Область техники изобретения
Настоящее изобретение относится к новому пептиду, который можно использовать в качестве пептида ракового антигена. Более конкретно, настоящее изобретение предлагает новый раковый пептидный антиген, содержащий 5 соединенных пептидов, способных индуцировать HLA-A-ограниченные CTL-ответы, а также фармацевтическую композицию, содержащую указанный антиген.
Уровень техники изобретения
Рак является основной причиной смерти в Японии. Примерно 350000 пациентов умирает от рака каждый год и в настоящее время рак еще остается серьезным заболеванием. Основные общепризнанные методы лечения рака включают в себя хирургическое удаление, лечение противораковыми препаратами и облучение. Однако такие стратегии лечения имеют недостатки, включающие в себя, например, рецидивы, ухудшение качества жизни (QOL) и отсутствие вариантов лечения в случае запущенных стадий рака, которые не поддаются лечению с помощью указанных выше стратегий.
Было выдвинуто предположение, что противораковую иммунотерапию (противораковые вакцины) можно использовать в качестве нового терапевтического метода в течение длительного периода времени, и в 1990-х годах, после идентификации пептидных эпитопов человеческих опухолевых антигенов, во всем мире начались исследования по разработке пептидных вакцин для лечения рака. Однако, в соответствии с результатами анализа клинических испытаний, проводимых путем введения пептида отдельно или в сочетании с другими средствами, величина ответа не превышала 2,7% в 1000 или более случаев (Rosenberg SA et al., Nature Med., 2004, 10(9): 909-15). Таким образом, были отмечены проблемы при практическом применении.
Тем временем в Японии в течение длительного периода времени проводятся клинические исследования по применению конкретных пептидных вакцин для лечения рака и постепенно раскрываются результаты таких исследований. В последние годы для улучшения результата лечения разрабатывается стратегия, связанная с ведением нескольких противораковых пептидов, вместо противоракового пептида одного типа. Например, предварительно анализируют антиген типа HLA и специфические иммунные ответы пациента, чтобы провести противораковое лечение по специальной схеме с использованием вакцин, содержащих несколько выбранных пептидов, подходящих для введения, и подтверждают их безопасность и противораковые эффекты. Более конкретно, введение специально изготовленных пептидных вакцин по отдельности, или в сочетании с противораковыми лекарственными средствами, дают превосходные результаты по клиническим эффектам и безопасности в случаях опухоли мозга, рака шейки матки, рака простаты и рака поджелудочной железы (Terasaki, M. Et al., J. Clin. Oncol., 2011, 29(3): 37-44; Noguchi, M. et al., Cancer Immunol. Immunother., 2010, 59(7): 1001-9; Yanagimoto, H. et al., Cancer Sci., 2007, 98(4): 605-11). Клеточный иммунитет, включающий в себя эпитоп-специфичные T-лимфоциты (далее обозначаемые CTL), которые рассматриваются как основные эффекторные клетки при лечении рака с использованием пептидных вакцин, является HLA-ограниченным. Соответственно, разработка пептидных вакцин для лечения рака была направлена исключительно на пациентов с конкретным типом HLA, таким как HLA-A2 или HLA-A24, поскольку он присутствует у большого числа пациентов.
Однако японцы, у которых присутствует HLA двух указанных типов, составляют примерно 40% и 60%, соответственно (Sette, A. Et al., Immunogenetics, 1999, 50(3-4) 201-12). Недостатком пептидных вакцин для лечения рака является то, что они не могут вызывать улучшение у пациентов с HLA других типов. Кроме того, начало лечения может откладываться из-за HLA-типирования, проводимого перед началом лечения, повышая нагрузку на пациентов. Следовательно, требуется проведение исследований и разработка пептидных вакцин для лечения рака, которые можно использовать для всех раковых пациентов без типирования по HLA.
Пептидные вакцины, используемые для лечения рака, помимо активации CTL, необходимой для развития клеточного иммунитета, индуцируют продукцию иммуноглобулинов, известную как гуморальный иммунитет, которую связывают с повышением выживания (Noguchi, M. et al., Cancer Biol. Ther., 2011, 10 (12): 1266-79).
Сущность изобретения
Цели настоящего изобретения
Целью настоящего изобретения является получение пептидного ракового антигена, который можно вводить в качестве пептидной вакцины для лечения рака широкому ряду раковых пациентов без необходимости HLA-типирования и независимо от типов HLA у пациентов.
Средства достижения целей
Авторами настоящего изобретения были проведены исследования, направленные на достижение вышеуказанных целей. В результате авторы обнаружили, что пептид, имеющий 5 соединенных эпитопов CTL, полученный путем соединения через линкеры 5 пептидов, выбранных из эпитопных пептидов CTL, которые, как описано, способны индуцировать CTL-ответ, ограниченный супертипом HLA-A2, HLA-A24, HLA-A26 или HLA-A3, или совокупность HLA-A-ограниченных CTL-ответов, можно вводить широкому ряду раковых пациентов без необходимости HLA-типирования и независимо от типов HLA у пациентов. Авторы также обнаружили, что введение такого пептида, содержащего 5 соединенных эпитопов CTL, может эффективно индуцировать CTL и иммуноглобулины, специфичные к пептидным эпитопам CTL, составляющим такой пептид. Таким образом авторы завершили настоящее изобретение.
Конкретно настоящее изобретение имеет нижеследующие признаки.
[1] Пептид, имеющий 5 эпитопов, соединенных через линкеры, где 5 эпитопов выбраны, необязательно с дублированием, из группы, включающей в себя следующие пептидные эпитопы CTL: пептид, описанный в SEQ ID NO: 1 (PEP1); пептид, описанный в SEQ ID NO: 2 (PEP2); пептид, описанный в SEQ ID NO: 3 (PEP3); пептид, описанный в SEQ ID NO: 4 (PEP4); пептид, описанный в SEQ ID NO: 5 (PEP5); пептид, описанный в SEQ ID NO: 6 (PEP6); и пептид, описанный в SEQ ID NO: 7 (PEP7); и
пептид, имеющий 5 соединенных эпитопов, характеризуется одним или несколькими из приведенных ниже признаков (1)-(12):
(1) пептид содержит последовательность, состоящую из PEP5 и PEP2, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(2) пептид содержит последовательность, состоящую из PEP2 и PEP4, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(3) пептид содержит последовательность, состоящую из PEP4 и PEP6, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(4) пептид содержит последовательность, состоящую из PEP6 и PEP3, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(5) пептид содержит последовательность, состоящую из PEP4 и PEP1, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(6) пептид содержит последовательность, состоящую из PEP1 и PEP3, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(7) пептид содержит последовательность, состоящую из PEP4 и PEP2, соединенных последовательно через линкер в указанном порядке, начиная от N-конца; -
(8) пептид содержит последовательность, состоящую из PEP1 и PEP4, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(9) пептид содержит последовательность, состоящую из PEP5 и PEP1, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(10) пептид содержит последовательность, состоящую из PEP6 и PEP5, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(11) пептид содержит PEP2 на C-конце; и
(12) пептид содержит PEP3 на C-конце.
[2] Пептид, имеющий 5 соединенных эпитопов, по пункту [1], который на N-конце содержит последовательность, состоящую из PEP5 и PEP2, PEP6 и PEP5, или PEP4 и PEP6, соединенных последовательно через линкер в указанном порядке, начиная от N-конца, и/или на C-конце последовательность, состоящую из PEP7 и PEP3, PEP4 и PEP3, PEP6 и PEP3, PEP1 и PEP3, PEP5 и PEP2, PEP4 и PEP2, или PEP5 и PEP3, соединенных последовательно через линкер в указанном порядке, начиная от N-конца.
[3] Пептид, имеющий 5 соединенных эпитопов, по пункту [2], который содержит последовательность, выбранную из приведенных ниже последовательностей (a)-(p):


где “-”обозначает линкер.
[4] Пептид, имеющий 5 соединенных эпитопов, по любому из пунктов [1]-[3], где линкер представляет собой аминокислотный линкер.
[5] Пептид, имеющий 5 соединенных эпитопов, по пункту [4], где аминокислотный линкер представляет собой димер аргинина, состоящий из двух остатков аргинина, соединенных друг с другом.
[6] CTL, полученный в результате стимуляции лимфоцитов периферической крови пептидом, имеющим 5 соединенных эпитопов, по любому из пунктов [1]-[5].
[7] Фармацевтическая композиция, используемая для лечения или профилактики рака, которая содержит, в качестве активного ингредиента, пептид, имеющий 5 соединенных эпитопов, по любому из пунктов [1]-[5], или CTL по пункту [6].
[8] Фармацевтическая композиция по пункту [7], которая представляет собой иммунотерапевтическое средство.
[9] Способ лечения рака, включающий в себя введение раковому пациенту пептида, имеющего 5 соединенных эпитопов, по любому из пунктов [1]-[5], или CTL по пункту [6].
[10] Способ противораковой иммунизации индивидуума, включающий в себя введение индивидууму пептида, имеющего 5 соединенных эпитопов, по любому из пунктов [1]-[5], или CTL по пункту [6].
Данное описание включает в себя частично или полностью содержание, раскрытое в описании и/или чертежах патентной заявки Японии № 2013-047271, которая является приоритетным документом по отношению к настоящей заявке.
Результаты изобретения
Настоящее изобретение предлагает пептид ракового антигена, который можно водить широкому ряду раковых пациентов в качестве пептидной вакцины против рака без необходимости HLA-типирования и независимо от типов HLA у пациентов.
Пептид, имеющий 5 соединенных эпитопов CTL, в соответствии с настоящим изобретением можно водить широкому ряду раковых пациентов без необходимости HLA-типирования. Примеры таких пациентов включают в себя пациентов, положительных по супертипу HLA-A2, пациентов, положительных по супертипу HLA-A24, пациентов, положительных по супертипу HLA-A26 и пациентов, положительных по супертипу HLA-A3. Описанный выше пептид можно использовать для лечения и/или профилактики у таких пациентов рака или вызываемых им заболеваний. Кроме того, экспрессия опухолевых антигенов, составляющих пептид настоящего изобретения, имеющий 5 соединенных эпитопов CTL, наблюдается при нескольких типах рака. Соответственно, пептид настоящего изобретения, имеющий 5 соединенных эпитопов CTL, можно использовать в виде фармацевтической композиции (более конкретно, в виде иммунотерапевтического средства) для лечения или профилактики ряда раковых заболеваний. Введение пептида настоящего изобретения, имеющего 5 соединенных эпитопов CTL, приводит к более интенсивной продукции CTL и иммуноглобинов, специфичных к пептидным эпитопам CTL, и к более эффективной активации противоопухолевого иммунитета, чем введение смеси эквивалентных количеств пептидных эпитопов CTL.
Краткое описание чертежей
На фиг. 1 показаны результаты определения индукции эпитоп-специфичных CTL у мышиных моделей, которым вводят пептид, имеющий 5 соединенных эпитопов (*: неисследованный).
На фиг. 2 показаны результаты определения титра эпитоп-специфичных антител IgG в сыворотке мышиных моделей, которым вводят пептид, имеющий 5 соединенных эпитопов.
Варианты осуществления изобретения
Далее настоящее изобретение описывается более подробно.
1. Пептид, имеющий 5 соединенных эпитопов
В соответствии с настоящим изобретением "пептид, имеющий 5 соединенных эпитопов" включает в себя 5 пептидов, выбранных из пептидных эпитопов CTL, присутствующих на одной молекуле опухолевого антигена и/или на разных молекулах опухолевых антигенов, линейно связанные через линкеры в составе одной молекулы.
"Пептидный эпитоп CTL, полученный из молекулы опухолевого антигена" представляет собой пептид, образовавшийся в результате разложения опухолевого антигена в опухолевой клетке, связанный с молекулой HLA класса I и презентированный на поверхности клетки. Следовательно, он распознается опухолеспецифическими CTL, и/или может индуцировать и/или активировать опухолеспецифические CTL. "Индукция опухолеспецифических CTL" включает в себя дифференциацию и/или пролиферацию CTL, способных специфически распознавать пептидные эпитопы CTL, полученные из молекул опухолевых антигенов in vitro или in vivo. А "активация опухолеспецифических CTL" включает в себя продукцию интерферона-γ (IFN-γ) после того, как CTL распознает антиген, презентированный молекулой HLA класса I. В настоящем описании выражение "пептидный эпитоп CTL, полученный из молекулы опухолевого антигена" иногда используется как эквивалентное выражению "пептидный эпитоп CTL".
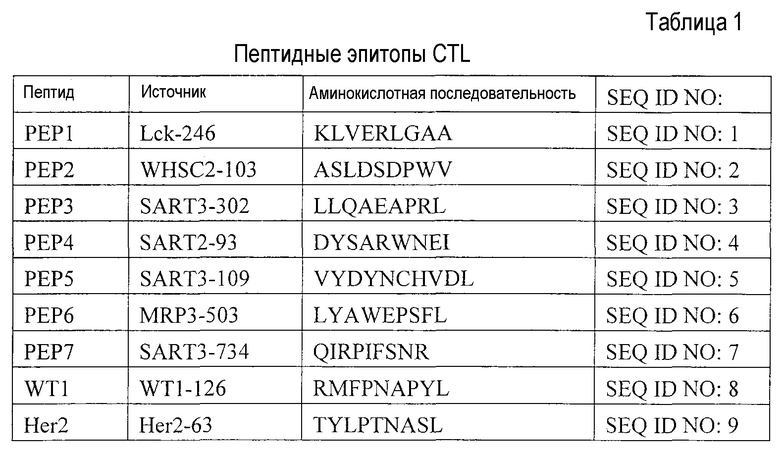
В качестве пептидных эпитопов CTL настоящего изобретения можно использовать известные пептиды, примеры которых включают в себя:
PEP1: KLVERLGAA (SEQ ID NO: 1 [WO 01/011044]);
PEP2: ASLDSDPWV (SEQ ID NO: 2 [WO 02/010369]);
PEP3: LLQAEAPRL (SEQ ID NO: 3 [WO 00/12701]);
PEP4: DYSARWNEI (SEQ ID NO: 4 [JP H11-318455A(1999)]);
PEP5: VYDYNCHVDL (SEQ ID NO: 5 [WO 00/12701]);
PEP6: LYAWEPSFL (SEQ ID NO: 6 [JP 2003-000270 A]);
PEP7: QIRPIFSNR (SEQ ID NO: 7 [Cancer Immunol, lmmunother., 2007, 56 (5), 689-698]).
В данном описании пептид, описанный в SEQ ID NO: 1, пептид, описанный в SEQ ID NO: 2, пептид, описанный в SEQ ID NO: 3, пептид, описанный в SEQ ID NO: 4, пептид, описанный в SEQ ID NO: 5, пептид, описанный в SEQ ID NO: 6, и пептид, описанный в SEQ ID NO: 7, иногда обозначают "PEP1", "PEP2", "PEP3", "PEP4", "PEP5", "PEP6" и "PEP7", соответственно.
В соответствии с настоящим изобретением в качестве "пептидного эпитопа CTL" можно использовать пептид, который содержит замену, инсерцию, делецию и/или добавление одной или нескольких аминокислот в аминокислотной последовательности PEP1, PEP2, PEP3, PEP4, PEP5, PEP6 или PEP7, и обладает способностью индуцировать CTL и способностью индуцировать продукцию иммуноглобулинов, эквивалентной способности исходного пептида, или превышающей ее. Термин "несколько" в данном случае относится к числу от 1 до 3, предпочтительно, к числу, равному 1 или 2. Примером такого пептида является пептид, полученный путем введения в качестве замены аминокислот, свойства которых подобны свойствам исходных аминокислот (т.е., пептид, полученный в результате консервативных аминокислотных замен).
PEP1, PEP2, PEP3, PEP4 и PEP5 улавливаются супертипом HLA-A2, PEP2, PEP4, PEP5 и PEP6 улавливаются супертипом HLA-A24, PEP2, PEP4, PEP5 и PEP7 улавливаются супертипом HLA-A3, PEP2 и PEP5 улавливаются супертипом HLA-A26, после чего может происходить индукция и/или активация CTL. Экспрессия генов, кодирующих такие пептидные эпитопы CTL, наблюдается при раковых заболеваниях нескольких типов (Yang, D. et al., Cancer Res., 1999, 59: 4056-63; Harashima, N. et al., Eur. J. Immunol., 2001, 31 (2), 323-32).
Пять пептидов, выбранных, необязательно с дублированием, из PEP1, PEP2, PEP3, PEP4, PEP5, PEP6 и PEP7, оединены линейно через линкеры.
Можно использовать любой линкер при условии, что он расщепляется после введения пептида, имеющего 5 соединенных эпитопов, в организм, с отделением пептидных эпитопов CTL друг от друга. Примеры способных к расщеплению элементов включают в себя сложноэфирную связь, эфирную связь, амидную связь, линкер, представляющий собой сахарную цепь, полиэтиленгликолевый линкер и аминокислотный линкер. Примеры аминокислотных последовательностей, используемых в качестве аминокислотных линкеров, включают в себя димер аргинина, димер лизина, димер глицина, пентамер глицина, гексамер глицина, аланин-аланин-тирозин (AAY), изолейцин-лейцин-аланин (ILA) и аргинин-валин-лизин-аргинин (RVKR), среди которых предпочтительным является димер аргинина.
Выбор пептидных эпитопов CTL и их порядок можно определить путем введения пептида, имеющего 5 соединенных эпитопов, полученного путем синтеза эпитопов в заданном сочетании и в заданном порядке, мышам, трансгенным по человеческому HLA-A, и оценки индукции CTL, специфичных к пептидным эпитопам CTL, in vivo.
Предпочтительно пептид настоящего изобретения, имеющий 5 соединенных эпитопов, характеризуется одним или несколькими из приведенных ниже признаков (1)-(12):
(1) пептид содержит последовательность, состоящую из PEP5 и PEP2, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(2) пептид содержит последовательность, состоящую из PEP2 и PEP4, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(3) пептид содержит последовательность, состоящую из PEP4 и PEP6, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(4) пептид содержит последовательность, состоящую из PEP6 и PEP3, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(5) пептид содержит последовательность, состоящую из PEP4 и PEP1, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(6) пептид содержит последовательность, состоящую из PEP1 и PEP3, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(7) пептид содержит последовательность, состоящую из PEP4 и PEP2, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(8) пептид содержит последовательность, состоящую из PEP1 и PEP4, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(9) пептид содержит последовательность, состоящую из PEP5 и PEP1, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(10) пептид содержит последовательность, состоящую из PEP6 и PEP5, соединенных последовательно через линкер в указанном порядке, начиная от N-конца;
(11) пептид содержит PEP2 на C-конце; и
(12) пептид содержит PEP3 на C-конце.
Предпочтительно пептид настоящего изобретения, имеющий 5 соединенных эпитопов, содержит: (I) на N-конце последовательность, состоящую из PEP5 и PEP2, PEP6 и PEP5, или PEP4 и PEP6, соединенных последовательно через линкер в указанном порядке, начиная от N-конца; и/или (II) на C-конце последовательность, состоящую из PEP7 и PEP3, PEP4 и PEP3, PEP6 и PEP3, PEP1 и PEP3, PEP5 и PEP2, PEP4 и PEP2, или PEP5 и PEP3, соединенных последовательно через линкер в указанном порядке, начиная от N-конца.
Более предпочтительно, пептид настоящего изобретения, имеющий 5 соединенных эпитопов, содержит последовательность, или состоит из последовательности, выбранной из приведенных ниже последовательностей (a)-(p), где “-” обозначает линкер:


Пептид настоящего изобретения, имеющий 5 соединенных эпитопов, с помощью которого можно индуцировать и/или активировать CTL, специфичные к пептидным эпитопам CTL, и индуцировать иммуноглобулины, специфичные к соответствующему пептидному эпитопу CTL, предпочтительно включает в себя два типа, более предпочтительно, три типа, еще более предпочтительно 4 типа, и наиболее предпочтительно 5 типов пептидных эпитопов CTL из 5 соединенных типов пептидных эпитопов CTL. В настоящем изобретении термин "иммуноглобулины" относится к IgG, IgM, IgA или IgD.
2. Получение пептида, имеющего 5 соединенных эпитопов
Пептид настоящего изобретения, имеющий 5 соединенных эпитопов, можно получить с помощью традиционных методов, включающих в себя, например, пептидный синтез, такой как жидкофазный синтез или твердофазный синтез, или пептидный синтез с помощью автоматизированного пептидного синтезатора (Kelley et al., Genetics Engineering Principles и Methods, Setlow, J. K. eds., Plenum Press NY., 1990, Vol. 12, pp. 1-19; Stewart et al., Solid-Phase Peptide Synthesis, 1989, W. H. Freeman Co.; Houghten, Proc. Natl. Acad. Sci., U.S.A., 1985, 82: p. 5132, "Shin Seikagaku Jikken Kouza (New Biochemical Experiment) 1, Protein IV, 1992, the Japanese Biochemical Society (ed.), Tokyo Kagaku Doujin). Пептидный синтез проводят путем получения аминокислот, в которых функциональные группы, отличные от α-аминогрупп и α-карбоксильных групп, используемых для соединения аминокислот, защищены, с последующим образованием пептидных связей между α-аминогруппами и α-карбоксильными группами аминокислот. Как правило, карбоксильную группу аминокислотного остатка, расположенного на C-конце пептида, присоединяют к твердой фазе через подходящий спейсер или линкер. Защитную группу на амино-конце дипептида, полученного по описанному выше способу, селективно удаляют и проводят реакцию образования пептидной связи между амино-концом и α-карбоксильной группой следующего аминокислотного остатка. Данную процедуру повторяют до получения пептида, содержащего защищенные боковые группы, после чего все защитные группы удаляют и на завершающей стадии полученный пептид отделяют от твердой фазы. Типы защитных групп, способы их получения и способы образования пептидных связей подробно описаны в указанных выше документах.
Альтернативно пептид можно получить методом генетической рекомбинации с использованием нуклеиновой кислоты, кодирующей пептид настоящего изобретения, имеющий 5 соединенных эпитопов, фагового дисплея, или с помощью других методов.
Метод генетической рекомбинации включает в себя вставку ДНК, кодирующей пептид настоящего изобретения, имеющий 5 соединенных эпитопов, в подходящий вектор экспрессии, введение вектора в подходящие клетки-хозяева, культивирование клеток и извлечение целевых пептидов из клеток или внеклеточной жидкости. Примеры векторов включают в себя, без ограничения, плазмиды, фаги, космиды, фагмиды и вирусные векторы. Векторы вводят в клетки-хозяева, такие как бактериальные клетки-хозяева (например, E. coli и Bacillus subtilis), дрожжевые клетки, клетки насекомых, клетки животных (например, клетки млекопитающих) и клетки растений. Трансформацию или трансфекцию таких клеток проводят, например, с помощью кальций-фосфатного метода, электропорации, липофекции, метода генной пушки, или с использованием ПЭГ. Трансформированные клетки культивируют с помощью метода, традиционно используемого для культивирования организмов-хозяев. Экспрессируемый пептид предпочтительно секретируется во внеклеточную среду, что позволяет облегчить извлечение пептида настоящего изобретения. Для достижения секреции ДНК, кодирующую пептидную последовательность, которая обеспечивает секрецию пептида из клеток, присоединяют к 5'-концевому фрагменту ДНК, кодирующей целевой пептид. Альтернативно можно выделять целевой пептид, накапливающийся в клетках. В таком случае клетки разрушают физическим или химическим способом и целевой пептид извлекают, используя методы очистки белков.
Полученный таким образом пептид можно выделить или очистить с помощью традиционных методов, таких как хроматографические методы, например, гель-фильтрационная хроматография, ионообменная колоночная хроматография, аффинная хроматография, колоночная хроматография на обращенной фазе, или ВЭЖХ, фракционирование сульфатом аммония, ультрафильтрация или иммуноадсорбция.
3. Цитотоксические T-лимфоциты
С использованием пептида настоящего изобретения, имеющего 5 соединенных эпитопов, можно получить CTL, специфичные к пептидному эпитопу CTL, которые способны разрушать раковые клетки, in vitro. В настоящем изобретении можно использовать описанный (например, в JP 2006-14637 A) способ индуцирования CTL с использованием пептидного эпитопа CTL in vitro. Например, мононуклеарные клетки периферической крови (PBMC), полученные от здоровых индивидуумов или раковых пациентов, высевают с прикреплением и культивируют в присутствии цитокинов, таких как GM-CSF или IL-4, чтобы индуцировать дендритные клетки (DC). Дендритные клетки сенсибилизируют пептидом настоящего изобретения, имеющим 5 соединенных эпитопов, и затем подвергают воздействию рентгеновского облучения, чтобы получить антиген-презентирующие клетки (стимуляторы). Если DC нельзя использовать, пептидом настоящего изобретения, имеющим 5 соединенных эпитопов, сенсибилизируют мононуклеарные клетки периферической крови (PBMC), полученные от здоровых индивидуумов или таких же раковых пациентов, с последующим воздействием рентгеновского облучения, и используют полученные клетки. Затем добавляют мононуклеарные клетки периферической крови (PBMC), полученные от здоровых индивидуумов, или мононуклеарные клетки периферической крови (PBMC) или лимфоциты из соответствующих лимфатических узлов (т.е., клетки-респондеры), полученные от раковых пациентов, и культивируют в присутствии цитокинов, таких как IL-2, IL-4 или IL-7. Затем антиген-перзентирующие клетки, полученные путем описанной выше сенсибилизации, снова стимулируют путем добавления пептида настоящего изобретения, имеющего 5 соединенных эпитопов, и культивируют в присутствии цитокинов, таких как IL-2.
В качестве культуральной среды для индукции CTL можно использовать любую среду, в которой могут жить T-лимфоциты. Например, можно использовать среду, полученную путем добавления разных цитокинов (например, IL-2) и фетальной телячьей сыворотки (FCS) к среде RHAMα (среда LAK, описанная в Kawai, K., Sasaki, T., Saijo-Kurita, K., Akaza, H., Koiso, K., и Ohno, T., Cancer Immunol. Immunother., 35, 225-229, 1992), среде AIMV (GIBCO BRL, Life Technologies, INC.), или среде RPMI 1640.
Культивирование можно проводить в условиях, хорошо известных в данной области. Например, температура культивирования составляет от 33°C до 41°C, предпочтительно 37°C. В качестве газообразной фазы можно использовать инертный газ, содержащий воздух или кислород в подходящей концентрации, и диоксид углерода в подходящей концентрации (например, 5% CO2), чтобы довести pH среды примерно до 7,4. Культивирование предпочтительно проводят в течение периода от 4 до 10 дней, более предпочтительно, в течение 7 дней. Некоторые CTL, индуцированные путем такого культивирования, являются специфичными к пептидным эпитопам CTL, предпочтительно относящимся к двум типам, более предпочтительно, к трем типам, еще более предпочтительно, к четырем типам, и, наиболее предпочтительно, к пяти типам пептидных эпитопов CTL, выбранным из пяти типов пептидных эпитопов CTL, составляющих пептид, имеющий 5 соединенных эпитопов, и, следовательно, они могут специфически разрушать раковые клетк.
4. Фармацевтическая композиция
Пептид настоящего изобретения, имеющий 5 соединенных эпитопов, можно использовать в качестве активного ингредиента фармацевтической композиции для противораковой иммунотерапии.
Фармацевтическая композиция настоящего изобретения может содержать, в качестве активного ингредиента (активных ингредиентов), один или несколько из пептидов, имеющих 5 соединенных эпитопов. Так, в результате включения в состав композиции нескольких пептидов, имеющих 5 соединенных эпитопов, можно ожидать более интенсивные эффекты.
Экспрессия генов, кодирующих PEP1, PEP2, PEP3, PEP4, PEP5, PEP6 и PEP7, входящих в состав пептида настоящего изобретения, имеющего 5 соединенных эпитопов, наблюдается при нескольких типах солидного рака и рака крови. Примеры солидного рака включают в себя опухоль мозга, рак легкого, рак молочной железы, рак щитовидной железы, рак шейки матки, рак тела матки, рак яичника, рак пищевода, рак желудка, GIST, рак поджелудочной железы, рак толстой кишки, рак прямой кишки, рак анального канала, рак почки, рак печени, рак желчных протоков, рак головы и шеи, рак мочевого пузыря, рак простаты, злокачественную меланому, рак кожи, рак языка, остеосаркому, хондросаркому, фибросаркому, липосаркому, ангиосаркому, рабдомиобластому и лейомиосаркому. Примеры рака крови включают в себя лейкоз, злокачественную лимфому и миелому. Соответственно, пептид настоящего изобретения, имеющий 5 соединенных эпитопов, можно использовать для лечения или профилактики таких раков. В данном описании термин "лечение или профилактика рака" относится к предотвращению развития/рецидива рака, подавлению развития/обострения рака, или улучшению состояния рака.
Фармацевтическая композиция настоящего изобретения может содержать фармацевтически приемлемые вещества, такие как разные, традиционно используемые органические или неорганические носители. Примеры подходящих для применения фармацевтических носителей включают в себя стабилизаторы, противобактериальные средства, буферы, средства, придающие изотоничность, хелатирующие средства, средства, регулирующие pH, поверхностно-активные вещества, наполнители, загустители, связующие средства, увлажнители, дезинтегрирующие средства, поверхностно-активные вещества, смазывающие средства, успокаивающие средства, разбавители и наполнители, которые обычно используются в соответствии со способом введения соответствующего фармацевтического препарата. Фармацевтические препараты предпочтительно получают в виде композиций, содержащих такие носители, с помощью традиционных способов.
Фармацевтическая композиция настоящего изобретения может содержать адъювант, традиционно используемый при введении вакцины. Примеры адъювантов включают в себя полный адъювант Фрейнда (CFA), неполный адъювант Фрейнда (IFA), алюминиевые квасцы, липид A, монофосфориллипид A, бактериальные препараты, такие как БЦЖ (бацилла Кальметта-Герена), препараты бактериальных компонентов, такие как туберкулин, природные полимеры, такие как гемоцианин лимфы улитки и дрожжевой маннан, мурамилтрипептид, мурамилдипептид, или их производные, алюминиевые квасцы, и неионные блок-сополимеры. Указанные адъюванты можно использовать по отдельности или в сочетаниях, содержащих два адъюванта или более. Адъюванты можно вводить одновременно с фармацевтической композицией настоящего изобретения в виде смеси или в виде эмульсии.
Помимо пептида, имеющего 5 соединенных эпитопов, фармацевтическая композиция настоящего изобретения может содержать один или несколько известных пептидных эпитопов CTL, полученных из молекул опухолевых антигенов, пептид, содержащий такие эпитопы, или пептид, содержащий пептидные эпитопы CTL, связанные друг с другом (далее называемые "известные пептидные эпитопы CTL, полученные из молекул опухолевых антигенов"). Примеры известных пептидных эпитопов CTL, полученных из молекул опухолевых антигенов, включают в себя, без ограничения, WT-1 p126-134, модифицированный (M236Y) WT-1 p235-243, NY-ESO-1 p157-165, модифицированный (T210M) gp100 p209-217, сурвивин-2B p80-88, Her-2/neu p63-71, VEGFR2 p169-177, MART-1 p26-35, глипикан-3 p298-306, и SPARC p143-151. В данном случае пептид настоящего изобретения, имеющий 5 соединенных эпитопов, и известные пептидные эпитопы CTL, полученные из молекул опухолевых антигенов, могут входить в состав одного препарата. Альтернативно препарат, содержащий в качестве активного ингредиента пептид настоящего изобретения, имеющий 5 соединенных эпитопов, можно использовать отдельно от препарата, содержащего в качестве активного ингредиента известные пептидные эпитопы CTL, полученные из молекул опухолевых антигенов.
Форму фармацевтической композиции настоящего изобретения выбирают в зависимости от способа введения. Типичные примеры лекарственных форм включают в себя, без ограничения, жидкие препараты, эмульсии, липосомальные препараты, липидные эмульсии, комплексы включения на основе циклодекстринов, суспензии, мази, кремы, чрезкожно абсорбируемые препараты, трансмукозально абсорбируемые препараты, таблетки, пилюли, капсулы, порошки, порошкообразные лекарственные средства, гранулы, мелкозернистые препараты и сиропы. В соответствии со способом введения такие лекарственные формы дополнительно подразделяют, например, на пероральные препараты, парентеральные препараты, трансназальные препараты, трансвагинальные препараты, суппозитории, подъязычные препараты, препараты для ингаляций, глазные капли или ушные капли, причем указанные препараты можно объединять, формовать, или получить с помощью традиционных методов. Помимо применения в жидком виде, такие препараты можно лиофилизировать с получением фармацевтического препарата, способного хорошо храниться. Перед применением такой фармацевтический препарат можно растворить, например, в буфере, содержащем воду и физиологический раствор, с получением подходящей концентрации.
Фармацевтическая композиция настоящего изобретения может содержать в качестве активного ингредиента CTL, индуцированные in vitro пептидом настоящего изобретения, имеющим 5 соединенных эпитопов. Такую фармацевтическую композицию предпочтительно получают в виде парентерального препарата.
5. Способ лечения
Фармацевтическую композицию настоящего изобретения можно вводить широкому ряду раковых пациентов, таких как пациенты, положительные по типам HLA, выбранным из группы, включающей в себя супертипы HLA-A2, HLA-A24, HLA-A26 и HLA-A3, причем лечение можно начинать без предварительного типирования по HLA.
При введении фармацевтической композиции настоящего изобретения раковому пациенту может происходить индукция и/или активация GTL, специфичных к двум или более, предпочтительно к 3 или более, более предпочтительно к 4 или более, и еще более предпочтительно к 5 или более типам пептидных эпитопов CTL, составляющих пептид, имеющий 5 соединенных эпитопов, входящий в состав фармацевтической композиции в качестве активного ингредиента. Кроме того, может индуцироваться продукция иммуноглобулинов, специфичных к соответствующим пептидным эпитопам CTL. Уровень индуцирования продукции иммуноглобулинов после введения пептида, имеющего 5 соединенных эпитопов, в качестве активного ингредиента, значительно превышает уровень индуцирования продукции иммуноглобулинов, наблюдающийся после введения смеси пептидных эпитопов CTL, входящих в состав пептида, имеющего 5 соединенных эпитопов, но не связанных друг с другом. Соответственно, с помощью пептида настоящего изобретения, имеющего 5 соединенных эпитопов, можно эффективно лечить или предотвращать рак у ракового пациента.
Способы введения фармацевтической композиции настоящего изобретения включают в себя, например, пероральное введение, внутривенное введение, внутриартериальное введение, внутримышечное введение, подкожное введение, внутрикожное введение, сублингвальное введение, внутрибрюшинное введение, ректальное введение, чрезкожное введение, трансмукозальное введение, трансназальное введение, трансвагинальное введение, глазное введение или введение путем вдыхания. Если препараты, содержащие в качестве активных ингредиентов несколько пептидов, имеющих 5 соединенных эпитопов, или известные пептидные эпитопы CTL, полученные из молекул опухолевых антигенов, используют в виде отдельных фармацевтических композиций, такие фармацевтические композиции можно вводить одновременно или не одновременно с помощью одинаковых или разных способов.
Дозу фармацевтической композиции настоящего изобретения можно корректировать в соответствии с таким факторами, как патологический статус/тяжесть рака, подлежащего лечению, возраст пациента, или масса пациента. Например, фармацевтическую композицию, содержащую пептид, который состоит из 5 соединенных эпитопов, можно вводить в количестве от 0,0001 мг до 1000 мг, предпочтительно от 0,001 мг до 100 мг, и более предпочтительно от 0,01 мг до 50 мг, один раз каждые несколько дней, каждые несколько недель, или каждые несколько месяцев. Если фармацевтическая композиция настоящего изобретения содержит в качестве активных ингредиентов CTL, индуцированные in vitro пептидом настоящего изобретения, имеющим 5 соединенных эпитопов, предпочтительно вводят от 2×106 до 2×108 CTL на кг массы тела в день с интервалами от 1 до 2 недель.
Фармацевтическую композицию настоящего изобретения можно вводить раковому пациенту в сочетании с фармацевтическими продуктами, широко используемыми для противораковой химиотерапии. Примеры таких фармацевтических продуктов включают в себя: алкилирующие средства, такие как циклофосфамид, темозоломид и бендамустин; антиметаболиты, такие как тегафур-урацил, тегафур-гимерацил-отерацил калия, метатрексат и гемцитабин; платина-содержащие средства, такие как цисплатин и оксалиплатин; препараты, содержащие алкалоиды растений, такие как иринотекан, эрибулин, паклитаксел, дорцетаксел и винкристин; канцеростатические антибиотики, такие как доксорубицин, блеомицин и актиномицин D; лекарственные средства, направленные на молекулярные мишени, такие как иматиниб, сунитиниб, гефитиниб, сорафениб, эверолимус, трастузумаб, бевацизумаб, ритуксимаб, цетуксимаб, панитумумаб и могамулизумаб; а также гормональные терапевтические средства, такие как бикалутамид, эстрамустин и эксеместан. Такие фармацевтические продукты и фармацевтическую композицию настоящего изобретения можно вводить одновременно или не одновременно с помощию одинаковых или разных способов введения.
Далее настоящее изобретение описывается более подробно с помощью нижеследующих примеров, которые никоим образом не предназначены для ограничения настоящего изобретения.
Примеры
Пример 1: Синтез и очистка пептидов
Пептидные эпитопы CTL и пептиды, имеющие 5 соединенных эпитопов, синтезируют с помощью коммерчески доступного пептидного синтезатора (Prelude, Protein Technologies, Inc.) методом твердофазного синтеза (Fmoc). Полученные разные синтетические пептиды очищают с использованием колонки YMC-Pack Pro C18 (YMC Co., Ltd.) и системы ВЭЖХ (Gilson), лиофилизируют, хранят при низкой температуре в темноте и затем используют в описанных ниже примерах.
В таблице 1 приведены аминокислотные последовательности синтезированных пептидных эпитопов CTL, а в таблице 2 приведены аминокислотные последовательности пептидов, имеющих 5 соединенных эпитопов.
WT1 (SEQ ID NO: 8) синтезируют в качестве контрольного пептида, способного связываться с HLA-A2, а Her2 (SEQ ID NO: 9) синтезируют в качестве контрольного пептида, способного связываться с HLA-A24.
Пример 2: Индукция у мышиной модели CTL, специфичных к пептидным эпитопам, и детекция CTL с использованием ELISPOT
Пептиды, имеющие 5 соединенных эпитопов, растворяют в дистиллированной воде Оцука (Otsuka Pharmaceutical Factory Inc.) с получением концентрации 2 мг/мл или 4 мг/мл, после чего полученный раствор помещают в шприц B Braun Injekt. Другой шприц заполняют равным количеством неполного адъюванта Фрейнда (IFA), затем шприцы соединяют с помощью коннектора для шприцев GP и раствор пептидов, имеющих 5 соединенных эпитопов, тщательно перемешивают с IFA до получения эмульсии. Эмульсию еженедельно вводят каждой мыши в количестве 100 мкл вблизи основания хвоста (используют мышей, трансгенных по HLA-A2.1 и HLA-A24 (Taconic)), всего проводят два введения. Через 1 неделю после последнего введения обследуют паховые лимфатические узлы мышей. Суспензию клеток лимфатического узла доводят до плотности 5×106 клеток/мл, используя полную среду (RPMI-1640, 10% инактивированной нагреванием FBS, 100 ед/мл пенициллина, 100 мкг/мл стрептомицина и 50 мкМ 2-меркаптоэтанол), добавляют целевой пептидный эпитоп CTL (конечная концентрация: 10 мкг/мл), рекомбинантный мышиный IL-15 (конечная концентрация: 100 нг/мл) и рекомбинантный мышиный IL-21 (конечная концентрация: 100 нг/мл), после чего клетки помещают в 24-луночный планшет в количестве 1 мл/лунку и культивируют в инкубаторе при 37°C в присутствии 5% CO2 в течение 8 дней. Затем клетки собирают и высевают в планшет, содержащий иммобилизованное антитело против IFN-γ, входящий в состав набора ELISpot для определения мышиного IFN-γ (GEN-PROBE), в количестве 1×105 клеток/лунку. Затем спленоциты, выделенные из селезенки изогенной мыши и получившие дозу рентгеновского излучения 30 Гр, высевают в тот же планшет в количестве 1×105 клеток/лунку как антиген-презентирующие клетки, добавляют целевой пептидный эпитоп CTL, или пептид, используемый в качестве отрицательного контроля (конечная концентрация: 10 мкг/мл), и инкубируют в инкубаторе при 37°C в присутствии 5% CO2 в течение ночи. На следующий день пятна клеток, продуцирующих IFN-γ, окрашивают в соответствии с инструкциями производителя. Число пятен IFN-γ-продуцирующих клеток определяют с помощью анализатора ELISPOT (Immunospot S6, Cellular Technology Ltd.). Индукцию CTL, специфичных к пептидному эпитопу CTL, определяют как положительную, если число пятен IFN-γ-продуцирующих клеток в лунках, содержащих целевые пептидные эпитопы CTL, значительно превышает число пятен, присутствующих в лунках, содержащих пептиды отрицательного контроля (критерий Стьюдента, p<0,05). В качестве пептида отрицательного контроля используют WT1 или Her2. Чтобы визуализировать уровень индукции CTL, результат нижеследующего уравнения обозначают "Δ" (среднее число пятен IFN-γ-продуцирующих клеток в лунках, содержащих целевые пептидные эпитопы CTL) - (среднее число пятен IFN-γ-продуцирующих клеток в лунках, содержащих пептиды отрицательного контроля). Результат считают положительным, если 10≤Δ<100; умеренно положительным, если 100≤Δ<200; и строго отрицательным, если 200≤Δ.
На фиг. 1 показаны результаты определения индукции CTL, специфичных к пептидному эпитопу CTL. Как показано на фиг. 1, пептид, имеющий 5 соединенных эпитопов, включающий в себя последовательность PEP5-RR-PEP2 или PEP4-RR-PEP2, или пептид, имеющий 5 соединенных эпитопов, с PEP3 на C-конце, индуцирует, по меньшей мере, 3 типа CTL. И наоборот, пептид, имеющий 5 эпитопов, такой как TPV18, индуцирует не более двух типов CTL.
Приведенные выше результаты демонстрируют, что введение мышам пептида, имеющего 5 соединенных эпитопов, полученного путем соединения известных пептидных эпитопов CTL через димеры аргинина, не всегда индуцирует эпитоп-специфичные CTL, специфичные ко всем пептидным эпитопам CTL.
Пример 3: Получение гранул с иммобилизованным пептидным эпитопом CTL
Пептиды иммобилизуют на микросферах xMAP Multi-Analyte COOH (Luminex Corporation; называемых далее "гранулы") с помощью описанного ниже способа. Гранулы промывают буфером MES (0,1M MES-NaOH; pH 7,0), супернатант удаляют путем центрифугирования. Указанный процесс промывания повторяют дважды и затем гранулы суспендируют в 75 мкл буфера MES. К суспензии гранул добавляют 100 мкл раствора пептидного эпитопа CTL (1 мг/мл) и 5 мкл раствора 10 мг/мл EDC (1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид), после чего тщательно перемешивают. Реакцию проводят в течение ночи при 30°C в темноте. На следующий день супернатант удаляют центрифугированием, добавляют 125 мкл 1M Tris-HCl и инкубируют при 30°C в темноте в течение 30 минут. Супернатант снова удаляют, гранулы дважды промывают буфером для промывания (PBS(-), 0,05% твин 20) и суспендируют в Immunoblock (DS Pharma Biomedical Co., Ltd.). Таким образом завершают иммобилизацию пептидного эпитопа CTL.
Пример 4: Измерение титра антител IgG, специфичных к эпитопу CTL
Пептиды настоящего изобретения, имеющие 5 соединенных эпитопов, растворяют в дистиллированной воде Оцука (Otsuka Pharmaceutical Factory Inc.) с получением концентрации 2 мг/мл, после чего полученный раствор помещают в шприц B Braun Injekt. Другой шприц заполняют равным количеством IFA, затем шприцы соединяют с помощью коннектора для шприцев GP и раствор пептидов, имеющих 5 соединенных эпитопов, тщательно перемешивают с IFA до получения эмульсии. Эмульсию еженедельно вводят в количестве 100 мкл вблизи основания хвоста каждой мыши CBF1 (C57BL/6×Balb/c F1), введение повторяют всего три раза. Через 1 неделю после последнего введения у мышей собирают кровь и получают образцы сыворотки. Контрольные образцы получают путем введения эмульсии, содержащей смесь пептидов PEP2, PEP3, PEP4, PEP5 и PEP7 (1 мг/мл каждого), по такой же схеме, что и пептид, имеющий 5 соединенных эпитопов (группа, получающая смесь).
Гранулы с иммобилизованными пептидными эпитопами CTL, разбавленные Immunoblock, распределяют в лунки 96-луночного фильтровального планшета. Распределенные гранулы промывают буфером для промывания, после чего во все лунки добавляют 100 мкл образцов мышиной сыворотки, разбавленных в 200 раз Immunoblock. Планшет инкубируют 90 минут при 30°C, перемешивая при 600 об/мин. После трехкратного промывания планшета буфером для промывания в каждую лунку добавляют 100 мкл биотинилированных антител против мышиных IgG (H+L) (Vector Laboratories), разведенных в 500 раз Immunoblock, и планшет инкубируют 60 минут при 30°C, перемешивая при 600 об/мин. После трехкратного промывания планшета буфером для промывания в каждую лунку добавляют 100 мкл конъюгата стрептавидин-R-фикоэритрин (Invitrogen), разведенного в 500 раз Immunoblock, и планшет инкубируют 30 минут при 30°C, перемешивая при 600 об/мин. После трехкратного промывания планшета буфером для промывания в каждую лунку добавляют 100 мкл буфера для промывания, чтобы суспендировать гранулы, и измеряют среднюю интенсивность флуоресценции PE, специфически связанного с соответствующими гранулами, используя систему Bio-Plex Suspension Array (BIO-RAD).
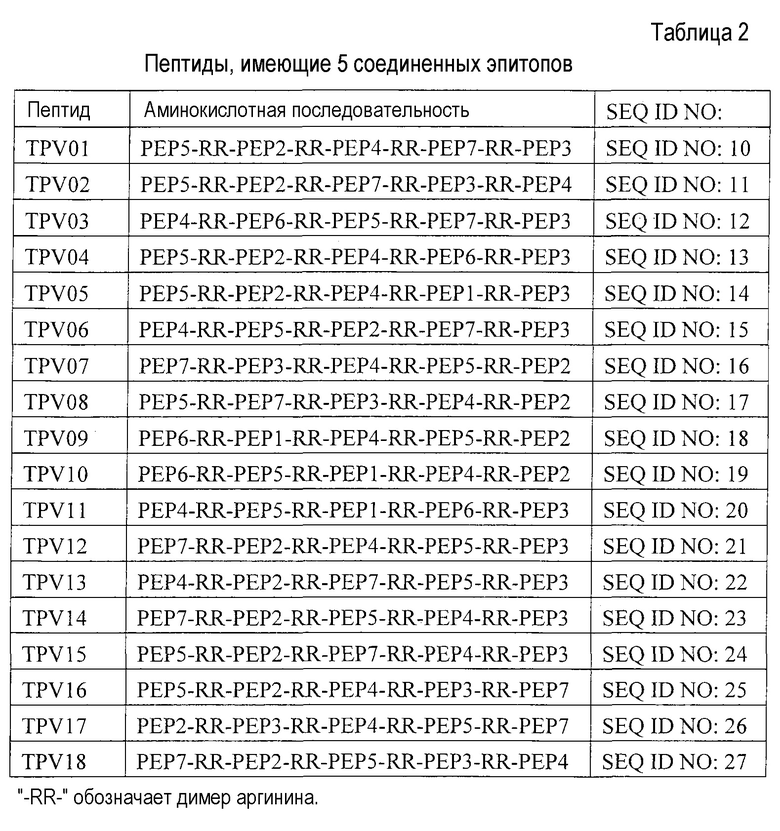
Результаты измерения титра IgG, специфичных к эпитопам CTL, приведены на фиг. 2. На фиг. 2 показана интенсивность продукции антител IgG, специфичных к пептидным эпитопам CTL, по сравнению с мышами из группы отрицательного контроля (далее обозначаемой как "группа IFA"). Результаты, полученные для мышей из группы IFA, которым вводят эмульсию, полученную путем смешивания равных количеств IFA и дистиллированной воды Оцука (Otsuka Pharmaceutical Factory Inc.), сравнивают с результатами, полученными путем введения по такой же схеме смеси пептидных эпитопов CTL или пептида, имеющего 5 соединенных эпитопов.
Как показано на фиг. 2, индуцирование продукции антител IgG, специфичных к эпитопам CTL, отсутствует в группе, получающей смесь, по сравнению с группой IFA. И наоборот, интенсивное индуцирование продукции антител IgG, специфичных к эпитопам CTL, часто наблюдается при введении пептида, имеющего 5 соединенных эпитопов. Кроме того, обнаружено, что превышение величины продукции IgG в значительной степени (например, превышение может варьировать в диапазоне от нескольких десятков раз до нескольких сотен раз) зависит от типа введенного пептида, имеющего 5 соединенных эпитопов. В случае пептида, имеющего 5 эпитопов, соединенных друг с другом в таком порядке, как TPV17, продукция антител IgG, специфичных к нескольким эпитопам CTL, не индуцируется.
Полученные результаты демонстрируют, что введение пептида, имеющего 5 соединенных эпитопов, может более интенсивно активировать противоопухолевый иммунитет, чем введение смеси пептидных эпитопов CTL, составляющих пептид, имеющий 5 соединенных эпитопов.
И индуцирование продукции IgG, специфичных к пептидным эпитопам CTL, и индукция CTL, специфичных к пептидным эпитопам, эффективно продлевают жизнь раковых пациентов, получающих лечение противораковой пептидной вакциной. Соответственно, эффекты настоящего изобретения, обеспечивающие продление жизни, превосходят соответствующие эффекты лечения пептидными вакцинами, содержащими известные пептидные эпитопы CTL, или их смеси. Следовательно, пептид настоящего изобретения, имеющий 5 соединенных эпитопов, подходит для применения в качестве терапевтического и/или профилактического средства против рака или вызванных им заболеваний и противораковых пептидных вакцин, которые могут обеспечивать результаты лечения, превосходящие результаты лечения рака с помощью пептидных вакцин, содержащих известные пептидные эпитопы CTL, или из смеси.
Все цитирующиеся здесь публикации, патенты и патентные заявки полностью включены в настоящее описание в качестве ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| АГЕНТ ДЛЯ АДЪЮВАНТНОЙ ТЕРАПИИ | 2020 |
|
RU2829433C1 |
| НОВЫЙ ПЕПТИД, ИМЕЮЩИЙ 4 СВЯЗАННЫХ CTL-ЭПИТОПА | 2014 |
|
RU2636549C1 |
| ЭМУЛЬСИОННЫЙ СОСТАВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2019 |
|
RU2793862C2 |
| ПРОТИВООПУХОЛЕВОЕ СРЕДСТВО И СПОСОБ ЕГО ОЦЕНКИ | 2019 |
|
RU2803148C2 |
| КЛЕТКА НИТЧАТЫХ ГРИБОВ С ДЕФИЦИТОМ ПРОТЕАЗ И СПОСОБЫ ЕЕ ПРИМЕНЕНИЯ | 2013 |
|
RU2645252C2 |
| СПОСОБ ФЕРМЕНТАТИВНОГО УДАЛЕНИЯ БИОПЛЕНКИ, КОМПОЗИЦИЯ И НАБОР | 2008 |
|
RU2495098C2 |
| ПЕПТИДНЫЕ ВАКЦИНЫ ДЛЯ РАКОВ, ЭКСПРЕССИРУЮЩИХ ОПУХОЛЕСПЕЦИФИЧЕСКИЕ АНТИГЕНЫ | 2008 |
|
RU2464275C2 |
| КОНЪЮГИРОВАННАЯ ВАКЦИНА НА ОСНОВЕ ПЕПТИДА АНТИГЕНА WT1 | 2014 |
|
RU2668560C2 |
| АНАЛИЗ РАСЩЕПЛЕНИЯ КЛЕТОЧНОГО VAMP | 2017 |
|
RU2807994C2 |
| ПЕПТИДЫ ЭПИТОПОВ MYBL2 И СОДЕРЖАЩИЕ ИХ ВАКЦИНЫ | 2009 |
|
RU2496787C2 |











Изобретение относится к области биотехнологии, конкретно к иммунологии, и может быть использовано в медицине для индуцирования противоопухолевого иммунитета против экспрессирующего Lck, WHSC2, SART2, SART3 или MRP3 рака. Получают пептид из 5 эпитопов CTL раковых антигенов, соединенных через аминокислотные линкеры. Полученный пептид используют для стимуляции лимфоцитов периферической крови с целью получения комбинации CTL специфичных к раковому антигену. Изобретение позволяет получить пептидную вакцину для лечения рака у широкого ряда раковых пациентов без необходимости HLA-типирования и независимо от типов HLA у пациентов. 5 н. и 1 з.п. ф-лы, 2 ил., 2 табл., 4 пр.
1. Пептид ракового антигена, имеющий 5 эпитопов, соединенных через линкеры, где 5 эпитопов выбраны из группы, включающей в себя следующие пептидные эпитопы CTL: пептид, описанный в SEQ ID NO: 1 (РЕР1); пептид, описанный в SEQ ID NO: 2 (РЕР2); пептид, описанный в SEQ ID NO: 3 (РЕР3); пептид, описанный в SEQ ID NO: 4 (РЕР4); пептид, описанный в SEQ ID NO: 5 (РЕР5); пептид, описанный в SEQ ID NO: 6 (РЕР6); и пептид, описанный в SEQ ID NO: 7 (РЕР7); и
где пептид, имеющий 5 соединенных эпитопов, содержит последовательность, выбранную из следующих последовательностей (а)-(р):
(a) РЕР5-РЕР2-РЕР4-РЕР7-РЕР3;
(b) РЕР5-РЕР2-РЕР7-РЕР3-РЕР4;
(c) РЕР4-РЕР6-РЕР5-РЕР7-РЕР3;
(d) РЕР5-РЕР2-РЕР4-РЕР6-РЕР3;
(e) РЕР5-РЕР2-РЕР4-РЕР1-РЕР3;
(f) РЕР4-РЕР5-РЕР2-РЕР7-РЕР3;
(g) РЕР7-РЕР3-РЕР4-РЕР5-РЕР2;
(h) РЕР5-РЕР7-РЕР3-РЕР4-РЕР2;
(i) РЕР6-РЕР1-РЕР4-РЕР5-РЕР2;
(j) РЕР6-РЕР5-РЕР1-РЕР4-РЕР2;
(k) РЕР4-РЕР5-РЕР1-РЕР6-РЕР3;
(l) РЕР7-РЕР2-РЕР4-РЕР5-РЕР3;
(m) РЕР4-РЕР2-РЕР7-РЕР5-РЕР3;
(n) РЕР7-РЕР2-РЕР5-РЕР4-РЕР3;
(о) РЕР5-РЕР2-РЕР7-РЕР4-РЕР3; или
(р) РЕР5-РЕР2-РЕР4-РЕР3-РЕР7,
где "-" обозначает линкер, который является аминокислотным линкером.
2. Комбинация CTL, специфичных к раковому антигену, полученная в результате стимуляции лимфоцитов периферической крови пептидом, имеющим 5 соединенных эпитопов, по п. 1.
3. Фармацевтическая композиция, используемая для лечения или профилактики рака, экспрессирующего Lck, WHSC2, SART2, SART3 или MRP3, которая содержит, в качестве активного ингредиента, пептид, имеющий 5 соединенных эпитопов, по п. 1 или комбинацию по п. 2.
4. Фармацевтическая композиция по п. 3, которая представляет собой иммунотерапевтическое средство.
5. Способ лечения рака, экспрессирующего Lck, WHSC2, SART2, SART3 или MRP3, включающий в себя введение раковому пациенту пептида, имеющего 5 соединенных эпитопов, по п. 1 или комбинации по п. 2.
6. Способ иммунизации индивидуума против рака, экспрессирующего Lck, WHSC2, SART2, SART3 или MRP3, включающий в себя введение индивидууму пептида, имеющего 5 соединенных эпитопов, по п. 1 или комбинации по п. 2.
| ОПОРНАЯ СИСТЕМА ДЛЯ УСИЛЕНИЯ ПРОМЫШЛЕННЫХ ЗДАНИЙ | 2001 |
|
RU2196209C2 |
| US 20080286228 A1, 20.11.2008 | |||
| ZHAO H.L | |||
| et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Pharm., 2012, V.9, N.3, P.664-670 | |||
| ПОСЛЕДОВАТЕЛЬНОСТИ ПЕПТИДОВ И ПЕПТИДНЫЕ КОМПОЗИЦИИ | 2008 |
|
RU2466737C2 |
| Способ подготовки кинолент перед обработкой их жидкостями | 1926 |
|
SU5404A1 |
| СКОСЫРЕВ В.С | |||
| и др | |||
| Зависимость стабильности гибридов зеленого флуоресцентного белка с обелином от природы составляющих их модулей и структуры аминокислотного линкера | |||
| Биоорган | |||
| химия, 2001, т.27, n.5, с.364-371 | |||
| LEE K.H | |||
| et al | |||
| Increased vaccine-specific T cell frequency after peptide-based vaccination correlates with increased susceptibility to in vitro stimulation but does not lead to tumor regression, J | |||
| Immunol., 1999, v.163, n.11, p.6292-6300 | |||
| GURA T | |||
| Systems for identifying new drugs are often faulty, Science, 1997, v.278, n.5340, p.1041-1042 | |||
| JAIN R.K | |||
| Barriers to drug delivery in solid tumors, Sci | |||
| Am., 1994, v.271, n.1, p.58-65 | |||
| HAIGH P.I | |||
| et al | |||
| Vaccine therapy for patients with melanoma, Oncology, 1999, v.13, n.11, p.1561-1574 | |||
| SPITLER L.E | |||
| Cancer vaccines: the interferon analogy, Cancer Biother., 1995, v.10, n.1, p.1-3. | |||
Авторы
Даты
2017-08-03—Публикация
2014-03-05—Подача