Группа изобретений относится к биотехнологии и медицине, в частности, к новым антителам, специфически связывающим рецептор 1 типа фактора роста фибробластов, применению антител для лечения онкологических заболеваний и их получению.
Известно, что в основе развития злокачественных новообразований лежит избыточная пролиферация клеток, а также образование кровеносных сосудов в опухоли, через которые происходит ее питание (ангиогенез).
Образование новых кровеносных сосудов происходит из уже существующего эндотелия и является важным компонентом многих заболеваний и нарушений, в том числе таких, как рост и метастазирование опухолей, ревматоидный артрит, псориаз, атеросклероз, диабетическая ретинопатия, ретролентальная фиброплазия, неоваскулярная глаукома, гемангиомы, иммунное отторжение трансплантированной роговицы и других тканей, а также хронические воспаления.
В случае роста опухолей ангиогенез имеет особенно важное значение при переходе от гиперплазии к неоплазии, а также для обеспечения питания растущей солидной опухоли (J. Folkman et al. Nature; 339, 58, 1989). Ангиогенез также позволяет опухолям находиться в контакте с кровеносной системой хозяина, в результате чего могут быть определены направления метастазирования для клеток опухоли. Данные, подтверждающие роль ангиогенеза в метастазировании клеток опухоли, были получены, в частности, в результате исследований, показавших зависимость между количеством и плотностью микрососудов в инвазивном раке молочной железы и фактическим наличием дистантных метастазов (N. Weidner et al. New Eng. J. Med., 324:1, 1991).
По многочисленным имеющимся данным пролиферация клеток опухоли, равно как и эндотелиальных клеток, может быть вызвана различными полипептидами, которые естественным образом встречаются в природе. Одним из них является семейство факторов роста фибробластов (fibroblast growth factor, FGF). Впервые FGF был обнаружен в экстрактах гипофиза в 1973 году (Н. Armelin. PNAS 70, 9, 1973).
FGF относятся к семейству гепарин-связывающих полипептидов, модулирующих функции различных клеток. FGF оказывает сильное влияние на пролиферацию и дифференцировку опухолевых и эндотелиальных клеток. В настоящее время выделяют 23 члена семейства FGF (FGF 1-23). Каждый член семейства имеет свои функциональные особенности. Наиболее хорошо изучены FGF 1 и 2 типов (кислый и основный). Для того чтобы оказать воздействие на клетки, FGF должен связаться с рецептором на ее поверхности. Существуют 4 типа рецепторов FGF (FGFR 1-4). С FGFR1 связываются не только FGF 1 и 2, но и большинство других членов этого семейства, поэтому роль этого рецептора в проведении сигнала в клетку считается наиболее значимой.
FGFR1 состоит из надмембранной, внутримембранной и внутриклеточной частей. Надмембранная часть рецептора состоит из 3 доменов (Д I-III), подобных иммуноглобулину. FGF, как правило, взаимодействуют с Д II и III; гепаран-сульфат, участвующий в формировании комплекса FGF/FGFR1, взаимодействует с Д III. Альтернативный мРНК сплайсинг способствует образованию на поверхности клетки нескольких вариантов FGFR1 (D Johnson, L. Williams. J Adv. Cancer Res., 60, 1, 1993; McKeehan et al. J Prog Nucleic Acid Res. Mol. Biol., 59, 135, 1998). Внутриклеточная часть рецептора представлена тирозинкиназой, при аутофосфорилировании которой происходит дальнейшее проведение сигнала в ядро и деление клетки.
Авторы настоящей заявки ранее предположили и подтвердили появление и достижение высокого уровня экспрессии FGFR1 как на клетках первичной почечно-клеточной опухоли, так и в метастазах почечно-клеточного рака (ПКР) (I. Tsimafeyeu et al. ESMO-ECCO 09, 2009; WO 2011000384). Более того, было продемонстрировано, что патологический путь FGF/FGFR1 является не только независимым в развитии ПКР, но и может определять устойчивость к существующей таргетной терапии опухолей.
Другие авторы также показали значение FGF/FGFR1 при развитии таких опухолей, как немелкоклеточный рак легкого, рак молочной железы, рак желудка и пищевода, рак предстательной железы, рак мочевого пузыря, опухоли головы и шеи, меланома (С. Behrens et al. J Clinical cancer research 14, 19, 2008; M. Koziczak et al. J Oncogene, 23, 20 2004; K. Freier J Oral Oncology 43, 1, 2007; E. Shin et al. J Cancer Res Clin Oncol. 126, 9, 2000; K. Sugiura et al. J Oncology reports 17, 3, 2007; E. Devilard et al. J BMC Cancer 6, 272, 2006; G. Lefèvre et al. J Investigative Ophthalmology and Visual Science 50, 2009).
Основываясь на вышеизложенном, можно предположить, что блокирование пути FGF/FGFR1 может привести к нарушению пролиферации опухолевых клеток и ингибированию ангиогенеза. Антагонисты FGFR1, в том числе человеческие моноклональные антитела, могут быть использованы для подавления роста опухоли и ее метастазов.
Сущность группы изобретений
Целью группы изобретений является создание новых антител для подавления пролиферации опухолевых клеток, ингибирования опухолевого ангиогенеза и лечения онкологических заболеваний. Также целью группы изобретений является расширение арсенала средств для подавления пролиферации опухолевых клеток, ингибирования опухолевого ангиогенеза и лечения онкологических заболеваний.
Объектом настоящего изобретения является антитело или его функциональный фрагмент, специфически связывающее рецептор 1 типа фактора роста фибробластов, включающее тяжелую цепь, содержащую
H-CDR1 с последовательностью SEQ ID NO: 1 или вариантом последовательности SEQ ID NO: 1, содержащим одну или две консервативные аминокислотные замены,
H-CDR2 с последовательностью SEQ ID NO: 2 или вариантом последовательности SEQ ID NO: 2, содержащим одну или две консервативные аминокислотные замены,
и H-CDR3 с SEQ ID NO: 3 или вариантом последовательности SEQ ID NO: 3, содержащим одну или две консервативные аминокислотные замены,
и легкую цепь, содержащую
L-CDR1 с последовательностью SEQ ID NO: 4 или вариантом последовательности SEQ ID NO: 4, содержащим одну или две консервативные аминокислотные замены,
L-CDR2 с последовательностью SEQ ID NO: 5 или вариантом последовательности SEQ ID NO: 5, содержащим одну или две консервативные аминокислотные замены,
и L-CDR3 с SEQ ID NO: 6 или вариантом последовательности SEQ ID NO: 6, содержащим одну или две консервативные аминокислотные замены.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что указанное антитело или его функциональный фрагмент специфически связывается с доменами II и IIIc рецептора 1 типа фактора роста фибробластов.
В частном случае выполнения антитело или его функциональный фрагмент связывает рецептор 1 типа фактора роста фибробластов с константой диссоциации Кd 2×10-9 M или менее.
В частном случае выполнения антитело или его функциональный фрагмент связывает рецептор 1 типа фактора роста фибробластов с константой диссоциации Kd 1.59×10-9 М.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его тяжелая цепь содержит вариабельный домен с последовательностью, гомологичной по меньшей мере на 90% SEQ ID NO: 7.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его тяжелая цепь содержит вариабельный домен с последовательностью SEQ ID NO: 7.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его легкая цепь содержит вариабельный домен с последовательностью, гомологичной по меньшей мере на 90% SEQ ID NO: 8.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его легкая цепь содержит вариабельный домен с последовательностью SEQ ID NO: 8.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его тяжелая цепь имеет последовательность, гомологичную по меньшей мере на 90% SEQ ID NO: 9.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его тяжелая цепь имеет последовательность SEQ ID NO: 9.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его легкая цепь имеет последовательность, гомологичную по меньшей мере на 90% SEQ ID NO: 10.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что его легкая цепь имеет последовательность SEQ ID NO: 10.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что указанное антитело является моноклональным.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что указанное антитело является химерным, гуманизированным или человеческим.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что указанное антитело относится к изотипу IgA, IgD, IgE, IgG1, IgG2, IgG3, IgG4 или IgM.
В частном случае выполнения антитело или его функциональный фрагмент характеризуется тем, что указанное антитело конъюгировано с цитотоксическим агентом.
Объектом настоящего изобретения является также фармацевтическая композиция для лечения онкологического заболевания, содержащая вышеописанное антитело или его функциональный фрагмент в эффективном количестве и фармацевтически приемлемый носитель.
В частном случае выполнения фармацевтическая композиция характеризуется тем, что онкологическим заболеванием является почечно-клеточный рак.
Объектом настоящего изобретения является также применение вышеописанного антитела или его функционального фрагмента для лечения онкологического заболевания.
В частном случае выполнения применение антитела или его функционального фрагмента характеризуется тем, что онкологическим заболеванием является почечно-клеточный рак.
Объектом настоящего изобретения является также способ лечения онкологического заболевания, включающий введение пациенту эффективного количества вышеописанного антитела или его функционального фрагмента или вышеописанной фармацевтической композиции.
Еще одним объектом настоящего изобретения является нуклеиновая кислота, кодирующая вышеописанное антитело или его функциональный фрагмент.
В частном случае выполнения нуклеиновая кислота характеризуется тем, что имеет последовательность, гомологичную по меньшей мере на 90% SEQ ID NO: 11.
В частном случае выполнения нуклеиновая кислота характеризуется тем, что имеет последовательность SEQ ID NO: 11.
В частном случае выполнения нуклеиновая кислота характеризуется тем, что имеет последовательность, гомологичную по меньшей мере на 90% SEQ ID NO: 12.
В частном случае выполнения нуклеиновая кислота характеризуется тем, что имеет последовательность SEQ ID NO: 12.
Еще одним объектом настоящего изобретения является линия клеток яичника китайского хомячка, содержащая вышеописанную нуклеиновую кислоту для получения вышеописанного антитела или его функционального фрагмента.
В частном случае выполнения линия клеток яичника китайского хомячка депонирована во Всероссийской коллекции промышленных микроорганизмов под регистрационным номером VKPM Н-134.
Еще одним объектом настоящего изобретения является способ получения антитела или его функционального фрагмента по изобретению, включающий культивирование линии клеток по изобретению в питательной среде и выделение антитела или его функционального фрагмента из вышеуказанных клеток и/или вышеуказанной среды.
Технический результат группы изобретений - достижение высокой эффективности и специфичности подавления пролиферации опухолевых клеток и ингибирования опухолевого ангиогенеза путем блокирования патологического пути FGF/FGFR1, что позволяет эффективно лечить онкологические заболевания.
В частном случае выполнения изобретения, представляющим собой создание гуманизированного антитела, достигается дополнительный технический результат - неожиданно высокая аффинность и специфичность антитела при практически полном отсутствии нежелательных антигенных (иммуногенных) свойств.
Подробное описание изобретения
Настоящее изобретение относится к антителам, в частности, как один из вариантов, к моноклональным гуманизированным антителам, которые специфически и с высокой аффинностью связываются с FGFR1. В некоторых вариантах изобретения антитела имеют конкретные структурные признаки, такие как области CDR, содержащие конкретные аминокислотные последовательности. Настоящее изобретение относится к выделенным антителам, к способам получения таких антител, к иммуноконъюгатам, включающим в себя указанные антитела, а также к фармацевтическим композициям, содержащим указанные антитела. Настоящее изобретение относится также к способам применения указанных антител, например, для лечения заболеваний, ассоциированных с экспрессией FGFR1, таких как онкологические заболевания.
В соответствии с этим настоящее изобретение относится также к способам применения анти- FGFR1-антител согласно изобретению для лечения различных онкологических заболеваний, например, для лечения почечно-клеточного рака, рака легкого, рака молочной железы.
Для лучшего понимания настоящего изобретения ниже приведены некоторые термины, использованные в настоящем описании изобретения.
В использованном здесь значении термин «антитело» означает полные антитела и любые антигенсвязывающие (функциональные) фрагменты (то есть антигенсвязывающие части) или одиночные цепи антител. Термин антитело означает гликопротеин, включающий по меньшей мере две тяжелые (Н) цепи и две легкие (L) цепи, соединенные дисульфидными связями, или его антигенсвязывающую часть. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов СН1, СН2 и СН3. Каждая легкая цепь состоит из вариабельной области легкой цепи (VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена CL. VH и VL-области могут быть далее подразделены на гипервариабельные участки, именуемые областями, определяющими комплементарность (H-CDR и L-CDR), разделенные более консервативными областями, именуемыми каркасными областями (FR). Каждая VH и VL область состоит из трех CDR и четырех FR, расположенных от аминоконца до карбоксиконца в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4.
Вариабельные области тяжелой и легкой цепей содержат домен связывания, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулинов с тканями или факторами хозяина, включающими разные клетки иммунной системы (например, эффекторные клетки) и первый компонент (C1q) классической системы комплементов.
Термин «функциональный фрагмент антитела» в использованном здесь значении означает один или несколько фрагментов антитела, которые сохраняют способность специфически связываться с антигеном (например, доменами II и IIIc FGFR1). Установлено, что антигенсвязывающую функцию антитела могут выполнять фрагменты непроцессированного антитела. Примеры связывающих фрагментов, входящих в определение термина антигенсвязывающая часть антитела, включают (i) Fab-фрагмент, одновалентный фрагмент, состоящий из VL, VH, CL и СН1 доменов; (ii) F(аb')2-фрагмент, двухвалентный фрагмент, включающий два Fab-фрагмента, связанных дисульфидным мостиком в шарнирной области; (iii) Fd-фрагмент, состоящий из VH и СН1 доменов; (iv) Fv-фрагмент, состоящий из VL и VH доменов одного плеча антитела; (v) фрагмент dAb (Ward et al., 1989, Nature 341:544-546), состоящий из VH или VL домена; и (vi) выделенную область, определяющую комплементарность (CDR). Кроме того, хотя два домена Fv-фрагмента, VL и VH, кодированы разными генами, они могут быть объединены методами рекомбинантных ДНК с использованием синтетического линкера, который позволяет получить одиночную белковую цепь, в которой VL и VH области спариваются с образованием одновалентных молекул (известен как одноцепочечный Fv-фрагмент (scFv); см., например, публикации Bird et al., 1988, Science 242:423-426; и Huston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883). Такие одноцепочечные антитела также входят в определение термина антигенсвязывающая часть антитела (фрагмент антитела). Указанные фрагменты антител получают обычными методами, известными специалистам в данной области, и исследуют в отношении их пригодности так же, как интактные антитела. В одном варианте осуществления изобретения фрагмент антитела выбирают из группы, состоящей из Fab, Fd, Fd', одноцепочечного Fv (scFv), scFva и домен-специфического антитела (dAb).
Кроме того, антитело или его функциональный фрагмент (антигенсвязывающая часть) может быть частью более крупной иммуноадгезивной молекулы, образованной путем ковалентного или нековалентного связывания антитела или части антитела с одним или несколькими другими белками или пептидами. Указанные другие белки или пептиды могут иметь функциональные группы, которые делают возможной очистку антител или их антигенсвязывающих частей либо их связывание друг с другом или с другими молекулами. Таким образом, примеры таких иммуноадгезивных молекул включают использование центральной области стрептавидина для получения молекул, содержащих тетрамерный одноцепочечный вариабельный фрагмент (scFv) (Kipriyanov et al., 1995, Human Antibodies and Hybridomas 6:93-101), и использование остатка цистеина, пептида-маркера и С-концевой полигистидиновой метки для создания двухвалентных и биотинилированных молекул scFv (Kipriyanov et al., 1994, Mol. Immunol. 31:1047-1058). Части антитела, такие как Fab и F(ab')2 фрагменты, могут быть получены из полных антител стандартными методами, такими как расщепление полных антител папаином или пепсином. Кроме того, антитела, части антител и иммуноадгезивные молекулы могут быть получены стандартными методами рекомбинантных ДНК.
Домены антитела являются комплементарными, так как они принадлежат к семейству структур, которые образуют родственные пары или группы или выделены из таких семейств и сохраняют указанный признак. Например, VH-домен и VL-домен антитела являются комплементарными; два VH-домена не являются комплементарными, и два VL-домена не являются комплементарными. Комплементарные домены могут быть найдены в других членах надсемейства иммуноглобулинов, такие как γ и δ (или гамма и дельта) домены Т-клеточного рецептора.
Термин «домен» означает складчатую структуру белка, которая сохраняет свою третичную структуру независимо от остального белка. Как правило, домены отвечают за отдельные функциональные свойства белков и во многих случаях могут быть добавлены, удалены или перенесены в другие белки без утраты функции остальной части белка и/или домена. Один вариабельный домен антитела является складчатым полипептидным доменом, включающим последовательности, характерные для вариабельных областей антитела. Поэтому антитело включает полные вариабельные домены и модифицированные вариабельные домены, в которых, например, одна или несколько петель заменены последовательностями, не характерными для вариабельных доменов антитела или вариабельных доменов антитела, которые были усечены или включают удлинения у Ν- или С-конца, а также складчатые фрагменты вариабельных доменов, которые сохраняют, по меньшей мере, частично связывающую активность и специфичность непроцессированного домена.
Вариабельные домены по настоящему изобретению могут быть объединены с образованием группы доменов; например, могут быть объединены комплементарные домены, в частности, VL-домены могут быть объединены с VH-доменами. Некомплементарные домены также могут быть объединены. Домены могут быть объединены разными способами, включающими связывание доменов ковалентными или нековалентными связями.
Термин «рекомбинантное антитело» означает антитела, полученные, экспрессированные, созданные или выделенные рекомбинантными методами, например, антитела, экспрессированные при помощи рекомбинантного экспрессирующего вектора, трансфицированного в клетку-хозяина; антитела, выделенные из комбинаторной библиотеки рекомбинантных антител; антитела, выделенные у животного (например, мыши), которое является трансгенным для генов иммуноглобулина человека (см., например, публикацию Taylor et al., 1992, Nucl. Acids Res. 20:6287-6295), или антитела, полученные, экспрессированные, созданные или выделенные любым другим способом, который включает сплайсинг конкретных последовательностей генов иммуноглобулина (таких как последовательности генов иммуноглобулина человека) в другие последовательности ДНК. Примеры рекомбинантных антител включают химерные, CDR-имплантированные и гуманизированные антитела.
Термин «человеческое антитело» означает антитела, имеющие вариабельные и константные области, соответствующие или выделенные из последовательностей иммуноглобулина зародышевой линии человека, описанные, например, Кабатом и др. (см. публикацию Kabat et al., 1991, Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication 91-3242). Однако человеческие антитела по настоящему изобретению могут включать аминокислотные остатки, не кодированные последовательностями иммуноглобулина зародышевой линии человека (например, мутации, введенные при помощи неспецифического или сайт-специфического мутагенеза in vitro или соматической мутации in vivo), например, в CDR-области и, в частности, в CDR3.
Рекомбинантные человеческие антитела по настоящему изобретению содержат вариабельные области и могут также включать константные области, выделенные из последовательностей иммуноглобулина зародышевой линии человека (см., публикацию Kabat et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication 91-3242). Однако в некоторых вариантах осуществления изобретения такие рекомбинантные человеческие антитела подвергают мутагенезу in vitro (или соматическому мутагенезу in vivo при использовании животного, трансгенного к последовательностям Ig человека), и, таким образом, аминокислотные последовательности VH- и VL-областей рекомбинантных антител являются последовательностями, которые, будучи выделенными и родственными последовательностям VH- и VL-областей зародышевой линии человека, могут не существовать в естественных условиях в спектре последовательностей антител зародышевой линии in vivo. Однако в некоторых вариантах осуществления изобретения такие рекомбинантные антитела являются результатом селективного мутагенеза, обратной мутации или того и другого вместе.
Термин «обратная мутация» означает процесс, в соответствии с которым некоторые или все соматически мутированные аминокислоты человеческого антитела заменяют соответствующими остатками из гомологичной последовательности антитела зародышевой линии. Последовательности тяжелой и легкой цепей человеческого антитела по настоящему изобретению отдельно подвергают сравнительному анализу с последовательностями зародышевой линии в базе данных VBASE для идентификации последовательностей, обладающих наибольшей гомологией. Отличающиеся аминокислоты человеческого антитела по настоящему изобретению возвращают в последовательность зародышевой линии путем мутации нуклеотидов в определенных положениях, кодирующих отличающуюся аминокислоту. Роль каждой аминокислоты, идентифицированной таким образом в качестве кандидата для обратной мутации, должна быть исследована в отношении прямого или непрямого связывания антигена, при этом любая аминокислота, которая, как установлено, после мутации воздействует на любые желаемые характеристики человеческого антитела, не должна быть включена в конечное человеческое антитело. Чтобы свести к минимуму число аминокислот, подвергаемых обратной мутации, аминокислоты в положениях, которые, как установлено, отличаются от ближайшей последовательности зародышевой линии, но являются идентичными соответствующей аминокислоте во второй последовательности зародышевой линии, могут оставаться при условии, что вторая последовательность зародышевой линии идентична и соответствует последовательности человеческого антитела по настоящему изобретению в отношении по меньшей мере 10, предпочтительно 12 аминокислот, с обеих сторон рассматриваемой аминокислоты. Обратная мутация может произойти на любой стадии оптимизации антитела.
Термин «химерное антитело» означает антитело, которое включает последовательности вариабельной области тяжелой и легкой цепей из одного вида и последовательности константной области из другого вида, например, антитела, включающие вариабельные области тяжелой и легкой цепей грызуна, связанные с константными областями человека.
Термин «гуманизированное антитело» означает антитела, которые включают последовательности вариабельной области тяжелой и легкой цепей из вида, отличного от человека, (например, мыши), но в которых, по меньшей мере, часть последовательности VH- и/или VL-областей была изменена, чтобы быть более похожей на человеческую, то есть более подобной вариабельным последовательностям зародышевой линии человека. Одним типом гуманизированного антитела является CDR-имплантированное антитело, в котором последовательности CDR человека вводят в последовательности VH- и VL-областей, отличные от человеческих, для замены соответствующих последовательностей CDR, отличных от человеческих. Методы гуманизации антител, отличных от человеческих, хорошо известны в данной области. Гуманизированное антитело обычно содержит один или несколько аминокислотных остатков, введенных в него из источника, отличного от человеческого. Указанные аминокислотные остатки, отличные от человеческих, часто определяются как чужеродные остатки, которые обычно получают из чужеродного вариабельного домена. Гуманизация может быть выполнена методом, разработанным Уинтером с соавторами (Jones et al., Nature, 321:522-525, 1986; Riechmann et al., Nature, 332:323-327, 1988; Verhoeyen et al., Science, 239:1534-1536, 1988), который включает замену соответствующих последовательностей человеческого антитела CDR-областями или последовательностями CDR, отличными от человеческих (например, грызунов). Таким образом, такие гуманизированные антитела являются химерными антителами (US 4816567), в которых по существу часть интактного вариабельного домена человека заменена соответствующей последовательностью вида, отличного от человека. На практике гуманизированные антитела обычно являются человеческими антителами, в которых некоторые остатки CDR и, возможно, некоторые остатки каркасной области (FR) заменены остатками аналогичных сайтов в антителах грызунов. Дополнительные материалы, в которых описан процесс гуманизации, включают публикации Sims et al., J. Immunol., 151:2296, 1993; Chothia et al., J. Mol. Biol., 196:901, 1987; Carter et al., Proc. Natl. Acad. Sci. USA, 89:4285, 1992; Presta et al., J. Immunol., 151:2623, 1993, которые включены в настоящее описание изобретения в качестве ссылки.
Термин «поликлональные антитела» обозначают антитела, которые обычно представляют собой смесь антител, специфичных к определенному антигену, но связывающихся с разными эпитопами на указанном антигене. Поликлональные антитела обычно образуются в организме животных в результате выполнения нескольких подкожных (sc) или внутрибрюшинных (ip) инъекций родственного антигена и адъюванта. Может оказаться полезным конъюгировать родственный антиген с белком, который является иммунногенным в иммунизируемом виде, таким как, например, гемоцианин лимфы улитки, сывороточный альбумин, бычий тироглобулин или ингибитор соевого трипсина, с использованием бифункционального или образующим производное агента, например, сложного эфира малеимидобензоилсульфосукцинимида (конъюгация по остаткам цистеина), N-гидроксисукцинимида (по остаткам лизина), глутаральдегида, янтарного альдегида, SOCl2 или R1NCNR, где R и R1 означают разные алкильные группы. Методы получения поликлональных антител известны в данной области и описаны, например, в публикации Antibodies: A Laboratory Manual, Lane and Harlow, 1988, которая включена в настоящее описание изобретения в качестве ссылки.
Термин «моноклональные антитела» в использованном здесь значении означает антитело, полученное из гибридомы (например, антитело, секретированное гибридомой, полученной методом гибридом, таким как стандартный метод гибридом Колера и Милстейна). Например, моноклональные антитела могут быть получены методом гибридом, впервые описанным в публикации Kohler et al., Nature, 256:495, 1975, или могут быть получены методами рекомбинантных ДНК (US 4816567). Моноклональные антитела получают из популяции по существу гомогенных антител, то есть отдельные антитела, образующие популяцию, являются идентичными за исключением возможных естественных мутаций, которые могут присутствовать в незначительных количествах. Таким образом, термин «моноклональное» определяет характер антитела, которое не является смесью отдельных антител.
Используемые здесь термины «антитело, распознающее антиген» и «антитело, специфичное к антигену», а также «антитело против антигена» являются синонимами термина «антитело, которое специфически связывается с антигеном».
Термин «производные антитела» означает любую модифицированную форму антитела (человеческого, гуманизированного, мышиного), например, конъюгат антитела с другим агентом или антителом.
Используемый здесь термин «антитело, специфически связывающее рецептор 1 типа фактора роста фибробластов (FGFR1)» означает антитело, которое связывается с человеческим FGFR1 с Kd=1×10-7 М или менее, более предпочтительно 1×10-8 М или менее, еще более предпочтительно 2×10-9 М или менее, а наиболее предпочтительно 1.59×10-9 М или менее.
Используемый здесь термин «высокая аффинность» антитела IgG означает, что данное антитело связывается с антигеном-мишенью с Kd, равным 1×10-7 М или менее, более предпочтительно 1×10-8 М или менее, еще более предпочтительно 2×10-9 М или менее, а наиболее предпочтительно 1.59×10-9 М или менее.
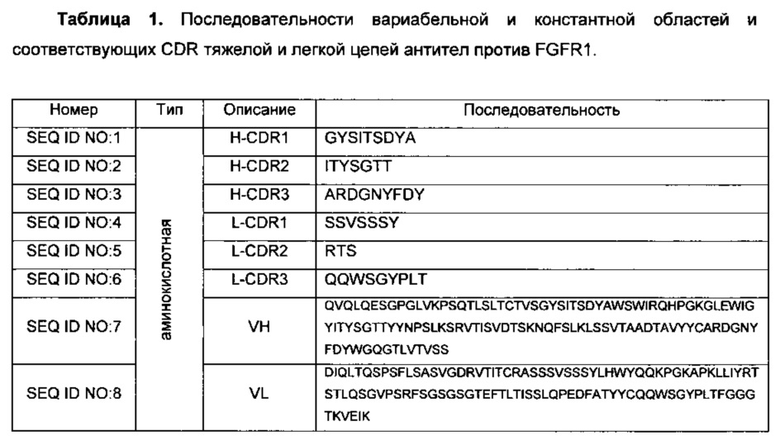
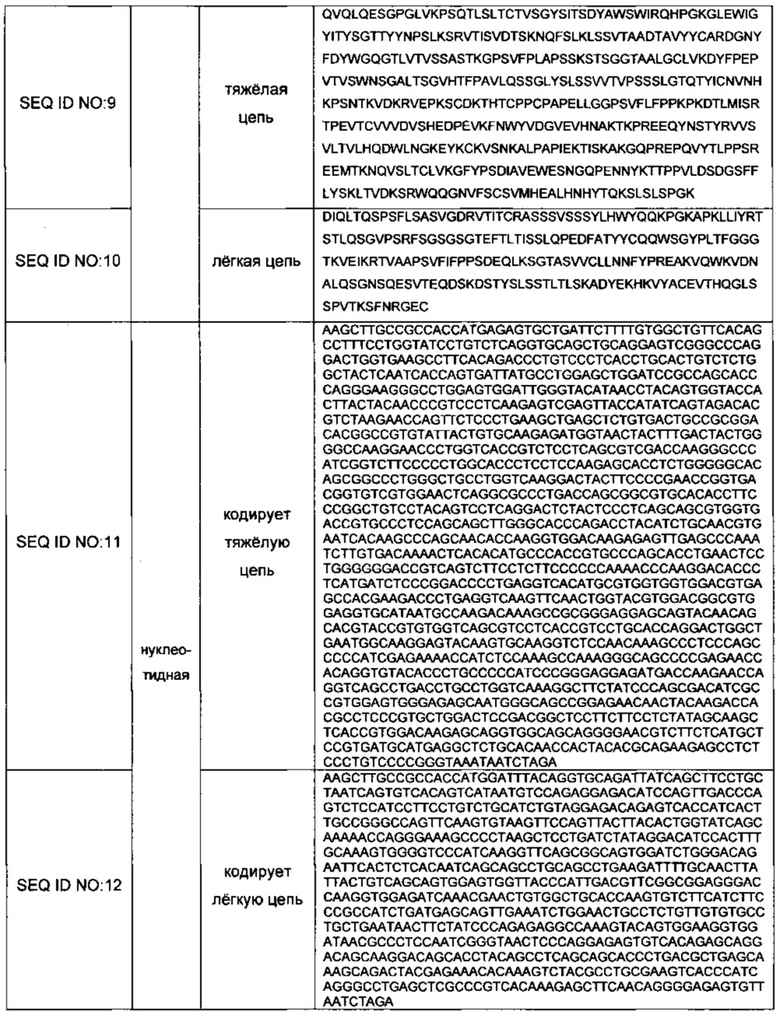
Каждая из вышеупомянутых аминокислотных и нуклеотидных последовательностей приводится в нижеследующей таблице 1 и в списке последовательностей.
Гомологичные антитела
В некоторых вариантах осуществления изобретения антитело согласно изобретению содержит вариабельные области тяжелой и легкой цепей, включающие в себя аминокислотные последовательности, гомологичные аминокислотным последовательностям описанных здесь предпочтительных антител, где указанные антитела сохраняют нужные функциональные свойства анти-FGFR1-антител согласно изобретению.
Гомологичные антитела могут быть получены путем мутагенеза (например, сайт-направленного или ПЦР-опосредуемого мутагенеза) соответствующих молекул нуклеиновых кислот с последующим тестированием кодируемого модифицированного антитела на сохранение его функций в соответствии с описанными здесь функциональными анализами.
Используемый здесь термин «процент гомологии двух аминокислотных последовательностей» эквивалентен термину «процент идентичности двух последовательностей». Процент идентичности двух последовательностей зависит от числа положений идентичных аминокислот в этих двух последовательностях (то есть % гомологии = % идентичных аминокислот в данных положениях/общее число положений ×100) с учетом числа пробелов и длины каждого пробела, которые необходимо ввести для оптимального сопоставления двух последовательностей путем выравнивания.
Процент идентичности двух аминокислотных последовательностей может быть определен с помощью алгоритма Е. Meyers and W. Miller (Comput. Appl. Biosci., 4:11-17, 1988), который был введен в программу ALIGN (version 2.0), с использованием таблицы «весов» остатков РАМ120, штрафа на пробел-удлинение =12, и штрафа на пробел-пропуск =4. Кроме того, процент идентичности двух аминокислотных последовательностей может быть определен с помощью алгоритма Needleman и Wunsch (J. Mol. Biol. 48:444-453, 1970), который был введен в программу GAP, входящую в пакет программ GCG (доступных на сайте www.gcg.com), с использованием либо матрицы Blossum 62, либо матрицы РАМ250 и «весов» пробелов-пропусков, составляющих 16, 14, 12, 10, 8, 6, или 4 и «весов» длин (участков), составляющих 1, 2, 3, 4, 5 или 6.
Дополнительно или альтернативно, последовательности белка согласно изобретению могут быть также использованы в качестве «запрашиваемой последовательности» для осуществления поиска в общедоступных базах данных, например, в целях идентификации родственных последовательностей. Такой поиск может быть проведен с помощью программы XBLAST (version 2.0) Altschul, et al., 1990, J. Mol.Biol. 215:403-10. Поиск белков BLAST может быть осуществлен с помощью программы XBLAST, где при «весовом коэффициенте» =50 и длине «слова» =3, могут быть получены аминокислотные последовательности, гомологичные последовательностям молекул антител согласно изобретению. Для осуществления выравнивания с пробелами в целях сопоставления последовательностей может быть использована программа Gapped BLAST, описанная Altschul et al., 1997, Nucleic Acids Res. 25(17):3389-3402. При работе с программами BLAST и Gapped BLAST могут быть использованы параметры по умолчанию, установленные в соответствующих программах (например, XBLAST и NBLAST). См. www.ncbi.nlm.nih.gov.
Молекулы нуклеиновых кислот, кодирующие антитела согласно изобретению
В другом своем аспекте настоящее изобретение относится к молекулам нуклеиновой кислоты, кодирующим антитела согласно изобретению. Такие нуклеиновые кислоты могут присутствовать в целых клетках, в клеточных лизатах или в частично очищенной или, по существу, в чистой форме. Нуклеиновая кислота является «выделенной» или «по существу чистой», если она очищена от других клеточных компонентов или других примесей, например, от других клеточных нуклеиновых кислот или белков, стандартными методами, включая обработку щелочью/ДСН, центрифугирование в градиенте плотности CsCl, колоночную хроматографию, электрофорез на агарозном геле и другие методы, хорошо известные специалистам. См. F. Ausubel, et al., ed., 1987, Current Protocols in Molecular Biology, Greene Publishing and Wiley Interscience, New York. Нуклеиновая кислота согласно изобретению, может представлять собой, например, ДНК или РНК, и может содержать, а может и не содержать, интронные последовательности. В предпочтительном варианте изобретения нуклеиновой кислотой является молекула кДНК.
Нуклеиновые кислоты согласно изобретению могут быть получены стандартными методами молекулярной биологии. Для антител, экспрессируемых гибридомами (например, гибридомами, полученными от трансгенных мышей, несущих гены человеческого иммуноглобулина), кДНК, кодирующие легкую и тяжелую цепи антитела, продуцируемого гибридомами, могут быть получены стандартными методами ПЦР-амплификации или клонирования кДНК. Для антител, полученных из библиотеки генов иммуноглобулина (например, с применением методов фагового представления), нуклеиновая кислота, кодирующая указанное антитело, может быть выделена из этой библиотеки.
Предпочтительными молекулами нуклеиновой кислоты согласно изобретению являются молекулы, кодирующие последовательности VH и VL моноклонального антитела против FGFR1. Последовательность ДНК, кодирующая последовательность VH антитела против FGFR1, представляет собой SEQ ID NO: 11. Последовательность ДНК, кодирующая последовательность VL антитела против FGFR1, представляет собой SEQ ID NO: 12. После получения фрагментов ДНК, кодирующих сегменты VH и VL, эти фрагменты ДНК могут быть затем модифицированы стандартными методами рекомбинантных ДНК, например, для конверсии генов вариабельной области в гены, кодирующие цепь полноразмерного антитела, в гены Fab-фрагмента или в ген scFv. При этих манипуляциях VL- или VH-кодирующий ДНК-фрагмент функционально присоединяют к другому ДНК-фрагменту, кодирующему другой белок, такой как константная область антитела или гибкий линкер. Термин «функционально присоединенный», используемый в данном контексте, означает, что два ДНК-фрагмента присоединены друг к другу так, что аминокислотные последовательности кодируются этими двумя ДНК-фрагментами с сохранением рамки считывания. Выделенная ДНК, кодирующая область VH, может быть трансформирована в ген, кодирующий полноразмерную тяжелую цепь, путем функционального присоединения VH-кодирующей ДНК к другой молекуле ДНК, кодирующей константные области тяжелой цепи (СН1, СН2 и СН3). Последовательности генов константной области человеческой тяжелой цепи известны специалистам (см., например, Kabat, Ε.Α., el al., 1991, Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication 91-3242), а ДНК-фрагменты, включающие в себя эти области, могут быть получены стандартным методом ПЦР-амплификации. Константной областью тяжелой цепи могут быть константные области IgG1, IgG2, IgG3, IgG4, IgA, IgE, IgM или IgD, а наиболее предпочтительно, константная область IgG1. Для гена Fab-фрагмента тяжелой цепи, VH-кодирующая ДНК может быть функционально присоединена к другой молекуле ДНК, кодирующей только константную область СН1 тяжелой цепи. Выделенная ДНК, кодирующая область VL, может быть превращена в ген полноразмерной легкой цепи (а также в ген легкой цепи Fab) путем функционального присоединения VL-кодирующей ДНК к другой молекуле ДНК, кодирующей константную область легкой цепи, CL. Константной областью легкой цепи может быть константная область каппа или лямбда, а наиболее предпочтительно константная область каппа. Для создания гена scFv, VH- и VL-кодирующие ДНК-фрагменты функционально присоединяют к другому фрагменту, кодирующему гибкий линкер, например, кодирующему аминокислотную последовательность (Gly4-Ser)3, так, чтобы последовательности VH и VL могли экспрессироваться в виде единого одноцепочечного белка, причем указанные области VL и VH присоединены друг к другу посредством гибкого линкера (см., например, Bird et al., 1988, Science 242:423-426; Huston et al., 1988, Proc. Natl. Acad. Sci. USA 85:5879-5883; McCafferty et al., 1990, Nature 348:552-554).
Продуцирование моноклональных антител согласно изобретению
Моноклональные антитела (mAb) согласно изобретению могут быть продуцированы различными методами, включая стандартную технологию получения моноклональных антител, например, стандартный метод гибридизации соматических клеток, описанный Kohler и Milstein, 1975, Nature 256:495. Могут быть применены и другие методы продуцирования моноклональных антител, например, вирусная или онкогенная трансформация. Предпочтительным животным, которое может быть использовано для получения гибридом, является грызун, например, мышь. Продуцирование гибридомы у мыши является хорошо разработанной процедурой. Протоколы иммунизации и методы выделения иммунизированных спленоцитов для слияния известны специалистам. Партнеры по слиянию клеток (например, мышиных миеломных клеток) и процедуры такого слияния также известны специалистам. При получении моноклональных антител гибридомным методом мышь или другое подходящее животное-хозяин иммунизируется антигеном посредством подкожной, внутриперитонеальной или внутримышечной инъекции с целью выявить лимфоциты, которые производят или же способны производить антитела, специфически связывающиеся с белком(ами), использованным(и) для иммунизации. В качестве альтернативы, лимфоциты могут быть иммунизированы in vitro. Затем лимфоциты сливают с клетками миеломы с использованием соответствующего агента, например такого, как полиэтиленгликоль, чтобы создать гибридомную клетку (J. Goding. Monoclonal Antibodies: Principles and Practice, pp.59-103, Academic Press, 1986).
В данном изобретении таким антигеном является FGFR1 (домены II и IIIc). Антиген может представлять собой фрагмент или часть FGFR1, обладающие одним или несколькими аминокислотными остатками, которые участвуют в связывании FGF.
Приготовленные таким образом гибридомные клетки высеваются и выращиваются в подходящей культуральной среде, которая предпочтительно должна содержать одно или несколько веществ, которые ингибируют рост или выживание неслитых, родительских клеток миеломы. Например, в случае, если в родительских клетках миеломы отсутствует фермент гипоксантингуанинфосфорибозилтрансфераза (ГГФРТ или ГФРТ), культуральная среда для гибридом обычно будет содержать гипоксантин, аминоптерин и тимидин (среда HAT), которые препятствуют росту клеток, не обладающих ГГФРТ. Предпочтительно выбирать такие клетки миеломы, которые эффективно сливаются, поддерживают стабильный высокий уровень экспрессии антител в отобранных клетках, производящих антитела, и являются чувствительными к средам, таким, например, как среда HAT. Среди таких клеток предпочтительными клеточными линиями являются: мышиные линии миеломы, такие как линии, происходящие от мышиных опухолей МОРС-21 и МРС-11, которые можно получить из Центра распределения клеток Института им. Солка в Сан-Диего (Калифорния, США); клетки SP-2, которые можно получить из Американской коллекции типовых культур в Роквилле (Мэриленд, США); и клетки P3X63Ag8U.1, описанные Йелтоном и др. (J Curr. Top. Microbiol. Immunol. 81, 1, 1978). Кроме того, были описаны клеточные линии человеческой миеломы и человеческо-мышиной гетеромиеломы, способные производить человеческие моноклональные антитела (D. Kozbor et al. J Immunol. 133, 3001, 1984; В. Brodeur, P. Tsang Monoclonal Antibody Production Techniques and Applications, pp.51-63, Marcel Dekker Inc., New York, 1987). Культуральная среда, в которой выращиваются клетки гибридомы, подвергается анализу для производства моноклональных антител, направленных против соответствующего антигена. Предпочтительно, чтобы специфичность связывания моноклональных антител, производимых клетками гибридомы, была высокой.
Данное изобретение включает те моноклональные антитела, которые показали высокую специфичность (2×10-9 и менее) связывания с указанными антигенами, определенную по стандартной методике «BIOCORE».
Химерные или гуманизованные антитела согласно изобретению могут быть получены на основе последовательности мышиного моноклонального антитела, полученного как описано выше. ДНК, кодирующая тяжелую и легкую цепи иммуноглобулина, может быть выделена из представляющей интерес нечеловеческой гибридомы и сконструирована стандартными методами молекулярной биологии так, чтобы она содержала гуманизированные последовательности иммуноглобулина. Так, например, для создания химерного антитела мышиные вариабельные области могут быть присоединены к человеческим константным областям методами, известными специалистам (см., например, US 4816567, Cabilly et al.). Для создания гуманизованного антитела мышиные области CDR могут быть встроены в человеческую каркасную область методами, известными специалистам (см., например, US 5225539, Winter и US 5530101; US 5585089; US 5693762 и US 6180370, Queen et al.). В предпочтительном варианте изобретения антителами согласно изобретению являются гуманизированные моноклональные антитела. В другом варианте изобретения человеческие антитела согласно изобретению могут быть продуцированы у мышей, имеющих последовательности человеческого иммуноглобулина в трансгенах и в трансхромосомах, например, у таких мышей, которые имеют трансген человеческой тяжелой цепи и трансхромосому человеческой легкой цепи. Такие мыши, называемые здесь мышами «КМ», подробно описаны в международной заявке WO 2002043478, Ishida et al. Кроме того, альтернативные системы трансгенных животных, экспрессирующие гены человеческого иммуноглобулина, известны специалистам и могут быть использованы для продуцирования анти-FGFR1-антител согласно изобретению. Так, например, может быть использована альтернативная трансгенная система, называемая Xenomouse (Abgenix, Inc.); и такие мыши описаны, например, в патентах US 5939598; US 6075181; US 6114598; US 6150584 и US 6162963, Kucherlapati et al. Более того, альтернативные системы трансхромосомных животных, экспрессирующие гены человеческого иммуноглобулина, известны специалистам и могут быть использованы для продуцирования анти-FGFR1-антител согласно изобретению. Так, например, могут быть использованы мыши, несущие трансхромосому тяжелой цепи и трансхромосому легкой цепи, и называемые «мышами ТС»; и такие мыши описаны в публикации Tomizuka et al., 2000, Proc. Natl. Acad. Sci. USA 97:722-727. Кроме того, для продуцирования анти-FGFR1-антитела согласно изобретению могут быть использованы коровы, несущие человеческие трансхромосомы тяжелой и легкой цепей, как было описано в литературе (Kuroiwa et al., 2002, Nature Biotechnology 20:889-894). Моноклональные антитела согласно изобретению могут быть также получены с применением методов фагового представления для скрининга библиотек генов иммуноглобулина. Такие методы фагового представления для выделения антител известны специалистам. См., например, патенты US 5223409; US 5403484 и US 5571698, Ladner et al.; патенты US 5427908 и US 5580717, Dower et al.; патенты US 5969108 и US 6172197, McCafferty et al.; и патенты US 5885793; US 6521404; US 6544731; US 6555313; US 6582915 и US 6593081, Griffiths et al.
Моноклональные антитела согласно изобретению могут быть также получены с использованием мышей SCID, которым были введены человеческие иммунные клетки, реконструированные так, чтобы у этих мышей, после иммунизации, вырабатывалось человеческое антитело. Такие мыши описаны, например, в патентах US 5476996 и US 5698767, Wilson et al.
Иммунизация мышей, вырабатывающих анти-FGFR1-антитело
Если для продуцирования антител согласно изобретению используются мыши, вырабатывающие Ig, то такие мыши могут быть иммунизованы FGFR1-экспрессирующей клеточной линией, очищенным антигеном FGFR1 или препаратом, обогащенным этим антигеном. Предпочтительно, чтобы после первой иммунизации, мыши имели возраст 6-16 недель. Так, например, для внутрибрюшинной иммунизации мышей, вырабатывающих, анти-FGFR1-антитело, может быть использован очищенный или рекомбинантный препарат (5-50 мкг) антигена FGFR1. Подробное описание процедур получения анти-FGFR1-антител приведено ниже в примере 1. Совокупные результаты экспериментов с различными антигенами показали, что у трансгенных мышей при проведении первичной внутрибрюшинной иммунизации (i.р.) антигеном в полном адъюванте Фрейнда, а затем i.р. иммунизации раз в две недели (всего 6 иммунизаций) антигеном в неполном адъюванте Фрейнда, наблюдалось вырабатывание иммунного ответа.
Однако было также обнаружено, что кроме адъюванта Фрейнда эффективными являются и другие адъюванты. Кроме того, было обнаружено, что в отсутствии адъюванта целые клетки являются в высокой степени иммуногенными. Мониторинг иммунного ответа может быть проведен во время проведения всей процедуры иммунизации пробами плазмы, полученными из ретроорбитальной области. Эта плазма может быть скринирована с помощью ELISA, и мыши, имеющие достаточно высокие титры анти-FGFR1-антител, могут быть затем использованы для слияния клеток. Мышам может быть повторно введен антиген путем внутривенной инъекции за 3 дня до умерщвления и взятия селезенки. При этом предполагается, что для каждой иммунизации могут потребоваться 2-3 процедуры слияния клеток. Обычно 6-24 мышей иммунизируют каждым антигеном. Для этого обычно используют штаммы НСо7 и НСо12. Генерирование мышиных штаммов НСо7 и НСо12 описано в патенте US 5770429 и в примере 2 международной заявки WO 2001009187, соответственно.
Кроме того, оба трансгена НСо7 и НСо12 могут быть переданы вместе одной мыши, имеющей два различных трансгена человеческой тяжелой цепи (НСо7/НСо12). Альтернативно или дополнительно, могут быть использованы мыши штамма КМ, описанные в международной заявке WO 2002043478.
Генерирование гибридом, продуцирующих анти-FGFR1-антитела согласно изобретению
Для генерирования гибридом, продуцирующих анти-FGFR1-антитела согласно изобретению, спленоциты и/или клетки лимфоузлов, взятые от иммунизованных мышей, могут быть выделены и подвергнуты слиянию с соответствующей иммортализованной клеточной линией, такой как клеточная линия мышиной миеломы. Полученные гибридомы могут быть скринированы на продуцирование антигенспецифических антител. Так, например, моноклеточные суспензии лимфоцитов селезенки, взятых от иммунизованных мышей, могут быть подвергнуты слиянию с 1/3 от числа несекретирующих клеток мышиной миеломы Sp2/0 (АТСС, CRL 1581), связанных с 50% ПЭГ. Альтернативно, моноклеточные суспензии лимфоцитов селезенки, взятых у иммунизованных мышей, могут быть подвергнуты слиянию с равным числом клеток мышиной миеломы Sp2/0 с применением метода электрослияния под действием электрического поля с использованием электропоратора для крупномасштабного слияния клеток Cyto Pulse large chamber cell fusion electroporator (Cyto Pulse Sciences, Inc., Glen Burnie, MD). Клетки высевают в концентрации примерно 1×105 клеток/лунку в плоскодонный микротитрационный планшет, а затем инкубируют в течение двух недель в селективной среде, содержащей 10% фетальную бычью сыворотку (Hyclone, Logan, UT), 10% P388DI-кондиционированную среду (АТСС, CRL TIB-63), 3-5% Origen (IGEN) в DMEM (Mediatech, CRL 10013, с высоким содержанием глюкозы, L-глутамина и пирувата натрия), а также 5 мМ HEPES, клетки могут быть культивированы в среде, где среда HAT (hypoxanthine-aminopterin-thymidine, гипоксантин-аминоптерин-тимидин) заменена средой HT. Затем отдельные лунки могут быть скринированы с помощью ELISA или FACS на моноклональные антитела IgG. Позитивные клоны могут быть затем скринированы на FGFR1-позитивные антитела с помощью ELISA или против FGFR1-экспрессирующих клеток. После интенсивного роста гибридом, обычно через 10-14 дней, проводят мониторинг среды. Антитело-секретирующие гибридомы могут быть засеяны повторно и снова скринированы, и при получении положительного результата на анти-FGFR1-антитело антитела могут быть субклонированы по меньшей мере два раза, путем лимитирующего разведения. Затем стабильные субклоны могут быть культивированы in vitro для генерирования небольших количеств антител в среде для культивирования тканей в целях их характеризации.
Для очистки анти-FGFR1-антител отобранные гибридомы могут быть культивированы в двухлитровых центрифужных колбах, предназначенных для очистки моноклональных антител.
Супернатанты могут быть отфильтрованы и концентрированы, а затем подвергнуты белковой аффинной хроматографии на А-сефарозе (Pharmacia, Piscataway, NJ). Для гарантии нужной чистоты, элюированный IgG может быть оценен с помощью гель-электрофореза и высокоэффективной жидкостной хроматографии. Буферный раствор может быть заменен на PBS, и концентрация может быть определена по OD280 с использованием коэффициента экстинкции 1,43. Моноклональные антитела могут быть разделены на аликвоты и положены на хранение при -80°С.
Генерирование трансфектом, продуцирующих моноклональные антитела согласно изобретению
Антитела согласно изобретению могут быть также продуцированы в трансфектоме клеток-хозяев с применением комбинированных методов рекомбинантных ДНК и трансфекции генов. Так, например, для экспрессии антител или их фрагментов ДНК, кодирующие неполные или полноразмерные легкие и тяжелые цепи, могут быть получены стандартными методами молекулярной биологии (например, посредством ПЦР-амплификации или клонирования кДНК с использованием гибридомы, экспрессирующей представляющее интерес антитело - подробное описание процедур получения рекомбинантного ДНК, кодирующего легкую или тяжелую цепи антитела, представленного в изобретении, приведено в примере 5), и эти ДНК могут быть встроены в экспрессирующие векторы так, чтобы такие гены были функционально присоединены к последовательностям регуляции транскрипции и трансляции. В этом контексте, термин «функционально присоединенный» означает, что ген антитела лигируют в вектор так, чтобы указанные последовательности регуляции транскрипции и трансляции в данном векторе выполняли присущую им функцию регуляции транскрипции и трансляции гена антитела. Экспрессирующий вектор и последовательности регуляции экспрессии выбирают так, чтобы они были совместимы с клеткой-хозяином, используемой для такой экспрессии. Ген легкой цепи антитела и ген тяжелой цепи антитела могут быть встроены в отдельные векторы, или, чаще всего, оба гена встраивают в один и тот же экспрессирующий вектор. Гены антитела встраивают в экспрессирующий вектор стандартными методами (например, путем лигирования по комплементарным рестрикционным сайтам в генные фрагменты антитела и в вектор, или путем лигирования по тупым концам, если такие рестрикционные сайты отсутствуют - подробное описание процедур получения плазмиды, содержащей рекомбинантную ДНК, кодирующую легкую и тяжелую цепи антитела, представленного в изобретении, приведено в примере 5). Описанные здесь вариабельные области легкой и тяжелой цепей антител могут быть использованы для создания полноразмерных генов, кодирующих антитело любого изотипа, путем их встраивания в экспрессирующие векторы, уже кодирующие константные области тяжелой и легкой цепей антитела нужного изотипа так, чтобы сегмент VH был функционально присоединен к сегменту(ам) СН в данном векторе, а сегмент VL был функционально присоединен к сегменту CL в данном векторе. Дополнительно или альтернативно, рекомбинантный экспрессирующий вектор может кодировать сигнальный пептид, облегчающий секрецию цепи антитела из клетки-хозяина. Указанный ген цепи антитела может быть клонирован в вектор так, чтобы сигнальный пептид был присоединен к амино-концу гена цепи антитела с сохранением рамки считывания. Таким сигнальным пептидом может быть сигнальный пептид иммуноглобулина или гетерологичный сигнальный пептид (то есть сигнальный пептид, происходящий от белка, не являющегося иммуноглобулином).
Рекомбинантные экспрессирующие векторы согласно изобретению, помимо генов цепи антител, несут регуляторные последовательности, которые регулируют экспрессию генов цепи антител в клетке-хозяине. Термин «регуляторная последовательность» включает в себя промоторы, энхансеры и другие элементы регуляции экспрессии (например, сигналы полиаденилирования), регулирующие транскрипцию или трансляцию генов цепей антител. Такие регуляторные последовательности описаны, например, в публикации Goeddel (Gene Expression Technology. Methods in Enzymology 185, Academic Press, San Diego, CA, 1990). Следует отметить, что конструирование экспрессирующего вектора, включая секрецию регуляторных последовательностей, может зависеть от таких факторов, как выбор трансформируемой клетки-хозяина, уровень экспрессии нужного белка и т.п. Предпочтительными регуляторными последовательностями, регулирующими экспрессию в клетках-хозяевах млекопитающих, являются вирусные элементы, которые обеспечивают высокие уровни экспрессии белка в клетках млекопитающих, такие как промоторы и/или энхансеры, происходящие от цитомегаловируса (CMV), обезьяньего вируса 40 (SV40), аденовируса (например, главный поздний промотор аденовируса (AdMLP)) и полиомавируса. Альтернативно, могут быть использованы невирусные регуляторные последовательности, такие как промотор убихитина или промотор β-глобина. Кроме того, могут быть использованы регуляторные элементы, состоящие из последовательностей, происходящих от различных источников, такие как промоторная система SR, содержащая последовательности раннего промотора SV40 и длинного концевого повтора вируса Т-клеточного человеческого лейкоза типа 1 (Takebe, Y. et al., 1988, Mol. Cell. Biol. 8:466-472).
Помимо генов цепей антител и регуляторных последовательностей рекомбинантные экспрессирующие векторы согласно изобретению могут содержать дополнительные последовательности, такие как последовательности, регулирующие репликацию вектора в клетках-хозяевах (например, ориджины репликации) и селективные маркерные гены. Селективный маркерный ген облегчает отбор клеток-хозяев, в которые был введен данный вектор (см., например, патенты US 4399216, US 4634665 и US 5179017, выданные Axel et al.). Так, например, обычно, селективный маркерный ген сообщает клеткам-хозяевам, в которые был введен данный вектор, резистентность к лекарственным средствам, таким как G418, гигромицин или метотрексат. Предпочтительными селективными маркерными генами являются ген дигидрофолат-редуктазы (DHFR) (вводимый в dhfr-клетки-хозяева при отборе/амплификации с использованием метотрексата) и ген neo (для отбора на резистентность к G418).
Для экспрессии легкой и тяжелой цепей экспрессирующий(е) вектор(ы), кодирующий(е) тяжелую и легкую цепи, переносят в клетку-хозяина стандартными методами. Термин «трансфекция» в его различных формах включает в себя методы широкого ряда, обычно используемые для введения экзогенной ДНК в прокариотические или эукариотические клетки-хозяева, например, электропорацию, преципитацию фосфатом кальция, трансфекцию, опосредуемую DEAE-декстраном. Хотя, теоретически, антитела согласно изобретению могут быть экспрессированы в любых прокариотических или эукариотических клетках-хозяевах, однако предпочтительными являются эукариотические клетки-хозяева, а наиболее предпочтительными являются клетки млекопитающих, поскольку такие эукариотические клетки, а в частности, клетки млекопитающих являются более подходящими для «правильной» сборки и секреции иммунологически активного антитела, чем прокариотические клетки. Сообщалось, что экспрессия генов антитела в прокариотических клетках оказалась неэффективной для продуцирования высоких уровней активного антитела (Boss, Μ.Α. & Wood, С.R., 1985, Immunology Today 6:12-13).
Предпочтительными клетками-хозяевами млекопитающих, подходящих для экспрессии рекомбинантных антител согласно изобретению, являются клетки яичника китайского хомячка (клетки СНО) (включая dhfr-клетки СНО, описанные в публикации Urlaub & Chasin, 1980, Proc. Natl. Acad. Sci. USA 77:4216-4220, и используемые с DHFR-селективным маркером, например, как описано в публикации R.J. Kaufman и P.A. Sharp, 1982, Mol. Biol. 159:601-621), клетки миеломы NSO, клетки COS и клетки SP2. В частности, для использования с миеломными клетками NSO, другой предпочтительной экспрессионной системой является экспрессионная система гена GS, описанная в WO 8704462, WO 8901036 и ЕР 338841. Если рекомбинантные экспрессирующие векторы, кодирующие гены антитела, вводят в клетки-хозяева млекопитающих, то антитела продуцируют путем культивирования указанных клеток-хозяев в течение периода времени, достаточного для осуществления экспрессии антитела в указанных клетках-хозяевах, а более предпочтительно для секреции указанного антитела в культуральную среду, в которой были культивированы эти клетки-хозяева. Антитела могут быть выделены из культуральной среды стандартными методами очистки белков.
Характеризация связывания антител с антигеном
Антитела согласно изобретению могут быть протестированы на связывание с FGFR1, например, с помощью проточной цитометрии. Вкратце, свежие FGFR1-экспрессирующие клетки собирают из колб для культивирования ткани и получают моноклеточную суспензию. Суспензии FGFR1-экспрессирующих клеток окрашивают «первым» антителом либо непосредственно, либо после фиксации 1% параформальдегидом в PBS. Приблизительно один миллион клеток ресуспендируют в PBS, содержащем, 0,5% BSA и 50-200 мкг/мл «первого» антитела, а затем инкубируют на льду в течение 30 мин. Клетки два раза промывают PBS, содержащим 0,1% BSA, 0,01% NaN3, ресуспендируют в 100 мкл разведенного 1:100 ФИТЦ-конъюгированного козьего антитела против человеческих IgG (Jackson ImmunoResearch, West Grove, PA) и инкубируют на льду в течение еще 30 мин. Затем клетки снова два раза промывают, ресуспендируют в 0,5 мл промывочного буфера и анализируют на флуоресцентное окрашивание на цитометре FACSCalibur (Becton-Dickinson, San Jose, CA).
Альтернативно, антитела согласно изобретению могут быть протестированы на связывание с FGFR1 с помощью стандартного ELISA. Вкратце, микротитрационные планшеты покрывают очищенным FGFR1 в концентрации 0,25 мкг/мл в PBS, а затем блокируют 5% альбумином бычьей сыворотки в PBS. В каждую лунку добавляют разведения антитела (например, разведения плазмы, взятой от FGFR1-иммунизованных мышей) и инкубируют в течение 1-2 ч при 37°С. Планшеты промывают PBS/твином, а затем инкубируют со «вторым» антителом (например, для человеческих антител, козьим поликлональным Fc-специфическим антителом против человеческого IgG), конъюгированным со щелочной фосфатазой, в течение 1 ч при 37°С. После промывки, в планшеты добавляют субстрат pNPP (1 мг/мл) для проявления окраски и анализируют при OD405-650. Обычно для слияния клеток предпочтительно использовать мышь, у которой вырабатываются наибольшие титры антител.
Для скрининга гибридом, которые обнаруживают положительную реактивность с иммуногеном FGFR1, можно также проводить анализы ELISA или FACS, · описанные выше. Гибридомы, которые связываются с FGFR1 с высокой авидностью, субклонируют, а затем охарактеризовывают. Один клон от каждой гибридомы, который сохраняет реактивность родительских клеток (на что указывает ELISA или FACS), может быть выбран для создания клеточного банка в 5-10 сосудах, которые помещают на хранение при -140°С и используют для очистки антител.
Для очистки анти-FGFR1-антител отобранные гибридомы могут быть культивированы в двухлитровых центрифужных колбах, предназначенных для очистки моноклональных антител.
Супернатанты могут быть подвергнуты фильтрации и концентрированию, а затем аффинной хроматографии на белке А-сефарозе (Pharmacia, Piscataway, NJ). Для гарантии нужной чистоты, элюированный IgG может быть оценен с помощью гель-электрофореза и высокоэффективной жидкостной хроматографии. Буферный раствор может быть заменен на PBS, и концентрация может быть определена по OD280 с использованием коэффициента экстинкции 1,43. Моноклональные антитела могут быть разделены на аликвоты и помещены на хранение при -80°С.
Для того чтобы определить, связываются ли выбранные моноклональные анти-FGFR1-антитела с уникальными эпитопами, каждое антитело может быть биотинилировано с использованием коммерчески доступных реагентов (Pierce, Rockford, IL). Исследования по конкурентному связыванию с использованием немеченых моноклональных антител и биотинилированных моноклональных антител могут быть проведены на FGFR1-сенсибилизированных ELISA-планшетах, описанных выше. Связывание биотинилированного mAb может быть детектировано с использованием стрептавидин-щелочной фосфатазы в качестве зонда. Альтернативно, исследования по конкурентному связыванию могут быть проведены с использованием радиоактивно меченого антитела, а немеченые конкурирующие антитела могут быть детектированы с помощью анализа по Скэтчарду.
Для определения изотипа очищенных антител ELISA-анализы на изотип антитела могут быть проведены с использованием реагентов, специфичных к антителам конкретного изотипа. Так, например, для определения изотипа человеческого моноклонального антитела лунки микротитрационных планшетов покрывают 1 мкг/мл антитела против человеческого иммуноглобулина и оставляют на ночь при 4°С. После блокирования 1%-ным BSA, планшеты подвергают реакции с 1 мкг/мл или менее тестируемых моноклональных антител или очищенных антител контрольного изотипа при комнатной температуре в течение 1-2 ч. Затем лунки могут быть подвергнуты реакции с антителами-зондами, специфичными к человеческому IgG1 или к человеческому IgM, и конъюгированными с щелочной фосфатазой. Планшеты проявляют и анализируют, как описано выше.
Физические свойства антител
Анти-FGFR1-антитела согласно изобретению могут быть также охарактеризованы на различные физические свойства. Различные классы таких антител могут быть идентифицированы и/или определены исходя из их физических свойств с помощью различных анализов.
В некоторых вариантах изобретения, антитела могут содержать один или несколько сайтов гликозилирования в вариабельной области легкой или тяжелой цепи. Присутствие одного или нескольких сайтов гликозилирования в вариабельной области может приводить к повышению иммуногенности антитела или к изменению рК антитела, обусловленному изменением уровня связывания с антигеном (Marshall et al., 1972, Annu. Rev. Biochem. 41:673-702; Gala F.A. & Morrison S.L., 2004, J. Immunol. 172:5489-94; Wallick et al., 1988, J. Exp.Med. 168:1099-109; Spiro R.G., 2002, Glycobiology 12:43R 56R; Parekh et al., 1985, Nature 316:452-7: Mimura et al., 2000, Mol. Immunol. 37:697-706). Известно, что гликозилирование происходит в мотивах, содержащих последовательность N-X-S/T. Гликозилирование вариабельной области может быть протестировано с помощью анализа Glycoblot, где тестируемое антитело расщепляют с получением Fab-фрагмента, а затем тестируют на гликозилирование с помощью анализа, в котором определяют уровень окисления периодатом и образование оснований Шиффа. Альтернативно, гликозилирование вариабельной области может быть протестировано посредством хроматографии (Dionex-LC) с измерением рассеяния света, где сахариды Fab расщепляют с получением моносахаридов и анализируют на содержание отдельных сахаридов. В некоторых случаях предпочтительно, чтобы анти- FGFR1-антитело не содержало сайтов гликозилирования в вариабельной области. Это может быть достигнуто либо путем отбора антител, не содержащих мотива гликозилирования в вариабельной области, либо путем мутации остатков в мотиве гликозилирования с применением стандартных методов, хорошо известных специалистам.
Каждое антитело имеет уникальную изоэлектрическую точку (pI), но обычно антитело имеет pI в интервале рН 6-9,5. pI для антитела IgG1 обычно составляет в пределах рН 7-9,5, a pI для антитела IgG4 обычно составляет в пределах рН 6-8. Антитела могут иметь pI, выходящую за пределы указанного интервала. Хотя влияние таких значений pI, по существу, неизвестно, однако существует мнение, что антитела со значением pI, выходящим за пределы нормальных интервалов, могут иметь до некоторой степени развернутую укладку и нестабильность в условиях in vivo. Изоэлектрическая точка может быть определена путем проведения анализа методом капиллярного изоэлектрического фокусирования, в котором создается градиент рН, а для большей точности может быть использовано лазерное фокусирование (Janiniet al., 2002, Electrophoresis 23:1605-11; Ma et al., 2001, Chromatographia 53:S75-89; Hunt et al., 1998, J. Chromatogr A 800:355-67). В некоторых случаях, предпочтительно, чтобы анти-FGFR1-антитело имело значение pI в нормальном интервале. Это может быть достигнуто либо путем отбора антител с pI в нормальном интервале, либо посредством мутации заряженных поверхностных остатков с применением стандартных методов, хорошо известных специалистам.
Каждое антитело имеет температуру плавления, которая является показателем его термостабильности (Krishnamurthy R. & Manning M.С, 2002, Curr. Pharm. Biotechnol. 3:361-71). Чем выше термостабильность антитела, тем выше его общая стабильность in vivo. Температура плавления антитела может быть измерена стандартными методами, такими как дифференциальная сканирующая калориметрия (Chen et al., 2003, Pharm. Res. 20:1952-60; Ghirlando et al., 1999, Immunol. Lett. 68:47-52). TM1 означает температуру начального развертывания антитела. ТМ2 означает температуру полного развертывания антитела. Обычно ТМ1 антитела согласно изобретению предпочтительно превышает 60°С, более предпочтительно превышает 65°С, а еще более предпочтительно превышает 70°С. Альтернативно, термостабильность антитела может быть измерена с использованием кругового дихроизма (Murray et al., 2002, J. Chromatogr Sci. 40:343-9). В предпочтительном варианте настоящего изобретения отбирают антитела, разложение которых происходит достаточно медленно. Фрагментация анти-FGFR1-антитела может быть измерена методами капиллярного электрофореза (КЭ) и MALDI-MS, хорошо известными специалистам (Alexander A.J. and Hughes D.E., 1995, Anal. Chem. 67:3626-32). В другом предпочтительном варианте изобретения отбирают антитела, подвергаемые минимальной агрегации. Агрегация может приводить к запуску нежелательного иммунного ответа и/или к вырабатыванию измененных или неблагоприятных фармакокинетических свойств. Обычно приемлемыми являются антитела, агрегация которых составляет 25% или менее, предпочтительно 20% или менее, еще более предпочтительно 15% или менее, еще более предпочтительно 10% или менее, а наиболее предпочтительно 5% или менее. Агрегация может быть измерена различными методами, хорошо известными специалистам, включая эксклюзионную колоночную хроматографию (ЭКХ), высокоэффективную жидкостную хроматографию (ВЭЖХ) и метод рассеяния света для идентификации мономеров, димеров, тримеров или мультимеров.
Иммуноконъюгаты
В другом своем аспекте настоящее изобретение относится к анти-FGFR1-антителу или к его фрагменту, конъюгированному с терапевтической молекулой, такой как цитотоксин, лекарственное средство (например, иммунодепрессант) или радиотоксин. Такие конъюгаты называются здесь «иммуноконъюгатами». Иммуноконъюгаты, которые включают в себя один или несколько цитотоксинов, называются «иммунотоксинами». Цитотоксин или цитотоксическое средство включает в себя любой агент, который оказывает негативное воздействие на клетку (например, разрушает клетку). Примерами являются таксол, цитохалазин В, грамицидин D, этидийбромид, эметин, митомицин, этопозид, тенопозид, винкристин, винбластин, колхицин, доксорубицин, даунорубицин, дигидроксиантрациндион, митоксантрон, митрамицин, актиномицин D, 1-дегидротестостерон, глюкокортикоиды, прокаин, тетракаин, лидокаин, пропранолол и пуромицин и их аналоги или гомологи. Терапевтическими средствами также являются, например, антиметаболиты (например, метотрексат, 6-меркаптопурин, 6-тиогуанин, цитарабин, 5-фторурацилдекарбазин), алкилирующие агенты (например, мехлорэтамин, тиотепа, хлорамбуцил, мелфалан, кармустин (BSNU) и ломустин (CCNU), циклофосфамид, бусульфан, дибромманнит, стрептозотоцин, митомицин С и цис-дихлордиаминплатина (II) (DDP), то есть цисплатин), антрациклины (например, даунорубицин (прежнее название: дауномицин) и доксорубицин), антибиотики (например, дактиномицин (прежнее название: актиномицин), блеомицин, митрамицин и антрамицин (АМС)) и антимитотические средства (например, винкристин и винбластин).
Другими предпочтительными примерами терапевтических цитотоксинов, которые могут быть конъюгированы с антителом согласно изобретению, являются дуокармицины, калихеамицины, майтанзины и ауристатины и их производные. Так, например, конъюгат «калихеамицин-антитело» является коммерчески доступным (Mylotarg®; Wyeth-Ayerst).
Цитотоксины могут быть конъюгированы с антителами согласно изобретению с применением линкерной технологии, известной специалистам. Примерами линкеров, которые могут быть использованы для конъюгирования цитотоксина с антителом, являются, но не ограничиваются ими, линкеры, содержащие гидразоны, тиоэфиры, сложные эфиры, дисульфиды и пептиды. Так, например, может быть выбран линкер, который является чувствительным к расщеплению при низком рН в лизосомном компартменте или чувствительным к расщеплению протеазами, такими как протеазы, преимущественно экспрессируемые в опухолевой ткани, такие как, катепсины (например, катепсины В, С, D).
Более подробное обсуждение типов цитотоксинов, линкеров и методов конъюгирования терапевтических средств с антителами можно также найти в публикациях Saito, G. et al., 2003, Adv. Drug Deliv. Rev. 55:199-215; Trail, P.A. et al., 2003, Cancer Immunol. Immunother. 52:328-337; Payne, G., 2003, Cancer Cell 3:207-212; Allen, T.M., 2002, Wat. Rev. Cancer 2:750-763; Pastan, I. and Kreitman, R.J., 2002, Curr. Opin. Investig. Drugs 3:1089-1091; Senter, P.D. и Springer, C.J., 2004, Adv. Drug Deliv. Rev. 53:247-264.
Антитела согласно изобретению могут быть также конъюгированы с радиоактивным изотопом с получением цитотоксических радиофармацевтических средств, также называемых радиоиммуноконъюгатами. Примерами радиоактивных изотопов, которые могут быть конъюгированы с антителами в целях их применения в диагностике или терапии, являются, но не ограничиваются ими, иод-131, иод-125, индий-111, иттрий-90 и лютеций-177. Метод получения радиоиммуноконъюгатов хорошо разработан специалистами.
Примерами радиоиммуноконъюгатов являются коммерчески доступные радиоиммуноконъюгаты, включая Zevalin® (IDEC Pharmaceuticals) и Bexxar® (Corixa Pharmaceuticals), и для получения радиоиммуноконъюгатов с использованием антител согласно изобретению могут быть применены аналогичные методы.
Конъюгаты антител согласно изобретению могут быть использованы для модификации данного биологического ответа, при этом выбор лекарственного средства необязательно должен ограничиваться классическими химическими терапевтическими средствами. Так, например, указанным лекарственным средством может быть белок или полипептид, обладающий нужной биологической активностью. Такими белками могут быть, например, ферментативно активный токсин или его активный фрагмент, такой как абрин, рицин А, экзотоксин Pseudomonas или дифтерийный токсин; белок, такой как фактор некроза опухоли или интерферон; или модификаторы биологических ответов, такие как, например, лимфокины, интерлейкин-1 (IL-1), интерлейкин-2 (IL-2), интерлейкин-6 (IL-6), гранулоцитарный-макрофагальный колониестимулирующий фактор (GM-CSF), гранулоцитарный колониестимулирующий фактор (G-CSF) или другие факторы роста. Методы конъюгирования таких терапевтических средств с антителами хорошо известны специалистам, см., например, Arnon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy," Monoclonal Antibodies and Cancer Therapy, Reisfeld et al. (eds.), pp.243-56 (Alan R. Liss, Inc. 1985); Hellstrom et al, "Antibodies For Drug Delivery," Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp.623-53 (Marcel Dekker, Inc. 1987); Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review," in Monoclonal Antibodies '84: Biological and Clinical Applications, Pinchera et al. (eds.), pp.475-506, 1985; "Analysis, Results and Future Prospective of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy," in Monoclonal Antibodies For Cancer Detection and Therapy, Baldwin et al. (eds.), pp.303-16 (Academic Press 1985) и Thorpe et al., “The Preparation and Cytotoxic Properties Of Antibodiy-Toxin Conjugates,” Immunol. Rev., 62:119-58, 1982.
Биспецифические молекулы
В другом своем аспекте настоящее изобретение относится к биспецифическим молекулам, содержащим анти-FGFR1-антитело согласно изобретению или его фрагмент. Антитело согласно изобретению или его антигенсвязывающая часть могут быть дериватизированы или присоединены к другой функциональной молекуле, например, к другому пептиду или белку (например, к другому антителу или рецептору) с получением биспецифической молекулы, которая связывается по меньшей мере с двумя различными сайтами связывания или с молекулами-мишенями. Антитело согласно изобретению может быть, фактически, дериватизировано или присоединено к более чем одной другой функциональной молекуле с получением мультиспецифических молекул, которые связываются с более чем двумя различными сайтами связывания и/или с молекулами-мишенями; и такие мультиспецифические молекулы также входят в определение используемого здесь термина «биспецифическая молекула». Для создания биспецифической молекулы согласно изобретению антитело согласно изобретению может быть функционально присоединено (например, посредством химического связывания, сцепления генов, нековалентного связывания или каким-либо иным методом связывания) к одной или нескольким другим связывающим молекулам, таким как другое антитело, фрагмент антитела, пептид или связывающий миметик, с получением нужной биспецифической молекулы. В соответствии с этим настоящее изобретение включает в себя биспецифические молекулы, обладающие по меньшей мере одной первой специфичностью связывания с FGFR1 и второй специфичностью связывания со вторым эпитопом-мишенью. В конкретном варианте изобретения указанным вторым эпитопом-мишенью является Fc-рецептор, например, человеческий FcγRI. Поэтому настоящее изобретение включает в себя биспецифические молекулы, способные связываться с FcγRI-экспрессирующими эффекторными клетками (например, моноцитами, макрофагами или полиморфонуклеарными клетками (ПМНК)) и с клетками-мишенями, экспрессирующими FGFR1. Такие биспецифические молекулы осуществляют доставку FGFR1-экспрессирующих клеток к эффекторным клеткам и стимулируют опосредуемую Fc-рецептором активность эффекторных клеток, такую как фагоцитоз FGFR1-экспрессирующих клеток, антитело-зависимая клеточно-опосредуемая цитотоксичность (ADCC), высвобождение цитокинов или образование супероксид-аниона. В варианте изобретения, в котором биспецифическая молекула является мультиспецифической, указанная молекула помимо специфичности связывания с Fc и специфичности связывания с FGFR1 может дополнительно обладать и третьей специфичностью связывания. В одном из вариантов изобретения такой третьей специфичностью связывания обладает область, направленная против фактора стимуляции (EF), например, молекула, которая связывается с поверхностным белком, участвующим в цитотоксической активности, и тем самым, усиливающим иммунный ответ против клетки-мишени. Такой «областью против фактора стимуляции» может быть антитело, фрагмент функционального антитела или лиганд, который связывается с данной молекулой, например с антигеном или рецептором, и, тем самым, способствует усилению связывания эпитопов для Fc-рецептора или антигена клетки-мишени. Такая «область против фактора стимуляции» может связываться с Fc-рецептором или антигеном клетки-мишени. Альтернативно, «область против фактора стимуляции» может связываться с молекулой, отличающейся от молекулы, с которой связываются области, обладающие первой и второй специфичностью связывания. Так, например, часть антитела против фактора стимуляции может связываться с цитотоксической Т-клеткой (например, посредством CD2, CD3, CD8, CD28, CD4, CD40, ICAM-1 или с другими иммунными клетками), что приводит к повышению иммунного ответа против клетки-мишени. В одном из вариантов изобретения указанные биспецифические молекулы согласно изобретению содержат в качестве молекулы, обладающей специфичностью связывания, по меньшей мере, одно антитело или его фрагмент, включая, например, Fab, Fab', F(ab')2/Fv, Fd, dAb или одноцепочечный Fv. Указанное антитело может также представлять собой димер легкой цепи или тяжелой цепи или любой их минимальный фрагмент, такой как Fv, или одноцепочечную конструкцию, описанную в патенте US 4946778, Ladner et al. В одном из вариантов изобретения специфичность связывания с Fc-рецептором обеспечивается моноклональным антителом, связывание которого не блокируется человеческим иммуноглобулином (IgG). Используемый здесь термин «IgG-рецептор» означает любой из восьми генов, кодирующих γ-цепь, и локализованных на хромосоме 1. Эти гены кодируют всего двенадцать трансмембранных или растворимых изоформ рецептора, которые подразделяются на три класса Fcγ-рецепторов: FcγRI (CD64), FcγRII (CD32) и FcγRIII (CD16). В одном из предпочтительных вариантов изобретения Fcγ-рецептором является человеческий высокоаффинный FcγRI. Человеческий FcγRI представляет собой молекулу размером 72 кДа, которая обладает высокой аффинностью к мономерному IgG (108-109 М-1). Продуцирование и характеризация некоторых предпочтительных моноклональных анти-Fc у антител описаны в международной заявке WO 88/00052, Fanger et al., и в патенте US 4954617. Эти антитела связываются с эпитопом FcγRI, FcyRII или FcγRIII в сайте, который отличается от сайта связывания Fcγ данного рецептора, а поэтому их связывание, по существу, не блокируется IgG на физиологическом уровне.
В еще одном предпочтительном варианте изобретения специфичность связывания с человеческим Fc-рецептором обеспечивается антителом, которое связывается с IgA-рецептором, например Fcα-рецептором (FcαRI, CD89), связывание которого предпочтительно не блокируется человеческим иммуноглобулином A (IgA). Используемый здесь термин "IgA-рецептор" означает любой генный продукт, кодируемый одним α-геном (FcαRI), локализованным на хромосоме 19. Известно, что этот ген кодирует несколько альтернативно сплайсированных трансмембранных изоформ, имеющих размер от 55 до 110 кДа. FcαRI (CD89) конститутивно экспрессируется на моноцитах/макрофагах, эозинофильных и нейтрофильных гранулоцитах, но не на популяциях не-эффекторных клеток. FcαRI имеет среднюю аффинность (5×107 М-1) для обоих IgА1 и IgА2, которая увеличивается под действием цитокинов, таких как G-CSF или GM-CSF (Morton, H.С. et al., 1996, Critical Reviews in Immunology 16:423-440). Были описаны четыре FcαRI-специфичных моноклональных антитела, идентифицированные как антитела A3, А59, А62 и А77, которые связываются с рецептором FcaRI, находящимся за пределами домена, связывающегося с лигандом IgA (Monteiro, R.C. et al., 1992, J. Immunol. 148:1764). FcγRI и FcαRI являются предпочтительными стимулирующими рецепторами, используемыми в биспецифических молекулах согласно изобретению, поскольку они (1) экспрессируются, главным образом, на иммунных эффекторных клетках, например, моноцитах, PMN, макрофагах и дендритных клетках; (2) экспрессируются на высоких уровнях (например, 5000-100000 на клетку); (3) являются медиаторами цитотоксической активности (например, ADCC, фагоцитоза) и (4) опосредуют повышенный уровень презентации антигенов, включая нацеленные на них аутоантигены. Хотя предпочтительными являются человеческие моноклональные антитела, однако в биспецифических молекулах согласно изобретению могут быть использованы и другие антитела, которыми являются мышиные, химерные и гуманизованные моноклональные антитела. Биспецифические молекулы согласно изобретению могут быть получены путем конъюгирования молекул, обладающих специфичностью связывания, например, с FcR и FGFR1, с применением методов, известных специалистам. Так, например, каждая биспецифическая молекула, обладающая специфичностью связывания, может быть продуцирована отдельно, а затем все эти молекулы могут быть конъюгированы друг с другом. Если молекулами, обладающими специфичностью связывания, являются белки или пептиды, то для ковалентного связывания может быть использован ряд связывающих или перекрестносшивающих агентов. Примерами перекрестносшивающих агентов являются белок А, карбодиимид, N-сукцинимидил-3-ацетил-тиоацетат (SATA), 5,5'-дитиобис(2-нитробензойная кислота) (DTNB), о-фенилендималеимид (oPDM), N-сукцинимидил-3-(2-пиридилдитио) пропионат (SPDP) и сульфосукцини-мидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC) (см., например, Karpovsky et al., 1984, J. Exp.Med. 160:1686; Liu, MA et al., 1985, Proc. Natl. Acad. Sci. USA 82:8648). Другими методами являются методы, описанные Paulus, 1985, Behring Ins. Mitt. №78, 118-132; Brennan et al., 1985, Science 229:81-83 и Glennie et al., 1987, J. Immunol. 139:2367-2375. Предпочтительными конъюгирующими агентами являются SATA и сульфо-SMCC, поставляемые Pierce Chemical Со. (Rockford, IL). Если специфически связывающимися молекулами являются антитела, то они могут быть конъюгированы посредством сульфгидрильной связи с С-концевыми шарнирными областями двух тяжелых цепей. В конкретном предпочтительном варианте изобретения шарнирную область модифицируют так, чтобы она содержала нечетное число сульфгидрильных остатков, а предпочтительно один остаток, а затем осуществляют конъюгирование. Альтернативно, обе специфически связывающиеся молекулы могут кодироваться в одном и том же векторе и могут экспрессироваться и подвергаться сборке в одной и той же клетке-хозяине. Этот метод является особенно подходящим в том случае, если биспецифической молекулой является гибридный белок mAb-mAb, mAb-Fab, Fab-F(ab')2 или лиганд-Fab. Биспецифической молекулой согласно изобретению может быть одноцепочечная молекула, содержащая одноцепочечное антитело и детерминанту связывания, или одноцепочечная биспецифическая молекула, содержащая две детерминанты связывания. Биспецифические молекулы могут содержать по меньшей мере две одноцепочечных молекулы. Методы получения биспецифических молекул описаны, например, в патенте US 5260203; в патенте US 5455030; в патенте US 4881175; в патенте US 5132405; в патенте US 5091513; в патенте US 5476786; в патенте US 5013653; в патенте US 5258498 и в патенте US 5482858. Связывание биспецифических молекул с их конкретными мишенями может быть подтверждено, например, с помощью иммуноферментного твердофазного анализа (ELISA), радиоиммуноанализа (РИА), FACS-анализа, биоанализа (например, на ингибирование роста) или вестерн-блот-анализа. В каждом из этих анализов обычно детектируют присутствие представляющих особый интерес комплексов «белок-антитело» с использованием меченого реагента (например, антитела), специфичного к представляющему интерес комплексу. Так, например, комплексы FcR-антитело могут быть детектированы с использованием, например, связанного с ферментом антитела или фрагмента антитела, которые распознают указанные комплексы «антитело-FcR» и специфически связываются с ними. Альтернативно, такие комплексы могут быть детектированы с помощью любого из ряда других иммуноанализов. Так, например, антитело может быть радиоактивно меченным и может быть использовано в радиоиммуноанализе (РИА) (см., например, публикацию Weintraub, В., Principles of Radioimmunoassays, Seventh Training Course on Radioligand Assay Techniques, The Endocrine Society, March, 1986). Радиоактивный изотоп может быть детектирован с помощью γ-счетчика или сцинтилляционного счетчика или посредством авторадиографии.
Фармацевтические композиции
В другом своем аспекте настоящее изобретение относится к композиции, например к фармацевтической композиции, содержащей одно моноклональное антитело согласно изобретению или его антиген связывающую(ие) часть (и) или их комбинации в сочетании с фармацевтически приемлемым носителем. Такие композиции могут включать одно антитело или их комбинации (например, два или более различных антител), или иммуноконъюгаты, или биспецифические молекулы согласно изобретению. Так, например, фармацевтическая композиция согласно изобретению может содержать комбинацию антител (или иммуноконъюгатов или биспецифических молекул), которые связываются с различными эпитопами на антигене-мишени или обладают дополнительной активностью. Фармацевтические композиции согласно изобретению могут быть также использованы в комбинированной терапии, то есть они могут быть введены в комбинации с другими средствами. Так, например, комбинированная терапия может включать введение анти-FGFR1-антитела согласно изобретению в комбинации по меньшей мере с одним другим противовоспалительным или иммуносупрессорным средством. Примеры терапевтических средств, которые могут быть использованы в комбинированной терапии, более подробно описаны ниже в разделе, относящемся к применению антител согласно изобретению. Используемый здесь термин «фармацевтически приемлемый носитель» включает в себя любые и все растворители, дисперсионные среды, материалы для покрытий, антибактериальные и противогрибковые средства, вещества, придающие изотоничность, и вещества, замедляющие абсорбцию, и т.п., которые являются физиологически совместимыми. Обычно таким носителем является носитель, подходящий для внутривенного, внутримышечного, подкожного, парентерального, интраспинального или интрадермального введения (например, путем инъекции или вливания). В зависимости от способа введения, активное соединение, то есть антитело, иммуноконъюгат или биспецифическая молекула могут иметь покрытие из материала, защищающего данное соединение от действия кислот и других условий окружающей среды, которые могут инактивировать данное соединение. Фармацевтические соединения согласно изобретению могут включать одну или несколько фармацевтически приемлемых солей. Термин «фармацевтически приемлемая соль» означает соль, которая сохраняет нужную биологическую активность исходного соединения и не обладает каким-либо нежелательным токсическим действием (см., например, Berge, S.M., et al., 1977, J. Pharm. Sci. 66:1-19). Примерами таких солей являются кислотно-аддитивные соли и основно-аддитивные соли. Кислотно-аддитивными солями являются соли, происходящие от нетоксичных неорганических кислот, таких как соляная, азотная, фосфорная, серная, бромистоводородная, иодистоводородная, фосфорная кислоты и т.п., а также от нетоксичных органических кислот, таких как алифатические моно- и дикарбоновые кислоты, замещенные фенилом алкановые кислоты, гидроксиалкановые кислоты, ароматические кислоты, алифатические и ароматические сульфоновые кислоты и т.п. Основно-аддитивными солями являются соли, происходящие от щелочноземельных металлов, таких как натрий, калий, магний, кальций и т.п., а также от нетоксичных органических аминов, таких как Ν,Ν'-дибензилэтилендиамин, N-метилглюкамин, хлорпрокаин, холин, диэтаноламин, этилендиамин, прокаин и т.п. Фармацевтическая композиция согласно изобретению может также включать фармацевтически приемлемый антиоксидант. Примерами фармацевтически приемлемых антиоксидантов являются: (1) водорастворимые антиоксиданты, такие как аскорбиновая кислота, гидрохлорид цистеина, бисульфат натрия, метабисульфит натрия, сульфит натрия и т.п.; (2) растворимые в масле антиоксиданты, такие как аскорбилпальмитат, бутилированный гидроксианизол (ВНА), бутилированный гидрокситолуол (ВНТ), лецитин, пропилгаллат, α-токоферол и т.п.; и (3) агенты, образующие хелатные комплексы с металлами, такие как лимонная кислота, этилендиаминтетрауксусная кислота (EDTA), сорбит, винная кислота, фосфорная кислота и т.п.
Примерами подходящих водных и безводных носителей, которые могут быть использованы в фармацевтических композициях согласно изобретению, являются вода, этанол, полиолы (такие как глицерин, пропиленгликоль, полиэтиленгликоль и т.п.) и их подходящие смеси, растительные масла, такие как оливковое масло, и органические сложные эфиры для инъекций, такие как этилолеат. Нужная текучесть может быть сохранена, например, путем нанесения покрытий из таких материалов, как лецитин, путем поддерживания требуемого размера частиц в случае дисперсий, и с использованием поверхностно активных веществ. Эти композиции могут также содержать адъюванты, такие как консерванты, смачивающие агенты, эмульгирующие агенты и диспергирующие агенты. Защита от микроорганизмов может быть достигнута, например, путем стерилизации или путем включения различных антибактериальных и противогрибковых средств, например, парабена, хлорбутанола, фенолсорбиновой кислоты и т.п. Может также оказаться желательным введение в композиции агентов, придающих изотоничность, таких как сахара, хлорид натрия, и т.п. Кроме того, пролонгированная абсорбция фармацевтического препарата для инъекции может быть достигнута путем включения веществ, замедляющих абсорбцию, таких как моностеарат алюминия и желатин. Фармацевтически приемлемыми носителями являются стерильные водные растворы или дисперсии и стерильные порошки для быстрого приготовления стерильных растворов или дисперсий для инъекций. Применение таких сред и агентов для приготовления фармацевтически активных веществ известно специалистам. В фармацевтических композициях согласно изобретению могут быть использованы любые стандартные среды или агенты, за исключением тех, которые являются несовместимыми с данным активным соединением. В такие композиции могут быть также введены дополнительные активные соединения. Терапевтические композиции должны быть стерильными и стабильными в условиях их приготовления и хранения. Такие композиции могут быть приготовлены в виде раствора, микроэмульсии, липосомы или других упорядоченных структур, подходящих для достижения высоких концентраций лекарственных средств. Носителем может быть растворитель или дисперсионная среда, содержащая, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полипропиленгликоль и т.п.) и их подходящие смеси. Нужная текучесть может быть сохранена, например, путем нанесения покрытий из таких материалов, как лецитин, путем поддерживания требуемого размера частиц в случае дисперсий, и с использованием поверхностно-активных веществ.
Стерильные растворы для инъекций могут быть получены путем включения в соответствующий растворитель активного соединения в требуемом количестве, взятого отдельно или в комбинации с ингредиентами, перечисленными выше, если это необходимо, с последующей микрофильтрацией путем стерилизации. Дисперсии обычно получают путем включения активного соединения в стерильный носитель, содержащий основную дисперсионную среду и другие необходимые ингредиенты из числа ингредиентов, перечисленных выше. В случае стерильных порошков, предназначенных для получения стерильных растворов для инъекций, предпочтительными методами получения таких препаратов являются вакуумная сушка и сушка вымораживанием (лиофилизация), в результате которой из указанного предварительно стерильно отфильтрованного раствора получают порошок, состоящий из активного ингредиента и любого другого нужного ингредиента.
Количество активного ингредиента, который может быть объединен с веществом-носителем в целях приготовления разовой лекарственной формы, может варьироваться в зависимости от индивидуума, подвергаемого лечению, и от конкретного способа введения. Количество активного ингредиента, который может быть объединен с веществом-носителем в целях получения разовой лекарственной формы, обычно представляет собой количество, включенное в композицию, которое продуцирует терапевтический эффект. В основном, такое количество, в расчете на 100% всего количества композиции, составляет в пределах примерно от 0,01 до 99% активного ингредиента, предпочтительно примерно от 0,1 до 70%, а наиболее предпочтительно примерно от 1 до 30% активного ингредиента в комбинации с фармацевтически приемлемым носителем. Схему приема лекарственного средства подбирают так, чтобы достигался оптимальный нужный ответ (например, терапевтический ответ). Так, например, может быть введена одна ударная доза или несколько дробных доз в течение определенного периода времени, либо эта доза может быть пропорционально уменьшена или увеличена в зависимости от терапевтических показаний.
Для облегчения введения и обеспечения равномерного введения доз, особенно предпочтительной композицией для парентерального введения является унифицированная лекарственная форма. Используемый здесь термин «унифицированная лекарственная форма» означает физически дискретную единицу, подходящую для однократного введения дозы индивидууму, подвергаемому лечению; причем каждая такая единица содержит заданное количество активного соединения, необходимое для достижения нужного терапевтического эффекта в комбинации с подходящим фармацевтическим носителем. Спецификация унифицированных лекарственных форм согласно изобретению определяется такими факторами и непосредственно зависит от таких факторов, как (а) уникальные свойства активного соединения и конкретно достигаемый терапевтический эффект, и (b) ограничения, с которыми сталкиваются специалисты при приготовлении такого активного соединения, и которые связаны с восприимчивостью индивидуума к применяемому лечению. Дозы вводимого антитела составляют в пределах примерно от 0,0001 до 100 мг/кг, а обычно от 0,01 до 25 мг/кг массы тела хозяина. Так, например, эти дозы могут составлять 0,3 мг/кг массы тела, 1 мг/кг массы тела, 3 мг/кг массы тела, 5 мг/кг массы тела или 10 мг/кг массы тела или в интервале 1-10 мг/кг. При необходимости могут быть введены более высокие дозы, например 15 мг/кг массы тела, 20 мг/кг массы тела или 25 мг/кг массы тела.
Репрезентативная схема лечения предусматривает введение дозы один раз в неделю, один раз в две недели, один раз в три недели, один раз в четыре недели, один раз в месяц, один раз в 3 месяца или один раз в 3-6 месяцев. Предпочтительная схема введения антитела согласно изобретению предусматривает внутривенное введение 1 мг/кг массы тела или 3 мг/кг массы тела, где указанное антитело вводят в соответствии со одной из следующих схем введения: (i) через каждые четыре недели, 6 доз, а затем через каждые три месяца; (ii) через каждые три недели; (iii) одну дозу в количестве 3 мг/кг массы тела, а затем одну дозу в количестве 1 мг/кг массы тела через каждые три недели.
В некоторых способах одновременно вводят два или более моноклональных анти-FGFR1-антител согласно изобретению с различными специфичностями связывания, и в данном случае доза каждого вводимого антитела составляет в пределах указанных значений. Антитело обычно вводят в виде многократных доз. Разовые дозы могут быть введены с интервалами раз в неделю, раз в месяц, раз в три месяца или раз в год. Интервалы введения доз могут быть также нерегулярными и могут устанавливаться в соответствии с измеряемыми уровнями антитела против антигена-мишени в крови данного пациента. В некоторых способах дозы могут быть скорректированы для достижения концентрации антитела в плазме в пределах примерно 1-1000 мкг/мл, а в некоторых способах, примерно 25-300 мкг/мл. В других способах, одно или несколько моноклональных анти-FGFR1-антител согласно изобретению вводят одновременно с антителом, обладающим другой специфичностью связывания, например, с таким антителом, как анти-СТLА-4-антитело и/или анти-PD-1-антитело, и в этом случае, каждое антитело вводят в дозе, величина которой входит в указанные интервалы. Альтернативно, антитело может быть введено в виде препарата пролонгированного высвобождения, и в этом случае требуется менее частое его введение. Доза и частота введения варьируются в зависимости от времени полужизни данного антитела в организме пациента. В общих чертах, человеческие антитела имеют наиболее продолжительное время полужизни, а за ними идут гуманизованные антитела, химерные антитела и нечеловеческие антитела. Доза и частота введения могут варьироваться в зависимости от того, является ли лечение профилактическим или терапевтическим. При профилактическом применении относительно низкую дозу антитела вводят через относительно большие интервалы в течение длительного периода времени. Некоторые пациенты проходят лечение в течение всей жизни. При терапевтическом применении иногда может потребоваться введение относительно высокой дозы через относительно короткие промежутки времени до замедления или прекращения прогрессирования заболевания, а предпочтительно до тех пор, пока у пациента не будет наблюдаться частичное ослабление или полное исчезновение симптомов заболевания. Затем пациенту может быть назначено профилактическое лечение. Фактические дозы активных ингредиентов в фармацевтических композициях согласно изобретению могут варьироваться в целях получения такого количества активного ингредиента, которое является эффективным для достижения нужного терапевтического ответа у данного пациента при соответствующем составе композиции и при соответствующем способе ее введения, и которое не оказывает токсического воздействия на пациента. Выбор доз зависит от ряда фармакокинетических факторов, включая активность конкретно используемых композиций согласно изобретению или их сложных эфиров, солей или амидов, способ введения, время введения, скорость выведения конкретно используемого соединения, продолжительность лечения, присутствие других лекарственных средств, соединений и/или веществ, используемых в комбинации с данными композициями, а также от возраста, пола, массы тела, тяжести заболевания, общего состояния здоровья и истории болезни пациента, подвергаемого лечению, и от других факторов, хорошо известных специалистам-медикам.
«Терапевтически эффективная доза» анти-FGFR1-антитела согласно изобретению, обычно способствует снижению тяжести симптомов заболевания, увеличению частоты и продолжительности ремиссий заболевания или предотвращению ухудшения состояния или наступления инвалидности, вызываемых данным заболеванием. Так, например, для лечения РGFR1+-опухолей, «терапевтически эффективная доза» предпочтительно, ингибирует рост клеток или опухолей по меньшей мере примерно на 20%, более предпочтительно по меньшей мере примерно на 40%, еще более предпочтительно по меньшей мере примерно на 60%, а наиболее предпочтительно по меньшей мере примерно на 80% по сравнению с индивидуумами, не подвергавшимися лечению. Способность соединения ингибировать рост опухоли может быть оценена на животном с предсказуемой моделью активного роста человеческих опухолей. Альтернативно, такое свойство композиции может быть оценено путем определения способности данного соединения ингибировать рост опухоли, где такое ингибирование in vitro осуществляют с помощью анализов, известных специалистам-практикам. Терапевтически эффективная доза терапевтического соединения может способствовать снижению размера опухоли или ослаблению каких-либо других симптомов у индивидуума. Средний специалист в данной области может самостоятельно определить нужные количества исходя из таких факторов, как масса тела индивидуума, тяжесть симптомов его заболевания, конкретный состав композиции или выбранный способ введения. Композиция согласно изобретению может быть введена одним или несколькими путями в соответствии с методикой, хорошо известной специалистам. Как известно специалистам, путь и/или способ введения может варьироваться в зависимости от желаемых результатов. Предпочтительными способами введения антител согласно изобретению являются внутривенное, внутримышечное, интрадермальное, внутрибрюшинное, подкожное и интраспинальное введение или другие способы парентерального введения, например, путем инъекции или вливания. Используемый здесь термин «парентеральное введение» означает способы введения, за исключением внутрикишечного и местного введения, обычно осуществляемые путем инъекции, и такими способами являются, но не ограничиваются ими, внутривенные, внутримышечные, внутриартериальные, интратекальные, интракапсулярные, интраорбитальные, внутрисердечные, интрадермальные, внутрибрюшинные, транстрахеальные, подкожные, субэпидермальные, внутрисуставные, субкапсулярные, субарахноидальные, интраспинальные, эпидуральные и интрастернальные инъекции и вливания. Альтернативно, антитело согласно изобретению может быть введено путем непарентерального введения, такого как местное или трансэпидермальное введение или введение через слизистую, например, путем интраназального, перорального, вагинального, ректального, подъязычного или местного введения.
Активные соединения могут быть получены в комбинации с носителями, которые защищают данное соединение от быстрого высвобождения, например, они могут быть получены в виде препарата с регулируемым высвобождением, включая имплантаты, чрескожные пластыри и микроинкапсулированные системы для доставки. Могут быть использованы биологически разлагаемые и биологически совместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Многие методы приготовления таких препаратов запатентованы или, по существу, известны специалистам. См., например, Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978. Терапевтические композиции могут быть введены с помощью медицинского оборудования, известного специалистам. Так, например, в предпочтительном варианте изобретения терапевтическая композиция согласно изобретению может быть введена с помощью безыгольного устройства для подкожных инъекций, такого как устройства, описанные в патентах US 5399163; US 5383851; US 5312335; US 5064413; US 4941880; US 4790824 или US 4596556. Примеры хорошо известных имплантатов и модулей, используемых в настоящем изобретении, можно найти в патенте US 4487603, где описан имплантируемый микроинфузионный насос для введения лекарственного средства с регулируемой скоростью; в патенте US 4486194, где описано терапевтическое устройство для чрескожного введения лекарственных средств; в патенте US 4447233, где описан медицинский инфузионный насос для введения лекарственного препарата с точно заданной скоростью вливания; в патенте US 4447224, где описан имплантируемый аппарат для непрерывного вливания лекарственного средства с различной скоростью потока; в патенте US 4439196, где описана осмотическая система доставки лекарственного средства, имеющая многокамерные отделения; и в патенте US 4475196, где описана осмотическая система доставки лекарственного средства. Эти патенты вводятся в настоящее описание посредством ссылки. Специалистам известны и многие другие подобные имплантаты, системы доставки и модули.
В некоторых вариантах изобретения человеческие моноклональные антитела согласно изобретению могут быть приготовлены так, чтобы они имели соответствующее распределение in vivo. Так, например, гематоэнцефалический барьер (ВВВ) не пропускает многие в высокой степени гидрофильные соединения. Для обеспечения прохождения терапевтических соединений согласно изобретению через ВВВ (если это необходимо), они могут быть приготовлены, например, в виде липосом. Методы получения липосом описаны, например, в патентах US 4522811; US 5374548 и US 5399331. Липосомы могут содержать одну или несколько молекул, которые селективно транспортируются в конкретные клетки или органы, что повышает эффективность направленной доставки лекарственных средств (см., например, V.V. Ranade, 1989, J. Clin. Pharmacol. 29:685). Репрезентативными нацеливающими молекулами являются фолат или биотин (см., например, патент США №5416016, Low et al.); маннозиды (Umezawa et al., 1988, Biochem. Biophys. Res. Commun. 153:1038); антитела (P.G. Bloeman et al., 1995, FEBS Lett. 357:140; M. Owais et al., 1995, Antimicrob. Agents Chemother. 39:180); поверхностно-активный рецепторный белок A (Briscoe et al., 1995, Am. J. Physiol. 1233: 134); p120 (Schreier et al., 1994, J. Biol. Chem. 269:9090): см. также К. Keinanen; M L. Laukkanen, 1994, FEBS Lett. 346:123; J.J. Killion; L.J. Fidler, 1994, Immunomethods 4:273.
Применение и способы согласно изобретению
Антитела, а в частности, гуманизированные антитела, композиции антител и способы согласно изобретению могут быть применены in vitro и in vivo в различных диагностических и терапевтических целях, например, для детектирования FGFR1, для лечения рака или для усиления иммунного ответа путем блокирования FGFR1. В предпочтительном варианте изобретения антителами согласно изобретению являются человеческие антитела. Так, например, эти молекулы могут быть введены в клеточную культуру, in vitro или ex vivo, или человеку, например, in vivo, для лечения, предупреждения и диагностики различных расстройств, или для повышения иммунитета при различных состояниях. Используемый здесь термин «индивидуум» включает в себя человека и животных. Такими животными являются все позвоночные, например млекопитающие и не млекопитающие, такие как приматы, не являющиеся человеком, овцы, собаки, кошки, коровы, лошади, куры, амфибии и рептилии. Предпочтительным индивидуумом является человек, а именно, пациент, страдающий расстройствами, ассоциированными с экспрессией FGFR1, или нуждающийся в усилении иммунного ответа. Указанные методы являются особенно подходящими для лечения человека, страдающего расстройством, ассоциированным с нарушением экспрессии FGFR1. Такие методы также являются особенно подходящими для лечения человека, страдающего расстройством, которое может быть подвергнуто лечению посредством повышения уровня Т-клеточно-опосредуемого иммунного ответа. Для достижения усиления антигенспецифического иммунного ответа анти-FGFR1-антитела могут быть введены вместе с представляющим интерес антигеном. Если антитела против FGFR1 вводят вместе с другим средством, то эти два компонента могут быть введены либо последовательно, либо одновременно. Принимая во внимание тот факт, что антитело согласно изобретению специфически связывается с FGFR1, следует отметить, что антитела согласно изобретению могут быть использованы для специфической детекции экспрессии FGFR1 на поверхности клеток, и, кроме того, они могут быть использованы для выделения FGFR1 посредством иммуноаффинной хроматографии.
Злокачественные опухоли
FGFR1 экспрессируется в различных злокачественных опухолях человека, включая немелкоклеточный рак легкого, рак молочной железы, рак желудка и пищевода, рак предстательной железы, рак мочевого пузыря, опухоли головы и шеи, меланома (С.Behrens et al. J Clinical cancer research 14, 19, 2008; M. Koziczak et al. J Oncogene, 23, 20, 2004; K. Freier J Oral Oncology 43, 1, 2007; E. Shin et al. J Cancer Res Clin Oncol. 126, 9, 2000; K. Sugiura et al. J Oncology reports 17, 3, 2007; E. Devilard et al. J BMC Cancer 6, 272, 2006; G.  et al. J Investigative Ophthalmology and Visual Science 50, 2009).
et al. J Investigative Ophthalmology and Visual Science 50, 2009).
Анти-FGFR1-антитело само может быть использовано для ингибирования роста опухолей. Альтернативно, анти-FGFR1-антитело может быть использовано в комбинации с другими иммуногенными средствами, со стандартной противораковой терапией или с другими антителами, описанными ниже. В проведенных исследованиях (KCRB-L01, WO 2011000384) была обнаружена экспрессия FGFR1 у пациентов с почечно-клеточным раком (ПКР). Иммуногистохимический анализ проводили на срезах парафиновых блоков опухолей у 140 больных ПКР. Результаты сравнивали с экспрессией FGFR1 у 40 здоровых доноров, которым ранее была произведена биопсия почки по разным причинам без последующего обнаружения заболеваний органа. Была выявлена экспрессия FGFR1 в 98% случаев на клетках первичной опухоли почки и в 82,5% случаев на клетках метастазов ПКР. Во всех случаях интенсивность окрашивания при иммуногистохимическом анализе была высокой (3+), что свидетельствует о сильной экспрессии рецептора. В 68% получено ядерное окрашивание. Экспрессия FGFR1 на клетках здоровой ткани почки выявлена в 1 случае (2,5%) за счет окрашивания сосудов. Таким образом, данное исследование подтвердило предположение о появлении и высокой экспрессии FGFR1 как на клетках первичной опухоли, так и в метастазах ПКР (I. Tsimafeyeu et al. ESMO-ECCO 09, 2009). В последующих исследованиях определяли концентрацию FGF 1 и 2, как основных факторов, обладающих митогенной активностью при связывании с FGFR1, в плазме крови 38 больных метастатическим ПКР до начала таргетной терапии, при прогрессировании болезни на таргетной терапии, а также в плазме крови 38 здоровых добровольцев (методом ELISA). Было установлено, что в крови здоровых людей уровни обоих FGF были достоверно ниже по сравнению с больными метастатическим ПКР. Наибольшие различия были продемонстрированы для FGF 2 (р<0,001). При прогрессировании заболевания на таргетной терапии (сунитиниб, сорафениб) происходило достоверное повышение FGF 2 - более чем на 50% (р<0,001) и FGF 1 - более чем на 30% (р<0,05) по сравнению с исходным уровнем FGF. При эффективности таргетной терапии изменение уровня обоих FGF достоверно не наблюдалось (р=0,3). Медиана концентрации FGF 2 в плазме пациентов при прогрессировании болезни и без - достоверно отличалась (р<0,001, фигура 1). Кроме того, в этом исследовании анализировался уровень мишени для сунитиниба/сорафениба - фактора роста эндотелия сосудов (ФРЭС). Статистических различий в концентрации ФРЭС в плазме пациентов с ПКР при прогрессировании болезни на терапии и исходным уровнем (р=0,2), а также корреляции с обоими FGF (р>0,1) не выявлено. Таким образом, результаты исследований KCRB-L01 и KCRB-L02 свидетельствуют о том, что патологический путь FGF/FGFR1 является не только независимым в развитии ПКР, но может определять устойчивость к существующей таргетной терапии опухолей. Основываясь на вышеизложенном, мы предположили, что блокирование пути FGF/FGFR1 может привести к нарушению пролиферации опухолевых клеток и ингибированию ангиогенеза. Антагонисты FGFR1, в том числе человеческие моноклональные антитела, могут быть использованы для подавления роста опухоли и ее метастазов. Кроме того, создание конъюгатов моноклонального антитела (его фрагментов) к FGFR1 и контрастных веществ может использоваться в диагностике злокачественных и других образований, клетки которых экспрессируют FGFR1 в большом количестве.
В одном из своих аспектов настоящее изобретение относится к лечению индивидуума in vivo с использованием анти-FGFR1-антитела, которое ингибирует рост раковых опухолей. Для ингибирования роста раковых опухолей может быть использовано лишь одно анти-FGFR1-антитело. Альтернативно, анти-FGFR1-антитело может быть использовано в комбинации с другими иммуногенными средствами, со стандартной противораковой терапией или с другими антителами, описанными ниже. В соответствии с этим, в одном из своих вариантов настоящее изобретение относится к способу ингибирования роста опухолевых клеток у индивидуума, где указанный способ включает в себя введение данному индивидууму терапевтически эффективного количества анти-FGFR1-антитела или его антигенсвязывающей части. Предпочтительным антителом является гуманизированное анти-FGFR1-антитело (например, любое из описанных здесь гуманизированных антител против человеческого FGFR1). Дополнительно или альтернативно, указанным антителом может быть химерное или человеческое анти-FGFR1-антитело. Предпочтительными раковыми опухолями, рост которых может ингибироваться антителами согласно изобретению, являются раковые опухоли, обычно восприимчивые к иммунотерапии. Не ограничивающими настоящее изобретение примерами раковых опухолей, предпочтительных для лечения антителами согласно изобретению, являются, почечно-клеточный рак, рак легкого, рак молочной железы (например, карцинома молочной железы), рак яичника (например, карцинома яичника).
Примерами других опухолевых заболеваний, которые могут быть подвергнуты лечению способами согласно изобретению, являются меланома (например, метастизирующая злокачественная меланома), рак предстательной железы, рак толстой кишки, опухоли костей, рак поджелудочной железы, рак кожи, опухоли головного мозга, хронический или острый лейкоз, включая острый миелоидный лейкоз, хронический миелоидный лейкоз, острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, лимфомы (например, ходжкинская лимфома и неходжкинская лимфома, лимфоцитарная лимфома, первичная лимфома ЦНС, Т-клеточная лимфома), карциномы носоглотки, рак головы и шеи, злокачественная меланома кожи или внутриглазная меланома, рак матки, рак прямой кишки, рак заднего прохода, рак желудка, рак яичек, рак матки, карцинома фаллопиевых труб, карцинома эндометрия, карцинома шейки матки, карцинома влагалища, карцинома вульвы, рак пищевода, рак тонкого кишечника, рак эндокринной системы, рак щитовидной железы, рак паращитовидной железы, рак коры надпочечника, саркома мягких тканей, рак уретры, рак пениса, солидные опухоли у детей, рак мочевого пузыря, рак почек или мочеточника, карцинома почечной лоханки, опухоль центральной нервной системы (ЦНС), опухолевый ангиогенез, опухоль позвоночника, глиома ствола головного мозга, аденома гипофиза, саркома Калоши, эпидермоидный рак, плоскоклеточный рак, раковые опухоли, индуцируемые влиянием окружающей среды, включая раковые опухоли, индуцируемые асбестом, например, мезотелиома и комбинации указанных раковых заболеваний.
Антитела против FGFR1 могут быть, но необязательно, объединены с иммуногенным агентом, таким как раковые клетки, очищенные опухолевые антигены (включая рекомбинантные белки, пептиды и углеводные молекулы), клетки, и клетки, трансфицированные генами, кодирующими иммуностимулирующие цитокины. Неограничивающими примерами подходящих для использования противоопухолевых вакцин являются вакцины на основе пептидов меланомных антигенов, таких как пептиды gp100, антигены MAGE, Trp-2, MART1 и/или тирозиназа, или вакцины на основе опухолевых клеток, которые были трансфицированы для экспрессии цитокина GM-CSF. Было обнаружено, что некоторые опухоли человека, такие как меланома, являются иммуногенными. При этом предполагается, что при увеличении порога активации Т-клеток посредством блокады FGFR1 можно активировать опухолевые ответы у хозяина.
Было разработано множество экспериментальных стратегий вакцинации против опухолей (см. Rosenberg, S., Development of Cancer Vaccines, ASCO Educational Book Spring: 60-62, 2000; Logothetis, ASCO Educational Book Spring: 300-302, 2000; Khayat, ASCO Educational Book Spring: 414-428, 2000; Foon, ASCO Educational Book Spring: 730-738, 2000; см. также Restifo, & Sznol, Cancer Vaccines, Ch. 61, pp.3023-3043 in DeVita, et al. (eds.), Cancer: Principles and Practice of Oncology, Fifth Edition, 1997). В одной из этих стратегий вакцину получают с использованием аутологичных или аллогенных опухолевых клеток. Обычно, эти клеточные вакцины являются наиболее эффективными при трансдукции опухолевых клеток в целях сообщения им способности экспрессировать GM-CSF. Было показано, что GM-CSF является сильным активатором презентации антигена и может быть использован для противоопухолевой вакцинации (Dranoff et al. Proc. Natl. Acad. Sci U.S.A. 90: 3539-43, 1993).
Исследование экспрессии генов и паттернов широкомасштабной экспрессии генов в различных опухолях позволило идентифицировать так называемые опухоль-специфические антигены (Rosenberg, Immunity 10: 281-7, 1999). Во многих случаях такие опухоль-специфические антигены представляют собой антигены дифференцировки, экспрессируемые в опухолях и в клетках, от которых произошли эти опухоли, например, антигены меланоцитов gp100, антигены MAGE и Тrр-2. Важно отметить, что многие из этих антигенов, как уже было показано, являются мишенями опухоль-специфических Т-клеток, присутствующих у хозяина. Блокада FGFR1 может быть осуществлена вместе с использованием набора рекомбинантных белков и/или пептидов, экспрессиируемых в опухоли для генерирования иммунного ответа на эти белки. Такие белки обычно распознаются иммунной системой как аутоантигены, а поэтому являются толерантными к ним. Опухолевым антигеном может быть также протеинтеломераза, которая необходима для синтеза хромосомных теломер, и которая экспрессируется в более чем 85% человеческих раковых опухолей и лишь в ограниченном числе соматических тканей (Kim et al. Science 266: 2011-2013, 1994) (эти соматические ткани могут быть защищены от иммунной атаки различными методами). Опухолевыми антигенами могут быть также «неоантигены», экспрессируемые в раковых клетках под влиянием соматических мутаций, которые модифицируют последовательность белка или приводят к образованию гибридных белков между двумя неродственными последовательностями (то есть bcr-abl в хромосоме Philadelphia) или идиотипа В-клеточных опухолей. Другие противоопухолевые вакцины могут включать белки вирусов, участвующих в образовании раковых опухолей у человека, таких как человеческие папиломавирусы (HPV), вирусы гепатита (HBV и HCV) и герпесвирус саркомы Капоши (KHSV). Другие формы опухоль-специфических антигенов, которые могут быть использованы в комбинации с блокадой FGFR1, представляют собой очищенные белки теплового шока (HSP), выделенные из самой опухолевой ткани. Эти белки теплового шока содержат фрагменты белков опухолевых клеток, и такие HSP являются в высокой степени эффективными при их доставке к антиген-презентирующим клеткам для вырабатывания противоопухолевого иммунитета (Suot & Srivastava, Science 269:1585-1588, 1995; Tamura et al. Science 278:117-120, 1997). Дендритные клетки (ДК) являются эффективными антиген-презентирующими клетками, которые могут быть использованы для стимуляции антигенспецифических ответов. ДК могут продуцироваться ex vivo и могут быть нагружены различными белковыми и пептидными антигенами, а также экстрактами опухолевых клеток (Nestle, F. et al., 1998, Nature Medicine A: 328-332). ДК могут быть также трансдуцированы генетическими методами для сообщения им способности экспрессировать опухолевые антигены. ДК были также непосредственно слиты с опухолевыми клетками в целях иммунизации (Kugler, A. et al., 2000, Nature Medicine 6:332-336). Иммунизация с использованием ДК, проводимая в целях вакцинации, может быть с успехом проведена в комбинации с блокадой PD-1 в целях активации более сильных противоопухолевых ответов. Блокада FGFR1 может быть также объединена со стандартной противораковой терапией. Блокада FGFR1 может быть с успехом осуществлена в комбинации с химиотерапией. В этих случаях может быть снижена доза вводимого химиотерапевтического средства (Mokyr, M. et al., 1998, Cancer Research 58: 5301-5304). Примером такой комбинации является комбинация анти-FGFR1-антитела с декарбазином, используемым для лечения различных раковых опухолей. Другим примером такой комбинации является комбинация анти-FGFR1-антитела с интерлейкином-2 (IL-2), используемым для лечения различных раковых опухолей. Помимо комбинированной терапии с применением блокады FGFR1 и химиотерапии, существует и другой научный подход, основанный на том, что гибель клеток, которая является следствием цитотоксического действия большинства химиотерапевтических соединений, должна приводить к повышению уровней опухолевого антигена на пути презентации антигена.
Другой комбинированной терапией, которая может давать синергетический эффект в сочетании с блокадой FGFR1 и, тем самым, приводить к гибели клеток, является лучевая терапия, хирургическая операция и антигормональная терапия. Каждая из этих стратегий позволяет создавать источник опухолевого антигена у хозяина. Блокада FGFR1 может быть также объединена с ингибированием ангиогенеза. Ингибирование ангиогенеза приводит к гибели опухолевых клеток, которые могут направлять опухолевый антиген на путь презентации антигена хозяина. FGFR1-блокирующие антитела могут быть также использованы в комбинации с биспецифическими антителами, которые направляют эффекторные клетки, экспрессирующие Feα- или Fcγ-рецепторы, к опухолевым клеткам (см., например, патенты US 5922845 и US 5837243). Биспецифические антитела могут быть использованы для доставки двух отдельных антигенов. Так, например, биспецифические антитела против Fc-рецептора/опухолевого антигена (например, Неr-2/neu) были использованы для доставки макрофагов в участки, пораженные опухолью. Такая направленная доставка может более эффективно активировать опухоль-специфические ответы. Блокада FGFR1 должна приводить к увеличению Т-клеточной составляющей этих ответов. Альтернативно, использование биспецифических антител, которые связываются с опухолевым антигеном и со специфическим маркером поверхности дендритных клеток, позволяет осуществлять непосредственную доставку антигена к ДК.
«Ускользание» опухолей от «иммунного надзора» хозяина происходит по различным механизмам широкого ряда. Многие из этих механизмов могут быть устранены путем инактивации белков, которые экспрессируются опухолями и являются иммуносупрессорными. Такими белками, среди прочих, являются TGF-бета (Kehrl, J. et al., 1986, J. Exp. Med. 163: 1037-1050), IL-10 (Howard, M. & O'Garra, Α., 1992, Immunology Today 13: 198-200) и лиганд Fas (Hahne, M. et al., 1996, Science 274: 1363-1365). Антитела против каждой из этих молекул могут быть использованы в комбинации с анти-PD-1 антителом для подавления действия иммуносупрессорного агента и индуцирования благоприятных противоопухолевых иммунных ответов у хозяина.
Другие антитела, которые могут активировать иммунные ответы у хозяина, могут быть использованы в комбинации с анти-FGFR1-антителами. Такими антителами являются молекулы, присутствующие на поверхности дендритных клеток и активирующие функцию ДК и презентацию антигена. Анти-СD40-антитела могут служить эффективной заменой активности Т-хелперных клеток (Ridge, J. et al., 1998, Nature 393: 474-478) и могут быть использованы в сочетании с анти-FGFR1-антителами. Активирующие антитела против Т-клеточных костимулирующих молекул, таких как CTLA-4 (например, патент US 5811097), ОХ-40 (Weinberg, A. et al., 2000, Immunol. 164: 2160-2169), 4-1 ВВ (Melero, I. et al., 1997, Nature Medicine 3: 682-685, 1997, PD-1 (del Rio et al., 2005, Eur. J. Immunol. 35:3545-60) и ICOS (Hutloff, A. et al., 1999, Nature 397: 262-266), могут быть также использованы для повышения уровней активации Т-клеток.
В настоящее время для лечения различных опухолей гемопоэтической системы применяется трансплантация костного мозга. Хотя осложнением такого лечения может быть реакция «трансплантат против хозяина», однако в результате вырабатывания у хозяина ответа «трансплантат против опухоли» может быть достигнут положительный терапевтический эффект. Блокада FGFR1 может быть использована для повышения эффективности трансплантированных донорам опухоль-специфических Т-клеток.
Было также разработано несколько экспериментальных стратегий терапии, которые предусматривают активацию ex vivo, экспансию антигенспецифических Т-клеток и адоптивный перенос этих клеток реципиенту для вырабатывания у него антигенспецифического Т-клеточного противоопухолевого ответа (Greenberg, R. & Riddell, S., 1999, Science 285: 546-51). Эти методы могут быть также применены для активации Т-клеточных ответов на инфекционные агенты, такие как CMV. Можно предположить, что ех vivo активация в присутствии анти-FGFR1-антител будет увеличивать число и активность адаптивно перенесенных Т-клеток. Принимая во внимание тот факт, что FGFR1 экспрессируются на различных опухолевых клетках, следует отметить, что человеческие антитела, композиции антител и способы согласно изобретению могут быть применены для лечения индивидуума, страдающего опухолевым заболеванием, например заболеванием, характеризующимся присутствием опухолевых клеток, экспрессирующих FGFR1, включая, например, почечно-клеточный рак, рак легкого, рак молочной железы (например, карциному молочной железы), рак яичника (например, карциному яичника). Примерами других опухолевых заболеваний, которые могут быть подвергнуты лечению способами согласно изобретению, являются меланома (например, метастизирующая злокачественная меланома), рак предстательной железы, рак толстой кишки и рак легких, опухоли костей, рак поджелудочной железы, рак кожи, опухоли головы и шеи, злокачественная меланома кожи или внутриглазная меланома, рак матки, рак прямой кишки, рак заднего прохода, рак желудка, рак яичек, карцинома фаллопиевых труб, карцинома эндометрия, карцинома шейки матки, карцинома влагалища, карцинома вульвы, болезнь Ходжкина, неходжкинская лимфома, острый миелоидный лейкоз (ALL), хронический лимфоцитарный лейкоз (CLL), лимфома Беркитта, анапластическая крупноклеточная лимфома (ALCL), множественная миелома, Т-клеточная лимфома кожи, нодулярная мелкоклеточная дифференцированная лимфома, лимфоцитарная лимфома, лимфомы периферических Т-клеток, лимфома Леннерта, иммунобластные лимфомы, Т-клеточный лейкоз/Т-клеточная лимфома (ATLL), Т-клеточный лейкоз взрослых (TALL), энтробластные/центроцитарные (cb/cc) фолликулярные лимфомы, диффузная крупноклеточная лимфома В-клеточной линии дифференцировки, Т-клеточная лимфома, подобная ангиоиммунобластной лимфоаденопатии (AILD), ВИЧ-ассоциированная лимфома полости тела, эмбриональные карциномы, недифференцированные карциномы носоглотки (например, опухоль Шминке), болезнь Каслмана, саркома Калоши, множественная миелома, макроглобулинемия Вальденстрема и другие В-клеточные лимфомы, рак пищевода, рак тонкого кишечника, опухоли эндокринной системы, опухоли щитовидной железы, опухоли паращитовидной железы, рак коры надпочечника, саркома мягких тканей, рак уретры, рак пениса, хронический или острый лейкоз, включая острый миелоидный лейкоз, хронический миелоидный лейкоз, острый лимфобластный лейкоз, хронический лимфоцитарный лейкоз, солидные опухоли у детей, лимфоцитарная лимфома, рак мочевого пузыря, рак почек или мочеточника, карцинома почечной лоханки, опухоль центральной нервной системы (ЦНС), первичная лимфома ЦНС, глиобластома, опухоли головного мозга, карциномы носоглотки, опухолевый ангиогенез, опухоль позвоночника, глиома ствола головного мозга, аденома гипофиза, саркома Капоши, эпидермоидный рак, плоскоклеточный рак, Т-клеточная лимфома, раковые опухоли, индуцируемые влиянием окружающей среды, включая раковые опухоли, индуцируемые асбестом, и комбинации указанных раковых заболеваний.
Настоящее изобретение может быть также применено для лечения метастазов злокачественных опухолей. В соответствии с этим, в одном из своих вариантов настоящее изобретение относится к способу ингибирования роста опухолевых клеток у индивидуума, где указанный способ включает в себя введение индивидууму терапевтически эффективного количества анти-FGFR1-антитела или его антигенсвязывающей части. Обычно, таким антителом является гуманизированное анти-FGFR1-антитело (например, любое гуманизированное антитело против FGFR1, описанное в настоящей заявке). Дополнительно или альтернативно, таким антителом может быть химерное или человеческое анти-FGFR1-антитело.
Вакцины
Анти-FGFR1-антитела могут быть использованы для стимуляции антигенспецифических иммунных ответов путем введения анти-FGFR1-антитела в комбинации с представляющим интерес антигеном (например, с вакциной). В соответствии с этим в другом своем аспекте настоящее изобретение относится к способу усиления иммунного ответа на антиген у индивидуума, включающего в себя введение указанному индивидууму: (i) антигена; и (ii) анти-FGFR1-антитела или его антигенсвязывающей части, в целях усиления иммунного ответа на указанный антиген у данного индивидуума. При этом предпочтительным антителом является гуманизированное антитело против человеческого FGFR1 (например, любое из описанных здесь гуманизированных анти-FGFR1-антител). Дополнительно или альтернативно, таким антителом может быть химерное или гуманизированное антитело. Указанным антигеном может быть, например, опухолевый антиген, вирусный антиген, бактериальный антиген или антиген, происходящий от патогена. Неограничивающими примерами таких антигенов являются антигены, обсуждаемые в вышеописанных разделах, такие как опухолевые антигены (или противоопухолевые вакцины), обсуждаемые выше, или антигены, происходящие от вирусов, бактерий или других патогенов. Подходящие способы in vivo и in vitro введения композиций антител (например, гуманизированных моноклональных антител, мультиспецифических и биспецифических молекул и иммуноконъюгатов) согласно изобретению хорошо известны специалистам и могут быть самостоятельно выбраны средним специалистом в данной области. Так, например, композиции антител могут быть введены путем инъекции (например, внутривенной или подкожной). Подходящие дозы используемых молекул зависят от возраста и массы тела индивидуума, а также от концентрации и/или состава данной композиции антител. Как было описано ранее, анти-FGFR1-антитела согласно изобретению могут быть введены в комбинации с одним или несколькими другими терапевтическими средствами, например, с цитотоксическим средством, радиоактивным токсическими средством или иммуносупрессорным средством.
Антитело может быть присоединено к указанному средству (в виде иммунокомплекса), либо оно может быть введено отдельно. В последнем случае (отдельное введение) указанное антитело может быть введено до, во время или после введения указанного средства, либо оно может быть введено в комбинации с проведением другой известной терапии, например противораковой терапии, а именно, лучевой терапии. Указанными терапевтическими средствами являются, среди прочих, противоопухолевые средства, такие как доксорубицин (адриамицин), цисплатин, сульфат блеомицина, кармустин, хлорамбуцил и циклофосфамидная соль гидроксимочевины, которые сами по себе являются эффективными только в концентрациях, токсичных или субтоксичных для пациента. Цисплатин вводят внутривенно в количестве 100 мг/мл на дозу один раз в четыре недели, а адриамицин вводят внутривенно в количестве 60-75 мг/мл на дозу один раз через каждые 21 день. Введение гуманизированных анти-FGFR1-антител или их антигенсвязывающих фрагментов согласно изобретению в комбинации с химиотерапевтическими средствами позволяет осуществлять доставку двух противораковых средств, которые действуют по различным механизмам и оказывают цитотоксическое действие на человеческие опухолевые клетки. Такое совместное введение позволяет решать проблемы, связанные с вырабатыванием резистентности к лекарственным средствам или с изменением антигенности опухолевых клеток, которое делает их невосприимчивыми к данному антителу.
Настоящее изобретение относится также к наборам, содержащим композиции антител согласно изобретению (например, гуманизированных антител, биспецифических или мультиспецифических молекул или иммуноконъюгатов) и инструкции по их применению. Такой набор может также содержать по меньшей мере один дополнительный реагент или одно или несколько дополнительных гуманизированных антител согласно изобретению (например, гуманизированное антитело, обладающее дополнительной активностью, направленной на связывание с эпитопом на антигене FGFR1 и отличающейся от активности первого гуманизированного антитела). Обычно такие наборы включают в себя этикетку, на которой приводится инструкция по применению содержимого данного набора. Термин «этикетка» включает в себя любой текст или отпечатанный материал, наклеенный на упаковку или вложенный в упаковку данного набора, или прилагаемый к данному набору в какой-либо иной форме.
Комбинированная терапия
В одном из вариантов изобретения настоящее изобретение относится к способу лечения гиперпролиферативного (онкологического) заболевания, включающему в себя введение индивидууму антитела против FGFR1 и антитела против CTLA-4 и/или PD-1. В других вариантах изобретения анти-FGFR1-антитело вводят в субтерапевтической дозе, анти-СТLА-4- и/или анти-PD-1-антитело вводят в субтерапевтической дозе, либо оба этих антитела вводят в субтерапевтической дозе. В другом своем варианте настоящее изобретение относится к способу подавления побочного эффекта, ассоциированного с лечением гиперпролиферативного заболевания иммуностимулирующим средством, где указанный способ включает в себя введение индивидууму анти-FGFR1-антитела и субтерапевтической дозы анти-СТLА-4- и/или анти-PD-1-антитела. В некоторых вариантах изобретения указанным индивидуумом является человек. В некоторых вариантах изобретения, указанным анти-СТLА-4-антителом является моноклональное антитело с человеческой последовательностью 10D1, а указанным анти-PD-1-антителом является моноклональное антитело с человеческой последовательностью, такие как 17D8, 2D3, 4Н1, 5С4 и 4А11. Моноклональное антитело с человеческой последовательностью 10D1 было выделено и структурно охарактеризовано, как описано в патенте US 6984720. Моноклональные антитела с человеческой последовательностью 17D8 2D3, 4Н1, 5С4 и 4А11 были выделены и структурно охарактеризованы, как описано в предварительной заявке на патент США №60/679466. Моноклональное анти-FGFR1-антитело, моноклональное анти-СТLА-4-антитело и моноклональное анти-PD-1-антитело и антитела с человеческой последовательностью согласно изобретению могут быть получены различными методами, включая стандартный метод получения моноклональных антител, например страндартный метод гибридизации соматических клеток, описанный Kohler и Milstein, 1975, Nature 256:495. При этом может быть применен любой метод получения моноклональных антител, например, метод вирусной или онкогенной трансформации В-лимфоцитов. Одним из животных, используемых для получения гибридом, является мышь. Получение гибридом у мышей является очень хорошо разработанной процедурой. Протоколы и методы иммунизации для выделения иммунизованных спленоцитов, проводимого в целях их последующего слияния, известны специалистам. Партнеры по слиянию (например, клетки мышиной миеломы) и процедуры слияния также известны специалистам (см., например, Harlow and Lane, 1988, Antibodies, A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor New York).
Комбинация антител может быть использована в целях усиления иммунного ответа для подавления гиперпролиферативного заболевания путем блокирования FGFR1 и PD-1 и/или CTLA-4. Так, например, эти молекулы могут быть введены в клеточные культуры, in vitro или ex vivo, или человеку, например, in vivo, для усиления иммунного ответа в различных ситуациях. В соответствии с этим в одном из своих аспектов настоящее изобретение относится к способу модификации иммунного ответа у индивидуума, включающему в себя введение данному индивидууму комбинации антител или комбинации их антигенсвязывающих частей согласно изобретению в целях модификации иммунного ответа у индивидуума. При этом предпочтительно, чтобы такой ответ усиливался, стимулировался или активировался. В другом своем варианте настоящее изобретение относится к способу устранения побочных эффектов, ассоциированных с лечением гиперпролиферативного заболевания иммуностимулирующим терапевтическим средством, где указанный способ включает в себя введение индивидууму анти-FGFR1 -антитело и субтерапевтической дозы анти-СТLА-4-антитела или анти-PD-1-антитела. Блокирование FGFR1, PD-1 и CTLA-4 антителами может усиливать иммунный ответ против раковых клеток у пациента. Злокачественными опухолями, рост которых может ингибироваться антителами согласно изобретению, являются злокачественные опухоли, обычно восприимчивые к иммунотерапии. Репрезентативными примерами злокачественных опухолей, для лечения которых может быть применена комбинированная терапия согласно изобретению, являются почечно-клеточный рак (ПКР), рак легкого, меланома (например, метастизирующая злокачественная меланома), рак предстательной железы, рак молочной железы, рак толстой кишки, рак легких и другие злокачественные опухоли, включая злокачественные опухоли, индуцируемые влиянием окружающей среды, в том числе злокачественные опухоли, индуцируемые асбестом, и комбинации указанных злокачественных опухолей.
Настоящее изобретение может быть также применено для лечения метастазов злокачественных опухолей. В некоторых вариантах изобретения обсуждаемая здесь комбинация терапевтических антител может быть введена одновременно в виде одной композиции в фармацевтически приемлемом носителе или одновременно в виде отдельных композиций каждого антитела в фармацевтически приемлемом носителе. В другом варианте изобретения такая комбинация терапевтических антител может быть введена последовательно. Так, например, анти-FGFR1-антитело и анти-PD-1-антитело могут быть введены последовательно, например, сначала может быть введено анти-FGFR1-антитело, а затем анти-PD-1-антитело, либо сначала может быть введено анти-PD-1-антитело, а затем анти-FGFR1-антитело. Кроме того, в случае последовательного введения более чем одной дозы комбинации терапевтических средств, порядок такого введения может быть обратным или одним и тем же для каждого времени введения, при этом последовательное введение может быть объединено с одновременным введением, либо оно может быть осуществлено в любой другой комбинации. Так, например, первое введение может быть осуществлено путем одновременного введения анти-FGFR1-антитела и анти-PD-1-антитела в комбинации друг с другом, при втором введении, сначала может быть введено анти-FGFR1-антитело, а затем анти-PD-1-антитело, а при третьем введении сначала может быть введено анти-PD-1-антитело, а затем анти-FGFR1-антитело и т.п. Другая репрезентативная схема может включать первое введение, при котором сначала вводят анти-PD-1-антитело, а затем анти-FGFR1-антитело, а во втором и последующих введениях эти антитела вводят одновременно.
Блокирование всех FGFR1 и PD-1 и/или CTLA-4 должно приводить к увеличению Т-клеточной составляющей опухоль-специфических ответов.
Альтернативно, использование биспецифических антител, которые связываются с опухолевым антигеном и со специфическим маркером поверхности дендритных клеток, позволяет осуществлять непосредственную доставку антигена к ДК.
В другом примере, антитела по изобретению могут быть использованы в комбинации с противоопухолевыми антителами, такими как Rituxan® (ритуксимаб), Herceptin® (трастузумаб), Веххаr® (тозитумомаб), Zevalin® (ибритумомаб), Campath® (алемтузумаб), Lymphocide® (эпратузумаб), Avastin® (бевацизумаб) и Tarceva® (эрлотиниб) и т.п.
В некоторых своих вариантах настоящее изобретение относится к способу устранения побочных эффектов, ассоциированных с лечением гиперпролиферативного заболевания иммуностимулирующим средством, где указанный способ включает в себя введение индивидууму анти-FGFR1-антитела и субтерапевтической дозы анти-СТLА-4-антитела. Так, например, настоящее изобретение относится к способу снижения частоты возникновения колита или диареи, индуцированных иммуностимулирующим терапевтическим антителом, где указанный способ включает в себя введение пациенту неабсорбируемого стероида. Поскольку у любого пациента, подвергаемого лечению иммуностимулирующим терапевтическим антителом, имеется риск развития колита или диареи, индуцированных введением такого антитела, то это означает, что терапия с применением способов согласно изобретению может оказаться эффективной для всего населения. Хотя стероиды были введены для лечения воспалительного заболевания кишечника (ВЗК) и для предупреждения осложнений при ВЗК, однако они не были использованы для предупреждения развития ВЗК (снижения частоты развития ВЗК) у пациентов, у которых ранее не было диагностировано ВЗК. Серьезные побочные эффекты, ассоциированные с введением стероидов, и даже с введением неабсорбируемых стероидов, не позволяют использовать их в профилактических целях.
В других вариантах изобретения, блокирование всех FGFR1 и PD-1 и/или CTLA-4 (т.е. использование иммуностимулирующих терапевтических антител против FGFR1 и PD-1 и/или CTLA-4) может быть также объединено с применением любых неабсорбируемых стероидов. Используемый здесь термин «неабсорбируемый стероид» означает глюкокортикоид, который сначала проходит интенсивный первый путь метаболизма, то есть после метаболизма в печени биологическая доступность такого стероида становится низкой, то есть менее чем примерно 20%. В одном из вариантов изобретения неабсорбируемым стероидом является будезонид. Будезонид представляет собой глюкокортикостероид местного действия, который после перорального введения подвергается интенсивному метаболизму, главным образом, в печени.
ENTOCORT ЕС® (Astra-Zeneca) представляет собой пероральный препарат будезонид, действие которого зависит от рН и от времени введения, и который был разработан для оптимизации доставки лекарственного средства в подвздошную кишку и через толстую кишку. В США ENTOCORT ЕС® был разрешен к применению для лечения болезни Крона легкой или средней тяжести, поражающей подвздошную кишку и/или восходящую толстую кишку. Обычно, пероральная доза препарата ENTOCORT ЕС® для лечения болезни Крона составляет 6-9 мг/день. ENTOCORT ЕС® высвобождается в тонкий кишечник, а затем адсорбируется и остается в слизистой кишечника. После прохождения через нужную ткань слизистой кишечника, ENTOCORT ЕС® подвергается интенсивному метаболизму под действием системы цитохрома Р450 в печени, в результате чего образуются метаболиты, обладающие незначительной глюкокортикоидной активностью. Поэтому его биологическая доступность является низкой (примерно 10%).
Низкая биологическая доступность будезонида обеспечивает лучший терапевтический индекс по сравнению с другими глюкокортикоидами с менее интенсивным первым этапом метаболизма. Будезонид дает меньшие побочные эффекты, включая меньшую степень подавления функции гипоталамуса-гипофиза, чем кортикостероиды системного действия. Тем не менее, постоянное введение ENTOCORT ЕС® может приводить к развитию системных глюкокортикоидных эффектов, таких как гиперкортицизм и подавление функций надпочечников. См. PDR 58th ed. 2004; 608-610.
В других вариантах изобретения блокирование комбинации FGFR1 и PD-1 и/или CTLA-4 (то есть иммуностимулирующими терапевтическими анти-FGFR1-антителом и анти-PD-1-антителом и/или антиСТLА-4-антителом), осуществляемое в сочетании с неабсорбируемым стероидом, может быть также проведено в сочетании с салицилатом. Салицилатами являются соединения 5-ASA, такие как, например: сульфасалазин (AZULFIDINE®, Pharmacia & UpJohn); олсалазин (DIPENTUM®, Pharmacia & UpJohn); балсалазид (COLAZAL®, Salix Pharmaceuticals, Inc.) и мезаламин (ASACOL®, Procter & Gamble Pharmaceuticals; PENTASA®, Shire US; CANASA®, Axcan Scandipharm, Inc.; ROWASA®, Solvay).
В способах согласно изобретению для снижения числа случаев возникновения колита, индуцированного иммуностимулирующими антителами, введение салицилата в комбинации с анти-FGFR1 антителом и анти-PD-1-антителом и/или с анти-СТLА-4-антителом и неабсорбируемым стероидом может быть осуществлено путем почти одновременного или последовательного введения салицилата и неабсорбируемого стероида. Так, например, в соответствии с настоящим изобретением способы снижения числа случаев возникновения колита, индуцированного иммуностимулирующими антителами, охватывают введение салицилата и неабсорбируемого стероида одновременно или последовательно (например, салицилат вводят через 6 ч. после введения неабсорбируемого стероида) или в любом другом порядке. Кроме того, в соответствии с настоящим изобретением, салицилат и неабсорбируемый стероид могут быть введены одним и тем же способом (например, они оба могут быть введены перорально) или различными способами (например, салицилат вводят перорально, а неабсорбируемый стероид вводят ректально), которые могут отличаться от способа(ов) введения анти-FGFR1-антитела, анти-PD-1-антитела и анти-СТLА-4-антитела.
Композиции согласно изобретению (например, человеческие антитела, мультиспецифические и биспецифические молекулы и иммуноконъюгаты), имеющие комплемент-связывающие сайты, такие как части, происходящие от IgG1, IgG2 или IgG3 или IgM, которые связываются с комплементом, могут быть также использованы в присутствии комплемента. В одном из вариантов изобретения ex vivo обработка популяции клеток, содержащей клетки-мишени, связывающим агентом согласно изобретению и соответствующими эффекторными клетками, может быть осуществлена вместе с введением комплемента или комплемент-содержащей сыворотки. Фагоцитоз клеток-мишеней, покрытых связывающим агентом согласно изобретению, может быть усилен посредством связывания с белками комплемента. В другом варианте изобретения клетки-мишени, покрытые указанными композициями согласно изобретению (например, человеческими антителами, мультиспецифическими и биспецифическими молекулами), могут быть также подвергнуты лизису под действием комплемента. В еще одном варианте изобретения указанные композиции согласно изобретению не активируют комплемент. Композиции согласно изобретению (например, человеческие антитела, мультиспецифические и биспецифические молекулы и иммуноконъюгаты) могут быть также введены в комбинации с комплементом. В соответствии с этим в объем настоящего изобретения входят композиции, содержащие человеческие антитела, мультиспецифические и биспецифические молекулы, и сыворотку или комплемент.
Эти композиции имеют то преимущество, что в них указанный комплемент локализован в непосредственной близости от человеческих антител, мультиспецифических и биспецифических молекул. Альтернативно, человеческие антитела, мультиспецифические и биспецифические молекулы согласно изобретению и комплемент или сыворотка могут быть введены отдельно.
В соответствии с этим пациентам, подвергаемым лечению композициями антител согласно изобретению, может быть дополнительно введено (до, во время или после введения человеческого антитела согласно изобретению) другое терапевтическое средство, такое как цитотоксическое или радиотоксическое лекарственное средство, которое усиливает или улучшает терапевтический эффект человеческого антитела.
Настоящее изобретение подробно проиллюстрировано нижеследующими примерами, которые не должны рассматриваться как ограничение изобретения. Описание всех публикаций, патентов и опубликованных патентных заявок, цитируемых в настоящей заявке, во всей своей полноте вводится в настоящее описание посредством ссылки.
Пример 1. Мышиное моноклональное антитело ОСХ-01 против FGFR1, полученное из гибридом
Мышиная гибридома РА255 клон 56 (Бюро по исследованию рака почек) была получена гибридомным методом G.  , С. Milstein. J Nature 256, 495 (1975) и выращена в модифицированной по способу Дульбекко среде Игла MegaCell™ (компания «Сигма Алдрич») с 1 ммоль/л глутамина, 10% ЭБС («Гибко»; «Инвитроген») и 50 мкг/мл гентамицина (компания «Сигма Алдрич») при температуре 37°С, 5% СO2. Клеточная линия млекопитающих CHO-S была куплена у компании «Инвитроген» и содержалась в среде CHO-S-SFM II («Гибко»; «Инвитроген») при температуре 37°С, 8% СO2. Мышиное моноклональное антитело ОСХ-01, полученное из клеточной линии мышиной РА255 клон 56, обладает способностью связываться с высокой степенью сродства (Kd=4,6 нМ) и возможностью оказывать влияние на биологическую активность FGF-рецептора.
, С. Milstein. J Nature 256, 495 (1975) и выращена в модифицированной по способу Дульбекко среде Игла MegaCell™ (компания «Сигма Алдрич») с 1 ммоль/л глутамина, 10% ЭБС («Гибко»; «Инвитроген») и 50 мкг/мл гентамицина (компания «Сигма Алдрич») при температуре 37°С, 5% СO2. Клеточная линия млекопитающих CHO-S была куплена у компании «Инвитроген» и содержалась в среде CHO-S-SFM II («Гибко»; «Инвитроген») при температуре 37°С, 8% СO2. Мышиное моноклональное антитело ОСХ-01, полученное из клеточной линии мышиной РА255 клон 56, обладает способностью связываться с высокой степенью сродства (Kd=4,6 нМ) и возможностью оказывать влияние на биологическую активность FGF-рецептора.
Пример 1.1. Изоляция м-РНК и обратная транскрипция
Все РНК были извлечены из клеток гибридомы с использованием системы Nucleospin RNA II (компания «Мачерей Нагел ГмбХ энд Ко КГ»), в соответствии с инструкциями производителя, кДНК синтезировались из 5 мкг извлеченных РНК с использованием системы First Strand cDNA Synthesis и набора праймеров мышиного Ig («Новаген»; «Мерк КГаА») в соответствии с инструкциями производителя.
Пример 1.2. Амплификация вариабельных областей тяжелой и легкой цепи мышиного Ig, клонирование и секвенирование
Мышиные последовательности VDJ и VJ для вариабельных областей тяжелой и легкой цепей были амплифицированы с применением синтезированных кДНК, набора праймеров мышиного Ig и ДНК-полимеразы NovaTаg («Новаген»; «Мерк КГаА»). Продукты ПЦР были очищены и клонированы в системе pSTBIue-1 AccepTor Vector и с применением ДНК-полимеразы NovaTaq («Новаген»; «Мерк КГаА») в соответствии с инструкциями производителя. Секвенирование плазмидной ДНК проводилось компанией «ЛГК Геномикс ГмбХ».
Последовательности мышиных VDJ или VJ-реаранжировок были связаны с широкодоступными последовательностями генеративной линии из генов тяжелой и легкой цепей мышиного Ig с использованием программного обеспечения IMGT/V_QUEST. Многочисленные связи VDJ или VJ и мышиных последовательностей были получены с помощью программного обеспечения ClustalW.
Пример 2. Получение вариантов гуманизированных антител
Гуманизированные версии моноклонального антитела РА255 клон 56, ОСХ-01, были сгенерированы с использованием иммуногенетической информации и инструментов иммуноинформационного моделирования, ставших доступными с помощью международной информационной системы ImMunoGeneTics® (IMGT®, http://www.imgt.org). Мышиные вариабельные последовательности тяжелой и легкой цепей (VH и VL соответственно) сравнивались с человеческими последовательностями генеративной линии с использованием инструментов IMGT/V_QUEST и IMGT/DomainGapAlign. Компоненты мышиных последовательностей, которые отличались от человеческих компонентов в исследуемых сегментах, были заменены, за исключением CDR и ключевых аминокислот. Предложенные изменения были проанализированы с применением систем IMGT/collier de perles и IMGT/3D Structure с целью сравнения с референтными мышиными и человеческими генеративными линиями. Отдельные аминокислоты из мышиного антитела использовались, если они рассматривались как играющие важную роль в формировании специфичности и сродства антитела. Гены со специфическими мутациями были синтезированы с применением системы GeneArt («Инвитроген»). После ДНК-секвенирования гуманизированные вариабельные области были помещены на производные векторы pCDNA3, а также экспрессионные векторы pHHU_HulgG1 и pHHU_Huk, содержащие человеческий IgG1-ген IGHG1*03 (База данных GenBank: Y14737) и к-ген IGKC*01 (База данных GenBank: J00241), представляющие константные домены тяжелой и легкой цепи антитела соответственно.
Первоначально были получены коды последовательностей нуклеотидов для различных доменов тяжелых (VH) и легких (VL) цепей мышиного моноклонального антитела после извлечения м-РНК из клеточной линии гибридомы клона 56. Синтез кДНК и амплификация вариабельной области кДНК с помощью полимеразной цепной реакции (ПЦР) были проведены с использованием подходящих наборов праймеров. Затем коды последовательностей нуклеотидов и аминокислот для различных доменов мышиного антитела были проанализированы с использованием инструментов IMGT/V-QUEST и IMGT/DomainGapAlign и наиболее близких человеческих V и J генов.
Были выявлены длины гипервариабельных участков для тяжелой цепи на уровне [9.7.9], а также наиболее близкий человеческий ген IGHV4-30-4*01 (База данных GenBank: Z14238). Имеются 19 отличий между OM-RCA-01 VH и человеческим геном IGHV4-30-4*01 (3, 5 и 11 в структурах FR1, FR2 и FR3 IMGT соответственно). В структуре FR4-IMGT остатки Т123 и L124 мышиного антитела VH были заменены на L123 и V124 (Рис. 1) с целью получения идентичной последовательности для человеческого IGHJ4-30-4*01.
Были выявлены длины гипервариабельных участков для легкой цепи на уровне [7.3.9], а также наиболее близкий человеческий ген IGKV1-9*01 (База данных GenBank: Z00013). Имеются 28 отличий между OM-RCA-01 VL и человеческим геном IGKV1-9*01 (12, 6 и 10 в структурах FR1, FR2 и FR3 IMGT соответственно). В структуре FR4-IMGT остаток L124 мышиного антитела VL был заменен на V124 с целью получения идентичной последовательности для человеческого IGKJ4*01.
Длины гипервариабельных участков ограничиваются расположением структур FR-IMGT (Лефранк с соавторами, 2003, 10). С целью сохранения расположения гипервариабельных участков, остатки ключевых и специфических мышиных аминокислот считались потенциально важными для сохранения строения вариабельной области, так как контакты с гипервариабельными участками должны были происходить в гуманизированной форме. С учетом этого критерия была создана структура, состоящая из двух гуманизированных вариабельных тяжелых цепей (VH3 и VH4) и трех гуманизированных легких цепей (VL3, VL4 и VL5) с целью их совместного использования и получения функционального гуманизированного моноклонального антитела (ОМ-RCA) с сохранением антигенсвязывающего сродства родительского мышиного антитела. Химерный организм, содержащий мышиные вариабельные легкую (mVL2) и тяжелую (mVH2) цепи, совмещенный с человеческими постоянными каппа и IgG1 тяжелыми цепями соответственно, использовался в качестве контрольного материала.
Экспрессионные векторы тяжелой и легкой цепи для вариантов гуманизированного антитела были трансфицированы в соотношении 1:1 в клетки CHO-S с использованием реагента Freestyle™ МАХ («Инвитроген»). 30×106 клеток были трансфицированы с 15 мкг каждого экспрессионного вектора и 30 мкл реагента трансфекции. Надосадочные жидкости были получены через 3 дня после трансфекции с помощью центрифугирования. Антитела были очищены на G-сефарозе (компания «ДжиИ Хелскер») и проанализированы с применением нитрата серебра SDS-PAGE.
Пример 2.1. Анализ связывания антител
Для оценки иммунореактивности химерного антитела и рекомбинантных гуманизированных вариантов с учетом FGFR1, титрационные микропланшеты (компания «Грейнер Био Уан») были покрыты 0,5 мкг/мл РА-269#37 рекомбинанта FGFR1 (антигена) или коммерческим рекомбинантным человеческим FGFR1 (компания «Сино Биолоджикалс», ссылка №10616-Н08Н) в 0,05 моль/л карбонатно-бикарбонатного буфера, рН 9,6. Связанные антитела были обнаружены с использованием легкой цепи каппа козьего противочеловеческого антитела, конъюгированного с пероксидазой хрена («Сигма Алдрич»), для гуманизированных вариантов или анти-мышиного IgG (ФК-специфичного) антитела («Сигма Алдрич») для химерного антитела. Всасываемость определялась на уровне 450 нм (Multiskan EX; «Термо Электрон Корпорейшн»).
Пример 2.2. Поверхностный плазмонный резонанс
Анализ поверхностного плазмонного резонанса был проведен на инструменте BIAcore Т100 («Бьякор»; «ДжиИ Хелскер»). Рекомбинантный человеческий FGFR1 антиген РА-269#37 или рекомбинантный человеческий FGFR1 («Сино Биолоджикалс», ссылка №10616-Н08Н) были лишены подвижности с помощью сенсорного чипа СМ5 (серия S, «Бьякор»; «ДжиИ Хелскер») в 10 ммоль/л ацетата натрия рН 5. Различные варианты антител были растворены в буфере HBS-P (10 ммоль/л HEPES, рН 7,4, 0,15 моль/л NaCl и 0,05% сурфактанта Р20) и проведены через сенсорный чип (25 мкл/мин). Сенсорная поверхность была промыта буфером HBS-P, а затем регенерирована с применением 10 ммоль/л глицина-HCl (рН 2). Различные концентрации антител были протестированы (0, 1, 2, 4, 8, 16, 32, 24 и 32 нМ). Были определены различные циклические кинетические свойства, и полученные результаты были проанализированы с применением модели 1:1 (Langmuir) с учетом константы скорости ассоциации (Кon), константы скорости диссоциации (Коff) и константы диссоциации (Kd) («Бьякор»; «ДжиИ Хелскер»).
Пример 2.3. Анализ пролиферации
Для оценки влияния нового гуманизированного анти-FGFR1 антитела (OM-RCA-01) на вызываемые FGF сигналы, человеческие FGFR1-экспрессирующие клетки почечной карциномы Caki-1 (компания «Чарльз Ривер») были помещены в 96-луночный микропланшет (Costar white, плоское дно №3917) в концентрации 90 мкл/лунка и инкубированы (0,5% ЭБС) с OM-RCA-01 в концентрации 100, 10 и 1 мкг/мл. Контрольные лунки были оставлены в необработанном состоянии. Через три часа был добавлен основной FGF в концентрации 50 нг/мл. Дополнительные контрольные лунки были обработаны OM-RCA-01 без FGF-стимуляции. Угнетение роста клеток было определено с использованием анализа Cell Titer-Glo® компании «Промега».
Пример 2.4. Ксенографтные модели
Самкам голой мыши Чарльз Ривер (в возрасте 6-12 недель) были подкожно введены фрагменты опухоли Caki-1 объемом 1 мм3. Мыши с выявленными опухолями (средний размер 80-120 мг) были случайным образом распределены по трем группам, принимавшим плацебо, неспецифический IgG (1 или 10 мг/кг) или OM-RCA-01 (1 или 10 мг/кг) по 10 животных в каждой группе. Размеры опухоли измерялись два раза в неделю с помощью штангенциркуля. Животные наблюдались ежедневно на наличие признаков токсичности и были гуманным образом убиты, при этом считалось, что заболевание прогрессировало, если размеры опухоли достигали ≥2000 мм3. Конечной целью было выявление существенных различий в росте опухоли. Различия считались статистически значимыми при Ρ<0,05.
Пример 2.5. Свойства химерных и гуманизированных антител против FGFR1
Варианты гуманизированных и химерных генов были клонированы для получения двух различных экспрессионных векторов млекопитающих (pHHU_HuIgG1 и pHHU_Huk), содержащих человеческий ген постоянной каппа-цепи IGKC*01 и человеческий ген постоянной IgG1 тяжелой цепи: IGHG1*03 и трансфицированы в клетки HEK-FS. ДНК-коды для всей легкой и тяжелой цепи каждого варианта были проверены с помощью дидезоксинуклеотидного секвенирования.
Шесть вариантов гуманизированного антитела и контрольное химерное антитело были очищены от культуральной среды с использованием хроматографии на G-сефарозе. Чистота и целостность определялись с помощью метода ДСН-ПААГ в восстановительных и невосстановительных условиях. В невосстановительных условиях была обнаружена крупная структура массой примерно 150 «Да, соответствующая нетронутому антителу. В восстановительных условиях все антитела образовывали две большие структуры с молекулярной массой примерно 50 кДа (тяжелые цепи) и 25 кДа (легкие цепи).
Связывающие свойства кандидатов на получение гуманизированного антитела были оценены качественно и количественно с применением иммуноферментного анализа и поверхностного плазмонного резонанса соответственно.
Химерное антитело (mVH2/mVL2) и варианты антител VH3/VL5 (OM-RCA-01) и VH4/VL5 (OM-RCA-02) могли связываться с рекомбинантным FGFR1-антигеном РА-269#37, обездвиженным на поверхности планшета во время проведения иммуноферментного анализа. Аналогичные результаты были получены при использовании коммерчески доступного рекомбинантного FGFR1-антигена («Сино Биолоджикал, ссылка №10616-Н03Н) для получения антител с помощью иммуноферментного анализа.
С целью количественного измерения взаимодействия химерного антитела и вариантов гуманизированного антитела с рекомбинантным FGFR1-антигеном, были определены константа диссоциации (Кd) и константа ассоциации (Ка). Связывающие способности mVH2/mVL2, VH3/VL5 (OM-RCA-01) и VH4/VL5 (OM-RCA-02) находились в пределах низкого наномолярного диапазона с показателями Kd на уровне 1,95 нМ, 1,59 нМ и 1,52 нМ соответственно. Два гуманизированных варианта и химерное контрольное антитело показали значения Kd, аналогичные таким значениям для родительского мышиного антитела, что свидетельствовало о том, что процесс гуманизации не оказывал влияния на связывающую способность родительского антитела.
Пример 2.6. OM-RCA-01 замедляет пролиферацию клеточной линии почечно-клеточной карциномы (ПКК) и фосфорилирование FGFR1
OM-RCA-01 был оценен на наличие антипролиферативного действия на человеческие клетки почечно-клеточной карциномы с FGFR1-экспрессией (Caki-1) в модели с наличием вызванных FGF сигналов. Основной FGF увеличивал пролиферацию клеток почечно-клеточной карциномы Caki-1 (Р=0,011). Клетки были обработаны с применением повышенных концентраций антитела OM-RCA-01 в диапазоне от 1 до 100 мкг/мл. Антитело значительно замедляло вызванную FGF пролиферацию клеток по сравнению с контрольным материалом (Р=0,02). Не было выявлено существенного влияния антитела на пролиферацию клеток без предыдущей FGF-стимуляции (Р=0,1). Более того, пролиферации клеток не происходило без стимуляции FGF или лечения. В связи с этим было сделано заключение, что пролиферация клеток ПКК с экспрессией FGFR1 требует экспрессии FGFR1, а также стимуляции FGF. Кроме того, полученные данные подтверждают, что активация FGF оказывает влияние на развитие ПКК.
Не было выявлено различий между разными дозировками OM-RCA-01 (Р=0,8, 0,6 для 10 и 100 мкг/мл по сравнению с 1 мкг/мл). Эти данные четко показывают, что низкая дозировка высокоизбирательного антитела достаточна для блокады FGFR1 в FGFR-зависимой системе.
Иммуноферментный анализ использовался для наблюдения за концентрацией фосфо-FGFR1 в клетках рака почек Caki-1 после инкубации с применением OM-RCA-01. OM-RCA-01 угнетал активность фосфо-FGFR1 при использовании концентрации 1-50 нмоль/л.
Пример 2.7. Эффективность в ксенографтных моделях человеческих опухолей
Противоопухолевое действие OM-RCA-01 было изучено в FGFR1-зависимых ксенографтных моделях ПКК. С этой целью мы использовали клетки Caki-1 с высоким уровнем экспрессии FGFR1. Моноклональное антитело OM-RCA-01 вводилось внутрибрюшинно два раза в неделю в группе 3 (1 мг/кг) и группе 4 (10 т/кг). Не наблюдалось никаких признаков потери средней массы тела или клинических проявлений токсичности во время исследования. В группах 3 и 4 лечение с применением 1 и 10 мг/кг OM-RCA-01 привело к наличию среднего объема опухоли на уровне 758,3 мм3 и 763,8 мм3 на 13 день соответственно. Этот объем был значительно меньше по сравнению с группой, принимавшей плацебо (963,9 мм3; Р=0,006, Р=0,021) (группа 1), и группой, принимавшей неспецифический IgG (1017 мм3; Р=0,003, Р=0,01) (группа 2). К 21 дню у 6 (60%) и 5 (50%) наблюдалось прогрессирование заболевания до увеличения объемов опухоли до 2000 мм3 в группах, принимавших плацебо и IgG. Опухоли у трех (30%) мышей в группе 3 и двух (20%) мышей в группе 4 увеличились до 2000 мм3. Все опухоли в группах 3 и 4 достигли целевого объема к 34 дню по сравнению с группой, принимавшей плацебо (24 день), и IgG (23 день), что соответствовало 90 и 92-процентным показателям замедления роста опухоли.
Пример 3. Исследования противоопухолевой и ангиогенной активности антитела OM-RCA-01 на моделях почечно-клеточного рака (ПКР).
В исследовании in vitro в среде bFGF без добавления OM-RCA-01 отмечена пролиферация клеток ПКР (Р=0.011). Антитело OM-RCA-01 полностью нивелировало эффекты стимуляции клеток.
In vivo, в группах мышей, которые не получали лечение или получали неспецифический иммуноглобулин, отмечен агрессивный рост опухоли до достижения объема 2000 мм3, после чего животные были подвергнуты эвтаназии. Моноклональное антитело OM-RCA-01 достоверно подавляло рост опухоли (таблица 2). Различий в эффективности доз 1 мг/кг и 10 мг/кг не выявлено (Р=0,917), что, по-видимому, свидетельствует о высокой ингибирующей активности антитела даже в малых дозах.
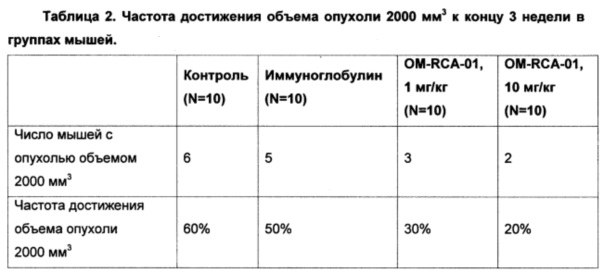
Все отличия между OM-RCA-01 (1 мг/кг), OM-RCA-01 (10 мг/кг) и группами контроля Р<0,05.
В эксперименте также оценена ранняя противоопухолевая активность OM-RCA-01. При сравнении объема опухоли уже на 13-й день от начала эксперимента были получены существенные достоверные отличия между группой основного контроля и лечебными группами OM-RCA-01 1 мг/кг (Р=0,006) и OM-RCA-01 10 мг/кг (Р=0,021). При этом средний объем опухоли в группе контроля, в которой лечение не проводилось, составил 963,9 мм3, а в группах с антителом OM-RCA-01 был 758,3 мм3 и 763,8 мм3 (для 1 мг/кг и 10 мг/кг, соответственно).
В течение всего периода лечения токсичности антитела не отмечено.
Проведено экспериментальное исследование антиангиогенной активности антитела OM-RCA-01, блокирующего активность рецептора FGFR-1, на модели имплантата Матригеля in vivo. В качестве образца сравнения использовали Бевацизумаб - гуманизированное моноклональное антитело против VEGF.
Установлено, что при трехкратном введении в дозе 10 мг/кг OM-RCA-01 статистически значимо блокирует ангиогенез, стимулированный bFGF, но не VEGF. Бевацизумаб в том же режиме применения был эффективен против VEGF-стимулированного ангиогенеза, но не при использовании bFGF.
В исследованиях in vitro и in vivo доказано, что OM-RCA-01 является моноклональным антителом с выраженной терапевтической активностью в отношении почечно-клеточного рака. Противоопухолевая эффективность антитела отмечается уже на 13-й день лечения.
Пример 4. Исследования противоопухолевой и ангиогенной активности антитела OM-RCA-01 на моделях различных видов опухолей
В работе были использованы следующие клеточные линии: А549 (рак легкого, АТСС #CCL-185), HS578T (рак молочной железы, АТСС # НТВ-126), T47D (рак молочной железы, АТСС #НТВ-1336), собственная линия метастатической меланомы кожи Mel Коr (патент РФ №2287578) и SVEC-4-10 (эндотелиальные клетки, АТСС #CRL-2181).
Клетки культивировали в среде RPMI-1640 (ПАНЭКО) (А549, HS578T, T47D, Mel-Kor) или DMEM (ПАНЭКО) (SVEC-4-10), содержащей 10% эмбриональной сыворотки крупного рогатого скота (FCS, HyClone), 2mM глутамина (ПАНЭКО), антибиотики (100 IU/mL пенициллина и 100 mg/ml стрептомицина (все ПАНЭКО)) при 37°С, 5% СO2.
Для проведения экспериментов использовали клетки при 70-80% монослое.
Оценка цитотоксичности антитела
Цитотоксичность оценивали в соответствии с ГОСТ Ρ ИСО 10993-5-2009.
Клетки (5-10×103) рассаживали в 96-луночные планшеты (Costar, США) в полной среде. На следующей день в лунки вносили различные концентрации исследуемых образцов, приготовленные путем их разбавления культуральной средой, или соответствующий растворитель (контроль). Объем вносимых веществ не превышал 5% объема среды в лунках. Каждую концентрацию исследуемых образцов изучали в триплетах. Клетки инкубировали с образцами в течение 72 часов. По окончании инкубации в лунки вносили 20 мкл тетразолиевой соли МТТ на 4 часа. О жизнеспособности клеток судили по цветной реакции, развивающейся при восстановлении тетразолия в формазан дегидрогеназами митохондрий. Оптическую плотность оценивали на спектрофотометре при длине волны возбуждения 540 нм. Показатели оптической плотности в лунках с каждой концентрацией испытуемых препаратов усредняли и вычисляли процент выживших клеток при той или иной концентрации исследуемого препарата.
Процент живых клеток вычисляли по формуле:
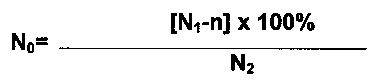
N0 - процент живых клеток;
N1 - средняя оптическая плотность лунок, содержащих клетки и тестируемое вещество;
N2 - средняя оптическая плотность контрольных лунок, содержащих только клетки;
n - оптическая плотность лунок, содержащих только тестируемое вещество.
Для каждого препарата строили график зависимости «доза-эффект» и определяли ИК50.
Концентрацию образцов, начиная с которой процент выживших клеток становился меньше 50% (IС50), вычисляли в программе GraphPad Prizm 5.
Эксперименты повторяли не менее 3-х раз по три повтора в опыте.
Антипролиферационный тест
Клетки высаживали в низкой плотности (30 т клеток/мл) в триплетах на 96-луночный планшет в среде, содержащей 0,1-0,5% сыворотки FCS. На следующий день в лунки добавляли тестируемое вещество в необходимых концентрациях, а через 6 часов - фактор роста фибробластов (100 нг/мл bFGF (BD Bioscience)). Среду, антибиотики и препараты меняли раз в 3 дня. Рост клеток определяли модифицированным «митогенным методом по Crystal Violet» на 7-е сутки после начала опыта. Клетки промывали PBS, фиксировали 1% параформальдегидом на PBS и окрашивали 0,5% раствором Crystal Violet (Sigma Chemical Co) на этаноле. Краситель растворяли в этаноле и измеряли на спектрофотометре при 540-560 нм.
Кривую ингибирования пролиферативной активности клеток строили по зависимости процента количества клеток (ось ординат) от концентрации исследуемого вещества в лунке планшета (ось абсцисс). Концентрацию образцов, начиная с которой процент выживших клеток становился меньше 50% (IС50) вычисляли в программе GraphPad Prizm 5.
Эксперименты повторяют не менее 3-х раз по три повтора в опыте.
Метод оценки блокирования миграционной способности клеток по методу «заживления раны»
Клетки SVEC-4-10 (3×105 клеток/мл) вносили в лунки 24-луночного планшета в среде полной DMEM и инкубировали до образования монослоя. Затем монослой нарушали путем соскабливания части клеток. Клетки инкубировали в среде DMEM, содержащей 10% FCS, 2 мМ глутамина и нецитотоксические дозы образцов, в течение 24 часов. В качестве отрицательного контроля использовали клетки в бессывороточной среде DMEM. Результаты оценивали как процент мигрирующих клеток в опыте по отношению к контролю.
Метод оценки блокирования формирования сосудисто-подобных структур (СПС) 24-луночную плашку покрывали Матригелем (100 мкл/лунка, плотность 8.4 мг/мл (BD Bioscience)) и инкубировали 20-30 минут при комнатной температуре до его полной полимеризации. Клетки SVEC-4-10 (5×105 клеток/мл) инкубировали в среде DMEM с добавлением нецитотоксических доз антитела в течение 30 минут при 37°С. Затем клетки переносили в лунки, покрытые Матригелем, и инкубировали в СO2-инкубаторе 4-6 часов. В качестве положительного контроля использовали клетки, инкубировавшиеся в среде DMEM без добавления антитела.
Проведено исследование цитотоксического действия антитела OM-RCA-01 на культурах опухолевых и эндотелиальных клеток. По результатам МТТ теста показано, что антитело OM-RCA-01 не является цитотоксическим и не вызывает гибели опухолевых клеток в изученных концентрациях (от 100 мкг/мл до 1,5 мкг/мл) (таблица 3).
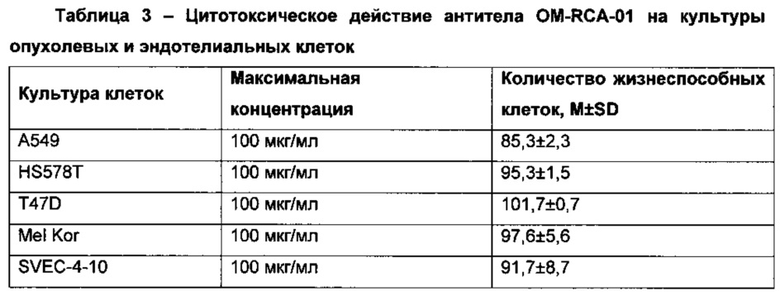
Противоопухолевая активность антитела OM-RCA-01
Проведено исследование антипролиферативной активности антитела OM-RCA-01 на опухолевых клеточных линиях, экспрессирующих FGFR1: А549 (рак легкого, АТСС #CCL-185), HS578T (рак молочной железы, АТСС # НТВ-126) и T47D (рак молочной железы, АТСС #НТВ-1336). Также была использована собственная линия метастатической меланомы кожи Mel Коr (патент RU 2287578) с неизвестной экспрессией FGFR1.
Количество клеток определяли на 6-е сутки после инкубации с исследуемым образцом в присутствии bFGF. Показано, что антитело OM-RCA-01 дозозависимо блокирует пролиферацию опухолевых клеток, экспрессирующих FGFR1 (таблица 4). Исследуемое антитело не блокировало пролиферативную активность клеточной линии метастатической меланомы Mel Коr.

Антиангиогенная активность антитела OM-RCA-01
Антиангиогенная активность антитела OM-RCA-01 изучена на клеточной линии эндотелиальных клеток мыши SVEC-4-10 (эндотелиальные клетки, АТСС #CRL-2181).
В таблице 5 приведены обобщенные результаты блокирования ангиогенной активности клеток в трех различных тестах: на ингибирование пролиферативной и миграционной активности, блокирования сосудисто-подобных структур (СПС).
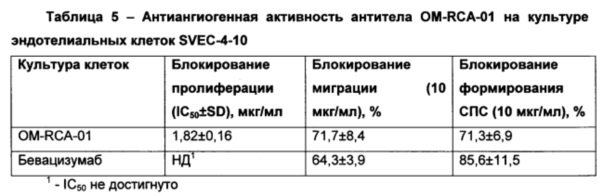
Показано, что антитело OM-RCA-01 блокирует ангиогенную активность в концентрациях, сравнимых с Бевацизумабом.
Миграционная активность была изучена в тесте «заживления раны». В качестве отрицательного контроля (точка максимального ингибирования миграции, «0» точка) использовали 0,1% FCS, в качестве положительного (точка максимальной миграционной активности, 100%) - 10% FCS. Исследованные антитела (100, 50 и 10 мкг/мл) добавляли к клеткам SVEC-4-10 в среде DMEM, содержащей 10% FCS. Способность антител блокировать миграцию клеток оценивали через 24 часа после добавления исследуемых образцов. Показано, что антитела OM-RCA-01 и Бевацизумаб блокируют миграционную активность эндотелиальных клеток в сравнимых концентрациях.
При инкубации на Матригеле эндотелиальные клетки формируют первичную сосудистую сеть - сосудисто-подобные структуры. При добавлении исследованных антител OM-RCA-01 и Бевацизумаб (10 мкг/мл) наблюдалось практически полное ингибирование формирования данных структур.
Проведено экспериментальное исследование противоопухолевой и антиангиогенной активности антитела OM-RCA-01, блокирующего активность рецептора FGFR1, на культурах опухолевых и эндотелиальных клеток in vitro. В качестве образца сравнения использовали Бевацизумаб - гуманизированное моноклональное антитело против VEGF.
Установлено, что OM-RCA-01 дозозависимо блокирует пролиферативную активность культур опухолевых и эндотелиальных клеток in vitro. Также антитело OM-RCA-01 блокирует миграцию эндотелиальных клеток и формирование ими сосудисто-подобных структур. Антиангиогенный профиль активности антитела OM-RCA-01 соответствует профилю Бевацизумаба.
Полученные данные свидетельствуют, что OM-RCA-01 является перспективным противоопухолевым и антиангиогенным веществом. Полученные результаты позволяют предположить, что антитело OM-RCA-01 может блокировать рост опухолей по двум независимым механизмам: блокируя пролиферацию опухолевых клеток и ингибируя ангиогенез в опухолевой ткани.
Пример 5. Получение стабильных клеточных линий, продуцирующих антитело против FGFR1
5.1 Получение кДНК, кодирующей антитело против FGFR1
Нуклеотидные последовательности кДНК генов, кодирующих тяжелую и легкую цепи антитела OM-RCA-01 (ОМ-1-НС и OM-1-LC, соответственно), были получены путем химико-ферментативного синтеза в компании GenScript (США). Ген ОМ-1-НС содержал 1418 п. о., ген OM-1-LC - 735 п. о. После завершения синтеза последовательности были проверены секвенированием в той же компании.
Рекомбинантная плазмидная ДНК pCBp2-OM1s содержит следующие последовательности: две копии промоторно-энхансерного участка предранних генов цитомегаловируса человека, две копии химерного интрона, две копии сигнала полиаденилирования поздних генов SV40, синтетические гены, кодирующие тяжелую и легкую цепи антитела OM-RCA-01, минимальный сайт инициации репликации SV40. В качестве селективных маркеров используются: ген бета-лактамазы (AmpR), обеспечивающий резистентность к ампициллину в клетках e.coli, и ген деаминазы бластицидина S (bsr), обеспечивающий резистентность к блистицидину у эукариот.
Плазмида pCBp2-OM1s характеризуется следующими параметрами:
- состоит из 8028 п. о.,
- имеет молекулярную массу 4,95 МДа,
- кодирует тяжелую и легкую цепи моноклонального антитела OM-RCA-01,
- обеспечивает устойчивость бактериальных клеток, трансформированных данной плазмидой, к ампицилину и клеток млекопитающих, трансфецированных указанной плазмидой, к бластицидину,
- содержит уникальные участки узнавания следующих эндонуклеаз рестрикции: NheI (1125 п. о.), MluI (1854 п. о.), XbaI (3288 п. о.), NotI (4698 п. о.).
Создание плазмиды pCBp2-OM1s выполнялось в несколько стадий клонирования.
На первом этапе использовалась коммерческая плазмида pCI-neo (Promega, США), из которой была получена плазмида рСВ путем введения второй экспрессионной кассеты в 3'-фланкирующий участок имеющейся экспрессионной кассеты. Обе экспрессионные кассеты имели в своем составе промоторно-энхансерные участки предранних генов цитомегаловируса человека, химерные интроны, сигналы полиаденилирования поздних генов SV40, полученные из плазмиды pCI-neo. При этом первая кассета содержала участки узнавания рестриктаз NheI и Mlul, вторая кассета - рестриктаз XbaI и NotI.
На втором этапе клонирования ген, кодирующий селективный маркер резистентности к антибиотику неомицину (Neo), был заменен на ген деаминазы бластицидина S (bsr), обуславливающий резистентность к антибиотику бластицидину. С этой целью в компании GenScript (США) была синтезирована оптимизированная нуклеотидная последовательность, кодирующая деаминазу бластицидина S, содержащая участки узнавания рестриктаз Avrll и BstBI. Синтезированный ген был вставлен в плазмиду рСВ по сайтам указанных рестриктаз вместо гена Neo для получения плазмиды рСВр2.
Синтезированные гены ОМ-1-НС и OM-1-LC, кодирующие тяжелую и легкую цепи антитела, соответственно, содержали на своих концах участки узнавания рестриктаз Nhel и MluI (для ОМ-1-НС) и XbaI и NotI (для OM-1-LC). Ген ОМ-1-НС был встроен в плазмиду рСВр2 по сайтам NheI и MluI для получения плазмиды рСВр2-НС, ген OM-1-LC - также в плазмиду рСВр2 по сайтам XbaI и NotI для получения плазмиды pCBp2-LC.
Плазмиды рСВр2-НС и pCBp2-LC были обработаны рестриктазами MluI и NotI и лигированы между собой для получения результирующей плазмиды pCBp2-OM1s. Последовательность гена ОМ-1-НС и OM-1-LC в составе данной плазмиды проверяли секвенированием с использованием следующих праймеров:
Праймеры для секвенирования гена OM1-LC:
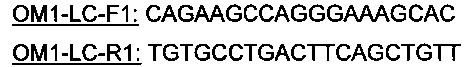
Праймеры для секвенирования гена ОМ1-НС:
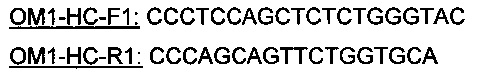
5.2 Трансфекция клеток CHO-ks1 pCBp2-OM1s плазмидой
Клетки трансфецированы с использованием прибора Electroporator («БиТиЭкс Гарвард Аппаратус», Холлистон, Массачусетс). 20 миллионов клеток перенесены в 50 мл пробирку фирмы «Фалкон» и процентрифугированы при 1000 оборотов в минуту в течение 5 минут. Среда убрана и клетки перерастворены в 100-800 мкл раствора для электропорации («БиТиЭкспресс», каталожный номер 45-8050, серия №ВТ1201626), смешанного с векторной ДНК. Клетки переданы в электропорационную кювету и применен импульс. Сразу же после импульса клетки были перенесены в колбу для клеточных культур Т150, содержащую 27 мл питательной среды. Трансфекция была произведена еще два раза (всего 60 млн. клеток) и клетки были собраны в одну колбу Т150. Все процедуры проводились в стерильных условиях. Клетки в колбе Т150 инкубировались в течение 2-х дней.
Селекция Бластицидином и генерация стабильного пула.
Плотность клеток: 2,26×106 клеток/мл
Жизнеспособность клеток: 85,2%
Средний диаметр клеток: 14,2 мкм
Общее количество живых клеток = 67 миллионов
Этот результат показывает, что клетки сохраняют высокую жизнеспособность после трансфекции.
- Клетки вычищены из колбы Т150 и перенесены в 50 мл пробирку фирмы «Фалкон».
- Клетки процентрифугированы и среда отделена от клеток.
- Клетки перерастворены в 30 мл среды CDM4CHO, содержащей 400 мкг/мл G-418 и 10 мкг/мл бластицидина (Инвитроген, каталожный номер А11139-03, серия №1145016).
- Клетки перенесены в 3 колбы CultiFlask (10 мл клеточной суспензии в каждой) и смешаны с 20 мл (на каждую колбу) дополнительной среды.
- Клетки инкубировались в СO2-инкубаторе на встряхивателе (улучшенный цифровой встряхиватель «ВиДабл-юА») при 179 об/мин.
Затем была произведена сортировка клеток стабильного пула ОМ1 с помощью MoFLo FACS.
Клонирование одиночных клеток в 96-луночных планшетах и иммуноферментный анализ
- Подпитка клеток ОМ1-7 (50 лунок) 100 мкл среды:
- Смесь 1:1 ExCellCHO и PowerCHO-2 с 400 мкг/мл G-418 и 10 мкг/мл бластицидина
- Это даст 50% от исходной концентрации антибиотиков.
- По результатам ИФА были отобраны 24 наиболее выраженных клона, они были размножены в 24-луночных планшетах в 1 мл среды на лунку.
- Из 24 предварительно отобранных клонов три показали наибольшую стабильность и продуктивность.
Клеточная линия СНО-ОМ8-21, полученная вышеописанным способом, имеет высокую продуктивность, равную 0,8 г/л антитела OM-RCA-01, и высокую аффинность антитела к рецептору FGFR1 равную 9,27×10-9 M.
Клеточная линия СНО-ОМ8-21, регистрационный номер VKPM Н-134, депонирована в Интернациональном депозитарии Российской Национальной Коллекции Промышленных Микроорганизмов ФГУП ГосНИИгенетика от 06 ноября 2012 года.
Клеточная линия СНО-ОМ8-21 произошла от стабильной анеуплоидной клеточной линии CHO-S (Invitrogen, кат. №R800-07), выделенной в виде отдельного субклона из клеточной линии СНО К1. Ткань - яичники китайского хомяка (СНО), эпителиоподобная.
Морфология клеточной линии.
В фазовый контраст и световой микроскоп культура представлена суспензией круглых клеток с овальным ядром, содержащих небольшие эндосомы. Время удвоения 20-22 часа.
Культуральные свойства, маркерные признаки.
Клетки адаптированы к росту в среде Power СНО 2CD без добавления сыворотки, белков, а также в химических средах без добавления компонентов животного или человеческого происхождения. Кроме того, клетки хорошо растут на традиционных средах с добавлением сыворотки.
Рекомендуемые условия для замораживания.
Замораживать клетки при плотности ≥2,0×106 живых клеток/мл. Центрифугировать клеточную суспензию, удалить супернатант и ресуспендировать клеточный осадок в культуральной среде с 7,5% ДМСО. Заморозить до -80°С с контролируемой скоростью 1°С/мин. Хранить клетки в криопробирках в жидком азоте.
Рекомендуемые условия для культивирования.
Клетки культивируют во флаконах 0,1-1,0 л (объем среды - 20-30% общего объема) на орбитальном шейкере при 100-120 об/мин в увлажненной атмосфере при 5% СO2. Пассирование клеток производят каждые 2-3 дня путем разбавления суспензии клеток свежей средой. Плотность посева 0,2-0,3×106 клеток/мл, максимальная плотность 3,0×106 клеток/мл. При необходимости можно проводить центрифугирование при 200×g.
Производимый продукт: моноклональное антитело для лечения рака.
Чувствительность к вирусам: везикулярный стоматит, арбовирусы.
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К РЕЦЕПТОРУ 2 ФАКТОРА РОСТА ФИБРОБЛАСТОВ | 2009 |
|
RU2546254C9 |
| БИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА | 2011 |
|
RU2573588C2 |
| ГУМАНИЗИРОВАННЫЕ АНТИТЕЛА К CXCR4 ДЛЯ ЛЕЧЕНИЯ РАКА | 2011 |
|
RU2595394C2 |
| МОЛЕКУЛЫ БИСПЕЦИФИЧЕСКИХ АНТИТЕЛ И Т-КЛЕТКИ, ТРАНСФЕЦИРОВАННЫЕ АНТИГЕНОМ, И ИХ ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2013 |
|
RU2693264C2 |
| АНТИТЕЛА, СПЕЦИФИЧНЫЕ К КЛАУДИНУ 6 (CLDN6) | 2010 |
|
RU2675997C2 |
| Антитело против PD-1 и его применение | 2017 |
|
RU2739610C1 |
| ГУМАНИЗИРОВАННЫЕ АНТИ-ТФР-БЕТА-АНТИТЕЛА | 2005 |
|
RU2386638C2 |
| ЛЕЧЕНИЕ РАКА ПРИ ПОМОЩИ НАПРАВЛЕННЫХ НА МИШЕНЬ АНТИТЕЛ IN VIVO | 2011 |
|
RU2642305C2 |
| СОЧЕТАННАЯ ТЕРАПИЯ АФУКОЗИЛИРОВАННЫМ АНТИТЕЛОМ К CD20 С АНТИТЕЛОМ К VEGF | 2011 |
|
RU2615459C2 |
| ANTI-CXCR4 АНТИТЕЛА И КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВО | 2014 |
|
RU2675516C2 |







Группа изобретений относится к области биотехнологии, а именно биохимии и медицине, и касается антител для лечения онкологических заболеваний. Антитела по изобретению специфически связывают и блокируют рецептор 1 типа фактора роста фибробластов (FGFR1) и характеризуются аминокислотными последовательностями H-CDR1, H-CDR2, H-CDR3, L-CDR1, L-CDR2 и L-CDR3. Предложены фармацевтическая композиция для лечения онкологических заболеваний, содержащая антитела по изобретению, и способ лечения онкологических заболеваний, включающий введение пациенту антител по изобретению. Также предложены способ получения антител, кодирующие их нуклеиновые кислоты и линии клеток для получения антител. Изобретения позволяют с высокой эффективностью и специфичностью подавлять пролиферацию опухолевых клеток и ингибировать опухолевый ангиогенез путем блокирования патологического пути FGF/FGFR1, что в свою очередь позволяет эффективно лечить онкологические заболевания. 7 н. и 15 з.п. ф-лы, 5 табл., 5 пр.
1. Антитело или его функциональный фрагмент, специфически связывающее рецептор 1 типа фактора роста фибробластов, включающее тяжелую цепь, содержащую
H-CDR1 с последовательностью SEQ ID NO:1,
H-CDR2 с последовательностью SEQ ID NO:2,
и H-CDR3 с последовательностью SEQ ID NO:3,
и легкую цепь, содержащую
L-CDR1 с последовательностью SEQ ID NO:4,
L-CDR2 с последовательностью SEQ ID NO:5,
и L-CDR3 с последовательностью SEQ ID NO:6.
2. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что указанное антитело или его функциональный фрагмент специфически связывается с доменами II и III с рецептора 1 типа фактора роста фибробластов.
3. Антитело или его функциональный фрагмент по п. 1, связывающее рецептор 1 типа фактора роста фибробластов с константой диссоциации Kd 2×10-9 М или менее.
4. Антитело или его функциональный фрагмент по п. 1, связывающее рецептор 1 типа фактора роста фибробластов с константой диссоциации Kd 1.59×10-9 М.
5. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что тяжелая цепь содержит вариабельный домен с последовательностью SEQ ID NO:7.
6. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что легкая цепь содержит вариабельный домен с последовательностью SEQ ID NO:8.
7. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что тяжелая цепь имеет последовательность SEQ ID NO:9.
8. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что легкая цепь имеет последовательность SEQ ID NO:10.
9. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что указанное антитело является моноклональным.
10. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что указанное антитело является химерным, гуманизированным или человеческим.
11. Антитело или его функциональный фрагмент по п. 1, характеризующееся тем, что указанное антитело относится к изотипу IgA, IgD, IgE, IgG1, IgG2, IgG3, IgG4 или IgM.
12. Фармацевтическая композиция для лечения онкологического заболевания, содержащая антитело или его функциональный фрагмент по любому из пп. 1-11 в эффективном количестве и фармацевтически приемлемый носитель.
13. Фармацевтическая композиция по п. 12, характеризующаяся тем, что онкологическим заболеванием является почечно-клеточный рак.
14. Применение антитела или его функционального фрагмента по любому из пп. 1-11 для лечения онкологического заболевания.
15. Применение антитела или его функционального фрагмента по п. 14, характеризующееся тем, что онкологическим заболеванием является почечно-клеточный рак.
16. Способ лечения онкологического заболевания, включающий введение пациенту эффективного количества антитела или его функционального фрагмента по любому из пп. 1-11 или фармацевтической композиции по п. 12 или 13.
17. Нуклеиновая кислота, кодирующая антитело или его функциональный фрагмент по любому из пп. 1-11.
18. Нуклеиновая кислота по п. 17, характеризующаяся тем, что включает последовательность SEQ ID NO:11.
19. Нуклеиновая кислота по п. 17, характеризующаяся тем, что включает последовательность SEQ ID NO:12.
20. Линия клеток яичника китайского хомячка, содержащая нуклеиновую кислоту по любому из пп. 17-18 для получения антитела или его функционального фрагмента по любому из пп. 1-11.
21. Линия клеток по п. 20, депонированная во Всероссийской коллекции промышленных микроорганизмов под регистрационным номером VKPM Н-134.
22. Способ получения антитела или его функционального фрагмента по любому из пп. 1-11, включающий культивирование линии клеток по п. 20 или 21 в питательной среде и выделение антитела или его функционального фрагмента из вышеуказанных клеток и/или вышеуказанной среды.
| US 20140086925 A1, 27.03.2014 | |||
| US 20070248605 A1, 25.10.2007 | |||
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К РЕЦЕПТОРУ 2 ФАКТОРА РОСТА ФИБРОБЛАСТОВ | 2009 |
|
RU2546254C9 |
| EP 2165715 A1, 24.03.2010 | |||
| ТИМОФЕЕВ И.В | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ФЕДЯНИН М.Ю., ХМЕЛЬКОВА Д.Н | |||
| и др | |||
| Рецепторы фактора роста фибробластов при злокачественных опухолях, ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ, 2014. | |||
Авторы
Даты
2017-12-13—Публикация
2015-09-28—Подача