Область техники, к которой относится изобретение
Изобретение касается способов и композиций для лечения ишемии или болезни или нарушения, вызывающего ишемию, включающие контактирование субъекта с цистеамином, производным цистеамина, цистамином или производным цистамина. В изобретении раскрыты также способы модулирования уровней адипонектина у субъекта, включающие контактирование субъекта с цистеамином, производным цистеамина, цистамином или производным цистамина.
Уровень техники
По подсчетам острый ишемический инсульт затрагивает ~2-2,5 из каждой тысячи человек, что влечет за собой приблизительно 4,5 миллиона смертей в год во всем мире и 9 миллионов пациентов, перенесших инсульт, при этом расходы в настоящее время превышают 50 биллионов $ только в США.
Раскрытие изобретения
Изобретение предоставляет способ лечения субъекта, страдающего от ишемического поражения или острого ишемического события, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли в количестве, эффективном для уменьшения ишемического повреждения. В одном варианте осуществления ишемическое поражение является результатом тромботического нарушения. В дополнительном варианте осуществления тромботическое нарушение является серповидноклеточной анемией, тромбозом глубоких вен, легочной эмболией, сердечной эмболией, состоянием гиперкоагуляции, тромбофилией, фактором V Ляйдена, дефицитом антитромбина III, дефицитом белка С, дефицитом белка S, мутацией гена протромбина (G20210A), гипергомоцистеинемией, синдромом антифосфолипидных антител (APS), синдромом антикардиолипиновых антител (ACLA) или синдромом волчаночного антикоагулянта (LA). В любом из упомянутых выше вариантов осуществления количество цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли является эффективным для уменьшения риска ишемического поражения, полученного в результате тромбоза.
Изобретение также предоставляет способ лечения субъекта с повышенным риском тромбообразования и возникающего в связи с этим ишемического поражения, включающий введение субъекту количества цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, эффективного для уменьшения риска ишемического поражения, полученного в результате тромбоза.
В любом из упомянутых выше вариантов субъект может иметь рак, миелопролиферативное заболевание, множественную миелому, мог перенести операцию или травму, может находиться в состоянии иммобилизации, принимать пероральный контрацептив, принимать талидомид или его родственные соединения необязательно в комбинации со стероидным гормоном, может иметь гепарин-индуцированную тромбоцитопению, может быть беременным, может иметь воспалительную болезнь кишечника, нефротический синдром, ночную пароксизмальную гемоглобинурию, синдром повышенной вязкости крови или макроглобулинемию Вальденстрема.
Изобретение также предоставляет способ лечения субъекта с повышенным риском тромбообразования, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли в количестве, эффективном для снижения риска ишемического поражения вследствие тромбоза. В одном варианте осуществления субъект имеет рак, миелопролиферативное заболевание, множественную миелому, перенес операцию, имел травму, находится в состоянии иммобилизации, принимает пероральное противозачаточное средство, субъекту вводят талидомид или его родственные соединения необязательно в комбинации со стероидным гормоном, имеет гепарин-индуцированную тромбоцитопению, является беременным, имеет воспалительную болезнь кишечника, имеет нефротический синдром, имеет ночную пароксизмальную гемоглобинурию, имеет синдром повышенной вязкости крови или макроглобулинемию Вальденстрема.
В любом из упомянутых выше вариантов осуществления ишемическое поражение может быть результатом повреждения ткани, болезни или инсульта. В дополнительном варианте осуществления поражение является реперфузионным повреждением. В другом варианте осуществления реперфузионное повреждение является результатом хирургического вмешательства или трансплантации органа. В другом варианте осуществления болезнь является серповидноклеточной анемией.
В любом из упомянутых выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в пределах 72 часов после ишемического события. В дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в течение длительного времени после ишемического события. В любом из упомянутых выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в течение длительного времени субъекту с повышенным риском ишемического события.
Данный вариант предоставляет способ увеличения отношения уровней адипонектина с низким молекулярным весом (LMW) к уровням адипонектина со средним молекулярным весом (MMW) и/или высоким молекулярным весом (HMW) у субъекта, нуждающегося в этом, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, в количестве, эффективном для увеличения отношения уровней адипонектина с низким молекулярным весом по сравнению с исходным уровнем до контактирования субъекта с цистеамином, производным цистеамина, цистамином, производным цистамина или их фармацевтически приемлемой солью, при этом субъект не страдает от гиперхолестеринемии или диабета II типа.
Изобретение также предоставляет способ лечения субъекта, имеющего не отвечающие нормам или ненормальные отношения адипонектина с высоким молекулярным весом (HMW) к адипонектину со средним молекулярным весом (MMW), адипонектина с HMW к адипонектину с низким молекулярным весом (LMW) или MMW : LMW, включающий введение субъекту цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, в количестве, эффективном для улучшения соотношений адипонектина у субъекта по сравнению с субъектом, не получавшим цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль.
В одном варианте осуществления упомянутый выше субъект имеет фактор риска возникновения ишемии, выбранный из группы, состоящей из гипертонической болезни, употребления табака, болезни сонной или других артерий, заболевания периферических артерий, мерцательной аритмии, другого заболевания сердца, преходящего ишемического нарушения (TIA), заболеваний крови, высокого уровня холестерина в крови, гиподинамии, ожирения, избыточного употребления алкоголя, использования запрещенных наркотиков, предшествующего инсульта, серповидно-клеточной анемии и предшествующего сердечного приступа. В другом варианте осуществления субъект ранее перенес ишемическое событие. В любом из упомянутых выше вариантов осуществления способ включает введение цистеамина, производного цистеамина или его фармацевтически приемлемой соли. В дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина, или фармацевтически приемлемая соль любого из вышеупомянутого вводится в концентрации в пределах примерно от 0,5 до 20 мг/кг веса тела указанного субъекта. В еще одном варианте осуществления общая ежедневная доза цистеамина, производного цистеамина, цистамина, производного цистамина или фармацевтически приемлемой соли любого из вышеупомянутого составляет около 0,5-4,0 г/м2. В еще одном дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или фармацевтически приемлемая соль любого из вышеупомянутого вводится перорально. В одном варианте осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или их фармацевтически приемлемая соль является лекарственной формой с замедленным или контролируемым высвобождением. В любом из упомянутых выше вариантов осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или их фармацевтически приемлемая соль вводится внутрибрюшинно. В дополнительном варианте осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или их фармацевтически приемлемая соль вводится внутривенно или внутриартериально. В любом из упомянутых выше вариантов осуществления введение приводит к уменьшению ишемически-реперфузионного повреждения или воспаления в результате ишемического события. В другом варианте осуществления способ дополнительно включает введение одного или более дополнительных средств, пригодных для лечения ишемии. В дополнительном варианте осуществления одно или более дополнительных средств выбирают из группы, состоящей из реперфузионного средства, ловушки свободных радикалов и спиновой ловушки, нейропротекторного средства, антикоагулирующего средства, антитромбоцитарного средства, нимодипина и налоксона. В другом варианте осуществления способ дополнительно включает введение одного или более средств, пригодных для лечения тромботического нарушения: антикоагулирующего средства, гепарина, антагониста витамина К, производных 4-гидроксикумарина, варфарина, аценокумарола, дикумарола, этилбискумацетата, фенпрокумона, стрептокиназы, урокиназы, тканевого активатора плазминогена (tPA), альтеплазы (рекомбинантной tPA), ретеплазы, тенектеплазы и аргатробана. В другом варианте осуществления цистеамин, производное цистеамина, цистамин или производное цистамина или фармацевтически приемлемую соль любого из вышеперечисленного вводят менее чем четыре раза в день. В еще одном варианте осуществления цистеамин, производное цистеамина, цистамин или цистамин вводят два раза в день. В любом из перечисленных выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль вводят непрерывно в течение дней, недель или месяцев.
Изобретение предоставляет способ лечения ишемического события, включающий контактирование субъекта, страдающего от ишемического события, с эффективным количеством цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли, при этом субъект имеет улучшенный поведенческий результат по сравнению с субъектом, который не получал цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль. В одном варианте осуществления уровни адипонектина у субъекта увеличиваются после контактирования с цистеамином, производным цистеамина, цистамином, производным цистамина или их фармацевтически приемлемой солью. В другом варианте осуществления общая ежедневная доза цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли составляет около 0,5-4,0 г/м2. В еще одном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится внутрибрюшинно. В следующем варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится перорально. В следующем варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль представляет собой лекарственную форму с замедленным или контролируемым высвобождением, которая обеспечивает увеличенную доставку цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли в тонкий кишечник. В еще одном варианте осуществления лекарственная форма с замедленным или контролируемым высвобождением содержит энтеросолюбильное покрытие, которое высвобождает цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемую соль, когда цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль достигает тонкого кишечника или участка желудочно-кишечного тракта субъекта, в котором значение pH больше чем около pH 4,5. В одном варианте осуществления энтеросолюбильное покрытие является покрытием, выбранным из группы, состоящей из полимеризованного желатина, шеллака, сополимера метакриловой кислоты типа С NF, фталат бутирата целлюлозы, гидрофталата целлюлозы, фталата пропионата целлюлозы, поливинилацетата фталата (PVAP), ацетата фталата целлюлозы (CAP), ацетата тримеллитата целлюлозы (CAT), фталата гидроксипропил метилцеллюлозы, ацетата гидроксипропил метилцеллюлозы, сукцината диоксипропил метилцеллюлозы, карбоксиметилэтилцеллюлозы (CMEC), гидроксипропилметилцеллюлозы ацетата сукцината (HPMCAS) и полимеров и сополимеров акриловой кислоты, таких как метилакрилат, этилакрилат, метилметакрилат и/или этилметакрилат с сополимерами сложных эфиров акриловой и метакриловой кислоты. В еще одном варианте осуществления, когда цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится перорально, цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в составе композиции с биодоступным железом. В любом из вышеперечисленных вариантов осуществления введение приводит к уменьшению воспаления, наблюдающегося вследствие ишемического события.
Изобретение также предоставляет способ увеличения уровней адипонектина у субъекта, включающий контактирование субъекта с эффективным количеством цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли с целью увеличения уровней адипонектина по сравнению с исходным уровнем до контактирования субъекта с цистеамином, производным цистеамина, цистамином, производным цистамина или их фармацевтически приемлемой солью. В одном варианте осуществления общие уровни адипонектина повышаются. В другом варианте осуществления отношение адипонектина с низким молекулярным весом к адипонектину со средним и/или высоким молекулярным весом повышается. В еще одном варианте осуществления субъект страдает ожирением и имеет низкие уровни LMW-адипонектина по сравнению со здоровыми субъектами. В одном варианте осуществления субъект имеет диабет и имеет низкие уровни LMW-адипонектина по сравнению со здоровыми субъектами. В еще одном варианте осуществления субъект страдает от ишемических событий.
Изобретение также предоставляет применение цистеамина, производного цистеамина, цистамина, производного цистамина или их фармацевтически приемлемой соли для лечения ишемии, ишемического повреждения, острого ишемического события, тромбоза или ишемического повреждения в результате тромбоза. В одном варианте осуществления ишемия или ишемическое повреждение является результатом тромботического нарушения. В другом варианте осуществления тромботическое нарушение является серповидно-клеточной анемией, тромбозом глубоких вен, легочной эмболией, состоянием гиперкоагуляции, тромбофилией, фактором V Ляйдена, дефицитом антитромбина III, дефицитом белка C, дефицитом белка S, мутацией гена протромбина (G20210A), гипергомоцистеинемией, синдромом антифосфолипидных антител (APS), синдромом антикардиолипиновых антител (ACLA) или синдромом волчаночного антикоагулянта (LA). В еще одном варианте осуществления применяют цистеамин, производное цистеамина или их фармацевтически приемлемую соль. В еще одном варианте осуществления ишемия возникает в результате фактора риска, выбранного из группы, состоящей из гипертонической болезни, употребления табака, болезни сонной или других артерий, заболевания периферических артерий, мерцательной аритмии, другого заболевания сердца, преходящего ишемического нарушения (TIA), заболеваний крови, высокого уровня холестерина в крови, гиподинамии, ожирения, избыточного употребления алкоголя, использования запрещенных наркотиков, предшествующего инсульта, серповидно-клеточной анемии и предшествующего сердечного приступа. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль заключается в состав для внутрибрюшинного введения. В любом из вышеперечисленных вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится внутрисосудистым способом. В еще одном варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль заключается в состав для перорального введения. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль имеет энтеросоюлюбильоне покрытие. В любом из перечисленных выше вариантов осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится в течение длительного времени. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль вводится до, одновременно с или после ишемического события/кризиса. В другом варианте осуществления цистеамин, производное цистеамина, цистамин, производное цистамина или их фармацевтически приемлемая соль используется для увеличения уровней адипонектина у субъекта.
Детали одного или более вариантов осуществления раскрытия изложены в прилагаемых чертежах и описании ниже. Другие признаки, цели и преимущества станут очевидны на основе описания и чертежей, а также пунктов формулы изобретения.
Краткое описание чертежей
Фигура 1 показывает обработку эксплантатов жировой ткани цистеамином 90 мкМ в течение 45 мин, 90 мин и 24 часов. Значимое увеличение уровня общего адипонектина при обработке цистеамином 90 мкМ в течение 45 мин.: p=0.002; значимое различие уровня адипонектина HMW при обработке цистеамином 90 мкМ 45 мин.: p=0.04; значимое различие уровня адипонектина HMW при обработке цистеамином 90 мкМ 90 мин.: p=0.02.
Фигура 2A-C показывает (A) схематическое изображение и относительный сдвиг подвижности LMW, MMW и HMW адипонектина; (В) показывает сыворотку, полученную при бандажировании желудка (GB), инкубированную при комнатной температуре, 37°C, 37°C + 45 мкМ цистеамина в течение 1 часа и получение мультимеров адипонектина. Не наблюдалось значимого различия между комнатной температурой и 37°C для любого мультимера. Однако: HMW значимо уменьшается при обработке цистеамином: p=0.009; MMW значимо изменяется при обработке цистеамином; и LMW значимо увеличивается при обработке цистеамином: p=0.05. (C) Средние значения BMI, ALT и AST, измеренные в начальный момент, через 24 недели обработки EC-цистеамином и затем через 16 недель после отмены ЕС-цистеамина). Значения P обозначаются как незначимые (ns), *P<.05, **P<.01. Среднее значение BMI не различалось достоверно в любых временных точках. Показана стандартная ошибка среднего (SEM).
Фигура 3 показывает in vivo действие цистеамина на мультимеризацию адипонектина у субъектов с NAFLD. Одиннадцать субъектов с NAFLD перорально лечили enteric-coated цистеамином с энтеросолюбильным покрытием в течение 24 недель и затем осуществляли контроль без лечения в течение 24 недель. Сыворотку анализировали в начальный момент времени, через 24 недели на фоне лечения и затем через 24 недели без лечения. Наблюдалось значимое увеличение общего, а также всех подформ адипонектина после 24 недель приема перорально ЕС-цистеамина, а затем значимое уменьшение через 24 недели после прекращения лечения.
Фигура 4 показывает уровень общего адипонектина in vivo при лечении цистеамином. Наблюдалось значимое увеличение общего адипонектина в течение 0-24 недель: p=0.05; значимое уменьшение абсолютного уровня в течение 24-40 недель: p=0.01; Не наблюдалось значимого различия между исходным уровнем и уровнем на 40 неделе.
Фигура 5 показывает аналогичные данные, как Фигура 3, но выраженные в виде среднего процентного изменения in vivo эффектов цистеамина на мультимеризацию адипонектина. Сыворотка от субъектов в момент времени 0 (исходный), через 24 недели обработки лечения и через 40 недель (после прекращения обработки цистеамином через 24 недели). Полуколичественный анализ проводили с помощью вестерн-блоттинга 1 мкл сыворотки в невосстанавливающих условиях. Данные субъекта нормировали, используя % изменения мультимеров адипонектина на 24 неделе в сравнении с исходным и на 40 неделе в сравнении с исходным.
Фигура 6 показывает in vitro эффекты цистеамина на абсолютные уровни адипонектина у худых (lean) контрольных субъектов. Безжировую контрольную сыворотку при комнатной температуре, 37°C, 37°C + 90 мкМ цистеамина инкубировали в течение 1 часа. Не наблюдалось значимого различия между комнатной температурой и 37°C; для любого мультимера HMW не наблюдалось значимого изменения при обработке цистеамином; наблюдалось значимое уменьшение абсолютного уровня MMW при обработке цистеамином; не наблюдалось значимого изменения абсолютного уровня LMW при обработке цистеамином (результаты проявляют тенденцию к значимому увеличению); значимое % изменение при обработке цистеамином.
Фигура 7 показывает безжировую контрольную сыворотку при комнатной температуре, 37°C, 37°C + 90 мкМ цистеамина после инкубации 1 час. Не наблюдалось значимого различия между комнатной температурой и 37°C для любого мультимера. Не наблюдалось значимого различия HMW при обработке цистеамином. Наблюдалось значимое различие абсолютного уровня MMW при обработке цистеамином; значимое процентное изменение при обработке цистеамином; и не наблюдалось значимого изменения абсолютного уровня LMW при обработке цистеамином (результаты проявляют тенденцию к значимому увеличению) значимое процентное изменение при обработке цистеамином.
Фигура 8 - графики, демонстрирующие эффект цистеамина in vitro на сыворотку, полученную от субъектов с бандажированием желудка. Концентрации цистеамина 0, 7,5, 15, 30, 45, 60, 90 мкМ при инкубации 1 час при 37°C.
Фигура 9 демонстрирует уровни адипонектина, измеренные через 1 час после добавления цистеамина (в различных концентрациях 0, 7,5, 15, 30, 45, 60 и 90 мкМ) к сыворотке 4 пациентов с ожирением.
Фигура 10 показывает процент изменения различных мультимеров адипонектина при разных концентрациях цистеамина.
Фигура 11 показывает среднее значение процентного изменения от исходного форм адипонектина после инкубации ВАТ1-16 сыворотки с разными концентрациями цистеамина в течение 1 час.
Фигура 12 показывает уровни всех форм мультимеров, повышенные после обработки цистеамином в течение 24 недель. Однако относительные пропорции каждого мультимера (которые давали повышение общего адипонектина) были значимо повышены для HMW, понижены для MMW и оставались неизмененными для LMW.
Фигура 13 показывает средние процентные изменения мультимеров адипонектина у субъектов (n=10) с NAFLD. Не наблюдалось значимого различия для любого мультимера, измеренного в пределах между комнатной температурой (RT белые столбики) и 37°C (темные столбики). В сыворотке, инкубированной с цистеамином при 45 мкМ при 37°C в течение одного часа (заштрихованные столбики), наблюдалось значимое уменьшение MMW и увеличение LMW по сравнению с необработанной сывороткой.
Фигура 14A-B демонстрирует эффекты цистеамина in vivo. (A) - график, показывающий значимое различие между обработкой цистеамином и контролем по площади ишемии в виде процента площади, подверженной риску (или участка сердечной мышцы с LAD артерией). (B) - график, показывающий значимое различие между обработкой цистеамином и контрольной группой по площади ишемии в виде процента площади левого желудочка.
Фигура 15A-B показывает диастолические объемы на моделях с обработкой цистеамином и без обработки. (A) показывает конечный диастолический объем в мкл на 24 час и 72 час в контрольной группе, получавшей только IV буфер. Не наблюдалось значимого различия в EDV между двумя временными точками, что указывает на то, что не наблюдалось улучшения в течение времени. (B) показывает конечный диастолический объем в мкл на 24 час и 72 час в контрольной группе, получавшей цистеамин в IV буфере. Наблюдалось значимое уменьшение EDV между двумя временными точками, свидетельствуя, что имелось улучшение с течением времени.
Фигура 16 - график, показывающий, что наблюдалось значимое различие между процентным изменением EDV между 24 час и 72 час. Уменьшение EDV говорит о меньшей дилатации желудочка после ишемии миокарда. Мыши теряли вес в пределах между 24 час и 72 час и были вялыми. Контрольные мыши потеряли 13%, а группа с цистеамином потеряла 14% веса тела.
Фигура 17A-B - графики конечного систолического объема (ESV) в контрольной и обработанной цистеамином группах животных с моделью ишемии. (A) показывает ESV в мкл на 24 час и 72 час в контрольной группе, получавшей только буфер IV. Наблюдалось значимое различие ESV. (B) показывает ESV в мкл на 24 час и 72 час в группе, получавшей IV цистеамин в буфере. Наблюдалось значимое различие ESV.
Фигура 18 - график процентного изменения ESV. Наблюдалось значимое различие процентного изменения ESV между 24 час и 72 час. Уменьшение ESV говорит от лучшем сокращении желудочков.
Осуществление изобретения
Использованные в описании и прилагаемых пунктах формулы изобретения формы единственного числа включают формы множественного числа, если контекст явно не диктует иначе. Таким образом, например, ссылка на "неопределенный (некоторый) антиоксидант" включает множество таких антиоксидантов, а ссылка на "конкретный (данный) антиоксидант" включает ссылку на один или более антиоксидантов и т.д.
Кроме того, использование "или" означает "и/или", если не указано иначе. Подобным образом, термины "содержать", "содержит", "содержащий", "включать", "включает" и "включающий" являются взаимозаменяемыми и не являются ограничивающими.
Кроме того, следует понимать, что в случаях, когда описания различных вариантов осуществления используют термин "содержащий", специалистам в данной области техники понятно, что в некоторых конкретных случаях вариант осуществления альтернативно может быть описан с использованием выражения "в основном состоящий из" или "состоящий из".
Если не указано иное, все технические и научные термины, использованные в описании, имеют то же самое значение, которое обычно понятно специалисту в той области техники, к которой относится данное раскрытие. Хотя при осуществлении на практике раскрытых способов и композиций могут использоваться способы и материалы, подобные или эквивалентные описанным здесь, типичные способы, устройства и материалы представлены в данном описании.
Рассмотренные выше или на всем протяжении текста публикации используются только для их раскрытия до даты подачи настоящей заявки. Ничто в данном описании не должно трактоваться как допущение, что изобретатели не имеют права датировать такое раскрытие на основании предшествующего раскрытия.
При использовании в описании ишемия относится к состоянию, являющемуся результатом уменьшения или отсутствия (недостаточности) тока крови и кислорода к части организма, например, мозгу, сердцу или другой ткани. Ишемическое повреждение имеет отношение в основном к ткани, которая является удаленной (дистальной) или по иным причинам находится под влиянием отсутствия тока крови и кислорода. Ишемическое повреждение часто является результатом недостатка кислорода и жидкостей, а также включает воспалительные каскады. Например, ишемия и ишемическое повреждение может происходить в результате сердечного, легочного или мозгового нарушения, трансплантации органа или хирургической процедуры, или болезни или расстройства (например, серповидноклеточной анемии или серповидноклеточной болезни).
Острая ишемия чаще всего наблюдается при инсультах и поражениях сердца. Однако существует целый ряд нарушений и травм, которые вызывают ишемические события, приводящие к гибели клеток и повреждению ткани. Например, острые сердечные приступы (т.е. инфаркты миокарда) представляют собой распространенное явление. Кроме того, индивидуум, у которого имеются признаки, указывающие на рецидивирующую умеренную сердечную ишемию (т.е. стенокардию), может получить пользу от применения цистеамина (вероятно в результате его длительного влияния на адипонектин). Инсульты, цереброваскулярные и сердечно-сосудистые осложнения являются результатом острого нарушения тока крови в участке мозга или сердца соответственно. В Соединенных Штатах наблюдается приблизительно 500000 случаев инсультов в год, из которых 30% являются фатальными, и, следовательно, инсульт является третьей из основных причин смерти в США. Приблизительно 80% инсультов являются "ишемическими" и происходят вследствие острой окклюзии (закупорки) мозговой артерии, в результате чего уменьшается ток крови. Остальная часть является "геморрагическими инсультами", происходящими вследствие разрыва мозговой артерии с кровоизлиянием в ткань мозга и последующей блокадой тока крови из-за отсутствия течения в дистальном участке разорванного сосуда и местного сдавливания ткани, создающего ишемию.
В большинстве случаев инсульт затрагивает индивидуумов старше 65-летнего возраста, при этом наиболее мощным фактором риска является повышенное кровяное давление. До недавнего времени не было утвержденного лечения острого инсульта, который лечили только общей медицинской поддержкой, а затем реабилитацией после повреждения. В 1996 FDA одобрило применение тканевого активатора плазминогена (tPA) в качестве терапии при остром ишемическом нарушении, исходя из небольшого количества контролируемых испытаний. Некоторые, но не все, из испытаний подтвердили 30-55% улучшение клинических результатов с общим снижением частоты осложнений, но не летальности. В связи с узким окном благоприятной возможности для лечения пациента с использованием tPA и существенных побочных эффектов, связанных с использованием tPA, данное лекарственное средство недоиспользуется. Даже при использовании tPA в тромболитической терапии лечение вызывает полную регрессию симптомов менее чем в 40% случаев, вот почему существует необходимость в дополнительных видах лечения. Многочисленные нейропротекторные стратегии были проверены в клинических испытаниях, но ни одна из них не была одобрена FDA для лечения ишемического инсульта.
Приблизительно восемьдесят процентов инсультов может быть вызвано тем, что слишком мало крови достигает участка мозга, что обычно связано с тромбом (сгустком крови), блокирующим кровеносный сосуд (т.е., например, тромбозом сосудов головного мозга). Это называется "ишемический инсульт". Этот тип инсульта иногда может приводить к кровоизлиянию в мозг, так как подвергнутая воздействию ткань мозга размягчается и это может приводить к разрушению небольших кровеносных сосудов. В дополнение к этому внутримозговое кровоизлияние может происходить в том случае, когда у людей имеются проблемы, связанные с образованием сгустков крови. Сгустки, представляющие собой способ остановки любого кровотечения в организме, образуются белками, называемыми факторами свертывания крови, и «липкими» клетками крови, называемыми тромбоцитами. Во всех случаях, когда факторы свертывания крови или тромбоциты плохо работают, или их количество является недостаточным, у человека может развиться склонность к чрезмерному кровотечению.
Ишемическим инсультам могут предшествовать преходящие нарушения мозгового кровообращения (транзиторные ишемические атаки) (TIA), причем по оценкам, около 300,000 людей в Соединенных Штатах страдает от TIA каждый год. Тромбообразование также способствует закупорке периферических артерий у пациентов с диабетом, серповидноклеточной анемией и других пациентов, при этом необходимы эффективные и безопасные средства против ишемического поражения у таких пациентов.
Приблизительно двадцать процентов инсультов включает кровотечение в мозг, повреждающее близлежащую ткань мозга (например, геморрагический инсульт). Геморрагический инсульт наблюдается при разрыве кровеносного сосуда внутри мозга. Мозг очень чувствителен к кровотечению, при этом повреждение может происходить очень быстро или по причине присутствия самой крови, или потому, что жидкость увеличивает давление на мозг и повреждает его, придавливая мозг к черепу. Кровотечение раздражает ткань мозга, вызывая отек. Окружающие ткани мозга сопротивляются распространению кровотечения, что отражается в образовании опухоли (например, внутримозговой гематомы). Отек и гематома сдавливают и смещают нормальную ткань мозга. Чаще всего геморрагический инсульт связан с высоким кровяным давлением, которое создает нагрузку на стенки артерий до тех пор, пока они не разрываются.
Ишемия при серповидноклеточной анемии является результатом закупорки капилляров и недопущения тока крови в ткань, которая лишается кислорода и глюкозы. Эта закупорка капилляров вызывается эритроцитами, которые утратили свою нормальную форму и гибкость, разрушились или деформировались в жесткие или полужесткие "серповидные" формы. Закупорка капилляров прекращает ток свежей крови через те участки органа или ткани, которые в норме обслуживаются заблокированными капиллярами.
У большинства пациентов серповидноклеточная анемия не является причиной постоянной или хронической боли. Однако большая часть пациентов с серповидноклеточной анемией страдает от спорадических повторяющихся приступов, которые иногда называются ишемическими кризисами. Во время таких кризисов пациент с серповидноклеточной анемией обычно испытывает сильную боль в одном или более местах, которые часто различаются между пациентами и между разными кризисами у отдельного пациента. Нередко случается, что один или более суставов становятся опухшими и болезненными, и/или пациент страдает от острой или разлитой боли в животе, которая, как предполагается, является следствием ишемических состояний в одном или более участках одного или более органов.
Как правило, многие пациенты с серповидноклеточной анемией переносят несколько таких ишемических кризисов в год. Во время этих кризисов пациента, как правило, госпитализируют, назначают постельный режим с небольшой нагрузкой или отсутствием физической нагрузки и лечат целым рядом лекарственных средств, включая сильные обезболивающие средства, такие как морфин, кодеин и меперидин, и антибиотики широкого спектра действия, и то и другое помогает контролировать какие-либо инфекции, которые могут вносить вклад в кризисы, и помогает предотвратить или уменьшить дополнительные инфекции в тканях или органах, которые ослабляются в результате ишемического кризиса.
Среди детей младшего возраста с серповидноклеточной анемией обычным является дактилит вследствие ишемического некроза небольших костей и хрящей кистей рук и ступней, а острая боль в животе часто является результатом накопления повреждений в селезенке. Острая боль в животе также может быть результатом инфаркта в печени или почке, или может быть связана с гематурией. Как правило, в возрасте 10 лет наблюдаются холецистит вследствие желчных камней, асептический некроз головки бедренной кости, радиологические данные об уширенном объеме костного мозга в черепе, остеопороз позвоночника и некроз мозгового вещества почки, а у пациентов старше 18 лет часто происходят патологические переломы, в частности головки бедренной кости и плечевой кости. Ножные язвы являются обычным явлением у взрослых пациентов, а также наблюдаются лобарная пневмония, инфаркты легкого, инсульт и поражение сетчатки глаза. Во всех случаях боль является тяжелой, часто блуждающей и распространенной.
Одной причиной геморрагического инсульта является аневризма. Это слабое место в стенке артерии, которое растягивается наружу вследствие давления крови, циркулирующей внутри пораженной артерии. Со временем это место может разорваться и вызвать серьезное повреждение. Более крупная аневризма скорее всего когда-то разорвется.
Симптомы инсульта в большинстве случаев начинаются внезапно и могут быстро становиться тяжелыми. Симптомы инсульта могут включать, но не ограничиваются этим: i) слабость или неспособность двигать частью тела; ii) онемение или потерю чувствительности; iii) ухудшение или потерю зрения (может быть частичную); iv) затрудненность речи; v) неспособность узнавать или идентифицировать хорошо знакомые предметы; vi) внезапную головная боль; vii) нарушение пространственной ориентировки; viii) головокружение; xi) нарушение координации; x) затрудненность глотания и xi) сонливость, оцепенение, летаргическое, коматозное и/или бессознательное состояние.
Случай инсульта можно определить с помощью неврологического исследования, которое предположительно может показать отклоняющиеся от нормы результаты. Кроме того, пациент может выглядеть сонным или растерянным. Проверка глаз показывает ненормальные движения глаз, при этом в результате исследования сетчатки могут быть обнаружены изменения (проверка глазного дна с помощью инструмента, называемого офтальмоскопом). Кроме того, у пациента могут наблюдаться ненормальные рефлексы. Изображения мозга, полученные при исследовании методом компьютерной томографии, подтвердят наличие мозгового кровоизлияния. Для лучшего понимания того, что вызвало кровоизлияние, позже может быть проведена магнитно-резонансная визуализация мозга (MRI). Для установления аневризмы или AVM может понадобиться обычная ангиография (например, рентгенологическое исследование артерий с использованием красителя). Другие исследования могут включать, но не ограничиваются этим: клинический анализ крови, время свертывания крови, протромбиновое/частичное тромбопластиновое время (PT/PTT) и исследование CSF (спинномозговой жидкости).
Тромбоз может определяться как образование, развитие или наличие сгустка крови (например, тромба) в кровеносном сосуде и считается распространенной тяжелой болезнью. Тромбообразование может быть вовлечено в возникновение целого ряда сосудистых нарушений, включая, но не ограничиваясь этим, инфаркт миокарда, сердечную ишемию и/или тромбоз глубоких вен.
Наиболее частым примером тромбообразования является коронарный тромбоз, который приводит к закупорке коронарных артерий и часто к инфаркту миокарда (сердечному приступу). Каждый год в Северной Америке по причине инфаркта миокарда подвергается госпитализации более 1,3 миллиона пациентов. Стандартным лечением является введение тромболитического белка путем вливания. По оценкам тромболитическое лечение острого инфаркта миокарда сохранят 30 жизней на 1000 подвергнутых лечению пациентов; тем не менее, 30-дневная летальность для этого нарушения остается значительной (Mehta et al., Lancet 356: 449-454 (2000), включенная в описание путем отсылки). Значительная часть повреждения ткани в результате тромбоза может быть отнесена за счет окислительного повреждения. Было бы целесообразно вводить антиоксиданты или средства, ингибирующие окислительное повреждение, с помощью болюсных инъекций, хронически или остро.
Нестабильная стенокардия, вызванная недостаточной доставкой кислорода к сердцу вследствие закупорки коронарных артерий, является наиболее частой причиной госпитализации, что составляет 1,5 миллионов случаев в год только в Соединенных Штатах.
Тромбоз глубоких вен - часто встречающееся осложнение после хирургических вмешательств, таких как артропластика бедер и коленей. Подобные соображения распространяются на тромбоз вен, связанный с беременностью и родами. Некоторые индивидуумы имеют склонность к повторным случаям тромбоза вен и в настоящее время их лечат антитромботическими средствами, такими как лекарственные средства типа кумарина. Дозировка таких лекарственных средств должна быть оттитрована для каждого пациента, причем интервал между эффективными антитромботическими дозировками и дозировками, увеличивающими кровоизлияние, является небольшим. Комбинированная терапия с применением антиоксиданта в качестве части терапии может помочь уменьшить окислительное повреждение, связанное с тромбообразованием и ишемией.
Тромбоз глубоких вен может быть установлен с помощью тестов, включая, но не ограничиваясь этим: i) ультразвуковое доплеровское исследование тока крови в конечностях; ii) венографию ног или iii) плетизмографию ног.
Легочная эмболия представляет собой закупорку артерии в ногах жиром, воздухом, сгустком крови или опухолевыми клетками. Легочную эмболию чаще всего вызывают сгустки крови в венах, в частности в венах ног или таза (бедер). Реже пузырьки воздуха, капли жира, амниотическая жидкость или скопления паразитов или опухолевых клеток могут закупорить легочные сосуды. Одной из причин легочной эмболии является сгусток крови в венах ног, называемый тромбозом глубоких вен (DVT) (выше). Многие тромбы «убираются» собственными силами, однако некоторые могут вызывать тяжелую болезнь или даже смерть.
Факторы риска для развития легочной эмболии могут включать, но не ограничиваются этим: i) длительный постельный режим или отсутствие активности (включая длительные путешествия на самолетах, машинах или поездах); ii) использование пероральных контрацептивов; iii) хирургическое вмешательство (в частности, операции на органах таза); iv) роды; v) тяжелую травму; vi) ожог; vii) рак; viii) инсульт; ix) инфаркт миокарда; x) операцию на сердце или xi) переломы шейки бедра или бедренной кости. Кроме того, повышенный риск также могут иметь индивидуумы с некоторыми нарушениями свертывания крови и/или аутоиммунными заболеваниями (т.е., например, с синдромом антител к кардиолипину).
Симптомы легочной эмболии могут быть смазанными или они могут походить на симптомы, связанные с другими болезнями. Симптомы могут включать, но не ограничиваются этим: i) внезапный кашель; ii) кровянистую мокроту (значительные количества видимой крови или мокроту с прожилками крови); iii) внезапное появление затрудненного дыхания в состоянии покоя или при физической нагрузке; iv) шинирование ребер при дыхании (наклон вперед или фиксация положения грудной клетки); v) боль в груди; vi) частое дыхание или vii) учащенное сердцебиение (тахикардия).
Легочная эмболия может быть установлена при помощи тестов, включая, но не ограничиваясь этим: i) анализ крови на газы; ii) пульсовую оксиметрию; iii) рентгенографию грудной клетки; iv) вентиляционно-перфузионную сцинтиграфию легких; v) ангиопульмонографию; vi) электрокардиограмму и v) компьютеризированную томографическую ангиограмму грудной клетки.
Тромбофлебит представляет собой опухание (отек, воспаление) вен, вызванное сгустком крови. Такие состояния являются обычно результатом сидения в течение длительного периода времени (например, длительного воздушного перелета). Нарушения, которые увеличивают возможность образования сгустков крови у субъекта, также приводят к тромбофлебиту. Поверхностный тромбофлебит затрагивает вены, расположенные близко к поверхности кожи.
Симптомы, связанные с поверхностным тромбофлебитом, могут включать, но не ограничиваются этим: i) раздражение (теплоту) и болезненность по всей поверхности вены; ii) боль в пораженной части тела; iii) покраснение кожи (не всегда присутствует) или iv) воспаление (опухание) пораженной части тела. Для установления тромбофлебита могут быть проведены объективные тесты, включая, но не ограничиваясь этим: i) ультразвуковое доплеровское исследование; ii) венографию и iii) анализ свертывания крови.
Когда начинается ишемический кризис, он приводит в движение каскад событий, который делает данный кризис еще более тяжелым и трудным для остановки и лечения. Следует отметить три аспекта каскадного эффекта и само-сохраняющую природу этих ишемических кризисов. В дополнение к уменьшению питательных веществ и кислорода в месте ишемического повреждения, данный процесс приводит к воспалительному повреждению и выработке активных форм кислорода. Например, окислительный стресс после ишемического инсульта приводит к образованию активных форм кислорода, таких как перекись водорода (H2O2), гидроксильный радикал (HO•) и супероксид-анион (O2•), которые вызывают перекисное окисление липидов и модификации белков, приводящие к повреждению нейронов и сосудов и клиническим нарушениям.
Ишемия также вызывает повреждение ткани, являющееся следствием воспалительного каскада, приводящего к выработке лейкотриена посредством активации липокигеназы. Липоксигеназы (LOX) являются диоксигеназами, которые вводят молекулярный кислород в полиненасыщенные жирные кислоты, такие как арахидоновая кислота, и, исходя из места включения кислорода, классифицируются как 5-, 12- или 15-LOX. Недавние исследования подтверждают, что 12/15-LOX может играть роль в вызванной ишемией потере нервных клеток. Кроме того, по-видимому, существует корреляция между ранним уменьшением уровней GSH при ишемии и активацией 12-LOX. С помощью in vitro исследований на клеточной культуре было показано, что ингибиторы 12-LOX блокируют гибель клеток, вызванную глутаматом, и 5- и 12-LOX ингибиторы препятствуют ишемическому поражению в культурах гиппокампальных срезов.
Данное раскрытие, как более подробно описано ниже, предоставляет способы и композиции, пригодные для лечения любого из упомянутых выше ишемических повреждений. В одном варианте осуществления раскрытие предоставляет применение продукта цистеамина (например, цистеамина, производного цистеамина, цистамина, производного цистамина или фармацевтически приемлемой соли любого из вышеперечисленного), который уменьшает ишемическое поражение прямо или косвенно. В одном варианте осуществления раскрытие предоставляет способы и композиции для лечения ишемического повреждения за счет стимулирования уровней адипонектина у субъекта, например, путем введения продукта цистеамина.
Адипонектин (иногда называемый GBP-28, apM1 AdipoQ и Acrp30) - это белок, который у людей кодируется геном ADIPOQ. Адипонектин является белковым гормоном, модулирующим некоторое количество метаболических процессов, включая уровни глюкозы, катаболизм жирных кислот и воспаление. Адипонектин секретируется из жировой ткани в кровяное русло и является наиболее часто встречающимся в плазме по сравнению со многими гормонами. Уровни гормона находятся в обратно пропорциональном соотношении с жиром в организме взрослых людей. Адипонектин выделяется в кровяное русло, где он составляет около 0,01% всего белка в плазме примерно 5-10 мкг/мл. Уровни адипонектина являются пониженными у диабетиков по сравнению с недиабетиками.
Адипонектин автоматически самосвязывается в большие структуры (например, мультимеры с большим молекулярным весом (HMW), средним молекулярным весом (MMW) и низким молекулярным весом (LMW)). Сначала три молекулы адипонектина связываются вместе с образованием гомотримера. Тримеры продолжают самосвязываться и образуют гексамеры или додекамеры. Мономеры адипонектина имеют три домена, N-концевую сигнальную последовательность, коллагеноподобный домен и C-концевой глобулярный домен. В коллагеноподобном домене каждого LMW тримера несвязанный Cys-36 остаток может связываться с другим тримером с образованием гексамера MMW, который в свою очередь может образовывать большой HMW олигомерный мультимер (смотри, например, фигуру 2A).
Мультимеры адипонектина собираются внутри жировых клеток с помощью процесса, вовлекающего реакции дисульфидного обмена (вероятно через hEROs и ERp44) затем высвобождаются в кровоток для распространения. Высвобождение этих белков во внеклеточное пространство зависит от правильной 3-D структурной конфигурации, которая достигается в ходе образования дисульфидных связей (например, путем переноса электрона и окисления). Избыточное окисление может приводить к агрегации и сверхнакоплению белков в клетке. Неспособность к сворачиванию в силу образования дисульфидных связей будет давать в результате белки адипонектина, остающиеся внутри клетки, где они деградируют. В человеческих клетках белки-шапероны Erol-Lальфа и Erol-Lбета (hEROs) окисляют опосредованное дисульфидизомеразой белков (PDI) образование дисульфидной связи с помощью ER-резидентного белка ERp44, который содержит домен тиоредоксина. ERp44 образует смешанные дисульфиды (вероятно через цистеиновые концы) с hEROs и cargo складывающиеся промежуточные продукты. При нормальных физиологических условиях LMW, MMW и HMW мультимеры адипонектина выделяются в кровоток, где они в норме не являются взаимопревращаемыми. Эта жестко контролируемая выработка и высвобождение адипонектина наряду с отсутствием внеклеточного взаимопревращения между мультимерами находится в соответствии с адипонектином, имеющим различные сигнал-индуцирующие функции в разных клетках. Показано, что форма LMW является биологически более активной, чем другие формы, в частности, способствует действию инсулина в печени и скелетных мышцах, тем самым уменьшая уровни сахара в крови. Кроме того, было показано, что адипонектин играет благотворную роль после ишемического повреждения. В дополнение к этому, было показано, что адипонектин обладает церебро-защитной функцией, благодаря его противовоспалительному действию. Однако доставка адипонектина трудна и требует дополнительного исследования и разработки.
Функция этих белков-шаперонов зависит от внутриклеточных условий и мягко окисляющей среды эндоплазматического ретикулума. Избыточное окисление может приводить к неправильному сворачиванию молекул адипонектина, агрегации, внутриклеточному накоплению и в конечном итоге к деградации. Поэтому, при состояниях, связанных с окислительным стрессом, таких как ожирение, диабет II типа, резистентность к инсулину, сердечно-сосудистое заболевание и неалкогольная жировая дистрофия печени (NAFLD), выработка и высвобождение адипонектина будут уменьшены. Кроме того, субъекты, страдающие ожирением, имеющие диабет, сердечно-сосудистое заболевание и неалкогольную жировую дистрофию печени, подвергаются большому риску ишемического повреждения/кризиса.
Как описано выше, биосинтез адипонектина зависит от образования и распада смешанных дисульфидных промежуточных соединений между адипонектином и белками-шаперонами эндоплазматического ретикулума (ER). Цистеамин и цистамин являются сульфгидрил-содержащими веществами со способностью обеспечивать восстанавливающие эквиваленты для клеточных процессов. Данное раскрытие демонстрирует, что лечение in vivo цистеамином значительно увеличивает уровни циркулирующего в крови адипонектина. Тем не менее, без желания быть связанными каким-либо конкретным механизмом действия, данные указывают на то, что цистеамин может высвобождать дисульфидную связь, "связанные" пулы клеточного адипонектина, выступая в качестве донора восстанавливающих эквивалентов. Альтернативно, цистеамин может оказывать содействие взаимопревращению циркулирующего мультимерного адипонектина, увеличивая концентрацию LMW адипонектина, обладающего самой значительной эффективностью действия на клеточном уровне. Кроме того, введение продуктов цистеамина может увеличить общее количество адипонектина, включая HWM адипонектин. Кроме того, цистеамин сам обладает антиокислительными свойствами, которые могут останавливать или уменьшать окислительное повреждение в месте ишемического повреждения. Несмотря на многочисленные механизмы, перечисленные выше, результаты показывают полезное действие продуктов цистеамина (например, цистеамина или его производных, или цистамина или его производных) на уменьшение ишемического повреждения.
Цистеамин (HS-CH2-CH2-NH2) может легко проникать через клеточные мембраны благодаря небольшому размеру. В настоящее время FDA одобрило применение цистеамина только для лечения цистиноза, болезни, связанной с внутри-лизосомальным накоплением цистина. При цистинозе цистеамин действует путем превращения цистина в цистеин и цистин-цистеамин смешанный дисульфид, которые оба затем способны покинуть лизосому через посредство транспортеров цистеина и лизина соответственно (Gahl et al., N Engl J Med, 347(2): 111-21, 2002). Показано, что лечение цистеамином приводит в результате к снижению внутриклеточных уровней цистина в циркулирующих лейкоцитах (Dohil et al., J. Pediatr, 148(6): 764-9, 2006). Ранее не было показано, что продукты цистеамина пригодны для лечения ишемии.
Изобретение предоставляет продукты цистеамина, пригодные при лечении болезней и нарушений, связанных с ишемическим повреждением. "Продукт цистеамина" относится к цистеамину или его производным или цистамину или его производным, их биологически активному метаболиту или комбинации цистеамина или цистамина, и включает фармацевтически приемлемые соли любого из перечисленного выше, сложные эфиры, амиды, алкилированные соединения, пролекарства, аналоги, фосфорилированные соединения, сульфатные соединения или другие химически модифицированные формы и тому подобное. Такие производные включают, например, биологически активные метаболиты, формы соединения, химически модифицированные с помощью таких методов, как этерификация, алкилирование (например, C1, C2 или C3), мечение (например, радионуклидами или различными ферментами), ковалентное присоединение полимера, такое как пегилирование (получение производных с полиэтиленгликолем) или их смеси. В некоторых вариантах осуществления продукты цистеамина включают, но не ограничиваются этим, хлористоводородные соли, кислые соли винной кислоты, фосфорилированные производные и сульфатированные производные. Примеры других продуктов цистеамина включают 2-аминопропан тиол-1,1-аминопропан тиол-2, N- и S-замещенный цистеамин, AET, аминоалкильные производные, фосфотионат, амифостин (патент США 4,816,482). В одном варианте осуществления продукт цистеамина, в частности, исключает N-ацетилцистеин. В одном варианте осуществления продукты цистеамина включают, но не ограничиваются этим, структуры I и/или II:
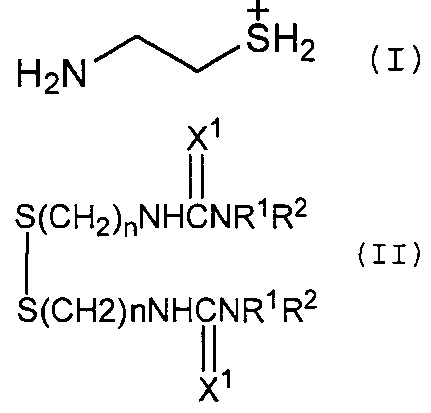
в которой n представляет 2 или 3, R1 и R2 каждый представляет атом водорода или алкильную группу, необязательно замещенную гидроксигруппой, аминогруппой, алкиламино или диалкиламиногруппой, или представляет циклоалкильную или арильную группу, и X1 выбирают из группы, состоящей из =N-CN, =N-NO2, =N-COR4, =N-NR-COOR4, =N-NR-CONH2, =N-SO2R4, =CH-NO2, -CH-SO2R4, =C(CN)2, =C(CN)COOR4 и =C(CN)CONH2, где R4 является алкильной или арильной группой. В другом аспекте продукт цистеамина может содержать радикал цистеамина, связанный с любым числом нетоксичных групп, выбранных из группы, состоящей из:
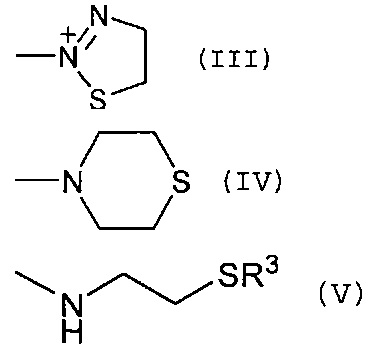
где R3 представляет атом водорода или алкильную группу с прямой или разветвленной цепью, имеющей от 1 до 10 атомов углерода.
Также рассматриваются фармацевтически приемлемые соли продуктов цистеамина, включая фармацевтически приемлемые анионы и/или катионы. Фармацевтически приемлемые катионы включают в числе прочих, катионы щелочных металлов (например, Li+, Na+, K+), катионы щелочноземельных металлов (например, Ca2+, Mg2+), катионы нетоксичных тяжелых металлов и аммония (NH4+) и замещенный аммоний (N(R')4+, где R' представляет собой водород, алкил или замещенный алкил, т.е. включая метил, этил или гидроксиэтил, в частности, катионы триметиламмония, триэтиламмония и триэтаноламмония). Фармацевтически приемлемые анионы включают в числе других галидов (например, Cl-, Br-), сульфат, ацетаты (например, ацетат, трифторацетат), аскорбаты, аспартаты, бензоаты, цитраты и лактат.
Раскрытие не ограничивается конкретной солью цистеамина или цистамина или сложного эфира или производного; композиции продукта цистеамина могут содержать любой цистеамин или цистамин, цистеамин или производное цистамина, или комбинацию цистеамина и цистамина. Активные вещества в композиции, например, цистеамин или цистамин, могут применяться в форме фармакологически приемлемой соли, сложного эфира, амида, пролекарства или аналога или в виде их комбинации. Соли, сложные эфиры, амиды, пролекарства и аналоги активных веществ можно получить с помощью стандартных методов, известных специалистам в области синтетической органической химии и описанных, например, в работе J. March, "Advanced Organic Chemistry: Reactions, Mechanisms and Structure," 4th Ed. (New York: Wiley-Interscience, 1992). Например, соли присоединения основания получают из нейтрального лекарственного средства с использованием обычных способов, затрагивающих взаимодействие одной или более свободных гидроксильных групп активных веществ с подходящим основанием. В большинстве случаев нейтральную форму лекарственного средства растворяют в полярном органическом растворителе, таком как метанол или этанол, и добавляют основание. Полученная соль или осаждается или может быть выделена из раствора путем добавления менее полярного растворителя. Подходящие основания для получения солей присоединения основания включают, но не ограничиваются этим, неорганические основания, такие как гидроксид натрия, гидроксид калия, гидроксид аммония, гидроксид кальция, триметиламин или тому подобное. Получение сложных эфиров затрагивает функционализацию гидроксильных групп, которые могут присутствовать в молекулярной структуре лекарственного средства. Сложные эфиры являются, как правило, ацил-замещенными производными свободных спиртовых групп, т.е. молекулами, которые получают из карбоновых кислот формулы R-COOH, где R является алкилом, и в большинстве случаев является низшим алкилом. Сложные эфиры могут быть возвращены в прежнее состояние свободных кислот, при необходимости, путем использования обычной процедуры гидрогенолиза или гидролиза. Получение амидов и пролекарств может осуществляться аналогичным образом. Другие производные и аналоги активных веществ можно получить с помощью стандартных методов, известных специалистам в области синтетической органической химии, или они могут быть получены согласно соответствующей литературе.
Продукты цистеамина могут заключаться в состав, предназначенный для целевой или длительной доставки. Например, цистеамин может быть покрыт энтеросолюбильной оболочкой для обеспечения доставки в тонкий кишечник или при желательном значении pH в нижний отдел желудочно-кишечного тракта. «Покрытое энтеросолюбильной оболочкой лекарственное средство или таблетка» имеет отношение, как правило, к лекарственному средству или таблетке, покрытой веществом ("энтеросолюбильной оболочкой"), которое остается неизменным или в основном неизменным, так что лекарственное средство или таблетка пропускается через желудок, но растворяется и высвобождает лекарственное средство в тонком кишечнике. В частности, композиции с доставкой в тонкий кишечник, с отсроченным высвобождением и замедленным высвобождением пригодны для лечения хронических ишемических болезней и нарушений, таких как серповидноклеточная анемия.
Любая из композиций раскрытия может быть введена в форме с замедленным высвобождением. Композиция с замедленным высвобождением имеет преимущество доставки в течение продолжительного периода времени без необходимости повторных введений композиции.
Замедленное высвобождение может достигаться, например, с помощью материалов, обеспечивающих замедленное высвобождение, таких как капсула-имплантат, иммуногранула, микронасос, или другого материала, который обеспечивает контролируемое медленное высвобождение продукта цистеамина или комбинированной композиции. Такие контролирующие высвобождение материалы хорошо известны в данной области техники и доступны из коммерческих источников. Кроме того, в состав с активными веществами данного изобретения может быть заключен биоразлагаемый или биодеградируемый материал, такой как полимолочная кислота, полигалактуроновая кислота, восстановленный коллаген, многослойные липосомы, или другие общепринятые депо-композиции могут быть имплантированы для медленного высвобождения продукта цистеамина, тромботического средства, спиновой ловушки и антагонистов NMDA. В данном изобретении также рассматривается применение инфузионньгх насосов, матричных систем включения и устройств для чрескожной доставки.
Активные вещества/композиции также могут быть заключены в мицеллы или липосомы. Технология инкапсулирования в липосомы хорошо известна. Липосомы могут быть нацелены на конкретную ткань, такую как нервная ткань, посредством использования рецепторов, лигандов или антител, способных связываться с антигеном или мишенью в желательной ткани. Получение этих композиций хорошо известно в данной области техники (смотри, например, Pardridge, выше (1991), и Radin and Metz, Meth Enzymol. 98: 613-618 (1983)).
Продукт цистеамина также может включать дополнительные фармацевтически приемлемые носители или основы. Фармацевтически приемлемый носитель или основа относится, как правило, к материалам, пригодным для введения субъекту, при этом носитель или основа не является биологически вредным, или в других случаях не вызывает нежелательных эффектов. Такие носители или основы, как правило, являются инертными ингредиентами медикамента. В большинстве случаев носитель или основа вводится субъекту вместе с активным ингредиентом, не вызывая каких-либо биологических эффектов или не взаимодействуя вредоносным образом с любых из других компонентов фармацевтической композиции, в которой он содержится.
Продукт цистеамина или другой активный ингредиент может включать фармацевтически приемлемую соль, сложный эфир или другое производное. Например, соли, сложные эфиры или другие производные включают биологически активные формы, обладающие сходными биологическими эффектами по сравнению с исходным соединением. Типичные соли включают хлористоводородную соль и битартратные соли.
Фармацевтические носители включают фармацевтически приемлемые соли, в частности, когда в соединении присутствует основная или кислотная группа. Например, в том случае, когда присутствует кислотный заместитель, такой как -COOH, для введения рассматривается использование солей аммония, натрия, калия, кальция и т.п. В дополнение к этому, в том случае, когда присутствует кислотная группа, в качестве предпочтительных форм соединений рассматриваются фармацевтически приемлемые сложные эфиры (например, метиловый, третбутиловый, пивалоилоксиметиловый, сукциниловый и тому подобные), такие сложные эфиры применяются в данной области техники для модификации растворимости и/или характеристик гидролиза при использовании композиций с замедленным высвобождением или пролекарственных композиций.
Когда присутствует основная группа (например, аминогруппа или основной гетероарильный радикал, такой как пиридил), тогда кислая соль, такая как гидрохлорид, гидробромид, ацетат, малеат, памоат, фосфат, метансульфонат, п-толуолсульфонат и т.п., рассматривается в качестве формы для введения.
В дополнение к этому, соединения могут образовывать сольваты с водой или общими органическими растворителями. Такие сольваты также рассматриваются.
Активный ингредиент, фармацевтическая или другая композиция раскрытия может содержать стабилизирующее вещество. «Стабилизирующие вещества», как правило, подразумевают соединения, которые уменьшают скорость, с которой деградирует фармацевтический препарат, в частности, фармацевтическая композиция для перорального приема при хранении в условиях окружающей среды. Некоторые стабилизирующие вещества пригодны для внутривенной доставки. Например, одно или более из следующих стабилизирующих веществ может использоваться при создании композиции с продуктом цистеамина для внутрисосудистой доставки: α-токоферол, 2,6-ди-трет-бутил-4-метилфенол (BHT), токоферол ацетат, 2-трет-бутил-4-гидроксианизол и/или 3-трет-бутил-4-гидроксианизол (BHA), додецилгаллат, ацетат и аскорбиновая кислота.
При использовании в описании термин "терапевтически эффективное количество" или "эффективное количество" относится к количеству цистеамина, производного цистеамина, цистамина, производного цистамина или их солей, достаточному для того, чтобы приводить к уменьшению интенсивности симптомов, например, исцелению, выздоровлению, предотвращению или улучшению соответствующего медицинского состояния, или увеличению скорости лечения, исцелению, предотвращению или улучшению таких состояний, как правило, обеспечению статистически значимого улучшения в леченой популяции. При ссылке на отдельный активный ингредиент, который вводится отдельно, терапевтически эффективная доза относится к этому одному ингредиенту. При ссылке на комбинацию, терапевтически эффективная доза относится к объединенным количествам активных ингредиентов, которые дают в результате терапевтический эффект, когда они вводятся в комбинации, включая периодическое или одновременное введение. В одном варианте осуществления терапевтически эффективное количество продукта цистеамина улучшает симптомы, включая, но не ограничиваясь этим, воспалительное повреждение, окислительное повреждение, уменьшение количества окислительных агентов, уменьшение ишемического повреждения, являющегося результатом острого или хронического ишемического события, увеличение уровней адипонектина и/или увеличение LMW адипонектина.
Использованный в описании термин "количество, уменьшающее (облегчающее) ишемическое повреждение", или "эффективное количество" означает количество композиции, содержащее продукт цистеамина, необходимое для уменьшения ишемического повреждения, будь то уменьшение повреждения ткани, улучшение поведения или оказание содействия реперфузии поврежденной ткани. Эффективное количество, которое следует вводить системно, зависит от веса тела субъекта. Как правило, эффективное количество, которое должно вводиться системно, составляет примерно от 0,1 мг/кг до 100 мг/кг (например, примерно от 0,5 мг/кг до 20 мг/кг). Эффективное количество, конечно, будет зависеть от целого ряда факторов, включая, например, возраст и вес субъекта (например, млекопитающего, такого как человек), определенного состояния, требующего лечения, и его тяжести, способа введения, и в конечном итоге будет отводиться на усмотрение врача или ветеринара.
Фармацевтические композиции раскрытия, включающие продукт цистеамина в качестве активного ингредиента, могут содержать фармацевтически приемлемые носители или добавки, зависящие от способа введения. Примеры таких носителей или добавок включают воду, фармацевтически приемлемый органический растворитель, коллаген, поливиниловый спирт, поливинилпирролидон, карбоксивиниловый полимер, натрий карбоксиметилцеллюлозу, полиакрилат натрия, альгинат натрия, водорастворимый декстран, карбоксиметилкрахмал натрия, пектин, метилцеллюлозу, этилцеллюлозу, ксантановую камедь, гуммиарабик, казеин, желатин, агар, диглицерин, глицерин, пропиленгликоль, полиэтиленгликоль, вазелин, парафин, стеариловый спирт, стеариновую кислоту, человеческий сывороточный альбумин (HSA), маннитол, сорбит, лактозу, фармацевтически приемлемое поверхностно-активное вещество и тому подобное. Добавки выбирают из перечисленного выше и их комбинаций, но не ограничиваясь этим, по необходимости, в зависимости от лекарственной формы раскрытия.
Состав фармацевтической композиции будет варьировать согласно выбранному способу введения (например, раствор, эмульсия, таблетка с покрытием). Предназначенная для введения подходящая композиция, содержащая продукт цистеамина, может быть приготовлена в физиологически приемлемом разбавителе (основе) или носителе. Подходящие носители для растворов и эмульсий включают, например, водные или спиртовые/водные растворы, эмульсии или суспензии, содержащие физиологический раствор и содержащую буфер среду. Разбавители для парентерального введения включают раствор хлорида натрия, раствор Рингера, декстрозы и хлорида натрия, раствор Рингера с лактатом или жирные масла. Носители для внутривенного введения могут включать различные добавки, консервирующие вещества, или жидкость, питательное вещество или электролитные наполнители.
Ряд водных носителей, например, вода, буферная вода, 0,4% физиологический раствор, 0,3% глицин или водные суспензии могут содержать активное соединение в смеси с эксципиентами, пригодными для изготовления водных суспензий. Такие эксципиенты представляют собой суспендирующие вещества, например, натрий карбоксиметилцеллюлозу, метилцеллюлозу, гидроксипропилметилцеллюлозу, альгинат натрия, поливинилпирролидон, трагакантовую камедь и гуммиарабик; диспергирующие или увлажняющие вещества могут быть природным фосфатидом, например, лецитином, или продуктами конденсации алкиленоксида с жирными кислотами, например, полиоксиэтилен стеаратом, или продуктами конденсации этиленоксида с алифатическими спиртами с длинной цепью, например, гептадекаэтиленоксицетанолом, или продуктами конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и гексита, такими как полиоксиэтилен сорбит моноолеат, или продуктами конденсации этиленоксида с неполными эфирами, полученными из жирных кислот и ангидридов гексита, например, полиэтилен сорбит моноолеат. Водные суспензии также могут содержать одно или более консервирующих веществ, например, этил или н-пропил, п-гидроксибензоат, один или более красителей, и один или более подсластителей, таких как сахароза или сахарин.
В некоторых вариантах осуществления продукт цистеамина этого раскрытия может быть лиофилизирован с целью хранения и может быть восстановлен в подходящем носителе перед применением. Может использоваться любой подходящий метод лиофилизации и восстановления. Специалистам понятно, что лиофилизация и восстановление могут приводить к различной степени потери активности, и что используемые уровни могут быть отрегулированы с учетом этого.
Диспергируемые порошки и гранулы, подходящие для приготовления водной суспензии путем добавления воды, предоставляют активное соединение в смеси с диспергирующим или увлажняющим веществом, суспендирующим веществом и одним или более консервирующими веществами. Примеры подходящих диспергирующих или увлажняющих веществ и суспендирующих веществ уже упоминались выше. Также могут присутствовать дополнительные эксципиенты, например, подсластители, вкусовые и красящие вещества.
В одном варианте осуществления раскрытие предоставляет применение композиции продукта цистеамина с энтеросолюбильным покрытием. Энтеросолюбильные покрытия отсрочивают высвобождение до тех пор, когда продукт цистеамина достигает кишечника, как правило, тонкого кишечника. Благодаря энтеросолюбильным покрытиям, доставка в тонкий кишечник улучшается, тем самым улучшая поглощение активного ингредиента, одновременно уменьшая побочные эффекты в желудке.
В некоторых вариантах осуществления покровный материал выбирают так, что терапевтически активное средство высвобождается, когда лекарственная форма достигает тонкого кишечника или области, в которой значение pH больше чем pH 4,5. Покрытие может быть pH-чувствительным материалом, который остается интактным при низком значении pH в среде желудка, но который разрушается или растворяется при обычном значении pH тонкого кишечника пациента. Например, материал энтеросолюбильного покрытия начинает растворяться в водном растворе при значении pH примерно от 4,5 до 5,5. Например, pH-чувствительные материалы не подвергаются значительному растворению до тех пор, пока лекарственная форма не выпускается из желудка. Значение pH тонкого кишечника постепенно увеличивается примерно от 4,5 до 6,5 в луковице двенадцатиперсной кишки примерно до 7,2 в дистальных участках тонкого кишечника. Для того, чтобы обеспечить предсказуемое растворение, соответствующее времени прохода через тонкий кишечник около 3 часов (например, 2-3 часа), и дать возможность воспроизводимого высвобождения, растворение покрытия должно начинаться в диапазоне значений pH, характерных для тонкого кишечника. Следовательно, количество энтеросолюбильного полимерного покрытия должно быть достаточным для того, чтобы в основном растворяться в течение приблизительно трех часов времени прохождения по тонкому кишечнику, например, проксимальной и средней кишке.
Энтеросолюбильные покрытия используются в течение многих лет для того, чтобы останавливать высвобождение лекарственного средства из форм для перорального приема. В зависимости от состава и/или толщины энтеросолюбильные покрытия являются устойчивыми к желудочной кислоте в течение необходимых периодов времени, до того, как они начнут разрушаться и обеспечат возможность высвобождения лекарственного средства в нижнем отделе желудка или в верхней части тонкого кишечника. Примеры некоторых энтеросолюбильных покрытий раскрыты в патенте США №5,225,202, который полностью включается в описание путем отсылки. Как установлено в патенте США №5,225,202, некоторыми примерами покрытий, применяемыми ранее, являются воск и глицерилмоностеарат; воск, шеллак и целлюлоза; цетиловый спирт, мастика и шеллак, а также шеллак и стеариновая кислота (патент США №2,809,918); поливинилацетат и этилцеллюлоза (патент США №3,835,221); и нейтральный сополимер сложных эфиров полиметакриловой кислоты (Eudragit® L30D) (F.W. Goodhart et al., Pharm. Tech., pp. 64-71, April 1984); сополимеры метакриловой кислоты и метилового эфира метакриловой кислоты (Eudragits), или нейтральный сополимер сложных эфиров полиметакриловой кислоты, содержащий стеараты металла (Mehta et al., патенты США №4,728,512 и 4,794,001). Такие покрытия содержат смеси жиров и жирных кислот, шеллака и производных шеллака и кислых фталатов целлюлозы, например, имеющих свободные карбоксильные группы. Смотри описания подходящих энтеросолюбильных покрытий в Remington's на странице 1590, и Zeitova et al. (патент США №4,432,966). Соответственно, увеличенная абсорбция в тонком кишечнике, происходящая благодаря энтеросолюбильным покрытиям композиций продукта цистеамина, может дать в результате улучшенную эффективность.
В большинстве случаев энтеросолюбильное покрытие содержит полимерный материал, который предотвращает высвобождение продукта цистеамина при низком значении pH в среде желудка, но который ионизирует при немного более высоком значении pH, как правило pH 4 или 5, и таким образом, растворяется достаточно в тонком кишечнике, чтобы постепенно высвобождать здесь активное вещество. Соответственно, к числу наиболее эффективных материалов для энтеросолюбильных покрытий относятся поликислоты, имеющие рКа в пределах примерно от 3 до 5. Подходящие материалы для энтеросолюбильных покрытий включают, но не ограничиваются этим, полимеризованный желатин, шеллак, сополимер метакриловой кислоты типа С NF, фталат бутирата целлюлозы, гидрофталат целлюлозы, фталат пропионата целлюлозы, поливинилацетат фталата (PVAP), ацетат фталата целлюлозы (CAO), ацетат тримеллитата целлюлозы (CAT), фталат гидроксипропил метилцеллюлозы, ацетат гидроксипропил метилцеллюлозы, сукцинат диоксипропил метилцеллюлозы, карбоксиметилэтилцеллюлоза (CMEC), гидроксипропилметилцеллюлозы ацетат сукцината (HPMCAS) и полимеры и сополимеры акриловой кислоты, как правило, образованные из метилакрилата, этилакрилата, метилметакрилата и/или этилметакрилата с сополимерами сложных эфиров акриловой и метакриловой кислот (Eudragit® NE, Eudragit® RL, Eudragit® RS). Например, энтеросолюбильное покрытие может содержать Eudragit® L30D, триэтилцитрат и гидроксипропилметилцеллюлозу (НРМС), при этом покрытие составляет от 10 до 13% окончательного продукта.
В одном варианте осуществления композиция продукта цистеамина вводится в форме таблетки. В различных вариантах осуществления таблетки изготавливаются сначала путем нанесения энтеросолюбильного покрытия на продукт цистеамина. Способом формования таблеток является прямое прессование порошков, содержащих продукт цистеамина с энтеросолюбильным покрытием, необязательно в комбинации с разбавителями, связующими веществами, смазывающими веществами, разрыхлителями, красящими веществами, стабилизирующими веществами или тому подобным. В различных вариантах осуществления таблетки изготавливаются путем перемешивания эксципиентов с продуктом цистеамина, прессования таблетки и нанесения энтеросолюбильного покрытия. В качестве альтернативы прямому прессованию, прессованные таблетки можно получить, используя процессы влажного гранулирования, сухого гранулирования и вальцевания. Кроме того, таблетки могут быть отлиты в форму, а не спрессованы, начиная с влажного материала, содержащего подходящее водорастворимое смазывающее вещество. Также в желудочную/пероральную композицию может быть включено биологически доступное железо для способствования потреблению продукта цистеамина.
Изобретение предоставляет способ лечения ишемического повреждения и воспаления, связанного с окислительным повреждением, включающий введение продукта цистеамина, например, цистеамина или его производного, или цистамина или его производного, в количестве, эффективном для уменьшения окислительного повреждения у субъекта в месте ишемического повреждения. Данные способы и композиции включают доставку продукта цистеамина субъекту до, одновременно с или после ишемического события. В некотором или любом вариантах осуществления продукт цистеамина доставляется одновременно с или сразу после острого ишемического события, в количестве, эффективном для уменьшения ишемического поражения. Введенные продукты цистеамина имеют один или более эффектов, включая уменьшение окислительного повреждения, оказание содействия выработке/циркуляции адипонектина с целью ингибирования окислительного повреждения.
Изобретение предоставляет способы и композиции для стимулирования уровней адипонектина у субъекта, включающие введение субъекту эффективного количества продукта цистеамина, например, цистеамина или его производного, или цистамина или его производного, или их фармацевтически приемлемой соли. Описание демонстрирует, что контактирование клетки или субъекта с продуктом цистеамина увеличивает уровень адипонектина по сравнению с той же самой клеткой или субъектом при отсутствии продукта цистеамина. В одном варианте осуществления цистеамин или его производное, или цистамин или его производное, или их фармацевтически приемлемая соль может способствовать выработке мультимера адипонектина с низким молекулярным весом.
Изобретение предоставляет способ лечения ишемического повреждения и воспаления, включающий введение продукта цистеамина, например, цистеамина или его производного, или цистамина или его производного, или их фармацевтически приемлемой соли в количестве, эффективном для увеличения уровней адипонектина и/или модулирования уровней GSH у субъекта. Способы и композиции включают доставку продукта цистеамина субъекту до, одновременно с или после ишемического события. В некоторых или каких-либо вариантах осуществления продукт цистеамина доставляется одновременно с или сразу после острого ишемического события в количестве, эффективном для уменьшения ишемического поражения и/или увеличения уровней адипонектина. В одном варианте осуществления повышенные уровни адипонектина являются повышенными уровнями мультимера адипонектина с низким молекулярным весом.
Изобретение предоставляет способы и композиции для увеличения уровней адипонектина и, в частности, LMW адипонектина. Кроме того, изобретение предоставляет способы и композиции для лечения ишемического повреждения. В другом варианте осуществления обеспечивается лечение субъекта, нуждающегося в повышении уровней адипонектина (например, LMW адипонектина) с помощью продукта цистеамина в количестве, эффективном для увеличения уровней адипонектина. Субъект может быть субъектом, у которого наблюдается острое ишемическое событие, ишемическое повреждение или возможно наблюдается острое ишемическое событие. Субъект может быть субъектом, страдающим тромболитическим заболеванием. Субъект может быть диабетиком (например, субъектом с диабетом II типа) или субъектом с ожирением. В некоторых вариантах осуществления субъект с диабетом или ожирением имеет низкие уровни LMW адипонектина, или высокие уровни HMW адипонектина по сравнению с популяцией здоровых субъектов (например, субъектами без диабета и без ожирения). В некоторых вариантах осуществления субъект не является субъектом с диабетом. В некоторых вариантах осуществления субъект не имеет гиперхолестеринемии.
Изобретение предоставляет способы и композиции для лечения хронических болезней, увеличивающих риск возникновения ишемии. Хронические болезни, несущие повышенный риск ишемического повреждения/кризиса, включают, но не ограничиваются этим, атеросклероз (нагруженные липидом бляшки, закрывающие просвет артерий); гипогликемию (более низкий, чем нормальный уровень глюкозы); тахикардию (ненормально быстрое биение сердца); гипотензию (низкое кровяное давление, например, септический шок, сердечная недостаточность); тромбоэболию (сгустки крови; например, связанные с раком); внешнее сдавливание кровеносного сосуда, например, опухолью или в случае артериомезентериальной компрессии; эмболию (инородные тела в кровотоке, например, эмболия амниотической жидкостью); серповидноклеточную анемию (эритроциты, имеющие неправильную форму); и анемию. При лечении такой хронической болезни композиции, которые даются менее частыми дозами, могут приниматься перорально в противовес IV, и, в частности, пригодными являются композиции с длительным/отсроченным высвобождением. Например, изобретение предоставляет продукты цистеамина с энтеросолюбильным покрытием, которые высвобождаются при значении pH выше чем 4,5, и которые назначаются менее часто, чем Cystagon®. Композиция для такой доставки также может включать добавку биодоступного железа или компонент, способствующий поглощению продукта цистеамина. Когда субъект находится в клинических условиях, может использоваться IV введение в течение продолжительных периодов времени. Например, продукт цистеамина может быть заключен в состав с фармацевтически приемлемым буфером, содержащим стабилизирующие вещества для IV введения.
Изобретение также предоставляет способ ингибирования повреждения с целью снижения возможности повреждения ткани во время реперфузии у млекопитающего, данный способ включает введение млекопитающему эффективного количества продукта цистеамина в отдельности или в комбинации с другими терапевтическими средствами (например, тромболитическим средством, ловушкой свободных радикалов и т.п.), как описано здесь.
Данные средства могут вводиться одновременно или последовательно в отдельных композициях или могут вводиться одновременно в одной композиции. В любом случае отсрочка введения второго или третьего или т.д. из множества средств не должна быть такой, при которой утрачивается польза от возможного эффекта комбинации средств in vivo при ингибировании повреждения ткани.
Как описано выше, композиции продукта цистеамина могут быть приготовлены для введения перорально, парентерально, трансокулярно, интраназально, чрескожно, через слизистую, с помощью средства для ингаляции, вагинально, ректально, через спинномозговую жидкость или путем внутричерепной инъекции. Использованный в описании термин «парентеральное введение» включает подкожные, внутривенные, внутримышечные, интрацистернальные инъекции или способы вливания. Также рассматривается введение с помощью внутривенной, внутрикожной, внутримышечной инъекции, инъекции внутрь молочной железы, внутрибрюшинной, подоболочечной, ретробульбарной, внутрилегочной инъекции и/или хирургической имплантации в определенное место. В большинстве случаев композиции, предназначенные для введения любым из вышеуказанных способов, являются апирогенными, а также не содержат других примесей, которые могут быть вредны для реципиента. Кроме того, композиции, предназначенные для парентерального введения, являются стерильными.
Прямое внутричерепное введение или введение в спинномозговую жидкость также может использоваться для введения эффективного количества продукта цистеамина. Продукт цистеамина можно комбинировать с другими терапевтическими средствами, как описано здесь.
Внутрисосудистые вливания обычно проводятся с использованием парентерального раствора, содержащегося в инфузионном мешке или флаконе или в шприце для вливания с электрическим управлением. Раствор может доставляться субъекту из инфузионного мешка или флакона под действием собственного веса или при помощи инфузионного насоса. Использование инфузионных систем подачи под собственным весом в некоторых случаях не может предоставить достаточный контроль скорости введения парентерального раствора и поэтому может быть желательно использование инфузионного насоса, в частности, при использовании растворов, содержащих относительно высокие концентрации спиновой ловушки/тромболитической композиции. Шприц для вливания с электрическим управлением может обеспечить гораздо больший контроль над скоростью введения.
Для лечения нейронного повреждения, связанного, например, с острым ишемическим инсультом, подходящая ежедневная системная дозировка композиции продукта цистеамина (например, содержащей цистеамин, цистамин или производное любого из вышеуказанного) основывается на весе тела субъекта и находится в пределах примерно от 0,1 мкг/кг до 100 мг/кг, хотя также рассматриваются дозировки примерно от 0,1 мг/кг до 100 мг/кг или примерно от 0,5 мг/кг до 20 мг/кг. Таким образом, для типичного человека весом 70 кг системная дозировка может составлять примерно от 7 мкг до 7000 мг ежедневно. Ежедневная дозировка вещества для местного введения будет составлять величину меньшего порядка, чем системная дозировка. Также рассматривается пероральное введение.
Продукт цистеамина может быть введен локально в место ишемического повреждения (например, острого ишемического повреждения) или может вводиться системно. В одном варианте осуществления продукт цистеамина может вводиться постоянно или в течение длительного периода времени субъекту, имеющему риск получения ишемического повреждения (например, субъекту с серповидноклеточной анемией). Способ введения и композиция может отличаться в зависимости от хронических или острых вариантов лечения.
В одном варианте осуществления продукт цистеамина может быть введен во время ишемического повреждения или в пределах периода времени сразу после ишемического события или ишемического повреждения. Период времени может составлять от нескольких минут (например, 1, 2, 3, 4, 5 или более минут) или 10, 20, 30, 60, 90 120 или более минут до нескольких часов после ишемического события (например, 3 часов, 6 часов, 10 часов, 12 часов или более). В одном варианте осуществления продукт цистеамина может вводиться в комбинации с одним или более дополнительными средствами, пригодными для лечения ишемии. Например, данный способ может включать введение с реперфузионным средством, ловушкой свободных радикалов, спиновой ловушкой или тому подобным.
В другом варианте осуществления субъект подвергается риску инсульта, ишемии сердца или другого ишемического поражения, например, испытывал или испытывает состояния, которые создают риск инсульта, ишемии сердца или легкого. Примеры таких состояний включают высокое кровяное давление; потребление табака; сахарный диабет; болезнь сонной или другой артерии; заболевание периферических артерий; мерцательную аритмию; другую болезнь сердца; преходящие ишемические нарушения (TIA); некоторые заболевания крови (например, высокое количество эритроцитов; серповидноклеточную анемию); высокий уровень холестерина в крови, гиподинамию, ожирение, избыточное употребление алкоголя, использование запрещенных наркотиков, предшествующий инсульт, серповидноклеточную анемию и предшествующий сердечный приступ.
При хронических состояниях (например, серповидноклеточной анемии), используются композиции с замедленным или контролируемым высвобождением. В острых состояниях (например, при ишемическом инсульте) подходят композиции с немедленным высвобождением, такие как IV доставка (или другая парентеральная доставка), локальная черепно-мозговая доставка и тому подобное. В некоторых вариантах осуществления композиция продукта цистеамина является лекарственной формой с замедленным или контролируемым высвобождением, обеспечивающей Cmax продукта цистеамина, то есть по меньшей мере примерно на 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85% или 100% выше, чем Cmax, предоставленная лекарственной формой с немедленным высвобождением, содержащей такое же количество продукта цистеамина. В некоторых вариантах осуществления Cmax является примерно на 75%, 100%, 125% или 150% выше, чем Cmax лекарственной формы с немедленным высвобождением. Cmax относится к максимальной дозе продукта цистеамина в крови после введения дозировки и обеспечивает показательного, что лекарственное средство поглощается системно.
В некоторых вариантах осуществления AUC лекарственной формы с замедленным или контролируемым высвобождением также увеличивается по меньшей мере примерно на 20%, 25%, 30%, 35%, 40%, 45% или 50%, или примерно до 50%, 60%, 75% или 100% относительно лекарственной формы с немедленным высвобождением. AUC или "площадь под кривой" относится к кинетической кривой, полученной после измерения концентрации лекарственного средства в плазме в зависимости от времени после введения дозы лекарственного средства.
Приготовление форм фармацевтических композиций с замедленным, контролируемым или длительным высвобождением с желательными фармакокинетическими характеристиками известно в данной области техники и может осуществляться с помощью целого ряда методов. Например, системы для пероральной контролируемой доставки включают высвобождение, контролируемое растворением (например, контроль растворения инкапсулированием или контроль растворения с помощью матрицы), диффузионно-контролируемое высвобождение (устройства с резервуаром или матрицей), ионообменные смолы, осмотически-контролируемое высвобождение или гастроретентивные системы. Контролируемое растворением высвобождение может быть получено, например, за счет медленной скорости растворения лекарственного средства в желудочно-кишечном тракте, включения лекарственного средства в нерастворимый полимер и покрытия частиц или гранул лекарственного средства полимерными материалами различной толщины. Диффузионно-контролируемое высвобождение может быть получено, например, за счет контролируемой диффузии через полимерную мембрану или полимерную матрицу. Осмотически-контролируемое высвобождение может быть получено, например, за счет контролируемого поступления растворителя через полупроницаемую мембрану, который в свою очередь перемещает лекарственное средство наружу через сформированное лазером отверстие. Осмотическое и гидростатическое давление отличается по обе стороны мембраны, управляющей транспортом жидкости. Длительное удерживание в желудке может быть достигнуто, например, путем изменения плотности композиций, биоадгезии к слизистой оболочке желудка или увеличением времени пребывания в желудке. Более подробно смотри руководство Handbook of Pharmaceutical Controlled Release Technology, Wise, ed., Marcel Dekker, Inc., New York, NY (2000), полностью включенное в описание путем отсылки, например, главу 22 ("An Overview of Controlled Release Systems").
Концентрация продукта цистеамина в этих композициях может широко варьировать, например, менее чем примерно от 0,5%, обычно или по меньшей мере от 1% вплоть до 15 или 20% по весу и выбирается главным образом, исходя из объемов жидкости, технологических характеристик, вязкости и т.д. в соответствии с конкретным выбранным способом введения. Современные способы получения композиций известны или очевидны специалистам в данной области техники и описаны более подробно, например, в Remington's Pharmaceutical Science, 15th ed., Mack Publishing Company, Easton, Pa. (1980).
Продукт цистеамина присутствует в композиции в терапевтически эффективном количестве; как правило, композиция заключена в стандартную лекарственную форму. Количество вводимого продукта цистеамина, конечно, будет зависеть от возраста, веса и общего состояния субъекта, тяжести заболевания, которое необходимо лечить, и заключения лечащего врача. Подходящие терапевтические количества хорошо известны специалистам в данной области и/или раскрыты в текстах пертинентных ссылок и литературе. Существующие дозировки без энтеросолюбильной оболочки составляют около 1,35 г/м площади поверхности тела и вводятся 4-5 раз в день. В одном варианте осуществления дозировка вводится или один раз в день или несколько раз в день при хронических состояниях болезни (например, серповидноклеточной анемии) и может вводиться в виде болюса или IV при острых состояниях (например, остром ишемическом повреждении). Продукт цистеамина может вводиться один, два, три или четыре раза в день. В отдельных вариантах осуществления продукт цистеамина дается менее чем четыре раза в день. В некоторых вариантах осуществления эффективная дозировка продукта цистеамина может составлять в пределах от 0,01 мг до 1000 мг на кг (мг/кг) веса тела в день, или примерно от 0,1 мг/кг до 100 мг/кг, или примерно от 0,5 мг/кг до 20 мг/кг веса тела в день. Кроме того, эффективная дозировка может составлять 0,5 мг/кг, 1 мг/кг, 5 мг/кг, 10 мг/кг, 15 мг/кг, 20 мг/кг/ 25 мг/кг, 30 мг/кг, 35 мг/кг, 40 мг/кг, 45 мг/кг, 50 мг/кг, 55 мг/кг, 60 мг/кг, 70 мг/кг, 75 мг/кг, 80 мг/кг, 90 мг/кг, 100 мг/кг, 125 мг/кг, 150 мг/кг, 175 мг/кг, 200 мг/кг и может увеличиваться с шагом 25 мг/кг вплоть до 1000 мг/кг или может находиться в диапазоне между любыми двумя из указанных выше значений. В некоторых вариантах осуществления продукт цистеамина вводится в общей суточной дозе приблизительно от 0,25 г/м2 до 4,0 г/м2 площади поверхности тела, например, по меньшей мере около 0.5, 0.6, 0.7, 0.8, 0.9, 1.0, 1.1, 1.2, 1.3, 1.4, 1.5, 1.6, 1.7, 1.8, 1.9 или 2 г/м2, или примерно до 0.8, 0.9, 1.0, 1.1, 1.2, 1.3, 1.4, 1.5, 1.6, 1.7, 1.8, 1.9, 2.0, 2.2, 2.5, 2.7, 3.0, или 3.5 г/м2. В некоторых вариантах осуществления продукт цистеамина вводится в общей суточной дозе примерно от 0,5 до 2,0 г/м2 площади поверхности тела, 1-1,5 г/м2 площади поверхности тела или 0,5-1 г/м2 площади поверхности тела, или около 0,7-0,8 г/м2 площади поверхности тела, или около 1,35 г/м2 площади поверхности тела. Соли или сложные эфиры одного и того же активного ингредиента могут варьировать по молекулярному весу в зависимости от типа и веса молекулы соли или сложного эфира. Для введения лекарственной формы, например, таблетки или капсулы или другой пероральной лекарственной формы, содержащей продукт цистеамина с энтеросолюбильным покрытием, используется общий вес в пределах приблизительно от 100 мг до 1000 мг. Лекарственная форма перорально вводится пациенту, страдающему, например, от (i) болезни, связанной с ненормальными или аномальными общими уровнями адипонектина, (ii) ненормальными или аномальными соотношениями HMW : MMW, HMW : LMW или MMW : LMW адипонектина, (iii) хронического ишемического риска или событий или (iv) острого ишемического повреждения (например, инсульта или другой сердечно-сосудистой болезни). Введение может продолжаться в течение нескольких часов, дней, недель, месяцев или лет в зависимости от болезни или нарушения (например, острого случая или хронической болезни).
Пригодные для введения композиции могут быть заключены в состав с веществами, усиливающими поглощение или абсорбцию, для увеличения их эффективности. Такие усилители включают, например, салицилат, гликохолят/линолеат, гликолят, апротинин, бацитрацин, SDS, капрат, железо и тому подобное. Смотри, например, Fix (J. Pharm. Sci., 85:1282-1285, 1996) и Oliyai and Stella (Ann. Rev. Pharmacol. Toxicol, 32: 521-544, 1993).
Продукт цистеамина с энтеросолюбильным покрытием может включать различные эксципиенты, как хорошо известно в области фармацевтики, при условии, что такие эксципиенты не оказывают дестабилизирующего воздействия на какие-либо компоненты в композиции. Таким образом, такие эксципиенты как связывающие вещества, объемообразующие вещества, разбавители, дезинтегрирующие вещества, смазывающие вещества, наполнители, носители и тому подобное могут быть объединены с продуктом цистеамина. Для твердых композиций, как правило, необходимы разбавители для увеличения объема таблетки, для того, чтобы обеспечить практичный размер для прессования. Подходящие разбавители включают дикальций фосфат, сульфат кальция, лактозу, целлюлозу, каолин, маннитол, хлорид натрия, сухой крахмал и порошкообразный сахар. Для придания составу для таблеток связующих свойств используются связующие вещества, и таким образом гарантировать, что таблетка остается интактной после прессования. Подходящие связывающие вещества включают, но не ограничиваются этим, крахмал (включая кукурузный крахмал и прежелатинизированный крахмал), желатин, сахара (включая сахарозу, глюкозу, декстрозу и лактозу), полиэтиленгликоль, воски и природные и синтетические камеди, например, гуммирарабик, альгинат натрия, поливинилпирролидон, полимеры на основе целлюлозы (включая гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, метилцеллюлозу, гидроксиэтилцеллюлозу и т.п.) и вигум (Veegum). Смазывающие вещества используются для облегчения производства таблеток; примеры подходящих смазывающих веществ включают, например, стеарат магния, стеарат кальция и стеариновую кислоту, и в большинстве случаев присутствуют в количестве не более чем около 1 весового процента относительно веса таблетки. Дезинтегрирующие вещества используются для облегчения распада таблетки после введения и представляют собой в большинстве случаев крахмалы, глины, целлюлозы, альгины, камеди или перекрестно-сшитые полимеры. При необходимости предназначенная для введения фармацевтическая композиция также может содержать минимальные количества вспомогательных веществ, таких как увлажняющие или эмульгирующие вещества, pH буферные вещества и тому подобные, например, ацетат натрия, сорбитанмонолаурат, триэтаноламин натрий ацетат, триэтаноламин олеат и тому подобное. При необходимости, также могут добавляться вкусовые, окрашивающие вещества и/или подсластители. Другие необязательные компоненты для включения в композицию, предназначенную для перорального приема, включают, но не ограничиваются этим, консервирующие вещества, суспендирующие вещества, загустители и тому подобное. Наполнители включают, например, нерастворимые вещества, такие как диоксид кремния, окись титана, окись алюминия, тальк, каолин, порошкообразную целлюлозу, микрокристаллическую целлюлозу и тому подобное, а также растворимые вещества, такие как маннитол, мочевину, сахарозу, лактозу, декстрозу, хлорид натрия, сорбит и тому подобное.
Фармацевтическая композиция также может содержать стабилизирующее средство, такое как гидроксипропилметилцеллюлоза или поливинилпирролидон, как раскрывается в патенте США №4,301,146. Другие стабилизирующие средства включают, но не ограничиваются этим, полимеры на основе целлюлозы, такие как гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, метилцеллюлоза, этилцеллюлоза, ацетат целлюлозы, ацетатфталат целлюлозы, ацетат-тримеллитат целлюлозы, фталат гидроксипропил метилцеллюлозы, микрокристаллическая целлюлоза и натрий карбоксиметилцеллюлоза; и виниловые полимеры и сополимеры, такие как поливинилацетат, поливинилацетат фталат, сополимер винилацетата и кротоновой кислоты и сополимеры этилена и винилацетата. Стабилизирующее средство присутствует в количестве, эффективном для обеспечения желательного стабилизирующего эффекта; как правило, это означает, что отношение продукта цистеамина к стабилизирующему средству составляет по меньшей мере примерно 1:500 масс./масс., в большинстве случаев около 1:99 масс./масс.
Таблетки могут изготавливаться сначала путем нанесения энтеросолюбильного покрытия на продукт цистеамина. В одном варианте осуществления способом получения таблеток является прямое прессование порошков, содержащих продукт цистеамина с энтеросолюбильным покрытием, необязательно в комбинации с разбавителями, связующими веществами, смазывающими веществами, разрыхлителями, красителями, стабилизирующими веществами или тому подобным. В различных вариантах осуществления таблетки изготавливают путем смешивания эксципиентов с продуктом цистеамина, прессованием таблеток и нанесением энтеросолюбильного покрытия. В качестве альтернативы прямому прессованию спрессованные таблетки можно изготовить с использованием процессов влажного гранулирования, сухого гранулирования или вальцевания. Кроме того, таблетки могут быть сформованы, а не спрессованы, начиная с влажного материала, содержащего подходящее водорастворимое смазывающее вещество.
В альтернативном варианте осуществления продукты цистеамина с энтеросолюбильным покрытием гранулируют, а гранулят спрессовывают в таблетки или заполняют им капсулы. Материалы для капсул могут быть твердыми или мягкими, как правило, капсулы герметически закупоривают, например, с помощью желатиновых полос или тому подобного. Таблетки и капсулы для перорального применения, как правило, включают один или более используемых обычно эксципиентов, как обсуждалось выше. В различных вариантах осуществления капсула представляет собой незапечатанную капсулу.
При введении лекарственной формы, т.е. таблетки или капсулы, содержащей продукт цистеамина с энтеросолюбильным покрытием, общий вес составляет приблизительно от 100 мг до 1000 мг. Лекарственная форма перорально вводится пациенту, страдающему от состояния, при котором, как правило, показан продукт цистеамина, включая, но не ограничиваясь этим, ишемические болезни и нарушения (например, серповидноклеточная анемия, острые ишемические события, инсульт, сердечный приступ и тому подобное).
Композиции продукта цистеамина раскрытия могут использоваться в комбинации с другими видами лечения, пригодными при лечении ишемических событий или болезни или нарушения, связанного с ненормальными уровнями или соотношениями адипонектина. Например, цистеамин может вводиться внутривенно в комбинации с тромболитическим средством, ловушкой свободных радикалов, спиновой ловушкой и т.п.
Комбинирование двух или более лекарственных средств с разными механизмами действия может обеспечить максимальную защиту от ишемического повреждения посредством аддитивных или синергетических эффектов или обеспечить дополнительную пользу за счет увеличения терапевтического окна для соединений или возможно за счет уменьшения побочных действий. Наряду с тем, что существует необходимость уменьшения последовательности активации ишемического каскада, необходимыми являются тромболитические препараты, так как они вызывают реканализацию. Это дает возможность не только реперфузии ишемической ткани, в том случае, когда инсульт является результатом тромбообразования или эмболии, но также обеспечивает улучшенный доступ небольших молекул, включая лекарственные средства и питательные вещества к периферическим отделам инфарктной ткани.
Способы и композиции по изобретению могут включать, в дополнение к продукту цистеамина, (1) антиоксидант; (2) тромболитическое средство, (3) антагонист NMDA рецептора и (4) спиновую ловушку; или (5) любую комбинацию вышеперечисленного.
Антиоксиданты включают, но не ограничиваются этим, нитроны (STAZN), полифенолы, флавонолы (например, байкалеин) и фенилпропаноиды (хлорогеновая кислота и физетин). Антиоксиданты используются в способах и композициях раскрытия в качестве нейропротекторов и для лечения ишемического повреждения в результате инсульта. В различных вариантах осуществления из числа антиоксидантов, комбинируемых с продуктом цистеамина, исключается N-ацетилцистеин.
Различные тромболитические средства, известные в данной области техники (например, тенектеплаза), также могут использоваться в способах или композициях изобретения в комбинации со спиновой ловушкой (например, NXY-059). В способах или композициях изобретения может использоваться целый ряд тромболитических средств. Примеры тромболитических средств, которые можно использовать в способах или композициях изобретения включают альтеплазу, тенектеплазу, ретеплазу, стрептазу, аббокиназу, памитеплазу, натеплазу, десмотеплазу, дутеплазу, монтеплазу, ретеплазу, ланотеплазу и Prolyse™). Другие тромболитические средства включают, например, микоплазмин, Bat-tPA, BB-10153 (разработанная форма человеческого плазминогена, активированного тромбином до плазмина) и активаторы плазминогена слюны Desmodus rotundus (DSPAs) (например, DSPAal).
Фенольные кислоты включают, например, кофеиновую кислоту, ванилин и кумаровую кислоту. Фенольные кислоты образуют разнотипную группу, включающую широко распространенные оксибензойную и гидроксикоричную кислоты. Соединения гидроксикоричной кислоты (p-кумаровая, кафеиновая, феруловая кислоты) чаще всего встречаются в виде простых эфиров с гидроксикарбоновыми кислотами или глюкозой, тогда как соединения оксибензойной кислоты (p-оксибензойная, галловая кислота, эллаговая кислота) присутствуют главным образом в форме глюкозидов. Во многих случаях фенольные кислоты встречаются в виде эфиров или гликозидов, конъюгированных с флавоноидами, спиртами, жирными гидроксикислотами, стеролами и глюкозидами.
Спиновые ловушки на основе нитрона, такие как NXY-059, и тромболитические средства, такие как тенектеплаза, в настоящее время разрабатываются для лечения острого ишемического инсульта (AIS), так как они являются двумя самыми многообещающими кандидатами в лекарственные средства.
Спиновые ловушки, такие как нитроксиды и нитроны, являются стабилизированными формами оксида азота, биологического посредника. В отличие от других антиоксидантов, спиновые ловушки не действуют как прооксиданты, и не распространяют свободнорадикальные цепные реакции. Более того, эти вещества ингибируют реакцию образования пероксинитрита из супероксида и оксида азота. Таким образом, комбинированная терапия с применением спиновых ловушек и терапевтических средств, разрабатываемая или используемая в настоящее время для лечения таких болезней и нарушений, как паркинсонизм, инсульт, ишемическое повреждение, сердечный приступ и старческая деменция, рассматривается изобретением.
Спиновые ловушки на основе нитрона и нитрозосоединений являются коммерчески доступными. Типичные спиновые ловушки на основе нитрона и нитрозо соединений включают динатрий 2,4-дисульфофенил-N-трет-бутилнитрон (NXY-059), N-t-бутил-α-фенилнитрон, 3,5-дибром-4-нитрозобензолсульфоновую кислоту, 5,5-диметил-1-пирролин N-оксид, 2-метил-2-нитрозопропан, нитрозодисульфоновую кислоту, α-(4-пиридил-1-оксид)-N-t-бутилнитрон, 3,3,5,5-тетраметилпирролин N-оксид, 2,4,6-три-t-бутилнитрозобензол, PTIYO (4-фенил-2,2,5,5-тетраметил имидазолин-1-илокси-5-оксид) и темпол (4-гидрокси 2,2,6,6-тетраметилпиперидин-1-оксил) и тому подобное.
В другом аспекте изобретения предоставляются способы и композиции, содержащие антагонисты NMDA (N-метил-D-аспартат) рецепторов, которые в комбинации с тромболитическим средством, улучшают поведенческую активность. Примеры антагонистов NMDA-рецепторов включают 3-альфа-ол-5-бета-прегнан-20-он гемисукцинат, кетамин, мемантин, декстрометорфан, декстрорфан и декстрометорфан гидробромид. Производные и аналоги пиперидина, замещенные фенолами или эквивалентами фенолов, обладающими NR2B селективной активностью NMDA антагониста, описаны в международных патентных заявках №WO 90/14087, WO 90/14088, WO 97/23202, WO 97/23214, WO 97/23215, WO 97/23216, WO 97/23458, WO 99/21539, WO 00/25109, Европейской патентной заявке № EP 648744 A1 и патенте США №5,436,255. Соединения, содержащие подструктуру 2-бензоксазолинона со сходной биологической активностью, описаны в международных патентных заявках WO 98/18793 и WO 00/00197. Другие NR2B селективные NMDA-антагонисты, имеющие конденсированные гетероциклические структуры, описаны в международных патентных заявках №WO 01/30330, WO 01/32171, WO 01/32174, WO 01/32177, WO 01/32179, 01/32615, WO 01/32634.
Определение эффективности отдельного лечения, включающего продукт цистеамина отдельно или в комбинации с одним или более дополнительными средствами, может проводиться на модели эмболического инсульта, которая позволяет контролировать поведенческие ожидаемые результаты и дает возможность сравнения эффективности соединения(ий). Также, кроме контролирования поведенческих результатов, могут использоваться гистохимические методы для количественной оценки ожидаемых результатов и патологии.
Кроме того, эффективность метода или композиции изобретения также может быть оценена путем измерения уровней адипонектина и/или соотношений различных мультимеров адипонектина. В дополнение к этому, эффективность может быть оценена путем клинических наблюдений, проведения диагностической проверки и тому подобного, что служит признаком повреждения ткани в результате ишемического повреждения. Подбор дозировки и лечения может осуществляться медицинским работником в зависимости, например, от тяжести ишемического события или болезни или нарушения, связанного с нарушенными или ненормальными уровнями адипонектина.
Для оценки эффективности лечения по изобретению могут использоваться некоторые животные модели ишемического повреждения. Например, эндотелии-1 представляет собой сильный вазоконстриктор (сосудосуживающее средство), который вырабатывается эндогенно во время ишемического инсульта и способствует общей потере клеток и потере трудоспособности. Экзогенный эндотелии-1 также может использоваться для индуцирования инсульта и гибели клетки после длительной вазоконстрикции (сужения сосудов) в сочетании с реперфузией. Его микроинъекция вызывает фокальный инсульт в небольших объемах ткани (например, сером веществе коры мозга, белом веществе или подкорковой ткани) или после инъекции около средней мозговой артерии. Его часто используют в качестве модели фокального инсульта с целью оценки возможного кандидата для про-регенеративной терапии. Одно преимущество этой модели инсульта заключается в том, что он вызывает инфаркты с высокой воспроизводимостью и очень низкой смертностью.
На другой животной модели ишемического инсульта закупорка средней мозговой артерии (MCA) осуществляется путем введения частиц, подобных сгусткам крови (тромбоэмболическая MCAO), или искусственных сфер в сонную артерию животных. Тромбоэмболическая MCAO достигается путем введения сгустков, которые были образованы in vitro или путем внутрисосудистой инсталляции тромбина для тромбообразования in situ. Тромбоэмболическая модель является ближайшей к патофизиологии кардиоэмболического инсульта у человека. При введении сфер в мозговое кровообращение их размер определяет образец инфаркта головного мозга: макросферы (300-400 мкм) вызывают инфаркты, подобные тем, которые вызывает закупорка проксимальной МСА, тогда как инъекция микросфер (~50 мкм) дает в результате дистальную, диффузную эмболию. Однако качество МСАО (и таким образом объем инфарктов мозга) является очень непостоянным, явление, которое дополнительно усиливается определенной скоростью спонтанного лизиса введенных сгустков крови.
В другой животной модели ишемического инсульта МСА рассекается хирургическим путем и в дальнейшем необратимо закупоривается, например, с помощью электрокаутеризации (метод прижигания ткани) или лигирования (перевязки). Окклюзия (закупорка) может осуществляться на проксимальном или дистальном участке МСА. В последнем случае ишемическое повреждение ограничивается корой головного мозга. МСАО может быть объединена с временной или постоянной закупоркой общей сонной артерии. Эти модели требуют небольшой краниотомии (трепанации черепа).
Может быть использована транзиторная (временная) транскраниальная МСАО модель, которая похожа на необратимую постоянную транскраниальную МСАО, при этом имеется реперфузия МСА после определенного периода фокальной церебральной ишемии. Подобно постоянной МСАО, требуется краниотомия и может быть присоединена общая закупорка сонной артерии (ССА). Закупорка одной МСА и обеих ССА называется моделью фокальной ишемии головного мозга, вызванной окклюзией трех сосудов.
Продукты цистеамина можно оценить в отношении их использования в любой из приведенных выше животных моделей путем введения терапевтического средства до, во время или после того, как вызвано ишемическое повреждение. Эффективность терапии можно оценить с помощью гистологии или путем оценки расстройств поведения по сравнению с контролем, не получавшим продукта цистеамина.
В других вариантах осуществления способы по изобретению могут быть оценены путем выделения адипоцитов и инкубирования адипоцитов с или без продуктов цистеамина. Продукт цистеамина может контактировать с адипоцитами в различных дозировках. Эффективность может быть оценена путем измерения изменения уровней адипонектина или мультимеров в культуре клеток, при этом увеличение адипонектина или изменение соотношения мультимеров адипонектина указывает на вещество, оказывающее влияние на уровни адипонектина.
Следующие примеры предназначаются для дополнительной иллюстрации изобретения, а не для ограничения вышеизложенного раскрытия и сопутствующих пунктов формулы изобретения.
Примеры
Капсулы цистеамина битартрата (Mylan Pharma, VA) были покрыты энтеросолюбильным покрытием компанией The Coating Place Inc. (Verona, WI) с помощью прибора Model 600 Wurster unit.
Пример 1
Образцы биопсии жировой ткани (AT) обрабатывали коллагеназой в течение 1 часа при 37°C во вращающейся водяной бане. Затем обработанную AT профильтровали через нейлоновое сито с размером ячейки 425 мкм для отделения жировых клеток. Выделенные жировые клетки (FC) дважды промыли физиологическим солевым буфером (Phillips 2008), профильтровали и снова дважды промыли. FC центрифугировали при 50×g с целью концентрирования. 1 мл FC ресуспендировали в 9 мл определенной культуральной среды (Phillips 2008) и дали возможность FC восстановиться × 10 час в течение ночи при 37°C.
Адипоциты выделяли и давали возможность восстановиться в течение ночи, затем культивировали с или без цистеамина 90 мкМ, а среду собирали в определенные моменты времени (45, 90, 180, 24 час). Проводили вестерн-блоттинг 20 мкл среды с использованием невосстанавливающего 5X загрузочного буфера. Делали блоты, блокировали и инкубировали с первичными антителами (анти-адипонектин мышиные моноклональные при разведении 1:500 в течение ночи). Блот промывали и инкубировали с вторичными антителами (козьи анти-мышиные IR 800) и измеряли оптическую плотность с помощью денситометра LICOR (смотри фигуру 1).
Для определения зависимости от времени эффектов цистеамина на адипонектин, среду заменяли и FC ресуспендировали в 9 мл определенной среды ±90 мкМ цистеамина. Содержание FC и секрецию адипонектина в среду оценивали в двух экземплярах в культуре через 0, 45, 90, 180 минут и 24 часа. Для анализа содержания FC, изолированные FC были получены, как описано ранее (Phillips, 2008). Белки выделяли, используя невосстанавливающий SDS PAGE электрофорез без термической денатурации, и переносили на нитроцеллюлозу для проведения иммуноблотинга с применением 1:500 первичных моноклональных анти-адипонектин антител (BD Transduction Laboratories) и 1:20,000 LiCOR Odyssey вторичных антител. Обнаружение сигнала и количественный анализ проводили с помощью прибора LiCOR Odyssey Machine (LiCOR, Lincoln, Небраска). Содержание мультимеров адипонектина в клетке определяли делением AU для мультимера на общую AU на образец. Содержание мультимеров в кондиционированной среде определяли, как и в случае содержания в клетке, затем этот процент умножали на общий адипонектин в среде, определенный методом ELISA (Millipore Billerica, Массачусетс).
Пример 2
В исследование было включено одиннадцать детей ≥10-летнего возраста, с подтвержденной биопсией NAFLD и уровнем аланин аминотрансферазы (ALT)≥60 IU/л. Диагноз был установлен впервые, или они не получали специфической терапии в отношении NAFLD, такой как витамин Е или инсулин-сенсибилизирующие лекарственные средства по меньшей мере в течение 3 месяцев до начала исследования. Все пациенты были подвергнуты стандартному изменению образа жизни, включая диету и комплекс упражнений в течение более чем 3 месяцев. Основным критерием эффективности исследования была нормализация (≤40 IU/л) или ≥50% уменьшение исходного ALT в сыворотке на 24 неделе терапии EC-цистеамином; эти субъекты считались ответившими на лечение.
Субъектов лечили в течение 24 недель и контролировали в течение 24 недель после прекращения лечения. Средняя доза принятого внутрь EC-цистеамина составляла 654 мг два раза в день или 15,2 мг/кг/день (средняя доза 900 мг) в течение 24 недель.
Во время пилотного исследования кровь отбирали с предварительно установленными интервалами. Сыворотку хранили при -80°C до исследования. Достаточные объемы сыворотки были отобраны у 10 из 11 субъектов с NAFLD и только до 16 недель после обработки.
Уровни общего адипонектина и мультимеров измеряли в сыворотке, полученной от: (1) субъекта с NAFLD, собранной на 0 и 24 неделе лечения цистеамином и повторно через 16 недель после прекращения лечения (т.е. на 40 неделе); (2) подвергнутых предварительной обработке на 0 неделе субъектов с NAFLD и взрослых без NAFLD при комнатной температуре и при 37°C, а также после инкубации с цистеамином 90 мкМ в течение 1 часа при 37°C; и (3) подвергнутых предварительной обработке на 0 неделе субъектов с NAFLD до и после инкубации с цистеамином при различных концентрациях (15, 30, 45, 60, 90, 120 мкМ) в течение 1 часа при 37°C для установления дозозависимого эффекта.
Электрофорез в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE) проводили согласно стандартному методу Лэмли. Буфер для образца для невосстанавливающих условий денатурации без нагревания содержал 3% SDS; 50 ммоль/л Трис-HCL, pH 6,8 и 20% глицерин. Белки были разделены с помощью 3-8% Трис-ацетатных гелей (Invitrogen, Carlsbad, Калифорния) с использованием трис-ацетатного подвижного буфера согласно инструкции производителя. Для иммуноблотинга белки переносили на нитроцеллюлозные мембраны. Мембраны промывали Твином (Трис-буферизированный физраствор, 0,1% Тритон-X-100) и инкубировали с моноклональными антителами (1:500 BD Transduction Laboratories, San Diego, Калифорния). После промывки Трис-буферизированным раствором с 0,1% Твином (4×5 мин) мембраны инкубировали с вторичными антителами L-COR (LI-COR Biotechnology, Lincoln, Небраска) при разведении 1:20000. Мультимеры адипонектина обнаруживали и количественно определяли с помощью устройства для визуализации LICOR и программного обеспечения для анализа. Относительное распределение мультимеров адипонектина определяли путем деления плотности полосы на общую плотность (клеточный адипонектин) или общий адипонектин, определенный с помощью ELISA (Millipore, Billerica, MA). Затем процент мультимера адипонектина был умножен на общий уровень адипонектина для вычисления абсолютного значения олигомера.
В другом эксперименте 25 мкл общего объема образца (5 мкл разведенной сыворотки + 15 мкл воды + 5 мкл 5X LB) инкубировали с или без цистеамина при 37°C × 1 час. Контроль приготавливали без цистеамина и инкубировали при комнатной температуре в течение 1 часа on the bench. Затем препараты «прогоняли» на 2 × 15-ячеечных 1,5 мм 3-8% трис-ацетатных гелях. Первичные антитела - мышиные анти-адипонектин 1:500, в течение ночи при 4°C и вторичные антитела - козьи анти-мышь IR800 1:20000.
Была проанализирована сыворотка, полученная от 10 субъектов в исходный момент времени и через 24 недели лечения цистеамином и повторно через 16 недель после окончания лечения (т.е. на 40 неделе после включения в исследование). Семь из 10 субъектов ответили на лечение. У трех субъектов наблюдалось уменьшение уровней AST/ALT, но не достигало ожидаемого результата исследования. По сравнению с исходным не наблюдалось значительного изменения в средних измерениях BMI на 24 неделе (P=.47) или на 40 неделе (P=.43). У всех исследованных субъектов наблюдалось уменьшение среднего ALT от исходного (123 IU/л) на 24 неделе (55 UI/л, P=.003) на 40 неделе (71 IU/L, P=0,055). Наблюдалось уменьшение среднего AST от исходного (60,9 IU/л) на 24 неделе (32 IU/л, P=0,001), и на 40 неделе (35 IU/л, P=0,012). У ответивших пациентов средние уровни лептина составляли 21,3; 15,7 и 19,5 нг/мл, соответственно, при этом наблюдалось значимое уменьшение между временными точками 0 и 24 неделя (P=0,04) (фигура 2В).
Здоровые субъекты - 1 час 90 мкМ цистеамина. Уровни HMW не были изменены по сравнению с исходными. Аналогично субъектам с NAFLD, был определен средний процент увеличения уровней LMW (P<0,005), а также средний процент уменьшения уровней MMW (P<0,01) по сравнению с исходным (фигура 7). Средний процент общего уровня адипонектина, который включал мультимеры HMW, MMW, LMW, изменялся от 42,9%, 46,0% и 11,1% соответственно до 42,7%, 39,3% и 18,0% соответственно после инкубации с цистеамином.
Чтобы определить пороговую дозу цистеамина, вызывающую уменьшение мультимеров адипонектина в сыворотке, собирали сыворотку и инкубировали с различными концентрациями цистеамина. Шесть микролитров разведенной GB сыворотки инкубировали с 24 мкл воды и разными концентрациями цистеамина. Образцы инкубировали в инкубаторе для культуры тканей в течение 1 часа при 37°C, при этом в контрольную пробирку не был добавлен цистеамин. Затем к каждой пробирке добавили 5 мкл 5X невосстанавливающего загрузочного буфера. Образцы перемешивали на вортексе и загружали в 3-8% трис-ацетатный гель и «пропускали» в течение 75 минут при постоянном токе 125 V. Гель переносили и блокировали. Затем блот инкубировали в течение ночи с анти-адипонектин антителами 1:500 в 3% BSA/TBS. Блот промывали и инкубировали с вторичными анти-мышиными антителами в течение 1 часа. Определение оптической плотности проводили на приборе LICOR. Проводили количественный анализ результатов, которые представлены на фигурах 8-9.
Мультимеры адипонектина-24 недели введения EC-цистеамина. У всех субъектов после 24 недель лечения битартратом цистеамина средний процент увеличения HMW, MMW, LMW и общего адипонектина от исходного составил 53% (P=0,02), 19% (P=0,02), 29.4% (P=0,03) и 49,3% (P=0,05) соответственно (фигуры 3 и 5). Между концом лечения на 24-неделе и временной точкой на 40-неделе наблюдался значимый средний процент уменьшения HMW (P=0,02), MMW (P=0,01), LMW (P=0,009) и общего адипонектина (P=0,01). Во временной точке 40 недель уровни всех мультимеров адипонектина составляли в пределах 2% исходного. Это не повторяло тенденцию средних уровней ALT и AST, которые не возвращались к исходным уровням на 40 неделе. Общие уровни адипонектина увеличивались от 0 недели на 49,3% на 24 неделе (P=0,05) и уменьшались с 24 недели к исходным уровням на 40 неделе (P=0,01). Несмотря на то, что уровни всех форм мультимеров увеличивались после 24 недель лечения цистеамином, относительные доли мультимеров адипонектина были значимо увеличены только для HMW (12,2%-14,9%, P=0,02), уменьшены для MMW (73,7%-70,3%, P=0,03) и оставались неизмененными для LMW (14,1%-14,8%). У 7 субъектов с NAFLD, которые отвечали на лечение, средний процент изменения для HMW, MMW, LMW и общего адипонектина на 24 неделе увеличился от исходного на 87,7%, 13,7%, 33,9% и 57,5% соответственно.
Мультимеры адипонектина - 1 час цистеамина. Не отмечалось различия между уровнями мультимеров адипонектина до обработки при комнатной температуре и 37°C (фигура 4). Инкубирование с цистеамином в течение 1 часа при 37°C приводило к среднему процентному увеличению уровней LMW (P<0,0001) и также среднему процентному уменьшению уровней MMW (P<0,0001) по сравнению с уровнями до обработки. Уровни HMW не были изменены по сравнению с исходными. Средний процент общего уровня адипонектина, который состоял из мультимеров HMW, MMW и LMW, изменялся от 8,2%, 63,3% и 28,5% соответственно до 8,6%, 54,7% и 36,7% соответственно после инкубации с цистеамином. Смотри фигуру 13.
Дозозависимый профиль. Уровни HMW повышались примерно на 10% выше исходного, когда сыворотку инкубировали при концентрациях цистеамина 15, 30, 45 и 60 мкМ. Уровни MMW были ниже, чем исходные при всех концентрациях цистеамина. Средние уровни LMW повышались на >60% выше исходного после обработки цистеамином при всех использованных концентрациях (фигура 11). Самый большой процент увеличения LMW (77%) был достигнут при концентрации цистеамина 120 мкМ, и это совпадало с уменьшением уровней HMW и MMW ниже исходного.
Пример 3
Вышеизложенные данные показывают, что цистеамин имел два эффекта на мультимеризацию адипонектина, (1) эффект in vivo - после ежедневного лечения у людей будут повышаться уровни всех мультиморов адипонектина, и (2) эффект in vitro - быстрое и значимое повышение LMW адипонектина в сыворотке человека, подвергнутой воздействию 90 мкМ цистеамина в течение 1 часа. На сегодняшний день существует только ограниченное число лекарственных средств, увеличивающих циркулирующие (находящиеся в кровотоке) уровни адипонектина, но ни одно из них не изменяет распределение мультимеров адипонектина.
Предыдущее исследование на нокаутных по адипонектину мышах, которые подвергались ишемии/реперфузии, показало, что животные, которые получили рекомбинантный адипонектин, имели менее значительное миокардиальное ишемическое повреждение, исходя из гистологии, с большим сохранением функции миокарда. Рекомбинантного адипонектина не имеется в наличии. Представленные выше данные показывают, что цистеамин быстро увеличивает уровни LMW адипонектина в сыворотке, полученной от людей с NAFLD, а также от здоровых взрослых (контролен). Кроме того, известно, что цистеамин является сильным антиоксидантом, а также показано, что он стимулирует глутатион, захватывает активные формы кислорода, ингибирует активность тканевой трансглутаминазы, а также обладает радиозащитными свойствами.
Для изучения лечения цистеамином ишемического повреждения было проведено исследование на мышах (C57BL/6-самцы-12 недель, 25 г), которых предварительно обрабатывали или никогда не обрабатывали цистеамином битартратом, как описано далее.
Предварительно обработанные животные получали внутрибрюшинно цистеамин, 60 мг/кг дважды (120 мг/кг/день) за 2 часа до хирургического лигирования LAD артерии. После периода лигирования в течение 60 минут нарушение проходимости устраняли и сразу давали другую дозу цистеамина в момент реперфузии, а также два раза в день в виде инъекций в течение 4 дней после реперфузии. Контрольная группа получила те же самые объемы контрольного раствора, введенного IV вместо цистеамина. Соответствующие объемы крови были собраны в начальной точке и в заранее установленные временные точки после ишемического инсульта, для того, чтобы определить уровни суррогатных маркеров воспаления и цистеамина в плазме. Электрокардиография/гемодинамические исследования животных проводились непосредственно после IR, и через 3 дня после IR. До умерщвления была снята закупорка LAD, и введен краситель синий Эвана через JVC для того, чтобы установить очертания площади, не затронутой ишемией. Миокардиальную ткань окрашивали 2,3,5 трифенилтетразолий хлоридом (для установления различия между метаболически активной и неактивной или инфарктной тканью), H&E, а также проводили TUNEL-окрашивание. Электрокардиография предоставляла показания объема желудочка, а также пристеночной функции. Исследования гемодинамики предоставили результаты сократительной способности мышцы (а именно, систолические данные).
Было исследовано семь мышей. Четыре получали контрольный раствор и 3 получали цистеамин. Средний исходный вес контрольных мышей составлял 25,8 г (в пределах 25-27 г) и конечный вес 22,5 г (21-24 г). Уменьшение составило 13%. Животные были вялыми после торакотомии и плохо ели.
Мыши, получавшие цистеамин, имели средний исходный вес 21,3 г (в пределах 21-22 г) и конечный вес 18,3 г (18-19 г). Уменьшение составило 14%. Животные были вялыми после торакотомии и плохо ели.
Животные получали регулярные болюсы физраствора подкожно после хирургического вмешательства, и все же могли быть частично обезвожены во время гемодинамических/эхо-исследований. Однако обе группы подвергались одинаковому воздействию. Обезвоживание может влиять на гемодинамические/эхо-исследования, уменьшая объем и функцию.
Ишемическое повреждение. Между группой с цистеамином и контрольной группой наблюдалось значительное уменьшение площади инфаркта (IA) относительно площади с повышенным риском (AAR) (т.е. IA/AAR) (p=0,004), и отношения IA/LV (левый желудочек) (p=0,008). Относительные количества ишемического повреждения составляли около половины при лечении цистеамином по сравнению с контрольными группами (смотри, например, фиг. 14A-B; первичные данные в таблицах A-B).
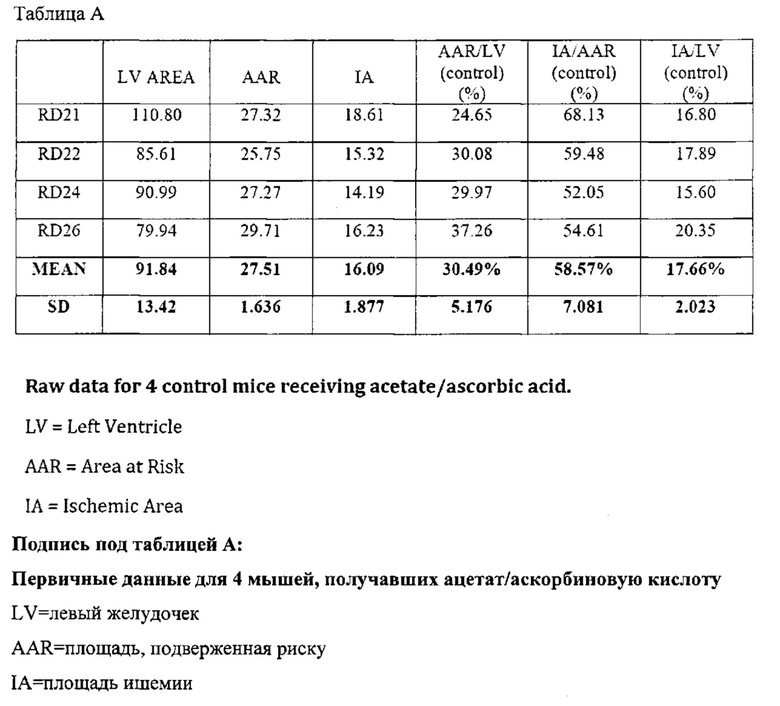
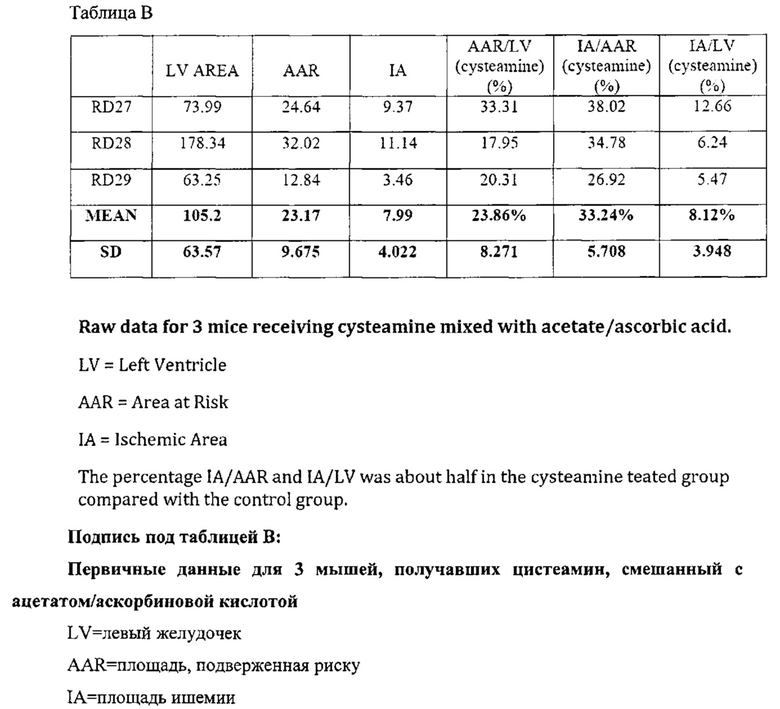
Процент IA/AAR и IA/LV составлял около половины в группе, получавшей цистеамин, по сравнению с контрольной группой.
Конечно-диастолический объем (EDV). Увеличение EDV после MI будет означать дилатацию желудочка вследствие ишемического повреждения. Интервал уменьшения (между 24 и 72 час) был бы желателен. Не наблюдалось значимого различия между средним EDV, измеренным на 24 часа и 72 часа, в контрольной группе (p=0,59). Однако наблюдалось значимое различие между средним EDV, измеренным на 24 часа и 72 часа, в группе с цистеамином (p=0,032) (смотри, например, фиг. 15A-B).
Процентное изменение EDV. Чтобы сравнить EDV в двух группах был вычислен процент изменения действительного объема желудочка (мкл) с момента времени 24 часа для каждой из двух групп. В группе, леченой цистеамином, имелось значительно большее процентное уменьшение EDV (по сравнению с 24 час) во временной точке 72 часа по сравнению с контрольной группой (p=0,04) (смотри фиг. 16).
Конечно-систолический объем (ESV). Увеличение ESV после MI будет означать уменьшение сократимости желудочка. Наблюдалось значимое различие между средним ESV, измеренным на 24 часа и 72 часа в контрольной группе (p=0,01) и группе с цистеамином (p=0,025) (смотри например, фиг. 17A-B).
Процентное изменение ESV. Чтобы сравнить ESV в двух группах, было сравнено процентное изменение действительного объема желудочка от временной точки 24 часа для каждой из двух групп. В группе, леченой цистеамином, имелось значительно большее процентное уменьшение ESV во временной точке 72 часа по сравнению с контрольной группой (p=0,039) (смотри, например, фиг. 18).
Приведенные выше примеры приводятся для того, чтобы предоставить специалистам в данной области техники раскрытие и описание того, как осуществить и использовать варианты осуществления способов, вариантов лечения и композиций изобретения, при этом примеры не предназначаются для ограничения рамок того, что изобретатели рассматривают как свое изобретение. Модификации описанных выше способов осуществления изобретения, которые понятны специалистам в данной области техники, включаются в рамки приведенных далее пунктов формулы изобретения. Все патенты и публикации, упомянутые в подробном описании, показывают специалистам уровень области техники, к которой относится изобретение. Все ссылки, приведенные в этом раскрытии, включаются путем отсылки в равной мере, как в том случае, когда каждая ссылка полностью включается путем отсылки.
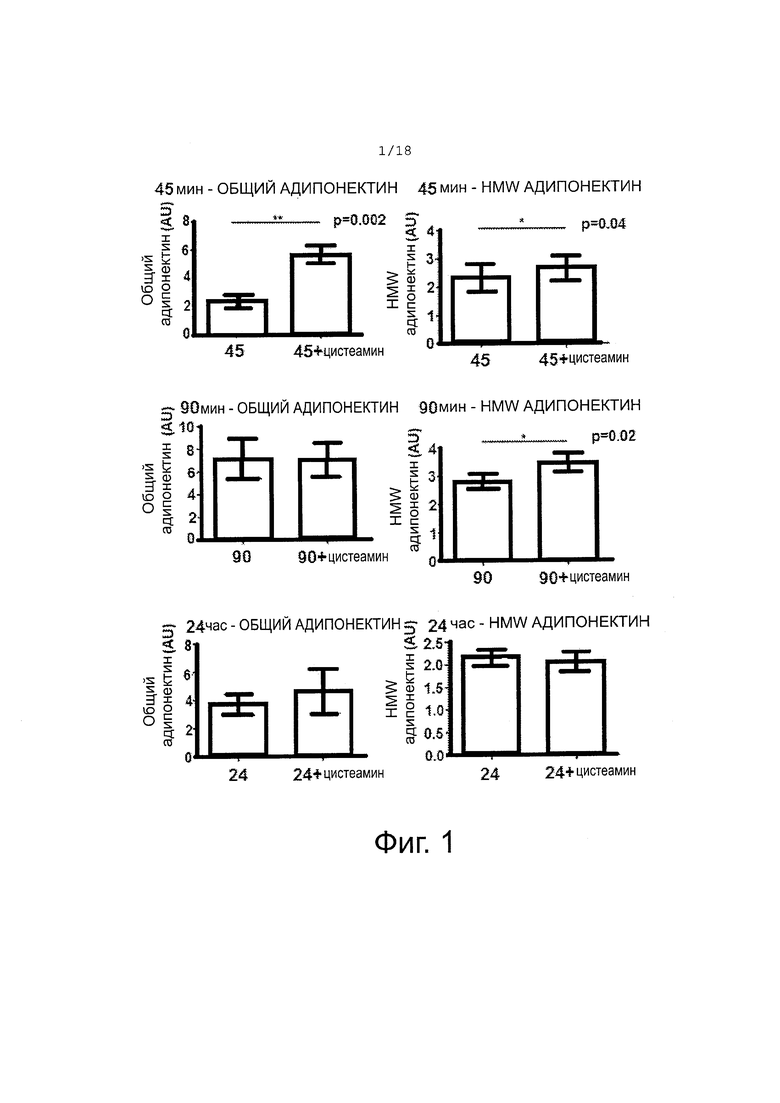
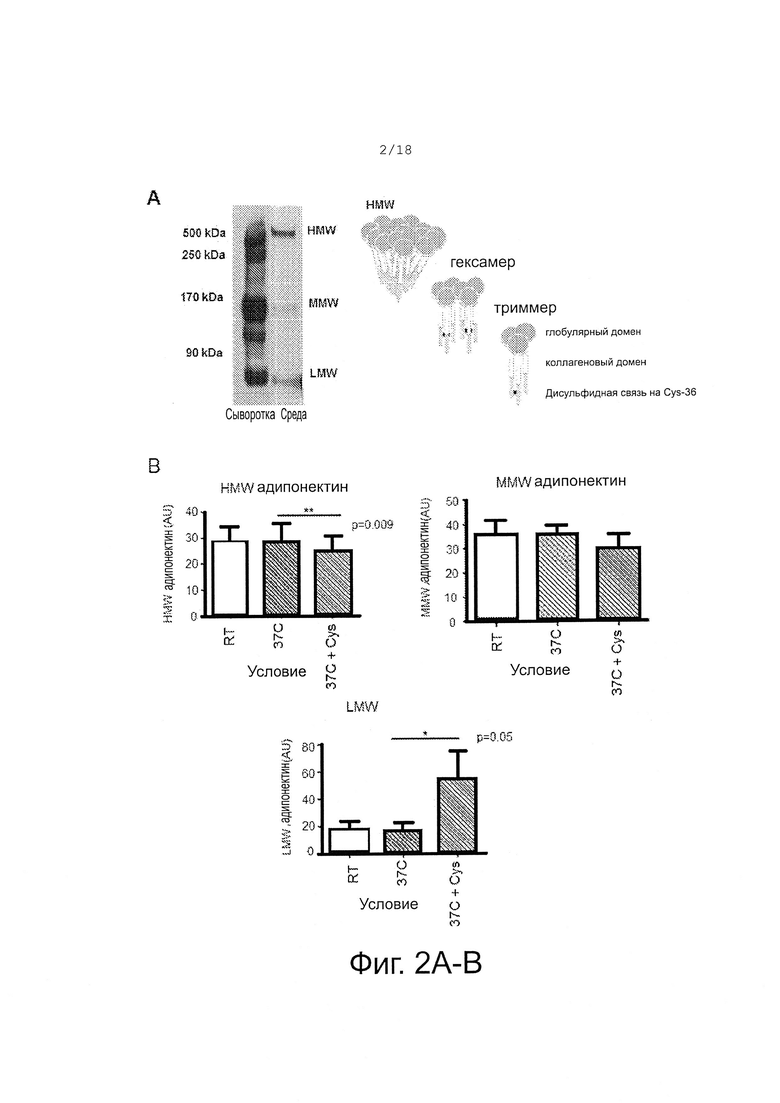
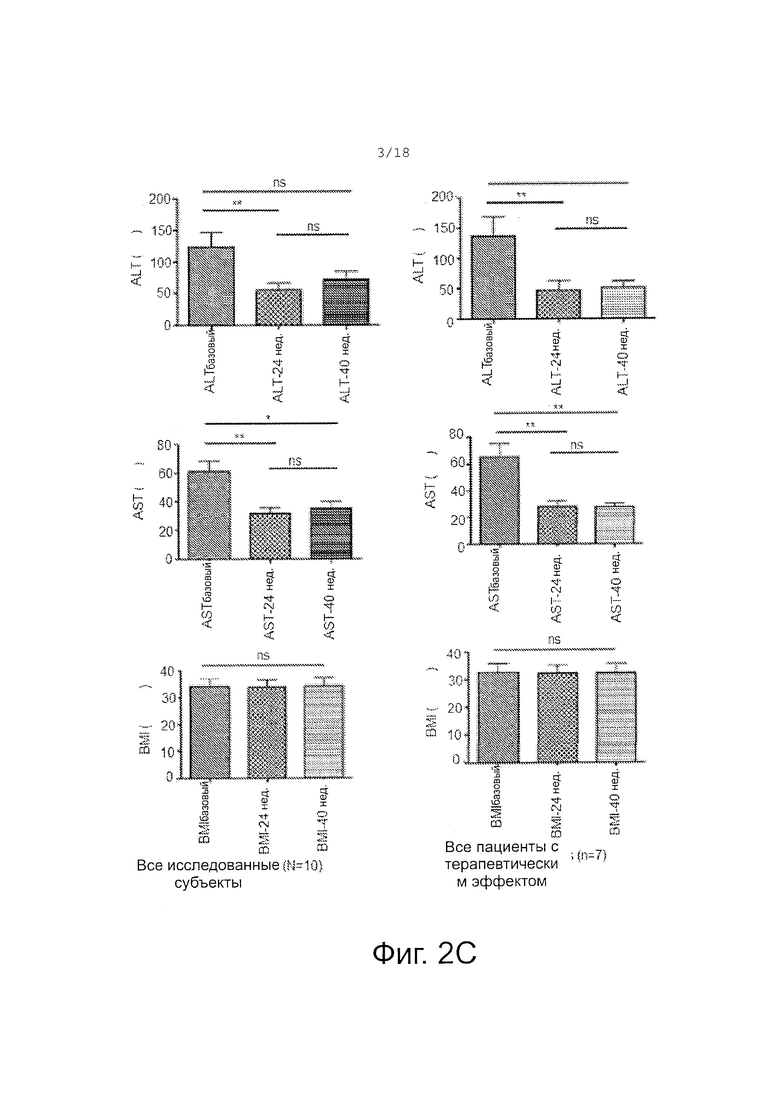
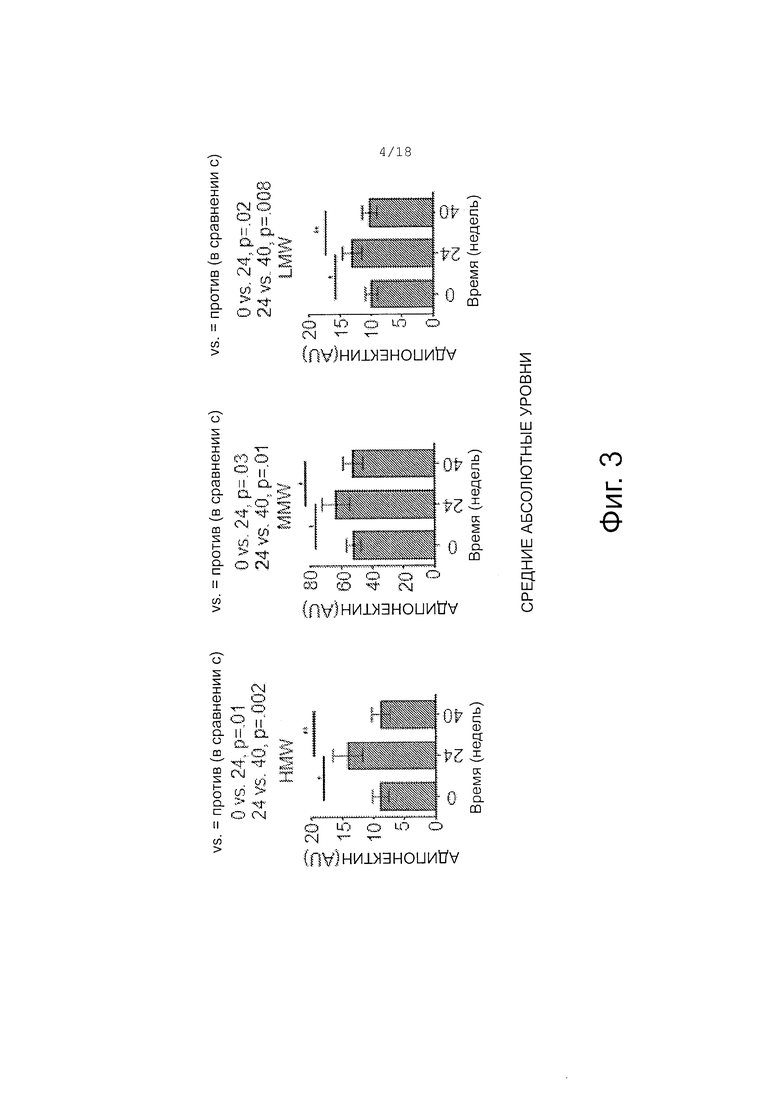
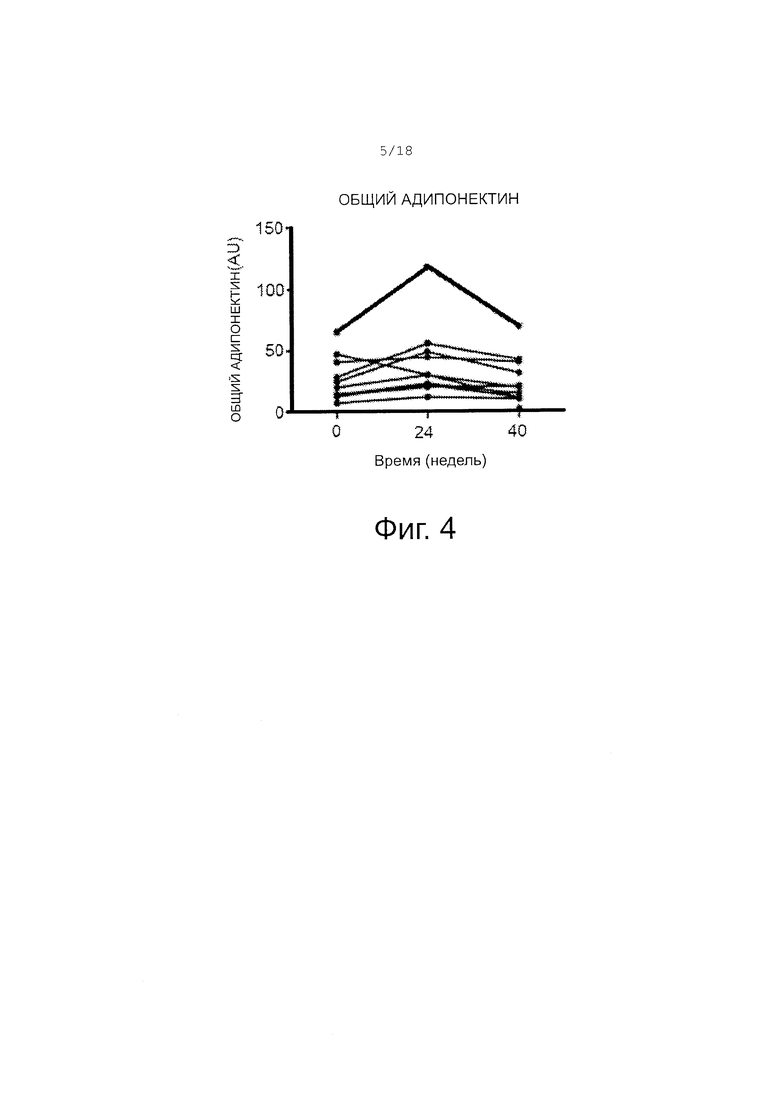
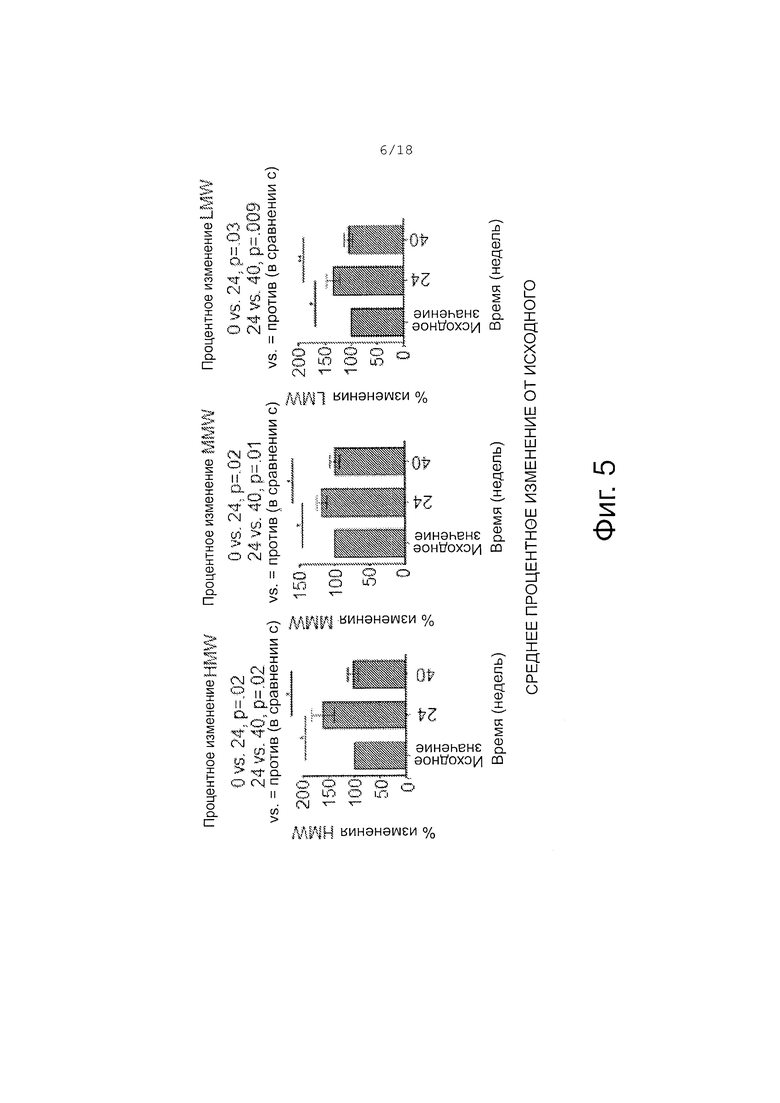
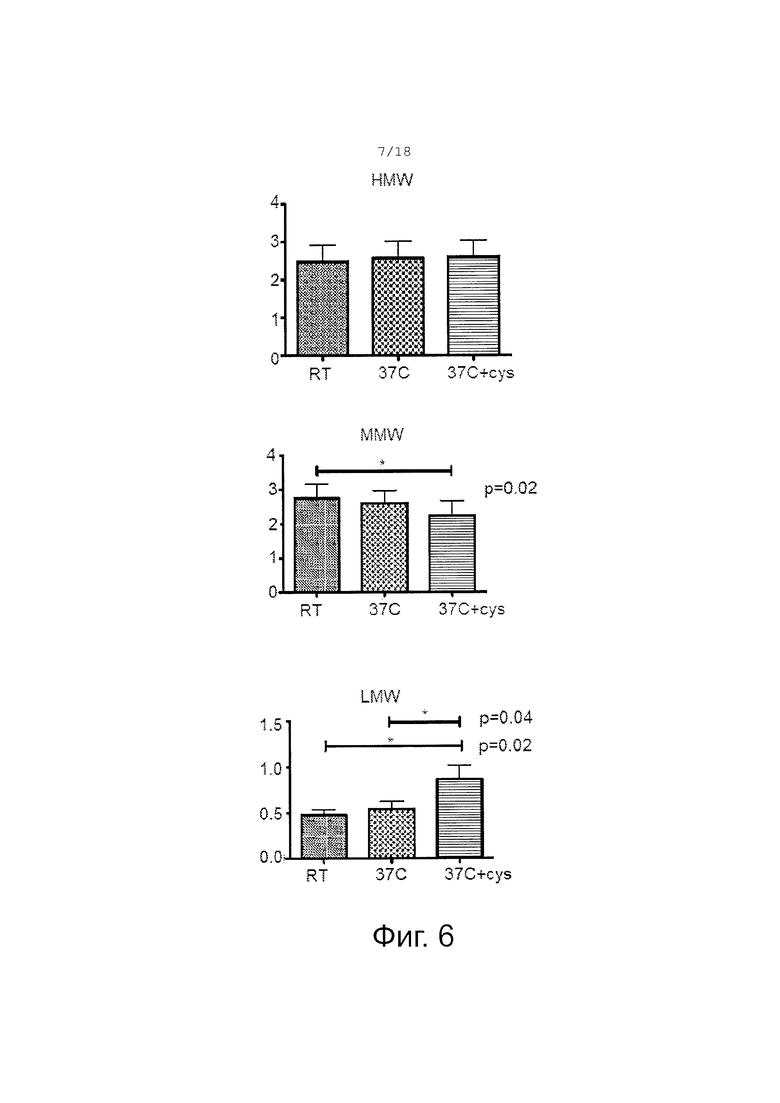
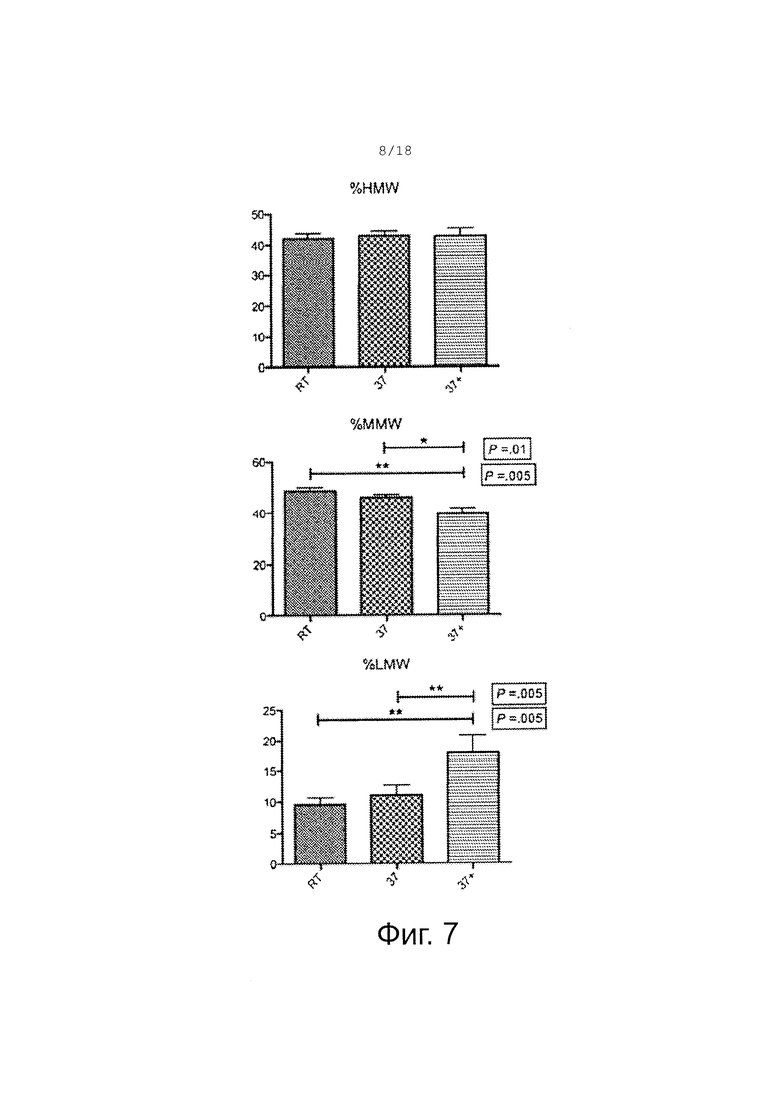
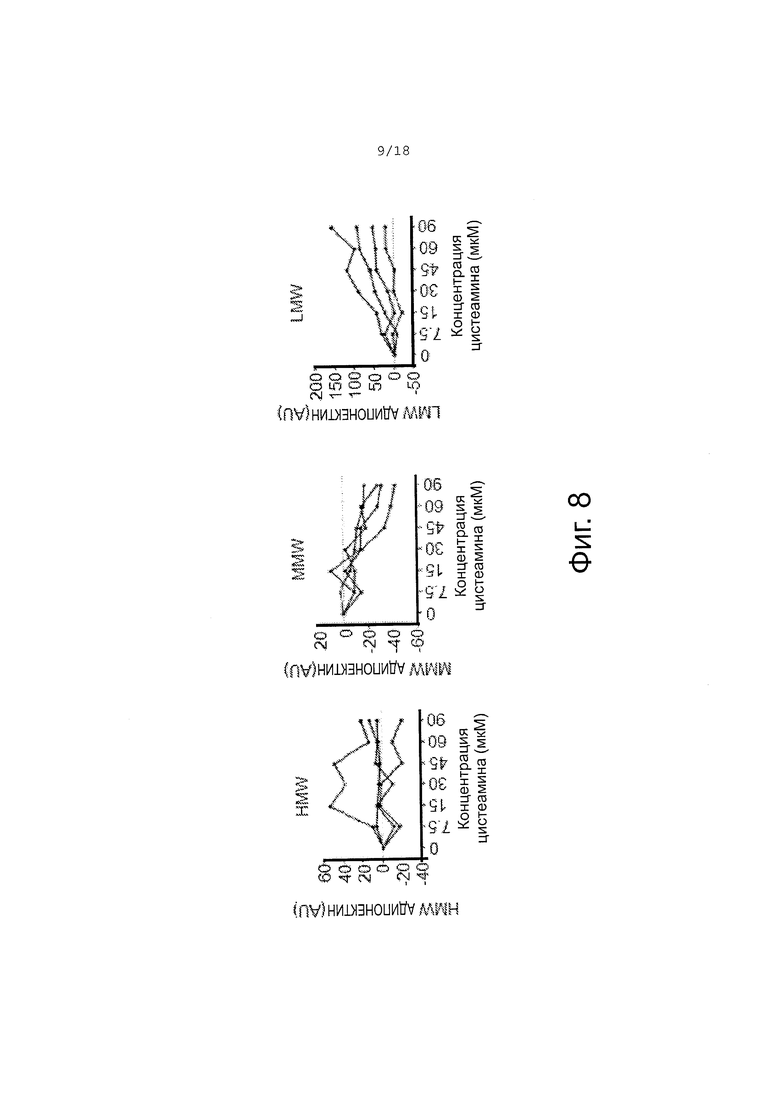
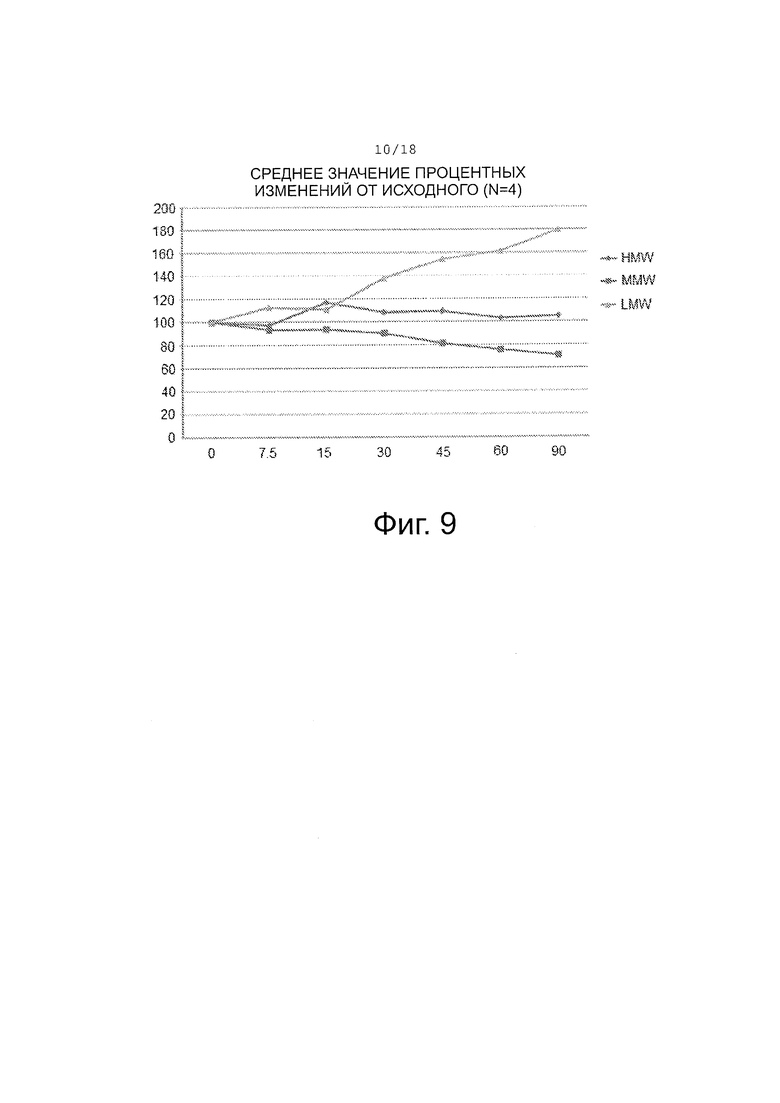
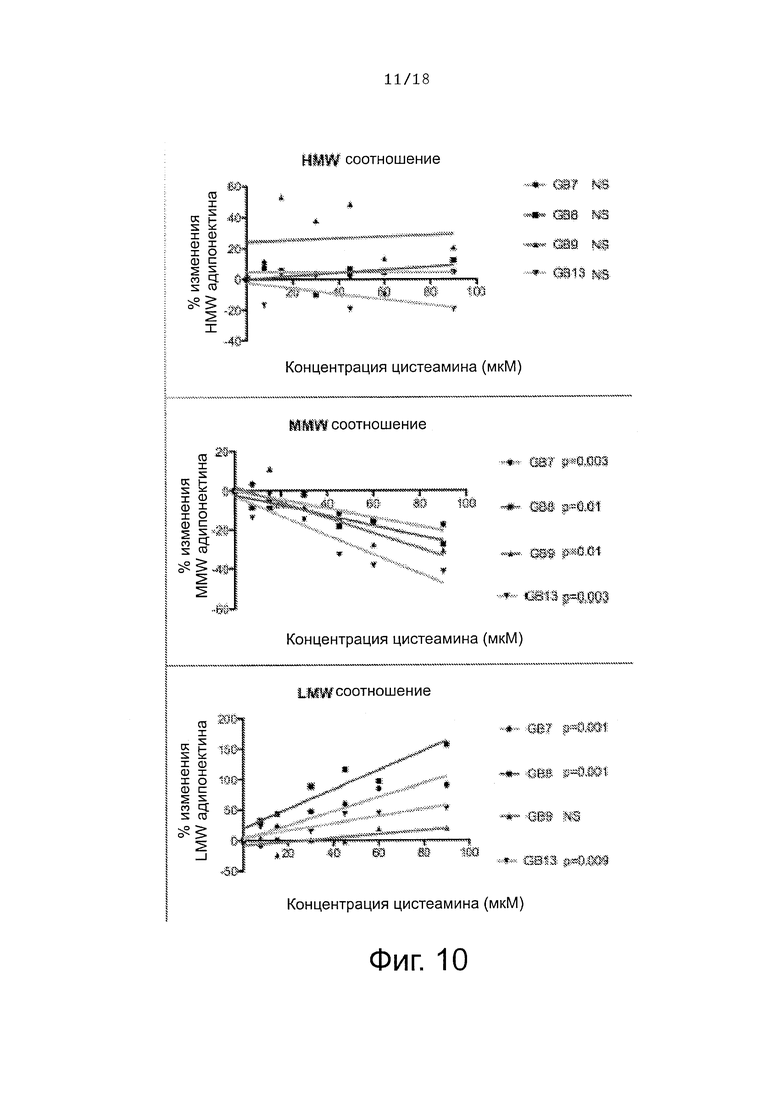
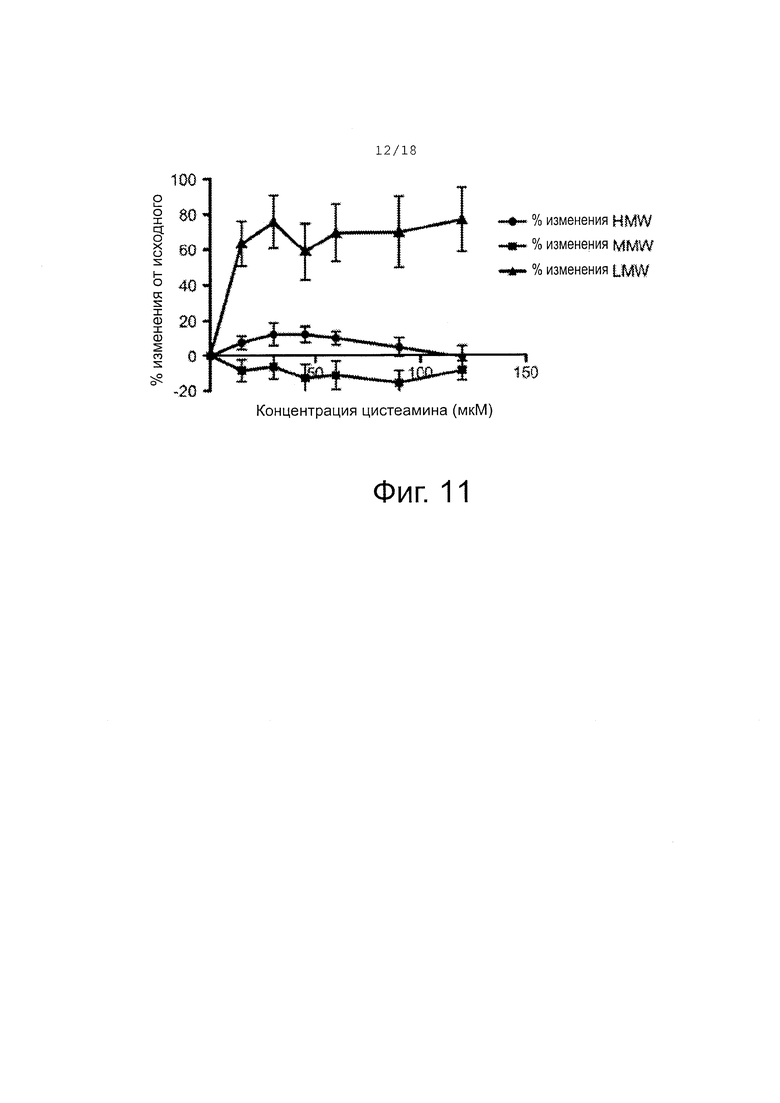
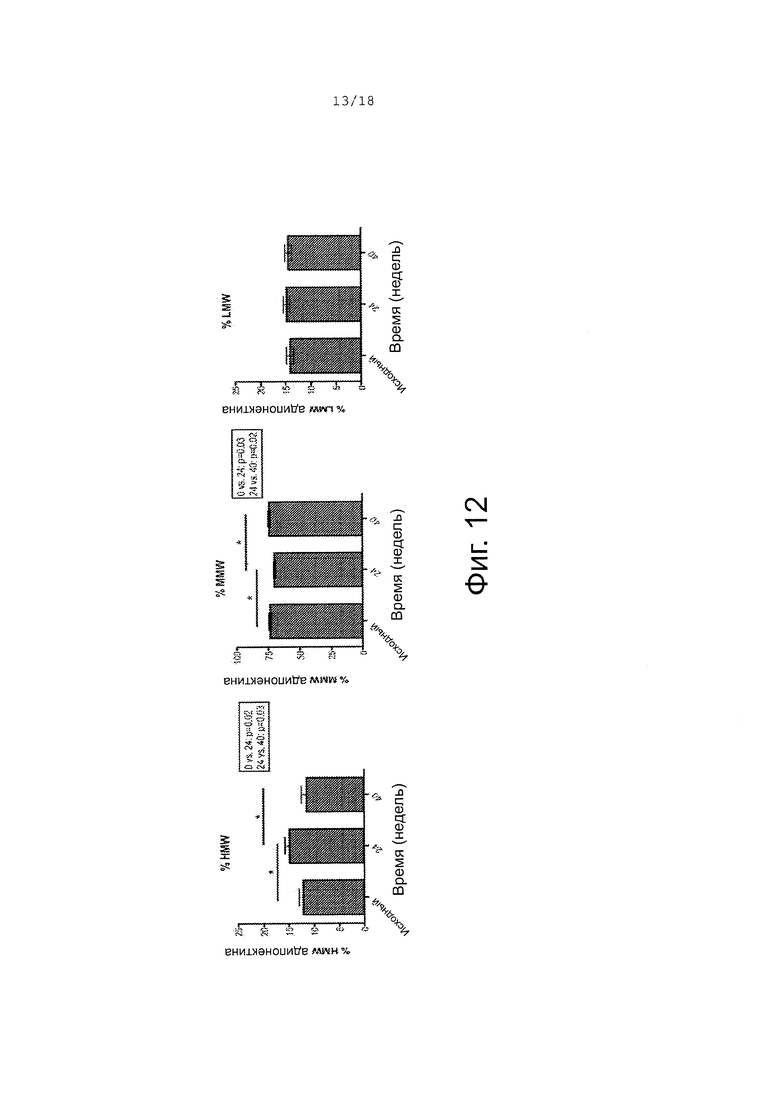
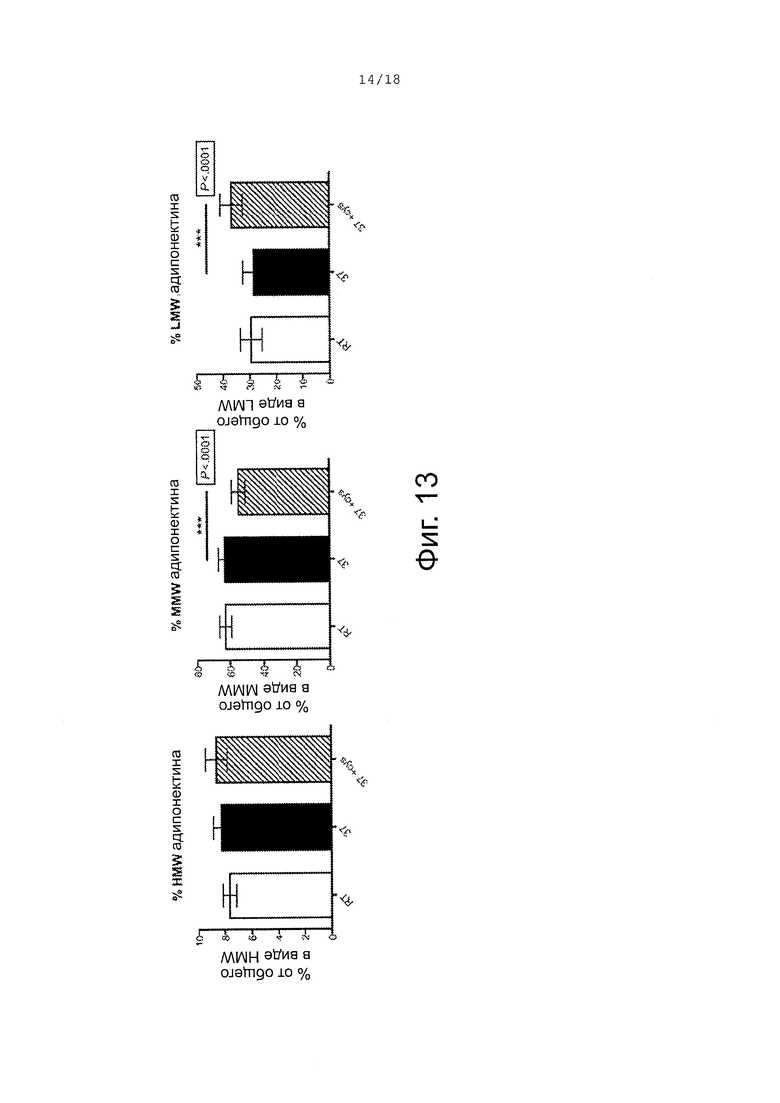
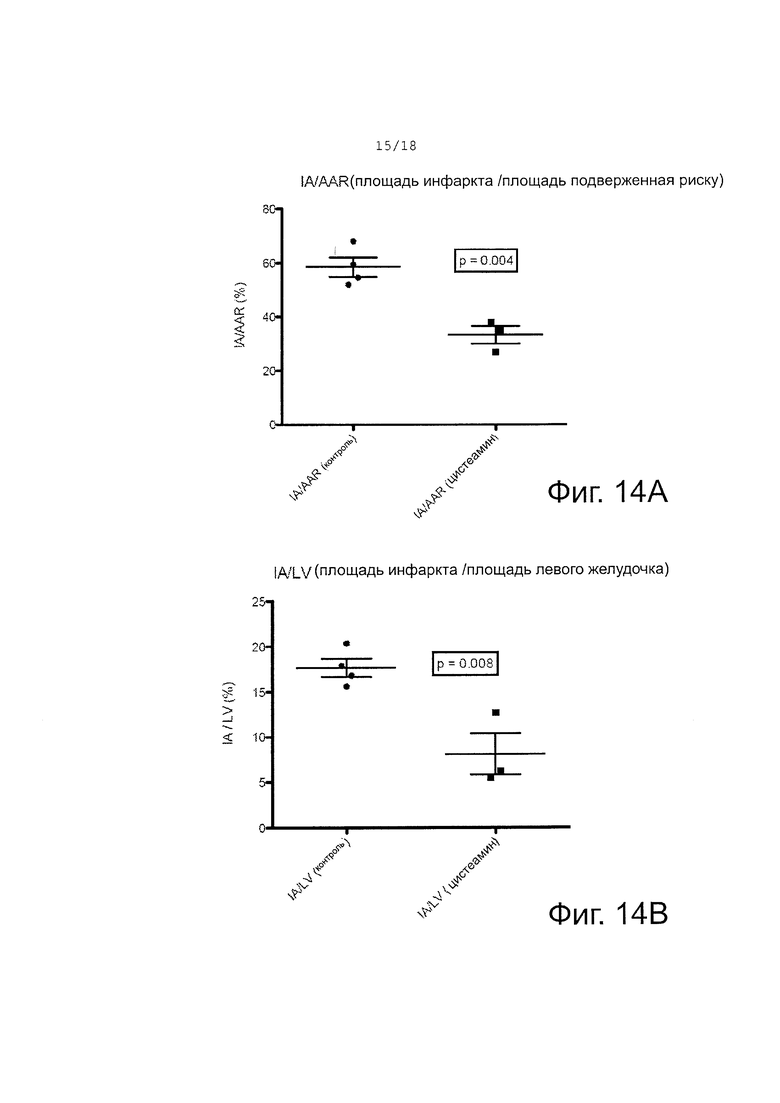
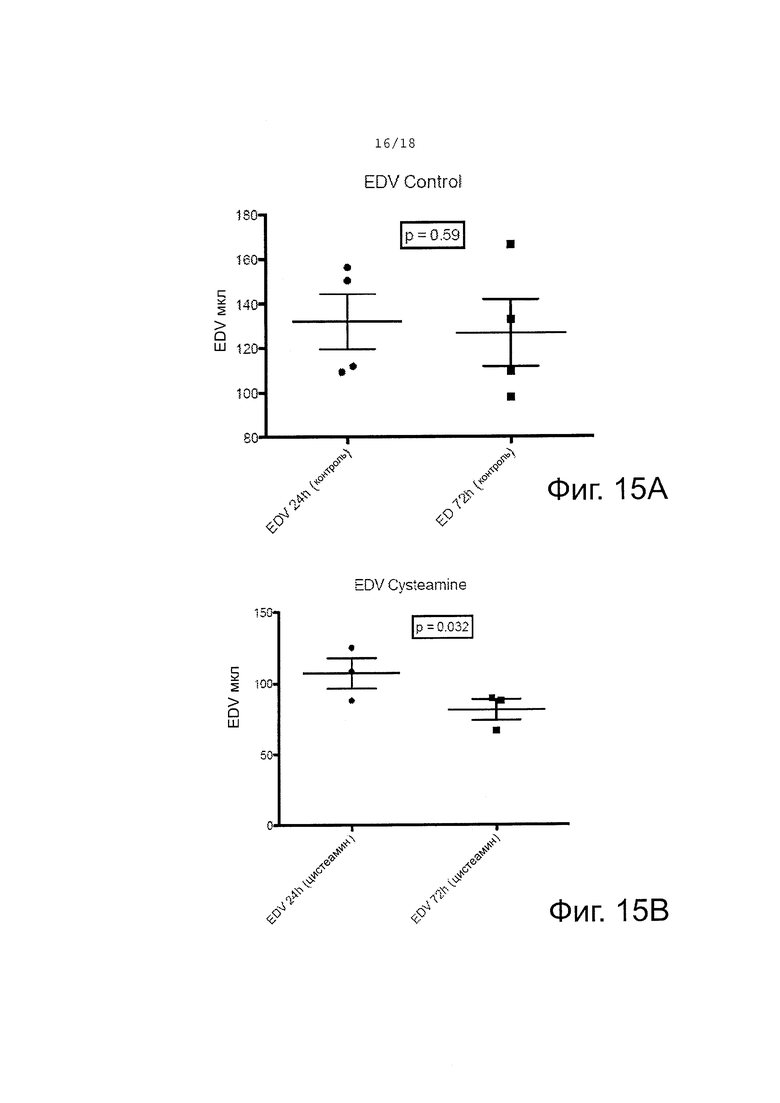
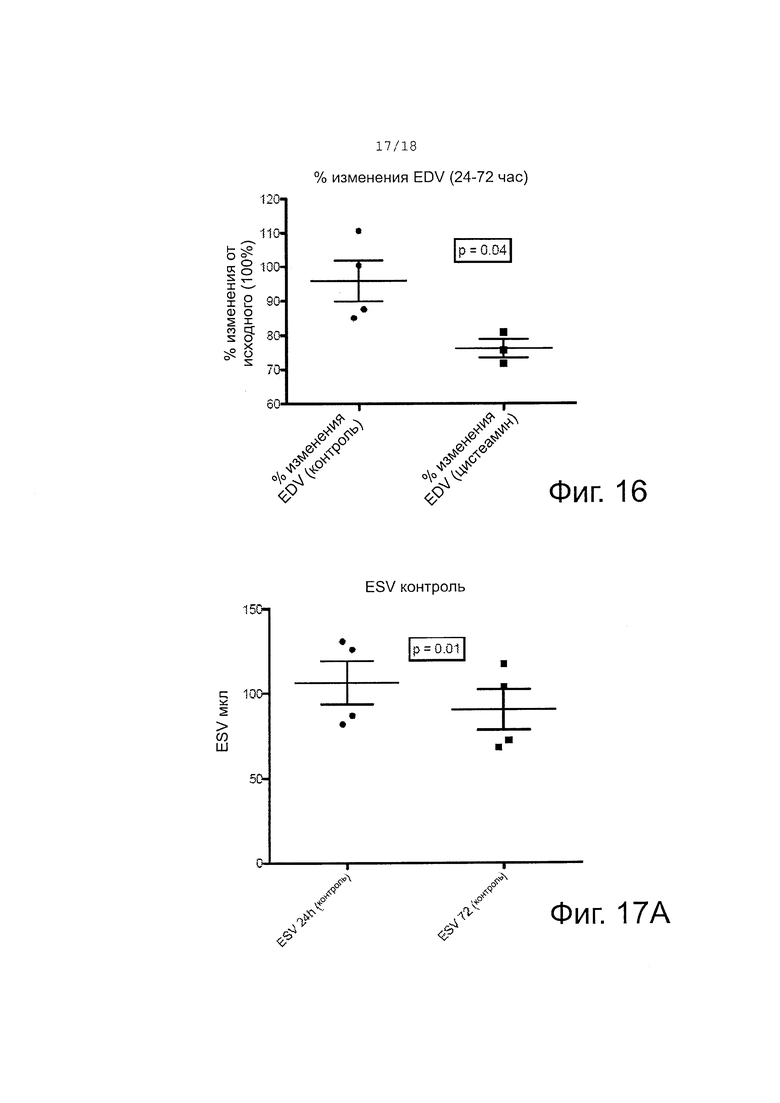
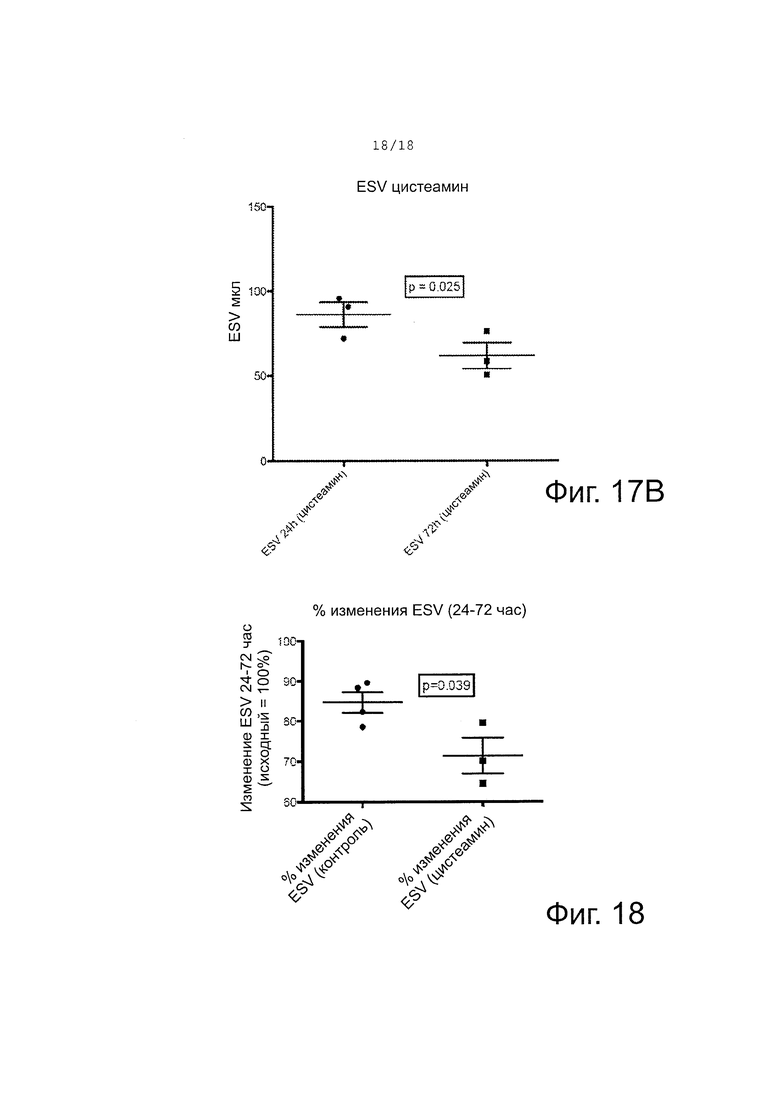
Группа изобретений касается фармакологии и медицины. Предложены: способ лечения субъекта, страдающего от ишемического повреждения или острого ишемического события, включающий введение цистеамина, цистамина или их соли до, одновременно с или сразу после ишемического события, в количестве, эффективном для уменьшения ишемического повреждения, причем субъект не страдает от гиперхолестеринэмии или диабетом II типа, где введение цистеамина, цистамина или их соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) (варианты); способ увеличения (варианты) уровней адипонектина LMW у указанной группы больных, включающий контактирование субъекта с эффективным количеством цистеамина, цистамина или их соли (варианты); применение цистеамина, цистамина или их соли при производстве медикамента при вышеуказанном лечении субъекта, страдающего от острого ишемического события и не страдающего от гиперхолестеринэмии или диабета II типа. Технический результат состоит в реализации заявленного назначения у указанной группы больных, при этом повышаются уровни всех мультиморов адипонектина, в течение 1 часа после воздействия цистеамина в сыворотке крови быстро и значимо повышался LMW адипонектина, введение цистеамина за 2 часа до ишемического инсульта значительно снижало площадь инфаркта и количество ишемических повреждений. 7 н. и 21 з.п. ф-лы, 18 ил., 2 табл., 3 пр.
1. Способ лечения субъекта, страдающего от ишемического повреждения или острого ишемического события, включающий введение субъекту цистеамина, цистамина или их фармацевтически приемлемой соли для уменьшения ишемического повреждения в результате острого ишемического события, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, причем
цистеамин, цистамин или их фармацевтически приемлемую соль вводят до, одновременно с или сразу после ишемического события, в количестве, эффективном для уменьшения ишемического повреждения, и причем
субъект не страдает от гиперхолестеринэмии или диабетом II типа.
2. Способ по п. 1, в котором субъект имеет тромботическое заболевание, которое факультативно представляет собой серповидноклеточную анемию, глубокий тромбоз вен, легочную эмболию, сердечную эмболию, состояние гиперкоагуляции, тромбофилию, фактор V Ляйдена, дефицит антитромбина III, дефицит белка С, дефицит белка S, мутацию гена протромбина (G20210A), гипергомоцистеинемию, синдром антифосфолипидных антител (APS), синдром антикардиолипиновых антител (ACLA) или синдром волчаночного антикоагулянта (LA).
3. Способ лечения субъекта с повышенным риском острого тромболитического события и ишемического повреждения, являющегося его результатом, включающий введение субъекту цистеамина, цистамина или их фармацевтически приемлемой соли, путем уменьшения риска ишемического повреждения, являющегося результатом острого тромболитического события, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, причем
цистеамин, цистамин или их фармацевтически приемлемую соль вводят до, одновременно с или сразу после ишемического события, в количестве, эффективном для уменьшения ишемического повреждения, и причем
субъект не страдает от гиперхолестеринэмии или диабетом II типа.
4. Способ по п. 3, в котором субъект имеет рак, миелопролиферативное заболевание, множественную миелому, перенес операцию, имел травму, находится в состоянии иммобилизации, принимает пероральное противозачаточное средство, субъекту вводят талидомид или его родственные соединения необязательно в комбинации со стероидным гормоном, имеет гепарин-индуцированную тромбоцитопению, является беременным, имеет воспалительную болезнь кишечника, имеет нефротический синдром, имеет ночную пароксизмальную гемоглобинурию, имеет синдром повышенной вязкости крови или макроглобулинемию Вальденстрема.
5. Способ по п. 1, в котором ишемическое повреждение является результатом поражения ткани, болезнью или инсультом.
6. Способ по п. 5, в котором повреждение представляет собой реперфузионное повреждение или серповидноклеточную анемию.
7. Способ по п. 1, в котором цистеамин, цистамин или их фармацевтически приемлемую соль вводят:
i) в интервале 72 часов после острого ишемического события;
ii) длительное время после острого ишемического события; или
iii) постоянно субъекту с повышенным риском острого ишемического события.
8. Способ увеличения отношения уровней адипонектина с низким молекулярным весом (LMW) к адипонектину со средним молекулярным весом (MMW) и/или высоким молекулярным весом (HMW) у субъекта, нуждающегося в этом, включающий введение субъекту цистеамина, цистамина или их фармацевтически приемлемой соли, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, при этом субъект не страдает гиперхолестеринемией или диабетом II типа.
9. Способ лечения субъекта, имеющего ненормальные или аномальные отношения адипонектин с высоким молекулярным весом (HMW) : адипонектин со средним молекулярным весом (MMW), HMW : адипонектин с низким молекулярным весом (LMW) или MMW:LMW, включающий введение субъекту цистеамина, цистамина, или их фармацевтически приемлемой соли, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, при этом субъект не страдает гиперхолестеринемией или диабетом II типа.
10. Способ по п. 8, в котором субъект имеет фактор риска развития ишемии, выбранный из группы, состоящей из высокого кровяного давления, употребления табака, болезни сонной или других артерий, заболевания периферических артерий, мерцательной аритмии, другого заболевания сердца, преходящего ишемического нарушения (TIA), заболеваний крови, высокого уровня холестерина в крови, гиподинамии, ожирения, избыточного употребления алкоголя, использования запрещенных наркотиков, предшествующего инсульта, серповидноклеточной анемии и предшествующего сердечного приступа.
11. Способ по п. 9, в котором субъект ранее страдал от острого ишемического события.
12. Способ по п. 1, включающий введение цистеамина или его фармацевтически приемлемой соли.
13. Способ по п. 1, в котором цистеамин, цистамин или их фармацевтически приемлемая соль вводится в концентрации в пределах около 0,5-20 мг/кг веса тела указанного субъекта.
14. Способ по п. 1, в котором общая ежедневная доза цистеамина, цистамина или их фармацевтически приемлемой соли составляет около 0,5-4,0 г/м2.
15. Способ по п. 14, в котором цистеамин, цистамин или их фармацевтически приемлемая соль представляет собой лекарственную форму с замедленным или контролируемым высвобождением.
16. Способ по п. 1, который дополнительно включает введение
i) одного или более дополнительных средств, полезных для лечения ишемии, или
ii) одного или более средств, полезных для лечения тромботических заболеваний, выбранных из группы, состоящей из необязательно антикоагулирующего средства, гепарина, антагониста витамина K, производных 4-гидроксикумарина, варфарина, аценокумарола, дикумарола, этилбискумацетата, фенпрокумона, стрептокиназы, урокиназы, тканевого активатора плазминогена (tPA), альтеплазы (рекомбинантной tPA), ретеплазы, тенектеплазы и аргатробана.
17. Способ по п. 15, в котором цистеамин, цистамин или их фармацевтически приемлемая соль вводится
i) меньше, чем четыре раза в день или
ii) дважды в день.
18. Способ лечения острого ишемического события, включающий:
контактирование субъекта, страдающего от острого ишемического события с эффективным количеством цистеамина, цистамина или их фармацевтически приемлемой соли, при этом субъект имеет улучшенный поведенческий результат по сравнению с субъектом, который не получал цистеамин, цистамин или их фармацевтически приемлемую соль, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, причем
цистеамин, цистамин или их фармацевтически приемлемую соль вводят до, одновременно с или сразу после ишемического события, в количестве, эффективном для уменьшения ишемического повреждения, и причем
субъект не страдает от гиперхолестеринэмии или диабетом II типа.
19. Способ по п. 18, в котором уровни адипонектина у субъекта увеличиваются после контактирования с цистеамином, цистамином или их фармацевтически приемлемой солью.
20. Способ по п. 18, в котором цистеамин, цистамин или их фармацевтически приемлемая соль представляет собой лекарственную форму с замедленным или контролируемым высвобождением, которая обеспечивает увеличенную доставку цистеамина, цистамина или их фармацевтически приемлемой соли в тонкий кишечник.
21. Способ по п. 20, в котором лекарственная форма с замедленным или контролируемым высвобождением содержит энтеросолюбильное покрытие, которое высвобождает цистеамин, цистамин или их фармацевтически приемлемую соль, когда цистеамин, цистамин или их фармацевтически приемлемая соль достигает тонкого кишечника или участка желудочно-кишечного тракта субъекта, в котором значение pH больше, чем около pH 4,5.
22. Способ по п. 10, в котором цистеамин, цистамин или их фармацевтически приемлемая соль вводится постоянно или остро (в остром случае).
23. Способ увеличения уровней адипонектина у субъекта, включающий контактирование субъекта с эффективным количеством цистеамина, цистамина или их фармацевтически приемлемой соли с целью увеличения уровней адипонектина по сравнению с исходным до контактирования субъекта с цистеамином, цистамином или их фармацевтически приемлемой солью, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, причем
субъект не страдает от гиперхолестеринэмии или диабетом II типа.
24. Способ по п. 23, в котором
i) уровни общего адипонектина повышаются или
ii) содержание адипонектина с более низким молекулярным весом увеличивается по отношению к адипонектину со средним молекулярным весом или адипонектину с высоким молекулярным весом.
25. Способ по п. 23, в котором субъект
i) является тучным и имеет низкие уровни LMW адипонектина по сравнению со здоровыми субъектами, или
ii) субъект имеет низкие уровни LMW адипонектина по сравнению со здоровыми субъектами, или
iii) субъект страдает от острых ишемических событий/приступов.
26. Применение цистеамина, цистамина или их фармацевтически приемлемой соли при производстве медикамента при лечении субъекта, страдающего от острого ишемического события, для уменьшения ишемического повреждения в результате острого ишемического события, где введение цистеамина, цистамина или их фармацевтически приемлемой соли приводит к увеличению у субъектов уровня адипонектина с низким молекулярным весом (LMW) по сравнению с этим уровнем до введения указанных веществ, причем
цистеамин, цистамин или их фармацевтически приемлемую соль вводят до, одновременно с или сразу после ишемического события, в количестве, эффективном для уменьшения ишемического повреждения, и причем
субъект не страдает от гиперхолестеринэмии или диабетом II типа.
27. Применение по п. 26, при котором субъект имеет тромботическое заболевание и при котором тромботическое заболевание факультативно является серповидноклеточной анемией, глубоким тромбозом вен, легочной эмболией, сердечной эмболией, состоянием гиперкоагуляции, тромбофилией, фактором V Ляйдена, дефицитом антитромбина III, дефицитом белка С, дефицитом белка S, мутацией гена протромбина (G20210A), гипергомоцистеинемией, синдромом антифосфолипидных антител (APS), синдромом антикардиолипиновых антител (ACLA) или синдромом волчаночного антикоагулянта (LA).
28. Применение по п. 26, при котором медикамент содержит цистеамин, цистамин или их фармацевтически приемлемую соль.
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА | 2004 |
|
RU2367423C2 |
| КОМБИНАЦИЯ ИНГИБИТОРОВ NO-СИНТЕТАЗЫ И УЛАВЛИВАТЕЛЕЙ РЕАКЦИОННОСПОСОБНЫХ ФОРМ КИСЛОРОДА | 1997 |
|
RU2174844C2 |
| СПОСОБ РАЗМЕРНОЙ ЭЛЕКТРОХИМИЧЕСКОЙ ОБРАБОТКИ | 0 |
|
SU306937A1 |
| GUO Z | |||
| et al | |||
| Effect of N-acetylcysteine on plasma adiponectin and renal adiponectin receptors in streptozotocin-induced diabetic rats | |||
| Eur.J.Pharmacol | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Mar | |||
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| WANG T | |||
| et al | |||
| N-acetylcysteine and allopurinol synergistically enhance cardiac adiponectin content and reduce myocardial reperfusion in diabetic rats | |||
| PLoS One | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Aug | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| РАДИОЗАЩИТНОЕ СРЕДСТВО | 2010 |
|
RU2428192C1 |
Авторы
Даты
2017-12-15—Публикация
2012-11-21—Подача