ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Бутадиен (1,3-бутадиен, CH2=CH-CH=CH2, CAS 106-99-0) представляет собой неразветвленный, конъюгированный 4-углеродный углеводород, как правило, получаемый (наряду с другими 4-углеродными молекулами) посредством парового крекинга нефтяных углеводородов. Этот процесс включает жесткие условия и высокие температуры (по меньшей мере приблизительно 850°C). Другие способы получения бутадиена включают токсические и/или дорогостоящие катализаторы, легковоспламеняющиеся и/или газообразные источники углерода и высокие температуры. На мировом уровне ежегодно получают несколько миллионов тонн содержащих бутадиен полимеров. Бутадиен можно полимеризовать с получением полибутадиена или подвергать реакции с цианистым водородом (синильной кислотой) в присутствии никелевого катализатора с получением адипонитрила, предшественника нейлона. Однако более часто бутадиен полимеризуют с другими олефинами с получением сополимеров, таких как сополимеры акрилонитрил-бутадиен-стирол (ABS), акрилонитрил-бутадиен (ABR) или стирол-бутадиен (SBR).
СУЩНОСТЬ
Настоящее изобретение в основном относится к микроорганизмам (например, неприродным микроорганизмам, также обозначаемым в настоящем документе как модифицированные микроорганизмы), содержащим один или несколько полинуклеотидов, кодирующих ферменты в одном или нескольких метаболических путей, которые катализируют превращение источника углерода в бутадиен, и к применениям таких микроорганизмов в производственных процессах, включая применение в получении бутадиена и получаемых из него продуктов.
Настоящее изобретение относится к способам получения бутадиена из ферментируемого источника углерода, включающим: получение ферментируемого источника углерода; приведение ферментируемого источника углерода в контакт с микроорганизмом, содержащим один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен в ферментационных средах; и экспрессию одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен в микроорганизме, с получением бутадиена.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, ферменты, которые катализируют превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, приведены в любой из таблиц 1-3.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, ферменты, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, приведены в любой из таблиц 1-3.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, бутадиен получают через промежуточные соединения ацетил-КоА и пропионил-КоА; промежуточное соединение кротонил-КоА; и/или промежуточное соединение муравьиную кислоту.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в кетовалерил-КоА, кодируют кетотиолазу, включая, например, кетотиолазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 58-78.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кетовалерил-КоА в (R) или (S) 3-гидроксиалерил-КоА, кодируют оксидоредуктазу, включая, например, оксидоредуктазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 103-123.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) гидроксиалерил-КоА в 2-пентеноил-КоА, кодируют дегидратазу, включая, например, дегидратазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 37-55.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение of 2-пентеноил-КоА to 2-пентенов кислота кодируют трансферазу или гидролазу, включая, например, трансферазу или гидролазу, кодируемые полинуклеотидами, как указано в любой из SEQ ID NO: 1-28 или 29-33, соответственно.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в бутадиен, кодируют декарбоксилазу, включая, например, декарбоксилазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 79-98.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в 4-пентеновую кислоту, кодируют изомеразу, включая, например, и изомеразу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 99-102.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-пентеновой кислоты в бутадиен, кодируют декарбоксилазу, включая, например, декарбоксилазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 79-98.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеноил-КоА в пент-2,4-диеноил-КоА, кодируют дегидрогеназу, включая, например, дегидрогеназу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 124-139.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пент-2,4-диеноил-КоА в пент-2,4-диеновую кислоту, кодируют трансферазу или гидролазу, включая, например, трансферазу или гидролазу, кодируемые полинуклеотидами, как указано в любой из SEQ ID NO: 1-28 или 29-33, соответственно.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2,4-пентеновой кислоты в бутадиен, кодируют декарбоксилазу, включая, например, декарбоксилазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 79-98.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротониловый спирт, кодируют оксидоредуктазу, включая, например, оксидоредуктазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 103-123.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротоновый альдегид, кодируют оксидоредуктазу, включая, например, оксидоредуктазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 103-123.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонового альдегида в кротониловый спирт, кодируют оксидоредуктазу или КоА-синтетазу, включая, например, оксидоредуктазу или синтетазу, кодируемые полинуклеотидами, как указано в любой из SEQ ID NO: 103-123 или SEQ ID NO: 34-36, соответственно.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонилового спирта в бутадиен, кодируют дегидратазу, включая, например, дегидратазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 37-55.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение CO2 в муравьиную кислоту, кодируют дегидрогеназу, включая, например, дегидрогеназу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 124-139.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата и КоА в ацетил-КоА и муравьиную кислоту, кодируют кетотиолазу, включая, например, кетотиолазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 58-78.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение муравьиной кислоты в формил-КоА, кодируют трансферазу или КоА-синтетазу, включая, например, трансферазу или КоА-синтетазу, кодируемые полинуклеотидами, как указано в любой из SEQ ID NO: 1-28 или 34-36, соответственно.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2 ацетил-КоА в ацетоацетил-КоА, кодируют кетотиолазу, включая, например, кетотиолазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 58-78.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетоацетил-КоА и формил-КоА в 3,5-кетовалерил-КоА, кодируют кетотиолазу, включая, например, кетотиолазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 58-78.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3,5-кетовалерил-КоА в (R)- или (S)-5-гидрокси-3-кетовалерил-КоА, кодируют оксидоредуктазу, включая, например, оксидоредуктазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 103-123.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R)- или (S)-5-гидрокси-3-кетовалерил-КоА в (R)- или (S)-3,5-дигидроксиалерил-КоА, кодируют оксидоредуктазу, включая, например, оксидоредуктазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 103-123.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R)- или (S)-3,5-дигидроксиалерил-КоА в (R) или (S) 3-гидрокси-4-пентеноил-КоА, кодируют дегидратазу, включая, например, дегидратазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 37-55.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R)- или (S)-3-гидрокси-4-пентеноил-КоА в 3-гидрокси-4-пентеновую кислоту, кодируют трансферазу или гидролазу, включая, например, трансферазу или гидролазу, кодируемые полинуклеотидами, как указано в любой из SEQ ID NO: 1-28 или 29-33, соответственно.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидрокси-4-пентеновой кислоты в бутадиен, кодируют декарбоксилазу, включая, например, декарбоксилазу, кодируемую полинуклеотидом, как указано в любой из SEQ ID NO: 79-98.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм представляет собой бактерию, выбранную из родов, состоящих из: Burkholderia, Propionibacterium, Propionispira, Clostridium, Bacillus, Escherichia, Pelobacter или Lactobacillus.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм представляет собой эукариотический организм, представляет собой дрожжи, нитевидные грибы, простейших или водоросли.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, дрожжи представляют собой Saccharomyces cerevisiae, Zymomonas mobilis или Pichia pastoris.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, источник углерода представляет собой сок сахарного тростника, патоку сахарного тростника, гидролизованный крахмал, гидролизованный лигноцеллюлозные вещества, глюкозу, сахарозу, фруктозу, лактат, лактозу, ксилозу, пируват или глицерин в любой их форме или смеси.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, источник углерода представляет собой моносахарид, олигосахарид или полисахарид.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм секретирует бутадиен в ферментационные среды.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, способы дополнительно могут включать извлечение бутадиена из ферментационных сред.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм генетически модифицирован так, чтобы экспрессировать один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, превращение ферментируемого источника углерода в бутадиен положительно по АТФ (например, в нем образуется свободный АТФ на моль продуцируемого бутадиена), и его дополнительно можно комбинировать с потребляющим NADH метаболическим путем для обеспечения анаэробного процесса получения бутадиена.
Настоящее изобретение также относится к микроорганизмам, содержащим один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, ферменты, которые катализируют превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, приведены в любой из таблиц 1-3.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, ферменты, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, приведены в любой из таблиц 1-3.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, бутадиен получают через промежуточные соединения ацетил-КоА и пропионил-КоА; промежуточное соединение кротонил-КоА и/или промежуточное соединение муравьиную кислоту.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм представляет собой бактерию, выбранную из родов, состоящих из: Burkholderia, Propionibacterium, Propionispira, Clostridium, Bacillus, Escherichia, Pelobacter или Lactobacillus.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм представляет собой эукариотический организм, представляет собой дрожжи, нитевидные грибы, простейших или водоросли.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, дрожжи представляют собой Saccharomyces cerevisiae, Zymomonas mobilis или Pichia pastoris.
В некоторых вариантах осуществления, которые можно комбинировать с любым из указанных выше или ниже вариантов осуществления, микроорганизм генетически модифицирован так, чтобы экспрессировать один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен.
Эти и другие варианты осуществления настоящего изобретения более подробно описаны далее в настоящем документе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Указанное выше краткое изложение, а также следующее далее подробное описание изобретения, будут лучше понятны при чтении в сочетании с приложенными фигурами. С целью иллюстрации изобретения на фигурах представлены предпочтительные в настоящем изобретении варианты осуществления. Однако следует понимать, что изобретение не ограничено представленными определенными схемами, примерами и средствами.
На фиг. 1 представлен иллюстративный метаболический путь получения бутадиена из ферментируемого источника углерода через промежуточные соединения ацетил-КоА и пропионил-КоА.
На фиг. 2 представлен иллюстративный метаболический путь получения бутадиена из ферментируемого источника углерода через промежуточное соединение кротонил-КоА.
На фиг. 3 представлен иллюстративный метаболический путь получения бутадиена из ферментируемого источника углерода через промежуточное соединение муравьиную кислоту.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретении в основном относится к микроорганизмам (например, неприродным микроорганизмам; модифицированным микроорганизмам), содержащим генетически модифицированный метаболический путь, и к применениям микроорганизмов для превращения ферментируемого источника углерода в бутадиен (см. фиг. 1-3). Такие микроорганизмы содержат один или несколько полинуклеотидов, кодирующих ферменты, которые катализируют превращение ферментируемого источника углерода в бутадиен через новые ферментативные метаболические пути. Необязательно получаемый бутадиен можно затем превращать в полибутадиен или любой ряд других содержащих бутадиен полимеров.
Частично настоящее изобретение относится к открытию новых ферментативных путей, включая, например, новые комбинации ферментативных путей получения бутадиена из источника углерода (например, ферментируемого источника углерода). Ферментативные пути, описываемые в настоящем документе, обеспечивают ферментативное получение бутадиена через: промежуточные соединения ацетил-КоА и пропионил-КоА; промежуточное соединение кротонил-КоА и/или промежуточное соединение муравьиную кислоту.
Предоставляемые в настоящем документе способы обеспечивают конечные результаты, сходные с результатами при стерилизации без высоких капиталовложений и непрерывных повышенных производственных затрат, которые, как правило, необходимы для установления и поддержания стерильности на протяжении всего способа получения. В этом отношении, наиболее промышленно значимые способы получения бутадиен используют в присутствии значительных количеств бактериальных загрязнителей вследствие аэробного характера их процессов. Полагают, что бактериальное загрязнение способов получения бутадиена вызывает снижение выхода продукта и ингибирование роста микроорганизма, продуцирующего бутадиен. В предлагаемых по настоящему заявлению способах такие недостатки предшествующих способов устранены, так как токсичная природа продуцируемого бутадиена уменьшает загрязнители в способе получения.
Ферментативные пути, описываемые в настоящем документе, имеют преимущество над известными предшествующими ферментативными путями получения бутадиена в том, что ферментативные пути, описываемые в настоящем документе, положительны по АТФ, и при комбинации с потребляющим NADH метаболическим путем это может обеспечить анаэробный метаболический путь бутадиена. Хотя для получения бутадиена возможно использовать аэробные процессы, анаэробные процессы являются предпочтительными вследствие риска потерь, когда олефины (которые по своему характеру являются взрывчатыми) в процессе ферментации, особенно при ферментации бутадиена, смешивают с кислородом. Кроме того, подача кислорода и азота в ферментер требует дополнительных инвестиций в воздушный компрессор, ферментеры (барботажная колонна или воздухоструйный ферментер), контроль температуры и азота. Присутствие кислорода также может катализировать полимеризацию бутадиена и может способствовать росту аэробных загрязнителей в ферментируемом бульоне. Кроме того, у процессов аэробной ферментации при получения бутадиена в промышленном масштабе (там, где технически сложно поддерживать асептические условия) существует несколько недостатков, таких как факты того, что: (i) получают большую биомассу, снижая общие выходы углерода для желаемых продуктов; (ii) присутствие кислорода способствуют росту загрязнителей (Weusthuis et al., 2011, Trends in Biotechnology, 2011, Vol. 29, No. 4, 153-158) и (iii) смесь кислорода и газообразных соединений, таких как бутадиен, создают серьезные риски взрыва, (iv) кислород может катализировать нежелательную реакцию полимеризации олефина и, наконец, (v) обеспечена повышенная стоимость ферментации и очистки в аэробных условиях. Кроме того, бутадиен, получаемый способами, описанными в настоящем документе, не разбавлен O2 и N2, таким образом, устраняя необходимость в потребляющей средства и время очистке получаемого бутадиена.
Следует понимать, что этапы, включенные в любой и все способы, описываемые в настоящем документе, можно проводить в любом порядке, и их не следует ограничивать лимитировать или ограничивать порядком, в котором они конкретно указаны. Например, настоящее изобретение относится к способам получения бутадиена из ферментируемого источника углерода, включающим: получение ферментируемого источника углерода; приведение ферментируемого источника углерода в контакт с микроорганизмом, содержащим один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, в ферментационных средах; и экспрессию в микроорганизме одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, с получением бутадиена. По существу, экспрессию в микроорганизме одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, с получением бутадиена можно проводить до или после приведения ферментируемого источника углерода в контакт с микроорганизмом, содержащим один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений в метаболическом пути получения бутадиена, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, в ферментационных средах.
Также следует понимать, что микроорганизмы, описываемые в настоящем документе, могут содержать целый метаболический путь, описанный на любой из фиг. 1-3, включая все полинуклеотиды, которые кодируют ферменты, которые катализируют превращение ферментируемого источника углерода в бутадиен. Альтернативно, также следует понимать, что микроорганизмы, описываемые в настоящем документе, могут содержать один или несколько из полинуклеотидов, кодирующих ферменты, которые катализируют превращение ферментируемого источника углерода в бутадиен на любой из фиг. 1-3 (например, микроорганизм может содержать 2, 3, 4, 5, 6, 7, 8, 9, 10 или более полинуклеотидов, которые кодируют ферменты, которые катализируют превращение ферментируемого источника углерода в бутадиен, как описано на любой из фиг. 1-3.
В некоторых вариантах осуществления отношение количества грамм получаемого бутадиена к количеству грамм ферментируемого источника углерода составляет 0,20, 0,21, 0,22, 0,23, 0,24, 0,25, 0,26, 0,27, 0,28, 0,29, 0,30, 0,31, 0,32, 0,33, 0,34, 0,35, 0,36, 0,37, 0,38, 0,39, 0,40, 0,41, 0,42, 0,43, 0,44, 0,45, 0,46, 0,47, 0,48, 0,49, 0,50, 0,51, 0,52, 0,53, 0,54, 0,55, 0,56, 0,57, 0,58, 0,59, 0,60, 0,61, 0,62, 0,63, 0,64, 0,65, 0,66, 0,67, 0,68, 0,69, 0,70, 0,71, 0,72, 0,73, 0,74, 0,75, 0,76, 0,77, 0,78, 0,79, 0,80, 0,81, 0,82, 0,83, 0,84, 0,85, 0,86, 0,87, 0,88, 0,89, 0,90, 0,91, 0,92, 0,93, 0,94, 0,95, 0,96, 0,97, 0,98, 0,99 или 1,00.
В некоторых вариантах осуществления количество моль углерода в получаемом бутадиене составляет 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 41%, 42%, 43%, 44%, 45%, 46%, 47%, 48%, 49%, 50%, 51%, 52%, 53%, 54%, 55%, 56%, 57%, 58%, 59%, 60%, 61%, 62%, 63%, 64%, 65%, 66%, 67%, 68%, 69%, 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% от количества моль углерода в ферментируемом источнике углерода.
Как используют в настоящем документе, "бутадиен" предназначен для обозначения бута-1,3-диена или 1,3-бутадиена (CAS 106-99-0)c общей формулой CH2=CH-CH=CH2 и молекулярной массой 54,09 г/моль.
Как используют в настоящем документе, термин "биологическая активность" или "функциональная активность", когда он относится к белку, полипептиду или пептиду, может означать, что белок, полипептид или пептид проявляют функциональность или свойство, полезное в отношении определенного биологического процесса, метаболического пути или реакции. Биологическая или функциональная активность может относиться, например, к способности к взаимодействию или ассоциации (например, связыванию) с другим полипептидом или молекулой, или она может относиться к способности катализировать или регулировать взаимодействие других белков или молекул (например, ферментативные реакции).
Как используют в настоящем документе, термин "культивирование" может относиться к выращиванию популяции клеток, например, микробных клеток, в подходящих условиях роста в жидкой или на твердой среде.
Как используют в настоящем документе, термин "полученный из" может включать термины происходящий из, полученный из, получаемый из, выделяемый из и сделанный из и, как правило, означает, что указанный материал имеет происхождение в другом указанном материале или имеет характеристики, которые можно описать со ссылкой на другой указанный материал.
Как используют в настоящем документе, термин "экспрессирующий вектор" может относиться к конструкции ДНК, содержащей полинуклеотид или последовательность нуклеиновой кислоты, кодирующую полипептид или белок, такую как кодирующая последовательность ДНК (например, последовательность гена), которая функционально связана с одной или несколькими подходящими контрольными последовательностями, способными влиять на экспрессию кодирующей последовательности у хозяина. Такие контрольные последовательности включают промотор для влияния на транскрипцию, необязательную управляющую последовательность для контроля такой транскрипции, последовательность, кодирующую подходящие участки связывания рибосом в мРНК, и последовательности, контролирующие терминацию транскрипции и трансляции. Вектор может представлять собой плазмиду, фаговую частицу или просто потенциальную геномную вставку. После трансформации в подходящего хозяина, вектор может реплицироваться и функционировать независимо от генома хозяина (например, автономный вектор или плазмида) или, в некоторых случаях, может самостоятельно интегрироваться в геном (например, интегрированный вектор). Наиболее широко используемой формой вектора является плазмида. Однако изобретение предназначено для включения других таких форм экспрессирующих векторов, которые выполняют эквивалентные функции и которые известны или станут известны в данной области.
Как используют в настоящем документе, термин "экспрессия" может относиться к процессу, посредством которого образуется полипептид на основе последовательности нуклеиновой кислоты, кодирующей полипептиды (например, гена). Процесс включает и транскрипцию, и трансляцию.
Как используют в настоящем документе, термин "ген" может относиться к участку ДНК, который участвует в продукции полипептида или белка (например, слитого белка) и включает области предшествующие и следующие за кодирующей областью, а также промежуточные последовательности (интроны) между отдельными кодирующими участками (экзонами).
Как используют в настоящем документе, термин "гетерологичный", по отношению к нуклеиновой кислоте, полинуклеотиду, белку или пептиду, может означать нуклеиновую кислоту, полинуклеотид, белок или пептид, которые в природе не встречаются в указанной клетке, например, клетке-хозяине. Следует понимать, что термин включает белки, которые кодируют природные гены, мутантные гены и/или синтетические гены. В отличие от этого, термин гомологичный, в отношении нуклеиновой кислоты, полинуклеотида, белка или пептида относится к нуклеиновой кислоте, полинуклеотиду, белку или пептиду, которые встречаются в клетке в природе.
Как используют в настоящем документе, термин "клетка-хозяин" может относиться к клетке или линии клеток, включая такие клетки, как микроорганизм, которые можно трансфицировать рекомбинантным экспрессирующим вектором для экспрессии полипептида или белка (например, слитого белка). Клетки-хозяева включают потомство одной клетки-хозяина, и потомство не обязательно может являться полностью идентичным (по морфологии или общей геномной комплементарной ДНК) исходной родительской клетке вследствие природной, случайной или преднамеренной мутации. Клетка-хозяин может включать клетки, трансфицированные или трансформированные экспрессирующим вектором in vivo.
Как используют в настоящем документе, термин "вносимая" в отношении встраиваемой в клетку последовательности нуклеиновой кислоты или полинуклеотидной последовательности, может включать трансфекцию, трансформацию или трансдукцию и относится к внесению последовательности нуклеиновой кислоты или полинуклеотидной последовательности в эукариотическую или прокариотическую клетку, где последовательность нуклеиновой кислоты или полинуклеотидная последовательность может встраиваться в геном клетки (например, хромосомную, плазмидную, пластидную или митохондриальную ДНК), превращаться в автономный репликон или экспрессироваться транзиторно.
Как используют в настоящем документе, термин "неприродный", когда его используют по отношению к микробному организму или микроорганизму по изобретению, предназначен для обозначения того, что микроорганизм содержит по меньшей мере одно генетическое изменение, в норме не встречающееся в природном штамме указанного вида, включая штаммы дикого типа указанного вида. Генетические изменения включают, например, модификации с внесением экспрессируемой нуклеиновой кислоты, кодирующей метаболические полипептиды, другие добавления нуклеиновых кислот, делеции нуклеиновых кислот и/или другие функциональные нарушения генетического материала микроорганизма. Такие модификации включают, например, кодирующие области и их функциональные фрагменты для гетерологичных, гомологичных или и гетерологичных, и гомологичных полипептидов для указанного вида. Дополнительные модификации включают, например, некодирующие регуляторные области, в которых модификации изменяют экспрессию гена или оперона. Неприродные микроорганизмы по изобретению могут нести стабильные генетические изменения, что означает микроорганизмы, которые можно культивировать в течение более чем пяти поколений без потери изменения. Как правило, стабильные генетические изменения включают модификации, которые сохраняются более чем у 10 поколений, в частности стабильные модификации могут сохраняться более чем приблизительно у 25 поколений, а более конкретно, стабильные генетические модификации присутствуют более чем у 50 поколений, включая бесконечное количество. Специалисты в данной области понимают, что генетические изменения, включая модификации метаболизма, проиллюстрированные в настоящем документе, описаны в отношении подходящего организма-хозяина, такого как E. coli и соответствующих их метаболических реакций, или подходящего организма-источника для желаемого генетического материала, такого как гены, для желаемого метаболического пути. Однако, учитывая полное секвенирование геномов широкого спектра организмов и высокого уровня профессионализма в области геномики, специалисты в данной области могут легко использовать способы и руководства, предоставленные в настоящем документе, по существу для всех остальных организмов. Например, метаболические изменения E. coli, проиллюстрированные в настоящем документе, можно легко использовать для других видов, внося ту же или аналогичную кодирующую нуклеиновую кислоту из вида, отличного от указанного вида. Такие генетические изменения включают, например, генетические изменения видовых гомологов, в общем и в частности, перестановки ортологичных, паралогичных или неортологичных генов.
Как используют в настоящем документе, "бутадиен" предназначен для обозначения сопряженного неразветвленного диена с молекулярной формулой C4H6, общей формулы CH2=CH-CH=CH2 и с молекулярной массой 54,09 г/моль. Бутадиен также известен в данной области как 1,3-бутадиен, бут-1,3-диен, биэтилен, эритрен, дивинил и винилэтилен.
Как используют в настоящем документе, термин "функционально связанный" может относиться к смежному положению или перестановке конкретных элементов, которые позволяют им для осуществления эффекта действовать совместно. Например, промотор может быть функционально связан с кодирующей последовательностью, если он контролирует транскрипцию кодирующей последовательности.
Как используют в настоящем документе, термин "промотор" может относиться к регуляторной последовательности, которая вовлечена в связывание РНК-полимеразы для инициации транскрипции гена. Промотор может быть индуцибельным промотором или конститутивным промотором. Индуцибельный промотор представляет собой промотор, который активен в определенных регулирующих условиях окружения или развития.
Как используют в настоящем документе, термин "полинуклеотид" или "последовательность нуклеиновой кислоты" может относиться к полимерной форме нуклеотидов любой длины и любой трехмерной структуры и одно- или многоцепочечной форме (например, одноцепочечной, двухцепочечной, трехспиральной и т.д.), которая содержит дезоксирибонуклеотиды, рибонуклеотиды и/или аналоги или модифицированные формы дезоксирибонуклеотидов или рибонуклеотидов, включая модифицированные нуклеотиды или основания или их аналоги. Такие полинуклеотиды или последовательности нуклеиновой кислоты могут кодировать аминокислоты (например, полипептиды или белки, такие как слитые белки). Вследствие вырожденности генетического кода для кодирования конкретной аминокислоты может быть использовано более одного кодона, и настоящее изобретение включает полинуклеотиды, кодирующие конкретную аминокислотную последовательность. Можно использовать модифицированный нуклеотид или аналог нуклеотида любого типа при условии, что полинуклеотид сохраняет желаемую функциональность в условиях использования, включая модификации, которые увеличивают устойчивость к нуклеазам (например, дезокси, 2’-O-Me, тиофосфаты и т.д.). Также, с целью детекции или захвата, можно встраивать метки, например, радиоактивные или нерадиоактивные метки или якоря, например, биотин. Термин "полинуклеотид" также включает пептидные нуклеиновые кислоты (ПНК). Полинуклеотиды могут быть природными или неприродными. Термины "полинуклеотид", "нуклеиновая кислота" и "олигонуклеотид" используют в настоящем документе взаимозаменяемо. Полинуклеотиды могут содержать РНК, ДНК или и РНК, и ДНК и/или их модифицированные формы и/или аналоги. Последовательность нуклеотидов может прерываться ненуклеотидными компонентами. Одну или несколько фосфодиэфирных связей можно заменять альтернативными связывающими группами. Эти альтернативные связывающие группы в качестве неограничивающих примеров включают варианты, где фосфат заменен на P(O)S (тиоат), P(S)S (дитиоат), (O)NR2 (амидат), P(O)R, P(O)OR’, COCH2 (формацеталь), в которых каждый R или R’ независимо представляет собой H или замещенный или незамещенный алкил (1-20 C), необязательно содержащую простой эфир (-O-) связь, арил, алкенил, циклоалкил, циклоалкенил или аралкил. Не все связи в полинуклеотиде должны быть одинаковыми. Полинуклеотиды могут быть линейными или кольцевыми или содержать комбинацию неразветвленных и кольцевых частей.
Как используют в настоящем документе, термин "белок" или "полипептид" может относиться к композиции, состоящей из аминокислот и признаваемой белком специалистами в данной области. В настоящем документе для аминокислотных остатков используют общепринятый однобуквенный или трехбуквенный код. В настоящем документе термины белок и полипептид используют взаимозаменяемо для обозначения полимеров аминокислот любой длины, включая полимеры аминокислот, содержащие связанные (например, слитые) пептиды/полипептиды (например, слитые белки). Полимер может быть неразветвленным или разветвленным, он может содержать модифицированные аминокислоты, и он может прерываться не являющимися аминокислотами молекулами. Термины также включают полимер из аминокислот, который может быть модифицирован в природе или посредством инструментального вмешательства; например, структурой дисульфидной связи, гликозилированием, липидизацией, ацетилированием, фосфорилированием или любой другой манипуляцией или модификацией, такой как конъюгация с меченым компонентом. Также в определение включены, например, полипептиды, содержащие один или несколько аналогов аминокислот (например, включая неприродные аминокислоты и т.д.), а также другие модификации, известные в данной области.
Как используют в настоящем документе, родственные белки, полипептиды или пептиды могут включать варианты белков, полипептидов или пептидов. Варианты белков, полипептидов или пептидов отличаются от исходного белка, полипептида или пептида и/или друг от друга по небольшому количеству аминокислотных остатков. В некоторых вариантах осуществления количество различных аминокислотных остатков представляет собой любое приблизительно из 1, 2, 3, 4, 5, 10, 20, 25, 30, 35, 40, 45 или 50. В некоторых вариантах осуществления варианты отличаются по аминокислотам приблизительно от 1 до приблизительно 10. Альтернативно или дополнительно варианты могут обладать определенной степенью идентичности последовательностей с исходными белком или нуклеиновой кислотой, например, как определяют с использованием средства выравнивания последовательностей, такого как BLAST, ALIGN и CLUSTAL (см., ниже). Например, варианты белков или нуклеиновых кислот могут обладать по меньшей мере приблизительно 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или даже 99,5% идентичности аминокислотных последовательностей с исходной последовательностью.
Как используют в настоящем документе, термин "восстановленный", "выделенный", "очищенный" и "отделенный" может относиться к материалу (например, белку, пептиду, нуклеиновой кислоте, полинуклеотиду или клетке), который отделяют по меньшей мере от одного компонента с которым он ассоциирован в природе. Например, эти термины могут относиться к материалу, который в значительной степени очищен или по существу не содержит компонентов, которые как выявляют, в норме сопровождают его в природном состоянии, например, таком как, интактная биологическая система.
Как используют в настоящем документе, термин "рекомбинантная" может относиться к последовательностям нуклеиновой кислоты или полинуклеотидам, полипептидам или белкам и клеткам на их основе, которые подвергнуты манипуляции человеком так, что они не являются такими же нуклеиновыми кислотами, полипептидами и клетками, как выявляют в природе. Рекомбинантный также может относиться к генетическому материалу (например, последовательностям нуклеиновых кислот или полинуклеотидам, к кодируемым ими полипептидам или белкам, и векторам и клеткам, содержащим такие последовательности нуклеиновых кислот или полинуклеотидов), который был модифицирован с изменением его последовательности или характеристик экспрессии, например, посредством мутирования кодирующей последовательности с получением измененного полипептида, слияния кодирующей последовательности с другой кодирующей последовательностью или геном, помещение гена под контроль другого промотора, экспрессии гена в гетерологичном организме, экспрессии ген на сниженном или повышенном уровнях, условной или конститутивной экспрессии гена, отличным от его природного профиля экспрессии характером, и т.п.
Как используют в настоящем документе, термин "селективный маркер" или "селектируемый маркер" может относиться к гену, способному к экспрессии в клетке-хозяине, который обеспечивает простоту отбора тех хозяев, которые содержат вводимую последовательность нуклеиновой кислоты, полинуклеотид или вектор. Примеры селектируемых маркеров в качестве неограничивающих примеров включают противомикробные вещества (например, гигромицин, блеомицин или хлорамфеникол) и/или гены, которые придают клетке-хозяину метаболическое преимущество, такое как преимущество в питании.
Как используют в настоящем документе, термин "в значительной степени сходный" и "по существу идентичный" в отношении по меньшей мере двух нуклеиновых кислот, полинуклеотидов, белков или полипептидов может означать, что нуклеиновая кислота, полинуклеотид, белок или полипептид содержат последовательности, которые по меньшей мере приблизительно на 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или даже на 99,5% идентичны по сравнению с исходными (например, дикого типа) нуклеиновой кислотой, полинуклеотидом, белком или полипептидом. Идентичность последовательностей можно определять с использованием известных программ, таких как BLAST, ALIGN и CLUSTAL с использованием стандартных параметров (см., например, Altshul et al. (1990) J. Mol. Biol. 215:403-410; Henikoff et al. (1989) Proc. Natl. Acad. Sci. 89:10915; Karin et al. (1993) Proc. Natl. Acad. Sci. 90:5873; и Higgins et al. (1988) Gene 73:237). Программное обеспечение для проведения анализа BLAST общедоступно в National Center for Biotechnology Information. Также можно проводить поиск по базам данных с использованием FASTA (Person et al. (1988) Proc. Natl. Acad. Sci. 85:2444-2448.) В некоторых вариантах осуществления по существу идентичные полипептиды отличаются только по одной или нескольким заменам консервативных аминокислот. В некоторых вариантах осуществления по существу идентичные полипептиды являются иммунологически перекрестно реактивными. В некоторых вариантах осуществления по существу идентичные молекулы нуклеиновой кислоты гибридизуются друг с другом в жестких условиях (например, в диапазоне от средней до высокой жесткости).
Как используют в настоящем документе, термин "трансфекция" или "трансформация" может относиться к введению экзогенной нуклеиновой кислоты или полинуклеотида в клетку-хозяина. Экзогенная нуклеинов кислота или полинуклеотид могут сохраняться в виде неинтегрированного вектора, например, плазмиды, или, альтернативно, могут интегрироваться в геном клетки-хозяина. Термин "трансфицирование" или "трансфекция" предназначен для включения всех общепринятых способов введения нуклеиновой кислоты или полинуклеотида в клетки-хозяева. Примеры способов трансфекции в качестве неограничивающих примеров включают осаждение фосфатом кальция, опосредованную DEAE-декстраном трансфекцию, липофекцию, электропорацию и микроинъекцию.
Как используют в настоящем документе, термины "трансформированная", "стабильно трансформированная" и "трансгенная" могут относиться к клетке, которая содержит неприродную (например, гетерологичную) последовательность нуклеиновой кислоты или полинуклеотидную последовательность, интегрированную в ее геном или в виде эписомной плазмиды, которая сохраняется в нескольких поколениях.
Как используют в настоящем документе, термин "вектор" может относиться к полинуклеотидной последовательности, сконструированной для введения нуклеиновой кислоты в один или несколько типов клеток. Векторы включают клонирующие векторы, экспрессирующие векторы, челночный векторы, плазмиды, фаговые частицы, одно и двухцепочечные кассеты и т.п.
Как используют в настоящем документе, термины "дикого типа", "природные" или "встречающиеся в природе" белки могут относиться к белкам, находимым в природе. Термин "последовательность дикого типа" относится к последовательности аминокислот или нуклеиновой кислоты, находящуюся в природе или встречающуюся в природе. В некоторых вариантах осуществления последовательность дикого типа представляет собой начальную точку программы инженерии белков, например, получения вариантов белков.
Если в настоящем документе не определено иначе, все технические и научные термины, используемые в настоящем документе, имеют то же значение, как обычно понимает специалист в области, к которой принадлежит настоящее изобретение. В Singleton, et al., Dictionary of Microbiology and Molecular Biology, second ed., John Wiley and Sons, New York (1994) и Hale & Markham, The Harper Collins Dictionary of Biology, Harper Perennial, NY (1991) специалисту предоставлен общий словарь многих терминов, используемых в настоящем описании. Кроме того, следует понимать, что любой из субстратов, в любом из описываемых в настоящем документе метаболических путей альтернативно может включать анион или катион этого субстрата.
Числовые диапазоны, приводимые в настоящем документе, являются включающими числа, определяющие диапазоны.
Если не указано иначе, последовательности нуклеиновых кислот записаны слева направо в ориентации от 5’ к 3’; аминокислотные последовательности записаны слева направо в ориентации от N-конца к C-концу, соответственно.
Хотя настоящее изобретения можно осуществлять в различных формах, ниже приведено описание нескольких вариантов осуществления с пониманием того, что настоящее описание следует рассматривать как иллюстрацию изобретения, и оно не предназначено для ограничения описания конкретными проиллюстрированными вариантам осуществления. Заголовки приведены исключительно для удобства и их не следует рассматривать, как какое-либо ограничение изобретения. Варианты осуществления, проиллюстрированные под любым из заголовков, можно комбинировать с вариантами осуществления, проиллюстрированными под любым другим заголовком.
Если явно не указано иначе, числовые значения в различных количественных величинах, определенных в настоящей заявке, использованы в виде приближенных значений так, как если бы минимальным и максимальным значениям в пределах указанных диапазонов предшествовало слово "приблизительно". Также описание диапазонов приведено в качестве непрерывного диапазона, включающего каждое значение между указанными минимальным и максимальным значениями, а также любые диапазоны, которые можно сформировать из таких значений. Также в настоящем документе описаны любое и все отношения (и диапазоны из таких отношений), которые можно сформировать, деля описанное числовое значение на любое другое описанное числовое значение. Таким образом, специалисту понятно, что из числовых значений, представленных в настоящем документе можно однозначно получить множество таких отношений, диапазонов и диапазонов отношений, и во всех случаях такие отношения, диапазоны и диапазоны отношений представляют различные варианты осуществления настоящего изобретения.
Модификация микроорганизма
Микроорганизм любым известным в данной области способом можно модифицировать (например, подвергать генетической инженерии) так, чтобы он содержал и/или экспрессировал (например, включая сверхэкспрессию) один или несколько полинуклеотидов (например, гетерологичные полинуклеотиды и/или негетерологичные полинуклеотиды), кодирующие ферменты одного или нескольких метаболических путей, способные к превращению ферментируемого источника углерода в бутадиен. Микроорганизм может экспрессировать все ферменты одного или нескольких метаболических путей, необходимые для превращения ферментируемого источника углерода в бутадиен, от природы, или его можно модифицировать для экспрессии, например, включая сверхэкспрессию одного или нескольких ферментов одного или нескольких метаболических путей. В некоторых вариантах осуществления микроорганизм может содержать не все ферменты в таком метаболическом пути, и полинуклеотиды, кодирующие отсутствующие ферменты можно вводить в микроорганизм генетически. Например, модифицированный микроорганизм можно модифицировать так, чтобы он содержал один или несколько полинуклеотидов, кодирующих ферменты, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в одно или несколько промежуточных соединений (например, ацетил-КоА и пропионил-КоА; кротонил-КоА и/или муравьиную кислоту) в метаболическом пути получения бутадиена. Дополнительно или альтернативно модифицированный микроорганизм можно модифицировать так, чтобы он содержал один или несколько полинуклеотидов, кодирующих ферменты, которые катализируют превращение одного или нескольких промежуточных соединений (например, ацетил-КоА и пропионил-КоА; кротонил-КоА и/или муравьиную кислоту) в бутадиен. В некоторых вариантах осуществления полинуклеотид может кодировать фермент, который катализирует превращение одного или нескольких промежуточных соединений в метаболическом пути получения бутадиена. В некоторых вариантах осуществления полинуклеотиды можно модифицировать (например, подвергать генетической инженерии) так, чтобы модулировать (например, увеличением или снижением) субстратной специфичности кодируемого фермента, или полинуклеотиды можно модифицировать так, чтобы изменять субстратную специфичность кодируемого фермента (например, полинуклеотид, который кодирует фермент со специфичностью к одному субстрату можно модифицировать так, чтобы фермент получил специфичность к другому субстрату). Предпочтительные микроорганизмы могут содержать полинуклеотиды, кодирующие один или несколько из ферментов, как указано в любой из таблиц 1-3 и на фиг. 1-3.
Микроорганизм может содержать один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в бутадиен. В некоторых вариантах осуществления один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в бутадиен, в качестве неограничивающих примеров могут включать:
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в кетовалерил-КоА, (например, тиолазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кетовалерил-КоА в (R) или (S) 3-гидроксиалерил-КоА (например, гидроксивалерил-КоА-дегидрогеназу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) гидроксиалерил-КоА в 2-пентеноил-КоА (например, гидроксивалерил-КоА-дегидратазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеноил-КоА в 2-пентеновую кислоту (например, пентеноил-КоА-гидролазу или -трансферазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в бутадиен (например, декарбоксилазу 2-пентеновой кислоты);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в 4-пентеновую кислоту (например, перемещающую связи C=C изомеразу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-пентеновой кислоты в бутадиен (например, декарбоксилазу 4-пентеновой кислоты);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеноил-КоА в пент-2,4-диеноил-КоА (например, пентеноил-КоА-дегидрогеназу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пент-2,4-диеноил-КоА в пент-2,4-диеновую кислоту (например, пент-2,4-диеноил-КоА-гидролазу или -трансферазу); и/или
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2,4-пентеновой кислоты в бутадиен (например, декарбоксилазу пент-2,4-диеновой кислоты).
В некоторых вариантах осуществления микроорганизм дополнительно содержит один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозу) в метилмалонил-КоА и /или акрилоил-КоА.
В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все указанные выше полинуклеотиды.
В таблице 1 ниже представлены иллюстративные ферменты, преобразующие ацетил-КоА и пропионил-КоА в бутадиен, а также субстраты, на которые они могут действовать, и продукты, которые они могут продуцировать. Номер фермента, представленного в таблице 1, соответствует нумерации фермента, используемой на фиг. 1, на которой схематически представлено ферментативное превращение ферментируемого источника углерода в бутадиен через промежуточные соединения ацетил-КоА и пропионил-КоА.
и пропионил-КоА
Микроорганизм может содержать один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в бутадиен. В некоторых вариантах осуществления один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в бутадиен, в качестве неограничивающих примеров могут включать:
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротониловый спирт (например, кротонил-КоА-редуктазу (бифункциональную));
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротоновый альдегид (например, дегидрогеназу кротонового альдегида);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонового альдегида в кротониловый спирт (например, дегидрогеназу кротонилового спирта); и/или
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонилового спирта в бутадиен (например, дегидратазу кротонилового спирта).
В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все из указанных выше полинуклеотидов.
В предпочтительных вариантах осуществления микроорганизм дополнительно содержит один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкоза) в кротонил-КоА.
В некоторых вариантах осуществления микроорганизм дополнительно может содержать один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозу) в 3-гидроксибутирил-КоА и/или 4-гидроксибутирил-КоА. В таких вариантах осуществления микроорганизм дополнительно содержит один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидроксибутирил-КоА в кротонил-КоА, и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-гидроксибутирил-КоА в кротонил-КоА.
В таблице 2 ниже представлены иллюстративные ферменты, преобразующие кротонил-КоА в бутадиен, а также субстраты, на которые они могут действовать, и продукты, которые они могут продуцировать. Номер фермента, представленного в таблице 2, соответствует нумерации фермента, используемой на фиг. 2, на которой схематически представлено ферментативное превращение ферментируемого источника углерода в бутадиен через промежуточное соединение кротонил-КоА.
Микроорганизм может содержать один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение муравьиной кислоты в бутадиен. В некоторых вариантах осуществления один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение муравьиной кислоты в бутадиен, в качестве неограничивающих примеров могут включать:
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение CO2 в муравьиную кислоту (например, формиатдегидрогеназу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата и КоА в ацетил-КоА и муравьиную кислоту (например, ацетил-КоА:формиат-C-ацетилтрансферазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение муравьиной кислоты в формил-КоА (например, формил-КоА-трансферазу или -синтетазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-ацетил-КоА в ацетоацетил-КоА (например, ацетоацетил-КоА-тиолазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетоацетил-КоА и формил-КоА в 3,5-кетовалерил-КоА (например, 3,5-кетовалерил-КоА-тиолазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3,5-кетовалерил-КоА в (R)- или (S)-5-гидрокси-3-кетовалерил-КоА (например, 3,5-кетовалерил-КоА-дегидрогеназу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R)- или (S)-5-гидрокси-3-кетовалерил-КоА в (R)- или (S)-3,5-дигидроксиалерил-КоА (например, 5-гидрокси-3-кетовалерил-КоА-дегидрогеназу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R)- или (S)-3,5-дигидроксиалерил-КоА в (R) или (S) 3-гидрокси-4-пентеноил-КоА (например, 3,5-гидроксивалерил-КоА-дегидратазу);
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R)- или (S)-3-гидрокси-4-пентеноил-КоА в 3-гидрокси-4-пентеновую кислоту (например, 3-гидрокси-4-пентеноил-КоА-гидролазу, -трансферазу или -синтетазу); и/или
- один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидрокси-4-пентеновой кислоты в бутадиен (например, декарбоксилазу 3-гидрокси-4-пентеновой кислоты).
В некоторых вариантах осуществления микроорганизм дополнительно содержит один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват.
В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных выше полинуклеотидов, включая все из указанных выше полинуклеотидов.
В таблице 3 ниже представлены иллюстративные ферменты, преобразующие муравьиную кислоту в бутадиен, а также субстраты, на которые они могут действовать, и продукты, которые они могут продуцировать. Номер фермента, представленного в таблице 3, соответствует нумерации фермента, используемой на фиг. 3, на которой схематически представлено ферментативное превращение ферментируемого источника углерода в бутадиен через промежуточное соединение муравьиную кислоту.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в ацетил-КоА и пропионил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в метилмалонил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение метилмалонил-КоА в пропионил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в акрилоил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение акрилоил-КоА в пропионил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в кетовалерил-КоА, (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кетовалерил-КоА в (R) или (S) 3- гидроксивалерил-КоА (например, гидроксивалерил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3-гидроксивалерил-КоА в 2-пентеноил-КоА (например, гидроксивалерил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеноил-КоА в 2-пентеновую кислоту (например, пентеноил-КоА-гидролазу, пентеноил-КоА-трансферазу или пентеноил-КоА-синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в 4-пентеновую кислоту (например, перемещающую связи C=C изомеразу); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-пентеновой кислоты в бутадиен (например, декарбоксилазу 4-пентеновой жирной кислоты или декарбоксилазу 2-пентеновой кислоты). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в этилмалонил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение этилмалонил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение пирувата в ацетил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ацетил-КоА в ацетоацетил-КоА (например, ацетоацетил-КоА-тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ацетоацетил-КоА в 3-гидроксибутирил-КоА (например, 3-гидроксибутирил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение 3-гидроксибутирил-КоА в кротонил-КоА (например, кротоназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение кротонил-КоА в этилмалонил-КоА (например, кротонил-КоА-карбоксилазу/редуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение кротонил-КоА в масляную кислоту (например, бутирил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение масляной кислоты в этилмалонил-КоА (например, лигазу бутаноил-КоА:диоксида углерода); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение этилмалонил-КоА в 2-(формол)бутановую кислоту (например, этилмалонил-КоА-редуктазу (формирующую альдегид)); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-(формол)бутановой кислоты в 2-(гидроксиметил)бутановую кислоту (например, редуктазу 2-(формил)бутановой кислоты (формирующую спирт)); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение этил малонил-КоА в 2-(гидроксиметил)бутановую кислоту (например, этилмалонил-КоА-редуктазу (формирующую спирт)); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-(гидроксиметил)бутановой кислоты в 2-(фосфанилоксиметил)бутановую кислоту (например, киназу 2-(гидроксиметил)бутановой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-(фосфанилоксиметил)бутановой кислоты в 2-(дифосфанилоксиметил)бутановую кислоту (например, киназу 2-(фосфанилоксиметил)бутановой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-(дифосфанилоксиметил)бутановой кислоты в [(E)-бут-2-енокси]фосфанилфосфан (например, декарбоксилазу 2-(дифосфанилоксиметил)бутановой кислоты); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение [(E)-бут-2-енокси]фосфанилфосфана в бутадиен (например, бутадиенсинтетазу). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных выше полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в 4-гидроксибутирил-КоА и 3-гидроксибутирил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-гидроксибутирил-КоА и 3-гидроксибутирил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в PEP; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение PEP в оксалоацетат (например, PEP-карбоксикиназа или PEP-карбоксилазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение PEP в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в ацетил-КоА (например, пируватдегидрогеназу или пируватферредоксиноксидоредуктазу) или оксалоацетат (например, PEP-карбоксикиназу или PEP-карбоксилазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА в ацетоацетил-КоА (например, ацетоацетил-КоА-тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетоацетил-КоА в 3-гидроксибутирил-КоА (например, 3-гидроксибутирил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение оксалоацетата в малат (например, малатдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение малата в фумарат (например, фумаразу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение фумарата в сукцинат (например, фумаратредуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение сукцинат в сукцинил-КоА (например, сукцинил-КоА-трансферазу или сукцинил-КоА-синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение сукцинил-КоА в янтарный полуальдегид (например, сукцинил-КоА-редуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение янтарного полуальдегида в 4-гидроксибутират (например, 4-гидроксибутиратдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение сукцината в 4-гидроксибутират (например, сукцинат редуктазу, фосфопанатеинилазу или 4-гидроксибутиратдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-гидроксибутирата в 4-гидроксибутирил-КоА (например, 4-гидроксибутирил-КоА-трансферазу или 4-гидроксибутирил-КоА-синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-гидроксибутирил-КоА в кротонил-КоА (например, 4-гидроксибутирил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидроксибутирил-КоА в кротонил-КоА (например, кротоназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротоновый альдегид (например, дегидрогеназу кротонового альдегида); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонового альдегида в кротониловый спирт (например, алкогольдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротониловый спирт (например, кротонил-КоА-редуктазу (бифункциональную); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонилового спирта в бутадиен (например, дегидратазу кротонилового спирта). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в акрилоил-КоА и ацетил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение акрилоил-КоА и ацетил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в лактат (например, лактатдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактата в лактоил-КоА (например, лактоил-КоА-трансферазу или -синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактоил-КоА в акрилоил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в ацетил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение акрилоил-КоА и ацетил-КоА в 3-кето-4-пентеноил-КоА (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-кето-4-пентеноил-КоА в (R) или (S) 3-гидрокси-4-пентеноил-КоА (например, 3-кето-4-пентеноил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3-гидрокси-4-пентеноил-КоА в 3-гидрокси-4-пентеновую кислоту (например, 3-гидрокси-4-пентеноил-КоА-трансферазу, -гидролазу или -синтетазу); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидрокси-4-пентеновой кислоты в бутадиен (например, декарбоксилазу 3-гидрокси-4-пентеновой кислоты). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в ацетил-КоА и 3-гидроксипропионил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и 3-гидроксипропионил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в лактат; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактата в лактоил-КоА (например, лактоил-КоА-трансферазу или -синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактоил-КоА в акрилоил-КоА (например, лактоил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение акрилоил-КоА в 3-гидроксипропионил-КоА (например, акрилоил-КоА-гидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в 3-гидроксипропионат; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидроксипропионат в 3-гидроксипропионил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и 3-гидроксипропионил-КоА в 5-гидрокси-3-кетовалерил-КоА (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 5-гидрокси-3-кетовалерил-КоА в (R) или (S) 3,5-дигидрокси-валерил-КоА (например, 5-гидрокси-3-кетовалерил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3,5-дигидрокси-валерил-КоА в (R) или (S) 3-гидрокси-4-пентеноил-КоА (например, 3,5-гидроксивалерил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3-гидрокси-4-пентеноил-КоА в 3-гидрокси-4-пентеновую кислоту (например, 3-гидрокси-4-пентеноил-КоА-гидролазу, -трансферазу или -синтетазу); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидрокси-4-пентеновой кислоты в бутадиен (например, декарбоксилазу 3-гидрокси-4-пентеновой кислоты). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в ацетоацетил-КоА и формил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетоацетил-КоА и формил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в ацетил-КоА и формиат (например, пируватформиатлиазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА в ацетоацетил-КоА (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение CO2 в формиат (например, формиатдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение формиата в формил-КоА (например, формил-КоА-трансферазу или формил-КоА-синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение формил-КоА и ацетоацетил-КоА в 3,5-кетовалерил-КоА (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3,5-кетовалерил-КоА в 5-гидрокси-3-кетовалерил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 5-гидрокси-3-кетовалерил-КоА в (R) или (S) 3,5-дигидрокси-валерил-КоА (например, 5-гидрокси-3-кетовалерил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3,5-дигидрокси-валерил-КоА в (R) или (S) 3-гидрокси-4-пентеноил-КоА (например, 3,5-гидроксивалерил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3-гидрокси-4-пентеноил-КоА в 3-гидрокси-4-пентеновую кислоту (например, 3-гидрокси-4-пентеноил-КоА-гидролазу, -трансферазу или -синтетазу); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидрокси-4-пентеновой кислоты в бутадиен (например, декарбоксилазу 3-гидрокси-4-пентеновой кислоты). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в ацетил-КоА и 3-гидроксипропионил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и 3-гидроксипропионил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в акрилоил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение акрилоил-КоА в 3-гидроксипропионил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в 3-гидроксипропионат; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3-гидроксипропионата в 3-гидроксипропионил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и 3-гидроксипропионил-КоА в 5-гидрокси-3-кетовалерил-КоА (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 5-гидрокси-3-кетовалерил-КоА в (R) или (S) 3,5-дигидрокси-валерил-КоА (например, 5-гидрокси-3-кетовалерил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение (R) или (S) 3,5-дигидрокси-валерил-КоА в 3,5-гидроксипентановую кислоту (например, киназу 3,5-гидроксипентановой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 3,5-гидроксипентановой кислоты в фосфат 3,5-гидроксипентановой кислоты (например, киназу 3,5-гидроксипентановой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение фосфата 3,5-гидроксипентановой кислоты в дифосфат 3,5-гидроксипентановой кислоты (например, киназу фосфата 3,5-гидроксипентановой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение дифосфата 3,5-гидроксипентановой кислоты в 1-бутенил-4-дифосфат (например, декарбоксилазу дифосфата гидроксипентановой кислоты); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 1-бутенил-4-дифосфата в бутадиен (например, бутадиенсинтетазу). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных выше полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в этилмалонил-КоА, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение этилмалонил-КоА в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение пирувата в ацетил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ацетил-КоА в ацетоацетил-КоА (например, ацетоацетил-КоА-тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ацетоацетил-КоА в 3-гидроксибутирил-КоА (например, 3-гидроксибутирил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение 3-гидроксибутирил-КоА в кротонил-КоА (например, кротоназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение кротонил-КоА в этилмалонил-КоА (например, кротонил-КоА-карбоксилазу/редуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение кротонил-КоА в масляную кислоту (например, бутирил-КоА-дегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение масляной кислоты в этилмалонил-КоА (например, лигазу бутаноил-КоА:диоксида углерода); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение этилмалонил-КоА в 2-гидроксиметилбутановую кислоту (например, этилмалонил-КоА-редуктазу, алкогольдегидрогеназу или альдегиддегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-гидроксиметилбутановой кислоты в 2-бутенил-4-дифосфат (например, 2-гидроксиметилбутаноаткиназу, киназу гидроксиметилбутаноатфосфата или декарбоксилазу 2-гидроксиметилбутаноатдифосфата); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-гидроксиметилбутановой кислоты в 2-бутенил-4-фосфат; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-бутенил-4-фосфата в бутадиен, и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-бутенил-4-дифосфата в бутадиен (например, бутадиенсинтетазу). В некоторых вариантах осуществления предоставлен микроорганизм, содержащий один или несколько из указанных выше полинуклеотидов, включая все из указанных выше полинуклеотидов.
Также предоставлен микроорганизм, содержащий один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в лактат и ацетил-КоА и оксалоацетат, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактат и ацетил-КоА и оксалоацетата в бутадиен, включая в качестве неограничивающих примеров: один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода (например, глюкозы) в PEP; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение PEP в пируват; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пирувата в ацетил-КоА; один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактата в лактоил-КоА (например, лактат КоА-трансферазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение лактоил-КоА в акрилоил-КоА (например, лактоил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение акрилоил-КоА в пропионил-КоА (например, акрилоил-КоА-оксидоредуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение пропионил-КоА в кетовалерил-КоА (например, тиолазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кетовалерил-КоА в 2-пентеноил-КоА (например, кетовалерил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеноил-КоА в 2-пентеновую кислоту (например, пентеноил-КоА-гидролазу, -трансферазу или -синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в бутадиен (например, декарбоксилазу 2-пентеновой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 2-пентеновой кислоты в 4-пентеновую кислоту (например, переносящую C=C связи изомеразу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-пентеновой кислоты в бутадиен (например, декарбоксилазу 4-пентеновой кислоты); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение оксалоацетата в малат (например, малатдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение малата в фумарат (например, фумаразу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение фумарата в сукцинат (например, фумаратредуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение сукцината в сукцинил-КоА (например, сукцинил-КоА-трансферазу/синтазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение сукцинил-КоА в янтарный полуальдегид (например, сукцинил-КоА-редуктазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение янтарного полуальдегида в 4-гидроксибутират (например, 4 гидроксибутиратдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-гидроксибутирата в 4-гидроксибутирил-КоА (например, 4-гидроксибутирил-КоА-трансферазу или 4-гидроксибутирил-КоА-синтетазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение 4-гидроксибутирил-КоА в кротонил-КоА (например, 4-гидроксибутирил-КоА-дегидратазу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротоновый альдегид (например, дегидрогеназу кротонового альдегида); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в кротониловый спирт (например, кротонил-КоА-редуктазу или бифункциональную алкогольдегидрогеназу); один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонового альдегида в кротониловый спирт (например, алкогольдегидрогеназу); и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонилового спирта в бутадиен (например, дегидратазу кротонилового спирта).
Любой из микроорганизмов, предоставленных в настоящем документе, необязательно может содержать один или несколько полинуклеотидов, кодирующих ферменты, которые обеспечивают сбалансированное по окислительно-восстановительным реакциям превращение ферментируемого источника углерода в бутадиен.
Микроорганизм могут представлять собой архей, бактерий или эукариот. В некоторых вариантах осуществления бактерии представляют собой Propionibacterium, Propionispira, Clostridium, Bacillus, Escherichia, Pelobacter или Lactobacillus, например, включая Pelobacter propionicus, Clostridium propionicum, Clostridium acetobutylicum, Lactobacillus, Propionibacterium acidipropionici или Propionibacterium freudenreichii. В некоторых вариантах осуществления эукариоты представляют собой дрожжей, нитевидных грибов, простейших или водоросли. В некоторых вариантах осуществления дрожжи представляют собой Saccharomyces cerevisiae, Zymomonas mobilis или Pichia pastoris.
В некоторых вариантах осуществления изобретение предусматривает модификацию (например, инженерию) одного или нескольких из ферментов, предоставленных в настоящем документе. Такую модификацию можно проводить для изменения субстратной специфичности фермента и/или для изменения (например, снижения) его активности в отношении других субстратов для увеличения его селективности в отношении данного субстрата. Дополнительно или альтернативно можно подвергать инженерии один или несколько ферментов, как предоставлено в настоящем документе, с изменением (например, увеличением, например, включая увеличение его каталитической активности или его субстратной специфичности) одного или нескольких из его свойств.
Для расширения или изменения субстратной специфичности фермента (например, переключения субстратной специфичности фермента с одного субстрата на другой субстрат) модифицировать (например, подвергать мутагенезу или получать варианты) можно любой из ферментов (например, полинуклеотид, кодирующий фермент) любым известным в данной области способом. Такие способы в качестве неограничивающих примеров включают EpPCR Pritchard et al., J. Theor. Biol. 234:497-509 (2005)); амплификацию по типу катящегося кольца с внесением ошибок (epRCA) Fujii et al., Nucleic Acids Res. 32:e145 (2004); и Fujii et al., Nat. Protoc. 1:2493-2497 (2006)); смешение ДНК или семейств Stemmer, Proc. Natl. Acad. Sci. U.S.A. 91:10747-10751 (1994); и Stemmer, Nature 370:389-391 (1994)); ступенчатую достройку (Этап) Zhao et al., Nat. Biotechnol. 16:258-261 (1998)); и/или рекомбинацию со случайными праймерами (RPR) Shao et al., Nucleic Acids Res 26:681-683 (1998)).
Дополнительные иллюстративные способы мутагенеза полинуклеотидов включают рекомбинацию гетеродуплексов (Volkov et al., Nucleic Acids Res. 27:e18 (1999); и Volkov et al., Methods Enzymol. 328:456-463 (2000)); случайный химерогенез на временных матрицах (RACHITT) (Coco et al., Nat. Biotechnol. 19:354-359 (2001)); рекомбинантную достройку на укороченных матрицах (RETT) (Lee et al., J. Molec. Catalysis 26:119-129 (2003)); генные перестановки с вырожденными олигонуклеотидами (DOGS) (Bergquist and Gibbs, Methods Mol. Biol. 352:191-204 (2007); Bergquist et al., Biomol. Eng. 22:63-72 (2005); Gibbs et al., Gene 271:13-20 (2001)); пошаговое укорочение для получения гибридных ферментов (ITCHY) (Ostermeier et al., Proc. Natl. Acad. Sci. U.S.A. 96:3562-3567 (1999); и Ostermeier et al., Nat. Biotechnol. 17:1205-1209 (1999)); пошаговое укорочение для получения гибридных ферментов с тионуклеотидами (THIO-ITCHY) (Lutz et al., Nucleic Acids Res. 29:E16 (2001)); SCRATCHY (Lutz et al., Proc. Natl. Acad. Sci U.S.A. 98:11248-11253 (2001)); мутагенез со случайным смещением (RNDM) (Bergquist et al., Biomol. Eng. 22:63-72 (2005)); насыщающий мутагенез последовательностей (SeSaM) (Wong et al., Biotechnol. J. 3:74-82 (2008); Wong et al., Nucleic Acids Res. 32:e26 (2004); и Wong et al., Anal. Biochem. 341:187-189 (2005)); синтетическая перестановка (Ness et al., Nat. Biotechnol. 20:1251-1255 (2002)); технология замены и вырезания нуклеотидов NexT (Muller et al., Nucleic Acids Res. 33:e117 (2005)). Дополнительные иллюстративные способы включают независимую от гомологии последовательностей рекомбинацию белков (SHIPREC) (Sieber et al., Nat. Biotechnol. 19:456-460 (2001)); насыщающий мутагенез участка гена™ (GSSM™) (Kretz et al., Methods Enymol. 388:3-11 (2004)); комбинаторный кассетный мутагенез (CCM) (Reidhaar-Olson et al., Methods Enymol. 208:564-586 (1991); и Reidhaar-Olson et al. Science 241:53-57 (1988)); комбинаторный мутагенез с несколькими кассетами (CMCM) (Reetz et al., Angew. Chem. Int. Ed Engl. 40:3589-3591 (2001)) и способ мутаторных штаммов (Selifonova et al., Appl. Environ. Microbiol. 67:3645-3649 (2001); Low et al., J. Mol. Biol. 260:359-3680 (1996)). Дополнительные иллюстративные способы включают сканирующий мутагенез (LTM) (Rajpal et al., Proc. Natl. Acad. Sci. U.S.A. 102:8466-8471 (2005)); технологию пересборки генов (настраиваемой пересборки генов™ (TGR™) поставляемую Verenium Corporaiton), автоматическое проектирование белков in silico (PDA) (Hayes et al., Proc. Natl. Acad. Sci. U.S.A. 99:15926-15931 (2002)) и пошаговый насыщающий мутагенез (ISM) (Reetz et al., Nat. Protoc. 2:891-903 (2007); и Reetz et al., Angew. Chem. Int. Ed Engl. 45:7745-7751 (2006)).
В некоторых вариантах осуществления для изменения одного или нескольких из ферментов, описываемых в настоящем документе, можно использовать выравнивание последовательностей и сравнительное моделирование белков. Гомологичное моделирование или сравнительное моделирование относится к построению модели желаемого белка в атомном разрешении из первичной аминокислотной последовательности и экспериментальной трехмерной структуры сходного белка. Эта модель может обеспечить определение участка связывания субстрата у фермента и идентификацию конкретных положений аминокислоты, которые можно заменять на другие природные аминокислоты для изменения его субстратной специфичности.
В практическом осуществлении изобретения можно использовать варианты или последовательности со значительной идентичностью или гомологией с полинуклеотидами, кодирующими ферменты, как описано в настоящем документе. Такие последовательности можно обозначать как варианты последовательностей или модифицированные последовательности. Другими словами, полинуклеотидную последовательность можно модифицировать так, чтобы она еще сохраняла способность кодировать полипептид, проявляющий желаемую активность. Таким образом, такие варианты последовательностей или модифицированные последовательности являются эквивалентами. Как правило, вариант последовательности или модифицированная последовательность может быть по меньшей мере приблизительно на 40%-60%, предпочтительно приблизительно на 60%-80%, более предпочтительно приблизительно на 80%-90% и даже более предпочтительно приблизительно на 90%-95% идентична с природной последовательностью.
В некоторых вариантах осуществления микроорганизм можно модифицировать для экспрессии, например, включая сверхэкспрессию, одного или нескольких ферментов, как предоставлено в настоящем документе. Микроорганизм можно модифицировать способами генетической инженерии (например, рекомбинантных технологий), классическими микробиологическими способами или комбинацией таких способов, а также для получения генетически модифицированного микроорганизма он может включать природные генетические варианты. Некоторые из таких способов в общих чертах описаны, например, в Sambrook et al., 1989, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Labs Press.
Микроорганизм может включать микроорганизм, в котором вставлен, удален или модифицирован (например, подвергнут мутации; например, посредством вставки, делеции, замены и/или инверсии нуклеотидов) полинуклеотид таким образом, что такие модификации обеспечивают в микроорганизме желаемый эффект экспрессии (например, сверхэкспрессии) одного или нескольких ферментов, как предоставлено в настоящем документе. Генетические модификации, которые приводят к усилению экспрессии или функции генов можно обозначать как амплификацию, сверхпродукцию, сверхэкспрессию, активацию, усиление, добавление или положительную регуляцию гена. Добавление клонированных генов для усиления экспрессии генов может включать поддержание клонированного гена(ов) на реплицирующихся плазмидах или интеграция клонированного гена(ов) в геном продуцирующего организма. Кроме того, усиление экспрессии желаемых клонированных генов может включать функциональное связывание клонированного гена(ов) с природными или гетерологичными элементами контроля транскрипции.
Когда желательно, экспрессия одного или нескольких из ферментов, предоставленных в настоящем документе, находится под контролем регуляторной последовательности, прямо или опосредованно контролирующей экспрессию фермента при реакции ферментации в зависимости от времени.
В некоторых вариантах осуществления микроорганизм трансформируют или трансфицируют генетическим переносчиком, таким как экспрессирующий вектор, содержащий экзогенную полинуклеотидную последовательность, кодирующую ферменты, предоставленные по настоящему документу.
Полинуклеотидные конструкции, получаемые для введения прокариотическому или эукариотическому хозяину, как правило, но не всегда, могут содержать систему репликации (например, вектор), распознаваемую хозяином, включая желаемый полинуклеотидный фрагмент, кодирующий желаемый полипептид, и предпочтительно, но необязательно, также могут включать последовательности регуляции инициации транскрипции и трансляции, функционально связанные с кодирующим полипептид участком. Экспрессирующие системы (экспрессирующие векторы) могут включать, например, участок начала репликации или последовательность автономной репликации (ARS) и последовательности контроля экспрессии, промотор, энхансер и необходимые участки обработки информации, такие как участки связывания рибосомы, участки сплайсинга РНК, участки полиаденилирования, последовательности терминации трансляции, последовательности стабилизации мРНК, нуклеотидные последовательности, гомологичные хромосомной ДНК хозяина и/или участок множественного клонирования. Также, при необходимости, можно включать сигнальные пептиды, предпочтительно из секретируемых полипептидов того же или родственного вида, которые позволяют белку пересекать клеточные мембраны и/или закрепляться в них или позволяют клетке секретировать их.
Векторы можно конструировать стандартными способами (см., например, Sambrook et al., Molecular Biology: A Laboratory Manual, Cold Spring Harbor, N.Y. 1989 и Ausubel, et al., Current Protocols in Molecular Biology, Greene Publishing, Co. N.Y, 1995).
Манипуляции с полинуклеотидами по настоящему изобретению, включая полинуклеотиды, кодирующие один или несколько из ферментов, описанных в настоящем документе, как правило, проводят в рекомбинантных векторах. Общеизвестными являются множество векторов, включая бактериальные плазмиды, бактериофаги, искусственные хромосомы, эписомные векторы и экспрессирующие гены векторы, которые все можно применять. Вектор, пригодный по настоящему изобретению, можно выбирать так, чтоб он вмещал кодирующую белок последовательность желаемого размера. После манипуляций по клонированию in vitro вектором можно трансформировать подходящую клетку-хозяина. Клетки-хозяева могут быть прокариотическими, такими как любой из ряда бактериальных штаммов, или могут быть эукариотическими, такими как дрожжи или клетки других грибов, клетки насекомых или амфибий или клетки млекопитающих, например, включая клетки грызунов, обезьян или человека. Каждый вектор содержит различные функциональные компоненты, которые, как правило, включают участок клонирования, участок начала репликации и по меньшей мере один ген селективного маркера. Если данный вектор является экспрессирующим вектором, он дополнительно несет один или несколько из следующего: энхансерный элемент, промотор, последовательности терминации транскрипции и сигнальные последовательности, где каждый расположен вблизи участка клонирования так, что они функционально связаны с геном, кодирующим представителя множества полипептидов по изобретению.
Векторы, включающие клонирующие и экспрессирующие векторы, могут содержать последовательности нуклеиновой кислоты, которые позволяют вектору реплицироваться в одном или нескольких выбранных клетках-хозяевах. Например, последовательность может представлять собой последовательность, которая позволяет вектору реплицироваться независимо от хромосомной ДНК хозяина и может включать участки начала репликации или последовательности автономной репликации. Такие последовательности хорошо известны для множества бактерий, дрожжей и вирусов. Например, участок начала репликации из плазмиды pBR322 подходит для большинства грамотрицательных бактерий, участок начала репликации 2-микронной плазмиды подходит для дрожжей, а различные вирусные участки начала репликации (например, SV 40, аденовируса) пригодны для клонирования векторов в клетках млекопитающих. Как правило, участок начала репликации не является необходимым для экспрессирующих векторов у млекопитающих, за исключением случаев, когда их используют в клетках млекопитающих, способных к репликации высоких уровней ДНК, таких как клетки COS.
Клонирующий или экспрессирующий вектор может содержать селективный ген, также обозначаемый как селектируемый маркер. Этот ген кодирует белок, необходимый для выживания или роста трансформированных клеток-хозяев, выращиваемых в селективной среде для культивирования. Таким образом, клетки-хозяева, не трансформированные вектором, содержащим селективный ген, не выживают в среде для культивирования. Типичные селективные гены кодируют белки, которые придают устойчивость к антибиотикам и другим токсинам, например, ампициллину, неомицину, метотрексату, гигромицину, тиострептону, апрамицину или тетрациклину, дополняют ауксотропную недостаточность или обеспечивают критически важные питательные вещества, недоступные в средах для выращивания.
Репликацию векторов можно проводить в E. coli (например, в штаммах TB1 или TG1, DH5α, DH10β, JM110). Использовать можно селектируемый маркер E. coli, например, ген β-лактамазы, который придает устойчивость к антибиотику ампициллину. Эти селектируемые маркеры можно получать из плазмид E. coli, таких как плазмиды pBR322 или pUC, такая как pUC18, или pUC19, или pUC119.
Экспрессирующие векторы могут содержать промотор, который распознает организм-хозяин. Промотор может быть функционально связан с представляющей интерес кодирующей последовательностью. Такой промотор может быть индуцибельным или конститутивным. Полинуклеотиды функционально связаны, когда эти полинуклеотиды находятся в зависимости, позволяющей им функционировать заданным для них способом.
Промоторы, пригодные для использования у прокариотических хозяев могут включать, например, промоторные системы α-лактамазы и лактозы, промоторные системы щелочной фосфатазы, триптофана (trp), промотор эритромицина, промотор апрамицина, промотор гигромицина, промотор метиленомицин и гибридные промоторы, такие как промотор tac. Кроме того, можно использовать конститутивные или индуцибельные у хозяина промоторы. Также промоторы для применения в бактериальных системах, как правило, содержат последовательность Шайна-Дальгарно, функционально связанную с кодирующей последовательностью.
Вирусные промоторы, получаемые из геномов вирусов, включают промоторы из вируса полиомы, вируса куриной оспы, аденовируса (например, аденовируса 2 или 5), вируса простого герпеса (промотор тимидинкиназы), вируса папилломы крупного рогатого скота, вируса саркомы птиц, цитомегаловируса, ретровируса (например, MoMLV или RSV LTR), вируса гепатита B, промотор миелопролиферативного вируса саркомы (MPSV), VISNA и вируса 40 обезьян (SV40). Гетерологичные промоторы млекопитающих включают, например, промотор актина, промотор иммуноглобулина, промоторы белков теплового шока.
Ранний и поздний промоторы вируса SV40 подходящим способом получают в качестве рестрикционного фрагмента, который также содержит участки участок начала репликации вируса SV40 (см., например, Fiers et al., Nature, 273:113 (1978); Mulligan and Berg, Science, 209:1422-1427 (1980); и Pavlakis et al., Proc. Natl. Acad. Sci. USA, 78:7398-7402 (1981)). Предранний промотор цитомегаловируса человека (CMV) подходящим способом получают в качестве рестрикционного фрагмента HindIII E (см., например, Greenaway et al., Gene, 18:355-360 (1982)). Для использования в экспрессирующих векторах по настоящему изобретению пригоден промотор с широким кругом хозяев, такой как ранний промотор SV40 или LTR вируса саркомы Рауса.
Как правило, можно использовать сильный промотор для обеспечения высокого уровня транскрипции и экспрессии желаемого продукта. Среди эукариотических промоторов, которые идентифицированы как сильные промоторы для высокоуровневой экспрессии, находятся ранний промотор SV40, основной поздний промотор аденовируса, промотор металлотионеина-I мыши, длинный концевой повтор вируса саркомы Рауса и предранний промотор цитомегаловируса человека (CMV или CMV IE). В одном из вариантов осуществления промотор представляет собой ранний промотор SV40 или CMV.
Используемые промоторы могут быть конститутивными или регулируемыми, например, индуцибельными. Иллюстративные индуцибельные промоторы включают промоторы jun, fos и металлотионеина и промоторы белков теплового шока. Индуцибельными могут быть один или оба промотора единиц транскрипции. В одном из вариантов осуществления с конститутивного промотора экспрессируется GFP, тогда как транскрипция гена, кодирующего один или несколько ферментов, как описано в настоящем документе, и/или амплифицируемого селектируемого маркера, находится под контролем индуцибельного промотора.
Область регуляции транскрипции у высших эукариот может содержать энхансерную последовательность. Известно множество энхансерных последовательностей генов млекопитающих, например, из генов глобина, эластазы, альбумина, α-фетопротеина и инсулина. Подходящим энхансером является энхансер вируса эукариотической клетки. Примеры включают энхансер SV40 на поздней стороне участка начала репликации (п.н. 100-270), энхансер предраннего промотора цитомегаловируса (Boshart et al. Cell 41:521 (1985)), энхансер полиомы на поздней стороне участка начала репликации и энхансеры аденовирусов (также об энхансерных элементах для активации эукариотических промоторов см., например, Yaniv, Nature, 297:17-18 (1982)). Энхансерные последовательности можно вводить в вектор в положении 5’ или 3’ от представляющего интерес гена, но предпочтительно они расположены в участке с 5’-конца от промотора.
Экспрессирующие векторы дрожжей и млекопитающих могут содержать прокариотические последовательности, которые облегчают размножение вектора в бактериях. Таким образом, вектор может содержать другие компоненты, такие как участок начала репликации (например, последовательность нуклеиновой кислоты, которая позволяет вектору реплицироваться в одной или нескольких выбранных клетках-хозяевах), гены устойчивости к антибиотикам для отбора в бактериях и/или стоп-кодон amber, который может позволить трансляции проходить через кодон. Дополнительно можно встраивать эукариотический селективный ген(ы). Как правило, в клонирующих векторах участок начала репликации представляет собой участок, который позволяет векторы реплицироваться независимо от хромосомной ДНК хозяина, и включает участки начала репликации или последовательности автономной репликации. Такие последовательности хорошо известны, например, участок начала репликации ColE1 у бактерий. Для клонирующих векторов в клетках млекопитающих пригодны различные вирусные участки начала репликации (например, SV40, полиомы, аденовируса, VSV или BPV). Как правило, для экспрессии в клетках млекопитающих эукариотический репликон не нужен кроме случаев, когда необходима экстрахромосомная (эписомальная) репликация (например, как правило, участок начала репликации SV40 можно использовать только потому, что он содержит ранний промотор).
Для облегчения вставки и экспрессии с конструкций и экспрессирующих векторов различных генов, кодирующие ферменты, как описано в настоящем документе, конструкции можно проектировать по меньшей мере с одним участком клонирования для вставки любого гена, кодирующего любой фермент, описываемый в настоящем документе. Участок клонирования может представлять собой участок множественного клонирования, например, содержащий несколько участков рестрикции.
Для получения количеств ДНК для этапов субклонирования или для введения в эукариотические клетки-хозяева плазмиды можно выращивать в бактериальных клетках-хозяевах. Трансфекцию эукариотических клеток-хозяев можно проводить любым способом, хорошо известным в данной области. Способы трансфекции включают липофекцию, электропорацию, соосаждение с фосфатом кальция, опосредуемая хлоридом рубидия или поликатионами трансфекция, слияние протопластов и микроинъекцию. Предпочтительно, трансфекция представляет собой стабильную трансфекцию. Предпочтителен способ трансфекции, который обеспечивает оптимальную частоту трансфекции и экспрессию конструкции в конкретных типе и линии клеток-хозяев. Подходящие способы можно определять посредством обычных процедур. Для получения стабильных трансфектантов конструкции интегрируют так, чтобы они стабильно сохранялись в хромосоме хозяина.
Векторы можно вводить в выбранные клетки-хозяева любым из ряда подходящих способов, известных специалистам в данной области. Например, векторные конструкции можно вводить в соответствующие клетки любым из ряда способов трансформации плазмидных векторов. Например, для введения в бактерии очищенной ДНК все еще широко используют стандартную трансформацию бактерий, опосредуемую хлоридом кальция (см., например, Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.), но также можно использовать электропорацию и конъюгацию (см., например, Ausubel et al., 1988, Current Protocols in Molecular Biology, John Wiley & Sons, Inc., NY, N.Y.).
Для введения векторных конструкций в дрожжи или клетки других грибов можно использовать способы химической трансформации (например, Rose et al., 1990, Methods in Yeast Genetics, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.). Трансформированные клетки можно выделять на селективных средах, соответствующих используемому селектируемому маркеру. Альтернативно или, кроме того, для идентификации трансформированных клонов, планшеты и фильтры, поднятые с планшетов, можно сканировать на флуоресценцию GFP.
Для введения в клетки млекопитающих векторов, содержащих дифференциально экспрессируемые последовательности, используемый способ может зависеть от формы вектора. Плазмидные векторы можно вводить любым из ряда способов трансфекции, включая, например, опосредуемую липидами трансфекцию ("липофекцию"), опосредуемую DEAE-декстраном трансфекцию, электропорацию или осаждение фосфатом кальция (см., например, Ausubel et al., 1988, Current Protocols in Molecular Biology, John Wiley & Sons, Inc., NY, N.Y.).
Широкодоступными являются реагенты для липофекции и способы, подходящие для транзиторной трансфекции широкого спектра трансформированных и нетрансформированных или первичных клеток, деля липофекцию привлекательным способом введения конструкций в эукариотические клетки, и в частности клетки млекопитающих, в культуре. Например, доступны наборы LipofectAMINE™ (Life Technologies) или LipoTaxi™ (Stratagene). Другие компании, предлагающие реагенты и способы для липофекции, включают Bio-Rad Laboratories, CLONTECH, Glen Research, InVitrogen, JBL Scientific, MBI Fermentas, PanVera, Promega, Quantum Biotechnologies, Sigma-Aldrich и Wako Chemicals USA.
Клетка-хозяин может быть способной экспрессировать конструкцию, кодирующую желаемый белок, процессировать белок и транспортировать секретируемый белок на клеточную поверхность для секреции. Процессинг включает одновременные с трансляцией и посттрансляционные модификации, такие как отщепление лидерного пептида, присоединение GPI, гликозилирование, убиквитинилирование и образование дисульфидных связей. Предпочтительными являются культуры иммортализованных клеток-хозяев, поддающихся трансфекции и культивированию клеток in vitro, и т.п., как правило, используемое в генетической инженерии. Примеры подходящих линий клеток-хозяев млекопитающих представляют собой линия почки обезьян CV1, трансформированная SV40 (COS-7, ATCC CRL 1651); линия эмбриональной почки человека (293 или производные 293, адаптированные для выращивания в суспензионной культуре, Graham et al., J. Gen Virol., 36:59 (1977); клетки почки детеныша хомяка (BHK, ATCC CCL 10); клетки яичника китайского хомяка DHFR (ATCC CRL-9096); клетки CHO dp12, производные CHO/DHFR- (EP 307247, опубликованный 15 марта 1989 года); клетки Сертоли мыши (TM4, Mather, Biol. Reprod., 23:243-251 (1980)); клетки почки обезьяны (CV1 ATCC CCL 70); клетки почки африканской зеленой мартышки (VERO-76, ATCC CRL-1587); клетки шейки матки карциномы человек (HELA, ATCC CCL 2); клетки почки собаки (MDCK, ATCC CCL 34); клетки печени серой крысы (BRL 3A, ATCC CRL 1442); клетки легкого человека (W138, ATCC CCL 75); клетки печени человека (Hep G2, HB 8065); опухоль молочной железы мыши (MMT 060562, ATCC CCL51); клетки TRI (Mather et al., Annals N.Y. Acad. Sci., 383:44-68 (1982)); линия клеток острого лимфобластного лейкоза человека PEER (Ravid et al. Int. J. Cancer 25:705-710 (1980)); клетки MRC 5; клетки FS4; линия гепатомы человека (Hep G2), клетки человека HT1080, клетки KB, клетки JW-2, клетки Detroit 6, клетки NIH-3T3, клетки гибридомы и миеломы, также являются подходящими эмбриональные клетки, используемые для получения трансгенных животных (например, зиготы и эмбриональные стволовые клетки).
Подходящие клетки-хозяева для клонирования или экспрессии полинуклеотидов (например, ДНК) в векторах могут включать, например, прокариот, дрожжи, или клетки высших эукариот. Подходящие для этой цели прокариоты включают эубактерии, такие как грамотрицательные или грамположительные организмы, например, Enterobacteriaceae, такие как Escherichia, например, E. coli, Enterobacter, Erwinia, Klebsiella, Proteus, Salmonella, например, Salmonella typhimurium, Serratia, например, Serratia marcescans, и Shigella, а также Bacilli, такие как B. subtilis и B. licheniformis (например, B. licheniformis 41 P, описанная в DD 266710, опубликованном 12 апреля 1989 года), Pseudomonas, такие как P. aeruginosa, и Streptomyces. Одним из предпочтительных клонирующих хозяев E. coli является E. coli 294 (ATCC 31446), хотя подходящими являются и другие штаммы, такие как E. coli B, E. coli X1776 (ATCC 31537), E. coli JM110 (ATCC 47013) и E. coli W3110 (ATCC 27325).
В дополнение к прокариотам, подходящими клонирующими или экспрессирующими хозяевами для векторов, содержащих полинуклеотиды, кодирующие один или несколько ферментов, могут быть эукариотические микроорганизмы, такие как нитевидные грибы или дрожжи. Наиболее широко используемыми из низших эукариотических микроорганизмов-хозяев являются Saccharomyces cerevisiae или обычные пекарские дрожжи. Однако общедоступным и пригодным по настоящему документу является ряд других родов, видов и штаммов, таких хозяев как Schizosaccharomyces pombe; Kluyveromyces, такие как, например, K. lactis, K. fragilis (ATCC 12424), K. bulgaricus (ATCC 16045), K. wickeramii (ATCC 24178), K. waltii (ATCC 56500), K. drosophilarum (ATCC 36906), K. thermotolerans и K. marxianus; Yarrowia (EP 402226); Pichia pastors (EP 183070); Candida; Trichoderma reesia (EP 244234); Neurospora crassa; Schwanniomyces, такие как Schwanniomyces occidentalis; и нитевидных грибов, например, таких хозяев, как, Neurospora, Penicillium, Tolypocladium и Aspergillus, такие как A. nidulans и A. niger.
Когда фермент гликозилирован, подходящие клетки-хозяева для экспрессии можно получить из многоклеточных организмов. Примеры клеток беспозвоночных включают клетки растений и насекомых. Идентифицировано множество бакуловирусных штаммов и вариантов и соответствующих пермиссивных клеток-хозяев насекомых таких, как Spodoptera frugiperda (гусеница), Aedes aegypti (комар), Aedes albopictus (комар), Drosophila melanogaster (плодовая мушка), и Bombyx mori (шелкопряд). Общедоступными для трансфекции является множество вирусных штаммов, например, вариант L-1 NPV Autographa californica и штамм Bm-5 NPV Bombyx mori, и такие вирусы можно использовать в качестве вируса по настоящему документе по настоящему изобретению, в частности для трансфекции клеток Spodoptera frugiperda.
В качестве клеток-хозяев также можно использовать культуры растительных клеток хлопка, кукурузы, картофеля, сои, петунии, томата, табака, ряски и других растительных клеток.
Примеры подходящих клеток-хозяев млекопитающих представляют собой клетки яичника китайского хомяка, включая клетки CHOK1 (ATCC CCL61), DXB-11, DG-44, и клетки яичника китайского хомяка/-DHFR (CHO, Urlaub et al., Proc. Natl. Acad. Sci. USA 77: 4216 (1980)); линия почки обезьяны CV1, трансформированная SV40 (COS-7, ATCC CRL 1651); линия эмбриональной почки человека (293 или клетки 293, субклонированные для выращивания в суспензионной культуре (Graham et al., J. Gen Virol. 36: 59, 1977); клетки почки детеныша хомяка (BHK, ATCC CCL 10); клетки Сертоли мыши (TM4, Mather, (Biol. Reprod. 23: 243-251, 1980); клетки почки обезьяны (CV1 ATCC CCL 70); клетки почки африканской зеленой мартышки (VERO-76, ATCC CRL-1587); клетки шейки матки карциномы человек (HELA, ATCC CCL 2); клетки почки собаки (MDCK, ATCC CCL 34); клетки печени серой крысы (BRL 3A, ATCC CRL 1442); клетки легкого человека (W138, ATCC CCL 75); клетки печени человека (Hep G2, HB 8065); опухоль молочной железы мыши (MMT 060562, ATCC CCL51); клетки TRI (Mather et al., Annals N.Y Acad. Sci. 383: 44-68 (1982)); клетки MRC 5; клетки FS4 и линия гепатомы человека (Hep G2).
Клетки-хозяева трансформируют или трансфицируют описанными выше экспрессирующими или клонирующими векторами с получением одного или нескольких ферментов, как описано в настоящем документе, или полинуклеотидами, кодирующими один или несколько ферментов, как описано в настоящем документе, и культивируют в общепринятых питательных средах, при необходимости модифицированных для индукции промоторов, отбора трансформантов или амплификации генов, кодирующих желаемые последовательности.
Клетки-хозяева, содержащие желаемые последовательности нуклеиновой кислоты, кодирующие описываемые ферменты, можно культивировать во множестве сред. Подходящими для культивирования клеток-хозяев являются коммерчески доступные среды, такие как среда Хэма F10 (Sigma), минимальная питательная среда ((MEM), Sigma), RPMI-1640 (Sigma) и модифицированная Дульбекко среда Игла ((DMEM), Sigma). Кроме того, в качестве среды для культивирования клеток-хозяев можно использовать любую из сред, описанных в Ham et al., Meth. Enz. 58: 44, (1979); Barnes et al., Anal. Biochem. 102: 255 (1980); патентах США №№ 4767704; 4657866; 4927762; 4560655 или 5122469; WO90103430; WO 87/00195; или патенте США с регистрационным № 30985. Любую из этих сред можно по мере необходимости дополнять гормонами и/или другими факторами роста (такими как инсулин, трансферрин или эпидермальный фактор роста), солями (такими как хлорид натрия, кальция, магния и фосфатом), буферами (такими как HEPES), нуклеотидами (такими как аденозин и тимидин), антибиотиками (такими как лекарственное средство гентамицин™), микроэлементами (определяемыми как неорганические соединения, как правило, находящиеся в конечных концентрациях в микромолярном диапазоне) и глюкозой или эквивалентным источником энергии. Также в подходящих концентрациях можно включать любые другие необходимые добавки, которые известны специалистам в данной области. Условия культивирования, такие как температура, pH и т.п., являются такими, как ранее использовали для клетки-хозяина, выбранной для экспрессии, и очевидны специалисту в данной области.
Полинуклеотиды и кодируемые ферменты
Для применения по настоящему изобретению предусмотрен любой известный полинуклеотид (например, ген), который кодирует фермент или его вариант, который способен катализировать ферментативное превращение, например, включая фермент, как указано в любой из таблиц 1-3 или на фиг. 1-3. Такие полинуклеотиды можно модифицировать (например, подвергать генетической инженерии) для модуляции (например, увеличения или снижения) субстратной специфичности кодируемого фермента, или полинуклеотиды можно модифицировать для изменения субстратной специфичности кодируемого фермента (например, полинуклеотид, который кодирует фермент со специфичность к субстрату можно модифицировать так, чтобы фермент получил специфичность к альтернативному субстрату). Предпочтительные микроорганизмы могут содержать полинуклеотиды, кодирующие один или несколько из ферментов, как указано в любой из таблиц 1-3 и на фиг. 1-3.
В некоторых вариантах осуществления микроорганизм может содержать оксидоредуктазу, такую как гидроксивалерил-КоА-дегидрогеназа, кротонил-КоА-редуктаза (бифункциональная), дегидрогеназа кротонового альдегида, дегидрогеназа кротонилового спирта, 3,5-кетовалерил-КоА-дегидрогеназа, или оксидоредуктазу, как указано в SEQ ID NO: 103-123. В некоторых вариантах осуществления микроорганизм может содержать трансферазу, такую как пентеноил-КоА-трансфераза, пент-2,4-диеноил-КоА-трансфераза, формил-КоА-трансфераза, 3-гидрокси-4-пентеноил-КоА-трансфераза, или трансферазу, как указано в SEQ ID NO: 1-28. В некоторых вариантах осуществления микроорганизм может содержать гидролазу, такую как пентеноил-КоА-гидролаза, пент-2,4-диеноил-КоА-гидролаза, 3-гидрокси-4-пентеноил-КоА-гидролаза, или гидролазу, как указано в SEQ ID NO: 29-33. В некоторых вариантах осуществления микроорганизм может содержать КоА-синтетазу, такую как формил-КоА-синтетаза, или КоА-синтетазу, как указано в SEQ ID NO: 34-36. В некоторых вариантах осуществления микроорганизм может содержать кетотиолазу, такую как тиолаза, ацетил-КоА:формиат-C-ацетилтрансфераза, ацетоацетил-КоА-тиолаза, 3,5-кетовалерил-КоА-тиолаза, или кетотиолазу, как указано в SEQ ID NO: 58-78. В некоторых вариантах осуществления микроорганизм может содержать дегидрогеназу, такую как пентеноил-КоА-дегидрогеназа, формиатдегидрогеназа, или дегидрогеназу, как указано в SEQ ID NO: 124-139. В некоторых вариантах осуществления микроорганизм может содержать дегидратазу, такую как гидроксивалерил КоА-дегидратаза, дегидратаза кротонилового спирта, 3,5-гидроксивалерил-КоА-дегидратаза, или дегидратазу, как указано в SEQ ID NO: 37-55. В некоторых вариантах осуществления микроорганизм может содержать изомеразу, такую как переносящая C=C связи изомераза, или изомеразу, как указано в SEQ ID NO: 99-102. В некоторых вариантах осуществления микроорганизм может содержать декарбоксилазу, такую как декарбоксилаза 2-пентеновой кислоты, декарбоксилаза 4-пентеновой кислоты, декарбоксилаза пент-2,4-диеновой кислоты, декарбоксилаза 3-гидрокси-4-пентеновой кислоты, или декарбоксилазу, как указано в SEQ ID NO: 79-98.
Ферменты для катализа превращений на фиг. 1-3 классифицированы в таблице 4 по номеру комиссии по ферментам (EC), функции и этапу на фиг. 1-3, в котором они катализируют превращение (таблица 4).
Этапы D и I на фиг. 1, и этапы C и I на фиг. 3 могут катализировать трансферазы из EC 2.8.3, например, включая трансферазу, которая катализирует обратимый перенос группы КоА с одной молекулы на другую. Для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий фермент КоА-трансферазу, например, включая полинуклеотиды, указанные в таблице 5 ниже.
Этапы D и I на фиг. 1 и этап I на фиг. 3 могут катализировать гидролазы из EC 3.1.2, например, включая гидролазы с широким диапазоном субстратов, способные гидролизовать 2-пентеноил-КоА, 2,4-пентеноил-КоА и 3-гидроксипентеноил-КоА в соответствующие им кислоты. Для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий гидролазу, например, включая полинуклеотиды, указанные в таблице 6 ниже.
Этап C на фиг. 3 может катализировать КоА-синтетаза из EC 6.2.1., например, включая КоА-синтетазу с широким диапазоном субстратов, способную активировать муравьиную кислоту в формил-КоА. Для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий КоА-синтетазу, например, включая полинуклеотиды, указанные в таблице 7 ниже.
Гидратацию двойной связи могут катализировать гидратазные ферменты из EC 4.2.1, а удаление воды с формированием двойной связи могут катализировать дегидратазные ферменты из EC 4.2.1. Гидратазные ферменты иногда являются обратимыми и также могут катализировать дегидратацию. Подобным образом, дегидратазные ферменты иногда являются обратимыми и также могут катализировать гидратацию. Добавление или удаление воды из данного субстрата необходимо на этапе C на фиг. 1, этапе D на фиг. 2 и этапе H на фиг. 3. Для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий гидратазу или дегидратазу, например, включая полинуклеотиды, указанные в таблице 8 ниже.
Линалоолдегидратаза-изомераза из штамма 65Phen Castellaniella defragrans катализирует стереоспецифическую гидратацию бета-мирцена в (3S)-линалоол, изомеризацию (3S)-линалоола в гераниол, и вовлечена в начальные этапы анаэробного разрушения монотерпена бета-мирцена. Кроме того, эта линалоолдегидратаза-изомераза катализирует обратные реакции, т.е. изомеризацию гераниола в линалоол и дегидратацию линалоола в мирцен. В этом направлении можно наблюдать образование мирцена из гераниола как процесс детоксикации монотерпенового спирта. Другие дегидратазы-изомеразы включают 4-гидроксибутирил-КоА-дегидратазу/винилацетил-КоА-дельтаизомеразу. Дегидратазу/изомеразу можно конструировать стандартными способами для акцептирования в качестве субстрата кротонилового спирта, таким образом представляя подходящего кандидата для этого этапа D на фиг. 2 ниже:
Этап A на фиг. 1 и этапы C, D и E на фиг. 3 требуют конденсации ацетил-КоА или ацетоацетил-КоА с формил-КоА или пропионил-КоА. Такую конденсацию может катализировать кетотиолаза, указанная в EC 2.3.1. Однако для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий кетотиолазу, например, включая полинуклеотиды, указанные в таблице 10 ниже.
Этапы E, G, и J на фиг. 1 и этап J на фиг. 2 может катализировать фермент декарбоксилаза, как указано в классе EC 4.1.1. для декарбоксилирования структурно сходных субстратов в 2-пентеновую кислоту, 2,4-пентендиеновую кислоту (фиг. 1) и 3-гидроксипентеновую кислоту (фиг. 3) охарактеризовано и представлено множество декарбоксилаз. Иллюстративные ферменты для этапа J на фиг. 1 включают декарбоксилазу сорбиновой кислоты и аконитатдекарбоксилазу, как указано в EC 4.1.1.16. Иллюстративные ферменты для этапов G и E на фиг. 1 могут включать декарбоксилазу p450 жирной кислоты из Jeotgalicoccus. Иллюстративные ферменты для этапа J на фиг. 3 могут включать ферменты, как указано в EC 4.1.1.33, такие как дифосфомевалонатдекарбоксилазу. Однако для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий декарбоксилазу, например, включая полинуклеотиды, указанные в таблице 11 ниже.
Этап F на фиг. 1 включает изомеразный фермент, как указано в EC 5.3.3. Иллюстративные ферменты для этого этапа включают изопентенилдифосфатдельтаизомеразу. Однако для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий изомеразу, например, включая полинуклеотиды, указанные в таблице 12 ниже.
Этап B на фиг. 1, этапы A, B и C на фиг. 2 и этапы F и G на фиг. 3 включают восстановление кетона в спирт, и его могут катализировать оксидоредуктазные ферменты из класса EC 1.1.1. Однако для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий оксидоредуктазу, например, включая полинуклеотиды, указанные в таблице 13 ниже.
Этап I на фиг. 1 и этап A на фиг. 3 включают дегидрогеназу, как указано в EC 1.3.1 или 1.2.99. Однако для применения по настоящему изобретению предусмотрен любой известный полинуклеотид, кодирующий дегидрогеназу, например, включая полинуклеотиды, указанные в таблице 14 ниже.
Способы получения бутадиена
Бутадиен (например, продукт ферментации) можно получать посредством приведения одного или нескольких генетически модифицированных микроорганизмов, предоставленных по настоящему документу, в контакт с ферментируемым источником углерода. Предпочтительно такие способы могут включать приведение ферментируемого источника углерода в ферментационных средах, включая подходящие условия и в течение подходящего периода времени, в контакт с микроорганизмом, содержащим один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в любое из промежуточных соединений, предоставленных в таблицах 1-3 или на фиг. 1-3, и один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений, предоставленных в таблицах 1-3 или на фиг. 1-3 в бутадиен; и экспрессию в микроорганизме одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или несколько промежуточных соединений, предоставленных в таблицах 1-3 или на фиг. 1-3, и одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений, предоставленных в таблицах 1-3 или на фиг. 1-3 в бутадиен, с получением бутадиена. В некоторых вариантах осуществления превращение ферментируемого источника углерода в бутадиен положительно по АТФ (например, в нем образуется свободный АТФ на моль продуцируемого бутадиена; продуцируется АТФ в качестве побочного продукта), и, при комбинации с потребляющим NADH метаболическим путем, это может обеспечить анаэробный процесс получения бутадиена. Например, превращение ферментируемого источника углерода, такого как глюкоза или фруктоза в бутадиен может давать приблизительно 1 моль АТФ на моль продуцируемого бутадиена.
Иллюстративные ферментируемые источники углерода в качестве неограничивающих примеров могут включать сок сахарного тростника, патоку сахарного тростника, гидролизованный крахмал, гидролизованные лигноцеллюлозные вещества, глюкозу, сахарозу, фруктозу, лактат, лактозу, ксилозу, пируват или глицерин в любой их форме или смеси. В некоторых вариантах осуществления источник углерода представляет собой моносахарид, олигосахарид или полисахарид.
Метаболические пути, приводящие к получению промышленно значимых соединений, таких как бутадиен, включают окислительно-восстановительные (редокс) реакции. Например, при ферментации глюкоза в ряду ферментативных реакций окисляется до меньших молекул с сопутствующим высвобождением энергии. Высвобождающиеся электроны из одной реакции в другую переносят универсальные переносчики электронов, такие как никотинамидадениндинуклеотид (NAD) и никотинамидадениндинуклеотидфосфат (NAD(P)), которые действуют в качестве кофакторов для оксидоредуктазных ферментов. При катаболизме у микроорганизмов глюкозу окисляют ферменты, использующие в качестве кофакторов окисленную форму кофакторов (NAD(P)+ и/или NAD+), таким образом, получая восстановительные эквиваленты в форме восстановленных кофакторов (NAD(P)H и NADH). Для продолжения ферментации, требуется сбалансированный по окислительно-восстановительным реакциям метаболизм, например, кофакторы необходимо регенерировать посредством восстановления метаболических соединений микробной клетки. В некоторых вариантах осуществления новые метаболические пути, описываемые в настоящем документе, являются преимущественными в том, что они обеспечивают превращение ферментируемого источника углерода в бутадиен по метаболическому пути, который перераспределяет конечные продукты с достижением окислительно-восстановительного баланса.
Некоторые ключевые параметры для эффективной ферментации ферментируемого источника углерода одним или несколькими модифицированными микроорганизмами, как описано в настоящем документе, включают: возможность выращивать микроорганизмы до большей плотности клеток, увеличенный выход желаемых продуктов, увеличенное количество объемной продуктивности, удаление нежелательных кометаболитов, улучшенная утилизация дешевых источников углерода и азота, адаптация к варьирующим условиям ферментера, увеличенная продукция первичного метаболита, увеличенная продукция вторичного метаболита, повышенная устойчивость к кислым условиям, повышенная устойчивость к основным условиям, повышенная устойчивость к органическим растворителям, повышенная устойчивость к высокосолевым условиям и повышенная устойчивость к высоким или низким температурам. Недостаточность по любому из этих параметров может приводить к высокой стоимости производства, неспособности к захвату или удержанию доли рынка и/или неспособности к поставке ферментируемых конечных продуктов на рынок.
Способы по настоящему изобретению можно адаптировать к общепринятым ферментационным биореакторам (например, периодическая ферментация, периодическая ферментация с добавлением субстрата, ферментация с рециркуляцией клеток и непрерывная ферментация). В некоторых вариантах осуществления микроорганизм (например, генетически модифицирован микроорганизм), как предоставляют по настоящему документу, культивируют в жидких ферментационных средах (например, погруженная культура), что приводит к выделению ферментируемого продукта(ов) в ферментационные среды. Ферментация может происходить в биореакторе, сконфигурированном в виде смесителя, барботажной колонны, воздухоструйного реактора или любой другой подходящей конфигурации, известной в данной области. В одном из вариантов осуществления конечный ферментируемый продукт(ы) можно выделять из ферментационных сред любым подходящим известным в данной области способом.
В некоторых вариантах осуществления получение ферментируемого продукта может происходить в течение начальной фазы быстрого роста микроорганизма. В одном из вариантов осуществления получение ферментируемого продукта может происходить в течение второго периода, в котором культуру поддерживают на стадии медленного роста или отсутствия роста. В одном из вариантов осуществления получение ферментируемого продукта может происходить в течение более чем одного периода роста микроорганизма. В таких вариантах осуществления количество ферментируемого продукта, получаемое в единицу времени в основном представляет собой функцию метаболической активности микроорганизма, физиологических условий культивирования (например, pH, температуры, состава среди) и количества микроорганизмов, присутствующих в процессе ферментации.
В некоторых вариантах осуществления продукт ферментации восстанавливают из периплазмы или среда для культивирования в качестве секретируемого метаболита. В одном из вариантов осуществления продукт ферментации выделяют из микроорганизма, например, когда у микроорганизма отсутствует секреторный сигнал, соответствующий продукту ферментации. В одном из вариантов осуществления микроорганизмы разрушают и среду для культивирования или лизат центрифугируют для удаления дебриса из частиц клеток. Затем, если необходимо, можно отделять мембранную фракцию и фракцию растворимых белков. Затем представляющий интерес продукт ферментации из оставшегося раствора или суспензии супернатанта можно выделять, например, посредством перегонки, фракционирования, хроматографии, осаждения, фильтрации и т.п. В одном из вариантов осуществления продукты ферментации выделяют посредством одного или нескольких из: перегонки, реакционной перегонки, азеотропной перегонки и экстрактивной перегонки.
Способы по настоящему изобретению предпочтительно проводят в анаэробных условиях. Можно ли проводить способ получения аэробно или анаэробно определяют степень восстановления продукта, а также необходимость АТФ для его синтеза. Для получения бутадиена посредством анаэробных превращений микроорганизмами или, по меньшей мере, используя способ с уменьшенным потреблением кислорода, следует избегать окислительно-восстановительного дисбаланса. Несколько типов этапов обмена веществ включают окислительно-восстановительные реакции, включая некоторые из превращений, как указано в таблицах 1-3 или на фиг. 1-3. Такие окислительно-восстановительные реакции включают перенос электронов, опосредуемый участием окислительно-восстановительных кофакторов, таких как NADH, NADPH и ферредоксин. Так как количества окислительно-восстановительных кофакторов в клетке ограничено, то для обеспечения продолжения прохождения метаболических процессов кофакторы необходимо восстанавливать. Во избежание такого окислительно-восстановительного дисбаланса следует конструировать альтернативные пути восстановления кофакторов, а в некоторых случаях можно предоставлять дополнительные источники получения АТФ. Альтернативно, процессы окисления и восстановления можно разделять пространственно в биоэлектрохимических системах (Rabaey and Rozendal, 2010, Nature reviews, Microbiology, vol 8: 706-716).
В определенном варианте осуществления окислительно-восстановительный дисбаланс можно устранять, используя субстраты (например, ферментируемые источники углерода), которые являются более окисленными или более восстановленными. Например, если утилизация субстрата приводит к дефициту или избытку электронов, необходимость в кислороде можно обойти использованием субстратов, которые являются более восстановленными или окисленными, соответственно. Например, глицерин, который является основным побочным продуктом получения биодизельного топлива, является более восстановленным, чем сахара и, таким образом, более подходящим для синтеза соединений, получение которых из сахара приводит к окислению кофакторов, таких как янтарная кислота. В некоторых вариантах осуществления, если превращение субстрата в продукт приводит к дефициту электронов, можно добавлять дополнительные субстраты, которые функционируют в качестве доноров электронов (Babel 2009, Eng. Life Sci. 9,285-290). Важным критерием для анаэробного использования дополнительных субстратов является то, что их окислительно-восстановительный потенциал является выше, чем окислительно-восстановительный потенциал NADH (Geertman et al., 2006, FEMS Yeast Res. 6, 1193-1203). Если превращение субстрата в продукты приводит к избытку электронов можно добавлять дополнительные субстраты, которые функционируют в качестве акцепторов электронов.
Способы получения полибутадиена и других соединений из бутадиена
Бутадиен при комнатной температуре или в условиях ферментирования (20-45°C) является газообразным, и его получение в процессе ферментации приводит к получению газа, который может накапливаться в свободном пространстве ферментационного резервуара, и который можно откачивать и концентрировать. Бутадиен можно очищать от ферментационных газов, включающих газообразный спирт, CO2 и другие соединения, посредством экстракции растворителем, низкотемпературных процессов, перегонки, фракционирования, хроматографии, осаждения, фильтрации и т.п.
Бутадиен, получаемый любым из процессов или способов, описываемых в настоящем документе, можно превращать в полибутадиен. Альтернативно, бутадиен, получаемый способами, описываемыми в настоящем документе, можно полимеризовать с другими олефинами с получением сополимеров, таких как сополимеры акрилонитрил-бутадиен-стирол (ABS), акрилонитрил-бутадиен (ABR) или стирол-бутадиен (SBR), бутилрезина BR (RB), полибутадиеновый каучук (PBR), нитриловый каучук и полихлоропрен (неопрен). Применения этих синтетических каучуков или пластиковых эластомеров включают производство шин, пластмасс, подметок, обувных каблуков, технических изделий, бытовых устройств, неопрена, бумажных покрытий, перчаток, прокладок и герметиков.
Без дополнительного описания полагают, что специалист в данной области, используя предыдущее описание и последующие иллюстративные примеры, может получать и использовать средства по настоящему изобретению и на практике осуществлять указанные в формуле изобретения способы. Приводимые далее демонстрационные примеры предназначены для облегчения практического осуществления настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие оставшуюся часть изобретения.
ПРИМЕРЫ
Пример 1: Модификация микроорганизма для получения бутадиена.
Микроорганизм, такой как бактерия, можно генетически модифицировать для получения бутадиена из ферментируемого источника углерода, например, включая глюкозу.
В иллюстративном способе микроорганизм можно подвергать генетической инженерии любыми известными в данной области способами так, чтобы он содержал: i.) один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в ацетил-КоА и пропионил-КоА, и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ацетил-КоА и пропионил-КоА в бутадиен; ii.) один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в кротонил-КоА, и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение кротонил-КоА в бутадиен; или iii.) один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение ферментируемого источника углерода в муравьиную кислоту, и/или один или несколько полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение муравьиной кислоты в бутадиен.
Альтернативно, микроорганизм, у которого отсутствует несколько ферментов (например, один или несколько функциональных ферментов, которые являются каталитически активными) для превращения ферментируемого источника углерода в бутадиен, можно генетически модифицировать так, чтобы он содержал один или несколько полинуклеотидов, кодирующих ферменты (например, функциональные ферменты, например, включая любой фермент, описываемый в настоящем документе) в метаболическом пути катализа превращения ферментируемого источника углерода в бутадиен, который отсутствует у микроорганизма.
Пример 2: Ферментация источника углерода посредством генетически модифицированного микроорганизма с получением бутадиена.
Генетически модифицированный микроорганизм, как получают в примере 1 выше, можно использовать для ферментации источника углерода с получением бутадиена.
В иллюстративном способе предварительно простерилизованную среду для культивирования, содержащую ферментируемый источник углерода (например, 9 г/л глюкозы, 1 г/л KH2PO4, 2 г/л (NH4)2HPO4, 5 мг/л FeSO4⋅7H2O, 10 мг/л MgSO4⋅7H2O, 2,5 мг/л MnSO4⋅H2O, 10 мг/л CaCl2⋅6H2O, 10 мг/л CoCl2⋅6H2O и 10 г/л дрожжевого экстракта) помещают в биореактор.
При ферментации анаэробные условия поддерживают, например, посредством пропускания через среду для культивирования азота. Подходящую для ферментации температуру (например, приблизительно 30°C) поддерживают любым известным в данной области способом. pH, близкий к физиологическому (например, приблизительно 6,5), поддерживают, например, посредством автоматического добавления гидроксида натрия. Среду в биореакторе перемешивают, например, приблизительно при 50 об/мин. Ферментацию проводят до завершения.
Затем полученный бутадиен общепринятыми способами выделяют из среды для культивирования. Когда продукты ферментации восстанавливают посредством перегонки, бутадиеновую фракцию необязательно можно полимеризовать с получением полибутадиена. Фракции после перегонки, содержащие другие промежуточные соединения метаболического пути бутадиена (если они присутствуют) можно подвергать дальнейшей ферментации в биореакторе с получением дополнительного бутадиена.
Если не указано иначе, все значения, выражающие количества ингредиентов, такие свойства, как молекулярная масса, условия реакции и т.д., используемые в описании и формуле изобретения, следует понимать как модифицируемые во всех случаях выражением "приблизительно". Таким образом, если не указано иначе, указанные в описании и приложенной формуле изобретения числовые параметры являются приближениями, которые могут варьировать в зависимости от желаемых свойств, которые необходимо получить по настоящему изобретению. Как минимум, и не в качестве попытки ограничения применение основных положений эквивалентов в объеме формулы изобретения, каждый численный параметр по меньшей мере следует рассматривать с учетом количества указанных значащих цифр и используя стандартные правила округления.
Несмотря на то, что числовые диапазоны и параметры, указывающие на широкую область изобретения, являются приближениями, числовые значения, указанные в конкретных примерах приведены настолько точно насколько возможно. Однако любое числовое значение, по существу содержит определенную погрешность, неизбежно возникающую вследствие среднеквадратического отклонения, выявляемого при его соответствующем опытном определении.
Формы единственного числа и подобные указания, используемые в контексте описания изобретения (особенно в контексте приводимой ниже формулы изобретения) следует рассматривать, как относящиеся к форме единственного числа и к форме множественного числа, если в настоящем документе не указано иначе или явно не диктуется контекстом. Перечисление диапазонов значений в настоящем документе предназначено только для того, чтобы служить в качестве способа сокращения отдельного указания каждого отдельного значения, попадающего в диапазон. Если в настоящем документе не указано иначе, каждое отдельное значение включено в описания, как если бы его отдельно указывали в настоящем документе. Если в настоящем документе не указано иначе или иным образом не очевидно из контекста, все способы, описываемые в настоящем документе, можно проводить в любом подходящем порядке. Использование любого и всех примеров или приблизительных формулировок (например, "такой как"), приводимых в настоящем документе, предназначено исключительно для лучшего описания изобретения и не предназначено для ограничения области изобретения, иначе чем формулой изобретения. Ни одну из формулировок в описании не следует рассматривать, как указывающую на какой-либо не входящий в формулу изобретения элемент, необходимый для практического осуществления изобретения.
Группировки альтернативных элементов или вариантов осуществления изобретения, описываемых в настоящем документе, не следует рассматривать, как ограничения. Каждого представителя группы можно указать и заявлять отдельно или в любой комбинации с другими представителями группы или другими элементами, представленными в настоящем документе. Полагают, что один или более представителей группы можно включать в группу или удалять из группы по причинам удобства и/или патентоспособности. Когда происходит любое такое включение или удаление, полагают, что описание содержит модифицированную группу, таким образом, удовлетворяя письменному описанию всех групп Маркуша, используемых в прилагаемой формуле изобретения.
Определенные варианты осуществления настоящего изобретения описаны в настоящем документе, включая лучший способ осуществления изобретения, известный авторам изобретения. Понятно, что специалистам в данной области после прочтения приведенного выше описания будут очевидны вариации этих описанных вариантов осуществления. Авторы изобретения рассчитывают, что специалисты в данной области при необходимости используют такие вариации, и авторы изобретения не предполагают практического осуществления изобретения иначе, чем конкретно описано в настоящем документе. Таким образом, настоящее описание включает все модификации и эквиваленты объекта изобретения, перечисленные в прилагаемой к нему формуле изобретения, в рамках применимого закона. Кроме того, если в настоящем документе не указано иначе или иным образом не вступает в явное противоречие с контекстом, в изобретение включена любая комбинация описанных выше элементов во всех их возможных вариациях.
Дополнительно конкретные варианты осуществления, описанные в настоящем документе, могут быть ограничены в формуле изобретения с использованием формулировок "состоящий из" и/или "по существу состоящий из". При использовании в формуле изобретения, или при подаче, или при добавлении поправок, связывающая формулировка "состоящий из" исключает любой элемент, этап или ингредиент, не указанный в формуле изобретения. Связывающая формулировка "по существу состоящий из" ограничивает область формулы изобретения указанными материалами или этапами и тем, что существенно не влияет на основные и новые характеристики. Приведенные таким образом в формуле изобретения варианты осуществления изобретения по существу или явно описаны и задействованы в настоящем документе.
Следует понимать, что варианты осуществления изобретения, описываемые в настоящем документе, являются иллюстрацией основных положений настоящего изобретения. В объеме изобретения находятся другие модификации, которые можно использовать. Таким образом, в качестве примера, а не в качестве ограничения, в соответствии с указаниями в настоящем документе можно использовать альтернативные конфигурации по настоящему изобретению. Таким образом, настоящее изобретение не ограничено тем, что точно представлено и описано.
Хотя настоящее изобретение описано и проиллюстрировано в настоящем документе посредством указания различных конкретных материалов, способов и примеров, следует понимать, что изобретение не ограничено конкретными комбинациями материалов и способов, выбранных для этой цели. Как понятно специалистам в данной области может подразумеваться множество вариаций таких характеристик. Следует понимать, что описание и примеры следует рассматривать исключительно как иллюстрацию, притом что точный объем и сущность изобретения указаны в приложенной ниже формуле изобретения. Все указанные в настоящей заявке ссылки, патенты и патентные заявки полностью включены в настоящий документ в качестве ссылки.









































































































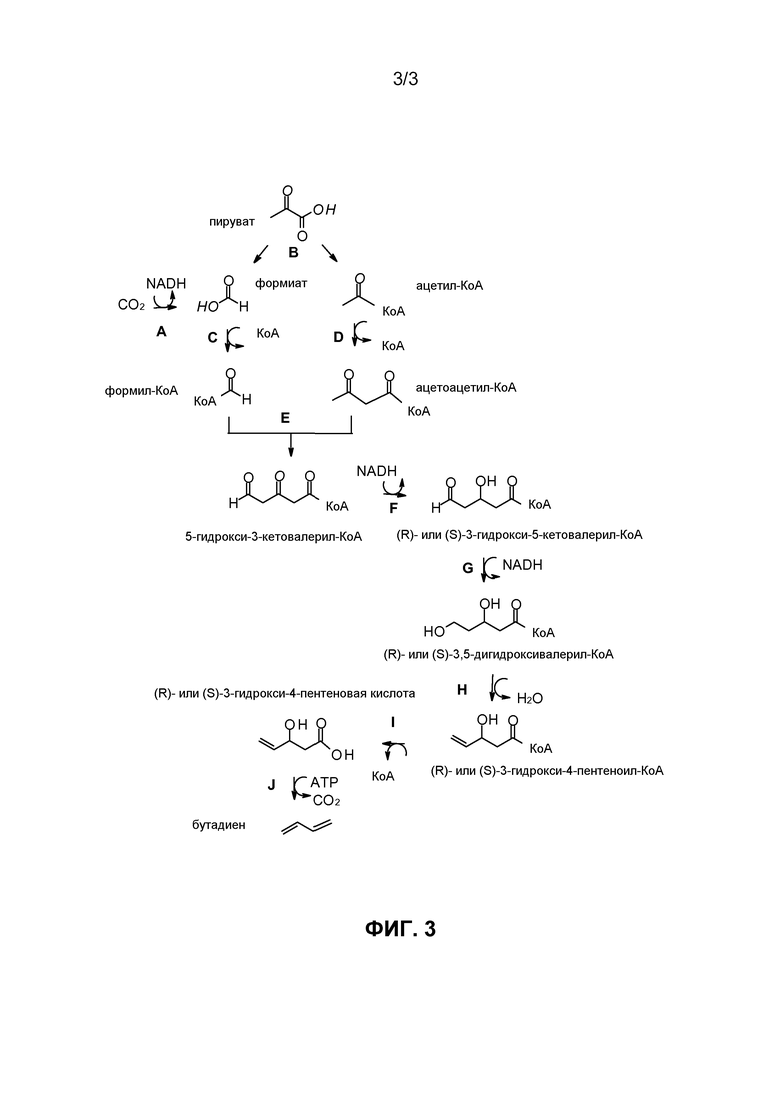
Группа изобретений относится к области биотехнологии. Представлен генетически модифицированный микроорганизм для получения бутадиена, представляющий собой бактерию, дрожжи, нитевидные грибы, простейшие или водоросли и содержащий один или более полинуклеотидов, кодирующих ферменты в метаболическом пути, катализирующие превращение ферментируемого источника углерода в кротонил-КоА, и один или более полинуклеотидов, кодирующих ферменты в метаболическом пути, катализирующие превращение кротонил-КоА в бутадиен, где указанными ферментами являются или кротонил-КоА-редуктаза (бифункциональная) (Е.С.1.1.1) и дегидратаза кротонилового спирта (Е.С.4.2.1, 4.2.1.127), или дегидрогеназа кротонилового альдегида (Е.С.1.2.1), дегидрогеназа кротонилового спирта (Е.С.1.1.1, 1.1.1.1) и дегидратаза кротонилового спирта (Е.С.4.2.1, 4.2.1.127). Представлен способ получения бутадиена из ферментируемого источника углерода путем его контактирования с указанным микроорганизмом. Группа изобретений позволяет осуществлять более экономичное анаэробное ферментативное получение бутадиена. 2 н. и 16 з.п. ф-лы, 3 ил., 14 табл., 2 пр.
1. Способ получения бутадиена из ферментируемого источника углерода, включающий:
a) обеспечение ферментируемого источника углерода;
b) приведение ферментируемого источника углерода в контакт с микроорганизмом, содержащим один или более полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или более промежуточных соединений в метаболическом пути получения бутадиена, и один или более полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, в ферментационных средах; и
c) экспрессию в микроорганизме одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или более промежуточных соединений в метаболическом пути получения бутадиена, и одного или нескольких полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или нескольких промежуточных соединений в бутадиен, с получением бутадиена,
где одно или более промежуточных соединений в метаболическом пути получения бутадиена представляет собой кротонил-КоА,
где все из ферментов выбираются из или (i) кротонил-КоА-редуктазы (бифункциональной) (Е.С.1.1.1) и дегидратазы кротонилового спирта (Е.С.4.2.1, 4.2.1.127), или (ii) дегидрогеназы кротонового альдегида (Е.С.1.2.1), дегидрогеназы кротонилового спирта (Е.С.1.1.1, 1.1.1.1) и дегидратазы кротонилового спирта (Е.С.4.2.1, 4.2.1.127),
где микроорганизм представляет собой бактерии, дрожжи, нитевидные грибы, простейшие или водоросли и
где источник углерода представляет собой сок сахарного тростника, патоку сахарного тростника, гидролизованный крахмал, гидролизованные лигноцеллюлозные вещества, глюкозу, сахарозу, фруктозу, лактат, лактозу, ксилозу, пируват или глицерин в любой их форме или смеси.
2. Способ по п.1, где микроорганизм представляет собой бактерию, выбранную из родов, состоящих из: Burkholderia, Propionibacterium, Propionispira, Clostridium, Bacillus, Escherichia, Pelobacter или Lactobacillus.
3. Способ по п.1, где микроорганизм представляет собой эукариотический организм, который выбран из дрожжей, нитевидных грибов, простейших или водорослей.
4. Способ по п.3, где дрожжи представляют собой Saccharomyces cerevisiae, Zymomonas mobilis или Pichia pastoris.
5. Способ по п.1, где источник углерода представляет собой моносахарид, олигосахарид или полисахарид.
6. Способ по п.1, где микроорганизм секретирует бутадиен в ферментационные среды.
7. Способ по п.6, дополнительно включающий извлечение бутадиена из ферментационных сред.
8. Способ по любому из пп.1-7, где способ является анаэробным.
9. Генетически модифицированный микроорганизм для получения бутадиена из ферментируемого источника углерода, содержащий один или более полинуклеотидов, кодирующих ферменты в метаболическом пути, который катализирует превращение ферментируемого источника углерода в одно или более промежуточных соединений в метаболическом пути получения бутадиена, и один или более полинуклеотидов, кодирующих ферменты в метаболическом пути, которые катализируют превращение одного или более промежуточных соединений в бутадиен, где одно или более промежуточных соединений в метаболическом пути получения бутадиена представляет собой кротонил-КоА, где все из ферментов выбираются из или (i) кротонил-КоА-редуктазы (бифункциональной) (Е.С.1.1.1) и дегидратазы кротонилового спирта (Е.С.4.2.1, 4.2.1.127), или (ii) дегидрогеназы кротонового альдегида (Е.С.1.2.1), дегидрогеназы кротонилового спирта (Е.С.1.1.1, 1.1.1.1) и дегидратазы кротонилового спирта (Е.С.4.2.1, 4.2.1.127), и
где микроорганизм представляет собой бактерии, дрожжи, нитевидные грибы, простейшие или водоросли и
где источник углерода представляет собой сок сахарного тростника, патоку сахарного тростника, гидролизованный крахмал, гидролизованные лигноцеллюлозные вещества, глюкозу, сахарозу, фруктозу, лактат, лактозу, ксилозу, пируват или глицерин в любой их форме или смеси.
10. Микроорганизм по п.9, где микроорганизм представляет собой бактерию, выбранную из родов, состоящих из: Burkholderia, Propionibacterium, Propionispira, Clostridium, Bacillus, Escherichia, Pelobacter или Lactobacillus.
11. Микроорганизм по п.9, где микроорганизм представляет собой эукариотический организм, который выбран из дрожжей, нитевидных грибов, простейших или водорослей.
12. Микроорганизм по п.11, где дрожжи представляют собой Saccharomyces cerevisiae, Zymomonas mobilis или Pichia pastoris.
13. Способ по п.1, где ферменты представляют собой кротонил-КоА-редуктазу (бифункциональную) (Е.С.1.1.1) и дегидратазу кротонилового спирта (Е.С.4.2.1, 4.2.1.127).
14. Способ по п.1, где ферменты представляют собой дегидрогеназу кротонового альдегида (Е.С.1.2.1), дегидрогеназу кротонилового спирта (Е.С.1.1.1, 1.1.1.1), дегидратазу кротонилового спирта (Е.С.4.2.1, 4.2.1.127).
15. Микроорганизм по п.9, где ферменты представляют собой кротонил-КоА-редуктазу (бифункциональную) (Е.С.1.1.1) и дегидратазу кротонилового спирта (Е.С.4.2.1, 4.2.1.127).
16. Микроорганизм по п.9, где ферменты представляют собой дегидрогеназу кротонового альдегида (Е.С.1.2.1), дегидрогеназу кротонилового спирта (Е.С.1.1.1, 1.1.1.1), дегидратазу кротонилового спирта (Е.С.4.2.1, 4.2.1.127).
17. Способ по п.1, где указанная дегидратаза кротонилового спирта представляет собой линалоолдегидратазу (4.2.1.127).
18. Микроорганизм по п.9, где указанная дегидратаза кротонилового спирта представляет собой линалоолдегидратазу (4.2.1.127).
| US20110300597 A1, 08.12.2011 | |||
| US20110262975 A1, 27.10.2011 | |||
| US20110165644 A1, 07.07.2011 | |||
| US20110172476 A1, 14.07.2011 | |||
| EA200700908 A1, 28.12.2007. |
Авторы
Даты
2017-12-21—Публикация
2012-12-17—Подача