Изобретение относится к области нанотехнологии, медицины и пищевой промышленности.
Ранее были известны способы получения микрокапсул.
В пат. 2173140, МПК A61K 009/50, A61K 009/127, РФ, опубл. 10.09.2001 предложен способ получения кремнийорганолипидных микрокапсул с использованием роторно-кавитационной установки, обладающей высокими сдвиговыми усилиями и мощными гидроакустическими явлениями звукового и ультразвукового диапазона для диспергирования.
Недостатком данного способа является применение специального оборудования - роторно-кавитационной установки, которая обладает ультразвуковым действием, что оказывает влияние на образование микрокапсул и при этом может вызывать побочные реакции в связи с тем, что ультразвук разрушающе действует на полимеры белковой природы, поэтому предложенный способ применим при работе с полимерами синтетического происхождения
В пат. 2359662, МПК A61K 009/56, A61J 003/07, B01J 013/02, A23L 001/00, опубл. 27.06.2009, РФ предложен способ получения микрокапсул хлорида натрия с использованием распылительного охлаждения в распылительной градирне Niro при следующих условиях: температура воздуха на входе 10°C, температура воздуха на выходе 28°C, скорость вращения распыляющего барабана 10000 об/мин. Микрокапсулы по изобретению обладают улучшенной стабильностью и обеспечивают регулируемое и/или пролонгированное высвобождение активного ингредиента.
Недостатками предложенного способа являются длительность процесса и применение специального оборудования, комплекс определенных условий (температура воздуха на входе 10°C, температура воздуха на выходе 28°C, скорость вращения распыляющего барабана 10000 об/мин).
Наиболее близким методом является способ, предложенный в пат. 2134967, МПК A01N 53/00, A01N 25/28, опубл. 27.08.1999, РФ (1999). В воде диспергируют раствор смеси природных липидов и пиретроидного инсектицида в весовом отношении 2-4:1 в органическом растворителе, что приводит к упрощению способа микрокапсулирования.
Недостатком метода является диспергирование в водной среде, что делает предложенный способ неприменимым для получения микрокапсул водорастворимых препаратов в водорастворимых полимерах.
Техническая задача - упрощение и ускорение процесса получения нанокапсул, уменьшение потерь при получении нанокапсул (увеличение выхода по массе).
Решение технической задачи достигается способом получения нанокапсул витаминов группы В, отличающимся тем, что в качестве оболочки нанокапсул используется каррагинан, а в качестве ядра - витамины (тиамина, рибофлавина, пиридоксина, фолиевой кислоты и карнитина) при получении нанокапсул методом осаждения нерастворителем с применением 1,2-дихлорэтана в качестве осадителя.
Отличительной особенностью предлагаемого метода является получение нанокапсул методом осаждения нерастворителем с использованием 1,2-дихлорэтана в качестве осадителя, а также использование каррагинана в качестве оболочки частиц и витаминов группы В в качестве ядра.
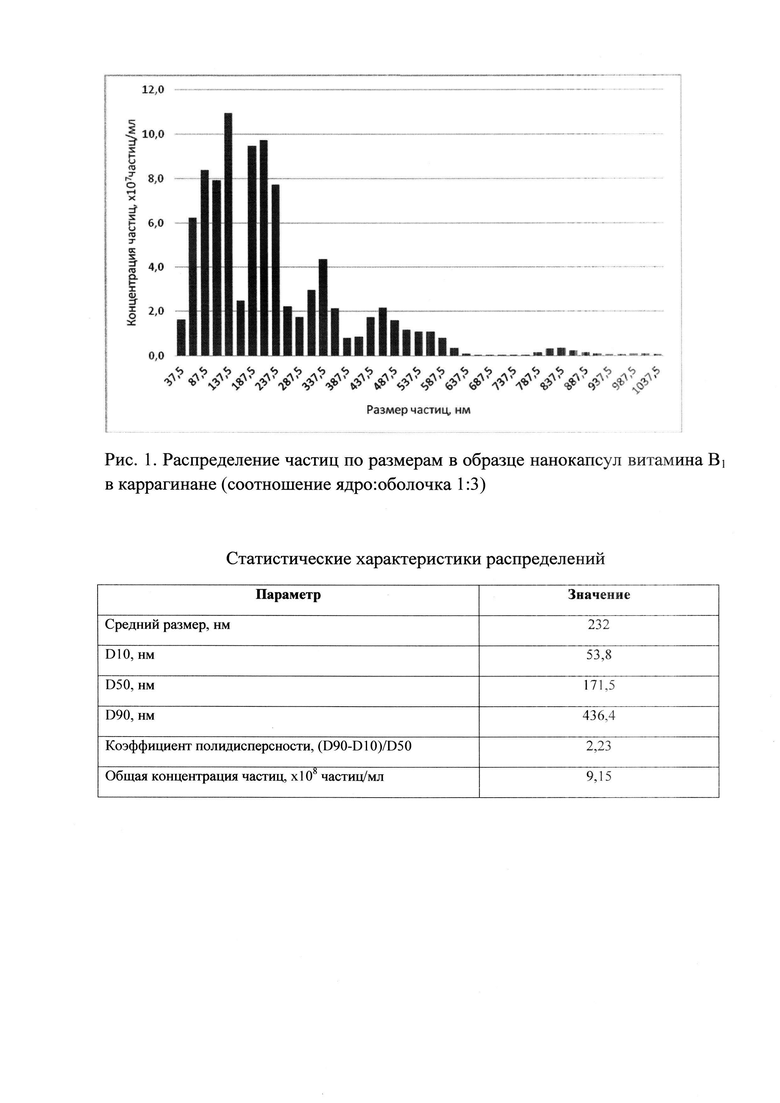
Результатом предлагаемого метода является получение нанокапсул витаминов группы В (см. рис. 1-3).
ПРИМЕР 1. Получение нанокапсул тиамина (В1), соотношение ядро:оболочка 1:3
100 мг тиамина добавляют в суспензию 300 мг каррагинана в бензоле в присутствии 0,01 г препарата Е472с (сложный эфир глицерина с одной-двумя молекулами пищевых жирных кислот и одной-двумя молекулами лимонной кислоты, причем лимонная кислота, как трехосновная, может быть этерифицирована другими глицеридами и как оксокислота - другими жирными кислотами. Свободные кислотные группы могут быть нейтрализованы натрием) в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,4 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 2. Получение нанокапсул тиамина (В1), соотношение ядро:оболочка 1:1
100 мг тиамина добавляют в суспензию 100 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,2 г порошка нанокапсул. Выход составил 100%.
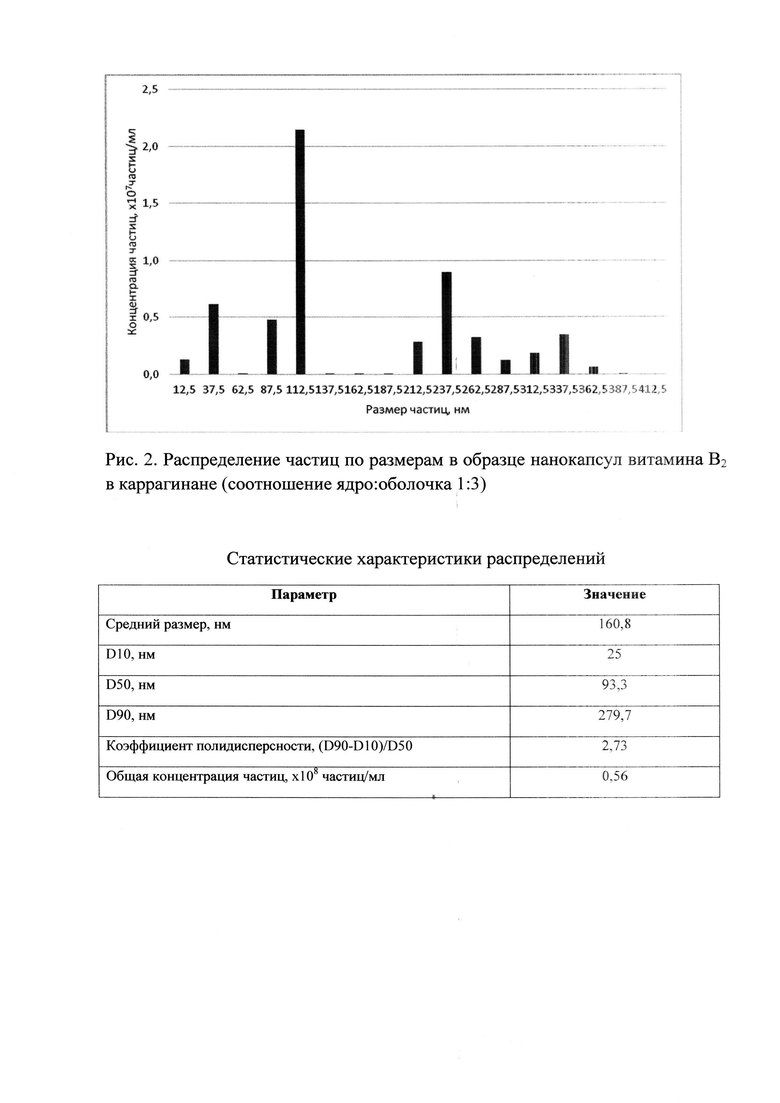
ПРИМЕР 3. Получение нанокапсул рибофлавина (В2), соотношение ядро:оболочка 1:3
100 мг рибофлавина добавляют в суспензию 300 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,4 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 4. Получение нанокапсул рибофлавина (В2), соотношение ядро:оболочка 1:1
100 мг рибофлавина добавляют в суспензию 100 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,2 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 5. Получение нанокапсул пиридоксина (В6), соотношение ядро:оболочка 1:3
100 мг пиридоксина добавляют в суспензию 300 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,4 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 6. Получение нанокапсул пиридоксина (В6), соотношение ядро:оболочка 1:1
100 мг пиридоксина добавляют в суспензию 100 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,2 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 7. Получение нанокапсул фолиевой кислоты (В9), соотношение ядро:оболочка 1:3
100 мг фолиевой кислоты добавляют в суспензию 300 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,4 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 8. Получение нанокапсул фолиевой кислоты (В9), соотношение ядро:оболочка 1:1
100 мг фолиевой кислоты добавляют в суспензию 100 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,2 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 9. Получение нанокапсул карнитина (В11), соотношение ядро:оболочка 1:3
100 мг карнитина добавляют в суспензию 300 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,4 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 10. Получение нанокапсул карнитина (В11), соотношение ядро:оболочка 1:1
100 мг карнитина добавляют в суспензию 100 мг каррагинана в бензоле, в присутствии 0,01 г препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин. Далее приливают 5 мл 1,2-дихлорэтана. Полученную суспензию отфильтровывают и сушат при комнатной температуре.
Получено 0,2 г порошка нанокапсул. Выход составил 100%.
ПРИМЕР 11. Определение размеров нанокапсул методом NTA.
Измерения проводили на мультипараметрическом анализаторе наночастиц Nanosight LM0 производства Nanosight Ltd (Великобритания) в конфигурации HS-BF (высокочувствительная видеокамера Andor Luca, полупроводниковый лазер с длиной волны 405 нм и мощностью 45 мВт). Прибор основан на методе анализа траекторий наночастиц (Nanoparticle Tracking Analysis, NTA), описанном bASTM E2834.
Оптимальным разведением для разведения было выбрано 1: 100. Для измерения были выбраны параметры прибора: Camera Level = 16, Detection Threshold = 10 (multi), Min Track Length:Auto, Min Expected Size: Auto. длительность единичного измерения 215s, использование шприцевого насоса.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения нанокапсул витаминов группы В в каппа-каррагинане | 2016 |
|
RU2618449C1 |
| Способ получения нанокапсул витаминов группы В в геллановой камеди | 2015 |
|
RU2616514C2 |
| Способ получения нанокапсул семян чиа (Salvia hispanica) в пектине | 2016 |
|
RU2647440C2 |
| Способ получения нанокапсул АЕКола | 2016 |
|
RU2644725C2 |
| Способ получения нанокапсул солей металлов в каррагинане | 2016 |
|
RU2627578C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКАПСУЛ ВИТАМИНОВ ГРУППЫ В | 2015 |
|
RU2605596C1 |
| Способ получения нанокапсул розмарина в каррагинане | 2017 |
|
RU2657766C1 |
| Способ получения нанокапсул АЕКола | 2016 |
|
RU2640128C1 |
| Способ получения нанокапсул АЕКола | 2016 |
|
RU2640129C1 |
| Способ получения нанокапсул АЕКола | 2016 |
|
RU2648747C2 |

Изобретение относится к медицине, в частности к способу получения нанокапсул витаминов группы В в каррагинане. Способ получения нанокапсул характеризуется тем, что в качестве оболочки используется каррагинан, а в качестве ядра - витамины группы В при массовом соотношении ядро:оболочка 1:3 или 1:1. При этом витамин добавляют в суспензию каррагинана в бензоле в присутствии препарата Е472с в качестве поверхностно-активного вещества при перемешивании. Осуществление изобретения позволяет упростить и ускорить процесс получения нанокапсул. 11 пр., 3 ил.
Способ получения нанокапсул витаминов группы В в каррагинане, характеризующийся тем, что в качестве оболочки используется каррагинан, а в качестве ядра - витамины группы В при массовом соотношении ядро:оболочка 1:3 или 1:1 при этом витамин добавляют в суспензию каррагинана в бензоле в присутствии препарата Е472с в качестве поверхностно-активного вещества при перемешивании 1300 об/мин, далее добавляют 1,2-дихлорэтан, полученную суспензию отфильтровывают и сушат при комнатной температуре.
| Солодовник В.Д | |||
| Микрокапсулирование | |||
| М., "Химия", 1980 | |||
| Nagavarma B.V.N | |||
| "Different techniques for preparation of polymeric nanoparticles", Asian Journal Pharm Clin Res, vol.5, suppl 3, 2012, pages 16-23 | |||
| Идентификация контактов с использованием распознавания речи | 2017 |
|
RU2682005C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОКАПСУЛ АСПИРИНА В КАРРАГИНАНЕ | 2014 |
|
RU2558084C1 |
| US 2014161892 A1, 12.06.2014. | |||
Авторы
Даты
2018-03-05—Публикация
2016-09-13—Подача