ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к медицинской технике, а именно к экстракорпоральным и имплантируемым устройствам механической поддержки кровообращения (МПК), основанным на применении роторных насосов (РН) крови (насосы непульсирующего потока (ННП)).
УРОВЕНЬ ТЕХНИКИ
Метод МПК с использованием РН, построенных на принципе центробежных, осевых и роликовых устройств, занял ведущее направление (94%) в мировой клинической практике для лечения больных с терминальной сердечной недостаточностью (ТСН). Это связано с существенными преимуществами данных насосов по сравнению с пульсирующими насосами, обусловленными, прежде всего, их малыми размерами, высокой энергетической эффективностью, большей надежностью и ресурсом. Данная технология успешно применяется при изолированной левожелудочковой недостаточности с высоким процентом выживаемости пациентов (85% в первый год имплантации).
Однако более чем в 30% случаев больные с ТСН имеют двусторонюю сердечную недостаточность и процент выживаемости этих пациентов значительно снижен. Поэтому решение данной проблемы состоит либо в бивентрикулярном обходе, либо в имплантации искусственного сердца (ИС) (Sunagawa G, Horvath D.J., Karimo J.H., Moazami N. et al. Future Prospects for the Total Artificial Heart //J Expert Review of Medical Device 2016 p 1-29).
В настоящее время в клинической практике единственным устройством искусственного сердца является SynCardia ТАН (CardioWest Inc), представляющее собой два имплантируемых искусственных желудочка сердца с внешними электропневмоприводом и системой энергопитания. Широкое внедрение данной технологии ограничивается теми же недостатками данной системы, что и поставило на второй план системы вспомогательного кровообращения с помощью РН: относительно большие габариты ИС, которые не позволили создать полностью имплантируему систему ИС, более низкая надежнсть и ресурс.
С другой стороны, клиническое применение имплантируемого электромеханического пульсируещего ИС Abiocor™ ТАН (Abiomed Inc) ограничивалось несколькими случаями. Одной из причиной этого была высокая стоимости системы. Поэтому в последние годы внимание разработчиков ИС было направлено на использование РН в силу их преимуществ перед насосами пульсирующего потока. При этом при создании ИС на основе правого и левого РН могли располагаться в одном корпусе и приводиться от одного бесконтактного двигателя постоянного тока. Не менее важным является относительно более низкая стоимость такого ИС.
Первые применения в качестве имплантируемого ИС двух РН, которые работали в неспульсирующем режиме, также не получили клинического внедрения, создавая в организме нефизиологический непульсирующий поток.
Известно устройство ИС (US 2014172087, А1) центробежного типа, ротор электрического двигателя которого вращает два рабочих колеса для подачи крови в большой и малый круг кровообращения.
Известно устройство ИС (US 2013331934, А1) центробежного типа. Устройство имеет крыльчатку с одной стороны импеллера и соответственно крыльчатку с другой стороны импеллера. Учитывая, что периферическое сопротивление большого и малого кругов кровообращения значительно отличаются в данном изобретении описан метод управления системой и конструкция крыльчатки для левого и правого канала.
Известно устройство ИС (US 9192702, В2), в котором раскрыта технология управления ИС с помощью встроенного микроконтроллера, который регулирует скорость двигателя в ответ на гемодинамические изменения артериального давления, физическую активность пациента.
Известно устройство ИС (US 8870951, В1), в котором обеспечивается автоматическое регулирование потоком крови для левого и правого насосов и поддержание баланса давлений за счет минимизации градиентов давлений при использовании высокой чувствительности потока крови к давлению в РН.
Описаны и другие системы РН, которые могут быть использованы для ИС с модуляцией скорости вращения рабочего колеса (US 2011178361, Al; US 9579435, В2; US 9345824, В2).
В качестве прототипа нами выбрано устройство и способ управления РН, описанные в US 8864644, В2. Устройство-прототип содержит насос роторного типа. В состав устройства входит привод, который периодически изменяет частоту вращения ротора насоса.
Недостатком описанных выше устройств, включая прототип, является периодическое изменение скорости вращения рабочего колеса насоса, которое может привести к травме крови. Кроме того, в данных устройствах из-за малой пульсации потока имеются проблемы, связанные с образованием тромбов в правым насосе, поскольку гидралическое сопротивление малого круга в несколько раз меньше гидравлического сопротивления большого круга, а левый и правый насос имеют один привод, то последовательо с правым насосом вводят дополнительное гидравлическое сопротивления для выравнивания расходов крови по двум кругам кровообращения. Данная стратегия принята и при подключении в качестве ИС двух независимых РН. При этом из-за меньшего перпада давлений на правом насосе согласно расходно-напорной характеристике РН в правом насосе снижается пульсация, что приводит к повышенному тромбообразованию в правом насосе по сравнению с левым насосом.
Кроме того, при использовании в качестве ИС существующих РН, разработанных ранее для левожелудочкового обхода с применением режима переменной скорости вращения требуются существенная переработка, доработка блоков управления насосами.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Предложено искусственное сердце, содержащее левый и правый роторный насосы крови, каждый из которых связан с блоком управления насосом, обеспечивающим поддержание заданной скорости вращения рабочего колеса насоса постоянной. К каждому из насосов параллельно входной и выходной магистралям подключен отдельный канал регулируемой рециркуляции крови, содержащий клапан. Клапаны связаны с блоком управления клапанами, включающим блок задания частоты и скважности работы раздельно для каждого клапана. Блок управления клапанами имеет возможность независимого регулирования потоком крови каждого канала рециркуляции с частичным или полным перекрытием и открытием его просвета.
В искусственном сердце может быть использован электромеханический клапан.
Канал регулируемой рециркуляции крови может быть подключен к входной и выходной магистралям насоса через тройники.
Для реализации режима искусственного сердца общие вход и выход правого насоса с каналом регулируемой рециркуляции крови подключены экстракорпорально или интракорпорально по схеме «правое предсердие-легочная артерия», а левого насоса с каналом регулируемой рециркуляции крови - по схеме «левое предсердие-аорта».
Технический результат, достигаемый при осуществлении настоящего изобретения, заключается в:
- обеспечении стабильности внутринасосной гидродинамики, минимизации травмы крови в системах ИС на базе РН за счет генерации ими на выходе из системы насос-шунт физиологического пульсирующего потока без изменения скорости вращения рабочего колеса насоса;
- улучшении условий внутринасосной гидродинамики правого насоса за счет увеличения пульсационной составляющей, что способствует снижению вероятности его тромбоза;
- предотвращении условий появления опасного режима разрежения и регургитации в диастолической фазе;
-реализации ИС на основе разработанных ранее конструкций ННП, предназначенных для левожелудочкового обхода.
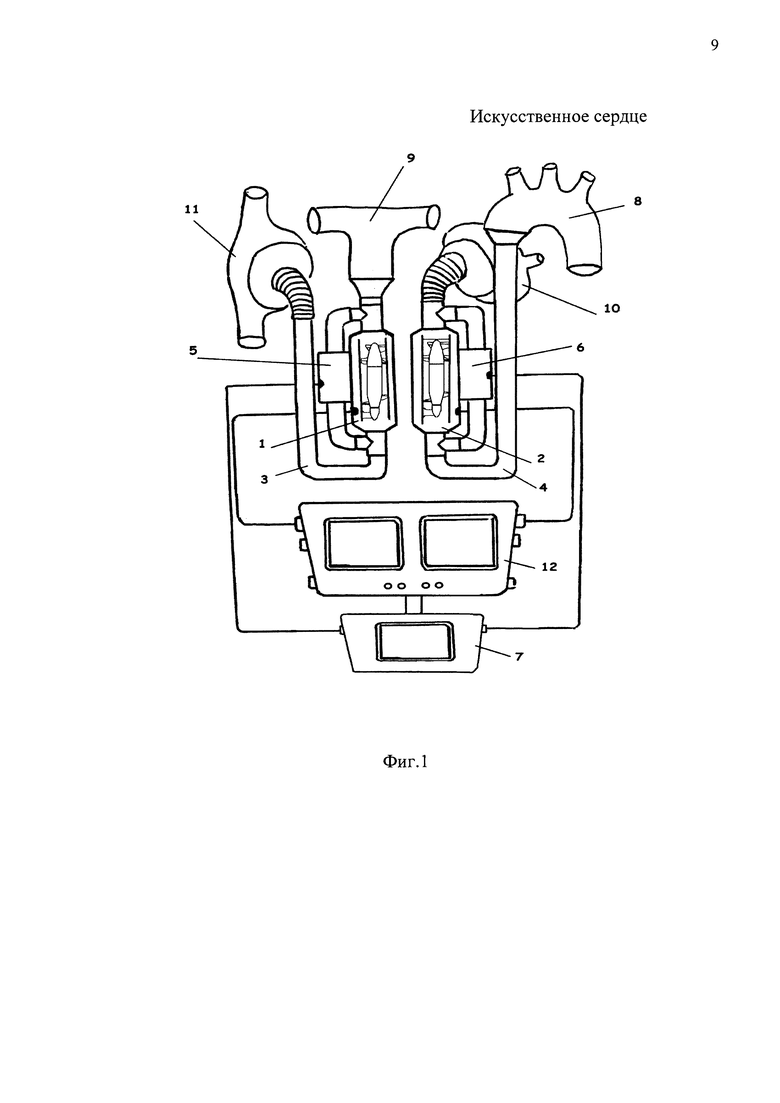
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ Существо изобретения поясняется на фигурах, где на фиг. 1 показана схема генерации пульсирующего потока в ИС с применением РН и канала рециркуляции (КР) с управляемым клапаном;
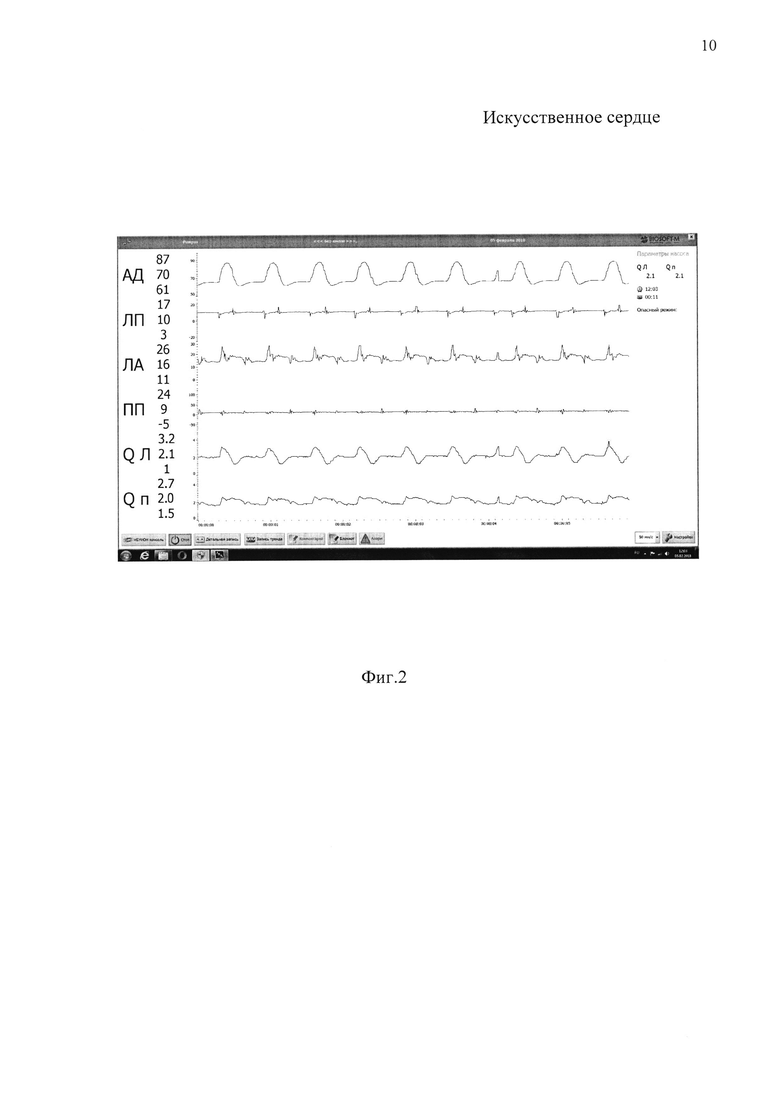
на фиг. 2 показана показана диаграмма давлений и расходов, полученных на двухкруговом гидродинамическом стенде, при работе левого и правого РН в пульсирующем с помощью системы насос-шунт режимах.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Патентуемое устройство содержит левый и правый РН 1, 2 (осевой или центробежный), при этом выход и вход каждого насоса через первый и второй тройники соединены с КР 3, 4 в виде трубок определенного сечения с установленным на нем электромагнитными клапанами 5,6 соединенными с блоком управления 7, обеспечивающим заданную частоту и скважность сокращений по левому и правому каналам.
При подключения КР 3, 4 к правому и левому РН 1, 2 клапаны 5, 6 частично или полностью их перекрывают, увеличивая поток крови на выходе системы в систолическую фазу, а в диастолическую фазу частино или полностью открывают КР 3, 4, уменьшая поток крови в аорту 8 и легочную артерию 9. В свою очередь входы систем РН 1, 2-КР 3, 4 подключены к левому 10 и правому 11 предсердиям. Таким образом, на выходе системы РН 1, 2-КР 3, 4 т.е. в аорте 8 и легочной артерии 9 формируется близкая к физиологической пульсация давления.
Кроме того, режим работы систем РН 1, 2-КР 3, 4 в диастолической фазе способствует устранению опасного режима, связанного с возникновением разрежения на входе насоса при работе РН в непульсирующем режиме при высоких оборотах рабочего колеса.
С другой стороны работа системы РН 1, 2-КР 3, 4 устраняет опасный режим обратной регургитации крови из артерии в желудочек, который имеет место при работе РН в непульсирующем рнжиме при малых оборотах ротора РН. Таким образом, на выходе заявляемой системы
ИС генерируется физиологический пульсирующий поток жидкости по правому и левому каналам при постоянной скорости вращения ротора за счет импульсной работы клапанов 5,6, которые управляют потоком жидкости (крови) в КР 3, 4.
Для реализации режима ИС сердца левая и правая системы РН 1, 2 - КР 3, 4 могут располагаться экстракорпорально или интракорпорально.
Для реализации режима ИС правый и левый насосы с каналами регулируемой рециркуляции крови подключены по схеме «правое предсердие-легочная артерия» для правого насоса с каналом регулируемой рециркуляции крови и по схеме «левое предсердие-аорта» для левого канала регулируемой рециркуляции крови.
В качестве подтверждения возможности реализации заявленного назначения и достижения указанного технического результата приводим следующие экспериментальные данные.
В качестве насосов в эксперименте на гидродинамическом стенде были использованы отечественные детские осевые насосы ДОН3 при расходе или минутном объеме сердца 1,8-1,9 л/мин, который соотвествует детям в возрасте 3-5 лет. При этом аортальный и легочные резервуары, имитирующие соотвественно аорту и легочную артерию, представляют собой емкости, заполненные жидкостью с воздушной подушкой, определяющей их эластичность (для легочного артерии эластичность равна 5,7 мл/мм рт.ст и для аорты эластичность аортального резервуара равна 2 мл/мм рт.ст). В качестве периферического сопротивления использовались гидравлические сопротивления (для малого круга кровообращения 0,4 мм рт.ст./мл/с и для большого круга кровобращения 1,2 мм. рт.ст/мл/с). Левое и правое предсердия имитировались открытыми резервуарами. При этом средний расход жидкости по левому каналу был больше среднего расхода жидкости по правому каналу на 0,1 л/мин с учетом бронхиального сброса. В условиях работы ИС данная разница расходов необходима для предотвращения отека легких.
Таким образом, работа системы РН 1, 2-КР3, 4 в гидродинамическом стенде по левому и правому каналам создает условия повышенного систолического потока крови и минимизирует диастолический поток, генерируя при этом физиологический поток жидкости крови по большому и малому кругам кровооьращения.
Полученный эффект работы системы РН 1, 2 - КР 3, 4 показан на диаграмме (фиг. 2).
Как видно из диаграммы в имитаторах аорты и легочной артерии создаются физиологическое пульсирующее давление АД (давление в аортальном резервуаре 92/66 мм. рт.ст) и ЛА (давление в легочном резервуаре 19/13 мм рт.ст) при пульсации потока жидкости в большом круге кровообращения ΔQл=2 л/мин и ΔQп=0.6 л/мин в малом круге кровообращени, что способствует созданию условий для внутринасосной гидродинамики, препятствующей образовнию в полостях левого 1 и правого 2 РН зон стагнации и рециркуляции.
Для специалистов в области кардиологии должно быть очевидно, что в настоящее изобретение могут быть внесены различные модификации и изменения, не отступая от сущности или объема формулы изобретения, которые не нашли отражения в приведенном примере осуществления изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Искусственное сердце | 2020 |
|
RU2732084C1 |
| Устройство и способ управления потоком крови роторных насосов | 2018 |
|
RU2665178C1 |
| Устройство и способ бивентрикулярного обхода сердца | 2020 |
|
RU2734142C1 |
| Устройство и способ управления потоком крови роторных насосов | 2020 |
|
RU2725083C1 |
| Устройство и способ управления потоком крови в аппаратах сердечно-легочного обхода | 2018 |
|
RU2665180C1 |
| Устройство управления потоком крови в аппаратах сердечно-легочного обхода | 2020 |
|
RU2732312C1 |
| Система и способ селективной билатеральной перфузии головного мозга при реконструктивной операции на дуге аорты, проводимой в условиях искусственного кровообращения | 2019 |
|
RU2734136C1 |
| Способ искусственного кровообращения при реконструктивной операции на дуге аорты | 2019 |
|
RU2724871C1 |
| Способ искусственного кровообращения у реципиента сердца при его трансплантации и система для его осуществления | 2024 |
|
RU2826522C1 |
| СПОСОБ ГЕМОДИНАМИЧЕСКОЙ РАЗГРУЗКИ ЛЕВОГО ЖЕЛУДОЧКА ПРИ ПРОВЕДЕНИИ ПЕРИФЕРИЧЕСКОЙ ВЕНО-АРТЕРИАЛЬНОЙ ЭКСТРАКОРПОРАЛЬНОЙ МЕМБРАННОЙ ОКСИГЕНАЦИИ | 2013 |
|
RU2526880C1 |
Изобретение относится к медицинской технике, а именно к экстракорпоральным и имплантируемым устройствам механической поддержки кровообращения, основанным на применении роторных насосов крови. Искусственное сердце содержит левый и правый роторные насосы крови, каждый из которых связан с блоком управления насосом, обеспечивающим заданную скорость вращения рабочего колеса насоса постоянной. Параллельно каждому насосу с одной стороны к входной части магистрали насоса, а с другой - к выходной части магистрали насоса подключен отдельный канал регулируемой рециркуляции крови, содержащий клапан. Каждый клапан связан с блоком управления клапанами, включающим блок задания частоты и скважности работы независимо для каждого клапана. Блок управления клапанами имеет возможность независимого регулирования потоком крови каждого канала рециркуляции крови с частичным или полным перекрытием и открытием его просвета. Технический результат состоит в обеспечении стабильности внутринасосной гемодинамики и минимизации травмы крови, тромбоза, регургитации в диастолической фазе. 2 з.п. ф-лы, 2 ил.
1. Искусственное сердце, содержащее левый и правый роторные насосы крови, каждый из которых связан с блоком управления насосом, обеспечивающим заданную скорость вращения рабочего колеса насоса постоянной, при этом параллельно каждому насосу с одной стороны к входной части магистрали насоса, а с другой к выходной части магистрали насоса подключен отдельный канал регулируемой рециркуляции крови, содержащий клапан; каждый клапан связан с блоком управления клапанами, включающим блок задания частоты и скважности работы независимо для каждого клапана, при этом блок управления клапанами имеет возможность независимого регулирования потоком крови каждого канала рециркуляции крови с частичным или полным перекрытием и открытием его просвета.
2. Искусственное сердце по п. 1, в котором использован клапан с электромеханическим приводом.
3. Искусственное сердце по п. 1, в котором канал регулируемой рециркуляции крови подключен к входной и выходной частям магистрали насоса через тройники.
| US 3533408 A, 13.10.1970 | |||
| US 8864644 B2, 21.10.2014 | |||
| US 9192702 B2, 24.11.2015 | |||
| US 2013331934 A1, 12.12.2013 | |||
| US 2014172087 A1, 19.06.2014 | |||
| Способ улучшения коммутации электрических машин | 1959 |
|
SU127315A1 |
Авторы
Даты
2018-08-28—Публикация
2018-02-06—Подача