ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к медицинской технике, а именно к аппаратам искусственного кровообращения (АИК) и системам экстракорпоральной мембранной оксигенации (ЭКМО), может быть использовано в аппаратах сердечно-легочного обхода при проведении искусственного или вспомогательного кровообращения, в том числе при проведении кардиохирургических вмешательств, а также до и после них.
УРОВЕНЬ ТЕХНИКИ
Многие факторы влияют на результаты операций с применением АИК и ЭКМО, особенно у педиатрических пациентов с врожденными пороками сердца. Преимущество пульсирующей перфузии по сравнению с непульсирующей является одним из таких факторов, который по-прежнему широко обсуждается среди исследователей, перфузиологов и хирургов (Agati S, Ciccarello G, Salvo D, et al. Pulsatile ECMO as bridge to recovery and cardiac transplantation in pediatric population: A comparative study. J Heart Lung Transplant 2007; 26: 8).
В частности преимущества пульсирующей перфузии у педиатрических пациентов при ЭКМО и АИК заключаются в увеличении кровотока жизненно важных органов, улучшении восстановления жизненно важных органов, что способствуют уменьшению постоперационных осложнений (Ungar A. Pulsatile Versus Nonpulsatile cardiopulmonary bypass procedures in neonates and infants: From bench to clinical practice. ASAIO 2005; 51: 6-10).
В настоящее время в литературе приводятся достаточно позитивные данные, полученные в результате пульсирующей перфузии у детей и взрослых, а также в экспериментальных моделях на животных.
Для сравнительной оценки непульсирующего и пульсирующего потока с точки зрения сравнения физиологических эффектов данных режимов в 1966 году Шепард и др. (Shepard RB, Simpson DC, Sharp JF: Energy equivalent pressure. Arch Surg 1966; 93: 730-74) предложили индекс энергетического эквивалентного давления (ЭЭД), который точно оценивает гемодинамическую энергию, которая определяется как соотношение между гемодинамической работой давления и объемом крови, перекачиваемой за тот же период времени;
ЭЭД=(ƒpdt)/(ƒdt),
где ƒpdt - гемодинамическая работа по давлению,
ƒdt - объем перкачиваемой крови.
При этом было показано, что пульсирующий поток, который создает более высокий уровень гемодинамической энергии, может лучше поддерживать микроциркуляцию и клеточный метаболизм, способствуя восстановлению жизненно важных органов после использования АИК и ЭКМО (Undar A, Masai Т, Beyer ЕА, Goddard-Finegold J, et al: Pediatric physiologic pulsatile pump enhances cerebral and renal blood flow during and after cardiopulmonary bypass Artif Org 2002; 26: 919-923).
Кроме того, считается, что пульсирующая перфузии положительно влияет на процесс восстановления, уменьшая синдром системной воспалительной реакции, и снижает продолжительность госпитализации (Alkan Т, Akc evin A, Undar A, et al: Benefits of pulsatile perfusion on vital organ recovery during and after pediatric open-heart surgery. ASAIO J, 2005; 3, 651-654).
Были предложены различные способы имитации в АИК и ЭКМО естественного пульсирующего кровотока, но ни один из них до сих пор не был признан удовлетворительным. Тем не менее, было проведено достаточно много исследований в области разработок пульсирующих систем для сердечно-легочного обхода.
Известно устройство (US 7850594 В2), которое содержит роторный насос (РН) с приводом, обеспечивающим пульсирующий режим работы насоса за счет периодического изменения с помощью контроллера скорости вращения рабочего колеса. Однако для реализации данного режима в АИК, в которых используются, главным образом, роликовые насосы, из-за инерции рабочего колеса на выходе формируется синусоидальный сигнал, отличающийся от естественной пульсации.
Описаны и другие системы управления РН с модуляцией скорости вращения рабочего колеса (US 9579435 В2, US 9345824 В2), обладающие теми же недостатками при использовании роликовых насосов.
Самый простой способ обеспечить импульсный поток - периодически пережимать и открывать входную или выходную линию артериального насоса аппарата АИК или ЭКМО.
Известны устройства (US 7238165 В2, US 8317499 В2, US 4492531 А), в которых для создания пульсирующего потока установлен клапан с приводом периодически частично или полностью пережимающий выходную артериальную или входную венозную магистраль. Недостатком указанных устройств, особенно при использовании роликовых насосов, является создание высокого давления при пережатии выходной магистрали и высокого разрежения при пережатии входной магистрали, за счет которых создаются условия травмы крови, а в некоторых случаях условия, способные вызывать кавитацию, которая потенциально высвобождает пузырьки газа в кровоток.
В качестве прототипа нами выбрано устройство US 6547753 В1, в котором пульсирующий кровоток в АИК создается за счет эластичной камеры (баллона), установленной в артериальной линии с программируемой ее компрессией для модулирования сердечного ритма.
Недостатком описанных выше устройств, включая прототип, является создание высокого давления при пережатии выходной магистрали и высокого разрежения при пережатии входной магистрали, за счет которых создаются условия травмы крови, периодическое изменение скорости вращения рабочего колеса насоса, синхронизированное с частотой сердечного цикла, может также привести к травме крови. Кроме того, недостатком прототипа является дополнительный объем крови, необходимый для заполнения пульсирующего баллона, увеличивающий общий объем заполнения кровью всего АИК. В конструкциях современных систем минимизация объема заполнения является одной из важных характеристик аппаратов сердечно-легочного обхода.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Предложено устройство управления потоком крови в аппарате сердечно-легочного обхода, включающее канал регулируемой рециркуляции крови (КР) или шунт с возможностью параллельного подключения к входной и выходной магистралям РН (или насоса непульсирующего потока (ННП)) с встроенным в него клапаном. Последний связан с блоком управления клапаном, обеспечивающим пульсацию с заданной частотой и скважностью потока крови, поступающего через оксигенатор в артериальную линию системы сердечно-легочного обхода путем частичного или полного перекрытия и открытия просвета КР.
В качестве аппарата сердечно-легочного обхода может быть использована система (аппарат) ЭКМО, в которой блок управления клапаном подключен к блоку кардиосинхронизации и выделения зубца R ЭКГ. Последний выполнен с возможностью регулирования потока крови с частичным или полным перекрытием и открытием просвета КР в соответствии с фазами сердечного цикла в режиме контрпульсации с сердцем пациента. При этом клапан в диастолическую фазу частично или полностью перекрывает КР, а в систолическую фазу - частично или полностью открывает КР.
Может быть использован клапан с электромеханическим приводом (электромеханический клапан).
КР может быть подключен к входной и выходной магистралям насоса через тройники.
КР может быть выполнен в виде эластичной трубки или сосудистого протеза.
Предложен также способ управления потоком крови в аппарате сердечно-легочного обхода, в котором устройство подключают параллельно входной и выходной магистралям РН аппарата сердечно-легочного обхода, соединенного с блоком управления насосом, обеспечивающим поддержание заданной скорости вращения рабочего колеса насоса постоянной, после чего подключают полученную систему по схеме «венозная линия - оксигенатор».
Технический результат, достигаемый при осуществлении предлагаемой группы изобретений, заключается в:
- создании физиологического пульсирующего потока в аппаратах сердечно-легочного обхода, например АИК или система ЭКМО, при постоянной заданной скорости вращения рабочего колеса насоса и обеспечении тем самым условий, минимизирующих травму форменных элементов крови и кавитацию с образованием опасных для организма пузырьков газа;
- универсальности предлагаемых устройства и способа, в которых в качестве базового РН насоса для АИК и ЭКМО может быть использован насос любой конструкции.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Существо изобретения поясняется на чертежах, где
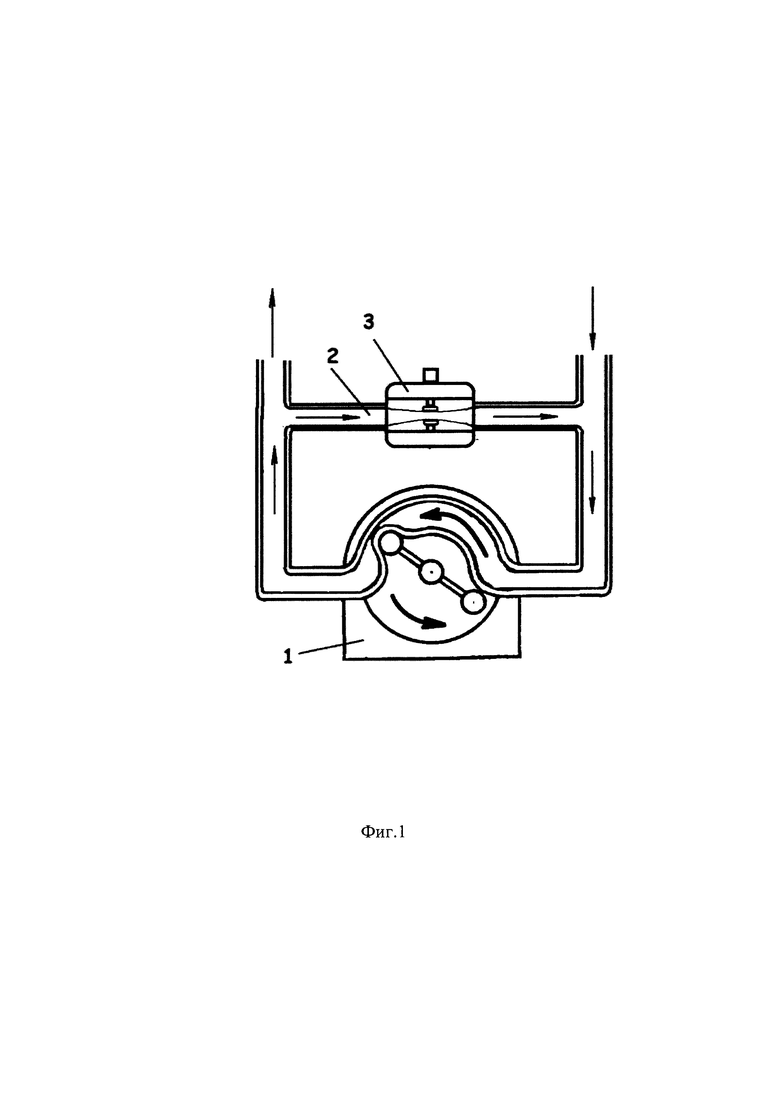
на фиг. 1 показана схема генерации пульсирующего потока в АИК и аппарате ЭКМО с применением РН (ННП) и КР (шунта) с встроенным клапаном, связанным с блоком управления, обеспечивающего заданную частоту и скважность управляющих импульсов;
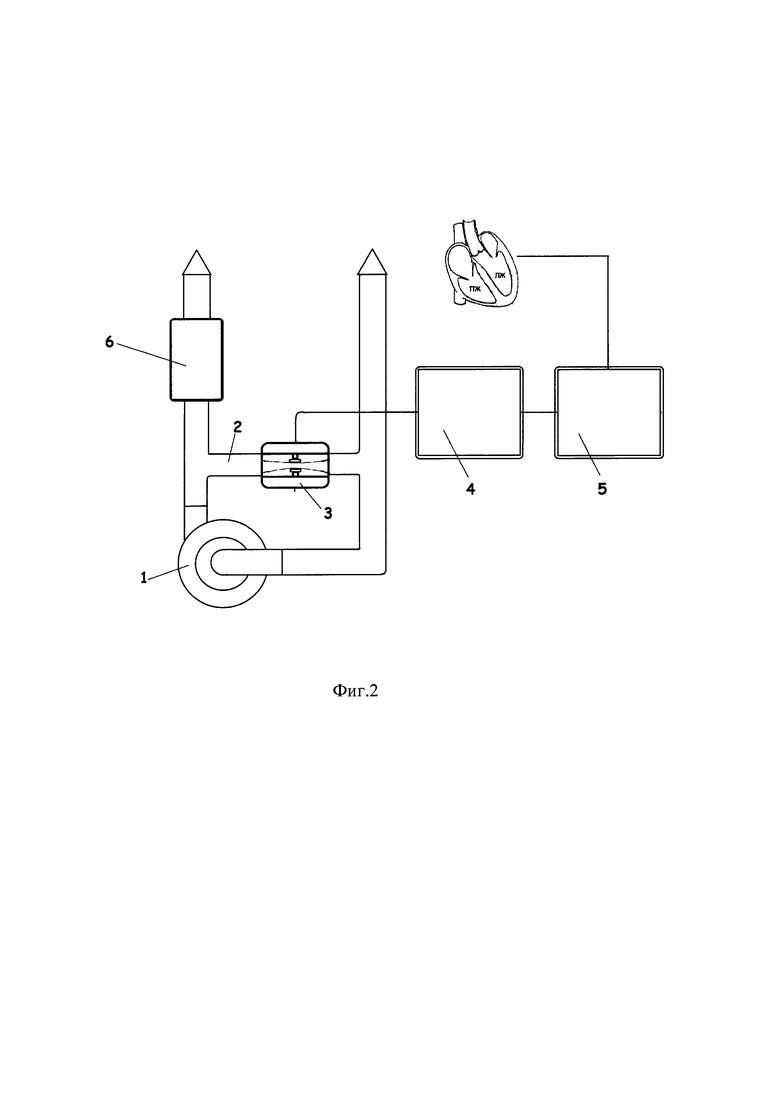
на фиг. 2 показана схема генерации пульсирующего потока в системах ЭКМО с применением РН (ННП) и КР (шунта) с встроенным клапаном, связанным с блоком управления клапаном, обеспечивающим заданную частоту и скважность управляющих импульсов и блоком кардиосинхронизации, обеспечивающий режим контрпульсации;
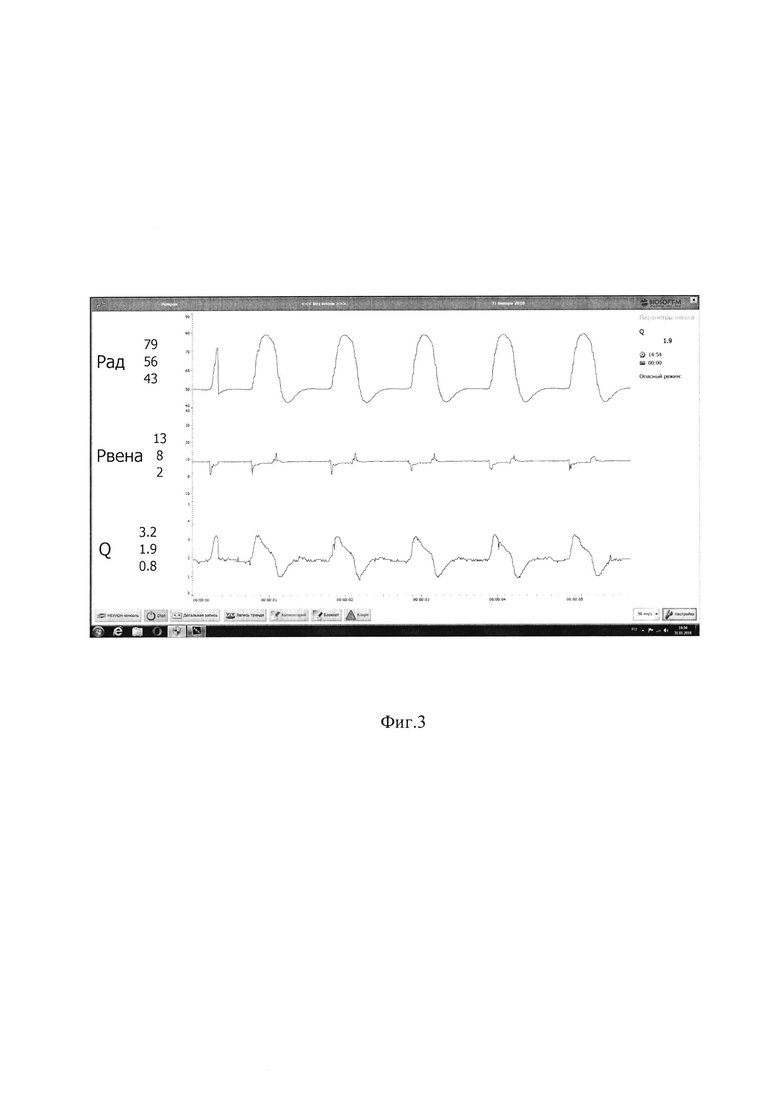
на фиг. 3 показана диаграмма давлений и расходов, полученная на гидродинамическом стенде, при моделировании с помощью заявленного устройства пульсирующего режима работы.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Устройство содержит РН 1, при этом выход и вход насоса параллельно соединены с управляемым КР 2 в виде трубки определенного сечения с установленным на ней клапаном 3, соединенными с блоком управления 4, обеспечивающим заданную частоту и скважность пульсаций, соответствующих сердечному циклу. Управляемый КР или шунт 2 подсоединен к РН 1 с помощью двух тройников, вход первого тройника подключен через систему трубок к венозной линии аппарата сердечно-легочного обхода, а вход второго тройника через систему трубок подключен к артериальной линии аппарата.
В другом варианте в системе ЭКМО блок управления клапаном связан с кардиосинхронизатом 5, подключенным к блоку выделения R- зубца ЭКГ.
Работа предлагаемого устройства и способ управления потоком крови роторного насоса могут быть представлены следующим образом.
В первом варианте подключения системы РН 1 - КР 2 в системе АИК по схеме «венозный резервуар-артериалтная линия» за счет блока управления 4 клапаном 3 с заданными частотой и скважностью, соответствующих сердечному ритму, клапан 3 частично или полностью перекрывает КР 2, увеличивая или уменьшая поток крови на выходе системы.
Во втором варианте подключения РН 1 - КР 2 в системе ЭКМО по схеме «венозная линия - оксигенатор 6», за счет блока управления 4 клапаном 3 с заданными частотой и скважностью, соответствующими сердечному ритму, клапан 3 частично или полностью перекрывает КР 2, увеличивая или уменьшая поток крови на выходе системы.
В третьем варианте подключения в системе ЭКМО РН 1 - КР 2 по схеме «венозная линия - оксигенатор 6», за счет блока управления 4 клапаном 3, подключенного к блоку кардиосинхронизации 5, при этом в фазе диастолы клапан 3 частично или полностью перекрывает шунт 2, увеличивая поток крови на выходе системы; в фазе систолы клапан 3 и частично или полностью открывает КР 2, уменьшая поток крови в артерию, таким образом реализуя режим контрпульсации. В систолическую фазу клапан частично или полностью открывает канал рециркуляции, уменьшая давление в артериальной линии, таким образом снижая постнагрузку или работу левого желудочка сердца.
На выходе системы РН 1- КР 2, т.е. в артериальной линии, формируются близкие к физиологическим пульсация и давление без изменения скорости вращения рабочего колеса РН1. Данный режим способствует минимизации травмы форменных элементов крови по сравнению с заявленными ранее устройствами и устранению режима разрежения на входе РН1 с возможной кавитацией крови и появлением газовых пузырьков потенциально опасных для мозгового кровообращения.
Таким образом, предложенная система, используемая для управления потоком крови в аппаратах АИК и ЭКМО, включает РН 1 с блоком управления насосом 4, обеспечивающим заданную скорость вращения рабочего колеса насоса, и КР 2. Последний подключен параллельно входной и выходной магистралям РН1 и снабжен клапаном 3, который подключен к блоку управления клапаном 4.
Предлагаемое устройство выполнено с возможностью регулирования потока крови через КР с частичным или полным перекрытием и открытием просвета, создавая условия регулируемого пульсового потока в аппаратах АИК и ЭКМО для модуляции заданного сердечного ритма.
В случаях использования устройства в аппаратах ЭКМО может быть установлен дополнительно блок кардиосинхронизации 5 и связанный с блоком управления клапаном 4. В этом случае блок управления клапаном 4 может работать с заданной задержкой относительно зубца R-ЭКГ, реализуя режим контрпульсации, который за счет повышения давления крови в артерии может способствовать увеличению коронарного кровотока.
Приводим данные, полученные на гидродинамическом стенде, подтверждающие возможность реализации заявленного назначения и достижения указанного технического результата.
Полученный эффект работы системы РН 1 - КР 2 с клапаном 3 и системой управления клапаном 3 показан на диаграмме давлений и расходов на фиг. 3. В данной работе на гидродинамическом стенде в качестве РК использовался насос Биопамп ВР-80 (Medtronic, США) с подключением КР с пневматическим клапаном 3, управляемым от системы привода искусственного сердца Синус-ИС.
Как видно из диаграммы, амплитуда пульсового давления в аортальном резервуаре при работе системы РН 1 - КР 2 находится в физиологических пределах (79/50 мм рт.ст) при среднем расходе жидкости 1,9 л/мин.
Кривая потока жидкости при этом также имеет выраженную пульсацию, что может позитивно сказаться при использовании системы у пациентов как при проведении операций на открытом сердце, так и при использовании при подключении ЭКМО в условиях терминальной сердечной недостаточности.
Для специалистов в области кардиологии должно быть очевидно, что в настоящее изобретение могут быть внесены различные модификации и изменения, не отступая от сущности или объема формулы изобретения, которые не нашли отражения в приведенном примере осуществления изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| Устройство управления потоком крови в аппаратах сердечно-легочного обхода | 2020 |
|
RU2732312C1 |
| Устройство и способ управления потоком крови роторных насосов | 2018 |
|
RU2665178C1 |
| Искусственное сердце | 2018 |
|
RU2665179C1 |
| Устройство и способ управления потоком крови роторных насосов | 2020 |
|
RU2725083C1 |
| Устройство и способ бивентрикулярного обхода сердца | 2020 |
|
RU2734142C1 |
| Искусственное сердце | 2020 |
|
RU2732084C1 |
| Способ искусственного кровообращения у реципиента сердца при его трансплантации и система для его осуществления | 2024 |
|
RU2826522C1 |
| Система и способ селективной билатеральной перфузии головного мозга при реконструктивной операции на дуге аорты, проводимой в условиях искусственного кровообращения | 2019 |
|
RU2734136C1 |
| Способ искусственного кровообращения при реконструктивной операции на дуге аорты | 2019 |
|
RU2724871C1 |
| Воздушный сепаратор к системе экстракорпорального кровообращения | 2023 |
|
RU2815528C1 |
Изобретение относится к медицинской технике, а именно к аппаратам искусственного кровообращения и системам экстракорпоральной мембранной оксигенации. Устройство управления потоком крови в аппарате сердечно-легочного обхода включает канал регулируемой рециркуляции крови с возможностью параллельного подключения к роторному насосу с одной стороны к входной части магистрали насоса, а с другой - к выходной части магистрали насоса. Канал регулируемой рециркуляции крови содержит клапан, связанный с блоком управления клапаном, обеспечивающим пульсацию с заданной частотой и скважностью потока крови, поступающего через оксигенатор в артериальную линию системы сердечно-легочного обхода путем частичного или полного перекрытия и открытия просвета канала регулируемой рециркуляции крови. Технический результат состоит в создании физиологичного пульсирующего потока при постоянной скорости вращения рабочего колеса насоса для минимизации травмы крови и кавитации при использовании насосов разных конструкций. 3 з.п. ф-лы, 3 ил.
1. Устройство управления потоком крови в аппарате сердечно-легочного обхода, включающее канал регулируемой рециркуляции крови с возможностью параллельного подключения к роторному насосу с одной стороны к входной части магистрали насоса, а с другой - к выходной части магистрали насоса, причем канал регулируемой рециркуляции крови содержит клапан, связанный с блоком управления клапаном, обеспечивающим пульсацию с заданной частотой и скважностью потока крови, поступающего через оксигенатор в артериальную линию системы сердечно-легочного обхода путем частичного или полного перекрытия и открытия просвета канала регулируемой рециркуляции крови.
2. Устройство по п. 1, в котором используют клапан с электромеханическим приводом.
3. Устройство по п. 1, в котором канал регулируемой рециркуляции крови подключен к входной и выходной частям магистрали насоса через тройники.
4. Устройство по п. 1, в котором канал регулируемой рециркуляции крови представляет собой эластичную трубку или сосудистый протез.
| US 3533408 A, 13.10.1970 | |||
| US 6547753 B1, 15.04.2003 | |||
| US 2016000983 A1, 07.01.2016 | |||
| US 2004015042 A1, 22.01.2004 | |||
| US 2015057488 A1, 26.02.2015 | |||
| US 2007265703 A1, 15.11.2007 | |||
| СПОСОБ ИСКУССТВЕННОГО КРОВООБРАЩЕНИЯ И АППАРАТ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2002 |
|
RU2226111C2 |
| Способ очистки антрахинона, 2-хлорантрахинона, этилантрахинона и хинизарина с помощью дистилляции | 1954 |
|
SU104462A1 |
Авторы
Даты
2018-08-28—Публикация
2018-02-06—Подача