Изобретение относится к технологии получения солей олова (IV) и может быть использовано в различных видах химической и иных практик, переработке вторичного сырья металлов, других утилизационных процессах, в научных исследованиях и в аналитическом контроле.
Известен способ получения карбоксилатов олова (Patent USA№6303808, опубл. 10/16/2001), в соответствии с которым металлическое олово в виде порошка и других форм вводят в контакт с некоторыми жирными кислотами в присутствии 1-20% от загрузок олова промотора как 4-трет-бутилкатехола или 2,5-ди-трет-бутилгидрохинона, которые добавляют индивидуально или в носителе типа диола, гликоля или карбоновой кислоты. Реакционную смесь сначала нагревают до 60˚C и подают кислородсодержащий газ, в частности воздух. Затем температуру повышают до 140-180˚C и в таком режиме ведут окисление до накопления определенного количества соединений олова. В зависимости от того, какой карбоксилат олова нужен ((II) или (IV)), процесс завершают, либо кислородсодержащий газ при 140-180˚C меняют на инертный (например, азот) и еще какое-то время продолжают в таком режиме процесс при контроле за составом продуктов. По завершении процесса реакционную смесь перерабатывают с выделением целевых продуктов и утилизацией отдельных ее компонентов и композиций.
Недостатками данного способа являются:
1. Нет четкого разграничения режимов на избирательное или по крайней мере приемлемое, но конкретное для получения либо карбоксилатов олова (II), либо карбоксилатов олова (IV). Да и вообще не ясно, могут ли быть достигнуты обозначенные избирательные получения, либо всегда смесь «больше-меньше» соединений олова (II) и олова (IV).
2. Цитируемый процесс требует в одном и том же реакторе поддерживать в течение определенного времени разные температурные режимы, в частности, 60˚C и 140-180˚C, что предполагает не только применение разных теплоносителей, но и разную организацию подвода внешнего тепла.
3. Процесс характеризуется многокомпонентной загрузкой, причем многие компоненты не вносят никакого вклада в массу целевого продукта. Это существенно усложняет выделение и очистку последнего, а также утилизацию отдельных компонентов из многокомпонентных систем.
4. Процесс требует не только проток через зону реакции кислородсодержащего газа или воздуха, но и замену его на инертный газ, причем при высоких (140-180˚C) температурах. В реакционной смеси есть довольно много наименований органических соединений, которые при такой температуре способны окисляться кислородом, а в инертной среде - соединениями олова (IV). Все эти процессы следует рассматривать как конкурентоспособные, причем не только обязательные в превращении Sn→ Sn2+→ Sn4+→ Sn2+, но и как сопутствующие, и побочные, увеличивающие ассортимент продуктов в реакционной смеси, снижающие избирательность по целевому продукту и степень полезного использования реагентов для его получения.
5. Данный процесс слишком сложен, чтобы его использовать для переработки олова как вторичного металлического сырья; сложны и аппаратурное оформление, а также переработка реакционной смеси и выделение целевого продукта. К тому же нет оснований считать, что какие-то удаляемые с помощью вакуум-ректификации и азеотропной перегонки компоненты и композиции могут быть возвращены в повторные процессы без дополнительных очисток, концентрирований и других операций.
6. Ассортимент используемых кислот ограничен жирными кислотами в довольно небольшом диапазоне числа углеродных атомов. Нет оснований полагать возможность реализации такого процесса с ароматическими кислотами и содержащими в своем составе фенильные радикалы в качестве заместителей.
Наиболее близким к заявляемому являются сведения о маршруте превращения олова в карбоксилаты олова (IV) через стадию окисления металла в водном растворе азотной или соляной кислоты в отсутствие и в присутствии соединений меди (II) с образованием и накоплением в основном гидроксидов олова (II) с примесями основных солей и последующим окислением этих продуктов в присутствии соответствующей кислоты в небольшом стехиометрическом избытке соединениями меди (II) в карбоксилаты олова (IV) (Агеева Л.С., Пожидаева С.Д., Иванов А.М. Глубокие и быстрые при комнатных температурах превращения олова, его оксидов, гидроксидов и солей в присутствии кислот и механической активации процессов. Материалы III Международной Российско-Казахстанской научно-практической конференции г. Новосибирск, 27-29 апреля 2017 г., Изд-во НГТУ, 2017. – 363 с. (С. 52-55)).
Недостатками данного способа являются:
1. В нем очерчен лишь маршрут, но не выделен способ как таковой с ограничением режимных и прочих характеристик по природе исходного сырья, концентрационным факторам и условиям проведения.
2. Нет ясности в вопросе перехода от окисления металла в водных и водно-солевых растворах к окислению получаемых продуктов в карбоксилаты олова (IV) в органических средах, т.е. реализуется ли весь маршрут в последовательных стадиях одного процесса, либо данный процесс является двухстадийным с неопределенным промежутком времени между стадиями, либо вообще реализуемым как отдельные два процесса.
3. Нет достаточных и надежных сведений о доступных и эффективных окислителях соединений олова (II) в соединения олова (IV), о возможности использования для этих целей отработанных окислителей металла в водных и водно-солевых растворах в гидроксид олова (II), а также продуктов окисления меди и ее сплавов в различных условиях.
4. Нет никаких сведений о выделении целевого продукта из реакционной смеси, его потерях и условиях проведения этой операции.
Задачей предлагаемого решения является подобрать такие условия окисления и взаимодействия с карбоновыми кислотами явно некондиционных продуктов глубокого окисления олова, в том числе и покровного, в отсутствие или в присутствии соединений меди (II) в водных растворах азотной или соляной кислот, содержащимися в них соединениями меди, а также продуктами окисления меди и ее сплавов в водных, водно-органических и органических средах и их взаимодействия с минеральными и карбоновыми кислотами, в которых обозначенный окислительно-восстановительный брутто-процесс с явно пониженной чувствительностью к составу и способу получения окислителя и восстановителя как вторичного сырья протекал бы не только быстро и количественно, но и с высокой избирательностью по средней соли олова (IV) в качестве целевого продукта, не загрязненного большими содержаниями медьсодержащих примесей.
Поставленная задача достигается тем, что в качестве оловосодержащего сырья используют продукты окисления олова, включая и покровное, в водных растворах разбавленной азотной или соляной кислоты в отсутствие или в присутствии соединений меди (II) в качестве окислителя с отделенным или неотделенным непрореагировавшим металлом, продукты неколичественного и неселективного взаимодействия первых с бензойной и замещенными бензойными кислотами в органических средах, продукты взаимодействия оксида олова (II) с бензойными и замещенными бензойными кислотами при использовании недостаточно активного и селективного трибохимического катализатора, а также любые комбинации перечисленных выше вариантов в любых массовых соотношениях между собой; в качестве окислителя берут часть полученного при окислении олова в водных кислотах в присутствии медьсодержащих соединений продукта, продукты глубокого окисления меди или ее сплавов в присутствии соляной или азотной кислоты в разных условиях, часть продуктов их взаимодействия с карбоновыми кислотами в присутствии неэффективного трибохимического катализатора, продукты глубокого коррозионного разрушения меди и ее сплавов, продукты неполного и неселективного взаимодействия оксида, гидроксида или основного карбоната меди (II) с минеральными и соответствующими бензойными кислотами, либо небольшую часть продуктов заявляемого процесса, проводимого при повышенных содержаниях медьсодержащего окислителя; оловосодержащих соединений берут в загрузку в количестве 0,25-0,6 моль/кг; медьсодержащих 10-3-5·10-2 моль/кг; загрузку ведут в последовательности: стеклянный бисер в массовом отношении с остальной загрузкой 1:1, растворитель жидкой фазы и расчетное количество кислоты в мольном соотношении с содержанием оловосодержащих соединений (4,0÷4,05):1, включают механическое перемешивание и ведут приготовление раствора-суспензии кислоты, затем загружают восстановитель и окислитель и ведут процесс при механическом перемешивании и подаче протока воздуха через газовое пространство реактора в отсутствие подвода внешнего тепла и(или) принудительного охлаждения при текущем контроле за расходованием кислоты до достижения предварительно находимого расчетного значения, после чего процесс прекращают, проводят отделение стеклянного бисера и непрореагировавшего металла (если он присутствовал в загрузке и остался), полученную суспензию реакционной смеси фильтруют, осадок промывают на фильтре промывным растворителем, отжимают и направляют на воздушную сушку или очистку путем перекристаллизации; при этом в качестве кислоты используют бензойную, салициловую, антраниловую, 5-аминосалициловую или п-толуиловую, а в качестве растворителя - толуол, о-ксилол, уайт-спирит, сольвент или керосин.
Характеристика используемого сырья:
Вторичное оловосодержащее сырье:
Восстановитель 1 - твердый продукт, получаемый взаимодействием олова (включая и покровное) с разбавленными водными растворами азотной или соляной кислоты в отсутствие или в присутствии соответствующих солей аммония при комнатных или близких к ним температурах в условиях больших стехиометрических недостатков кислоты. Содержит в основном (до 95%) гидроксид олова (II) формулы SnО⋅хН2О (х – переменная величина) с примесями основных солей типа Sn(ОН)А, где А - анион рабочей кислоты.
Получение [в.1.1] Пожидаева С.Д., Григорьев Д.А., Агеева Л.С., Иванов А.М. Быстрое и глубокое разрушение белого олова под воздействием суспендированного малахита в подкисленном водном растворе нитрата аммония. Технология металлов. 2017, №7, С. 12-18.
Восстановитель 2 – аналогичный п.1 продукт, полученный в описанных выше условиях в присутствии соединений меди (II) в качестве окислителей в водных растворах азотной или соляной кислоты в условиях довольно интенсивного контакта хорошо перемешиваемой суспензии реакционной смеси с воздухом (содержание меди в продукте до 0,25 моль/кг). Получение: по п.1[в.1.1] и [в.2.1] Агеева Л.С., Пожидаева С.Д., Иванов А.М. Глубокие и быстрые при комнатных температурах превращения олова, его оксидов, гидроксидов и солей в присутствии кислот и механической активации процессов. Химические технологии функциональных материалов: Материалы III Международной Российско-Казахстанской научно-практической конференции. – Новосибирск: изд-во НГТУ, 2017. – 363 с; (С.52-55).
Восстановители 1 и 2 могут содержать и непрореагировавший твердый металл в различном мольном соотношении с оловосодержащими соединениями.
Восстановитель 3 (а и б) – оловосодержащие продукты взаимодействия восстановителя 1 (а) или 2 (б) с карбоновыми кислотами в присутствии недостаточно активного и селективного трибохимического катализатора; содержит смеси непрореагировавших гидроксида и основных солей олова (II) с карбоновой кислотой, а также основные и средние продукты-карбоксилаты в различных мольных соотношениях. Получение: п.2 [в.2.1] и [в.3.1] Пожидаева С.Д., Агеева Л.С., Иванов А.М. Избирательное получение бензоатов олова (II и IV) из металла, его оксидов и продуктов окисления в различных условиях. Технология металлов. 2017, №10, С.2-5.
Восстановитель 4 – продукт взаимодействия оксида олова (II) при использовании недостаточно активного и селективного (на основную или среднюю соль) трибохимического катализатора (смесь непрореагировавшего SnО и солей Sn(ОН)А и SnА2 (НА- кислота) в различных мольных соотношениях. Получение: источник п.3 [в.3.1].
Вторичные медьсодержащие окислители:
Окислитель 1 - содержащие соединения меди оловосодержащие продукты восстановителя 2; загрузка оловосодержащих продуктов (восстановителя) требует учета и их во вводимом окислителе 1. Получение: источники п.2 раздела восстановители [в.1.1] и [в.2.1].
Окислитель 2 - продукты глубокого окисления оловосодержащих бронз. Получение: [о.2.1] Патент РФ №2577878, опубл. 20.03.2016; [о.2.2] Пожидаева С.Д., Иванов А.М., Сотникова Д.А., Елисеева А.Ю. Взаимодействие оксида меди (II) с одноосновными минеральными кислотами в модельных условиях и в присутствии металлической меди. Журнал Неорганической химии. 2014, т.59, №1, С. 21-27); [о.2.3] Пожидаева С.Д., Елисеева А.Ю. Сотникова Д.А., Иванов А.М. Об использовании отходов меди и бронзы как вторичного сырья. Химическая технология. 2014, Т.15, №6, С.356-363; [о.2.4] Пожидаева С.Д., Елисеева А.Ю., Иванов А.М. Аномально глубокое и быстрое разрушение меди и бронзы под воздействием присутствующих на них продуктов коррозии. Технология металлов. 2014, №10, С.13-21; [о.2.5] Пожидаева С.Д., Иванов А.М. Оксиды марганца, железа и свинца в инициировании быстрого и глубокого разрушения меди и ее сплавов. Технология металлов. 2015, №8, С. 2-11; [о.2.6] Pozhidaeva S.D., Eliseeva A.Yu. Ivanov A.M., Anomalously Deep and Fast Failure of Copper and Bronze under the Action of the Corrosion Products Existing on Them RUSSIAN METALLURGY (METALLY). Vol. 2015, No. 13, Pp.1117-1123.
Как и в предыдущем случае содержащиеся в нем оловосодержащие продукты должны быть учтены в загрузке восстановителя.
Окислитель 3 - продукты глубокого окисления меди, богатые Сu(ОН)А как доминирующим в их составе [о.3.1] Иванов А.М., Кликин Е.Г., Пожидаева С.Д. Глубокое окисление меди оксидом меди (II) в подкисленных водно-солевых растворах. Часть 1. Макрокинетические характеристики процесса в зависимости от геометрической конфигурации корпуса. Известия Юго-Западного государственного университета. 2014, №5 (56), С.35-41; [о.3.2] Иванов А.М., Кликин Е.Г., Пожидаева С.Д. Глубокое окисление меди оксидом меди (II) в подкисленных водно-солевых растворах. Часть II. Влияние начального содержания хлорида аммония. Известия Юго-Западного государственного университета. 2015, №1 (58), С.26-35; [о.3.3] Пожидаева С.Д., Сотникова Д.А., Елисеева А.Ю., Иванов А.М. Об идентификации основных солей меди (II) в растворах, суспензиях и твердых фазах. Известия Юго-Западного государственного университета. 2013, №3(48), С.220- 227.
Окислитель 4 - продукты окисления меди с повышенным содержанием основных солей Сu(ОН)А⋅mСu(ОН)2 и (или) СuА2⋅nСu(ОН)2, где m=2 и менее, а n чаще всего 3. [о.3.2]; [о.3.3] и [о.4.1] Пожидаева С.Д., Елисеева А.Ю., Сотникова Д.А. Иванов А.М. Получение, выделение и анализ основных солей меди с формулой CuA2∙nCu(OH)2. Известия Юго-Западного государственного университета. 2013, №1(46), С.175- 180.
Окислитель 5 - продукты глубокого окисления иных сплавов меди (неоловянных бронз, латуней). [о.2.5].
Окислитель 6 - продукты неполного и неселективного взаимодействия малахита СuСО3⋅Сu(ОН)2 с кислотами. [в.1.1].
Окислитель 7 - продукты глубокого, но неселективного взаимодействия оксида меди (II) с карбоновыми кислотами. [о.7.1] Пожидаева С.Д., Сотникова Д.А., Елисеева А.Ю., Лазарева В.А., Иванов А.М Взаимодействия оксида меди (II) с кислыми солями двухосновных кислот в водных растворах в отсутствие и в присутствии металлической меди и ее сплавов. Известия Юго-Западного университета. 2012, №5(44), Ч.2, С.187- 193; [о.7.2] Пожидаева С.Д., Елисеева А.Ю., Сотникова Д.А., Иванов А.М. Взаимодействие оксидов металлов с кислотами в модельных условиях и в качестве промежуточной стадии сложных окислительно-восстановительных процессов. Известия Юго-Западного государственного университета. Серия Физика и химия. 2011, №2, С.38- 45.
Окислитель 8 – продукты глубокого превращения оксида меди (II) в присутствии минеральных кислот [о.2.2]; [о.8.1] Пожидаева С.Д., Сотникова Д.А., Иванов А.М. Взаимодействие оксида, гидроксида и основного карбоната меди (II) с концентрированными растворами фтороводородной кислоты. Известия Юго-Западного государственного университета. 2012, №3(42), Ч.1, С.126-132; [о.8.2] Пожидаева С.Д., Сотникова Д.А., Иванов А.М. Кинетика и продукты взаимодействия оксида (гидроксида) меди (II) с азотной кислотой. Известия Юго-Западного государственного университета. 2012, №5(44), Ч.2, С.176- 181; [о.8.3] Способ получения концентрированных водных растворов хлоркупрата меди (II) Cu[CuCl4]. Патент РФ №2528685, опубл. 20.09.2014, Бюл. № 26; [о.8.4] Способ получения основного хлорида или нитрата меди (II). Патент РФ №2476380, опубл. 27.02.2013, Бюл. № 6.
Кислоты:
Бензойная ГОСТ 6413-77
Салициловая ГОСТ 624-70
Антраниловая ТУ 6-09-3821-74
5-Аминосалициловая ТУ 6-09-07-691-76
п-Толуиловая ТУ 6-09-14-1974-78
Уайт-спирит ГОСТ 3134-78
Сольвент ГОСТ 10214-78
Керосин ГОСТ 18499-73
Проведение процесса заявляемым способом следующее. В бисерную мельницу вертикального типа с высокооборотной механической мешалкой вводят расчетные количества растворителя жидкой фазы, стеклянного бисера как перетирающего агента и кислоты-реагента. Включают механическое перемешивание и в течение определенного времени готовят раствор-суспензию кислоты. По истечении обозначенного времени, не прекращая перемешивания, вводят расчетные количества восстановителя и окислителя, подают проток воздуха через газовое пространство реактора и этот момент принимают за начало процесса. Контроль за его ходом ведут методом отбора проб реакционной смеси и определения в них непрореагировавшей кислоты. По достижению близкого к полному расходованию этого реагента или какой-либо расчетной величины этой характеристики процесс прекращают, проводят отделение суспензии реакционной смеси от перетирающего агента и непрореагировашего металла (если он брался в составе восстановителя и полностью не прореагировал), отделенную суспензию фильтруют, осадок на фильтре обрабатывают промывным растворителем, тщательно отжимают, снимают с фильтра и сушат или отправляют на очистку путем перекристаллизации.
Пример №1
В бисерную мельницу с цилиндрическим стеклянным корпусом с плоским дном и высокооборотной (1560 об/мин) механической мешалкой и входным отверстием 57 мм (общий объем 500 мл, размер лопасти из текстолита 53×26,7×2,6 мм) загружают 150,8 г о-ксилола, 200 г стеклянного бисера и 37,5 г бензойной кислоты. Включают механическое перемешивание и в течение 10 мин готовят раствор-суспензию кислоты. Далее, не прекращая перемешивания, вводят 10 г восстановителя 1 и 1,7 г восстановителя 2. Выполненный анализ показал содержание соединений Sn2+ в исходной загрузке 0,37 моль/кг и медьсодержащего окислителя 10-3 моль/кг. Через газовое пространство подают проток воздуха с расходом 0,59 л/(мин⋅кг) и этот момент принимают за начало эксперимента. По ходу процесса отбирают пробы реакционной смеси, в которых определяют содержание непрореагировавшей бензойной кислоты. Одновременно контролируют и температуру в зоне протекания процесса. Полученные данные представлены в таблице 1.
Таблица 1
По достижении остаточного значения кислоты 0,05 моль/кг перемешивание реакционной смеси и проток воздуха прекращают, корпус реактора отсоединяют от крышки с мешалкой и опускают в гнезде каркасной рамы настолько, чтобы нижняя кромка лопасти мешалки оказалась выше уровня реакционной смеси (РС), давая возможность остаткам РС стечь с лопасти и вала мешалки в течение 5 мин. Далее содержимое корпуса переносят в узел отделения РС от стеклянного бисера с сеткой с размерами ячеек 0,3×0,3 мм в качестве фильтровальной перегородки. Отделяемый бисер снимают с сетки и возвращают в корпус бисерной мельницы, который помещают на свое место в каркасной раме, мельницу собирают вновь, добавляют 50 г растворителя, включают механическое перемешивание и проводят отмывку перетирающего агента и элементов реактора от остатков РС. Далее проводят повторное отделение перетирающего агента от промывного растворителя. Бисер снимают с сетки, сушат и отправляют на загрузку повторного процесса.
Суспензию РС фильтруют, осадок на фильтре промывают промывным растворителем, хорошо отжимают и далее сушат до достижения постоянной массы, которая оказалась равной 43,33 г. При необходимости продукт направляют на дополнительную очистку путем перекристаллизации. Выход выделенного продукта без перекристаллизации составил 97,1%, после перекристаллизации 92,7% (41,36 г).
Примеры №2-12
Реактор, величина загрузки, природа кислоты, перетирающего агента, растворителя и окислителя, последовательности операций при загрузке, приготовлении раствора-суспензии кислоты, проведении, текущем контроле и завершении процесса, отделении и очистке от остатков РС перетирающего агента, выделении продукта и работы с ним аналогичны описанным в примере 1. Отличаются природой и содержанием восстановителя и начальным содержанием окислителя в исходной загрузке. Характеристики загрузки и проведенного процесса сведены в таблицу 2.
Таблица 2
проводимого процесса
природа (х+у)
металл, % от загрузки
загрузке, моль/кг
раствора-суспензии кислоты, мин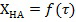
процесса, мин
Примеры №13-22
Реактор, величина загрузки, природа кислоты, растворителя, перетирающего агента и восстановителя, последовательности операций при загрузке, приготовлении раствора-суспензии кислоты, проведении текущего контроля и завершении процесса, отделении и очистке перетирающего агента, выделении продукта и работы с ним аналогичны описанным в примере 1. Отличаются природой и содержанием окислителя в исходной загрузке. Характеристики загрузки и проведения процесса сведены в таблицу 3.
Таблица 3
природа (х+у+…)
загрузке, моль/кг
металл, % от загрузки
исходной загрузке, моль/кг
загрузке, моль/кг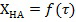
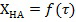
Продолжение таблицы 3
реактора от остатков РС:
% от исходной загрузки
продукта, г
продукта, %
Примеры №23-32
Реактор, величина загрузки, природа перетирающего агента и его количество, последовательности операций при загрузке, приготовлении раствора-суспензии кислоты, проведении процесса и текущего контроля за ним, его завершении, отделении перетирающего агента от суспензии продукта, выделении продукта и работы с ним аналогичны описанным в примере 1. Отличаются природой используемой кислоты и растворителя, присутствием в начальной стадии непрореагировавшего при получении восстановителя металла и количественными характеристиками основных реагентов в исходной загрузке. Указанные различия и полученные характеристики процессов сведены в таблицу 4.
Таблица 4
природа (х+у)
соединений в загрузке, моль/кг
Продолжение таблицы 4
% от загрузки
раствора-суспензии кислоты, мин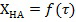
% от исходной загрузки
Положительный эффект предлагаемого решения состоит в том, что:
1. Основным сырьем (и восстановитель, и окислитель) являются выделенные в виде соответствующих твердых фаз продукты иных процессов, представляющие собой сложные многокомпонентные смеси переменного состава, не имеющие без разделения и очистки компонентов постоянного целевого использования. В предлагаемом решении из сложной смеси оловосодержащих продуктов получается с хорошим выходом один продукт: бензоат или замещенный бензоат олова (IV). При этом происходит значимое (в десятки раз) уменьшение в продукте медьсодержащих соединений, что во многих случаях значительно облегчает очистку от них.
2. Медьсодержащие продукты в продуктах окисления олова, меди и ее сплавов по эффективности их как окислителей в рассматриваемых брутто-процессах не уступают индивидуальным соединениям меди (II), но являются более стабильными к дезактивации, что предопределяет использование их в меньших количествах, вплоть до близких к каталитическим.
3. Избытки начальных дозировок кислоты сказываются на некотором увеличении растворимости продукта в жидкой фазе реакционной смеси, что способствует некоторому снижению выхода выделяемого целевого продукта. Но поскольку отделяемые жидкие фазы, как и промывные растворители возвращаются на загрузку повторных процессов без их разделения и концентрирования, обозначенные потери относятся лишь к конкретному варианту и во многом нивелируются в серии.
4. Предлагаемые решения реализуются в отсутствии подвода внешнего тепла и использования принудительного охлаждения. Они легко управляемы и контролируемы. Причем кинетический вариант их проведения позволяет легко устанавливать целесообразный момент прекращения окислительно-восстановительного брутто-процесса.
5. Предлагаемое решение приемлемо не только для бензойной кислоты, но и для ряда замещенных бензойных кислот, что является благоприятным фактором. Это допускает использование ряда растворителей, что облегчает применение получаемых суспензий солей олова (IV) в качестве окислителей металла без выделения конкретного карбоксилата, его очистки и сушки.
6. Оборудование для предлагаемого решения простое, в нем нет котлонадзорных элементов и его довольно просто изготовить.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения соли олова (IV) с анионами азотной и бензойной кислот | 2020 |
|
RU2735433C1 |
| Двухстадийный способ получения карбоксилатов олова (II) из металла | 2017 |
|
RU2678092C1 |
| Способ получения карбоксилатов олова (II) | 2017 |
|
RU2670199C1 |
| Способ получения нитрата олова (IV) путем окисления нитрата олова (II) | 2019 |
|
RU2717810C1 |
| Способ получения бензоата и замещенных бензоатов олова (IV) | 2017 |
|
RU2660905C1 |
| Способ получения нитрата олова (II) при окислении металла | 2020 |
|
RU2744006C1 |
| Способ получения основного бензоата олова (II) | 2017 |
|
RU2650893C1 |
| Способ получения основного нитрата олова (IV) Sn(OH)(NO) | 2017 |
|
RU2680065C1 |
| Способ получения карбоксилатов олова (II) | 2017 |
|
RU2671197C1 |
| Способ получения ацетата или оксалата свинца из его оксида (II) | 2023 |
|
RU2807759C1 |
Изобретение относится к усовершенствованному способу получения бензоата и замещенных бензоатов олова (IV) из вторичного сырья путем окисления соединений олова (II) соединениями меди (II) в бисерной мельнице вертикального типа с протоком воздуха через газовое пространство реактора и стеклянным бисером в качестве перетирающего агента, в котором оловосодержащие и медьсодержащие реагенты являются твердыми продуктами других окислительно-восстановительных процессов без какого-либо разделения и концентрирования, т.е. по-существу вторичным сырьем. В частности, в качестве оловосодержащего сырья используют продукты окисления олова, включая и покровное, в водных растворах разбавленной азотной или соляной кислоты в отсутствие или в присутствии соединений меди (II) в качестве окислителя с отделенным или неотделенным непрореагировавшим металлом, продукты неколичественного и неселективного взаимодействия первых с бензойной и замещенными бензойными кислотами в органических средах, продукты взаимодействия оксида олова (II) с бензойными и замещенными бензойными кислотами при использовании недостаточно активного и селективного трибохимического катализатора, а также любые комбинации перечисленных выше вариантов в любых массовых соотношениях между собой. В качестве же окислителя берут часть полученного при окислении олова в водных кислотах в присутствии медьсодержащих соединений продукта, продукты глубокого окисления меди или ее сплавов в присутствии соляной или азотной кислоты в различных условиях, часть продуктов их взаимодействия с карбоновыми кислотами в присутствии неэффективного трибохимического катализатора, продукты глубокого коррозионного разрушения меди и ее сплавов, продукты неполного и неселективного взаимодействия оксида, гидроксида или основного карбоната с минеральными и соответствующими бензойными кислотами, либо небольшую часть продуктов заявляемого процесса, проводимого при повышенных содержаниях медьсодержащего окислителя. В загрузку оловосодержащих соединений берут в количестве 0,25-0,60 моль/кг, медьсодержащих 5·10-2-10-3 моль/кг, загрузку ведут в последовательности: стеклянный бисер в массовом соотношении с остальной загрузкой 1:1, растворитель жидкой фазы и расчетное количество кислоты в мольном соотношении с содержанием оловосодержащих соединений (4,0÷4,05):1. Включают механическое перемешивание и ведут приготовление раствора-суспензии кислоты. Затем загружают восстановитель и окислитель и ведут процесс при механическом перемешивании и подаче протока воздуха через газовое пространство реактора в отсутствие подвода внешнего тепла и(или) принудительного охлаждения при текущем контроле за расходованием кислоты до достижения предварительно находимого расчетного значения. После этого процесс прекращают, проводят отделение стеклянного бисера и непрореагировавшего металла (если он присутствовал в загрузке и остался), суспензию реакционной смеси фильтруют, осадок промывают на фильтре растворителем, отжимают и направляют на воздушную сушку или очистку путем перекристаллизации. 2 з.п. ф-лы, 4 табл., 12 пр.
1. Способ получения бензоата и замещенных бензоатов олова (IV) из вторичного сырья в бисерной мельнице вертикального типа с высокооборотной механической мешалкой лопастного типа в присутствии стеклянного бисера как перетирающего агента путем окисления смесей соединений олова (II) соединениями меди (II), отличающийся пониженной чувствительностью к природе и способу получения как восстановителя, так и окислителя, в котором в качестве оловосодержащего сырья используют продукты окисления олова, включая и покровное, в водных растворах разбавленной азотной или соляной кислоты в отсутствие или в присутствии соединений меди (II) в качестве окислителя с отделенным или неотделенным непрореагировавшим металлом, продукты неколичественного и неселективного взаимодействия первых с бензойной и замещенными бензойными кислотами в органических средах, продукты взаимодействия оксида олова (II) с бензойными и замещенными бензойными кислотами при использовании недостаточно активного и селективного трибохимического катализатора, а также любые комбинации перечисленных выше вариантов в любых массовых соотношениях между собой; в качестве окислителя берут часть полученного при окислении олова в водных кислотах в присутствии медьсодержащих соединений продукта, продукты глубокого окисления меди или ее сплавов в присутствии соляной или азотной кислоты в разных условиях, часть продуктов их взаимодействия с карбоновыми кислотами в присутствии неэффективного трибохимического катализатора, продукты глубокого коррозионного разрушения меди и ее сплавов, продукты неполного и неселективного взаимодействия оксида, гидроксида или основного карбоната меди (II) с минеральными и соответствующими бензойными кислотами, либо небольшую часть продуктов заявляемого процесса, проводимого при повышенных содержаниях медьсодержащего окислителя; оловосодержащих соединений берут в загрузку в количестве 0,25-0,6 моль/кг; медьсодержащих 5⋅10-2÷10-3 моль/кг, загрузку ведут в последовательности: стеклянный бисер в массовом отношении с остальной загрузкой 1:1, растворитель жидкой фазы и расчетное количество кислоты в мольном соотношении с содержанием оловосодержащих соединений (4,0÷4,05):1, включают механическое перемешивание и ведут приготовление раствора-суспензии кислоты, затем загружают восстановитель и окислитель и ведут процесс при механическом перемешивании и подаче протока воздуха через газовое пространство реактора в отсутствие подвода внешнего тепла и(или) принудительного охлаждения при текущем контроле за расходованием кислоты до достижения предварительно находимого расчетного значения, после чего процесс прекращают, проводят отделение стеклянного бисера и непрореагировавшего металла (если он присутствовал в загрузке и остался), полученную суспензию реакционной смеси фильтруют, осадок промывают на фильтре промывным растворителем, отжимают и направляют на воздушную сушку или очистку путем перекристаллизации.
2. Способ по п.1, отличающийся тем, что в качестве кислоты используют бензойную, салициловую, антраниловую, 5-аминосалициловую или п-толуиловую.
3. Способ по п.1, отличающийся тем, что в качестве растворителя используют толуол, о-ксилол, уайт-спирит, сольвент или керосин.
| Vasanta, E | |||
| N | |||
| et al | |||
| "Synthesis and reactions of tin tetracarboxylates" | |||
| Inorganica Chimica Acta, 26(1), 47-50, 1978, реферат CAS 88:145335 | |||
| Ol'dekop, Yu | |||
| A | |||
| et al | |||
| "Acylates of mercury(I) oxide in an anion exchange reaction: synthesis of tin tetraacylates and some organometallic acylates" | |||
| Vestsi Akademii Navuk BSSR, Seryya Khimichnykh Navuk (4), 128-31, 1979, реферат CAS 91:175460 | |||
| Reichle, Walter T | |||
| "Pyrolysis of phenyltin benzoates and related substances" | |||
| Journal of Organometallic Chemistry, 18(1), 105-15, 1969, реферат CAS 71:50131 | |||
| Moore, McDonald et al | |||
| "Organotin esters." Quarterly Journal of the Florida Academy of Sciences, 29, 73-6, 1966, реферат CAS 66:28483 | |||
| Способ получения бензоата олова (II) | 2016 |
|
RU2630310C1 |
Авторы
Даты
2018-11-27—Публикация
2017-11-08—Подача