Область техники
Настоящее изобретение относится к рекомбинантным антигенам, содержащим суперспиральные домены или антигенам, слитым с белками, содержащими суперспирали, где эти суперспирали модифицированы. Модификация улучшает иммуногенность таких антигенов. Одновременно она повышает их способность связываться с отрицательно заряженными полимерами, такими как нуклеиновые кислоты, включая ДНК и РНК, а также с гепарином.
Предшествующий уровень техники
Суперспираль представляет собой структурный мотив в белках, в котором альфа-спирали скручены вместе, как пряди каната. Суперспиральные домены часто встречаются в природных белках (1, 2) и могут быть распространенным способом организации олигомеризованных белков. Суперспирали состоят из двух или более альфа-спиралей, закрученных вокруг друг друга в суперспираль, простую, но универсальную укладку белка (3). Типичная суперспирализованная первичная последовательность является повторяющейся, состоящей из семичленных повторов, так называемых «гептад».
Многие белки суперспирального типа принимают участие в важных биологических функциях. Особый интерес для настоящего изобретения представляют те из них, которые обнаружены в антигенах или белках-носителях.
Примеры суперспиралей, обнаруженные в антигенах включают, без ограничений:
I) димерные суперспирали, обнаруженные в семействе ОСА (где ОСА означает олигомерный суперспиральный адгезии, от англ. oligomeric coiled coil adhesin): примерами которого являются NadA, защитный антиген из менингококка Neisseria meningitidis (4); адгезии YadA из иерсинии Yersinia enterocolitica (5); адгезии UspA2 из диплококка Moraxella catarrhalis (6); адгезии BadA из бартонеллы Bartonella henselae (7) и адгезии HadA из гемофильной палочки Haemophilus influenzae (8).
II) тримерные суперспирали, обнаруженные, среди прочего, в белке НА2, гемагглютинине вируса гриппа А (9), гликопротеине F респираторно-синцитиального вируса (10), в гликопротеинах gp41 вирусов иммунодефицита человека ВИЧ-1 (11) и ВИЧ-2 (12), и гликопротеине gp1,2 эболавируса Ebolavirus (13).
III) тетрамерные суперспирали, обнаруженные в гликопротеине HN (от англ. hemagglutinin-neuraminidase - гемагглютинин-нейраминидаза) вируса болезни Ньюкасла и других парамиксовирусов (14 и ссылки в этом источнике).
Белки-носители применяются, в частности, для повышения иммуногенности антигенов. Белки-носители, содержащие суперспирали, были описаны ранее, в частности, пентамер, полученный из олигомерного матриксного белка хряща СОМР (15), и искусственные последовательности, которые также образуют пентамеры (34), и гептамеры, полученные из доменов олигомеризации млекопитающих C4bp, таких как мышиный домен IMX108 (16), или птичьи домены олигомеризации C4bp (16, WO 2005/077976 и WO 2007/062819). Гибрид птичьего домена олигомеризации, называемый IMX313 (WO 2007/062819), используется в настоящем описании в качестве примера.
На предшествующем уровне техники суперспирали были предметом обширных исследований с целью понять, чем определяется у них состояние олигомеризации и соответствующая ориентация (параллельная или антипараллельная) их спиралей (35). Однако, исследования с целью улучшить иммуногенность антигенов, модифицируя их суперспирали, не проводились. Два примечательных примера из предшествующего уровня техники относятся к работающим в производстве вакцин группам, которым требовалось выделить для целей вакцинации два отдельных антигена, содержащих суперспирали (10, 36, 37); но ни одна из этих групп не модифицировала суперспирали в антигене.
Как было показано на предшествующем уровне техники, некоторые специфические пептиды улучшают связывающие свойства мономерных белков, не имеющих суперспиралей. Было показано, что рекомбинантные белки легче очистить с помощью ионообменной хроматографии, если с ними слит концевой участок полиаргинина (17, 18). При прошлом применении дополнительные остатки аргинина были удалены после очистки энзимологическими средствами (17, 18) или, в ином случае, были оставлены на своем месте и использовались для иммобилизации ферментов и/или рефолдинга (19, 20). Для иммобилизации мономерного фермента на колонке с гепарин-сефарозой был использован короткий пептид длиной в шесть последовательных остатков аргинина, что предотвращало агрегацию мономеров путем связывания матрицы и позволяло повторное использование фермента (19, 20). Fuchs и Raines показали, что полиаргининовая метка из девяти аминокислот может быть использована для иммобилизации мономерного фермента (РНКазы А) на различных носителях, таких как стекло и силикагелевая смола (22).
Были описаны другие пептиды, связывающие нуклеиновые кислоты, например, мотив SPKK, который был идентифицирован в 1980 в качестве ДНК-связывающего мотива, и пептиды, содержащие мотив SPKK, которые могут связывать двухцепочечную ДНК (21). Тем не менее, связывание с РНК или одноцепочечной ДНК не было продемонстрировано, причем, данные Suzuki убедительно показывают, что связывание с одноцепочечной ДНК не будет происходить, поскольку малая бороздка существует только в молекулах в форме двойной спирали.
Другие пептиды, для которых было продемонстрировано связывание ДНК, включают протамин-подобный домен ядерного антигена вируса гепатита В (38), который содержит пептидную последовательность SPRRRRS, используемую в некоторых примерах настоящего описания.
Однако концевые участки полиаргинина очень чувствительны к расщеплению под действием протеаз, особенно сериновых протеаз, поэтому они при обычном применении как для целей очистки, так и в целях иммобилизации были заменены полигистидиновыми метками (45).
Дополнительно, на предшествующем уровне технике пептиды были слиты с мономерными белками для того, чтобы улучшить их иммуногенность. Shibagaki с коллегами показали, что домены белковой трансдукции (ДБТ) могут быть использованы для улучшения трансдукции дендритных клеток (ДК) in vitro, и что при введении трансдуцированных ДК животным достигается улучшение иммуногенности антигена (43). Кроме того, Shimada с коллегами показали, что полиаргининовые пептиды могут улучшать иммуногенность белка, яичного альбумина, с которым они слиты (42), либо при введении непосредственно в опухоль, экспрессирующую белок, либо при внутрикожном введении (41).
Большинство очищенных антигенов являются слабо иммуногенными. Для повышения их иммуногенности были использованы адъюванты. Ранее было продемонстрировано применение небольших, содержащих суперспираль, доменов белков C4bp для повышения иммуногенности антигенов:
- в патенте WO 2007/062819 описаны комплексы, содержащие в качестве первого компонента домен птичьего белка C4bp, а в качестве второго компонента антиген, причем все упомянутые элементы были в форме слитого белка или являлись нековалентно связанными. Этот комплекс показывает повышенную иммуногенность антигена при введении в организм.
- в патенте WO 2011/045612 описан слитый белок, содержащий фрагмент куриного белка C4bp и микобактериальный антиген 85А. Этот слитый белок повышает иммуногенность 85А не только у таких животных, как грызуны, но также и у приматов.
Кроме того, для совершенствования методов иммунизации также имеет большое значение индукция сигналы через толл-подобные рецепторы (ТПР), но не менее важно иметь возможность ограничения такой сигнализации. Толл-подобные рецепторы (ТПР) представляют собой класс белков, которые играют ключевую роль в иммунной системе. После того, как микробы нарушили физические барьеры организмов, они распознаются ТПР. Отличительные признаки для распознавания микробов включают двухцепочечную РНК вирусов, неметилированные CpG сайты бактериальной и вирусной ДНК и некоторые другие молекулы РНК и ДНК.
Существует значительная заинтересованность в таких нуклеиновых кислотах, поскольку они являются лигандами класса толл-подобных рецепторов (далее ТПР), и, в частности, таких рецепторов, как ТПР3, ТПР7, ТПР8, ТПР9 и ТПР13 (23 и ссылки в нем). Иногда они классифицируются как «внутриклеточные толл-подобные рецепторы», но, по меньшей мере, ТПР3 присутствует также на поверхности некоторых клеток (24). ТПР7 и ТПР9 локализованы во внутриклеточных компартментах (в частности, в эндоплазматическом ретикулуме и эндосомах), и было четко показано для рецепторов ТПР9 и ТПР7, что отщепление рецептора необходимо для активации MyD88, через который лиганды рецепторов передают сигнал (25, 26). Поскольку это отщепление происходит только в эндолизосомах, то возможно, что оно представляет собой эволюционную адаптацию для предотвращения нежелательных сигналов от отдельных нуклеиновых кислот.
ТПР3 экспрессируется в различных эпителиальных клетках, включая клетки дыхательных путей, матки, роговицы, влагалища, шейки матки, желчные и кишечные эпителиальные клетки, и по-видимому, эти клетки экспрессируют ТПР3 на их клеточной поверхности (24). Возможно поэтому не является удивительным то, что введение Poly(I:С) сопровождалось рядом побочных эффектов (26). В этом исследовании использовали его повторное введение в дозах 3 мг на грамм. Если средняя мышь имеет массу около 35 г, то повторно вводимая доза 100 мг может вызвать такие эффекты. Для иммунизации, описанной в настоящем изобретении, требуется только 2,5 мкг Poly(I:C) на дозу.
Важно то, что ограничение сигналов через эти рецепторы, и в частности рецептор ТПР3, зависит от дозы. Таким образом, существенным является преимущество прочного связывания нуклеиновых лигандов с антигеном. Поэтому прочно связанные лиганды внутриклеточных ТПР намного предпочтительнее препаратов, в которых связывание является менее прочным. Вот почему, специалисты в данной области техники ведут поиск антигенных композиций, способных эффективно связывать лиганды ТПР так, что они не отделяются от антигена прежде, чем антиген поступает в клетки, где он будет вызвать иммунный ответ, с целью уменьшения потенциальных побочных эффектов, опосредованных связыванием лигандов рецепторов ТПР в других местах.
Краткое описание изобретения
Изобретение относится к белкам, содержащим суперспиральные домены, которые модифицированы путем связывания положительно заряженного пептида с суперспиральным доменом. Модифицированные белки суперспирального типа имеют повышенную иммуногенность и одновременно улучшенные свойства связывания с отрицательно заряженными полимерами, такими как гепарин и нуклеиновые кислоты. Все суперспиральные белки являются рекомбинантными, а модификации получены путем слияния коротких пептидных последовательностей с концами суперспиральных доменов. В приведенных в настоящем изобретении примерах модификация осуществляется с помощью методов генной инженерии, но существуют и другие способы получения модифицированных суперспиралей, такие как пептидный синтез.
Этот положительно заряженный пептид содержит преимущественно аргинин, но вместо последнего может также содержать лизины или комбинацию аргинина и лизина. Этот пептид является коротким, состоящим из семи или менее аминокислот, в частности, 5, 6 или 7 аминокислот. Один или более пептидов могут быть использованы для каждой цепи суперспирали.
Связь осуществляется непосредственно с суперспиральным доменом или через линкерный пептид, содержащий одну или более аминокислот, которые не влияют на технические эффекты суперспирального домена, положительно заряженного пептида и их комбинацию. Линкеры могут содержать любые аминокислоты, но предпочтительные линкеры содержат глицин, серии или пролин или их комбинации.
В одном наборе примеров модифицированный белок IMX313 является белком-носителем, полученным из куриных белков C4bp.
Изобретение также относится к слитому белку, содержащему модифицированный суперспиральный белок-носитель, слитый с антигеном.
Изобретение также относится к модифицированному антигену, содержащему модифицированный суперспиральный домен.
Изобретение также относится к иммуногенной композиции, содержащей модифицированный слитый белок или модифицированный антиген и лиганды на основе нуклеиновых кислот для внутриклеточных ТПР.
Изобретение также относится к подложке, несущей модифицированный белок по настоящему изобретению, при этом связь с подложкой образуется посредством пептида, связанного с суперспиральным доменом. Подложка на основе гепарина может быть использована in vitro или in vivo. Способы с использованием гепарина для повышения иммуногенности положительно заряженных белков хорошо известны (47, и ссылки в нем).
Настоящая заявка также относится к применению модифицированного антигена или модифицированного слитого белка или иммуногенной композиции, таких, как описанные выше, для индукции иммунного ответа у пациента.
Модифицированный белок суперспирального типа в соответствии с настоящей патентной заявкой, в котором положительно заряженный пептид связан с суперспиральным доменом модифицированного белка, имеет преимущества по сравнению с соответствующим немодифицированным белком, а именно:
- лучшее связывание с отрицательно заряженными хроматографическими колонками, такими как катионная ионообменная колонка SP FF и, особенно, колонками с гепарин-сефарозой;
- лучшее связывание с нуклеиновыми кислотами;
- в случае белков-носителей и антигенов, повышенная иммуногенность антигенов, которые представляют собой модифицированные белки суперспирального типа, или повышенная иммуногенность антигенов, ассоциированных с модифицированными белками-носителями.
Подробное описание изобретения
Перед подробным описанием настоящего изобретения следует понять, что данное изобретение не ограничивается лишь приведенными в качестве примеров способами и, безусловно, может изменяться. В частности, настоящее изобретение относится к модифицированным антигенам, обладающим суперспиральными доменами, а не ограничивается конкретными белками-носителями или специфическими антигенами, содержащими суперспирали.
Все публикации, патенты и патентные заявки, цитируемые в настоящем изобретении, как приведенные выше, так и следующие ниже, включены в данное изобретение посредством ссылки во всей своей полноте. Тем не менее, публикации, упомянутые в настоящем документе, приводятся с целью описания и раскрытия протоколов, реагентов и векторов, которые представлены в публикации и могут быть использованы в связи с настоящим изобретением.
Кроме того, для осуществления настоящего изобретения используются, если не указано иное, обычные методы очистки белков и молекулярно-биологические методы, известные в данной области техники. Такие методы хорошо известны специалистам в данной области техники, и описаны в литературе. В формуле изобретения, которая следует ниже, и в последовательном описании изобретения, за исключением случаев, когда контекст требует иного толкования для того, чтобы передать язык или необходимый смысл, слова «охватывать», «содержать», «включать» или «включать в себя» или варианты, такие как «содержит», «заключающий в себе», «содержащий», «включенный», «включает», «включающий», используются в широком смысле, т.е. для того, чтобы указать присутствие указанных элементов, но не для того, чтобы исключить наличие или добавление дополнительных функций в различные формы осуществления изобретения.
Следующим ниже терминам даны определения для лучшего понимания изобретения:
«Белок суперспирального типа», также называемый «белок, содержащий суперспирали» или «белок, обладающий суперспиральным доменом», обозначает белок, содержащий суперспиральный мотив, т.е., по меньшей мере, две альфа-спиральные нити, закрученные вокруг друг друга в суперспираль. Некоторые белки, содержащие такие суперспирали, были описаны в литературе. Согласно изобретению, предпочтительными белками суперспирального типа являются антигены и белки-носители.
«Белок-носитель» обозначает, как правило, белок с которым антигены конъюгированы или слиты и тем самым приведены в более иммуногенное состояние. Здесь этот термин специально используется в значении «белок, несущий антиген». Функцией этого белка является повышение иммуногенности антигена, с которым он конъюгирован или слит. Слияние имеет то преимущество, что оно создает однородный продукт. Более формально «конъюгация» может быть описана с генетической точки зрения: ДНК, кодирующую про-иммуногенную метку или белок-носитель, подвергают сплайсингу с ДНК, кодирующей антиген. При использовании традиционных химических методов конъюгации не всегда можно точно контролировать то, в какой позиции антиген соединяется с белком. Данный подкласс белков-носителей в этой форме также называют «про-иммуногенные метки» или даже «адъювант» (16) или «генетический адъювант».
Согласно изобретению, термин «модифицированный белок» обозначает белок, имеющий модифицированную последовательность по сравнению с последовательностью дикого типа, с добавлением или частичным замещением положительно заряженного пептида по изобретению. Разница между немодифицированным белком и модифицированным белком по изобретению заключается в положительно заряженном пептиде, связанном с суперспиральным доменом, к которому он либо присоединен, либо частично его замещает. Специалист в данной области техники поймет, что модифицированный белок по настоящему изобретению представляет собой рекомбинантный белок или химеру, не обнаруживаемую в природе. Природные белки, содержащие суперспиральный домен и заряженный пептидный домен, модифицированный в каком-либо другом месте, кроме заряженного пептидного домена, не входят в объем настоящего изобретения.
Изобретение относится к модифицированному белку, содержащему (i) белок, имеющий суперспиральный домен и (ii), по меньшей мере, один положительно заряженный пептид, связанный с суперспиральным доменом, причем, этот положительно заряженный пептид имеет последовательность ZXBBBBZ (SEQ ID NO: 1), где:
- Z представляет собой любую аминокислоту или отсутствует;
- X представляет собой любую аминокислоту;
- В представляет собой аргинин (R) или лизин (К).
Если требуется защитить пептид от разрушения экзопротеазами, такими как карбоксипептидаза В, то последней аминокислотой пептида не может быть ни остаток аргинина, ни остаток лизина.
Если модифицированный белок по изобретению содержит более одного положительно заряженного пептида SEQ ID NO: 1, то предпочтительно, чтобы эти пептиды были слиты вместе для того, чтобы образовать один положительно заряженный пептид, являющийся повторением последовательности SEQ ID NO: 1 с формулой (ZXBBBBZ)n, где n является целым числом от 1 или более, по меньшей мере, до 6, в частности 1, 2, 3, 4, 5 или 6, предпочтительно 2.
В другой форме осуществления настоящего изобретения 2, 3, 4, 5 или 6 пептидов могут быть разделены одним или более линкерами, как определено ниже.
В предпочтительной форме осуществления настоящего изобретения пептид имеет последовательность, выбранную из группы, состоящей из последовательностей SPRRRRS (SEQ ID NO: 2), GRRRR (SEQ ID NO: 3), SPKKKK (SEQ ID NO: 4), GKKKK (SEQ ID NO: 5) и GRRRRRS (SEQ ID NO: 36), в частности, для гептамерных суперспиралей. Для тримерных суперспиралей слияние двух положительно заряженных пептидов является особенно предпочтительным, более предпочтительно с последовательностью, выбранной из группы, состоящей из последовательностей SPRRRRRRRRRS (SEQ ID NO: 37), комбинации первого пептида SPRRRR (SEQ ID NO: 38) со вторым пептидом RRRRRS (SEQ ID NO: 39) и GRRRRRRRRRRS (SEQ ID NO: 40), комбинации первого пептида GRRRR (SEQ ID NO: 41) с пептидом RRRRRS (SEQ ID NO: 39).
Пептид может быть присоединен к суперспирали на С-конце или на N-конце. Слияние пептида с белком может быть выполнено с помощью линкера (короткой пептидной последовательности, связывающей пептид и белок) или без линкера. Линкеры могут содержать любые аминокислоты, но предпочтительные линкеры содержат глицин, серин или пролин, или их комбинации.
В конкретной форме осуществления настоящего изобретения несколько аминокислот С-конца белка могут быть удалены и заменены одной или более копиями пептида ZXBBBBZ.
В предпочтительном аспекте изобретения пептид связан с суперспиралью на его С-конце.
В одном аспекте настоящего изобретения модифицированный белок имеет функцию белка-носителя, в частности, действует как носитель для антигенов.
В предпочтительном аспекте изобретения модифицированный белок является куриным С4-связывающим белком-носителем, называемым IMX313, который содержит гептамерную суперспираль, описанную в патентной заявке WO 2007/062819.
Специфический модифицированный белок по изобретению представляет собой белок IMX313, в котором пептид GRRRR (SEQ ID NO: 3) связан с суперспиральным доменом белка IMX313.
Другой специфический модифицированный белок по изобретению представляет собой белок IMX313, в котором пептид SPKKKK (SEQ ID NO: 4) связан с суперспиральным доменом белка IMX313.
Еще одним специфическим модифицированным белком по изобретению является белок IMX313, в котором пептид GKKKK (SEQ ID NO: 5) связан с суперспиральным доменом белка IMX313.
Предпочтительный конкретный модифицированный белок по изобретению представляет собой белок IMX313 в котором пептид SPRRRRS (SEQ ID NO: 2) связан с суперспиральным доменом белка IMX313.
Аминокислотные последовательности белков IMX313, IMX313T и IMX313P показаны ниже (знак * означает стоп-кодон):
 (SEQ ID NO: 6)
(SEQ ID NO: 6)

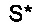 (SEQ ID NO: 7)
(SEQ ID NO: 7)
 (SEQ ID NO: 42).
(SEQ ID NO: 42).
В предпочтительной форме осуществления настоящего изобретения белок, имеющий функцию белка-носителя, представляет собой IMX313P (SEQ ID NO: 42). Белок, содержащий последовательность IMX313P (SEQ ID NO: 42), в чистом виде также является объектом настоящего изобретения, отдельно или слитым с одним или более положительно заряженным пептидом и антигеном или другим белком.
В наиболее предпочтительной форме осуществления настоящего изобретения суперспиральный домен белка IMX313P (SEQ ID NO: 42) связан с двумя слитыми положительно заряженными пептидами SEQ ID NO: 1, более предпочтительно с пептидом, имеющим последовательность SPRRRRRRRRRS (SEQ ID NO: 37) или пептидом, имеющим последовательность GRRRRRRRRRRS (SEQ ID NO: 40).
В другом аспекте настоящего изобретения модифицированный белок не является белком-носителем, а представляет собой антиген. Этот олигомерный антиген, в частности, выбирают из группы, состоящей из:
гемагглютинина вируса гриппа НА,
гликопротеина F респираторно-синцитиального вируса,
гликопротеина gp41 вируса иммунодефицита человека ВИЧ-1,
гликопротеина gp41 вируса иммунодефицита человека ВИЧ-2,
гликопротеина gp1,2 эболавируса Ebolavirus,
защитного антигена NadA из менингококка Neisseria meningitidis,
адгезина YadA из иерсинии Yersinia enterocolitica,
адгезина UspA2 из диплококка Moraxella catarrhalis,
адгезина BadA из бартонеллы Bartonella henselae, и
адгезина HadA из гемофильной палочки Haemophilus influenzae.
Изобретение также относится к связи между модифицированным белком-носителем и антигеном. Такая связь белка-носителя (IMX313) и антигена, как уже было показано, повышает иммуногенность антигена (см. патентную заявку WO 2007/062819). С применением модифицированного белка-носителя увеличение иммуногенности даже выше, чем с применением немодифицированного белка IMX313.
В частности, модифицированный белок-носитель, связанный с антигеном представляет собой белок IMX313P, имеющий последовательность SEQ ID NO: 42.
В одном альтернативном варианте два связанных компонента являются нековалентно связанными друг с другом. В предпочтительном альтернативном варианте два связанных компонента химически сопряжены и находятся в форме слитого белка. Специалисту в данной области техники известно, как соединить два пептидных компонента с целью получения слитого белка.
Изобретение, в частности, относится к слитому белку, содержащему белок-носитель с модифицированной суперспиралью и один или более антигенов.
В предпочтительном аспекте изобретения один из следующих антигенов слит с модифицированными белками IMX313T или IMX313P:
i) протеин А золотистого стафилококка Staphylococcus aureus, мутированный, как описано в (27, 44), или альфа-гемолизин золотистого стафилококка Staphylococcus aureus или белок ClfB золотистого стафилококка Staphylococcus aureus или белок сортаза F золотистого стафилококка Staphylococcus aureus;
ii) белок 85А, секретируемый микобактерией туберкулеза Mycobacterium tuberculosis (28);
iii) аутоантиген GnRH;
iv) криптоспоридиальный антиген СР15;
v) нуклеопротеин вируса гриппа.
Специфический слитый белок по настоящему изобретению представляет собой белок IMX313P (SEQ ID NO: 42), где пептид GRRRRRS (SEQ ID NO: 36) связан с суперспиральным доменом из белка IMX313, а модифицированный белок слит с протеином А золотистого стафилококка Staphylococcus aureus.
Другим специфическим слитый белком по настоящему изобретению является белок IMX313P (SEQ ID NO: 42), в котором пептид GRRRRRS (SEQ ID NO: 36) связан с суперспиральным доменом белка IMX313, а модифицированный белок слит с белком 85А.
Еще одним специфическим слитым белком по настоящему изобретению является белок IMX313 (SEQ ID NO: 6), в котором пептид SPKKKK (SEQ ID NO: 4) связан с суперспиральным доменом белка IMX313, а модифицированный белок слит с протеином А золотистого стафилококка Staphylococcus aureus.
Другим специфическим слитым белком по настоящему изобретению является белок IMX313 (SEQ ID NO: 6), в котором пептид SPKKKK (SEQ ID NO: 4) связан с суперспиральным доменом белка IMX313, а модифицированный белок слит с белком 85А.
Еще одним специфическим слитым белком по настоящему изобретению является белок IMX313 (SEQ ID NO: 6), в котором пептид GKKKK (SEQ ID NO: 5) связан с суперспиральным доменом белка IMX313, и модифицированный белок слит с протеином А золотистого стафилококка Staphylococcus aureus.
Еще одним специфическим слитым белком по настоящему изобретению является белок IMX313 (SEQ ID NO: 6), в котором пептид GKKKK (SEQ ID NO: 5) связан с суперспиральным доменом белка IMX313, а модифицированный белок слит с белком 85А.
Другим специфическим слитым белком по настоящему изобретению является белок IMX108T (SEQ ID NO: 64), в котором пептид SPRRRRS (SEQ ID NO: 2) слит с суперспиральным доменом белка IMX108 (SEQ ID NO: 63).
Предпочтительный специфический модифицированный белок по изобретению представляет собой белок IMX313 (SEQ ID NO: 6), в котором пептид SPRRRRS (SEQ ID NO: 2) связан с суперспиральным доменом белка IMX313, а модифицированный белок слит с протеином А золотистого стафилококка Staphylococcus aureus.
Другим предпочтительным специфическим модифицированным белком по изобретению является белок IMX313 (SEQ ID NO: 6), в котором пептид SPRRRRS (SEQ ID NO: 2) связан с суперспиральным доменом белка IMX313, а модифицированный белок слит с белком 85А.
Как показано в примерах, эти два модельных антигена были использованы для того, чтобы продемонстрировать, что модификация суперспиралей повышает их иммуногенность. Как В-клеточный, так и Т-клеточный ответы были улучшены. Кроме того, модифицированные суперспирали были более иммуногенными при введении в форме либо белков, либо нуклеиновых кислот.
Изобретение также относится к иммуногенной композиции, содержащей модифицированный белок суперспирального типа, такой, как описано выше, или слитый белок, как описано выше, и лиганды внутриклеточных ТПР на основе нуклеиновых кислот. Эти лиганды ТПР на основе нуклеиновых кислот находятся преимущественно в комплексе с модифицированным белком-носителем. То, что лиганды на основе нуклеиновых кислот связаны с модифицированным белком, является преимуществом, хотя соответствующий немодифицированный белок-носитель не был способен существенно связывать лиганды ТПР на основе нуклеиновых кислот.
Изобретение также относится к иммуногенной композиции, содержащей модифицированный белок спирального типа, такой, как описано выше, или слитый белок, такой, как описано выше, и гепарин. Гепарин находится преимущественно в комплексе с модифицированным белком-носителем. То, что гепарин связан с модифицированным белком, является преимуществом, хотя соответствующий немодифицированный белок-носитель не был способен существенно связывать гепарин.
Изобретение также относится к твердой подложке, несущей модифицированный белок, причем, этот белок связывается с подложкой с помощью пептида ZXBBBBZ. Действительно, избыток зарядов в пептиде является достаточным для прочного связывания модифицированного белка с поверхностью.
Изобретение также относится к способу увеличения способности к связыванию с подложкой белка, содержащего спиральный домен, причем, этот способ включает связывание, по меньшей мере, одного пептида ZXBBBBZ с суперспиральным доменом, в котором:
- Z представляет собой любую аминокислоту, или отсутствует,
- X представляет собой любую аминокислоту;
- В представляет собой аргинин (R) или лизин (К).
В частности, подложка представляет собой хроматографическую колонку. Все модифицированные растворимые суперспиральные белки могут быть связаны с такими колонками с использованием положительно заряженного пептида в качестве аффинной метки. Исполнитель может изменить количество аргинина в пептиде с основной последовательностью ZXBBBBZ для того, чтобы усилить или уменьшить связывание. Кроме того, исполнитель может изменить число пептидов с общей последовательностью ZXBBBBZ для усиления связывания. Чем меньше количество белковых цепей в олигомере, тем больше количество остатков аргинина в пептиде или пептидов, которые должны быть использованы. Так, например, в тримерной суперспирали желательно использовать девять или более остатков аргинина в цепи для того, чтобы обеспечить аналогичную очистку на гепарин-сефарозе.
Изобретение также относится к способу повышения иммуногенности белка-носителя или антигена, который содержит суперспиральный домен, включающему связывание, по меньшей мере, одного пептида ZXBBBBZ суперспиральным доменом этого белка, где:
- Z представляет собой любую аминокислоту, или отсутствует,
- X представляет собой любую аминокислоту;
- В представляет собой аргинин (R) или лизин (К).
Изобретение также относится к способу увеличения иммуногенности антигена, включающему:
- получение модифицированного белка-носителя, например, как описано выше; и
- связывание антигена с этим модифицированным белком-носителем и лигандами внутриклеточных ТПР на основе нуклеиновых кислот или гепарином.
Изобретение, в частности, относится к способу увеличения Th1 иммуногенности антигена, характеризующемуся очень высоким отношением IgG2a к IgG1, таким, как то, что проиллюстрировано ниже, причем, этот способ включает:
- получение модифицированного белка-носителя, например, как описано выше; и
- связывание этого антигена с модифицированным белком-носителем и лигандами внутриклеточных ТПР на основе нуклеиновых кислот или гепарином.
Изобретение также относится к модифицированному антигену по настоящему изобретению или слитому белку по настоящему изобретению для применения в качестве вакцины.
Настоящее изобретение также относится к способу индукции иммунного ответа у нуждающегося в этом пациента, который включает введение пациенту вакцинной композиции, содержащей слитый белок, включающий модифицированный белок-носитель и антиген.
Настоящее изобретение также относится к способу индукции иммунного ответа у нуждающегося в этом пациента, включающему введение пациенту вакцинной композиции, содержащей иммуногенную композицию, включающую модифицированный белок и лиганды внутриклеточных ТПР на основе нуклеиновых кислот или гепарин.
Изобретение также относится к молекулам нуклеиновой кислоты, кодирующим модифицированные белки и слитые белки, такие как описанные выше.
Кроме того, настоящее изобретение относится к вакцинной композиции, содержащей, по меньшей мере, одну молекулу нуклеиновой кислоты, такую, как описанные выше. Вакцинные композиции, содержащие молекулы нуклеиновых кислот, хорошо известны специалистам в данной области техники, и, в частности, описаны в патентной заявке WO 2008/122817, включенной в настоящее изобретение путем ссылки.
Такие нуклеиновые кислоты могут быть использованы в чистом виде или могут быть введены в вирусные векторы, которые также описаны в патентной заявке WO 2008/122817. Некоторые вирусные векторы были модифицированы для получения нуклеиновых кислот, которые могут затем связываться с модифицированными антигенами, кодирующимися вирусными векторами. Модификация вирусных векторов для получения нуклеиновых кислот описана в патентной заявке WO 2007/100908, включенной в настоящее изобретение путем ссылки.
Настоящее изобретение также относится к способу очистки модифицированных белков суперспирального типа, таких как описанные выше, включающему следующие последовательные стадии:
- нанесение модифицированного белка на хроматографическую колонку с гепарин-сефарозой, и
- вымывание этого белка элюентом с концентрацией соли превосходящей 500 мМ.
Краткое описание графических материалов
Фигура 1. Хроматограмма белка IMX313T, очищенного на колонке Hi Trap heparin HP. Колонка с гепарин-сефарозой четко отделяет загрязняющие примеси (пики А и В) от практически чистого белка IMX313T (пик С). Пунктирная линия показывает градиент соли, используемый для элюирования модифицированного белка.
Фигура 2. Лиганды ТПР9 и белок IMX497 (PAm-IMX313T) - гель-электрофорез в агарозном геле (с концентрацией 0,8% в ТАЕ буфере). Положение в геле, до которого мигрировал олигонуклеотид, наблюдали в ультрафиолетовом свете, окрашивая гель бромистым этидием.
Фигура 3. Лиганды ТПР7 и ТПР3 и белок IMX497 (PAm-IMX313T) - гель-электрофорез в агарозном геле (с концентрацией 0,8% в ТАЕ буфере).
Фигура 4. Лиганды ТПР7 и белки IMX495 (PAm), IMX494 (PAm-IMX313) и IMX497 (PAm-IMX313T) - гель-электрофорез в агарозном геле (с концентрацией 0,8% в ТАЕ буфере).
Фигура 5. Группы самок мышей линии BALB/C (n=5) подкожно иммунизировали дважды с интервалом в четырнадцать дней антигенами PAm, PAm-IMX313, PAm-IMX313T или PAm, приготовленными сначала в полном адъюванте Фрейнда (CFA), а затем в неполном адъюванте Фрейнда (IFA). Двадцать восемь дней спустя после первой иммунизации определяли титры PAm-специфического иммуноглобулина IgG в сыворотке с использованием иммуносорбентного ферментного анализа (ELISA, от англ. enzyme-linked immunosorbent assay), при котором планшеты покрывали антигеном PAm. Результаты выражали в виде оптической плотности образцов, измеренной при длине волны 405 нм + СОС (стандартная ошибка среднего). Значимые различия между значениями разных групп определяли с помощью однофакторного дисперсионного анализа ANOVA с последующим сравнением при помощи критерия множественного сравнения Тьюки. Р-значение <0,05 считали статистически значимым, при этом Р-значение представляли при помощи различных знаков *, где знак *** представляет р<0,001, а знак ** представляет р<0,01.
Фигура 6. Уровни экспрессии интерферона γ (IFN-γ) в общей популяции Т-клеток. 85А-специфические клеточные иммунные ответы у внутримышечно иммунизированных мышей. Группы самок мышей линии BALB/C (n=5), иммунизировали дважды с интервалом в 14 дней плазмидами, экспрессирующими антигены: 85А, 85A-IR14, 85A-TL18, 85А-85А или IMX313-IMX313T. Через две недели после последней иммунизации мышей умерщвляли и выделяли Т-клетки селезенки. Клетки культивировали совместно с рекомбинантным белком 85А. Значимые различия между значениями разных групп определяли с помощью однофакторного дисперсионного анализа ANOVA с последующим сравнением при помощи критерия множественного сравнения Тьюки. Р-значение <0,05 считали статистически значимым. Ответы IFN-γ в супернатантах совместной культуры выражали как число клеток, секретирующих IFN-γ на миллион клеток.
Фигура 7. Уровни экспрессии интерферона IFN-γ в популяции CD8 + Т-клеток. 85А-специфические клеточные иммунные ответы у внутримышечно иммунизированных мышей. Группы самок мышей линии BALB/C (n=5), иммунизировали дважды с интервалом в 14 дней плазмидами, экспрессирующими антигены: 85А, 85A-IR14, 85A-TL18, 85А-85А или IMX313-IMX313T. Через две недели после последней иммунизации мышей умерщвляли и выделяли CD8 + T-клетки. Клетки культивировали совместно с пептидом р11 из антигена 85А. Значимые различия между значениями разных групп определяли с помощью однофакторного дисперсионного анализа ANOVA с последующим сравнением при помощи критерия множественного сравнения Тьюки. Р-значение <0,05 считали статистически значимым. Ответы IFN-γ в супернатантах совместной культуры выражали как число клеток, секретирующих IFN-γ на миллион клеток.
Фигура 8. Уровни экспрессии интерферона IFN-γ в популяции CD8 + Т-клеток. 85А-специфические клеточные иммунные ответы у внутримышечно иммунизированных мышей. Группы самок мышей линии BALB/C (n=5), иммунизировали дважды с интервалом в 14 дней плазмидами, экспрессирующими антигены: 85А, 85A-IR14, 85A-TL18, 85А-85А или IMX313-IMX313T. Через две недели после последней иммунизации мышей умерщвляли и выделяли CD8 + Т-клетки. Клетки культивировали совместно с пептидом р15 из антигена 85А. Значимые различия между значениями разных групп определяли с помощью однофакторного дисперсионного анализа ANOVA с последующим сравнением при помощи критерия множественного сравнения Тьюки. Р-значение <0,05 считали статистически значимым. Ответы IFN-γ в супернатантах совместной культуры выражали как число клеток, секретирующих IFN-γ на миллион клеток.
Фигура 9. Группы самок мышей линии BALB/C (n=5) иммунизировали внутримышечно дважды с интервалом 14 дней плазмидой 85A-IMX313, плазмидой 85A-IMX313T и более короткими последовательностями 85A-IR14 и 85A-TL18. Двадцать восемь дней спустя после первой иммунизации определяли титры 85А-специфического иммуноглобулина IgG в сыворотке с использованием 85А-специфического ELISA. Результаты выражали в виде оптической плотности образцов, измеренной при длине волны 405 нм + СОС (стандартная ошибка среднего). Существенные различия между значениями разных групп определяли с помощью однофакторного дисперсионного анализа ANOVA с последующим сравнением при помощи критерия множественного сравнения Тьюки. Р-значение <0,05 считали статистически значимым. NS означает «статистически незначимый»; статистически значимые уровни значений показаны при помощи «звездочек»: *** (р<0,001), ** (р<0,01), * (р<0,05).
Фигура 10. Карта исходной плазмиды pcDNA3 NP - данную плазмиду и ее производные, сконструированные, как описано в примерах, использовали для ДНК-вакцинации.
Фигура 11. Сравнение общих количеств Т-клеток, секретирующих IFN-γ в ответ на иммунизацию плазмидами, кодирующими нуклеопротеин NP, для нуклеопротеина NP, слитого с IMX313.
Фигура 12. Сравнение общих количеств CD8 и CD4 Т-клеток, секретирующих IFN-γ в ответ на иммунизацию, плазмидой, кодирующей NP или плазмидой, кодирующей NP слитый с IMX313.
Фигура 13. Сравнение ответов антител IgG на рекомбинантный NP индуцируемый плазмидной ДНК, кодирующей либо NP, либо NP, слитый с IMX313.
Фигура 14. Сравнение ответов антител подкласса IgG на рекомбинантный NP, индуцируемый плазмидной ДНК, кодирующей либо NP, либо NP, слитый с IMX313.
Фигура 15. Сравнение ответов общих количеств Т-клеток на плазмиды, кодирующие NP, мономерный NP (NP-M), мономерный NP, слитый с IMX313 (NP-M-IMX313) и мономерный NP, слитый с IMX313T (NP-M-IMX313T).
Фигура 16. Сравнение ответов CD8+ и CD4+ Т-клеток на плазмиды, кодирующие NP, мономерный NP (NP-M), мономерный NP, слитый с IMX313 (NP-M-IMX313) и мономерный NP, слитый с IMX313T (NP-M-IMX313T).
Фигура 17. Сравнение ответов антител IgG, измеренных методом ELISA с использованием рекомбинантного NP, на плазмиды, кодирующие NP, мономерный NP (NP-M), мономерный NP, слитый с IMX313 и мономерный NP, слитый с IMX313T.
Фигура 18. Сравнение ответов антитела подкласса IgG, измеренное с помощью рекомбинантного NP, на плазмиды, кодирующие NP, мономерный NP (NP-М), мономерный NP, слитый с IMX313 и мономерный NP, слитый с IMX313T.
Фигура 19. Влияние секреции различных слитых белков NP, опосредованной сигнальным пептидом tPA. Общее число Т-клеток измеряли при помощи анализа секреции гамма-интерферона посредством метода иммуноферментных пятен (IFNγ ELISpots), сравнивая NP, секретируемый NP (tPA-NP), секретируемый мономерный NP (tPA-NP-M), секретируемый NP, слитый с IMX313 (tPA-NP-IMX313), секретируемый мономерный NP, слитый с IMX313 и секретируемый мономерный NP, слитый с IMX313T (tPA-NP-M-IMX313T).
Фигура 20. Влияние секреции, опосредованной сигнальным пептидом tPA, на CD8+ и CD4+ ответы на различные слитые белки NP, измеренное при помощи сравнения методом IFNγ ELISpots: нуклеопротеин NP, секретируемый NP (tPA-NP), секретируемый мономерный NP (tPA-NP-M), секретируемый NP, слитый с IMX313 ((tPA-NP-IMX313), секретируемый мономерный NP, слитый с IMX313 и секретируемый мономерный NP, слитый с IMX313T (tPA-NP-M-IMX313T).
Фигура 21. Влияние секреции, опосредованной сигнальным пептидом tPA, на ответы иммуноглобулина IgG на различные слитые белки NP, измеренное при помощи сравнения методом ELISA: нуклеопротеин NP, секретируемый NP (tPA-NP), секретируемый мономерный NP (tPA-NP-M), секретируемый NP, слитый с IMX313 ((tPA-NP-IMX313), секретируемый мономерный NP, слитый с IMX313 и секретируемый мономерный NP, слитый с IMX313T (tPA-NP-M-IMX313T).
Фигура 22. Влияние секреции, опосредованной сигнальным пептидом tPA, на ответы иммуноглобулина подкласса IgG на различные слитые белки NP, измеренное при помощи сравнения методом ELISA: на нуклеопротеин NP, секретируемый NP (tPA-NP), секретируемый мономерный NP (tPA-NP-M), секретируемый NP, слитый с IMX313 ((tPA-NP-IMX313), секретируемый мономерный NP, слитый с IMX313 и секретируемый мономерный NP, слитый с IMX313T (tPA-NP-M-IMX313T).
Фигура 23. Фигура показывает, что белок IMX743 прочно связывает ДНК олигонуклеотид ODN1826, тогда как IMX744 слабо связывает тот же олигонуклеотид. Электрофорез в агарозном геле проводили в 0,8% ТАЕ буфере. Положение в геле, к которому олигонуклеотид мигрировал, наблюдали в ультрафиолетовом свете, окрашивая гель бромистым этидием. Различные комбинации ТПР9 лиганда ODN1826 с белками IMX744 и IMX743 получали, как описано в приведенной над гелем Таблице, образование комплексов анализировали с помощью электрофореза в агарозном геле. Образование комплексов четко обнаруживалось, поскольку комплексы мигрировали гораздо медленнее, чем не участвующие в комплексах лиганды. Поскольку концентрация белка была снижена, наблюдаемые комплексы стали лучше диффундировать, и полоса несвязанного лиганда ТПР стал видимой. На геле видно, что сдвиг в геле является воспроизводимым для IMX743 (сравнивая полосы 6 и 12), однако белок IMX744 (полосы 3-5) дает такой сдвиг, который почти незаметен в геле.
ПРИМЕРЫ
1. Получение белков IMX313, IMX313T и IMX313P
IMX313 получали путем клонирования домена олигомеризации в экспрессионный вектор на основе Т7 стандартными способами. ПЦР-продукт содержал сайт NdeI на N-конце и сайт HindIII, перекрывающий второй стоп-кодон. Нуклеотидная последовательность была следующей:
SEQ ID NO: 8:
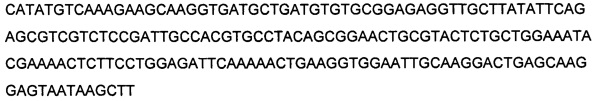
Этот ген кодирует следующую белковую последовательность (SEQ ID NO: 9): 
Звездочки означают стоп-кодоны. Серин во втором положении дает возможность полного удаления инициирующего метионина, что определяется при помощи масс-спектрометрии.
IMX313 экспрессировали в штамме C43(DE3) кишечной палочки Escherichia coli. Трансформированные клетки выращивали в среде Terrific Broth при 37°С до оптической плотности OD600, равной примерно 0,6, затем индуцировали экспрессию изопропил-β-D-1-тиогалактопиранозидом (ИПТГ) в концентрации 1 мМ, и культуры выращивали в течение ночи при 37°С. Выращенные бактерии подвергали лизису путем обработки ультразвуком в буфере, содержащем 50 мМ фосфата натрия, pH 7,4, и центрифугировали при 18000 оборотах в минуту в течение 30 минут при 4°С. Белок IMX313 обнаруживали в растворимой фракции.
IMX313T получали путем замены последних пяти С-концевых аминокислот (GLSKE) белка IMX313 на положительно заряженный пептид (SPRRRRS) следующим образом: непосредственно перед аминокислотами, которые должны быть заменены (GLSKE), создавали сайт рестрикции PstI (CTGCAG: кодирующий аминокислоты лейцин и глутамин) путем сайт-направленного мутагенеза. Это позволяет провести замену последних пяти аминокислот IMX313 на любые аминокислоты, кодируемые двумя комплементарными олигонуклеотидами, которые могут быть подвергнуты отжигу и лигированы в сайт PstI и сайт Hind III непосредственно ниже стоп-кодона.
В следующих фосфорилированных олигонуклеотидах заменяли последовательность, кодирующую LQGLSKE** (SEQ ID NO: 10), на последовательность LQSPRRRRS** (SEQ ID NO: 11, где знак * означает стоп-кодон), в процессе отжига и клонирования ее между сайтами PstI и HindIII:
SEQ ID NO 12: 5' GTCTCCGCGTCGCCGTCGCTCCTAATA 3' и
SEQ ID NO: 13: 5' AGCTTATTAGGAGCGACGGCGACGCGGAGACTGCA 3'.
Нуклеотидная последовательность, кодирующая IMX313T, является следующей (SEQ ID NO: 14):

IMX313T экспрессировали также в штамме C43(DE3) кишечной палочки Escherichia coli. Трансформированные клетки выращивали в среде Terrific Broth при 37°С до оптической плотности OD600, равной примерно 0,6, затем индуцировали экспрессию путем добавления ИПТГ до 1 мМ и культуру выращивали в течение ночи при 37°С. Бактерии лизировали путем обработки ультразвуком в буфере, содержащем 50 мМ фосфата натрия, pH 7,4, и центрифугировали при 18000 оборотах в минуту в течение 30 минут при 4°С. Белок IMX313T также обнаруживали в растворимой фракции.
IMX313P сконструировали путем мутации плазмиды, экспрессирующей IMX313T, с помощью олигонуклеотидов:
 (SEQ ID NO: 43) и
(SEQ ID NO: 43) и
 (SEQ ID NO: 44).
(SEQ ID NO: 44).
ПЦР-продукт встраивали по методу Geiser (29) в вектор Т7, экспрессирующий белок IMX313T.
Нуклеотидная последовательность, кодирующая IMX313P, была следующей (SEQ ID NO: 45):

Белок IMX313P выделяли и получали таким же образом, как и белок IMX313T, за исключением того, что буфер для лизиса содержал 1М NaCl. Очищенный бактериальный лизат нагревали при 80°С в течение 20 минут и снова очищали центрифугированием при 18000 оборотов в минуту в течение 30 минут при 4°С.
2. IMX313P и IMX313T также, как и IMX313, являются гептамерными
Белок IMX313T выделяли на колонке Hi Trap SP FF объемом 5 мл, уравновешенной 50 мМ фосфата натрия, pH 7,4. Белок элюировали в градиенте от 0 до 1 М NaCl. Фракции, содержащие белок IMX313T, объединяли, подвергали диализу против 1 × натрий-фосфатного буфера (НФБ) и наносили на колонку Hi Load 26/60 Superdex с чувствительностью 75 пг, уравновешенную 1×НФБ. Элюирующий объем для IMX313T (Ve 170 мл) был очень близок к элюирующему объему IMX313 (Ve 162 мл).
Белок IMX313P выделяли на колонке с гепарин-сефарозой. Перед нанесением на колонку белок сначала подвергали диализу против раствора Трис-HCl с pH 8,0 и 150 мМ NaCl. Затем колонку обрабатывали Трис-HCl с pH 8,0 и 2М NaCl. Элюированные фракции белка IMX313P объединяли, подвергали диализу против НФБ, содержащего 500 мМ NaCl, и наносили на колонку Hi 26/60 Superdex, чувствительностью 75 пг, уравновешенную 1×НФБ, содержащего 500 мМ NaCl. Элюирующий объем был неотличим от такового для IMX313T.
Чтобы продемонстрировать образование гептамера на ПААГ-электрофорезе, очищенные белки IMX313T и IMX313P анализировали в нативных, денатурирующих и восстанавливающих условиях. В отсутствие восстанавливающего агента IMX313T and IMX313P были олигомеризованы так же, как и IMX313, и все мигрировали с гораздо более высокой молекулярной массой, чем их мономеры.
3. Слияние короткого положительно заряженного пептида с белком IMX313 облегчает очистку белков
Затем белок IMX313T, очищенный, как описано выше, наносили на колонку HiTrap Heparin HP объемом 5 мл в буфере, состоящем из 10 мМ трис-HCl и 150 мМ NaCl, pH 7,5. Элюирование связанных белков проводили градиентом соли: 15-ю объемами колонки 2М раствора NaCl в том же буфере. Положительно заряженный белок IMX313T связывали с гепарином колонки и элюировали примерно 1М NaCl. В отдельном анализе на колонке было показано, что IMX313 не связывается с гепарин-сефарозой колонки, но вместо этого обнаруживается в потоке через фракцию.
Колонка с гепарин-сефарозой представляет собой колонку для аффинной хроматографии. Она широко применяется для очистки белков сыворотки, включая факторы свертывания крови, липазы, липопротеины и гормональные рецепторы, а также была успешно использована для очистки факторов роста. Полианионная структура гепарина, который служит в качестве аналога ДНК и РНК, позволила провести очистку многих видов белков, которые взаимодействуют с ДНК или РНК, включая полимеразы, киназы и рибосомные белки.
В настоящем изобретении авторы показали, что модификация суперспирали путем слияния с ней положительно заряженного пептида (например, концевого участка полиаргинина), придает ей полезное свойство связываться с отрицательно заряженной гепарин-сефарозой на колонке, что значительно упрощает очистку.
Это оказалось неожиданным, поскольку, когда Stempfer и др. (19, 20) использовали шесть остатков аргинина, слитые с ферментом с целью иммобилизации этого фермента на гепарин-сефарозе, фермент мог быть элюирован из колонки только 0.35М NaCl. При этой концентрации соли другие белки в клеточных экстрактах также элюируются, как показано в Примере 4, и существует значительное преимущество, состоящее в возможности элюирования подавляющего большинства белков, которые связываются с колонкой, имеющей концентрацию соли, например, менее чем 500 мМ NaCl, а кроме того, в элюировании модифицированного суперспирального слитого белка практически в чистом виде с использованием еще более высокой концентрации соли. Это позволяет провести очистку путем ступенчатого градиента или на установке периодического действия. Таким образом, колонки с гепарин-сефарозой могут быть использованы в качестве аффинных колонок для белков, слитых с IMX313T и других суперспиралей, модифицированных по способу, описанному в настоящем изобретении.
По сравнению с катионообменными колонками, такими как Hi Trap SP FF, колонки с гепарин-сефарозой более пригодны, поскольку они являются более специфичными для модифицированных суперспиралей. В настоящем исследовании, белок IMX313T, который элюировали с катионообменной колонки (Hi Trap SP FF; pH 7,4), не был полностью чистым. Когда этот очищенный на SP FF и S75 белок наносили на колонку с гепарин-сефарозой (HiTrap Heparin HP), следы загрязняющих веществ удалялись с потоком через нее, и белок IMX313T элюировали с чистотой >98%, показывающей, что колонка с гепарином более специфична, чем SP FF, для суперспирали, модифицированной добавлением пептида SPRRRRS, хотя белок элюировали из обеих колонок с помощью аналогичных концентраций NaCl.
4. Колонка с гепарин-сефарозой действует как аффинная колонка для модифицированных суперспиралей
IMX313 получали, как описано в Примере 1. Растворимую фракцию, получали после обработки ультразвуком лизата бактерий в буфере, содержащем 10 мМ Трис-HCl, 150 мМ NaCl, pH 7,5, и центрифугировали при 18000 оборотах в минуту в течение 30 минут при 4°С в роторе SS34 центрифуги Sorvall.
Супернатант, содержащий слитый белок, наносили на колонку Hi Trap heparin HP, уравновешенную 10 мМ Трис-HCl и 150 мМ NaCl, pH 7,5. Элюирование проводили градиентом соли: 2М NaCl в том же буфере. Почти все загрязняющие вещества были удалены в потоке через колонку или с использованием низкой концентрации соли; и после этого белок IMX313T элюировали примерно 1М NaCl с очень высокой степенью чистоты (примерно 95%) за одну хроматографическую стадию. Дальнейшая очистка с помощью гель-фильтрации давала, по существу, чистый белок. Результаты представлены на Фигуре 1.
5. Другие короткие положительно заряженные пептиды, слитые с IMX313
Три другие модификации IMX313T получали для того, чтобы сравнить различные линкеры (глицин по сравнению с серином и пролином) или для сравнения аргинина и лизина. Плазмиду, экспрессирующую IMX313T, подвергали мутации путем амплификации с олигонуклеотидами:
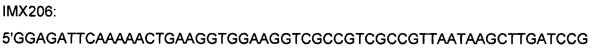
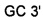 (SEQ ID NO: 46) или
(SEQ ID NO: 46) или
 (SEQ ID NO: 47) или
(SEQ ID NO: 47) или
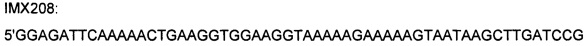
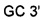 (SEQ ID NO: 48) и
(SEQ ID NO: 48) и
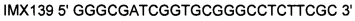 (SEQ ID NO: 49),
(SEQ ID NO: 49),
и ПЦР-продукт встраивали по методу Geiser (29) в экспрессионный вектор Т7 белка IMX313T.
Полученные плазмиды, называемые pIMX427, pIMX428 и pIMX429, кодируют белки:
IMX427:
 (SEQ ID NO: 50)
(SEQ ID NO: 50)
IMX428:
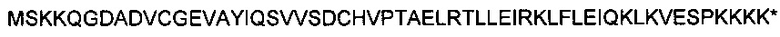 (SEQ ID NO: 51)
(SEQ ID NO: 51)
IMX429:
 (SEQ ID NO: 52)
(SEQ ID NO: 52)
Их очищали так же, как IMX313P, а затем исследовали их поведение в сравнении с IMX313T и IMX313P на колонке объемом 5 мл с гепарин-сефарозой.


Условия были следующими: загрузочный буфер 20 мМ Трис, pH 7,5, 150 мМ NaCl. Затем проводили градиентное элюирование с использованием второго буфера. Второй буфер содержал 20 мМ Трис, pH 7,5 и 2М NaCl.
Эти результаты можно сравнить с экспериментами Fromm и коллег (47), которые показали, что пептид из семи остатков аргинина элюируется с гепарин-сефарозы при концентрации NaCl от 820 мМ, а пептид из семи остатков лизина элюируется при концентрации NaCl, равной 640 мМ. Очевидно, что слияние положительно заряженных пептидов с суперспиралью улучшает их связывание с гепарином.
6. Получение и очистка антигена PAm и слитых белков PAm-IMX313 и PAm-IMX313T
Для получения антигена PAm, слитого с IMX313, протеин А из открытой рамки считывания золотистого стафилококка Staphylococcus aureus амплифицировали из плазмиды pEZZ18 (Amersham Pharmacia) с использованием олигонуклеотидов:
SEQ ID NO: 15 - IMX1078: 5'
CTTTAAGAAGGAGATATACATATGgctgatgcgcaacaaaataac 3' и
SEQ ID NO: 16 - IMX1079: 5' CCGCACACatcagcatcaccttgcttttttggtgcttgagcatcatttagc 3'
и ПЦР-продукт длиной ~233bp пар оснований встраивали с помощью метода Geiser (29) в экспрессионный вектор Т7 белка IMX313. Затем протеин А из рамки считывания подвергали мутации с использованием олигонуклеотидов:
SEQ ID NO: 17 - IMX1080: 5' cttcaacaaagaAAaaAaGaAcgccttctatg 3' и
SEQ ID NO: 18 - IMX1081: 5' gcgctttggcttggagccgcttttaagctttgg 3'
для того, чтобы ввести в него мутации, описанные Kim и др. (27), создав экспрессионный вектор pIMX494, который имеет следующую кассету экспрессии (SEQ ID NO: 19):

Он кодирует следующий белок:
(SEQ ID NO: 20):

Следует отметить, что для облегчения интерпретации плановой иммунизации в этой версии IMX313 не хватает последних пяти аминокислот (GLSKE), обнаруживаемых в версии с пятьюдесятью пятью аминокислотами. Слитый белок IMX494 (PAm-IMX313) экспрессировали в штамме C43(DE3) с индукцией при помощи ИПТГ. Клеточный дебрис лизировали ультразвуком в 20 мМ Трис-HCl, pH 7, и центрифугировали при 18000 оборотах в минуту в течение пятнадцати минут при 4°С. Слитый белок обнаруживали в дебрисе, который затем обрабатывали ультразвуком в буфере, содержащем 50 мМ Трис-HCl, 3М мочевины, pH 7,4, и снова центрифугировали при 18000 оборотах в минуту. На этот раз слитый белок был в супернатанте, который наносили на колонку Hi Trap Q FF объемом 5 мл и хроматографировали эту колонку градиентом 1М NaCl.
Фракции, содержащие белок IMX494, собирали, диализовали против НФБ и дополнительно очищали гель-фильтрацией на колонке Hi Load 26/60 Superdex 75.
Для получения антигена PAm неслитого с белком-носителем последовательность, кодирующую IMX313, удаляли из вектора pIMX494 с использованием олигонуклеотидов:
SEQ ID NO: 21 - IMX1279 5' gcagccggatcaagcttattattttggtgcttgagcatc 3' и
SEQ ID NO: 22 - T7 (прямой): 5' TAATACGACTCACTATAGGG 3'.
ПЦР-продукт встраивали (27) в исходный вектор, получая плазмиду pIMX495.
500 мл культуры pIMX495 в штамме C43(DE3) индуцировали с помощью 1 мМ ИПТГ и выращивали в течение ночи. Выращенные бактерии подвергали лизису путем обработки ультразвуком в буфере: 50 мМ фосфата натрия, pH 7,4, и центрифугировали при 18000 оборотах в минуту в течение 15 минут при 4°С в роторе SS34 центрифуги Sorvall. Белок IMX495 (PAm без его N-концевого метионина) обнаруживали в супернатанте, и очищали путем нагревания в супернатанте при 76°С в течение пятнадцати минут с последующим вторым центрифугированием при 18000 оборотах в минуту в течение 15 минут. Снова обнаруживали IMX495 в супернатанте, который подвергали диализу против 50 мМ буферного раствора 2-(N-морфолино)этансульфоновой кислоты (MES), pH 6. Супернатант наносили на колонку Hi Trap SP FF объемом 5 мл и элюировали градиентом NaCl. И наконец, белок IMX495 подвергали тонкой очистке путем гель-фильтрации в НФБ на колонке PBS on a Hi prep 26/60 sephacryl S-100 HR.
Для получения вектора pIMX497, кодирующего слитый белок PAm-IMX313T, модифицировали вектор pIMX494 путем синонимичной мутации последовательности, кодирующей две последние аминокислоты лейцин и глутамин, из TTGCAA в CTGCAG, а затем путем клонирования перекрывающих второй стоп-кодон между вновь созданным сайтом Pst I и сайтом Hind III олигонуклеотидов:
SEQ ID NO: 23 - 5' GTCTCCGCGTCGCCGTCGCTCCTAATA 3' и
SEQ ID NO: 24 - 5' AGCTTATTAGGAGCGACGGCGACGCGGAGACTGCA 3'
изменяя С-конец IMX313 с последовательности LQ** на последовательность LQSPRRRRS** (SEQ ID NO: 11).
Кодируемый белок IMX497 экспрессировали в штамме С43 (DE3) и очищали путем лизиса бактериального дебриса в 50 мМ фосфата натрия, pH 7,4, и центрифугировали при 18000 оборотах в минуту. Слитый белок обнаруживали в дебрисе и ресуспендировали путем обработки ультразвуком в 50 мМ фосфата натрия, 8М мочевины, pH 7,4. После дальнейшего центрифугирования супернатант подвергали диализу против 50 мМ фосфата натрия, pH 7,4 и диализат центрифугировали. Супернатант нагревали до 75°С в течение пятнадцати минут, а затем снова центрифугировали. Супернатант очищали на колонке Hi Trap SP FF, хроматографированной градиентом NaCl до 2М, и фракции, содержащие слитый белок IMX497, объединяли, подвергали диализу против НФБ и тонкой фильтрации с помощью гель-фильтрации на колонке Hi Load 26/60 superdex 75.
7. Связывание внутриклеточных лигандов ТПР
Чтобы определить, могут ли эти белки связывать внутриклеточные лиганды ТПР, проводили анализ сдвига электрофоретической подвижности (EMSA, от англ. Electrophoretic Mobility Shift Assay).
Приготавливали различные комбинации внутриклеточных лигандов ТПР и белка IMX497 (PAm-IMX313T) и анализировали образование комплекса с помощью электрофореза в агарозном геле.
Лиганды ТПР были следующими:
- Для ТПР3: Poly(I:C), представляющий собой дуплекс полинуклеотида полиинозиновой кислоты, гибридизованный с полицитидиловой кислотой, аналог двухцепочечной РНК. Длина цепи была равна двадцать нуклеотидов для каждой нити.
- Для ТПР7: олигонуклеотид, называемый ssRNA40, с последовательностью
5'GsCsCsCsGsUsCsUsGsUsUsGsUsGsUsGsAsCsUsC 3', где «s» представляет собой фосфотиоатную связь (SEQ ID NO: 25);
- Для ТПР9: олигонуклеотид, называемый ODN1826 с последовательностью: 5' tccatgacgttcctgacgtt 3' (SEQ ID NO: 26).
Для лигандов ТПР9, результаты представлены на Фигуре 2. Слева направо:
Полоса 1: Маркер длин фрагментов с низкой молекулярной массой (NEB);
Полоса 2: Белок IMX497 (1 мг/мл);
Полоса 3: FITC CpG ODN (Eurogentec) 10 мкМ;
Полоса 4: Белок IMX497 (1 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 5: Белок IMX497 (0,5 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 6: Белок IMX497 (0,25 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 7: Белок IMX497 (0,125 мг/мл) и FITC CpG ODN 10 мкМ.
Образование комплекса было четко обнаруживаемо, так как комплексы мигрировали гораздо медленнее, чем не участвующий в комплексах лиганд, таким образом, возникал «сдвиг» лиганда в геле. Поскольку концентрация белка снижалась, наблюдаемые комплексы становились более способными к диффузии, и полоса несвязанного лиганда ТПР становилась видимой (они мигрировали на такое же расстояние, что и образец, содержащий только лиганд ТПР, используемый в качестве контроля).
Комбинации белка IMX497 с лигандами ТПР7 и ТПР3 показаны на Фигуре 3; эти нуклеиновые кислоты также образовывали комплексы, которые были легко обнаруживаемы при помощи EMSA.
Пояснение к Фигуре 3 (лиганды ТПР7 или лиганды ТПР3 + IMX497):
Полоса 1: Маркер длин фрагментов с низкой молекулярной массой (NEB);
Полоса 2: Белок IMX497 (1 мг/мл);
Полоса 3: FITC ssRNA (Eurogentec) 10 мкМ;
Полоса 4: Белок IMX497 (1,5 мг/мл) / FITC ssRNA 10 мкМ;
Полоса 5: Белок IMX497 (1 мг/мл) / FITC ssRNA 10 мкМ;
Полоса 6: Белок IMX497 (0,5 мг/мл) / FITC ssRNA 10 мкМ;
Полоса 7: Белок IMX497 (0,25 мг/мл) / FITC ssRNA 10 мкМ;
Полоса 8: Белок IMX497 (0,125 мг/мл) / FITC ssRNA 10 мкМ;
Полоса 9: FITC ssRNA 10 мкМ;
Полоса 10: Отрицательный контроль;
Полоса 11: Poly(I:C) (R&D Tocris Bioscience) 0,5 мг/мл;
Полоса 12: Белок IMX497 (1,5 мг/мл) / Poly(I:C), 0,5 мг/мл;
Полоса 13: Белок IMX497 (1 мг/мл) / Poly(I:C), 0,5 мг/мл;
Полоса 14: Белок IMX497 (1 мг/мл) / Poly(I:C), 0,25 мг/мл;
Полоса 15: Белок IMX497 (0,5 мг/мл) / Poly(I:C), 0,5 мг/мл;
Полоса 16: Белок IMX497 (0,5 мг/мл) / Poly(I:C), 0,25 мг/мл
Полоса 17: Белок IMX497 (0,25 мг/мл) / Poly(I:C), 0,5 мг/мл
Авторы также рассмотрели, могут ли IMX494 (PAm-IMX313) и IMX495 (PAm) производить такой же «сдвиг» в геле с олигонуклеотидом CpG (лиганды ТПР9). Результаты показаны на Фигуре 4.
Пояснение к Фигуре 4:
Полоса 1: Маркер длин фрагментов с низкой молекулярной массой (NEB);
Полоса 2: Белок IMX497 (1 мг/мл);
Полоса 3: Белок IMX494 (1 мг/мл)
Полоса 4: Белок IMX495 (1 мг/мл)
Полоса 5: FITC CpG ODN (Eurogentec) 10 мкМ;
Полоса 6: Белок IMX497 (1,5 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 7: Белок IMX497 (1 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 8: Белок IMX497 (0,5 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 9: Белок IMX497 (0,25 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 10: Белок IMX494 (1 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 11: Белок IMX494 (0,5 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 12: Белок IMX494 (0,25 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 13: Белок IMX495 (1 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 14: Белок IMX495 (0,5 мг/мл) и FITC CpG ODN 10 мкМ;
Полоса 15: Белок IMX495 (0,25 мг/мл) и FITC CpG ODN 10 мкМ
Гель на Фигуре 4 показывает, что сдвиг в геле является воспроизводимым для белка IMX497, но белок IMX495 (полосы 13-15) не производит в геле никакого обнаруживаемого сдвига и сдвиги в геле, наблюдаемые для белка IMX494 (полосы 10-12), являются трудно обнаруживаемыми и гораздо менее заметными, чем сдвиги для белка IMX497.
Разница между IMX494 и IMX497 обусловлена наличием последовательности SPRRRRS, присутствующей в белке IMX497 и слитой с С-концом суперспирали этого белка.
Вывод: в отсутствие этого пептида слитый белок IMX313 и антиген PAm не могут связывать лиганды ТПР на основе нуклеиновых кислот.
8. Иммуногенность антигенов, связанных с IMX313T
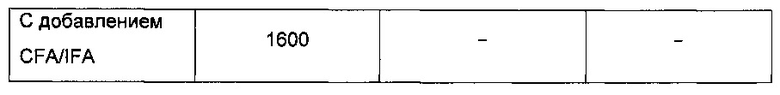
Затем проводили иммунизацию мышей для того, чтобы определить иммуногенность PAm, в индивидуальном виде или слитого с IMX313 или IMX313T, и находящегося или не находящегося в одном препарате с внутриклеточными лигандами ТПР. PAm, приготовленный в одном препарате с полным или неполным адъювантом Фрейнда (CFA/IFA) использовали в качестве контроля.
С этой целью самок мышей линии BALB/C (n=5) подкожно иммунизировали дважды с интервалом в четырнадцать дней, используя 2 наномоля на инъекцию каждого из белков PAm, PAm-IMX313, PAm-IMX313T или PAm, приготовленных сначала в CFA, а затем в IFA. Двадцать восемь дней спустя после первой иммунизации определяли титры PAm-специфического иммуноглобулина IgG в сыворотке с использованием ELISA, при котором планшеты покрывали антигеном PAm. Результаты выражали в виде оптической плотности (ОП) образцов, измеренной при длине волны 405 нм + СОС (стандартная ошибка среднего). Значимые различия между значениями разных групп определяли с помощью однофакторного дисперсионного анализа ANOVA с последующим сравнением при помощи критерия множественного сравнения Тьюки. Р-значение <0,05 считали статистически значимым, при этом Р-значение представляли при помощи различных знаков *, где знак *** представляет р<0,001, а знак ** представляет р<0,01.
Результаты показаны на Фигуре 5. Мыши, иммунизированные одним лишь PAm не имели антител IgG против PAm или имели очень низкие их уровни в сыворотке. В противоположность им, мыши, иммунизированные PAm-IMX313 или PAm-IMX313T, показывали высокие уровни системных ответов посредством PAm-специфических антител IgG; однако, мыши, иммунизированные PAm-IMX313T имели значительно более высокие ответы посредством антител IgG (р<0,001) по сравнению с ответами мышей, иммунизированных PAm-IMX313; ответы, аналогичные ответам на PAm-IMX313T были получены на PAm + CFA/IFA в качестве адъювантов.
Это показывает, что добавление пептида SPRRRRS придает антигену существенно повышенную иммуногенность по сравнению с исходной последовательностью IMX313.
Если антиген PAm была приготовлен с внутриклеточными лигандами ТПР (либо с одноцепочечной ДНК или РНК, либо с двухцепочечной РНК), его иммуногенность была существенно повышенной, и подобные усовершенствования наблюдались, когда антиген был слит с IMX313 до приготовления препарата. Тем не менее, очевидно, что лучшие результаты были наблюдаемы, когда антиген был слит с IMX313T до приготовления его в препарате с лигандами ТПР.
Результаты приведены в Таблице 1 и показаны в виде диаграммы ниже.
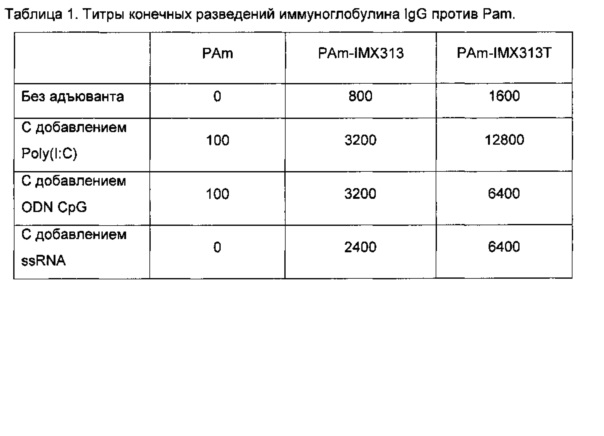
Возникает интересный вопрос, изменяют ли эти улучшения типы иммунных ответов, полученные против антигена, в данном случае PAm. Являются ли Th1 или Th2 ответы избирательно повышенными? Чтобы ответить на этот вопрос, авторы сравнивали ответы иммуноглобулина IgG1 с ответами иммуноглобулина IgG2a, поскольку титры IgG1 представляют ответы Th2 типа, тогда как IgG2a представляют ответы Th1 типа. Результаты представлены в Таблице 2.
Очевидно, что PAm сам по себе индуцирует почти равные Th1 и Th2 ответы, однако его композиции с полным адъювантом Фрейнда резко изменяют это в сторону преобладания Th2 ответа (IgG1). Слияние PAm с IMX313 показывает, что как ответ Th1, так и ответ Th2 усиливаются, и значительное изменение в типе ответа отсутствует. При использовании IMX313T начинает преобладать Th1 ответ (IgG2a), но эффект гораздо менее заметен, чем с адъювантом Фрейнда и ориентирован в обратном направлении. Консенсус среди иммунологов сводится к тому, что Th1 ответы предпочтительнее Th2 ответов.
Затем, проводя этот анализ, авторы исследовали может ли препарат с внутриклеточными лигандами ТПР быть использован для того, чтобы перенаправить иммунную систему на производство либо Th1 ответа, либо Th2 ответа. Данные об антителе изотипа IgG использовали для оценки типа Th-ответа с преобладанием IgG2a или IgG1 антител, указывающих на Th1-подобный или Th2-подобный ответ, соответственно. Th1-подобные ответы имели очень высокие соотношения IgG2a/IgG1, так что среднее значение по группе также было высоким. Отношение IgG2a/IgG1 использовали в качестве индикатора того, является ли ответ преимущественно Th1 ответом (IgG2a>IgG1), преимущественно Th2 ответом (IgG1>IgG2a), или смешанным Th1/Th2 ответом (Th0, IgG1,=IgG2a).
Результаты показаны в Таблице 2 ниже.
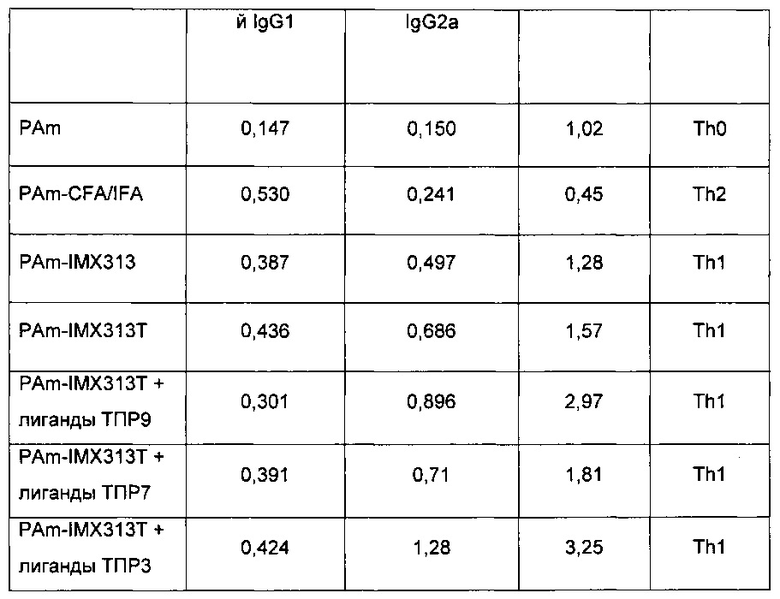
Сразу становится понятно, что препарат PAm-IMX313T с лигандами ТПР увеличивает тенденцию к преобладанию Th1 ответа с каждым из трех лигандов; эффект наиболее выражен с лигандом ТПР3 Poly(I:C) и почти так же выражен с лигандом ТПР9.
9. Т-клеточные ответы
Чтобы определить, может ли модификация суперспирали IMX313 с положительно заряженным пептидом также улучшать Т-клеточные ответы, использовали микобактериальный антиген 85А в качестве модели, поскольку было показано, что IMX313 улучшает ответы Т-клеток на этот антиген у мышей и обезьян (28). Получали серию рекомбинантных плазмид, экспрессирующих антиген 85А индивидуально, или слитым с IMX313T, или слитым с двумя усеченными версиями IMX313, содержащими только четырнадцать или восемнадцать аминокислот, при помощи первого субклонирования кодирующей последовательности 85A-IMX313 из вектора pSG2-85A-IMX313, описанного Спенсер и др. (28), в плазмиду pENTR4-LP по технологии Gateway. Были сделаны производные по главной цепи плазмиды pENTR4 для того, чтобы или удалить, или модифицировать IMX313.
Аминокислотные последовательности вариантов IMX313 приведены ниже:
 (SEQ ID NO: 27)
(SEQ ID NO: 27)
 (SEQ ID NO: 28)
(SEQ ID NO: 28)
 (SEQ ID NO: 6)
(SEQ ID NO: 6)
 (SEQ ID NO: 7).
(SEQ ID NO: 7).
В 14-мерный и 18-мернйе фрагменты IMX313 выбирали потому, что они остаются гептамерными при 37°С, (и даже 42°С) и, таким образом, должны образовывать гептамерные слитые белки при экспрессии после ДНК вакцинации. Модификации IMX313 проводились следующим образом:
Прямые праймеры IMX043 и IMX044 и обратный праймер IMX045 применяли для амплификации фрагментов IMX313 и этот ПЦР-продукт использовали (29) для того, чтобы заменить IMX313 в исходной плазмиде.
IMX043: 5' gaagcccgacctgcaacgtggatccATACGAAAACTCTTCCTGGAGA 3' (SEQ ID NO: 29)
IMX044: 5' gaagcccgacctgcaacgtggatccACTCTGCTGGAAATACGA 3' (SEQ ID NO: 30)
IMX045: 5' agggccctctagatgcatgctcgagcggccgcttattaTTCCACCTTCAGTTTTTG 3' (SEQ ID NO: 31)
Последовательность, кодирующую IMX313, удаляли, используя праймеры IMX037 и IMX047 и исходную плазмиду в качестве матрицы; затем полученный ПЦР-продукт применяли (29) для того, чтобы заменить последовательность IMX313.
IMX037: 5' cagaatagaatgacacctactcag 3' (SEQ ID NO: 32)
IMX047: 5' GAAGCCCGACCTGCAACGTTAATAAgcggccgctcgagcatg 3' (SEQ ID NO: 33)
Для того, чтобы получить 85A-IMX313T, применяли следующие ниже олигонуклеотиды для амплификации IMX313T из плазмиды pIMX497; затем ПЦР-продукт встраивали (29) в исходную плазмиду:
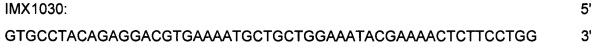
(SEQ ID NO: 34)
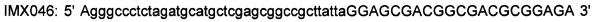 (SEQ ID NO: 35)
(SEQ ID NO: 35)
Эти пять плазмид (кодирующие 85А, 85A-IR14, 85A-TL18, 85А-85А и IMX313-IMX313T) затем применяли для ДНК иммунизации.
Пять групп мышей линии BALB/C иммунизировали внутримышечно каждой из пяти плазмид в дни 0 и 14, используя 25 мкг на инъекцию. Индукция антиген-специфических ответов Т-клеток была измерена при помощи ELISPOTs с использованием спленоцитов на 28-ой день. Выделенные из иммунизированных мышей очищенные CD4+, CD8+ Т-клетки и общее количество Т-клеток селезенки культивировали совместно либо с рекомбинантным белком 85А (Clinibiosciences), либо с пептидами р11 или р15 (26), полученными от компании Eurogentec.
Анализы ELISPOT: плоскодонные, нитроцеллюлозные 96-луночные планшеты (Millititer; Millipore) покрывали IFN-γ mAb (15 мкг/мл; Mabtech, Стокгольм) и инкубировали в течение ночи при 4°С. После промывки НФБ, планшеты блокировали добавлением 10% фетальной бычьей сыворотки в течение одного часа при 37°С. Клетки в концентрации 2×106 на лунку стимулировали соответствующими пептидами в конечной концентрации 2 мкг/мл (CD8 эпитоп р11, CD4 эпитоп р15 или белок 85А) на IPVH мембранах с покрытием антителами к человеческому IFN-γ в концентрации 15 мкг/мл и инкубировали в течение 20 ч. После инкубации планшеты тщательно промывали НФБ для удаления клеток и прибавляли IFN-γ mAb (с добавлением 1 мкг/мл биотина, МАВТЕСН) в каждую лунку. После инкубации в течение 2 ч при 37°С планшеты промывали и детектировали с помощью стрептавидина, конъюгированного с пероксидазой хрена (1 мкг/мл; МАВТЕСН) в течение одного часа при комнатной температуре. После промывки добавляли субстрат (3-амино-9-этилкарбазол (Sigma)) и инкубировали в течение 15 минут. После дополнительной промывки подсчитывали под микроскопом пятна красного цвета.
Выделенные из иммунизированных 85A-IMX313, 85A-IR14 или 85A-TL18 или 85A-IMX313T мышей очищенные CD4+, CD8+ Т-клетки и общее количество Т-клеток селезенки показали значительно более высокие IFNγ ответы, по сравнению с ответами аналогичных Т-клеток из мышей, иммунизированных 85а, что подтвердило способность IMX313 и других модифицированных последовательностей к усилению ответов Т-клеток. Кроме того, CD4+, CD8+ Т-клетки и общее количество Т-клеток селезенки селезенки из мышей, вакцинированных 85A-IMX313T, производили значительно больше IFNγ, чем Т-клетки из любых других иммунизированных групп (р<0,001) (Фигуры 6, 7, 8).
CD8+ Т-клетки демонстрировали иной цитокиновый профиль по сравнению с CD4+ Т-клетками; преобладающей наблюдаемой цитокин-продуцирующей популяцией были CD8+ Т-клетки, которые продуцировали IFN-γ (Фигуры 7 и 8).
Следует отметить, что ответы как CD4+, так и CD8+-антиген-специфических Т-клеток усиливается, когда IMX313 заменяют на IMX313T.
В заключение, Т-клеточные ответы на антиген 85А, которые улучшаются при помощи IMX313, дополнительно улучшаются за счет использования вместо него пептида IMX313T.
10. Ответы В-клеток, индуцированные ДНК-вакцинацией
Титры антител к антигену 85А измеряли с помощью ELISA в сыворотке мышей, иммунизированных ДНК-вакцинами (Фигура 9).
У мышей, иммунизированных плазмидой 85A-IMX313, плазмидой 85а-IMX313T и более короткими версиями IMX313 (IR14 и TL18, развиваются значительно более высокие титры общего антиген-специфического иммуноглобулина IgG (Фигура 9), чем у мышей, иммунизированных плазмидой, экспрессирующей 85А. Группа, иммунизированная 85A-IMX313T, показывала более высокие IgG ответы (р<0,001). Мыши, иммунизированные одним белком 85А, имели очень низкие уровни антител IgG против белка 85А в сыворотке.
При добавлении положительно заряженного короткого пептида SPRRRRS наблюдали также перенаправление иммунных ответов в сторону ответов Th1 типа, когда для вакцинации использовали ДНК. Содержание изотипов иммуноглобулина IgG, специфичных для белка 85а, измеряли с помощью ELISA (Таблица 3). У мышей линии BALB/C изотип IgG2a связан с Th1 типом иммунного ответа, а изотип IgG1 связан с Th2 типом иммунного ответа.
Следует отметить, что применение либо IMX313, либо IMX313T, привело к смещению ответов в направлении Т хелпера типа 1 (Th1), связанного с антиген-специфическими IgG, со значительно повышенными уровнями IgG2a и сниженными уровнями IgG1 по сравнению с одиночным антигеном 85А (Таблица 3), и эти результаты представляют собой прямое доказательство Th1-поляризации; причем, такие результаты согласуются с результатами, полученными для клеточных иммунных ответов.
Таблица 3. Группы самок мышей линии BALB/C (n=5) иммунизировали внутримышечно дважды с интервалом в 14 дней плазмидами, экспрессирующими 85A-IMX313, 85A-IMX313T, более короткими IMX313 последовательностями белков 85А-85А и IR14-TL18, и одним белком 85А. Двадцать восемь дней спустя после первой иммунизации определяли уровни 85А-специфических иммуноглобулинов IgG1 and IgG2a в сыворотке с помощью 85А-специфического ELISA. Результаты выражали в виде оптической плотности образцов, измеренной при длине волны 405 нм + СОС. Анализируя, как указано выше, те же самые данные для того, чтобы классифицировать данные изотипа, получили следующее:
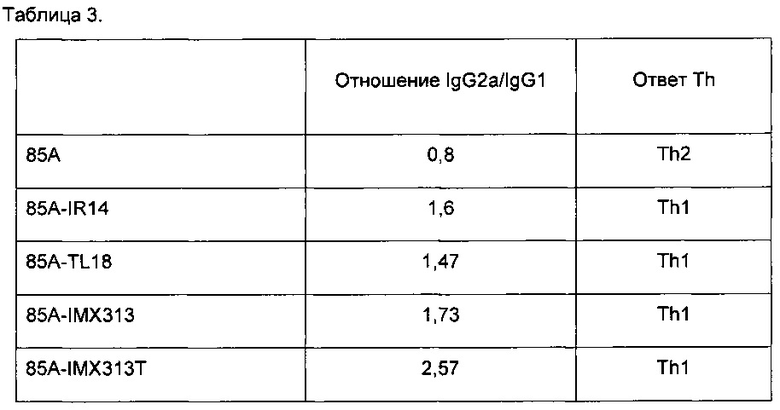
Очевидно, что все версии IMX313 имеют тенденцию к увеличению предпочтительно ответов Th1 типа, и этот эффект наиболее выражен у версии IMX313T, которая имеет короткий положительно заряженный пептид, слитый с суперспиралью.
11. Применение специфического слитого белка «IMX313T + нуклеопротеиновый (NP) антиген вируса гриппа»
Для ДНК-вакцинации исходная плазмида pcDNA3-NP, показанная на Фигуре 10, была изменена, как описано в примере ниже.
11.1. Вставка IMX313 в плазмиду, кодирующую нуклеопротеин NP
Последовательность, кодирующую IMX313, амплифицировали из плазмиды pIMX494, используя олигонуклеотидные праймеры IMX1289 5' caatgcagaggagtacgacaatggatccaagaagcaaggtgatgctgatg 3' (SEQ ID NO: 53) и IMX1290 5' GTAGAAACAAGGGTATTTTTCTTtattactccttgctcagtccttgc 3' (SEQ ID NO: 54), и встраивали в плазмиду pcDNA3-NP, как описано Geiser (29).
11.2. Вставка сигнального пептида tPA
Сигнальный пептид tPA амплифицировали из вектора pSG2-85A (28), используя олигонуклеотиды IMX1305 5' cactgagtgacatcaaaatcatgGATGCAATGAAGAGAGGGC 3' (SEQ ID NO: 55) и 5' IMX1306 cgtaagaccgtttggtgccttggctagctcttctgaatcgggcatggatttcc 3' (SEQ ID NO: 56), и встраивали его в рамку считывания со стороны N-конца последовательности, кодирующей NP, некоторых плазмид, как описано Geiser (29).
11.3. Создание двух точечных мутаций нуклеопротеина NP для того, чтобы сделать его мономерным
Для амплификации внутреннего фрагмента гена белка NP использовали олигонуклеотидные праймеры IMX1287 5' ccattctgccgcatttgCagatctaagag 3' (SEQ ID NO: 57) и IMX1288 5' CAAAAGGGAGATTTGCCTGTACTGAGAAC 3' (SEQ ID NO: 58), и полученный ПЦР-продукт встраивали в плазмиду, кодирующую NP, как описано Geiser. Поскольку оба олигонуклеотида недостаточно соответствовали гену белка NP, вставка продукта ПЦР образовала две точечных мутации. IMX1287 праймер создал мутацию Е339А (замена GAA на GCA), тогда как праймер IMX1288 создал мутацию R416A в гене NP (замена AGA на GCA).
11.4. Вставка IMX313T
Последовательность, кодирующую IMX313T, амплифицировали из плазмиды pIMX497, используя олигонуклеотидные праймеры IMX1289 (SEQ ID NO: 53) и IMX051 5' GTAGAAACAAGGGTATTTTTCTTtattaggagcgacggcgacgc 3' (SEQ ID NO: 59) и встраивали в различные плазмиды, полученные из плазмиды pcDNA3-NP так, как описано у Geiser.
11.5. ДНК-иммунизация нуклеиновыми кислотами по настоящему изобретению
11.5.1. Протокол
Группы из пяти самок мышей линии BALB/C иммунизировали внутримышечно дважды с интервалом 14 дней различными плазмидными ДНК, используя 20 мкг каждой плазмиды на инъекцию. Иммунные ответы измеряли спустя 28 день для того, чтобы определить влияние различных модификаций: +/- IMX313 или IMX313T; +/- сигнальный пептид ТАП; +/- мономеризованные мутации.
Антиген-специфические Т-клеточные ответы были измерены при помощи метода ELISPOT с использованием спленоцитов на 28-ой день. Очищенные CD4+, CD8+ Т-клетки и общее количество Т-клеток селезенки, выделенные из иммунизированных мышей, культивировали совместно с пептидом NP вируса гриппа А (аминокислоты 366-374), приобретенным от компании Eurogentec.
Анализы ELISPOT: плоскодонные, нитроцеллюлозные 96-луночные планшеты (Millititer; Millipore) покрывали IFN-γ mAb (15 мкг/мл; Mabtech, Стокгольм) и инкубировали в течение ночи при 4°С. После промывки НФБ планшеты блокировали добавлением 10% фетальной бычьей сыворотки в течение одного часа при 37°С. Клетки в концентрации 2×106 на лунку стимулировали соответствующими пептидами в конечной концентрации 2 мкг/мл (пептид NP вируса гриппа А) на IPVH мембранах с покрытием антителами к человеческому IFN-γ в концентрации 15 мкг/мл и инкубировали в течение 20 ч. После инкубации планшеты тщательно промывали НФБ для удаления клеток и прибавляли IFN-γ mAb (с добавлением 1 мкг/мл биотина, МАВТЕСН) в каждую лунку. После инкубации в течение 2 ч при 37°С планшеты промывали и детектировали с помощью стрептавидина, конъюгированного с пероксидазой хрена (1 мкг/мл; МАВТЕСН) в течение одного часа при комнатной температуре. После промывки добавляли субстрат (3-амино-9-этилкарбазол (Sigma)) и инкубировали в течение 15 минут. После дополнительной промывки подсчитывали под микроскопом пятна красного цвета.
Для изучения гуморального иммунного ответа оценивали уровень антител методом ELISA, специфическим для суммарного количества иммуноглобулинов IgG, и отдельно для каждого иммуноглобулина IgG1 и IgG2a оценивали относительные пропорции Th1 и Th2 ответов у мышей линии BALB/C на вакцины против вируса гриппа с Th2-типом иммунного ответа, который связан со стимуляцией IgG1 антител. Однако, главным изотипом антител, присутствующих в сыворотках мышей, выживших при вирусных инфекциях, является иммуноглобулин IgG2a, который стимулируется во время иммунных ответов Th1-типа (32). Стимуляция антител IgG2a была связана с увеличением эффективности вакцинации против гриппа.
Для проведения ELISA антигены разбавляли до концентрации 5 мг/мл в 0,1М растворе натрия карбоната/бикарбоната (pH 9,6), а затем применяли для покрытия лунок планшета MaxiSorb (Nunc-Immulon, Denmark). В лунки добавляли двухкратные серийные разведения тестируемых сывороток и после промывания обнаруживали связанные антитела с использованием антител против мышиных IgG, или антител против мышиного IgG1, или антител против мышиного IgG2a (Sigma), конъюгированных с пероксидазой хрена. Поглощение при длине волны 490 нм определяли после добавления о-фенилендиамина (Sigma) и H2O2; реакции останавливали путем добавления 1М серной кислоты.
Результаты показаны на Фигурах 11-14.
11.5.2. В предварительных экспериментах тестировали суммарные Т-клеточные ответы на NP, индуцированные ДНК-вакцинами, кодирующими или NP, или NP слитый с IMX313. Общее количество Т-клеток, выделенных из мышей, иммунизированных NP-IMX313, свидетельствовало о значительно более высоких IFNγ ответах по сравнению с аналогичными ответами у мышей, иммунизированных NP, и подтверждало способность IMX313 усиливать Т-клеточные ответы.
Фигура 11 показывает, что слияние исходного гена нуклеопротеина NP с геном IMX313 усиливает Т-клеточные ответы на NP.
11.5.3. Чтобы определить, был ли обнаруженный при проведении ELISPOT интерферон у (IFN-γ) произведен CD4 Т-клетками или CD8 Т-клетками, подвергали очистке CD4+ и CD8+ Т-клетки селезенки из иммунизированных мышей, и культивировали их совместно с пептидом NP гриппа А. Обнаруживали значительное увеличение продукции IFN-γ CD8+ Т-клетками в группе, иммунизированной NP-IMX313. Процентное содержание антиген-специфических CD8+ клеток, продуцирующих IFN-γ было выше, чем соответствующая популяция CD4+ Т (Фиг. 12).
Фигура 12 показывает, что слияние гена антигена NP с геном IMX313 улучшает как CD4+, так и CD8+ ответы на антиген NP.
11.5.4. Затем исследовали ответ антител на NP после иммунизации и через 14 дней после последней иммунизации, для чего измеряли ответы NP-специфических антител IgG в сыворотке. Контрольные по антигену NP мыши и мыши, получавшие NP-IMX313, демонстрировали умеренное количество NP-специфических антител IgG (Фиг. 13), которое были выше в группе, иммунизированной NP-IMX313.
Фигура 13 показывает, что слияние гена NP с геном IMX313 повышает ответ антител IgG на антиген NP.
11.5.5. Сыворотки также исследовали на присутствие NP-специфических антител IgG1 и IgG2a (представляющих Th2 и Th1 типы ответа у мышей линии BALB/C, соответственно). NP-специфические антитела изотипов IgG1 и IgG2a были обнаружены в сыворотке мышей, иммунизированных NP-IMX313; однако образцы сыворотки из мышей, получавших только NP, демонстрировали низкие уровни антител IgG1 и IgG2a (Фиг. 14).
На Фигуре 14 показаны распределения подкласса антител, индуцированных против антигена NP. Слияние с геном IMX313 улучшает ответ антител IgG2a сильнее, чем ответ антител IgG1, преобразуя Th2-обусловленный ответ против NP в Th1-обусловленный ответ против NP-IMX313.
11.6. Получение рекомбинантного белка NP-M-IMX313T
Синтетический ген, кодирующий белок NP-M-IMX313T, синтезировали с помощью кодонов, оптимизированных для экспрессии в кишечной палочке Escherichia coli. Этот синтетический ген был клонирован в экспрессионный вектор pIMX04 на основе Т7 (он представляет собой вектор pRsetC от Invitrogen, в котором точка начала репликации f1 была заменена локусом par плазмиды pSC101). Экспрессию индуцировали в нескольких стандартных средах (лизогенный бульон (LB), среда для аутоиндукции по Studier) и суперэкспрессированный белок очищали сначала так, как описано Ye (30) и Tarus (31) для осветления и стадий ионообменной хроматографии, но на конечной стадии слитый белок очищали при помощи аффинной хроматографии на гепарин-сефарозе, как описано выше.
11.7. Рекомбинантный белок NP-M-IMX313T применяли для иммунизации следующим образом:
Группы из пяти самок мышей линии BALB/C иммунизировали внутримышечно дважды с интервалом в 14 дней различными белковыми препаратами (с применением препарата лигандов ТПР или без него), используя 2 нмоль белка на инъекцию. Иммунный ответ измеряли на 28-й день, используя спленоциты для определения антиген-специфических Т-клеточных реакций, (измеряли при помощи ELISPOTs). Ответы антител перед иммунизацией и на 28-й день измеряли при помощи ELISA с применением NP в качестве антигена.
Результаты:
Фигура 15 показывает, что мономеризация NP незначительно повышает его иммуногенность, при этом последняя дополнительно улучшается путем слияния NP с геном IMX313, но самое большое улучшение достигается путем слияния мономерного NP с геном IMX313T.
Фигура 16 показывает, что, на основании анализа CD4+ и CD8+ ответов, при том же самом порядке ранжирования, как на Фигуре 6, наблюдалось следующее: мономеризация NP незначительно улучшает иммуногенность NP; при этом последняя дополнительно улучшается путем слияния NP с геном IMX313, однако, самое большое улучшение достигается путем слияния мономерного NP с геном IMX313T.
Фигура 17 показывает, что для В-клеточных ответов наблюдался тот же самый порядок ранжирования, что и для Т-клеточных ответов (как для CD4+, так и для CD8+) на Фигурах 6 и 7. Ответы суммарных IgG против NP были выше при использовании IMX313T, чем при использовании IMX313.
Фигура 18 показывает распределение подклассов антител, индуцированных против мономерного антигена NP. Слияние NP с геном IMX313 увеличивает ответ IgG2a больше, чем ответ IgG1, преобразуя Th2-обусловленный ответ на NP в Th1-обусловленный на NP-IMX313. Особый интерес представляет то, что смена Th2-типа ответа на Th1-тип ответа была амплифицирована путем слияния с белком IMX313T, а не с белком IMX313. Экспрессия антител IgG2a в вакцинах против вируса гриппа коррелирует с клиренсом вируса и повышенной защитой от летального инфицирования вирусом гриппа. Увеличение индукции обоих изотипов антител, как свидетельствуют измерения с помощью ELISA, является лучшим коррелятом для эффективности вакцины, чем одна лишь нейтрализация (32).
11.8. Секреция нуклеопротеина NP улучшала его иммуногенность
Получали серию конструктов ДНК-вакцин нуклеопротеина NP, содержащих секреторную сигнальную последовательность тканевого активатора плазминогена (tPA): tPA-NP, tPA-NP-M, tPA-NP-M-IMX313 и tPA-NP-V-IMX313T. Анализировали воздействие слияния tPA и NP на гуморальные и клеточные иммунные ответы иммунизированных животных.
Мыши, иммунизированные конструктами, содержащими tPA, показывали значительно более высокие ответы IFNγ по сравнению с ответами мышей, иммунизированных NP, что подтверждало способность IMX313T и мономеризующих мутаций усиливать Т-клеточные ответы.
Фигура 19 показывает, что усиление секреции антигена NP улучшало его иммуногенность (NP по сравнению с tPA-NP), независимо от того, был ли он мономерным или нет (tPA-NP по сравнению с tPA-NP-M). Однако слияние с IMX313 показало, что использование мономерной версии NP было более иммуногенным, чем использование немодифицированного антигена (tPA-NP-IMX313 сравнению tPA-NP-M-IMX313). А замена IMX313 на IMX313T дополнительно улучшала иммуногенность NP (tPA-NP-M-IMX313 по сравнению с tPA-NP-M-IMX313T).
На Фигуре 20 показаны ответы CD8+ и CD4+ на различные секретируемые версии NP. Виден тот же порядок ранжирования, как на Фигуре 19, и снова явно выражена эффективность мономеризации антигена при добавлении IMX313. Как и на предыдущих фигурах, наибольшие иммунные ответы наблюдаются, когда IMX313T используется вместо IMX313.
На Фигуре 21 показаны ответы суммарного количества IgG на антиген NP, что побуждает к таким же выводам, как Т-клеточные ответы на Фигуре 20: наибольшие ответы наблюдаются при использовании IMX313T, но секреция (NP по сравнению с tPA-NP) и мономеризация (tPA-NP-IMX313 по сравнению с tPA-NP-M-IMX313) также вносят в них важный вклад.
Мыши, иммунизированные одним лишь антигеном NP не имели никаких антител IgG против NP или имели очень низкие уровни этих антител в сыворотке (Фигура 21) Мыши, иммунизированные NP-M-IMX313, tPA-NP-M-IMX313, NP-M-IMX313T или tPA-NP-M-IMX313T, напротив, демонстрировали высокие уровни системных ответов NP-специфических антител IgG; однако, мыши, иммунизированные tPA-NP-M-IMX313T, имели значительно более высокие (р<0,001) ответы антител IgG по сравнению со всеми группами иммунизированных мышей. Это показывает, что сочетание всех модификаций (мономеризующие мутации, tPA и IMX313T) придает антигену значительно улучшенную иммуногенность по сравнению с иммуногенностью исходной последовательности или других комбинаций.
На Фигуре 22 показан анализ подклассов В-клеточных ответов на NP, и эта Фигура иллюстрирует, что начальная тенденция к Th2-типу ответов на использование одного лишь NP обращается при использовании IMX313 и IMX313T. Несмотря на то, что секреция сама по себе оказывает мало влияния (NP по сравнению с tPA-NP), мономеризация (tPA-NP-IMX313 по сравнению с tPA-NP-M-IMX313), а затем замена IMX313 на IMX313T (tPA-NP-M-IMX313 по сравнению с tPA-NP-M-IMX313T) вносят свой вклад в усиление Th1 (IgG2a) ответов по сравнению с Th2 (IgG1) ответами.
Очень важно, что tPA-NP-M-IMX313T сам по себе почти эквивалентно улучшает Th1 и Th2 ответы. Слияние NP и IMX313 показывает, что как Th1 ответы, так и Th2 ответы усиливаются и не существует никакого значительного изменения в типе ответов. Но при использовании IMX313T и мономеризующих мутаций Th1-тип ответа (IgG2a) начинает преобладать. Консенсус среди иммунологов заключается в том, что ответы Th1 предпочтительнее ответов Th2 (Фигура 22).
11.9. IMX313T не разрушается протеазами при прохождении через пути секреции
Результаты, полученные при ДНК-иммунизации плазмидами, содержащими IMX313T, убедительно свидетельствуют о том, что конечный участок молекулы не расщепляется протеазами, когда она проходит через пути секреции, где в избытке имеются протеазы. Чтобы изучить этот вопрос более полно, проводили трансфекцию клеток СНО K1 с помощью плазмиды, используемой для экспрессии NP-M-IMX313T in vivo. Трансфекцию проводили, как описано в (33).
От восемнадцати до двадцати четырех часов спустя супернатанты трансфицированных клеток выделяли центрифугированием и фильтровали перед нанесением на колонку с гепарин-сефарозой, как описано выше.
Обнаруживали небольшой «пик С», который, как было доказано с помощью электрофореза в полиакриламидном геле с додецилсульфонатом натрия и Вестерн-блоттинга, содержит белок NP-M-IMX313T.
12. Модификация тримерной суперспирали
Для того, чтобы определить, может ли изменение тримерной суперспирали улучшить иммуногенность антигена, конструировали две плазмиды с использованием синтетического гена НА2, кодирующего тримерную суперспираль гемагглютинина вируса гриппа.
Первая плазмида представляла собой плазмиду рIМХ743, в которой суперспираль НА2 была модифицирована путем слияния с пептидом: SPRRRRRRRRRS (SEQ ID NO: 37).
Следующий после Nde I и до Hind III рестрикционный фрагмент клонировали в экспрессионный вектор Т7:

 (SEQ ID NO: 60)
(SEQ ID NO: 60)
Кодируемая белковая последовательность была следующей:

 (SEQ ID NO:61)
(SEQ ID NO:61)
Контрольную плазмиду pIMX744 создавали путем удаления пептида с использованием олигонуклеотидных праймеров IMX203: 5' GTTAGCAGCCGGATCAAGCTTATTAGGCATTGTTCTTCAGCTGGC 3' (SEQ ID NO: 62) и T7F для амплификации НА2 вставки, которую затем вновь встраивали в исходную плазмиду.
Нуклеотидная последовательность была следующей:

 (SEQ ID NO: 63)
(SEQ ID NO: 63)
А кодируемая белковая последовательность была следующей:

 (SEQ ID NO: 64)
(SEQ ID NO: 64)
Затем оба белка очищали сначала на аффинной колонке IMAC, а после этого на колонке с гепарин-сефарозой. Белок IMX743 элюировали при более высокой концентрации соли (NaCl), чем белок IMX744: белок IMX743 элюировали при концентрации соли 1,4 М (sic), тогда как белок IMX744 элюировали при концентрации соли 600 мМ.
Затем оба белка были использованы для иммунизации четырех групп самок мышей линии BALB/C в возрасте 5-6 недель в дни 0 и 14, в количестве 20 мкг на инъекцию. На 21-ой день забирали образцы сыворотки и селезенок для проведения ELISA и ELISPOTs. Две группы получали белок в адъюванте Addavax, тогда как две другие группы были иммунизированы без адъюванта. Белок IMX744 был использован в качестве антигена для ELISA, а также для стимуляции клеток селезенки.
Результаты показаны в Таблице 4 ниже.
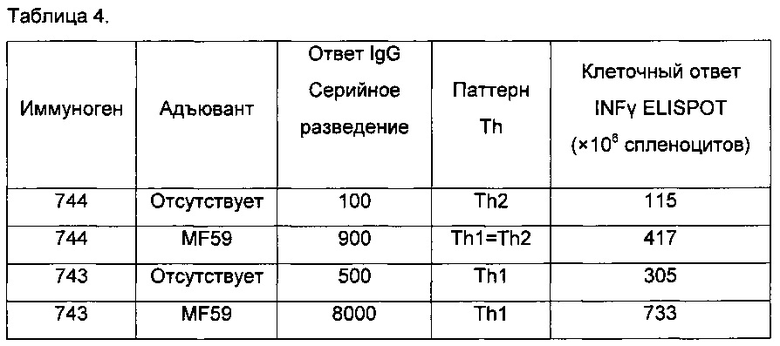
Результаты ясно показывают, что положительно заряженный пептид (SEQ ID NO: 37), представленный только в белке IMX743, делает белок IMX743 гораздо более иммуногенным, чем другой идентичный белок IMX744, независимо от того, использован адъювант или нет. Кроме того, применение адъюванта дополнительно повышает иммуногенность суперспирали, содержащей антиген.
13. Модификация мышиного домена олигомеризации C4bp белка IMX108
Суперспираль слитого белка DsbA-IMX108, описанного в ссылке 16, модифицировали для того, чтобы определить, приобрел ли он тоже улучшенные свойства, приданные белку IMX313. Для того, чтобы модифицировать его, амплифицировали ген DsbA-IMX108 с олигонуклеотидами IMX212: 5' GGAGCGACGGCGACGCGGAGActggagctgtagtagttcaacctcc 3' (SEQ ID NO: 65) и T7F и встраивали (29) в плазмиду, экспрессирующую IMX313T, вместо IMX313. Белок очищали при помощи ионообменной хроматографии, а затем на колонке с гепарин-сефарозой, с которой он связывался, тогда как исходный конструкт DsbA-IMX108 не связывался.
Ниже исходную последовательность IMX108 (SEQ ID NO: 66) выравнивали с последовательностью IMX108T (SEQ ID NO: 67);
IMX108: EASEDLKPALTGNKTMQYVPNSHDVKMALEIYKLTLEVELLQLQIQKEKHTEAH*
IMX108T: EASEDLKPALTGNKTMQYVPNSHDVKMALEIYKLTLEVELLQLQSPRRRRS*
Модифицированный белок IMX108 эффективен для иммунизации домашней птицы, где следует избегать потенциальных аутоиммунных эффектов от использования модифицированных слитых белков IMX313 (16). Другие домены олигомеризации млекопитающих C4bp (перечисленные в ссылке 16 и патенте WO 2007/062819) также могут быть модифицированы, как описано в настоящем изобретении для этой цели.
14. Слитые белки, содержащие N-конец стафилококкового альфа-гемолизина и модифицированные белки IMX313
Для того, чтобы продемонстрировать, что слияние с модифицированными белками IMX313 может улучшить иммуногенность N-концевого домена стафилококкового токсина альфа-гемолизина (Hla), усеченный ген гемолизина амплифицировали из геномной ДНК штамма Newman и клонировали в экспрессионный вектор T7. Были использованы олигонуклеотиды:
 (SEQ ID NO: 68) и
(SEQ ID NO: 68) и
 (SEQ ID NO: 69).
(SEQ ID NO: 69).
Для слияния N-концевой шестьдесят третьей аминокислоты зрелого токсина с модифицированным белком IMX313 амплифицировали IMX313T с использованием праймеров:
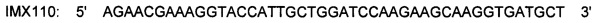 (SEQ ID NO: 70) и
(SEQ ID NO: 70) и 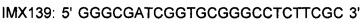 (SEQ ID NO: 44) из плазмиды экспрессии IMX313T, а ПЦР-продукт использовали для дополнительного транкирования гена токсина Hla во время слияния аминокислоты 63 с модифицированным геном IMX313. Полученная в результате этого плазмида экспрессирует слитый белок, называемый Hla63-IMX313T, который имеет следующую аминокислотную последовательность:
(SEQ ID NO: 44) из плазмиды экспрессии IMX313T, а ПЦР-продукт использовали для дополнительного транкирования гена токсина Hla во время слияния аминокислоты 63 с модифицированным геном IMX313. Полученная в результате этого плазмида экспрессирует слитый белок, называемый Hla63-IMX313T, который имеет следующую аминокислотную последовательность:
 (SEQ ID NO: 71) и кодируется следующей нуклеотидной последовательностью:
(SEQ ID NO: 71) и кодируется следующей нуклеотидной последовательностью:
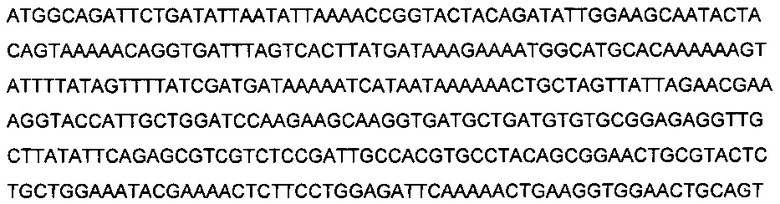
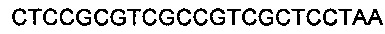 (SEQ ID NO: 72).
(SEQ ID NO: 72).
Для получения этого белка 500 мл культуры штамма C43(DE3) индуцировали с использованием 1 мМ ИПТГ и выращивали в течение ночи. Выращенные бактерии подвергали лизису путем обработки ультразвуком, а нерастворимый белок ресуспендировали в 50 мМ Трис, pH 7,5, 150 мМ NaCl и 6 М мочевине (буфер А). Этот белок наносили на колонку Hi-Trap SP FF и элюировали буфером А, содержащим 1М NaCl. Частично очищенный белок подвергали диализу против буфера, содержащего 50 мМ Трис, pH 7,5, 150 мМ NaCl и наносили на колонку с гепарин-сефарозой, из которой его элюировали градиентом NaCl (50 мМ Трис, pH 7,5, 1 М NaCl). Элюированный белок подвергали диализу против НФБ и дополнительно очищали гель-фильтрацией.
N-концевой фрагмент (отсутствующий в IMX313T) модифицировали путем клонирования С-концевой метки из шести остатков гистидина и очищали с помощью металл-аффинной хроматографии (IMAC, от англ. - immobilized-metal affinity chromatography) на никеле и гель-фильтрации.
Затем оба очищенных белка использовали для иммунизации мышей, в присутствии и в отсутствие адъюванта.
Четыре группы из пяти самок мышей линии BALB/C в возрасте 5-6 недель иммунизировали, используя или 5 ммоль белка Hla63, или 5 ммоль этого же антигена, слитого с IMX313T, в дни 0 и 14. На 28 день забирали образцы сыворотки и селезенок для проведения ELISA и ELISPOT. Белок 63 Hla 6 His использовали в качестве антигена для ELISA, а также для стимуляции клеток селезенки.
Результаты показаны в Таблице 5.
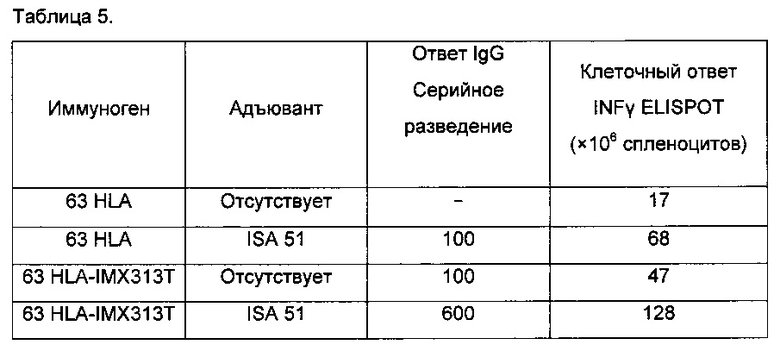
Результаты ясно показывают, что N-концевой фрагмент альфа-гемолизина (HLA) является более иммуногенным, когда он слит с белком IMX313T, независимо от того, присутствует адъювант или нет.
15. Полноразмерный стафилококковый протеин А, слитый с модифицированными IMX313 белками
Чтобы определить, могут ли белки IMX313T и IMX313P улучшить иммуногенность полноразмерного стафилококкового антигена протеина A (SpA), синтетический ген, кодирующий пять гомологичных доменов (мутантный, как описано в ссылке 44) клонировали в виде фрагмента Nde I-Hind III в экспрессионный вектор T7. Нуклеотидная последовательность была следующей:

 (SEQ ID NO: 73)
(SEQ ID NO: 73)
А кодированная белковая последовательность была следующей:

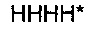 (SEQ ID NO: 74)
(SEQ ID NO: 74)
Для того, чтобы слить антиген и белки IMX313T и IMX313P, фрагмент BamH I-Hind III, кодирующий С-концевую гистидиновую метку, заменяли на фрагмент BamH I-Hind III, кодирующий белки 313.
Белки очищали следующим образом: SpA-6His получали путем продукции его в бактериальном штамме BLR и бактериальный дебрис лизировали в буфере А (1×НФБ, 1М NaCl, 20 мМ имидазола, 1 мМ, фенилметилсульфонил фторида (ФМСФ)), бактериальный лизат нагревали до 75°С в течение 15 минут, а затем очищали центрифугированием перед нанесением на колонку с никелем для IMAC. Белок элюировали градиентом имидазола в буфере В (1×НФБ, 500 мМ имидазола). Белок дополнительно очищали методом гель-фильтрации.
Белки SpA-IMX313T и SpA-IMX313P также экспрессировали в штамме BLR, и бактериальные лизаты нагревали до 75°С в течение 15 минут и осветляли центрифугированием. После этого оба белка очищали на ионообменной колонке SP, а затем на колонке с гепарин-сефарозой.
Эти три белки использовали для иммунизации шести групп самок мышей линии BALB/C в возрасте 5-6 недель в дни 0 и 14. Для иммунизации использовали 5 ммоль каждого белка с адъювантом AddaVax или без него. На 28-й день забирали образцы сыворотки и селезенки для ELISA и ELISPOT. Белок SpA-6His применяли в качестве антигена для ELISA, а также для стимуляции клеток селезенки.
Результаты показаны в Таблице 6 ниже. Очевидно, что антиген SpA, слитый с IMX313T или Р, является более иммуногенным, чем не подвергнутый слиянию антиген, a IMX313P версия является немного более иммуногенной, чем IMX313T версия.
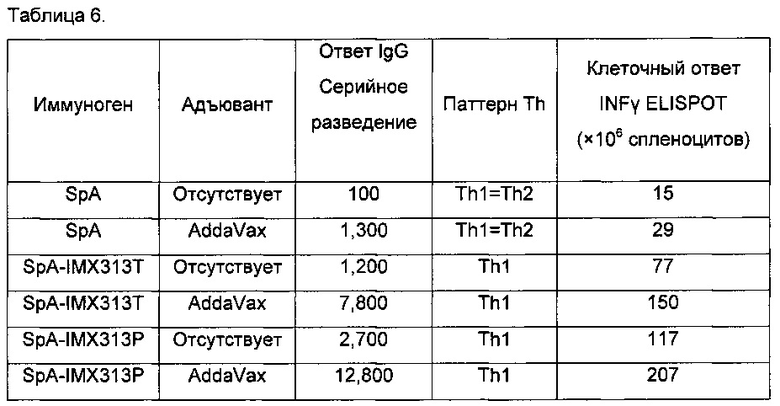
16. Слитые белки ClfB и модифицированные белки IMX313
Для улучшения иммуногенности стафилококкового антигена ClfB домены N2N3 амплифицировали с помощью следующих олигонуклеотидов:
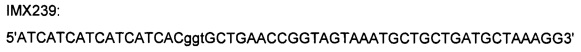 (SEQ ID NO: 75) и
(SEQ ID NO: 75) и
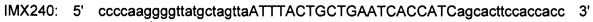 (SEQ ID NO: 76),
(SEQ ID NO: 76),
а ПЦР-продукт клонировали в экспрессионный вектор Т7 с N-концевой гистидиновой меткой (27).
Нуклеотидная последовательность фрагмента N2N3 была следующей:

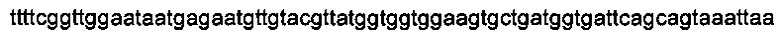 (SEQ ID NO: 77)
(SEQ ID NO: 77)
а последовательность белка была следующей:
 (SEQ ID NO: 78)
(SEQ ID NO: 78)
Затем домены IMX313T и IMX313P амплифицировали с олигонуклеотидами:
 (SEQ ID NO: 79) и IMX139 и клонировали С-концевой фрагмент в домен N3. Немодифицированные домены N2N3 и слитые белки N2N3-IMX313T и IMX313P экспрессировали следующим образом:
(SEQ ID NO: 79) и IMX139 и клонировали С-концевой фрагмент в домен N3. Немодифицированные домены N2N3 и слитые белки N2N3-IMX313T и IMX313P экспрессировали следующим образом:
500 мл культуры штамма C43(DE3) индуцировали с помощью 1 мМ ИПТГ и после индукции в течение ночи бактериальные дебрис лизировали в буфере А (1×НФБ, 1М NaCl, 20 мМ имидазола, 1 мМ ФМСФ), а затем очищали центрифугированием перед нанесением на колонку с никелем для IMAC. Белок элюировали градиентом имидазола в буфере В (1×НФБ, 500 мМ имидазола). Слитые белки дополнительно очищали с помощью аффинной хроматографии на гепарин-сефарозе с последующей гель-фильтрацией на геле Sephacryl S-300 HR, тогда как не подвергнутый слиянию протеин дополнительно очищали гель-фильтрацией на колонке для гель-фильтрации S-75.
17. Слитые белки сортазы А и модифицированные белки IMX313
Для улучшения иммуногенности стафилококковой протеазы, известной как сортаза А или SrtA, инактивированную версию клонировали в рамку считывания белков IMX313, IMX313T и IMX313P следующим образом: дикий тип гена сортазы А амплифицировали из геномной ДНК штамма Newman с олигонуклеотидами:
 (SEQ ID NO: 80), и
(SEQ ID NO: 80), и
 (SEQ ID NO: 81)
(SEQ ID NO: 81)
и клонировали в экспрессионный вектор Т7. Активный сайт остатка цистеина был заменен на активный сайт серина с помощью олигонуклеотида  (SEQ ID NO 82).
(SEQ ID NO 82).
Затем гены IMX313, 313Т и 313Р амплифицировали с олигонуклеотидами 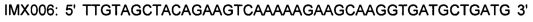 (SEQ ID NO 83) и
(SEQ ID NO 83) и  (SEQ ID NO: 44) из соответствующих экспрессионных векторов и встраивали в рамку считывания с помощью инактивированного гена протеазы (29).
(SEQ ID NO: 44) из соответствующих экспрессионных векторов и встраивали в рамку считывания с помощью инактивированного гена протеазы (29).
Слитые белки IMX313T и IMX313P очищали с помощью ионобменнной хроматографии на колонке SP, а затем на колонке с гепарин-сефарозой.
18. ДНК-иммунизация антигеном Ср15
Для того, чтобы определить, могут ли модифицированные белки IMX313 дополнительно улучшить иммуногенность криптоспоридиального антигена Ср15 сверх улучшения, полученного с помощью исходного IMX313, три плазмиды, предназначенные для того, чтобы экспрессировать Ср15, Ср15-IМХ313 и IMX313T в кишечной палочке Escherichia coli, применяли для приготовления векторов pCDNA3 в виде ДНК-вакцин. Праймеры, используемые для амплификации трех генов из экспрессионных векторов Т7 с целью вставки в вектор pcDNA3 ниже сигнального пептида tPA, были следующими:
IMX092: 5' ggaaatccatgcccgattcagaaga GCGCGTGTTCTGATCAAAGAGAAGC 3' (SEQ ID NO: 84) и
IMX093: 5' gccagtgtgatggatggcggtagttattgctcagcggtgg 3' (SEQ ID NO: 85).
Эти три ПЦР-продукта встраивали по отдельности в вектор pcDNA3, который содержит N-концевой сигнальный пептид tPA.
Три кодирующие последовательности были следующие:
Для CP15:

 (SEQ ID NO: 86).
(SEQ ID NO: 86).
Для CP15-IMX313:


 (SEQ ID NO 87).
(SEQ ID NO 87).
А для CP15-IMX313T:

 (SEQ ID NO 88).
(SEQ ID NO 88).
Вектор PcDNA3, не имеющий никаких вставок, использовали в качестве контрольной плазмиды. Эти четыре плазмиды применяли для иммунизации четырех группы мышей-самок линии BALB/C в возрасте 5-6 недель в дни 0 и 14. Двадцать пять микрограммов каждой плазмиды вводили внутримышечно при каждой иммунизации. На 28-й день забирали образцы сыворотки и селезенок для ELISA и ELISPOTs. Белок Cp15-6His, выделенный из кишечной палочки Escherichia coli, использовали в качестве антигена для ELISA, а также для стимуляции клеток селезенки.
Результаты ELISA и ELISPOT приведены в таблице 7 ниже.

Эти результаты показывают, что IMX313 улучшает как титры антител, так и ответы интерферона γ на антиген СР15, но эти ответы дополнительно улучшаются за счет использования IMX313T вместо IMX313.
19. Иммунизация продуктами слияния аутоантигенов и модифицированного белка IMX313: GnRH-IMX313T
Для дальнейшего улучшения иммунных ответов, индуцированных аутоантигеном GnRH при слиянии с IMX313, получали белок GnRH-IMX313T. Последовательность, кодирующая белок, была следующей:

 (SEQ ID NO: 89),
(SEQ ID NO: 89),
а последовательность белка была следующей:
 (SEQ ID NO: 90)
(SEQ ID NO: 90)
20. Синергизм адъювантов с модифицированными IMX313 белками и антигенами
Для того, чтобы определить, может ли улучшенная иммуногенность полученная с использованием модифицированных белков IMX313, быть дополнительно улучшена за счет применения классического адъюванта, и действительно ли это может быть сделано путем применения двух адъювантов, получали следующие белки: PAm, PAm-IMX313 и PAm-IMX313T (приготовленный, как описано в Примере 6 выше), как указано в колонке «адъювант» в Таблице ниже. Затем полученные белки применяли для иммунизации семи групп самок мышей линии BALB/C в возрасте 5-6 недель в дни 0 и 14. Для иммунизации применяли 5 ммоль каждого белка с добавлением адъюванта AddaVax или без него, и с добавлением или без добавления ТПР-лиганда Poly(I:C). В седьмой группе ТПР-лиганд Poly(I:C) сначала был приготовлен совместно с белком PAm-IMX313T, а затем с адъювантом AddaVax.
На 28-й день брали образцы сыворотки и селезенки для ELISA и ELISPOTs. Белок PAm применяли в качестве антигена для ELISA, а также для стимуляции клеток селезенки.
Результаты представлены ниже в таблице (Таблица 8).
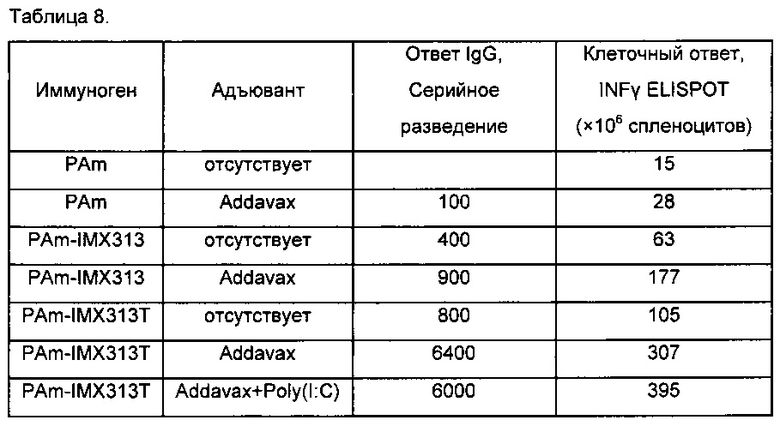
Очевидно, что существует преимущество в использовании адъюванта совместно с модифицированным белком IMX313, а иммуногенность может быть дополнительно улучшена путем использования второго адъюванта, Poly(I:C).
Ссылки
1) Odgren PR, Harvie LW Jr, Fey EG. 1996. Phylogenetic occurrence of coiled coil proteins: implications for tissue structure in metazoan via coiled coil tissue matrix. Proteins 24:467-484.
2) Rose A, Schraegle SJ, Stahlberg EA, Meier I. 2005. Coiled-coil protein composition of 22 proteomes--differences and common themes in subcellular infrastructure and traffic control. BMC Evol Biol. 5:66.
3) Burkhard P, Stetefeld J, Strelkov SV. 2001. Coiled coils: a highly versatile protein folding motif. Trends Cell Biol. 11:82-88.
4) Tavano R, Capecchi B, Montanari P, Franzoso S, Marin O, Sztukowska M, Cecchini P, Segat D, Scarselli M,  , Papini E. 2011. Mapping of the Neisseria meningitidis NadA cell-binding site: relevance of predicted {alpha}-helices in the NH2-terminal and dimeric coiled-coil regions. J Bacteriol. 193:107-115.
, Papini E. 2011. Mapping of the Neisseria meningitidis NadA cell-binding site: relevance of predicted {alpha}-helices in the NH2-terminal and dimeric coiled-coil regions. J Bacteriol. 193:107-115.
5) El Tahir Y, & Skurnik M. 2001. YadA, the multifaceted Yersinia adhesin. Int. J. Med. Microbiol. 291:209-218.
6) Cotter SE, Surana NK, St. Geme III JW. 2005. Trimeric autotransporters: a distinct subfamily of autotransporter proteins. Trends Microbiol. 13:199-205.
7) Szczesny P, Linke D, Ursinus A,  , Schwarz H, Riess TM, Kempf VA, Lupas AN, Martin J, Zeth K. 2008. Structure of the head of the Bartonella adhesin BadA. PLoSPathog. 4:e1000119.
, Schwarz H, Riess TM, Kempf VA, Lupas AN, Martin J, Zeth K. 2008. Structure of the head of the Bartonella adhesin BadA. PLoSPathog. 4:e1000119.
8) Serruto D, Spadafina T, Scarselli M, Bambini S, Comanducci M,  , Kilian M, Veiga E, Cossart P, Oggioni MR, Savino S, Ferlenghi I, Taddei AR, Rappuoli R, Pizza M, Masignani V,
, Kilian M, Veiga E, Cossart P, Oggioni MR, Savino S, Ferlenghi I, Taddei AR, Rappuoli R, Pizza M, Masignani V, 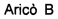 . 2009. HadA is an atypical new multifunctional trimeric coiled-coil adhesin of Haemophilus influenzae biogroup aegyptius, which promotes entry into host cells. Cell Microbiol. 11:1044-1063.
. 2009. HadA is an atypical new multifunctional trimeric coiled-coil adhesin of Haemophilus influenzae biogroup aegyptius, which promotes entry into host cells. Cell Microbiol. 11:1044-1063.
9) Chen J, Wharton SA, Weissenhorn W, Calder LJ, Hughson FM, Skehel JJ, Wiley DC. 1995. A soluble domain of the membrane-anchoring chain of influenza virus hemagglutinin (HA2) folds in Escherichia coli into the low-pH-induced conformation. Proc Natl Acad Sci USA. 92:12205-12209.
10) Swanson KA, Settembre EC, Shaw CA, Dey AK, Rappuoli R, Mandl CW, Dormitzer PR, Carfi A. 2011. Structural basis for immunization with postfusion respiratory syncytial virus fusion F glycoprotein (RSV F) to elicit high neutralizing antibody titers. Proc Natl Acad Sci USA. 108:9619-9624.
11) Tan K, Liu J, Wang J, Shen S, Lu M. 1997. Atomic structure of a thermostable subdomain of HIV-1 gp41. Proc Natl Acad Sci USA. 94:12303-12308.
12) Chen YH, Christiansen A,  , Dierich MP. 1995. HIV-2 transmembrane protein gp36 like HIV-1 gp41 binds to human lymphocytes and monocytes. AIDS 9:1193-1194.
, Dierich MP. 1995. HIV-2 transmembrane protein gp36 like HIV-1 gp41 binds to human lymphocytes and monocytes. AIDS 9:1193-1194.
13) Lee JE, Fusco ML, Hessell AJ, Oswald WB, Burton DR, Saphire EO. 2008. Structure of the Ebola virus glycoprotein bound to an antibody from a human survivor. Nature 454:177-182.
14) Yuan P, Swanson KA, Leser GP, Paterson RG, Lamb RA, Jardetzky TS. 2011. Structure of the Newcastle disease virus hemagglutinin-neuraminidase (HN) ectodomain reveals a four-helix bundle stalk. Proc Natl Acad Sci USA. 108:14920-14925.
15) Chambers RS, Johnston SA. (2003) High-level generation of polyclonal antibodies by genetic immunization. Nat Biotechnol. 21:1088-1092.
16) Ogun SA, Dumon-Seignovert L, Marchand JB, Holder AA, Hill F. 2008. The oligomerization domain of C4-binding protein (C4bp) acts as an adjuvant, and the fusion protein comprised of the 19-kilodalton merozoite surface protein 1 fused with the murine C4bp domain protects mice against malaria. Infect Immun. 76:2817-3823.
17) Sassenfeld HM & Brewer SJ. 1984. A polypeptide fusion designed for the purification of recombinant proteins. Biotechnology. 2:76-81.
18) Smith JC, Derbyshire RB, Cook E, Dunthorne L, Viney J, Brewer SJ, Sassenfeld HM, Bell LD. 1984. Chemical synthesis and cloning of a poly(arginine)-coding gene fragment designed to aid polypeptide purification. Gene. 32:321-327.
19) Stempfer G,  , Rudolph R. 1996. Improved refolding of an immobilized fusion protein. Nat Biotechnol. 14:329-334.
, Rudolph R. 1996. Improved refolding of an immobilized fusion protein. Nat Biotechnol. 14:329-334.
20) Stempfer G,  , Kopetzki E, Rudolph R. 1996. A fusion protein designed for noncovalent immobilization: stability, enzymatic activity, and use in an enzyme reactor. Nat Biotechnol. 14:481-484.
, Kopetzki E, Rudolph R. 1996. A fusion protein designed for noncovalent immobilization: stability, enzymatic activity, and use in an enzyme reactor. Nat Biotechnol. 14:481-484.
21) Suzuki M. 1989. SPKK, a new nucleic acid-binding unit of protein found in histone. EMBO J. 8:797-804.
22) Fuchs SM & Raines RT. 2005. Polyarginine as a multifunctional fusion tag. Protein Science 14:1538-1544.
23) Blasius AL & Beutler B. 2010. Intracellular Toll-like Receptors. Immunity 32:305-315.
24) Akira S, Uematsu S, Takeuchi O. 2006. Pathogen recognition and innate immunity. Cell 124:783-801.
25) Ewald SE, Lee BL, Lau L, Wickliffe KE, Shi GP, Chapman HA, Barton GM. 2008. The ectodomain of Toll-like receptor 9 is cleaved to generate a functional receptor. Nature 456:658-662.
26) Mendlowski B, Field AK, Tytell AA, Hilleman MR. 1975. Safety assessment of poly I:C in NZB/NZW mice. Proc Soc Exp Biol Med. 148:476-483.
27) Kim HK, Cheng AG, Kim HY, Missiakas DM, Schneewind O. 2010. Nontoxigenic protein A vaccine for methicillin-resistant Staphylococcus aureus infections in mice. J Exp Med. 207:1863-1870.
28) Spencer AJ, Hill F, Honeycutt JD, Cottingham MG, Bregu M, Rollier CS, Furze J, Draper SJ, Sogaard KС, Gilbert SC, Wyllie DH,. 2012. Fusion of the Mycobacterium tuberculosis antigen 85A to an oligomerization domain enhances its immunogenicity in both mice and non-human primates. PLoS One 7:e33555.
29) Geiser M,  ; Drewello D, Schmitz R. 2001. Integration of PCR fragments at any specific site within cloning vectors without the use of restriction enzymes and DNA ligase. Biotechniques 31:88-92.
; Drewello D, Schmitz R. 2001. Integration of PCR fragments at any specific site within cloning vectors without the use of restriction enzymes and DNA ligase. Biotechniques 31:88-92.
30) Ye Q, Krug RM, Tao YJ. (2006) The mechanism by which influenza A virus nucleoprotein forms oligomers and binds RNA. Nature. 444:1078-1082.
31) Tarus B, Bakowiez O, Chenavas S, Duchemin L, Estrozi LF, Bourdieu C, Lejal N, Bernard J, Moudjou M, Chevalier C, Delmas B, Ruigrok RW, Di Primo C, Slama-Schwok A. (2012) Oligomerization paths of the nucleoprotein of influenza A virus. Biochimie. 94:776-785.
32) Huber VC, McKeon RM, Brackin MN, Miller L, Keating R, Brown SA, Makarova N, Perez DR, MacDonald GH, McCullers JA. 2006 Distinct Contributions of Vaccine-Induced Immunoglobulin G1 (IgG1) and IgG2a Antibodies to Protective Immunity against Influenza. CLINICAL AND VACCINE IMMUNOLOGY 13: 981-990.
33) Krammer F, Pontiller J, Tauer C, Palmberger D, Maccani A, Baumann M, Grabherr R. (2010) Evaluation of the influenza A replicon for transient expression of recombinant proteins in mammalian cells. PLoS One. 5:e13265.
34) Yang Y, Ringler P,  , Burkhard P. (2012) Optimizing the refolding conditions of self-assembling polypeptide nanoparticles that serve as repetitive antigen display systems. J Struct Biol. 177:168-176.
, Burkhard P. (2012) Optimizing the refolding conditions of self-assembling polypeptide nanoparticles that serve as repetitive antigen display systems. J Struct Biol. 177:168-176.
35) Parry DA, Fraser RD, Squire JM. (2008) Fifty years of coiled-coils and alpha-helical bundles: a close relationship between sequence and structure. J Struct Biol. 163:258-269.
36) Bommakanti G, Citron MP, Hepler RW, Callahan C, Heidecker GJ, Najar ТА, Lu X, Joyce JG, Shiver JW, Casimiro DR, ter Meulen J, Liang X, Varadarajan R. (2010) Design of an HA2-based Escherichia coli expressed influenza immunogen that protects mice from pathogenic challenge. Proc Natl Acad Sci USA. 107:13701-13706.
37) Bommakanti G, Lu X, Citron MP, Najar ТА, Heidecker GJ, ter Meulen J, Varadarajan R, Liang X. (2012) Design of Escherichia coli-expressed stalk domain immunogens of H1N1 hemagglutinin that protect mice from lethal challenge. J Virol. 86:13434-13444.
38) Birnbaum F, Nassal M. (1990) Hepatitis В virus nucleocapsid assembly: primary structure requirements in the core protein. J Virol. 64:3319-3330.
39) Mulcahy ME, Geoghegan JA, Monk IR, O'Keeffe KM, Walsh EJ, Foster TJ, McLoughlin RM. (2012) Nasal colonisation by Staphylococcus aureus depends upon clumping factor В binding to the squamous epithelial cell envelope protein loricrin. PLoS Pathog. 8(12):e1003092.
40) Shibagaki N, Okamoto T, Mitsui H, Inozume T, Kanzaki M, Shimada S. (2010) Novel immunotherapeutic approaches to skin cancer treatments using protein transduction technology. J Dermatol Sci. 61:153-161.
41) Mitsui H, Okamoto T, Kanzaki M, Inozume T, Shibagaki N, Shimada S. (2010) Intradermal injections of polyarginine-containing immunogenic antigens preferentially elicit Tc1 and Th1 activation and antitumour immunity. Br J Dermatol. 162:29-41
42) Mitsui H, Inozume T, Kitamura R, Shibagaki N, Shimada S. (2006) Polyarginine-mediated protein delivery to dendritic cells presents antigen more efficiently onto MHC class I and class II and elicits superior antitumor immunity. J Invest Dermatol. 126:1804-1812.
43) Shibagaki N, Udey MC. (2002) Dendritic cells transduced with protein antigens induce cytotoxic lymphocytes and elicit antitumor immunity. J Immunol. 168:2393-2401.
44) O'Seaghdha M, van Schooten CJ, Kerrigan SW, Emsley J, Silverman GJ, Cox D, Lenting PJ, Foster TJ. (2006) Staphylococcus aureus protein A binding to von Willebrand factor A1 domain is mediated by conserved IgG binding regions. FEBS J. 273:4831-4841.
45) Arnau J, Lauritzen C, Petersen GE, Pedersen J. (2006) Current strategies for the use of affinity tags and tag removal for the purification of recombinant proteins. Protein Expr Purif. 48:1-13.
46) Fromm JR, Hileman RE, Caldwell EE, Weiler JM, Linhardt RJ. (1995) Differences in the interaction of heparin with arginine and lysine and the importance of these basic amino acids in the binding of heparin to acidic fibroblast growth factor. Arch Biochem Biophys. 323:279-287.
47) Chudasama SL, Espinasse B, Hwang F, Qi R, Joglekar M, Afonina G, Wiesner MR, Welsby IJ, Ortel TL, Arepally GM. (2010) Heparin modifies the immunogenicity of positively charged proteins. Blood. 116:6046-6053.
Ссылки на патенты
WO 2007/062819
WO 2007/100908
WO 2011/045612
WO 2008/122817
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНЫ НА ОСНОВЕ НУКЛЕОПРОТЕИНА ВИРУСА ГРИППА | 2014 |
|
RU2662667C2 |
| СЛИТЫЙ БЕЛОК ТЕЛОМЕРАЗНОЙ ОБРАТНОЙ ТРАНСКРИПТАЗЫ, КОДИРУЮЩИЕ ЕГО НУКЛЕОТИДЫ И ИХ ПРИМЕНЕНИЕ | 2007 |
|
RU2473691C2 |
| АГЕНТЫ И СПОСОБЫ, ОСНОВАННЫЕ НА ПРИМЕНЕНИИ ДОМЕНА EDA ФИБРОНЕКТИНА | 2006 |
|
RU2430738C2 |
| Иммуногенная композиция, включающая ее вакцина, набор для приготовления вышеуказанной композиции и способ лечения заболеваний, связанных с патологией секреции гастрина | 2014 |
|
RU2664197C2 |
| ИММУНОРЕГУЛЯТОРНАЯ ВАКЦИНА | 2013 |
|
RU2650709C2 |
| МОДИФИЦИРОВАННЫЙ БИОТИН-СВЯЗЫВАЮЩИЙ БЕЛОК, СЛИТЫЕ БЕЛКИ НА ЕГО ОСНОВЕ И ИХ ПРИМЕНЕНИЕ | 2012 |
|
RU2632651C2 |
| СЛИТЫЕ БЕЛКИ С FC-ФРАГМЕНТОМ ИММУНОГЛОБУЛИНА ДЛЯ ПОВЫШЕНИЯ ИММУНОГЕННОСТИ БЕЛКОВЫХ И ПЕПТИДНЫХ АНТИГЕНОВ | 2000 |
|
RU2248214C2 |
| ИММУНОГЕННАЯ КОМПОЗИЦИЯ ПРЕЗЕНТАЦИИ МНОЖЕСТВЕННЫХ АНТИГЕНОВ, ОТНОСЯЩИЕСЯ К НЕЙ СПОСОБЫ И ПРИМЕНЕНИЯ | 2012 |
|
RU2619176C2 |
| Универсальная противогриппозная вакцина | 2015 |
|
RU2618918C2 |
| АНТИГЕННЫЕ МАТРИЦЫ ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ КОСТЕЙ | 2002 |
|
RU2322258C2 |

































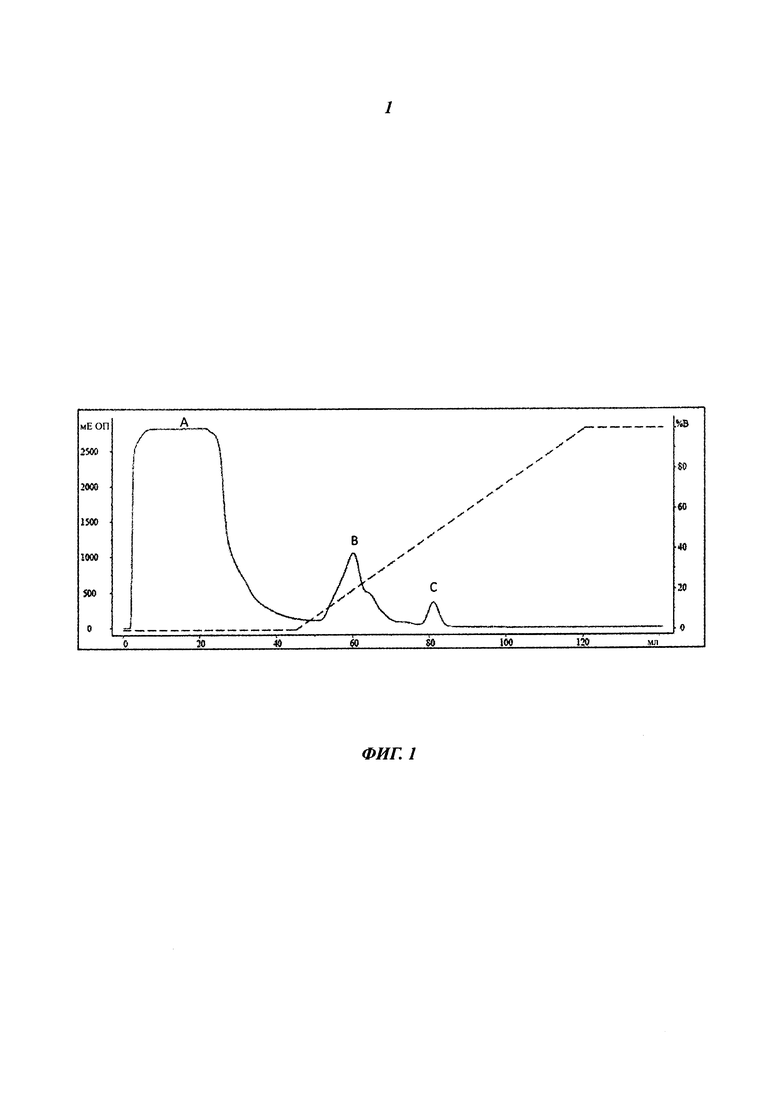
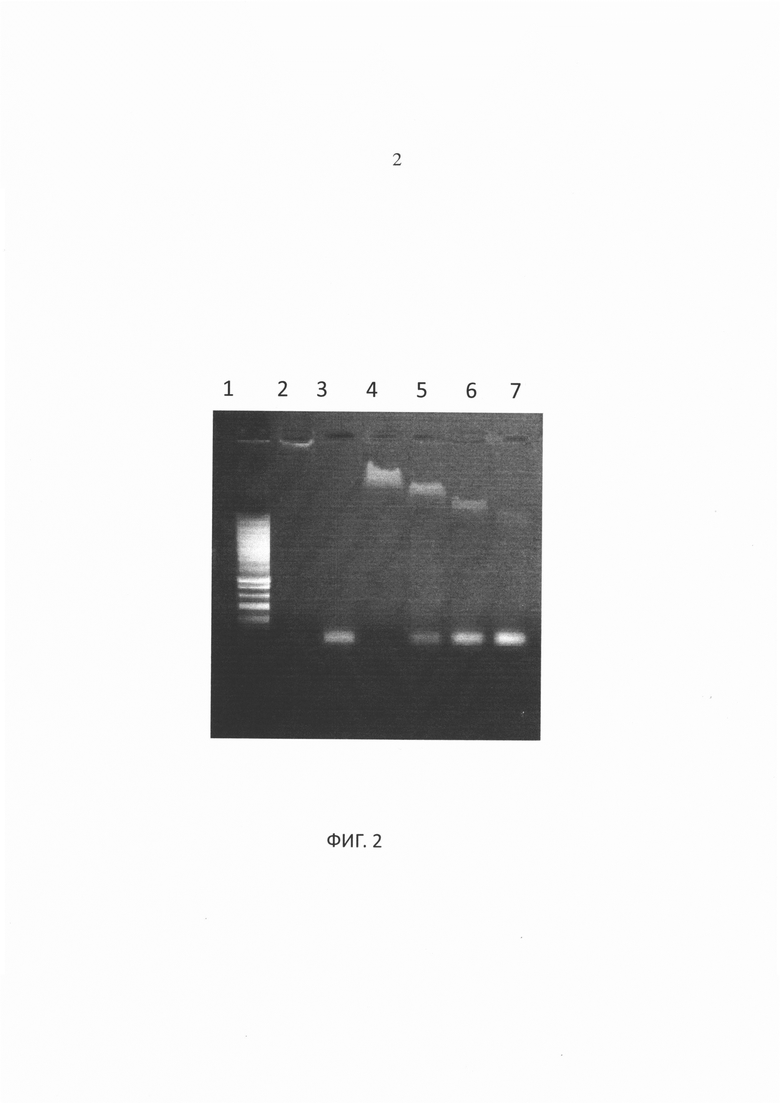
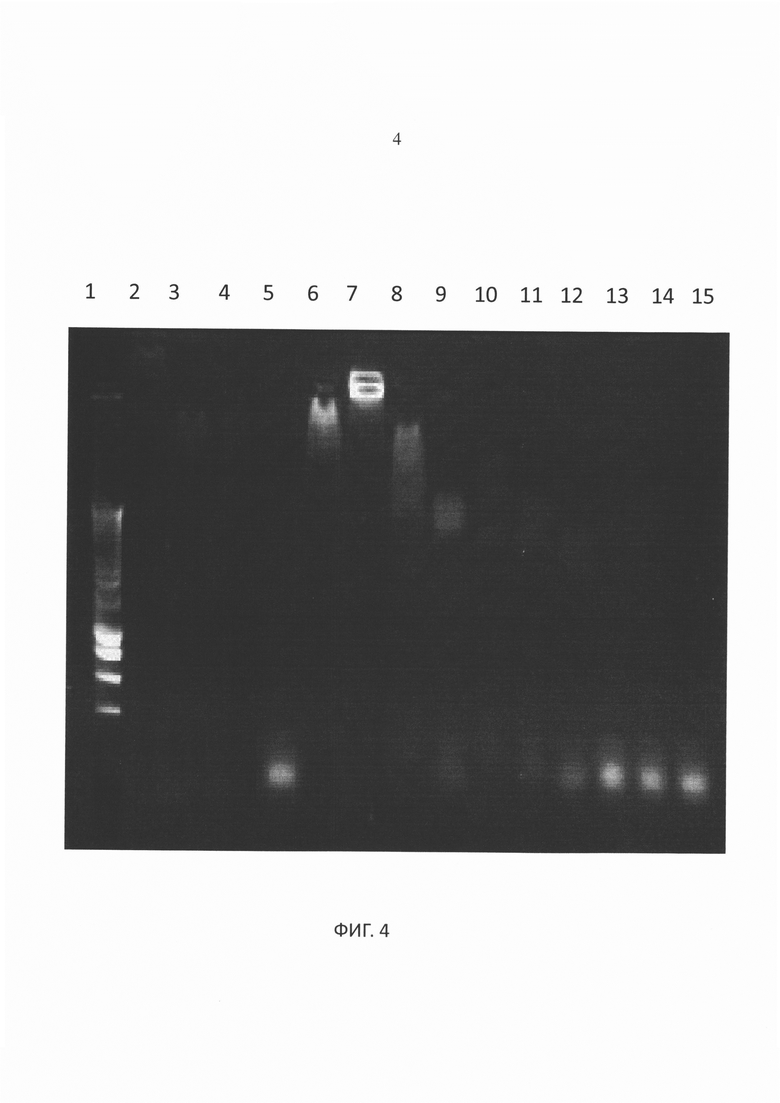
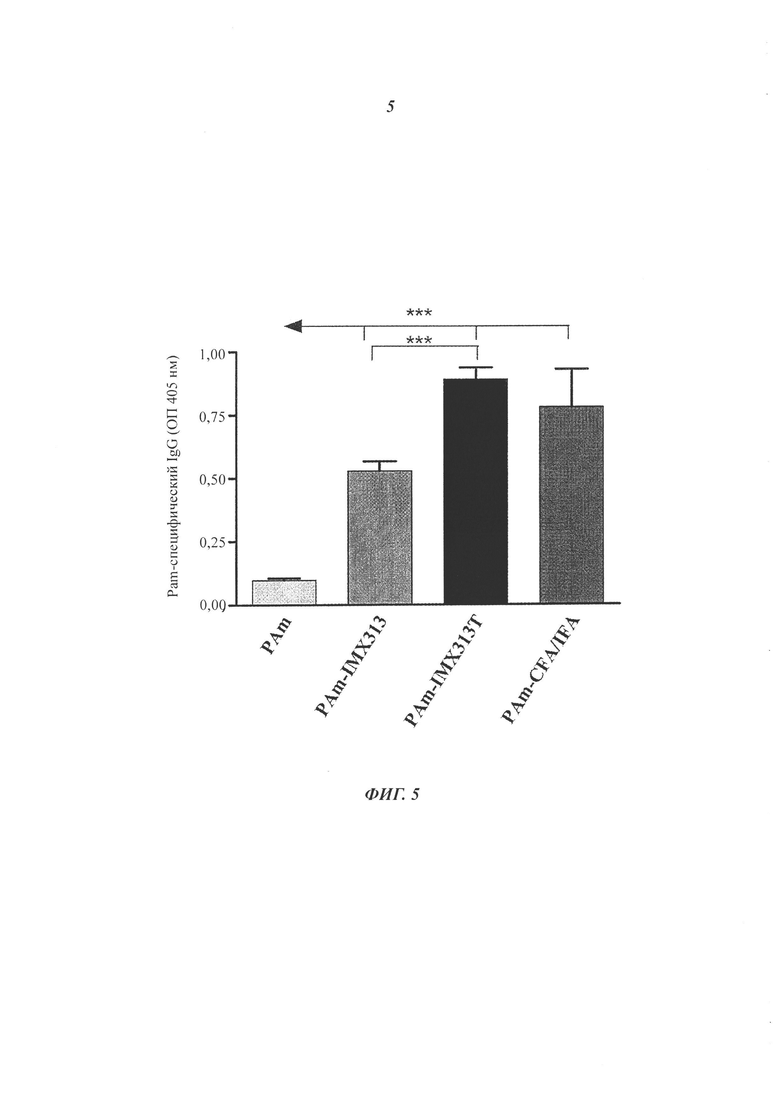

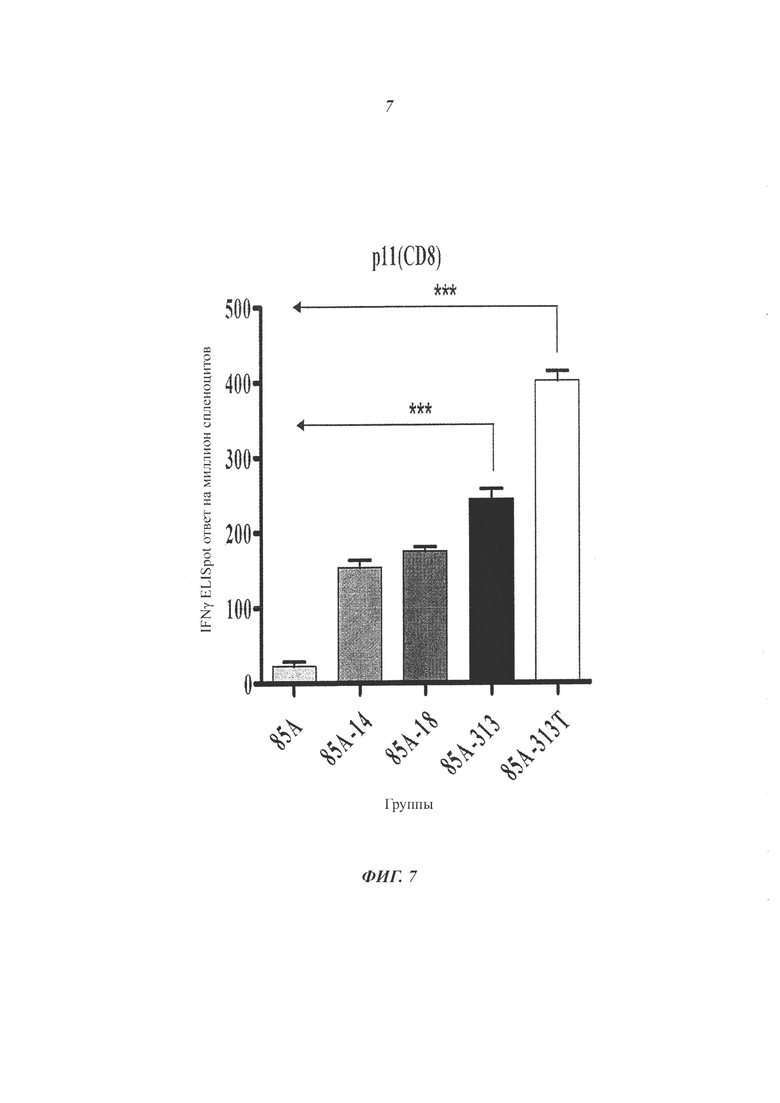
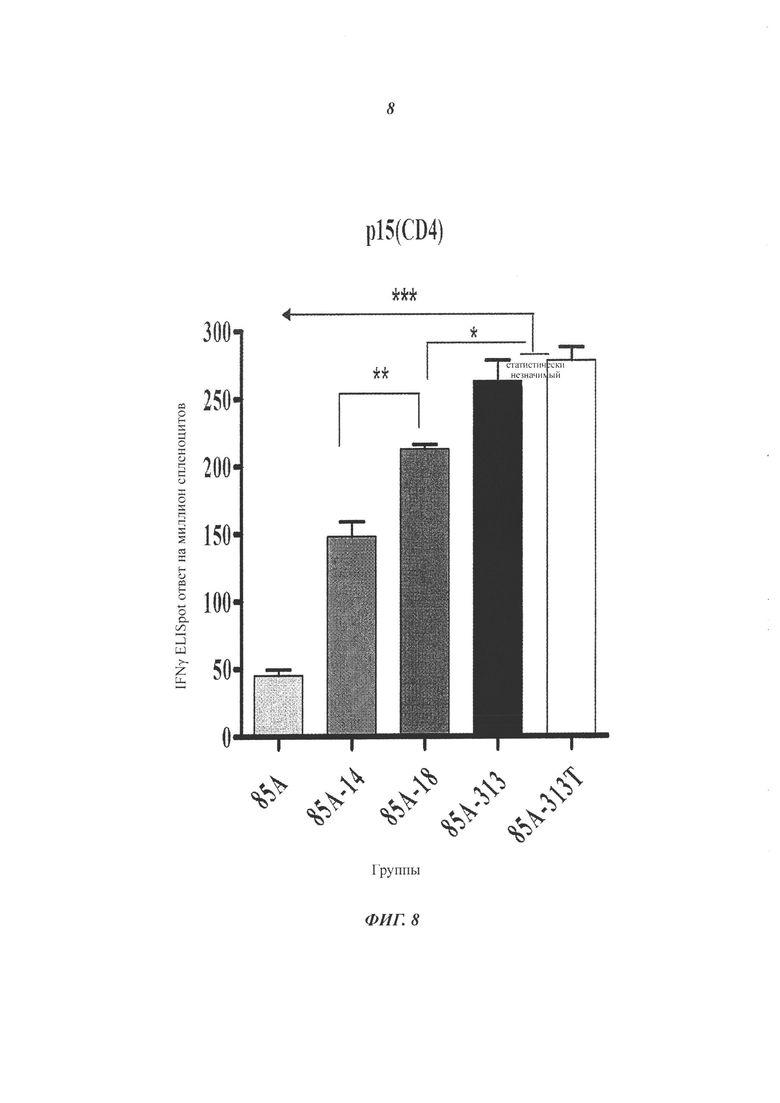
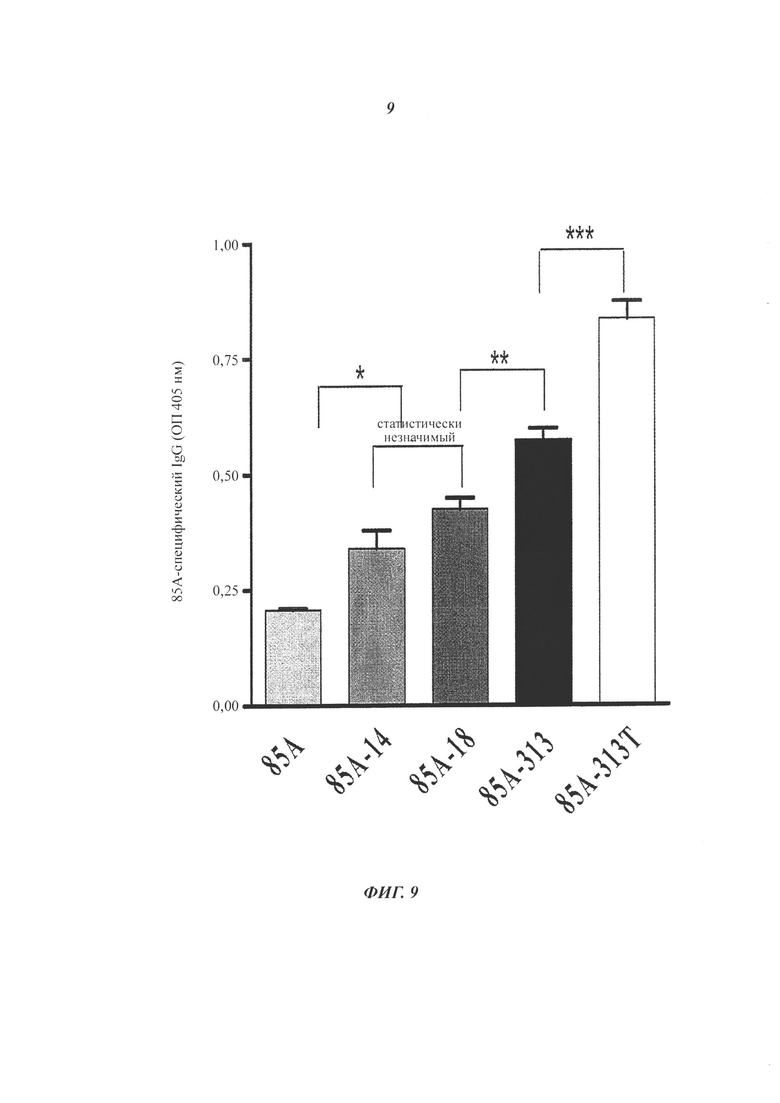
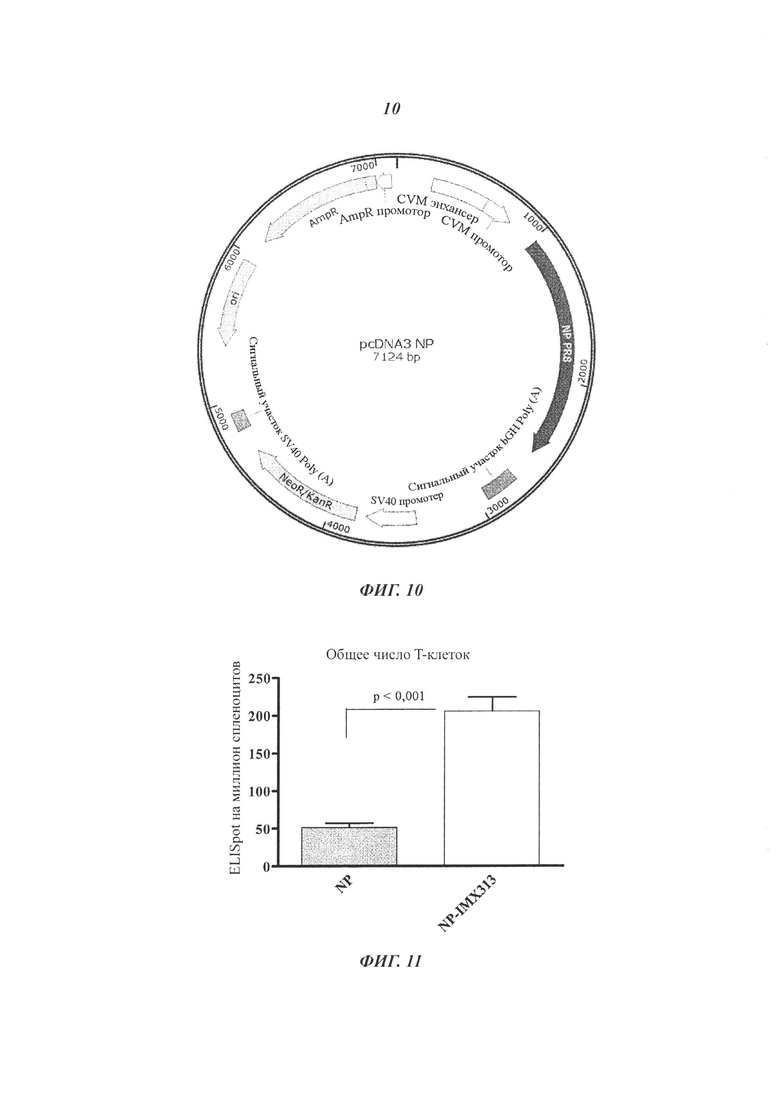
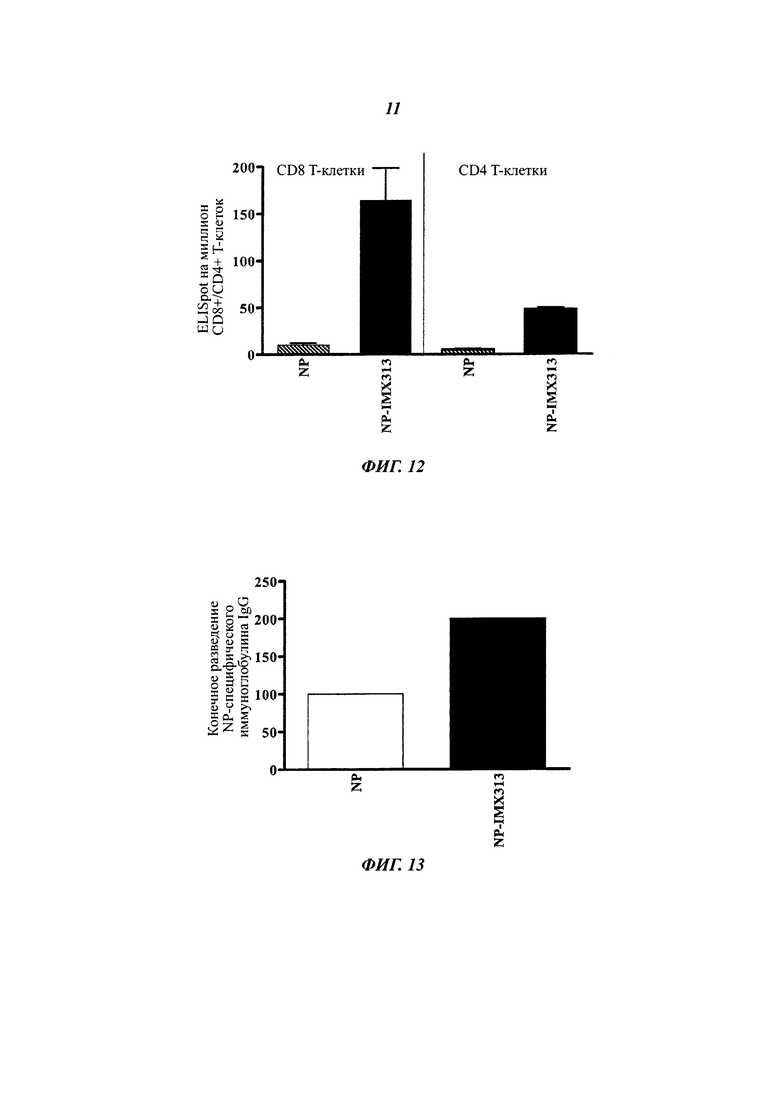
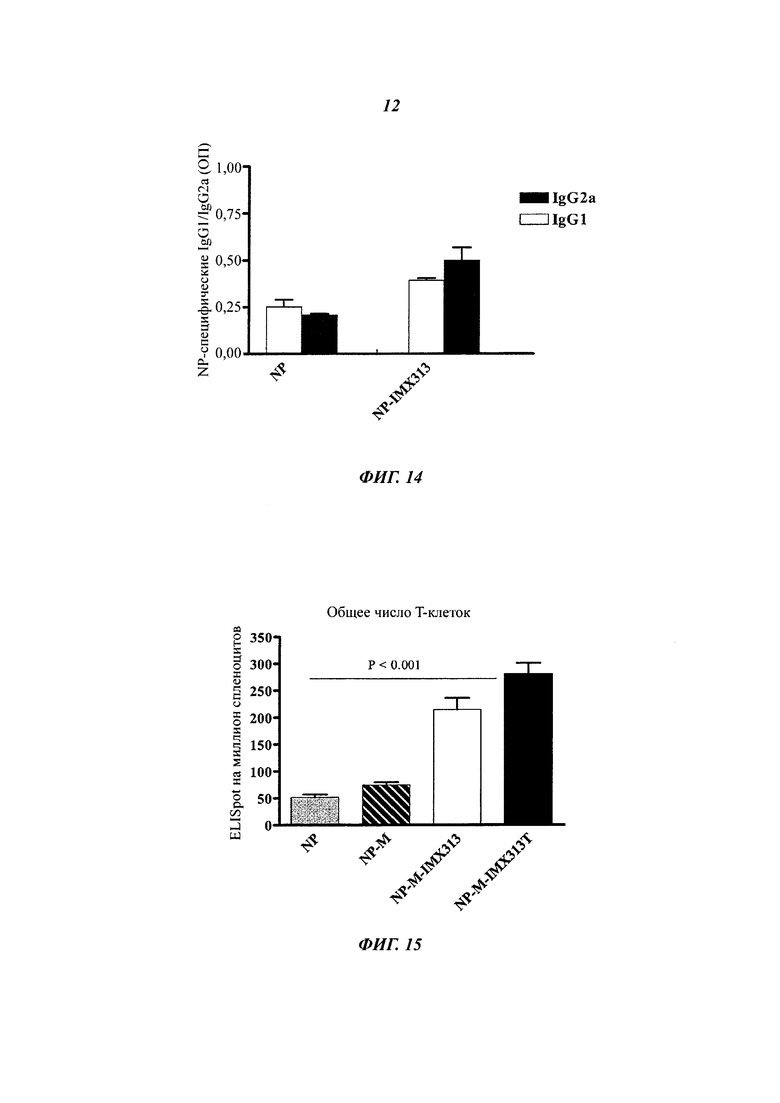
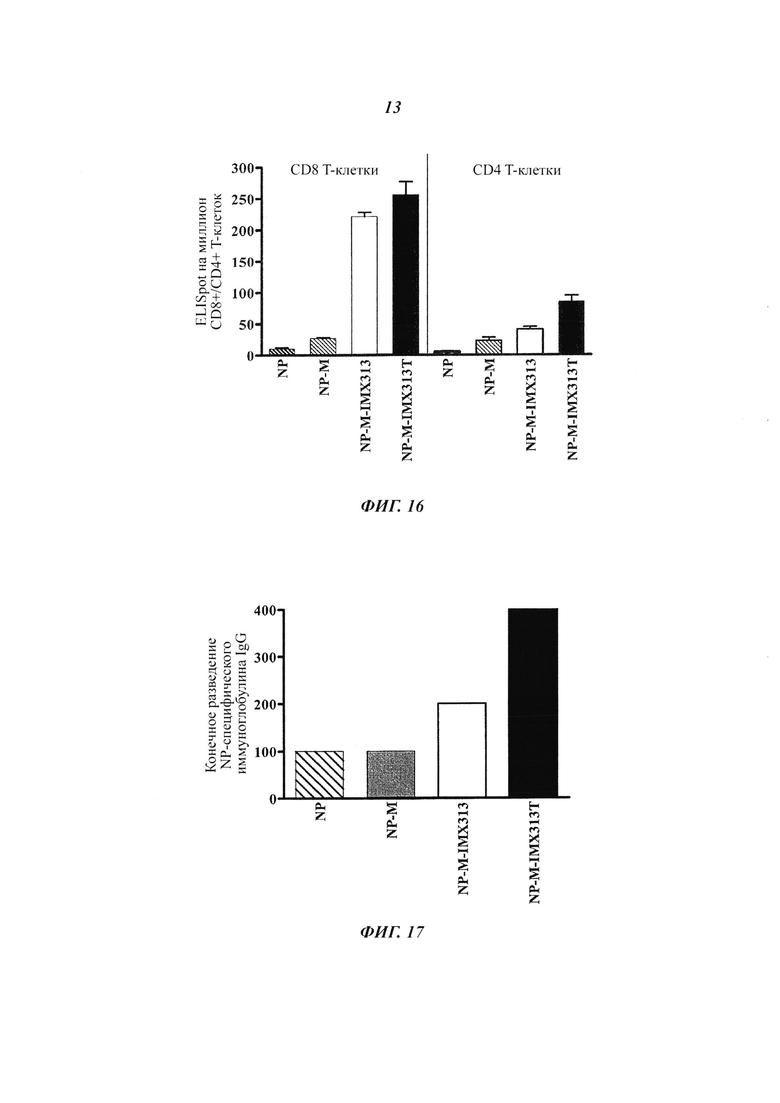

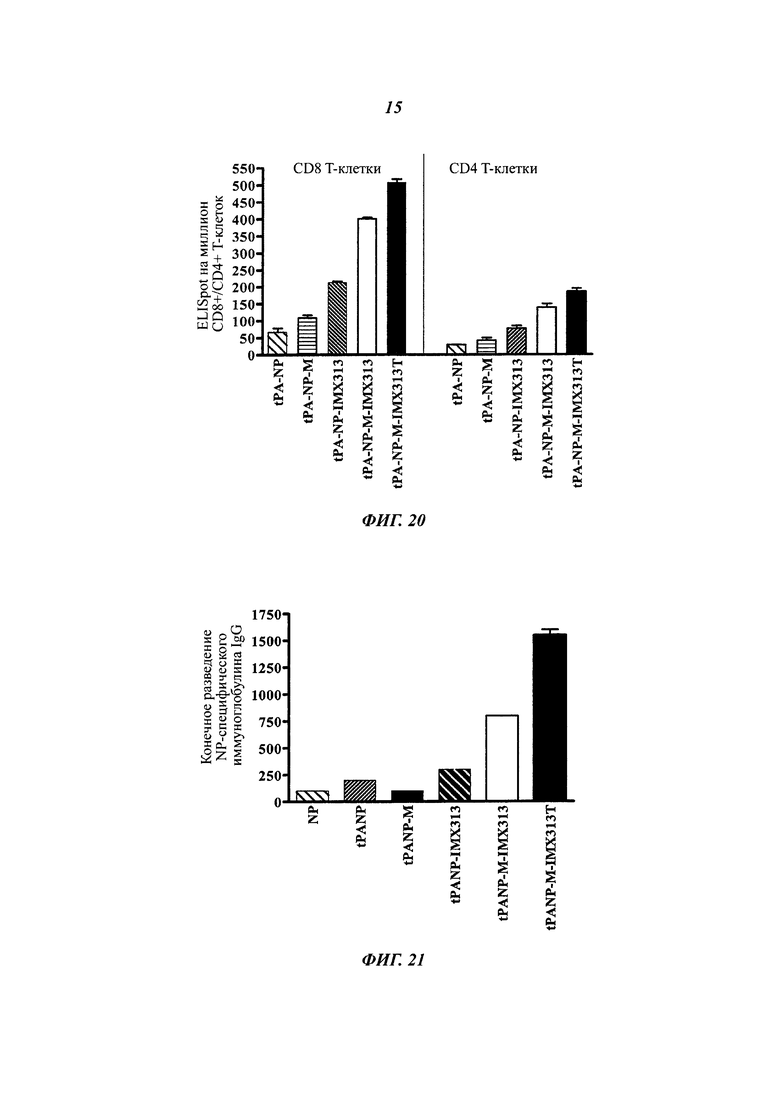
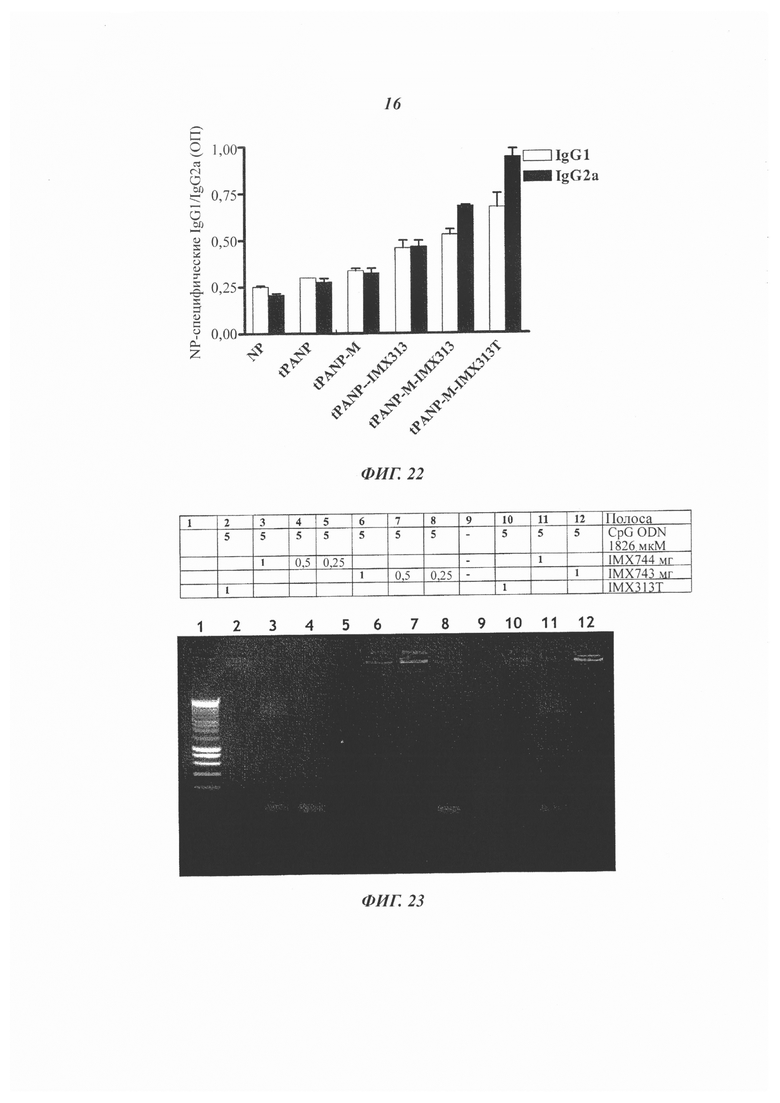
Изобретение относится к биотехнологии, в частности к иммунологии, и представляет собой иммуногенный модифицированный белок, содержащий (i) белок, имеющий суперспиральный домен, и (ii), по меньшей мере, один положительно заряженный пептид, связанный с С-концом или N-концом суперспирального домена, где указанный модифицированный белок имеет последовательность, как показано в SEQ ID NO: 42 (IMX313P), или имеет последовательность, как показано в SEQ ID NO: 7. Изобретение относится также к иммуногенному модифицированному белку, который является белком, имеющим тримерный суперспиральный домен, непосредственно связанный с последовательностью SEQ ID NO: 37 (SPRRRRRRRRRS), причем белок имеет последовательность, как показано в SEQ ID NO: 61. Модифицированные белки имеют повышенное сродство к отрицательно заряженным полимерам, таким как нуклеиновые кислоты или гепарин, и проявляют повышенную иммуногенность. 5 н. и 3 з.п. ф-лы, 23 ил., 8 табл., 19 пр.
1. Иммуногенный модифицированный белок, содержащий (i) белок, имеющий суперспиральный домен, и (ii), по меньшей мере, один положительно заряженный пептид, связанный с С-концом или N-концом суперспирального домена, где указанный модифицированный белок имеет последовательность, как показано в SEQ ID NO: 42 (IMX313P), или имеет последовательность, как показано в SEQ ID NO: 7 (IMX313T).
2. Иммуногенный модифицированный белок, который является белком, имеющим тримерный суперспиральный домен, непосредственно связанный с последовательностью SEQ ID NO: 37 (SPRRRRRRRRRS), причем белок имеет последовательность, как показано в SEQ ID NO: 61.
3. Иммуногенный слитый белок, включающий иммуногенный модифицированный белок по п. 1 или 2 и один или более антигенов.
4. Иммуногенный слитый белок по п. 3 для применения при производстве вакцины.
5. Иммуногенная композиция, содержащая эффективное количество иммуногенного модифицированного белка по п. 1 или 2 и лиганды внутриклеточных ТПР на основе нуклеиновых кислот.
6. Иммуногенная композиция по п. 5 для применения при производстве вакцины.
7. Иммуногенная композиция, содержащая эффективное количество слитого белка по п. 3 или 4 и лиганды внутриклеточных ТПР на основе нуклеиновых кислот.
8. Иммуногенная композиция по п. 7 для применения при производстве вакцины.
| A | |||
| J | |||
| SPENCER et al., FUSION OF THE MYCOBACTERIUM TUBERCULOSIS ANTIGEN 85A TO AN OLIGOMERIZATION DOMAIN ENHANCES ITS IMMUNOGENICITY IN BOTH MICE AND NON-HUMAN PRIMATES, PLOS ONE, 2012, vol | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Пружинный затвор для букс с отъемной нижней частью | 1933 |
|
SU33555A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| R | |||
| RICCO et al., HEPATITIS B VIRUS AND HOMO SAPIENS PROTEOMEWIDE ANALYSIS: A PROFUSION OF VIRAL PEPTIDE OVERLAPS IN NEURON-SPECIFIC HUMAN RPOTEINS, BIOLOGICS: TARGETS & THERAPY, 2010:4, p | |||
| Фальцовая черепица | 0 |
|
SU75A1 |
| J | |||
| C | |||
| SMITH et al, CHEMICAL SYNTHESIS AND CLONING OF A POLY(ARGININE)-CODING GENE FRAGMENT DESIGNED TO AID POLYPEPTIDE PURIFICATION, GENE, 1984, vol | |||
| Способ образования коричневых окрасок на волокне из кашу кубической и подобных производных кашевого ряда | 1922 |
|
SU32A1 |
| Плуг для снега | 1924 |
|
SU1165A1 |
| Обогреваемый отработавшими газами карбюратор для двигателей внутреннего горения | 1921 |
|
SU321A1 |
| WO 2004070012 A2, 19.08.2004 | |||
| G | |||
| DATTA et al., THE RECEPTOR BINDING DOMAIN OF APOLIPOPROTEIN E, LINKED TO A MODEL CLASS A AMPHIPATHIC HELIX, ENHANCES INTERNALIZATION AND DEGRADATION OF LDL BY FIBROBLASTS, BIOCHEMISTRY 2000, vol | |||
| Машина для изготовления проволочных гвоздей | 1922 |
|
SU39A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кулиса для фотографических трансформаторов и увеличительных аппаратов | 1921 |
|
SU213A1 |
| С | |||
| Ю | |||
| БЕЛИЦКАЯ и др., КОНСТРУИРОВАНИЕ ХИМЕРНЫХ БЕЛКОВ НА ОСНОВЕ ПЕНТАМЕРНОГО СУПЕРСПИРАЛЬНОГО ФРАГМЕНТА СОМР: II | |||
| СВОЙСТВА ГИБРИДА, СОДЕРЖАЩЕГО АНТИГЕН VNTR (MUC1) ОПУХОЛЕЙ ЧЕЛОВЕКА, БИООРГАНИЧЕСКАЯ ХИМИЯ, 2004, т | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
Авторы
Даты
2019-01-21—Публикация
2013-12-11—Подача