Область техники
Изобретение относится к генной инженерии и может быть использовано в биотехнологии, медицине и сельском хозяйстве для создания препаратов генной терапии. То есть, созданный генотерапевтический ДНК-вектор с целевым геном может быть использован для введения в клетки организма животных и человека, характеризующихся сниженной или недостаточной экспрессией данного гена, обеспечивая таким образом достижение терапевтического эффекта.
Уровень техники
Генная терапия - это современный медицинский подход, направленный на лечение наследственных и приобретенных заболеваний путем введения нового генетического материала в клетки пациента с целью компенсации или подавления функции мутантного гена и/или исправления генетического дефекта.
Переносчики генетического материала (генотерапевтические векторы) разделяют на вирусные и невирусные. В качестве вирусных векторов с успехом применяют ретровирусы, лентивирусы, аденоассоциированный вирус, герпесвирусы, поксвирусы и аденовирусы (Lukashev AN, Zamyatnin АА Jr. Viral Vectors for Gene Therapy: Current State and Clinical Perspectives. Biochemistry (Mosc). 2016. 81: 700-708.). В невирусной доставке генетического материала лидируют плазмидные векторы, несущие терапевтический ген в комплексе с различными носителями -липидами, катионными полимерами, дендримерами, полипептидами, наночастицами (Mintzer MA, Simanek ЕЕ. Nonviral vectors for gene delivery. Chem Rev. 2009. 109: 259-302).
Несмотря на то, что вирус, в силу своей природы, является почти идеальным агентом по скорости и эффективности доставки рекомбинантной ДНК в клетку, существуют практические ограничения для широкого использования вирусной системы доставки. Это трудности, связанные с промышленным производством, отсутствием селективности, возникновением иммунного ответа, потенциальной угрозой канцерогенеза, а также воспалением, возникающим после трансдукции клеток. Часть этих проблем остается до сих пор нерешенной. Поэтому в последнее время в генной терапии все большее внимание уделяется разработке невирусных систем доставки генетического материала.
Плазмидный вектор - автономно реплицирующаяся внехромосомная кольцевая ДНК. Плазмидные векторы могут иметь в своем составе гены устойчивости к антибиотикам, ионам тяжелых металлов, а также гены, контролирующие катаболизм некоторых органических соединений (Lipps G. (editor). (2008). Plasmids: Current Research and Future Trends. Caister Academic Press. ISBN 978-1-904455-35-6). Плазмидные вектора - своего рода мобильные генетические элементы, могут передаваться от одной бактериальной клетки к другой путем конъюгации, являясь средством горизонтального переноса генов.
Плазмидные векторы лишены недостатков, присущих вирусным векторам. В клетке-мишени они существуют в эписомальной форме, не интегрируясь в геном, производство их достаточно дешево, отсутствие иммунного ответа и побочных реакций на введение плазмидного вектора делают их удобным инструментом генетической терапии (перенос терапевтических генов) и генетической профилактики (ДНК-вакцины) (Li L, Petrovsky N. Molecular mechanisms for enhanced DNA vaccine immunogenicity. Expert Rev Vaccines. 2016; 15 (3): 313-29).
Помимо того, что плазмидные векторы являются весьма перспективным средством доставки в генетической терапии, уже долгое время они служат важным инструментом в молекулярно-биологических и биотехнологических научных лабораториях и с успехом применяются в области молекулярного клонирования и получения рекомбинантных белков (Russell, David W.; Sambrook, Joseph (2001), Molecular cloning: a laboratory manual. Cold Spring Harbor, N.Y; Cold Spring Harbor Laboratory)
Несмотря на очевидную перспективность для генной терапии, критическим ограничением для использования плазмидных векторов в качестве терапевтических средств является наличие в их составе: i) генов устойчивости к антибиотикам для наработки в штаммах-носителях, ii) различных регуляторных элементов, представленных последовательностями вирусных геномов. Еще одним ограничением является размер терапевтического плазмидного вектора, определяющий эффективность проникновения вектора в клетку-мишень.
Как известно, на протяжении последних лет во всем мире отмечается значительный рост устойчивости возбудителей инфекционных заболеваний к антимикробным препаратам. Возникновение антимикробной резистентности является естественным биологическим ответом на использование антибиотиков, которые создают селективное давление, способствующее отбору, выживанию и размножению резистентных штаммов микроорганизмов. Резистентность к антибиотикам имеет большое социально-экономическое значение и рассматривается как угроза национальной безопасности (MacPherson D.W., Gushulak B.D., Baine W.B., Bala S., Gubbins P.O., Holtom P., Segarra-Newnham M. 2009. Population mobility, globalization, and antimicrobial drug resistance. Emerg Infect Dis 15: 1727-1732). Именно с помощью плазмидных векторов обеспечивается механизм горизонтального переноса генов, в том числе и антибиотикорезистентности, внутри популяции микроорганизмов, что обеспечивает им селективное преимущество. Таким образом, с горизонтальным переносом генов связывают распространение устойчивых к современным антибиотикам возбудителей инфекционных заболеваний человека (Ramirez MS, Traglia GM, Lin DL, Tran T, Tolmasky ME. Plasmid-Mediated Antibiotic Resistance and Virulence in Gram-Negatives: the Klebsiella pneumoniae Paradigm. Microbiol Spectr. 2014 (5).
В связи с этим, Европейское агентство по лекарственным средствам считает необходимым избегать введения маркеров антибиотикорезистентности в разрабатываемые плазмидные векторы для генной терапии (Reflection paper on design modifications of gene therapy medicinal products during development / 14 December 2011 EMA/CAT/GTWP/44236/2009 Committee for advanced therapies).
Другим существенным ограничением использования терапевтических плазмидных векторов является наличие в их составе регуляторных элементов для повышения экспрессии целевых генов (промоторы, энхансеры, посттрансляционные регуляторные элементы), которые в большинстве случаев представляют собой нуклеотидные последовательности геномов различных вирусов (Draft Guideline on the quality, non-clinical and clinical aspects of gene therapy medicinal products, http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_quid_eline/2015/05/WC500187020.pdf).
Еще одним недостатком существующих плазмидных векторов для генетической терапии является их размер (длина). Известно, что чем больше длина плазмидного вектора, тем менее эффективно он проникает в клетку-мишень. Существующие плазмидные векторы зачастую перегружены нефункциональными участками, серьезно увеличивающими размер вектора (Mairhofer J, Grabherr R. Rational vector design for efficient non-viral gene delivery: challenges facing the use of plasmid DNA. Mol Biotechnol. 2008. 39 (2): 97-104).
Известен способ накопления плазмидных векторов в штаммах Escherichia coli без использования антибиотиков (Cranenburgh RM, Hanak JA, Williams SG, Sherratt DJ. Escherichia coli strains that allow antibiotic-free plasmid selection and maintenance by repressor titration. Nucleic Acids Res. 2001. 29 (5): E26). Были созданы штаммы Escherichia coli DH1lacdapD и DH1lacP2dapD, в которых ген dapD, кодирующий фермент 2,3,4,5-тетрагидропиридин-2,6-дикарбоксилат-N-сукцинилтрансферазу, участвующий в биосинтезе L-лизина, находится под контролем lac-промотора. В отсутствие индуктора IPTG (изопропил-β-D-1-тиогалактопиранозид) эти штаммы подвержены лизису. При введении мультикопийного вектора pORT, содержащего lac-оператор, индуцируется экспрессия гена dapD и, таким образом, трансформированные клоны могут быть отобраны и размножены. Однако, эти штаммы характеризуются низким уровнем трансформации и ее нестабильностью.
Известен также способ получения штаммов Escherichia coli для наработки плазмидных векторов без использования селекции с антибиотиками (Mairhofer J, Pfaffenzeller I, Merz D, Grabherr R. A novel antibiotic free plasmid selection system: advances in safe and efficient DNA therapy. Biotechnol J. 2008. 3 (1): 83-89). Выбранные бактериальные штаммы (например DG5α, JM109, MG1655) были модифицированы таким образом, что ингибитор репликации плазмидных векторов RNA I мог подавлять трансляцию генов, необходимых для жизнедеятельности бактерий (например, murA, кодирующего фермент UDP-N-ацетилглюкозамин 1-карбоксивинил-трансферазу, участвующего в биосинтезе пептидогликана клеточной стенки бактерий) путем образования дуплекса РНК/антисенс-РНК. Ген murA находился под контролем белка репрессора tetR и мог экспрессироваться только в присутствии сконструированного плазмидного вектора, несущего RNA I. Однако было обнаружено, что добавление индуктора IPTG приводило к появлению колоний Escherichia coli, не содержащих целевого плазмидного вектора. Механизм ингибирования селекции остается неизвестным.
Известен способ получения минимального по длине вектора. Была получена небольшая, имеющая суперскрученную форму молекула ДНК, лишенная всех прокариотических нуклеотидных последовательностей, содержащая только ориджин репликации и ген устойчивости к антибиотикам (так называемое «миникольцо»). Вектор был получен путем интеграза-опосредованной внутримолекулярной интеграции с использованием фага ϕС31 (Chen ZY, Не CY, Ehrhardt A, Kay MA. Minicircle DNA vectors devoid of bacterial DNA result in persistent and high-level transgene expression in vivo. Mol Ther. 2003. 8 (3): 495-500). Недостатком такого рода плазмидных векторов является трудоемкость их получения и невозможность наработки в промышленных масштабах.
Известно решение по патентной заявке US 2011152377/10, описывающей получение экспрессионного плазмидного вектора без устойчивости к антибиотику, которая содержит полинуклеотид, кодирующий белок-репрессор. Экспрессия указанного белка-репрессора регулирует экспрессию токсичного генного продукта, встроенного в участок генома E. coli. Однако, как и все методы селекции, основанные на использовании белков-репрессоров, данный метод отличается нестабильностью трансформации и ее низкой эффективностью.
Известен патент (US 9,644,211), описывающий получение минимального по размеру вектора («миникольца»). Данный вектор не содержит прокариотических последовательностей и продуцируется путем parA-опосредованной рекомбинации, проходящей в специально полученном штамме E. coli. Недостатком данного метода получения минимального по размеру вектора является невозможность его использования при масштабировании производства.
Прототипом настоящего изобретения в части использования рекомбинантных ДНК-векторов для генной терапии является способ получения рекомбинантного вектора для генетической иммунизации (US 9,550,998). Плазмидный вектор представляет собой суперскученный плазмидный ДНК-вектор и предназначен для экспрессии клонированных генов в клетках животных и человека. Вектор состоит из ориджина репликации, регуляторных элементов, включающих промотор и энхансер цитомегаловируса человека, регуляторные элементы из Т-лимфотропного вируса человека.
Накопление вектора производят в специальном штамме E. coli без использования антибиотиков за счет антисенс-комплементации гена sacB, введенного в штамм посредством бактериофага. Ограничением использования данного ДНК-вектора для генетической терапии является наличие в его составе регуляторных элементов, представляющих собой последовательности вирусных геномов.
Раскрытие изобретения
Задачей изобретения является конструирование генотерапевтического ДНК-вектора для генетической модификации клеток животных и человека, оптимально сочетающего в себе:
I) возможность безопасного использования для генетической терапии человека и животных за счет отсутствия в составе геннотерапевтического ДНК-вектора генов антибиотикорезистентности.
II) длину, обеспечивающую эффективное проникновение в клетку-мишень;
III) наличие регуляторных элементов, обеспечивающих эффективную экспрессию целевых генов и, в то же время, не представляющих собой нуклеотидные последовательности вирусных геномов;
IV) технологичность получения и возможность наработки в промышленных масштабах.
Пункт I является обязательным, и предусмотрен в данном техническом решении в соответствии с требованиями государственных регуляторов к лекарственным средствам для генной терапии, в частности, Европейского Агентства по лекарственным средствам касательно отказа от введения маркеров антибиотикорезистентности в разрабатываемые плазмидные векторы для генной терапии (Reflection paper on design modifications of gene therapy medicinal products during development / 14 December 2011 EMA/CAT/GTWP/44236/2009 Committee for advanced therapies).
Поставленная задача решается за счет того, что вначале конструируют генотерапевтический ДНК-вектор VTvaf17 размером 3165 п.н., предназначенный для генетической модификации клеток животных и человека с нуклеотидной последовательностью SEQ ID №1. При этом способ получения генотерапевтического ДНК-вектора VTvaf17 размером 3165 п.н., заключается в том, что, сначала на следующем этапе конструируют вектор размером 4182 п.н., содержащий промоторную область гена человеческого фактора элонгации EF1A с собственным энхансером размером 1188 п.н., полилинкер, имеющий сайты для эндонуклеаз рестрикции BamHI, EcoRV, SalI, HindIII, KpnI, EcoRI размером 35 п.н., терминатор транскрипции и сайт полиаденилирования гена фактора роста человека размером 466 п.н., регуляторный элемент PHK-out транспозона Tn10, обеспечивающий возможность положительной селекции без использования антибиотиков размером 136 п.н., ориджин репликации, служащий для автономной репликации с однонуклеотидной заменой для повышения копийности вектора в клетках большинства штаммов Eshcerichia coli размером 1299 п.н., ген устойчивости к канамицину размером 1010 п.н., а затем выщепляют его по сайтам рестрикции SpeI, после чего оставшийся фрагмент лигируют сам на себя. Поставленная задача решается также за счет того, что конструируют штамм Escherichia coli SCS110-AF для наработки генотерапевтического ДНК-вектора VTvaf17 или генотерапевтических ДНК-векторов на его основе с возможностью положительной селекции без использования антибиотиков. При этом способ получения штамма Escherichia coli SCS 110-AF для наработки генотерапевтического ДНК-вектора VTvaf17 или генотерапевтических ДНК-векторов на его основе, заключается в том, что конструируют линейный фрагмент ДНК, содержащий регуляторный элемент RNA-in транспозона Tn10 для селекции без применения антибиотиков размером 64 п.н., ген левансахаразы sacB, продукт которого обеспечивает селекцию на сахарозо-содержащей среде размером 1422 п.н., ген устойчивости к хлорамфениколу catR, необходимый для отбора клонов штамма, в которых прошла гомологичная рекомбинация размером 763 п.н. и две гомологичные последовательности, обеспечивающие процесс гомологичной рекомбинации в области гена recA с одновременной его инактивацией размером 329 п.н. и 233 п.н., после чего проводят трансформацию клеток Escherichia coli путем электропорации и отбирают клоны, выжившие на среде, содержащей 10 мкг/мл хлорамфеникола. Конструируют также штамм Escherichia coli SCS110-AF/VTvaf17 (регистрационный № ВКПМ В-12990, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 42801), несущий генотерапевтический ДНК-вектор VTvaf17 для его наработки с возможностью селекции без использования антибиотиков. При этом способ получения штамма Escherichia coli SCS110-AF/VTvaf17 (регистрационный № ВКПМ В-12990, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 42801), несущего генотерапевтический ДНК-вектор VTvaf17, заключается в том, что получают электрокомпетентные клетки штамма Escherichia coli SCS110-AF и проводят электропорацию этих клеток генотерапевтическим ДНК-вектором VTvaf17, после чего клетки высеивают на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола.
Изобретение поясняется чертежами.
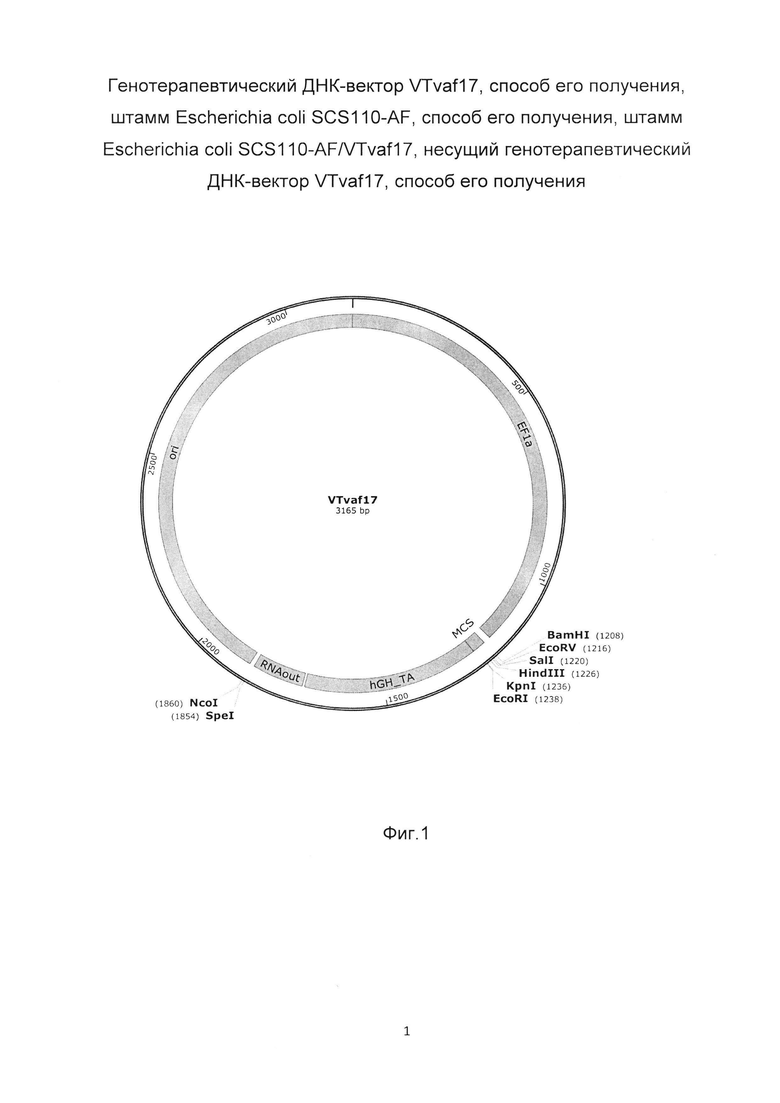
На фиг. 1 приведена схема генотерапевтического ДНК-вектора VTvaf17, который представляет собой кольцевую двуцепочечную молекулу ДНК размером 3165 п.н., способную к автономной репликации в клетках бактерии Eshcerichia coli.
На фиг. 1 отмечены следующие структурные элементы вектора:
(1) EF1a (позиция 1-1188 п.н) - промоторная область гена человеческого фактора элонгации EF1A с собственным энхансером, содержащимся в первом интроне гена. Служит для обеспечения высокого уровня транскрипции рекомбинантного гена в большинстве тканей человека.
(2) MCS (позиция 1208-1243 п.н.) - полилинкер (сайт множественного клонирования), содержащий последовательно сайты рестрикции BamHI, EcoRV, SalI, HindIII, KpnI, EcoRI и предназначенный для клонирования целевых терапевтических генов.
(3) hGH-TA (позиция 1244-1710 п.н.) - терминатор транскрипции и сайт полиаденилирования гена фактора роста человека;
(4) RNA-out (позиция 1717-1853 п.н.) - регуляторный элемент PHK-out транспозона Tn 10, обеспечивающий возможность положительной селекции без использования антибиотиков при использовании штамма Eshcerichia coli SCS 110;
(5) ori (позиция 1866-3165 п.н.) - ориджин репликации, служащий для автономной репликации с однонуклеотидной заменой для повышения копийности плазмиды в клетках большинства штаммов Eshcerichia coli.
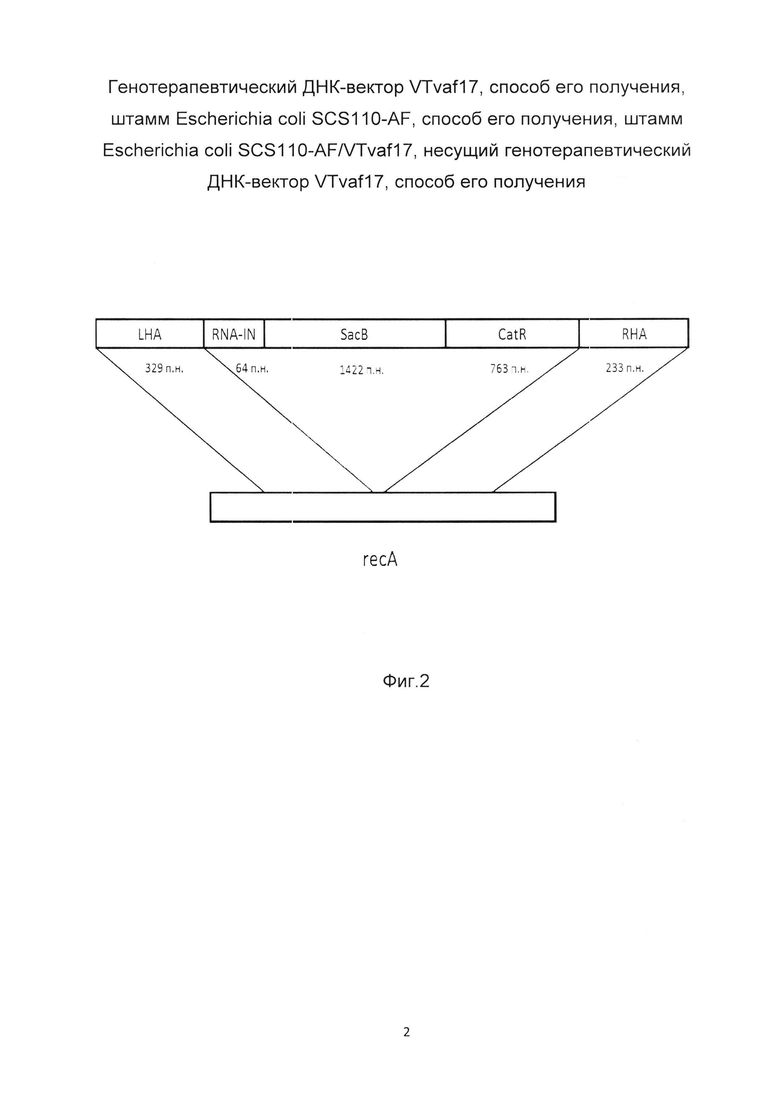
На фиг. 2 изображена структура фрагмента ДНК для гомологичной рекомбинации в области гена recA Eshcerichia coli для получения штамма Eshcerichia coli SCS 110;
линейный фрагмент состоит из кассеты, несущей в себе регуляторный элемент RNA-in транспозона Tn10 для селекции без применения антибиотиков (64 п.н.), ген левансахаразы sacB, продукт которого обеспечивает селекцию на сахарозо-содержащей среде (1422 п.н.), ген устойчивости к хлорамфениколу catR, необходимый для отбора клонов штамма, в которых прошла гомологичная рекомбинация (763 п.н.). Кассета фланкирована двумя гомологичными плечами, обеспечивающими процесс рекомбинации в области гена recA с одновременной его инактивацией (329 п.н. и 233 п.н. для левого и правого плеча, соответственно).
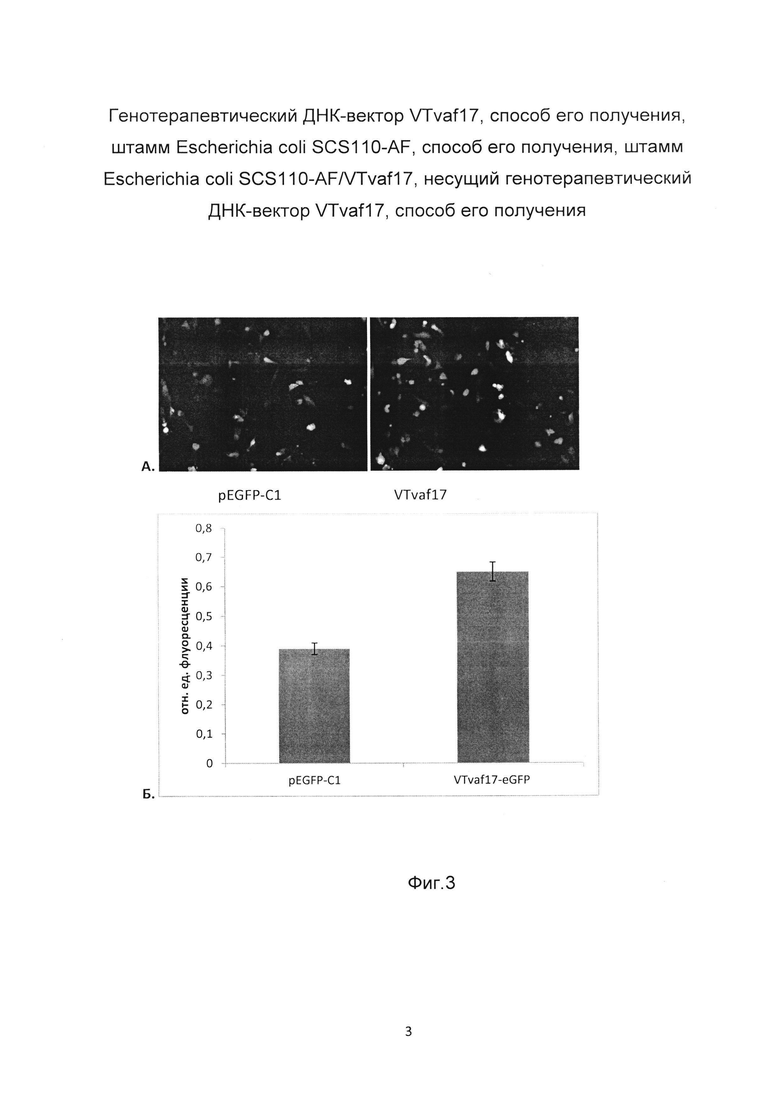
На фиг. 3 приведены микрофотографии культуры клеток НЕK-293 с использованием флуоресцентной микроскопии через 48 часов после их трансфекции плазмидным вектором pEFGP-C1 (Clontech) и ДНК-вектором VTvaf17-eGFP (А) и диаграмма уровня флуоресценции выделенного из клеток НЕK-293 белка через 48 часов после их трансфекции плазмидным вектором pEFGP-C1 (Clontech) и ДНК-вектором VTvaf17-eGFP (Б) с целью сравнения уровня накопления продукта целевого гена, например, зеленого флуоресцентного белка (GFP) в клетках НЕK-293 через 48 часов после их трансфекции плазмидным вектором pEFGP-C1 (Clontech) и ДНК-вектором VTvaf17-eGFP.
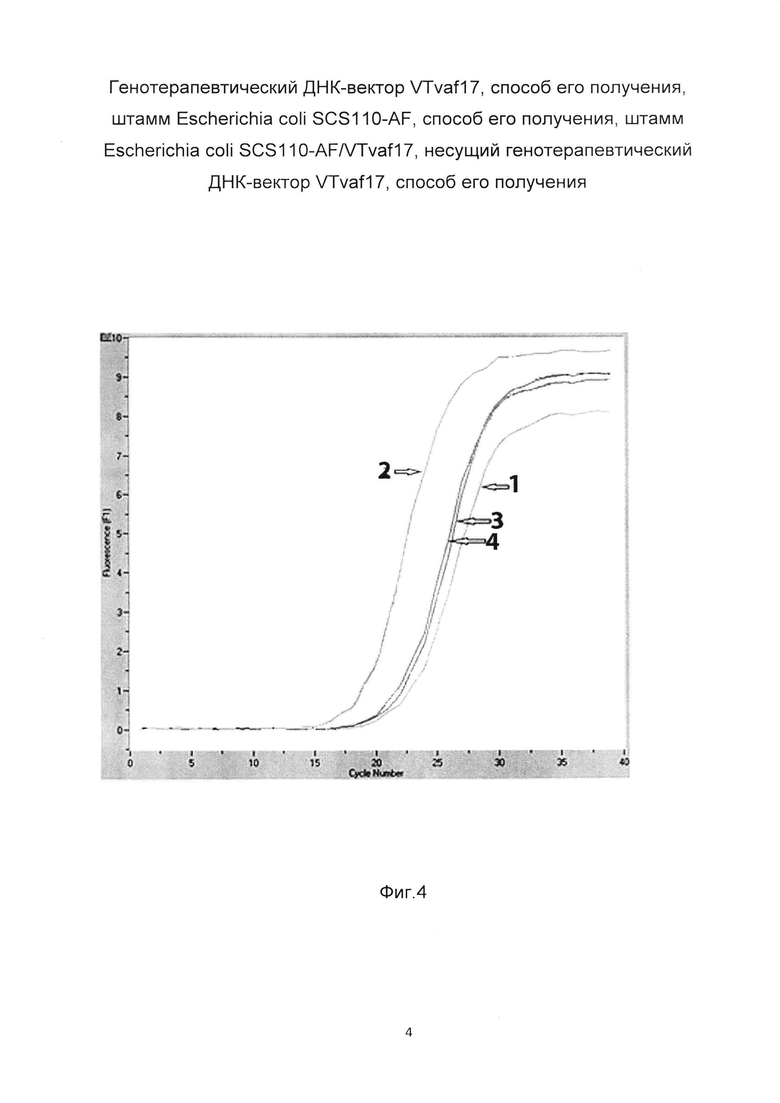
На фиг. 4 показаны графики накопления мРНК гена эластина в клетках кератиноцитов НаСаТ до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17-ELN, несущим участок, кодирующий ген эластина человека с целью оценки изменения накопления мРНК целевого гена, например, гена эластина, в клетках кератиноцитов НаСаТ до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17-ELN, несущим участок, кодирующий ген эластина человека.
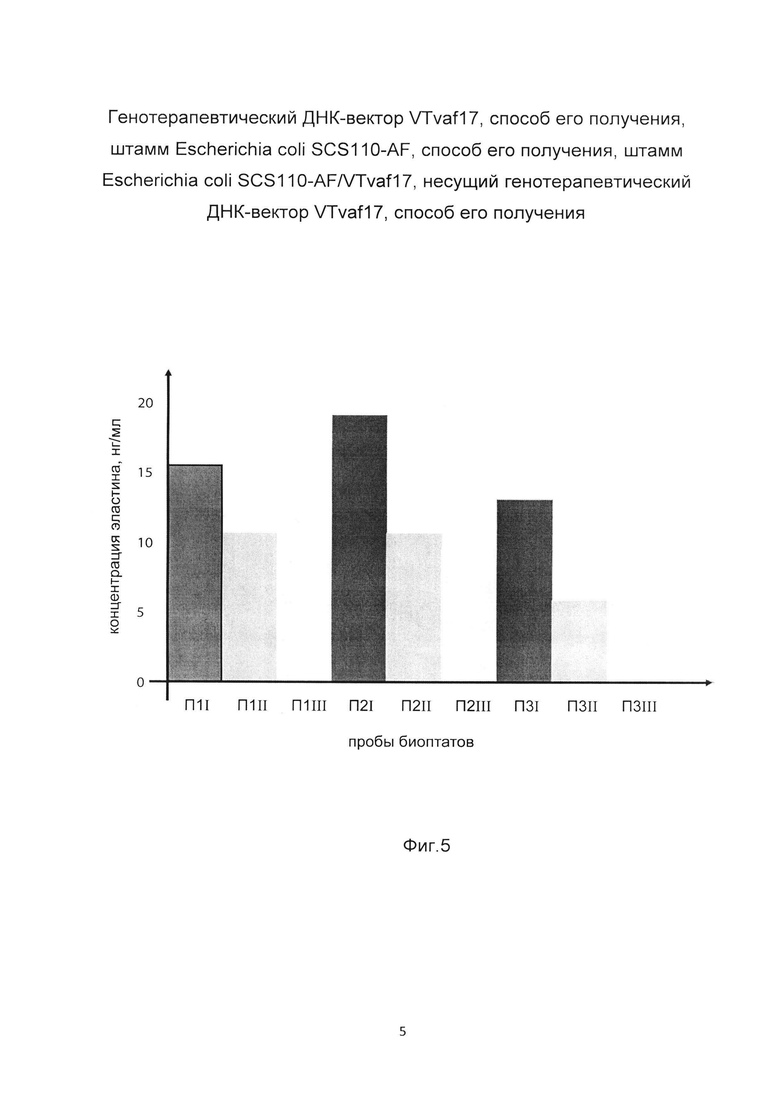
На фиг 5. показана диаграмма концентрации белка эластина в биоптатах кожи трех пациентов после введения в кожу этих пациентов генотерапевтического ДНК-вектора VTvaf17-ELN, несущего участок, кодирующий ген эластина человека для оценки изменения количества белка эластина в коже человека при введении в кожу человека генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, например, ген эластина человека.
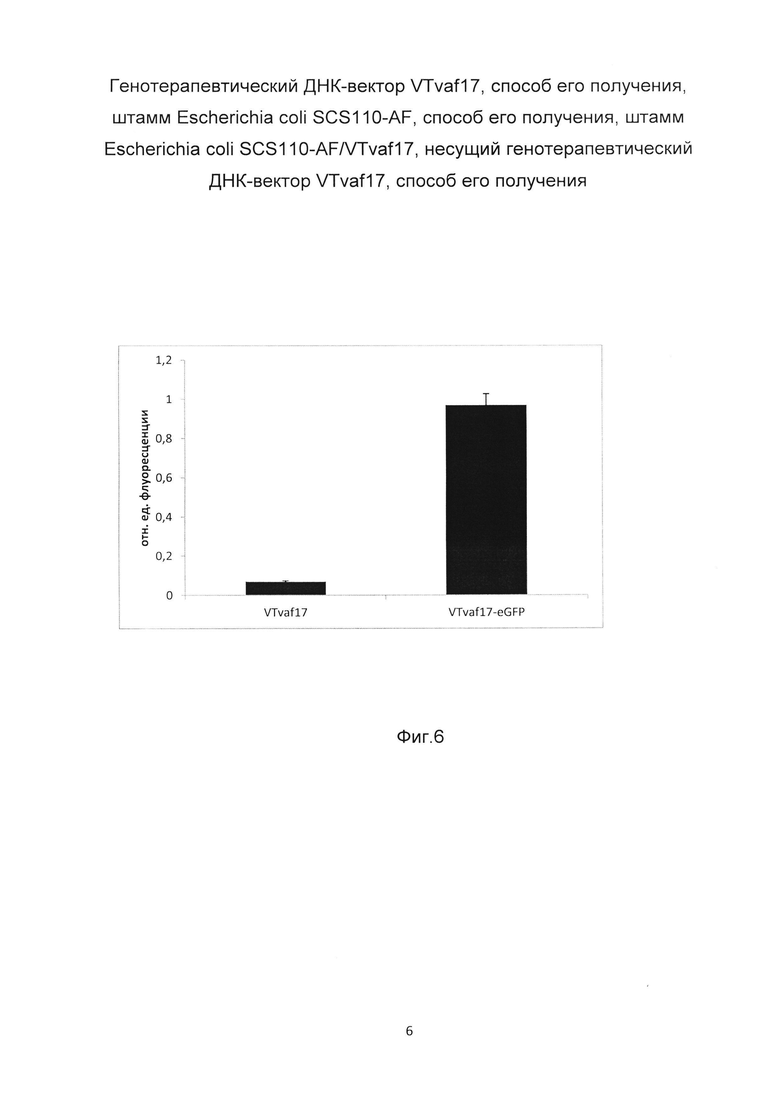
На фиг. 6 приведена диаграмма изменения количества зеленого флуоресцентного белка в клетках почки быка MDBK через 48 часов после их трансфекции ДНК-вектором VTvaf17 и ДНК-вектором VTvaf17-eGFP, несущим участок, кодирующий ген зеленого флуоресцентного белка с целью сравнения уровня накопления продукта целевого гена, например, зеленого флуоресцентного белка (GFP) в клетках почки быка MDBK через 48 часов после их трансфекции ДНК-вектором VTvaf17 и ДНК-вектором VTvaf17-eGFP, несущим участок, кодирующий ген зеленого флуоресцентного белка.
Реализация изобретения
Изобретение поясняется следующими примерами.
Пример 1
Получение генотерапевтического ДНК-вектора VTvaf17, содержащего промотор человеческого гена фактора элонгации EF1a с собственным энхансером, полилинкер, терминатор транскрипции и сигнала полиаденилирования гена фактора роста человека, регуляторный элемента PHК-out транспозона Tn10, ориджин репликации с однонуклеотидной заменой для повышения копийности плазмиды.
Генотерапевтический ДНК-вектор VTvaf17 конструировали объединением шести фрагментов ДНК, полученных из разных источников:
(а) ориджин репликации получали путем ПЦР-амплификации участка коммерческой плазмиды pBR322 с внесением точечной мутации с использованием олигонуклеотидов Ori-F, Ori-R, Ori-M1, Ori-M2 (перечень последовательностей, (1)-(4));
(б) промоторный регион EF1a получали путем ПЦР-амплификации участка геномной ДНК человека с использованием олигонуклеотидов EF1-F и EF1-R (перечень последовательностей, (5) и (6));
(в) терминатор транскрипции hGH-TA получали путем ПЦР-амплификации участка геномной ДНК человека с использованием олигонуклеотидов hGH-F и hGH-R (перечень последовательностей, (7) и (8));
(г) регуляторный участок транспозона Tn10 PHК-out получали путем синтеза из олигонуклеотидов RO-F, RO-R, RO-1, RO-2, RO-3 (перечень последовательностей, (9)-(13));
(д) ген устойчивости к канамицину получали путем ПЦР-амплификации участка коммерческой плазмиды рЕТ-28 человека с использованием олигонуклеотидов Kan-F и Kan-R (перечень последовательностей, (14) и (15));
(е) полилинкер получали отжигом двух синтетических олигонуклеотидов MCS1, MCS2 (перечень последовательностей, (15) и (16)).
ПЦР-амплификацию проводили с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs) в соответствии с инструкцией производителя. Фрагменты имеют перекрывающиеся области для возможности их объединения с последующей ПЦР-амплификацией. Объединяли фрагменты (а) и (б) с использованием олигонуклеотидов Ori-F и EF1-R (перечень последовательностей, (1) и (6)) а так же фрагменты (в), (г) и (д) с использованием олигонуклеотидов hGH-F и Kan-R (перечень последовательностей, (7) и (15)). Далее, полученные участки объединяли путем рестрикции с последующим лигированием по сайтам BamHI и NcoI. В результате получали плазмиду, пока еще не содержащую полилинкер. Для его введения проводили расщепление плазмиды по сайтам BamHI и EcoRI и лигирование с фрагментом (е). Таким образом, получали вектор размером 4182 п.н., несущий ген устойчивости к канамицину, который фланкирован сайтами рестрикции SpeI. Далее этот участок выщепляли по сайтам рестрикции SpeI, после чего оставшийся фрагмент лигировали сам на себя. Таким образом, получали генотерапевтический ДНК-вектор VTvaf17 размером 3165 п.н., который является рекомбинантным, с возможностью селекции без антибиотиков (SEQ ID №1).
Пример 2
Для подтверждения эффективности ДНК-вектора VTvaf17 клонировали в полилинкер целевой ген, например, ген зеленого флуоресцирующего белка (GFP).
Получение генотерапевтического ДНК-вектора VTvaf17-eGFP, несущего участок, кодирующий целевой ген, например, ген, кодирующий зеленый флуоресцирующий белок (GFP). Кодирующую часть гена зеленого флуоресцентного белка получали путем ПЦР-амплификации коммерческой плазмиды pEGFP-C1 (Clontech) с использованием олигонуклеотидов MVGFP-F и MVGFP-R (перечень последовательностей, (30) и (31)). Полученный ПЦР-фрагмент расщепляли эндонуклеазами рестрикции BamHI и EcoRI и лигировали с ДНК-вектором размером 4182 п.н., несущим ген устойчивости к канамицину, расщепленным теми же ферментами. Далее, из полученного вектора удаляли ген устойчивости к канамицину, как это описано в примере 1. В результате получали ДНК-вектор VTvaf17-eGFP размером 3874 п.о. с возможностью селекции без антибиотиков
Пример 3
Для подтверждения эффективности ДНК-вектора VTvaf17 клонировали в полилинкер целевой ген, например, ген кодирующий эластин человека.
Получение ДНК-вектора VTvaf17-ELN, несущего участок, кодирующий целевой ген, например, ген, кодирующий эластин человека. Кодирующую часть гена эластина (SEQ ID №2) размером 2175 п.о. получали путем выделения суммарной РНК из биопсийного образца кожи пациента с последующим проведением реакции обратной транскрипции и ПЦР-амплификации. Взятие биопсии осуществляли из участков интактной кожи в области предплечья, используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL). Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составил около 2×2×2 мм, масса - до 20 мг. Образец помещали в 1 мл Trizol Reagent (ThermoFisher Scientific) и гомогенизировали с последующим прогреванием в течении 5 мин при 65°C. Далее образец центрифугировали при 14000 g в течении 10 мин и снова прогревали в течении 10 мин при 65°C. Далее добавляли 200 мкл хлороформа, плавно перемешивали и центрифугировали при 14000 g в течении 10 мин. Затем отбирали водную фазу, добавляли к ней 1/10 объема 3М ацетата натрия pH 5.2 и равный объем изопропилового спирта. Инкубировали образец при -20°C в течении 10 мин с последующим центрифугированием при 14000 g в течении 10 мин. Осадок промывали 1 мл 70% этилового спирта, высушивали на воздухе и растворяли в 10 мкл воды, свободной от РНКаз. Для получения первой цепи кДНК гена эластина человека использовали обратную транскриптазу Mint (Евроген, Россия). К 6 мкл суммарной РНК добавляли 4 мкл буфера Mint, 2 мкл дитиотреитола и 2 мкл смеси dNTP, по 2 мкл олигонуклеотидов ELN-F и ELN-R (перечень последовательностей, (32) и (33)), 2 мкл ревертазы Mint и инкубируют при 42°C в течении 2 часов. Полученную кДНК использовали как матрицу при ПЦР-амплификации с использованием олигонуклеотидов ELN-F и ELN-R (перечень последовательностей, (32) и (33)) при условиях 94°C - 3 мин; 30 циклов: 94°C - 20 сек, 60°C - 20 сек и 72°C - 60 сек, с финальной элонгацией 72°C - 5 мин. Полученный ПЦР-фрагмент расщепляли эндонуклеазами рестрикции BamHI и EcoRI и лигировали с вектором размером 4182 п.н., несущим ген устойчивости к канамицину, расщепленный теми же ферментами. Далее, из полученного вектора удаляли ген устойчивости к канамицину, как это описано в примере 1. В результате получали генотерапевтический ДНК-вектор VTvaf17-ELN несущий участок, кодирующий ген эластина, размером 5322 п.о. с возможностью селекции без антибиотиков.
Пример 4
Получение штамма Escherichia coli SCS 110-AF для продукции генотерапевтического ДНК-вектора VTvaf17 - и генотерапевтических векторов на его основе.
Штамм Escherichia coli SCS 110-AF для продукции генотерапевтического ДНК-вектора VTvaf17 и генотерапевтических векторов на его основе получали методом гомологичной рекомбинации путем введения в его хромосому в область гена recA линейного фрагмента, содержащего регуляторный элемент RNA-in транспозона Tn10 для селекции без применения антибиотиков (64 п.н.), ген левансахаразы sacB, продукт которого обеспечивает селекцию на сахарозо-содержащей среде (1422 п.н.), ген устойчивости к хлорамфениколу catR, необходимый для отбора клонов штамма, в которых прошла гомологичная рекомбинация (763 п.н.) и две гомологичные последовательности (плечи гомологии), обеспечивающих процесс гомологичной рекомбинации в области гена recA с одновременной его инактивацией (329 п.н. и 233 п.н. для левого и правого плеча, соответственно).
Для получения левого и правого плеч гомологии проводили ПЦР амплификацию фрагментов гена recA с использованием геномной ДНК Eshcerichia coli SCS 110 (Agilent Technologies) в качестве матрицы. Для получения левого плеча гомологии использовали праймеры LHA-F и LHA-R (перечень последовательностей, (18) и (19)), для получения правого плеча гомологии используют праймеры RHA-F и RHA-R (перечень последовательностей, (28) и (29)). Фрагмент RNA-in достраивали из синтетических олигонуклеотидов IN-F, IN-1, IN-2, IN-R (перечень последовательностей, (20), (21), (22), (23)). Ген sacB получали ПЦР-амплификацией с использованием геномной ДНК B.subtilis 168НТ в качестве матрицы и SacB-F и SacB-R в качестве праймеров (перечень последовательностей, (24) и (25)). Для получения гена catR проводли ПЦР-амплификацию с использованием штамма Eshcerichia coli BL21 pLysS в качестве матрицы и CatR-F и CatR-R (перечень последовательностей, (26) и (27)) в качестве праймеров. ПЦР продукты LHA (левое плечо гомологии), SacB, RHA (правое плечо) амплифицировали при условиях 94°C - 3 мин; 30 циклов: 94°C - 20 сек, 60°C - 20 сек и 72°C - 60 сек, с финальной элонгацией 72°C - 5 мин. ПЦР продукт RNA-in получали при условиях 94°C - 3 мин; 30 циклов: 94°C - 10 сек, 60°C - 10 сек и 72°C - 10 сек использованием IN-F, IN-1, IN-2, IN-R олигонуклеотидов (перечень последовательностей, (20), (21), (22), (23)) для сборки фрагмента, при этом использовали 10 мкМ праймеров IN-F и IN-R, и 5 мкМ праймеров IN-1 и IN-2. ПЦР-амплификацию проводили с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (Thermo Fisher Scientific) в соответствии с инструкцией производителя.
Линейный фрагмент для гомологичной рекомбинации получали путем объединения пяти продуктов ПЦР амплификации. Все пять продуктов имели перекрывающиеся области для дальнейшей сборки в единый фрагмент. Все фрагменты смешивали в количестве 10 нг в объеме 50 мкл. ПЦР продукт получали при условиях 94°C - 3 мин; 10 циклов: 94°C - 30 сек, 60°C - 30 сек и 72°C - 2 мин без добавления праймеров, затем добавляли праймеры LHA-F, RHA-R (перечень последовательностей, (18), (19)), после чего проводили дополнительно 25 циклов ПЦР: 94°C - 30 сек, 60°C - 30 сек и 72°C - 2 мин с финальной элонгацией 72°C - 5 мин. В результате получали ПЦР фрагмент длиной 2811 п.н. следующей структуры: LHA-RNA-IN-SacB-CatR-RHA. Данный фрагмент выделяли препаративно из агарозного геля с помощью набора для элюции ДНК из агарозного геля (BioSilica, Россия) согласно рекомендациям производителя.
Для получения штамма Escherichia coli SCS 110-AF готовили элетрокомпетентные клетки. Для этого, одиночной колонией штамма Eshcerichia coli SCS 110 (Agilent Technologies) заражали 10 мл среды LB и культивируют ночь в орбитальном шейкере при 150 об/мин и 37°C. На следующий день пересеивали 1/20 в 100 мл среды LB и культивировали в орбитальном шейкере при 150 об/мин и 37°C до достижения OD600=0,5. По достижении необходимой оптической плотности, клетки охлаждали до 0°C и центрифугировали 10 мин при 4000 g. Далее, удаляли среду, клетки отмывали от остатков среды охлажденной во льду 100 мл бидистилированной водой дважды, затем промывали 20 мл 10% глицерина. После этого, клетки ресуспендировали в 1 мл 10% глицерина и использовали для трансформации.
Трансформацию полученным линейным фрагментом проводили методом электропорации в кюветах 1 мм при 2 кВ, 200 Ом, 25 мкФ на приборе Gene Pulser Xcell (Bio-Rad, США). Время импульса составло от 4,9 до 5,1 мсек. После чего клетки культивировали в течение 2,5 часов в среде SOC в шейкере-инкубаторе при 30°C. Затем, клетки высеивали на чашки Петри с агаризованной средой LB, содержащей 10 мкг/мл хлорамфеникола. Клетки культивировали 48 часов при 30°C. Отобранные клоны проверяли на выживаемость на селективной среде, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола. Полученный штамм имеет генотип recA rpsL (Strr) thr leu endA thi-1 lacY galK galT ara tonA tsx dam dcm supE44 Δ(lac-proAB) [F' traD36 proAB laclq ZΔM15]ChmR sacB+
Пример 5
Получение штамма Escherichia coli SCS110-AF/VTvaf 17 (регистрационный № ВКПМ B-12990, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 42801), несущего генотерапевтический ДНК-вектор VTvaf17 для его наработки.
Для приготовления электрокомпетентных клеток штамма Escherichia coli SCS 110-AF, одиночной колонией заражали 10 мл среды LB и культивировали ночь в орбитальном шейкере при 150 об/мин и 37°C. На следующий день пересеивали 1/20 в 100 мл среды LB и культивировали в орбитальном шейкере при 150 об/мин и 37°C до достижения OD600=0,5. По достижении необходимой оптической плотности, клетки охлаждали до 0°C и центрифугировали 10 мин при 4000 g. Далее, удаляли среду, клетки отмывали от остатков среды охлажденной во льду 100 мл бидистилированной водой дважды, затем промывали 20 мл 10% глицерина. После этого, клетки ресуспендировали в 1 мл 10% глицерина и использовали для трансформации методом электропорации. Электропорацию проводли в кюветах 1 мм при 2 кВ, 200 Ом, 25 мкФ на приборе Gene Pulser Xcell (Bio-Rad, США). Время импульса составляло от 4,9 до 5,1 мсек, с использованием 1-10 нг вектора. После чего клетки культивировали в течение 2,5 часов в среде SOC в шейкере-инкубаторе при 30°C. Затем, клетки высеивали на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола. Таким образом получали штамм Escherichia coli SCS110-AF/VTvaf17 (регистрационный № ВКПМ В-12990, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 42801), несущий генотерапевтический ДНК-вектор VTvaf17. Через 48 часов одиночной колонией заражали 10 мл жидкой селективной среды, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола, и культивировали ночь в орбитальном шейкере при 150 об/мин и 37°C. На следующий день клетки осаждали центрифугированием и выделяли ДНК-вектор методом щелочного лизиса с помощью набора Gene JET Plasmid Miniprep Kit (Thermo Fisher Scientific) согласно рекомендациям производителя.
Пример 6
Для подтверждения эффективности генотерапевтический ДНК-вектора VTvaf17 клонируют в полилинкер целевой ген, например, ген кодирующий зеленого флуоресцентного белка (GFP)
Сравнение уровня накопления продукта целевого гена, например, зеленого флуоресцентного белка (GFP) в клетках НЕK-293 через 48 часов после их трансфекции плазмидным вектором pEFGP-C1 (Clontech) и генотерапевтическим ДНК-вектором VTvaf17-eGFP.
Для оценки уровня накопления зеленого флуоресцентного белка GFP в клетках НЕK-293 (клетки почки эмбриона человека, трансформированные ДНК аденовируса типа 5, АТСС CRL-1573) проводили их трансфекцию плазмидным вектором pEFGP-C1 (Clontech) и генотерапевтическим ДНК-вектором VTvaf17-eGFP.
Клетки выращивали в среде DMEM (ThermoFisher Scientific, США), содержащей 10% сыворотки эмбрионов коров (ThermoFisher Scientific, США), 4,5 г/л глюкозы и 10 мкг/мл гентамицина в атмосфере 5% CO2 при 37°C. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 4*104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). В пробирке №1 к 25 мкл среды Opti-MEM (Gibco) добавляли 1 мкл раствора плазмидного вектора pEFGP-C1 и генотерапевтического ДНК-вектора VTvaf17-eGFP (концентрация каждого 500 нг/мкл) и 1 мкл реагента Р3000. Аккуратно перемешивали легким встряхиванием. В пробирке №2 к 25 мкл среды Opti-MEM (Gibco) добавляли 1 мкл раствора Lipofectamine 3000. Аккуратно перемешивали легким встряхиванием. Добавляли содержимое пробирки №1 к содержимому пробирки №2, инкубировали 5 мин при комнатной температуре. Полученный раствор по каплям добавляли к клеткам в объеме 40 мкл.
Учет результатов проводили через 48 часов с использованием флуоресцентного микроскопа Olympus ix53 (Япония) с парой фильтров 485 нм и 535 нм (фиг. 3А). Данные результаты подтверждают, что трансфекция клеток НЕK-293 генотерапевтическим ДНК-вектором VTvaf17-eGFP приводит к значительному увеличению накопления зеленого флуоресцентного белка по сравнению с трансфекцией этих клеток плазмидным вектором pEFGP-C1 (Clontech).
Учет результатов также проводили путем измерения флуоресценции белка, выделенного из трансфицированной линии клеток. Для этого клетки из лунки смывали пипетированием и осаждали центрифугированием на 6000 об/мин в течение 10 мин, дважды промывали и затем ресуспендировали осадки в 1 мл натрий-фосфатного буфера. Клетки разрушали с помощью трехкратного замораживания-оттаивания при -70°C. Далее гомогенат разрушенных клеток осаждали центрифугированием при 13000 g в течение 15 мин. Полученные супернатанты переносили в 96-луночный планшет (Grainer Bio-one), в четырех технических повторах для каждого образца, после чего оценивали относительную флуоресценцию белка GFP в пробе (поглощение 455 нм / испускание 538 нм) с помощью флуориметра Fluoroskan Ascent (Labsystems). Нормировку полученных значений осуществляли в зависимости от суммарной концентрации белка в пробе, которую определяли методом Бредфорд. Для этого в качестве красителя использовали Coomassie Brilliant Blue R-250. Каждый технический повтор в ячейках 96-луночного планшета (4 повтора для каждого образца) разводили водой в 100 раз, после чего добавляли краситель. Затем с помощью сканера Multiskan Ascent (Thermo) проводили оценку оптической плотности всех проб на длине волны 620 нм. Полученные значения сравнивали с калибровочной кривой, построенной для бычьего сывороточного альбумина (Bio-Rad) с использованием серии разведений от 20 до 2,5 мкг/мл. Расчет осуществляли по формуле:
∑количество белка (мкг)={[x]-σ}÷k*М,
где [x] - среднее значение OD620 из четырех повторов для каждого образца, σ - среднее отклонение, k - коэффициент наклона калибровочной кривой для БСА, М - число раз, в которое был разведен образец.
Исходя из полученных значений суммарного количества белка, выделенного из клеток, нормировку флуоресценции GFP в образцах осуществляли по формуле:
OEn=[ОЕ]÷∑количество белка (мг),
где [ОЕ] - среднее значение из четырех повторов для каждого образца в относительных единицах флуоресценции.
Результаты приведены на фиг. 3Б, откуда следует, что трансфекция клеток НЕK-293 генотерапевтическим ДНК-вектором VTvaf17-eGFP приводит к двукратному увеличению накопления зеленого флуоресцентного белка по сравнению с трансфекцией этих клеток плазмидным вектором pEFGP-C1 (Clontech).
Пример 7
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17 клонировали в полилинкер целевой ген, например, ген кодирующий эластин.
Оценка изменения накопления мРНК целевого гена, например, гена эластина, в клетках кератиноцитов НаСаТ через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-ELN, несущим участок, кодирующий ген эластина человека.
Клетки линии НаСаТ (иммортализованные кератиноциты человека, ThermoFisher Scientific, США) выращивали в среде DMEM (ThermoFisher Scientific, США), содержащей 10% сыворотки эмбрионов коров (ThermoFisher Scientific, США), 4,5 г/л глюкозы, 2 мМ глутамина в атмосфере 5% CO2 при 37°C. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5*104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-ELN, экспрессирующим ген эластина человека проводили как описано в примере 6. В качестве контроля использовали клетки НаСаТ, трансфицированные генотерапевтическим ДНК-вектором VTvaf17. Суммарную РНК из трансфицированных клеток и построение первой цепи кДНК проводили как описано в примере 3. Для определения уровня экспрессии мРНК гена эластина после трансфекции использовали метод ПЦР в режиме реального времени (SYBR GreenRealTimePCR). Для амплификации кДНК, специфичной для гена эластина человека, использовалиолигонуклеотиды EL1F и EL1 R (перечень последовательностей, (34), (35)). Длина продукта амплификации - 227 п.о. В качестве референтного гена использовали ген бета-2-микроглобулина В2М.
ПЦР-амплификацию проводили с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, США) или другого набора для ПЦР в режиме реального времени в 20 мкл амплификационной смеси, содержащей: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 mM хлорида магния, по 0,5 мкМ каждого праймера, 5 мкл суммарной РНК. Реакцию осуществлли на амплификаторе CFX96 (Bio-Rad, USA) при следующих условиях: 1 цикл обратной транскрипции при 42°C 30 минут, денатурация 98°C - 15 мин, затем 40 циклов, включающих денатурацию 94°C - 15 сек, отжиг праймеров 60°C - 30 сек и элонгацию 72°C - 30 сек. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов ELN и В2М. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов ELN и В2М, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1.
С целью подтверждения увеличения экспрессии гена ELN в клетках кератиноцитов человека после трансфекции данных клеток генотерапевтическим ДНК-вектором VTvaf17-ELN, несущим участок, кодирующий ген эластина на фиг. 3 приведены графики накопления ПЦР-продуктов, соответствующих:
1 - кДНК гена ELN после трансфекции генотерапевтическим вектором VTvaf17;
2 - кДНК гена ELN после трансфекции генотерапевтическим вектором VTvaf17-ELN, несущим участок, кодирующий ген эластина;
3 - кДНК гена В2М после трансфекции генотерапевтическим вектором VTvaf17;
4 - кДНК гена В2М после трансфекции генотерапевтическим вектором VTvaf17-ELN, несущим участок, кодирующий ген эластина
Из фигуры следует, что в результате трансфекции генотерапевтическим ДНК-вектором VTvaf17-ELN, несущим целевой ген, например, ген эластина человека, уровень специфической мРНК гена эластина человека вырос многократно.
Пример 8
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17 клонировали в полилинкер целевой ген, например, ген кодирующий эластин.
Оценивали изменения количества белка эластина в коже человека при введении в кожу человека генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, например, ген эластина человека.
С целью анализа изменения количества белка эластина трем пациентам с видимыми возрастными изменениями кожи вводили в кожу предплечья генотерапевтический ДНК-вектор VTvaf17-ELN, несущий участок, кодирующий ген эластина и параллельно вводили плацебо, представляющее собой генотерапевтический ДНК-вектор VTvaf 17, не содержащий кДНК гена ELN. Пациент 1, женщина, 56 лет, мелкоморщинистый тип старения (П1); пациент 2, женщина, 67 лет, деформационный, или крупноморщинистый тип старения (П2); пациент 3, мужчина, 60 лет, деформационный тип старения (П3).
Генотерапевтический ДНК-вектор VTvaf17 (плацебо) и генотерапевтический ДНК вектор VTvaf17-ELN, несущий участок, кодирующий ген эластина вводили в количестве 1 мг для каждой генетической конструкции тоннельным методом иглой 30G на глубину 3 мм. Объем вводимого раствора генотерапевтического ДНК-вектора VTvaf17 (плацебо) и генотерапевтического ДНК вектора VTvaf17-ELN, несущего участок, кодирующий ген эластина - 0,3 мл для каждой генетической конструкции. Очаги введения каждой генетической конструкции располагали на расстоянии 5-10 см друг от друга.
Биопсийные образцы отбирали на 2 сутки после введения генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков кожи пациентов в зоне введения генотерапевтического ДНК вектора VTvaf17-ELN, несущего участок, кодирующий ген эластина (I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (II), а также из участков интактной кожи (III), используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL). Кожу пациентов предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 2×2×2 мм, масса - до 10 мг. Образец помещают в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000 g. Отбирали супернатант и использовали его для количественного определения целевого белка.
Количество белка эластина оценивали в биоптатах кожи пациентов методом твердофазного иммуноферментного анализа, используя набор Enzyme-linked Immunosorbent Assay Kit For Elastin (ELN) (SEB337Hu, Cloud - Clone Corp., США).
В наборе были использованы высоко специфичные антитела к белку эластин, адсорбированные на лунках микропланшета. В лунки добавляли по 100 мкл разведенных стандартных образцов и тестируемых образцов и инкубировали 2 часа при 37°C. Затем добавляли 100 мкл реагента А, закрывали планшет клейкой лентой и инкубировали 1 час при 37°C. Далее лунки промывали трехкратно 350 мкл промывочного буфера и добавляли 100 мкл реагента В с последующей инкубацией в течение 30 мин при 37°C. После инкубации проводили пятикратную отмывку 350 мкл промывочного буфера, затем добавляли 90 мкл раствора субстрата и инкубировали 20-25 мин при 37°C. Реакцию останавливали добавлением 50 мкл стоп-раствора и измеряли оптическую плотность при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США). Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка эластин, входящим в состав набора. Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/).
Показано, что в коже всех трех пациентов в области введения генотерапевтического ДНК вектора VTvaf17, несущего целевой ген, например, ген эластина человека, произошло увеличение количества белка эластина в сравнении с количеством белка эластина в области введения генотерапевтического ДНК-вектора VTvaf17 (плацебо), не содержащего участок, кодирующий ген эластина человека. Результаты измерений концентрации эластина в коже пациентов П1, П2, П3 отражены на фиг. 5.
Пример 9
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17 клонировали в полилинкер целевой ген, например, ген кодирующий зеленый флуоресцентный белок (GFP) в клетках почки быка MDBK.
Оценивали уровень накопления продукта целевого гена, например, зеленого флуоресцентного белка (GFP) в клетках почки быка MDBK через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-eGFP.
Для оценки уровня накопления зеленого флуоресцентного белка GFP в клетках MDBK (клетки почки быка, АТСС CLL-22) проводили их трансфекцию генотерапевтическим ДНК-вектором VTvaf17-eGFP.
Клетки выращивали в среде MEM (ThermoFisher Scientific, США), содержащей 10% сыворотки эмбрионов коров (ThermoFisher Scientific, США), 1 г/л глюкозы и 2 мМ глутамина в атмосфере 5% CO2 при 37°C. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 3*104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию проводили как описано в примере 6. В качестве контроля использовали рекомбинантный генотерапевтический вектор VTvaf17, не содержащий гена зеленого флуоресцентного белка. Учет результатов также проводили путем измерения флуоресценции белка, выделенного из трансфицированной линии клеток как описано в примере 6.
Результаты приведены на фиг. 6, откуда следует, что трансфекция линии клеток почки быка MDBK генотерапевтическим ДНК-вектором VTvaf17-eGFP несущим ген зеленого флуоресцентного белка приводит к увеличению накопления зеленого флуоресцентного белка по сравнению с трансфекцией этих клеток генотерапевтическим вектором VTvaf17, не содержащим ген зеленого флуоресцентного белка.
Пример 10
Для подтверждения технологичности получения и возможности наработки генотерапевтического ДНК-вектора VTvaf17 в промышленных масштабах проводили масштабную ферментацию штамма Escherichia coli SCS110-AF/VTvaf17 (регистрационный № ВКПМ В-12990, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 42801), несущего генотерапевтический ДНК-вектор VTvaf17.
Проводили ферментацию штамма Escherichia coli SCS110-AF/VTvaf17 несущего генотерапевтический ДНК-вектор VTvaf17 в ферментере объемом 10 л с последующим выделением генотерапевтического ДНК-вектора VTvaf17.
Для ферментации штамма Escherichia coli SCS110-AF/VTvaf17 готовили среду, содержащую на 10 л: 100 г триптон, 50 г дрожжевой экстракт (Becton Dickinson), доводили водой до 8800 мл и автоклавировали при 121°C 20 мин, затем добавляли 1200 мл 50% (вес/объем) сахарозы. Далее засевали в колбу затравочную культуру штамма Escherichia coli SCS110-AF/VTvaf17 в объеме 100 мл. Инкубировали в шейкере-инкубаторе 16 ч при 30°C. Переносили затравочную культуру в ферментер Techfors S (Infors НТ, Швейцария), растили до достижения стационарной фазы. Контроль осуществляли измерением оптической плотности культуры при длине волны 600 нм. Клетки осаждали центрифугированием 30 мин при 5000-10000 g. Супернатант удаляли, клеточную массу ресуспендировали в 10% по объему фосфатно-солевого буфера. Повторно центрифугировали 30 мин при 5000-10000 g. Супернатант удаляли, к клеточной массе добавллит раствор 20 мМ TrisCl, 1 мМ ЭДТА, 200 г/л сахароза, рН 8,0 в объеме 1000 мл, тщательно перемешивали до образования гомогенной суспензии. Добавляли раствор яичного лизоцима до конечной концентрации 100 мкг/мл. Инкубировали 20 мин на льду при бережном перемешивании. Далее, добавляли 2500 мл раствора 0,2 М NaOH, 10 г/л додецилсульфат натрия, инкубировали 10 мин на льду при бережном перемешивании, затем добавляли 3500 мл раствора 3М ацетат натрия, 2М уксусная кислота, рН 5-5,5, инкубировали 10 мин на льду при бережном перемешивании. Полученный образец центрифугировали 20-30 мин при 15000 g или более. Раствор аккуратно декантировали, от остатков осадка избавляли фильтрацией через грубый фильтр (фильтровальную бумагу). Добавляли РНКазу А (Sigma) до конечной концентрации 20 нг/мл, инкубировали ночь 16 ч при комнатной температуре. Раствор центрифугировали 20-30 мин при 15000 g, затем фильтровали через мембранный фильтр с порами 0,45 мкм (Millipore). Далее проводили ультрафильтрацию через мембрану размером отсечения 100 кДа (Millipore) и разбавляли до начального объема буфером 25 мМ TrisCl, рН 7.0. Операцию повторяли три - четыре раза. Наносили раствор, на колонку с 250 мл сорбента DEAE sepharose HP (GE, США), уравновешенную раствором 25 мМ TrisCl, рН 7.0. После нанесения образца колонку промывали тремя объемами этого же раствора, а затем проводили элюцию генотерапевтического ДНК-вектора VTvaf17 линейным градиентом от раствора 25 мМ TrisCl, рН 7.0 до раствора 25 мМ TrisCl, рН 7.0, 1М NaCl в объеме пяти объемов колонки. Контроль элюции осуществляли по оптической плотности сходящего раствора при 260 нм. Хроматографические фракции, содержащие генотерапевтический ДНК-вектор VTvaf17, объединяли и проводили гель-фильтрацию на сорбенте Superdex 200 (GE, США). Колонку уравновешивали фосфатно-солевым буфером. Контроль элюции осуществляли по оптической плотности сходящего раствора при 260 нм, фракции анализируют электрофорезом в агарозном геле. Фракции, содержащие генотерапевтический ДНК-вектор VTvaf17 объединяли и хранили при -20°C. Выход конечного продукта достаточен для организации масштабного промышленного производства генотерапевтического ДНК-вектора VTvaf17.
Таким образом, задача, поставленная в данном изобретении, а именно: конструирование генотерапевтического ДНК-вектора для генетической модификации клеток животных и человека, оптимально сочетающего в себе:
I) возможность безопасного использования для генетической терапии человека и животных за счет отсутствия в составе геннотерапевтического ДНК-вектора генов антибиотикорезистентности;
II) длину, обеспечивающую эффективное проникновение в клетку-мишень;
III) наличие регуляторных элементов, обеспечивающих эффективную экспрессию целевых генов и, в то же время, не представляющих собой нуклеотидные последовательности вирусных геномов;
IV) технологичность получения и возможность наработки в промышленных масштабах, -
решена, что подтверждается примерами: для п. I - пример 1; для п. II - пример 1, 6, 7, 8; 9; для п. III - пример 1, 6, 7, 8, 9; для п. IV - пример 5, 10.
Промышленная применимость
Все представленные выше примеры подтверждают промышленную применимость предлагаемого генотерапевтического ДНК-вектора VTvaf17, способа его получения, генетически-модифицированного штамма Escherichia coli SCS110-AF для наработки ДНК-вектора VTvaf17 и генотерапевтических ДНК векторов, несущих целевые гены, на его основе, способа получения штамма Escherichia coli SCS110-AF, генетически-модифицированного штамма Escherichia coli SCS110-AF/VTvaf17 (регистрационный № ВКПМ В-12990, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 42801), несущего генотерапевтический ДНК-вектор VTvaf17 для его наработки, способа получения штамма Escherichia coli SCS110-AF/VTvaf17.







Изобретение относится к генной инженерии и биотехнологии, в частности к генотерапевтическому ДНК-вектору VTvaf17 размером 3165 п.н. и способу его получения. Указанный ДНК-вектор VTvaf17 предназначен для генетической модификации клеток животных и человека и имеет нуклеотидную последовательность SEQ ID No: 1. Настоящее изобретение также относится к штамму Escherichia coli SCS110-AF, к штамму Escherichia coli SCS110-AF/VTvaf17 и к способам их получения. Штамм E. coli SCS110-AF предназначен для наработки генотерапевтического ДНК-вектора VTvaf17 или генотерапевтических ДНК-векторов на его основе и содержит в хромосоме в области гена rесА линейный фрагмент, содержащий регуляторный элемент RNA-in транспозона Тn10. Штамм E. coli SCS110-AF/VTvaf17 содержит генотерапевтический ДНК-вектор VTvaf17 и предназначен для его наработки. Указанный штамм E. coli SCS110-AF/VTvaf17 получен путем электропорации клеток штамма E. coli SCS110-AF ДНК-вектором VTvaf17. Изобретение позволяет получать ДНК-вектор для генетической модификации клеток животных и человека. 6 н.п. ф-лы, 6 ил., 10 пр.
1. Генотерапевтический ДНК-вектор VTvaf17 размером 3165 п.н., предназначенный для генетической модификации клеток животных и человека, с нуклеотидной последовательностью SEQ ID №1.
2. Способ получения генотерапевтического ДНК-вектора VTvaf17 размером 3165 п.н. по п. 1, заключающийся в том, что сначала конструируют вектор размером 4182 п.н., содержащий промоторную область гена человеческого фактора элонгации EF1A с собственным энхансером размером 1188 п.н., полилинкер, имеющий сайты для эндонуклеаз рестрикции BamHI, EcoRV, SalI, HindIII, KpnI, EcoRI размером 35 п.н., терминатор транскрипции и сайт полиаденилирования гена фактора роста человека размером 466 п.н., регуляторный элемент PHK-out транспозона Тn10, обеспечивающий возможность положительной селекции без использования антибиотиков размером 136 п.н., ориджин репликации, служащий для автономной репликации с однонуклеотидной заменой для повышения копийности вектора в клетках большинства штаммов Eshcerichia coli размером 1299 п.н., ген устойчивости к канамицину размером 1010 п.н., а затем выщепляют его по сайтам рестрикции Spel, после чего оставшийся фрагмент лигируют сам на себя.
3. Способ получения штамма Escherichia coli SCS 110-AF для наработки генотерапевтического ДНК-вектора VTvaf17 по п. 1 или генотерапевтических ДНК-векторов на его основе, заключающийся в том, что конструируют линейный фрагмент ДНК, содержащий регуляторный элемент RNA-in транспозона Тn10 для селекции без применения антибиотиков размером 64 п.н., ген левансахаразы sacB, продукт которого обеспечивает селекцию на сахарозо-содержащей среде размером 1422 п.н., ген устойчивости к хлорамфениколу catR, необходимый для отбора клонов штамма, в которых прошла гомологичная рекомбинация, размером 763 п.н. и две гомологичные последовательности, обеспечивающие процесс гомологичной рекомбинации в области гена rесА с одновременной его инактивацией размером 329 п.н. и 233 п.н., причем указанные гомологичные последовательности являются последовательностями, полученными путем проведения ПЦР амплификации фрагментов гена rесА с использованием геномной ДНК Eshcerichia coli SCS 110 в качестве матрицы и пары праймеров LHA-F (5'-GCTGACGCTGCAGGTGATC) и LHA-R (5'-GACAAGATGTGTGTCTACCGCTTCAGGTTACCCGCCAG) и пары праймеров RHA-F (5'-TGGCAGGGCGGGGCGTAACTACGCCTCTGTTCGTCTCGA) и RHA-R (5'-CTCAGCAGCAACTCACGTAC), после чего проводят трансформацию клеток Escherichia coli путем электропорации и отбирают клоны, выжившие на среде, содержащей 10 мкг/мл хлорамфеникола.
4. Штамм Escherichia coli SCS110-AF, полученный способом по п. 3, для наработки генотерапевтического ДНК-вектора VTvaf17 по п.1 или генотерапевтических ДНК-векторов на его основе с возможностью положительной селекции без использования антибиотиков, и содержащий в хромосоме в области гена rесА линейный фрагмент, содержащий регуляторный элемент RNA-in транспозона Тn10, ген левансахарозы sacB и ген устойчивости к хлорамфениколу catR.
5. Способ получения штамма Escherichia coli SCS110-AF/VTvaf17, несущего генотерапевтический ДНК-вектор VTvaf17 по п. 1, заключающийся в том, что получают электрокомпетентные клетки штамма Escherichia coli SCS110-AF по п. 3 и проводят электропорацию этих клеток генотерапевтическим ДНК-вектором VTvaf17, после чего клетки высеивают на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола.
6. Штамм Escherichia coli SCS110-AF/VTvaf17, полученный способом по п. 5, несущий генотерапевтический ДНК-вектор VTvaf17 по п.1 для его наработки с возможностью селекции без использования антибиотиков.
| OLIVEIRA P.H | |||
| et al | |||
| Marker-free plasmids for biotechnological applications-implications and perspectives | |||
| Trends in biotechnology, 2013 | |||
| HARDEE C.L | |||
| et al | |||
| Advances in non-viral DNA vectors for gene therapy | |||
| Genes, 2017 | |||
| LUKE J | |||
| et al | |||
| Improved antibiotic-free DNA vaccine vectors utilizing a novel RNA based plasmid selection system | |||
| Vaccine, 2009 | |||
| ЕФРЕМОВ А.М | |||
| и др | |||
| Невирусная регенеративная генотерапия повреждений кожных покровов млекопитающих | |||
| Цитология, 2010. |
Авторы
Даты
2019-01-31—Публикация
2017-08-25—Подача