Область техники
Изобретение относится к генной инженерии и может быть использовано в биотехнологии, медицине и сельском хозяйстве для создания препаратов генной терапии. То есть, созданный генотерапевтический ДНК-вектор с целевым геном может быть использован для введения в клетки организма животных и человека, характеризующихся сниженной или недостаточной экспрессией данного гена, обеспечивая таким образом достижение терапевтического эффекта.
Уровень техники
Генная терапия - это современный медицинский подход, направленный на лечение наследственных и приобретенных заболеваний путем введения нового генетического материала в клетки, ткани, органы пациента с целью компенсации или подавления функции мутантного гена и/или исправления генетического дефекта. Целью генной терапии является, в большинстве случаев, введение в организм генов, обеспечивающих транскрипцию и последующую трансляцию белковых молекул, кодируемых этими генами. В рамках описания настоящего изобретения под экспрессией гена подразумевается продукция белковой молекулы, аминокислотная последовательность которой кодируется этим геном.
Гены, выбранные из группы генов COL1A1, COL1A2, ВМР2, ВМР7, играют важную роль в формированием костной и хрящевой тканей организма человека и животных. Показана связь низких/недостаточных концентраций этих белков с различными заболеваниями человека, которая, в ряде случаев, подтверждена нарушениями в нормальной экспрессии генов, кодирующих эти белки. Например, мутации в генах COL1A1, COL1A2 приводят к наследственным заболеваниям соединительной ткани - несовершенным остеогенезам, которые сопровождаются частыми переломами костей (Яхяева Г.Т. С соавт., Вопросы современной педиатрии. 2016; 15 (2): 175-179). Результатом генетически обусловленной недостаточности BMP 2 являются повышенная хрупкость костей, нарушения энхондрального остеогенеза и минерализации костного матрикса (Chen G., Deng С., Li Y.P. Int. J. Biol. Sci. 2012; 8 (2): 272-88). Таким образом, повышение экспрессии гена, выбранного из группы генов COL1A1, COL1A2, ВМР2, ВМР7, и введенного в организм геннотерапевтическим способом, актуально для коррекции состояний человека и животных, связанных с нарушением действия вышеназванных генов.
Для целей генной терапии используют специально сконструированные генотерапевтические векторы, которые разделяют на вирусные и невирусные. В последнее время все большее внимание уделяется разработке невирусных систем доставки генетического материала, среди которых лидируют плазмидные векторы. Данные векторы лишены недостатков, присущих вирусным векторам: в клетке-мишени они существуют в эписомальной форме, поэтому не происходит интеграции в геном; их производство достаточно дешево; отсутствие иммунного ответа и побочных реакций на введение плазмидного вектора делают их удобным инструментом генной терапии и генетической профилактики в качестве ДНК-вакцины (Li L, Petrovsky N. Molecular mechanisms for enhanced DNA vaccine immunogenicity. Expert Rev Vaccines. 2016; 15(3):313-29).
При этом имеются ограничения для использования плазмидных векторов для генной терапии: 1) наличие генов устойчивости к антибиотикам для наработки в штаммах-носителях, 2) наличие различных регуляторных элементов, представленных последовательностями вирусных геномов, 3) размер терапевтического плазмидного вектора, определяющий эффективность проникновения вектора в клетку-мишень.
Известно, что Европейское агентство по лекарственным средствам считает необходимым избегать введения маркеров антибиотикорезистентности в разрабатываемые плазмидные векторы для генной терапии (Reflection paper on design modifications of gene therapy medicinal products during development / 14 December 2011 EMA/CAT/GTWP/44236/2009 Committee for advanced therapies), а также рекомендует избегать наличия в составе терапевтических плазмидных векторов регуляторных элементов для повышения экспрессии целевых генов (промоторов, энхансеров, посттрансляционных регуляторных элементов), которые являются частями геномов различных вирусов (Guideline on the quality, non-clinical and clinical aspects of gene therapy medicinal products / 23 March 2015, EMA/CAT/80183/2014, Committee for Advanced Therapies).
Также, существенным моментом является размер генотерапевтического вектора. Известно, что современные плазмидные векторы зачастую перегружены нефункциональными участками, серьезно увеличивающими размер вектора (Mairhofer J, Grabherr R. Rational vector design for efficient non-viral gene delivery: challenges facing the use of plasmid DNA. Mol Biotechnol. 2008. 39(2):97-104), что порой не позволяет встраивать в состав вектора целевой ген нужного размера.
Известен способ накопления плазмидных векторов в штаммах Escherichia coli без использования антибиотиков (Cranenburgh RM, Hanak JA, Williams SG, Sherratt DJ. Escherichia coli strains that allow antibiotic-free plasmid selection and maintenance by repressor titration. Nucleic Acids Res. 2001. 29(5):E26). Были созданы штаммы Escherichia coli DH1lacdapD и DH1lacP2dapD, в которых ген dapD, кодирующий фермент 2,3,4,5-тетрагидропиридин-2,6-дикарбоксилат-N-сукцинилтрансферазу, участвующий в биосинтезе L-лизина, находится под контролем lac-промотора. В отсутствие индуктора IPTG (изопропил-β-D-1-тиогалактопиранозид) эти штаммы подвержены лизису. Однако при введении мультикопийного вектора pORT, содержащего lac-оператор, индуцируется экспрессия гена dapD и, таким образом, трансформированные клоны могут быть отобраны и размножены. Однако, эти штаммы характеризуются низким уровнем трансформации и ее нестабильностью.
Известно решение по патентной заявке RU 2011152377 A, описывающей получение экспрессионного плазмидного вектора без устойчивости к антибиотику, которая содержит полинуклеотидную последовательность, кодирующую белок-репрессор. Экспрессия указанного белка-репрессора регулирует экспрессию токсичного генного продукта, встроенного в участок генома E.coli. Однако, как и все методы селекции, основанные на использовании белков-репрессоров, данный метод отличается нестабильностью трансформации и ее низкой эффективностью.
В патенте US 9644211 B2 описано получение минимального по размеру вектора. Данный вектор не содержит бактериальных геномных последовательностей и продуцируется путем parA-опосредованной рекомбинации, проходящей в специально полученном штамме E.coli. Недостатком данного метода получения минимального по размеру вектора является невозможность его использования при масштабировании производства.
Известно получение генотерапевтических векторов, в состав которых включены нуклеотидные последовательности, кодирующие структурные белки человека или факторы роста, связанные с репарацией костной и хрящевой тканей. Так ген COL1A1 кодирует белок альфа1-цепи коллагена I типа, а ген COL1A2 кодирует белок альфа2-цепи коллагена I типа, которые являются потенциально значимым в формировании генетической предрасположенности к остеопорозу и хрупкости костей с риском переломов. Это связано с тем, что коллаген I типа входит в состав костей, сухожилий, связок, кожи и других соединительных тканей.
В заявке WO 2015035395 описано использование терапевтического полинуклеотида для получения хондроцитов или клеток хрящевого типа в суставе индивидуума, при этом полинуклеотид создан на основе вирусных и невирусных векторов с генами COL1A1 и COL1A2 под контролем промотора, подходящим для активности в бессосудистой, безнейронной или низко-кислородной среде.
Костные морфогенетические белки (BMPs; bone morphogenetic proteins) являются самыми важными факторами регенерации кости и хряща. Белки семейства BMP действуют на рецепторы клеточной мембраны и играют важную роль в регуляции роста, дифференцировки и апоптоза различных типов клеток включая остеобласты, хондробласты, нервные и эпителиальные клетки. Эти белки стимулируют увеличение числа клеток, а также вызывают ускоренную дифференцировку мезенхимальных стволовых клеток в хондробласты и остеобласты, усиливают синтез коллагена, повышают активность щелочной фосфатазы, увеличивают синтез остеокальцина, стимулируют синтез внеклеточного матрикса и его последующую минерализацию (Katagiri Т, Watabe Т. Bone Morphogenetic Proteins. Cold Spring Harb Perspect Biol. 2016, 8(6)).
В настоящее время некоторые члены семейства BMP используются в медицине. Так, современные биологические методы повышения остеоиндуктивности костных имплантатов акцентированы на поставку значительных концентраций BMP на различных типах носителей (Lowery JW, Rosen V. Bone Morphogenetic Protein-Based Therapeutic Approaches. Cold Spring Harb Perspect Biol. 2018, 10(4)). Применение рекомбинантных BMP для индукции остеогенеза в клинике ограничено быстрой деградацией этих белков в месте введения и в кровяном русле, а также опасностью развития гетеротопической оссификации.
Наиболее полно изученными из этой группы белков являются белки ВМР-2 и ВМР-7. В патенте RU 2408727 описана рекомбинантная плазмида pCollbd-BMP-2 размером 3447 п.н., которая находится в штамме Escherichia coli М15 и обеспечивает в нем экспрессию рекомбинантного белка Collbd-BMP-2, состоящего из коллагенсвязывающего домена Collbd из внеклеточного кальций-зависимого белка SPARC человека, спейсера из остатков глицина и серина и костного морфогенетического белка ВМР-2. Созданный искусственный бактериальный оперон химерных белков находится под контролем промоторной области раннего промотора бактериофага Т5. Полученная рекомбинантная плазмида содержит бактериальный оперон bla, кодирующий белок бета-лактамазу, являющуюся селективным маркером для отбора клонов-трансформантов E.coli методом контрселекции.
В источнике ЕР 2228071 (А1) описан рекомбинантный вектор, созданный на основе коммерческой плазмиды VR1012 (J. Hartikka et al. Human Gene Therapy 1996, 7, 1205-1217), экспрессирующий белок ВМР-7 (слитый с сигнальным пептидом для облегчения секреции ВМР-7 в экстраклеточную среду) в клетках хозяина, а также - фармацевтические композиции на основе таких рекомбинантных векторов для лечения почечной недостаточности у млекопитающих. Описанный вектор, содержит в себе полинуклеотид, кодирующий белок ВМР-7 млекопитающего или человека, функционально связанный с промоторным элементом. Промоторы и энхансеры, которые могут быть использованы в данном изобретении, включают, но не ограничиваются следующими элементами: промоторы и энхансеры LTR вируса саркомы Rous, ген ТК HSV-1, ранние или поздние промоторы SV40, аденовирусный промотор (MLP), гены фосфоглицераткиназы, гены металлотионеина, гены α-1-антитрипсина, гены альбумина, гены коллагеназы, гены эластазы I, гены β-актина, гены β-глобина, гены γ-глобина, гены α-фетопротеинов и гены мышечной креатинкиназы. Предпочтительным промотором для экспрессии гена белка ВМР-7 является ранний промотор цитомегаловируса (CMV-IE) человеческого или мышиного происхождения. Таким образом, в данном изобретении промотор имеет либо вирусное, либо клеточное происхождение. Вектор в изобретении может быть любым подходящим рекомбинантным вирусом или вирусным вектором, таким как поксвирус, аденовирус, герпесвирус, бакуловирус, ретровирус и т.д. или вектор может быть плазмидой.
Прототипом настоящего изобретения в части использования рекомбинантных ДНК-векторов для генной терапии является патент, US 9550998 (В2), в котором описан способ получения рекомбинантного вектора для генетической иммунизации. Полученный вектор представляет собой суперскрученный плазмидный ДНК-вектор, который предназначен для экспрессии клонированных генов в клетках животных и человека. Вектор состоит из области начала репликации (origin), регуляторных элементов, включающих промотор и энхансер цитомегаловируса человека, регуляторные элементы из Т-лимфотропного вируса человека. Накопление вектора производят в специальном штамме E.coli без использования антибиотиков за счет антисенс-комплементации гена sacB, введенного в штамм посредством бактериофага. Ограничением использования данного ДНК - вектора для генетической терапии является наличие в его составе регуляторных элементов, представляющих собой последовательности вирусных геномов.
Раскрытие изобретения.
Задачей изобретения является конструирование генотерапевтических ДНК-векторов на основе специально сконструированного генотерапевтического ДНК-вектора для повышения уровня экспрессии гена, выбранного из группы генов - гена COL1A1 белка альфа1-цепи коллагена I типа, гена COL1A2 белка альфа2-цепи коллагена I типа, гена костного морфогенетического белка ВМР-2, гена костного морфогенетического белка ВМР-7, а также - конструирование штаммов, несущих эти генотерапевтические ДНК-векторы для производства их промышленных масштабах.
При этом ДНК-векторы должны оптимально сочетать в себе следующие свойства:
I) возможность безопасного использования для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора генов антибиотикорезистентности.
II) длину, обеспечивающую эффективное проникновение в клетку-мишень;
III) наличие регуляторных элементов, обеспечивающих эффективную экспрессию целевых генов и, в то же время, не представляющих собой нуклеотидные последовательности вирусных геномов;
IV) технологичность получения и возможность наработки в промышленных масштабах.
Пункты I и III предусмотрены в данном техническом решении в соответствии с рекомендациями государственных регуляторов к лекарственным средствам для генной терапии, в частности, Европейского Агентства по лекарственным средствам.
Поставленная задача решается за счет того, что создан генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, для повышения уровня экспрессии этого целевого гена в организме человека и животных, при этом генотерапевтический ДНК-вектор VTvaf17-COL1A1, или VTvaf17- COL1A2, или VTvaf17-ВМР2, или VTvaf17-ВМР7, имеет нуклеотидную последовательность SEQ ID №1 или SEQ ID №2 или SEQ ID №3 или SEQ ID №4 соответственно. Каждый из созданных генотерапевтических ДНК-векторов: VTvaf17- COL1A1, или VTvaf17- COL1A2, или VTvaf17- ВМР2, или VTvaf17- ВМР7 за счет ограниченного размера векторной части VTvaf17, не превышающего 3200 п.н, обладает способностью эффективно проникать в клетки и экспрессировать клонированный в него целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7. В составе генотерапевтического ДНК-вектора отсутствуют нуклеотидные последовательности вирусного происхождения и отсутствуют гены антибиотикорезистентности, обеспечивая возможность его безопасного применения для генетической терапии человека и животных.
Создан также способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: COL1A1, COL1A2, ВМР2, ВМР7, который заключается в том, что каждый генотерапевтический ДНК-вектор: VTvaf17- COL1A1, или VTvaf17- COL1A2, или VTvaf17- ВМР2, или VTvaf17- ВМР7, получают следующим образом: кодирующую часть целевого гена из группы генов COL1A1, COL1A2, ВМР2, ВМР7, клонируют в ДНК-вектор VTvaf17 и получают генотерапевтический ДНК-вектор VTvaf17-COL1A1, SEQ ID №1, или VTvaf17- COL1A2, SEQ ID №2 или VTvaf17- BMP2, SEQ ID №3, или VTvaf17- BMP7, SEQ ID №4 соответственно.
Способ применения созданного генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: COL1A1, COL1A2, ВМР2, ВМР7, для повышения уровня экспрессии этих целевых генов заключается во введении выбранного генотерапевтического ДНК-вектора или нескольких выбранных генотерапевтических ДНК-векторов в клетки, органы и ткани человека или животного, и/или во введении в органы и ткани человека или животного аутологичных клеток человека или животного, трансфицированных выбранным генотерапевтическим ДНК-вектором или несколькими выбранными генотерапевтическими ДНК-векторами, или в сочетании обозначенных способов.
Способ получения штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1 или штамма Escherichia coli SCS110-AF/VTvaf17-COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17-BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7 заключается в электропорации компетентных клеток штамма Escherichia coli SCS110-AF созданным генотерапевтическим ДНК-вектором и последующей селекцией стабильных клонов штамма с использованием селективной среды.
Заявлен штамм Escherichia coli SCS110-AF/VTvaf17-COL1A1, или штамм Escherichia coli SCS110-AF/VTvaf17-COL1A2, или штамм Escherichia coli SCS110-AF/VTvaf17-BMP2, или штамм Escherichia coli SCS110-AF/VTvaf17-BMP7, несущий генотерапевтический ДНК-вектор для его наработки с возможностью культивирования штамма без использования антибиотиков.
Способ производства в промышленных масштабах генотерапевтического ДНК-вектора заключается в масштабировании бактериальной культуры штамма до количеств, необходимых для наращивания бактериальной биомассы в промышленном ферментере, после чего биомассу используют для выделения фракции, содержащей целевой ДНК-продукт - генотерапевтический ДНК-вектор VTvaf17-COL1A1 или VTvaf17-COL1A2 или VTvaf17- VTvaf17-BMP2 или VTvaf17-BMP7, многостадийно фильтруют и очищают хроматографическими методами.
При этом специалистам в данной области техники известно свойство вырожденности генетического кода, из которого следует, что под объем настоящего изобретения также подпадают варианты нуклеотидных последовательностей, отличающихся инсерцией, делецией или заменой нуклеотидов, которые не приводят к изменению полипептидной последовательности, кодируемой целевым геном, и/или не приводят к потере функциональной активности регуляторных элементов вектора VTvaf17. При этом специалистам в данной области техники известно явление генетического полиморфизма, из которого следует, что под объем настоящего изобретения также подпадают варианты нуклеотидных последовательностей генов из группы генов COL1A1, COL1A2, ВМР2, ВМР7, которые при этом кодируют различные варианты аминокислотных последовательностей белков COL1A1, COL1A2, ВМР2, ВМР7, не отличающихся от приведенных по своей функциональной активности при физиологических условиях.
Способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, заключается в том, что кодирующую часть целевого гена COL1A1, или COL1A2, или ВМР2, или ВМР7 получают путем выделения РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции и ПЦР-амплификации кДНК с использованием специфических олигонуклеотидов и расщеплением продукта амплификации эндонуклеазами рестрикции, причем клонирование в генотерапевтический ДНК-вектор VTvaf17 проводят по сайтам рестрикции, обеспечивающим попадание рамки считывания целевых генов в экспрессионную кассету вектора VTvaf17.
Известно, что способность ДНК-векторов проникать в эукариотические клетки обусловлена, главным образом, размером вектора. При этом ДНК-вектора с наименьшим размером обладают более высокой проникающей способностью. Таким образом, отсутствие в составе вектора элементов, которые не несут функциональной нагрузки, но при этом увеличивают размер ДНК вектора, является предпочтительным. Данные особенности ДНК-векторов были учтены при получении генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, путем отсутствия в составе вектора крупных нефункциональных последовательностей и генов антибиотикорезистентности, что позволило, помимо технологических преимуществ и преимуществ в плане безопасности применения, значительно уменьшить размер полученного генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7. Таким образом, способность проникать в эукариотические клетки полученного генотерапевтического ДНК-вектора обусловлена ограниченным размером векторной части VTvaf17 (в которую входит промотор, ориджин репликации, сигнал полиаденилирования, полилинкер, элемент RNA-out), не превышающим 3200 п.н.
Способность проникать в эукариотические клетки и проявлять функциональную активность, то есть способность экспрессировать целевой ген, полученного генотерапевтического ДНК-вектора VTvaf17-COL1A1 или VTvaf17-COL1A2 или VTvaf17-ВМР2 или VTvaf17-BMP7 подтверждают путем введения в эукариотические клетки полученного вектора и последующим анализом экспрессии специфической мРНК и/или белкового продукта целевого гена. При этом наличие специфической мРНК в клетках, в которые был введен генотерапевтический ДНК-вектор VTvaf17-COL1A1 или VTvaf17-COL1A2 или VTvaf17-BMP2 или VTvaf17-BMP7 свидетельствует как о способности полученного вектора проникать в эукариотические клетки, так и о его способности экспрессировать мРНК целевого гена. При этом, как известно специалистам в данной области техники, наличие мРНК гена является обязательным условием, но не является доказательством трансляции белка, кодируемого целевым геном. Поэтому для подтверждения свойства генотерапевтического ДНК-вектора VTvaf17- COL1A1, или VTvaf17- COL1A2, или VTvaf17-ВМР2, или VTvaf17- ВМР7 экспрессировать целевой ген на уровне белка в эукариотических клетках, в которые был введен генотерапевтический ДНК-вектор, проводят с использованием иммунологических методов анализ концентрации белков, кодируемых целевыми генами. Наличие белка COL1A1, или COL1A2, или ВМР2, или ВМР7 подтверждает эффективность экспрессии целевых генов в эукариотических клетках и возможность повышения уровня концентрации белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7.
Способ применения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, для повышения уровня экспрессии этих целевых генов, заключается во введении генотерапевтического ДНК-вектора, несущего целевой ген или нескольких выбранных генотерапевтических ДНК-векторов, в клетки, органы и ткани человека или животного, и/или во введении в органы и ткани человека или животного аутологичных клеток, в которые был введен генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 или несколько выбранных генотерапевтических ДНК-векторов, или в сочетании обозначенных способов.
Указанные способы применения характеризуются отсутствием потенциальных рисков для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора регуляторных элементов, представляющих собой нуклеотидные последовательности вирусных геномов и за счет отсутствия в составе генотерапевтического ДНК-вектора генов устойчивости к антибиотикам, что подтверждается отсутствием участков, гомологичных вирусным геномам и генам антибиотикорезистентности в нуклеотидных последовательностях генотерапевтического ДНК-вектора VTvaf17- COL1A1, или генотерапевтического ДНК-вектора VTvaf17- COL1A2, или генотерапевтического ДНК-вектора VTvaf17- ВМР2, или генотерапевтического ДНК-вектора VTvaf17- ВМР7 (SEQ ID №1 или SEQ ID №2 или SEQ ID №3 или SEQ ID №4 соответственно).
Как известно специалистам в данной области техники, гены антибиотикорезистентности в составе генотерапевтических ДНК-векторов используются с целью получения этих векторов в препаративных количествах путем наращивания бактериальной биомассы в питательной среде, содержащей селективный антибиотик. В рамках настоящего изобретения в целях возможности безопасного применения генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A1, или COL1A2, или ВМР2, или ВМР7, использование селективных питательных сред, содержащих антибиотик, не представляется возможным. В качестве технологического решения для получения генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, для возможности масштабирования до промышленных масштабов получения генотерапевтических векторов предлагается способ получения штаммов для наработки указанных генотерапевтических векторов на основе бактерии Escherichia coli SCS110-AF. Способ получения штамма Escherichia coli SCS110-AF/VTvaf17- COL1A1 или штамма Escherichia coli SCS110-AF/VTvaf17- COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7 заключается в получении компетентных клеток штамма Escherichia coli SCS110-AF с введением в эти клетки генотерапевтического ДНК-вектора VTvaf17- COL1A1, или ДНК-вектора VTvaf17- COL1A2, или ДНК-вектора VTvaf17- ВМР2, или ДНК-вектора VTvaf17- ВМР7, соответственно с помощью методов трансформации (электропорации). Полученные штаммы используются для наработки генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, с возможностью использования сред без содержания антибиотиков.
Способ масштабирования получения бактериальной массы до промышленных масштабов для выделения генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, заключается в том, что затравочную культуру штамма Escherichia coli SCS110-AF/VTvaf17- COL1A1 или штамма Escherichia coli SCS110-AF/VTvaf17- COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7 инкубируют в объеме питательной среды без содержания антибиотика обеспечивающим подходящую динамику накопления биомассы, по достижению достаточного количества биомассы в логарифмической фазе роста, бактериальную культуру переносят в промышленный ферментер, после чего растят до достижения стационарной фазы роста, затем выделяют фракцию, содержащую целевой ДНК-продукт генотерапевтический ДНК-вектор VTvaf17- COL1A1, или ДНК-вектор VTvaf17- COL1A2, или ДНК-вектор VTvaf17- ВМР2, или ДНК-вектор VTvaf17- ВМР7, многостадийно фильтруют и очищают хроматографическими методами. При этом специалистам в данной области техники понятно, что условия культивирования штаммов, состав питательных сред (за исключением содержания антибиотиков), используемое оборудование, методы очистки ДНК могут варьировать в рамках стандартных операционных процедур в зависимости от отдельно взятой производственной линии, но известные подходы к масштабированию, промышленному получению и очистке ДНК-векторов с использованием штамма Escherichia coli SCS110-AF/VTvaf17- COL1A1, или штамма Escherichia coli SCS110-AF/VTvaf17- COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7 подпадают под объем настоящего изобретения.
Изобретение поясняется чертежами, где
На фиг. 1 представлена схема генотерапевтического ДНК-вектора VTvaf17, несущего целевой гена человека, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, который представляет собой кольцевую двуцепочечную молекулу ДНК, способную к автономной репликации в клетках бактерии Eshcerichia coli.
На фиг. 1 приведены схемы, соответствующие:
А - генотерапевтический ДНК-вектор VTvaf17-COL1A1,
В - генотерапевтический ДНК-вектор VTvaf17-COL1A2,
С - генотерапевтический ДНК-вектор VTvaf17-ВМР2,
D - генотерапевтический ДНК-вектор VTvaf17-ВМР7.
На схемах отмечены следующие структурные элементы вектора:
EF1a - промоторная область гена человеческого фактора элонгации EF1A с собственным энхансером, содержащимся в первом интроне гена. Служит для обеспечения высокого уровня транскрипции рекомбинантного гена в большинстве тканей человека.
Рамка считывания целевого гена, соответствующая кодирующей части гена COL1A1 (фиг. 1А), или COL1A2 (фиг. 1В), или ВМР2 (фиг. 1С), или ВМР7 (фиг. 1D), соответственно;
hGH-TA - терминатор транскрипции и сайт полиаденилирования гена фактора роста человека;
(4) RNA-out - регуляторный элемент РНК-out транспозона Tn 10, обеспечивающий возможность положительной селекции без использования антибиотиков при использовании штамма Eshcerichiacoli SCS 110;
ori - область начала репликации, участок служащий для автономной репликации с однонуклеотидной заменой для повышения копийности плазмиды в клетках большинства штаммов Eshc
Отмечены уникальные сайты рестрикции Eshcerichia coli.
На фиг. 2 представлены графики накопления мРНК целевого гена, а именно, гена COL1A1 человека, в клетках первичной культуры фибробластов кожи человека HDFa (АТСС PCS-201-012) до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17- COL1A1, с целью подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-COL1A1, несущего целевой ген COL1A1, где
1 - кДНК гена COL1A1 до трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A1,
2 - кДНК гена COL1A1 после трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A1;
3 - кДНК гена В2М до трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A1;
4 - кДНК гена В2М после трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A1;
В качестве референтного гена использовали ген В2М (Бета-2-микроглобулин) приведенного в базе данных GenBank под номером NM 004048.2.
На фиг. 3 представлены графики накопления мРНК целевого гена, а именно гена COL1A2 человека, в клетках культуры фибробластов кожи человека до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17- COL1A2, с целью подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего целевой ген COL1A2, где
1 - кДНК гена COL1A2 до трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A2,
2 - кДНК гена COL1A2 после трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A2,
3 - кДНК гена В2М до трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A2,
4 - кДНК гена В2М после трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A2.
В качестве референтного гена использовали ген В2М (Бета-2-микроглобулин) приведенного в базе данных GenBank под номером NM 004048.2. где
На фиг. 4 представлены графики накопления мРНК целевого гена, а именно гена ВМР2 человека в клетках остеосаркомы человека MG-63 (АТСС CRL-1427) до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17- ВМР2 с целью подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- ВМР2, несущего целевой ген ВМР2, где
1 - кДНК гена ВМР2 до трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР2;
2 - кДНК гена ВМР2 после трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР2;
3 - кДНК гена В2М до трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР2;
4 - кДНК гена В2М после трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР2.
В качестве референтного гена использовали ген В2М (Бета-2-микроглобулин) приведенного в базе данных GenBank под номером NM 004048.2.
На фиг. 5 представлены графики накопления мРНК целевого гена, а именно гена ВМР7 человека, в клетках остеобластов человека hFOB 1.19 (АТСС CRL-11372) до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17- ВМР7 с целью подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- ВМР7, несущего целевой ген ВМР7, где
1 - кДНК гена ВМР7 до трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР7
2 - кДНК гена ВМР7 после трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР7
3 - кДНК гена В2М до трансфекции генотерапевтическим ДНК-вектором VTvaf17- BMP7
4 - кДНК гена В2М в клетках после трансфекции генотерапевтическим ДНК-вектором VTvaf17- ВМР7
В качестве референтного гена использовали ген В2М (Бета-2-микроглобулин) приведенного в базе данных GenBank под номером NM 004048.2.
На фиг. 6 представлена диаграмма концентрации белка альфа-1 цепи коллагена I типа в культуральной среде клеток первичной культуры фибробластов кожи человека HDFa (АТСС PCS-201-012) после трансфекции этих клеток ДНК-вектором VTvaf17- COL1A1, с целью оценки изменения количества белка альфа-1 цепи коллагена I типа в культуральной среде клеток первичной культуры фибробластов кожи человека HDFa, при трансфекции этих клеток ДНК-вектором VTvaf17- COL1A1, несущим ген COL1A1, где
культура А - первичная культура фибробластов кожи человека HDFa, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль)
культура В - первичная культура фибробластов кожи человека HDFa, трансфицированных ДНК-вектором VTvaf17
культура С - первичная культура фибробластов кожи человека HDFa, трансфицированных ДНК-вектором VTvaf17-COL1A1, несущим ген COL1A1
На фиг. 7 представлена диаграмма концентрации белка альфа-2 цепи коллагена I типа в культуральной среде клеток культуры фибробластов кожи человека после трансфекции этих клеток ДНК-вектором VTvaf17- COL1A2, с целью оценки изменения количества белка альфа-2 цепи коллагена I типа в культуральной среде клеток культуры фибробластов кожи человека, при трансфекции этих клеток ДНК-вектором VTvaf17-COL1A2, несущим ген COL1A2, где
культура А - культура фибробластов кожи человека, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль)
культура В - культура фибробластов кожи человека, трансфицированных ДНК-вектором VTvaf17
культура С - культура фибробластов кожи человека, трансфицированных ДНК-вектором VTvaf17- COL1A2, несущим ген COL1A2.
На фиг. 8 представлена диаграмма концентрации костного морфогенетического белка 2 в культуральной среде клеток остеосаркомы человека MG-63 (АТСС CRL-1427) после трансфекции этих клеток ДНК-вектором VTvaf17- ВМР2, с целью оценки изменения количества костного морфогенетического белка 2 в культуральной среде клеток остеосаркомы человека MG-63 (АТСС CRL-1427), при трансфекции этих клеток ДНК-вектором VTvaf17- ВМР2, несущим ген ВМР2, где
культура А - культура клеток остеосаркомы человека MG-63, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль)
культура В - культура клеток остеосаркомы человека MG-63, трансфицированных ДНК-вектором VTvaf17
культура С - культура клеток остеосаркомы человека MG-63, трансфицированных ДНК-вектором VTvaf17- ВМР2, несущим ген ВМР2.
На фиг. 9 представлена диаграмма концентрации костного морфогенетического белка 7 в культуральной среде клеток остеобластов человека hFOB 1.19 (АТСС CRL-11372) после трансфекции этих клеток ДНК-вектором VTvaf17- ВМР7, с целью оценки изменения количества костного морфогенетического белка 7 в культуральной среде клеток остеобластов человека hFOB 1.19 (АТСС CRL-11372), при трансфекции этих клеток ДНК-вектором VTvaf17- ВМР7, несущим ген ВМР7, где
культура А - культура клеток остеобластов человека hFOB 1.19, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль)
культура В - культура клеток остеобластов человека hFOB 1.19, трансфицированных ДНК-вектором VTvaf17
культура С - культура клеток остеобластов человека hFOB 1.19, трансфицированных ДНК-вектором VTvaf17- ВМР7, несущим ген ВМР7.
На фиг. 10 представлена диаграмма концентрации белка COL1A2 в биоптатах кожи трех пациентов после введения в кожу этих пациентов генотерапевтического ДНК-вектора VTvaf17- COL1A2 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A2.
На фиг. 12 отмечены следующие элементы:
П1I - биоптат кожи пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A2
П1II - биоптат кожи пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо)
П1III- биоптат кожи пациента П1 из интактного участка,
П2I - биоптат кожи пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A2
П2II - биоптат кожи пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо)
П2III - биоптат кожи пациента П2 из интактного участка,
П3I - биоптат кожи пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A2
П3II - биоптат кожи пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо)
П3III - биоптат кожи пациента П3 из интактного участка
На фиг. 11 представлена диаграмма концентрации белка COL1A1 в биоптатах хрящевой ткани трех пациентов после введения в хрящевую ткань этих пациентов генотерапевтического ДНК-вектора VTvaf17- COL1A1 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A1.
На фиг. 13 отмечены следующие элементы:
П1I - биоптат хрящевой ткани пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A1
П1II - биоптат хрящевой ткани пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо)
П1III - биоптат хрящевой ткани пациента П1 из интактного участка,
П2I - биоптат хрящевой ткани пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A1
П2II - биоптат хрящевой ткани пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо)
П2III - биоптат хрящевой ткани пациента П2 из интактного участка,
П3I - биоптат хрящевой ткани пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A1
П3II - биоптат хрящевой ткани пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо)
П3III - биоптат хрящевой ткани пациента П3 из интактного участка.
На фиг. 12 представлена диаграмма концентрации белка COL1A1 в биоптатах кожи человека после введения в кожу культуры аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17- COL1A1 с целью демонстрации способа применения путем введения аутологичных клеток, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-COL1A1
На фиг. 15 отмечены следующие элементы:
П1А - биоптат кожи пациента П1 в зоне введения культуры аутогенных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-COL1A1
П1В - биоптат кожи пациента П1 в зоне введения аутогенных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17
П1С - биоптат кожи пациента П1 из интактного участка.
На фиг. 13:
На фигуре 13А представлена диаграмма изменения количества белков: белка альфа-1 цепи коллагена I типа (COL1A1), белка альфа-2 цепи коллагена I типа (COL1A2) в костных биоптатах крыс в зоне хирургически-смоделированной травмы после инъекционного введения в травмированную зону крысы:
в 1-й группе смеси генотерапевтических ДНК-векторов VTvaf17- COL1A1, VTvaf17- COL1A2, VTvaf17- ВМР2, VTvaf17-BMP7,
во 2-й группе - неочищенного кальций-фосфатный преципитата генотерапевтических ДНК-векторов VTvaf17-COL1A1, VTvaf17- COL1A2, VTvaf17- ВМР2, VTvaf17- BMP7,
в 3-й группе (контрольной) - физраствора,
 COL1A1
COL1A1
 COL1A2
COL1A2
На фигуре 13В представлена диаграмма изменения количества белков: костного морфогенетического белка 2 (ВМР2), костного морфогенетического белка 7 (ВМР7) в костных биоптатах крыс в зоне хирургически-смоделированной травмы после инъекционного введения в травмированную зону крысы:
в 1-й группе смеси генотерапевтических ДНК-векторов VTvaf17- COL1A1, VTvaf17- COL1A2, VTvaf17- ВМР2, VTvaf17- BMP7,
во 2-й группе - неочищенного кальций-фосфатный преципитата генотерапевтических ДНК-векторов VTvaf17- COL1A1, VTvaf17- COL1A2, VTvaf17- ВМР2, VTvaf17- BMP7,
в 3-й группе (контрольной) - физраствора,
 ВМР2
ВМР2
 ВМР7
ВМР7
На фиг. 14 представлены графики накопления мРНК целевого гена ВМР2 в культуральной среде клеток остеобластов собаки CnOb до трансфекции ДНК-вектором VTvaf17- ВМР2 и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17- ВМР2, где
1 - кДНК гена ВМР2 в клетках остеобластов собаки CnOb до трансфекции ДНК-вектором VTvaf17- BMP2,
2 - кДНК гена ВМР2 в клетках остеобластов собаки CnOb после трансфекции ДНК-вектором VTvaf17- ВМР2,
3 - кДНК гена ACT в клетках остеобластов собаки CnOb до трансфекции ДНК-вектором VTvaf17- ВМР2,
4 - кДНК гена ACT в клетках остеобластов собаки после трансфекции ДНК-вектором VTvaf17-BMP2,
В качестве референтного гена использовали ген актина собаки (ACT), приведенного в базе данных GenBank под номером DQ131478.1.
Реализация изобретения
На основе генотерапевтического ДНК-вектора VTvaf17 размером 3165 п.н. созданы генотерапевтические ДНК-векторы, несущие целевые гены человека - ген COL1A1 белка альфа1-цепи коллагена I типа, или ген COL1A2 белка альфа2-цепи коллагена I типа, или ген костного морфогенетического белка ВМР-2, или ген костного морфогенетического белка ВМР-7, предназначенные для повышения уровня экспрессии этих целевых генов в тканях человека и животных. При этом способ получения каждого генотерапевтического ДНК-вектора, несущего целевые гены человека заключается в том, что в полилинкер генотерапевтического ДНК-вектора VTvaf17 клонируют белок-кодирующую последовательность целевого гена, выбранного из группы генов: COL1A1, COL1A2, ВМР2, ВМР7.
Способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: COL1A1, COL1A2, ВМР2, ВМР7 заключается в том, что:
1. кодирующую часть гена COL1A1 размером 4422 п.н., или гена COL1A2 размером 4128 п.н., или гена ВМР2 размером 1219 п.н., или гена ВМР7 размером 1322 п.н. получали путем выделения суммарной РНК из биологического образца ткани здорового человека с последующим проведением реакции обратной транскрипции и ПЦР-амплификации, с использованием созданных для этого методом химического синтеза олигонуклеотидов, с последующим расщеплением продукта амплификации эндонуклеазами рестрикции  и
и 
2. кодирующую часть целевого гена COL1A1, или COL1A2, или ВМР2, или ВМР7 клонировали в полилинкер генотерапевтического ДНК-вектора VTvaf17 по сайтам  и
и  и получали генотерапевтический ДНК-вектор VTvaf17-COL1A1, SEQ ID №1, или VTvaf17- COL1A2, SEQ ID №2 или VTvaf17-BMP2, SEQ ID №3, или VTvaf17- BMP7, SEQ ID №4. Полученным генотерапевтическим ДНК-вектором VTvaf17, несущий целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7 трансформировали методом электропорации бактерии Escherichia coli SCS110-AF, а селекцию полученных клонов проводили без антибиотиков.
и получали генотерапевтический ДНК-вектор VTvaf17-COL1A1, SEQ ID №1, или VTvaf17- COL1A2, SEQ ID №2 или VTvaf17-BMP2, SEQ ID №3, или VTvaf17- BMP7, SEQ ID №4. Полученным генотерапевтическим ДНК-вектором VTvaf17, несущий целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7 трансформировали методом электропорации бактерии Escherichia coli SCS110-AF, а селекцию полученных клонов проводили без антибиотиков.
3. для подтверждения эффективности созданного генотерапевтического ДНК-вектора VTvaf17- COL1A1, SEQ ID №1, или VTvaf17- COL1A2, SEQ ID №2 или VTvaf17-BMP2, SEQ ID №3, или VTvaf17- BMP7, SEQ ID №4 оценивали:
A) изменение накопления мРНК целевых генов в клетках человека и животного, после трансфекции различных клеточных линий генотерапевтическими ДНК-векторами (методом ПЦР в реальном времени-RT-PCR);
B) изменение количественного уровня целевых белков в культуральной среде клеток человека, после трансфекции различных клеточных линий генотерапевтическими ДНК-векторами (методом иммуноферментного анализа - ИФА);
C) изменение количественного уровня целевых белков в супернатанте биоптатов тканей человека и животного, после введения в эти ткани генотерапевтических ДНК-векторов (методом ИФА);
D) изменение количественного уровня целевых белков в супернатанте биоптатов тканей человека, после введения в эти ткани аутологичных клеток этого человека, трансфицированных генотерапевтическими ДНК-векторами (методом ИФА);
Для подтверждения реализуемости способа применения созданного генотерапевтического ДНК-вектора VTvaf17- COL1A1, SEQ ID №1, или VTvaf17- COL1A2, SEQ ID №2 или VTvaf17-BMP2, SEQ ID №3, или VTvaf17- BMP7, SEQ ID №4 выполняли:
A) трансфекцию генотерапевтическими ДНК-векторами различных клеточных линий человека;
B) введение генотерапевтических ДНК-векторов в различные ткани человека и животного;
C) введение в ткани животного смеси генотерапевтических ДНК-векторов;
D) введение в ткани человека аутологичных клеток, трансфицированных генотерапевтическими ДНК-векторами.
Для подтверждения получения штамма Escherichia coli SCS110-AF/VTvaf17- COL1A1, или штамма Escherichia coli SCS110-AF/VTvaf17- COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7, проводили трансформацию, селекцию и последующее наращивание с выделением плазмидной ДНК.
Для подтверждения технологичности получения и возможности производства в промышленных масштабах генотерапевтического ДНК-вектора VTvaf17- COL1A1, SEQ ID №1, или VTvaf17- COL1A2, SEQ ID №2 или VTvaf17-BMP2, SEQ ID №3, или VTvaf17- BMP7, SEQ ID №4 выполняли:
А) ферментацию в промышленном масштабе штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1 или штамма Escherichia coli SCS110-AF/VTvaf17-COL1A2 или штамма Escherichia coli SCS110-AF/VTvaf17-BMP2, или штамма Escherichia coli SCS 110-AF/VTvaf17- BMP7, каждый из которых содержит генотерапевтический ДНК-вектор VTvaf17, несущий белок-кодирующую последовательность целевого гена, выбранного из группы генов: COL1A1, COL1A2, ВМР2, ВМР7.
Пример 1.
Получение генотерапевтического ДНК-вектора VTvaf17-COL1A1, несущего целевой ген COL1A1.
Генотерапевтический ДНК-вектор VTvaf17-COL1A1 конструировали клонированием кодирующей части гена COL1A1 в ДНК-вектор VTvaf17 по сайтам рестрикции  и
и  . Кодирующую часть гена COL1A1 размером 4422 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
. Кодирующую часть гена COL1A1 размером 4422 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
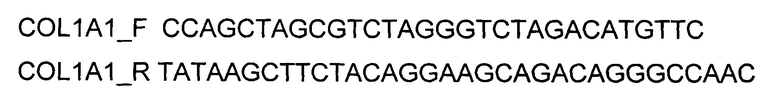
и ПЦР-амплификации с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США) и созданных олигонуклеотидов
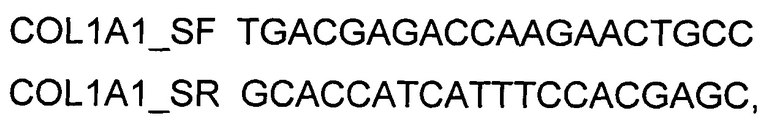
Расщепление продукта амплификации кодирующей части гена COL1A1 и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции  и
и  (New England Biolabs, США).
(New England Biolabs, США).
В результате получали ДНК-вектор VTvaf17- COL1A1 с нуклеотидной последовательностью SEQ ID №1, несущий целевой ген, а именно, ген COL1A1, размером 4422 п.н. с возможностью селекции без антибиотиков со структурой изображенной на фиг. 1.А.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали объединением шести фрагментов ДНК, полученных из разных источников:
(а) область начала репликации (ori) получали путем ПЦР-амплификации участка коммерческой плазмиды pBR322 с внесением точечной мутации;
(б) промоторный регион EF1a получали путем ПЦР-амплификации участка геномной ДНК человека;
(в) терминатор транскрипции hGH-TA получали путем ПЦР-амплификации участка геномной ДНК человека;
(г) регуляторный участок транспозона Tn10 РНК-out получали путем синтеза из олигонуклеотидов;
(д) ген устойчивости к канамицину получали путем ПЦР-амплификации участка коммерческой плазмиды рЕТ-28 человека;
(е) полилинкер получали отжигом двух синтетических олигонуклеотидов.
ПЦР-амплификацию проводили с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs) в соответствии с инструкцией производителя. Фрагменты имеют перекрывающиеся области для возможности их объединения с последующей ПЦР-амплификацией. Объединяли фрагменты (а) и (б) с использованием олигонуклеотидов Ori-F и EF1-R, а также фрагменты (в), (г) и (д) с использованием олигонуклеотидов hGH-F и Kan-R. Далее, полученные участки объединяли путем рестрикции с последующим лигированием по сайтам BamHI и  . В результате получали плазмиду, пока еще не содержащую полилинкер. Для его введения проводили расщепление плазмиды по сайтам
. В результате получали плазмиду, пока еще не содержащую полилинкер. Для его введения проводили расщепление плазмиды по сайтам  и
и 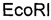 , и лигирование с фрагментом (е). Таким образом, получали вектор размером 3165 п.н., несущий ген устойчивости к канамицину, который фланкирован сайтами рестрикции
, и лигирование с фрагментом (е). Таким образом, получали вектор размером 3165 п.н., несущий ген устойчивости к канамицину, который фланкирован сайтами рестрикции  . Далее этот участок выщепляли по сайтам рестрикции
. Далее этот участок выщепляли по сайтам рестрикции  , после чего оставшийся фрагмент лигировали сам на себя. Таким образом получали генотерапевтический ДНК-вектор VTvaf17 размером 3165 п.н., который является рекомбинантным, с возможностью селекции без антибиотиков.
, после чего оставшийся фрагмент лигировали сам на себя. Таким образом получали генотерапевтический ДНК-вектор VTvaf17 размером 3165 п.н., который является рекомбинантным, с возможностью селекции без антибиотиков.
Пример 2.
Получение генотерапевтического ДНК-вектора VTvaf17-COL1A2, несущего целевой ген COL1A2.
Генотерапевтический ДНК-вектор VTvaf17- COL1A2 конструировали клонированием кодирующей части гена COL1A2 в ДНК-вектор VTvaf17 по сайтам рестрикции  и
и  . Кодирующую часть гена COL1A2 размером 4128 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
. Кодирующую часть гена COL1A2 размером 4128 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
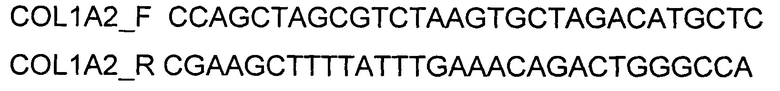
и ПЦР-амплификации с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США) и созданных олигонуклеотидов
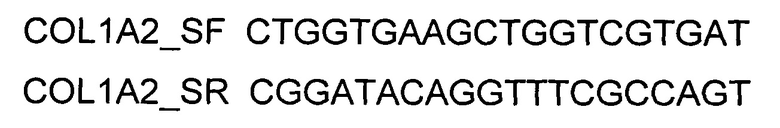
Расщепление продукта амплификации кодирующей части гена COL1A1 и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции  и
и  (New England Biolabs, США).
(New England Biolabs, США).
В результате получили ДНК-вектор VTvaf17- COL1A2 размером 7269 п.н. с нуклеотидной последовательностью SEQ ID №2, несущий целевой ген, а именно, ген COL1A2, размером 4128 п.н. с возможностью селекции без антибиотиков, со структурой изображенной на фиг. 1.В.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали по Примеру 1.
Пример 3
Получение ДНК-вектора VTvaf17-ВМР2, несущего целевой ген ВМР2 человека.
Генотерапевтический ДНК-вектор VTvaf17- ВМР2 конструировали клонированием кодирующей части гена ВМР2 в ДНК-вектор VTvaf17 по сайтам рестрикции  и
и  . Кодирующую часть гена ВМР2 размером 1219 п.н. получали путем выделения суммарной РНК из биопсийного образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
. Кодирующую часть гена ВМР2 размером 1219 п.н. получали путем выделения суммарной РНК из биопсийного образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
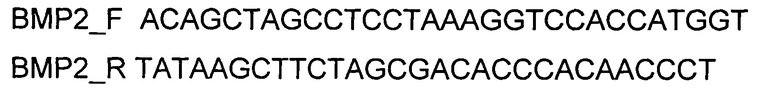
и ПЦР-амплификации с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США) и созданных олигонуклеотидов
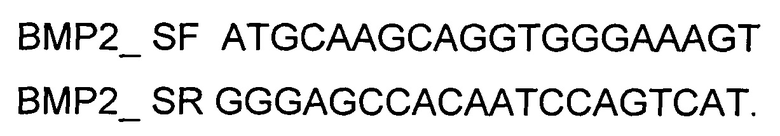
Расщепление продукта амплификации кодирующей части гена COL1A1 и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции  и
и  (New England Biolabs, США).
(New England Biolabs, США).
В результате получили генотерапевтический ДНК-вектор VTvaf17-ВМР2 размером 4360 п.н. с нуклеотидной последовательностью SEQ ID №3 несущий целевой ген ВМР2, размером 1219 п.н. с возможностью селекции без антибиотиков, со структурой изображенной на фиг. 1.С.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали по Примеру 1.
Пример 4.
Получение генотерапевтического ДНК-вектора VTvaf17-ВМР7, несущего целевой ген ВМР7.
Генотерапевтический ДНК-вектор VTvaf17- ВМР7 конструировали клонированием кодирующей части гена ВМР7 в ДНК-вектор VTvaf17 по сайтам рестрикции  и
и  . Кодирующую часть гена ВМР7 размером 1322 п.н. получали путем выделения суммарной РНК из биопсийного образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
. Кодирующую часть гена ВМР7 размером 1322 п.н. получали путем выделения суммарной РНК из биопсийного образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и созданных олигонуклеотидов
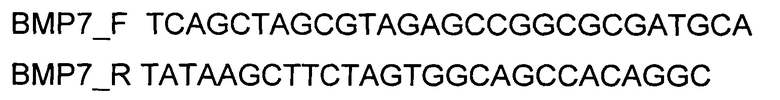
и ПЦР-амплификации с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США) и созданных олигонуклеотидов
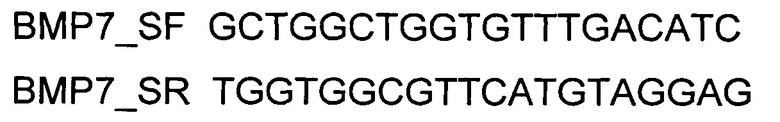
Расщепление продукта амплификации кодирующей части гена COL1A1 и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции  и
и  (New England Biolabs, США).
(New England Biolabs, США).
В результате получили ДНК-вектор VTvaf17- ВМР7 размером 4463 п.н. с нуклеотидной последовательностью SEQ ID №4, несущий целевой ген, а именно, ген ВМР7, размером 1322 п.н. с возможностью селекции без антибиотиков со структурой изображенной на фиг. 1.D.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали по Примеру 1.
Пример 5.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего целевой ген COL1A1. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген COL1A1.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1 оценивали изменения накопления мРНК целевого гена COL1A1, в клетках первичной культуры фибробластов кожи человека HDFa (АТСС PCS-201-012) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17- COL1A1.
Клетки первичной культуры фибробластов кожи человека HDFa выращивали в среде Fibroblast Basal Medium (АТСС PCS-201-030) с добавлением компонентов входящих в состав набора Fibroblast Growth Kit-Serum-Free (АТСС PCS-201-040) в атмосфере 5% CO2 при 37°С. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку.
Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17- COL1A1 проводили следующим образом. В пробирке №1 к 25 мкл среды Opti-MEM (Gibco) добавляли 1 мкл раствора ДНК-вектора VTvaf17-COL1A1 (концентрация 500 нг/мкл) и 1 мкл реагента Р3000. Аккуратно перемешивали легким встряхиванием. В пробирке №2 к 25 мкл среды Opti-MEM (Gibco) добавляли 1 мкл раствора Lipofectamine 3000. Аккуратно перемешивали легким встряхиванием. Добавляли содержимое пробирки №1 к содержимому пробирки №2, инкубировали 5 мин при комнатной температуре. Полученный раствор по каплям добавляли к клеткам в объеме 40 мкл.
В качестве контроля использовали фибробласты кожи человека HDFa, трансфицированные генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена (кДНК гена COL1A1 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано для упрощения визуализации). Подготовку контрольного вектора VTvaf17 для трансфекции проводили как описано выше.
Суммарную РНК из трансфицированных клеток выделяли следующим образом. В лунку с клетками добавляли 1 мл Trizol Reagent (ThermoFisher Scientific) и гомогенизировали с последующим прогреванием в течение 5 мин при 65°С. Далее образец центрифугировали при 14000 g в течение 10 мин и снова прогревали в течение 10 мин при 65°С. Далее добавляли 200 мкл хлороформа, плавно перемешивали и центрифугировали при 14000 g в течение 10 мин. Затем отбирали водную фазу, добавляли к ней 1/10 объема 3М ацетата натрия рН5.2 и равный объем изопропилового спирта. Инкубировали образец при -20°С в течение 10 мин с последующим центрифугированием при 14000 g в течение 10 мин. Осадок промывали 1 мл 70% этилового спирта, высушивали на воздухе и растворяли в 10 мкл воды, свободной от РНКаз. Для определения уровня экспрессии мРНК гена COL1A1 после трансфекции использовали метод ПЦР в режиме реального времени (SYBR GreenRealTimePCR). Для амплификации кДНК, специфичной для гена COL1A1 человека, использовали олигонуклеотиды COL1A1_SF и COL1A1_SR согласно Примеру 1. Длина продукта амплификации - 756 п.н. В качестве референтного гена использовали ген бета-2-микроглобулина В2М.
ПЦР-амплификацию проводили с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, США) в режиме реального времени в 20 мкл амплификационной смеси, содержащей: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 mM хлорида магния, по 0,5 мкМ каждого праймера, 5 мкл суммарной РНК. Реакцию осуществляли на амплификаторе CFX96 (Bio-Rad, USA) при следующих условиях: 1 цикл обратной транскрипции при 42°С 30 минут, денатурация 98°С - 15 мин, затем 40 циклов, включающих денатурацию 94°С - 15 сек, отжиг праймеров 60°С - 30 сек и элонгацию 72°С - 120 сек. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов COL1A1 и В2М. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов COL1A1 и В2М, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager2.1.
С целью подтверждения увеличения экспрессии гена COL1A1 в культуре клеток фибробластов кожи человека HDFa после трансфекции данных клеток генотерапевтическим ДНК-вектором VTvaf17- COL1A1 на фиг. 2 приведены графики накопления ПЦР-продуктов, из которых следует, что в результате трансфекции первичной культуры фибробластов кожи человека HDFa генотерапевтическим ДНК-вектором VTvaf17- COL1A1, уровень специфической мРНК гена COL1A1 человека вырос многократно. Это свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-COL1A1 для повышения уровня экспрессии гена COL1A1 в эукариотических клетках.
Пример 6.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего целевой ген COL1A2. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген COL1A2.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего целевой ген COL1A2, оценивали изменения накопления мРНК целевого гена COL1A2 в фибробластах кожи человека через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-COL1A2.
Культуру фибробластов кожи человека выращивали следующим образом. Брали биопсийный образец из зоны за мочкой уха пациента используя устройство для взятия биопсии DERMO PUNCH (компания Medax, USA). Кожу пациента в зоне отбора биоптата предварительно дезинфицировали 70% раствором этанола, промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 10 куб. мм, масса - около 11 мг. Образец помещали в буферный раствор, содержащий 0,05% трипсин (Gibco), 10 мМ ЭДТА. Клетки инкубировали при помешивании на магнитной мешалке при 37°С. Далее суспензию клеток фильтровали, используя фильтры с диамером пор 100 мкм (Nalgen, США), центрифугировали в течение 10 мин 130 g, осадок ресуспендировали в 15 мл среды Fibroblast Basal Medium (АТСС PCS-201-030) с добавлением компонентов входящих в состав набора Fibroblast Growth Kit-Serum-Free (АТСС PCS-201-040), помещали во флакон площадью 75 см2 (Eppendorf) и инкубировали в течение 36-72 часов при 37°С в атмосфере 5% CO2. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 4*104 клеток/лунку в среде того же состава. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17- COL1A2, экспрессирующим ген COL1A2 человека проводили, как описано в примере 5. В качестве контроля использовали эти же клетки, трансфицированные генотерапевтическим ДНК-вектором VTvaf17 (кДНК гена COL1A2 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано для упрощения визуализации). Выделение суммарной РНК из трансфицированных клеток и построение первой цепи кДНК проводили как описано в примере 5. Для определения уровня экспрессии мРНК гена COL1A2 после трансфекции использовали метод ПЦР в режиме реального времени (SYBR GreenRealTimePCR). Для амплификации кДНК, специфичной для гена COL1A2 человека, использовали олигонуклеотиды COL1A2_SF и COL1A2_SR согласно Примеру 2. Длина продукта амплификации - 853 п.н. В качестве референтного гена использовали ген бета-2-микроглобулина В2М.
ПЦР-амплификацию проводили с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, США) в режиме реального времени в 20 мкл амплификационной смеси, содержащей: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 mM хлорида магния, по 0,5 мкМ каждого праймера, 5 мкл суммарной РНК. Реакцию осуществляли на амплификаторе CFX96 (Bio-Rad, USA) при следующих условиях: 1 цикл обратной транскрипции при 42°С - 30 минут, денатурация 98°С - 15 мин, затем 40 циклов, включающих денатурацию 94°С - 15 сек, отжиг праймеров 60°С - 30 сек и элонгацию 72°С - 120 сек. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов COL1A2 и В2М. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов COL1A2 и В2М, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager2.1.
С целью подтверждения увеличения экспрессии гена COL1A2 в культуре фибробластов кожи человека после трансфекции данных клеток генотерапевтическим ДНК-вектором VTvaf17-COL1A2, на фиг. 3 приведены графики накопления ПЦР-продуктов, из которых следует, что в результате трансфекции клеток культуры фибробластов кожи человека генотерапевтическим ДНК-вектором VTvaf17-COL1A2, несущим целевой ген COL1A2 человека, уровень специфической мРНК гена COL1A2 человека вырос многократно. Это свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-COL1A2. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-COL1A2 для повышения уровня экспрессии гена COL1A2 в эукариотических клетках.
Пример 7.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР2, несущего целевой ген ВМР2. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген ВМР2.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-BMP2, несущего целевой ген ВМР2, оценивали изменения накопления мРНК целевого гена ВМР2 в клетках остеосаркомы человека MG-63 (АТСС CRL-1427) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-BMP2.
Клетки остеосаркомы человека MG-63 культивировали в среде DMEM (Gibco) с добавлением 10% сыворотки эмбрионов коров (Gibco) и 10 мкг/мл гентамицина при 37 С в атмосфере 5% CO2. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17- ВМР2, экспрессирующим ген ВМР2 человека, проводили как описано в примере 5. В качестве контроля использовали клетки остеосаркомы человека MG-63, трансфицированные генотерапевтическим ДНК-вектором VTvaf17 (кДНК гена ВМР2 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано для упрощения визуализации). Выделение суммарной РНК из трансфицированных клеток и построение первой цепи кДНК проводили как описано в примере 5. Для определения уровня экспрессии мРНК гена ВМР2 после трансфекции использовали метод ПЦР в режиме реального времени (SYBR GreenRealTimePCR). Для амплификации кДНК, специфичной для гена ВМР2 человека, использовали олигонуклеотиды BMP2_SF и BMP2_SR согласно Примеру 3. Длина продукта амплификации -353 п.н. В качестве референтного гена использовали ген бета-2-микроглобулина В2М.
ПЦР-амплификацию проводили с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, США) в режиме реального времени в 20 мкл амплификационной смеси, содержащей: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 mM хлорида магния, по 0,5 мкМ каждого праймера, 5 мкл суммарной РНК. Реакцию осуществляли на амплификаторе CFX96 (Bio-Rad, USA) при следующих условиях: 1 цикл обратной транскрипции при 42°С - 30 минут, денатурация 98°С - 15 мин, затем 40 циклов, включающих денатурацию 94°С - 15 сек, отжиг праймеров 60°С - 30 сек и элонгацию 72°С - 30 сек. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов ВМР2 и В2М. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов ВМР2 и В2М, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager2.1.
С целью подтверждения увеличения экспрессии гена ВМР2 в клетках остеосаркомы человека MG-63 после трансфекции данных клеток генотерапевтическим ДНК-вектором VTvaf17- ВМР2 на фиг. 4 приведены графики накопления ПЦР-продуктов, из которых следует, что в результате трансфекции клеток остеосаркомы человека MG-63 генотерапевтическим ДНК-вектором VTvaf17- ВМР2, несущим целевой ген ВМР2 человека, уровень специфической мРНК гена ВМР2 человека вырос многократно. Это свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17- ВМР2. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-ВМР2 для повышения уровня экспрессии гена ВМР2 в эукариотических клетках.
Пример 8.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР7, несущего целевой ген. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген ВМР7..
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР7 оценивали изменения накопления мРНК целевого гена ВМР7 в первичной культуре остеобластов человека hFOB 1.19 (АТСС CRL-11372) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-ВМР7.
Линию первичной культуры остеобластов человека hFOB 1.19 выращивают в смеси сред F12 (Gibco, США) и DMEM (Gibco, США) (1:1), содержащей 2 мМ L-глутамина, 0.3 мг/мл G418 и 10% сыворотки эмбрионов коров (Gibco, США) в атмосфере 5% CO2 при 37°С. Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку.
Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-ВМР7, экспрессирующим ген ВМР7 человека, проводили как описано в примере 5. В качестве контроля использовали клетки остеобластов человека hFOB 1.19, трансфицированные генотерапевтическим ДНК-вектором VTvaf17 (кДНК гена ВМР7 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано для упрощения визуализации). Выделение суммарной РНК из трансфицированных клеток и построение первой цепи кДНК проводили как описано в примере 5. Для определения уровня экспрессии мРНК гена ВМР7 после трансфекции использовали метод ПЦР в режиме реального времени (SYBR GreenRealTimePCR). Для амплификации кДНК, специфичной для гена ВМР7 человека, использовали олигонуклеотиды BMP7_SF и BMP7_SR согласно Примеру 4. Длина продукта амплификации - 459 п.н. В качестве референтного гена использовали ген бета-2-микроглобулина В2М.
ПЦР-амплификацию проводили с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, США) в режиме реального времени в 20 мкл амплификационной смеси, содержащей: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 mM хлорида магния, по 0,5 мкМ каждого праймера, 5 мкл суммарной РНК. Реакцию осуществляли на амплификаторе CFX96 (Bio-Rad, USA) при следующих условиях: 1 цикл обратной транскрипции при 42°С 30 минут, денатурация 98°С - 15 мин, затем 40 циклов, включающих денатурацию 94°С - 15 сек, отжиг праймеров 60°С - 30 сек и элонгацию 72°С - 30 сек. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов ВМР7 и В2М. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов ВМР7 и В2М, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1.
С целью подтверждения увеличения экспрессии гена ВМР7 в клетках остеобластов человека hFOB 1.19 после трансфекции данных клеток генотерапевтическим ДНК-вектором VTvaf17-ВМР7, несущим целевой ген ВМР7 на фиг. 5 приведены графики накопления ПЦР-продуктов, из которых следует, что в результате трансфекции первичной культуры остеобластов человека hFOB 1.19 генотерапевтическим ДНК-вектором VTvaf17- ВМР7, несущим целевой ВМР7 человека, уровень специфической мРНК гена ВМР7 человека вырос многократно. Это свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР7 и подтверждает реализуемость способа его использования. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-ВМР7 для повышения уровня экспрессии гена ВМР7 в эукариотических клетках.
Пример 9.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего целевой ген, а именно, ген COL1A1 и реализуемости способа его использования.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего целевой ген, а именно, ген COL1A1 и реализуемости способа его использования оценивали изменение количества белка альфа-1 цепи коллагена I типа в культуральной среде клеток первичной культуры фибробластов кожи человека HDFa (АТСС PCS-201-012) после трансфекции этих клеток ДНК-вектором VTvaf17- COL1A1, несущим ген COL1A1 человека.
Для оценки изменения количества белка альфа-1 цепи коллагена I типа, использовали клетки первичной культуры фибробластов кожи человека HDFa, которые выращивали по примеру 5.
В качестве транспортной молекулы использовали дендримеры SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия), в качестве контроля - водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена COL1A1 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17-COL1A1, несущий ген COL1A1 человека SEQ ID No: 1 (С). Приготовление комплекса ДНК/дендример проводили по методике производителя (QIAGEN, SuperFect Transfection Reagent Handbook, 2002) с некоторыми изменениями. Для трансфекции клеток в одной лунке 24-луночного планшета к 1 мкг ДНК-вектора, растворенного в буфере ТЕ, добавляли среду DMEM не содержащую антибиотиков, до конечного объема 60 мкл, затем добавляли 5 мкл SuperFect Transfection Reagent и осторожно перемешивали пятикратным пипетированием. Комплекс инкубировали при комнатной температуре в течение 10-15 мин. Далее отбирали из лунок культуральную среду, лунки промывали 1 мл буфера PBS. К образовавшемуся комплексу добавляли 350 мкл полной среды DMEM, содержащей 10 мкг/мл гентамицина, осторожно перемешивали и добавляли к клеткам. Клетки инкубировали с комплексом 2-3 часа при 37°С в атмосфере, содержащей 5% CO2.
Затем осторожно удаляли среду, промывали клеточный монослой 1 мл буфера PBS. Затем добавляли полную среду DMEM, содержащую 10 мкг/мл гентамицина и инкубировали 24-48 часов при 37°С в атмосфере 5% CO2.
После трансфекции к 0,5 мл культуральной жидкости приливали 0,1 мл 1N HCl, тщательно перемешивали и инкубировали 10 минут при комнатной температуре. Затем нейтрализовали смесь, добавляя 0,1 мл 1.2N NaOH/0.5M HEPES (рН 7-7,6) и тщательно перемешивали. Отбирали супернатант и использовали его для количественного определения целевого белка. Количественное определение белка COL1A1 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human collagen, type I, alpha 1 (COL1A1) ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка альфа-1 цепи коллагена I типа, входящим в состав набора. Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/).
Диаграмма, полученная в результате анализа представлена на фиг. 6, из которой следует, что трансфекция клеток первичной культуры фибробластов кожи человека HDFa генотерапевтическим ДНК-вектором VTvaf17-COL1A1, несущим ген COL1A1, приводит к увеличению количества белка альфа-1 цепи коллагена I типа по сравнению с контрольными образцами, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-COL1A1 и подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген COL1A1 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17- COL1A1 для повышения уровня экспрессии COL1A1 в эукариотических клетках.
Пример 10.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего целевой ген, а именно, ген COL1A2 и реализуемости способа его использования.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего целевой ген, а именно, ген COL1A2 и реализуемости способа его использования оценивали изменение количества белка альфа-2 цепи коллагена I типа в культуральной среде клеток культуры фибробластов кожи человека после трансфекции этих клеток ДНК-вектором VTvaf17-COL1A2, несущим ген COL1A2 человека.
Для оценки изменения количества белка альфа-2 цепи коллагена I типа клетки культуры фибробластов кожи человека выращивали как описано в примере 6. В качестве транспортной молекулы использовали дендримеры SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия), в качестве контроля - водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена COL1A2 (В), в качестве трансфицирующих агентов - ДНК-вектор VTvaf17- COL1A2, несущий ген COL1A2 человека SEQ ID No: 2 (С). Приготовление комплекса ДНК-дендример и трансфекцию культуры клеток фибробластов кожи человека проводили как описано в примере 9.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение продукта гена COL1A2 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human Collagen Type I Alpha 2 (COL1A2) ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка альфа-2 цепи коллагена I типа, входящим в состав набора
Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/).
Диаграмма, полученная в результате анализа представлена на фиг. 7, из которой следует, что трансфекция клеток фибробластов кожи человека генотерапевтическим ДНК-вектором VTvaf17-COL1A2, несущим ген COL1A2, приводит к увеличению количества белка альфа-2 цепи коллагена I типа по сравнению с контрольными образцами, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A2 и подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген COL1A2 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-COL1A2 для повышения уровня экспрессии COL1A2 в эукариотических клетках.
Пример 11.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17- ВМР2, несущего целевой ген, а именно, ген ВМР2 и реализуемости способа его использования.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР2, несущего целевой ген ВМР2, и реализуемости способа его использования оценивали изменение количества костного морфогенетического белка 2 в культуральной среде клеток остеосаркомы человека MG-63 (АТСС CRL-1427) после трансфекции этих клеток ДНК-вектором VTvaf17- ВМР2, несущим ген ВМР2 человека.
Для оценки изменения количества костного морфогенетического белка 2 культуру клеток остеосаркомы человека MG-63 выращивали как описано в примере 7. В качестве транспортной молекулы использовали дендримеры SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия), в качестве контроля - водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена ВМР2 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17- ВМР2, несущий целевой ген ВМР2 человека SEQ ID No: 3 (С). Приготовление комплекса ДНК-дендример и трансфекцию клеток остеосаркомы человека MG-63 проводили согласно Примеру 9.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение продукта гена ВМР-2 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human ВМР-2, ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией костного морфогенетического белка 2, входящим в состав набора
Диаграмма, полученная в результате анализа представлена на фиг. 8, из которой следует, что трансфекция клеток остеосаркомы человека MG-63 генотерапевтическим ДНК-вектором VTvaf17- ВМР2, несущим ген ВМР2, приводит к увеличению количества костного морфогенетического белка 2 по сравнению с контрольными образцами, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР2 и подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген ВМР2 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17- ВМР2 для повышения уровня экспрессии ВМР2 в эукариотических клетках.
Пример 12.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17- ВМР7, несущего целевой ген, а именно, ген ВМР7 и реализуемости способа его использования.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР7, несущего целевой ген ВМР7, и реализуемости способа его использования оценивали изменение количества костного морфогенетического белка 7 в культуральной среде клеток остеобластов человека hFOB 1.19 (АТСС CRL-11372) после трансфекции этих клеток ДНК-вектором VTvaf17-ВМР7, несущим ген ВМР7 человека.
Для оценки изменения количества костного морфогенетического белка 7 культуру клеток остеобластов человека hFOB 1.19 выращивали как описано в примере 8. В качестве транспортной молекулы использовали дендримеры SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия), в качестве контроля - водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена ВМР7 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17-ВМР7, несущий целевой ген ВМР7 человека SEQ ID No: 4 (С). Приготовление комплекса ДНК-дендример и трансфекцию клеток остеобластов человека hFOB 1.19 проводили согласно Примеру 9.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение продукта гена ВМР-7 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human ВМР-7, ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией костного морфогенетического белка 7, входящим в состав набора
Диаграмма, полученная в результате анализа представлена на фиг. 9, из которой следует, что трансфекция клеток клеток остеобластов человека hFOB 1.19 генотерапевтическим ДНК-вектором VTvaf17- ВМР7, несущим ген ВМР7, приводит к увеличению количества костного морфогенетического белка 7 по сравнению с контрольными образцами, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР7 и подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген ВМР7 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17- ВМР7 для повышения уровня экспрессии ВМР7 в эукариотических клетках.
Пример 13.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего ген COL1A2, для повышения экспрессии белка COL1A2 в тканях человека
С целью анализа изменения количества белка альфа-2 цепи коллагена I типа трем пациентам вводили в кожу предплечья генотерапевтический ДНК-вектор VTvaf17- COL1A2, несущий ген COL1A2 и параллельно вводили плацебо, представляющее собой генотерапевтический ДНК-вектор VTvaf17, не содержащий ген COL1A2.
Пациент 1, мужчина 65 лет, (П1); пациент 2, женщина 67 лет, (П2); пациент 3, мужчина, 62 года, (П3). В качестве транспортной системы использовали полиэтиленимин Transfection reagent cGMP grade in-vivo-jetPEI (Polyplus Transfection, Франция). Генотерапевтический ДНК-вектор VTvaf17- COL1A2, который содержит ген COL1A2 и генотерапевтический ДНК-вектор VTvaf17, используемый в качестве плацебо, растворяли в стерильной воде степени очистки Nuclease-Free. Комплексы ДНК- cGMP grade in-vivo-jetPEI готовили в соответствии с рекомендациями производителя.
Генотерапевтический ДНК-вектор VTvaf17 (плацебо) и генотерапевтический ДНК вектор VTvaf17- COL1A2 вводили в количестве 1 мг для каждой генетической конструкции тоннельным методом иглой 30G на глубину 3 мм. Объем вводимого раствора генотерапевтического ДНК-вектора VTvaf17 (плацебо) и генотерапевтического ДНК вектора VTvaf17-COL1A2 -0,3 мл для каждой генетической конструкции. Очаги введения каждой генетической конструкции располагались на участке предплечья на расстоянии 8-10 см друг от друга.
Биопсийные образцы отбирали на 2-е сутки после введения генетических конструкций генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков кожи пациентов в зоне введения генотерапевтического ДНК вектора VTvaf17-COL1A2, несущего ген COL1A2 (I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (II), а также из интактных участков кожи (III), используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL, Италия). Кожу пациентов в зоне отбора биоптата предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 10 куб. мм, масса - около 11 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000 g. Отбирали супернатант и использовали его для количественного определения целевого белка альфа-2 цепи коллагена I типа методом твердофазного иммуноферментного анализа (ELISA), используя набор Human Collagen Type I Alpha 2 (COL1A2) ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка альфа-2 цепи коллагена I типа, входящим в состав набора. Диаграммы, полученные в результате анализа представлены на фиг. 10.
Из фигуры 10 следует, что в коже всех трех пациентов в области введения генотерапевтического ДНК вектора VTvaf17-COL1A2, несущего целевой ген COL1A2 человека, произошло увеличение количества белка альфа-2 цепи коллагена I типа в сравнении с количеством белка альфа-2 цепи коллагена I типа в области введения генотерапевтического ДНК-вектора VTvaf17 (плацебо), не содержащего ген COL1A2 человека, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-COL1A2 и подтверждает реализуемость способа его применения, в частности при введении генотерапевтического ДНК-вектора в ткани/ органы человека.
Пример 14.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего ген COL1A1, для повышения экспрессии белка COL1A1 в тканях человека
С целью анализа изменения количества белка альфа-1 цепи коллагена I типа трем пациентам вводили в хрящевую ткань ушных раковин с тыльной стороны генотерапевтический ДНК-вектор VTvaf17- COL1A1, несущий ген COL1A1 и параллельно вводили плацебо, представляющее собой генотерапевтический ДНК-вектор VTvaf17, не содержащий ген COL1A1.
Пациент 1, мужчина 65 лет, (П1); пациент 2, женщина 67 лет, (П2); пациент 3, мужчина, 62 года, (П3). В качестве транспортной системы использовали полиэтиленимин Transfection reagent cGMP grade in-vivo-jetPEI (Polyplus Transfection, Франция). Генотерапевтический ДНК-вектор VTvaf17- COL1A1, который содержит ген COL1A1 и генотерапевтический ДНК-вектор VTvaf17, используемый в качестве плацебо, растворяли в стерильной воде степени очистки Nuclease-Free. Комплексы ДНК- cGMP grade in-vivo-jetPEI готовили в соответствии с рекомендациями производителя.
Генотерапевтический ДНК-вектор VTvaf17 (плацебо) и генотерапевтический ДНК вектор VTvaf17- COL1A1 вводили в количестве 1 мг для каждой генетической конструкции тоннельным методом иглой 30G на глубину 1-2 мм в хрящевую ткань ушных раковин с тыльной стороны. Объем вводимого раствора генотерапевтического ДНК-вектора VTvaf17 (плацебо) и генотерапевтического ДНК вектора VTvaf17- COL1A1 - 0,2 мл для каждой генетической конструкции. Очаги введения биологически активной генно-терапевтической субстанции и плацебо располагались на расстоянии 2-3 см друг от друга.
Биопсийные образцы отбирали на 3-е сутки после введения генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков кожи пациентов в зоне введения генотерапевтического ДНК вектора VTvaf17- COL1A1, несущего ген COL1A1 (I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (II), а также из интактных участков (III), методом чрескожной пункционного биопсии при помощи одноразовой ручной биопсийной иглы и далее проводили манипуляции по примеру 13.
Количество белка альфа-1 цепи коллагена I типа оценивали в супернатантах биоптатов хрящевой ткани пациентов методом твердофазного иммуноферментного анализа (ИФА ELISA), используя набор Human collagen, type I, alpha 1 (COL1A1) ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка альфа-1 цепи коллагена I типа, входящим в состав набора. Диаграммы, полученные в результате анализа представлены на фиг. 11.
Из фигуры 11 следует, что в хрящевой ткани всех трех пациентов в области введения генотерапевтического ДНК вектора VTvaf17- COL1A1, несущего целевой ген COL1A1 человека, произошло увеличение количества белка альфа-1 цепи коллагена I типа в сравнении с количеством белка альфа-1 цепи коллагена I типа в области введения генотерапевтического ДНК-вектора VTvaf17 (плацебо), не содержащего ген COL1A1 человека, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1 и подтверждает реализуемость способа его применения, в частности при введении генотерапевтического ДНК-вектора в хрящевую ткань человека.
Пример 15.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17-COL1A1, несущего ген COL1A1 и реализуемости способа его применения для повышения уровня экспрессии белка COL1A1 в тканях человека путем введения аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17- COL1A1.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего ген COL1A1 и реализуемости способа его применения оценивали изменения количества белка COL1A1 в коже человека при введении в кожу пациента культуры аутогенных фибробластов этого пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-COL1A1.
Пациенту вводили в кожу предплечья соответствующую культуру аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17- COL1A1, несущим ген COL1A1, и параллельно вводили плацебо, представляющее собой культуру аутогенных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим ген COL1A1.
Первичную культуру фибробластов человека выделяли из биоптатов кожи пациента. Используя устройство для взятия биопсии кожи Epitheasy 3.5 (Medax SRL, Италия) брали образец биоптата кожи из зоны, защищенной от действия ультрафиолета, а именно за ушной раковиной или с боковой внутренней поверхности в зоне локтевого сустава, размером около 10 кв. мм, массой - около 11 мг. Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Культивирование первичной культуры клеток осуществляли при 37°С в атмосфере, содержащей 5% CO2 в среде DMEM с 10% фетальной телячьей сывороткой и ампициллином 100 Ед/мл. Пересев культуры и смену культуральной среды осуществляли каждые 2 дня. Общая продолжительность роста культуры не превышала 25-30 дней. Из культуры клеток отбирали аликвоту, содержащую 5×104 клеток. Культуру фибробластов пациента трансфицировали генотерапевтическим ДНК-вектором VTvaf17- COL1A1, несущим ген COL1A1 или плацебо - вектор VTvaf17, не несущий целевой ген COL1A1.
Трансфекцию осуществляли с помощью катионного полимера полиэтиленимина JETPEI (Polyplus transfection, Франция), согласно инструкции фирмы-производителя. Клетки культивировали 72 часа и затем вводили пациенту. Введение пациенту культуры аутогенных фибробластов этого пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-COL1A1, и плацебо, представляющее собой культуру аутогенных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, осуществляли туннельным методом в область предплечья иглой 30G длиной 13 мм на глубину около 3 мм. Концентрация модифицированных аутогенных фибробластов в вводимой суспензии составляла примерно 5 млн клеток на 1 мл суспензии, количество вводимых клеток не превышало 15 млн. Очаги введения культуры аутогенных фибробластов располагались на расстоянии 8-10 см друг от друга.
Биопсийные образцы отбирали на 4-е сутки после введения культуры аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17- COL1A1, несущим целевой ген, а именно, ген COL1A1 и плацебо. Взятие биопсии осуществляли из участков кожи пациента в зоне введения культуры аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17- COL1A1, несущим целевой ген COL1A1 (С), культуры аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим целевой ген COL1A1 (плацебо) (В), а также из участков интактной кожи (А), используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL, Италия) и далее проводили манипуляции по примеру 13.
Количество белка альфа-1 цепи коллагена I типа оценивали в супернатантах биоптатов кожи пациентов методом твердофазного иммуноферментного анализа (ИФА ELISA), используя набор Human collagen, type I, alpha 1 (COL1A1) ELISA Kit (MyBioSource, США) согласно методике производителя с детекцией оптической плотности при длине волны 450 нм при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка альфа-1 цепи коллагена I типа, входящим в состав набора. Диаграммы, полученные в результате анализа, представлены на фиг. 12.
Из фигуры 12 следует, что в коже пациента в области введения культуры аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-COL1A1, несущим ген COL1A1, произошло увеличение количества белка COL1A1 в сравнении с количеством белка COL1A1 в области введения культуры аутогенных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим ген COL1A1 (плацебо), что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-COL1A1 и подтверждает реализуемость способа его применения для повышения уровня экспрессии COL1A1 в тканях/ органах человека, в частности при введении в кожу аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17- COL1A1.
Пример 16.
Подтверждение эффективности и реализуемости способа сочетанного применения генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего целевой ген COL1A1, генотерапевтического ДНК-вектора VTvaf17- COL1A2, несущего целевой ген COL1A2, генотерапевтического ДНК-вектора VTvaf17-ВМР2, несущего целевой ген ВМР2, генотерапевтического ДНК-вектора VTvaf17- ВМР7, несущего целевой ген ВМР7 для повышения уровня экспрессии белков COL1A1, COL1A2, ВМР2 и ВМР7 в тканях млекопитающих..
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего целевой ген COL1A1, ДНК-вектора VTvaf17- COL1A2, несущего целевой ген, COL1A2, ДНК-вектора VTvaf17- ВМР2, несущего целевой ген ВМР2, ДНК-вектора VTvaf17- ВМР7, несущего целевой ген ВМР7 и реализуемости способа использования данных векторов оценивали изменение количества белков: белка альфа-1 цепи коллагена I типа, белка альфа-2 цепи коллагена I типа, костного морфогенетического белка 2, костного морфогенетического белка 7 соответственно в зоне предварительно хирургически-смоделированной травмы большеберцовой кости крысы Вистар (самцы, в возрасте 22-24 недель).
Было сформировано 3 группы животных по 11 особей в каждой.
Всем животным под анестезией была сделана хирургическая операция по созданию дефекта большеберцовой кости. В частности, по наружной поверхности правой голени был произведен разрез кожи длиной до 3.0 см. Далее были раздвинуты мышцы и осуществлен доступ к большеберцовой кости. В диафизарной области сверлом диаметром 2 мм вручную была произведена остеотомия до костного канала. После этого с помощью стального мандрена - иглы диаметром 1.6 мм по направлению к коленному эпифизу был пробит дефект глубиной примерно 10 мм. Дефект был заполнен через катетер РЕ-50 с помощью гамильтоновского шприца:
в 1-й группе смесью генотерапевтических ДНК-векторов VTvaf17- COL1A1, VTvaf17- COL1A2, VTvaf17- ВМР2, VTvaf17-BMP7 в объеме 20 мкл. (50 мкг.), причем раствор готовили из лиофилизата смеси кДНК и физраствора,
во 2-й группе - неочищенным кальций-фосфатный преципитатом смеси генотерапевтических ДНК-векторов VTvaf17-COL1A1, VTvaf17- C0L1A2, VTvaf17- BMP2, VTvaf17- BMP7 в объеме 20 мкл. (50 мкг.),
в 3-й группе (контрольной) - физраствором в объеме 20 мкл..
После моделирования дефекта большеберцовой кости и введения тестируемых ДНК-векторов и физраствора дефект герметизировали хирургическим воском.
Биопсийные образцы отбирали через 72 часа после введения смеси генотерапевтических ДНК-векторов и плацебо. Взятие биопсии осуществляли после некропсии животных из участков травмы в зоне введения смеси четырех генотерапевтических ДНК-векторов, несущих целевые гены COL1A1, COL1A2, ВМР2, ВМР7 (1-й группы), в зоне введения неочищенного кальций-фосфатного преципитата смеси четырех генотерапевтических ДНК-векторов, несущих целевые гены COL1A1, COL1A2, ВМР2, ВМР7 (2-й группы), в зоне введения физраствора (3-й группы). Масса каждого биопсийного образца составляла около 20 мг. Далее проводили манипуляции по примеру 13.
Количественное определение продуктов генов COL1A1, COL1A2, ВМР2, ВМР7 проводили методом твердофазного иммуноферментного анализа (ELISA), используя наборы Human collagen, type I, alpha 1 (COL1A1) ELISA Kit (MyBioSource, США), Human Collagen Type I Alpha 2 (COL1A2) ELISA Kit (MyBioSource, США, Human BMP-2, ELISA Kit (MyBioSource, США), Human BMP-7, ELISA Kit (MyBioSource, США). Подготовку тестируемых образцов, измерение и обработку результатов проводили как описано в Примерах 9, 10, 11, 12.
Диаграммы, полученные в результате анализа представлены на фиг. 13А и 13В, на которых показано, что в травмированной зоне животных в области введения преципитата смеси четырех генотерапевтических ДНК-векторов: VTvaf17-COL1A1, несущего целевой ген, COL1A1 человека, VTvaf17-COL1A2, несущего целевой COL1A2 человека, VTvaf17- ВМР2, несущего целевой ген ВМР2 человека, VTvaf17- ВМР7, несущего целевой ген ВМР7 человека в 1-й группе животных произошло существенное увеличение количества белков: белка альфа-1 цепи коллагена I типа, белка альфа-2 цепи коллагена I типа, костного морфогенетического белка 2, костного морфогенетического белка 7 в сравнении соответственно с количеством белков COL1A1 альфа-1 цепи коллагена I типа, альфа-2 цепи коллагена I типа, костного морфогенетического белка 2, костного морфогенетического белка 7 в контрольной 3-й группе. Также показано, что что в травмированной зоне животных в области введения смеси четырех генотерапевтических ДНК-векторов: VTvaf17- COL1A1, несущего целевой ген, COL1A1 человека, VTvaf17- COL1A2, несущего целевой COL1A2 человека, VTvaf17- ВМР2, несущего целевой ген ВМР2 человека, VTvaf17- ВМР7, несущего целевой ген ВМР7 человека в 2-й группе животных произошло умеренное увеличение количества белков: белка альфа-1 цепи коллагена I типа, белка альфа-2 цепи коллагена I типа, костного морфогенетического белка 2, костного морфогенетического белка 7 соответственно в сравнении с количеством белков COL1A1 альфа-1 цепи коллагена I типа, альфа-2 цепи коллагена I типа, костного морфогенетического белка 2, костного морфогенетического белка 7 в контрольной 3-й группе. Приведенные результаты подтверждает реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17- COL1A1, несущего целевой ген COL1A1, генотерапевтического ДНК-вектора VTvaf17-COL1A2, несущего целевой ген, COL1A2, генотерапевтического ДНК-вектора VTvaf17- ВМР2, несущего целевой ген ВМР2, генотерапевтического ДНК-вектора VTvaf17- ВМР7, несущего целевой ген ВМР7 для повышения уровня экспрессии белков COL1A1, COL1A2, ВМР2 и ВМР7 в тканях животного, в частности при введении этих генотерапевтических ДНК-векторов в костную ткань млекопитающих и свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17- COL1A1, генотерапевтического ДНК-вектора VTvaf17- COL1A2, генотерапевтического ДНК-вектора VTvaf17- ВМР2, генотерапевтического ДНК-вектора VTvaf17- ВМР7.
Пример 17.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР2, несущего целевой ген ВМР2 и реализуемости способа его применения для повышения уровня экспрессии костного морфогенетического белка 2 в клетках млекопитающих.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР2, несущего целевой ген ВМР2 человека, оценивали изменение накопления мРНК целевого гена ВМР2 в клетках остеобластов собаки CnOb (Cell Applications, Inc., USA) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-ВМР2.
Клетки линии остеобластов собак (CnOb) выращивали согласно методики производителя (https://www.cellapplications.com/canine-osteoblasts-cnob). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-ВМР2, несущим целевой ген ВМР2 человека и ДНК-вектором VTvaf17, не несущим ген ВМР2 человека (контороль) проводили как описано в примере 8. Суммарную РНК из трансфицированных клеток и построение первой цепи кДНК проводили как описано в примере 5. Для определения уровня экспрессии мРНК гена ВМР2 после трансфекции использовали метод ПЦР в режиме реального времени (SYBR GreenRealTimePCR) как описано в примере 3. В качестве референтного гена использовали ген актина собаки (ACT).
В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности генов ВМР2 и ACT. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов ВМР2 и ACT, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1. (Bio-Rad, USA).
Графики накопления ПЦР-продуктов, полученные в результате анализа представлены на фиг. 14., на которых показано, что в результате трансфекции клеток остеобластов собаки CnOb генотерапевтическим ДНК-вектором VTvaf17- ВМР2, несущим целевой ген ВМР2 человека, уровень специфической мРНК гена ВМР2 вырос многократно, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-ВМР2. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-ВМР2 для повышения уровня экспрессии гена ВМР2 в клетках млекопитающих.
Пример 18.
Штамм Escherichia coli SCS110-AF/VTvaf17-COL1A1 или штамм Escherichia coli SCS110-AF/VTvaf17-COL1A2 или штамм Escherichia coli SCS110-AF/VTvaf17-BMP2 или штамм Escherichia coli SCS110-AF/VTvaf17-BMP7, несущий генотерапевтический ДНК-вектор, способ его получения.
Конструирование штамма для наработки в промышленных масштабах генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A1 или COL1A2 или ВМР2 или ВМР7: а именно штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1, или штамма Escherichia coli SCS110-AF/VTvaf17-COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17-BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7, несущего генотерапевтический ДНК-вектор VTvaf17- COL1A1, или VTvaf17- COL1A2, или VTvaf17-ВМР2, или VTvaf17- ВМР7 соответственно для его наработки с возможностью селекции без использования антибиотиков заключается в получении электрокомпетентных клеток штамма Escherichia coli SCS110-AF с проведением электропорации этих клеток генотерапевтическим ДНК-вектором VTvaf17- COL1A1, или ДНК-вектором VTvaf17- COL1A2, или ДНК-вектором VTvaf17-ВМР2, или ДНК-вектором VTvaf17- ВМР7, после чего клетки высеивали на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола. При этом штамм Escherichia coli SCS110-AF для наработки генотерапевтического ДНК-вектора VTvaf17 или генотерапевтических ДНК-векторов на его основе с возможностью положительной селекции без использования антибиотиков получали путем конструирования линейного фрагмента ДНК, содержащего регуляторный элемент RNA-in транспозона Tn10 для селекции без применения антибиотиков размером 64 п.н., ген левансахаразы sacB, продукт которого обеспечивает селекцию на сахарозо-содержащей среде размером 1422 п.н., ген устойчивости к хлорамфениколу catR, необходимый для отбора клонов штамма, в которых прошла гомологичная рекомбинация размером 763 п.н. и две гомологичные последовательности, обеспечивающие процесс гомологичной рекомбинации в области гена recA с одновременной его инактивацией размером 329 п.н. и 233 п.н., после чего проводили трансформацию клеток Escherichia coli путем электропорации и отбирали клоны, выжившие на среде, содержащей 10 мкг/мл хлорамфеникола.
Пример 19.
Способ производства в промышленных масштабах генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7.
Для подтверждения технологичности получения и возможности производства в промышленных масштабах генотерапевтического ДНК-вектора VTvaf17- COL1A1 (SEQ ID №1), или VTvaf17- COL1A2 (SEQ ID №2), или VTvaf17-BMP2 (SEQ ID №3), или VTvaf17- BMP7 (SEQ ID №4), каждый из которых несет целевой ген, а именно, COL1A1, или COL1A2, или ВМР2, или ВМР7 проводили масштабную ферментацию штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1 (регистрационный № ВКПМ В-13165, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 43033 или штамма Escherichia coli SCS110-AF/VTvaf17-COL1A2 (регистрационный № ВКПМ B-13164, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 43035 или штамма Escherichia coli SCS110-AF/VTvaf17-BMP2 (регистрационный № ВКПМ В-13167, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 43034), или штамма Escherichia coli SCS110-AF/VTvaf17- BMP7 (регистрационный № ВКПМ B-13166, INTERNATIONAL DEPOSITARY AUTHORITY № NCIMB 43036), каждый из которых содержит генотерапевтический ДНК-вектор VTvaf17, несущий целевой ген, а именно COL1A1, или COL1A2, или ВМР2, или ВМР7. Каждый штамм Escherichia coli SCS110-AF/VTvaf17-COL1A1, или Escherichia coli SCS110-AF/VTvaf17-COL1A2, или Escherichia coli SCS110-AF/VTvaf17- BMP2, или Escherichia coli SCS 110-AF/VTvaf17- BMP7 получали на базе штамма Escherichia coli SCS110-AF (Cell and Gene Therapy LLC, PIT Ltd) по примеру 18 путем электропорации компетентных клеток этого штамма генотерапевтическим ДНК-вектором VTvaf17-COL1A1, или VTvaf17- COL1A2, или VTvaf17-ВМР2, или VTvaf17-ВМР7, несущим целевой ген, а именно, COL1A1, или COL1A2, или ВМР2, или ВМР7, с последующим высевом трансформированных клеток на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы и отбором отдельных клонов.
Ферментацию полученного штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1, несущего генотерапевтический ДНК-вектор VTvaf17- COL1A1 проводили в ферментере объемом 10 л с последующим выделением генотерапевтического ДНК-вектора VTvaf17- COL1A1.
Для ферментации штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1 готовили среду, содержащую на 10 л: 100 г триптон, 50 г дрожжевой экстракт (Becton Dickinson), доводили водой до 8800 мл и автоклавировали при 121°С 20 мин, затем добавляли 1200 мл 50% (вес/объем) сахарозы. Далее засевали в колбу затравочную культуру штамма Escherichia coli SCS110-AF/VTvaf17- COL1A1 в объеме 100 мл. Инкубировали в шейкере-инкубаторе 16 ч при 30°С. Переносили затравочную культуру в ферментер Techfors S (Infors НТ, Швейцария), растили до достижения стационарной фазы. Контроль осуществляли измерением оптической плотности культуры при длине волны 600 нм. Клетки осаждали центрифугированием 30 мин при 5000-10000 g. Супернатант удаляли, клеточную массу ресуспендировали в 10% по объему фосфатно-солевого буфера. Повторно центрифугировали 30 мин при 5000-10000 g. Супернатант удаляли, к клеточной массе добавляли раствор 20 мМ TrisCl, 1 мМ ЭДТА, 200 г/л сахароза, рН 8,0 в объеме 1000 мл, тщательно перемешивали до образования гомогенной суспензии. Добавляли раствор яичного лизоцима до конечной концентрации 100 мкг/мл. Инкубировали 20 мин на льду при бережном перемешивании. Далее, добавляли 2500 мл раствора 0,2 М NaOH, 10 г/л додецилсульфат натрия, инкубировали 10 мин на льду при бережном перемешивании, затем добавляли 3500 мл раствора 3 М ацетат натрия, 2 М уксусная кислота, рН 5-5,5, инкубировали 10 мин на льду при бережном перемешивании. Полученный образец центрифугировали 20-30 мин при 15000 g или более. Раствор аккуратно декантировали, от остатков осадка избавлялись фильтрацией через грубый фильтр (фильтровальную бумагу). Добавляли РНКазу A (Sigma) до конечной концентрации 20 нг/мл, инкубировали ночь 16 ч при комнатной температуре. Раствор центрифугировали 20-30 мин при 15000 g, затем фильтровали через мембранный фильтр с порами 0,45 мкм (Millipore). Далее проводили ультрафильтрацию через мембрану размером отсечения 100 кДа (Millipore) и разбавляли до начального объема буфером 25 мМ TrisCl, рН 7.0. Операцию повторяли три-четыре раза. Наносили раствор, на колонку с 250 мл сорбента DEAE sepharose HP (GE, США), уравновешенную раствором 25 мМ TrisCl, рН 7.0. После нанесения образца колонку промывали тремя объемами этого же раствора, а затем проводили элюцию генотерапевтического ДНК-вектора VTvaf17- COL1A1 линейным градиентом от раствора 25 мМ TrisCl, рН 7.0 до раствора 25 мМ TrisCl, рН 7.0, 1М NaCl в объеме пяти объемов колонки. Контроль элюции осуществляли по оптической плотности сходящего раствора при 260 нм. Хроматографические фракции, содержащие генотерапевтический ДНК-вектор VTvaf17- COL1A1, объединяли и проводили гель-фильтрацию на сорбенте Superdex 200 (GE, США). Колонку уравновешивали фосфатно-солевым буфером. Контроль элюции осуществляли по оптической плотности сходящего раствора при 260 нм, фракции анализировали электрофорезом в агарозном геле. Фракции, содержащие генотерапевтический ДНК-вектор VTvaf17-COL1A1 объединяли и хранили при -20°С. Для оценки воспроизводимости техпроцесса обозначенные технологические операции повторяли пятикратно. Все технологические операции для штаммов Escherichia coli SCS110-AF/VTvaf17-COL1A2, или Escherichia coli SCS110-AF/VTvaf17- BMP2, или Escherichia coli SCS110-AF/VTvaf17- BMP7 проводили аналогичным образом.
Воспроизводимость техпроцесса и количественные характеристики выхода конечного продукта подтверждают технологичность получения и возможность производства в промышленных масштабах генотерапевтического ДНК-вектора VTvaf17- COL1A1, или VTvaf17- COL1A2, или VTvaf17-ВМР2, или VTvaf17- ВМР7.
Таким образом, задача, поставленная в данном изобретении, а именно: конструирование генотерапевтических ДНК-векторов, несущих целевые гены человека на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, связанных с необходимостью повышения уровня экспрессии этих целевых генов оптимально сочетающего в себе:
I) возможность безопасного использования для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора генов антибиотикорезистентности;
II) длину, обеспечивающую эффективное проникновение в клетку-мишень;
III) наличие регуляторных элементов, обеспечивающих эффективную экспрессию целевых генов и, в то же время, не представляющих собой нуклеотидные последовательности вирусных геномов;
IV) технологичность получения и возможность наработки в промышленных масштабах, а также задача по конструированию штаммов, несущих эти генотерапевтические ДНК-вектора для производства в промышленных масштабах этих генотерапевтических ДНК-векторов решена, что подтверждается примерами: для п. I - пример 1, 2, 3, 4, 5; для п. II - пример 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17; для п. III - пример 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17; для п. IV - пример 18, 19.
Промышленная применимость:
Все представленные выше примеры подтверждают промышленную применимость предлагаемого генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7 для повышения уровня экспрессии этих целевых генов, способа его получения и использования, штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1 или Escherichia coli SCS110-AF/VTvaf17-COL1A2 или Escherichia coli SCS110-AF/VTvaf17-BMP2 или Escherichia coli SCS110-AF/VTvaf17-BMP7, несущего генотерапевтический ДНК-вектор, способа его получения, способа производства в промышленных масштабах генотерапевтического ДНК-вектора.
Перечень сокращений
VTvaf17 - вектор генотерапевтический, не содержащий последовательностей вирусных геномов и маркеров антибиотико-резистентности (vector therapeutic virus-antibiotic-free)
ДНК - дезоксирибонуклеиновая кислота
кДНК - комплементарная дезоксирибонуклеиновая кислота
РНК - рибонуклеиновая кислота
мРНК - матричная рибонуклеиновая кислота
п.н. - пар нуклеотидов
ПЦР - полимеразная цепная реакция
RT-PCR - ПЦР в режиме реального времени
мл - миллилитр, мкл - микролитр
куб. мм - кубический миллиметр
л - литр
мкг – микрограмм
мг – миллиграмм
г – грамм
мкМ – микромоль
мМ – миллимоль
мин – минута
сек - секунда
об/мин - обороты в минуту
нм – нанометр
см – сантиметр
мВт - милливатт
о.е. ф-относительная единица флуоресценции
РВС - фосфатно-солевой буфер









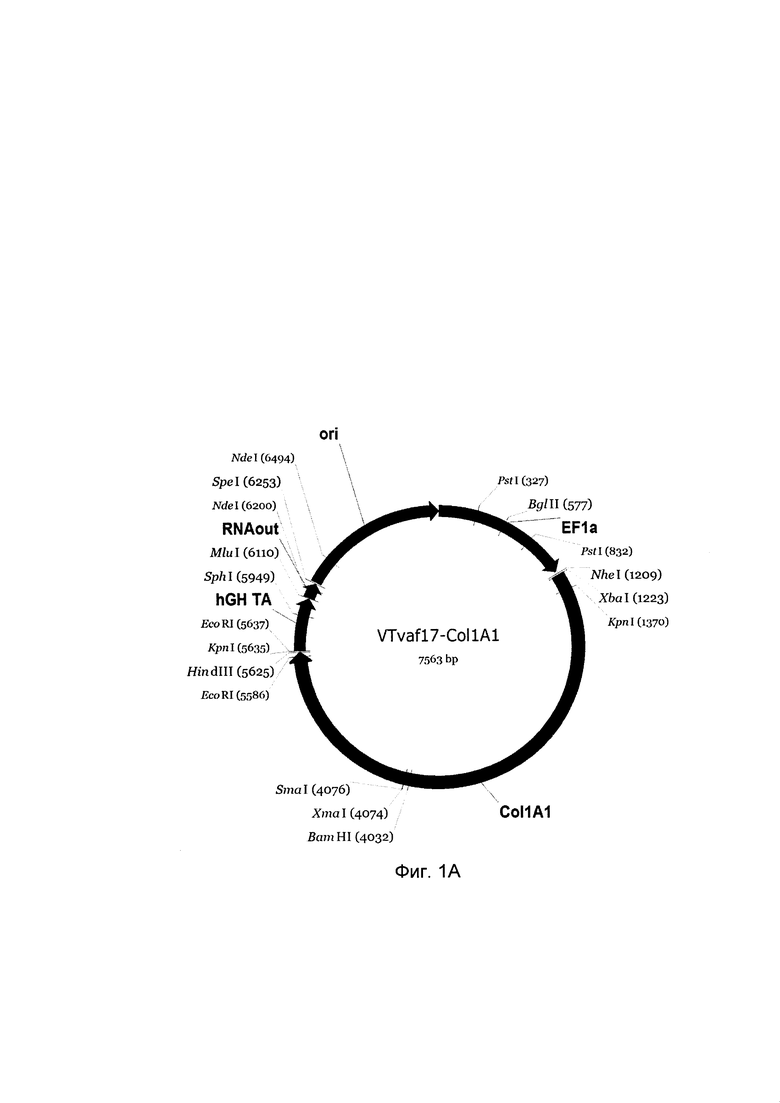

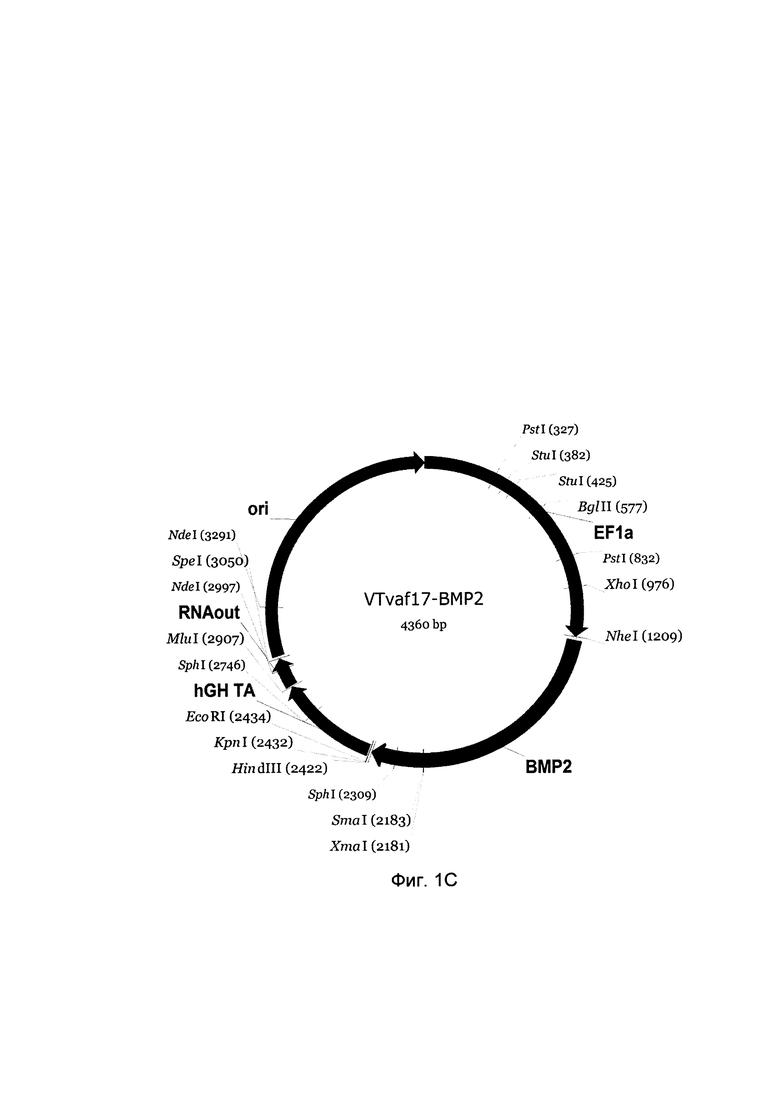
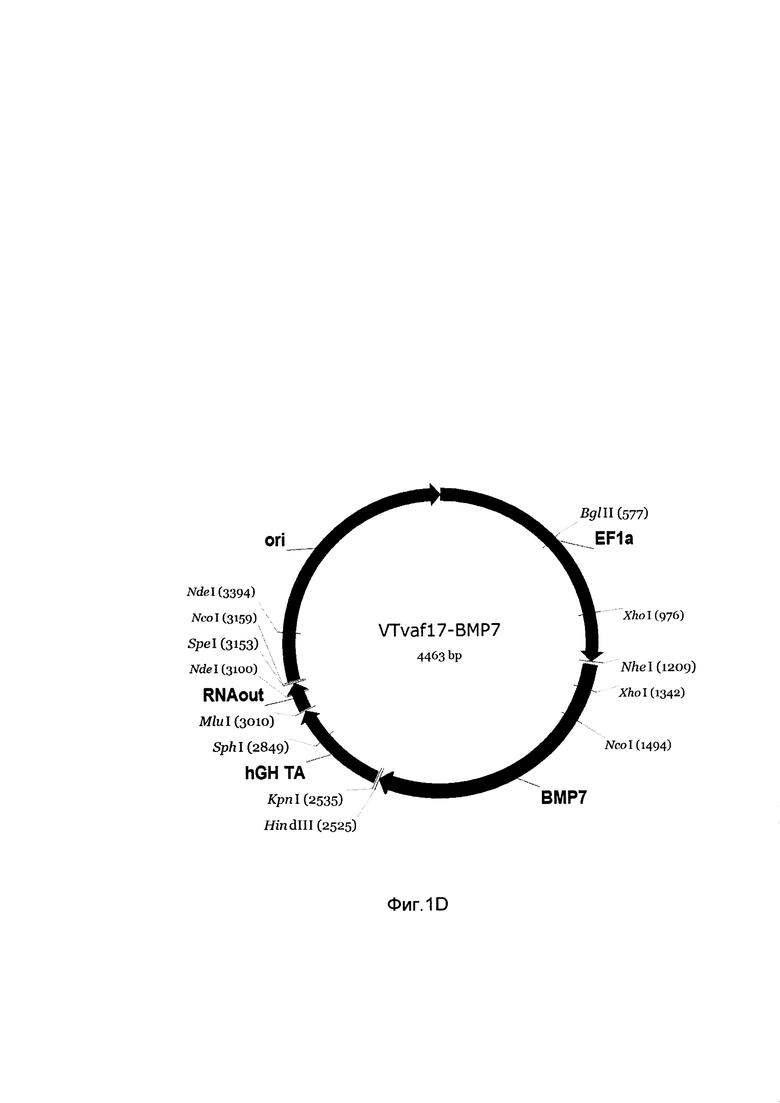
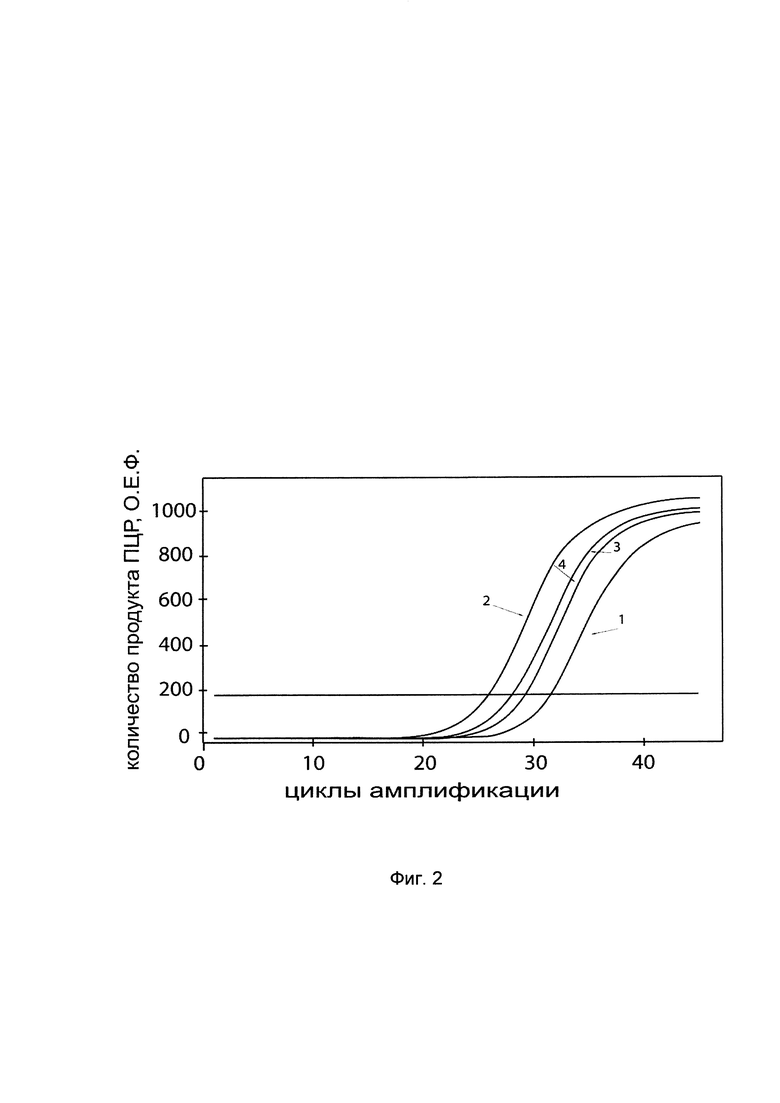
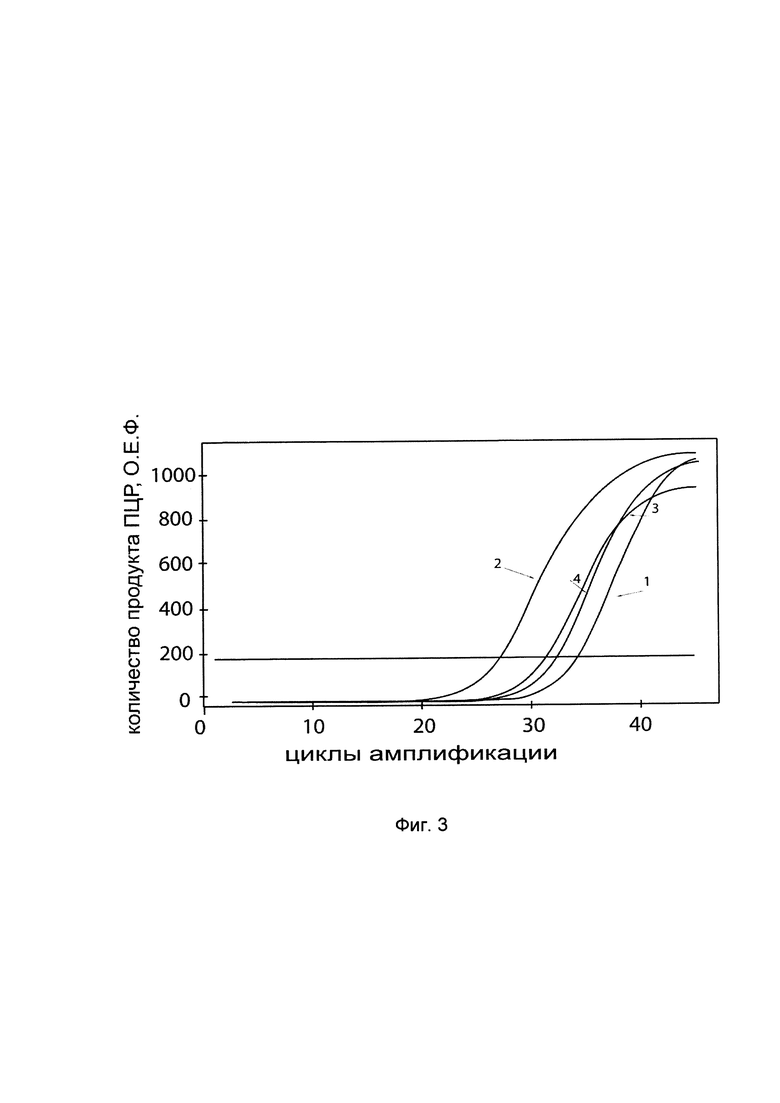
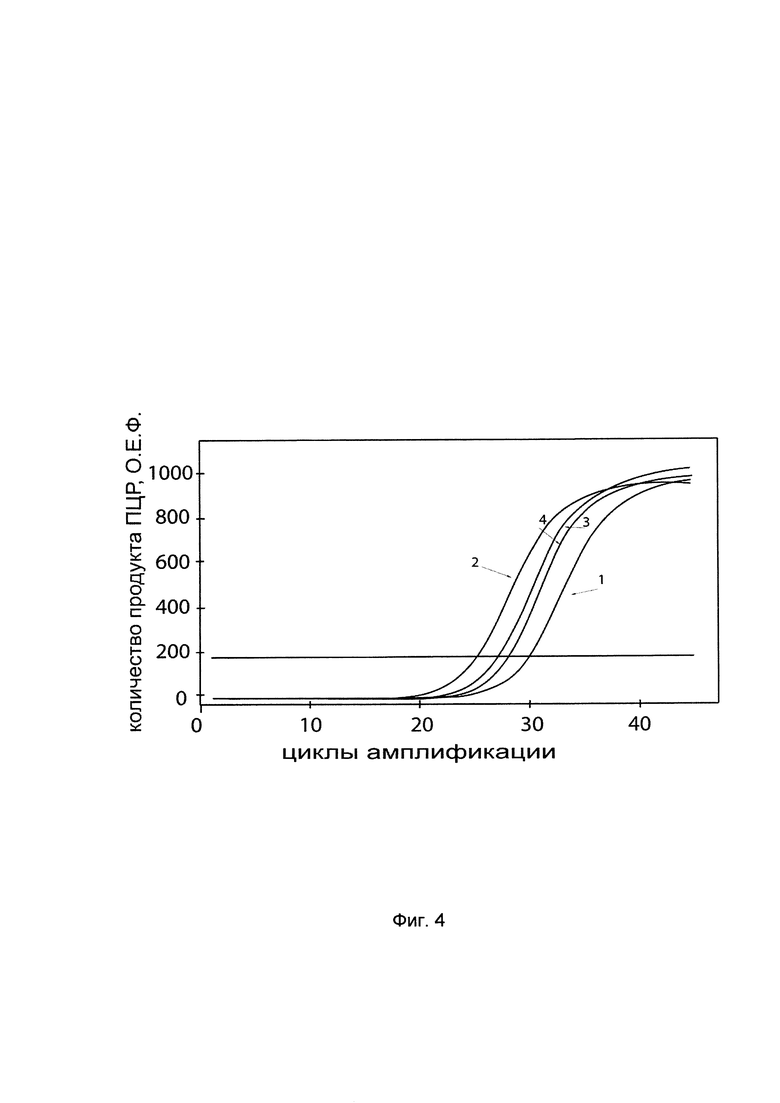
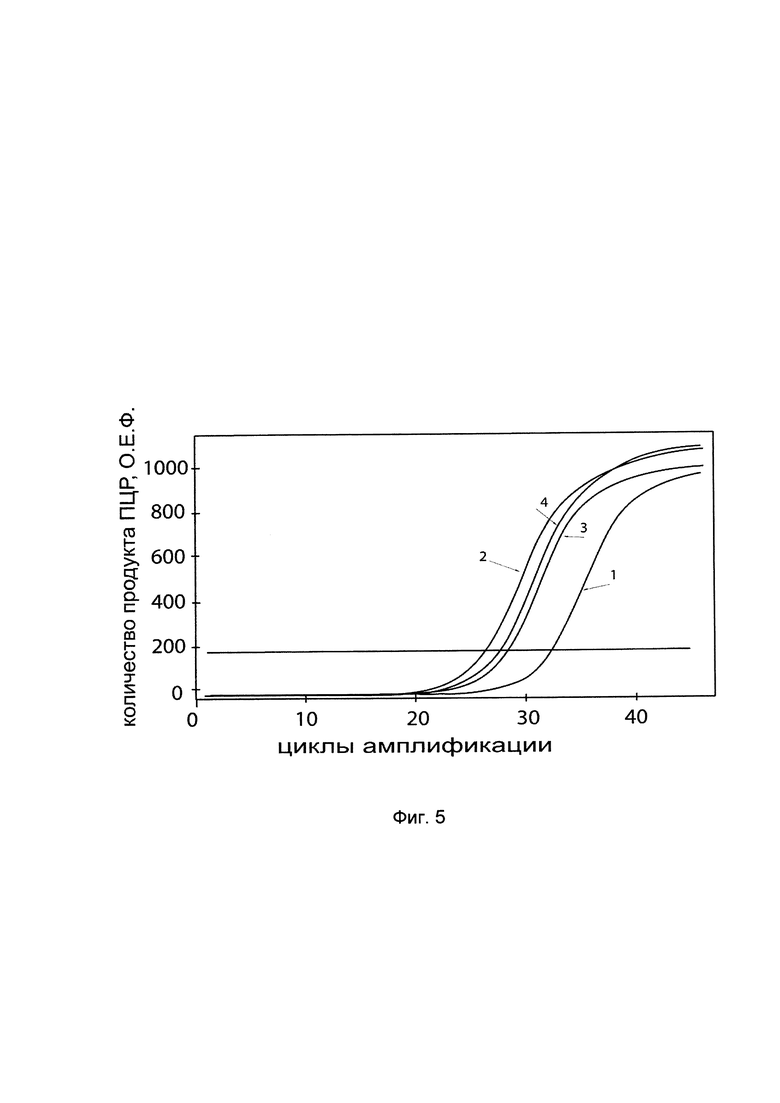
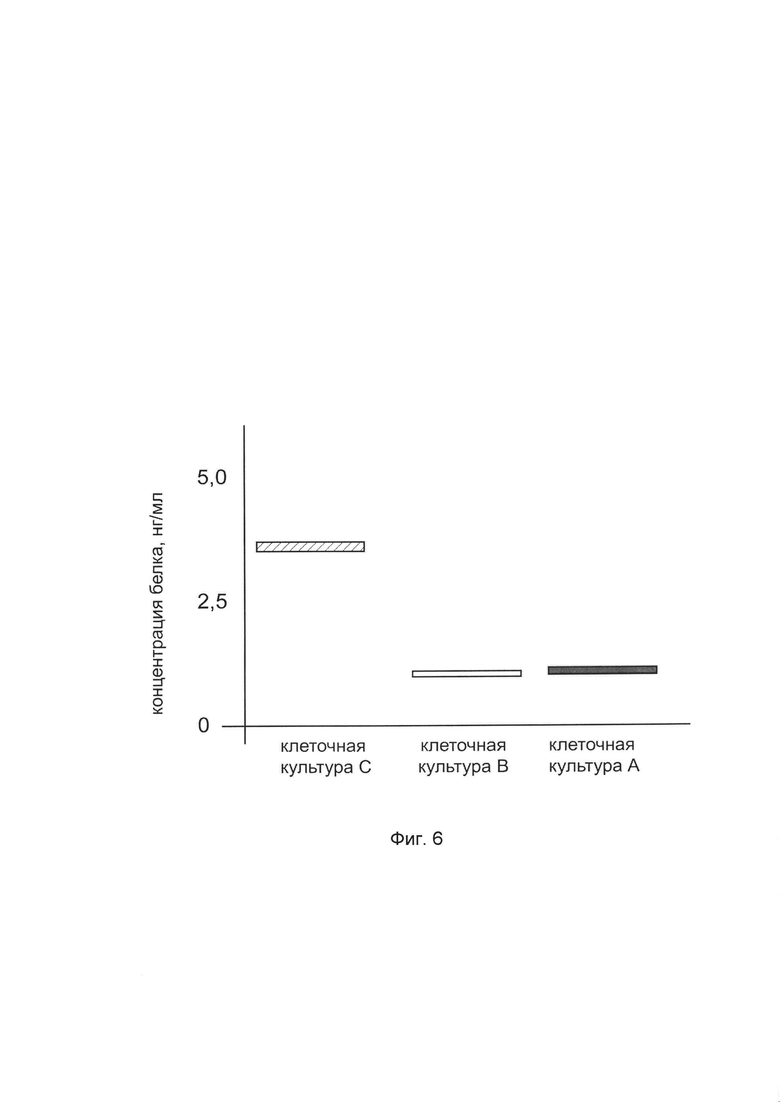
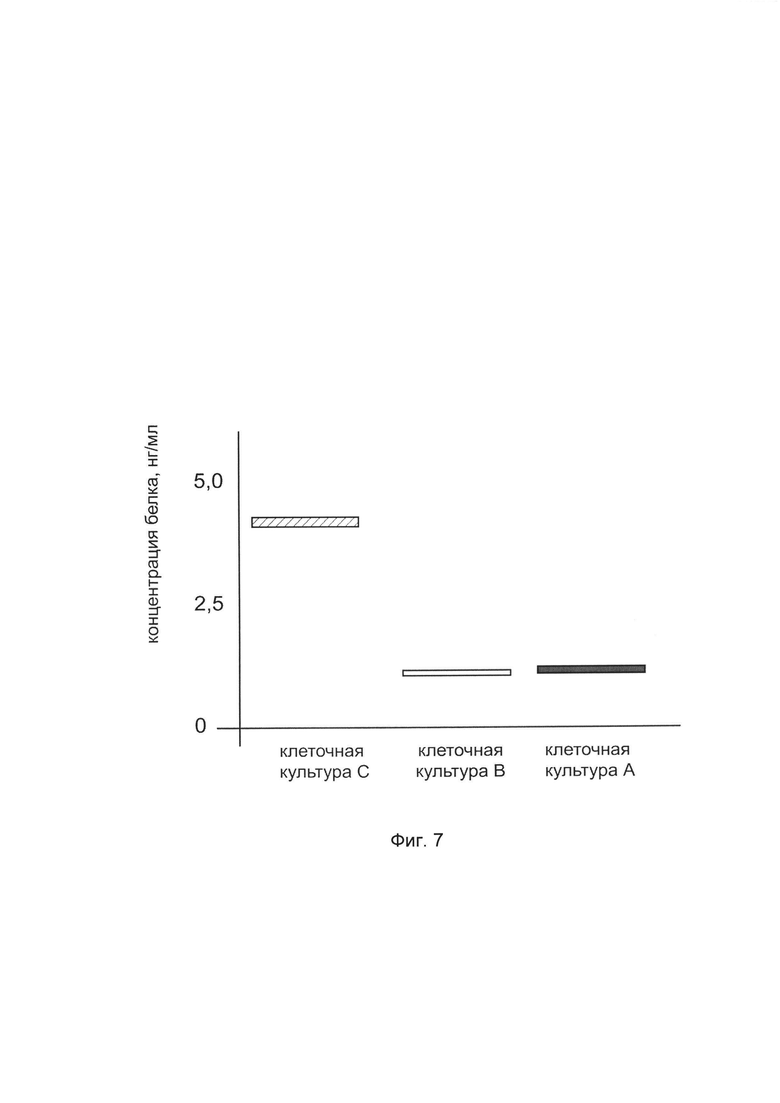
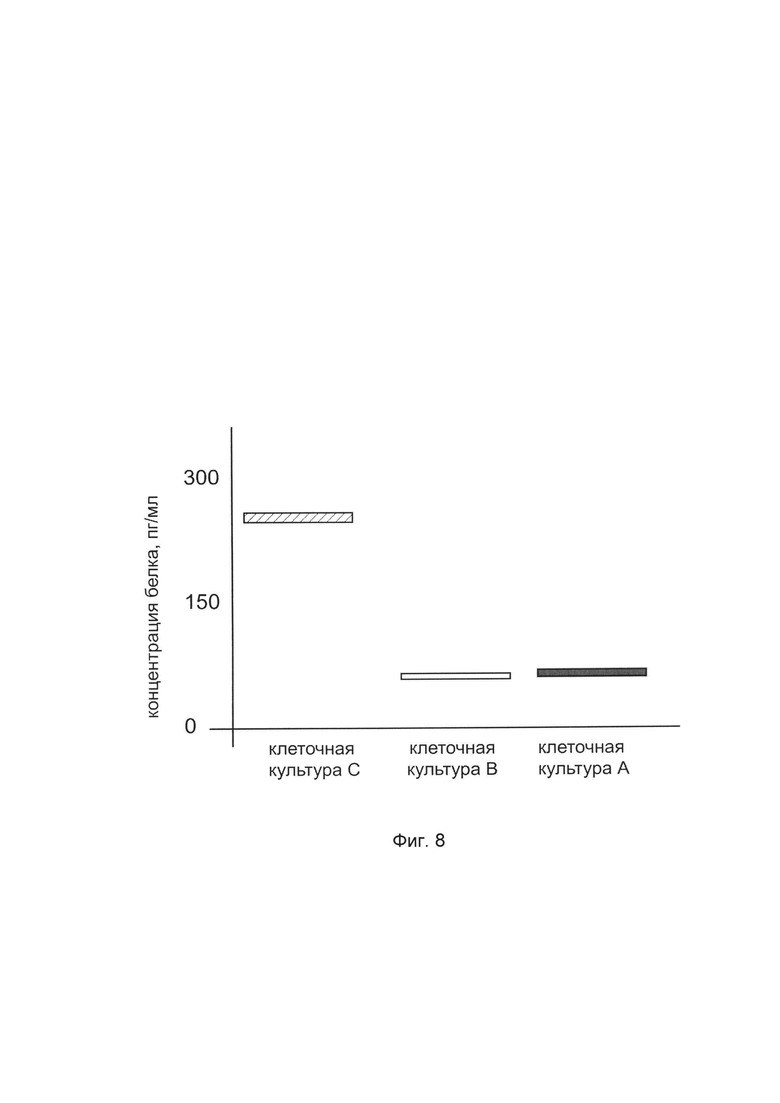
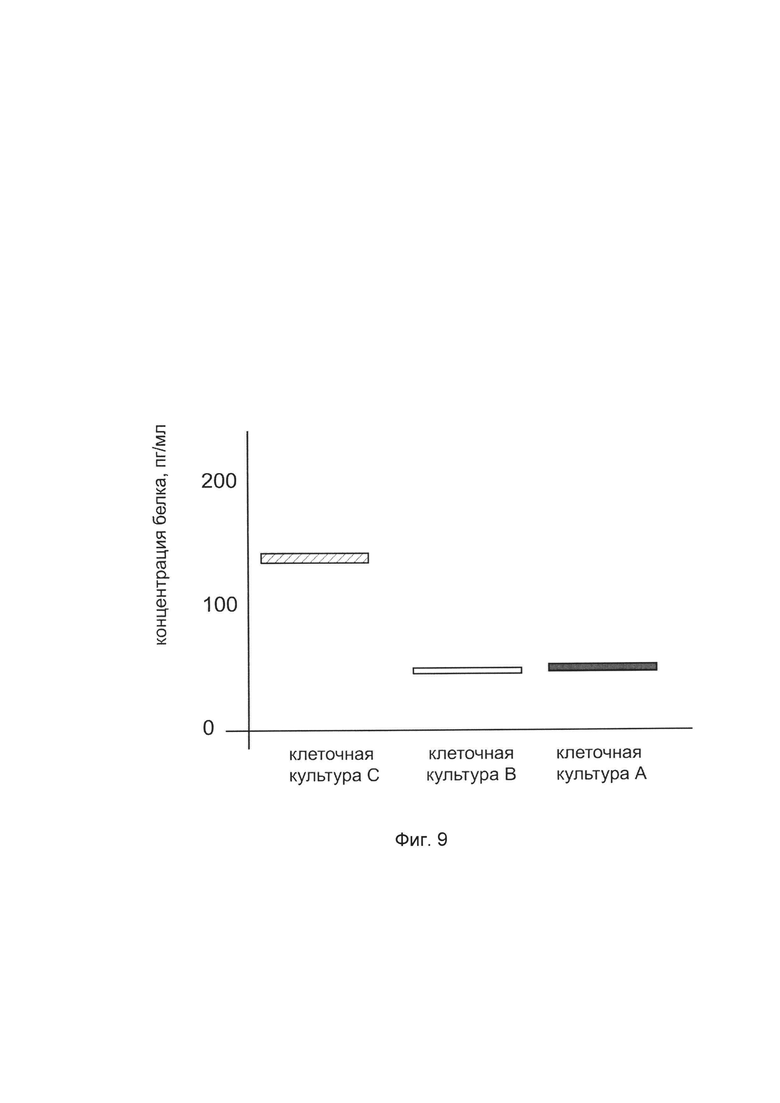
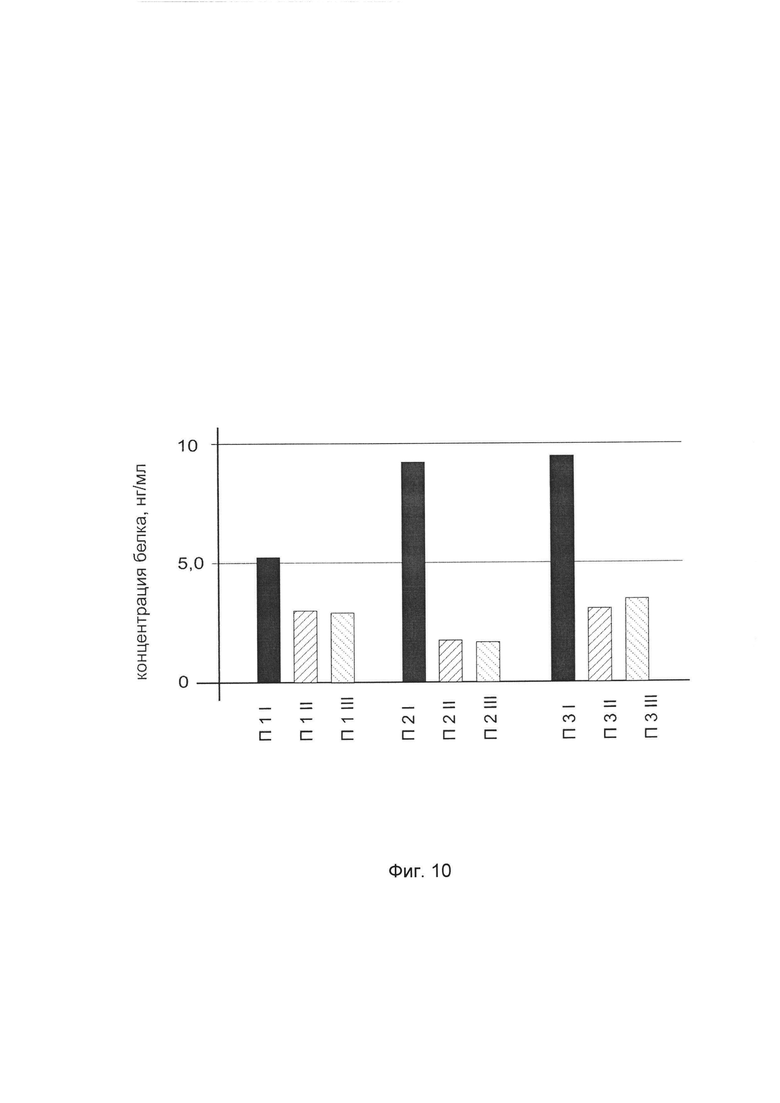

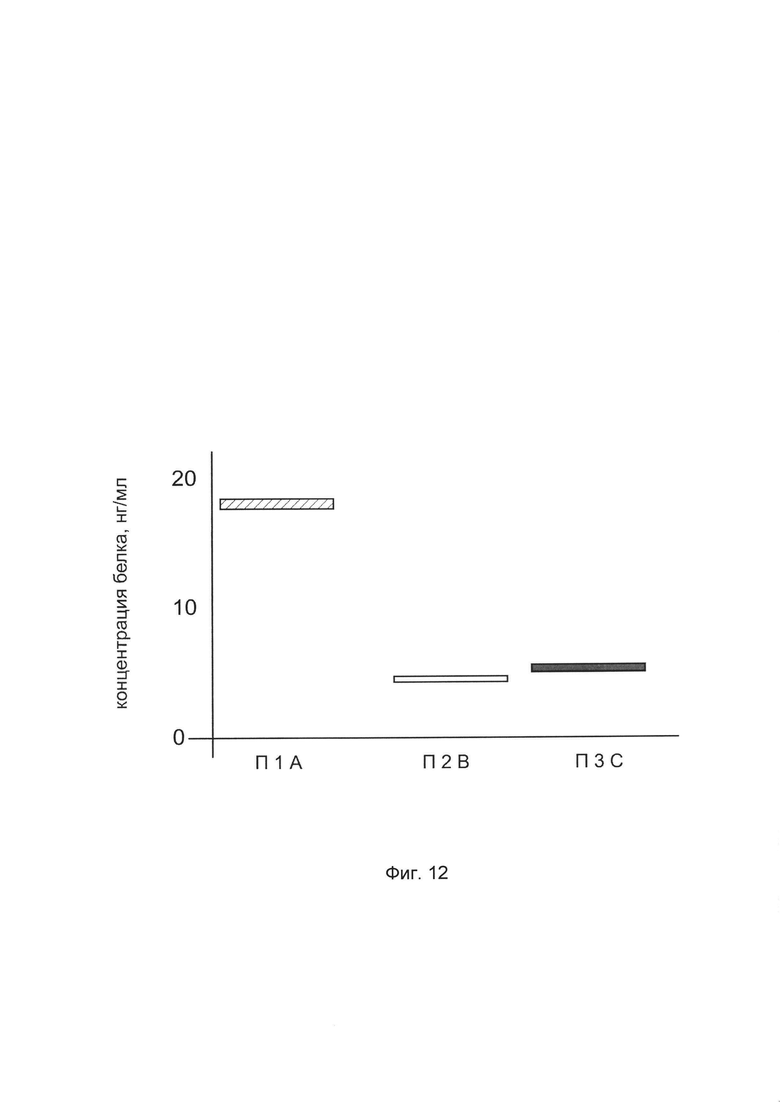
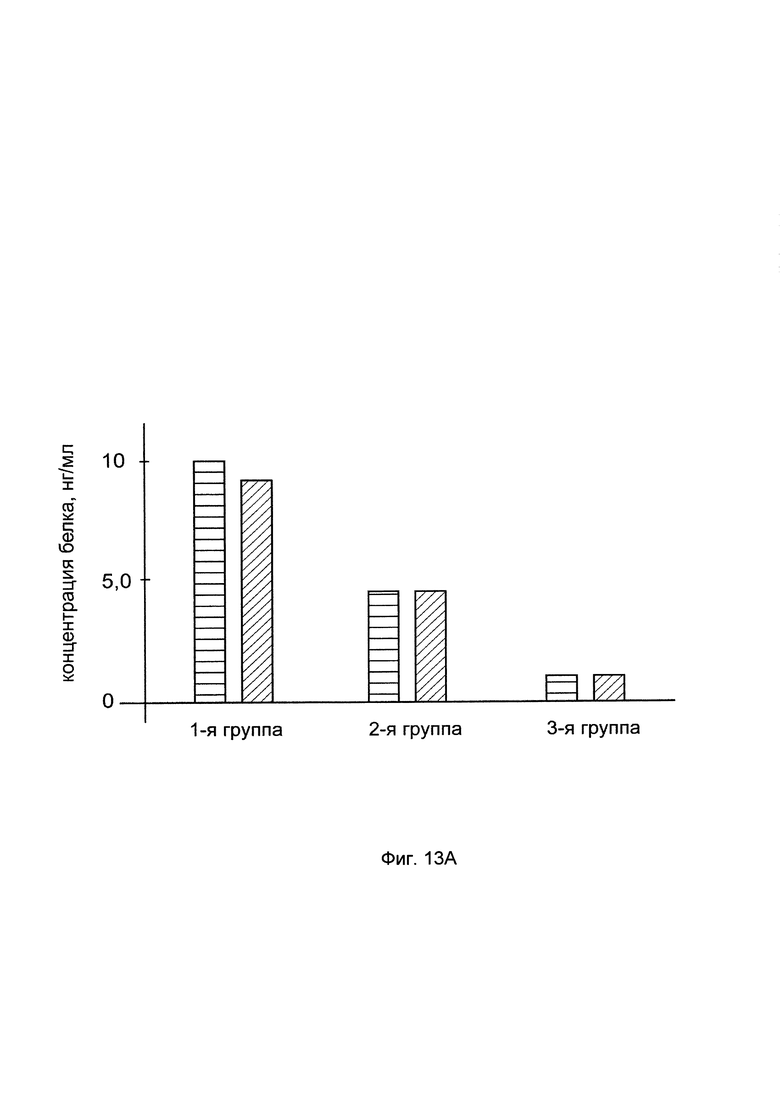
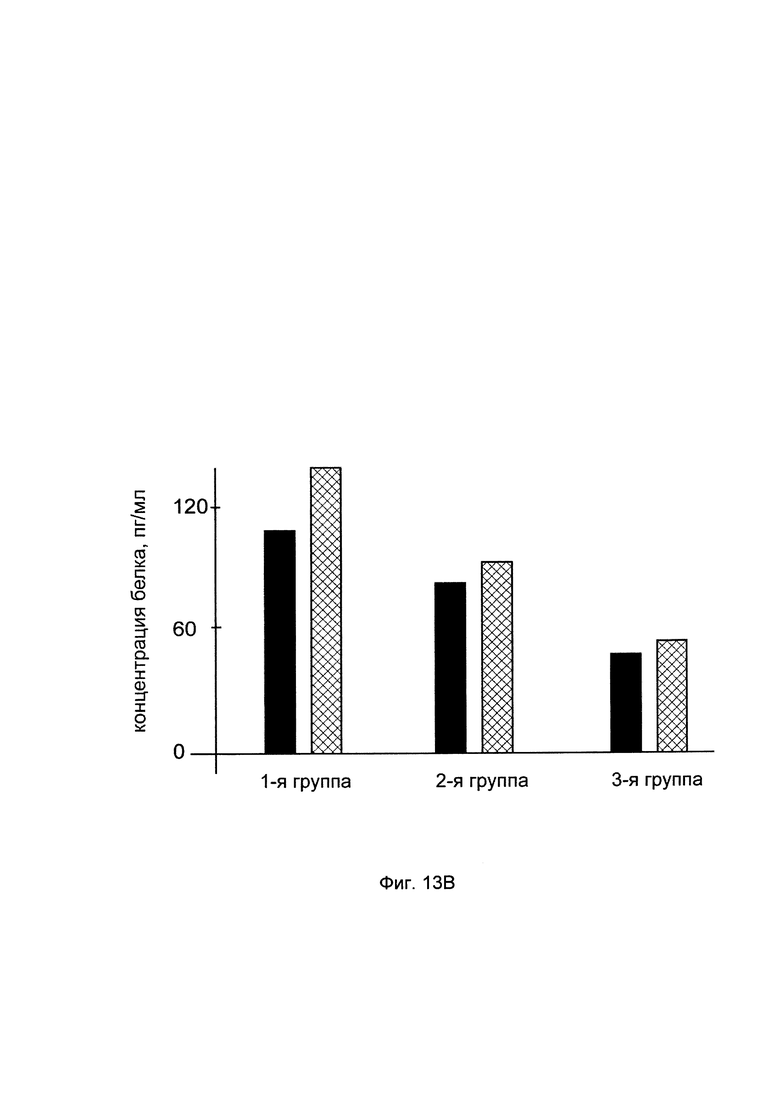
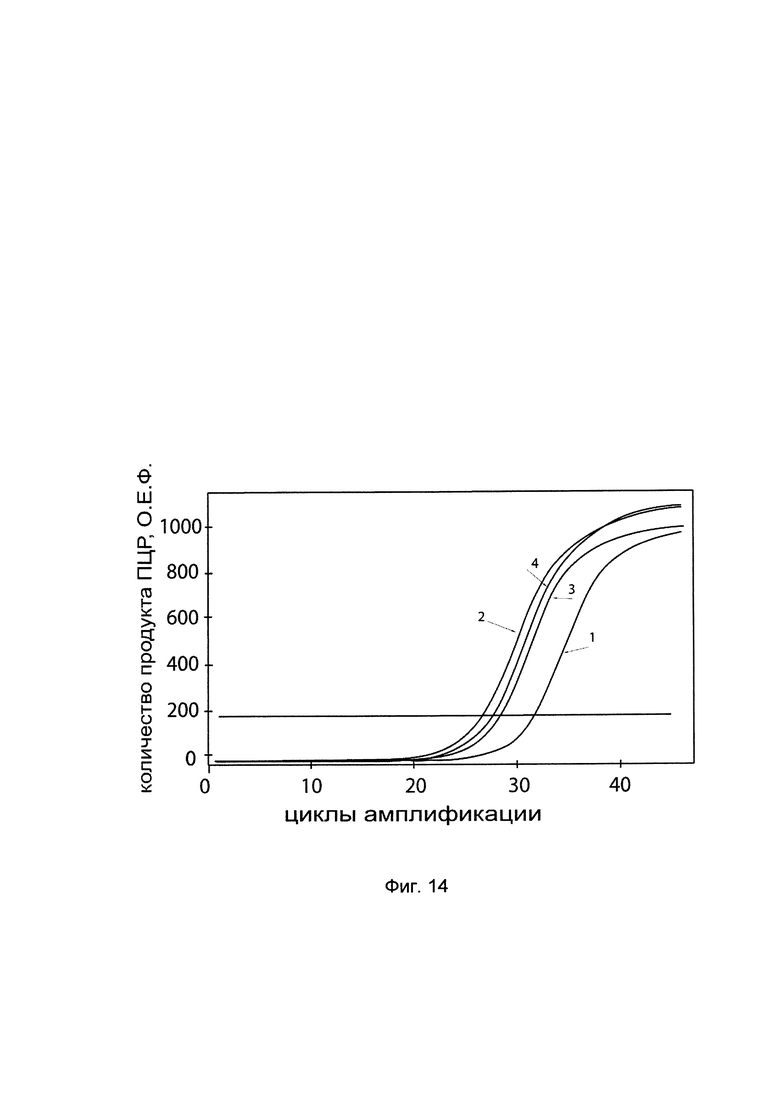
Изобретение относится к генной инженерии. Описан генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7, для повышения уровня экспрессии этого целевого гена в организме человека и животных, при этом генотерапевтический ДНК-вектор VTvaf17-COL1A1, или VTvaf17- COL1A2, или VTvaf17- ВМР2, или VTvaf17-ВМР7 имеет нуклеотидную последовательность SEQ ID №1 или SEQ ID №2 или SEQ ID №3 или SEQ ID №4 соответственно. Каждый из созданных генотерапевтических ДНК-векторов: VTvaf17-COL1A1, или VTvaf17-COL1A2, или VTvaf17-ВМР2, или VTvaf17-ВМР7 за счет ограниченного размера векторной части VTvaf17, не превышающего 3200 п.н, обладает способностью эффективно проникать в клетки и экспрессировать клонированный в него целевой ген, выбранный из группы генов COL1A1, COL1A2, ВМР2, ВМР7. В составе генотерапевтического ДНК-вектора отсутствуют нуклеотидные последовательности вирусного происхождения и отсутствуют гены антибиотикорезистентности, обеспечивая возможность его безопасного применения для генетической терапии человека и животных. Создан также способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: COL1A1, COL1A2, ВМР2, ВМР7, который заключается в том, что каждый генотерапевтический ДНК-вектор: VTvaf17-COL1A1, или VTvaf17-COL1A2, или VTvaf17-ВМР2, или VTvaf17-ВМР7, получают следующим образом: кодирующую часть целевого гена из группы генов COL1A1, COL1A2, ВМР2, ВМР7 клонируют в ДНК-вектор VTvaf17 и получают генотерапевтический ДНК-вектор VTvaf17-COL1A1, SEQ ID №1, или VTvaf17-COL1A2, SEQ ID №2 или VTvaf17-BMP2, SEQ ID №3, или VTvaf17-BMP7, SEQ ID №4 соответственно. Способ применения созданного генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: COL1A1, COL1A2, ВМР2, ВМР7, для повышения уровня экспрессии этих целевых генов заключается во введении выбранного генотерапевтического ДНК-вектора или нескольких выбранных генотерапевтических ДНК-векторов в клетки, органы и ткани человека или животного, и/или во введении в органы и ткани человека или животного аутологичных клеток человека или животного, трансфицированных выбранным генотерапевтическим ДНК-вектором или несколькими выбранными генотерапевтическими ДНК-векторами, или в сочетании обозначенных способов. Представлен способ получения штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1 или штамма Escherichia coli SCS110-AF/VTvaf17-COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17-BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17-BMP7 заключается в электропорации компетентных клеток штамма Escherichia coli SCS110-AF созданным генотерапевтическим ДНК-вектором и последующей селекцией стабильных клонов штамма с использованием селективной среды. Представлен штамм Escherichia coli SCS110-AF/VTvaf17-COL1A1, или штамм Escherichia coli SCS110-AF/VTvaf17-COL1A2, или штамм Escherichia coli SCS110-AFA/Tvaf17-BMP2, или штамм Escherichia coli SCS110-AF/VTvaf17-BMP7, несущий генотерапевтический ДНК-вектор для его наработки с возможностью культивирования штамма без использования антибиотиков. Способ производства в промышленных масштабах генотерапевтического ДНК-вектора заключается в масштабировании бактериальной культуры штамма до количеств, необходимых для наращивания бактериальной биомассы в промышленном ферментере, после чего биомассу используют для выделения фракции, содержащей целевой ДНК-продукт - генотерапевтический ДНК-вектор VTvaf17-COL1A1, или VTvaf17-COL1A2, или VTvaf17-VTvaf17-BMP2, или VTvaf17-BMP7, многостадийно фильтруют и очищают хроматографическими методами. Изобретение может быть использовано в биотехнологии, медицине и сельском хозяйстве для создания препаратов генной терапии. 12 н. и 2 з.п. ф-лы, 14 ил., 19 пр.
1. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, путем повышения уровня экспрессии целевого гена COL1A1 в организме человека и животных, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена COL1A1, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-COL1A1, с нуклеотидной последовательностью SEQ ID №1.
2. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации, путем повышения уровня экспрессии целевого гена COL1A2 в организме человека и животных, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена COL1A2, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-COL121, с нуклеотидной последовательностью SEQ ID №2.
3. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации, путем повышения уровня экспрессии целевого гена ВМР2 в организме человека и животных, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена ВМР2, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-BMP2, с нуклеотидной последовательностью SEQ ID №3.
4. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации, путем повышения уровня экспрессии целевого гена ВМР7 в организме человека и животных, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена ВМР7, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-BMP7, с нуклеотидной последовательностью SEQ ID №. 4.
5. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген COL1A1, COL1A2, ВМР2, ВМР7 по пп. 1-3 или 4, отличающийся тем, что каждый из созданных генотерапевтических ДНК-векторов: VTvaf17-COL1A1, или VTvaf17-COL1A2, или ВМР2, или VTvaf17-ВМР7 по пп. 1-3 или 4, за счет ограниченного размера векторной части VTvaf17, не превышающей 3200 п.н., обладает способностью эффективно проникать в клетки человека и животных и экспрессировать клонированный в него целевой ген COL1A1, или COL1A2, или ВМР2, или ВМР7.
6. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген COL1A1, COL1A2, ВМР2, ВМР7 по пп. 1-3 или 4, отличающийся тем, что в составе каждого из созданных генотерапевтических ДНК-векторов: VTvaf17-COL1A1, или VTvaf17-COL1A2, или ВМР2, или VTvaf17-ВМР7 по пп. 1-3 или 4, в качестве структурных элементов используют нуклеотидные последовательности, не являющиеся генами антибиотикорезистентности, вирусными генами и регуляторными элементами вирусных геномов, обеспечивая возможность его безопасного применения для генетической терапии человека и животных.
7. Способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A1, или COL1A2, или ВМР2, или ВМР7 по пп. 1-3 или 4, заключающийся в том, что каждый из генотерапевтических ДНК-векторов: VTvaf17-COL1A1, или VTvaf17-COL1A2, или VTvaf17-ВМР2, или VTvaf17-ВМР7 получают следующим образом: кодирующую часть целевого гена COL1A1, или COL1A2, или ВМР2, или ВМР7 по пп. 1-3 или 4 клонируют в генотерапевтический ДНК-вектор VTvaf17 и получают генотерапевтический ДНК-вектор VTvaf17-COL1A1, SEQ ID №1, или VTvaf17-COL1A2, SEQ ID №2, или VTvaf17-BMP2, SEQ ID №3, или VTvaf17-BMP7, SEQ ID №4, соответственно, при этом кодирующую часть целевого гена COL1A1, или COL1A2, или ВМР2, или ВМР7 получают путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции и ПЦР-амплификации с использованием созданных олигонуклеотидов и расщеплением продукта амплификации соответствующими эндонуклеазами рестрикции, причем клонирование в генотерапевтический ДНК-вектор VTvaf17 проводят по сайтам рестрикции Nhel и Hindlll, причем селекцию проводят без антибиотиков, при этом при получении генотерапевтического ДНК-вектора VTvaf17-COL1A1, SEQ ID №1 для проведения реакции обратной транскрипции и ПЦР-амплификации, в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
COL1A1_F CCAGCTAGCGTCTAGGGTCTAGACATGTTC
COL1A1_R TATAAGCTTCTACAGGAAGCAGACAGGGCCAAC,
а расщепление продукта амплификации и клонирование кодирующей части гена COL1A1 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции Nhel и Hindlll,
причем при получении генотерапевтического ДНК-вектора VTvaf17-COL1A2, SEQ ID №2 для проведения реакции обратной транскрипции и ПЦР-амплификации, в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
COL1A2_F CCAGCTAGCGTCTAAGTGCTAGACATGCTC
COL1A2_R CGAAGCTTTTATTTGAAACAGACTGGGCCA,
а расщепление продукта амплификации и клонирование кодирующей части гена COL1A2 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции Nhel и Hindlll,
причем при получении генотерапевтического ДНК-вектора VTvaf17-BMP2, SEQ ID №3 для проведения реакции обратной транскрипции и ПЦР-амплификации, в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
BMP2_F ACAGCTAGCCTCCTAAAGGTCCACCATGGT
BMP2_R TATAAGCTTCTAGCGACACCCACAACCCT,
а расщепление продукта амплификации и клонирование кодирующей части гена ВМР2 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции Nhel и Hindlll,
причем при получении генотерапевтического ДНК-вектора VTvaf17-BMP7, SEQ ID №4 для проведения реакции обратной транскрипции и ПЦР-амплификации, в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
BMP7_F TCAGCTAGCGTAGAGCCGGCGCGATGCA
BMP7_R TATAAGCTTCTAGTGGCAGCCACAGGC,
а расщепление продукта амплификации и клонирование кодирующей части гена ВМР7 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции Nhel и Hindlll.
8. Способ применения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A1, или COL1A2, или ВМР2, или ВМР7 по пп. 1-3 или 4, для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации, путем повышения уровня экспрессии целевого гена COL1A1, или COL1A2, или ВМР2, или ВМР7 в организме человека и животных, заключающийся в трансфекции выбранным генотерапевтическим ДНК-вектором, несущим целевой ген на основе генотерапевтического ДНК-вектора VTvaf17, или несколькими выбранными генотерапевтическими ДНК-векторами, несущими целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, из созданных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, клеток органов и тканей пациента или животного, и/или во введении в органы и ткани пациента или животного аутологичных клеток этого пациента или животного, трансфицированных выбранным генотерапевтическим ДНК-вектором, несущим целевой ген на основе генотерапевтического ДНК-вектора VTvaf17, или несколькими выбранными генотерапевтическими ДНК-векторами, несущими целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, из созданных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, и/или во введении в органы и ткани пациента или животного выбранного генотерапевтического ДНК-вектора, несущего целевой ген на основе генотерапевтического ДНК-вектора VTvaf17, или нескольких выбранных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, из созданных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, или в сочетании обозначенных способов.
9. Способ получения штамма для производства генотерапевтического ДНК-вектора по пп. 1-3 или 4 для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации, путем повышения уровня экспрессии целевого гена COL1A1, или COL1A2, или ВМР2, или ВМР7 в организме человека и животных, заключающийся в получении электрокомпетентных клеток штамма Escherichia coliSCS110-AF с последующим проведением электропорации этих клеток генотерапевтическим ДНК-вектором VTvaf17-COL1A1, или ДНК-вектором VTvaf17-COL1A2, или ДНК-вектором VTvaf17-ВМР2, или ДНК-вектором VTvaf17-ВМР7, после чего клетки высеивают на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола с получением в результате штамма Escherichia coli SCS110-AF/VTvaf17-COL1A1, или штамма Escherichia coli SCS110-AF/VTvaf17-COL1A2, или штамма Escherichia coli SCS110-AF/VTvaf17-BMP2, или штамма Escherichia coli SCS110-AF/VTvaf17-BMP7.
10. Штамм Escherichia coliSCS110-AFA/Tvaf17-COL1A1, полученный способом по п. 9, несущий генотерапевтический ДНК-вектор VTvaf17-COL1A1, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации.
11. Штамм Escherichia coliSCS110-AF/VTvaf17-COL1A2, полученный способом по п. 9, несущий генотерапевтический ДНК-вектор VTvaf17-COL1A2, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации.
12. Штамм Escherichia coliSCS110-AF/VTvaf17-BMP2, полученный способом по п. 9, несущий генотерапевтический ДНК-вектор VTvaf17- ВМР2, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации.
13. Штамм Escherichia coliSCS110-AFA/Tvaf17-BMP7, полученный способом по п. 9, несущий генотерапевтический ДНК-вектор VTvaf17-ВМР7, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации.
14. Способ производства в промышленных масштабах генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL1A1, или COL1A2, или ВМР2, или ВМР7 по пп. 1-3 или 4, для лечения заболеваний, характеризующихся нарушением процессов остеогенеза, формирования и регенерации костной и хрящевой ткани, обусловленных дерегуляцией роста, дифференцировки и апоптоза различных типов клеток, включая остеобласты, хондробласты, замедлением дифференцировки мезенхимальных стволовых клеток в хондробласты и остеобласты, снижением синтеза коллагена, активности щелочной фосфатазы, синтеза остеокальцина, синтеза внеклеточного матрикса и его последующей минерализации в том числе при переломах костей, повышенной хрупкости костей, снижении минерализации костей, для повышения остеоиндуктивности костных имплантатов, а также в качестве альтернативы лекарственным средствам на основе рекомбинантных остеогенных факторов с целью снижения риска гетеротопической оссификации, заключающийся в том, что генотерапевтический ДНК-вектор VTvaf17-COL1A1, или генотерапевтический ДНК-вектор VTvaf17-COL1A2, или генотерапевтический ДНК-вектор VTvaf17-ВМР2, или генотерапевтический ДНК-вектор VTvaf17-BMP7 получают путем того, что засевают в колбу с приготовленной средой затравочную культуру, выбранную из штамма Escherichia coliSCS110-AF/VTvaf17-COL1A1, или штамма Escherichia coliSCS110-AF/VTvaf17-COL1A2, или штамма Escherichia coliSCS110-AF/VTvaf17-BMP2, или штамма Escherichia coliSCS110-AF/VTvaf17-ВМР7, затем инкубируют затравочную среду в шейкере-инкубаторе и переносят ее в промышленный ферментер, после чего растят до достижения стационарной фазы, затем выделяют фракцию, содержащую целевой ДНК-продукт, многостадийно фильтруют и очищают хроматографическими методами.
| RU 2016101664 A, 24.07.2017 | |||
| RU 2016101660 A, 25.07.2017 | |||
| OLIVEIRA P.H | |||
| et al | |||
| Marker-free plasmids for biotechnological applications-implications and perspectives | |||
| Trends in biotechnology, 2013 | |||
| HARDEE C.L | |||
| et al | |||
| Advances in non-viral DNA vectors for gene therapy | |||
| Genes, 2017 | |||
| LUKE J | |||
| et al | |||
| Improved antibiotic-free DNA vaccine vectors |
Авторы
Даты
2019-11-27—Публикация
2018-09-04—Подача