Область техники
Изобретение относится к генной инженерии и может быть использовано в биотехнологии, медицине и сельском хозяйстве для создания препаратов генной терапии.
Уровень техники
Генная терапия - это современный медицинский подход, направленный на лечение наследственных и приобретенных заболеваний путем введения нового генетического материала в клетки пациента с целью компенсации или подавления функции мутантного гена и/или исправления генетического дефекта. Конечным продуктом экспрессии гена может являться молекула РНК или белка. Однако осуществление большей части физиологических процессов в организме связано с функциональной активностью белковых молекул, тогда как молекулы РНК являются либо промежуточным продуктом в синтезе белков, либо осуществляют регуляторные функции. Таким образом целью генной терапии является, в большинстве случаев, введение в организм генов, обеспечивающих транскрипцию и последующую трансляцию белковых молекул, кодируемых этими генами. В рамках описания настоящего изобретения под экспрессией гена подразумевается продукция белковой молекулы, аминокислотная последовательность которой кодируется этим геном.
Гены KRT5, KRT14, LAMB3, COL7A1 входящие в группу генов, играют ключевую роль в ряде процессов в организме человека и животных. Показана связь низких/недостаточных концентраций этих белков с различными неблагоприятными состояниями человека, которая, в ряде случаев, подтверждена нарушениями в нормальной экспрессии генов, кодирующих эти белки. Таким образом, генотерапевтическое повышение экспрессии гена, выбранного из группы генов KRT5, KRT14, LAMB3, COL7A1 обладает потенциалом для коррекции различных состояний человека и животных.
Коллаген VII типа кодируется геном COL7A1. Три белковые цепи pro-α1 (VII) скручиваются вместе, образуя трехцепочечную молекулу проколлагена. Молекулы проколлагена секретируются клеткой и обрабатываются ферментами для удаления дополнительных сегментов белка с концов. Как только эти концевые сегменты удалены формируются длинные тонкие пучки зрелого коллагена VII.
Мутации в гене COL7A1 вызывают буллезный эпидермолиз дистрофического типа. Буллезные поражения чаще всего возникают в зонах, подверженных незначительному травмированию, например, разгибательные поверхности локтей и тыльные поверхности рук и ног. При заживлении возникают шрамы, поверхностные эпидермальные кисты и гиперпигментация. У некоторых пациентов наблюдается дистрофия ногтей. Часто встречаются внекожные проявления, включающие поражения желудочно-кишечного и мочеполового трактов, внешних оболочек глаза, хроническую анемию, остеопороз, задержку роста. У пациентов с булезным эпидермолизом наблюдается высокий риск онкологических заболеваний, в частности образования агрессивных плоскоклеточных карцином. Изучением и лечением буллезного эпидермолиза во всем мире занимается Международная ассоциация DEBRA International, которая была основана в 1978 г. в Великобритании. По данным DEBRA International в мире рождается один больной на 50-100 тысяч человек.
В настоящее время в мире ведутся различные исследования по лечению буллезного эпидермолиза в трех направлениях: генная терапия, терапия с применением рекомбинантных белков и клеточная терапия (использование стволовых клеток). Все эти виды лечения находятся на разных этапах разработки.
Генотерапевтические подходы к лечению буллезного эпидермолиза включают различные экспериментальные подходы. В ряде работ для коррекции мутаций в гене COL7A1 были успешно использованы ex vivo технологии редактирования генома (Mencia et al., 2018), микроинъекции линейных молекул ДНК, кодирующих ген COL7A1 (Mecklenbeck et al., 2002), интеграция кДНК с использованием ферментов-интеграз (Ortiz-Urda et al., 2003), интрадермальные инъекции лентивирусных векторов (Woodley et al., 2004), технология репарации мутаций на основе TALEN нуклеаз (Osborn et al., 2013), а также введение аутологичных клеток - фибробластов или кератиноцитов, модифицированных с использованием различных ретровирусных векторов ( et al., 2016, Georgiadis et al., 2016, Goto et al., 2006). В настоящее время клинические испытания подобных подходов находятся на различных фазах исследований (NCT01263379, NCT02810951).
et al., 2016, Georgiadis et al., 2016, Goto et al., 2006). В настоящее время клинические испытания подобных подходов находятся на различных фазах исследований (NCT01263379, NCT02810951).
Гены KRT5 и KRT14 кодируют белки кератин 5 и кератин 14 соответственно. Кератины представляют собой группу жестких волокнистых белков, которые определяют структурную организацию кожи, волос и ногтей. Кератин 5 вырабатывается в клетках кератиноцитах. Кератин 5 с кератином 14 образуют молекулы, называемые кератиновыми промежуточными волокнами. Эти нити собираются в сетчатую структуру, которая необходима для прикрепления кератиноцитов и соединения эпидермиса с подстилающим слоям кожи. Сеть кератиновых промежуточных волокон обеспечивает прочность и упругость кожи и защищает ее от повреждения при трении и других механических нагрузках. Мутации в генах KRT5 и KRT14 вызывают около 75% случаев буллезного эпидермолиза, при этом тяжесть заболевания зависит от того, в каком участке гена находится мутация (Bolling, Lemmink, Jansen, & Jonkman, 2011; Pfendner et al., 2016). У мышей, нокаутных по гену KRT5, наблюдается полное отсутствие соединения дермы и эпидермиса (Cao et al., 2001; Peters, Kirfel,  , Vidal & Magin, 2001).
, Vidal & Magin, 2001).
Мутации в генах KRT5 и KRT14 помимо буллезного эпидермолиза вызывают такие заболевания как сетчатая пигментированная аномалия сгибаний (болезнь Доулинг-Дегоса), дерматопатия пигментная ретикулярная (Оберста-Лена-Хаусса пигментная дерматопатия), синдром Франческетти-Ядассона-Негели (Coulombe PA et al., 2017).
Ген LAMB3 кодирует белок ламинин бета 3 - субъединицу ламинина. Ламинины представляют собой группу белков, которые регулируют рост клеток, движение и адгезию клеток. Они также участвуют в формировании и организации базальных мембран, которые представляют собой тонкие листовидные структуры, которые отделяют и поддерживают клетки во многих тканях. Ламинин является основным компонентом волокон, называемых анкерными нитями, которые соединяют два слоя мембраны основания и помогают формировать единую структуру кожи, а мутации в гене LAMB3 вызывают буллезный эпидермолиз. Исследования показывают, что ламинин также имеет несколько других функций. Этот белок, по-видимому, важен для заживления ран и развития зубной эмали.
Также в литературе имеются данные, что мутации в гене LAMB3 может вызывать несовершенный амелогенез (Poulter et al., 2014), а отдельные редкие аллели этого гена ассоциированы с болезненным ожирением и риском диабета 2 типа (Jiao H et al., 2016).
В экспериментальной работе у пациента-добровольца с буллезным эпидермолизом было показано, что трансплантация клеток, трансфицированных ретровирусным вектором, экспрессирующим ген LAMB3, приводила к значительному улучшению в местах введения, которое сохранялось не менее года (Mavilio et al., 2006).
В клинических испытаниях I/II фазы было показано, что введение аутологичных генетически модифицированных эпителиальных клеток, экспрессирующих ген LAMB3, представляется перспективным подходом к терапии буллезного эпидермолиза (De Rosa L et al., 2013).
Таким образом предшествующий уровень техники свидетельствует о том, что мутации в генах KRT5, KRT14, LAMB3, COL7A1 или недостаточная экспрессия белков, кодируемых этими генами, связаны с развитием спектра заболеваний, включающих в себя, но не ограничивающихся, заболеваниями соединительной ткани, заживлением ран, наследственными и приобретенными патологическими процессами, такими, например, как буллезный эпидермолиз, и другими неблагоприятными для организма состояниями. Этим обусловлено объединение генов KRT5, KRT14, LAMB3, COL7A1 в рамках данного патента в группу генов. Генетические конструкции, обеспечивающие экспрессию белков, кодируемых генами из группы KRT5, KRT14, LAMB3, COL7A1, могут быть использованы для разработки лекарственных препаратов для предотвращения и терапии различных заболеваний и патологических состояний.
Более того, приведенные данные свидетельствуют о том, что недостаточная экспрессия белков, кодируемых генами KRT5, KRT14, LAMB3, COL7A1, входящими в группу генов, связана не только с патологическими состояниями, но и с предрасположенность к их развитию. Также приведенные данные свидетельствуют о том, что недостаточная экспрессия данных белков может не проявляться в явном виде в форме патологии, которая может быть однозначно описана в рамках существующих стандартов клинической практики (например, с применением кода МКБ), однако при этом вызывать состояния, которые неблагоприятны для человека и животных и связанны с ухудшением качества жизни.
Анализ подходов для повышения экспрессии целевых генов подразумевает возможность использования различных генотерапевтических векторов.
Генотерапевтические векторы разделяют на вирусные, клеточные и ДНК-векторы (Guideline on the quality, non-clinical and clinical aspects of gene therapy medicinal Products EMA/COL7A1/80183/2014). В последнее время в генной терапии все большее внимание уделяется разработке невирусных систем доставки генетического материала, среди которых лидируют плазмидные векторы. Плазмидные векторы лишены недостатков, присущих клеточным и вирусным векторам. В клетке-мишени они существуют в эписомальной форме, не интегрируют в геном, производство их достаточно дешево, отсутствие иммунного ответа и побочных реакций на введение плазмидного вектора делают их удобным инструментом генной терапии и генетической профилактики (ДНК-вакцины) (Li L, Petrovsky N. // Expert Rev Vaccines. 2016;15(3):313-29).
Тем не менее, ограничениями для использования плазмидных векторов для генной терапии являются: 1) наличие генов устойчивости к антибиотикам для наработки в бактериальных штаммах, 2) наличие различных регуляторных элементов, представленных последовательностями вирусных геномов 3) размер терапевтического плазмидного вектора, определяющий эффективность проникновения вектора в клетку-мишень.
Известно, что Европейское агентство по лекарственным средствам считает необходимым избегать введения маркеров антибиотикорезистентности в разрабатываемые плазмидные векторы для генной терапии (Reflection paper on design modifiCOL7A1ions of gene therapy medicinal products during development / 14 December 2011 EMA/COL7A1/GTWP/44236/2009 Committee for advanced therapies). Данная рекомендация связана, в первую очередь, с потенциальной опасностью проникновения ДНК-вектора или горизонтального переноса генов антибиотикорезистентности в клетки бактерий, представленных в организме в составе нормальной или оппортунистической микрофлоры. Помимо этого, наличие генов антибиотикорезистентности значительно увеличивает размер ДНК-вектора, что приводит к снижению эффективности его проникновения в эукариотические клетки.
Необходимо отметить, что гены антибиотикорезистентности также вносят принципиальный вклад в способ получения ДНК-векторов. В случае наличия генов антибиотикорезистентности штаммы для наработки ДНК-векторов обычно культивируются в среде, содержащей селективный антибиотик, что создает риск наличия следовых количеств антибиотика в недостаточно очищенных препаратах ДНК-векторов. Таким образом, получение ДНК-векторов для генной терапии, в которых отсутствуют гены антибиотикорезистентности, связано с получением штаммов, обладающих такой отличительной особенностью как способность к стабильной амплификации целевых ДНК-векторов в среде без содержания антибиотиков.
Кроме того, Европейское Медицинское Агентство рекомендует избегать наличия в составе терапевтических плазмидных векторов регуляторных элементов для повышения экспрессии целевых генов (промоторов, энхансеров, посттрансляционных регуляторных элементов), являющихся нуклеотидными последовательностями геномов различных вирусов (Draft Guideline on the quality, non-clinical and clinical aspects of gene therapy medicinal products, http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2015/05/WC500187020.pdf). Данные последовательности, хотя и могут увеличивать уровень экспрессии целевого трансгена, однако создают риск рекомбинации с генетическим материалом вирусов дикого типа и интеграции в геном эукариотической клетки. Более того, целесообразность гиперэкспрессии того или иного гена в целях терапии остается нерешенным вопросом.
Также, существенным моментом является размер терапевтического вектора. Известно, что современные плазмидные векторы зачастую перегружены нефункциональными участками, серьезно увеличивающими размер вектора (Mairhofer J, Grabherr R. // Mol Biotechnol. 2008.39(2):97-104). Например, ген устойчивости к ампициллину в векторах серии pBR322, как правило, состоит из не менее чем 1000 п.н., что составляет более 20% от размера самого вектора. При этом наблюдается обратная зависимость между размером вектора и его способностью проникать в эукариотические клетки - ДНК-векторы с небольшим размером эффективней проникают в клетки человека и животных. Так, например, в серии экспериментов по трансфекции клеток HELA ДНК-векторами с размером от 383 до 4548 п.н. было показано, что разница в эффективности проникновения может достигать двух порядков (отличаться в 100 раз) (Hornstein BD et al. // PLoS ONE. 2016;11(12): e0167537.).
Таким образом при выборе ДНК-вектора в целях безопасности и наибольшей эффективности следует отдавать предпочтение тем конструкциям, в которых не содержатся гены устойчивости к антибиотикам, последовательности вирусного происхождения и размер которых позволяет эффективно проникать в эукариотические клетки. Штамм для получения такого ДНК-вектора в количествах, достаточных для целей генной терапии, должен обеспечивать возможность стабильной амплификации ДНК-вектора с использованием питательных сред, не содержащих антибиотики.
Примером использования рекомбинантных ДНК-векторов для генной терапии является способ получения рекомбинантного вектора для генетической иммунизации по патенту US 9550998 В2. Плазмидный вектор представляет собой суперскученный плазмидный ДНК-вектор и предназначен для экспрессии клонированных генов в клетках животных и человека. Вектор состоит из ориджина репликации, регуляторных элементов, включающих промотор и энхансер цитомегаловируса человека, регуляторные элементы из Т-лимфотропного вируса человека.
Накопление вектора проводят в специальном штамме E.coli без использования антибиотиков за счет антисенс-комплементации гена sacB, введенного в штамм посредством бактериофага. Недостатком данного изобретения является наличие в составе ДНК-вектора регуляторных элементов, представляющих собой последовательности вирусных геномов.
Прототипом настоящего изобретения в части использования генотерапевтических подходов для повышения уровня экспрессии генов из группы KRT5, KRT14, LAMB3, COL7A1 является следующая заявка.
В заявке US20020064876A1 описывается изобретение, в основе которого лежит введение комплексного олигонуклеотида, состоящего из РНК и ДНК, для коррекции нарушений экспрессии генов из группы, включающей гены KRT5, KRT14, LAMB3, COL7A1, для коррекции патологических состояний кожи, в том числе наследственных заболеваний, таких как буллезный эпидермолиз. Недостатком данного изобретения является способ коррекции нарушений в генах, который изменяет последовательность нуклеотидов этих генов, тогда как не все нарушения ограничиваются мутациями в кодирующих областях генов, а также могут быть связаны с недостаточной функциональной активностью, которая обусловлена не мутациями или такими мутациями, которые не могут быть скорректированы данным способом.
Раскрытие изобретения
Задачей изобретения является конструирование генотерапевтических ДНК-векторов для повышения уровня экспрессии группы генов KRT5, KRT14, LAMB3, COL7A1 в организме человека и животных, сочетающих в себе следующие свойства:
I) Эффективность генотерапевтического ДНК-вектора для повышения уровня экспрессии целевых генов в эукариотических клетках.
II) Возможность безопасного применения для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора регуляторных элементов, представляющих собой нуклеотидные последовательности вирусных геномов.
III) Возможность безопасного применения для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора генов антибиотикорезистентности.
IV) Технологичность получения и возможность наработки генотерапевтического ДНК-вектора в промышленных масштабах.
Пункты II и III предусмотрены в данном техническом решении в соответствии с рекомендациями государственных регуляторов к лекарственным средствам для генной терапии, в частности, Европейского Агентства по лекарственным средствам касательно отказа от введения маркеров антибиотикорезистентности в разрабатываемые плазмидные векторы для генной терапии (Reflection paper on design modifiCOL7A1ions of gene therapy medicinal products during development / 14 December 2011, EMA/COL7A1/GTWP/44236/2009 Committee for advanced therapies) и касательно отказа от введения в разрабатываемые плазмидные векторы для генной терапии элементов вирусных геномов (Guideline on the quality, non-clinical and clinical aspects of gene therapy medicinal products / 23 March 2015, EMA/COL7A1/80183/2014, Committee for Advanced Therapies).
Задачей изобретения также является конструирование штаммов, несущих эти генотерапевтические ДНК-вектора, для наработки и производства в промышленных масштабах генотерапевтических ДНК-векторов.
Поставленная задача решается за счет того, что создан генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1, для повышения уровня экспрессии этого целевого гена в организме человека и животных, при этом генотерапевтический ДНК-вектор VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 имеет нуклеотидную последовательность SEQ ID №1 или SEQ ID №2 или SEQ ID №3 или SEQ ID №4 соответственно. При этом каждый из созданных генотерапевтических ДНК-векторов: VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 за счет ограниченного размера векторной части VTvaf17, не превышающей 3200 п.н., обладает способностью эффективно проникать в клетки и экспрессировать клонированный в него целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1 соответственно. В составе генотерапевтического ДНК-вектора отсутствуют нуклеотидные последовательности вирусного происхождения и отсутствуют гены антибиотикорезистентности, обеспечивая возможность его безопасного применения для генетической терапии человека и животных.
Создан также способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: ген KRT5, ген KRT14, ген LAMB3, ген COL7A1, который заключается в том, что каждый из генотерапевтических ДНК-векторов: VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 получают следующим образом: кодирующую часть целевого гена из группы KRT5, или KRT14, или LAMB3, или COL7A1 клонируют в ДНК-вектор VTvaf17 и получают генотерапевтический ДНК-вектор VTvaf17-KRT5, SEQ ID №1, или VTvaf17-KRT14, SEQ ID №2 или VTvaf17-LAMB3, SEQ ID №3, или VTvaf17-COL7A1, SEQ ID №4 соответственно.
Способ применения созданного генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: ген KRT5, ген KRT14, ген LAMB3, ген COL7A1 для повышения уровня экспрессии этих целевых генов, заключается во введении выбранного генотерапевтического ДНК-вектора или нескольких выбранных генотерапевтических ДНК-векторов в клетки, органы и ткани человека или животного, и/или во введении в органы и ткани человека или животного аутологичных клеток человека или животного, трансфицированных выбранным генотерапевтическим ДНК-вектором или несколькими выбранными генотерапевтическими ДНК-векторами, или в сочетании обозначенных способов.
Способ получения штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1 заключается в электропорации компетентных клеток штамма Escherichia coli SCS110-AF созданным генотерапевтическим ДНК-вектором и последующей селекцией стабильных клонов штамма с использованием селективной среды.
Заявлен штамм Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамм Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамм Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамм Escherichia coli SCS110-AF/VTvaf17-COL7A1, несущий генотерапевтический ДНК-вектор для его наработки с возможностью культивирования штамма без использования антибиотиков.
Способ производства в промышленных масштабах генотерапевтического ДНК-вектора заключается в масштабировании бактериальной культуры штамма до количеств, необходимых для наращивания бактериальной биомассы в промышленном ферментере, после чего биомассу используют для выделения фракции, содержащей целевой ДНК-продукт - генотерапевтический ДНК-вектор VTvaf17-KRT5 или VTvaf17-KRT14 или VTvaf17-LAMB3 или VTvaf17-COL7A1 многостадийно фильтруют и очищают хроматографическими методами.
Изобретение поясняется чертежами, где:
На фиг.1
приведена схема генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1, который представляет собой кольцевую двуцепочечную молекулу ДНК, способную к автономной репликации в клетках бактерии Escherichia coli.
На фиг.1 приведены схемы, соответствующие:
A - генотерапевтический ДНК-вектор VTvaf17-KRT5;
B - генотерапевтический ДНК-вектор VTvaf17-KRT144;
C - генотерапевтический ДНК-вектор VTvaf17-LAMB3;
D - генотерапевтический ДНК-вектор VTvaf17-COL7A1.
На схемах отмечены следующие структурные элементы вектора:
EF1a - промоторная область гена человеческого фактора элонгации EF1A с собственным энхансером, содержащимся в первом интроне гена. Служит для обеспечения высокого уровня транскрипции рекомбинантного гена в большинстве тканей человека;
Рамка считывания целевого гена, соответствующая кодирующей части гена KRT5 (фиг.1A), или KRT14 (фиг.1B), или LAMB3 (фиг.1C), или COL7A1 (фиг.1D) соответственно;
hGH-TA - терминатор транскрипции и сайт полиаденилирования гена фактора роста человека;
ori - ориджин репликации, служащий для автономной репликации с однонуклеотидной заменой для повышения копийности плазмиды в клетках большинства штаммов Escherichia coli;
RNA-out - регуляторный элемент РНК-out транспозона Tn 10, обеспечивающий возможность положительной селекции без использования антибиотиков при использовании штамма Escherichia coli SCS 110.
Отмечены уникальные сайты рестрикции.
На фиг.2
показаны графики накопления ампликонов кДНК целевого гена, а именно, гена KRT5, в первичной культуре клеток фибробластов кожи человека HDFa (ATCC PCS-201-012) до их трансфекции и через 48 часов после трансфекции этих клеток генотерапевтическим ДНК-вектором VTvaf17-KRT5 с целью оценки способности проникать в эукариотические клетки и функциональной активности, то есть экспрессии целевого гена на уровне мРНК.
На фиг.2 отмечены кривые накопления ампликонов в ходе реакции, соответствующие:
1 - кДНК гена KRT5 в первичной культуре клеток фибробластов кожи человека HDFa до трансфекции ДНК-вектором VTvaf17-KRT5;
2 - кДНК гена KRT5 в первичной культуре клеток фибробластов кожи человека HDFa после трансфекции ДНК-вектором VTvaf17-KRT5;
3 - кДНК гена B2M в первичной культуре клеток фибробластов кожи человека HDFa до трансфекции ДНК-вектором VTvaf17-KRT5;
4 - кДНК гена B2M в первичной культуре клеток фибробластов кожи человека HDFa после трансфекции ДНК-вектором VTvaf17-KRT5;
В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2.
На фиг.3
показаны графики накопления ампликонов кДНК целевого гена, а именно гена KRT14, в первичной культуре первичной культуры кератиноцитов эпидермиса человека HEKa (ATCC PCS-200-011) до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17-KRT14 с целью оценки способности проникать в эукариотические клетки и функциональной активности, то есть экспрессии целевого гена на уровне мРНК.
На фиг.3 отмечены кривые накопления ампликонов в ходе реакции, соответствующие:
1 - кДНК гена KRT14 в первичной культуре первичной культуры кератиноцитов эпидермиса человека HEKa до трансфекции ДНК-вектором VTvaf17-KRT14;
2 - кДНК гена KRT14 первичной культуре первичной культуры кератиноцитов эпидермиса человека HEKa после трансфекции ДНК-вектором VTvaf17-KRT14;
3 - кДНК гена B2M в первичной культуре первичной культуры кератиноцитов эпидермиса человека HEKa до трансфекции ДНК-вектором VTvaf17-KRT14;
4 - кДНК гена B2M первичной культуре первичной культуры кератиноцитов эпидермиса человека HEKa после трансфекции ДНК-вектором VTvaf17-KRT14;
В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2.
На фиг.4
показаны графики накопления ампликонов кДНК целевого гена, а именно гена LAMB3 в клетках скелетных миобластов человека Human Skeletal Myoblasts (HSKM) (GIBCO® Кат. A12555) до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17-LAMB3 с целью оценки способности проникать в эукариотические клетки и функциональной активности, то есть экспрессии целевого гена на уровне мРНК.
На фиг.4 отмечены кривые накопления ампликонов в ходе реакции, соответствующие:
1 - кДНК гена LAMB3 в клетках скелетных миобластов человека линии HSKM до трансфекции ДНК-вектором VTvaf17-LAMB3;
2 - кДНК гена LAMB3 клетках скелетных миобластов человека линии HSKM после трансфекции ДНК-вектором VTvaf17-LAMB3;
3 - кДНК гена B2M клетках скелетных миобластов человека линии HSKM до трансфекции ДНК-вектором VTvaf17-LAMB3;
4 - кДНК гена B2M клетках скелетных миобластов человека линии HSKM после трансфекции ДНК-вектором VTvaf17-LAMB3.
В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2.
На фиг.5
показаны графики накопления ампликонов кДНК целевого гена, а именно гена COL7A1, в первичной культуре клеток эндотелия человека линии Primary Umbilical Vein Endothelial Cells; Normal, Human (HUVEC) (ATCC® PCS-100-010™) до их трансфекции и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17-COL7A1 с целью оценки способности проникать в эукариотические клетки и функциональной активности, то есть экспрессии целевого гена на уровне мРНК.
На фиг.5 отмечены кривые накопления ампликонов в ходе реакции, соответствующие:
1 - кДНК гена COL7A1 в первичной культуре клеток эндотелия человека линии HUVEC до трансфекции ДНК-вектором VTvaf17-COL7A1;
2 - кДНК гена COL7A1 в первичной культуре клеток эндотелия человека линии HUVEC после трансфекции ДНК-вектором VTvaf17-COL7A1;
3 - кДНК гена B2M в первичной культуре клеток эндотелия человека линии HUVEC до трансфекции ДНК-вектором VTvaf17-COL7A1;
4 - кДНК гена B2M в первичной культуре клеток эндотелия человека линии HUVEC после трансфекции ДНК-вектором VTvaf17-COL7A1.
В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2.
На фиг.6
показана диаграмма концентрации белка KRT5 в клеточном лизате первичной культуры фибробластов кожи человека HDFa (ATCC PCS-201-01) после трансфекции этих клеток ДНК-вектором VTvaf17- KRT5 с целью оценки функциональной активности, то есть экспрессии на уровне белка, по изменению количества белка KRT5 в лизате клеток.
На фиг.6 отмечены следующие элементы:
культура А - культура клеток первичных фибробластов кожи человека HDFa, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль);
культура B - культура клеток первичных фибробластов кожи человека HDFa, трансфицированных ДНК-вектором VTvaf17;
культура C - культура клеток первичных фибробластов кожи человека HDFa, трансфицированных ДНК-вектором VTvaf17-KRT5.
На фиг.7
показана диаграмма концентрации белка KRT14 в лизате клеток первичной культуры кератиноцитов эпидермиса человека HEKa (ATCC PCS-200-01), после трансфекции этих клеток ДНК-вектором VTvaf17-KRT14 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген KRT14.
На фиг.7 отмечены следующие элементы:
культура А - первичная культура клеток кератиноцитов эпидермиса человека HEKa, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль);
культура B - первичная культура клеток кератиноцитов эпидермиса человека HEKa, трансфицированных ДНК-вектором VTvaf17;
культура C - первичная культура клеток кератиноцитов эпидермиса человека HEKa, трансфицированных ДНК-вектором VTvaf17-KRT14.
На фиг.8
показана диаграмма концентрации белка LAMB3 в лизате клеток скелетных миобластов человека Human Skeletal Myoblasts (HSKM) (GIBCO® Кат.A12555) после трансфекции этих клеток ДНК-вектором VTvaf17-LAMB3 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген LAMB3.
На фиг.8 отмечены следующие элементы:
культура А - культура скелетных миобластов человека линии HSKM, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль);
культура B - культура скелетных миобластов человека линии HSKM, трансфицированных ДНК-вектором VTvaf17;
культура C - культура скелетных миобластов человека линии HSKM, трансфицированных ДНК-вектором VTvaf17-LAMB3.
На фиг.9
показана диаграмма концентрации белка COL7A1 в лизате клеток первичной культуры эндотелия человека линии Primary Umbilical Vein Endothelial Cells; Normal, Human (HUVEC) (ATCC® PCS-100-010™) после трансфекции этих клеток ДНК-вектором VTvaf17-COL7A1 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL7A1.
На фиг.9 отмечены следующие элементы:
культура А - культура клеток эндотелия человека линии HUVEC, трансфицированных водным раствором дендримеров без плазмидной ДНК (контроль);
культура B - культура клеток эндотелия человека линии HUVEC, трансфицированных ДНК-вектором VTvaf17;
культура C - культура клеток эндотелия человека линии HUVEC, трансфицированных ДНК-вектором VTvaf17-COL7A1.
На фиг.10
показана диаграмма концентрации белка COL7A1 в биоптатах кожи трех пациентов после введения в кожу этих пациентов генотерапевтического ДНК-вектора VTvaf17-COL7A1 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген COL7A1.
На фиг.10 отмечены следующие элементы:
П1I - биоптат кожи пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17-COL7A1;
П1II - биоптат кожи пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П1III - биоптат кожи пациента П1 из интактного участка;
П2I - биоптат кожи пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17-COL7A1;
П2II - биоптат кожи пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П2III - биоптат кожи пациента П2 из интактного участка;
П3I - биоптат кожи пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17-COL7A1;
П3II - биоптат кожи пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П3III - биоптат кожи пациента П3 из интактного участка.
На фиг.11
показана диаграмма концентрации белка LAMB3 в биоптатах икроножной мышцы трех пациентов после введения в икроножную мышцу этих пациентов генотерапевтического ДНК-вектора VTvaf17- LAMB3, с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген LAMB3.
На фиг.11 отмечены следующие элементы:
П1I - биоптат икроножной мышцы пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17- LAMB3;
П1II - биоптат икроножной мышцы пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П1III - биоптат интактного участка икроножной мышцы пациента П1;
П2I - биоптат икроножной мышцы пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17- LAMB3;
П2II - биоптат икроножной мышцы пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П2III - биоптат интактного участка икроножной мышцы пациента П2;
П3I - биоптат икроножной мышцы пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17- LAMB3;
П3II - биоптат икроножной мышцы пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П3III - биоптат интактного участка икроножной мышцы пациента П3.
На фиг.12
показана диаграмма концентрации белка KRT14 в биоптатах кожи трех пациентов после введения в кожу этих пациентов генотерапевтического ДНК-вектора VTvaf17-KRT14 с целью оценки функциональной активности, то есть экспрессии целевого гена на уровне белка, и возможности повышения уровня экспрессии белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген KRT14.
На фиг.12 отмечены следующие элементы:
П1I - биоптат кожи пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17-KRT14;
П1II - биоптат кожи пациента П1 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П1III - биоптат кожи пациента П1 из интактного участка;
П2I - биоптат кожи пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17-KRT14;
П2II - биоптат кожи пациента П2 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П2III - биоптат кожи пациента П2 из интактного участка;
П3I - биоптат кожи пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17-KRT14;
П3II - биоптат кожи пациента П3 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
П3III - биоптат кожи пациента П3 из интактного участка.
На фиг.13
показана диаграмма концентрации белка KRT14 в биоптатах кожи человека после введения в кожу культуры аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14 с целью демонстрации способа применения путем введения аутологичных клеток, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14.
На фиг.13 отмечены следующие элементы:
П1С - биоптат кожи пациента П1 в зоне введения культуры аутологичных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14;
П1B - биоптат кожи пациента П1 в зоне введения аутологичных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17;
П1А - биоптат кожи пациента П1 из интактного участка.
На фиг.14
показана диаграмма концентраций белков: белка KRT5 человека, белка KRT14 человека, белка LAMB3 человека, белка COL7A1 человека в биоптатах кожи трех крыс после инъекционного введения смеси генотерапевтических векторов: генотерапевтического ДНК-вектора VTvaf17- KRT5, генотерапевтического ДНК-вектора VTvaf17-KRT14, генотерапевтического ДНК-вектора VTvaf17-LAMB3, генотерапевтического ДНК-вектора VTvaf17-COL7A1 с целью демонстрации способа применения смеси генотерапевтических ДНК-векторов.
На фиг.14 отмечены следующие элементы:
К1I - биоптат кожи крысы К1 в зоне введения смеси генотерапевтических ДНК векторов: VTvaf17- KRT5, VTvaf17- KRT14, VTvaf17- LAMB3 и VTvaf17- COL7A1;
К1II - биоптат кожи крысы К1 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
К1III - биоптат контрольного интактного участка кожи крысы К1;
К2I - биоптат кожи крысы К2 в зоне введения смеси генотерапевтических ДНК векторов: VTvaf17-KRT5, VTvaf17-KRT14, VTvaf17-LAMB3 и VTvaf17-COL7A1;
К2II - биоптат кожи крысы К2 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
К2III - биоптат контрольного интактного участка кожи крысы К2;
К3I - биоптат кожи крысы К3 в зоне введения смеси генотерапевтических ДНК векторов: VTvaf17- KRT5, VTvaf17- KRT14, VTvaf17- LAMB3 и VTvaf17- COL7A1;
К3II - биоптат кожи крысы К3 в зоне введения генотерапевтического ДНК вектора VTvaf17 (плацебо);
К3III - биоптат контрольного интактного участка кожи крысы К3.
На фиг.15
показаны графики накопления ампликонов кДНК целевого гена LAMB3 в клетках эпителия почки коровы MDBK (NBL-1) (ATCC® CCL-22™) до и через 48 часов после трансфекции этих клеток ДНК-вектором VTvaf17-LAMB3 с целью демонстрации способа применения путем введения генотерапевтического ДНК-вектора животным
На фиг.15 отмечены кривые накопления ампликонов в ходе реакции, соответствующие:
1 - кДНК гена LAMB3 в клетках MDBK до трансфекции генотерапевтическим ДНК-вектором VTvaf17-LAMB3;
2 - кДНК гена LAMB3 в клетках MDBK после трансфекции генотерапевтическим ДНК-вектором VTvaf17-LAMB3;
3 - кДНК гена ACT в клетках MDBK до трансфекции генотерапевтическим ДНК-вектором VTvaf17-LAMB3;
4 - кДНК гена ACT в клетках MDBK после трансфекции генотерапевтическим ДНК-вектором VTvaf17-LAMB3.
В качестве референтного гена использовали ген актина быка/коровы (АСТ), приведенного в базе данных GenBank под номером AH001130.2.
Реализация изобретения
На основе ДНК-вектора VTvaf17 размером 3165 п.н. созданы генотерапевтические ДНК-векторы, несущие целевые гены человека, предназначенные для повышения уровня экспрессии этих целевых генов в тканях человека и животных. При этом способ получения каждого генотерапевтического ДНК-вектора, несущего целевые гены заключается в том, что в полилинкер генотерапевтического ДНК-вектора VTvaf17 клонируют белок-кодирующую последовательность целевого гена, выбранного из группы генов: ген KRT5 (кодирует белок KRT5), ген KRT14 (кодирует белок KRT14), ген LAMB3 (кодирует белок LAMB3), ген COL7A1 (кодирует белок COL7A1) человека. Известно, что способность ДНК-векторов проникать в эукариотические клетки обусловлена, главным образом, размером вектора. При этом ДНК-вектора с наименьшим размером обладают более высокой проникающей способностью. Таким образом, предпочтительным является отсутствие в составе вектора элементов, которые не несут функциональной нагрузки, но при этом увеличивают размер ДНК-вектора. Данные особенности ДНК-векторов были учтены при получении генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1 путем отсутствия в составе вектора крупных нефункциональных последовательностей и генов антибиотикорезистентности, что позволило, помимо технологических преимуществ и преимуществ в плане безопасности применения, значительно уменьшить размер полученного генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1. Таким образом, способность проникать в эукариотические клетки полученного генотерапевтического ДНК-вектора обусловлена его небольшими размерами.
Каждый из генотерапевтических ДНК-векторов: ДНК-вектор VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 получали следующим образом: кодирующую часть целевого гена KRT5, или KRT14, или LAMB3, или COL7A1 клонировали в генотерапевтический ДНК-вектор VTvaf17 и получали генотерапевтический ДНК-вектор VTvaf17-KRT5, SEQ ID №1, или VTvaf17-KRT14, SEQ ID №2 или VTvaf17-LAMB3, SEQ ID №3, или VTvaf17-COL7A1, SEQ ID №4 соответственно. Кодирующую часть гена KRT5 размером 1776 п.н., или гена KRT14 размером 1422 п.н., или гена LAMB3 размером 3521 п.н., или гена COL7A1 размером 8838 п.н. получали путем выделения суммарной РНК из биологического образца ткани здорового человека. Для получения первой цепи кДНК генов KRT5, KRT14, LAMB3, COL7A1 человека использовали реакцию обратной транскрипции. Амплификацию проводили с использованием созданных для этого методом химического синтеза олигонуклеотидов. Расщепление продукта амплификации специфическими эндонуклеазами рестрикции проводили с учетом оптимальной процедуры дальнейшего клонирования, причем клонирование в генотерапевтический ДНК-вектор VTvaf17 проводили по сайтам рестрикции BamHI, SalI, EcoRI, HindIII расположенными в полилинкере вектора VTvaf17. Выбор сайтов рестрикции проводили таким образом, чтобы клонированный фрагмент попадал в рамку считывания экспрессионной кассеты вектора VTvaf17, при этом белок-кодирующая последовательность не содержала сайты рестрикции для выбранных эндонуклеаз. При этом специалистам в данной области техники понятно, что методическая реализация получения генотерапевтического ДНК-вектора VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 может варьировать в рамках выбора известных методов молекулярного клонирования генов, при этом эти способы подпадают под объем настоящего изобретения. Так, например, могут быть использованы различные последовательности олигонуклеотидов для амплификации гена KRT5, или KRT14, или LAMB3, или COL7A1 различные эндонуклеазы рестрикции или такие лабораторные техники как безлигазное клонирование генов.
Генотерапевтический ДНК-вектор VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 обладает нуклеотидной последовательностью SEQ ID №1 или SEQ ID №2 или SEQ ID №3 или SEQ ID №4 соответственно. При этом специалистам в данной области техники известно свойство вырожденности генетического кода, из которого следует, что под объем настоящего изобретения также подпадают варианты нуклеотидных последовательностей, отличающихся инсерцией, делецией или заменой нуклеотидов, которые не приводят к изменению полипептидной последовательности, кодируемой целевым геном, и/или не приводят к потере функциональной активности регуляторных элементов вектора VTvaf17. При этом специалистам в данной области техники известно явление генетического полиморфизма, из которого следует, что под объем настоящего изобретения также подпадают варианты нуклеотидных последовательностей генов из группы генов KRT5, KRT14, LAMB3, COL7A1, которые при этом кодируют различные варианты аминокислотных последовательностей белков KRT5, KRT14, LAMB3, COL7A1, не отличающихся от приведенных по своей функциональной активности при физиологических условиях.
Способность проникать в эукариотические клетки и функциональную активность, то есть способность экспрессировать целевой ген, полученного генотерапевтического ДНК-вектора VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 подтверждают путем введения в эукариотические клетки полученного вектора и последующим анализом экспрессии специфической мРНК и/или белкового продукта целевого гена. Наличие специфической мРНК в клетках, в которые был введен генотерапевтический ДНК-вектор VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 свидетельствует как о способности полученного вектора проникать в эукариотические клетки, так и о его способности экспрессировать мРНК целевого гена. При этом, как известно специалистам в данной области техники, наличие мРНК гена является обязательным условием, но не доказательством трансляции белка, кодируемого целевым геном. Поэтому для подтверждения свойства генотерапевтического ДНК-вектора VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 экспрессировать целевой ген на уровне белка в эукариотических клетках, в которые был введен генотерапевтический ДНК-вектор, проводят анализ концентрации белков, кодируемых целевыми генами, с использованием иммунологических методов. Наличие белка KRT5, или KRT14, или LAMB3, или COL7A1 подтверждает эффективность экспрессии целевых генов в эукариотических клетках и возможность повышения уровня концентрации белка с помощью генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1. Таким образом для подтверждения эффективности экспрессии созданного генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего целевой ген, а именно, ген KRT5, генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген, а именно, ген KRT14, генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген, а именно, ген LAMB3, генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген, а именно, ген COL7A1 использовали следующие методы:
А) ПЦР в реальном времени - изменение накопления ампликонов кДНК целевых генов в лизате клеток человека и животного, после трансфекции различных клеточных линий человека и животного генотерапевтическим ДНК-векторами;
B) Иммуноферментный анализ - изменение количественного уровня целевых белков в лизате или среде клеток человека, после трансфекции различных клеточных линий человека генотерапевтическими ДНК-векторами;
C) Иммуноферментный анализ - изменение количественного уровня целевых белков в супернатанте биоптатов тканей человека и животного, после введения в эти ткани генотерапевтических ДНК-векторов;
D) Иммуноферментный анализ - изменение количественного уровня целевых белков в супернатанте биоптатов тканей человека, после введения в эти ткани аутологичных клеток этого человека, трансфицированных генотерапевтическими ДНК-векторами.
Для подтверждения реализуемости способа применения созданного генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего целевой ген, а именно, ген KRT5, генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген, а именно, ген KRT14, генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген, а именно, ген LAMB3, генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген, а именно, ген COL7A1 выполняли:
А) трансфекцию генотерапевтическими ДНК-векторами различных клеточных линий человека и животного;
B) введение генотерапевтических ДНК-векторов в различные ткани человека и животного;
С) введение в ткани животного смеси генотерапевтических ДНК-векторов;
D) введение в ткани человека аутологичных клеток, трансфицированных генотерапевтическими ДНК-векторами.
Указанные способы применения характеризуются отсутствием потенциальных рисков для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора регуляторных элементов, представляющих собой нуклеотидные последовательности вирусных геномов, и за счет отсутствия в составе генотерапевтического ДНК-вектора генов устойчивости к антибиотикам, что подтверждается отсутствием участков, гомологичных вирусным геномам и генам антибиотикорезистентности в нуклеотидных последовательностях генотерапевтического ДНК-вектора VTvaf17-KRT5, или генотерапевтического ДНК-вектора VTvaf17-KRT14, или генотерапевтического ДНК-вектора VTvaf17-LAMB3, или генотерапевтического ДНК-вектора VTvaf17-COL7A1 (SEQ ID №1 или SEQ ID №2 или SEQ ID №3 или SEQ ID №4 соответственно).
Как известно специалистам в данной области техники, гены антибиотикорезистентности в составе генотерапевтических ДНК-векторов используются с целью получения этих векторов в препаративных количествах путем наращивания бактериальной биомассы в питательной среде, содержащей селективный антибиотик. В рамках настоящего изобретения в целях возможности безопасного применения генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген KRT5 или KRT14, или LAMB3 или COL7A1, использование селективных питательных сред, содержащих антибиотик, не представляется возможным. В качестве технологического решения для получения генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1 для возможности масштабирования до промышленных масштабов получения генотерапевтических векторов предлагается способ получения штаммов для наработки указанных генотерапевтических векторов на основе бактерии Escherichia coli SCS110-AF. Способ получения штамма Escherichia coli SCS110-AF/VTvaf17-KRT5 или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1 заключается в получении компетентных клеток штамма Escherichia coli SCS110-AF с введением в эти клетки генотерапевтического ДНК-вектора VTvaf17-KRT5, или ДНК-вектора VTvaf17-KRT14, или ДНК-вектора VTvaf17-LAMB3, или ДНК-вектора VTvaf17-COL7A1 соответственно с помощью методов трансформации (электропорации), общеизвестных специалистам в данной области техники. Полученный штамм Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамм Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамм Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамм Escherichia coli SCS110-AF/VTvaf17-COL7A1 используется для наработки генотерапевтического ДНК-вектора VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 соответственно с возможностью использования сред без содержания антибиотиков.
Для подтверждения получения штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1 проводили трансформацию, селекцию и последующее наращивание с выделением плазмидной ДНК.
Для подтверждения технологичности получения и возможности масштабирования до промышленного производства генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего целевой ген, а именно, ген KRT5, генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген, а именно, ген KRT14, генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген, а именно, ген LAMB3 генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген, а именно, ген COL7A1, выполняли ферментацию в промышленном масштабе штамма Escherichia coli SCS110-AF/VTvaf17-KRT5 или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14 или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1, каждый из которых содержит генотерапевтический ДНК-вектор VTvaf17, несущий целевой ген, а именно KRT5, или KRT14, или LAMB3, или COL7A1.
Способ масштабирования получения бактериальной массы до промышленных масштабов для выделения генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1, заключается в том, что затравочную культуру штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1 инкубируют в объеме питательной среды без содержания антибиотика обеспечивающим подходящую динамику накопления биомассы, по достижению достаточного количества биомассы в логарифмической фазе роста, бактериальную культуру переносят в промышленный ферментер, после чего растят до достижения стационарной фазы роста, затем выделяют фракцию, содержащую целевой ДНК-продукт - генотерапевтический ДНК-вектор VTvaf17-KRT5, или генотерапевтический ДНК-вектор VTvaf17-KRT14, или генотерапевтический ДНК-вектор VTvaf17-LAMB3, или генотерапевтический ДНК-вектор VTvaf17-COL7A1 многостадийно фильтруют и очищают хроматографическими методами. При этом специалистам в данной области техники понятно, что условия культивирования штаммов, состав питательных сред (за исключением содержания антибиотиков), используемое оборудование, методы очистки ДНК могут варьировать в рамках стандартных операционных процедур в зависимости от отдельно взятой производственной линии, но известные подходы к масштабированию, промышленному получению и очистке ДНК-векторов с использованием штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1, или подпадают под объем настоящего изобретения.
Описанное раскрытие изобретения подтверждается примерами реализации настоящего изобретения.
Изобретение поясняется следующими примерами
Пример 1.
Получение генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего целевой ген, а именно, гена KRT5.
Генотерапевтический ДНК-вектор VTvaf17-KRT5 конструировали клонированием кодирующей части гена KRT5 размером 1776 п.н. в ДНК-вектор VTvaf17 размером 3165 п.н. по сайтам рестрикции BamHI и HindIII. Кодирующую часть гена KRT5 размером 1776 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и ПЦР-амплификации с использованием олигонуклеотидов:
KRT5_F TTTGGATCCACCATGTCTCGCCAGTCAAGTGTGTCCTTC
KRT5_R AATAAGCTTCTAGCTCTTGAAGCTCTTCCGGGAGG
и коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США).
Генотерапевтический ДНК-вектор VTvaf17 конструировали объединением шести фрагментов ДНК, полученных из разных источников:
(а) ориджин репликации получали путем ПЦР-амплификации участка коммерческой плазмиды pBR322 с внесением точечной мутации;
(б) промоторный регион EF1a получали путем ПЦР-амплификации участка геномной ДНК человека;
(в) терминатор транскрипции hGH-TA получали путем ПЦР-амплификации участка геномной ДНК человека;
(г) регуляторный участок транспозона Tn10 РНК-out получали путем синтеза из олигонуклеотидов;
(д) ген устойчивости к канамицину получали путем ПЦР-амплификации участка коммерческой плазмиды pET-28 человека;
(е) полилинкер получали отжигом двух синтетических олигонуклеотидов.
ПЦР-амплификацию проводили с использованием коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США) в соответствии с инструкцией производителя. Фрагменты имеют перекрывающиеся области для возможности их объединения с последующей ПЦР-амплификацией. Объединяли фрагменты (а) и (б) с использованием олигонуклеотидов Ori-F и EF1-R, а также фрагменты (в), (г) и (д) с использованием олигонуклеотидов hGH-F и Kan-R. Далее полученные участки объединяли путем рестрикции с последующим лигированием по сайтам BamHI и NcoI. В результате получали плазмиду, пока еще не содержащую полилинкер. Для его введения проводили расщепление плазмиды по сайтам BamHI и EcoRI, и лигирование с фрагментом (е). Таким образом, получали вектор размером 4182 п.н., несущий ген устойчивости к канамицину, который фланкирован сайтами рестрикции SpeI. Далее этот участок выщепляли по сайтам рестрикции SpeI, после чего оставшийся фрагмент лигировали сам на себя. Таким образом получали генотерапевтический ДНК-вектор VTvaf17 размером 3165 п.н., который является рекомбинантным, с возможностью селекции без антибиотиков.
Расщепление продукта амплификации кодирующей части гена KRT5 и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции BamHI и HindIII (New England Biolabs, США).
В результате получали ДНК-вектор VTvaf17-KRT5 размером 4929 п.н. с нуклеотидной последовательностью SEQ ID №1 и общей структурой изображенной на фиг.1A.
Пример 2.
Получение генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген, а именно, гена KRT14.
Генотерапевтический ДНК-вектор VTvaf17-KRT14 конструировали клонированием кодирующей части гена KRT14 размером 1422 п.н. в ДНК-вектор VTvaf17 размером 3165 п.н. по сайтам рестрикции BamHI и HindIII. Кодирующую часть гена KRT14 размером 1422 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и ПЦР-амплификации с использованием олигонуклеотидов:
KRT14_F TTTGGATCCACCATGACCACCTGCAGCCGCCAG
KRT14_R AATAAGCTTTCAGTTCTTGGTGCGAAGGACCTGC
и коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США), расщепление продукта амплификации и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции BamHI и HindIII (New England Biolabs, США).
В результате получали ДНК-вектор VTvaf17-KRT14 размером 4575 п.н. с нуклеотидной последовательностью SEQ ID №2 и общей структурой изображенной на фиг.1B.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали по Примеру 1.
Пример 3
Получение ДНК-вектора VTvaf17-LAMB3, несущего целевой ген, а именно, гена LAMB3 человека.
Генотерапевтический ДНК-вектор VTvaf17-LAMB3 конструировали клонированием кодирующей части гена LAMB3 размером 3521 п.н. в ДНК-вектор VTvaf17 размером 3165 п.н. по сайтам рестрикции SalI и EcoRI. Кодирующую часть гена LAMB3 размером 3521 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген, Россия) и ПЦР-амплификации с использованием олигонуклеотидов:
LAMB3_F TTAGTCGACCACCATGAGACCATTCTTCCTCTTG
LAMB3_R ATAGAATTCACTTGCAGGTGGCATAGTAGAG
и коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США), расщепление продукта амплификации и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции SalI и EcoRI (New England Biolabs, США).
В результате получали ДНК-вектор VTvaf17-LAMB3 размером 6674 п.н. с нуклеотидной последовательностью SEQ ID №3 и общей структурой изображенной на фиг.1C.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали по Примеру 1.
Пример 4.
Получение генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген, а именно, гена COL7A1.
Генотерапевтический ДНК-вектор VTvaf17-COL7A1 конструировали клонированием кодирующей части гена COL7A1 размером 8838 п.н. в ДНК-вектор VTvaf17 размером 3165 п.н. по сайтам рестрикции SalI и EcoRI. Кодирующую часть гена COL7A1 размером 8838 п.н. получали путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции с использованием коммерческого набора Mint-2 (Евроген) и ПЦР-амплификации с использованием олигонуклеотидов:
COL7A1_F ATCGTCGACCACCATGACGCTGCGGCTTCTGGT
COL7A1_R ATAGAATTCAGTCCTGGGCAGTACCTGTC
и коммерческого набора Phusion® High-Fidelity DNA Polymerase (New England Biolabs, США), расщепление продукта амплификации и ДНК-вектора VTvaf17 проводили эндонуклеазами рестрикции SalI и EcoRI (New England Biolabs, США).
В результате получали ДНК-вектор VTvaf17-COL7A1 размером 11990 п.н. с нуклеотидной последовательностью SEQ ID №4 и общей структурой изображенной на фиг.1D.
При этом генотерапевтический ДНК-вектор VTvaf17 конструировали по Примеру 1.
Пример 5.
Подтверждение способности генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего целевой ген, а именно, ген KRT5, проникать в эукариотические клетки и подтверждение его функциональной активности на уровне экспрессии мРНК целевого гена. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген.
Оценивали изменения накопления мРНК целевого гена KRT5, в первичной культуре фибробластов кожи человека HDFa (ATCC PCS-201-01) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-KRT5, несущим ген KRT5 человека. Количество мРНК определяли по динамике накопления ампликонов кДНК в реакции ПРЦ в реальном времени.
Для оценки изменения накопления мРНК целевого гена KRT5, использовалась первичная культура фибробластов кожи человека HDFa. Клеточную культуру HDFa выращивали в стандартных условиях (37°С, 5% СО2) с использованием питательной среды Fibroblast Growth Kit-Serum-Free (ATCC® PCS-201-040). В процессе культивирования каждые 48 ч происходила смена ростовой среды.
Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку. Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-KRT5, экспрессирующим ген KRT5 человека, проводили с использованием Lipofectamine 3000 (ThermoFisher Scientific, США) согласно рекомендациям производителя. В пробирке №1 к 25 мкл среды Opti-MEM (Gibco, США) добавляли 1 мкл раствора ДНК-вектора VTvaf17-KRT5 (концентрация 500 нг/мкл) и 1 мкл реагента Р3000. Аккуратно перемешивали легким встряхиванием. В пробирке №2 к 25 мкл среды Opti-MEM (Gibco, США) добавляли 1 мкл раствора Lipofectamin 3000. Аккуратно перемешивали легким встряхиванием. Добавляли содержимое пробирки №1 к содержимому пробирки №2, инкубировали 5 мин при комнатной температуре. Полученный раствор по каплям добавляли к клеткам в объеме 40 мкл.
В качестве контроля использовали клетки HDFa, трансфицированные генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена (кДНК гена KRT5 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано). Подготовку контрольного вектора VTvaf17 для трансфекции проводили как описано выше.
Суммарную РНК из клеток HDFa выделяли с использованием Trizol Reagent (Invitrogen, США) согласно рекомендациям производителя. В лунку с клетками добавляли 1 мл Trizol Reagent и гомогенизировали с последующим прогреванием в течении 5 мин при 65°С. Далее образец центрифугировали при 14 000g в течении 10 мин и снова прогревали в течении 10 мин при 65°С. Далее добавляли 200 мкл хлороформа, плавно перемешивали и центрифугировали при 14000g в течении 10 мин. Затем отбирали водную фазу, добавляли к ней 1/10 объема 3М ацетата натрия, рН 5.2 и равный объем изопропилового спирта. Инкубировали образец при -20°С в течении 10 мин с последующим центрифугированием при 14000g в течении 10 мин. Осадок промывали 1 мл 70% этилового спирта, высушивали на воздухе и растворяли в 10 мкл воды, свободной от РНКаз. Определение уровня экспрессии мРНК гена KRT5 после трансфекции проводили путем оценки динамики накопления ампликонов кДНК методом ПЦР в режиме реального времени. Для получения и амплификации кДНК, специфичной для гена KRT5 человека, использовали олигонуклеотиды KRT5_SF и KRT5_SR:
KRT5_SF CGAAGCCGAGTCCTGGTATC
KRT5_SR TTGGCGCACTGTTTCTTGAC
Длина продукта амплификации - 162 п.н.
Реакцию обратной транскрипции и ПЦР-амплификацию проводили с помощью набора реагентов SYBR GreenQuantitect RT-PCR Kit (Qiagen, США) для ПЦР в режиме реального времени. Реакцию проводили в объеме 20 мкл, содержащих: 25 мкл QuantiTect SYBR Green RT-PCR MasterMix, 2,5 мМ хлорида магния, по 0,5 мкМ каждого праймера, 5 мкл РНК. Реакцию осуществляли на амплификаторе CFX96 (Bio-Rad, США) при следующих условиях: 1 цикл обратной транскрипции при 42°С - 30 минут, денатурация 98°С - 15 мин, затем 40 циклов, включающих денатурацию 94°С - 15 сек, отжиг праймеров 60°C - 30 сек и элонгацию 72°С - 30 сек. В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов KRT5 и B2M. В качестве отрицательного контроля использовали деионизированную воду. Количество динамику накопления ампликонов кДНК генов KRT5 и B2M оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1 (Bio-Rad, США). Графики, полученные в результате анализа представлены на фиг.2.
Из фигуры 2 следует, что в результате трансфекции первичной культуры клеток фибробластов человека HDFa генотерапевтическим ДНК-вектором VTvaf17-KRT5, уровень специфической мРНК гена KRT5 человека вырос многократно, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген KRT5 на уровне мРНК. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-KRT5 для повышения уровня экспрессии гена KRT5 в эукариотических клетках.
Пример 6.
Подтверждение способности генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген, а именно, ген KRT14, проникать в эукариотические клетки и подтверждение его функциональной активности на уровне экспрессии мРНК целевого гена. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген.
Оценивали изменения накопления мРНК целевого гена KRT14, в первичной культуре кератиноцитов эпидермиса человека HEKa (ATCC PCS-200-011) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-KRT14, несущим ген KRT14 человека. Количество мРНК определяли по динамике накопления ампликонов кДНК в реакции ПРЦ в реальном времени.
Первичную культуру клеток кератиноцитов эпидермиса человека HEKa выращивали в среде Keratinocyte Growth Kit (ATCC® PCS-200-040™) в стандартных условиях (37°С, 5% СО2). Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-KRT14, экспрессирующим ген KRT14 человека, проводили как описано в примере 5. В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2. В качестве контроля использовали культуру клеток HEKa, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим целевой ген (кДНК гена KRT14 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано). Выделение РНК, реакцию обратной транскрипции и ПЦР в реальном времени проводили как описано в примере 5, за исключением олигонуклеотидов с отличающимися от примера 5 последовательностями. Для амплификации кДНК, специфичной для гена KRT14 человека, использовали олигонуклеотиды KRT14_SF и KRT14_SR:
KRT14_SF TCCAGGAGATGATTGGCAGC
KRT14_SR GGATGACTGCGATCCAGAGG
Длина продукта амплификации - 197 п.н.
В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов KRT14 и B2M. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов KRT14 и B2M, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1 (Bio-Rad, США). Графики, полученные в результате анализа представлены на фиг.3.
Из фигуры 3 следует, что в результате трансфекции культуры клеток HEKa генотерапевтическим ДНК-вектором VTvaf17-KRT14, уровень специфической мРНК гена KRT14 человека вырос многократно, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген KRT14 на уровне мРНК. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-KRT14 для повышения уровня экспрессии гена KRT14 в эукариотических клетках.
Пример 7.
Подтверждение способности генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген, а именно, ген LAMB3, проникать в эукариотические клетки и подтверждение его функциональной активности на уровне экспрессии мРНК целевого гена. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген.
Оценивали изменения накопления мРНК целевого гена LAMB3 в культуре клеток скелетных миобластов человека Human Skeletal Myoblasts (HSKM) (GIBCO® Кат.A12555) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-LAMB3, несущим ген LAMB3 человека. Количество мРНК определяли по динамике накопления ампликонов кДНК в реакции ПРЦ в реальном времени.
Культуру клеток скелетных миобластов человека линии HSKM выращивали в среде Dulbecco's Modified Eagle's Medium (DMEM) (ATCC® 30-2002™) с добавлением 2% лошадиной сыворотки (Gibco Кат.16050130) в стандартных условиях (37°С, 5% СО2). Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-LAMB3, экспрессирующим ген LAMB3 человека, проводили как описано в примере 5. В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2. В качестве контроля использовали культуру клеток HSKM, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим целевой ген (кДНК гена LAMB3 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано). Выделение РНК, реакцию обратной транскрипции и ПЦР в реальном времени проводили как описано в примере 5, за исключением олигонуклеотидов с отличающимися от примера 5 последовательностями. Для амплификации кДНК, специфичной для гена LAMB3 человека, использовали олигонуклеотиды LAMB3_SF и LAMB3_SR:
LAMB3_SF CAGAGGAGCTGTTTGGGGAG
LAMB3_SR CCCATTGATGTGGTCACGGA
Длина продукта амплификации - 155 п.н.
В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов LAMB3 и B2M. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов LAMB3 и B2M, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1 (Bio-Rad, США). Графики, полученные в результате анализа представлены на фиг.4.
Из фигуры 4 следует, что в результате трансфекции культуры клеток скелетных миобластов человека линии HSKM генотерапевтическим ДНК-вектором VTvaf17-LAMB3 уровень специфической мРНК гена LAMB3 человека вырос многократно, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген LAMB3 на уровне мРНК. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-LAMB3 для повышения уровня экспрессии гена LAMB3 в эукариотических клетках.
Пример 8.
Подтверждение способности генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген, а именно, ген COL7A1, проникать в эукариотические клетки и подтверждение его функциональной активности на уровне экспрессии мРНК целевого гена. Данный пример также демонстрирует реализуемость способа применения генотерапевтического ДНК-вектора, несущего целевой ген.
Оценивали изменения накопления мРНК целевого гена COL7A1, в первичной культуре клеток эндотелия человека линии Primary Umbilical Vein Endothelial Cells; Normal, Human (HUVEC) (ATCC® PCS-100-010™) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-COL7A1, несущим ген COL7A1 человека. Количество мРНК определяли по динамике накопления ампликонов кДНК в реакции ПРЦ в реальном времени.
Культуру клеток эндотелия человека линии HUVEC выращивали в среде Vascular Cell Basal Medium (ATCC PCS-100-030) с добавлением Endothelial Cell Growth Kit-BBE (ATCC® PCS-100-040™) в стандартных условиях (37°С, 5% СО2). Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку. Для трансфекции использовали реагент Lipofectamine 3000 (ThermoFisher Scientific, США). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-COL7A1, экспрессирующим ген COL7A1 человека, проводили как описано в примере 5. В качестве контроля использовали культуру клеток эндотелия человека линии HUVEC, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим целевой ген (кДНК гена COL7A1 до и после трансфекции генотерапевтическим ДНК-вектором VTvaf17, не содержащим вставку целевого гена на фигурах не показано). Выделение РНК, реакцию обратной транскрипции и ПЦР в реальном времени проводили как описано в примере 5, за исключением олигонуклеотидов с отличающимися от примера 5 последовательностями. Для амплификации кДНК, специфичной для гена COL7A1 человека, использовали олигонуклеотиды COL7A1_SF и COL7A1_SR:
COL7A1_SF CAAAGGAGAGATGGGGGAGC
COL7A1_SR ATCATTTCCACTGGGGCCTG
Длина продукта амплификации - 184 п.н.
В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности кДНК генов COL7A1 и B2M. В качестве референтного гена использовали ген B2M (Бета-2-микроглобулин) приведенный в базе данных GenBank под номером NM 004048.2. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов COL7A1 и B2M, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1 (Bio-Rad, США). Графики, полученные в результате анализа представлены на фиг.5.
Из фигуры 5 следует, что в результате трансфекции культуры клеток эндотелия человека линии HUVEC генотерапевтическим ДНК-вектором VTvaf17-COL7A1, уровень специфической мРНК гена COL7A1 человека вырос многократно, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген COL7A1 на уровне мРНК. Представленные результаты также подтверждают реализуемость способа применения генотерапевтическим ДНК-вектором VTvaf17-COL7A1 для повышения уровня экспрессии гена COL7A1 в эукариотических клетках.
Пример 9.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего ген KRT5, для повышения экспрессии белка KRT5 в клетках млекопитающих.
Оценивали изменение количества белка KRT5 в лизате фибробластов кожи человека HDFa (ATCC PCS-201-01) после трансфекции этих клеток ДНК-вектором VTvaf17-KRT5, несущим ген KRT5 человека.
Клеточную культуру фибробластов кожи человека выращивали как это описано в примере 5.
Для получения 90% конфлюэнтности, за 24 часа до постановки трансфекции клетки высевали в 24-луночный планшет из расчета 5×104 клеток/лунку. Для трансфекции использовали реагент SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия). В качестве контроля использовали водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена KRT5 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17-KRT5, несущий ген KRT5 человека (С). Приготовление комплекса ДНК/дендример проводили по методике производителя (QIAGEN, SuperFect Transfection Reagent Handbook, 2002) с некоторыми изменениями. Для трансфекции клеток в одной лунке 24-луночного планшета к 1 мкг ДНК-вектора, растворенного в буфере ТЕ, добавляли культуральную среду до конечного объема 60 мкл, затем добавляли 5 мкл SuperFect Transfection Reagent и осторожно перемешивали пятикратным пипетированием. Комплекс инкубировали при комнатной температуре в течении 10-15 мин. Далее отбирали из лунок культуральную среду, лунки промывали 1 мл буфера PBS. К образовавшемуся комплексу добавляли 350 мкл среды, содержащей 10 мкг/мл гентамицина, осторожно перемешивали и добавляли к клеткам. Клетки инкубировали с комплексом 2-3 часа при 37°С в атмосфере, содержащей 5% СО2.
Затем осторожно удаляли среду, промывали клеточный монослой 1 мл буфера PBS. Затем добавляли среду, содержащую 10 мкг/мл гентамицина, и инкубировали 24-48 часов при 37°С в атмосфере 5% СО2.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение белка KRT5 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human KRT5 / CK5 / Cytokeratin 5 ELISA Kit (Sandwich ELISA) (LifeSpan BioSciences Кат.LS-F8194-1, США) согласно методике производителя с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка KRT5, входящим в состав набора. Чувствительность метода составляла не менее 15,6 пг/мл, диапазон измерения - от 15,6 пг/мл до 1000 пг/мл. Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). Графики, полученные в результате анализа представлены на фиг.6.
Из фигуры 6 следует, что трансфекция клеток фибробластов кожи человека HDFa генотерапевтическим ДНК-вектором VTvaf17-KRT5 приводит к увеличению количества белка KRT5 по сравнению с контрольными образцами, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген KRT5 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-KRT5 для повышения уровня экспрессии KRT5 в эукариотических клетках.
Пример 10.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего ген KRT14, для повышения экспрессии белка KRT14 в клетках млекопитающих.
Оценивали изменение количества белка KRT14 в лизате клеток первичной культуры кератиноцитов эпидермиса человека HEKa (ATCC PCS-200-01) после трансфекции этих клеток ДНК-вектором VTvaf17-KRT14, несущим ген KRT14 человека. Клетки выращивали как описано в примере 6.
Для трансфекции использовали реагент SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия). В качестве контроля использовали водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена KRT14 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17-KRT14, несущий ген KRT14 человека (С). Приготовление комплекса ДНК-дендример и трансфекцию клеток HEKa проводили как описано в примере 9.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка. Количественное определение белка KRT14 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human KRT14 / CK14 / Cytokeratin 14 ELISA Kit (Sandwich ELISA) (LifeSpan BioSciences Кат.LS-F7936, США) согласно методике производителя с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка KRT14, входящим в состав набора. Чувствительность метода составляла не менее 156 пг/мл, диапазон измерения - от 156 пг/мл до 10000 пг/мл. Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). Графики, полученные в результате анализа представлены на фиг.7.
Из фигуры 7 следует, что трансфекция первичной культуры клеток кератиноцитов эпидермиса человека HEKa генотерапевтическим ДНК-вектором VTvaf17-KRT14 приводит к увеличению количества белка KRT14 по сравнению с контрольными образцами, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген KRT14 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-KRT14 для повышения уровня экспрессии KRT14 в эукариотических клетках.
Пример 11.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего ген LAMB3, для повышения экспрессии белка LAMB3 в клетках млекопитающих.
Оценивали изменение количества белка LAMB3 в лизате клеток скелетных миобластов человека Human Skeletal Myoblasts (HSKM) (GIBCO® Кат.A12555) после трансфекции этих клеток ДНК-вектором VTvaf17-LAMB3, несущим ген LAMB3 человека. Клетки культивировали как описано в примере 7.
Для трансфекции использовали реагент SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия). В качестве контроля использовали водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена LAMB3 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17-LAMB3, несущий ген LAMB3 человека (С). Приготовление комплекса ДНК-дендример и трансфекцию клеток HSKM проводили как описано в примере 9.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение белка LAMB3 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human LAMB3 / Laminin Beta 3 ELISA Kit (Sandwich ELISA) (LifeSpan BioSciences Кат.LS-F33141, США) согласно методике производителя с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка LAMB3, входящим в состав набора. Чувствительность метода составляла не менее 9,375 пг/мл, диапазон измерения - от 15,625 пг/мл до 8000 пг/мл. Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). Графики, полученные в результате анализа представлены на фиг.8.
Из фигуры 8 следует, что трансфекция культуры клеток скелетных миобластов человека линии HSKM генотерапевтическим ДНК-вектором VTvaf17-LAMB3 приводит к увеличению количества белка LAMB3 по сравнению с контрольными образцами, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген LAMB3 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-LAMB3 для повышения уровня экспрессии LAMB3 в эукариотических клетках.
Пример 12.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего ген COL7A1, для повышения экспрессии белка COL7A1 в клетках млекопитающих.
Оценивали изменение количества белка COL7A1 в лизате культуры клеток первичной культуры эндотелия человека линии Primary Umbilical Vein Endothelial Cells; Normal, Human (HUVEC) (ATCC® PCS-100-010™) после трансфекции этих клеток ДНК-вектором VTvaf17-COL7A1, несущим ген COL7A1 человека. Клетки культивировали как описано в примере 8.
Для трансфекции использовали реагент SuperFect Transfection Reagent 6-го поколения (Qiagen, Германия). В качестве контроля использовали водный раствор дендримеров без ДНК-вектора (А), ДНК-вектор VTvaf17, не содержащий кДНК гена COL7A1 (В), в качестве трансфицируемых агентов - ДНК-вектор VTvaf17-COL7A1, несущий ген COL7A1 человека (С). Приготовление комплекса ДНК-дендримеры и трансфекцию клеток HUVEC проводили как описано в примере 9.
После трансфекции клетки промывали три раза PBS, далее к клеткам добавляли 1 мл PBS и подвергали трехкратному замораживанию/оттаиванию. Далее суспензию центрифугировали при 15000 об/мин в течение 15 мин, отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение белка COL7A1 проводили методом твердофазного иммуноферментного анализа (ELISA), используя набор Human COL7A1 / Collagen VII ELISA Kit (Sandwich ELISA) (LifeSpan BioSciences Кат.LS-F11164, США) согласно методике производителя с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Численное значение концентрации определяли с помощью калибровочной кривой, построенной по стандартным образцам с известной концентрацией белка COL7A1, входящим в состав набора. Чувствительность метода составляла не менее 156 пг/мл, диапазон измерения - от 156 пг/мл до 10000 пг/мл. Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). Графики, полученные в результате анализа, представлены на фиг.9.
Из фигуры 9 следует, что трансфекция клеток первичной культуры эндотелия человека линии HUVEC генотерапевтическим ДНК-вектором VTvaf17-COL7A1 приводит к увеличению количества белка COL7A1 по сравнению с контрольными образцами, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген COL7A1 на уровне белка. Представленные результаты также подтверждают реализуемость способа применения генотерапевтического ДНК-вектора VTvaf17-COL7A1 для повышения уровня экспрессии COL7A1 в эукариотических клетках.
Пример 13.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего ген COL7A1, для повышения экспрессии белка COL7A1 в тканях человека.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген, а именно, ген COL7A1 и реализуемости способа его применения оценивали изменения количества белка COL7A1 в коже человека при введении в кожу человека генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего ген человека COL7A1.
С целью анализа изменения количества белка COL7A1 трем пациентам вводили в кожу предплечья генотерапевтический ДНК-вектор VTvaf17-COL7A1, несущий ген COL7A1 и параллельно вводили плацебо, представляющее собой генотерапевтический ДНК-вектор VTvaf17, не содержащий кДНК гена COL7A1.
Пациент 1, женщина 44 года, (П1); пациент 2, женщина 50 лет, (П2); пациент 3, мужчина, 53 года, (П3). В качестве транспортной системы использовали полиэтиленимин Transfection reagent cGMP grade in-vivo-jetPEI (Polyplus Transfection, Франция). Генотерапевтический ДНК-вектор VTvaf17-COL7A1, который содержит кДНК гена COL7A1 и генотерапевтический ДНК-вектор VTvaf17, используемый в качестве плацебо, который не содержит кДНК гена COL7A1, каждый из которых растворяли в стерильной воде степени очистки Nuclease-Free. Для получения генетической конструкции готовили комплексы ДНК- cGMP grade in-vivo-jetPEI в соответствии с рекомендациями производителя.
Генотерапевтический ДНК-вектор VTvaf17 (плацебо) и генотерапевтический ДНК вектор VTvaf17-COL7A1, несущий ген COL7A1 вводили в количестве 1 мг для каждой генетической конструкции тоннельным методом иглой 30G на глубину 2-3 мм. Объем вводимого раствора генотерапевтического ДНК-вектора VTvaf17 (плацебо) и генотерапевтического ДНК вектора VTvaf17-COL7A1, несущего ген COL7A1 - 0,3 мл для каждой генетической конструкции. Очаги введения каждой генетической конструкции располагались на участке предплечья на расстоянии 8-10 см друг от друга.
Биопсийные образцы отбирали на 2-е сутки после введения генетических конструкций генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков кожи пациентов в зоне введения генотерапевтического ДНК вектора VTvaf17-COL7A1, несущего ген COL7A1 (I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (II), а также из интактных участков кожи (III), используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL, Италия). Кожу пациентов в зоне отбора биоптата предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 10 куб. мм, масса - около 11 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000g. Отбирали супернатант и использовали его для количественного определения целевого белка методом твердофазного иммуноферментного анализа (ELISA). Количественное определение белка COL7A1 проводили методом твердофазного иммуноферментного анализа (ELISA) как это описано в примере 12 с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). согласно методике производителя с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США). Графики, полученные в результате анализа, представлены на фиг.10.
Из фигуры 10 следует, что в коже всех трех пациентов в области введения генотерапевтического ДНК вектора VTvaf17-COL7A1, несущего целевой ген COL7A1 человека, произошло увеличение количества белка COL7A1 в сравнении с количеством белка COL7A1 в области введения генотерапевтического ДНК-вектора VTvaf17 (плацебо), не содержащего ген COL7A1 человека, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-COL7A1 и подтверждает реализуемость способа его применения, в частности при внутрикожном введении генотерапевтического ДНК-вектора в ткани человека.
Пример 14.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего ген LAMB3, для повышения экспрессии белка LAMB3 в тканях человека.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген LAMB3 и реализуемости способа его применения оценивали изменение количества белка LAMB3 в мышечной ткани человека при введении генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген, а именно, ген LAMB3 человека.
С целью анализа изменения количества белка LAMB3 трем пациентам вводили в ткань икроножной мышцы генотерапевтический ДНК-вектор VTvaf17- LAMB3, несущий ген LAMB3 с транспортной молекулой, и параллельно вводили плацебо, представляющее собой генотерапевтический ДНК-вектор VTvaf17, не содержащий кДНК гена LAMB3 с транспортной молекулой.
Пациент 1, женщина 40 лет, (П1); пациент 2, женщина 43 года (П2); пациент 3, мужчина 54 года, (П3). В качестве транспортной системы использовали полиэтиленимин Transfection reagent cGMP grade in-vivo-jetPEI (Polyplus Transfection, Франция), пробоподготовку проводили в соответствии с рекомендациями производителя.
Генотерапевтический ДНК-вектор VTvaf17 (плацебо) и генотерапевтический ДНК вектор VTvaf17-LAMB3, несущий ген LAMB3 вводили в количестве 1 мг для каждой генетической конструкции тоннельным методом иглой 30G на глубину около 10 мм. Объем вводимого раствора генотерапевтического ДНК-вектора VTvaf17 (плацебо) и генотерапевтического ДНК вектора VTvaf17- LAMB3, несущего ген LAMB3 - 0,3 мл для каждой генетической конструкции. Очаги введения каждой генетической конструкции располагали медиально на расстоянии 8-10 см друг от друга.
Биопсийные образцы отбирали на 2-е сутки после введения генетических конструкций генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков мышечной ткани пациентов в зоне введения генотерапевтического ДНК вектора VTvaf17-LAMB3, несущего ген LAMB3 (I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (II), а также из интактного участка икроножной мышцы (III), используя устройство для взятия биопсии MAGNUM (BARD, США). Кожу пациентов в зоне отбора биоптата предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 20 куб. мм, масса - около 22 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000g. Отбирали супернатант и использовали его для количественного определения целевого белка.
Количественное определение белка LAMB3 проводили методом твердофазного иммуноферментного анализа (ELISA) как это описано в примере 11 с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). Графики, полученные в результате анализа представлены на фиг.11.
Из фигуры 11 следует, что в икроножной мышце всех трех пациентов в области введения генотерапевтического ДНК вектора VTvaf17-LAMB3, несущего целевой ген, а именно, ген LAMB3 человека, произошло увеличение количества белка LAMB3 в сравнении с количеством белка LAMB3 в области введения генотерапевтического ДНК-вектора VTvaf17 (плацебо), не содержащего ген LAMB3 человека, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-LAMB3 и подтверждает реализуемость способа его применения, в частности при внутримышечном введении генотерапевтического ДНК-вектора в ткани человека.
Пример 15.
Подтверждение эффективности и реализуемости способа применения генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего ген KRT14, для повышения экспрессии белка KRT14 в тканях человека.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген, а именно, ген KRT14 и реализуемости способа его применения оценивали изменения количества белка KRT14 в коже человека при введении в кожу человека генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего ген человека KRT14.
С целью анализа изменения количества белка KRT14 трем пациентам вводили в кожу предплечья генотерапевтический ДНК-вектор VTvaf17-KRT14, несущий ген KRT14 и параллельно вводили плацебо, представляющее собой генотерапевтический ДНК-вектор VTvaf17, не содержащий кДНК гена KRT14.
Пациент 1, женщина 39 лет (П1); пациент 2, мужчина 61 год (П2); пациент 3, мужчина, 38 лет (П3). В качестве транспортной системы использовали полиэтиленимин Transfection reagent cGMP grade in-vivo-jetPEI (Polyplus Transfection, Франция). Генотерапевтический ДНК-вектор VTvaf17-KRT14, который содержит кДНК гена KRT14 и генотерапевтический ДНК-вектор VTvaf17, используемый в качестве плацебо, который не содержит кДНК гена KRT14, каждый из которых растворяли в стерильной воде степени очистки Nuclease-Free. Для получения генетической конструкции готовили комплексы ДНК- cGMP grade in-vivo-jetPEI в соответствии с рекомендациями производителя.
Генотерапевтический ДНК-вектор VTvaf17 (плацебо) и генотерапевтический ДНК вектор VTvaf17-KRT14, несущий ген KRT14 вводили в количестве 1 мг для каждой генетической конструкции тоннельным методом иглой 30G на глубину 1,5 - 2 мм. Объем вводимого раствора генотерапевтического ДНК-вектора VTvaf17 (плацебо) и генотерапевтического ДНК вектора VTvaf17-KRT14, несущего ген KRT14 - 0,3 мл для каждой генетической конструкции. Очаги введения каждой генетической конструкции располагались на участке предплечья на расстоянии 8-10 см друг от друга.
Биопсийные образцы отбирали на 2-е сутки после введения генетических конструкций генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков кожи пациентов в зоне введения генотерапевтического ДНК вектора VTvaf17-KRT14, несущего ген KRT14 (I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (II), а также из интактных участков кожи (III), используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL, Италия). Кожу пациентов в зоне отбора биоптата предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 10 куб. мм, масса - около 11 мг.Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000g. Отбирали супернатант и использовали его для количественного определения целевого белка методом твердофазного иммуноферментного анализа (ELISA) по примеру 10 с детекцией оптической плотности при помощи автоматического биохимического и иммуноферментного анализатора ChemWell (Awareness Technology Inc., США).
Статистическую обработку полученных результатов осуществляли с помощью программного обеспечения для статистической обработки и визуализации данных R, версия 3.0.2 (https://www.r-project.org/). Графики, полученные в результате анализа, представлены на фиг.12.
Из фигуры 12 следует, что в коже всех трех пациентов в области введения генотерапевтического ДНК вектора VTvaf17-KRT14, несущего целевой ген KRT14 человека, произошло увеличение количества белка KRT14 в сравнении с количеством белка KRT14 в области введения генотерапевтического ДНК-вектора VTvaf17 (плацебо), не содержащего ген KRT14 человека, что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-KRT14 и подтверждает реализуемость способа его применения, в частности при внутрикожном введении генотерапевтического ДНК-вектора в ткани человека.
Пример 16.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего ген KRT14 и реализуемости способа его применения для повышения уровня экспрессии белка KRT14 в тканях человека путем введения аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего ген KRT14 и реализуемости способа его применения оценивали изменения количества белка KRT14 в коже человека при введении в кожу пациента культуры аутологичных фибробластов этого пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14.
Пациенту вводили в кожу предплечья соответствующую культуру аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14, несущим ген KRT14, и параллельно вводили плацебо, представляющее собой культуру аутологичных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим ген KRT14.
Первичную культуру фибробластов человека выделяли из биоптатов кожи пациента. Используя устройство для взятия биопсии кожи Epitheasy 3.5 (Medax SRL, Италия) брали образец биоптата кожи из зоны, защищенной от действия ультрафиолета, а именно за ушной раковиной или с боковой внутренней поверхности в зоне локтевого сустава, размером около 10 кв. мм, массой - около 11 мг. Кожу пациента предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Культивирование первичной культуры клеток осуществляли при 37°С в атмосфере, содержащей 5% СО2 в среде DMEM с 10% фетальной телячьей сывороткой и ампициллином 100 Ед/мл. Пересев культуры и смену культуральной среды осуществляли каждые 2 дня. Общая продолжительность роста культуры не превышала 25-30 дней. Из культуры клеток отбирали аликвоту, содержащую 5×104 клеток. Культуру фибробластов пациента трансфицировали генотерапевтическим ДНК-вектором VTvaf17-KRT14, несущим ген KRT14 и плацебо - вектором VTvaf17, не несущим целевой ген KRT14.
Трансфекцию осуществляли с помощью катионного полимера полиэтиленимина JETPEI (Polyplus Transfection, Франция), согласно инструкции фирмы-производителя. Клетки культивировали 72 часа и затем вводили пациенту. Введение пациенту культуры аутологичных фибробластов этого пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14, и плацебо, представляющее собой культуру аутологичных фибробластов пациента, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, осуществляли туннельным методом в область предплечья иглой 30G длиной 13 мм на глубину около 3 мм. Концентрация модифицированных аутологичных фибробластов в вводимой суспензии составляла примерно 5 млн клеток на 1 мл суспензии, количество вводимых клеток не превышало 15 млн. Очаги введения культуры аутологичных фибробластов располагались на расстоянии 8-10 см друг от друга.
Биопсийные образцы отбирали на 4-е сутки после введения культуры аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14, несущим целевой ген, а именно, ген KRT14 и плацебо. Взятие биопсии осуществляли из участков кожи пациента в зоне введения культуры аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14, несущим целевой ген, а именно, ген KRT14 (C), культуры аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим целевой ген KRT14 (плацебо) (B), а также из участков интактной кожи (A), используя устройство для взятия биопсии Epitheasy 3.5 (Medax SRL, Италия). Кожу в зоне отбора биоптата пациентов предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер биопсийного образца составлял около 10 куб. мм, масса - около 11 мг. Образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000g. Отбирали супернатант и использовали его для количественного определения целевого белка как это описано в примере 15.
Графики, полученные в результате анализа, представлены на фиг.13.
Из фигуры 13 следует, что в коже пациента в области введения культуры аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14, несущим ген KRT14, произошло увеличение количества белка KRT14 в сравнении с количеством белка KRT14 в области введения культуры аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17, не несущим ген KRT14 (плацебо), что свидетельствует об эффективности генотерапевтического ДНК-вектора VTvaf17-KRT14 и подтверждает реализуемость способа его применения для повышения уровня экспрессии KRT14 в тканях человека, в частности при введении аутологичных фибробластов, трансфицированных генотерапевтическим ДНК-вектором VTvaf17-KRT14.
Пример 17.
Подтверждение эффективности и реализуемости способа сочетанного применения генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего ген KRT5, генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего ген KRT14, генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего ген LAMB3, генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего ген COL7A1, для повышения уровня экспрессии белков KRT5, KRT14, LAMB3 и COL7A1 в тканях млекопитающих.
Оценивали изменение количества белков KRT5, KRT14, LAMB3 и COL7A1 в зоне кожи крысы линии Вистар при введении в эту зону смеси генотерапевтических векторов.
В качестве транспортной системы использовали полиэтиленимин Transfection reagent cGMP grade in-vivo-jetPEI (Polyplus Transfection, Франция). Эквимолярную смесь четырех генотерапевтических ДНК-векторов, а также генотерапевтический ДНК-вектор VTvaf17 в качестве плацебо, растворяли в стерильной воде степени очистки Nuclease-Free. Для получения генетической конструкции готовили комплексы ДНК-cGMP grade in-vivo-jetPEI в соответствии с рекомендациями производителя. Объем вводимого раствора каждой генетический конструкции (смеси генотерапевтических ДНК-векторов и плацебо) составлял 0,3 мл с суммарным количеством ДНК 100 мкг. Введение раствора осуществляли тоннельным методом инсулиновым шприцом на глубину 1-1,5 мм в зону кожи крысы.
Биопсийные образцы отбирали на 2 сутки после введения генотерапевтических ДНК-векторов. Взятие биопсии осуществляли из участков на коже животных в зоне введения смеси четырех генотерапевтических ДНК-векторов, несущих гены KRT5, KRT14, LAMB3, COL7A1 (зона I), генотерапевтического ДНК-вектора VTvaf17 (плацебо) (зона II), а также из аналогичного участка кожи, не подвергавшегося никаким манипуляциям (зона III), используя устройство для взятия биопсии кожи Epitheasy 3.5 (Medax SRL). Зону отбора биоптата предварительно промывали стерильным физиологическим раствором и анестезировали раствором лидокаина. Размер каждого биопсийного образца составлял около 10 куб. мм, масса - около 11 мг. Каждый образец помещали в буферный раствор, содержащий 50 мМ Трис-HCl рН 7.6, 100 мМ NaCl, 1 мМ ЭДТА и 1 мМ фенилметилсульфонилфторид, и гомогенизировали до получения однородной суспензии. Полученную суспензию центрифугировали в течение 10 мин при 14000g. Отбирали супернатант и использовали его для количественного определения целевых белков как это описано в примере 9 (количественное определение белка KRT5), примере 10 (количественное определение белка KRT14), примере 11 (количественное определение белка LAMB3), примере 12 (количественное определение белка COL7A1). Графики, полученные в результате анализа, представлены на фиг.14.
Из фигуры 14 следует, что в зоне кожи крыс (зона I), в которую вводилась смесь генотерапевтических векторов: генотерапевтического ДНК-вектора VTvaf17-KRT5, несущего целевой ген KRT5, генотерапевтического ДНК-вектора VTvaf17-KRT14, несущего целевой ген KRT14, генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего целевой ген LAMB3, генотерапевтического ДНК-вектора VTvaf17-COL7A1, несущего целевой ген COL7A1, произошло увеличение количества белков KRT5, KRT14, LAMB3 и COL7A1 по сравнению с зоной II (зона плацебо) и зоной III (интактная зона). Полученные результаты свидетельствуют об эффективности сочетанного применения генотерапевтических ДНК-векторов и подтверждает реализуемость способа применения для повышения уровня экспрессии целевых белков в тканях млекопитающих.
Пример 18.
Подтверждение эффективности генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего ген LAMB3 и реализуемости способа его применения для повышения уровня экспрессии белка LAMB3 в клетках млекопитающих.
Для подтверждения эффективности генотерапевтического ДНК-вектора VTvaf17-LAMB3, несущего ген LAMB3 оценивали изменение накопления мРНК целевого гена LAMB3 в клетках эпителия почки коровы MDBK (NBL-1) (ATCC® CCL-22™) через 48 часов после их трансфекции генотерапевтическим ДНК-вектором VTvaf17-LAMB3, несущим ген LAMB3 человека.
Клетки эпителия почки коровы MDBK (NBL-1) выращивали в среде Eagle's Minimum Essential Medium (EMEM) (ATCC® 30-2003™) с добавлением 10% сыворотки Horse Serum (ATCC® 30-2040™). Трансфекцию генотерапевтическим ДНК-вектором VTvaf17-LAMB3, несущим ген LAMB3 человека и ДНК-вектором VTvaf17, не несущим ген LAMB3 человека (контроль), выделение РНК, реакцию обратной транскрипции, ПЦР амплификации и анализ данных проводили как описано в примере 7. В качестве референтного гена использовали ген актина быка/коровы (АСТ), приведенного в базе данных GenBank под номером AH001130.2. В качестве положительного контроля использовали ампликоны, получаемых при ПЦР на матрицах, представляющих собой плазмиды в известных концентрациях, содержащие последовательности генов LAMB3 и ACT. В качестве отрицательного контроля использовали деионизированную воду. Количество ПЦР продуктов - кДНК генов LAMB3 и ACT, полученных в результате амплификации, оценивали в режиме реального времени с помощью программного обеспечения амплификатора Bio-RadCFXManager 2.1. (Bio-Rad, USA).
Графики, полученные в результате анализа представлены на фиг.15.
Из фигуры 15 следует, что в результате трансфекции клеток эпителия почки коровы MDBK генотерапевтическим ДНК-вектором VTvaf17-LAMB3, уровень специфической мРНК гена LAMB3 человека вырос многократно, что подтверждает способность вектора проникать в эукариотические клетки и экспрессировать ген LAMB3 на уровне мРНК. Представленные результаты подтверждают реализуемость способа применения генотерапевтическим ДНК-вектором VTvaf17-LAMB3 для повышения уровня экспрессии гена LAMB3 в клетках млекопитающих.
Пример 19.
Штамм Escherichia coli SCS110-AF/VTvaf17-KRT5 или штамм Escherichia coli SCS110-AF/VTvaf17-KRT14 или штамм Escherichia coli SCS110-AF/VTvaf17-LAMB3 или штамм Escherichia coli SCS110-AF/VTvaf17-COL7A1, несущий генотерапевтический ДНК-вектор, и способ его получения.
Конструирование штамма для наработки в промышленных масштабах генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: KRT5, KRT14, LAMB3, COL7A1, а именно штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1, несущего генотерапевтический ДНК-вектор VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 соответственно для его наработки с возможностью селекции без использования антибиотиков заключается в получении электрокомпетентных клеток штамма Escherichia coli SCS110-AF с проведением электропорации этих клеток генотерапевтическим ДНК-вектором VTvaf17-KRT5, или ДНК-вектором VTvaf17-KRT14, или ДНК-вектором VTvaf17-LAMB3, или ДНК-вектором VTvaf17-COL7A1, после чего клетки высеваются на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола. При этом штамм Escherichia coli SCS110-AF для наработки генотерапевтического ДНК-вектора VTvaf17 или генотерапевтических ДНК-векторов на его основе с возможностью положительной селекции без использования антибиотиков получали путем конструирования линейного фрагмента ДНК, содержащего регуляторный элемент RNA-in транспозона Tn10 для селекции без применения антибиотиков размером 64 п.н., ген левансахаразы sacB, продукт которого обеспечивает селекцию на сахарозо-содержащей среде размером 1422 п.н., ген устойчивости к хлорамфениколу COL7A1R, необходимый для отбора клонов штамма, в которых прошла гомологичная рекомбинация размером 763 п.н. и две гомологичные последовательности, обеспечивающие процесс гомологичной рекомбинации в области гена recA с одновременной его инактивацией размером 329 п.н. и 233 п.н., после чего проводили трансформацию клеток Escherichia coli путем электропорации и отбирали клоны, выжившие на среде, содержащей 10 мкг/мл хлорамфеникола.
Полученные штаммы для наработки были внесены в коллекции Национального биоресурсного центра - Всероссийская коллекция промышленных микроорганизмов (НБЦ ВКПМ), РФ и NCIMB Patent Deposit Service, UK с присвоением регистрационных номеров:
штамм Escherichia coli SCS110-AF/VTvaf17-KRT5 - регистрационный №ВКПМ B-13386, дата депонирования: 14.12.2018; accession № NCIMB: 43310, дата депонирования: 13.12.2018;
штамм Escherichia coli SCS110-AF/VTvaf17-KRT14 - регистрационный № ВКПМ B-13345, дата депонирования: 22.11.2018; accession №NCIMB: 43282, дата депонирования: 22.11.2018.
Пример 20.
Способ масштабирования получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: KRT5, KRT14, LAMB3, COL7A1 до промышленного масштаба.
Для подтверждения технологичности получения и возможности производства в промышленных масштабах генотерапевтического ДНК-вектора VTvaf17-KRT5 (SEQ ID №1), или VTvaf17-KRT14 (SEQ ID №2), или VTvaf17-LAMB3 (SEQ ID №3), или VTvaf17-COL7A1 (SEQ ID №4) проводили масштабную ферментацию штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1, каждый из которых содержит генотерапевтический ДНК-вектор VTvaf17, несущий целевой ген, а именно KRT5, или KRT14, или LAMB3, или COL7A1. Каждый штамм Escherichia coli SCS110-AF/VTvaf17-KRT5, или Escherichia coli SCS110-AF/VTvaf17-KRT14, или Escherichia coli SCS110-AF/VTvaf17-LAMB3, или Escherichia coli SCS110-AF/VTvaf17-COL7A1 получали на базе штамма Escherichia coli SCS110-AF (Cell and Gene Therapy LLC, Великобритания) по примеру 19 путем электропорации компетентных клеток этого штамма генотерапевтическим ДНК-вектором VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1, несущим целевой ген, а именно, KRT5, или KRT14, или LAMB3, или COL7A1 с последующим высевом трансформированных клеток на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы и отбором отдельных клонов.
Ферментацию полученного штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, несущего генотерапевтический ДНК-вектор VTvaf17-KRT5 проводили в ферментере объемом 10 л с последующим выделением генотерапевтического ДНК-вектора VTvaf17-KRT5.
Для ферментации штамма Escherichia coli SCS110-AF/VTvaf17-KRT5 готовили среду, содержащую на 10 л: 100 г триптон, 50 г дрожжевой экстракт (Becton Dickinson, США), доводили водой до 8800 мл и автоклавировали при 121°С 20 мин, затем добавляли 1200 мл 50% (вес/объем) сахарозы. Далее засевали в колбу затравочную культуру штамма Escherichia coli SCS110-AF/VTvaf17-KRT5 в объеме 100 мл. Инкубировали в шейкере-инкубаторе 16 ч при 30°С. Переносили затравочную культуру в ферментер Techfors S (Infors HT, Швейцария), растили до достижения стационарной фазы. Контроль осуществляли измерением оптической плотности культуры при длине волны 600 нм. Клетки осаждали центрифугированием 30 мин при 5000-10000 g. Супернатант удаляли, клеточную массу ресуспендировали в 10% по объему фосфатно-солевого буфера. Повторно центрифугировали 30 мин при 5000-10000g. Супернатант удаляли, к клеточной массе добавляли раствор 20 мМ TrisCl, 1 мМ ЭДТА, 200 г/л сахароза, рН 8,0 в объеме 1000 мл, тщательно перемешивали до образования гомогенной суспензии. Добавляли раствор яичного лизоцима до конечной концентрации 100 мкг/мл. Инкубировали 20 мин на льду при бережном перемешивании. Далее, добавляли 2500 мл раствора 0,2 М NaOH, 10 г/л додецилсульфат натрия, инкубировали 10 мин на льду при бережном перемешивании, затем добавляли 3500 мл раствора 3M ацетат натрия, 2М уксусная кислота, рН 5-5,5, инкубировали 10 мин на льду при бережном перемешивании. Полученный образец центрифугировали 20-30 мин при 15000 g или более. Раствор аккуратно декантировали, от остатков осадка избавлялись фильтрацией через грубый фильтр (фильтровальную бумагу). Добавляли РНКазу А (Sigma, США) до конечной концентрации 20 нг/мл, инкубировали ночь 16 ч при комнатной температуре. Раствор центрифугировали 20-30 мин при 15000g, затем фильтровали через мембранный фильтр с порами 0,45 мкм (Millipore, США). Далее проводили ультрафильтрацию через мембрану размером отсечения 100кДа (Millipore, США) и разбавляли до начального объема буфером 25 мМ TrisCl, pH 7.0. Операцию повторяли три - четыре раза. Наносили раствор, на колонку с 250 мл сорбента DEAE sepharose HP (GE, США), уравновешенную раствором 25 мМ TrisCl, pH 7.0. После нанесения образца колонку промывали тремя объемами этого же раствора, а затем проводили элюцию генотерапевтического ДНК-вектора VTvaf17-KRT5 линейным градиентом от раствора 25 мМ TrisCl, pH 7.0 до раствора 25 мМ TrisCl, pH 7.0, 1М NaCl в объеме пяти объемов колонки. Контроль элюции осуществляли по оптической плотности сходящего раствора при 260 нм. Хроматографические фракции, содержащие генотерапевтический ДНК-вектор VTvaf17-KRT5, объединяли и проводили гель-фильтрацию на сорбенте Superdex 200 (GE, США). Колонку уравновешивали фосфатно-солевым буфером. Контроль элюции осуществляли по оптической плотности сходящего раствора при 260 нм, фракции анализировали электрофорезом в агарозном геле. Фракции, содержащие генотерапевтический ДНК-вектор VTvaf17-KRT5 объединяли и хранили при -20°С. Для оценки воспроизводимости техпроцесса обозначенные технологические операции повторяли пятикратно. Все технологические операции для штаммов Escherichia coli SCS110-AF/VTvaf17-KRT14, или Escherichia coli SCS110-AF/VTvaf17-LAMB3, или Escherichia coli SCS110-AF/VTvaf17-COL7A1 проводили аналогичным образом.
Воспроизводимость техпроцесса и количественные характеристики выхода конечного продукта подтверждают технологичность получения и возможность производства в промышленных масштабах генотерапевтического ДНК-вектора VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1.
Таким образом, созданный генотерапевтический ДНК-вектор с целевым геном может быть использован для введения в клетки организма животных и человека, характеризующихся сниженной или недостаточной экспрессией белка, кодируемого данным геном, обеспечивая таким образом достижение терапевтического эффекта.
Задача, поставленная в данном изобретении, а именно: конструирование генотерапевтических ДНК-векторов для повышения уровня экспрессии генов KRT5, KRT14, LAMB3, COL7A1, сочетающих в себе следующие свойства:
I) Эффективность повышения экспрессии целевых генов в эукариотических клетках за счет полученных генотерапевтических векторов с размером векторной части не превышающей 3200 п.н.;
II) Возможность безопасного применения для генетической терапии человека и животных за счет отсутствия в составе генотерапевтического ДНК-вектора регуляторных элементов, представляющих собой нуклеотидные последовательности вирусных геномов и генов антибиотикорезистентности;
III) Технологичность получения и возможность наработки в штаммах в промышленных масштабах;
IV) также задача по конструированию штаммов, несущих эти генотерапевтические ДНК-вектора для производства этих генотерапевтических ДНК-векторов решена, что подтверждается примерами:
для п. I - пример 1, 2, 3, 4, 5; 6; 7; 8; 9; 10; 11; 12; 13; 14; 15; 16; 17; 18;
для п. II - пример 1, 2, 3, 4;
для п. III и п. IV - пример 19, 20.
Промышленная применимость:
Все представленные выше примеры подтверждают промышленную применимость предлагаемого генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген, выбранный из группы генов: ген KRT5, ген KRT14, ген LAMB3, ген COL7A1 для повышения уровня экспрессии этих целевых генов, штамма Escherichia coli SCS110-AF/VTvaf17-KRT5 или Escherichia coli SCS110-AF/VTvaf17-KRT14 или Escherichia coli SCS110-AF/VTvaf17-LAMB3 или Escherichia coli SCS110-AF/VTvaf17-COL7A1, несущего генотерапевтический ДНК-вектор, способа получения генотерапевтического ДНК-вектора, способа производства в промышленных масштабах генотерапевтического ДНК-вектора.
Перечень сокращений
VTvaf17 - вектор генотерапевтический, не содержащий последовательностей вирусных геномов и маркеров антибиотико-резистентности (vector therapeutic virus-antibiotic-free)
ДНК - дезоксирибонуклеиновая кислота
кДНК - комплементарная дезоксирибонуклеиновая кислота
РНК - рибонуклеиновая кислота
мРНК - матричная рибонуклеиновая кислота
п.н. - пар нуклеотидов
ПЦР - полимеразная цепная реакция
мл - миллилитр, мкл - микролитр
куб. мм - кубический миллиметр
л - литр
мкг - микрограмм
мг - миллиграмм
г - грамм
мкМ - микромоль
мМ - миллимоль
мин - минута
сек - секунда
об/мин - обороты в минуту
нм - нанометр
см - сантиметр
мВт - милливатт
о.е. ф-относительная единица флуоресценции
РВС - фосфатно-солевой буфер.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110>Селл энд Джин Терапи Лтд (CELL and GENE THERAPY Ltd), Общество с ограниченной ответственностью «Прорывные Инновационные Технологии»,
<120>Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1 для повышения уровня экспрессии этих целевых генов, способ его получения и применения, штамм Escherichia coli SCS110-AF/VTvaf17-KRT5 или Escherichia coli SCS110-AF/VTvaf17-KRT14 или Escherichia coli SCS110-AF/VTvaf17-LAMB3 или Escherichia coli SCS110-AF/VTvaf17-COL7A1, несущий генотерапевтический ДНК-вектор, способ его получения, способ производства в промышленных масштабах генотерапевтического ДНК-вектора.
<160>4
<170>BiSSAP 1.3.6
<210>1
<211>4929
<212>DNA
<213>Homo Sapiens
<400>1
cgtgaggctc cggtgcccgt cagtgggcag agcgcacatc gcccacagtc cccgagaagt 60
tggggggagg ggtcggcaat tgaaccggtg cctagagaaa gtggcgcggg gtaaactggg 120
aaagtgatgt cgtgtactgg ctccgccttt ttcccgaggg tgggggagaa ccgtatataa 180
gtgcagtagt cgccgtgaac gttctttttc gcaacgggtt tgccgccaga acacaggtaa 240
gtgccgtgtg tggttcccgc gggcctggcc tctttacggg ttatggccct tgcgtgcctt 300
gaattacttc cacgcccctg gctgcagtac gtgattcttg atcccgagct tcgggttgga 360
agtgggtggg agagttcgag gccttgcgct taaggagccc cttcgcctcg tgcttgagtt 420
gaggcctggc ctgggcgctg gggccgccgc gtgcgaatct ggtggcacct tcgcgcctgt 480
ctcgctgctt tcgataagtc tctagccatt taaaattttt gatgacctgc tgcgacgctt 540
tttttctggc aagatagtct tgtaaatgcg ggccaagatc tgcacactgg tatttcggtt 600
tttggggccg cgggcggcga cggggcccgt gcgtcccagc gcacatgttc ggcgaggcgg 660
ggcctgcgag cgcggccacc gagaatcgga cgggggtagt ctcaagctgg ccggcctgct 720
ctggtgcctg gcctcgcgcc gccgtgtatc gccccgccct gggcggcaag gctggcccgg 780
tcggcaccag ttgcgtgagc ggaaagatgg ccgcttcccg gccctgctgc agggagctca 840
aaatggagga cgcggcgctc gggagagcgg gcgggtgagt cacccgcaca aaggaaaagg 900
gcctttccgt cctcagccgt cgcttcatgt gactccacgg agtaccgggc gccgtccagg 960
cacctcgatt agttctcgag cttttggagt acgtcgtctt taggttgggg ggaggggttt 1020
tatgcgatgg agtttcccca cactgagtgg gtggagactg aagttaggcc agcttggcac 1080
ttgatgtaat tctccttgga atttgccctt tttgagtttg gatcttggtt cattctcaag 1140
cctcagacag tggttcaaag tttttttctt ccatttcagg tgtcgtgaaa actaccccta 1200
aaagccagga tccaccatgt ctcgccagtc aagtgtgtcc ttccggagcg ggggcagtcg 1260
tagcttcagc accgcctctg ccatcacccc gtctgtctcc cgcaccagct tcacctccgt 1320
gtcccggtcc gggggtggcg gtggtggtgg cttcggcagg gtcagccttg cgggtgcttg 1380
tggagtgggt ggctatggca gccggagcct ctacaacctg gggggctcca agaggatatc 1440
catcagcacc agtggtggca gcttcaggaa ccggtttggt gctggtgctg gaggcggcta 1500
tggctttgga ggtggtgccg gtagtggatt tggtttcggc ggtggagctg gtggtggctt 1560
tgggcttggt ggcggagctg gctttggagg tggcttcggt ggccctggct ttcctgtctg 1620
ccctcctgga ggtatccaag aggtcactgt caaccagagt ctcctgactc ccctcaacct 1680
gcaaatcgac cccagcatcc agagggtgag gaccgaggag cgcgagcaga tcaagaccct 1740
caacaataag tttgcctcct tcatcgacaa ggtgcggttc ctggagcagc agaacaaggt 1800
tctggacacc aagtggaccc tgctgcagga gcagggcacc aagaccgtga ggcagaacct 1860
ggagccgttg ttcgagcagt acatcaacaa cctcaggagg cagctggaca gcatcgtggg 1920
ggaacggggc cgcctggact cagagctaag aaacatgcag gacctggtgg aagacttcaa 1980
gaacaagtat gaggatgaaa tcaacaagcg taccactgct gagaatgagt ttgtgatgct 2040
gaagaaggat gtagatgctg cctacatgaa caaggtggag ctggaggcca aggttgatgc 2100
actgatggat gagattaact tcatgaagat gttctttgat gcggagctgt cccagatgca 2160
gacgcatgtc tctgacacct cagtggtcct ctccatggac aacaaccgca acctggacct 2220
ggatagcatc atcgctgagg tcaaggccca gtatgaggag attgccaacc gcagccggac 2280
cgaagccgag tcctggtatc agaccaagta tgaggagctg cagcagacag ctggccggca 2340
tggcgatgac ctccgcaaca ccaagcatga gatctctgag atgaaccgga tgatccagag 2400
gctgagagcc gagattgaca atgtcaagaa acagtgcgcc aatctgcaga acgccattgc 2460
ggatgccgag cagcgtgggg agctggccct caaggatgcc aggaacaagc tggccgagct 2520
ggaggaggcc ctgcagaagg ccaagcagga catggcccgg ctgctgcgtg agtaccagga 2580
gctcatgaac accaagctgg ccctggacgt ggagatcgcc acttaccgca agctgctgga 2640
gggcgaggaa tgcagactca gtggagaagg agttggacca gtcaacatct ctgttgtcac 2700
aagcagtgtt tcctctggat atggcagtgg cagtggctat ggcggtggcc tcggtggagg 2760
tcttggcggc ggcctcggtg gaggtcttgc cggaggtggc agtggaagct actactccag 2820
cagcagtggg ggtgtcggcc taagtggtgg gctcagtgtg gggggctctg gcttcagtgc 2880
aagcagtggc cgagggctgg gggtgggctt tggcagtggc gggggtagca gctccagcgt 2940
caaatttgtc tccaccacct cctcctcccg gaagagcttc aagagctaga agcttggtac 3000
cgaattccct gtgacccctc cccagtgcct ctcctggccc tggaagttgc cactccagtg 3060
cccaccagcc ttgtcctaat aaaattaagt tgcatcattt tgtctgacta ggtgtccttc 3120
tataatatta tggggtggag gggggtggta tggagcaagg ggcaagttgg gaagacaacc 3180
tgtagggcct gcggggtcta ttgggaacca agctggagtg cagtggcaca atcttggctc 3240
actgcaatct ccgcctcctg ggttcaagcg attctcctgc ctcagcctcc cgagttgttg 3300
ggattccagg catgcatgac caggctcagc taatttttgt ttttttggta gagacggggt 3360
ttcaccatat tggccaggct ggtctccaac tcctaatctc aggtgatcta cccaccttgg 3420
cctcccaaat tgctgggatt acaggcgtga accactgctc ccttccctgt ccttacgcgt 3480
agaattggta aagagagtcg tgtaaaatat cgagttcgca catcttgttg tctgattatt 3540
gatttttggc gaaaccattt gatcatatga caagatgtgt atctacctta acttaatgat 3600
tttgataaaa atcattaact agtccatggc tgcctcgcgc gtttcggtga tgacggtgaa 3660
aacctctgac acatgcagct cccggagacg gtcacagctt gtctgtaagc ggatgccggg 3720
agcagacaag cccgtcaggg cgcgtcagcg ggtgttggcg ggtgtcgggg cgcagccatg 3780
acccagtcac gtagcgatag cggagtgtat actggcttaa ctatgcggca tcagagcaga 3840
ttgtactgag agtgcaccat atgcggtgtg aaataccgca cagatgcgta aggagaaaat 3900
accgcatcag gcgctcttcc gcttcctcgc tcactgactc gctgcgctcg gtcgttcggc 3960
tgcggcgagc ggtatcagct cactcaaagg cggtaatacg gttatccaca gaatcagggg 4020
ataacgcagg aaagaacatg tgagcaaaag gccagcaaaa ggccaggaac cgtaaaaagg 4080
ccgcgttgct ggcgtttttc cataggctcc gcccccctga cgagcatcac aaaaatcgac 4140
gctcaagtca gaggtggcga aacccgacag gactataaag ataccaggcg tttccccctg 4200
gaagctccct cgtgcgctct cctgttccga ccctgccgct taccggatac ctgtccgcct 4260
ttctcccttc gggaagcgtg gcgctttctc atagctcacg ctgtaggtat ctcagttcgg 4320
tgtaggtcgt tcgctccaag ctgggctgtg tgcacgaacc ccccgttcag cccgaccgct 4380
gcgccttatc cggtaactat cgtcttgagt ccaacccggt aagacacgac ttatcgccac 4440
tggcagcagc cactggtaac aggattagca gagcgaggta tgtaggcggt gctacagagt 4500
tcttgaagtg gtggcctaac tacggctaca ctagaagaac agtatttggt atctgcgctc 4560
tgctgaagcc agttaccttc ggaaaaagag ttggtagctc ttgatccggc aaacaaacca 4620
ccgctggtag cggtggtttt tttgtttgca agcagcagat tacgcgcaga aaaaaaggat 4680
ctcaagaaga tcctttgatc ttttctacgg ggtctgacgc tcagtggaac gaaaactcac 4740
gttaagggat tttggtcatg agattatcaa aaaggatctt cacctagatc cttttaaatt 4800
aaaaatgaag ttttaaatca atctaaagta tatatgagta aacttggtct gacagttacc 4860
aatgcttaat cagtgaggca cctatctcag cgatctgtct atttcgttca tccatagttg 4920
cctgactcc 4929
<210>2
<211>4575
<212>DNA
<213>Homo Sapiens
<400>2
cgtgaggctc cggtgcccgt cagtgggcag agcgcacatc gcccacagtc cccgagaagt 60
tggggggagg ggtcggcaat tgaaccggtg cctagagaaa gtggcgcggg gtaaactggg 120
aaagtgatgt cgtgtactgg ctccgccttt ttcccgaggg tgggggagaa ccgtatataa 180
gtgcagtagt cgccgtgaac gttctttttc gcaacgggtt tgccgccaga acacaggtaa 240
gtgccgtgtg tggttcccgc gggcctggcc tctttacggg ttatggccct tgcgtgcctt 300
gaattacttc cacgcccctg gctgcagtac gtgattcttg atcccgagct tcgggttgga 360
agtgggtggg agagttcgag gccttgcgct taaggagccc cttcgcctcg tgcttgagtt 420
gaggcctggc ttgggcgctg gggccgccgc gtgcgaatct ggtggcacct tcgcgcctgt 480
ctcgctgctt tcgataagtc tctagccatt taaaattttt gatgacctgc tgcgacgctt 540
tttttctggc aagatagtct tgtaaatgcg ggccaagatc tgcacactgg tatttcggtt 600
tttggggccg cgggcggcga cggggcccgt gcgtcccagc gcacatgttc ggcgaggcgg 660
ggcctgcgag cgcggccacc gagaatcgga cgggggtagt ctcaagctgg ccggcctgct 720
ctggtgcctg gcctcgcgcc gccgtgtatc gccccgccct gggcggcaag gctggcccgg 780
tcggcaccag ttgcgtgagc ggaaagatgg ccgcttcccg gccctgctgc agggagctca 840
aaatggagga cgcggcgctc gggagagcgg gcgggtgagt cacccacaca aaggaaaagg 900
gcctttccgt cctcagccgt cgcttcatgt gactccacgg agtaccgggc gccgtccagg 960
cacctcgatt agttctcgag cttttggagt acgtcgtctt taggttgggg ggaggggttt 1020
tatgcgatgg agtttcccca cactgagtgg gtggagactg aagttaggcc agcttggcac 1080
ttgatgtaat tctccttgga atttgccctt tttgagtttg gatcttggtt cattctcaag 1140
cctcagacag tggttcaaag tttttttctt ccatttcagg tgtcgtgaaa actaccccta 1200
aaagccagga tccaccatga ccacctgcag ccgccagttc acctcctcca gctccatgaa 1260
gggctcctgc ggcatcgggg gcggcatcgg gggcggctcc agccgcatct cctccgtcct 1320
ggccggaggg tcctgccgcg cccccagcac ctacgggggc ggcctgtctg tctcatcctc 1380
ccgcttctcc tctgggggag cctatgggtt ggggggcggc tatggcggtg gcttcagcag 1440
cagcagcagc agctttggta gtggctttgg gggaggatat ggtggtggcc ttggtgctgg 1500
cttgggtggt ggctttggtg gtggctttgc tggtggtgat gggcttctgg tgggcagtga 1560
gaaggtgacc atgcagaacc tcaacgaccg cctggcctcc tacctggaca aggtgcgtgc 1620
tctggaggag gccaacgccg acctggaagt gaagatccgt gactggtacc agaggcagcg 1680
gcctgctgag atcaaagact acagtcccta cttcaagacc attgaggacc tgaggaacaa 1740
gattctcaca gccacagtgg acaatgccaa tgtccttctg cagattgaca atgcccgtct 1800
ggccgcggat gacttccgca ccaagtatga gacagagttg aacctgcgca tgagtgtgga 1860
agccgacatc aatggcctgc gcagggtgct ggacgaactg accctggcca gagctgacct 1920
ggagatgcag attgagagcc tgaaggagga gctggcctac ctgaagaaga accacgagga 1980
ggagatgaat gccctgagag gccaggtggg tggagatgtc aatgtggaga tggacgctgc 2040
acctggcgtg gacctgagcc gcattctgaa cgagatgcgt gaccagtatg agaagatggc 2100
agagaagaac cgcaaggatg ccgaggaatg gttcttcacc aagacagagg agctgaaccg 2160
cgaggtggcc accaacagcg agctggtgca gagcggcaag agcgagatct cggagctccg 2220
gcgcaccatg cagaacctgg agattgagct gcagtcccag ctcagcatga aagcatccct 2280
ggagaacagc ctggaggaga ccaaaggtcg ctactgcatg cagctggccc agatccagga 2340
gatgattggc agcgtggagg agcagctggc ccagctccgc tgcgagatgg agcagcagaa 2400
ccaggagtac aagatcctgc tggacgtgaa gacgcggctg gagcaggaga tcgccaccta 2460
ccgccgcctg ctggagggcg aggacgccca cctctcctcc tcccagttct cctctggatc 2520
gcagtcatcc agagatgtga cctcctccag ccgccaaatc cgcaccaagg tcatggatgt 2580
gcacgatggc aaggtggtgt ccacccacga gcaggtcctt cgcaccaaga actgaaagct 2640
tggtaccgaa ttccctgtga cccctcccca gtgcctctcc tggccctgga agttgccact 2700
ccagtgccca ccagccttgt cctaataaaa ttaagttgca tcattttgtc tgactaggtg 2760
tccttctata atattatggg gtggaggggg gtggtatgga gcaaggggca agttgggaag 2820
acaacctgta gggcctgcgg ggtctattgg gaaccaagct ggagtgcagt ggcacaatct 2880
tggctcactg caatctccgc ctcctgggtt caagcgattc tcctgcctca gcctcccgag 2940
ttgttgggat tccaggcatg catgaccagg ctcagctaat ttttgttttt ttggtagaga 3000
cggggtttca ccatattggc caggctggtc tccaactcct aatctcaggt gatctaccca 3060
ccttggcctc ccaaattgct gggattacag gcgtgaacca ctgctccctt ccctgtcctt 3120
acgcgtagaa ttggtaaaga gagtcgtgta aaatatcgag ttcgcacatc ttgttgtctg 3180
attattgatt tttggcgaaa ccatttgatc atatgacaag atgtgtatct accttaactt 3240
aatgattttg ataaaaatca ttaactagtc catggctgcc tcgcgcgttt cggtgatgac 3300
ggtgaaaacc tctgacacat gcagctcccg gagacggtca cagcttgtct gtaagcggat 3360
gccgggagca gacaagcccg tcagggcgcg tcagcgggtg ttggcgggtg tcggggcgca 3420
gccatgaccc agtcacgtag cgatagcgga gtgtatactg gcttaactat gcggcatcag 3480
agcagattgt actgagagtg caccatatgc ggtgtgaaat accgcacaga tgcgtaagga 3540
gaaaataccg catcaggcgc tcttccgctt cctcgctcac tgactcgctg cgctcggtcg 3600
ttcggctgcg gcgagcggta tcagctcact caaaggcggt aatacggtta tccacagaat 3660
caggggataa cgcaggaaag aacatgtgag caaaaggcca gcaaaaggcc aggaaccgta 3720
aaaaggccgc gttgctggcg tttttccata ggctccgccc ccctgacgag catcacaaaa 3780
atcgacgctc aagtcagagg tggcgaaacc cgacaggact ataaagatac caggcgtttc 3840
cccctggaag ctccctcgtg cgctctcctg ttccgaccct gccgcttacc ggatacctgt 3900
ccgcctttct cccttcggga agcgtggcgc tttctcatag ctcacgctgt aggtatctca 3960
gttcggtgta ggtcgttcgc tccaagctgg gctgtgtgca cgaacccccc gttcagcccg 4020
accgctgcgc cttatccggt aactatcgtc ttgagtccaa cccggtaaga cacgacttat 4080
cgccactggc agcagccact ggtaacagga ttagcagagc gaggtatgta ggcggtgcta 4140
cagagttctt gaagtggtgg cctaactacg gctacactag aagaacagta tttggtatct 4200
gcgctctgct gaagccagtt accttcggaa aaagagttgg tagctcttga tccggcaaac 4260
aaaccaccgc tggtagcggt ggtttttttg tttgcaagca gcagattacg cgcagaaaaa 4320
aaggatctca agaagatcct ttgatctttt ctacggggtc tgacgctcag tggaacgaaa 4380
actcacgtta agggattttg gtcatgagat tatcaaaaag gatcttcacc tagatccttt 4440
taaattaaaa atgaagtttt aaatcaatct aaagtatata tgagtaaact tggtctgaca 4500
gttaccaatg cttaatcagt gaggcaccta tctcagcgat ctgtctattt cgttcatcca 4560
tagttgcctg actcc 4575
<210>3
<211>6674
<212>DNA
<213>Homo Sapiens
<400>3
cgtgaggctc cggtgcccgt cagtgggcag agcgcacatc gcccacagtc cccgagaagt 60
tggggggagg ggtcggcaat tgaaccggtg cctagagaaa gtggcgcggg gtaaactggg 120
aaagtgatgt cgtgtactgg ctccgccttt ttcccgaggg tgggggagaa ccgtatataa 180
gtgcagtagt cgccgtgaac gttctttttc gcaacgggtt tgccgccaga acacaggtaa 240
gtgccgtgtg tggttcccgc gggcctggcc tctttacggg ttatggccct tgcgtgcctt 300
gaattacttc cacgcccctg gctgcagtac gtgattcttg atcccgagct tcgggttgga 360
agtgggtggg agagttcgag gccttgcgct taaggagccc cttcgcctcg tgcttgagtt 420
gaggcctggc ctgggcgctg gggccgccgc gtgcgaatct ggtggcacct tcgcgcctgt 480
ctcgctgctt tcgataagtc tctagccatt taaaattttt gatgacctgc tgcgacgctt 540
tttttctggc aagatagtct tgtaaatgcg ggccaagatc tgcacactgg tatttcggtt 600
tttggggccg cgggcggcga cggggcccgt gcgtcccagc gcacatgttc ggcgaggcgg 660
ggcctgcgag cgcggccacc gagaatcgga cgggggtagt ctcaagctgg ccggcctgct 720
ctggtgcctg gcctcgcgcc gccgtgtatc gccccgccct gggcggcaag gctggcccgg 780
tcggcaccag ttgcgtgagc ggaaagatgg ccgcttcccg gccctgctgc agggagctca 840
aaatggagga cgcggcgctc gggagagcgg gcgggtgagt cacccgcaca aaggaaaagg 900
gcctttccgt cctcagccgt cgcttcatgt gactccacgg agtaccgggc gccgtccagg 960
cacctcgatt agttctcgag cttttggagt acgtcgtctt taggttgggg ggaggggttt 1020
tatgcgatgg agtttcccca cactgagtgg gtggagactg aagttaggcc agcttggcac 1080
ttgatgtaat tctccttgga atttgccctt tttgagtttg gatcttggtt cattctcaag 1140
cctcagacag tggttcaaag tttttttctt ccatttcagg tgtcgtgaaa actaccccta 1200
aaagccagga tccgatatcg tcgaccacca tgagaccatt cttcctcttg tgttttgccc 1260
tgcctggcct cctgcatgcc caacaagcct gctcccgtgg ggcctgctat ccacctgttg 1320
gggacctgct tgttgggagg acccggtttc tccgagcttc atctacctgt ggactgacca 1380
agcctgagac ctactgcacc cagtatggcg agtggcagat gaaatgctgc aagtgtgact 1440
ccaggcagcc tcacaactac tacagtcacc gagtagagaa tgtggcttca tcctccggcc 1500
ccatgcgctg gtggcagtca cagaatgatg tgaaccctgt ctctctgcag ctggacctgg 1560
acaggagatt ccagcttcaa gaagtcatga tggagttcca ggggcccatg cccgccggca 1620
tgctgattga gcgctcctca gacttcggta agacctggcg agtgtaccag tacctggctg 1680
ccgactgcac ctccaccttc cctcgggtcc gccagggtcg gcctcagagc tggcaggatg 1740
ttcggtgcca gtccctgcct cagaggccta atgcacgcct aaatgggggg aaggtccaac 1800
ttaaccttat ggatttagtg tctgggattc cagcaactca aagtcaaaaa attcaagagg 1860
tgggggagat cacaaacttg agagtcaatt tcaccaggct ggcccctgtg ccccaaaggg 1920
gctaccaccc tcccagcgcc tactatgctg tgtcccagct ccgtctgcag gggagctgct 1980
tctgtcacgg ccatgctgat cgctgcgcac ccaagcctgg ggcctctgca ggcccctcca 2040
ccgctgtgca ggtccacgat gtctgtgtct gccagcacaa cactgccggc ccaaattgtg 2100
agcgctgtgc acccttctac aacaaccggc cctggagacc ggcggagggc caggacgccc 2160
atgaatgcca aaggtgcgac tgcaatgggc actcagagac atgtcacttt gaccccgctg 2220
tgtttgccgc cagccagggg gcatatggag gtgtgtgtga caattgccgg gaccacaccg 2280
aaggcaagaa ctgtgagcgg tgtcagctgc actatttccg gaaccggcgc ccgggagctt 2340
ccattcagga gacctgcatc tcctgcgagt gtgatccgga tggggcagtg ccaggggctc 2400
cctgtgaccc agtgaccggg cagtgtgtgt gcaaggagca tgtgcaggga gagcgctgtg 2460
acctatgcaa gccgggcttc actggactca cctacgccaa cccgcagggc tgccaccgct 2520
gtgactgcaa catcctgggg tcccggaggg acatgccgtg tgacgaggag agtgggcgct 2580
gcctttgtct gcccaacgtg gtgggtccca aatgtgacca gtgtgctccc taccactgga 2640
agctggccag tggccagggc tgtgaaccgt gtgcctgcga cccgcacaac tccctcagcc 2700
cacagtgcaa ccagttcaca gggcagtgcc cctgtcggga aggctttggt ggcctgatgt 2760
gcagcgctgc agccatccgc cagtgtccag accggaccta tggagacgtg gccacaggat 2820
gccgagcctg tgactgtgat ttccggggaa cagagggccc gggctgcgac aaggcatcag 2880
gccgctgcct ctgccgccct ggcttgaccg ggccccgctg tgaccagtgc cagcgaggct 2940
actgtaatcg ctacccggtg tgcgtggcct gccacccttg cttccagacc tatgatgcgg 3000
acctccggga gcaggccctg cgctttggta gactccgcaa tgccaccgcc agcctgtggt 3060
cagggcctgg gctggaggac cgtggcctgg cctcccggat cctagatgca aagagtaaga 3120
ttgagcagat ccgagcagtt ctcagcagcc ccgcagtcac agagcaggag gtggctcagg 3180
tggccagtgc catcctctcc ctcaggcgaa ctctccaggg cctgcagctg gatctgcccc 3240
tggaggagga gacgttgtcc cttccgagag acctggagag tcttgacaga agcttcaatg 3300
gtctccttac tatgtatcag aggaagaggg agcagtttga aaaaataagc agtgctgatc 3360
cttcaggagc cttccggatg ctgagcacag cctacgagca gtcagcccag gctgctcagc 3420
aggtctccga cagctcgcgc cttttggacc agctcaggga cagccggaga gaggcagaga 3480
ggctggtgcg gcaggcggga ggaggaggag gcaccggcag ccccaagctt gtggccctga 3540
ggctggagat gtcttcgttg cctgacctga cacccacctt caacaagctc tgtggcaact 3600
ccaggcagat ggcttgcacc ccaatatcat gccctggtga gctatgtccc caagacaatg 3660
gcacagcctg tggctcccgc tgcaggggtg tccttcccag ggccggtggg gccttcttga 3720
tggcggggca ggtggctgag cagctgcggg gcttcaatgc ccagctccag cggaccaggc 3780
agatgattag ggcagccgag gaatctgcct cacagattca atccagtgcc cagcgcttgg 3840
agacccaggt gagcgccagc cgctcccaga tggaggaaga tgtcagacgc acacggctcc 3900
taatccagca ggtccgggac ttcctaacag accccgacac tgatgcagcc actatccagg 3960
aggtcagcga ggccgtgctg gccctgtggc tgcccacaga ctcagctact gttctgcaga 4020
agatgaatga gatccaggcc attgcagcca ggctccccaa cgtggacttg gtgctgtccc 4080
agaccaagca ggacattgcg cgtgcccgcc ggttgcaggc tgaggctgag gaagccagga 4140
gccgagccca tgcagtggag ggccaggtgg aagatgtggt tgggaacctg cggcagggga 4200
cagtggcact gcaggaagct caggacacca tgcaaggcac cagccgctcc cttcggctta 4260
tccaggacag ggttgctgag gttcagcagg tactgcggcc agcagaaaag ctggtgacaa 4320
gcatgaccaa gcagctgggt gacttctgga cacggatgga ggagctccgc caccaagccc 4380
ggcagcaggg ggcagaggca gtccaggccc agcagcttgc ggaaggtgcc agcgagcagg 4440
cattgagtgc ccaagaggga tttgagagaa taaaacaaaa gtatgctgag ttgaaggacc 4500
ggttgggtca gagttccatg ctgggtgagc agggtgcccg gatccagagt gtgaagacag 4560
aggcagagga gctgtttggg gagaccatgg agatgatgga caggatgaaa gacatggagt 4620
tggagctgct gcggggcagc caggccatca tgctgcgctc agcggacctg acaggactgg 4680
agaagcgtgt ggagcagatc cgtgaccaca tcaatgggcg cgtgctctac tatgccacct 4740
gcaagtgaat tccctgtgac ccctccccag tgcctctcct ggccctggaa gttgccactc 4800
cagtgcccac cagccttgtc ctaataaaat taagttgcat cattttgtct gactaggtgt 4860
ccttctataa tattatgggg tggagggggg tggtatggag caaggggcaa gttgggaaga 4920
caacctgtag ggcctgcggg gtctattggg aaccaagctg gagtgcagtg gcacaatctt 4980
ggctcactgc aatctccgcc tcctgggttc aagcgattct cctgcctcag cctcccgagt 5040
tgttgggatt ccaggcatgc atgaccaggc tcagctaatt tttgtttttt tggtagagac 5100
ggggtttcac catattggcc aggctggtct ccaactccta atctcaggtg atctacccac 5160
cttggcctcc caaattgctg ggattacagg cgtgaaccac tgctcccttc cctgtcctta 5220
cgcgtagaat tggtaaagag agtcgtgtaa aatatcgagt tcgcacatct tgttgtctga 5280
ttattgattt ttggcgaaac catttgatca tatgacaaga tgtgtatcta ccttaactta 5340
atgattttga taaaaatcat taactagtcc atggctgcct cgcgcgtttc ggtgatgacg 5400
gtgaaaacct ctgacacatg cagctcccgg agacggtcac agcttgtctg taagcggatg 5460
ccgggagcag acaagcccgt cagggcgcgt cagcgggtgt tggcgggtgt cggggcgcag 5520
ccatgaccca gtcacgtagc gatagcggag tgtatactgg cttaactatg cggcatcaga 5580
gcagattgta ctgagagtgc accatatgcg gtgtgaaata ccgcacagat gcgtaaggag 5640
aaaataccgc atcaggcgct cttccgcttc ctcgctcact gactcgctgc gctcggtcgt 5700
tcggctgcgg cgagcggtat cagctcactc aaaggcggta atacggttat ccacagaatc 5760
aggggataac gcaggaaaga acatgtgagc aaaaggccag caaaaggcca ggaaccgtaa 5820
aaaggccgcg ttgctggcgt ttttccatag gctccgcccc cctgacgagc atcacaaaaa 5880
tcgacgctca agtcagaggt ggcgaaaccc gacaggacta taaagatacc aggcgtttcc 5940
ccctggaagc tccctcgtgc gctctcctgt tccgaccctg ccgcttaccg gatacctgtc 6000
cgcctttctc ccttcgggaa gcgtggcgct ttctcatagc tcacgctgta ggtatctcag 6060
ttcggtgtag gtcgttcgct ccaagctggg ctgtgtgcac gaaccccccg ttcagcccga 6120
ccgctgcgcc ttatccggta actatcgtct tgagtccaac ccggtaagac acgacttatc 6180
gccactggca gcagccactg gtaacaggat tagcagagcg aggtatgtag gcggtgctac 6240
agagttcttg aagtggtggc ctaactacgg ctacactaga agaacagtat ttggtatctg 6300
cgctctgctg aagccagtta ccttcggaaa aagagttggt agctcttgat ccggcaaaca 6360
aaccaccgct ggtagcggtg gtttttttgt ttgcaagcag cagattacgc gcagaaaaaa 6420
aggatctcaa gaagatcctt tgatcttttc tacggggtct gacgctcagt ggaacgaaaa 6480
ctcacgttaa gggattttgg tcatgagatt atcaaaaagg atcttcacct agatcctttt 6540
aaattaaaaa tgaagtttta aatcaatcta aagtatatat gagtaaactt ggtctgacag 6600
ttaccaatgc ttaatcagtg aggcacctat ctcagcgatc tgtctatttc gttcatccat 6660
agttgcctga ctcc 6674
<210>4
<211>11990
<212>DNA
<213>Homo Sapiens
<400>4
cgtgaggctc cggtgcccgt cagtgggcag agcgcacatc gcccacagtc cccgagaagt 60
tggggggagg ggtcggcaat tgaaccggtg cctagagaaa gtggcgcggg gtaaactggg 120
aaagtgatgt cgtgtactgg ctccgccttt ttcccgaggg tgggggagaa ccgtatataa 180
gtgcagtagt cgccgtgaac gttctttttc gcaacgggtt tgccgccaga acacaggtaa 240
gtgccgtgtg tggttcccgc gggcctggcc tctttacggg ttatggccct tgcgtgcctt 300
gaattacttc cacgcccctg gctgcagtac gtgattcttg atcccgagct tcgggttgga 360
agtgggtggg agagttcgag gccttgcgct taaggagccc cttcgcctcg tgcttgagtt 420
gaggcctggc ttgggcgctg gggccgccgc gtgcgaatct ggtggcacct tcgcgcctgt 480
ctcgctgctt tcgataagtc tctagccatt taaaattttt gatgacctgc tgcgacgctt 540
tttttctggc aagatagtct tgtaaatgcg ggccaagatc tgcacactgg tatttcggtt 600
tttggggccg cgggcggcga cggggcccgt gcgtcccagc gcacatgttc ggcgaggcgg 660
ggcctgcgag cgcggccacc gagaatcgga cgggggtagt ctcaagctgg ccggcctgct 720
ctggtgcctg gcctcgcgcc gccgtgtatc gccccgccct gggcggcaag gctggcccgg 780
tcggcaccag ttgcgtgagc ggaaagatgg ccgcttcccg gccctgctgc agggagctca 840
aaatggagga cgcggcgctc gggagagcgg gcgggtgagt cacccacaca aaggaaaagg 900
gcctttccgt cctcagccgt cgcttcatgt gactccacgg agtaccgggc gccgtccagg 960
cacctcgatt agttctcgag cttttggagt acgtcgtctt taggttgggg ggaggggttt 1020
tatgcgatgg agtttcccca cactgagtgg gtggagactg aagttaggcc agcttggcac 1080
ttgatgtaat tctccttgga atttgccctt tttgagtttg gatcttggtt cattctcaag 1140
cctcagacag tggttcaaag tttttttctt ccatttcagg tgtcgtgaaa actaccccta 1200
aaagccagga tccgatatcg tcgaccacca tgacgctgcg gcttctggtg gccgcgctct 1260
gcgccgggat cctggcagag gcgccccgag tgcgagccca gcacagggag agagtgacct 1320
gcacgcgcct ttacgccgct gacattgtgt tcttactgga tggctcctca tccattggcc 1380
gcagcaattt ccgcgaggtc cgcagctttc tcgaagggct ggtgctgcct ttctctggag 1440
cagccagtgc acagggtgtg cgctttgcca cagtgcagta cagcgatgac ccacggacag 1500
agttcggcct ggatgcactt ggctctgggg gtgatgtgat ccgcgccatc cgtgagctta 1560
gctacaaggg gggcaacact cgcacagggg ctgcaattct ccatgtggct gaccatgtct 1620
tcctgcccca gctggcccga cctggtgtcc ccaaggtctg catcctgatc acagacggga 1680
agtcccagga cctggtggac acagctgccc aaaggctgaa ggggcagggg gtcaagctat 1740
ttgctgtggg gatcaagaat gctgaccctg aggagctgaa gcgagttgcc tcacagccaa 1800
cctccgactt cttcttcttc gtcaatgact tcagcatctt gaggacacta ctgcccctcg 1860
tttcccggag agtgtgcacg actgctggtg gcgtgcctgt gacccgacct ccggatgact 1920
cgacctctgc tccacgagac ctggtgctgt ctgagccaag cagccaatcc ttgagagtac 1980
agtggacagc ggccagtggc cctgtgactg gctacaaggt ccagtacact cctctgacgg 2040
ggctgggaca gccactgccg agtgagcggc aggaggtgaa cgtcccagct ggtgagacca 2100
gtgtgcggct gcggggtctc cggccactga ccgagtacca agtgactgtg attgccctct 2160
acgccaacag catcggggag gctgtgagcg ggacagctcg gaccactgcc ctagaagggc 2220
cggaactgac catccagaat accacagccc acagcctcct ggtggcctgg cggagtgtgc 2280
caggtgccac tggctaccgt gtgacatggc gggtcctcag tggtgggccc acacagcagc 2340
aggagctggg ccctgggcag ggttcagtgt tgctgcgtga cttggagcct ggcacggact 2400
atgaggtgac cgtgagcacc ctatttggcc gcagtgtggg gcccgccact tccctgatgg 2460
ctcgcactga cgcttctgtt gagcagaccc tgcgcccggt catcctgggc cccacatcca 2520
tcctcctttc ctggaacttg gtgcctgagg cccgtggcta ccggttggaa tggcggcgtg 2580
agactggctt ggagccaccg cagaaggtgg tactgccctc tgatgtgacc cgctaccagt 2640
tggatgggct gcagccgggc actgagtacc gcctcacact ctacactctg ctggagggcc 2700
acgaggtggc cacccctgca accgtggttc ccactggacc agagctgcct gtgagccctg 2760
taacagacct gcaagccacc gagctgcccg ggcagcgggt gcgagtgtcc tggagcccag 2820
tccctggtgc cacccagtac cgcatcattg tgcgcagcac ccagggggtt gagcggaccc 2880
tggtgcttcc tgggagtcag acagcattcg acttggatga cgttcaggct gggcttagct 2940
acactgtgcg ggtgtctgct cgagtgggtc cccgtgaggg cagtgccagt gtcctcactg 3000
tccgccggga gccggaaact ccacttgctg ttccagggct gcgggttgtg gtgtcagatg 3060
caacgcgagt gagggtggcc tggggacccg tccctggagc cagtggattt cggattagct 3120
ggagcacagg cagtggtccg gagtccagcc agacactgcc cccagactct actgccacag 3180
acatcacagg gctgcagcct ggaaccacct accaggtggc tgtgtcggta ctgcgaggca 3240
gagaggaggg ccctgctgca gtcatcgtgg ctcgaacgga cccactgggc ccagtgagga 3300
cggtccatgt gactcaggcc agcagctcat ctgtcaccat tacctggacc agggttcctg 3360
gcgccacagg atacagggtt tcctggcact cagcccacgg cccagagaaa tcccagttgg 3420
tttctgggga ggccacggtg gctgagctgg atggactgga gccagatact gagtatacgg 3480
tgcatgtgag ggcccatgtg gctggcgtgg atgggccccc tgcctctgtg gttgtgagga 3540
ctgcccctga gcctgtgggt cgtgtgtcga ggctgcagat cctcaatgct tccagcgacg 3600
ttctacggat cacctgggta ggggtcactg gagccacagc ttacagactg gcctggggcc 3660
ggagtgaagg cggccccatg aggcaccaga tactcccagg aaacacagac tctgcagaga 3720
tccggggtct cgaaggtgga gtcagctact cagtgcgagt gactgcactt gtcggggacc 3780
gcgagggcac acctgtctcc attgttgtca ctacgccgcc tgaggctccg ccagccctgg 3840
ggacgcttca cgtggtgcag cgcggggagc actcgctgag gctgcgctgg gagccggtgc 3900
ccagagcgca gggcttcctt ctgcactggc aacctgaggg tggccaggaa cagtcccggg 3960
tcctggggcc cgagctcagc agctatcacc tggacgggct ggagccagcg acacagtacc 4020
gcgtgaggct gagtgtccta gggccggctg gagaagggcc ctctgcagag gtgactgcgc 4080
gcactgagtc acctcgtgtt ccaagcattg aactacgtgt ggtggacacc tcgatcgact 4140
cggtgacttt ggcctggact ccagtgtcca gggcatccag ctacatccta tcctggcggc 4200
cactcagagg ccctggccag gaagtgcctg ggtccccgca gacacttcca gggatctcaa 4260
gctcccagcg ggtgacaggg ctagagcctg gcgtctctta catcttctcc ctgacgcctg 4320
tcctggatgg tgtgcggggt cctgaggcat ctgtcacaca gacgccagtg tgcccccgtg 4380
gcctggcgga tgtggtgttc ctaccacatg ccactcaaga caatgctcac cgtgcggagg 4440
ctacgaggag ggtcctggag cgtctggtgt tggcacttgg gcctcttggg ccacaggcag 4500
ttcaggttgg cctgctgtct tacagtcatc ggccctcccc actgttccca ctgaatggct 4560
cccatgacct tggcattatc ttgcaaagga tccgtgacat gccctacatg gacccaagtg 4620
ggaacaacct gggcacagcc gtggtcacag ctcacagata catgttggca ccagatgctc 4680
ctgggcgccg ccagcacgta ccaggggtga tggttctgct agtggatgaa cccttgagag 4740
gtgacatatt cagccccatc cgtgaggccc aggcttctgg gcttaatgtg gtgatgttgg 4800
gaatggctgg agcggaccca gagcagctgc gtcgcttggc gccgggtatg gactctgtcc 4860
agaccttctt cgccgtggat gatgggccaa gcctggacca ggcagtcagt ggtctggcca 4920
cagccctgtg tcaggcatcc ttcactactc agccccggcc agagccctgc ccagtgtatt 4980
gtccaaaggg ccagaagggg gaacctggag agatgggcct gagaggacaa gttgggcctc 5040
ctggcgaccc tggcctcccg ggcaggaccg gtgctcccgg cccccagggg ccccctggaa 5100
gtgccactgc caagggcgag aggggcttcc ctggagcaga tgggcgtcca ggcagccctg 5160
gccgcgccgg gaatcctggg acccctggag cccctggcct aaagggctct ccagggttgc 5220
ctggccctcg tggggacccg ggagagcgag gacctcgagg cccaaagggg gagccggggg 5280
ctcccggaca agtcatcgga ggtgaaggac ctgggcttcc tgggcggaaa ggggaccctg 5340
gaccatcggg cccccctgga cctcgtggac cactggggga cccaggaccc cgtggccccc 5400
cagggcttcc tggaacagcc atgaagggtg acaaaggcga tcgtggggag cggggtcccc 5460
ctggaccagg tgaaggtggc attgctcctg gggagcctgg gctgccgggt cttcccggaa 5520
gccctggacc ccaaggcccc gttggccccc ctggaaagaa aggagaaaaa ggtgactctg 5580
aggatggagc tccaggcctc ccaggacaac ctgggtctcc gggtgagcag ggcccacggg 5640
gacctcctgg agctattggc cccaaaggtg accggggctt tccagggccc ctgggtgagg 5700
ctggagagaa gggcgaacgt ggacccccag gcccagcggg atcccggggg ctgccagggg 5760
ttgctggacg tcctggagcc aagggtcctg aagggccacc aggacccact ggccgccaag 5820
gagagaaggg ggagcctggt cgccctgggg accctgcagt ggtgggacct gctgttgctg 5880
gacccaaagg agaaaaggga gatgtggggc ccgctgggcc cagaggagct accggagtcc 5940
aaggggaacg gggcccaccc ggcttggttc ttcctggaga ccctggcccc aagggagacc 6000
ctggagaccg gggtcccatt ggccttactg gcagagcagg acccccaggt gactcagggc 6060
ctcctggaga gaagggagac cctgggcggc ctggcccccc aggacctgtt ggcccccgag 6120
gacgagatgg tgaagttgga gagaaaggtg acgagggtcc tccgggtgac ccgggtttgc 6180
ctggaaaagc aggcgagcgt ggccttcggg gggcacctgg agttcggggg cctgtgggtg 6240
aaaagggaga ccagggagat cctggagagg atggacgaaa tggcagccct ggatcatctg 6300
gacccaaggg tgaccgtggg gagccgggtc ccccaggacc cccgggacgg ctggtagaca 6360
caggacctgg agccagagag aagggagagc ctggggaccg cggacaagag ggtcctcgag 6420
ggcccaaggg tgatcctggc ctccctggag cccctgggga aaggggcatt gaagggtttc 6480
ggggaccccc aggcccacag ggggacccag gtgtccgagg cccagcagga gaaaagggtg 6540
accggggtcc ccctgggctg gatggccgga gcggactgga tgggaaacca ggagccgctg 6600
ggccctctgg gccgaatggt gctgcaggca aagctgggga cccagggaga gacgggcttc 6660
caggcctccg tggagaacaa ggcctccctg gcccctctgg tccccctgga ttaccgggaa 6720
agccaggcga ggatgggaaa cctggcctga atggaaaaaa cggagaacct ggggaccctg 6780
gagaagacgg gaggaaggga gagaaaggag attcaggcgc ctctgggaga gaaggtcgtg 6840
atggccccaa gggtgagcgt ggagctcctg gtatccttgg accccagggg cctccaggcc 6900
tcccagggcc agtgggccct cctggccagg gttttcctgg tgtcccagga ggcacgggcc 6960
ccaagggtga ccgtggggag actggatcca aaggggagca gggcctccct ggagagcgtg 7020
gcctgcgagg agagcctgga agtgtgccga atgtggatcg gttgctggaa actgctggca 7080
tcaaggcatc tgccctgcgg gagatcgtgg agacctggga tgagagctct ggtagcttcc 7140
tgcctgtgcc cgaacggcgt cgaggcccca agggggactc aggcgaacag ggccccccag 7200
gcaaggaggg ccccatcggc tttcctggag aacgcgggct gaagggcgac cgtggagacc 7260
ctggccctca ggggccacct ggtctggccc ttggggagag gggccccccc gggccttccg 7320
gccttgccgg ggagcctgga aagcctggta ttcccgggct cccaggcagg gctgggggtg 7380
tgggagaggc aggaaggcca ggagagaggg gagaacgggg agagaaagga gaacgtggag 7440
aacagggcag agatggccct cctggactcc ctggaacccc tgggcccccc ggaccccctg 7500
gccccaaggt gtctgtggat gagccaggtc ctggactctc tggagaacag ggaccccctg 7560
gactcaaggg tgctaagggg gagccgggca gcaatggtga ccaaggtccc aaaggagaca 7620
ggggtgtgcc aggcatcaaa ggagaccggg gagagcctgg accgaggggt caggacggca 7680
acccgggtct accaggagag cgtggtatgg ctgggcctga agggaagccg ggtctgcagg 7740
gtccaagagg cccccctggc ccagtgggtg gtcatggaga ccctggacca cctggtgccc 7800
cgggtcttgc tggccctgca ggaccccaag gaccttctgg cctgaagggg gagcctggag 7860
agacaggacc tccaggacgg ggcctgactg gacctactgg agctgtggga cttcctggac 7920
cccccggccc ttcaggcctt gtgggtccac aggggtctcc aggtttgcct ggacaagtgg 7980
gggagacagg gaagccggga gccccaggtc gagatggtgc cagtggaaaa gatggagaca 8040
gagggagccc tggtgtgcca gggtcaccag gtctgcctgg ccctgtcgga cctaaaggag 8100
aacctggccc cacgggggcc cctggacagg ctgtggtcgg gctccctgga gcaaagggag 8160
agaagggagc ccctggaggc cttgctggag acctggtggg tgagccggga gccaaaggtg 8220
accgaggact gccagggccg cgaggcgaga agggtgaagc tggccgtgca ggggagcccg 8280
gagaccctgg ggaagatggt cagaaagggg ctccaggacc caaaggtttc aagggtgacc 8340
caggagtcgg ggtcccgggc tcccctgggc ctcctggccc tccaggtgtg aagggagatc 8400
tgggcctccc tggcctgccc ggtgctcctg gtgttgttgg gttcccgggt cagacaggcc 8460
ctcgaggaga gatgggtcag ccaggcccta gtggagagcg gggtctggca ggccccccag 8520
ggagagaagg aatcccagga cccctggggc cacctggacc accggggtca gtgggaccac 8580
ctggggcctc tggactcaaa ggagacaagg gagaccctgg agtagggctg cctgggcccc 8640
gaggcgagcg tggggagcca ggcatccggg gtgaagatgg ccgccccggc caggagggac 8700
cccgaggact cacggggccc cctggcagca ggggagagcg tggggagaag ggtgatgttg 8760
ggagtgcagg actaaagggt gacaagggag actcagctgt gatcctgggg cctccaggcc 8820
cacggggtgc caagggggac atgggtgaac gagggcctcg gggcttggat ggtgacaaag 8880
gacctcgggg agacaatggg gaccctggtg acaagggcag caagggagag cctggtgaca 8940
agggctcagc cgggttgcca ggactgcgtg gactcctggg accccagggt caacctggtg 9000
cagcagggat ccctggtgac ccgggatccc caggaaagga tggagtgcct ggtatccgag 9060
gagaaaaagg agatgttggc ttcatgggtc cccggggcct caagggtgaa cggggagtga 9120
agggagcctg tggccttgat ggagagaagg gagacaaggg agaagctggt cccccaggcc 9180
gccccgggct ggcaggacac aaaggagaga tgggggagcc tggtgtgccg ggccagtcgg 9240
gggcccctgg caaggagggc ctgatcggtc ccaagggtga ccgaggcttt gacgggcagc 9300
caggccccaa gggtgaccag ggcgagaaag gggagcgggg aaccccagga attgggggct 9360
tcccaggccc cagtggaaat gatggctctg ctggtccccc agggccacct ggcagtgttg 9420
gtcccagagg ccccgaagga cttcagggcc agaagggtga gcgaggtccc cccggagaga 9480
gagtggtggg ggctcctggg gtccctggag ctcctggcga gagaggggag caggggcggc 9540
cagggcctgc cggtcctcga ggcgagaagg gagaagctgc actgacggag gatgacatcc 9600
ggggctttgt gcgccaagag atgagtcagc actgtgcctg ccagggccag ttcatcgcat 9660
ctggatcacg acccctccct agttatgctg cagacactgc cggctcccag ctccatgctg 9720
tgcctgtgct ccgcgtctct catgcagagg aggaagagcg ggtaccccct gaggatgatg 9780
agtactctga atactccgag tattctgtgg aggagtacca ggaccctgaa gctccttggg 9840
atagtgatga cccctgttcc ctgccactgg atgagggctc ctgcactgcc tacaccctgc 9900
gctggtacca tcgggctgtg acaggcagca cagaggcctg tcaccctttt gtctatggtg 9960
gctgtggagg gaatgccaac cgttttggga cccgtgaggc ctgcgagcgc cgctgcccac 10020
cccgggtggt ccagagccag gggacaggta ctgcccagga ctgaattccc tgtgacccct 10080
ccccagtgcc tctcctggcc ctggaagttg ccactccagt gcccaccagc cttgtcctaa 10140
taaaattaag ttgcatcatt ttgtctgact aggtgtcctt ctataatatt atggggtgga 10200
ggggggtggt atggagcaag gggcaagttg ggaagacaac ctgtagggcc tgcggggtct 10260
attgggaacc aagctggagt gcagtggcac aatcttggct cactgcaatc tccgcctcct 10320
gggttcaagc gattctcctg cctcagcctc ccgagttgtt gggattccag gcatgcatga 10380
ccaggctcag ctaatttttg tttttttggt agagacgggg tttcaccata ttggccaggc 10440
tggtctccaa ctcctaatct caggtgatct acccaccttg gcctcccaaa ttgctgggat 10500
tacaggcgtg aaccactgct cccttccctg tccttacgcg tagaattggt aaagagagtc 10560
gtgtaaaata tcgagttcgc acatcttgtt gtctgattat tgatttttgg cgaaaccatt 10620
tgatcatatg acaagatgtg tatctacctt aacttaatga ttttgataaa aatcattaac 10680
tagtccatgg ctgcctcgcg cgtttcggtg atgacggtga aaacctctga cacatgcagc 10740
tcccggagac ggtcacagct tgtctgtaag cggatgccgg gagcagacaa gcccgtcagg 10800
gcgcgtcagc gggtgttggc gggtgtcggg gcgcagccat gacccagtca cgtagcgata 10860
gcggagtgta tactggctta actatgcggc atcagagcag attgtactga gagtgcacca 10920
tatgcggtgt gaaataccgc acagatgcgt aaggagaaaa taccgcatca ggcgctcttc 10980
cgcttcctcg ctcactgact cgctgcgctc ggtcgttcgg ctgcggcgag cggtatcagc 11040
tcactcaaag gcggtaatac ggttatccac agaatcaggg gataacgcag gaaagaacat 11100
gtgagcaaaa ggccagcaaa aggccaggaa ccgtaaaaag gccgcgttgc tggcgttttt 11160
ccataggctc cgcccccctg acgagcatca caaaaatcga cgctcaagtc agaggtggcg 11220
aaacccgaca ggactataaa gataccaggc gtttccccct ggaagctccc tcgtgcgctc 11280
tcctgttccg accctgccgc ttaccggata cctgtccgcc tttctccctt cgggaagcgt 11340
ggcgctttct catagctcac gctgtaggta tctcagttcg gtgtaggtcg ttcgctccaa 11400
gctgggctgt gtgcacgaac cccccgttca gcccgaccgc tgcgccttat ccggtaacta 11460
tcgtcttgag tccaacccgg taagacacga cttatcgcca ctggcagcag ccactggtaa 11520
caggattagc agagcgaggt atgtaggcgg tgctacagag ttcttgaagt ggtggcctaa 11580
ctacggctac actagaagaa cagtatttgg tatctgcgct ctgctgaagc cagttacctt 11640
cggaaaaaga gttggtagct cttgatccgg caaacaaacc accgctggta gcggtggttt 11700
ttttgtttgc aagcagcaga ttacgcgcag aaaaaaagga tctcaagaag atcctttgat 11760
cttttctacg gggtctgacg ctcagtggaa cgaaaactca cgttaaggga ttttggtcat 11820
gagattatca aaaaggatct tcacctagat ccttttaaat taaaaatgaa gttttaaatc 11880
aatctaaagt atatatgagt aaacttggtc tgacagttac caatgcttaa tcagtgaggc 11940
acctatctca gcgatctgtc tatttcgttc atccatagtt gcctgactcc 11990
<---
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ ОЛИГОНУКЛЕОТИДОВ
(1) KRT5_F TTTGGATCCACCATGTCTCGCCAGTCAAGTGTGTCCTTC
(2) KRT5_R AATAAGCTTCTAGCTCTTGAAGCTCTTCCGGGAGG
(3) KRT5_SF CGAAGCCGAGTCCTGGTATC
(4) KRT5_SR TTGGCGCACTGTTTCTTGAC
(5) KRT14_F TTTGGATCCACCATGACCACCTGCAGCCGCCAG
(6) KRT14_R AATAAGCTTTCAGTTCTTGGTGCGAAGGACCTGC
(7) KRT14_SF TCCAGGAGATGATTGGCAGC
(8) KRT14_SR GGATGACTGCGATCCAGAGG
(9) LAMB3_F TTAGTCGACCACCATGAGACCATTCTTCCTCTTG
(10) LAMB3_R ATAGAATTCACTTGCAGGTGGCATAGTAGAG
(11) LAMB3_SF CAGAGGAGCTGTTTGGGGAG
(12) LAMB3_SR CCCATTGATGTGGTCACGGA
(13) COL7A1_F ATCGTCGACCACCATGACGCTGCGGCTTCTGGT
(14) COL7A1_R ATAGAATTCAGTCCTGGGCAGTACCTGTC
(15) COL7A1_SF CAAAGGAGAGATGGGGGAGC
(16) COL7A1_SR ATCATTTCCACTGGGGCCTG

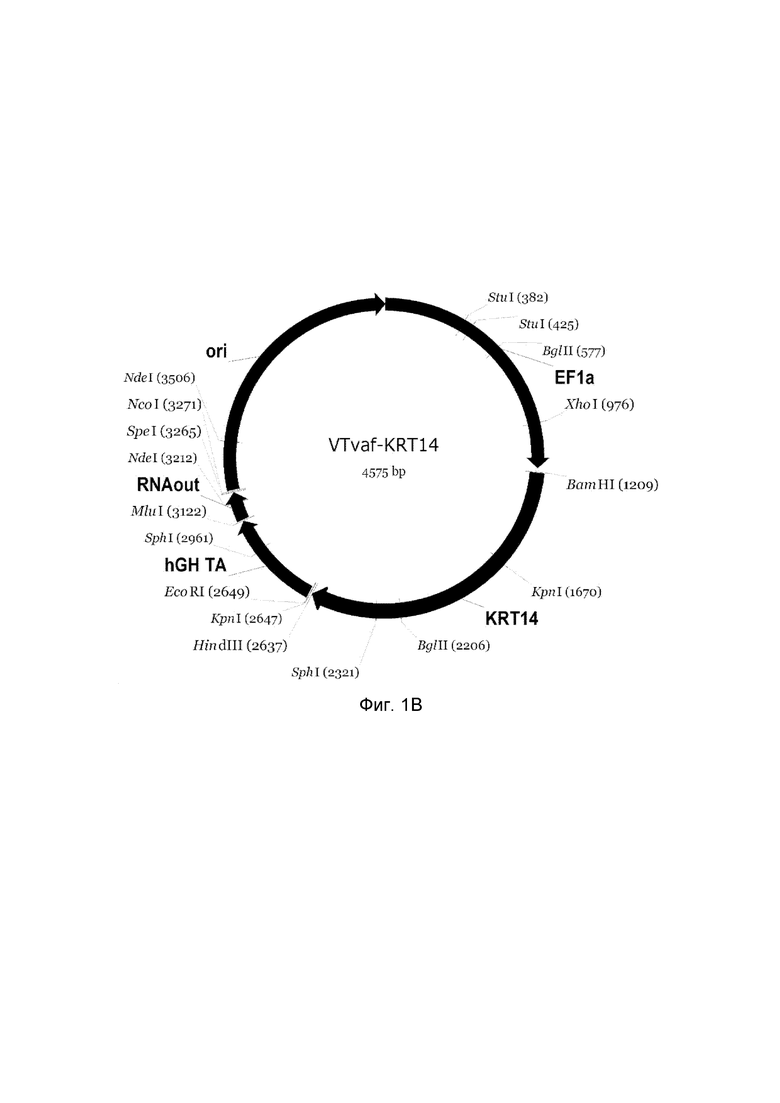
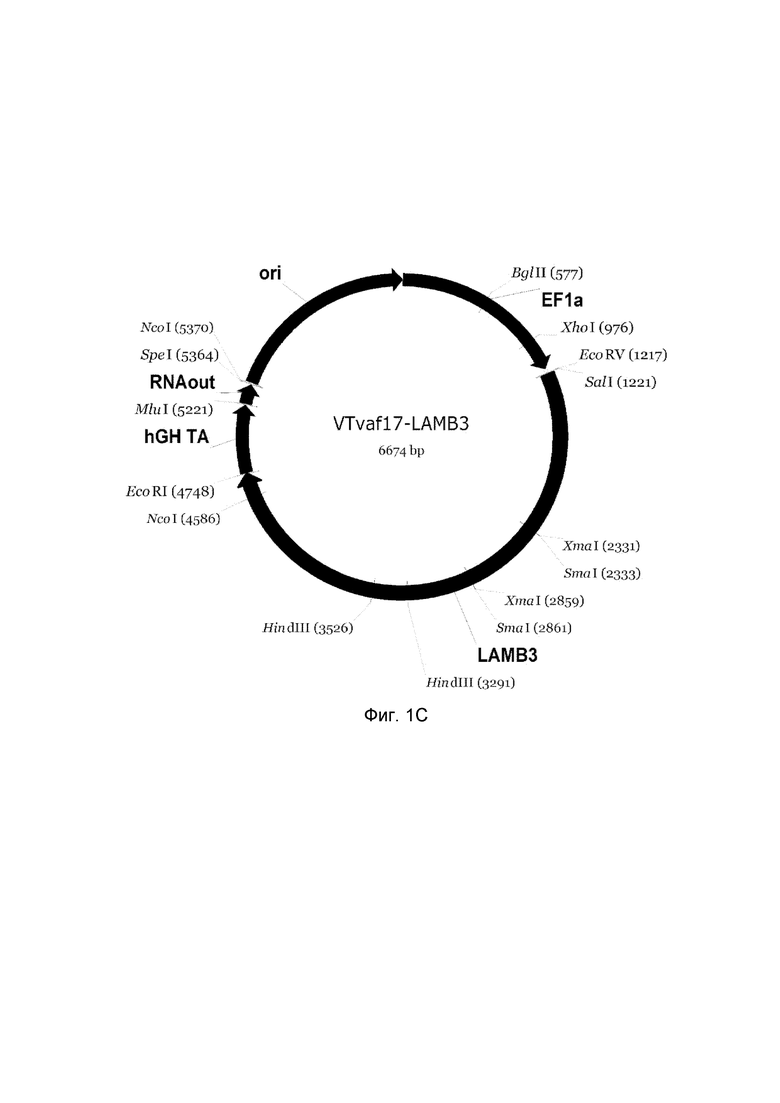
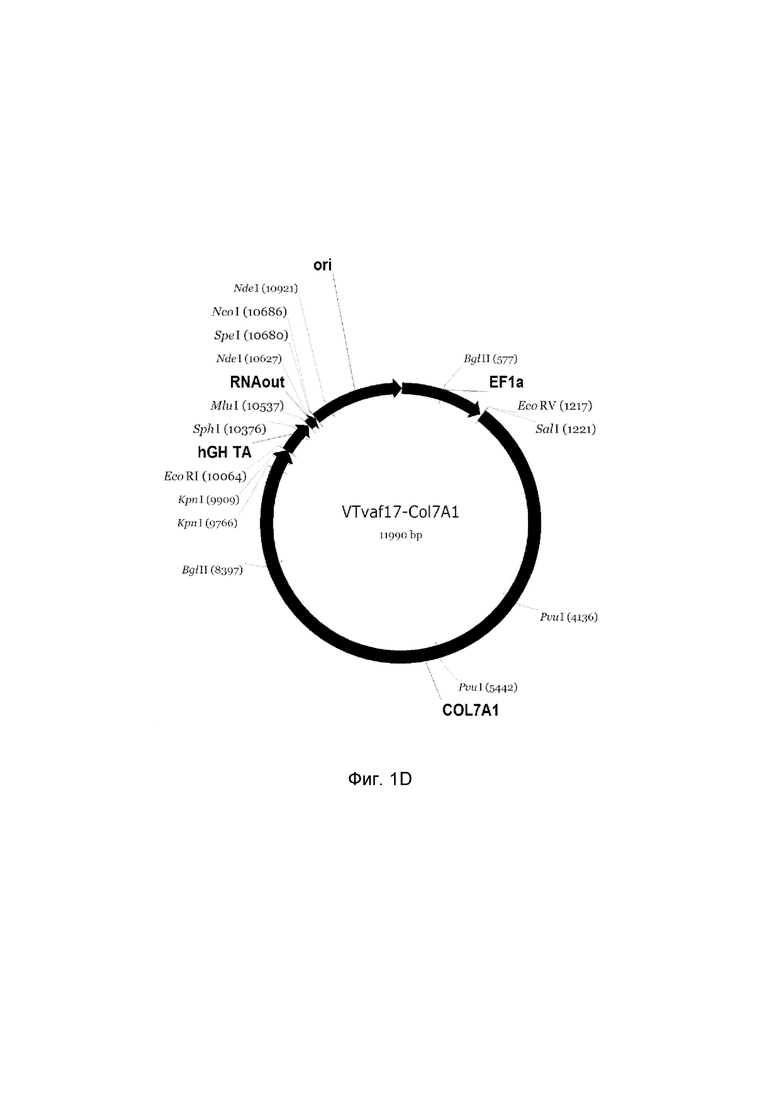
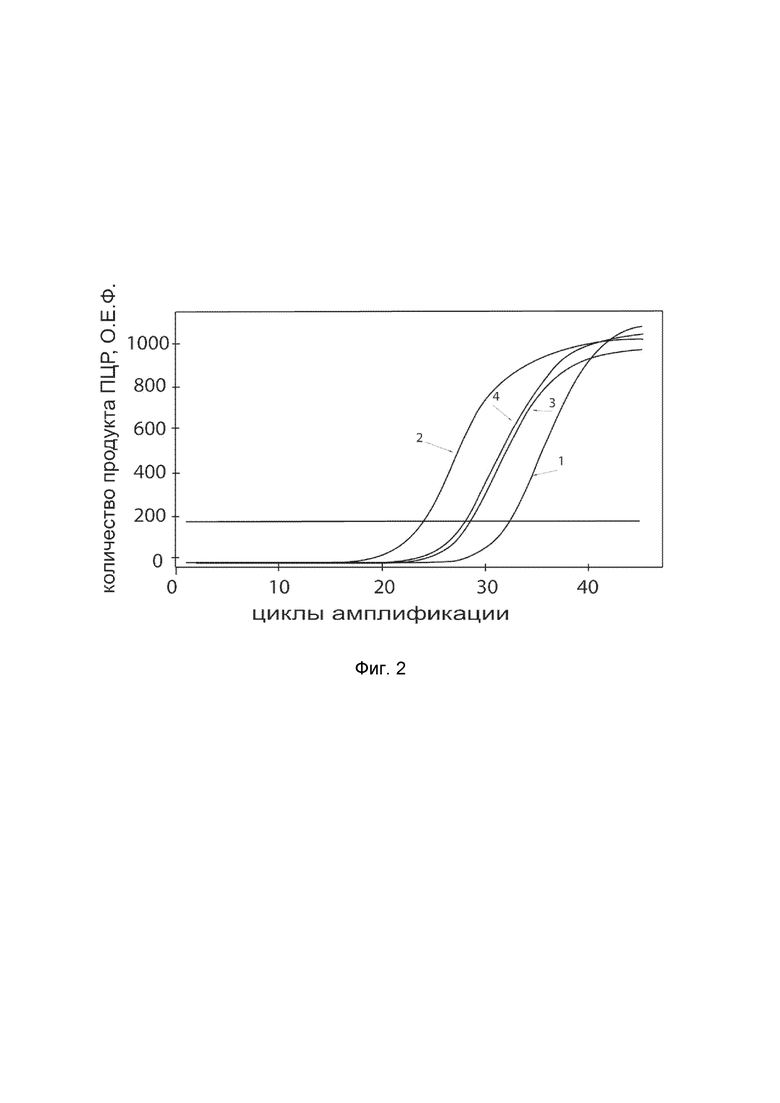
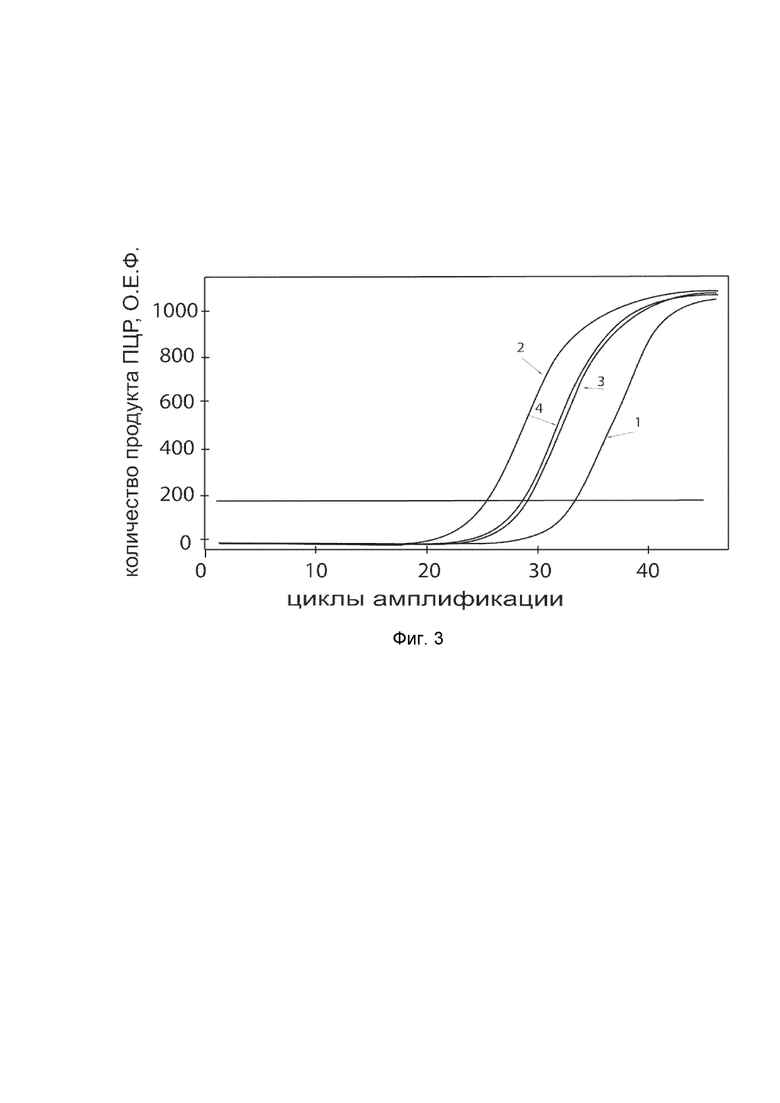
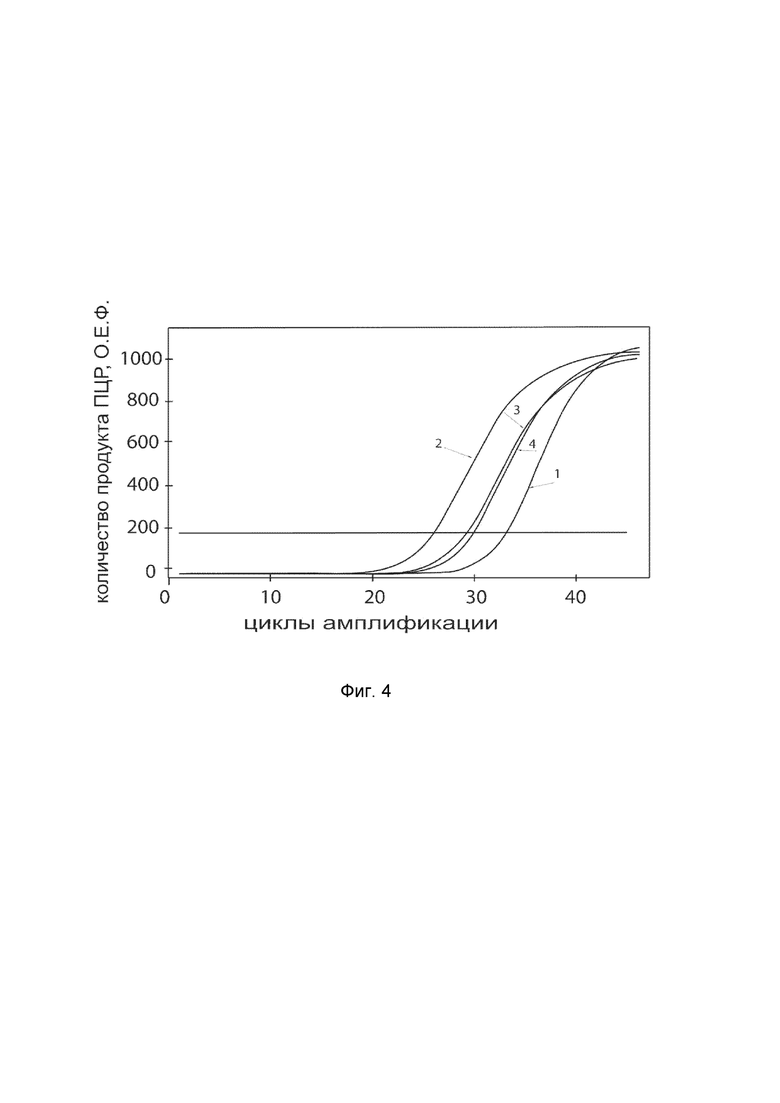
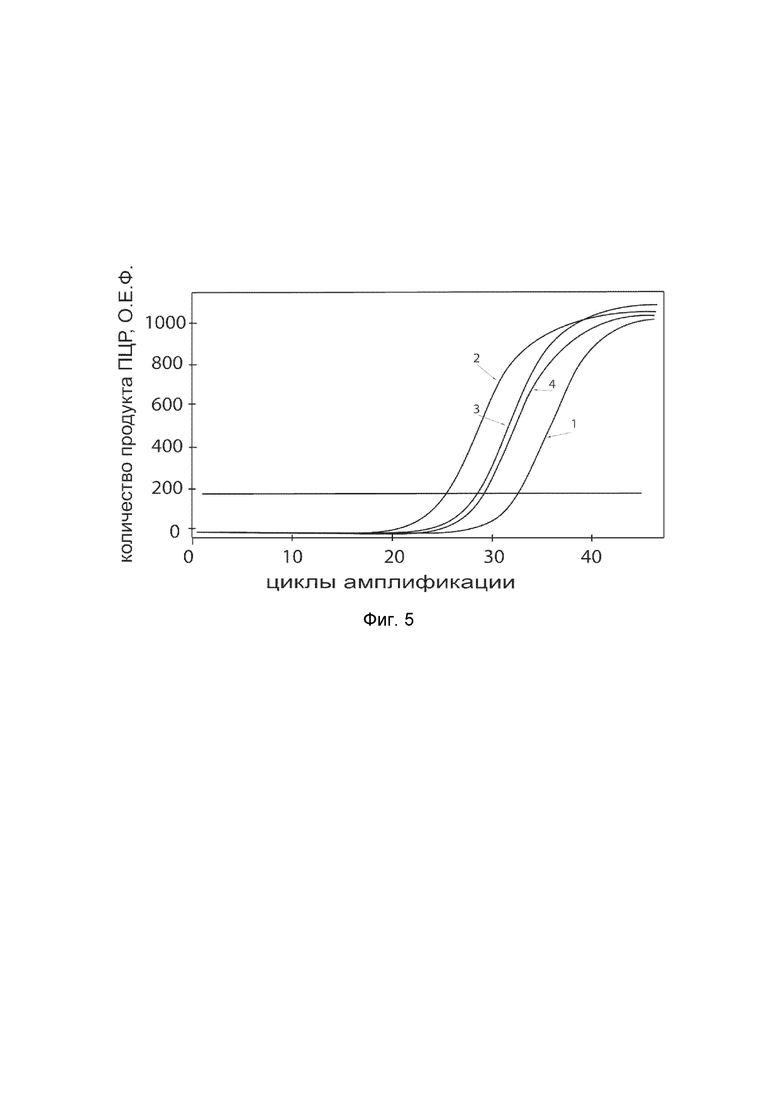
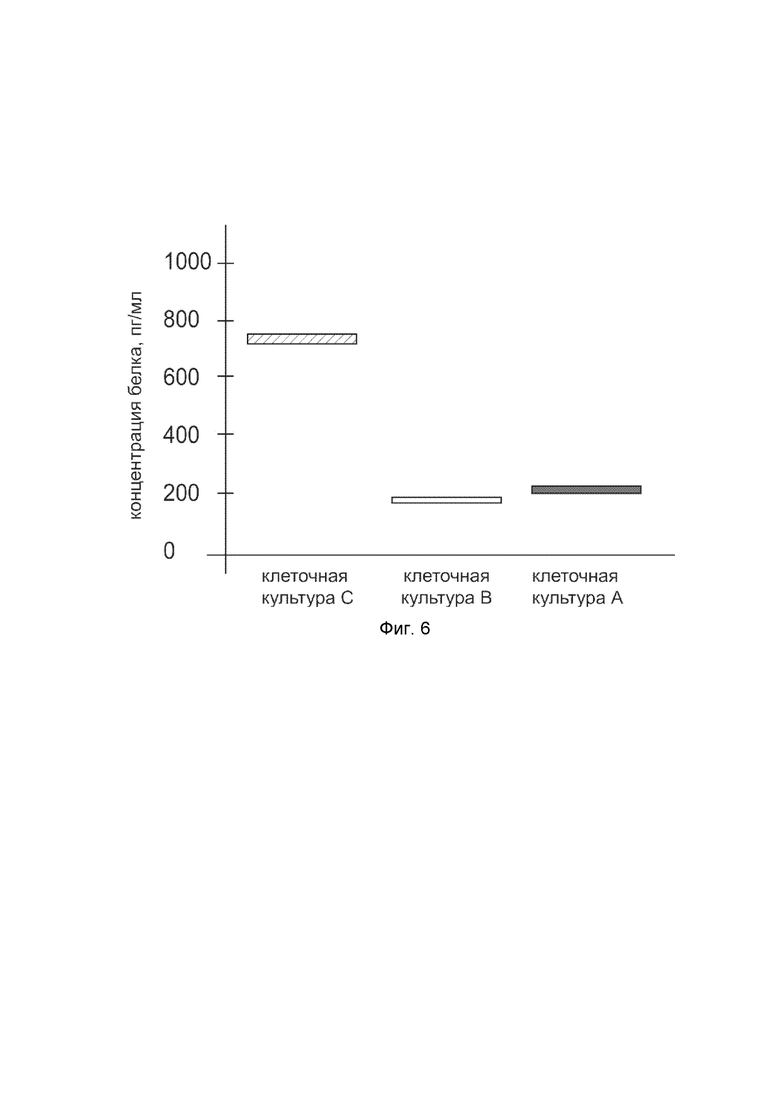
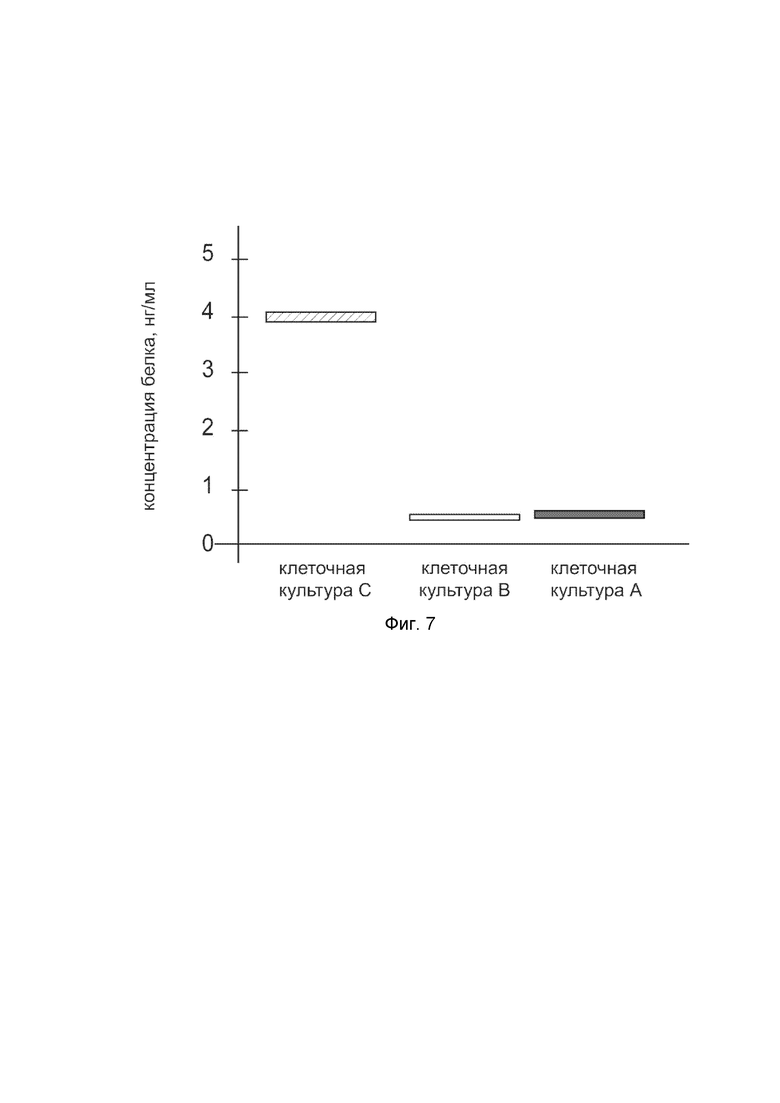
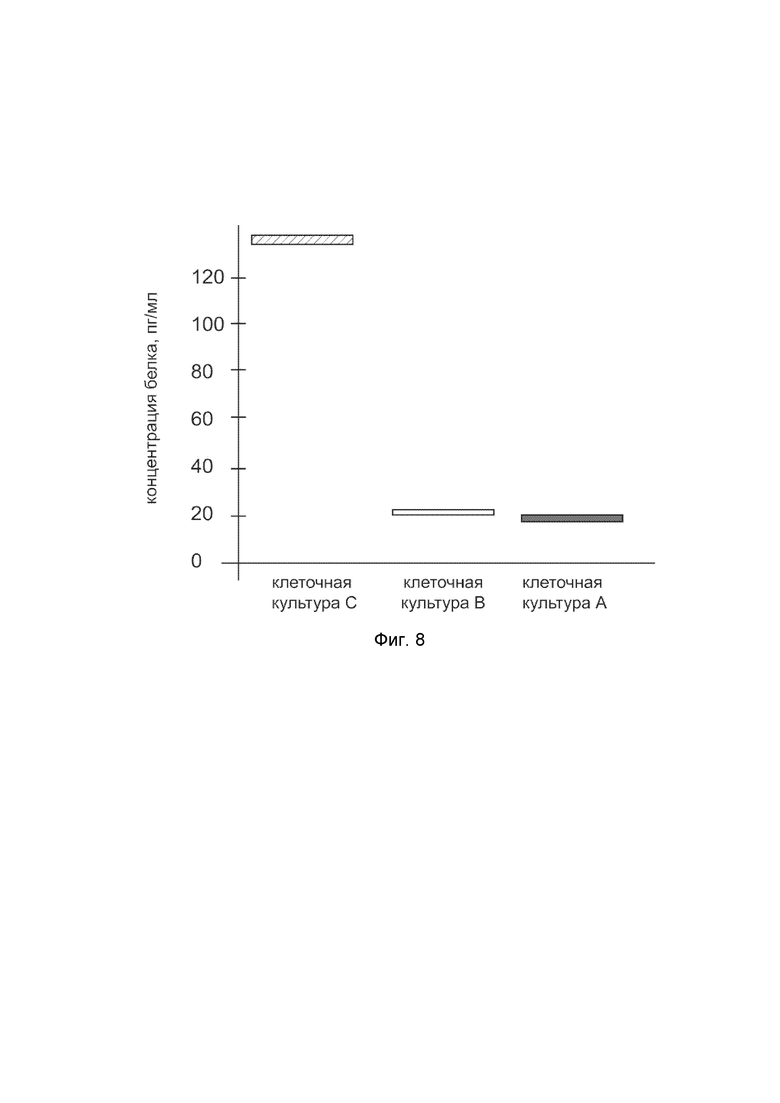
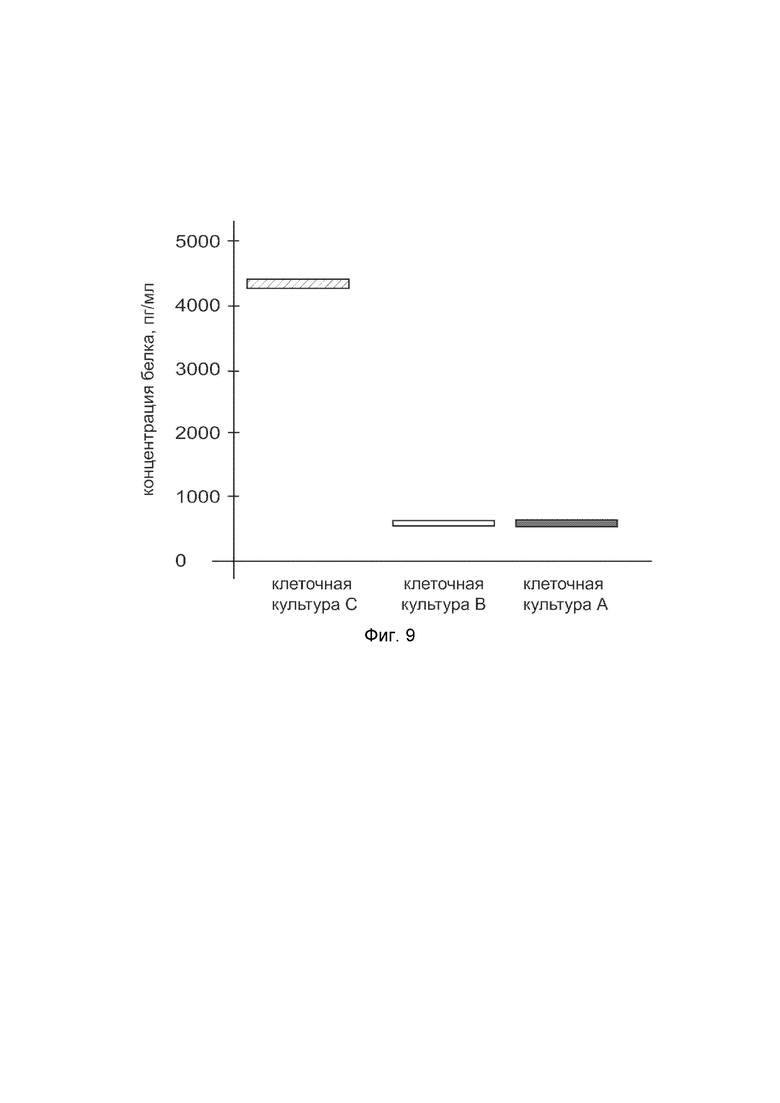
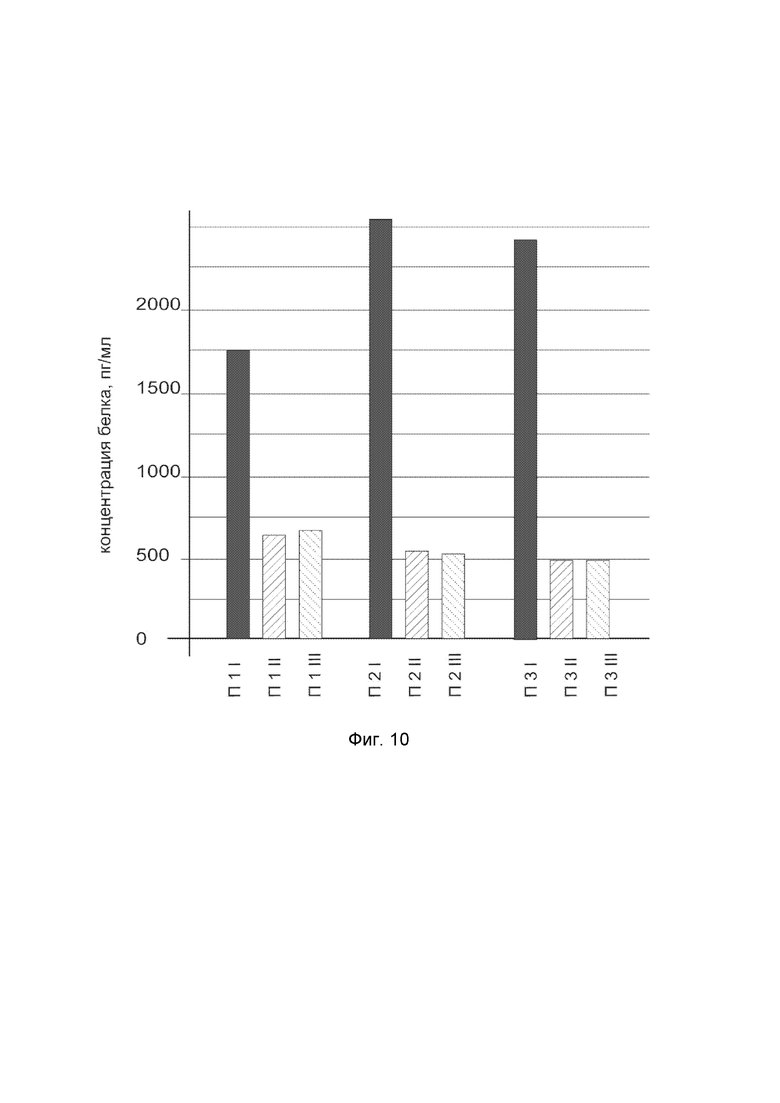
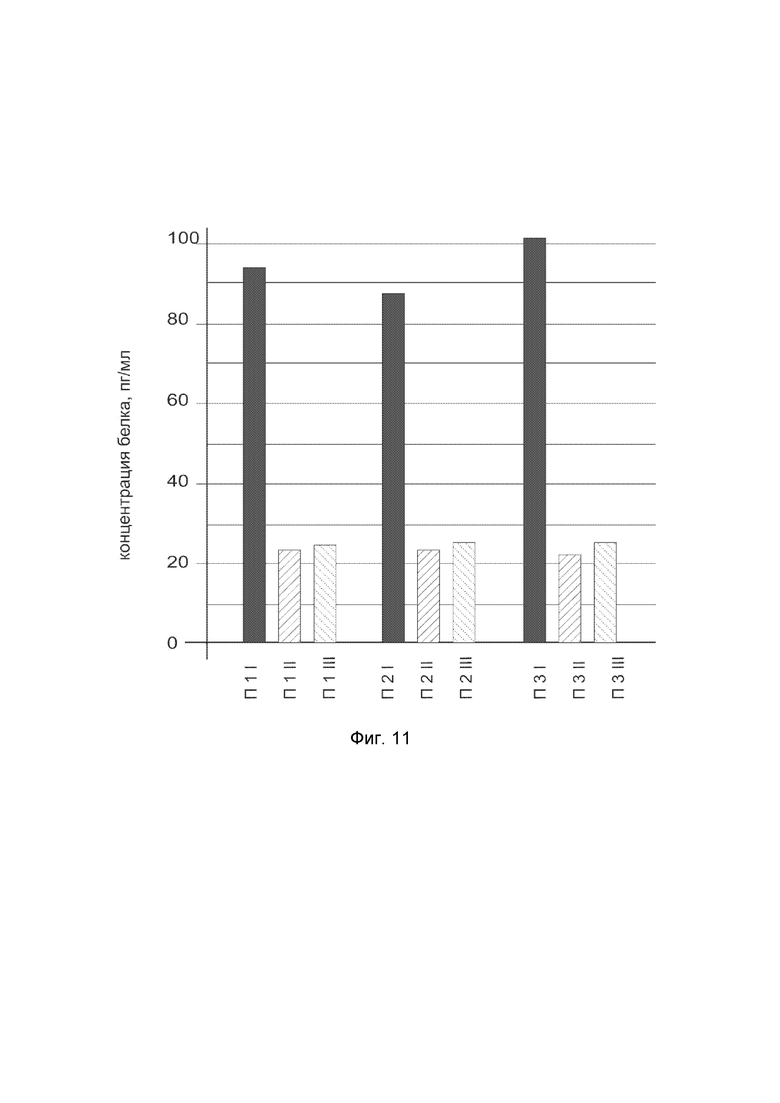
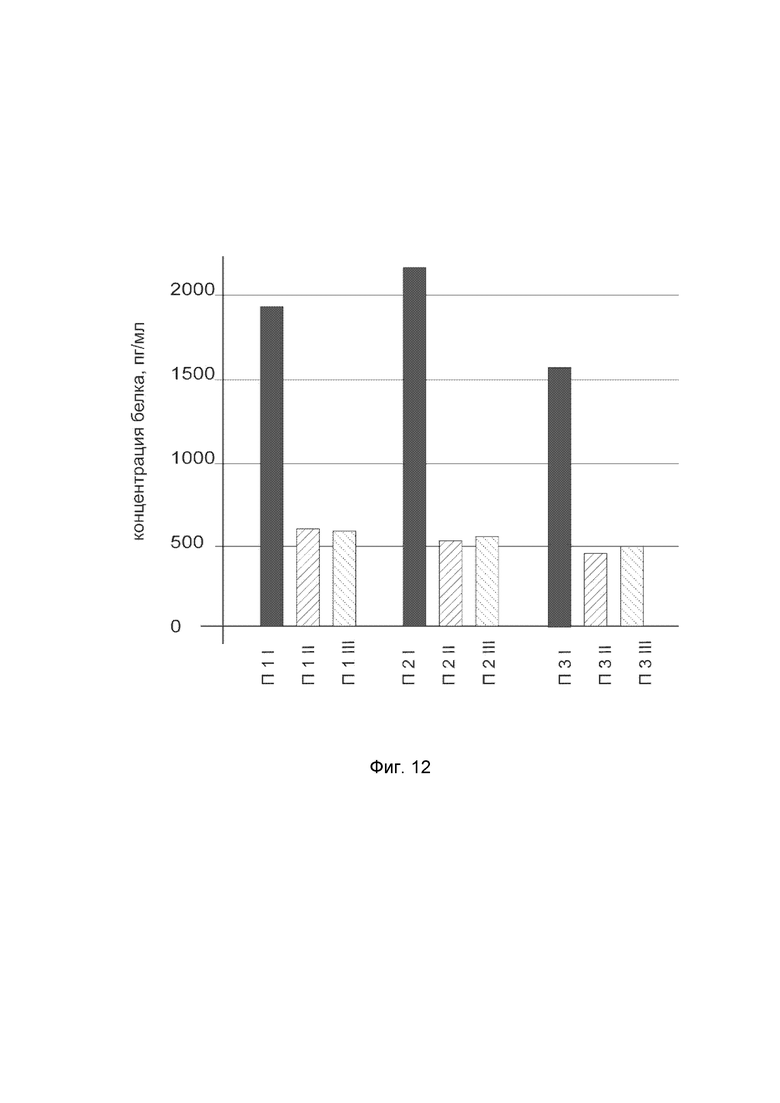
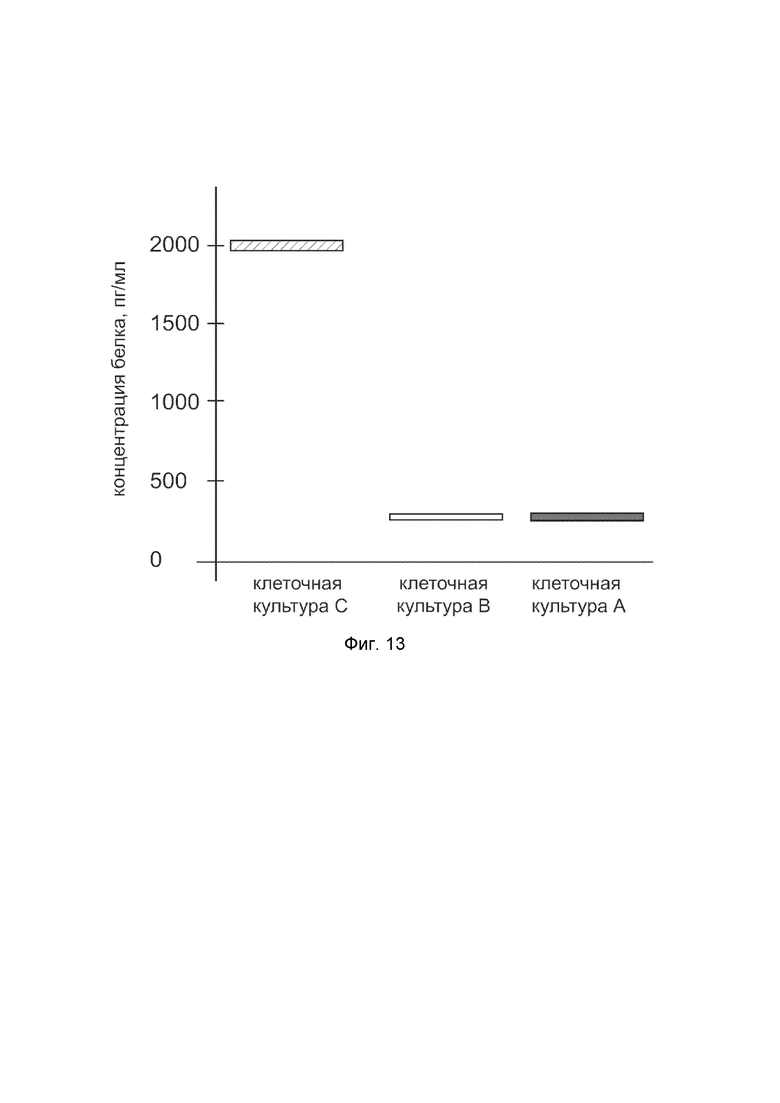
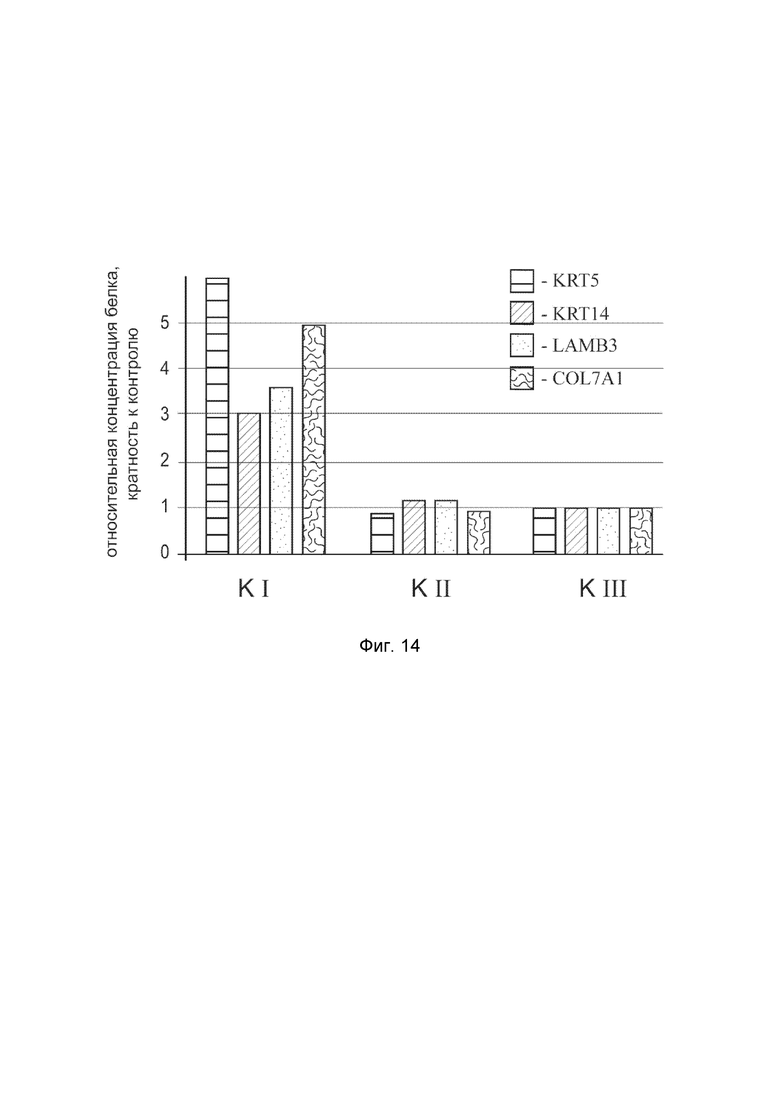
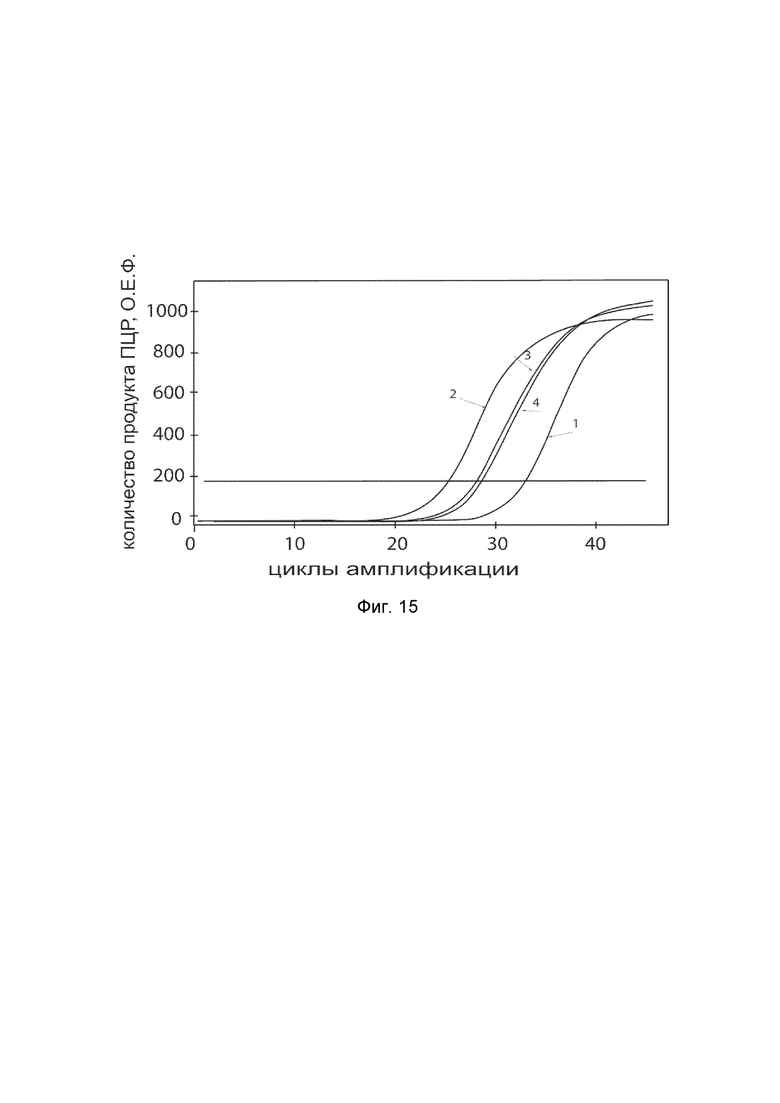
Изобретение относится к генной инженерии и может быть использовано в биотехнологии, медицине и сельском хозяйстве для создания препаратов генной терапии. Предложен генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген, выбранный из группы генов KRT5, KRT14, LAMB3, COL7A1, для повышения уровня экспрессии этого целевого гена в организме человека и животных. При этом генотерапевтический ДНК-вектор VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-LAMB3, или VTvaf17-COL7A1 имеет нуклеотидную последовательность SEQ ID №1, или SEQ ID №2, или SEQ ID №3, или SEQ ID №4 соответственно. Предложены также способ получения указанного вектора, применение вектора, штамм Escherichia coli, несущий указанный вектор, а также способ производства в промышленных масштабах указанного вектора. Изобретение может быть использовано для безопасного применения для генетической терапии человека и животных. 12 н. и 2 з.п. ф-лы, 15 ил., 20 пр.
1. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена KRT5, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-KRT5, размером 4929 п.н., с нуклеотидной последовательностью SEQ ID №1.
2. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена KRT14, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-KRT14, размером 4575 п.н., с нуклеотидной последовательностью SEQ ID №2.
3. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена LAMB3, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-LAMB3, размером 6674 п.н., с нуклеотидной последовательностью SEQ ID №3.
4. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17 для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, при этом генотерапевтический ДНК-вектор содержит кодирующую часть целевого гена COL7A1, клонированную в генотерапевтический ДНК-вектор VTvaf17, с получением генотерапевтического ДНК-вектора VTvaf17-COL7A1, размером 11990 п.н., с нуклеотидной последовательностью SEQ ID № 4.
5. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген KRT5, KRT14, LAMB3, COL7A1 по пп.1, 2, 3 или 4, отличающийся тем, что каждый из созданных генотерапевтических ДНК-векторов: VTvaf17-KRT5, или VTvaf17-KRT14, или VTvaf17-AMB3, или VTvaf17-COL7A1 по пп.1, 2, 3 или 4, за счет ограниченного размера векторной части VTvaf17, не превышающей 3200 п.н., обладает способностью эффективно проникать в клетки человека и животных и экспрессировать клонированный в него целевой ген KRT5, или KRT14, или LAMB3, или COL7A1.
6. Генотерапевтический ДНК-вектор на основе генотерапевтического ДНК-вектора VTvaf17, несущий целевой ген KRT5, KRT14, LAMB3, COL7A1 по пп.1, 2, 3 или 4, отличающийся тем, что в составе каждого из созданных генотерапевтических ДНК-векторов: VTvaf17- KRT5, или VTvaf17- KRT14, или VTvaf17-LAMB3, или VTvaf17- COL7A1 по пп.1, 2, 3 или 4, в качестве структурных элементов используются нуклеотидные последовательности, которые не являются генами антибиотикорезистентности, вирусными генами и регуляторными элементами вирусных геномов, обеспечивая возможность его безопасного применения для генетической терапии человека и животных.
7. Способ получения генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген KRT5, KRT14, LAMB3, COL7A1 по пп.1, 2, 3 или 4, заключающийся в том, что каждый из генотерапевтических ДНК-векторов: VTvaf17- KRT5, или VTvaf17- KRT14, или VTvaf17- LAMB3, или VTvaf17- COL7A1 получают следующим образом: кодирующую часть целевого гена KRT5, KRT14, LAMB3, COL7A1 по пп.1, 2, 3 или 4, клонируют в генотерапевтический ДНК-вектор VTvaf17 и получают генотерапевтический ДНК-вектор VTvaf17- KRT5, SEQ ID №1, или VTvaf17- KRT14, SEQ ID №2, или VTvaf17- LAMB3, SEQ ID №3, или VTvaf17- COL7A1, SEQ ID №4, соответственно, при этом кодирующую часть целевого гена KRT5, или KRT14, или LAMB3, или COL7A1 получают путем выделения суммарной РНК из биологического образца ткани человека с последующим проведением реакции обратной транскрипции и ПЦР-амплификации с использованием созданных олигонуклеотидов и расщеплением продукта амплификации соответствующими эндонуклеазами рестрикции, причем клонирование в генотерапевтический ДНК-вектор VTvaf17 проводят по сайтам рестрикции BamHII и HindIII, или по сайтам рестрикции SalI и EcoRI, причем селекцию проводят без антибиотиков, при этом при получении генотерапевтического ДНК-вектора VTvaf17-KRT5, SEQ ID №1 для проведения реакции обратной транскрипции и ПЦР-амплификации, в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
KRT5_F TTTGGATCCACCATGTCTCGCCAGTCAAGTGTGTCCTTC
KRT5_R AATAAGCTTCTAGCTCTTGAAGCTCTTCCGGGAGG,
а расщепление продукта амплификации и клонирование кодирующей части гена KRT5 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции BamHII и HindIII,
причем при получении генотерапевтического ДНК-вектора VTvaf17-KRT14, SEQ ID №2, для проведения реакции обратной транскрипции и ПЦР-амплификации в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
KRT14_F TTTGGATCCACCATGACCACCTGCAGCCGCCAG
KRT14_R AATAAGCTTTCAGTTCTTGGTGCGAAGGACCTGC,
а расщепление продукта амплификации и клонирование кодирующей части гена KRT14 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции BamHII и HindIII,
причем при получении генотерапевтического ДНК-вектора VTvaf17-LAMB3, SEQ ID №3, для проведения реакции обратной транскрипции и ПЦР-амплификации в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
LAMB3_F TTAGTCGACCACCATGAGACCATTCTTCCTCTTG
LAMB3_R ATAGAATTCACTTGCAGGTGGCATAGTAGAG,
а расщепление продукта амплификации и клонирование кодирующей части гена LAMB3 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции SalI и EcoRI,
причем при получении генотерапевтического ДНК-вектора VTvaf17-COL7A1, SEQ ID №4, для проведения реакции обратной транскрипции и ПЦР-амплификации в качестве созданных для этого олигонуклеотидов используют олигонуклеотиды
COL7A1_F ATCGTCGACCACCATGACGCTGCGGCTTCTGGT
COL7A1_R ATAGAATTCAGTCCTGGGCAGTACCTGTC,
а расщепление продукта амплификации и клонирование кодирующей части гена COL7A1 в генотерапевтический ДНК-вектор VTvaf17 проводят с использованием эндонуклеаз рестрикции SalI и EcoRI.
8. Способ использования генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген KRT5, KRT14, LAMB3, COL7A1 по пп.1, 2, 3 или 4, для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, заключающийся в трансфекции выбранным генотерапевтическим ДНК-вектором, несущим целевой ген на основе генотерапевтического ДНК-вектора VTvaf17, или несколькими выбранными генотерапевтическими ДНК-векторами, несущими целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, из созданных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, клеток органов и тканей пациента или животного, и/или во введении в органы и ткани пациента или животного аутологичных клеток этого пациента или животного, трансфицированных выбранным генотерапевтическим ДНК-вектором, несущим целевой ген на основе генотерапевтического ДНК-вектора VTvaf17 или несколькими выбранными генотерапевтическими ДНК-векторами, несущими целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, из созданных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17 и/или во введении в органы и ткани пациента или животного выбранного генотерапевтического ДНК-вектора, несущего целевой ген на основе генотерапевтического ДНК-вектора VTvaf17 или нескольких выбранных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, из созданных генотерапевтических ДНК-векторов, несущих целевые гены на основе генотерапевтического ДНК-вектора VTvaf17, или в сочетании обозначенных способов.
9. Способ получения штамма для производства генотерапевтического ДНК-вектора по пп.1, 2, 3 или 4 для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, заключающийся в получении электрокомпетентных клеток штамма Escherichia coli SCS110-AF с последующим проведением электропорации этих клеток генотерапевтическим ДНК-вектором VTvaf17-KRT5, или ДНК-вектором VTvaf17-KRT14, или ДНК-вектором VTvaf17- LAMB3, или ДНК-вектором VTvaf17- COL7A1, после чего клетки высеивают на чашки Петри с агаризованной селективной средой, содержащей дрожжевой экстракт, пептон, 6% сахарозы, а также 10 мкг/мл хлорамфеникола с получением в результате штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1.
10. Штамм Escherichia coli SCS110-AF/VTvaf17-KRT5, полученный способом по п.9, несущий генотерапевтический ДНК-вектор VTvaf17-KRT5, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, связанных с недостаточной экспрессией целевого гена.
11. Штамм Escherichia coli SCS110-AF/VTvaf17-KRT14, полученный способом по п.9, несущий генотерапевтический ДНК-вектор VTvaf17-KRT14, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, связанных с недостаточной экспрессией целевого гена.
12. Штамм Escherichia coli SCS110-AF/VTvaf17-LAMB3, полученный способом по п.9, несущий генотерапевтический ДНК-вектор VTvaf17-LAMB3, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, связанных с недостаточной экспрессией целевого гена.
13. Штамм Escherichia coli SCS110-AF/VTvaf17-COL7A1, полученный способом по п.9, несущий генотерапевтический ДНК-вектор VTvaf17-COL7A1, для его наработки с возможностью селекции без использования антибиотиков при получении генотерапевтического ДНК-вектора для лечения заболеваний, связанных с недостаточной экспрессией целевого гена.
14. Способ производства в промышленных масштабах генотерапевтического ДНК-вектора на основе генотерапевтического ДНК-вектора VTvaf17, несущего целевой ген KRT5, KRT14, LAMB3, COL7A1 по пп.1, 2, 3 или 4, для лечения заболеваний, связанных с недостаточной экспрессией целевого гена, заключающийся в том, что генотерапевтический ДНК-вектор VTvaf17-KRT5, или генотерапевтический ДНК-вектор VTvaf17-KRT14, или генотерапевтический ДНК-вектор VTvaf17-LAMB3, или генотерапевтический ДНК-вектор VTvaf17-COL7A1, получают путем того, что засевают в колбу с приготовленной средой затравочную культуру, выбранную из штамма Escherichia coli SCS110-AF/VTvaf17-KRT5, или штамма Escherichia coli SCS110-AF/VTvaf17-KRT14, или штамма Escherichia coli SCS110-AF/VTvaf17-LAMB3, или штамма Escherichia coli SCS110-AF/VTvaf17-COL7A1, затем инкубируют затравочную среду в шейкере-инкубаторе и переносят ее в промышленный ферментер, после чего растят до достижения стационарной фазы, затем выделяют фракцию, содержащую целевой ДНК-продукт, многостадийно фильтруют и очищают хроматографическими методами.
| US 20020064876 A1, 30.05.2002 | |||
| WO 2018220211 A1, 06.12.2018 | |||
| GORELL E | |||
| et al | |||
| Gene Therapy for Skin Diseases | |||
| Cold Spring Harb Perspect Med | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| БЕЙЛИН А.К.и др | |||
| Методы генной терапии для лечения врожденного буллезного эпидермолиза | |||
| ВЕСТН | |||
| МОСК | |||
| УН-ТА, СЕР | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| БИОЛОГИЯ, 2018, Т | |||
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
Авторы
Даты
2020-08-24—Публикация
2018-12-26—Подача