Изобретение относится к области аналитической химии и может быть использовано в контрольно-аналитических, клинических лабораториях для определения концентрации цефотаксима, для стандартизации и контроля качества лекарственных средств, для определения антибиотиков в образцах биологического происхождения с целью изучения фармакокинетики, лекарственного мониторинга для регулирования введения оптимальных доз антибиотиков при лечении различных инфекционных заболеваний.
Для определения цефотаксима используют масс-спектрометрию, диффузию в агар, высокоэффективную жидкостную хроматографию (ВЭЖХ), а также потенциометрические методы с применением ионоселективных электродов с различными видами электродно-активных соединений [1].
Для качественного и количественного анализа антибиотиков в фармацевтических формах и биологических жидкостях наиболее перспективным является использование высокоэффективной жидкостной хроматографии в обращенно-фазном режиме. Метод отличается селективностью, точностью и воспроизводимостью, а также высоким уровнем автоматизации.
Известно использование ультрафиолетовой спектрофотометрии для количественного определения цефалоспоринов в биологических средах. Способ заключается в снятии спектров поглощения антибиотика в пробе после удаления из нее твердых элементов и осаждения белков. К недостаткам данного способа можно отнести низкие показатели специфичности и чувствительности (2 мкг/мл) [2].
Известен способ определения цефотаксима методом ультрафиолетовой спектрофотометрии для количественного определения цефалоспоринов в биосредах. Предложенный метод основан на свойстве азотсодержащих органических соединений образовывать окрашенные соединения с солями переходных металлов в водных растворах. Основными недостатками этого способа являются трудоемкая пробоподготовка, низкая специфичность и визуальный учет результата исследования, что может существенно снизить воспроизводимость результатов. Кроме того, для образцов с концентрацией аналита менее 10 мкг/мл применяется дополнительная стадия концентрирования пробы, что еще сильнее затрудняет ход анализа [3].
Наиболее близким к заявляемому изобретению является методика определения цефотаксима натрия методом ВЭЖХ в изократическом режиме с использованием хроматографической колонки размером 250×4 мм, заполненной сорбентом С8 с размером частиц 5 мкм, в качестве подвижной фазы используют смесь раствора ацетата аммония (рН=6,8) с ацетонитрилом в соотношении 85:15. Недостатками метода являются небольшая чувствительность и низкое удерживание цефотаксима в данных хроматографических условиях. Кроме того, низкая буферная емкость раствора ацетата аммония при рН=6,80 может приводить к уширенным и ассиметричным пикам, что существенно осложняет проведение количественного анализа [4].
Целью предлагаемого изобретения является разработка способа определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии.
Технический результат достигается с помощью способа определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии, в котором изократический режим элюирования с использованием хроматографической колонки, заполненной сорбентом с размером частиц 5 мкм, в качестве подвижной фазы используют смесь раствора ацетата аммония с ацетонитрилом, при этом хроматографическое разделение производится на колонке размером 250×3 мм, заполненной сорбентом С18, с использованием в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония рН=4,7 с ацетонитрилом в соотношении 90:10 с применением ультрафиолетового детектора при длине волны 252 нм и объеме вводимой пробы 10 мкл.
Сущность способа определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии, включающий изократический режим элюирования с использованием хроматографической колонки, заполненной сорбентом с размером частиц 5 мкм, в качестве подвижной фазы используют смесь раствора ацетата аммония с ацетонитрилом, при этом хроматографическое разделение производится на колонке размером 250×3 мм, заполненной сорбентом С18, с использованием в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония рН=4,7 с ацетонитрилом в соотношении 90:10 с применением ультрафиолетового детектора при длине волны 252 нм и объеме вводимой пробы 10 мкл.
Использование в качестве неподвижной фазы хроматографической колонки размером 250×3 мм, заполненной сорбентом С18 с размером частиц 5 мкм, позволяет получить эффективное разделение цефотаксима с примесными соединениями пробы. Меньший внутренний диаметр колонки позволяет уменьшить расход подвижной фазы с сохранением эффективности, а большая гидрофобность сорбента С18 по сравнению с С8 обеспечивает большее удерживание цефотаксима, что повышает разрешающую способность метода.
Применения в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония (рН=4,70) с ацетонитрилом в соотношении 90:10 позволяет достигнуть высокой симметрии и остроты пиков за счет высокой буферной емкости аммоний-ацетатного буфера при рН=4,70.
Заявляемый способ обладает следующими отличительными от прототипа признаками:
- Высокая чувствительность метода (предел обнаружения 27 нг/мл);
- Повышенная экономическая эффективность анализа: расход подвижной фазы и ацетонитрила ниже в 2 и 1,5 раза соответственно.
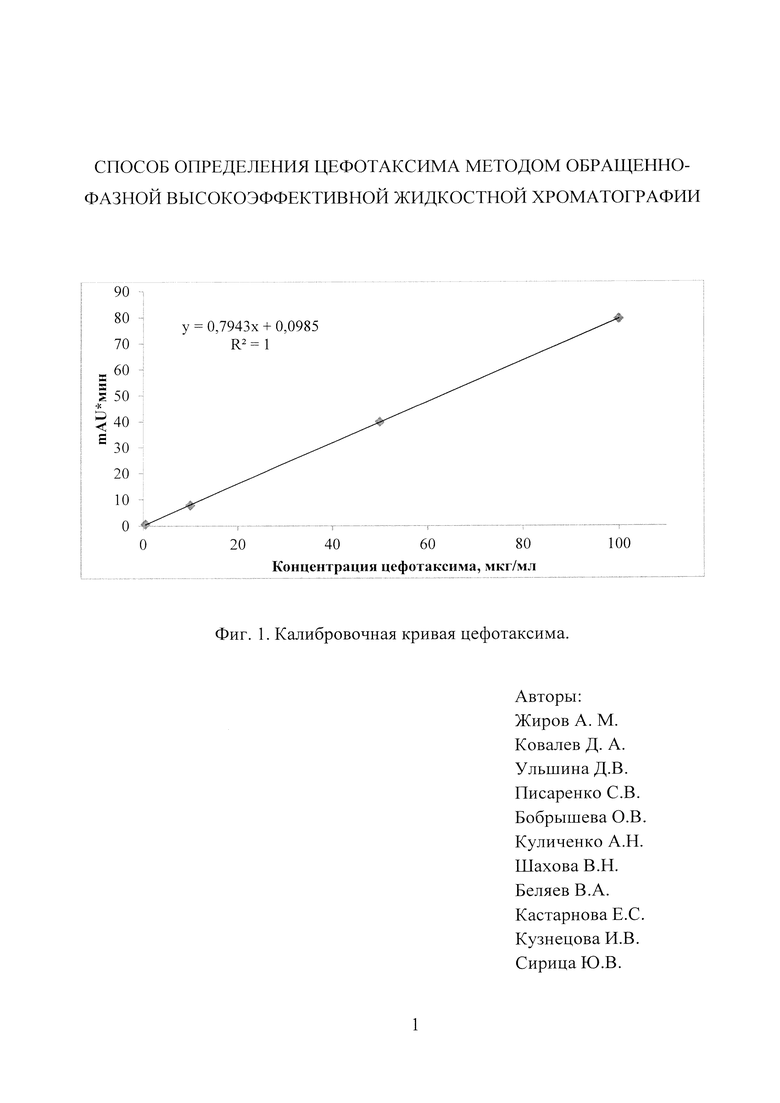
На фиг. 1, дан способ определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии, калибровочная кривая цефотаксима.
На фиг. 2, дан способ определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии, хроматограмма цефотаксима.
Способ осуществляется следующим образом.
Исследуемый образец растворяется в смеси 0,02 М раствора ацетата аммония (рН=4,70) с ацетонитрилом в соотношении 90:10, фильтруется через 0,2 мкм фильтр и анализируется на приборе «Ultimate 3000» Dionex с ультрафиолетовым детектором при длине волны 252 нм, хроматографической колонкой размером 250×3 мм, заполненной сорбентом С18 с размером частиц 5 мкм. Режим элюирования изократический, с использованием в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония (рН=4,70) с ацетонитрилом в соотношении 90:10, температура термостата колонки 25°С, объем вводимой пробы 10 мкл. Проводится не менее пяти измерений для каждого раствора.
Концентрацию цефотаксима в препаратах определяли с использованием предварительно построенной калибровочной кривой зависимости площади пика аналита от концентрации (фиг. 1).
Возможность практического применения заявленного способа подтверждается примером его конкретного выполнения с использованием совокупности заявляемых признаков.
Пример 1.
200 мкл плазмы крови смешивается с 800 мкл смеси 0,02 М раствора ацетата аммония (рН=4,70) с ацетонитрилом в соотношении 90:10, фильтруется через 0,2 мкм фильтр и анализируется на приборе «Ultimate 3000» Dionex с ультрафиолетовым детектором при длине волны 252 нм, хроматографической колонкой размером 250×3 мм, заполненной сорбентом С18 с размером частиц 5 мкм. Режим элюирования изократический, с использованием в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония (рН=4,70) с ацетонитрилом в соотношении 90:10, температура термостата колонки 25°С, объем вводимой пробы 10 мкл. Проводится не менее пяти измерений для каждого раствора.
На представленной хроматограмме образца предел обнаружения цефотаксима составляет 27 нг/мл, время удерживания 9,92±0,12 мин (фиг. 2.).
Используемая литература
1. Кулапина, Е.Г. Современные методы определения антибиотиков в биологических и лекарственных средах / Е.Г. Кулапина, О.В. Баринова, О.И. Кулапина, И.А. Утц, СВ. Снесарев // Антибиотики и химиотерапия. - 2009. - Т. 54. - №9-10. - С. 53-60.
2. Патент РФ №2445624. Опубликован 20.03.2012 Бюл. №8.
3. Патент РФ №2567335. Опубликован 10.11.2015 Бюл. №31.
4. Lalitha, N. Development and validation of RP-HPLC method for estimation of cefotaxime sodium in marketed formulations / N. Lalitha, P.S. Pai // J. Basic Clin. Pharm. - 2009. - Vol.1. - P. 26-28.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения аминогликозидных антибиотиков методом обращенно-фазной высокоэффективной жидкостной хроматографии | 2022 |
|
RU2786839C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦИПРОФЛОКСАЦИНА МЕТОДОМ ОБРАЩЕННО-ФАЗНОЙ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2020 |
|
RU2751338C1 |
| Способ определения скорости высвобождения инкапсулированного в ниосомы цефотаксима in vitro | 2020 |
|
RU2754850C1 |
| Способ определения амиодарона и его основного метаболита дезэтиламиодарона в сыворотке крови человека | 2020 |
|
RU2749566C1 |
| Способ количественного определения декспантенола и хитозана при их совместном присутствии в геле | 2021 |
|
RU2760525C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ РИВАРОКСАБАНА В КРОВИ МЕТОДОМ ВЫСОКОЭФФЕКТИВНОЙ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ | 2025 |
|
RU2839935C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ЭСТРОГЕНА И ДЕКСПАНТЕНОЛА В ДВУХКОМПОНЕНТНОМ ЛЕКАРСТВЕННОМ ПРЕПАРАТЕ МЕТОДОМ ВЭЖХ | 2011 |
|
RU2476873C1 |
| СПОСОБ УВЕЛИЧЕНИЯ СРОКА ЭКСПЛУАТАЦИИ СОРБЕНТА ПРИ ПРОМЫШЛЕННОЙ ОЧИСТКЕ ГЕННО-ИНЖЕНЕРНОГО ИНСУЛИНА ЧЕЛОВЕКА | 2008 |
|
RU2383624C2 |
| Способ количественного определения фтивазида | 2024 |
|
RU2828350C1 |
| СПОСОБ ОЧИСТКИ ТРИПТОРЕЛИНА | 2015 |
|
RU2585105C1 |

Настоящее изобретение относится к способу определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии, включающему изократический режим элюирования с использованием хроматографической колонки, заполненной сорбентом с размером частиц 5 мкм, в качестве подвижной фазы используют смесь раствора ацетата аммония с ацетонитрилом, отличающийся тем, что хроматографическое разделение производится на колонке размером 250×3 мм, заполненной сорбентом С18, с использованием в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония рН=4,7 с ацетонитрилом в соотношении 90:10 с применением ультрафиолетового детектора при длине волны 252 нм и объеме вводимой пробы 10 мкл. Технический результат – эффективное разделение цефотаксима с примесными соединениями пробы и обеспечение большого удержания цефотаксима, что повышает чувствительность и разрешающую способность метода, уменьшение расхода подвижной фазы, что повышает экономическую эффективность анализа. 2 ил., 1 пр.
Способ определения цефотаксима методом обращенно-фазной высокоэффективной жидкостной хроматографии, включающий изократический режим элюирования с использованием хроматографической колонки, заполненной сорбентом с размером частиц 5 мкм, в качестве подвижной фазы используют смесь раствора ацетата аммония с ацетонитрилом, отличающийся тем, что хроматографическое разделение производится на колонке размером 250×3 мм, заполненной сорбентом С18, с использованием в качестве подвижной фазы смеси 0,02 М раствора ацетата аммония рН=4,7 с ацетонитрилом в соотношении 90:10 с применением ультрафиолетового детектора при длине волны 252 нм и объеме вводимой пробы 10 мкл.
| N | |||
| Lalitha, P.S | |||
| Pai: "Development and validation of RP-HPLC method for estimation of cefotaxime sodium in marketed formulations", J | |||
| Basic Clin | |||
| Pharm., 2009., vol.1, pp.26-28 | |||
| L.I | |||
| Sokolova, I.V | |||
| Chuchalina: "Preconcentration of the antibiotics Cephazolin, Cefotaxime and Levomycetin on modified silicas", Journal of Analytical Chemistry, 2006, vol.61, no.12, pp.1140-1143, DOI: 10.1134/S1061934806120021 | |||
| CN 101592637 A, 02.12.2009 | |||
| CN 101592636 A, 02.12.2009 | |||
| Е.Г | |||
| Кулапина и др.: "Современные методы определения антибиотиков в биологических и лекарственных средах (обзор)", антибиотики и химиотерапия, 2009, т | |||
| Видоизменение прибора для получения стереоскопических впечатлений от двух изображений различного масштаба | 1919 |
|
SU54A1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦЕФАЛОСПОРИНОВЫХ АНТИБИОТИКОВ В БИОСРЕДАХ | 2010 |
|
RU2445624C2 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ЦИПРОФЛОКСАЦИНА В ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ | 2009 |
|
RU2416792C1 |
Авторы
Даты
2019-05-14—Публикация
2018-10-08—Подача