Настоящее изобретение относится к способу получения сложных эфиров альфа-гидроксикарбоновых кислот (HCE) путем алкоголиза соответствующих альфа-гидроксикарбоксамидов (HCA) в газовой фазе.
Получение HCE посредством алкоголиза HCA в достаточной мере известно из уровня техники. В DE 2454497 описана соответствующая реакция с применением соединений свинца в качестве катализатора. В данном контексте также упоминаются варианты непрерывного способа, но без обеспечения технического решения, в которых продукты получают с высокой эффективностью.
В DE 2528524 описан способ получения HCE с применением катализаторов, включая inter alia соединения лантана. Упоминается также, что способы можно осуществлять непрерывно, но без обеспечения удовлетворительных решений для задач, которые возникают при длительной эксплуатации.
В EP 0945423 раскрыт способ получения HCE, при котором HCA вводят в реакцию со спиртом в присутствии катализатора в жидкой фазе, при этом концентрация аммиака в реакционном растворе поддерживается на уровне ≤ 0,1% по весу. Следовательно, образованный аммиак постоянно практически полностью удаляют из реакционного раствора. Для этой цели реакционный раствор нагревают до кипения и газообразный реактив для удаления барботируют через реакционный раствор. Недостатки существующего способа заключаются в том, что эффективное удаление аммиака требует использования исключительно эффективной разделительной колонны и, следовательно, исключительного уровня технической сложности.
Применение инертного газообразного реактива для удаления улучшает удаление аммиака, но при затратах на дополнительный компонент способа, обработка с помощью него означает дополнительную обработку. Более того, если альфа-гидроксиизобутирамид и метанол применяют в качестве соответствующих реагентов, аммиак и остаточный метанол, образовавшиеся при условиях, определенных в публикации, можно отделить друг от друга только с очень большими трудностями. Дополнительная обработка дополнительного потока (разделение газообразного реактива для удаления/аммиака) также неизбежно означает, что предложенная процедура представляет относительно низкий экономический интерес, поэтому данный способ до сих пор не реализован в промышленности. В случае данного каталитического выполнения в жидкой фазе происходит дополнительное образование побочных продуктов, например N-метилгидроксиизобутирамида или триметиламина, которые необходимо удалять из желаемого продукта на основе метилгидроксиизобутирата очень сложным путем с применением соответствующих способов.
Недавно в EP 2415750 был раскрыт способ, который описывает алкоголиз HCA в газовой фазе. Было показано, что значительно более высокие значения степени превращения, до 90% HCA, можно получить «за один проход», что уже приводит к значительному улучшению в потреблении пара при получении HCE, поскольку получают меньшие циркуляционные потоки. Однако было обнаружено, что значения селективности HCE намного ниже, и существует повышенная частота возникновения побочных продуктов, например, ацетона и 2-амино-2-метилпропионитрила (AMPN). Таким образом, способ в газовой фазе, описанный в данном документе, можно оценивать как лучший с точки зрения энергетических показателей по сравнению со способами в жидкой фазе, но при этом значения селективности неудовлетворительны, и в результате относительно высокая концентрация побочных продуктов в некоторых случаях неблагоприятна для длительной эксплуатации.
С учетом уровня техники задачей, рассматриваемой в настоящем изобретении, являлось обеспечение способов получения HCE, которые можно осуществлять энерго- и ресурсосберегающим образом и, следовательно, легко и без лишних затрат. Дополнительная задача, которая рассматривается в настоящем изобретении, заключалась в обеспечении способов, в которых HCE можно получать с высокой степенью селективности. Другая задача, которая рассматривается в настоящем изобретении, заключалась в обеспечении способа получения HCE, в котором отсутствуют побочные продукты или получают только небольшие количества побочных продуктов. В то же время продукт должен, насколько это возможно, быть получен при высоких значениях выхода и, если смотреть в целом, с низким потреблением энергии.
Данные задачи и дополнительные проблемы, которые не указаны явно, решают путем обеспечения способа получения HCE посредством алкоголиза в газовой фазе соответствующего HCA над гетерогенным катализатором, характеризующегося тем, что молярное отношение спирта к HCA составляет 2-25 моль/моль, и превращение осуществляют в присутствии воды.
Применимые HCA в реакции по настоящему изобретению обычно включают все такие карбоксамиды, которые несут по меньшей мере одну гидроксильную группу в альфа-положении по отношению к карбоксамидной группе.
В свою очередь, карбоксамиды хорошо известны в данной области техники. Как правило, под ними понимают соединения, несущие группы, имеющие формулу -CONR’R”-, в которой каждый из R’ и R” независимо представляет собой водород или группу, содержащую 1-30, более предпочтительно 1-20, предпочтительно 1-10 и более предпочтительно 1-5 атомов углерода, особенное предпочтение отдают амидам, где R’ и R’’ представляют собой водород. Карбоксамид может нести 1, 2, 3, 4 или больше групп, имеющих формулу -CONR’R’’-. Данные включают, в частности, соединения, имеющие формулу R(-CONR’R’’)n, где радикал R представляет собой группу, содержащую 1-30, более предпочтительно 1-20, предпочтительно 1-10, более предпочтительно 1-5 и более предпочтительно 2-3 атома углерода, R’ и R’’ определены выше, и n представляет собой целое число в диапазоне 1-10, предпочтительно 1-4 и более предпочтительно равняется 1 или 2.
Выражение «группа, содержащая 1-30 атомов углерода» обозначает радикалы органических соединений, содержащие 1-30 атомов углерода. Оно включает не только ароматические и гетероароматические группы, но также алифатические и гетероалифатические группы, например алкильные, циклоалкильные, алкокси-, циклоалкокси-, циклоалкилтио- и алкенильные группы. Данные указанные группы могут быть разветвленными или неразветвленными.
В соответствии с настоящим изобретением ароматические группы представляют собой радикалы моно- или полициклических ароматических соединений, предпочтительно содержащих 6-20, более предпочтительно 6-12 атомов углерода.
Гетероароматические группы представляют собой арильные радикалы, в которых по меньшей мере одна CH-группа замещена посредством N, и/или по меньшей мере две смежные CH-группы замещены посредством S, NH или O.
Предпочтительные в соответствии с настоящим изобретением ароматические или гетероароматические группы получены из бензола, нафталина, бифенила, дифенилового эфира, дифенилметана, дифенилдиметилметана, бисфенона, дифенилсульфона, тиофена, фурана, пиррола, тиазола, оксазола, имидазола, изотиазола, изоксазола, пиразола, 1,3,4-оксадиазола, 2,5-дифенил-1,3,4-оксадиазола, 1,3,4-тиадиазола, 1,3,4-триазола, 2,5-дифенил-1,3,4-триазола, 1,2,5-трифенил-1,3,4-триазола, 1,2,4-оксадиазола, 1,2,4-тиадиазола, 1,2,4-триазола, 1,2,3-триазола, 1,2,3,4-тетразола, бензо[b]тиофена, бензо[b]фурана, индола, бензо[c]тиофена, бензо[c]фурана, изоиндола, бензоксазола, бензотиазола, бензимидазола, бензизоксазола, бензизотиазола, бензопиразола, бензотиадиазола, бензотриазола, дибензофурана, дибензотиофена, карбазола, пиридина, бипиридина, пиразина, пиразола, пиримидина, пиридазина, 1,3,5-триазина, 1,2,4-триазина, 1,2,4,5-триазина, тетразина, хинолина, изохинолина, хиноксалина, хиназолина, циннолина, 1,8-нафтиридина, 1,5-нафтиридина, 1,6-нафтиридина, 1,7-нафтиридина, фталазина, пиридопиримидина, пурина, птеридина или хинолизина, 4H-хинолизина, дифенилового эфира, антрацена, бензопиррола, бензооксатиадиазола, бензооксадиазола, бензопиридина, бензопиразина, бензопиразидина, бензопиримидина, бензотриазина, индолизина, пиридопиридина, имидазопиримидина, пиразинопиримидина, карбазола, акридина, феназина, бензохинолина, феноксазина, фенотиазина, акридизина, бензоптеридина, фенантролина и фенантрена, каждый из которых также может быть необязательно замещен.
Предпочтительные алкильные группы включают метил, этил, пропил, изопропил, 1-бутил, 2-бутил, 2-метилпропил, трет-бутил, пентил, 2-метилбутил, 1,1-диметилпропил, гексил, гептил, октил, 1,1,3,3-тетраметилбутил, нонил, 1-децил, 2-децил, ундецил, додецил, пентадецил и эйкозил.
Предпочтительные циклоалкильные группы включают циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил, каждый из которых может быть необязательно замещен разветвленными или неразветвленными алкильными группами.
Предпочтительные алкенильные группы включают винил, аллил, 2-метил-2-пропенил, 2-бутенил, 2-пентенил, 2-деценил и 2-эйкозенил.
Предпочтительные гетероалифатические группы включают вышеупомянутые предпочтительные алкильные и циклоалкильные радикалы, в которых по меньшей мере одно углеродное звено замещено O-, S-, или NR8-, или NR8R9-группой, и каждый из R8 и R9 независимо представляет собой алкильную группу, содержащую 1-6 атомов углерода, алкокси-группу, содержащую 1-6 атомов углерода, или арильную группу.
Наиболее предпочтительно в соответствии с настоящим изобретением, когда карбоксамиды несут разветвленные или неразветвленные алкильные или алкокси-группы, содержащие 1-20 атомов углерода, предпочтительно 1-12, преимущественно 1-6 и, в частности, 1-4 атома углерода, и циклоалкильные или циклоалкилокси-группы, содержащие 3-20 атомов углерода, предпочтительно 5-6 атомов углерода.
Радикал R может нести заместители. Предпочтительные заместители включают галогены, особенно фтор, хлор, бром, а также алкокси- или гидроксильные радикалы.
HCA можно применять в способе по настоящему изобретению отдельно или в виде смеси двух, или трех, или более различных HCA. Особенно предпочтительные HCA включают альфа-гидроксиизобутирамид и/или альфа-гидроксиизопропионамид.
Кроме того, особый интерес в одном варианте способа по настоящему изобретению представляет применение HCA, получаемых из кетонов или альдегидов и цианистого водорода посредством циангидринного синтеза. Первая стадия указанного синтеза предусматривает осуществление реакции карбонильного соединения, например кетона, в частности ацетона, или альдегида, например ацетальдегида, пропаналя или бутаналя, с цианистым водородом с получением определенного циангидрина. Особенно предпочтительно, когда упомянутый синтез предусматривает осуществление реакции ацетона и/или ацетальдегида характерным образом в присутствии небольшого количества щелочи или амина в качестве катализатора. На дополнительной стадии полученный таким образом циангидрин вводят в реакцию с водой с получением HCA.
Успешно применяемые в способах по настоящему изобретению спирты включают любые спирты, известные специалисту в данной области, а также соединения-предшественники спиртов, способные подвергаться реакции по типу алкоголиза с HCA при заданных условиях давления и температуры. Реакцию с HCA предпочтительно проводят путем алкоголиза со спиртом, предпочтительно содержащим 1-10 атомов углерода, более предпочтительно содержащим 1-5 атомов углерода. Предпочтительные спирты включают метанол, этанол, пропанол, бутанол, в частности н-бутанол и 2-метил-1-пропанол, пентанол, гексанол, гептанол, 2-этилгексанол, октанол, нонанол и деканол и их смеси. Особенно предпочтительно, когда применяемым спиртом является метанол и/или этанол, метанол является наиболее предпочтительным. Применение предшественников спирта также, по сути, возможно. Таким образом, например, можно применять алкилформиаты. Метилформиат или смесь метанола и монооксида углерода являются особенно подходящими.
Также предпочтительными являются способы, которые характеризуются тем, что применяемый HCA представляет собой гидроксиизобутирамид (HIBA), и применяемый спирт представляет собой метанол, в таком случае данные соединения реагируют с получением целевого продукта, метилгидроксиизобутирата (MHIB).
Подходящими катализаторами для способа по настоящему изобретению являются диоксиды циркония, легированные элементами из групп 2-4, 7 или 9-13 периодической таблицы или с помощью La, Sb или Bi. Также подходящими являются нелегированные диоксиды циркония. Предпочтительными легирующими элементами для диоксида циркония являются элементы из групп 3, 7, 9, 10 или 13 периодической таблицы или элементы, которые выбраны из группы, включающей B, Al, Mn, Co, Ni, Y, La или Yb. Особое предпочтение отдают легирующим элементам Ce, K, La, Mo, P, S, Si, Ti, W, Y и Zn, наибольшее предпочтение отдают Ce, K или La. Содержание легирующих веществ составляет 0-50%, предпочтительно 0,2-20% и более предпочтительно 0,4-15% по весу.
Способ по настоящему изобретению представляет собой реакцию в газовой фазе, причем гетерогенный катализатор находится в форме неподвижного слоя, подвижного слоя или псевдоожиженного слоя. Подходящие решения для устройств для конфигурации слоя катализатора описаны в Ullmann's Encyclopedia of Industrial Chemistry, Wiley 2012, p. 293 ff. (DOI: 10.1002/14356007.b04_087).
В реакции в газовой фазе по настоящему изобретению, достигали более высоких значений степени превращения по сравнению с реакцией в жидкой фазе, поскольку равновесие реакции смещается сильнее от реагентов к продуктам в газовой фазе. В контексте настоящего изобретения выражение «реакция в газовой фазе» необходимо понимать как такую реакцию, которая проходит главным образом в газовой фазе, при этом доля присутствующей жидкой фазы составляет <10%, предпочтительно <5%, более предпочтительно <2% и наиболее предпочтительно 0% по весу, исходя из общего количества реагентов.
HCA и спиртовые реагенты можно преобразовать в газовую фазу до подачи в реактор или внутри самого реактора. Кроме того, реагенты можно подавать в реактор отдельно или в виде смеси. Реакцию можно, по сути, также осуществлять в присутствии инертного газа, например азота, который облегчает преобразование реагентов в газовую фазу благодаря снижению значений парциального давления реагентов. Однако в предпочтительном варианте не требуется инертный газ, поскольку, таким образом, нет необходимости в дополнительной обработке инертного газа. Предпочтительными типами реакторов являются трубчатые реакторы.
Для разделения продуктов реакции, образовавшихся из непрореагировавших реагентов, побочных продуктов и/или других компонентов, можно применять стандартные способы, известные специалистам в данной области, например ректификацию.
Температуру реакции выбирают таким образом, чтобы происходило достаточное выпаривание реагентов, которое зависит главным образом от природы реагентов и выбранного значения давления реакции. В предпочтительном способе осуществления реакции HIBA с метанолом температура реакции составляет 150-300°C, предпочтительно 160-250°C, более предпочтительно 180-230°C.
Давление реакции при осуществлении реакции HIBA с метанолом составляет 0,1-3 бар, предпочтительно 0,2-3 бар, более предпочтительно 0,3-1,5 бар.
Способ в газовой фазе по настоящему изобретению осуществляют в присутствии воды. Неожиданно было обнаружено, что, например, в случае осуществления реакции HIBA с метанолом в присутствии воды образование побочных продуктов, особенно ацетона или 2-амино-2-метилпропионионитрила (AMPN), очень значительно уменьшалось, и селективность в отношении MHIB и срок эксплуатации катализатора существенно повышались. Воду либо можно добавлять к исходной реакционной смеси, либо подавать непосредственно в реактор. Молярное отношение воды к HCA составляет 0,1-10, предпочтительно 0,3-5 и более предпочтительно 0,5-1 моль/моль.
Молярное отношение спирта к HCA составляет 2-25, предпочтительно 7-20 и более предпочтительно 10-15 моль/моль.
WHSV (среднечасовая скорость подачи сырья), исходя из HCA, составляет 0,05-2, предпочтительно 0,1-1,5, более предпочтительно 0,1-0,6 ч-1.
В дополнительном предпочтительном варианте способа по настоящему изобретению перед выпариванием потоки реагентов обрабатывают с помощью катионообменника. Это может быть необходимо, когда, в случае применения каталитических способов, которые применяют при получении предшественников гидроксикарбоновых кислот, применяют ионы металлов из катализаторов или вторичные вспомогательные средства остаются в сырье для метанолиза. Таким образом, в случае получения гидроксиизобутирамида из ацетонциангидрина с помощью гидролиза над гетерогенными катализаторами на основе диоксида марганца вспомогательное вещество, а именно стабилизатор pH (обычно гидроксид щелочного металла, предпочтительно лития, натрия или калия), может оставаться в продукте даже после обработки; таким образом, данные следовые количества щелочи при последующем метанолизе в газовой фазе обычно приводят к комкованию в испарителе, при этом любые следовые количества, которые попадают в катализатор, будут его повреждать, или иначе они будут оказывать общее неблагоприятное воздействие на реакцию в ходе выпаривания и катализа. Аналогичные взаимосвязи применимы к другим минеральным веществам, которые попадают в гидроксикарбоновую кислоту, применяемую в качестве реагента, в виде следовых количеств от предшественника(предшественников), например, ионы марганца (из катализатора на основе диоксида марганца) и SiO2 (применяют в качестве вспомогательного вещества при получении диоксида марганца), которые приведены в качестве примера лишь нескольких примесей.
Это используется в первую очередь для отделения соединений металлов, которые, возможно, вымываются из катализатора, особенно ионы щелочных металлов или щелочно-земельных металлов, из сырья. Более конкретно, применяют соединения металлов из групп I А, II А, IV A периодической таблицы элементов и переходных элементов, в особенности из группы VII В. Подходящие стадии обработки с помощью ионообменников в достаточной мере хорошо известны из уровня техники. Подходящими ионообменниками являются, например, ионообменники, поставляемые на рынок компанией Rohm & Haas под торговым названием Amberlyst. Неожиданно было обнаружено, что, особенно в случае осуществления реакции HIBA с метанолом с получением MHIB, возможно, таким образом, уменьшить или полностью избежать образования отложений или любой тенденции к засорению на участке выпаривания установки. Значение pH потоков реагентов после прохождения через ионообменник составляет 3-7.
В качестве альтернативы для предварительной обработки сырья с помощью ионообменника, испаритель, который применяют перед подачей в реактор, в котором входное сырье выпаривают, можно заменить на парциальный испаритель, из которого отводят высококипящую фракцию, содержащую указанные примеси металлов из катализатора. Отводимая высококипящая фракция в данном случае составляет 0,1-20%, предпочтительно 0,2-10% и более предпочтительно 0,5-5% по весу, исходя из общего количества сырья. При необходимости, отводимую высококипящую фракцию можно подвергать дальнейшей дополнительной стадии выпаривания, в случае которого, низкокипящие соединения подают обратно в вышеупомянутый парциальный испаритель. Также в данном случае возможно применение других способов, известных специалистам в данной области, с целью восстановления дополнительного исходного материала.
Аммиак, высвобождаемый в предпочтительных вариантах способа по настоящему изобретению можно рециркулировать, например, в способ получения цианистого водорода. Например, аммиак можно вводить в реакцию с метанолом с получением цианистого водорода. Это подробно описано, например, в EP 0941984. Кроме того, цианистый водород можно получать из аммиака и метана с помощью способа BMA или способа Андрусова, при этом данные способы описаны в Ullmann’s Encyclopedia of Industrial Chemistry 5th edition, 1995, на CD-ROM, название записи «Inorganic Cyano Compounds». Таким же образом можно рециркулировать аммиак в способ аммоксидирования, например, синтез в промышленных масштабах акрилонитрила из аммиака, кислорода и пропена. Синтез акрилонитрила описан в Industrial Organic Chemistry, 1997, K. Weissermel and H.-J. Arpe, на страницах 307 и далее, название записи «Sohio process».
При необходимости, выделенный аммиак вводят в вышеупомянутые способы получения цианистого водорода или аммоксидирования после стадии очистки, которая, в частности, включает применение твердых адсорбентов. Пригодный твердый адсорбент более предпочтительно представляет собой активированный уголь.
Активированный уголь можно применять во всех возможных структурных формах, в форме порошка, в гранулированной форме или в виде цилиндрических или сферических гранул. Предпочтение отдают гранулированным активированным углям, которые характеризуются значениями поверхностной величины 1000-1500 м2/г, более предпочтительно 1200-1400 м2/г. Наряду с активированном углем, активированном химически с помощью хлорида цинка или фосфорной кислоты, предпочтительными являются активированные угли, которые активировали газом с применением солей щелочных металлов, щелочных металлов, хлоридов, сульфатов и ацетатов.
Возможными адсорбентами являются адсорбенты неподвижного слоя, подвижного слоя или псевдоожиженного слоя. Иллюстрированные решения для устройств описаны, например, в Ullmann's Encyclopedia of Industrial Chemistry, Wiley 2012, p 293 ff. (DOI: 10.1002/14356007.b04_087). Процедуру можно осуществлять непрерывно или периодически, причем предпочтение отдается первому.
Адсорбцию осуществляют в диапазоне температур 0-150°C, предпочтительно 30-100°C, более предпочтительно 35-50°C и при значениях давления 0,1-5 бар, предпочтительно 0,5-4 бар, более предпочтительно 1-3 бар.
Способ по настоящему изобретению также включает регенерацию катализатора для алкоголиза. Это осуществляют с помощью среды при 200-600°C, предпочтительно при 350-500°C.
Подходящими средами для регенерации являются воздух, водяной пар, инертные газы, например азот, аргон, ксенон, или газообразные продукты сгорания, например CO2 или оксиды азота, а также их смеси. Насыщенную или истощенную среду для регенерации можно подавать в подходящие обычные способы утилизации, например, на установку биологической очистки сточных вод или в термический окислитель.
Регенерацию можно осуществлять либо при восстановительных, либо при окислительных условиях, и ее эффект, по сути, состоит в том, что кислотно-основные свойства свежего катализатора восстанавливаются.
Значения температуры регенерации составляют 200-600°C, предпочтительно 300-500°C, более предпочтительно 350-450°C.
Время регенерации составляет 1-24 ч, предпочтительно 2-18 ч, более предпочтительно 3-12 ч.
WHSV (среднечасовая скорость подачи сырья) среды для регенерации через катализатор, подлежащий регенерации, составляет 0,01-10, предпочтительно 0,1-5, более предпочтительно 0,4-1,5 ч-1.
Приведенные далее примеры предназначены для иллюстрации, но никоим образом не ограничивают настоящее изобретение.
Сравнительные примеры 1-4
Раствор 20% по весу HIBA в метаноле подавали с помощью HPLC-насоса (Knauer) со скоростью потока 1 г/мин. в испаритель, включающий капиллярную трубку из нержавеющей стали длиной 1 м, намотанную вокруг нагревательного цилиндра мощностью 500 Вт. Смесь газов, которая возникала, подавали в реактор с неподвижным слоем длиной 33 см и внутренним диаметром 1 см. Загрузка катализатора включает 100 г легированного иттрием диоксида циркония (концентрация легирующей примеси составляет 8,3% по весу). Соответствующая WHSV, исходя из HIBA, составляет 0,2 ч-1. Результаты экспериментов в отношении степени превращения и селективности, которые осуществляли при четырех различных значениях температуры реактора, каждое при давлении реакции в 400 мбар, указаны в табл. 1.
Табл. 1. Степень превращения и селективность при различных температурах без воды
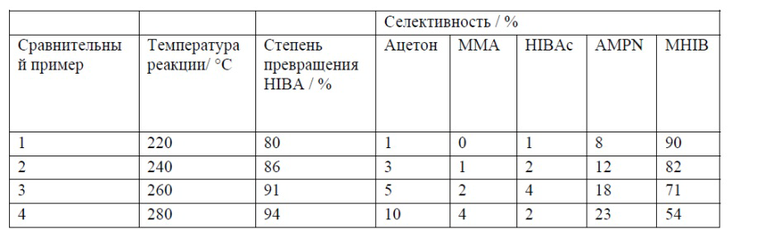
HIBAc = гидроксиизомасляная кислота
MMA = метилметакрилат
Когда температуру реакции повышали на 60°C, степень превращения HIBA увеличивалась от 80% до 94%. В то же время селективность для желаемого целевого продукта MHIB уменьшалась от 90% до 54%, и селективность для, например, нежелательного побочного продукта AMPN вырастала от 8% до 23%. Без добавления или без присутствия воды (согласно патентной публикации EP 2415750 Mitsubishi Gas Chem.) не найдено ни одной точки оптимизации, посредством чего уменьшалось бы получение побочного продукта AMPN, уменьшалось бы отделение ацетона от гидроксиизобутирамида и при этом достигалось бы значение селективности >93%.
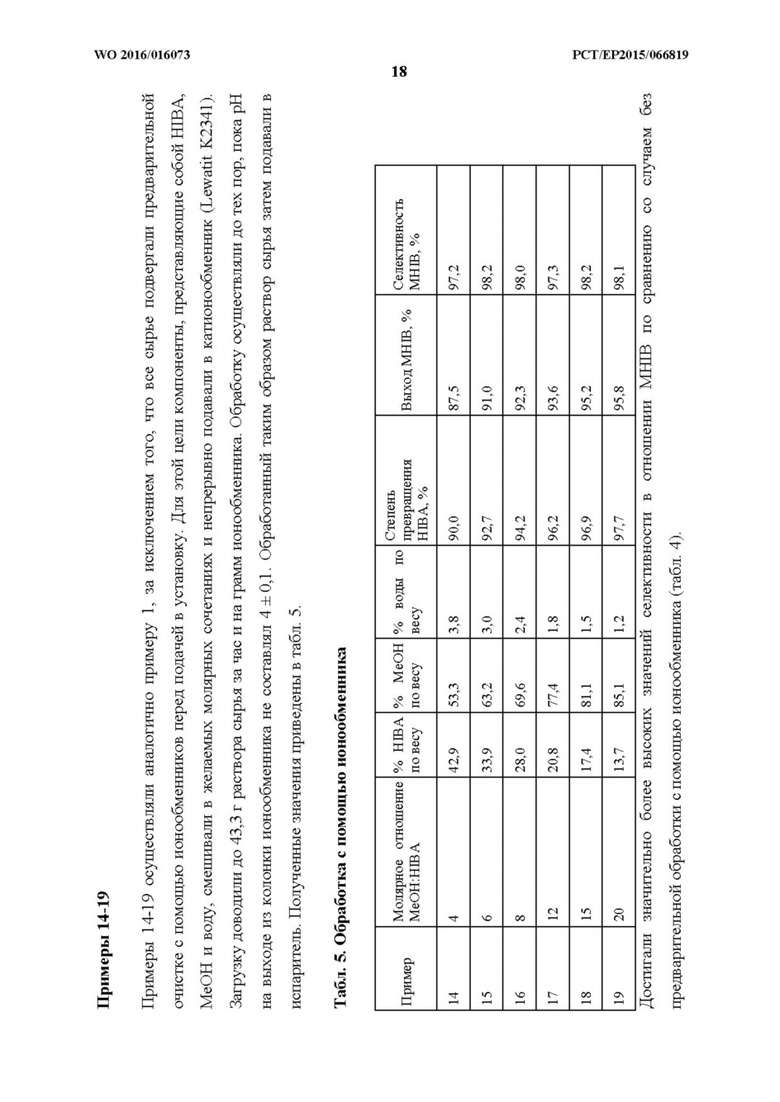
Примеры 1-9
Примеры 1-9 осуществляли в том же устройстве, что и сравнительные примеры 1-4. Однако добавляли 1% по весу воды к сырью за счет метанола. Температура реакции составляла 220°C. Результаты в отношении степени превращения HIBA и селективности MHIB для катализаторов на основе диоксида циркония, легированных различными оксидами, показаны в табл. 2.
Табл. 2. Различные катализаторы на основе диоксида циркония с 1% воды
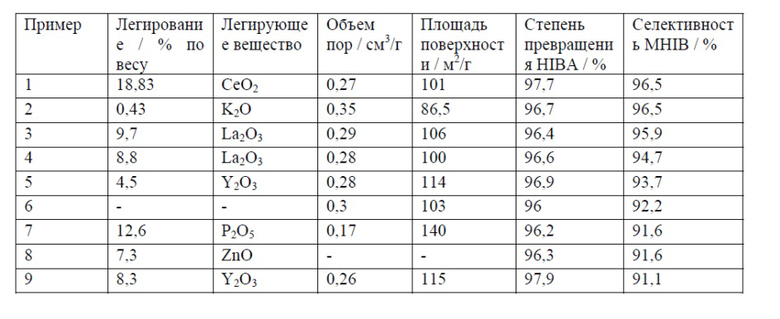
Что заметно, отчетливо повышены значения степени превращения и значения селективности по сравнению со сравнительными примерами 1-4 без воды в сырье. Особенно хорошие значения демонстрировали катализаторы, легированные Ce, K и La.
Даже небольшое каталитическое вспомогательное содержание воды при прочих одинаковых или идентичных условиях реакции обеспечивает эффективное подавление отделения ацетона и существенное сокращение образования нежелательного побочного продукта AMNP. Таким образом, селективность продукта значительно повышается.


Настоящее изобретение относится к способу получения сложных эфиров альфа-гидроксикарбоновых кислот с высокой степенью селективности путем алкоголиза соответствующего альфа-гидроксикарбоксамида в газовой фазе над гетерогенным катализатором, где молярное отношение спирта к альфа-гидроксикарбоксамиду составляет 2-25 моль/моль, и превращение осуществляют в присутствии 0,01-10 моль/моль воды относительно альфа-гидроксикарбоксамида. 4 з.п. ф-лы, 5 табл., 19 пр.
1. Способ получения сложных эфиров альфа-гидроксикарбоновых кислот путем алкоголиза соответствующего альфа-гидроксикарбоксамида в газовой фазе над гетерогенным катализатором, отличающийся тем, что молярное отношение спирта к альфа-гидроксикарбоксамиду составляет 2-25 моль/моль, и превращение осуществляют в присутствии 0,01-10 моль/моль воды относительно альфа-гидроксикарбоксамида.
2. Способ по п. 1, отличающийся тем, что реакцию осуществляют в присутствии катализатора на основе диоксида циркония.
3. Способ по любому из предыдущих пунктов, отличающийся тем, что температура реакции составляет 150-300°С.
4. Способ по любому из предыдущих пунктов, отличающийся тем, что реагенты перед выпариванием обрабатывают с помощью катионообменника.
5. Способ по любому из предыдущих пунктов, отличающийся тем, что применяемый альфа-гидроксикарбоксамид представляет собой гидроксиизобутирамид, и применяемый спирт представляет собой метанол.
| СПОСОБ И УСТРОЙСТВО ДЛЯ ИЗГОТОВЛЕНИЯ ПРЕФОРМЫ | 2007 |
|
RU2415750C2 |
| RU 2009105882 A, 27.08.2010 | |||
| US 4161609 A, 17.07.1979. | |||
Авторы
Даты
2019-05-16—Публикация
2015-07-23—Подача