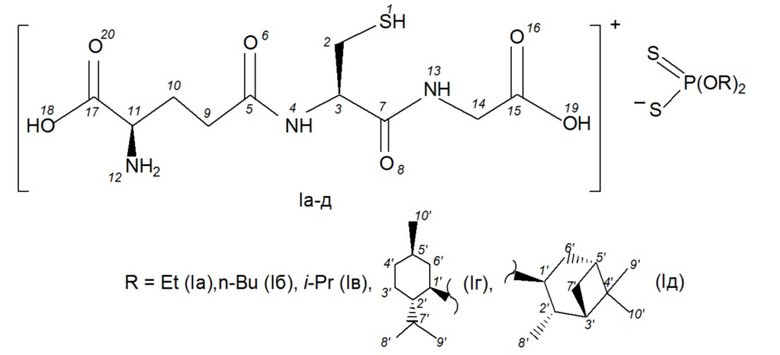
Изобретение относится к химии фосфорорганических соединений, а именно, к глутатионаммониевым солям O,O-диорганилдитиофосфорных кислот общей формулы (Iа-д), обладающим антиоксидантной и противоопухолевой активностью.
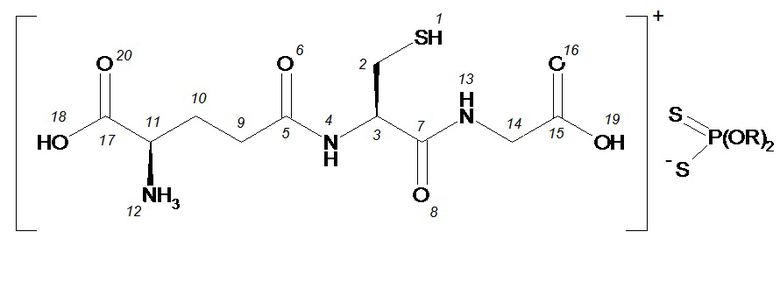
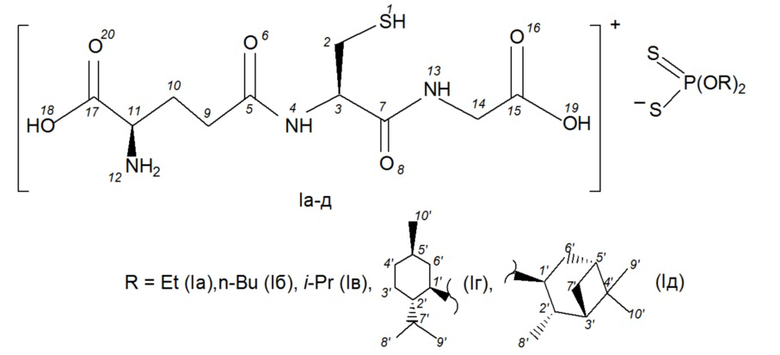
Изобретение может быть использовано в различных областях медицины, ветеринарии и фармацевтики, например, для создания лекарственных средств, используемых для лечения опухолевых, инфекционных и дегенеративных заболеваний.
Из исследованного заявителем уровня техники известно, что глутатион (2-амино-5-{[2-[(карбоксиметил)амино]-1-(меркаптометил)-2-оксоэтил]амино}-5-оксопентаноевая кислота) - представляет собой трипептид гамма-глутамилцистеинилглицин. Значение глутатиона в живых организмах определяется его антиоксидантными свойствами. Глутатион не только защищает клетку от токсичных свободных радикалов, но и определяет окислительно-восстановительные характеристики внутриклеточной среды [Lucente, G. Design and synthesis of glutathione analogues (Разработка и синтез аналогов глутатиона) / G. Lucente, G. Luisi, F. Pinnen // Farmaco. - 1998. - V. 53. - P. 721-735]. [информация общего характера о глутатионе размещена на сайте http://mir-herb.ru/poleznye-stati/glutation-biologicheskaya-rol-polza-dlya-organizma.html].
Из уровня техники известно, что глутатион защищает клетки и ткани живых организмов от воздействия токсикантов и свободных радикалов [Estrela, J.M. Glutathione in cancer biology and therapy (Глутатион в области биологии и терапии рака) / J.M. Estrela, A. Ortega, Е. Obrador // Crit. Rev. Clin. Lab. Sci. - 2006. - V. 43. - P. 143-181], и способен оказывать лечебный эффект при почечной дисфункции и нефротоксичности, болезнях Паркинсона и Альцгеймера, заболевании печени и легких, опухолевых болезнях, аллергии и СПИДе [Lomaestro, В.М. Glutathione in health and disease: pharmacotherapeutic issues (Глутатион в области здоровья и болезней: фармакотерапевтические проблемы) // В.М. Lomaestro, М. Malone // Ann. Pharmacother. - 1995. - V. 29. - P. 1263-1273].
При этом глутатион обладает недостатками при его использовании по назначению в качестве лекарственного средства, а именно, обладает плохими фармакокинетическими свойствами, к их числу относятся:
- низкая стабильность, т.е. быстрая деградация в результате химических и ферментативных реакций;
- низкой способностью проникать через биологические барьеры, такие как клеточные мембраны и живые ткани, т.е. обладает плохими транспортными свойствами [Fraternale, A. GSH and analogs in antiviral therapy (GSH и аналоги в противовирусной терапии) // A. Fraternale, M.F. Paoletti, A. Casabianca, L. Nencioni, E. Garaci, A.T. Palamara, M. Magnani // Mol. Aspects Med. - 2009. - V. 30. - P. 99-110].
Указанные выше недостатки снижают эффективность использования глутатиона в качестве лекарственного средства при пероральном и парентеральном применении.
Из исследованного уровня техники заявителем выявлено, что, в отличие от самого глутатиона его химические производные обладают улучшенными фармакокинетическими свойствами, среди них производные S-ацилглутатиона, используемые против индуцированного амилоидом окислительного стресса и связанной с ним болезни Альцгеймера [A. Pensalfini, С.Cecchi, М. Zampagni, М. Becatti, F. Favilli, P. Paoli, S. Catarzi, S. Bagnoli, B. Nacmias, S. Sorbi, G. Liguri. Protective effect of new S-acylglutathione derivatives against amyloid-induced oxidative stress // Free Rad. Biol. Med. - 2008. - V. 44. - P. 1624-1636; M. Zampagni, D. Wright, R. Cascella, G.  , F. Casamenti, E. Evangelisti, F. Cardona, A. Goti, B. Nacmias, S. Sorbi, G. Liguri, C. Cecchi. Novel S-acyl glutathione derivatives prevent amyloid oxidative stress and cholinergic dysfunction in Alzheimer disease models // Free Rad. Biol. Med. - 2012. - V. 52. - P. 1362-1371].
, F. Casamenti, E. Evangelisti, F. Cardona, A. Goti, B. Nacmias, S. Sorbi, G. Liguri, C. Cecchi. Novel S-acyl glutathione derivatives prevent amyloid oxidative stress and cholinergic dysfunction in Alzheimer disease models // Free Rad. Biol. Med. - 2012. - V. 52. - P. 1362-1371].
Химические производные глутатиона обладают противоопухолевой активностью за счет ингибирования свободных радикалов, участвующих в развитии опухолевых заболеваний, инактивации глутатион-зависимых ферментов, отвечающих за повышение устойчивости опухолевых клеток к химиотерапии [Burg, D. Glutathione conjugates and their synthetic derivatives as inhibitors of glutathione-dependent enzymes involved in cancer and drug resistance // D. Burg, G.J. Mulder // Drug Metabol. Rev. - 2002. - V. 34 - P. 821-863].
Из исследованного уровня техники заявителем выявлены технические решения, предназначенные для улучшения фармакокинетических свойств глутатиона и создания на его основе производных глутатиона и лекарственных средств.
В группе изобретений по патенту US 6627732 «Производные глутатиона и лекарственные средства на его основе» «Glutathione derivatives and their dosage forms», сущностью по первому пункту является состав - S-бензильные и сложноэфирные по фенилглициновому фрагменту производные глутатиона общей формулы 1 и их композиции с фармацевтическими носителями, где А - Н или С1-С20 ацильная группа, R1 -С1-С26 алкильная группа, R2 - Н, С1-С26 алкильная группа или С3-С26 алкильная группа.
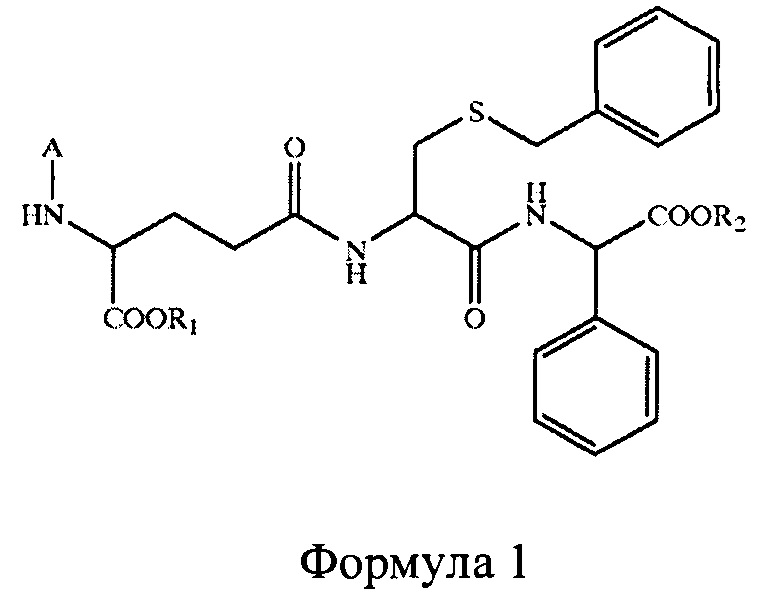
Сущностью изобретения являются производные глутатиона и их лекарственные формы, которые обеспечивают эффективную экспрессию промотирующей гематопоэз активности в месте действия костного мозга, когда они вводятся в живой организм с целью стимулирования гемопоэза. При этом происходит увеличение стабильности in vivo, не влияя на биологическую активность гамма-глутамил-S-бензил-цистеинил-R-(-)-фенилглицина общей формулы 1, содержащего длинноцепочечный алкильный или алкениловый эфирный заместители с 12 атомами углерода или более, а также придается структура, которая способна распределяться в костном мозге. Недостатком известного изобретения является наличие неполярных ковалентных связей в эфирных производных глутатиона, что ухудшает их проходимость через биологические мембраны и снижает их биологическую активность.
В изобретении по патенту US 7029695 «Терапевтические композиции, содержащие аналоги глутатиона» «Therapeutic compositions containing glutathione analogs», сущностью является получение диэтиловых эфиров гамма-глютамил-S-бенилцистенил-R-фенилглицина общей формулы 2, обладающих гепатопротекторными свойствами, где R1 и R2 - С1-С25 линейные или разветвленные алкильные группы, R3 - алкильная или бензильная группы.
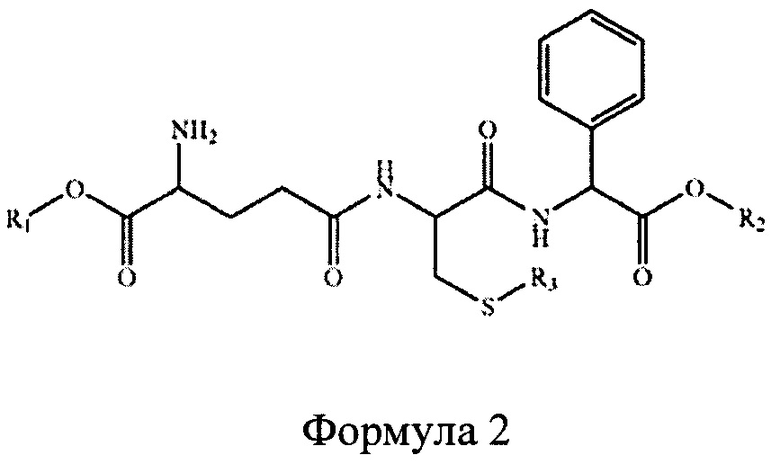
Недостатком известного изобретения является наличие сложноэфирных групп вместо карбоксильных групп, что придает этим соединениям неполярный характер и пониженную проницаемость через биологические мембраны. Кроме того, наличие S-алкильной группы вместо свободной сульфгидрильной группы цистеинового фрагмента, которая могла бы связывать свободные радикалы, делает невозможным использовать эти соединения в качестве противоопухолевых препаратов.
Из исследованного уровня техники выявлена группа изобретений, представленная в патенте РФ 2043994 «Глутатионалкиловые эфиры окисленного типа и способ их получения», сущностью которой является глутатионалкиловые эфиры окисленного типа общей формулы 3, где R - низший алкил.
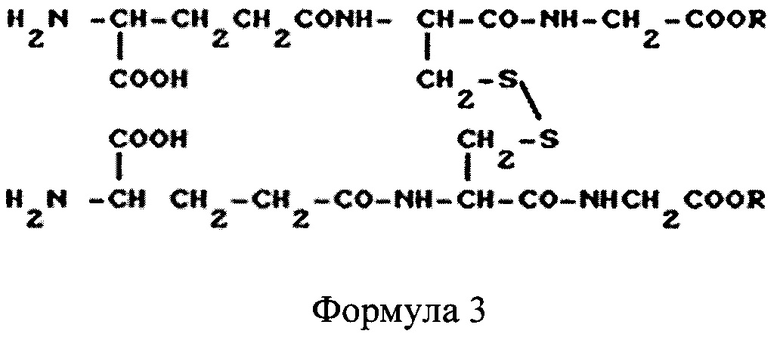
Эти соединения представляют собой димерные дисульфидные формы моноалкиловых эфиров глутатиона, обладающие гепатопротекторной активностью. Недостатком известного изобретения является наличие в их молекулах дисульфидного мостика сера-сера и отсутствие свободных сульфгидрильных групп, что исключает проявление антиоксидантной активности.
Из исследованного уровня техники выявлена группа изобретений по патенту US 5646177 «Глутатионовые производные антрациклинов» «Glutathione derivatives of anthracyclines», сущностью которой являются антрациклиновые S-эфиры глутатиона общей формулы 4, которые используются для ингибирования роста болезнетворных микроорганизмов.
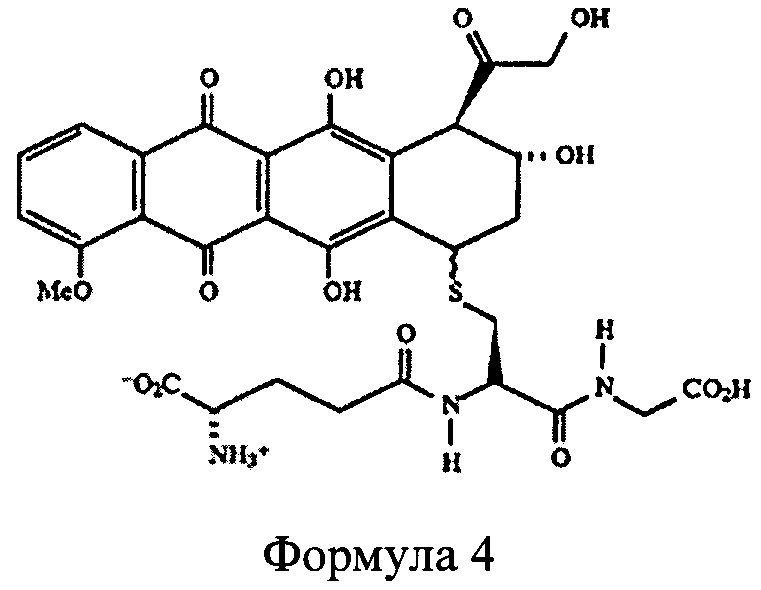
Недостатками известного изобретения является отсутствие свободной сульфгидрильной группы в соединениях общей формулы 4, необходимость применения многостадийных способов синтеза и очистки целевых продуктов.
Сопоставительный анализ исследованного заявителем уровня техники позволяет рассматривать вышеуказанные изобретения в качестве аналогов по назначению, при этом заявителем не выявлены технические решения, совпадающие с заявленным техническим решением по составу, вследствие чего заявителем не выбран наиболее близкий аналог, который мог бы быть выбран в качестве прототипа, поскольку сущностью известных, описанных выше изобретений являются ковалентносвязанные производные глутатиона, тогда как сущностью заявленного технического решения являются глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот, т.е. производные глутатиона, обладающие ионной (солевой, нековалентной) структурой.
В патентной и научной литературе заявителем не выявлены сведения о получении и свойствах солевых производных O,O-диорганилдитиофосфорных кислот на основе глутатиона, что позволяет сделать вывод о том, что глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот являются новым классом соединений, обладают высокой биологической и фармакологической активностью.
В связи с этим целью и техническим результатом заявленного технического решения являются новые производные глутатиона с O,O-диорганилдитиофосфорными кислотами, обладающие солевой структурой, преодолевающие недостатки ковалентносвязанных аналогов, которые (производные глутатиона) могут быть использованы для получения лекарственных средств, обладающих антиоксидантной и противоопухолевой активностью.
Заявленное техническое решение иллюстрируется Фиг. 1 и Фиг. 2.
На Фиг. 1 представлена Таблица 1, в которой представлены данные об усиленных антиоксидантных свойствах глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот - полумаксимальные эффективные концентрации (ЕС50, μM) глутатиона и глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот по данным DPPH-теста;
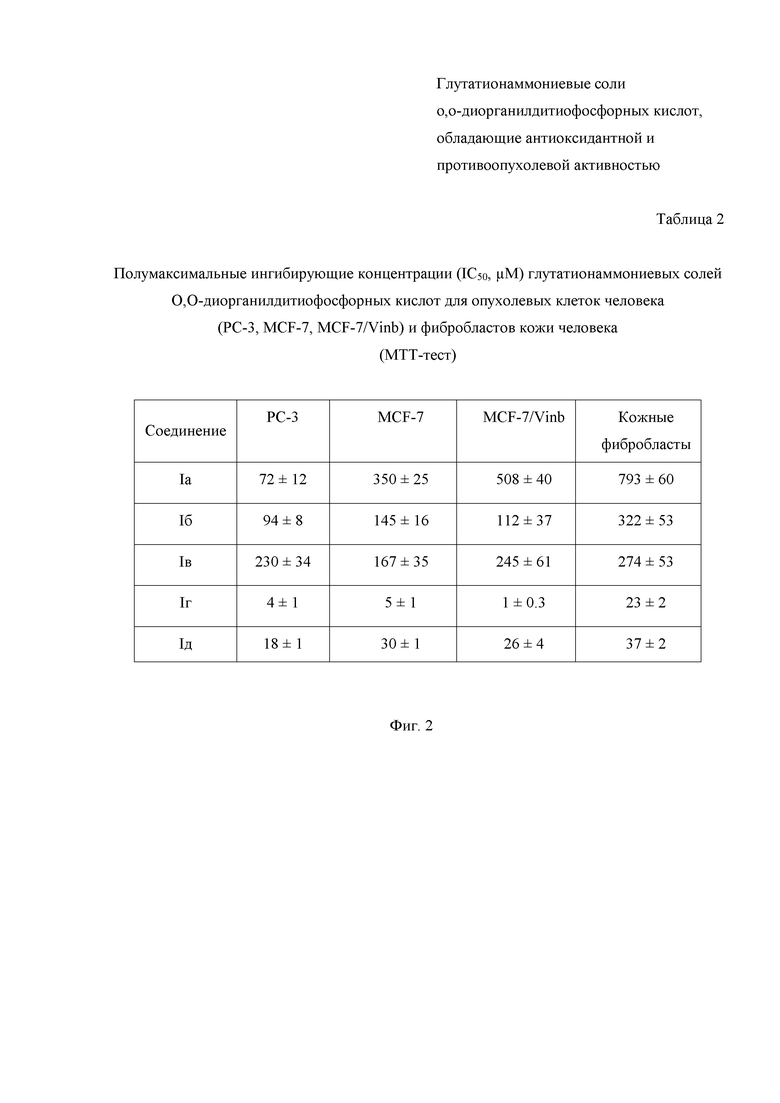
На Фиг. 2 представлена Таблица 2, в которой представлены данные о противоопухолевых свойствах глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот в отношении опухолевых клеток человека и условно нормальных клеток (фибробластов кожи человека) - полумаксимальные ингибирующие концентрации (IC50, μМ) глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот для опухолевых клеток человека (РС-3, MCF-7, MCF-7/Vinb) и условно нормальных клеток (фибробластов кожи человека) (МТТ-тест).
Таким образом, сущностью предлагаемого изобретения является получение биологически активных производных глутатиона в виде солей, в которых глутатион преобразуется в аммониевый катион, а анионом является O,O-диорганилдитиофосфат-анион, на основе которых ожидается создание лекарственных средств для лечения опухолевых, инфекционных и дегенеративных заболеваний.
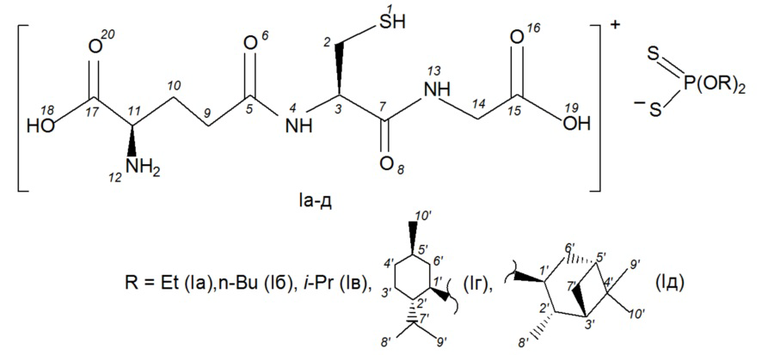
O,O-Диорганилдитиофосфорные кислоты содержат различные органильные группы, такие как О-алкильные или О-терпенильные группы, которые усиливают транспорт производных глутатиона через клеточные мембраны. Терпенильные группы наряду с усилением транспорта обладают дополнительными полезными видами фармакологической активности, такими как антиоксидантная, противовоспалительная и обезболивающая активность [ da Silveira е
da Silveira е  , R. A Review on anti-inflammatory activity of monoterpenes (Обзор противовоспалительной активности монотерпенов) / R. de
, R. A Review on anti-inflammatory activity of monoterpenes (Обзор противовоспалительной активности монотерпенов) / R. de  da Silveira e Sa, N.L. Andrade, P.D. de Sousa // Molecules. - 2013. - V. 18. - P. 1227-1254; Gonzalez-Burgos, E. Terpene compounds in nature: A review of their potential antioxidant activity (Терпеновые соединения в природе: обзор их потенциальной антиоксидантной активности) / Е. Gonzalez-Burgos, М.Р. Gomez-Serranillos // Curr. Med. Chem. - 2012. V. 19. - P. 5319-5341].
da Silveira e Sa, N.L. Andrade, P.D. de Sousa // Molecules. - 2013. - V. 18. - P. 1227-1254; Gonzalez-Burgos, E. Terpene compounds in nature: A review of their potential antioxidant activity (Терпеновые соединения в природе: обзор их потенциальной антиоксидантной активности) / Е. Gonzalez-Burgos, М.Р. Gomez-Serranillos // Curr. Med. Chem. - 2012. V. 19. - P. 5319-5341].
Заявленные производные глутатиона получают одностадийной обработкой глутатиона O,O-диорганилдитиофосфорными кислотами в органическом растворителе в мягких условиях, т.е. при нормальном давлении, умеренном нагревании (например, при 50°С) и коротком времени реакции (например, 1.5-2 ч), что предотвращает нежелательные побочные превращения глутатиона, такие как окисление, полимеризация и рацемизация. Образование глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот происходит путем квартенизации атома азота глутатиона за счет миграции протона сульфгидрильной группы дитиофосфорной кислоты и не сопровождается изменением скелетной структуры глутатиона. Предложенный способ характеризуется высоким выходом целевых продуктов (83-88%). При растворении заявленные производные глутатиона в водных растворах обладают повышенной биологической активностью по сравнению с глутатионом. Полученные по предлагаемому изобретению глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот заявляются в качестве соединений, обладающих антиоксидантной и противоопухолевой активностью.
Чистота полученных соединений и полнота протекания реакций подтверждены данными ЯМР 31Р, 1Н, 13С, ИК спектроскопии, масс-спектрометрии электрораспылительной ионизации, поляриметрии и данными элементного анализа.
Изобретение иллюстрируется следующими примерами.
Пример 1. Получение глутатионаммониевой соли O,O-диэтилдитиофосфорной кислоты (Iа)
К раствору 0.15 г (0.81 ммоль) O,O-диэтилдитиофосфорной кислоты в 10 мл безводного этанола при 20°С при перемешивании в токе сухого аргона прибавляют порциями 0.25 г (0.81 ммоль) глутатиона. Смесь перемешивают в течение 1.5 ч при 50°С. Образовавшийся осадок отфильтровывают. Фильтрат вакуумируют в течение 1 ч при 40°С в вакууме 0.5 мм рт.ст. и при 0.02 мм рт.ст. при 40°С в течение 1 ч. Получено 0.34 г (85%) глутатионаммониевой соли O,O-диэтилдитиофосфорной кислоты (Iа), [α]20D -4.5° (с 1.1, ацетон). ИК спектр (жидкая пленка, ν, см-1): 3336 о. с. о. ш [ν(NH3+)], 2978 с, 2937 с [νas,s(CH3, СН2)], 2635 сл [ν(S-H)], 1735 о. с [ν(O=C-O)], 1659 о. с [ν (NHC=O, амид I)], 1536 ср [ν(CNH, амид II)], 1444 ср [δasCH3)], 1388 с [δs(CH3)], 1028 о. с {ν[(P)O-C]}, 936 с [ν(OC-C), О-С], 678 с [ν(P=S)], 572 ср [ν(P-S)]. Спектр ЯМР 1Н (ацетон-d6, δ, м.д., J, Гц): 1.22 д (6Н, СН3СН2О, 3JHH 7.1), 1.91 м (2Н, С10Н2), 2.22 м (2Н, С10Н2), 2.42 т (2Н, СН2С9Н2С=O, 3JHH 7.8), 2.43 т (2Н, СН2С9Н2С=O, 3JHH 7.8), 2.87-2.93 м (2Н, HSC2H2CH), 2.95 с (2Н, С14Н2СООН), 2.96 с (2Н, C14H2COOH), 3.74 м (С11НСН2), 4.14 д. к (4Н, CH3CH2OP, 3JHH 6.2, 3JPH 14.4), 4.64 м (1H, С3НСН2). Спектр ЯМР 31Р-{1Н} (этанол), δР, м.д.: 112.0. Найдено, %: С 33.78; Н 6.03; N 8.24; Р 5.91; S 19.78. C14H28N3O8PS3. Вычислено, %: С 34.07; Н 5.72; N 8.51; Р 6.28; S 19.49.
Пример 2. Получение глутатионаммониевой соли O,O-дибутилдитиофосфорной кислоты (16)
К раствору 0.2 г (0.7 ммоль) глутатиона в 5 мл безводного этанола при 20°С при перемешивании в токе сухого аргона прибавляют по каплям 0.16 г (0.7 ммоль) O,O-дибутилдитиофосфорной кислоты. Смесь нагревают в течение 1.5 ч при 50°С, выдерживают 12 ч и фильтруют. Фильтрат выпаривают при 40°С в течение 1 ч в вакууме (0.5 мм рт.ст.) и 1 ч при 0.02 мм рт.ст. В остатке получено 0.3 г (83%) глутатионаммониевой соли O,O-дибутилдитиофосфорной кислоты (Iб), [α]20D-3.5° (с 1.10, ацетон). ИК спектр (жидкая пленка, ν, см-1): 3333 о. с. о. ш [ν(NH3+)], 2958 с, 2876 с [νas,s(CH3, СН2)], 2637 сл [ν(S-H)], 1736 с [ν(O=C-O)], 1656 с [ν (NHC=O, амид I)], 1536 с [ν(CNH, амид II)], 1461 ср [δas(CH3)], 1380 ср [δs(CH3)], 1030 ср {ν[(P)O-C]}, 971 с [ν(OC-С), О-С], 677 с [ν(P=S)], 561 ср [ν(P-S)]. Спектр ЯМР 1Н (ацетон-d6, δ, м.д., J, Гц): 0.93 т (12Н, CH3CH2CH2CH2O, 3JHH 7.4), 1.42 т.к (4Н, СН3СН2СН2СН2О, 3JHH 7.4), 1.60 т. т (4Н, CH3CH2CH2CH2O, 3JHH 6.5), 1.91 м (2Н, НСС10Н2СН2), 2.22 м (2Н, С10Н2), 2.43 м (2Н, СН2С9Н2С=O), 2.89-2.98 м (2Н, HSC2H2CH), 2.95 с (2Н, С14Н2СООН), 2.96 с (2Н, С14Н2СООН), 3.74 м (1Н, С11НСН2), 4.13 д. к (4Н, СН3СН2ОР, 3JHH 6.5 Hz, 3JPH 10.9 Hz), 4.64 м (1Н, С3НСН2). Спектр ЯМР 31Р-{1Н} (этанол), δP, м.д.: 112.2. Масс-спектр электрораспылительной ионизации, ацетон, m/z: 591.0 [М+K+Н]+. Найдено, %: С 32.98; Н 6.87; N 7.87; Р 5.35; S 17.89. C18H36NO8PS3. Вычислено, %: С 33.33; Н 6.60; N 7.64; Р 5.64; S 17.50. М 549.7.
Пример 3. Получение глутатионаммониевой соли О.О-диизопропилдитио-фосфорной кислоты (Iв)
К раствору 0.2 г (0.65 ммоль) глутатиона в 5 мл безводного этанола при 20°С при перемешивании в токе сухого аргона прибавляют по каплям 0.14 г (0.65 ммоль) O,O-диизопропилдитиофосфорной кислоты. Смесь нагревают 1.5 ч при 50°С. Смесь выдерживают 12 ч и фильтруют. Фильтрат вакуумируют при 40°С 11 ч (0.5 мм рт.ст.) и 1 ч при 0.02 мм рт.ст. В остатке получено 0.3 г (88%) глутатионаммониевой соли O,O-диизопропилдитиофосфорной кислоты (Iв), [α]20D+0.4° (с 1.10, бензол). ИК спектр (жидкая пленка, ν, см-1): 3318 с [ν(NH3+)], 2976 о.с, 2935 с [νas,s(СH3, СН2)], 2637 сл [ν(S-Н)], 1735 с [ν(O=C-O)], 1658 с [ν (NHC=O, амид I)], 1538 с [ν (CNH, амид II)], 1413 ср [δas(СН3)], 1383 ср, 1373 ср [δs(CH3)2C гем.], 1040 с {ν[(P)O-C]}, 963 с [ν(OC-C), О-С], 669 с [ν(P=S)], 557 ср [ν(P-S)]. Спектр ЯМР 1Н (ацетон-d6, δ, м.д., J, Гц): 1.26 т [12Н, (СН3)2СН, 3JHH 6.2], 1.91 м (2Н, С10Н2), 2.22 м (2Н, НСС10Н2СН2), 2.43 м (2Н, СН2С9Н2С=O), 2.87-2.93 м (2Н, HSC2H2CH), 2.97 с (2Н, С14Н2СООН), 2.98 с (2Н, С14Н2СООН), 3.74 м (1Н, С11НСН2), 4.13 д. т (2Н, CHOP, 3JHH 6.2, 3JPH 10.9), 4.64 м (1H, C3HCH2). Спектр ЯМР 31P-{1H} (этанол), δР, м.д.: 108.0. Масс-спектр электрораспылительной ионизации, ацетон, m/z: 565.0 [М+K+Н]+. Найдено, %: С 32.55; Н 5.87; N 8.39; Р 6.19; S 18.76. C16H32N3O8PS3. Вычислено, %: С 36.84; Н 6.18; N 8.06; Р 5.94; S 18.44. М 521.6.
Пример 4. Получение глутатионаммониевой соли O,O-ди-(-)-(1R,2S,5R)-2-изо-пропил-5-метилциклогекс-1-илдитиофосфорной кислоты (Iг)
К раствору 0.2 г (0.65 ммоль) глутатиона в 10 мл безводного этанола при 20°С при перемешивании в токе сухого аргона прибавляют по каплям 0.26 г (0.64 ммоль) O,O-ди-(-)-(1R,2S,5R)-2-изопропил-5-метилциклогекс-1-илдитиофосфорной кислоты, полученной из (S)-(-)-ментола. Смесь нагревают 2 ч при 20°С, выдерживают 12 ч и фильтруют. Фильтрат вакуумируют при 40°С 1 ч (0.5 мм рт.ст.) и 1 ч при 0.02 мм рт.ст. В остатке получено 0.4 г (87%) глутатионаммониевой соли O,O-ди-(-)-(1R,2S,5R)-2-изопропил-5-метилциклогекс-1-илдитиофосфорной кислоты (Iг), [α]20D+25.5° (с 0.99, этанол). ИК спектр (жидкая пленка, ν, см-1): 3355 с [ν(NH3+)], 2955 о. с, 2930 с, 2870 с [νas,s(CH3, СН2)], 2600 сл [ν(S-H)], 1730 с [ν(O=C-O)], 1653 с [ν (NHC=O, амид I)], 1538 с [ν (CNH, амид II)], 1454 с [δas(CH3)], 1387 ср, 1370 ср [δs(CH3)2C гем.], 1044 с {ν[(P)O-C]}, 959 с [ν(OC-С), О-С], 670 с [ν(P=S)], 550 ср [ν(P-S)]. Спектр ЯМР 1Н (ацетон-d6, 5, м.д., J, Гц): 0.66 д (6Н, С10'Н3СН, 3JHH 6.9); 0.75 д [12Н, (С8',9'H3)2СН, 3JHH 6.6]; 0.76 д [12Н, (С8',9'Н3)2СН, 3JHH 6.1]; 0.99 м (2Н, С2'Н); 1.26 м [2Н, (СН3)2С7'Н]; 1.42 м (2Н, СН3С5'Н); 1-52 м (4Н, С3'Н2); 2.14 д.т (2Н, НСС10Н2СН2, 3JHH 7.1 Hz, 3JHH 6.9), 3.19 м (2Н, HSC2H2CH), 3.42 с (2Н, С14Н2СООН), 3.60 м (1Н, С11НСН2), 3.99 м (2Н, РОС1Н), 4.34 м (1H, С3НСН2). Спектр ЯМР 31Р-{1Н} (этанол), δP, м.д.: 105.8. Найдено, %: С 50.76; Н 8.23; N 6.16; Р 4.65; S 13.76. C30H56N3O8PS3. Вычислено, %: С 50.47; Н 7.91; N 5.89; Р 4.34; S 13.47.
Пример 5. Получение глутатионаммониевой соли O,O-ди(1S,2S,3S,5R)-(+)-2,6,6-триметилбицикло[3.1.1]гепт-3-илдитиофосфорной кислоты (Iд)
К раствору 0.2 г (0.65 ммоль) глутатиона в 10 мл безводного этанола при 20°С при перемешивании в токе сухого аргона прибавляют по каплям 0.26 г (0.65 ммоль) O,O-ди(1S,2S,3S,5R)-(+)-2,6,6-триметилбицикло[3.1.1]гепт-3-илдитиофосфорной кислоты, полученной из (1S,2S,3S,5R)-(+)-изопинокамфеола. Смесь нагревают 1.5 ч при 50°С, выдерживают 12 ч и фильтруют. Фильтрат вакуумируют при 40°С 1 ч (0.5 мм рт. ст.) и 1 ч при 0.02 мм рт.ст. В остатке получено 0.4 г (87%) глутатионаммониевой соли O,O-ди(1S,2S,3S,5R)-(+)-2,6,6-триметилбицикло[3.1.1]гепт-3-илдитиофосфорной кислоты (Iд).
Синтезированные глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот прошли испытания на антиоксидантную и противоопухолевую активность.
Пример 6. Антиоксидантные свойства глутатионаммониевых солей О,О-диорганилдитиофосфорных кислот
Антиоксидантные свойства глутатиона и глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот (Ia-д) оценивали по их способности связывать хромогенный DPPH-радикал (2,2-дифенил-1-пикрилгидразил). Исходный раствор DPPH растворяют в метаноле в концентрации 4 мМ. Реакционный раствор содержит DPPH в конечной концентрации 250 мкМ и исследуемое соединение в серийных разведениях в диапазоне концентраций от 60 нМ до 2.5 мМ в фосфатно-солевом буфере (ФСБ). Смесь выдерживают в течение 60 мин при 20°С. Оптическое поглощение раствора измеряли на 96-луночном планшете при длине волны 515 нм на микропланшетном анализаторе Infinite М200 PRO (TECAN). Антиоксидантную способность соединений определяли по уменьшению величины оптического поглощения. Для этого строили сигмоидальные зависимости оптического поглощения от концентрации соединения относительно контрольного раствора без антиоксиданта (100%) и вычисляли полумаксимальные эффективные (ингибирующие) концентрации (ЕС50) с использованием программного обеспечения OriginPro 8.0 (Таблица 1 на Фиг. 1).
По данным DPPH-теста глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот (Iа-д) обладают более низкими значениями ЕС50 - от 18 до 186 мкМ по сравнению с глутатионом (ЕС50 248 мкМ). Это показывает, что заявленные производные глутатиона обладают значительно более высокой антиоксидантной способностью, проявляющейся в связывании свободных радикалов.
Пример 7. Противоопухолевые свойства глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот
Цитотоксичность глутатиона и глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот (Ia-д) для различных клеток человека исследовали с помощью стандартного МТТ-теста. Опухолевые клетки человека (рака груди MCF-7, рака простаты РС-3, устойчивые к винбластину клетки рака груди MCF-7/Vinb), а также условно нормальные фибробласты кожи человека культивируют в питательной среде DMEM в стандартных асептических условиях в 96-ти луночном планшете. Стерильные серийно разбавленные растворы соединений (60 нМ - 2.5 мМ) вносят в питательную среду к клеткам, которые далее культивируют в течение 72 ч.
Жизнеспособность клеток выявляют следующим образом:
- добавляют 3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолийбромид - реагент МТТ (0.5 мг/мл) в течение 3 ч;
- растворяют образующийся продукт в ДМСО;
- детектируют оптическое поглощение раствора на микропланшетном анализаторе Infinite М200 PRO (Tecan) при длине волны 555 нм.
Жизнеспособность клеток рассчитывают относительно контрольных клеток, выращенных без испытуемых соединений (жизнеспособность 100%). Влияние соединений на жизнеспособность клеток оценивали по величине полумаксимальной ингибирующей концентрации на пролиферацию клеток (IC50) (Таблица 2 на Фиг. 2).
Установлено, что глутатион не понижает, а наоборот, значительно повышает жизнеспособность опухолевых клеток в широком диапазоне концентраций, например, для клеток MCF-7 до 20%, для клеток РС-3 до 40%, а для резистентных клеток MCF-7/Vinb на 60-100%. Это показывает, что немодифицированный глутатион ускоряет рост опухолей и поэтому не может быть использован при онкологических заболеваниях.
В отличие от этого, глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот существенно ингибируют жизнеспособность опухолевых клеток. Значения IC50 соединений (Iа), (Iб) и (Iв), в которых O,O-диорганилдитиофосфорные кислоты содержат О-алкильные заместители, для опухолевых клеток MCF-7, РС-3 и MCF-7/Vinb составили от 508 до 72 мкМ. В тех же условиях, значения IC50 соединений (Iг) и (Iд), имеющих О-терпенильные заместители, были еще ниже и составили от 30 до 1 мкМ.
Таким образом, модификация глутатиона O,O-диорганилдитиофосфорными кислотами придает значительную противоопухолевую активность, которая особенно выражена при использовании глутатионаммониевых солей O,O-диорганилдитиофосфорных кислот, содержащих О-терпенильные заместители. Наблюдаемая противоопухолевая активность разработанных дитиофосфорильных производных глутатиона объясняется их повышенным проникновением через клеточные мембраны и накоплением внутри опухолевых клеток.
Наибольший эффект проявляет глутатионаммониевая соль дитиофосфорной кислоты (Iг), содержащий (S)-(-)-ментильный заместитель, в отношении опухолевых клеток рака груди, устойчивых к противоопухолевому препарату винбластину (IC50 1 мкМ).
При этом разработанные глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот обладают значительно меньшей цитотоксической активностью (т.е. большими значениями IC50) в отношении фибробластов кожи человека (Фиг. 2), являющихся моделью нормальных клеток. Это показывает, что заявленные соединения обладают избирательным цитотоксическим действием для опухолевых клеток и относительной безопасностью для нормальных клеток, благодаря избирательному накоплению и нарушению окислительно-восстановительного метаболизма в опухолевых клетках.
Заявленное техническое решение позволяет достигнуть поставленные цели и заявленный технический результат, а именно - получить новые глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот, характеризующиеся следующими преимущественными характеристиками:
- нековалентной ионной структурой, не изменяющей скелетную структуру глутатиона, и тем самым уменьшающей вероятность возникновения побочных эффектов при применении заявленных производных глутатиона;
- простым одностадийным способом получения заявленных производных глутатиона в мягких условиях с высокими выходами целевых продуктов;
- повышенной антиоксидантной активностью заявленных производных глутатиона по сравнению с самим глутатионом;
- избирательной цитотоксической активностью заявленных производных глутатиона в отношении опухолевых клеток, в том числе, резистентных к известным цитостатикам.
Заявленное техническое решение соответствует критерию «новизна», предъявляемое к изобретениям, т.к. из исследованного уровня техники не выявлены технические решения, обладающие заявленной совокупностью признаков и полученными техническими результатами.
Заявленное техническое решение соответствует критерию «изобретательский уровень», предъявляемое к изобретениям, так как не является очевидным для специалистов в данной области науки и техники, а в существующем уровне техники специалистам не были известны биологически активные глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот.
Заявленное техническое решение соответствует критерию «промышленная применимость», предъявляемое к изобретениям, т.к. заявленное техническое решение может быть реализовано в специализированных химических и фармацевтических предприятиях с применением известных материалов и технологического оборудования.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДЛИННОЦЕПНЫХ S-АЛКИЛОВЫХ ЭФИРОВ О, О-ДИАЛКИЛДИТИОФОСФОРНЫХ КИСЛОТ, ОБЛАДАЮЩИХ АНТИКОРРОЗИОННОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2337913C1 |
| Производные пиридоксина и ацетона с противоопухолевой активностью | 2017 |
|
RU2639879C1 |
| 7-ТРИАЗОЛИЛ-ЗАМЕЩЕННЫЕ ГИДРОКСИСПИРОСТАНЫ, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ ОПУХОЛЕВЫХ КЛЕТОК ЧЕЛОВЕКА | 2023 |
|
RU2798105C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИЙ ПОЛИЭФИРОВ АРИЛДИТИОФОСФОНОВЫХ КИСЛОТ И ИХ АММОНИЕВЫХ СОЛЕЙ ИЗ ГИПЕРРАЗВЕТВЛЕННЫХ ПОЛИЭФИРПОЛИОЛОВ, КОМПОЗИЦИИ ПОЛИЭФИРОВ АРИЛДИТИОФОСФОНОВЫХ КИСЛОТ И ИХ АММОНИЕВЫЕ СОЛИ, ОБЛАДАЮЩИЕ АНТИКОРРОЗИОННОЙ АКТИВНОСТЬЮ | 2009 |
|
RU2427584C2 |
| Фосфониевые соли на основе бетулиновой кислоты, обладающие цитотоксической активностью в отношении аденокарциномы предстательной железы | 2018 |
|
RU2665922C1 |
| Бромсодержащие пространственно-затрудненные фенолы, обладающие противоопухолевой активностью | 2023 |
|
RU2822270C1 |
| Способ получения S-триметилсилиловых эфиров дитио- или тетратиофосфорных кислот | 1990 |
|
SU1735300A1 |
| ФОСФОРСЕРООРГАНИЧЕСКИЙ ИНГИБИТОР КОРРОЗИИ СТАЛИ НА ОСНОВЕ АЛЬФА-ОЛЕФИНОВ ПРОМЫШЛЕННОЙ ФРАКЦИИ C, C | 2011 |
|
RU2449056C1 |
| СПОСОБ ПОЛУЧЕНИЯ S-ТРИАЛКИЛСИЛИЛОВЫХ И СТАННИЛОВЫХ ЭФИРОВ 4-МЕТОКСИФЕНИЛДИТИО- ИЛИ ТРИТИОФОСФОНОВЫХ КИСЛОТ | 1991 |
|
RU2005723C1 |
| Фосфониевые соли на основе салициловой и ацетилсалициловой кислот, обладающие антибактериальной и антиоксидантной активностью" | 2019 |
|
RU2704025C1 |

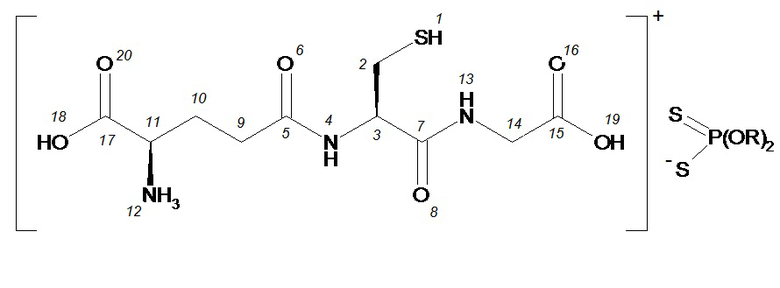
Изобретение относится к глутатионаммониевым солям O,O-диорганилдитиофосфорных кислот общей формулы (Iа-д), обладающим антиоксидантной и противоопухолевой активностью, которые могут быть использованы в медицине, ветеринарии и фармацевтике:
Предложены новые соединения с выраженной противоопухолевой и антиоксидантной активностью. 7 пр., 2 ил.
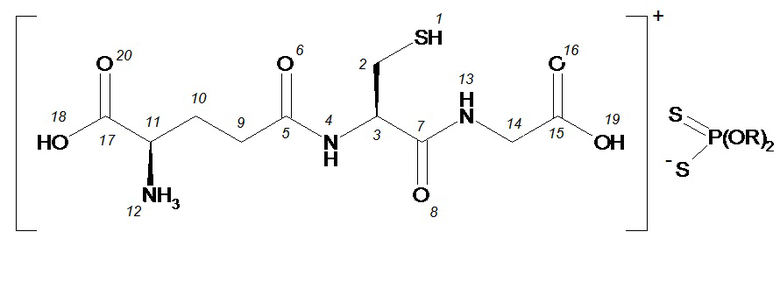
Глутатионаммониевые соли O,O-диорганилдитиофосфорных кислот, обладающие антиоксидантной и противоопухолевой активностью, общей формулы (Iа-д)
| Rezeda A.Akhmadishina et al | |||
| Peptides, Vol | |||
| Прибор, замыкающий сигнальную цепь при повышении температуры | 1918 |
|
SU99A1 |
| Gino Lucente et al | |||
| Il Farmaco, 1998, 53(12), 721-735 | |||
| E | |||
| Gonzalez-Burgos et al | |||
| Current Medicinal Chemistry, 2012, 19(31), 5319-5341 | |||
| ГЛУТАТИОНАЛКИЛОВЫЕ ЭФИРЫ ОКИСЛЕННОГО ТИПА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1991 |
|
RU2043994C1 |
| US 6627732 B1, 30.09.2003 | |||
| US 5646177 A1, 08.07.1997 | |||
| US 7029695 A1, 08.07.1997. | |||
Авторы
Даты
2019-06-20—Публикация
2018-04-05—Подача