Изобретение относится к области органической химии, а именно гетероциклическим азотсодержащим соединениям, являющимся активной основой ингибиторов коррозии газо- и нефтепромыслового оборудования и трубопроводов транспортировки нефти, работающих в высокоминерализованных сероводородсодержащих средах.
Известно применение смеси хлоргидратов аминопарафинов в качестве ингибиторов коррозии оборудования, находящегося в сероводородной среде (А.С. №652315, К1 У21В 43/00, 1979).
Однако недостатком заявленного ингибитора является невысокий защитный эффект при дозировке до 100 мг/л.
Известен также ингибитор коррозии для защиты оборудования в сероводородсодержащих средах, в котором в качестве активной основы -продукт взаимодействия одного моль жирной кислоты с числом углеродных атомов С10-С20 и 0,1-1 моль аминопарафинов с числом атомов углерода С8-С20 в соотношении взаимодействия 10÷50 (А.С. №2061091, кл.6 C23F 11/00,1996).
Недостатками ингибитора коррозии являются недостаточно высокий защитный эффект при дозировке 50 мл/л, а также применение метилового спирта, который имеет низкую температуру кипения и применяется в количестве 80 мл на 10 г активной основы.
Близкими по структуре (прототипами) являются ингибиторы коррозии, содержащие в качестве активной основы смесь модифицированных имидазолинов с альдиминами или основаниями Шиффа (Патент RU 2394941, C23F 11/14, 2010).
Недостатками указанных ингибиторов коррозии является недостаточно высокая эффективность при малых дозировках, ограниченность сырьевой базы.
Изобретение решает задачу расширение ассортимента ингибиторов коррозии, применяемых в высокоминерализованных средах.
Поставленная задача решается тем, что в качестве активной основы ингибиторов коррозии применяются производные несимметричных аминотриазинов общей формулы
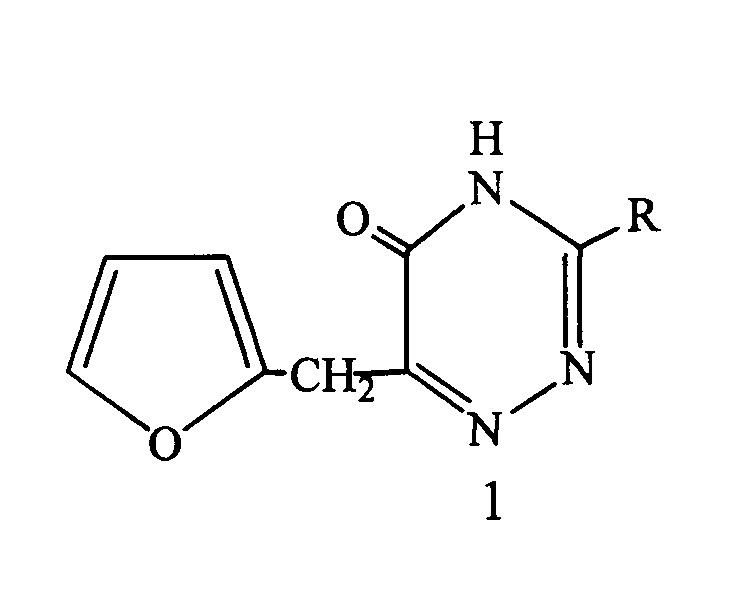
где R - NH-CH2-C2H3O (2), N=CHC6H5 (3), N=HC-C4H3O (4)
Сущность изобретения заключается в создании ингибитора коррозии, содержащего в качестве активной основы аминопроизводные 1,2,4-триазинов, полученные на основе монохлоруксусной кислоты:
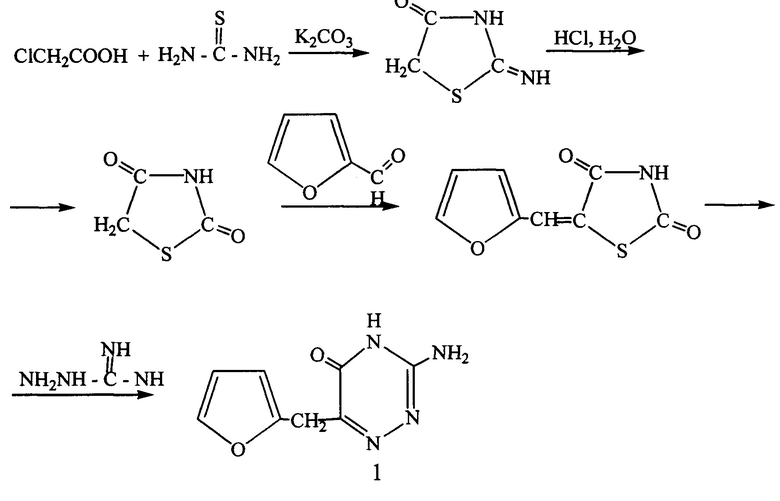
Химические превращения соединения (1):
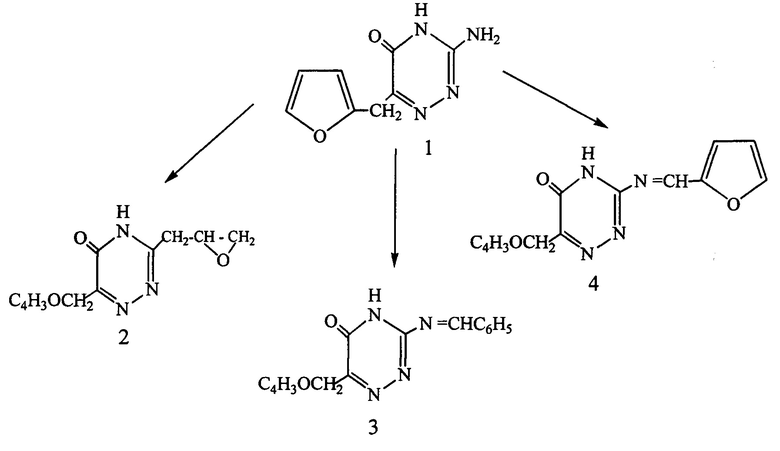
Получение новых соединений иллюстрируется следующими примерами.
Пример 1. Получение 3-амино-6-фурфурил-1,2,4-триазинона-5.
3-Амино-6-фурфурил-1,2,4-триазинон-5 получали в три стадии. На первой стадии в трехгорлую колбу, снабженную механической мешалкой, обратным холодильником и термометром, помещают 3,6 г (0,05 моль) тиомочевины, 6,9 г (0,05 моль) карбоната калия, 10 мл воды и порциями в течение десяти минут при температуре 50-55°С прибавляют 6,6 г (0,05 моль) 20%-ый водный раствор хлорацетата калия. Реакционную массу выдерживают при температуре 80°С в течение 60 минут. Затем выпавший осадок отфильтровывают, промывают гексаном и перекристаллизовывают из спирта. Получают 2-аминотиазолидинон-4 с выходом 92%.
5,8 г (0,05 моль) синтезированного продукта помещают в трехгорлую колбу, снабженную механической мешалкой, обратным холодильником и термометром, добавляют 15 мл 13%-ого раствора соляной кислоты и кипятят шесть часов. Реакционную смесь концентрируют до выпадения первых кристаллов, охлаждают и отфильтровывают полученный продукт. Тиазолидиндион-2,4 экстрагируют диизпропиловым эфиром в аппарате Сокслетта, выход 90%
На второй стадии получают 5-фурфурилидентиазолидиндион-2,4. В трехгорлую колбу, снабженную механической мешалкой, обратным холодильником и термометром загружают 20 мл этанола, 5.85 г (0,05 моль) тиазолидиндина-2,4, 4,2 мл (0,05 моль) фурфурола, пиперидин в количестве 1% от массы тиазолидиндиона-2,4. Реакционную массу выдерживают при температуре 80°С в течение 4 часов. Затем реакционную смесь охлаждают, целевой продукт отфильтровывают, промывают ацетоном, сушат на воздухе и перекристаллизовывают из этилового спирта. Выход продукта 92%.
На третьей стадии проводят конденсацию 5-фурфурилидентиазолидиндиона-2,4 с аминогуанидином. В трехгорлую колбу, снабженную механической мешалкой, обратным холодильником и термометром загружают 46 мл 30%-ого раствора гидроксида калия, 9,75 (0,05 моль) 5-фурфурилидентиазолидиндион-2,4 и 10,9 г (0,08 моль) бикарбоната аминогуанидина. Реакционную массу нагревают при 75°С в течение трех часов. Полученный продукт после охлаждения реакционной смеси отфильтровывают, промывают ацетоном, сушат на воздухе и перекристаллизовывают из этилового спирта.
Физико-химические характеристики 3-амино-6-фурфурил-1,2,4-триазинона-5:
Выход: 80%.
Т. пл. °С: 240-241.
ИК-спектр, см-1: 1630, 1690, 1590.
УФ-спектр, нм: 235.
Масс-спектр, m/z: 232, 189, 172, 60, 43, 28.
Пример 2. Химические превращения 3-амино-6-фурфурил-1,2,4-триазинона-5.
Получение 3-глицидиламино-6-фурфурил-1,2,4-триазинона 5 (2). В колбу загружают 1 г (моль) соединения (1), 3 мл эпихлоргидрина и 1 мл воды. Перемешивают при комнатной температуре в течение 5 часов, затем нагревают с обратным холодильником в течение 2 часов. Реакционную массу охлаждают до комнатной температуры, добавляют 0,2 г (моль) гидроксида натрия в небольшом количестве воды. Смесь перемешивают в течение одного часа, добавляют этиловый спирт и воду до появления мути. Полученный осадок отфильтровывают, промывают спиртом, сушат на воздухе.
Физико-химические характеристики 3-глицидиламино-6-фурфурил-1,2,4-триазинона-5:
Выход: 65%.
Т. пл. °С: 212-213.
ИК-спектр, см-1: 1620, 1650, 1510.
УФ-спектр, нм: 230, 270.
Масс-спектр, m/z: 248, 187, 133, 115, 61.
Получение 3-бензилиденамино-6-фурфурил-1,2.4-триазинона-5 (3) и 3-фурфурилиденамино-6-фурфурил-1,2,4-триазинона-5 (4). В трехгорлую колбу, снабженную механической мешалкой, обратным холодильником и термометром загружают 0,5 моль соединения (1), 0,5 моль соответствующего альдегида, n-толуолсульфокислоту в количестве 1% от массы общей загрузки. Реакционную массу кипятят до прекращения выделения воды, затем ее охлаждают, толуол отгоняют под вакуумом. Полученный продукт промывают диизопропиловым эфиром и сушат на воздухе.
Физико-химические характеристики 3-бензилиденамино-6-фурфурил-1,2,4-триазинона-5:
Выход: 67%.
Т. пл. °С: 230-233.
ИК-спектр, см-1: 1620, 1690, 1590.
УФ-спектр, нм: 236, 290.
Масс-спектр, m/z: 280, 161, 147, 133, 119.
Физико-химические характеристики 3-фурфурилиденамино-6-фурфурил-1,2,4-триазинона-5:
Выход: 69%.
Т. пл. °С: 265-266.
ИК-спектр, см-1: 1700, 1660, 1590.
УФ-спектр, нм: 239, 289.
Масс-спектр, m/z: 270, 161, 137, 109, 103.
Пример 3. Испытания заявленного ингибитора коррозии.
Испытания проводили по программе, приведенной в ГОСТ 9.905-82, двумя методами.
При электрохимическом методе испытания по определению плотности коррозионного тока, соответствующего скорости коррозии, проводили на потенциостате типа ПИ-50-1 в электрохимической ячейке с исследуемым электродом, изготовленного из стали марки Ст20 и хлорсеребряным электродом сравнения, снабженным платиновым вспомогательным электродом при концентрации соединений 100 мг/л в модельной и кислой (рН=3) среде. Плотность коррозионного тока определяли экстраполяцией участка Тафеля до значения потенциала коррозии на поляризационной кривой. Защитный эффект соединений оценивали сравнением плотностей, снятых в неингибированной и ингибированной средах.
При гравиметрическом методе испытания проводили в аппарате с перемешивающим устройством со скоростью течения испытуемой среды 1,0 м/с на образцах, изготовленных из стали марки Ст20.
Результаты опытов представлены в таблице 1. 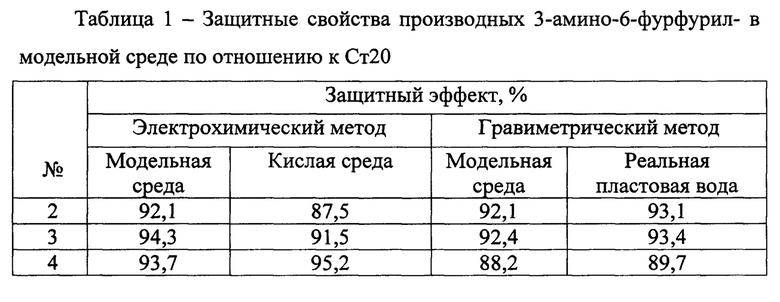
Пример 4.
Ингибитор коррозии получают следующим образом; смесь 10 г активной формы (соединение 2), 5 г неонола марки АФ-9-9 и 85 г растворителя (кубовые остатки бутиловых спиртов) перемешивают при температуре 30-40°С в течение часа (продукт 1).
Пример 5.
Ингибитор коррозии получают следующим образом; смесь 20 г активной формы (соединение 3), 4 г неонола марки АФ-9-10 и 85 г растворителя (кубовые остатки бутиловых спиртов) перемешивают при температуре 40-45°С в течение часа (продукт 2).
Пример 6.
Ингибитор коррозии получают следующим образом; смесь 12 г активной формы (соединение 4), 5 г неонола марки АФ-9-10 и 90 г растворителя (кубовые остатки бутиловых спиртов) перемешивают при температуре 40-45°С в течение часа (продукт 3).
В таблице 2 представлен результаты испытаний продуктов - ингибиторов коррозии на защитную активность Исследования проводили по методике, описанной в примере 3.

Таким образом, заявленные соединения обладают защитной способностью, и полученные результаты свидетельствуют о перспективности использования аминопроизводных несимметричных триазинов в качестве ингибиторов коррозии.
| название | год | авторы | номер документа |
|---|---|---|---|
| Ингибитор коррозии | 2023 |
|
RU2806401C1 |
| ГЕРБИЦИДНОЕ СРЕДСТВО | 2017 |
|
RU2645760C1 |
| Ростстимулирующее средство для предпосевной обработки семян | 2020 |
|
RU2746139C1 |
| ПРОИЗВОДНЫЕ 3-МЕРКАПТО-1,2,4-ТРИАЗИНОНА-5, ОБЛАДАЮЩИЕ РОСТРЕГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1990 |
|
SU1800810A1 |
| РОСТСТИМУЛИРУЮЩЕЕ СРЕДСТВО ДЛЯ ПРЕДПОСЕВНОЙ ОБРАБОТКИ СЕМЯН | 2008 |
|
RU2379891C1 |
| РОСТСТИМУЛИРУЮЩЕЕ СРЕДСТВО ДЛЯ ПРЕДПОСЕВНОЙ ОБРАБОТКИ СЕМЯН | 2012 |
|
RU2507744C1 |
| ПРОИЗВОДНЫЕ 1,2,4-ТРИАЗИНОНОВ, ПРОЯВЛЯЮЩИЕ ГЕРБИЦИДНУЮ АКТИВНОСТЬ | 2021 |
|
RU2766696C1 |
| ИНГИБИТОР КОРРОЗИИ | 2019 |
|
RU2706927C1 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛИЧЕСКИХ ПРОИЗВОДНЫХ ЦЕЛЛЮЛОЗЫ | 1997 |
|
RU2148059C1 |
| АЗОМЕТИНЫ 1,2,4-ТРИАЗИНОНОВ-5, ОБЛАДАЮЩИЕ РОСТРЕГУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 1999 |
|
RU2146252C1 |
Изобретение относится к области защиты металлов от коррозии и может быть использовано для ингибирования коррозии газо- и нефтепромыслового оборудования и трубопроводов транспортировки нефти, работающих в высокоминерализованных сероводородсодержащих средах. Ингибитор коррозии содержит в качестве активной основы производные 3-амино-6-фурфурил-1,2,4-триазинона-5 общей формулы
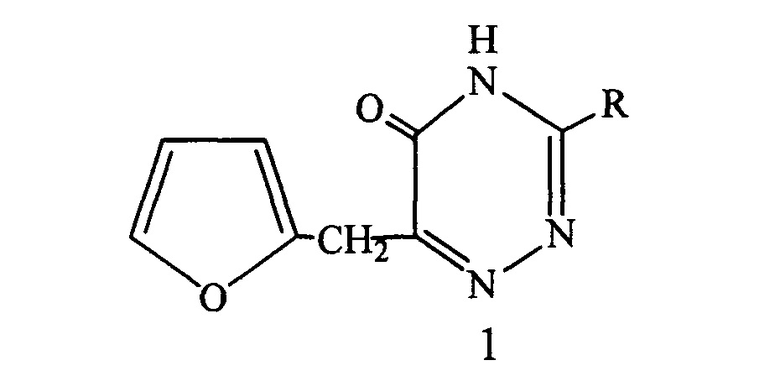 ,
,
где R - NH-CH2-C2H3O (2), N=CHC6H5 (3), N=HC-C4H3O (4). Технический результат: расширение ассортимента ингибиторов коррозии. 2 табл., 6 пр.
Ингибитор коррозии, содержащий в качестве активной основы производные 3-амино-6-фурфурил-1,2,4-триазинона-5 общей формулы
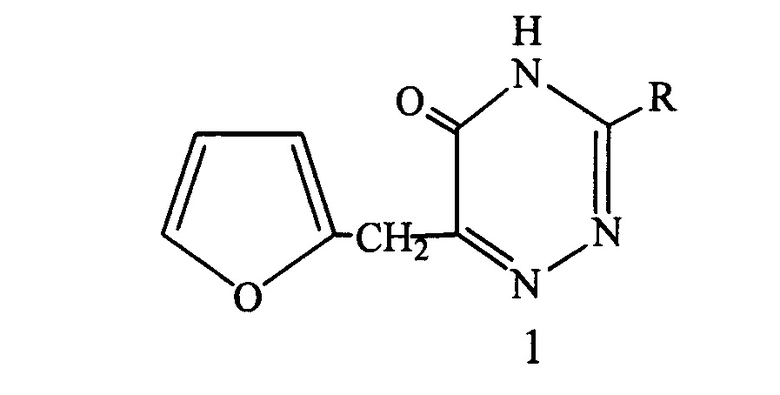 ,
,
где R - NH-CH2-C2H3O (2), N=CHC6H5 (3), N=HC-C4H3O (4)
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРОВ КОРРОЗИИ | 2008 |
|
RU2394941C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНГИБИТОРА КОРРОЗИИ И НАВОДОРАЖИВАНИЯ МЕТАЛЛОВ | 1997 |
|
RU2135483C1 |
| ИНГИБИТОР СЕРОВОДОРОДНОЙ КОРРОЗИИ | 2003 |
|
RU2243292C1 |
| Реагент для предотвращения образования сероводорода в заводняемом нефтяном пласте | 1977 |
|
SU652315A1 |
Авторы
Даты
2019-09-03—Публикация
2018-12-26—Подача