РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает преимущество приоритета по предварительной заявке на патент США №61/977,037, поданной 8 апреля 2014 г., которая включена в настоящий документ посредством ссылки во всей своей полноте.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Fc-рецепторы (FcR) представляют собой белки, обнаруживаемые на поверхности клеток иммунной системы, которые выполняют разнообразные функции иммунной системы у млекопитающих. Существует множество типов FcR, которые присутствуют на различных клетках и опосредуют разнообразные иммунные функции, такие как, например, связывание с антителами, присоединенными к инфицированным клеткам или инвазивным патогенам, стимулирование фагоцитарных или цитотоксических клеток к уничтожению микроорганизмов или инфицированных клеток путем опосредованного антителами фагоцитоза или антителозависимой клеточноопосредованной цитотоксичности (ADCC).
ADCC представляет собой процесс, посредством которого эффекторные клетки иммунной системы лизируют клетку-мишень, связанную антителами. Данный процесс зависит от предшествующего воздействия инородного антигена или клетки, вызывающего образование антител. ADCC может быть опосредована эффекторными клетками, такими как, например, натуральные клетки-киллеры (NK-клетки), путем связывания FcR, экспрессированных на поверхности эффекторной клетки, с Fc-участком антитела, которое само связано с чужеродным антигеном или клеткой. Передача сигнала через высокоаффинный рецептор FcγR1 играет важную роль в регуляции иммунной системы и функции эффектной клетки.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В основе настоящего изобретения лежит понимание целесообразности создания не относящихся к человеку животных, таких как мыши, для экспрессии человеческого или гибридного белка FcγRI для обеспечения экспериментального изучения человеческих иммунных эффекторных ответов, которое нельзя выполнять на людях.
В основе настоящего изобретения также лежит понимание целесообразности замещения эндогенного мышиного гена FcγRI гуманизированным (человеческим или гибридным) геном FcγRI.
В некоторых вариантах осуществления в изобретении предложена мышь, которая экспрессирует белок FcγRI, содержащий внеклеточный участок человеческой α-цепи FcγRI и внутриклеточный участок мышиной α-цепи FcγRI. В некоторых вариантах осуществления внеклеточный участок человеческой α-цепи FcγRI содержит домен ЕС1, домен ЕС2, домен ЕС3 или их комбинацию.
В некоторых вариантах осуществления домен ЕС1 кодируется экзоном по меньшей мере на 50%, 70%, 85%, 90% или 95% идентичным экзону 3 SEQ ID NO: 3.
В некоторых вариантах осуществления домен ЕС2 кодируется экзоном по меньшей мере на 50%, 70%, 85%, 90% или 95% идентичным экзону 4 SEQ ID NO: 3.
В некоторых вариантах осуществления домен ЕС3 кодируется экзоном по меньшей мере на 50%, 70%, 85%, 90% или 95% идентичным экзону 5 SEQ ID NO: 3.
В некоторых вариантах осуществления в изобретении предложена мышь, которая экспрессирует белок FcγRI, содержащий внеклеточный участок человеческой α-цепи FcγRI и внутриклеточный участок мышиной α-цепи FcγRI, причем мышь не экспрессирует полноразмерную мышиную α-цепь FcγRI на обнаруживаемом уровне. В некоторых вариантах осуществления внутриклеточный участок α-цепи FcγRI содержит весь цитоплазматический домен мышиной α-цепи FcγRI или его часть. В некоторых вариантах осуществления мышь дополнительно экспрессирует α-цепь FcγRI, содержащую весь трансмембранный домен мышиной α-цепи FcγRI или его часть.
В некоторых вариантах осуществления в изобретении предложена мышь, которая экспрессирует аминокислотную последовательность α-цепи FcγRI по меньшей мере на 70%, 85%, 90% или 95% идентичную SEQ ID NO: 5. В некоторых вариантах осуществления человеческий или гибридный белок FcγRI экспрессируется на обнаруживаемом уровне на моноцитах, макрофагах, нейтрофилах, дендритных клетках и/или их комбинации.
В некоторых вариантах осуществления уровень человеческого белка FcγRI повышается при введении мышиного гранулоцитарного колониестимулирующего фактора (мГ-КСФ). В некоторых вариантах осуществления уровень мышиного белка FcγRI не повышается в моноцитах, нейтрофилах или дендритных клетках при введении мышиного гранулоцитарного колониестимулирующего фактора (мГ-КСФ).
В некоторых вариантах осуществления в изобретении предложена мышь, которая экспрессирует ген FcγRI, который содержит один или более экзонов человеческого гена FcγRI, функционально связанных с одним или более экзонов мышиного гена FcγRI. В некоторых вариантах осуществления экзоны человеческого гена FcγRI кодируют один или более внеклеточных участков человеческого белка FcγRI. В некоторых вариантах осуществления экзоны мышиного гена FcγRI кодируют один или более внутриклеточных участков мышиного белка FcγRI. В некоторых вариантах осуществления экзоны человеческого FcγRI выбирают из группы, состоящей из экзонов 3,4, 5 и их комбинаций.
В некоторых вариантах осуществления внутриклеточный участок мышиного FcγRI функционально связан с одним или более мышиными каскадами внутриклеточной сигнализации.
В некоторых вариантах осуществления в изобретении предложена мышь, которая экспрессирует человеческий FcγRI, причем в клетках зародышевой линии мыши отсутствует функциональный мышиный ген FcγRI. В некотором варианте осуществления в изобретении предложена мышь, которая экспрессирует человеческий FcγRI, причем в клетках зародышевой линии мыши отсутствует какой-либо мышиный ген FcγRI.
В некоторых вариантах осуществления в изобретении предложена эмбриональная стволовая клетка, геном которой содержит ген FcγRI, который кодирует внеклеточный участок человеческого белка FcγRI и внутриклеточный участок мышиного белка FcγRI. В некоторых вариантах осуществления ген FcγRI содержит экзоны 3, 4 и 5 человеческого гена FcγRI. В некоторых вариантах осуществления ген FcγRI дополнительно содержит одну или более человеческих нетранслируемых областей на 5'-конце, фланкирующих человеческий экзон 1. В некоторых вариантах осуществления внеклеточный участок человеческого белка FcγRI содержит один или более из доменов ЕС1, ЕС2 и ЕС3.
В некоторых вариантах осуществления в изобретении предложена эмбриональная стволовая клетка, геном которой содержит аминокислотную последовательность цепи FcγRIα по меньшей мере на 70%, 85%, 90% или 95% идентичную SEQ ID NO: 5.
В некоторых вариантах осуществления эмбриональная стволовая клетка содержит ген FcγRI, содержащий аминокислотные остатки экзона 6 мышиного гена FcγRI. В некоторых вариантах осуществления внутриклеточный участок мышиного белка FcγRI содержит весь цитоплазматический домен мышиного белка FcγRI или его часть.
В некоторых вариантах осуществления в изобретении предложена эмбриональная стволовая клетка, содержащая человеческий ген FcγRI, причем человеческий ген FcγRI расположен в эндогенном локусе FcγRI, который обнаруживается в мышином геноме в природе.
В некоторых вариантах осуществления в изобретении предложен эмбрион мыши, созданный из эмбриональной стволовой клетки, как описано в настоящем документе.
В некоторых вариантах осуществления в изобретении предложено применение мышиной эмбриональной стволовой клетки, описанной в настоящем документе, для создания трансгенной мыши.
В некоторых вариантах осуществления описаны способы создания мыши, которая экспрессирует белок FcγRI, содержащий внеклеточный участок человеческого белка FcγRI и внутриклеточный участок мышиного белка FcγRI, причем способ включает следующие этапы: (а) получение мышиной эмбриональной стволовой клетки; (b) замещение в эмбриональной клетке эндогенного мышиного гена FcγRI фрагментом генома, содержащим молекулу нуклеиновой кислоты, которая кодирует участок человеческого белка FcγRI, имеющий человеческие внеклеточные области; и (с) создание мыши с использованием эмбриональной клетки этапа (b).
В некоторых вариантах осуществления в изобретении предложен фрагмент генома, содержащий молекулу нуклеиновой кислоты, которая кодирует участок человеческого белка FcγRI, имеющего человеческие внеклеточные области, и молекулу нуклеиновой кислоты, которая кодирует внутриклеточный участок мышиного белка FcγRI.
В настоящей заявке термины «около» и «приблизительно» используются как синонимы. Все цифры, используемые в настоящей заявке с терминами «около/приблизительно» или без них, охватывают любые нормальные колебания, известные обычному специалисту в соответствующей области.
Другие характеристики, цели и преимущества настоящего изобретения станут понятны из следующего подробного описания. Однако следует понимать, что несмотря на указание вариантов осуществления настоящего изобретения, подробное описание приведено только в качестве примера, но не ограничения. Специалисту в данной области из подробного описания станут очевидными разнообразные изменения и модификации в пределах объема изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Чертежи, включенные в настоящий документ, приведены только в качестве примера, но не ограничения.
На Фиг. 1 показано генотипирование мышиного аллеля FcγRI у экспериментальных мышей и контрольных мышей дикого типа.
На Фиг. 2 показано относительное число копий человеческого гена FcγRI у экспериментальных мышей и контрольных мышей дикого типа.
На Фиг. 3 показаны преобразованные данные для чисел копий гена на основании наличия у мышей Het (+/-) одной копии человеческого FcγRI и калиброванные по среднему ΔCt.
На Фиг. 4 показана экспрессия рецепторов FcγRI в клетках от доноров человеческой крови.
На Фиг. 5 показана схематическая иллюстрация (без соблюдения масштаба) человеческого гена FcγRI, мышиного гена FcγRI и гуманизированного гена FcγRI.
На Фиг. 6 показана схематическая иллюстрация (без соблюдения масштаба) процесса получения кассеты MAID 6074.
На Фиг. 7 показаны нормальные частоты клеток в селезенке и крови у мышей, имеющих гуманизированный ген FcγRI.
На Фиг. 8 показаны популяции миелоидных клеток в селезенке у мышей, имеющих гуманизированный ген FcγRI.
На Фиг. 9 показано исчезновение экспрессии мышиного FcγRI на макрофагах из селезенки мышей, имеющих гуманизированный ген FcγRI.
На Фиг. 10 показано появление экспрессии человеческого FcγRI на моноцитах из селезенки мышей, имеющих гуманизированный ген FcγRI.
На Фиг. 11 показана стратегия селекции при проведении анализа флуоресцентно-активированной сортировки клеток (FACS) макрофагов, очищенных из брюшной полости мышей, имеющих эндогенные мышиные гены FcγRI (MAID 6074 WT), и мышей, гомозиготных по гуманизированному гену FcγRI (MAID 6074 НО).
На Фиг. 12 показана экспрессия человеческого FcγRI и мышиного FcγRI в макрофагах из брюшной полости мышей, имеющих эндогенные мышиные гены FcγRI (MAID 6074 WT), и мышей, гомозиготных по гуманизированному гену FcγRI (MAID 6074 НО).
На Фиг. 13 показана стратегия селекции при проведении анализа FACS макрофагов, полученных из костного мозга мышей, имеющих эндогенные мышиные гены FcγRI (MAID 6074 WT), и мышей, гомозиготных по гуманизированному гену FcγRI (MAID 6074 НО).
На Фиг. 14 показана экспрессия человеческого FcγRI и мышиного FcγRI в макрофагах, полученных из костного мозга мышей, имеющих эндогенные мышиные гены FcγRI (MAID 6074 WT), и мышей, гомозиготных по гуманизированному гену FcγRI (MAID 6074 НО).
На Фиг. 15 показана стратегия селекции при проведении анализа FACS макрофагов, полученных из костного мозга мышей, имеющих эндогенные мышиные гены FcγRI (контроль 75/25), и мышей, гетерозиготных по гуманизированному гену FcγRI (MAID 6074 НЕТ).
На Фиг. 16 показана экспрессия человеческого FcγRI и мышиного FcγRI в макрофагах, полученных из костного мозга мышей, имеющих эндогенные мышиные гены FcγRI (контроль 75/25), и мышей, гетерозиготных по гуманизированному гену FcγRI (MAID 6074 НЕТ).
На Фиг. 17 показаны популяции миелоидных клеток крови у мышей MAID 6074 НО по сравнению с MAID 6074 WT через 48 часов после обработки натрий-фосфатным буфером (PBS).
На Фиг. 18 показаны популяции миелоидных клеток крови у мышей MAID 6074 НО по сравнению с MAID 6074 WT через 48 часов после обработки мГ-КСФ.
На Фиг. 19 показано исчезновение экспрессии человеческого FcγRI в крови мышей MAID 6074 WT и мышей MAID 6074 НО через 48 часов после обработки PBS.
На Фиг. 20 показана экспрессия человеческого FcγRI в крови мышей MAID 6074 НО по сравнению с мышами MAID 6074 WT через 48 часов после обработки мГ-КСФ.
На Фиг. 21 показано исчезновение экспрессии мышиного FcγRI в крови мышей MAID 6074 WT и MAID 6074 НО через 48 часов после обработки PBS.
На Фиг. 22 показана экспрессия мышиного FcγRI в крови мышей MAID 6074 WT по сравнению с мышами MAID 6074 НО через 48 часов после обработки мГ-КСФ.
На Фиг. 23 показаны популяции миелоидных клеток селезенки у мышей MAID 6074 НО по сравнению с мышами MAID 6074 WT через 48 часов после обработки PBS.
На Фиг. 24 показаны популяции миелоидных клеток селезенки у мышей MAID 6074 НО по сравнению с мышами MAID 6074 WT через 48 часов после обработки мГ-КСФ.
На Фиг. 25 показано исчезновение экспрессии человеческого FcγRI в моноцитах селезенки у мышей MAID 6074 НО и мышей 6074 WT через 48 часов после обработки PBS.
На Фиг. 26 показана экспрессия человеческого FcγRI в селезенке мышей MAID 6074 НО по сравнению с мышами MAID 6074 WT через 48 часов после обработки мГ-КСФ.
На Фиг. 27 показана экспрессия мышиного FcγRI в селезенке мышей MAID 6074 WT по сравнению с мышами MAID 6074 НО через 48 часов после обработки PBS.
На Фиг. 28 показана экспрессия мышиного FcγRI в селезенке мышей MAID 6074 WT по сравнению с мышами MAID 6074 НО через 48 часов после обработки мГ-КСФ.
На Фиг. 29 показана сводная таблица экспрессии человеческого FcγRI в клеточных популяциях мышей MAID 6074 WT и MAID 6074 НО после обработки PBS или мГ-КСФ.
На Фиг. 30 показана положительная регуляция мРНК человеческого FcγRI в крови и селезенке мыши MAID 6074 НО, индуцированная мГ-КСФ и нормализованная по mHPRT1.
На Фиг. 31 показана положительная регуляция мРНК человеческого FcγRI в крови и селезенке мыши MAID 6074 НО, индуцированная мГ-КСФ.
На Фиг. 32 изображена в виде схемы иллюстративная стратегия гуманизации FcγRI мыши.
ОПРЕДЕЛЕНИЯ
Настоящее изобретение не ограничивается конкретными способами и описанными экспериментальными условиями, так как такие способы и условия могут изменяться. Также следует понимать, что терминология, используемая в настоящем документе, служит только для описания конкретных вариантов осуществления и не ограничивает объем настоящего изобретения, который определяется формулой изобретения.
При отсутствии иных указаний все термины и фразы, используемые в настоящем документе, включают значения, которые эти термины и фразы имеют в данной области, кроме случаев, когда иное значение четко указано или очевидно из контекста, в котором используется термин или фраза. В настоящем документе описаны конкретные способы и материалы, хотя для проверки или анализа настоящего изобретения могут быть использованы любые способы и материалы, подобные или эквивалентные тем, которые описаны в настоящем документе.
Термин «приблизительно», примененный в настоящем документе к одной или более интересующим величинам, обозначает величину, которая подобна указанной эталонной величине. В некоторых вариантах осуществления термин «приблизительно» или «около» обозначает диапазон величин, которые лежат в пределах 25%, 20%, 19%, 18%, 17%, 16%, 15%, 14%, 13%, 12%, 11%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1% или меньше в обе стороны (большую и меньшую) от заданной эталонной величины, кроме случаев, когда указано иное значение или иное значение очевидно из контекста (за исключением ситуаций, в которых такое число превышает 100% от возможной величины).
Термин «биологически активный» в контексте настоящего документа обозначает характеристику любого агента, который обладает активностью в биологической системе in vitro или in vivo (например, в организме). Например, биологически активным считается агент, который при нахождении в организме оказывает биологический эффект внутри этого организма. В конкретных вариантах осуществления, в которых белок или полипептид является биологически активным, участок этого белка или полипептида, который связан по меньшей мере с одним биологическим действием белка или полипептида, обычно называется «биологически активным» участком.
Термин «сравнимый» в контексте настоящего документа обозначает два или более агентов, объектов, ситуаций, наборов условий и т.п., которые могут не быть идентичными друг другу, но являются в достаточной мере схожими, чтобы можно было их сравнить и сделать правильный вывод на основании наблюдаемых различий или сходств. Обычным специалистам в данной области будет понятно из контекста, какая степень идентичности требуется в любых конкретных обстоятельствах, чтобы два или более таких агентов, объектов, ситуаций, наборов условий и т.п. можно было считать сравнимыми.
Термин «консервативный», используемый в настоящем документе для описания консервативного аминокислотного замещения, обозначает замещение аминокислотного остатка другим аминокислотным остатком, имеющим R-группу боковой цепи со схожими химическими свойствами (например, зарядом или гидрофобностью). В большинстве случаев консервативное аминокислотное замещение по существу не изменит интересующие функциональные свойства белка, например способность рецептора к связыванию с лигандом. Примеры групп аминокислот, которые имеют боковые цепи со схожими химическими свойствами, включают аминокислоты с алифатическими боковыми цепями, такие как глицин, аланин, валин, лейцин и изолейцин; аминокислоты с гидроксилированными алифатическими боковыми цепями, такие как серии и треонин; аминокислоты с амидосодержащими боковыми цепями, такие как аспарагин и глутамин; аминокислоты с ароматическими боковыми цепями, такие как фенилаланин, тирозин и триптофан; аминокислоты с основными боковыми цепями, такие как лизин, аргинин и гистидин; аминокислоты с кислыми боковыми цепями, такие как аспарагиновая кислота и глутаминовая кислота; и аминокислоты с серосодержащими боковыми цепями, такие как цистеин и метионин. Группы консервативного аминокислотного замещения включают, например, валин/лейцин/изолейцин, фенилаланин/тирозин, лизин/аргинин, аланин/валин, глутамат/аспартат и аспарагин/глутамин. В некоторых вариантах осуществления консервативным аминокислотным замещением может быть замещение любого нативного остатка в белке аланином, как, например, при аланин-сканирующем мутагенезе. В некоторых вариантах осуществления выполняется консервативное замещение, которое имеет положительную величину в логарифмической матрице правдоподобия РАМ250, описанной в публикации Gonnet et al. (1992) Exhaustive Matching of the Entire Protein Sequence Database, Science 256:1443-45, включенной в настоящий документ путем ссылки. В некоторых вариантах осуществления замещение является умеренно консервативным и имеет неотрицательную величину в логарифмической матрице правдоподобия РАМ250.
Термин «разрыв» в контексте настоящего документа обозначает результат события гомологичной рекомбинации с молекулой ДНК (например, с эндогенной гомологичной последовательностью, такой как ген или локус гена). В некоторых вариантах осуществления разрыв может приводить к вставке, делеции, замещению, замене, миссенс-мутации или сдвигу рамки считывания последовательности (-ей) ДНК или их комбинации или представлять собой их. Вставки могут представлять собой вставку генов целиком или фрагментов генов, например экзонов, источником которых могут быть не эндогенные последовательности. В некоторых вариантах осуществления разрыв может увеличивать экспрессию и/или активность гена или генного продукта (например, кодируемого геном белка). В некоторых вариантах осуществления разрыв может уменьшать экспрессию и/или активность гена или генного продукта. В некоторых вариантах осуществления разрыв может изменять последовательность гена или кодируемого генного продукта (например, кодируемого белка). В некоторых вариантах осуществления разрыв может укорачивать или фрагментировать ген или кодируемый генный продукт (например, кодируемый белок). В некоторых вариантах осуществления разрыв может удлинять ген или кодируемый генный продукт; в некоторых вариантах осуществления разрыв может приводить к сборке слитного белка. В некоторых вариантах осуществления разрыв может изменять количество гена или генного продукта, но не влиять на их активность. В некоторых вариантах осуществления разрыв может изменять активность гена или генного продукта, но не влиять на их количество. В некоторых вариантах осуществления разрыв может не оказывать значимого влияния на количество гена или генного продукта. В некоторых вариантах осуществления разрыв может не оказывать значимого влияния на активность гена или генного продукта. В некоторых вариантах осуществления разрыв может не оказывать значимого влияния ни на количество, ни на активность гена или генного продукта.
Фраза «эндогенный локус» или «эндогенный ген» в контексте настоящего документа обозначает генетический локус, обнаруживаемый в исходном или эталонном организме перед внесением разрыва, делеции, замены, перестройки или модификации, как описано в настоящем документе. В некоторых вариантах осуществления эндогенный локус имеет последовательность, обнаруживаемую в природе. В некоторых вариантах осуществления эндогенный локус представляет собой локус дикого типа. В некоторых вариантах осуществления эталонный организм представляет собой организм дикого типа. В некоторых вариантах осуществления эталонный организм представляет собой искусственно созданный организм. В некоторых вариантах осуществления эталонный организм представляет собой выведенный в лаборатории организм (искусственно созданный или дикого типа).
Фраза «эндогенный промотор» в контексте настоящего документа обозначает промотор, который естественно связан, например, в организме дикого типа, с эндогенным геном.
Термин «белок FcγRI» в контексте настоящего документа обозначает высокоаффинный иммуноглобулиновый Fc-рецептор, содержащий α-цепь, имеющую три внеклеточных домена, трансмембранный домен и внутриклеточный домен.
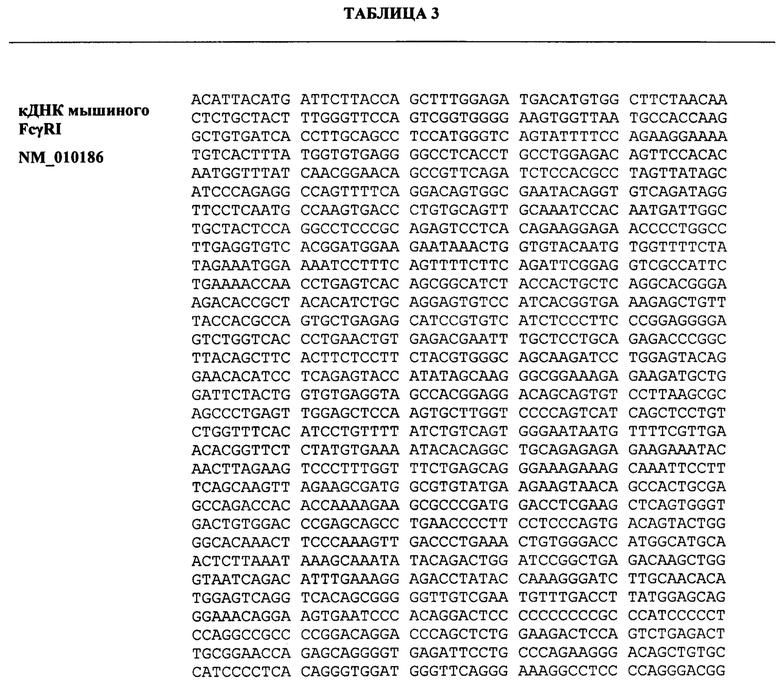
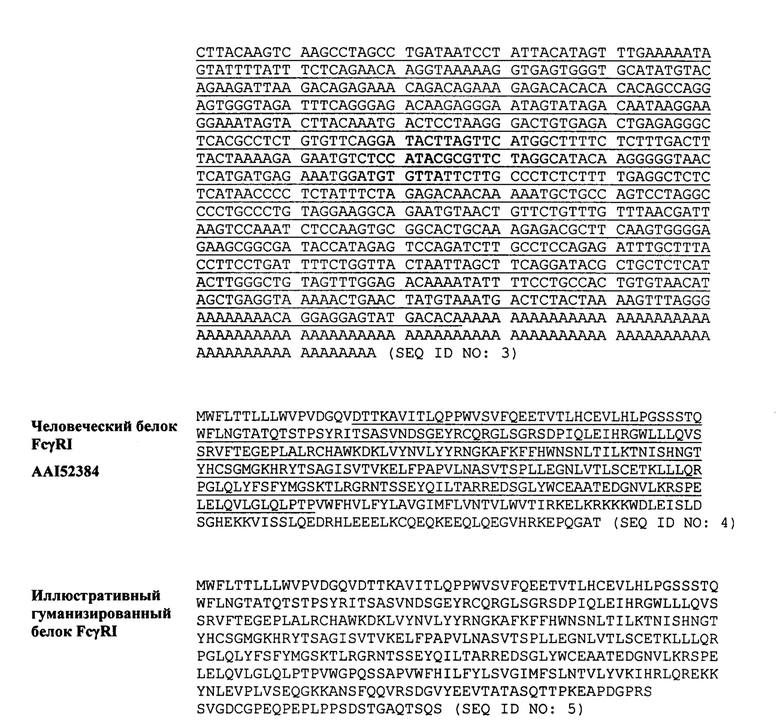
В качестве иллюстрации в таблице 3 приведены репрезентативные нуклеотидные и аминокислотные последовательности мышиных и человеческих генов FcγRIa. После прочтения этого описания специалистам будет понятно, что один или более эндогенных генов рецептора FcγRI в геноме (или все) могут быть замещены одним или более гетерологичными генами FcγRI (например, полиморфными разновидностями, подтипами или мутантами, генами от других видов и т.д.).
Термин «FcγRI-экспрессирующая клетка» в контексте настоящего документа обозначает клетку, которая экспрессирует FcγRI. В некоторых вариантах осуществления FcγRI-экспрессирующая клетка экспрессирует на своей поверхности рецептор FcγRI. В некоторых вариантах осуществления рецептор FcγRI экспрессируется на поверхности клетки в количестве, достаточном для опосредования межклеточных взаимодействий посредством белка FcγRI, экспрессированного на поверхности клетки. Примеры FcγRI-экспрессирующих клеток включают лимфоциты, миелоидные клетки, макрофаги, нейтрофилы и натуральные клетки-киллеры (NK-клетки). FcγRI-экспрессирующие клетки регулируют взаимодействие иммунных клеток с целью регулирования иммунного ответа на различные чужеродные антигены или патогены. В некоторых вариантах осуществления регулирование иммунных клеток не относящихся к человеку животных настоящего изобретения осуществляется посредством гуманизированных рецепторов FcγRI, экспрессированных на поверхности одной или более клеток не относящегося к человеку животного.
Термин «гетерологичный» в контексте настоящего документа обозначает агент или объект из другого источника. Например, при использовании со ссылкой на полипептид, ген или генный продукт или наличие в конкретной клетке или организме термин указывает, что соответствующий полипептид, ген или генный продукт: 1) создан человеком; 2) введен в клетку или организм (или его предшественник) человеком (например, посредством генной инженерии); и/или 3) не образован естественным путем или не присутствует в естественных условиях в соответствующей клетке или организме (например, соответствующем типе клетки или типе организма).
Термин «клетка-хозяин» в контексте настоящего документа обозначает клетку, в которую была введена гетерологичная (например, экзогенная) нуклеиновая кислота или белок. После прочтения этого описания специалистам будет понятно, что эти термины обозначают не только конкретную указанную клетку, но также используются для обозначения потомства такой клетки. Так как в последующих поколениях могут возникнуть некоторые модификации вследствие либо мутации, либо воздействий среды, такое потомство фактически может быть не идентичным исходной клетке, но оно также может быть включено в объем используемого в настоящем документе термина «клетка-хозяин». В некоторых вариантах осуществления клетка-хозяин представляет собой или содержит прокариотическую или эукариотическую клетку. Как правило, клетка-хозяин представляет собой любую клетку, пригодную для получения и/или продуцирования гетерологичной нуклеиновой кислоты или белка, вне зависимости от царства, к которому принадлежит клетка. Примеры клеток включают прокариоты и эукариоты (одноклеточные или многоклеточные), бактериальные клетки (например, штаммы Е. coli, Bacillus spp., Streptomyces spp.и т.д.), клетки микобактерий, клетки грибов, дрожжевые клетки (например, S. cerevisiae, S. pombe, P. pastoris, P. methanolica и т.д.), клетки растений, клетки насекомых (например, SF-9, SF-21, инфицированные бакуловирусом клетки насекомых, Trichoplusia ni и т.д.), клетки не относящихся к человеку животных, клетки человека или слияния клеток, такие как, например гибридомы или квадромы. В некоторых вариантах осуществления клетка представляет собой клетку человека, обезьяны, человекообразной обезьяны, хомяка, крысы или мыши. В некоторых вариантах осуществления клетка представляет собой эукариотическую клетку, выбранную из следующих клеток: СНО (например, СНО K1, DXB-11 СНО, Veggie-CHO), COS (например, COS-7), клетка сетчатки, Vero, CV1, клетка почек (например, НЕК293, 293 EBNA, MSR 293, MDCK, HaK, ВНК), HeLa, HepG2, WI38, MRC 5, Colo205, НВ 8065, HL-60, (например, ВНК21), Jurkat, Daudi, А431 (эпидермальная), CV-1, U937, 3Т3, L-клетка, клетка С127, SP2/0, NS-0, ММТ 060562, клетка Сертоли, клетка BRL 3А, клетка НТ1080, миеломная клетка, опухолевая клетка и клеточная линия, полученная из вышеупомянутых клеток. В некоторых вариантах осуществления клетка содержит один или более вирусных генов, например, клетка сетчатки, которая экспрессирует вирусный ген (например, клетка PER.C6™). В некоторых вариантах осуществления клетка-хозяин представляет собой или содержит изолированную клетку. В некоторых вариантах осуществления клетка-хозяин представляет собой часть ткани. В некоторых вариантах осуществления клетка-хозяин представляет собой часть организма.
Фраза «человеческий ген FcγRI» в контексте настоящего документа обозначает, в зависимости от контекста, нуклеотидную последовательность, кодирующую полностью человеческий, по существу человеческий или гуманизированный участок белка FcγRI. В некоторых вариантах осуществления фраза «человеческий ген FcγRI» обозначает гуманизированный ген FcγRI в противоположность полностью мышиному гену FcγRI. В некоторых вариантах осуществления человеческий ген FcγRI содержит одну или более замен, добавлений, делеций или мутаций. В некоторых вариантах осуществления человеческий ген FcγRI представляет собой FcγRIA (CD64A), FcγRIB (CD64B), FcγRIC (CD64C) или их комбинацию.
Фраза «человеческий белок FcγRI» в зависимости от контекста обозначает белок, кодируемый полностью человеческим, по существу человеческим или гуманизированным геном FcγRI. В некоторых вариантах осуществления фраза «человеческий белок FcγRI» обозначает гуманизированный белок FcγRI в противоположность полностью мышиному белку FcγRI. В некоторых вариантах осуществления человеческий белок FcγRI содержит одну или более аминокислотных замен, добавлений, делеций или мутаций. В некоторых вариантах осуществления белок FcγRI представляет собой FcγRIA (CD64A), FcγRIB (CD64B), FcγRIC (CD64C) или их комбинацию.
Фраза «гибридный ген FcγRI» или «гибридный белок FcγRI» обозначает ген или белок FcγRI, который включает последовательность FcγRI по меньшей мере двух различных видов животных. В некоторых вариантах осуществления гибридный ген FcγRI включает участок человеческой нуклеотидной последовательности и участок мышиной нуклеотидной последовательности. В некоторых вариантах осуществления гибридный белок FcγRI включает участок человеческой аминокислотной последовательности и участок мышиной аминокислотной последовательности.
Термин «гуманизированный» в контексте настоящего документа используется согласно принятому в данной области значению для обозначения нуклеиновых кислот или белков, структуры которых (например, нуклеотидные или аминокислотные последовательности) включают в себя участки, которые по существу соответствуют или являются идентичными структурам конкретного гена или белка, обнаруживаемого в природе у не относящегося к человеку животного, а также включают в себя участки, которые отличаются от обнаруживаемых в соответствующем конкретном нечеловеческом гене или белке, но более точно соответствуют сравнимым структурам, обнаруживаемым в соответствующем человеческом гене или белке. В некоторых вариантах осуществления «гуманизированный» ген кодирует полипептид, имеющий аминокислотную последовательность, по существу идентичную последовательности человеческого полипептида (например, человеческого белка или его участка (например, характерного участка)). В качестве одного из примеров, в случае мембранного рецептора «гуманизированный» ген может кодировать полипептид, имеющий внеклеточный участок, аминокислотная последовательность которого аналогична человеческому внеклеточному участку, а оставшаяся последовательность аналогична нечеловеческому (например, мышиному) полипептиду. В некоторых вариантах осуществления гуманизированный ген содержит по меньшей мере участок последовательности ДНК человеческого гена. В некоторых вариантах осуществления гуманизированный ген содержит полную последовательность ДНК человеческого гена. В некоторых вариантах осуществления гуманизированный белок содержит последовательность, имеющую участок, который присутствует в человеческом белке. В некоторых вариантах осуществления гуманизированный белок содержит полную последовательность человеческого белка и экспрессируется из эндогенного локуса не относящегося к человеку животного, который соответствует гомологу или ортологу человеческого гена.
Термин «идентичность», используемый в настоящем документе для сравнения последовательностей, обозначает идентичность, определенную по нескольким различным алгоритмам, известным в данной области, которые можно использовать для измерения идентичности нуклеотидной и/или аминокислотной последовательности. В некоторых вариантах осуществления идентичность определяется с помощью программы выравнивания ClustalW v. 1.83 (медленное выравнивание) со штрафом за открытие гэпа 10.0 и штрафом за продолжение гэпа 0.1 и с помощью матрицы правдоподобности Гоннета (MACVECTOR™ 10.0.2, MacVector Inc., 2008).
Термины «внутриклеточный сигнальный каскад» или «внутриклеточная сигнальная трансдукция» в контексте настоящего документа обозначают передачу сигнала от поверхности клетки к одной или более внутриклеточных мишеней. В некоторых вариантах осуществления внутриклеточная сигнальная трансдукция представляет собой физиологический ответ в клетке, который вызывается посредством связывания молекулы-мишени (например, Fc-области иммуноглобулина) с внеклеточным компонентом рецептора FcγRI.
Термин «изолированный» в контексте настоящего документа обозначает вещество и/или объект, который был: (1) отделен по меньшей мере от некоторых компонентов, с которыми он был связан при изначальной продукции (в природе и/или в экспериментальных условиях); и/или (2) создан, продуцирован, получен и/или произведен человеком. Изолированные вещества и/или объекты могут быть отделены от приблизительно 10%, приблизительно 20%, приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более чем приблизительно 99% других компонентов, с которыми они были изначально связаны. В некоторых вариантах осуществления изолированные агенты имеют степень чистоты, равную приблизительно 80%, приблизительно 85%, приблизительно 90%, приблизительно 91%, приблизительно 92%, приблизительно 93%, приблизительно 94%, приблизительно 95%, приблизительно 96%, приблизительно 97%, приблизительно 98%, приблизительно 99% или более чем приблизительно 99%. В контексте настоящего документа вещество является «чистым», если оно по существу не содержит других компонентов. В некоторых вариантах осуществления, как будет понятно специалистам в данной области, вещество может по-прежнему рассматриваться как «изолированное» или даже «чистое» после объединения с некоторыми другими компонентами, такими как, например, один или более носителей или эксципиентов (например, буфер, растворитель, вода и т.д.); в таких вариантах осуществления процент изолирования или чистоты вещества рассчитывается без включения таких носителей или эксципиентов. В качестве одного из примеров, в некоторых вариантах осуществления биологический полимер, такой как полипептид или полинуклеотид, встречающийся в природе, считается «изолированным», если: а) в связи со своим происхождением или источником получения он не связан с некоторыми или всеми компонентами, вместе с которыми он существует в нативном состоянии в природе; b) он по существу не содержит других полипептидов или нуклеиновых кислот тех же видов, которые продуцируют его в природе; с) он экспрессируется или находится в иной связи с компонентами клетки или другой экспрессирующей системы, которая не относится к видам, которые продуцируют его в природе. Таким образом, в некоторых вариантах осуществления полипептид, полученный путем химического синтеза или синтеза в клеточной системе, отличной от продуцирующей его в природе, считается «изолированным» полипептидом. Альтернативно или дополнительно в некоторых вариантах осуществления полипептид, который был подвергнут очистке с использованием одного или более способов, может рассматриваться как «изолированный» полипептид в соответствии со степенью его отделения от других компонентов: а) с которыми он связан в природе; и/или b) с которыми он был связан при изначальной продукции.
Фраза «мышиный ген FcγRI» в контексте настоящего документа обозначает ген, содержащий молекулу нуклеиновой кислоты, показанную в SEQ ID NO: 1, или молекулу нуклеиновой кислоты, по существу идентичную молекуле, показанной в SEQ ID NO: 1.
Фраза «мышиный белок FcγRI» в контексте настоящего документа обозначает белок, содержащий аминокислотную последовательность, показанную в SEQ ID NO: 2, включая белок, по существу идентичный белку, показанному в SEQ ID NO: 2.
Фраза «не относящееся к человеку животное» в контексте настоящего документа обозначает любой позвоночный организм, кроме человека. В некоторых вариантах осуществления не относящееся к человеку животное представляет собой круглоротое, костную рыбу, хрящевую рыбу (например, акулу или ската), амфибию, рептилию, млекопитающее и птицу. В некоторых вариантах осуществления не относящееся к человеку животное представляет собой примата, козу, овцу, свинью, собаку, корову или грызуна. В некоторых вариантах осуществления не относящееся к человеку животное представляет собой грызуна, такого как крыса или мышь.
Фраза «нуклеиновая кислота» в контексте настоящего документа в широком смысле обозначает любое соединение и/или вещество, которое находится в олигонуклеотидной цепи или может быть введено в нее. В некоторых вариантах осуществления нуклеиновая кислота представляет собой соединение и/или вещество, которое находится в олигонуклеотидной цепи или может быть введено в нее посредством фосфодиэфирной связи. Как будет понятно из контекста, в некоторых вариантах осуществления фраза «нуклеиновая кислота» обозначает отдельные остатки нуклеиновой кислоты (например, нуклеотиды и/или нуклеозиды); в некоторых вариантах осуществления фраза «нуклеиновая кислота» обозначает олигонуклеотидную цепь, содержащую отдельные остатки нуклеиновой кислоты. В некоторых вариантах осуществления «нуклеиновая кислота» представляет собой или содержит РНК; в некоторых вариантах осуществления «нуклеиновая кислота» представляет собой или содержит ДНК. В некоторых вариантах осуществления нуклеиновая кислота представляет собой, или содержит один или более остатков природной нуклеиновой кислоты, или состоит из них. В некоторых вариантах осуществления нуклеиновая кислота представляет собой, или содержит один или более аналогов нуклеиновой кислоты, или состоит из них. В некоторых вариантах осуществления аналог нуклеиновой кислоты отличается от нуклеиновой кислоты тем, что в нем отсутствует фосфодиэфирный остов. Например, в некоторых вариантах осуществления нуклеиновая кислота представляет собой, или содержит одну или более «пептидных нуклеиновых кислот», или состоит из этих кислот, известных в данной области, в остове которых присутствуют пептидные связи вместо фосфодиэфирных связей, при этом они находятся в пределах объема настоящего изобретения. Альтернативно или дополнительно в некоторых вариантах осуществления нуклеиновая кислота имеет одну или более тиофосфатных и/или 5'-N-фосфорамидитных связей вместо фосфодиэфирных связей. В некоторых вариантах осуществления нуклеиновая кислота представляет собой, или содержит один или более природных нуклеозидов (например, аденозин, тимидин, гуанозин, цитидин, уридин, дезоксиаденозин, дезокситимидина, дезоксигуанозин и дезоксицитидин) или состоит из них. В некоторых вариантах осуществления нуклеиновая кислота представляет собой, или содержит один или более нуклеозидных аналогов (например, 2-аминоаденозин, 2-тиотимидин, инозин, пирролопиримидин, 3-метиладенозин, 5-метилцитидин, С5-пропинилцитидин, С5-пропинилуридин, 2-аминоаденозин, С5-бромуридин, С5-фторуридин, С5-йодуридин, С5-пропинилуридин, С5-пропинилцитидин, С5-метилцитидин, 2-аминоаденозин, 7-дезазааденозин, 7-дезазагуанозин, 8-оксоаденоизн, 8-оксогуанозин, O(6)-метилгуанин, 2-тиоцитидин, метилированные основания и их комбинаций), или состоит из них. В некоторых вариантах осуществления нуклеиновая кислота содержит один или более модифицированных сахаров (например, 2'-фторрибозу, рибозу, 2'-дезоксирибозу, арабинозу и гексозу) по сравнению с сахарами в природных нуклеиновых кислотах. В некоторых вариантах осуществления нуклеотидная последовательность нуклеиновой кислоты кодирует функциональный генный продукт, такой как РНК или белок. В некоторых вариантах осуществления нуклеиновая кислота включает в себя один или более интронов. В некоторых вариантах осуществления нуклеиновые кислоты получают посредством одного или более из изолирования из природного источника, ферментативного синтеза путем полимеризации на основании комплементарной матрицы (in vivo или in vitro), репродукции в рекомбинантной клетке или системе и химического синтеза. В некоторых вариантах осуществления нуклеиновая кислота состоит по меньшей мере из 3, 4, 5, 6, 7, 8, 9,10, 15, 20, 25, 30, 35,40,45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, 110, 120,130, 140, 150,160, 170, 180, 190, 20, 225, 250, 275, 300, 325, 350, 375,400, 425, 450, 475, 500, 600, 700, 800, 900, 1000, 1500, 2000, 2500, 3000, 3500, 4000, 4500, 5000 или более остатков. В некоторых вариантах осуществления нуклеиновая кислота является одноцепочечной; в некоторых вариантах осуществления нуклеиновая кислота является двухцепочечной. В некоторых вариантах осуществления нуклеотидная последовательность нуклеиновой кислоты содержит по меньшей мере один элемент, который кодирует последовательность, кодирующую полипептид, или комплементарен ей. В некоторых вариантах осуществления нуклеиновая кислота обладает ферментативной активностью.
Фраза «функционально связанный» в контексте настоящего документа обозначает смежное положение, в котором описанные компоненты находятся во взаимосвязи, позволяющей им функционировать надлежащим образом. Управляющая последовательность, «функционально связанная» с кодирующей последовательностью, лигирована таким образом, что экспрессия кодирующей последовательности осуществляется в условиях, которые подходят для управляющих последовательностей. «Функционально связанные» последовательности включают в себя как последовательности управления экспрессией, которые примыкают к интересующему гену, так и последовательности управления экспрессией, которые выполняют регулирование интересующего гена в транс-положении или на расстоянии. Термин «последовательность управления экспрессией» в контексте настоящего документа обозначает полинуклеотидные последовательности, необходимые для осуществления экспрессии и процессинга кодирующих последовательностей, с которыми они лигированы. Последовательности управления экспрессией включают в себя соответствующие последовательности инициации и терминации транскрипции, промотора и энхансера; эффективные сигналы процессинга РНК, такие как сигналы сплайсинга и полиаденилирования; последовательности, которые стабилизируют цитоплазматическую мРНК; последовательности, которые усиливают эффективность трансляции (например, консенсусную последовательность Козак); последовательности, которые усиливают стабильность белка; и, при желании, последовательности, которые усиливают секрецию белка. Природа таких управляющих последовательностей отличается в зависимости от организма-хозяина. Например, у прокариот такие управляющие последовательности по существу включают в себя промотор, рибосомный сайт связывания и последовательность терминации транскрипции, тогда как у эукариот такие управляющие последовательности обычно включают в себя промоторы и последовательность терминации транскрипции. Термин «управляющие последовательности» включает компоненты, наличие которых является обязательным для экспрессии и процессинга, а также может включать дополнительные компоненты, наличие которых является преимуществом, например лидерные последовательности и последовательности партнеров слияния.
Термин «полипептид» в контексте настоящего документа обозначает любую полимерную цепь аминокислот. В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, которая встречается в природе. В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, которая не встречается в природе. В некоторых вариантах осуществления полипептид имеет аминокислотную последовательность, которая является искусственно созданной, то есть она была сконструирована и/или получена в результате деятельности человека.
Термин «рекомбинантный» в контексте настоящего документа обозначает полипептиды (например, сигнально-регуляторные белки, описанные в настоящем документе), которые сконструированы, произведены, получены, экспрессированы, созданы или изолированы с помощью рекомбинантных средств, например полипептиды, экспрессированные с использованием рекомбинантного вектора экспрессии, трансфицированного в клетку-хозяина, полипептиды, изолированные из рекомбинантной, комбинаторной библиотеки человеческих полипептидов (Hoogenboom Н.R., (1997) TIB Tech. 15: 62-70; Azzazy Н., and Highsmith W.E., (2002) Clin. Biochem. 35: 425-445; Gavilondo J.V., and Larrick J.W. (2002) BioTechniques 29: 128-145; Hoogenboom H., and Chames P. (2000) Immunology Today 21: 371-378), антитела, изолированные из животного (например, мыши), трансгенного в отношении генов человеческого иммуноглобулина (см. например, Taylor, L.D., et al. (1992) Nucl. Acids Res. 20: 6287-6295; Kellermann S-A., and Green L.L. (2002) Current Opinion in Biotechnology 13: 593-597; Little M. et al (2000) Immunology Today 21: 364-370) или полипептиды, полученные, экспрессированные, созданные или изолированные другими средствами, которые включают в себя сплайсинг выбранных элементов последовательности друг с другом. В некоторых вариантах осуществления один или более таких выбранных элементов последовательности встречаются в природе. В некоторых вариантах осуществления один или более таких выбранных элементов последовательности сконструированы с помощью компьютерного моделирования. В некоторых вариантах осуществления один или более таких выбранных элементов последовательности получены в результате мутагенеза (например, in vivo или in vitro) известного элемента последовательности, например, из природного или искусственного источника. Например, в некоторых вариантах осуществления рекомбинантный полипептид состоит из последовательностей, встречающихся в геноме исходного интересующего организма (например, человека, мыши и т.д.). В некоторых вариантах осуществления аминокислотная последовательность рекомбинантного полипептида получена посредством мутагенеза (например, in vivo или in vitro у не относящегося к человеку животного), в результате чего аминокислотные последовательности рекомбинантных полипетидов представляют собой последовательности, которые хотя и происходят из полипетидных последовательностей и являются родственными им, могут не существовать в природе в геноме не относящегося к человеку животного in vivo.
Термин «замена» используется в настоящем документе для обозначения процесса, посредством которого «заменяемая» нуклеотидная последовательность (например, ген), находящаяся в локусе организма-хозяина (например, в геноме), удаляется из этого локуса, а на ее месте размещается другая «заменяющая» нуклеиновая кислота. В некоторых вариантах осуществления заменяемая нуклеотидная последовательность и заменяющие нуклеотидные последовательности являются сравнимыми друг с другом в том смысле, что они, например, являются гомологичными друг другу и/или содержат соответствующие элементы (например, кодирующие белок элементы, регуляторные элементы и т.д.). В некоторых вариантах осуществления заменяемая нуклеотидная последовательность включает в себя один или более промоторов, энхансеров, донорных сайтов сплайсинга, принимающих сайтов сплайсинга, интронов, экзонов, нетранслируемых областей (UTR); в некоторых вариантах осуществления заменяющая нуклеотидная последовательность включает в себя одну или более кодирующих последовательностей. В некоторых вариантах осуществления заменяющая нуклеотидная последовательность представляет собой гомолог заменяемой нуклеотидной последовательности. В некоторых вариантах осуществления заменяющая нуклеотидная последовательность представляет собой ортолог заменяемой последовательности. В некоторых вариантах осуществления заменяющая нуклеотидная последовательность представляет собой или содержит человеческую нуклеотидную последовательность. В некоторых вариантах осуществления, включая таковые, в которых заменяющая нуклеотидная последовательность представляет собой или содержит человеческую нуклеотидную последовательность, заменяемая нуклеотидная последовательность представляет собой или содержит последовательность грызуна (например, мышиную последовательность). Вставленная этим способом нуклеотидная последовательность может включать в себя одну или более регуляторных последовательностей, которые являются частью исходной нуклеотидной последовательности, используемой для получения вставленной этим способом последовательности (например, промоторов, энхансеров, нетранслируемых областей на 5 - или 3'-конце и т.д.). Например, в различных вариантах осуществления замена представляет собой замещение эндогенной последовательности гетерологичной последовательностью, что приводит к продукции генного продукта из вставленной этим способом нуклеотидной последовательности (содержащей гетерологичную последовательность), но не экспрессии эндогенной последовательности; замена представляет собой замену эндогенной геномной последовательности нуклеотидной последовательностью, которая кодирует белок, который выполняет такую же функцию, что и белок, кодируемый эндогенной последовательностью (например, эндогенная геномная последовательность кодирует белок FcγRI, а фрагмент ДНК кодирует один или более человеческих белков FcγRI). В различных вариантах осуществления эндогенный ген или его фрагмент заменяется соответствующим человеческим геном или его фрагментом. Соответствующий человеческий ген или его фрагмент представляет собой человеческий ген или его фрагмент, который является ортологом или по существу схожим или аналогичным по структуре и/или функции заменяемому эндогенному гену или его фрагменту.
Термин «по существу» в контексте настоящего документа обозначает качественное состояние проявления в полной или практически полной мере или степени интересующей характеристики или свойства. Обычному специалисту в области биологии будет понятно, что биологические и химические явления редко или почти никогда не стремятся к завершенности и/или не протекают до завершения или не достигают или не отрицают абсолютного результата. Таким образом, термин «по существу» используется в настоящем документе для обозначения потенциального отсутствия завершенности, присущего многим биологическим и химическим явлениям.
Фраза «по существу гомологичный» в контексте настоящего документа обозначает сравнение между аминокислотными или нуклеотидными последовательностями. Как будет понятно обычным специалистам в данной области, две последовательности в большинстве случаев рассматриваются как «по существу гомологичные», если они содержат гомологичные остатки в соответствующих положениях. Гомологичные остатки могут быть идентичными. Альтернативно, гомологичные остатки могут быть неидентичными, но будут иметь схожие соответствующие структурные и/или функциональные характеристики. Например, как хорошо известно обычным специалистам в данной области, некоторые аминокислоты обычно разделяют на «гидрофобные» или «гидрофильные» аминокислоты и/или на имеющие «полярные» или «неполярные» боковые цепи. Замещение аминокислоты другой аминокислотой аналогичного типа часто рассматривается как «гомологичное» замещение. В таблицах 1 и 2 приведены типичные классификации аминокислот.



Как хорошо известно в данной области, аминокислотные или нуклеотидные последовательности можно сравнивать с использованием различных алгоритмов, включая алгоритмы, реализованные в коммерческих компьютерных программах, таких как BLASTN для нуклеотидных последовательностей и BLASTP, BLAST с использованием гэпов и PSI-BLAST для аминокислотных последовательностей. Примеры таких программ описаны в Altschul, et al, Basic local alignment search tool, J. Mol. Biol., 215(3): 403-410, 1990; Altschul, et al, Methods in Enzymology; Altschul, et al, "Gapped BLAST and PSI-BLAST: a new generation of protein database search programs", Nucleic Acids Res. 25:3389-3402, 1997; Baxevanis, et al, Bioinformatics: A Practical Guide to the Analysis of Genes and Proteins, Wiley, 1998; и Misener, et al., (eds.), Bioinformatics Methods and Protocols (Methods in Molecular Biology, Vol. 132), Humana Press, 1999. Кроме выявления гомологичных последовательностей вышеупомянутые программы обычно обеспечивают определение степени гомологии. В некоторых вариантах осуществления две последовательности считаются по существу гомологичными, если по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более их соответствующих остатков являются гомологичными на протяжении достаточного отрезка из остатков. В некоторых вариантах осуществления достаточный отрезок равен полной последовательности. В некоторых вариантах осуществления достаточный отрезок составляет по меньшей мере 9, 10, 11, 12, 13, 14, 15, 16, 17 или более остатков. В некоторых вариантах осуществления достаточный отрезок включает в себя непрерывные остатки вдоль полной последовательности. В некоторых вариантах осуществления достаточный отрезок включает в себя прерывающиеся остатки вдоль всей последовательности. В некоторых вариантах осуществления достаточный отрезок составляет по меньшей мере 10, 15, 20, 25, 30, 35, 40, 45, 50 или более остатков.
Фраза «по существу идентичные» в контексте настоящего документа обозначает сравнение между аминокислотными или нуклеотидными последовательностями. Как будет понятно обычным специалистам в данной области, две последовательности в большинстве случаев рассматриваются как «по существу идентичные», если они содержат идентичные остатки в соответствующих положениях. Как хорошо известно в данной области, аминокислотные или нуклеотидные последовательности можно сравнивать с использованием различных алгоритмов, включая алгоритмы, реализованные в коммерческих компьютерных программах, таких как BLASTN для нуклеотидных последовательностей и BLASTP, BLAST с использованием гэпов и PSI-BLAST для аминокислотных последовательностей. Примеры таких программ описаны в Altschul, et al., Basic local alignment search tool, J. Mol Biol., 215(3): 403-410, 1990; Altschul, et al, Methods in Enzymology; Altschul et al, Nucleic Acids Res. 25: 3389-3402, 1997; Baxevanis et al, Bioinformatics: A Practical Guide to the Analysis of Genes and Proteins, Wiley, 1998; и Misener, et al., (eds.), Bioinformatics Methods and Protocols (Methods in Molecular Biology, Vol. 132), Humana Press, 1999. Кроме выявления идентичных последовательностей вышеупомянутые программы обеспечивают определение степени идентичности. В некоторых вариантах осуществления две последовательности считаются по существу идентичными, если по меньшей мере 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более их соответствующих остатков являются идентичными на протяжении достаточного отрезка из остатков. В некоторых вариантах осуществления достаточный отрезок равен полной последовательности. В некоторых вариантах осуществления достаточный отрезок составляет по меньшей мере 10, 15, 20, 25, 30, 35, 40, 45, 50 или более остатков.
Фраза «нацеливающий вектор» или «нацеливающий конструкт» в контексте настоящего документа обозначает полинуклеотидную молекулу, которая содержит нацеливающую область. Нацеливающая область содержит последовательность, идентичную или по существу идентичную последовательности в целевой клетке, ткани или животном и обеспечивает встраивание нацеливающего конструкта в положение внутри генома клетки, ткани или животного посредством гомологичной рекомбинации. Также включены нацеливающие области, которые осуществляют нацеливание с использованием сайтов распознавания сайт-специфичной рекомбиназы (например, сайтов loxP или Frt). В некоторых вариантах осуществления нацеливающий конструкт настоящего изобретения дополнительно содержит нуклеотидную последовательность или особо интересующий ген, селектируемый маркер, управляющие и/или регуляторные последовательности и другие нуклеотидные последовательности, позволяющие выполнять рекомбинацию, опосредованную экзогенным добавлением белков, которые способствуют или облегчают рекомбинацию с участием таких последовательностей. В некоторых вариантах осуществления нацеливающий конструкт настоящего изобретения дополнительно содержит весь интересующий ген или его часть, причем интересующий ген представляет собой гетерологичный ген, кодирующий весь белок или его часть, который выполняет функцию, аналогичную функции белка, кодируемого эндогенной последовательностью.
Термин «разновидность» в контексте настоящего документа обозначает объект, который демонстрирует выраженную структурную идентичность с эталонным объектом, но имеет структурные отличия от эталонного объекта в присутствии или при определенном уровне содержания одного или более химических фрагментов по сравнению с эталонным объектом. Во многих вариантах осуществления разновидность также функционально отличается от эталонного объекта. В целом решение, является ли конкретный объект «разновидностью» эталонного объекта, основывается на степени его структурной идентичности эталонному объекту. Как будет понятно специалистам в данной области, любой биологический или химический эталонный объект имеет конкретные характерные структурные элементы. Разновидность по определению представляет собой отдельный химический объект, который включает в себя один или более таких характерных структурных элементов. Можно привести следующие примеры: небольшая молекула может иметь характерный основной структурный элемент (например, макроциклическое ядро) и/или один или более характерных боковых фрагментов так, что разновидностью небольшой молекулы является молекула, включающая в себя основной структурный элемент и характерные боковые фрагменты, но имеющая отличающиеся другие боковые фрагменты и/или типы связей (одиночная или двойная, Е или Z и т.д.) внутри центральной части; полипептид может иметь характерный элемент последовательности, содержащий множество аминокислот, имеющих определенные положения по отношению друг к другу в линейном или трехмерном пространстве и/или выполняющих конкретную биологическую функцию; нуклеиновая кислота может иметь характерный элемент последовательности, содержащий множество нуклеотидных остатков, имеющих определенные положения по отношению друг к другу в линейном или трехмерном пространстве. Например, разновидность полипептида может отличаться от эталонного полипептида вследствие одного или более отличий в аминокислотной последовательности и/или одного или более отличий в химических фрагментах (например, углеводах, липидах и т.д.), ковалентно связанных с полипептидным остовом. В некоторых вариантах осуществления общая идентичность последовательности разновидности полипептида с эталонным полипептидом составляет по меньшей мере 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97% или 99%. Альтернативно или дополнительно в некоторых вариантах осуществления разновидность полипептида не имеет по меньшей мере одной общей характерной последовательности с эталонным полипептидом. В некоторых вариантах осуществления эталонный полипептид выполняет одно или более биологических действий. В некоторых вариантах осуществления разновидность полипептида выполняет одно или более общих биологических действий с эталонным полипептидом. В некоторых вариантах осуществления разновидность полипептида не может выполнять одно или более общих биологических действий с эталонным полипептидом. В некоторых вариантах осуществления разновидность полипептида демонстрирует сниженный уровень одного или более биологических действий по сравнению с эталонным полипептидом. Во многих вариантах осуществления интересующий полипептид считается «разновидностью» исходного или эталонного полипептида, если аминокислотная последовательность интересующего полипептида идентична аминокислотной последовательности исходного полипептида, но имеет небольшое число изменений последовательности в определенных положениях. Обычно в разновидности замещено менее 20%, 15%, 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2% остатков по сравнению с исходным соединением. В некоторых вариантах осуществления разновидность имеет 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1 замещенный остаток по сравнению с исходным соединением. Часто разновидность имеет очень малое число (например, меньше 5, 4, 3, 2 или 1) замещенных функциональных остатков (т.е. остатков, которые участвуют в конкретном биологическом действии). Кроме того, разновидность обычно имеет не более 5, 4, 3, 2 или 1 добавления или делеции и часто не имеет добавлений или делеций по сравнению с исходным соединением. Более того, количество любых добавлений или делеций составляет обычно менее чем приблизительно 25, приблизительно 20, приблизительно 19, приблизительно 18, приблизительно 17, приблизительно 16, приблизительно 15, приблизительно 14, приблизительно 13, приблизительно 10, приблизительно 9, приблизительно 8, приблизительно 7, приблизительно 6 и чаще всего менее чем приблизительно 5, приблизительно 4, приблизительно 3 или приблизительно 2 остатка. В некоторых вариантах осуществления исходный или эталонный полипептид представляет собой встречающийся в природе полипептид. Как будет понятно обычным специалистам в данной области, множество разновидностей конкретного интересующего полипетида в большинстве случаев могут встречаться в природе, в особенности если интересующий полипептид представляет собой полипептид инфекционного агента.
Термин «вектор» в контексте настоящего документа обозначает молекулу нуклеиновой кислоты, способную транспортировать другую нуклеиновую кислоту, с которой она связана. В некоторых вариантах осуществления векторы способны выполнять экстрахромосомную репликацию и/или экспрессию нуклеиновых кислот, с которыми они связаны в клетке-хозяине, такой как эукариотическая и/или прокариотическая клетка. Векторы, способные направлять экспрессию функционально связанных генов, называются в настоящем документе «векторами экспрессии».
Термин «дикий тип» в контексте настоящего документа имеет значение, соответствующее принятому в данной области и обозначает объект, имеющий такую структуру и/или вид действия, которые встречаются в природе в «нормальном» (в противоположность мутантному, болезненному, поврежденному) состоянии или контексте. Обычным специалистам в данной области будет понятно, что гены и полипептиды дикого типа часто существуют во множестве различных форм (например, аллелей).
В следующих разделах подробно описаны различные аспекты изобретения. Использование разделов не является ограничивающим изобретение. Каждый раздел можно применять к любому аспекту изобретения. В этой заявке применение союза «или» означает «и/или», если не указано иное.
ПОДРОБНОЕ ОПИСАНИЕ
В настоящем изобретении предложены, в числе прочего, улучшенные и/или искусственно созданные не относящиеся к человеку животные, имеющие гуманизированный генетический материал, кодирующий рецептор FcγRI, которые предназначены для проведения экспериментов по изучению человеческих или человекоподобных иммунных эффекторных ответов. Fc-рецепторы
Рецепторы для Fc-участков (то есть константных участков) иммуноглобулинов (FcR) играют важную роль в регуляции иммунного ответа. FcR присутствуют на А-клетках иммунной системы организма-хозяина для облегчения удаления чужеродных антигенов, связанных антителом. FcR также играют важные роли в уравновешивании активирующих и ингибирующих ответов А-клеток иммунной системы. FcR участвуют в фагоцитозе макрофагами, дегрануляции тучных клеток, поглощении комплексов «антиген-антитело» и модуляции иммунного ответа, а также в других процессах иммунной системы.
У мышей и людей отдельные FcR дифференцированно экспрессируются на поверхности различных А-клеток, каждая из которых является специфичной в отношении изотипов иммуноглобулина, присутствующих в составе экспрессированных антител. Например, антитела иммуноглобулины G (IgG) опосредуют эффекторные функции через рецепторы IgG (FcγR). FcγR разделяются на четыре группы: высокоаффинные активирующие FcγRI (CD64), низкоаффинные ингибирующие FcγRIIb (CD32b), низкоаффинные активирующие FcgRIIa/c (CD32a/c) и низкоаффинные активирующие FcγRIII (CD 16). Хотя каждая группа имеется как у мышей, так и у человека, число изоформ и субпопуляций иммунных клеток, на которых они присутствуют, различны. Например, Fcγ RIIA и FcγRIIIB экспрессируются на А-клетках у людей, но, по имеющимся данным, отсутствуют у мышей. Кроме того, аффинности различных изотипов IgG (например, IgG 1) для каждого FcγR у мышей и людей отличаются. Высокоаффинный человеческий FcγRI
Человеческий высокоаффинный FcγRI (CD64) представляет собой встроенный в мембрану гликопротеин, который связывается с мономерными антителами типа IgG с высокой аффинностью (Ka обычно составляет приблизительно от 10-8 до 10-9 М). После связывания с IgG CD64 взаимодействует со вспомогательной цепью, известной как общая γ-цепь (γ-цепь), имеющей иммунорецепторный тирозиновый активирующий мотив (ITAM), который запускает клеточную активацию. Сообщается, что у людей CD64 конститутивно экспрессируется на макрофагах и моноцитах и индуцируемо экспрессируется на полиморфно-ядерных лейкоцитах посредством цитокинов, таких как IFNy и Г-КСФ.
Последовательности FcγRI
Примеры последовательностей человеческого, мышиного и гибридизированного FcγRI приведены в таблице 3. В последовательностях кДНК следующие друг за другом экзоны разделяются чередующимся подчеркнутым текстом. В последовательностях белка подчеркнуты внеклеточные последовательности. Эталонные последовательности являются иллюстративными; специалисты в данной области смогут определить и сравнить элементы последовательности или степени идентичности, чтобы распознать дополнительные мышиные или человеческие последовательности.

Не относящиеся к человеку животные с гуманизированным FcγRI
Предложены не относящиеся к человеку животные, которые экспрессируют гуманизированные белки рецептора FcγRI на поверхности иммунных клеток (например, миелоидных клеток) не относящихся к человеку животных, созданные посредством генетической модификации эндогенного локуса не относящегося к человеку животного, который кодирует белок FcγRI. Подходящие примеры, описанные в настоящем документе, включают грызунов, в частности мышей.
Гуманизированный эндогенный ген FcγRI в некоторых вариантах осуществления содержит генетический материал гетерологичного вида (например, людей), причем гуманизированный эндогенный ген FcγRI кодирует белок FcγRI, который содержит кодируемый участок генетического материала гетерологичного вида. В некоторых вариантах осуществления гуманизированный эндогенный ген FcγRI настоящего изобретения содержит геномную ДНК гетерологичного вида, соответствующую внеклеточному участку белка FcγRI, который экспрессируется на плазматической мембране клетки. Также предложены не относящиеся к человеку животные, эмбрионы, клетки и нацеливающие конструкты для создания не относящихся к человеку животных, нечеловеческих эмбрионов и клеток, содержащих указанный гуманизированный эндогенный ген FcγRI.
В некоторых вариантах осуществления эндогенный локус FcγRI удален. В некоторых вариантах осуществления эндогенный локус FcγRI изменен, причем участок эндогенного локуса FcγRI заменен гетерологичной последовательностью (например, полной последовательностью человеческого FcγRI или ее частью). В некоторых вариантах осуществления весь или по существу весь эндогенный локус FcγRI заменен гетерологичным локусом (например, человеческим локусом FcγRI). В некоторых вариантах осуществления участок гетерологичного локуса FcγRI вставлен в эндогенный нечеловеческий локус FcγRI. В некоторых вариантах осуществления гетерологичный локус представляет собой человеческий локус.
Не относящееся к человеку животное настоящего изобретения в эндогенном нечеловеческом локусе FcγRI содержит весь человеческий ген FcγRI или его часть. Таким образом, такое не относящееся к человеку животное можно описать как имеющее гетерологичный ген FcγRI. Замененный, вставленный или модифицированный эндогенный локус FcγRI можно обнаружить с помощью различных способов, включая, например, полимеразную цепную реакцию (ПНР), вестерн-блоттинг, саузерн-блоттинг, полиморфизм длин рестрикционных фрагментов (ПДРФ) или анализ на приобретение или утрату аллеля.
В различных вариантах осуществления гуманизированный ген FcγRI в соответствии с настоящим изобретением представляет собой ген FcγRI, который имеет третий, четвертый и пятый экзон, причем последовательность каждого по меньшей мере на 50% (например, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более) идентична третьему, четвертому и пятому экзону, присутствующему в гене человеческого FcγRI SEQ ID NO: 3.
В различных вариантах осуществления гуманизированный ген FcγRI в соответствии с настоящим изобретением представляет собой ген FcγRI, который имеет нуклеотидную кодирующую последовательность (например, последовательность кДНК) по меньшей мере на 50% (например, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более) идентичную нуклеотидам, присутствующим в SEQ ID NO: 5.
В различных вариантах осуществления гуманизированный белок FcγRI, продуцированный не относящимся к человеку животным настоящего изобретения, имеет внеклеточный участок, имеющий последовательность, которая по меньшей мере на 50% (например, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более) идентична внеклеточному участку человеческого белка FcγRI, представленного в таблице 3.
В различных вариантах осуществления гуманизированный белок FcγRI, продуцированный не относящимся к человеку животным настоящего изобретения, имеет внеклеточный участок, имеющий последовательность, которая по меньшей мере на 50% (например, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более) идентична аминокислотным остаткам 18-288, присутствующим в человеческом белке FcγRI SEQ ID NO: 4.
В различных вариантах осуществления гуманизированный белок FcγRI, продуцированный не относящимся к человеку животным настоящего изобретения, имеет аминокислотную последовательность, которая по меньшей мере на 50% (например, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более) идентична аминокислотной последовательности гуманизированного белка FcγRI, как, например, в SEQ ID NO: 5.
Предложены композиции и способы создания не относящихся к человеку животных, которые экспрессируют гуманизированный белок FcγRI, включая специфические полиморфные формы или разновидности аллелей (например, одиночные различия в аминокислотах), включая композиции и способы создания не относящихся к человеку животных, которые экспрессируют такие белки с человеческого промотора и человеческой регуляторной последовательности. В некоторых вариантах осуществления также предложены композиции и способы создания не относящихся к человеку животных, которые экспрессируют такие белки с эндогенного промотора и эндогенной регуляторной последовательности. Способы включают вставку полностью или частично генетического материала, кодирующего человеческий белок FcγRI, в точное местоположение в геноме не относящегося к человеку животного, которое соответствует эндогенному гену FcγRI, что приводит к созданию гуманизированного гена FcγRI, который экспрессирует белок FcγRI, являющийся полностью или частично человеческим. В некоторых вариантах осуществления способы включают вставку геномной ДНК, соответствующей экзонам 3-5 гуманизированного гена, кодирующего белок FcγRI, который содержит человеческий участок, содержащий аминокислоты, кодируемые вставленными экзонами.
Техника создания гуманизированного эндогенного гена FcγRI включает в себя относительно минимальную модификацию эндогенного гена и в различных вариантах осуществления приводит к природным FcγRI-опосредованным эффекторным ответам у не относящегося к человеку животного, поскольку геномная последовательность последовательностей FcγRI модифицируется в одном фрагменте и, следовательно, сохраняет нормальную функциональность вследствие включения необходимых регуляторных последовательностей. Таким образом, в этих вариантах осуществления модификация гена FcγRI не влияет на другие окружающие гены или другие эндогенные гены FcγRI. Кроме того, в различных вариантах осуществления модификация не влияет на сборку функционального рецептора на плазматической мембране и сохраняет нормальные эффекторные функции посредством связывания и последующей передачи сигнала через цитоплазматический участок рецептора, который в результате модификации изменяется минимально или не изменяется вообще.
На Фиг. 5 представлена схематическая иллюстрация (без соблюдения масштаба) эндогенного мышиного гена FcγRI и гуманизированного эндогенного гена FcγRI. Как показано на фигуре, геномная ДНК, содержащая экзоны 3-5 человеческого гена FcγRI, вставляется в локус эндогенного мышиного гена FcγRI посредством нацеливающего конструкта. Эта геномная ДНК включает в себя участок гена, который кодирует одну или более областей внеклеточных доменов (например, аминокислотные остатки 28-362) человеческого белка FcγRI, участвующих в связывании Fc.
Не относящееся к человеку животное (например, мышь), имеющая гуманизированный эндогенный ген FcγRI, может быть создана с помощью любого способа, известного в данной области. Например, может быть создан нацеливающий вектор, который встраивает весь человеческий ген FcγRI или его часть вместе с селектируемым маркерным геном. На Фиг. 5 показан геном мыши, содержащий вставку экзонов 1-5 человеческого FcγRI. Как показано на фигуре, нацеливающий конструкт содержит гомологичный участок на 5'-конце, содержащий последовательность перед экзоном 1 эндогенного мышиного гена FcγRI, затем фрагмент геномной ДНК, содержащий экзоны 1-5 человеческого гена FcγRI, кассету для отбора по чувствительности к лекарственному средству (например, ген устойчивости к неомицину, фланкированный с обеих сторон последовательностями loxF) и гомологичный участок на 3'-конце, содержащий последовательность за экзоном 6 эндогенного мышиного гена FcγRI. При гомологичной рекомбинации экзоны 1-5 и участок экзона 6 эндогенного мышиного гена FcγRI заменяются последовательностью, содержащейся в нацеливающем векторе. Создается гуманизированный эндогенный ген FcγRI, что приводит к получению клетки или не относящегося к человеку животного, которое экспрессирует гуманизированный белок FcγRI, содержащий аминокислоты, кодируемые экзонами 1-5 человеческого гена FcγRI. Кассета для отбора по чувствительности к лекарственному средству может быть необязательно удалена последующим добавлением рекомбиназы (например, обработкой Cre).
Кроме описанных в настоящем документе мышей, имеющих гуманизированные гены FcγRI, также предложены другие генетически модифицированные не относящиеся к человеку животные, которые содержат гуманизированные гены FcγRI. В некоторых вариантах осуществления такие не относящиеся к человеку животные содержат гуманизированный ген FcγRI, функционально связанный с эндогенным промотором FcγRI. В некоторых вариантах осуществления такие не относящиеся к человеку животные экспрессируют гуманизированный белок FcγRI с эндогенного локуса, причем гуманизированный белок FcγRI содержит аминокислотные остатки 16-290 человеческого белка FcγRI.
Таких не относящихся к человеку животных можно выбрать из группы, состоящей из мыши, крысы, кролика, свиньи, крупного рогатого скота (например, коровы, быка, буйвола), оленя, овцы, козы, цыпленка, кота, собаки, хорька, примата (например, мартышки, макаки-резус). В случае не относящихся к человеку животных, для которых отсутствуют легкодоступные приемлемые генетически модифицируемые эмбриональные стволовые (ЭС) клетки, для создания не относящегося к человеку животного, содержащего генетические модификации, описанные в настоящем документе, применяют другие способы. Такие способы включают, например, модификацию генома другой клетки, кроме эмбриональной стволовой (например, фибробласта или индуцированной плюрипотентной клетки), и использование ядерного переноса для переноса модифицированного генома в приемлемую клетку, например ооцит, и постепенное созревание модифицированной клетки (например, модифицированного ооцита) в не относящемся к человеку животном в приемлемых условиях для формирования эмбриона.
В некоторых вариантах осуществления не относящееся к человеку животное настоящего изобретения представляет собой млекопитающее. В некоторых вариантах осуществления не относящееся к человеку животное настоящего изобретения представляет собой мелкое млекопитающее, например, из надсемейства Dipodoidea или Muroidea. В некоторых вариантах осуществления генетически модифицированное животное настоящего изобретения представляет собой грызуна. В некоторых вариантах осуществления грызун настоящего изобретения выбран из мыши, крысы и хомяка. В некоторых вариантах осуществления грызун настоящего изобретения выбран из надсемейства Muroidea. В некоторых вариантах осуществления генетически модифицированное животное настоящего изобретения выбрано из семейства Calomyscidae (например, мышевидные хомячки), Cricetidae (например, хомяк, мыши и крысы Нового света, полевка), Muridae (мыши и крысы, песчанки, иглистые мыши, косматые хомяки), Nesomyidae (рипидомисы, скальные крысы, белохвостые крысы, малагасийские крысы и мыши), Platacanthomyidae (например, колючие соневидные хомяки) и Spalacidae (например, слепыши, бамбуковые крысы и цокоры). В некоторых вариантах осуществления генетически модифицированный грызун настоящего изобретения выбран из мыши или крысы (семейство Muridae), песчанки, иглистой мыши и косматого хомяка. В некоторых конкретных вариантах осуществления генетически модифицированная мышь настоящего изобретения является представителем семейства Muridae. В некоторых вариантах осуществления не относящееся к человеку животное настоящего изобретения представляет собой грызуна. В некоторых вариантах осуществления грызун настоящего изобретения выбран из мыши и крысы. В некоторых вариантах осуществления не относящееся к человеку животное настоящего изобретения представляет собой мышь.
В некоторых вариантах осуществления не относящееся к человеку животное настоящего изобретения представляет собой грызуна, который является мышью линии C57BL, выбранной из C57BL/A, C57BL/An, C57BL/GrFa, C57BL/KaLwN, C57BL/6, C57BL/6J, C57BL/6ByJ, C57BL/6NJ, C57BL/10, C57BL/10ScSn, C57BL/10Cr и C57BL/01a. В некоторых конкретных вариантах осуществления мышь настоящего изобретения представляет собой мышь линии 129, выбранную из группы, состоящей из линий 129Р1, 129Р2, 129Р3, 129Х1, 129S1 (например, 129S1/SV, 129S1/SvIm), 129S2, 129S4,129S5, 129S9/SvEvH, 129/SvJae, 129S6 (129/SvEvTac), 129S7, 129S8, 129T1, 129T2 (см., например, Festing et al., 1999, Mammalian Genome 10:836; Auerbach et al., 2000, Biotechniques 29(5): 1024-1028, 1030, 1032). В некоторых конкретных вариантах осуществления генетически модифицированная мышь настоящего изобретения представляет собой смесь вышеупомянутой линии 129 и вышеупомянутой линии C57BL/6. В некоторых конкретных вариантах осуществления мышь настоящего изобретения представляет собой смесь вышеупомянутых линий 129 или смесь вышеупомянутых линий BL/6. В некоторых конкретных вариантах осуществления линия 129 смеси, описанной в настоящем документе, представляет собой линию 129S6 (129/SvEvTac). В некоторых вариантах осуществления мышь настоящего изобретения представляет собой мышь линии BALB, например, линии BALB/c. В некоторых вариантах осуществления мышь настоящего изобретения представляет собой смесь линии BALB и другой вышеупомянутой линии.
В некоторых вариантах осуществления не относящееся к человеку животное настоящего изобретения представляет собой крысу. В некоторых конкретных вариантах осуществления крыса настоящего изобретения выбрана из крысы линии Вистар, линии LEA, линии Спрег-Доули, линии Фишер, F344, F6 и линии темные Агути. В некоторых конкретных вариантах осуществления линия крыс, описанная в настоящем документе, представляет собой смесь двух или более линий, выбранных из группы, состоящей из линий Вистар, LEA, Спрег-Доули, Фишер, F344, F6 и темные Агути. Не относящиеся к человеку животные, имеющие гуманизированные гены FcγRI
Мутантные и трансгенные по гену FcγR не относящиеся к человеку животные (например, мыши) описаны, например, van de Winkel et al в патенте США №6,111,166.
Таких животных использовали в анализах по оценке молекулярных аспектов экспрессии, функции и регуляции FcγRI. Однако они имеют ограничения и недостатки. Например, мышь, описанная в патенте '166, содержит человеческий FcγRI, случайным образом вставленный в ее геном, что: (1) может непреднамеренно нарушить экспрессию и/или функцию других генов (нарушение может быть выявлено или не выявлено); и (2) привести к экспрессии как полностью человеческого, так и полностью мышиного FcγRI, что усложняет или нарушает конкретное исследование отдельного типа FcγR. Более того, внутриклеточная сигнальная область α-цепи FcγRI может быть повреждена, разорвана или может иным образом не соответствовать нормальному FcγRI у мыши, описанной в патенте '116, так как внутриклеточная область α-цепи FcγRI, которая участвует в передаче сигнала, является человеческой, а не мышиной.
В настоящем изобретении предложены средства устранения этих и других недостатков. В настоящем изобретении предложен, среди прочего, гуманизированный трансген FcγRI, вставленный в эндогенный мышиный локус для замены мышиного FcγRI человеческим или гибридным геном FcγRI. В некоторых вариантах осуществления гибридный ген FcγRI вставлен в эндогенный мышиный локус, причем внеклеточный домен содержит человеческую последовательность, а внутриклеточный домен содержит мышиную последовательность. В некоторых вариантах осуществления вставка гибридного гена FcγRI в эндогенный локус мышиного гена FcγRI обеспечивает экспрессию белка FcγRI на иммунных клетках, которая имеет большее сходство с распределением человеческого белка FcγRI на клетках иммунной системы по сравнению с распределением экспрессии человеческого белка FcγRI на иммунных клетках мыши, на которых дополнительно экспрессируется эндогенный мышиный белок FcγRI. В некоторых вариантах осуществления вставка гибридного гена FcγRI в эндогенный локус мышиного гена FcγRI обеспечивает экспрессию белка FcγRI на иммунных клетках, которая индуцируется и регулируется соответствующими сигналами и стимулами.
В некоторых вариантах осуществления опосредованная α-цепью FcγRI презентация антигенов главного комплекса гистосовместимости (МНС) класса II функционально сохраняется у мышей, имеющих гибридный белок FcγRI с гуманизированной внеклеточной областью и внутриклеточной областью мышиной α-цепи FcγRI. В некоторых вариантах осуществления внутриклеточный процессинг интернализированного FcγRI сохраняется у мыши, имеющей гибридный белок FcγRI с мышиной внутриклеточной областью, по сравнению с мышью, имеющей полностью человеческий белок FcγRI или белок FcγRI с не мышиной внутриклеточной областью.
Не относящиеся к человеку животные настоящего изобретения обеспечивают улучшенную in vivo систему и источник биологических материалов (например, клеток), экспрессирующих человеческий FcγRI, который используется для различных анализов. В различных вариантах осуществления не относящиеся к человеку животные настоящего изобретения используются для разработки лекарственных средств, которые оказывают целевое воздействие на FcγRI и/или модулируют FcγRI-опосредованную передачу сигналов и иммунные эффекторные ответы. В различных вариантах осуществления мыши настоящего изобретения используются для скрининга и разработки потенциальных лекарственных средств (например, антител), которые связываются с FcγRI. В различных вариантах осуществления не относящиеся к человеку животные настоящего изобретения используются для определения иммунного эффекторного ответа, связанного с конкретным терапевтическим антителом.
Генетически модифицированные не относящиеся к человеку животные, которые не экспрессируют эндогенные высокоаффинные мышиные гены FcγR, используются, например, для изучения различных функций отдельных высокоаффинных генов FcγR в иммунном ответе, для измерения эффективности человеческого терапевтического антитела посредством клеточного иммунитета (например, ADCC), для определения роли FcγR в иммунных заболеваниях или расстройствах, для использования в качестве моделей иммунных заболеваний или расстройств, для создания антител к одному или более белкам FcγR и для разведения с целью создания других генетически модифицированных мышей, представляющих интерес.
В одном варианте осуществления мышь в соответствии с настоящим изобретением может использоваться для определения потери цитотоксического эффекта (по сравнению с мышью дикого типа) мышью, которая не экспрессирует высокоаффинные гены FcγR, посредством введения такой мыши агента, который обладает известной способностью запускать FcγR-зависимый цитотоксический эффект у мышей дикого типа. В одном варианте осуществления мыши настоящего изобретения имплантируют опухолевые клетки и через некоторое время вводят с помощью инъекции антитело, специфичное к антигену, экспрессированному на поверхности опухолевых клеток. Изотип антитела известен до выполнения инъекции, и животных анализируют на нарушение FcγR-зависимой ADCC по сравнению с ADCC, наблюдаемой у животных дикого типа.
В одном аспекте мышей, дефицитных по эндогенным высокоаффинным рецепторам, можно объединять (например, посредством селекции) с другими иммунодефицитными мышами для создания in vivo моделей аутоиммунного заболевания. Например, в данной области часто используются мыши с тяжелым комбинированным иммунодефицитом (SCID) в качестве моделей организмов для исследования внутренней системы. У мышей Scm нарушена способность продукции Т- или В-лимфоцитов или активации некоторых компонентов системы комплемента, и они не могут эффективно бороться с инфекциями, уничтожать опухоли и отторгать трансплантаты. Мыши настоящего изобретения, дефицитные по гену а-субъединицы высокоаффинного FcγR, могут скрещиваться с мышами со SCID для обеспечения уменьшения количества клеток в животном-хозяине в ответ на введение терапевтического антитела (например, противоопухолевого антитела), что позволит определить роли ADCC и комплемент-зависимой цитотоксичности (CDC) в уменьшении опухолевых клеток in vivo.
В некоторых вариантах осуществления предложены генетически модифицированные не относящиеся к человеку животные, у которых эндогенные высокоаффинные гены FcγR заменены высокоаффинными человеческими генами FcγR. Таких животных можно использовать для исследования фармакокинетики полностью человеческих антител и FcγR-опосредованной ADCC. Кроме того, показано, что человеческие гены FcγR имеют полиморфные или аллельные разновидности, связанные с заболеванием. Таким образом, генетически модифицированные не относящиеся к человеку животные, у которых эндогенные высокоаффинные гены FcγR заменены определенными аллельными или полиморфными формами человеческих генов FcγR, могут использоваться для исследования человеческих аутоиммунных заболеваний и характерных особенностей, связанных с полиморфизмом, у животных. В некоторых вариантах осуществления аллельные формы человеческих генов FcγR связаны с повышенной эффективностью человеческого IgG.
В некоторых вариантах осуществления определяют влияние полиморфизма человеческого высокоаффинного FcγR на эффективность человеческого терапевтического антитела. В некоторых вариантах осуществления противоопухолевое антитело вводят первой гуманизированной мыши, содержащей первый полиморфизм человеческого FcγR, а также второй гуманизированной мыши, содержащей второй полиморфизм человеческого FcγR, причем как первая, так и вторая мыши содержат человеческую опухолевую клетку; и противоопухолевую активность противоопухолевого антитела оценивают у первой мыши и у второй мыши.
В некоторых вариантах осуществления тип лечения выбирает врач с учетом лечения человека, имеющего первый или второй полиморфизм, и имеющего опухоль, соответствующую человеческой опухолевой клетке, на основании оценки эффективности противоопухолевого антитела у первой мыши и у второй мыши.
Способ замены α-цепи эндогенного FcγRI включает относительно минимальное нарушение сигнальной трансдукции, опосредованной природным FcγRI, у животного. В различных вариантах осуществления геномная последовательность α-цепей FcγR заменена в одном фрагменте и, следовательно, сохраняет нормальную функциональность посредством включения необходимых регуляторных последовательностей. Таким образом, в таких вариантах осуществления модификация α-цепи FcγR не влияет на другие эндогенные FcR, зависимые от молекул функциональной γ-цепи FcR. Дополнительно, в различных вариантах осуществления модификация не влияет на сборку функционального комплекса рецептора, включающего в себя α-цепь FcγR и эндогенную γ-цепь FcR, что может иметь важное значение для правильной экспрессии некоторых α-цепей FcγR на поверхности клетки и для передачи далее определенных сигналов, возникающих в связи с активацией рецептора. В связи с тем, что γ-цепь FcR не удалена, в различных вариантах осуществления животные, у которых эндогенные гены α-цепи FcγR заменены человеческими генами α-цепи FcγR, могут воспроизводить нормальные эффекторные функции антител посредством связывания Fc-участка иммуноглобулинов IgG с человеческими α-цепями FcγR, присутствующими на поверхности А-клеток.
Не относящиеся к человеку животные настоящего изобретения экспрессируют гуманизированный белок FcγRI, поэтому могут быть созданы клетки, клеточные линии и клеточные культуры в качестве источника гуманизированного FcγRI для использования в анализах связывания и функциональных анализах, например, для оценки связывания или реакции FcγRI на потенциальное терапевтическое антитело. В различных вариантах осуществления гуманизированный белок FcγRI, экспрессируемый не относящимся к человеку животным, в соответствии с настоящим описанием может содержать разновидность аминокислотной последовательности. Сообщается о разновидностях человеческих белков FcγRI, имеющих вариации, связанные с остатками, связывающими лиганд. В различных вариантах осуществления не относящиеся к человеку животные настоящего изобретения экспрессируют разновидность гуманизированного белка FcγRI. В различных вариантах осуществления разновидность является полиморфной в положении аминокислоты, ассоциированном со связыванием лиганда. В различных вариантах осуществления не относящиеся к человеку животные настоящего изобретения используются для определения иммунного эффекторного ответа терапевтического антитела посредством взаимодействия с полиморфной разновидностью человеческого FcγRI.
Клетки не относящихся к человеку животных настоящего изобретения могут быть изолированы и использованы для данного конкретного случая или могут быть сохранены в культуре в течение многих поколений. В различных вариантах осуществления клетки не относящегося к человеку животного настоящего изобретения являются иммортализованными и поддерживаются в культуре неопределенно долго (например, в последовательных культурах).
Не относящиеся к человеку животные настоящего изобретения обеспечивают улучшенную in vivo систему для изучения механизмов антителозависимой клеточноопосредованной цитотоксичности.
ПРИМЕРЫ
Следующие примеры приведены для того, чтобы описать обычным специалистам в данной области, как создать и использовать способы и композиции изобретения. Эти примеры не предназначены для ограничения объема того, что авторы рассматривают в качестве их изобретения. При отсутствии иных указаний температура приведена в градусах по Цельсию, а давление равно или приблизительно равно атмосферному.
Пример 1. Гуманизация эндогенного гена FcγRI
В данном примере продемонстрированы иллюстративные способы гуманизации эндогенного гена, кодирующего высокоаффинный FcγRI, у не относящегося к человеку млекопитающего, такого как грызун (например, мышь). Создание нацеливающего вектора гуманизации FcγRI (MAID 6074)
Крупный нацеливающий вектор (LTVEC) был создан с использованием человеческого гена Fc-гамма-рецептора 1 (область промотора, сигнальная область плюс область эктодомена) для замены эквивалентной последовательности мыши на мышиной хромосоме 3.
Создание нацеливающих векторов на основе ВАС (МАЮ 6073)
Мышиная ВАС RP23-477p23 и человеческая ВАС CTD-2339o22, содержащие ген FcγRI, были идентифицированы с помощью концевой последовательности бласта и ВАС на основании базы данных NCBI и Ensemble.
Техника создания нацеливающих векторов, а именно LTVEC, содержащего человеческую последовательность от промотора (25 т.п.о.) гена FcγRI (дистальный 5'-конец) до проксимального 3'-конца на ко доне W290 (перед трансмембранным доменом (ТМ)) человеческого гена FcγRI (за которым расположены мышиный трансмембранный домен и оставшаяся часть гена), включает описанные ниже этапы.
На первом этапе путем гомологичной рекомбинации в бактериях удаляют 5'-конец человеческой последовательности из человеческой BAC(CTD-2339o22) и оставляют сайт I-Ceul и область промотора гена FcγRI размером 25 т.п.о., 3'-конец человеческой последовательности удаляют с помощью кассеты loxped pgk-Neo, расположенной в интроне 5 (404 п. о. в направлении против хода транскрипции от домена ТМ) гена FcγR1, за которым находится сайт AsiS1.
На втором этапе путем гомологичной рекомбинации в бактериях (в мышиной ВАС RP23-477p23) удаляют мышиный ген FcγRI (от промотора (20 т.п.о.) до трансмембранного домена) с помощью кассеты Spec (перед мышиным ТМ добавляют 8 АА домена ЕС3 человеческой последовательности FcγRI (до кодона W290)), фланкированной сайтами I-Ceul и AsiS1.
На третьем этапе выполняют расщепление и лигирование сайтов I-Ceul и AsiS1 для создания LTVEC (MAID 6073), содержащего человеческую последовательность от промотора (25 т.п.о.) гена FcγRI (дистальный 5'-конец) до проксимального 3'-конца на кодоне W290 (перед трансмембранным доменом) человеческого гена FcγRI, за которым расположены мышиный трансмембранный домен и оставшаяся часть гена.
На Фиг. 32 изображена в виде схемы иллюстративная стратегия гуманизации FcγRI мыши. MAID 6074 представляет собой версию MAID 6073 с удаленной кассетой. Соединительные последовательности показаны на Фиг. 6. Выбор целевых эмбриональных стволовых клеток
LTVEC MAID 6074 был внедрен путем электропорации в мышиную линию эмбриональных стволовых клеток F1H4.
Пример 2. Создание гуманизированных мышей с высокоаффинным FcγRI
В данном примере показаны способы трансформации и разведения мышей. LTVEC с эктодоменом hFcgRI (MAID 6073) был внедрен путем электропорации в исходные мышиные эмбриональные стволовые (ЭС) клетки F1H4. Колонии, выжившие в результате отбора по чувствительности к лекарственному средству G418, собрали и подвергли скринингу на наличие гомологичной рекомбинации человеческой последовательности FcγRI в мышиный локус FcγRI. Определили, что восемь клонов имеют подходящую модификацию и являются гетерозиготными по человеческому эктодомену FcγRI, один из них представлял собой клон 6073F-D2. Все эти клоны содержали кассету neo.
Клон 6073F-D2 подвергли электропорации с 2 мкг плазмиды Cre для удаления кассеты neo. Колонии собрали, а затем подвергли скринингу на отсутствие кассеты пео. Из тех клонов, в которых определили, что кассета neo была удалена, клонам ЭС-клеток 6074 В-А1 и 6074 В-А10 выполнили микроинъекции с использованием способа VelociMouse.
Из клонов 6074 В-А1 и 6074 В-А10 создали самцов и самок (самок XY) VelociMice поколения F0. Этих мышей F0 разводили, спаривая их друг с другом внутри одного клона и между клонами. Создали мышей F1, и эти мыши были гетерозиготными и гомозиготными (и дикого типа) по человеческому FcγRI. Внешний вид мышей F1 был нормальным, и соотношение гомозиготных мышей к гетерозиготным и к мышам дикого типа (Нот: Het: WT) соответствовало расчетному менделевскому соотношению 1:2:1. Когорты самцов и самок дикого типа и гомозиготных по человеческому гену FcγRI использовали для исследования.
Пример 3. Определение характеристик гуманизированных мышей с высокоаффинным FcγRI
В данном примере показана типичная экспрессия высокоаффинного белка FcγRI на поверхности клеток не относящихся к человеку животных, искусственно созданных и содержащих гуманизированный конструкт гена FcγRI, описанный в примере 1 в эндогенном локусе FcγRI.
Определение генотипических характеристик гуманизированных мышей с высокоаффинным FcγRI показано на Фиг. 1-3. Транскрипт для мышиного FcγRI не обнаружен у мышей, гомозиготных по гуманизированному FcγRI.
Результаты характеризации по фенотипу представлены на Фиг. 4 и 7-16.
Пример 4. Определение фенотипических характеристик гуманизированных мышей с высокоаффинным FcγRI, которым вводили мышиный гранулоцитарный колониестимулирующий фактор (мГ-КСФ)
Выполнили анализ фенотипа мышей МАШ 6074 (hFcγRI) НО, которым вводили мышиный Г-КСФ (мГ-КСФ), по сравнению с контрольными животными, получавшими натрий-фосфатный буфер (PBS). Мышей исследовали через 48 часов после подкожной инъекции. Данные показаны для мышей MAID 6074 WT в возрасте 6-7 недель, которым вводили PBS (n=2) или мГ-КСФ (n=2), по сравнению с мышами MAID 6074 НО, которым вводили PBS (n=2) или мГ-КСФ (n=3). Результаты были схожими для мышей MAID 6074 WT в возрасте 16-17 недель, которым вводили PBS (n=1) или мГ-КСФ (n=1), по сравнению с мышами MAID 6074 НО, которым вводили PBS (n=1) или мГ-КСФ (n=1). На Фиг. 17-31 показана исходная (PBS) и индуцированная мГ-КСФ экспрессия мышиного и гибридизированного FcγRI на моноцитах, макрофагах, нейтрофилах и дендритных клетках в крови и селезенке мышей MAID 6074 WT и MAID 6074 НО.
Мыши MAID 6074 НО, которым не вводили никаких препаратов, экспрессируют мРНК FcγRI (CD64) в крови, хотя белок не был обнаружен с помощью FACS. Г-КСФ (48 часов) индуцировал увеличение мРНК FcγRI (CD64) в крови и селезенке, а также белка при определении с помощью FACS.
Пример 5. Определение фенотипических характеристик мышей, экспрессирующих гуманизированные высокоаффинные и низкоаффинные рецепторы Fcγ
С использованием стандартных техник разведения создали мышей, которые экспрессируют гуманизированные высокоаффинные и низкоаффинные рецепторы Fcγ. А именно, мышей, экспрессирующих гуманизированные высокоаффинные FcγRI, созданных, как описано в примерах 1 и 2, скрестили с мышами, экспрессирующими гуманизированные низкоаффинные FcγRIIa, FcγRIIb, FcγRIIc, FcγRIIIa и FcγRIIIb, созданными, как описано в примерах 1-6 и показано на Фиг. 1-6 заявки на патент США №2014/0154701, которая включена в настоящий документ путем ссылки. Полученных мышей разводили до достижения гомозиготности.
После введения мышиного Г-КСФ (мГ-КСФ) или натрий-фосфатного буфера (PBS) выполнили фенотипический анализ у гуманизированных мышей с высокоаффинными и низкоаффинными FcγR. Мышам вводили подкожную инъекцию PBS или мГ-КСФ (62 мкг подкожно, однократная доза). Через 48 часов у получавших инъекции мышей собирали кровь и селезенки и определяли фенотипические характеристики с помощью FACS, как описано в примере 4. Фенотип клеточной поверхности мышей с гуманизированными высокоаффинными и низкоаффинными FcγR был схожим с фенотипом, наблюдаемым у мышей с гуманизированными высокоаффинными FcγR. Также, подобно мышам с гуманизированным высокоаффинным рецептором Fcγ, мыши, у которых был гуманизирован как высокоаффинный, так и низкоаффинный рецептор Fcγ, демонстрировали увеличение экспрессии человеческого FcγRI в моноцитах, макрофагах и нейтрофилах крови и селезенки. Итак, гуманизация низкоаффинных рецепторов Fcγ у мышей с гуманизированным FcγRI не приводила к выраженному изменению фенотипа.
Эквиваленты
Таким образом, после описания нескольких аспектов по меньшей мере одного варианта осуществления настоящего изобретения, специалистам в данной области должно быть понятно, что можно легко выполнить различные изменения, модификации и улучшения. Предполагается, что такие изменения, модификации и улучшения будут частью настоящего описания и будут находиться в рамках сущности и объема изобретения. Соответственно, вышеизложенное описание и чертежи приведены только в качестве примера, а изобретение подробно описано в приведенной ниже формуле изобретения.
Использование обозначающих порядок терминов, таких как «первый», «второй», «третий» и т.д., в формуле изобретения для определения заявляемого элемента формулы изобретения само по себе не подразумевает какой-либо приоритет, предшествование или расположение в определенном порядке одного элемента формулы изобретения по сравнению с другим или временной порядок, в котором выполняются этапы способа, но используется исключительно в качестве отметки с целью отличить один элемент формулы изобретения, имеющий определенное название, от другого элемента с таким же названием (кроме использования обозначающего порядок термина) для различения элементов формулы изобретения.
При использовании в настоящем описании и в формуле настоящего изобретения форм единственного числа, при отсутствии ясных иных указаний, они обозначают включение множества объектов. Пункты формулы изобретения или описания, которые включают союз «или» между одним или более элементов группы, являются выполненными, если один, более одного или все элементы группы присутствуют, используются или иным образом связаны с данным продуктом или процессом, если не указано противоположное или из контекста не очевидно иное. Изобретение включает варианты осуществления, в которых ровно один элемент группы присутствует, используется или иным образом связан с данным продуктом или процессом. Изобретение также включает варианты осуществления, в которых более одного или все элементы группы присутствуют, используются или иным образом связаны с данным продуктом или процессом. Кроме того, следует понимать, что настоящее изобретение охватывает все варианты, комбинации и перестановки, в которых одно или более ограничений, элементов, условий, описательных терминов и т.п.из одного или более перечисленных пунктов формулы изобретения включены в другой пункт формулы изобретения, зависимый от того же исходного пункта (или, если применимо, любого другого пункта), если не указано иное или если специалисту в данной области не будет очевидно, что возникнет противоречие или несоответствие. Если элементы представлены в виде перечней (например, в группе Маркуша или схожем формате), следует понимать, что также описана каждая подгруппа элементов, и любой(-ые) элемент(-ы) можно удалить из группы. Следует понимать, что в целом, если изобретение или аспекты изобретения содержат конкретные элементы, признаки и т.д., конкретные варианты осуществления изобретения или аспекты изобретения состоят, или по существу состоят из таких элементов, признаков и т.д. С целью упрощения эти варианты осуществления в настоящем документе специально не были описаны в каждом случае именно таким образом. Также следует понимать, что любой вариант осуществления или аспект изобретения может быть в прямой форме исключен из формулы изобретения, вне зависимости от того, присутствует ли в описании такое особое исключение.
Специалистам в данной области будут понятны типичные стандартные отклонения или погрешности, относящиеся к величинам, полученным в анализах или других процессах, описанных в настоящем документе.
| название | год | авторы | номер документа |
|---|---|---|---|
| ОПОСРЕДОВАННЫЕ ГУМАНИЗИРОВАННЫМИ Т-КЛЕТКАМИ ИММУННЫЕ ОТВЕТЫ У НЕ ОТНОСЯЩИХСЯ К ЧЕЛОВЕКУ ЖИВОТНЫХ | 2016 |
|
RU2732628C2 |
| ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫЕ МЫШИ, ЭКСПРЕССИРУЮЩИЕ ХИМЕРНЫЕ МОЛЕКУЛЫ ГЛАВНОГО КОМПЛЕКСА ГИСТОСОВМЕСТИМОСТИ | 2012 |
|
RU2660564C2 |
| ГЕНЕТИЧЕСКИ МОДИФИЦИРОВАННЫЕ МЫШИ, ЭКСПРЕССИРУЮЩИЕ ХИМЕРНЫЕ МОЛЕКУЛЫ ГЛАВНОГО КОМПЛЕКСА ГИСТОСОВМЕСТИМОСТИ | 2012 |
|
RU2797549C2 |
| ГУМАНИЗИРОВАННЫЕ ГРЫЗУНЫ ДЛЯ ТЕСТИРОВАНИЯ ТЕРАПЕВТИЧЕСКИХ АГЕНТОВ | 2019 |
|
RU2805212C2 |
| ГУМАНИЗИРОВАННАЯ МОДЕЛЬ НАРУШЕНИЙ СО СТОРОНЫ ПОЧЕК И ПЕЧЕНИ | 2018 |
|
RU2772583C2 |
| ЖИВОТНЫЕ, СОДЕРЖАЩИЕ ГУМАНИЗИРОВАННУЮ ДИПЕПТИДИЛПЕПТИДАЗУ IV (DPP4) | 2015 |
|
RU2648166C1 |
| ЖИВОТНЫЕ С ГУМАНИЗИРОВАННЫМ ГЕНОМ IL-15 | 2014 |
|
RU2674910C2 |
| ГУМАНИЗИРОВАННЫЕ ЖИВОТНЫЕ ПО С5 И С3 | 2015 |
|
RU2713327C2 |
| ГУМАНИЗИРОВАННЫЕ FCγR МЫШИ | 2010 |
|
RU2549695C2 |
| ЖИВОТНЫЕ С ГУМАНИЗИРОВАННЫМИ IL-4 И IL-4Rα | 2015 |
|
RU2788523C2 |
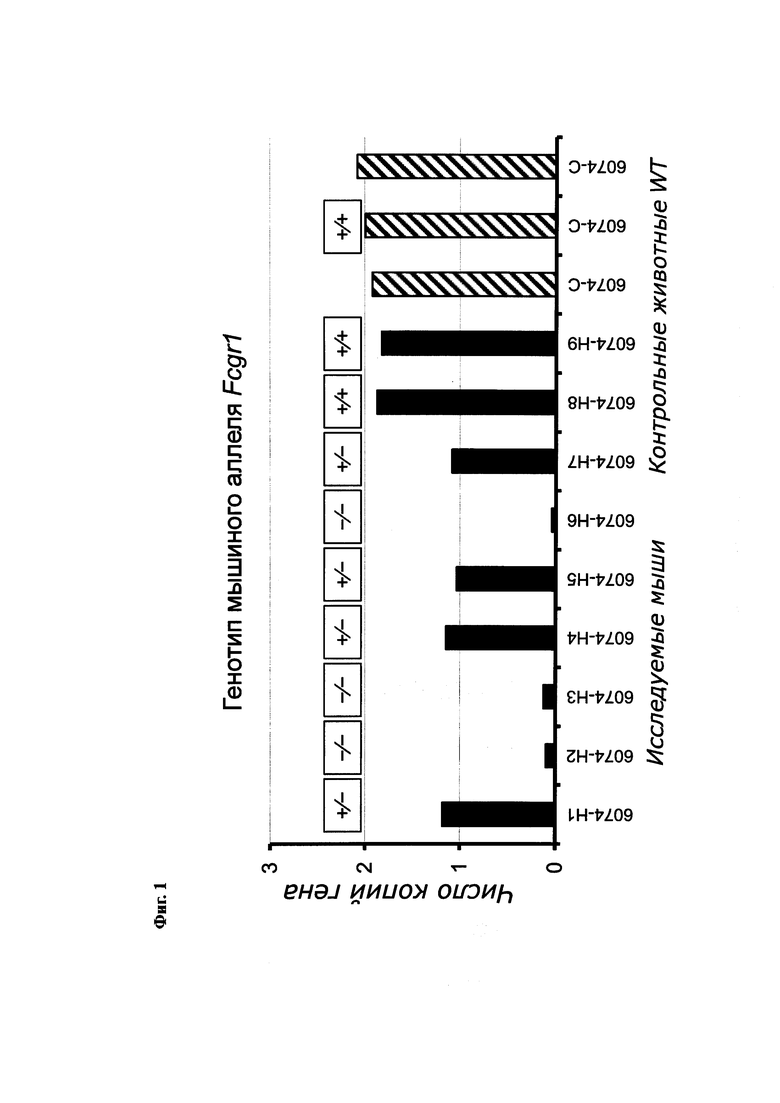

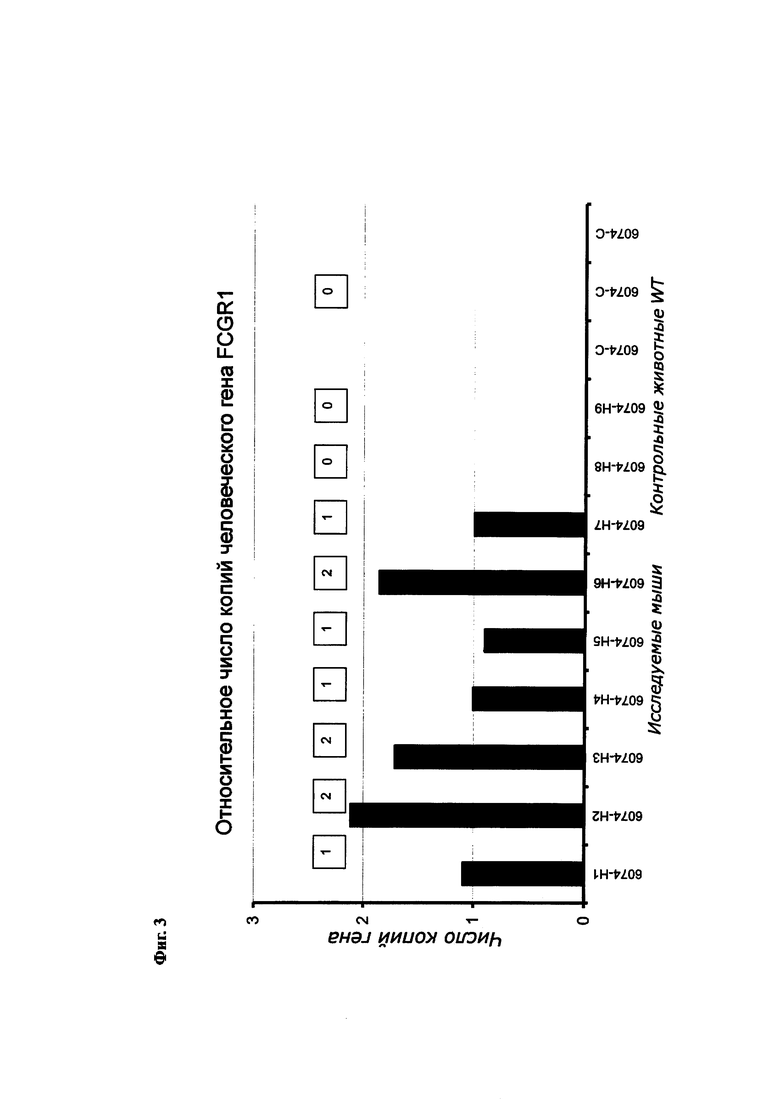
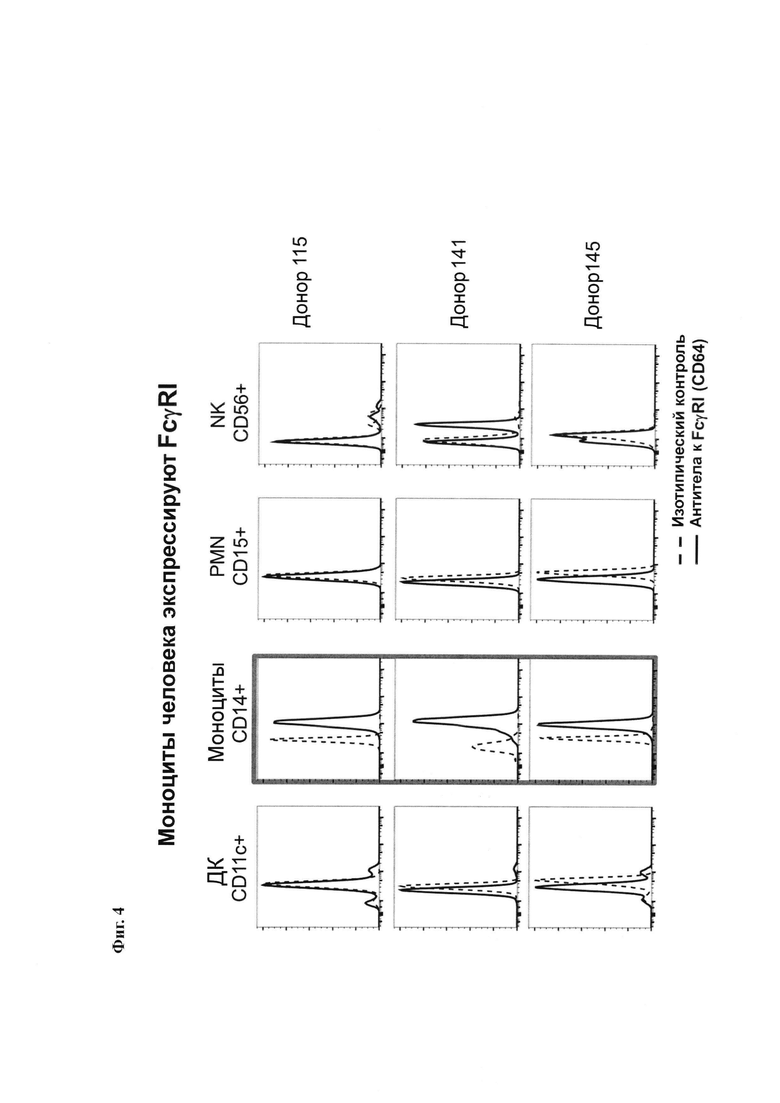
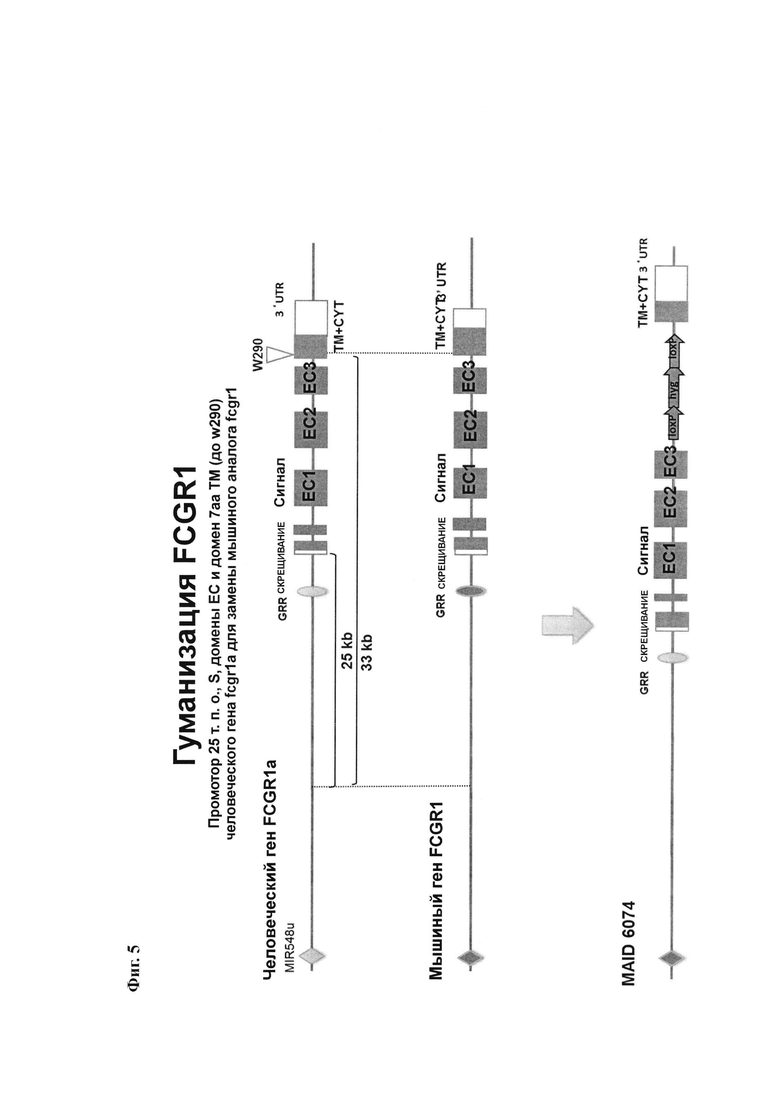

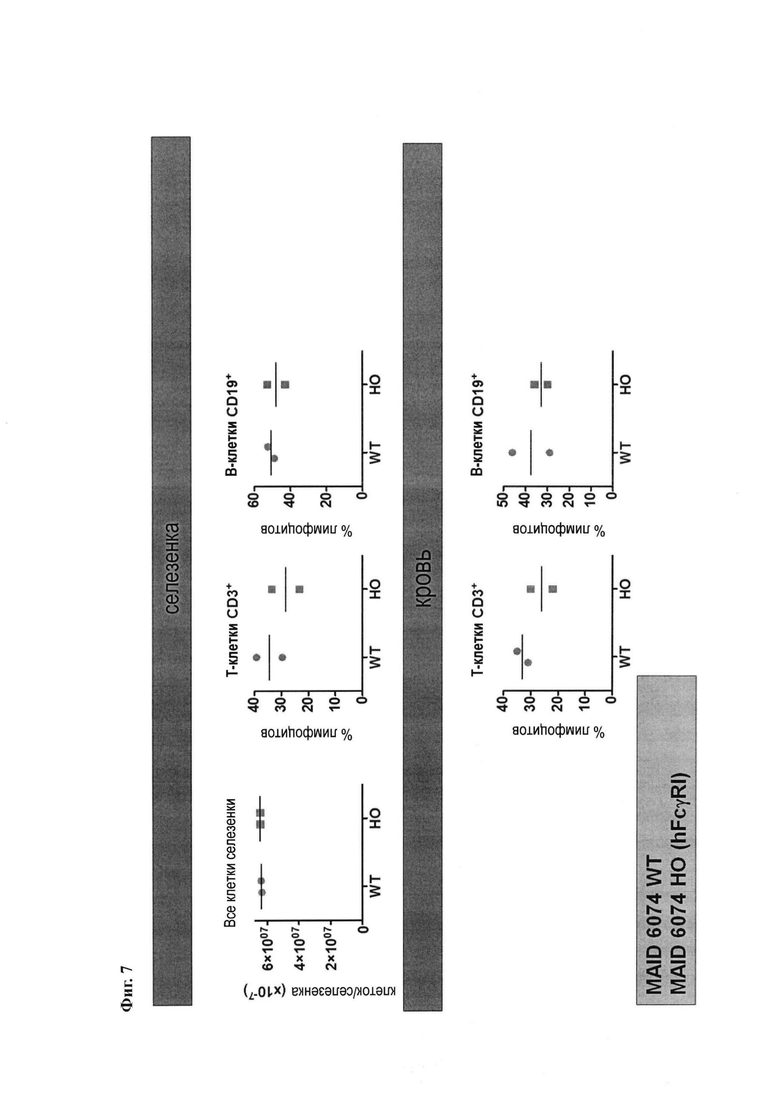

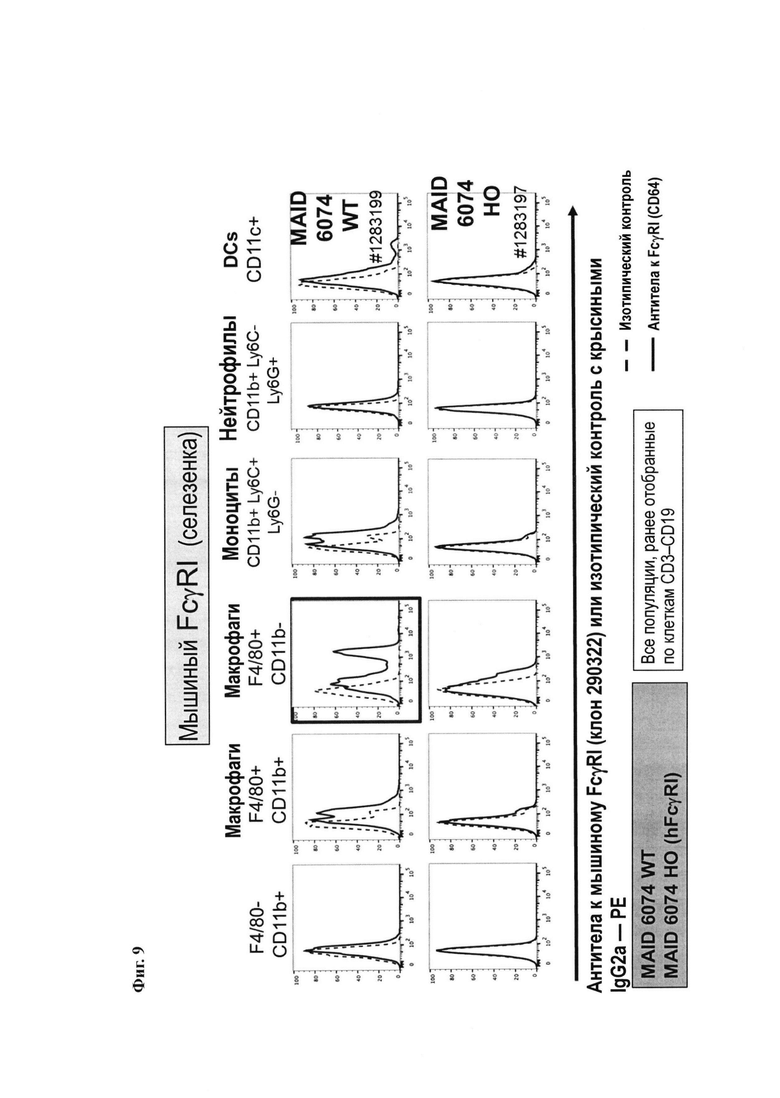
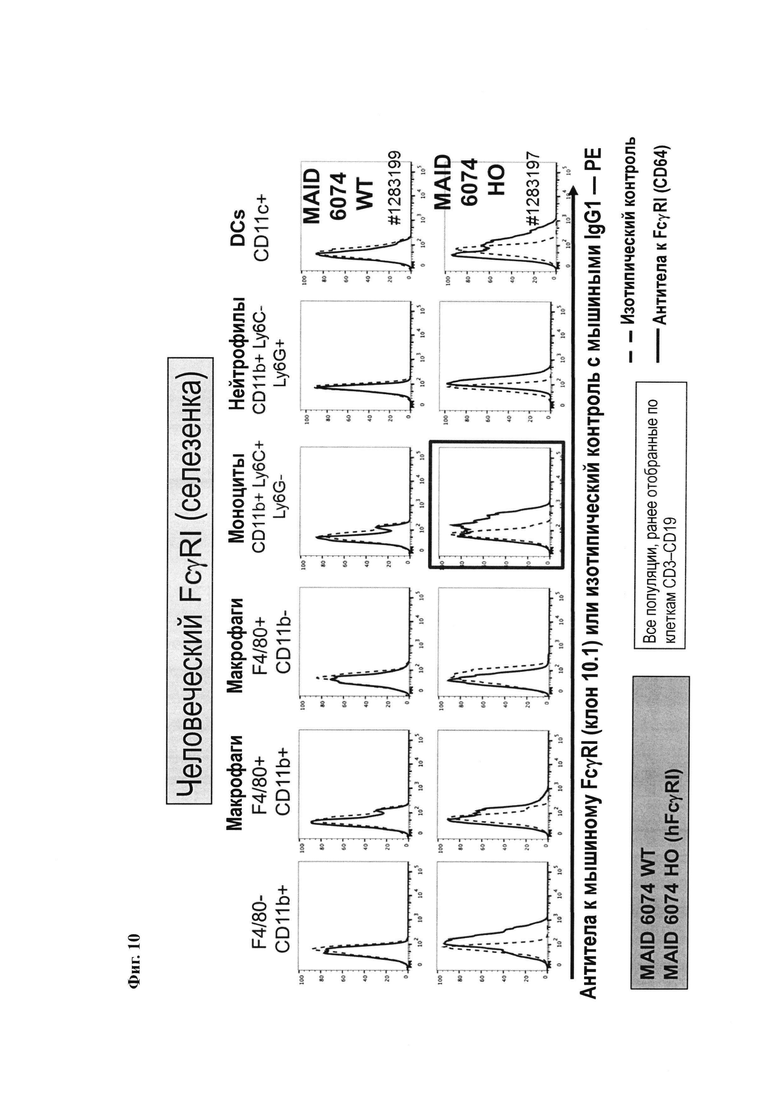

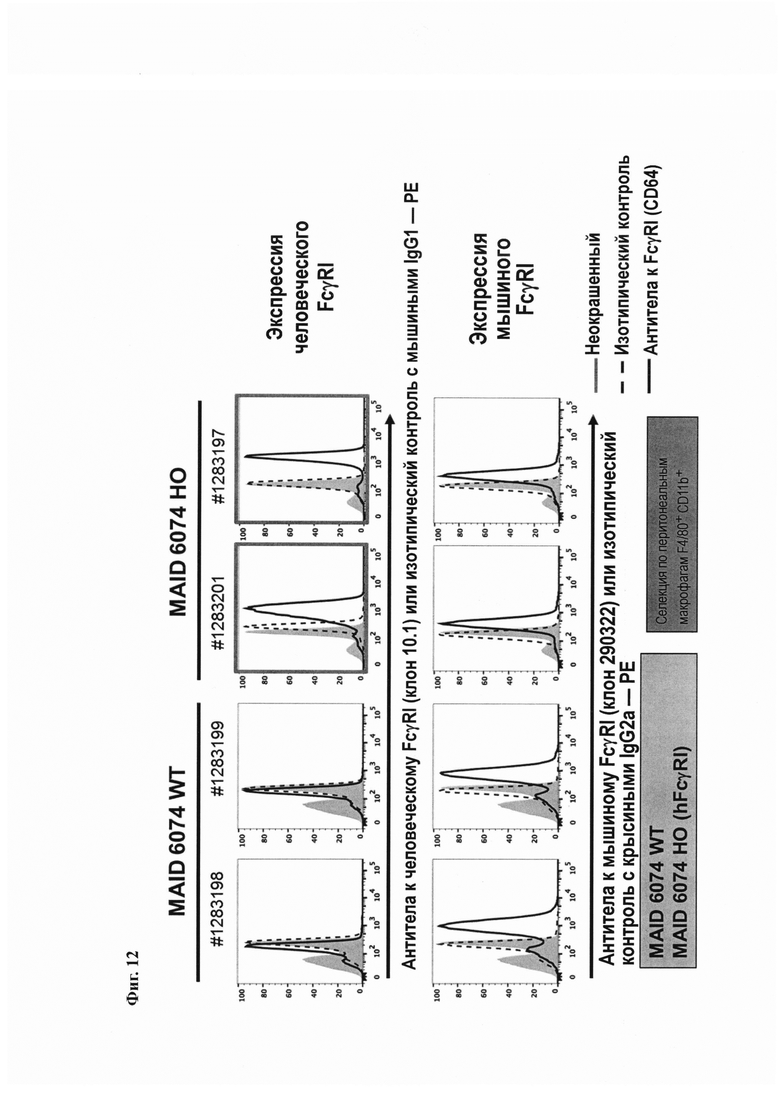

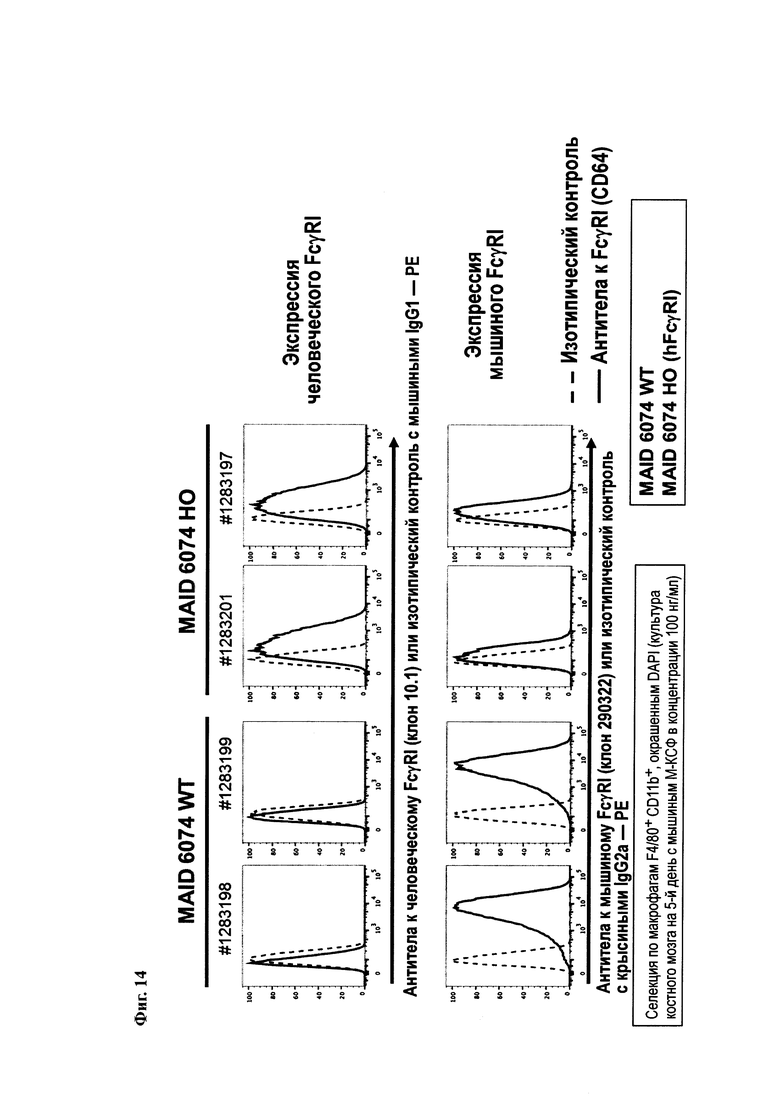
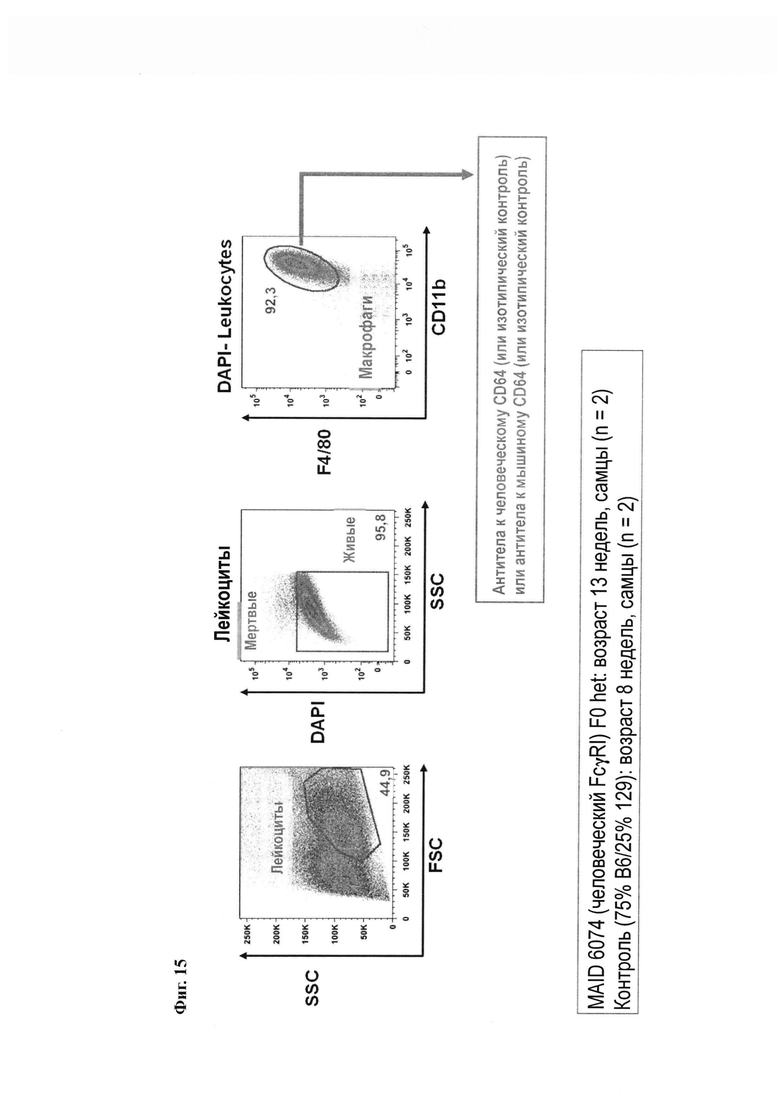
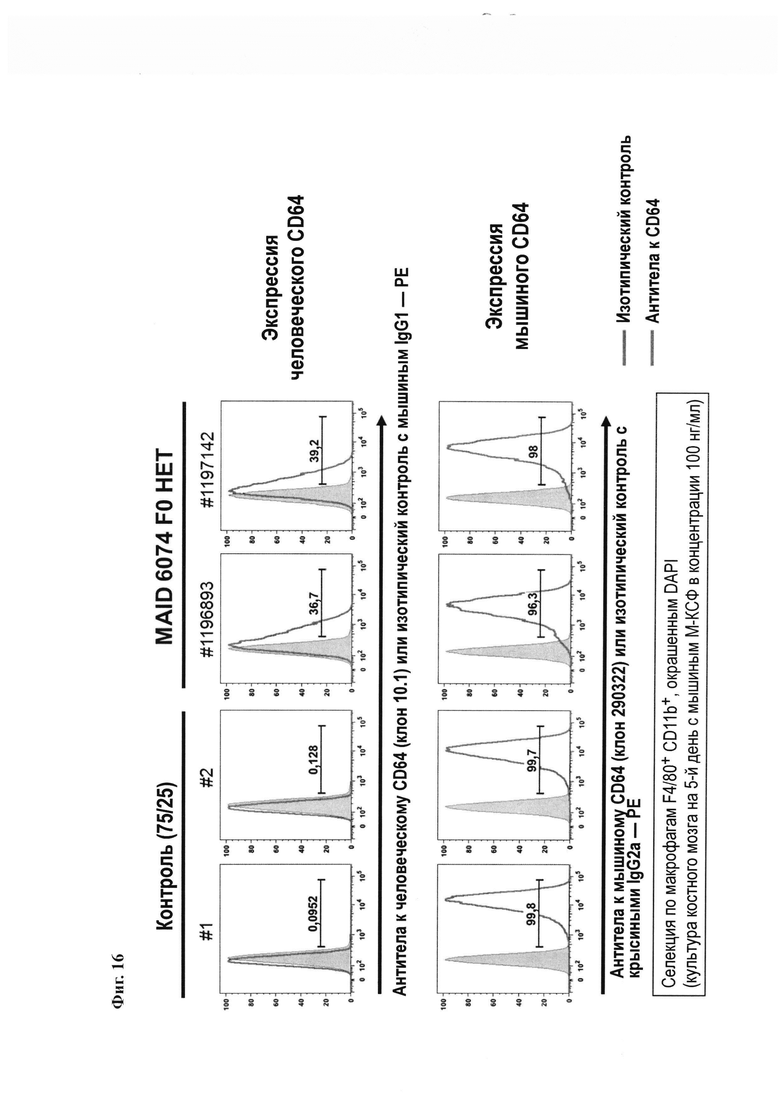
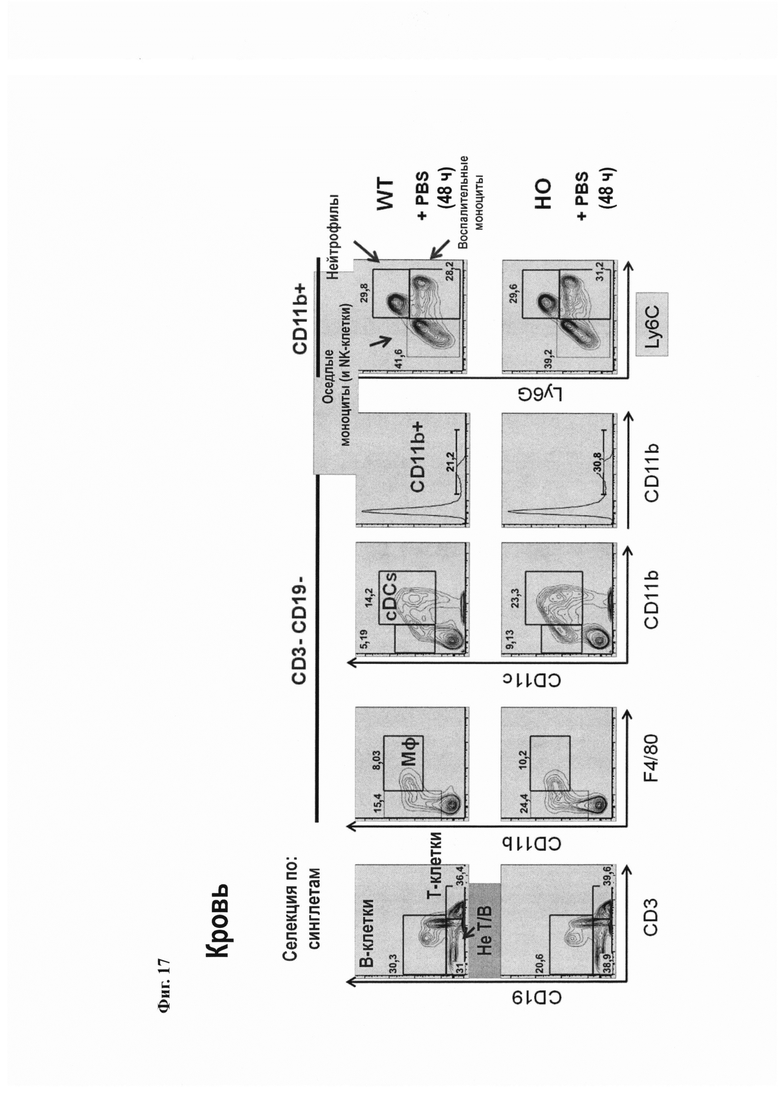






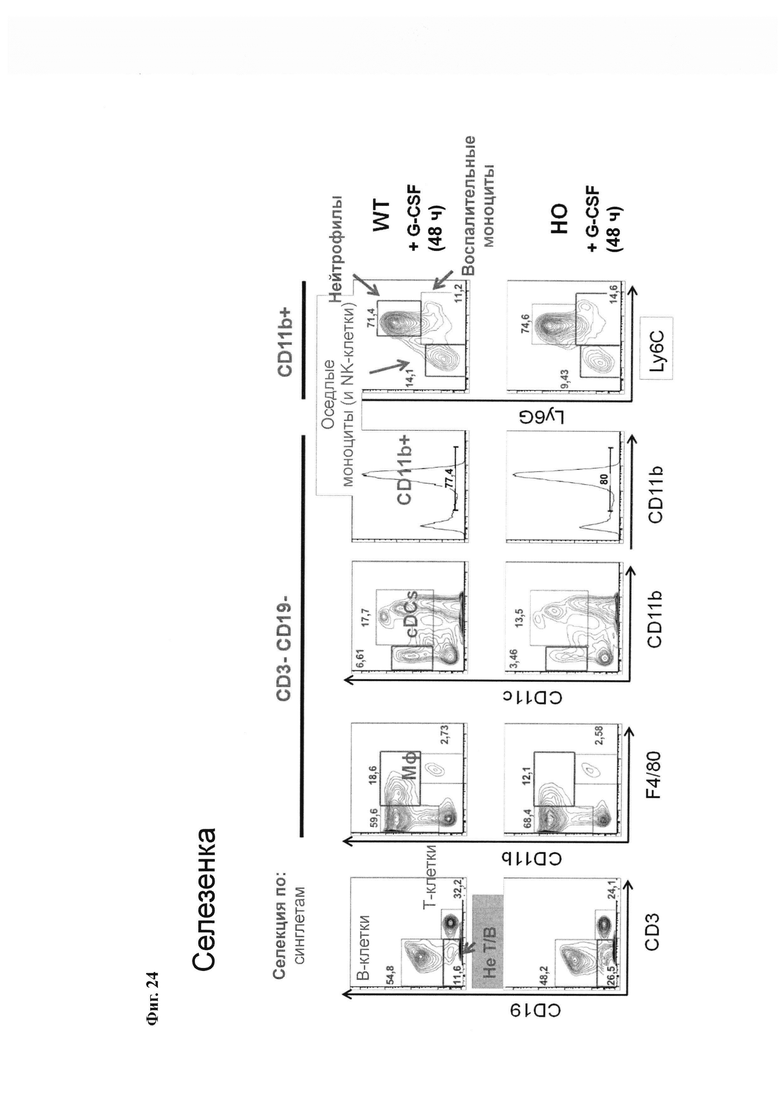




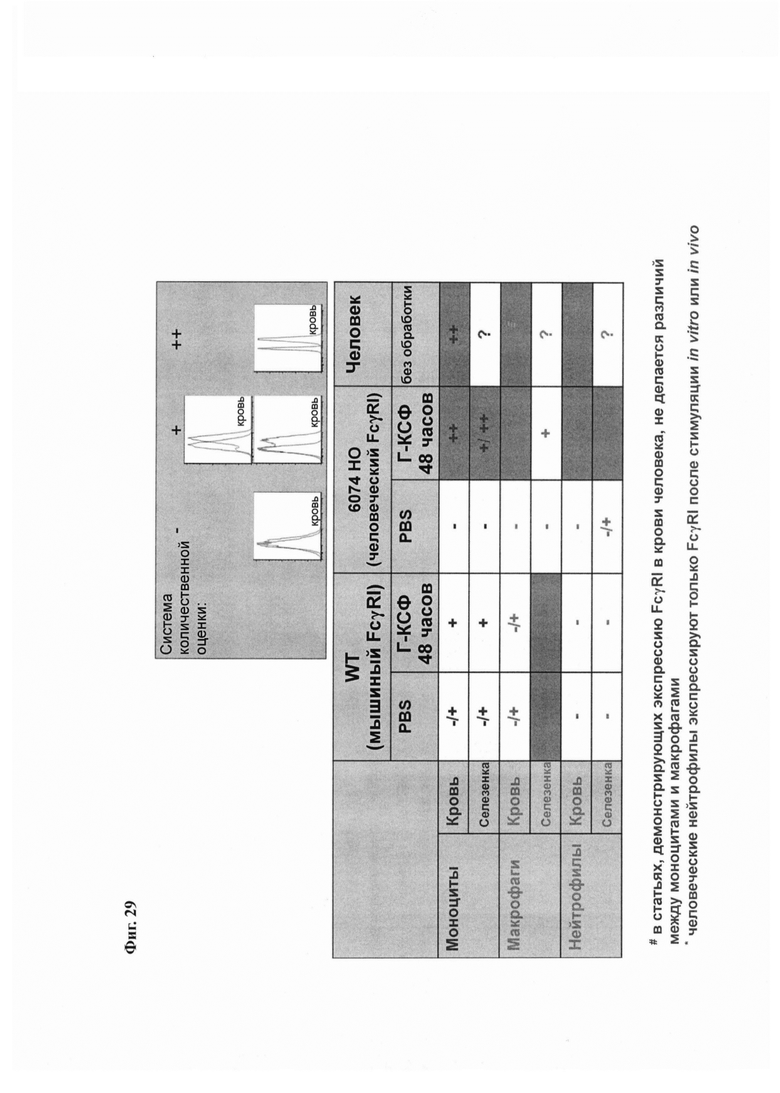
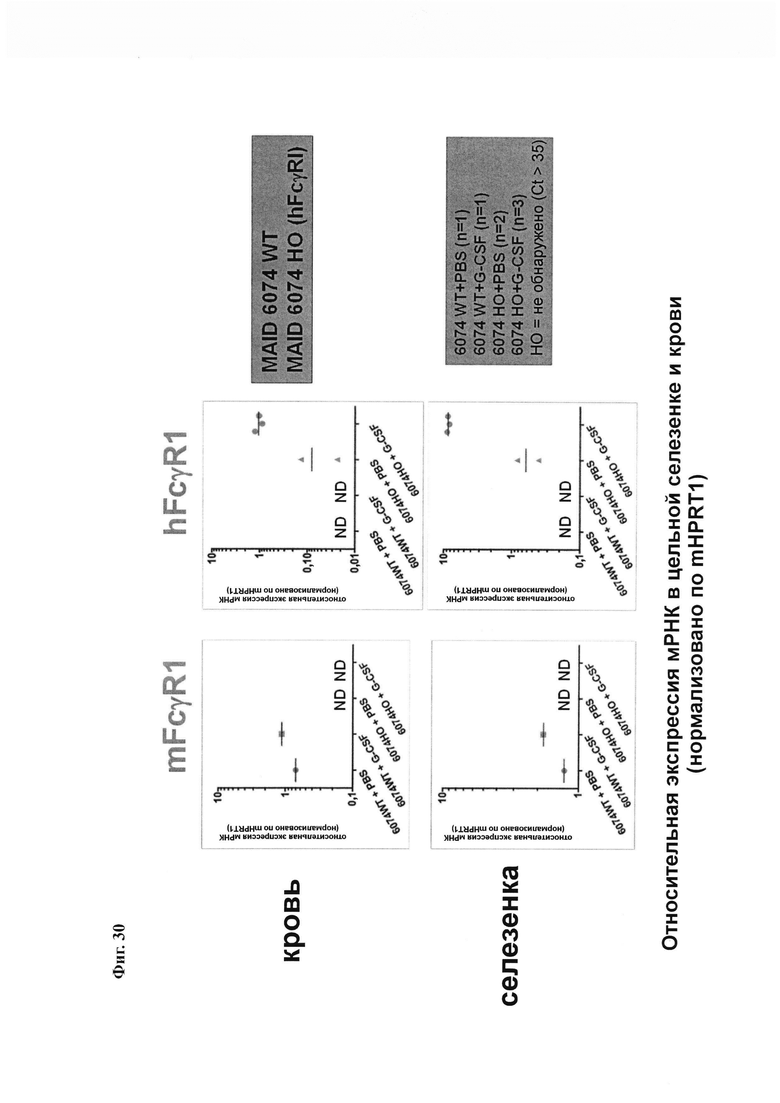
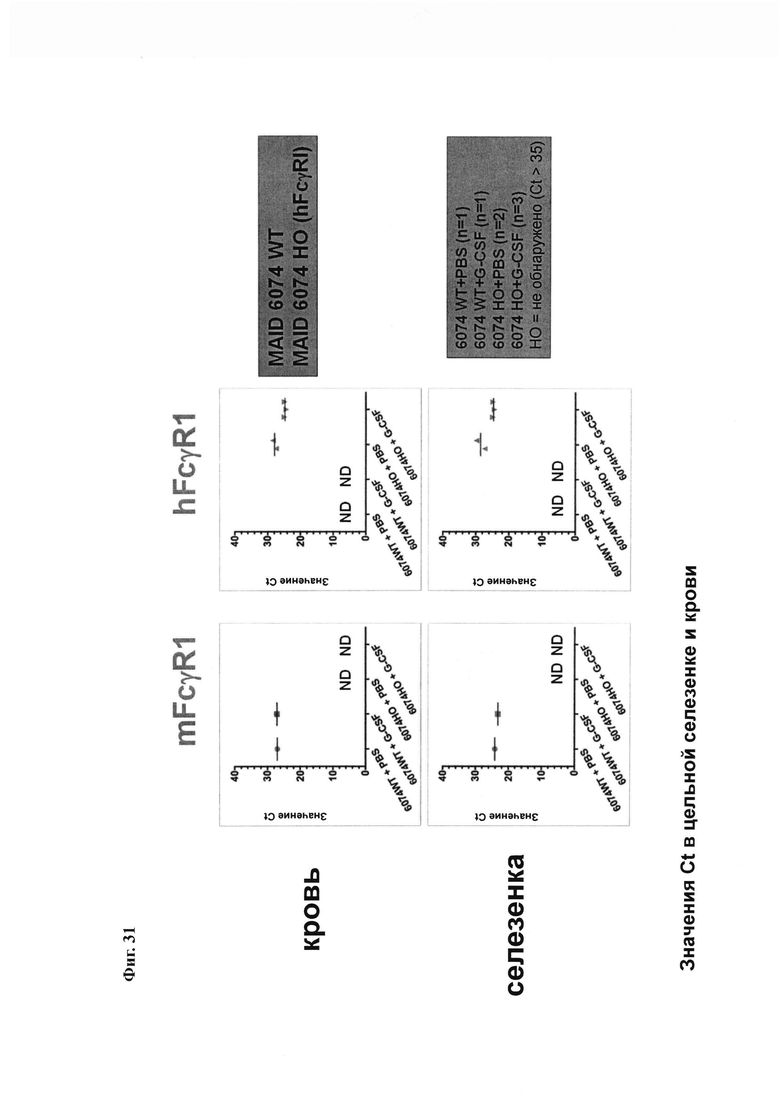

Изобретение относится к области биохимии, в частности к мыши, содержащей в эндогенном локусе α-цепи FcγRI промотор α-цепи FcγRI и регуляторную последовательность, функционально связанные с геном α-цепи FcγRI, кодирующим α-цепь FcγRI, а также к способу ее создания. Также раскрыта эмбриональная стволовая клетка мыши для создания мыши, которая экспрессирует функциональный белок FcγRI, содержащий внеклеточный участок человеческой α-цепи FcγRI и внутриклеточный участок мышиной α-цепи FcγRI. Изобретение также относится к эмбриону мыши для создания мыши, которая экспрессирует функциональный белок FcγRI, содержащий внеклеточный участок человеческой α-цепи FcγRI и внутриклеточный участок мышиной α-цепи FcγRI. Изобретение позволяет эффективно получать мышь, которая экспрессирует белок FcγRI, содержащий внеклеточный участок α-цепи FcγRI человека и внутриклеточный участок α-цепи FcγRI мыши. 5 н. и 19 з.п. ф-лы, 32 ил., 3 табл., 5 пр.
1. Мышь, содержащая в эндогенном локусе α-цепи FcγRI промотор α-цепи FcγRI и регуляторную последовательность, функционально связанные с геном α-цепи FcγRI, кодирующим α-цепь FcγRI, содержащую аминокислотную последовательность, по меньшей мере на 90% идентичную SEQ ID NO: 5, так, что мышь экспрессирует функциональный белок FcγRI, содержащий α-цепь FcγRI, содержащую аминокислотную последовательность, по меньшей мере на 90% идентичную SEQ ID NO: 5.
2. Мышь по п. 1, у которой α-цепь FcγRI содержит домен ЕС1, кодируемый экзоном, по меньшей мере на 90% идентичным экзону 3 SEQ ID NO: 3.
3. Мышь по п. 1, у которой α-цепь FcγRI содержит домен ЕС2, кодируемый экзоном, по меньшей мере на 90% идентичным экзону 4 SEQ ID NO: 3.
4. Мышь по п. 1, у которой α-цепь FcγRI содержит домен ЕС3, кодируемый экзоном, по меньшей мере на 90% идентичным экзону 5 SEQ ID NO: 3.
5. Мышь по п. 1, которая не экспрессирует полноразмерную мышиную α-цепь FcγRI на обнаруживаемом уровне.
6. Мышь по п. 1, у которой α-цепь FcγRI содержит весь цитоплазматический домен мышиной α-цепи FcγRI или его часть.
7. Мышь по п. 1, у которой белок FcγRI содержит аминокислотную последовательность α-цепи FcγRI, идентичную SEQ ID NO: 5.
8. Мышь по п. 1, у которой белок FcγRI экспрессирован на моноцитах, макрофагах, нейтрофилах или дендритных клетках.
9. Мышь по п. 8, у которой экспрессия белка FcγRI увеличивается при введении мышиного гранулоцитарного колониестимулирующего фактора (мГ-КСФ) мыши.
10. Эмбриональная стволовая клетка мыши для создания мыши, которая экспрессирует функциональный белок FcγRI, содержащий внеклеточный участок человеческой α-цепи FcγRI и внутриклеточный участок мышиной α-цепи FcγRI, при этом геном эмбриональной стволовой клетки содержит в эндогенном локусе α-цепи FcγRI промотор α-цепи FcγRI и регуляторную последовательность, функционально связанные с геном α-цепи FcγRI, который кодирует α-цепь FcγRI, содержащую аминокислотную последовательность, по меньшей мере на 90% идентичную SEQ ID NO: 5.
11. Клетка по п. 10, в которой ген α-цепи FcγRI содержит экзоны 3, 4 и 5 гена α-цепи FcγRI человека.
12. Клетка по п. 10, в которой эндогенный локус α-цепи FcγRI дополнительно содержит одну или более человеческих нетранслируемых областей на 5'-конце, фланкирующих человеческий экзон 1.
13. Клетка по п. 10, содержащая аминокислотную последовательность α-цепи FcγRI, идентичную SEQ ID NO: 5.
14. Клетка по п. 10, в которой ген α-цепи FcγRI содержит экзон 6 мышиного гена FcγRI.
15. Эмбрион мыши для создания мыши, которая экспрессирует функциональный белок FcγRI, содержащий внеклеточный участок человеческой α-цепи FcγRI и внутриклеточный участок мышиной α-цепи FcγRI, при этом геном эмбриона содержит в эндогенном локусе α-цепи FcγRI промотор α-цепи FcγRI и регуляторную последовательность, функционально связанные с геном α-цепи FcγRI, кодирующим α-цепь FcγRI, содержащую аминокислотную последовательность, по меньшей мере на 90% идентичную SEQ ID NO: 5.
16. Способ создания мыши, которая экспрессирует белок FcγRI, содержащий внеклеточный участок α-цепи FcγRI человека и внутриклеточный участок α-цепи FcγRI мыши, включающий следующие этапы:
(a) получение мышиной эмбриональной стволовой клетки по п. 10; и
(b) создание мыши с использованием эмбриональной клетки со стадии (а).
17. Способ создания мыши, которая экспрессирует функциональный белок FcγRI, содержащий внеклеточный участок α-цепи FcγRI человека и внутриклеточный участок α-цепи FcγRI мыши, предусматривающий модификацию мыши методами генной инженерии для содержания в ее геноме эндогенного локуса α-цепи FcγRI промотора α-цепи FcγRI и регуляторной последовательности, функционально связанных с геном α-цепи FcγRI, кодирующим α-цепь FcγRI, содержащую аминокислотную последовательность, по меньшей мере на 90% идентичную SEQ ID NO: 5.
18. Способ по п. 17, в котором α-цепь FcγRI содержит домен ЕС1, кодируемый экзоном, по меньшей мере на 90% идентичным экзону 3 SEQ ID NO: 3.
19. Способ по п. 17, в котором α-цепь FcγRI содержит домен ЕС2, кодируемый экзоном, по меньшей мере на 90% идентичным экзону 4 SEQ ID NO: 3.
20. Способ по п. 17, в котором α-цепь FcγRI содержит домен ЕС3, кодируемый экзоном, по меньшей мере на 90% идентичным экзону 5 SEQ ID NO: 3.
21. Способ по п. 17, в котором мышь не экспрессирует полноразмерную мышиную α-цепь FcγRI на обнаруживаемом уровне.
22. Способ по п. 17, в котором белок FcγRI содержит аминокислотную последовательность α-цепи FcγRI, идентичную SEQ ID NO: 5.
23. Способ по п. 17, в котором белок FcγRI экспрессируется на моноцитах, макрофагах, нейтрофилах или дендритных клетках.
24. Способ по п. 23, в котором экспрессия белка FcγRI увеличивается при введении мышиного гранулоцитарного колониестимулирующего фактора (мГ-КСФ) мыши.
| INGMAR A | |||
| F | |||
| M | |||
| HEIJNEN et al., Antigen Targeting to Myeloid-specific Human FcgRI/CD64 Triggers Enhanced Antibody Responses in Transgenic Mice, J | |||
| Clin | |||
| Invest, 1996, Vol | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Накладной висячий замок | 1922 |
|
SU331A1 |
| US 6111166 A, 29.08.2000 | |||
| WO 2009158696 A1, 30.12.2009 | |||
| US 2010035280 A1, 11.02.2010 | |||
| СПОСОБ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ МЫШЕЙ | 2009 |
|
RU2425880C2 |
Авторы
Даты
2019-09-17—Публикация
2015-04-08—Подача