Изобретение относится к области медицины, микробиологии, молекулярной генетики и биотехнологии и может быть использовано в медицинской промышленности при производстве живых вакцин для профилактики и лечения пневмонии, вызываемой пневмококками Streptococcus pneumoniae.
Проблема вакцинной профилактики инфекций, вызываемых стрептококками, стафилококками и пневмококками, только в последнее время стала рассматриваться в качестве актуальной проблемы в медицинской науке.
Streptococcus pneumoniae является наиболее частым (в 20-60%) возбудителем опасного заболевания - внебольничной пневмонии, смертность от которой составляет 5%. Кроме того, Streptococcus pneumoniae может вызывать такие заболевания человека, как средний отит, острый негнойный синусит, ринит, ларингит, бронхит, менингит, сепсис, остеомилит, септический артрит, эндокардит, перитонит и другие. Streptococcus pneumoniae является вторым (после HaemophilusHYPERLINK "http://www.gastroscan.ru/handbook/118/7781" HYPERLINK "http://www.gastroscan.ru/handbook/118/7781"influenzae) по распространённости и важности пневмотропным микроорганизмом в микробном спектре при хронических бронхолегочных заболеваниях у детей в период обострения.
Для пневмококков характерна мощная полисахаридная капсула, которая выполняет функцию защиты микроорганизма от опсонизации и последующего фагоцитоза. Вследствие того, что капсула пневмококков является основным поверхностным элементом, распознаваемым системой иммунитета, капсульный полисахарид характеризуется наибольшей вариабельностью. К настоящему времени обнаружен 91 различный капсульный тип пневмококков, но большинство (более 90%) инвазивных пневмококковых заболеваний вызывается 23 наиболее распространенными серотипами. Большое количество иммунологических вариантов капсульного полисахарида является фактором, осложняющим создание эффективных полисахаридных вакцинных препаратов.
Заболеть пневмококковой инфекцией может любой человек, но существуют группы риска, в большей степени подверженные заболеванию, это лица в возрасте от 65 лет, маленькие дети, лица, имеющие определенные проблемы со здоровьем, лица с ослабленной иммунной системой, курильщики. Пневмококковая инфекция нередко с трудом поддается лечению, поскольку многие циркулирующие эпидемические штаммы пневмококков приобрели множественную лекарственную устойчивость к антибиотикам. Поскольку пневмония считается распространенным заболеванием как у взрослых, так и у детей, она требует ответственного проведения диагностических и лечебных мероприятий.
Для предупреждения развития заболевания используются вакцины. Согласно позиции ВОЗ (Всемирная Организация Здравоохранения) и Российского респираторного общества, «Вакцинация - единственная возможность предотвратить развитие пневмококковой инфекции».
На данный момент FDA (Food and Drug Administration) одобрило 2 типа вакцин: пневмококковую полисахаридную вакцину и пневмококковую конъюгированную вакцину.
На территории России используется несколько препаратов для защиты от пневмококка. В их составе и установленном графике проведения прививок существуют значительные различия. Но имеющиеся вакцины защищают лишь от наиболее опасных серотипов Streptococcus pneumoniae. Пневмококковая вакцина, выпускаемая под торговым названием «Пневмо 23» (ППСВ), производится во Франции компанией «Санофи Пастер» и зарегистрирована в России. Она предназначена для вакцинирования детей, которым уже исполнилось 2 года, и взрослых, которые попадают в группу риска и болеют вирусными респираторными заболеваниями, пневмониями, отитами, диабетом.
У большинства здоровых взрослых людей, прошедших вакцинацию ППСВ, вырабатывается сопротивляемость большинству типов бактерий (антигены которых имеются в вакцине) в течение 2-3 недель после прививки. У лиц очень пожилого возраста, детей до 2 лет и людей с хроническими заболеваниями вакцинация может не привести к созданию стойкого иммунитета, либо иммунитет к заболеванию не возникает совсем (http://www.nlm.nih.gov/medlineplus/languages/pneumococcalinfections.html#Russian). Для детей до 2 лет одновременно с вакцинацией показана профилактика с использованием антибиотиков [Bade A, Diot P, Lemarie E. Rev Pneumol Clin. 53(3): 128-37, (1997)].
После вакцинации могут возникнуть осложнения: покраснение, болезненные ощущения в месте инъекции, высокая температура, мышечные боли или более серьезные местные реакции [Donalisio MR, Rodrigues SM, Mendes ET, Krutman M. J Bras Pneumol. 33(1):51-6 (2007)].
ППСВ оказалась достоверно эффективна лишь для людей с низким риском заболевания пневмококковой инфекцией. Оказалось, что ППСВ не уменьшает частоту пневмонии и связанную с ней смертность и лишь немного уменьшает риск заражения тяжелой пневмококковой инфекцией. Также показано, что данная вакцина не защищает от пневмококков, чувствительных к пенициллину в больших концентрациях [Pneumococcal vaccine: a second look. Solution for SC or IM injection: pneumococcal vaccine. Prescrire Int. 7 (33):16-8, (1998)]. Такие же результаты были показаны и для людей страрше 65 лет (Pneumococcal vaccination for elderly subjects: license extension. Still no proof of clinical efficacy. Prescrire Int. 9 (48):106-9, (2000)].
Действующим веществом ППСВ являются полисахариды 23 серотипов Streptococcus, вызывающих до 90% инвазивных заболеваний пневмококковой этиологии. Полисахарид - это антиген, не связанный с реакцией Т-клеток, потому вызывает лишь краткосрочный иммунитет без иммунной памяти; вакцины, содержащие только данные вещества, неэффективны, что показано у детей до 2 лет (Greenwood В М et al., Trans R Soc Trop Med Hyg, 74:756-760 (1980)]; международная заявка на изобретение WO 2010120921 A1, дата приоритета 16.04.2009). Также тот факт, что существует порядка 90 серотипов пневмококков, поскольку возбудители заболеваний в разных областях земного шара различаются, затрудняет создание универсальной вакцины на основе полисахаридов.
Вакцина «Превенар», которая используется на территории Федерации, изготавливается в США компанией «Вайет». Она считается более иммуногенной. Это означает, что антигены патогенных микроорганизмов дольше удерживаются в организме. Вакцина «Превенар» предназначена для детей от 2 месяцев до 5 лет. Она начала широко использоваться с 2000 года в США. На сегодня она применяется в 88 странах и в 42 странах включена в национальные календари вакцинации. В России вакцина зарегистрирована в конце 2008 г. Это другой тип вакцин для профилактики пневмококковой инфекции - конъюгированная вакцина. Кусочки полисахаридной оболочки семи различных типов пневмококка соединили со специальным белком-носителем, что сделало эту вакцину эффективной у малышей с 2-х мес. жизни. В неё включены 7 так называемых «педиатрических» серотипов бактерии, которые чаще всего вызывают пневмококковую инфекцию в той или иной форме у детей раннего возраста.
В конъюгированной вакцине, показанной детям, наряду с полисахаридами 7 серотипов пневмококков, которые наиболее часто вызывают заболевания среди детей, также содержится белок-носитель CRM 197 (мутант дифтерийного токсина), в качестве адъюванта. Благодаря наличию адъюванта в препарате вакцины данный антигенный комплекс хорошо распознается Т-клетками, обеспечивая устойчивый иммунитет [Schneerson R, Barrera O, Sutton A, Robbins JB. J Exp Med. 152(2):361-76, (1980)]. CRM 197 связывается с гепарин-связывающим эпидермальным фактором роста и может его ингибировать. Несмотря на то, что токсичность CRM197 примерно в 106 раз меньше, чем дифтерийного токсина, все же его использование должно быть осторожным, особенно в высоких дозировках [Takuya Kageyama, Minako Ohishil, Shingo Miyamoto, Hiroto Mizushima, Ryo Iwamoto and Eisuke Mekada. Diphtheria Toxin Mutant CRM197 Possesses Weak EF2-ADP-ribosyl Activity that Potentiates its Anti-tumorigenic Activity. Received April 16, 2007. Accepted May 2, 2007]. Кроме того, после вакцинации могут возникнуть осложнения: покраснение, чувствительность или припухлость в месте введения препарата, температура выше 38-39С, а также беспокойность, сонливость, потеря аппетита. Более того, вакцинацию рекомендуют проводить детям до 2 лет четыре раза, от 2 до 5 лет - в зависимости от возраста ребенка, В общей сложности для вакцинации ребенка требуется введение как минимум 4 доз, что дорого и небезопасно.
Известна вакцина, двумя главными компонентами которой являются полисахарид оболочки N. meningitidi и белок PsaA S.pneumoniae (может также использоваться белок PspA) (международная заявка на изобретение WO2010120921 A1, дата приоритета 16.04.2009). Ввиду невозможности выработки иммунной памяти на полисахариды, использование полисахарида оболочки N. meningitidi в качестве компонента вакцины является неоправданным.
В качестве вакцинных препаратов целесообразнее использовать поверхностные антигены пневмококков, которые способны вызывать и иммунный ответ, и формирование иммунологической памяти. Центральное место в такой разработке занимают белки пневмококков, полученные с использованием методов молекулярной биологии и рекомбинантной ДНК. По литературным данным, в качестве вакцинных кандидатов белковой природы наиболее перспективными антигенами являются три поверхностных белка пневмококков: PsaA, PspA, Spr1895 [Suvorov A., Dukhovlinov I., Leontieva G., Kramskaya T., Koroleva I., Grabovskaya K., Fedorova E., Chernyseva E., Klimov N., Orlov A., Uversky V. J Vaccines Vaccin, 6, 6: 1-8, (2015)].
Белок PsaA высоко консервативен среди различных серотипов пневмококков и обусловливает адгезию бактерии и ее вирулентность [Berry AM, and Paton JC. Infect Immun. 64:5255-5262, (1996)]. Показано, что антитела к PsaA обладают перекрестной активностью относительно всех серотипов S. pneumonia.
PspA - это холин-связывающий поверхностный антиген, который ингибирует комплемент-опосредованный фагоцитоз, связывается с лактоферрином и предотвращает лактоферрин-опосредованную элиминацию бактериальных клеток [Hammerschmidt S., Bethe G., Remane P.H., Chhatwal G.S. Infect Immun 67:1683-1687, (1999)]. В данной статье также указывается белок PsaA, как перспективный для создания вакцины.
Белок PsaA считают перспективным иммуногеном и авторы международной заявки на изобретение WO 2004102199 A2, дата приоритета 16.05.2003. Авторы приводят данный белок и еще несколько белков (SlrA - ротамаза липопротеинов, IgA1 - протеаза, PpmA - белок созревания стрептококков) или их компонентов в качестве основы для создания вакцины. Описан гибридный белок, включающий PsaA и В-субъединицу холерный токсин в качестве адъюванта [Areas АР, Oliveira ML, Miyaji EN, Leite LC, Aires KA, Dias WO, Ho PL. Biochem Biophys Res Commun. 13; 321(1):192-6 (2006)]. Однако, использование холерного токсина, либо его компонентов в качестве компонента вакцины не безопасно, ввиду того, что люди высокочувствительны к холерному токсину, и даже 8 мкг токсина может вызвать сильную диарею.
Существуют и другие подходы при создании пневмококковых вакцин. Для доставки пневмококкового антигена используют пузырьки грамотрицательных микроорганизмов. Создан гибрид гена PspA и -лактамазы сальмонеллы. Иммунизация мышей пузырьками внешней мембраны, содержащие PspA, обеспечивает полную защиту против летальной дозы S. pneumonia.
Одним из способов доставки антигена являются молочнокислые бактерии. Назальная иммунизация мышей Lactobacillus casei, экспрессирующих N-терминальный участок PspA приводит к образованию анти-PspA IgG в сыворотке, которые защищали мышей от последующей пневмококковой инфекции [Tarahomjoo, J Mol Microbiol Biotechnol. 24:215-2272014, (2014)].
Описана вакцина, в которой в качестве главных компонентов используются белки PsaA, PspA и белок Spr 1895, закодированный в гене фосфат-связывающего белка фосфатного ABC транспортера. Данный белок является жизненно важным для бактерий, константным, что обуславливает его выбор для создания вакцины от пневмонии, вызываемой S. pneumonia. В этой вакцине авторы используют белок флагеллин (FliC) в качестве адъюванта. В результате создана вакцина на основе гибридного белка PSPF, включающего фрагменты белков Streptococcus pneumoniae PsaA и PspA и Spr 1895, а также компоненты флагеллина, соединенные гибкими мостиками. Вакцина обеспечивает эффективную профилактику и терапию пневмонии за счет того, что гибридный белок вакцины составлен из различных иммуногенных эпитопов, на которые вырабатывается специфический иммунный ответ с формированием иммунологической памяти [Суворов А.Н., Духовлинов И. В., Орлов А. И. Байгузин Е. Я. патент RU 2510281 С2, (2014)].
Эта вакцина принята в качестве первого прототипа заявляемого изобретения. В настоящем изобретении использовали плазмиду, кодирующую гибридный вакцинный белок для профилактики инфекции, вызванной Streptococcus pneumoniae.
Эффективное применение и белковых и полисахаридных вакцинных препаратов предусматривает двух- или трехкратную иммунизацию путем подкожных или внутримышечных инъекций с адъювантом, что может быть сопряжено с осложнениями и требует серьезных организационных и финансовых затрат.
Альтернативой использованию химических адъювантов для вакцинации является применение так называемых живых бактериальных вакцин на основе пробиотиков. Живые вакцины применяют, как правило, однократно, вводят подкожно, накожно или внутримышечно, а некоторые вакцины перорально и ингаляционно. Главным преимуществом живых вакцин является то, что они активируют все компоненты иммунной системы, вызывая сбалансированный прочный иммунный ответ.
Пробиотики - препараты, оказывающие общее благотворное влияние на организм человека (чаще всего молочнокислые бактерии). Установлено, что некоторые пробиотики являются эффективными неспецифическими стимуляторами выработки специфических иммуноглобулинов против различных инфекций [Vintini E.O., Medina M.S., BMC Immunol., 12: 46 (2011), Bermudez-Hurnarun L.G., Kharrat P., Chatel J.M., Microb. Cell. Fact., 10: 17-24 (2011)]. Пробиотики стали использоваться в качестве векторов, в часть из которых успешно внесены плазмидные конструкции, обеспечивающие зкспрессию антигенов патогенных бактерий [ME Y., Luo Y., Huang X., Song F., Liu G. Microbiology, 158: 498-504 (2012), De Azevedo M., Karczzewski J., Lefeure F. Et al. BMC Microbiol. 12: 299 (2011)].
Разработана вакцина против Enterohemorrhagic Escherihia coli (EHEC), вызывающей уремический синдром [Ahmed, M. Loos, D. Vanrompay, E. Cox. Vaccine, 32: 3909-3916 (2014). Он является причиной острой почечной недостаточности у детей и пожилых людей. В своей вакцине авторы используют пробиотический штамм Lactococcus lactis, который является безопасной бактерией и может служить платформой для пероральной вакцинации. В работе создан рекомбинантный штамм, в котором Lactococcus lactis экспрессирует антиген EHEC, EspB, в цитоплазме. Эта вакцина может быть особенно полезна для детей и пожилых людей, находящихся в группе высокого риска заболеваемости.
Персистенция подобных вариантов пробиотиков в организме способна не только стимулировать выработку протективных иммуноглобулинов, специфичных в отношении целевых антигенов возбудителя, но и обеспечить благоприятный фон для борьбы с инфекцией за счет усиления защитных реакций врожденного иммунитета.
Пробиотические микроорганизмы рассматриваются в настоящее время как хорошая основа для получения рекомбинантных живых вакцин, экспрессирующих вакцинные антигены возбудителей актуальных инфекций [Vintini E.O., Medina M.S., BMC Immunol., 12: 46 (2011); Bermudez-Hurnarun L.G., Kharrat P., Chatel J.M., Microb. Cell. Fact., 10: 17-24 (2011); ME Y., Luo Y., Huang X., Song F., Liu G. Microbiology, 158: 498-504 (2012), De Azevedo M., Karczzewski J., Lefeure F. Et al. BMC Microbiol. 12: 299 (2011)].
Описано создание живой вакцины на основе штамма пробиотика Enterococcus faecium L3 для профилактики вагинальной инфекции, вызванной Streptococcus agalactiae (СГБ). На основе штамма пробиотика Enterococcus faecium L3 сконструирована первая генно-инженерная живая вакцина со встроенным в хромосому участком гена белка патогенного СГБ. [Гупалова Т.В., Леонтьева Г.Ф., Ермоленко Е.И. и др. Медицинский академический журнал, 13: 64-70, (2013)].
Также описано создание живой вакцины против СГВ, в которой использовался подход, основанный на введении bac гена патогенных СГВ в хромосомную ДНК пробиотического штамма Enterococcus faecium L3 при экспрессии в пилях. Пили из энтерококков являются идеальными кандидатами для вакцин из-за их экспозиции на клеточной поверхности. Они выступают за пределы бактериальных клеток и способны проникать сквозь капсулу, которая экранирует большинство белков-антигенов. Пили состоят из мономеров, способных к агрегации за счет чего увеличивается доза антигена, что способствует увеличению титров антител, специфичных к встраиваемому в структуру поверхностного белка энтерококка полипептидного фрагмента штамма патогенного СГВ. Поэтому способ введения гена патогенных стрептококков в пили пробиотического штамма Enterococcus faecium L3 выгодно отличается тем, что рекомбинантный белок экспрессируется не на поверхности, а в цитоплазме бактерии [Суворов А.Н., Гупалова Т.В., Леонтьева Г.Ф. и др., патент № RU 2640250].
Способ введения генов патогенных стрептококков в хромосомную ДНК пробиотического штамма Enterococcus faecium L3 для экспрессии в пилях, описанный в этом патенте, использовался в качестве второго прототипа настоящего изобретения.
Отличие данного исследования от других экспериментальных работ с живыми вакцинами на основе пробиотиков заключается в том, что обычно пробиотики используют в качестве природных адъювантов иммунного ответа, а антиген вводится отдельно.
Настоящее исследование представляет собой интеграцию участка ДНК, кодирующего антигенный фрагмент белка патогенного микроорганизма, в структуру хромосомной ДНК энтерококка. При этом задача генетической части работы состояла в осуществлении интеграции гетерологичного участка ДНК в структуру гена поверхностного белка пробиотика без нарушения открытой рамки считывания и повреждения участков кодирования компонентов, участвующих в процессинге поверхностного белка PilF. В данном исследовании в качестве бактерии-реципиента использовался хорошо изученный пробиотический штамм Enterococcus faecium L3, обладающий целым рядом уникальных биологических свойств.
Штамм Enterococcus faecium L3 обладает выраженной антагонистической активностью в отношении грамположительных и грамотрицательных бактерий, способностью восстанавливать микробиоценоз кишечника на фоне дисбиотических состояний [Yermolenko E., Suvorov A., Chernush A., et al. International Congress Series, 1289: 363-366 (2006)], а также оказывать иммуномодулирующее действие на организм хозяина [Tarasova E., Yermolenko E., Donets V. et al. Beneficial Microbs, 1: 265-270, (2010)]. Осуществлено физическое картирование штамма Enterococcus faecium L3 [Suvorov A., Simanenkov V., Gromova L. et al. Prebiotics and probiotics potencial for human health, 104-112, (2011)]. В экспериментах на здоровых самках мышей показано, что интравагинальное введение высоких доз штамма Enterococcus faecium L3 не только не оказывает токсического действия на организм, но и не влияет на состояние слизистой оболочки влагалища [Суворов А.Н., Алехина Г.Г., Пигаревский П.В. и др. Гастробюллетень, 4: 29-31, (2001)], способствует экспрессии IL-10 клетками слизистой оболочки влагалища крыс с экспериментальным вагинитом, вызванном S.agalactiae и Staphylococcus aureus [Tarasova E., Yermolenko E., Donets V. et al. Beneficial Microbs, 1: 265-270, (2010)].
В штамме Enterococcus faecium L3, как и у других грамположительных бактерий, были найдены пили, которые представляют собой фимбрии длиной 0,3-3 m и диаметром 2-10nm [Telford JL, Barocchi MA, Margarit I et al. Nature Reviews Microbiology 4: 509-519, (2006)]. Это длинные белок подобные полимеры, тянущиеся на поверхности бактерий, представляют собой субъединицы белка пилина, соединенные ковалентной связью. Они играют большую роль в адгезии колонизации хозяина. Пили являются высокоиммуногенными структурами, которые находятся под селективным давлением иммунных реакций хозяина [Camille Danne, Shaynoor Dramsi. Research in Microbiology, 163: 645-658, (2012)]. Принцип модификации пилей энтерококков вакцинными антигенами является идеальным подходом при создании эффективных живых вакцин благодаря экспозиции целевого антигена на поверхности энтерококка.
В качестве вакцинного антигена Streptococcus pneumoniae в настоящем изобретении использовался гибридный белок, включающий иммуногенные фрагменты белков PspA, PsaA и Spr1895. В отличие от гибридного белка, используемого в описанной вакцине для профилактики инфекции, вызванной Streptococcus pneumoniae [Суворов А.Н., Гупалова Т.В., Леонтьева Г.Ф. и др., патент № RU2640250], он не содержал фрагментов флагеллина.
В гибридном белке представлены антигенные детерминанты консервативных белков пневмококка, которые присутствуют у всех серотипов данного микроорганизма, поэтому иммунный ответ, который вырабатывается после вакцинации, будет эффективен в отношении любого серологического варианта пневмококка. Использование эпитопов нескольких белков позволит увеличить эффективность вакцины. Наличие в сыворотке крови человека протективных антител к S. pneumoniae приведет к тому, что человек не заболеет или легко перенесет болезнь. Ранее была показана защита от пневмококков за счет того, что белок вакцины составлен из иммуногенных эпитопов нескольких консервативных белков пневмококков, на которые вырабатывается специфический иммунный ответ с формированием иммунологической памяти [Suvorov A., Dukhovlinov I., Leontieva G., Kramskaya T., Koroleva I., Grabovskaya K., Fedorova E., Chernyseva E., Klimov N., Orlov A., Uversky V. J Vaccines Vaccin, 6, 6: 1-8, (2015)].
Задачей данного изобретения явилась создание живой вакцины на основе биологически активного штамма Enterococcus faecium L3 за счет включения в структуру его пилей гибридного поливалентного антигена клинически патогенного микроорганизма Streptococcus pneumoniae. Создание такой вакцины против инфекции, вызываемой пневмококками, основано на введении участка ДНК, кодирующего антигенный фрагмент иммуногенных эпитопов нескольких консервативных белков пневмококков, в структуру пилей пробиотика.
Задача решалась конкретно на примере введения гена pspf патогенных пневмококков в хромосомную ДНК пробиотического штамма Enterococcus faecium L3 для экспрессии в пилях:
а) получение слитого гена entF-pspf и его клонирование
б) выявление бактериальных клонов, экспрессирующих ген слитого белка PSPF белок в пилях
в) интраназальная вакцинация мышей живой пробиотической вакциной
г) определение PSPF-специфических антител в крови и вагинальных смывах.
д) исследование протективной эффективности и вакцинации живой пробиотической вакциной
Сущностью предлагаемого изобретения является создание живой вакцины против пневмококков, обладающей выраженным иммуногенным и протективным эффектами.
Авторами заявляемого изобретения на основе штамма пробиотика Enterococcus faecium L3, содержащего пили на своей поверхности, сконструирована генно-инженерная живая вакцина со встроенным в хромосому участком гена pspf патогенного Streptococcus pneumoniae. Интраназальное введение вакцины Enterococcus faecium L3-PSPF+ стимулировало развитие специфического системного и местного иммунного ответа. На модели интравазальной летальной пневмококковой инфекции у мышей СВА было показано, что трехкратная интравазальная вакцинация созданной живой пробиотической вакциной повышала защиту от летальной пневмококковой инфекции.
Конструирование живой вакцины на основе биологически активного пробиотического штамма Enterococcus faecium L3 за счет включения в его пили антигенов Streptococcus pneumoniae позволило объединить в одном препарате эффективность полезных свойств пробиотика и специфического антигенного стимула.
Поставленная задача решалась получением слитого гена entF-pspf и его клонированием. Для этого были сконструированы уникальные праймеры, представленные в таблице.
Таблица 1. Олигонуклеотидные праймеры
Подчеркнутые звенья нуклеотидной последовательности указывают на сайты рестрикции.
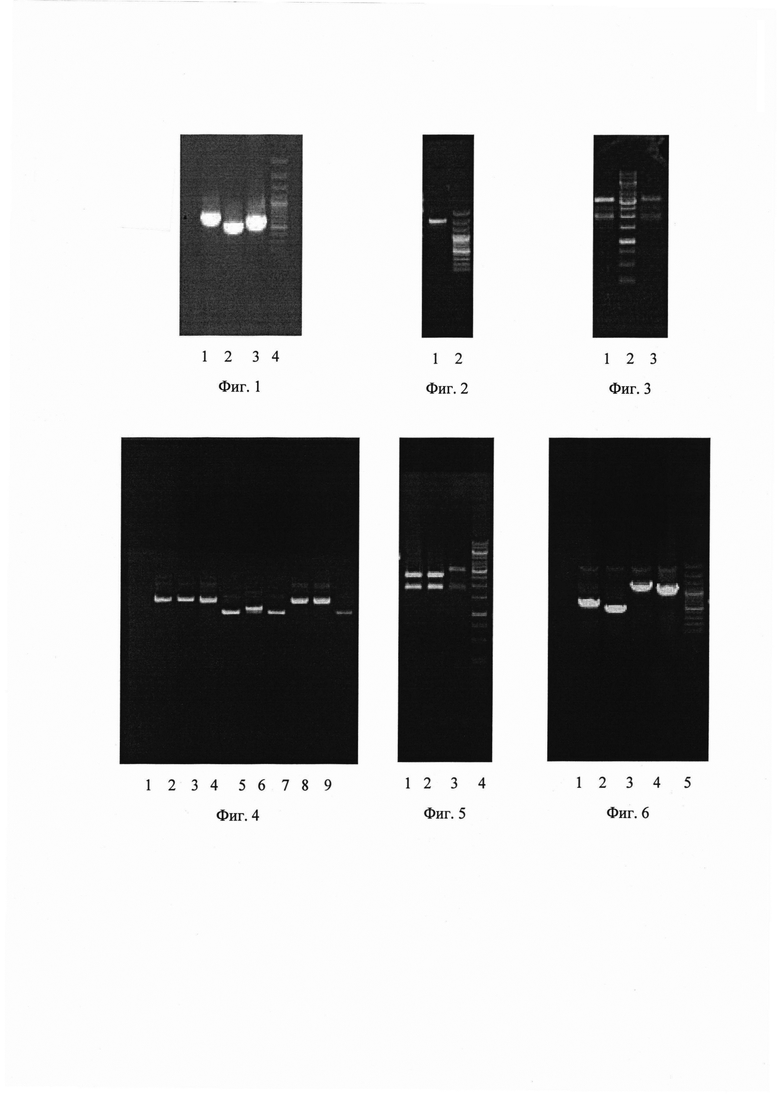
Фрагменты ДНК, соответствующие фрагментам гена пилей Enterococcus faecium L3 и плазмидной ДНК, кодирующей три пневмококковых белка PspA, PsaA и Spr1895 без компонентов флагеллина, были амплифицированы в ПЦР с помощью Taq полимеразы («Ampli Taq», Perkin-Elmer, Cetus, USA) и амплификатора (BIO-RAD, USA). Проведена амплификация отдельных двух фрагментов гена пилей Enterococcus faecium L3 с праймерами А1 и В1 и с праймерами С1 и D1 и фрагмента гена pspf с праймерами E1 и F1. Синтез слитого фрагмента осуществляли с праймерами A1 и D1. Одна пара праймеров представлена одновременно участком ДНК энтерококков, а другая участком гена pspf. Дизайн праймеров предполагал образование слитого гена без стоп-кодонов в местах сшивок. В результате постановки двух последовательных этапов ПЦР сначала получены отдельные части конструкции, а затем и целый слитый фрагмент ДНК (фиг. 1 и фиг. 2). Клонирование амплифицированного фрагмента ДНК осуществляли с использованием плазмиды pJET1.2, используя Clone JET PCR Cloning Kit (Fermentas). В результате клонирования была создана уникальная гибридная ДНК entF-pspf с использованием плазмиды pJET1.2. Наличие в ней нужной вставки было подтверждено реакцией гидролиза ферментами BamHI и XbaI (фиг. 3). Гибридная ДНК entF-pspf из плазмиды pJET1.2 была переклонирована в суицидную плазмиду pT7ERMB с геном устойчивости к эритромицину. Для этого была проведена амплификация гибридной плазмиды с праймерами A1 и D1. В результате клонирования были получена плазмида pentF-pspf с ожидаемой вставкой и геном устойчивости к эритромицину. Наличие вставки подтверждалось гидролизом плазмиды ферментами BamHI и XbaI (фиг. 4 и фиг. 5). Наличие фрагментов гена пилей Enterococcus faecium L3 и фрагмента гена pspf подтвердила ПЦР с праймерами A1 и B1, C1 и D1, A1 и F1, E1 и D1 (фиг. 6).
В результате электропорации энтерококков созданной интегративной плазмидой были получены 2 трансформанта. Они были проверены в реакции ПЦР со специально сконструированными праймерами SeqF и SeqR. Для этого из трансформантов выделяли ДНК, используя набор ДНК-экспресс (Литех, Россия). Положительный ответ дал только один трансформант, обозначенный как PSPF+ клон (фиг. 7). Было проведено секвенирование ДНК, выделенной из PSPF+ клона с праймерами, соответствующими последовательности гена pspf (праймер seqR) и последовательности хромосомной ДНК энтерококков (праймер В2) для подтверждения интеграции плазмидной ДНК pentF-pspf в хромосомную ДНК энтерококка.
Этот клон энтерококков PSPF+, экспрессирующий ген слитого белка PSPF белок, выбран в качестве вакцинного препарата для дальнейшего исследования.
Вакцинацию живой пробиотической вакциной проводили на мышах CBA, самках 16-18 г. Мыши экспериментальной группы (n=16) были вакцинированы интраназально введением в обе ноздри взвеси Enterococcus faecium L3-PSPF в дозе 5 х 108 КОЕ. Бактерии вводили два дня подряд, процедуру вакцинации проводили три раза с интервалом в три недели. Контрольные группы мышей получали по той же схеме пробиотический штамм Enterococcus faecium L3 (n=16) или ЗФР (n=16). Через 18 дней после второй и третьей вакцинации у мышей определяли содержание PSPF-специфических IgA в носовых смывах и PSPF-специфических IgG в сыворотке крови.
Уровень специфических антител определяли в реакции ИФА.
Было показано, что в сыворотке крови уже после второй вакцинации присутствовали специфические IgG (фиг. 8). Через 18 дней после третьей вакцинации специфические антитела в сыворотке крови продолжали циркулировать (фиг. 9).
Анализ секреторных IgA показал, что накануне заражения в носовых секретах мышей, вакцинированных живой вакциной присутствовали PSPF-специфические антитела в титре 1:5-1:10, в контролях специфические антитела не обнаруживались (фиг. 10).
В результате показано, что после проведения курса вакцинации живой вакциной происходит стимуляция местного и системного PSPF-специфического иммунного ответа, что выражается в накоплении в носовых секретах и сыворотке специфических антител класса А и G.
Для оценки протективной эффективности живой вакцины Enterococcus faecium L3-PSPF мышей заражали S.pneumoniae штамм 73 (серотип 3). С этой целью 20 мкл суспензии бактерий вводили иммунным и контрольным животным интраназально, каждая доза содержала 6 x 104 КОЕ. Через 4 часа после заражения у части мышей получали легкие для последующего подсчета бактерий в легочной ткани, остальных мышей оставляли для оценки уровня падежа от пневмококковой инфекции.
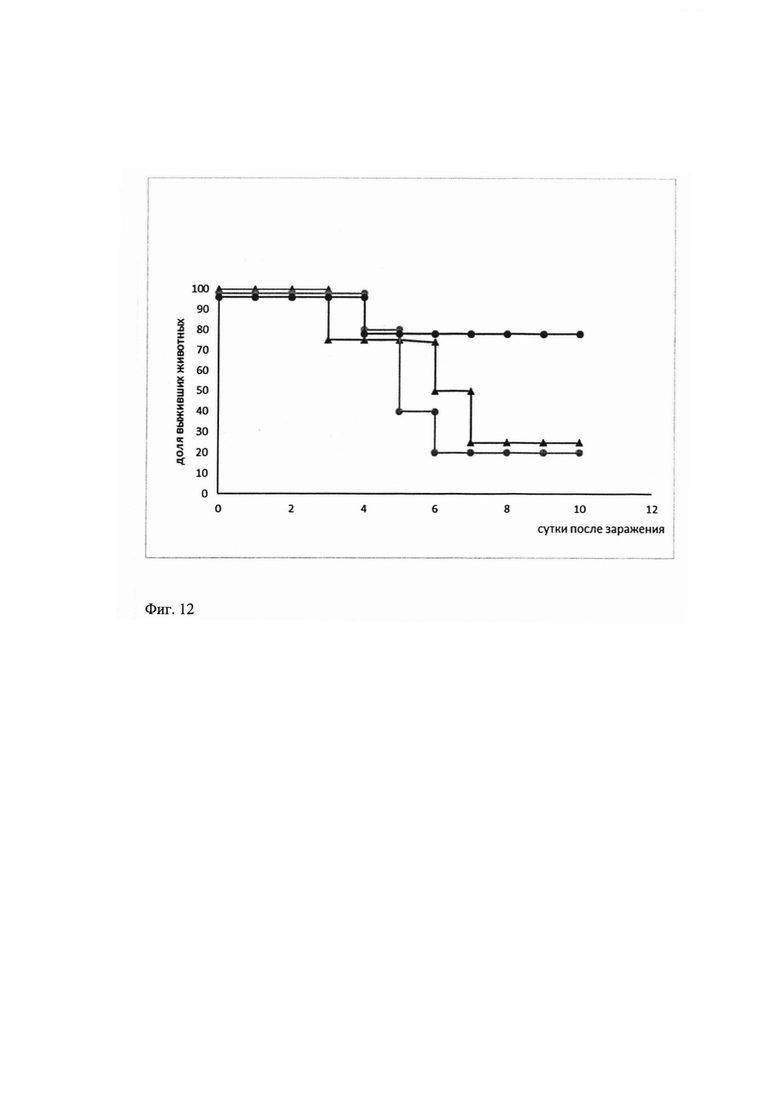
Через 4 часа после заражения в легких мышей, вакцинированных живой вакциной наблюдалось снижение количества бактерий по сравнению с обеими контрольными группами (фиг. 11). Через 10 дней после заражения в группе вакцинированных живой вакциной мышей падеж составил 40 %, тогда как смертность в контрольных группах составила 75 и 80 % (фиг. 12).
На основании проведенных иммунологических исследований можно заключить, что живая вакцина на основании штамма L3 пробиотика Enterococcus faecium, содержащая химерную последовательность иммунодоминантных участков ряда поверхностных белков пневмококка (PSPF), стимулировала развитие иммунного ответа, достаточного для снижения смертности от летальной пневмококковой инфекции на 40%.
Таким образом, на основе штамма пробиотика Enterococcus faecium L3 сконструирована генно-инженерная живая вакцина со встроенным в хромосому участком гена белка PSPF патогенного Streptococcus pneumoniae. Белок PSPF был встроен в структуру пилей. Интраназальное введение вакцины Enterococcus faecium L3-PSPF+ стимулировало развитие специфического системного и местного иммунного ответа. На модели интраназальной летальной пневмококковой инфекции у мышей СВА было показано, что трехкратная интраназальная вакцинация созданной живой пробиотической вакциной повышала защиту от летальной пневмококковой инфекции.
Описано создание живой вакцины на основе введении слитого гена, состоящего из двух участков гена пилей энтерококка и фрагмента гена, кодирующего PSPF белок патогенных пневмококков в структуру пробиотиков.
Пример 1. Получение фрагментов гена Enterococcus faecium L3 и фрагмента гена pspf
Для работы были выбран пробиотический штамм Enterococcus faecium L3, хромосомную ДНК которого использовали в качестве матрицы в полимеразной цепной реакции (ПЦР). Для выделения хромосомной ДНК клетки микроба лизировали 50 мМ ЭДТА (Serva, Германия) и лизоцимом в концентрации 1мг/мл. ДНК депротеинезировали фенолом и хлороформом, а затем экстрагировали спиртом. Для амплификации фрагмента гена pspf использовали гибридную плазмидную ДНК pspf.
Фрагменты ДНК, соответствующие фрагментам гена Enterococcus faecium L3 и фрагменту гена pspf, были амплифицированы в ПЦР с помощью Taq полимеразы («Ampli Taq», Perkin-Elmer, Cetus, USA) и амплификатора (BIO-RAD, USA). Олигонуклеотидные праймеры представлены в таблице 1. Проведена амплификация отдельных двух фрагментов гена Enterococcus faecium L3 с праймерами А1 и В1 и с праймерами С1 и D1 и фрагмента гена pspf с праймерами E1 и F1. В пробирки с 0,25 мкг геномной ДНК добавляли по 10 М каждого из специфических праймеров, фланкирующих исследуемую последовательность, буфер с магнием для полимеразы, по 0,2 мМ четырех дезоксирибонуклеотидтрифосфатов, объем доводили водой до 25 мкл и добавляли 0,5 мкл термостабильной Taq полимеразы. Пробирки помещали в амплификатор и инкубировали при 94С 2 мин. Программа ПЦР состояла из: денатурации при 94С - 30 сек, отжига праймеров - 55С - 1 мин и синтеза - 72С - 1 мин. Этот цикл повторяли 30 раз, после чего смесь инкубировали при 72С 10 мин. ПЦР продукты разделяли в 1% агарозном геле в горизонтальном электрофорезе. Выделение амплифицированных участков ДНК проводили с использованием набора «QIAquick Gel Extraction Kit» (Qiagen, США). Анализ размера полученных фрагментов ДНК проводили, исходя из сравнения их электрофоретических подвижностей с элетрофоретической подвижностью маркера молекулярных весов (100 п.н. ДНК-маркер, Хеликон).
На фиг. 1 представлена электрофореграмма амплифицированных ДНК-фрагментов, где цифрами обозначено:
1 - 100 п.н. ДНК - маркер (сверху вниз: 3000, 2000, 1000, 900, 800, 700, 600, 500, 400, 300, 200 и 100 нуклеотидных пар).
2 - продукт ПЦР с праймерами А1 и В1
3 - продукт ПЦР с праймерами С1 и D1
4 - продукт ПЦР с праймерами E1 и F1
Пример 2. Получение слитого гена entF-pspf и его клонирование.
Синтез слитого фрагмента осуществляли с праймерами A1 и D1. Программа ПЦР состояла из: денатурации при 94С - 30 сек, отжига праймеров - 55 С - 1 мин и синтеза - 72С - 2 мин. Этот цикл повторялся 30 раз, после чего смесь инкубировалась при 72С 10 мин. ПЦР продукты разделяли в 1% агарозном геле в горизонтальном электрофорезе. Выделение амплифицированного участка ДНК проводили с использованием набора «QIAquick Gel Extraction Kit» (Qiagen, США). Анализ размера полученного фрагмента ДНК проводили, исходя из сравнения их электрофоретических подвижностей с элетрофоретической подвижностью маркера молекулярных весов (100 п.н. ДНК-маркер, Хеликон).
Электрофореграмма амплифицированного слитого фрагмента ДНК представлена на фиг. 2, где цифрами обозначено:
1 - 100 п.н. ДНК - маркер (сверху вниз: 3000, 2000, 1000, 900, 800, 700, 600, 500, 400, 300, 200 и 100 нуклеотидных пар).
2 - Продукт ПЦР (слитый фрагмент).
Пример 3. Клонирование слитого фрагмента ДНК
Клонирование амплифицированного фрагмента ДНК осуществляли с использованием плазмиды pJET1.2, используя Clone JET PCR Cloning Kit (Fermentas). Реакционная смесь состояла из 1мкл PCR- продукта, 1 мкл ДНК-вектора pJET1.2 (50 ng/l), 10 мкл лигазного буфера, 1 мкл T4 ДНК-лигазы и 7 мкл бидистиллированной воды. Лигазную смесь инкубировали при 220 С 5 мин. Лигазную смесь использовали для трансформации в гетерологичную систему E.coli DH5. Среда для отбора трансформантов содержала 100 мкг/мл ампициллина. Получили трансформанты, из которых были выделены плазмидные ДНК, с которыми поставлена реакция ПЦР с праймерами А1 и D2. Вставку содержали 2 плазмиды. Эти плазмиды были рестрицированы ферментами BamHI и XbaI (фиг. 3).
На фиг.3. представлена электрофореграмма рестрицированных плазмид BamHI и XbaI, где цифрами обозначено:
1 - плазмида 1,
3 - плазмида 2,
2 - 1 kb маркер (сверху вниз: 10000, 8000, 6000, 5000, 4000, 3500, 3000, 2500, 2000, 1500, 1000, 750, 500 и 250 нуклеотидных пар).
Как следует из рисунка, нужный фрагмент содержали обе плазмиды. Была выбрана плазмида 1 и обозначена, как pentF-pspf
Гибридная ДНК (entF-pspf) была переклонирована в суицидную плазмиду pT7ERMB с геном устойчивости к эритромицину. Для этого была проведена амплификация плазмиды 1 с праймерами A1 и D1. ПЦР-продукт и плазмида pT7ERMB были рестрицированы ферментами BamHI и Xba. Продукты рестрикции разделяли с помощью электрофореза в 1% агарозном геле. ДНК рестрикты выделяли из агарозы с помощью набора «QIAquick Gel Extraction Kit» (Qiagen, USA), лигировали и трансформировали в гетерологичную систему E.coli DH5. Среда для отбора содержала 500 мкг/мл эритромицина. Из полученных клонов после трансформации были выделены ДНК, которые были проверены в реакции ПЦР с праймерами A1 и D1. 8 трансформантов дали положительный ответ. Из них были выделены плазмиды, 5 из которых содержали ожидаемую вставку. На фиг. 4 показана электрофореграмма плазмид, выделенных из 8 трансформантов, где цифрами 1-8 обозначены плазмиды с 1 по 8, а цифрой 9 обозначена эритромициновая плазмида pT7ERMB. Как следует из рисунка, вставка есть в 1, 2, 3, 7 и 8 плазмидах.
Рестрикция этих плазмид BamHI и XbaI подтвердила наличие нужной вставки. На фиг. 5 представлена электрофореграмма рестрицированных плазмид BamHI и XbaI, где цифрами обозначено:
1 - плазмида 7, 2 - плазмида 8, 3 - плазмида 1 pJET,
4 - 1kb маркер (сверху вниз: 10000, 8000, 6000, 5000, 4000, 3500, 3000, 2500, 2000, 1500, 1000, 750, 500 и 250 нуклеотидных пар). Для дальнейшей работы выбрали плазмиду, выделенную из клона 7 и обозначенную как pentF-pspf.
Наличие фрагментов гена пилей Enterococcus faecium L3 и фрагмента гена pspf ПЦР было подтверждено ПЦР плазмиды pentF-pspf с праймерами A1 и B1, C1 и D1, A1 и F1, E1 и D1.
Электрофореграмма амплифицированной плазмиды pentF-pspf) приведена на фиг. 6, где цифрами обозначено:
1 - ПЦР продукт с праймерами A1 и B1
2 - ПЦР продукт с праймерами C1 и D1
3 - ПЦР продукт с праймерами A1 и F1
4 - ПЦР продукт с праймерами E1 и D1
5 - 100 п.н. ДНК - маркер (сверху вниз: 3000, 2000, 1000, 900, 800, 700, 600, 500, 400, 300, 200 и 100 нуклеотидных пар).
Пример 4. Электропорация энтерококков.
Для электропорации энтерококков культуру Enterococcus faecium L3 сеяли в 3 мл бульона Tood-Hewitt (THB) («HiMedia», Индия) и выращивали в течение ночи при 37С, затем пересевали в 50 мл бульона THB 1 мл ночной культуры и выращивали ее до оптической плотности при длине волны 650 нм 0.3. После этого культуру помещали в лед и затем отмывали трижды в 20 мл 10% глицерола при температуре 4С, полученный осадок суспендировали в 0.5 мл стерильного раствора глицерола, переосаждали и конечный осадок ресуспендировали в 0.3 мл того же раствора, разлили по 50 мкл в пробирки и проводили электропорацию в кювете с расстоянием между электродами 1 мм при напряжении 2100 В. Во льду к клеткам добавили ДНК (полученную интегративную плазмиду pentF-pspf плазмиду, 300 нг). Оптимальная продолжительность импульса составила 4-5 миллисекунд. После проведения разряда тока в кювету добавляли 1 мл THB, инкубировали 1 час и высевали на чашки с селективной средой, которая содержала 2.5 мкг/мл эритромицина. Затем ожидали появления трансформантов через 24 часа.
В результате электропорации энтерококков созданной интегративной плазмидой были получены 2 трансформанта. Они были проверены в реакции ПЦР со специально сконструированными праймерами SeqF и SeqR. Для этого из трансформантов выделяли ДНК, используя набор ДНК-экспресс (Литех, Россия). Положительный ответ дал только один трансформант, обозначенный как PSPF+ клон. Электрофореграмма амплифицированных ДНК-фрагментов показана на фиг. 7, где цифрами обозначено:
1 - 100 п.н. ДНК - маркер (сверху вниз: 3000, 2000, 1000, 900, 800, 700, 600, 500, 400, 300, 200 и 100 нуклеотидных пар).
2 - продукт ПЦР клона 1 с праймерами SeqF и SeqR
3 - продукт ПЦР клона 2 с праймерами SeqF и SeqR
4 - продукт ПЦР плазмидной ДНК pentF-pspf с праймерами SeqF и SeqR
Было проведено секвенирование ДНК, выделенной из PSPF+ клона с праймерами, соответствующими последовательности гена pspf (праймер seqR) и последовательности хромосомной ДНК энтерококков (праймер В2), чтобы подтвердить интеграцию плазмидной ДНК pentF-pspf в хромосомную ДНК энтерококка.
Нуклеотидная последовательность ПЦР продукта, состоящая из 1713 п.н. и соответствующая последовательности двух фрагментов гена энтерококка и встроенному между ними фрагменту pspf гена, приведена в Перечне последовательностей как SEQ ID NO: 1.
Аминокислотная последовательность слитого белка, состоящая из 571 аминокислотного остатка, приведена в Перечне последовательностей как SEQ ID NO: 2.
Клон энтерококков PSPF+, экспрессирующий ген слитого PSPF белка, выбран в качестве вакцинного препарата для дальнейшего исследования.
Пример 5. Вакцинация мышей живой пробиотической вакциной.
Исследование выполнялось на мышах CBA, самках 16-18 г. Мыши экспериментальной группы (n=16) были вакцинированы интраназально введением в обе ноздри взвеси Enterococcus faecium L3-PSPF в дозе 5 х 108 КОЕ. Бактерии вводили два дня подряд, процедуру вакцинации проводили три раза с интервалом в три недели. Контрольные группы мышей получали по той же схеме пробиотический штамм Enterococcus faecium L3 (n=16) или ЗФР (n=16). Через 18 дней после второй и третьей вакцинации у мышей определяли содержание PSPF-специфических IgA в носовых смывах и PSPF-специфических IgG в сыворотке крови.
Уровень специфических антител определяли в реакции ИФА.
Было показано, что в сыворотке крови уже после второй вакцинации присутствовали специфические IgG. На фиг. 8 показано сравнение уровня PSPF-специфических IgG антител в сыворотке крови мышей после двух циклов интраназального введения, где
■- E. faecium L3-PSPF
● - E.. Faecium L3
▲- ФСБ
* - различия средних значений достоверны (р0,05)
Через 18 дней после третьей вакцинации специфические антитела в сыворотке крови продолжали циркулировать. Сравнение уровня PSPF-специфических IgG антител в сыворотке крови мышей после трех циклов интраназального введения показано на фиг. 9, где
■ - E.. faecium L3-PSPF
●- E.. faecium L3
▲- ФСБ
* - различия средних значений достоверны (р0,05).
Каждая точка представляет собой среднее значение из четырех или пяти мышей на группу . Сравнение независимых выборок проводили методом ANOVA. Статистически достоверные отличия значений ОД450 при анализе сывороток в соответствующих разведениях указаны звездочками, уровень статистической значимости p0,05.
Анализ секреторных IgA показал, что накануне заражения в носовых секретах мышей, вакцинированных живой вакциной присутствовали PSPF-специфические антитела в титре 1:5-1:10, в контролях специфические антитела не обнаруживались. На фиг. 10 показано сравнение уровня PSPF-специфических IgA антител в индивидуальных сыворотках крови мышей после трех циклов интраназального введения, где
• - E. faecium L3-PSPF
● - E. faecium L3
▲ - ФСБ
— - среднее значение
Таким образом, после проведения курса вакцинации живой вакциной происходит стимуляция местного и системного PSPF-специфического иммунного ответа, что выражается в накоплении в носовых секретах и сыворотке специфических антител класса А и G.
Пример 6. Изучение протективной эффективности живой вакцины.
Для оценки протективной эффективности живой вакцины Enterococcus faecium L3-PSPF мышей заражали S.pneumoniae штамм 73 (серотип 3). С этой целью 20 мкл суспензии бактерий вводили иммунным и контрольным животным интраназально, каждая доза содержала 6 х 104 КОЕ. Через 4 часа после заражения у части мышей получали легкие для последующего подсчета бактерий в легочной ткани, остальных мышей оставляли для оценки уровня падежа от пневмококковой инфекции.
Через 4 часа после заражения в легких мышей, вакцинированных живой вакциной наблюдалось снижение количества бактерий по сравнению с обеими контрольными группами. На фиг. 11 приведено сравнение показателей выделения S.pneumoniae из легких мышей, вакцинированных интраназально различными препаратами, через 4 часа после заражения.
• - E. faecium L3-PSPF
● - E. faecium L3
▲ - ФСБ
— - среднее значение
Через 10 дней после заражения в группе вакцинированных живой вакциной мышей падеж составил 40 %, тогда как смертность в контрольных группах составила 75 и 80 %. На фиг. 12 показано изменение доли выживших животных после интраназальной инфекции S.pneumoniae.
• - E. faecium L3-PSPF
●- E. faecium L3
▲- ФСБ
Таким образом на основании проведенных иммунологических исследований можно заключить, что живая вакцина на основании штамма L3 пробиотика Enterococcus faecium, содержащая химерную последовательность иммунодоминантных участков ряда поверхностных белков пневмококка (PSPF), стимулировала развитие иммунного ответа, достаточного для снижения смертности от летальной пневмококковой инфекции на 40%.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ создания рекомбинантного штамма энтерококка L3-SARSN1 на основе биологически активного штамма Enterococcus faecium L3 | 2022 |
|
RU2820058C1 |
| Способ создания живой вакцины против коронавирусной инфекции COVID-19 на основе пробиотического штамма Enterococcus faecium L3 и живая вакцина Enterococcus faecium L3-pentF-covid-19 | 2020 |
|
RU2745626C1 |
| Способ создания живого штамма энтерококка L3-SARS на основе биологически активного штамма Е. faecium L3 | 2021 |
|
RU2782529C1 |
| Способ создания рекомбинантного штамма энтерококка L3-SARS"XBB.1.5" на основе биологически активного штамма Enterococcus faecium L3 | 2023 |
|
RU2840971C1 |
| СПОСОБ ВВЕДЕНИЯ ГЕНОВ ПАТОГЕННЫХ СТРЕПТОКОККОВ В ХРОМОСОМНУЮ ДНК ПРОБИОТИЧЕСКОГО ШТАММА ENTEROCOCCUS FAECIUM L3 ДЛЯ ЭКСПРЕССИИ В ПИЛЯХ | 2015 |
|
RU2640250C2 |
| Штамм вируса гриппа ИнфлюБакт-H7/PspA для производства комбинированной вакцины против вируса гриппа А и бактериальной пневмонии, вызываемой Streptococcus pneumoniae | 2021 |
|
RU2776196C1 |
| Рекомбинантная ДНК, обеспечивающая получение рекомбинантного белка Cov1, обладающего иммуногенными свойствами в отношении вируса SARS-CoV-2 | 2021 |
|
RU2776484C1 |
| ВАКЦИНА ПРОТИВ ПНЕВМОНИИ, ВЫЗЫВАЕМОЙ Streptococcus pneumoniae, НА ОСНОВЕ ГИБРИДНОГО БЕЛКА | 2012 |
|
RU2510281C2 |
| ШТАММ Lactobacillus fermentum Z, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРОИЗВОДСТВА ПРОБИОТИЧЕСКИХ МОЛОЧНОКИСЛЫХ ПРОДУКТОВ | 2008 |
|
RU2412239C2 |
| Штамм энтерококков Enterococcus faecium L-3 для лечения и профилактики бактериальных и вирусных инфекций с использованием изготовленных на его основе лечебно-профилактических средств и продуктов питания и способ культивирования штамма энтерококков Enterococcus faecium L-3 | 2022 |
|
RU2800359C1 |





Настоящая группа изобретений относится к медицине, а именно к микробиологии, молекулярной генетике и биотехнологии, и касается создания живой вакцины на основе штамма Enterococcus faecium L3 для профилактики и лечения пневмонии, вызываемой пневмококками Streptococcus pneumoniae. Для этого в структуру пилей Еnterococcus faecium L3 включают антиген клинически актуального патогенного микроорганизма. Это достигалось введением гена pspf патогенных пневмококков в хромосомную ДНК пробиотического штамма Еnterococcus faecium L3. Вакцина, созданная на основе пробиотического штамма микроорганизмов, обладает выраженным иммуногенным и протективным эффектами, что обеспечивает ее эффективность в отношении любого серологического варианта пневмококка. 3 н.п. ф-лы, 12 ил., 1 табл., 6 пр.
1. Способ создания живой вакцины на основе биологически активного штамма E. faecium L3 за счет включения в структуру его пилей антигена клинически актуального патогенного микроорганизма, заключающийся в получении слитого гена enta-pspf и его клонировании, выявлении бактериальных клонов, экспрессирующих нужный белок в пилях, иммунизации мышей живой пробиотической вакциной и определении белок-специфических антител в крови и носовых смывах.
2. Рекомбинантная плазмидная ДНК penta-pspf, представляющая собой плазмидную ДНК, полученную в результате вставки суммарного фрагмента ДНК, состоящего из двух отдельных фрагментов гена пробиотика Enterococcus faecium L3 и фрагмента гена pspf и имеющего нуклеотидную последовательность SEQ ID NO: 1, в суицидную плазмиду PT7ERMB по сайтам BamHI и XbaI, используемая для создания живой вакцины по п. 1.
3. Вакцинный препарат Enterococcus faecium L3-PSPF+, полученный после электропорации плазмидной ДНК pentF-pspf по п. 2, в котором Enterococcus faecium L3 экспрессирует ген слитого белка PSPF, имеющий аминокислотную последовательность SEQ ID NO: 2, способный вызывать синтез анти-PSPF, причем образующиеся специфические антитела обладают протективными свойствами в отношении Streptococcus pneumonie.
| СПОСОБ ВВЕДЕНИЯ ГЕНОВ ПАТОГЕННЫХ СТРЕПТОКОККОВ В ХРОМОСОМНУЮ ДНК ПРОБИОТИЧЕСКОГО ШТАММА ENTEROCOCCUS FAECIUM L3 ДЛЯ ЭКСПРЕССИИ В ПИЛЯХ | 2015 |
|
RU2640250C2 |
| ВАКЦИНЫ И КОМПОЗИЦИИ ПРОТИВ STREPTOCOCCUS PNEUMONIAE | 2012 |
|
RU2623174C2 |
| US 2006263846 A1, 23.11.2006 | |||
| ВАСИЛЬЕВА В.А | |||
| и др | |||
| "Молекулярная эпидемиология инфекций, вызываемых стрептококками группы В у беременных и новорожденных, и разработка профилактических вакцин" | |||
| Журнал акушерства и женских болезней, 2018, т.67, вып.5, с.62-73, принята к печати 19.10.2018 | |||
| ГУПАЛОВА Т.В | |||
| и др | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| SHARMA K | |||
| et al | |||
| "Development of probiotic-based immunoparticles for pulmonary immunization against Hepatitis B" | |||
| J Pharm Pharmacol | |||
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
Авторы
Даты
2019-10-01—Публикация
2018-12-14—Подача