Область техники
Настоящее изобретение относится в целом к иминосахарам и способам их применения и, в частности, к N-замещенным соединениям дезоксинойиримицина и их применению для лечения и/или профилактики вирусных инфекций.
Сущность изобретения
Один вариант осуществления представляет собой соединение формулы (I):
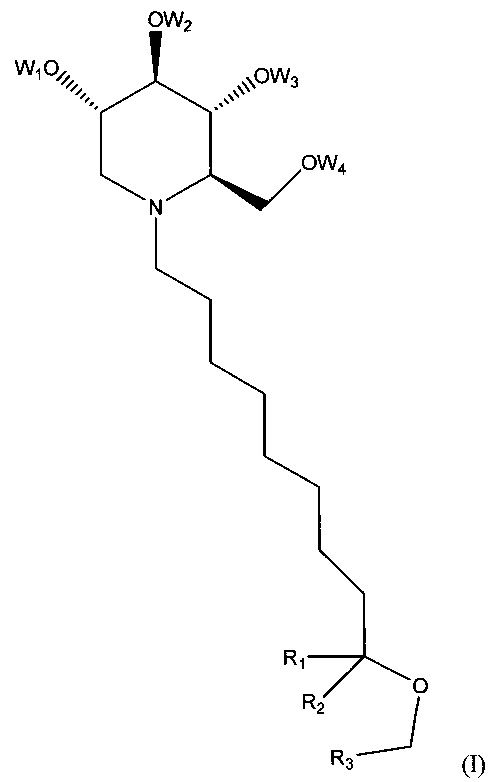
или его фармацевтически приемлемую соль, где W1-4 и R1-3 каждый независимо выбран из водорода и С1-3-алкильных групп и где по меньшей мере один из R1-3 представляет собой не водород.
Еще один вариант осуществления представляет собой способ лечения заболевания или состояния, вызванного или связанного с вирусом, принадлежащим к семейству Orthomyxoviridae, предусматривающий введение нуждающемуся в этом субъекту соединения формулы (I) или его фармацевтически приемлемой соли.
И еще один вариант осуществления представляет собой способ лечения заболевания или состояния, вызванного или связанного с вирусом денге, предусматривающий введение нуждающемуся в этом субъекту соединения формулы (I) или его фармацевтически приемлемой соли.
Краткое описание чертежей
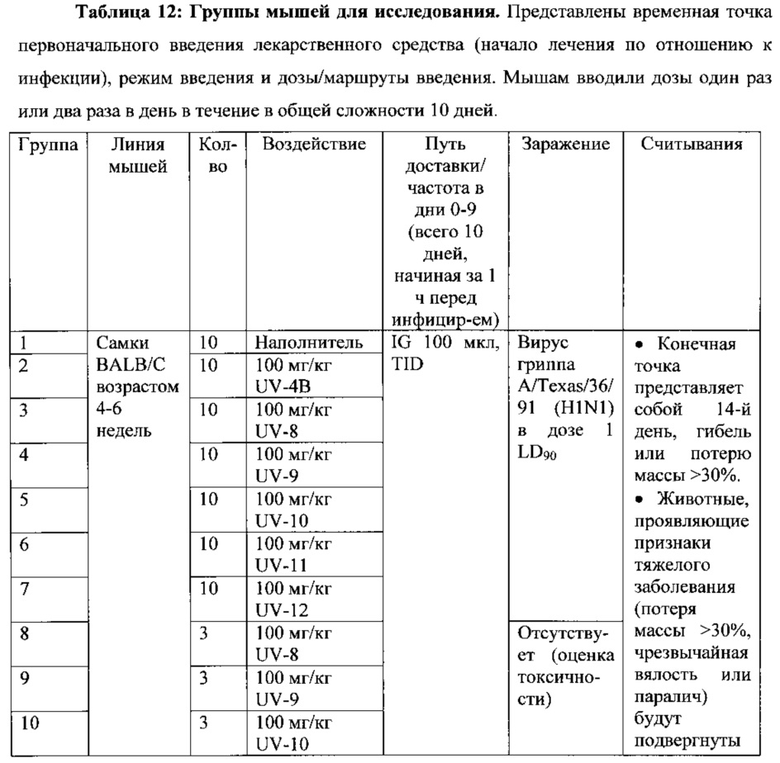
Фигура 1: Выживаемость инфицированных мышей, сгруппированных по лечению. Группы мышей (n=10) получали лечение TID, начиная за 1 час до инфицирования; мышей заражали интраназально гриппом в дозе ~1 LD90. Данные по выживаемости представлены на графике в виде процента выживаемости по отношению к дням после заражения. На графике показана выживаемость животных в каждой группе.
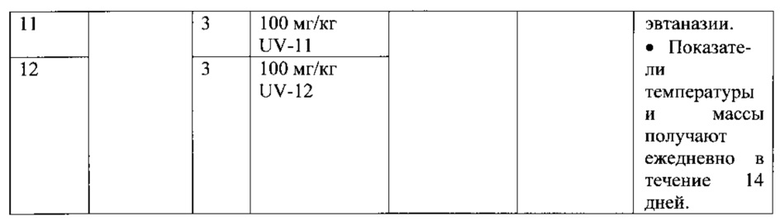
Фигура 2: Массы инфицированных мышей, сгруппированных по лечению. Группы мышей (n=10) получали лечение TID, начиная за 1 час до инфицирования; мышей заражали интраназально гриппом в дозе ~1 LD90. Данные масс представлены на графике в виде процента от первоначальной массы по отношению к количеству дней после инфицирования.
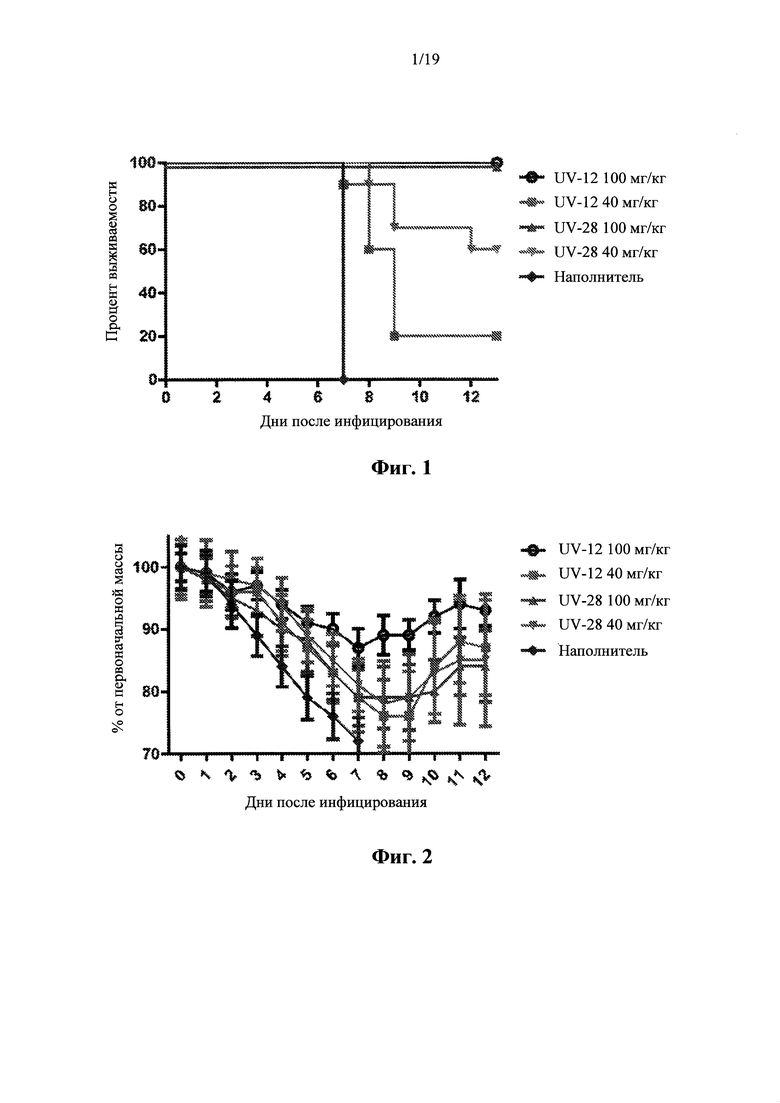
Фигура 3: Температуры инфицированных мышей, сгруппированных по лечению. Группы мышей (n=10) получали лечение TID, начиная за 1 час до инфицирования; мышей заражали интраназально гриппом в дозе ~1 LD90. Температурные данные представлены на графике в виде процента от исходной температуры по отношению к количеству дней после инфицирования.
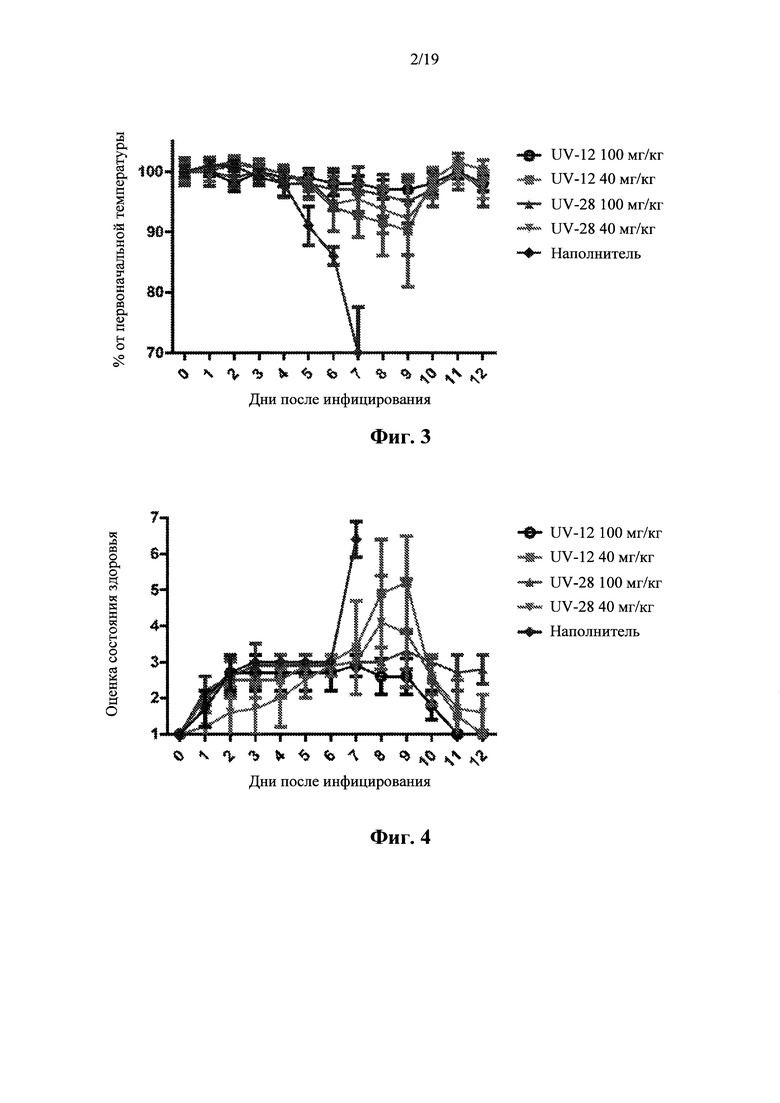
Фигура 4: Состояние здоровья инфицированных мышей, сгруппированных по лечению. Группы мышей (n=10) получали лечение TID, начиная за 1 час до инфицирования; мышей заражали интраназально гриппом в дозе ~1 LD90. Данные о состоянии здоровья представлены на графике в виде показателя состояния здоровья по отношению к дням после заражения.
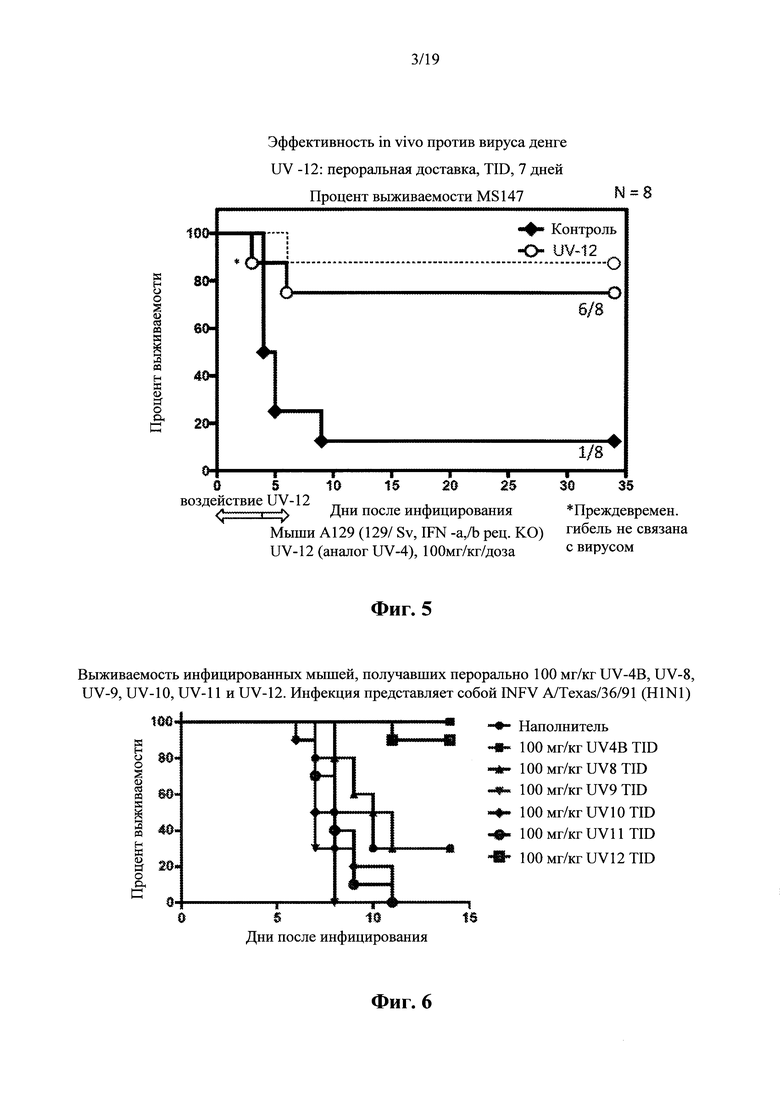
На фигуре 5 представлен график, демонстрирующий эффективность in vivo UV-12 против вируса денге.
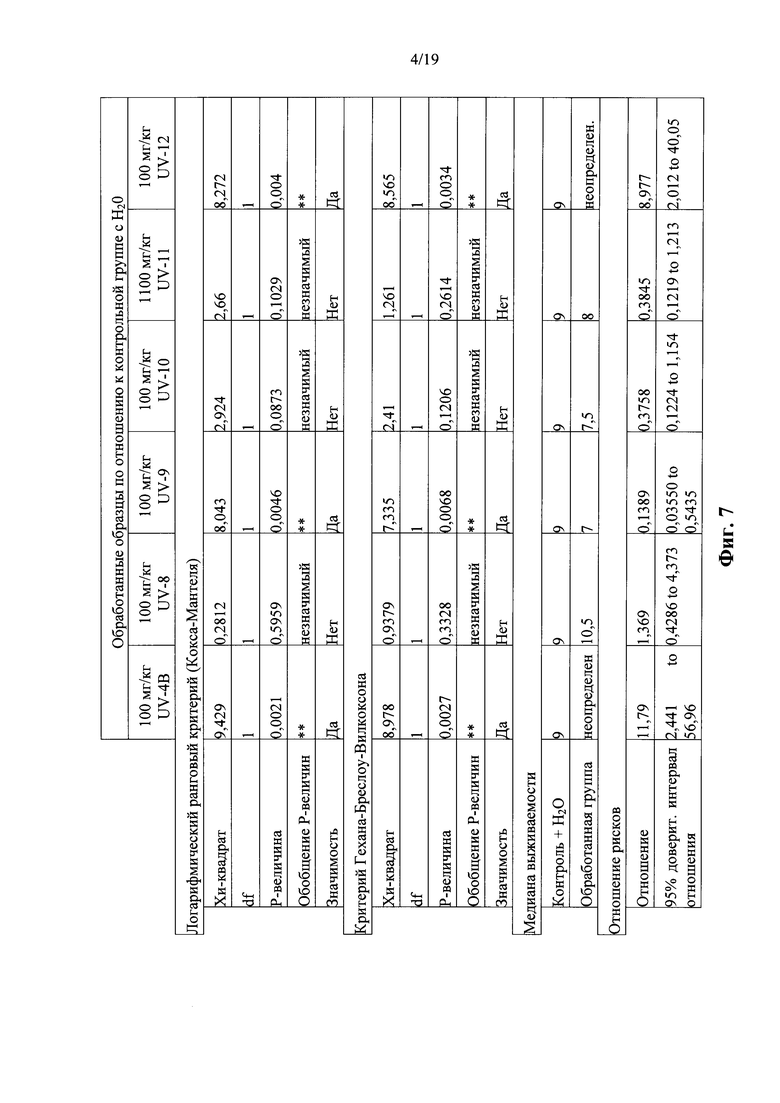
Фигура 6: Выживаемость мышей, сгруппированных по маршруту доставки лечения. Группы мышей (n=10) получали первую дозу воздействия соединения в воде за 1 ч до интраназального инфицирования вирусом гриппа A/Texas/36/91 (H1N1) в дозе ~1 LD90. Данные по выживаемости представлены на графике в виде процента выживаемости по отношению к дням после инфицирования. (А) Воздействие 100 мг/кг UV-4B, UV-8, UV-9, UV-10, UV-11 и UV-12, предполагая начальный вес ~20 г на мышь. График включает в себя кривую выживаемости контрольной группы, получавшей только наполнитель.
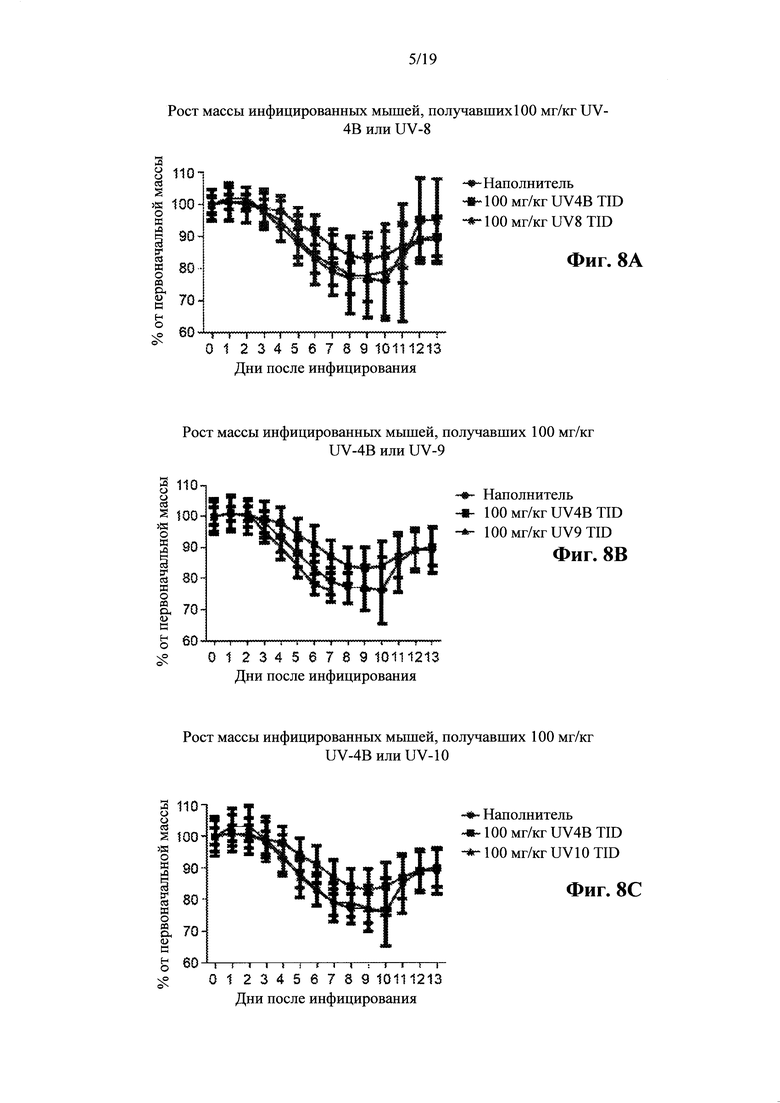
Фигура 7: Статистический анализ выживаемости инфицированных мышей. Данные выживаемости, приведенные на фиг. 6, анализировали с использованием критериев Кокса-Мантеля и Гехана-Бреслоу-Вилкоксона. (А) Статистический анализ проводили путем сравнения обработанных групп с контролем, получавшим носитель Н2О. Статистическая значимость указана в виде р-величины <0,05.
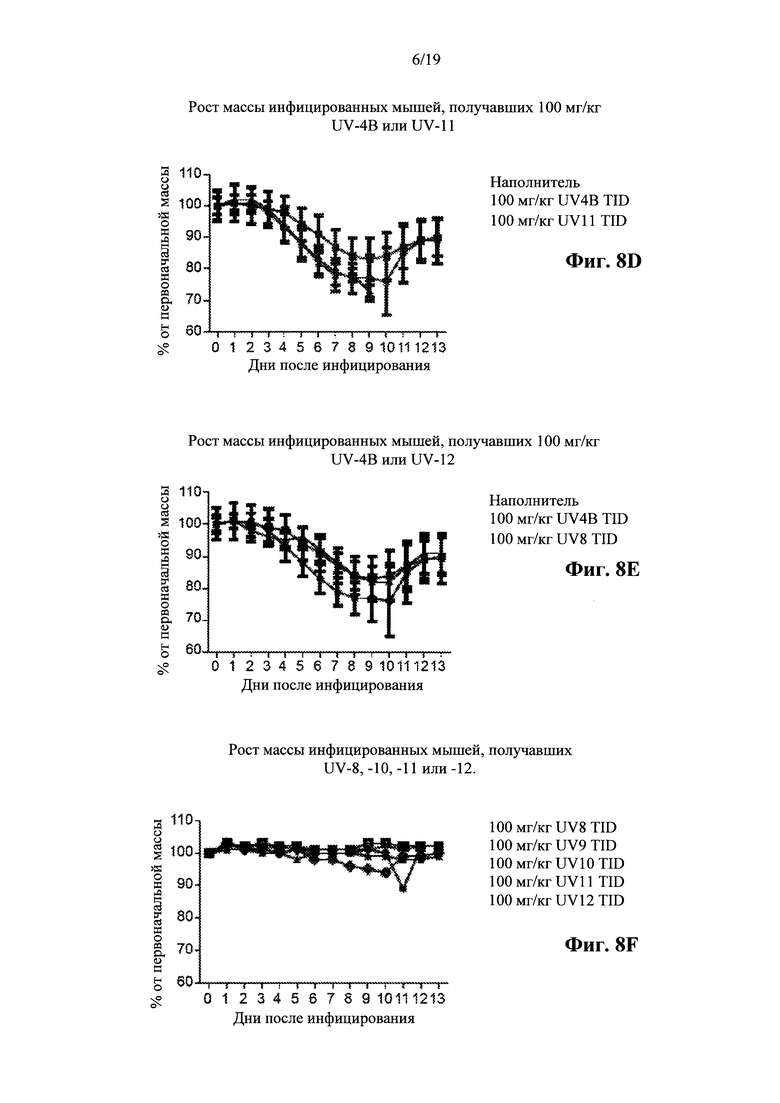
Фигуры 8A-F: Анализ масс.Мыши получали первую дозу соединения в Н2О за 1 час до интраназального инфицирования гриппом A/Texas/36/91 (H1N1) в дозе ~1 LD90. Средние массы для каждой группы приведены на графиках в виде процентов от масс в день 0 (исходный уровень) со стандартными отклонениями. (А) Воздействие на инфицированных мышей UV-4B или UV-8, (В) воздействие на инфицированных мышей UV-4B или UV-9, (С) воздействие на инфицированных мышей UV-4B или UV-10, (D) воздействие на инфицированных мышей UV-4B или UV-11, (Е) воздействие на инфицированных мышей UV-4B или UV-12 и (F) воздействие на инфицированных мышей UV-8, -9, - 10, - 11 или -12, без стандартных отклонений.
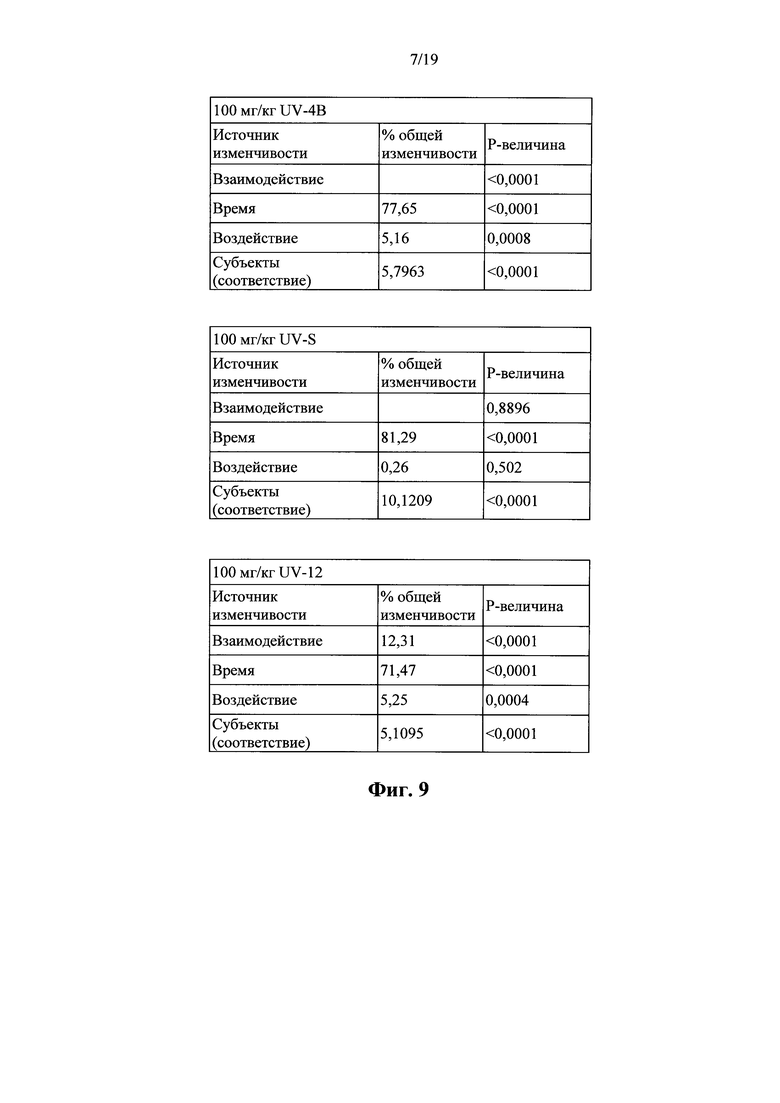
Фигура 9: Статистический анализ данных масс. Данные о массах для инфицированных гриппом мышей, приведенные на фиг.8, анализировали с использованием повторных измерений 2-факторного дисперсионного анализа (GraphPad Prism) по отношению к контролю-наполнителю. Данные анализировали только в течение 7 дней после инфицирования (p.i.) из-за смертности в более поздние моменты времени. Соединения UV-9, UV-10 и UV-11 характеризовались выживаемостью, составляющей 0%, и MTD<9 дней и были, таким образом, исключены из дальнейшего статистического анализа. Статистическая значимость указана в виде р-величины ниже, чем 0,05 (р<0,05).
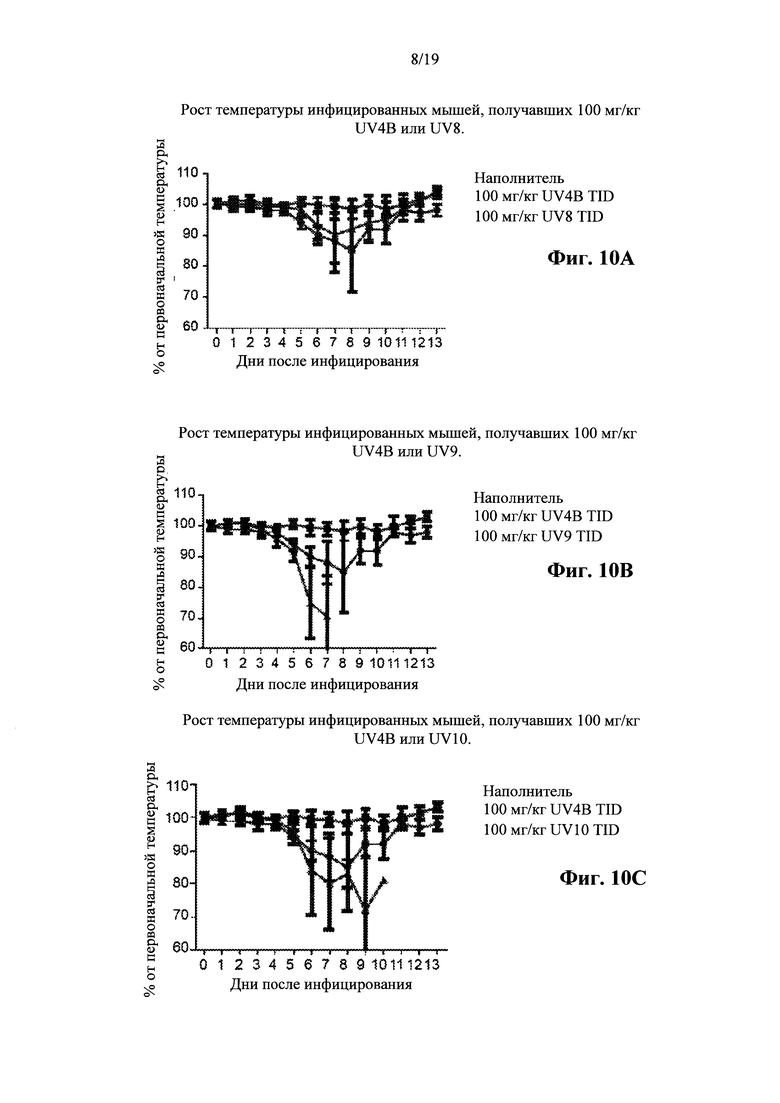
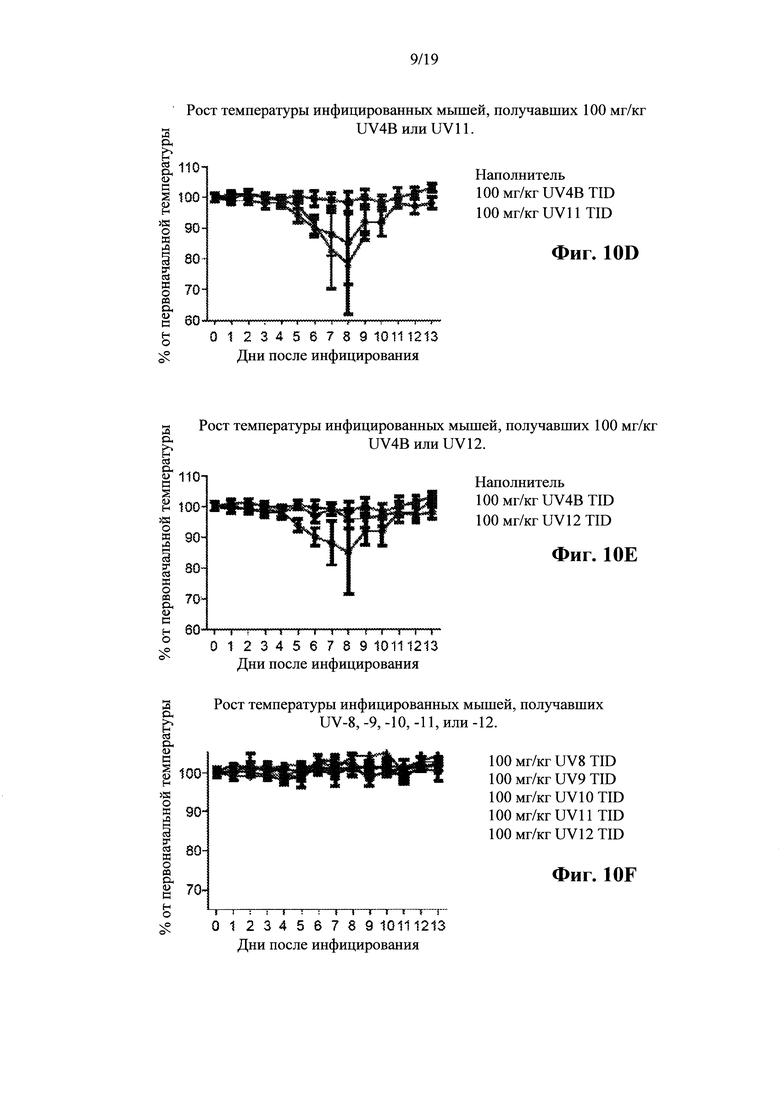
Фигура 10: Анализ температур. Мыши получали первую дозу соединения в Н2О на 1 час до интраназального инфицирования гриппом A/Texas/36/91 (H1N1) в дозе ~1 LD90. Средние температуры для каждой группы приведены на графиках в процентах от массы в день 0 (исходный уровень) со стандартными отклонениями. (А) Воздействие на инфицированных мышей UV-4B или UV-8, (В) воздействие на инфицированных мышей UV-4B или UV-9, (С) воздействие на инфицированных мышей UV-4B или UV-10, (D) воздействие на инфицированных мышей UV-4B или UV-11, (Е) воздействие на инфицированных мышей UV-4B или UV-12 и (F) воздействие на инфицированных мышей UV-8, -9, - 10, - 11 или -12, без стандартных отклонений.
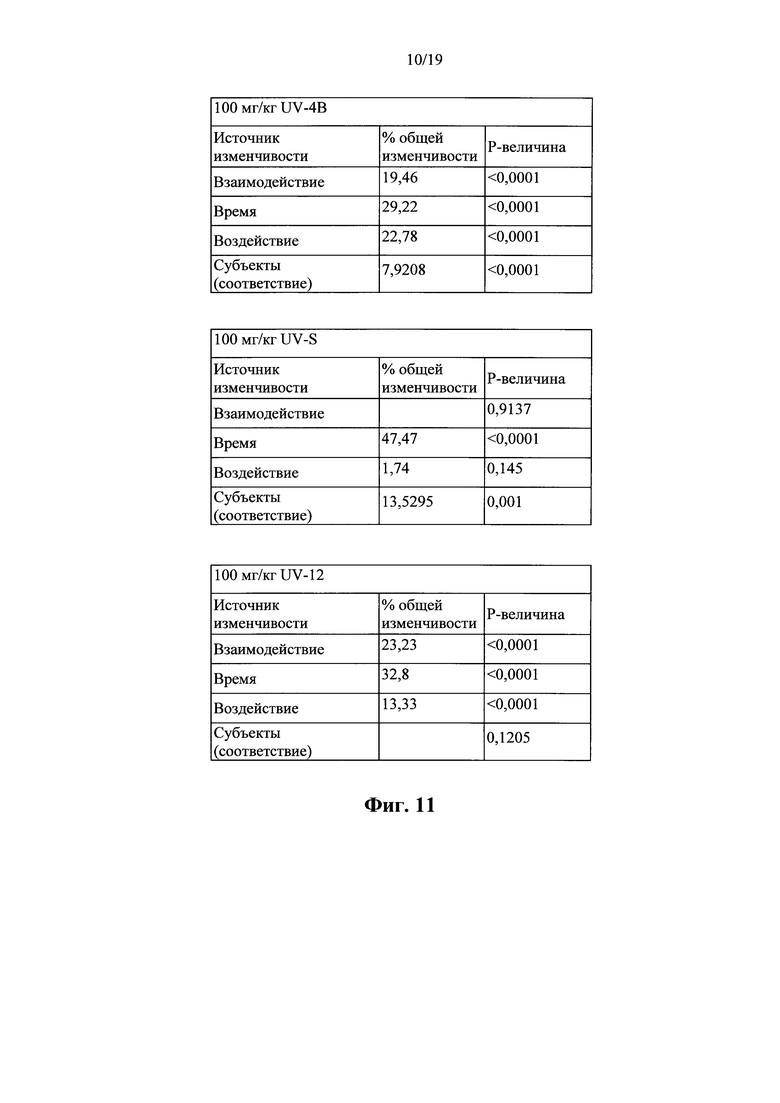
Фигура 11: Статистический анализ температурных данных. Температурные данные для инфицированных гриппом мышей, приведенные на фиг. 10, анализировали с использованием повторных измерений 2-факторного дисперсионного анализа (GraphPad Prism) по отношению к контролю-наполнителю. Данные анализировали только в течение 7 дней после инфицирования (p.i.) из-за смертности в более поздние моменты времени. Соединения UV-9, UV-10 и UV-11 характеризовались выживаемостью, составляющей 0%, и MTD<9 дней и были, таким образом, исключены из дальнейшего статистического анализа. Статистическая значимость указана в виде р-величины ниже, чем 0,05 (р<0,05).
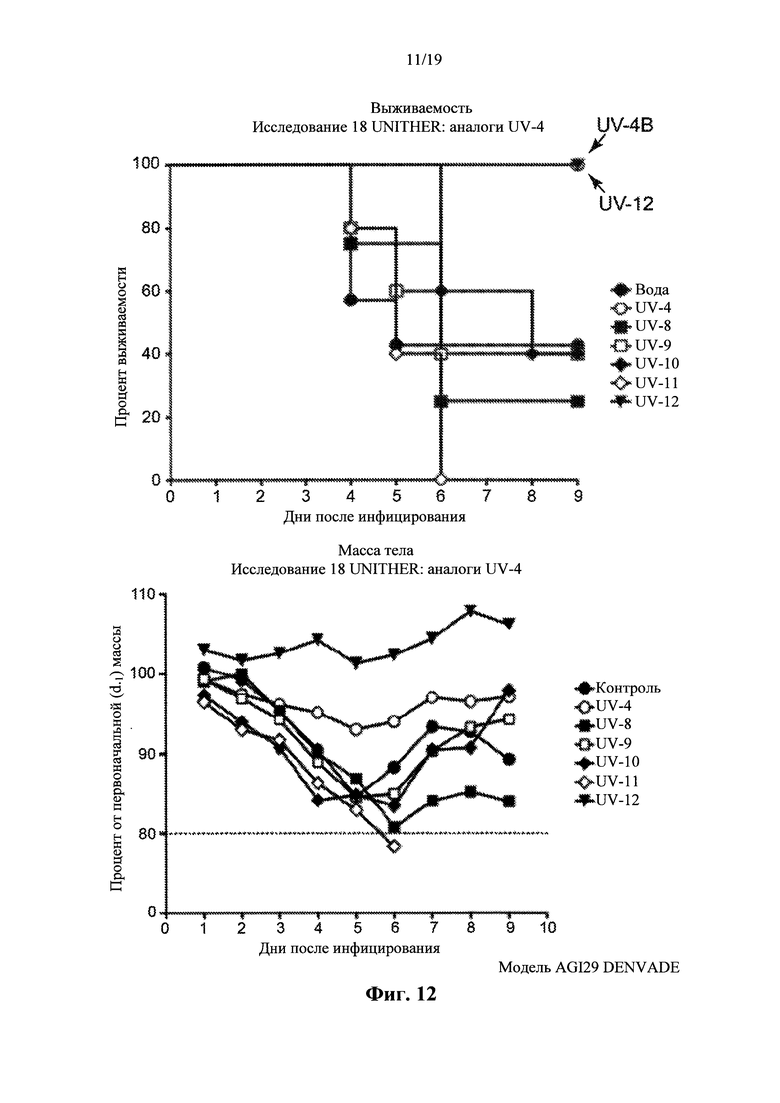
На фиг. 12 представлены результаты исследования, выполненного в примере 4. Это исследование представляло собой определение выживаемости инфицированных вирусом денге мышей. Данные о выживании и массе тела животных показаны на фиг. 12. Все соединения вводили в воде пероральным путем (3 раза в день внутрижелудочно через желудочный зонд - IG) до достижения общего количества 7 дней после начала приема лекарственного средства. Доза лекарственного средства составляла 50 мг/кг UV-4B, UV-8, UV-9, UV-10, UV-11 и UV-12. Группы мышей получали первую дозу воздействия соединения за 0,5-1 ч до внутривенной инфекции вирусом денге в дозе ~1 LD90. Выживаемость и массу тела измеряли до достижения 3 дней после введения дозы.
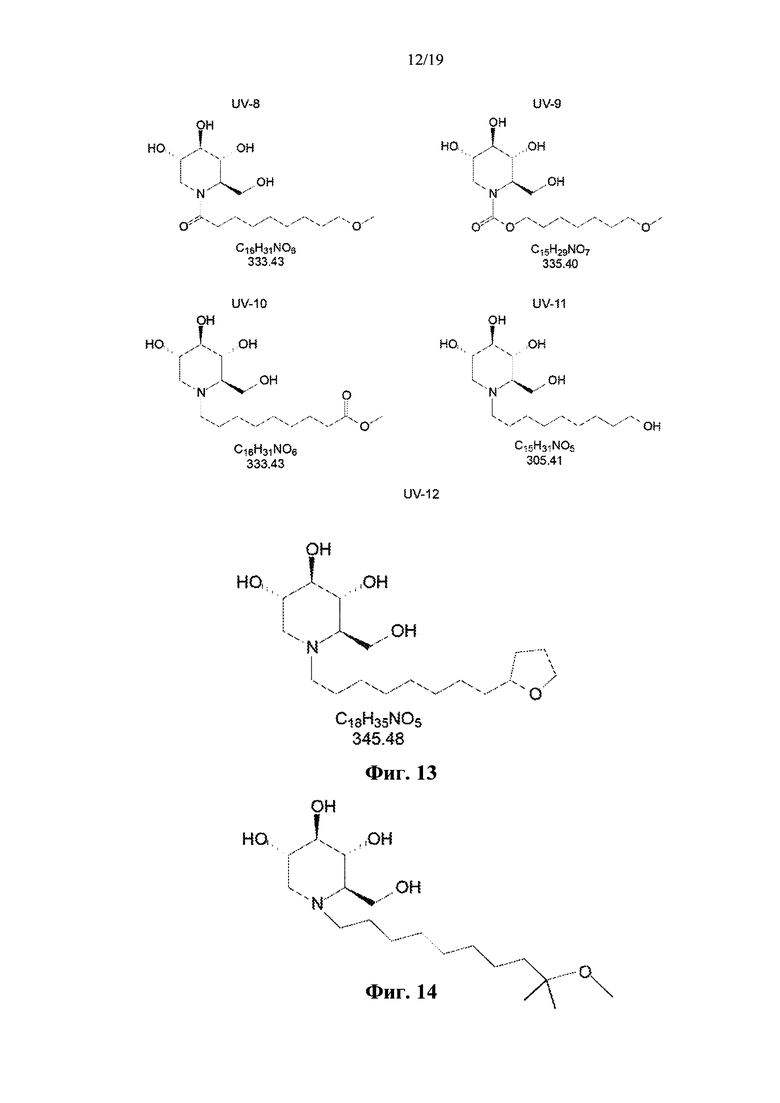
На фиг. 13 приведены химические формулы соединений UV-8, UV-9, UV-10, UV-11 hUV-12.
Фигура 14 представляет собой химическую формулу UV-28.
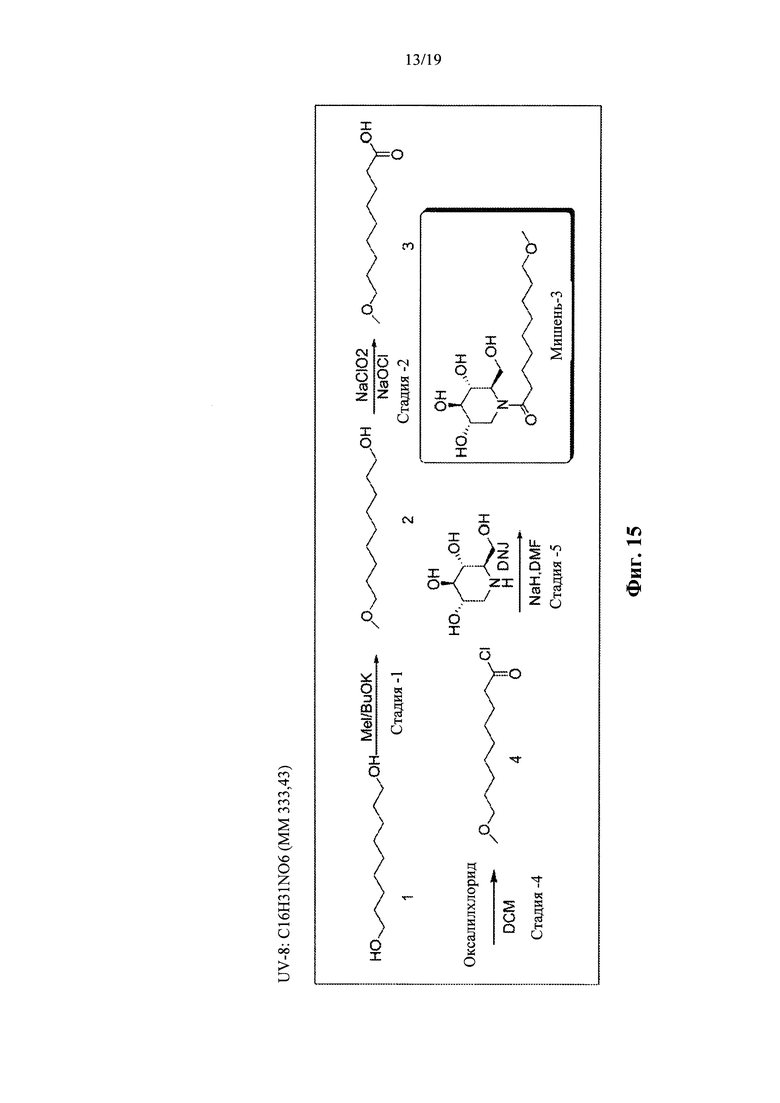
На фиг. 15 представлена схема синтеза для UV-8.
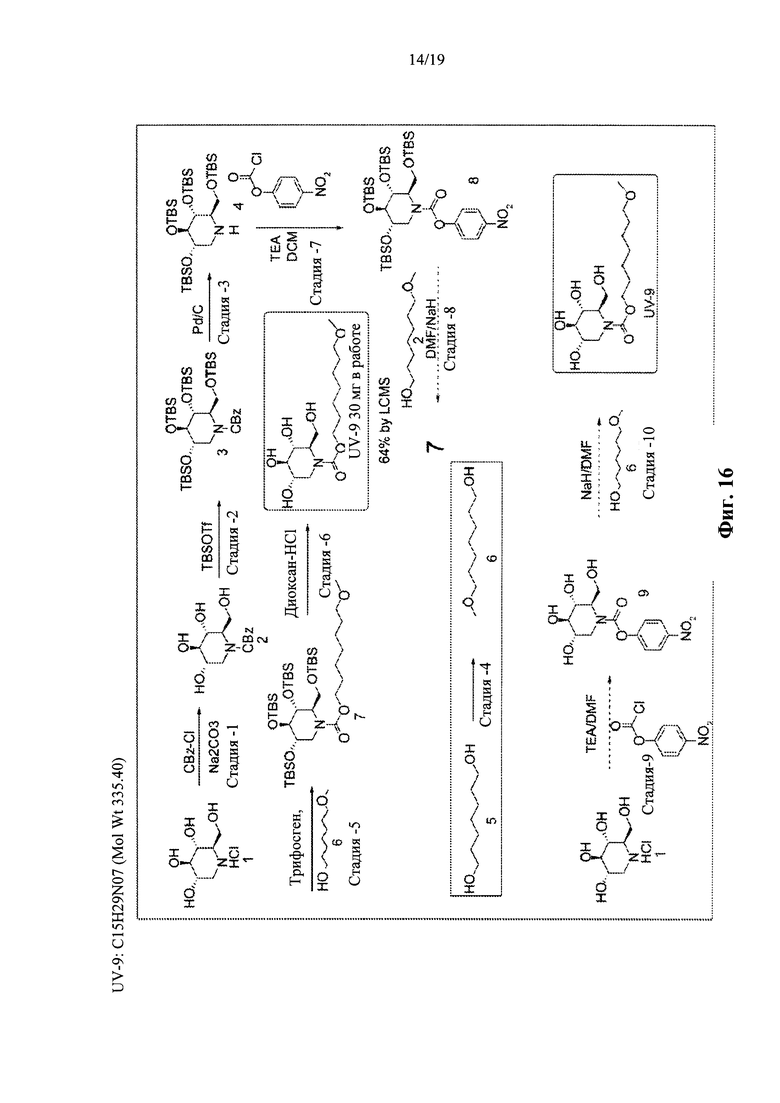
На фиг. 16 представлена схема синтеза для UV-9.
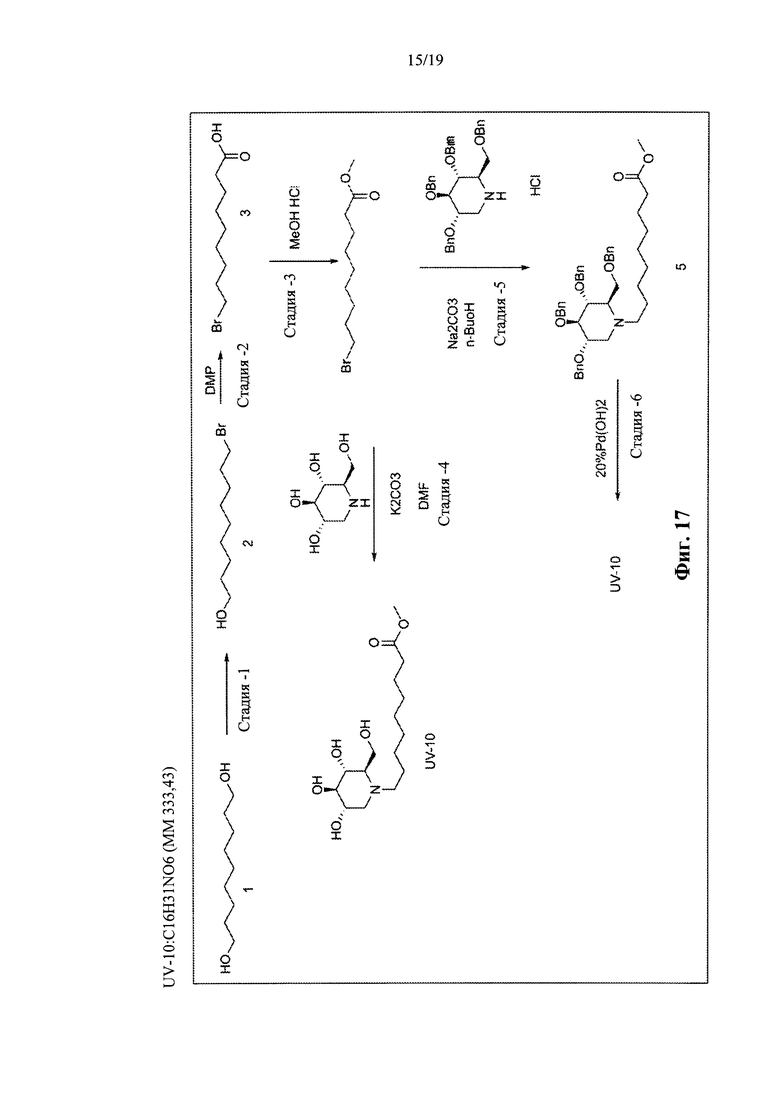
На фиг. 17 представлена схема синтеза для UV-10.
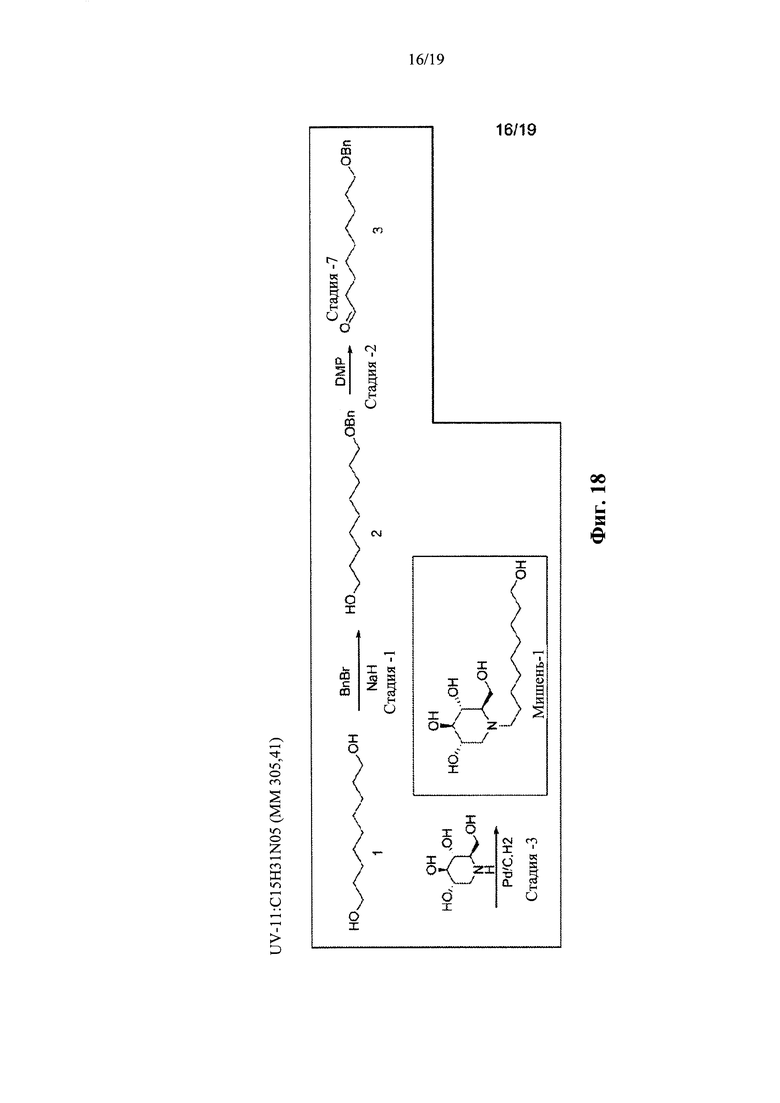
На фиг. 18 представлена схема синтеза для UV-11.
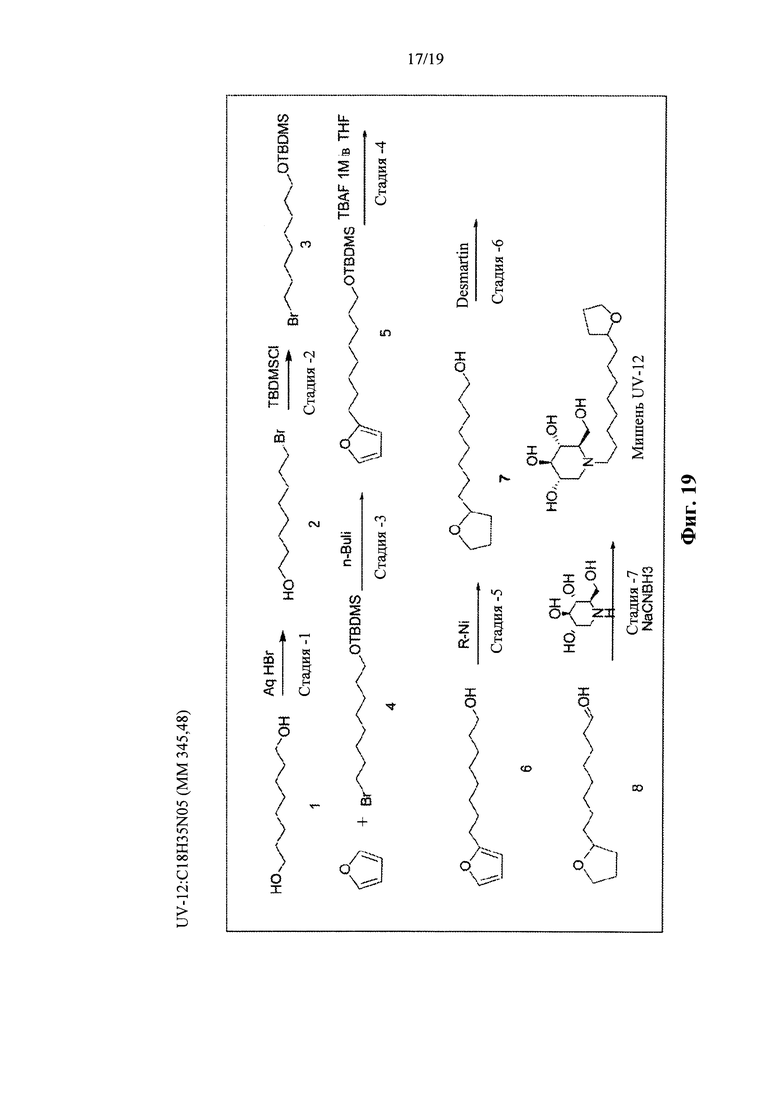
На фиг. 19 представлена схема синтеза для UV-12.
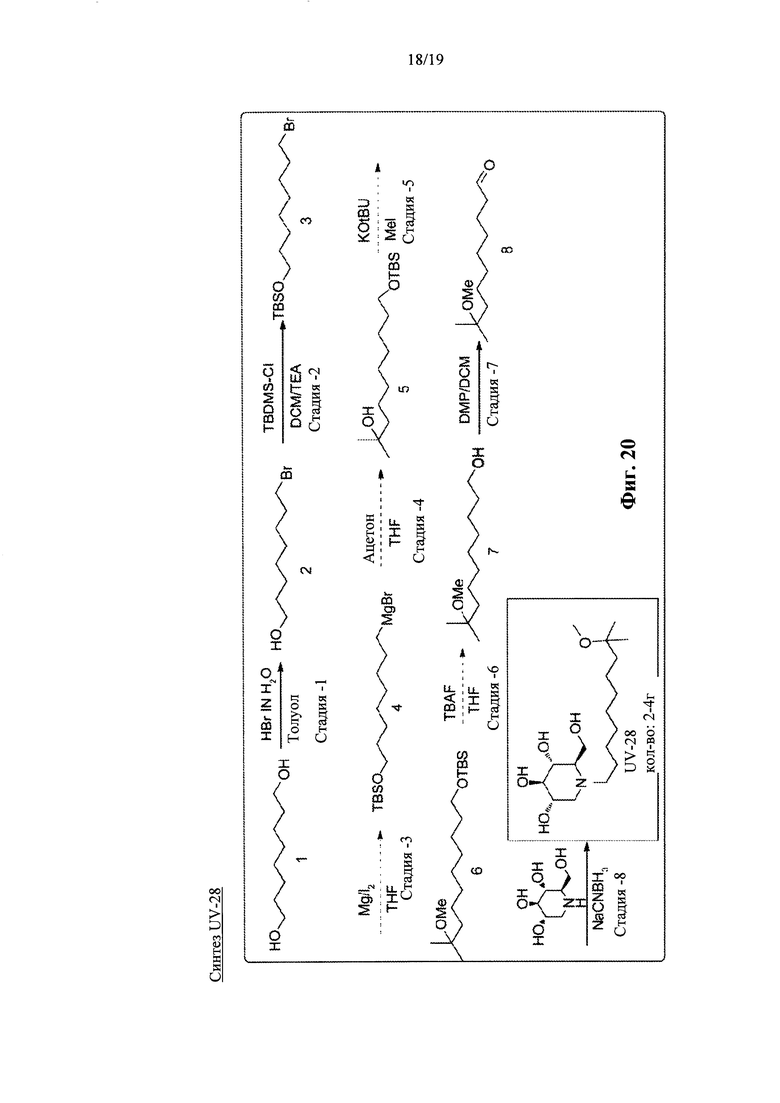
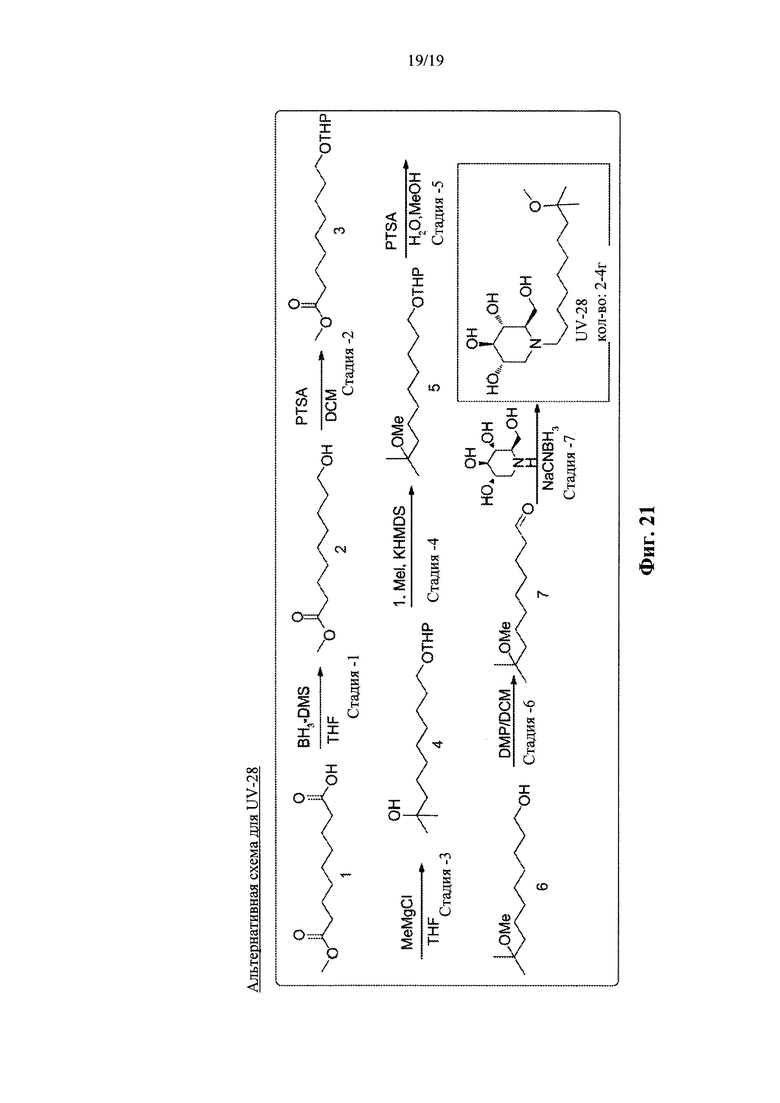
На фиг. 20 представлена схема синтеза для UV-28.
На фиг. 21 представлена альтернативная схема синтеза для UV-28.
Подробное описание
Родственные документы
Следующие патентные документы, каждый из которых полностью включен в настоящий документ посредством ссылки, могут быть применимы для понимания настоящего раскрытия:
Патенты США №6545021; 6809803; 6689759; 6465487; 5622972; 7816650; 7256005; 8450345; 7612093 и 8426445; Американские публикации патентных заявок №20110184019; 20130150405; 20100222384; 20110065754; 20110065753; 20110065752 и 2007-0275998 и заявка на патент США №13/870341, поданная 25 апреля 2013 г.
Значение терминов
Если не указано иное, неопределенный артикль единственного числа означает "один или несколько".
Используемый в настоящем документе термин "вирусная инфекция" описывает патологическое состояние, при котором вирус проникает в здоровую клетку, использует репродуктивный механизм клетки для размножения или репликации и, в конечном счете, лизирует клетку, приводя к клеточной гибели, высвобождению вирусных частиц и заражению других клеток посредством вновь образовавшегося вирусного потомства. Латентная инфекция некоторыми вирусами представляет собой также возможный результат вирусной инфекции.
Используемый в настоящем документе термин "лечение или профилактика вирусной инфекции" означает ингибирование репликации конкретного вируса, ингибирование вирусной трансмиссии или предотвращение обоснования вируса в своем хозяине и смягчение или облегчение симптомов заболевания, вызванного вирусной инфекцией. Лечение считается терапевтическим, если наблюдается снижение вирусной нагрузки, снижение смертности и/или заболеваемости.
IC50 или IC90 (ингибирующая концентрации 50 или 90) представляет собой концентрацию терапевтического средства, такого как иминосахар, используемую для достижения 50% или 90% снижения вирусной нагрузки, соответственно.
LD90 (смертельная доза 90%) представляет собой оцененную дозу средства, при которой, как ожидается, 90% популяции погибнет.
DENV обозначает вирус денге.
INFV обозначает вирус гриппа.
IV обозначает внутривенное введение.
IG обозначает внутрижелудочное введение.
IP обозначает внутрибрюшинное введение.
PFU обозначает бляшкообразующую единицу.
PBS обозначает фосфатный буферный солевой раствор.
ANOVA обозначает дисперсионный анализ.
Раскрытие изобретения
Авторы настоящего изобретения обнаружили, что некоторые производные дезоксинойиримицина могут быть эффективны против одного или нескольких вирусов, которые могут представлять собой, например, вирус лихорадки денге и/или вирус, принадлежащий к семейству Orthomyxoviridae, такой как вирус гриппа А.
В частности, такие производные дезоксинойиримицина могут быть применимы для лечения заболевания или состояния, вызванного или связанного с одним или несколькими вирусами, которые могут представлять собой, например, вирус лихорадки денге и/или вирус, принадлежащий к семейству Orthomyxoviridae, такой как вирус гриппа А. Согласно некоторым вариантам осуществления производные дезоксинойиримицина могут увеличивать процент или вероятность выживаемости субъекта, инфицированного одним или несколькими вирусами, которые могут представлять собой, например, вирус лихорадки денге и/или вирус, принадлежащий к семейству Orthomyxoviridae, такой как вирус гриппа А.
Вирусы денге
Вирус денге принадлежит к роду Flavivirus семейства Flaviridae и вызывает геморрагическую лихорадку денге (DHF). Вирус денге включает в себя четыре тесно связанных серотипа, как правило, называемые денге 1, денге 2, денге 3 и денге 4. Восстановление после инфицирования обеспечивает пожизненный иммунитет против этого серотипа, но лишь частичную и временную защиту от инфекции другими тремя. Существует убедительное доказательство, что непрерывная инфекция увеличивает риск развития более серьезных заболеваний, что приводит к DHF. Возникающие эпидемии DHF вызывают все большее беспокойство в Северной и Южной Америке и в Азии, где все четыре вируса лихорадки денге представляют собой эндемичные. DHF стала ведущей причиной госпитализации и смертности среди детей в нескольких странах. В 2007 году было зарегистрировано более 890000 случаев заболевания денге в Северной и Южной Америке, из которых 26000 случаев представляли собой DHF.
Денге передается в первую очередь комарами Aedes aegypti и представляет собой наиболее распространенное передаваемое комарами вирусное заболевание человека. Во всем мире 2,5 миллиарда человек - 40% населения мира - живут в теплых областях, где распространен желтолихорадочный комар и может быть передана лихорадка денге. Быстрый рост тропических городов и их человеческих и комариных популяций приводит к тому, что все большее число людей контактирует с этим переносчиком. Географическое распространение, как комаров-переносчиков, так и вируса привело к глобальному всплеску эпидемии лихорадки денге и появлению геморрагической лихорадки денге (DHF).
Семейство Orthomyxoviridae
Семейство Orthomyxoviridae представляет собой семейство РНК-содержащих вирусов, которое включает в себя пять родов: Influenzavirus A, Influenzavirus В, Influenzavirus С, Isavirus и Thogotovirus. Первые три рода содержат вирусы, которые могут вызывать грипп у позвоночных, включая в себя птиц, людей и других млекопитающих.
Род Influenzavirus А включает в себя единственный вид, который может вызывать грипп у птиц и некоторых млекопитающих, включающих в себя людей, свиней, кошек, собак и лошадей.
Вирусы гриппа А представляют собой вирусы с отрицательно направленной, одноцепочечной, сегментированной РНК. Существует несколько подтипов вируса гриппа А, маркированные в соответствии с числом Н (для типа гемагглютинина) и числом N (для типа нейраминидазы). В настоящее время известно 16 различных антигенов Н (от HI до H16) и девять различных антигенов N (от N1 до N9). Серотипы и подтипы вируса гриппа А включают в себя грипп A H1N1; грипп A H1N2; грипп A H2N2; грипп A H3N1; грипп А H3N2; грипп A H3N8; грипп A H5N1; грипп A H5N2; грипп A H5N3; грипп A H5N8; грипп A H5N9; грипп A H5N9, грипп A H7N1; грипп A H7N2; грипп A H7N3; грипп А H7N4; грипп A H7N7; грипп A H9N2; грипп A H10N7.
Род Influenzavirus В включает в себя один вид, который может вызывать грипп у человека и тюленей.
Род Influenzavirus С включает в себя один вид, который может вызывать грипп у людей и свиней.
Производные дезоксинойиримицина
Согласно некоторым вариантам осуществления производное дезоксинойиримицина может представлять собой соединение, принадлежащее к роду, определяемому формулой (I):
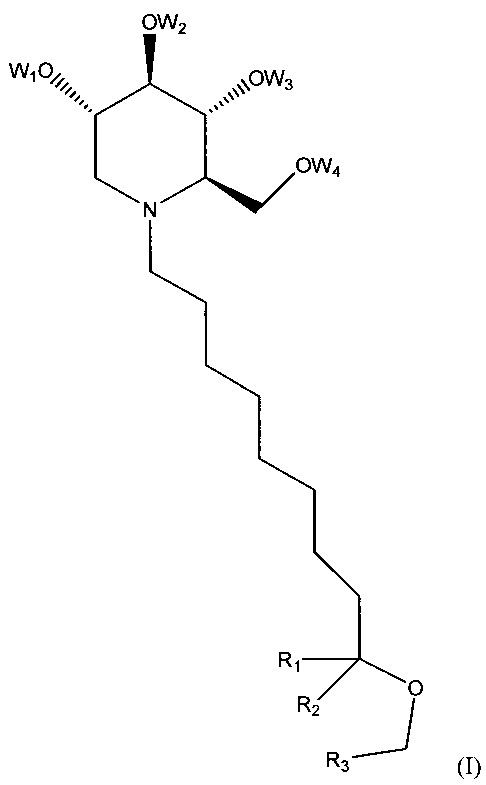
где W1-4 и R1-3 каждый независимо выбран из водорода и С1-3-алкильных групп, где по меньшей мере один из R1-3 представляет собой не водород. C1-3-алкильные группы включают в себя метил, этил и пропил. Согласно некоторым вариантам осуществления R2 и R3 могут быть такими, что они образуют вместе одну из следующих групп: -СН2-, -СН2-СН2- или -СН2-СН2-СН2-.
Соединение формулы (I) с каждым из W1-4 и R1-3, которые представляют собой водород, представляет собой N-(9-метоксинонил)дезоксинойиримицин, который также известен как N9-DNJ или UV-4. Соединения согласно определенному выше роду можно рассматривать как производные UV-4. Соединения согласно определенному выше роду, такие как соединения UV-12 и UV-28 (смотрите фигуры 13-14), могут характеризоваться одним или несколькими преимуществами, по сравнению с другими производными UV-4, такими как, например, соединения UV-8, UV-9, UV-10 и UV-11 (смотрите фиг. 13). Например, соединения согласно определенному выше роду, такие как соединения UV-12 и UV-28, могут быть более эффективными, по сравнению с другими производными UV-4, такими как соединения UV-8, UV-9, UV-10 и UV-11, против одного или нескольких вирусов, которые могут представлять собой, например, вирус лихорадки денге и/или вирус, принадлежащий к семейству Orthomyxoviridae, такой как вирус гриппа А.
Производные UV-4, такие как UV-8, UV-9, UV-10, UV-11, UV-12 и UV-28, могут быть синтезированы, как показано на фиг. 15-21.
Способы синтеза производных дезоксинойиримицина раскрыты также, например, в патентах США №5622972, 5200523, 5043273, 4994572, 4246345, 4266025, 4405714 и 4806650 и опубликованной заявке на патент США №2007/0275998, которые включены в настоящий документ посредством ссылки.
Согласно некоторым вариантам осуществления производное дезоксинойиримицина может быть в форме соли, полученной из неорганической или органической кислоты. Фармацевтически приемлемые соли и способы получения солевых форм, раскрыты, например, в Berge et al. (J. Pharm. Sci. 66: 1-18, 1977). Примеры соответствующих солей включают в себя без ограничения следующие соли: ацетат, адипат, альгинат, цитрат, аспартат, бензоат, бензолсульфонат, бисульфат, бутират, камфорат, камфорсульфонат, диглюконат, циклопентанпропионат, додецилсульфат, этансульфонат, глюкогептаноат, глицерофосфат, гемисульфат, гептаноат, гексаноат, фумарат, гидрохлорид, гидробромид, гидроиодид, 2-гидроксиэтансульфонат, лактат, малеат, метансульфонат, никотинат, 2-нафталсульфонат, оксалат, пальмоат, пектинат, персульфат, 3-фенилпропионат, пикрат, пивалат, пропионат, сукцинат, тартрат, тиоцианат, тозилат, мезилат и ундеканоат.
Согласно некоторым вариантам осуществления производное дезоксинойиримицина может быть также использовано в форме пролекарства. Пролекарства производных DNJ, таких как 6-фосфорилированных производных DNJ, раскрыты в патентах США №5043273 и 5103008.
Согласно некоторым вариантам осуществления производное дезоксинойиримицина может быть использовано в виде части композиции, которая дополнительно содержит фармацевтически приемлемый носитель и/или компонент, применимый для доставки композиции животному. Многочисленные фармацевтически приемлемые носители, применимые для доставки композиции человеку, и компоненты, применимые для доставки композиции другим животным, таким как крупный рогатый скот, известны в настоящей области техники. Добавление таких носителей и компонентов в композицию согласно настоящему изобретению находится в пределах обычной квалификации в настоящей области техники.
Согласно некоторым вариантам осуществления фармацевтическая композиция может состоять по существу из N-замещенного дезоксинойиримицина, что может означать, что N-замещенный дезоксинойиримицин представляет собой единственный активный ингредиент в композиции.
Тем не менее, согласно некоторым вариантам осуществления, N-замещенный дезоксинойиримицин можно вводить с одним или несколькими дополнительными противовирусными соединениями.
Согласно некоторым вариантам осуществления производное дезоксинойиримицина может быть использовано в липосомальной композиции, такой как те, которые раскрыты в публикациях США №2008/0138351, 2009/0252785 и 2010/0266678.
Производное DNJ можно вводить в клетку или животному, пораженному вирусом. Производное DNJ может ингибировать морфогенез вируса или он может лечить индивидуума. Лечение может уменьшать, ослаблять или снижать вирусную инфекцию у животного.
Согласно некоторым вариантам осуществления животное может представлять собой животное, инфицированное вирусом денге, которое может представлять собой позвоночное животное, такое как млекопитающее, которое может представлять собой, например, грызуна или примата, такого как человек.
Согласно некоторым вариантам осуществления количество производного DNJ, вводимое животному или в клетку животного согласно способам по настоящему изобретению может представлять собой количество, эффективное для ингибирования морфогенеза вируса денге в клетке. Используемый в настоящем документе термин "ингибирование" может относиться к обнаруживаемому уменьшению и/или ликвидации биологической активности, проявляемой в отсутствие иминосахара. Термин "эффективное количество" может относиться к такому количеству производного DNJ, необходимому для достижения указанного эффекта. Используемый в настоящем документе термин "лечение" может относиться к уменьшению или облегчению симптомов у субъекта, профилактике ухудшения или прогрессирования симптомов, ингибированию или устранению возбудителя или профилактике инфекции или нарушения, связанного с вирусом денге, у субъекта, который освобождается от него посредством этого.
Согласно некоторым вариантам осуществления животные могут представлять собой животное, инфицированное вирусом, который принадлежит к семейству Orthomyxoviridae, которое может представлять собой позвоночное, например, птицу или млекопитающее, включающее в себя приматов, таких как люди; кошачьих; лошадей и собачьих.
Согласно некоторым вариантам осуществления количество производного DNJ, вводимое животному или в клетку животного согласно способам по настоящему изобретению, может представлять собой количество, эффективное для ингибирования морфогенеза вируса, принадлежащего семейству Orthomyxoviridae в клетке.
Используемый в настоящем документе термин "ингибирование" может относиться к обнаруживаемому уменьшению и/или ликвидации биологической активности, проявляемой в отсутствие производного DNJ. Термин "эффективное количество" может относиться к такому количеству производного DNJ, необходимому для достижения указанного эффекта. Используемый в настоящем документе термин "лечение" может относиться к уменьшению или облегчению симптомов у субъекта, профилактике ухудшения или прогрессирования симптомов, ингибированию или устранению возбудителя или профилактике инфекции или нарушения, связанного с вирусом, принадлежащего семейству Orthomyxoviridae, у субъекта, который освобождается от него посредством этого.
Лечение заболевания, вызванного или связанного с вирусом, который может представлять собой, например, вирус лихорадки денге или вирус, принадлежащий к семейству Orthomyxoviridae, такой как вирус гриппа А, может предусматривать уничтожение возбудителя, ингибирование или вмешательство в его рост или созревание, а также нейтрализацию его патологических эффектов. Количество производного DNJ, которое может быть введено в клетку или животному, предпочтительно представляет собой количество, которое не вызывает токсических эффектов, которые перевешивают сопутствующие его введению преимущества.
Фактические дозировки активных ингредиентов в фармацевтических композициях могут варьировать таким образом, чтобы вводить количество активного соединения(й), которое эффективно для достижения желаемого терапевтического ответа у конкретного пациента.
Выбранная дозировка может зависеть от активности производного DNJ, пути введения, тяжести подлежащего лечению состояния, а также состояния и предшествующей истории болезни подлежащего лечению пациента. Тем не менее, специалисту в настоящей области техники понятно, что необходимо начинать дозы соединения(й) с более низким содержанием, чем требуется для достижения желаемого терапевтического эффекта, и постепенно повышать дозировку, пока желаемый эффект не будет достигнут. Если это желательно, эффективная суточная доза может быть разделена на несколько доз для целей введения, например, от двух до четырех доз в день. Следует понимать, однако, что конкретная дозировка для любого конкретного пациента может зависеть от множества факторов, включающих в себя массу тела, общее состояние здоровья, диету, время и способ введения и комбинацию с другими терапевтическими средствами, а также тяжести подлежащего лечению состояния или заболевания. У взрослого человека суточная дозировка может находиться в диапазоне от приблизительно одного микрограмма до приблизительно грамма или от приблизительно 10 до 100 мг производного DNJ на 10 килограмм массы тела. Согласно некоторым вариантам осуществления общая суточная доза может составлять от 0,1 мг/кг массы тела до 100 мг/кг веса тела, или от 1 мг/кг массы тела до 60 мг/кг массы тела, или от 2 мг/кг массы тела до 50 мг/кг массы тела, или от 3 мг/кг массы тела до 30 мг/кг массы тела. Суточную дозу можно вводить в один или несколько приемов введения в течение дня. Например, согласно некоторым вариантам осуществления суточная доза может быть распределена на два (BID) события введения в день, три события введения в день (TID) или четыре события введения (QID). Согласно некоторым вариантам осуществления одна доза события введения, находящаяся в диапазоне от 1 мг/кг массы тела до 10 мг/кг массы тела, может быть введена BID или TID в организм человека, получая общую дневную дозу от 2 мг/кг массы тела до 20 мг/кг массы тела или от 3 мг/кг массы тела до 30 мг/кг массы тела. Конечно, количество производного DNJ, которое должно быть введено в клетку или животному, может зависеть от многочисленных факторов, хорошо понимаемых специалистом в настоящей области техники, таких как молекулярная масса производного DNJ и способ введения.
Фармацевтические композиции, которые применимы в способах согласно настоящему изобретению, можно вводить системно в пероральных твердых композициях, офтальмологических, суппозиториях, аэрозольных, местных или других подобных составах. Например, она может быть в физической форме порошка, таблетки, капсулы, пастилки, геля, раствора, суспензии, сиропа или т.п. В дополнение к производному DNJ такие фармацевтические композиции могут содержать фармацевтически приемлемые носители и другие ингредиенты, известные как улучшающие и облегчающие введение лекарственного средства. Другие возможные составы, такие как наночастицы, липосомы, эритроциты в качестве переносчиков и иммунологические системы также могут быть использованы для введения производного DNJ. Такие фармацевтические композиции могут вводиться несколькими путями. Используемый в настоящем документе термин "парентеральный" включает в себя подкожное, внутривенное, внутриартериальное, интратекальное введение и техники инъекции и инфузии, без ограничений. В качестве примера, фармацевтические композиции могут быть введены перорально, местно, парентерально, системно или ингаляционным путем.
Эти композиции могут быть введены в виде однократной дозы или в виде нескольких доз, которые вводят в разное время. Поскольку ингибирующее действие композиции на вирус может сохраняться, режим дозирования может быть отрегулирован таким образом, чтобы замедлялось распространение вируса, в то же время оказывая минимальное влияние на клетку-хозяина. В качестве примера, животному можно вводить дозу композиции согласно настоящему изобретению один раз в неделю, в результате чего распространение вируса замедляется на протяжении всей недели, в то время как функции клетки-хозяина подавляются только в течение короткого периода один раз в неделю.
Описанные в настоящем документе варианты осуществления дополнительно иллюстрируются, хотя ни в коей мере не ограничиваются следующими демонстрационными примерами.
ДЕМОНСТРАЦИОННЫЕ ПРИМЕРЫ
Пример 1
Эффективность UV-12 и UV-28 против заражения INFV A/Texas/36/91 (H1N1) у мышей
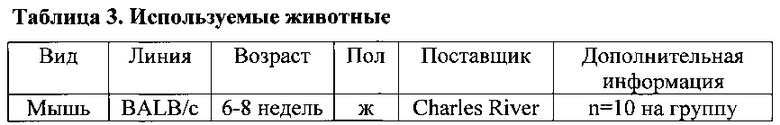
Краткое раскрытие исследования: В настоящем исследовании изучали способность иминосахаров UV-12 и UV-28 защищать мышей от летальной инфекции гриппа (грипп A/Texas/36/91 (H1N1) в дозе ~1 LD90, вводимой интраназально). Соединения вводили за 30-60 минут до вирусного заражения пероральным (IG) путем в дозе 100 или 40 мг/кг и продолжали три раза в день в течение 10 дней. Использовали мышей с массой ~20 грамм, 6-8 недельных самок мышей линии BALB/C, в группах по 10 для изучения эффективности (сводная информация по исследуемым группам приведена в таблице 1). Температуру и массу тела определяли ежедневно. Конечная точка представляла собой 14-й день после инфицирования, смерть или эвтаназию. Животных, проявляющих признаки тяжелого заболевания, что определялось потерей массы >30%, крайней вялостью или параличом, подвергали эвтаназии.
I. Введение
Запланированная цель: Цель настоящего исследования заключалась в определении эффективности малых молекул UV-12 и UV-28 in vivo против смертельного вируса гриппа A/Texas/36/91 (H1N1).
II. Материалы и способы
Материалы



Дизайн исследования
В настоящем исследовании изучали способность UV-12 и UV-28 защищать мышей от летальной инфекции гриппа. Использовали мышей в возрасте 6-8 недель, самок мышей BALB/c в группах по 10 (смотрите таблицу 5 ниже). Мышам вводили 100 или 40 мг/кг лекарственного средства три раза в день (TID) путем IG, начиная приблизительно за 30-60 минут до заражения. Мышей заражали гриппом A/Texas/36/91 (H1N1) в дозе ~1 LD90, вводимой интраназально (IN). Конечная точка представляла собой 14-й день после инфицирования, смерть или эвтаназию. Животных, проявляющих признаки тяжелого заболевания, что определялось потерей массы >30%, крайней вялостью или параличом, подвергали эвтаназии. Температуру и массу тела определяли ежедневно.


Стандартные протоколы
Стандартный протокол для интраназального инфицирования мышей
1. Мышей-самок BALB/C возрастом 6-8 недель содержали в группах по 5 мышей. Мышей помещали на карантин в исследовательском центре (Noble Life Sciences, Gaithersburg, MD) на время не менее 3-х дней до начала исследования.
2. Пищу и воду предоставляли без ограничения.
3. Группы мышей, зараженных INFV, инфицировали интраназально (IN) в дозе ~IXLD90 в 100 мкл разбавления 1:500 INFV в PBS под легкой анестезией (изофлураном).
4. После инфицирования мышей помещали обратно в свои клетки для наблюдения и последующего дозированного введения средств.
Протокол для перорального введения через желудочный зонд мышам для доставки исследуемого лекарственного средства
1. Мышам вводили 100 или 40 мг/кг исследуемого соединения посредством IG пути в 100 мкл воды (таблица 5 для режимов введения) три раза в день в течение 10 дней.
2. После введения дозы мышей возвращали в их клетки и контролировали возникновение любых дистрессов, связанных с введением лекарственных средств.
Наблюдение мышей
1. Мышей наблюдали в течение 13 дней после инфицирования (всего 14 дней, 0-13 дней после инфицирования).
2. Мышей взвешивали ежедневно на весах Ohause и записывали массы.
3. Всем животным имплантировали чипы по меньшей мере за 3 дня до заражения вирусом, которые контролировали температуру тела. Температуры регистрировали ежедневно.
4. Выживаемость и состояние здоровья каждой мыши оценивали один раз в день с использованием шкалы оценок 1-7.
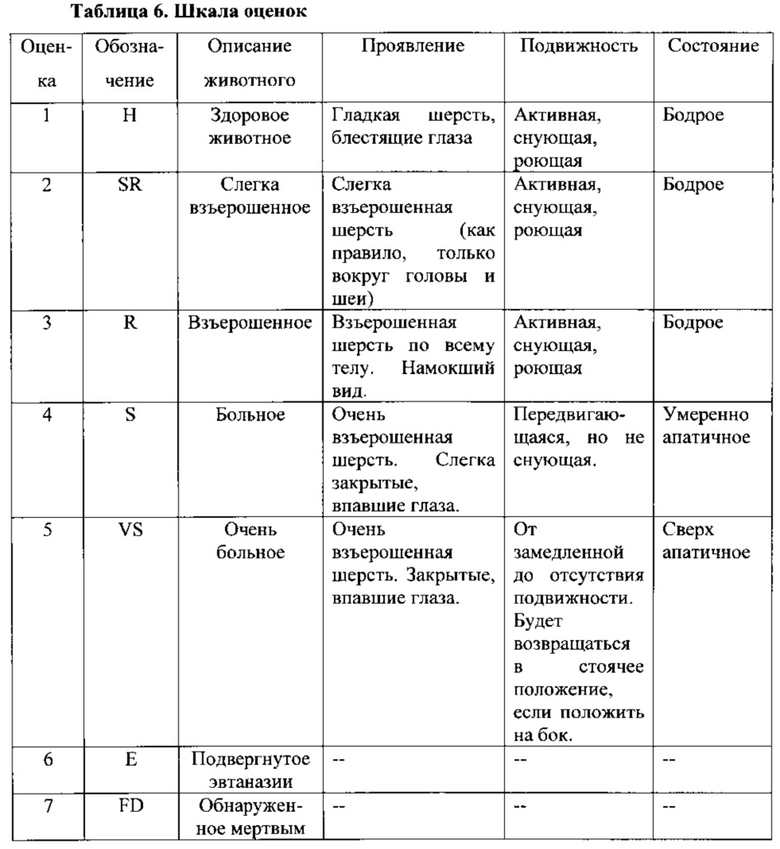
III. РЕЗУЛЬТАТЫ
Выживаемость
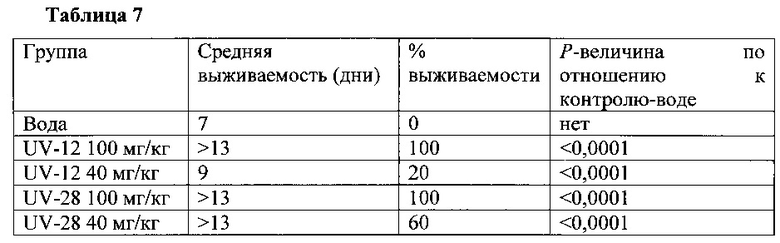
Мышей инфицировали гриппом A/Texas/36/91 (H1N1) в дозе ~1 LD90 и подвергали воздействию UV-12 или UV-28 в дозе 100 или 40 мг/кг три раза в день в течение 10 дней. Выживаемость в каждой инфицированной группе лечения рассчитывали как процент выживаемости по отношению к дням после инфицирования, как показано на фиг. 1 и в таблице 7. Инфицированные группы, которые подвергали воздействию 100 мг/кг как UV-12, так и UV-28, показали 100% выживаемость. Зараженные группы, которые подвергали воздействию 40 мг/кг как UV-12, так и UV-28, показали 20 и 60% выживаемость, соответственно. Необработанная контрольная группа показала 0% выживаемости и все животные "были обнаружены мертвыми" или "подвергнуты эвтаназии" на 7-й день после заражения.
Фигура 1 представляет собой график, на котором представлены данные выживаемости инфицированных мышей, сгруппированных по лечению. В таблице 7 представлены результаты анализа выживаемости инфицированных мышей. Данные выживаемости, приведенные на фиг. 1, анализировали с использованием критерия Кокса-Мантеля (логарифмический ранговый критерий) в GraphPad Prism.
Биометрический анализ
В ходе настоящего исследования, индивидуальную массу, оценку состояния здоровья и температуру контролировали ежедневно для каждой группы. Средняя масса для каждой группы мышей показана на фиг. 2. Каждое животное было помечено чипом для выполнения ежедневных считываний показаний температуры с помощью сканера BMDS; средние температуры показаны на фиг. 3. Оценки состояния здоровья показаны на фиг. 4.
ВЫВОДЫ
Инфицированных гриппом мышей подвергали воздействию UV-12 или UV-28 в дозе 100 или 40 мг/кг через желудочный зонд три раза в день в течение 10 дней. Обе группы, которые получали дозу 100 мг/кг, показали 100% выживаемость, а группы, которые получали дозу 40 мг/кг, показал выживаемость 60 и 20% для UV-28 и UV-12, соответственно. В то время как лекарственное средство UV-28 показало, по всей видимости, лучшую эффективность в дозе 40 мг/кг, оно, по-видимому, более токсично, чем UV-12 (фиг. 4). В то время как мыши, которые получали UV-12 в дозе 100 мг/кг, полностью восстанавливались после инфекции и возвращались к нормальной жизни, мыши, которые получали UV-28 в дозе 100 мг/кг, никогда не восстанавливали свой показатель состояния здоровья и оставались «взъерошенными» в ходе всего исследования.
В сочетании с более высокой оценкой состояния здоровья, указывая на тяжесть заболевания, мыши, которые получали UV-28 не восстанавливали свою массу в полной мере, в то время как мыши, получавшие UV-12, почти полностью выздоравливали. Мыши, которые подвергались воздействию только наполнителя, все поддались инфекции к 7-му дню после инфицирования, демонстрируя выживаемость, составляющую 0%.
Пример 2
Анализ выживаемости с использованием лекарственного средства UV-12 на модели А129 ADE
Цель: В настоящем исследовании определяли эффективность UV-12 в стимуляции выживаемости мышей, зараженных вирусом денге. Соединение вводили перорально (3 раза в сутки внутрижелудочно через желудочный зонд - IG) до достижения общего количества 7 дней после начала приема лекарственного средства. В эксперименте использовали модель А129 ADE инфекции. (Prestwood TR, Morar MM, Zellweger RM, Miller R, May MM, Yauch LE, Lada SM, Shresta S. Gamma interferon (IFN-γ) receptor restricts systemic dengue virus replication and prevents paralysis in IFN-α/β receptor-deficient mice. J Virol. 2012 Dec; 86(23): 12561-70). Животные получали дозу заражения вирусом ~1 LD90 в день 0. Первую дозу вводили за 0,5-1 ч до заражения вирусом. Выживаемость оценивали в течение 30 дней после инфицирования.
Иминосахар-кандидат: UV-12.
Экспериментальный дизайн исследования:
Контроль, H2O DENV (S221) [10 мышей]
UV-12 (100 мг/кг/доза)+DENV (S221) [10 мышей]
Мыши: соответствующего пола возрастом 5-6 недель А129 (129/SV IFN-α, -β рецептор-/-)
Маршрут введения:
Иминосахар: Перорально 3 раза в день (через желудочный зонд (IG)) каждые 8
часов
Антитело: IP
Вирус: IV
Антитело и соединение иминосахара вводили одновременно, затем вирус в течение 30 минут после заражения вирусом:
Антитело: 100 мкг 2Н2 (IgG2a aHTH-DENVl-4 prM) из АТСС, день 0 и день 1 в 40 мкл
Вирус: штамм DENV2 S221 (v512) (Zellweger RM, Prestwood TR, Shresta S. Enhanced infection of liver sinusoidal endothelial cells in a mouse model of antibody-induced severe dengue disease. Cell Host Microbe, 2010 Feb 18; 7(2): 128-39)
Доза: 1E11 GE (геномные эквиваленты) на животное
Считывание:
Выживаемость животных. Животных, у которых проявляется тяжелое заболевание (как определено посредством 20% потери веса, крайней вялости, взъерошенной шерсти или паралича), усыпляют.
Ресурсы:
Мыши А129, антитело 2Н2 и вирус S221 поставлялись Институтом аллергии и иммунологии Sujan Shresta, La Jolla
Поставка Unither Virology: UV-12
На фиг. 5 представлены результаты этого исследования. Мыши получали UV-12, разведенного в 50 мкл воды, перорально три раза в день в общей сложности 7 дней. Лечение начиналось за 1 час до внутривенного заражения вирусом. Получившие UV-12 мыши А129 проявляли повышенную выживаемость по сравнению с контрольными животными, которым вводили перорально только 50 мкл воды три раза в день.
Пример 3
Эффективность выбранных иминосахаров у мышей: заражение гриппом A/Texas/36/91 (H1N1)
Краткое раскрытие исследования: В настоящем исследовании анализировали токсичность и эффективность UV-8, UV-9, UV-10, UV-11 и UV-12 у мышей во время инфекции гриппа H1N1. Ранее, исследования, которые выполняли с пероральной доставкой UV-4B два раза в день (TID) в дозе 100 мг/кг, приводили к эффективности против H1N1 и не показали каких-либо заметных признаков токсичности. В текущем исследовании авторы настоящего исследования изучали дозы доставки UV-4B, UV-8, UV-9, UV-10, UV-11 и UV-12 в дозе 100 мг/кг, поставляемые три раза в день перорально (внутрижелудочно через желудочный зонд или IG). Небольшие группы (n=3), которые были включены для изучения общей токсичности, получали 100 мг/кг иминосахаров, но без вирусного заражения. UV-4B, UV-8, UV-9, UV-10, UV-11 или UV-12 вводили животным, начиная за 1 час до интраназальной инфекции (IN) гриппом A/Texas/36/91 (H1N1) в дозе ~1 LD90. Животные затем получали TID в течение всего 10 дней (дни 0-9 после заражения). Эффективность оценивали путем сравнения выживаемости, изменения температуры и увеличения/потери веса по отношению к зараженной необработанной контрольной группе. Мыши, которые получали UV-8, -9, -10 или -11, не показали улучшения выживаемости по сравнению с необработанной контрольной группой, в то время как группа, получавшая UV-12, и положительная контрольная группа, получавшая UV-4B, показали значительное увеличение выживаемости.
I. Введение
Целью настоящего исследования было определение эффективности UV-8, UV-9, UV-10, UV-11 и UV-12 при введении перорально в дозе 100 мг/кг TID против летальной интраназальной инфекции вирусом гриппа A/Texas/36/91 (H1N1) на модели мышей BALB/c. В дополнение к группе эффективности, каждый из иминосахаров испытывали в небольшой группе животных с той же схемой лечения (100 мг/кг, перорально через зонд, TID) в отсутствие вирусной инфекции, чтобы исследовать общую токсичность каждого аналога (оценки общего состояния здоровья, массы, температуры и смертности).
II. Материалы и способы
Материалы
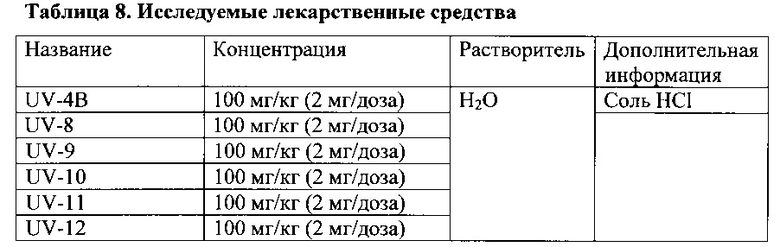

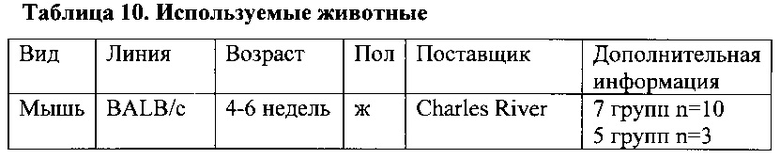


Дизайн исследования
UV-8, -9, -10, -11, -12 и UV-4B готовили в Н2О в концентрации 20 мг/мл для вводимой дозы 100 мг/кг, при условии, что мыши массой ~20 г получали 0,1 мл соединения, на группы мышей BALB/c воздействовали за один час до (-1 час) интраназальной инфекции с INFV A/Texas/36/91 (H1N1) в дозе ~1 LD90, а затем соединения вводили три раза в день в течение в общей сложности 10 дней (таблица 12 для сводной информации постановки исследования). Массу, температуру и выживаемость контролировали и применяли для оценки защитной эффективности и токсичности каждого аналога.
Стандартные протоколы
Стандартный протокол для интраназального инфицирования мышей
1. Мышей-самок BALB/C возраста 6-8 недель содержали в группах по 3-5 мышей. Мышей помещали на карантин в исследовательском центре (Noble Life Sciences, Gaithersburg, MD) на время не менее 3-х дней до начала исследования.
2. Пищу и воду предоставляли без ограничения.
3. Группы мышей, зараженных гриппом, анестезировали с помощью 5% изофлурана и поддерживали при 2,5% перед интраназальным введением INFV в дозе ~1×LD90 в 100 мкл PBS.
4. После инфицирования мышей помещали обратно в свои клетки для наблюдения и последующего дозированного введения средств.
Протокол для перорального введения через желудочный зонд мышам для доставки исследуемого лекарственного средства
1. Мышам вводили, начиная за 1 час перед инфицированием, 100 мкл исследуемого соединения в H2O (смотрите таблицу 12 для режимов введения лекарственных средств) три раза в день в течение 10 дней в дозе 100 мг/кг соединения UV-4B, UV-8, UV-9, UV-10, UV-11 или UV-12, вводимого пероральным путем (внутрижелудочно через желудочный зонд).
2. После введения дозы мышей возвращали в свои клетки и контролировали возникновение любых дистрессов, связанных с введением лекарственных средств.
Наблюдение мышей
1. Мышей наблюдали в течение 13 дней после инфицирования (всего 14 дней, 0-13 дней после инфицирования).
2. Мышей взвешивали ежедневно на весах Ohause и записывали массы.
3. Всем животным имплантировали чипы, которые контролировали температуру тела. Температуры регистрировали ежедневно.
4. Выживаемость и состояние здоровья каждой мыши оценивали один раз в день с использованием шкалы оценок 1-7.
5. Мышей подвергали эвтаназии, когда оценка состояния здоровья составляла 5 или выше (очень болен, очень взъерошенная шерсть; закрытые, впавшие глаза; движения от медленных до их отсутствия; возврат в вертикальное положение, если положить на бок, крайняя вялость животного).
III. РЕЗУЛЬТАТЫ
Выживаемость
Мышей инфицировали вирусом гриппа A/Texas/36/91 (H1N1) в дозе ~1 LD90 через один час после первой дозы аналогов UV-4B или UV-4, как описано выше. Таблицы выживаемости, рассчитанные, как процент выживаемости по отношению к дням после инфицирования, показаны на фиг. 6. Как и ожидалось на основании предыдущих исследований, группы, которым вводили перорально TID UV-4B в дозе 100 мг/кг, показали выживаемость 100% и MTD>13 дней (фиг. 7). Мыши, которые получали перорально UV-12 в дозе 100 мг/кг, показали уровень выживаемости 90% и MTD>13 дней (фиг.6, 7). Мыши, подвергнутые воздействию UV-8, UV-9, UV-10 или UV-11, проявляли MTD 10,5, 7, 7,5 и 8 дней, соответственно, и выживаемость 0%, за исключением UV-8 (30%) (фиг. 6, 7). Мыши отрицательного контроля, которым вводили дозы наполнителя (Н2О), продемонстрировали выживаемость 30% и MTD 9 дней (фиг. 6, 7).
Мыши, которые получали UV-8, -9, -10, -11 или -12 в дозе 100 мг/кг без вирусного заражения, чтобы исследовать общую токсичность, проявляли 100% выживаемость (данные не показаны).
Биометрический анализ
В ходе этого исследования, индивидуальные массы и температуры контролировали ежедневно для каждой группы. Средняя масса для каждой группы мышей показана на фиг. 8 со статистическим анализом, показанным на фиг. 9. Средние температуры показаны на фиг. 10 со статистическим анализом, показанным на фиг. 11.
В качестве второго биометрического анализа оценивали температуры животных. Каждое животное было помечено чипом для выполнения ежедневных считываний показаний температуры с использованием сканера. Графики на фиг. 10 показывают температуру тела для каждой исследуемой группы. Значимость, показанная по отношению к наполнителю-контролю, указана на фиг. 11.
ВЫВОДЫ
Группа инфицированных мышей, которой вводили перорально TID UV-4B в дозе 100 мг/кг, проявляла 100% выживаемость, причем группы, которым вводили перорально UV-9, UV-10 и UV-11 в дозе 100 мг/кг, проявляли выживаемость 0%. Статистический анализ масс и температур для этих групп не был выполнен из-за более низкой выживаемости и MTD, чем у контрольных групп, получавших наполнитель. Мыши, которым вводили перорально UV-8, проявляли выживаемость30% и, таким образом, не характеризовались существенным отличием от контрольной группы. Мыши, которым вводили перорально UV-12 в дозе 100 мг/кг, проявляли выживаемость 90%, а также значительное увеличение общей температуры и массы. Средство UV-12 также показало умеренную токсичность с устойчивой потерей массы в неинфицированной группе, но неинфицированные мыши, которым вводили дозы UV-12, не теряли более 10% массы в целом и они смогли полностью восстановиться после того, как график лечения был завершен. Статистический анализ не был выполнен ни по одному из параметров, рассматриваемому для неинфицированных групп мышей (общая токсичность), поскольку число мышей в группе было ограничено (n=3) и не было неинфицированной, контрольной группы без воздействия для сравнения. Пример 4
Анализ выживаемости с использованием лекарственного средства UV-4 и UV-12 на модели ADE
Цель: В настоящем исследовании определяли эффективность UV-4 и UV-12 в стимуляции выживаемости мышей, зараженных вирусом денге. Все соединения вводили перорально (3 раза в день внутрижелудочно через желудочный зонд - IG) до достижения общего количества 7 дней после начала приема лекарственного средства. В эксперименте использовали модель ADE инфекции, разработанную в лаборатории (Zellweger et al. CellHostMicrob 7; ppl-12 (2010)). Животные получали дозу заражения вирусом ~1 LD90 в день 0. Первую дозу вводили за 0,5-1 ч до заражения вирусом. Выживаемость оценивали в течение 3 дней после завершения графика лечения. В настоящем исследовании использовали соль HC1UV-4, которая эквивалентна "UV-4B".
Иминосахара-кандидаты:
1. N-9-метоксинонилдезоксинойиримицин (UV-4) (соль НСl), UV-4B
2. UV-12
3. Контроль, H2O
Экспериментальный дизайн исследования
1. Контроль, H2O+DENV (S221) [7 мышей]
2. UV-4, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
3. UV-12, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
Мыши: Соответствующий пол возрастом 5-6 недель
AG 129 (129/SV IFN-α, β и γ-рецептор-/-), разведенный в LIAI от Sujan Shresta (также общедоступны The Jackson Laboratory, Bar Harbor, Maine)
Путь:
Иминосахар: Перорально 3 раза в день (через желудочный зонд (IG)) каждые 8 часов
Антитело: IP (внутрибрюшинно)
Вирус: IV
Антитело и соединение вводили одновременно, затем вирус в течение 30 минут
Заражение вирусом:
Антитело: 5 мкг 2112 (анти-PRM), доступное от АТСС
Вирус: штамм S221 DENV2 (v476) (Zellweger R М, Prestwood TR, Shresta S. Enhanced infection of liver sinusoidal endothelial cells in a mouse model of antibody-induced severe dengue disease. Cell Host Microbe, 2010 Feb 18; 7(2): 128-39)
Доза: 1E9 GE (геномные эквиваленты) на одно животное
Считывание:
Выживаемость животных. Животных, проявляющих признаки тяжелого заболевания (что определяли посредством 20% потери веса, крайней вялости, взъерошенной шерсти или паралича), подвергали эвтаназии.
На фиг. 12 представлены результаты настоящего исследования. Все группы подвергались воздействию той же дозой соединений:
Экспериментальный дизайн исследования
1. Контроль, H2O+DENV (S221) [7 мышей]
2. UV-4, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
3. UV-8, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
4. UV-9, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
5. UV-10, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
6. UV-11, 1 мг (50 мг кг/доза)+DENV (S221) [5 мышей]
7. UV-12, 1 мг (50 мг/кг/доза)+DENV (S221) [5 мышей]
В настоящем исследовании определяли эффективность UV-4 и его аналогов в стимуляции выживаемости мышей, зараженных вирусом денге. Все соединения вводили перорально (3 раза в день внутрижелудочно через желудочный зонд - IG) до достижения общего количества 7 дней после начала приема лекарственного средства. В эксперименте использовали модель ADE инфекции (Zellweger et al. CellHostMicrob 7; ppl-12 (2010)). Животные получали дозу заражения вирусом ~1 LD90 в день 0. Первую дозу соединения вводили за 0,5-1 ч до заражения вирусом. Выживание оценивали в течение 3 дней после завершения графика лечения.
Хотя вышеизложенное относится к конкретным предпочтительным вариантам осуществления, следует понимать, что настоящее изобретение этим не ограничено. Обычным специалистам в настоящей области техники будет понятно, что могут быть сделаны различные модификации в соответствии с раскрытыми вариантами осуществления и что такие модификации предназначены, чтобы находиться в пределах объема настоящего изобретения.
Все публикации, патентные заявки и патенты, цитируемые в настоящем документе, полностью включены в настоящий документ посредством ссылки.
Изобретение относится к новым иминосахарам, имеющим формулы:
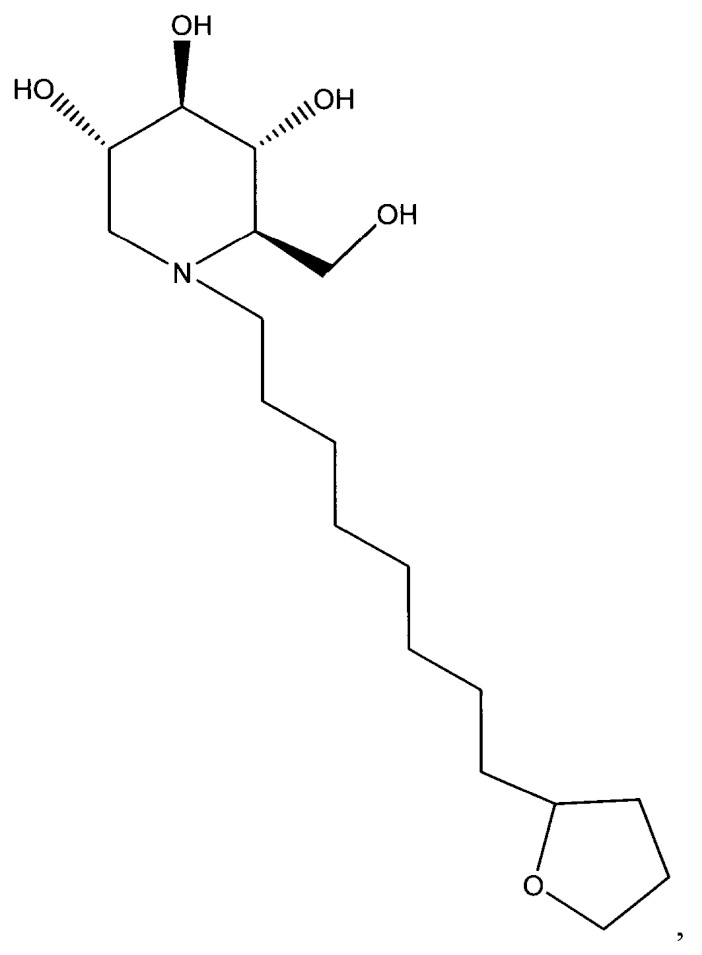
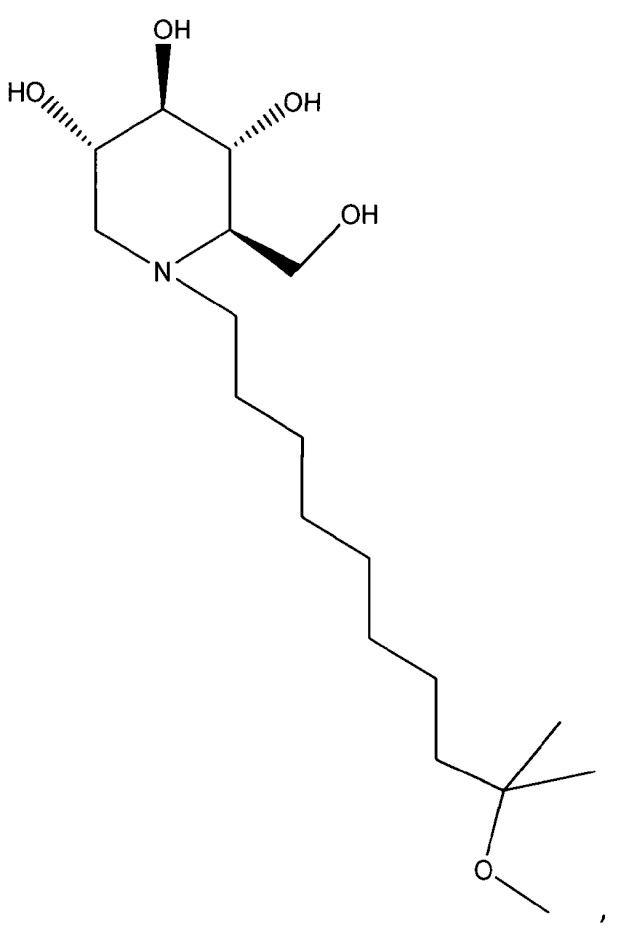
или их фармацевтически приемлемым солям и их применению для лечения вирусных инфекций, таких как инфекция денге и инфекция гриппа А. 8 н. и 14 з.п. ф-лы, 21 ил., 12 табл., 3 пр.
1. Соединение, имеющее формулу
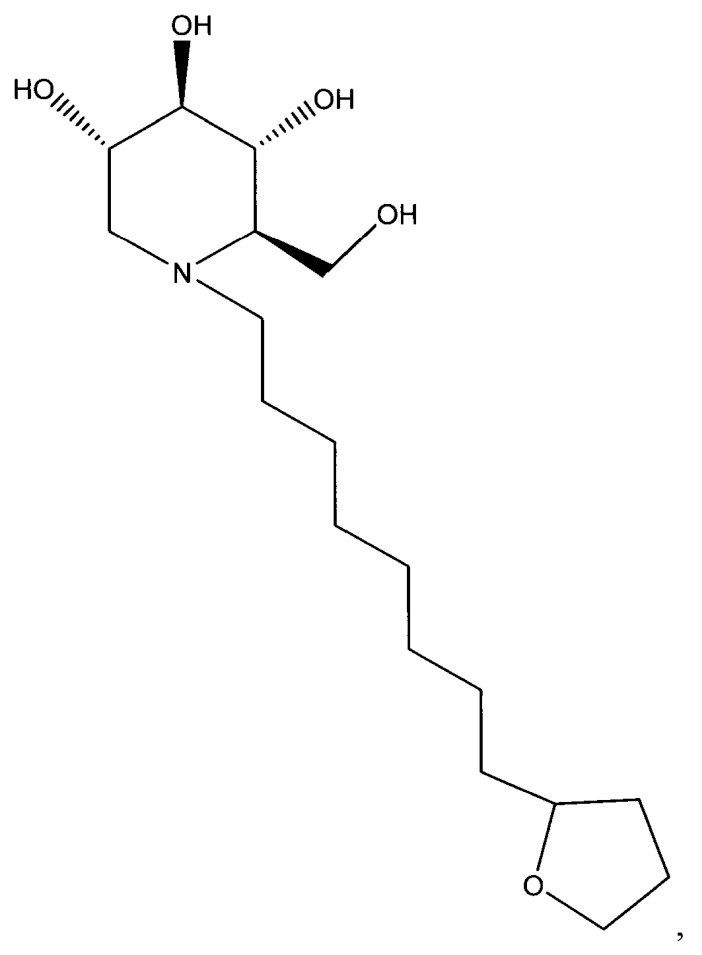
или его фармацевтически приемлемая соль.
2. Соединение, имеющее формулу
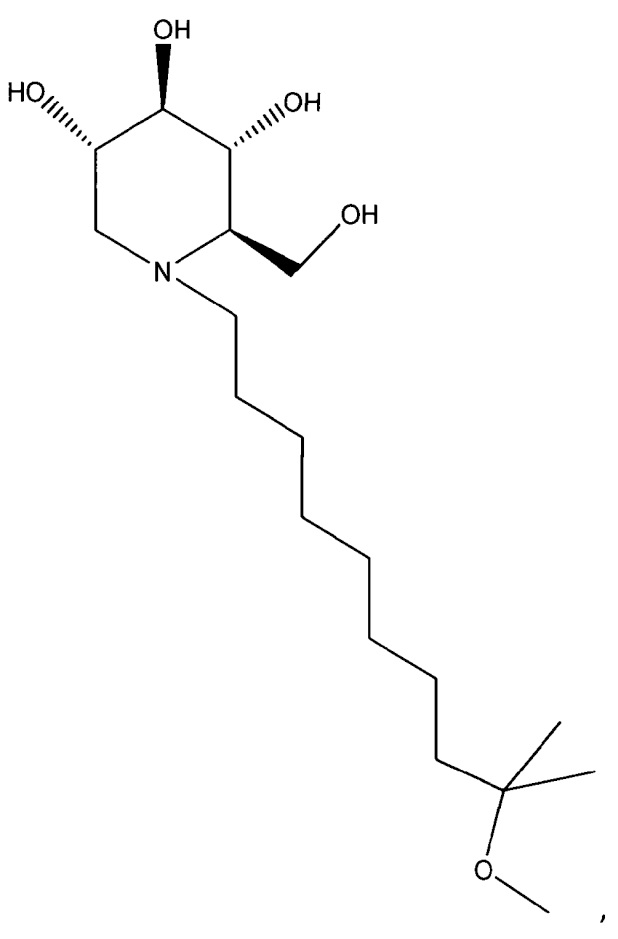
или его фармацевтически приемлемая соль.
3. Фармацевтическая композиция для лечения или предотвращения вирусной инфекции денге, содержащая а) фармацевтически эффективное количество соединения по п. 1 или 2 и b) фармацевтически приемлемый носитель.
4. Способ лечения или профилактики вирусной инфекции денге, предусматривающий введение нуждающемуся в этом субъекту соединения по п. 1 или его фармацевтически приемлемой соли.
5. Способ по п. 4, в котором вирусная инфекция денге вызвана или связана с вирусом денге 2.
6. Способ по п. 4, в котором субъект представляет собой млекопитающее.
7. Способ по п. 6, в котором субъект представляет собой человека.
8. Способ лечения заболевания или состояния, вызванного или связанного с вирусом, принадлежащим к семейству Orthomyxoviridae, предусматривающий введение нуждающемуся в этом субъекту соединения по п. 1 или его фармацевтически приемлемой соли.
9. Способ по п. 8, в котором вирус представляет собой вирус гриппа.
10. Способ по п. 9, в котором вирус представляет собой вирус гриппа А.
11. Способ по п. 10, в котором вирус представляет собой подтип H3N2 вируса гриппа А.
12. Способ по п. 10, в котором вирус представляет собой подтип H1N1 вируса гриппа А.
13. Фармацевтическая композиция для лечения заболевания или состояния, вызванного или связанного с вирусом, принадлежащим к семейству Orthomyxoviridae, содержащая а) фармацевтически эффективное количество соединения по п. 1 или 2 и b) фармацевтически приемлемый носитель.
14. Способ лечения или предотвращения вирусной инфекции денге, предусматривающий введение нуждающемуся в этом субъекту соединения по п. 2 или его фармацевтически приемлемой соли.
15. Способ по п. 14, в котором вирусная инфекция денге вызвана или связана с вирусом денге 2.
16. Способ по п. 14, в котором субъект представляет собой млекопитающее.
17. Способ по п. 16, в котором субъект представляет собой человека.
18. Способ лечения заболевания или состояния, вызванного или связанного с вирусом, принадлежащим к семейству Orthomyxoviridae, предусматривающий введение нуждающемуся в этом субъекту соединения по п. 2 или его фармацевтически приемлемой соли.
19. Способ по п. 18, в котором вирус представляет собой вирус гриппа.
20. Способ по п. 19, в котором вирус представляет собой вирус гриппа А.
21. Способ по п. 20, в котором вирус представляет собой подтип H3N2 вируса гриппа А.
22. Способ по п. 20, в котором вирус представляет собой подтип H1N1 вируса гриппа А.
| WO 2010027996 A1 11.03.2010 | |||
| US 20090042268 A1 12.02.2009 | |||
| Способ получения производных 3,4,5-триоксипиперидина | 1981 |
|
SU1014470A3 |
| Способ получения производных 3,4,5-тригидроксипиперидина | 1981 |
|
SU1014471A3 |
| ПРИМЕНЕНИЕ ИНГИБИТОРОВ ГЛЮКОЗИДАЗЫ ДЛЯ ТЕРАПИИ МУКОВИСЦИДОЗА | 2004 |
|
RU2358725C2 |
Авторы
Даты
2019-10-04—Публикация
2014-09-15—Подача