РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет предварительной заявки США № 61/976350, зарегистрированной 7 апреля 2014 года, которая полностью включена в настоящий документ в качестве ссылки.
ОБЛАСТЬ ТЕХНИКИ
Объект изобретения, описываемый в настоящем документе, в числе прочего относится к содержащим карбазол амидным, карбаматным и карбамидным производным, фармацевтическим композициям, содержащим эти соединения, способам их применения при лечении опосредуемых криптохромами заболеваний или нарушений и к способу их получения. Также предоставлены способы диагностики, детекции или мониторинга прогресса зависимых от криптохромов заболеваний у индивидуумов, получающих соединения и композиции, описываемые в настоящем документе.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Циркадные часы представляют собой врожденный хронометрический механизм, который контролирует суточные ритмы множества физиологических процессов, таких как режим сна/бодрствования, температура тела, секреция гормонов и метаболизм (Takahashi, J. S. et al. Nat. Rev. Genet. 2008, 9, 764; Green, C. B. et al. Cell, 2008, 134, 728; Zhang, E. E. et al. Nat. Rev. Mol. Cell. Biol. 2010, 11, 764). Клетки генерируют циркадные ритмы автономно посредством транскрипционных регуляторных сетей генов часов. В основном цикле обратной связи факторы транскрипции CLOCK и BMAL1 активируют экспрессию генов Period (Per1 и Per2) и Cryptochrome (Cry1 и Cry2). После трансляции и локализации в ядре, белки PER и CRY ингибируют функцию CLOCK-BMAL1, что приводит к устойчивой ритмической экспрессии генов. Под контролем циркадных часов находится множество физиологических путей (Panda, S. et al. Cell, 2002, 109, 307), включая прямую регуляцию множества процессов в печени (Rey, G. et al. PLoS Biol. 2011, 9, e1000595; Bugge, A. et al. Genes Dev. 2012, 26, 657).
Рассинхронизация циркадных часов ассоциирована с нарушенной чувствительностью к инсулину (Spiegel, K. et al. J. Appl. Physiol. 2005, 99, 2008; Spiegel, K. et al. Lancet, 1999, 354, 1435), сниженными уровнями лептина и приводит к гипергликемии, гиперинсулинемии и реакциям глюкозы после приема пищи, сравнимым с реакциями при преддиабетическом состоянии (Scheer, F. A. et al. Proc. Natl. Acad. Sci. USA, 2009, 106, 4453). Несколько полногеномных исследований ассоциаций привели к открытию возможной важности Cry2 в регуляции уровней глюкозы у млекопитающих (Dupuis, J. et al. Nat. Genet. 2010, 42, 105; Liu, C. et al. PLoS One, 2011, 6, e21464; Barker, A. et al. Diabetes, 2011, 60, 1805).
Концентрации глюкозы в крови являются высокоритмичными вследствие изменений чувствительности к инсулину и способности эндокринной поджелудочной железы к секреции инсулина (Polonsky, K. S. et al. N. Engl. J. Med. 1988, 318, 1231). У мышей с мутацией ClockΔ19 развивается зависимая от возраста гипергликемия и у этих животных также развивается чувствительность к индуцированному диетой ожирению, и присутствуют несоответственно низкие концентрации инсулина (Turek, F. W. et al. Science, 2005, 308, 1043), и выявлено резкое падение сахара в крови в ответ на обработку инсулином, включая то, что у этих животных выявлена увеличенная чувствительность к инсулину, таким образом, маскирующая недостаточность β-клеток (Marcheva, B. et al. Nature, 2010, 466, 627). Специфичная для печени делеция Bmal1 у мышей приводит к нарушенной толерантности к глюкозе и увеличенной чувствительности к инсулину (Lamia, K. A. et al. Proc. Natl. Acad. Sci. USA, 2008, 105, 15172). Индивидуумы с диабетом 2 типа и даже их родственники первой степени, еще не подверженные заболеванию, демонстрируют измененную ритмичность толерантности к глюкозе (Boden, G. et al. Diabetes, 1999, 48, 2182). У людей с диабетом 2 типа по сравнению с людьми без заболевания также значительно снижена экспрессия Per2, Per3 и Cry2 (Stamenkovich, J. A. et al. Metabolism, 2012, 61, 978). Гены глюконеогенеза фосфоенолпируваткарбоксикиназы (Pck1) и глюкозо-6-фосфатазы (G6pc) находятся под контролем CRY и регулятора гена Bmal1 REV-ERB (Zhang, E. E. et al. Nat. Med. 2010, 16, 1152; Lamia, K. A. et al. Nature, 2011, 480, 552; Yin, L. et al. Science, 2007, 318, 1786). Глюконеогенез строго контролируется несколькими механизмами передачи сигналов и, кроме того, исследования на мышах выявили, что модуляция Cry1 и Cry2 может изменять глюконеогенез и регулировать уровни сахара в крови (Zhang, E. E. et al. Nat. Med. 2010, 16, 1152).
В условиях монотерапевтического или комбинированного лечения новые и широко известные пероральные противодиабетические средства обладают неоднородной и ограниченной эффективностью. Пероральные противодиабетические средства обладают плохим или ограниченным гликемическим контролем или плохим соблюдением пациентами схемы лечения вследствие нежелательного побочного действия, такого как отек, увеличение массы или даже более серьезные осложнения, подобные гипогликемии. Метформин, замещенный бигуанид, может вызывать диарею и дискомфорт желудочно-кишечного тракта. В заключение, с введением некоторых тиазолидин-2,4-дионовых противодиабетических средств (например, росиглитазона и пиоглитазона) связаны отек, увеличение массы и, в некоторых случаях, гепатотоксичность и кардиотоксичность. Комбинированное лечение с использованием двух или более из указанных выше средств является частым, но, как правило, приводит только к инкрементальным улучшениям гликемического контроля.
Cry1 и Cry2 также взаимодействуют с рецептором глюкокортикоидов (GR) с общим изменением транскрипционного ответа на глюкокортикоиды (Lamia, K. A. et al. Nature, 2011, 480, 552). Потеря Cry1 и/или Cry2 приводит к отсутствию толерантности к глюкозе и конститутивно высоким уровням циркулирующего кортикостерона, свидетельствующего о сниженной супрессии гипоталамо-гипофизарно-надпочечниковой оси в сочетании с увеличенной трансактивации глюкокортикоидов в печени. На геномном уровне, Cry1 и Cry2 гормонозависимо ассоциированы с элементом ответа на глюкокортикоиды в промоторе Pck1, и печени с недостаточностью криптохромов выраженно увеличена индуцируемая дексаметазоном транскрипция гена Pck1. Это позволяют предположить, что нежелательное метаболическое побочное действие глюкокортикоидов (например, гипергликемию, резистентность к инсулину и подавление функции надпочечников), используемых для подавления воспаления, можно смягчить посредством комбинации их со средствами, которые могут стабилизировать Cry1 и/или Cry2.
СУЩНОСТЬ
Объект изобретения в настоящем документе относится к модулирующим криптохромы (Cry) соединениям, фармацевтическим композициям, содержащим модулирующие Cry соединения, и к способам лечения связанных с Cry заболеваний или нарушений, таких как, например, диабет, ожирение, метаболический синдром, синдром Иценко-Кушинга и глаукома, посредством введения модулирующих Cry соединений.
В одном из аспектов объект изобретения, описанный в настоящем документе, относится к соединению формулы I:
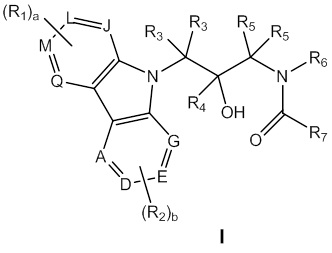
или к его фармацевтически приемлемой соли или гидрату, где:
каждый из A, D, E, G, J, L, M, и Q независимо представляет собой N или C;
каждый из R1 и R2, когда A, D, E, G, J, L, M и Q представляет собой C, независимо выбран из H, галогена, циано, нитро, -CF3, -CHF2, -CH2F, трифторметокси, азидо, гидроксила, (C1-C6)алкокси, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R8, -(C=O)-O-R8, -O-(C=O)-R8, -NR8(C=O)-R10, -(C=O)-NR8R9, -NR8R9, -NR8OR9, -S(O)cNR8R9, -S(O)d(C1-C8)алкила, -O-SO2-R8, NR8-S(O)c, -(CR8R9)d(3-10)-членного циклоалкила, -(CR8R9)e(C6-C10)арила, -(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)f(C=O)(CR8R9)e(C6-C10)арила, -(CR8R9)f(C=O)(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)eO(CR8R9)f(C6-C10)арила, -(CR8R9)eO(CR8R9)f(4-10)-членного гетероциклила, -(CR8R9)fS(O)d(CR8R9)e(C6-C10)арила и -(CR8R9)fS(O)d(CR8R9)e(4-10)-членного гетероциклила;
каждый из R3 и R5 независимо выбран из H, циано, -CF3, -CHF2, -CH2F, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R8, -(C=O)-O-R8, -(C=O)-NR8R9, -S(O)cNR8R9, -S(O)d(C1-C8)алкила, -(CR8R9)d(3-10)-членного циклоалкила, -(CR8R9)e(C6-C10)арила, -(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)f(C=O)(CR8R9)e(C6-C10)арила, -(CR8R9)f(C=O)(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)eO(CR8R9)f(C6-C10)арила, -(CR8R9)eO(CR8R9)f(4-10)-членного гетероциклила, -(CR8R9)fS(O)d(CR8R9)e(C6-C10)арила и -(CR8R9)fS(O)d(CR8R9)e(4-10)-членного гетероциклила;
где каждая из групп R3 необязательно связана друг с другом, образуя 4-12-членной моно- или бициклическую структуру;
где каждая из групп R5 необязательно связаны друг с другом, образуя 4-12-членную моно- или бициклическую структуру;
R4 представляет собой H, -CF3, -CHF2, -CH2F, (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, -(C=O)-R8, -(C=O)-O-R8, -(C=O)-NR8R9, -(CR8R9)d(3-10)-членный циклоалкил, -(CR8R9)e(C6-C10)арил, -(CR8R9)e(4-10)-членный гетероциклил, -(CR8R9)f(C=O)(CR8R9)e(C6-C10)арил, -(CR8R9)f(C=O)(CR8R9)e(4-10)-членный гетероциклил, -(CR8R9)eO(CR8R9)f(C6-C10)арил, -(CR8R9)eO(CR8R9)f(4-10)-членный гетероциклил, -CR8R9)fS(O)d(CR8R9)e(C6-C10)арил и -(CR8R9)fS(O)d(CR8R9)e(4-10)-членный гетероциклил;
где R6 и R7 связаны друг с другом, образуя 4-12-членную моно- или бициклическую структуру;
каждый из R8, R9 и R10 независимо выбран из H, (C1-C6)алкила, -(CR11R12)e(3-10)-членного циклоалкила, -(CR11R12)g(C6-C10)арила и -(CR11R12)g(4-10)-членного гетероциклила;
любой из атомов углерода (C1-C6)алкила, (3-10)-членного циклоалкила, (C6-C10)арила и (4-10)-членного гетероциклила указанных выше R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16 независимо необязательно замещен 1-3 заместителями R14, где каждый независимо выбран из галогена, циано, нитро, -CF3, -CHF2, -CH2F, трифторметокси, азидо, гидроксила, -O-R15, (C1-C6)алкокси, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R11, -(C=O)-R15, -(C=O)-O-R11, -(C=O)-O-R15, -O-(C=O)-R11, -O-(C=O)-R15, -NR11(C=O)-R13, -(C=O)-NR11R12, -(C=O)-NR11R15, -NR11R12, -NR11R15, -NR11OR12, -NR11OR15, -S(O)cNR11R12, -S(O)cNR11R15, -S(O)d(C1-C6)алкила, -S(O)dR15, -O-SO2-R11, -O-SO2-R15, -NR11-S(O)c, -NR15-S(O)c, -(CR11R12)e(3-10)-членного циклоалкила, -(CR11R12)e(C6-C10)арила, -(CR11R12)e(4-10)-членного гетероциклила, -(CR11R12)f(C=O)(CR11R12)e(C6-C10)арила, -(CR11R12)f(C=O)(CR11R12)e(4-10)-членного гетероциклила, -(CR11R12)eO(CR11R12)f(C6-C10)арила, -(CR11R12)eO(CR11R12)f(4-10)-членного гетероциклила, -(CR11R12)fS(O)d(CR11R12)e(C6-C10)арила и -(CR11R12)fS(O)d(CR11R12)e(4-10)-членного гетероциклила;
любой из атомов углерода (C1-C6)алкила, (3-10)-членного циклоалкила, (C6-C10)арила и (4-10)-членного гетероциклила указанного выше R14 независимо необязательно замещен 1-3 заместителями R16, где каждый R16 независимо выбран из галогена, циано, нитро, -CF3, -CHF2, -CH2F, трифторметокси, азидо, (CH2)eOH, (C1-C6)алкокси, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R11, -(C=O)-R15, -(C=O)-O-R11, -(C=O)-O-R15, -O-(C=O)-R11, -O-(C=O)-R15, -NR11(C=O)-R13, -(C=O)-NR11R12, -NR11R12 и -NR11R15;
любой из атомов азота (4-10)-членного гетероциклила указанных выше R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R14 и R15 независимо необязательно замещен (C1-C6)алкилом, (C2-C6)алкенилом, (C2-C6)алкинилом, -(C=O)-R11, -(C=O)-O-R11, -(C=O)-NR11R12, -(CR11R12)e(3-10)-членным циклоалкилом, -(CR11R12)e(C6-C10)арилом, -(CR11R12)e(4-10)-членным гетероциклилом, -(CR11R12)f(C=O)(CR11R12)e(C6-C10)арилом или -(CR11R12)f(C=O)(CR11R12)e(4-10)-членным гетероциклилом;
каждый из R11, R12 и R13 независимо представляет собой H или (C1-C6)алкил;
R15 представляет собой -(CR11R12)e(3-10)-членный циклоалкил, -(CR11R12)e(C6-C10)арил или -(CR11R12)e(4-10)-членный гетероциклил;
каждый из a и b независимо представляет собой 1, 2, 3 или 4;
c представляет собой 1 или 2;
d представляет собой 0, 1 или 2; и
каждый из e, f и g независимо представляет собой 0, 1, 2, 3, 4 или 5.
В определенных вариантах осуществления каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической амидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В других вариантах осуществления каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической карбамидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В определенных вариантах осуществления соединение формулы I представляет собой один из энантиомеров с (R)-конфигурацией в C-3, где каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической амидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В других вариантах осуществления объекта изобретения, описываемого в настоящем документе, соединение формулы I представляет собой один из энантиомеров с (R)-конфигурацией в C-3, где каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической карбамидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
Другие варианты осуществления объекта изобретения, описываемого в настоящем документе, представляют собой соединения, выбранные из группы, состоящей из:
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
2-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
(1R,4S)-2-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(R)-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
(S)-1-((S)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она или их фармацевтически приемлемых солей или гидратов.
В другом аспекте соединения, описываемые в настоящем документе, модулируют Cry1 или Cry2. Модуляция Cry1 или Cry2 включает любое из следующего: связывание с Cry1 или Cry2; ингибирование модификации Cry1 или Cry2; изменение локализации Cry1 или Cry2; увеличение или уменьшение стабилизации Cry1 или Cry2; увеличение или уменьшение связывания Cry1 или Cry2 с мишенью; увеличение или уменьшение активности Cry1 или Cry2 и увеличение или уменьшение активности мишени Cry1 или Cry2. Мишени Cry1 и/или Cry2 в качестве неограничивающих примеров включают Per1, Per2, рецептор глюкокортикоидов (GR), CLOCK, BMAL1 или промоторную последовательность CLOCK-BMAL1.
В другом аспекте объект изобретения, описываемый в настоящем документе, относится к фармацевтической композиции, содержащей соединение формулы I или его фармацевтически приемлемую соль или гидрат и фармацевтически приемлемый носитель, вспомогательное средство или разбавитель. В определенных вариантах осуществления фармацевтическая композиция дополнительно содержит одно или несколько дополнительных терапевтических средств. Примеры дополнительных терапевтических средств в качестве неограничивающих примеров включают ингибиторы DPP-IV, такие как ситаглиптин, алоглиптин, вилдаглиптин, саксаглиптин и линаглиптин; агонисты GLP-1, такие как эксенатид, лираглутид и альбиглютид; ингибиторы SGLT2, такие как канаглифлозин, эртуглифлозин и дапаглифлозин); метформин и сульфонилкарбамиды, такие как глибурид. Другие примеры дополнительных терапевтических средств включают сигнифор®, кетоконазол, метирапон, митотан, этомидат, корлим®, ингибиторы эпидермального фактора роста, ингибитор альдостеронсинтазы/11β-гидроксилазы LCI699 и кевокетоконазол (COR-003).
В других аспектах предоставлен способ лечения опосредуемого Cry заболевания или нарушения у индивидуума посредством введения индивидууму терапевтически эффективного количества фармацевтической композиции, описываемой в настоящем документе. В дополнительном аспекте настоящее изобретение относится к способу облегчение симптомов опосредуемого Cry заболевания или нарушения у индивидуума посредством введения индивидууму терапевтически эффективного количества фармацевтической композиции, описываемой в настоящем документе. Заболевание или нарушение можно выбирать из группы, состоящей из диабета, осложнений диабета, таких как диабетическая нейропатия, диабетическая ретинопатия, диабетическая нефропатия, формирование катаракты, глаукома, диабетическая ангиопатия, атеросклероз; неалкогольный стеатогепатит (NASH); неалкогольная жировая болезнь печени (NAFLD); астма; хроническое обструктивное заболевание легких (COPD); метаболический синдром; синдром резистентности к инсулину; ожирение; глаукома; синдром Иценко-Кушинга; психотическая депрессия; болезнь Альцгеймера; нейропатическая боль; лекарственная зависимость; остеопороз; злокачественная опухоль; дегенерация желтого пятна и миопатия.
Любой из способов, описываемых в настоящем документе, также может включать введение индивидууму одного или нескольких дополнительных терапевтических средств. Примеры дополнительных терапевтических средств в качестве неограничивающих примеров включают ингибиторы DPP-IV, такие как ситаглиптин, алоглиптин, вилдаглиптин, саксаглиптин и линаглиптин; агонисты GLP-1, такие как эксенатид, лираглутид и альбиглютид; ингибиторы SGLT2, такие как канаглифлозин, эртуглифлозин и дапаглифлозин); метформин; сульфонилкарбамиды, такие как глибурид; сигнифор®; кетоконазол; метирапон; митотан; этомидат; корлим®; ингибиторы эпидермального фактора роста; ингибитор альдостеронсинтазы/11β-гидроксилазы LCI699 и кевокетоконазол (COR-003)
В другом аспекте предоставлен способ мониторинга прогресса или прогноза опосредуемого Cry заболевания или нарушения у индивидуума, включающий определение эффективного количества одного или нескольких криптохромов или регулируемых криптохромами генов в первом образце, полученном у индивидуума, в первый период времени; определение эффективного количества одного или нескольких криптохромов или регулируемых криптохромами генов во втором образце, полученном у индивидуума, во второй период времени и сравнение количества одного или нескольких криптохромов или регулируемых криптохромами генов, детектированных в первом образце с количеством одного или нескольких криптохромов или регулируемых криптохромами генов, детектированных во втором образце или с эталонным значением. Примеры регулируемых криптохромами генов включают гены, которые содержат в своих промоторах последовательность E-бокс. Такие гены в качестве неограничивающих примеров включают Dbp, Rev-erb альфа, Rev-erb бета, Ror альфа, Ror бета, Ror гамма, Per1, Per2, Per3, Cry1, Cry2, Pck1, G6Pc, Avp, Vip, Cck, SP (субстанция P), AA-Nat, PK2 (прокинектин 2), c-Myc, MyoD и Nampt.
В определенных вариантах осуществления мониторинг включает оценку изменений риска развития опосредуемого Cry заболевания или нарушения у индивидуума.
Полагают, что оптимальным временем для дозирования у людей является вечер, соответствующий пику экспрессии Cry у человека и концу активного (дневного) периода.
Индивидуумы могут включать индивидуумов, у которых ранее лечили опосредуемое Cry заболевание или нарушение, индивидуумов, у которых ранее не лечили опосредуемое Cry заболевание или нарушение, или индивидуумов, у которых ранее не диагностировали опосредуемое Cry заболевания или нарушения. Образец может представлять собой цельную кровь, сыворотку, плазму, клетки крови, эндотелиальные клетки, биоптаты тканей, лимфу, асцитную жидкость, межклеточную жидкость, костный мозг, цереброспинальную жидкость (CSF), семенную жидкость, слюну, слизь, мокроту, пот или мочу.
В определенных вариантах осуществления первый образец получают у индивидуума до лечения опосредуемого Cry заболевания или нарушения, а второй образец получают у индивидуума после лечения опосредуемого Cry заболевания или нарушения. В других вариантах осуществления индивидуума лечат фармацевтической композицией, содержащей соединения формулы I, описываемые в настоящем документе. В определенных вариантах осуществления мониторинг дополнительно включает выбор лечения для индивидуума и/или мониторинг эффективности лечения опосредуемого Cry заболевания или нарушения, где лечение опосредуемого Cry заболевания или нарушения включает хирургическое вмешательство, введение фармацевтической композиции, как определено в настоящем документе, отдельно или в комбинации с одним или несколькими дополнительными терапевтическими средствами, хирургическое вмешательство после или перед введением фармацевтической композиции, предоставляемой в настоящем документе, или в комбинации с одним или несколькими дополнительными терапевтическими средствами, или отсутствие дополнительных действий.
В других вариантах осуществления эталонное значение включает заданное значение, значение, получаемое на основе одного или нескольких алгоритмов прогноза риска опосредуемого Cry заболевания или нарушения, значение, получаемое у индивидуума без опосредуемого Cry заболевания или нарушения, или значение, получаемое у индивидуума с диагностированным опосредуемым Cry заболеванием или нарушением. В определенных вариантах осуществления определение включает детекцию присутствия или отсутствия одного или нескольких криптохромов, определение количества одного или нескольких криптохромов, определение типа одного или нескольких криптохромов и оценку способности одного или нескольких криптохромов связываться с мишенью. Мишень может представлять собой Per1, Per2 или промоторную последовательность CLOCK-BMAL1.
Как описано в настоящем документе, опосредуемое Cry заболевание или нарушение можно выбирать из группы, состоящей из диабета, осложнений диабета, таких как диабетическая нейропатия, диабетическая ретинопатия, диабетическая нефропатия, формирование катаракты, глаукома, диабетическая ангиопатия, атеросклероз; неалкогольного стеатогепатита (NASH); неалкогольной жировой болезни печени (NAFLD); астмы; хронического обструктивного заболевания легких (COPD); метаболического синдрома; синдрома резистентности к инсулину; ожирения; глаукомы; синдрома Иценко-Кушинга; психотической депрессии; болезни Альцгеймера; нейропатической боли; лекарственной зависимости; остеопороза; злокачественной опухоли; дегенерации желтого пятна и миопатии.
В одном из вариантов осуществления в соединениях формулы I, описываемых в настоящем документе, A, D, E, G, J, L, M и Q представляют собой углерод. В другом варианте осуществления в соединениях формулы I R1 и R2 представляют собой водород. В других вариантах осуществления в соединениях формулы I R1 и R2 представляют собой фтор, а a и b представляют собой 1. В дополнительных вариантах осуществления в соединениях формулы I R3 и R5 представляют собой водород.
В другом варианте осуществления в соединениях формулы I R3, R4 и R5 представляют собой водород. В определенных вариантах осуществления в соединениях формулы I R6 и R7 связаны, образуя необязательно замещенную моноциклическую структуру.
В других вариантах осуществления в соединениях формулы I R6 и R7 связаны, образуя необязательно замещенную конденсированную бициклическую структуру, необязательно замещенную соединенную мостиковой связью бициклическую структуру, необязательно замещенную бициклическую спироструктуру, необязательно замещенную пирролидиноновую циклическую структуру, необязательно замещенную имидазолидиноновую циклическую структуру, необязательно замещенную пиперидиноновую циклическую структуру и/или необязательно замещенную пиримидиноновую циклическую структуру. Подобным образом, в любом из этих вариантов осуществления циклическая структура, формируемая R6 и R7, может быть замещена исключительно фтором, метильными группами, этильными группами, изопропильными группами, C3-6-циклоалканами или фенильными группами.
Если не определено иначе, все технические и научные термины, используемые в настоящем документе, имеют то же значение, как обычно понимает специалист в области, к которой принадлежит настоящее изобретение. Хотя в практическом осуществлении настоящего изобретения можно использовать способы и материалы, подобные или эквивалентные, способам и материалам, описываемым в настоящем документе, ниже описаны подходящие способы и материалы. Все публикации, патентные заявки, патенты и другие ссылки, указываемые в настоящем документе, явным образом включены в качестве ссылки полностью. В случае конфликта руководствоваться следует настоящим описанием, включая определения. Кроме того, материалы, способы и примеры, описываемые в настоящем документе, являются только иллюстративными и не предназначены для ограничения.
Другие характеристики и преимущества изобретения будут очевидны из приводимых ниже подробного описания и формулы изобретения.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фигуры 1A-H представляют собой ряд диаграмм, демонстрирующих экспрессию основных генов часов у мышей после введения соединения 72. Экспрессию иРНК основных генов часов Per2 (A и B), Bmal1 (C и D), Cry1 (E и F) и Cry2 (G и H) измеряли в течение 24 часов с шестичасовыми интервалами в печени мышей C57Bl/6J DIO (A, C, E, G) или Balb/c (B, D, F, H), обработанных носителем (H2O) или соединением 72. Уровни транскриптов определяли посредством кПЦР-РВ и сравнивали с носителем в ZT8 с заштрихованным периодом темноты. Уровни иРНК у обработанных соединением 72 животных для каждого момента времени сравнивали с носителем посредством T-теста: * < 0,05, ** < 0,01, *** < 0,001, **** < 0,0001.
Фигуры 2A-D представляют собой ряд диаграмм, демонстрирующих экспрессию генов глюконеогенеза у мышей после введения соединения 72. Экспрессия иРНК генов глюконеогенеза Pck1 (PEPCK; A и B), G6Pc (каталитическая субъединица глюкозо-6-фосфатаза; C и D) через шестичасовые интервалы в течение 24 часов в печени мышей C57Bl/6J DIO (A и C) или Balb/c (B и D), обработанных носителем (H2O) или соединением 72. Уровни транскриптов определяли посредством кПЦР-РВ и сравнивали с носителем в ZT8 с заштрихованным периодом темноты. Уровни иРНК у обработанных соединением 72 животных для каждого момента времени сравнивали с носителем посредством T-теста: * < 0,05, ** < 0,01, *** < 0,001, **** < 0,0001.
Фигуры 3A-C представляют собой ряд диаграмм, демонстрирующих экспрессию основных генов часов в печени мышей ICR после введения соединения 72, соединения 48, соединения 9 или соединения 57. Экспрессию иРНК основных генов часов Per2 (A), Bmal1 (B), и Cry2 (C) измеряли в печени мышей ICR, обрабатываемых в течение 4 суток дважды в сутки соединением 72, соединением 48, соединением 9, соединением 57 или носителем. Уровни иРНК определяли посредством кПЦР-РВ в образцах, полученных в ZT6 после последней дозы в ZT0. Уровни иРНК у обработанных соединением 72 животных для каждого момента времени сравнивали с носителем посредством T-теста: * < 0,05, ** < 0,01, *** < 0,001, **** < 0,0001.
Фигура 4 представляет собой диаграмму, демонстрирующую экспрессию гена Dbp после трех суточных доз соединения 72 на пике экспрессии Cry1. Экспрессию иРНК Dbp измеряли в ZT7,5 в цельной крови у мышей db/db после трех суточных доз 100 мг/кг соединения 72. Уровни транскриптов определяли посредством кПЦР-РВ и сравнивали с кровью у мышей, обработанных носителем (10% коллифор) в ZT7,5. Уровни иРНК после каждой обработки соединением сравнивали с носителем посредством T-теста (***; p ≤ 0,001).
Фигуры 5A-D представляют собой ряд диаграмм, демонстрирующих экспрессию основных генов часов после однократной дозы соединения 72 на пике или низшей точке экспрессии Cry1. Экспрессию иРНК основных генов часов Per2 (A), Bmal1 (B), Cry1 (C) и Cry2 (D) измеряли в ZT7,5 (пик экспрессии Cry1) или ZT17,5 (низшая точка экспрессии Cry1) в печени у мышей C57Bl/6J DIO после однократной дозы 100 мг/кг соединения 72. Уровни транскриптов определяли посредством кПЦР-РВ и сравнивали с печенью у обработанных носителем (10% коллифор) животных. Уровни иРНК у обработанных соединением 72 животных для каждого момента времени сравнивали с носителем посредством T-теста: * < 0,05, ** < 0,01, *** < 0,001, **** < 0,0001.
Фигура 6 представляет собой ряд диаграмм, демонстрирующих действие соединения 72 на пероральный тест толерантности к глюкозе (OGTT) у мышей db/db. Соединение 72 (50 мг/кг, п/о) или 10% коллифор (контроль) вводили в виде однократной дозы или на пике (ZT0) (A), или в низшей точке (ZT10) (B) экспрессии генов Cry1 и Bmal1.
Фигура 7 представляет собой диаграмму, демонстрирующую действие соединения 72 на площадь под кривой глюкозы (AUC) у мышей db/db. Соединение 72 (50 мг/кг, п/о) или 10% коллифор (контроль) вводили в виде однократной дозы на пике (ZT0) экспрессии генов Cry1 и Bmal1.
Фигуры 8A-C представляют собой ряд диаграмм, демонстрирующих действие соединения 72, вводимого в течение 7 суток, на метаболизм глюкозы у мышей db/db. Соединение 72 (50 мг/кг, п/о) или 10% коллифор (контроль) вводили в течение 7 суток. A) Уровни глюкозы в крови натощак; B) пероральный тест толерантности к глюкозе (OGTT); C) AUC глюкозы.
Фигуры 9A-B представляют собой ряд диаграмм, демонстрирующих действие соединения 72, вводим в течение 7 суток, на уровни инсулина у мышей db/db. Вводили соединение 72 (50 мг/кг, п/о) или 10% коллифор (контроль). A) Уровни инсулина перед (на 0 час) и после нагрузки глюкозой (через 2 часа); B) Модельная оценка гомеостаза с расчетом резистентности к инсулину (HOMA-IR).
Фигура 10 представляет собой диаграмму, демонстрирующую уровни соединения для соединения 72, измеряемые в плазме и печени приблизительно через 8 часов после введения последней дозы (50 мг/кг, п/о). Концентрация EC50 соединения 72 в анализе Per2 обозначена на диаграмме пунктирной линией.
Фигуры 11A-C представляют собой ряд диаграмм, демонстрирующих действие увеличивающихся доз соединения 72 (10 мг/кг, 50 мг/кг и 100 мг/кг) на метаболизм глюкозы у мышей db/db. В качестве контрольного носителя использовали 10% коллифор. A) Уровни глюкозы в крови натощак; B) OGTT; C) AUC глюкозы.
Фигуры 12A-B представляют собой ряд диаграмм, демонстрирующих действие увеличивающихся доз соединения 72 (10 мг/кг, 50 мг/кг и 100 мг/кг) на уровни инсулина у мышей db/db. В качестве контрольного носителя использовали 10% коллифор. A) Уровни инсулина до (на 0 час) и после нагрузки глюкозой (через 2 часа); B) Модельная оценка гомеостаза с расчетом резистентности к инсулину (HOMA-IR).
Фигура 13 представляет собой диаграмму, демонстрирующую уровни соединения для соединения 72, измеряемые в плазме и печень приблизительно через 8 часов после введения последней дозы при увеличивающихся дозах (10 мг/кг, 50 мг/кг и 100 мг/кг). Концентрация EC50 соединения 72 в анализе Per2 обозначена на диаграмме пунктирной линией.
Фигуры 14A-C представляют собой ряд диаграмм, демонстрирующих действие увеличивающихся доз соединения 9 (30 мг/кг, 100 мг/кг и 300 мг/кг) на метаболизм глюкозы у мышей db/db. В качестве контроля использовали 10% коллифор. A) Уровни глюкозы в крови натощак; B) OGTT; C) AUC глюкозы.
Фигуры 15A-B представляют собой ряд диаграмм, демонстрирующих действие варьирующих доз соединения 9 (30 мг/кг, 100 мг/кг и 300 мг/кг) на уровни инсулина у мышей db/db. В качестве контроля использовали 10% коллифор. A) Уровни инсулина до (на 0 час) и после нагрузки глюкозой (через 2 часа); B) Модельная оценка гомеостаза с расчетом резистентности к инсулину (HOMA-IR).
Фигура 16 представляет собой диаграмму, демонстрирующую уровни соединения для соединения 9 в плазме и печени приблизительно через 8 часов после введения последней дозы при увеличивающихся дозах (30 мг/кг, 100 мг/кг и 300 мг/кг). Концентрация EC50 для соединения 9 в анализе Per2 обозначена на диаграмме пунктирной линией.
Фигуры 17A-C представляют собой диаграммы, демонстрирующие действие соединения 72 на метаболизм глюкозы у мышей C57/Bl6J DIO. Соединение 72 (100 мг/кг, п/о), 10% коллифор (контроль) или росиглитазон (30мг/кг) вводили в течение 7 суток. A) Уровни глюкозы в крови натощак; B) OGTT; C) AUC глюкозы.
Фигуры 18A-B представляют собой ряд диаграмм, демонстрирующих действие соединения 72 на уровни инсулина у мышей C57/Bl6J DIO. Соединение 72 (100 мг/кг, п/о), 10% коллифор (контроль) или росиглитазон (30мг/кг) вводили в течение 7 суток. A) Уровни инсулина перед (на 0 час) и после нагрузки глюкозой (через 2 часа); B) Модельная оценка гомеостаза с расчетом резистентности к инсулину (HOMA-IR).
Фигура 19 представляет собой ряд диаграмм, демонстрирующих действие соединения 72 на модели индуцированной кортизоном резистентности к инсулину на крысах. Кортизон (30мг/кг, п/к) вводили с носителем, соединением 72 (50 мг/кг, п/о) или мифепристоном (30 мг/кг, п/о) в течение 7 суток. (A) Уровни глюкозы в плазме натощак и (B) уровни инсулина в плазме натощак.
Фигура 20 представляет собой диаграмму, демонстрирующую действие соединения 72 (50 мг/кг, п/о), вводимого в течение 7 суток, на HOMA-IR в модели индуцированной кортизоном резистентности к инсулину на крысах. Кортизон (30мг/кг, п/к) вводили с носителем, соединением 72 (50 мг/кг, п/о) или мифепристоном (30 мг/кг, п/о) в течение 7 суток.
Фигура 21 представляет собой диаграмму, демонстрирующую действие соединения 72 на термостабильность связывающий FAD домен CRY1 in vitro. Обработка очищенного связывающего FAD домена CRY1 соединением 72 вызывала зависимое от дозы увеличение температуры плавления белка, как определяли посредством анализа дифференциальной сканирующей флуорометрии ("тепловой сдвиг").
Фигуры 22A-C представляют собой ряд диаграмм, демонстрирующих действие увеличивающихся доз соединения 72 (10 мг/кг, 30 мг/кг и 100 мг/кг) на метаболизм глюкозы у мышей DIO. Соединение 72 (100 мг/кг, п/о), 10% коллифор (контроль) или росиглитазон (30мг/кг) вводили в течение 7 суток. A) Уровни глюкозы в крови натощак; B) OGTT; C) AUC глюкозы.
ПОДРОБНОЕ ОПИСАНИЕ
Каждые из заявок и патентов, цитируемых в тексте настоящего документа, а также каждые документ или ссылка, цитируемые в каждых из заявок и патентов (включая цитаты при ведении каждого выданного патента; "цитируемые при подаче заявки документы"), и каждые из заявок США и иностранных заявок или патентов, соответствующих и/или притязающих на приоритет на основе любых из этих заявок и патентов, и каждые из документов, цитируемых или указываемых в каждых из цитируемых в заявках документах, таким образом, явно включены в настоящий документ в качестве ссылки. В более общем смысле, документы или ссылки цитируют в тексте настоящего документа или в списке ссылок перед формулой изобретения, или в самом тексте; и каждый из этих документов или ссылок ("цитируемых в настоящем документе ссылок"), а также каждые документ или ссылка, цитируемые в каждой из цитируемых в настоящем документе ссылок (включая любые характеристики, инструкции и т.д. производителей), таким образом, явно включены в настоящий документ в качестве ссылки. Документы, включаемые в текст настоящего документа в качестве ссылки, можно использовать в практическом осуществлении изобретения. Особенности, структуры или характеристики, описываемые на всем протяжении настоящего описания, можно комбинировать любым подходящим образом в одном или нескольких вариантах осуществления. Например, использование фраз "иллюстративные варианты осуществления", "примеры вариантов осуществления" "определенные варианты осуществления" или другие сходные формулировки на всем протяжении настоящего описания относится к тому факту, что конкретную особенность, структуру или характеристику, описанные в отношении какого-либо варианта осуществления, можно включать по меньшей мере в один из вариантов осуществления, описываемых в настоящем документе. Таким образом, наличие фраз "иллюстративные варианты осуществления", "примеры вариантов осуществления", "в определенных вариантах осуществления", "в других вариантах осуществления" или другие сходные формулировки на всем протяжении настоящего описания не все обязательно относятся к одной и той же группе вариантов осуществления, и описанные особенности, структуры или характеристики можно комбинировать любым подходящим образом в одном или нескольких вариантах осуществления.
Для облегчения понимания настоящего описания ниже определен ряд терминов. Термины, определенные в настоящем документе, имеют значения, обычно понимаемые специалистом в областях, относящихся к сущности, описываемой в настоящем документе. Формы единственного числа не предназначены для обозначения исключительно единственного числа, но включают общий класс, из которого можно использовать конкретный пример для иллюстрации. Терминологию в настоящем документе используют для описания конкретных вариантов осуществления объекта изобретения, описываемого в настоящем документе, но их использование не ограничивает объект изобретения, за исключением того, что указано в формуле изобретения.
Как используют в настоящем документе, термины "содержащий", "включающий" или "обладающий" используют в их открытом, неограничивающем смысле.
Как используют в настоящем документе, если не указано иначе, термин "галоген" означает фтор, хлор, бром или йод.
Как используют в настоящем документе, если не указано иначе, термин "алкил" включает насыщенные одновалентные углеводородные радикалы с неразветвленными или разветвленными молекулами.
Как используют в настоящем документе, термин "алкенил" представляет собой одновалентные группы с неразветвленными или разветвленными цепями, если не указано иначе, с количеством атомов углерода от 2 до 6, содержащих одну или несколько двойных связей углерод-углерод и иллюстрируемых этенилом, 1-пропенилом, 2-пропенилом, 2-метил-1-пропенилом, 1-бутенилом, 2-бутенилом и т.п.
Как используют в настоящем документе, термин "алкинил" представляет собой одновалентные группы с неразветвленными или разветвленными цепями с количеством атомов углерода от двух до шести, содержащие тройную связь углерод-углерод и иллюстрируемых этинилом, 1-пропинилом и т.п.
Как используют в настоящем документе, если не указано иначе, термин "алкокси" включает O-алкильные группы, где алкил является таким, как определено выше.
Термин "Me" означает метил, а "Et" означает этил.
Как используют в настоящем документе, если не указано иначе, термин "циклоалкил" относится к неароматическим, насыщенным или частично насыщенным, моноциклическим или конденсированным, спиро или неконденсированным бициклическим или трициклическим углеводородам, указанным в настоящем документе, содержащим всего от 3 до 10 атомом углерода. Иллюстративные примеры циклоалкилов являются производными, но не ограничиваясь ими, из следующего:
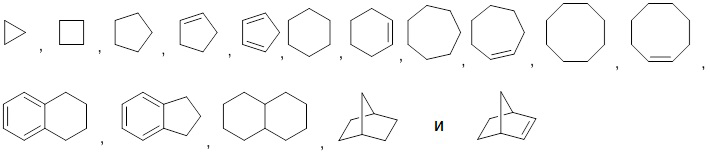
Как используют в настоящем документе, если не указано иначе, термин "арил" включает органические радикалы, получаемые из ароматических углеводородов посредством удаления одного атома водорода, такие как фенил или нафтил.
Как используют в настоящем документе, если не указано иначе, термин "(4-12)-членный гетероциклил" включает ароматические и неароматические гетероциклические группы, содержащие от одного до четырех гетероатомов, где каждый выбран из O, S и N, где каждая гетероциклическая группа в своей циклической системе содержит 4-12 атомов, и при условии, что циклическая структура указанной группы не содержит двух соседних атомов O или S. Неароматические гетероциклические группы включают группы, содержащие в своей циклической системе только 3 атома, но ароматические гетероциклические группы должны содержать в своей циклической системе по меньшей мере 5 атомов. Гетероциклические группы включают конденсированные с бензолом циклические системы. Примером 3-членной гетероциклической группы является азиридин, примером 4-членной гетероциклической группы является азетидинил (производное азетидина). Примером 5-членной гетероциклической группы является тиазолил, примером 7-членной циклической структуры является азепинил, и примером 10-членной гетероциклической группы является хинолинил. Примерами неароматических гетероциклических групп являются пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидинo, морфолино, тиоморфолино, тиоксанил, пиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 1,2,3,6-тетрагидропиридинил, 2-пирролинил, 3-пирролинил, индолинил, 2H-пиранил, 4H-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3.1.0]гексанил, 3-азабицикло[4.1.0]гептанил, 3H-индолил и хинолизинил. Примерами ароматических гетероциклических групп являются пиридинил, имидазолил, пиримидинил, пиразолил, триазолил, пиразинил, тетразолил, фурил, тиенил, изоксазолил, тиазолил, оксазолил, изотиазолил, пирролил, хинолинил, изохинолинил, индолил, бензимидазолил, бензофуранил, ционнолинил, индазолил, индолизинил, фталазинил, пиридазинил, триазинил, изоиндолил, птеридинил, пуринил, оксадиазолил, тиадиазолил, фуразанил, бензофуразанил, бензотиофенил, бензотиазолил, бензоксазолил, хиназолинил, хиноксалинил, нафтиридинил и фуропиридинил. Указанные выше группы, как получают из приведенных выше списков, могут быть C-связанными или N-связанными, когда такое возможно. Например, группа, производная пиррола, может представлять собой пиррол-1-ил (N-связанная) или пиррол-3-ил (C-связанная). Кроме того, группа, производная имидазола, может представлять собой имидазол-1-ил (N-связанная) или имидазол-3-ил (C-связанная). 4-12-членный гетероцикл может являться необязательно замещенной по любому циклическому атому(ам) углерода, серы или азота одним или двумя оксо на циклическую структуру. Примером гетероциклической группы, где 2 циклических атома замещены оксо-группами, является 1,1-диоксотиоморфолинил. Другими иллюстративными примерами 4-12-членных гетероциклов является производны, но не ограничиваясь этим, следующего:
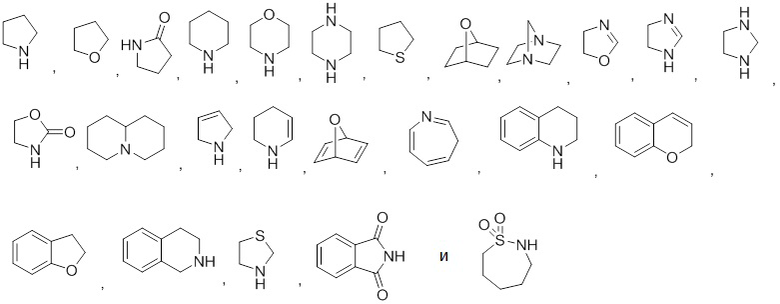
Как используют в настоящем документе, термин "замещенный" означает, что любой один или несколько атомов водорода в указанном атоме замещены любой выбранной из указанных групп, при условии, что не превышается нормальная валентность указанного атома и что замена приводит к стабильному соединению. Когда заместитель представляет собой кето (например, =O), тогда на атоме замещены 2 атома водорода. Кетозаместители не представлены в ароматических функциональных группах. Как используют в настоящем документе, циклические двойные связи представляют собой двойные связи, которые сформированы между двумя соседними циклическими атомами (например, C=C, C=N или N=N). Неограничивающие примеры таких групп в качестве неограничивающих примеров включают H, CH3, NO2, SO2N(CH3)2, SO2N((CH3)SO2), COOH, COOCH3, CO(N(CH3)), алкил, алкенил, алкинил, арил, аралкил, циклоалкил, гетероциклил, алкиларил, гетероарил, гетероциклоалкил, алкокси (например, метокси, этокси и т.д.), алкилкарбонилокси, арилкарбонилокси, алкоксикарбонилокси, арилоксикарбонилокси, карбоксилат, алкилкарбонил, алкиламинокарбонил, аралкиламинокарбонил, алкениламинокарбонил, алкилкарбонил, арилкарбонил, аралкилкарбонил, алкенилкарбонил, алкоксикарбонил, аминокарбонил, алкилтиокарбонил, трифторметил, пентафторэтил, галоген (например, хлор, фтор, бром, йод), циано, тио, амидо, простой эфир, сложный эфир, гидроксил, гидроксиалкил, насыщенные или ненасыщенные жирные кислоты, азидо, фосфонамидо, сульфонамидо, лактам, фосфат, фосфонато, фосфинато, амино (включая алкиламино, диалкиламино, ариламино, диариламино и алкилариламино), ациламино (включая алкилкарбониламино, арилкарбониламино, карбамоил и уреидо), амидино, имино, гуанидино, сульфгидрил, алкилтио, арилтио, тиокарбоксилат, сульфаты, алкилсульфинил, сульфонaто, сульфамоил, сульфонамидо, нитро, циано, азидо и т.д.
Объект изобретения, описываемые в настоящем документе, относится к карбазолсодержащим сульфонамидным соединениям, которые модулируют молекулы одного или нескольких криптохромов. Эти соединения обладают общей структурой, указанной в формуле I:

или ее фармацевтически приемлемой солью или гидратом, где
каждый из A, D, E, G, J, L, M и Q независимо представляет собой N или C;
каждый из R1 и R2, когда A, D, E, G, J, L, M и Q представляет собой C, независимо выбран из H, галогена, циано, нитро, -CF3, -CHF2, -CH2F, трифторметокси, азидо, гидроксила, (C1-C6)алкокси, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R8, -(C=O)-O-R8, -O-(C=O)-R8, -NR8(C=O)-R10, -(C=O)-NR8R9, -NR8R9, -NR8OR9, -S(O)cNR8R9, -S(O)d(C1-C8)алкила, -O-SO2-R8, NR8-S(O)c, -(CR8R9)d(3-10)-членного циклоалкила, -(CR8R9)e(C6-C10)арила, -(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)f(C=O)(CR8R9)e(C6-C10)арила, -(CR8R9)f(C=O)(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)eO(CR8R9)f(C6-C10)арила, -(CR8R9)eO(CR8R9)f(4-10)-членного гетероциклила, -(CR8R9)fS(O)d(CR8R9)e(C6-C10)арила и -(CR8R9)fS(O)d(CR8R9)e(4-10)-членного гетероциклила;
каждый из R3 и R5 независимо выбран из H, циано, -CF3, -CHF2, -CH2F, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R8, -(C=O)-O-R8, -(C=O)-NR8R9, -S(O)cNR8R9, -S(O)d(C1-C8)алкила, -(CR8R9)d(3-10)-членного циклоалкила, -(CR8R9)e(C6-C10)арила, -(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)f(C=O)(CR8R9)e(C6-C10)арила, -(CR8R9)f(C=O)(CR8R9)e(4-10)-членного гетероциклила, -(CR8R9)eO(CR8R9)f(C6-C10)арила, -(CR8R9)eO(CR8R9)f(4-10)-членного гетероциклила, -(CR8R9)fS(O)d(CR8R9)e(C6-C10)арила и -(CR8R9)fS(O)d(CR8R9)e(4-10)-членного гетероциклила;
каждая из групп R3 необязательно связаны друг с другом в виде 4-12-членной моно- или бициклической структуры;
каждая из групп R5 необязательно связаны друг с другом в виде 4-12-членной моно- или бициклической структуры;
R4 представляет собой H, -CF3, -CHF2, -CH2F, (C1-C6)алкил, (C2-C6)алкенил, (C2-C6)алкинил, -(C=O)-R8, -(C=O)-O-R8, -(C=O)-NR8R9, -(CR8R9)d(3-10)-членный циклоалкил, -(CR8R9)e(C6-C10)арил, -(CR8R9)e(4-10)-членный гетероциклил, -(CR8R9)f(C=O)(CR8R9)e(C6-C10)арил, -(CR8R9)f(C=O)(CR8R9)e(4-10)-членный гетероциклил, -(CR8R9)eO(CR8R9)f(C6-C10)арил, -(CR8R9)eO(CR8R9)f(4-10)-членный гетероциклил, -CR8R9)fS(O)d(CR8R9)e(C6-C10)арил и -(CR8R9)fS(O)d(CR8R9)e(4-10)-членный гетероциклил;
где R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической структуры;
каждый из R8, R9 и R10 независимо выбран из H, (C1-C6)алкила, -(CR11R12)e(3-10)-членного циклоалкила, -(CR11R12)g(C6-C10)арила и -(CR11R12)g(4-10)-членного гетероциклила;
любой из атомов углерода (C1-C6)алкила, (3-10)-членного циклоалкила, (C6-C10)арила и (4-10)-членного гетероциклила указанных выше R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, R13, R14, R15 и R16 независимо необязательно замещен 1-3 заместителями R14, где каждый независимо выбран из галогена, циано, нитро, -CF3, -CHF2, -CH2F, трифторметокси, азидо, гидроксила, -O-R15, (C1-C6)алкокси, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R11, -(C=O)-R15, -(C=O)-O-R11, -(C=O)-O-R15, -O-(C=O)-R11, -O-(C=O)-R15, -NR11(C=O)-R13, -(C=O)-NR11R12, -(C=O)-NR11R15, -NR11R12, -NR11R15, -NR11OR12, -NR11OR15, -S(O)cNR11R12, -S(O)cNR11R15, -S(O)d(C1-C6)алкила, -S(O)dR15, -O-SO2-R11, -O-SO2-R15, -NR11-S(O)c, -NR15-S(O)c, -(CR11R12)e(3-10)-членного циклоалкила, -(CR11R12)e(C6-C10)арила, -(CR11R12)e(4-10)-членного гетероциклила, -(CR11R12)f(C=O)(CR11R12)e(C6-C10)арила, -(CR11R12)f(C=O)(CR11R12)e(4-10)-членного гетероциклила, -(CR11R12)eO(CR11R12)f(C6-C10)арила, -(CR11R12)eO(CR11R12)f(4-10)-членного гетероциклила, -(CR11R12)fS(O)d(CR11R12)e(C6-C10)арила и -(CR11R12)fS(O)d(CR11R12)e(4-10)-членного гетероциклила;
любой из атомов углерода (C1-C6)алкила, (3-10)-членного циклоалкила, (C6-C10)арила и (4-10)-членного гетероциклила указанного выше R14 независимо необязательно замещен 1-3 заместителями R16, где каждый независимо выбран из галогена, циано, нитро, -CF3, -CHF2, -CH2F, трифторметокси, азидо, (CH2)eOH, (C1-C6)алкокси, (C1-C6)алкила, (C2-C6)алкенила, (C2-C6)алкинила, -(C=O)-R11, -(C=O)-R15, -(C=O)-O-R11, -(C=O)-O-R15, -O-(C=O)-R11, -O-(C=O)-R15, -NR11(C=O)-R13, -(C=O)-NR11R12, -NR11R12 и -NR11R15;
любой из атомов азота (4-10)-членного гетероциклила указанных выше R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R14 и R15 независимо необязательно замещен (C1-C6)алкилом, (C2-C6)алкенилом, (C2-C6)алкинилом, -(C=O)-R11, -(C=O)-O-R11, -(C=O)-NR11R12, -(CR11R12)e(3-10)-членным циклоалкилом, -(CR11R12)e(C6-C10)арилом, -(CR11R12)e(4-10)-членным гетероциклилом, -(CR11R12)f(C=O)(CR11R12)e(C6-C10)арилом или -(CR11R12)f(C=O)(CR11R12)e(4-10)-членным гетероциклилом;
каждый из R11, R12 и R13 независимо представляет собой H или (C1-C6)алкил;
R15 представляет собой -(CR11R12)e(3-10)-членный циклоалкил, -(CR11R12)e(C6-C10)арил или -(CR11R12)e(4-10)-членный гетероциклил;
каждый из a и b независимо представляет собой 1, 2, 3 или 4;
c представляет собой 1 или 2;
d представляет собой 0, 1 или 2; и
каждый из e, f и g независимо представляет собой 0, 1, 2, 3, 4 или 5.
В иллюстративных вариантах осуществления соединений формулы I каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической амидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В определенных вариантах осуществления каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической карбамидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В определенных вариантах осуществления объекта изобретения, описываемого в настоящем документе, соединение формулы I представляет собой один из энантиомеров c (R)-конфигурацией в C-3, где каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической амидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В других вариантах осуществления соединение формулы I представляет собой один из энантиомеров c (S)-конфигурацией в C-3, где каждый из A, D, E, G, J, L, M и Q представляет собой C; каждый из R1 и R2 независимо выбран из H или галогена; R4 представляет собой H или (C1-C6)алкил, R3 и R5 представляют собой H; R6 и R7 связаны друг с другом в виде 4-12-членной моно- или бициклической карбамидной структуры; R8, R9, R10, R11, R12, R13, R14, R15, R16, a, b, c, d, e и f являются такими, как определено в настоящем документе.
В определенных вариантах осуществления соединение можно выбирать из группы, состоящей из:
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
2-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
(1R,4S)-2-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(R)-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
(S)-1-((S)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она или их фармацевтически приемлемых солей или гидратов.
Как используют в настоящем документе, термин "фармацевтически приемлемый" относится к такому веществу, как носитель или разбавитель, который не нейтрализует биологической активности или свойств соединений, описываемых в настоящем документе, и является относительно нетоксичным, например, вещество можно вводить индивидууму без вызова нежелательного биологического действия или без вредного взаимодействия с любым из компонентов композиции, в которой оно содержится.
Как используют в настоящем документе, термин "фармацевтически приемлемые соли" относится к солям, которые сохраняют биологическую эффективность свободных кислот и оснований указанных соединений и которые не являются биологически или иным образом нежелательными. Фармацевтически приемлемые соли соединений формулы I включают их соли присоединения кислот и оснований. Подходящие соли присоединения кислот формируют кислоты, которые формируют нетоксические соли. Примеры включают соли ацетат, адипат, арабогалактансульфонат, аскорбат, аспартат, бензоат, безилат, бикарбонат/карбонат, бисульфат/сульфат, борат, камзилат, холат, цитрат, эдизилат, эстолат, эзилат, формиат, фумарат, галактуронат, глюцептат, глюконат, глюкуронат, глутаминат, гексафторфосфат, гибензат, гиппурат, гидрохлорид/хлорид, гидробромид/бромид, йодогидрат/йодид, 3-гидрокси-2-нафтоат, 1-гидрокси-2-нафтоат, изетионат, лактат, лактобионат, малат, малеат, малонат, соль миндальной кислоты, мезилат, метилсульфат, соль муциновой кислоты, нападизилат, нафталат, 2-напсилат, никотинат, нитрат, олеат, оротат, оксалат, пальмитат, памоат, фосфат/водород фосфат/дигидрофосфат, сахарат, салицилат, стеарат, сукцинат, сульфосалицилат, тартрат, тозилат, трифторацетат и триптофанат.
Подходящие основные соли формируют основания, которые формируют нетоксичные соли. Примеры включают соли аденина, алюминия, 2-амино-2-метилпропан-1-ола, аргинина, бентамина, бензатина, кальция, холина, цитозина, диэтиламина, диоламина, эполамина, эрбумина, этилендиамина, глюкозамина, глицина, гуанидина, гуанина, гидрабамина, лизина, магния, меглумина, морфолина, никотинамида, оламина, омитина, пиперазина, калия, прокаина, пролина, пиридоксина, серина, серебра, натрия, трогламина, трометамина, тирозина, валина и цинка. Для обзора подходящих солей, см. "Handbook of Pharmaceutical Salts: Properties, Selection, and Use" by Stahl and Wermuth (Wiley-VCH, Weinheim, Germany, 2002).
Фармацевтически приемлемую соль соединения формулы I можно легко получать, смешивая растворы соединения формулы I и желаемой кислоты или основания, соответственно. Соль можно осаждать из раствора и собирать посредством фильтрования или можно восстанавливать посредством выпаривания растворителя. Степень ионизации соли может варьировать от полностью ионизированной до почти неионизированной.
Соединения формулы I могут существовать в различных кристаллических формах, известных как полиморфы. Полиморфы включают различные структуры укладки кристаллов соединения одного и того же химического состава. Полиморфы могут обладать различными профилями рентгенодифракции, инфракрасными спектрами, температурами плавления, плотностью, жесткостью, формой кристаллов, оптическими и электрическими свойствами, стабильностью, сольватами и растворимостью. Доминирование одной кристаллической формы могут обеспечивать различные факторы, такие как растворитель при перекристаллизации, скорость кристаллизации и температура хранения.
"Сольват" предназначен для обозначения формы фармацевтически приемлемого сольвата указанного соединения, которая сохраняет биологическую эффективность такого соединения. Примеры сольватов включают соединения по изобретению в комбинации с водой, изопропанолом, этанолом, метанолом, диметилсульфоксидом, этилацетатом, уксусной кислотой или этаноламином. Термин "гидрат" относится к сольвату, где растворителем является вода. Термин "алкоголят" относится к сольвату, где растворителем является спирт. Гидраты сформированы посредством комбинации одной или нескольких молекул воды с одной молекулой вещества, в которой вода сохраняет свое молекулярное состояние в виде H2O. Неограничивающие примеры гидратов включают моногидраты, дигидраты и т.д.
Соединения по изобретению включают соединения формулы I, как определено в настоящем документе, их полиморфы, пролекарственные средства и изомеры (включая оптические, геометрические и таутомерические изомеры), а также меченные изотопами соединения формулы I.
Соединения по настоящему изобретению можно вводить в виде пролекарственных средств. Таким образом, определенные производные соединений формулы I, которые сами могут обладать небольшой или вообще не обладать фармакологической активностью, при введение в организм или на тело, могут преобразовываться в соединения формулы I с желаемой активностью, например, посредством гидролитического расщепления. Такие производные обозначают как "пролекарственные средства". Дополнительную информацию по использованию пролекарственных средств можно найти в "Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T. Higuchi and W. Stella) и "Bioreversible Carriers in Drug Design", Pergamon Press, 1987 (Ed. E. B. Roche, American Pharmaceutical Association). Например, пролекарственные средства можно получать, заменяя соответствующие функциональные группы, находящиеся в соединениях формулы I, определенными функциональными группами, известными специалистам в данной области как "профункциональные группы", как описано, например, в "Design of Prodrugs" by H. Bundgaard (Elsevier, 1985).
Определенные примеры таких пролекарственных средства, когда соединение формулы I содержит функциональную группу карбоновой кислоты (-CO2H), включают ее сложные эфиры, например, замещение водорода (C1-C8)алкилом; когда соединение формулы I содержит спиртовую функциональную группу (-OH), ее простой эфир, например, замещение водорода (C1-C8)алканоилоксиметилом; и когда соединение формулы I содержит вторичную функциональную аминогруппу (-NHR, когда R не является H), ее амид, например, замещение одного из атомов водорода (C1-C10)алканоилом. Специалистам в данной области известны дополнительные примеры замещающих групп в соответствии с указанными выше примерами и примеры других типов пролекарственных средств.
Соединения формулы I содержат один или несколько ассиметричных атомов углерода. Следует понимать, что все энантиомеры и/или диастереомеры, соответствующие соединениям формулы I, можно получать аналогичными способами. Все оптические изомеры и стереоизомеры соединений формулы I и их смеси, представляют собой считают включенными в объем изобретения. В отношении соединений формулы I изобретение включает использование рацемата, одной или нескольких энантиомерных форм, одной или нескольких диастереоизомерных форм или их смесей. Также соединения формулы I могут существовать в виде таутомеров. Настоящее изобретение относится к использованию всех таких таутомеров и их смесей.
Определенные функциональные группы, содержащиеся в соединениях по настоящему изобретению, можно замещать биоизостерическими группами, которые представляют собой группы, которые обладают сходными пространственными требованиями или необходимостью в электронах относительно исходной группы, но демонстрируют другие или улучшенные физико-химические или другие свойства. Подходящие примеры хорошо известны специалистам в данной области и в качестве неограничивающих примеров включают функциональные группы, описанные в Patini, et al. Chem Rev. 1996, 96, 3147-3176 и цитируемых там ссылках.
В объем заявляемых соединений формулы I включены фармацевтически приемлемые соли добавления кислот или оснований, где противоион является оптически активным, например, D-лактат или L-лизин или рацемат, например, DL-тартрат или DL-аргинин. Цис/транс изомеры можно разделять общепринятыми способами, хорошо известными специалистам в данной области, например, хроматографией и фракционной кристаллизацией. Общепринят способы получения/выделения индивидуальных энантиомеров включают хиральный синтез из подходящего оптически чистого предшественника или разделение рацемата (или рацемата соли или производного), например, с использованием хиральной высокоэффективной жидкостной хроматографии (ВЭЖХ).
Альтернативно, рацемат (или рацемический предшественник) можно подвергать реакции с подходящим оптически активным соединением, например, спиртом или, в случае, когда соединение формулы I содержит кислотную или основную функциональную группу, кислотой или основанием, такими как винная кислота или 1-фенилэтиламин. Полученную смесь диастереоизомеров можно разделять посредством хроматографии и/или фракционной кристаллизации и преобразовывать диастереомеры в соответствующие чистые энантиомеры и/или диастереомеры хорошо известными специалистам способами. Хиральные соединения по изобретению (и их хиральные предшественники) можно получать в энантиомерно- и/или диастереомерно обогащенной форме с использованием хроматографии, как правило ВЭЖХ, на ассиметричной смоле с подвижной фазой, состоящей из углеводорода, как правило, гептана или гексана, содержащего от 0 до 50% изопропанола, как правило, от 2 до 20%, и от 0 до 5% алкиламина, как правило, 0,1% диэтиламина. Концентрация элюата обеспечивает обогащенную смесь. Смеси энантиомеров и/или диастереомеры можно разделять общепринятыми способами, известными специалистам в данной области. См., например, "Stereochemistry of Organic Compounds" by E. L. Eliel (Wiley, New York, 1994).
Соединения формулы I могут быть изотопно мечеными, где один или несколько атомы замещены атомами с тем же атомным номером, но с атомной массой или массовым числом, отличающимся от атомной массы или массового числа, в основном присутствующего в природе. Примеры изотопов, подходящих для включения в соединения по изобретению, включают изотопы водорода, такие как 2H и 3H, углерода, такие как 11C, 13C и 14C, хлора, такие как 36Cl, фтора, такие как 18F, йода, такие как 123I и 125I, азота, такие как 13N и 15N, кислорода, такие как 15O, 17O и 18O, фосфора, такие как 32P, и серы, таки как 35S. Определенные изотопно меченые соединения формулы I, например, соединения, с включением радиоактивного изотопа, пригодны в исследованиях распределения лекарственного средства и/или субстрата в тканях. Особенно пригодны для этой цели радиоактивные изотопы тритий, например, 3H, и углерод-14, например, 14C, ввиду простоты их включения и готовых средств детекции. Замещение более тяжелыми изотопами, такими как дейтерий, например, 2H, может обеспечить определенные терапевтические преимущества, являющиеся результатом большей метаболической стабильности, например, увеличенного времени полужизни in vivo или сниженной необходимости дозирования, и, таким образом, в некоторых обстоятельствах могут быть предпочтительными. Замещение испускающими позитроны изотопами, такими как 11C, 18F, 15O и 13N, может быть полезно для исследований позитронно-эмиссионной томографии (PET) для проверки занятия субстратом рецепторов. Изотопно меченые соединения формулы I, как правило, можно получать общепринятыми способами, известными специалистам в данной области, или способами, аналогичными способам, описанным в сопровождающем разделе "Примеры и Препараты" с использованием вместо применяемых ранее немеченых реагентов соответствующих изотопно меченых реагентов.
Соединения по настоящему изобретению модулируют Cry1 и/или Cry2. Как используют в настоящем документе, "модуляция" относится к повышению, снижению или изменению функционирования, активности или собственных характеристик Cry1 и Cry2. Модуляция Cry1 или Cry2 включает любое из следующего: связывание с Cry1 или Cry2; ингибирование модификации Cry1 или Cry2; изменение локализации Cry1 или Cry2; повышение или снижение стабилизации Cry1 или Cry2; увеличение или уменьшение связывания Cry1 или Cry2 с мишенью; повышение или снижение активности Cry1 или Cry2 и увеличение или уменьшение активности мишени Cry1 или Cry2.
Модуляция Cry1 и Cry2 включает связывание соединения по настоящему изобретению с Cry1 и/или Cry2, посредством прямого взаимодействия или непрямого взаимодействия. В определенных аспектах соединение по настоящему изобретению может связываться с комплексом, содержащим Cry1 и/или Cry2. Способы детекции взаимодействия низкомолекулярных соединений и белков известны в данной области, например, способы иммунопреципитации, хроматография и различные форматы панелей.
Соединениями по настоящему изобретению можно изменять собственные характеристики Cry1 и Cry2, такие как посттрансляционная модификация, стабильность или локализация. Посттрансляционные модификации Cry1 и Cry2 могут играть решающую роль в определении активности, стабильности или клеточной локализации Cry1 и Cry2. В определенных исследованиях показано, что фосфорилирование может изменять стабильность Cry1 и Cry2. Соединения по настоящему изобретению могут предотвращать или увеличивать посттрансляционную модификацию Cry1 и Cry2, например, фосфорилирование, убиквитинирование, ацетилирование, гликозилирование, рибозилирование или сумоилирование.
Специалист в данной области может легко осуществлять способы детекции посттрансляционных модификаций Cry1 или Cry2. Такие способы детекции включают вестерн-блоттинг и радиоиммунологический анализ. Cry1 и Cry2 локализуются в ядре в конкретных состояниях, например, после гетеродимеризации с Per1 и Per2. После прохождения в ядро Cry1 и Cry2 играют роль в прерывании инициации транскрипции ядерного комплекса CLOCK-BMAL1, таким образом, снижая экспрессию генов циркадных ритмов в петле отрицательной обратной связи, которая является ключевой для поддержания суточных колебаний. Специалист в данной области может легко определить локализацию белков, например, посредством иммунофлуоресцентного анализа, анализов субклеточного фракционирования и вестерн-блоттинга. Снижение экспрессии Cry1 и Cry2 также является решающим для суточных колебания и опосредовано на транскрипционном и белковом уровнях. Стабильность Cry1 и Cry2 можно измерять известными в данной области способами, а также способами, представленными в примерах 5-8.
Как используют в настоящем документе, активность Cry1 и Cry2 включает связывание Cry1 или Cry2 с мишенью и активность расположенной ниже по цепи мишени Cry1 или Cry2. Соединения по настоящему изобретению могут повышать или снижать связывание Cry1 или Cry2 с мишенью. Мишени, которые связываются с Cry1 и/или Cry2, известны в данной области и включают Per1, Per2, рецептор глюкокортикоидов, промоторную последовательность CLOCK-BMAL1 и промоторную последовательность VEGF. Другие мишени включают гены, экспрессию которых модулируют Cry1 или Cry2, включая гены, которые содержат в своих промоторах последовательность E-бокс. Такие гены в качестве неограничивающих примеров включают Dbp, Rev-erb альфа, Rev-erb бета, Ror альфа, Ror бета, Ror гамма, Per1, Per2, Per3, Cry1, Cry2, Pck1, G6Pc, Avp, Vip, Cck, SP (субстанция P), AA-Nat, PK2 (прокинектин 2), c-Myc, MyoD и Nampt. Мишени Cry1 и Cry2, указанные в настоящем документе, также включают мишени, которые еще не идентифицированы.
Связывание Cry1 или Cry2 с мишенями можно определять, например, посредством иммунопреципитации, дрожжевой двухгибридной системы, аффинной хроматографии. Нисходящая активность мишеней Cry1 или Cry2 включает опосредованную CLOCK-BMAL1 транскрипцию, связывание Cry1 или Cry2 с промотором CLOCK-BMAL-1, связывание Cry1 или Cry2 с промотором промотор VEGF, локализацию или стабильность Per1 или Per2, димеризацию CLOCK-BMAL1, экспрессию генов-мишеней CLOCK-BMAL1, таких как Cry1, Cry2, Per1, Per2, Rev-erb α и β, Rora, белки TIM и VEGF. Способы детекции активности промоторов можно проводить посредством иммунопреципитации хроматина, анализа изменения электрофоретической подвижности или анализов промоторов с люциферазой, как описано в примерах 3 и 4. Способы определения экспрессии генов-мишеней включают анализ экспрессии генов и микропанели, которые легко может проводить специалист в данной области.
В определенных вариантах осуществления для идентификации из соединений, описываемых в настоящем документе, конкретных соединений, которые подходят для лечения или облегчения симптомов опосредуемых Cry заболеваний или нарушений, пригодными могут являться способы или анализы определения предполагаемой эффективности. В одном из аспектов в анализе in vitro, в котором определяют действие соединения на экспрессию основных генов часов, можно определять концентрацию соединения, индуцирующую половину ответа между исходным уровнем и максимумом после указанного времени воздействия (обозначаемую в настоящем документе как значение или концентрация EC50). В клетки, которые обрабатывают соединениями по настоящему изобретению, вводят (например, посредством трансфекции, трансдукции, инфекции) люциферазные репортеры, функционально связанные с промоторными последовательностями основных генов часов (например, Per1, Per2, Cry1, Cry2 или Bmal1), и измеряют люминесценцию (или экспрессию под контролем генов часов) в зависимости от времени. Конкретно определяют период, амплитуду и фазу люминесценции по сравнению с ожидаемой экспрессией, коррелирующей с циркадным ритмом. Значение EC50 соединения можно рассчитывать легкодоступными специалисту в данной области способами. Пример такого анализа описан в настоящем документе в примере 3. Значения EC50 пригодны для оценки активности соединений по настоящему изобретению.
В другом аспекте соединения по настоящему изобретению с увеличенной эффективностью можно определять посредством анализа in vivo. Соединения вводят индивидууму (например, модель на мышах) в течение определенного периода времени. Выделяют биологический образец, полученный у индивидуума, и определяют уровни концентрации соединения, присутствующие в биологическом образце. Биологический образец представляет собой, например, цельную кровь или любую ее фракцию (например, сыворотку или плазму), или ткань, такую как ткань, которая поражена опосредуемым Cry заболеванием или нарушением. Концентрацию, определяемую в образце обрабатываемых индивидуумов, сравнивают со значением концентрации EC50 того же соединения, тестируемой в соответствующем анализе in vitro (как описано выше и в примере 3). Соединения с измеренной концентрацией соединения in vivo, превышающей определенное значение EC50, являются предпочтительными соединениями по настоящему изобретению. Эти предпочтительные соединения могут демонстрировать повышенную эффективность при лечении или облегчении симптомов опосредуемых Cry заболеваний или нарушений.
В других аспектах объекта изобретения, описываемого в настоящем документе, предоставлена фармацевтическая композиция, содержащая соединение по формуле I и фармацевтически приемлемый носитель, вспомогательное средство или разбавитель. Способы получения различных фармацевтических композиций с указанным количеством активного соединения известны или очевидны специалистам в данной области. Кроме того, специалисты в данной области хорошо знакомы со способами составления или введения. Такие темы описаны, например, в "The Pharmaceutical Basis of Therapeutics" Goodman и Gilman, текущее издание, Pergamon Press; и "Remington's Pharmaceutical Sciences", текущее издание, Mack Publishing, Co., Easton, PA. Эти способы можно использовать в соответствующих аспектах и вариантах осуществления способов и композиций, описываемых в настоящем документе. Фармацевтические композиции предпочтительно производят в условиях GMP. Приводимые ниже примеры предоставлены исключительно с иллюстративными целями и не предназначены для того, чтобы служить в качестве ограничений настоящего изобретения.
Так как соединения, описываемые в настоящем документе, предназначены для применения в фармацевтических композициях, легко понять, что каждое из них предоставлено по существу в очищенной форме, например, по меньшей мере на 50% чистой, по меньшей мере на 55% чистой, по меньшей мере на 60% чистой, по меньшей мере на 65% чистой, по меньшей мере на 70% чистой, по меньшей мере на 75% чистой, по меньшей мере на 80% чистой, по меньшей мере на 85%, по меньшей мере на 90% чистой, по меньшей мере на 95% чистой, по меньшей мере на 96% чистой, по меньшей мере на 97% чистой, по меньшей мере на 98% чистой, или по меньшей мере на 99% чистой. Проценты в настоящем документе предоставлены на основе отношения массы к массе. Неочищенные препараты соединений можно использовать для получения более чистых форм, используемых в фармацевтических композициях; эти менее чистые препараты соединений должны содержать по меньшей мере 1%, более удовлетворительно по меньшей мере 5%, например, от 10 до 49% соединения формулы I.
Соединения формулы I можно предоставлять в подходящих местных, пероральных, назальных, офтальмологических, мукозальных, ректальных, вагинальных и парентеральных фармацевтических составах для применения при лечении опосредованных Cry заболеваний. Соединения по настоящему изобретению можно вводить перорально в виде таблеток или капсул, в виде масляных или водных суспензий, таблеток-леденцов, пастилок, порошков, гранул, эмульсий, сиропов или эликсиров. Композиции для перорального применения могут включать одно или несколько средств для ароматизации, подслащивания, придания цвета и предохранения для получения фармацевтически приемлемых и приятных на вкус препаратов. Таблетки могут содержать фармацевтически приемлемые эксципиенты, носители, разбавители и вспомогательные средства для помощи в производстве таких таблеток. Как общепринято в данной области, эти таблетки можно покрывать фармацевтически приемлемым растворяющимся в кишечнике покрытием, таким как глицерилмоностеарат или глицерилдистеарат, для замедления дезинтеграции и всасывания в желудочно-кишечном тракте с обеспечением длительного действие в течение долгосрочного периода. Скорость растворения плохо растворимых в воде соединений можно увеличивать посредством использования высушенных распылением дисперсий, таких как дисперсии, описанные в Takeuchi, H. et al. J. Pharm. Pharmacol. 1987, 39, 769-773.
Составы для перорального применения могут находиться в форме твердых желатиновых капсул, где активный ингредиент смешивают с твердым инертным разбавителем, например, карбонатом кальция, фосфатом кальция или каолином. Они также могут находиться в форме мягких желатиновых капсул, где активный ингредиент смешивают с водной или масляной средой, такой как арахисовое масло, парафиновое масло или оливковое масло.
Водные суспензии в норме содержат активные ингредиенты в смеси с эксципиентами, подходящими для получения водной суспензии. Такие эксципиенты могут представлять собой суспендирующие средства, такие как коллифор, карбоксиметилцеллюлоза натрия, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, камедь трагакант и гуммиарабик; диспергирующее средство или средство для смачивания, которое может представлять собой природный фосфолипид, такой как лецитин, продукт конденсации этиленоксида и длинноцепочечной жирной кислоты, например, полиоксиэтиленстеарат, продукт конденсации этиленоксида и длинноцепочечного алифатического спирта, такой как гептадекаэтиленоксицетанол, продукт конденсации этиленоксида и сложного эфира, получаемого из жирной кислоты и гексита, такой как полиоксиэтиленсорбитмоноолеат или ангидриды жирных кислот и гекситов, такие как полиоксиэтиленсорбитанмоноолеат.
Фармацевтические композиции могут находиться в форме стерильных инъецируемых водных или масляных суспензий. Эту суспензию можно формулировать известными способами в виде водных изотонических растворов или суспензий, а из жировых эмульсий или суспензий можно получать суппозитории. Композиции можно стерилизовать, и/или они могут содержать вспомогательные средства, такие как консерванты, стабилизаторы, увлажнители или эмульгаторы, ускорители растворения, соли для регуляции осмотического давления и/или буферы. Кроме того, они также могут содержать другие терапевтически значимые вещества. Стерильный инъецируемый препарат также можно формулировать в виде суспензии в нетоксическом приемлемом для парентерального применения разбавителе или растворителе, например, в виде раствора в 1,3-бутандиоле. В ряду приемлемых носителей и растворителей, которые можно применять, находятся вода, раствор Рингера и изотонический раствор хлорида натрия. Для этой цели можно использовать любое безвкусное жирное масло, включая синтетические моно- или диглицериды. Кроме того, при получении инъецируемых препаратов находят применение жирные кислоты, такие как олеиновая кислота.
Соединения формулы I также можно вводить в форме суппозиториев для ректального введения лекарственных средств. Эти композиции можно получать посредством смешивания лекарственного средства с подходящим нераздражающим эксципиентом, который является твердым приблизительно при 25°C, но жидким при ректальной температуре и, таким образом, плавится в прямой кишке с высвобождением лекарственного средства. Такие материалы включают масло какао и другие глицериды.
Для препаратов для местного или трансдермального применения, например, кремов, мазей, желе, применяют растворы или суспензии, содержащие соединения по настоящему изобретению. Подходящие составы для трансдермальных применений содержат эффективное количество соединения по настоящему изобретению с носителем. Носитель может включать впитываемые фармакологически приемлемые растворители для помощи в прохождении через кожу хозяина. Например, трансдермальные устройства существуют в форме повязки, содержащей поддерживающий элемент, резервуар, содержащий соединение, необязательно с носителями, необязательно с контролирующим скорость барьером для доставки соединения на кожу хозяина с контролируемой и предопределенной скоростью в течение длительного периода времени, и средства для закрепления устройства на коже. Также можно использовать матриксные трансдермальные составы и устройства для ионтофореза. Подходящие составы для местного применения, например, для кожи и глаз, предпочтительно представляют собой водные растворы, мази, кремы или гели, хорошо известные в данной области. Они могут содержать солюбилизаторы, стабилизаторы, средства увеличения тоничности, буферы и консерванты.
Активные соединения можно получать с фармацевтически приемлемыми носителями, которые защищают соединение от быстрого выведения из организма, такими как состав с контролируемым высвобождением, включая имплантаты и микроинкапсулированные системы доставки. Можно использовать биоразлагаемые, биосовместимые полимеры, такие как этиленвинилацетат, полиангидриды, полигликолевая кислота, коллаген, полиортоэфиры и полимолочная кислота. Способы получения таких составов известны специалистам в данной области.
Соединения формулы I также можно получать в форме липосомных систем доставки, таких как малые однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы можно формировать из ряда фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолин.
Подходящей формой продленного высвобождения любого из активных фармацевтических ингредиентов или их совместного высвобождения может представлять собой содержащая матрикс таблетированная или капсулированная композиция. Подходящие формирующие матрикс материалы включают, например, воска (например, карнаубский воск, пчелиный воск, парафиновый воск, церезин, шеллачный воск, жирные кислоты и жирные спирты), масла, гидрогенизированные масла или жиры (например, гидрогенезированное рапсовое масло, касторовое масло, говяжье сало, пальмовое масло и соевое масло) и полимеры (например, гидроксипропилцеллюлоза, поливинилпирролидон, гидроксипропилметилцеллюлоза и полиэтиленгликоль). Другие подходящие матриксные таблетирующие материалы представляют собой микрокристаллическую целлюлозу, порошковую целлюлозу, гидроксипропилцеллюлозу, этилцеллюлозу с другими носителями и наполнителями. Таблетки также могут содержать грануляты, порошки с покрытием или окатыши. Таблетки также могут являться многослойными. Многослойные таблетки являются особенно предпочтительными, когда у активных ингредиентов существует значительно отличающиеся фармакокинетические профили. Необязательно, готовая таблетка может содержать покрытие или не содержать покрытия.
Как правило, покрывающая композиция содержит нерастворимый мактриксный полимер (приблизительно 15-85% по массе покрывающей композиции) и водорастворимый материал (например, приблизительно 15-85% по массе покрывающей композиции). Необязательно можно использовать или включать растворимый в кишечнике полимер (приблизительно от 1 до 99% по массе покрывающей композиции). Подходящие водорастворимые материалы включают полимеры, такие как полиэтиленгликоль, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, поливинилпирролидон, поливиниловый спирт, и мономерные материалы, такие как сахара (например, лактоза, сахароза, фруктоза, маннит и т.п.), соли (например, хлорид натрия, хлорид калия и т.п.), органические кислоты (например, фумаровая кислота, янтарная кислота, молочная кислота и винная кислота) и их смеси. Подходящие растворимые в кишечнике полимеры включают гидроксипропилметилцеллюлозу, ацетатсукцинат, гидроксипропилметилцеллюлозу, фталат, фталат поливинилацетата, ацетатфталат целлюлозы, тримеллитат ацетилцеллюлозы, шеллак, зеин и полиметакрилаты, содержащие карбоксильные группы.
Покрывающую композицию можно пластифицировать в соответствии со свойствами покрывающей смеси, такими как температура стеклования основного компонента или смеси компонента или растворителя, используемой для нанесения покрывающих композиций. Подходящие пластификаторы можно добавлять в количестве от 0 до 50% по массе покрывающей композиции, и они включают, например, диэтилфталат, сложные цитратные эфиры, полиэтиленгликоль, глицерин, ацетилированные глицериды, ацетилированные цитратные сложные эфиры, дибутилсебацинат и касторовое масло. При желании, покрывающая композиция может содержать наполнитель. Количество наполнителя может составлять от 1% до приблизительно 99% по массе от общей массы покрывающей композиции и может представлять собой нерастворимый материал, такой как диоксид кремния, диоксид титана, тальк, каолин, оксид алюминия, крахмал, порошковую целлюлозу, MCC, или полакрилин калия. Покрывающую композицию можно наносить в виде раствора или латекса в органических растворителях или водных растворителях или их смесях. Если наносят растворы, растворитель может присутствовать в количествах приблизительно 25-99% по массе от общей массы растворенных твердых веществ. Подходящие растворители представляют собой воду, низшие спирты, низшие хлорированные углеводороды, кетоны или их смеси. Если наносят латексы, растворитель присутствует в количествах приблизительно 25-97% по массе от количества полимерного материала в латексе. Растворитель преимущественно может представлять собой воду.
Уровни дозирования соединений по настоящему изобретению составляют порядка приблизительно от 0,5 мг/кг массы тела до приблизительно 100 мг/кг массы тела или любое приращение между ними. Предпочтительная дозировка представляет собой приблизительно от 30 мг/кг массы тела до приблизительно 100 мг/кг массы тела. Общую суточную дозу можно вводить в одной или дробных дозах. Подходящие терапевтические дозы соединений формулы I могут находиться в диапазоне от 1 микрограмма (мкг) до 1000 миллиграммов (мг) на килограмм массы тела реципиента в сутки и составлять любое приращение между ними, такое как, например, 1, 2, 3, 5, 10, 25, 50, 75, 100, 200, 300, 400, 500, 600, 700, 800, 900 или 1000 мкг (1 мг); 2, 3, 5, 10, 25, 50, 75, 100, 200, 300, 400, 500, 600, 700, 800, 900 или 1000 мг. Однако следует понимать, что конкретный уровень дозирования для любого конкретного пациента зависит от ряда факторов, включая активность конкретного вводимого соединения, возраст, массу тела, общее состояние здоровья, пол, диету, время введения, маршрут введения, скорость выведения, комбинацию лекарственных средств и тяжесть конкретного заболевания, подвергаемого лечению.
Для обеспечения оптимального желаемого ответа можно регулировать режимы дозирования. Например, можно вводить одну разовую дозу, можно вводить несколько дробных доз в течение определенного периода времени или дозу можно пропорционально снижать или повышать в зависимости от требований терапевтического момента. Для простоты введения и постоянства дозирования особенно предпочтительно формулировать парентеральные композиции в стандартной лекарственной форме. Как используют в настоящем документе, стандартная лекарственная форма относится к физически дискретным единицам, подходящим в качестве единичных доз для являющихся млекопитающими индивидуумов, подвергаемых лечению; где каждая единица содержит предопределенное количество активного соединения, которое по расчетам обеспечивает желаемое терапевтическое действие, в ассоциации с требуемым фармацевтическим носителем. Характеристики стандартных лекарственных форм по изобретению продиктованы и напрямую зависят от (a) уникальных характеристик терапевтического средства и конкретного терапевтического или профилактического действия, которое необходимо достигнуть, и (b) ограничений, свойственных области составления, таких активных соединений для лечения чувствительности у индивидуумов. Таким образом, специалист в данной области, на основе приведенного в настоящем документе описания, может понять, что дозу и режим дозирования регулируют хорошо известными в терапевтической области способами. Т.е., как возможные временные требования для введения каждого средства для обеспечения детектируемого положительного терапевтического действия на пациента можно легко установить максимальную переносимую дозу, а также можно определить эффективное количество, обеспечивающее детектируемое положительное терапевтическое действие на пациента. Таким образом, хотя в настоящем документе проиллюстрированы конкретные режимы дозирования и введения, эти примеры никаким образом не ограничивают режимы дозирования и введения, которые можно предоставлять для пациента в практическом осуществлении настоящего изобретения.
В определенных вариантах осуществления соединения и композиции, описываемые в настоящем документе, вводят индивидууму приблизительно перед временем отхода ко сну или во время сна ночью. Предпочтительно, соединения и композиции, описываем в настоящем документе, вводят индивидууму в пределах 6 часов, 5 часов, 4 часов, 3 часов, 120 минут, 90 минут, 60 минут, 45 минут, 30 минут, 25 минут, 20 минут, 15 минут, 10 минут, 5 минут или непосредственно перед или после времени отхода ко сну. Предпочтительно, соединения и композиции по настоящему изобретению вводят индивидууму в пределах от 2 часов до момента непосредственно перед временем отхода ко сну. Как используют в настоящем документе, "время отхода ко сну" относится к времени ночи, когда индивидуум ложится с намерением отдохнуть или уснуть.
В других вариантах осуществления соединения и композиции, описываемые в настоящем документе, можно вводить с пищей или без. Когда соединения или композиции вводят с пищей, предпочтительным может являться вводить соединения или композиции в пределах 4 часов перед или после приемом пищи, таким как завтрак, обед, ужин или полдник. Например, соединения или композиции по настоящему изобретению вводят в пределах 6 часов, в пределах 5 часов, в пределах 4 часов, в пределах 3 часов, в пределах 120 минут, в пределах 90 минут, в пределах 60 минут, в пределах 45 минут, в пределах 30 минут, в пределах 25 минут, в пределах 20 минут, в пределах 15 минут, в пределах 10 минут, в пределах 5 минут или непосредственно перед или после приема пищи. Предпочтительно, соединения и композиции по настоящему изобретению вводят индивидууму в пределах 4 часов, в пределах 3 часов, в пределах 120 минут, в пределах 90 минут или в пределах 60 минут после ужина.
В другом аспекте объекта изобретения, описываемого в настоящем документе, предоставлен способ лечения опосредуемого Cry заболевания или нарушения, включающий введение терапевтически эффективного количества соединения по формуле I, как описано в любом из приведенных ранее в настоящем документе вариантов осуществления. Предпочтительным вариантом осуществления настоящего изобретения является способ лечения опосредуемого Cry заболевания или нарушения, где заболевание или нарушение, характеризующиеся аномальными уровнями Cry, выбраны из группы, состоящей из диабета, осложнений, ассоциированных с диабетом, метаболического синдрома, синдрома резистентности к инсулину, ожирения, глаукомы, синдрома Иценко-Кушинга, воспалительных нарушений, митохондриальных нарушения, атаксии Фридрейха, психотической депрессии, болезни Альцгеймера, нейропатической боли, лекарственной зависимости, остеопороза, злокачественной опухоли, дегенерации желтого пятна и миопатии. Особенно предпочтительные опосредованные Cry заболевания или нарушения, подвергаемые лечению соединениями, описываемыми в настоящем документе, включают диабет, осложнения диабета, такие как диабетическая нейропатия, диабетическая ретинопатия, диабетическая нефропатия, формирование катаракты, глаукома, диабетическая ангиопатия, атеросклероз; неалкогольный стеатогепатит (NASH); неалкогольную жировую болезнь печени (NAFLD); астму и хроническое обструктивное заболевание легких (COPD).
Как используют в настоящем документе, термины "вводить", "введение" и т.п. относятся к способам, которые можно использовать для обеспечения доставки соединений или композиции в желаемый участок биологического действия. Эти способы в качестве неограничивающих примеров включают пероральное, парентеральное, местное, мукозальное, глазное, офтальмологическое, вагинальное и ректальное введение. Специалисты в данной области хорошо знакомы со способами введения, которые можно использовать для соединений и способов, описываемых в настоящем документе, например, как описано в Goodman and Gilman, The Pharmacological Basis of Therapeutics, current ed.; Pergamon; and Remington's, Pharmaceutical Sciences (текущее издание), Mack Publishing Co., Easton, Pa. Как используют в настоящем документе, "парентеральное введение" фармацевтической композиции включает любой маршрут введения, характеризуемый физическим разрушением ткани индивидуума и введением фармацевтической композиции через разрушенную ткань. Таким образом, парентеральное введение в качестве неограничивающих примеров включает введение фармацевтической композиции посредством инъекции композиции, посредством введения композиции через хирургический разрез, посредством введения композиции через проникающую в ткань нехирургическую рану и т.п. В частности, парентеральное введение предусмотрено для включения в качестве неограничивающих примеров подкожной, интраперитонеальной, внутримышечной и внутригрудинной инъекции и способов почечной диализной инфузии.
"Индивидуум" в контексте настоящего изобретения предпочтительно представляет собой млекопитающее. Млекопитающее может представлять собой человека, не являющегося человеком примата, мышь, крысу, собаку, кошку, лошадь или корову, но не ограничено этими примерами. Млекопитающие, отличающиеся от людей, преимущественно можно использовать в качестве индивидуумов, которые представляют собой модели опосредуемого Cry заболевания или нарушения на животных, такие как мыши ob/ob. Индивидуум может быть мужского или женского пола. Индивидуум может представлять собой индивидуума, которого ранее диагностировали или идентифицировали как страдающего опосредуемым Cry заболеванием или нарушением, и который необязательно уже проходил или проходит терапевтические мероприятия или лечение этого заболевания или нарушения. Альтернативно, индивидуум также может представлять собой индивидуума, которого ранее не диагностировали как страдающего опосредуемым Cry заболеванием или нарушением. Например, индивидуум может представлять собой индивидуума, подверженного одному или нескольким факторам риска опосредуемого Cry заболевания или нарушения, или индивидуума, который не подвержен факторам риска опосредуемого Cry заболевания или нарушения, или индивидуума, у которого не выявляют симптомов опосредуемого Cry заболевания или нарушения. Также индивидуум может представлять собой индивидуума, страдающего или подверженного риску развития опосредуемого Cry заболевания или нарушения или страдающего или подверженного риску развития рецидива опосредуемого Cry заболевания или нарушения. Также индивидуум может представлять собой индивидуума, которого ранее лечили от опосредуемого Cry заболевания или нарушения, посредством введения соединений и композиций, описываемых в настоящем документе, отдельно или в комбинации с другими терапевтическими средствами, хирургическим вмешательством или посредством любой комбинация из указанных выше. Как используют в настоящем документе, термин "индивидуум" и "пациент" можно использовать взаимозаменяемо.
"Опосредуемое Cry заболевание или нарушение" в качестве неограничивающих примеров может включать диабет (включая без ограничения инсулинзависимый диабет "I типа", инсулиннезависимый диабет "II типа", гестационный диабет и связанные с диабетом осложнения, такие как диабетическая нейропатия, диабетическая ретинопатия, диабетическая кардиомиопатия, диабетическая нефропатия, пародонтоз и диабетический кетоацидоз), метаболический синдром, синдром резистентности к инсулину, ожирение, глаукома, синдром Иценко-Кушинга, психотическую депрессию, болезнь Альцгеймера, нейропатическую боль, лекарственную зависимость, остеопороз, злокачественную опухоль, дегенерацию желтого пятна и миопатию.
Как используют в настоящем документе, термины "лечение", "лечить" или "обработка" включают профилактическое (например, профилактическое), паллиативное, вспомогательное лечение и лечение при заболевании. Например, как используют в настоящем документе, лечение диабета 2 типа означает, что пациента с диабетом 2 типа или с риском наличия диабета 2 типа можно лечить способами, описываемыми в настоящем документе. Для пациентов, проходящих профилактическое лечение, измеримым результатом профилактического лечения является итоговое снижение частоты случаев заболевания, подвергаемого профилактическому лечению.
Как используют в настоящем документе, термин "облегчение" или "облегчать" описывает процесс, посредством которого происходит снижение, уменьшение или подавление тяжести признака или симптома нарушения. Важно, что симптом можно облегчать без устранения. В предпочтительном варианте осуществления введение фармацевтических композиций по изобретению приводит к устранению симптома, однако устранение не является необходимым. Ожидают, что терапевтически эффективные количества соединений или фармацевтических композиций, описываемых в настоящем документе, снижают тяжесть симптомов.
Как используют в настоящем документе термин "симптом" определен как показатель заболевания, болезни, повреждения или того, что в организме происходит что-либо ненадлежащее. Симптомы ощущает или замечает индивидуум, испытывающий симптомы, но их не так просто могут заметить другие индивидуумы. Другие индивидуумы представляют собой профессиональных работников медобеспечения или клиницистов.
Как используют в настоящем документе, термин "метаболический синдром", если не указано иначе, означает псориаз, сахарный диабет, заживление ран, воспаление, нейродегенеративные заболевания, галактоземию, болезнь кленового сиропа, фенилкетонурию, гиперсаркозинемию, тиминурацилурию, сульфинурию, изовалериановую ацидемию, сахаропуринурию, 4-гидроксимасляную ацидурию, недостаточность глюкозо-6-фосфатдегидрогеназы и недостаточность пируватдегидрогеназы.
Как используют в настоящем документе, термин "ожирение" или "тучность", как правило, относится к индивидуумам, с массой, по меньшей мере приблизительно на 20-30% превышающей среднюю массу для их возраста, пола и роста. Технически, "тучность" определяют для мужчин, как индивидуумов, индекс массы тела которых составляет более 27,8 кг/м2, а для женщин, как индивидуумов, индекс массы тела которых составляет более 27,3 кг/м2. Специалисты в данной области легко поймут, что способ по изобретению не ограничен индивидуумами, попадающими в пределы указанных выше критериев. Фактически, способ по изобретению также можно преимущественно практиковать у индивидуумов, которые не попадают в эти традиционные критерии, например, у индивидуумов, которые могут быть предрасположены к ожирению.
Как используют в настоящем документе, термин "воспалительные нарушения" относится к таким нарушениям, как астма, хроническое обструктивное заболевание легких (COPD), ревматоидный артрит, анкилозирующий спондилит, псориатический артрит, псориаз, хондрокальциноз, подагра, воспалительное заболевание кишечника, язвенный колит, болезнь Крона, фибромиалгия и кахексия.
Как используют в настоящем документе, термин "синдром Иценко-Кушинга" относится к совокупности признаков и симптомов, являющихся результатом длительного воздействия повышенных уровней кортизола. Синдром Иценко-Кушинга может являться результатом эндогенных или экзогенных причин. Причины эндогенного синдрома Иценко-Кушинга включают опухоли гипофиза (также называемые болезнью Кушинга), опухоли надпочечников и эктопическую секрецию адренокортикотропного гормона (АКТГ) и/или кортикотропин-высвобождающего гормона (CRH) у других опухолей (включая в качестве неограничивающих примеров, мелкоклеточный рак легких). Экзогенный (или ятрогенный) синдром Иценко-Кушинга является результатом использования кортикостероидов для лечения ряда нарушений, включая воспалительные нарушения, включая в качестве неограничивающих примеров астму, псориаз и ревматоидный артрит.
Как используют в настоящем документе, термин "митохондриальные заболевания" относится к таким заболеваниям, как митохондриальная энцефаломиопатия, лактоацидоз и подобные инсультам эпизоды (MELAS), миоклоническая эпилепсия с разорванными красными волокнами (MERRF), синдром Кирнса-Сейра, хроническая прогрессирующая наружная офтальмоплегия, врожденная оптическая нейропатия Лебера, синдром Лейга, диабет, глухота, нейрогенная мышечная слабость, атаксия и пигментный ретинит (NARP) и мионейрогенная желудочно-кишечная энцефалопатия.
Как используют в настоящем документе, термин "злокачественная опухоль" относится к нарушениям и заболеваниям, характеризуемым неконтролируемым клеточным ростом и/или пролиферацией, и включает доброкачественные и злокачественные опухоли, гипопролиферативные нарушения и заболевания и метастазы. Примеры особенно предпочтительных злокачественных опухолей включают солидные злокачественные опухоли или эпителиальные злокачественные опухоли, включая в качестве неограничивающих примеров: рак легких; рак головного мозга; рак поджелудочной железы; рак головы и шеи (например, плоскоклеточную карциному); рак молочной железы; колоректальный рак; рак печени; рак желудка; рак почки; рак яичника; рак предстательной железы или аденокарциному. Другие злокачественные опухоли представляют собой опухоли с увеличенной экспрессией VEGF, увеличенным ангиогенезом или гипоксические опухоли.
Как используют в настоящем документе, фраза "терапевтически эффективное количество" относится к количеству лекарственного средства или фармацевтического средства, которое вызывает биологический или медицинский ответ в ткани, в системе, у животного или человека, который стремился получить исследователь, ветеринар, лечащий врач или другой индивидуум.
Как используют в настоящем документе, фраза "количеств, эффективное для снижения уровней глюкозы в крови" относится к уровням соединения, достаточным для обеспечения циркулирующих концентраций, достаточно высоких для осуществления желаемого действия. Как правило, такие концентрации находятся в диапазоне приблизительно от 10 нМ до 2 мкМ; где предпочтительными являются концентрации в диапазоне приблизительно от 100 нМ до 500 нМ. Как указано ранее, так как активность различных соединений, которые находятся в пределах определения формулы I, как указано выше, может значительно варьировать, и так как у разных индивидуумов могут существовать значительные колебания тяжести симптомов, определение ответа индивидуума на лечение и соответствующее варьирование дозировок находится на усмотрении практикующего врача.
Как используют в настоящем документе, фраза "резистентность к инсулину" относится к сниженной чувствительности к действию инсулина во всем организме или конкретных тканях, таких как ткань скелетных мышц, ткань миокарда, жировая ткань или ткань печени. Резистентность к инсулину встречается у множества индивидуумов с сахарным диабетом и без него.
Как используют в настоящем документе, фраза "синдром резистентности к инсулину" относится к группе проявлений, которые включают резистентность к инсулину, гиперинсулинемию, инсулиннезависимый сахарный диабет (NIDDM), артериальную гипертензию, центральное (висцеральное) ожирение и дислипидемию.
Соединения по настоящему изобретению также могут быть пригодными при лечении других нарушений обмена веществ, ассоциированных с нарушенными утилизацией глюкозы и резистентностью к инсулину, включая основные осложнения NIDDM на поздних стадиях, такие как диабетическая ангиопатия, атеросклероз, неалкогольный стеатогепатит (NASH), неалкогольная жировая болезнь печени (NAFLD), диабетическая нефропатия, диабетическая нейропатия и диабетические офтальмологические осложнения, такие как ретинопатия, формирование катаракты и глаукома, и многие другие осложнения, связанные с NIDDM, включая дислипидемию, индуцированную глюкокортикоидами резистентность к инсулину, синдром поликистоза яичников, ожирение, гипергликемию, гиперлипидемию, гиперхолестеринемию, гипертриглицеридемию, гиперинсулинемию и гипертензию. Краткие описания этих состояний доступны в любом медицинском словаре, например, "Stedman's Medical Dictionary" (Xth Ed.).
Соединения и композиции, описываемые в настоящем документе, можно вводить в терапевтически эффективных количествах в комбинации с одним или несколькими дополнительными терапевтическими средствами, как определено в настоящем документе. Например, может происходить синергическое действие с другими веществами, используемыми при лечении опосредованных Cry заболеваний или нарушений. Когда соединения по изобретению вводят в сочетании с другими терапевтическими средствами, дозы совместно вводимых соединений, конечно же варьируют в зависимости от типа совместно применяемого лекарственного средства, от конкретного применяемого лекарственного средства, от состояния, подвергаемого лечению, и т.д.
Как используют в настоящем документе, термины "комбинированное лечение", "комбинированная терапия", "комбинированная обработка" или "комбинаторное лечение", используемые взаимозаменяемо, относятся к лечению индивидуума по меньшей мере двумя различными терапевтическими средствами. Как используют в настоящем документе, термины "совместное введение" или "комбинированное введение" или т.п. предназначены для включения введение выбранных терапевтических средств одному индивидууму и предназначены для включения схем дозирования, в которых средства не обязательно вводят одним и тем же маршрутом введения или одновременно. Комбинированное лечение, описываемое в настоящем документе, предназначено для обеспечения положительного воздействия на основе совместного действия соединений и композиций, описываемых в настоящем документе, и одного или нескольких дополнительных терапевтических средств. Положительное воздействие комбинации в качестве неограничивающих примеров включает фармакокинетическое или фармакодинамическое совместное действие, являющееся результатом комбинации соединений, описываемых в настоящем документе, и терапевтических средств. Введение этих терапевтических средств в комбинации, как правило, проводят в течение определенного периода времени (как правило, минут, часов, суток или недель в зависимости от выбранной комбинации). В определенных вариантах осуществления соединения по настоящему изобретению вводят в комбинации с одним или несколькими дополнительными терапевтическими средствами одновременно или последовательно. При одновременном введении соединение(я) по настоящему изобретению можно вводить, например, в той же капсуле, что и дополнительное терапевтическое средство. Альтернативно, соединение по настоящему изобретению и дополнительное терапевтическое средство содержатся в раздельных композициях (например, капсулах), которые предназначены для одновременного введения. При последовательном введении соединение(я) по настоящему изобретению можно вводить до или после введения дополнительного терапевтического средства. Термин "фармацевтическая комбинация" означает продукт, который является результатом смешивания или комбинирования более одного активного ингредиента и включает фиксированные и нефиксированные комбинации активных ингредиентов. "Фиксированная комбинация" означает, что активные ингредиенты, например, соединение, как описано в настоящем документе, и дополнительное терапевтическое средство, вводят пациенту одновременно в форме единого целого или дозы. "Нефиксированная комбинация" означает, что активные ингредиенты, например, соединение, как описано в настоящем документе, и дополнительное терапевтическое средство, вводят пациенту в виде раздельных единиц параллельно, одновременно или последовательно без конкретных временных пределов, где такое введение обеспечивает терапевтически эффективные уровни 2 соединений в организме пациента. Последнее также применимо к смешанной терапии, например, введению 3 или более активных ингредиентов.
Терапевтические средства для лечения диабета, метаболического синдрома, ожирения, синдрома резистентности к инсулину, осложнений диабета или злокачественной опухоли в качестве неограничивающих примеров включают следующее: инсулин, гипогликемические средства, противодиабетические средства, противовоспалительные средства, восстановители липидов, антигипертензивные средства, такие как блокаторы кальциевых каналов, блокаторы β-адренергических рецепторов, ингибиторы циклооксигеназы-2, ингибиторы ангиотензиновой системы, ингибиторы АПФ, ингибиторы ренина, химиотерапевтические средства, лучевую терапию, модулирующие гормоны средства, иммуномодулирующие средства, антиангиогенные средства вместе с другими общими модификаторами факторов риска.
Инсулин включает быстродействующие формы, такие как инсулин лизпро, получаемый из рДНК: хумалог (1,5 мл, 10 мл, Eli Lilly and Company, Indianapolis, Ind.), инъекцию инсулина (инсулин регуляр) коровы и свиньи (илетин I регуляр, Eli Lilly], человека: рДНК: хумулин R (Eli Lilly), новолин R (Novo Nordisk), полусинтетический: велосулин человека (Novo Nordisk), рДНК человека, буферизованный: велосулин BR, свиной: инсулин регуляр (Novo Nordisk), очищенный свиной: Pork Regular ILETIN II (Eli Lilly), инсулин регуляр очищенный свиной (Novo Nordisk) и регуляр (концентрированный) илетин II U-500 (500 единиц/мл, Eli Lilly); промежуточно действующие формы, такие как суспензия коровьего и свиного инсулина с цинком,: илетин ленте G I (Eli Lilly), человека, рДНК: хумулин L (Eli Lilly), новолин L (Novo Nordisk), очищенный свиной: илетин ленте II (Eli Lilly), суспензия инсулина изофана (NPH): коровьего и свиного: илетин NPH I (Eli Lilly), человека, рДНК: хумулин N (Eli Lilly), новолин N (Novo Nordisk), очищенный свиной: свиной илетин NPH II (Eli Lilly), NPH-N (Novo Nordisk) и длительно действующие формы, такие как суспензия инсулина с цинком, длительного действия (ультраленте, Eli Lilly), человека, рДНК: хумулин U (Eli Lilly).
Гипогликемические средства в качестве неограничивающих примеров включают сульфонилкарбамиды: ацетогексамид (димелор), хлорпропамид (диабинез), толбутамид (ориназа); сульфонилкарбамиды второго поколения: глипизид (глюкотрол, глюкотрол XL), глибурид (диабета; микроназа; глиназа), глимепирид (амарил); бигуаниды: метформин (глюкофаж); ингибиторы α-глюкозидазы: акарбоза (прекоза), миглитол (глисет), тиазолидиндионы: росиглитазон (авандия), пиоглитазон (актос), троглитазон (резулин); меглитиниды: репаглинид (прандин) и другие гипогликемические средства, такие как акарбоза; буформин; гидрохлорид бутоксамина; камиглибоза; циглитазон; энглитазон натрия; дарглитазон натрия; гидрохлорид этоформина; глиамилид; глибомурид; глицетанил гликлазид натрия; глифлумид; глюкагон; глигексамид; глимидин натрия; глиоктамид; глипарамид; линоглирид; фумарат линоглирида; метилпальмоксират; пальмоксират натрия; тартрат пироглирида; проинсулин человека; ацетат сеглитида; толазамид; толпирамид; зополрестат.
Противодиабетические средства в качестве неограничивающих примеров включают ингибиторы дипептидилпептидазы IV, такие как ситаглиптин, алоглиптин, вилдаглиптин, саксаглиптин, линаглиптин, анаглиптин, тенелиглиптин, гемиглиптин, дутоглиптин или любые другие глиптины, находящиеся в настоящее время в разработке, берберин и лупеол; и агонисты GLP-1, такие как эксенатид, лираглутид, альбиглютид, таспогенитид и AVE0010.
Противовоспалительные средства включают алклофенак; дипропионат алклометазона; алгестон ацетонид; α-амилаза; амцинафал; амцинафид; амфенак натрия; гидрохлорид амиприлозы; анакинра; аниролак; анитразафен; апазон; двунатриевый балсалазид; бендазак; беноксапрофен; гидрохлорид бензидамина; бромелайн; броперамол; будезонид; карпрофен; циклопрофен; цинтазон; клипрофен; пропионат клобетазола; бутират клоберазона; клопирак; пропионат клотиказона; ацетат корметазона; кортодоксон; дефлазакорт; дезонид; дезоксиметазон; дипропионат дексаметазона; диклофенак калия; натрия диклофенак; диацетат дифлоразона; дифлумидон натрия; дифлунизал; дифлупреднат; дифталон; диметилсульфоксид; дроцинонид; эндризон; энлимомаб; эноликам натрия; эпиризол; этодолак; этофенамат; фелбинак; фенамол; фенбуфен; фенклофенак; фенклорак; фендозал; фенпипалон; фентиазак; флазалон; флуазакорт; флуфенамовую кислоту; флумизол; ацетат флунизолида; флуниксин; флуниксин меглумин; флуокортинбутил; ацетат фторметолона; флукуазон; флурбипрофен; флуретофен; пропионат флутиказона; фурапрофен; фуробуфен; галцинонид; пропионат галобетазола; ацетат галопредона; ибуфенак; ибупрофен; ибупрофен алюминия; ибупрофен пиконол; илонидап; индометацин; индометацин натрия; индопрофен; индоксол; интразол; ацетат изофлупредона; изоксепак; изоксикам; кетопрофен; гидрохлорид лофемизола; лорноксикам; лотепреднол этабонат; меклофенамат натрия; меклофенамовую кислоту; дибутират меклоризона; мефенамовую кислоту; месаламин; мезеклазон; сулептанат метилпреднизолона; морнифлумат; набуметон; напроксен; напроксен натрия; напроксол; нимазон; олсалазин натрия; орготеин; орпаноксин; оксапрозин; оксифенбутазон; гидрохлорид паранилина; полисульфат пентозана натрия; глицерат фенбутазона натрия; пирфенидон; пироксикам; пироксикам циннамат; пироксикам оламин; пипрофен; предназат; прифелон; продоловую кислоту; проквазон; проксазол; цитрат проксазола; римексолон; ромазарит; салколекс; салнацедин; салсалат; салицилаты; хлорид сангвинария; секлазон; серметацин; судоксикам; сулиндак; супрофен; талметацин; талнифлумат; талосалат; тебуфелон; тенидап; тенидап натрия; теноксикам; тезикам; тезимид; тетридамин; тиопинак; пивалат тиксокортола; толметин; толметин натрия; триклонид; трифлумидат; зидометацин; глюкокортикоиды; зомепирак натрия. Важным противовоспалительным средством является аспирин.
Другие противовоспалительные средства представляют собой ингибиторы цитокинов, включая антагонисты цитокинов (например, антагонисты рецепторов IL-6), азаалкиллизофосфолипиды (AALP) и ингибиторы фактора некроза опухоли-α (TNF-α), такие как антитела к TNF-α, растворимый рецептор TNF, TNF-α, антисмысловые молекулы нуклеиновой кислоты, поливалентный гуанилгидразон (CNI-1493), N-ацетилцистеин, пентоксифиллин, окпентифилин, карбоциклические аналоги нуклеозидов, низкомолекулярное соединение S9a, RP 55778 (ингибитор синтеза TNF-α), дексанабинол (HU-211), MDL 201,449A (9-[(1R, 3R)-транс-циклопентан-3-ол]аденин и триходимерол (BMS-182123). Другие ингибиторы TNF-α включают этанерцепт (энбрел, Immunex, Seattle) и инфликсимаб (ремикейд, Centocor, Malvern, Pa.).
Восстановители липидов включают гемфиброзил, холистирамин, колестипол, никотиновую кислоту и ингибиторы HMG-КоА-редуктазы. Ингибиторы HMG-КоА-редуктазы, пригодные для введения или совместного введения с другими средствами по изобретению, в качестве неограничивающих примеров включают симвастатин (патент США № 4444784), ловастатин (патент США № 4231938), правастатин натрия (патент США № 4346227), флувастатин (патент США № 4739073), аторвастатин (патент США № 5273995) и церивастатин.
Блокаторы кальциевых каналов включают дигидропиридины, такие как нифедипин, фенилалкиламины, такие как верапамил, и бензотиазепины, такие как дилтиазем. Другие блокаторы кальциевых каналов в качестве неограничивающих примеров включают амринон, амлодипин, бенциклан, фелодипин, фендилин, флунаризин, исрадипин, никардипин, нимодипин, пергексилен, галлопамил, тиапамил и аналоги тиапамила (такие как 1993RO-11-2933), фенитоин, барбитураты и пептиды динорфин, омега-конотоксин и омега-агатоксин, и т.п. и/или их фармацевтически приемлемые соли.
Средства, блокирующие β-адренергические рецепторы, в качестве неограничивающих примеров включают, атенолол, ацебутолол, алпренолол, бефунолол, бетаксолол, бунитролол, картеолол, целипролол, гедроксалол, инденолол, лабеталол, левобунолол, мепиндолол, метипранол, метиндол, метопролол, метризоранолол, окспренолол, пиндолол, пропранолол, практолол, зоталолнадолол, типренолол, томалолол, тимолол, бупранолол, пенбутолол, тримепранол, 2-(3-(1,1-диметилэтил)-амино-2-гидроксипропокси)-3-пирединкарбонитрил·HCl, 1-бутиламино-3-(2,5-дихлорфенокси)-2-пропанол, 1-изопропиламино-3-(4-(2-циклопропилметоксиэтил)фенокси)-2-пропанол, 3-изопропиламино-1-(7-метилиндан-4-илокси)-2-бутанол, 2-(3-трет-бутиламино-2-гидроксипропилтио)-4-(5-карбамоил-2-тиенил)тиазол, 7-(2-гидрокси-3-трет-бутиламинопропокси)фталид. Указанные выше соединения можно использовать в качестве изомерных смесей или в их соответствующих левовращающих или правовращающих формах.
В данной области известен ряд селективных ингибиторов COX-2, и в качестве неограничивающих примеров они включают ингибиторы COX-2, описанные в патенте США № 5474995; патенте США № 5521213; патенте США № 5536752; патенте США № 5550142; патенте США № 5552422; патенте США № 5604253; патенте США № 5604260; патенте США № 5639780; патенте США № 5677318; патенте США № 5691374; патенте США № 5698584; патенте США № 5710140; патенте США № 5733909; патенте США № 5789413; патенте США № 5817700; патенте США № 5849943; патенте США № 5861419; патенте США № 5922742; патенте США № 5925631 и в патенте США № 5643933. Ряд из указанных выше ингибиторы COX-2 представляют собой пролекарственные средства селективных ингибиторов COX-2, и включают средства, описанные в WO 95/00501, WO 95/18799 и в патенте США № 5474995, выданном 12 декабря 1995 года.
Примеры антагонистов ангиотензина II включают: пептидные соединения (например, саралазин, октапептид [(San1)(Val5)(Ala8)]-ангиотензин-(1-8) и родственные аналоги); N-замещенный имидазол-2-он (патент США № 5087634); производные имидазолацетата, включая 2-N-бутил-4-хлор-1-(2-хлорбензил)имидазол-5-уксусную кислоту (см. Long et al., J. Pharmacol. Exp. Ther. 247(1), 1-7 (1988)); 4,5,6,7-тетрагидро-1H-имидазо[4,5-c]пиридин-6-карбоновую кислоту и аналогичные производные (патент США № 4816463); аналоги N2-тетразол β-глюкуронида (патент США № 5085992); замещенные пирролы, пиразолы и триазолы (патент США № 5081127); фенольные и гетероциклические производные, такие как 1,3-имидазолы (патент США № 5073566); конденсированные с имидазо 7-членные гетероциклы (патент США № 5064825); пептиды (например, патент США № 4772684); антитела к ангиотензину II (например, патент США № 4302386) и аралкилимидазольные соединения, такие как замещенные бифенилметилом имидазолы (например, EP 253310, 20 января 1988 года); ES8891 (N-морфолиноацетил-(1-нафтил)-L-аланил-(4, тиазолил)-L-аланил-(35,45)-4-амино-3-гидрокси-5-циклогексапентаноил-N-гексиламид, Sankyo Company, Ltd., Tokyo, Japan); SKF108566 (E-α-2-[2-бутил-1-(карбоксифенил)метил]-1H-имидазол-5-ил[метилан]-2-тиофенпропионовая кислота, Smith Kline Beecham Pharmaceuticals, Pa.); лозартан (DUP753/MK954, DuPont Merck Pharmaceutical Company); ремикирин (RO42-5892, F. Hoffman LaRoche AG); агонисты A2 (Marion Merrill Dow) и определенные непептидные гетероциклы (G. D. Searle and Company).
Ингибиторы ангиотензинпревращающего фермента (АПФ) включают аминокислоты и их производные, пептиды, включая ди- и трипептиды, и антитела к АПФ? которые препятствуют ренин-ангиотензиновой системе, ингибируя активность АПФ, таким образом, снижая или устраняя формирование повышающего кровяное давление вещества ангиотензина II. Другие ингибиторы АПФ включают ацилмеркапто- и меркаптоалканоилпролины, такие как каптоприл (патент США № 4105776) и зофеноприл (патент США № 4316906), карбоксиалкильные дипептиды, такие как эналаприл (патент США № 4374829), лизиноприл (патент США № 4374829), хинаприл (патент США № 4344949), рамиприл (патент США № 4587258) и периндоприл (патент США № 4508729), миметики карбоксиалкильных дипептидов, такие как цилазаприл (патент США № 4512924) и беназаприл (патент США № 4410520), фосфинилалканоилпролины, такие как фозиноприл (патент США № 4337201) и трандолоприл.
Ингибиторы ренина включают аминокислоты и их производные, пептиды и их производные и антитела к ренину. Другие ингибиторы ренина включают производные мочевины пептидов (патент США № 5116835); аминокислоты, связанные непептидными связями (патент США № 5114937); ди- и трипептидные производные (патент США № 5106835); аминокислоты и их производные (патенты США №№ 5104869 и 5095119); диолсульфонамиды и сульфинилы (патент США № 5098924); модифицированные пептиды (патент США № 5095006); пептидил-β-аминоациламинодиолкарбаматы (патент США № 5089471); пиролимидазолоны (патент США № 5075451); фтор- и хлорстатин или -статон-содержащие пептиды (патент США № 5066643); пептидиламинодиолы (патенты США №№ 5063208 и 4845079); производные N-морфолино (патент США № 5055466); пепстатиновые производные (патент США № 4980283); N-гетероциклические спирты (патент США № 4885292); моноклональные антитела к ренину (патент США № 4780401) и ряд других пептидов и их аналоги (патенты США №№ 5071837, 5064965, 5063207, 5036054, 5036053, 5034512 и 4894437).
Другие терапевтические средства, пригодные при лечении диабета и связанных нарушений, в качестве неограничивающих примеров включают ингибиторы липаз, такие как цетилистат (ATL-962); синтетические аналоги амилина, такие как симлин прамлинтид с рекомбинантным лептином или без; ингибиторы контранспортера натрия-глюкозы 2 (SGLT2), такие как серглифлозин (869682; KGT-1251), YM543, канаглифлозин, эртуглифлозин, дапаглифлозин, молекула GlaxoSmithKline 189075 и молекула Sanofi-Aventis AVE2268; двойные активаторы адипозотриглицеридлипазы и PI3-киназы, такие как адивиа (ID 1101); антагонисты рецепторов нейропептидов Y2, Y4 и Y5, такие как молекула Nastech PYY3-36, синтетические аналоги гормонов человека PYY3-36 и панкреатического полипептида (молекула 7TM TM30338); молекула Shionogi S-2367; антагонисты каннабиноидного рецептора CB1, такие как римонабант (акомпила), таранабант, CP-945598, молекула Solvay SLV319, молекула Vernalis V24343; гормоны, такие как олеоилэстрон; ингибиторы серотонина, дофамина и норадреналина (также известные в данной области как тройные ингибиторы обратного захвата моноаминов), такие как тезофензин (молекула Neurosearch NS2330); ингибиторы обратного захвата норадреналина и дофамина, такие как контрав (бупропион плюс антагонист опиоидов налтрексон) и экскалиа (бупропион плюс противосудорожное средство зонисамид); ингибиторы 11β-гидроксистероиддегидрогеназы типа 1 (11b-HSD1), такие как молекула Incyte INCB13739; ингибиторы синтеза кортизола, такие как кетоконазол (молекула DiObex DIO-902); ингибиторы глюконеогенеза, такие как молекула Metabasis/Daiichi CS-917; активаторы глюкокиназы, такие как молекула Roche R1440; антисмысловые ингибиторы тирозинфосфатазы белков 1B, такие как ISIS 113715; а также другие средства, такие как молекула NicOx NCX 4016; инъекции аналогов гастрина и эпидермального фактора роста (EGF), такие как Islet Neogenesis Therapy (E1-I.N.T.); бетагистин (молекула Obecure OBE101); вещества, усиливающее экскрецию желчных кислот (например, холестирамин и колестипол), витамин B3 (также известный как никотиновая кислота или ниацин), витамин B6 (пиридоксин), витамин B12 (цианокобаламин), производные фиброевой кислоты (например, гемфиброзил, клофибрат, фенофибрат и бензафибрат), пробукол, нитроглицерин и ингибиторы всасывания холестерина (например, β-ситостерин и ингибиторы ацил-КоA-холестеринацилтрансферазы (ACAT), такие как мелинамид), ингибиторы HMG-КоA-синтетазы, ингибиторы скваленэпоксидазы и ингибиторы скваленсинтетазы.
Примеры средств, используемых для лечения синдрома Иценко-Кушинга, в качестве неограничивающих примеров включают нейромодуляторы (сигнифор® (пасиреотид, каберголин); ингибиторы стероидогенез в надпочечниках (кетоконазол, метирапон, митотан, этомидат) и модуляторы ядерных рецепторов (корлим® (мифепристон), ретиноевая кислота). Другие средства в качестве неограничивающих примеров включают ингибиторы рецепторов эпидермального фактора роста (например, гефинитиб), ингибитор альдостеронсинтазы/11β-гидроксилазы LCI699 и левокетоконазол (COR-003).
Примеры анальгетических средств, часто используемых для лечения боли, включая нейропатическую боль, в качестве неограничивающих примеров включают опиоидные или неопиоидные анальгетические средства. Подходящие опиоидные анальгетические средства в качестве неограничивающих примеров включают морфин, героин, гидроморфон, гидрокодон, оксиморфон, оксикодон, метопон, апоморфин, норморфин, эторфин, бупренорфин, меперидин, лоперамид, анилеридин, этогептазин, пиминидин, бетапродин, дифеноксилат, фентанил, суфентанил, альфентанил, ремифентанил, леворфанол, декстрометорфан, феназоцин, пентазоцин, циклазоцин, метадон, изометадон и пропоксифен. Подходящие неопиоидные анальгетические средства в качестве неограничивающих примеров включают аспирин, целекоксиб, рофекоксиб, диклофенак, дифлусинал, этодолак, фенопрофен, флурбипрофен, ибупрофен, кетопрофен, индометацин, кеторолак, меклофенамат, мефенамовую кислоту, набуметон, напроксен, пироксикам и сулиндак.
Примеры терапевтических средств, часто используемых для лечения глаукомы включают агонисты холинергических рецепторов (например, пилокарпин и карбахол), ингибиторы холинэстеразы (например, физостигмин, неостигмин, демакариум, йодид эхотиофата и изофлуорофат), ингибиторы карбоангидразы (например, ацетазоламид, дихлорофенамид, метазоламид, этоксозоламид и дорзоламид), неселективные агонисты адренергических рецепторов (например, эпинефрин и дипивефрин), селективные агонисты α2-адренергических рецепторов (например, апраклонидин и бримонидин), β-блокаторы (например, тимолол, бетазолол, левобунолол, картеолол и метипранолол), аналоги простагландинов (например, латанопрост) и осмотические диуретики (например, глицерин, маннит и изосорбид); кортикостероиды, такие как беклометазон, метилпреднизолон, бетаметазон, преднизон, преднизолон, дексаметазон, флутиказон и гидрокортизон, и аналоги кортикостероидов, такие как будезонид.
Примеры терапевтических средств, часто используемых для лечения болезни Альцгеймера включают ингибиторы β-секретазы или ингибиторы γ-секретазы; ингибиторы транспорта глицина, ингибиторы фосфорилирования тау-белка; блокаторы формирования олигомеров Aβ; ингибиторы p25/CDK5; ингибиторы HMG-КоA-редуктазы; агонисты PPARγ, такие как пиоглитазон и росиглитазон; антагонисты рецепторов NK1/NK3; NSAID, включая ибупрофен; витамин E; антитела к амилоиду, включая гуманизированные моноклональные антитела к амилоиду; ингибиторы COX-2; противовоспалительные соединения, такие как (R)-флурбипрофен; антагонисты рецепторов CB-1 или обратные агонисты рецепторов CB-1; антибиотики, такие как доксициклин и рифампин; антагонисты рецепторов N-метил-D-аспартата (NMDA), такие как мемантин и нерамексан; антагонисты NR2B; модуляторы рецепторов андрогенов; ингибиторы ацетилхолинэстеразы, такие как галантамин, ривастигмин, донепезил и такрин; модуляторы mGluR5; стимуляторы секреции гормона роста, такие как ибутаморен, мезилат ибутаморена и капроморелин; антагонисты H3-гистаминовых рецепторов; агонисты AMPA; ингибиторы PDE IV; обратные агонисты ГАМКA; лиганды α5-рецепторов ГАМКA; лиганды рецепторов ГАМКB; блокаторы калиевых каналов; нейрональные агонисты никотинчувствительных рецепторов; ингибиторы P-450, такие как ритонавир.
Примеры терапевтических средств, часто используемых для лечения аффективных расстройств, таких как депрессия, в качестве неограничивающих примеров включают амитриптилин, оксид амитриптилина, дезипрамин, дибензепин, досулепин, доксепин, хлоримипрамин, имипрамин, нортриптилин, миансерин, мапротилин, тримипрамин, CP-122721, эльзасонан, PD-171729, MK-869, DOV-216303, DOV-21947, ликарбазепин, амфебутамон, радафаксин, вилазодон, GSK-679769, GW-597599, NS-2359, GSK-876008, прамипексол, дулоксетин, атомоксетин, LY-628535, десвенлафаксин, эсциталопрам, LU-AA21004, саредутант, SR-58611, SSR-149415, SSR-146977, моклобемид, R-673, R-1204, BMS-469458, DPC-368, Org-34517, Org-34850, ингибиторы рецепторов CRH, ONO-2333Ms, NBI-876008, AAG-561, NBI-34041, DPC-368, PD-171729, SSR-125543, вилоксазин, тразодон, нефазодон, митразапин, венлафаксин, ребоксетин, транилципромин, брофаромин, моклобемид, циталопрам, эсциталопрам, пароксетин, флуоксетин, флувоксамин, сертралин, зверобой (зверобой обыкновенный), алпразолам, клоназепам, диазепам, лоразепам, галазепам, хлордиазэпоксид и другие лекарственные средства, такие как буспирон, клонидин, пагоклон, рисперидон, оланзапин, кветиапин, зипрасидон, целекоксиб, пироксикам, парекоксиб, валдекоксиб, PMI-001, PH-686464, SC-58236, эторикоксиб, рофекоксиб, L-776967, лумиракоксиб, GW-406381, GW-644784, мелоксикам, SVT-2016, PAC-10649, CS-706, LAS-34475, цимикоксиб, A-183827.0 или нимесулид.
Примеры терапевтических средств, часто используемых для лечения аддикции и лекарственной зависимости в качестве неограничивающих примеров включают, фенелзин, фенилалкилгидразин (патент США № 4786653), дисульфирам ("антабуз"), 2-имино-5-фенил-4-оксазолидинон, α-метилпаратирозин или фузаровую кислоту, производные пиперазина (патент США № 4325952), клонидин в сочетании с трициклическими антидепрессантами (патент США № 4788189), γ-пироны, такие как мальтол или этилмальтол (патент США № 4276890), акампросат, габапентин, вигабатрин, баклофен, N-ацетилцистеин, нокаин, моданафил, пароксетин, бупропион, митразапин, топирамат, ондансетрон, варениклин, антагонисты опиоидных рецепторов, такие как налтрексон, налоксон, налмефин, антаксон, L-α-ацетил метадол, пентазоцин, буторфанол, налбуфин, бупренорфин и метадон.
Примеры терапевтических средств, часто используемых при лечении остеопороза и способных модулировать минеральный состав костей в качестве неограничивающих примеров включают бисфосфонаты, такие как аледронат (фосамакс®), ризедронат (актонель®), этидронат (дидронел®), памидронат, тилудронат (скелид®), клодронат (бонефос®; лорон®), неридронат, олпадронат, золедронат (зомета®) и ибандронат (бонива®), селективные модуляторы эстрогеновых рецепторов (SERM), такие как ралоксифен (эвиста®), арзоксифен, кломифен, базедоксифен, лазофоксифен, ормелоксифен, тамоксифен и торемифен, анаболическе лекарственные средства, такие как терипаратид (фортео®; рекомбинантный паратиреоидный гормон) и ранелат стронция, и рекомбинантные пептидные фрагменты паратиреоидного гормона, лекарственные средства, замещающие эстроген/прогестерон, моноклональные антитела, ингибиторы лиганда рецептора активатора ядерного фактора kB (RANKL), такие как деносумаб, остеопротегерин и пепстатин A, ингибиторы катепсина K, такие как, но не ограничиваясь ими, OST-4077 (фуран-2-карбоновая кислота-(1-{1-[4-фтор-2-(2-оксо-пирролидин-1-ил)-фенил]-3-оксо-пиперидин-3-илкарбамоил}циклогексил)амид), лейпептин, Cbz-Phe-Ala-CHN2, Cbz-Leu-Leu-Leu-альдегид, цистатин, необратимые ингибиторы цистеиновых протеаз, такие как пептидные галогенметилкетоны, пептидные диазометилкетоны, и эпоксиды, устойчивые необратимые ингибиторы цистеиновых протеаз, такие как ацилоксиметилкетоны, азапептиды, акцепторы Михаэля, такие как пептидные виниловые сложные эфиры, сульфоны и сульфонаты, обратимые ингибиторы цистеиновых протеаз, такие как пептидные альдегиды, a-кетоэфиры и a-кетоамиды, пептидные метилкетоны и их гидроксильные, алкилоксильные, арилокси, алкилтио и арилтио производные, 1,3-бис-(ациламино)-2-пропанoны, 1,3-бис-(ацилгидразино)карбонилы, ациламинопиразолоны, пиперидиноны и тиазонкарбонилгидразиды, антагонисты интегрина Avb3 (также известные в данной области как витронектин), кальцийлитические соединения (антагонисты рецепторов Ca2+, которые увеличивают секрецию PTH), кальцитонин (МиакальцинÒ), нитраты, включая в качестве неограничивающих примеров мононитрат изосорбида (ISMO) или нитроглицериновую мазь (NTG), и пищевые добавки, такие как кальций и витамин D, и их сочетания.
Другим вариантом осуществления настоящего изобретения является способ идентификации пациентов, нуждающихся в лечении, на основе определения уровней экспрессии генов часов (например, Cry1 и Cry2) в образцах, полученных у индивидуумов (Bjarnason, G. A. et al. Am. J. Pathol. 2001, 158, 1793; Akashi, M. et. al. Proc. Natl. Acad. Sci. USA, 2010, 107, 15643). Профили ритмической экспрессии иРНК для генов часов человека, включая Cry1 и Cry2, определяемые в образцах, полученных у индивидуума, означают, что циркадные часы присутствует в периферических тканях (Mohawk, J. A. et al. Ann. Rev. Neurosci. 2012, Epub ahead of print). Показано, что в этих образцах экспрессия связанных с циркадными часами генов варьирует в течение суток. Кроме того, профили экспрессии генов часов (например, Cry1 и Cry2) изменены в мононуклеарных клетках периферической крови у людей с такими заболеваниями, как ожирение (Tahira, K. et al. Arch. Med. Sci. 2011, 7, 933). Изменения экспрессии генов часов (например, Cry1 и Cry2) в мононуклеарных клетках периферической крови могут коррелировать с уровнями сывороточных лептина, адипонектина, инсулина и hsCRP, уровнями липидов, глюкозы, мелатонина и кортизола в плазме и, у животных, с экспрессией генов часов (например, Cry1 и Cry2) в тканях, включая печень, жировую ткань, поджелудочную железу и скелетные мышцы. Посредством контакта образцов, получаемых у подвергаемого лечению индивидуума, с соединением формулы I и измерения профилей ритмической экспрессии иРНК или белка можно идентифицировать пациентов, нуждающихся в лечении, и можно оценивать фармакологическую активность. В других вариантах осуществления можно оценивать активность одного или нескольких криптохромов, например, способность криптохромов связываться с мишенью, такой как Per1, Per2, рецептор глюкокортикоидов (GR) или промоторная последовательность, содержащая участки распознавания Cry, например, такая как промотор CLOCK-BMAL1.
Таким образом, один из аспектов объекта изобретения, описываемого в настоящем документе, относится к способу мониторинга прогресса или прогноза опосредуемого Cry заболевания или нарушения у индивидуума, включающему определение эффективного количества одного или нескольких криптохромов в первом образце, полученном у индивидуума в первый период времени; определение эффективного количества одного или нескольких криптохромов во втором образце, полученном у индивидуума, во второй период времени; и сравнение количества одного или нескольких криптохромов, детектированных в первом образце, с количеством одного или нескольких криптохромов, детектированных во втором образце, или с эталонным значением.
"Диагноз", "постановка диагноза", "прогнозирование" или "прогноз" не ограничен безусловным или почти безусловным определением того, что у индивидуума присутствует заболевание, но также включает определение, что у индивидуума существует вероятность наличия или развития заболевания по сравнению со здоровыми индивидуумами или со всей популяцией.
Как используют в настоящем документе, "экспрессия" и "уровни экспрессии" в качестве неограничивающих примеров включают одно или несколько из следующего: транскрипция гена в иРНК-предшественник; сплайсинг и другой процессинг иРНК-предшественника с получением зрелой иРНК; стабильность иРНК; трансляция зрелой иРНК в белок (включая использование кодонов и доступность тРНК) и гликозилирование и/или другие модификации продукта трансляции, если они необходимы для правильной экспрессии и функционирования.
"Формула", "алгоритм" или "модель" представляют собой любое математическое уравнение, алгоритмический, аналитический или программируемый процесс или статистический способ, которые принимают один или несколько непрерывных или категорийных аргумента (в настоящем документе называемых "параметрами") и рассчитывают выходное значение, иногда, обозначаемое как "индекс" или "заданное значение". Неограничивающие примеры "алгоритмов" включают суммы, отношения и регрессионные операторы, такие как коэффициенты или экспоненты, трансформация и нормализация значений (включая, без ограничения, схемы нормализации на основе клинических параметров, таких как пол, возраст, индекс массы тела или этническая принадлежность), правила и руководства, статистические классификационные модели и нейронные сети, тренируемые на ретроспективных группах. Как определено в настоящем документе, конкретное применение в измерениях Cry находят линейные и нелинейные уравнения и уравнения анализов статистической классификации для выявления "корреляционной" зависимости между уровнями Cry, детектируемыми в образце индивидуума и риском развития у индивидуума опосредуемого Cry заболевания или нарушения.
"Измерение" или "определение величины" означает оценку присутствия, отсутствия, величины или количества (которое может представлять собой эффективное количество) любого данного вещества в клиническом или полученном у индивидуума образце, включая получение качественных или количественных уровней концентрации таких веществ, или иную оценку значений или ранжирование клинических параметров индивидуума. Также измерение или определение величины может включать квалификацию типа или идентификацию вещества. Также измерение или определение величины может включать способность одного или нескольких Cry связываться с мишенью, где мишень может представлять собой периодические гены или белки Per1 и Per2, рецептор глюкокортикоидов (GR), или промоторная область гена CLOCK-BMAL1. Измерение Cry можно использовать для диагностики, детекции или идентификации опосредуемого Cry заболевания или нарушения у индивидуума, для мониторинга прогресса или прогноза опосредуемого Cry заболевания или нарушения у индивидуума, для прогноза рецидива опосредуемого Cry заболевания или нарушения у индивидуума или для классификации индивидуума, как индивидуума с низким риском или с высоким риском развития опосредуемого Cry заболевания или нарушения или рецидива опосредуемого Cry заболевания или нарушения.
В рамках настоящего изобретения "риск" относится к вероятности того, что определенное событие произойдет в течение определенного периода времени, как при развитии опосредуемого Cry заболевания или нарушения, и может означать "абсолютный" риск и "относительный" риск у индивидуума. Абсолютный риск можно измерять в отношении фактического наблюдения после измерения в группе в течение соответствующего времени, или в отношении заданных значений, получаемых в статистически обоснованных ретроспективных группах, за которыми наблюдали в течение соответствующего периода времени. Относительный риск относится к отношению абсолютных рисков индивидуума по сравнению с абсолютными рисками с группами с низким риском или со средним риском в популяции, которые могут варьировать в зависимости от оцениваемых клинических факторов риска. Также широко используется отношения шансов, отношение положительных исходов к отрицательным исходам для данного результата теста (шансы рассчитывают по формуле p/(1-p), где p представляет собой вероятность события, а (1- p) представляет собой вероятность отсутствия события) по отношению к отсутствию конверсии. Альтернативные непрерывные меры, которые можно определять в рамках настоящего изобретения, включают время до развития опосредуемого Cry заболевания или нарушения или прогрессирования в другую стадию опосредуемого Cry заболевания или нарушения, включая прогрессирование или развитие опосредуемого Cry заболевания или нарушения и снижение степени риска терапевтической конверсии.
"Оценка рисков" или "оценка риска" в контексте объекта изобретения, описываемого в настоящем документе, включает получение прогноза вероятности, шансов или возможности того, что событие или состояние болезни может возникнуть, частоты возникновения события или конверсии из одного состояния болезни в другое, например, из "нормального" состояния к состоянию с риском развития опосредуемого Cry заболевания или нарушения, или от состояния с риском к опосредуемому Cry заболеванию или нарушению, или развитие рецидива заболевания или нарушения. Оценка риска также может включать прогноз других показателей опосредуемого Cry заболевания или нарушения, в абсолютных или относительных единицах по отношению к ранее определенной группе. Способы по настоящему изобретению можно использовать для проведения непрерывных или категорийных измерения риска конверсии опосредуемого Cry заболевания или нарушения, таким образом, диагностируя и определяя спектр риска категории индивидуумов, определенных как индивидуумов с риском развития заболевания или нарушения. При категорийном варианте изобретение можно использовать для различения между группами обычных индивидуумов и индивидуумов с риском. В других вариантах осуществления настоящее изобретение можно использовать для различения состояний с риском от состояний заболевания или состояний заболевания от нормы.
Как используют в настоящем документе, "образец" представляет собой биологический образец, полученный у индивидуума, и в качестве примера, а не ограничения может включать цельную кровь, сыворотку, плазму, клетки крови, эндотелиальные клетки, биоптаты тканей, лимфу, асцитную жидкость, межклеточную жидкость (также известную как "внеклеточная жидкость" и включать жидкость, находящуюся в пространствах между клетками, в числе прочего включая зубодесневую жидкость), костный мозг, семенную жидкость, цереброспинальную жидкость (CSF), слюну, слизь, мокроту, пот, мочу или любой другой секрет, экскрет или другие жидкости организма.
Под "статистически значимым" подразумевают, что изменение превосходит то, что можно было бы ожидать только вследствие случайности (что могло бы быть "ложноположительным"). Статистическую значимость можно определять любым известным в данной области способом. Общепринятые меры значимости включают значение p, которое представляет собой вероятность получения значения по меньшей мере такого же экстремального, как полученной значение, в предположении, что значение является результатом только случайных изменений. Часто результат считают высокозначимым при значении p 0,05 или менее.
Риск опосредуемого Cry заболевания или нарушения можно детектировать определяя "эффективное количество" одного или нескольких криптохромов в образце (например, в полученном у индивидуума образце) и сравнивая эффективные количества с эталонными значениями, часто с использованием математических алгоритмов или формул с комбинированием информации из результатов для нескольких индивидуумов в одно определение. Индивидуумов, идентифицированных как индивидуумов с повышенным риском опосредуемого Cry заболевания или нарушения, необязательно можно выбирать для проведения схем лечения или терапевтического вмешательства, таких как введение соединений формулы I, как определено в настоящем документе, в качестве монотерапии или в комбинации с одним или несколькими дополнительными терапевтическими средствами, или проведения хирургического вмешательства (которое может следовать или предшествовать введению соединений формулы I, отдельно или в комбинации с дополнительными терапевтическими средства или другими способами лечения).
У способов детекции этих криптохромов в образце существует множество применений. Например, один или несколько криптохромов можно измерять в помощь диагнозу или прогнозу опосредуемого Cry заболевания или нарушения. В другом примере способы детекции криптохромов можно использовать для мониторинга ответа у индивидуума на лечение опосредуемого Cry заболевания или нарушения. В другом примере способы можно использовать для анализа и для идентификации соединений, которые модулируют экспрессию криптохромов in vivo или in vitro.
Настоящее изобретение можно использовать для проведения непрерывных или категорийных определений риска конверсии в опосредуемое Cry заболевание или нарушение, таким образом, диагностируя и определяя спектр риска категории индивидуумов, определенных как индивидуумов с риском развития заболевания или нарушения. При категорийном варианте изобретение можно использовать для различения между группами обычных индивидуумов и индивидуумов с риском. В других вариантах осуществления настоящее изобретение можно использовать для различения состояний с риском от заболевания или заболевания от нормы. Такое различное применение может требовать различных комбинаций панелей или профилей индивидуумов, математических алгоритмов и/или граничных точек, но быть объектом тех же указанных выше измерений точности для назначаемого применения.
Идентификация индивидуумов с риском обеспечивает выбор и начало терапевтических вмешательств или схем лечения с целью задержки, ослабления или предотвращение прохождение у индивидуума конверсии в опосредуемое Cry заболевание или нарушение. Уровни эффективного количества белков, нуклеиновых кислот, полиморфизмов, метаболитов или других анализируемых веществ криптохромов также обеспечивают мониторинг курса лечения. В этом способе биологический образец можно получать у индивидуума, подвергаемого схемам лечения, например, терапевтическому лечению опосредуемого Cry заболевания или нарушения. Такие схемы лечения в качестве неограничивающих примеров могут включать хирургическое вмешательство и лечение терапевтическими средствами, используемыми для индивидуумов, у которых диагностировано или идентифицировано опосредуемое Cry заболевание или нарушение, например, соединениями формулы I, описываемыми в настоящем документе. При желании, биологические образцы получают у индивидуума в различные моменты времени до, в течение или после лечения. Например, определение статуса заболевания посредством сравнения профиля криптохромов индивидуума с эталонным профилем криптохромов можно повторять более одного раза, где профиль индивидуума можно получать из отдельных образцов, получаемый каждый раз при повторении способа. Образцы можно получать у индивидуума с различными временными интервалами, например, такими как 4 часа, 8 часов, 12 часов, 24 часа, 48 часов, 72 часа или любой подходящий временной интервал, как могут выполнить специалисты в данной области.
Различия генетического строения индивидуумов могут приводить к различиям их способностей метаболизировать различные лекарственные средства, которые могут модулировать симптомы или факторы риска опосредуемого Cry заболевания или нарушения. Индивидуумы с опосредуемым Cry заболеванием или нарушением, или с риском развития опосредуемого Cry заболевания или нарушение могут различаться по возрасту, этнической принадлежности и другим параметрам. Таким образом, определение эффективных количеств одного или нескольких криптохромов, как определено в настоящем документе, отдельно и в комбинации с известными генетическими факторами метаболизма лекарственных средств, обеспечивают предопределенный уровень прогнозирования, что предполагаемое терапевтическое или профилактическое средство для тестирования у выбранного индивидуума подходит для лечения или профилактики у индивидуума опосредуемого Cry заболевания или нарушение.
Для идентификации терапевтических средств или лекарственных средств, которые пригодны для конкретного индивидуума, тестируемый образец, полученный у индивидуума, также можно подвергать воздействию терапевтического средства или лекарственного средства и можно определять уровень или активность одного или нескольких из белков, нуклеиновых кислот, полиморфизмов, вариантов сплайсинга, метаболитов или других анализируемых веществ криптохромов. Также можно определять другие гены или белки, которые подвержены действию или которые прямо или опосредованно связываются с одним или несколькими криптохромами (например, Per1, Per2, GR, промотор CLOCK-BMAL1 и т.д.). Уровень одного или нескольких криптохромов можно сравнивать с образцом, полученным у индивидуума, до и после лечения у индивидуума опосредуемого Cry заболевания или нарушение, например, лечения или подвергания действию терапевтического средства или лекарственного средства, или можно сравнивать с образцами, полученными у одного или нескольких индивидуумов, продемонстрировавших улучшение в отношении факторов риска в результате такого лечения или воздействия.
Нуклеиновые кислоты можно получать из образцов множеством способов, известных специалисту в данной области, например, способами экстракции, включая например, экстракцию растворителем, аффинную очистку и центрифугирование. Также нуклеиновые кислоты можно очищать посредством селективного осаждения. Также можно использовать способы хроматографии, включая гель-фильтрацию, ионообменную хроматографию, селективную адсорбцию или аффинное связывание. Нуклеиновые кислоты могут представлять собой, например, РНК, ДНК или можно синтезировать кДНК. Нуклеиновые кислоты можно детектировать с использованием способов с микропанелями, которые хорошо известны в данной области, например, панели Affymetrix с последующим способом многомерного шкалирования. См. R. Ekins, R. and Chu, F.W. (1999) Trends Biotechnol. 17: 217-218; D. D. Shoemaker, et al., (2001) Nature 409(6822): 922-927 и патент США № 5750015.
При желании образец можно получать для увеличения детектируемости одного или нескольких криптохромов, например, посредством префракционирования. Способы префракционирования включают, например, агарозную хроматографию с Cibacron синим, эксклюзионную хроматографию, ионообменную хроматографию, хроматография с гепарином, хроматографию с лектином, аффинную хроматографию, аффинную хроматография одноцепочечных ДНК, последовательную экстракцию, электрофорез в геле и жидкостную хроматографию. Также анализируемые вещества до детекции можно модифицировать. Образец можно префракционировать посредством удаления белков, которые присутствуют в большом количестве или которые могут препятствовать детекции в образце представляющих интерес молекул. Например, в образце сыворотки крови в большом количестве присутствует сывороточный альбумин, и он может препятствовать анализу одного или нескольких криптохромов. Таким образом, образец сыворотки крови можно префракционировать, удаляя сывороточный альбумин с использованием, например, субстрата, который содержит адсорбенты, которые специфически связывают сывороточные альбумин, можно использовать аффинную колонку или антитела к сывороточному альбумину.
В других вариантах осуществления представляющие интерес молекулы в образце можно разделять посредством электрофореза высокого разрешения, например, одно- или двумерного электрофореза в геле. Можно выделять фракцию и дополнительно анализировать посредством ионной спектрометрии в газовой фазе. Предпочтительно, двумерный электрофорез в геле используют для получения двумерных паналей точек, содержащих один или несколько криптохромов. См., например, Jungblut and Thiede, (1997) Mass Spectr. Rev. 16: 145-162. Двумерный электрофорез в геле можно проводить известными в данной области способами. См., например, Deutscher ed., Methods in Enzymology vol. 182. Как правило, образец можно разделять, например, посредством изоэлектрофокусирования, в течение которого один или несколько криптохромов в образце разделяют в градиенте pH до достижения точки, где их суммарный заряд представляет собой ноль (например, изоэлектрической точки). Этот первый этап разделения приводит к получению одномерной панели. Молекулы в одномерной панели дополнительно разделяют способом, как правило, отличающимся от способа, применяемого на первом этапе разделения. Например, во втором измерении представляющие интерес молекулы, разделенные посредством изоэлектрофокусирования, дополнительно разделяют с использованием полиакриламидного геля, например, посредством электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE). Гель после SDS-PAGE обеспечивает дополнительное разделение на основе молекулярной массы. Как правило, двумерный электрофорез в геле может разделять химически различные представляющие интерес молекулы в диапазоне молекулярных масс 1000-200000 Да в сложных смесях.
Представляющие интерес молекулы в двумерной панели можно детектировать с использованием любых подходящих известных в данной области способов. Например, представляющие интерес молекулы в геле можно метить или окрашивать (например, посредством окрашивания Кумасси синим или серебром). Если при электрофорезе в геле получают точки, соответствующие молекулярной массе одного или нескольких криптохромов по изобретению, точку можно вырезать и дополнительно анализировать, например, посредством ионной спектрометрии в газовой фазе, масс-спектрометрия или высокоэффективной жидкостной хроматографии. Альтернативно, гель, содержащий представляющие интерес молекулы, можно переносить на инертную мембрану, прикладывая электрическое поле. Затем точку на мембране, которая приблизительно соответствует молекулярной массе представляющей интерес молекулы можно анализировать, например, посредством ионной спектрометрии в газовой фазе, масс-спектрометрии или ВЭЖХ.
Необязательно, представляющую интерес молекулу до анализа можно модифицировать для улучшения ее разрешения или для определения ее подлинности. Например, образец до анализа можно подвергать протеолитическому расщеплению. Можно использовать любую протеазу. Особенно пригодны такие протеазы, как трипсин, которые с определенной вероятностью расщепляют белки на определенное количество отдельных фрагментов. Фрагменты, которые являются результатом расщепления, могут функционировать для представляющих интерес молекул в качестве "отпечатков пальцев", таким образом, обеспечивая их непрямую детекцию. Это особенно пригодно, где для предпочтительной молекулы присутствуют представляющие интерес молекулы со сходными молекулярными массами, которые можно спутать, например, рассматриваемые криптохромы. Также протеолитическая фрагментация пригодна для высокомолекулярных молекул, так как молекулы меньших размеров легче разрешать посредством масс-спектрометрии. В другом примере молекулы можно модифицировать для улучшения разрешения детекции. Например, можно использовать нейраминидазу для удаления концевых остатков сиаловой кислоты из гликопротеинов для улучшения связывания с анионным адсорбентом (например, катионообменные панели) и для улучшения разрешения детекции. В другом примере молекулы можно модифицировать, присоединением меток с конкретной молекулярной массой, которые специфически связывается с другой молекулярной структурой, обеспечивая их дополнительное различение. Необязательно, после детекции таких модифицированных представляющих интерес молекул, подлинность молекул можно дополнительно определять, сопоставляя физические и химические характеристики модифицированных версий в базе данных белков (например, SwissProt).
После захвата на субстрате, например, биочипе или антителе, для определения одного или нескольких криптохромов в образце можно использовать любой подходящий способ, такой как способы, описываемые в настоящем документе, а также другие известные в данной области способы. Фактическое определение уровней или количеств таких молекул можно проводить любым известным в данной области способом. Эти способы в качестве неограничивающих примеров включают масс-спектрометрию (например, масс-спектрометрию с лазерной десорбцией/ионизацией), флуоресценцию (например, иммунологический "сэндвич"-анализ), поверхностный плазмонный резонанс, эллипсометрию и атомно-силовую микроскопию. Способы могут дополнительно включать один или несколько из микропанелей, способов ПЦР, масс-спектрометрии (включая, например и без ограничения, ESI-MS, ESI-MS/MS, ESI-MS/(MS)n, лазерную десорбцию/ионизацию с помощью матрицы с время-пролетной масс-спектрометрией (MALDI-TOF-MS), время-пролетную масс-спектрометрию с усиленной поверхностью лазерной десорбцией/ионизацией (SELDI-TOF-MS), десорбцию/ионизацию на кремнии (DIOS), масс-спектрометрию вторичных ионов (SIMS), квадрупольное время пролета (Q-TOF), масс-спектрометрию с химической ионизацией при атмосферном давлении (APCI-MS), APCI-MS/MS, APCI-(MS)n, масс-спектрометрию с фотоионизацией при атмосферном давлении (APPI-MS), APPI-MS/MS и APPI-(MS)n, квадрупольную масс-спектрометрию, масс-спектрометрию с преобразованием Фурье (FTMS) и масс-спектрометрию с ионной ловушкой), чипы нуклеиновых кислот, "нозерн"-блот гибридизацию, TMA, SDA, NASBA, ПЦР, ПЦР с детекцией в реальном времени, ПЦР с обратной транскриптазой, ПЦР с обратной транскриптазой и детекцией в реальном времени, ПЦР in situ, хроматографическое разделение в сочетании с масс-спектрометрией, захват белков с использованием иммобилизованных антител или посредством традиционных иммунологических анализов. См. например, патенты США №№ 5723591; 5801155 и 6084102 и Higuchi, 1992 и 1993. Анализы ПЦР можно проводить, например, в форматах планшетов с множеством лунок или на чипах, например, чипах BioTrove OPEN ARRAY Chips (BioTrove, Woburn, MA).
Например, можно использовать последовательности в записях базы данных последовательностей, соответствующих криптохромам для конструирования зондов для детекции последовательностей РНК, например, в анализах гибридизации "нозерн"-блота или в способах, которыми специфически и, предпочтительно, количественно амплифицируют конкретные последовательности нуклеиновой кислоты. В качестве другого пример, последовательности можно использовать для конструирования праймеров, которые специфически или селективно гибридизуются с последовательностями криптохромов и которые используют для амплификации таких последовательностей, например, в основанных на амплификации способах детекции, таких как полимеразная цепная реакция на основе обратной транскрипции (ОТ-ПЦР), например, количественная ОТ-ПЦР с детекцией в реальном времени. Когда изменения экспрессии генов ассоциированы с амплификацией генов, делециями, полиморфизмами и мутациями, сравнения последовательностей в тестовых и эталонных группах можно проводить посредством сравнения относительных количеств исследуемых последовательностей ДНК индивидуума и эталонных групп клеток. Как используют в настоящем документе, термин "специфически (или селективно) гибридизуется" в отношении нуклеиновых кислот, относится к реакции связывания, которая определяет присутствие конкретной нуклеиновой кислоты в гетерогенной группе нуклеиновых кислот. Таким образом, в указанных условиях анализа, специфический зонд нуклеиновой кислоты (включая ингибирующие нуклеиновые кислоты) может связываться или гибридизоваться с конкретной представляющей интерес нуклеиновой кислотой по меньшей мере в два раза выше фонового уровня и по существу не связывается или не гибридизуется в значимом количестве с другими нуклеиновыми кислотами, находящимися в образце.
Уровни криптохромов также можно определять посредством иммунологического анализа. Антитело может быть моноклональным, поликлональным, химерным или фрагментом указанного выше, как подробно описано в настоящем документе, и этап детекции продукта реакции можно проводить любым подходящим иммунологическим анализом. Фраза "специфически (или селективно) связывается" с антителом или "специфически (или селективно) иммунореактивный" в отношении белка или пептида относится к реакции связывания, которой определяют присутствие белка в гетерогенной группе белков и других биологических молекул. Таким образом, в указанных условия иммунологического анализа специфические антитела связываются с конкретным белком по меньшей мере в два раза выше фонового уровня и по существу не связываются в значимом количестве с другими белками, находящимися в образце. Специфическое связывание с антителом в таких условиях может требовать антитела, которое выбрано по его специфичности в отношении конкретного белка. Например, можно выбирать поликлональные антитела, индуцированные криптохромами конкретных видов, таких как крыса, мышь или человек с получением только тех поликлональных антител, которые специфически иммунореактивны в отношении конкретного криптохрома, а не других белков, за исключением полиморфных вариантов и аллелей криптохрома. Такой выбор можно получать, удаляя антитела, перекрестно реагирующие с криптохромами других видов.
Иммунологические анализы, проводимые в соответствии с настоящим изобретением, могут представлять собой гомогенные анализы или гетерогенные анализы. В гомогенном анализе иммунная реакция, как правило, включает специфическое антитело (например, антитело к белку криптохрома), меченое анализируемое вещество и представляющий интерес образец. Сигнал, поступающий от метки прямо или опосредовано модифицируется при связывании антитела с меченым анализируемым веществом. Иммунную реакцию и детекцию ее степени можно проводить в гомогенном растворе. Иммунохимические метки, которые можно использовать, включают свободные радикалы, радиоактивные изотопы, флуоресцентные красители, ферменты, бактериофаги или коферменты.
В подходе гетерогенного анализа реагенты, как правило, представляют собой образец, антитело и средства получения детектируемого сигнала. Образцы можно использовать, как описано выше. Антитело можно иммобилизовать на подложке, такой как гранулы (такие как агарозные гранулы с белком A и белком G), планшет или стекло, и приводить в контакт с образцом, в котором полагают наличие антигена в жидкой фазе. Затем подложку отделяют от жидкой фазы и фазу подложки или жидкую фазу исследуют на детектируемый сигнал с использованием средств получения такого сигнала. Сигнал связан с присутствием в образце анализируемого вещества. Средства получения детектируемого сигнала включают использование детектируемых меток. Иллюстративные детектируемые метки включают магнитные гранулы (например, DYNABEADS™), флуоресцентные красители, ферменты (например, пероксидаза хрена, щелочная фосфатаза и другие общепринятые в ELISA ферменты), радиоактивные метки (например, 35S, 125I, 131I) и флуоресцентные метки (например, флуоресцеин, Alexa, зеленый флуоресцентный белок, родамин) и колориметрические метки, такие как коллоидное золото или цветное стекло или пластиковые гранулы в соответствии с известными способами.
Альтернативно, представляющие интерес молекулы в образце можно детектировать с использованием непрямого анализа, например, где для детекции связанного с криптохромом специфичного антитела используют второе меченое антитело, и/или в конкурентном анализе или анализе с ингибированием, например, где одновременно со смесью инкубируют моноклональное антитело, которое связывается с определенным эпитопом криптохрома. Например, если антиген для детекции содержит второй участок связывания, то антитело, которое связывается с этим участком, можно конъюгировать с детектируемой группой и перед этапом разделения добавлять в реакционной раствор жидкой фазы. Присутствие детектируемой метки на твердой подложке указывает на присутствие антигена в тестируемом образце. Способы определения количества или присутствия комплексов антитело-антиген включают, например, детекцию флуоресценции, люминесценции, хемилюминесценции, оптической плотности, отражения, пропускания, двойного преломления или показателя преломления (например, поверхностный плазмонный резонанс, эллипсометрия, способ резонансного зеркала, способ с волноводом с решетчатым светоделителем или интерферометрия). Оптические способы включают микроскопию (конфокальную и неконфокальную), способы получения изображения и способы без получения изображения. Электрохимические способы включают способы вольтамперометрии и амперометрии. Радиоволновые способы включают мультиполярную резонансную спектроскопию. Примеры подходящих иммунологических анализов в качестве неограничивающих примеров включают иммуноблоттинг (например, вестерн-блоттинг, анализ слот-блоттинг), иммунопреципитацию, иммунофлуоресцентные способы, хемилюминесцентные способы, электрохемилюминесценцию (ECL) или иммуноферментные анализы, например, твердофазный иммуноферментный анализ (ELISA) и радиоиммунологический анализ (RIA). В основном см. E. Maggio, Enzyme-Immunoassay, (1980) (CRC Press, Inc., Boca Raton, Fla.); также см. патенты США №№ 4727022; 4659678; 4376110; 4275149; 4233402 и 4230767. Эти способы также описаны, например, в Methods in Cell Biology: Antibodies in Cell Biology, volume 37 (Asai, ed. 1993); Basic and Clinical Immunology (Stites & Terr, eds., 7th ed. 1991); и Harlow & Lane, выше. Все они включены в настоящий документ в качестве ссылки.
Иммунологические анализы можно использовать для определения присутствия или отсутствия одного или нескольких криптохромов в образце, а также их количества в образце. Количество комплекса антитело-маркер можно определять, сравнивая со стандартом. Стандарт может представлять собой, например, известное соединение или другой белок, для которого известно, что он присутствует в образце. Как указано выше, при условии, что единицу измерения можно сравнивать с контролем, необходимости определять тестируемое количество одного или нескольких криптохромов в абсолютных единицах нет.
Белки, часто присутствующие в образце во множестве различных форм, характеризуются детектируемо различными массами. Эти формы могут являться результатом любой из пре- и посттрансляционных модификаций или и пре-, и посттрансляционных модификаций вместе. Претрансляционно модифицированные формы включают аллельные варианты, варианты сплайсинга и формы с редактированием РНК. Посттрансляционно модифицированные формы включают формы, являющиеся результатом протеолитического расщепления (например, фрагментами исходного белка), гликозилирования, фосфорилирования, липидирования, окисления, метилирования, цистинилирования, сульфирования и ацетилирования. Антитела также могут быть пригодны для детекции посттрансляционных модификаций белков, полипептидов, мутаций и полиморфизмов, таких как фосфорилирование тирозина, фосфорилирование треонина, фосфорилирование серина, гликозилирование (например, O-GlcNAc). Такие антитела специфически детектируют фосфорилированные аминокислоты в представляющих интерес белке или белках, и их можно использовать в анализы иммуноблоттинга, иммунофлуоресценции и ELISA, описываемых в настоящем документе. Эти антитела хорошо известны специалистам в данной области и коммерчески доступны. Посттрансляционные модификации также можно определять с использованием метастабильных ионов в рефлекторной времяпролетной масс-спектрометрии с лазерной десорбцией/ионизацией с помощью матрицы (MALDI-TOF) (Wirth, U. et al. (2002) Proteomics 2(10): 1445-51). Набор белков, включая конкретный белок и все его модифицированные формы, обозначают в настоящем документе как "белковый кластер". Набор всех модифицированных форм конкретного белка, исключая сам конкретный белок, обозначают в настоящем документе как "кластер модифицированных белков". В способах, описываемых в настоящем документе, также можно использовать сами модифицированные формы любого криптохрома. В определенных случаях модифицированные формы могут демонстрировать лучшую селективную способность в диагнозе, чем конкретные формы, указанные в настоящем документе. Модифицированные формы исходно можно детектировать любым способом, известным в данной области.
Альтернативно можно определять метаболиты белков и нуклеиновых кислот криптохромов. Термин "метаболит" включает любой химический или биохимический продукт метаболического процесса, такой как любое соединений, получаемое при процессинге, расщеплении или потреблении биологической молекулы (например, белка, нуклеиновой кислоты, углевода или липида). Метаболиты можно детектировать рядом способов, известных специалисту в данной области, включая рефракционную спектроскопию (RI), спектроскопию в ультрафиолетовом излучении (UV), анализ флуоресценции, радиохимический анализ, спектроскопию в ближней инфракрасной области спектра (ближней ИК области спектра), ядерную магнитно-резонансную спектроскопию (ЯМР), анализ светорассеяния (LS), масс-спектрометрию, масс-спектрометрию с пиролизом, нефелометрию, дисперсионную раман-спектроскопию, газовую хроматографию, комбинированную с масс-спектрометрией, жидкостную хроматографию (включая высокоэффективную жидкостную хроматографию (ВЭЖХ)), которые можно комбинировать с масс-спектрометрией, времяпролетную лазерную десорбцию/ионизацию с помощью матрицы (MALDI-TOF), комбинированную с масс-спектрометрией, ионоспрейную спектроскопию, комбинированную с масс-спектрометрией, капиллярный электрофорез, спектрометрию ионной подвижности, усиленную поверхностью лазерную десорбцию/ионизацию (SELDI), оптические способы, электрохимические способы, атомно-силовую микроскопию, радиоволновые способы, поверхностный плазмонный резонанс, эллипсометрию, детекцию ЯМР и IR. (См., публикации международных заявок №№ WO 04/056456 и WO 04/088309, каждая из которых, таким образом, полностью включена в качестве ссылки). В этом отношении, указанными выше способами детекции или другими способами, известными специалисту в данной области, можно определять другие анализируемые вещества. Например, в образце можно детектировать циркулирующие ионы кальция (Ca2+) с использованием флуоресцентных красителей, таких как, наряду с другими, серия Fluo, Fura-2A, Rhod-2. Подобным образом, можно детектировать другие метаболиты с использованием реагентов, которые конкретно разработаны или приспособлены для детекции таких метаболитов.
Опосредуемое Cry заболевание или нарушение может включать изменения активности одного или нескольких криптохромов или способности одного или нескольких криптохромов связываться с мишенью. Не желая быть связанными теорией, полагают, что белки криптохромов связываются с белками Period Per 1 и/или Per2 в виде гетеродимера, который затем связывается с промоторной областью гена CLOCK-BMAL1, способствуя репрессии транскрипции в петле обратной связи, которая может воздействовать на множество метаболических процессов. Таким образом, определение эффективного количества одного или нескольких криптохромов способами по изобретению может включать оценку увеличения или уменьшения способности белков Cry связываться с Per1 и/или Per2, с рецептором глюкокортикоидов (GR) или с любой другой мишенью связывания Cry, известной специалистам в данной области. Определение белок-белковых взаимодействий можно обеспечивать любым известным в данной области способом, включая коиммунопреципитацию, анализ дрожжевой двухгибридной системы, поверхностный плазмонный резонанс, бимолекулярную комплементацию флуоресценции, тандемную аффинную очистку, фаговый дисплей, поляризацию/анизотропию флуоресценции, интерферометрию двойной поляризации, флуоресцентную корреляционную спектроскопию, резонансный перенос энергии флуоресценции и т.п.
Активность одного или нескольких криптохромов также можно определять по увеличению или уменьшению способности связываться с последовательностью ДНК, например, промоторной областью гена CLOCK-BMAL1 или другого гена, который содержит участки связывания, распознаваемые одним или несколькими криптохромами. "Промотор", "промоторная последовательность" или "промоторная область" относятся к последовательности ДНК, способной к связыванию в клетке с РНК-полимеразой, инициации транскрипции расположенной ниже (в направлении 3') кодирующей последовательности, таким образом, контролируя ее экспрессию. Для целей определения настоящего изобретения промоторная последовательность на своем 3'-конце ограничена участком инициации транскрипции и расположена выше (в направлении 5'), включая минимальное количество оснований или элементов, необходимых для инициации транскрипции на уровнях, детектируемых выше фона. В пределах промоторной последовательности находится участок инициации транскрипции (в целях удобства определенный, например, посредством картирования с использованием нуклеазы S1), а также связывающие белки домены (консенсусные последовательности), ответственные за связывание РНК-полимеразы. Промоторы могут полностью происходить из природного гена или состоять из различных элементов, получаемых из различных промоторов, выявляемых в природе, или даже синтетические участки ДНК. В большинстве случаев точные границы регуляторных последовательностей полностью не определены, идентичной промоторной активностью могут обладать фрагменты ДНК различной длины.
Промотор CLOCK-BMAL1 (или любая другая промоторная область, содержащая участки связывания или распознавания Cry) может быть "функционально связанной" с репортерным геном. Термин "функционально связанный" относится к ассоциации последовательностей нуклеиновых кислот на одном из фрагментов нуклеиновой кислоты так, что функционирование одного из них влияет на другой. Например, промотор функционально связан с кодирующей последовательностью, когда он способен влиять на экспрессию этой кодирующей последовательности (например, эта кодирующая последовательность находится под транскрипционным контролем промотора). Кодирующие последовательности могут быть функционально связанными с регуляторными последовательностями в смысловой или антисмысловой ориентации. Термин "репортерный ген" означает нуклеиновую кислоту, кодирующую идентификационный фактор, который можно идентифицировать в зависимости от действия репортерного гена, где действие используют для слежения за наследованием представляющей интерес нуклеиновой кислоты, для идентификации клетки или организма, содержащих унаследованную представляющую интерес нуклеиновую кислоту, и/или для определения индукции экспрессии или транскрипции гена. Примеры репортерных генов, известных и используемых в данной области включают: люциферазу (Luc), зеленый флуоресцентный белок (GFP), щелочную фосфатазу (ALP), хлорамфениколацетилтрансферазу (CAT), β-галактозидазу (LacZ), β-глюкуронидазу (Gus) и т.п. Гены селективных маркеров также можно считать репортерными генами. Конструкция промотор-репортерный ген может содержаться в плазмиде или экспрессирующем векторе, который переносят или трансфицируют в клетку. Экспрессию репортерного гена можно детектировать, определяя активность продукта гена, например, ферментативную активность в случае использования репортерного гена из представленных выше примеров.
Термин "плазмида" относится к внехромосомному элементу, часто несущему ген, который не является частью основного метаболизма клетки, и, как правило, находящемуся в форме кольцевой двухцепочечной молекулы ДНК. Такие элементы могут представлять собой автономно реплицирующиеся последовательности, интегрируемые в геном последовательности, фаговые или нуклеотидные последовательности, линейные, кольцевые или суперскрученные с одно- или двухцепочечной ДНК или РНК, получаемые из любого источника, в которых ряд нуклеотидных последовательностей связан или рекомбинирован в уникальную конструкцию, которая способна к внесению в клетку промоторного фрагмента и последовательности ДНК выбранного продукта гена вместе с соответствующей 3'-нетранслируемой последовательностью. Термин "экспрессирующий вектор" означает вектор, плазмиду или носитель, сконструированные для обеспечения экспрессии вставленной последовательности нуклеиновой кислоты после трансформации хозяину. Векторы можно вносить в желаемые клетки-хозяева известными в данной области способами, например, трансфекцией, электропорацией, микроинъекцией, трансдукцией, слиянием клеток, DEAE-декстраном, осаждением с фосфатом кальция, липофекцией (слиянием лизосом), использованием генной пушки или ДНК-вектора-транспортера. Для проведения анализов репортеров можно использовать любую клетку, такую как прокариотическая клетка или эукариотическая клетка. Предпочтительно клетка может представлять собой бактериальную клетку, клетку гриба, дрожжевую клетку, клетку нематоды, клетку насекомого, клетку рыбы, клетку растения, клетка птицы, клетку животного и клетку млекопитающего. Клетки могут представлять собой первичные клетки или их можно непрерывно пересевать в качестве линий клеток. Иллюстративные клетки и линии клеток известны специалистам в данной области.
Другие способы определения активности или способности одного или нескольких криптохромов связываться с последовательностью ДНК включают анализ иммунопреципитации хроматина, анализ изменения электрофоретической подвижности, анализ осаждения ДНК, захват и детекцию на микропланшете и т.п.
Затем можно определять уровни эффективного количества белков криптохромов, нуклеиновых кислот, полиморфизмов, метаболитов или других анализируемых веществ или активности белков криптохромов или мишеней, которые прямо или опосредованно связываются с белками криптохромов, и сравнивать с эталонным значением, например, с контрольным индивидуумом или группой, статус заболевания которых известен, или с заданным значением или исходным значением. Эталонный образец или заданное значение или исходное значение можно брать или получать у одного или нескольких индивидуумов, которых подвергали лечению, или можно брать или получать у одного или нескольких индивидуумов, которые представляют собой индивидуумов с низким риском развития опосредуемого Cry заболевания или нарушения, или можно брать или получать у индивидуумов, продемонстрировавших улучшение факторов риска заболевания в результате проведенного лечения. Альтернативно, эталонный образец или заданное значение или исходное значение можно брать или получать у одного или нескольких индивидуумов, которых не подвергали лечению. Например, образцы можно получать у индивидуумов, которым проводили исходное лечение опосредуемого Cry заболевания или нарушения и последующее лечение заболевания или нарушение для контроля прогресса лечения. В определенных вариантах осуществления первый образец можно получать у индивидуума в первый период времени, например, до лечения соединением формулы I, как определено в настоящем документе, отдельно или в комбинации с одним или несколькими дополнительными терапевтическими средствами, с последующим определением или детекцией одного или нескольких криптохромов (или мишеней криптохромов), как описано в настоящем документе. Затем у индивидуума во второй период времени можно получать второй образец, например, после лечения соединением формулы I, как определено в настоящем документе, отдельно или в комбинации с одним или несколькими дополнительными терапевтическими средствами, и определять один или несколько криптохромов или мишеней криптохромов. Для оценки эффективности курса лечения можно получать любое количество образцов с любыми временными интервалами на всем его протяжении.
Эталонное значение также может включать значение, получаемое на основе алгоритмов прогноза риска или рассчитанных индексов на основе популяционных исследований, таких как описаны в настоящем документе. Подобный термин в этом контексте представляет собой "контроль", который может представлять собой, например, среднее или медианное количество криптохромов, находящихся в сравниваемых образцах представляющих норму индивидуумов у представляющих норму индивидуумов или у индивидуумов без заболевания, таких как индивидуумы, у которых опосредуемое Cry заболевание или нарушение не детектируют. Контрольное количество определяют в тех же или в значительной степени сходных экспериментальных условиях, что и при определении тестируемого количества. Корреляция может учитывать присутствие или отсутствие криптохромов в тестируемом образце и частоту детекции тех же молекул у контроля. Для содействия определению статуса заболевания корреляция может учитывать оба этих фактора.
Также описываемыми в настоящем документе способами можно получать эталонный профиль индивидуумов, у которых нет опосредуемого Cry заболевания или нарушение и у которых не ожидают развития опосредуемого Cry заболевания или нарушения. Определение одного или нескольких криптохромов также можно использовать для получения "профиля индивидуума" у индивидуумов с опосредуемым Cry заболеванием или нарушением. Профили индивидуумов можно сравнивать с эталонным профиль для диагностики или идентификации индивидуумов с риском развития опосредуемого Cry заболевания или нарушения, для контроля за прогрессированием заболевания, а также скорости прогрессирования заболевания и для контроля эффективности способов лечения или ухода за индивидуумами.
Эталонные профили и профили индивидуумов по настоящему изобретению могут находиться на машиночитаемых носителях, таких как, наряду с другими, но не ограниченном ими, аналоговые или цифровые кассеты, такие как кассеты читаемые VCR, CD-ROM, DVD-ROM, флэш-носители USB. Такие машиночитаемые носители также могут содержать дополнительные результаты тестирования, такие как, без ограничения, определения клинических параметров и традиционных лабораторных факторов риска. Альтернативно или дополнительно машиночитаемые носители также могут содержать информацию об индивидууме, такую как история болезни (анамнез) и любой соответствующий семейный анамнез. Машиночитаемые носители также могут содержать информацию о других алгоритмах риска и рассчитанных индексах, таких как описаны в настоящем документе.
В любом из способов, описываемых в настоящем документе, данные из образца можно непосредственно со средств детекции отправлять в компьютер, содержащий диагностический алгоритм. Альтернативно, полученные данные можно отправлять вручную или автоматизированными средствами в отдельный компьютер, который содержит диагностический алгоритм. Таким образом, варианты осуществления изобретения включают способы, включающие выявление корреляции детекции криптохромов с возможным диагнозом опосредуемого Cry заболевания или нарушения. Корреляция может учитывать количество одного или нескольких криптохромов в образце в сравнении с количеством у контроля (повышение или снижение экспрессии криптохромов) (например, у представляющих норму индивидуумов, у которых опосредуемое Cry заболевание или нарушение не детектируют). Корреляция может учитывать присутствие или отсутствие криптохромов в тестируемом образце и частоту детекции тех же молекул у контроля. Для содействия определению наличия или отсутствия у индивидуума опосредуемого Cry заболевания или нарушения корреляция может учитывать оба этих фактора.
Анализ данных может включать этапы определения силы сигнала (например, высоты пиков) от детектируемого маркера и удаление "выбросов" (данных, отклоняющихся от предопределенного статистического распределения). Наблюдаемые пики можно нормализовать, процесс в котором рассчитывают высоту каждого из пиков относительно определенной точки отсчета. Например, точка отсчета может представлять собой фоновый шум, генерируемый устройством и химическими соединениями (например, энергопоглощающими молекулами), которые устанавливают как ноль на шкале. Силу сигнала, детектируемая для каждой представляющей интерес молекулы, можно выражать в форме относительных интенсивностей по желаемой шкале (например, 100). Альтернативно, с образцом можно вводить стандарт (например, сывороточный белок) так, что для расчета относительных интенсивностей наблюдаемых сигналов каждой представляющей интерес детектируемой молекулы в качестве эталона можно использовать пик стандарта.
Полученные данные для отображения можно трансформировать или конвертировать в различные форматы. В одном из форматов, обозначаемом как "спектральный вид или карта концентрата", можно отображать стандартный спектральный вид, где на изображении представлено количество достигающих детектора молекул с каждой конкретной молекулярной массой. В другом формате, обозначаемом как "карта пиков", из спектрального вида сохраняют только информацию о высоте пиков и массе, получая более четкое изображение и обеспечивая более четкое отображение представляющих интерес молекул с почти идентичными молекулярными массами. В другом формате, обозначаемом как "вид геля", каждую массу из вида пиков на основе высоты каждого пика можно преобразовывать в изображение с градациями серого, получая вид, сходный с полосами на электрофоретических гелях. В еще одном формате, обозначаемом как "3-D наложения", можно накладывать несколько спектров для исследования незаметных изменений относительных высот пиков. В еще одном формате, обозначаемом как "вид дифференциальной карты", можно сравнивать два или более спектра, в целях удобства подсвечивая уникальные представляющие интерес молекулы с повышенной или сниженной экспрессией в разных образцах. Профили (спектры) любых двух образцов можно сравнивать визуально. В другом формате, можно использовать диаграмму рассеяния Spotfire, где представляющие интерес детектированные молекулы нанесены в виде точек на диаграмму, где одна ось диаграммы представляет собой видимую молекулярную массу детектированных криптохромов, а другая ось представляет интенсивность сигнала детектированных криптохромов. Для каждого образца, представляющие интерес молекулы, которые были детектированы, и в образце присутствует определенное количество этих молекул, можно сохранять на машиночитаемом носителе. Затем эти данные можно сравнивать с контрольным или эталонным профилем или эталонным значением (например, с профилем или количеством молекул, детектированных в контроле, например, у индивидуумов, у которых опосредуемое Cry заболевание или нарушение не детектируют).
Данные, которые получают в способах, описываемых в настоящем документе, можно классифицировать с использованием способа распознавания профилей, к котором используют классифицирующую модель. В определенных вариантах осуществления данные, получаемые с использованием таких образцов, как "известные образцы" затем можно использовать для "обучения" классифицирующей модели. "Известный образец" представляет собой образец, который предварительно классифицирован (например, заболевание или отсутствие заболевания). Затем данные, полученные с использованием известных образцов, можно использовать для "обучения" классифицирующей модели. "Известный образец" представляет собой образец, который предварительно классифицирован. Данные, которые можно использовать для формирования классифицирующей модели, можно обозначать как "набор обучающих данных". После обучения, классифицирующая модель может распознавать профили в данных, получаемые с использованием неизвестных образцов. Затем классифицирующую модель можно использовать для классификации неизвестных образцов по классам. Это можно использовать, например, при прогнозе того ассоциирован ли конкретный биологический образец с определенным биологическим состоянием (например, болезнь в сравнении с отсутствием болезни) или нет. Набор обучающих данных, который используют для формирования классифицирующей модель может содержать исходные данные или предварительно обработанные данные. В определенных вариантах осуществления исходные данные можно получать непосредственно из время-пролетных спектров или масс-спектров, а затем можно необязательно подвергать "предварительной обработке" любым подходящим способом. Этапы предварительной обработки, такие как эти, можно использовать для уменьшения количества данных, которые используют для обучения классифицирующей модели.
Классифицирующие модели можно формировать с использованием любого подходящего способа статистической классификации (или "обучения"), в котором предпринимается попытка разделить массивы данных на классы на основе реальных параметров, представленных в данных. Способы классификации могут быть или контролируемые или неконтролируемые. Примеры контролируемых и неконтролируемых способов классификации описаны в Jain, "Statistical Pattern Recognition: A Review", IEEE Transactions on Pattern Analysis and Machine Intelligence, Vol. 22, No. 1, January 2000, которая полностью включена в настоящий документ в качестве ссылки. В контролируемой классификации для обучаемого механизма, который изучает несколько наборов зависимостей, которые определяют каждый из известных классов, предоставляют обучающие данные, содержащие примеры известных категорий. Затем в обучаемом механизме можно использовать новые данные, после чего механизм классифицирует новые данные с использованием изученных зависимостей.
Примеры контролируемых способов классификации включают способ линейной регрессии (например, множественную линейную регрессию (MLR), регрессию частных наименьших квадратов (PLS) и регрессию основных компонентов (РОК)), бинарное дерево решений (например, способы рекурсивного секционирования, такие как CART - деревья классификации и регрессии), искусственные нейронные сети, такие как нейронная сеть с обучением по алгоритму обратного распространения, дискриминационный анализ (например, байессовский классификатор или анализ по Фишеру), логистические классификаторы и классификаторы на основе поддерживающих векторов (метод опорных векторов). Предпочтительным контролируемым способом классификации является способ рекурсивного секционирования (публикация патентной заявки США № 20020138208). В неконтролируемой классификации стремятся получить классификацию на основе сходства в наборе обучающих данных без предварительной классификации спектров из которых получают набор обучающих данных. Неконтролируемые способы обучения включают кластерные анализы. В кластерном анализе стремятся разделить данные на "кластеры" или группы, которые в идеале должны содержать члены, которые являются очень сходными друг с другом и очень непохожи на членов других кластеров. Затем сходство определяют с использованием какого-либо критерия расстояния, который определяет расстояние между элементами данных и кластеры тесно связанных элементов данных, которые расположены ближе друг с другом. Способы кластеризации включают алгоритм обучения методом k-средних MacQueen и алгоритм самоорганизующихся карт Kohonen. Алгоритмы обучения, утвержденные для применения в классификации биологической информации, описаны, например, в публикации международной заявки № WO 01/31580 и в публикациях патентных заявок США №№ 20020193950, 20030004402 и 20030055615. Другой способ классификации включает многопараметрические прогностические модели с использованием нелинейной версии классификаторов на основе анализа разделяемости унифицированных максимумов ("USMA"). Подробности классификаторов USMA описаны в публикации патентной заявки США № 20030055615.
Другие алгоритмы и формулы классификации в качестве неограничивающих примеров, наряду с другими, включают анализ главных компонент (PCA), перекрестную корреляцию, чередование факторов, логистическую регрессию (LogReg), линейный дискриминантный анализ (LDA), линейный дискриминантный анализ Eigengene (ELDA), случайный лес (RF), дерево рекурсивного секционирования (RPART), а также другие родственные способы классификации на основе деревьев принятия решений, стянутые центроиды (SC), StepAIC, K-ый ближайший сосед, усиление, деревья принятия решений, нейронные сети, байесовские сети, методы опорных векторов, исключение по одному (LOO), 10-кратную перекрестную проверку (10-кратную CV) и скрытые марковские модели.
Детекцию и корреляцию одного или нескольких криптохромов также можно анализировать с использованием любых подходящих средств, включая пакеты программного обеспечения, например, Applied Maths, GenExplore™, 2-мерный кластерный анализ, анализ основных компонент, дискриминационный анализ, самоорганизующиеся карты; BioDiscovery, Inc., Los Angeles, California (ImaGene™, программное обеспечение по особой обработке изображений и экстракции данных, разработанное MatLab®; GeneSight: иерархическая кластеризация, искусственная нейронная сеть (SOM), анализ основных компонент, временные ряды; AutoGene™; CloneTracker™); GeneData AG (Basel, Switzerland); веб-сайт распознавания молекулярных профилей в Whitehead Genome Center MIT; Rosetta Inpharmatics, Kirkland, Washington. Resolver™ Expression Data Analysis System; Scanalytics, Inc., Fairfax, VA. Его MicroArray Suite позволяет исследователям получать, визуализировать, обрабатывать и анализировать данные микропанелей с экспрессией генов; TIGR (The Institute for Genome Research) предлагает инструментарий программного обеспечения для анализа массивов. Для примеров, также см. Eisen and Brown, (1999) Methods Enzymol. 303: 179-205.
В определенных вариантах осуществления способов квалификации статуса заболевания способы дополнительно включают организацию или модификацию клинического лечения индивидуума на основе статуса заболевания или нарушения. Например, если результат способов по настоящему изобретению является малоубедительным или существует повод полагать, что необходимо подтверждение статуса, лечащий врач может назначить дополнительные тесты (например, срезы КТ, сканирование PET, сканирование MRI, PET-срезы КТ, рентгенограмма, биопсия, анализы крови. Альтернативно, если статус свидетельствует об уместности лечения, лечащий врач может запланировать лечение индивидуума. В других случаях для индивидуума могут применять терапевтическое лечение (такое как введение терапевтических средств (например, таких как соединения формулы I, определенные в настоящем документе, отдельно или в комбинации с одним или несколькими дополнительными терапевтическими средствами), вместо или в дополнение к хирургическому вмешательству. Никакое дополнительное действие не может быть гарантировано. Кроме того, если результаты демонстрируют, что лечение было успешным, необходимыми могут являться поддерживающее лечение или отсутствие дополнительных действий.
Объект изобретения, описываемый в настоящем документе, также предусматривает такие способы, когда криптохромы снова определяют после клинического лечения индивидуума. В этих случаях способы используют для контроля статуса опосредуемого Cry заболевания или нарушения, например, ответа на лечение, ремиссии заболевания или прогрессирования заболевания. Способы можно повторять после каждого проходимого индивидуумом лечения, обеспечивая лечащему врачу контроль эффективности курса лечения. Если результаты демонстрируют, что лечение является неэффективным, курс лечения соответствующим образом можно изменять.
Изобретение относится к наборам для определения статуса заболевания и/или детекции или диагностики заболевания, где наборы можно использовать для детекции одного или нескольких криптохромов. Например, наборы можно использовать для детекции любого одного или нескольких криптохромов, описываемых в настоящем документе, где один или несколько криптохромов дифференциально представлены в образцах индивидуумов с заболеванием и у представляющих норму индивидуумов. Наборы по изобретению имеют множество применений. Например, наборы можно использовать в любом из способов по изобретению, описываемых в настоящем документе, в числе прочего, например, для определения наличия у индивидуума опосредуемого Cry заболевания или нарушения или наличия отрицательного диагноза, таким образом, способствуя диагнозу. В другом примере, наборы можно использовать для идентификации соединений, которые модулируют экспрессию одного или нескольких криптохромов, соединений, которые модулируют активность одного или нескольких криптохромов (например, которые влияют на способность одного или нескольких криптохромов связываться с мишенью, такой как Per1, Per2, рецептор глюкокортикоидов (GR) или промоторная последовательность, распознаваемая криптохромами, такая как промотор CLOCK-BMAL1 или любая другая промоторная последовательность), используя модели опосредуемого Cry заболевания или нарушение на животных in vitro или in vivo. В другом примере наборы можно использовать для идентификации мишеней связывания одного или нескольких белков криптохромов, как определено в настоящем документе.
Наборы по настоящему изобретению могут содержать реагент для детекции, например, нуклеиновые кислоты, которые специфически идентифицируют одну или несколько нуклеиновых кислот криптохромов вследствие наличия гомологичных последовательностей нуклеиновых кислот, таких как олигонуклеотидные последовательности, праймеры или аптамеры, комплементарные к частям нуклеиновых кислот, или антител к белкам, кодируемым нуклеиновыми кислотами, упакованных совместно. Олигонуклеотиды могут представлять собой фрагменты генов. Олигонуклеотиды могут быть одноцепочечными или двухцепочечными. Например, длина олигонуклеотидов может составлять 200, 150, 100, 50, 25, 10 или менее нуклеотидов. Альтернативно, реагент для детекции может представлять собой одно или несколько антител, которые специфически или селективно связываются с одним или несколькими белками криптохромов или их мишенями. Набор может в отдельных контейнерах содержать нуклеиновые кислоты или антитела (уже связанные с твердым матриксом или раздельно упакованные с реагентами для связывания их с матриксом), контрольные составы (положительные и/или отрицательные) и/или детектируемую метку, такую как, наряду с другими, флуоресцеин, зеленый флуоресцентный белок, родамин, цианиновые красители, красители Alexa, люцифераза, радиоактивные метки. В набор можно включать инструкции (например, написанные, кассета, VCR, CD-ROM и т.д.) для проведения анализа и установления корреляции со статусом заболевания.
Например, реагенты для детекции могут быть иммобилизованы на твердом матриксе, таком как пористая полоска с формированием по меньшей мере одного участка детекции. Область определения или детекции пористой полоски может содержать множество участков, содержащих нуклеиновую кислоту. Тестовая полоска также может содержать участки для отрицательных и/или положительных контролей. Альтернативно, контрольные участки могут располагаться на отдельной от тестовой полоске. Необязательно, различные участки детекции могут содержать различные количества иммобилизованных нуклеиновых кислот, например, большее количество в первом участке детекции и меньшие количества в последующих участках. После добавления тестируемого образца, количество участков с выявляемым детектируемым сигналом обеспечивает количественную оценку количества криптохромов, присутствующих в образце. Участки детекции можно конфигурировать в любой подходящей детектируемой форме и, как правило, находятся в форме полосы или точки, занимающих всю ширину тестовой полоски. Субстратная панель может находиться, например, на твердом субстрате, например, "чипе", как описано в патенте США № 5744305. Альтернативно, субстратная панель может представлять собой панель растворов, например, xMAP (Luminex, Austin, TX), Cyvera (Illumina, San Diego, CA), CellCard (Vitra Bioscience, Mountain View, CA) и Quantum Dots' Mosaic (Invitrogen, Carlsbad, CA). Набор также может содержать реагенты и/или ферменты для амплификации или выделения образца ДНК. Наборы могут содержать реагенты для ПЦР с детекцией в реальном времени, например, зонды и/или праймеры TaqMan и ферменты.
В определенных вариантах осуществления набор содержит: (a) субстрат, содержащий на нем адсорбент, где адсорбент удерживает или иным образом подходит для связывания криптохрома, и (b) инструкции для детекции криптохрома посредством приведения образца в контакт с адсорбентом и детекции криптохрома, удерживаемого адсорбентом. В определенных вариантах осуществления набор может содержать элюент (в качестве альтернативы или в комбинации с инструкциями) или инструкции для получения элюента, где комбинация адсорбента и элюента обеспечивает детекцию криптохрома с использованием ионной спектрометрии в газовой фазе.
В других вариантах осуществления набор может содержать первый субстрат, содержащий на нем адсорбент (например, частицу, функционализированную адсорбентом), и второй субстрат, на котором можно располагать первый субстрат с формированием зонда, который можно удалять и вставлять в устройство, например, такое как ионный спектрометр в газовой фазе. В других вариантах осуществления набор может содержать один субстрат, который находится в форме зонда с адсорбентами на субстрате, который можно вынимать и вставлять в устройство. В еще одном варианте осуществления набор может дополнительно содержать префракционированную центрифужную колонку (например, агарозную колонку с Cibacron синим, агарозную колонку с антителом к HSA, эксклюзионную колонку размера K-30, центрифужную колонку для Q-анионного обмена, колонку с одноцепочечной ДНК, колонку с лектинами и т.д.). В другом варианте осуществления набор содержит (a) антитело, которое специфически связывается с одним или несколькими криптохромами; и (b) реагент для детекции. Антитело может представлять собой, например, антитело к продуктам генов криптохромов.
Необязательно набор может дополнительно содержать стандартную или контрольную информацию так, что тестируемый образец можно сравнивать с контрольным информационным стандартом с определением того, представляет ли тестируемое количество одного или нескольких криптохромов, детектируемых в образце, диагностическое количество, согласующееся с диагнозом опосредуемого Cry заболевания или нарушения.
Хотя выше подробно описано только небольшое количество вариантов, возможны другие модификации или дополнения. В частности, в дополнение к характеристикам и/или вариантам, указанным в настоящем документе, могут быть предоставлены дополнительные характеристикам и/или варианты. Например, описанные выше реализации можно применять к различным комбинациям и субкомбинациям описанных характеристик и/или комбинациям и субкомбинациям нескольких дополнительных характеристик, описанных выше. Кроме того, логический алгоритм, описываемый в настоящем документе, для достижения желаемых результатов не требует конкретного представленного порядка или последовательного порядка. В объеме формулы изобретения могут находиться другие варианты осуществления.
ПРИМЕРЫ
Пример 1: Схемы реакций для синтеза соединений
На приводимых ниже схемах реакций, схемах реакций I, II, III, IV, V и VI, приведены способы синтеза соединений формулы I. Если не указано иначе, в общих способах получения соединений формулы I, переменные R1, R2, R3, R4, R5, R6, R7, a и b являются такими, как определено ранее для соединения формулы I. Схемы реакций, описанные в настоящем документе, предназначены для предоставления общего описания методологии, применяемой при получении множества приводимых соединений. Однако из приводимых подробных описаний очевидно, что применяемые способы получения не исчерпываются общими способами, описываемыми в настоящем документе. В частности, следует отметить, что соединения, получаемые в соответствии со схемами, можно дополнительно модифицировать с получением новых соединений, находящихся в объеме настоящего изобретения. Реагенты и промежуточные соединения, использованные в приводимых ниже соединениях, являются или коммерчески доступными, или их могут получать специалисты в области органического синтеза стандартными описанными в литературе способами.
На схеме реакции I, ниже, приведен синтез соединений формулы I. Обработка соответствующим образом замещенного бромидного производного формулы IV соответствующим карбазолом формулы V, в соответствующем растворителе, таком как N,N-диметилформамид или N,N-диметилацетамид, в пределах температурного диапазона приблизительно от 0°C до 150°C в течение периода приблизительно от 5 минут до 24 часов позволяет получать соответствующее оксирановое соединение формулы III. Предпочтительные условия для проведения реакции бромидного соединения формулы IV с карбазолом формулы V с получением соединения формулы III включают проведение реакции в N,N-диметилформамиде при температурах от 0°C до комнатной температуры в присутствии гидроксида калия в течение периода от 20 до 24 часов с последующей экстрактивной обработкой. Обработка соединения формулы III соответствующим амидом или карбамидом формулы II в соответствующем растворителе, таком как N,N-диметилформамид, диметилсульфоксид или N,N-диметилацетамид, в пределах температурного диапазона приблизительно от комнатной температуры до 150°C в течение периода приблизительно от 5 минут до 3 суток позволяет получить соответствующий амидное или карбамидное соединение формулы I. Предпочтительные условия для проведения реакции оксиранового соединения формулы III с получением соединения формулы I включают проведение реакции в N,N-диметилформамиде с гидридом натрия при комнатной температуре в течение периода от 20 до 24 часов с последующей экстрактивной обработкой. Альтернативно, оксирановое соединение формулы III можно подвергать реакции с амидом или карбамидом формулы II в соответствующем растворителе, таком как диметилсульфоксид, соответствующем основании, таком как трет-бутоксид калия, при комнатной температуре в течение 3 суток с получением соединения формулы I.
Схема реакции I
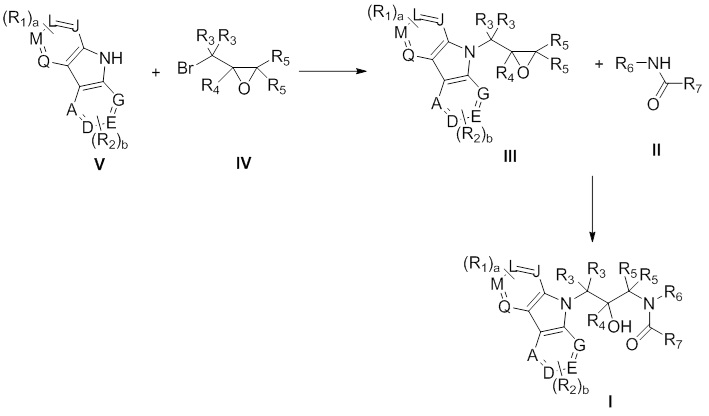
На схеме реакции II ниже приведен альтернативный синтез соединений формулы I. Обработка соответствующим образом замещенного оксиранового производного формулы III соответствующим диамином формулы VII в соответствующем растворителе, таком как этанол, в пределах температурного диапазона от 0°C до 150°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее диаминовое соединение формулы VI. Предпочтительные условия для проведения реакции оксиранового соединения формулы III с диамином формулы VII с получением соединения формулы VI включают проведение реакции в этаноле при 40°C в течение периода от 20 до 24 часов. Обработка соединения формулы VI соответствующим карбонилирующим средством, таким как 1,1'-карбонилдиимидазол, в соответствующем растворителе, таком как тетрагидрофуран, при комнатной температуре в течение периода от 5 минут до 24 часов позволяет получить соответствующее соединение формулы I.
Схема реакции II
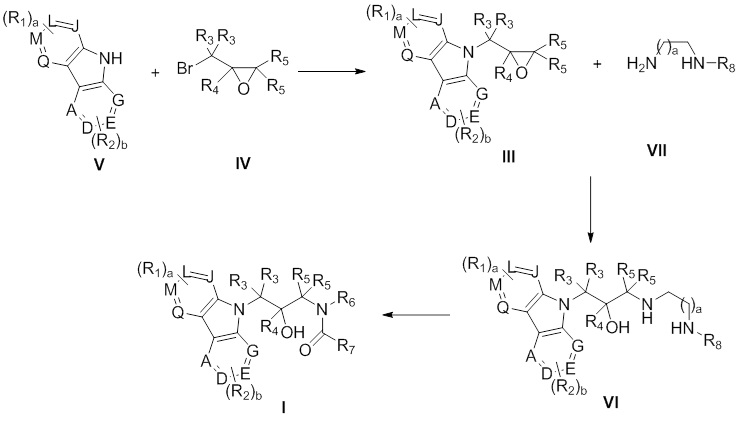
На схеме реакции III ниже приведен альтернативный синтез соединений формулы I. Обработка амидного или карбамидного соединения формулы II соответствующим образом замещенным бромидным производным формулы IX в соответствующем растворителе, таком как тетрагидрофуран, в пределах температурного диапазона приблизительно от 0°C до 65°C в течение периода приблизительно от 5 минут до 24 часов позволяет получать соответствующее оксирановое соединение формулы VIII. Предпочтительные условия для проведения реакции бромидного соединения формулы IX с амидом или карбамидом формулы II с получением соединения формулы VIII включают проведение реакции в тетрагидрофуране при температурах от 0°C до комнатной температуры в присутствии гидрида натрия в течение периода от 20 до 24 часов с последующей экстрактивной обработкой. Обработка соединения формулы VIII соответствующим карбазолом формулы V в соответствующем растворителе, таком как N,N-диметилформамид, в пределах температурного диапазона от 0°C до 70°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее соединение формулы I. Предпочтительные условия для проведения реакции оксиранового соединения формулы VIII карбазолом формулы V с получением соединения формулы I включают проведение реакции в N,N-диметилформамиде при температурах от комнатной температуре до 70°C в присутствии гидрида натрия в течение периода от 20 до 24 часов с получением соединения формулы I.
Схема реакции III
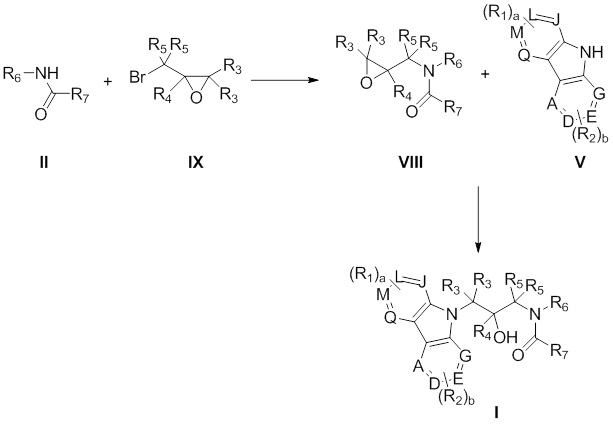
На схеме реакции IV ниже приведен альтернативный синтез соединений формулы I. Обработка соединения Boc-защищенной аминокислоты формулы XIII аммиаком, соответствующим связывающим реагентом, таким как гексафторфосфат N,N,N',N'-тетраметил-O-(1H-бензотриазол-1-ил)урония, соответствующим основанием, таким как N,N-диизопропилэтиламин и соответствующим растворителем, таким как диметилформамид, в пределах температурного диапазона приблизительно от 0°C до 65°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее амидное соединение формулы XII. Обработка Boc-защищенного аминоамидного соединения формулы XII соответствующим восстановителем, таким как бористый водород, в соответствующем растворителе, таком как тетрагидрофуран, в пределах температурного диапазона приблизительно от 0°C до 100°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее Boc-защищенное диаминовое соединение формулы XI. Предпочтительные условия для проведения реакции оксиранового соединения формулы III с Boc-защищенным диамином формулы XI с получением соединения формулы X включают проведение реакции в этаноле при 70°C в течение периода от 16 до 24 часов. Обработка соединения формулы X соответствующим основанием, таким как трет-бутоксид калия, в соответствующем растворителе, таком как тетрагидрофуран, в пределах температурного диапазона приблизительно от 0°C до 100°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее соединение формулы I.
Схема реакции IV
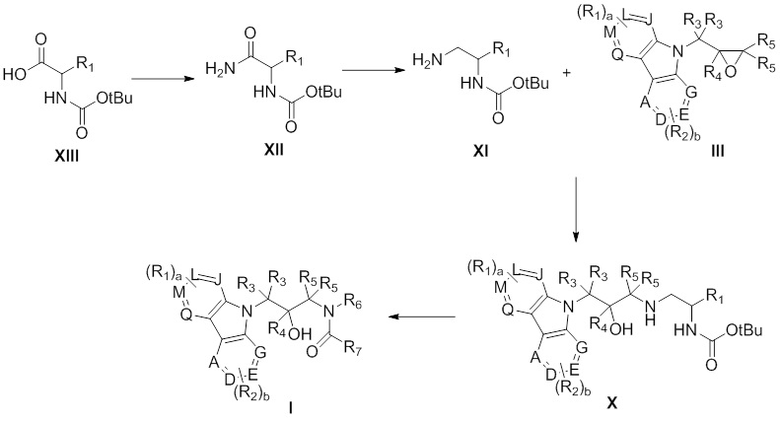
На схеме реакции V ниже приведен альтернативный синтез соединений формулы I. Обработка защищенного бензилом диаминового соединения формулы XVI соответствующим карбанилирующим средством, таким как 1,1'-карбонилдиимидазол, в соответствующем растворителе, таком как тетрагидрофуран, при комнатной температуре в течение периода от 5 минут до 24 часов позволяет получить соответствующее соединение формулы XV. Предпочтительные условия для проведения реакции оксиранового соединения формулы III с защищенным бензилом карбамидом формулы XV с получением соединения формулы XIV включает проведение реакции в N,N-диметилформамиде при температурах от комнатной температуре до 70°C в присутствии гидрида натрия в течение периода от 16 до 24 часов. Обработка замещенного бензилом карбамидного соединения формулы XIV водородом при 6,9-344,7 кПа в присутствии соответствующего катализатора, такого как гидроксид палладия на углероде, соответствующей кислотой, такой как уксусная кислота, в соответствующем растворителе, таком как тетрагидрофуран, в пределах температурного диапазона приблизительно от комнатной температуры до 100°C в течение периода приблизительно от 5 минут до 5 суток позволяет получить соответствующее соединение формулы I.
Схема реакции V
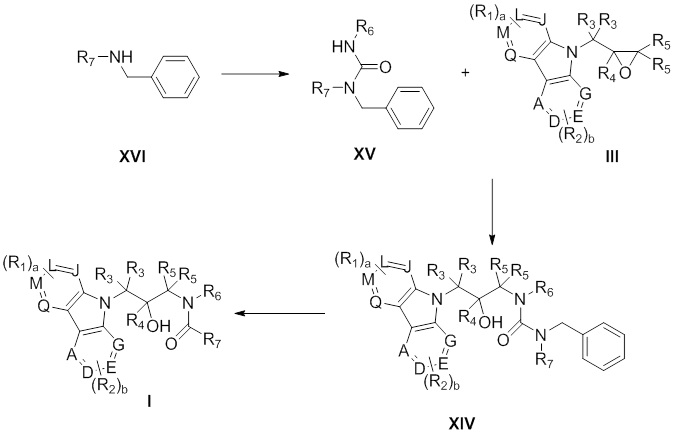
На схеме реакции VI ниже приведен альтернативный синтез соединений формулы I. Обработка соответствующим образом замещенного хирального оксиранового производного формулы XVII или XVIII соответствующим амидным или карбамидным соединением формулы II, соответствующим основанием, таким как гидрид натрия, в соответствующем растворителе, таком как N,N-диметилформамид или тетрагидрофуран, в пределах температурного диапазона от 0°C до 150°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее хиральное амидное или карбамидное соединение формулы I.
Схема реакции VI
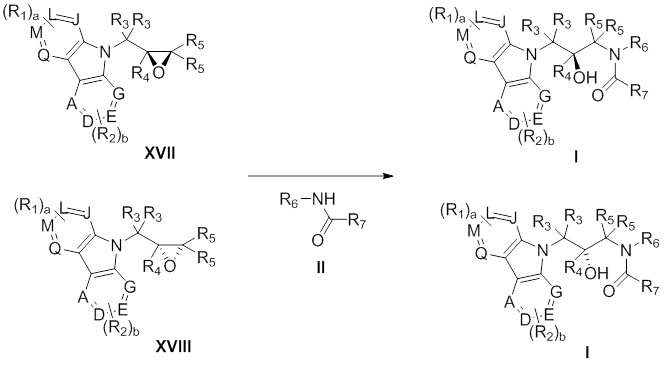
На схеме реакции VII ниже приведен альтернативный синтез соединений формулы I. Обработка соответствующим образом замещенного хирального оксиранового производного формулы XVII или XVIII соответствующим диамином формулы VII в соответствующем растворителе, таком как этанол, в пределах температурного диапазона от 0°C до 150°C в течение периода приблизительно от 5 минут до 24 часов позволяет получить соответствующее хиральное диаминовое соединение формулы VI. Предпочтительные условия для проведения реакции оксиранового соединения формулы XVII или XVIII с диамином формулы VII с получением соединения формулы VI включает проведение реакции в этанол при 55°C в течение периода от 5 до 24 часов. Обработка соединения формулы VI соответствующим карбанилирующим средством, таким как 1,1'-карбонилдиимидазол, в соответствующем растворителе, таком как тетрагидрофуран, при комнатной температуре в течение периода от 5 минут до 24 часов позволяет получить соответствующее соединение формулы I.
Схема реакции VII
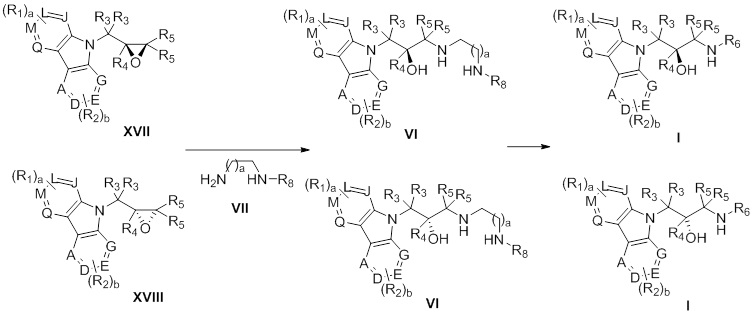
В схемах реакций, описываемых в настоящем документе, следует понимать, что гидроксильные группы в промежуточных соединениях, пригодные для получения соединений формулы I, по мере необходимости можно защищать общепринятыми группами, известными специалистам в данной области. Например, промежуточные соединения, содержащие гидроксильные группы, можно защищать в виде соответствующего трет-бутилдиметилсилильного простого эфира, а затем производить снятие защиты посредством обработки фторидом тетра-н-бутиламмония с получением свободного гидроксильного производного. Подходящие защитные группы и способы их удаления проиллюстрированы в "Protective Groups in Organic Synthesis", 3rd Ed., T. W. Greene and P. G. M. Wuts (Wiley & Sons, 1999).
Спектры ядерного магнитного резонанса (ЯМР) 1H во всех случаях соответствовали предлагаемым структурам. Характеристические химические сдвиги (δ) приведены в виде частей на миллион в сторону слабого поля от тетраметилсилана с использованием общепринятых сокращений для обозначения основных пиков: например, с, синглет; д, дублет; т, триплет; кв., квадруплет; м, мультиплет; ушир., уширенный. Масс-спектры (масса/заряд) записаны с использованием ионизации распылением в электрическом поле (ESI) или химической ионизации при атмосферном давлении (APCI). Когда использована тонкослойная хроматография (TLC) это относится к TLC в силикагеле с использованием планшетов с силикагелем 60 F254, Rf представляет собой расстояние, проходимое соединением, деленое на расстояние, проходимое фронтом растворителя на планшете для TLC. ВЭЖХ относится к высокоэффективной жидкостной хроматографии.
Приводимые ниже конкретные примеры включены в иллюстративных целях и их не следует рассматривать как ограничение настоящего изобретения.
Получение промежуточных соединений
Получение 1: 2-хлор-4-фтор-N-(4-фторфенил)анилин
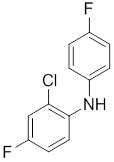
В круглодонную колбу помещали 1-бром-4-фторбензол (13,0 г, 74,3 ммоль), 2-хлор-4-фторанилин (11,354 г, 78,0 ммоль), безводный толуол (200 мл) и трет-бутоксид калия(10,003 г, 89,1 ммоль). Смесь дегазировали и заполняли азотом, а затем добавляли трис(дибензилиденацетон)дипалладий(0) (2,041 г, 2,2 ммоль) и три-трет-бутилфосфин (0,902 г, 4,5 ммоль) и реакционную смесь перемешивали в атмосфере азота при 100°C в течение 16 часов. После охлаждения смесь обрабатывали 6 M водной соляной кислотой до кислого pH, а затем снова доводили до основного pH твердым карбонатом натрия. Смесь сушили (безводный сульфат магния), фильтровали через целит и осадок на фильтре промывали этилацетатом. Фильтрат концентрировали и остаток очищали посредством хроматографии в силикагеле (0-20% этилацетат/гексан) с получением желтоватого масла (14 г, 79%). 1H ЯМР (300 МГц, CDCl3): δ 7,14 (дд, 1H, J=8,4, 3,0 Гц), 7,12-6,98 (м, 5H), 6,88 (тд, 1H, J=8,7, 3,0 Гц), 5,80 (ушир. с, 1H).
Получение 2:3,6-дифтор-9H-карбазол
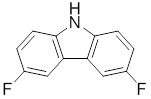
Смесь карбоната калия (26,528 г, 191,9 ммоль), 2-хлор-4-фтор-N-(4-фторфенил)анилина (23,0 г, 96,0 ммоль), тетрафторбората трициклогексилфосфиния (3,534 г, 9,6 ммоль), диацетат палладия (1,077 г, 4,8 ммоль) и безводного N,N-диметилацетамида (200 мл) перемешивали в атмосфере азота при 130°C в течение 16 часов. После охлаждения смесь концентрировали и остаток обрабатывали этилацетатом, фильтровали через целит и осадок на фильтре промывали этилацетатом. Фильтрат концентрировали и остаток очищали посредством короткой колонки с силикагелем (20-50% метиленхлорид/гексан) с получением неочищенного продукта, который перекристаллизовывали из гексана-метиленхлорида с получением чистого продукта в виде белого порошка (17,2 г, 88%). 1H ЯМР (300 МГц, CDCl3): δ 8,00 (ушир. с, 1H), 7,67 (дд, 2H, J=8,7, 2,7 Гц), 7,36 (дд, 2H, J=8,7, 4,2 Гц), 7,19 (тд, 2H, J=9,0, 2,7 Гц).
Получение 3: 9-(оксиран-2-илметил)-9H-карбазол
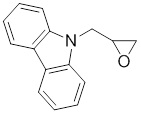
Порошковый гидроксид калия (3,36 г, 60 ммоль) добавляли в раствор карбазола (8,36 г, 50 ммоль) в безводном N,N-диметилформамиде (50 мл) и перемешивали при температуре окружающей среды в течение 1 часа. Реакционную смесь охлаждали в ледяной бане и добавляли эпибромгидрин (10,3 мл, 125 ммоль). Ледяную баню удаляли и реакционную смесь перемешивали при комнатной температуре в течение 20 часов. Смесь разделяли между этилацетатом и водой. Органический слой последовательно промывали водой и насыщенным раствором водного хлорида натрия, сушили (безводный сульфат натрия), фильтровали и концентрировали. Неочищенное вещество растирали с гексаном и перекристаллизовывали из этилацетата/гексана с получением желаемого продукта в виде белых игл (6,41 г, выход 58%). Из маточного раствора кристаллизовали вторую партию кристаллов с получением дополнительного продукта (1,2 г, 11%). 1H ЯМР (300 МГц, CDCl3) δ 8,11-8,08 (м, 2H), 7,46-7,44 (м, 4H), 7,28-7,25 (м, 2H), 4,68-4,62 (дд, 1H, J=3,1, 15,8 Гц) 4,45-4,38 (дд, 1H, J=4,8, 15,9 Гц), 3,37 (м, 1H), 2,84-2,81 (дд, 1H, J=4,2, 4,3 Гц), 2,60-2,57 (дд, 1H, J=2,5, 5,0 Гц); анализ ВЭЖХ: (C18, 5-95% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 7,83 мин, 98,7%.
Приводимые ниже соединения получали аналогичным образом:
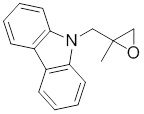
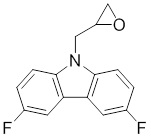
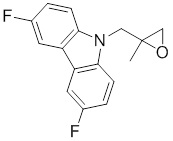
Получение 4: 1-бензоилпирролидин-2-он
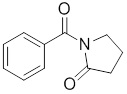
К охлажденному до 0°C раствору 2-пирролидинона (4,4 г, 51,7 ммоль, 1,0 эквив.) и триэтиламина (15,4 мл, 111,2 ммоль, 2,1 эквив.) в безводном тетрагидрофуране (120 мл) добавляли 4-диметиламинопиридин (0,075 г) и бензоилхлорид (6,9 мл, 59,5 ммоль, 1,1 эквив.). Полученную смесь перемешивали в течение 16 часов при комнатной температуре. Смесь выливали в воду и экстрагировали этилацетатом. Органическую фракцию промывали 0,1 M водной соляной кислотой, насыщенным водным бикарбонатом натрия и насыщенным раствором водного хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением красного масла. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 20-65% этилацетата в гексане с получением почти белого твердого вещества (5,63 г, 58%). 1H ЯМР (300 МГц, CDCl3): δ 7,61-7,57 (м, 2H), 7,53-7,47 (тт, 1H, J=1,5, 7,5 Гц), 7,42-7,37 (м, 2H), 3,98-3,94 (т, 2H, J=7,1 Гц), 2,61-2,58 (т, 2H, J=8,0 Гц), 2,20-2,10 (квинт., 2H, J=7,5 Гц). ESI (масса/заряд): 190,1 (M+H).
Получение 5: 1-бензоил-3-фторпирролидин-2-он
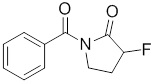
К раствору 1-бензоилпирролидин-2-она (1 г, 5,3 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (26 мл) при -78°C добавляли диизопропиламида лития (3,382 мл 2 M раствора в тетрагидрофуране, 6,8 ммоль, 1,3 эквив.) и смесь перемешивали при -78°C в течение 30 минут. Медленно добавляли раствор н-фторбензолсульфонимида (2,5 г, 7,9 ммоль, 1,5 эквив.) в безводном тетрагидрофуране (5 мл) при -78°C и реакционную смесь перемешивали в течение 1 часа при -40°C. Добавляли насыщенный водный гидрокарбонат натрия, раствор нагревали до комнатной температуры и экстрагировали этилацетатом. Органический слой промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением желтого твердого вещества. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции из силикагеля в градиенте 15-60% этилацетата в гексане с получением белого твердого вещества (0,595 г, 54%). 1H ЯМР (300 МГц, CDCl3): δ 7,64-7,61 (м, 2H), 7,57-7,52 (тт, 1H, J=1,5, 7,5 Гц), 7,45-7,39 (м, 2H), 5,28-5,06 (дт, 1H, J=7,8, 51 Гц), 4,15-4,07 (м, 1H), 3,87-3,78 (м, 1H), 2,68-2,56 (м, 1H), 2,45-2,27 (м, 1H). 19F ЯМР (282 МГц, CDCl3): δ от -188,9 до -189,2 (ддд, J=12,1, 24,2, 51,8 Гц).
Получение 6: 3-фторпирролидин-2-он

К раствору 1-бензоил-3-фторпирролидин-2-она (0,282 г, 1,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (5 мл) добавляли октиламин (0,259 мл, 1,6 ммоль, 1,1 эквив.) и реакционную смесь перемешивали в течение 16 часов при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении с получением желтого масла. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 70-100% этилацетата в гексане с получением белого твердого вещества. (0,104 г, выход 74%). 1H ЯМР (300 МГц, CDCl3): δ 7,81 (ушир. с, 1H), 5,11-4,89 (ддд, 1H, J=6,3, 7,8, 52,8 Гц), 3,49-3,42 (м, 1H), 3,36-3,27 (м, 1H), 2,57-2,41 (м, 1H), 2,34-2,13 (м, 1H). 13C ЯМР (75 МГц, CDCl3): δ 173,5-173,3 (д, J=20 Гц), 89,9-87,4 (д, J=182 Гц), 39,1 (д, J=4 Гц), 28,6-28,4 (д, J=20 Гц). 19F ЯМР (282 МГц, CDCl3): δ от -190,1 до -190,4 (ддд, J=15, 27, 52 Гц).
Получение 7: трет-бутил-2-оксопиперидин-1-карбоксилат
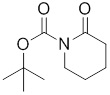
К перемешиваемому раствору пиперидин-2-она (5 г, 50,4 ммоль, 1,0 эквив.), триэтиламина (14,022 мл, 100,9 ммоль, 2,0 эквив.) и N,N-4-диметиламинопиридина (0,123 г, 1,0 ммоль) в метиленхлориде (100 мл) при 0°C добавляли ди-трет-бутилдикарбонат (16,512 г, 75,7 ммоль, 1,5 эквив.). Смесь медленно нагревали до комнатной температуры и перемешивали в течение 48 часов. Реакцию гасили водой и органический слой последовательно промывали 1 Н водной соляной кислотой, насыщенным водным бикарбонатом натрия и насыщенным водным хлоридом натрия и сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-100% этилацетат/гексан) с получением желаемого продукта в виде желтого масла (8,5 г, 85%). 1H ЯМР (300 МГц, CDCl3): δ 3,72-3,62 (м, 2H), 2,58-2,48 (м, 2H), 1,90-1,78 (м, 4H), 1,55 (с, 9H).
Получение 8: трет-бутил-3-фтор-2-оксопиперидин-1-карбоксилат
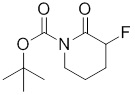
К перемешиваемому раствору трет-бутил-2-оксопиперидин-1-карбоксилата (3 г, 15,1 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (70 мл) в атмосфере азота при -78°C капельно добавляли бис(триметилсилил)амид натрия (22,586 мл 1 M раствора в тетрагидрофуране, 22,6 ммоль, 1,5 эквив.) в течение периода 30 минут. Полученный раствор перемешивали в течение 45 минут при -78°C, а затем капельно добавляли раствор н-фторбензолсульфонимида (7,122 г, 22,6 ммоль, 1,5 эквив.) в безводном тетрагидрофуране (30 мл) в течение периода 30 минут. Реакционную смесь перемешивали при -78°C в течение 1 часа, а затем оставляли медленно нагреваться до комнатной температуры в течение 2 часов и перемешивали при комнатной температуре в течение 1 часа. Реакцию гасили насыщенным водным хлоридом аммония и экстрагировали этилацетатом. Органическую фазу промывали насыщенным водным хлоридом натрия и сушили над безводным сульфатом магния, фильтровали и концентрировали при пониженном давлении. Остаток обрабатывали простым диэтиловым эфиром и удаляли твердые вещества. Раствор концентрировали и остаток очищали посредством хроматографии на колонке с силикагелем (0-100% этилацетат/гексан) с получением фракций неочищенного продукта и побочного дифторного продукта в виде белого твердого вещества (1,5 г). Фракцию неочищенного продукта дополнительно очищали посредством второго прохода хроматографии в силикагеле с получением желаемого продукта в виде густого масла (0,46 г, 14%). 1H ЯМР (300 МГц, CDCl3): δ 4,92 (ддд, 1H, J=47,4, 8,7, 6,3 Гц), 3,78-3,60 (м, 2H), 2,35 (м, 1H), 2,15-1,80 (м, 3H), 1,55 (с, 9H). 19F ЯМР (282 МГц, CDCl3): δ -185,2 (дт, J=45,7, 15,5 Гц).
Получение 9: 3-фторпиперидин-2-он
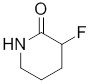
К охлажденному до 0°C раствору трет-бутил-3-фтор-2-оксопиперидин-1-карбоксилата (0,450 г, 2,1 ммоль, 1,0 эквив.) в метиленхлориде (5 мл) добавляли трифторуксусную кислоту (1 мл, 13,5 ммоль, 6,5 эквив.) и полученный раствор перемешивали в течение 3 часов. Реакционную смесь концентрировали при пониженном давлении и остаток очищали на колонке с силикагелем (0-100% этилацетат/гексан, а затем 0-20% метанол/этилацетат) с получением желаемого продукта в виде белого порошка (0,23 г, 95%). 1H ЯМР (300 МГц, CDCl3): δ 6,36 (ушир. с, 1H), 4,85 (ддд, 1H, J=46,8, 8,1, 5,4 Гц), 3,50-3,20 (м, 2H), 2,40-1,70 (м, 4H). 19F ЯМР (282 МГц, CDCl3): δ -186,5 (дт, J=46,5, 15,5 Гц).
Получение 10: 3,3-дифторпиперидин-2-он
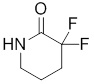
3,3-дифторпиперидин-2-он получали в соответствии с опубликованными способами (Kim, B. C. et al. Synthesis 2012, 44, 3165-3170).
Получение 11: 1-бензоил-3,3-дифторпирролидин-2-он
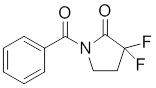
К охлажденному до -78°C раствору 1-бензоил-3-фторпирролидин-2-она после получения 21B (0,3 г, 1,4 ммоль, 1,0 эквив.) и н-фторбензолсульфонимида (0,639 г, 2,0 ммоль, 1,4 эквив.) в безводном тетрагидрофуране (10 мл) добавляли диизопропиламид лития (0,905 мл 2 M раствора в тетрагидрофуране, 1,8 ммоль, 1,3 эквив.) и смесь перемешивали при -78°C в течение 30 минут. Добавляли дополнительные порции раствора диизопропиламида лития (0,5 эквив.) и н-фторбензолсульфонимида (0,5 эквив. в 0,5 мл безводного тетрагидрофурана) и смесь перемешивали в течение 1 часа при -78°C. Добавляли насыщенный водный гидрокарбонат натрия, смесь нагревали до комнатной температуры и экстрагировали этилацетатом. Органический слой промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 15-50% этилацетата в гексане с получением белого твердого вещества (0,09 г, 23%). 1H ЯМР (300 МГц, CDCl3): δ 7,66-7,61 (м, 2H), 7,59-7,55 (м, 1H), 7,47-7,44 (м, 2H), 4,02-3,97 (м, 2H), 2,70-2,56 (тт, 2H, J=6,6, 14,7 Гц). 19F ЯМР (282 МГц, CDCl3): δ от -106,0 до -106,1 (т, J=15 Гц).
Получение 12: 3,3-дифторпирролидин-2-он
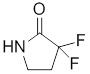
К раствору 1-бензоил-3,3-дифторпирролидин-2-она (0,085 г, 0,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (1 мл) добавляли октиламин (0,075 мл, 0,5 ммоль, 1,1 эквив.) и реакционную смесь перемешивали в течение 16 часов при комнатной температуре. Смесь концентрировали при пониженном давлении с получением желтого масла. Неочищенный остаток очищали посредством хроматографии на колонке с силикагелем элюции в градиенте 50-100% этилацетата в гексане с получением белого твердого вещества (0,024 г, выход 52%). 1H ЯМР (300 МГц, CDCl3): δ 7,93 (ушир. с, 1H), 3,50-3,46 (ушир. т, 2H, J=6,0 Гц), 2,63-2,48 (тт, 2H, J=6,6, 15,2 Гц). 19F ЯМР (282 МГц, CDCl3): δ от -107,33 до -107,44 (т, J=15,2 Гц). 13C ЯМР (75 МГц, CDCl3): δ 167,5-166,7 (т, J=31 Гц), 121,1-114,4 (т, J=248 Гц), 37,1 (т, J=3,3 Гц), 31,2-30,6 (т, J=23,1 Гц).
Получение 13: 1-бензил-3-метилпирролидин-2-он; общий способ
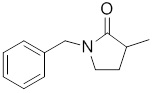
К охлажденному до -78°C раствору 1-бензил-2-пирролидинона (0,422 г, 2,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (15 мл) добавляли диизопропиламид лития (2,4 мл 2 M раствора, 4,8 ммоль, 2,0 эквив.) и полученный красный раствор перемешивали в течение 30 минут при -78°C и добавляли йодметан (0,6 мл, 9,6 ммоль, 4,0 эквив.). Раствор перемешивали при -78°C в течение 1 часа и оставляли медленно нагреваться до комнатной температуры в течение 16 часов. Добавляли насыщенный водный хлорида аммония и смесь экстрагировали этилацетатом. Органическую фракцию промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 35-80% этилацетата в гексане с получением продукта в виде желтовато-коричневой жидкости (0,374 г, 82%). 1H ЯМР (300 МГц, CDCl3): δ 7,37-7,34 (м, 5H), 4,52-4,41 и 4,46-4,41 (ABq, 2H, J=14,6 Гц), 3,27-3,15 (м, 2H), 2,60-2,46 (м, 1H), 2,28-2,15 (м, 1H), 1,68-1,58 (м, 1H), 1,28-1,25 (д, 3H, J=7,2 Гц).
Приводимые ниже соединения получали аналогичным образом:
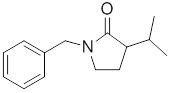
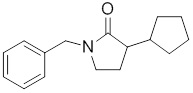
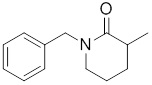
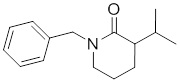
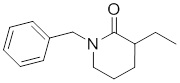
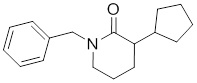
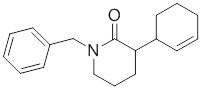
Получение 14: 1-бензил-3-циклогексилпиперидин-2-он
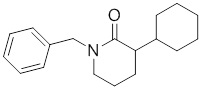
в раствор 1-бензил-3-(циклогекс-2-ен-1-ил)пиперидин-2-она (0,6 г, 2,3 ммоль) в этаноле (10 мл) в атмосфере азота добавляли 10% палладий на углероде (0,09 г). Смесь помещали в атмосфере водорода и перемешивали в течение 2 суток. Суспензию фильтровали через целит и концентрировали при пониженном давлении с получением желаемого продукта в виде прозрачной жидкости (0,578 г, 98%). 1H ЯМР (300 МГц, CDCl3): δ 7,33-7,22 (м, 5H), 4,66-4,61 и 4,59-4,54 (ABq, 2H, J=14,7 Гц), 3,19-3,14 (м, 2H), 2,34-2,21 (м, 2H), 1,86-1,52 (м, 9H), 1,39-1,04 (м, 5H); ESI (масса/заряд): 272,2 (M+H).
Получение 15: 1-бензил-3-фенилпиперидин-2-он
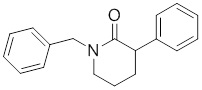
Синтезировано в соответствии со способом из de Filippis, A. et al. Tetrahedron, 2004, 60, 9757. К охлажденному (-20°C) перемешиваемому раствору н-бензил-2-пиперидинона (1,326 г, 7,0 ммоль, 2,2 эквив.) в безводном тетрагидрофуране (14 мл, 0,5 M) добавляли бис(триметилсилил)амид лития (6,4 мл 1 M раствора в безводном тетрагидрофуране, 6,4 ммоль, 2,0 эквив.) и смесь перемешивали в течение 20 минут при -20°C. Добавляли раствор хлорида цинка (0,955 г, 7,0 ммоль, 2,2 эквив.) в безводном тетрагидрофуране (8 мл) и раствор перемешивали в течение 20 минут при -20°C. Полученный раствор канюлировали в раствор 2-дициклогексилфосфино-2'-(N,N-диметиламино)бифенила (0,094 г), трис(дибензилиденацетон)дипалладия(0) (0,092 г) и бромбензола (0,335 мл, 3,2 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (6 мл) и полученную смесь нагревали при 70°C в течение 6 часов. Реакцию гасили водным хлоридом аммония и экстрагировали этилацетатом. Органическую фракцию промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 15-60% этилацетата в гексане с получением желтой жидкости (0,629 г, 74%). 1H ЯМР (300 МГц, CDCl3): δ 7,38-7,21 (м, 10H), 4,74-4,69 и 4,66-4,61 (AB, 2H, J=14,4 Гц), 3,77-3,72 (дд, 1H, J=6,0, 8,1 Гц), 3,41-3,28 (м, 2H), 2,23-2,13 (м, 1H), 2,05-1,69 (м, 3H).
Получение 16: 3-метилпирролидин-2-он
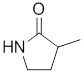
В раствор 1-бензил-3-метилпирролидин-2-она (0,323 г, 1,7 ммоль, 1,0 эквив.) в толуоле (2 мл, 1 M) добавляли трифторметансульфоновую кислоту (0,604 мл, 6,8 ммоль, 4,0 эквив.). Смесь нагревали при 195°C в микроволновом реакторе в течение 25 минут. Смесь выливали в небольшое количество насыщенного водного бикарбоната натрия, экстрагировали этилацетатом, промывали насыщенным водным хлоридом натрия и комбинированные водные слои снова экстрагировали этилацетатом. Комбинированные органические фракции сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Неочищенный остаток очищали посредством хроматографии на колонке с силикагелем, элюцией 0-10% метанолом в метиленхлориде с получением желаемого продукта (0,087 г). 1H ЯМР (300 МГц, CDCl3): δ 6,49 (ушир. с), 3,37-3,26 (м, 2H), 2,53-2,28 (м, 2H), 1,80-1,65 (м, 1H), 1,21-1,19 (д, 3H, J=6,6 Гц).
Приводимые ниже соединения получали аналогичным образом:
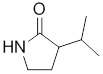
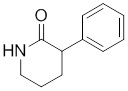
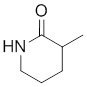
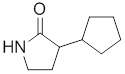
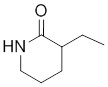
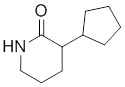
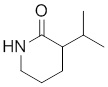
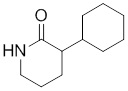
Получение 17: 1-бензил-3-(1-гидроксициклобутил)пирролидин-2-он
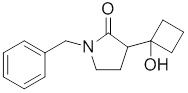
К охлажденному (-78°C) раствору 1-бензил-2-пирролидинона (1,0 г, 5,7 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (19 мл) добавляли диизопропиламид лития (3,15 мл 2 M раствора в тетрагидрофуране, 1,1 эквив.) и смесь перемешивали в течение 1 часа при -78°C. Добавляли циклобутанон (0,426 мл, 5,7 ммоль, 1,0 эквив.) и диэтилэфирaт трифторида бора (0,704 мл, 5,7 ммоль, 1,0 эквив.) и реакционную смесь перемешивали при -78°C в течение 4 часов. Реакцию гасили насыщенным водным хлоридом аммония и экстрагировали этилацетатом. Органическую фракцию промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем элюции из силикагеля в градиенте 50-100% этилацетата в гексане с получением белого твердого вещества (0,714 г, 51%). 1H ЯМР (300 МГц, CDCl3): δ 7,36-7,20 (м, 5H), 4,56-4,51 и 4,42-4,37 (AB, 2H, J=14,7 Гц), 4,24 (с, 1H), 3,28-3,21 (м, 2H), 2,78-2,72 (т, 1H, J=2,7 Гц), 2,34-1,89 (м, 7H), 1,66-1,52 (м, 1H); ESI (масса/заряд): 246,0 (M+H).
Приводимое ниже соединение получали аналогично:
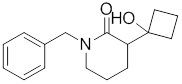
Получение 18: 1-бензил-3-циклобутилиденпирролидин-2-он:
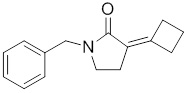
К охлажденному (0°C) раствору 1-бензил-3-(1-гидроксициклобутил)пирролидин-2-она (0,7 г, 2,9 ммоль, 1,0 эквив.) в безводном метиленхлориде (12 мл) добавляли N,N-диизопропилэтиламин (2,485 мл, 14,3 ммоль, 5,0 эквив.), N,N-4-диметиламинопиридин (0,07 г, 0,6 ммоль, 0,2 эквив.) и метансульфонилхлорид (0,331 мл, 4,3 ммоль, 1,5 эквив.). Смесь перемешивали при 0°C в течение 2 часов, при комнатной температуре 16 часов и при кипячении с обратным холодильником в течение 3 часов. Смесь охлаждали до комнатной температуры и разделяли между этилацетатом и насыщенным водным хлоридом аммония. Органический слой промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением оранжевого масла. Неочищенный продукт очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 20-60% этилацетата в гексане с получением желтого масла (0,25 г, 38%). 1H ЯМР (300 МГц, CDCl3): δ 7,33-7,23 (м, 5H), 4,47 (с, 2H), 3,27-3,19 (м, 4H), 2,75-2,69 (м, 2H), 2,52-2,46 (м, 2H), 2,18-2,08 (квинт., 2H, J=7,8 Гц); ESI (масса/заряд): 228,2 (M+H).
Приводимое ниже соединение получали аналогично:
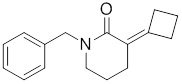
Получение 19: 1-бензил-3-циклобутилпирролидин-2-он
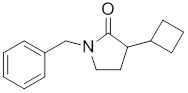
К раствору 1-бензил-3-циклобутилиденпирролидин-2-она (0,25 г, 1,0 ммоль) в этаноле (11 мл) добавляли 10% палладий на углероде (0,05 г) и реакционную смесь перемешивали в атмосфере водорода в течение 72 часов. Смесь фильтровали через целит и концентрировали при пониженном давлении с получением прозрачного масла (0,242 г, 100%). 1H ЯМР (300 МГц, CDCl3): δ 7,34-7,20 (м, 5H), 4,49-4,47 и 4,40-4,35 (ABq, 2H, J=14,4 Гц), 3,18-3,13 (м, 2H), 2,69-2,47 (м, 2H), 2,20-1,64 (м, 8H); ESI (масса/заряд): 230,2 (M+H).
Приводимое ниже соединение получали аналогично:
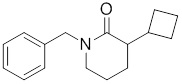
Получение 20: 3-циклобутилпирролидин-2-он:
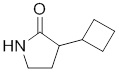
Получали из 1-бензил-3-циклобутилпирролидин-2-она аналогично получению 18. 1H ЯМР (300 МГц, CDCl3): δ 5,45 (ушир. с, 1H), 3,34-3,27 (м, 2H), 2,65-2,54 (м, 1H), 2,43-2,35 (м, 1H), 2,28-1,79 (м, 8H).
Приводимое ниже соединение получали аналогично:
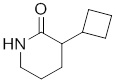
Получение 21: N1-циклогексилэтан-1,2-диамин
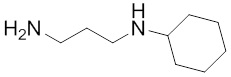
К смеси циклогексанона (6,26 г, 63,8 ммоль), этилендиамина (42,64 мл, 637,8 ммоль, 10,0 эквив.), уксусной кислоты (36,515 мл, 637,8 ммоль, 10,0 эквив.) и 4Å молекулярных сит (25 г) в безводном метаноле (250 мл) добавляли цианоборогидрид натрия (8,017 г, 127,6 ммоль, 2,0 эквив.). Смесь перемешивали в течение 48 часов, фильтровали для удаления твердых веществ и концентрировали до полутвердого состояния. Неочищенное вещество растворяли в 3 Н водном гидроксиде натрия (150 мл) и три раза экстрагировали метиленхлоридом. Комбинированные органические фракции немного промывали основным насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением бледно-желтой жидкости, которую очищали посредством вакуумной перегонки с получением прозрачной жидкости (4,1 г, 45%). 1H ЯМР (300 МГц, CDCl3): δ 2,80-2,76 (тд, 2H, J=0,9, 6,0 Гц), 2,68-2,64 (тд, 2H, J=0,9, 6,0 Гц), 2,43-2,34 (м, 1H), 1,89-1,83 (м, 2H), 1,74-1,70 (м, 2H), 1,62-1,57 (м, 1H), 1,32-0,98 (м, 8H).
Получение 22: 3-(циклобутиламино)пропаннитрил
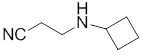
Циклобутиламин (5,90 мл, 59,8 ммоль, 1,0 эквив.) при комнатной температуре в течение 15 минут капельно добавляли к раствору акрилонитрила (4,76 г, 89,7 ммоль, 1,5 эквив.) в метаноле (7 мл). Смесь перемешивали при комнатной температуре в течение 30 минут и при кипячении с обратным холодильником в течение 1 часа, охлаждали до комнатной температуры, концентрировали при пониженном давлении и желаемый продукт перегоняли в вакууме с получением прозрачной жидкости (7,7 г, 98%). 1H ЯМР (300 МГц, CDCl3): δ 3,29-3,21 (м, 1H), 2,88-2,83 (т, 2H, J=6,6 Гц), 2,50-2,46 (т, 2H, J=6,6 Гц), 2,26-2,20 (м, 2H), 1,76-1,63 (м, 4H), 1,30 (ушир. с, 1H).
Получение 23: N1-циклобутилпропан-1,3-диамин
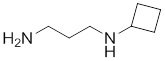
К охлаждаемой (0°C) суспензии гидрида лития алюминия (3,056 г, 80,5 ммоль, 2,0 эквив.) в простом безводном эфире (120 мл) капельно добавляли раствор 3-(циклобутиламино)пропаннитрила (5,0 г, 40,3 ммоль, 1,0 эквив.) в простом безводном диэтиловом эфире (40 мл) в течение 45 минут. Реакционную смесь перемешивали при комнатной температуре в течение 15 минут и при кипячении с обратным холодильником в течение 4 часов, охлаждали до комнатной температуры и перемешивали в течение 1 часа. Смесь охлаждали до 0°C и интенсивно перемешивали при капельном добавлении воды (3,1 мл) с последующим 15% водным гидроксидом натрия (3,1 мл) и в заключение водой (9,3 мл). Полученную взвесь нагревали до комнатной температуры, перемешивали в течение 15 минут и добавляли сульфат магния, перемешивая в течение дополнительных 15 минут. Твердые вещества удаляли посредством фильтрации через пористый стеклянный фильтр, несколько раз промывая теплым метиленхлоридом, и органический раствор концентрировали при пониженном давлении с получением желаемого продукта в виде бледно-желтой жидкости (3,44 г, 66%). 1H ЯМР (300 МГц, CDCl3): δ 3,14 (м, 1H), 2,69-2,62 (м, 2H), 2,53-2,45 (м, 2H), 2,13-2,10 (м, 2H), 1,56-1,48 (м, 6H), 1,33 (ушир. с, 3H).
Получение 24: 3-(циклопентиламино)пропаннитрил
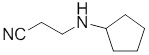
Циклопентиламин (5,794 мл, 58,7 ммоль, 1,0 эквив.) при комнатной температуре капельно добавляли к раствору акрилонитрила (5,79 мл, 88,1 ммоль, 1,5 эквив.) в метаноле (7 мл). Раствор перемешивали при комнатной температуре в течение 30 минут и при кипячении с обратным холодильником в течение 1 часа, охлаждали до комнатной температуры, концентрировали при пониженном давлении и желаемый продукт перегоняли в вакууме с получением прозрачной жидкости (7,4 г, 91%). 1H ЯМР (300 МГц, CDCl3): δ 3,14-3,04 (квинт., 1H, J=6,3 Гц), 2,91-2,87 (т, 2H, J=6,9 Гц), 2,53-2,48 (тд, 2H, J=0,9, 6,9 Гц), 1,88-1,78 (м, 2H), 1,73-1,49 (м, 4H), 1,36-1,24 (м, 2H), 1,19 (ушир. с, 1H).
Получение 25: N1-циклопентилпропан-1,3-диамин
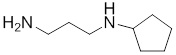
К охлаждаемой (0°C) суспензии гидрида лития алюминия (3,295 г, 86,8 ммоль, 2,0 эквив.) в простом безводном диэтиловом эфире (150 мл) капельно добавляли раствор 3-(циклопентиламино)пропаннитрила (6,0 г, 43,4 ммоль, 1,0 эквив.) в простом безводном диэтиловом эфире (40 мл) в течение 45 минут. Реакционную смесь перемешивали при комнатной температуре в течение 15 минут и при кипячении с обратным холодильником в течение 4 часов, охлаждали до комнатной температуры и перемешивали в течение 1 часа. Смесь охлаждали до 0°C и интенсивно перемешивали при капельном добавлении воды (3,4 мл) с последующим 15% водным гидроксидом натрия (3,4 мл) и в заключение водой (10,2 мл). Полученную взвесь нагревали до комнатной температуры, перемешивали в течение 15 минут и добавляли сульфат магния, перемешивая в течение дополнительных 15 минут. Твердые вещества удаляли посредством фильтрации через пористый стеклянный фильтр, несколько раз промывая теплым метиленхлоридом, и органический раствор концентрировали при пониженном давлении с получением желаемого продукта в виде прозрачного масла (4,5 г, 73%). 1H ЯМР (300 МГц, CDCl3): δ 3,05-2,96 (квинт., 1H, J=6,6 Гц), 2,74-2,71 (т, 2H, J=6,6 Гц), 2,68-2,58 (т, 2H, J=6,9 Гц), 1,85-1,68 (м, 2H), 1,62-1,42 (м, 6H), 1,34 (ушир. с, 3H), 1,30-1,21 (м, 2H).
Получение 26: 1-((3-(циклогексиламино)пропил)амино)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-метилпропан-2-ол; общий способ
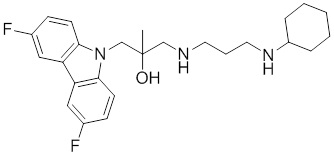
К раствору н-циклогексил-1,3-пропандиамина (или другого н-замещенного 1,3-пропандиамина, 8,0 эквив.) в этаноле (1 M) добавляли 3,6-дифтор-9-((2-метилоксиран-2-ил)метил)-9H-карбазол (1,0 эквив., или альтернативно 3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазол) и реакционную смесь перемешивали при 70°C в течение 16 часов или до определения завершения реакции посредством LCMS, охлаждали до комнатной температуры, концентрировали при пониженном давлении с получением неочищенного остатка, который очищали посредством хроматографии на колонке, элюируя из HP силикагеля соответствующим градиентом метанола в метиленхлориде и 0,1% триэтиламине с получением желаемого продукта.
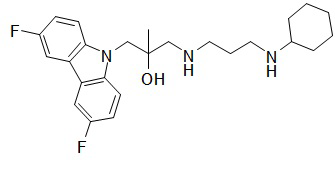
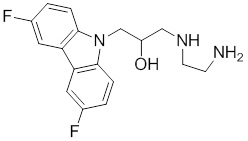
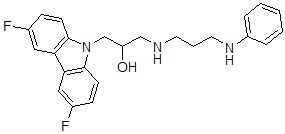
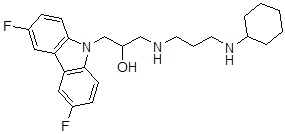
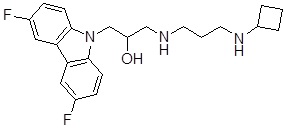
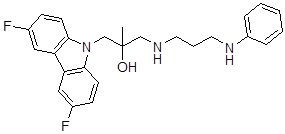
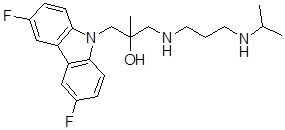
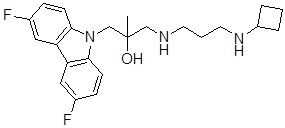
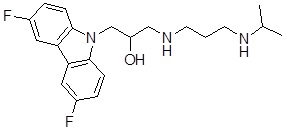
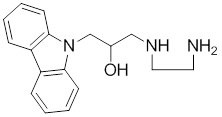
Получение 27: трет-бутил (1-амино-1-оксопропан-2-ил)карбамат
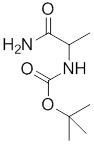
Смесь Boc-DL-аланина (5,0 г, 26,4 ммоль, 1,0 эквив.), гексафторфосфата N,N,N',N'-тетраметил-O-(1H-бензотриазол-1-ил)урония (15,033 г, 39,6 ммоль, 1,5 эквив.), N,N-диизопропилэтиламина (8,735 мл, 52,9 ммоль, 2,0 эквив.) и безводного диметилформамида (50 мл) перемешивали при комнатной температуре в течение 20 минут, а затем охлаждали ледяной водой, и в смесь медленно барботировали аммиак (2,250 г, 132,1 ммоль, 5,0 эквив.). Реакционную смесь перемешивали при комнатной температуре в течение 3 часов в герметичном сосуде. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органические слои промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Полученные твердые вещества промывали холодным этилацетатом и простым эфиром и сушили с получением продукта в виде белого порошка (2,9 г, 58%). 1H ЯМР (300 МГц, CDCl3): δ 6,20 (ушир. с, 1H), 5,50 (ушир. с, 1H), 5,00 (ушир. с, 1H), 4,20 (м, 1H), 1,47 (с, 9H), 1,40 (д, 3H, J=7,2 Гц).
Получение 28: трет-бутил (1-аминопропан-2-ил)карбамат
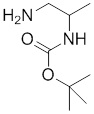
Трет-бутил (1-амино-1-оксопропан-2-ил)карбамат (2,2 г) растворяли в безводном тетрагидрофуране (100 мл) и добавляли бористый водород (40 мл 1 M раствора в тетрагидрофуране). Смесь перемешивали при комнатной температуре в течение 2 часов, а затем нагревали при 90°C в течение 2 часов. После охлаждения до комнатной температуры, реакцию гасили метанолом до отсутствия пузырьков. Смесь нагревали при 90°C в течение 1 часа, а затем концентрировали досуха с получением неочищенного продукта в виде сиропа (2,2 г), который использовали непосредственно на следующем этапе реакции. 1H ЯМР (300 МГц, CDCl3): δ 4,60 (ушир. с, 1H), 3,65 (м, 1H), 2,76 (дд, 1H, J=12,9, 5,1 Гц), 2,64 (дд, 1H, J=12,9, 6,3 Гц), 1,47 (с, 9H), 1,14 (д, 3H, J=6,9 Гц).
Получение 29: трет-бутил (1-((3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)амино)пропан-2-ил)карбамат
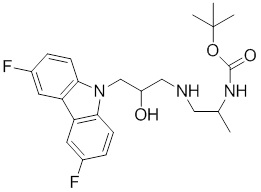
Раствор 3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазола (0,7 г) и трет-бутил-(1-аминопропан-2-ил)карбамата (1,5 г) в этаноле (50 мл) в атмосфере азота перемешивали при 70°C в течение 16 часов. Смесь концентрировали при пониженном давлении и очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 0-20% метанола в метиленхлориде с получением грязнобелой пены (1,28 г). Продукт использовали непосредственно на следующем этапе без дополнительной очистки: 1H ЯМР (300 МГц, CDCl3): δ 7,67 (дд, 2H, J=8,7, 2,7 Гц), 7,42-7,37 (м, 2H), 7,22 (тд, 2H, J=9,0, 2,7 Гц), 4,55-4,30 (м, 3H), 4,13 (м, 1H), 3,78 (ушир. с, 1H), 2,88 и 2,82 (дд, 1H, J=12,0, 3,6 Гц), 2,70-2,50 (м, 3H), 1,45 (с, 9H), 1,13 и 1,11 (д, 3H, J=6,6 Гц); ESI (масса/заряд): 434,0 (M+H).
Получение 30: 3-(циклопропиламино)пропаннитрил
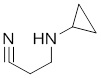
Циклопропиламин (4,214 мл, 60,8 ммоль, 1,0 эквив.) медленно добавляли к раствору акрилонитрила (4,840 г, 91,2 ммоль, 1,5 эквив.) в метаноле (7 мл) при комнатной температуре и перемешивали в течение 30 минут. Реакционную смесь нагревали до кипения с обратным холодильником и перемешивали в течение 1 часа, охлаждали, концентрировали и перегоняли в вакууме с получением 5,5 г прозрачной жидкости (5,5 г, 82%). 1H ЯМР (300 МГц; CDCl3): δ 2,99 (т, 2H, J=6,3 Гц), 2,51 (т, 2H, J=6,3 Гц), 2,12 (м, 1H), 1,78 (ушир. с, 1H), 0,49-0,32 (м, 4H); ESI (масса/заряд): 111,5 (M+H).
Получение 31: N1-циклопропилпропан-1,3-диамин
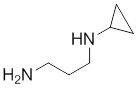
К охлаждаемой (0°C) суспензии гидрида лития алюминия (3,445 г, 90,8 ммоль, 2,0 эквив.) в безводном тетрагидрофуране (120 мл) в течение десяти минут медленно добавляли раствор 3-(циклопропиламино)пропаннитрила (5,000 г, 45,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (20 мл). Реакционную смесь перемешивали при комнатной температуре в течение 15 минут, затем нагревали до кипения с обратным холодильником и перемешивали в течение 3 часов. Смесь охлаждали до комнатной температуры и добавляли декагидрат сульфата натрия до остановки пенообразования. Суспензию перемешивали в течение 10 минут и твердые вещества отфильтровывали (промывая тетрагидрофураном). Раствор концентрировали при пониженном давлении с получением неочищенного продукта, который использовали непосредственно на следующем этапе. 1H ЯМР (300 МГц, CDCl3): δ 2,74-2,69 (м, 4H), 2,10-2,04 (м, 1H), 1,65-1,56 (м, 2H), 0,43-0,27 (м, 4H); ESI (масса/заряд): 115,4 (M+H).
Получение 32: 1-этилтетрагидропиримидин-2(1H)-он; общий способ синтеза карбамидов из диаминов
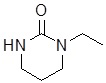
Соответствующий н-замещенный 1,3-пропандиамин или 1,2-этилендиамин (10,0 ммоль, 1,0 эквив.) с интенсивным перемешиванием добавляли в раствор 1,1'-карбонилдиимидазола (1,622 г, 10,0 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (0,05 M), который поддерживали при 0°C с внешней ледяной баней. Раствор оставляли медленно нагреваться до комнатной температуры и перемешивали в течение 16 часов. Смесь обрабатывали любым из следующих действий: i) смесь концентрировали при пониженном давлении и очищали посредством хроматографии на колонке, элюции из силикагеля в градиенте метанола в метиленхлориде с получением желаемого продукта; или ii) смесь разбавляли этилацетатом и дважды последовательно промывали 1 Н водной соляной кислотой и однократно насыщенным водным хлоридом натрия, проводили однократную обратную экстракцию органического слоя этилацетатом, сушили комбинированные органические фракции над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением желаемого продукта, который использовали без дополнительной очистки.

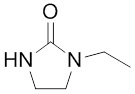
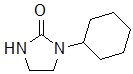
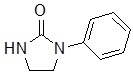
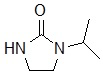
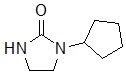
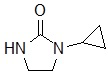
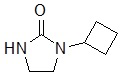
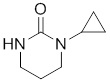
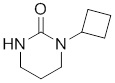
Получение 31: 1-этил-3-(оксиран-2-илметил)тетрагидропиримидин-2(1H)-он; общий способ получения (оксиран-2-илметил)-замещенных карбамидов
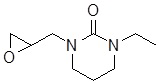
К раствору 1-этилтетрагидропиримидин-2(1H)-она или альтернативно циклического карбамида, полученного в получении 6 (1,0 эквив.), в безводном тетрагидрофуране (0,2 M) добавляли 60% гидрид натрия в минеральном масле (1,1 эквив.) и полученную суспензию перемешивали в течение 1 часа при комнатной температуре. Добавляли эпибромгидрин (3,0 эквив.) и смесь перемешивали в течение 24 часов при комнатной температуре или при 35°C. Добавляли силикагель и суспензию концентрировали при пониженном давлении и непосредственно очищали посредством хроматографии на колонке с силикагелем - элюирования желаемого продукта соответствующим градиентом метанола в метиленхлориде.

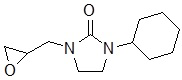
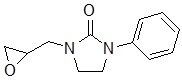
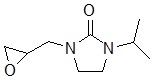
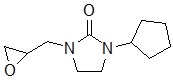
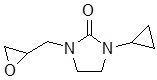
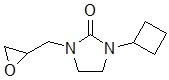
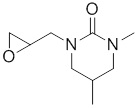
Получение 32: 1-этил-3-((2-метилоксиран-2-ил)метил)тетрагидропиримидин-2(1H)-он; общий способ получения замещенных N-((2-метилоксиран-2-ил)метилом) карбамидов
К раствору циклического карбамида, полученного в получении 7 (1,0 эквив.), в безводном тетрагидрофуране (0,2 M) добавляли 60% гидрид натрия в минеральном масле (1,1 эквив.) и полученную суспензию перемешивали в течение 1 часа при комнатной температуре. Добавляли 2-(хлорметил)-2-метилоксиран (4,0 эквив.) при комнатной температуре и смесь перемешивали при 70-90°C в герметичной пробирке в течение ночи. Добавляли силикагель и суспензию концентрировали при пониженном давлении и непосредственно очищали посредством хроматографии на колонке с силикагелем - элюции желаемого продукта в градиенте метанола в метиленхлориде.
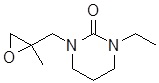
Получение 33: 3-(метиламино)бутаннитрил
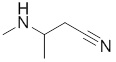
Смесь метиламина (158,584 мл 40% масс./масс. водный раствор, 1842,3 ммоль, 10,0 эквив.) и хромнитрила (15 мл, 184,2 ммоль, 1,0 эквив.) перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь экстрагировали метиленхлоридом (3 × 100 мл) и объединенные органические слои сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением желаемого продукта в виде бесцветного масла (18 г, 100%). 1H ЯМР (300 МГц, CDCl3): δ 2,96 (м, 1H), 2,47 (д, 2H, J=6,0 Гц), 2,46 (с, 3H), 1,36 (д, 3H, J=6,6 Гц).
Получение 34: N3-метилбутан-1,3-диамин
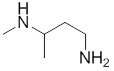
В смесительную колбу Парра помещали метанол (100 мл), охлаждали до 0°C и барботировали аммиаком. 3-(метиламино)бутаннитрил (4,8 г, 48,9 ммоль, 1,0 эквив.) и добавляли полную ложку Ni Ренея. Реакционную смесь перемешивали в атмосфере водорода при 344,7 кПа в течение 10 часов. Реакционную смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении с получением прозрачного масла (5,0 г, 100%). 1H ЯМР (300 МГц, CDCl3): δ 2,90-2,60 (м, 3H), 2,43 (с, 3H), 1,70-1,40 (м, 2H), 1,08 (д, 3H, J=6,0 Гц).
Получение 35: 1,6-диметилтетрагидропиримидин-2(1H)-он
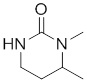
К перемешиваемому раствору N3-метилбутан-1,3-диамина (5,0 г, 48,9 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (100 мл) при 0°C добавляли 1,1'-карбонилдиимидазол (7,935 г, 48,9 ммоль, 1,0 эквив.). Смесь медленно нагревали до комнатной температуры и перемешивали в течение 16 часов. Реакционную смесь концентрировали при пониженном давлении и остаток обрабатывали насыщенным водным хлоридом аммония и дважды экстрагировали метиленхлоридом. Объединенные органические слои промывали насыщенным водным хлоридом натрия, сушили над безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-20% этанол/метиленхлорид) с получением желаемого продукта в виде белого твердого вещества (1,8 г, 29%). 1H ЯМР (300 МГц, CDCl3): δ 4,66 (ушир. с, 1H), 3,53-3,35 (м, 2H), 3,25 (м, 1H), 2,95 (с, 3H), 2,05 (м, 1H), 1,70 (м, 1H), 1,24 (д, 3H, J=6,3 Гц).
Получение 36: 2-(аминометил)-н-бензиланилин
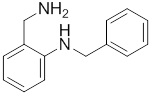
Раствор 2-(бензиламино)бензонитрила (4,0 г, 19,2 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (25 мл) в атмосфере азота медленно добавляли к холодной (0°C) суспензии гидрида лития алюминия (2,187 г, 57,6 ммоль, 3,0 эквив.) в безводном тетрагидрофуране (60 мл). Смесь охлаждали и добавляли декагидрат сульфата натрия до остановки пенообразования (охлаждение внешней водной/ледяной баней). Смесь фильтровали для удаления твердых веществ и раствор концентрировали при пониженном давлении до прозрачной жидкости (3,2 г, 79%). 1H ЯМР (300 МГц, CDCl3): δ 7,42-7,23 (м, 5H), 7,17-7,11 (тд, 1H, J=1,8, 7,5 Гц), 7,07-7,04 (м, 1H), 6,68-6,61 (м, 2H), 6,29 (ушир. с, 1H), 4,40 (с, 2H), 3,99 (с, 2H), 1,31 (ушир. с, 2H).
Получение 37: 1-бензил-3,4-дигидрохиназолин-2(1H)-он
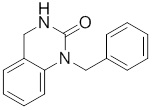
К раствору 2-(аминометил)-н-бензиланилина (1,5 г, 7,1 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (142 мл) добавляли 1,1'-карбонилдиимидазол (1,318 г, 8,1 ммоль, 1,1 эквив.) и раствор перемешивали при комнатной температуре в течение 24 часов. Добавляли 1 Н водную соляную кислоту (20 мл) и смесь три раза экстрагировали этилацетатом. Органические фракции сушили безводным сульфатом натрия, фильтровали и концентрировали при пониженном давлении с получением белого твердого вещества (1,68 г, 99%). 1H ЯМР (300 МГц, CDCl3): δ 7,33-7,20 (м, 5H), 7,11-7,03 (м, 2H), 6,95-6,91 (м, 1H), 6,74-6,71 (д, 1H, J=8,1 Гц), 5,13 (с, 2H), 4,54 (с, 2H), 1,60 (ушир. с, 2H). ESI (масса/заряд): 239,2 (M+H).
Получение 38: 1-бензил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,4-дигидрохиназолин-2(1H)-он
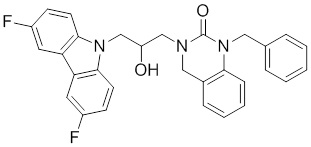
К перемешиваемому раствору 1-бензил-3,4-дигидрохиназолин-2(1H)-она (0,105 г, 0,4 ммоль, 1,8 эквив.) в безводном диметилформамиде (1 мл) добавляли 60% гидрид натрия в минеральном масле (0,01 г, 0,3 ммоль, 1,0 эквив.) и смесь перемешивали в течение 30 минут. Добавляли 3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазол (0,065 г, 0,3 ммоль, 1,0 эквив.) и смесь перемешивали в течение 16 часов при 55°C. Смесь выливали в насыщенный водный хлорид аммония и три раза экстрагировали этилацетатом. Органические фракции сушили над безводным сульфатом натрия, фильтровали и концентрировали с получением желтовато-коричневого масла. Неочищенный остаток очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 20-60% этилацетата/гексана с получением продукта, который использовали непосредственно на следующем этапе без дополнительной очистки (35%). ESI (масса/заряд): 498,2 (M+H); анализ ВЭЖХ: (C18, 5-95% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 15,2 минут, 51%.
Получение 39: 1-бензил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3,4-дигидрохиназолин-2(1H)-он
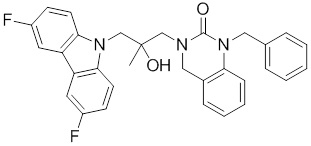
К перемешиваемому раствору 1-бензил-3,4-дигидрохиназолин-2(1H)-она (0,099 г, 0,4 ммоль, 1,8 эквив.) в безводном диметилформамиде (1 мл) добавляли 60% гидрид натрия в минеральном масле (0,01 г, 0,3 ммоль, 1,0 эквив.) и смесь перемешивали в течение 30 минут. Добавляли 3,6-дифтор-9-((2-метилоксиран-2-ил)метил)-9H-карбазол (0,065 г, 0,2 ммоль, 1,0 эквив.) и смесь перемешивали при 55°C в течение 16 часов. Смесь выливали в насыщенный водный хлорид аммония и три раза экстрагировали этилацетатом. Органические фракции сушили над сульфатом натрия, фильтровали и концентрировали с получением желтовато-коричневого масла. Неочищенный остаток очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 20-60% этилацетата/гексана с получением почти белого твердого вещества (0,086 г, 65%). 1H ЯМР (300 МГц, CDCl3): δ 7,66-7,62 (дд, 2H, J=2,4, 8,7 Гц), 7,45-7,40 (дд, 2H, J=4,1, 8,9 Гц), 7,30-7,09 (м, 8H), 7,04-6,93 (м, 2H), 6,75-6,72 (д, 1H, J=8,1 Гц), 5,20-5,15 и 5,08-5,03 (ABq, 2H, J=16,6 Гц), 4,74-4,69 и 4,59-4,54 (ABq, 2H, J=14,3 Гц), 4,39-4,34 и 4,32-4,26 (ABq, 2H, J=15,3 Гц), 4,09 (с, 1H), 3,97-3,93 и 3,51-3,47 (ABq, 2H, J=14,4 Гц), 1,36 (с, 3H); ESI (масса/заряд): 512,3 (M+H).
Получение 40: (R)-(2-метилоксиран-2-ил)метанол
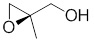
Смесь размолотых 4Å активированных молекулярных сит (15,0 г) и метиленхлорида (300 мл) охлаждали до -10°C, шприцом добавляли изопропоксид титана (IV) (2,072 мл, 7,0 ммоль, 0,05 эквив.) и (-)-диэтил-D-тартрат (2,126 г, 10,3 ммоль, 0,07 эквив.) с последующим 80% гидропироксидом кумола (50,000 г, 262,8 ммоль, 1,8 эквив.). Смесь перемешивали при -10°C в течение 30 минут. Смесь охлаждали до -35°C и шприцом добавляли раствор 2-метил-2-пропен-1-ола (10,620 г, 147,3 ммоль, 1,0 эквив.) в дихлорметане (10 мл), в 1-2 мл частях в течение 30 минут. Реакционную смесь перемешивали при -35°C в течение 1 часа, а затем помещали в холодильник на -20°C в течение 3 суток. Смесь нагревали до 0°C, добавляли воду и перемешивали в течение 30 минут при комнатной температуре. Смесь охлаждали до 0°C и добавляли раствор 30% гидроксида натрия в насыщенном водном хлориде натрия (10 мл) и перемешивали при этой температуре в течение 1 часа. Смесь фильтровали через слой целита и промывали метиленхлоридом (50 мл). Водную часть отделяли и экстрагировали метиленхлоридом (3 × 30 мл). Органический слой комбинировали и сушили (безводный сульфат магния), фильтровали и концентрировали при пониженном давлении до бесцветной жидкости. Неочищенный остаток очищали посредством хроматографии на колонке с силикагелем, элюции в градиенте 20-100% простого диэтилового эфира/гексана с получением бесцветного масла (6,2349 г 48%). 1H ЯМР (300 МГц, CDCl3): δ 3,76 (дд, 1H, J=4,5, 12,3 Гц), 3,6 (дд, 1H, J=8,1, 12,3 Гц), 2,92 (д, 1H, J=4,5 Гц), 2,66 (д, 1H, J=4,8 Гц), 1,79 (ушир. м, 1H), 1,36 (с, 3H).
(S)-энантиомер синтезировали сходным образом из (+)-диэтилтартрата.
Получение 41: 3-нитробензолсульфонат (S)-(2-метилоксиран-2-ил)метила
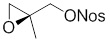
К перемешиваемому раствору (R)-(2-метилоксиран-2-ил)метанола (5,000 г, 56,8 ммоль, 1,0 эквив.), N,N-4-диметиламинопиридина (0,100 г, 0,8 ммоль, 1,4 моль%) и N,N-диизопропилэтиламина (15,776 мл, 88,9 ммоль, 2,0 эквив.) в безводном метиленхлориде (100 мл) при -20°C малыми частями в течение 15 минут медленно добавляли 3-нитробензолсульфонилхлорид (15,092 г, 68,1 ммоль, 1,2 эквив.). Смеси позволяли достигать 0°C и перемешивали в течение 3 часов. Реакцию гасили водой и экстрагировали метиленхлоридом. Объединенные органические слои промывали последовательно водой, 1 Н водной соляной кислотой, насыщенным водным бикарбонатом натрия и насыщенным водным хлоридом натрия. Органический слой сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении. Неочищенный остаток очищали на колонке с силикагелем (0-80% этилацетат/гексан) с получением желаемого продукта в виде желтого масла (6,73 г, 43,4%). 1H ЯМР (300 МГц, CDCl3): δ 8,77 (т, 1H, J=1,8 Гц), 8,54 (м, 1H), 8,27 (м, 1H), 7,84 (т, 1H, J=7,95 Гц), 4,29 (д, 1H, J=11,1 Гц), 4,05 (д, 1H, J=11,1 Гц), 2,73 (дд, 2H, J=17,7, 4,8 Гц), 1,37 (с, 3H).
(R)-энантиомер синтезировали сходным образом.
Получение 42: (S)-9-(оксиран-2-илметил)-9H-карбазол
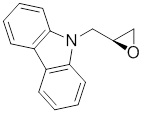
К перемешиваемому раствору карбазола (5,15 г, 30,8 ммоль, 1,0 эквив.) в безводном диметилформамиде (100 мл) при 0°C добавляли 60% гидрид натрия в минеральном масле (1,355 г, 33,9 ммоль, 1,1 эквив.) и смесь перемешивали при 0°C в течение 1 часа. Добавляли (R)-(-)-глицидилнозилат (9,981 г, 38,5 ммоль, 1,3 эквив.) и реакционную смесь перемешивали в течение 1 часа, а затем медленно нагревали до комнатной температуры и перемешивали в течение 16 часов. Смесь разделяли между водой и этилацетатом. Органический слой промывали насыщенным водным хлоридом натрия, сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением красного масла. Неочищенный остаток очищали на колонке с силикагелем (15-80% метиленхлорид/гексан) с получением желаемого продукта в виде белого твердого вещества (4,95 г, 72%). 1H ЯМР (300 МГц, CDCl3): δ 8,11-8,08 (дт, 2H, J=0,9, 7,5 Гц), 7,48-7,46 (м, 4H), 7,28-7,23 (м, 2H), 4,67-4,61 (дд, 1H, J=2,4, 15,9 Гц), 4,45-4,38 (дд, 1H, J=5,0, 15,9 Гц), 3,39-3,34 (м, 1H), 2,83-2,80 (т, 1H, J=4,2 Гц), 2,60-2,57 (дд, 1H, J=2,4, 4,8 Гц). Анализ ВЭЖХ: (C18, 5-95% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 13,2 минут, 99,5%. Хиральный анализ ВЭЖХ: (Chiralcel AD-H, 5-15% изопропанол в гексане в течение 20 минут: время удержания, % площади при 254 нм): 8,12 минут, 3,8%; 8,54 минут, 96,1% (92,2% эи).
Приводимые ниже соединения получали аналогичным образом:
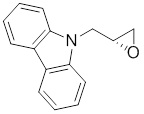
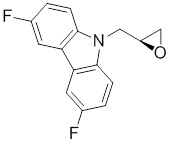
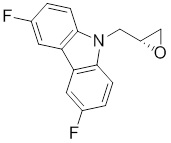
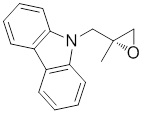
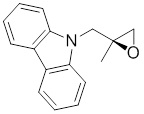
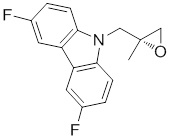
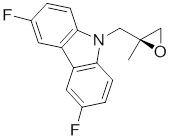
Получение 43: (1S,4R)-2-азабицикло[2.2.1]гептан-3-он
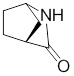
Смесь (1R)-(-)-2-азабицикло[2.2.1]гепт-5-ен-3-она (1,0 г, 9,2 ммоль) и 10% палладия на углероде (0,4 г) в метаноле (50 мл) перемешивали в атмосфере водорода в течение 3 часов. Смесь фильтровали через целит и осадок на фильтре промывали метанолом. Комбинированные органические фазы концентрировали при пониженном давлении с получением требуемого продукта (1 г, 98%). 1H ЯМР (300 МГц, CDCl3): δ 5,91 (ушир. с, 1H), 3,89 (с, 1H), 2,74 (с, 1H), 1,96-1,59 (м, 5H), 1,42-1,37 (м, 1H).
Получение 44: (1R,4S)-2-азабицикло[2.2.1]гептан-3-он
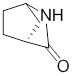
Смесь (1S)-(+)-2-азабицикло[2.2.1]гепт-5-ен-она (1,0 г, 9,2 ммоль, 1,0 эквив.) и 10% палладия на углероде (0,4 г) в метаноле (40 мл) перемешивали в атмосфере водорода при температуре окружающей среды в течение 2 часов. Смесь фильтровали через целит и осадок на фильтре промывали метанолом. Комбинированные органические фазы концентрировали при пониженном давлении с получением требуемого продукта (1 г, 98%). 1H ЯМР (300 МГц, CDCl3): δ 5,83 (ушир. с, 1H), 3,89 (с, 1H), 2,74 (с, 1H), 1,96-1,59 (м, 5H), 1,42-1,38 (м, 1H).
Получение 45: п-толуолсульфонат (R)-5-(гидроксиметил)-2-пирролидинона
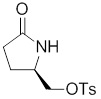
(R)-(-)-5-(гидроксиметил)-2-пирролидинон (1,0 г, 8,7 ммоль, 1,0 эквив.) растворяли в метиленхлориде (40 мл). Добавляли триэтиламин (1,569 мл, 11,3 ммоль, 1,3 эквив.), п-толуолсульфонилхлорид (1,904 г, 10,0 ммоль, 1,1 эквив.) и 4-(диметиламино)пиридин (0,12 г) с охлаждением на льду и смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь концентрировали при пониженном давлении, добавляли 0,5 Н водную соляную кислоту и смесь экстрагировали этилацетатом. Органический слой промывали 0,5 Н водной соляной кислотой, водой, насыщенным водным гидрокарбонатом натрия, и насыщенным водным хлоридом натрия. Органическую фракцию сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением белого твердого вещества (1,91 г, 81%). 1H ЯМР (300 МГц, CDCl3): δ 7,79-7,76 (м, 2H), 7,38-7,35 (м, 2H), 5,73 (ушир. с, 1H), 4,08-4,04 (дд, 1H, J=3,5, 9,5 Гц), 3,98-3,93 (м, 1H), 3,85-3,82 (дд, 1H, J=7,5, 9,5 Гц), 2,47 (с, 3H), 2,36-2,22 (м, 3H), 1,81-1,73 (м, 1H).
Получение 46: (S)-5-(йодметил)пирролидин-2-он
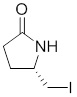
(S)-(5-оксопирролидин-2-ил)метил-4-метилбензолсульфонат (4,5 г, 16,7 ммоль, 1,0 эквив.) растворяли в безводном ацетонитриле (140 мл), добавляли натрий йодид (5,009 г, 33,4 ммоль, 2,0 эквив.) и смесь нагревали до кипения с обратным холодильником в течение 8 часов. Реакционную смесь охлаждали до комнатной температуры, концентрировали при пониженном давлении, добавляли воду и смесь экстрагировали этилацетатом. Органический слой промывали насыщенным водным тиосульфатом натрия, водой и насыщенным водным хлоридом натрия. Органическую фракцию сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением указанного в заголовке соединения в виде белого твердого вещества (2,0 г, 53%). 1H ЯМР (300 МГц, CDCl3): δ 6,42 (ушир. с, 1H), 3,90-3,82 (с, 1H), 3,27-3,16 (м, 2H), 2,53-2,29 (м, 3H), 1,88-1,17 (м, 1H).
Получение 47: (R)-5-(йодметил)пирролидин-2-он
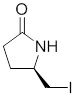
п-толуолсульфонат (R)-5-(гидроксиметил)-2-пирролидинона (1,9 г, 7,1 ммоль, 1,0 эквив.) растворяли в безводном ацетонитриле (60 мл), добавляли натрий йодид (2,09 г) и смесь нагревали при кипячении с обратным холодильником в течение 8 часов. Реакционную смесь охлаждали до комнатной температуры, концентрировали при пониженном давлении, добавляли воду и смесь экстрагировали этилацетатом. Органический слой промывали насыщенным водным тиосульфатом натрия, водой и насыщенным водным хлоридом натрия. Органическую фракцию сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением указанного в заголовке соединения в виде почти белого твердого вещества (0,97 г, 61%). 1H ЯМР (300 МГц, CDCl3): δ 5,92 (ушир. с, 1H), 3,89-3,85 (м, 1H), 3,28-3,15 (м, 2H), 2,53-2,30 (м, 3H), 1,88-1,78 (м, 1H).
Получение 48: (R)-5-метилпирролидин-2-он
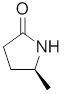
(S)-5-(йодметил)пирролидин-2-он (2,0 г, 8,9 ммоль, 1,0 эквив.) растворяли в этаноле (60 мл), добавляли карбонат натрия (1,036 г, 9,8 ммоль, 1,1 эквив.) и 10% палладий на углероде (0,4 г) и смесь перемешивали в течение 16 часов в атмосфере водорода. Смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении с получением оранжевого полутвердого вещества. К полученному остатку добавляли 5% водный тиосульфат натрия и смесь экстрагировали этилацетатом. Органический слой сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением указанного в заголовке соединения в виде бледно-желтого масла (0,564 г, 64%). 1H ЯМР (300 МГц, CDCl3): δ 6,61 (ушир. с, 1H), 3,82-3,72 (секст., 1H, J=6,6 Гц), 2,45-2,22 (м, 3H), 1,71-1,59 (м, 1H), 1,23-1,21 (д, 3H, J=6,6 Гц).
Получение 49: (S)-5-метилпирролидин-2-он
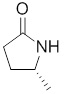
(S)-5-йодметилпирролидин-2-он (1,12 г) растворяли в этаноле (30 мл), добавляли карбонат натрия (0,53 г) и 10% палладий на углероде (0,22 г) и смесь перемешивали в течение 8 часов в атмосфере водорода. Смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении. К полученному остатку добавляли 5% водный тиосульфат натрия и смесь экстрагировали этилацетатом. Органический слой сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением указанного в заголовке соединения (0,263 г, 61%). 1H ЯМР (300 МГц, CDCl3): δ 6,34 (ушир. с, 1H), 3,83-3,72 (секст., 1H, J=6,3 Гц), 2,46-2,21 (м, 3H), 1,72-1,60 (м, 1H), 1,23-1,21 (д, 3H, J=6,0 Гц).
Получение 50: (S)-1-((2-аминоэтил)амино)-3-(3,6-дифтор-9H-карбазол-9-ил)пропан-2-ол
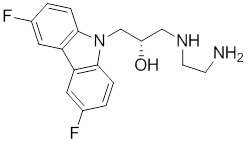
Смесь (R)-3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазола (0,1 г, 0,4 ммоль, 1,0 эквив.) и этилендиамина (0,232 г, 3,9 ммоль, 10,0 эквив.) в этаноле (2 мл) перемешивали при 55°C в течение 5 часов. Реакционную смесь охлаждали до комнатной температуры и концентрировали при пониженном давлении с получением светло-желтого сиропа, который медленно отверждался с формированием почти белого твердого вещества (0,122 г, 96%). 1H ЯМР (300 МГц, CDCl3): δ 7,68 (дд, 2H, J=8,7, 2,7 Гц), 7,42 (дд, 2H, J=8,7, 4,2 Гц), 7,22 (тд, 2H, J=9,0, 2,7 Гц), 4,33-4,31 (д, 2H, J=5,4 Гц), 4,15 (м, 1H), 2,85-2,55 (м, 6H) 1,84 (ушир. с, 4H). ESI (масса/заряд): 320,2 (M+H).
Получение 51: (R)-4-бензил-3-(4-бромбутаноил)оксазолидин-2-он
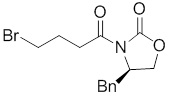
В круглодонную колбу помещали 4-броммасляную кислоту (19,226 г, 115,1 ммоль, 1,0 эквив.) и безводный простой диэтиловый эфир (500 мл). Полученный раствор охлаждали до -78°C и добавляли триэтиламин (16,473 мл, 118,5 ммоль, 1,1 эквив.) с последующим триметилацетилхлоридом (14,596 мл, 118,5 ммоль, 1,1 эквив.). Формировался белый осадок, после чего холодную баню удаляли и реакционную смесь оставляли нагреваться до 0°C и перемешивали в течение 2 часов, взвесь повторно охлаждали до -78°C. В отдельный реакционный сосуд к раствору (R)-4-бензил-2-оксазолидинона (20,000 г, 112,9 ммоль, 1,0 эквив.), перемешиваемому в безводном тетрагидрофуране (170 мл) при -78°C, капельно добавляли 2,5 M раствор н-бутиллития в гексане (45,146 мл, 112,9 ммоль, 1,0 эквив.). Через 10 минут посредством широкогорлой канюли полученную взвесь добавляли в перемешиваемый ангидрид (промывали приблизительно 100 мл безводного тетрагидрофурана). Через 15 мин при -78°C смеси позволяли нагреваться до 0°C в течение 30 мин, а затем поддерживали при этой температуре в течение 1 часа. Затем взвесь осторожно гасили водой (180 мл), перемешивали в течение дополнительных 5 минут, а затем нагревали до комнатной температуры. Полученный раствор экстрагировали этилацетатом (2 × 500 мл). Комбинированные органические экстракты промывали водой, насыщенным водным бикарбонатом натрия (500 мл), насыщенным водным хлоридом натрия (400 мл), сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении. Неочищенный остаток очищали посредством флэш-хроматографии (силикагель, 10-50% этилацетат/гексан) с получением прозрачного масла (26,0 г, 71%). 1H ЯМР (300 МГц, CDCl3): δ 7,19-7,37 (м, 5H), 4,63-4,71 (м, 1H), 4,16-4,25 (м, 2H), 3,52 (т, 2H, J=6,5 Гц), 3,29 (дд, 1H, J=3,3, 13,5 Гц), 3,08-3,18 (м, 2H), 2,78 (дд, 1H, J=9,6, 13,5 Гц), 2,21-2,30 (м, 2H).
The (S) энантиомер синтезировали сходным образом.
Получение 52: (R)-3-(4-азидобутаноил)-4-бензилоксазолидин-2-он
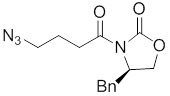
Азид натрия (7,623 г, 117,3 ммоль, 1,5 эквив.) добавляли к перемешиваемому раствору (R)-4-бензил-3-(4-бромбутаноил)оксазолидин-2-она (25,500 г, 78,2 ммоль, 1,0 эквив.) в безводном N,N-диметилформамиде (225 мл). Полученный раствор нагревали при 55°C в течение 15 минут и 2 часа при 70°C. После охлаждения до комнатной температуры раствор выливали в насыщенный водный хлорид натрия/этилацетат (1,4 л) и промывали водой и насыщенным водным хлоридом натрия, сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением масла (22,0 г, 98%), которое использовали без дополнительной очистки. 1H ЯМР (300 МГц, CDCl3): δ 7,36- 7,19 (м, 5H), 4,62-4,72 (м, 1H), 4,10-4,25 (м, 2H), 3,41 (т, 2H, J=6,6 Гц), 3,30 (дд, 1H, J=3,3, 13,2 Гц), 2,99-3,10 (м, 2H), 2,79 (дд, 2H, J=9,9, 13,5 Гц), 1,93-2,02 (м, 2H); анализ ВЭЖХ: (C18, 10-90% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 12,3 мин, 95%.
The (S) энантиомер синтезировали сходным образом.
Получение 53: (R)-3-((R)-4-азидо-2-метилбутаноил)-4-бензилоксазолидин-2-он
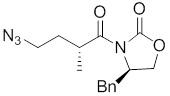
К раствору (R)-3-(4-азидобутаноил)-4-бензилоксазолидин-2-она (20,600 г, 71,5 ммоль, 1,0 эквив.), перемешиваемом в безводном тетрагидрофуране при -78°C (125 мл), медленно добавляли 1,0 M раствор бис(триметилсилил)амида натрия в тетрагидрофуране (119,088 мл, 71,5 ммоль, 1,0 эквив.). Через 15 минут полученный раствор обрабатывали йодметаном (4,671 мл, 75,0 ммоль, 1,0 эквив.). Охлаждающую баню удаляли и через 5 минут реакционный сосуд помещали в ледяную баню и перемешивали в течение дополнительных 15 минут. Реакцию гасили насыщенным водным бикарбонатом натрия (300 мл) и экстрагировали этилацетатом (2 × 300 мл). Комбинированные органические экстракты промывали насыщенным водным хлоридом натрия (2 × 200 мл), сушили (безводный сульфат магния), фильтровали и концентрировали при пониженном давлении. Очисткой посредством флэш-хроматографии (400 г силикагель, 10-50% этилацетат/гексан) получали желаемый продукт в виде прозрачного масла (9,7 г, 45%). 1H ЯМР (300 МГц, CDCl3): δ 7,20-7,38 (м, 5H), 4,65-4,72 (м, 1H), 4,15-4,26 (м, 2H), 3,85-3,79 (м, 1H), 3,35 (app. t, 2H, J=6,0 Гц), 3,25 (дд, 1H, J=13,5, 3,6 Гц), 2,78 (дд, 1H, J=13,0 Гц, 9,0 Гц), 2,04-2,18 (м, 1H), 1,67-1,78 (м, 1H), 1,27 (д, 3H, J=6,9 Гц); анализ ВЭЖХ: (C18, 10-90% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 13,0 мин, 99,4%.
The (S) энантиомер синтезировали сходным образом.
Получение 54: (R)-3-метилпирролидин-2-он
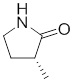
К раствору (R)-3-((R)-4-азидо-2-метилбутаноил)-4-бензилоксазолидин-2-она (9,650 г, 31,9 ммоль, 1,0 эквив.), перемешиваемому в безводном тетрагидрофуране (125 мл), при комнатной температуре добавляли трифенилфосфин (16,744 г, 63,8 ммоль, 2,0 эквив.). Через 5 минут (раствор становился желтым и пузырился) добавляли воду (0,575 мл, 31,9 ммоль, 1,0 эквив.) и реакционную смесь перемешивали при 25°C в течение 18 часов. Смесь концентрировали и полученный остаток очищали посредством флэш-хроматографии (силикагель, 75-100% этилацетат/гексан, затем градиент от 100% до 90% этилацетата/метанола) с получением желаемого продукта (2,98 г, 95%). 1H ЯМР (300 МГц, CDCl3): δ 6,10 (ушир. с, 1H), 3,25-3,35 (м, 2H), 2,27-2,50 (м, 2H), 1,68-1,80 (м, 1H), 1,20 (д, 3H, J=7,5 Гц).
The (S) энантиомер синтезировали сходным образом.
Получение 55: (S)-3-((триметилсилил)окси)пирролидин-2-он
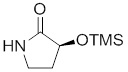
В соответствии со способом Harris, B. D. et al. Synth. Commun. 1986, 16, 1815. триметилсилилхлорид (0,805 мл, 6,3 ммоль, 0,1 эквив.) добавляли к перемешиваемой смеси (S)-(-)-4-амино-2-гидроксимасляной кислоты (15,000 г, 125,9 ммоль, 1,0 эквив.) в ксилоле (1 л) и гексаметилдисилазане (184,757 мл, 881,5 ммоль, 7,0 эквив.) при комнатной температуре. Реакционную смесь нагревали до кипения с обратным холодильником в течение 4 часов, охлаждали до комнатной температуры и разбавляли абсолютным этанолом/метанолом (1 л). Растворители удаляли при пониженном давлении с получением неочищенного продукта, который очищали посредством хроматографии на колонке с использованием этилацетата/метиленхлорида (30-80% градиент) в качестве элюэнта с получением белого твердого вещества. (17,9 г, 82%). 1H ЯМР (300 МГц, CDC13): δ 6,49 (ушир. с, 1H), 4,28-4,23 (т, 1H, J= 7,7 Гц), 3,40-3,21 (м, 2H), 2,42-2,32 (м, 2H), 2,08-1,95 (м, 2H), 0,18 (с, 9H).
Получение 56: (S)-трет-бутил-2-оксо-3-((триметилсилил)окси)пирролидин-1-карбоксилат
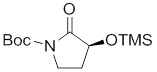
В соответствии со способом DiRocco, D. A. et al. J. Am. Chem. Soc. 2009, 131, 10872 & DiRocco, D. A. et al. WO 2012/009372. К раствору (S)-3-(триметилсилилокси)пирролидин-2-она (6,00 г, 34,62 ммоль, 1,0 эквив.) в безводном метиленхлориде (150 мл) добавляли ди-трет-бутилдикарбонат (15,11 г, 69,24 ммоль, 2,0 эквив.), триэтиламин (4,82 мл, 34,62 ммоль, 1,0 эквив.) и 4-диметиламинопиридин (4,23 г, 34,62 ммоль, 1,0 эквив.). Смесь перемешивали в течение ночи при комнатной температуре, затем добавляли 1 Н водной соляной кислоты (100 мл) и разделяли слои. Органический слой промывали 1 Н водной соляной кислотой (2 × 50 мл) и насыщенным водным хлоридом натрия (1 × 50 мл), сушили (безводный сульфат натрия) и фильтровали. Раствор концентрировали при пониженном давлении с получением неочищенного масла, которое очищали посредством хроматографии в силикагеле (элюируя 0-15% этилацетатом/гексаном) с получением прозрачного вязкого масла, которое отверждали в холодильнике. (3,93 г, 42%). 1H ЯМР (300 МГц, CDCl3): δ 4,32-4,26 (дд, 1H, J=8,4, 9,3 Гц), 3,82-3,74 (ддд, 1H, J=2,1, 9,0, 11,1 Гц), 3,50-3,41 (м, 1H), 2,28-2,25 (м, 1H), 1,94-1,87 (м, 1H), 1,51 (с, 9H), 0,18 (с, 9H).
Получение 57: (R)-3-фторпирролидин-2-он
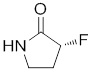
Раствор (S)-трет-бутил-2-оксо-3-((триметилсилил)окси)пирролидин-1-карбоксилата (3 г, 11 ммоль) в безводном метиленхлориде (55 мл) охлаждали до -78°C после чего капельно добавляли трифторид диэтиламиносеры (2,9 мл, 22 ммоль, 2,0 эквив.). Затем раствору позволяли медленно нагреваться до комнатной температуры и затем добавляли насыщенный водный бикарбонат натрия (50 мл) для гашения реакции. Слои разделяли и затем органический слой промывали насыщенным водным хлоридом аммония (2 × 25 мл), сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением неочищенного твердого вещества. Затем это неочищенное вещество растворяли в метиленхлориде (40 мл) и добавляли трифторуксусную кислоту (2,5 мл, 33 ммоль, 3,0 эквив.). Раствор перемешивали в течение 3 часов после чего образование газа прекращалось. Посредством концентрации при пониженном давлении получали желтовато-коричневую жидкость, которую очищали посредством хроматографии в силикагеле (элюируя 0-10% метанолом/метиленхлоридом) с получением желаемого продукта в виде белого твердого вещества (0,77 г, 68%). 1H ЯМР (300 МГц, CDC13): δ 7,35 (ушир. с, 1H), 5,15-4,93 (дт, 1H, J=7,6, 53,4 Гц), 3,50-3,34 (м, 2H), 2,53 (м, 1H), 2,39-2,21 (м, 1H).
Получение 58: (R)-3-гидроксипирролидин-2-он
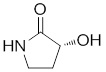
К перемешиваемой смеси 4-нитробензойной кислоты (9,273 г, 55,5 ммоль, 1,1 эквив.) и (S)-(-)-3-гидрокси-2-пирролидона (5,100 г, 50,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (175 мл) в атмосфере азота добавляли трифенилфосфин (26,461 г, 100,9 ммоль, 2,0 эквив.). К этой реакционной смеси капельно добавляли диизопропилазодикарбоксилат (14,898 мл, 75,7 ммоль, 1,5 эквив.) (с внешним охлаждением холодной водной баней). Реакционную смесь перемешивали при комнатной температуре в течение ночи. Реакционную смесь концентрировали при пониженном давлении с получением неочищенного остатка. К остатку при комнатной температуре добавляли метанол (130 мл) с последующим карбонатом калия (0,38 г). Реакционную смесь перемешивали при комнатной температуре в течение 8 часов. Реакционную смесь разбавляли метиленхлоридом и фильтровали через целит. Слой целита промывали 1% метанолом в метиленхлориде. Фильтраты комбинировали и концентрировали досуха. Остаток разделяли между этилацетатом:разбавленной водной соляной кислотой (20 мл, 9:1) и перемешивали в течение 15 минут. Слои разделяли и водный слой промывали этилацетатом три раза. Водный слой концентрировали досуха и получали твердый остаток получали. Неочищенный остаток промывали 1-2% метанолом в метиленхлориде (3 × 50 мл), сушили (безводный сульфат натрия), фильтровали и концентрировали с получением желтовато-коричневого масла (3,3 г, 60%). 1H ЯМР (300 МГц, CDCl3): δ 4,32-4,27 (т, 1H, J=8,5 Гц), 3,36-3,19 (м, 2H), 2,48-2,40 (м, 1H), 2,07-1,93 (м, 1H), 1,16-1,14 (д, 1H, J=6,3 Гц).
Получение 59: (R)-3-((триметилсилил)окси)пирролидин-2-он
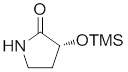
К перемешиваемой суспензии (R)-3-гидрокси-2-пирролидона (3,200 г, 31,7 ммоль, 1,0 эквив.), ксилола (45 мл) и гексаметилдисилазана (39,8 мл, 189 ммоль, 6,0 эквив.) при комнатной температуре добавляли триметилсилилхлорид (0,405 мл, 3,2 ммоль, 0,1 эквив.). Реакционную смесь нагревали при температуре кипения с обратным холодильником в течение 5 часов и разбавляли абсолютным этанолом (50 мл). Растворители удаляли при пониженном давлении. Неочищенный продукт очищали посредством хроматографии на колонке с использованием этилацетата в метиленхлориде (30-80% градиент) в качестве элюэнта с получением прозрачного масла, которое отверждается до почти белого твердого вещества при отстаивании. (2,57 г, 47%). 1H ЯМР (300 МГц, CDC13): δ 6,89 (ушир. с, 1H), 4,28-4,23 (т, 1H, J=8,1 Гц), 3,40-3,21 (м, 2H), 2,42-2,32 (м, 1H), 2,08-1,95 (м, 1H), 0,18 (с, 9H).
Получение 60: (R)-трет-бутил-2-оксо-3-((триметилсилил)окси)пирролидин-1-карбоксилат
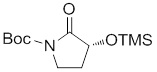
К раствору (R)-3-((триметилсилил)окси)пирролидин-2-она (2,770 г, 16,0 ммоль, 1,0 эквив.) в безводном метиленхлориде (75 мл) добавляли ди-трет-бутилдикарбонат (6,971 г, 31,9 ммоль, 2,0 эквив.), триэтиламин (2,222 мл, 16,0 ммоль, 1,0 эквив.) и N,N-4-диметиламинопиридин (1,953 г, 16,0 ммоль, 1,0 эквив.). Смесь перемешивали в течение ночи при комнатной температуре, затем разбавляли метиленхлоридом и промывали 0,1 Н водной соляной кислотой (100 мл). Органический слой промывали 0,1 Н водной соляной кислотой (2 × 100 мл) и насыщенным водным хлоридом натрия (1 × 100 мл), сушили (безводный сульфат натрия) и фильтровали. Раствор концентрировали при пониженном давлении и очищали посредством хроматографии в силикагеле (элюируя 0-15% этилацетатом/гексаном) с получением прозрачного вязкого масла (2,1 г, 48%). 1H ЯМР (300 МГц, CDCl3): δ 4,32-4,26 (дд, 1H, J=8,1, 9,3 Гц), 3,82-3,74 (ддд, 1H, J=2,1, 9,0, 11,1 Гц), 3,50-3,41 (м, 1H), 2,32-2,23 (м, 1H), 1,97-1,87 (м, 1H), 1,54 (с, 9H), 0,18 (с, 9H).
Получение 61: (S)-3-фторпирролидин-2-он
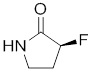
Раствор (R)-трет-бутил-2-оксо-3-((триметилсилил)окси)пирролидин-1-карбоксилата (2,100 г, 7,7 ммоль, 1,0 эквив.) в безводном метиленхлориде (37 мл) охлаждали до -78°C после чего капельно добавляли трифторид диэтиламиносеры (2,030 мл, 15,4 ммоль, 2,0 эквив.). Затем раствору позволяли медленно нагреваться до комнатной температуры и затем добавляли насыщенный водный бикарбонат натрия (33 мл) для гашения реакции. Слои разделяли и органический слой промывали насыщенным водным хлоридом аммония (2 × 16 мл), сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением неочищенного твердого вещества. Затем это неочищенное вещество растворяли в дихлорметане (30 мл) и добавляли трифторуксусную кислоту (1,7 мл, 33 ммоль, 3,0 эквив.). Раствор перемешивали в течение 3 часов после чего образование газа прекращалось. Посредством концентрации при пониженном давлении и очисткой посредством хроматографии в силикагеле (элюируя 0-10% метанолом/метиленхлоридом) получали желаемый продукт в виде почти белого твердого вещества (0,71 г, 90%). 1H ЯМР (300 МГц, CDC13): δ 7,35 (ушир. с, 1H), 5,15-4,93 (дт, 1H, J=7,6, 53,4 Гц), 3,50-3,34 (м, 2H), 2,53 (м, 1H), 2,39-2,21 (м, 1H).
Получение 62: метил 4-метил-5-оксопентаноат
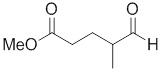
В соответствии со способом Oikawa, M. et al. Tetrahedron, 1995, 51, 62377. Колбу, содержащую пиперидин (54,425 мл, 551,0 ммоль, 2,0 эквив.) и карбонат калия (13,774 г, 99,7 ммоль, 0,4 эквив.) помещали в водяную баню и добавляли пропионовый альдегид (16,000 г, 275,5 ммоль, 1,0 эквив.) в течение 20 минут с интенсивным перемешиванием. После перемешивания в течение 18 часов нерастворимое вещество удаляли посредством фильтрации через слой целита (слой промывали простым диэтиловым эфиром). Фильтрат сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении. Полученный таким образом неочищенный енамин растворяли в ацетонитриле (150 мл) и к этой смеси капельно добавляли метилацилат (47,433 г, 551,0 ммоль, 2,0 эквив.). Реакционную смесь перемешивали при кипячении с обратным холодильником в течение 24 часов с последующим добавлением уксусной кислоты (31,541 мл, 551,0 ммоль, 2,0 эквив.) и воды (150 мл). После перемешивания при кипячении с обратным холодильником в течение 24 часов, его насыщали хлоридом натрия и экстрагировали простым диэтиловым эфиром (3 × 100 мл). Комбинированные органические экстракты сушили (безводный сульфат магния), фильтровали и концентрировали при пониженном давлении. Посредством очистки с использованием флэш-хроматографии на силикагеле (0-20% этилацетат/гексан) получали аддукт в виде бесцветного масла (22 г, 55%). 1H ЯМР (300 МГц, CDC13): δ 9,64 (д, 1H, J=1,8 Гц), 3,69 (с, 3H), 2,50-2,35 (м, 3H), 2,07 (секст., 1H, J=7,2 Гц), 1,71 (секст., 1H, J=7,2 Гц), 1,14 (д, 3H, J=7,2 Гц).
Получение 63: (3R,8S,8aR)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-он и (3R,8R,8aS)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-он
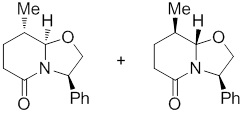
В соответствии со способом Amat, M. et al. J. Org. Chem. 2014, 79, 2792. К перемешиваемому раствору метила 4-метил-5-оксопентаноата (5,780 г, 40,1 ммоль, 1,0 эквив.) в толуоле (100 мл) добавляли (R)-(-)-фенилглицинол (5,500 г, 40,1 ммоль, 1,0 эквив.). Реакционную смесь нагревали при кипячении с обратным холодильником в течение 25 часов с азеотропным удалением получаемой воды устройством Дина-Старка. После охлаждения смесь концентрировали при пониженном давлении и остаток очищали на колонке с силикагелем (колонку предварительно обрабатывали TEA, затем элюировали 0-70% этилацетатом/гексаном) с получением желаемых продуктов: (3R,8S,8aS)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-она в виде светло-желтого твердого вещества (1,3 г, 14%) и (3R,8S,8aR)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-он в виде бесцветного сиропа (6,5 г, 70%). (3R,8S,8aS)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-он: 1H ЯМР (300 МГц, CDCl3): δ 7,40-7,20 (м, 5H), 5,25 (т, 1H, J=7,5 Гц), 4,61 (д, 1H, J=8,4 Гц), 4,48 (т, 1H, J=8,7 Гц), 3,75 (дд, 1H, J=9,0, 7,8 Гц), 2,55 (дд, 1H, J=18,0, 6,0 Гц), 2,46-2,33 (м, 1H), 1,88-1,51 (м, 3H), 1,19 (д, 3H, J=5,7 Гц); ESI (масса/заряд): 232,7 (M+H). (3R,8S,8aR)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-он: 1H ЯМР (300 МГц, CDCl3): δ 7,40-7,20 (м, 5H), 4,93 (д, 1H, J=6,3 Гц), 4,44 (д, 1H, J=9,3 Гц), 4,14 (дд, 1H, J=8,7, 6,3 Гц), 4,01 (дд, 1H, J=8,7, 1,2 Гц), 2,47-2,25 (м, 2H), 2,05-1,87 (м, 2H), 1,60-1,43 (м, 1H), 1,20 (д, 3H, J=6,6 Гц); ESI (масса/заряд): 232,7 (M+H).
Получение 64: (S)-1-((R)-2-гидрокси-1-фенилэтил)-5-метилпиперидин-2-он
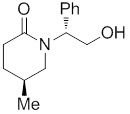
В соответствии со способом Amat, M. et al. J. Org. Chem. 2014, 79, 2792. К перемешиваемому раствору (3R,8S,8aR)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-она (3,600 г, 15,6 ммоль, 1,0 эквив.) в безводном метиленхлориде (100 мл) добавляли триэтилсилан (7,458 мл, 46,7 ммоль, 3,0 эквив.) и хлорид титана (IV) (7,697 мл, 70,0 ммоль, 4,5 эквив.) и смесь перемешивали при 50°C в течение 24 часов. Затем добавляли дополнительный хлорид титана (IV) (7,7 мл) и триэтилсилан (7,5 мл) и перемешивание продолжали при 50°C в течение 24 часов. Смесь выливали в насыщенный водный бикарбонат натрия (100 мл). Водную фазу фильтровали через целит и экстрагировали метиленхлоридом. Комбинированные органические экстракты сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением остатка, который подвергали хроматографии в силикагеле (0-100% этилацетат/гексан, затем чистый этилацетат) с получением желаемого продукта в виде бесцветного масла (1,6 г, 44%) и восстанавливали исходное вещество (0,6 г). 1H ЯМР (300 МГц, CDCl3): δ 7,40-7,20 (м, 5H), 5,80 (дд, 1H, J=9,6, 4,8 Гц), 4,20-4,00 (м, 2H), 2,97 (ддд, 1H, J=11,7, 4,8, 2,4 Гц), 2,84 (дд, 1H, J=11,7, 9,9 Гц), 2,70 (ушир. с, 1H), 2,59 (ддд, 1H, J=17,7, 6,3, 3,0 Гц), 2,47 (ддд, 1H, J=17,7, 11,1, 6,6 Гц), 1,90-1,75 (м, 2H), 1,50 (м, 1H), 0,93 (д, 3H, J=6,3 Гц).
Получение 65: (S)-5-метилпиперидин-2-он
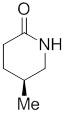
В двухгорлую колбу, оснащенную конденсатором сухого льда, помещали (S)-1-((R)-2-гидрокси-1-фенилэтил)-5-метилпиперидин-2-он (1,600 г, 6,9 ммоль, 1,0 эквив.) и безводный тетрагидрофуран (20 мл). Смесь охлаждали до -78°C в атмосфере азота, а затем конденсировали аммиак (50 мл). Температуру реакции поднимали до -33°C. Добавляли небольшие порции металлического натрия пока оставалась синяя окраска и смесь перемешивали при -33°C в течение 5 минут. Реакцию гасили добавлением твердого хлорида аммония до исчезновения синей окраски. Смесь перемешивали при комнатной температуре в течение 5 часов и добавляли метиленхлорид. Смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-100% этилацетат/гексан, а затем 20% метанол/этилацетат) с получением желаемого продукта в виде бесцветного масла (0,480 г, 62%). 1H ЯМР (300 МГц, CDCl3): δ 5,84 (ушир. с, 1H), 3,10 (м, 1H), 2,94 (т, 1H, J=10,8 Гц), 2,50-2,28 (м, 2H), 2,05-1,80 (м, 2H), 1,50 (м, 1H), 1,03 (д, 3H, J=6,9 Гц).
Получение 66: (R)-1-((R)-2-гидрокси-1-фенилэтил)-5-метилпиперидин-2-он
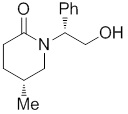
В соответствии со способом Amat, M. et al. J. Org. Chem. 2014, 79, 2792. К перемешиваемому раствору (3R,8R,8aS)-8-метил-3-фенилтетрагидро-2H-оксазолo[3,2-a]пиридин-5(3H)-она (1,000 г, 4,3 ммоль, 1,0 эквив.) в безводном метиленхлориде (50 мл) добавляли триэтилсилан (2,072 мл, 13,0 ммоль, 3,0 эквив.) и хлорид титана (IV) (2,138 мл, 19,5 ммоль, 4,5 эквив.) и смесь перемешивали при 50°C в течение 6 часов. Смесь выливали в насыщенный водный бикарбонат натрия (50 мл). Водную фазу фильтровали через целит и экстрагировали метиленхлоридом. Комбинированные органические экстракты сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении с получением остатка, который подвергали хроматографии (0-100% этилацетат/гексан, а затем этилацетат) с получением желаемого продукта в виде бесцветного сиропа (0,200 г, 20%). 1H ЯМР (300 МГц, CDCl3): δ 7,40-7,20 (м, 5H), 5,67 (дд, 1H, J=7,8, 6,3 Гц), 4,20-4,05 (м, 2H), 3,15-3,00 (м, 2H), 2,65-2,40 (м, 3H), 2,00-1,75 (м, 2H), 1,40 (м, 1H), 0,89 (д, 3H, J=6,9 Гц).
Получение 67: (R)-5-метилпиперидин-2-он
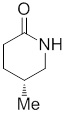
В двухгорлую колбу, оснащенную конденсатором сухого льда, помещали (R)-1-((S)-2-гидрокси-1-фенилэтил)-5-метилпиперидин-2-он (0,200 г, 0,9 ммоль, 1,0 эквив.) и безводный тетрагидрофуран (5 мл). Смесь охлаждали до -78°C в атмосфере азота, а затем конденсировали аммиак (15 мл). Температуру реакции поднимали до -33°C. Добавляли небольшие порции металлического натрия пока оставалась синяя окраска и смесь перемешивали при -33°C в течение 5 минут. Реакцию гасили добавлением твердого хлорида аммония до исчезновения синей окраски. Смесь перемешивали при комнатной температуре в течение 5 часов и добавляли метиленхлорид. Смесь фильтровали через целит и фильтрат концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-100% этилацетат/гексан, а затем 20% метанол/этилацетат) с получением желаемого продукта в виде желтого масла (0,080 г, 82%). 1H ЯМР (300 МГц, CDCl3): δ 5,85 (ушир. с, 1H), 3,10 (м, 1H), 2,93 (т, 1H, J=10,8 Гц), 2,50-2,28 (м, 2H), 2,05-1,80 (м, 2H), 1,50 (м, 1H), 1,03 (д, 3H, J=6,6 Гц).
Получение 68: (S)-трет-бутил (1-амино-1-оксопропан-2-ил)карбамат
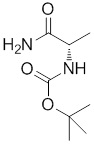
Смесь Boc-Ala-OMe (5,000 г, 24,6 ммоль, 1,0 эквив.) и 28% водного гидроксида аммония (100,00 мл, 1479,7 ммоль, 60,1 эквив.) в метаноле (100 мл) перемешивали в течение 16 часов при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении с получением желаемого продукта в виде белого твердого вещества (4,65 г, 100%). 1H ЯМР (300 МГц, CDCl3): δ 6,15 (ушир., 1H), 5,55 (ушир., 1H), 4,95 (ушир., 1H), 4,20 (ушир., 1H), 1,46 (с, 9H), 1,39 (д, 3H, J=7,2 Гц).
Получение 69: (S)-трет-бутил-(1-аминопропан-2-ил)карбамат
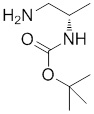
К перемешиваемому раствору Boc-Ala-NH2 (4,600 г, 24,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (100 мл) в атмосфере азота добавляли 1,0 M комплекс боран-тетрагидрофуран в тетрагидрофуране (85,536 мл, 85,5 ммоль, 3,5 эквив.). Смесь перемешивали в течение 16 часов при комнатной температуре, а затем нагревали при 70°C в течение 2 часов. После охлаждения, реакцию гасили метанолом до прекращения образования пузырей. Смесь нагревали при 70°C в течение 2 часов, а затем концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-100% этилацетат/гексан, а затем 0-30% метанол/метиленхлорид) с получением желаемого продукта в виде полутвердого вещества (1,4 г, 33%). 1H ЯМР (300 МГц, CDCl3): δ 4,60 (ушир. с, 1H), 3,65 (м, 1H), 2,76 (дд, 1H, J=12,9, 4,8 Гц), 2,64 (дд, 1H, J=12,9, 6,6 Гц), 1,45 (с, 9H), 1,13 (д, 3H, J=6,9 Гц).
Получение 70: трет-бутил-((S)-1-(((S)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)амино)пропан-2-ил)карбамат
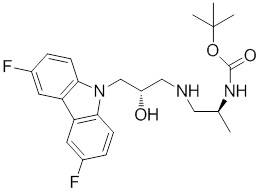
Смесь (R)-3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазола (0,600 г, 2,3 ммоль, 1,0 эквив.) и (S)-трет-бутил-(1-аминопропан-2-ил)карбамата (1,210 г, 6,9 ммоль, 3,0 эквив.) в этаноле (10 мл) перемешивали при 70°C. Через 15 часов реакционную смесь концентрировали при пониженном давлении и очищали на колонке с силикагелем (0-100% этилацетат/гексан, затем 0-30% метанол/метиленхлорид) с получением желаемого продукта в виде белой пены (0,750 г, 75%) и восстанавливали исходный амин (0,2 г). 1H ЯМР (300 МГц, CDCl3): δ 7,67 (дд, 2H, J=8,7, 2,4 Гц), 7,42 (дд, 2H, J=8,7, 3,9 Гц), 7,22 (тд, 2H, J=9,0, 2,7 Гц), 4,50-4,25 (м, 3H), 4,13 (м, 1H), 3,78 (ушир. с, 1H), 2,86 (дд, 1H, J=12,0, 3,6 Гц), 2,70-2,50 (м, 3H), 1,43 (с, 9H), 1,10 (д, 3H, J=6,3 Гц); ESI (масса/заряд): 434,0 (M+H).
Получение 71: трет-бутил-((S)-1-(((S)-3-(9H-карбазол-9-ил)-2-гидроксипропил)амино)пропан-2-ил)карбамат
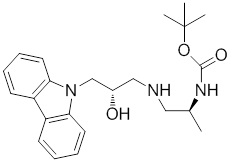
Смесь (R)-9-(оксиран-2-илметил)-9H-карбазола (0,150 г, 0,7 ммоль, 1,0 эквив.) и (S)-трет-бутил (1-аминопропан-2-ил)карбамата (0,200 г, 1,1 ммоль, 1,7 эквив.) в этаноле (5 мл) перемешивали при 70°C. Через 15 часов реакционную смесь концентрировали при пониженном давлении и очищали на колонке с силикагелем (0-100% этилацетат/гексан) с получением желаемого продукта в виде белой пены (0,120 г, 45%). 1H ЯМР (300 МГц, CDCl3): δ 8,09 (д, 2H, J=7,8 Гц), 7,52-7,41 (м, 4H), 7,25-7,20 (м, 2H), 4,50-4,35 (м, 3H), 4,17 (м, 1H), 3,73 (м, 1H), 2,83 (дд, 1H, J=11,7, 3,6 Гц), 2,66-2,47 (м, 3H), 1,43 (с, 9H), 1,08 (д, 3H, J=6,6 Гц); ESI (масса/заряд): 398,1 (M+H).
Получение 72: (R)-трет-бутил-(1-амино-1-оксопропан-2-ил)карбамат
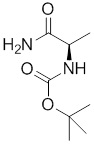
Смесь Boc-D-Ala-OMe (5,000 г, 24,6 ммоль, 1,0 эквив.) и 28% водного гидроксида аммония (100 мл, 1479,7 ммоль, 60,1 эквив.) в метаноле (100 мл) перемешивали в течение 16 часов при комнатной температуре. Реакционную смесь концентрировали при пониженном давлении с получением желаемого продукта в виде белого твердого вещества (4,65 г, 100%). 1H ЯМР (300 МГц, CDCl3): δ 6,15 (ушир., 1H), 5,60 (ушир., 1H), 5,00 (ушир., 1H), 4,20 (ушир., 1H), 1,46 (с, 9H), 1,39 (д, 3H, J=6,9 Гц).
Получение 73: (R)-трет-бутил-(1-аминопропан-2-ил)карбамат
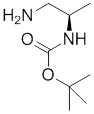
К перемешиваемому раствору Boc-D-Ala-NH2 (4,600 г, 24,4 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (100 мл) в атмосфере азота добавляли 1,0 M комплекс боран-тетрагидрофуран в тетрагидрофуране (97,756 мл, 97,8 ммоль, 4,0 эквив.). Смесь перемешивали в течение 16 часов при комнатной температуре, а затем нагревали при 70°C в течение 2 часов. После охлаждения реакцию гасили метанолом до прекращения образования пузырей. Смесь нагревали при 70°C в течение 2 часов, а затем концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-30% метанол/метиленхлорид) с получением желаемого продукта в виде бесцветного масла (1,5 г, 35%). 1H ЯМР (300 МГц, CDCl3): δ 4,60 (ушир. с, 1H), 3,65 (м, 1H), 2,75 (дд, 1H, J=12,9, 5,1 Гц), 2,63 (дд, 1H, J=12,9, 6,6 Гц), 1,45 (с, 9H), 1,41 (с, 2H), 1,12 (д, 3H, J=6,3 Гц).
Получение 74: трет-бутил-((R)-1-(((S)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)амино)пропан-2-ил)карбамат
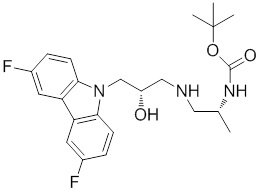
Смесь (R)-3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазола (0,200 г, 0,8 ммоль, 1,0 эквив.) и (R)-трет-бутил-(1-аминопропан-2-ил)карбамата (0,403 г, 2,3 ммоль, 3,0 эквив.) в этаноле (10 мл) перемешивали при 70°C. Через 15 часов реакционную смесь концентрировали при пониженном давлении и очищали на колонке с силикагелем (0-30% метанол/метиленхлорид) с выделением желаемого продукта в виде белого порошка (0,250 г, 75%). 1H ЯМР (300 МГц, CDCl3): δ 7,68 (дд, 2H, J=8,7, 2,7 Гц), 7,41 (дд, 2H, J=9,3, 4,2 Гц), 7,22 (тд, 2H, J=9,3, 2,4 Гц), 4,43 (ушир. с, 1H), 4,35 (д, 2H, J=5,7 Гц), 4,12 (м, 1H), 3,78 (ушир. с, 1H), 2,80 (дд, 1H, J=12,3, 3,6 Гц), 2,63 (дд, 1H, J=12,3, 5,7 Гц), 2,57 (д, 2H, J=7,2 Гц), 1,44 (с, 9H), 1,11 (д, 3H, J=6,6 Гц); ESI (масса/заряд): 434,0 (M+H).
Получение 75: трет-бутил-((R)-1-(((S)-3-(9H-карбазол-9-ил)-2-гидроксипропил)амино)пропан-2-ил)карбамат
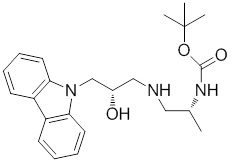
Смесь (R)-9-(оксиран-2-илметил)-9H-карбазола (0,150 г, 0,7 ммоль, 1,0 эквив.) и (R)-трет-бутил-(1-аминопропан-2-ил)карбамата (0,351 г, 2,0 ммоль, 3,0 эквив.) в этаноле (10 мл) перемешивали при 70°C. Через 15 часов реакционную смесь концентрировали при пониженном давлении и очищали на колонке с силикагелем (0-30% метанол/метиленхлорид) с выделением желаемого продукта в виде белой пены (0,210 г, 78%). 1H ЯМР (300 МГц, CDCl3): δ 8,10 (д, 2H, J=7,5 Гц), 7,55-7,40 (м, 4H), 7,27-7,20 (м, 2H), 4,60-4,30 (м, 3H), 4,16 (м, 1H), 3,78 (м, 1H), 2,80 (дд, 1H, J=12,3, 3,6 Гц), 2,67 (дд, 1H, J=12,0, 8,4 Гц), 2,60-2,50 (м, 2H), 1,44 (с, 9H), 1,10 (д, 3H, J=6,6 Гц); ESI (масса/заряд): 398,1 (M+H).
Пример 2: Получение соединений формулы I
Соединение 1: 1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)пиперидин-2-он
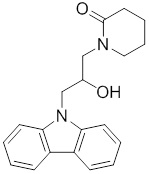
К перемешиваемому раствору пиперидин-2-она (0,133 г, 1,3 ммоль) в диметилсульфоксиде (5 мл) добавляли трет-бутоксид калия(0,151 г, 1,3 ммоль) и смесь перемешивали при комнатной температуре в течение 1 часа. Добавляли 9-(оксиран-2-илметил)-9H-карбазол (0,150 г, 0,7 ммоль) и смесь перемешивали при комнатной температуре в течение 16 часов. Смесь разбавляли водой и экстрагировали этилацетатом. Органический слой промывали насыщенным водным хлоридом натрия, сушили (безводный сульфат натрия), фильтровали и концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (50-100% этилацетат/гексан), а затем посредством препаративной ВЭЖХ (C18, 30-80% ацетонитрил/вода с 0,1% муравьиной кислотой в течение 0-8 минут) с получением продукта в виде белой пены (0,098 г, 45%). 1H ЯМР (300 МГц, CDCl3): δ 8,08 (д, 2H, J=7,8 Гц), 7,50-7,40 (м, 4H), 7,28-7,18 (м, 2H), 4,60-4,25 (м, 4H), 3,87 (дд, 1H, J=14,1, 7,8 Гц), 3,15-2,95 (м, 3H), 2,36 (т, 2H, J=5,7 Гц), 1,85-1,55 (м, 4H); ESI (масса/заряд): 323,2 (M+H).
Соединения от 2 до 72:
Соединения от 2 до 72 получали способами, аналогичными способам, используемым для соединения 1, или с использованием вместо трет-бутоксида калия гидрида натрия (0,4 эквив.). Альтернативно, вместо трет-бутоксида калия также можно использовать фосфазеновое основание P4-t-Bu. В случаях, когда исходные вещества для указанных ниже целей не были коммерчески доступными, в предшествующих примерах получения описан синтез.
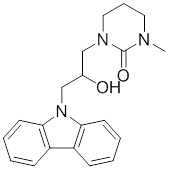
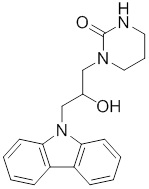
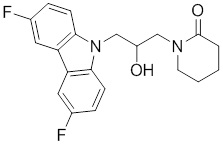
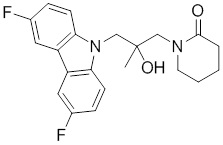
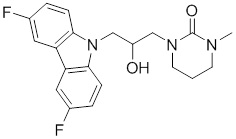
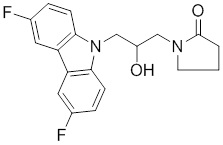
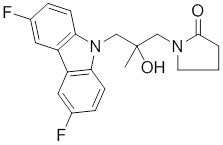
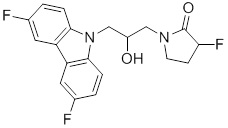
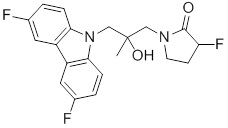
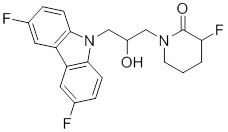
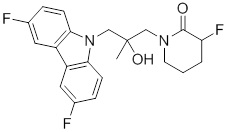
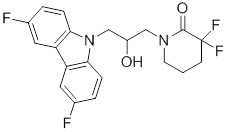
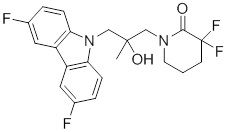
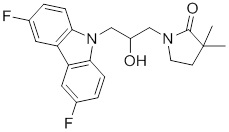
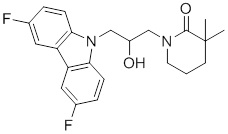
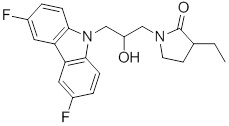
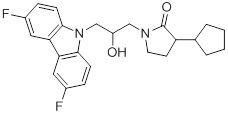
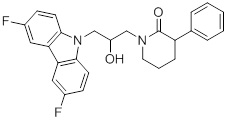
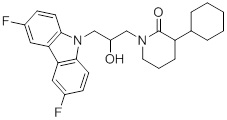
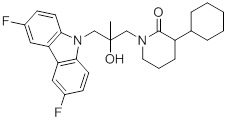
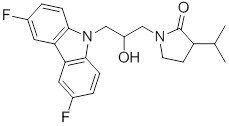
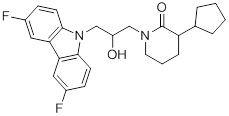
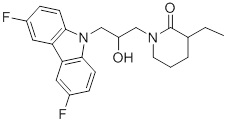
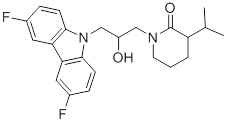
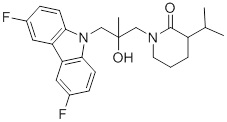
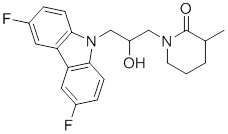
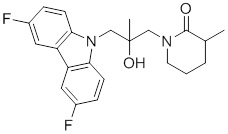
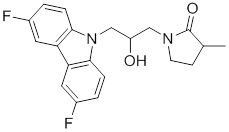
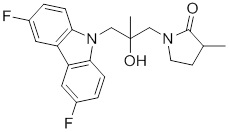
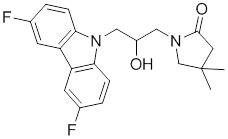
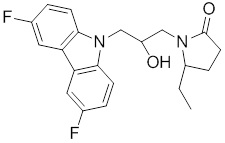
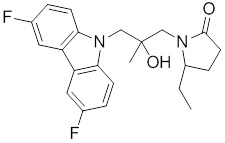
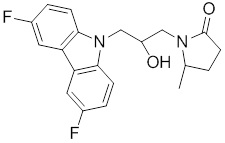
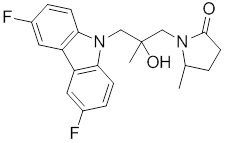
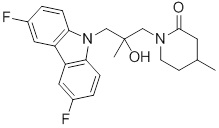
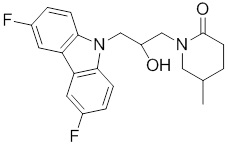
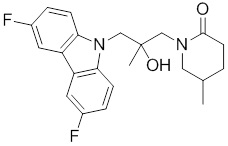
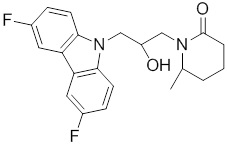
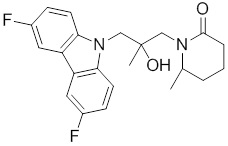
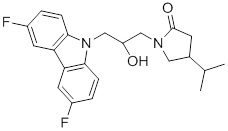
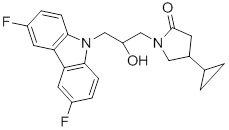
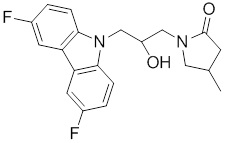
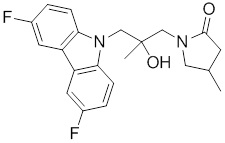
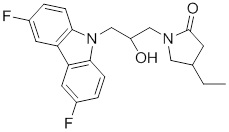
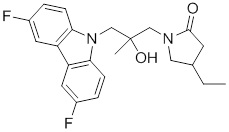
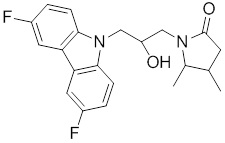
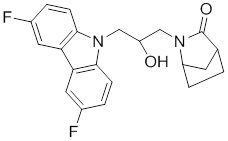
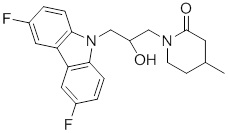
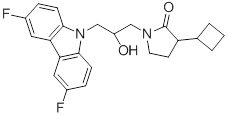
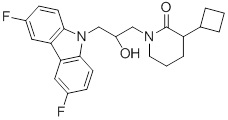
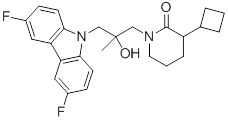
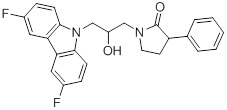
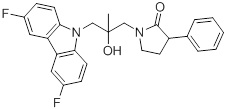
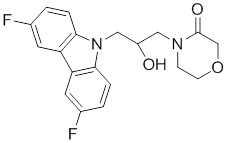
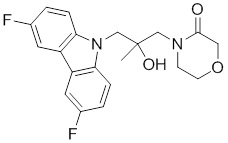
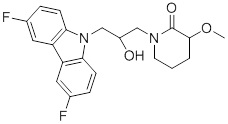
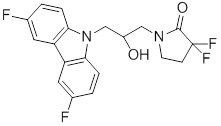
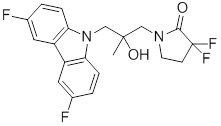
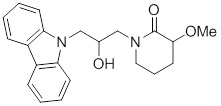
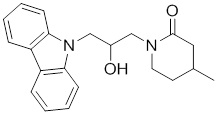
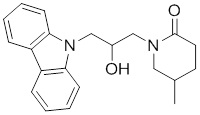
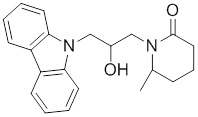
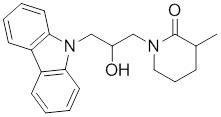
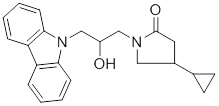
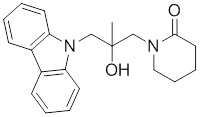
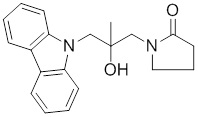
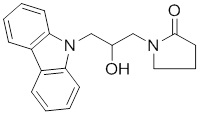
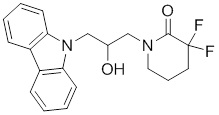
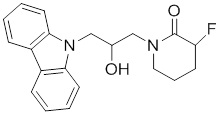
Соединение 71: 1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-он
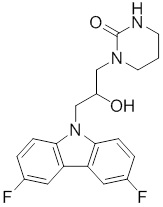
Смесь 3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазола (0,06 г, 0,2 ммоль) и 1,3-диаминопропана (0,195 мл, 2,3 ммоль) в этаноле (2 мл) перемешивали при 40°C в течение 5 часов. Реакционную смесь концентрировали при пониженном давлении с получением светло-желтого масла. ESI (масса/заряд): 334,2 (M+H). Остаток растворяли в метиленхлориде (10 мл) при 0°C добавляли 4-диметиламинопиридин (0,005 г) и 1,1'-карбонилдиимидазол (0,056 г, 0,3 ммоль). Смесь нагревали до комнатной температуры и перемешивали в течение 16 часов. Реакционную смесь концентрировали при пониженном давлении и остаток очищали посредством хроматографии в силикагеле (0-10% метанол/метиленхлорид) с получением желаемого продукта в виде белого порошка (0,060 г, 72%). 1H ЯМР (300 МГц, d6-DMSO): δ 7,99 (дд, 2H, J=9,6, 2,7 Гц), 7,56 (дд, 2H, J=9,0, 4,2 Гц), 7,30 (тд, 2H, J=9,0, 2,7 Гц), 6,29 (с, 1H), 5,24 (д, 1H, J=5,4 Гц), 4,35 (дд, 1H, J=15,0, 3,6 Гц), 4,24 (дд, 1H, J=15,0, 8,1 Гц), 4,07 (м, 1H), 3,55-3,05 (м, 6H), 1,90-1,70 (м, 2H); ESI (масса/заряд): 360,1 (M+H).
Соединения от 72 до 84:
Соединения от 72 до 84 получали способами, аналогичными способам, используемым для соединения 71 с использованием вместо 1,3-диаминопропана соответствующего диамина, такого как н-метил-1,3-диаминопропан, этилендиамин, н-этилэтилендиамин, N1-циклогексилпропан-1,3-диамин, N1-циклобутилпропан-1,3-диамин, N1-циклопентилпропан-1,3-диамин или пропан-1,2-диамин. Получение используемых коммерчески недоступных диаминов описано в получении промежуточных соединений.
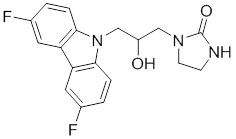
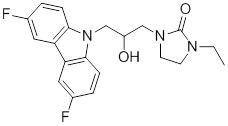
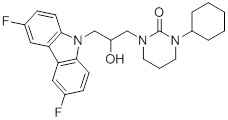
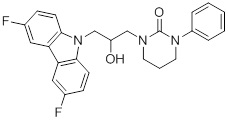
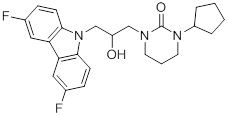
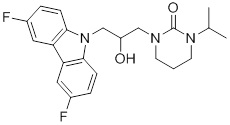
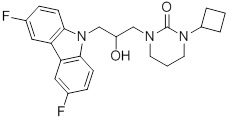
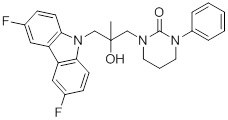
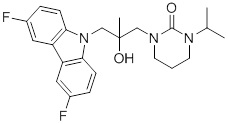
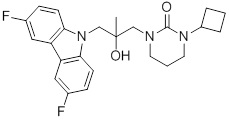
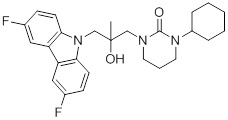
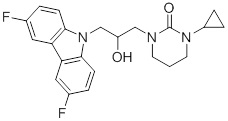
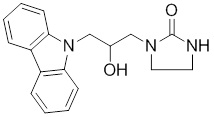
Соединение 85: 1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-он
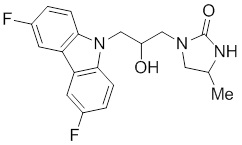
Смесь трет-бутил-(1-((3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)амино)пропан-2-ил)карбамата (1,400 г, 80% чистоты, 2,6 ммоль, 1,0 эквив.) и трет-бутоксида калия (0,290 г, 2,6 ммоль, 1,0 эквив.) в безводном тетрагидрофуране (270 мл) перемешивали при кипячении с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли уксусную кислоту (0,1 мл) и силикагель и смесь концентрировали при пониженном давлении до взвеси. Неочищенный остаток очищали посредством хроматографии на колонке с силикагелем посредством элюции в градиенте 0-10% метанола/метиленхлорида с получением твердого вещества. Твердое вещество кристаллизовали из этилацетата с получением белого твердого вещества (0,673 г, 72%). 1H ЯМР (300 МГц, CDCl3; смесь диастереомеров): δ 7,69-7,65 (дд, 2H, J=2,7, 8,7 Гц), 7,40-7,35 (дд, 2H, J=4,1, 9,0 Гц), 7,24-7,18 (тд, 2H, J=2,7, 9,0 Гц), 4,47-4,19 (м, 5H), 3,82 (ушир. м, 1H), 3,58-2,93 (м, 4H), 1,26-1,24 (д, 3H, J=6,3 Гц); ESI (масса/заряд): 360,9 (M+H).
Соединение 86: 1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-этилтетрагидропиримидин-2(1H)-он
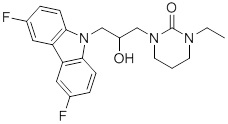
К раствору 3,6-дифтор-9H-карбазола (0,065 г, 0,3 ммоль) в безводном N,N-диметилформамиде (0,3 мл) добавляли 60% гидрид натрия в минеральном масле (0,009 г, 0,2 ммоль) и смесь перемешивали при комнатной температуре в течение 30 минут. Добавляли раствор 1-этил-3-(оксиран-2-илметил)тетрагидропиримидин-2(1H)-она (0,055 г, 0,3 ммоль) в безводном N,N-диметилформамиде (0,3 мл) и смесь нагревали при 70°C в течение 8 часов. Реакционную смесь разбавляли метанолом, фильтровали и очищали посредством препаративной ВЭЖХ (C18, 30-95% ацетонитрил в воде) с получением белого твердого вещества (0,072 г, 62%). 1H ЯМР (300 МГц, CDCl3): δ 7,67-7,63 (дд, 2H, J=2,6, 9,0 Гц), 7,39-7,35 (дд, 2H, J=4,2, 8,7 Гц), 7,23-7,16 (тд, 2H, J=2,4, 9,0 Гц), 5,52 (д, 1H, J=2,7 Гц), 4,37-4,21 (м, 3H), 3,86-3,79 (м, 1H), 3,43-2,98 (м, 6H), 2,88-2,83 (дд, 1H, J=1,8, 14,7 Гц), 1,91-1,83 (квинт., 2H, J=5,9 Гц), 1,12-1,07 (т, 3H, J=7,4 Гц); ESI (масса/заряд): 388,1 (M+H); анализ ВЭЖХ: (C18, 10-90% ацетонитрил в воде в течение 20 минут: время удержания, % площади при 254 нм): 12,8 мин, 100%.
Соединения 87-100:
Соединения 87-100 получали способами, аналогичными способам, используемым для соединения 88.
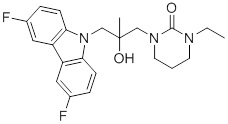
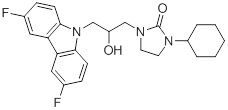
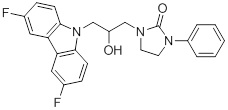
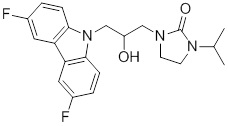
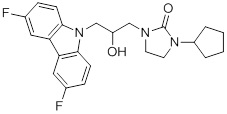
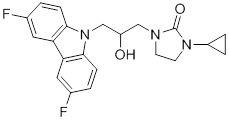
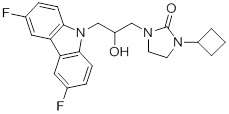
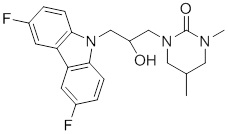
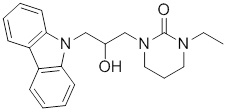
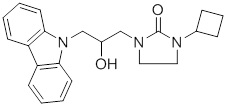
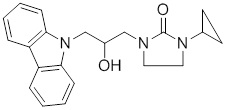
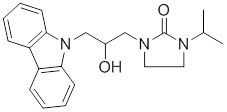
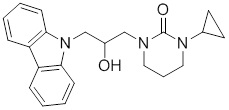
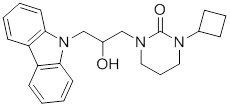
Соединение 101: 1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,4-диметилтетрагидропиримидин-2(1H)-он
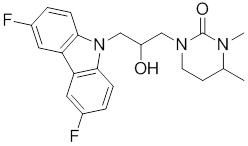
К перемешиваемому раствору 3,6-дифтор-9H-карбазола (0,38 г, 1,9 ммоль, 1,2 эквив.) в безводном N,N-диметилацетамиде (2 мл) добавляли 60% гидрид натрия в минеральном масле (0,075 г, 1,9 ммоль, 1,2 эквив.). После перемешивания при комнатной температуре в течение 2 часов полученный раствор карбазола натрий был готов к применению.
К перемешиваемому раствору 1,6-диметилтетрагидропиримидин-2(1H)-она (0,2 г, 1,6 ммоль, 1,0 эквив.) в безводном N,N-диметилацетамиде (3 мл) при 0°C добавляли 60% гидрид натрия в минеральном масле (0,075 г, 1,9 ммоль, 1,2 эквив.) и смесь перемешивали в течение 1 часа при комнатной температуре. Добавляли эпибромгидрин (0,155 мл, 1,9 ммоль, 1,2 эквив.) при 0°C и смесь медленно нагревали до комнатной температуры и перемешивали в течение 16 часов. Добавляли Раствор карбазола натрия и смесь нагревали при 70°C в течение 5 часов. Реакционную смесь разбавляли водой и экстрагировали этилацетатом. Органические слои промывали насыщенным водным хлоридом натрия, сушили над сульфатом натрия, фильтровали и концентрировали при пониженном давлении. Остаток очищали на колонке с силикагелем (0-100% этилацетат/гексан) с получением чистого продукта в виде белой пены (0,116 г, 19%). 1H ЯМР (300 МГц, CDCl3): (смесь двух диастереомеров) δ 7,68 (дд, 2H, J=8,7, 2,7 Гц), 7,40 (дд, 2H, J=9,0, 4,2 Гц), 7,27-7,18 (м, 2H), 5,51 и 5,06 (д, 1H, J=2,7 Гц), 4,50-4,20 (м, 3H), 3,90-3,74 (м, 1H), 3,50-2,75 (м, 7H), 2,05 (м, 1H), 1,60 (м, 1H), 1,21 и 1,17 (д, 3H, J=6,6 Гц); ESI (масса/заряд): 388,2 (M+H).
Соединение 102: 3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3,4-дигидрохиназолин-2(1H)-он
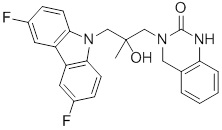
Смесь 1-бензил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3,4-дигидрохиназолин-2(1H)-она (0,102 г, 0,2 ммоль, 1,0 эквив.) и 20% гидроксида палладия на углероде (0,035 г) в уксусной кислоте (4 мл) и тетрагидрофуране (2 мл) перемешивали при 344,7 кПа водорода в течение 48 часов. Добавляли 20% гидроксид палладия на углероде (0,02 г) и 10% палладий на углероде (0,01 г) и реакционную смесь перемешивали при 344,7 кПа водорода в течение 72 часов. Смесь фильтровали, концентрировали и очищали посредством препаративной ВЭЖХ (C18, 40-80% ацетонитрил в воде) с получением белого твердого вещества (0,013 г, 15%). 1H ЯМР (300 МГц, CD3OD): δ 7,73-7,70 (дд, 2H, J=2,6, 8,6 Гц), 7,55-7,51 (дд, 2H, J=4,1, 9,2 Гц), 7,27-7,05 (м, 3H), 7,07-7,05 (д, 1H, J=7,2 Гц), 6,96-6,91 (тд, 1H, J=1,1, 7,5 Гц), 6,81-6,78 (д, 1H, J=8,1 Гц), 4,71 (с, 2H), 4,33 (с, 2H) 3,75-3,70, 3,59-3,54 (ABq, 2H, J=14,4 Гц), 1,22 (с, 3H); ESI (масса/заряд): 422,1 (M+H); анализ ВЭЖХ: (C18, 5-95% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 13,5 мин, 91,5%.
Приводимые ниже соединение получали способами, аналогичными способам, используемым для соединения 102.
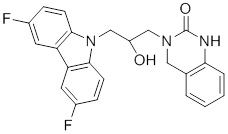
Соединение 104: (1S,4R)-2-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-он
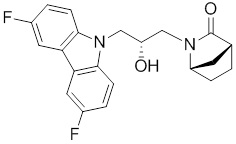
К перемешиваемому раствору (1S,4R)-2-азабицикло[2.2.1]гептан-3-она (0,051 г, 0,5 ммоль, 2,0 эквив.) в безводном тетрагидрофуране (1,5 мл) добавляли 60% гидрид натрия в минеральном масле (0,009 г, 0,2 ммоль, 1,0 эквив.) и смесь перемешивали при комнатной температуре в течение 60 минут. Добавляли (R)-3,6-дифтор-9-(оксиран-2-илметил)-9H-карбазол (0,060 г, 0,2 ммоль, 1,0 эквив.) и смесь перемешивали при 80°C в герметичной пробирке в течение 16 часов. Смесь охлаждали до комнатной температуры и добавляли 1 Н уксусную кислоту (0,02 мл) в метаноле, а затем концентрировали при пониженном давлении. Неочищенный остаток очищали посредством препаративной ВЭЖХ (C18, 30-95% ацетонитрил в воде) с получением белого твердого вещества (0,053 г, 61%). 1H ЯМР (300 МГц, CDCl3): δ 7,68-7,65 (дд, 2H, J=2,6, 8,6 Гц), 7,38-7,33 (дд, 2H, J=4,1, 8,9 Гц), 7,24-7,17 (тд, 2H, J=2,5, 9,0 Гц), 4,38-4,28 (м, 4H), 3,64 (ушир. с, 1H), 3,43-3,38 (дд, 1H, J=2,7, 14,1 Гц), 3,02-2,96 (дд, 1H, J=2,7, 14,4 Гц), 2,90-2,89 (м, 1H), 1,96-1,40 (м, 6 H); ESI (масса/заряд): 371,1 (M+H); анализ ВЭЖХ: (C18, 5-95% ацетонитрил в воде+0,1% трифторуксусная кислота в течение 20 минут: время удержания, % площади при 254 нм): 12,2 мин, 100%; хиральный анализ ВЭЖХ (Chiralcel AD-H, 15% этанол в гексане в течение 42 минут: время удержания, % площади при 254 нм): 7,7 мин, 98,5%; 12,6 мин, 0,7% (98,5% ди).
Соединения 105-138:
Соединения 105-138 получали способами, аналогичными способам, используемым для соединения 104.
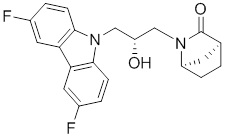
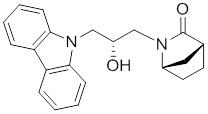
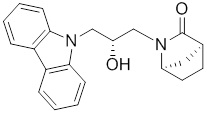
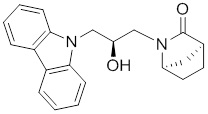
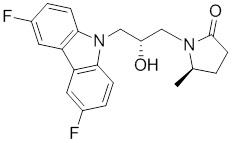
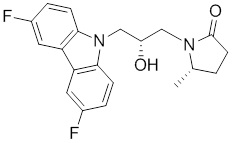
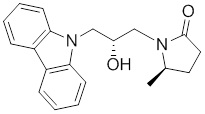
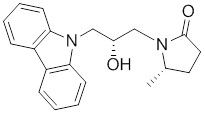
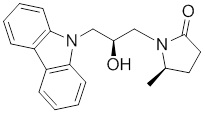
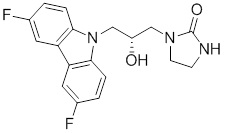
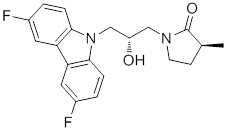
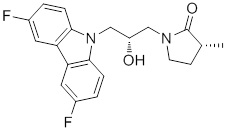
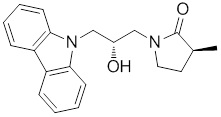
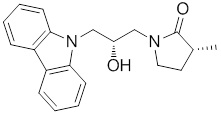
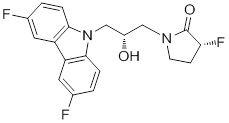
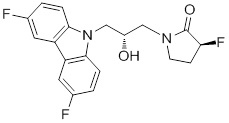
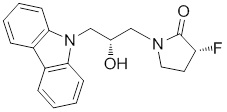
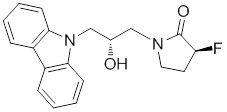
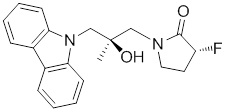
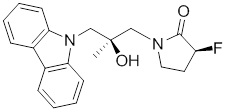
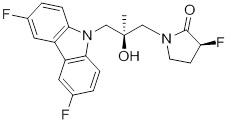
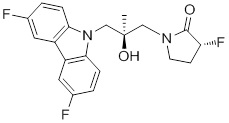
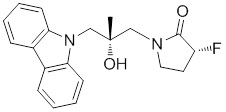
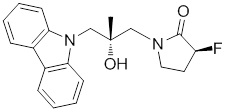
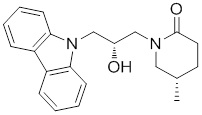
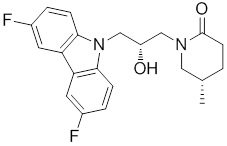
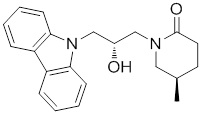
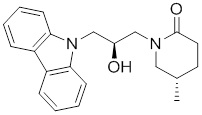
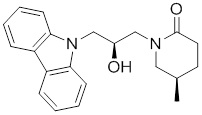
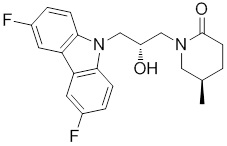
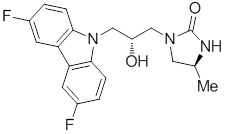
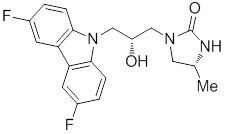
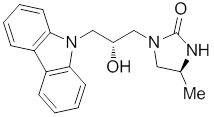
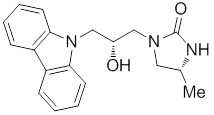
Конкретные анализы, пригодные для оценки соединений формулы I, включают анализ Per2 для оценки активности тестируемых соединений и анализ Cry1 для оценки мишеней тестируемых соединений, как описано ниже.
Пример 3: Анализ Per2 для оценки активности тестируемых соединений
Соединения подвергали скринингу с использованием высокопроизводительной системы анализа циркадных ритмов, как описано ранее в Zhang, E. E. et al. Cell, 2009, 139, 199-210. В кратком изложении, стабильные репортерные клетки U2OS, несущие Per2-dLuc высевали с плотностью 30000 клеток/лунку в 96-луночные твердые белые плоскодонные обработанные TC микропланшеты Corning (Corning®) и инкубировали в течение 48 часов при 37°C в присутствии 5% CO2 в модифицированной Дульбекко среде Игла (DMEM), дополненной 10% эмбриональной телячьей сывороткой (FBS) и пенициллином (100 единиц/мл)-стрептомицином (100 мкг/мл). Соединения формулы I разводили в диметилсульфоксиде (DMSO), как правило в концентрации 2 мг/мл. Затем маточные растворы DMSO серийно разводили в DMSO, как правило, разводя в 3 раза на каждом этапе разведения. Через период 48 часов из клеток на планшете удаляли среду для культивирования клеток и клетки синхронизировали 200 мкл/лунку полной среды для культивирования клеток (описанной выше), дополненной 5 мкМ форсколином (Tocris®) и 1 мМ люциферина жука (Promega®). Непосредственно после синхронизации в каждую лунку добавляют 1 мкл разведения соединения. Планшеты герметизируют, немного перемешивают и за экспрессией генов наблюдают, непрерывно измеряя люминесценцию (Tecan® Infinite M200 или Tecan® Infinite M200 Pro) в течение минимум 3 суток при 35°C. Необработанные данные люминесценции (числа) сначала анализируют с использованием программного обеспечения Multicycle™ (Actimetrics, Inc.) с определением амплитуды (амп.), периода и фазы (фз.) для каждой концентрации соединения. Длительность периода для контрольных лунок (т.е. в отсутствии соединения, только с DMSO) должна составлять 26-30 часов. Затем данные амп. наносят на диаграмму в зависимости от логарифма концентрации соединения (M) и анализируют посредством нелинейного регрессионного анализа с определением EC50.
Приводимая ниже таблица позволяет получать данные EC50 для Per2 для указанных соединений. EC50 приведены в виде микромолярной концентрации.
Таблица 1
Анализ данных Per2
Специалист в данной области может легко оптимизировать этот анализ с определением данных EC50 для Per2 для любых описываемых в настоящем документе соединений.
Пример 4: Анализ связывания посредством теплового сдвига
Связывание соединений с выделенным FAD-связывающим доменом белка CRY1 человека (hCRY1) определяли с использованием анализа дифференциальной сканирующей флуорометрии ("теплового сдвига") (Pantoliano et al. (2001) J. Biomol. Screening 6, 429; Niesen et al. (2007) Nature Protocols 2, 2212). FAD-связывающий домен hCRY1 (аминокислотные остатки 1-494) с C-концевой меткой Myc-DDK (FADBD) получали посредством транзиторной трансфекции клеток HEK293T (каталожный № CRL-3216, American Type Culture Collection) и очищали посредством аффинной хроматографией с антителами к FLAG (каталожный № A2220, Sigma-Aldrich). FADBD (0,5 мкг на лунку) инкубировали с разведениями соединений в DMSO (конечная концентрация DMSO в реакционной смеси 5%) в 17,5 мкл забуференного Tris солевого раствора (TBS) в течение 10 минут на льду, затем в каждую лунку добавляли 2,5 мкл 8× красителя Sypro-Orange Dye (Life Technologies). Для каждой концентрации соединения оценивали три лунки. Температуры плавления измеряли в устройстве для количественной ПЦР ABI7500 с использованием режима кривой плавления с термическим профилем 2 минуты при 25°C, с последующей скоростью линейного изменения 1°C/минута до 99°C. Температуру плавления для каждой лунки определяли на основании первой производной кривой плавления. Изменение температуры плавления (ΔTm) получали вычитая температуру плавления FADBD только в 5% DMSO. Как представлено на фиг. 21, для соединения 72 наблюдали зависимое от дозы увеличение ΔTm, что указывает на то, что соединение физически ассоциируется с FADBD белка hCRY1.
Пример 5: Действие на гены часов и экспрессия генов глюконеогенеза in vivo
В этом примере исследовали действие содержащих карбазол амидов, карбаматов и карбамидов на экспрессию генов часов и глюконеогенеза в различных моделях на мышах. Конкретно, использовали четыре различных модели на мышах: мыши ICR, мыши Balb/c, мыши C57Bl/6J DIO (индуцированное диетой ожирение) и мыши db/db. Мыши C57Bl/6J DIO и db/db представляют собой принятые в данной области модели диабета, ожирения и дислипидемии. У мышей с индуцированным диетой ожирением (DIO), которые демонстрируют фенотип диабета II типа, в ответ на кормление с высоким содержанием жиров развивается ожирение, гиперинсулинемия, резистентность к инсулину и нарушение толерантности к глюкозе (Srinivasan and Ramarao, 2007). Мышь db/db (мышь leprdb ) несет мутацию в гене мышей db, который кодирует рецептор лептина. Db/db являются спонтанно прожорливыми и приобретают ожирение, гипергликемию, гиперинсулинемию и резистентность к инсулину.
Исследования in vivo, где исследовали влияние модулирующих Cry соединений на экспрессию генов, проводили различными экспериментальными способами, описанными ниже.
Четерехсуточное исследование. Самцов мышей ICR (с массой 30-35 г), полученных в Charles River Laboratories (Hollister, CA), использовали для эксперимента после акклиматизации в течение по меньшей мере 3 суток. Мышам дозировали носитель (WFI или 10% коллифор) или соединение (50 мг/кг, объем дозы 5 мл/кг, п/о) в течение 4 суток дважды в сутки (дважды в сутки), начиная во второй половине дня первых суток. Последнюю дозу соединения или носителя вводили утром суток сбора. На сутки сбора (6 часов после последней дозы), мышей подвергали эвтаназии посредством удушения CO2 и вырезали 50 мг ткани печени и помещали в пробирку, содержащую 500 мкл RNALater.
Исследования экспрессии генов в течение 24 часов. Самцов мышей C57Bl/6J DIO приобретали в возрасте 17 недель (The Jackson Laboratory, Sacramento, CA) и перед использованием в эксперименте акклиматизировали в течение периода 2 недель. Общий размер группы составлял 15 особей на обработку, разделяемых на 5 временных точек с получением конечного размера группы 3 мыши. Мышам дозировали носитель (вода для инъекций (WFI) или модулирующее Cry соединение, соединение 72 (50 мг/кг в WFI) в объеме дозы 5 мл/кг, дважды в сутки, посредством перорального принудительного кормления в течение 2 суток, с последней пятой дозой, вводимой за 12 часов перед сбором.
Всего каждая мышь в течение эксперимента получала 5 доз соединения. Мышей взвешивали и случайным образом распределяли по каждому из видов обработки на основе массы вечером перед началом исследования. Начиная с суток 3 в 15:00, группу животных из групп, обрабатываемых носителем и соединением 72, подвергали эвтаназии с использованием удушения CO2, вырезали по 50 мг печени, эпидидимальной жировой ткани и скелетных мышц, соответственно, и помещали в пробирку, содержащую 500 мкл RNALater. Эту процедуру проводили для оставшейся части полученных на основе временных точек групп в соответствующие им времена сбора. Также у каждого животного получали образцы плазмы и замораживали для использования для последующего определения уровней соединения.
Получение тотальной РНК печени мыши. Для получения и выделения РНК из образцов печени использовали наборы для выделения тотальной РНК E.Z.N.A.® HP (R6812-01 и протокол, описанный в руководстве, пересмотрено в 2010 году). Для получения образцов РНК, 10-30 мг образца отбирали из РНКLater и помещали в 1,5 мл микроцентрифужную пробирку. К ткани, которую гомогенизировали в роторно-статорном гомогенизаторе (например, Tissue-Tearor, модель № 985370 BioSpec Products с 4,5 мм датчиком, кат. № 985370-04) добавляли лизирующий буфер GTC (700 мкл), а затем центрифугировали на полной скорости (≥ 13000×g) в течение 5 минут. Очищенный супернатант пипеткой переносили в колонку для очистки ДНК предварительно встроенную в 2 мл пробирку для сбора. Собранную колонку центрифугировали при 13000×g в течение 1 минуты и фильтрат сохраняли. в лизат добавляли равный объем (700 мкл) 70% этанола и перемешивали. Затем образец вносили в центрифужную колонку для РНК HiBind, помещенную в 2 мл пробирку для сбора, которую центрифугировали при 10000×g в течение 60 секунд при комнатной температуре. Непосредственно в новую колонку для РНК HiBind, помещенную в 2 мл пробирка для сбора, пипеткой добавляли отмывочный буфер для РНК I (250 мкл). Собранную колонку центрифугировали при 10000×g в течение 60 секунд. Колонку для РНК помещали в новую 2 мл пробирку для сбора. непосредственно на поверхность смолы для РНК HiBind в каждой колонке пипеткой наносили исходный раствор ДНКазы I (75 мкл) (с использованием расщепления ДНКазой не содержащим РНКаз набором ДНКаз (E1091): для каждой колонка для РНК HiBind исходный раствор ДНКазы I получали следующим образом: буфер для расщепления ДНКазой I E.Z.N.A.® 73,5 мкл, не содержащая РНКаз ДНКаза I (20 единиц Кунитца/мкл) 1,5 мкл=общий объем 75 мкл.). Колонку со связанной РНК инкубировали при комнатной температуре (25-30°C) в течение 15 минут. В колонку добавляли отмывочный буфер для РНК I (500 мкл) и колонку помещали на стол на 2 минуты. После центрифугирования при 10000×g в течение 60 секунд, удаления фильтрата, добавляли 500 мкл отмывочного буфера для РНК II и центрифугировали при 10000×g в течение 60 секунд. Добавляли дополнительные 500 мкл отмывочного буфера для РНК II и собранную колонку центрифугировали при 10000×g в течение 60 секунд. Колонку центрифугировали в течение 2 минут при максимальной скорости до полного высушивания матрикса HiBind. Колонку помещали в чистую 1,5 мл микроцентрифужную пробирку и добавляли 40-70 мкл воды, удовлетворяющей требованиям молекулярной биологии. После осаждения в течение 1 минуты колонку центрифугировали в течение 2 минут при максимальной скорости для элюции РНК. Выделенную РНК собирали в пробирку для сбора.
Получение тотальной РНК крови мыши. Для исследований РНК цельной крови использовали самцов мышей db/db (в возрасте 9 недель, The Jackson Laboratory, Bar Harbor, Maine) в эксперименте с n=8 мышами в каждой экспериментальной группе. Мышам дозировали соединение 72 (100 мг/кг, п/о; объем дозы 5 мл/кг, в 10% коллифоре) или 10% коллифор, раз в сутки в течение трех суток в ZT0 (7:00) (ZT относится к времени таймера и означает время, в которое включали свет с форсированием суток в виварии для мышей). В последние сутки в ZT7,5 (14:30) животных подвергали эвтаназии с использованием удушения CO2, и собирали кровь из сердца посредством сердечной пункции. Кровь помещали в раствор RNALater в общем объеме 1,5 мл. Тотальную РНК получали с использованием набора для изоляции РНК из крови Ambion Mouse RiboPure Blood RNA Isolation Kit AM1951 как указано далее. Образцы центрифугировали в течение 3 минут, удаляя супернатант. Добавляли два мл лизирующего раствора и перемешивали, переносили в 15 мл пробирку с последующим добавлением нескольких микролитров 3M ацетата натрия. Добавляли лизирующий буфер до общего объема 3,8 мл и перемешивали. Смесь образца экстрагировали 1,5 мл кислого фенола:хлороформа и восстанавливали водную фазу. После добавления 0,5 объема 100% этанола и перемешивания, образцы пропускали через фильтрующую колонку, предоставляемую в наборе и промывали 750 микролитрами отмывочного буфера 1. Фильтр промывали, пропуская 2 раза 750 микролитров отмывочного буфера 2/3 и сушили. РНК элюировали в 200 микролитров воды, удовлетворяющей требованиям молекулярной биологии (не содержащей РНКаз).
Количественное определение тотальной РНК. С использованием набора для количественного определения РНК RediPlate 96 RiboGreen RNA Quantification Kit (Invitrogen) (Invitrogen) получали стандартную кривую RediPlate, перенося 20 мкл восстановленного стандарта РНК в лунку RediPlate, восстановленную в 180 мкл буфера TE RediPlate. Для РНК печени, получаемой из 30-100 мг ткани с использованием набора, подобного Omega Bio-Tek HP Total RNA Kit, и элюируемой в не содержащую РНКаз воду в объеме 50 мкл (микролитров), 5 мкл тотальной РНК разбавляют в 195 мкл буфера TE RediPlate (разведение РНК 1:40 РНК), перемешивают. После перенесения 5 мкл в лунку RediPlate, восстановленную в 195 мкл буфера TE, и инкубации 10 минут при комнатной температуре, определяли интенсивность флуоресценции в лунках со стандартами и образцами в Tecan M200 с возбуждением, установленным на 480 нм, и испусканием, установленным на 520 нм, с коэффициентом усиления, установленным на ≈70%. Альтернативно, можно использовать FlexStation 3 с возбуждением 488 нм и испусканием 525 нм и порогом 515 нм. Стандартную кривую получали в GraphPad Prism и показатели для образцов (неизвестные) интерполировали посредством линейного регрессионного анализа, и рассчитывали концентрации в образцах РНК.
Получение кДНК. 10× буфер RT из набора для высокопроизводительной обратной транскрипции кДНК (Invitrogen) (40-70 мкл), dNTP и случайные праймеры размораживали на льду. С использованием одинакового количества добавляемой в каждый образец РНК (как правило, 0,5-4,0 мкг) проводили реакции в общем объеме 40 мкл. Смешивали соответствующие количества тотальной РНК и не содержащей нуклеаз H2O с получением общего объема 20 мкл. Получали готовую смесь с использованием 4,2 мкл не содержащей РНКаз H2O, 2 мкл 10× буфера RT, 0,8 мкл 25× dNTP и 2 мкл случайных праймеров для каждой из реакций (необязательно, можно добавлять на 10% больше, чем общее количество для реакций, которые необходимо провести, для гарантии достаточного объема). Для каждой из реакций добавляли обратную транскриптазу (1 мкл) и осторожно смешивали без встряхивания. Определенные дублирующие образцы (всего ≈10%) включали в группу RT(-) и получали достаточное количество готовой смеси без обратной транскриптазы для включения этих контролей. К постоянно добавляемым 20 мкл образцов РНК добавляли готовую смесь (20 мкл) (или готовую смесь RT(-)). Реакционные смеси инкубировали при 37°C в течение 2 часов, нагревали до 85°C в течение 5 минут и помещали на лед. Образцы кДНК хранили при 4°C, если использовали на следующие сутки, или хранили при -20°C в течение более длительных периодов.
ОТ-ПЦР. Для анализа ПЦР используемым набором являлась готовая смесь TaqMan® Fast Universal Master Mix (2×), No AmpErase® UNG. Для реакций, проводимых на ABI 7500, в каждую лунку добавляли 2 мкл матричной кДНК или контроля матричной кДНК RT(-). Получали готовую смесь, содержащую 1,0 мкл TaqMan Expression Assay (праймеры/зонды) и 7 мкл не содержащей нуклеаз H2O для каждого анализируемого образца, и на каждые 2 мкл образца добавляли 18 мкл готовой смеси+Expression Assay+не содержащей нуклеаз H2O, перемешивали пипеткой. Планшет герметизировали, центрифугировали и помещали в ABI 7500. В каждую группу исследуемых образцов РНК включали анализ экспрессии иРНК по меньшей мере одного гена домашнего хозяйства (например, GAPDH; Mm03302249_g1 или Hs02758991_g1).
Действие модулирующего Cry соединения 72 на функцию основных часов исследовали у мышей с диабетом и у мышей без диабета. Самцов мышей C57Bl/6J DIO в возрасте 17 недель (The Jackson Laboratory, Sacramento, CA) содержали на диете с высоким содержанием жиров (HFD) и перед обработкой для подтверждения диабета и ожирения акклиматизировали в течение периода 2 недель. Трех мышей обрабатывали соединением или носителем в каждый из 5 моментов времени. Мышам дозировали носитель (вода для инъекций (WFI) или соединение 72 (50 мг/кг в WFI) в объеме дозы 5 мл/кг, дважды в сутки посредством перорального принудительного кормления. Всего каждая мышь в ходе эксперимента получала 5 доз соединения. Мышей взвешивали и случайным образом распределяли по каждому из видов обработки на основе массы вечером перед началом исследования. Начиная с суток 3 в 15:00, группу животных из групп, обрабатываемых носителем и соединением 72, подвергали эвтаназии с использованием удушения CO2, вырезали по 50 мг печени, эпидидимальной жировой ткани и скелетных мышц, соответственно, для получения РНК.
Действие соединения 72 также исследовали у нормальных мышей Balb/c на циркадных иРНК в течение 24 часов. Мышам в возрасте 8 недель, полученным из Charles River, позволяли акклиматизироваться в течение 2 недель. Мышам дважды в сутки в течение 3 суток дозировали всего 7 доз каждому животному с последней дозой за 12 часов перед получением тканей. Мышам дозировали носитель (WFI) или соединение 72 (50 мг/кг в WFI) в объеме дозы 5 мл/кг, дважды в сутки, посредством перорального принудительного кормления. Начиная с суток 3 в 15:00, группу животных из групп, обрабатываемых носителем и соединением 72, умерщвляли и вырезали приблизительно по 50 мг печени, легкого, почки, надпочечника, селезенки, эпидидимальной жировой ткани и бурой жировой ткани и помещали в RNALater.
иРНК основных часов у мышей C57Bl/6J DIO, обработанных носителем, демонстрировала характерный циркадный профиль экспрессии (фиг. 1). Однако при обработке соединением 72 иРНК Per2 была супрессирована у обеих пород мышей C57Bl/6J DIO и Balb/c в течение 24 часов, и наиболее сильно она была снижена в ZT8 и снова в ZT8 через 24 часа (фиг. 1 A и B). иРНК Bmal1 при обработке соединением 72 значительно снижалась через ZT8 и 32 часа после начального ZT0 у обеих пород мышей. Также транскрипты Bmal1 демонстрировали значительную задержку фазы у мышей C57Bl/6J DIO и в меньшей степени у мышей Balb/c (фиг. 1C и D). иРНК Cry1 была супрессирована в течение ее пика экспрессии в течение периода темноты (фиг. 1E и F, заштрихованные области). Опережение по фазе транскриптов Cry1 у мышей, обработанных носителем, наблюдаемое у DIO относительно обработанных носителем мышей Balb/c частично может являться следствием известного действия диеты с высоким содержанием жиров на многие суточные профили (Eckel-Mahan et al. (2013) Cell). В отличие от иРНК Cry1, иРНК Cry2 у обработанных носителем животных выходила на пик в дневные часы, но это было сильно ослаблено при обработке соединением 72 у обеих пород мышей C57Bl/6J DIO и Balb/c (фиг. 1G и H).
В тех же 24 часовых исследованиях, описанных выше, соединение 72 значительно изменяло суточный профиль иРНК генов глюконеогенеза Pck1 (PEPCK) и G6Pc (каталитической субъединицы глюкозо-6-фосфатаза) у мышей C57Bl/6J DIO относительно носителя (фиг. 2A и C). Обработанные носителем мыши демонстрировали профиль, который был сглажен и опережал по фазе профиль, наблюдаемый у получающих корм мышей C57Bl/6J из других исследований (Hughes et al. (2009)). Обработанные соединением 72 мыши C57Bl/6J DIO демонстрировали пик экспрессии обоих этих генов глюконеогенеза ранним вечером (ZT14), что находится ближе к времени пика экспрессии, который наблюдают у получающих корм животных (Hughes et al. (2009)). Соединение 72 изменяло суточные профили экспрессии Pck1 и G6Pc у мышей C57Bl/6J DIO относительно носителя в большей степени, чем это происходило у мышей Balb/c (фиг. 2B и D).
У мышей ICR исследовали действие нескольких модулирующих Cry соединений, соединения 72, соединения 48 соединения 9 и соединения 57. Мышей обрабатывали 50 мг/кг каждого из соединений (соединения 72, соединения 48, соединения 9 и соединения 57), п/о (пероральное введение) в объеме дозы 5 мл/кг в течение 4 суток, дважды в сутки, или контрольным носителем. Каждое соединение супрессировало экспрессию Per2 в печени (фиг. 3A). Обработка соединением 48 приводила к 8-кратному увеличению иРНК Bmal1 в ZT6, обработанные соединением 72 и соединением 9 мыши демонстрировали 4-кратное увеличение, и обработанные соединением 57 мыши демонстрировали по меньшей мере 2-кратное увеличение (фиг. 3B). Соединение 72, соединение 48 и соединение 9 также вызывали снижение транскриптов Cry2 (фиг. 3C).
Уровни иРНК основных генов часов в цельной крови могут обеспечивать неинвазивный способ определения действия соединений у обрабатываемых индивидуумов. В каждой экспериментальной группе использовали по n=8 самцов мышей db/db (в возрасте 9 недель, The Jackson Laboratory, Bar Harbor, Maine). Мышам дозировали соединение 72 (100 мг/кг, п/о; объем дозы 5 мл/кг, в 10% коллифоре) или 10% коллифор, раз в сутки в течение трех суток в ZT0 (7:00) (ZT относится к времени таймера и означает время, в которое включали свет с форсированием суток в виварии для мышей). В последние сутки в ZT7,5 (14:30) животных подвергали эвтаназии с использованием удушения CO2, и собирали кровь из сердца посредством сердечной пункции. Цельную кровь переносили в пробирку, содержащую RNALater для анализа посредством кПЦР-РВ.
Связывающий D-бокс белок Dbp подвержен выраженной суточной регуляции. Соединение 72 в настоящем исследовании вызывало статистически значимую супрессию экспрессии гена Dbp (фиг. 4), демонстрируя, что лейкоциты мышей, обработанных такими соединениями, могут предоставлять информацию о действии соединений на основной механизм часов во всем организме. Такую информацию можно использовать в качестве диагностического маркера или в качестве биомаркера для оценки действия модуляторов Cry и других терапевтических средств, которые влияют на основной циркадный механизм.
Для соединений, которые напрямую взаимодействуют с основным механизмом часов, время дозирования может являться решающим для максимизации их действия. Мышей db/db обрабатывали однократной дозой соединения 72 (50 мг/кг), вводимой в ZT0 или ZT10. Первое (ZT0) совпадало с пиком белков Cry1 и Bmal1 в печени мыши, а последнее (ZT10) приблизительно соответствовало низшей точке Cry1 и Bmal1. Для каждого момента через 7,5 часов получали ткань печени и образцы исследовали на иРНК основных ген часов посредством кПЦР-РВ. Так как соединение 72 обладало большим относительным действием на иРНК часов на пике по сравнению с низшей точкой (фиг. 5), дозирование примерно такой же момент времени, как первый, позволяет обеспечить большее действие на механизм часов, и это может дополнительно приводить на большее действие на метаболическую продукцию часов.
Пример 6: Действие однократной дозы соединения 72, вводимого на пике или в низшей точке экспрессии генов часов в модели диабета на мышах
Оценивали действие соединения 72 на метаболизм глюкозы при введении в виде однократной дозы, вводимой или на пике, или в низшей точке экспрессии основных генов часов Cry1/Bmal1, в модели диабета II типа на мышах db/db.
Самцов мышей db/db, гомозиготных по Leprdb (в возрасте 6 недель), получали в The Jackson Laboratory (Bar Harbor, Maine). Мышей в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к стандартному гранулированному корму для мышей и воде. Животные перед экспериментированием привыкали к таким условиям в течение 2 недель. Мышей разделяли на две исследуемых группы для дозирования на пике или в низшей точке экспрессии генов Cry1 и Bmal1. Мышам однократно дозировали носитель (10% коллифор, Sigma-Aldrich) или соединение 72 (50 мг/кг в 10% коллифоре в воде) в объеме дозы 5 мл/кг, раз в сутки, посредством перорального принудительного кормления, в ZT0 (пик, 7:00) или ZT10 (низшая точка, 17:00). Животных взвешивали на сутки 0 и случайно распределяли по группам обработки так, чтобы каждая группа содержала сходные средние начальные массы. Мыши, дозируемые в ZT0, голодали в течение ночи, начиная с 22:30, когда их переносили в чистую клетку и предоставляли свободный доступ к вода, но не к пище в течение периода 12 часов. Мыши, дозируемые в ZT10, голодали, начиная с 8:30 таким же образом. На сутки исследования после дозирования, мышам за 2 часа до определения глюкозы крови натощак проводили разрез хвоста для обеспечения восстановления после любого стресса, который может вызывать эта процедура. Глюкозу крови натощак (FBG) оценивали у животных в 10:30 или 20:30 с использованием глюкометра AlphaTRAK (Abbott Laboratories, USA). В 11:30 (дозируемые на пике мыши) или 21:30 (дозируемые в низшей точке мыши) каждое животное дозировали 0,5 г/кг глюкозы, затем определяли глюкозу крови через t=15, 30, 60, 90 и 120 минут после глюкозной нагрузки. После последнего сбора крови животных умертвляли и собирали ткани и кровь для других определений.
Значения глюкозы крови натощак и измерения глюкозы, проводимые при OGTT, усредняли и наносили на диаграмму (GraphPad Prism, GraphPad Software, La Jolla, CA). Для каждого отдельного животного рассчитывали площадь под кривой (AUC). Статистический анализ проводили с использованием одностороннего дисперсионного анализа с последующим соответствующим послеэкспериментальным тестом. Значимость допускали при p < 0,05. Данные представлены как среднее и S.E.M.
Введение соединения 72 (50 мг/кг, п/о) в однократной дозе, вводимого на пике экспрессии генов Cry1 и Bmal1 мышам db/db, приводило к видимому влиянию на измерение при OGTT (фиг. 6A) по сравнению с контрольным носителем, но при дозировании в низшей точке влияния не наблюдали (фиг. 6B). AUC, рассчитанная у животных, подвергаемых OGTT, дозируемых на пике экспрессии гена, продемонстрировала, что обработка соединением 72 приводила к меньшему повышению глюкозы на 14% (от 74098 +/- 4194 до 63842 +/- 4318; фиг. 7).
Пример 7: Действие однократной дозы соединения 72, вводимого в течение 7 суток, в модели диабета на мышах
Оценивали действие соединения 72 на метаболизм глюкозы и уровни инсулина при введении в виде однократной дозы, вводимой в течение 7 суток, в модели диабета II типа на мышах db/db.
Самцов мышей db/db, гомозиготных по Leprdb (в возрасте 6 недель), получали в The Jackson Laboratory (Bar Harbor, Maine). Мышей в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к стандартному гранулированному корму для мышей и воде. Животные перед экспериментированием привыкали к таким условиям в течение 2 недель. Мышам дозировали носитель (10% коллифор, Sigma-Aldrich) или соединение 72 (50 мг/кг в 10% коллифоре в воде) в объеме дозы 5 мл/кг, раз в сутки, посредством перорального принудительного кормления, в ZT0 (7:00) в течение семи суток. Мышей взвешивали на сутки 0 и случайно распределяли по группам обработки так, чтобы каждая группа содержала сходные средние начальные массы. Вечером в 22:30 до последнего измерения мышей помещали в чистые клетки и перед измерением глюкозы крови натощак обеспечивали свободный доступ к воде, но не к пище в течение периода 12 часов. На конечные сутки исследования животных дозировали как обычно, а затем за 2 часа до определения глюкозы крови натощак проводили разрез хвоста, для обеспечения восстановления после любого стресса, который может вызывать эта процедура. Глюкозу крови натощак (FBG) у животных оценивали в 10:30 с использованием глюкометра AlphaTRAK (Abbott Laboratories, USA). После определения FBG у каждой мыши способом забора из хвоста собирали кровь в капиллярную трубку. Капиллярные трубки центрифугировали в устройстве для определения гематокрита (BD Triac 0200) и полученную плазму переносили в пробирку Eppendorff. Этот образец, помеченный как t=0 часов, замораживали при -80°C для обеспечения более позднего определения инсулина. В 11:30 каждому животному дозировали 0,5 г/кг глюкозы, затем определяли глюкозу крови через t=15, 30, 60, 90 и 120 минут после глюкозной нагрузки. В конце OGTT собирали кровь для определение инсулина в t=2 часа, как описано выше. После последнего сбора крови животных умерщвляли и собирали ткани и кровь для других определений (подробно описанных ниже). Плазму и ткань печени обработанных соединением 72 животных передавали в CRO для определения уровней соединений с использованием LC/MS/MS и сравнения со стандартной кривой известных количеств соединений.
Значения глюкозы крови натощак и измерения глюкозы, проводимые при OGTT, усредняли и наносили на диаграмму (GraphPad Prism, GraphPad Software, La Jolla, CA). Для каждого отдельного животного рассчитывали площадь под кривой (AUC). Уровни инсулина в плазме определяли с использованием ультрачувствительного ELISA инсулина (ALPCO, Salem, NH). HOMA-IR (модельную оценку гомеостаза-резистентность к инсулину) рассчитывали с использованием следующей формулы: (FPI (мкЕд/л) × FPG (ммоль/л))/22,5, где FPI и FPG означают инсулин в плазме натощак и глюкозу в плазме натощак, соответственно. Данные по инсулину также представляли в формате GraphPad Prism. Статистический анализ проводили с использованием одностороннего дисперсионного анализа с последующим соответствующим послеэкспериментальным тестом. Значимость допускали при p < 0,05. Данные представлены как среднее и S.E.M.
Введение соединения 72 (50 мг/кг, п/о) мышам db/db в течение 7 суток приводило к значимому снижению FBG при сравнении с контрольным носителем (484,9 +/- 34,37 мг/дл до 385,0 +/- 29,69 мг/дл; фиг. 8A). При измерениях в OGTT, у обработанных соединением 72 животных наблюдали меньшие уровни, чем в обработанной контрольным носителем группе (фиг. 8B). The AUC, рассчитанная на основе OGTT, продемонстрировала, что введение соединения 72 приводило к значимо меньшему повышению глюкозы (от 54845 +/- 4112 до 35942 +/- 3192; фиг. 8C).
Определения инсулина в плазме проводили в образцах, полученных в t=0 и t=2 часа, и они представлены на фиг. 9A. Инсулин при обработке соединением 72 был снижен в обеих временных точках t=0 и t=2 часа на 20% и 21%, соответственно (от 4,70 +/- 0,76 до 3,78 +/- 0,69 нг/мл и от 3,17 +/- 0,67 до 2,53 +/- 0,50 нг/мл, соответственно). HOMA-IR (показатель восстановления чувствительности к инсулину) был снижен на 33% с 139,91 +/- 26,57 до 93,69 +/- 23,60 единиц (фиг. 9B).
Уровни соединения 72 оценивали в образцах, полученных в конце исследования, и они представлены на фиг. 10 вместе со значениями EC50, определяемыми в анализе Per2, как описано в примере 3, с целями сравнения. Соединение 72 выявлено в плазме и в печени приблизительно через 8 часов после введения последней дозы (плазма: 0,53 +/- 0,03 мкМ; печень: 0,67 +/- 0,05 мкМ, представлено как среднее и S.E.M). В обоих случаях уровни соединений были немного выше, чем значение EC50 для Per2, определенное для соединения 72 (0,4 мкМ; в 1,3 раза и в 1,7 раза выше, чем значение EC50 в плазме и печени, соответственно).
Пример 8: Действие увеличивающихся доз соединения 72 в модели диабета на мышах
Действие соединения 72 оценивали по увеличению доз, вводимых в течение 7 суток, на метаболизме глюкозы и уровнях инсулина в модели диабета II типа на мышах db/db.
Самцов мышей db/db, гомозиготных по Leprdb (в возрасте 5 недель), получали в The Jackson Laboratory (Bar Harbor, Maine). Мышей в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к стандартному гранулированному корму для мышей и воде. Животные перед экспериментированием привыкали к таким условиям в течение 2 недель. Мышам дозировали носитель (10% коллифор, Sigma-Aldrich) или соединение 72 при 10, 50 или 100 мг/кг (в 10% коллифоре в воде) в объеме дозы 5 мл/кг, раз в сутки, посредством перорального принудительного кормления в ZT0 (7:00) в течение семи суток. Проводимые экспериментальные процедуры были такими же, как процедуры, подробно описанные в примере 11. Уровни соединения в плазма и ткани печени у обработанных соединением 72 животных измеряли с использованием LC/MS/MS и сравнивали со стандартными кривыми известных количеств соединения.
Введение соединения 72 мышам db/db в увеличивающихся дозах в течение 7 суток приводило к снижению уровней глюкозы в крови натощак по сравнению с группой контрольного носителя при 50 и 100 мг/кг, хотя это и не достигало статистической значимости (контрольный носитель: 491,0 +/- 51,30 мг/дл, 50 мг/кг: 402,8 +/- 25,25 мг/дл, 100 мг/кг: 420,7 +/- 26,44 мг/дл; фиг. 11A). Соединение 72, вводимое в дозе 10 мг/кг, не демонстрировало снижения уровней глюкозы в крови натощак (503,5 +/- 49,68 мг/дл). При измерениях в OGTT обработанные соединением 72 животные демонстрировали зависимое от дозы действие на повышение глюкозы у животных после глюкозной нагрузки (фиг. 11B). Площадь под кривой, рассчитанная на основе OGTT, продемонстрировала, что введение соединения 72 снижала AUC глюкозы зависимым от дозы образом, что было значимым при 100 мг/кг (носитель: 46088 +/- 3303, 10 мг/кг: 39771 +/- 4244, 50 мг/кг: 35527 +/- 3215, 100 мг/кг: 28499 +/- 3079; фиг. 11C).
Определения инсулина в плазме проводили в образцах, полученных в t=0 и t=2 часа, и они представлены на фиг.12A. При обработке соединением 72, дозируемым при 100 мг/кг, в момент времени t=0 инсулин был снижен (с 5,68 +/- 0,43 до 4,63 +/- 0,17 нг/мл (носитель и группа 100 мг/кг, соответственно)). HOMA-IR после введения соединения 72 снижался зависимым от дозы образом (носитель: 169,3 +/- 18,41, 10 мг/кг: 172,7 +/- 16,61, 50 мг/кг: 149,2 +/- 16,49, 100 мг/кг: 111,9 +/- 9,02 единиц; фиг. 12B). При 100 мг/кг действие соединения 72 было значимым (34% снижение по сравнению с группой контрольного носителя).
Уровни соединения 72 оценивали в образцах, полученных в конце исследования, и они представлены на фиг. 13, вместе со значением EC50 для Per2 (как описано в примере 3) с целями сравнения. Соединение 72 было выявлено в плазме и печени приблизительно через 8 часов после введения последней дозы с уровнями экспонирования, которые были увеличены относительно увеличения вводимой дозы (плазма, 10 мг/кг: 0,09 +/- 0,01 мкМ; 50 мг/кг: 0,57 +/- 0,03 мкМ; 100 мг/кг: 1,22 +/- 0,17 мкМ; печень, 10 мг/кг: 0,12 +/- 0,01 мкМ; 50 мг/кг: 0,78 +/- 0,06 мкМ; 100 мг/кг: 1,81 +/- 0,22 мкМ). В плазме и печени уровни экспонирования были в 1,4 раза и в 1,95 раза выше при 50 мг/кг и в 3 раза и в 4,5 раза выше при 100 мг/кг, чем значение EC50 для Per2 в плазме и печени, соответственно.
Пример 9: Действие увеличивающихся доз соединения 9 в модели диабета на мышах
Действие соединения 9 оценивали по увеличению доз, вводимых в течение 7 суток, на метаболизме глюкозы и уровнях инсулина в модели диабета II типа на мышах db/db.
Самцов мышей db/db, гомозиготных по Leprdb (в возрасте 5 недель), получали в The Jackson Laboratory (Bar Harbor, Maine). Мышей в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к стандартному гранулированному корму для мышей и воде. Животные перед экспериментированием привыкали к таким условиям в течение 2 недель. Мышам дозировали носитель (10% коллифор, Sigma-Aldrich) или соединение 9 при 30, 100 или 300 мг/кг или росиглитазон при 30 мг/кг (в 10% коллифоре в воде) в объеме дозы 5 мл/кг раз в сутки посредством перорального принудительного кормления в ZT0 (7:00) в течение семи суток. Росиглитазон представляет собой антидиабетическое терапевтическое средство, которое использовали в качестве положительного контроля. Проводимые экспериментальные способы были такими же как способы, подробно описанные в примере 11. Уровни соединения в плазме и ткани печени у обработанных соединением 9 животных измеряли с использованием LC/MS/MS и сравнивали со стандартными кривыми известных количеств соединения.
Введение соединения 9 мышам db/db в увеличивающихся дозах в течение 7 суток приводило к снижению уровней глюкозы в крови натощак при 100 мг/кг по сравнению с группой контрольного носителя (с 492,8 +/- 48,07 до 403,1 +/- 39,73 мг/дл; фиг. 14A), но абсолютного статистически достоверного действия не наблюдали. Соединение 9, вводимое в дозе 30 и 100 мг/кг, демонстрировало зависимое от дозы снижение уровней глюкозы при измерениях во время OGTT, без увеличения наблюдаемого действия при наибольшей тестируемой дозе 300 мг/кг (фиг. 14B). Площадь под кривой, рассчитанная на основе OGTT, продемонстрировала, что введение соединения 9 снижало AUC глюкозы зависимым от дозы образом, что было значимым при 100 и 300 мг/кг (носитель: 56046 +/- 3204, 30 мг/кг: 44442 +/- 3895, 100 мг/кг: 33643 +/- 4822, 300 мг/кг: 33650 +/- 4688; фиг. 8C). AUC глюкозы относительно группы контрольного носителя снижалась на 21%, 40% и 40% при 30, 100 и 300 мг/кг, соответственно. Росиглитазон, используемый для модели на животных в качестве положительного контроля, значимо снижал глюкозу крови натощак (с 492,8 +/- 48,07 до 280,4 +/- 13,66 мг/дл; фиг. 14A) и AUC глюкозы (с 56046 +/- 3204 до 11502 +/- 2118 единиц; фиг. 14C).
Определения инсулина в плазме проводили в образцах, полученных в t=0 и t=2 часа, и они представлены на фиг. 15A. Инсулин после обработки соединением 9 снижался в t=0 (носитель: 14,89 +/- 2,93, 30 мг/кг: 10,94 +/- 1,62, 100 мг/кг: 7,71 +/- 1,26, 300 мг/кг: 10,54 +/- 1,6 нг/мл) и в t=2 часа (носитель: 7,44 +/- 0,92, 30 мг/кг: 5,76 +/- 0,11, 100 мг/кг: 3,70 +/- 0,29, 300 мг/кг: 4,01 +/- 0,44 нг/мл). HOMA-IR после введения соединения 9 снижался зависимым от дозы образом, хотя наблюдали меньшее действие соединения на этот конечный показатель при 300 мг/кг (носитель: 438,8 +/- 87,88, 30 мг/кг: 289,9 +/- 24,40, 100 мг/кг: 175,3 +/- 27,52, 300 мг/кг: 301,4 +/- 52,66 единиц; фиг. 15B). При 100 мг/кг действие соединения 9 было значимым (60% снижения по сравнению с группой контрольного носителя). Росиглитазон снижал уровни инсулина в t=0 и t=2 часа (до 3,05 +/- 0,14 и 2,28 +/- 0,08 нг/мл, соответственно; фиг. 15A), а также значимо снижал HOMA-IR (до 50,58 +/- 3,52 единиц, фиг. 15B).
Уровни соединения 9 в тканях оценивали в образцах печени, получаемых в конце исследования, и они представлены на фиг. 16 вместе со значением EC50 для Per2 с целями сравнения. Соединение 9 выявлено в печени приблизительно через 8 часов после введения последней дозы с уровнями экспонирования, которые были увеличены относительно увеличения дозы, вводимой между дозами 30 мг/кг и 100 мг/кг. Уровни экспонирования при 300 мг/кг указывали на накопление лекарственного средства (увеличение в 7,1 раз а не в 3 раза, как и ожидалось). Уровни соединения в образцах печени животных, которым вводили 30, 100 или 300 мг/кг соединения 9, составляли 0,19 +/- 0,02 мкМ, 0,67 +/- 0,05 мкМ и 4,77 +/- 1,06 мкМ, соответственно. Уровни экспонирования в печени после введения 30 мг/кг соединение 9 были приблизительно в 1,6 раза ниже значения EC50 для Per2 (0,3 мкМ), тогда как при 100 мг/кг и 300 мг/кг уровни были выше в 2,2 раза и в 15,9 раза, соответственно.
Пример 10: Действие соединения 72 в модели индуцированного диетой ожирения на мышах
Действие соединения 72 исследовали в модели диабета II типа на мышах с индуцированным диетой ожирением (DIO).
Самцов мышей C57/Bl6J DIO получали в The Jackson Laboratory (Sacramento, CA). Мышей в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к питанию с высоким содержанием жиров (D12492 (60ккал% жира), Research Diets, Inc.) и воде. Животные перед экспериментированием привыкали к таким условиям в течение по меньшей мере 2 недель и их использовали в возрасте приблизительно 24 недели. Мышам дозировали носитель (10% коллифор, Sigma-Aldrich), соединение 72 (100 мг/кг в 10% коллифоре в воде) или росиглитазон (30 мг/кг в 10% коллифоре в воде) в объеме дозы 5 мл/кг раз в сутки посредством перорального принудительного кормления в ZT0 (7:00) в течение семи суток. Росиглитазон представляет собой антидиабетическое терапевтическое средство, которое использовали в качестве положительного контроля. Мышей взвешивали на сутки 0 и случайно распределяли по группам обработки так, чтобы каждая группа содержала сходные средние начальные массы. Вечером в 22:30 перед измерением конечных показателей мышей помещали в чистые клетки и обеспечивали свободный доступ к воде, но не к пище, в течение периода 12 часов перед измерением глюкозы крови натощак. На конечные сутки исследования, животным проводили дозирование как обычно, а затем проводили разрез хвоста за 2 часа до определения глюкозы крови натощак для обеспечения восстановления после любого стресса, который может вызывать эта процедура. Глюкозу крови натощак (FBG) у животных оценивали в 10:30 с использованием глюкометра AlphaTRAK (Abbott Laboratories, USA). После определения FBG у каждой мыши способом забора из хвоста собирали кровь в капиллярную трубку. Капиллярные трубки центрифугировали в устройстве для определения гематокрита (BD Triac 0200) и полученную плазму переносили в пробирки Eppendorff. Этот образец, помеченный t=0 часов, замораживали при -80 для обеспечения более позднего определения инсулина. В 11:30 каждому животному дозировали 1,5 г/кг глюкозы, затем измеряли глюкозу крови в t=15, 30, 60, 90 и 120 минут после глюкозной нагрузки. В конце OGTT собирали кровь для определения инсулина в t=2 часа, как описано выше. После последнего сбора крови животных умерщвляли и собирали ткани и кровь для других определений.
Значения глюкозы крови натощак и измерения глюкозы, проводимые при OGTT, усредняли и наносили на диаграмму (GraphPad Prism, GraphPad Software, LA Jolla, CA). Для каждого отдельного животного рассчитывали площадь под кривой (AUC). Уровни инсулина в плазме определяли с использованием ультрачувствительного ELISA инсулина (ALPCO, Salem, NH). HOMA-IR (модельную оценку гомеостаза-резистентность к инсулину) рассчитывали с использованием следующей формулы: (FPI (мкЕд/л) × FPG (ммоль/л))/22,5, где FPI и FPG означают инсулин в плазме натощак и глюкозу в плазме натощак, соответственно. Данные по инсулину также представляли в формате GraphPad Prism. Статистический анализ проводили с использованием одностороннего дисперсионного анализа с последующим соответствующим послеэкспериментальным тестом. Значимость допускали при p < 0,05. Данные представлены как среднее и S.E.M.
Введение соединения 72 (100 мг/кг, п/о) мышам C57/Bl6J DIO в течение 7 суток приводило к значимому снижению уровней глюкозы в крови натощак по сравнению с контрольным носителем (с 237,2 +/- 15,29 мг/дл до 177,1 +/- 8,28 мг/дл; фиг. 17A). При измерениях в OGTT, у обработанных соединением 72 животных наблюдали намного меньшие уровни, чем в группе контрольного носителя (фиг. 17B). AUC, рассчитанная на основе OGTT, продемонстрировала, что введение соединения 72 приводило к значимо меньшему повышению глюкозы (с 31511 +/- 1670 до 17055 +/- 769,1; фиг. 17C). Росиглитазон, используемый в качестве положительного контроля в модели на животных, снижал глюкозу крови натощак до 153,9 +/- 5,05 мг/дл и AUC глюкозы до 11500 +/- 1104 единиц.
Определения инсулина в плазме проводили в образцах, полученных в t=0 и t=2 часа, и они представлены на фиг. 18A. Инсулин после обработки соединением 72 был снижен в t=0 (носитель: 5,00 +/- 0,92, 100 мг/кг: 3,12 +/- 0,24, нг/мл) и t=2 часа (носитель: 4,82 +/- 0,60, 100 мг/кг: 2,88 +/- 0,21 нг/мл). HOMA-IR после введения соединения 72 был значимо снижен (носитель: 70,76 +/- 11,30, 100 мг/кг: 32,54 +/-3,37 единиц; фиг. 18B). Росиглитазон (30 мг/кг) снижал инсулин в t=0 и t=2 часа (до 2,70 +/-0,12 и 2,30 +/- 0,06 нг/мл, соответственно) и значимо снижал HOMA-IR (до 24,60 +/- 1,42 единиц).
Пример 11: Действие соединения 72 на развитие индуцированной кортизоном резистентности к инсулину у крыс
Повторное введение кортизона крысам в течение 6 суток индуцирует значимое снижение массы тела, которое ассоциировано со значительным повышением инсулина и глюкозы в плазме. Это действие опосредовано кортизолом, образуемым вследствие активности 11-βHSD1. Антагонисты рецепторов глюкокортикоидов, такие как мифепристон, улучшают действие кортизола на резистентность к инсулину. Целью этих экспериментов являлось определение действия соединения 72 на развитие индуцированной кортизоном резистентности к инсулину у крыс.
Животным дозировали кортизон (30 мг/кг п/к раз в сутки) в комбинации с тестируемыми соединениями в течение 6 суток, а затем умерщвляли через 27 часов после последней дозы кортизона. Также включали эталонный стандарт (мифепристон). Кортизон-21-ацетат (Sigma C-3130) получали в RenaSci и вводили в объеме дозы 5 мл/кг посредством подкожного маршрута в виде высокодисперсной суспензии в 1% метилцеллюлозе. Соединение 72 (50 мг/кг в 10% коллифоре в воде) дозировали раз в сутки в объеме дозы 5 мл/кг посредством перорального принудительного кормления. Мифепристон (Sigma M8046) получали в RenaSci.
Определения глюкозы и инсулин проводили в образцах плазмы, получаемых посредством отбора крови из хвостовой вены, проводимого после 12 часов голодания приблизительно через 27 час после последней дозы кортизона. Животных умерщвляли и получали последний (из сердца) образец крови, из которого получали плазму.
Тридцать четыре самца крыс Sprague Dawley (диапазон масс 200-250 г) получали в Charles River, Margate, Kent, UK. Крысы в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к стандартному гранулированному корму для крыс и водопроводной воде в любое время. Животные перед экспериментированием привыкали к таким условиям в течение 2 недель. Затем, у животных был базовый период в течение 3 суток, в течение которого им раз в сутки дозировали носитель в t=0 час (07:00). Выявлено, что эта процедура снижает частоту связанных со стрессом эффектов в исследовании. Все лекарственные средства вводили в течение 6 суток, как представлено в таблице 2 ниже. Массу тела регистрировали непосредственно перед дозированием, начинавшимся в 07:00 (t=0 часов). Кортизон вводили посредством подкожного маршрута (п/к), тогда как соединение 72 и мифепристон вводили перорально посредством принудительного кормления непосредственно после введения кортизона в t=0 часов.
Таблица 2
На сутки 6 дозирования крысы голодали в течение 12 часов, начиная с 22:30 (рассчитано в соответствии с окончанием на сутки 7). На сутки 7 крысам вводили носитель, но не кортизон (п/к) с последующим пероральным введением носителя/соединение 72/мифепристона как обычно в 07:00. В 10:30 на сутки 7, через 27 часов после последней дозы кортизона, из боковой хвостовой вены отбирали образцы крови (300 мкл) в пробирки, содержащие ЭДТА (Sarstedt 16,444). Кровь центрифугировали и полученные аликвоты плазмы хранили при -75°C. Животных подвергали эвтаназии посредством удушения CO2 с последующим смещением шейных позвонков. Собирали последний образец крови (приблизительно 10 мл) посредством сердечной пункции в пробирки, содержащие ЭДТА (Sarstedt 5 мл 32.332), а затем центрифугировали и плазму хранили при -75°C. Плазму хвостовой вены анализировали на глюкозу (n=2) с использованием коммерческого клинического реагента (реагент для глюкозы Thermoelectron Infinity (TR15421) и на инсулин (n=1) с использованием ультрачувствительного ELISA инсулина крыс Mercodia (10-1251-10).
Глюкозу и инсулин плазмы анализировали посредством устойчивой регрессии или общей линейной модели с обработкой в качестве независимой переменной и порядком забора крови и исходной массой тела в качестве ковариант. Если было необходимо использовали логарифмическую трансформацию. Для определения значимых отличий от группы носителя и от группы кортизона использовали соответствующие критерии множественного сравнения (двухсторонние). Статистически значимым считали значение p<0,05.
Введение крысам соединения 72 значимо снижало возрастание глюкозы и инсулина плазмы, вызываемое введением кортизона. Уровни глюкозы в плазме после обработки кортизоном возрастали с 6,28 +/- 0,30 мМ до 10,17 +/- 0,51 мМ, что соединение 72 (50 мг/кг) значимо уменьшало до 8,55 +/- 0,3 мМ (p < 0,01; среднее и S.E.M). Уровни инсулина в плазме после обработки кортизоном возрастали с 0,70 +/- 0,11нг/мл до 8,19 +/- 0,91нг/мл, что соединение 72 (50 мг/кг) снижало до 5,24 +/- 1,11 нг/мл (p < 0,05; данные представлены как среднее и S.E.M; фиг. 19). Мифепристон, используемый в качестве положительного контроля в модели на животных, значимо снижал глюкозу плазмы и инсулин плазмы до 7,43 +/- 0,27 нг/мл и 3,62 +/- 0,29 нг/мл, соответственно.
Значения HOMA-IR рассчитывали, как описано для соединения 9, и данные представлены на фиг. 20. Обработка кортизоном увеличивала HOMA-IR до 95,57 +/- 11,4 единиц по сравнению с носителем: группа контрольного носителя (5,27 +/- 1,04 единиц). Введение соединения 72 (50 мг/кг) и мифепристона значимо снижало значение HOMA-IR у резистентных к инсулину крыс до 56,94 +/- 11,18 единиц и 29,99 +/- 2,54 единиц, соответственно.
Пример 12: Фармакокинетический (PK) анализ соединения 9 и соединения 72
Для эксперимента использовали самцов мышей ICR (с массой 30-40 г, Charles River Laboratories) с n=3 мышами в каждой экспериментальной группе (всего 27 мышей в исследовании). Мышам дозировали модулирующие Cry соединение 9 или соединение 72 (50 мг/кг, п/о; объем дозы 5 мл/кг, в 10% коллифоре). В указанные далее моменты времени после введения получали кровь и ткань печени: 15, 30, 60, 90 минут, 3, 6, 12 и 24 часов. Также образцы получали у контрольной группы животных (T0). Животных подвергали эвтаназии с использованием CO2 и с использованием сердечной пункции собирали кровь из сердца, переносили в пробирку с ЭДТА, а затем центрифугировали при 5400 об./мин. в течение 5 минут при 4°C. Полученную плазму замораживали с использованием сухого льда, а затем хранили при -80°C до готовности к анализу. У каждого животного получали ткань печени, 0,5 г помещали в пробирку Eppendorff, замораживали и подвергали фармакокинетическим измерениям. Плазму и ткань печени каждого животного отправляли в CRO для определения уровней соединений с использованием LC/MS/MS и сравнения со стандартными кривыми известных количеств соединения в плазме и печени. Исходные данные для установления параметров PK анализировали с использованием WinNonLin (Cмакс, Tмакс, t1/2 выведения, MRT (средняя продолжительность обработки), AUC (площадь под кривой) -(0- последнее и экстраполированные %).
Для эксперимента использовали самцов крыс SD (с массой 250-300 г, Charles River Laboratories) с n =4 крысами в каждой экспериментальной группе. Крысам дозировали соединение 72 (50 мг/кг, п/о; объем дозы 5 мл/кг, в 10% коллифоре). Собирали кровь в указанные далее моменты времени после введения: 15, 30, 60, 90 минут, 3, 6, 12 и 24 часов. Также получали образец перед дозированием. Технический персонал Charles River канюлировал животных до приведения в спокойное состояние. Цельную кровь (0,3 мл) собирали из канюли в правой общей яремной вене в каждую из временных точек. Цельную кровь переносили в пробирку с ЭДТА, а затем центрифугировали при 5400 об./мин. в течение 5 минут при 4°C. Полученную плазму замораживали с использованием сухого льда, а затем хранили при -80°C до готовности к анализу. После каждого забора крови для восполнения жидкости вводили 0,9% хлорида натрия (0,3 мл). После временной точки 12 часов в качестве останавливающего раствора использовали 0,1 мл гепарина натрия (500 МЕ/мл). Образцы анализировали, как описано выше. Результаты анализов обобщены в таблицах 3 и 4.
Таблица 3
PK параметры соединения 9 и соединения 72
*Означает данные после 4 экспериментов, приведенные в виде среднего и S.E.M.
Таблица 4
Данные для экспонирования несвязанного
*Означает данные после 4 экспериментов, приведенные в виде среднего и S.E.M.
Пример 13: Действие увеличивающихся доз соединения 72 в модели на мышах с индуцированным диетой ожирением
Действие соединения 72 оценивали по увеличению доз в модели диабета II типа на мышах с индуцированным диетой ожирением (DIO).
Самцов мышей C57/Bl6J DIO получали в The Jackson Laboratory (Sacramento, CA). Мышей в группах содержали при нормальном цикле чередования света/темноты (включенный свет: 07:00-19:00 часов) со свободным доступом к питанию с высоким содержанием жиров (D12492 (60ккал% жира), Research Diets, Inc.) и воде. Животные перед экспериментированием привыкали к таким условиям в течение по меньшей мере 2 недель и их использовали в возрасте приблизительно 26 недель. Мышам дозировали носитель (10% коллифор, Sigma-Aldrich), соединение 72 (10, 30 или 100 мг/кг в 10% коллифоре в воде) или росиглитазон (30 мг/кг в 10% коллифоре в воде) в объеме дозы 5 мл/кг раз в сутки посредством перорального принудительного кормления в ZT0 (7:00) в течение семи суток. Проводимые экспериментальные способы были такими же, как способы, подробно описанные в примере 10.
Введение соединения 72 мышам C57/Bl6J DIO в увеличивающихся дозах в течение 7 суток приводило к снижению уровней глюкозы в крови натощак по сравнению с контрольным носителем, что достигало значимости при 100 мг/кг (контрольный носитель: 226,9 +/- 13,11 мг/дл, 10 мг/кг: 206,8 +/- 8,36 мг/дл, 30 мг/кг: 197,5 +/- 12,06 мг/дл, 100 мг/кг: 176,3 +/- 7,83 мг/дл, фиг. 22A. При измерениях в OGTT, обработанные соединением 72 животные демонстрировали меньшее повышение глюкозы после глюкозной нагрузки (фиг. 22B. Площадь под кривой, рассчитанная на основе OGTT, продемонстрировала, что введение соединения 72 снижало AUC глюкозы, демонстрируя значимость при 30 и 100 мг/кг (носитель: 26090 +/- 1917, 10 мг/кг: 22563 +/- 1224, 30 мг/кг: 19033 +/- 1934, 100 мг/кг: 19502 +/- 2404 единиц; фиг. 22C). Росиглитазон, используемый в качестве положительного контроля в модели на животных, значимо снижал глюкозу крови натощак (с 226,9 +/- 13,11 до 161,1 +/- 8,06 мг/дл; фиг. 22A и AUC глюкозы (с 26090 +/- 1917 до 9858 +/- 1281 единиц; фиг. 22C).
| название | год | авторы | номер документа |
|---|---|---|---|
| КАРБАЗОЛСОДЕРЖАЩИЕ СУЛЬФОНАМИДЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ КРИПТОХРОМА | 2013 |
|
RU2654484C1 |
| НОВЫЕ СОЕДИНЕНИЯ, ИХ ИЗОМЕР ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ В КАЧЕСТВЕ АНТАГОНИСТА ВАНИЛОИДНОГО РЕЦЕПТОРА И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2007 |
|
RU2448108C2 |
| ФЕНИЛКАРБАМАТЫ И ИХ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ ФЕРМЕНТА ГИДРОЛАЗЫ АМИДОВ ЖИРНЫХ КИСЛОТ (FAAH) И МОДУЛЯТОРОВ D3 ДОПАМИНОВОГО РЕЦЕПТОРА (D3DR) | 2014 |
|
RU2693457C2 |
| ЗАМЕЩЕННЫЕ ХРОМАНЫ | 2015 |
|
RU2718060C2 |
| 4-АМИНО-6-(4-ЗАМЕЩЕННЫЕ-ФЕНИЛ)-ПИКОЛИНАТЫ И 6-АМИНО-2-(4-ЗАМЕЩЕННЫЕ-ФЕНИЛ)-ПИРИМИДИН-4-КАРБОКСИЛАТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2014 |
|
RU2771326C2 |
| 4-АМИНО-6-(4-ЗАМЕЩЕННЫЕ-ФЕНИЛ)-ПИКОЛИНАТЫ И 6-АМИНО-2-(4-ЗАМЕЩЕННЫЕ-ФЕНИЛ)-ПИРИМИДИН-4-КАРБОКСИЛАТЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2014 |
|
RU2652132C2 |
| ДИПИКОЛИЛАМИННЫЕ ПРОИЗВОДНЫЕ И ИХ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2015 |
|
RU2703454C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С NTRK | 2016 |
|
RU2744974C2 |
| ИНДОЛОПИРРОЛОКАРБАЗОЛЬНЫЕ ПРОИЗВОДНЫЕ САХАРОВ, СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ РОСТА ОПУХОЛЕЙ | 1997 |
|
RU2167880C2 |
| ЦИКЛОАЛКАНОВОЕ ПРОИЗВОДНОЕ | 2013 |
|
RU2635354C2 |
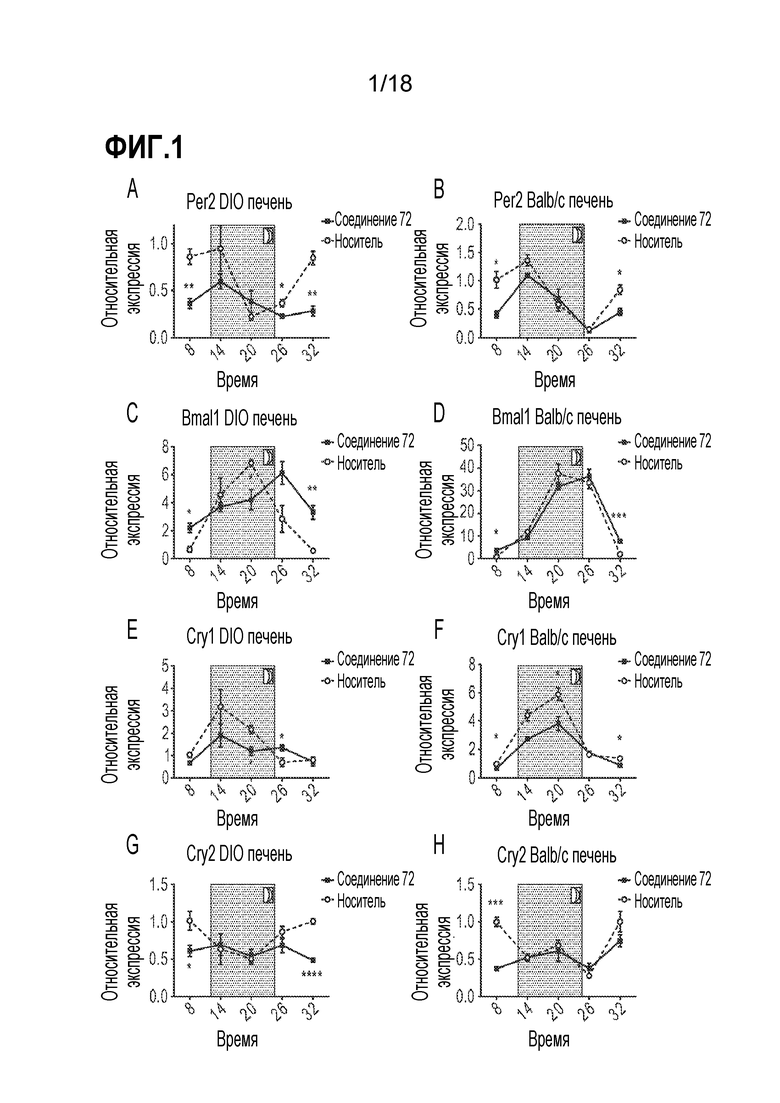
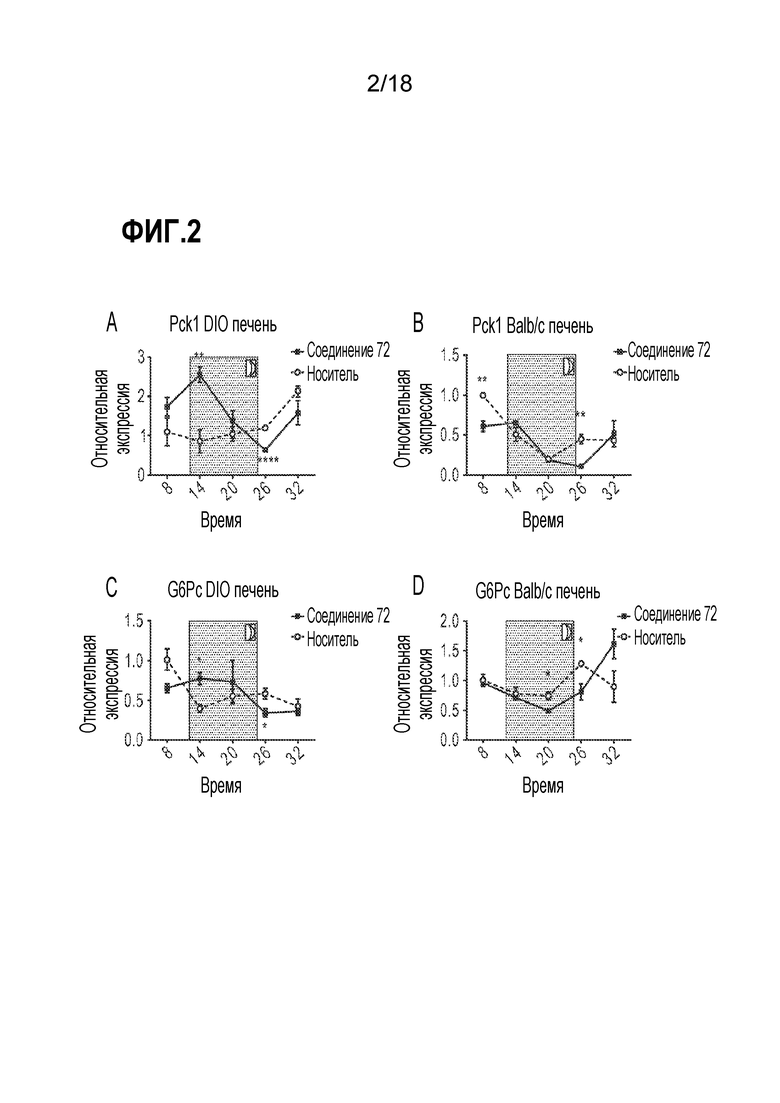
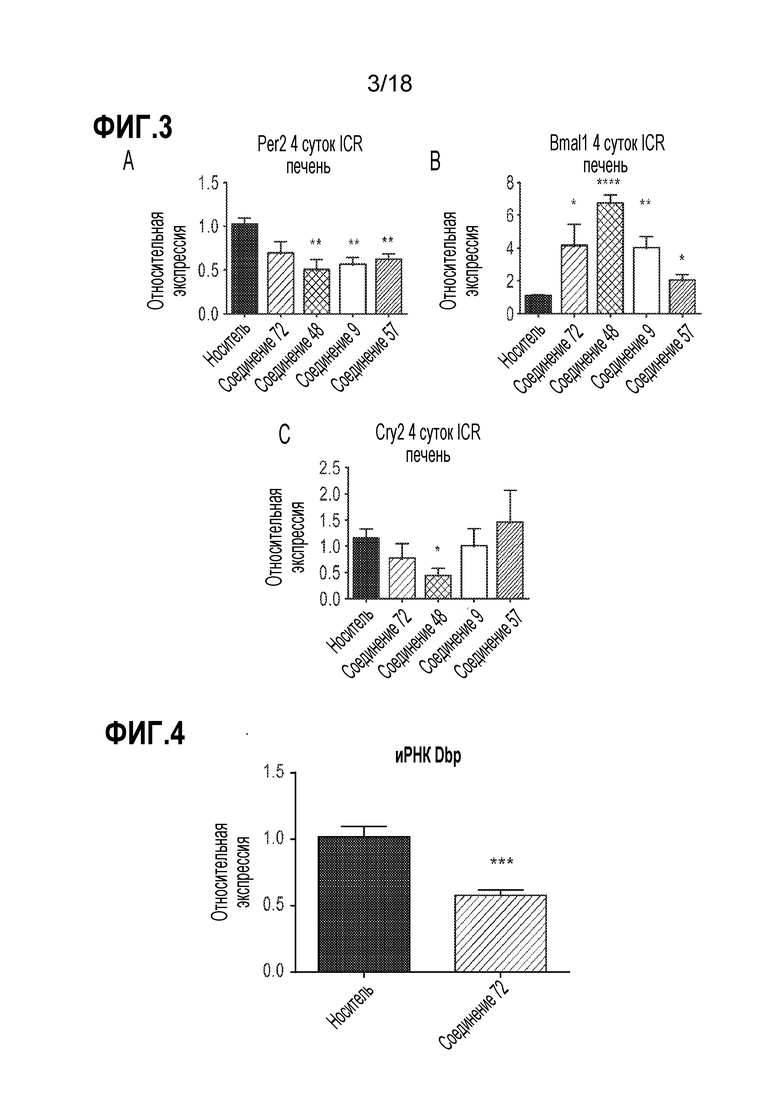
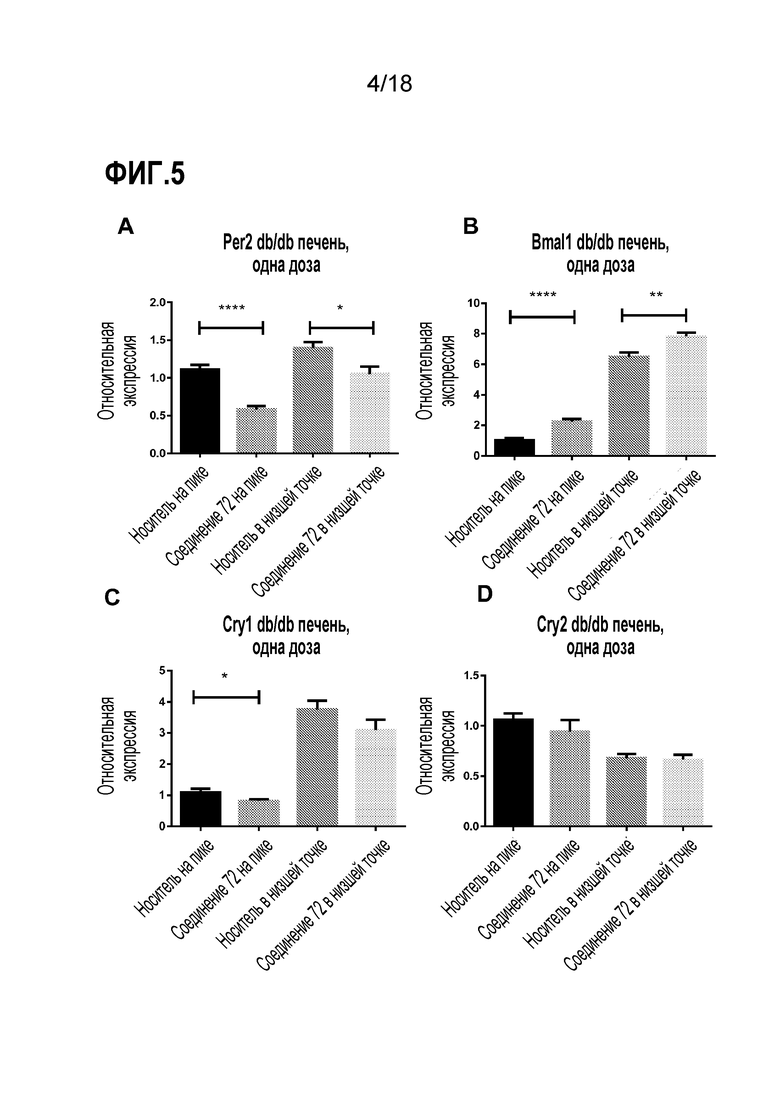
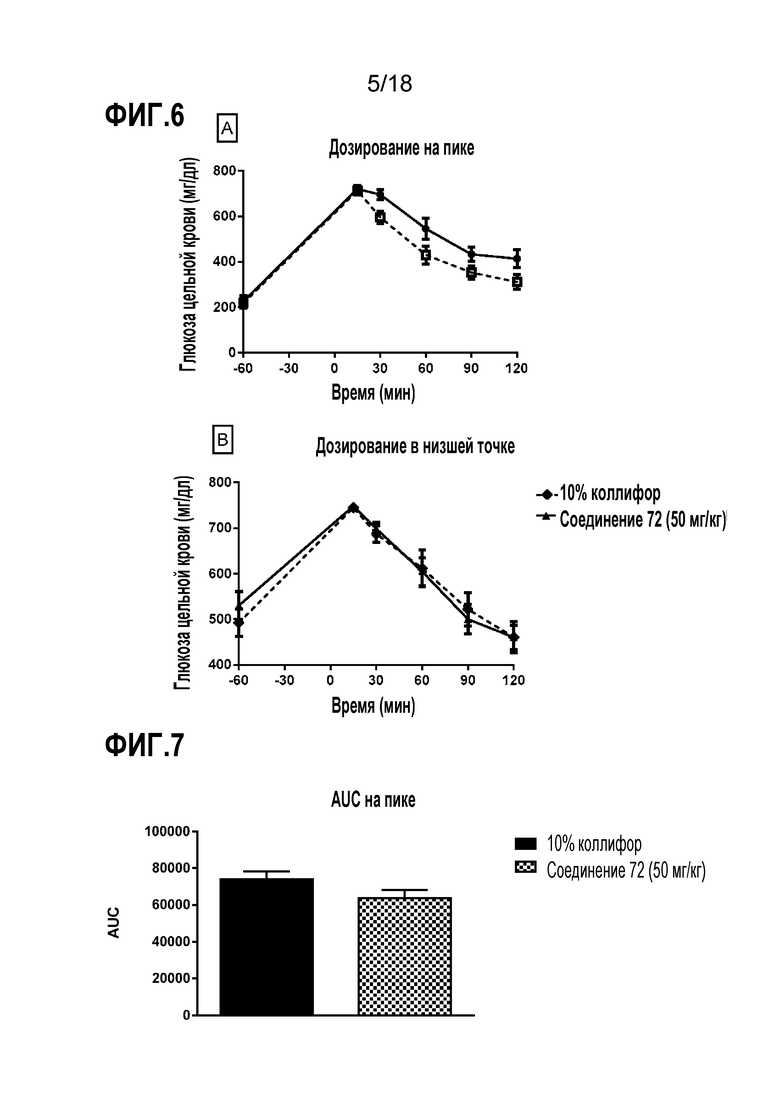
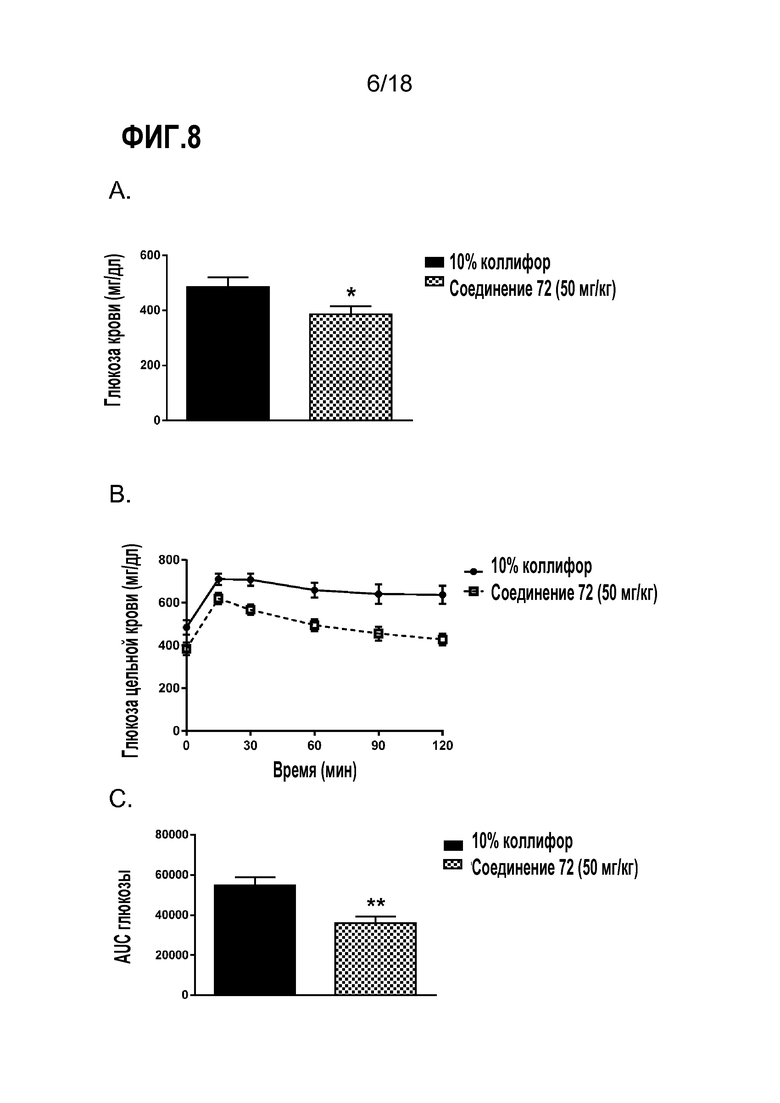
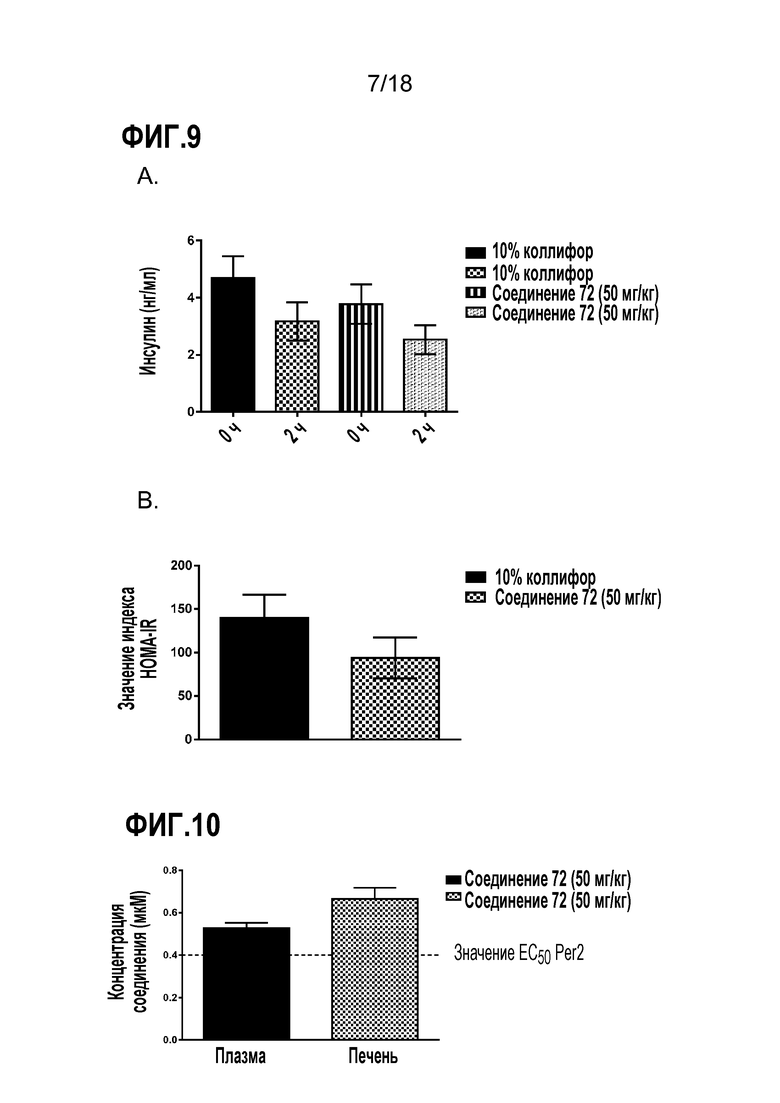
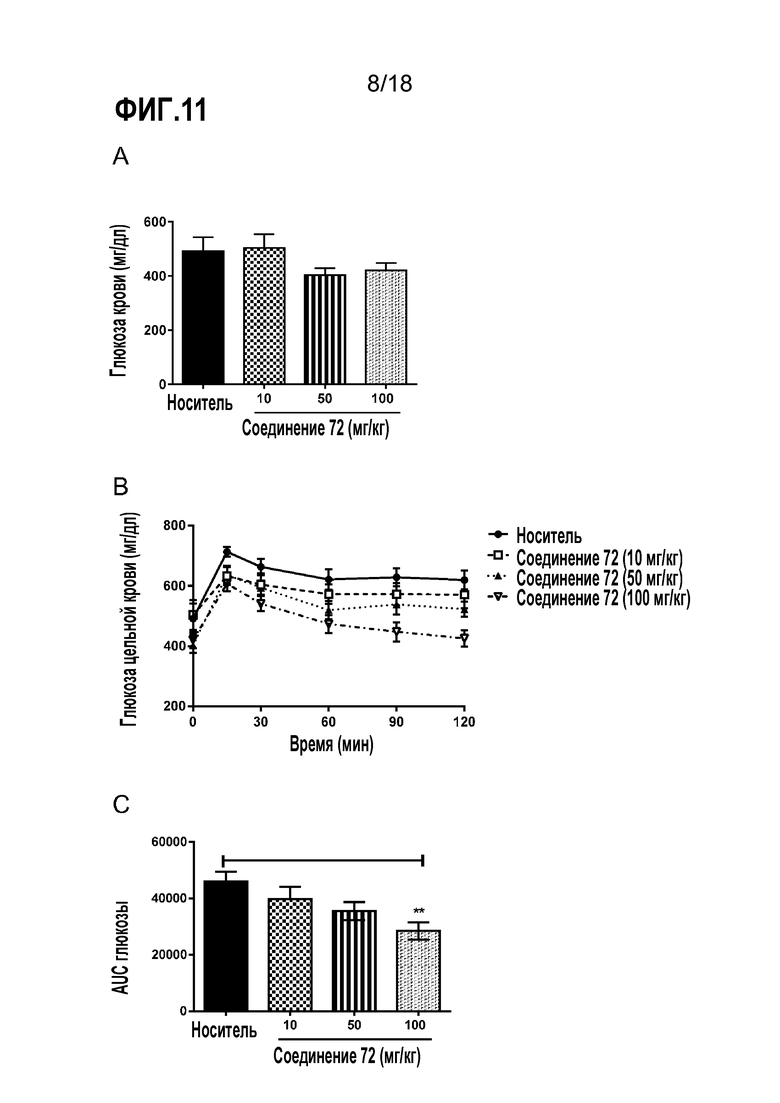
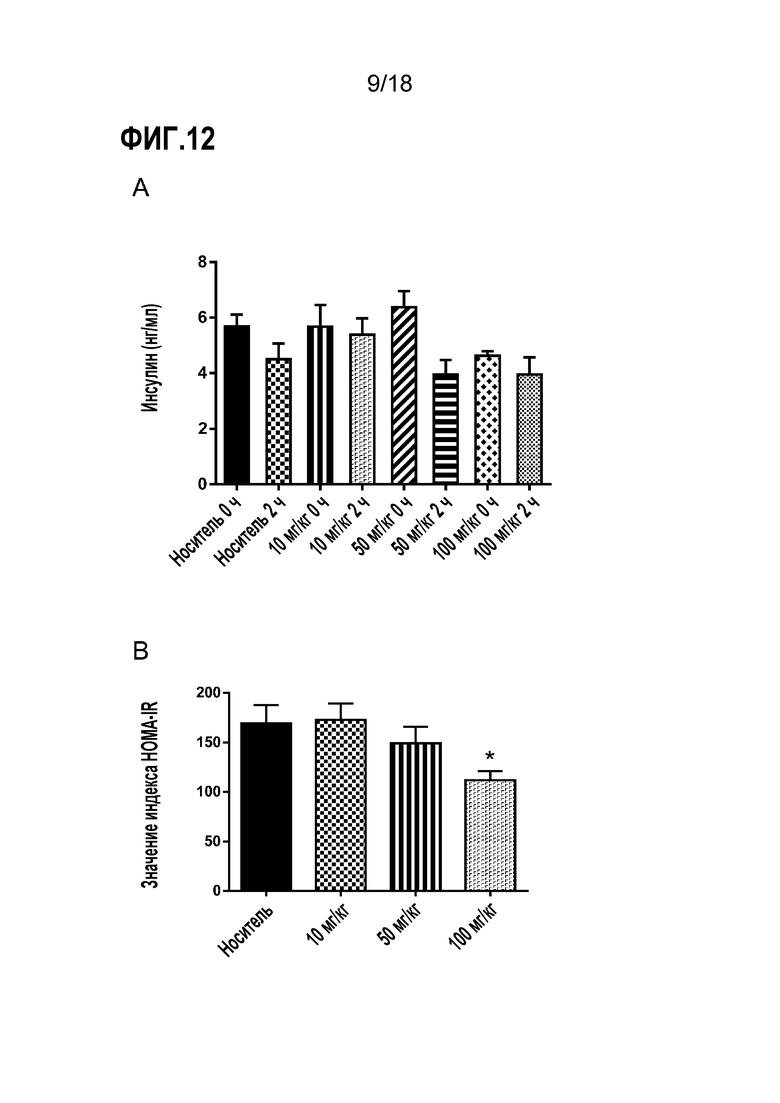
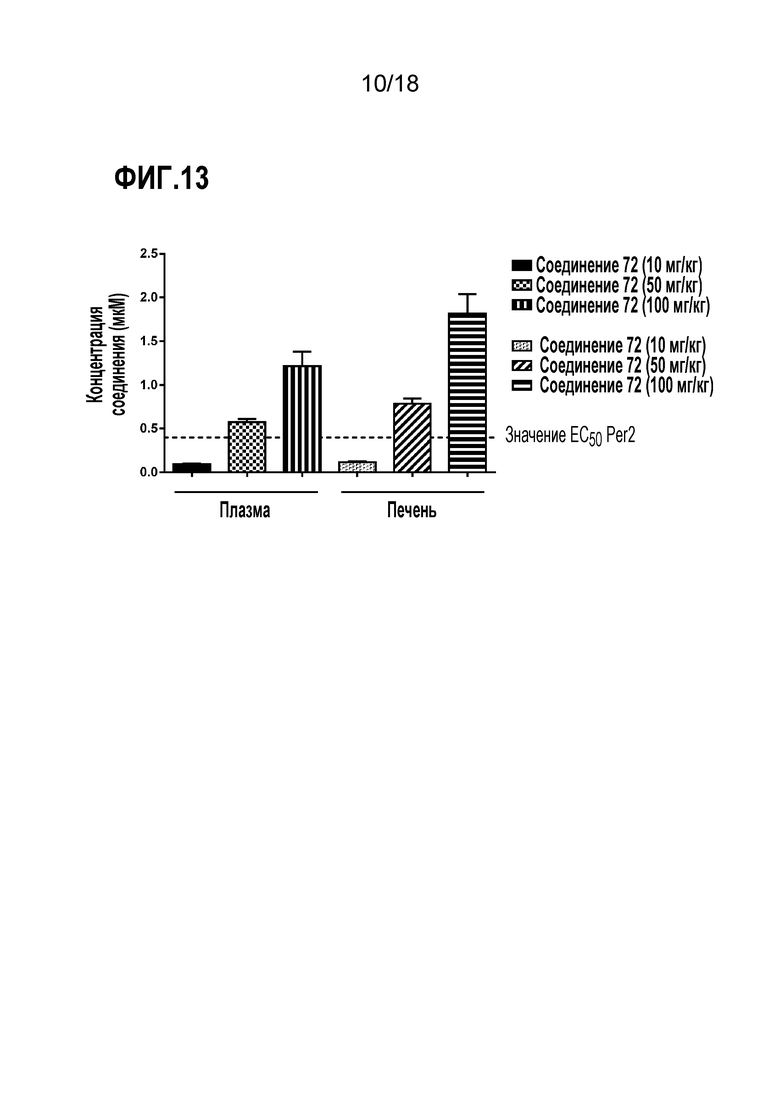
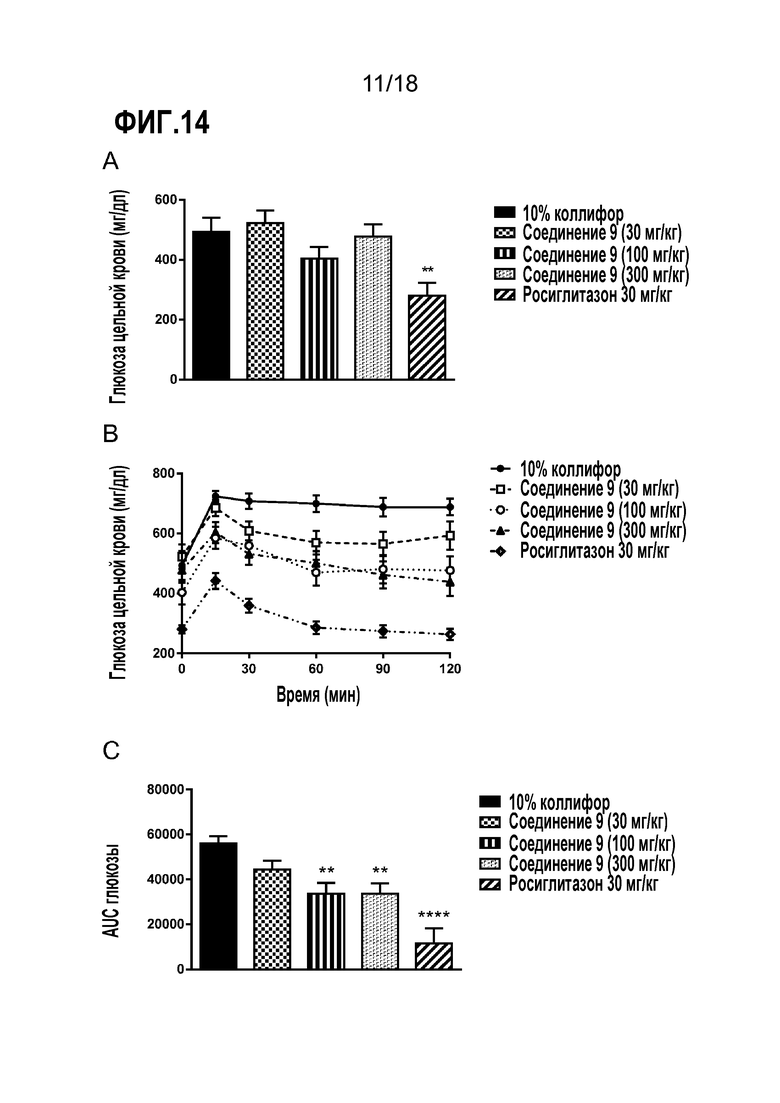
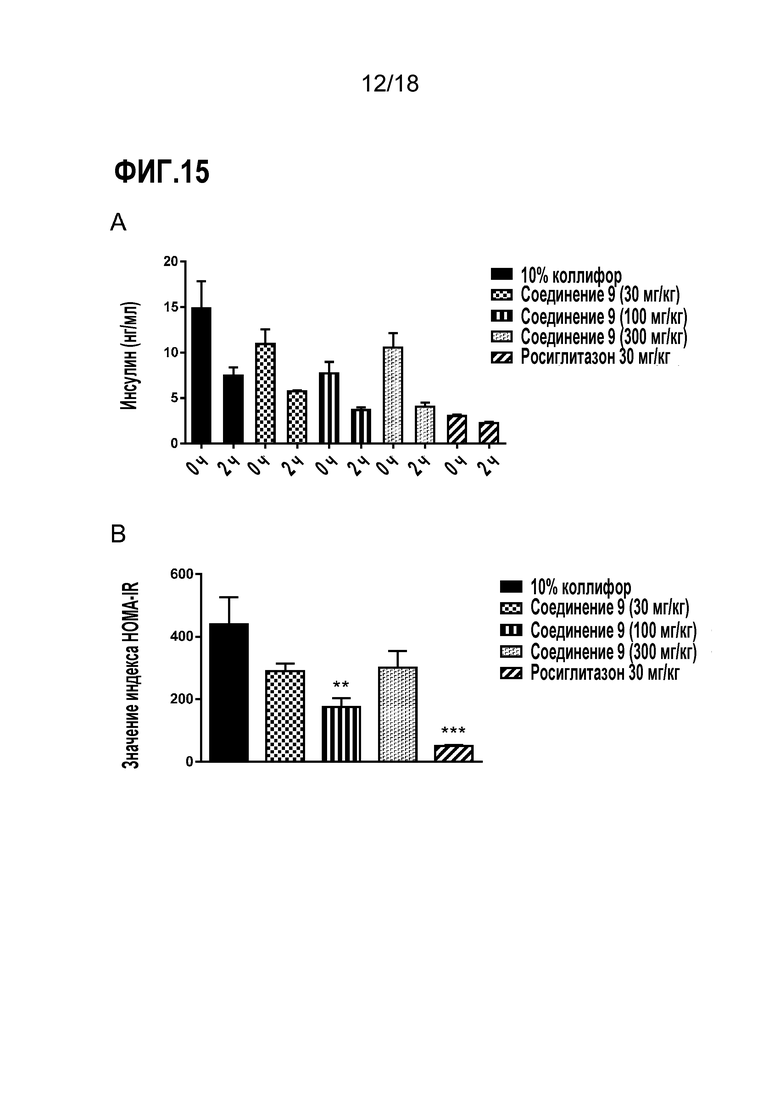
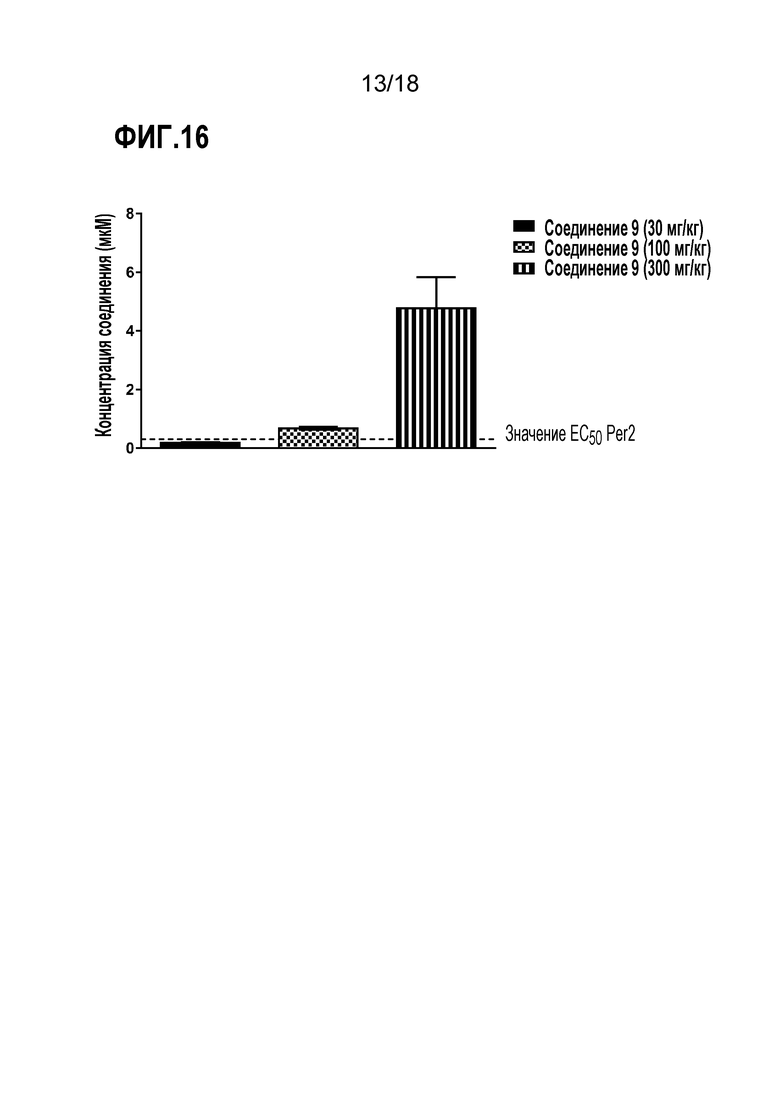
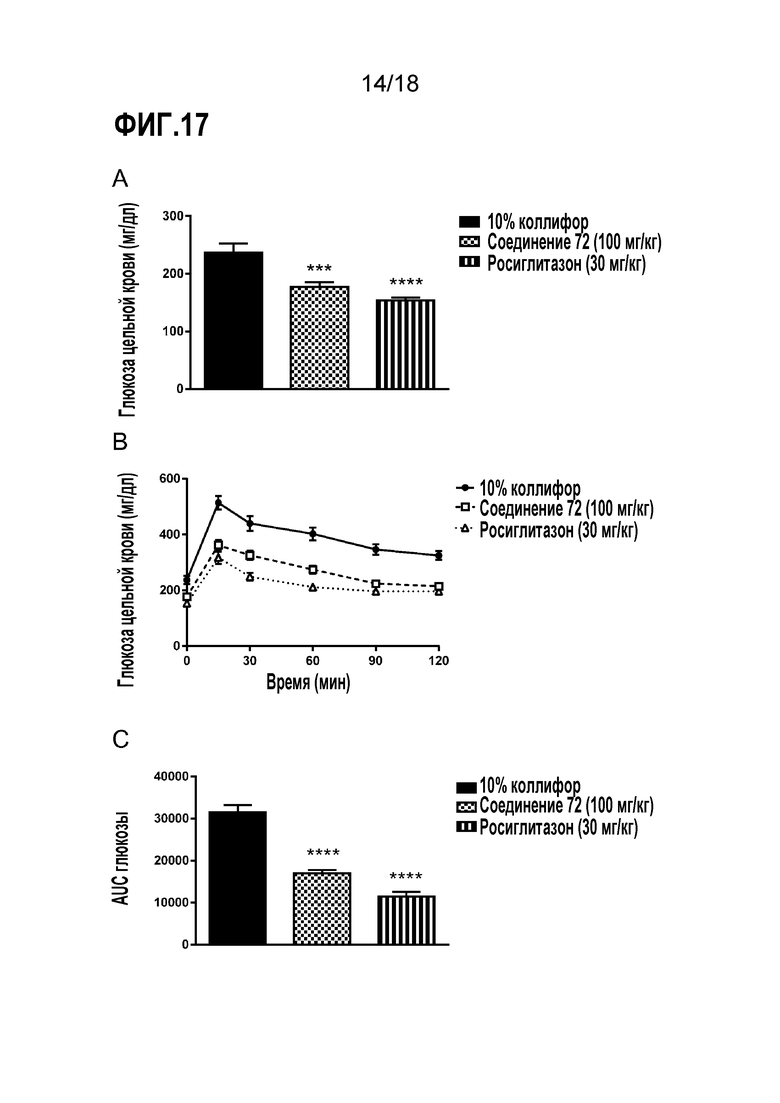
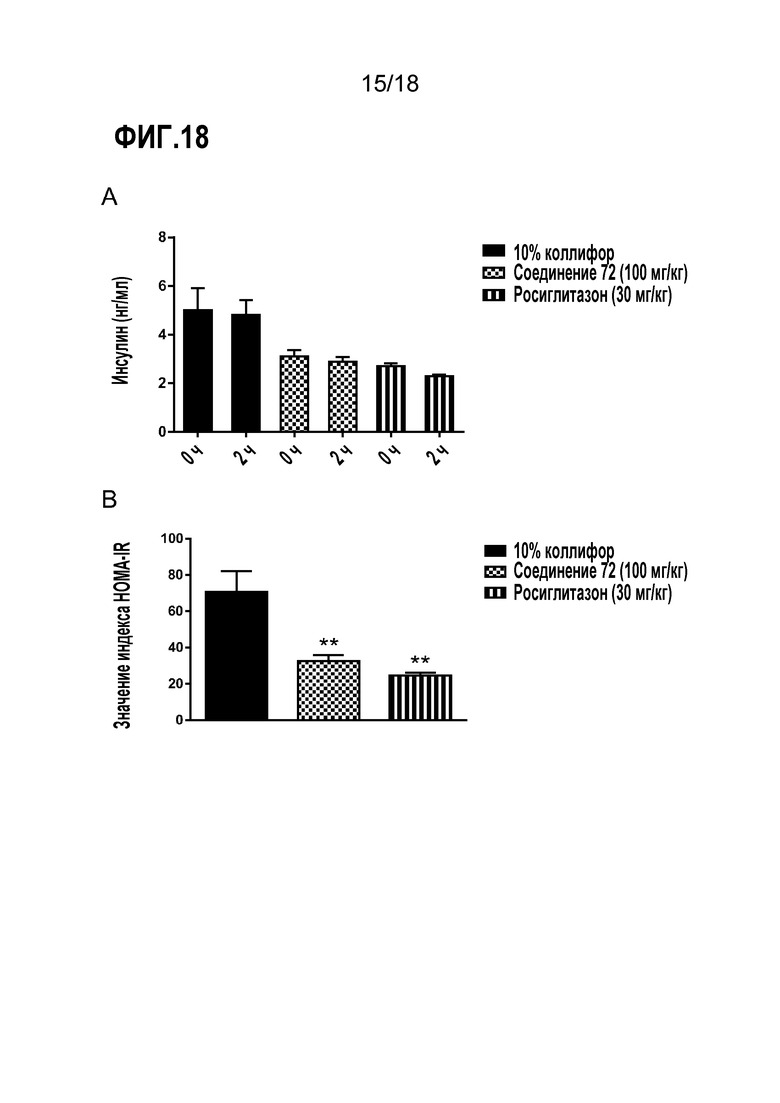
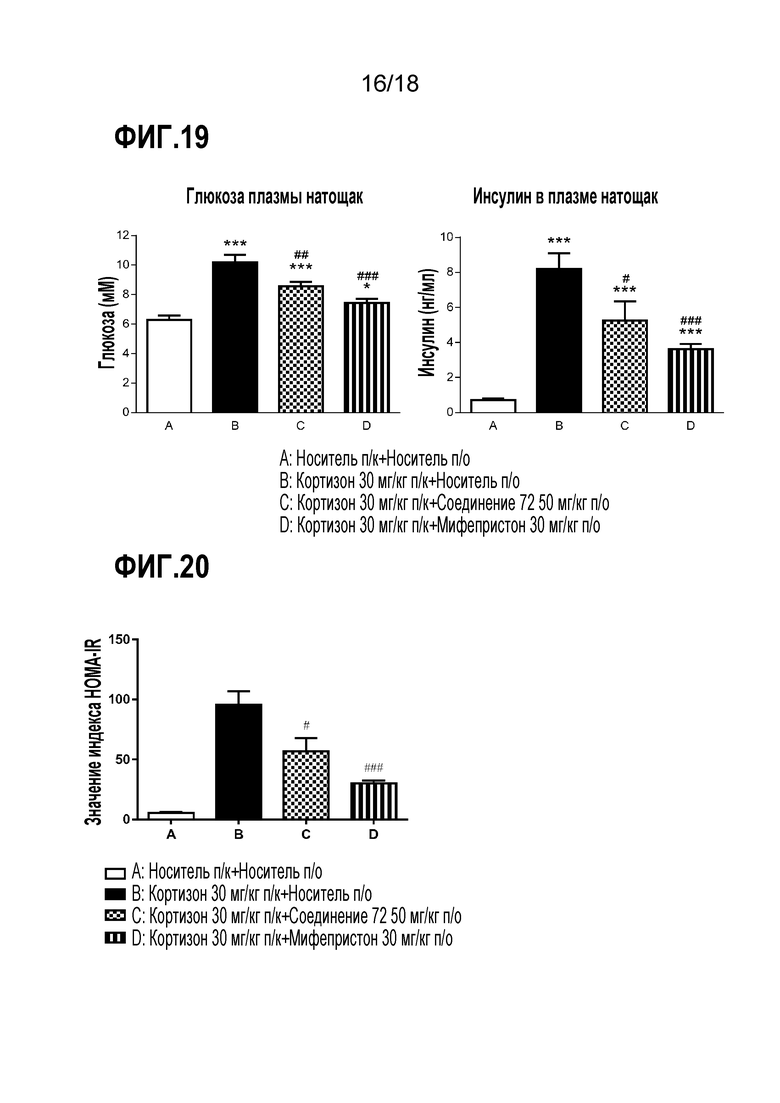
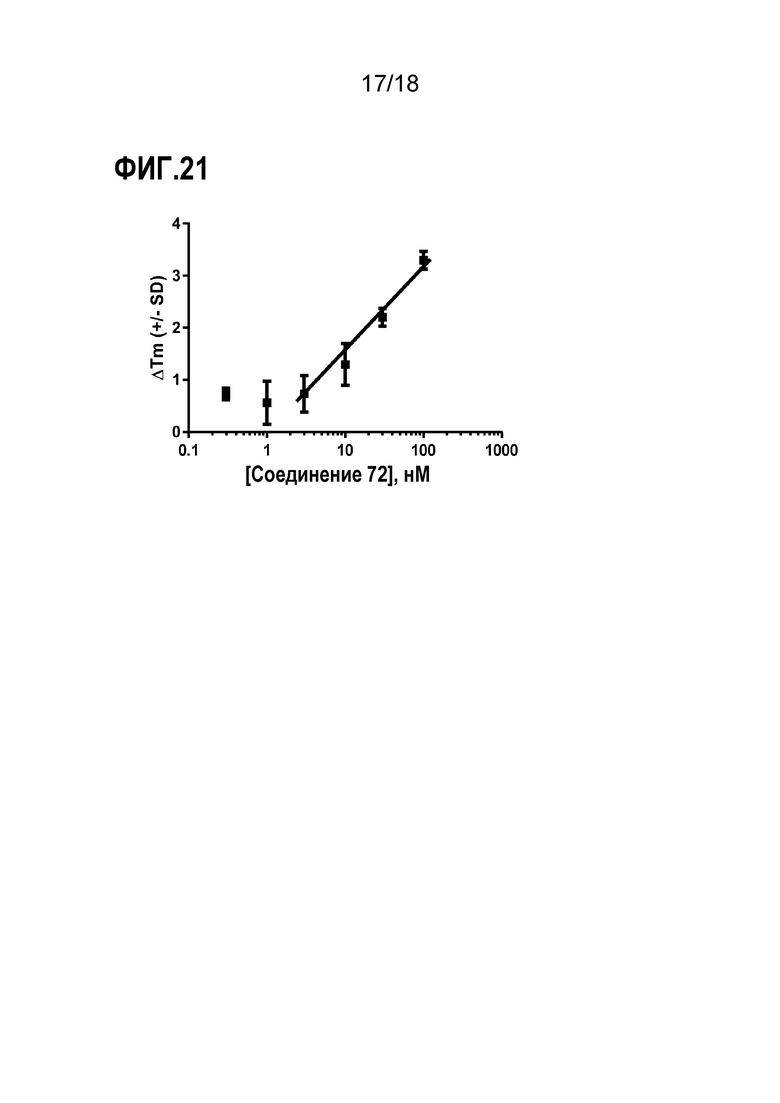
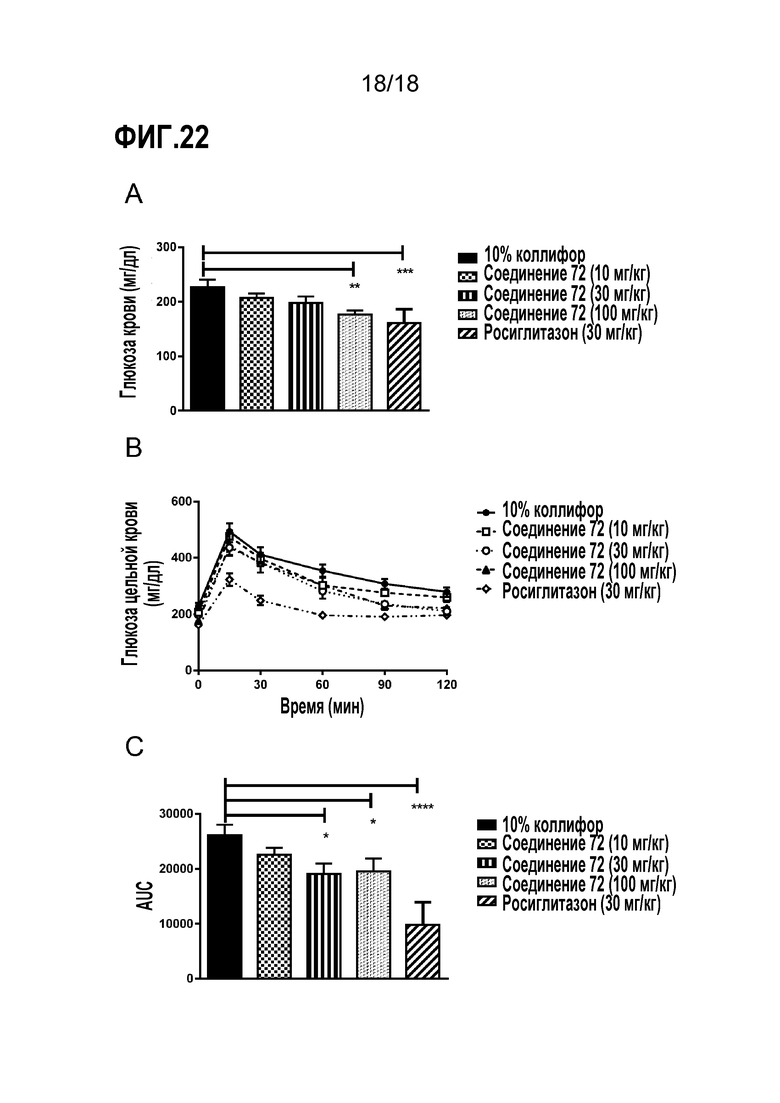
Изобретение относится к соединению формулы I
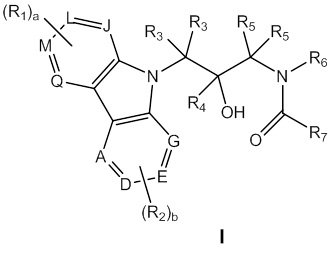
или его фармацевтически приемлемой соли. В формуле I: каждый из A, D, E, G, J, L, M и Q представляет атом углерода; каждый из R1 и R2 независимо выбран из водорода и галогена; каждый из R3 и R5 представляет собой водород; R4 выбирают из водорода и (C1-C6)алкила; R6 и R7 связаны друг с другом в виде кольца пирролидинона, кольца имидазолидинона, 7-членного моно- или бициклического кольца или 10-членного моно- или бициклического кольца, необязательно замещенного одним или более галогеном, (C1-C6)алкилом, (C1-C6)алкокси, (C3-C10)циклоалкилом или (C6-C10)арилом. Любой из атомов углерода (C1-C6)алкила, (C1-C6)алкокси, (3-10)-членного циклоалкила, (C6-C10)арила, кольца пирролидинона, кольца имидазолидинона, 7-членного моно- или бициклического кольца или 10-членного моно- или бициклического кольца независимо необязательно замещен 1-3 заместителями R14, где каждый R14 независимо выбран из галогена, (C1-C6)алкокси, (C1-C6)алкила, -(CR11R12)e(3-10)-членного циклоалкила и -(CR11R12)e(C6-C10)арила. Любой из атомов азота кольца пирролидинона, кольца имидазолидинона, 7-членного моно- или бициклического кольца или 10-членного моно- или бициклического кольца независимо необязательно замещен (C1-C6)алкилом, -(CR11R12)e(3-10)-членным циклоалкилом и -(CR11R12)e(C6-C10)арилом. R11 и R12 независимо представляют собой водород или (C1-C6)алкил, a и b независимо представляют собой 1, 2, 3 или 4 и e представляет собой 0, 1, 2, 3, 4 или 5. Также предложены варианты соединения формулы I, фармацевтическая композиция, способы лечения и способы смягчения опосредуемого Cry заболевания или нарушения. Предложенные соединения способны модулировать криптохомы (Cry) и могут быть использованы для лечения связанных с Cry заболеваний или нарушений. 9 н. и 37 з.п. ф-лы, 22 ил., 4 табл., 13 пр.
1. Соединение формулы I
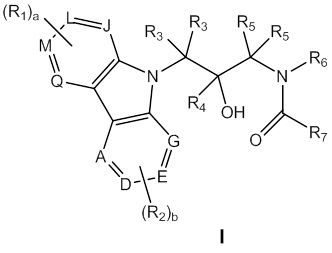
или его фармацевтически приемлемая соль, где
каждый из A, D, E, G, J, L, M и Q представляет атом углерода;
каждый из R1 и R2 независимо выбран из водорода и галогена;
каждый из R3 и R5 представляет собой водород;
R4 выбирают из водорода и (C1-C6)алкила;
где R6 и R7 связаны друг с другом в виде кольца пирролидинона, кольца имидазолидинона, 7-членного моно- или бициклического кольца или 10-членного моно- или бициклического кольца, необязательно замещенного одним или более галогеном, (C1-C6)алкилом, (C1-C6)алкокси, (C3-C10)циклоалкилом или (C6-C10)арилом;
любой из атомов углерода (C1-C6)алкила, (C1-C6)алкокси, (3-10)-членного циклоалкила, (C6-C10)арила, кольца пирролидинона, кольца имидазолидинона, 7-членного моно- или бициклического кольца или 10-членного моно- или бициклического кольца указанных выше R4, R6 и R7 независимо необязательно замещен 1-3 заместителями R14, где каждый R14 независимо выбран из галогена, (C1-C6)алкокси, (C1-C6)алкила, -(CR11R12)e(3-10)-членного циклоалкила и -(CR11R12)e(C6-C10)арила;
любой из атомов азота кольца пирролидинона, кольца имидазолидинона, 7-членного моно- или бициклического кольца или 10-членного моно- или бициклического кольца указанных выше R6 и R7 независимо необязательно замещен (C1-C6)алкилом, -(CR11R12)e(3-10)-членным циклоалкилом и -(CR11R12)e(C6-C10)арилом;
каждый из R11 и R12 независимо представляет собой водород или (C1-C6)алкил;
каждый из a и b независимо представляет собой 1, 2, 3 или 4; и
каждый из e представляет собой 0, 1, 2, 3, 4 или 5.
2. Соединение по п. 1, где R4 представляет собой водород или метил и R6 и R7 связаны друг с другом в виде кольца пирролидинона.
3. Соединение по п. 1, где R4 представляет собой водород или метил и R6 и R7 связаны друг с другом в виде кольца имидазолидинона.
4. Соединение по п. 1, где R4 представляет собой водород или метил и R6 и R7 связаны друг с другом в виде 7-членного моно- или бициклического кольца.
5. Соединение по п. 1, где R4 представляет собой водород или метил и R6 и R7 связаны друг с другом в виде 10-членного моно- или бициклического кольца.
6. Соединение по п. 1, выбранное из группы, состоящей из:
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
2-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
(1R,4S)-2-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(R)-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
(S)-1-((S)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)пирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,3-диметилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-этилпирролидин-2-она;
3-циклопентил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-изопропилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-метилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4,4-диметилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-этилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-5-этилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-5-метилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-изопропилпирролидин-2-она;
4-циклопропил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-метилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-4-метилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-этилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-4-этилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4,5-диметилпирролидин-2-она;
3-циклобутил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фенилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фенилпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,3-дифторпирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3,3-дифторпирролидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-циклопропилпирролидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)пирролидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)пирролидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-этилимидазолидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она;
1-циклогексил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фенилимидазолидин-2-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-изопропилимидазолидин-2-она;
1-циклопентил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
1-циклопропил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
1-циклобутил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-циклобутилимидазолидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-циклопропилимидазолидин-2-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-изопропилимидазолидин-2-она;
3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3,4-дигидрохиназолин-2(1H)-она;
3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,4-дигидрохиназолин-2(1H)-она;
(1S,4R)-2-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(1S,4R)-2-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(1R,4S)-2-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(1R,4S)-2-((S)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-она;
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпирролидин-2-она;
(S)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпирролидин-2-она;
(S)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпирролидин-2-она;
(R)-1-((S)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпирролидин-2-она;
(S)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпирролидин-2-она;
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпирролидин-2-она;
(S)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпирролидин-2-она;
(S)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
(S)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-она;
(R)-1-((S)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(S)-1-((S)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(R)-1-((S)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(S)-1-((R)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-она;
(S)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она;
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она и
(S)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-она
или их фармацевтически приемлемых солей.
7. Соединение по п. 6, которое представляет собой 1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-он или его фармацевтически приемлемую соль.
8. Соединение по п. 6, которое представляет собой 2-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-он или его фармацевтически приемлемую соль.
9. Соединение по п. 6, которое представляет собой 1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-он или его фармацевтически приемлемую соль.
10. Соединение по п. 6, которое представляет собой (1R,4S)-2-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-2-азабицикло[2.2.1]гептан-3-он или его фармацевтически приемлемую соль.
11. Соединение по п. 6, которое представляет собой (R)-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)имидазолидин-2-он или его фармацевтически приемлемую соль.
12. Соединение по п. 6, которое представляет собой (R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпирролидин-2-он или его фармацевтически приемлемую соль.
13. Соединение по п. 6, которое представляет собой (S)-1-((S)-3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпирролидин-2-он или его фармацевтически приемлемую соль.
14. Соединение по п. 6, которое представляет собой (R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-метилимидазолидин-2-он или его фармацевтически приемлемые соль или гидрат.
15. Соединение по п. 1, где R1 и R2 представляют собой водород.
16. Соединение по п. 1, где R1 и R2 представляют собой галоген.
17. Соединение по п. 1, где a и b представляют собой 1.
18. Соединение по п. 1, где R1 и R2 представляют собой фтор и a и b представляют собой 1.
19. Соединение по п. 1, где R4 представляет собой водород.
20. Соединение по п. 1, где R6 и R7 связаны друг с другом с образованием необязательно замещенного кольца пирролидинона.
21. Соединение по п. 1, где R6 и R7 связаны друг с другом с образованием необязательно замещенного кольца имидазолидинона.
22. Соединение по п. 1, где R6 и R7 связаны друг с другом с образованием необязательно замещенного 7-членного моно- или бициклического кольца.
23. Соединение по п. 1, где R6 и R7 связаны друг с другом с образованием необязательно замещенного 10-членного моно- или бициклического кольца.
24. Соединение по п. 1, где кольцо, образованное R6 и R7, замещено одной или более группой, выбранной из фтора, метила, этила, изопропила, С3-6 циклоалкила или фенила.
25. Соединение формулы I
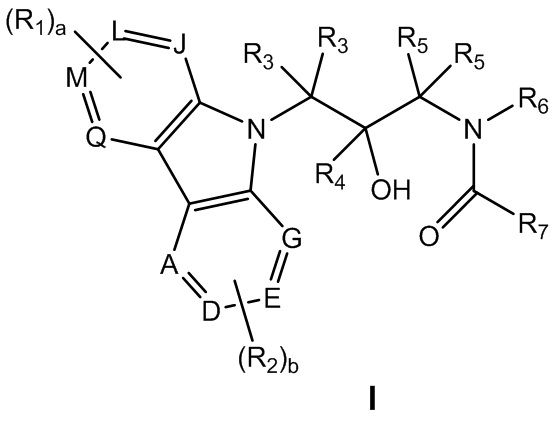
или его фармацевтически приемлемая соль, где
каждый из A, D, E, G, J, L, M и Q представляет атом углерода;
каждый из R1 и R2 независимо выбран из водорода и галогена;
каждый из R3 и R5 представляет собой водород;
R4 выбирают из водорода и (C1-C6)алкила;
где R6 и R7 связаны друг с другом в виде кольца пиперидинона, необязательно замещенного одним или более галогеном, (C1-C6)алкилом, (C1-C6)алкокси, (C3-C10)циклоалкилом или (C6-C10)арилом;
любой из атомов углерода (C1-C6)алкила, (C1-C6)алкокси, (3-10)-членного циклоалкила, (C6-C10)арила и кольца пиперидинона указанных выше R4, R6 и R7 независимо необязательно замещен 1-3 заместителями R14, где каждый R14 независимо выбран из галогена, (C1-C6)алкокси, (C1-C6)алкила, -(CR11R12)e(3-10)-членного циклоалкила и -(CR11R12)e(C6-C10)арила;
любой из атомов азота кольца пиперидинона указанных выше R6 и R7 независимо необязательно замещен (C1-C6)алкилом, -(CR11R12)e(3-10)-членным циклоалкилом и -(CR11R12)e(C6-C10)арилом;
каждый из R11 и R12 независимо представляет собой водород или (C1-C6)алкил;
каждый из a и b независимо представляет собой 1, 2, 3 или 4 и
каждый из e представляет собой 0, 1, 2, 3, 4 или 5.
26. Соединение по п. 25, где каждый R1 и R2 представляет собой водород.
27. Соединение по п. 25, где R4 выбирают из водорода и метила.
28. Соединение по п. 25, выбранное из:
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)пиперидин-2-она (1);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пиперидин-2-она (4);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)пиперидин-2-она (5);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпиперидин-2-она (11);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фторпиперидин-2-она (12);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,3-дифторпиперидин-2-она (13);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3,3-дифторпиперидин-2-она (14);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,3-диметилпиперидин-2-она (16);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фенилпиперидин-2-она (19);
3-циклогексил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пиперидин-2-она (20);
3-циклогексил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)пиперидин-2-она (21);
3-циклопентил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пиперидин-2-она (23);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-этилпиперидин-2-она (24);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-изопропилпиперидин-2-она (25);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-изопропилпиперидин-2-она (26);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпиперидин-2-она (27);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-метилпиперидин-2-она (28);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-4-метилпиперидин-2-она (36);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (37);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-5-метилпиперидин-2-она (38);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-6-метилпиперидин-2-она (39);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-6-метилпиперидин-2-она (40);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-4-метилпиперидин-2-она (49);
3-циклобутил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)пиперидин-2-она (51);
3-циклобутил-1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)пиперидин-2-она (52);
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-метоксипиперидин-2-она (57);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-метоксипиперидин-2-она (60);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-4-метилпиперидин-2-она (61);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (62);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-6-метилпиперидин-2-она (63);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-метилпиперидин-2-она (64);
1-(3-(9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)пиперидин-2-она (66);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3,3-дифторпиперидин-2-она (69);
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-фторпиперидин-2-она (70);
(S)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (129);
(S)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (130);
(R)-1-((R)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (131);
(S)-1-((S)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (132);
(R)-1-((S)-3-(9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (133) и
(R)-1-((R)-3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-5-метилпиперидин-2-она (134);
или его фармацевтически приемлемая соль.
29. Соединение формулы I

или его фармацевтически приемлемая соль, где
каждый из A, D, E, G, J, L, M и Q представляет атом углерода;
каждый из R1 и R2 представляет собой фтор;
каждый из R3 и R5 представляет собой водород;
R4 выбирают из водорода и (C1-C6)алкила;
где R6 и R7 связаны друг с другом в виде насыщенного кольца пиримидинона, необязательно замещенного одним или более галогеном, (C1-C6)алкилом, (C1-C6)алкокси, (C3-C10)циклоалкилом или (C6-C10)арилом;
любой из атомов углерода (C1-C6)алкила, (C1-C6)алкокси, (3-10)-членного циклоалкила, (C6-C10)арила и насыщенного кольца пиримидинона указанных выше R4, R6 и R7 независимо необязательно замещен 1-3 заместителями R14, где каждый R14 независимо выбран из галогена, (C1-C6)алкокси, (C1-C6)алкила, -(CR11R12)e(3-10)-членного циклоалкила и -(CR11R12)e(C6-C10)арила;
любой из атомов азота насыщенного кольца пиримидинона указанных выше R6 и R7 независимо необязательно замещен (C1-C6)алкилом, -(CR11R12)e(3-10)-членным циклоалкилом и -(CR11R12)e(C6-C10)арилом;
каждый из R11 и R12 независимо представляет собой водород или (C1-C6)алкил;
каждый из a и b независимо представляет собой 1, 2, 3 или 4 и
каждый из e представляет собой 0, 1, 2, 3, 4 или 5.
30. Соединение по п. 29, выбранное из:
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-метилтетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-она;
1-циклогексил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-фенилтетрагидропиримидин-2(1H)-она;
1-циклопентил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-изопропилтетрагидропиримидин-2(1H)-она;
1-циклобутил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-фенилтетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-изопропилтетрагидропиримидин-2(1H)-она;
1-циклобутил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)тетрагидропиримидин-2(1H)-она;
1-циклогексил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)тетрагидропиримидин-2(1H)-она;
1-циклопропил-3-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3-этилтетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)-3-этилтетрагидропиримидин-2(1H)-она;
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,5-диметилтетрагидропиримидин-2(1H)-она и
1-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)-3,4-диметилтетрагидропиримидин-2(1H)-она;
или его фармацевтически приемлемая соль.
31. Соединение, выбранное из:
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-метилтетрагидропиримидин-2(1H)-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)тетрагидропиримидин-2(1H)-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-этилтетрагидропиримидин-2(1H)-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-циклопропилтетрагидропиримидин-2(1H)-она;
1-(3-(9H-карбазол-9-ил)-2-гидроксипропил)-3-циклобутилтетрагидропиримидин-2(1H)-она;
4-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидроксипропил)морфолин-3-она и
4-(3-(3,6-дифтор-9H-карбазол-9-ил)-2-гидрокси-2-метилпропил)морфолин-3-она;
или его фармацевтически приемлемая соль.
32. Соединение по любому из пп. 1-31, где указанное соединение модулирует Cry1 или Cry2.
33. Соединение по п. 32, где указанная модуляция включает одно из следующего:
(i) связывание с Cry1 или Cry2;
(ii) ингибирование модификации Cry1 или Cry2;
(iii) изменение локализации Cry1 или Cry2;
(iv) увеличение или уменьшение стабилизации Cry1 или Cry2;
(v) увеличение или уменьшение связывания Cry1 или Cry2 с мишенью;
(vi) увеличение или уменьшение активности Cry1 или Cry2 и
(vii) увеличение или уменьшение активности мишени Cry1 или Cry2.
34. Соединение по п. 33, где указанная мишень представляет собой Per1, Per2, рецептор глюкокортикоидов (GR), CLOCK, BMAL1 или последовательность промотора CLOCK-BMAL1.
35. Фармацевтическая композиция, содержащая соединение по любому из пп. 1-31 или его фармацевтически приемлемую соль и фармацевтически приемлемые носитель, вспомогательное средство или разбавитель, предназначенная для лечения заболевания или расстройства, опосредованного Cry, у пациента или смягчения симптома заболевания или расстройства, опосредованного Cry, у пациента, где заболевание или расстройство выбирают из группы, состоящей из диабета, осложнений диабета, таких как диабетическая нейропатия, диабетическая ретинопатия, диабетическая нефропатия и диабетическая ангиопатия; неалкогольного стеатогепатита (NASH); неалкогольной жировой болезни печени (NAFLD); метаболического синдрома; синдрома резистентности к инсулину и ожирения.
36. Фармацевтическая композиция по п. 35, дополнительно содержащая одно или несколько дополнительных терапевтических средств.
37. Фармацевтическая композиция по п. 36, где указанное одно или несколько дополнительных терапевтических средств выбраны из группы, состоящей из ингибиторов DPP-IV, ингибиторов SGLT2, метформина и сульфонилкарбамидов.
38. Фармацевтическая композиция по п. 36, где указанное одно или несколько дополнительных терапевтических средств выбран из группы, состоящей из сигнифора®, кетоконазола, метирапона, митотана, этомидата, корлима®, ингибиторов рецептора эпидермального фактора роста, ингибитора альдостеронсинтазы/11β-гидроксилазы LCI699 и левокетоконазола (COR-003).
39. Способ лечения опосредуемого Cry заболевания или нарушения у индивидуума, включающий введение индивидууму терапевтически эффективного количества соединения по любому из пп. 1-31 или его фармацевтически приемлемой соли.
40. Способ лечения опосредуемого Cry заболевания или нарушения у индивидуума, включающий введение индивидууму фармацевтической композиции по п. 35.
41. Способ смягчения симптома опосредуемого Cry заболевания или нарушения у пациента, включающий введение индивидууму терапевтически эффективного количества соединения по любому из пп. 1-31 или его фармацевтически приемлемой соли.
42. Способ смягчения симптома опосредуемого Cry заболевания или нарушения у пациента, включающий введение индивидууму фармацевтической композиции по п. 35.
43. Способ по пп. 39-42, где опосредуемое Cry заболевание или нарушение выбрано из группы, состоящей из диабета, осложнения диабета, такого как диабетическая нейропатия, диабетическая ретинопатия, диабетическая нефропатия, диабетическая ангиопатия; неалкогольного стеатогепатита (NASH); неалкогольной жировой болезни печени (NAFLD); метаболического синдрома; синдрома резистентности к инсулину и ожирения.
44. Способ по пп. 39-42, дополнительно включающий введение пациенту одного или нескольких дополнительных терапевтических средств.
45. Способ по п. 44, где указанные одно или несколько дополнительных терапевтических средств выбраны из группы, состоящей из ингибиторов DPP-IV, ингибиторов SGLT2, метформина и сульфонилкарбамидов.
46. Способ по п. 44, где указанные одно или несколько дополнительных терапевтических средств выбраны из группы, состоящей из сигнифора®, кетоконазола, метирапона, митотана, этомидата, корлима®, ингибиторов рецепторов эпидермального фактора роста, ингибитора альдостеронсинтазы/11β-гидроксилазы LCI699 и левокетоконазола (COR-003).
| WO 2003105759 A2, 24.12.2003 | |||
| WO 2014039515 A2, 13.03.2014 | |||
| MOLETTE J | |||
| et al, Identification and Optimization of an Aminoalcohol-Carbozole Series with Antimalarial Properties, ACS Med | |||
| Chem | |||
| Lett., 2013, v | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| ФИГУРНЫЕ КЛЮЧЕВИНЫ ДЛЯ ЗАМКОВ | 1924 |
|
SU1037A1 |
| База данных REGISTRY [online], RN 1222876-06-3, 13.05.2010, найдено из STN | |||
| US 2013303524 A1, 14.11.2013 | |||
| HIROTA T | |||
| et al, Identification of Small Molecule Activators of Cryptochrome, SCIENCE, 2012, v | |||
| Ленточный тормозной башмак | 1922 |
|
SU337A1 |
| ПРИБОР ДЛЯ СООБЩЕНИЯ ВИНТООБРАЗНОГО ДВИЖЕНИЯ ВОЗДУХУ | 1925 |
|
SU1094A1 |
| CHUN S.K | |||
| et al, Identification and Validation of Cryptochrome Inhibitops That Modulate the Molecular Circadian Clock, ACS Chem | |||
| Biol., 03.01.2014 | |||
| КАРБАЗОЛЬНЫЕ СОЕДИНЕНИЯ И ТЕРАПЕВТИЧЕСКИЕ ПРИМЕНЕНИЯ СОЕДИНЕНИЙ | 2009 |
|
RU2497807C2 |
Авторы
Даты
2019-11-05—Публикация
2015-04-06—Подача