Изобретение относится к области органической химии, в частности, к процессам конденсации органических алкил(арил)спиртов с третичными гидропероксидами и может быть использовано для производства органических пероксидов.
Органические пероксиды являются источником свободных радикалов для инициации процесса полимеризации ненасыщенных мономеров. Они широко применяются в полимерной промышленности. Также, пероксиды используются для сшивки полимеров с получением изделий из каучука и полиолефинов с высокими механическими, термическими и химическими свойствами, таких, как: кабель, изоляция, полупроводниковые слои, автомобильные и промышленные рукава, профили, уплотнители, подошвы обуви на основе этилвинилацетата, трубы и контейнеры. А также в качестве источника активного кислорода, в процессах горения, воспламенения, в том числе в двигателях внутреннего сгорания.
Существует несколько основных способов синтеза -алкил(арил)пероксидов (см., например, Рахимов А.И. Химия и технология органических перекисных соединений. // Москва. Изд-во "Химия". 1979. 392 С.): самоконденсация третичных алкил(арил)гидроперекисей; конденсация третичных алкил(арил)гидроперекисей с третичными алкил(арил)спиртами, эфирами, непредельными соединениями; реакция третичных алкил(арил)спиртов с Н2О2; реакция третичных алкил(арил)хлоридов с H2O2; окисление третичных алкил(арил)олефинов третичными алкил(арил)гидропероксидами; окисление третичных алкил(арил)олефинов кислородом или воздухом.
Среди них существенное отражение в промышленности нашел способ, основанный на конденсации третичных алкил(арил)гидропероксидов с органическими спиртами, эфирами, непредельными соединениями (см., например Рахимов А.И. Химия и технология органических перекисных соединений. // Москва. Изд-во "Химия". 1979. 392 С).
Этот способ осуществляется в присутствии кислотного катализатора. В результате реакции выделяется вода или спирт. Как правило, реакционную воду или спирт необходимо убирать из зоны реакции, т.к. они существенно снижают скорость конденсации (см. уравнения реакций 1-3):
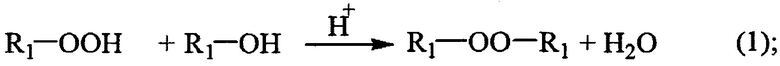
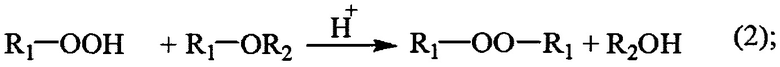
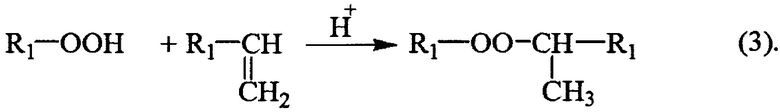
где R1=Алкил или арил.
R2=Алкил.
Из патента США 2668180 известен способ получения пероксида общей формулой (4):
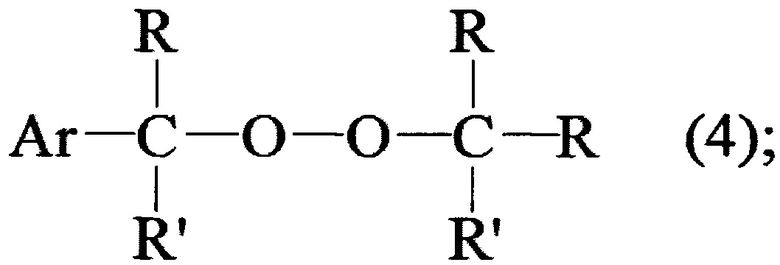
где Ar - арильный радикал, R-алифатический радикал, а R'-радикал группы, состоящей из алифатического и арильного радикалов, отличающихся от Ar. Способ заключается во взаимодействии гидропероксида и не превышающего двухмольного избытка спирта при 50-120°С в присутствии каталитического количества до 0,5% кислотного катализатора (серная кислота 25%-ый водный раствор, n-толуолсульфокислота, эфират трехфтористого бора).
Из патента США 3310588 известен, способ получения органических пероксидов, который включает взаимодействие спирта с гидропероксидом в присутствии кислотно-реагирующего катализатора и удаление образующейся при этом воды. Реакция, улучшение, включающее использование безводной щавелевой кислоты как в качестве катализатора, так и в качестве обезвоживающего агента в количестве, достаточном для поглощения воды, уже присутствующей в исходных компонентах реакции, и количества воды, теоретически образующейся во время реакции, в качестве дигидрата щавелевой кислоты и механического удаления гидратированной щавелевой кислоты.
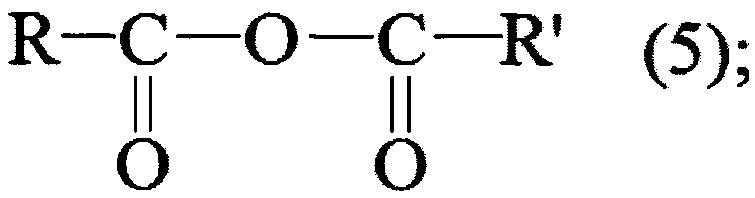
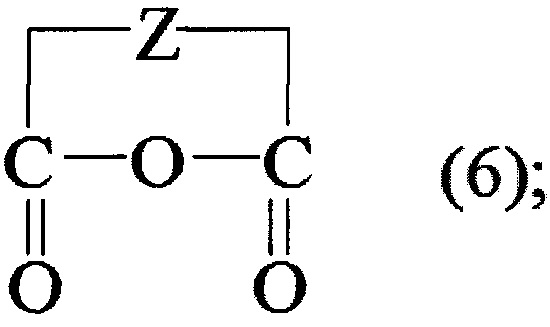
Из патента США 4198528 известен способ получения ди-третичных пероксидов взаимодействием третичного арил- или алкилгидропероксида с третичным арилом или алкиловым спиртом в присутствии сильного кислотного катализатора, усовершенствование которого заключается в проведении указанного взаимодействия в присутствии по крайней мере одного легкогидролизуемого ангидрида карбоновых кислот, имеющего pKa>2,85, при молярном соотношении гидропероксид : спирт : ангидрид около 1,0:0,2-2,5: 0,2-2,0 при температуре около от минус 10°С. до примерно плюс 120°С., ангидрид имеет общую формулу 5, в котором каждый из R и R' выбран из группы, состоящей из алкильных групп, имеющих от 1 до 4 атомов углерода или арилами, содержащий, по крайней мере один электроотрицательных заместителей и от 6 до 10 атомов углерода, и структуру (6), где Z представляет собой двухвалентный радикал, выбранный из группы, состоящей из алкиленов радикалов, имеющих от 2 до 10 атомов углерода, циклоалкилен радикалов, имеющих от 5 до 6 атомов углерода, или о-фенилен.
Из патента США 4374280 известен способ получения перекиси дикумила взаимодействием гидропероксида кумола с диметилфенилкарбинолом в присутствии каталитического количества от 0,5 до 2% галогенида фосфора или оксигалогенида при температуре от 20 до 100°С, с удалением образующийся в реакции воды.
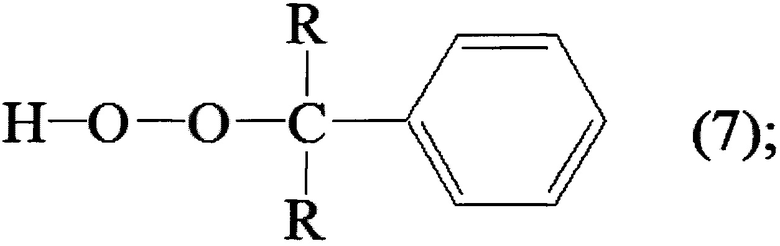
Из патента США 3254130 известен способ получения пероксидов, заключающийся во взаимодействия третичного гидропероксида формулы (7), в которой R представляет собой алкил, с членом группы, состоящей из спиртов α,α-диметилфенилкарбинола и трифенилкарбинола, в присутствии исключительно хлорной кислоты.
Известен из патента США 3337639 способ производства органических пероксидов, осуществляющий взаимодействием (а) гидропероксида, выбранного из группы, состоящей из насыщенных алкильных моногидропероксидов, насыщенных алкил полигидропероксидов, циклоалкилмоногидроперекисей, циклоалкилполигидроперекисей, циклоалкиларилмоногидроперекисей, циклоалкиларилполигидроперекисей, алкил-арилмоногидроперекисей, арил и алкил полигидроперекисей, (б) спирта, выбранного из класса, состоящего из алкильных одноатомных спиртов, многоатомных спиртов алкил, арилалкил одноатомных спиртов и арилалкил многоатомных спиртов в мольном соотношении 1:1-1,5; и (С) катализатора - сильная кислота при температуре от 20 до 80°С, а также удаления воды из реакционной смеси в ходе реакции путем отгонки.
Недостатком известных из уровня техники представленных выше способов проведения синтезов является то, что они происходят с применением сильных кислот. В результате реакций образуется большое количество кислых стоков и побочных продуктов.
Также существуют способы, в которых α-метилстирол взаимодействует с третичными алкил(арил)гидропероксидами в присутствии кислого катализатора, например, патенты Германии 2035127 и 2016108. Применение α-метилстирола приводит к его димеризации, что значительно усложняет данный процесс.
Известным из патентов США 5288919 и 7034189 способом синтеза диалкилпероксидов является взаимодействие органического спирта и/или олефина с органическим гидропероксидом в присутствии гетерополикислого и/или изополикислого катализатора.
Существенными недостатками этих способов являются, малодоступность катализатора и сложность аппаратурного оформления.
Из патента США 3833664 известна реакция между гидропероксидом и спиртом, которая катализируется 70%-ой хлорной кислотой, а образующаяся в результате реакции вода связывается безводным сульфатом магния.
Недостатком данного способа является использование большого количества твердого сульфата магния для связывания реакционной воды, что значительно усложняет технологический процесс.
Из патента США 4266081 известен способ получения органических пероксидов при взаимодействии органических гидропероксидов и третичных спиртов в присутствии ZnCl2. Образующаяся вода отдувается из реакционной зоны азотом, либо отгоняется в вакууме.
Недостатком данного способа является низкая производительность, большое количество инертного газа и невозможностью повторного использования катализатора.
Самым близким по своей технической сущности к заявленному изобретению является способ синтеза алкил(арил)-пероксидов описанный в патенте ЕР 0967194 В1 где при конденсации трет-гидропероксида и третичного спирта в присутствии ароматических сульфокислот:
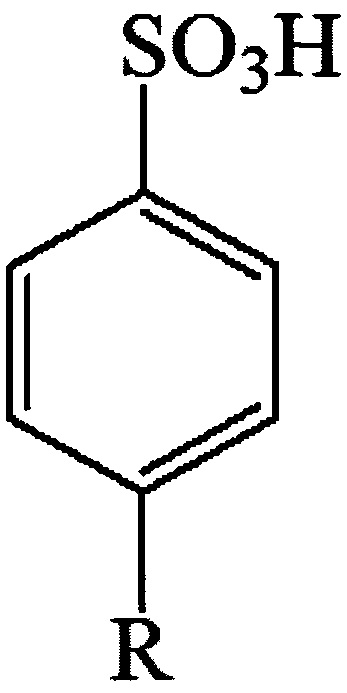
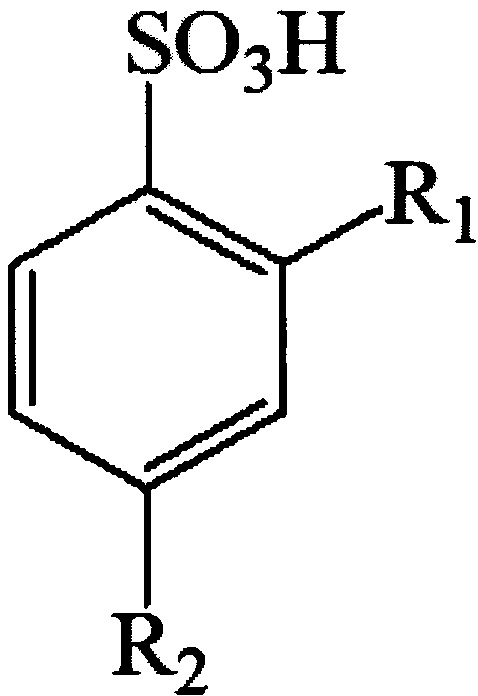
где R - алкильная группа с числом атомов от 2 до 9, предпочтительно от 2 до 6; R1 и R2-алкильные группы с числом углеродных атомов от 1 до 9, преимущественно от 1 до 6.
Основным недостатком этого способа является однократное использование большого количества дорогого катализатора.
Техническим результатом, на который направлено заявленное изобретение, является снижения расхода катализатора за счет его повторного использования при получении органических алкил(арил)пероксидов.
Поставленная задача решается за счет того, что для получения органических алкил(арил)пероксидов используют в качестве катализатора смесь следующего состава:
причем в качестве арилсульфокислот используют смесь пара- и мета- толуолсульфокислот в соотношении от 1:0,01 до 1:1.
Катализатор может повторно использоваться в процессе.
Способ получения органических алкил(арил)пероксидов осуществляется следующим образом. В реактор с мешалкой и обогревом загружают органический алкил(арил) спирт, третичный алкил(арил)гидропероксид и полисульфокислоту. Затем при перемешивании прикапывают водный раствор растворимого катализатора при температуре 40-75°С в течение 1 -2 часов. После чего смесь дополнительно выдерживают еще 1-4 часа при этой же температуре, затем отключают перемешивание и после того как слои разделились на органический слой - сверху и водно-катализаторный - снизу, слои разделяют. Из верхнего слоя выделяют пероксид, а нижний слой отправляют на укрепление (отгонку лишней воды). Полисульфокислота после реакции отфильтровывается. Катализатор (растворимый слой и полисульфокислота) может использоваться повторно. Условия синтеза и основные параметры процессов указаны в таблице 1.
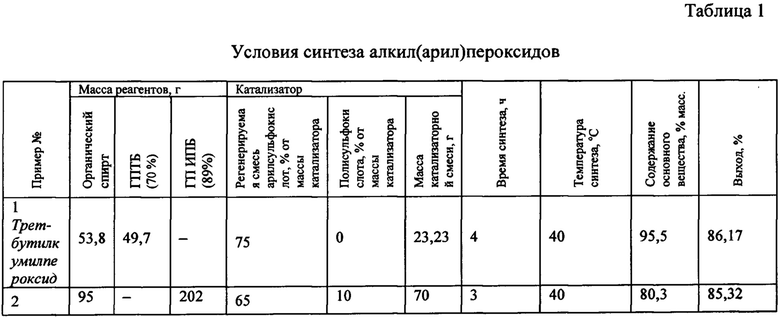
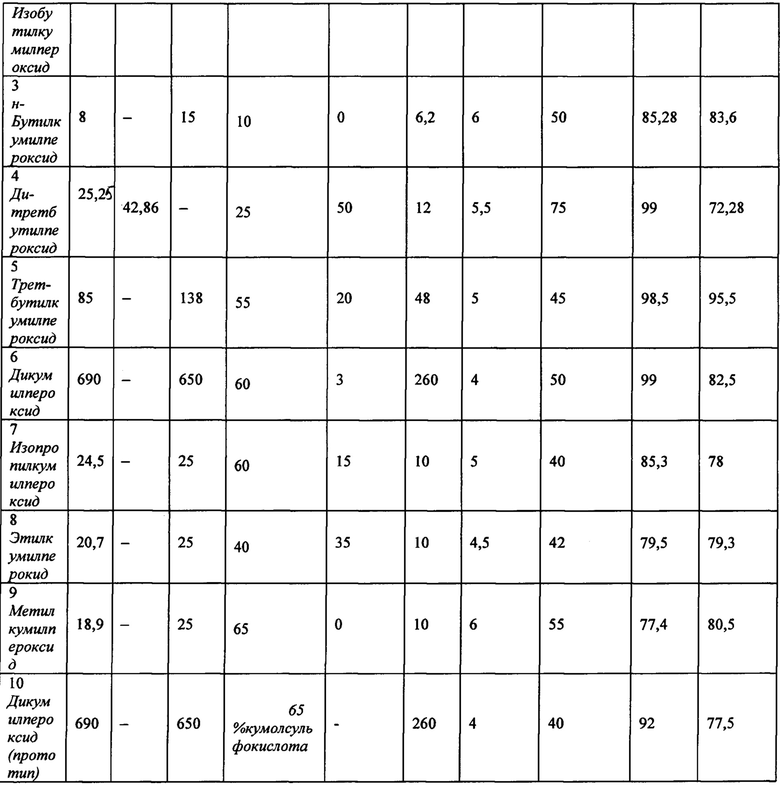
Органический спирт:
Пример №1, 6 и 10=диметилфенилкарбинол 93%;
Пример №2=изобутиловый спирт 98%;
Пример №3=бутиловый спирт 98%;
Пример №4 и 5=трет-бутиловый спирт 98%;
Пример 7=изопропиловый спирт 87%;
Пример 8=этиловый спирт 96%;
Пример 9=метиловый спирт 99%.
ГПТБ - гидропероксид трет-бутила, ГП ИПБ - гидропероксид изопропилбензола, КСК - кумолсульфокислота.
Примеры 3-10, указанные в таблице, методически и принципиально аналогичны примеру 1 и 2 указанному ниже. Они демонстрируют синтез различных алкил(арил)пероксидов по заявленному способу получения органических алкил(арил)пероксидов. Условия синтезов по примерам 1-10 представлены в таблице 1. Пример 10 описывает получение дикумилпероксида по прототипу для сравнения.
Осуществление заявленного способа получения органических алкил(арил)пероксидов подтверждается примерами.
Пример 1. Получения органических алкил(арил)пероксидов без использования полисульфокислоты.
В реактор с мешалкой и обогревом загружают 53,8 г диметилфенилкарбинола (содержание основного вещества 93%) и 49,7 г технического гидропероксида трет-бутила (содержание основного вещества 70%). Затем при перемешивании прикапывают 23,23 г регенерируемую смесь арилсульфокислот (75% водный раствор) при температуре 40°С в течение 1 часа. Смесь дополнительно выдерживают еще 3 часа при этой же температуре. Затем отбирают пробу реакционной массы из верхнего органического слоя на анализ -определение остаточного гидропероксида трет-бутила йодометрически. При содержании остаточного гидропероксида трет-бутила не более 1,0-1,5% масс, перемешивание останавливают. После этого разделяют слои: верхний - органический (трет-бутилкумилпероксид) и нижний - водный (разбавленный раствор катализатора). Органический слой последовательно промывают 3 раза 15%-ным водным раствором гидроксида натрия и 3 раза водой до рН водного слоя 6-7. После этого делают дополнительную промывку с отстаиванием верхнего слоя не менее 1 часа. Сырой продукт после окончания промывок сушат безводным сульфатом магния. Содержание основного вещества 95,5% масс. Выход 86,17%.
Пример 2. Получения органических алкил(арил)пероксидов с использованием полисульфокислоты.
В реактор с мешалкой и обогревом загружают 95 г изо-бутилового спирта (содержание основного вещества 98%) и 202 г технического гидропероксида изопропилбензола (содержание основного вещества 89%). Добавляют полисульфокислоту 7 г так, чтобы реакционная масса омывала катализатор, но не разрушала его. Затем при перемешивании прикапывают 63 г регенерируемую смесь арилсульфокислот (водный 72,22% раствор) при температуре 40°С в течение 1 часа. Смесь дополнительно выдерживают еще 2 часа при этой же температуре. Затем отбирают пробу реакционной массы из верхнего органического слоя на анализ - определение остаточного гидропероксида изопропилбензола йодометрически. При содержании остаточного гидропероксида изопропилбензола не более 1,0-1,5% масс, перемешивание останавливают. Отфильтровывают полисульфокислоту, пропуская через фильтр всю реакционную массу. После этого разделяют слои: верхний - органический (изо-бутилкумилпероксид) и нижний - водный (разбавленный раствор катализатора). Органический слой последовательно промывают 3 раза 15%-ным водным раствором гидроксида натрия и 3 раза водой до рН водного слоя 6-7. После этого делают дополнительную промывку с отстаиванием верхнего слоя не менее 1 часа. Сырой продукт после окончания промывок сушат безводным сульфатом магния. Содержание основного вещества 80,3% масс. Выход 85,32%.
Отфильтрованную полисульфокислоту и регенерируемый водный раствор катализатора используется повторно для последующих синтезов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ОРГАНИЧЕСКИХ ПЕРОКСИДОВ ИЛИ ПЕРОКСИКЕТАЛЕЙ | 2020 |
|
RU2755085C1 |
| Пероксидная цетаноповышающая присадка к дизельному топливу и способ ее получения | 2022 |
|
RU2800120C1 |
| Способ разложения гидропероксида изопропилбензола с получением диметилфенилкарбинола | 2020 |
|
RU2750718C1 |
| Способ получения этилацетата | 2021 |
|
RU2771241C1 |
| Способ получения фенола | 2023 |
|
RU2829821C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ФЕНОЛА, АЦЕТОНА И АЛЬФА-МЕТИЛСТИРОЛА | 1992 |
|
RU2068404C1 |
| Эффективный способ получения фенола | 2023 |
|
RU2838431C2 |
| Способ очистки отходов спиртового производства | 2021 |
|
RU2775964C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНОЛА И АЦЕТОНА | 2014 |
|
RU2565764C1 |
| Топливная композиция дизельного топлива | 2021 |
|
RU2795859C1 |
Изобретение относится к способу получения органических алкил(арил)пероксидов путем взаимодействия органических алкил(арил)спиртов с гидропероксидами и может быть использовано для производства органических пероксидов. Техническим результатом, на который направлено изобретение, является снижение расхода катализатора за счет его повторного использования при получении органических алкил(арил)пероксидов. Поставленная задача решается за счет того, что в качестве катализатора используют смесь пара- и мета-арилсульфокислоты в массовом соотношении компонентов от 1:0,001 до 1:1 в виде водного 10-75% раствора, которая представляет собой регенерируемую смесь следующего состава: арилсульфокислота 10-75 мас.%; полисульфокислота 0-50 мас.%; вода 5-90 мас.%. 1 табл., 2 пр.
Способ получения органических алкил(арил)пероксидов, заключающийся во взаимодействии гидропероксида и спирта с использованием катализатора, отличающийся тем, что в качестве катализатора используют смесь пара- и мета-арилсульфокислоты в массовом соотношении компонентов от 1:0,001 до 1:1 в виде водного 10-75% раствора, которая представляет собой регенерируемую смесь следующего состава, мас.%:
| ЕР 0967194 А1, 29.12.1999 | |||
| Преобразователь давления | 1977 |
|
SU628546A1 |
| US 5371278 А, 06.12.1994 | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Способ получения перекиси дикумила | 1989 |
|
SU1776256A3 |
Авторы
Даты
2019-11-28—Публикация
2019-04-26—Подача