Изобретение относится к области сельского хозяйства, в частности ветеринарной гельминтологии, и может быть использовано для лечения гельминтозов животных.
Гельминтозы животных широко распространены в России и в других странах и причиняют большой экономический ущерб животноводству вследствие снижения всех видов продуктивности, отставания в росте и развитии молодняка и гибели животных, особенно молодняка [5].
Одним из широко применяемых антигельминтиков для борьбы с гельминтозами является фенбендазол (син.: панакур, фебтал, фенкур), который, в основном, обладает нематодоцидным действием в дозе 5-10 мг/кг [1, 3].
Фенбендазол применяют на овцах, козах и крупном рогатом скоте против гельминтозов, включая желудочно-кишечные стронгилятозы, диктиокаулез, стронгилидоз, трихоцефалез; лошадям против параскаридоза, стронгилидозов; плотоядным против токсокароза, токсаскаридоза, унцинариоза и других нематодозов. Препарат безопасен для организма животных, не обладает побочным действием. Применяют перорально с кормом в дозе 5 мг/кг овцам, молодняку крупного рогатого скота в дозе 10 мг/кг, собакам в дозе 50 мг/кг три дня подряд, лошадям в дозе 10-15 мг/кг [1, 3].
Недостатком этого препарата является низкая растворимость, плохая абсорбция слизистой оболочкой кишечника и, как следствие, плохая биодоступность и высокие дозы против гельминтозов, особенно, плотоядных животных [6, 7].
Нами (Варламова А.И., Архипов И.А., Халиков С.С.и др., 2015) в 2015 году получен Патент на изобретение «Антигельминтное средство и способ его получения» [4], касающийся получения супрамолекулярного комплекса фенбендазола с арабиногалактаном (СКФА) по механохимической технологии. Полученный препарат обладает повышенной растворимостью в воде, биодоступностью и эффективностью. Однако, до сих пор антигельминтное средство (СКФА) не производится из-за резкого повышения цены арабиногалактана и его производства в ограниченном количестве, что затрудняет применение препарата в ветеринарии. Высокая цена арабиногалактана снижает экономическую эффективность супрамолекулярного комплекса фенбендазола. Кроме того, нами в предварительном опыте установлено средство - диоктилсульфосукцината натрия, который в большей степени повышает растворяемость и эффективность фенбендазола.
Сравнивая способы получения, выбор полимера и решение вопроса растворимости, наиболее близким техническим решением, выбранным в качестве прототипа, является СКФА, производимый по механохимической технологии [2, 4].
С целью совершенствования прототипа СКФА, нами предложен способ получения твердой дисперсии фенбендазола с повышенной эффективностью с использованием механохимической технологии и адресной доставки.
Предлагаемая твердая дисперсия (ТД) получается путем механохимической обработки фенбендазола (ФБЗ), поливинилпирролидона (ПВП) и диоктилсульфосукцината натрия (ДССН) в весовом соотношении 10:899:0,10 в измельчителях ударно-истирающего типа. Эта ТД фенбендазола, обозначенная нами как ТДФПД, представляет собой порошок светло-серого цвета.
Способ получения ТДФПД включает в себя последовательное смешение расчетных количеств фенбендазола, ПВП и ДССН с дальнейшей механохимической обработкой в измельчителе-активаторе ударно-истирающего типа до образования твердых агрегатов наноразмерного диапазона. Полученные ТДФПД состава ФБЗ : ПВП : ДССН=10:88,85-89,95:0,05-0,15 обладают повышенной растворимостью в воде, большей антигельминтной активностью и имеют следующие преимущества:
1. В синтезе ТДФПД используется водорастворимый, доступный, дешевый полимер - ПВП, который позволяет улучшить гидрофильность, смачиваемость и растворимость фенбендазола.
2. Снижается стоимость ТДФПД по сравнению с прототипом СКФА за счет использования дешевого полимера ПВП и снижения терапевтической дозы.
3. В процессе синтеза ТДФПД субстанция фенбендазола за счет его смешивания с ПВП и ДССН, а также дальнейшей механохимической обработки легко распределяется в порах и на стенке полимерного носителя (ПВП), что значительно изменяет свойства конечного продукта (ТДФПД), в частности, повышается его водорастворимость, проницаемость, биодоступность и антигельминтная эффективность.
4. Целевой продукт ТДФПД в виде наноразмерных агрегатов получается в одну стадию при твердофазной механообработке в ударно-истирающей мельнице без участия жидких фаз и процесса сушки. При этом исключено образование отходов.
В связи с тем, что наиболее значимой и важной характеристикой предлагаемого продукта является его дисперсность и водорастворимость, нами проводилась оценка этих показателей.
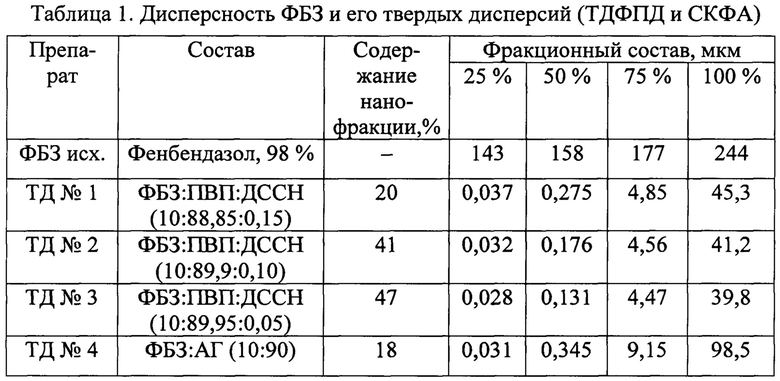
Анализ дисперсности ТДФПД, полученных при твердофазной механообработке трехкомпонентной смеси (ФБЗ, ПВП, ДССН), проводили на лазерном анализаторе размеров частиц "SALD-7101" (SALD-7101 Nanoparticle Size Analyzer) компании "Shimadzu". Обработку данных осуществляли по методике стандартного программного обеспечения Windows ХР Professional. Полученные результаты (см. табл. 1) указывают на то, что включение в состав твердых дисперсий ПВП и ДССН позволяет получать нанодисперсные агломераты фенбендазола в целевых продуктах серии ТДФПД. Содержание нанофракций в предлагаемой серии ТДФПД составляет 20-47%, тогда как в прототипе (СКФА) - лишь 18%. При этом, 50% фракций в ТДФПД составляют агломераты в диапазоне 131-275 нм.
Изучение водорастворимости различных по составу образцов ТДФПД в воде по сравнению с прототипом (СКФА) проводили методом ВЭЖХ на хроматографе Agilent 1200 при следующих условиях:
- колонка Zorbax Eclipse XDB-C18, 4,6×150 мм;
- температура колонки 30°С;
- элюент - 25% ацетонитрил + 75% вода; скорость потока - 1 мкл/мин;
- детектор диодно-матричный, детектирование в диапазоне 230-280 нм.
На основании интегральной интенсивности пика со временем удерживания ФБЗ (4,645 мин) рассчитали показатель водорастворимости анализируемых комплексов. Результаты приведены в таблице 2 и они показали, что наблюдается существенное увеличение растворимости ТДФПД в зависимости от соотношения компонентов.

Наибольшая растворимость отмечена у ТДФПД состава ФБЗ : ПВП : ДССН (10:88,85:0,15). Однако, это значение растворимости не столь значимо по сравнению с ТДФПД состава ФБЗ : ПВП : ДССН (10:89,9:0,10) - сравнить 24,0 и 21,2 и поэтому оптимальным составом выбран ТД №2.
Эффективность предлагаемой ТД №2 состава ФБЗ : ПВП : ДССН (10:89,9:0,10) демонстрируется примерами:
Пример 1. Получение антигельминтного средства - ТДФПД состава ФБЗ : ПВП : ДССН (10:89,9:0,10),
В металлический барабан валковой шаровой мельницы типа LE-101 объемом 800 мл последовательно при периодическом перемешивании загружали 800 г металлических шаров (диаметр 12 мм), 2.1 г ФБЗ, 20,9 г ПВП, 0,10 г ДССН. В результате такой операции в барабане была получена физическая смесь компонентов. Барабан устанавливали на валках и проводили обработку смеси в течение 2 ч при вращении барабана со скоростью 70 об./мин. Полученный продукт - ТДФПД состава ФБЗ : ПВП : ДССН (10:89,9:0,10) в виде светло-серого сыпучего порошка выгружали из барабана и изучали его эффективность на лабораторной модели при трихинеллезе белых мышей.
Пример 2. Аналогично примера 1 из 2,1 г ФБЗ, 20,85 г ПВП и 0,15 г ДССН получали сыпучий порошок - ТДФПД состава ФБЗ : ПВП : ДССН (10:88,85:0,15), который затем изучали на эффективность при трихинеллезе белых мышей.
Пример 3. Аналогично примера 1 из 2,1 г ФБЗ, 20,95 г ПВП и 0,05 г ДССН получали светло-серый сыпучий порошок - антигельминтное средство - ТДФПД состава ФБЗ : ПВП : ДССН (10:89,95:0,05), который испытали при трихинеллезе белых мышей.
Пример 4. Изучение антигельминтной эффективности ТД на модели Trichinella spiralis. Изучение нематодоцидной активности заявляемых препаратов проводили на лабораторной модели трихинеллеза на белых мышах, экспериментально инвазированных Т. spiralis в возрасте 1,5-2 месяцев в дозе 200 личинок на животное. Животных заражали через рот введением суспензии с личинками с помощью шприца с канюлей. На 3-и сутки после заражения мышам подопытных групп (по 10 голов в каждой) вводили перорально однократно 3 твердые дисперсии фенбендазола (ТД №1, ТД №2, ТД №3), полученные при различном соотношении субстанции фенбендазола, полимера ПВП и ДССН (см. табл. 1). Мыши этих групп получали антигельминтные средства №1, №2 и №3 в дозе 10 мг/кг по препарату или 0,9 мг/кг по субстанции фенбендазола. Мыши четвертой группы получали прототип - ТД №4 в дозе 10 мг/кг по препарату. Животные контрольной группы получали дистиллированную воду в соответствующих объемах.
Животных убивали декапитацией на 2-е сутки после введения препаратов. Нематодоцидную активность испытуемых препаратов учитывали по результатам гельминтологического вскрытия кишечника, взятия соскобов слизистой оболочки, переваривания в растворе искусственного желудочного сока и подсчета под бинокулярной лупой. Учитывали обнаруженное при этом количество трихинелл. Учет эффективности препаратов проводили по типу «контрольный тест» с расчетом среднего количества обнаруженных нематод и интенсэффективности (ИЭ). Результаты приведены в таблице 3.
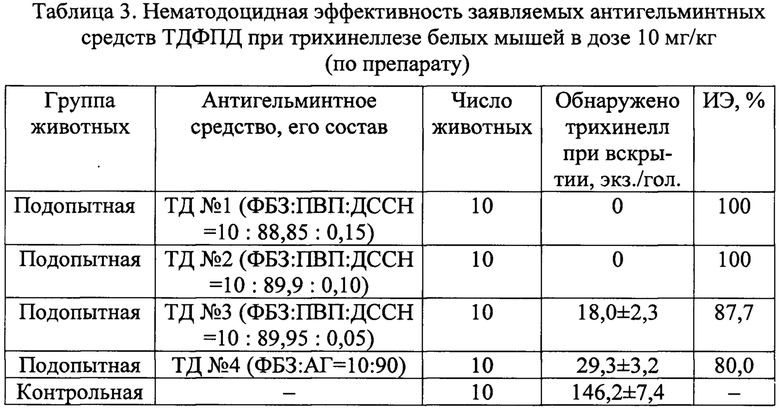
Антигельминтное средство - ТД №2 (ФБЗ : ПВП : ДССН=10:89,9:0,10) в дозе 10 мг/кг (в пересчете на субстанцию фенбендазола 0,9 мг/кг), оказал 100%-ную эффективность при экспериментальном трихинеллезе мышей.
Антигельминтные средства - ТД №1 (ФБЗ : ПВП : ДССН=10:88,85:0,15) и ТД №3 (ФБЗ : ПВП : ДССН=10:89,95:0,05) в дозе 10 мг/кг по препарату или 0,9 мг/кг по фенбендазолу, показали соответственно 100 и 87,7%-ную эффективность против имагинальных трихинелл. Эффективность базового препарата в дозе 10 мг/кг по препарату или 0,9 мг/кг по ДВ оказалась недостаточной и составила 80,0%. У животных контрольной группы обнаруживали в среднем по 146,2±7,4 экз. трихинелл.
Таким образом, антигельминтное средство - ТДФПД состава ФБЗ : ПВП : ДССН=10:89,9:0,10 в дозе 10 мг/кг (в пересчете на фенбендазол 0,9 мг/кг) показал 100%-ную эффективность при экспериментальном трихинеллезе мышей.
Пример 5. Изучение эффективности заявляемого антигельминтного средства на модели Hymenolepis nana. Испытание на цестодоцидную активность нового антигельминтного средства в дозе 10 мг/кг (по препарату) проводили на белых мышах, экспериментально инвазированных Н. nana. Мышей заражали перорально с помощью шприца, снабженного специальной канюлей, из расчета 200 инвазионных яиц на животное. Для этого собранных от предшествующего заражения цестод Н. nana растирали пестиком в ступке или разрушали в небольшом объеме водопроводной воды посредством неоднократного насасывания в шприц с насаженной на него иглой-канюлей для перорального заражения. На 13-е сутки после заражения в желудок мышей трех первых подопытных групп вводили тестируемые препараты (ТД №1, ТД №2 и ТД №3) однократно в дозе 10 мг/кг в 1%-ном крахмальном геле. Животные четвертой группы получали прототип (ТД №4) - СКФА в дозе 1,0 мг/кг по фенбендазолу или 10 мг/кг по препарату. Животным контрольной группы вводили крахмальный гель в соответствующих объемах. На 4-е сутки после введения препаратов мышей убивали декапитацией.
Активность препаратов учитывали по результатам гельминтологического вскрытия кишечника. Извлеченных при вскрытии цестод подсчитывали. Учет эффективности препаратов проводили по типу «контрольный тест» с расчетом среднего количества обнаруженных цестод и интенсэффективности (ИЭ). Результаты приведены в таблице 4.
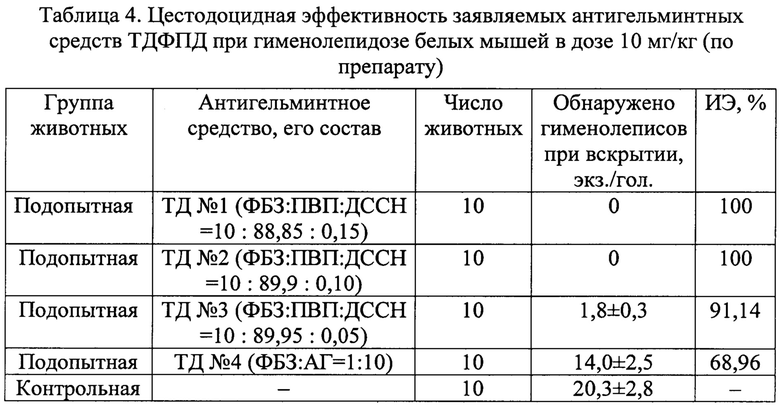
100%-ю эффективность при гименолепидозе мышей проявили заявляемые антигельминтные средства - ТД №1 (ФБЗ : ПВП : ДССН=10:88,85:0,15) и ТД №2 (ФБЗ : ПВП : ДССН=10:89,9:0,10). Препараты были активны как против имагинальных, так и неполовозрелых цестод. При вскрытии кишечника мышей, получавших этот препарат, цестод не обнаруживали. После введения антигельминтного средства ТД №3 (ФБЗ : ПВП : ДССН=10:89,95:0,05) в кишечнике животных находили нежизнеспособных гименолеписов и единичные экземпляры подвижных цестод. Эффективность составила 91,14%.
Базовый препарат ТД №4 (ФБЗ : АГ=10:90) в испытанной дозе проявил меньшую активность против Н. nana (68,96%).
В кишечнике животных контрольной группы обнаруживали в среднем по 20,3±2,8 экз./гол. Н. nana, из них 30% составили неполовозрелые цестоды.
Пример 6. Изучение острой токсичности антигельминтного средства - твердой дисперсии фенбендазола. Для определения параметров острой токсичности исследуемые препараты вводили в желудок однократно беспородным белым мышам в дозах 6000, 12000, 18000 и 24000 мг/кг. Исследование каждой дозы проводили на 10 белых мышах. В течение 14 суток проводили наблюдение за общим состоянием и поведением животных, проявлением симптомов интоксикации и возможной гибели. Павших животных подвергали патологоанатомическому вскрытию.
Результаты изучения острой токсичности антигельминтных средств при введении в желудок белым мышам приведены в таблице 5.
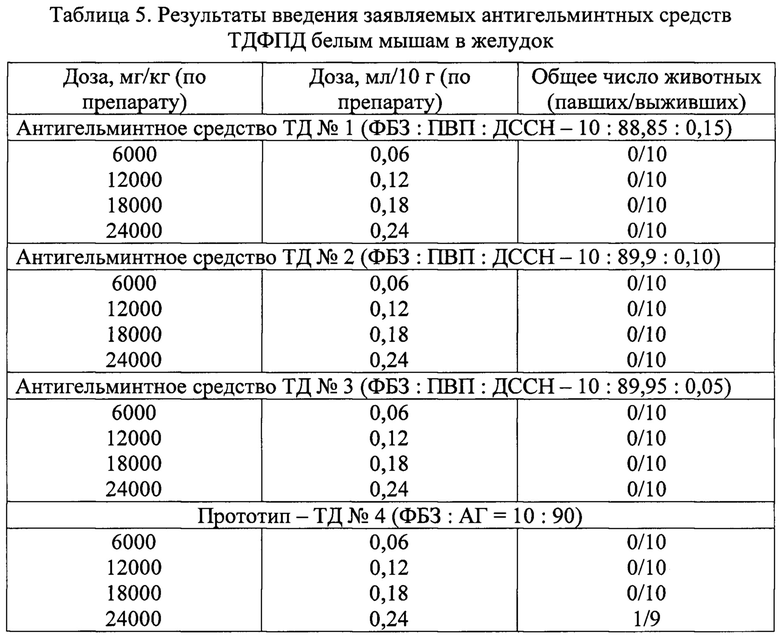
Результаты изучения острой токсичности препаратов показали, что все заявляемые средства в виде твердых дисперсий (ТД №1, ТД №2 ТД №3) оказались нетоксичными для организма белых мышей при введении в желудок. Дозу 24000 мг/кг вводили животным в два этапа равными порциями с интервалом 20 минут. Доза 24000 мг/кг является максимально возможной для перорального введения мышам. В связи с этим, LD50 тестируемых препаратов будет превышать эту дозу. Ни одна мышь не пала после введения препарата в дозе 24000 мг/кг. Базовый препарат - прототип ТД №4 проявил токсичность. От дозы 24000 мг/кг пала одна мышь. При вскрытии павшего животного отмечали гиперемию стенок желудка и тонкого кишечника, точечные кровоизлияния на печени и почках. Таким образом, антигельминтные средства в виде твердых дисперсий (ТД №1, ТД №2, ТД №3), содержащие в своем составе ФБЗ, ПВП и ДССН в различном соотношении, оказались безопасными для организма животных в дозах от 6000 до 24000 мг/кг, в то время как базовый препарат (прототип) в дозе 24000 мг/кг вызвал падеж одного из 10 животных.
Полученные результаты показывают, что из разработанных и испытанных заявляемых антигельминтных средств ТДФПД состава ФБЗ : ПВП : ДССН=10:89,9:0,10 наиболее экономичен и обеспечивает повышение антигельминтной эффективности против нематод, расширение спектра действия, включая нематод и цестод, снижение терапевтической дозы на 20-31% и токсичности по сравнению с прототипом - СКФА.
Литература
1. Архипов И.А. Антигельминтики: фармакология и применение. - М.: Изд-во РАСХН, 2009. - 405 с.
2. Варламова А.И., Лимова Ю.В., Садов К.М., Садова А.К., Белова Е. Е., Радионов А.В., Халиков С.С., Чистяченко Ю.С., Душкин А.В., Скира В.Н., Архипов И.А. Эффективность супрамолекулярного комплекса фенбендазола при нематодозах овец // Российский паразитологический журнал. - М., 2016. - Т. 35, Вып. 1. - С. 76-81.
3. Инструкция о мероприятиях по предупреждению и ликвидации заболеваний животных гельминтозами. - М.: Информагротех, 1999. - 72 с.
4. Патент РФ №2558922 (2014). Антигельминтное средство и способ его получения / Варламова А.И., Архипов И.А., Халиков С.С., Душкин А.B., Чистяченко Ю.С., Халиков М.С., Данилевская Н.В. Заявл. Заявка: 2014118329/15 от 07.05.2014. Опубл. 10.08.2015. бюл. №22.
5. Сафиуллин Р.Т. Распространение и экономический ущерб от основных гельминтозов жвачных животных // Ветеринария. - 1997. - №6. - C. 28-32.
6. Bossche Н., Rochette F., Horig С.Anthelmintic efficacy of fenbendazole // Vet. Rec. - 1982. - V. 78, No 3. - P. 876-877.
7. The Biopharmaceutics Classification System (BCS) Guidance, Available at: // www.fda.gov/About FDA/Center Offices/CDER/ucm 128219, htm (accessed 25 May 2009).
| название | год | авторы | номер документа |
|---|---|---|---|
| Комплексное твердодисперсное антигельминтное средство | 2023 |
|
RU2811699C1 |
| ПРОТИВОПАРАЗИТАРНОЕ СРЕДСТВО НА ОСНОВЕ АЛЬБЕНДАЗОЛА И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ ДЛЯ ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ МЛЕКОПИТАЮЩИХ | 2014 |
|
RU2546535C1 |
| АНТИГЕЛЬМИНТНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2558922C1 |
| Противопаразитарное средство и способ терапии овец при паразитарных инвазиях | 2022 |
|
RU2815424C1 |
| Супрамолекулярный антигельминтный комплекс для лечения и профилактики животных при основных гельминтозах | 2019 |
|
RU2732293C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ ЖИВОТНЫХ | 2016 |
|
RU2635514C1 |
| СУПРАМОЛЕКУЛЯРНЫЙ КОМПЛЕКС С НИКЛОЗАМИДОМ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2015 |
|
RU2588368C1 |
| АНТИГЕЛЬМИНТНОЕ СРЕДСТВО | 2011 |
|
RU2452489C1 |
| АНТИГЕЛЬМИНТНОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ КАБАНОВ | 2009 |
|
RU2422142C2 |
| Средство для лечения гельминтозов диких свиней | 2021 |
|
RU2786792C1 |
Изобретение относится к ветеринарии, в частности к ветеринарной гельминтологии, и может быть использовано для лечения гельминтозов животных. Изобретение касается состава твердой дисперсии фенбендазола, ПВП и ДССН при следующем соотношении по массе: 10:89,9:0,10 и заявляемого способа получения, заключающегося в совместной механохимической обработке в валковой шаровой мельнице с добавлением 800 г металлических шаров в течение 2 часов при вращении барабана со скоростью 70 оборотов в минуту до получения твердодисперсного порошка с размером частиц до 10 μn. Заявленный препарат обладает повышенной растворимостью в воде, увеличенной биодоступностью, повышенной эффективностью, пониженной токсичностью, расширенным спектром действия при снижении терапевтической дозы. 2 н.п. ф-лы, 5 табл., 7 пр.
1. Антигельминтное средство в виде твердодисперсного порошка, включающее фенбендазол, отличающееся тем, что оно дополнительно включает поливинилпирролидон и диоктилсульфосукцинат натрия при следующем соотношении компонентов, масс. %:
фенбендазол - 10,
поливинилпирролидон - 89,9,
диоктилсульфосукцинат натрия - 0,10.
2. Способ получения антигельминтного средства по п. 1, отличающийся тем, что фенбендазол, поливинилпирролидон и диоктилсульфосукцинат натрия подвергают совместной механохимической обработке в валковой мельнице с добавлением 800 г металлических шаров диаметром 12 мм в течение 2 часов при вращении барабана со скоростью 70 об/мин.
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ КОМПЛЕКСНЫХ ПРЕПАРАТОВ ИЗ НЕРАСТВОРИМЫХ В ВОДЕ СУБСТАНЦИЙ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2013 |
|
RU2524652C1 |
| Автоматическая сцепка для железнодорожных вагонов | 1929 |
|
SU22068A1 |
| Лимова Ю | |||
| В | |||
| и др., АНТИГЕЛЬМИНТНАЯ ЭФФЕКТИВНОСТЬ НОВЫХ ЛЕКАРСТВЕННЫХ ФОРМ ФЕНАСАЛА НА ОСНОВЕ СУПРАМОЛЕКУЛЯРНЫХ, НАНОРАЗМЕРНЫХ СИСТЕМ ДОСТАВКИ DRUG DELIVERY SYSTEM ПРИ АНОПЛОЦЕФАЛИДОЗАХ ЛОШАДЕЙ, РОССИЙСКИЙ ПАРАЗИТОЛОГИЧЕСКИЙ ЖУРНАЛ, Том 40, Выпуск 2/2017, стр | |||
| Поршень для воздушных тормозов с сжатым воздухом | 1921 |
|
SU188A1 |
Авторы
Даты
2019-12-13—Публикация
2019-01-29—Подача