Изобретение относится к области медицины, а именно к области воспроизведения болезней человека в эксперименте, и может быть использовано для моделирования нарушений свертывающей системы крови на фоне действия цитостатиков.
Основную роль в патогенезе тромботических осложнений у больных злокачественными новообразованиями играют изменения в системе гемостаза, вызываемые как самой опухолью, так и методами лечения [1]. Известно, что для больных злокачественными новообразованиями получающих химиотерапию характерен высокий риск развития побочных эффектов. Наиболее распространенными токсическими эффектами являются панцитопения периферической крови и гипоплазия костного мозга, а так же нарушение функции печени, что влечет за собой нарушение гемостаза и приводит к повышению риска образования тромбов [2, 3].
Известен способ моделирования тромбообразования у подопытных животных, [4] характеризующийся тем, что открывают сонную артерию для индукции тромбоза и яремную вену для введения исследуемого образца антикоагулянта или контрольного раствора у наркотизированных животных, под сонную артерию подкладывают изолирующий ее от окружающих тканей материал, затем вводят препарат антикоагулянта или контрольного раствора в яремную вену, после чего приводят сонную артерию в соприкосновение с тонкой стальной иглой, соединенной с источником постоянного тока и выполняющей функцию первого электрода, при этом второй электрод вводят подкожно в область бедра животного и пропускают через него ток силой 200-250 микроампер в течение одной минуты, затем осуществляют под микроскопом видеосъемку, в результате которой отснятый видеоматериал анализируют посредством компьютерной программы для определения размера образовавшегося тромба.
Недостатком данного способ является то, что он не подходит для моделирования нарушений гемостаза, наблюдаемых при противоопухолевой терапии. Способ моделирования тромбообразования включает в себя проведение хирургических манипуляций с животными, что предполагает владение определенными навыками и использование дорогостоящего оборудования, что значительно усложняет способ.
Известен способ моделирования тромбоэмболии легочной артерии у крыс [5]. Для моделирования тромбоэмболии легочной артерии перекрывают кровоток в нижней полой вене крысы. При этом для развития тромбоэмболии мелких ветвей легочной артерии на уровне сегментарных артерий окклюзию вены сохраняют в течение 1,5-3,0 часов. Для формирования тромбоэмболии на уровне долевых артерий окклюзию вены сохраняют в течение 3,1-6,0 часов с последующим открытием кровотока.
Недостатком данного способа является то, что он не показывает влияние противоопухолевых препаратов на систему гемостаза. Данный метод предполагает инвазивное хирургическое вмешательство, что требует определенных навыков, а так же моделирует только тромбоэмболии легочной артерии и ее мелких ветвей, наш же способ предполагает системное нарушение гемостаза под влиянием цитостатика.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задачей решаемой настоящим изобретением является создание модели тромбообразования для изучения возможности фармакологической коррекции нарушений свертывающей системы крови.
Поставленная задача решается путем введения самкам аутбредных мышей внутрибрюшинно цисплатина в максимально переносимой дозе (МПД) 10 мг/кг, самкам аутбредных крыс - 4 мг/кг. На 10 сутки после введения цитостатика осуществляют забор крови и анализ показателей активности коагуляционного звена гемостаза.
Новым в предлагаемом изобретении является то, что для постановки модели используются самки аутбредных мышей которым вводиться цисплатин МПД 10 мг/кг и самки аутбредных крыс, которым вводили по 4 мг/кг, а так же то, что показатели гемостаза анализируют на 10 сутки после введения цисплатина.
Новые признаки проявили в заявляемой совокупности новые свойства явным образом не вытекающие из уровня техники в данной области и неочевидные для специалиста. Идентичной совокупности признаков не обнаружено в патентной и научно -медицинской литературе.
Предлагаемый в качестве изобретения способ может быть использован для изучения возможности фармакологической коррекции нарушений свертывающей системы крови.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Изобретение будет понятно из следующего описания.
Самкам аутбредных мышей внутрибрюшинно вводят цисплатин в (МПД) 10 мг/кг, самкам аутбредных крыс - 4 мг/кг, затем на 10 сутки осуществляют забор крови и анализ показателей коагуляционного звена гемостаза.
Способ осуществляется следующим образом. Самкам аутбредных мышей внутрибрюшинно вводят цисплатин в МПД 10 мг/кг, самкам аутбредных крыс - 4 мг/кг, затем на 10 сутки осуществляют забор крови путем пункции сердца, в пластиковые пробирки с добавлением в качестве стабилизатора крови 3,8%-го раствора цитрата натрия в соотношении 9:1. Кровь центрифугируют для получения плазмы в течение 15 минут на 3000 об/мин. Далее осуществляют анализ показателей активности коагуляционного звена - активированное парциальное тромбопластиновое время (АПТВ), протромбиновое время (ПВ), международное нормализованное отношение (MHO), концентрация фибриногена на полуавтоматическом коагулометре Helena С-4 (Helena Biosciences Europe, Великобритания) с использованием реактивов фирмы «Технология-Стандарт» (г.Барнаул, Россия).
Достигаемый технический результат заключается в том, что введение цисплатина на 10 сутки вызывает значимые изменения в свертывающей системе крови, которые свидетельствуют о сдвиге параметров гемостаза в сторону тромбообразования.
Пример
При проведении экспериментов аутбредные мыши и крысы были распределены по группам:
1. Контроль мыши - аутбредные мыши, которым внутрибрюшинно вводили физиологический раствор по 0,5 мл.
2. Цисплатин мыши - аутбредные мыши, которым внутрибрюшинно вводили цисплатин в максимально переносимой дозе 10 мг/кг.
3. Контроль крысы - аутбредные крысы, которым внутрибрюшинно вводили физиологический раствор по 3 мл.
4. Цисплатин крысы - аутбредные крысы, которым внутрибрюшинно вводили цисплатин в максимально переносимой дозе 4 мг/кг.
Забор крови для исследования осуществляли в пластиковые пробирки путем пункции сердца. В качестве стабилизатора крови использовался 3,8% раствор цитрата натрия в соотношении 9:1. Кровь центрифугировали для получения плазмы в течение 15 минут на 3000 об/мин.
Исследование показателей системы коагуляционного гемостаза выполняли на поуавтоматическом коагулометре Helena С-4 (Helena Biosciences Europe, Великобритания) с использованием реактивов фирмы «Технология-Стандарт» (г.Барнаул, Россия). Показателями активности коагуляционного звена системы гемостаза явились: активированное парциальное тромбопластиновое время, протромбиновое время, международное нормализованное отношение, концентрация фибриногена.
Статистическую обработку полученных результатов проводили с использованием пакета программ. Межгрупповые различия были оценены с помощью непараметрического критерия Манна-Уитни. Различия определяются при 0,05% уровне достоверности и отражаются значком *.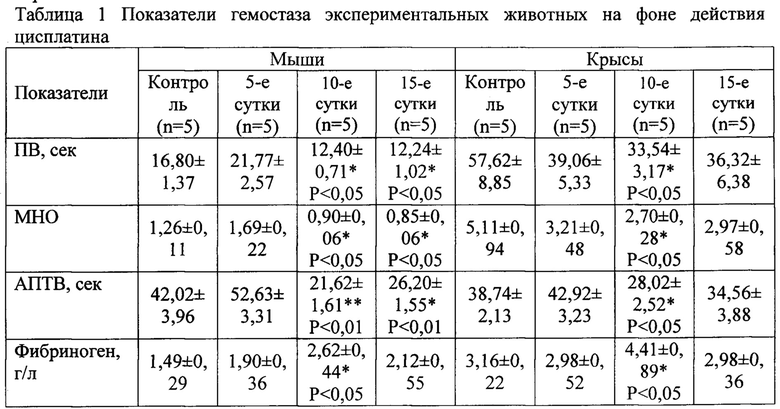
Примечание: Р<0,05 - *; Р<0,01 - ** при сравнении полученных данных у животных, получавших цисплатин с соответствующими значениями у контрольных животных.
В эксперименте на мышах-самках показано, что при внутрибрюшинном введении животным цисплатина в максимально переносимой дозе 10 мг/кг на 10-е и 15-е сутки исследования, отмечалось снижение протромбинового времени (на 26% и 27% Р<0,05), MHO (на 29% и 33% Р<0,05) и АПТВ (на 49% и 38% Р<0,01), повышение фибриногена на 10-е сутки (на 75% Р<0,05).
В эксперименте на крысах-самках показано, что при внутрибрюшинном введении животным цисплатина в максимально переносимой дозе 4 мг/кг на 10-е сутки исследования, отмечалось снижение протромбинового времени (на 42%, Р<0,05), MHO (на 47%, Р<0,05) и АПТВ (на 27%, Р<0,05), повышение фибриногена (на 40%, Р<0,05).
Способ обеспечивает приближенную к клиническим условиям картину тромбообразования при воспроизведении нарушений системы гемостаза вследствие применения противоопухолевых препаратов, и может быть использовано для моделирования и коррекции патологических состояний системы гемостаза.
Список литературы
1. Khorana A.A. Thromboembolism is a leading cause of death in cancer patients receiving outpatient chemotherapy / A.A. Khorana, C.W. Francis, E.Culakova // J. Thromb. Haemost, 2007. - Vol.5. - P. 632-634(632-633).
2. Птушкин В.В. Профилактика осложнений химиотерапии // Русский медицинский журнал. - 2004.- Т. 12. - №11. - 680-684 с (680).
3. Патент РФ №2570162, опубл. 10.12.2015.
4. Патент РФ №2610212, опубл. 08.02.2017.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования нарушений гемостаза при сочетанном поражении легких бактериальным воспалением и тромбозом легочных сосудов | 2023 |
|
RU2800645C1 |
| Способ коррекции гиперкоагуляционного состояния при введении противоопухолевого препарата цисплатина | 2020 |
|
RU2743848C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ КОАГУЛОПАТИИ У ЖИВОТНЫХ В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2746831C1 |
| Способ усиления противометастатического действия цисплатина и снижения его побочного действия на систему гемостаза | 2023 |
|
RU2825825C1 |
| СПОСОБ ПРОФИЛАКТИКИ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2023 |
|
RU2829177C2 |
| Способ коррекции тромбообразования резвератролом при ADMA-подобной модели преэклампсии | 2019 |
|
RU2722273C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ХРОНИЧЕСКОЙ ТОКСИЧЕСКОЙ КОАГУЛОПАТИИ У КРЫС | 2023 |
|
RU2800860C1 |
| Способ коррекции тромбообразования никорандилом при ADMA-подобной модели преэклампсии | 2019 |
|
RU2721291C1 |
| Способ моделирования хронической токсической коагулопатии у экспериментальных животных | 2017 |
|
RU2661722C1 |
| СПОСОБ КОРРЕКЦИИ НАРУШЕНИЙ ГЕМОСТАЗА У ДЕТЕЙ С ГЕМАНГИОМАМИ ПЕЧЕНИ | 2012 |
|
RU2483737C1 |
Изобретение относится к медицине, а именно к области воспроизведения болезней человека в эксперименте, и может быть использовано для моделирования нарушений свертывающей системы крови на фоне действия цитостатиков. Цисплатин вводят внутрибрюшинно однократно мышам по 10 мг/кг, крысам по 4 мг/кг, на 10 сутки после введения цисплатина забирают кровь и анализируют показатели активности коагуляционного звена гемостаза. Способ обеспечивает приближенную к клиническим условиям картину тромбообразования при воспроизведении нарушений системы гемостаза вследствие применения противоопухолевых препаратов за счет введения цисплатина. 1 табл.
Способ моделирования нарушений коагуляционного звена системы гемостаза, характеризующийся тем, что цисплатин вводят внутрибрюшинно однократно мышам по 10 мг/кг, крысам по 4 мг/кг, на 10 сутки после введения цисплатина забирают кровь и анализируют показатели активности коагуляционного звена гемостаза.
| СПОСОБ МОДЕЛИРОВАНИЯ ТРОМБООБРАЗОВАНИЯ У МЫШЕЙ ДЛЯ ОЦЕНКИ ДЕЙСТВИЯ ПРЕПАРАТОВ АНТИКОАГУЛЯНТА | 2014 |
|
RU2570162C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ТРОМБОЭМБОЛИИ ЛЕГОЧНОЙ АРТЕРИИ У КРЫС | 2015 |
|
RU2610212C1 |
| Способ моделирования ишемии миокарда | 1980 |
|
SU1045250A1 |
| Паровой котел | 1925 |
|
SU8832A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ | 2008 |
|
RU2359338C1 |
Авторы
Даты
2020-02-18—Публикация
2019-03-04—Подача