Изобретение относится к технологии производства медицинских иммунобиологических препаратов и может быть использовано в практике производства вакцины туляремийной живой сухой.
В настоящее время иммунизация является самым надежным способом профилактики туляремии.
Известна живая туляремийная вакцина Nik-sp. Francisella tularensis (Пат.2308969 РФ) [1], обладающая низкой реактогенностью, высокой стабильностью, возможностью использования стандартных сред и технологий для культивирования, хранения и приготовления. Однако для данной вакцины не раскрыт ни состав биофармацевтической композиции, ни способ получения готовой лекарственной формы.
Известна живая туляремийная вакцина 15 НИИЭГ F. tularensis и ее биофармацевтическая композиция (состав приведен на 1 мл):
активный компонент: клетки F. tularensis штамма 15 НИИЭГ - 20±10 млрд клеток;
и вспомогательные вещества:
сахароза - 0,099 г;
натрия глутамата моногидрат - 0,1485 г;
тиомочевина - 0,0495 г;
желатин - 0,099 г [2].
Данная вакцина используется в качестве средства специфической профилактики туляремии на территории России. Вакцина включена в Национальный календарь профилактических прививок по эпидемическим показаниям в соответствии с Приказом Минздрава России №229 от 27.06.2001 г.
Известен способ получения данной вакцины, который предусматривает получение посевных культур I, II и III генерации штамма F. tularensis 15 НИИЭГ, процесса накопления биомассы, необходимой для приготовления микробной взвеси определенной концентрации, последующим розливом, замораживанием, сублимационным высушиванием, герметизацией и упаковкой препарата, при этом количество микробных клеток в 1 мл готовой лекарственной формы препарата должно быть 20±10 млрд [2].
Известен способ получения концентрата микробных клеток для получения живой туляремийной вакцины (Патент 2528878 РФ) [3]. Однако лиофилизированная биофармацевтическая композиция, полученная по данному способу, после года хранения не соответствует нормативным требованиям по показателю «Процент живых микробных клеток». Было установлено, что значение данного показателя снижается до 30-35% к концу первого года и до 10-15% к концу второго года хранения при температуре 4°С [4].
Известно, что выживаемости клеток способствует заморозка до температуры меньше температуры эвтектики или стеклования; сохраняемость бактерий после высушивания определяется составом защитной среды, остаточной влажностью бактериального продукта, способом его герметизации и условиями хранения [5].
Известно, что хранение лиофилизированных микроорганизмов в условиях вакуума обеспечивает их большую выживаемость в сравнении с теми препаратами, которые были загерметизированы в первичной упаковке в условиях доступа атмосферного воздуха, а оптимальная остаточная влажность для хранения лиофилизатов бактерий составляет от 1 до 5% [6, 7].
Известна зависимость электрического сопротивления жидкости при ее замораживании и оттаивании [8].
Задачей изобретения является разработка способа получения лиофилизата живой туляремийной вакцины соответствующего нормативным требованиям Фармакопейной статьи ФС.3.3.1.0019.15 «Вакцина туляремийная живая» [2].
Технический результат заключается в реализации указанного назначения. Технический результат достигается тем, что смешивают подготовленные в необходимой концентрации клетки F. tularensis штамма 15 НИИЭГ и вспомогательные вещества при следующем соотношении компонентов (состав приведен на 1 мл):
клетки F. tularensis штамма 15 НИИЭГ - 10±5 млрд клеток;
трегалоза - 0,035 г;
реополиглюкин (декстран со средней молекулярной массой 30000-40000) - 0,0075 г;
хитозан - 0,0075 г,
полученную смесь разливают по 2 мл во флаконы, замораживают до температуры полного замерзания минус 35-45°С, выдерживают при ней 2-3 ч, осуществляют сублимационное высушивание при глубине вакуума (0,1±0,01) мbar со скоростью повышения температуры полок не более 5°С в час до температуры смеси 24-26°С, выдерживают при ней 1-2 ч, после чего герметизируют в условиях вакуума.
Для достижения технического результата разработаны состав вспомогательных веществ, соотношение компонентов лиофилизата и технологические режимы, обеспечивающие требуемое качество вакцины в условиях промышленного производства.
Клетки F. tularensis штамма 15 НИИЭГ получены известным способом (патент РФ 2528878) [3], согласно которому туляремийный микроб выращивают на питательной среде, содержащей, г/л: сухой ферментативный гидролизат фибрина, приготовленный из отхода производства антирабического иммуноглобулина 50-55, глюкозу 10, пантотенат кальция 0,05, содержание аминного азота не менее 320 мг %, при температуре 37°С в течение 20±2 часов с последующим концентрированием микробной массы путем микрофильтрации культуры туляремийного микроба через мембраны с размером пор 0,2 мкм в режиме тангенциального потока жидкости. Концентрирование микробной массы необходимо для получения достаточной концентрации живых микробных клеток F. tularensis штамма 15 НИИЭГ в готовой лекарственной форме вакцины. На этапе добавления среды высушивания концентрация микробной массы должна составлять 80±10 млрд клеток в 1 мл. Если концентрация клеток после проведения процедуры выращивания составляет большую величину, то концентрирование не проводят.
Вспомогательное вещество хитозан разрешен для применения в России в качестве пищевой добавки, трегалоза описана в качестве вспомогательного вещества в Европейской, Японской Фармакопеях, а реополиглюкин (декстран со средней молекулярной массой 30000-40000) зарегистрирован в РФ в качестве активной фармацевтической субстанции.
Замораживание на полках сублимационной сушильной установки до температуры полного замерзания и сублимационное высушивание при оптимальных технологических режимах (глубина вакуума, температурно-временные параметры нагрева туляремийной вакцины) позволяет обеспечить максимальную выживаемость клеток F. tularensis 15 НИИЭГ в процессе лиофилизации.
Герметизация в условиях вакуума лиофилизированных микроорганизмов позволяет обеспечить их большую выживаемость в сравнении с теми препаратами, которые при производстве были загерметизированы в первичной упаковке в условиях доступа атмосферного воздуха.
Возможность реализации заявляемого способа подтверждается примерами.
Пример 1. Приготовление лиофилизата вакцины туляремийной живой.
Взвешивают на весах хитозан в количестве 10,0 г, заливают 25 мМ калий-фосфатным буфером рН 8,0 в количестве 500 мл и оставляют на 30-40 мин для набухания при комнатной температуре. Затем раствор нагревают на слабом огне до полного растворения хитозана, добавляют навеску трегалозы (45 г) и 10% раствор реополиглюкина (100 мл). После полного растворения ингридиентов среду переливают в мерный цилиндр, доводят объем до 1 л тем же буфером и разливают по градуированным флаконам. Среду высушивания стерилизуют в паровом стерилизаторе водяным паром при (110±2)°С в течение 30 мин, давление (0,05±0,02) Мпа. Среда должна быть прозрачной или слегка опалесцирующей, без осадка, соломенно-желтоватого цвета. Стерильность среды проверяют путем выдерживания при температуре (37±1)°С в течение 48 ч.
Перед смешением компонентов вакцины флаконы, пробки и колпачки для флаконов моют проточной водой, затем кипятят в 0,1% растворе натрия углекислого кислого. После кипячения пробки и колпачки промывают проточной водой и кипятят в очищенной (дистиллированной) воде в течение 2 ч. Вымытые колпачки и пробки сушат в термостатной комнате при температуре (38,5±1,5)°С. Пробки стерилизуют насыщенным водяным паром при температуре (120±2)°С в течение 30 мин, давление (0,10±0,02) МПа в паровом стерилизаторе. Колпачки и флаконы стерилизуют горячим сухим воздухом при температуре (180±2)°С в течение 120 мин в воздушном стерилизаторе.
Живую культуру вакцинного штамма F. tularensis 15 НИИЭГ в концентрации 80±10 млрд микробных клеток в 2 см3 добавляют в среду высушивания в соотношении 1:4. Процесс смешения проводят за лабораторным столом с соблюдением правил асептики. После добавления компонентов проводят перемешивание смеси в течение 10-15 мин на шуттель-аппарате. В конечном итоге, в 2 см3 вакцины содержится 20±10 млрд микробных клеток F. tularensis 15 НИИЭГ, 0,068 г трегалозы, 0,015 г хитозана и 0,015 г реополиглюкина.
Фасовку препарата проводят с использованием автоматического дозатора во флаконы вместимостью 10,0 см3 по 2,0 см3 над пламенем спиртовки за лабораторным столом с соблюдением правил асептики. Во флаконы вставляют специальные пробки для лиофилизации таким образом, чтобы боковые прорези в пробках не перекрывались полностью горлышком флакона. По окончании фасовки флаконы передают на сушку.
За 3-4 ч до начала высушивания включают сублимационную сушильную установку Martin Christ Epsilon 2-6D. Конденсатор-вымораживатель охлаждают до температуры минус (65±5)°С, полки установки - до температуры минус (45±5)°С.
Флаконы с препаратом устанавливают на полки сублимационной сушильной установки, закрывают крышку и замораживают до температуры полного замерзания препарата минус (40±5)°С.При этой температуре препарат выдерживают в течение 2-3 ч. Затем включают вакуумный насос и создают остаточное давление в сушильной установке (0,1±0,01) мbаr. Через 1 ч после создания в сублиматоре сушильной установки указанного остаточного давления включают систему подогрева полок камеры. Процесс сублимации ведут от температуры минус (40±5)°С до (25±1)°С со скоростью повышения температуры полок не более 5°С в час. оптимальный температурно-временной режимы замораживания и лиофилизации в течение всего технологического процесса высушивания поддерживается благодаря онлайн контролю электрического сопротивления LyoRx в пределах 96-97% с использованием технологии Lyocontrol, разработанной специалистами немецкой компании «Мартин Крист» [9].
При достижении температуры препарата (25±1)°С его выдерживают 1-2 ч, флаконы герметизируют непосредственно в камере сушильной установки, используя винтовой прижиматель пробок, являющийся конструктивным элементом сушильной установки. После герметизации флаконов давление в установке выравнивают с атмосферным подачей воздуха через стерильный фильтр и влагопоглотитель (силикагель). Производят выгрузку флаконов и обкатку их алюминиевыми колпачками.
Закатанные флаконы с препаратом контролируют на наличие вакуума в соответствии с требованиями ОФС 1.8.1.0002.15 [10]. Проверка выявила соответствие контролируемого параметра требованиям ОФС 1.8.1.0002.15.
Полученный лиофилизат представляет собой пористую массу белого с желтоватым оттенком цвета. При растворении - гомогенную мутную суспензию белого с желтоватым оттенком цвета без посторонних примесей, осадка или хлопьев.
Пример 2. Проверка свойств лиофилизата вакцины туляремийной живой.
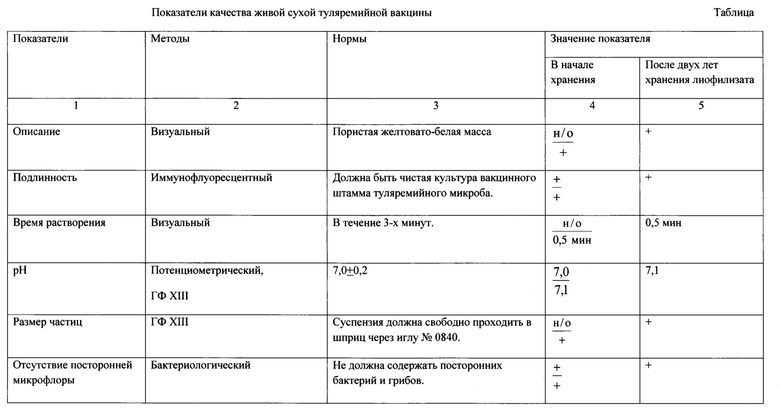
По заявленному способу был получен лиофилизат для приготовления серии вакцины туляремийной живой, проверены ее свойства в начале и после двух лет хранения в соответствии с требованиями нормативной документации [2]. Результаты проверки качества препаратов представлены в таблице, где «+» - соответствие нормативным показателям, «н/о» - не определяли, в числителе - значение показателей до высушивания, в знаменателе - после высушивания.
В полученных лиофилизатах не происходит ухудшения характеристик (в сравнении с культурой вакцинного штамма F. tularensis 15 НИИЭГ перед сублимационным высушиванием). Характеристики вакцины, нормируемые только для сухой формы, соответствуют нормативным требованиям. После двух лет хранения лиофилизаты также соответствуют требованиям нормативной документации [2].
Таким образом, заявляемый способ позволяет получить лиофилизат живой туляремийную вакцины, отвечающий требованиям Фармакопейной статьи ФС.3.3.1.0019.15 «Вакцина туляремийная живая».
ЛИТЕРАТУРА
1. Пат. 2308969 Российская Федерация, МПК А61К 39/02. Живая туляремийная вакцина Nik-sp. Francisella tularensis [Текст] / Н.Н. Кисличкин, О.И. Кисличкина; заявитель и патентообладатель. -№2006121120/15; заявл. 16.06.2006; опубл. 27.10.2007.
2. Вакцина туляремийная живая. Фармакопейная статья ФС.3.3.1.0019.15 / Государственная фармакопея Российской Федерации XIII издание (Том III). - М.: ФЭМБ. 2015. С. 952-957.
3. Пат. 2528878 Российская Федерация, МПК А61К 39/00. Способ получения концентрата микробных клеток для получения живой туляремийной вакцины [Текст] / О.А. Волох, А.В. Комиссаров, А.К. Никифоров, Ю.И. Самохвалова, Н.Г. Авдеева; заявитель и патентообладатель РосНИПЧИ «Микроб» - №2013129146/15; заявл. 25.06.2013; опубл. 20.09.2014.
4. Волох, О.А. Совершенствование технологии получения живой туляремийной вакцины [Текст] / О.А. Волох, А.В. Комиссаров, М.В. Антонычева и др. // Проблемы особо опасных инф. - 2016. - Вып.3. - С. 81-84.
5. Грачева, И.В. Механизмы повреждений бактерий при лиофилизации и протективное действие защитных сред [Текст] / И.В. Грачева, А.В. Осин // Проблемы особо опасных инф. - 2016. - Вып.3. - С. 5-12.
6. Похиленко, В.Д. Методы длительного хранения коллекционных культур микроорганизмов и тенденции развития [Текст] / В.Д. Похиленко, А.М. Баранов, К.В. Детушев // Известия высших учебных заведений. Поволжский регион. - 2009. - №4(12). - С. 99-118.
7. Матвеева, Е.В. Сохранение генофонда фитопатогенных бактерий методом лиофилизации [Текст] / Е.В. Матвеева // АГРО XXI. - 2007. - №10-12. - С. 28.-30.
8. Rey, L.R. Study of the freezing and drying of tissues at very low temperatures. In: Recent research in freezing and drying / L.R. Rey, edit, by A. Parkers, A. Smith. - Blackwell, Oxford, 1960.-P. 40-62.
9. Лиофилизаторы MARTIN CHRIST: надежная и быстрая сублимационная сушка [Текст] // Фармацевтическая отрасль. - 2010. - №5(22). - С. 48-52.
10. Иммунобиологические лекарственные препараты. Фармакопейная статья ОФС 1.8.1.0002.15 / Государственная фармакопея Российской Федерации XIII издание (Том I). - М.: ФЭМБ. 2015.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОТУЛЯРЕМИЙНОЙ ГИПЕРИММУННОЙ СЫВОРОТКИ И СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ЭРИТРОЦИТАРНОГО ТУЛЯРЕМИЙНОГО ИММУНОГЛОБУЛИНОВОГО СУХОГО | 2002 |
|
RU2240822C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНЦЕНТРАТА МИКРОБНЫХ КЛЕТОК ДЛЯ ПОЛУЧЕНИЯ ЖИВОЙ ТУЛЯРЕМИЙНОЙ ВАКЦИНЫ | 2013 |
|
RU2528878C1 |
| Способ длительного сохранения (консервирования) облигатно анаэробных бактерий высушиванием из замороженного состояния | 2023 |
|
RU2822476C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА НА ОСНОВЕ ВАКЦИННОГО ШТАММА ЧУМНОГО МИКРОБА | 2012 |
|
RU2510825C2 |
| УНИВЕРСАЛЬНАЯ СРЕДА ВЫСУШИВАНИЯ ДЛЯ СТАБИЛИЗАЦИИ ЭРИТРОЦИТАРНЫХ ДИАГНОСТИКУМОВ ТУЛЯРЕМИЙНЫХ | 2019 |
|
RU2708636C1 |
| ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ ГЛУБИННОГО КУЛЬТИВИРОВАНИЯ ТУЛЯРЕМИЙНОГО МИКРОБА | 2013 |
|
RU2518282C1 |
| ЖИВАЯ ТУЛЯРЕМИЙНАЯ ВАКЦИНА Nik-sp. Francisella tularensis | 2006 |
|
RU2308969C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИМИТАТОРОВ ПАТОГЕННЫХ БИОЛОГИЧЕСКИХ АГЕНТОВ | 2015 |
|
RU2607369C1 |
| ШТАММ БАКТЕРИЙ GALLIBACTERIUM ANATIS, ПРЕДНАЗНАЧЕННЫЙ ДЛЯ ПОЛУЧЕНИЯ МОНО- И ПОЛИВАЛЕНТНЫХ ИММУНОГЕННЫХ КОМПОЗИЦИЙ, НАПРАВЛЕННЫХ НА СПЕЦИФИЧЕСКУЮ ПРОФИЛАКТИКУ ГАЛЛИБАКТЕРИОЗА СЕЛЬСКОХОЗЯЙСТВЕННЫХ ПТИЦ | 2022 |
|
RU2787392C1 |
| ШТАММ Francisella tularensis 15/23-1ΔrecA СО СНИЖЕННОЙ РЕАКТОГЕННОСТЬЮ ДЛЯ СОЗДАНИЯ ЖИВОЙ ТУЛЯРЕМИЙНОЙ ВАКЦИНЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2014 |
|
RU2567810C2 |
Изобретение относится к технологии производства медицинских иммунобиологических препаратов и касается способа получения лиофилизата живой туляремийной вакцины. Для этого смешивают подготовленные в необходимой концентрации клетки F. tularensis штамма 15 НИИЭГ и вспомогательные вещества при следующем соотношении компонентов (состав приведен на 1 мл): клетки F. tularensis штамма 15 НИИЭГ - 10±5 млрд клеток; трегалоза - 0,034 г; реополиглюкин (декстран со средней молекулярной массой 30000-40000) - 0,0075 г; хитозан - 0,0075 г, полученную смесь разливают по 2 мл во флаконы, замораживают на полках сублимационной сушильной установки до температуры полного замерзания минус 35-45°С, выдерживают при ней 2-3 ч, осуществляют сублимационное высушивание при глубине вакуума (0,1±0,01) мбар со скоростью повышения температуры полок не более 5°С в час до температуры препарата 24-26°С, выдерживают при ней 1-2 ч, после чего герметизируют в условиях вакуума. Изобретение обеспечивает получение лиофилизата живой туляремийной вакцины, обеспечивающее требуемое качество вакцины. 1 табл., 1 пр.
Способ получения лиофилизата вакцины туляремийной живой, характеризующийся тем, что смешивают подготовленные в необходимой концентрации клетки F. tularensis штамма 15 НИИЭГ и вспомогательные вещества при следующем соотношении компонентов (состав приведен на 1 мл):
клетки F. tularensis штамма 15 НИИЭГ - 10±5 млрд клеток;
трегалоза - 0,034 г;
реополиглюкин (декстран со средней молекулярной массой 30000-40000) - 0,0075 г;
хитозан - 0,0075 г,
полученную смесь разливают по 2 мл во флаконы, замораживают на полках сублимационной сушильной установки до температуры полного замерзания минус 35-45°С, выдерживают при ней 2-3 ч, осуществляют сублимационное высушивание при глубине вакуума (0,1±0,01) мбар со скоростью повышения температуры полок не более 5°С в час до температуры препарата 24-26°С, выдерживают при ней 1-2 ч, после чего герметизируют в условиях вакуума.
| ЖИВАЯ ТУЛЯРЕМИЙНАЯ ВАКЦИНА Nik-sp. Francisella tularensis | 2006 |
|
RU2308969C1 |
| US 20070264233 A1, 15.11.2007 | |||
| Вакцина туляремийная живая | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| - М.: ФЭМБ | |||
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| С | |||
| Приспособление для автоматического перевода трамвайных стрелок | 1924 |
|
SU952A1 |
| Волох О.А | |||
| и др | |||
| Совершенствование технологии получения живой туляремийной вакцины // Проблемы особо опасных инф | |||
| - | |||
Авторы
Даты
2020-03-12—Публикация
2019-06-24—Подача