Положение относительно финансируемых из федерального бюджета исследований
Это изобретение выполнено при поддержке правительства Соединенных Штатов по грантам NIH 1R43AR061902-01 и 1P20RR20152-01; и грантам Министерства обороны ОС073102 и ОС 110218. Правительство обладает определенными правами на изобретение.
Сущность изобретения
Изобретение относится к новым способам культивирования стволовых клеток и терапии, и к композициям среды для культивирования для целей индукции, активации или примирования дискретных однородных фенотипов клеток для избирательной стимуляции или супрессии воспаления и иммунитета, предоставляя значительные преимущества по сравнению с известными средами и способами культивирования, используемыми в клеточной терапии. Изобретение можно использовать для получения более однородных и предсказуемых размноженных и индуцированных, примированных или активированных ex-vivo популяций мезенхимальных стволовых клеток (MSC), которые можно использовать для клеточной терапии. В данной области существует давно назревшая потребность в улучшенном способе для получения большого количества однородных и эффективных стволовых клеток, необходимых для клеточной терапии. Преимуществом различных вариантов осуществления изобретения является то, что их можно использовать для индукции, активации или примирования культур мезенхимальных стволовых клеток до однородных и дискретных фенотипов с предсказуемым поведением при введении пациенту.
В соответствии с конкретными вариантами осуществления в настоящем документе описана индукционная среда для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, где индукционная среда содержит: лиганд Toll-подобного рецептора 3 (TLR3), эритропоэтин и 0,5-2% кислород или миметик гипоксии, где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов. В соответствии с конкретными вариантами осуществления лиганд Toll-подобного рецептора 3 (TLR3) представляет собой поли(I:С). В соответствии с конкретными вариантами осуществления лиганд Toll-подобного рецептора 3 (TLR3) представляет собой поли(A:U). В соответствии с конкретными вариантами осуществления эритропоэтин присутствует в концентрации менее 10 нг/мл. В соответствии с конкретными вариантами осуществления миметик гипоксии представляет собой хлорид кобальта. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации между 5 мкМ и 500 мкМ. В соответствии с конкретными вариантами осуществления индукционная среда дополнительно содержит интерлейкин 4 (IL-4). В соответствии с конкретными вариантами осуществления индукционная среда дополнительно содержит интерлейкин 13 (IL-13). В соответствии с конкретными вариантами осуществления индукционная среда не содержит сыворотку, полученную от человека или животного. В соответствии с конкретными вариантами осуществления индукционная среда представляет собой концентрированный раствор. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток человека, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток собаки, кошки или лошади, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой, где в клетках отмечена увеличенная экспрессия мРНК CXCL9 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой, где в клетках отмечена увеличенная экспрессия мРНК OAS1 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой, где в клетках отмечена увеличенная экспрессия мРНК ISG15 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе описана композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную индукционной средой, где заболевание представляет собой воспалительное или аутоиммунное нарушение. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой ревматоидный артрит. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой воспалительное заболевание кишечника. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой острый неврит зрительного нерва. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой болезнь Краббе. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой диабетическую ретинопатию. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой болезнь Крона. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой острое повреждение легких.
В соответствии с конкретными вариантами осуществления в настоящем документе описана индукционная среда для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, где индукционная среда содержит: лиганд Toll-подобного рецептора 4 (TLR4), эритропоэтин и 0,5-2% кислорода или миметик гипоксии, где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает провоспалительными характеристиками, отмеченными экспрессией провоспалительных медиаторов. В соответствии с конкретными вариантами осуществления лиганд Toll-подобного рецептора 4 (TLR4) представляет собой липополисахарид (LPS). В соответствии с конкретными вариантами осуществления лиганд Toll-подобного рецептора 4 (TLR4) представляет собой аминоалкилглюкозаминид-4-фосфат.В соответствии с конкретными вариантами осуществления эритропоэтин присутствует в концентрации менее 10 нг/мл. В соответствии с конкретными вариантами осуществления миметик гипоксии представляет собой хлорид кобальта. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации между 5 мкМ и 500 мкМ. В соответствии с конкретными вариантами осуществления индукционная среда дополнительно содержит интерферон. В соответствии с конкретными вариантами осуществления индукционная среда дополнительно содержит фактор некроза опухолей альфа (TNFα). В соответствии с конкретными вариантами осуществления индукционная среда не содержит сыворотку, полученную от человека или животного. В соответствии с конкретными вариантами осуществления индукционная среда представляет собой концентрированный раствор. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток человека, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток собаки, кошки или лошади, обработанная индукционной средой. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой, где мезенхимальные стволовые клетки получены из плюрипотентных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе описана популяция мезенхимальных стволовых клеток, обработанная индукционной средой, где в клетках отмечена увеличенная экспрессия мРНК TNFSF10 (TRAIL) по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе описана композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную индукционной средой, где заболевание представляет собой злокачественную опухоль. В соответствии с конкретными вариантами осуществления злокачественная опухоль представляет собой рак яичника. В соответствии с конкретными вариантами осуществления злокачественная опухоль представляет собой увеальную меланому. В соответствии с конкретными вариантами осуществления в настоящем документе описана композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную индукционной средой, где заболевание представляет собой вызванное вирусом состояние. В соответствии с конкретными вариантами осуществления в настоящем документе описана композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную индукционной средой, где заболевание представляет собой бактериальную инфекцию.
В соответствии с конкретными вариантами осуществления в настоящем документе описана индукционная среда для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, где индукционная среда содержит: поли(I:С) в концентрации между 0,1 мкг/мл и 100 мкг/мл, эритропоэтин в концентрации менее 10 нг/мл, и хлорид кобальта в концентрации между 5 мкМ и 500 мкМ, где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками и отмечена увеличенной экспрессией мРНК CXCL9, OAS1 и ISG15 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток.
В соответствии с конкретными вариантами осуществления в настоящем документе описана индукционная среда для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, где индукционная среда содержит: LPS в концентрации между 0,1 нг/мл и 1 мкг/мл, эритропоэтин в концентрации менее 10 нг/мл, и хлорид кобальта в концентрации между 5 мкМ и 500 мкМ, где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает провоспалительными характеристиками и отмечена увеличенной экспрессией TNFSF10 (TRAIL) по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток.
В соответствии с конкретными вариантами осуществления в настоящем документе описан способ получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, где способ предусматривает: приведение нестимулированной популяции мезенхимальных стволовых клеток в контакт с композицией, содержащей: лиганд Toll-подобного рецептора 3 (TLR3), эритропоэтин и вызывающей гипоксию или содержащей миметик гипоксии, где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов. В соответствии с конкретными вариантами осуществления лиганд TLR3 представляет собой поли(I:С). В соответствии с конкретными вариантами осуществления лиганд TLR3 представляет собой поли(А:U). В соответствии с конкретными вариантами осуществления эритропоэтин присутствует в концентрации менее 10 нг/мл. В соответствии с конкретными вариантами осуществления миметик гипоксии представляет собой хлорид кобальта. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации между 5 мкМ и 500 мкМ. В соответствии с конкретными вариантами осуществления композиция дополнительно содержит интерлейкин 4 (IL-4). В соответствии с конкретными вариантами осуществления композиция дополнительно содержит интерлейкин 13 (IL-13). В соответствии с конкретными вариантами осуществления композиция не содержит сыворотку, полученную от человека или животного. В соответствии с конкретными вариантами осуществления композиция представляет собой концентрированный раствор. В соответствии с конкретными вариантами осуществления нестимулированную популяцию мезенхимальных стволовых клеток приводят в контакт с лигандом Toll-подобного рецептора 3, эритропоэтином и подвергают воздействию гипоксии или миметика гипоксии одновременно. В соответствии с конкретными вариантами осуществления композицию приводят в контакт с нестимулированной популяцией мезенхимальных стволовых клеток по меньшей мере на 30 минут, но менее чем на 8 часов. В соответствии с конкретными вариантами осуществления способ дополнительно предусматривает мониторирование экспрессии CXCL9 на уровне либо РНК, либо белка. В соответствии с конкретными вариантами осуществления способ дополнительно предусматривает мониторирование экспрессии OAS1 на уровне либо РНК, либо белка. В соответствии с конкретными вариантами осуществления способ дополнительно предусматривает мониторирование экспрессии ISG15 на уровне либо РНК, либо белка. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанных этим способом. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток человека, обработанная этим способом. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток собаки, кошки или лошади, обработанная этим способом. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом, где мезенхимальные стволовые клетки получены из плюрипотентных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом, где в клетках отмечена увеличенная экспрессия мРНК CXCL9 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом, где в клетках отмечена увеличенная экспрессия мРНК OAS1 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом, где в клетках отмечена увеличенная экспрессия мРНК ISG15 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе представлена композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную этим способом, где заболевание представляет собой воспалительное или аутоиммунное нарушение. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой ревматоидный артрит. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой воспалительное заболевание кишечника. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой острый неврит зрительного нерва. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой болезнь Краббе. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой диабетическую ретинопатию. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой болезнь Крона. В соответствии с конкретными вариантами осуществления воспалительное или аутоиммунное нарушение представляет собой острое повреждение легких.
В соответствии с конкретными вариантами осуществления в настоящем документе описан способ получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, где способ предусматривает: приведение нестимулированной популяции мезенхимальных стволовых клеток в контакт с композицией, содержащей: лиганд Toll-подобного рецептора 4 (TLR4), эритропоэтин и вызывающей гипоксию или содержащей миметик гипоксии, где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает провоспалительными характеристиками, отмеченными экспрессией провоспалительных или иммуносупрессивных медиаторов. В соответствии с конкретными вариантами осуществления лиганд TLR4 представляет собой липополисахарид (LPS). В соответствии с конкретными вариантами осуществления лиганд TLR4 представляет собой аминоалкилглюкозаминид-4-фосфат. В соответствии с конкретными вариантами осуществления эритропоэтин присутствует в концентрации 1 нг/мл. В соответствии с конкретными вариантами осуществления миметик гипоксии представляет собой хлорид кобальта. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации между 5 мкМ и 500 мкМ. В соответствии с конкретными вариантами осуществления композиция дополнительно содержит интерферон. В соответствии с конкретными вариантами осуществления композиция дополнительно содержит фактор некроза опухолей альфа (TNFα). В соответствии с конкретными вариантами осуществления композиция не содержит сыворотку, полученную от человека или животного. В соответствии с конкретными вариантами осуществления композиция представляет собой концентрированный раствор. В соответствии с конкретными вариантами осуществления нестимулированную популяцию мезенхимальных стволовых клеток приводят в контакт с лигандом Toll-подобного рецептора 4, эритропоэтином и подвергают воздействию гипоксии или миметика гипоксии одновременно. В соответствии с конкретными вариантами осуществления композицию приводят в контакт с нестимулированной популяцией мезенхимальных стволовых клеток по меньшей мере на 30 минут, но менее чем на 8 часов. В соответствии с конкретными вариантами осуществления способ дополнительно предусматривает мониторирование экспрессии TNFSF10 (TRAIL) на уровне либо РНК, либо белка. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток человека, обработанная этим способом. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток собаки, кошки или лошади, обработанная этим способом. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом, где мезенхимальные стволовые клетки получены из плюрипотентных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе представлена популяция мезенхимальных стволовых клеток, обработанная этим способом, где в клетках отмечена увеличенная экспрессия мРНК TNFSF10 (TRAIL) по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток. В соответствии с конкретными вариантами осуществления в настоящем документе представлена композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную этим способом, где заболевание представляет собой злокачественную опухоль. В соответствии с конкретными вариантами осуществления злокачественная опухоль представляет собой рак яичника. В соответствии с конкретными вариантами осуществления злокачественная опухоль представляет собой увеальную меланому. В соответствии с конкретными вариантами осуществления в настоящем документе представлена композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную этим способом, где заболевание представляет собой вызванное вирусом состояние. В соответствии с конкретными вариантами осуществления в настоящем документе представлена композиция для лечения заболевания, содержащая популяцию мезенхимальных стволовых клеток, обработанную этим способом, где заболевание представляет собой бактериальную инфекцию.
Полезность изобретения
Существует необходимость в улучшенных терапевтических способах и улучшенных способах культивирования клеток, и в среде для индукции, активации или примирования однородных популяций MSC - стволовых клеток, мезенхимальных стволовых клеток, стромальных клеток мозга, мультипотентных стромальных клеток, мультипотентных стволовых клеток - полученных из различных взрослых тканей. Клинические применения MSC требуют воспроизводимых способов культивирования клеток и способов размножения клеток, обеспечивающих адекватное количество клеток подходящего качества и соответствующие терапевтические преимущества. С различными средами и способами для культивирования добивались успеха в различной степени. Остается необходимость дальнейших улучшений среды и способов для культивирования MSC, обеспечивающих повышенные уровни примированных, активированных или индуцированных клеток, используемых в клеточной терапии, оказывающих безопасные и постоянно воспроизводимые терапевтические эффекты.
Активность или терапевтическое преимущество индуцированных, активированных или примированных MSC по сравнению с неиндуцированными общепринятыми MSC показано в доклинических моделях заболеваний. Терапия противовоспалительными индуцированными MSC облегчала боль и воспаление в моделях болезненной диабетической периферической невропатии, ревматоидного артрита, воспалительного заболевания кишечника и острого повреждения легких значительно улучшенным способом по сравнению с общепринятой терапией MSC. Кроме того, терапия противовоспалительными индуцированными MSC улучшала клинические показатели, походку и двигательные функции в доклинических моделях рассеянного склероза (ЕАЕ) и болезни Краббе. В модели рака яичника на иммунокомпетентных мышах, клеточная иммунотерапия проимунными противоопухолевыми индуцированными MSC приводила к ослаблению роста и распространения опухоли, в то время как общепринятая терапия MSC стимулировала рост и распространение опухоли.
Научное обоснование изобретения
Стимуляция Toll-подобных рецепторов (TLR) влияет на иммуномодулирующие ответы MSC. Toll-подобные рецепторы узнают сигналы «опасности», и их активация приводит к значительным клеточным и системным ответам, мобилизующим врожденные и адаптивные иммуноциты хозяина. Сигналы «опасности», которые запускают TLR, высвобождаются в ходе большинства патологий тканей. Поскольку сигналы опасности привлекают иммуноциты к участкам повреждения, авторы изобретения заключили, что MSC могут быть привлечены сходным образом. Авторы изобретения наблюдали, что MSC экспрессируют несколько TLR (например, TLR3 и TLR4, известных в данной области), и что на их миграцию, инвазию и секрецию иммуномодулирующих факторов существенно влияет привлечение специфических агонистов TLR. В частности, авторы изобретения наблюдали разнообразные последствия для MSC после стимуляции TLR3 по сравнению с TLR4 посредством способа кратковременного примирования низкими уровнями TLR. На основании этих обнаружений, авторы изобретения предложили новую парадигму для MSC, на основании информации из литературы о моноцитах. Конкретно, эти MSC можно поляризовать (индуцировать, активировать или примировать) посредством нижележащей передачи сигналов TLR на два однородных по действию фенотипа, классифицированных как MSC1 и MSC2. Примированные посредством TLR4 MSC, или MSC1, в основном экспрессируют проиммунные воспалительные медиаторы, в то время как примированные посредством TLR3 MSC, или MSC2, в основном экспрессируют противовоспалительные или иммуносупрессивные медиаторы. Кроме того, авторы изобретения показали, что совместное культивирование аллогенных (не собственных) MSC, примированных посредством TLR, с мононуклеарными клетками периферической крови (РВМС) предсказуемо приводит к активации супрессивных Т-лимфоцитов после совместного культивирования с MSC2 и к активации пермиссивных Т-лимфоцитов при совместном культивировании с MSC1. Индукция MSC до проиммунного фенотипа MSC1 посредством активации TLR4 или до противовоспалительного фенотипа MSC2 посредством активации TLR3 обеспечивает однородные и определенные клетки, что решает проблемы индустрии посредством предоставления определенных и предсказуемых клеток для применения в клеточной терапии.
Эритропоэтин, также известный как ЕРО, представляет собой гликопротеиновый гормон, контролирующий эритропоэз, или образование эритроцитов. Он представляет собой цитокин или передающую сигнал клеткам молекулу для предшественников эритроцитов (красных кровяных клеток) в костном мозге. ЕРО человека обладает молекулярной массой 34 кДа, и его называют также гематопоетин или гемопоэтин. ЕРО продуцируют интерстициальные фибробласты в почке в тесной ассоциации с перитубулярными капиллярами и эпителиальными канальцами и в перисинусоидальных клетках в печени. В то время как продукция в печени преобладает на ранних стадиях развития (в фетальном и перинатальном периоде), почка является преобладающим участком продукции ЕРО у взрослых. В дополнение к эритропоэзу, эритропоэтин обладает также другими известными биологическими функциями. Например, он играет важную роль в ответе головного мозга на повреждение нейронов посредством подачи способствующего выживанию сигнала против апоптоза (программируемой гибели клеток). ЕРО вовлечен также в процесс заживления ран. Синтетический эритропоэтин получают также способом рекомбинантной ДНК в культуре клеток. Кроме того, доступно несколько различных фармацевтических средств, подобных ЕРО, со множеством паттернов гликозилирования, и вместе их называют стимулирующими эритропоэз средствами (ESA). ЕРО используют по этому изобретению в качестве средства для предотвращения преждевременной гибели клеток и продления выживаемости полученных примированных, активированных или индуцированных клеток, используемых в клеточной терапии.
Постоянное снабжение кислородом является важным фактором, влияющим на все основные аспекты биологии клетки, включая выживаемость, пролиферацию, дифференцировку и миграцию. Как правило, клетки млекопитающих (не стволовые клетки) требуют постоянного снабжения кислородом для поддержания надежного производства энергии, и для сохранения нормального функционирования клетки и выживаемости клетки. В отличие от этого, стволовые клетки млекопитающих, по-видимому, размножаются и персистируют в гипоксическом окружении (с давлением кислорода в диапазоне от 0,5% до 7%) костного мозга. В нескольких исследованиях показано, что гипоксическое окружение необходимо для сохранения способности к пролиферации и самоподдержанию стволовых клеток в костном мозге. В частности, описаны эффекты пониженного давления кислорода даже после кратковременного культивирования MSC в качестве общего способа улучшения их способности к приживлению трансплантата в способах клеточной терапии. Гипоксическое окружение используют по этому изобретению в качестве средства для сохранения самоподдержания и пролиферативного потенциала полученных примированных, активированных или индуцированных клеток, используемых в клеточной терапии.
Определения и предпочтительные значения
Для ясного понимания, термины определены и предпочтительные значения указаны в настоящем документе, а также на всем протяжении текста, где необходимо.
Термин «злокачественная опухоль» обозначает любое заболевание, вызванное неконтролируемым делением клеток в части организма. Злокачественные опухоли включают в себя, но без ограничения, лейкоз, лимфому, меланому, карциному, саркому, аденому или любую другую злокачественную опухоль или неоплазию, вызванную генетическим, связанным с внешней средой или стохастическим механизмом.
Термин «стволовая клетка» обозначает клетку, способную давать начало множеству различных типов клеток. Термин «мезенхимальная стволовая клетка» или «MSC» обозначает стволовую клетку, первоначально происходящую из мезенхимы. Термин относится к клетке, способной к дифференцировке в по меньшей мере два или более из остеобласта, хондроцита, адипоцита или миоцита. MSC можно выделять из любого типа взрослой ткани. Как правило, MSC выделяют из костного мозга, жировой ткани, пуповины или периферической крови. В предпочтительном аспекте изобретения, MSC получают из костного мозга или липоаспиратов, которые сами получены из жировой ткани.
Термин «мультипотентная» и альтернативный термин «плюрипотентная» обозначает клетку, способную давать начало множеству различных типов клеток из линий клеток различных тканей. Термин «мультипотентная» или «плюрипотентная» включает в себя также индуцированные мультипотентные стволовые клетки или индуцированные плюрипотентные стволовые клетки, или клетки, индуцированные до стадии плюрипотентности с использованием любых химических или генетических средств. В соответствии с конкретными вариантами осуществления мультипотентные или плюрипотентные стволовые клетки по описанию представляют собой мезенхимальные стволовые клетки.
Клетки по этому описанию получены из любых клеток любых видов млекопитающих, включая человека, примата, собаку, кошку, лошадь, корову, козу, овцу и свинью. Клетка может представлять собой первичную клетку или иммортализованную линию клеток.
Термин «клеточная терапия» или «терапия на основе клеток» обозначает трансплантацию клеток человека или животного для предотвращения, лечения или облегчения одного или нескольких симптомов, ассоциированных с заболеванием или нарушением, например, но без ограничения, замену или репарацию поврежденных тканей или органов, модуляцию иммунных ответов и уменьшение симптомов воспаления и злокачественных опухолей.
Термин «субъект» относится к животному, предпочтительно, млекопитающему, включая не относящихся к приматам (например, корову, свинью, лошадь, кошку, собаку, крысу или мышь) или примата (например, обезьяну или человека). В предпочтительном варианте осуществления субъект представляет собой человека.
Термины «лечить», «лечение» и «подвергание лечению» при использовании непосредственно по отношению к пациенту или субъекту обозначает облегчение одного или нескольких симптомов, ассоциированных с нарушением, включая, но без ограничения, любую злокачественную опухоль, любую опухоль или неоплазию, воспалительное нарушение, аутоиммунное заболевание или иммунологически опосредованное заболевание, включая отторжение трансплантированных органов и тканей, где облегчение происходит в результате введения иммуномодулирующих клеток, полученных по изобретению, или фармацевтической композиции, содержащей иммуномодулирующие клетки, полученные по изобретению, субъекту, нуждающемуся в таком лечении.
Термин «нестимулированная» относится к популяции клеток, не подвергавшейся обработке, поляризации или индукции способами по этому описанию. Первичные выделенные мезенхимальные стволовые клетки, являющиеся свежими или замороженными, считают нестимулированными. Клетки, которые ранее обрабатывали с использованием соединения или композиции, лишенных по меньшей мере одного из лиганда toll-подобного рецептора, эритропоэтина, гипоксии или миметика гипоксии, считают нестимулированными.
Термины «подвергание репарации» и «репарация» при использовании непосредственно по отношению к поврежденным тканям обозначает облегчение такого повреждения посредством прямых механизмов, таких как регенерация поврежденной ткани, а также посредством непрямых механизмов, например, уменьшения воспаления, таким образом, позволяя формирование ткани.
«Аллогенный» означает происходящий из различных индивидуумов одного и того же вида. Когда индивидуумы обладают генами, отличающимися по одному или нескольким локусам, указывают, что они являются аллогенными. В отличие от этого, «аутологичный» означает происходящий из одного и того же индивидуума.
Термин «иммунное заболевание» относится к состоянию субъекта, характеризующемуся повреждением клеток, тканей и/или органов, вызванных иммунной реакцией субъекта.
Термин «аутоиммунное нарушение» относится к состоянию субъекта, характеризующемуся повреждением клеток, тканей и/или органов, вызванных иммунной реакцией субъекта на его собственные клетки, ткани и/или органы. Иллюстративные, неограничивающие примеры аутоиммунных заболеваний, которые можно лечить с использованием иммуномодулирующих клеток, полученных по изобретению, включают в себя очаговую алопецию, анкилозирующий спондилит, антифосфолипидный синдром, аутоиммунную болезнь Аддисона, аутоиммунные заболевания надпочечников, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунный оофорит и орхит, аутоиммунную тромбоцитопению, болезнь Бехчета, буллезный пемфигоид, кардиомиопатию, спру-целиакию-дерматит, синдром хронической усталости и иммунной дисфункции (CF1DS), хроническую воспалительную демиелинизирующую полиневропатию, синдром Черджа-Стросс, рубцовый пемфигоид, синдром CREST, болезнь холодовой агглютинации, дискоидную волчанку, эссенциальную смешанную криоглобулинемию, фибромиалгию-фибромиозит, гломерулонефрит, болезнь Грэйвса, синдром Гийена-Барре, тиреоидит Хашимото, идиопатический пульмонарный фиброз, идиопатическую тромбоцитопеническую пурпуру (ITP), IgA-невропатию, ювенильный артрит, красный плоский лишай, болезнь Меньера, смешанное заболевание соединительной ткани, рассеянный склероз, сахарный диабет 1 типа или иммуноопосредованный сахарный диабет, миастению, обыкновенную пузырчатку, пернициозную анемию, узелковый полиартериит, полихондрит, полигландулярные синдромы, ревматическую полимиалгию, полимиозит и дерматомиозит, первичную агаммаглобулинемию, первичный биллиарный цирроз, псориаз, псориатический артрит, феномен Рейно, синдром Рейтера, саркоидоз, склеродермию, прогрессирующий системный склероз, синдром Шегрена, синдром Гудпасчера, синдром мышечной скованности, системную красную волчанку, красную волчанку, артериит Такаясу, темпоральный артериит/гигантоклеточный артериит, язвенный колит, увеит, васкулиты, такие как герпетиформный дерматит-васкулит, витилиго, гранулематоз Вегенера, гломерулонефрит с образованием антител к базальной мембране, антифосфолипидный синдром, аутоиммунные заболевания нервной системы, семейную средиземноморскую лихорадку, миастенический синдром Ламберта-Итона, симпатическую офтальмию, полиэндокринопатию, псориаз и т.д.
«Иммунные нарушения» включают в себя аутоиммунные заболевания и иммунологически опосредованные воспалительные заболевания.
«Иммуноопосредованное воспалительное заболевание» обозначает любое заболевание, характеризующееся хроническим или острым воспалением, возникающее в результате дисрегуляции, ассоциированное с дисрегуляцией или запускаемое посредством дисрегуляции нормального иммунного ответа; например, болезнь Крона, сахарный диабет 1 типа, ревматоидный артрит, воспалительное заболевание кишечника, псориаз, псориатический артрит, анкилозирующий спондилит, системная красная волчанка, болезнь Хашимото, реакция трансплантат против хозяина, синдром Шегрена, пернициозная анемия, болезнь Аддисона, склеродермия, синдром Гудпасчера, язвенный колит, аутоиммунная гемолитическая анемия, бесплодие, миастения, рассеянный склероз, базедова болезнь, тромбоцитопеническая пурпура, синдром Гийена-Барре, аллергия, астма, атопическое заболевание, артериосклероз, миокардит, кардиомиопатия, гломерулонефрит, гипопластическая анемия и отторжение после трансплантации органов.
Термин «иммуномодулирующий» относится к модификации, амплификации, ингибированию или уменьшению одного или нескольких видов биологической активности иммунной системы, которые включают в себя, но без ограничения, отрицательную регуляцию иммунного ответа, усиление иммунных ответов и изменения воспалительных состояний, опосредованных изменениями цитокинового профиля, цитотоксической активности и продукции антител, и их эффектов на иммунные и связанные с иммунитетом клетки.
Термин «воспалительные нарушения» относится к состояниям субъекта, характеризующимся воспалением, например, хроническим воспалением. Иллюстративные, неограничивающие примеры воспалительных нарушений включают в себя, но без ограничения, острый неврит зрительного нерва, диабетическую невропатию, болезнь Краббе, острое повреждение легких, болезнь Крона, глютенчувствительную целиакию, ревматоидный артрит (RA), воспалительное заболевание кишечника (IBD), астму, энцефалит, хроническое обструктивное заболевание легких (COPD), воспалительный остеолиз, аллергические нарушения, септический шок, пульмонарный фиброз (например, идиопатический пульмонарный фиброз), воспалительные васкулиты (например, узелковый полиартериит, гранулематоз Вегнера, артериит Такаясу, височный артериит и лимфогранулематоз), постравматическую ангиопластику сосудов (например, рестеноз после ангиопластики), недифференцированную спондилоартропатию, недифференцированную артропатию, артрит, воспалительный остеолиз, хронический гепатит и хроническое воспаление, возникающее в результате хронических вирусных или бактериальных инфекций.
Термин «вызванное вирусом состояние» относится к любому заболеванию, вызванному вирусом. Подходящие заболевания включают в себя, но без ограничения: грипп, аденовирусные инфекции, респираторно-синцитиальную инфекцию, риновирусные инфекции, простой герпес, ветряную оспу (ветрянку), корь (коревую краснуху), германскую корь (краснуху), свинку (эпидемический паротит), черную оспу (натуральную оспу), болезнь Кавасаки, желтую лихорадку, лихорадку Денге, гепатит А, гепатит В, гепатит не-А/не-В, вирусный гастроэнтерит, вирусную лихорадку, цитомегаловирусную инфекцию, СПИД (ВИЧ), бешенство, полиомиелит, инфекцию вирусом Эбола, геморрагическую лихорадку, инфекцию вирусом Эпштейна-Барр и заболевание, включая злокачественные опухоли, вызванное вирусом, вызывающим любое из вышеперечисленных заболеваний.
Термин «бактериальная инфекция» относится к любой инфекции, вызванной важными с медицинской точки зрения бактериями, включая, но без ограничения, коклюш, лепру, туберкулез, синдром токсического шока, пищевое отравление, сальмонеллезную инфекцию, отравление, вызванное Е. coli, инфекцию Staphylococcus aureus, инфекцию Clostridium difficile, сепсис, болезнь Лайма, холеру, дизентерию и другие.
«Выделенная популяция клеток» обозначает популяцию клеток, выделенную из организма человека или животного, которая является в основном свободной от одной или нескольких других популяций клеток, в норме ассоциированных с этой популяцией клеток in vivo или in vitro.
Термин «индуктор лиганда» обозначает средство или средства, вызывающие увеличенную продукцию такого лиганда. Индуктор лиганда для лиганда Toll-подобного рецептора (TLR) приводит к увеличенному уровню лиганда TLR, и таким образом, по существу является эквивалентным собственно лиганду TLR.
Термин «МНС» (главный комплекс гистосовместимости) относится к подгруппе генов, кодирующих антигенпредставляющие белки поверхности клеток. У человека эти гены обозначают как гены лейкоцитарных антигенов человека (HLA). Сокращения МНС или HLA используют взаимозаменяемо.
Термин «популяция клеток» обозначает любое количество клеток, превышающее 1, однако, составляет по меньшей мере 1×103 клеток, по меньшей мере 1×104 клеток, по меньшей мере 1×105 клеток, по меньшей мере 1×106 клеток, по меньшей мере 1×107 клеток, по меньшей мере 1×108 клеток, или по меньшей мере 1×109 или более клеток. Популяция клеток относится также к клеткам, периодически образуемым при выращивании в биореакторах или в других промышленных способах, предназначенных для культивирования большого количества клеток
В предпочтительных вариантах осуществления этого изобретения, по меньшей мере 50%, по меньшей мере 55%, по меньшей мере 60%, по меньшей мере 65%, по меньшей мере 70%, по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 85%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94% или по меньшей мере 95% стволовых клеток (% от количества клеток) в исходной популяции клеток составляют недифференцированные MSC.
Термин «значительная экспрессия» или эквивалентные ему термины «положительный» и «+» при использовании по отношению к поверхностному маркеру клеток, означает, что в популяции клеток более 20%, предпочтительно, более 30%, 40%, 50%, 60%, 70%, 80%, 90% 95%, 98%, 99%, или даже 100% клеток экспрессируют поверхностный маркер клеток.
Экспрессию поверхностных маркеров клеток можно определять, например, посредством проточной цитометрии для специфического поверхностного маркера клеток с использованием общепринятых способов и устройств (например, системы BECKMAN COULTER EPICS XL FACS, используемой с коммерчески доступными антителами и стандартными протоколами, известными в данной области), показывающей сигнал для специфического поверхностного маркера клеток при проточной цитометрии выше фонового сигнала с использованием общепринятых способов и устройств. Фоновый сигнал определяют как интенсивность сигнала, получаемого посредством неспецифического антитела такого же изотипа, как специфическое антитело, используемое для детекции каждого поверхностного маркера в общепринятом анализе FACS. Чтобы считать маркер положительным, наблюдаемый специфический сигнал должен быть сильнее на 20%, предпочтительно, сильнее на 30%, 40%, 50%, 60%, 70%, 80%, 90%, 500%, 1000%, 5000%, 10000% или более, чем интенсивность фонового сигнала с использованием общепринятых способов и устройств. Кроме того, коммерчески доступные и известные моноклональные антитела против указанных поверхностных маркеров клеток (например, клеточных рецепторов и трансмембранных белков) можно использовать для идентификации соответствующих клеток.
Экспрессию мРНК определяют любым подходящим способом, включая, но без ограничения, массивы для анализа экспрессии генов (генные чипы), мРНК-SEQ, «нозерн»-блоттинг или полимеразную цепную реакцию (ПЦР), включая способы количественной ПЦР (кПЦР), включающие в себя использование обратной транскриптазы. Способы кПЦР включают в себя, но без ограничения: количественную оценку на основе зондов, например, TaqMan®; количественную оценку на основе красителей, например, SYBR green; цифровую ПЦР. Способ кПЦР может представлять собой способ с использованием оценки абсолютного количества, или способ относительной количественной оценки, требующий нормализации по генам домашнего хозяйства, таким как гены актина, GAPDH или рибосомальных субъединиц.
Включение в качестве ссылки
Содержание всех публикаций, патентов и патентных заявок, упомянутых в этом описании, включено в настоящий документ в качестве ссылки в той же степени, как если бы было конкретно и индивидуально указано, что содержание каждой индивидуальной публикации, патента или патентной заявки включено в качестве ссылки.
Краткое описание чертежей
На фиг. 1 показаны данные для экспрессии генов, полученные с использованием массива для ПЦР, для MSC, поляризованных, чтобы обладать противовоспалительными характеристиками, с использованием лиганда TLR3 поли(I:С). Серым обозначена по меньшей мере двукратная индукция экспрессии гена; черным обозначено двукратное снижение экспрессии гена; и толстыми рамками обозначены гены, обладающие более чем двукратной повышающей регуляцией и избранные для дальнейшего подтверждения (за исключением PIAS2, экспрессия которого была снижена по меньшей мере в два раза) на фиг. 2.
На фиг. 2 показано подтверждение избранных генов из эксперимента на фиг. 1 с использованием кПЦР (А и В). Планки погрешностей обозначают SEM.
На фиг. 3 показана индукция секреции IL-6 и IL-8 в клетках MSC после обработки лигандом TLR4 (MSC1) или лигандом TLR4 плюс ЕРО и хлорид кобальта (MSC1*).
На фиг. 4 показана индукция секреции CCL5 и CXCL10 в клетках MSC после обработки лигандом TLR3 (MSC2) или лигандом TLR3 плюс ЕРО и хлорид кобальта (MSC2*).
На фиг. 5 показана индукция фенотипа MSC1, по экспрессии TNFSF10 (TRAIL) в клетках MSC от различных доноров-людей, после обработки лигандом TLR4 (без*) или лигандом TLR4 плюс ЕРО и хлорид кобальта (с*).
На фиг. 6 показана индукция фенотипа MSC2, по экспрессии CXCL9 в клетках MSC от различных доноров-людей, после обработки лигандом TLR3 (без *) или лигандом TLR3 плюс ЕРО и хлорид кобальта (с *).
На фиг. 7 показана индукция экспрессии TNFSF10 (TRAIL) в клетках MSC с течением времени, для MSC после обработки лигандом TLR4 (MSC1) или лигандом TLR4 плюс ЕРО и хлорид кобальта (MSC1*).
На фиг. 8 показана индукция экспрессии CXCL9 в клетках MSC с течением времени, для MSC после обработки лигандом TLR3 (MSC2) или лигандом TLR3 плюс ЕРО и хлорид кобальта (MSC2*).
На фиг. 9 показан анализ миграции в системе transwell для MSC, которые являются нестимулированными (отрицательный контроль), по сравнению с MSC, стимулированными с использованием лиганда TLR4 (MSC1), лиганда TLR4 плюс ЕРО и хлорид кобальта (MSC1*), лиганда TLR3 (MSC2) и лиганда TLR3 плюс ЕРО и хлорид кобальта MSC2*). Планки погрешностей обозначают SEM.
На фиг. 10 показан анализ пролиферации/жизнеспособности клеток для MSC, которые являются нестимулированными (отрицательный контроль), по сравнению с MSC, стимулированными с использованием лиганда TLR4 (MSC1), лиганда TLR4 плюс ЕРО и хлорид кобальта(М8С1*), лиганда TLR3 (MSC2), и лиганда TLR3 плюс ЕРО и хлорид кобальта (MSC2*). Планки погрешностей обозначают SEM.
На ФИГ. 11 показано подтверждение анализа кПЦР для измерения экспрессии TNFSF10 (TRAIL): показан агарозный гель с продуктами амплификации ПЦР с праймерами для TNFSF10 (TRAIL).
На фиг. 12 (А) показана экспрессия CXCL9 с течением времени в MSC, поляризованных до MSC2; на (В) показан агарозный гель с продуктами амплификации ПЦР с праймерами для CXCL9.
Подробное описание изобретения
В практическом осуществлении этого изобретения применяют - за исключением собственно изобретения - общепринятые способы культивирования клеток, молекулярной биологии и микробиологии, находящиеся в компетенции специалистов в данной области.
Изобретение относится к индуцирующей, активирующей, поляризующей или примирующей индукционной среде для культивирования для популяции мезенхимальных стволовых клеток, содержащей лиганд Toll-подобного рецептора (TLR) или индуктор лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии, плюс дополнительные, стандартные компоненты среды для культивирования клеток, известные в данной области и описанные в настоящем документе.
Изобретение относится также к индукционной добавке к среде для культивирования, содержащей лиганд Toll-подобного рецептора (TLR) или индуктор лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии, которую можно добавлять в другие, существующие среды для культивирования. Такая добавка может являться пригодной, когда необычные компоненты или концентрации других компонентов являются пригодными в определенных условиях.
Изобретение относится также к герметично закрытому сосуду для культивирования, содержащему индукционную среду для культивирования или индукционную добавку к среде для культивирования по изобретению.
Изобретение относится также к способу получения индукционной среды для культивирования, как описано в настоящем документе, предусматривающему стадии: (а) получения среды для культивирования; и (b) добавления лиганда Toll-подобного рецептора (TLR) или индуктора лиганда TLR в комбинации с эритропоэтином (ЕРО) и воздействием гипоксии или миметика гипоксии к среде для культивирования.
Изобретение относится также к композиции, содержащей: (а) среду для культивирования по изобретению; и (b) стволовые клетки.
Изобретение относится также к композиции, содержащей: (а) среду для культивирования по изобретению; и (b) твердую поверхность. В соответствии с конкретными вариантами осуществления твердая поверхность представляет собой любую совместимую с культурой тканей поверхность, включая планшеты для культивирования тканей, колбы и бутыли любого размера для применения в 2D культуре клеток. В соответствии с конкретными вариантами осуществления твердая поверхность представляет собой микроноситель или любой другой поддерживающий матрикс для клеток, применяемый в 3D культуре.
Изобретение относится также к применению среды для культивирования по изобретению для индукции, активации или примирования популяции мезенхимальных стволовых клеток.
Изобретение относится также к способу индукции, активации или примирования ех-vivo популяции мезенхимальных стволовых клеток, предусматривающему: (а) получение популяции мезенхимальных стволовых клеток; (b) получение среды для культивирования по изобретению; (с) приведение стволовых клеток в контакт со средой для культивирования; и (d) культивирование клеток в подходящих условиях.
В одном из аспектов изобретение относится к применению лиганда Toll-подобного рецептора (TLR) или индуктора лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии в изготовлении лекарственного средства для клеточной терапии. Соответственно, в одном варианте осуществления изобретение относится также к способу изготовления лекарственного средства для клеточной терапии, предусматривающему: (а) получение популяции мезенхимальных стволовых клеток; (b) получение среды для культивирования по изобретению; (с) приведение стволовых клеток в контакт со средой для культивирования; и (d) культивирование клеток в подходящих условиях. Изобретение относится также к применению композиции, содержащей: (а) среду для культивирования по изобретению; и (b) стволовые клетки, для изготовления лекарственного средства для клеточной терапии. Изобретение относится также к применению композиции, содержащей: (а) среду для культивирования по изобретению; и (b) твердую поверхность, для изготовления лекарственного средства для клеточной терапии.
Указанные лекарственные средства можно использовать для лечения, репарации, профилактики, и/или улучшения поврежденных тканей, или одного или нескольких симптомов, ассоциированных с воспалительными и/или иммунными нарушениями, такими как, но без ограничения, аутоиммунные заболевания, воспалительные нарушения, и иммунологически опосредованные заболевания, включая отторжение трансплантированных органов и тканей и злокачественную опухоль. Лекарственное средство для клеточной терапии по изобретению содержит профилактически или терапевтически эффективное количество стволовых клеток и фармацевтический носитель. Особенно предпочтительными являются стволовые клетки мезенхимального происхождения. Примеры доз и режимов дозирования для каждого из этих типов клеток известны в данной области. Подходящие фармацевтические носители известны в данной области и предпочтительно представляют собой носители, одобренные федеральными регулирующими органами США или регулирующими органами штата, или перечисленные в Фармакопее США, или Европейской фармакопее, или в другой общепризнанной фармакопее для применения для животных, и более конкретно, для человека. Термин «носитель» относится к разбавителю, вспомогательному средству, наполнителю или переносчику, с которым вводят лекарственное средство. Композиция, если желательно, может содержать также незначительное количества забуферивающих pH средств. Примеры подходящих фармацевтических носителей описаны в «Remington's Pharmaceutical Sciences » от E W Martin. Такие композиции могут содержать профилактически или терапевтически эффективное количество профилактического или терапевтического средства, предпочтительно, в очищенной форме, вместе с подходящим количеством носителя, так чтобы обеспечивать форму для надлежащего введения субъекту. Состав должен соответствовать способу введения. В предпочтительном варианте осуществления лекарственные средства являются стерильными и находятся в подходящей форме для введения субъекту, предпочтительно, субъекту-животному, более предпочтительно, субъекту-млекопитающему, и наиболее предпочтительно, субъекту-человеку.
В соответствии с конкретными вариантами осуществления способы, клетки и индукционная среда по этому описанию предназначены для лечения острой боли или хронической боли. В соответствии с конкретными вариантами осуществления боль не является ассоциированной с конкретным диагнозом. В соответствии с конкретными вариантами осуществления боль является ассоциированной с травмой. В соответствии с конкретными вариантами осуществления боль представляет собой позвоночную боль. В соответствии с конкретными вариантами осуществления боль является ассоциированной с грыжей межпозвонкового диска или с дегенеративным заболеванием межпозвонковых дисков. В соответствии с конкретными вариантами осуществления боль является нейропатической. В соответствии с конкретными вариантами осуществления боль обусловлена ишиасом.
В соответствии с конкретными вариантами осуществления способы, клетки и индукционная среда по описанию предназначены для лечения злокачественной опухоли. В соответствии с конкретными вариантами осуществления способы, клетки и индукционная среда по этому описанию предназначены для лечения опухолей. В соответствии с конкретными вариантами осуществления способы, клетки и индукционная среда по этому описанию предназначены для дополнения лечения злокачественной опухоли. В соответствии с конкретными вариантами осуществления злокачественная опухоль представляет собой острый лимфобластный лейкоз, взрослых; острый лимфобластный лейкоз, детский; острый миелоидный лейкоз, взрослых; острый миелоидный лейкоз, детский; адренокортикальную карциному; ассоциированные со СПИД злокачественные опухоли; ассоциированную со СПИД лимфому; злокачественную опухоль анального канала; злокачественную опухоль аппендикса; астроцитомы; атипичную тератоидно-рабдоидную опухоль; базально-клеточную карциному; злокачественную опухоль желчного протока, за пределами печени; рак мочевого пузыря; злокачественную опухоль кости, остеосаркому и злокачественную фиброзную гистиоцитому; глиому ствола головного мозга; опухоль мозга; эмбриональные опухоли центральной нервной системы; астроцитомы; краниофарингиому; эпендимобластому; опухоль мозга, эпендимому; медуллобластому; медуллоэпителиому; опухоли паренхимы эпифиза с промежуточной дифференцировкой; супратенториальную примитивную нейроэктодермальную опухоль и пинеабластому; опухоли головного мозга и спинного мозга; рак молочной железы; рак молочной железы, у мужчин; опухоли бронхов; лимфому Беркитта; карциноидную опухоль; атипичную тератоидно-рабдоидную опухоль центральной нервной системы; эмбриональные опухоли центральной нервной системы; лимфому центральной нервной системы (ЦНС), рак шейки матки; первичный; рак шейки матки; детский рак; хордому; хронический лимфоцитарный лейкоз; хронический миелогенный лейкоз; хронические миелопролиферативные нарушения; рак толстого кишечника; колоректальный рак; краниофарингиому; Т-клеточную лимфому кожи; эмбриональные опухоли центральной нервной системы; рак эндометрия; эпендимобластому; эпендимому; рак пищевода; эстезионейробластому; опухоли семейства саркомы Юинга; экстракраниальную герминогенную опухоль; внегонадную герминогенную опухоль; злокачественную опухоль желчных протоков за пределами печени; злокачественную опухоль глаза, внутриглазную меланому; злокачественную опухоль глаза, ретинобластому; рак желчного пузыря; гастральную злокачественную опухоль (желудка); карциноидную опухоль желудочно-кишечного тракта; стромальную опухоль желудочно-кишечного тракта (GIST); герминогенные опухоли, экстракраниальные; герминогенные опухоли, внегонадные; герминогенные опухоли, яичников; гестационную трофобластическую опухоль; глиому; волосатоклеточный лейкоз; рак головы и шеи; злокачественную опухоль сердца; гепатоклеточную злокачественную опухоль (печени), взрослых (первичную); гепатоклеточную злокачественную опухоль (печени); гистиоцитоз, клеток Лангерганса; лимфому Ходжкина, взрослых; лимфому Ходжкина, детскую; гипофарингиальный рак; внутриглазную меланому; опухоль клеток островков поджелудочной железы (эндокринной ткани поджелудочной железы); саркому Капоши; рак почки (почечноклеточный); рак почки; гистиоцитоз клеток Лангерганса; рак гортани; рак гортани, детский; лейкоз, острый лимфобластный, взрослых; лейкоз, острый лимфобластный, детский; лейкоз, острый миелоидный, взрослых; лейкоз, острый миелоидный, детский; лейкоз, хронический лимфоцитарный; лейкоз, хронический миелогенный; лейкоз, волосатоклеточный; злокачественную опухоль губ и полости рта; рак печени, взрослых (первичный); рак печени; рак легкого, немелкоклеточный; рак легкого, мелкоклеточный; лимфому, ассоциированную со СПИД; лимфому, Беркитта; лимфому, Т-клеточную кожи; лимфому, Ходжкина, взрослых; лимфому, Ходжкина, детскую; лимфому, неходжкинскую, взрослых; Лимфому, неходжкинскую, детскую; лимфому, первичную центральной нервной системы (ЦНС); макроглобулинемию, Вальденстрема; злокачественную фиброзную гистиоцитому кости и остеосаркому; медуллобластому; медуллоэпителиому; меланому; меланому, внутриглазную (глаза); карциному из клеток Меркеля; мезотелиому, злокачественную, взрослых; мезотелиому; метастазирующую плоскоклеточную злокачественную опухоль шеи с неизвестной локализацией первичного очага; злокачественную опухоль ротовой полости; синдром множественных эндокринных неоплазий; множественную миелому/неоплазию плазматических клеток; фунгоидный микоз; миелодиспластические синдромы; миелодиспластические/миелопролиферативные неоплазий; миелогенный лейкоз, хронический; миелоидный лейкоз, взрослых, острый; миелоидный лейкоз, детский, острый; миелому, множественную; миелопролиферативные нарушения, хронические; злокачественную опухоль носовой полости и околоносовых пазух; рак носоглотки; нейробластому; неходжкинскую лимфому, взрослых; неходжкинскую лимфому, детскую; немелкоклеточный рак легкого; злокачественную опухоль полости рта; злокачественную опухоль полости рта и губ; рак ротоглотки; остеосаркому и злокачественную фиброзную гистиоцитому кости; рак яичника; эпителиальный рак яичника; герминогенные опухоли яичников; опухоль яичников с низким злокачественным потенциалом; рак поджелудочной железы; рак поджелудочной железы, опухоли клеток островков поджелудочной железы; папилломатоз; злокачественную опухоль околоносовых пазух и носовой полости; рак паращитовидной железы; рак полового члена; фарингеальный рак; опухоли паренхимы эпифиза с промежуточной дифференцировкой; опухоль гипофиза; неоплазию плазматических клеток/множественную миелому; плевролегочную бластому; рак молочной железы при беременности; первичную лимфому центральной нервной системы (ЦНС); рак предстательной железы; рак прямой кишки; почечноклеточный рак (почки); переходноклеточный рак почечной лоханки и мочеточника; злокачественную опухоль дыхательных путей с изменениями хромосомы 15; ретинобластому; рабдомиосаркому; злокачественную опухоль слюнной железы; злокачественную опухоль слюнной железы; саркому, опухоли семейства саркомы Юинга; саркому, Капоши; саркому мягких тканей, взрослых; саркому, мягких тканей, детскую; саркому, матки; синдром Сезари; рак кожи (не относящийся к меланоме); рак кожи; рак кожи (меланому); карциному кожи, из клеток Меркеля; мелкоклеточный рак легкого; злокачественную опухоль тонкого кишечника; саркому мягких тканей, взрослых; саркому мягких тканей, детскую; плоскоклеточную карциному; плоскоклеточную злокачественную опухоль шеи с неизвестной локализацией первичного очага, метастазирующую; злокачественную опухоль желудка (гастральную); супратенториальные примитивные нейроэктодермальные опухоли; Т-клеточную лимфому, кожи; рак яичка; злокачественную опухоль глотки; тимому и карциному тимуса; рак щитовидной железы; переходноклеточный рак почечной лоханки и мочеточника; трофобластическую опухоль, гестационную; карциному с неизвестной локализацией первичного очага; переходноклеточный рак мочеточника и почечной лоханки; злокачественную опухоль мочеиспускательного канала; рак тела матки, эндометриальный; саркому матки; увеальную меланому; рак влагалища; рак вульвы; макроглобулинемию Вальденстрема или опухоль Вильмса.
В соответствии с конкретными вариантами осуществления способы, клетки и индукционная среда по этому описанию предназначены для введения субъекту, нуждающемуся в лечении злокачественной опухоли, аутоиммунного нарушения или воспалительного нарушения. В конкретных вариантах осуществления, способы для клеток и индукционной среды по этому описанию включают в себя различные способы введения. В соответствии с конкретными вариантами осуществления способы введения представляют собой подкожное, интрапариетальное, внутримышечное, внутривенное введение, введение внутрь опухоли, внутриглазное введение, введение в сетчатку, в стекловидное тело или интракраниальное введение.
В соответствии с конкретными вариантами осуществления способы, клетки и индукционная среда по этому описанию предназначены для введения субъекту, нуждающемуся в лечении злокачественной опухоли, аутоиммунного нарушения или иммуноопосредованного воспалительного заболевания. В конкретных вариантах осуществления, способы для клеток и индукционной среды по этому описанию включают в себя различную частоту дозирования. В соответствии с конкретными вариантами осуществления клетки и лекарственные средства по этому описанию вводят один раз в сутки, один раз в неделю, один раз в месяц или один раз в год. В соответствии с конкретными вариантами осуществления клетки и способы по этому описанию применяют дважды в сутки, дважды в неделю, дважды в месяц или дважды в год. В соответствии с конкретными вариантами осуществления клетки и способы по этому описанию применяют три раза в сутки, три раза в неделю, три раза в месяц или три раза в год. В соответствии с конкретными вариантами осуществления клетки и способы по этому описанию предназначены для применения четыре раза в сутки, четыре раза в неделю, четыре раза в месяц или четыре раза в год. В соответствии с конкретными вариантами осуществления за первичным лечением следует поддерживающая доза 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 раз в год. В соответствии с конкретными вариантами осуществления введение поддерживающей дозы продолжают в течение по меньшей мере 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более лет. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 1×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 2×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 3×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 4×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 5×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 6×106 клеток на дозу. В соответствии с конкретными вариантами осуществления клетки вводят. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 7×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 8×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 9×106 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 1×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 2×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 3×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 4×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 5×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 6×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 7×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 8×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 9×107 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 1×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 2×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 3×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 4×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 5×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 6×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 7×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 8×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 9×108 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 1×109 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 2×109 клеток на дозу. В соответствии с конкретными вариантами осуществления вводят по меньшей мере 3×109 клеток на дозу.
Лекарственное средство по изобретению может находиться во множестве форм. Они включают в себя, например, полутвердые и жидкие лекарственные формы, такие как лиофилизированные препараты, жидкие растворы или суспензии, пригодные для инъекции и пригодные для инфузии растворы и т.д., лекарственное средство предпочтительно является пригодным для инъекции.
В соответствии с конкретными вариантами осуществления лекарственные средства предназначены для лечения или репарации поврежденной ткани (предпочтительно, мезенхимальной ткани), и/или для лечения, модуляции, профилактики и/или облегчения одного или нескольких симптомов, ассоциированных с воспалительными и/или иммунными нарушениями. Соответственно, способы и клетки по изобретению являются пригодными для лечения любого нарушения, характеризующегося любым или всеми из указанных симптомов. Репрезентативный не исчерпывающий список таких нарушений представлен в разделе определения. Особенно предпочтительным является лекарственное средство для лечения иммуноопосредованных воспалительных заболеваний. Кроме того, предпочтительным является лекарственное средство для лечения сахарного диабета, ревматоидного артрита (RA), воспалительного заболевания кишечника (IBD, включая болезнь Крона и/или язвенный колит) и рассеянного склероза (MS). Изобретение относится также к применению лиганда Toll-подобного рецептора (TLR) или индуктора лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии для культивирования мезенхимальных стволовых клеток.
Конкретные ингредиенты и соотношения ингредиентов среды для культивирования, добавок и композиций по изобретению можно менять в соответствии с конкретной необходимостью и применениями. Подобным образом, точные стадии способов по изобретению можно менять в соответствии с конкретной необходимостью и применениями. Среду для культивирования, добавки, способы, композиции и применения по этому изобретению можно оптимизировать посредством общепринятых экспериментов. Например, если желательным исходом является противовоспалительный терапевтический эффект, тогда среда для культивирования, добавка или композиция специально содержат лиганд TLR3 или индуктор лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина) в отличие от этого, если желательным исходом является проиммунный терапевтический эффект, тогда среда для культивирования, добавка или композиция специально содержат лиганд TLR4 или индуктор лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии. Количество каждого из ингредиентов, описанных в настоящем документе, можно оптимизировать независимо от других ингредиентов посредством общепринятой оптимизации, или один или несколько ингредиентов можно добавлять или удалять. Среду для культивирования можно тестировать по ее способности поддерживать индукцию, активацию или примирование мезенхимальных стволовых клеток, посредством ее тестирования параллельно с известной средой для культивирования или способом или вместо них. Среда для культивирования, добавки, способы, композиции и применения по изобретению более подробно описаны ниже.
Индукционная среда по изобретению содержит лиганд Toll-подобного рецептора (TLR) или индуктор лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии. В одном из аспектов индукционная среда по изобретению содержит лиганд Toll-подобного рецептора (TLR) или индуктор лиганда TLR. В альтернативном аспекте индукционная среда по изобретению содержит эритропоэтин и оказывает воздействие гипоксии или миметика гипоксии. В следующем аспекте индукционная среда по изобретению содержит лиганд Toll-подобного рецептора (TLR) или индуктор лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии. В соответствии с конкретными вариантами осуществления лиганд TLR представляет собой лиганд TLR4. В соответствии с конкретными вариантами осуществления лиганд TLR представляет собой лиганд TLR3.
Индукционная среда по изобретению может содержать две или более, три или более, 4-, 5-, 6-, 7-, 8-, 9-, 10- или более, комбинаций лиганда Toll-подобного рецептора (TLR) или индуктора лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии.
Индукционная среда по изобретению может содержать между приблизительно 0,10 пикомолярным (пМ) и приблизительно 100 миллимолярным (мМ) количеством лиганда TLR или индуктора лиганда TLR в комбинации с между приблизительно 0,5 мед./мл и приблизительно 100 мед./мл эритропоэтина (ЕРО) и с воздействием условий от приблизительно 0,5 до приблизительно 2% кислорода (гипоксии) или миметика гипоксии, такого как хлорид кобальта или дезферриоксамин, в концентрации приблизительно от 10 микромолярной до приблизительно 1 мМ, или любую другую комбинацию вышеуказанного лиганда TLR или индуктора лиганда TLR, эритропоэтина и гипоксии.
Лиганд TLR3, используемый в индукционной среде для культивирования, может представлять собой IL4, IL13, поли(А:Ц), поли(I:С), и их сочетания, и его можно доставлять посредством инкубации, трансфекции, трансдукции, посредством молекул носителя или посредством их сочетания. Предпочтительно, лиганд или агонист TLR3 представляет собой поли(I:С).
Лиганд TLR4, используемый в индукционной среде для культивирования, может представлять собой аминоалкилглюкозаминид-4-фосфаты, интерфероны, TNF-альфа, GM-CSF, липополисахарид (LPS), и их сочетания, и его можно доставлять посредством инкубации, трансфекции, трансдукции, посредством молекул носителя или посредством их сочетания. Предпочтительно, лиганд или агонист TLR4 представляет собой LPS.
Лиганд или агонист TLR3 можно предоставлять в количестве от приблизительно 10 пг/мл до приблизительно 100 мкг/мл, от приблизительно 100 пг/мл до приблизительно 100 мкг/мл, от приблизительно 1 нг/мл до приблизительно 100 мкг/мл, от приблизительно 5 нг/мл до приблизительно 100 мкг/мл, от приблизительно 10 нг/мл до приблизительно 100 мкг/мл, от приблизительно 100 нг/мл до приблизительно 100 мкг/мл, от приблизительно 0,1 мкг/мл до приблизительно 50 мкг/мл, от приблизительно 0,1 мкг/мл до приблизительно 10 мкг/мл, от приблизительно 0,25 мкг/мл до приблизительно 7,5 мкг/мл, приблизительно от 0,5 мкг/ мл до приблизительно 5 мкг/мл, от приблизительно 1 мкг/мл до приблизительно 2,5 мкг/мл, и предпочтительно, от приблизительно 1 мкг/мл до приблизительно 1,5 мкг/мл в среде для культивирования или добавке, как указано выше.
В соответствии с конкретными вариантами осуществления лиганд TLR3 представляет собой поли(I:С) и предоставлен в количестве от приблизительно 10 пг/мл до приблизительно 100 мкг/мл, от приблизительно 100 пг/мл до приблизительно 100 мкг/мл, от приблизительно 1 нг/мл до приблизительно 100 мкг/мл, от приблизительно 5 нг/мл до приблизительно 100 мкг/мл, от приблизительно 10 нг/мл до приблизительно 100 мкг/мл, от приблизительно 100 нг/мл до приблизительно 100 мкг/мл, от приблизительно 0,1 мкг/мл до приблизительно 50 мкг/мл, от приблизительно 0,1 мкг/мл до приблизительно 10 мкг/мл, от приблизительно 0,25 мкг/мл до приблизительно 7,5 мкг/мл, приблизительно от 0,5 мкг/ мл до приблизительно 5 мкг/мл, от приблизительно 1 мкг/мл до приблизительно 5 мкг/мл, и от приблизительно 1 мкг/мл до приблизительно 2,5 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 1 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 2 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 3 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 4 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 5 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 6 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 7 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 8 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 9 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве приблизительно 10 мкг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве менее приблизительно 100 нг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве менее приблизительно 50 нг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве менее приблизительно 20 нг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве менее приблизительно 10 нг/мл. В соответствии с конкретными вариантами осуществления поли(I:С) предоставлен в количестве менее приблизительно 50 нг/мл.
Лиганд или агонист TLR4 можно предоставлять в количестве от приблизительно 10 пг/мл до приблизительно 10 мкг/мл, от приблизительно 100 пг/мл до приблизительно 10 мкг/мл, от приблизительно 1 нг/мл до приблизительно 1 мкг/мл, от приблизительно 5 нг/мл до приблизительно 1 мкг/мл, от приблизительно 10 нг/мл до приблизительно 1 мкг/мл, от приблизительно 100 нг/мл до приблизительно 1 мкг/мл, предпочтительно от приблизительно 5 нг/мл до приблизительно 50 нг/мл, а также предпочтительно от приблизительно 5 нг/мл до приблизительно 25 нг/мл в среде для культивирования или добавке, как указано выше.
В соответствии с конкретными вариантами осуществления лиганд TLR4 представляет собой LPS. В соответствии с конкретными вариантами осуществления LPS присутствует в количестве от приблизительно 10 пг/мл до приблизительно 10 мкг/мл, от приблизительно 100 пг/мл до приблизительно 10 мкг/мл, от приблизительно 1 нг/мл до приблизительно 1 мкг/мл, от приблизительно 5 нг/мл до приблизительно 1 мкг/мл, от приблизительно 10 нг/мл до приблизительно 1 мкг/мл, от приблизительно 100 нг/мл до приблизительно 1 мкг/мл, предпочтительно, от приблизительно 5 нг/мл до приблизительно 50 нг/мл, а также предпочтительно, от приблизительно 5 нг/мл до приблизительно 25 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 5 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 10 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 15 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 20 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 25 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 30 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 35 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 40 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 45 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации приблизительно 50 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации менее приблизительно 100 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации менее приблизительно 50 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации менее приблизительно 20 нг/мл. В соответствии с конкретными вариантами осуществления LPS присутствует в концентрации менее приблизительно 10 нг/мл.
В соответствии с конкретными вариантами осуществления индукционная среда для культивирования по изобретению обеспечивает инкубацию в гипоксическом окружении или в окружении с истощенным кислородом. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает менее 2% кислорода. В соответствии с конкретными вариантами осуществления а гипоксическое окружение обладает менее 1,5% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает менее 1,0% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает менее 0,5% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает эффективной концентрацией 0% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает от 0,5% до 2,0% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает от 0,5% до 1,5% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает от 0,5% до 1,0% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает от 1,0% до 2,0% кислорода. В соответствии с конкретными вариантами осуществления гипоксическое окружение обладает от 1,5% до 2,0% кислорода.
В соответствии с конкретными вариантами осуществления индукционная среда для культивирования по изобретению содержит хлорид кобальта. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 50 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 100 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 200 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 400 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 500 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 600 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 700 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 800 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 900 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно 1 мМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 10 мкМ до приблизительно 1 мМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации приблизительно от 10 мкМ приблизительно 800 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 10 мкМ до приблизительно 500 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 10 мкМ до приблизительно 400 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 10 мкМ до приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 50 мкМ до приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 100 мкМ до приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления хлорид кобальта присутствует в концентрации от приблизительно 150 мкМ до приблизительно 300 мкМ.
В соответствии с конкретными вариантами осуществления индукционная среда для культивирования по изобретению содержит дезферриоксамин. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 50 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 200 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 400 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 500 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 600 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 700 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 800 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 900 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации приблизительно 1 мМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 10 мкМ до приблизительно 1 мМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 10 мкМ до приблизительно 800 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 10 мкМ до приблизительно 500 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 10 мкМ до приблизительно 400 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 10 мкМ до приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 50 мкМ до приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 100 мкМ до приблизительно 300 мкМ. В соответствии с конкретными вариантами осуществления дезферриоксамин присутствует в концентрации от приблизительно 150 мкМ до приблизительно 300 мкМ.
В соответствии с конкретными вариантами осуществления индукционная среда для культивирования по изобретению по изобретению содержит эритропоэтин. В соответствии с конкретными вариантами осуществления индукционная среда для культивирования по изобретению содержит рекомбинантный эритропоэтин. В соответствии с конкретными вариантами осуществления индукционная среда для культивирования по изобретению содержит рекомбинантный человеческий эритропоэтин. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,1 нг/мл и приблизительно 1,0 мг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,1 нг/мл и приблизительно 100 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,1 нг/мл и приблизительно 50 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,1 нг/мл и приблизительно 10 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,1 нг/мл и приблизительно 1,0 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,2 нг/мл и приблизительно 0,8 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет между приблизительно 0,3 нг/мл и приблизительно 0,6 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 10 мг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 5 мг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 1 мг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 100 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 30 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 10 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 5 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 4 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 1 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 0,8 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 1 нг/мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 5 ед./мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 1 ед./мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 0,5 ед./мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 0,1 ед./мл. В соответствии с конкретными вариантами осуществления количество эритропоэтина составляет менее 0,05 ед./мл.
Индукционная среда для клеток, как правило, содержит большое количество ингредиентов, необходимых для обеспечения поддержания культивируемых клеток. Индукционная среда по изобретению, таким образом, в норме содержит множество других ингредиентов в дополнение к лиганду Toll-подобного рецептора (TLR) или индуктору лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина). Специалист в данной области может легко составлять подходящие комбинации ингредиентов, учитывая следующее описание. Индукционная среда по изобретению, как правило, представляет собой раствор питательных веществ, содержащий стандартные для культивирования клеток ингредиенты, такие как аминокислоты, витамины, металлы в следовых количествах, неорганические соли, углеродный источник энергии и буфер, как более подробно описано ниже.
Индукционная среда по изобретению может содержать сыворотку. Сыворотка содержит клеточные и внеклеточные факторы и компоненты, которые могут являться необходимыми для жизнеспособности и размножения. Можно использовать сыворотку, полученную из любого подходящего источника, включая эмбриональную бычью сыворотку (FBS), бычью сыворотку (BS), телячью сыворотку (CS), эмбриональную телячью сыворотку (FCS), сыворотку новорожденных телят (NCS), козью сыворотку (GS), лошадиную сыворотку (HS), свиную сыворотку, овечью сыворотку, кроличью сыворотку, крысиную сыворотку (RS) и т.д. В объем изобретения включено также то, что если указанные MSC имеют человеческое происхождение, индукционную среду для клеток дополняют человеческой сывороткой, предпочтительно, аутологичного происхождения. Понятно, что сыворотку можно инактивировать нагреванием при 55-65°C, если кажется необходимым инактивировать компоненты каскада реакций комплемента. Когда используют заменитель сыворотки, его можно использовать в количестве между приблизительно 2% и приблизительно 40% от объема среды, в соответствии с общепринятыми способами.
В других вариантах осуществления индукционная среда по изобретению может содержать заменитель сыворотки. Различные варианты составов заменителей сыворотки являются коммерчески доступными и известными специалисту в данной области, такие как, но без ограничения, сывороточный альбумин, сывороточный трансферрин, селен и рекомбинантные белки, включая, но без ограничения, инсулин, фактор роста тромбоцитов (PDGF) и основной фактор роста фибробластов (bFGF). Когда используют заменитель сыворотки, его можно использовать в количестве между приблизительно 2% и приблизительно 40% от объема среды, в соответствии с общепринятыми способами. В других вариантах осуществления индукционная среда по изобретению может являться бессывороточной и/или не содержать заменителя сыворотки. Бессывороточная среда представляет собой среду, не содержащую сыворотки животного никакого типа. Бессывороточная среда может являться предпочтительной, чтобы избегать возможной ксеноконтаминации стволовых клеток. Не содержащая заменителя сыворотки среда представляет собой среду, не дополненную никаким коммерческим составом заменителя сыворотки.
Индукционную среду по изобретению в норме можно составлять на деионизированной, дистиллированной воде. Индукционную среду по изобретению, как правило, стерилизуют перед использованием для предотвращения контаминации, например, посредством ультрафиолетового света, нагревания, радиоактивного облучения или фильтрации. Индукционную среду можно замораживать (например, при -20°C или -80°C) для хранения или транспортировки. Противомикробные средства также, как правило, используют в среде для уменьшения бактериальной, микоплазменной и грибковой контаминации. Среда может содержать одно или несколько противомикробных средств или антибиотиков для предотвращения контаминации. Как правило, используемые антибиотики или противогрибковые соединения представляют собой смеси пенициллина/стрептомицина, но могут также включать в себя, но без ограничения, амфотерицин (Фунгизон®), ампициллин, гентамицин, блеомицин, гигромицин, канамицин, митомицин и т.д.
В одном варианте осуществления изобретения среда для культивирования представляет собой среду, кондиционированную посредством добавления клеток, индуцированных посредством лиганда Toll-подобного рецептора (TLR) или индуктора лиганда TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина). Кондиционированную среду получают посредством культивирования популяции указанных клеток в индукционной среде в течение периода времени, достаточного для кондиционирования среды, затем сбора кондиционированной среды. Когда используют кондиционированную среду, среду можно кондиционировать на клетках млекопитающих, например, клетках мыши или клетках человека. Множество различных типов клеток млекопитающих можно использовать для получения кондиционированной среды, пригодной для индукции мезенхимальных стволовых клеток.
Индукционная среда может иметь 1х состав или концентрированный состав, например, 2х-250х концентрированный состав среды. В 1х составе каждый ингредиент в среде присутствует в концентрации, предназначенной для индукции клеток. В концентрированном составе один или несколько ингредиентов присутствуют в более высокой концентрации, чем предназначено для индукции клеток. Индукционную среду можно концентрировать с использованием известных способов, например, осаждение солью или избирательная фильтрация. Концентрированную среду можно разводить для применения водой (предпочтительно, деионизированной и дистилированной) или любым пригодным раствором, например, водно-солевым раствором, водным буфером или средой для культивирования.
Индукционная среда, как описано в настоящем документе, может являться способной к индукции, активации или примированию популяции стволовых клеток в мультипотентом, недифференцированном и пролиферативном состоянии в течение только единственного пассажа или удвоения популяции в подходящих условиях. Стволовые клетки считают находящимися в мультипотентом, недифференцированном и пролиферативном состоянии, если они обладают конкретными характеристиками, как описано более подробно в других местах настоящего документа. Специалист в данной области может выбирать подходящие условия из используемых в норме для культивирования мезенхимальных стволовых клеток.
Как отмечено в другом месте настоящего документа, изобретение относится также к герметично закрытому сосуду, содержащему индукционную среду по изобретению. Герметично закрытые сосуды могут являться предпочтительными для транспортировки или хранения индукционной среды, для предотвращения контаминации. Сосуд может представлять собой любой пригодный сосуд, такой как биореактор, колба, планшет, бутыль, банка, флакон или пакет. Как отмечено в другом месте настоящего документа, изобретение относится также к способу получения индукционной среды, предусматривающему стадии: (а) получения среды для культивирования; и (b) добавления лиганда Toll-подобного рецептора (TLR) или индуктора лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина) к среде для культивирования. Предусмотрено множество различных способов получения индукционной среды, в зависимости от конкретных ингредиентов, подлежащих включению в индукционную среду. Например, способ получения индукционной среды может включать в себя стадии: (а) получения среды для культивирования; и (b) добавления лиганда TLR или индуктора лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина) к среде для культивирования. В одном варианте осуществления способ получения индукционной среды может включать в себя стадии: (а) получения среды для культивирования; и (b) добавления лиганда TLR, ЕРО и хлорида кобальта в среду для культивирования.
Индукционную среду по изобретению можно использовать для индукции, активации или примирования популяции мезенхимальных стволовых клеток. Соответственно, изобретение относится к применению любой индукционной среды, как описано в настоящем документе, для индукции, активации или примирования популяции мезенхимальных стволовых клеток до дискретных однородных фенотипов для клеточной терапии.
В соответствии с конкретными вариантами осуществления индукционная среда, описанная в настоящем документе, индуцирует или уменьшает экспрессию конкретных генов, которую можно измерять способами, известными специалисту в данной области, включая, но без ограничения: ПЦР; кПЦР; qRT-ПЦР; полуколичественную RT-ПЦР; цифровую ПЦР; «нозерн»-блоттинг; мРНК-SEQ; микромассивы; и другие. В соответствии с конкретными вариантами осуществления индукционная среда, описанная в настоящем документе, увеличивает или уменьшает уровни белков, которые можно измерять способами, известными специалисту в данной области, включая, но без ограничения: анализы на основе антител; твердофазный иммуноферментный анализ (ELISA); иммуноблоттинг или вестерн-блоттинг; проточную цитометрию, масс-спектрометрию и другие. В соответствии с конкретными вариантами осуществления индукционная среда, описанная в настоящем документе, индуцирует активацию или ослабление путей передачи сигналов в клетках, которые можно измерять способом, известным специалисту в данной области, включая, но без ограничения: анализ киназы; измерения фосфорилирования/дефосфорилирования белка; измерения убиквитинилирования/деубиквитинилирования белка; измерения ацетилирования/деацетилирования белка; измерения деградации/стабильности белка; измерения вторичных мессенджеров, таких как кальций или диацилглицерин; или мониторирования расщепления от неактивной до активной формы.
В соответствии с конкретными вариантами осуществления индукционная среда, описанная в настоящем документе, приводит к поддающимся измерению изменениям в экспрессии генов, уровнях белков или путях передачи сигналов в клетках, для популяции клеток. В соответствии с конкретными вариантами осуществления изменение представляет собой увеличение экспрессии генов, уровней белков или усиление передачи сигналов в клетках. В соответствии с конкретными вариантами осуществления изменение представляет собой любое статистически значимое изменение, как измерено при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой увеличение по меньшей мере в 2 раза, в 3 раза, в 4 раза, в 5 раз, в 6 раз, в 7 раз, в 8 раз, в 9 раз, в 10 раз или более. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой увеличение по меньшей мере в 100 раз или более. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой уменьшение по меньшей мере в 2 раза, в 3 раза, в 4 раза, в 5 раз, в 6 раз, в 7 раз, в 8 раз, в 9 раз, в 10 раз или более. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой уменьшение по меньшей мере в 100 раз или более.
В соответствии с конкретными вариантами осуществления индукционная среда, содержащая лиганд TLR3, индуцирует экспрессию мРНК любого из следующих генов по меньшей мере в 2 раза по сравнению с нестимулированной популяцией клеток: CXCL9; EGFR; IRF1; А2М; FAS; IL2RG; ММРЗ; GBP 1; ISG15; FCGR1; NFKB1; NOS2A; USF1; YY1; JAK2; STA2, STAT4; STAT5; SOCS1; или IRF1. В соответствии с конкретными вариантами осуществления индукционная среда, содержащая лиганд TLR3, уменьшает экспрессию мРНК любого из следующих генов по меньшей мере в 2 раза по сравнению с нестимулированной популяцией клеток: EPOR; F2R; STAM; PDGFRA; PIAS2; MYC; SH2B1; или CSF2RB. В соответствии с конкретными вариантами осуществления индукционная среда, содержащая лиганд TLR3, индуцирует экспрессию мРНК любого из следующих генов по меньшей мере в 10 раз по сравнению с нестимулированной популяцией клеток: CXCL9; GBP1; ISG15; SOCS1; ММР3; JAK2 или IRF1. В соответствии с конкретными вариантами осуществления индукционная среда, содержащая лиганд TLR3, индуцирует экспрессию мРНК любого из следующих генов по меньшей мере в 20 раз по сравнению с нестимулированной популяцией клеток: CXCL9; GBP1; ISG15; или SOCS1. В соответствии с конкретными вариантами осуществления индукционная среда, содержащая лиганд TLR3, индуцирует экспрессию мРНК CXCL9 по меньшей мере в 100 раз по сравнению с нестимулированной популяцией клеток.
В соответствии с конкретными вариантами осуществления индукционная среда, содержащая лиганд TLR4, индуцирует экспрессию мРНК TNFSF10 (TRAIL) по меньшей мере в 2 раза, в 10 раз, в 100 раз или в 1000 раз по сравнению с нестимулированной популяцией клеток.
Изобретение относится также к способу индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, предусматривающему: (а) получение популяции мезенхимальных стволовых клеток; (b) получение индукционной среды, как описано в настоящем документе; (с) приведение стволовых клеток в контакт с индукционной средой; и (d) культивирование стволовых клеток в подходящих условиях.
В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, индуцируют или уменьшают экспрессию конкретных генов, которую можно измерять способами, известными специалисту в данной области, включая, но без ограничения,: ПЦР; кПЦР; qRT-ПЦР; полуколичественную RT-ПЦР; цифровую ПЦР; «нозерн»-блоттинг; мРНК-SEQ; микромассивы; и другие. В соответствии с конкретными вариантами осуществления индукционная среда, описанная в настоящем документе, увеличивает или уменьшает уровни белка, которые можно измерять способами, известными специалисту в данной области, включая, но без ограничения: анализы на основе антител; твердофазный иммуноферментный анализ (ELISA); иммуноблоттинг или вестерн-блоттинг; проточную цитометрию, масс-спектрометрию и другие. В соответствии с конкретными вариантами осуществления способ индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанной в настоящем документе, предусматривает активацию или ослабление путей передачи сигналов в клетках, которые можно измерять способом, известным специалисту в данной области, включая, но без ограничения: анализ киназы; измерения фосфорилирования/дефосфорилирования белка; измерения убиквитинилирования/деубиквитинилирования белка; измерения ацетилирования/деацетилирования белка; измерения деградации/стабильности белка; измерения вторичных мессенджеров, таких как кальций или диацилглицерин; или мониторирование расщепления от неактивной до активной формы.
В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, получают поддающиеся измерению изменения в экспрессии генов, уровнях белков или путях передачи сигналов в клетках, для популяции стволовых клеток. В соответствии с конкретными вариантами осуществления изменение представляет собой увеличение экспрессии генов, уровней белков или усиление передачи сигналов в клетках. В соответствии с конкретными вариантами осуществления изменение представляет собой любое статистически значимое изменение, как измерено при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой увеличение по меньшей мере в 2 раза, в 3 раза, в 4 раза, в 5 раз, в 6 раз, в 7 раз, в 8 раз, в 9 раз, в 10 раз или более. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой увеличение по меньшей мере в 100 раз или более. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой уменьшение по меньшей мере в 2 раза, в 3 раза, в 4 раза, в 5 раз, в 6 раз, в 7 раз, в 8 раз, в 9 раз, в 10 раз или более. В соответствии с конкретными вариантами осуществления изменение при сравнении нестимулированного или контрольного образца и стимулированного или тестируемого образца представляет собой уменьшение по меньшей мере в 100 раз или более.
В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, предусматривающим лиганд TLR3, индуцируют экспрессию мРНК любого из следующих генов по меньшей мере в 2 раза по сравнению с нестимулированной популяцией клеток: CXCL9; EGFR; IRF1; А2М; FAS; IL2RG; ММР3; GBP1; ISG15; FCGR1; NFKB1; NOS2A; USF1; YY1; JAK2; STA2, STAT4; STAT5; SOCS1; или IRF1. В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, предусматривающим лиганд TLR3, уменьшают экспрессию мРНК любого из следующих генов по меньшей мере в 2 раза по сравнению с нестимулированной популяцией клеток: EPOR; F2R; STAM; PDGFRA; PIAS2; MYC; SH2B1; или CSF2RB. В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, предусматривающим лиганд TLR3, индуцируют экспрессию мРНК любого из следующих генов по меньшей мере в 10 раз по сравнению с нестимулированной популяцией клеток: CXCL9; GBP1; ISG15; SOCS1; ММР3; JAK2 или IRFT. В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, предусматривающим лиганд TLR3, индуцируют экспрессию мРНК любого из следующих генов по меньшей мере в 20 раз по сравнению с нестимулированной популяцией клеток: CXCL9; GBP1; ISG15; или SOCS1. В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, предусматривающим лиганд TLR3, индуцируют экспрессию мРНК CXCL9 по меньшей мере в 100 раз по сравнению с нестимулированной популяцией клеток.
В соответствии с конкретными вариантами осуществления способом индукции, активации или примирования ex-vivo популяции мезенхимальных стволовых клеток, описанным в настоящем документе, предусматривающим лиганд TLR4, индуцируют экспрессию мРНК TNFSF10 (TRAIL) по меньшей мере в 2 раза, в 10 раз, в 100 раз или в 1000 раз по сравнению с нестимулированной популяцией клеток.
Изобретение относится также к способу клеточной терапии, предусматривающему: (а) получение популяции мезенхимальных стволовых клеток; (b) получение индукционной среды по изобретению; (с) приведение популяции стволовых клеток в контакт с индукционной средой; и (d) культивирование клеток в подходящих условиях.
Способы по изобретению могут включать в себя культивирование клеток в контакте с твердой поверхностью, как описано в другом месте настоящего документа. Например, изобретение относится к способу, предусматривающему: (а) получение популяции мезенхимальных стволовых клеток; (b) получение индукционной среды, как описано в настоящем документе; (с) приведение стволовых клеток в контакт с индукционной средой; и (d) культивирование клеток в подходящих условиях и в контакте с твердой поверхностью. Изобретение относится также к применению индукционной среды, как описано в настоящем документе, и твердой поверхности для размножения популяции мезенхимальных стволовых клеток. Мезенхимальные стволовые клетки могут проявлять адгезию, прикрепляться к указанной подложке или являться высеянными на указанную подложку. Как правило, клетки высевают с желательной плотностью, такой как от приблизительно 100 клеток/см2 до приблизительно 100000 клеток/см2 (такой как от приблизительно 500 клетки/см2 до приблизительно 50000 клеток/см2, или, более конкретно, от приблизительно 1000 клеток/см2 до приблизительно 20000 клеток/см2) до индукции, активации или примирования стволовых клеток. В конкретном варианте осуществления плотность клеток составляет между 200-10000 клеток/см2.
Следует понимать, что стадии способов, описанных в настоящем документе, можно проводить в любом подходящем подрядке или одновременно, при необходимости, и нет необходимости проводить их в том порядке, в котором они перечислены. Например, в вышеописанном способе стадию получения популяции мезенхимальных стволовых клеток можно проводить до, после или одновременно со стадией получения индукционной среды.
Способы и применения по изобретению могут включать в себя любую индукционную среду или добавку, как описано в настоящем документе. Соответственно, в некоторых вариантах осуществления способы по изобретению могут представлять собой способы без сыворотки и/или заменителя сыворотки. В некоторых вариантах осуществления способы по изобретению можно использовать для индукции клеток в отсутствие контакта со слоем фидерных клеток.
Предпочтительные способы и применения по изобретению предназначены для индукции, активации или примирования популяции мезенхимальных стволовых клеток, происходящих, как только клетки подвергли размножению и перед криоконсервацией и применением в клеточной терапии.
Предпочтительно, чтобы указанная популяция стволовых клеток происходила из взрослого источника, и кроме того, является предпочтительным, чтобы указанные клетки представляли собой популяцию мезенхимальных стволовых клеток, как в происходящих из костного мозга или в происходящих из жировой ткани клетках.
Условия культивирования стволовых клеток известны специалисту в данной области. Предпочтительно, чтобы культивирование проводили в присутствии твердой подложки, пригодной для адгезии мезенхимальных стволовых клеток.
Указанный способ изготовления может, необязательно, дополнительно содержать стадии: (а) пассирования клеток в среде для культивирования, как описано в настоящем документе; (b) дальнейшего культивирования клеток в подходящих условиях и (с) индукции, активации или примирования клеток.
Показано, что размножение MSC ex vivo без индукции дифференцировки можно проводить в течение продолжительных периодов времени, например, с использованием специально подвергнутой скринингу подходящей сыворотки (такой как эмбриональная бычья сыворотка или человеческая сыворотка). Способы измерения жизнеспособности и выхода известны в данной области (например, исключение трипанового синего).
Любую из стадий и процедур для выделения клеток из популяции клеток по изобретению можно проводить вручную, при желании. Альтернативно, процесс выделения таких клеток можно облегчать и/или автоматизировать посредством одного или нескольких подходящих устройств, примеры которых известны в данной области.
Практическое осуществление изобретения можно выполнять с использованием любого пригодного сосуда для культивирования клеток в качестве подложки. Сосуды для культивирования клеток различных форм и размеров (например, колбы, одно- или многолуночные планшеты, одно- или многолуночные чашки, бутыли, банки, флаконы, пакеты, биореакторы) и сконструированные из множества различных материалов (например, пластика, стекла) известны в данной области. Специалист в данной области может легко выбрать подходящий сосуд для культивирования клеток.
Изобретение относится также к индукционной добавке к среде для культивирования, которую можно использовать для получения индукционной среды для культивирования, как описано в настоящем документе. «Индукционная добавка к среде для культивирования» представляет собой смесь ингредиентов, которая сама неспособна поддерживать мезенхимальные стволовые клетки, но которая позволяет или улучшает культивирование мезенхимальных стволовых клеток при комбинации с другими ингредиентами среды для культивирования клеток. Добавку, таким образом, можно использовать для получения функциональной среды для культивирования клеток по изобретению посредством ее комбинации с другими ингредиентами среды для культивирования клеток для получения подходящего состава среды. Применение добавок к среде для культивирования хорошо известно в данной области. Изобретение относится к индукционной добавке к среде для культивирования, содержащей добавление лиганда TLR или индуктора лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина). Добавка может содержать любые лиганды, описанные в настоящем документе. Добавка может также содержать один или несколько дополнительных ингредиентов для культивирования клеток, например, один или несколько ингредиентов для культивирования клеток, выбранных из группы, состоящей из аминокислот, витаминов, неорганических солей, микроэлементов, углеродных источников энергии и буферов.
Индукционная добавка к среде для культивирования может представлять собой концентрированную жидкую добавку (например, 2х-250х концентрированную жидкую добавку) или может представлять собой сухую добавку. Как жидкие, так и сухие типы добавок хорошо известны в данной области. Добавка может являться лиофилизированной.
Индукционную добавку к среде для культивирования по изобретению, как правило, стерилизуют перед использованием для предотвращения контаминации, например, посредством ультрафиолетового света, нагревания, радиоактивного облучения или фильтрации. Индукционную добавку к среде для культивирования можно замораживать (например, при -20°C или -80°C) для хранения или транспортировки.
Изобретение относится также к герметично закрытому сосуду, содержащему добавку к среде для культивирования по изобретению. Герметично закрытые сосуды могут являться предпочтительными для транспортировки или хранения добавок к среде для культивирования, описанных в настоящем документе, для предотвращения контаминации. Сосуд может представлять собой любой пригодный сосуд, такой как биореактор, колба, планшет, бутыль, банка, флакон или пакет.
Множество веществ используют в качестве поверхностей для адгерентной культуры стволовых клеток, и специалист в данной области может легко выбирать подходящий материал. Предпочтительно, твердая поверхность содержит пластик, но может альтернативно содержать стекло, внеклеточный матрикс. Поверхность может являться плоской, трубчатой или иметь форму каркасной структуры, бусины или волокна.
Композиции по изобретению могут содержать сыворотку или могут не содержать сыворотки и/или заменителя сыворотки, как описано в другом месте настоящего документа.
Мезенхимальные стволовые клетки для применения по изобретению можно получать с использованием хорошо известных способов (см. ниже). Предусмотрено, что различные типы мезенхимальных стволовых клеток можно использовать в сочетании с изобретением, вне зависимости от того, получены ли они из эмбриональной, фетальной или взрослой ткани, но предпочтительно они происходят из источников взрослой ткани.
Индукционную среду, описанную в настоящем документе, можно использовать для культивирования стволовых клеток млекопитающих, в частности, взрослых стволовых клеток человека. Взрослые стволовые клетки человека, которые можно использовать в сочетании с изобретением, предпочтительно представляют собой мезенхимальные стволовые клетки. Можно использовать также стволовые клетки мыши или примата. В предпочтительных вариантах осуществления стволовые клетки представляют собой происходящие из костного мозга человека стволовые клетки (MSC).
Мезенхимальные стволовые клетки можно идентифицировать по их способности к дифференцировке в клетки всех трех зародышевых листков, например, посредством определения способности клеток к дифференцировке в клетки, обладающие поддающейся детекции экспрессии маркеров, специфических для всех трех зародышевых листков. Ссылки на единственное число (например, на «клетку» и эквивалентные ссылки) включают в себя множественное число (например, «клетки»), если контекст не требует иного.
индукционную среду по изобретению можно использовать для индукции, активации или примирования популяции мезенхимальных стволовых клеток. Соответственно, изобретение относится к применению любой индукционной среды, как описано в настоящем документе, для индукции, активации или примирования популяции мезенхимальных стволовых клеток до дискретных однородных фенотипов для клеточной терапии. Эти дискретные и однородные фенотипы могут представлять собой противовоспалительный фенотип MSC (MSC2) и однородный и дискретный проиммунный противоопухолевый фенотип MSC (MSC1).
Предпочтительным способом индукции для однородного и дискретного противовоспалительного фенотипа MSC (MSC2) является инкубация MSC с средой для культивирования, содержащей лиганд Toll-подобного рецептора-3 (TLR3), такой как полиинозиновая : полицитидиловая кислота (или поли(I:С); 1 мкг/мл) в комбинации с эритропоэтином (1 мед./мл или 5 нг/мл) и с воздействием гипоксии (1% кислорода) или миметика гипоксии (хлорида кобальта или дезферриоксамина, каждый при 200 мкМ) в течение 1 часа при 70-90% конфлюэнтном росте.
Предпочтительным способом индукции для однородного и дискретного проиммунного противоопухолевого фенотипа MSC (MSC1) является инкубация MSC с средой для культивирования, содержащей лиганд Toll-подобного рецептора-4 (TLR4), такой как липополисахарид (LPS, эндотоксин при 10 нг/мл) в комбинации с эритропоэтином (1 мед./мл или 5 нг/мл) и с воздействием гипоксии (1% кислорода) или миметика гипоксии (хлорида кобальта или дезферриоксамина, каждый при 200 мкМ)) в течение 1 часа при 70-90% конфлюэнтном росте.
Лиганды TLR в комбинации с эритропоэтином и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина) добавляют к свежей среде для культивирования, или в форме добавки для культивирования и инкубируют клетки в течение 1 час.После этой стадии индукции, MSC промывают дважды в среде для культивирования или подходящем забуференном солевом растворе без лигандов TLR для удаления клеточного и культурального дебриса. Без желания быть связанными теорией, короткие периоды времени инкубации (<1 час) и минимальное воздействие лиганда TLR в указанных выше концентрациях (или более низких) являются важными для достижения желательных фенотипов и кроме того, этот способ имитирует градиент сигналов опасности, с которым сталкиваются и на который отвечают эндогенные MSC на расстоянии от участка повреждения. После промывки, индуцированные, активированные или примированные MSC можно собирать общепринятыми способами, например, с использованием трипсина и ЭДТА в течение между 5 секунд и 15 минут при 37°C или с использованием заменителя трипсина (например, TrypLE от Invitrogen), коллагеназы, диспазы, аккутазы или других реагентов, известных специалисту в данной области. После сбора клеток примированные, активированные или индуцированные MSC можно подвергать криоконсервации стандартными способами.
Агонисты TLR3 или агонисты TLR4 можно доставлять посредством инкубации, трансфекции, трансдукции, посредством молекул носителя, или другими способами, известными специалистам в данной области.
Клетки можно инкубировать с лигандом или агонистом лиганда TLR в комбинации с эритропоэтином (ЕРО) и с воздействием гипоксии или миметика гипоксии (хлорида кобальта или дезферриоксамина) в течение от приблизительно 1 минуты до приблизительно 480 минут, от приблизительно 5 минут до приблизительно 475 минут, от приблизительно 10 минут до приблизительно 470 минут, от приблизительно 15 минут до приблизительно 400 минут, от приблизительно 20 минут до приблизительно 120 минут, от приблизительно 25 минут до приблизительно 90 минут, от приблизительно 30 минут до приблизительно 80 минут, от приблизительно 35 минут до приблизительно 70 минут, от приблизительно 40 минут до приблизительно 65 минут, от приблизительно 45 минут до приблизительно 60 минут, от приблизительно 55 минут до приблизительно 60 минут, и предпочтительно, приблизительно 60 минут.
Примеры
Пример 1 - Индукция характерного для MSC2 профиля экспрессии генов в первичных MSC человека
Для этого эксперимента первичные MSC человека инкубировали при 37°C и 5% CO2, в бессывороточной среде, содержащей 2 мкг/мл поли(I:С), в течение 6 часов. Затем клетки дважды промывали, РНК выделяли с использованием набора RNeasy Mini (Qiagen, Valencia, CA) и затем обрабатывали с использованием набора TURBO DNA-free (Ambion, Austin, TX). РНК подвергали обратной транскрипции, и полученную кДНК использовали в массиве для анализа путей передачи сигнала JAK/STAT посредством ПЦР - JAK/STAT Signaling Pathway RT2 ProfilerTM PCR Array (SuperArray Bioscience, Frederick, MD), в соответствии с инструкциями производителя, в системе для ПЦР с детекцией в реальном времени iCycler iQ5 (Bio-Rad, Hercules, CA). Необработанные данные для необработанных и обработанных групп анализировали с использованием программного обеспечения GEarray Analyzer (SuperArray Inc., Bethesda, MD). С использованием этого массива измеряют уровни экспрессии РНК 84 различных генов в пути передачи сигнала JAK/STAT. Результаты показаны на фиг. 1. Гены, для которых показана 2-кратная или большая индукция, заключены в серые рамки, гены, для которых показано 2-кратное или большее снижение экспрессии, заключены в черные рамки, и гены, обладающие более чем двукратной индукцией и избранные для дальнейшего подтверждения, показаны в толстых рамках (за исключением PIAS2, экспрессия которого была снижена более чем в 2 раза). На фиг. 2 показано дальнейшее подтверждение по кПЦР генов, избранных на фиг. 1. Проверку проводили посредством кПЦР с использованием готовой смеси SYBR green Master Mix с геноспецифическими праймерами на тех же образцах, что анализировали на фиг. 1.
Пример-2 Поляризация первичных MSC человека до MSC1 и MSC2
Первичные MSC доноров-людей подвергали поляризации до MSC1 или MSC2. MSC человека подвергали поляризации с использованием среды, содержащей 10 нг/мл LPS либо в отсутствие (MSC1), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC1*). Клетки MSC2 получали при поляризации с использованием среды, содержащей 2 мкг/мл поли(I:С) либо в отсутствие (MSC2), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC2*). Культуральные супернатанты собирали и затем анализировали по экспрессии хемокинов/цитокинов посредством bio-plex, как описано ранее. Кратко, MSC высевали при плотности 50000 клеток в 24-луночные планшеты, позволяли адгезию в течение ночи, затем примировали с использованием агонистов TLR в течение 1 час, как указано. Кондиционированную среду собирали через 48 час и анализировали с использованием анализов цитокинов Bio-Plex (Human Group I & II; Bio-Rad, Hercules, CA), в соответствии с инструкциями производителя. Эти эксперименты проводили по меньшей мере три раза для пулов MSC трех индивидуальных доноров. Индукция MSC1 вне зависимости от формулы приводит к значимой секреции цитокинов, включая IL6 и IL8 (фиг. 3), в то время как индукция MSC2 вне зависимости от формулы приводит к значимой секреции IP 10 (CXCL10) и RANTES (CCL5) (фиг. 4). Планки погрешностей обозначают +/- SEM.
Пример 3 - Поляризация MSC1 и MSC2 является постоянной среди множества источников MSC
MSC доноров-людей из 3 различных коммерческих источников и от максимум шести различных доноров подвергали поляризации до MSC1. MSC человека подвергали поляризации с использованием среды, содержащей 10 нг/мл LPS, либо в отсутствие (MSC1), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC1*). Тотальную РНК выделяли, очищали и подвергали обратной транскрипции до кДНК. Количественную ПЦР с детекцией в реальном времени проводили с использованием готовой смеси SYBR Green Master Mix. Данные анализированы с использованием способа количественного сравнения СТ с нормализацией экспрессии гена-мишени по экспрессии гена домашнего хозяйства 18S рРНК, и показаны как кратность увеличения по сравнению с контролем без обработки. Экспрессия гена Trail являлась значимо увеличенной после индукции MSC1 для всех доноров, включая смешанные образцы (фиг. 5). Планки погрешностей представляют собой +/- стандартную ошибку среднего (SEM). Праймеры, использованные для кДНК человека: Cxcl9 Прямой - CTTTCCTGG СТА СТС CAT GTT Обратный - GTT GGT CACTGG CTG АТС ТАТ АА; Trail Прямой - СТТ САС AGT GCT ССТ GCA GT Обратный - ТТА GCC AACTAA AAA GGC ССС; 18S рРНК Прямой - GAGGGAGCCTGAGAAACGG, Обратный-GTCGGGAGTGGGTAATTTGC с протоколом: 1:95,0°C в течение 0:30,2:95,0°C в течение 0:10,3:68,0°C в течение 0:30, считывание планшета, 4: переход к стадии 2, еще 39 раз.
MSC доноров-людей из 3 различных коммерческих источников и от максимум шести различных доноров подвергали поляризации до MSC2. MSC человека подвергали поляризации с использованием среды, содержащей 2 мкг/мл поли(I:С), либо в отсутствие (MSC2), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC2*). Тотальную РНК выделяли, очищали и подвергали обратной транскрипции до кДНК. Количественную ПЦР с детекцией в реальном времени проводили с использованием готовой смеси SYBR Green Master Mix. Данные анализированы с использованием способа количественного сравнения СТ с нормализацией экспрессии гена-мишени по экспрессии гена домашнего хозяйства 18S рРНК и показаны как кратность увеличения по сравнению с контролем без обработки. Экспрессия гена CXCL9 являлась значимо увеличенной после индукции MSC2 для всех доноров, включая смешанные образцы (фиг. 6). Планки погрешностей представляют собой +/- стандартную ошибку среднего (SEM).
Пример 4 - Поляризация MSC1 и MSC2 с течением времени.
MSC доноров-людей подвергали поляризации до MSC1. MSC человека подвергали поляризации с использованием среды, содержащей 10 нг/мл LPS, либо в отсутствие (MSC1), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC1*). Клетки собирали в различные периоды времени, как указано. Тотальную РНК выделяли, очищали и подвергали обратной транскрипции до кДНК. Количественную ПЦР с детекцией в реальном времени проводили с использованием готовой смеси SYBR Green Master Mix. Данные анализированы с использованием способа количественного сравнения СТ с нормализацией экспрессии гена-мишени по экспрессии гена домашнего хозяйства 18S рРНК и показаны как кратность увеличения по сравнению с контролем без обработки. Экспрессия гена Trail являлась значимо увеличенной через 4 часа после индукции MSC1 (фиг. 7). Планки погрешностей представляют собой +/- стандартную ошибку среднего (SEM).
MSC доноров-людей подвергали поляризации до MSC2. MSC человека подвергали поляризации с использованием среды, содержащей 2 мкг/мл поли(I:С) либо в отсутствие (MSC2), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC2*). Клетки собирали в различные периоды времени, как указано. Тотальную РНК выделяли, очищали и подвергали обратной транскрипции до кДНК. Количественную ПЦР с детекцией в реальном времени проводили с использованием готовой смеси SYBR Green Master Mix. Данные анализированы с использованием способа количественного сравнения СТ с нормализацией экспрессии гена-мишени по экспрессии гена домашнего хозяйства 18S рРНК и показаны как кратность увеличения по сравнению с контролем без обработки, экспрессия гена Схс19 являлась значимо увеличенной через 4 часа после индукции MSC2 (фиг. 8). Планки погрешностей представляют собой +/- стандартную ошибку среднего (SEM).
Пример 5 - Биораспределение клеток MSC1 и MSC2
Проводили эксперимент для определения эффективности in vivo поляризованных MSC по сравнению с наивными MSC. Для этого эксперимента, наивные MSC человека, MSC1 и MSC2 (1 миллионов клеток) вводили посредством IP инъекции мышам дикого типа, и через 4 часа собирали все органы. Затем выполняли анализ выделенной РНК по GAPDH человека и сравнивали с ДНК GAPDH мыши для определения хоминга в тканях. Результаты показаны ниже в таблице 1.
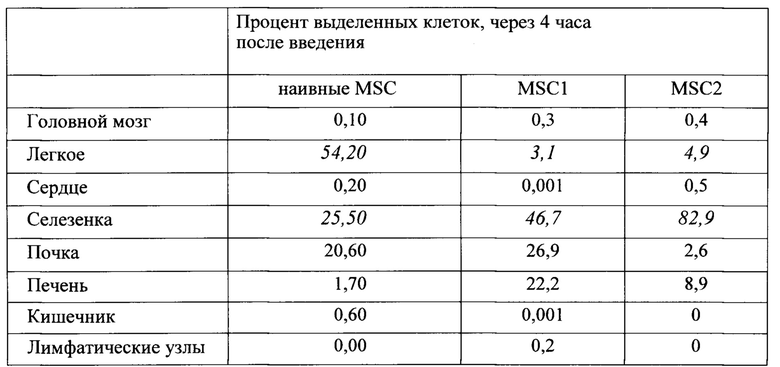
Пример 6 - Инкубация с эритропоэтином и хлоридом кобальта в ходе поляризации MSC увеличивает миграцию, пролиферацию/жизнеспособность клеток MSC1 и MSC2
Для определения способности к миграции MSC, культивированные в присутствии или в отсутствие эритропоэтина и гипоксии, наивные клетки MSC человека и поляризованные клетки MSC1 или MSC2 добавляли в индивидуальные вставки transwell (поры 8 мкм, 50000 клеток/вставку). Клетки MSC1 подвергали поляризации с использованием среды, содержащей 10 нг/мл LPS либо в отсутствие (MSC1), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC1*). Клетки MSC2 подвергали поляризации с использованием среды, содержащей 2 мкг/мл поли (I:С) либо в отсутствие (MSC2), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC2*). Мембраны опускали в 24-луночные сопровождающие планшеты, содержащие либо отрицательный контроль, бессывороточную среду (SFM), либо положительный контроль, содержащую сыворотку среду для выращивания (ССМ), либо соответствующую индукционную среду, как указано. Микрофотографии получали через 16 часов инкубации с помощью инвертированного флуоресцентного микроскопа Nikon Eclipse ТЕ300. На фиг. 9 показаны репрезентативные данные для мигрировавших MSC, подсчитанных в 4 репрезентативных квадрантах изображения для более чем трех независимо проведенных экспериментов, выполненных в трех повторах (n=3). Планки погрешностей обозначают SEM.
Анализ пролиферации использовали для определения способности к пролиферации и жизнеспособности MSC, культивированных в присутствии или в отсутствие эритропоэтина и гипоксии. MSC человека подвергали поляризации с использованием среды, содержащей 10 нг/мл LPS либо в отсутствие (MSC1), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC1*). Клетки MSC2 подвергали поляризации с использованием среды, содержащей 2 мкг/мл поли(I:С) либо в отсутствие (MSC2), либо в присутствии 0,5 нг/мл рекомбинантного человеческого эритропоэтина и 200 мкМ хлорида кобальта (MSC2*). Клетки инкубировали с указанной средой в течение 48 часов. Пролиферацию и жизнеспособность клеток из каждого образца измеряли посредством анализа CyQUANT (Life Technologies, CA) и анализа трипанового синего, соответственно. Для пролиферации клеток, клетки высевали в 96-луночные планшеты при 1×103 клеток в 50 мкл на лунку в трех повторах и культивировали при 37°C, 5% СО2. Образцы отбирали через 0, 24, 48, 72 и 96 час после обработки и обрабатывали, как описано производителем (CyQUANT assay, Life Technologies, CA). Показанные данные выражены относительно контроля без обработки. Анализ пролиферации клеток проводили по меньшей мере в трех отдельных экспериментах, где каждый образец повторяли в 8 лунках 96-луночного планшета (n=3). Планки погрешностей обозначают SEM. Результаты показаны на фиг. 10.
Пример 7 Подтверждение анализа кПЦР для CXCL9 и TNFSF10
Проводили индукцию MSC человека до MSC1. Тотальную РНК выделяли, очищали и подвергали обратной транскрипции до кДНК. Количественную ПЦР с детекцией в реальном времени проводили с использованием готовой смеси SYBR Green Master Mix. Данные анализированы с использованием способа количественного сравнения СТ с нормализацией экспрессии гена-мишени по экспрессии гена домашнего хозяйства 18S рРНК и показаны как кратность увеличения по сравнению с контролем без обработки. Экспрессия гена Trail являлась значимо увеличенной после индукции MSC1. Планки погрешностей представляют собой +/- стандартную ошибку среднего (SEM). Подтверждали эффективность праймеров и специфичность продукта (фиг. 11).
Проводили индукцию MSC человека до MSC2. Тотальную РНК выделяли, очищали и подвергали обратной транскрипции до кДНК. Количественную ПЦР с детекцией в реальном времени проводили с использованием готовой смеси SYBR Green Master Mix. Данные анализированы с использованием способа количественного сравнения СТ с нормализацией экспрессии гена-мишени по экспрессии гена домашнего хозяйства 18S рРНК и показаны как кратность увеличения по сравнению с контролем без обработки. Экспрессия гена Схс19 являлась значимо увеличенной после индукции MSC2. Планки погрешностей представляют собой +/- стандартную ошибку среднего (SEM). Подтверждали экспрессию гена с течением времени (фиг. 12А) и специфичность продукта (фиг. 12В).
В то время как это изобретение подробно описано с конкретными ссылками на предпочтительные варианты его осуществления, принципы и способы действия изобретения также описаны в этом описании. Изобретение не следует рассматривать как ограниченное описанными конкретными формами, которые являются иллюстративными, а не ограничивающими. Специалисты в данной области могут осуществлять модификации, варианты и изменения без отклонения от содержания и объема изобретения, как описано в следующей формуле изобретения.
В то время как предпочтительные варианты осуществления настоящего изобретения показаны и описаны в настоящем документе, специалистам в данной области очевидно, что такие варианты осуществления представлены только в качестве примера. Специалисты в данной области в настоящее время могут осуществлять многочисленные варианты, изменения и замены без отклонения от изобретения. Следует понимать, что различные альтернативы вариантам осуществления изобретения, описанным в настоящем документе, можно применять в практическом осуществлении изобретения. Подразумевают, что следующая формула изобретения определяет объем изобретения, и что оно, таким образом, охватывает способы и структуры в объеме этих пунктов формулы изобретения и их эквивалентов.
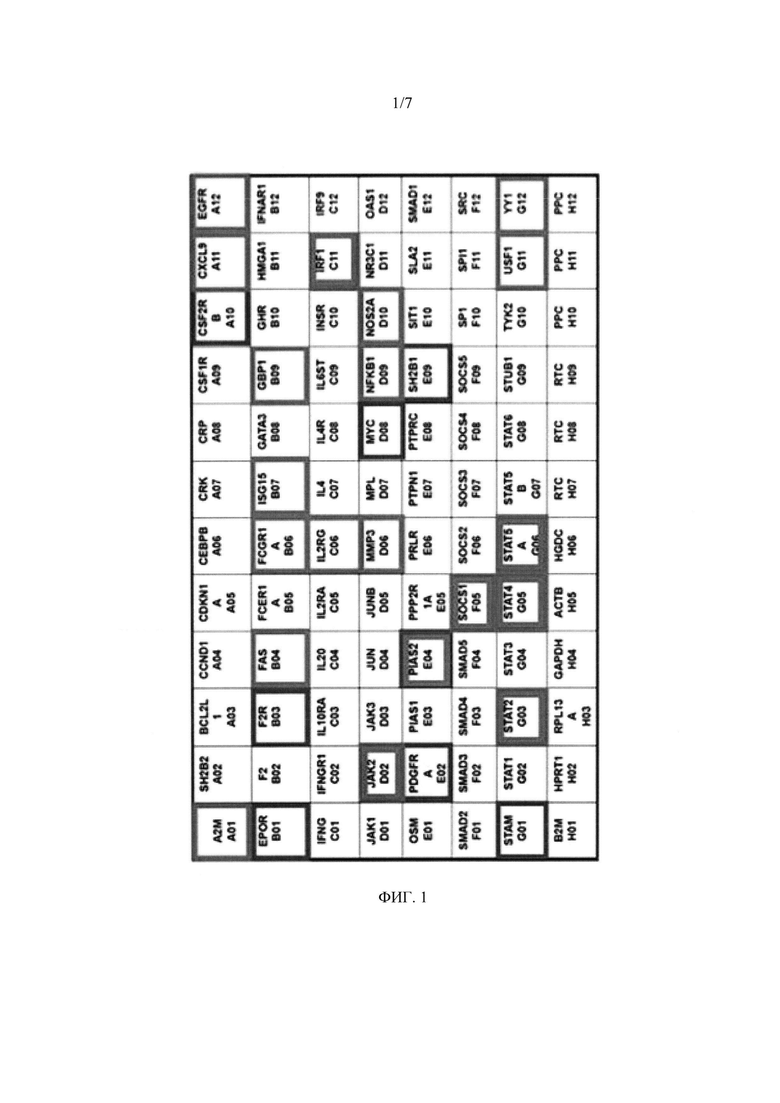
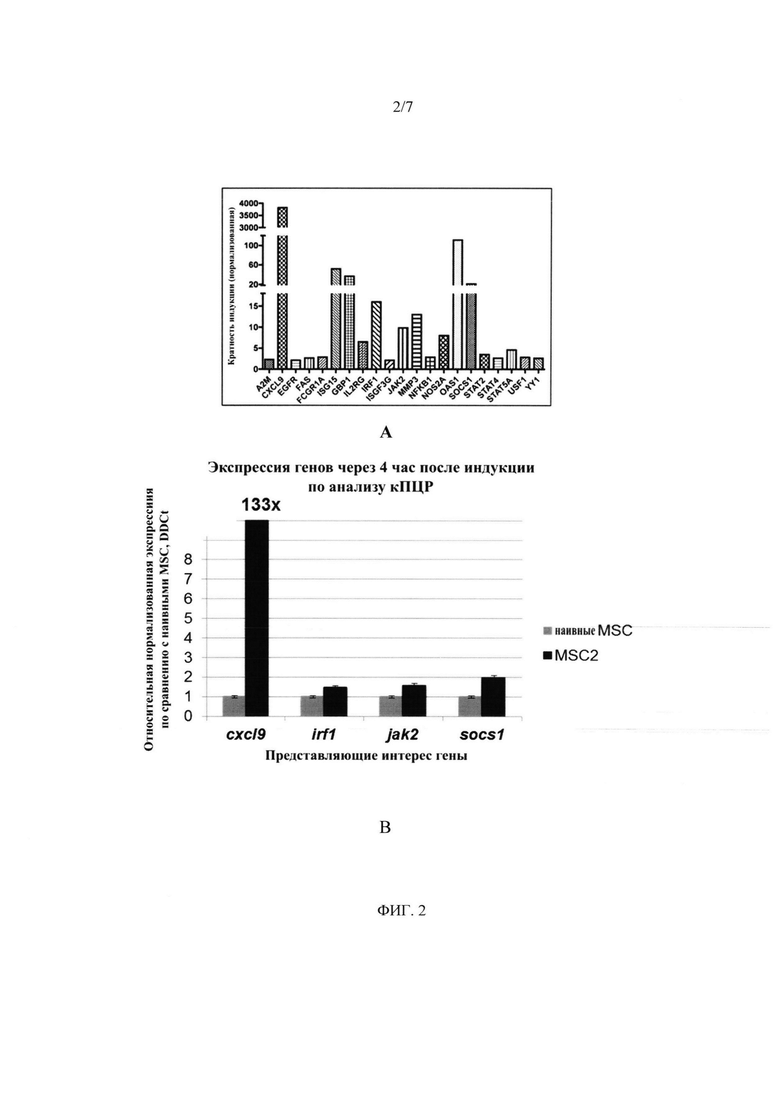
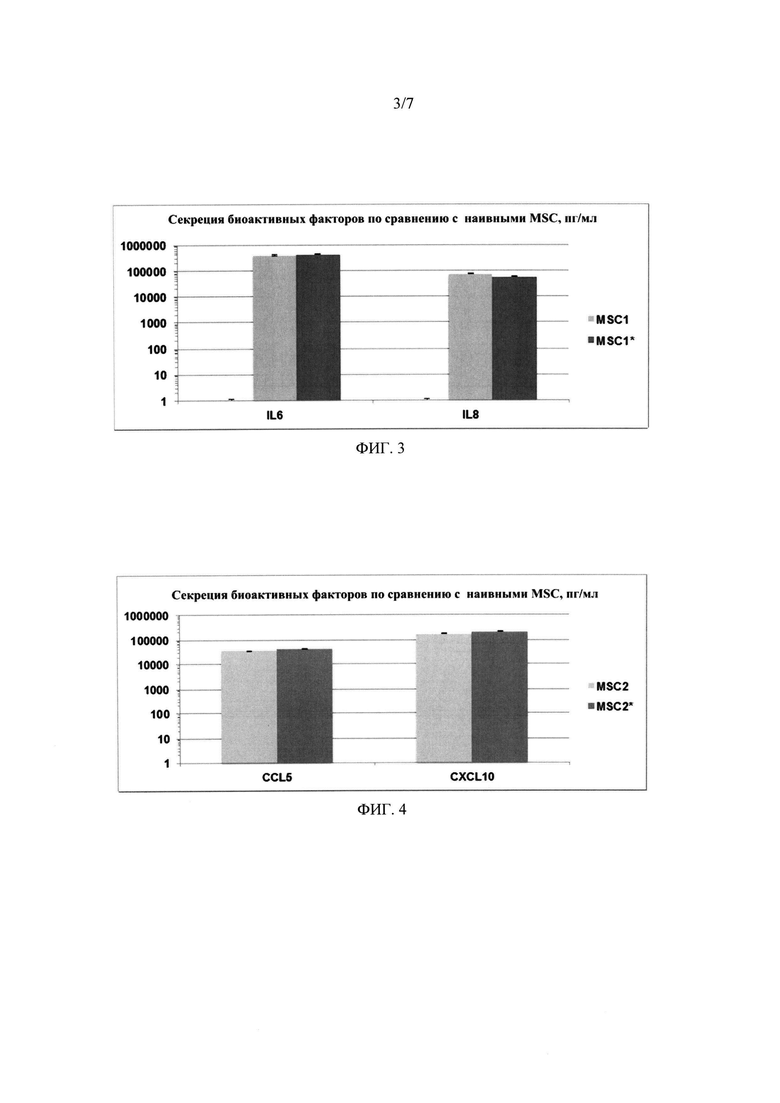
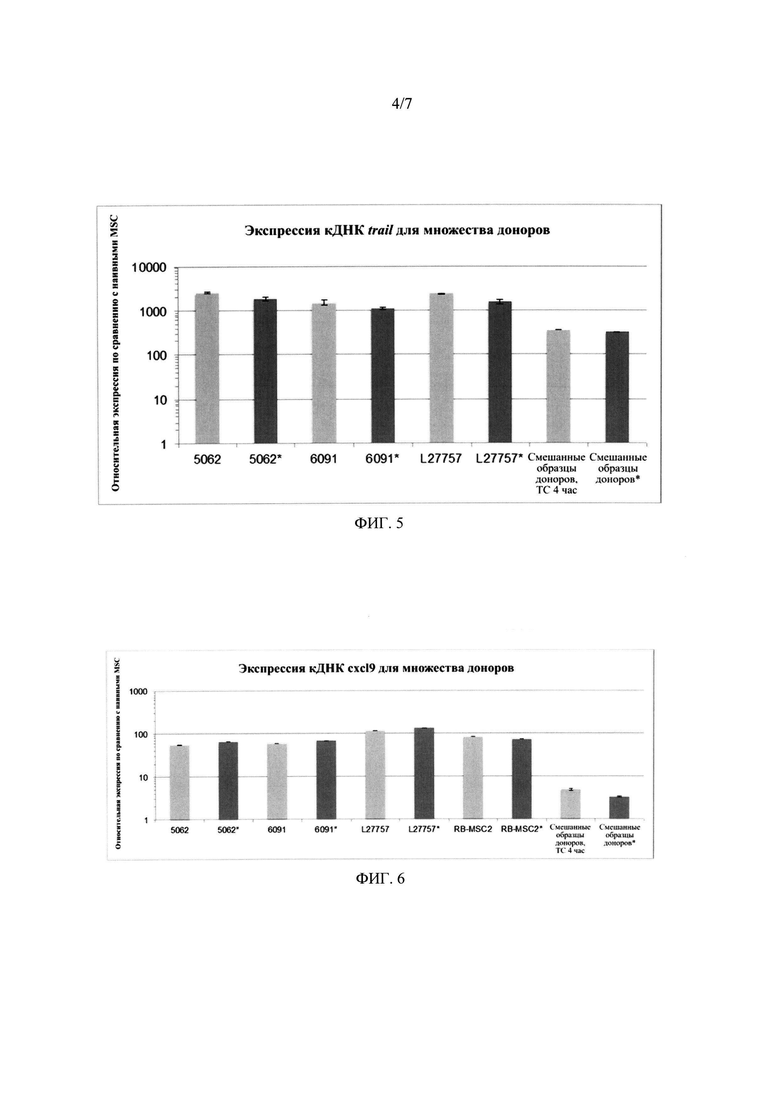
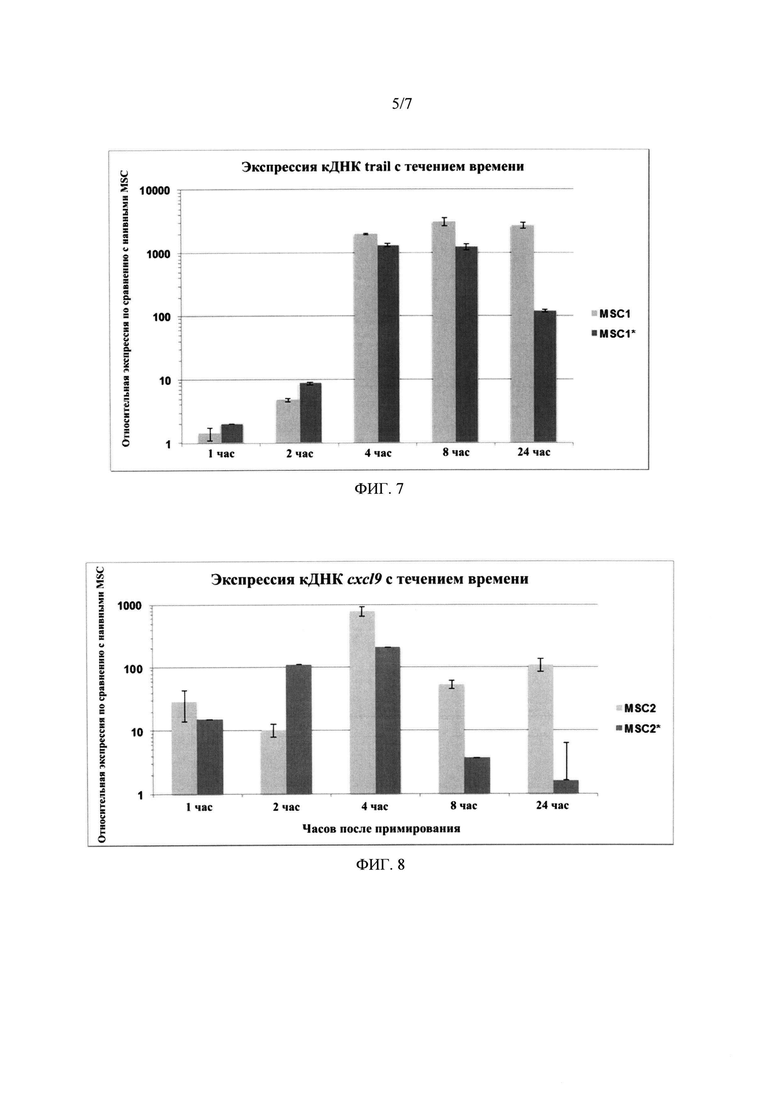
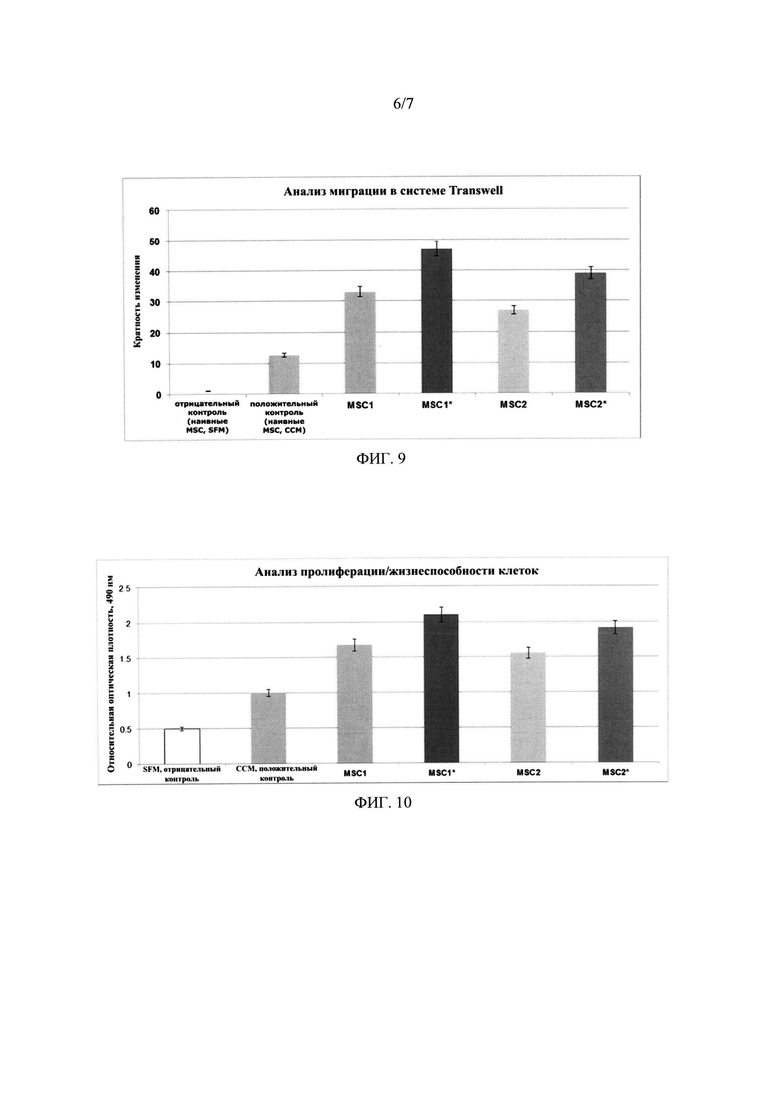
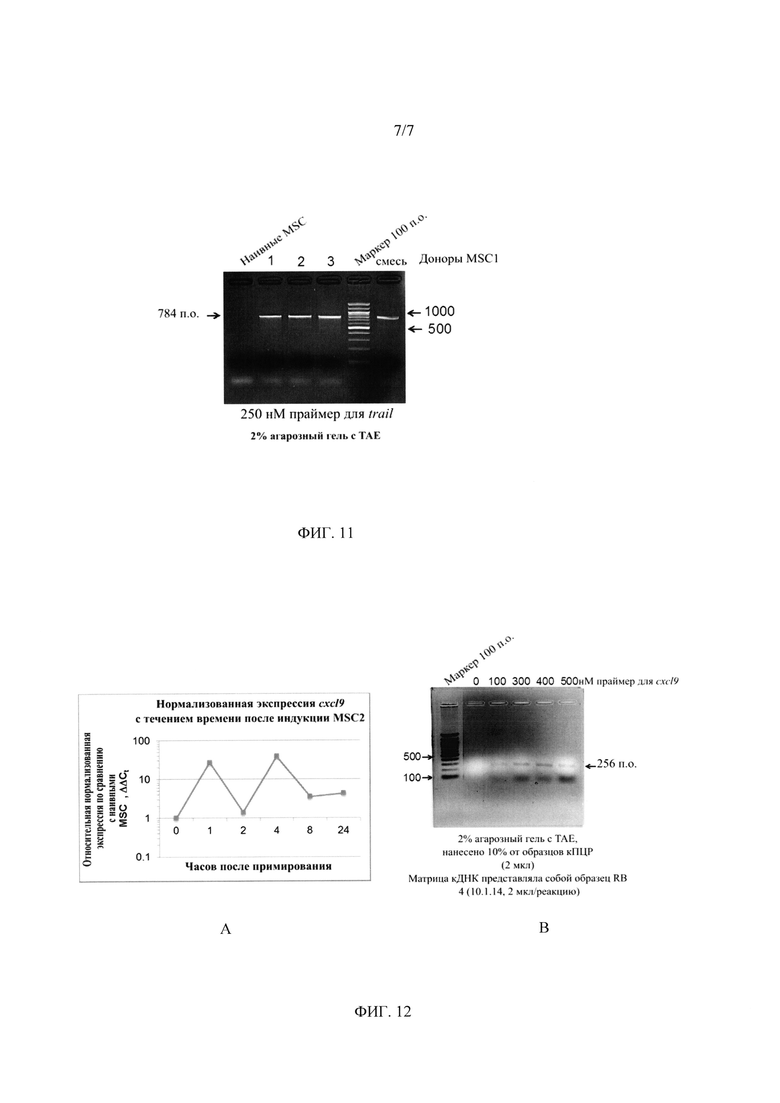
Изобретение относится к области биотехнологии, а именно к индукционным средам для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, иммунологически поляризованным популяциям мезенхимальных стволовых клеток и лечению заболеваний у субъекта. Индукционная среда содержит лиганд Toll-подобного рецептора 3 (TLR3) в концентрации между 1 мкг/мл и 2,5 мкг/мл, эритропоэтин в концентрации между 0,1 нг/мл и 1,0 нг/мл или 5 нг/мл, и 0,5-2% кислорода или миметик гипоксии. Иммунологически поляризованная популяция мезенхимальных стволовых клеток, обладающая противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов, получена обработкой указанной средой, в которой TLR3 представлен поли(I:С), который доставлен в нестимулированную популяцию мезенхимальных стволовых клеток путем трансфекции. Способ лечения воспалительных нарушений или аутоиммунных нарушений у субъекта включает введение субъекту указанных популяций. Изобретение позволяет расширить арсенал технических средств. 19 н. и 37 з.п. ф-лы, 12 ил., 1 табл., 7 пр.
1. Индукционная среда для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, причем индукционная среда содержит:
a. лиганд Toll-подобного рецептора 3 (TLR3) в концентрации между 1 мкг/мл и 2,5 мкг/мл,
b. эритропоэтин в концентрации между 0,1 нг/мл и 1,0 нг/мл, и
c. 0,5-2% кислорода или миметик гипоксии,
где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов.
2. Индукционная среда по п. 1, причем лиганд Toll-подобного рецептора 3 (TLR3) представляет собой поли(I:С).
3. Индукционная среда по п. 1, причем лиганд Toll-подобного рецептора 3 (TLR3) представляет собой поли(А:U).
4. Индукционная среда по п. 1, причем миметик гипоксии представляет собой хлорид кобальта, присутствующий в концентрации между 100 мкМ и 300 мкМ.
5. Индукционная среда по п. 1, дополнительно содержащая интерлейкин 4 (IL-4) в концентрации между 1 мкг/мл и 2,5 мкг/мл.
6. Индукционная среда по п. 1, дополнительно содержащая интерлейкин 13 (IL-13) в концентрации между 1 мкг/мл и 2,5 мкг/мл.
7. Индукционная среда по п. 1, которая не содержит сыворотку, полученную от человека или животного.
8. Индукционная среда по п. 1, которая представляет собой концентрированный раствор.
9. Иммунологически поляризованная популяция мезенхимальных стволовых клеток, обладающая противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов; причем иммунологически поляризованная популяция мезенхимальных стволовых клеток получена обработкой нестимулированной популяции мезенхимальных стволовых клеток индукционной средой по п. 2, причем поли(I:С) доставлен в нестимулированную популяцию мезенхимальных стволовых клеток путем трансфекции.
10. Композиция для лечения заболевания, содержащая иммунологически поляризованную популяцию мезенхимальных стволовых клеток по п. 9, причем заболевание представляет собой воспалительное нарушение.
11. Композиция для лечения заболевания, содержащая иммунологически поляризованную популяцию мезенхимальных стволовых клеток по п. 9, причем заболевание представляет собой аутоиммунное нарушение.
12. Композиция по п. 11, причем аутоиммунное нарушение представляет собой ревматоидный артрит.
13. Композиция по п. 10, причем воспалительное нарушение представляет собой воспалительное заболевание кишечника.
14. Композиция по п. 10, причем воспалительное нарушение представляет собой острый неврит зрительного нерва.
15. Композиция по п. 10, причем воспалительное нарушение представляет собой болезнь Краббе.
16. Композиция по п. 11, причем аутоиммунное нарушение представляет собой диабетическую ретинопатию.
17. Композиция по п. 10, причем воспалительное нарушение представляет собой болезнь Крона.
18. Композиция по п. 10, причем воспалительное нарушение представляет собой острое повреждение легких.
19. Индукционная среда для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, причем индукционная среда содержит:
a. поли(I:С) в концентрации 1 мкг/мл,
b. эритропоэтин в концентрации 5 нг/мл или 1 мЕД/мл, и
c. хлорид кобальта в концентрации 200 мкМ,
где иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками и отмечена увеличенной экспрессией мРНК CXCL9, OAS1 и ISG15 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток.
20. Способ получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, причем способ предусматривает: приведение нестимулированной популяции мезенхимальных стволовых клеток в контакт с композицией, содержащей: лиганд Toll-подобного рецептора 3 (TLR3) в концентрации между 1 мкг/мл и 2,5 мкг/мл, эритропоэтин в концентрации между 0,1 нг/мл и 1,0 нг/мл, и подвергание воздействию гипоксии или миметика гипоксии, причем иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками, отмеченными экспрессией противоспалительных или иммуносупрессивных медиаторов.
21. Способ по п. 20, причем лиганд Toll-подобного рецептора 3 (TLR3) представляет собой поли(I:С).
22. Способ по п. 20, причем лиганд Toll-подобного рецептора 3 (TLR3) представляет собой поли(А:U).
23. Способ по п. 20, причем миметик гипоксии представляет собой хлорид кобальта, присутствующий в концентрации между 100 мкМ и 300 мкМ.
24. Способ по п. 20, причем композиция дополнительно содержит интерлейкин 4 (IL-4) в концентрации между 1 мкг/мл и 2,5 мкг/мл.
25. Способ по п. 20, причем композиция дополнительно содержит интерлейкин 13 (IL-13) в концентрации между 1 мкг/мл и 2,5 мкг/мл.
26. Способ по п. 20, причем композиция не содержит сыворотку, полученную от человека или животного.
27. Способ по п. 20, причем композиция получена из концентрированного раствора.
28. Способ по п. 20, причем нестимулированную популяцию мезенхимальных стволовых клеток приводят в контакт с лигандом Toll-подобного рецептора 3 (TLR3), эритропоэтином и подвергают воздействию гипоксии или миметика гипоксии одновременно.
29. Способ по п. 20, причем композицию приводят в контакт с нестимулированной популяцией мезенхимальных стволовых клеток по меньшей мере на 30 минут, но менее чем на 8 часов.
30. Способ по п. 20, дополнительно предусматривающий мониторирование экспрессии CXCL9 на уровне либо РНК, либо белка.
31. Способ по п. 20, дополнительно предусматривающий мониторирование экспрессии OAS1 на уровне либо РНК, либо белка.
32. Способ по п. 20, дополнительно предусматривающий мониторирование экспрессии ISG15 на уровне либо РНК, либо белка.
33. Иммунологически поляризованная популяция мезенхимальных стволовых клеток, полученная способом по п. 21, обладающая противовоспалительными характеристиками и отмеченная увеличенной экспрессией мРНК CXCL9, OAS1 и ISG15 по сравнению с нестимулированной популяцией мезенхимальных стволовых клеток, причем поли(I:С) доставлен в нестимулированную популяцию мезенхимальных стволовых клеток путем трансфекции.
34. Способ лечения заболевания у субъекта, предусматривающий введение указанному субъекту иммунологически поляризованной популяции мезенхимальных стволовых клеток по п. 33, причем заболевание представляет собой воспалительное нарушение.
35. Способ лечения заболевания у субъекта, предусматривающий введение указанному субъекту иммунологически поляризованной популяции мезенхимальных стволовых клеток по п. 33, причем заболевание представляет собой аутоиммунное нарушение.
36. Способ по п. 35, причем аутоиммунное нарушение представляет собой ревматоидный артрит.
37. Способ по п. 34, причем воспалительное нарушение представляет собой воспалительное заболевание кишечника.
38. Способ по п. 34, причем воспалительное нарушение представляет собой острый неврит зрительного нерва.
39. Способ по п. 34, причем воспалительное нарушение представляет собой болезнь Краббе.
40. Способ по п. 35, причем аутоиммунное нарушение представляет собой диабетическую ретинопатию.
41. Способ по п. 34, причем воспалительное нарушение представляет собой болезнь Крона.
42. Способ по п. 34, причем воспалительное нарушение представляет собой острое повреждение легких.
43. Применение индукционной среды по п. 1 для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, причем иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов.
44. Применение индукционной среды по п. 19 для получения иммунологически поляризованной популяции мезенхимальных стволовых клеток из нестимулированной популяции мезенхимальных стволовых клеток, причем иммунологически поляризованная популяция мезенхимальных стволовых клеток обладает противовоспалительными характеристиками, отмеченными экспрессией противовоспалительных или иммуносупрессивных медиаторов.
45. Применение популяции мезенхимальных стволовых клеток по п. 9 для лечения воспалительного нарушения.
46. Применение популяции мезенхимальных стволовых клеток по п. 9 для лечения аутоиммунного нарушения.
47. Применение популяции мезенхимальных стволовых клеток по п. 9 для изготовления лекарственного средства для лечения воспалительного нарушения.
48. Применение популяции мезенхимальных стволовых клеток по п. 9 для изготовления лекарственного средства для лечения аутоиммунного нарушения.
49. Применение иммунологически поляризованной популяции мезенхимальных стволовых клеток по п. 33 для лечения воспалительного нарушения.
50. Применение иммунологически поляризованной популяции мезенхимальных стволовых клеток по п. 33 для лечения аутоиммунного нарушения.
51. Применение иммунологически поляризованной популяции мезенхимальных стволовых клеток по п. 33 для изготовления лекарственного средства для лечения воспалительного нарушения.
52. Применение иммунологически поляризованной популяции мезенхимальных стволовых клеток по п. 33 для изготовления лекарственного средства для лечения аутоиммунного нарушения.
53. Популяция мезенхимальных стволовых клеток по п. 9, дополнительно содержащая фармацевтический носитель, разбавитель, вспомогательное средство или наполнитель.
54. Композиция по п. 10, дополнительно содержащая фармацевтический носитель, разбавитель, вспомогательное средство или наполнитель.
55. Композиция по п. 11, дополнительно содержащая фармацевтический носитель, разбавитель, вспомогательное средство или наполнитель.
56. Иммунологически поляризованная популяция мезенхимальных стволовых клеток по п. 33, дополнительно содержащая фармацевтический носитель, разбавитель, вспомогательное средство или наполнитель.
| US 20140017787 A1, 16.01.2014 | |||
| НОВОХАТСКИЙ А.С., и др | |||
| "Проблема контаминации клетками и новые подходы к контролю перевиваемых линий", Вопросы вирусологии | |||
| Шеститрубный элемент пароперегревателя в жаровых трубках | 1918 |
|
SU1977A1 |
| ВЕЧКАНОВ Е.М, и др | |||
| Основы клеточной инженерии: Учебное пособие | |||
| - Ростов-на-Дону, 2012 | |||
| Регулятор для ветряного двигателя в ветроэлектрических установках | 1921 |
|
SU136A1 |
| US 20050265980 A1, 01.12.2005. | |||
Авторы
Даты
2020-03-27—Публикация
2015-09-24—Подача