Изобретение относится к области биотехнологии и может быть использовано для восстановления кишечной микрофлоры при заболеваниях желудочно-кишечного тракта.
Экосистема кишечника вовлечена во все процессы организма человека и является «вторым мозгом», контролирующим как иммунные процессы, так и метаболические. На сегодняшний день идет постоянные рост числа людей страдающих синдром раздраженного кишечника, аутоиммунными заболеваниями, болезнью Крона, язвенным колитом, инфекционными и другими заболеваниями, которые вызывают или являются следствием нарушения состава или соотношения микробиоты в кишечнике.
Нарастающая антибиотикорезистентность штаммов Clostridium difficile (возбудителя псевдомембранозного колита) ставит под угрозу жизни практически всех людей, перенесших операции, находящихся на длительной госпитализации, либо принимающих курсом антибиотики, так как псевдомембранозный колит (ПМК) является одной из самых распространенных внутрибольничных инфекций, и летальность этого заболевания при некоторых типах течения достигает более 50%. В настоящее время, инфекция Clostridium difficile является показанием к трансплантации фекальной микробиоты (ТФМ). Кроме этого ТФМ позволяет лечить и другие кишечные заболевания. Группа исследователей провела рандомизированное открытое контролируемое клиническое исследование, которое показало 81% улучшения или полного исчезновения диареи уже после первого введения препарата, в отличие от антибиотикотерапиим [1].
Еще одним серьезным заболевание страдают около 20% населения Земли, это синдромом раздраженного кишечника (СРК). Лечение СРК до сих пор проходит только симптоматически, применяется диетотерапия, хотя ТФМ показала отличные результаты, с частотой лечения 36-60% и ремиссией основных симптомов СРК, сохраняющихся более полугода [2]. Более того, регулярно появляются новые данные о том, что ТФМ может привести к значительному клиническому улучшению при таких заболеваниях, как: метаболический синдром на фоне сахарного диабета второго типа [3], рассеянного склероза [4] и расстройств аутического спектра [5].
Широкие возможности применения трансплантации фекальной микробиоты при инфекционных, неврологических и гастроэнтерологических заболеваниях делает ее одним из наиболее перспективных направлений для терапии желудочно-кишечных расстройств.
Во многих странах, в том числе и в России (ФНКЦ ФМБА России г. Москва; ЦНМТ г. Новосибирск) проводится трансплантация фекальной микробиоты. Но до последнего времени в клиниках использовали только свежие пробы доноров, что вызывает сложности при обращении нескольких пациентов и значительно увеличивает стоимость процедуры.
Известен способ фекалотрансплантации, заключающийся в гомогенизировании фекалий донора с физиологическим раствором, с последующей фильтрацией от крупных частиц непереваренной пищи через сито, затем полученную смесь вводят пациентам в течение двух часов [6]. Пациент может получать материал двумя способами – ректальное введение (250-500 мл) или через верхние отделы желудочно-кишечного тракта (с помощью назогастроэнтерального зонда) (50–75 мл) [7]. Известен способ получения композиции, содержащей культивируемую в анаэробных условиях микробиоту кишечника человека [8]. Изобретение относится к композициям анаэробно культивируемой микробиоты, представляющим собой функциональную посевную культуру для восстановления нормального состояния нарушенного микробиома человека, для профилактики и лечения желудочно-кишечных заболеваний.
Также известны способы получения композиций фекальной микробиоты и устройства для их доставки [9]. Трансплантация фекалий достигается посредством перорального приема, назогастрального вливания или клизмы.
В изобретении по подготовки донорского фекального материала к трансплантации описано устройство, которое содержат несколько камер с механизмами перемешивания, фильтрации, с насосами, где происходит подготовка фекалий донора к трансплантации (гомогенизируют фекальную массу с физиологическим раствором и фильтруют ее, с возможностью получения фекального материала различного состава и консистенции) [10].
Недостатками этих способов являются отсутствие возможности хранения микробиоты.
Альтернативой фекальной трансплантации являются препараты пробиотиков, однако, было установлено, что до толстой кишки (основной ареал обитания нормофлоры) в среднем доходит живой всего 1 из 1000000 бактерий в составе пробиотика, более того, пробиотические клетки, способны вступать в антагонистические взаимоотношения с аутоштаммами микроорганизмов пациента. Даже дошедшие до толстой кишки в жизнеспособном состоянии бактерии пробиотиков не способны прижиться на поверхности слизистой оболочке кишечника.
Прототипом заявленного способа является способ получения аутопробиотика, содержащего живые бифидобактерии и лактобактерии [11]. Способ предусматривает выделение бифидобактерий и лактобактерий из фекалий хозяина, после выделения изолированных колоний бифидобактерий и лактобактерий их пересевают на жидкие накопительные питательные среды и вносят биомассу бактерий рода Bacillus.
К недостаткам данного способа относится ограниченный состав микробиоты, низкая концентрация бактерий и продолжительное время ожидания культивирования перед введением препарата, что снижает возможность использования метода при острых заболеваниях, а также использование лабораторных штаммов, которые плохо приживаются и вступают в антагонистические отношения с собственной микробиотой кишечника пациента.
На данный момент не существует стандартизированной методики и способов хранения фекальной микробиоты в оптимальных условиях, что не позволяет произвести трансфер технологии в клиники, тогда как в ней имеется острая необходимость (особенно учитывая возрастающее количество антибиотикорезистентных штаммов Clostridium difficile).
Решением данной проблемы является способ выделения тотальной микробиоты кишечника донора и ее сохранение, что позволит использовать в клинической практике предварительно замороженную готовую к трансплантации микробиоту кишечника.
Техническая задача изобретения - разработка способа выделения и криоконсервации микробиоты кишечника, проверка сохранения их жизнеспособности после криоконсервации и определение КОЕ бифидо- и лактобактерий.
Для решения поставленной задачи предлагается выделить тотальную микробиоту кишечника доноров и криоконсервировать в среде с эмбриональной бычьей сывороткой и с последующим хранением при -80 °C. После чего клетки размораживают при +37°C на водяной бане. Далее микробиоту ресуспендируют в натрий-фосфатном буфере и вводят реципиенту ректально.
Способ включает в себя выделение микробиоты кишечника донора методами фильтрации и центрифугирования в фосфатно-солевом растворе и на градиенте перколла, которую затем промывают 1% фосфатно-солевым раствором и концентрируют центрифугированием при 13000g 20 мин. Полученную клеточную фракцию замораживают в среде с эмбриональной бычьей сывороткой с последующим хранением при -80 ˚С. Полученная тотальная микробиота кишечника восстанавливает собственную микробиоту кишечника пациента и нормальное функционирование желудочно-кишечного тракта.
Метод осуществляют следующим образом:
1. Выделение микробиоты кишечника из фекалий донора.
Для выделения микробиоты кишечника, из 5 г фекалий донора, биоматериал ресуспендировали в 15 мл 1 % раствора PBS с помощью ступки и пестика. Полученную взвесь пропускали через стрейнер с порами 100 мкм (Cell strainer 100 μm Nylon Falcon Acorning Brand) в стерильный фалькон на 50 мл. Осадок, оставшийся на стрейнере, промывали 15 мл 1 % раствора PBS. Затем, для осаждения крупных частиц и удаления непереваренных частиц пищи, полученную массу центрифугировали (Sigma 3-30 ks, Германия) в течение 10 минут с ускорением 5 000g при температуре +4°C.
Надосадочную жидкость отбирали в новый фалькон на 50 мл. Для удаления растворимых солей и других веществ к надосадочной жидкости с микробиотой кишечника добавляли 1% раствор PBS, доводя объем до 30 мл. Далее полученную жидкость, для осаждения микроорганизмов, центрифугировали 15 мин с ускорением 14000g при температуре +4°C. Надосадочную жидкость аспирировали, а осадок микробиоты кишечника ресуспендировали в 5 мл 1 % раствора PBS.
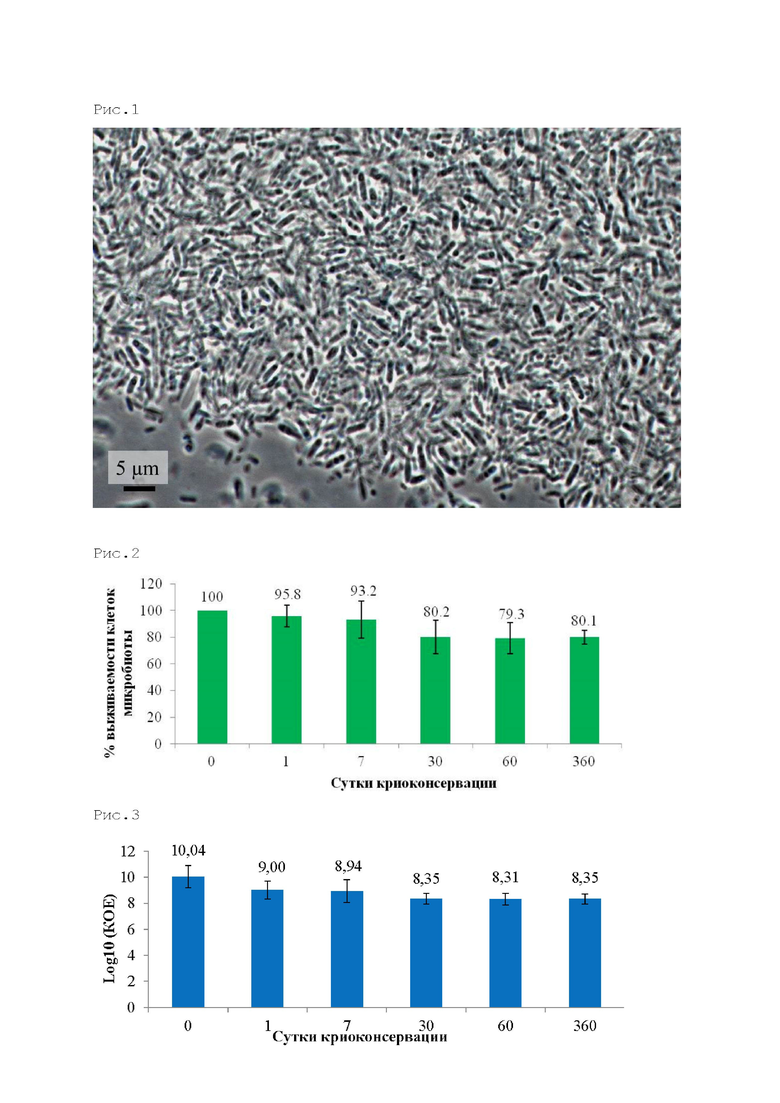
Полученную взвесь с микробиотой наслаивали на градиентную жидкость – 5 мл перколла, плотностью 1,13 г/мл (Sigma, США). Полученный градиент центрифугировали в течение 60 минут с ускорением 10000g при температуре +4°C. Далее пипеткой Пастера собирали клеточную фракцию микроорганизмов на границе раздела фаз (мутно-белое кольцо) и переносили в новые стерильные фальконы объемом 50 мл (рис.1).
Для отмывки полученных клеток от примесей перколла объем клеточной суспензии доводили до 30 мл раствором 1% PBS и центрифугировали 30 минут с ускорением 12 000 g при температуре +4°C. После удаляли надосадочную жидкость, а осажденную микробиоту ресуспендировали в 1 мл раствора 1% PBS. Полученный объем смеси повторно доводили до 30 мл раствором 1% PBS и концентрировали центрифугированием при 13 000 об/мин 15 мин, при температуре +4°C. После чего сливают надосадочную жидкость, а осадок клеток ресуспедируют в 1 мл среды для криозаморозки. Микрофотографии микробиоты кишечника донора представлены на рисунке 1.
2. Криоконсервация микробиоты кишечника
Смесь для криозаморозки содержит в себе 70% эмбриональной телячьей сыворотки, 10 % диметилсульфоксида (ДМСО), 20 % раствор 1% PBS. Подготовленную микробиоту в среде для криозаморозки переносят в криопробирки и сразу переносят в низкотемпературный морозильник (-80°С) на длительное хранение.
3. Подготовка микробиоты кишечника к последующей трансплантации
После криоконсервации донорскую микробиоту кишечника размораживали на водяной бане при +37°С. Суспензию микробиоты переносили в новые 15 мл пробирки, доводили объем до 10 мл раствором 1% PBS и центрифугировали в течение 10 минут с ускорением 10000g при температуре 20°С. Надосадочную жидкость аспирировали, а осадок ресуспендировали в 5 мл раствора 1% PBS. Концентрированную клеточную суспензию микробиоты можно вводить реципиенту непосредственно в кишечник.
4. Исследование жизниспособности микробиоты после криоконсервации
Оценку жизнеспособности бактериальной культуры проводили с помощью реагента МТТ (Sigma, США), который представляет собой тиазолий синий тетразолий бромид (3-(4,5-диметилтиазол-2-ил)-2,5-дифенилтетразолиний бромид).
Непосредственно перед проведением теста на жизнеспособность готовили раствор МТТ: 30 мг МТТ-реагента растворили в 15 мл раствора PBS, аккуратно перемешивали избегая образования пены. После полного растворения реагента МТТ раствор фильтровали через бумажный фильтр. К хранению данный раствор не предназначен.
Тесты на жизнеспособность проводили в трех повторностях для каждого образца, после чего брали среднее значение. В качестве положительного контроля, для достоверности положительной реакции реагента МТТ и энергетических молекул внутри живой клетки, использовали культуру Escherichia coli Rossetta DE3. В качестве отрицательного контроля использовали убитые бактериальные клетки реагентом DMSO, для этого к 10 мкл образца вносили 90 мкл реагента DMSO и нагревали до 50°С в течении 10 минут. В качестве нулевого контроля использовали раствор МТТ, который в последующем вычитался из значений испытуемых образцов в качестве погрешностей.
В эппендорфы на 1,5 мл вносили образцы и растворы по следующей схеме:
1. К0: раствор МТТ,
2. К+: 10 мкл культуры Е. Coli, 90 мкл 1% PBS и 100 мкл р-ра МТТ,
3. К-: 10 мкл исследуемого образца 1, 90 мкл DMSO, 10 мин при 60°С, затем добавиляли 100 мкл р-ра МТТ,
4-6. Образец 1 (10): 10 мкл образца 1, 90 мкл 1% PBS и 100 мкл р-ра МТТ,
7-9. Образец 2 (10): 10 мкл образца 1, 90 мкл 1% PBS и 100 мкл р-ра МТТ,
10-12. Образец 3 (10): 10 мкл образца 1, 90 мкл 1% PBS и 100 мкл р-ра МТТ и т.д.
Растворы аккуратно перемешивали, плотно закрывали эппендорфы и инкубировали 1 час при температуре +4°С.
После инкубации к образцам добавляли по 200 мкл DMSO для разрушения бактериальных клеток и выхода кристаллов формазана в раствор, тщательно перемешивали наконечником пипетки. Затем образцы центрифугировали (Sigma Eppendorf Minispin) 5 мин при 5000 g, для осаждения остатков клеток. Надосадочную жидкость переносили в планшет на 96 лунок и измеряли оптическую плотность на автоматическом микропланшетном фотометре Sunrise (микропланшетный ридер) (Tecan, Австрия) при длине волны 540 нм.
Повторили выполнения МТТ-теста для каждого образца в течение всего эксперимента, а именно МТТ-тест:
1. непосредственно после выделения тотальной микробиоты кишечника - «свежий образец»,
2. через 1 сутки после криозаморозки,
3. через 7 суток после криозаморозки,
4. через 30 суток после криозаморозки,
5. через 60 суток после криозаморозки,
6. через 1 год (360 суток) после криозаморозки.
За 100% на калибровочном графике принимали оптическую плотность образцов, которые не проходили этап криоконсервации - «свежий образец», с этими показателями сравнивали оптическую плотность образцов после криоконсервации. По истечению суток кроиконсеравации процент жизнеспособных клеток составлял 95,82±8,20; 7 суток - 93,17±14,08, 30 суток - 80,12±12,52; 60 суток - 79,23±11,55; 360 суток - 80,08±5,22. Данные представлены на рис. 2.
Колониеобразующие единицы лакто- и бифидобактерий из микробиоты кишечника до (0 суток) и после (1, 7, 30, 60 и 360 суток) криоконсервации при -80С0 представлены на рис. 3 (десятичный логарифм (Log10) КОЕ). По истечению 1 и 7 суток криозаморозки жизнеспособность микробиоты кишечника во всех образцах практически не меняется и сохраняется около 100-95% от «свежих образцов» (в «свежем образце» КОЕ составлял 3,3438*1010, в образцах после 1 и 7 суток - 2,2605*109 и 2,44865*109 соответственно). По истечению 30 и 60 суток криозаморозки жизнеспособность микробиоты падает незначительно и составляет около 80% (30 суток - 3,26*108, 60 суток - 3,01*108). Образцы по истечению одного года криозаморозки по своей жизнеспособности не отличались от образцов, замороженных на 30 и 60 суток, и составляли также около 80% живых микроорганизмов (360 суток - 3,13*108).
5. Исследование терапевтического потенциала микробиоты кишечника после криоконсервации
Для оценки терапевтического потенциала донорской микробиоты кишечника после криоконсервации проводили исследование in vitro на среде MRS-arap для бифидо- и лактобактерий с установлением количества КОЕ бифидо- и лактобактерий. В качестве контрольных образцов брали фармацевтические препараты Бифидумбактерин и Лактобактерий.
С этой целью 1 мл микробиоты высевали методом предельных разведений в столбике агара (до 10-10) на среде MRS и Блаурокка и культивировали при +37°С в течение 5-10 суток. Контрольные препараты Бифидумбактерин и Лактобактерий перед тем как высевать на среду готовили к посеву: 1 капсулу растворяли в 1 мл 1% PBS. Затем проводили подсчет КОЕ.
Подсчет КОЕ проводили в каждом образце в нескольких вариантах:
1. непосредственно после выделения микробиоты кишечника - «свежий образец»,
2. через 1 сутки после криозаморозки,
3. через 7 суток после криозаморозки,
4. через 30 суток после криозаморозки,
5. через 60 суток после криозаморозки,
6. через 1 год (360 суток) после криозаморозки.
Исследование КОЕ в образцах показало максимальное количество колоний в «свежем образце» - 3,3*1010, в образцах после криоконсервации 1 и 7 суток 2,2*109 и 2,4*109, соответственно. В образцах после 30 суток и 1 года криоконсервации количество КОЕ практически не изменялось и составляло 3,01-3,26*108, что говорит о высоком потенциале способа криоконсервации микробиоты, сохранение ее терапевтических и пробиотических свойств по сравнению с аналогами.
Таким образом, разработанный способ выделения и сохранения тотальной микробиоты кишечника человека показывает высокую концентрацию микроорганизмов по сравнению с аналогами, а также высокий процент жизнеспособности микроорганизмов после криозаморозки. Одним из главных достоинств данного способа является его простота и доступность, что позволит увеличить количество лиц с положительными результатами лечения заболеваний ЖКТ и сокращение периода ожидания и лечения. Полученные результаты свидетельствуют о перспективности данного способа для применения в клинической практике для трансплантации микробиоты кишечника донора реципиентам с заболеваниями ЖКТ.
Источники информации:
1. Van Nood Е. Duodenal infusion of donor feces for recurrent Clostridium difficile / Van Nood E., A. Vrieze, M. Nieuwdorp et al. // New England Journal of Medicine. - 2013. - №368. - P. 407-415.
2. Smits L.P. Therapeutic potential of fecal microbiota transplantation / L.P. Smits, K.E. Bouter, W.M. de Vos et al. // Gastroenterology. - 2013. - №145. - Issue 5. - P. 946-953.
3. Vrieze A. Transfer of intestinal microbiota from lean donors increases insulin sensitivity in individuals with metabolic syndrome / A. Vrieze, E. Van Nood, F. Holleman et al. // Gastroenterology. - 2012. - №143(4). - P. 913-916.
4. Borody T.J. Fecal microbiota transplantation (FMT) in multiple sclerosis (MS) [abstract] / T.J. Borody, S.M. Leis, J. Campbell et al. // The American journal of Gastroenterology. - 2011. - №106. - P. 352.
5. Aroniadis O.C. Fecal microbiota transplantation: past, present and future / O.C. Aroniadis, L.J. Brandt // Current opinion in Gastroenterology. - 2013. - №29. - P. 79-84.
6. Hamilton M.J. Standardized frozen preparation for transplantation of fecal microbiota for recurrent Clostridium difficile infection / M.J. Hamilton, A.R. Weingarden, M.J. Sadowsky et al. // The American journal of Gastroenterology. - 2012. - №107. - P. 761-767.
7. Brandt L.J. An overview of fecal microbiota transplantation: technigues, indications, and outcomes / L.J. Brandt, O.C. Aroniadis // Gastrointestinal Endoscopy. - 2013. - №78. - P. 240-249
8. Патент EA 201490512 «Композиции, содержащие культивируемую в анаэробных условиях микробиоту кишечника человека».
9. Патент WO 2012016287 «Композиции для трансплантации фекальной флоры и способы их получения и применения и устройства для их доставки».
10. Патент RU 2659417 «Устройство для подготовки донорского фекального материала к трансплантации».
11. Патент RU 2580002 «Способ получения аутопробиотика, содержащего живые бифидобактерий и лактобактерий».
Приложение
Рисунок 1. Микрофотографии тотальной микробиоты кишечника.
Рисунок 2. Процент живых клеток микробиоты кишечника после криоконсервации.
Рисунок 3. Колониеобразующие единицы лакто- и бифидобактерий из микробиоты кишечника до и после криоконсервации при -80С.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ восстановления собственной кишечной микробиоты после антибиотикотерапии | 2021 |
|
RU2775887C1 |
| Способ получения лиофильно высушенного препарата фекалий для трансплантации фекальной микробиоты | 2021 |
|
RU2809736C2 |
| СПОСОБ ОЦЕНКИ ЭФФЕКТИВНОСТИ ТРАНСПЛАНТАЦИИ ФЕКАЛЬНОЙ МИКРОБИОТЫ У ПАЦИЕНТОВ С ИММУННОЙ РЕАКЦИЕЙ ПОСЛЕ ТРАНСПЛАНТАЦИИ ГЕМОПОЭТИЧЕСКИХ СТВОЛОВЫХ КЛЕТОК | 2019 |
|
RU2728241C1 |
| Способ приготовления аутопробиотика на основе анаэробного консорциума бактерий | 2018 |
|
RU2734896C2 |
| СПОСОБ КОРРЕКЦИИ СОСТАВА МИКРОФЛОРЫ КИШЕЧНИКА У ДЕТЕЙ | 2022 |
|
RU2801611C1 |
| Штамм Meyerozyma (Pichia) guilliermondii (варианты), используемый для изготовления пре-, про- и аутопробиотических препаратов и продуктов для человека и животных, лечебно-профилактическое средство на его основе и способ его получения (варианты) | 2021 |
|
RU2771136C1 |
| Штамм бактерий Bifidobacterium longum 174 для приготовления регион-специфичных пробиотических препаратов для профилактики и персонализированного лечения заболеваний желудочно-кишечного тракта у жителей Карачаево-Черкесской республики и/или для обогащения традиционного кисломолочного напитка "Гыпы айран" на основе индигенных кефирных зерен | 2023 |
|
RU2803350C1 |
| Способ коррекции дисбиоза кишечника в комплексной терапии вульгарного псориаза | 2023 |
|
RU2823057C1 |
| Защитная среда для криохранения для анаэробных, аэробных, факультативно анаэробных и микроаэрофильных микроорганизмов в фекальной микробиоте | 2019 |
|
RU2726299C1 |
| КОМПОЗИЦИЯ ФЕКАЛЬНОЙ МИКРОБИОТЫ ДЛЯ ПРИМЕНЕНИЯ ДЛЯ УМЕНЬШЕНИЯ ИНДУЦИРОВАННОГО ЛЕЧЕНИЕМ ВОСПАЛЕНИЯ | 2019 |
|
RU2816462C2 |
Изобретение относится к биотехнологии и может быть использовано для восстановления кишечной микрофлоры при заболеваниях желудочно-кишечного тракта, связанного с нарушением процесса переваривания пиши, микрофлоры и наличием кишечных инфекций. Способ предусматривает выделение методами фильтрации через стрейнеры с ячейками 100 мкм и градиентного центрифугирования в фосфатно-солевом растворе и в градиентной жидкости перколл. После чего клетки отмывают 1% фосфатно-солевым раствором и концентрируют центрифугированием при 13 000 об/мин 15 мин и замораживают в крио-среде с эмбриональной бычьей сывороткой с последующим хранением при температуре -80°С. Изобретение позволяет сохранять микробиоту кишечной микрофлоры при заболеваниях желудочно-кишечного тракта. 3 ил.
Способ выделения тотальной микробиоты кишечника человека для трансплантации, включающий выделение микробиоты кишечника медотами фильтрации и центрифугирования, отличающийся тем, что микробиоту кишечника донора выделяют методами фильтрации через стрейнеры с ячейками 100 мкм и градиентного центрифугирования в фосфатно-солевом растворе и в градиентной жидкости перколл, после чего клетки отмывают 1% фосфатно-солевым раствором и концентрируют центрифугированием при 13 000 об/мин 15 мин, после чего клеточную фракцию замораживают в среде с эмбриональной бычьей сывороткой.
| СПОСОБ ПОЛУЧЕНИЯ АУТОПРОБИОТИКА, СОДЕРЖАЩЕГО ЖИВЫЕ БИФИДОБАКТЕРИИ И ЛАКТОБАКТЕРИИ | 2015 |
|
RU2580002C1 |
| ЮДИН С.М | |||
| и др | |||
| Анализ микробиоты человека | |||
| Российский и зарубежный опыт, Международный журнал прикладных и фундаментальных исследований, 2018, N 11, ч.1, с | |||
| Ручной прибор для загибания кромок листового металла | 1921 |
|
SU175A1 |
| НИКОНОВ Е.Л., ГУРЕВИЧ К.Г | |||
| Микробиота различных локусов организма | |||
| Научный доклад, М., 2017, с | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| СПОСОБ ПОЛУЧЕНИЯ АУТОПРОБИОТИКА, СОДЕРЖАЩЕГО ЖИВЫЕ БИФИДОБАКТЕРИИ И ЛАКТОБАЦИЛЛЫ | 1999 |
|
RU2139070C1 |
Авторы
Даты
2020-07-21—Публикация
2019-10-24—Подача