Область техники, к которой относится изобретение
[0001] Настоящее изобретение в целом относится к области иммунологии, воспалительных заболеваний и онкоиммунологии. Более конкретно, настоящее изобретение относится к биологически активным биомиметическим молекулам, содержащим Fc-домены иммуноглобулина, к композициям, содержащим такие биомиметики, а также к способам использования таких биомиметиков.
[0002] Изобретение также относится к лечению и профилактике патологических состояний, опосредованных клетками, происходящими из моноцитов, и, более конкретно, к применению стабилизированных функциональных частей Fc-фрагментов IgG при таком лечении и профилактике.
Уровень техники
[0003] Препараты иммуноглобулина из плазмы человека используют с начала 1950-ых для лечения заболеваний, связанных с иммунодефицитом, а позже и более широко для лечения аутоиммунных и воспалительных заболеваний.
[0004] Первоначально препараты иммуноглобулина вводили путем внутримышечной инъекции. Позже использовали иммуноглобулин для внутривенного введения (IVIG), который, как первоначально было показано, являлся эффективным при лечении аутоиммунного заболевания - идиопатической тромбоцитопенической пурпуры (ИТП) (Imbach Р, Barandun S, d'Apuzzo V, et al: High-dose intravenous gammaglobulin for idiopathic thrombocytopenic purpura in childhood. Lancet 1981 Jun 6; 1(8232): 1228-31). IVIG человека (обозначенный в настоящей заявке как "hIVIG") представляет собой препарат на основе стерильного, очищенного иммуноглобулина G (IgG), полученного из смешанной плазмы человека, который обычно содержит более чем 95% немодифицированного IgG, с небольшим и переменным количеством иммуноглобулина A (IgA) или иммуноглобулина М (IgM) (см., например, Rutter A, Luger ТА: High-dose intravenous immunoglobulins: an approach to treat severe immune-mediated and autoimmune diseases of the skin. J. Am. Acad. Dermatol. 2001 Jun; 44(6): 1010-24). На сегодняшний день единственным наиболее распространенным клиническим применением hIVIG является лечение ИТП.
[0005] Несмотря на то, что лечение hIVIG являлось клинически эффективным, у препаратов на основе hIVIG имеется ряд недостатков, к которым относилась вероятность недостаточной стерильности, наличие примесей, недостаточную доступность, а также разброс характеристик препаратов от партии к партии. В частности, в препаратах hIVIG может значительно изменяться содержание иммуноглобулина A (IgA), что может представлять опасность, поскольку IgA вызывает аллергические и анафилактические реакции у реципиентов с дефицитом IgA.
[0006] Ввиду негативных свойств hIVIG существует потребность в улучшенных способах лечения аутоиммунных и воспалительных заболеваний.
[0007] Кроме того, клетки, происходящие из моноцитов, опосредуют многочисленные патологические состояния различных типов. Простое терапевтическое и/или профилактическое средство, предназначенное для применения во многих, если не во всех, таких состояниях было бы бесценным. Сущность изобретения
[0008] Иммунорегуляторные свойства IVIG обусловлены Fc-доменом молекул IgG. Например, в мышиных моделях ИТП немодифицированный IVIG, как и один Fc-фрагмент, демонстрирует терапевтическую эффективность в восстановлении количества тромбоцитов, тогда как выделеннные Fab-фрагменты IVIG не являются терапевтически эффективными (Samuelsson, A., Towers, Т.L. & Ravetch, J.V. Anti-inflammatory Activity of IVIG Mediated Through the Inhibitory Fc Receptor. Science 291, 484-486 (2001)). Более того, Fc, а не Fab-фрагменты IVIG также являются терапевтически эффективными при лечении идиопатической тромбоцитопенической пурпуры как у детей, так и у взрослых (Follea, G. et al. Intravenous plasmin-treated gammaglobulin therapy in idiopathic thrombocytopenic purpura. Nouv Rev Fr Hematol 27, 5-10 (1985); Solal-Celigny, P., Bernard, J., Herrera, A. & Biovin, P. Treatment of adult autoimmune thrombocytopenic purpura with high-dose intravenous plasmin-cleaved gammaglobulins. Scand J Haematol 31, 39-44 (1983); Debre, M. & Bonnet, M.-C. Infusion of Gcgamma fragments for treatment of children with acute immune thrombocytopenic purpura. Lancet 342, 945-49 (1993); Burdach, S.E., Evers, K. & Geurson, R. Treatment of acute idiopathic thrombocytopenic purpura of childhood with intravenous immunoglobulin G: Comparative efficacy of 7S and 5S preparations. J Pediatr 109, 770-775 (1986)).
[0009] Терапевтический эффект IVIG первоначально опосредуется Fc-гамма-рецептором (FcγR) и основан на перекрестном взаимодействии с дендритными клетками (DC) и макрофагами, что обуславливает их долговременный толерогенный эффект. FcγRIIIa играет важную роль в фазе инициации, a FcγRIIb участвует в эффекторной фазе в моделях ИТП на мышах (Samuelsson, A., Towers, T.L. & Ravetch, J.V. Anti-inflammatory Activity of IVIG Mediated Through the Inhibitory Fc Receptor. Science 291, 484-486 (2001); Siragam, V. et al. Intravenous immunoglobulin ameliorates ITP via activating Fc[gamma] receptors on dendritic cells. Nat Med 12, 688 (2006)). Аналогично, исследования на людях показали, что антитела против Fcγ-рецептора эффективны при лечении резистентной формы ИТП (Clarkson, S. et al. Treatment of refractory immune thrombocytopenic purpura with an anti-Fc gamma-receptor antibody. N Engl J Med 314, 1236-1239 (1986)). Важно то, что долговременные толерогенные эффекты обусловлены межклеточными взаимодействиями, как и адаптивный перенос IVIG-обработанных DC эффективен при лечении в моделях ИТП на мышах (Siragam, V. et al. Intravenous immunoglobulin ameliorates ITP via activating Fc[gamma] receptors on dendritic cells. Nat Med 12, 688 (2006)).
[0010] Иммунномодуляторные эффекты IVIG требуют агрегации FcγR. Агрегацию FcγR вызывают димеры IgG, присутствующие в IVIG (5-15% от общего IVIG) (Bleeker, W.K. et al. Vasoactive side effects of intravenous immunoglobulin preparations in a rat model and their treatment with recombinant platelet-activating factor acetylhydrolase. Blood 95, 1856-1861 (2000)). Например, в модели ИТП на мышах обработка IVIG с высоким содержанием "димеров" (димеров полноразмерных молекул иммуноглобулина) приводила к повышению количества тромбоцитов, тогда как "мономеры" IVIG (полноразмерные молекулы иммуноглобулина) не были эффективны (reeling, J.L. et al. Therapeutic efficacy of intravenous immunoglobulin preparations depends on the immunoglobulin G dimers: studies in experimental immune thrombocytopenia. Blood 98, 1095-1099 (2001)). Кроме того, несмотря на то, что фракционирование на ионообменной смоле и полиэтиленгликоле широко используют при получении IVIG для удаления агрегатов IgG, клиническая эффективность IVIG коррелирует с присутствием димеров в сыворотках пациента (Augener, W., Friedman, В. & Brittinger, G. Are aggregates of IgG the effective part of high-dose immunoglobulin therapy in adult idiopathic thrombocytopenic purpura (ITP)? Blut 50, 249-252 (1985)). Важно то, что процентное содержание димеров также коррелирует с вазоактивными побочными эффектами, которые поддаются терапии с применением ацетилгидролазы (Bleeker, W.K. et al. Vasoactive side effects of intravenous immunoglobulin preparations in a rat model and their treatment with recombinant platelet-activating factor acetylhydrolase. Blood 95, 1856-1861 (2000)).
[0011] Настоящее изобретение относится к биологически активным биомиметическим молекулам, к содержащим их композициям, а также к способам их применения. Указанные биомиметики находят широкое применение для лечения иммунологических и воспалительных заболеваний, включая, помимо прочих, аутоиммунные заболевания, а также в качестве биоиммунотерапевтических средств для лечения злокачественной опухоли. Кроме того, некоторые из указанных биомиметиков также находят применение в качестве реагентов, предназначенных, например, для применения в иммунологическом анализе, осуществляющем проверку функции иммуноцитов, а также при диагностике заболевания. Кроме того, биомиметики и композиции по настоящему изобретению обладают преимуществом, которое состоит в преодолении вышеуказанных ограничений hIVIG. Изобретение также относится к лечению и профилактике патологических состояний, опосредованных клетками, происходящими из моноцитов, и, более конкретно, к применению стабилизированных функциональных частей Fc-фрагментов IgG при таком лечении и профилактике.
[0012] В первом варианте осуществления настоящее изобретение направлено на выделенные последовательные страдомеры, содержащие два или более соединенных мономеров страдомера, где каждый из мономеров страдомера включает два или более мономера Fc-домена, где соединение двух или более мономеров страдомера приводит к формированию двух или более Fc-доменов, и где последовательный страдомер специфично связывается с первым Fcγ-рецептором через первый из двух или более Fc-доменов и со вторым Fcγ-рецептором через второй из двух или более Fc-доменов. В предпочтительном варианте осуществления два или более мономеров страдомера связаны через ковалентную связь, дисульфидную связь или посредством химического поперечного сшивания.
[0013] В предпочтительном варианте осуществления настоящего изобретения выделенные последовательные страдомеры состоят из двух соединенных мономеров страдомера. В другом предпочтительном варианте осуществления выделенные последовательные страдомеры состоят из двух соединенных мономеров страдомера, где оба мономера страдомера включают два мономера Fc-домена и где соединение двух мономеров страдомера приводит к формированию двух Fc-доменов. В первом конкретном примере данных вариантов осуществления, направленном на выделенные последовательные страдомеры, по меньшей мере один из двух Fc-доменов включает шарнирную область IgG и СН2 домен IgG. Во втором конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG и СН2 домен IgG. В третьем конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. В четвертом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. В пятом конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. В шестом конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, а также СН2 домен IgG1 или СН2 домен IgG3. В седьмом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. В восьмом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG1. В девятом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG3, СН2 домен IgG3 и СН3 домен IgG3. В десятом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG3.
[0014] Также в указанном первом варианте осуществления каждый из двух или более Fc-доменов относятся к одному классу Fc иммуноглобулина, причем класс Fc иммуноглобулина выбран из группы, состоящей из IgG1, IgG2, IgG3 и IgG4. Альтернативно каждый из двух или более Fc-доменов относятся к различным классам Fc иммуноглобулина, причем указанный класс Fc иммуноглобулина выбран из группы, состоящей из IgG1, IgG2, IgG3 и IgG4.
[0015] Кроме того, в указанном первом варианте осуществления первый и второй Fc-γ пецепторы независимо представляют собой Fc-γ пецептор I, Fc-γ пецептор II, Fc-γ пецептор III или Fc-γ пецептор IV. Предпочтительно и первый, и второй Fc-γ пецепторы являются Fc-γ пецептором IIIa.
[0016] Во втором варианте осуществления настоящее изобретение направлено на выделенные последовательные страдомеры, включающие два соединенных мономера страдомера, где каждый из мономеров страдомера включает два мономера Fc-домена, где соединение двух мономеров страдомера приводит к формированию двух Fc-доменов, где каждый из указанных двух Fc-доменов независимо включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG, и где последовательный страдомер специфично связывается с первым Fc-γ пецептором через первый из двух Fc доменов и со вторым Fc-γ пецептором через второй из двух Fc-доменов. В предпочтительном варианте осуществления два или более мономера страдомера соединены через ковалентную связь, дисульфидную связь или посредством химического поперечного сшивания.
[0017] В первом конкретном примере указанного второго варианта осуществления каждый из двух Fc-доменов относится к одному классу Fc иммуноглобулина, причем класс Fc иммуноглобулина выбран из группы, состоящей из IgG1, IgG2, IgG3 и IgG4. Во втором конкретном примере каждый из двух Fc-доменов относится к различным классам Fc иммуноглобулина, причем указанный класс Fc иммуноглобулина выбран из группы, состоящей из IgG1, IgG2, IgG3 и IgG4. В третьем конкретном примере по меньшей мере один из Fc-доменов включает шарнирную область IgG и СН2 домен IgG. В четвертом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG и СН2 домен IgG. В пятом конкретном примере по меньшей мере один из Fc-доменов включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. В шестом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. В седьмом конкретном примере по меньшей мере один из Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. В восьмом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. В девятом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG1. В десятом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG3, СН2 домен IgG3 и СН3 домен IgG3. В одиннадцатом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG3.
[0018] В третьем варианте осуществления настоящее изобретение относится к выделенным последовательным страдомерам, дополнительно включающим Fab-домен, где каждый из мономеров страдомера включает тяжелую цепь Fab-фрагмента и два мономера Fc-домена, где тяжелая цепь Fab-фрагмента расположена на N-конце или С-конце двух мономеров Fc-домена, где легкая цепь Fab-фрагмента независимо связана с каждой тяжелой цепью Fab-фрагмента, и где Fab-домен обладает антигенсвязывающей активностью. В предпочтительном варианте осуществления каждый из мономеров страдомера дополнительно включает мономер шарнирной области иммуноглобулина, и где мономер шарнирной области иммуноглобулина расположен между тяжелой цепью Fab-фрагмента и двумя мономерами Fc-домена.
[0019] В четвертом варианте осуществления настоящее изобретение направлено на кор-страдомеры, включающие кор-группу, связанную с двумя или более кор-страдомерными единицами, где каждая из двух или более кор-страдомерных единиц включает по меньшей мере один Fc-домен и где каждая из кор-страдомерных единиц независимо выбрана из группы, состоящей из:
(а) Fc-фрагмента, где указанный Fc-фрагмент включает два соединенных мономера Fc-фрагмента, где каждый из указанных мономеров Fc-фрагмента включает мономер Fc-домена и где соединение двух мономеров Fc-фрагмента приводит к формированию Fc-домена,
(b) неполного Fc-фрагмента, где указанный неполный Fc-фрагмент включает два соединенных неполных мономера Fc-фрагмента, где каждый указанный неполный мономер Fc-фрагмента включает мономер Fc-домена и где соединение двух неполных мономеров Fc-фрагмента приводит к формированию Fc-домена,
(c) Fc-домена, где указанный Fc-домен включает два соединенных мономера Fc-домена и где соединение двух мономеров Fc-домена приводит к формированию Fc-домена,
(d) последовательного страдомера, где указанный последовательный страдомер включает два или более соединенных мономеров страдомера, где каждый из указанных мономеров страдомера включает два или более мономеров Fc-домена и где соединение двух или более мономеров страдомера приводит к формированию двух или более Fc-доменов, и
(e) кластерного страдомера, где указанный кластерный страдомер включает два или более мультимеризованных кластерных страдомерных единиц, где каждая указанная кластерная страдомерная единица включает мультимеризирующую область и по меньшей мере один Fc-домен, где каждая указанная кластерная страдомерная единица включает два соединенных мономера кластерной страдомерной единицы, где каждый указанный мономер кластерной страдомерной единицы включает мономер мультимеризирующей области и по меньшей мере один мономер Fc-домена, где соединение двух мономеров кластерной страдомерной единицы приводит к формированию мультимеризирующей области и по меньшей мере одного Fc-домена, и где мультимеризирующие области двух или более кластерных страдомерных единиц мультимеризованы с формированием кластерного страдомера, и
где кор-страдомер специфично связывается с первым Fc-γ пецептором через первую из двух или более кор-страдомерных единиц и со вторым Fc-γ пецептором через вторую из двух или более кор-страдомерных единиц.
[0020] Предпочтительно в указанном четвертом варианте осуществления кор-группа выбрана из группы, состоящей из J-цепи иммуноглобулина, альбумина, липосомы, частицы, пептида и полиэтиленгликоля.
[0021] В предпочтительных вариантах осуществления, относящихся к кор-страдомерам, каждая из двух или более кор-страдомерных единиц независимо является Fc-фрагментом. В альтернативном варианте каждая из двух или более кор-страдомерных единиц независимо является последовательным страдомером.
[0022] В другом предпочтительном варианте осуществления, направленном на кор-страдомеры, кор-страдомер включает две кор-страдомерных единицы, где каждая из двух кор-страдомерных единиц независимо является последовательным страдомером, где последовательный страдомер включает два соединенных мономера страдомера, где оба из указанных мономеров страдомера включают два мономера Fc-домена, и где соединение двух мономеров страдомера приводит к формированию двух Fc-доменов. В первом конкретном примере указанного варианта осуществления по меньшей мере один из Fc-доменов двух или более кор-страдомерных единиц включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. Во втором конкретном примере по меньшей мере один из Fc-доменов двух или более кор-страдомерных единиц включает шарнирную область IgG1 или шарнирную область IgG3, а также СН2 домен IgG1. В третьем конкретном примере каждый из Fc-доменов двух или более кор-страдомерных единиц независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG1. В четвертом конкретном примере по меньшей мере один из Fc-доменов двух или более кор-страдомерных единиц включает шарнирную область IgG и СН2 домен IgG. В пятом конкретном примере каждый из Fc-доменов двух или более кор-страдомерных единиц независимо включает шарнирную область IgG и СН2 домен IgG. В шестом конкретном примере каждый из Fc-доменов двух или более кор-страдомерных единиц независимо включает шарнирную область IgG3, СН2 домен IgG3 и СН3 домен IgG3. В седьмом конкретном примере каждый из Fc-доменов двух или более кор-страдомерных единиц независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG3.
[0023] В указанном варианте осуществления и первый, и второй Fc-γ пецептор независимо представляет собой Fc-γ пецептор I, Fc-γ пецептор II, Fc-γ пецептор III или Fc-γ пецептор IV. Предпочтительно, и первый, и второй Fc-γ пецептор является Fc-γ пецептором IIIa.
[0024] В пятом варианте осуществления настоящее изобретение относится к кластерным страдомерам, включающим две или более мультимеризованные кластерные страдомерные единицы, где каждая кластерная страдомерная единица включает мультимеризирующую область и по меньшей мере один Fc-домен, где каждая кластерная страдомерная единица включает два соединенных мономера кластерной страдомерной единицы, где каждый мономер кластерной страдомерной единицы включает мономер мультимеризирующей области и по меньшей мере один мономер Fc-домена, где соединение двух мономеров кластерной страдомерной единицы приводит к формированию мультимеризирующей области и по меньшей мере одного Fc-домена, где мультимеризирующие области двух или более кластернных страдомерных единиц мультимеризованы с формированием кластерного страдомера, и где кластерный страдомер специфично связывается с первым Fc-γ пецептором через первый Fc-домен и со вторым Fc-γ пецептором через второй Fc-домен.
[0025] В предпочтительных вариантах осуществления мультимеризирующая область выбрана из группы, состоящей из шарнирной области IgG2, СН2 домена IgE, лейциновой, изолейциновой "молнии" и цинкового пальца.
[0026] В другом предпочтительном варианте осуществления кластерные страдомеры включают две, три, четыре или пять мультимеризованных кластерных страдомерных единиц.
[0027] В первом конкретном примере указанного пятого варианта осуществления по меньшей мере один из Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. Во втором конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG1. В третьем конкретном примере по меньшей мере один из Fc-доменов включает шарнирную область IgG и СН2 домен IgG. В четвертом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG и СН2 домен IgG. В пятом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG3, СН2 домен IgG3 и СН3 домен IgG3. В шестом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG3. В седьмом конкретном примере каждый из Fc-доменов независимо включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. В восьмом конкретном примере по меньшей мере одна из кластерных страдомерных единиц включает два или более Fc-домена. В девятом конкретном примере каждая кластерная страдомерная единица включает два или более Fc-домена.
[0028] В указанном варианте осуществления и первый, и второй Fc-γ пецептор независимо представляет собой Fc-γ пецептор I, Fc-γ пецептор II, Fc-γ пецептор III или Fc-γ пецептор IV. Предпочтительно и первый, и второй Fc-γ пецептор являются Fc-γ пецептором IIIa.
[0029] В шестом варианте осуществления настоящее изобретение направлено на страдотела, включающие два или более соединенных мономеров страдомера и Fab-домен, где каждый из мономеров страдомера включает тяжелую цепь Fab-фрагмента и два или более мономеров Fc-домена, где тяжелая цепь Fab-фрагмента расположена на N-конце или С-конце двух или более мономеров Fc-домена, где соединение двух или более мономеров страдомера приводит к формированию двух или более Fc-доменов, где легкая цепь Fab-фрагмента независимо соединена с тяжелой цепью Fab-фрагмента каждого мономера страдомера, где Fab-домен обладает антигенсвязывающей активностью и где страдотело специфично связывается с первым Fc-γ пецептором через первый из двух или более Fc-доменов и со вторым Fc-γ пецептором через второй из двух или более Fc-доменов.
[0030] В предпочтительных вариантах осуществления два или более мономера страдомера связаны через ковалентную связь, дисульфидную связь или посредством химического поперечного сшивания.
[0031] В другом предпочтительном варианте осуществления каждый из указанных мономеров страдомера в страдотелах дополнительно включает мономер шарнирной области иммуноглобулина, и где мономер шарнирной области иммуноглобулина расположен между тяжелой цепью Fab-фрагмента и двумя мономерами Fc-домена.
[0032] В конкретном варианте осуществления страдотело включает два соединенных мономера страдомера, где каждый из указанных мономеров страдомера включает тяжелую цепь Fab-фрагмента и два мономера Fc-домена, и где соединение двух мономеров страдомера приводит к формированию двух Fc-доменов. В первом конкретном примере указанного варианта осуществления по меньшей мере один из двух Fc-доменов включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. Во втором конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG, СН2 домен IgG и СН3 домен IgG. В третьем конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG и СН3 домен IgG. В четвертом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG и СН3 домен IgG. В пятом конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. В шестом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG1 или шарнирную область IgG3, СН2 домен IgG1 или СН2 домен IgG3, а также СН3 домен IgG1 или СН3 домен IgG3. В седьмом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG1. В восьмом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG3, СН2 домен IgG3 и СН3 домен IgG3. В девятом конкретном примере каждый из двух Fc-доменов независимо включает шарнирную область IgG1, СН2 домен IgG1 и СН3 домен IgG3. В десятом конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, а также СН2 домен IgG1 или СН2 домен IgG3. В одиннадцатом конкретном примере по меньшей мере один из двух Fc-доменов включает шарнирную область IgG1 или шарнирную область IgG3, а также СН2 домен IgG1.
[0033] В указанном варианте осуществления и первый, и второй Fc-γ пецепторы независимо представляет собой Fc-γ пецептор I, Fc-γ пецептор II, Fc-γ пецептор III или Fc-γ пецептор IV. Предпочтительно и первый, и второй Fc-γ пецептор являются Fc-γ пецептором IIIa.
[0034] В седьмом варианте осуществления настоящее изобретение направлено на способы изменения иммунного ответа у индивида, включающие введение индивиду, при необходимости, фармацевтической композиции, содержащей терапевтически эффективное количество последовательного страдомера, а также носитель или разбавитель. В предпочтительном варианте осуществления фармацевтическая композиция содержит терапевтически эффективное количество гетерогенной смеси последовательных страдомеров, а также носитель или разбавитель.
[0035] В восьмом варианте осуществления настоящее изобретение относится к способам изменения иммунного ответа у индивида, включающие введение индивиду, при необходимости, фармацевтической композиции, включающей терапевтически эффективное количество кор-страдомера, а также носитель или разбавитель. В предпочтительном варианте осуществления фармацевтическая композиция содержит терапевтически эффективное количество гетерогенной смеси кор-страдомеров, а также носитель или разбавитель.
[0036] В девятом варианте осуществления настоящее изобретение относится к способам изменения иммунного ответа у индивида, включающие введение индивиду, при необходимости, фармацевтической композиции, включающей терапевтически эффективное количество кластерного страдомера, а также носитель или разбавитель. В предпочтительном варианте осуществления фармацевтическая композиция содержит терапевтически эффективное количество гетерогенной смеси кластерных страдомеров, а также носитель или разбавитель.
[0037] В десятом варианте осуществления настоящее изобретение относится к способам изменения иммунного ответа у индивида, включающие введение индивиду, при необходимости, фармацевтической композиции, включающей терапевтически эффективное количество страдотела, а также носитель или разбавитель. В предпочтительном варианте осуществления фармацевтическая композиция включает терапевтически эффективное количество гетерогенной смеси страдотел, а также носитель или разбавитель.
[0038] В одиннадцатом варианте осуществления настоящее изобретение относится к способам скрининга антитела на предмет специфичной активности в отношении клетки иммунной системы, включающим: (а) контакт гомогенной популяции клеток иммунной системы с антителом-кандидатом, (b) измерение активности популяции клеток (а), (с) контакт с гомогенной популяцией клеток того же типа клеток, как в (а), с последовательным страдомером по п. 1, (d) измерение активности популяции клеток (с), и (е) сравнение активности, измеренной в (b), с активностью, измеренной в (d), осуществляя, таким образом, скрининг антитела на предмет специфичной активности в отношении клетки иммунной системы. В предпочтительном варианте осуществления антитело-кандидат и последовательный страдомер подбирают в соответствии с видами и изотипом. В другом предпочтительном варианте осуществления сравнение в (е) является отношением активности, измеренной в (d), к активности, измеренной в (b).
[0039] В двенадцатом варианте осуществления настоящее изобретение относится к способам ингибирования активности клетки, происходящей из моноцита (MDC). Способ включает контакт клетки с композицией, содержащей подложку, с которой связан Fc-реагент. Контакт может быть осуществлен in vitro, in vivo или ex vivo. Клетка может находиться в организме животного, например, животного с заболеванием, опосредованным клетками, происходящими из моноцитов (MDCMC), или животного, которое подвергается риску, развития указанного заболевания. Клетка может являться, например, дендритной клеткой, макрофагом, моноцитом или остеокластом.
[0040] В тринадцатом варианте осуществления настоящее изобретение относится к способам лечения, которые включают введение животному композиции, включающей подложку, с которой связан Fc-реагент, причем животное страдает заболеванием, опосредованным клетками, происходящими из моноцитов (MDCMC), или подвергается риску его развития.
[0041] Ниже приведены варианты осуществления, общие для двух указанных способов (двенадцатого и тринадцатого варианта осуществления).
[0042] Животное может являться, например, человеком.
[0043] Fc-реагент может содержать или представлять собой функциональную часть Fc-фрагмента человека, например, Fc-фрагмент IgG1 человека, Fc-фрагмент IgG3 человека, IgG2 человека или Fc-фрагмент IgG4 человека. Кроме того, он может содержать или представляет собой молекулу IgG. Fc-реагент может также являться или включать функциональную часть Fc-фрагмента не человека.
[0044] Подложка может представлять собой или содержать синтетический полимер, например, нейлон, тефлон, дакрон, поливинилхлорид,, ПЭУ (полиэфируретан), ПТФЭ (политетрафторэтилен) или ПММА (полиметилметакрилат). Подложка может содержать или представлять собой металл или металлический сплав, например, нержавеющую сталь, платину, иридий, титан, тантал, никельтитановый сплав или кобальтохромовый сплав. Подложка может содержать или представлять собой ткань животных или препарат ткани животных, например, тканевый или органный трансплантат, кость (например, остеогенную ткань) или хрящ. Подложка может содержать или представлять собой белок, например, коллаген или кератин. Подложка может также представлять собой или содержать полисахарид, например, агарозу. Кроме того, подложка может содержать или представлять собой тканевый матрикс, например, ацеллюлярный тканевый матрикс. Подложка может содержать или представлять собой клетку животного (например, клетку, восстанавливающую ткань, такую как фибробласты или мезенхимальная стволовая клетка). Подложка может содержать или представлять собой соль, например, сульфат кальция. Кроме того, подложка может представлять собой или содержать гель или крем. Также она может содержать или представлять собой силикон или силастик. Также она может содержать или представлять собой натуральное волокно, например, шелк, хлопок или шерсть.
[0045] Подложка может представлять собой комплекс, формирующий поры в мембране или имплантируемое медицинское устройство, такое как стент (например, сосудистый стент, такой как коронарный стент; стент, размещаемый в дыхательных путях, такой как эндотрахеальный или назальный стент; желудочно-кишечный стент, такой как билиарный или панкреатический стент; или мочеточниковый стент, такой как уретральный стент). Также она может являться хирургической нитью (например, шелковой нитью, хромированным кетгутом, нейлоновой, полимерной или металлической нитью, или хирургическим зажимом (например, зажимом при аневризме)). Кроме того, подложка может являться искусственным бедром, искусственным тазобедренным суставом, искусственным коленом, искусственным коленным суставом, искусственным плечом, искусственным плечевым суставом, искусственным пальцевым суставом (руки или ноги), костной пластинкой, костным штифтом, имплантом при переломе кости, имплантом межпозвоночного диска, костным цементом, или прослойкой из костного цемента. Она может являться артериально-венозным шунтом, имплантируемой проволокой, кардиостимулятором, искусственным сердцем, прибором, поддерживающим работу сердца, кохлеарным имплантом, имплантируемым дефибриллятором, стимулятором спинного мозга, стимулятором центральной нервной системы, имплантом перифирического нерва, зубным протезом или зубной коронкой. Кроме того, подложка может являться устройством или сеткой для защиты больших сосудов от эмболии, подкожным устройством, кожным пластырем или пластырем на подслизистую, или имплантируемым устройством для доставки лекарственного средства.
[0046] Подложка может также являться трансплантатом большого кровеносного сосуда, где кровеносный сосуд является, например, сонной артерией, бедренной артерией или аортой. Также она может являться подкожным имплантом, корнеальным имплантом, искусственным хрусталиком или контактной линзой.
[0047] Подложка может находиться в форме, например, листа, гранулы, сетки, частицы порошка, нити, гранулы или волокна. Подложка может содержать или представлять собой твердое, полутвердое или гелеобразное вещество. Таким образом, подложка содержит вещества, которые практически нерастворимы в водных растворителях, например, жирорастворимый липид, такой как липосома.
[0048] MDCMC может являться воспалительным заболеванием, аутоиммунным заболеванием, злокачественной опухолью, нарушением плотности кости, острой инфекцией или хронической инфекцией.
[0049] MDCMC может являться гематоиммунологическим процессом, например, идиопатической тромбоцитопенической пурпурой, аллоиммунной/аутоиммунной тромбоцитопенией, приобретенной иммунной тромбоцитопенией, аутоиммунной нейтропенией, аутоиммунной гемолитической анемией, Парвовирус В19-ассоциированной эритроцитарной аплазией, приобретенным аутоиммунитетом против фактора VIII, приобретенной болезнью фон Виллебранда, множественной миеломой и моноклональной гаммапатией неизвестной этиологии, сепсисом, апластической анемией, истинной эритроцитарной аплазией, анемией Даймонда-Блекфана, гемолитической болезнью новорожденных, иммуноопосредованной нейтропенией, невосприимчивостью к переливанию тромбоцитарной массы, неонатальной посттрансфузионной пурпурой, гемолитическим уремическим синдромом, системными васкулитами, тромбоцитопенической тромбогемолитической пурпурой или синдромом Эвана.
[0050] Альтернативно, MDCMC может являться нейроиммунологическим процессом, например, синдром Гийена-Барре, хронической воспалительной демиелинизирующей полирадикулоневропатией, парапротеинемической IgM демиелинизирующей полиневропатией, миастеническим синдромом Ламберта-Итона, миастенией гравис, многоочаговой двигательной невропатией, боковым амиотрофическим склерозом, ассоциируемым с антителами против GM1, демиелинизацией, рассеянным склерозом и невритом зрительного нерва, синдромом мышечной скованности, паранеопластической дегенерацией мозжечка, вызванной анти-Yo антителами, паранеопластическим энцефаломиелитом, сенсорной невропатией, вызванной анти-Hu антителами, эпилепсией, энцефалитом, миелитом, миелопатией, особенно связанной с Т-лимфотропным вирусом человека первого типа, аутоиммунной диабетической невропатией или острой идиопатической вегетативной невропатией.
[0051] MDCMC может являться ревматическим процессом, например, болезнью Кавасаки, ревматоидным артритом, синдромом Фелти, АНЦА-положительным васкулитом, спонтанным полимиозитом, дерматомиозитом, антифосфолипидными синдромами, повторным самопроизвольным абортом, системной красной волчанкой, ювенильным идиопатическим артритом, синдромом Рейно, CREST-синдромом или увеитом.
[0052] Кроме того, MDCMC может являться дерматоиммунологическим процессом, например, эпидермальным некролизом, гангреной, гранулемой, аутоиммунными заболеваниями кожи с развитием нарывов, включая вульгарную пузырчатку, буллезный пемфигоид и эксфолиативную пузырчатку, витилиго, синдромом стрептококкового токсического шока, склеродермией, системным склерозом, включая диффузный и локальный кожный системный склероз, атопическим дерматитом или стероидозависимым атопическим дерматитом.
[0053] Кроме того, MDCMC может являться скелетно-мышечным иммунологическим заболеванием, например, миозитом с включенными тельцами, некротизирующим фасцитом, воспалительными миопатиями, миозитом, анти-декорин (BJ антиген) миопатией, паранеопластической некротической миопатией, вакуолизирующей миопатией, сцепленной с Х-хромосомой, пеницилламин-индуцированным полимиозитом, атеросклерозом, ишемической болезнью сердца или кардиомиопатией.
[0054] MDCMC может также являться желудочно-кишечным иммунологическим процессом, например, пернициозной анемией, аутоиммунным хроническим активным гепатитом, первичным биллиарным циррозом печени, глютеновой энтеропатией, герпетиформным дерматитом, криптогенным циррозом печени, реактивным артритом, болезнью Крона, болезнью Уипла, язвенным колитом или склерозирующим холангитом.
[0055] MDCMC может являться, например, гомологичной болезнью (РТПХ), антитело-опосредованным отторжением трансплантата, отторжением трансплантата костного мозга, постинфекционным воспалением, лимфомой, лейкозом, неоплазией, астмой, сахарным диабетом I типа с антителами против бета-клеток, синдромом Шегрена, смешанным поражением соединительной ткани, болезнью Аддисона, синдромом Фогта-Коянаги-Харады, мембранозно-пролиферативным гломерулонефритом, синдромом Гудпасчера, болезнью Грейвса, тиреоидитом Хашимото, гранулематозом Вегенера, микрополиартеритом, синдромом Черджа-Стросс, узелковым полиартериитом или полиорганной недостаточностью.
[0056] Когда MDCMC является злокачественной опухолью, тогда MDCMC может быть фибросаркомой, миксосаркомой, липосаркомой, хондросаркомой, остеобластической саркомой, хордомой, ангиосаркомой, эндотелиосаркомой, лимфангиосаркомой, лимфангиоэндотелиосаркомой, синовиомой, мезотелиомой, саркомой Юинга, лейомиосаркомой, рабдомиосаркомой, карциномой толстой кишки, раком поджелудочной железы, раком молочной железы, раком яичников, раком предстательной железы, плоскоклеточной карциномой, базальноклеточной карциномой, аденокарциномой, карциномой потовой железы, карциномой сальной железы, папиллярной карциномой, папиллярными аденокарциномами, цистаденокарциномой, медуллярной карциномой, бронхогенной карциномой, почечноклеточной карциномой, гепатомой, карциномой желчных протоков, хориокарциномой, семиномой, таратокарциномой, опухолью Вилмса, раком шейки матки, опухолью яичка, карциномой легкого, мелкоклеточной карциномой легкого, карциномой мочевого пузыря, эпителиальной карциномой, глиомой, астроцитомой, медуллобластомой, краниофарингиомой, эпендимомой, пинеаломой, гемангиобластомой, невромой слухового нерва, олигодендроглиомой, менингиомой, меланомой, нейробластомой, ретинобластомой, лейкозом, лимфомой, множественной миеломой, макроглобулинемией Вальденстрема, миелодиспластической болезнью, болезнью тяжелых цепей, нейроэндокринными опухолями или шванномой.
[0057] Если MDCMC является заболеванием, связанным с нарушением плотности кости, то MDCMC может являться остеопорозом, остеопенией, врожденным остеопетрозом, идиопатическим гипогонадотропным гипогонадизмом, нервной анорексией, незаживающим переломом, постклимактерическим остеопорозом, дефицитом или избытком витамина D, первичным или вторичным гиперпаратиреозом, болезнью щитовидной железы или токсичностью бисфосфоната.
[0058] Когда MDCMC является острой инфекцией, тогда MDCMC может являться: грибковым заболеванием, включая кандидоз, кандидемию или аспергиллез; бактериальным заболеванием, включающим инфекции, вызванные стафилококком, включая метициллин-устойчивый Staphylococcus aureus, стрептококковые инфекции кожи и орофарингеальные заболевания или сепсис, вызванный грамм-отрицательными бактериями; микобактериальной инфекцией, включая туберкулез; вирусной инфекцией, включая мононуклеоз, респираторную синцитиальную вирусную инфекцию или опоясывающий герпес; паразитарной инфекцией, включая малярию, шистосомоз или трипаносомоз.
[0059] Когда MDCMC является хронической инфекцией, тогда MDCMC может являться онихомикозом; бактериальным заболеванием, включая инфекцию Helicobacter pylori; микобактериальной инфекцией, включая туберкулез; вирусной инфекцией, включая инфекцию, вызванную вирусом Эпштейна-Барра, инфекцию, вызванную вирусом папилломы человека, или инфекцию, вызванную вирусом простого герпеса; или паразитарной инфекцией, включая малярию или шистосомоз.
[0060] В четырнадцатом варианте осуществления настоящее изобретение относится к композиции, которая содержит или является имплантируемым или присоединяемым медицинским устройством и Fc-реагентом, связанным с ним.
[0061] В пятнадцатом варианте осуществления настоящее изобретение относится к набору, который содержит имплантируемое или присоединяемое медицинское устройство и Fc-реагент. В обоих указанных вариантах осуществления имплантируемое или присоединяемое медицинское устройство и Fc-реагент могут являться любыми из описанных в настоящей заявке. Набор может дополнительно содержать подходящий контейнер.
[0062] Дополнительные преимущества и признаки настоящего изобретения будут очевидны из последующего подробного описания, фигур и примеров, которые иллюстрируют предпочтительные варианты осуществления изобретения.
[0063] Вышеизложенное в общих чертах довольно широко описывает признаки и технические преимущества настоящего изобретения, чтобы последующее подробное описание изобретения могло быть лучше понято. Дополнительные признаки и преимущества изобретения, которые образуют объект настоящего изобретения, будут описаны далее. Для специалиста в данной области очевидно, что концепция и конкретные раскрытые варианты осуществления изобретения могут использоваться как основа для изменения или проектирования других структур, осуществляя те же самые задачи настоящего изобретения. Для специалиста в данной области очевидно, что такие эквивалентные структуры не выходят за рамки объема и не изменяют сущность настоящего изобретения, сформулированного в прилагаемой формуле изобретения. Новые признаки, которые, как полагают, являются существенными для изобретения, а также его структуры и способа осуществления, вместе с другими объектами и преимуществами, будут более понятны из последующего описания, рассматриваемого в совокупности с сопровождающими фигурами. Впрочем, следует учитывать, что каждая из фигур приведена исключительно в целях иллюстрации и описания, и не должна рассматриваться как ограничивающая настоящее изобретение.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[0064] На фиг. 1А схематически показаза нативная структура мономера Fc-фрагмента из IgG1, шарнирная область которого связана с СН2 доменом, который связан с СН3 доменом; на фиг. 1В показан самоагрегированный, нативный Fc-фрагмент IgG1, сформированный из двух связанных мономеров Fc-фрагмента.
[0065] На фиг. 1С схематически показана нативная структура мономера Fc-фрагмента из IgG3, шарнирная область которого связана с СН2 доменом, который связан с СН3 доменом; на фиг. 1D показан самоагрегированный, нативный Fc-фрагмент IgG3, сформированный из двух связанных мономеров Fc-фрагмента.
[0066] На фиг. 2А и 2В показаны агрегаты более высокого порядка нативной структуры мономера Fc-фрагмента, показанной на фиг. 1В. Фрагменты Fc могут естественно мультимеризоваться в димеры димера (то есть тетрамеры) или даже в агрегаты-мультимеры еще более высокого порядка.
[0067] На фиг. 3А схематично показано нативное антитело IgG1, имеющее нативный Fab фрагмент, связанный с Fc-фрагментом в шарнирной области Fc-фрагмента; на фиг. 3В показана аналогичная структура IgG3.
[0068] На фиг. 4А показан мономер страдомер, состоящий из двух мономеров Fc-домена IgG1; на фиг. 4В показана альтернативная структура мономера страдомера, в котором IgG1 Fc - IgG3 Fc - IgE Fc связаны последовательно.
[0069] На фиг. 5А и В показаны мономеры страдомера из фиг. 4А и В, автодимеризованные в последовательный страдомер благодаря способности, свойственной составляющим мономерам Fc-домена.
[0070] На фиг. 6А показан мономер страдомера, содержащий IgG1 Fc - IgG1 (шарнирная область-СН2); на фиг. 6В показан страдомер, содержащий IgG1 (шарнирная область-СН2) - IgG3 (шарнирная область-СН2) - IgE (шарнирная область-СН2).
[0071] На фиг. 7А и В показаны мономеры страдомера 6А и В, автодимеризованные в последовательный страдомер благодаря способности, свойственной составляющим мономерам Fc-домена.
[0072] На фиг. 7С показан последовательный страдомер, содержащий IgE (шарнирная область)-IgG1 Fc-IgG1 (шарнирная область-СН2)-IgE (СН3). На фиг. 7D показан последовательный страдомер, содержащий IgG3Fc - IgG1Fc.
[0073] На фиг. 8А показана конструкция страдотела, содержащая Fab с последовательной структурой страдомера, при этом каждый мономер страдомера содержит два мономера IgG1 СН2-СН3, происходящих из Fc-домена; на фиг. 8В показана конструкция страдотела, как и в 8А, но при этом в структуре страдомера содержится IgG1 Fc, связанный с IgG3 Fc, связанным с IgE Fc.
[0074] На фиг. 9А показано страдотело IgG1 Fc - IgG1 (шарнирная область-СН2); на фиг. 9В показано страдотело IgG1 (шарнирная область-СН2) - IgG3 (шарнирная область-СН2) - IgE (шарнирная область-СН2)3.
[0075] На фиг. 10А показан мономер страдомера IgG1 (шарнирная область-СН2) - IgG3 СН3-IgM СН4 и белок J-цепи; на фиг. 10В показан кор-страдомер на основе пентамерного страдомера фиг. 10А, сформированного в результате соединения через СН4 домен IgM к J-цепи.
[0076] На фиг. 10С показан мономер страдомера IgG1 Fc - IgG1 Fc - IgM CH4 и белок J-цепи; На фиг. 10D показан кор-страдомер на основе пентамерного страдомера фиг. 10С, сформированного в результате соединения через СН4 домен IgM к J-цепи.
[0077] На фиг. 11А показан мономер страдомера IgG1 Fc - IgG1 (шарнирная область-СН2). На фиг. 11В показано, как мономер страдомера из фиг. 11А может автодимеризоваться, формируя последовательный страдомер. На фиг. 11С показано, как в том же мономере страдомера из фиг. 11А мономерные Fc-домены могут выравниватся с теми же или подобными мономерами Fc-домена на другом мономере страдомера, но не автодимере, формируя, таким образом, страдомер, состоящий из того же мономера страдомера, как и автодимер, но со структурой с эффектом молнии.
[0078] На фиг. 12А показан мономер IgG3 Fc - IgG1 Fc страдомера. На фиг. 12В показано, что добавление второго IgG3 Fc, сопровождаемое автодимеризацией, может приводить к формированию разветвленного структурированного страдомера IgG3 Fc - IgG1 Fc -IgG3 Fc.
[0079] На фиг. 13А показан мономер IgE CH2 - IgG1 Fc - IgG1 (шарнирная область-СН2) - IgE CH4 страдомера. На фиг. 13В показан автодимер мономера фиг. 13А и выделены два сформированных сайта связыванию FcγR.
[0080] На фиг. 14А показан страдомер, состоящий из двух Fc-доменов IgG1, к которым присоединен линкер. На фиг. 14В показан страдомер, состоящий из двух последовательных страдомеров (а именно в каждом случае страдомера 2 (IgG1 Fc)), соединенных линкером.
[0081] На фиг. 15А показаны нуклеотидная (SEQ ID NO: 1) и аминокислотная (SEQ ID NO: 2) последовательности Fc-фрагмента IgG1 человека. На фиг. 15В показаны нуклеотидная (SEQ ID NO: 3) и аминокислотная (SEQ ID NO: 4) последовательности Fc-фрагмента IgG2 человека. На фиг. 15С показаны нуклеотидная (SEQ ID NO: 5) и аминокислотная (SEQ ID NO: 6) последовательности Fc-фрагмента IgG3 человека. На фиг. 15D показаны нуклеотидная (SEQ ID NO: 7) и аминокислотная (SEQ ID NO: 8) последовательности Fc-фрагмента IgG4 человека.
[0082] На фиг. 16 показаны нуклеотидная (SEQ ID NO: 17) и аминокислотная (SEQ ID NO: 18) последовательности конструкции, включающей (сигнальную последовательность IgK - Fc-фрагмент IgG1 Fc-фрагмент IgG1). Аминокислотная последовательность IgK сигнала выделена жирным шрифтом. Аминокислотная последовательность первого Fc-фрагмента IgG1 подчеркнута одинарной линией. Аминокислотная последовательность второго Fc-фрагмента IgG1 подчеркнута двойной линией. Серии и лизин, отмеченные звездочкой, являются аминокислотами, которые могут быть подвергнуты мутации с целью изменения связывания с Fc-γ пецептором.
[0083] На фиг. 17 показаны нуклеотидная (SEQ ID NO: 19) и аминокислотная (SEQ ID NO: 20) последовательности конструкции, включающей (сайты рестрикции - сигнальную последовательность IgK сайты рестрикции - IgG1 (шарнирная область-СН2-СН3) - сайты рестрикции - эпитоп таги (V5 и His) - STOP). Аминокислотная последовательность IgK сигнала выделена жирным шрифтом. Аминокислотная последовательность Fc-фрагмента IgG1 подчеркнута одинарной линией. Аминокислотная последовательность V5-тага подчеркнута пунктирной линией. Аминокислотная последовательность His-тага подчеркнута жирной линией.
[0084] На фиг. 18 показаны нуклеотидная (SEQ ID NO: 21) и аминокислотная (SEQ ID NO: 22) последовательности конструкции, включающей {сайты рестрикции - сигнал IgK - сайты рестрикции - IgG1 (шарнирная область-СН2-СН3)- сайт XbaI - IgG1 (шарнирная область-СН2-СН3) - STOP}. Аминокислотная последовательность сигнала IgK выделена жирным шрифтом. Аминокислотная последовательность первого Fc-фрагмента IgG1 подчеркнута одинарной линией. Аминокислотная последовательность второго Fc-фрагмента IgG1 подчеркнута двойной линией.
[0085] На фиг. 19 показаны нуклеотидная (SEQ ID NO: 23) и аминокислотная (SEQ ID NO: 24) последовательности конструкции, включающей {сайты рестрикции - сигнал IgK - сайты рестрикции - IgG1 (шарнирная область-СН2-СН3) сайт XbaI - IgG1 (шарнирная область-СН2-СН3) - эпитоп таги (V5 и His) - STOP}. Аминокислотная последовательность сигнала IgK выделена жирным шрифтом. Аминокислотная последовательность первого Fc-фрагмента IgG1 подчеркнута одинарной линией. Аминокислотная последовательность второго Fc-фрагмента IgG1 подчеркнута двойной линией. Аминокислотная последовательность V5-тага подчеркнута пунктирной линией. Аминокислотная последовательность His-тага подчеркнута жирной линией.
[0086] На фиг. 20А показаны нуклеотидная (SEQ ID NO: 31) и аминокислотная (SEQ ID NO: 32) последовательности N-концевой сигнальной последовательности FcRgammaIIIa, в которой полиморфизм фенилаланина (F) выделен жирным шрифтом и подчеркнут.Вариабельная нуклеиновая кислота также выделена жирным шрифтом и подчеркнута. На фиг. 20В показаны нуклеотидная (SEQ ID NO: 33) и аминокислотная (SEQ ID NO: 34) последовательности N-концевой сигнальной последовательности FcRgammaIIIa, в которой полиморфизм валина (V) выделен жирным шрифтом и подчеркнут. Вариабельная нуклеиновая кислота также выделена жирным шрифтом и подчеркнута. Обе конструкции содержат С-концевой гекса-His-Tar для очистки.
[0087] На фиг. 21 показаны нуклеотидная (SEQ ID NO: 25) и аминокислотная (SEQ ID NO: 26) последовательности конструкции, включающей {сайты рестрикции - сигнал IgK - сайт EcoRV - IgG3 (шарнирная область-СН2-СН3)-IgG1 (шарнирная область-СН2-СН3) сайты рестрикции - эпитоп таги (V5 и His) - STOP}. Аминокислотная последовательность сигнала IgK выделена жирным шрифтом. Аминокислотная последовательность Fc-фрагмента IgG3 подчеркнута одинарной линией. Аминокислотная последовательность Fc-фрагмента IgG1 подчеркнута двойной линией. Аминокислотная последовательность V5-тага подчеркнута пунктирной линией. Аминокислотная последовательность His-тага подчеркнута жирной линией.
[0088] На фиг. 22 показаны нуклеотидная (SEQ ID NO: 27) и аминокислотная (SEQ ID NO: 28) последовательности конструкции, включающей {сайты рестрикции - сигнал IgK - сайт EcoRV - IgE (СН2) - IgG1 (шарнирная область-СН2-СН3) - IgG1 (шарнирная область-СН2) - IgE (СН4) - STOP}. Аминокислотная последовательность сигнала IgK выделена жирным шрифтом. Аминокислотная последовательность IgE(CH2) домена подчеркнута одинарной линией. Аминокислотная последовательность IgG1 (шарнирная область-Н2-СН3) домена подчеркнута двойной линией. Аминокислотная последовательность IgG1 (Шарнирная область-СН2) домена подчеркнута пунктирной линией. Аминокислотная последовательность IgE(CH4) домена подчеркнута волнистой линией.
[0089] На фиг. 23А показан Fc-фрагмент, а также показано, что такой Fc-фрагмент состоит из двух мономеров Fc-фрагмента и дополнительно включает Fc-домен (пунктирный круг) и неполные Fc-домены (шарнирная область, СН2 и СН3, как обозначено). На фиг. 23В показан состав последовательного страдомера, состоящего из двух мономеров страдомера, которые связаны интер-мономер страдомерной связью. Последовательный страдомер включает по меньшей мере два Fc-домена (обозначенных пунктирными кругами) и может необязательно включать область связывания доменов. На фиг. 23С показан состав кор-страдомера, включающего кор-группу, с которой связаны кор-страдомерные единицы, каждая из которых содержит по меньшей мере один Fc-домен. Кор-страдомерные единицы могут являться Fc-фрагментом, последовательным страдомером или кластерной страдомерной единицей. На фиг. 23D показан состав кластерного страдомера, включающего мультимеризованные кластерные страдомерные единицы, каждая из которых имеет мультимеризирующую область и область, содержащую по меньшей мере один Fc-домен. Кластерная страдомерная единица может являться Fc-фрагментом или последовательным страдомером. Мультимеризирующая область при мультимеризации формирует головку кластерного страдомера. Ножки кластерного страдомера сформированы областями Fc-доменов кластерных страдомерных единиц, которые пространственно менее сжаты, чем мультимеризованная головка кластерного страдомера.
[0090] На фиг. 24 показаны аминокислотные последовательности страдомера, описанного в Таблице 3.
[0091] На фиг. 25 показаны аминокислотные последовательности мономеров неполных Fc-доменов (шарнирная область, СН2 и СН3) IgG1, IgG2, IgG3 и IgG4 человека (Kabat, ЕА, Wu, ТТ, Perry, НМ, Gottesman, KS, and Foeller, C. 1991. Sequences of proteins of immunological interest 5th Ed. US Public Health Services, NIH, Bethesda).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0092] Подход к рациональному молекулярному дизайну соединений, описанных в настоящей заявке, которые предназначены для замены hIVIG, включает рекомбинантное и/или биохимическое получение иммунологически активного биомиметика(ов). В предпочтительных способах соединения-заменители тестировали in vitro, чтобы оценить эффективность каждого соединения-заменителя при связывании Fcγ-рецептора и модулировании иммунной функции. Отдельные соединения-заменители отбирали для дальнейшего анализа in vivo, а также оптимизации дозировки/введения. Соединения заменители могут применяться при лечении, например, аутоиммунных заболеваний, воспалительных заболеваний, остеопороза и злокачественной опухоли. Каждая фаза подробно описана ниже вместе с конкретными примерами осуществлениями.
[0093] Используемые в оригинальном тексте настоящей заявки артикли "а" или "an", при использовании вместе с термином "включающий" в пунктах формулы и/или в описании могут означать "один", но при этом также не исключается значение "один или более, " "по меньшей мере один" и "одир. или более чем один".
[0094] Используемые в настоящем описании термины "биомиметик", "биомиметическая молекула", "биомиметическое соединение", а также подобные термины, относятся к искусственному соединению, которое имитуирует функцию другого соединения, например, смешанных hIVIG, моноклонального антитела или Fc-фрагмента антитела. "Биологически активные" биомиметики являются соединениями, которые обладают биологическими активностями, которые идентичны или по существу идентичны соответствующим природным аналогам. "Иммунологически активные" биомиметики являются биомиметиками, которые проявляют иммунологическую активность, которая по существу идентична активности природных иммунологически активных молекул, таких как антитела, цитокины, интерлейкины и другие иммунологические молекулы, известные в уровне техники. В предпочтительных вариантах осуществления биомиметики настоящего изобретения представляют собой страдомеры и страдотела, определенные в настоящей заявке.
[0095] Иммунологически активные биомиметики настоящего изобретения разработаны таким образом, что они обладают одной или несколькими иммуномодулирующими активностями Fc-домена IgG и включают по меньшей мере (i) первый Fc-домен, способный к связыванию с FcγR, включая FcγRI, FcγRII, FcγRIII и FcγRIV, и (ii) второй Fc-домен, способный к связыванию с FcγR, включая FcγRI, FcγRII, FcγRIII и FcγRIV.
[0096] В следующих параграфах определены элементарные звенья биомиметиков настоящего изобретения как структурно, так и функционально, а также определены биомиметики непосредственно. Однако следует отметить, что, как обозначено выше, каждый из биомиметиков настоящего изобретения имеет по меньшей мере два Fc-домена. Как минимум, Fc-домен является димерным полипептидом (или димерной областью более крупного полипептида), который включает две пептидных цепи или звена (мономера), которые соединены, формируя функциональный сайт связывания Fcγ-рецептора. Таким образом, функциональная форма индивидуальных фрагментов и доменов, описанных в настоящей заявке, существует обычно в димерной (или мультимерной) форме. Мономеры индивидуальных фрагментов и доменов, описанные в настоящей заявке, представляют собой одиночные цепи или звенья, которые должны соединяться со второй цепью или звеном, для того чтобы формировать функциональную димерную структуру. Fc-фрагмент
[0097] "Fc-фрагмент" является термином из уровня техники, который используется для того, чтобы описать область белка или свернутой структуры белка, которая обычно находится на С-конце иммуноглобулинов (см. фиг. 3А - 3В). Fc-фрагмент может быть выделен из Fab фрагмента моноклонального антитела с помощью расщепления папаином, что является неполным и несовершенным процессом (см. Mihaesco С and Seligmann М. Papain Digestion Fragments Of Human IgM Globulins. Journal of Experimental Medicine, Vol 127, 431-453 (1968)). Вместе с Fab фрагментом (содержащим связывающий домен антитела) Fc-фрагмент составляет холо-антитело, что в данном контексте означает полное антитело. Fc-фрагмент состоит из С-концевых частей тяжелых цепей антитела. Каждая из цепей в Fc фрагменте имеет размер приблизительно 220-265 аминокислот, при этом цепи часто связаны через дисульфидную связь. Fc-фрагмент часто содержит одну или несколько независимых структурных петель или функциональных субдоменов. В частности, Fc-фрагмент включает Fc-домен, определенный в настоящей заявке, как минимальная структура, которая связывается с Fcγ-рецептором (см., например, фиг. 1В и 1D). Выделенный Fc-фрагмент состоит из двух мономеров Fc-фрагмента (например, двух С-концевых частей тяжелых цепей антитела, также определенных в настоящей заявке), которые димеризованы. Образующийся при соединении двух мономеров Fc-фрагмента, Fc-фрагмент обладает связывающей активностью в отношении Fcγ-рецептора.
Неполный Fc-фрагмент
[0098] "Неполный Fc-фрагмент" является доменом, включающим неполноразмерный Fc-фрагмент антитела, который все же сохраняет структуру, которая достаточна для того, чтобы обладать такой же активностью, как и Fc-фрагмент, включая Fcγ-рецептор связывающую активность. Неполный Fc-фрагмент, таким образом, может быть лишен части или всей шарнирной области, части или всего СН2 домена, части или всего СН3 области, и/или части или всего СН4 области, в зависимости от изотипа антитела, из которого получен неполный Fc-домен. Пример неполного Fc-фрагмента включает молекулу, включающую верхнюю, центральную и нижнюю шарнирные области плюс СН2 домен IgG3 (Tan, LK, Shopes, RJ, Oi, VT and Morrison, SL, Influence of the hinge region on complement activation, Clq binding, and segmental flexibility in chimeric human immunoglobulins, Proc Natl Acad Sci USA. 1990 January; 87(1): 162-166). Таким образом, в данном примере неполный Fc-фрагмент не содержит СН3 домен, который присутствует в Fc-фрагменте IgG3. Неполные Fc-фрагменты состоят из двух мономеров неполного Fc-фрагмента. Как далее определено в настоящей заявке, при соединении двух таких мономеров неполного Fc-фрагмента образующийся неполный Fc-фрагмент обладает Fcγ-рецептор связывающей активностью.
Fc-домен
[0099] Используемый в настоящей заявке "Fc-домен" описывает минимальную область (в контексте более крупного полипептида) или наименьшую свернутую белковую структуру (в контексте изолированного белка), которая может связаться с или быть связанна Fcγ-рецептором. Как в Fc-фрагменте, так и в неполном Fc-фрагменте Fc-домен является минимальной связывающей областью, которая обеспечивает связывание молекулы с Fcγ-рецептором. Хотя Fc-домен может быть ограничен до отдельного полипептида, который может связываться Fcγ-рецептором, все же следует понимать, что Fc-домен может являться частью или всем фрагментом Fc, так же как частью или целым неполным Fc-фрагментом. Когда термин "Fc-домен" используется в настоящем изобретении, квалифицированный специалист будет понимать под этим термином более чем один Fc-домен. Fc-домен состоит из двух мономеров Fc-домена. Как дополнительно определено в настоящей заявке, Fc-домен, образующийся при соединении двух таких мономеров Fc-домена, обладает Fcγ-рецептор связывающей активностью. Таким образом, Fc-домен является димерной структурой, которая функционально может связывать Fcγ-рецептор. Неполный Fc-домен
[00100] Используемый в настоящей заявке "неполный Fc-домен" описывает часть Fc-домена. Неполные Fc-домены включают отдельные домены константной области тяжелой цепи (например, CH1, СН2, СН3 и СН4 домены), а также шарнирные области иммуноглобулинов различных классов и подклассов. Таким образом, неполные Fc-домены настоящего изобретения включают СН1 домены IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE, CH2 домены IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE, CH3 домены IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE, CH4 домены IgM и IgE и шарнирные области IgG1, IgG2, IgG3, IgG4, IgM, IgA1, IgA2, IgD и IgE. Неполный Fc-домен настоящего изобретения может дополнительно включать комбинацию более чем одного из указанных доменов и шарнирных областей. Однако отдельные неполные Fc-домены настоящего изобретения и их комбинации не способны связывать FcγR. Таким образом, неполные Fc-домены и их комбинации включают менее чем один Fc-домен. Неполные Fc-домены могут быть соединены с формированием пептида, который обладает Fcγ-пецептор-связывающей активностью, формируя, таким образом, Fc-домен. В настоящем изобретении неполные Fc-домены используются вместе с Fc-доменами в качестве элементарных звеньев для создания биомиметиков настоящего изобретения, определенных в настоящей заявке. Каждый неполный Fc-домен состоит из двух мономеров неполного Fc-домена. Когда два таких мономера неполного Fc-домена соединяются, формируется неполный Fc-домен.
[00101] Как указано выше, каждый из Fc-фрагментов, неполных Fc-фрагментов, Fc-доменов и неполных Fc-доменов являются димерными белками или доменами. Таким образом, каждая из указанных молекул состоит из двух мономеров, которые при соединении формируют димерный белок или домен. Хотя свойства и активность димерных форм были описаны выше, мономерные пептиды описаны далее.
Мономер Fc-фрагмента
[00102] Используемый в настоящей заявке "мономер Fc-фрагмента" является одноцепочечным белком, который в соединении с другим мономером Fc-фрагмента составляет Fc-фрагмент. Мономер Fc-фрагмента, таким образом, является С-концевой частью одной из тяжелых цепей антитела, которые составляют Fc-фрагмент холо-антитела (например, смежной частью тяжелой цепи, которая включает шарнирную область, СН2 домен и СН3 домен IgG) (см. фиг. 1А и фиг. 1С)). В одном варианте осуществления мономер Fc-фрагмента включает, как минимум, одну цепь шарнирной области (мономер шарнирной области), одну цепь СН2 домена (мономер СН2 домена) и одну цепь области СН3 (мономер СН3 домена), соединенные последовательно с формированием пептида. В другом варианте осуществления мономер Fc-фрагмента включает по меньшей мере одну цепь шарнирной области, одну цепь СН2 домена, одну цепь СН3 домена и одну цепь СН4 домена (мономер СН4 домена), соединенные последовательно с формированием пептида. Мономер Fc-домена
[00103] Используемый в настоящей заявке "мономер Fc-домена" описывает одноцепочечный белок, который, в соединении с другим мономером Fc-домена, включает Fc-домен, который может связаться с Fcγ-рецептором. При соединении двух мономеров Fc-домена образуется один Fc-домен. Мономер Fc-домена, сам по себе, включающий только одну сторону Fc-домена, не может связать Fcγ-рецептор.
Мономер неполного Fc-домена
[00104] Используемый в настоящей заявке "неполный мономер Fc-домена" описывает одноцепочечный белок, который в соединении с другим неполным мономером Fc-домена составляет неполный Fc-домен. Аминокислотные последовательности шарнирной области неполного Fc-домена, мономеров СН2 и СН3 для IgG1, IgG2, IgG3 и IgG4 приведены на фиг. 25. Соединение двух неполных мономеров Fc-домена приводит к образованию одного неполного Fc-домена.
Страдомеры
[00105] В конкретных вариантах осуществления биомиметики настоящего изобретения включают страдомеры. Страдомеры представляют собой биомиметические соединения, способные связывать два или более Fcγ-рецепторов (см., например, фиг. 13В). В предпочтительном варианте осуществления страдомеры настоящего изобретения используются для связывания Fcγ-рецепторов на эффекторных клетках, таких как NK-клетки, незрелые дендритные клетки и другие клетки, происходящие из моноцитов. В одном варианте осуществления Fcγ-рецепторы являются Fcγ-рецепторами низкой аффинности. Страдомер может иметь четыре различных физических конформации: последовательную, кластерную, кор- или Fc-фрагмент, каждая из которых описана в следующих параграфах. Как будет очевидно, Fc-фрагменты, неполные Fc-фрагменты, Fc-домены и неполные Fc-домены, описанные выше, используются при конструировании различных конформации страдомеров. Кроме того, именно отдельные мономеры Fc-домена и мономеры неполного Fc-домена, также описанные выше, после получения самоассоциациируют, формируя димерные структуры, которые и являются страдомерами настоящего изобретения. Последовательный страдомер
[00106] "Последовательный страдомер" является димерым полипептидом, состоящим из двух линейных мономеров страдомера, которые при соединении формируют два или более Fc-домена. Fc-домены страдомера являются функциональными только в том случае, когда две цепи пептида (мономеры страдомера) связаны (то есть нефункциональные в мономерном состоянии). Таким образом, последовательный страдомер представляет собой биомиметическое соединение, способное связывать два или более Fcγ-рецепторов. В различных вариантах осуществления последовательный страдомер может включать два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать или более Fc-доменов, а также неполных Fc-доменов. Fc-домены и неполные Fc-домены в последовательном страдомере могут быть связаны доменными связями, как определено ниже.
[00107] Используемый в настоящей заявке "димер страдомера" является определенной формой страдомера, состоящей только из двух страдомеров. В одном- варианте осуществления димеры страдомера представляют собой молекулы, сформированные в результате самоагрегации соответствующих мономеров страдомера. В другом варианте осуществления мономеры страдомера в димерах страдомера физически связаны через интер-мономер страдомерные связи, как определено в настоящем описании. "Мультимерный страдомер" состоит из трех или более страдомеров, сформированных в результате самоагрегации мономеров страдомера или образования интер-мономер страдомерных связей, как определено в настоящем описании.
Мономер страдомера
[00108] Используемый в настоящей заявке термин "мономер страдомера" относится к одиночной, цельной пептидной молекуле, которая при соединении по меньшей мере со вторым мономером страдомера формирует полипептид, включающий по меньшей мере два Fc-домена (см., например, фиг. 6А - 6В, фиг. 12А). Хотя в предпочтительных вариантах осуществления последовательные страдомеры состоят из двух соединенных мономеров страдомера (см., например, фиг. 5А, 5В, 7А, 7В, 1С, 7D), последовательный страдомер может также содержать три (см. фиг. 11С) или более мономеров страдомера. Мономеры страдомера могут быть соединены с формированием страдомеров посредством образования интер-мономер страдомерных связей, или они могут формировать страдомеры посредством самоагрегации.
[00109] Мономер страдомера может иметь такую аминокислотную последовательность, что при соединении с другим мономером страдомера образуется один, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать или более Fc-доменов, и формируется страдомер. Мономер страдомера может также иметь такую аминокислотную последовательность, что при соединении с другим мономером страдомера образуется один, два, три, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать, четырнадцать или более неполных Fc-доменов, и формируется страдомер.
[00110] Области мономеров страдомера, которые формируют Fc-домены и неполные Fc-домены в контексте страдомера, могут быть просто расположены от С-конца до N-конца в виде последовательных областей молекулы мономера страдомера (см., например, фиг. 4А - 4В). В альтернативе, последовательные области мономеров страдомера могут быть связаны через последовательность пептида, которую в настоящей заявке называют "доменной связью". Взаимное расположение отдельных мономеров Fc-домена и мономеров неполного Fc-домена, составляющих мономер страдомера, не является критическим. Однако указанное расположение должно позволять формирование двух функциональных Fc-доменов при соединении двух мономеров страдомера.
[00111] В одном варианте осуществления страдомеров настоящего изобретения получают мономеры страдомера, которые на N-конце пептида содержат мономер Fc-домена или мономер неполного Fc-домена, такие как один или два концевых мономера СН2 домена IgE или мономер неполной шарнирной области IgG3, которые сильно связываются сами с собой, образуя Fc-домен или неполный Fc-домен, соответственно. Каждый из указанных мономеров страдомера имеет необходимое дополнение к мономерам Fc-домена и/или мономерам неполного Fc-домена, чтобы после формирования страдомер мог связывать два Fc-гамма рецептора. Страдомеры, которые образуются в результате соединения таких мономеров страдомера, представляют собой биомиметики, способные связывать два или более Fc-гамма рецепторов. В предпочтительном варианте осуществления N-концевые Fc-домен или неполный Fc-домен содержат дополнительный сайт гликозилирования, например, такой как содержится в СН2 домене IgE.
[00112] В качестве пояснительного примера, квалифицированный специалист поймет, что молекулы страдомеров настоящего изобретения могут быть сконструированы путем получения полинуклеотидной молекулы, которая кодирует различные комбинации мономеров Fc-домена и мономеров неполного Fc-домена, однако комбинация должна быть такой, которая дает минимум два мономера Fc-домена. Такая полинуклеотидная молекула может быть встроена в экспрессионный вектор, который может применяться для трансформации популяции бактерий. Затем мономеры страдомера могут быть получены путем выращивания трансформированных бактерий в соответствующих условиях. Затем мономеры страдомера могут формировать функциональные страдомеры либо посредством самоагрегации мономеров страдомера, либо посредством соединения мономеров страдомера с помощью интер-мономер страдомерных связей. Настоящее изобретение охватывает оба страдомера, сформированные посредством соединения мономеров страдомера, имеющих идентичные аминокислотные последовательности, мономеров страдомера, имеющих по существу аналогичные аминокислотные последовательности, или мономеров страдомера, имеющих различные последовательности. В последнем варианте осуществления аминокислотная последовательность мономеров страдомера, составляющих страдомер, должна иметь лишь такое подобие, чтобы образовывались два или более функциональных Fcγ-рецепторсвязывающих сайта.
[00113] Как указано выше, Fc-домен может функционально определяться своей способностью к связыванию Fcγ-рецептора. В результате конкретная аминокислотная последовательность Fc-домена изменится на основе неполных Fc-доменов, которые составляют Fc-домен. Однако в одном варианте осуществления настоящего изобретения Fc-домен включает шарнирную область и СН2 домен молекулы иммуноглобулина. В другом варианте осуществления Fc-домен включает шарнирную область, СН2 домен и СН3 домен молекулы иммуноглобулина. В другом варианте осуществления Fc-домен включает шарнирную область, СН2 домен, СН3 домен и СН4 домен молекулы иммуноглобулина. В еще одном варианте осуществления Fc-домен включает шарнирную область, СН2 домен и СН4 домен молекулы иммуноглобулина.
Доменная связь
[00114] Как указано выше, "доменная связь" является пептидной связью между мономерами Fc-домена и/или мономерами неполного Fc-домена, которые составляют каждый из отдельных мономеров страдомера последовательных страдомеров или страдотел настоящего изобретения. Доменная связь может включать 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот. Доменная связь не присутствует между мономерами неполного Fc-домена, которые расположены в своей естественной последовательности. Таким образом, когда используются части мономеров Fc-домена, связанные в естественном порядке, например, шарнирная область, СН2 домен и СН3 домен IgG, данные мономеры неполного Fc-домена включают смежную последовательность, поэтому доменная связь между указанными элементами не нужна. Напротив, например, когда два или более мономеров Fc-домена или мономеров неполного Fc-домена соединены в таком порядке, в котором обычно не расположены, и формируют в результате отдельный мономер страдомера, могут использоваться доменные связи. Примером может являться связь между двумя пептидами шарнирная область/СН2/СН3 с получением отдельного мономера страдомера, составляющего страдомер, который включает: шарнирную область/СН2/СН3/L/шарнирную область/СН2/СН3, где "L" обозначает доменную связь (см., например., фиг. 4А, где доменная связь (не показана) образована между СН3 доменом IgG1 и шарнирной областью IgG1). В различных описанных случаях доменная связь может являться одной из природных частей тяжелой цепи, которая присоединяется к шарнирной области СН доменам в мономере Fc-домена антитела. В альтернативе, доменная связь может являться любой другой аминокислотной последовательностью, которая обеспечивает необходимый интервал и гибкость между мономерами Fc-домена и мономерами неполного Fc-домена отдельного мономера страдомера, и которая позволяет отдельным мономерам страдомера соединяться друг с другом, формируя страдомеры настоящего изобретения.
[00115] Квалифицированный специалист сумеет понять, что идентичность доменной связи не особенно важна, при условии что она позволяет двум или более отдельным мономерам страдомера формировать биомиметические соединения настоящего изобретения, и что образующиеся соединения обладают способностью поперечно связывать более одного FcγR. Предполагается, что каждое иммунологически активное биомиметическое соединение предпочтительно содержит по меньшей мере одну доменную связь в каждом мономере страдомера последовательного страдомера или страдотела, которая функционирует так, что поддерживает Fc-домены иммунологически активного биомиметика в пределах ограниченной пространственной области, и которая повышает активность при активации FcγR, например, посредством агрегации Fcγ-рецепторов путем связывания с Fc-доменами в иммунологически активном биомиметике. Предпочтительно, доменные связи обеспечивают такую же или более высокую степень конформационной вариабельности, которую обеспечивает шарнирная область молекул IgG. Все вышеупомянутые связи известны в уровне техники.
Интер-мономер страдомерная связь
[00116] Отдельной связью, присутствующей в биомиметических соединениях настоящего изобретения, является "интер-мономер страдомерная связь", которая расположена между двумя или более отдельными мономерами страдомера, которые составляют страдомеры и страдотела настоящего изобретения. Тогда как доменные связи представляют собой короткие аминокислотные последовательности, которые служат для связывания друг с другом мономеров Fc-домена и мономеров неполного Fc-домена, которые составляют индивидуальные мономеры страдомера биомиметических соединений, интер-мономер страдомерные связи служат для соединения двух или более отдельных мономеров страдомера, которые составляют биомиметические соединения. Интер-мономер страдомерная связь может являться любой связью, способной к стабильному соединению отдельных мономеров страдомера. В некоторых вариантах осуществления интер-мономер страдомерная связь может являться ковалентной связью между мономерами страдомера. В альтернативе, интер-мономер страдомерная связь между мономерами страдомера может являться прямым химическим сшиванием. В предпочтительных вариантах осуществления структуры мономеров страдомера обладают преимуществом возможности природной самоагрегации мономеров Fc-домена, что позволяет создать самоагрегирующие страдомеры. В таких вариантах осуществления между отдельными мономерами страдомера образуются дисульфидные связи, что приводит к формированию страдомеров (см., например, фиг. 5А, где интермономер страдомерные связи (не показаны) служат для соединения двух отдельных мономеров страдомера, составляющих страдомер). Дисульфидные связи образуются между остатками цистеина мономеров Fc-домена, которые составляют биомиметические молекулы, с использованием остатков цистеина, присутствующих в последовательности природного мономера Fc-домена, либо остатков цистеина, введенных в мономер Fc-домена с помощью сайт-направленного мутагенеза. Такие природные свойства самоагрегации могут также использоваться с целью формирования интер-мономер страдомерной связи между отдельными мономерами страдомера в мультимерах страдомера. Альтернативные варианты осуществления включают интер-мономер страдомерные связи, где дисульфидные связи образуются между остатками цистеина, введенными посредством сайт-направленного мутагенеза в аминокислотную последовательность, составляющую отдельные мономеры страдомера.
[00117] Как описано выше, в предпочтительном варианте осуществления интер-мономер страдомерная связь, с помощью которой формируется страдомер, представляет собой связь, которая образуется в результате самоагрегации мономеров страдомера. В одном варианте осуществления два мономера страдомера, которые составляют страдомер, являются идентичными пептидами, то есть два отдельных мономера страдомера, которые составляют страдомер, имеют идентичные последовательности. Впрочем, квалифицированный специалист сумеет понять, что другие варианты осуществления включают такие страдомеры, в которых мономеры страдомера отличаются друг от друга по аминокислотным последовательностям.
[00118] Два мономера страдомера могут сформировать страдомер, например, выстраиваясь параллельно, таким образом, соединение происходит между идентичными мономерами неполного Fc-домена в мономерах страдомера (см., например, фиг. 5А-В). Однако настоящее изобретение также включает варианты осуществления, в которых соединение происходит между неидентичными мономерами неполного Fc-домена, а также варианты осуществления (см. фиг. 11С), в которых соединение происходит между идентичными мономерами неполного Fc-домена в мономерах страдомера, но в которых при этом выравнивание двух мономеров страдомера происходит со смещением.
[00119] Для регуляции продукции и самодимеризации мономера страдомера могут использоваться "копирующие области". Например, последовательность мономера страдомера может включать следующие неполные Fc-домены: СН2 IgE/шарнирную область IgG1/CH2 IgG1/СН3 IgG1/шарнирную область IgG1/CH2 IgG1/CH4 IgE (см. фиг. 13А), где домены IgE служат кэпом, который предотвращает "эффект застегивания". Эффект застегивания может возникнуть, когда мономер страдомера (см. фиг. 11А) может автодимеризоваться (см. фиг. 11В) или может ориентировать себя не в виде автодимера, а в виде параллельных чередующихся мономеров (см. фиг. 11С). Средний специалист в данной области осведомлен, что для того, чтобы вызвать автодимеризацию страдомера и предотвратить эффект застегивания, при необходимости могут использоваться различные неполные Fc-домены, такие как шарнирная область любого иммуноглобулина или СН4 домен IgM, или IgE, отдельно или в комбинации. Другие непоследовательные структуры могут содержать молекулы с разветвленной цепью (см. фиг. 12В), два или более страдомеров, расположенных параллельно и соединенных линкерами, например, посредством простой ковалентной связи, пептидных линкеров или непептидных линкеров (см. фиг. 14А и 14В).
Кор-страдомер
[00120] "Кор-страдомер" состоит из кор-группы, с которой связаны две или более кор-страдомерных единицы, где каждая кор-страдомерная единица включает по меньшей мере один Fc-домен, формируя, таким образом, биомиметическое соединение, способное связывать два или более Fcγ-рецепторов. Fc-фрагмент, неполный Fc-фрагмент, последовательный страдомер или кластерная страдомерная единица могут независимо служить в качестве одной или обоих (если они включают два Fc-домена) кор-страдомерных единиц в кор-страдомере, поскольку каждая из указанных молекул содержит по меньшей мере один Fc-домен. Таким образом, кор-страдомер может включать кор-группу, с которой связан по меньшей мере один последовательный страдомер.
[00121] Используемая в настоящей заявке кор-группа кор-страдомера является любой физической структурой, с которой могут быть соединены или ковалентно связаны кор-страдомерные единицы. Предпочтительные полипептиды, которые могут служить в качестве кор-группы, включают гемоцианин лимфы улитки, бычий сывороточный альбумин и овальбумин. Химическое перекрестное сшивание между такими кор-группами и кор-страдомерными единицами (например, Fc-фрагментом, неполным Fc-фрагментом, Fc-доменом, последовательным, страдомером и кластерной страдомерной единицей) может осуществляться посредством различных химических реагентов с использованием известных методов. Примеры химических реагентов, которые стандартно применяют в перекрестном сшивании, включают глутаральдегид, карбодиимид, сложные эфиры сукцинимиды (например, MBS, SMCC), бензидин, периодат, изотиоцианат; ПЭО (полиэтиленоксид)/ПЭГ (полиэтиленгликоль) спейсеры, такие как бис(NHS)PEO5, DFDNB (1,5-дифтор-2,4-динитробензол); и аминореактивные гомобифункциональные поперечно-сшивающие реагенты, включая альдегид-активированный декстран, бис(сульфосукцинимидил)суберат, бис[2-(сукцинимидооксикарбонил-окси)этил]сульфон, диметиладипимидат⋅2 HCl, диметилпимелимидат⋅2 HCl, диметилсуберимидат⋅2 HCl, дисукцинимидил глутарат, дитиобис(сукцинимидил)пропионат, дисукцинимидилсуберат, дисукцинимидилтартрат, диметил-3,31-дитиобиспропионимидат⋅2 HCl, 3,3'-дитиобис(сульфосукцинимидилпропионат), этиленгликоль бис[сукцинимидилсукцинат], этиленгликоль бис[сульфосукцинимидил-сукцинат], β-[трис(гидроксиметил)фосфино]пропионовая кислота и трис-сукцинимидиламинотриацетат. Специалист в данной области сумеет подобрать соответствующий сшивающий реагент и условия на основе конкретной выбранной кор-группы и последовательности Fc-домен-содержащих полипептидов, соединяемых с формированием иммунологически активного биомиметика. См., например, Wong, Shan S. Chemistry of protein conjugation and cross-linking. Boca Raton: CRC Press, c1991 (ISBN 0849358868).
[00122] В другом предпочтительном варианте осуществления в качестве кор-группы может использоваться полипептид соединительной (J) цепи. Когда в качестве кор-группы используется J-цепь, цистеиновые мостики могут использоваться для соединения отдельных кор-страдомерных единиц с образованием кор-страдомера (См. фиг. 10A - 10D). В одном из вариантов осуществления кор-страдомер, последовательные страдомеры (служащие в качестве кор-страдомерных единиц), содержащие концевой СН4 домен IgM, соединены J-цепью с образованием кор-страдомера. Включение СН4 домена IgM приводит к самоагрегации страдомеров, включающих данный наполный Fc-домен с J-цепью, с формированием биомиметика, способное связывать несколько Fc-гамма рецепторов. Другим примером кор-страдомера является кор-страдомер, включающий Fc-домены (служащие в качестве кор-страдомерных единиц), где Fc-домены имеют следующую структуру: шарнирная область IgG3/CH2 IgG3/CH3 IgG3/CH4 IgM. Fc-домены, составляющие данную молекулу, не могут по отдельности связывать более одного Fc-гамма рецептора, а уже полная структура может связывать пять Fc-гамма рецепторов, когда составляющие Fc-домены соединены J-цепью.
[00123] В другом варианте осуществления кор-группа может являться неполипептидной молекулой. С кор-страдомерными единицами могут быть физически связаны различные подходящие композиции, обеспечивая получение иммунологически активного биомиметика. Могут использоваться нетоксичные гранулы, гиперразветвленные полимеры и дендримеры, наночастицы, а также различные соединения, которые классифицированы FDA как полностью безопасные (например, пропиленгликоль, сорбит, липосомы и силикат кальция). См., например, Nanoparticulates as Drug Carriers (Vladimir P. Torchilin (Редактор)), Imperial College Press (Сент. 2006) ISBN: 1860946305/ISBN-13: 978186094 6301.
[00124] Предпочтительные кор-группы настоящего изобретения включают гранулу, альбумин, липосому, пептид и полиэтиленгликоль.
Кластерный страдомер
[00125] "Кластерный страдомер" является биомиметиком, который имеет осьминогоподобную форму с центральной группой, "головкой" и двумя или более "ножками", где каждая ножка включает один или более Fc-доменов, которые способны связывать по меньшей мере один Fc-гамма рецептор, образуя, таким образом, биомиметик, способный связывать два или более Fc-гамма рецептора. Каждый кластерный страдомер состоит больше чем из одного димерного белка, который называется "кластерной страдомерной единицей". Каждая кластерная страдомерная единица состоит из области, которая мультимеризуется, и области "ножки", которая включает по меньшей мере один функциональный Fc-домен. Мультимеризирующая область образует "головку" кластерного страдомера при мультимеризации с мультимеризирующей областью другой кластерной страдомерной единицы. Область ножки способна связывать столько Fcγ-рецепторов, сколько Fc-доменов содержится в каждой области ножки. Таким образом, кластерный страдомер представляет собой биомиметическое соединение, способное связывать два или более Fcγ-рецепторов.
[00126] Мультимеризирующая область может являться пептидной последовательностью, которая вызывает дальнейшую мультимеризацию димерных белков, или, в альтернативе, мультимеризирующая область может являться гликозилированием, увеличивающим мультимеризацию димерных белков. Примеры пептидных мультимеризирующих областей включают шарнирную область IgG2, СН2 домен IgE, изолейциновую молнию и цинковые пальцы. Влияние гликозилирования на мультимеризацию пептидов хорошо описано в уровне техники (например, Role of Carbohydrate in Multimeric Structure of Factor VIII/V on Willebrand Factor Protein. Harvey R. Gralnick, Sybil B. Williams and Margaret E. Rick. Proceedings of the National Academy of Sciences of the United States of America, Vol. 80, No. 9, [Part 1: Biological Sciences] (May 1, 1983), pp. 2771-2774; Multimerization and collagen binding of vitronectin is modulated by its glycosylation. Kimie Asanuma, Fumio Arisaka and Haruko Ogawa. International Congress Series Volume 1223, December 2001, Pages 97-101).
[00127] Опытный специалист осведомлен, что кластерная страдомерная единица сама может включать последовательный страдомер (содержащий два или более Fc-доменов) наряду с мультимеризирующей областью. Таким образом, "ножки" кластерного страдомера могут состоять из последовательных страдомеров любого из типов, описанных в настоящей заявке, и/или одного или нескольких Fc-фрагментов IgG1, и/или Fc-фрагментов IgG3, и/или одного Fc-домена. Опытный специалист осведомлен, что каждый из Fc-фрагментов IgG1 и каждый Fc-фрагмент IgG3 в таких биомиметиках может быть модифицирован так, что будет включать неполные Fc-фрагменты из любого иммуноглобулина. Мономеры, которые составляют кластерную страдомерную единицу (которая, как указано выше, существует в виде димерного комплекса двух пептидов), являются "мономерами кластерной страдомерной единицы". Примером сконструированного кластерного страдомера, кластерная страдомерная единица которого связывает не более чем один Fc-гамма рецептор низкой аффинности перед мультимеризацией, является СН2 IgE/шарнирная область IgG1/CH2 IgG1/СН3 IgG1.
[00128] Опытный специалист осведомлен, что когда последовательный страдомер используется в качестве "ножки" кластерного страдомера, каждая "ножка" способна связывать больше одного Fc-гамма рецептора (поскольку в последовательном страдомере присутствует по меньшей мере два Fc-домена), то в результате образуется биомиметик, способный связывать больше одного Fc-гамма рецептора. Неполные Fc-домены, другие последовательности иммуноглобулинов и неиммуноглобулиновые последовательности могут быть помещены на концы отдельных мономеров кластерных страдомерных единиц, которые составляет ножки, с получением кластерного страдомера, в котором каждая ножка расположена на необходимом расстоянии, что повышает их доступность при связывании с одним или более чем одним Fc-гамма рецептором.
[00129] Мультимеризирующая область может являться пептидной последовательностью, которая вызывает димеризацию или мультимеризацию пептидов и включает шарнирную область IgG2, СН2 домен IgE, изолейциновую молнию и цинковый палец. Как известно из уровня техники, шарнирная область IgG2 человека может формировать ковалентно связанные димеры (Yoo, Е.М. et al. J. Immunol. 170, 3134-3138 (2003); Salfeld Nature Biotech. 25, 1369-1372 (2007)). Формирование димеров IgG2 потенциально опосредуется структурой шарнирной области IgG2 при образовании С-С связей (Yoo et al, 2003), что позволяет предположить, что структура одной лишь шарнирной области может вызывать образование димеров. Таким образом, последовательные страдомеры, содержащие шарнирную область IgG2 (и, таким образом, служащие в качестве кластерных страдомерных единиц), будут формировать кластерный страдомер, который может включать два последовательных страдомера или даже три последовательных страдомера.
[00130] Аминокислотная последовательность мономера шарнирной области IgG2 человека является следующей: ERKCCVECPPCP (SEQ ID NO: 36). Ключевой структурой шарнирной области является часть С-Х-Х-С мономера шарнирной области. Таким образом, мономеры страдомера настоящего изобретения могут включать полную последовательность мономера шарнирной области IgG2 из 12 аминокислот, либо четыре главных аминокислоты, наряду с мономерами Fc-домена. Хотя Х-Х в ключевой структуре может обозначать любую аминокислоту, в предпочтительном варианте осуществления последовательность Х-Х представляет собой V-E или Р-Р. Для квалифицированного специалиста очевидно, что мономерная шарнирная область IgG2 может состоять из любой части последовательности шарнирной области в дополнение к основной структуре из четырех аминокислот, включая полную последовательность шарнирной области IgG2, а также часть или полную последовательность мономеров СН2 и СН3 домена IgG2. Конкретные примеры возможных конструкций последовательных страдомеров на основе шарнирной области IgG2-Fс-домена IgG1 являются следующими:


[00131] Это лишь несколько из многих примеров. Любой из Fc-доменов IgG1 может быть заменен, например, Fc-доменом IgG3. Дополнительные белки с димеризационными доменами IgG2 включают химерные белки IgG2-IgG1 с дополнительными N- и/или С-концевыми последовательностями, включающими последовательности мономеров доменов IgM или IgE. Указанные N- и С-концевые последовательности могут являться шарнирными областями, константными областями или и тем, и другим.
[00132] Как указано выше, лейциновые и изолейциновые молнии также могут использоваться в качестве мультимеризирующей области. Лейциновые и изолейциновые молнии (спирально скрученные домены), как известно, способствуют образованию белковых димеров, тримеров и тетрамеров (Harbury et al. Science 262: 1401-1407 (1993); О'Shea et al. Science 243: 538 (1989)). Кластерные страдомеры, обладающие преимуществом природной тенденции изолейциновой молнии образовывать тример, могут быть получены с использованием последовательных страдомеров, включающих изолейциновую молнию. Ассоциирование трех или более последовательных страдомеров (как кластерных страдомерных единиц), содержащих изолейциновые молнии, приводит к формированию кластерных страдомеров, имеющих по меньшей мере шесть областей, связывающих Fc-гамма рецепторы.
[00133] Хотя для квалифицированного специалиста очевидно, что могут использоваться различные типы лейциновых и изолейциновых молний, в предпочтительном варианте осуществления используется изолейциновая молния из модифицированного регулятора транскрипции GCN4 (описанного в статье Morris et al., Mol. Immunol. 44: 3112-3121 (2007); Harbury et al. Science 262: 1401-1407 (1993)): 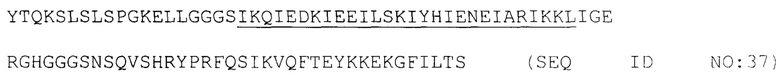 . Приведенная последовательность изолейциновой молнии является лишь одной из нескольких возможных последовательностей, которые могут использоваться для мультимеризации мономеров Fc-домена. Хотя может использоваться вся последовательность, приведенная в SEQ ID NO: 37, подчеркнутая часть последовательности представляет ключевую последовательность изолейциновой молнии, которая может использоваться в кластерных страдомерах настоящего изобретения. Таким образом, мономеры страдомера настоящего изобретения могут включать либо полную последовательность из 88 аминокислот изолейциновой молнии (ILZ), либо 2 8 ключевых аминокислот, наряду с одним или несколькими мономерами Fc-домена. Квалифицированному специалисту также очевидно, что изолейциновая молния может состоять из любой части молнии в дополнение к основной структуре из 28 аминокислот и, таким образом, может состоять больше чем из 28 аминокислот, но менее чем 88 аминокислот изолейциновой молнии. Конкретные примеры возможных конструкций на основе ILZ-Fc-домена IgG1 приведены далее.
. Приведенная последовательность изолейциновой молнии является лишь одной из нескольких возможных последовательностей, которые могут использоваться для мультимеризации мономеров Fc-домена. Хотя может использоваться вся последовательность, приведенная в SEQ ID NO: 37, подчеркнутая часть последовательности представляет ключевую последовательность изолейциновой молнии, которая может использоваться в кластерных страдомерах настоящего изобретения. Таким образом, мономеры страдомера настоящего изобретения могут включать либо полную последовательность из 88 аминокислот изолейциновой молнии (ILZ), либо 2 8 ключевых аминокислот, наряду с одним или несколькими мономерами Fc-домена. Квалифицированному специалисту также очевидно, что изолейциновая молния может состоять из любой части молнии в дополнение к основной структуре из 28 аминокислот и, таким образом, может состоять больше чем из 28 аминокислот, но менее чем 88 аминокислот изолейциновой молнии. Конкретные примеры возможных конструкций на основе ILZ-Fc-домена IgG1 приведены далее.

[00134] Это лишь несколько из многих примеров. Любой из доменов IgG1 может быть заменен, например, доменами IgG3. Дополнительные белки с ILZ доменами включают химерные белки IgG1 с дополнительными N- и/или С-концевыми последовательностями из других молекул Ig, таких как IgM или IgE. Указанные N- и С-концевые последовательности могут являться шарнирными областями, константными областями или и тем, и другим.
Fc-фрагмент-страдомер
[00135] "Fc-фрагмент-страдомер" состоит более чем из одного Fc-фрагмента. При некоторых обстоятельствах, относящихся к посттрансляционной модификации Fc-фрагмента, Fc-фрагмент с достаточной силой связывается с другим Fc-фрагментом, обеспечивая формирование молекулы, которая связывается более чем с одним Fcγ-рецептором. Посттрансляционная модификация, которая обеспечивает такое связывание, включает гликозилирование и метилирование. Идентичность клеточной линии, в которой получают рекомбинантные Fc-фрагменты, а также условия, при которых их получают, определяют, будут ли Fc-фрагменты формировать Fc-фрагмент-страдомеры. Например, рекомбинантный Fc-фрагмент, полученный в транзиентно трансфицированных СНО клетках FreestyleMax, образует мультимеры, которые визуально регистрируются на вестерн-блотах, связывается согласно бивалентному стандарту в анализе связывания методом плазмонного резонанса, и демонстрирует биологическую активность в анализе на дендритных клетках, сопоставимую с активностью IVIG. Напротив, такой же рекомбинантный Fc-фрагмент, полученный в стабильной линии клеток СНО не образует мультимеров Fc-фрагмента, детектируемых на вестерн-блотах, связывается согласно моновалентному стандарту в анализе связывания методом плазмонного резонанса, и не демонстрирует сопоставимую биологическую активность. Таким образом, Fc-фрагмент-страдомер является биомиметическим соединением, способным связывать два или более Fcγ-рецепторов.
[00136] Также используемый в настоящей заявке термин "Fc-димер" обозначает димер Fc-фрагментов (см. фиг. 2А), термин "Fc-тример" обозначает тример Fc-фрагментов и термин "Fc-мультимер" обозначает мультимер Fc-фрагментов (см. фиг. 2В).
Страдотело
[00137] Настоящее изобретение также охватывает страдотела. Используемое в настоящей заявке "страдотело" относится к молекуле, включающей два или более Fc-доменов, предпочтительно в контексте страдомера (включая последовательные страдомеры, кор-страдомеры, кластерные страдомеры и Fc-фрагмент-страдомеры), к которому присоединен один или несколько Fab-доменов (см., например, фиг. 8А-В и 9А-В). Таким образом, благодаря присутствию таких Fab-доменов страдотела обладают и антигенсвязывающей способностью, и страдомерной Fcγ-рецептор-связывающей активностью. В некоторых вариантах осуществления Fcγ-рецептор-связывающая активность может быть обусловлена способностью связывать и перекрестно связывать FcγR в равной или большей степени по сравнению с Fc-частью нативной структуры холо-антитела. Предпочтительно Fab-часть страдотела включает и тяжелую и легкую цепи. Вариабельная тяжелая цепь и легкая цепь могут независимо происходить из любого совместимого иммуноглобулина, например, IgA1, IgA2, IgM, IgD, IgE, IgG1, IgG2, IgG3 или IgG4, и могут относиться к тому же или другому изотипу Ig, но предпочтительно они относятся к тому же изотипу Ig. Легкие цепи каппа или лямбда также могут происходить из различных изотипов Ig. Страдотела, как и страдомеры, могут связывать два или более Fcγ-рецепторов и модулировать иммунную функцию.
[00138] В одном из вариантов осуществления страдомеры могут содержать Fab иммуноглобулина, связанный с Fc шарнирным (Н) доменом страдомера, образуя страдотело (например, фиг. 8А и В). В другом варианте осуществления страдотело может состоять из Fc IgG1 - (шарнирной области - СН2) IgG1 (например, фиг. 9А). В других вариантах осуществления страдотело может состоять из домена и шарнирной области IgG1, домена и шарнирной области IgG3 и домена и шарнирной области IgGE (например, фиг. 9В). Fab включает и тяжелую, и легкую цепь, присутствующие в нативной структуре иммуноглобулинов (фиг. 3А-В).
[00139] Страдотела обладают антигенсвязывающими свойствами Fab части и вышеописанными свойствами страдомеров. Такая комбинация служит для связывания, перекрестного связывания и активации Fcγ-рецепторов на эффекторных клетках с более высокой скоростью, чем может быть достигнуто Fc-основой холо-антитела, особенно в среде с низкой экспрессией эпитопов (например, у 90% пациентов с раком молочной железы, опухоли которых не классифицированы, как экспрессирующие her/2-neu с высоким уровнем), индуцируя у пациентов АЗКЦ с более высоким процентом. Как указано выше, один или несколько антигенсвязывающих Fab-фрагментов могут быть введены в страдомеры с формированием страдотел. Предпочтительно, полипептиды (кроме связей, описанных в настоящей заявке), вводимые в страдомеры, не являются целыми неиммуноглобулиновыми полипептидами или их частями.
[00140] Fab может являться химерной структурой, состоящей из константных областей, относящихся к человеку, и не относящихся к человеку вариабельных областей, таких как вариабельная область, происходящая из антитела мыши, крысы, кролика, обезьяны или козы. Средний специалист в данной области способен получить различные Fab-химерные структуры с целью их включения в страдотела с использованием методик, существующих на сегодняшний день и описанных в научной литературе применительно к таким конструкциям. Таким образом, "гуманизированные" страдотела могут быть созданы аналогично "гуманизированным" моноклональным антителам.
Варианты и гомологи
[00141] Квалифицированному специалисту очевидно, что могут быть разработаны страдомеры и другие биомиметики настоящего изобретения, включающие специфические Fc-домены иммуноглобулинов, такие как два Fc-домена из IgG1 (то есть шарнирная область IgG1/CH2 IgG1/СН3 IgG1/шарнирная область IgG1/CH2 IgG1/СН3 IgG1). Такой страдомер может быть сконструирован посредством получения в начале полинуклеотида, кодирующего два мономера Fc-домена IgG1 (то есть мономер шарнирной области IgG1/мономер СН2 IgG1/мономер СН3 IgG1/мономер шарнирной области IgG1/мономер СН2 IgG1/мономер СН3 IgG1), а экспрессии с него мономеров страдомера. Затем при ассоциировании двух таких мономеров страдомера образуется последовательный страдомер, включающий два Fc-домена IgG1.
[00142] Страдомеры и другие биомиметики настоящего изобретения могут быть также созданы на основе идентичности определенных неполных Fc-доменов иммуноглобулина, которые составляют Fc-домены. Например, может быть получен последовательный страдомер, содержащий два Fc-домена, где первый Fc-домен включает шарнирную область IgG1/CH2 IgG3/CH3 IgG1, а второй Fc-домен включает шарнирную область IgG3/CH2 IgG1/СН3 IgG3.
[00143] Следует понимать, что страдомеры и другие биомиметические молекулы, раскрытые в настоящей заявке, могут быть получены из организмов любых различных видов. Фактически Fc-домены или неполные Fc-домены в любых биомиметических молекулах настоящего изобретения могут быть получены из иммуноглобулина, происходящего более чем из одного (например, из двух, трех, четырех, пяти или более) видов. Однако обычно они происходят из одного вида. Кроме того, следует понимать, что любой из способов, раскрытых в настоящей заявке (например, способов лечения), может быть применен к любому виду. В основном все компоненты биомиметиков, применяемых к целевому виду, происходят из того же вида. Впрочем, также могут применяться биомиметики, в которых все компоненты происходят из различных видов или более чем из одного вида (включая или не включая виды, к которым применяется рассматриваемый способ).
[00144] Определенные CH1, СН2, СН3 и СН4 домены и шарнирные области, которые включают Fc-домены и неполные Fc-домены страдомеров и других биомиметиков настоящего изобретения, могут быть независимо выбраны как на основе подкласса иммуноглобулинов, так и на основе организма, из которого они получены. Таким образом, страдомеры и другие биомиметики, раскрытые в настоящей заявке, могут включать Fc-домены и неполные Fc-домены, которые независимо происходят из иммуноглобулинов различных типов, например, IgG1, IgG2, IgG3, IgG4, IgA1, IgA2, IgD, IgE и IgM. Аналогично, каждый Fc-домен и неполный Fc-домен могут быть получены из различных видов, предпочтительно видов млекопитающих, включая всех приматов кроме человека (например, обезьян, бабуинов и шимпанзе), людей, мышей, крыс, крупный рогатый скот, лошадей, кошачих, собачих, свиней, кроликов, коз, оленей, овец, хорьков, песчанок, морских свинок, хомяков, летучих мышей, птиц (например, кур, индеек и уток), рыб и рептилий, используемых для получения видоспецифичных или химерных молекул страдомеров.
[00145] Отдельные Fc-домены и неполные Fc-домены могут быть также гуманизированы. Специалисту в данной области очевидно, что различные Fc-домены и неполные Fc-домены обеспечивают функциональные свойства различных типов. Например, Fcγ-рецепторы специфично связываются с иммуноглобулинами IgG и никакими другими классами иммуноглобулинов. Таким образом, специалист в данной области, намереваясь создать страдомер, обладающий способностью связывания множественных Fcγ-рецепторов, будет создавать Fc-области страдомера, которые включают по меньшей мере хорошо описанные последовательности IgG, связывающие Fcγ-рецептор, включая соответствующие последовательности из шарнирной области IgG и СН2 и СН3 домены IgG. Специалисту в данной области также очевидно, что с применением конкретных доменов Ig могут быть связаны различные нежелательные последствия, например, анафилаксия, связанная с инъекциями IgA. Биомиметики, раскрытые в настоящей заявке, в целом необходимо разрабатывать так, чтобы избегать подобных эффектов, хотя в определенных обстоятельствах такие эффекты могут являться желательными.
[00146] Настоящее изобретение также охватывает страдомеры, включающие Fc-домены и неполные Fc-домены, которые содержат аминокислоты, которые отличаются от природной аминокислотной последовательности Fc-домена или неполного Fc-домена. Предпочтительные Fc-домены, включаемые в биомиметические соединения настоящего изобретения, обладают детектируемой специфичной связывающей аффинностью либо в отношении к холо-Fcγ-рецептору, или к растворимой внеклеточной части домена FcγR. Первичные аминокислотные последовательности и полученные с помощью рентгенокристаллографии структуры различных Fc-доменов и мономеров Fc-домена известны в уровне техники. См., например, Woof JM, Burton DR. Human antibody-Fc receptor interactions illuminated by crystal structures. Nat Rev Immunol. 2004 Feb; 4(2): 89-99. Типичные Fc-домены с Fcγ-рецепторсвязывающей способностью включают Fc-домены из иммуноглобулина G человека изотипов 1-4 (hIgG1-4) (SEQ ID NOS: 1, 3, 5 и 7 соответственно; см. также фиг. 15А-D). (См. фиг. 2 в статье Robert L. Shields, et al. High Resolution Mapping of the Binding Site on Human IgG1 for FcγRI, FcγRII, FcγRIII, and FcRn and Design of IgG1 Variants with Improved Binding to the FcγR. J. Biol. Chem., Feb 2001; 27 6: 6591-6604). Указанные нативные последовательности были подвергнуты обширному структурно-функциональному анализу, включая картирование сайт-направленного мутагенеза функциональных последовательностей 14. На основе указанных предшествующих структурно-функциональных исследований и доступных данных кристаллографии специалист в данной области может создать функциональные варианты последовательности Fc-домена (например, SEQ ID NOS: 1, 3, 5 и 7) с сохранением Fcγ-рецепторсвязывающей способности Fc-домена.
[00147] Аминокислотные замены могут быть обнаружены по ходу всей последовательности Fc-домена или локализованы до конкретных неполных Fc-доменов, которые составляют Fc-домен. Функциональные варианты Fc-домена, используемые в страдомерах и других биомиметиках настоящего изобретения, обладают по меньшей мере приблизительно 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности по отношению к нативному Fc-домену. Аналогично, функциональные варианты неполных Fc-доменов, используемые в страдомерах и других биомиметиках настоящего изобретения, обладают по меньшей мере приблизительно 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности по отношению к нативному неполному Fc-домену.
[00148] Квалифицированному специалисту очевидно, что настоящее изобретение также охватывает применение функциональных вариантов мономеров Fc-домена в конструировании мономеров Fc-фрагмента, мономеров неполного Fc-фрагмента, мономеров страдомера и других мономеров настоящего изобретения. Функциональные варианты мономеров Fc-домена обладают по меньшей мере приблизительно 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности по отношению к последовательности нативного мономера Fc-домена.
[00149] Аналогично, настоящее изобретение также охватывает применение функциональных вариантов мономеров неполного Fc-домена в конструировании мономеров Fc-фрагмента, мономеров неполного Fc-фрагмента, мономеров Fc-доменов, мономеров страдомера и других мономеров настоящего изобретения. Функциональные варианты мономеров неполного Fc-домена обладают по меньшей мере приблизительно 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичности последовательности по отношению к последовательности нативного мономера неполного Fc-домена.
[00150] Аминокислотные замены могут уменьшать, увеличивать или никак не изменять аффинность связывания страдомера с Fcγ-рецептором. Предпочтительно такие аминокислотные замены являются заменами консервативных аминокислот, однако такие замены включают делеции, добавления и другие замены. Замены консервативных аминокислот обычно включают замены в пределах следующих групп: глицин и аланин; валин, изолейцин и лейцин; аспарагиновая кислота и глутаминовая кислота; аспарагин, глутамин, серии и треонин; лизин, гистидин и аргинин; а также фенилаланин и тирозин.
[00151] Термин "функциональный вариант", используемый в настоящей заявке, относится к последовательности, родственной по гомологии с исходной последовательностью, которая способна опосредовать те же биологические эффекты, что и исходная последовательность (в случае полипептида), или которая кодирует полипептид, способный опосредовать те же биологические эффекты, как и полипептид, кодируемый исходной последовательностью (в случае полинуклеотида). Например, функциональный вариант любого из биомиметиков, описанных в настоящей заявке, обладает заданной гомологией или идентичностью и способен к иммунной модуляции дендритных клеток. Функциональные варианты последовательности включают и полинуклеотиды, и полипептиды. Идентичность последовательности обычно оценивают с помощью BLAST 2.0 (Basic Local Alignment Search Tool), работая с параметрами по умолчанию: Filter - On, Scoring Matrix - BLOSUM62, Word Size - 3, E value - 10, Gap Costs - 11,1 и Alignments - 50.
[00152] На основе вышесказанного следует понимать, что страдомеры настоящего изобретения включают страдомеры, содержащие: (а) только природные Fc-домены; (b) смесь природных Fc-доменов и Fc-доменов с измененными аминокислотными последовательностями; и (с) только Fc-домены с измененными аминокислотными последовательностями. Необходимо лишь, чтобы страдомеры, содержащие измененные аминокислотные последовательности, обладали по меньшей мере 25%, 30%, 4 0%, 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99%, 99,5% или 100% или даже большей способностью по сравнению со страдомером, включающим Fc-домены с природными последовательностями, связываться с двумя или более Fcγ-рецепторами.
[00153] Последовательности вышеуказанных Fcγ-рецепторсвязывающих сайтов, присутствующих в страдомерах и страдотелах настоящего изобретения, могут быть изменены с помощью генной инженерии в целях прогнозируемого получения связывающих сайтов с измененной связывающей способностью и аффинностью по сравнению с нативной последовательностью. Например, определенные остатки могут быть изменены, что снижает связывание Fc-домена биомиметических соединений с FcγRIT, повышая связывание с FcγRIIIa. Пример развернутого структурно-функционального анализа на основе мутагенеза для Fcγ-рецепторсвязывающих последовательностей hIgG можно найти в статье Robert L. Shields, et al. High Resolution Mapping of the Binding Site on Human IgG1 for FcγRI, FcγRII, FcγRIII, and FcRn and Design of IgG1 Variants with Improved Binding to the FcγR. J. Biol. Chem., Feb 2001; 276: 6591-6604. Подобные исследования. были выполнены на Fc IgG мыши (mIgG Fc). На основе гомологии структуры и первичной последовательности нативных Fc-доменов IgG различных видов специалист в данной области может перенести обширную информацию по структурно-функциональным свойствам hIgG Fc и mIgG Fc в рациональный мутагенез всех последовательностей нативных Fcγ-пецепторсвязывающих сайтов в биомиметических соединениях настоящего изобретения, создав связывающие сайты с заданной специфичностью и аффинностью связывания к Fcγ-рецептору.
[00154] В дополнение к составу аминокислотной последовательности нативных областей Fc-доменов содержание углеводов в Fc-домене, как известно, оказывает большое влияние на структуру Fc-домена и взаимодействие с FcγR. См., например, Robert L. Shields, et al. Lack of Fucose on Human IgG1 N-Linked Oligosaccharide Improves Binding to Human Fc RIII and Antibody-dependent Cellular Toxicity. J. Biol. Chem., Jul 2002; 277: 26733-26740 (doi:10.1074/jbe.M202069200); Ann Wright and Sherie L. Morrison. Effect of C2- Associated Carbohydrate Structure on Ig Effector Function: Studies with Chimeric Mouse-Human IgG1 Antibodies in Glycosylation Mutants of Chinese Hamster Ovary Cells. J. Immunol, Apr 1998; 160: 3393-3402. Содержание углеводов можно регулировать, используя, например, конкретные системы экспрессии белков, включая конкретные клеточные линии или энзиматическую модификацию in vitro. Таким образом, настоящее изобретение включает страдомеры и страдотела, включающие Fc-домены с нативным содержанием углеводов холо-антитела, из которого были получены указанные домены, а также биомиметические соединения, в которых изменено содержание углеводов.
[00155] Введение дополнений в полипептидную цепь неполного Fc-домена, мультимеризационная область или изменения в гликозилировании могут вызвать конформационное изменение в Fc-домене, приводящее к повышению связывания Fc-домена с Fcγ-рецептором. Таким образом, кажущиеся незначительными модификации полипептида могут также привести к получению страдомера, способного связывать несколько Fcγ-рецепторов.
Неполные домены и неполные фрагменты
[00156] Квалифицированному специалисту также очевидно, что Fc-домены и неполные Fc-домены, используемые в вариантах осуществления настоящего изобретения, могут и не быть полноразмерными вариантами. Таким образом, настоящее изобретение охватывает применение мономеров Fc-домена и мономеров неполного Fc-домена, не содержащих N-концевые, С-концевые аминокислоты или аминокислоты из центральной части конкретных мономеров Fc-домена и мономеров неполного Fc-домена, которые составляют страдомеры и другие биомиметики настоящего изобретения.
[00157] Например, был описан сайт связывания Fcγ-рецепторов на иммуноглобулинах IgG человека (например, Radaev, S., Sun, P., 2001. Recognition of Immunoglobulins by Fey Receptors. Molecular Immunology 38, 1073-1083; Shields, R.L. et. al., 2001. High Resolution Mapping of the Binding Site on Human IgG1 for FcγRI, FcγRII, FcγRIII, and FcRn and Design of IgG1 Variants with Improved Binding to the FcγR. J. Biol. Chem. 276 (9), 6591-6604). На основе данной информации можно удалить аминокислоты из Fc-домена указанных иммуноглобулинов и определить влияние, оказываемое на взаимодействие между Fc-доменом и рецептором. Таким образом, настоящее изобретение охватывает Fc-домены IgG, содержащие по меньшей мере приблизительно 90% аминокислот, включая положения 233-338 нижней шарнирной области и СН2, как определено в статье Radaev, S., Sun, P., 2001.
[00158] Неполные Fc-домены иммуноглобулинов IgG согласно настоящему изобретению включают всю шарнирную область или ее часть, весь СН2 домен или его часть, а также весь СН3 домен или его часть.
[00159] Неполные Fc-домены IgG, содержащие только часть шарнирной области, часть СН2 домена или часть СН3 домена, сконструированы из мономеров неполного Fc-домена. Таким образом, настоящее изобретение включает мономеры шарнирной области IgG, полученные из N-концевой части шарнирной области или С-концевой части шарнирной области. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61 или 62 (до 15 для IgG1, до 12 для IgG2, до 62 для IgG3, до 12 для IgG4) аминокислоты шарнирной области.
[00160] Настоящее изобретение также включает мономеры СН2 домена IgG, полученные из N-концевой части СН2 домена или С-концевой части СН2 домена. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109 или 110 (до 110 для IgG1 и IgG3, до 109 для IgG2 и IgG4) аминокислот СН2 домена.
[00161] Настоящее изобретение дополнительно включает мономеры СН3 домена IgG, полученные из N-концевой части СН3 домена или С-концевой части СН3 домена. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107 (до 106 для IgG1 и IgG3, до 107 для IgG2 и IgG4) аминокислот СН3 домена.
[00162] Неполные Fc-домены иммуноглобулинов IgA1, IgA2 и IgD настоящего изобретения включают всю шарнирную область или ее часть, весь СН2 домен или его часть, а также весь СН3 домен или его часть. Кроме того, в качестве неполных Fc-доменов может использоваться весь СН1 домен иммуноглобулина IgA1, IgA2 или IgD, или его часть.
[00163] Неполные домены IgA1, IgA2 и IgD, содержащие только часть шарнирной области, часть СН1 домена, часть СН2 домена или часть СН3 домена, сконструированы из мономеров неполного Fc-домена. Таким образом, настоящее изобретение включает мономеры шарнирной области, полученные из N-концевой части шарнирной области или С-концевой части шарнирной области IgA1, IgA2 или IgD. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63 или 64 (до 26 для IgA1, до 13 для IgA2, до 64 для IgD) аминокислоты шарнирной области.
[00164] Настоящее изобретение включает мономеры СН2 домена, полученные из N-концевой части СН2 домена или С-концевой части СН2 доменов IgA1, IgA2 или IgD. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106 или 107 (до 102 для IgA1, до 96 для IgA2, до 107 для IgD) аминокислот СН2 домена.
[00165] Настоящее изобретение включает СН3 домены, полученные из N-концевой части СН3 домена или С-концевой части СН3 доменов IgA1, IgA2 или IgD. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130 или 131 (до 113 для IgA1, до 131 для IgA2, до 110 для IgD) аминокислоту СН3 домена.
[00166] Неполные Fc-домены иммуноглобулинов IgM и IgE настоящего изобретения включают всю шарнирную область/СН2 домен или их часть, весь СН3 домен или его часть, а также весь СН4 домен или его часть, из указанных молекул. Кроме того, в качестве неполных Fc-доменов может использоваться весь СН1 домен, или его часть, из иммуноглобулинов IgM и IgE.
[00167] Неполные домены IgM и IgE, содержащие только часть шарнирной области/СН2 домена, часть СН3 домена или часть СН4 домена, сконструированы из мономеров неполного Fc-домена. Таким образом, настоящее изобретение включает мономеры шарнирной области/СН2 домена, полученные из N-концевой части шарнирной области/СН2 домена или С-концевой части шарнирной области/СН2 домена IgM или IgE. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111 или 112 (до 112 для IgM, до 109. для IgE) аминокислот шарнирной области / СН2 домена.
[00168] Настоящее изобретение включает мономеры СН3 домена IgM и IgE, полученные из N-концевой части СН3 домена или С-концевой части СН3 домена IgM или IgE. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105 или 106 (до 106 для IgM, до 105 для IgE) аминокислот СН3 домена.
[00169] Настоящее изобретение включает мономеры СН4 домена IgM и IgE, полученные из N-концевой части СН4 домена или С-концевой части СН4 домена IgM или IgE. Они, таким образом, могут содержать, например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56, 57, 58, 59, 60, 61, 62, 63, 64, 65, 66, 67, 68, 69, 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99, 100, 101, 102, 103, 104, 105, 106, 107, 108, 109, 110, 111, 112, 113, 114, 115, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129 или 130 (до 130 для IgM, до 105 для IgE) аминокислот СН4 домена. Однако размер частей СH4 домена IgM или IgE, которые включают С-конец СН4 домена, предпочтительно превышает 18 аминокислот и более предпочтительно превышает 30 аминокислот, а наиболее предпочтительно превышает 50 аминокислот.
[00170] Из вышеуказанного очевидно, что различные варианты осуществления настоящего изобретения включают страдомеры, содержащие: (а) полноразмерные Fc-домены; (b) комбинацию полноразмерных Fc-доменов и неполных Fc-доменов; и (с) неполные Fc-домены. В каждом из указанных вариантов осуществления страдомеры могут дополнительно включать СН1 домены. Как описано в настоящей заявке, в каждом варианте осуществления страдомеров настоящего изобретения страдомеры обладают способностью связывать два или более Fcγ-рецепторов.
Предпочтительные варианты осуществления страдомеров и мономеров страдомеров
[00171] Ниже приведены примеры мономеров страдомеров настоящего изобретения:
1. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1
2. Шарнирная область IgG1 - СН2 IgG3 - СН3 IgG1- шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1
3. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG3 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1
4. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1
5. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG3 - СН3 IgG1
6. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG3
7. Шарнирная область IgG1 - СН2 IgG3 - СН3 IgG1 - шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1
8. Шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1
9. Шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1
10. Шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG3 - шарнирная область IgG1 -СН2 IgG3 - СН3 IgG3
11. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG3 - СН2 IgG3 - СН3 IgG3 - шарнирная область IgG1 -СН2 IgG1 - СН3 IgG1
12. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG3 - шарнирная область IgG1 - СН2 IgG3 - СН3 IgG3 -шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1
13. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG3 - СН2 IgG3 - СН3 IgG3 - шарнирная область IgG1 -СН2 IgG2 - СН3 IgG3.
14. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG4 - СН2 IgG4 - СН3 IgG4 - шарнирная область IgG1 -СН2 IgG1 - СН3 IgG1
[00172] Следует понимать, что в каждом из указанных вариантов осуществления, а также в других вариантах осуществления, представленных в настоящей заявке, доменные связи могут использоваться для связи отдельных мономеров неполных Fc-доменов, которые формируют отдельные мономеры неполных Fc-доменов, которые формируют мономеры страдомеров. В одном из вариантов осуществления мономеры неполного Fc-домена для каждого из мономеров страдомера, перечисленных выше, являются мономерами неполного Fc-домена человека.
[00173] Настоящее изобретение включает страдомеры, включающие два или более мономеров страдомера, перечисленных выше. В предпочтительных вариантах осуществления настоящее изобретение включает последовательные страдомеры, включающие два -идентичных мономера страдомера, приведенные выше.
[00174] Как указано выше, функциональные свойства страдомера касательно связывания более чем одного Fcγ-рецептора также могут обеспечиваться введением J цепи в качестве кор-группы в кор-страдомер, аналогичный или молекуле природных IgM, или IgA. В нативных иммуноглобулинах IgA и IgM соединительная (J) цепь представляет собой 15 кДа пептид, который соединяет тяжелую и легкую цепи IgA и IgM с 18 аминокислотами "секреторной концевой части" Fc-частей антител через дисульфидные мостики. Braathen, R., et al., The Carboxyl-terminal Domains of IgA and IgM Direct I sotype-specifïс Polymerization and Interaction with the Polymeric Immunoglobulin Receptor, J. Bio. Chem. 277(45), 42755-42762 (2002).
[00175] Такие кор-страдомеры могут состоять из мономеров страдомера, содержащих природные СН4 Fc-домены, предпочтительно из иммуноглобулинов IgM, обеспечивая таким образом ассоциацию подобных мономеров страдомера с J цепью (см. фиг. 10А - 10D). Ниже приведены примеры мономеров страдомера, которые могут самодимеризоваться, образуя страдомер, а затем соединяться с J цепью, формируя кор-страдомер, состоящий из множества (например, двух, трех, четырех, пяти, шести, семи, восеми, девяти, десяти, одиннадцати, двенадцати, пятнадцати, восемнадцати, двадцати или более) страдомеров:
1. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - CH4 IgM (см. фиг. 10С - 10D)
2. Шарнирная область IgG1 - СН2 IgG3 - СН3 IgG1 - шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - CH4 IgM
3. Шарнирная область IgG1 - CH2 IgG1 - СН3 IgG3 - шарнирная область IgG1 - CH2 IgG1 - СН3 IgG1 - CH4 IgM (см. фиг. 10A - 10B)
4. Шарнирная область IgG1 - CH2 IgG1 - СН3 IgG1 - шарнирная область IgG3 - CH2 IgG1 - СН3 IgG1 - CH4 IgM
5. Шарнирная область IgG1 - CH2 IgG1 - CH3 IgG1 - шарнирная область IgG1 - CH2 IgG3 - CH3 IgG1 - CH4 IgM
6. Шарнирная область IgG1 - CH2 IgG1 - CH3 IgG1 - шарнирная область IgG1 - CH2 IgG1 - CH3 IgG1 - CH4 IgM
7. Шарнирная область IgG1 - CH2 IgG1 - CH3 IgG1 - шарнирная область IgG1 - CH2 IgG1 - CH3 IgG3 - CH4 IgM
8. Шарнирная область IgG1 - CH2 IgG3 - CH3 IgG1 - шарнирная область IgG3 - CH2 IgG1 - CH3 IgG1 - CH4 IgM
9. Шарнирная область IgG3 - CH2 IgG1 - CH3 IgG1 - шарнирная область IgG1 - CH2 IgG1 - CH3 IgG1 - CH4 IgM
10. Шарнирная область IgG3 - CH2 IgG1 - CH3 IgG1 - шарнирная область IgG3 - CH2 IgG1 - CH3 IgG1 - CH4 IgM
11. Шарнирная область IgG3 - CH2 IgG1 - CH3 IgG1 - шарнирная область IgG1 - CH2 IgG1 - шарнирная область IgG1 - CH2 IgG3 - CH3 IgG3 - CH4 IgM
[00176] Следует понимать, что в каждом из указанных вариантов осуществления, а также в других вариантах осуществления, представленных в настоящей заявке, доменные связи могут использоваться для связи отдельных мономеров неполных Fc-доменов, которые формируют отдельные мономеры неполных Fc-доменов, которые формируют мономеры страдомеров. В одном из вариантов осуществления мономеры неполного Fc-домена для каждого из мономеров страдомера, перечисленных выше, являются мономерами неполного Fc-домена человека.
[00177] Кор-страдомеры на основе J цепи также могут состоять из Fc-фрагментов, неполных Fc-фрагментов и/или Fc-доменов, которые содержат СН4 Fc-домен. В данном примере, каждый из Fc-фрагментов, неполных Fc-фрагментов и/или Fc-доменов, СН4 Fc-домен которых связан с кор-группой, может содержать только один Fcγ-рецепторсвязывающий сайт, однако в контексте такого кор-страдомера, образует биологически активный биомиметик, содержащий больше одного Fcγ-рецепторсвязывающего сайта. Квалифицированному специалисту очевидно, что неполные Fc-домены из различных нативных иммуноглобулинов могут использоваться для получения функциональных Fc-фрагментов, неполных Fc-фрагментов и Fc-доменов такого кор-страдомера. Ниже приведены примеры мономеров Fc-фрагментов, неполных Fc-фрагментов и Fc-доменов, которые могут самодимеризоваться, а затем ассоциироваться с J цепью, формируя кор-страдомер:
1. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - СН4 IgM
2. Шарнирная область IgG3 - СН2 IgG1 - СН3 IgG1 - СН4 IgM
3. Шарнирная область IgG1 - СН2 IgG3 - СН3 IgG1 - CH4 IgM
4. Шарнирная область IgG1 - CH2 IgG1 - СН3 IgG3 - CH4 IgM
5. Шарнирная область IgG1 - CH2 IgG3 - CH3 IgG3 - CH4 IgM
6. Шарнирная область IgG3 - CH2 IgG3 - CH3 IgG1 - CH4 IgM
7. Шарнирная область IgG3 - CH2 IgG3 - CH3 IgG1 - CH4 IgM
8. Шарнирная область IgG1 - CH2 IgG3 - CH3 IgG2 - CH4 IgM
9. Шарнирная область IgG1 - шарнирная область IgG3 - СН2 IgG3 - СН3 IgG2 - СН4 IgM
10. Шарнирная область IgG1 - СН2 IgG1 - СН3 IgG1 - СН4 IgE -CH4 IgM
[00178] Следует понимать, что в каждом из указанных вариантов осуществления, а также в других вариантах осуществления, представленных в настоящей заявке, доменные связи могут использоваться для связи отдельных мономеров неполных Fc-доменов, которые формируют отдельные мономеры неполных Fc-доменов, которые формируют мономеры страдомеров. В одном из вариантов осуществления мономеры неполного Fc-домена для каждого из мономеров страдомера, перечисленных выше, являются мономерами неполного Fc-домена человека.
[00179] Как следует из вышеприведенных примеров, мономеры страдомеров могут иметь различную длину и состав, в соответствии с целью, образуя кор-страдомер, содержащий более одного Fcγ-рецепторсвязывающего сайта при соединении посредством самоагрегации или интер-мономер страдомерных связей со вторым мономером страдомера и при соединении с J цепью. Данные примеры никоим образом не ограничивают изобретение, при этом специалисту в данной области очевидно, что страдомеры могут иметь множество других конфигураций. Fcγ-рецепторы
[00180] Термины "FcγR" и "Fcγ-рецептор", используемые в настоящей заявке, включают каждого представителя семейства Fc гамма рецепторных белков, экспрессируемых на поверхности иммуноноцитов, как описано в Nimmerjahn F and Ravetch JV. Fcgamma receptors: old friends and new family members. Immunity. 2006 Jan; 24(1): 19-28, или которые могут быть описаны позже. Предполагается, что термин "FcγR", описанный в настоящей заявке, охватывает всех представителей Fc гамма семейств RI, RII и RIII. Fcγ-рецептор включает Fcγ-рецепторы низкой аффинности и высокой аффинности, включая, помимо прочих, FcγRI (CD64); FcγRII (CD32) и его изотипы, и аллотипы FcγRIIa LR, FcγRIIa HR, FcγRIIb и FcγRIIc; FcγRIII (CD16) и его изотипы FcγRIIIa и FcγRIIIb. Квалифицированному специалисту очевидно, что настоящее изобретение, которое включает соединения, которые связывают FcγR, относится к будущим FcγR рецепторам и соответствующим изотипам и аллотипам, которые еще неизвестны на сегодняшний день.
[00181] Было описано, что IVIG связывается и полностью насыщает неонатальный Fc-рецептор ("FcRn") и что такое конкурентов ингибирование FcRn может играть важную роль в биологической активности IVIG (например, Mechanisms of Intravenous Immunoglobulin Action in Immune Thrombocytopenic Purpura. F. Jin, J. Balthasar. Human Immunology, 2005, Volume 66, Issue 4, Pages 403-410.) Поскольку иммуноглобулины, которые связываются с Fcγ-рецепторами, также связываются по меньшей мере в некоторой степени, с FcRn, то квалифицированному специалисту очевидно, что страдомеры, которые способны связываться с более чем одним Fcγ-рецептором, также будут связывать и могут полностью насыщать FcRn.
[00182] "Иммунологическая активность нативного агрегированного IgG" относится к свойствам мультимеризованного IgG, которые влияют на функционирование иммунной системы при воздействии на иммунную систему агрегатов IgG. Специфические свойства нативного мультимеризованного IgG включают измененное специфическое связывание с FcγR рецепторами, перекрестное связывание с FcγR рецепторами на поверхности иммуноцитов или эффекторные функциональные свойства мультимеризованного IgG, такие как антителозависимая клеточно-опосредованная цитотоксичность (АЗКЦ), фагоцитоз (ADCP) или связывание комплимента (см., например, Nimmerjahn F, Ravetch JV. The antiinflammatory activity of IgG: the intravenous IgG paradox. J Exp Med. 2007; 204: 11-15; Augener W, Friedman B, Brittinger G. Are aggregates of IgG the effective part of high-dose immunoglobulin therapy in adult idiopathic thrombocytopenic purpura (ITP)? Blut. 1985; 50: 249-252; Arase N, Arase H, Park SY, Ohno H, Ra C, Saito T. Association with FcRgamma is essential for activation signal through NKR-P1 (CD 161) in natural killer (NK) cells and NKl.1+ T cells. J Exp Med. 1997; 186: 1957-1963; Teeling JL, Jansen-Hendriks T, Kuijpers TW, et al. Therapeutic efficacy of intravenous immunoglobulin preparations depends on the immunoglobulin G dimers: studies in experimental immune thrombocytopenia. Blood. 2001; 98: 1095-1099; Anderson CF, Mosser DM. Cutting edge: biasing immune responses by directing antigen to macrophage Fc gamma receptors. J Immunol. 2002; 168: 3697-3701; Jefferis R, Lund J. Interaction sites on human IgG-Fc for Fc[gamma]R: current models. Immunology Letters. 2002; 82: 57; Banki Z, Kacani L, Mullauer B, et al. Cross-Linking of CD32 Induces Maturation of Human Monocyte - Derived Dendritic Cells Via NF-{kappa} В Signaling Pathway. J Immunol. 2003; 170: 3963-3970; Siragam V, Brine D, Crow AR, Song S, Freedman J, Lazarus AH. Can antibodies with specificity for soluble antigens mimic the therapeutic effects of intravenous IgG in the treatment of autoimmune disease? J Clin Invest. 2005; 115: 155-160). Обычно указанные свойства оценивают посредством сравнения со свойствами мономерного IgG.
[00183] "Сопоставимый или превосходящий перекрестное связывание Fey рецептора или эффекторные функциональные свойства множества природных, агрегированных иммуноглобулинов IgG", как используется в настоящей заявке, означает, что страдомер показывает в анализе результат порядка 70% или более по сравнению с результатом, получаемым для IVIG. В других вариантах осуществления результат анализа находится по меньшей мере в пределах стандартной среднеквадратической ошибки результатов анализа, получаемых для IVIG. В других вариантах осуществления результат анализа составляет 110% или выше по сравнению с результатом, получаемым для IVIG. Анализы на перекрестное связыванием FcγR известны средним специлистам в данной области (см. например, Falk Nimmerjahn and Jeffrey Ravetch. Fey receptors as regulators of immune responses. Nature Reviews Immunology, опубликовано онлайн, 7 декабря 2007 г.).
[00184] "Иммуномодулирующие активности", "модулирующий иммунный ответ", "модулирующий иммунную систему" и "иммуномодуляция" означают воздействие на иммунные системы с измением активностей, функциональных свойств и относительного количества одного или нескольких иммуноцитов, включая созревание клетки какого-либо типа в пределах своего типа клеток или с превращением в другие типы клеток. Например, иммуномодуляция незрелых моноцитов может приводить к увеличению популяции более зрелых моноцитов, дендритных клеток, макрофагов или остеокластов, которые образуются из незрелых моноцитов. Например, рецепторы иммуноцитов могут быть связаны иммунологически активными биомиметиками и могут активировать внутриклеточную передачу сигналов, индуцируя различные изменения иммуноцитов, отдельно упомянутые как "активация иммуномодуляции". Блокирование рецепторов иммуноцитов с целью предотвращения активации рецепторов также включено в рамки "иммуномодуляции" и может отдельно упоминаться как "ингибиторная иммуномодуляция".
[00185] Модуляция созревания моноцита относится к дифференцировке моноцита в зрелую DC, макрофаг или остеокласт. Дифференцировка может модулироваться с целью ускорения созревания и/или увеличения числа моноцитов, подвергаемых дифференцировке. В альтернативе, дифференцировка может быть снижена в отношении скорости дифференцировки и/или количества клеток, подвергающихся дифференцировке.
[00186] Используемый в настоящей заявке термин "выделенный" полипептид или пептид относится к полипептиду или пептиду, который не имеет какого-либо природного аналога, либо был выделен или получен при очистке от компонентов, которые обычно окружают его, например, в тканях, таких как поджелудочная железа, печень, селезенка, яичник, яичко, мышца, ткань сустава, нервная ткань, гастроинтестинальная ткань, ткань молочной железы или опухолевая ткань (например, ткань рака молочной железы), или в физиолигических жидкостях, таких как кровь, сыворотка или моча. Как правило, полипептид или пептид считаются "выделенными", когда степень их чистоты от белков и других природных органических молекул, с которыми они обычно связаны, составляет по меньшей мере 70% по сухому весу. Предпочтительно, препарат полипептида (или пептида) изобретения содержит по меньшей мере 80%, более предпочтительно по меньшей мере 90% и наиболее предпочтительно по меньшей мере 99% по сухому весу полипептида (пептида) изобретения соответственно. Поскольку полипептид или пептид, синтезированный химически, по свой природе отделен от компонентов, которые сопровождают его в природе, синтетический полипептид или пептид являются "выделенными".
[00187] Выделенный полипептид (или пептид) изобретения может быть получен, например, посредством экстракции из природного источника (например, из тканей или физиологических жидкостей); посредством экспрессии рекомбинантной нуклеиновой кислоты, кодирующей полипептид или пептид; или с помощью химического синтеза. Полипептид или пептид, который получен в клеточной системе, отличной от источника, из которого он происходит в природе, являются "выделенным", так как он в обязательном порядке не будет содержать компоненты, которые сопровождают его в природе. Степень очистки или чистоты может быть определена любым подходящим методом, например, с помощью колоночной хроматографии, электрофореза в полиакриламидном геле или ВЭЖХ анализа.
Фармацевтические композиции
[00188] Введение иммунологически активных биомиметических композиций, описанных в настоящей заявке, осуществляется любым обычным путем - перорально, парентерально или местно. Примеры путей введения включают, помимо прочих, пероральный, назальный, буккальный, ректальный, вагинальный, глазной, подкожный, внутримышечный, внутрибрюшинный, внутривенный, внутриартериальный, внутриопухолевый, спинальный, интратекальный, внутрисуставной, внутриартериальный, субарахноидальный, сублингвальный, на слизистую ротовой полости, бронхиальный, лимфатический, внутриматочный, подкожный, внутриопухолевый, интегрируемый на имплантируемом устройстве, интрадуральный, интракортикальный или кожный. Такие композиции обычно вводят в форме фармацевтически приемлемых композиций, как описано в настоящей заявке. В предпочтительном варианте осуществления выделенный иммунологически активный биомиметик вводят внутривенно.
[00189] Термин "фармацевтически приемлемый носитель", используемый в настоящей заявке, включает все без исключения растворители, диспергирующие среды, покрытия, антибактериальные и противогрибковые агенты, изотонические агенты, замедлители абсорбции и т.п. Применение таких сред и агентов в сочетании с фармацевтически активными веществами известно в уровне техники. За исключением тех случаев, когда какие-либо обычные среды или агенты являются несовместимыми с векторами или клетками настоящего изобретения, их применение в терапевтических композициях предусмотрено. Также в композиции могут быть включены дополнительные активные компоненты.
[00190] Иммунологически активные биомиметические композиции настоящего изобретения могут быть приготовлены в нейтральной форме или в форме соли. Фармацевтически приемлемые соли включают соли присоединения кислот (образованные со свободными аминогруппами белка) и соли, образованные с неорганическими кислотами, такими как, например, хлороводородная или фосфорная кислоты, или такими органическими кислотами как уксусная, щавелевая, винная, миндальная и т.п. Соли, образованные свободными карбоксильными группами, также могут быть получены с неорганическими основаниями, такими как, например, гидроксиды натрия, калия, аммония, кальция или гидрат оксида железа, а также с такими органическими основаниями как изопропиламин, триметиламин, гистидин, прокаин и т.п.
[00191] Стерильные растворы для инъекций получают путем введения в необходимом количестве иммунологически активных биомиметиков в подходящий растворитель, при необходимости вместе с другими различными компонентами, перечисленными выше, с последующей стерилизацией фильтрованием. Обычно дисперсии получают путем введения различных стерилизованных активных компонентов в стерильную среду, которая содержит базовую дисперсионную среду и другие необходимые компоненты из вышеперечисленного. В случае стерильных порошков для приготовления стерильных растворов для инъекций предпочтительные способы приготовления включают методы вакуумной сушки и лиофильной сушки, которые приводят к получению порошка активного компонента, содержащего также какой-либо дополнительный требуемый компонент из соответствующего, ранее простерилизованного фильтрованием раствора.
[00192] Кроме того, один из вариантов осуществления относится к иммунологически активной биомиметической композиции, подходящей для перорального введения, которая приготовлена в фармацевтически приемлемом носителе с или без инертного разбавителя. Носитель должен являться усвояемым или съедобным, и включает жидкие, полутвердые, то есть пастообразные, или твердые носители. За исключением тех случаев, когда какие-либо обычные среды, агенты, разбавители или носители являются нежелательными касательно реципиента или терапевтической эффективности иммунологически активного биомиметического препарата, содержащегося в них, их использование в перорально вводимой иммунологически активной биомиметической композиции, применяемой при осуществлении способов настоящего изобретения, предусмотрено. Примеры носителей или разбавителей включают жиры, масла, воду, соляные растворы, липиды, липосомы, смолы, связующие вещества, наполнители и т.п., или комбинации перечисленного. Термин "пероральное введение", используемый в настоящей заявке, включает пероральное, буккальное, энтеральное или внутрижелудочное введение.
[00193] В одном из вариантов осуществления композицию объединяют с носителем любым удобным и практичным способом, то есть путем растворения, суспендирования, эмульгирования, смешивания, инкапсулирования, микрокапсулирования, абсорбции и т.п. Подобные операции являются стандартными для специалистов в данной области.
[00194] В конкретном варианте осуществления иммунологически активную биомиметическую композицию в порошковой форме объединяют или тщательно смешивают с полутвердым или твердым носителем. Смешивание может быть выполнено любым удобным способом, например, растиранием. В процессе смешивания также могут быть добавлены стабилизаторы для предохранения композиции от потери терапевтической активности в ходе применения, то есть от денатурации в желудке. Примеры стабилизаторов, применяемых в перорально вводимой композиции, включают буферы, антагонисты секреции желудочных кислот, аминокислоты, такие как глицин и лизин, углеводы, такие как декстроза, манноза, галактоза, фруктоза, лактоза, сахароза, мальтоза, сорбит, маннит и т.д., ингибиторы протеолитических ферментов и т.п. Более предпочтительно, стабилизатор для перорально вводимой композиции может также включать антагонисты секреции желудочных кислот.
[00195] Кроме того, иммунологически активная биомиметическая композиция для перорального введения, объединенная с полутвердым или твердым носителем, может быть также приготовлена в форме желатиновых капсул, таблеток или пилюль с твердой или мягкой оболочкой. Более предпочтительно, желатиновые капсулы, таблетки или пилюли имеют кишечнорастворимое покрытие. Кишечнорастворимые покрытия предотвращают денатурацию композиции в желудке или верхней кишке, где рН является кислым. См., например, патент США 5,629,001. При попадании в тонкую кишку с основным рН покрытие растворяется,. и композиция высвобождается, взаимодействуя с клетками кишечника, например, М-клетками пейеровых бляшек.
[00196] В другом варианте осуществления иммунологически активная биомиметическая композиция в порошковой форме объединена или тщательно смешана с материалами, которые образуют наночастицы, инкапсулирующие иммунологически активный биомиметик, или к которым присоединен иммунологически активный биомиметик. Каждая наночастица имеет размер меньше или равный 100 микронам. Наночастица может обладать мукоадгезивными свойствами, которые обеспечивают абсорбцию иммунологически активного биомиметика в желудочно-кишечном тракте, который в ином случае не был бы биодоступен при пероральном введении.
[00197] В другом варианте осуществления порошковая композиция объединена с жидким носителем, таким как, например, вода или физиологический раствор, с или без стабилизатора.
[00198] Конкретная лекарственная форма иммунологически активного биомиметика, которая может применяться, является раствором иммунологически активного биомиметического белка в гипотоническом буфере на основе фосфатов, который не содержит калия, где состав буфера является следующим: 6 мМ моногидрат одноосновного фосфата натрия, 9 мМ гептагидрат двухосновного фосфата натрия, 50 мМ хлорид натрия, рН 7,0+/-0,1. Концентрация иммунологически активного биомиметического белка в гипотоническом буфере может изменяться в пределах от 10 микрограммов/мл до 100 миллиграммов/мл. Указанную лекарственную форму можно вводить любым путем введения, например, помимо прочего, внутривенно.
[00199] Кроме того, иммунологически активная биомиметическая композиция для местного применения, объединенная с полутвердым носителем, может быть также приготовлена в форме крема или геля. Предпочтительным носителем для приготовления геля является гель-полимер. Предпочтительные полимеры, используемые для приготовления композиции настоящего изобретения в форме геля, включают, помимо прочих, карбопол, карбоксиметилцеллюлозу и плюрониловый полимеры. В частности, порошковую композицию, содержащую Fc-мультимер, объединяют с гелем на водной основе, содержащим полимеризационный агент, такой как Карбопол 980, в концентрации от 0,5% до 5% вес/об, для нанесения на кожу для лечения заболевания или под кожу. Термин "местное применение", используемый в настоящей заявке, включает нанесение на поверхность кожи, эпидермиса, подкожного слоя или слизистой.
[00200] В процессе приготовления лекарственной формы растворы вводят способом, совместимым с приготовлением дозированной лекарственной формы, и в таком количестве, которое является терапевтически эффективным и приводит к облегчению или устранению симптомов. Лекарственные формы обычно вводят в различных дозированных формах, таких как растворы для внутреннего применения, лекарственные капсулы и т.п. Некоторое изменение дозировки может происходить в зависимости от состояния подвергаемого лечению индивида. Лицо, ответственное за введение, может, в любом случае, определить подходящую дозу для отдельного индивида. Кроме того, для введения человеку препараты должны соответствовать стандартам стерильности, полной безопасности и чистоты, требуемым Департаментом стандартов биопрепаратов FDA.
[00201] Путь введения изменяется, как и следовало ожидать, в соответствии с локализацией и природой заболевания, подвергаемого лечению, и может включать, например, внутрикожный, трансдермальный, парентеральный, внутривенный, внутримышечный, внутриназальный, подкожный, чрескожный, внутритрахеальный, внутрибрюшинный, внутриопухолевый, перфузию, промывку, прямую инъекцию и пероральное введение.
[00202] Термин "парентеральное введение", используемый в настоящей заявке, включает любую форму введения, в которой соединение абсорбируется в организме индивида, исключая абсорбцию через кишечный тракт. Примеры способов парентерального введения, используемых в настоящем изобретении, включают, помимо прочих, внутримышечное, внутривенное, внутрибрюшинное, внутриопухолевое, внутриглазное или внутрисуставное введение.
[00203] Ниже приведены конкретные примеры различных категорий фармацевтических форм и предпочтительных путей введения, как указано, для конкретных примеров заболеваний:
[00204] Буккальная или подъязычная растворимая таблетка: ангина, узелковый полиартериит.
[00205] Внутривенно: идиопатическая тромбоцитопеническая пурпура, миозит с включенными тельцами, парапротеинемическая IgM демиелинизирующая полиневропатия, некротизирующий фасцит, вульгарная пузырчатка, гангрена, дерматомиозит, гранулема, лимфома, сепсис, апластическая анемия, полиорганная недостаточность, множественная миелома и моноклональная гаммапатия неизвестной этиологии, хроническая воспалительная демиелинизирующая полирадикулоневропатия, воспалительные миопатии, тромбическая тромбоцитопеническая пурпура, миозит, анемия, неоплазия, гемолитическая анемия, энцефалит, миелит, миелопатия, особенно связанная с Т-лимфотропным вирусом человека первого типа, лейкоз, рассеянный склероз и неврит зрительного нерва, астма, эпидермальный некролиз, миастенический синдром Ламберта-Итона, миастения гравис, невропатия, увеит, синдром Гийена-Барре, гомологичная болезнь, синдром мышечной скованности, паранеопластическая дегенерация мозжечка, вызванная анти-Yo антителами, паранеопластический энцефаломиелит и сенсорная невропатия, вызванная анти-Hu антителами, системный васкулит, системная красная волчанка, аутоиммунная диабетическая невропатия, острая идиопатическая вегетативная невропатия, синдром Фогта-Коянаги-Харады, многоочаговая двигательная невропатия, боковой амиотрофический склероз, ассоциируемый с антителами против GM1, демиелинизация, мембранозно-пролиферативный гломерулонефрит, кардиомиопатия, болезнь Кавасаки, ревматоидный артрит и синдром Эвана IM-ИТП, CIDP, MS, дерматомиозит, миастения гравис, мышечная дистрофия. Термин "внутривенное введение", используемый в настоящей заявке, включает все способы доставки соединения или композиции настоящего изобретения в системный кровоток посредством внутривенной инъекции или инфузии.
[00206] Кожный гель, лосьон, крем или пластырь: витилиго, опоясывающий герпес, акне, хейлит.
[00207] Ректальный суппозиторий, гель или инфузия: язвенный колит, воспаление геморроидальных узлов.
[00208] Пероральная форма, такая как пилюля, пастилка, инкапсулированная или с кишечнорастворимым покрытием: болезнь Крона, глютеновая энтеропатия, синдром раздраженного кишечника, воспалительная болезнь печени, пищевод Барретта.
[00209] Интракортикальный: эпилепсия, болезнь Алыдгеймера, рассеянный склероз, болезнь Паркинсона, хорея Хантингтона.
[00210] Внутрибрюшинная инфузия или имплант: эндометриоз.
[00211] Интравагинальный гель или суппозиторий: бактериальный, трихомонадный или грибковый вагинит.
[00212] Медицинские устройства: введенный на коронарную артерию стент, протезные соединения.
[00213] Иммунологически активные биомиметики, описанные в настоящей заявке, могут вводить в дозировках приблизительно от 0,01 мг в расчете на кг до приблизительно 300 мг в расчете на кг массы тела и особенно от 0,01 мг в расчете на кг массы тела до приблизительно 300 мг в расчете на кг массы тела, и могут вводить по меньшей мере ежедневно, еженедельно, раз в две недели или ежемесячно. Может использоваться двухфазная схема введения, когда первая фаза введения включает приблизительно от 0,1% до приблизительно 10% от второй фазы введения.
Терапевтические применения страдомеров и страдотел
[00214] На основе рационального дизайна и тестов in vitro и in vivo иммунологически активные биомиметики настоящего изобретения могут служить важными биопрепаратами для лечения аутоиммунных заболеваний и для модуляции иммуной функции в других различных контекстах, например, в биоиммунотерапии рака и воспалительных заболеваний. Патологические состояния, подходящие для лечения иммунологически активными биомиметиками, описанными в настоящей заявке, включают заболевания, которые на сегодняшний день обычно подвергают лечению с применением hIVIG, или заболевания, при которых hIVIG, как установлено, являлся клинически эффективным, такие как аутоиммунные цитопении, синдром Гийена-Барре, миастения гравис, аутоиммунные заболевания с аутоиммунитетом против фактора VIII, дерматомиозит, васкулит и увеит (См., F.G. van der Meche, P.I. Schmitz, N. Engl. J. Med. 326, 1123 (1992); P. Gajdos et al, Lancet i, 406 (1984); Y. Sultan, M.D. Kazatchkine, P. Maisonneuve, U.E. Nydegger, Lancet ii, 765 (1984); M.C. Dalakas et al., N. Engl. J. Med. 329, 1993 (1993); D.R. Jayne, M.J. Davies, C.J. Fox, С.M. Black, С.M. Lockwood, Lancet 337, 1137 (1991); P. LeHoang, N. Cassoux, F. George, N. Kullmann, M.D. Kazatchkine, Ocul. Immunol. Inflamm. 8, 49 (2000)), а также те типы онкологических или воспалительных заболеваний, при которых может применяться или уже находится в клиническом применении моноклональное антитело. Также заболевания, которые можно эффективно лечить соединениями, которые являются объектом настоящего изобретения, включают воспалительное заболевание с нарушением баланса путей цитокинов, аутоиммунное нарушение, опосредованное патогенными аутоантителами или аутоагрессивными Т-клетками, или острую или хроническую фазу хронического рецидивирующего аутоиммунного, воспалительного или инфекционного заболевания или процесса.
[00215] Кроме того, лечению иммунологически активными биомиметиками могут успешно подвергаться другие патологические состояния с воспалительным фактором, такие как амиотрофический боковой склероз, болезнь Хантингтона, болезнь Альцгеймера, болезнь Паркинсона, инфаркт миокарда, инсульт, гепатит В, гепатит С, воспаление, связанное с вирусом иммуннодефицита человека, адренолейкодистрофия и эпилептические заболевания, в особенности такие, которые считаются связанными с поствирусным энцефалитом, включая синдром Расмуссена, синдром Веста и синдром Леннокса-Гасто.
[00216] Общий подход к терапии с применением выделенных иммунологически активных биомиметиков, описанных в настоящей заявке, включает введение индивиду с заболеванием или патологическим состоянием терапевтически эффективного количества выделенного иммунологически активного биомиметика с целью осуществления лечения. В некоторых вариантах осуществления заболевания или патологические состояния могут быть ориентировочно отнесены к категории воспалительных заболеваний с нарушением баланса путей цитокинов, аутоиммунного нарушения, опосредованного патогенными аутоантителами или аутоагрессивыыми Т-клетками, или острой или хронической фазы хронического рецидивирующего заболевания или процесса.
[00217] Термин "лечение", используемый в настоящей заявке, относится к введению индивиду терапевтически эффективного количества биомиметика настоящего изобретения, в результате чего у индивида наблюдается улучшение течения заболевания или патологического состояния, или симптома заболевания или патологического состояния. Улучшением является любое улучшение или устранение заболевания или патологического состояния, или симптома заболевания или патологического состояния. Улучшение является заметным или поддающимся измерению улучшением, либо может являться улучшением общего самочувствия индивида. Таким образом, специалисту в данной области очевидно, что лечение может улучшить течение заболевания, однако может и не приводить к полному выздоровлению. В частности, улучшения у индивидов могут включать одно или несколько из следующего: уменьшение воспаления; уменьшение воспалительных аналитических маркеров, таких как С-реактивный белок; уменьшение аутоиммунных реакций, о чем свидетельствует одно или несколько из следующего: улучшение картины аутоиммунных маркеров, например, аутоантител или числа тромбоцитов, числа лейкоцитов или эритроцитов, уменьшение сыпи или пурпуры, уменьшение слабости, онемения или покалывания, увеличение уровней глюкозы у пациентов с гипергликемией, уменьшение боли в суставах, воспаления, припухлости или деградации, уменьшение частоты и интенсивности судорог и диареи, уменьшение ангины, уменьшение воспаления ткани или уменьшение частоты пароксизмов; уменьшение тяжести раковой опухоли, замедление прогрессии опухоли, уменьшение болей при раке, увеличение выживаемости или улучшение качества жизни; или задержка прогрессии или улучшение течения остеопороза.
[00218] Термин "терапевтически эффективное количество", используемый в настоящей заявке, относится к количеству, которое приводит к улучшению или устранению симптомов заболевания или патологического состояния.
[00219] Используемая в настоящей заявке "профилактика" может означать полное предотвращение симптомов заболевания, задержку развития симптомов заболевания или уменьшение тяжести симптомов заболевания, развивающегося впоследствии.
[00220] Термин "индивид", используемый в настоящей заявке, используется для обозначения любого пациента-млекопитающего, которому вводят биомиметики настоящего изобретения согласно способам, описанным в настоящей заявке. В конкретном варианте осуществления способы настоящего описания используют для лечения человека. Способы настоящего описания могут также применяться для обработки всех приматов за исключением человека (например, обезьян, бабуинов и шимпанзе), мышей, крыс, крупного рогатого скота, лошадей, кошачих, собачих, свиней, кроликов, коз, оленей, овец, хорьков, песчанок, морских свинок, хомяков, летучих мышей, птиц (например, кур, индеек и уток), рыб и рептилий, с целью получения видоспецифичных или химерных молекул страдомеров.
[00221] В частности, биомиметики настоящего изобретения могут применяться для лечения патологических состояний, включающих, помимо прочих, ишемическую болезнь сердца (ИБС), васкулит, розацеа, акне, экзему, миокардит и другие поражения миокарда, системную красную волчанку, диабет, спондилопатии, синовиальные фибробласты и строму костного мозга; потерю костной массы; болезнь Паджета, остеокластому; множественную миелому; рак молочной железы; дисфункциональную остеопению; недостаточность питания, парадонтоз, синдром Гоше, гистиоцитоз из клеток Лангерганса, поражение спинного мозга, острый септический артрит, остеомаляция, синдром Иценко-Кушинга, монооссальную фиброзную дисплазию, полиоссальную фиброзную дисплазию, реконструкцию периодонта и переломы кости; саркоидоз; остеолитические формы рака, рак легкого, рак почки и ректальный рак; метастазы кости, регуляцию болей в кости, а также гуморальную злокачественную гиперкальцемию, анкилозирующий спондилит и другие спондилоартропатии; отторжение трансплантата, вирусные инфекции, гематологические неоплазии и заболевания наподобие неопластических, например, лимфому Ходжкина; неходжскинские лимфомы (лимфому Беркитта, мелкоклеточную лимфоцитарную лимфому/хронический лимфолейкоз, грибовидную гранулему, лимфому из клеток мантийной зоны, фолликулярную лимфому, диффузную В-крупноклеточную лимфому, лимфому краевой зоны, гистиоцитарный ретикулоэндотелиоз и лимфоплазмацитарный лейкоз), опухоли из клеток-предшественников лимфоцитов, включающие В-клеточный острый лимфобластный лейкоз/лимфому и Т-клеточный острый лимфобластный лейкоз/лимфому, тимому, опухоли из зрелых Т- и NK-клеток, включающие узловой Т-клеточный лейкоз, Т-клеточный лейкоз/Т-клеточные лимфомы взрослых и Т-клеточный лейкоз из крупных гранулярных лимфоцитов, лангергансоклеточный гистиоцитоз (X), миелоидные неоплазии, такие как острый миелобластный лейкоз, включая ОМЛ с созреванием, ОМЛ без дифференцировки, острый промиелоцитарный лейкоз, острый миеломоноцитарный лейкоз и острый моноцитарный лейкоз, миелодиспластические синдромы и хронические миелопролиферативные заболевания, включая хронический миелогенный лейкоз, опухоли центральной нервной системы, например, опухоли головного мозга (глиому, нейробластому, астроцитому, медуллобластому, эпендимому и ретинобластому), солидные опухоли (носоглоточный рак, базально-клеточную карциному, рак поджелудочной железы, рак желчных протоков, саркому Капоши, рак яичка, маточный, вагинальный или цервикальный рак, рак яичников, первичный рак печени или эндометриальный рак, опухоли сосудистой системы (ангиосаркому и гемангиоперицитому)) или другие формы рака.
[00222] В настоящей заявке "злокачественная опухоль" относится к или описывает физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток. Примеры злокачественной опухоли включают, помимо прочего, карциному, лимфому, бластому, саркому (включая липосаркому, остеобластическую саркому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, лейомиосаркому, рабдомиосаркому, фибросаркому, миксосаркому, хондросаркому), нейроэндокринные опухоли, мезотелиому, хордому, синовиому, шванному, менингиому, аденокарциному, меланому и лейкоз или лимфолейкоз. Более конкретные примеры таких форм злокачественной опухоли включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточную карциному легкого, мелкоклеточную карциному легкого, рак брюшной полости, гепатоцеллюлярный рак, рак желудка, включая рак желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, цервикальный рак, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнной железы, рак почки, рак простаты, рак вульвы, рак щитовидной железы, карциному печени, анальную карциному, карциному полового члена, рак яичка, рак пищевода, опухоли желчного тракта, опухоль Юинга, базально-клеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярные аденокарциномы, цистаденокарциному, медуллярную карциному, бронхогенную карциному, почечноклеточную карциному, гепатому, карциному желчных протоков, хориокарциному, семиному, таратокарциному, опухоль Вильмса, опухоль яичка, карциному легкого, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, неврому слухового нерва, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкоз, лимфому, множественную миелому, макроглобулинемию Вальденстрема, миелодиспластическую болезнь, болезнь тяжелых цепей, нейроэндокринные опухоли, Шванному и другие карциномы, а также рак головы и шеи.
[00223] Биомиметики настоящего изобретения могут применяться для лечения аутоиммунных заболеваний. Термин "аутоиммунное заболевание", используемый в настоящей заявке, относится к большой группе, включающей свыше 80 различных заболеваний и патологических состояний. Основная проблема при таких заболеваниях и патологических состояниях состоит в том, что иммунная система атакует собственный организм. Аутоиммунные заболевания затрагивают все основные системы организма, включая соединительную ткань, нервы, мышцы, эндокринную систему, кожу, кровь, дыхательную и желудочно-кишечную системы. Аутоиммунные заболевания включают, например, системную красную волчанку, ревматоидный артрит, рассеянный склероз, миастению гравис и диабет I типа.
[00224] Заболевание и патологическое состояние, поддающееся лечению с применением композиций и способов настоящего изобретения, могут являться гематоиммунологическим процессом, включающим, помимо прочего, идиопатическую тромбоцитопеническую пурпуру, аллоиммунную/аутоиммунную тромбоцитопению, приобретенную иммунную тромбоцитопению, аутоиммунную нейтропению, аутоиммунную гемолитическую анемию, Парвовирус В19-ассоциированную эритроцитарную аплазию, приобретенный аутоиммунитет против фактора VIII, приобретенную болезнь фон Виллебранда, множественную миелому и моноклональную гаммапатию неизвестной этиологии, сепсис, апластическую анемию, истинную эритроцитарную аплазию, анемию Даймонда-Блекфана, гемолитическую болезнь новорожденного, иммуноопосредованную нейтропению, невосприимчивость к переливанию тромбоцитарной массы, неонатальную посттрансфузионную пурпуру, гемолитический уремический синдром, системный васкулит, тромбическую тромбоцитопеническую пурпуру или синдром Эвана.
[00225] Заболевание и патологическое состояние могут также являться нейроиммунологическим процессом, включающим, помимо прочего, синдром Гийена-Барре, хроническую воспалительную демиелинизирующую полирадикулоневропатию, парапротеинемическую IgM демиелинизирующую полиневропатию, миастенический синдром Ламберта-Итона, миастению гравис, многоочаговую двигательную невропатию, боковой амиотрофический склероз, ассоциируемый с антителами против GM1, демиелинизацию, рассеянный склероз и неврит зрительного нерва, синдром мышечной скованности, паранеопластическую дегенерацию мозжечка, вызванную анти-Yo антителами, паранеопластический энцефаломиелит, сенсорную невропатию, вызванную анти-Hu антителами, эпилепсию, энцефалит, миелит, миелопатию, особенно связанную с Т-лимфотропным вирусом человека первого типа, аутоиммунную диабетическую невропатию или острую идиопатическую вегетативную невропатию.
[00226] Заболевание и патологическое состояние могут также являться ревматическим процессом, включающим, помимо прочего, болезнь Кавасаки, ревматоидный артрит, синдром Фелти, АНЦА-положительный васкулит, спонтанный полимиозит, дерматомиозит, антифосфолипидный синдром, повторные самопроизвольные аборты, системную красную волчанку, ювенильный идиопатический артрит, синдром Рейно, CREST-синдром или увеит.
[00227] Заболевание и патологическое состояние могут также являться дерматоиммунологическим процессом, включающим, помимо прочего, токсический эпидермальный некролиз, гангрену, гранулему, аутоиммунное заболевание кожи с развитием нарывов, включая вульгарную пузырчатку, буллезный пемфигоид и эксфолиативную пузырчатку, витилиго, синдром стрептококкового токсического шока, склеродермию, системный склероз, включая диффузный и локальный кожный системный склероз или атонический дерматит (особенно стероидозависимый атопический дерматит).
[00228] Заболевание и патологическое состояние могут также являться скелетно-мышечным иммунологическим заболеванием, включающим, помимо прочего, миозит с включенными тельцами, некротизирующий фасцит, воспалительные миопатии, миозит, анти-декорин (BJ антиген) миопатию, паранеопластическую некротическую миопатию, вакуолизирующую миопатию, сцепленную с Х-хромосомой, пеницилламин-индуцированный полимиозит, атеросклероз, ишемическую болезнь сердца или кардиомиопатию.
[00229] Заболевание и патологическое состояние могут также являться желудочно-кишечным иммунологическим процессом, включающим, помимо прочего, пернициозную анемию, аутоиммунный хронический активный гепатит, первичный биллиарный цирроз печени, глютеновую энтеропатию, герпетиформный дерматит, криптогенный цирроз печени, реактивный артрит, болезнь Крона, болезнь Уипла, язвенный колит или склерозирующий холангит.
[00230] Заболевание и патологическое состояние могут также являться гомологичной болезнью (РТПХ), антитело-опосредованным отторжением трансплантата, отторжением трансплантата костного мозга, постинфекционным воспалением, лимфомой, лейкозом, неоплазией, астмой, сахарным диабетом I типа с антителами против бета-клеток, синдромом Шегрена, смешанным поражением соединительной ткани, болезнью Аддисона, синдромом Фогта-Коянаги-Харады, мембранозно-пролиферативным гломерулонефритом, синдромом Гудпасчера, болезнью Грейвса, тиреоидитом Хашимото, гранулематозом Вегенера, микрополиартериитом, синдромом Черджа-Стросс, узелковым полиартериитом или полиорганной недостаточностью.
[00231] В другом варианте осуществления страдомеры, описанные в настоящей заявке, могут применяться в примирующей системе, в которой кровь отбирают у пациента и подвергают короткому контакту со страдомером (страдомерами) в течение промежутка времени продолжительностью приблизительно от получаса до приблизительно трех часов, после чего кровь обратно вводят пациенту. В данной форме клеточной терапии собственные эффекторные клетки пациента подвергаются контакту со страдомером, который иммобилизован на матриксе ex vivo, с целью модуляции эффекторных клеток посредством контакта эффекторных клеток со страдомером. Затем кровь, содержащую модулированные эффекторные клетки, вводят обратно пациенту. Такая примирующая система может найти различные клинические и терапевтические применения.
Терапевтические применения страдотел в онкологии
[00232] В дополнение к наличию клинического применения для лечения иммунологических заболеваний страдотела находят терапевтическое применение в лечении злокачественной опухоли и воспалительных заболеваний. Страдотела могут применяться по существу согласно известным протоколам для любого соответствующего терапевтического антитела. Страдотела обычно создаются с целью усиления эффекта, демонстрируемого эффекторными клетками под воздействием моноклонального антитела, например, АЗКЦ при злокачественной опухоли или уменьшение моноцитов и созревания DC при пониженной секреции цитокинов в аутоиммунном заболевании и, таким образом, потенцирования иммунного ответа против рака, который развивался, например, в результате применения моноклонального антитела, послужившего источником Fab-части страдотела.
[00233] Примеры Fab-доменов моноклональных антител, на основе которых может быть создано страдотело, включают цетуксимаб, ритуксимаб, муромонаб-CD3, абциксимаб, даклизумаб, базиликсимаб, паливизумаб, инфликсимаб, трастузумаб, гемтузумаб озогамицин, алемтузумаб, тиуксетан ибритумомаба, адалимумаб, омализумаб, тозитумомаб, 1-131 тозитумомаб, эфализумаб, бевацизумаб, панитумумаб, пертузумаб, натализумаб, этанерцепт, IGN101, волоциксимаб, анти-CD80 mAb, анти-CD23 mAb, САТ-3888, CDP-791, эпратузумаб, MDX-010, MDX-060, MDX-070, матузумаб, СР-675,206, CAL, SGN-30, занолимумаб, adecatumumab, ореговомаб, нимотузумаб, АВТ-874, деносумаб, AM 108, АМС 714, фонтолизумаб, даклизумаб, голимумаб, CNTO 1275, окрелизумаб, HuMax-CD20, белимумаб, эпратузумаб, MLN 1202, визилизумаб, тоцилизумаб, окрелизумаб, цертолизумаб пэгол, экулизумаб, пекселизумаб, абциксимаб, ранибизумаб, меполизумаб и TNX-355, MYO-029.
[00234] Страдомеры и страдотела, в совокупности иммунологически активные биомиметики, раскрытые в настоящей заявке, имеют множество других применений. Изменение иммунных ответов
[00235] Иммунологически активные биомиметики, раскрытые в настоящей заявке, могут также успешно применяться для изменения ответов иммунной системы в различных ситуациях для специфических изменений профилей иммунного ответа. Изменение или модуляция иммунного ответа у индивида относятся к увеличению, уменьшению или изменению соотношения или компонентов иммунного ответа. Например, уровни выработки или секреции цитокинов при необходимости могут быть увеличены или уменьшены путем направленного воздействия на соответствующую комбинацию Fc-рецепторов страдомера, созданного для взаимодействия с указанными рецепторами. Выработка антител также может быть увеличена или уменьшена; может быть изменено соотношение двух или более цитокинов или рецепторов иммуноцитов; или может быть индуцирована выработка дополнительных типов цитокинов или антител. Иммунный ответ может также являться эффекторной функцией иммуноцита, экспрессирующего FcγR, включая увеличенный или уменьшенный фагоцитный потенциал моноцит макрофаг производных клеток, повышенную или пониженную функцию остеокластов, повышенное или пониженное презентирование антигена антиген-презентирующими клетками (например, дендритными клетками), повышенную или пониженную функцию NK-клеток, повышенную или пониженную функцию В-клеток, по сравнению с иммунным ответом, который не подвергался модулированию с применением иммунологически активных биомиметиков, раскрытых в настоящей заявке.
[00236] В предпочтительном варианте осуществления иммунный ответ индивида со злокачественной опухолью или аутоиммунным или воспалительным заболеванием изменен, что включает стадию введения индивиду терапевтически эффективного количества иммунологически активного биомиметика, описанного в настоящей заявке, где терапевтически эффективное количество иммунологически активного биомиметика изменяет иммунный ответ у индивида. В идеальном случае подобное вмешательство служит лечением заболевания и патологического состояния у индивида. Измененный иммунный ответ может являться увеличенным или уменьшенным ответом и может включать измененные уровни цитокинов, включая уровни любого из IL-6, IL-10, IL-8, IL-23, IL-7, IL-4, IL-12, IL-13, IL-17, TNF-альфа и IFN-альфа. Впрочем, изобретение не ограничивается каким-либо специфическим механизмом действия описанных биомиметиков. Измененный иммунный ответ может являться измененным уровнем аутоантител у индивида. Измененный иммунный ответ может являться измененным уровнем аутоагрессивных Т-клеток у индивида.
[00237] Например, снижение количества выработки TNF-альфа при аутоиммунных заболеваниях может оказывать терапевтическое воздействие. Практическим применением данного способа является терапия анти-TNF-альфа антителами (например, REMICADE®), который, как доказано в клинических испытаниях, является эффективным при лечении пятнистого псориаза, ревматоидного артрита, псориатического артрита, болезни Крона, язвенного колита и анкилозирующего спондилита. Перечисленные аутоиммунные заболевания имеют различную этиологию, но при этом включают общие ключевые иммунологические компоненты процессов болезни, связанных с воспалением и активностью иммунных клеток. Страдомер, предназначенный для снижения выработки TNF-альфа, аналогичным образом будет эффективен при указанных и, возможно, при других аутоиммунных заболеваниях. Измененный профиль иммунного ответа может также являться прямой или косвенной модуляцией, вызывающей снижение выработки антител, например аутоантител, атакующих собственные ткани индивида, или изменением уровня аутоагрессивных Т-клеток у индивида. Например, рассеянный склероз является аутоиммунным нарушением, вовлекающим аутореактивные Т-клетки, которое можно лечить с помощью терапии бета-интерфероном. См., например, Zafranskaya М, et al., Interferon-beta therapy reduces CD4+ and CD8+ T-cell reactivity in multiple sclerosis, Immunology 2007 May; 121(1): 29-39-Epub 18 декабря 2006 г. Конструкция страдомера, направленная на уменьшение уровня аутореактивных Т-клеток аналогичным образом будет эффективна при рассеянном склерозе и, возможно, при других аутоиммунных заболеваниях, вовлекающих аутореактивные Т-клетки. Применения в иммунологическом анализе
[00238] Иммунологически активные биомиметики, раскрытые в настоящей заявке, могут применяться при выполнении иммунологического анализа с целью тестирования функций иммуноцитов, для модуляции которых созданы иммунологически активные биомиметики.
[00239] Передача сигналов через пути Fcγ-рецепторов низкой аффинности требует агрегации рецепторов и перекрестного связывания на поверхности клеток. Указанные параметры агрегации и перекрестного связывания, как предполагают, выполняются при Fab-связывании с антигенспецифичной мишенью с последующим взаимодействием между Fc-областью и Fcγ-рецепторами низкой аффинности на поверхности отреагировавших клеток. В данном случае антитела способны вызывать клеточные ответы двумя различными путями: 1. Fab-взаимодействие/блокирование эпитопспецифичной мишени и 2. Fc-взаимодействия с Fc-рецепторами. Несмотря на приведенные механизмы, существующие средства контроля для большинства терапевтических исследований с использованием моноклональных антител, применяемых in vivo, потенциал взаимодействий Fc : Fcγ-рецептора как участников наблюдаемых функциональных эффектов используют не на должном уровне. Многие стратегии в настоящее время направлены на устранение взаимодействий Fc : FcR как нежелательных переменных. Например, в некоторых исследованиях используются Scv (одноцепочечные вариабельные области) или Fab-фрагменты, которые сохраняют эпитоп-специфичность, но при этом не имеют Fc-домена. Данные подходы ограничены коротким периодом полужизни указанных реагентов и их ограниченным потенциалом при индукции передачи сигналов. В других исследованиях используют слитые белки, состоящие из рецептора или лиганда, слитого с Fc-фрагментом. Хотя указанные методы помогают дифференцировать Fab-специфичные эффекты от эффектов, наблюдаемых при лиганд-рецепторных взаимодействиях, они не позволяют эффективно регулировать Fc-опосредованные эффекты. При оценке терапевтических средств на основе антител в животных моделях также могут использоваться антитела контрольного изотипа с каким-либо другим посторонним связывающим сайтом Fab. Обоснование данного выбора основано на предполагаемом функциональном подобии между антителами одного и того же изотипа, независимо от их Fab специфичности или аффинности. Впрочем, данное применение посторонних контрольных изотипов имеет несколько существенных недостатков:
1. Если Fab-фрагменты указанных антител не могут связывать лиганд или антигенный эпитоп, то, скорее всего, Fc-фрагменты не будут стимулировать передачу сигналов через взаимодействия FcR низкой аффинности из-за отсутствия перекрестного связывания Fcγ-рецептора. Таким образом, наблюдаемые функциональные различия между экспериментальным и контрольным антителами нельзя будет безошибочно отнести к Fab-взаимодействию с эпитоп-специфической мишенью, лишенной способности поперечно связывать FcγR.
2. Если данные изотипы получены в клетках, которые дают различные гликоформы или другой процентное соотношение отдельных гликоформ по сравнению с исходных антителом, то связывание с Fc-рецепторами как низкой, так и высокой аффинности, будет изменено, даже если Fab-аффинность будет идентичной.
[00240] Хотя какого-либо точного способа контроля, чтобы решить данную проблему, не сушествут, одним из возможных вариантов является применение изотип-специфичных страдомеров, полученных в тех же клетках, что и исходные антитела, и взятых в дозе, пропорциональной уровням экспрессии эпитопа, к которому специфично экспериментальное антитело. Например, соответствующим контролем для эпитоп-специфичного антитела, полученного в крысе, может являться крысиный изотип-специфичный страдомер, способный связывать Fcγ-рецептор на поверхности эффекторных клеток.
[00241] Обычно иммуноцит подвергают контакту с эффективным количеством иммунологически активного биомиметика, модулирующего активность иммуноцита известным способом, при этом указанную иммуномодуляцию сравнивают с тестируемым соединением или молекулой, чтобы определить, обладает ли тестируемое соединение подобной иммуномодулирующей активностью.
[00242] В другом варианте осуществления термоагрегированные страдомеры и агрегированные иммуноглобулины могут применяться в качестве реагентов для лабораторного контроля в различных иммунологических анализах, описанных в настоящей заявке и известных средним специалистам в данной области.
[00243] Иммунологические анализы могут являться анализами in vitro или in vivo и могут включать человеческие или нечеловеческие иммуноциты с использованием видоспецифических или не видоспецифических иммунологически активных биомиметиков. В одном варианте осуществления иммунологический анализ проводят с использованием эффективного количества иммунологически активного биомиметика, модулирующего активность иммуноцита, а затем проводят сравнение данной модуляции с модуляцией иммуноцита под действием тестируемого соединения. Страдомер или страдотело могут выполнять функцию реагента положительного контроля в анализах, включающих испытание других соединений на предмет иммунологического действия. В анализе могут сравнивать эффект, производимый тестируемым моноклональным антителом в сравнении со страдомером при связывании с Fcγ-рецепторами эффекторных клеток, а также функциональный ответ, измеряемый изменениями уровня экспресии рецептора, секреции цитокинов, и функциональные свойства, например, используя реакцию смешанной культуры лимфоцитов. В данном случае, если страдомер (который не содержит Fab) дает ответ, который частично подобен ответу моноклонального антитела, то тогда эффект моноклонального антитела, в некоторой степени, не обусловлен специфичностью его Fab, а является следствием общего эффекта связывания и поперечного связывания более чем одного Fcγ-рецептора на эффекторной клетке. Страдотело, которое содержит и тот же страдомер, и Fab из того же моноклонального антитела, также может помочь отличить специфичность Fab моноклонального антитела от общего эффекта связывания и поперечного связывания более чем одного Fcγ-рецептора на эффекторной клетке.
[00244] Если биологическая активность видоспецифического и изотип-специфического антитела частично или полностью воспроизводится видоспецифичным и изотип-специфичным страдомером, то тогда очевидно, что Fc-Fcγ-рецептор активность составляет часть наблюдаемой биологической активности, относящейся к видоспецифичному и изотип-специфичному страдомеру. Таким образом, видоспецифичные и изотип-специфичные страдомеры могут применяться в оценке потенциальных терапевтических антител для определения, относится ли и в какой степени наблюдаемая биологическая активность к Fab-части тестируемого антитела или же к неспецифичному эффекту Fc-части от молекулярного связывания и поперечного связывания более чем одного Fcγ-рецептора.
[00245] В одном варианте осуществления выделенный иммунологически активный биомиметик настоящего изобретения включает по меньшей мере один страдомер, который включает по меньшей мере два Fc-домена или соответствующие неполные домены, из того же класса Fc иммуноглобулина, где класс Fc иммуноглобулина выбран из группы, состоящей из IgG1, IgG2, IgG3, IgG4 и их комбинаций. Такие биомиметики также способны специфично связываться с первым FcγRx1, где x1 обозначает I, II, III или IV, и со вторым FcγRx2, где х2 обозначает I, II, III или IV. Указанные биомиметики могут дополнительно характеризоваться наличием иммунологической активности, включающей поперечное связывание Fcγ-рецептора или эффекторные функциональные свойства, сопоставимые или превосходящие перекрестное связывание Fcγ-рецептора или эффекторные функциональные свойства множества природных, агрегированных иммуноглобулинов IgG.
[00246] В другом варианте осуществления настоящее изобретение включает выделенный иммунологически активный биомимети, который включает по меньшей мере один страдомер, включающий по меньшей мере два Fc-домена из различных классов иммуноглобулина, или соответствующие неполные домены, где биомиметик специфично связывается с первым FcγRx1, где x1 обозначает I, II, III или IV, и со вторым FcγRx2, где х2 обозначает I, II, III или IV. Указанный биомиметик может дополнительно характеризоваться наличием иммунологической активности, включающей перекрестное связывание Fcγ-рецептора или эффекторные функциональные свойства, сопоставимые или превосходящие перекрестное связывание Fcγ-рецептора или эффекторные функциональные свойства множества природных, агрегированных иммуноглобулинов IgG в отношении Fcγ-рецепторов.
[00247] В следующем варианте осуществления настоящее изобретение включает выделенный иммунологически активный биомиметик, который включает один или более страдомеров, каждый из которых независимо включает три или более Fc-домена, где три или более Fc-домена включают: а) первый Fc-домен, где первый Fc-домен включает Fc-шарнирную область (Н) первого иммуноглобулина, b) второй Fc-домен, где второй Fc-домен включает константную область 2 (СН2) второго иммуноглобулина, где второй Fc-домен способен специфично связываться с FcγRx1, где х1 обозначает I, II, III или IV; с) третий Fc-домен, где третий Fc-домен включает константную область 3 (СН3) третьего иммуноглобулина, где третий Fc-домен способен специфично связываться с FcγRx2, где х2 обозначает I, II, III или IV. Указанные биомиметики могут необязательно включать четвертый Fc-домен, где четвертый Fc-домен включает константную область 4 (СН4) четвертого иммуноглобулина IgM. В данной молекуле Fc-шарнирная область может содержать по меньшей мере один цистеин.
[00248] В еще одном варианте осуществления настоящее изобретение включает выделенный иммунологически активный биомиметик, который включает: а) первый Fc-домен или соответствующий неполный Fc-домен, где первый Fc-домен включает Fc-шарнирную область (Н) область из первого иммуноглобулина, где Fc-шарнирная область включает по меньшей мере один цистеин, где первый Fc-домен вносит вклад в специфичность связывания с FcγRx, где х обозначает I, II, III или IV; и по меньшей мере один из: i) второго Fc-домена или соответствующего неполного домена, где второй Fc-домен включает константную область 2 (СН2) из второго иммуноглобулина, который может являться, или не являться таким же, как и первый иммуноглобулин, где второй Fc-домен вносит вклад в специфичность связывания с FcγRx, где х обозначает I, II или III, IV; и, необязательно, ii) третьего Fc-домена или соответствующего неполного домена, где третий Fc-домен включает константную область 3 (СН3) из третьего иммуноглобулина, где третий Fc-домен вносит вклад в специфичность связывания с FcγRx, где х обозначает I, II, III или IV; и b) необязательно, четвертый Fc-домен или соответствующий неполный домен, где специфичность четвертого Fc-домена обусловлена константной областью 4 (СН4) из иммуноглобулина IgM.
[00249] В другом варианте осуществления выделенный иммунологически активный биомиметик является страдомером, где иммуноглобулин, послуживший источником Fc-доменов, является одинаковым или разным, и включает изотипы IgA, изотипы IgG, IgD, IgE и IgM. Другим вариантом осуществления страдомера является выделенный иммунологически активный биомиметик, включающий секреторную сигнальную последовательность.
[00250] В одном из предпочтительных вариантов осуществления терапевтически эффективное количество выделенных иммунологически активных биомиметиков настоящего изобретения является количеством, достаточным для связывания биомиметиков с двумя или более FcγRx, где х обозначает I, II, III или IV, на поверхности иммуноцита, вызывавая, таким образом, агрегацию FcγRx. Иммуноцит может являться любой эффекторной иммунной клеткой, например, моноцитом, дендритной клеткой, макрофагом, остеокластом или NK-клеткой. Созревание эффекторного иммуноцита может модулироваться иммунологически активным биомиметиком. На иммуноците также может быть изменено отношение FcγRIIa к FcγRIIb. Иммуноцит может быть расположен в плазме, костном мозге, кишечнике, костной ткани, лимфоидной ткани, тимусе, мозге, участке инфекции или опухоли. Функциональная активность макрофага, дендритной клетки, остеокласта или NK-клетки может быть смодулирована.
[00251] Терапевтически эффективное количество выделенного иммунологически активного биомиметика, описанного выше в настоящей заявке, можно вводить ex vivo в иммуноцит с целью получения обработанного иммуноцита, с последующей стадией введения обработанного иммуноцита индивиду. Обработанный иммуноцит может являться дендритной клеткой, макрофагом, остеокластом или моноцитом.
[00252] Дополнительную иммунотерапию можно проводить в сочетании с любым из выделенных иммунологически активных биомиметиков, описанных в настоящей заявке, вводимых в терапевтически эффективном количестве индивиду. Дополнительная иммунотерапия может включать, например, одну или несколько костимулирующих молекул, моноклональное антитело, поликлональное антитело, слитый белок, биоспецифичное антитело, цитокин, иммунологически узнаваемый антиген, низкомолекулярное противоопухолевое средство или антипролиферативное средство. Дополнительную иммунотерапию можно проводить одновременно с, или отдельно от введения иммунологически активного биомиметика.
[00253] Уровни цитокинов (включая вышеуказанные цитокины) могут быть изменены, например, посредством введения одного или нескольких целевых цитокинов, одного или нескольких других цитокинов, которые модулируют уровень одного или нескольких целевых цитокинов, и/или антител (любого из типов и классов, описанных в настоящей заявке), специфичных к одному или нескольким любым цитокинам из двух вышеуказанных категорий.
[00254] Иммунологически активные биомиметики, описанные в настоящей заявке, могут применяться для модуляции экспрессии костимулирующих молекул в иммуноците, включающем дендритную клетку, макрофаг, остеокласт, моноцит или NK-клетку, или ингибировать в тех же иммуноцитах дифференцировку, созревание или секрецию цитокинов, включая интерлейкин-12 (IL-12), или повышать секрецию цитокинов, включая интерлейкин-10 (IL-10) или интерлейкин-6 (IL-6). Квалифицированный специалист может также оценить эффективность иммунологически активного биомиметика, подвергая иммуноцит контакту с иммунологически активным биомиметиком с последующим измерением модуляции функции иммуноцита, где иммуноцит является дендритной клеткой, макрофагом, остеокластом или моноцитом. В одном варианте осуществления иммуноцит подвергают контакту с иммунологически активным биомиметиком in vitro, после чего следует стадия определения количества рецепторов на поверхности клетки или уровня выработки цитокинов, где изменение количества рецепторов на поверхности клетки или уровня выработки цитокина определяет модуляцию функции иммуноцита. В другом варианте осуществления иммуноцит подвергают контакту с иммунологически активным биомиметиком in vivo в животном, служащим моделью аутоиммунного заболевания, с дополнительной стадией оценки степени улучшения при аутоиммунном заболевании.
[00255] "Способный специфично связываться с FcγRx", используемый в настоящей заявке, относится к связыванию с FcγR, таким как FcγRIII. Специфичное связывание обычно определяется как количество меченого лиганда, вытесняемого последующим избытком немеченого лиганда в анализе связывания. Однако это не исключает другие способы оценки специфичного связывания, которые хорошо известны в уровне техники (например, Mendel CM, Mendel DB, 'Non-specific' binding. The problem, and a solution. Biochem J. 1985 May 15; 228(1): 269-72). Специфичное связывание может быть измерено различными способами, известными в уровне техники, например, с помощью технологии поверхностного плазмонного резонанса (SPR) (доступной посредством BIACORE"), позволяющей характеризовать константы связывания и диссоциации иммунологически активных биомиметиков (Asian K, Lakowicz JR, Geddes С. Plasmon light scattering in biology and medicine: new sensing approaches, visions and perspectives. Current Opinion in Chemical Biology 2005, 9: 538-544).
Способы с применением иммобилизованного Fc
[00256] Чтобы понять роль Fc : Fc-гамма-рецепторного (FcγR, Fc-рецептора для Fc IgG) взаимодействия и важность функции IVIG в отношении его Fc, биологически иммобилизованного в молекуле иммуноглобулина, авторы изобретения сравнивали влияние IVIG, а также иммобилизованной формы рекомбинантного Fc-фрагмента IgG1 (rFCF) и растворимой формы рекомбинантного Fc-фрагмента IgG1 (sFc), содержащих шарнирную область-СН2-СН3 домены, на функции моноцитов в процессе дифференцировки из моноцитов в незрелые дендритные клетки (iDC).
[00257] Воздействие на моноциты, выращиваемые в присутствии гранулоцитарно-макрофагального колониестимулирующего фактора (ГМКСФ) и интерлейкина-4 (IL-4), иммобилизованного rFCF и иммобилизованного IVIG, а не растворимого IVIG в малых дозах, повышало экспрессию CD86, замедляло экспрессию CD11c и подавляло экспрессию CD1a на клетках. Кроме того, указанные изменения, вероятно, не являются следствием неспецифичной белковой иммобилизации rFCF на полимере, поскольку растворимый термоагрегированный (sHA) IVIG, sHA rFCF или IVIG в большой дозе (как известно, содержащий мультимерные Fc) вызвали изменения, подобные наблюдаемым для иммобилизованного rFCF.
[00258] В совокупности, полученные данные указывают, что воздействие на iDC IVIG, иммобилизованного на поверхности твердой, полутвердой или гелеобразной подложки, приводит к получению уникальной популяции дендритных клеток (с высоким содержанием CD86 и низким CD1a), способных индуцировать развитие иммунной толерантности, и что иммобилизованные молекулы, которые включают функциональную часть Fc-фрагментов иммуноглобулина G (IgG), могут применяться в качестве миметиков IVIG для лечения местного и системного воспаления, а также широкого ряда других патологических состояний, которые, прямо или косвенно, опосредованы клетками, происходящими из моноцитов (MDC), такими как iDC. Кроме того, иммобилизация функциональной части Fc IgG на устройствах, описанных в настоящей заявке как "устройства с покрытием", которые имплантированы в тела или присоединены к телам животных (например, людей), с молекулами, содержащими функциональную часть Fc-фрагмента IgG, может уменьшать, если не предотвращать, воспалительный ответ на такие устройства.
[00259] Изобретение обеспечивает способ ингибированил активности клетки, происходящей из моноцита (MDC). Способ включает контакт клетки с композицией, включающей основу, с которой связан Fc реагент. Контакт может происходить in vitro, in vivo или ex vivo. В альтернативе, клетка может находиться в организме животного. Животное может являться животным, которое имеет, или подвергается риску развития заболевания, опосредованного клетками, происходящими из моноцитов (MDCMC). MDC может являться, например, дендритной клеткой, макрофагом, моноцитом или остеокластом.
[00260] Изобретение также обеспечивает способ лечения или профилактики. Способ включает введение животному композиции, содержащей основу, с которой связан Fc-реагент, где животное является животным, который имеет, или подвергается риску развития MDCMC.
[00261] Используемый в настоящей заявке термин "заболевание, опосредованное клетками, происходящими из моноцитов (MDCMC)" относится к патологическому состоянию, которое прямо или косвенно, частично или полностью, обусловлено активностью клеток, происходящих из моноцитов, или к факторам, вызванным ими. Клетки, происходящие из моноцитов, включают, помимо прочих, моноциты, макрофаги, интердигитальные дендритные клетки (обычно упоминаемые в настоящей заявке как "дендритные клетки", включая дендритоподобные клетки и фолликулярные дендритныхподобные клетки) (зрелые и незрелые), остеокласты, микроглиоцито-подобные клетки, вырабатывающие инсулин моноцит-производные инсулоцито-подобные клетки, моноцит-производные незрелые тучные клетки и моноцит-производные микрочастицы.
[00262] Касательно применения способов с использованием иммобилизованных Fc, термин "Fc-реагент" относится к любой молекуле или молекулярному комплексу, который включает одну или более (например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12, 15, 18, 20 или более) функциональных частей Fc-фрагмента иммуноглобулина G (IgG). Fc-фрагмент IgG состоит из С-концевых частей двух тяжелых цепей IgG, соединенных вместе, которые в свою очередь состоят из шарнирных областей, СН2 доменов и СН3 доменов обеих тяжелых цепей, соединенных вместе. "Функциональная часть Fc-фрагмента IgG" состоит из шарнирных областей, СН2 доменов и, необязательно, всех или некоторых из (например, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48 или 49) первых 50 (начиная с N-конца) аминокислот СН3 доменов обеих соединенных тяжелых цепей. У людей (а) шарнирная область IgG1 содержит 15 аминокислот, СН2 домен содержит 110 аминокислот и СН3 домен содержит 106 аминокислот; (b) шарнирная область IgG2 содержит 12 аминокислот, СН2 домен содержит 109 аминокислот и СН3 домен содержит 107 аминокислот; (с) шарнирная область IgG3 содержит 62 аминокислоты, СН2 домен содержит 104 аминокислоты и СН3 домен содержит 106 аминокислот; и (d) шарнирная область IgG4 содержит 12 аминокислот, СН2 домен содержит 109 аминокислот и СН3 домен содержит 107 аминокислот.
[00263] Как и в молекулах IgG дикого типа, в вышеописанных Fc-реагентах две полипептидных цепи, происходящие из тяжелых цепей IgG, обычно, но не обязательно, являются идентичными. Таким образом, Fc-реагент может являться, без ограничения, полноразмерной молекулой IgG, полноразмерной молекулой IgG, связанной с полипептидом, происходящим не из иммуноглобулина, Fc-фрагментом IgG, Fc-фрагментом IgG, связанным с полипептидом, происходящим не из иммуноглобулина, функциональной частью Fc-фрагмента IgG, функциональной частью Fc-фрагмента IgG, связанной с полипептидом, происходящим не из иммуноглобулина, или мультимерами (например, димерами, тримерами, тетрамерами, пентамерами, гексамерами, гептамерами, октамерами, нонамерами или декамерами) любого из перечисленного. Fc-реагенты могут также являться вышеописанными страдомерами и страдотелами, при условии что они находятся в рамках приведеного выше определения Fc-реагента.
[00264] В иммобилизованном Fcγ компоненты тяжелых цепей иммуноглобулина Fc-реагентов могут иметь аминокислотные последовательности дикого типа, или они могут являться аминокислотными последовательностями дикого типа, содержащими не более 20 (например, не более 19, 18, 17, 16, 15, 14, 13, 12, 11, 10, 9, 8, 7, 6, 5, 4, 3, 2 или 1) аминокислотных замен. Такие замены предпочтительно, но не обязательно, являются консервативными заменами. Консервативные замены обычно включают замены в пределах следующих групп: глицин и аланин; валин, изолейцин и лейцин; аспарагиновая кислота и глутаминовая кислота; аспарагин, глутамин, серии и треонин; лизин, гистидин и аргинин; а также фенилаланин и тирозин.
[00265] "Fc-реагент" изобретения обладает по меньшей мере 25% (например, по меньшей мере: 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95%, 98%, 99%, 99,5% или 100%, или даже больше) способности молекулы IgG, из которой IgG были получены компоненты тяжелых цепей Fc-реагента (исходной молекулы IgG), связываться с целевым Fc-рецептором. В случае, когда "Fc-реагент" содержит компоненты тяжелых цепей, полученные из молекулы более чем одного типа IgG, исходная молекула IgG является молекулой IgG, которая связывается с соответствующим целевым Fc-рецептором с наибольшей авидностью.
[00266] Используемый в настоящей заявке "иммобилизованный Fc", относится к Fc-реагенту, который связан с "подложкой", как определено ниже. Термины "иммобилизованный Fc, " "связанный Fc" и "стабилизированный Fc" являются синонимами. Иммобилизованный Fc состоит из функциональной части Fc (включающей, помимо прочего, любой полипептид, который включает функциональную часть Fc), присоединенной к подложке. Иммобилизованный Fc включает, например, как прямое связывание, так и опосредованное связывание Fc через полимеры с подложкой; введение полноразмерных Fc IgG в выделенное; введение только функциональных доменов Fc IgG или введение полноразмерных Fc IgG или функциональных доменов Fc IgG как часть более крупного полипептида, например, антитела, страдомера или страдотела.
[00267] Применительно к иммобилизованному Fc, термин "подложка" относится к твердому, полутвердому или гелеобразному объекту. Подложка может быть имплантирована в или присоединена (или прикреплена) к поверхности тела животного. Подложки могут включать, например, жидкие или газообразные компоненты, однако по меньшей мере часть подложки является твердой, полутвердой, или гелеобразной. Таким образом, подложка может являться веществом, которое по существу нерастворимо в водном растворителе, но растворимо в неводном растворителе. Такие вещества включают липиды (например, фосфолипиды), жирные кислоты и другие жирорастворимые, нерастворимые в водных растворителях соединения. Из настоящего очевидно, что подложки включают липосомы. Подложка может являться пористой или непористой. В конкретных вариантах осуществления подложка инертна по отношению к поверхности и/или телу, в которое она имплантирована, присоединена или прикреплена.
[00268] Подложка может содержать или быть изготовлена из синтетического полимера, например, нейлона, тефлона, дакрона, поливинилхлорида, ПЗУ (полиэфируретана), ПТФЭ (политетрафторэтилена), ПММА (полиметилметакрилата), ПЭЭК, термоэластопластов, радионепроницаемых полимеров, полиэфирсульфона, силиконов, поликарбонатов, полиуретанов, полиизобутилена и его сополимеров, сложных полиэфиров, полиолефинов, полиизобутилена, сополимеров этилена - альфа-олефинов, акриловых полимеров и сополимеров, винилгалогенидных полимеров и сополимеров, таких как поливинилхлорид, поливиниловых эфиров, поливинилметилового эфира, поливинилиденгалогенидов, поливинилиденфторида, поливинилиденхлорида, полиакрилонитрила, поливинилкетонов, поливинилароматических соединений, полистирола, сложных поливиниловых эфиров, поливинилацетата, сополимеров виниловых мономеров, сополимеров виниловых мономеров и олефинов, этилен-метил метакрилатных сополимеров, сополимеров акрилонитрила-стирола, АБС-смол, этилен-виниловацетатных сополимеров, полиамидов, Нейлона 66, поликапролактона, алкидных смол, полиоксиэтиленов, полиимидов, полиэфиров, эпоксидных смол, триацетатного искусственного шелка, целлюлозы, ацетата целлюлозы, бутирата целлюлозы, бутирата ацетата целлюлозы, целлофана, нитроцеллюлозы, пропионата целлюлозы, эфиров целлюлозы, карбоксиметилцеллюлозы, коллагенов, хитинов, полимолочной кислоты, полигликолевой кислоты, сополимеров полимолочной кислоты и полиэтиленоксида, полисилоксанов, замещенных полисилоксанов, сополимеры этилена-винилацетата, полиолефиновых эластомеров, а также этилен-пропилен-монодиенового каучука и их комбинаций.
[002 69] Подложка может также содержать или быть изготовлена из металла или металлического сплава, например, нержавеющей стали, платины, иридия, титана, тантала, никельтитанового сплава или кобальтохромового сплава. Кроме того, подложка может включать или являться тканью животных или продуктом из ткани животных, например, тканевым или органным трансплантатом. Ткань животных может являться, например, костью (например, остеогенной тканью) или хрящем. Кроме того, подложка может содержать белок, например, коллаген или кератин. Подложка может также являться или содержать тканевый матрикс, например, ацеллюлярный тканевый матрикс. Дисперсные и недисперсные ацеллюлярные матриксы подробно описаны, например, в патентах США 5,336,616 и 6,933,326, описания которых в полном объеме включены в настоящую заявку путем отсылки. Подложка может также являться, или включать клетку животного (например, клетку, восстанавливающую ткани, такую как фибробласты или мезенхимальную стволовую клетку), и может представлять собой, например, комплекс, формирующий поры в мембране. Подложка может содержать или являться полисахаридом, например, агарозой. Она может также содержать или являться солью, предпочтительно относительно нерастворимой солью, например, сульфатом кальция. Подложка может являться гелем или кремом. Кроме того, она может содержать силикон или силастик. Подложки могут также содержать натуральное волокно, например, шелк, хлопок или шерсть.
[00270] Кроме того, подложка может являться имплантируемым медицинским устройством. Она может являться, например, стентом (например, сосудистым стентом, таким как коронарный стент; стентом, размещаемым в дыхательных путях, таким как эндотрахеальный или назальный стент; желудочно-кишечным стентом, таким как билиарный или панкреатический стент; или мочеточниковым стентом, таким как уретральный стент) или хирургической нитью (например, шелковой нитью, хромированным кетгутом, нейлоновой, полимерной или металлической нитью), или хирургическим зажимом (например, зажимом при аневризме). Подложка может являться, например, искусственным бедром, искусственным тазобедренным суставом, искусственным коленом, искусственным коленным суставом, искусственным плечом, искусственным плечевым суставом, искусственным пальцевым суставом (руки или ноги), костной пластинкой, костным штифтом, имплантом при переломе кости, имплантом межпозвоночного диска, костным цементом или прослойкой из костного цемента. Она может являться артериально-венозным шунтом, имплантируемой проволокой, кардиостимулятором, искусственным сердцем, прибором, поддерживающим работу сердца, кохлеарным имплантом, имплантируемым дефибриллятором, стимулятором спинного мозга, стимулятором центральной нервной системы, имплантом перифирического нерва. Другими подложками являются зубные протезы или зубные коронки.
[00271] В других вариантах осуществления подложка может являться устройством или сеткой для защиты больших сосудов от эмболии, подкожным устройством, кожным пластырем или пластырем на подслизистую, или имплантируемым устройством для доставки лекарственного средства. Подложка может также являться трансплантатом большого кровеносного сосуда, где кровеносный сосуд является, например, сонной артерией, бедренной артерией или аортой. Также она может являться подкожным имплантом, корнеальным имплантом, искусственным хрусталиком или контактной линзой.
[00272] Подложка может находиться в форме, например, листа, гранулы, сетки, частицы порошка, нити, гранулы или волокна. Подложка может содержать или являться твердым, полутвердым или гелеобразным веществом.
[00273] Полимеры, применяемые в изобретении, предпочтительно являются такими полимерами, которые являются биостабильными, биосовместимыми, особенно в процессе введения или имплантации устройства в тело, и не вызывают раздражения тканей тела.
[00274] Fc-реагенты могут быть нанесены (то есть иммобилизованы или стабилизированы) на подложку любым доступным способом. Например, они могут быть нанесены непосредственно на поверхности подложек, к которым они прикрепляются, например, посредством гидрофобных взаимодействий. Ниже описаны несколько других методик ((a)-(e)), включающих применение полимеров:
(a) Fc-реагент смешивают с совместимой полимерной смесью, которую затем слоями наносят на поверхность имплантируемого синтетического материала, стабилизируя, таким образом, Fc-реагент. Мономеры, обычно используемые в уровне техники для получения полимерных смесей, включают PLMA [поли(лаурилметакрилат)]; ПЭГ [полиэтиленгликоль], ПЭО [полиэтиленосид]; алкилированные функционализированные метакрилатные полимеры ПММА, ПЭМА, ППМА и ПБМА; итаконаты; фумараты и стироловые полимеры.
(b) Полимерный грунтовочный слой или пленку нанометровой толщины закрепляют на поверхности подложки, а затем на полимерном грунтовочном слое или пленке нанометровой толщины закрепляют Fc-реагент, стабилизируя, таким образом, Fc-реагент.
(c) Тонкий слой мономера полимера наносят на поверхность имплантируемой подложки, после чего мономер полимеризуют.Такие мономеры включают, например, метан, тетрафторэтилен, бензол, метанол, этиленоксид, тетраглим, акриловую кислоту, аллиламин, гидроксиэтилметакрилат, N-винилпирролидон и меркаптоэтанол. Затем Fc-реагент прикрепляют к полученному мономеру.
(d) Подложку покрывают белком, таким как А-белок или альбумин, который прикрепляется к Fc-реагенту, стабилизируя, таким образом, Fc на поверхности подложки.
(e) Fc-реагент может быть помечен цепью гидрофобных аминокислот, которые связываются с имплантируемыми синтетическими материалами и обеспечивают однонаправленную ориентацию Fc.
[00275] Способы изобретения могут быть применены к любым видам животных, а молекулы IgG, из которых получены IgG-производные части Fc-реагентов, могут происходить из любых видов животных. Обычно подходящие виды животных включают те виды, в которых присутствуют IgG или IgG-подобные молекулы. В основном виды, к которым применяются способы, и виды, из которых происходят IgG-производные части Fc-реагентов, применяемых в способах, являются одинаковыми. Однако они не обязательно являются одинаковыми. Подходящими видами животных предпочтительно являются млекопитающие, при этом они включают, без ограничения, людей, всех приматов кроме человека (например, обезьян, бабуинов и шимпанзе), лошадей, крупный рогатый скот (например, быков, коров или волов) свиней, коз, овец, собак, кошек, кроликов, песчанок, хомяков, крыс и мышей. Не относящиеся к млекопитающим виды включают, например, птиц (например, кур, индеек и уток) и рыб.
[00276] Термины "лечение" и "профилактика" имеют одно и то же значение применительно к иммобилизованному Fc, как описано выше для страдомеров и страдотел.
[00277] В случае, когда иммобилизованные Fc являются имплантируемыми устройствами, покрытыми Fc-реатентами, они могут быть имплантированы в, присоединены к или закреплены на соответствующих внутренних органах или тканях, или поверхностях тела соответствующих индивидов, с использованием способов, известных в уровне техники. Когда они приготовлены в такой форме, как, например, суспензии, порошки, они могут быть приготовлены и введены так же, как описано выше для страдомеров и страдотел.
[00278] Иммобилизованные Fc-реагенты настоящего изобретения могут применяться для лечения или профилактики патологических состояний, включающих, помимо прочих, злокачественную опухоль, ишемическую болезнь сердца (ИБС), васкулит, розацеа, акне, экзему, миокардит и другие поражения миокарда, системную красную волчанку, диабет, спондилопатии, синовиальные фибробласты и строму костного мозга; потерю костной массы; болезнь Паджета, гипертрофическую остеопатию; дисфункциональную остеопению; недостаточность питания, парадонтоз, синдром Гоше, гистиоцитоз из клеток Лангерганса, поражение спинного мозга, острый септический артрит, остеомаляцию, синдром Иценко-Кушинга, монооссальную фиброзную дисплазию, полиоссальную фиброзную дисплазию, реконструкцию периодонта и переломы кости, регуляцию болей в кости, а также гуморальную злокачественную гиперкалыдемию, анкилозирующий спондилит и другие спондилоартропатии; отторжение трансплантата и вирусные инфекции.
[00279] Все аутоиммунные заболевания, частично или полностью, могут представлять собой MDCMD. Термин "аутоиммунное заболевание", используемый в настоящей заявке, относится к большой группе, включающей свыше 80 различных хронических заболеваний. Основная проблема при таких заболеваниях состоит в том, что иммунная система атакует собственный организм. Аутоиммунные заболевания затрагивают все основные системы организма, включая соединительную ткань, нервы, мышцы, эндокринную систему, кожу, кровь, дыхательную и желудочно-кишечную системы.
[00280] Аутоиммунное заболевание и патологическое состояние могут являться гематоиммунологическим процессом, включающим, помимо прочего, идиопатическую тромбоцитопеническую пурпуру, аллоиммунную/аутоиммунную тромбоцитопению, приобретенную иммунную тромбоцитопению, аутоиммунную нейтропению, аутоиммунную гемолитическую анемию, Парвовирус В19-ассоциированную эритроцитарную аплазию, приобретенный аутоиммунитет против фактора VIII, приобретенную болезнью фон Виллебранда, множественную миелому и моноклональную гаммапатию неизвестной этиологии, сепсис, апластическую анемию, истинную эритроцитарную аплазию, анемию Даймонда-Блекфана, гемолитическую болезнь новорожденного, иммуноопосредованную нейтропению, невосприимчивость к переливанию тромбоцитарной массы, неонатальную посттрансфузионную пурпуру, гемолитический уремический синдром, системный васкулит, тромбическую тромбоцитопеническую пурпуру или синдром Эвана.
[00281] Аутоиммунное заболевание и патологическое состояние могут являться нейроиммунологическим процессом, включающим, помимо прочего, синдром Гийена-Барре, хроническую воспалительную демиелинизирующую полирадикулоневропатию, парапротеинемическую IgM демиелинизирующую полиневропатию, миастенический синдром Ламберта-Итона, миастению гравис, многоочаговую двигательную невропатию, боковой амиотрофический склероз, ассоциируемый с антителами против GM1, демиелинизацию, рассеянный склероз и неврит зрительного нерва, синдром мышечной скованности, паранеопластическую дегенерацию мозжечка, вызванную аыти-Yo антителами, паранеопластический энцефаломиелит, сенсорную невропатию, вызванную анти-Hu антителами, эпилепсию, энцефалит, миелит, миелопатию, особенно связанную с Т-лимфотропным вирусом человека первого типа, аутоиммунную диабетическую невропатию или острую идиопатическую вегетативную невропатию.
[00282] Аутоиммунное заболевание и патологическое состояние могут являться ревматическим процессом, включающим, помимо прочего, болезнь Кавасаки, ревматоидный артрит, синдром Фелти, АНЦА-положительный васкулит, спонтанный полимиозит, дерматомиозит, антифосфолипидные синдромы, повторные самопроизвольные аборты, системную красную волчанку, ювенильный идиопатический артрит, синдром Рейно, CREST-синдром или увеит.
[00283] Аутоиммунное заболевание и патологическое состояние могут являться дерматоиммунологическим процессом, включающим, помимо прочего, токсический эпидермальный некролиз, гангрену, гранулему, аутоиммунное заболевание кожи с развитием нарывов, включая вульгарную пузырчатку, буллезный пемфигоид и эксфолиативную пузырчатку, витилиго, синдром стрептококкового токсического шока, склеродермию, системный склероз, включая диффузный и локальный кожный системный склероз или атопический дерматит (особенно стероидозависимый атопический дерматит).
[00284] Аутоиммунное заболевание и патологическое состояние могут являться скелетно-мышечным иммунологическим процессом, включающим, помимо прочего, миозит с включенными тельцами, некротизирующий фасцит, воспалительные миопатии, миозит, анти-декорин (BJ антиген) миопатию, паранеопластическую некротическую миопатию, вакуолизирующую миопатию, сцепленную с Х-хромосомой, пеницилламин-индуцированный полимиозит, атеросклероз, ишемическую болезнь сердца или кардиомиопатию.
[00285] Аутоиммунное заболевание и патологическое состояние могут являться желудочно-кишечным иммунологическим процессом, включающим, помимо прочего, пернициозную анемию, аутоиммунный хронический активный гепатит, первичный биллиарный цирроз печени, глютеновую энтеропатию, герпетиформный дерматит, криптогенный цирроз печени, реактивный артрит, болезнь Крона, болезнь Уипла, язвенный колит или склерозирующий холангит.
[00286] Аутоиммунное заболевание и патологическое состояние могут являться гомологичной болезнью (РТПХ), антитело-опосредованным отторжением трансплантата, отторжением трансплантата костного мозга, постинфекционным воспалением, лимфомой, лейкозом, неоплазией, астмой, сахарным диабетом I типа с антителами против бета-клеток, синдромом Шегрена, смешанным поражением соединительной ткани, болезнью Аддисона, синдромом Фогта-Коянаги-Харады, мембранозно-пролиферативным гломерулонефритом, синдромом Гудпасчера, болезнью Грейвса, тиреоидитом Хашимото, гранулематозом Вегенера, микрополиартериитом, синдромом Черджа-Стросс, узелковым полиартериитом или полиорганной недостаточностью.
[00287] В настоящей заявке "злокачественная опухоль" относится к или описывает физиологическое состояние у млекопитающих, которое обычно характеризуется нерегулируемым ростом клеток. Примеры злокачественной опухоли включают, помимо прочего, карциному, лимфому, бластому, саркому (включая липосаркому, остеобластическую саркому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, лейомиосаркому, рабдомиосаркому, фибросаркому, миксосаркому, хондросаркому), остеокластому, нейроэндокринные опухоли, мезотелиому, хордому, синовиому, шванному, менингиому, аденокарциному, меланому и лейкоз или лимфолейкоз. Более конкретные примеры таких форм злокачественной опухоли включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), рак легкого, включая эпителиальный плоскоклеточный рак), рак легкого, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточную карциному легкого, мелкоклеточную карциному легкого, рак брюшной полости, гепатоцеллюлярный рак, рак желудка, включая рак желудочно-кишечного тракта, рак-поджелудочной железы, глиобластому, цервикальный рак, рак яичников, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, карциному эндометрия или матки, карциному слюнной железы, рак почки, рак простаты, рак вульвы, рак щитовидной железы, карциному печени, анальную карциному, карциному полового члена, рак яичка, рак пищевода, опухоли желчного тракта, опухоль Юинга, базально-клеточную карциному, аденокарциному, карциному потовых желез, карциному сальных желез, папиллярную карциному, папиллярные аденокарциномы, цистаденокарциному, медуллярную карциному, бронхогенную карциному, почечноклеточную карциному, гепатому, карциному желчных протоков, хориокарциному, семиному, таратокарциному, опухоль Вильмса, опухоль яичка, карциному легкого, карциному мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, неврому слухового нерва, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкоз, лимфому, множественную миелому, макроглобулинемию Вальденстрема, миелодиспластическую болезнь, болезнь тяжелых цепей, нейроэндокринные опухоли, Шванному и другие карциномы, рак головы и шеи, миелоидные неоплазии, такие как острый миелобластный лейкоз, включая ОМЛ с созреванием, ОМЛ без дифференцировки, острый промиелоцитарный лейкоз, острый миеломоноцитарный лейкоз и острый моноцитарный лейкоз, миелодиспластические синдромы и хронические миелопролиферативные заболевания, включая хронический миелогенный лейкоз, опухоли центральной нервной системы, например, опухоли головного мозга (глиому, нейробластому, астроцитому, медуллобластому, эпендимому и ретинобластому), солидные опухоли (носоглоточный рак, базально-клеточную карциному, рак поджелудочной железы, рак желчных протоков, саркому Капоши, рак яичка, маточный, вагинальный или цервикальный рак, рак яичников, первичный рак печени или эндометриальный рак, опухоли сосудистой системы (ангиосаркому и гемангиоперицитому)), гематологические неоплазии и заболевания наподобие неопластических, например, лимфому Ходжкина; не-ходжскинские лимфомы (лимфому Беркитта, мелкоклеточную лимфоцитарную лимфому/хронический лимфолейкоз, грибовидную гранулему, лимфому из клеток мантийной зоны, фолликулярную лимфому, диффузную В-крупноклеточную лимфому, лимфому краевой зоны, гистиоцитарный ретикулоэндотелиоз и лимфоплазмацитарный лейкоз), опухоли из клеток-предшественников лимфоцитов, включающие В-клеточный острый лимфобластный лейкоз/лимфому и Т-клеточный острый лимфобластный лейкоз/лимфому, тимому, опухоли из зрелых Т- и NK-клеток, включающие узловой Т-клеточный лейкоз, Т-клеточный лейкоз/Т-клеточные лимфомы взрослых и Т-клеточный лейкоз из крупных гранулярных лимфоцитов, остеолитические формы рака и костный метастаз.
[00288] Используемый в настоящей заявке индивид "с риском развития заболевания, опосредованного клетками, происходящими из моноцитов (MDCMD)" является индивидом, который имеет предрасположенность к развитию MDCMD, то есть генетическую предрасположенность к развитию MDCMD, или который был подвергнут воздействию условий, которые могут привести к MDCMD. Индивид "подозреваемый на наличие MDCMD" является индивидом, имеющим один или более симптомов MDCMD. Из вышесказанного очевидно, что ни индивиды "с риском развития MDCMD", ни индивиды, "подозреваемые на наличие MDCMD", не являются всеми лицами в рамкам целевого вида.
[00289] В любом из вышеописанных способов MDCMC может являться заболеванием, вызванным подложкой, и Fc-реагент служит для предотвращения MDCMC или улучшения состояния при MDCMC.
Пример 1 - Конструкция иммунологически активных биомиметиков
[00290] Последовательность, кодирующую мономер Fc-фрагмента из IgG1 человека (SEQ ID NO: 1), клонировали в экспрессионный вектор (pCDNA 3.1D/V5 His ТОРО Invitrogen), включающий отобранные сайты рестрикции, сигнальную последовательность IgK (дополнительно определенную ниже) и эпитоп таги, получив последовательность мономера IgG1 {сайты рестрикции-сигнал IgK-сайты рестрикции-(шарнирная область-СН2-СН3) IgG1-сайты рестрикции-эпитоп таги (V5 и His)-STOP}, показанную на фиг. 17 (SEQ ID NO: 19). Конструкцию трансфицировали в клетки СНО (СНО-002) с целью продукции белка. Дополнительно, создавали несколько страдомерных конструкций с общими структурами:
a) {сайты рестрикции-сигнал IgK-сайты рестрикции-(шарнирная область-СН2-СН3)IgG1-сайт XbaI (шарнирная область-СН2-СН3)IgG1-ST0P} (SEQ ID NO: 21) (см. также фиг. 4А и фиг. 18);
b) {сайты рестрикции-сигнал IgK-сайты рестрикции-(шарнирная область-СН2-СН3)IgG1-сайт XbaI (шарнирная область-СН2-СН3)IgG1-сайты рестрикции-эпитоп таги (V5 и His)-STOP} (SEQ ID NO: 23) (см. также фиг. 19);
с) {сайты рестрикции-сигнал IgK-сайт EcoRV-(шарнирная область-СН2-СН3)IgG3-(шарнирная область-СН2-СН3)IgG1-сайты рестрикции-эпитоп таги (V5 и His)-STOP} (SEQ ID NO: 25) (см. также фиг. 21); и
d) (сайты рестрикции-сигнал IgK-сайт EcoRV-(СН2) IqE-(шарнирная область-СН2-СН3)IgG1-(шарнирная область-СН2)IgG1-(СН4) IgE-STOP} (SEQ ID NO: 27) (см. также фиг. 22).
[00291] Страдомерную конструкцию на основе IgG1 a) (SEQ ID NO: 21; фиг. 18) создавали с использованием ПЦР. Праймеры, комплементарные последовательности шарнирной области (на 5'-конце) IgGi (SEQ ID NO: 29) и С-концу Igd (на 3'-конце) (SEQ ID NO: 30), использовали для амплификации шарнирной-Fc области IgG. Сайты рестрикции вводили в праймеры, чтобы обеспечить клонирование внутри рамки второго Fc-домена последовательно с первым, который клонировали в pcDNA клонирующий вектор (pCDNA 3.1D/N5 His ТОРО, Invitrogen). Стоп-кодон встраивали перед сайтом рестрикции С-концевого праймера, чтобы предотвратить считывание фланкирующих последовательностей данной конструкции.
[00292] Страдомерная конструкция b) (SEQ ID NO: 23; фиг. 19), полученная аналогичным образом, содержала Fc IgG1 - Fc IgG1, как описано выше, а также два эпитоп тага, добавленные к С-концу конструкции. Данные эпитоп таги использовали для идентификации или очистки белка. В данной второй конструкции два эпитоп тага, V5 и His таг, присутствуют в рамке считывания перед стоп-кодоном.
[00293] Белки, которые обычно секретируются, содержат, как правило, гидрофобную сигнальную последовательность на N-конце белка. Для страдомерных конструкций использовали сигнальную последовательность IgK METDTLLLWVLLLWVPGSTG (SEQ ID NO: 35), которая удаляется из белка при секреции клетками млекопитающих, такими как клетки яичников китайских хомячков. Предполагаемый сайт расщепления определяли на основе алгоритмов для предсказания сайта расщепления сигнальной последовательности (SignalP 3.0).
[00294] Сконструировали дополнительные страдомерные конструкции, подобные а) и b) выше, которые содержали структуру Fc IgG1 - Fc IgG1, как описано выше (с и без эпитоп тага), но с использованием шарнирного домена IgG3 в конструкции: Fc IgG1 - шарнирная область IgG3-(СН2-СН3)IgG1.
Пример 2 - Конструкция и тестирование иммунологически активных биомиметиков
IVIG и Fc, наносимые в форме покрытий, вызывают аналогичныо фенотипические изменения
[00295] IVIG и Fc, при нанесении на стенки и дно лунок стерильного планшета, вызывают практически идентичные изменения уровней CD1a и CD86 на незрелых DC и замедляют активацию CD11c. Из-за общепризнанной критической роли DC в ИТП указанные данные обеспечивают рациональную модель для оценки функции IVIG-миметиков, таких как страдомеры. Также сделали заключение, что тот факт, что фенотипические изменения, вызываемые IVIG, полностью воспроизводятся рекомбинантным Fc, позволяет предположить, что действие IVIG на DC, вполне вероятно, является Fc-опосредованным.
Получение страдомеров
[00296] Сконструировали страдомеры четырех различных классов, воспроизводящие эффекты IVIG на незрелую DC. Получили все последовательные страдомеры, кластерные страдомерные единицы, составляющие кластерные страдомеры, кор-страдомерные единицы, включающие кор-страдомеры, а также Fc-фрагмент-страдомеры, приведенные ниже в Таблице 3, за исключением обозначенных случаев. Для получения соответствующих последовательностей для каждой из конструкций человека, перечисленных ниже, синтезировали кДНК из суммарной РНК, выделенной из МПК (мононуклеаров периферической крови) человека. Для получения указанных последовательностей из других видов РНК выделяли из ткани соответствующих видов. Для получения кДНК использовали рандомные праймеры. кДНК использовали для амплификации целевых фрагментов, используя ПЦР для синтеза, клонирования, а также для последующего анализа последовательности фрагментов ДНК. Конечные конструкции получали либо соединением перекрывающихся ПЦР фрагментов (Horton RM, Hunt HD, Но SN, Pullen, JK and Pease LR. Engineering hybrid genes without the use of restriction enzymes: gene splicing by overlap extension. Gene 77: 61-68, 1989), либо с использованием подходящих присутствующих сайтов рестрикции, с получением соответствующих слитых фрагментов.
[00297] Например, при клонировании G-007 СН4 домен IgE слили непосредственно с СН2 доменом IgG1 на 3'-конце белка. Это выполняли, получив праймеры, которые содержали перекрывающиеся последовательности IgG1CH2 (С-конец) с N-концевыми аминокислотами IgECH4. В одном случае гибридный праймер использовали для амплификации 5' с последовательностями IgG1, и комплементарный праймер - для амплификации 3'-праймерами с С-конца IgECH4. Продукты двух реакций смешивали, и использовали фланкирующие праймеры для амплификации слитого белка. Анализ последовательности подтвердил правильность конструкции.
[00298] Во многих случаях использовали сайты рестрикции, которые удобно располагались на концах соединяемых молекул. Когда сайты рестрикции встроены, на концах связываемых молекул находятся определяемые остаточные рестрикционные последовательности. Такой подход использовали для большинства конструкций, приведенных ниже в Таблице 3. Аминокислотные последовательности страдомеров, показанные в Таблице 3, приведены на фиг. 24. Некоторые последовательности показаны с His-тагами, известными в уровне техники, которые применяются при очистке белков.




Экспрессия белка страдомера
[00299] Для экспрессии белка страдомеров плазмидную ДНК, кодирующую страдомеры, описанные выше, трансфицировали в суспензионную культуру клеток СНО (система экспрессии Freestyle™ МАХ СНО, Invitrogen СА). После экспрессии белка экспрессированные страдомеры выделяли из среды культивирования с помощью аффинной колоночной хроматографии с использованием аффинных колонок с А-белком или G-белком. Очищенные страдомеры анализировали с помощью электрофореза в ДСН-ПААГ (полиакриламидном геле с додецилсульфатом натрия) с восстановлением, с последующим окрашиванием кумасси голубым, подтверждая присутствие полос мономерных белков ожидаемого размера, как показано: G-002: полоса приблизительно 35KD, G-004 полоса приблизительно 70KD, G-010: полоса приблизительно 45KD, G-011: полоса приблизительно 80KD, G-012: полоса приблизительно 85KD, G-018 полоса приблизительно 70KD, G-019: приблизительно 35KD, G-028: полоса приблизительно 37KD. Плазмидная ДНК, кодирующая описанные страдомеры, также может быть трансфицирована в другие клетки млекопитающих, такие как НЕК 2 93, клетки ВНК, мышиные клетки NSO и мышиные клетки SP2/0.
Образование мультимера
[00300] Было замечено, что данные конструкции при трансфекции, культивировании и очистке, могут давать белки ожидаемого размера в неденатурирующем и денатурирующем белковом анализе. Кроме того, наблюдали, что некоторые соединения также показывали полосы большего размера, которые в соответствии с критериями определения размера являются мультимерами белка, ожидаемого в димерной форме.
[00301] Образование соединений более высокого порядка из выбранных страдомеров анализировали электрофорезом в ДСН-ПААГ с последующим вестерн-блоттингом без восстановления (А) и с восстановлением (В). Анализ с помощью электрофореза в ДСН-ПААГ выявил образование высокомолекулярных соединений страдомеров G-002, G-010 и G-019 без восстановления по сравнению с восстановлением:
- G-002: полоса приблизительно 35KD в условиях восстановления - полосы приблизительно 70KD (димер) и 135KD (тетрамер) без восстановления.
- G-010: полоса приблизительно 45KD в условиях восстановления - полосы приблизительно 90KD (димер) и 180KD (тетрамер) без восстановления.
- G-019: полоса приблизительно 35KD в условиях восстановления - полосы приблизительно 70KD (димер), 140KD (тетрамер) без восстановления.
[00302] Предполагается, что тетрамеры и другие мультимеры более высокого порядка, образуемые из димерного белка, будут существенно повышать биологическую активность соединения при измерении в анализе на незрелых дендритных клетках (см. ниже).
Мономеры страдомеров, страдомеры и мультимеры страдомеров более высокого порядка сохраняют сайты узнавания
[00303] Каждый из белков в Таблице 3 узнавался кроличьим антителом против человеческого IgG (Fc) [Thermo Scientific 31789]. Из этого сделали вывод, что каждый из указанных белков сохраняет сайты узнавания для данного антитела.
Визуализация методом плазмонного резонанса
[00304] Способность страдомеров, показанных в Таблице 3, связывать FcγRIIIa оценивали, используя метод поверхностного плазмонного резонанса (SPR) (доступный в продаже как Biacore®). Человек FcγRIIIa иммобилизовали непосредственно путем связывания амина на чипе СМ5 Biacore, разбавив лиганд в ацетате рН 5,0 до концентрации 5 мкг/мл. Лиганды пропускали через определенную проточную ячейку при скорости потока 5 мкл/мл, пока не было достигнуто 250 RU (резонансные единицы Biacore, соотв. ~1 пг белка на мм биосенсора). Затем проточные ячейки блокировали этаноламином. Страдомеры и IVIG разбавляли до 1000 нМ в HBS-EP (0,01 М HEPES, рН 7,4; 0,15 М NaCl; 3 мМ ЭДТА; 0,0 0 5% поверхностно-активной добавки Р20) и получали серийные разведения 500 нМ, 250 нМ, 125 нМ и, наконец, 62,5 нМ. Также включали фоновую пробу, содержащую только буфер (HBS-EP). Скорость потока 20 мкл/мин использовали для всех проб. В общей сложности вводили 60 мкл пробы в течение 3 минут. Восстановление обеспечивали путем пропускания тока буфера через проточные ячейки в течение увеличенного промежутка времени продолжительностью приблизительно 10 минут.
[00305] При 500 нМ измеренное значение Req (равновесное) относительно базовой линии для страдомерной конструкции G-010 составило 24,9 RU при пропускании над FcγRIIIa человека, а КГ) составила 1,95е-7 с использованием модели связывания 1:1. IVIG при 500 нМ над FcγRIIIa человека показал Req 63,6 RU и KD 1,89е-7 с использованием модели связывания 1:1. Таким образом, определили, что G-010 связывался с FcγRIIIa. Подобную связывающую способность выявили у других биомиметических соединений. Ниже приведены некоторые другие примеры:
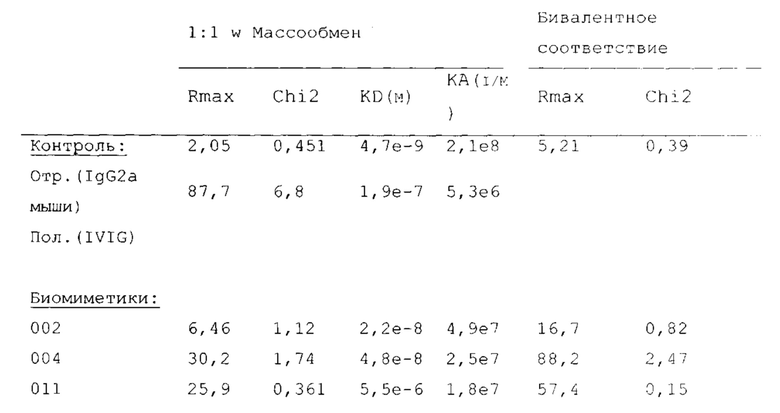
[00306] Сделали заключение, что указанные белки различались по способности связываться с рекомбинантным FcγRIIIa в анализе с методом плазмонного резонанса, и что некоторые соединения, такие как G-010, соответствовали бивалентной кривой, подобной кривым для бивалентных антител, что указывает на то, что страдомер может показывать мульти-валентное связывание с FcγRIIIa.
Страдомеры воспроизводят биологический эффект IVIG
[00307] Оценивали биологическую функцию указанных страдомеров. С целью определения способности каждого страдомера из Таблицы 3 воспроизводить функциональные свойства IVIG у лиц с ИТП, проводили in vitro анализ с использованием незрелых дендритных клеток (iDC). Основанием для выбора iDC в качестве целевых клеток послужили опубликованные данные, продемонстрировавшие, что адоптивный перенос DC из мышей, обработанных IVIG, индуцировал развитие защиты от развития ИТП у интактных животных (Siragam, V. et al. Intravenous immunoglobulin ameliorates ITP via activating Fc [gamma] receptors on dendritic cells. Nat Med 12, 688 (2006)). В своих первоначальных исследованиях авторы изобретения оценивали воздействие нанесенных, т.е. иммобилизованных на пластинке, рекомбинантных Fc (rFc) и IVIG на экспрессию различных маркеров активации, созревания и костимулиряции на человеческих CD14+ клетках, культивируемых в присутствии IL-4 и ГМКСФ. При сравнении с клетками, выращенными в присутствии только цитокинов, клетки, контактировавшие с покрытиями IVIG или rFc, демонстриривали заметное повышение экспрессии CD8 6 и подавление экспрессии CD1a, а также задержку активации CD11c.
[00308] Затем определяли, воспроизводили ли страдомеры, указанные в Таблице 3, описанный эффект иммобилизованных IVIG или Fc в отношении iDC. Указанные соединения при нанесении на стенки и дно лунок планшета действительно воспроизводили указанный эффект: G-002, G-004, G-005, G-014, G-018 и G-019. Следующие соединения при нанесении на стенки и дно лунок планшета не воспроизводили указанный эффект: G-010, G-011 и G-012.
[00309] Указанные соединения в растворе воспроизводили эффект иммобилизованных IVIG или Fc в отношении iDC: G-002, G-010, G-014, G-018 и G-019. Следующие соединения в растворе не воспроизводили указанный эффект: G-004, G-005, G-011 и G-012.
[00310] Можно проверить, действительно ли обработка iDC иммобилизованным IVIG влияет на последующий ответ на провоспалительные стимулы.
[00311] Из полученных данных сделали следующие выводы:
i. выбранные страдомеры, нанесенные на культуральный планшет, воспроизводят функциональную способность иммобилизованного IVIG активировать экспрессию CD8 6 и подавлять экспрессию CD1a на незрелой DC,
ii. выбранные страдомеры, вводимые при низкой дозе в растворимой форме, воспроизводят функциональную способность иммобилизованного IVIG активировать экспрессию CD8 6 и подавлять экспрессию CD1a на iDC,
iii. некоторые страдомеры могут индуцировать фенотипическое изменение как в растворимой, так и в иммобилизованной форме, а другие страдомеры, например, G-010, могут индуцировать фенотипическое изменение в растворимой, но не в иммобилизованной форме,
iv. страдомеры разной структуры могут являться биологически активными, что подтверждается на примере Fc-фрагмент-страдомера, образованного из G-002, и кластерного страдомера, образованного из G-010,
v. белковый анализ выявил более крупные структуры, чем ожидалось при димеризации мономеров страдомеров, причем указанные мультимерные структуры могут согласовываться с биологической активностью, сравнимой с активностью IVIG, и
VI. страдомеры, сформированные из димеризованных мономеров страдомеров, могут демонстрировать бивалентное соответствие в условиях плазмонного резонанса, что согласуется со связыванием нескольких Fcγ-рецепторов и предполагает присутствие мультимерных третичных структур страдомеров.
Пример 3 - Термоагрегированные биомиметики более эффективыы по сравнению с IVIG
[00312] Страдомер является биологически активным миметиком агрегированного иммуноглобулина и в особенности агрегированных Fc-фрагментов данного иммуноглобулина. В некоторых случаях термоагрегация биомиметиков, описанных в настоящей заявке, может повышать биологическую активность. Можно сделать вывод, что термоагрегированные биомиметики, как описанные в настоящей заявке, могут являться столь же эффективными, что и IVIG.
Пример 4 - Fc-фрагмент проявляет несколько активностей
[00313] Fc-фрагмент использовали в качестве положительного контроля в экспериментах, описанных выше, в которых белок, который наносили и, таким образом, иммобилизовали на полимере, проявлял такие биологические свойства, которые воспроизводили свойства иммобилизованного IVIG. Fc-фрагмент может также применяться в качестве кор-страдомерной единицы, когда его присоединяют к кор-группам, таким как липосомы, частицы или альбумин. Кроме того, авторы изобретения демонстрировали, что Fc-фрагмент при культивировании в некоторых системах экспрессии и некоторых типах клеток, таких как система транзиентной трансфекции Invitrogen FreestyleMax на основе клеток CHO-S, может формировать мультимеры более высокого порядка в белковом анализе, показывать биваленетный профиль связывания при визуализации в условиях плазмонного резонанса и проявлять мощную биологическую активность в растворимой форме, сопоставимой с активностью иммобилизованного IVIG, в анализе на незрелых DC. Таким образом, можно сделать вывод, что при некоторых тщательно контролируемых условиях Fc-фрагмент формирует Fc-фрагмент-страдомер. Данный эффект может происходить в результате посттрансляционных модификаций, таких как изменения в гликозилировании.
Пример 5 - Кор-страдомер, который представляет собой Fc-покрытую частицу, может менять фагоцитный потенциал в сравнении с частицами без покрытия
[00314] МПК выделяли из лейкотромбоцитарного слоя здоровых доноров, используя центрифугирование в градиенте плотности фиколла-гипака. После выделения МПК дважды промывали PBS. Затем CD14+ клетки очищали, используя разделительную колонку MACS (Miltenyi). Очищенные клетки подсчитывали и ресуспендировали до плотности 2×105/мл в полной среде RPMI, содержащей 800 мкг/мл ГМКСФ и 5 нг/мл IL-4. Затем клетки высевали в лунки обычных (не для культур тканей), но стерильных 6-луночных планшетов. После посева CD14+ клеток в планшеты к ним добавляли, в соотношении 1:1, полистирольные ФИТЦ-микрогранулы (0,52 мкм), покрытые насыщающим или ненасыщающим количеством Fc или IVIG, и инкубировали в течение 6 дней при 37°С, 5,0% СО2, а затем анализировали на предмет фагоцитоза микросфер посредством измерения флуоресценции отсортированных клеток.
[00315] Частицы, покрытые как IVIG, так и Fc, функционировали как кор-страдомеры и, таким образом, могли изменять фагоцитный потенциал в сравнении с частицами без покрытия.
Пример 6 - Конструкция иммунологически активных биомиметиков с измененными аффинностями связывания FcγRIII
[00316] Было показано, что общий набор остатков IgG1 вовлечен в связывание со всеми Fcγ-рецепторами. Также демонстрировали, что дополнительные остатки в молекулах IgG1 участвуют в связывании и с FcγRII, и с FcγRIII. Некоторые остатки при изменении ингибировали связывание одного или нескольких рецепторов. Примечательно, что специфическая двойная мутация S298A/K334A усиливала связывание с FcγIIIa и снижала связывание с FcγIIb. Указанные остатки были помечены на конструкции страдомера, показанной на фиг. 16 (звездочкой на обеих аминокислотах). Таким образом, можно использовать сайт-направленный мутагенез, чтобы получить страдомерную молекулу со структурой, кодируемой в соответствии с SEQ ID NO: 17, но с соответствующими мутациями S298A/K334A.
Пример 7 - Экспрессия рекомбинантных белков
[00317] Существуют многочисленные системы экспрессии, которые подходят для применения при получении композиций, описанных выше. В частности, системы экспрессии на основе эукариотических клеток могут использоваться для получения нуклеотидных последовательностей или соответствующих полипептидов, белков и пептидов. Многие такие системы широко доступны в продаже.
[00318] В предпочтительном варианте осуществления страдомеры, описанные в настоящей заявке, получены с использованием клеток яичников китайских хомячков -(СНО), широко применяемых для получения рекомбинантных иммуноглобулинов в соответствии со стандартными методами. В альтернативном варианте для получения человеческих страдомеров, описанных в настоящей заявке, могут применяться, например, трансгенные животные, обычно посредством экспрессии в молоке животного, с использованием общеизвестных методов экспрессии в трансгенных животных (Lonberg N. Human antibodies from transgenic animals. Nat Biotechnol. 2005 Sep; 23(9): 1117-25; Kipriyanov SM, Le Gall F. Generation and production of engineered antibodies. Mol. Biotechnol. 2004 Jan; 26(1): 39-60; см. также Ko K, Koprowskj Н. Plant biopharming of monoclonal antibodies. Virus Res. 2005 Jul; 111(1): 93-100.
[00319] Система на основе бакуловирусов в клетках насекомых может обеспечивать высокий уровень экспрессии белков с фрагмента гетерологичной нуклеиновой кислоты, как описанного в патентах США 5,871,986 и 4,879,236, включенных в полном объеме в настоящую заявку путем отсылки, и может быть приобретена, например, под маркой МАХВАС® 2.0 у Invitrogen® и BACPACK™ Baculovirus Expression System у Clontech®.
[00320] Другие примеры систем экспрессии включают систему индуцируемой экспрессии в клетках млекопитающих от Stratagene®, в которой используется синтетический экдизон-индуцируемый рецептор. Другим примером индуцируемой системы экспрессии является система T-REX™ от Invitrogen®, тетрациклин-регулируемая индуцируемая система экспрессии в клетках млекопитающих, в которой используется полноразмерный промотор ЦМВ. Invitrogen® также предлагает дрожжевую систему экспрессии, Pichia methanolica, которая разработана для получения с высоким уровнем рекомбинантных белков в метилотрофных дрожжах Pichia methanolica. Специалисту в данной области известно, как осуществлять экспрессию векторов, таких как экспрессионные конструкции, описанные в настоящей заявке, получать их кодирующую нуклеотидную последовательность или соответствующий полипептид, белок или пептид. См. обзоры Recombinant Gene Expression Protocols, Rocky S. Tuan, Humana Press (1997), ISBN 0896033333; Advanced Technologies for Biopharmaceutical Processing, Roshni L. Dutton, Jeno M. Scharer, Blackwell Publishing (2007), ISBN 0813805171; Recombinant Protein Production With Prokaryotic and Eukaryotic Cells By Otto-Wilhelm Merten, Contributor European Federation of Biotechnology, Section on Microbial Physiology Staff, Springer (2001), ISBN 0792371372.
Пример 8 - Экспрессия и очистка иммунологически активных биомиметиков
[00321] Конструкции нуклеиновых кислот, описанные в Примерах 1 и 2, трансфицировали в клеточные линии, которые в естественном состоянии не экспрессируют Ig. Кодируемые полипептиды экспрессировались в виде секретируемых белков благодаря наличию секреторных лидерных последовательностей, которые обычно удаляются эндогенными протеазами в процессе транспорта из клеток или могут быть впоследствии отщеплены и удалены способами, известными в уровне техники. Данные секретируемые, иммунологически активные биомиметики очищали с помощью хроматографических методов на основе А-белка или His-тагов, широко известных в уровне техники, а размер подтверждали с помощью электрофореза в ДСН-ПААГ (полиакриламидном геле с додецилсульфатом натрия) в восстанавливающих и/или не восстанавливающих условиях.
Пример 9 - Экспрессия и очистка иммунологически активных биомиметиков для крупномасштабного производства
[00322] Тогда как для получения больших количеств определенного белка могут использоваться различные системы, включающие бактерии, клетки насекомых или дрожжи, экспрессия в клетках млекопитающих может свести к минимуму проблемы, обусловленные измененным гликозилированием белков. Клетки млекопитающих, такие как клетки СНО, использовали для оверпродукции различных белков, слитых с Ig основой. Fc-домен в конструкции становится тагом, который обеспечивает последующую очистку из клеточного супернатанта с помощью очистки на аффинной колонке (Harris, CL, DM Lublin and BP Morgan Efficient generation of monoclonal antibodies for specific protein domains using recombinant immunoglobulin fusion proteins: pitfalls and solutions., J. Immunol. Methods 268: 245-258, 2002). Много слитых белков были непосредственно клонированы в рамке с константной областью Ig, а именно мономерами неполных СН2 и СН3 Fc-доменов. Конкретный пример экспрессии внеклеточного домена рецептора гамма-интерферона, экспрессируемого с Ig, использовали для получения больших количеств функционально активного белка (Fountoulakis, М, С. Mesa, G. Schmid, R. Gentz, M. Manneberg, M. Zulauf, Z. Dembic and G. Garotta, Interferon gamma receptor extracellular domain expressed as IgG fusion protein in Chinese hamster ovary cells: Purification, biochemical, characterization and stoichiometry of binding, J. Biol. Chem. 270: 3958-3964, 1995).
Пример 10 - Конструкция иммунологически активных биомиметиков с измененным Fc гликозилированием
[00323] С помощью метода, по существу аналогичного описанному Shields et al. для гомо-антител, дефукозилироваиные Fc-домены могут быть получены в мутантных СНО клетках с дефицитом ферментативной активности, обеспечивающей добавление фукозы к углеводам белка. Их используют для экспрессии страдомеров, обладающих более высокой аффинностью к FcγRIII, по сравнению с фукозилированной формой той же молекулы. (Robert L. Shields, et al. Lack of Fucose on Human IgG1 N-L inked Oligosaccharide Improves Binding to Human Fc RIR and Antibody-dependent Cellular Toxicity. J. Biol. Chem., Jul 2002; 277: 26733-26740 (doi:10.1074/jbc.M202069200)).
[00324] Было показано, что изменения в сиалировании Fc N-гликана может повысить биологическую активность (Kaneko Y, Nimmerjahn F, Ravetch JV. Science. 2006 Aug 4; 313 (5787): 627-8). Таким образом, с использованием подобных методов может быть получена молекула страдомера с измененным сиалированием.
[00325] Альтернативные способы изменения гликозилирования Fc-доменов страдомера включают хемоэнзиматические способы получения полипептидов с определенной структурой гликозилирования. См., Li, В., Song, Н., Hauser, S., and Wang, L.X. 2006. A Highly Efficient Chemoenzymatic Approach Toward Glycoprotein Synthesis. Org. Lett. 8: 3081-3084; См. также, заявку на международный патент PCT/US07/70818.
Пример 11 - Слитые конструкции с (176 V/F) полиморфизмом FcγIIIa
[00326] Как описано ранее, противовоспалительная активность IVIG зависит от первичных взаимодействий между Fc-доменом и FcγIIIa. Указанные взаимодействия можно эффективно оценить посредством количественного анализа с использованием метода ПНР для определения констант связывания и диссоциации иммунологически активных биомиметиков с двумя узнанаваемыми полиморфными вариантами FcγIIIa (176 V/F). Для определения аффинности связывания и диссоциации мономерного контрольного Fc-домена и страдомерных конструкций настоящего изобретния в клетках СНО необходимо получить слитые FcγIIIa-His-таг белки обоих V (SEQ ID NO: 33) и F (SEQ ID NO: 31), полиморфных по положению 176, вариантов (фиг. 20). Данные последовательности могут быть встроены в pCDNA 3.1 и трансфицированы в клетки СНО. Указанные слитые белки FcγIIIa очищали от супернатантов трансфицированных клеток, используя аффинные Nit'-колонки для очистки белков. Все слитые белки FcγIIIa характеризовали секвенированием кДНК и электрофорезом в ДСН-ПААГ.
[00327] Для экспрессии FcγIIIa и описания взаимодействия с иммунологически активным биомиметиком могут использоваться другие методы, известные в уровне техники. См., например, раздел "материалы и методы" в статье Robert L. Shields, et al. High Resolution Mapping of the Binding Site on Human IgG1 for FcγR-1/FcγRII/FcγRIII, and FcRn and Design of IgG1 Variants with Improved Binding to the FcγR. J. Biol. Chem., Feb 2001; 276: 6591-6604 (doi:10.1074/jbc.M009483200).
Пример 12 - Скрининг функции иммунологически активных биомиметиков in vitro
[00328] Для проверки функции иммунологически активных биомиметиков, таких как представленные в Примере 1, разработали in vitro анализ для определения возможного механизма, согласно которому нативные Fc-домены уменьшают воспаление in vivo. Недавно было продемонстрировано, что hIVIG ингибирует созревание дендритных клеток и изменяет профиль секреции IL-10, IL-12 и TNF-альфа (Bayry, J, et al., Inhibition of maturation and function of dendritic cells by intravenous immunoglobulin, Blood 101(2): 758-765 (2003)). Страдомеры настоящего изобретения опосредуют эффекты в отношении DC аналогично hIVIG. Ингибирование созревания DC и изменение секреции цитокина in vitro может служить эффективным способом определения некоторых биологических активностей многих конструкций страдомеров. Конструкции страдомеров, описанные выше, могут быть также проверены с использованием следующих экспериментальных параметров:

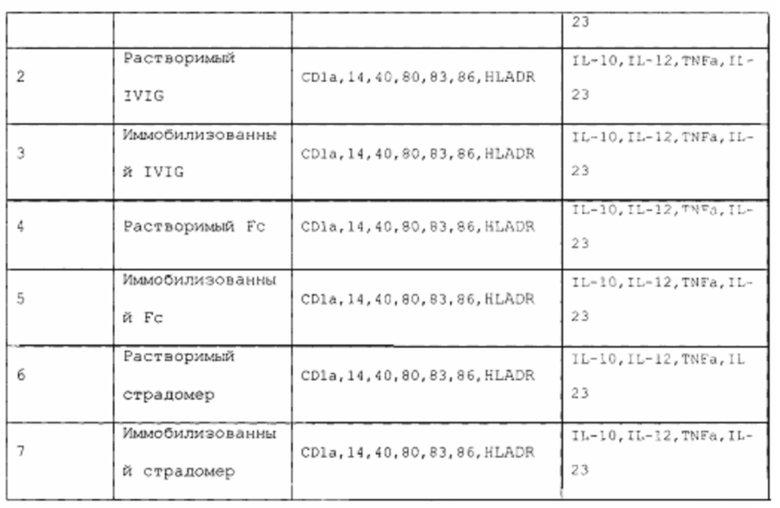
[00329] В одном предпочтительном in vitro анализе, показанном в Таблице 4, измеряли воздействие на человеческий фенотип DC растворимых, иммунологически активных биомиметиков, обладающих необходимыми аффинностями связывания. Растворимые не перекрестно-связанные конструкции на основе природной последовательности Fc-домена могут служить в качестве контроля. Оценивали специфичные DC маркеры на поверхности DC, включая маркеры активации (CD80, CD83 и CD86), а также Fcγ-рецепторы. См. Prechtel AT, Turza NM, Theodoridis AA, Steinkasserer A. CD83 knockdown in monocyte-derived DCs by small interfering RNA leads to a diminished T cell stimulation. J Immunol. 2007 May 1; 178(9): 5454-64. Кроме того, мультиплексный анализ может использоваться для оценки воздействия иммунологически активных биомиметиков настоящего изобретения на выработку цитокинов в DC (Jongbloed, Sarah L., et al. Enumeration and phenotypic analysis of distinct dendritic cell subsets in psoriatic arthritis and rheumatoid arthritis. Arthritis Res Ther. 2006;8 (1):R15 (Опубликовано онлайн 16 декабря 2005 г. doi:10.1186/ar1864)). Наконец, для подтверждения взаимодействия дендритных клеток с моноцитами, как ожидается, контрольные дендритные клетки и дендритные клетки, обработанные иммунологически активными биомиметиками, культивировали с очищенными моноцитами и с помощью поточной цитометрии оценивали изменения уровней активации рецепторов FcγRIIa и других клеточных поверхностных детерминант, связанных с состоянием активации моноцитов.
[00330] В конкретных вариантах осуществления страдомеры могут уменьшать число рецепторов FcγRIIa на иммунной клетке, увеличивая, таким образом, соотношение рецепторов FcγRIIb, ингибиторных в отношении рецепторов FcγRIIa, что приводит к ингибированию функций иммуноцита.
Пример 13 - Скрининг функции иммунологически активных биомиметиков in vivo
[00331] Многочисленные аутоиммунные заболевания, такие как идиопатическая тромбоцитопеническая пурпура, рассеянный склероз, астма и воспалительные болезни кишечника, являются признанными, общеизвестными моделями для испытания на животных in vivo (Wu GF, Laufer TM. The role of dendritic cells in multiple sclerosis. Curr Neural Neurosci Rep. 2007 May; 7(3): 245-52; Targan SR, Karp LC. Defects in mucosal immunity leading to ulcerative colitis. Immunol Rev. 2005 Aug; 206: 296-305). Например, в настоящее время доступны многочисленные модели ИТП. См., например, Crow AR, et al. IVIG inhibits reticuloendothelial system function and ameliorates murine passive immune thrombocytopenia independent of anti-idiotype reactivity. Br J Haematol. 2001; 115: 679-686. Иммунологически активные биомиметики, предназначенные для модуляции иммунной системы, как подходящие для каждого конкретного аутоиммунного заболевания, могут быть оценены в таких in vivo моделях. Важно то, что во многих из указанных моделей введение hIVIG скорее всего будет приводить к иммунному ответу на чужеродные (например, у мышей) человеческие антитела, который может заглушить или дать ложноположительный результат, связанный с противовоспалительными эффектами.
[00332] Мышиную модель идиопатической тромбоцитопенической пурпуры разрабатывали согласно следующей методике: число тромбоцитов у мышей C57BL6 измеряли, периодически производя надрез хвостовой вены, 10 мкл крови разводили в 15 мкл цитратного буфера. Затем в образцах анализировали абсолютное число тромбоцитов с помощью цитометра HemaVet 950. У мышей в ИТП контрольной группе, начиная со 2-го дня, ежедневно уменьшали число тромбоцитов, делая внутрибрюшинную инъекцию 2 мкг анти-тромбоцитного крысиного антитела против CD41 мышей (MWReg30) (BD Biosciences pharmingen). Мыши в IVIG профилактической контрольной группе каждое утро получали в/б инъекцию 2 г/кг (40 мг/мышь) человеческого IVIG и MWReg30 в той же дозе, как и в ИТП контрольной группе. Определили, что IVIG обеспечивает эффективную защиту числа тромбоцитов в данной модели индуцированной ИТП, и сделали вывод, что данная модель может применяться для тестирования страдомеров в сравнении с IVIG на предмет относительной степени защиты от уменьшения числа тромбоцитов. Страдомер может быть оценен в данной модели при различных концентрациях, чтобы оценить защиту по сравнению с IVIG, следующим образом:
Группы в эксперименте
1) Контроль - нет ИТП, нет IVIG
2) ИТП контрольная группа - 2 мкг MWReg30 каждый вечер, начиная со 2-го дня
3) Группа IVIG профилактики - 4 0 мг IVIG каждое утро и 2 мкг MWReg30 каждый вечер, начиная со 2-го дня
4) Страдомер, эквивалентный 101\12 Fc-доменам IV каждое утро
5) Страдомер, эквивалентный 101\11 Fc-доменам IV каждое утро
6) Страдомер, эквивалентный 101\10 Fc-доменам IV каждое утро
7) Страдомер, эквивалентный 101\9 Fc-доменам IV каждое утро
8) Страдомер, эквивалентный 101\8 Fc-доменам IV каждое утро
9) Страдомер, эквивалентный 101\7 Fc-доменам IV каждое утро
10) Страдомер, эквивалентный 101\6 Fc-доменам IV каждое утро
Пример 14 - Оценка эффективности иммунологически активных биомиметиков in vivo при лечении ИТП
[00333] В другой мышиной модели ИТП могут использоваться мыши с дефицитом нормальной функции В-клеток. Дефицит нормальной функции В-клеток служит для устранения идиотип-антиидиотипических эффектов мышиных антител против человеческого Fc-фрагмента, которые вырабатываются при введении мыши Fc-фрагмента или неполного Fc-фрагмента человека и приводят к ложноположительным результатам. Дефицит функции В-клеток может быть вызван, например, путем введения антител против В-клеток или получен в генно-инженерных линиях мышей, таких как нокаутные мыши (Jackson Labs, линия В6.129S2-Igh6tmlCgn/J) с дефицитом зрелых В-клеток.
[00334] Иммунную систему иммунодефицитных мышей восстанавливают либо посредством немодифицированных, либо очищенных от В-клеток МПК из иммунокомпетентных животных. Затем указанных животных обрабатывают антителами к тромбоцитам, воспроизводя ИТП с использованием общеизвестных способов из уровня техники. После этого животных обрабатывают иммунологически активными биомиметиками согласно следующей схеме:
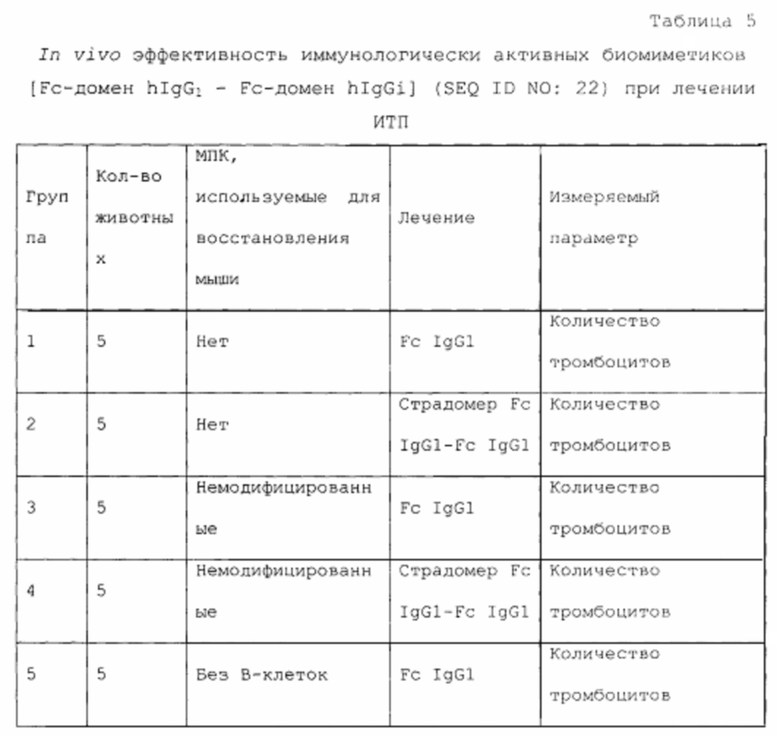

[00335] Ожидали, что в группах 1 и 2 ИТП не будет развиваться при введении антитела, поскольку в них у мышей нет В-клеток, чтобы вырабатывать антитела против тромбоцитов, необходимые для разрушения тромбоцитов. Ожидали, что в группах 3 и 4 и страдомерный полипептид {Fc hIgG1 - Fc hIgG1}, и мономерный полипептид Fc hIgG1 будут эффективно улучшать состояние при ИТП, поскольку эндогенные мышиные антитела, взаимодействуя с эпитопами Fc-домена hIgG1, перекрестно связывают мономерные полипептиды Fc hIgG1. Напротив, в отсутствие эндогенных мышиных антител страдомерный полипептид {Fc hIgG1 - Fc hIgG1} (группа 6) являлся более эффективным, чем не перекрестно-связанный мономерный полипептид Fc IgG1 (группа 5) в улучшении ИТП. Группа 7 служила положительным контролем эффекта лечения.
Пример 15 - Лечение пациентов с ИТП с использованием внутривенных форм страдомерных белков (SEQ ID NO: 18 и 22)
[00336] В схемах лечения ИТП с применением примеров страдомерных белков, кодируемых SEQ ID NO: 17 и 21, использовали методики на основе нормативных руководств для hIVIG терапии ИТП, таких как практическое руководство Исполнительного комитета американского Общества Гематологии для диагностики и терапии первичной иммунной тромбоцитопенической пурпуры. См. George, JN, et al. Idiopathic thrombocytopenic purpura: a practice guideline developed by explicit methods for the American Society of Hematology. Blood. 1996 Jul 1; 88(1): 3-40; См. также руководства педиатров гематологов Италии (2000), руководства гематологов Великобритании (2003) и руководства педиатров гематологов Японии (2006). В альтернативе, схемы применения страдомера IV при ИТП могут включать фазу начального введения дозировок, составляющих от приблизительно 0,1 до приблизительно 0,001 от вышеуказанных дозировок схемы лечения. Начальная фаза с низкой дозой предназначена для минимизации каких-либо кратковременных провоспалительных эффектов при введении страдомеров, все еще являясь достаточной, чтобы вызывать длительный противовоспалительный эффект, который впоследствии усиливается и поддерживается в ходе второй фазы стандартной дозировки, описанной выше. Обоснованием данного альтернативного подхода является то, что некоторые варианты осуществления страдомеров могут оказывать и кратковременный воспалительный эффект, и длительный противовоспалительный эффект посредством снижения экспрессии FcγRIIa. Начальная низкая доза (или начальные низкие дозы) может использоваться для стимуляции длительного противовоспалительного эффекта, минимизируя кратковременный воспалительный эффект.
[00337] Эффективная доза страдомера обычно составляет от приблизительно 0,01% до приблизительно 15% эффективной дозы hIVIG, более предпочтительно, от приблизительно 0,1% до приблизительно 3% эффективной дозы hIVIG. Эффективная доза hIVIG при ИТП обычно находится в диапазоне от приблизительно 100 мг/кг до приблизительно 2 грамм/кг, вводимых каждые 10-21 дней.
[00338] Лекарственная форма страдомера для внутривенного введения по существу является такой же, как и лекарственные формы hIVIG, одобренные FDA, однако может не содержать стабилизаторы, присутствующие в некоторых лекарственных формах hIVIG. См., например, листок-вкладыш препарата Gamrnagard S/D, распространяемого корпорацией Baxter Healthcare и одобренного FDA для терапии ИТП.
Пример 16 - Лечение пациентов с ИТП с использованием внутрибрюшинного введения кор-страдомера
[00339] Схемы лечения для ИТП с применением примеров страдомерных белков, которые представляют собой Fc-фрагменты, присоединенные к кор-группе, такой как липосома, включают внутрибрюшинное введение с дозировками, составляющими от приблизительно 1% до приблизительно 0,001% стандартных дозировок в схемах для внутривенного IVIG. Обоснованием для данного альтернативного подхода является то, что кор-страдомеры, состоящие из связанных фрагментов Fc, доставляемых в стабильной лекарственной форме внутрь брюшной полости, делают доступным воздействие множественных Fc-доменов на моноцит-производные эффекторные клетки, подобно IVIG, но в существенно более низких дозах.
Пример 17 - Конструкция иммунологически активных биомиметиков (страдотел)
[00340] Сконструировали и трансфицировали два страдотела. Для каждого страдотела на основе суммарной РНК, полученной из гибридомных клеточных линий, экспрессирущих целевое антитело, синтезировали кодирующую кДНК. Создание гибридомных клеточных линий известно в уровне техники. Амплификацию целевой кДНК, кодирующей тяжелые и легкие вариабельные области антитела, выполняли с помощью набора для амплификации BD SMART™ RACE (Clontech СА). Для получения кДНК, кодирующей тяжелые и легкие цепи вариабельных областей антител, доступны другие многочисленные методы (Sassano, М. et. al., 1994. Nucleic Acids Res. May 11; 22(9): 1768-9; Jones, S.T., Bendig, M.M., 1991. Biotechnology (NY) Jan: 9(1): 88-9). Для получения страдотела тяжелые области вариабельной цепи сливают со страдомерными конструкциями либо с помощью ПЦР с удлинением перекрывающихся фрагментов (Hutton и Pease), либо используют присутствующие совместимые сайты рестрикции для сливания соответствующих фрагментов. Страдотела экспрессировали в клетках CHO-S и выделяли из клеточных супернатантов путем аффинной очистки на колонке с А-белком. Связывание очищенного страдотела с целевым антигеном подтверждали путем анализов на связывание с помощью поточной цитометрии, используя клеточные линии, экспрессирующие антиген.
[00341] Стандартный анализ АЗКЦ с использованием NK-клеток в качестве эффекторов, а антиген-экспрессирующих опухолевых клеток в качестве мишени в различных соотношениях эффектор/мишень, применяли для сравнения эффективности страдотела и моноклонального антитела (Mab), имеющих один и тот же Fab-домен, в индукции АЗКЦ против опухолевых клеточных линий, экспрессирующих антиген с высоким и низким уровнем. Для дальнейшего совершенствования выбирали страдотела, которые демонстрировали результаты, сходные с результатами спаренного Mab в NK-анализе против клеточной линии с высоким уровнем экспрессии эпитопов, но превосходные результаты по сравнению со спаренным Mab в NK-анализе против клеточной линии с низким уровнем экспрессии эпитопов.
Пример 18 - Лечение пациентов с раком молочной железы с использованием внутривенных лекарственных форм страдотела, содержащего антигенсвязывающий домен Трастузумаба
[00342] В схемах лечения рака молочной железы с применением примера страдотела, содержащего Fab, аналогичный Fab из коммерческого препарата трастузумаб, который обладает активностью против эпитопа her2/neu, использовали методики на основе нормативных руководств для терапии рака молочной железы. См. Romond, EH et. al. Trastuzumab plus Adjuvant Chemotherapy for Operable HER2-Positive Breast Cancer. NEJM. 2005 Oct. 20; 353: 1673-1684; Seidman, AD et. al. Weekly Trastuzumab and Paclitaxel Therapy for Metastatic Breast Cancer With Analysis of Efficacy by HER2 Immunophenotype and Gene Amplification. Journal of Clinical Oncology. Vol 19, Issue 10 (May), 2001: 2587-2595; Vogel, CL et. al. Journal of Clinical Oncology. Vol 20, Issue 3 (February), 2002: 719-726
[00343] Ожидается, что эффективная доза страдотела варьирует в пределах от приблизительно 1% до приблизительно 500% эффективной дозы моноклонального антитела, Fab в котором аналогичен Fab страдотела, более предпочтительно, от приблизительно 50% до приблизительно 100% эффективной дозы моноклонального антитела. В клинической терапии рака эффективная доза моноклонального антитела варьирует. Для моноклонального антитела к Her-2 neu доза обычно находится в диапазоне от приблизительно 2 мг/кг до приблизительно 4 мг/кг, вводимых каждые 7-21 дней.
Пример 19 - Лечение пациентов с раком головы и шеи или раком толстой кишки с использованием внутривенных лекарственных форм страдотела, содержащего антигенсвязывающий домен Цетуксимаба
[00344] Ожидается, что схемы лечения рака молочной железы с применением примера страдотела, содержащего Fab, который является или аналогичен Fab из коммерческого препарата цетуксимаб, обладающий активностью против эпитопа РЭФР, включают методики на основе нормативных руководств для терапии рака головы и шеи и рака толстой кишки. См. Robert, F et. al. Phase 1 Study of Anti-Epidermal Growth Factor Receptor Antibody Cetuximab in Combination With Radiation Therapy in Patients With Advanced Head and Neck Cancer. Journal of Clinical Oncology, Vol 19, Issue 13 (July), 2001: 3234-3243; Bonner, JA et. al. Cetuximab prolongs survival in patients with locoregionally advanced squamous cell carcinoma of head and neck: A phase III study of high dose radiation therapy with or without cetuximab. Journal of Clinical Oncology, 2004 ASCO Annual Meeting Proceedings (Post-Meeting Edition). Vol 22, No 14S (July 15 Supplement), 2004: 5507; Shin, DM et. al. Epidermal Growth Factor Receptor-targeted Therapy with C225 and Cisplatin in Patients with Head and Neck Cancer. Clinical Cancer Research Vol. 7, 1204-1213, May 2001; Cunningham, D et al. Cetuximab Monotherapy and Cetuximab plus Irinotecan in I-rinotecan-Ref ractory Metastatic Colorectal Cancer. NEJM. Volume 351: 337-345, 2004.
[00345] Ожидается, что эффективная доза страдотела к РЭФР/HER1 варьирует в пределах от приблизительно 1% до приблизительно 500% эффективной дозы моноклонального антитела, Fab которого аналогичен Fab страдотела, более предпочтительно, от приблизительно 50% до приблизительно 100% эффективной дозы моноклонального антитела. В клинической терапии рака эффективная доза моноклонального антитела варьирует. Для моноклонального антитела РЭФР доза обычно находится в диапазоне приблизительно 250-400 мг/квадратный метр, что составляет приблизительно 5 мг/кг - 25 мг/кг, вводимых каждые 7-21 дней.
Пример 20 - Увеличенная мультимеризация в результате измененного гликозилирования может повысить активность иммунологически активных биомиметиков
[00346] Профили гликозилирования экспрессируемых белков зависят от клеточной линии, в которой экспрессируется белок. Клетка яичника китайского хомячка (клетка СНО), обычно используемая для экспрессии белка и очистки, дает профиль гликозилирования, который отличается, например, от гликозилирования в клетках HEK 293, которые имеют человеческое происхождение и также широко используются для экспрессии эндогенных белков. Поскольку профиль гликозилирования может влиять на свойства связывания Fc-фрагментов и кор-страдомерных единиц, увеличенная мультимеризация и, как следствие, повышенная биологическая активность экспрессируемых пептидов может быть достигнута при экспрессии в иных клеточных линиях, нежели СНО, или в клеточных линиях, включающих генетически модифицированные СНО с измененным профилем гликозилирования на N-гликане, что способствует повышенной агрегации между Fc-фрагментами или пептидами, содержащими Fc-домен. Увеличенная мультимеризация Fc-фрагмента или выбранных кластерных страдомерных единиц путем изменения профилей гликозилирования может повысить способность иммунологически активных биомиметиков к воспроизведению эффектов hIVIG.
Пример 21 - Изменяет ли IVIG или rFcF (рекомбинантные Fc-фрагменты) фенотип зрелых DC (mDC) при их обработке?
[00347] Фрагменты rFCF из человеческого IgG1, используемые в данном эксперименте, были получены с помощью стандартных методов генной инженерии белков. Каждая из двух цепей человеческого rFCF состояла из шарнирной области (15 аминокислот), СН2 домена (110 аминокислот) и СН3 домена (106 аминокислот) тяжелой цепи IgG1 человека.
[00348] CD14+ клетки могут быть выделены из мононуклеаров периферической крови (МПК), полученных из крови здоровых людей-доноров, с использованием разделительной колонки Miltenyi MACS. Клетки культивировали при конечной концентрации 2×105/мл в присутствии ГМКСФ (800 МЕ/мл) и IL-4 (5 нанограмм/мл) в течение 5 дней при 37°С. Среды во всех культурах обновляли на 3-й день культивирования. На 5-й день в подходящие культуры добавляли липополисахарид (ЛПС; 10 мкг/мл), чтобы вызвать созревание в зрелые дендритные клетки. Зрелые дендритные клетки, как известно из уровня техники, не экспрессируют существенные уровни CD16, CD32 или CD64. Затем клетки культивировали в течение еще двух дней и анализировали аликвоты на экспрессию CD11c, CD80, CD83, CD86, CD1a и CD14 посредством двумерной флюоресцентной поточной цитометрии (FFC). Затем оставшиеся клетки, культивировавшиеся с ЛПС, помещали в лунки с растворимым или иммобилизованным IVIG или человеческим rFcF (все в концентрации 10 мкг/мл) на 24 часа при 37°С, после чего собирали и анализировали экспрессию вышеуказанных маркеров с помощью двумерного FFC.
[00349] Экспериментальные группы являлись следующими:
(1) CD14+ клетки; ГМКСФ; IL-4; без ЛПС ("7d-ЛПС")
(2) CD14+ клетки: ГМКСФ; IL-4; ЛПС ("7d+ЛПС")
(3) CD14+ клетки; ГМКСФ; IL-4; ЛПС; иммоблилизованный IVIG ("cIVIG")
(4) CD14+ клетки; ГМКСФ; IL-4; ЛПС; растворимый IVIG ("sIVIG")
(5) CD14+ клетки; ГМКСФ; IL-4; ЛПС; иммоблилизованный rFcF ("cFc")
(6) CD14+ клетки; ГМКСФ; IL-4; ЛПС; растворимый rFcF ("sFc")
(7) CD14+ клетки; ГМКСФ; IL-4; ЛПС ("Контроль")
Пример 22 - Приводит ли обработка iDC иммобилизованным IVIG к ингибированию фагоцитоза опсонизированных эритроцитов?
[00350] CD14+ клетки очищали от человеческих МПК здорового человека-донора, как описано в Примере 21, и культивировали при 37°С в течение 6 дней в присутствии ГМКСФ и IL-4 в концентрациях, указанных в предыдущих примерах, а также в присутствии или отсутствие иммобилизованного или растворимого IVIG. Затем клетки собирали и инкубировали при 37°С, либо при 4°С в течение двух часов с человеческими резус-положительными (Rho+) эритроцитами, непокрытыми или покрытыми антителами против D-фактора (Rho), конъюгированными флуоресцеинизотиоцианатом (ФИТЦ). После инкубирования с эритроцитами CD14+ клетки окрашивали АФЦ-конъюгированным CD1a. Затем фагоцитоз оценивали с помощью двумерного FFC, измеряя боковое рассеяние (SSC-A), прямое рассеяние (FSC-A), флюоресценцию ФИТЦ (FITC-A) и флюоресценцию АФЦ (CDla).
Пример 23 - Приводит ли обработка иммобилизованным IVIG к уменьшению способности iDC стимулировать реакцию аллогенной смешанной культуры лимфоцитов
[00351] CD14+ клетки выделяли из крови здорового человека-донора, как описано в предыдущих примерах. Затем их культивировали при 37°С в течение 6 дней с ГМКСФ и IL-4 в присутствии или отсутствие растворимого и иммобилизованного IVIG. Концентрации всех указанных реагентов такие же, как описано выше. Затем клетки собирали и высевали в лунки 96-луночных микропланшетов для культур тканей в различной плотности (максимальная доза составляла 2,5×104 клеток в лунке). CD3+ Т-клетки очищали от МПК второго человека-донора, который являлся HLA-несовместимым с донором, от которого были получены CD14+ клетки. Т-клетки вносили в каждую лунку 96-луночных планшетов для культур тканей (105 Т-клеток на лунку). Через пять дней совместного культивирования в каждую лунку добавляли 1 мкКи 3Н-тимидина. Затем культуры инкубировали еще в течение 6 часов, после чего измеряли поглощение 3Н-тимидина ("имп/мин") как показатель степени пролиферации клеток в культурах. Тестировали три различных iDC стимуляторных популяции: одну, полученную при культивировании только с ГМКСФ и IL-4, одну, полученную при культивировании с ГМКСФ, IL-4 и иммобилизованным IVIG, и одну, полученную при культивировании с ГМКСФ, IL-4 и растворимым IVIG.
Пример 24 - Влияние обработки iDC иммобилизованными и растворимыми rFcF и IVIG на экспрессию цитокинов в iDC и mDC
[00352] Культуры, содержащие CD14+ клетки, ГМКСФ и IL-4, и либо rFcF (иммобилизованный или растворимый), либо IVIG (иммобилизованный или растворимый), выдерживали при условиях, описанных в предыдущих примерах. Вместо тестирования клеток на предмет экспрессии поверхностных клеточных маркеров оценивали фагоцитную способность или способность стимулировать аллогенные СКЛ-реакции, а также выработку цитокинов, продуцируемых клетками. Ожидалось, что иммобилизованный rFcF модулирует продукцию цитокинов в клетках аналогично IVIG, но не аналогично растворимому rFcF. Таким образом, ожидалось, что уровень цитокинов, которые ингибируют воспалительные ответы (например, интерлейкин-4, интерлейкин-6 и интерлейкин-12) повысится при обработке клеток иммобилизованным rFcF. Кроме того, ожидалось, что обработка клеток иммобилизованным rFcF приведет к уменьшению уровня выработки клетками цитокинов, которые усиливают воспалительные ответы (например, интерферон, интерлейкин-23 и фактор некроза опухолей-1).
Пример 25 - Рекомбинантные мышиные Fc-фрагменты
[00353] Рекомбинантные Fc-фрагменты (rFcF) из IgG2a мыши получали, используя стандартные методы клонирования и экспрессии рекомбинантных белков. Каждая из двух цепей мышиных rFcF состояла из шарнирной области (21 аминокислота), СН2 домена (110 аминокислот) и СН3 домена (107 аминокислот) тяжелой цепи мышиного IgG2a. Мышиный IgG2a являлся активным в анализе на iDC человека, когда был нанесен на стенки и дно лунок планшета.
[00354] Хотя настоящее изобретение и его преимущества были подробно описаны, следует понимать, что в настоящее изобретение могут быть внесены различные изменения, замены и модификации без отступления от сущности и объема изобретения, определенных в соответствии с прилагаемой формулой. Кроме того, объем настоящего заявления не должен ограничиваться конкретными вариантами осуществления способов, устройств, способов производства, композиции, средств, способов и стадий, изложенных в описании. Среднему специалисту в данной области техники из описания настоящего изобретения очевидно, что способы, устройства, способы производства, композиции, средства, способы или стадии, которые присутствуют по состоянию на данный момент или могут быть разработаны позже, выполняющие по существу ту же функцию или достигающие по существу того же результата, что и соответствующие варианты осуществления, описанные в настоящей заявке, могут применяться согласно настоящему изобретению. Таким образом, прилагаемая формула изобретения включает в себя такие способы, устройства, способы производства, композиции, средства, способы или стадии. Все патенты США и иностранные патенты, заявки на патент и непатентная литература (включающие, помимо прочего, рефераты, статьи в научных журналах, книги, товаросопроводительную литературу и руководства), упомянутые или процитированные в настоящей заявке, настоящим полностью включены путем отсылки.
СПИСОК ЛИТЕРАТУРЫ
Следующие ссылки полностью включены путем отсылки.
1. Smiley, D. & MG, Т. Southwestern internal medicine conference: High dose intravenous gamma globulin therapy: How does it work? Am JMed Sci 309, 295-303 (1995).
2. Nimmerjahn, F. & Ravetch, J.V. The antiinflammatory activity of IgG: the intravenous IgG paradox. J. Exp. Med. 204, 11-15 (2007).
3. Samuelsson, A., Towers, T.L. & Ravetch, J.V. Antiinflammatory Activity of IVIG Mediated Through the Inhibitory Fc Receptor. Science 291, 484-486 (2001).
4. Follea, G. et al. Intravenous plasmin-treated gammaglobulin therapy in idiopathic thrombocytopenic purpura. Nouv Rev Fr Hematol 27, 5-10 (1985).
5. Solal-Celigny, P., Bernard, J., Herrera, A. & Biovin, P. Treatment of adult autoimmune thrombocytopenic purpura with high-dose intravenous plasmin-cleaved gammaglobulins. Scand J Haematol 31, 39-44 (1983).
6. Debre, M. & Bonnet, M.-C. Infusion of Gcgamma fragments for treatment of children with acute immune thrombocytopenic purpura. Lancet 342, 945-49 (1993).
7. Burdach, S.E., Evers, K. & Geurson, R. Treatment of acute idiopathic thrombocytopenic purpura of childhood with intravenous immunoglobulin G: Comparative efficacy of 7S and 5S preparations. J Pediatr 109, 770-775 (1986).
8. Siragam, V. et al. Intravenous immunoglobulin ameliorates ITP via activating Fe[gamma] receptors on dendritic cells. Nat Med 12, 688 (2006).
9. Clarkson, S. et al. Treatment of refractory immune thrombocytopenic purpura with an anti-Fe gamma-receptor antibody. NEngl JMed 314, 1236-1239 (1986).
10. Bleeker, W.K. et al. Vasoactive side effects of intravenous immunoglobulin preparations in a rat model and their treatment with recombinant platelet-activating factor acetylhydrolase. Blood 95, 1856-1861 (2000).
11. Teeling, J.L. et al. Therapeutic efficacy of intravenous immunoglobulin preparations depends on the immunoglobulin G dimers: studies in experimental immune thrombocytopenia. Blood 98, 1095-1099 (2001).
12. Augener, W., Friedman, B. & Brittinger, G. Are aggregates of IgG the effective part of high-dose immunoglobulin therapy in adult idiopathic thrombocytopenic purpura (ITP)? Blut: 50, 249-252 (1985).
13. Tankersley, D.L., Preston, M.S. & Finlayson, J.S. Immunoglobulin G dimer: An idiotypeanti-idiotype complex. Molecular Immunology 25, 41 (1988).
14. Robert L. Shields, Angela K. Namenuk, Kyu Hong, Y. Gloria Meng, Julie Rae, John Briggs, Dong Xie, Jadine Lai, Andrew Stadlen, Betty Li, Judith A. Fox, and Leonard G. Presta. High Resolution Mapping of the Binding Site on Human IgG1 for FcγRI, FcγRII, FcγRIII, and FcRn and Design of IgG1 Variants with Improved Binding to the FOR J. Biol. Chem., Feb 2001; 276: 6591-6604; doi:10.1074/jbe.M009483200
15. Sondermann, P., Huber, R., Oosthuizen, V., and Jacob, U. (2000) Nature 406, 267-273
16. Robert L. Shields, Jadine Lai, Rodney Keck, Lori Y. O'Connell, Kyu Hong, Y. Gloria Meng, Stefanie H.A. Weikert, and Leonard G. Presta Lack of Fucose on Human IgG1 N-Linked Oligosaccharide Improves Binding to Human FcγRIII and Antibody-dependent Cellular Toxicity. J. Biol. Chem., Jul 2002; 277: 26733-26740; oi:10.1074/jbe.M202069200
17. Ann Wright and Sherie L. Morrison. Effect of C2-Associated Carbohydrate Structure on Ig Effector Function: Studies with Chimeric Mouse-Human IgG1 Antibodies in Glycosylation Mutants of Chinese Hamster Ovary Cells. J. Immunol., Apr 1998; 160: 3393-3402.
18. Crow AR, et al. IVIg inhibits reticuloendothelial system function and ameliorates murine passive immune thrombocytopenia independent of antiidiotype reactivity. Br J Haematol. 2001; 115: 679-686.
19. Inhibition of maturation and function of dendritic cells by intravenous immunoglobulin Jagadeesh Bayry, Sebastien Lacroix-Desmazes, Cedric Carbonneil, Namita Misra, Vladimira Donkova, Anastas Pashov, Alain Chevailler, Luc Mouthon, Bernard Weill, Patrick Bruneval, Michel D. Kazatchkine, and Srini V. Kaveri Blood 2003 101: 758-765. Prepublished online August 29, 2002; DOI 10.1182/blood-2002-05-1447
20. R. Deng and J.P. Balthasar. Comparison of the effects of antibody-coated liposomes, IVIG, and anti-RBC immunotherapy in a murine model of passive chronic immune thrombocytopenia. Blood, March 15, 2007; 109(6): 2470-2476. Prepublished online as a Blood First Edition Paper on November 28, 2006; DOI 10.1182/blood-2006-04-018093.
21. Kabat, E.A., Wu, Т.Т., Perry, H.M., Gottesman, K.S., and Foeller, C. (1991) Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda
22. U.S. Published Patent Application 20060074225.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> СТРОМ Скотт Е.
ШУЛЬЦ Дан Х.
БЛОК Дэвид С.
<120> СРЕДСТВА НА ОСНОВЕ КОНСТАНТНОЙ ОБЛАСТИ ИММУНОГЛОБУЛИНА, СВЯЗЫВАЮЩИЕ Fc-РЕЦЕПТОР
<130> 70089.0021WOU1
<150> 60/941,644
<151> 2007-06-01
<150> 61/015,547
<151> 2007-12-20
<150> 61/015,127
<151> 2007-12-19
<160> 98
<170> PatentIn version 3.4
<210> 1
<211> 699
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> домен Fc IgG1
<220>
<221> CDS
<222> (1)..(699)
<400> 1
agt gag ccc aaa tct tgt gac aaa act cac aca tgc cca ccg tgc cca 48
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
gca cct gaa ctc ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa 96
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
20 25 30
ccc aag gac acc ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg 144
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
35 40 45
gtg gtg gac gtg agc cac gaa gac cct gag gtc aag ttc aac tgg tac 192
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
50 55 60
gtg gac ggc gtg gag gtg cat aat gcc aag aca aag ccg cgg gag gag 240
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
65 70 75 80
cag tac aac agc acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac 288
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
85 90 95
cag gac tgg ctg aat ggc aag gag tac aag tgc aag gtc tcc aac aaa 336
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
100 105 110
gcc ctc cca gcc ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag 384
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
115 120 125
ccc cga gaa cca cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg 432
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
130 135 140
acc aag aac cag gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc 480
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
145 150 155 160
agc gac atc gcc gtg gag tgg gag agc aat ggg cag ccg gag aac aac 528
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
165 170 175
tac aag acc acg cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc 576
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
180 185 190
tac agc aag ctc acc gtg gac aag agc agg tgg cag cag ggg aac gtc 624
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
195 200 205
ttc tca tgc tcc gtg atg cat gag gct ctg cac aac cac tac acg cag 672
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
210 215 220
aag agc ctc tcc ctg tct ccg ggt aaa 699
Lys Ser Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 2
<211> 233
<212> Белок
<213> Homo sapiens
<400> 2
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
20 25 30
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
35 40 45
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
50 55 60
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
65 70 75 80
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
85 90 95
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
100 105 110
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
115 120 125
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
130 135 140
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
145 150 155 160
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
165 170 175
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
180 185 190
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
195 200 205
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
210 215 220
Lys Ser Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 3
<211> 684
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> домен Fc IgG2
<220>
<221> CDS
<222> (1)..(684)
<400> 3
gag cgc aaa tgt tgt gtc gag tgc cca ccg tgc cca gca cca cct gtg 48
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
gca gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag gac acc ctc 96
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
atg atc tcc cgg acc cct gag gtc acg tgc gtg gtg gtg gac gtg agc 144
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
35 40 45
cac gaa gac ccc gag gtc cag ttc aac tgg tac gtg gac ggc gtg gag 192
His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
gtg cat aat gcc aag aca aag cca cgg gag gag cag ttc aac agc acg 240
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
65 70 75 80
ttc cgt gtg gtc agc gtc ctc acc gtt gtg cac cag gac tgg ctg aac 288
Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn
85 90 95
ggc aag gag tac aag tgc aag gtc tcc aac aaa ggc ctc cca gcc ccc 336
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro
100 105 110
atc gag aaa acc atc tcc aaa acc aaa ggg cag ccc cga gaa cca cag 384
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
gtg tac acc ctg ccc cca tcc cgg gag gag atg acc aag aac cag gtc 432
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
130 135 140
agc ctg acc tgc ctg gtc aaa ggc ttc tac ccc agc gac atc gcc gtg 480
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
gag tgg gag agc aat ggg cag ccg gag aac aac tac aag acc aca cct 528
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
ccc atg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc aag ctc acc 576
Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
180 185 190
gtg gac aag agc agg tgg cag cag ggg aac gtc ttc tca tgc tcc gtg 624
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
195 200 205
atg cat gag gct ctg cac aac cac tac acg cag aag agc ctc tcc ctg 672
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
tct ccg ggt aaa 684
Ser Pro Gly Lys
225
<210> 4
<211> 228
<212> Белок
<213> Homo sapiens
<400> 4
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
35 40 45
His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
65 70 75 80
Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn
85 90 95
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro
100 105 110
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
130 135 140
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
195 200 205
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Pro Gly Lys
225
<210> 5
<211> 837
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> домен Fc IgG3
<220>
<221> CDS
<222> (1)..(837)
<400> 5
gag ctc aaa acc cca ctt ggt gac aca act cac aca tgc cca cgg tgc 48
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
cca gag ccc aaa tct tgt gac aca cct ccc ccg tgc cca cgg tgc cca 96
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
gag ccc aaa tct tgt gac aca cct ccc cca tgc cca cgg tgc cca gag 144
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
ccc aaa tct tgt gac aca cct ccc cca tgc cca cgg tgc cca gca cct 192
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Ala Pro
50 55 60
gaa ctc ctg gga gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag 240
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
65 70 75 80
gat acc ctt atg att tcc cgg acc cct gag gtc acg tgc gtg gtg gtg 288
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
85 90 95
gac gtg agc cac gaa gac ccc gag gtc cag ttc aag tgg tac gtg gac 336
Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Lys Trp Tyr Val Asp
100 105 110
ggc gtg gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag ttc 384
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
115 120 125
aac agc acg ttc cgt gtg gtc agc gtc ctc acc gtc ctg cac cag gac 432
Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
130 135 140
tgg ctg aac ggc aag gag tac aag tgc aag gtc tcc aac aaa gcc ctc 480
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
145 150 155 160
cca gcc ccc atc gag aaa acc atc tcc aaa acc aaa gga cag ccc cga 528
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg
165 170 175
gaa cca cag gtg tac acc ctg ccc cca tcc cgg gag gag atg acc aag 576
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
180 185 190
aac cag gtc agc ctg acc tgc ctg gtc aaa ggc ttc tac ccc agc gac 624
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
195 200 205
atc gcc gtg gag tgg gag agc agc ggg cag ccg gag aac aac tac aac 672
Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro Glu Asn Asn Tyr Asn
210 215 220
acc acg cct ccc atg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc 720
Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
225 230 235 240
aag ctc acc gtg gac aag agc agg tgg cag cag ggg aac atc ttc tca 768
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Ile Phe Ser
245 250 255
tgc tcc gtg atg cat gag gct ctg cac aac cgc ttc acg cag aag agc 816
Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser
260 265 270
ctc tcc ctg tct ccg ggt aaa 837
Leu Ser Leu Ser Pro Gly Lys
275
<210> 6
<211> 279
<212> Белок
<213> Homo sapiens
<400> 6
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Ala Pro
50 55 60
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
65 70 75 80
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
85 90 95
Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Lys Trp Tyr Val Asp
100 105 110
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
115 120 125
Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
130 135 140
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
145 150 155 160
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg
165 170 175
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
180 185 190
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
195 200 205
Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro Glu Asn Asn Tyr Asn
210 215 220
Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
225 230 235 240
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Ile Phe Ser
245 250 255
Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser
260 265 270
Leu Ser Leu Ser Pro Gly Lys
275
<210> 7
<211> 687
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> домен Fc IgG4
<220>
<221> CDS
<222> (1)..(687)
<400> 7
gag tcc aaa tat ggt ccc ccg tgc cca tca tgc cca gca cct gag ttc 48
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro Glu Phe
1 5 10 15
ctg ggg gga cca tca gtc ttc ctg ttc ccc cca aaa ccc aag gac act 96
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
ctc atg atc tcc cgg acc cct gag gtc acg tgc gtg gtg gtg gac gtg 144
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
agc cag gaa gac ccc gag gtc cag ttc aac tgg tac gtg gat ggc gtg 192
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag ttc aac agc 240
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
acg tac cgt gtg gtc agc gtc ctc acc gtc gtg cac cag gac tgg ctg 288
Thr Tyr Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu
85 90 95
aac ggc aag gag tac aag tgc aag gtc tcc aac aaa ggc ctc ccg tcc 336
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
tcc atc gag aaa acc atc tcc aaa gcc aaa ggg cag ccc cga gag cca 384
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
cag gtg tac acc ctg ccc cca tcc cag gag gag atg acc aag aac cag 432
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
gtc agc ctg acc tgc ctg gtc aaa ggc ttc tac ccc agc gac atc gcc 480
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
gtg gag tgg gag agc aat ggg cag ccg gag aac aac tac aag acc acg 528
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc agg cta 576
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
acc gtg gac aag agc agg tgg cag gag ggg aat gtc ttc tca tgc tcc 624
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
gtg atg cat gag gct ctg cac aac cac tac acg cag aag agc ctc tcc 672
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
ctg tct ctg ggt aaa 687
Leu Ser Leu Gly Lys
225
<210> 8
<211> 229
<212> Белок
<213> Homo sapiens
<400> 8
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys
225
<210> 9
<211> 48
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> шарнирная область IgG1
<220>
<221> CDS
<222> (1)..(48)
<400> 9
agt gag ccc aaa tct tgt gac aaa act cac aca tgc cca ccg tgc cca 48
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 10
<211> 16
<212> Белок
<213> Homo sapiens
<400> 10
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 11
<211> 36
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> шарнирная область IgG2
<220>
<221> CDS
<222> (1)..(36)
<400> 11
gag cgc aaa tgt tgt gtc gag tgc cca ccg tgc cca 36
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 12
<211> 12
<212> Белок
<213> Homo sapiens
<400> 12
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 13
<211> 186
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> шарнирная область IgG3
<220>
<221> CDS
<222> (1)..(186)
<400> 13
gag ctc aaa acc cca ctt ggt gac aca act cac aca tgc cca cgg tgc 48
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
cca gag ccc aaa tct tgt gac aca cct ccc ccg tgc cca cgg tgc cca 96
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
gag ccc aaa tct tgt gac aca cct ccc cca tgc cca cgg tgc cca gag 144
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
ccc aaa tct tgt gac aca cct ccc cca tgc cca cgg tgc cca 186
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 14
<211> 62
<212> Белок
<213> Homo sapiens
<400> 14
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 15
<211> 36
<212> ДНК
<213> Homo sapiens
<220>
<221> иной признак
<223> шарнирная область IgG4
<220>
<221> CDS
<222> (1)..(36)
<400> 15
gag tcc aaa tat ggt ccc ccg tgc cca tca tgc cca 36
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 16
<211> 12
<212> Белок
<213> Homo sapiens
<400> 16
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 17
<211> 1588
<212> ДНК
<213> Искусственная последовательность
<220>
<223> IgK/Fc IgG1/Fc IgG1
<220>
<221> CDS
<222> (45)..(1550)
<400> 17
gtcagttaag cttggtaccg agctcggatc cagtaccctt cacc atg gag aca gac 56
Met Glu Thr Asp
1
aca ctc ctg cta tgg gta ctg ctg ctc tgg gtt cca ggt tcc act ggt 104
Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly Ser Thr Gly
5 10 15 20
gac gcg gca gat atc cag cac agt ggc ggc cgc tcg agt gag ccc aaa 152
Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser Ser Glu Pro Lys
25 30 35
tct tgt gac aaa act cac aca tgc cca ccg tgc cca gca cct gaa ctc 200
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
40 45 50
ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag gac acc 248
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
55 60 65
ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg gtg gtg gac gtg 296
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
70 75 80
agc cac gaa gac cct gag gtc aag ttc aac tgg tac gtg gac ggc gtg 344
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
85 90 95 100
gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag tac aac agc 392
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
105 110 115
acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac cag gac tgg ctg 440
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
120 125 130
aat ggc aag gag tac aag tgc aag gtc tcc aac aaa gcc ctc cca gcc 488
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
135 140 145
ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag ccc cga gaa cca 536
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
150 155 160
cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg acc aag aac cag 584
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
165 170 175 180
gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc agc gac atc gcc 632
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
185 190 195
gtg gag tgg gag agc aat ggg cag ccg gag aac aac tac aag acc acg 680
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
200 205 210
cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc aag ctc 728
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
215 220 225
acc gtg gac aag agc agg tgg cag cag ggg aac gtc ttc tca tgc tcc 776
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
230 235 240
gtg atg cat gag gct ctg cac aac cac tac acg cag aag agc ctc tcc 824
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
245 250 255 260
ctg tct ccg ggt aaa agt cta gac ccc aaa tct tgt gac aaa act cac 872
Leu Ser Pro Gly Lys Ser Leu Asp Pro Lys Ser Cys Asp Lys Thr His
265 270 275
aca tgc cca ccg tgc cca gca cct gaa ctc ctg ggg gga ccg tca gtc 920
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
280 285 290
ttc ctc ttc ccc cca aaa ccc aag gac acc ctc atg atc tcc cgg acc 968
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
295 300 305
cct gag gtc aca tgc gtg gtg gtg gac gtg agc cac gaa gac cct gag 1016
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
310 315 320
gtc aag ttc aac tgg tac gtg gac ggc gtg gag gtg cat aat gcc aag 1064
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
325 330 335 340
aca aag ccg cgg gag gag cag tac aac agc acg tac cgg gtg gtc agc 1112
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
345 350 355
gtc ctc acc gtc ctg cac cag gac tgg ctg aat ggc aag gag tac aag 1160
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
360 365 370
tgc aag gtc tcc aac aaa gcc ctc cca gcc ccc atc gag aaa acc atc 1208
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
375 380 385
tcc aaa gcc aaa ggg cag ccc cga gaa cca cag gtg tac acc ctg ccc 1256
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
390 395 400
cca tcc cgg gat gag ctg acc aag aac cag gtc agc ctg acc tgc ctg 1304
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
405 410 415 420
gtc aaa ggc ttc tat ccc agc gac atc gcc gtg gag tgg gag agc aat 1352
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
425 430 435
ggg cag ccg gag aac aac tac aag acc acg cct ccc gtg ctg gac tcc 1400
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
440 445 450
gac ggc tcc ttc ttc ctc tac agc aag ctc acc gtg gac aag agc agg 1448
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
455 460 465
tgg cag cag ggg aac gtc ttc tca tgc tcc gtg atg cat gag gct ctg 1496
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
470 475 480
cac aac cac tac acg cag aag agc ctc tcc ctg tct ccg ggt aaa acc 1544
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Thr
485 490 495 500
ggt tga catcatcacc atcaccattg atgagttaaa cccgctga 1588
Gly
<210> 18
<211> 501
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 18
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys Thr Gly
500
<210> 19
<211> 952
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность мономера IgG1
<220>
<221> CDS
<222> (45)..(932)
<400> 19
gtcagttaag cttggtaccg agctcggatc cagtaccctt cacc atg gag aca gac 56
Met Glu Thr Asp
1
aca ctc ctg cta tgg gta ctg ctg ctc tgg gtt cca ggt tcc act ggt 104
Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly Ser Thr Gly
5 10 15 20
gac gcg gca gat atc cag cac agt ggc ggc cgc tcg agt gag ccc aaa 152
Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser Ser Glu Pro Lys
25 30 35
tct tgt gac aaa act cac aca tgc cca ccg tgc cca gca cct gaa ctc 200
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
40 45 50
ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag gac acc 248
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
55 60 65
ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg gtg gtg gac gtg 296
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
70 75 80
agc cac gaa gac cct gag gtc aag ttc aac tgg tac gtg gac ggc gtg 344
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
85 90 95 100
gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag tac aac agc 392
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
105 110 115
acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac cag gac tgg ctg 440
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
120 125 130
aat ggc aag gag tac aag tgc aag gtc tcc aac aaa gcc ctc cca gcc 488
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
135 140 145
ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag ccc cga gaa cca 536
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
150 155 160
cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg acc aag aac cag 584
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
165 170 175 180
gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc agc gac atc gcc 632
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
185 190 195
gtg gag tgg gag agc aat ggg cag ccg gag aac aac tac aag acc acg 680
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
200 205 210
cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc aag ctc 728
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
215 220 225
acc gtg gac aag agc agg tgg cag cag ggg aac gtc ttc tca tgc tcc 776
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
230 235 240
gtg atg cat gag gct ctg cac aac cac tac acg cag aag agc ctc tcc 824
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
245 250 255 260
ctg tct ccg ggt aaa agt cta gag ggc ccg cgg ttc gaa ggt aag cct 872
Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys Pro
265 270 275
atc cct aac cct ctc ctc ggt ctc gat tct acg cgt acc ggt cat cat 920
Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His His
280 285 290
cac cat cac cat tgatgagtta aacccgctga 952
His His His His
295
<210> 20
<211> 296
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 20
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
260 265 270
Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg
275 280 285
Thr Gly His His His His His His
290 295
<210> 21
<211> 1588
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность димера IgG1 без маркеров
<220>
<221> CDS
<222> (45)..(1550)
<400> 21
gtcagttaag cttggtaccg agctcggatc cagtaccctt cacc atg gag aca gac 56
Met Glu Thr Asp
1
aca ctc ctg cta tgg gta ctg ctg ctc tgg gtt cca ggt tcc act ggt 104
Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly Ser Thr Gly
5 10 15 20
gac gcg gca gat atc cag cac agt ggc ggc cgc tcg agt gag ccc aaa 152
Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser Ser Glu Pro Lys
25 30 35
tct tgt gac aaa act cac aca tgc cca ccg tgc cca gca cct gaa ctc 200
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
40 45 50
ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag gac acc 248
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
55 60 65
ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg gtg gtg gac gtg 296
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
70 75 80
agc cac gaa gac cct gag gtc aag ttc aac tgg tac gtg gac ggc gtg 344
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
85 90 95 100
gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag tac aac agc 392
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
105 110 115
acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac cag gac tgg ctg 440
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
120 125 130
aat ggc aag gag tac aag tgc aag gtc tcc aac aaa gcc ctc cca gcc 488
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
135 140 145
ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag ccc cga gaa cca 536
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
150 155 160
cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg acc aag aac cag 584
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
165 170 175 180
gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc agc gac atc gcc 632
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
185 190 195
gtg gag tgg gag agc aat ggg cag ccg gag aac aac tac aag acc acg 680
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
200 205 210
cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc aag ctc 728
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
215 220 225
acc gtg gac aag agc agg tgg cag cag ggg aac gtc ttc tca tgc tcc 776
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
230 235 240
gtg atg cat gag gct ctg cac aac cac tac acg cag aag agc ctc tcc 824
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
245 250 255 260
ctg tct ccg ggt aaa agt cta gac ccc aaa tct tgt gac aaa act cac 872
Leu Ser Pro Gly Lys Ser Leu Asp Pro Lys Ser Cys Asp Lys Thr His
265 270 275
aca tgc cca ccg tgc cca gca cct gaa ctc ctg ggg gga ccg tca gtc 920
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
280 285 290
ttc ctc ttc ccc cca aaa ccc aag gac acc ctc atg atc tcc cgg acc 968
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
295 300 305
cct gag gtc aca tgc gtg gtg gtg gac gtg agc cac gaa gac cct gag 1016
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
310 315 320
gtc aag ttc aac tgg tac gtg gac ggc gtg gag gtg cat aat gcc aag 1064
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
325 330 335 340
aca aag ccg cgg gag gag cag tac aac agc acg tac cgg gtg gtc agc 1112
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
345 350 355
gtc ctc acc gtc ctg cac cag gac tgg ctg aat ggc aag gag tac aag 1160
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
360 365 370
tgc aag gtc tcc aac aaa gcc ctc cca gcc ccc atc gag aaa acc atc 1208
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
375 380 385
tcc aaa gcc aaa ggg cag ccc cga gaa cca cag gtg tac acc ctg ccc 1256
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
390 395 400
cca tcc cgg gat gag ctg acc aag aac cag gtc agc ctg acc tgc ctg 1304
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
405 410 415 420
gtc aaa ggc ttc tat ccc agc gac atc gcc gtg gag tgg gag agc aat 1352
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
425 430 435
ggg cag ccg gag aac aac tac aag acc acg cct ccc gtg ctg gac tcc 1400
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
440 445 450
gac ggc tcc ttc ttc ctc tac agc aag ctc acc gtg gac aag agc agg 1448
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
455 460 465
tgg cag cag ggg aac gtc ttc tca tgc tcc gtg atg cat gag gct ctg 1496
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
470 475 480
cac aac cac tac acg cag aag agc ctc tcc ctg tct ccg ggt aaa acc 1544
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Thr
485 490 495 500
ggt tga catcatcacc atcaccattg atgagttaaa cccgctga 1588
Gly
<210> 22
<211> 501
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 22
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys Thr Gly
500
<210> 23
<211> 1636
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность димера IgG1 с эпитопными маркерами
<220>
<221> CDS
<222> (45)..(1616)
<400> 23
gtcagttaag cttggtaccg agctcggatc cagtaccctt cacc atg gag aca gac 56
Met Glu Thr Asp
1
aca ctc ctg cta tgg gta ctg ctg ctc tgg gtt cca ggt tcc act ggt 104
Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly Ser Thr Gly
5 10 15 20
gac gcg gca gat atc cag cac agt ggc ggc cgc tcg agt gag ccc aaa 152
Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser Ser Glu Pro Lys
25 30 35
tct tgt gac aaa act cac aca tgc cca ccg tgc cca gca cct gaa ctc 200
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
40 45 50
ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag gac acc 248
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
55 60 65
ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg gtg gtg gac gtg 296
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
70 75 80
agc cac gaa gac cct gag gtc aag ttc aac tgg tac gtg gac ggc gtg 344
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
85 90 95 100
gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag tac aac agc 392
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
105 110 115
acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac cag gac tgg ctg 440
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
120 125 130
aat ggc aag gag tac aag tgc aag gtc tcc aac aaa gcc ctc cca gcc 488
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
135 140 145
ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag ccc cga gaa cca 536
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
150 155 160
cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg acc aag aac cag 584
Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln
165 170 175 180
gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc agc gac atc gcc 632
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
185 190 195
gtg gag tgg gag agc aat ggg cag ccg gag aac aac tac aag acc acg 680
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
200 205 210
cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc aag ctc 728
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
215 220 225
acc gtg gac aag agc agg tgg cag cag ggg aac gtc ttc tca tgc tcc 776
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
230 235 240
gtg atg cat gag gct ctg cac aac cac tac acg cag aag agc ctc tcc 824
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
245 250 255 260
ctg tct ccg ggt aaa agt cta gac ccc aaa tct tgt gac aaa act cac 872
Leu Ser Pro Gly Lys Ser Leu Asp Pro Lys Ser Cys Asp Lys Thr His
265 270 275
aca tgc cca ccg tgc cca gca cct gaa ctc ctg ggg gga ccg tca gtc 920
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
280 285 290
ttc ctc ttc ccc cca aaa ccc aag gac acc ctc atg atc tcc cgg acc 968
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
295 300 305
cct gag gtc aca tgc gtg gtg gtg gac gtg agc cac gaa gac cct gag 1016
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
310 315 320
gtc aag ttc aac tgg tac gtg gac ggc gtg gag gtg cat aat gcc aag 1064
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
325 330 335 340
aca aag ccg cgg gag gag cag tac aac agc acg tac cgg gtg gtc agc 1112
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
345 350 355
gtc ctc acc gtc ctg cac cag gac tgg ctg aat ggc aag gag tac aag 1160
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
360 365 370
tgc aag gtc tcc aac aaa gcc ctc cca gcc ccc atc gag aaa acc atc 1208
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
375 380 385
tcc aaa gcc aaa ggg cag ccc cga gaa cca cag gtg tac acc ctg ccc 1256
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
390 395 400
cca tcc cgg gat gag ctg acc aag aac cag gtc agc ctg acc tgc ctg 1304
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
405 410 415 420
gtc aaa ggc ttc tat ccc agc gac atc gcc gtg gag tgg gag agc aat 1352
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
425 430 435
ggg cag ccg gag aac aac tac aag acc acg cct ccc gtg ctg gac tcc 1400
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
440 445 450
gac ggc tcc ttc ttc ctc tac agc aag ctc acc gtg gac aag agc agg 1448
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
455 460 465
tgg cag cag ggg aac gtc ttc tca tgc tcc gtg atg cat gag gct ctg 1496
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
470 475 480
cac aac cac tac acg cag aag agc ctc tcc ctg tct ccg ggt aaa ttc 1544
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Phe
485 490 495 500
gaa ggt aag cct atc cct aac cct ctc ctc ggt ctc gat tct acg cgt 1592
Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg
505 510 515
acc ggt cat cat cac cat cac cat tgatgagtta aacccgctga 1636
Thr Gly His His His His His His
520
<210> 24
<211> 524
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 24
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu
500 505 510
Asp Ser Thr Arg Thr Gly His His His His His His
515 520
<210> 25
<211> 1763
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность димера IgG3/IgG1 с эпитопными маркерами
<220>
<221> CDS
<222> (45)..(1760)
<400> 25
gtcagttaag cttggtaccg agctcggatc cagtaccctt cacc atg gag aca gac 56
Met Glu Thr Asp
1
aca ctc ctg cta tgg gta ctg ctg ctc tgg gtt cca ggt tcc act ggt 104
Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly Ser Thr Gly
5 10 15 20
gac gcg gca gat atc gag ctc aaa acc cca ctt ggt gac aca act cac 152
Asp Ala Ala Asp Ile Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His
25 30 35
aca tgc cca cgg tgc cca gag ccc aaa tct tgt gac aca cct ccc ccg 200
Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro
40 45 50
tgc cca cgg tgc cca gag ccc aaa tct tgt gac aca cct ccc cca tgc 248
Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys
55 60 65
cca cgg tgc cca gag ccc aaa tct tgt gac aca cct ccc cca tgc cca 296
Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro
70 75 80
cgg tgc cca gca cct gaa ctc ctg gga gga ccg tca gtc ttc ctc ttc 344
Arg Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
85 90 95 100
ccc cca aaa ccc aag gat acc ctt atg att tcc cgg acc cct gag gtc 392
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
105 110 115
acg tgc gtg gtg gtg gac gtg agc cac gaa gac ccc gag gtc cag ttc 440
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe
120 125 130
aag tgg tac gtg gac ggc gtg gag gtg cat aat gcc aag aca aag ccg 488
Lys Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
135 140 145
cgg gag gag cag ttc aac agc acg ttc cgt gtg gtc agc gtc ctc acc 536
Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr
150 155 160
gtc ctg cac cag gac tgg ctg aac ggc aag gag tac aag tgc aag gtc 584
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
165 170 175 180
tcc aac aaa gcc ctc cca gcc ccc atc gag aaa acc atc tcc aaa acc 632
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr
185 190 195
aaa gga cag ccc cga gaa cca cag gtg tac acc ctg ccc cca tcc cgg 680
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
200 205 210
gag gag atg acc aag aac cag gtc agc ctg acc tgc ctg gtc aaa ggc 728
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
215 220 225
ttc tac ccc agc gac atc gcc gtg gag tgg gag agc agc ggg cag ccg 776
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro
230 235 240
gag aac aac tac aac acc acg cct ccc atg ctg gac tcc gac ggc tcc 824
Glu Asn Asn Tyr Asn Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser
245 250 255 260
ttc ttc ctc tac agc aag ctc acc gtg gac aag agc agg tgg cag cag 872
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
265 270 275
ggg aac atc ttc tca tgc tcc gtg atg cat gag gct ctg cac aac cgc 920
Gly Asn Ile Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg
280 285 290
ttc acg cag aag agc ctc tcc ctg tct ccg ggt aaa ggc ggc cgc tcg 968
Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Gly Gly Arg Ser
295 300 305
agt gag ccc aaa tct tgt gac aaa act cac aca tgc cca ccg tgc cca 1016
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
310 315 320
gca cct gaa ctc ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa 1064
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
325 330 335 340
ccc aag gac acc ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg 1112
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
345 350 355
gtg gtg gac gtg agc cac gaa gac cct gag gtc aag ttc aac tgg tac 1160
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
360 365 370
gtg gac ggc gtg gag gtg cat aat gcc aag aca aag ccg cgg gag gag 1208
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
375 380 385
cag tac aac agc acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac 1256
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
390 395 400
cag gac tgg ctg aat ggc aag gag tac aag tgc aag gtc tcc aac aaa 1304
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
405 410 415 420
gcc ctc cca gcc ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag 1352
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
425 430 435
ccc cga gaa cca cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg 1400
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
440 445 450
acc aag aac cag gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc 1448
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
455 460 465
agc gac atc gcc gtg gag tgg gag agc aat ggg cag ccg gag aac aac 1496
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
470 475 480
tac aag acc acg cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc 1544
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
485 490 495 500
tac agc aag ctc acc gtg gac aag agc agg tgg cag cag ggg aac gtc 1592
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
505 510 515
ttc tca tgc tcc gtg atg cat gag gct ctg cac aac cac tac acg cag 1640
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
520 525 530
aag agc ctc tcc ctg tct ccg ggt aaa agt cta gag ggc ccg cgg ttc 1688
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
535 540 545
gaa ggt aag cct atc cct aac cct ctc ctc ggt ctc gat tct acg cgt 1736
Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg
550 555 560
acc ggt cat cat cac cat cac cat tga 1763
Thr Gly His His His His His His
565 570
<210> 26
<211> 572
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 26
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Leu Lys Thr Pro Leu Gly
20 25 30
Asp Thr Thr His Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp
35 40 45
Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr
50 55 60
Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro
65 70 75 80
Pro Pro Cys Pro Arg Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
85 90 95
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
100 105 110
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
115 120 125
Glu Val Gln Phe Lys Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
130 135 140
Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val
145 150 155 160
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
165 170 175
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
180 185 190
Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
195 200 205
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
210 215 220
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
225 230 235 240
Ser Gly Gln Pro Glu Asn Asn Tyr Asn Thr Thr Pro Pro Met Leu Asp
245 250 255
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
260 265 270
Arg Trp Gln Gln Gly Asn Ile Phe Ser Cys Ser Val Met His Glu Ala
275 280 285
Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
305 310 315 320
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
325 330 335
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
340 345 350
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
355 360 365
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
370 375 380
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
385 390 395 400
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
405 410 415
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
420 425 430
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
435 440 445
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
450 455 460
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
465 470 475 480
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
485 490 495
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
500 505 510
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
515 520 525
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu
530 535 540
Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu
545 550 555 560
Asp Ser Thr Arg Thr Gly His His His His His His
565 570
<210> 27
<211> 2224
<212> ДНК
<213> Искусственная последовательность
<220>
<223> слияние IgE(CH2)/IgG1(шарнир-CH2-CH3)/IgG1 (шарнир-CH2)/IgE(CH4) без
эпитопных маркеров
<220>
<221> CDS
<222> (45)..(2183)
<400> 27
gtcagttaag cttggtaccg agctcggatc cagtaccctt cacc atg gag aca gac 56
Met Glu Thr Asp
1
aca ctc ctg cta tgg gta ctg ctg ctc tgg gtt cca ggt tcc act ggt 104
Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro Gly Ser Thr Gly
5 10 15 20
gac gcg gca gat atc gtc tgc tcc agg gac ttc acc ccg ccc acc gtg 152
Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr Pro Pro Thr Val
25 30 35
aag atc tta cag tcg tcc tgc gac ggc ggc ggg cac ttc ccc ccg acc 200
Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe Pro Pro Thr
40 45 50
atc cag ctc ctg tgc ctc gtc tct ggg tac acc cca ggg act atc aac 248
Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly Thr Ile Asn
55 60 65
atc acc tgg ctg gag gac ggg cag gtc atg gac gtg gac ttg tcc acc 296
Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp Leu Ser Thr
70 75 80
gcc tct acc acg cag gag ggt gag ctg gcc tcc aca caa agc gag ctc 344
Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln Ser Glu Leu
85 90 95 100
acc ctc agc cag aag cac tgg ctg tca gac cgc acc tac acc tgc cag 392
Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr Thr Cys Gln
105 110 115
gtc acc tat caa ggt cac acc ttt gag gac agc acc aag aag tgt gca 440
Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys Lys Cys Ala
120 125 130
ggc ggc cgc tcg agt gag ccc aaa tct tgt gac aaa act cac aca tgc 488
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
135 140 145
cca ccg tgc cca gca cct gaa ctc ctg ggg gga ccg tca gtc ttc ctc 536
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
150 155 160
ttc ccc cca aaa ccc aag gac acc ctc atg atc tcc cgg acc cct gag 584
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
165 170 175 180
gtc aca tgc gtg gtg gtg gac gtg agc cac gaa gac cct gag gtc aag 632
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
185 190 195
ttc aac tgg tac gtg gac ggc gtg gag gtg cat aat gcc aag aca aag 680
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
200 205 210
ccg cgg gag gag cag tac aac agc acg tac cgg gtg gtc agc gtc ctc 728
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
215 220 225
acc gtc ctg cac cag gac tgg ctg aat ggc aag gag tac aag tgc aag 776
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
230 235 240
gtc tcc aac aaa gcc ctc cca gcc ccc atc gag aaa acc atc tcc aaa 824
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
245 250 255 260
gcc aaa ggg cag ccc cga gaa cca cag gtg tac acc ctg ccc cca tcc 872
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
265 270 275
cgg gat gag ctg acc aag aac cag gtc agc ctg acc tgc ctg gtc aaa 920
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
280 285 290
ggc ttc tat ccc agc gac atc gcc gtg gag tgg gag agc aat ggg cag 968
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
295 300 305
ccg gag aac aac tac aag acc acg cct ccc gtg ctg gac tcc gac ggc 1016
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
310 315 320
tcc ttc ttc ctc tac agc aag ctc acc gtg gac aag agc agg tgg cag 1064
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
325 330 335 340
cag ggg aac gtc ttc tca tgc tcc gtg atg cat gag gct ctg cac aac 1112
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
345 350 355
cac tac acg cag aag agc ctc tcc ctg tct ccg ggt aaa agt cta gac 1160
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp
360 365 370
ccc aaa tct tgt gac aaa act cac aca tgc cca ccg tgc cca gca cct 1208
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
375 380 385
gaa ctc ctg ggg gga ccg tca gtc ttc ctc ttc ccc cca aaa ccc aag 1256
Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
390 395 400
gac acc ctc atg atc tcc cgg acc cct gag gtc aca tgc gtg gtg gtg 1304
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
405 410 415 420
gac gtg agc cac gaa gac cct gag gtc aag ttc aac tgg tac gtg gac 1352
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
425 430 435
ggc gtg gag gtg cat aat gcc aag aca aag ccg cgg gag gag cag tac 1400
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
440 445 450
aac agc acg tac cgg gtg gtc agc gtc ctc acc gtc ctg cac cag gac 1448
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
455 460 465
tgg ctg aat ggc aag gag tac aag tgc aag gtc tcc aac aaa gcc ctc 1496
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
470 475 480
cca gcc ccc atc gag aaa acc atc tcc aaa gcc aaa ggg cag ccc cga 1544
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
485 490 495 500
gaa cca cag gtg tac acc ctg ccc cca tcc cgg gat gag ctg acc aag 1592
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
505 510 515
aac cag gtc agc ctg acc tgc ctg gtc aaa ggc ttc tat ccc agc gac 1640
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
520 525 530
atc gcc gtg gag tgg gag agc aat ggg cag ccg gag aac aac tac aag 1688
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
535 540 545
acc acg cct ccc gtg ctg gac tcc gac ggc tcc ttc ttc ctc tac agc 1736
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
550 555 560
aag ctc acc gtg gac aag agc agg tgg cag cag ggg aac gtc ttc tca 1784
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
565 570 575 580
tgc tcc gtg atg cat gag gct ctg cac aac cac tac acg cag aag agc 1832
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
585 590 595
ctc tcc ctg tct ccg ggt aaa ggc ccg cgt gct gcc ccg gaa gtc tat 1880
Leu Ser Leu Ser Pro Gly Lys Gly Pro Arg Ala Ala Pro Glu Val Tyr
600 605 610
gcg ttt gcg acg ccg gag tgg ccg ggg agc cgg gac aag cgc acc ctc 1928
Ala Phe Ala Thr Pro Glu Trp Pro Gly Ser Arg Asp Lys Arg Thr Leu
615 620 625
gcc tgc ctg atc cag aac ttc atg cct gag gac atc tcg gtg cag tgg 1976
Ala Cys Leu Ile Gln Asn Phe Met Pro Glu Asp Ile Ser Val Gln Trp
630 635 640
ctg cac aac gag gtg cag ctc ccg gac gcc cgg cac agc acg acg cag 2024
Leu His Asn Glu Val Gln Leu Pro Asp Ala Arg His Ser Thr Thr Gln
645 650 655 660
ccc cgc aag acc aag ggc tcc ggc ttc ttc gtc ttc agc cgc ctg gag 2072
Pro Arg Lys Thr Lys Gly Ser Gly Phe Phe Val Phe Ser Arg Leu Glu
665 670 675
gtg acc agg gcc gaa tgg gag cag aaa gat gag ttc atc tgc cgt gca 2120
Val Thr Arg Ala Glu Trp Glu Gln Lys Asp Glu Phe Ile Cys Arg Ala
680 685 690
gtc cat gag gca gcg agc ccc tca cag acc gtc cag cga gcg gtg tct 2168
Val His Glu Ala Ala Ser Pro Ser Gln Thr Val Gln Arg Ala Val Ser
695 700 705
gta aat ccc ggt aaa tgacatcatc accatcacca ttgatgagtt aaacccgctg a 2224
Val Asn Pro Gly Lys
710
<210> 28
<211> 713
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 28
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Ala Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Ser Leu Asp Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
370 375 380
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
385 390 395 400
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
405 410 415
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
420 425 430
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
435 440 445
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
450 455 460
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
465 470 475 480
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
485 490 495
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
500 505 510
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
515 520 525
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
530 535 540
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
545 550 555 560
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
565 570 575
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
580 585 590
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Gly Pro Arg Ala Ala
595 600 605
Pro Glu Val Tyr Ala Phe Ala Thr Pro Glu Trp Pro Gly Ser Arg Asp
610 615 620
Lys Arg Thr Leu Ala Cys Leu Ile Gln Asn Phe Met Pro Glu Asp Ile
625 630 635 640
Ser Val Gln Trp Leu His Asn Glu Val Gln Leu Pro Asp Ala Arg His
645 650 655
Ser Thr Thr Gln Pro Arg Lys Thr Lys Gly Ser Gly Phe Phe Val Phe
660 665 670
Ser Arg Leu Glu Val Thr Arg Ala Glu Trp Glu Gln Lys Asp Glu Phe
675 680 685
Ile Cys Arg Ala Val His Glu Ala Ala Ser Pro Ser Gln Thr Val Gln
690 695 700
Arg Ala Val Ser Val Asn Pro Gly Lys
705 710
<210> 29
<211> 31
<212> ДНК
<213> Искусственная последовательность
<220>
<223> праймер ПЦР
<400> 29
gtctctagag gagcccaaat cttgtgacaa a 31
<210> 30
<211> 34
<212> ДНК
<213> Искусственная последовательность
<220>
<223> праймер ПЦР
<400> 30
gcgtaccggt tcatttaccc ggggacaggg agag 34
<210> 31
<211> 603
<212> ДНК
<213> Искусственная последовательность
<220>
<223> N-концевой Fc-гамма-рецептор IIIa - фенилаланиновый полиморфный
вариант
<220>
<221> CDS
<222> (1)..(600)
<400> 31
atg tgg cag ctg ctc ctc cca act gct ctg cta ctt cta gtt tca gct 48
Met Trp Gln Leu Leu Leu Pro Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
ggc atg cgg act gaa gat ctc cca aag gct gtg gtg ttc ctg gag cct 96
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
20 25 30
caa tgg tac agg gtg ctc gag aag gac agt gtg act ctg aag tgc cag 144
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
gga gcc tac tcc cct gag gac aat tcc aca cag tgg ttt cac aat gag 192
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
50 55 60
agc ctc atc tca agc cag gcc tcg agc tac ttc att gac gct gcc aca 240
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
65 70 75 80
gtc gac gac agt gga gag tac agg tgc cag aca aac ctc tcc acc ctc 288
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
85 90 95
agt gac ccg gtg cag cta gaa gtc cat atc ggc tgg ctg ttg ctc cag 336
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
100 105 110
gcc cct cgg tgg gtg ttc aag gag gaa gac cct att cac ctg agg tgt 384
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
115 120 125
cac agc tgg aag aac act gct ctg cat aag gtc aca tat tta cag aat 432
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
130 135 140
ggc aaa ggc agg aag tat ttt cat cat aat tct gac ttc tac att cca 480
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
145 150 155 160
aaa gcc aca ctc aaa gac agc ggc tcc tac ttc tgc agg ggg ctt ttt 528
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Phe
165 170 175
ggg agt aaa aat gtg tct tca gag act gtg aac atc acc atc act caa 576
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
180 185 190
ggt ttg cat cat cac cat cat cat tag 603
Gly Leu His His His His His His
195 200
<210> 32
<211> 200
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 32
Met Trp Gln Leu Leu Leu Pro Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
20 25 30
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
50 55 60
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
65 70 75 80
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
85 90 95
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
100 105 110
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
115 120 125
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
130 135 140
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
145 150 155 160
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Phe
165 170 175
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
180 185 190
Gly Leu His His His His His His
195 200
<210> 33
<211> 603
<212> ДНК
<213> Искусственная последовательность
<220>
<223> N-концевой Fc-гамма-рецептор IIIa - валиновый полиморфный вариант
<220>
<221> CDS
<222> (1)..(600)
<400> 33
atg tgg cag ctg ctc ctc cca act gct ctg cta ctt cta gtt tca gct 48
Met Trp Gln Leu Leu Leu Pro Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
ggc atg cgg act gaa gat ctc cca aag gct gtg gtg ttc ctg gag cct 96
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
20 25 30
caa tgg tac agg gtg ctc gag aag gac agt gtg act ctg aag tgc cag 144
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
gga gcc tac tcc cct gag gac aat tcc aca cag tgg ttt cac aat gag 192
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
50 55 60
agc ctc atc tca agc cag gcc tcg agc tac ttc att gac gct gcc aca 240
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
65 70 75 80
gtc gac gac agt gga gag tac agg tgc cag aca aac ctc tcc acc ctc 288
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
85 90 95
agt gac ccg gtg cag cta gaa gtc cat atc ggc tgg ctg ttg ctc cag 336
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
100 105 110
gcc cct cgg tgg gtg ttc aag gag gaa gac cct att cac ctg agg tgt 384
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
115 120 125
cac agc tgg aag aac act gct ctg cat aag gtc aca tat tta cag aat 432
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
130 135 140
ggc aaa ggc agg aag tat ttt cat cat aat tct gac ttc tac att cca 480
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
145 150 155 160
aaa gcc aca ctc aaa gac agc ggc tcc tac ttc tgc agg ggg ctt gtt 528
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
165 170 175
ggg agt aaa aat gtg tct tca gag act gtg aac atc acc atc act caa 576
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
180 185 190
ggt ttg cat cat cac cat cat cac tag 603
Gly Leu His His His His His His
195 200
<210> 34
<211> 200
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая конструкция
<400> 34
Met Trp Gln Leu Leu Leu Pro Thr Ala Leu Leu Leu Leu Val Ser Ala
1 5 10 15
Gly Met Arg Thr Glu Asp Leu Pro Lys Ala Val Val Phe Leu Glu Pro
20 25 30
Gln Trp Tyr Arg Val Leu Glu Lys Asp Ser Val Thr Leu Lys Cys Gln
35 40 45
Gly Ala Tyr Ser Pro Glu Asp Asn Ser Thr Gln Trp Phe His Asn Glu
50 55 60
Ser Leu Ile Ser Ser Gln Ala Ser Ser Tyr Phe Ile Asp Ala Ala Thr
65 70 75 80
Val Asp Asp Ser Gly Glu Tyr Arg Cys Gln Thr Asn Leu Ser Thr Leu
85 90 95
Ser Asp Pro Val Gln Leu Glu Val His Ile Gly Trp Leu Leu Leu Gln
100 105 110
Ala Pro Arg Trp Val Phe Lys Glu Glu Asp Pro Ile His Leu Arg Cys
115 120 125
His Ser Trp Lys Asn Thr Ala Leu His Lys Val Thr Tyr Leu Gln Asn
130 135 140
Gly Lys Gly Arg Lys Tyr Phe His His Asn Ser Asp Phe Tyr Ile Pro
145 150 155 160
Lys Ala Thr Leu Lys Asp Ser Gly Ser Tyr Phe Cys Arg Gly Leu Val
165 170 175
Gly Ser Lys Asn Val Ser Ser Glu Thr Val Asn Ile Thr Ile Thr Gln
180 185 190
Gly Leu His His His His His His
195 200
<210> 35
<211> 20
<212> Белок
<213> Homo sapiens
<220>
<221> иной признак
<223> сигнальная последовательность IgK
<400> 35
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly
20
<210> 36
<211> 12
<212> Белок
<213> Homo sapiens
<400> 36
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 37
<211> 88
<212> Белок
<213> Saccharomyces cerevisiae
<400> 37
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Glu Leu Leu Gly
1 5 10 15
Gly Gly Ser Ile Lys Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser
20 25 30
Lys Ile Tyr His Ile Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile
35 40 45
Gly Glu Arg Gly His Gly Gly Gly Ser Asn Ser Gln Val Ser His Arg
50 55 60
Tyr Pro Arg Phe Gln Ser Ile Lys Val Gln Phe Thr Glu Tyr Lys Lys
65 70 75 80
Glu Lys Gly Phe Ile Leu Thr Ser
85
<210> 38
<211> 524
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 38
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Gly Gly Arg Ser Ser
20 25 30
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
35 40 45
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
50 55 60
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
65 70 75 80
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
85 90 95
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
100 105 110
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
115 120 125
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
130 135 140
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
145 150 155 160
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
165 170 175
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
180 185 190
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
195 200 205
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
210 215 220
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
225 230 235 240
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
245 250 255
Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp Glu Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu
500 505 510
Asp Ser Thr Arg Thr Gly His His His His His His
515 520
<210> 39
<211> 499
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 39
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Gly Gly Arg Ser Ser
20 25 30
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
35 40 45
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
50 55 60
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
65 70 75 80
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
85 90 95
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
100 105 110
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
115 120 125
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
130 135 140
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
145 150 155 160
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
165 170 175
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
180 185 190
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
195 200 205
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
210 215 220
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
225 230 235 240
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
245 250 255
Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Glu Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys
<210> 40
<211> 628
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 40
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Ala Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
370 375 380
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
385 390 395 400
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
405 410 415
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
420 425 430
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
435 440 445
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
450 455 460
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
465 470 475 480
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Pro
485 490 495
Arg Ala Ala Pro Glu Val Tyr Ala Phe Ala Thr Pro Glu Trp Pro Gly
500 505 510
Arg Asp Lys Arg Thr Leu Ala Cys Leu Ile Gln Asn Phe Met Pro Glu
515 520 525
Asp Ile Ser Val Gln Trp Leu His Asn Glu Val Gln Leu Pro Asp Ala
530 535 540
Arg His Ser Thr Thr Gln Pro Arg Lys Thr Lys Gly Ser Gly Phe Phe
545 550 555 560
Val Phe Ser Arg Leu Glu Val Thr Arg Ala Glu Trp Glu Gln Lys Asp
565 570 575
Glu Phe Ile Cys Arg Ala Val His Glu Ala Ala Ser Pro Ser Gln Thr
580 585 590
Val Gln Arg Ala Val Ser Val Asn Pro Gly Lys Phe Glu Gly Lys Pro
595 600 605
Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His His
610 615 620
His His His His
625
<210> 41
<211> 629
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 41
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Gly Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Ser Leu Asp Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
370 375 380
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
385 390 395 400
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
405 410 415
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
420 425 430
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
435 440 445
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
450 455 460
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
465 470 475 480
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
485 490 495
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
500 505 510
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
515 520 525
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
530 535 540
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
545 550 555 560
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
565 570 575
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
580 585 590
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Phe Glu Gly Lys
595 600 605
Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His
610 615 620
His His His His His
625
<210> 42
<211> 713
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 42
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Gly Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Ser Leu Asp Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
370 375 380
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
385 390 395 400
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
405 410 415
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
420 425 430
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
435 440 445
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
450 455 460
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
465 470 475 480
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
485 490 495
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
500 505 510
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
515 520 525
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
530 535 540
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
545 550 555 560
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
565 570 575
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
580 585 590
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Gly Pro Arg Ala
595 600 605
Ala Pro Glu Val Tyr Ala Phe Ala Thr Pro Glu Trp Pro Gly Arg Asp
610 615 620
Lys Arg Thr Leu Ala Cys Leu Ile Gln Asn Phe Met Pro Glu Asp Ile
625 630 635 640
Ser Val Gln Trp Leu His Asn Glu Val Gln Leu Pro Asp Ala Arg His
645 650 655
Ser Thr Thr Gln Pro Arg Lys Thr Lys Gly Ser Gly Phe Phe Val Phe
660 665 670
Ser Arg Leu Glu Val Thr Arg Ala Glu Trp Glu Gln Lys Asp Glu Phe
675 680 685
Ile Cys Arg Ala Val His Glu Ala Ala Ser Pro Ser Gln Thr Val Gln
690 695 700
Arg Ala Val Ser Val Asn Pro Gly Lys
705 710
<210> 43
<211> 733
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 43
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Gly Gly Arg Ser Ser
20 25 30
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
35 40 45
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
50 55 60
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
65 70 75 80
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
85 90 95
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
100 105 110
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
115 120 125
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
130 135 140
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
145 150 155 160
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
165 170 175
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
180 185 190
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
195 200 205
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
210 215 220
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
225 230 235 240
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
245 250 255
Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp Glu Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys Phe Glu Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
500 505 510
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
515 520 525
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
530 535 540
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
545 550 555 560
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
565 570 575
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
580 585 590
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
595 600 605
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
610 615 620
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
625 630 635 640
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
645 650 655
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
660 665 670
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
675 680 685
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
690 695 700
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
705 710 715 720
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
725 730
<210> 44
<211> 566
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 44
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Ser Ser Lys Pro His Leu Val
20 25 30
Thr Gln Leu Thr His Ala His Gly Cys Pro Glu Pro Lys Ser Cys Asp
35 40 45
Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr
50 55 60
Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro
65 70 75 80
Pro Pro Cys Pro Arg Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
85 90 95
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
100 105 110
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
115 120 125
Glu Val Gln Phe Lys Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
130 135 140
Lys Thr Lys Leu Arg Glu Glu Gln Tyr Asn Ser Thr Phe Arg Val Val
145 150 155 160
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
165 170 175
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
180 185 190
Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
195 200 205
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
210 215 220
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
225 230 235 240
Asn Gly Gln Pro Glu Asn Asn Tyr Asn Thr Thr Pro Pro Met Leu Asp
245 250 255
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
260 265 270
Arg Trp Gln Gln Gly Asn Ile Phe Ser Cys Ser Val Met His Glu Ala
275 280 285
Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
305 310 315 320
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
325 330 335
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
340 345 350
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
355 360 365
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
370 375 380
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
385 390 395 400
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
405 410 415
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
420 425 430
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
435 440 445
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
450 455 460
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
465 470 475 480
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
485 490 495
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
500 505 510
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
515 520 525
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Phe Glu Gly
530 535 540
Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly
545 550 555 560
His His His His His His
565
<210> 45
<211> 529
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 45
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Gly Gly Arg Ser Ser
20 25 30
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
35 40 45
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
50 55 60
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
65 70 75 80
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
85 90 95
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
100 105 110
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
115 120 125
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
130 135 140
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
145 150 155 160
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
165 170 175
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
180 185 190
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
195 200 205
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
210 215 220
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
225 230 235 240
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
245 250 255
Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe Glu
260 265 270
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
275 280 285
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
290 295 300
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
305 310 315 320
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
325 330 335
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
340 345 350
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
355 360 365
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
370 375 380
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
385 390 395 400
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
405 410 415
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
420 425 430
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
435 440 445
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
450 455 460
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
465 470 475 480
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
485 490 495
Ser Leu Ser Leu Ser Pro Gly Lys Phe Glu Gly Lys Pro Ile Pro Asn
500 505 510
Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His His His His His
515 520 525
His
<210> 46
<211> 559
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 46
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Leu Lys Thr Pro Leu Gly
20 25 30
Asp Thr Thr His Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp
35 40 45
Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr
50 55 60
Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro
65 70 75 80
Pro Pro Cys Pro Arg Cys Pro Gly Gly Arg Ser Ser Glu Pro Lys Ser
85 90 95
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
100 105 110
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
115 120 125
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
130 135 140
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
145 150 155 160
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
165 170 175
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
180 185 190
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
195 200 205
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
210 215 220
Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val
225 230 235 240
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
245 250 255
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
260 265 270
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
275 280 285
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
290 295 300
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
305 310 315 320
Ser Pro Gly Lys Ser Leu Asp Glu Pro Lys Ser Cys Asp Lys Thr His
325 330 335
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val
340 345 350
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
355 360 365
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
370 375 380
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
385 390 395 400
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
405 410 415
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
420 425 430
Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile
435 440 445
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
450 455 460
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
465 470 475 480
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
485 490 495
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
500 505 510
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
515 520 525
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
530 535 540
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
545 550 555
<210> 47
<211> 806
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 47
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Leu Lys Thr Pro Leu Gly
20 25 30
Asp Thr Thr His Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp
35 40 45
Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr
50 55 60
Pro Pro Pro Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro
65 70 75 80
Pro Pro Cys Pro Arg Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
85 90 95
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
100 105 110
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
115 120 125
Glu Val Gln Phe Lys Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
130 135 140
Lys Thr Lys Leu Arg Glu Glu Gln Tyr Asn Ser Thr Phe Arg Val Val
145 150 155 160
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
165 170 175
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
180 185 190
Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
195 200 205
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
210 215 220
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
225 230 235 240
Asn Gly Gln Pro Glu Asn Asn Tyr Asn Thr Thr Pro Pro Met Leu Asp
245 250 255
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
260 265 270
Arg Trp Gln Gln Gly Asn Ile Phe Ser Cys Ser Val Met His Glu Ala
275 280 285
Leu His Asn Arg Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
305 310 315 320
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
325 330 335
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
340 345 350
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
355 360 365
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
370 375 380
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
385 390 395 400
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
405 410 415
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
420 425 430
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
435 440 445
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
450 455 460
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
465 470 475 480
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
485 490 495
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
500 505 510
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
515 520 525
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu
530 535 540
Gly Pro Arg Phe Glu Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
545 550 555 560
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
565 570 575
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
580 585 590
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
595 600 605
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
610 615 620
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
625 630 635 640
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
645 650 655
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
660 665 670
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
675 680 685
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
690 695 700
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
705 710 715 720
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
725 730 735
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
740 745 750
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
755 760 765
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Phe Glu Gly
770 775 780
Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly
785 790 795 800
His His His His His His
805
<210> 48
<211> 394
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 48
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Asp Thr Cys Gly Glu Leu
20 25 30
Glu Phe Gln Asn Asp Glu Ile Val Lys Thr Ile Ser Val Lys Val Ile
35 40 45
Asp Asp Glu Glu Tyr Glu Lys Asn Lys Thr Phe Phe Leu Glu Ile Gly
50 55 60
Lys Pro Arg Leu Val Glu Met Ser Glu Lys Lys Ala Leu Leu Leu Asn
65 70 75 80
Glu Leu Gly Gly Phe Thr Ile Thr Gly Lys Tyr Leu Phe Gly Gln Pro
85 90 95
Val Phe Arg Lys Val His Ala Arg Glu His Pro Ile Leu Ser Thr Val
100 105 110
Ile Thr Ile Ala Asp Glu Tyr Asp Asp Lys Gln Pro Leu Thr Ser Lys
115 120 125
Glu Lys Glu Glu Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser
370 375 380
Thr Arg Thr Gly His His His His His His
385 390
<210> 49
<211> 634
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 49
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Asp Thr Cys Gly Glu Leu
20 25 30
Glu Phe Gln Asn Asp Glu Ile Val Lys Thr Ile Ser Val Lys Val Ile
35 40 45
Asp Asp Glu Glu Tyr Glu Lys Asn Lys Thr Phe Phe Leu Glu Ile Gly
50 55 60
Lys Pro Arg Leu Val Glu Met Ser Glu Lys Lys Ala Leu Leu Leu Asn
65 70 75 80
Glu Leu Gly Gly Phe Thr Ile Thr Gly Lys Tyr Leu Phe Gly Gln Pro
85 90 95
Val Phe Arg Lys Val His Ala Arg Glu His Pro Ile Leu Ser Thr Val
100 105 110
Ile Thr Ile Ala Asp Glu Tyr Asp Asp Lys Gln Pro Leu Thr Ser Lys
115 120 125
Glu Lys Glu Glu Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Ser Leu Glu Gly Pro Arg Phe Glu Glu Pro Lys Ser Cys Asp Lys
370 375 380
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
385 390 395 400
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
405 410 415
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
420 425 430
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
435 440 445
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
450 455 460
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
465 470 475 480
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
485 490 495
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
500 505 510
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
515 520 525
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
530 535 540
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
545 550 555 560
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
565 570 575
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
580 585 590
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
595 600 605
Lys Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser
610 615 620
Thr Arg Thr Gly His His His His His His
625 630
<210> 50
<211> 296
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 50
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
260 265 270
Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg
275 280 285
Thr Gly His His His His His His
290 295
<210> 51
<211> 252
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 51
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
20 25 30
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
35 40 45
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
50 55 60
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
65 70 75 80
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
85 90 95
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
100 105 110
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
115 120 125
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
130 135 140
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
145 150 155 160
Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
165 170 175
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
180 185 190
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
195 200 205
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
210 215 220
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
225 230 235 240
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
245 250
<210> 52
<211> 336
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 52
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
260 265 270
Glu Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg
275 280 285
Cys Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys
290 295 300
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
305 310 315 320
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Ala
325 330 335
<210> 53
<211> 738
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 53
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Gly Gly Arg Ser Ser
20 25 30
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
35 40 45
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
50 55 60
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
65 70 75 80
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
85 90 95
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
100 105 110
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
115 120 125
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
130 135 140
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
145 150 155 160
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr
165 170 175
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
180 185 190
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
195 200 205
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
210 215 220
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
225 230 235 240
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
245 250 255
Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Asp Glu Pro Lys Ser Cys
260 265 270
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
275 280 285
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
290 295 300
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
305 310 315 320
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
325 330 335
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
340 345 350
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
355 360 365
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
370 375 380
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
385 390 395 400
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
405 410 415
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
420 425 430
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
435 440 445
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
450 455 460
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
465 470 475 480
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
485 490 495
Pro Gly Lys Phe Glu Asp Gln Asp Ile Ala Ile Arg Val Phe Ala Ile
500 505 510
Pro Pro Ser Phe Ala Ser Ile Phe Leu Thr Lys Ser Thr Lys Leu Thr
515 520 525
Cys Leu Val Thr Asp Leu Thr Thr Tyr Asp Ser Val Thr Ile Ser Trp
530 535 540
Thr Arg Gln Asn Gly Glu Ala Val Lys Thr His Thr Asn Ile Ser Glu
545 550 555 560
Ser His Pro Asn Ala Thr Phe Ser Ala Val Gly Glu Ala Ser Ile Cys
565 570 575
Glu Asp Asp Trp Asn Ser Gly Glu Arg Phe Thr Cys Thr Val Thr His
580 585 590
Thr Asp Leu Pro Ser Pro Leu Lys Gln Thr Ile Ser Arg Pro Lys Gly
595 600 605
Val Ala Leu His Arg Pro Asp Val Tyr Leu Leu Pro Pro Ala Arg Glu
610 615 620
Gln Leu Asn Leu Arg Glu Ser Ala Thr Ile Thr Cys Leu Val Thr Gly
625 630 635 640
Phe Ser Pro Ala Asp Val Phe Val Gln Trp Met Gln Arg Gly Gln Pro
645 650 655
Leu Ser Pro Glu Lys Tyr Val Thr Ser Ala Pro Met Pro Glu Pro Gln
660 665 670
Ala Pro Gly Arg Tyr Phe Ala His Ser Ile Leu Thr Val Ser Glu Glu
675 680 685
Glu Trp Asn Thr Gly Glu Thr Tyr Thr Cys Val Val Ala His Glu Ala
690 695 700
Leu Pro Asn Arg Val Thr Glu Arg Thr Val Asp Lys Ser Thr Gly Lys
705 710 715 720
Pro Thr Leu Tyr Asn Val Ser Leu Val Met Ser Asp Thr Ala Gly Thr
725 730 735
Cys Tyr
<210> 54
<211> 510
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 54
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Gln His Ser Gly Gly Arg Ser
20 25 30
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
35 40 45
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
260 265 270
Glu Asp Gln Asp Ile Ala Ile Arg Val Phe Ala Ile Pro Pro Ser Phe
275 280 285
Ala Ser Ile Phe Leu Thr Lys Ser Thr Lys Leu Thr Cys Leu Val Thr
290 295 300
Asp Leu Thr Thr Tyr Asp Ser Val Thr Ile Ser Trp Thr Arg Gln Asn
305 310 315 320
Gly Glu Ala Val Lys Thr His Thr Asn Ile Ser Glu Ser His Pro Asn
325 330 335
Ala Thr Phe Ser Ala Val Gly Glu Ala Ser Ile Cys Glu Asp Asp Trp
340 345 350
Asn Ser Gly Glu Arg Phe Thr Cys Thr Val Thr His Thr Asp Leu Pro
355 360 365
Ser Pro Leu Lys Gln Thr Ile Ser Arg Pro Lys Gly Val Ala Leu His
370 375 380
Arg Pro Asp Val Tyr Leu Leu Pro Pro Ala Arg Glu Gln Leu Asn Leu
385 390 395 400
Arg Glu Ser Ala Thr Ile Thr Cys Leu Val Thr Gly Phe Ser Pro Ala
405 410 415
Asp Val Phe Val Gln Trp Met Gln Arg Gly Gln Pro Leu Ser Pro Glu
420 425 430
Lys Tyr Val Thr Ser Ala Pro Met Pro Glu Pro Gln Ala Pro Gly Arg
435 440 445
Tyr Phe Ala His Ser Ile Leu Thr Val Ser Glu Glu Glu Trp Asn Thr
450 455 460
Gly Glu Thr Tyr Thr Cys Val Val Ala His Glu Ala Leu Pro Asn Arg
465 470 475 480
Val Thr Glu Arg Thr Val Asp Lys Ser Thr Gly Lys Pro Thr Leu Tyr
485 490 495
Asn Val Ser Leu Val Met Ser Asp Thr Ala Gly Thr Cys Tyr
500 505 510
<210> 55
<211> 394
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 55
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Gly Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys
130 135 140
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
145 150 155 160
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
165 170 175
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
180 185 190
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
195 200 205
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
210 215 220
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
225 230 235 240
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
245 250 255
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
260 265 270
Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr
275 280 285
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
290 295 300
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
305 310 315 320
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
325 330 335
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
340 345 350
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
355 360 365
Lys Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser
370 375 380
Thr Arg Thr Gly His His His His His His
385 390
<210> 56
<211> 362
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 56
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Val Cys Ser Arg Asp Phe Thr Pro Pro Thr Val Lys
20 25 30
Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe Pro Pro Thr Ile
35 40 45
Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly Thr Ile Asn Ile
50 55 60
Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp Leu Ser Thr Ala
65 70 75 80
Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln Ser Glu Leu Thr
85 90 95
Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr Thr Cys Gln Val
100 105 110
Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys Lys Cys Glu Pro
115 120 125
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
130 135 140
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
145 150 155 160
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
165 170 175
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
180 185 190
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
195 200 205
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
210 215 220
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
225 230 235 240
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
245 250 255
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn
260 265 270
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
275 280 285
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
290 295 300
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
305 310 315 320
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
325 330 335
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
340 345 350
Ser Leu Ser Pro Gly Lys Phe Glu Gly Lys
355 360
<210> 57
<211> 519
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 57
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Arg Lys Cys Cys Val Glu
20 25 30
Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu
35 40 45
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
50 55 60
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln
65 70 75 80
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
85 90 95
Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu
100 105 110
Thr Val Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
115 120 125
Val Ser Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
130 135 140
Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
145 150 155 160
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
165 170 175
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
180 185 190
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly
195 200 205
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
210 215 220
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
225 230 235 240
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Arg Ser Ser
245 250 255
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
260 265 270
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
275 280 285
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
290 295 300
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
305 310 315 320
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
325 330 335
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
340 345 350
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
355 360 365
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
370 375 380
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
385 390 395 400
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
405 410 415
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
420 425 430
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
435 440 445
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
450 455 460
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
465 470 475 480
Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe Glu
485 490 495
Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr
500 505 510
Gly His His His His His His
515
<210> 58
<211> 488
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 58
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Arg Lys Cys Cys Val Glu
20 25 30
Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu
35 40 45
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
50 55 60
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln
65 70 75 80
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
85 90 95
Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu
100 105 110
Thr Val Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
115 120 125
Val Ser Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
130 135 140
Thr Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
145 150 155 160
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
165 170 175
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
180 185 190
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly
195 200 205
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
210 215 220
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
225 230 235 240
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Arg Ser Ser
245 250 255
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
260 265 270
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
275 280 285
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
290 295 300
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
305 310 315 320
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
325 330 335
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
340 345 350
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
355 360 365
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
370 375 380
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
385 390 395 400
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
405 410 415
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
420 425 430
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
435 440 445
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
450 455 460
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
465 470 475 480
Ser Leu Ser Leu Ser Pro Gly Lys
485
<210> 59
<211> 303
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 59
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Arg Lys Cys Cys Val Glu
20 25 30
Cys Pro Pro Cys Pro Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
35 40 45
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
50 55 60
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
65 70 75 80
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
85 90 95
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
100 105 110
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
115 120 125
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
130 135 140
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
145 150 155 160
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
165 170 175
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
180 185 190
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
195 200 205
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
210 215 220
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
225 230 235 240
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
245 250 255
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
260 265 270
Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu
275 280 285
Leu Gly Leu Asp Ser Thr Arg Thr Gly His His His His His His
290 295 300
<210> 60
<211> 272
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 60
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Arg Lys Cys Cys Val Glu
20 25 30
Cys Pro Pro Cys Pro Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
35 40 45
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
50 55 60
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
65 70 75 80
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
85 90 95
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
100 105 110
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
115 120 125
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
130 135 140
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
145 150 155 160
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
165 170 175
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
180 185 190
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
195 200 205
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
210 215 220
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
225 230 235 240
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
245 250 255
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
260 265 270
<210> 61
<211> 264
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 61
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
35 40 45
Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
50 55 60
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
65 70 75 80
Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val
85 90 95
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
100 105 110
Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
115 120 125
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala
130 135 140
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
145 150 155 160
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr
165 170 175
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
180 185 190
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
195 200 205
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
210 215 220
Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe
225 230 235 240
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
245 250 255
Ser Leu Ser Leu Ser Pro Gly Lys
260
<210> 62
<211> 538
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 62
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Arg Lys Cys Cys Val Glu
20 25 30
Cys Pro Pro Cys Pro Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
35 40 45
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
50 55 60
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
65 70 75 80
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
85 90 95
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
100 105 110
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
115 120 125
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
130 135 140
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
145 150 155 160
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
165 170 175
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
180 185 190
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
195 200 205
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
210 215 220
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
225 230 235 240
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
245 250 255
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
260 265 270
Ser Leu Asp Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
275 280 285
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
290 295 300
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
305 310 315 320
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
325 330 335
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
340 345 350
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
355 360 365
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
370 375 380
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
385 390 395 400
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
405 410 415
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
420 425 430
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
435 440 445
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
450 455 460
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
465 470 475 480
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
485 490 495
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro
500 505 510
Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser
515 520 525
Thr Arg Thr Gly His His His His His His
530 535
<210> 63
<211> 507
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 63
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Glu Arg Lys Cys Cys Val Glu
20 25 30
Cys Pro Pro Cys Pro Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
35 40 45
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
50 55 60
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
65 70 75 80
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
85 90 95
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
100 105 110
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
115 120 125
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
130 135 140
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
145 150 155 160
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
165 170 175
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
180 185 190
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
195 200 205
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
210 215 220
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
225 230 235 240
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
245 250 255
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
260 265 270
Ser Leu Asp Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
275 280 285
Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro
290 295 300
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
305 310 315 320
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
325 330 335
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
340 345 350
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
355 360 365
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
370 375 380
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
385 390 395 400
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
405 410 415
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
420 425 430
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
435 440 445
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
450 455 460
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
465 470 475 480
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
485 490 495
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
500 505
<210> 64
<211> 511
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 64
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Gly Gly Gly Asp Ile Val Cys Ser Arg Asp Phe Thr Pro
130 135 140
Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe
145 150 155 160
Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly
165 170 175
Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp
180 185 190
Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln
195 200 205
Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr
210 215 220
Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys
225 230 235 240
Lys Cys Gly Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
245 250 255
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
260 265 270
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
275 280 285
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
290 295 300
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
305 310 315 320
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
325 330 335
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
340 345 350
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
355 360 365
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
370 375 380
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
385 390 395 400
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
405 410 415
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
420 425 430
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
435 440 445
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
450 455 460
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
465 470 475 480
Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu
485 490 495
Leu Gly Leu Asp Ser Thr Arg Thr Gly His His His His His His
500 505 510
<210> 65
<211> 480
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 65
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Val Cys Ser Arg Asp Phe Thr
20 25 30
Pro Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His
35 40 45
Phe Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro
50 55 60
Gly Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val
65 70 75 80
Asp Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr
85 90 95
Gln Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr
100 105 110
Tyr Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr
115 120 125
Lys Lys Cys Gly Gly Gly Asp Ile Val Cys Ser Arg Asp Phe Thr Pro
130 135 140
Pro Thr Val Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe
145 150 155 160
Pro Pro Thr Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly
165 170 175
Thr Ile Asn Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp
180 185 190
Leu Ser Thr Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln
195 200 205
Ser Glu Leu Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr
210 215 220
Thr Cys Gln Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys
225 230 235 240
Lys Cys Gly Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
245 250 255
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
260 265 270
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
275 280 285
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
290 295 300
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
305 310 315 320
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
325 330 335
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
340 345 350
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
355 360 365
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
370 375 380
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
385 390 395 400
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
405 410 415
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
420 425 430
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
435 440 445
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
450 455 460
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
465 470 475 480
<210> 66
<211> 332
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 66
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Gly Gly Gly Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
65 70 75 80
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
85 90 95
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
100 105 110
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
115 120 125
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
130 135 140
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
145 150 155 160
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
165 170 175
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
180 185 190
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
195 200 205
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
210 215 220
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
225 230 235 240
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
245 250 255
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
260 265 270
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
275 280 285
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu
290 295 300
Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu
305 310 315 320
Asp Ser Thr Arg Thr Gly His His His His His His
325 330
<210> 67
<211> 301
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 67
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Gly Gly Gly Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
65 70 75 80
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
85 90 95
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
100 105 110
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
115 120 125
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
130 135 140
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
145 150 155 160
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
165 170 175
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
180 185 190
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
195 200 205
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
210 215 220
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
225 230 235 240
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
245 250 255
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
260 265 270
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
275 280 285
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
290 295 300
<210> 68
<211> 444
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 68
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Gly Gly Gly Asp Ile Val Cys Ser Arg Asp Phe Thr Pro Pro Thr Val
65 70 75 80
Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe Pro Pro Thr
85 90 95
Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly Thr Ile Asn
100 105 110
Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp Leu Ser Thr
115 120 125
Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln Ser Glu Leu
130 135 140
Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr Thr Cys Gln
145 150 155 160
Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys Lys Cys Gly
165 170 175
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
180 185 190
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
195 200 205
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
210 215 220
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
225 230 235 240
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
245 250 255
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
260 265 270
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
275 280 285
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
290 295 300
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
305 310 315 320
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
325 330 335
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
340 345 350
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
355 360 365
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
370 375 380
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
385 390 395 400
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu
405 410 415
Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu
420 425 430
Asp Ser Thr Arg Thr Gly His His His His His His
435 440
<210> 69
<211> 413
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 69
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Gly Gly Gly Asp Ile Val Cys Ser Arg Asp Phe Thr Pro Pro Thr Val
65 70 75 80
Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe Pro Pro Thr
85 90 95
Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly Thr Ile Asn
100 105 110
Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp Leu Ser Thr
115 120 125
Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln Ser Glu Leu
130 135 140
Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr Thr Cys Gln
145 150 155 160
Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys Lys Cys Gly
165 170 175
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
180 185 190
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
195 200 205
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
210 215 220
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
225 230 235 240
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
245 250 255
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
260 265 270
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
275 280 285
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
290 295 300
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
305 310 315 320
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
325 330 335
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
340 345 350
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
355 360 365
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
370 375 380
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
385 390 395 400
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
405 410
<210> 70
<211> 565
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 70
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Ile Leu Gly Gly Gly Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro
65 70 75 80
Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro
85 90 95
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
100 105 110
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn
115 120 125
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
130 135 140
Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val
145 150 155 160
Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
165 170 175
Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys
180 185 190
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
195 200 205
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
210 215 220
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
225 230 235 240
Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe
245 250 255
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
260 265 270
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
275 280 285
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Arg Ser Ser Glu Pro
290 295 300
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
305 310 315 320
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
325 330 335
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
340 345 350
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
355 360 365
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
370 375 380
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
385 390 395 400
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
405 410 415
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
420 425 430
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
435 440 445
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
450 455 460
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
465 470 475 480
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
485 490 495
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
500 505 510
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
515 520 525
Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys
530 535 540
Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His
545 550 555 560
His His His His His
565
<210> 71
<211> 534
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 71
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Ile Leu Gly Gly Gly Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro
65 70 75 80
Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro
85 90 95
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
100 105 110
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn
115 120 125
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
130 135 140
Glu Glu Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val
145 150 155 160
Val His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
165 170 175
Asn Lys Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys
180 185 190
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
195 200 205
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
210 215 220
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
225 230 235 240
Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe
245 250 255
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
260 265 270
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
275 280 285
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Arg Ser Ser Glu Pro
290 295 300
Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu
305 310 315 320
Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
325 330 335
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
340 345 350
Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
355 360 365
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
370 375 380
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
385 390 395 400
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
405 410 415
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
420 425 430
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn
435 440 445
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
450 455 460
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
465 470 475 480
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
485 490 495
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
500 505 510
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
515 520 525
Ser Leu Ser Pro Gly Lys
530
<210> 72
<211> 344
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 72
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Arg Ser
65 70 75 80
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
85 90 95
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
100 105 110
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
115 120 125
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
130 135 140
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
145 150 155 160
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
165 170 175
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
180 185 190
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
195 200 205
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
210 215 220
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
225 230 235 240
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
245 250 255
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
260 265 270
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
275 280 285
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
290 295 300
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
305 310 315 320
Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg
325 330 335
Thr Gly His His His His His His
340
<210> 73
<211> 313
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 73
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Arg Ser
65 70 75 80
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
85 90 95
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
100 105 110
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
115 120 125
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
130 135 140
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
145 150 155 160
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
165 170 175
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
180 185 190
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
195 200 205
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
210 215 220
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
225 230 235 240
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
245 250 255
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
260 265 270
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
275 280 285
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
290 295 300
Lys Ser Leu Ser Leu Ser Pro Gly Lys
305 310
<210> 74
<211> 372
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 74
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Ile Leu Gly Gly Gly Ser Ile Lys Gln Ile Glu Asp Lys Ile Glu Glu
65 70 75 80
Ile Leu Ser Lys Ile Tyr His Ile Glu Asn Glu Ile Ala Arg Ile Lys
85 90 95
Lys Leu Ile Gly Glu Arg Gly His Gly Gly Gly Ser Ser Glu Pro Lys
100 105 110
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
115 120 125
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
130 135 140
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
145 150 155 160
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
165 170 175
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
180 185 190
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
195 200 205
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
210 215 220
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
225 230 235 240
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
245 250 255
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
260 265 270
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
275 280 285
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
290 295 300
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
305 310 315 320
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
325 330 335
Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys Pro
340 345 350
Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His His
355 360 365
His His His His
370
<210> 75
<211> 341
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 75
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Asp Ile Leu Gly Gly Gly Ser Ile Lys
20 25 30
Gln Ile Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile
35 40 45
Glu Asn Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His
50 55 60
Ile Leu Gly Gly Gly Ser Ile Lys Gln Ile Glu Asp Lys Ile Glu Glu
65 70 75 80
Ile Leu Ser Lys Ile Tyr His Ile Glu Asn Glu Ile Ala Arg Ile Lys
85 90 95
Lys Leu Ile Gly Glu Arg Gly His Gly Gly Gly Ser Ser Glu Pro Lys
100 105 110
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu
115 120 125
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
130 135 140
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
145 150 155 160
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
165 170 175
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
180 185 190
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
195 200 205
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
210 215 220
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
225 230 235 240
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
245 250 255
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
260 265 270
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
275 280 285
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
290 295 300
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
305 310 315 320
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
325 330 335
Leu Ser Pro Gly Lys
340
<210> 76
<211> 412
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 76
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Val Cys Ser Arg Asp Phe Thr Pro Pro Thr Val
35 40 45
Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe Pro Pro Thr
50 55 60
Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly Thr Ile Asn
65 70 75 80
Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp Leu Ser Thr
85 90 95
Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln Ser Glu Leu
100 105 110
Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr Thr Cys Gln
115 120 125
Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys Lys Cys Gly
130 135 140
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
145 150 155 160
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
165 170 175
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
180 185 190
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
195 200 205
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
210 215 220
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
225 230 235 240
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
245 250 255
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
260 265 270
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
275 280 285
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
290 295 300
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
305 310 315 320
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
325 330 335
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
340 345 350
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
355 360 365
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu
370 375 380
Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu
385 390 395 400
Asp Ser Thr Arg Thr Gly His His His His His His
405 410
<210> 77
<211> 381
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 77
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Val Cys Ser Arg Asp Phe Thr Pro Pro Thr Val
35 40 45
Lys Ile Leu Gln Ser Ser Cys Asp Gly Gly Gly His Phe Pro Pro Thr
50 55 60
Ile Gln Leu Leu Cys Leu Val Ser Gly Tyr Thr Pro Gly Thr Ile Asn
65 70 75 80
Ile Thr Trp Leu Glu Asp Gly Gln Val Met Asp Val Asp Leu Ser Thr
85 90 95
Ala Ser Thr Thr Gln Glu Gly Glu Leu Ala Ser Thr Gln Ser Glu Leu
100 105 110
Thr Leu Ser Gln Lys His Trp Leu Ser Asp Arg Thr Tyr Thr Cys Gln
115 120 125
Val Thr Tyr Gln Gly His Thr Phe Glu Asp Ser Thr Lys Lys Cys Gly
130 135 140
Gly Gly Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
145 150 155 160
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
165 170 175
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
180 185 190
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
195 200 205
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
210 215 220
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
225 230 235 240
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
245 250 255
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
260 265 270
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
275 280 285
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
290 295 300
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
305 310 315 320
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
325 330 335
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
340 345 350
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
355 360 365
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
370 375 380
<210> 78
<211> 575
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 78
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Leu Gly Gly Gly Ser Ile Lys Gln Ile Glu Asp
35 40 45
Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile Glu Asn Glu Ile
50 55 60
Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His Gly Gly Gly Ser
65 70 75 80
Ser Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro
85 90 95
Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
100 105 110
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
115 120 125
Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
130 135 140
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
145 150 155 160
Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu
165 170 175
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala
180 185 190
Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro
195 200 205
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
210 215 220
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
225 230 235 240
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
245 250 255
Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
260 265 270
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
275 280 285
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
290 295 300
Leu Ser Pro Gly Lys Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
305 310 315 320
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
325 330 335
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
340 345 350
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
355 360 365
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
370 375 380
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
385 390 395 400
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
405 410 415
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
420 425 430
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
435 440 445
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
450 455 460
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
465 470 475 480
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
485 490 495
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
500 505 510
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
515 520 525
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
530 535 540
Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu
545 550 555 560
Leu Gly Leu Asp Ser Thr Arg Thr Gly His His His His His His
565 570 575
<210> 79
<211> 544
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 79
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Leu Gly Gly Gly Ser Ile Lys Gln Ile Glu Asp
35 40 45
Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile Glu Asn Glu Ile
50 55 60
Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His Gly Gly Gly Ser
65 70 75 80
Ser Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro
85 90 95
Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
100 105 110
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
115 120 125
Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
130 135 140
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
145 150 155 160
Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu
165 170 175
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala
180 185 190
Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro
195 200 205
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
210 215 220
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
225 230 235 240
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
245 250 255
Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
260 265 270
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
275 280 285
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
290 295 300
Leu Ser Pro Gly Lys Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr
305 310 315 320
His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser
325 330 335
Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg
340 345 350
Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro
355 360 365
Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala
370 375 380
Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val
385 390 395 400
Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr
405 410 415
Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr
420 425 430
Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu
435 440 445
Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys
450 455 460
Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser
465 470 475 480
Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp
485 490 495
Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser
500 505 510
Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala
515 520 525
Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
530 535 540
<210> 80
<211> 315
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 80
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
35 40 45
Pro Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
50 55 60
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
65 70 75 80
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
85 90 95
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
100 105 110
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
115 120 125
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
130 135 140
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
145 150 155 160
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
165 170 175
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
180 185 190
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
195 200 205
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
210 215 220
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
225 230 235 240
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
245 250 255
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
260 265 270
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly
275 280 285
Pro Arg Phe Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp
290 295 300
Ser Thr Arg Thr Gly His His His His His His
305 310 315
<210> 81
<211> 284
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 81
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
35 40 45
Pro Arg Ser Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro
50 55 60
Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe
65 70 75 80
Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val
85 90 95
Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe
100 105 110
Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro
115 120 125
Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr
130 135 140
Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val
145 150 155 160
Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala
165 170 175
Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg
180 185 190
Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly
195 200 205
Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro
210 215 220
Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser
225 230 235 240
Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln
245 250 255
Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His
260 265 270
Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
275 280
<210> 82
<211> 344
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 82
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Leu Gly Gly Gly Ser Ile Lys Gln Ile Glu Asp
35 40 45
Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile Glu Asn Glu Ile
50 55 60
Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His Gly Gly Gly Ser
65 70 75 80
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
85 90 95
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
100 105 110
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
115 120 125
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
130 135 140
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
145 150 155 160
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
165 170 175
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
180 185 190
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
195 200 205
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
210 215 220
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
225 230 235 240
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
245 250 255
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
260 265 270
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
275 280 285
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
290 295 300
Lys Ser Leu Ser Leu Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe
305 310 315 320
Glu Gly Lys Pro Ile Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg
325 330 335
Thr Gly His His His His His His
340
<210> 83
<211> 313
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 83
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Leu Gly Gly Gly Ser Ile Lys Gln Ile Glu Asp
35 40 45
Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile Glu Asn Glu Ile
50 55 60
Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly His Gly Gly Gly Ser
65 70 75 80
Ser Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
85 90 95
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
100 105 110
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
115 120 125
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
130 135 140
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
145 150 155 160
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
165 170 175
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
180 185 190
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
195 200 205
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
210 215 220
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
225 230 235 240
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
245 250 255
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
260 265 270
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
275 280 285
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
290 295 300
Lys Ser Leu Ser Leu Ser Pro Gly Lys
305 310
<210> 84
<211> 531
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 84
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
35 40 45
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Arg Ser Ser Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly Lys Ser Leu Glu Gly Pro Arg Phe Glu Gly Lys Pro Ile
500 505 510
Pro Asn Pro Leu Leu Gly Leu Asp Ser Thr Arg Thr Gly His His His
515 520 525
His His His
530
<210> 85
<211> 500
<212> Белок
<213> Искусственная последовательность
<220>
<223> химически синтезированный страдомерный мономер
<400> 85
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp Ala Ala Glu Arg Lys Cys Cys Val Glu Cys Pro
20 25 30
Pro Cys Pro Asp Ile Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys
35 40 45
Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
50 55 60
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
65 70 75 80
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
85 90 95
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
100 105 110
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His
115 120 125
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
130 135 140
Gly Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln
145 150 155 160
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
165 170 175
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
180 185 190
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
195 200 205
Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu
210 215 220
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
225 230 235 240
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
245 250 255
Lys Ser Leu Ser Leu Ser Pro Gly Lys Arg Ser Ser Glu Pro Lys Ser
260 265 270
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu
275 280 285
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
290 295 300
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
305 310 315 320
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
325 330 335
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
340 345 350
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
355 360 365
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
370 375 380
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
385 390 395 400
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
405 410 415
Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
420 425 430
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
435 440 445
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
450 455 460
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
465 470 475 480
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
485 490 495
Ser Pro Gly Lys
500
<210> 86
<211> 159
<212> Белок
<213> Homo sapiens
<400> 86
Met Lys Asn His Leu Leu Phe Trp Gly Val Leu Ala Val Phe Ile Lys
1 5 10 15
Ala Val His Val Lys Ala Gln Glu Asp Glu Arg Ile Val Leu Val Asp
20 25 30
Asn Lys Cys Lys Cys Ala Arg Ile Thr Ser Arg Ile Ile Arg Ser Ser
35 40 45
Glu Asp Pro Asn Glu Asp Ile Val Glu Arg Asn Ile Arg Ile Ile Val
50 55 60
Pro Leu Asn Asn Arg Glu Asn Ile Ser Asp Pro Thr Ser Pro Leu Arg
65 70 75 80
Thr Arg Phe Val Tyr His Leu Ser Asp Leu Cys Lys Lys Cys Asp Pro
85 90 95
Thr Glu Val Glu Leu Asp Asn Gln Ile Val Thr Ala Thr Gln Ser Asn
100 105 110
Ile Cys Asp Glu Asp Ser Ala Thr Glu Thr Cys Tyr Thr Tyr Asp Arg
115 120 125
Asn Lys Cys Tyr Thr Ala Val Val Pro Leu Val Tyr Gly Gly Glu Thr
130 135 140
Lys Met Val Glu Thr Ala Leu Thr Pro Asp Ala Cys Tyr Pro Asp
145 150 155
<210> 87
<211> 15
<212> Белок
<213> Homo sapiens
<400> 87
Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
1 5 10 15
<210> 88
<211> 110
<212> Белок
<213> Homo sapiens
<400> 88
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 89
<211> 107
<212> Белок
<213> Homo sapiens
<400> 89
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp
1 5 10 15
Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
100 105
<210> 90
<211> 11
<212> Белок
<213> Homo sapiens
<400> 90
Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro
1 5 10
<210> 91
<211> 109
<212> Белок
<213> Homo sapiens
<400> 91
Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
1 5 10 15
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
20 25 30
Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
35 40 45
Asp Gly Met Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
50 55 60
Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Val His Gln
65 70 75 80
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
85 90 95
Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys
100 105
<210> 92
<211> 107
<212> Белок
<213> Homo sapiens
<400> 92
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
1 5 10 15
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
100 105
<210> 93
<211> 62
<212> Белок
<213> Homo sapiens
<400> 93
Glu Leu Lys Thr Pro Leu Gly Asp Thr Thr His Thr Cys Pro Arg Cys
1 5 10 15
Pro Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
20 25 30
Glu Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro Glu
35 40 45
Pro Lys Ser Cys Asp Thr Pro Pro Pro Cys Pro Arg Cys Pro
50 55 60
<210> 94
<211> 110
<212> Белок
<213> Homo sapiens
<400> 94
Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser His Glu Asp Pro Glu Val Gln Phe Lys Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Phe Asn Ser Thr Phe Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys
100 105 110
<210> 95
<211> 107
<212> Белок
<213> Homo sapiens
<400> 95
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
1 5 10 15
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Ser Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Asn Thr Thr Pro Pro Met Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
65 70 75 80
Asn Ile Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn Arg Phe
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
100 105
<210> 96
<211> 12
<212> Белок
<213> Homo sapiens
<400> 96
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro
1 5 10
<210> 97
<211> 110
<212> Белок
<213> Homo sapiens
<400> 97
Ala Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
1 5 10 15
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
20 25 30
Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr
35 40 45
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
50 55 60
Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
65 70 75 80
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
85 90 95
Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
100 105 110
<210> 98
<211> 107
<212> Белок
<213> Homo sapiens
<400> 98
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
1 5 10 15
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
20 25 30
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
35 40 45
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
50 55 60
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
65 70 75 80
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
85 90 95
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
100 105
<---
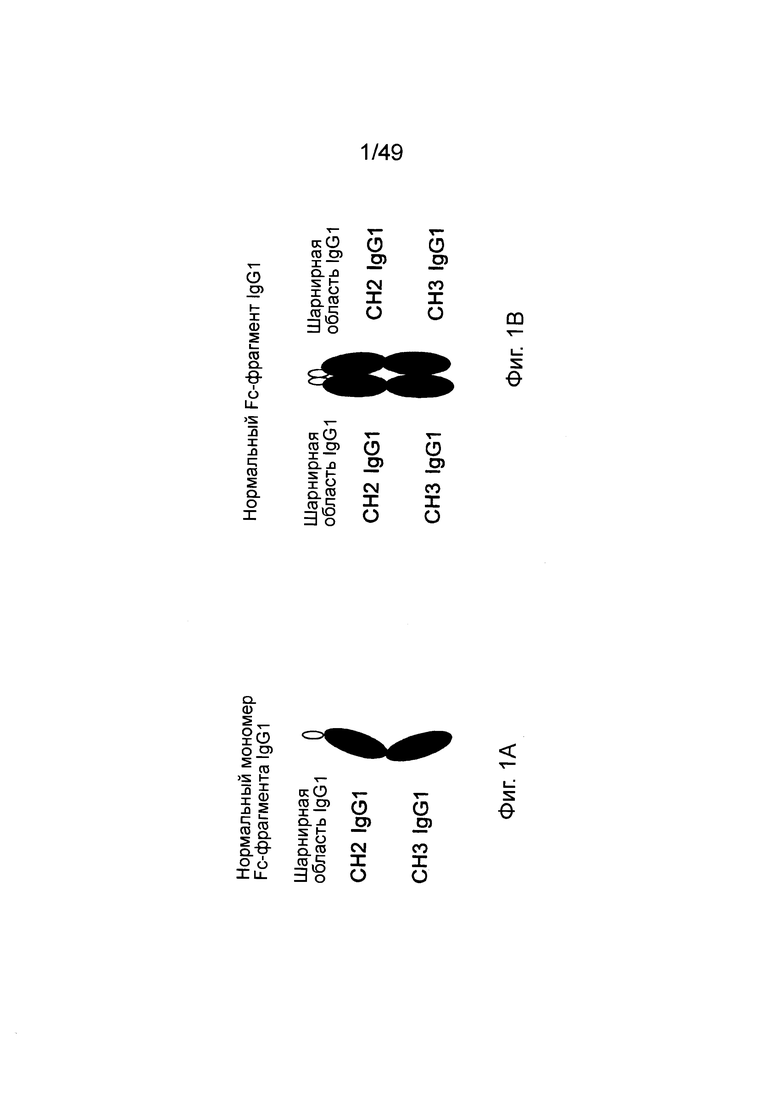
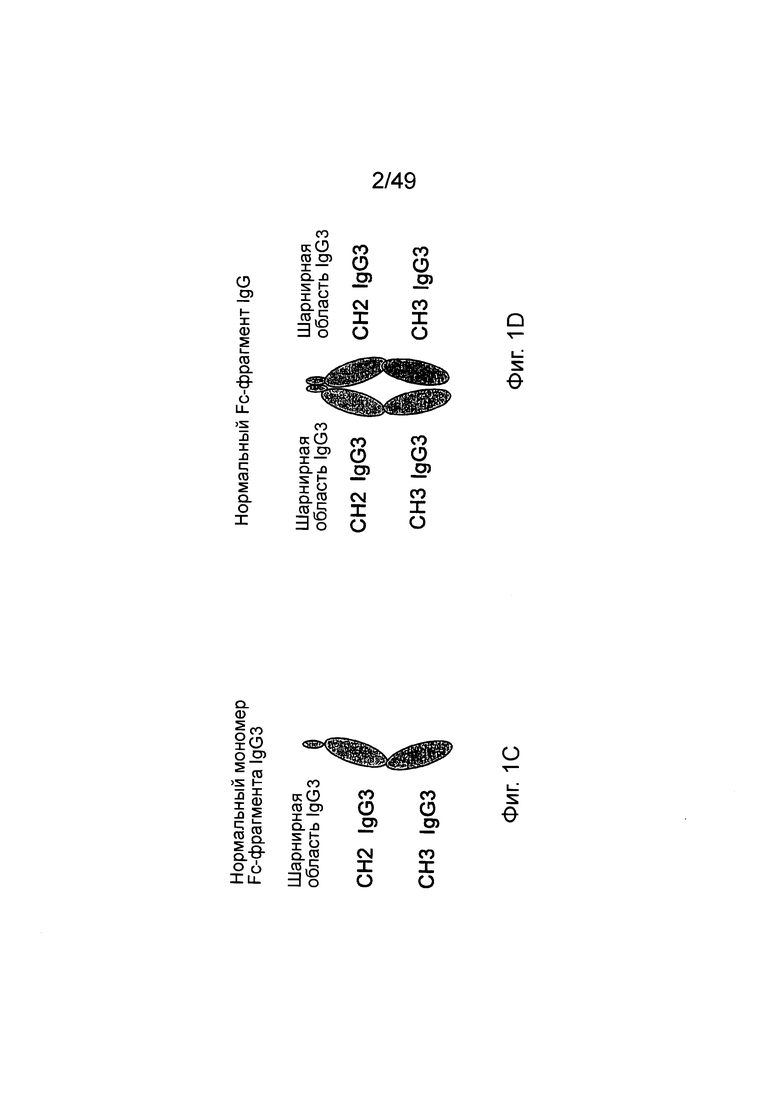

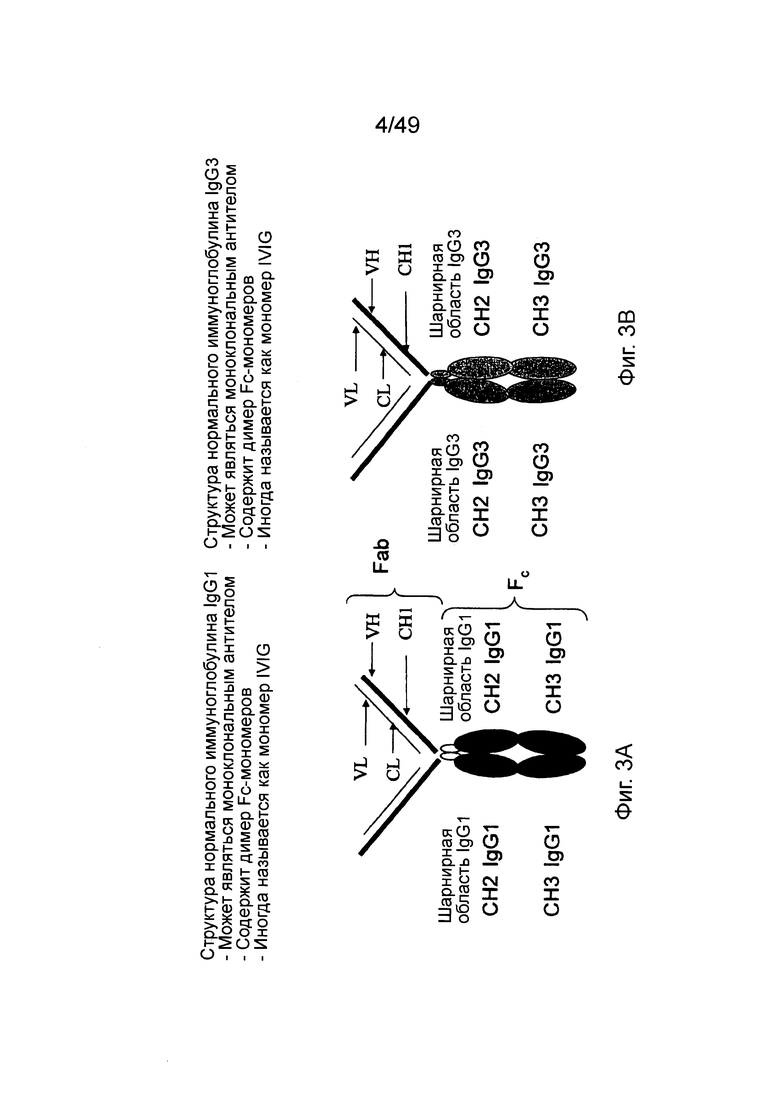
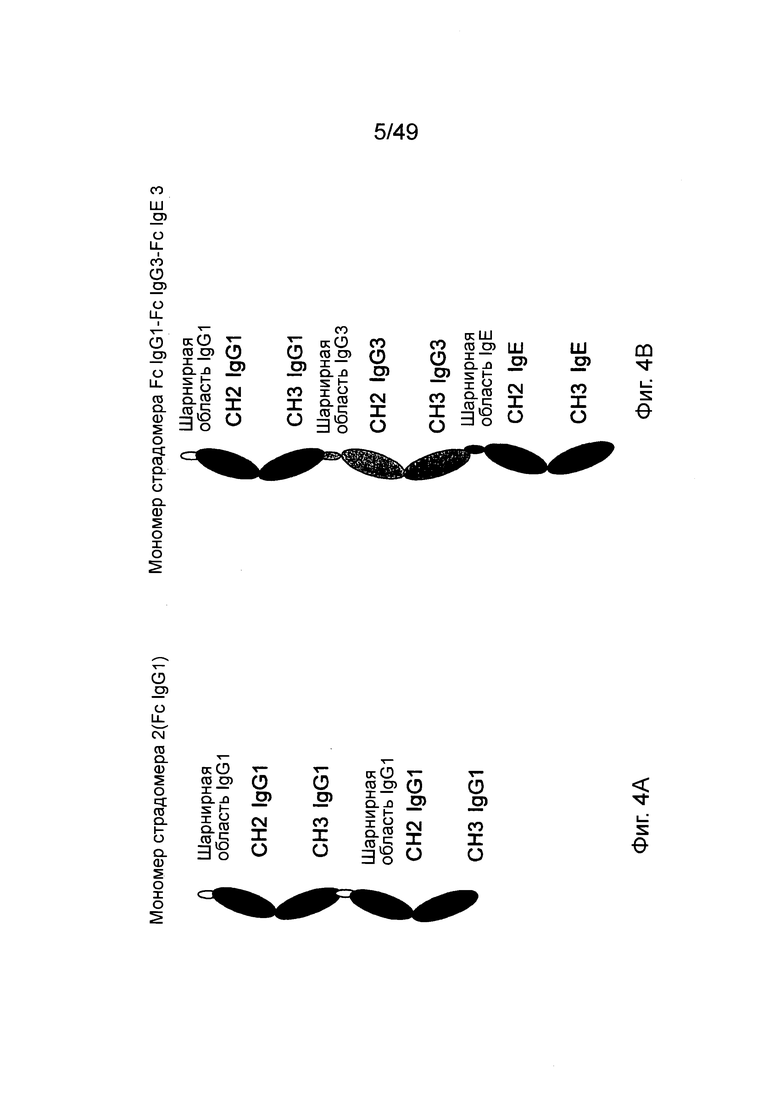
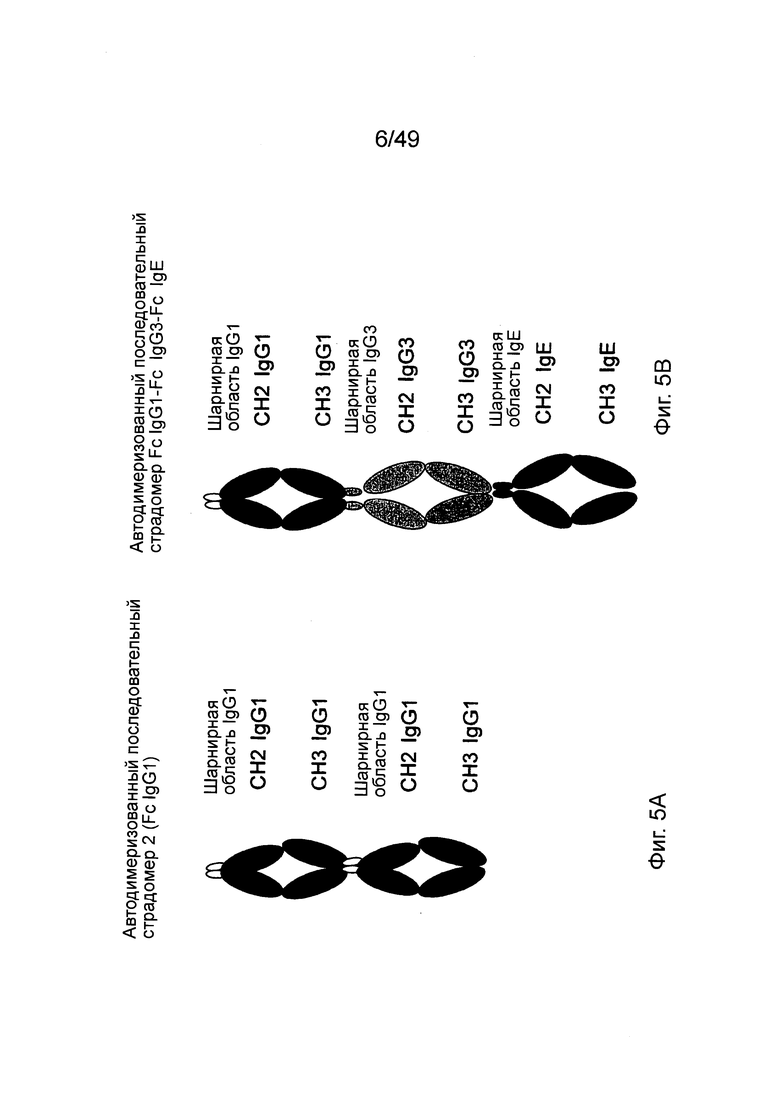



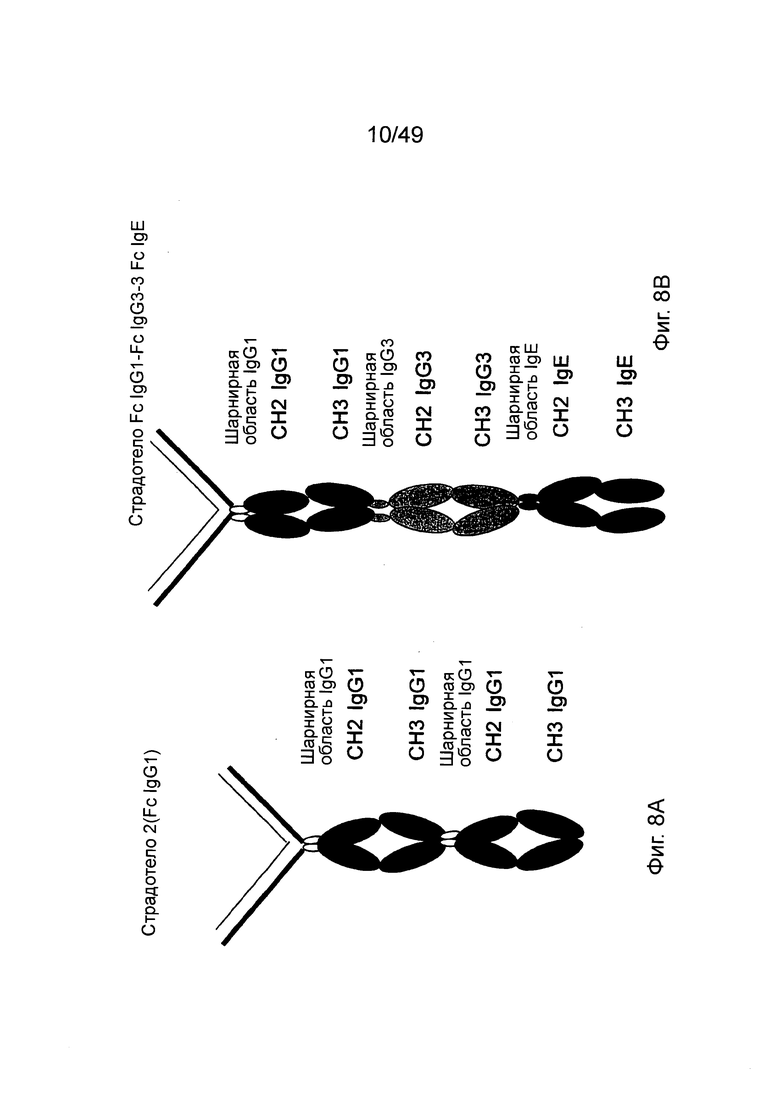
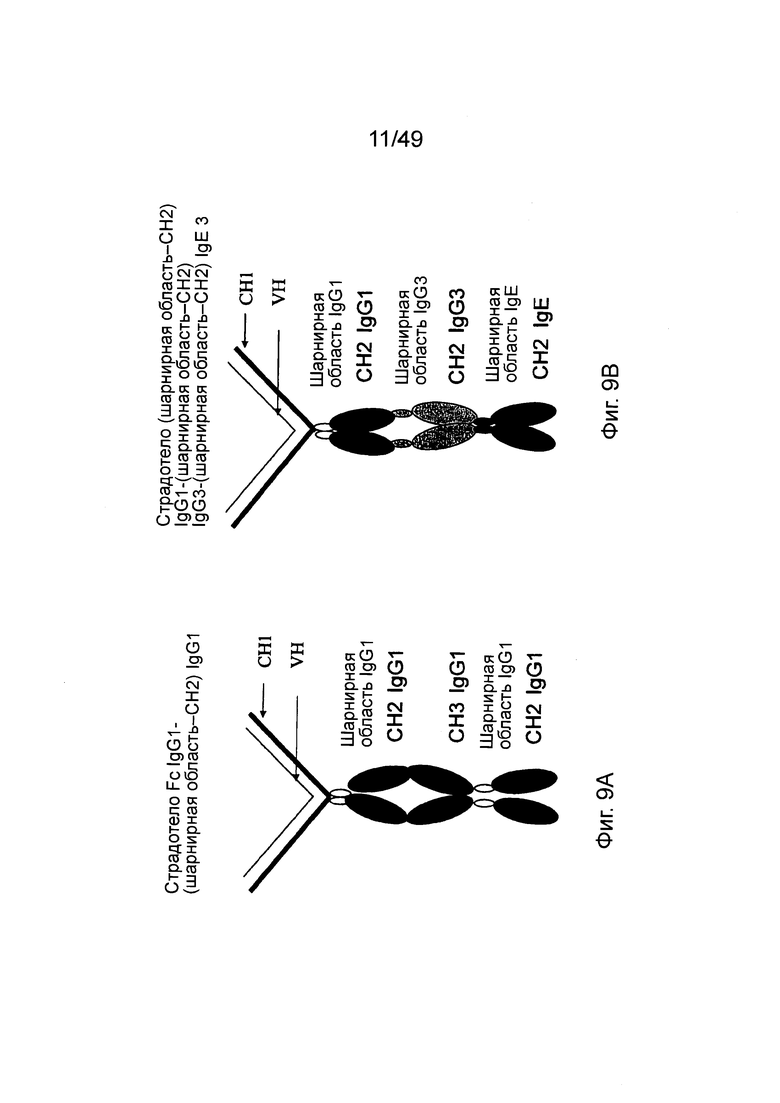
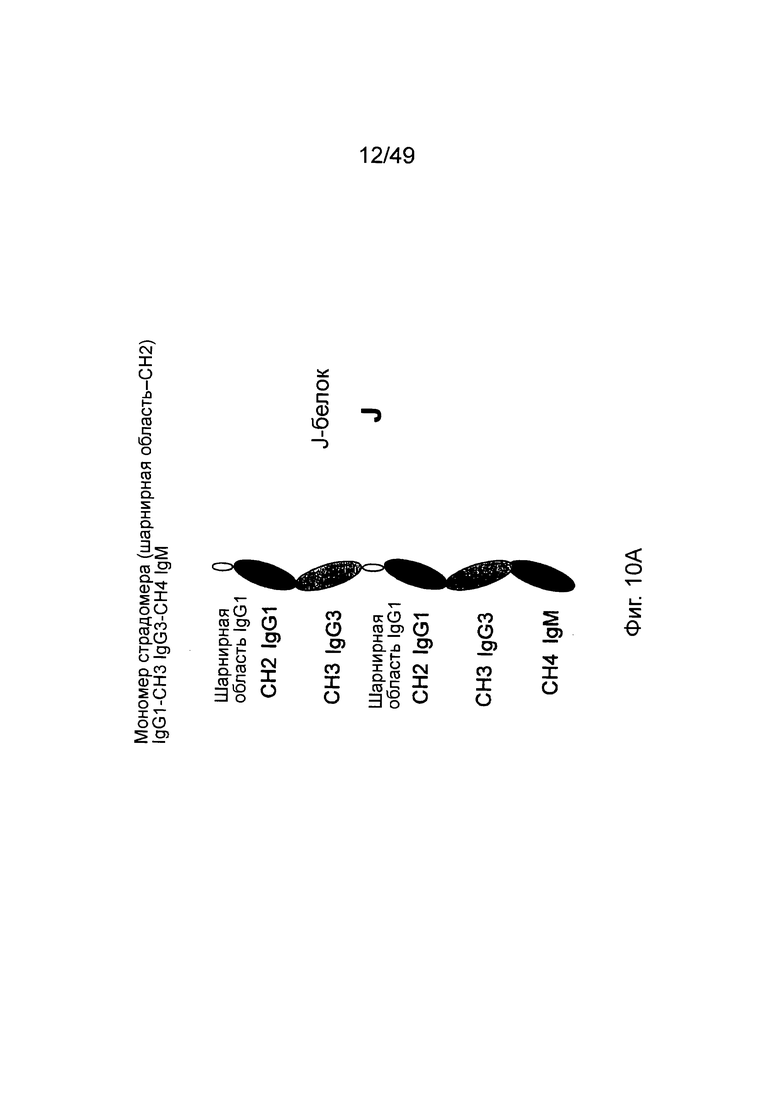

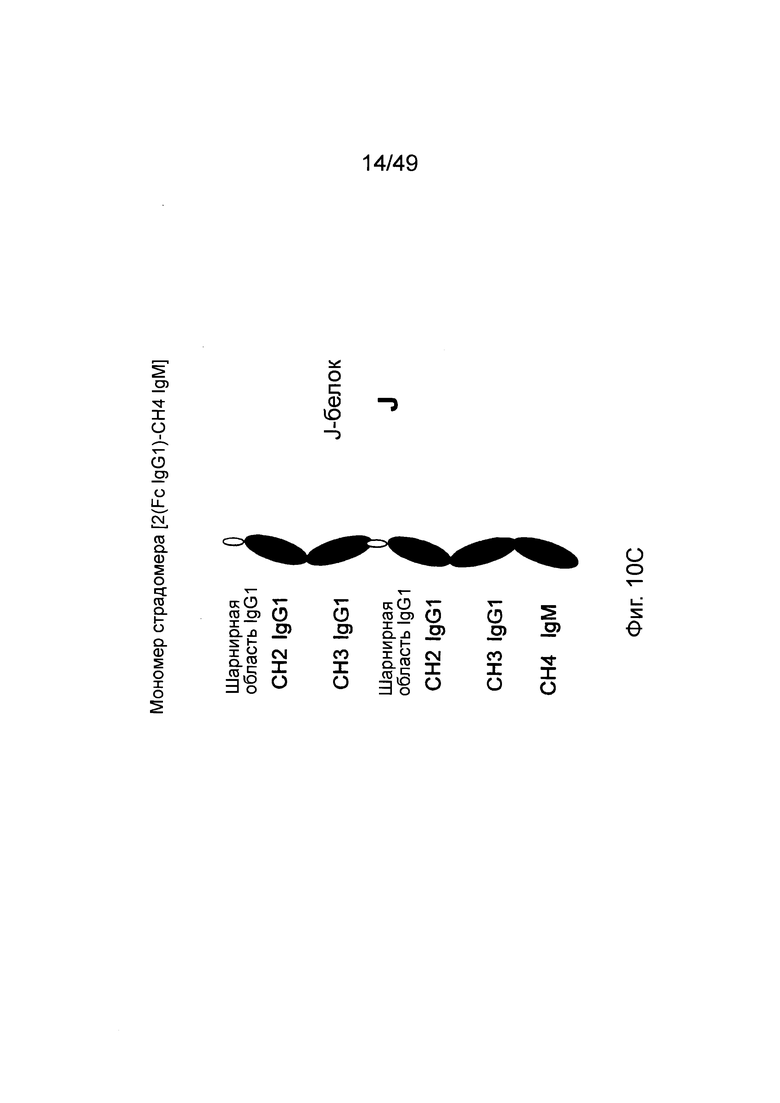


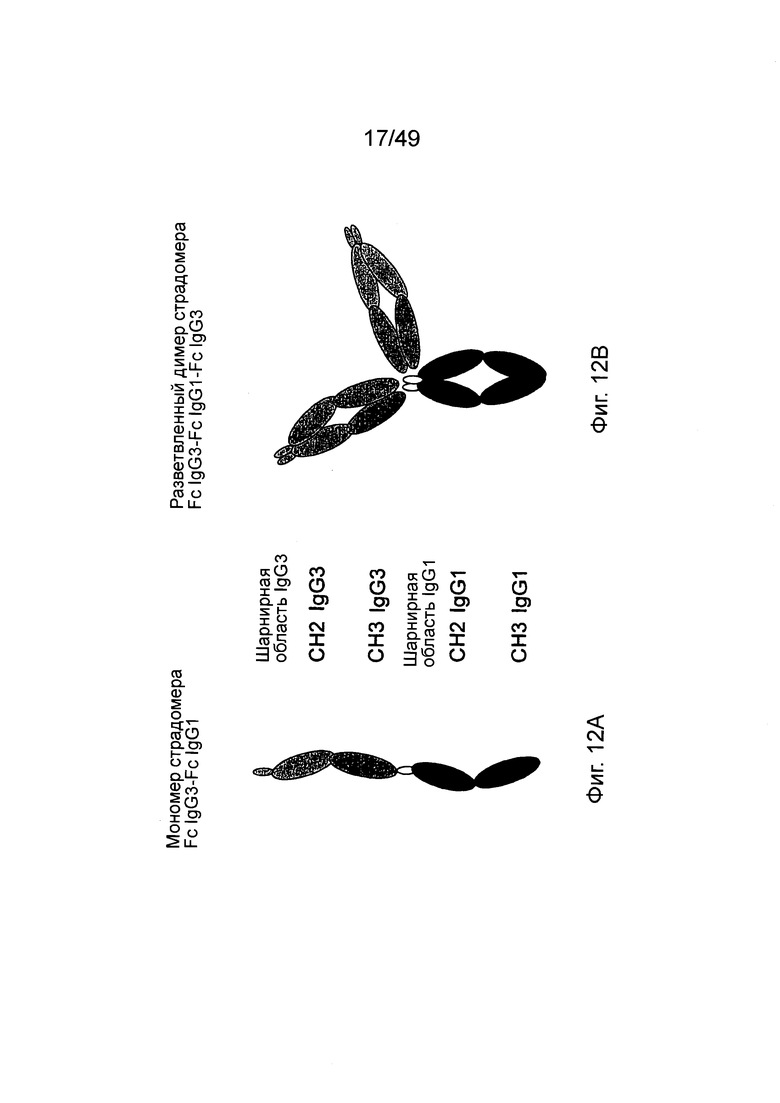
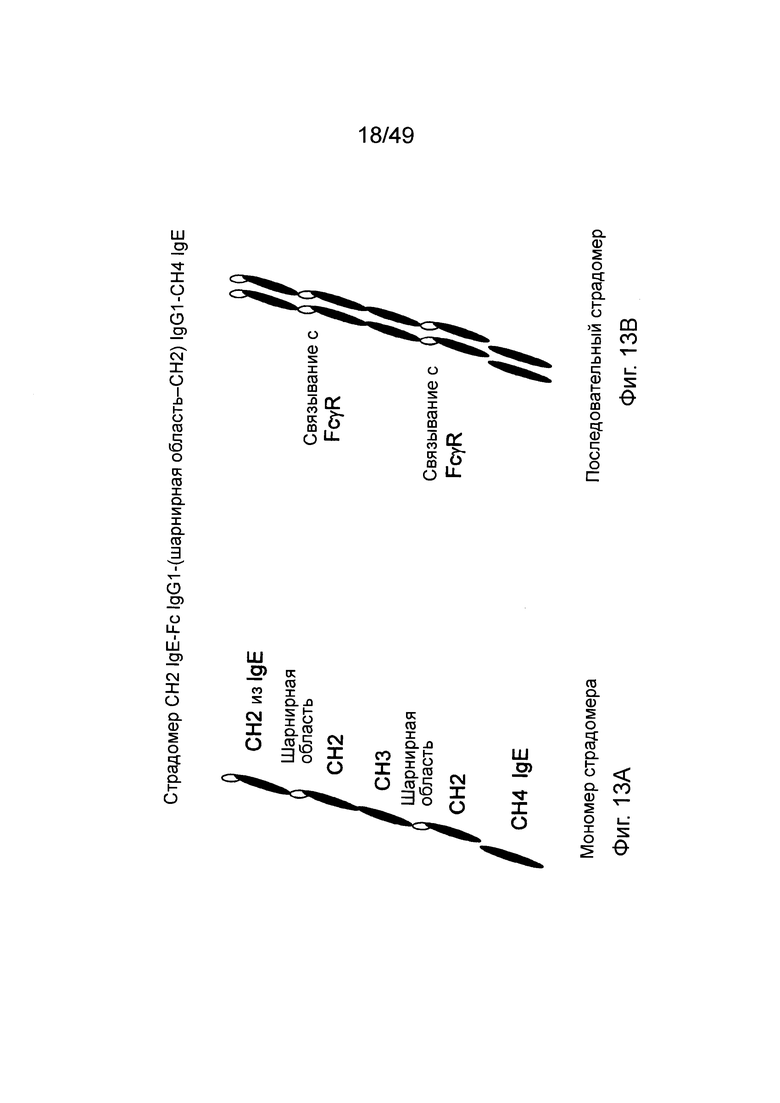


















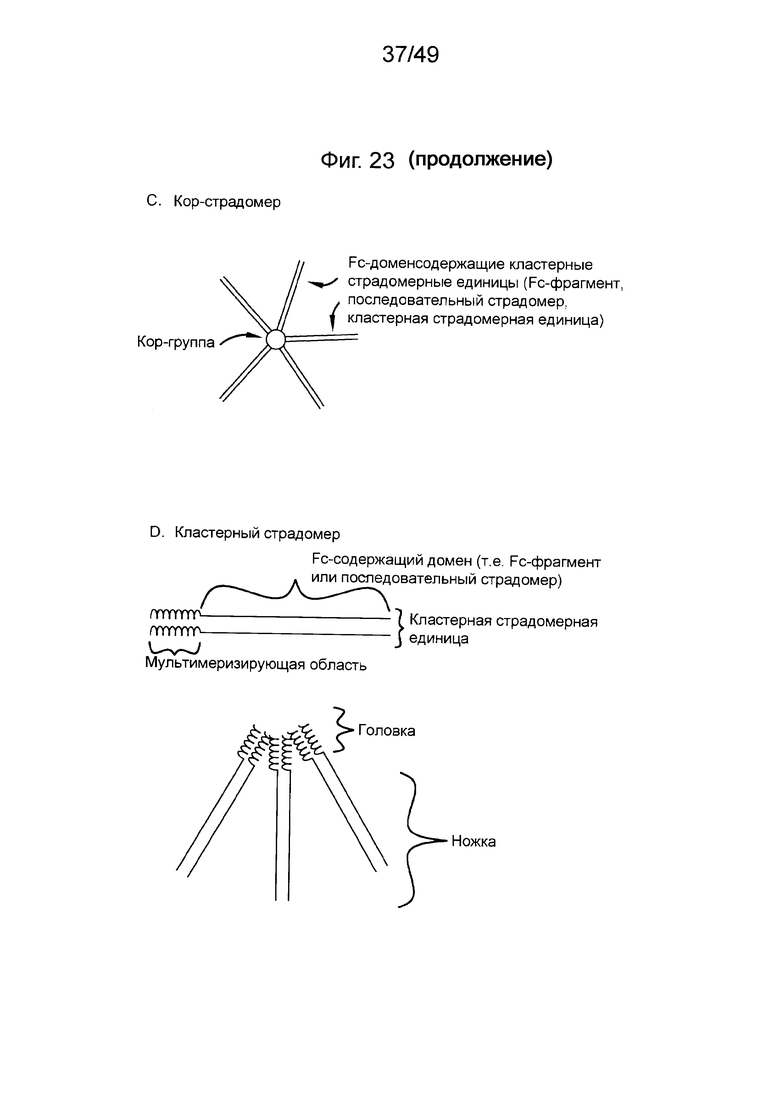












Изобретение относится к области биотехнологии. Предложены димерные соединения для образования мультимеров, содержащие идентичные мономеры. Каждый мономер содержит от N-конца до С-конца мономер мультимеризующей области и мономер Fc-домена, который при димеризации с другим мономером Fc-домена формирует Fc-домен, способный к связыванию с Fcγ-рецептором и/или неонатальным Fc-рецептором (FcRN). Также предложены мультимерные соединения для воспроизведения эффекторной функции агрегированного IgG, содержащие от двух до пяти мультимеризованных димерных соединений. Кроме того, изобретение относится к способу лечения аутоиммунного заболевания, включающему введение указанных димерных или мультимерных соединений. Изобретение позволяет получить иммунологически активные биомиметики. 7 н. и 6 з.п. ф-лы, 46 ил., 5 табл., 25 пр.
1. Димерное соединение для образования мультимера, способного к воспроизведению эффекторной функции агрегированного IgG при мультимеризации через мультимеризирующую область, где димерное соединение содержит идентичные мономеры, и где каждый мономер содержит от N-конца до С-конца:
(a) мономер мультимеризирующей области, который при димеризации с другим мономером мультимеризирующей области формирует мультимеризирующую область, и где мультимеризирующая область представляет собой шарнирную область IgG2; и
(b) мономер Fc-домена, содержащий мономер домена шарнирной области, мономер домена СН2 и мономер домена СН3 из IgG1, который при димеризации с другим мономером Fc-домена формирует Fc-домен, способный к связыванию с Fcγ-рецептором и/или неонатальным Fc-рецептором (FcRN).
2. Димерное соединение по п.1, где соединение не содержит антигенсвязывающий Fab-домен.
3. Димерное соединение по п.1, где Fcγ-рецептор представляет собой Fcγ-рецептор I человека, Fcγ-рецептор II человека, Fcγ-рецептор III человека, Fcγ-рецептор IV человека, FcRN человека или их нечеловеческие эквиваленты.
4. Димерное соединение по п.3, где Fcγ-рецептор III человека представляет собой FcγRIIIa.
5. Димерное соединение по п.1, где идентичные мономеры содержат белок SEQ ID NO: 61.
6. Димерное соединение по п.1, где идентичные мономеры содержат белок SEQ ID NO: 67.
7. Мультимерное соединение для воспроизведения эффекторной функции агрегированного IgG, содержащее два мультимеризованных димерных соединения по п.1, где димерные соединения мультимеризованы через мультимеризирующий домен.
8. Мультимерное соединение для воспроизведения эффекторной функции агрегированного IgG, содержащее три мультимеризованных димерных соединения по п.1, где димерные соединения мультимеризованы через мультимеризирующий домен.
9. Мультимерное соединение для воспроизведения эффекторной функции агрегированного IgG, содержащее четыре мультимеризованных димерных соединения по п.1, где димерные соединения мультимеризованы через мультимеризирующий домен.
10. Мультимерное соединение для воспроизведения эффекторной функции агрегированного IgG, содержащее пять мультимеризованных димерных соединений по п.1, где димерные соединения мультимеризованы через мультимеризирующий домен.
11. Димерное соединение для образования мультимера, способного к воспроизведению эффекторной функции агрегированного IgG при мультимеризации через мультимеризирующую область, где димерное соединение содержит идентичные мономеры, при этом каждый мономер содержит от N-конца до С-конца:
(a) мономер мультимеризирующей области, который при димеризации с другим мономером мультимеризирующей области образует мультимеризирующую область, и где мультимеризирующая область представляет собой шарнирную область IgG2; и
(b) мономер Fc-домена, содержащий мономер домена СН2 IgG1 и мономер домена СН3 IgG1, который при димеризации с другим мономером Fc-домена формирует Fc-домен, способный к связыванию с Fcγ-рецептором или неонатальным Fc-рецептором (FcRN).
12. Способ лечения аутоиммунного заболевания у пациента, который в этом нуждается, включающий введение димерного соединения по п.1 или мультимерного соединения по пп.7-10.
13. Способ по п.12, где аутоиммунное заболевание представляет собой увеит.
| СОВМЕЩЕННАЯ 3/1-ФАЗНАЯ ОБМОТКА ЯКОРЯ | 1992 |
|
RU2072608C1 |
| US 2007041972 A1, 22.02.2007 | |||
| GREENWOOD J | |||
| et al | |||
| Engineering multiple-domain forms of the therapeutic antibody CAMPATH-IH: effects on complement lysis, THERAPEUTIC IMMUNOLOGY, 1994, vol | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| CHAPPEL M.S | |||
| et al | |||
| Identification of the Fcγ receptor class I binding site in human IgG through the use of | |||
Авторы
Даты
2020-08-12—Публикация
2008-05-30—Подача