Область техники, к которой относится изобретение
В настоящем изобретении предложены средства и способы лечения ассоциированных с интерлейкином 18 (IL-18) заболеваний и нарушений. В частности, в настоящей заявке описаны антитела, специфические в отношении свободного IL-18, и IL-18-связывающего белка (IL-18BP), предназначенные для применения в указанных способах лечения и для диагностирования симптомов.
Предпосылки создания изобретения
Интерлейкин-18 (IL-18), известный также как интерферон-гамма-индуцирующий фактор, представляет собой цитокин, который продуцируется активированными макрофагами, клетками Купфера и другими клетками. IL-18 связывается с рецептором IL-18 и индуцирует клеточно-опосредованный иммунитет. Нарушения (например, «выключение») рецептора цитокина IL-18 или цитокина IL-18 приводят к нарушению активности естественных клеток-киллеров (NK) и ТН1-ответов. Помимо своей физиологической роли, IL-18 может также индуцировать серьезные воспалительные нарушения. Следовательно, для цели ранней диагностики таких нарушений необходимо количественно оценивать уровни свободного IL-18 в общей воде организма индивидуума, у которого предполагается такое нарушение.
Однако, в настоящее время количественную оценку уровней IL-18 в общей воде организма, как правило, осуществляют методом ELISA, с использованием антител, не обладающих специфичностью в отношении обнаружения свободного IL-18. Результат, достигаемый при использовании ELISA, ограничен специфичностью применяемого первичного антитела, которое связывается с антигеном-мишенью. До настоящего времени имелась возможность обнаруживать с использованием поступающих в продажу антител уровни только общего IL-18, однако до сих пор не были известны антитела к свободному IL-18. Обнаружение общего IL-18 не позволяет адекватно оценивать уровни свободного IL-18, поскольку IL-18, входящий в комплекс, например, связанный с его встречающимся в естественных условиях антагонистом, а именно IL-18-связывающим белком (IL-18BP), обладает пониженной аффинностью к рецептору IL-18. Кроме того, известно, что повышенные уровни IL-18 часто ассоциированы с повышенными уровнями IL-18BP.
С учетом указанных выше причин, определение общего IL-18 является недостаточным для установления адекватного диагноза ассоциированных с IL-18 заболеваний. Это означает, что для того, чтобы иметь возможность оценивать уровни свободного IL-18 в общей воде организма индивидуума и устанавливать адекватный диагноз ассоциированного с IL-18 заболевания, необходимо иметь средство обнаружения, которое специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс. Поэтому в настоящее время не существует эффективного метода лечения ассоциированных с IL-18 заболеваний или нарушений.
В настоящем изобретении предложены такие средства обнаружения в форме связывающей IL-18 молекулы, прежде всего IL-18-связывающего белка (IL-18BP) или антитела, которое специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс. Таким образом, настоящее изобретение позволяет удовлетворить потребность в адекватных средствах, которые позволяют обнаруживать свободный IL-18 и диагностировать заболевания и нарушения, ассоциированные со свободным IL-18, присутствующим в общей воде организма.
Это открывает возможность осуществления эффективного персонализированного медицинского подхода. В частности, в результате создания настоящего изобретения впервые оказывается возможным идентифицировать популяцию пациентов, страдающих от заболеваний или нарушений, которые ассоциированы с присутствием свободного IL-18 в тканях организма, и прежде всего, в общей воде организма, и эффективно лечить указанных пациентов путем введения связывающих молекул, которые специфически связываются со свободным IL-18.
Таким образом, в настоящем изобретении предложены также эффективные терапевтические средства для лечения и предупреждения ассоциированных с IL-18 заболеваний и нарушений у популяции пациентов, страдающих от заболеваний или нарушений, которые ассоциированы с присутствием свободного IL-18 в тканях организма, и, прежде всего, в общей воде организма. Таким образом, настоящее изобретение позволяет удовлетворить также потребность в эффективном лечении заболеваний или нарушений, которые ассоциированы с присутствием свободного IL-18 в тканях организма, прежде всего, в общей воде организма, путем создания IL-18-связывающих молекул, прежде всего, (1) IL-18BP и/или (2) антител, которые обладают специфичностью в отношении свободного IL-18 и не обладают перекрестной реактивностью с IL-18, входящим в состав комплекса.
IL-18-связывающие молекулы, прежде всего IL-18BP и IL-18-специфические антитела, предлагаемые в настоящем изобретении, обладают способностью уменьшать и/или устранять связывание свободного IL-18 с его рецептором и оказывать терапевтические благоприятные действия на пациента, страдающего от ассоциированного с IL-18 заболевания или нарушения.
Проведенные в последние годы неклинические и клинические исследования выявили очень важную роль провоспалительного цитокина интерлейкина 18 (IL-18) в патогенезе хронического обструктивного заболевания легких, и они позволяют предположить, что IL-18 действует в качестве главного регулятора деструктивных и ремоделирующих процессов.
Хроническое обструктивное заболевание легких (COPD), известное также как хроническое обструктивное легочное заболевание (COLD), хроническая обструкция дыхательных путей (COAD), хроническое ограничение воздушного потока (CAL) и хроническое обструктивное респираторное заболевание (CORD), представляет собой случай хронического бронхита или эмфиземы, двух обычно встречающихся вместе заболеваний легких, при которых с течением времени происходит сужение дыхательных путей. Это приводит к ограничению воздушного потока в легкое и из легкого, которое рассматривается как не полностью обратимое, и которое с течением времени может постепенно ухудшаться. Курение обусловливает 90% случаев COPD в Европе и в Соединенных Штатах. Хотя COPD может развиться не у всех курильщиков, но оценки показывают, что оно может развиться у 20%. Коэффициенты смертности у курильщиков, страдающих COPD, выше, чем у некурильщиков, страдающих COPD. У курильщиков проявляются также более часто респираторные симптомы (кашель, одышка и т.д.), и для них характерно большее нарушение легочной функции, чем у некурильщиков. Другими факторами риска являются, например, генетическая чувствительность (например, дефицит α1-антитрипсина, а также области на хромосоме 4 вблизи HHIP и в FAM13A, и на хромосоме 15 в CHRNA и IREB2), предшествующее заболевание туберкулезом, загрязнение воздуха, связанное с профессиональной деятельностью воздействие пыли и дыма (присутствующие в воздухе частицы), воздействие пассивного курения и вдыхание дыма сжигаемой биомассы. Понятие COPD включает главным образом два родственных заболевания: хронический бронхит и эмфизему. Хронический бронхит представляет собой воспаление и в конечном итоге рубцевание слизистой оболочки, выстилающей бронхиальные трубки. Когда бронхи воспаляются и/или инфицируются, то в легкие и из легких может протекать меньшее количество воздуха, при этом отхаркивается значительное количество слизи или мокроты. Эмфизема начинается с разрушения альвеол (воздушные мешочки в легких, в которых происходит обмен кислорода воздуха на диоксид углерода, присутствующий в крови), обусловленного, в частности, патологическим воспалительным ответом легкого на вредные частицы или газы, главным образом, на табачный дым. Стенки воздушных мешочков являются тонкими и хрупкими. Повреждение воздушных мешочков является необратимым и приводит к перманентным лакунам в тканях нижних долей легких. Когда воздушные мешочки разрушаются, легкие становятся способными передавать все меньше и меньше кислорода в кровоток, что вызывает одышку. Легкие теряют также свою эластичность, которая важна для поддержания дыхательных путей в открытом состоянии. В результате пациент испытывает большие трудности при выдохе. Как при хроническом бронхите, так и при эмфиземе, обструкция и разрушение ткани, как правило, являются перманентными прогрессирующими. У пациентов с COPD часто происходят обострения. Понятие «обострение» относится к ухудшению симптомов или увеличению серьезности заболевания. Продолжительность периода обострения может варьироваться в широких пределах - от нескольких часов до нескольких дней. Обострения могут вызывать симптомы, специфические для усиления процесса дыхания. Пациент может испытывать усиление одышки, у него может иметь место продуктивный кашель с измененным составом мокроты и жар. Количество мокроты может увеличиваться или она может становиться гнойной и изменять цвет. Пациент может испытывать также неспецифические симптомы, такие как недомогание, усталость, бессонница, сонливость или депрессия. Обострения COPD часто вызываются инфекцией нижних дыхательных путей. Наиболее распространенными причинами инфекции являются: аэробные грамположительные и грамотрицательные бактерии, атипичные бактерии, респираторный вирус, риновирус, вирус гриппа, RSV (респираторный синтициальный вирус) или комбинация патогенов. Обусловленные вирусами обострения являются более серьезными, более длительными, и они ассоциированы с более высокими уровнями воспаления и потери легочной функции, чем обострения, обусловленные другими причинами (Wedzicha, 2004, PATS; Seemungel и др., 2001, AM. J. RCCM; Tan и др., 2003, Am. J. Med. Donaldson и др., 2000, Thorax). Каждый страдающий COPD пациент, испытывает, по-видимому, от 1 до 4 обострений в год. Хотя такие обострения испытывают многие пациенты, оценки показывают, что они сообщают лечащему врачу только о примерно 50% всех эпизодов. Частые обострения ассоциированы с низким качеством жизни и большими экономическими проблемами.
Исследования на моделях заболевания COPD, посвященные индуцированному IL-18 легочному воспалению при индуцированной сигаретным дымом (CS) и индуцированной пассивным курением легочной эмфиземе, и воспалению и его ассоциации с COPD у курильщиков, продемонстрировали, что IL-18 и пути передачи сигнала IL-18 через IL-18R значительно активируются при воздействии сигаретного дыма, что было установлено на созданных на животных моделях и путем изучения воспаления и увеличения воздушных пространств в легких человека при индуцированной сигаретным дымом легочной эмфиземе. Результаты подтверждают важную роль альвеолярных макрофагов в качестве основного клеточного источника высвобождения IL-18.
Установлено, что IL-18 индуцирует ремоделирование дыхательных путей и сосудов у трансгенных по IL-18-индуцибельному гену, специфическому для легких, мышей, а также воспаление ткани, эмфизему, метаплазию слизистой оболочки и гипертрофию правого желудочка сердца.
Кроме того, было установлено, что IL-18 индуцирует эмфизему и цитотоксический ответ посредством IFNγ-зависимого механизма, фиброзное ремоделирование дыхательных путей, метаплазию слизистой оболочки и ремоделирование сосудов посредством IL-17A- и IL-13-зависимого пути. Существуют важные взаимодействия между этими путями, при которых имеет место IL-18-обусловленная индукция IL-13 посредством 1b-17А-зависимого механизма и взаимная негативная регуляция IFNγ- и 1b-17А/1b-13-ответов. Следовательно, IL-18 играет центральную роль в модуляции многих воспалительных каскадов.
Системные уровни IL-18 в организме пациентов с COPD позволяют предположить, что источником присутствующего в кровотоке IL-18 при COPD являются альвеолярные макрофаги, было установлено, что у пациентов с COPD повышены уровни IL-18 в кровотоке и в образующейся мокроте.
Повышенные уровни IL-18 при сопутствующих с COPD заболеваниях, по-видимому, ассоциированы с системным воспалением.
Кроме того, была установлена выраженная корреляция между уровнями IL-18 в сыворотке и легочной функцией.
В целом, результаты неклинических и клинических исследований убедительно свидетельствуют в пользу ингибирования/нейтрализации IL-18 как потенциальной предшествующей процессу мишени, позволяющего/позволяющей предупреждать или ограничивать как деструктивные, так и ремоделирующие процессы, которые, как правило, приводят к проявлению и развитию заболевания COPD.
На основе результатов проведенных в последние годы клинических исследований уровней IL-18 в кровотоке и мокроте пациентов с COPD установлено, что уровни IL-18 в легких пациентов с COPD значимо повышены и коррелируют с серьезностью заболевания.
Данные о присутствии IL-18 в мокроте пациентов с COPD позволяют предположить, что альвеолярные макрофаги являются основным источником IL-18 при COPD и что имеет место значимая сверхэкспрессия IL-18 в легких у пациентов с COPD по сравнению с контролями.
Проведенные в последние годы исследования роли инфламмасомы NLRP3 в стимулировании активации каспазы-1 после высвобождения зрелой формы провоспалительных цитокинов IL-1b и IL-18 позволили дополнительно изучить воздействия табачного дыма на воспаление дыхательных путей (Rastrick и др., 2013).
Было проведено исследование активации каспазы-1 и высвобождения IL-18 на мышах, которых подвергали воздействию сигаретного дыма дважды в день (Eltom и др., 2011).
На основе сравнения воздействия табачного дыма и обычного воздуха была продемонстрирована индуцируемая дымом повышающая регуляция IL-18 в результате активации каспазы-1.
В целом, IL-18 представляет собой предпочтительную предшествующую процессу мишень для перспективных терапевтических средств против COPD, позволяющих препятствовать деструктивным и ремоделирующим процессам в пораженных COPD легких, и поэтому является перспективным кандидатом для модифицирующего болезнь подхода к лечению COPD.
Поэтому в WO 2008/150431 А1 предложено лечить COPD и ассоциированные сопутствующие заболевания, возникающие в результате повышения уровней IL-18, IFN-γ или PKR у индивидуумов, страдающих COPD ассоциированными сопутствующими заболеваниями путем введения указанным индивидуумам ингибитора IL-18, ингибитора IL-18Rα и ингибитора IFNγ, ингибитора PKR и любой их комбинации.
Ингибирование IL-18, например, моноклональными антителами, мишенью которых является передача сигнала IL-18, путем блокады рецептора приводит к продолжительному действию, обусловленному продолжительным временем полужизни указанных агентов, при этом они оказывают воздействие не только на вредные виды активности IL-18, но также оказывают неблагоприятное влияние и на полезные с точки зрения защиты хозяина эффекты, приводя тем самым к нежелательным побочным действиям с точки зрения ответа, направленного на патогены (вирусы, бактерии, грибы и другие паразиты), в результате подавления IFN-гамма и хелперных Т-лимфоцитов типа 1.
При создании настоящего изобретения неожиданно было установлено, что указанных нежелательных побочных действий можно избежать с помощью альтернативного подхода, а именно, путем введения встречающегося в естественных условиях IL-18-связывающего белка (IL-18BP), который обладает высокой аффинностью связывания с интерлейкином 18 (IL-18) и принципиально другим механизмом действия в отношении IL-18 по сравнению, например, с известными в данной области моноклональными антителами.
В конкретном варианте осуществления изобретения IL-18-связывающий белок (IL-18BP) обладает аффинностью связывания, составляющей от 20 до 30пМ по данным измерений с помощью устройства BIAcore, как продемонстрировано в примере 4.4.2.
Таким образом, один из вариантов осуществления настоящего изобретения относится к IL-18-связывающей молекуле, которая специфически связывается со свободным IL-18 и не обладает перекрестной реактивностью с IL-18, входящим в комплекс (в дальнейшем в настоящем описании обозначена как «специфически связывающая свободный IL-18 молекула»), прежде всего к специфически связывающей свободный IL-18 молекуле, представляющей собой ингибитор IL-18, который снижает и/или устраняет связывание свободного IL-18 с его рецептором (в дальнейшем в настоящем описании обозначен как «ингибитор IL-18»), прежде всего IL-18BP, предназначенной для применения при лечении ассоциированного с IL-18 заболевания или нарушения у индивидуума, у которого диагностировано наличие аномальных уровней свободного IL-18 и/или аномального соотношения свободный IL-18/IL-18BP в общей воде организма по сравнению с уровнями в общей воде организма здорового контрольного индивидуума.
В частности, указанный аномальный уровень свободного IL-18 в общей воде организма превышает уровень в общей воде организма здорового индивидуума на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100%.
В другом варианте осуществления настоящего изобретения предложена специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, прежде всего IL-18BP, для применения согласно настоящему изобретению и согласно способам, представленным в настоящем описании, где указанные аномальные уровни свободного IL-18 в образцах, взятых из организма, прежде всего в общей воде организма, определены с применением IL-18-связывающей молекулы, прежде всего, IL-18-связывающего белка (IL-18BP) или антитела, которые специфически связываются со свободным IL-18, но не с IL-18, входящим в комплекс, согласно настоящему изобретению и согласно способам, представленным в настоящем описании в конкретных вариантах осуществления изобретения.
Кроме того, в одном из вариантов настоящего изобретения предложена специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, прежде всего IL-18BP, для применения, описанного в одном из предыдущих вариантов осуществления изобретения, в котором индивидуум, подлежащий лечению, относится к группе индивидуумов, у которых были выявлены повышенные уровни свободного IL-18 и/или аномальное соотношение свободный IL-18/IL-18BP в образцах, взятых из организма, прежде всего, в образце, выбранном из группы, состоящей из жидкости бронхоальвеолярного лаважа (BALF), жидкостей кровеносной системы, секреторных жидкостей, биопсии и гомогенизированной ткани, прежде всего, сыворотки, мочи, слез, слюны, желчи, пота, выделяемых продуктов, выдыхаемых продуктов, мокроты, бронхоальвеолярной жидкости, секрета сальных желез, клеточных, железистых, слизистых и тканевых выделений, по сравнению с уровнями в образцах, взятых из организма здоровых индивидуумов.
Указанные повышенные уровни свободного IL-18 в образце, взятом из организма больного пациента или индивидуума, составляют ≥5 пг/мл и вплоть до 10000 пг/мл или выше. В частности, указанные повышенные уровни свободного IL-18 в образце, взятом из организма больного пациента или индивидуума, находятся в пределах от ≥5 пг/мл до 10000 пг/мл, прежде всего в пределах от 100 пг/мл до 10000 пг/мл, прежде всего в пределах от 200 пг/мл до 10000 пг/мл, прежде всего в пределах от 300 пг/мл до 10000 пг/мл, прежде всего в пределах от 400 пг/мл до 10000 пг/мл, прежде всего в пределах от 500 пг/мл до 10000 пг/мл, прежде всего в пределах от 600 пг/мл до 10000 пг/мл, прежде всего в пределах от 700 пг/мл до 10000 пг/мл, прежде всего в пределах от 800 пг/мл до 10000 пг/мл, прежде всего в пределах от 900 пг/мл до 10000 пг/мл, прежде всего в пределах от 1000 до 10000 пг/мл, прежде всего в пределах от 1500 пг/мл до 10000 пг/мл, прежде всего в пределах от 2000 пг/мл до 10000 пг/мл, прежде всего в пределах от 3000 пг/мл до 10000 пг/мл, прежде всего в пределах от 4000 пг/мл до 10000 пг/мл, прежде всего в пределах от 5000 пг/мл до 10000 пг/мл. Количество свободного IL-18 в сыворотке здорового индивидуума, прежде всего здорового человека, составляет ≤5 пг/мл, прежде всего ≤4 пг/мл, прежде всего ≤1 пг/мл, прежде всего≤0,5 пг/мл, прежде всего, находится ниже предела обнаружения.
Еще одним объектом настоящего изобретения является специфически связывающая свободный IL-18 молекула, прежде всего, ингибитор IL-18, прежде всего, IL-18BP, предназначенная для применения по одному из предыдущих вариантов осуществления изобретения, в котором указанное ассоциированное с IL-18 заболевание или нарушение представляет собой заболевание или нарушение, выбранное из группы, состоящей из болезни Стилла взрослых, болезни Стилла детей, хронического обструктивного заболевания легких (COPD), связанного с трансфузией повреждения легких, бронхолегочной дисплазии (BPD), респираторного дистресс-синдрома взрослых (ARDS), интерстициальной болезни легких (ILD), идиопатического легочного фиброза, муковисцидоза, легочной артериальной гипертензии, астмы, бронхоэктаза, сердечной недостаточности, амиотрофического бокового склероза (ALS), синдрома сухого глаза (DED), кератита, язвы и истирания роговицы, неоваскуляризации роговицы, патологической внутриглазной неоваскуляризации, ирита, глаукомы, дегенерации желтого пятна, синдрома Шегрена, аутоиммунного увеита, болезни Бехчета, конъюнктивита, аллергического конъюнктивита, дерматита века, диабета типа 2, болезни жирной печени неалкогольной группы (NAFLD), стеатогепатита, трансплантации солидного органа и гематологической трансплантации, повреждения, вызванного ишемией-реперфузией, семейной средиземноморской лихорадки, периодических синдромов, ассоциированных с рецептором 1 фактора некроза опухоли, криопирин-ассоциированных периодических синдромов лихорадки, гипер-IgD-синдромов, подагры, синдрома Шнитцлера, гранулематоза Вегенера, называемого также гранулематозом с полиангиитом (GPA), тиреоидита Хашимото, болезни Крона, неспецифического язвенного колита, связанных с иммуноглобулином-4 (IgG4) заболеваний и терапий на основе стволовых клеток.
В конкретном варианте осуществления настоящего изобретения предложена специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, прежде всего IL-18BP, предназначенная для применения по одному из предыдущих вариантов осуществления изобретения, в котором указанное ассоциированное с IL-18 заболевание или нарушение индуцировано курением или воздействием пассивного курения, прежде всего, воздействием табачного дыма.
В другом конкретном варианте осуществления настоящего изобретения предложена специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, прежде всего IL-18BP, предназначенная для применения по одному из предыдущих вариантов осуществления изобретения, в котором указанное ассоциированное с IL-18 заболевание или нарушение индуцировано вирусной инфекцией.
Следующим объектом настоящего изобретения является специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, прежде всего IL-18BP, предназначенная для применения по одному из предыдущих вариантов осуществления изобретения, в котором указанное ассоциированное с IL-18 заболевание или нарушение представляет собой индуцированное IL-18 системное проявление воспаления и ассоциированных сопутствующих заболеваний, выбранных из группы, состоящей из эмфиземы, воспаления тканей, деструкции тканей, резекции легкого, исчезновения сосудов, апоптоза эндотелиальных клеток, метаплазии слизистой оболочки, гипертрофии сердца, снижения уровня VEGF в ткани легких, утраты легочных сосудов, мускуляризации сосудов, ремоделирования сосудов, отложения коллагена, наличия патологических слоев эластина в легких, фиброзного ремоделирования дыхательных путей, увеличения воздушного пространства, хронического ремоделирования дыхательных путей и легочных сосудов и снижения легочной функции.
Следующим объектом настоящего изобретения является специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, предназначенная для применения по одному из предыдущих вариантов осуществления изобретения, которая представляет собой антитело, прежде всего антитело, обладающее специфичностью в отношении свободного IL-18, прежде всего антагонистическое антитело, которое предупреждает связывание свободного IL-18 с рецептором IL-18, прежде всего связывание свободного IL-18 с IL-18Rα.
IL-18-специфическое антитело, предлагаемое в настоящем изобретении, включая любое функционально эквивалентное ему антитело или его фрагменты, связывается с IL-18 в сайте связывания IL-18BP или вблизи сайта связывания IL-18 ВР, или представляет собой конформационное антитело, которое связывается по меньшей мере с двумя эпитопами на молекуле IL-18, содержащими не являющиеся смежными аминокислоты, которые сближаются друг с другом в трехмерной конформации и взаимодействуют с паратопом рецептора таким образом, что сайт связывания IL-18BP на молекуле IL-18 оказывается блокированным.
В одном из вариантов осуществления изобретения IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, предлагаемое в настоящем изобретении и описанное в различных вариантах осуществления изобретения, представленных в настоящем описании, связывается со свободным белком IL-18, но не связывается с комплексами IL-18/IL-18BP.
В частности, IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, предлагаемое в настоящем изобретении характеризуется перекрестной реактивностью с комплексом IL-18/IL-18BP, составляющей от ≤0,01 до ≤0,05%, прежде всего от≤0,1 до ≤0,2%, прежде всего от ≤0,2 до ≤0,5%, прежде всего от ≤0,5 до ≤1%, прежде всего от ≤1 до ≤2%, по данным анализа с помощью ELISA в условиях конкуренции.
В конкретном варианте осуществления изобретения IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, предлагаемое в настоящем изобретении характеризуется перекрестной реактивностью с комплексом IL-18/IL-18BP, составляющей ≤0,1% по данным анализа с помощью ELISA в условиях конкуренции.
В одном из вариантов осуществления изобретения IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, описанное в одном из предыдущих вариантов осуществления изобретения, стерически препятствует связыванию IL-18BP с IL-18.
Еще в из вариантов осуществления изобретения IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, описанное в одном из предыдущих вариантов осуществления изобретения, специфически связывается с одним эпитопом, комбинацией двух эпитопов или комбинацией 3 эпитопов, содержащихся в последовательности, выбранной из группы последовательностей, которые представлены в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3 соответственно.
В конкретном варианте осуществления изобретения антитело, предлагаемое в изобретении, специфически связывается с одним эпитопом, содержащемся в последовательности, выбранной из группы последовательностей, которые представлены в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3.
В другом конкретном варианте осуществления изобретения антитело, предлагаемое в изобретении, специфически связывается с двумя эпитопами, содержащимися в последовательности, выбранной из группы последовательностей, которые представлены в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3 соответственно.
В частности антитело связывается с двумя эпитопами, содержащимися в последовательности (a) SEQ ID NO: 1 и SEQ ID NO: 2 соответственно, (б) SEQ ID NO: 1 и SEQ ID NO: 3 соответственно, (в) SEQ ID NO: 2 и SEQ ID NO: 3 соответственно.
В другом конкретном варианте осуществления изобретения антитело, предлагаемое в изобретении, специфически связывается с тремя эпитопами, содержащимися в последовательности, которая представлена в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3 соответственно.
В одном из вариантов осуществления настоящего изобретения предложено IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, описанное в одном из предыдущих вариантов осуществления изобретения, где антитело специфически связывается с одним эпитопом, комбинацией двух эпитопов или комбинацией трех эпитопов, выбранных из группы, состоящей из SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
В частности, настоящее изобретение относится также к указанному IL-18-специфическому антителу, включая любое функционально эквивалентное антитело или его фрагменты, где указанный эпитоп имеет последовательность, которая идентична на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности, представленной в SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6.
В конкретном варианте осуществления изобретения антитело, предлагаемое в изобретении, специфически связывается с одним эпитопом, содержащемся в последовательности, выбранной из группы последовательностей, представленных в SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
В другом конкретном варианте осуществления изобретения антитело, предлагаемое в изобретении, специфически связывается с двумя эпитопами, содержащимися в последовательности, выбранной из группы последовательностей, представленных в SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
В частности, антитело связывается с двумя эпитопами, содержащимися в последовательности (a) SEQ ID NO: 4 и SEQ ID NO: 5 соответственно, (б) SEQ ID NO: 4 и SEQ ID NO: 6 соответственно (в) SEQ ID NO: 5 и SEQ ID NO: 6 соответственно.
В другом конкретном варианте осуществления изобретения антитело, предлагаемое в изобретении, специфически связывается с тремя эпитопами, содержащимися в последовательности SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6 соответственно.
В конкретном варианте осуществления изобретения антитело, предлагаемое в настоящем изобретении, которое представлено в настоящем описании в различных вариантах осуществления изобретения, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержит по меньшей мере один, по меньшей мере два или все три гипервариабельных участка (CDR) вариабельной области легкой цепи, представленные в SEQ ID NO: 10, 12, 14, 16, 17, 19, 22, 24 и 26 соответственно, и/или меньшей мере один, по меньшей мере два или все три гипервариабельных участка (CDR) вариабельной области тяжелой цепи, представленные в SEQ ID NO: 9, 11, 13, 15, 18, 20, 21, 23 и 25 соответственно, где указанное антитело, эквивалентное антитело или его антигенсвязывающий участок связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP, но не связывается с комплексами IL-18/IL-18BP.
В частности, антитело, предлагаемое в настоящем изобретении, которое представлено в настоящем описании в различных вариантах осуществления изобретения, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержит гипервариабельные участки (CDR) вариабельной области легкой цепи, представленные в SEQ ID NO: 10, 12, 14, 16, 17, 19, 22, 24 и 26 соответственно, и гипервариабельные участки (CDR) вариабельной области тяжелой цепи, представленные в SEQ ID NO: 9, 11, 13, 15, 18, 20, 21, 23 и 25 соответственно, где указанное антитело, эквивалентное антитело или его антигенсвязывающий участок связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP, но не связывается в какой-либо значительной степени с комплексами IL-18/IL-18BP.
В конкретном варианте осуществления изобретения антитело, предлагаемое в настоящем изобретении, которое представлено в настоящем описании в различных вариантах осуществления изобретения, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержит по меньшей мере один, по меньшей мере два или все три гипервариабельных участка (CDR) вариабельной области легкой цепи, представленные на фиг. 11, и/или меньшей мере один, по меньшей мере два или все три гипервариабельных участка (CDR) вариабельной области тяжелой цепи, представленные на фиг. 11, где указанное антитело, эквивалентное антитело или его антигенсвязывающий участок связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP, но не связывается с комплексами IL-18/IL-18BP.
В частности, антитело, предлагаемое в настоящем изобретении, которое представлено в настоящем описании в различных вариантах осуществления изобретения, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержит гипервариабельные участки (CDR) вариабельной области легкой цепи, представленные на фиг. 11, и гипервариабельные участки (CDR) вариабельной области тяжелой цепи, представленные на фиг. 11, где указанное антитело, эквивалентное антитело или его антигенсвязывающий участок связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP, но не связывается в какой-либо значительной степени с комплексами IL-18/IL-18ВР.
В конкретном варианте осуществления изобретения гипервариабельные участки (CDR) определяют согласно системе нумерации остатков вариабельного домена, предложенной Кэботом.
В другом конкретном варианте осуществления изобретения гипервариабельные участки (CDR) определяют согласно системе нумерации остатков вариабельного домена, предложенной Хотиа.
В другом конкретном варианте осуществления изобретения гипервариабельные участки (CDR) определяют с помощью системы IMGT.
Антитело, предлагаемое в настоящем изобретении, которое представлено в настоящем описании в различных вариантах осуществления изобретения, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержит следующие гипервариабельные участки (CDR):
a. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 27, SEQ ID NO: 28 и SEQ ID NO: 29 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 30, SEQ ID NO: 31 и SEQ ID NO: 32 соответственно; или
б. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 33, SEQ ID NO: 34 и SEQ ID NO: 35 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 36, SEQ ID NO: 37 и SEQ ID NO: 38 соответственно; или
в. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 39, SEQ ID NO: 40 и SEQ ID NO: 41 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 42, SEQ ID NO: 43 и SEQ ID NO: 44 соответственно; или
г. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 45, SEQ ID NO: 46 и SEQ ID NO: 47 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 48, SEQ ID NO: 49 и SEQ ID NO: 50 соответственно; или
д. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 45, SEQ ID NO: 46 и SEQ ID NO: 47 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 51, SEQ ID NO: 52 и SEQ ID NO: 53 соответственно; или
е. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 54, SEQ ID NO: 55 SEQ ID NO: 56, соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 57, SEQ ID NO: 58 и SEQ ID NO: 59 соответственно; или
ж. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 60, SEQ ID NO: 61 и SEQ ID NO: 62 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 66, SEQ ID NO: 67 и SEQ ID NO: 68 соответственно; или
з. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 63, SEQ ID NO: 64 и SEQ ID NO: 65 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 66, SEQ ID NO: 67 и SEQ ID NO: 68 соответственно; или
и. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 69, SEQ ID NO: 70 и SEQ ID NO: 71 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 72, SEQ ID NO: 73 и SEQ ID NO: 74 соответственно; или
к. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную в SEQ ID NO: 75, SEQ ID NO: 78 и SEQ ID NO: 77 соответственно; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную в SEQ ID NO: 78, SEQ ID NO: 79 и SEQ ID NO: 80 соответственно.
л. CDR1, CDR2 и CDR 3 вариабельной области тяжелой цепи, которые имеют последовательность, представленную на фиг. 11; и CDR1, CDR2 и CDR 3 вариабельной области легкой цепи, которые имеют последовательность, представленную на фиг. 11.
В одном из вариантов осуществления изобретения антитело имеет вариацию в одной или нескольких последовательностях CDR, степень которой такова, что антитело, содержащее указанные варианты CDR, все еще обладает специфической связывающей активностью, присущей антителу, предлагаемому в настоящем изобретении, которое характеризуется тем, что связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP, но не связывается с комплексами IL-18/IL-18BP.
В другом конкретном варианте осуществления изобретения указанное антитело представляет собой человеческое или гуманизированное антитело, прежде всего человеческое или гуманизированное антитело, в котором CDR, встроенные в человеческий «каркас» антитела, происходят из одного или нескольких человеческого(их) иммуноглобулина(ов).
Еще в одном конкретном варианте осуществления изобретения предложено антитело, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержащее по меньшей мере вариабельную область легкой цепи, последовательность которой идентична на 75%, 80%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% последовательности, представленной в SEQ ID NO: 10, 12, 14, 16, 17, 19, 22, 24, 26 и на фиг. 11 соответственно и/или по меньшей мере вариабельную область тяжелой цепи, последовательность которой идентична на 75%, 80%, 82%, 83%,84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% последовательности, представленной в SEQ ID NO: 9, 11, 13, 15, 18, 20, 21, 23, 25 и на фиг. 11 соответственно, где указанное антитело, эквивалентное антитело или его антигенсвязывающий участок связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18 ВР или вблизи сайта связывания IL-18BP, но не связывается с комплексами IL-18/IL-18BP.
Еще в одном конкретном варианте осуществления изобретения предложено антитело, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, содержащее по меньшей мере вариабельную область легкой цепи, последовательность которой идентична на 75%, 80%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% последовательности, представленной в SEQ ID NO: 10, 12, 14, 16, 17, 19, 22, 24, 26 и на фиг. 11 соответственно, и/или по меньшей мере вариабельную область тяжелой цепи, последовательность которой идентична на 75%, 80%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% последовательности, представленной в SEQ ID NO: 9, 11, 13, 15, 18, 20, 21, 23, 25 и на фиг. 11 соответственно, при условии, что последовательности CDR вариабельной области легкой цепи и/или вариабельной области тяжелой цепи сохранены в неизмененном виде и где указанное антитело, эквивалентное антитело или его антигенсвязывающий участок связывается со свободным белком IL-18, прежде всего в сайте связывания IL-18ВР или вблизи сайта связывания IL-18BP, но не связывается с комплексами IL-18/IL-18BP.
В одном из вариантов осуществления настоящего изобретения предложено IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, для применения по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент представляет собой моноклональное антитело или поликлональное антитело.
В конкретном варианте осуществления настоящего изобретения предложено IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, для применения по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент представляет собой химерное, одноцепочечное, биспецифическое антитело, антитело с трансплантированными участками обезьяньего антитела, человеческое или гуманизированное антитело.
В частности, указанное антитело представляет собой гуманизированное антитело, прежде всего гуманизированное антитело, в котором определенные аминокислоты в каркасном участке и константных доменах вариабельных областей тяжелой и легкой цепи и/или константных областях тяжелой и легкой цепи подвергнуты мутации для избегания или устранения иммунного ответа у человека.
В частности, IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, предлагаемое в настоящем изобретении, характеризуется перекрестной реактивностью с комплексом IL-18/IL-18BP, составляющей от ≤0,01 до ≤0,05%, прежде всего от ≤0,1 до ≤0,2%, прежде всего от ≤0,2 до ≤0,5%, прежде всего от ≤0,5 до ≤1%, прежде всего от ≤1 до ≤2%, по данным анализа методом ELISA в условиях конкуренции.
В конкретном варианте осуществления изобретения IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его антигенсвязывающий участок, предлагаемое в настоящем изобретении, характеризуется перекрестной реактивностью с комплексом IL-18/IL-18BP, составляющей ≤0,1% по данным анализа методом ELISA в условиях конкуренции.
В другом конкретном варианте осуществления настоящего изобретения предложено IL-18-специфическое антитело, включая функционально эквивалентное антитело или его фрагменты, представленное в одном из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент связывается с человеческим IL-18.
Еще одним объектом настоящего изобретения является IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, представленное в одном из предыдущих вариантов осуществления изобретения, которое снижает связывание IL-18 с субъединицей рецептора IL-18 альфа (IL-18Rα) и бета (IL-18Rβ), прежде всего связывание с IL-18Rα, по меньшей мере на 5%, прежде всего, по меньшей мере на 10%, прежде всего, по меньшей мере на 15%, прежде всего, по меньшей мере на 20%, прежде всего, по меньшей мере на 25%, прежде всего, по меньшей мере на 30%, прежде всего, по меньшей мере на 40%, прежде всего, по меньшей мере на 45%, прежде всего, по меньшей мере на 50%, прежде всего, по меньшей мере на 55%, прежде всего, по меньшей мере на 60%, прежде всего, по меньшей мере на 65%, прежде всего, по меньшей мере на 70%, прежде всего, по меньшей мере на 75%, прежде всего, по меньшей мере на 80%, прежде всего, по меньшей мере на 85%, прежде всего, по меньшей мере на 90%, прежде всего, по меньшей мере на 95%, прежде всего, по меньшей мере на 96%, прежде всего, по меньшей мере на 97%, прежде всего, по меньшей мере на 98%, прежде всего, по меньшей мере на 99%, прежде всего, по меньшей мере на 100%.
Следующим объектом настоящего изобретения является специфически связывающая свободный IL-18 молекула, прежде всего ингибитор IL-18, прежде всего IL-18BP, прежде всего IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, представленное в одном из предыдущих вариантов осуществления изобретения, для применения при лечении ассоциированного с IL-18 заболевания или нарушения у популяции индивидуумов, у которых диагностировано наличие аномальных уровней свободного IL-18 и/или аномального соотношения свободный IL-18/IL-18BP в образцах, взятых из организма, прежде всего в общей воде организма, по сравнению с уровнями в общей воде организма здорового контрольного индивидуума, где указанная специфически связывающая свободный IL-18 молекула, ингибитор, IL-18BP или IL-18-специфическое антитело или его фрагмент нейтрализует действие свободного IL-18 посредством ограничения или предупреждения связывания IL-18 с рецептором IL-18 (IL-18R), прежде всего связывание свободного IL-18 с IL-18Rα.
В одном из вариантов осуществления настоящего изобретения предложено IL-18-специфическое антитело, включая любое функционально эквивалентное антитело или его фрагменты, представленное в одном из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагменты
а) специфически связывается(ются) с одним эпитопом, комбинацией двух эпитопов или комбинацией 3 эпитопов, который(ые) содержится(атся) в последовательности, выбранной из группы последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3; и/или
б) специфически связывается(ются) с эпитопом, последовательность которого идентична на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности, представленной в SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6; и
в) специфически связывается(ются) с IL-18 в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP; и
г) специфически связывается(ются) со свободным белком IL-18, но не с комплексами IL-18/IL-18BP; и
д) создает(ют) стерическую помеху для связывания IL-18BP с IL-18; и
е) снижает(ют) связывание IL-18 с рецептором IL-18, прежде всего связывание с IL-18Rα по меньшей мере на 5%, прежде всего, по меньшей мере на 10%, прежде всего, по меньшей мере на 15%, прежде всего, по меньшей мере на 20%, прежде всего, по меньшей мере на 25%, прежде всего, по меньшей мере на 30%, прежде всего, по меньшей мере на 40%, прежде всего, по меньшей мере на 45%, прежде всего, по меньшей мере на 50%, прежде всего, по меньшей мере на 55%, прежде всего, по меньшей мере на 60%, прежде всего, по меньшей мере на 65%, прежде всего, по меньшей мере на 70%, прежде всего, по меньшей мере на 75%, прежде всего, по меньшей мере на 80%, прежде всего, по меньшей мере на 85%, прежде всего, по меньшей мере на 90%, прежде всего, по меньшей мере на 95%, прежде всего, по меньшей мере на 96%, прежде всего, по меньшей мере на 97%, прежде всего, по меньшей мере на 98%, прежде всего, по меньшей мере на 99%, прежде всего, по меньшей мере на 100%.
В частности, конкретно определенное выше антитело характеризуется перекрестной реактивностью с комплексом IL-18/IL-18BP, составляющей от ≤0,01 до ≤0,05%, прежде всего от ≤0,1 до ≤0,2%, прежде всего от ≤0,2 до ≤0,5%, прежде всего от ≤0,5 до ≤1%, прежде всего от ≤1 до ≤2%, по данным анализа методом ELISA в условиях конкуренции.
В некоторых вариантах осуществления изобретения IL-18BP и/или специфическое в отношении свободного IL-18 антитело, представленный(ое) в одном из различных вариантов осуществления изобретения, можно применять в качестве ингибитора IL-18.
В другом конкретном варианте осуществления изобретения IL-18ВР и/или специфическое в отношении свободного IL-18 антитело, представленный(ое) в одном из различных вариантов осуществления изобретения, можно применять в качестве захватывающей молекулы в анализе для обнаружения свободного IL-18 в образце, взятом из организма, прежде всего в образце, выбранном из группы, состоящей из жидкости бронхоальвеолярного лаважа (BALF), жидкостей кровеносной системы, секреторных жидкостей, биопсии и гомогенизированной ткани, прежде всего, сыворотки, мочи, слез, слюны, желчи, пота, выделяемых продуктов, выдыхаемых продуктов, мокроты, бронхоальвеолярной жидкости, секрета сальных желез, клеточных, железистых, слизистых и тканевых секретов.
Один из вариантов осуществления изобретения относится к полинуклеотиду, который кодирует антитело, предлагаемое в изобретении, которое описано в различных вариантах осуществления изобретения, представленных в настоящем описании.
В одном из вариантов осуществления изобретения полинуклеотид кодирует вариабельную тяжелую цепь, представленную в SEQ ID NO: 9, 11, 13, 15, 18, 20, 21, 23, 25 и на фиг. 11.
В одном из вариантов осуществления изобретения полинуклеотид кодирует вариабельную легкую цепь, представленную в SEQ ID NO: 10, 12, 14, 16, 17, 19, 22, 24, 26 и на фиг. 11.
В одном из вариантов осуществления изобретения полинуклеотид кодирует CDR-участки, представленные в SEQ ID NO: 27-80.
В частности, изобретение относится к полинуклеотиду, который кодирует вариабельную область тяжелой цепи и/или легкой цепи антитела, предлагаемого в изобретении, которые имеют последовательность, идентичную на 75%, 80%, 82%, 83%,84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% последовательности, представленной на фиг 11.
Кроме того, настоящее изобретение относится также к ингибитору IL-18, предлагаемому в настоящем изобретении, предназначенному для применения по одному из предыдущих вариантов осуществления изобретения, где ингибитор представляет собой IL-18-связывающий белок (IL-18BP), прежде всего человеческий IL-18BP (hIL-18 BP), прежде всего IL-18BP, включая любой его функциональный эквивалент или фрагменты, прежде всего IL-18BP, представленный в SEQ ID NO: 7.
Под объем изобретения подпадают также транскрипционные варианты, кодирующие IL-18BP.
В одном из вариантов осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, где ингибитор представляет собой IL-18-связывающий белок (IL-18BP), последовательность которого идентична на 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности, представленной в SEQ ID NO: 7.
Еще одним объектом настоящего изобретения является ингибитор IL-18, предназначенный для применения по одному из предыдущих вариантов осуществления изобретения, где лечение представляет собой предупреждение, остановку, ослабление или реверсию симптомов, ассоциированных с указанным заболеванием или нарушением.
В другом варианте осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, в котором ограничивают или ингибируют связывание IL-18, в частности, связывание свободного IL-18 с IL-18R, прежде всего связывание свободного IL-18 с IL-18Rα.
В другом варианте осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, в котором модифицируют, прежде всего, ингибируют IL-18-зависимые низлежащие пути передачи сигнала.
Еще в одном варианте осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, в котором модифицируют, прежде всего, ингибируют, повышенную экспрессию IFNγ, IL-13 или IL-17A по сравнению с экспрессией у не подвергнутых лечению индивидуумов, страдающих указанным заболеванием или нарушением.
Еще в одном варианте осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, в котором ингибитор IL-18 компенсирует дисбаланс IL-18/IL-18BP посредством «улавливания» избытка свободного IL-18 в ткани и кровотоке.
В одном варианте осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, в котором ингибитор IL-18 ингибирует инфильтрацию нейтрофилов в легкое, прежде всего, посредством снижения высвобождения G-CSF в легочных дыхательных путях.
Еще в одном варианте осуществления настоящего изобретения предложен ингибитор IL-18 для применения по одному из предыдущих вариантов осуществления изобретения, который представляет собой полноразмерный белок или мутеин, функциональное производное, функциональный фрагмент, биологически активный пептид, фракцию, полученное в результате циклической перестановки производное, слитый белок, его изоформу или соль.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении хронического обструктивного заболевания легких (COPD), заболевания сердца, синдрома сухого глаза и/или диабета типа II.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении хронического обструктивного заболевания легких (COPD).
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении заболевания сердца.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении синдрома сухого глаза.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении амиотрофического бокового склероза (ALS).
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении диабета типа II.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении болезни Стилла взрослых.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении связанного с трансфузией повреждения легких.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении болезни Стилла детей.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении бронхолегочной дисплазии (BPD).
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении острого респираторного дистресс-синдрома (ARDS).
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении интерстициального заболевания легких (ILD).
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении идиопатического фиброза легких.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении муковисцидоза.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего антагонистическое антитело, прежде всего IL-18BP, по одному из предыдущих вариантов осуществления изобретения для применения при лечении легочной артериальной гипертензии.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении астмы.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении бронхоэктаза.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении сердечной недостаточности.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении кератита.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении язвы роговицы.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении неовакуляризации роговицы.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении патологической внутриглазной неоваскуляризации.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении ирита.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего антагонистическое антитело, прежде всего IL-18BP, по одному из предыдущих вариантов осуществления изобретения для применения при лечении глаукомы.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении дегенерации желтого пятна.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении синдрома Шегрена.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего антагонистическое антитело, прежде всего IL-18BP, по одному из предыдущих вариантов осуществления изобретения для применения при лечении аутоиммунного увеита.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении болезни Бехчета.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении конъюнктивита.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении дерматита века.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении болезни жирной печени неалкогольного типа (NAFLD).
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении стеатогепатита.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении нарушений, связанных трансплантацией солидного органа и гематологической трансплантацией.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении обусловленного ишемией-реперфузией нарушения.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из описанных выше вариантов осуществления изобретения для применения при лечении семейной средиземноморской лихорадки.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении ассоциированных с рецептором 1 фактора некроза опухоли периодических синдромов.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении криопирин-ассоциированных периодических синдромов лихорадки.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении гипер-IgD-синдромов.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении подагры.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении синдрома Шнитцлера.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении гранулематоза Вегенера.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении тиреоидита Хашимото.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении болезни Крона.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении язвенного колита.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении связанных с иммуноглобулином 4 (IgG4) заболеваний.
В настоящем изобретении предложен также ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения при лечении с использованием терапии на основе стволовых клеток.
В другом варианте настоящего изобретения предложен ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих выше вариантов осуществления изобретения, в котором указанное заболевание или нарушение индуцировано курением или воздействием пассивного курения, прежде всего воздействием табачного дыма.
В другом варианте настоящего изобретения предложен ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из описанных выше вариантов осуществления изобретения, в котором указанное заболевание или нарушение индуцировано вирусной инфекцией.
В другом варианте настоящего изобретения предложен ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих вариантов осуществления изобретения, в котором указанное заболевание или нарушение представляет собой индуцированное IL-18 системное проявление воспаления и ассоциированных сопутствующих заболеваний, выбранных из группы, которая состоит из эмфиземы, воспаления тканей, деструкции тканей, резекции легкого, исчезновения сосудов, апоптоза эндотелиальных клеток, метаплазии слизистой оболочки, гипертрофии сердца, снижения уровня VEGF в ткани легких, утраты легочных сосудов, мускуляризации сосудов, ремоделирования сосудов, отложения коллагена, наличия патологических слоев эластина в легких, фиброзного ремоделирования дыхательных путей, увеличения воздушного пространства, хронического ремоделирования дыхательных путей и легочных сосудов и снижения легочной функции.
Еще одним объектом настоящего изобретения является ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих вариантов осуществления изобретения, в котором ограничивают или ингибируют связывание IL-18, прежде всего связывание свободного IL-18 с IL-18R, прежде всего связывание свободного IL-18 с IL-18Rα.
Еще одним объектом настоящего изобретения является ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих вариантов осуществления изобретения, в котором модифицируют, прежде всего, ингибируют IL-18-зависимые пути передачи сигнала в обратном направлении.
Еще одним объектом настоящего изобретения является ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих вариантов осуществления изобретения, в котором модифицируют, прежде всего, ингибируют повышенную экспрессию IFNγ, IL-13 или IL-17A по сравнению с экспрессией у не подвергнутых лечению индивидуумов, страдающих указанным заболеванием или нарушением.
Еще одним объектом настоящего изобретения является ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих вариантов осуществления изобретения, в котором ингибитор IL-18 компенсирует дисбаланс IL-18/IL-18BP посредством захвата избытка свободного IL-18 в ткани или кровотоке.
Еще одним объектом настоящего изобретения является ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения для применения по одному из предыдущих вариантов осуществления изобретения, в котором лечение представляет собой предупреждение, остановку, облегчение или реверсию симптомов, ассоциированных с указанным заболеванием или нарушением.
Кроме того, в настоящем изобретении предложена также фармацевтическая композиция, предназначенная для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, где указанная композиция содержит ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое антитело, по одному из предыдущих вариантов осуществления изобретения, прежде всего в сочетании с фармацевтически приемлемым носителем и/или эксципиентом, прежде всего в профилактически и/или терапевтически эффективном количестве.
В частности, в настоящем изобретении предложена фармацевтическая композиция по предыдущему варианте осуществления изобретения, где указанная фармацевтическая композиция необязательно дополнительно содержит другой ингибитор провоспалительного цитокина или его функциональный фрагмент, или регуляторный фактор, который индуцирует in-situ экспрессию указанного ингибитора провоспалительного цитокина или его функционального фрагмента, терапевтические средства для совместного применения, такие как противовоспалительные, бронходилататорные, антигистаминные, противозастойные или противокашлевые лекарственные субстанции.
В одном из вариантов осуществления настоящего изобретения предложена фармацевтическая композиция по одному из предыдущих вариантов осуществления изобретения, которая содержит фармацевтически приемлемый носитель и/или эксципиент.
В конкретном варианте осуществления настоящего изобретения предложена фармацевтическая композиция, предназначенная для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, у индивидуума, страдающего такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, где указанная композиция содержит связывающий интерлейкин-18 белок (IL-18BP) по одному или нескольким из предыдущих вариантов осуществления изобретения, прежде всего в сочетании с фармацевтически приемлемым носителем и/или эксципиентом, прежде всего в профилактически и/или терапевтически эффективном количестве.
В другом конкретном варианте осуществления настоящего изобретения предложена фармацевтическая композиция, предназначенная для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, где указанная композиция содержит антагонистическое специфическое в отношении свободного IL-18 антитело по одному из предыдущих вариантов осуществления изобретения, прежде всего антагонистическое специфическое в отношении свободного IL-18 антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, которое(ые) характеризуется(ются) перекрестной реактивностью с комплексом IL-18/IL-18BP, составляющей от ≤0,01 до ≤0,05%, прежде всего от ≤0,1 до ≤0,2%, прежде всего от ≤0,2 до ≤0,5%, прежде всего от ≤0,5 до ≤1%, прежде всего от ≤1 до ≤2, по данным анализа методом ELISA в условиях конкуренции, прежде всего в сочетании с фармацевтически приемлемым носителем и/или эксципиентом, прежде всего в профилактически и/или терапевтически эффективном количестве.
В конкретном варианте осуществления настоящего изобретения предложена фармацевтическая композиция по предыдущему варианту осуществления изобретения, где указанная композиция необязательно дополнительно содержит другой ингибитор провоспалительного цитокина или его функциональный фрагмент, или регуляторный фактор, который индуцирует in-situ экспрессию указанного ингибитора провоспалительного цитокина или его функционального фрагмента, терапевтические средства для совместного применения, такие как противовоспалительные, бронходилататорные, антигистаминные, противозастойные или противокашлевые лекарственные субстанции.
Еще одним объектом настоящего изобретения является фармацевтическая композиция по одному из предыдущих вариантов осуществления изобретения, которая содержит фармацевтически приемлемый носитель и/или эксципиент.
В настоящем изобретении предложен также экспрессионный вектор, содержащий кодирующую последовательность ингибитора IL-18, или экспрессионный вектор, содержащий антисмысловую последовательность IL-18 (антисмысловой экспрессионный вектор IL-18), по одному из предыдущих вариантов осуществления изобретения, который после введения индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, приводит к экспрессии in situ ингибитора IL-18, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения.
В настоящем изобретении предложен также экспрессионный вектор, представляющий собой антисмысловой экспрессионный вектор IL-18, который после введения индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления настоящего изобретения, приводит к ингибированию in situ экспрессии IL-18, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения.
В настоящем изобретении предложен также экспрессионный вектор, содержащий кодирующую последовательность регуляторного фактора, который после введения индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, приводит к экспрессии in situ указанного регуляторного фактора, модулирующего вышележащие пути передачи сигналов, которые контролируют экспрессию ингибитора IL-18 по одному из предыдущих вариантов осуществления изобретения, где, указанный регуляторный фактор прежде всего, индуцирует клеточную экспрессию ингибитора IL-18, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения.
В частности, указанный экспрессионный вектор по одному из предыдущих вариантов осуществления изобретения, который предназначен для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, вводят индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, индивидуально или в сочетании с ингибитором IL-18 по одному из предыдущих вариантов осуществления изобретения, связывающим интерлейкин-18 белком (IL-18BP) по одному из предыдущих вариантов осуществления изобретения, или фармацевтической композицией по одному из предыдущих вариантов осуществления изобретения.
В настоящем изобретении предложен также экспрессионный вектор, содержащий кодирующую последовательность IL-18 по одному из предыдущих вариантов осуществления изобретения, который после введения индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, приводит к экспрессии in situ IL-18BP, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения.
В настоящем изобретении предложен также экспрессионный вектор, содержащий кодирующую последовательность регуляторного фактора, который после введения индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, приводит к экспрессии in situ указанного регуляторного фактора, модулирующего вышележащие пути передачи сигналов, которые контролируют экспрессию IL-18BP, по одному из предыдущих вариантов осуществления изобретения, где указанный регуляторный фактор, прежде всего, индуцирует клеточную экспрессию IL-18BP, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения.
В частности, указанный экспрессионный вектор по одному из предыдущих вариантов осуществления изобретения, который предназначен для применения при лечении заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, вводят индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, индивидуально или в сочетании с ингибитором IL-18 по одному из предыдущих вариантов осуществления изобретения, связывающим интерлейкин-18 белком (IL-18BP) по одному из предыдущих вариантов осуществления изобретения, или фармацевтической композицией по одному из предыдущих вариантов осуществления изобретения.
Еще одним объектом настоящего изобретения является ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое специфическое в отношении свободного IL-18 антитело, или фармацевтическая композиция, содержащая ингибитор IL-18, прежде всего IL-18BP, прежде всего антагонистическое специфическое в отношении свободного IL-18 антитело, или экспрессионный вектор, предназначенные для применения по одному из предыдущих вариантов осуществления изобретения, где их вводят индивидууму в профилактически и/или терапевтически эффективном количестве путем системного, интраназального, внутриглазного, интравитреального введения, с помощью глазных капель, трансбуккального, орального введения, введения через слизистую оболочку, внутритрахеального, внутривенного, подкожного введения, введения в мочевой тракт, интраректального, интравагинального, подъязычного, внутрибронхиального, внутрилегочного, чрескожного или внутримышечного введения, прежде всего, путем бронхолегочного введения.
В частности, указанный индивидуум представляет собой млекопитающее, прежде всего, указанный индивидуум представляет собой человека.
Настоящее изобретение относится также к способу лечения заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, заключающемуся в том, что вводят указанному индивидууму в терапевтически или профилактически эффективном количестве ингибитор IL-18, прежде всего IL-18BP, прежде всего, антагонистическое специфическое в отношении свободного IL-18 антитело, или фармацевтическую композицию, содержащую ингибитор IL-18, прежде всего IL-18BP, прежде всего, антагонистическое специфическое в отношении свободного IL-18 антитело, или экспрессионный вектор по одному из предыдущих вариантов осуществления изобретения.
Настоящее изобретение относится также к способу определения количества свободного IL-18 в образце или in situ, заключающемуся в том, что выявляют специфическое связывание специфически связывающей свободный IL-18 молекулы по одному из предыдущих вариантов осуществления изобретения со свободным белком IL-18 в образце или in situ, который включает стадии, на которых:
а) приводят образец или специфическую часть организма или область организма, в котором/которой предполагается присутствие свободного IL-18, в контакт со специфически связывающей свободный IL-18 молекулой по одному из предыдущих вариантов осуществления изобретения, которая специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс, и функционирует в качестве захватывающей молекулы для свободного IL-18;
б) дают связываться специфически связывающей свободный IL-18 молекуле со свободным IL-18;
в) выявляют связывание IL-18 со специфически связывающей свободный IL-18 молекулой и определяют количество свободного IL-18 в образце.
В другом варианте осуществления изобретения предложен способ диагностирования заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, у пациента, заключающийся в том, что выявляют специфическое связывание специфически связывающей свободный IL-18 молекулы по одному из предыдущих вариантов осуществления изобретения со свободным белком IL-18 в образце или in situ, который включает стадии, на которых:
а) приводят образец или специфическую часть организма или область организма, в котором/которой предполагается присутствие свободного IL-18, в контакт со специфически связывающей свободный IL-18 молекулой по одному из предыдущих вариантов осуществления изобретения, которая специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс, и функционирует в качестве захватывающей молекулы для свободного IL-18;
б) дают связываться специфически связывающей свободный IL-18 молекуле со свободным IL-18;
в) выявляют связывание IL-18 со специфически связывающей свободный IL-18 молекулой и определяют количество свободного IL-18 в образце;
г) сравнивают количество свободного IL-18 в образце, полученном из организма индивидуума, страдающего от заболеваний или нарушения по одному из предыдущих вариантов осуществления изобретения, с его количеством в образце, полученном из организма здорового индивидуума.
Еще в одном варианте осуществления изобретения предложен способ диагностирования предрасположенности пациента к заболеваниям или нарушению, указанным(ому) в одном из предыдущих вариантов осуществления изобретения, заключающийся в том, что выявляют специфическое связывание специфически связывающей свободный IL-18 молекулы по одному из предыдущих вариантов осуществления изобретения со свободным белком IL-18 в образце или in situ, который включает стадии, на которых:
а) приводят образец или специфическую часть организма или область организма, в котором/которой предполагается присутствие свободного IL-18, в контакт со специфически связывающей свободный IL-18 молекулой по одному из предыдущих вариантов осуществления изобретения, которая специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс, и функционирует в качестве захватывающей молекулы для свободного IL-18;
б) дают связываться специфически связывающей свободный IL-18 молекуле со свободным IL-18;
в) выявляют связывание IL-18 со специфически связывающей свободный IL-18 молекулой и определяют количество свободного IL-18 в образце;
г) сравнивают количество свободного IL-18 в образце, полученном из организма индивидуума, страдающего от заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, с его количеством в образце, полученном из организма здорового индивидуума;
где увеличение количества указанного свободного IL-18 в образце по сравнению с контрольным нормальным значением, полученным для здорового индивидуума, свидетельствует о том, что указанный пациент страдает от заболевания или нарушения, указанного в одном из предыдущих вариантов осуществления изобретения, или имеет риск его развития.
Кроме того, в настоящем описании представлен способ мониторинга минимальной остаточной болезни у пациента после лечения с использованием ингибитора IL-18, фармацевтической композиции или экспрессионного вектора по одному из предыдущих вариантов осуществления изобретения, где указанный способ заключается в том, что:
а) приводят образец или специфическую часть организма или область организма, в котором/которой предполагается присутствие свободного IL-18, в контакт со специфически связывающей свободный IL-18 молекулой по одному из предыдущих вариантов осуществления изобретения, которая специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс, и функционирует в качестве захватывающей молекулы для свободного IL-18;
б) дают связываться специфически связывающей свободный IL-18 молекуле со свободным IL-18;
в) выявляют связывание IL-18 со специфически связывающей свободный IL-18 молекулой и определяют количество свободного IL-18 в образце;
г) сравнивают количество свободного IL-18 в образце, полученном из организма индивидуума, страдающего от заболеваний или нарушения по одному из предыдущих вариантов осуществления изобретения, с его количеством в образце, полученном из организма здорового индивидуума;
где увеличение количества указанного свободного IL-18 в образце по сравнению с контрольным нормальным значением, полученным для здорового индивидуума, свидетельствует о том, что указанный пациент все еще страдает от минимальной остаточной болезни.
Изобретение относится также к способу прогнозирования чувствительности пациента к лечению с использованием ингибитора IL-18, фармацевтической композиции или экспрессионного вектора по одному из предыдущих вариантов осуществления изобретения, где указанный способ заключается в том, что:
а) приводят образец или специфическую часть организма или область организма, в котором/которой предполагается присутствие свободного IL-18, в контакт со специфически связывающей свободный IL-18 молекулой по одному из предыдущих вариантов осуществления изобретения, которая специфически связывается со свободным IL-18, но не с IL-18, входящим в комплекс, и функционирует в качестве захватывающей молекулы для свободного IL-18;
б) дают связываться специфически связывающей свободный IL-18 молекуле со свободным IL-18;
в) выявляют связывание IL-18 со специфически связывающей свободный IL-18 молекулой и определяют количество свободного IL-18 в образце;
г) сравнивают количество свободного IL-18 в образце, полученном из организма индивидуума, страдающего от заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, с его количеством в образце, полученном из организма здорового индивидуума;
где уменьшение количества указанного свободного IL-18 в образце свидетельствует о том, что указанный пациент с высокой вероятностью может обладать чувствительностью к лечению.
Любой из способов может включать на стадии а) дополнительную стадию, на которой применяют специфически связывающую IL-18BP молекулу, которая связывается с сайтом IL-18BP, отличным от сайта, с которым связывается захватывающая молекула, прежде всего, когда одна из указанных молекул связывается с сайтом IL-18BP, который связывается с IL-18.
Кроме того, любой из указанных выше способов может включать также дополнительную стадию, на которой определяют присутствие свободного IL-18ВР в образце посредством применения на стадии а) специфически захватывающей IL-18BP молекулы и специфически идентифицирующей IL-18BP молекулы, которая связывается с сайтом IL-18BP, отличным от сайта, с которым связывается захватывающая молекула, прежде всего, когда одна из указанных 1b-18ВР-связывающих молекул связывается с сайтом IL-18BP, который связывается с IL-18, посредством определения на стадии в) количества свободного и общего IL-18 и свободного и общего IL-18BP, связанного с захватывающей молекулой в образце; и посредством сравнения на стадии г) количества свободного и/или общего IL-18 и свободного и/или общего IL-18BP в образце, взятом из организма пациента, страдающего от заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, с количеством в образце, взятом из организма здорового индивидуума.
Захватывающая молекула, применяемая в любом из представленных выше способов, может представлять собой специфическую в отношении свободного IL-18 связывающую молекулу по одному из предыдущих вариантов осуществления изобретения, прежде всего IL-18BP, указанный в настоящем описании, или связывающее свободный IL антитело, предлагаемое в изобретении и представленное в настоящем описании.
Образец, применяемый в любом из указанных выше способов, может представлять собой образец, выбранный из группы, которая состоит из жидкости бронхоальвеолярного лаважа (BALF), жидкостей кровеносной системы, секреторных жидкостей, биопсии и гомогенизированной ткани, прежде всего, сыворотки, мочи, слез, слюны, желчи, пота, выделяемых продуктов, выдыхаемых продуктов, мокроты, бронхоальвеолярной жидкости, секрета сальных желез, клеточных, железистых, слизистых и тканевых выделений и т.д.
В одном из вариантов осуществления изобретения количество свободного IL-18 в образце, взятом из организма индивидуума, прежде всего человека, страдающего от любого из указанных в настоящем описании заболеваний, составляет от ≥5 пг/мл и вплоть до 10000 пг/мл или более. В частности, указанные повышенные уровни свободного IL-18 в образце, взятом из организма больного пациента или индивидуума, составляют от ≥5 пг/мл до 10000 пг/мл, прежде всего от 100 пг/мл до 10000 пг/мл, прежде всего от 200 пг/мл до 10000 пг/мл, прежде всего от 300 пг/мл до 10000 пг/мл, прежде всего от 400 пг/мл до 10000 пг/мл, прежде всего от 500 пг/мл to 10000 пг/мл, прежде всего от 600 пг/мл до 10000 пг/мл, прежде всего от 700 пг/мл до 10000 пг/мл, прежде всего от 800 пг/мл до 10000 пг/мл, прежде всего от 900 пг/мл до 10000 пг/мл, прежде всего от 1000 до 10000 пг/мл, прежде всего от 1500 пг/мл до 10000 пг/мл, прежде всего от 2000 пг/мл до 10000 пг/мл, прежде всего от 3000 пг/мл до 10000 пг/мл, прежде всего от 4000 пг/мл до 10000 пг/мл, прежде всего от 5000 пг/мл до 10000 пг/мл. Количество свободного IL-18 в сыворотке здорового индивидуума, прежде всего здорового человека, составляет ≤5 пг/мл, прежде всего ≤4 пг/мл, прежде всего ≤1 пг/мл, прежде всего ≤0.5 pg/m, прежде всего, находится на уровне ниже предела обнаружения.
В частности, количество свободного IL-18 в образце, выделенном из организма индивидуума, прежде всего человека, страдающего от любого из указанных в настоящем описании заболеваний, составляет ≥5 пг/мл и, прежде всего, вплоть до 10000 пг/мл, в то время как количество свободного IL-18 в образце, взятом из организма здорового индивидуума, прежде всего здорового человека, составляет ≤4 пг/мл.
В другом варианте осуществления изобретения предложен набор биомаркеров, предназначенный для применения в любом из указанных выше способов обнаружения для дополнительной характеризации заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, для диагностирования предрасположенности к заболеванию или нарушению, указанному в одном из предыдущих вариантов осуществления изобретения, для мониторинга минимальной остаточной болезни у индивидуума или для прогнозирования чувствительности индивидуума к лечению с использованием ингибитора IL-18, фармацевтической композиции или экспрессионного вектора по одному из предыдущих вариантов осуществления изобретения, заключающегося в том, что определяют профиль биомаркеров и устанавливают корреляцию полученного профиля с конкретным заболеванием или нарушением.
В частности, биомаркер можно применять в способе диагностирования заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, для диагностирования предрасположенности к заболеванию или нарушению, указанному в одном из предыдущих вариантов осуществления изобретения, для мониторинга минимальной остаточной болезни у индивидуума или для прогнозирования чувствительности индивидуума к лечению с использованием ингибитора IL-18 по одному из предыдущих вариантов осуществления изобретения, IL-18BP по одному из предыдущих вариантов осуществления изобретения, или содержащей ингибитор IL-18 фармацевтической композиции по одному из предыдущих вариантов осуществления изобретения, заключающемся в том, что осуществляют стадии, на которых:
а) получают профиль биомаркеров для индивидуума, подлежащего обследованию, для чего берут образец общей воды организма указанного индивидуума;
б) получают профиль биомаркеров для здоровой референс-популяции;
в) получают профиль биомаркеров для популяции, страдающей от указанного заболевания или нарушения, и
г) сравнивают профиль биомаркеров, полученный на стадии а), с профилями, полученными на стадии б) и стадии в).
Еще одним объектом настоящего изобретения является набор биомаркеров, предназначенный для применения при диагностировании заболеваний или нарушения, указанных(ого) в одном из предыдущих вариантов осуществления изобретения, для диагностирования предрасположенности к заболеванию или нарушению, указанному в одном из предыдущих вариантов осуществления изобретения, или для применения для мониторинга минимальной остаточной болезни у индивидуума, или для прогнозирования чувствительности индивидуума к лечению с использованием ингибитора IL-18 по одному из предыдущих вариантов осуществления изобретения, IL-18BP по одному из предыдущих вариантов осуществления изобретения, или содержащей ингибитор IL-18 фармацевтической композиции по одному из предыдущих вариантов осуществления изобретения, включающий a) IL-18, IL-18BP, IL-13, IL-17A, IL-8, IL-1β, IL-2, IL-12, IL-4, IL-6, INF-γ, TNF-α, VEGF, EGF, HB-EGF, TGF-α, MMP-9, MMP-12, миелопероксидазу, кальпротектин, измеряемые с помощью иммуноанализа, TGF-α, тканевый ингибитор металлопротеиназ (TIMP-1), фактор роста гепатоцитов (HGF), индуцируемый гипоксией фактор 1 альфа (HIF-1α), фактор фон Виллебранда (vWF), EN-RAGE, S-RAGE, сурфактантный белок D, HsCRP, фибриноген, эндотелиальные микрочастицы и б) газы, включающие NO, СО, алканы, пентаны, этаны, измеряемые в композиции выдыхаемого воздуха.
Еще одним объектом настоящего изобретения является фармацевтический набор, содержащий ингибитор IL-18 по одному из предыдущих вариантов осуществления изобретения, связывающий интерлейкин-18 белок (IL-18BP) по одному из предыдущих вариантов осуществления изобретения, или фармацевтическую композицию, которая содержит ингибитор IL-18 по одному из предыдущих вариантов осуществления изобретения, и фармацевтически приемлемый носитель и/или эксципиент, предлагаемый в настоящем изобретении, в виде раздельных содержащих стандартную дозу форм, где указанные формы пригодны для введения в эффективных количествах.
В одном из вариантов осуществления настоящего изобретения предложен диагностический набор для обнаружения свободного IL-18, содержащий специфически связывающую свободный IL-18 молекулу по одному из предыдущих вариантов осуществления изобретения в качестве захватывающей молекулы, и вторую специфически связывающую IL-18 молекулу в качестве идентифицирующей молекулы и, необязательно, вторую специфически захватывающую IL-18 молекулу, где идентифицирующая молекула связывается с сайтами IL-18, отличными от тех, с которыми связывается захватывающая молекула.
В другом варианте осуществления изобретения предложен диагностический набор для обнаружения общего IL-18 или общего IL-18BP, содержащий первую специфически связывающую IL-18BP молекулу, которая не связывается с сайтом IL-18, с которым связывается IL-18BP, и вторую специфически связывающую IL-18 молекулу, которая не связывается с сайтом IL-18BP, с которым связывается IL-18.
Под объем изобретения подпадает также диагностический набор для обнаружения свободного IL-18BP, содержащий первую IL-18ВР-специфическую связывающую молекулу в качестве захватывающей молекулы, и вторую IL-18-специфическую связывающую молекулу в качестве идентифицирующей молекулы, где указанная идентифицирующая молекула связывается с сайтами IL-18BP, отличными от сайтов, с которыми связывается захватывающая молекула.
В одном из вариантов осуществления изобретения диагностический набор включает комбинацию нескольких или всех связывающих молекул, содержащихся в указанных выше диагностических наборах.
Еще одним объектом настоящего изобретения является диагностический набор для обнаружения свободного IL-18, содержащий IL-18-специфическое антитело по одному из предыдущих вариантов осуществления изобретения, в качестве захватывающего антитела или IL-18BP в качестве альтернативной захватывающей молекулы, и второе IL-18-специфическое идентифицирующее антитело или IL-18-специфическое антитело по одному из предыдущих вариантов осуществления изобретения, в качестве идентифицирующего антитела и второе IL-18-специфическое захватывающее антитело, где идентифицирующее антитело связывается с сайтами IL-18, отличными от сайтов, с которыми связывается захватывающая молекула.
Следующим объектом настоящего изобретения является диагностический набор для обнаружения общего IL-18 или общего IL-18BP, содержащий первое моноклональное IL-18ВР-специфическое антитело, которое не связывается с сайтом IL-18BP, с которым связывается IL-18, и второе IL-18-специфическое антитело, которое не связывается с сайтом IL-18, с которым связывается IL-18 ВР.
Еще одним объектом настоящего изобретения является диагностический набор для обнаружения свободного IL-18BP, содержащий первое моноклональное 1b-18ВР-специфическое захватывающее антитело и IL-18BP-специфическое идентифицирующее антитело, которое связывается с сайтом IL-18ВР, отличным от сайта, с которым связывается захватывающее антитело.
В другом варианте осуществления настоящего изобретения предложен диагностический набор, который содержит все диагностические наборы, представленные в любом из предыдущих вариантов осуществления изобретения.
Таким образом, в настоящем изобретении предложен IL-18BP, предназначенный для применения при лечении ассоциированного с IL-18 заболевания или нарушения у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, путем введения указанному индивидууму в терапевтически эффективном количестве по меньшей мере одного IL-18BP.
Следует иметь в виду, что в контексте настоящего изобретения IL-18BP включает также мутеины IL-18BP, функциональные фрагменты или производные IL-18BP, полученные в результате циклической перестановки производные IL-18 ВР, слитые белки, содержащие IL-18BP, изоформы IL-18BP или его соли.
IL-18BP можно получать в форме индивидуальной субстанции или в форме композиции, прежде всего фармацевтической композиции. Такие композиции могут содержать дополнительные медицинские средства, фармацевтические средства, носители, буферы, диспергирующие агенты, разбавители, совместно применяемые терапевтические средства, такие как противовоспалительные, бронходилататорные, антигистаминные, противозастойные или противокашлевые лекарственные субстанции и т.п. в зависимости от предполагаемого применения и пути введения.
Так, в настоящем изобретении предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, предназначенный/предназначенная для применения при лечении ассоциированного с IL-18 заболевания или нарушения у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к такому заболеванию или нарушению.
Кроме того, в настоящем изобретении предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для лечения ассоциированного с IL-18 заболевания или нарушения у индивидуума, нуждающегося в таком лечении, где ассоциированное с IL-18 заболевание или нарушение обусловлено избыточной экспрессией IL-18 в конкретных тканях и/или компартментах организма, которая приводит к дисбалансу IL-18/IL-18BP в указанных тканях и/или компартментах. Например, повышенная экспрессия IL-18, указанная в настоящем описании, приводит к повышенным уровням IL-18 в легком, сыворотке, мокроте, жидкости бронхоальвеолярного лаважа (BALF) или в кровотоке у указанного индивидуума по сравнению со здоровыми служащими в качестве контроля индивидуумами, прежде всего, к повышенным уровням IL-18 в мокроте и/или сыворотке.
Ассоциированное с IL-18 заболевание или нарушение, указанное в настоящем описании в различных вариантах осуществления настоящего изобретения, обусловлено повышенной экспрессией IL-18. Таким образом, как указано в настоящем описании, повышенная экспрессия IL-18 приводит к повышенным уровням IL-18 в легких, сыворотке, мокроте, жидкости бронхоальвеолярного лаважа (BALF) и/или кровотоке у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, по сравнению со здоровыми контрольными индивидуумами. Кроме того, повышенные уровни IL-18 приводят к дисбалансу IL-18/IL-18BP у индивидуума, страдающего от такого заболевания или нарушения.
В конкретном варианте осуществления настоящего изобретения предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения с целью компенсации дисбаланса IL-18/IL-18BP у индивидуума, страдающего от ассоциированного с IL-18 заболевания или нарушения, указанного в различных вариантах осуществления настоящего изобретения, или предрасположенного к такому заболеванию или нарушению, посредством улавливания избытка IL-18. В частности, IL-18BP позволяет снижать уровни IL-18 по сравнению с уровнями у не подвергнутого лечению индивидуума.
В другом варианте осуществления настоящего изобретения предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения при лечении ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем изобретении, где IL-18BP приводит к ингибированию экспрессии IL-18. В частности, IL-18BP позволяет снижать уровни IL-18 в направлении уровней у не подвергнутого лечению индивидуума.
В настоящем изобретении предложен/предложена также IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения при лечении индуцированных IL-18 местных или системных проявлений воспаления.
В настоящем изобретении предложен/предложена также IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения при лечении индуцированных IL-18 местных или системных проявлений воспаления и ассоциированных сопутствующих заболеваний, таких как эмфизема, воспаление тканей, разрушение тканей, резекция легкого, исчезновение сосудов, метаплазия слизистой оболочки, гипертрофия сердца, снижение уровня VEGF в ткани легких, утрата легочных сосудов, мускуляризация сосудов, отложение коллагена, наличие патологических слоев эластина в легких, фиброзное ремоделирование дыхательных путей, увеличение воздушного пространства, хроническое ремоделирование дыхательных путей и легочных сосудов и снижение легочной функции.
Согласно другому объекту настоящего изобретения повышенные уровни IL-18, указанные в настоящем изобретении, индуцируют повышенную экспрессию IFNγ, IL-13 или IL-17A у индивидуумов, страдающих от указанного ассоциированного с IL-18 заболевания или нарушения, по сравнению со здоровыми контрольными индивидуумами. Таким образом, в настоящем изобретении предложен/предложена также IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для модулирования, прежде всего, для снижения экспрессии и/или производства IFNγ, IL-13 или IL-17A у индивидуума.
В конкретных вариантах осуществления настоящего изобретения IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, приводит к ингибированию связывания IL-18 с рецептором IL-18 (IL-18R), прежде всего, связывания IL-18 с рецептором-α IL-18 (IL-18Rα).
Проявление ассоциированного с IL-18 заболевания или нарушения индуцируется Th1-цитокиновым ответом и/или Th2-цитокиновым ответом. Таким образом, применение согласно настоящему изобретению IL-18BP или фармацевтической композиции, содержащей IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, приводит к ингибированию Th1-цитокинового ответа и/или Th2-цитокинового ответа.
В конкретных вариантах осуществления настоящего изобретения IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, приводит к модуляции IL-18-зависимых низлежащих путей передачи сигнала, например, таких путей, которые регулируют производство и/или высвобождение TNF-альфа, IL-1-бета, IL-8, макрофагального воспалительного белка-альфа (MIP-альфа), IL-12, IL-15 и оксида азота. В частности, осуществляют ингибирование указанных сигнальных путей.
В одном из вариантов осуществления настоящего изобретения IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, предупреждает активацию каспазы. В частности, указанная каспаза представляет собой каспазу-1.
В одном из вариантов осуществления настоящего изобретения предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения при лечении ассоциированного с IL-18 заболевания, такого как хроническое обструктивное заболевание легких (COPD), заболевание сердца и диабет типа 2.
В одном из вариантов осуществления настоящего изобретения предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения при лечении ассоциированного с IL-18 заболевания, такого как хроническое обструктивное заболевание легких (COPD), связанное с трансфузией повреждение легких, бронхолегочная дисплазия (BPD), острый респираторный дистресс-синдром (ARDS), болезнь Стилла взрослых, болезнь Стилла детей, интерстициальная болезнь легких (ILD), идиопатический легочный фиброз, муковисцидоз, легочная артериальная гипертензия, астма, бронхоэктаз, сердечная недостаточность, амиотрофический боковой склероз (ALS), синдром сухого глаза (DED), кератит, язва и истирание роговицы, неоваскуляризация роговицы, патологическая внутриглазная неоваскуляризация, ирит, глаукома, дегенерация желтого пятна, синдром Шегрена, аутоиммунный увеит, болезнь Бехчета, конъюнктивит, аллергический конъюнктивит, дерматит века, диабет типа 2, болезнь жирной печени неалкогольной группы (NAFLD), стеатогепатит, трансплантация солидного органа и гематологическая трансплантация, повреждение, вызванное ишемией-реперфузией, семейная средиземноморская лихорадка, периодические синдромы, ассоциированные с рецептором 1 фактора некроза опухоли, криопирин-ассоциированные периодические синдромы лихорадки, гипер-IgD-синдромы, подагра, синдром Шнитцлера, гранулематоз Вегенера, называемый также гранулематозом с полиангиитом (GPA), тиреоидит Хашимото, болезнь Крона, неспецифический язвенный колит, связанные с иммуноглобулином-4 (IgG4) заболевания и терапии на основе стволовых клеток.
В конкретном варианте осуществления настоящего изобретения предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения при лечении ассоциированного с IL-18 заболевания легких, заболевания или нарушения сердца или сахарного диабета типа 2, указанных в настоящем описании.
Более конкретно, указанное подлежащее лечению ассоциированное с IL-18 заболевание или нарушение проявляется в легких индивидуума и может приводить к развитию хронического обструктивного заболевания легких (COPD), ассоциированного с системными проявлениями воспаления, и ассоциированных сопутствующих заболеваний, таких как эмфизема, воспаление тканей, деструкция тканей, резекция легкого, исчезновение сосудов, метаплазия слизистой оболочки, гипертрофия сердца, снижение уровня VEGF в ткани легких, утрата легочных сосудов, мускуляризация легочных сосудов, отложение коллагена в легких, наличие патологических слоев эластина в легких, фиброзное ремоделирование дыхательных путей, увеличение воздушного пространства, хроническое ремоделирование дыхательных путей и легочных сосудов и/или снижение легочной функции. В частности, указанное проявление представляет собой индуцированное дымом легочное воспаление. В конкретном варианте осуществления настоящего изобретения предложен/предложена IL-18BP или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для применения согласно настоящему изобретению при лечении хронического обструктивного заболевания легких (COPD).
Наблюдаемый дисбаланс IL-18/IL-18BP в организме индивидуума и, как следствие, заболевание или нарушение, указанное в настоящем описании, такое как COPD, может вызываться курением или воздействием пассивного курения, прежде всего воздействием табачного дыма, и/или вирусной инфекцией. В частности, воздействие сигаретного дыма может приводить к развитию индуцированных дымом эмфиземы и/или воспаления легких.
Согласно другому объекту настоящего изобретения ассоциированное с IL-18 заболевание или нарушение, подлежащее лечению, индуцируется продолжительным воздействием загрязнения воздуха.
Таким образом, в настоящем изобретении предложен/предложена также IL-18 ВР или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для лечения индуцированного IL-18 ремоделирования дыхательных путей и сосудов, и тем самым предупреждения проявления и развития заболевания, представляющего собой COPD.
Один из объектов настоящего изобретения относится к альвеолярным макрофагам, которые являются важным фактором повышения уровня IL-18. Так, предложенный/предложенная в настоящем изобретении IL-18BP или фармацевтическая композиция, содержащая IL-18ВР и фармацевтически приемлемый носитель и/или эксципиент, позволяет снижать экспрессию и/или производство IL-18 альвеолярными макрофагами.
В настоящем изобретении предложен/предложена также IL-18ВР или фармацевтическая композиция, содержащая IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, для предупреждения и/или ингибирования индуцированной дымом формой клеточной гибели клеток ткани легких и/или эпителиальных клеток, пораженных ассоциированным с IL-18 заболеванием или нарушением, указанным в настоящем описании. В частности, указанная индуцированная дымом форма клеточной гибели представляет собой апоптоз.
В одном из вариантов осуществления настоящего изобретения фармацевтическую композицию, предлагаемую в изобретении и представленную в настоящем описании, вводят в профилактических целях.
В другом варианте осуществления настоящего изобретения фармацевтическую композицию, предлагаемую в изобретении и представленную в настоящем описании, вводят в терапевтических целях.
В одном из вариантов осуществления настоящего изобретения фармацевтическую композицию, предлагаемую в изобретении и описанную в различных вариантах осуществления изобретения, вводят индивидууму, страдающему от ассоциированного с IL-18 заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, путем системного, интраназального, внутриглазного, интравитреального введения, с помощью глазных капель, трансбуккального, орального введения, введения через слизистую оболочку, внутритрахеального, внутривенного, подкожного введения, введения в мочевой тракт, интраректального, интравагинального, подъязычного, внутрибронхиального, внутрилегочного, чрескожного или внутримышечного введения. В частности, фармацевтическую композицию, предлагаемую в изобретении и описанную в различных вариантах осуществления изобретения, вводят путем бронхолегочного введения.
Фармацевтическую композицию, предлагаемую в изобретении и описанную в различных вариантах осуществления изобретения, представленных в настоящем описании, можно приготавливать в виде жидкости, жидкого спрея, микросфер, полутвердой субстанции, геля или порошка для введения через слизистую оболочку, например, интраназального, трансбуккального введения, введения через слизистую оболочку ротовой полости, внутритрахеального, введения в мочевой тракт, интравагинального, подъязычного, внутрибронхиального, внутрилегочного и/или чрескожного введения. Кроме того, композиция может находиться в виде твердой формы лекарственного средства для трансбуккального введения, введения через слизистую оболочку в ротовой полости и/или подъязычного введения. Интраназальное, трансбуккальное введение, внутритрахеальное введение через ротовую полость, введение в мочевой тракт, интравагинальное введение, введение через слизистую оболочку и подъязычное введение приводит к расщеплению представленной в настоящем описании композиции в ротовой полости при температуре тела и необязательно может приводить к ее прилипанию в ротовой полости к ткани организма. Кроме того, представленная в настоящем описании композиция может включать один или несколько эксципиентов, разбавителей, связующих веществ, замасливателей, улучшающих скольжение веществ, разрыхлителей, десенсибилизаторов, эмульгаторов, адгезивов для слизистой оболочки, солюбилизаторов, суспендирующих агентов, модификаторов вязкости, обеспечивающих ионную тоничность агентов, буферов, носителей, сурфактантов, ароматизаторов или их смесь.
В конкретном варианте осуществления настоящего изобретения композицию приготавливают в форме для парентерального, внутривенного введения, в форме таблетки, пилюли, биоадгезивного пластыря, капель, губки, пленки, пастилки, твердого леденца, вафли, шарика, в форме «леденца на палочке», дискообразной структуры, суппозитория или спрея.
Введение через слизистую оболочку, как правило, является быстрым благодаря обширной сосудистой сети в слизистой оболочке и отсутствию роговичного слоя, присутствующего в эпидермисе. Такой путь транспортирования лекарственного средства, как правило, обеспечивает быстрое увеличение концентраций в крови и позволяет также избегать попадания в энтерогепатический кровоток и немедленного расщепления кислотами желудочного сока или частично эффектов «первого прохождения» через стенку кишечника и метаболизма в печени. Для лекарственных средств, как правило, требуется обеспечивать их продолжительное воздействие на поверхность слизистой оболочки для того, чтобы имела место значительная абсорбция лекарственного средства.
Пути введения через слизистую оболочку могут оказаться также более эффективными, чем оральный путь, поскольку эти пути могут обеспечивать относительно быструю абсорбцию и начало терапевтического действия. Кроме того, пути введения через слизистую оболочку могут оказаться предпочтительными для применения при лечении пациентов, которым трудно проглатывать таблетки, капсулы или другие твердые оральные формы, или у которых вследствие заболевания нарушена кишечная абсорбция. Таким образом, введение IL-18BP или фармацевтической композиции, содержащей IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, через слизистую оболочку имеет целый ряд преимуществ.
В случае интраназального или трансбуккального путей введения, абсорбцию лекарственного средства можно задерживать или пролонгировать, или поглощение можно осуществлять почти так же быстро, как и в случае внутривенного болюсного введения. Благодаря высокой проницаемости, обеспечиваемой интенсивным кровоснабжением, подъязычный путь введения может обеспечивать быстрое начало действия.
Интраназальные композиции можно вводить любым пригодным для их формы методом. Композицию, включающую микросферы или порошок, можно вводить с помощью назального инсуффлятора. Примеры таких устройств хорошо известны специалистам в данной области и включают поступающие в продажу системы для порошка, такие как Fisons Lomudal System. Инсуффлятор создает облако из тонко распыленного порошка или микросфер. Инсуффлятор предпочтительно снабжен механизмом, гарантирующим введение композиции в практически фиксированном количестве. Порошок или микросферы можно применять непосредственно с помощью инсуффлятора, который снабжен флаконом или контейнером для порошка или микросфер. Альтернативно этому, порошком или микросферами можно заполнять капсулу, такую как желатиновая капсула, или другое однодозовое устройство, пригодное для назального введения. Инсуффлятор предпочтительно имеет механизм для вскрытия капсулы или другого устройства. Кроме того, композиция может обеспечивать сначала быстрое высвобождение действующего вещества и затем замедленное высвобождение действующего вещества, например, путем применения более одного типа микросфер или порошка. Кроме того, обычному специалисту в данной области должны быть хорошо известны альтернативные методы, пригодные для введения композиции в носовую полость. Можно применять любой пригодный метод. Более подробное описание пригодных методов изложено в ЕР 2112923, ЕР 1635783, ЕР 1648406, ЕР 2112923 (полное содержание которых включено в настоящее описание в качестве ссылки).
В одном из вариантов осуществления настоящего изобретения фармацевтическую композицию, предлагаемую в изобретении и описанную в различных вариантах осуществления изобретения, представленных в настоящем описании, можно вводить также интраназально, т.е. путем ингаляции, и, таким образом, ее можно приготавливать в форме, пригодной для интраназального введения, т.е. в виде аэрозоля, формы в виде сухого порошка или жидкого препарата.
Примеры пригодных фармацевтических носителей, эксципиентов и/или разбавителей хорошо известны в данной области и включают (но, не ограничиваясь только ими) камедь, крахмал (например, кукурузный крахмал, предварительно желированный крахмал), сахар (например, лактозу, маннит, сахарозу, декстрозу), производные целлюлозы (например, микрокристаллическую целлюлозу), акрилат (например, полиметилакрилат), карбонат кальция, оксид магния, тальк или их смеси.
Фармацевтически приемлемые носители для жидких препаратов представляют собой водные или неводные растворы, суспензии, препараты на основе сухого порошка, эмульсии или масла. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль и инъекционные сложные органические эфиры, такие как этилолеат. Примерами масел являются масла животного, растительного или синтетического происхождения, например, арахисовое масло, соевое масло, оливковое масло, подсолнечное масло, рыбий жир, другие масла из морепродуктов или липиды из молока или яиц.
Настоящее изобретение относится также к транслегочному введению посредством ингаляции фармацевтической композиции, предлагаемой в изобретении и описанной в различных вариантах осуществления изобретения, представленных в настоящем описании, в форме сухого порошка, газообразных или летучих препаративных форм в системный кровоток через дыхательные пути. Абсорбция происходит практически с такой же скоростью, с какой препарат может поступать в альвеолы легких, поскольку альвеолярные и сосудистые эпителиальные мембраны являются хорошо проницаемыми, поток крови является обильным и имеется очень большая поверхность для адсорбции. Например, аэрозоли можно вводить с помощью упакованных под давлением дозирующих ингаляторов (MDI).
Фармацевтическую композицию, предлагаемую в изобретении и описанную в различных вариантах осуществления изобретения, представленных в настоящем описании, как правило, следует вводить в смеси с пригодным фармацевтическим эксципиентом, разбавителем или носителем, выбранным с учетом предполагаемых средств введения и стандартной фармацевтической практики.
В другом варианте осуществления изобретения препарат IL-18ВР или препарат фармацевтической композиции, содержащей IL-18BP, находится в форме сухого порошка, необязательно в сочетании по меньшей мере с одним состоящим из частиц фармацевтически приемлемым носителем, которым может являться один или несколько материалов, известных в качестве фармацевтически приемлемых носителей, предпочтительно выбранных из материалов, которые известны в качестве носителей, применяемых в композициях в виде сухого порошка для ингаляции, например, сахариды, включая моносахариды, дисахариды, полисахариды и сахарные спирты, такие как арабиноза, глюкоза, фруктоза, рибоза, манноза, сахароза, трегалоза, лактоза, мальтоза, крахмалы, декстран, маннит или сорбит. Наиболее предпочтительным носителем является лактоза, например, моногидрат лактозы или безводная лактоза. Сухой порошок может содержаться в виде стандартных доз в капсулах, например, желатиновых или пластиковых, или в блистерах (например, алюминиевых или пластиковых), предназначенных для применения в ингаляционном устройстве для сухого порошка, которое может представлять собой однодозовое или многодозовое устройство, предпочтительно в виде стандартных доз вместе с носителем, взятым в количествах, достаточных для доведения общей массы порошка в капсуле до 5-50 мг. Альтернативно этому сухой порошок может содержаться в резервуаре адаптированного для введения многих доз ингаляционного устройства для сухого порошка (MDDPI).
Можно применять любой другой терапевтически эффективный путь введения, например, абсорбцию через эпителиальную или эндотелиальную ткани, или генную терапию, при которой пациенту вводят (например, с использованием экспрессионного вектора) молекулу ДНК, кодирующую активный агент, что приводит к экспрессии активного агента и его секреции in vivo.
В организме экспрессию IL-18BP можно индуцировать путем модулирования вышележащих путей передачи сигнала, которые контролируют экспрессию IL-18BP. Например, IL-18BP специфически индуцируется IFN-гамма в качестве компонента петли негативной обратной связи, которая регулирует индукцию IFN-гамма с помощью IL-18. Другими известными факторами, которые, как известно, регулируют экспрессию IL-18BP, являются IL-18, IL-27, IFN-альфа и STAT1.
Так, в одном из вариантов осуществления настоящего изобретения клеточную экспрессию IL-18BP индуцируют косвенным образом путем модификации одного или нескольких вышележащих путей передачи сигнала, которые контролируют экспрессию IL-18BP. В частности, экспрессию IL-18BP индуцируют косвенным образом путем модификации по меньшей мере одного вышележащего пути передачи сигнала.
Изобретение относится также к экспрессионному вектору, содержащему кодирующую последовательность IL-18BP, в препарате лекарственного средства, предназначенного для лечения ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения.
Конкретный вариант осуществления настоящего изобретения относится к экспрессионному вектору, содержащему кодирующую последовательность регуляторного фактора, который модулирует вышележащие пути передачи сигнала, регулирующие экспрессию IL-18BP. Таким образом, указанный регуляторный фактор индуцирует экспрессию IL-18BP посредством модулирования по меньшей мере одного вышележащего пути передачи сигнала.
Изобретение относится также экспрессионному вектору, содержащему кодирующую последовательность регуляторного фактора, который модулирует вышележащие пути передачи сигнала, регулирующие экспрессию IL-18BP, в препарате лекарственного средства, предназначенного для лечения ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании, у индивидуума, страдающего таким заболеванием или нарушением, или предрасположенному к развитию такого заболевания или нарушения.
Изобретение относится также к экспрессионному вектору, содержащему кодирующую последовательность регуляторного фактора, который индуцирует экспрессию IL-18BP, предназначенному для лечения ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения. В частности, оно относится к экспрессионному вектору, содержащему кодирующую последовательность регуляторного фактора, который индуцирует экспрессию IL-18BP в легких, предназначенному для лечения ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения.
В настоящем изобретении необязательно предложен второй экспрессионный вектор, содержащий кодирующую последовательность второго встречающегося в естественных условиях ингибитора провоспалительных цитокинов или регуляторного фактора, который модулирует по меньшей мере один вышележащий путь передачи сигнала, регулирующего экспрессию указанных провоспалительных цитокинов. В частности, указанный регуляторный фактор индуцирует экспрессию указанного ингибитора цитокинов.
В частности, экспрессию IL-18 модулируют с помощью РНК-интерференции (PHKi) или антисмыслового экспрессионного вектора IL-18. Более конкретно, экспрессию IL-18 модулируют с помощью РНК-интерференции (PHKi), при этом осуществляют понижающую регуляцию экспрессии IL-18 посредством посттранскрипционного «молчания» гена (PTGS). В частности, осуществляют понижающую регуляцию экспрессии IL-18 в легких индивидуума, страдающего от указанного в настоящем описании заболевания или нарушения. Механизм РНК-интерференции заключается в осуществлении любого посттрансляционного события, приводящего, к «молчанию» гена, прежде всего любого приводящего, к «молчанию» гена посттрансляционного события, которое индуцируется микроРНК (miPHK) или малой интерферирующей РНК (siPHK). Экспрессию микроРНК (miPHK) и малых интерферирующих РНК (siPHK) можно осуществлять с использованием экспрессионных векторов, предлагаемых в изобретении и представленных в настоящем описании.
Таким образом, терапевтический подход, основанный на применении генов, можно применять для лечения ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании и описанного в различных вариантах осуществления изобретения. В этом случае экспрессия IL-18BP происходит in situ, следовательно, имеет место нейтрализация IL-18 непосредственно в ткани или клетках, пораженных указанным заболеванием или нарушением. В частности, экспрессию IL-18BP, указанного в настоящем описании, индуцируют в легких.
Фармацевтическую композицию, предлагаемую в изобретении и представленную в настоящем описании в различных вариантах осуществления изобретения, можно применять для лечения ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании и представленного в различных вариантах осуществления изобретения, в медицине человека и в ветеринарной медицине для лечения человека и животных, включая птиц, приматов кроме человека, собак, кошек, свиней, коз, овец, коров, лошадей, мышей, крыс и кроликов.
В конкретном варианте осуществления настоящего изобретения предложена фармацевтическая композиция, предлагаемая в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, для применения при лечении ассоциированного с IL-18 заболевания или нарушения, указанного в настоящем описании в различных вариантах осуществления изобретения, где индивидуум представляет собой млекопитающее, в частности, индивидуум представляет собой человека.
В другом конкретном варианте осуществления изобретения фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, вводят в терапевтически эффективном количестве в сочетании с пригодной дозой по меньшей мере второго ингибитора провоспалительных цитокинов. В частности, указанный ингибитор обладает специфичностью в отношении IL-1, IL-6, IL-13, IL-17A, IFNγ или TNFα.
Водные носители включают воду, спиртовые/водные растворы, эмульсии или суспензии, в том числе физиологический раствор и забуференные среды, такие как забуференные фосфатом физиологические растворы, вода, эмульсии, такие как эмульсии типа масло/вода, различные типы смачивающих агентов, стерильные растворы и т.д. Композиции, содержащие такие носители, можно приготавливать с помощью хорошо известных общепринятых методов. Пригодные носители могут включать любой материал, который при объединении с биологически активным соединением, предлагаемым в изобретении, сохраняет его биологическую активность.
В данной области предпринимались усилия для осуществления химической модификации барьерных свойств кожи с целью обеспечения проникновения определенных агентов, повышения эффективности доставляемых агентов, увеличения времени доставки, снижения доставляемых доз, уменьшения побочных действий, обусловленных различными методами доставки, уменьшения реакций пациентов и т.д.
В этой связи для увеличения проницаемости кожи для лекарственных средств применяли усиливающие проникновение вещества, которые часто представляли собой растворители, являющиеся акцепторами протонов, такие как диметилсульфоксид (ДМСО) и диметилацетамид. Другие усиливающие проникновение вещества, которые были изучены и оказались эффективными, включают 2-пирролидин, N,N-диэтил-м-толуамид (Deet), 1-додекалазациклогептан-2-он, N,N-диметилформамид, N-метил-2-пирролидин, тиогликолят кальция, гексанол, жирное кислоты и сложные эфиры, производные пирролидона, производные 1,3-диоксанов и 1,3-диоксоланов, 1-N-додецил-2-пирролидон-5-карбоновую кислоту, 2-пентил-2-оксопирролидинуксусную кислоту, 2-додецил-2-оксо-1-пирролидинуксусную кислоту, 1-азациклогептан-2-он-2-додецилуксусную кислоту и производные аминоспиртов, включая, среди прочего, производные 1,3-диоксанов.
Препараты для введения через слизистую оболочку могут включать стерильные водные и неводные растворы, суспензии, препараты на основе сухого порошка и эмульсии. Примерами неводных растворителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и инъекционные сложные органические эфиры, такие как этилолеат. Водные носители включают воду, спиртовые/водные растворы, эмульсии или суспензии, включая физиологический раствор и забуференные среды. Наполнители, применяемые для введения через слизистую оболочку, могут включать раствор хлорида натрия, декстрозу Рингера, декстрозу и хлорид натрия, лактированный раствор Рингера или нелетучие масла. Могут присутствовать также консерванты и другие добавки, включая, например, противомикробные средства, антиоксиданты, хелатирующие агенты и инертные газы и т.п. Кроме того, фармацевтическая композиция, предлагаемая в настоящем изобретении, может содержать белковые носители, такие, например, как сывороточный альбумин или иммуноглобулин, предпочтительно человеческого происхождения.
Фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, можно наносить местно на участки поверхности тела и, таким образом, ее следует приготавливать в форме, пригодной для местного нанесения. Пригодные препараты для местного применения включают гели, мази, кремы, лосьоны, капли и т.п. Для местного применения фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, получают и применяют в виде раствора, суспензии или эмульсии в физиологически приемлемом разбавителе с использованием фармацевтического носителя или без него.
Фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, можно вводить также в виде композиций с контролируемым высвобождением, т.е. композиций, из которых высвобождение действующего вещества происходит в течение некоторого периода времени после введения. Композиции с контролируемым или продолжительным высвобождением включают препараты, включенные в липофильные депо (например, жирные кислоты, воски, масла). В другом варианте осуществления изобретения композиция представляет собой композицию с немедленным высвобождением, т.е. композицию, из которой все действующее вещество высвобождается сразу после введения.
Другие примеры пригодных препаративных форм приведены в WO 2006/085983, полное содержание которой включено в настоящее описание в качестве ссылки. Например, фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, согласно настоящему изобретению можно приготавливать в виде липосомальных препаративных форм. Технология получения липосомальных суспензий хорошо известна в данной области. Применяемый липидный слой может иметь любой общепринятый состав и может, как содержать холестерин, так и не содержать холестерин. Размер липосом можно уменьшать путем использования стандартных методов облучения ультразвуком и гомогенизации. Липосомальные препаративные формы, содержащие фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, можно лиофилизировать с получением лиофилизата, который можно восстанавливать с использованием фармацевтически приемлемого носителя, такого как вода, для восстановления липосомальной суспензии. Фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, можно вводить индивидууму в пригодной дозе. Схему дозирования должен определять лечащий врач с учетом клинических факторов. Как хорошо известно, в области медицины, дозы для любого конкретного индивидуума должны зависеть от многих факторов, включая размер индивидуума, площадь поверхности тела, конкретного подлежащего введению соединения, пола, продолжительности и пути введения, общего состояния здоровья и других одновременно вводимых лекарственных средств.
Кроме того, следует иметь в виду, что, в зависимости от предполагаемого применения фармацевтической композиции, фармацевтическая композиция, предлагаемая в изобретении, может содержать дополнительные биологически активные субстанции. Указанные дополнительные биологически активные субстанции могут представлять собой, например, антитела, фрагменты антител, гормоны, факторы роста, ферменты, связывающие молекулы, цитокины, хемокины, молекулы нуклеиновой кислоты и лекарственные средства. В предпочтительном варианте осуществления изобретения фармацевтическую композицию, предлагаемую в настоящем изобретении, следует вводить совместно с агонистом бета-адренорецептора длительного действия (LABA), мускариновыми антагонистами длительного действия (LAMA), стероидами, кортикостероидом, глюкокортикоидом и глюкокортикоидными агонистами, ингибиторами фосфодиэстеразы, киназными ингибиторами, цитокиновыми и хемокиновыми ингибиторами или антагонистами, или протеазными ингибиторами, или их комбинациями.
Доза фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, должна зависеть от состояния, подлежащего лечению, конкретной применяемой композиции и других клинических факторов, таких как вес, размер и состояние индивидуума, площадь поверхности тела, конкретное соединение или композиция, предназначенное/предназначенная для введения, другие одновременно вводимые лекарственные средства и путь введения.
Фармацевтическую композицию предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, можно вводить в сочетании с другими биологически активными субстанциями и процедурами для лечения симптомов, связанных с ассоциированным с IL-18 заболеванием, таким как хроническое обструктивное заболевание легких (COPD), связанное с трансфузией повреждение легких, бронхолегочная дисплазия (BPD), острый респираторный дистресс-синдром (ARDS), болезнь Стилла взрослых, болезнь Стилла детей, интерстициальная болезнь легких (ILD), идиопатический легочный фиброз, муковисцидоз, легочная артериальная гипертензия, астма, бронхоэктаз, сердечная недостаточность, амиотрофический боковой склероз (ALS), синдром сухого глаза (DED), кератит, язва и истирание роговицы, неоваскуляризация роговицы, патологическая внутриглазная неоваскуляризация, ирит, глаукома, дегенерация желтого пятна, синдром Шегрена, аутоиммунный увеит, болезнь Бехчета, конъюнктивит, аллергический конъюнктивит, дерматит века, диабет типа 2, болезнь жирной печени неалкогольной группы (NAFLD), стеатогепатит, трансплантация солидного органа и гематологическая трансплантация, повреждение, вызванное ишемией-реперфузией, семейная средиземноморская лихорадка, периодические синдромы, ассоциированные с рецептором 1 фактора некроза опухоли, криопирин-ассоциированные периодические синдромы лихорадки, гипер-IgD-синдромы, подагра, синдром Шнитцлера, гранулематоз Вегенера, называемый также гранулематозом с полиангиитом (GPA), тиреоидит Хашимото, болезнь Крона, неспецифический язвенный колит, связанные с иммуноглобулином-4 (IgG4) заболевания и терапии на основе стволовых клеток. Другие биологически активные субстанции могут представлять собой часть одной и той же композиции, уже содержащей композицию, предлагаемую в изобретении, в форме смеси, в которой композиция, предлагаемая в изобретении, и другая биологически активная субстанция смешаны в одном и том же фармацевтически приемлемом растворителе и/или носителе, или с ним, или могут находиться по отдельности в виде части раздельных композиций, которые могут поставляться по отдельности или вместе в форме набора компонентов.
Фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, можно вводить одновременно с другой(ими) биологически активной(ыми) субстанцией или субстанциями, поочередно или последовательно. Например, композицию, предлагаемую в изобретении, можно вводить одновременно с первой дополнительной биологически активной субстанцией или последовательно после или до введения указанной композиции. Если выбирают схему введения, при которой вводят более одной дополнительной биологически активной субстанции и по меньшей мере одну композицию, предлагаемую в изобретении, то часть соединений или субстанций можно вводить одновременно, а часть последовательно в различных комбинациях.
Так, другим объектом настоящего изобретения являются смеси, включающие фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, необязательно содержащие одну или несколько дополнительных биологически активных субстанций в терапевтически или профилактически эффективном количестве, а также способы применения такой композиции, предлагаемой в изобретении, или включающих ее смесей для предупреждения и/или терапевтического лечения, и/или облегчения воздействий хронического обструктивного заболевания легких (COPD), заболевания сердца и диабета типа 2.
Так, еще объектом настоящего изобретения являются смеси, включающие фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, необязательно содержащие одну или несколько дополнительных биологически активных субстанций в терапевтически или профилактически эффективном количестве, а также способы применения такой композиции, предлагаемой в изобретении, или включающих ее смесей для предупреждения и/или терапевтического лечения, и/или облегчения воздействий хронического обструктивного заболевания легких (COPD), связанного с трансфузией повреждения легких, бронхолегочной дисплазии (BPD), острого респираторного дистресс-синдрома (ARDS), болезни Стилла взрослых, болезни Стилла детей, интерстициальной болезни легких (ILD), идиопатического легочного фиброза, муковисцидоза, легочной артериальной гипертензии, астмы, бронхоэктаза, сердечной недостаточности, амиотрофического бокового склероза (ALS), синдрома сухого глаза (DED), кератита, язвы и истирания роговицы, неоваскуляризации роговицы, патологической внутриглазной неоваскуляризации, ирита, глаукомы, дегенерации желтого пятна, синдрома Шегрена, аутоиммунного увеита, болезни Бехчета, конъюнктивита, аллергического конъюнктивита, дерматита века, диабета типа 2, болезни жирной печени неалкогольной группы (NAFLD), стеатогепатита, трансплантации солидного органа и гематологической трансплантации, повреждения, вызванного ишемией-реперфузией, семейной средиземноморской лихорадки, периодических синдромов, ассоциированных с рецептором 1 фактора некроза опухоли, криопирин-ассоциированных периодических синдромов лихорадки, гипер-IgD-синдромов, подагры, синдрома Шнитцлера, гранулематоза Вегенера, называемого также гранулематозом с полиангиитом (GPA), тиреоидита Хашимото, болезни Крона, неспецифического язвенного колита, связанных с иммуноглобулином-4 (IgG4) заболеваний и терапии на основе стволовых клеток.
Другая биологически активная субстанция или соединение может оказывать свое биологическое действие посредством того же самого механизма, что и композиция, предлагаемая в изобретении, или сходного с ним механизма, или посредством неродственного механизма, или посредством нескольких родственных и/или неродственных механизмов действия.
В целом, другое биологически активное соединение может включать антитела, выработанные против INF-гамма, IL-17A, IL-13, IL-1-бета, IL-6, IL-2, IL-4, IL-12, TNF-альфа и связывающиеся с ними. В частности, смесь, предлагаемая в изобретении, может содержать IL-18BP (IL-18BP) или предлагаемую в изобретении и представленную в настоящем описании фармацевтическую композицию, которая содержит IL-18BP (IL-18BP) и фармацевтически приемлемый носитель и/или эксципиент.
Пригодные дозы фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, могут варьироваться в зависимости от состояния, возраста и вида индивидуума, и их легко могут определять специалисты в данной области. Общие суточные дозы, применяемые как в ветеринарии, так и в медицине человека, могут соответственно находиться в пределах 0,01-2000 мг/кг веса тела, предпочтительно от 0,1 до 1000 мг/кг веса тела, предпочтительно от 1 до 100 мг/кг, и их можно вводить в виде однократных или разделенных доз, кроме того, верхний предел может быть также превышен, если установлено, что это показано. Указанные дозы следует регулировать в каждом конкретном случае с учетом индивидуальных требований, включая конкретное(ые) соединение(я), подлежащее(ие) введению, путь введения, состояние, подлежащее лечению, а также индивидуума, подвергающегося лечению. Однако соединения можно вводить также в виде препаратов в форме депо (имплантатов, препаративных форм с медленным высвобождением и т.д.) еженедельно, ежемесячно или даже с еще более продолжительными интервалами времени. В таких случаях доза может быть намного больше, чем суточная доза, и она должна быть адаптирована к форме введения, весу тела и конкретному показанию. Соответствующую дозу можно определять путем осуществления общепринятых тестов на моделях, предпочтительно на созданных на животных моделях. Эффективная доза действующего(их) вещества(веществ) зависит по меньшей мере от природы состояния, подлежащего лечению, токсичности, от того, применяют соединение(я) для профилактики или для лечения активной инфекции или состояния, от метода введения и от фармацевтической препаративной формы, и ее должен определять клиницист на основе общепринятых опытов с использованием повышающихся доз. Следует ожидать, что она может составлять от примерно 0,01 мг до примерно 1 г/кг веса тела в день. Например, для местного применения предполагаемая суточная доза для взрослого человека с весом тела примерно 70 кг может находиться в пределах от примерно 1 мг до примерно 500 мг, как правило, от примерно 5 мг до примерно 40 мг, и ее можно вводить в виде однократной дозы или в виде нескольких доз, или в одно или несколько мест введения. Для интраназального введения можно ожидать, что предполагаемая доза может составлять от примерно 0,01 мг до примерно 1 г/кг веса тела в день.
Кроме того, функциональные производные IL-18 ВР можно конъюгировать с полимерами для улучшения характеристик белка, таких как стабильность, время полужизни, биодоступность, переносимость человеческим организмом или иммуногенность. Для достижения указанной цели IL18-BP можно связывать, например, с полиэтиленгликолем (ПЭГ). ПЭГилирование можно осуществлять с помощью известных методов, которые описаны, например, в WO 92/13095.
Таким образом, в следующем варианте осуществления настоящего изобретения IL-18BP является ПЭГилированным.
Еще в одном варианте осуществления изобретения IL-18BP представляет собой слитый белок, содержащий полный IL-18BP или его часть, слитый/слитую с полным иммуноглобулином или его частью.
В другом варианте осуществления изобретения IL-18BP является ПЭГилированным, слитым с полным иммуноглобулином или его частью, предпочтительно с константной областью иммуноглобулина, где слитый белок все еще обладает способностью связываться с IL-18. Более конкретно, иммуноглобулин может быть IgG1- или IgG2-изотипа.
Специалисту в данной области должно быть очевидно, что полученный слитый белок сохраняет биологическую активность IL-18BP, в частности, способность связываться с IL-18. Слияние может быть непосредственным или через короткий линкерный пептид, имеющий длину от 1 до 3 или более аминокислотных остатков. Указанный линкер может представлять собой трипептид, например, имеющий последовательность E-F-M (Glu-Phe-Met) (SEQ ID NO: 9), или состоящую из 13 аминокислот линкерную последовательность, содержащую Glu-Phe-Gly-Ala-Gly-Leu-Val-Leu-Gly-Gly-Gln-Phe-Met (SEQ ID NO: 8), которая интродуцирована между последовательностью IL-18BP и последовательностью иммуноглобулина. Полученный слитый белок обладает улучшенными характеристиками, такими как удлиненное время нахождения в общей воде организма (время полужизни), повышенная специфическая активность, повышенный уровень экспрессии, или слитый белок может легче поддаваться очистке.
Предпочтительно его сливают с областями тяжелой цепи, такими, например, как СН2- и СН3-домены человеческого IgG1. Получение специфических слитых белков, содержащих IL-18BP и часть иммуноглобулина, описано, например, в примере 11 WP 99/09063. Для создания слитых белков, предлагаемых в изобретении, можно применять также и другие изоформы молекул Ig, такие как изоформы IgG2 или IgG4, Ig других классов, например, типа IgM или IgA. Слитые белки могут быть мономерными или мультимерными, гетеро- или гомомультимерными.
В других конкретных вариантах осуществления настоящего изобретения предложен способ лечения индивидуума, страдающего от заболевания или нарушения, ассоциированного с избыточной экспрессией IL-18, указанного в настоящем описании в различных вариантах осуществления настоящего изобретения, или предрасположенного к развитию указанного заболевания или нарушения, заключающийся в том, что указанному индивидууму вводят в терапевтически эффективном количестве фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения.
Серологические анализы хорошо известны в данной области, и они стали полезным инструментом для обнаружения антигенов в общей воде организма, такой как сыворотка, жидкость бронхоальвеолярного лаважа (BAL) и мокрота. Однако, до настоящего времени не существовало функционального диагностического анализа для обнаружения IL-18 с использованием специфических антител. Таким образом, существует конкретная потребность в диагностическом методе обнаружения IL-18 в общей воде организма, прежде всего в сыворотке.
Таким образом, в настоящем изобретении предложены способы и наборы для обнаружения и диагностирования ассоциированных с IL-18 заболеваний или состояний, указанных в настоящем описании, для диагностирования предрасположенности к ассоциированному с IL-18 заболеванию или состоянию, указанному в настоящем описании, или для мониторинга минимальной остаточной болезни у индивидуума, или для прогнозирования чувствительности индивидуума к лечению с использованием фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения и описана выше. Указанные способы включают известные иммунологические методы, которые обычно применяют для обнаружения или количественной оценки субстанций в биологических образцах или в условиях in situ.
В одном из вариантов осуществления настоящего изобретения предложен также способ диагностирования ассоциированного с IL-18 заболевания, указанного в настоящем описании, или диагностирования предрасположенности к ассоциированному с IL18 заболеванию, указанному в настоящем описании, или мониторинга минимальной остаточной болезни у индивидуума, или прогнозирования чувствительности индивидуума к лечению с использованием IL-18BP или фармацевтической композиции, содержащей IL-18BP (IL-18BP) и фармацевтически приемлемый носитель и/или эксципиент, по одному из предыдущих вариантов осуществления изобретения, заключающийся в том, что осуществляют стадии, на которых:
а) получают образец общей воды организма пациента, страдающего указанным заболеванием;
б) анализируют указанный образец в отношении присутствия IL-18 путем использования IL-18BP, указанного в настоящем описании, или IL-18-специфического антитела, предлагаемого в настоящем изобретении, в качестве захватывающей молекулы;
в) определяют количество IL-18, связанного с захватывающей молекулой в образце;
г) сравнивают количество IL-18 в образце, взятом из организма индивидуума, страдающего от указанного заболевания, с количеством в образце, взятом из организма здорового индивидуума.
Количество свободного IL-18 в сыворотке, выделенной из организма индивидуума, прежде всего человека, страдающего от указанного заболевания, находится в пределах от 5 до 10000 пг/мл, прежде всего в пределах от 100 до 10000 пг/мл, прежде всего в пределах от 200 до 10000 пг/мл, прежде всего в пределах от 300 до 10000 пг/мл, прежде всего в пределах от 400 до 10000 пг/мл, прежде всего в пределах от 500 до 10000 пг/мл, прежде всего в пределах от 600 до 10000 пг/мл, прежде всего в пределах от 700 до 10000 пг/мл, прежде всего в пределах от 800 до 10000 пг/мл, прежде всего в пределах от 900 до 10000 пг/мл, прежде всего в пределах от 1000 до 10000 пг/мл, прежде всего в пределах от 1500 до 10000 пг/мл, прежде всего в пределах от 2000 до 10000 пг/мл, прежде всего в пределах от 3000 до 10000 пг/мл, прежде всего в пределах от 4000 до 10000 пг/мл, прежде всего в пределах от 5000 до 10000 пг/мл. Количество свободного IL-18 в сыворотке здорового индивидуума, прежде всего здорового человека, составляет ≤40 пг/мл, прежде всего ≤30 пг/мл, прежде всего ≤25 пг/мл, прежде всего ≤20 пг/мл, прежде всего ≤10 пг/мл, прежде всего ≤5 пг/мл, прежде всего ≤1 пг/мл, прежде всего ≤0,5 пг/мл. Таким образом, индивидуум, у которого обнаруживаемая концентрация IL-18 в сыворотке составляет от 5 до 10000 пг/мл, страдает от ассоциированного с IL-18 заболевания, указанного в настоящем описании. Количество IL-18 в сыворотке и другой общей воде организма можно определять с помощью диагностического способа, представленного в настоящем описании, с использованием линейной стандартной кривой, которую рассчитывают для заранее определенных концентраций IL-18 в диапазоне от 5 до 200 пг/мл.
Диагностирование ассоциированного с IL-18 заболевания или состояния или определение предрасположенности к ассоциированному с IL-18 заболеванию или состоянию, указанному в настоящем описании, у индивидуума можно осуществлять путем обнаружения связывания IL-18BP, указанного в настоящем описании, с IL-18, или иммуноспецифического связывания моноклонального антитела или его активного фрагмента, указанного в настоящем описании, с эпитопом IL-18 в образце или in situ, заключающегося в том, что приводят образец или специфическую часть организма или область организма, который/которая, как предполагается, содержит антиген IL-18, в контакт с IL-18BP и/или антителом, которое связывается с эпитопом белка IL-18 или его фрагмента, дают связываться IL-18BP или антителу с антигеном IL-18 с образованием иммунологического комплекса, обнаруживают образование иммунологического комплекса и устанавливают корреляцию между присутствием или отсутствием иммунологического комплекса и присутствием или отсутствием антигена IL-18 в образце или в специфической части организма или области организма, необязательно сравнивают количество указанного иммунологического комплекса с нормальным контрольным значением, при этом увеличение количества указанного агрегата по сравнению с нормальным контрольным значением свидетельствует о том, что указанный индивидуум страдает от ассоциированного с IL-18 заболевания или состояния, или имеет риск его развития.
Мониторинг минимальной остаточной болезни у индивидуума после лечения с применением IL-18BP или фармацевтической композиции, содержащей IL-18BP и фармацевтически приемлемый носитель и/или эксципиент, по любому из предыдущих вариантов осуществления изобретения и описанной выше можно осуществлять путем обнаружения связывания IL-18BP, указанного в настоящем описании, с IL-18, или иммуноспецифического связывания моноклонального антитела или его активного фрагмента, указанного в настоящем описании, с эпитопом белка IL-18 или его фрагмента в образце или in situ, заключающегося в том, что приводят образец или специфическую часть организма или область организма, который/которая, как предполагается, содержит антиген IL-18, в контакт с IL-18BP и/или антителом, которое связывается с эпитопом белка IL-18 или его фрагмента, дают связываться IL-18ВР или антителу с антигеном IL-18 с образованием иммунологического комплекса, обнаруживают образование иммунологического комплекса и устанавливают корреляцию между присутствием или отсутствием иммунологического комплекса и присутствием или отсутствием антигена IL-18 в образце или в специфической части организма или области организма, необязательно сравнивают количество указанного иммунологического комплекса с нормальным контрольным значением, при этом увеличение количества указанного агрегата по сравнению с нормальным контрольным значением свидетельствует о том, что указанный индивидуум все еще может страдать от минимальной остаточной болезни.
Прогнозирование чувствительности индивидуума к лечению с помощью фармацевтической композиции, предлагаемой в изобретении и представленной в настоящем описании в различных вариантах осуществления изобретения, можно осуществлять путем обнаружения связывания IL-18BP, указанного в настоящем описании, с IL-18, или иммуноспецифического связывания моноклонального антитела или его активного фрагмента, указанного в настоящем описании, с эпитопом белка IL-18 или его активного фрагмента в образце или in situ, заключающегося в том, что приводят образец или специфическую часть организма или область организма, который/которая, как предполагается, содержит антиген IL-18, в контакт с IL-18BP и/или антителом, которое связывается с эпитопом белка IL-18 или его фрагмента, дают связываться IL-18ВР или антителу с антигеном IL-18 с образованием иммунологического комплекса, обнаруживают образование иммунологического комплекса и устанавливают корреляцию между присутствием или отсутствием иммунологического комплекса и присутствием или отсутствием антигена IL-18 в образце или в специфической части организма или области организма, необязательно сравнивают количества указанного иммунологического комплекса, определенные до и после начала лечения, при этом уменьшение количества указанного агрегата свидетельствует о том, что указанный индивидуум с большой вероятностью может являться чувствительным к лечению.
Биологические образцы, которые можно использовать при диагностировании ассоциированного с IL-18 заболевания или состояния, указанного в настоящем описании, для диагностирования предрасположенности к ассоциированному с IL-18 заболеванию или состоянию, или для мониторинга минимальной остаточной болезни, указанной в настоящем описании, у индивидуума или для прогнозирования чувствительности индивидуума к лечению с применением фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, представляют собой, например, жидкости, такие как сыворотка, плазма, слюна, желудочный секрет, слизь, спинномозговая жидкость, лимфатическая жидкость и т.п., или образцы ткани или клеток, полученные из организма, например, из нервной ткани, ткани головного мозга, легких, сердечной или сосудистой ткани. Для определения присутствия или отсутствия антигена IL-18, прежде всего свободного антигена IL-18 в образце можно применять любой иммуноанализ, известный специалистам в данной области (см. Harlow и Lane, Antibodies: A Laboratory Manual, изд-во Cold Spring Harbor Laboratory, New York 1988, cc. 555-612). Можно применять, например, анализы, в которых используются непрямые методы обнаружения с использованием вторичных реагентов для обнаружения, различные варианты ELISA и анализы иммунопреципитации и агглютинации. Подробное описание этих анализов приведено, например, в WO 96/13590 на имя Maertens и Stuyver, Zrein и др. (1998) и в WO 96/29605.
Для установления диагноза in situ IL-18BP, указанный в настоящем описании, и/или IL-18-специфическое антитело или любой его активный и функциональный фрагмент, указанное/указанный в настоящем описании, можно вводить в организм, который требуется диагностировать, с помощью методов, известных в данной области, таких, например, как внутривенная, интраназальная, внутрибрюшинная, интрацеребральная, внутриартериальная инъекция, таким образом, чтобы имелась возможность для специфического связывания IL-18BP и/или специфического антитела с областью эпитопа на антигене IL-18. Комплекс IL18ВР/антиген или антител о/антиген можно обнаруживать с помощью метки, присоединенной к антителу или его функциональному фрагменту.
Иммуноанализы, применяемые для установления диагноза или для выявления предрасположенности к ассоциированному с IL-18 заболеванию или состоянию, указанному в настоящем описании, или для мониторинга минимальной остаточной болезни у индивидуума, или для прогнозирования чувствительности индивидуума к лечению с применением фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, как правило, основаны на использовании меченых антигенов, антител или вторичных реагентов для обнаружения. Такие белки или реагенты можно метить с помощью соединений, хорошо известных специалистам в данной области, они включают ферменты, радиоизотопы и флуоресцентные, люминесцентные и хромогенные субстанции, включая окрашенные частицы, такие как коллоидные золотые и латексные гранулы. Из перечисленных подходов подход, основанный на использовании радиоактивной метки, можно применять почти для всех типов анализов, и он допускает наибольшие вариации. Конъюгированные с ферментом метки наиболее пригодны в тех случаях, когда необходимо избегать применения радиоактивности или когда требуется быстро получить результат. Флуорохромы, хотя они и требуют для своего применения дорогостоящего оборудования, обеспечивают очень высокую чувствительность метода обнаружения. Антитела, которые можно применять в таких анализах, включают моноклональные антитела, поликлональные антитела и подвергнутые аффинной очистке поликлональные антитела.
Альтернативно этому антитело можно метить косвенным образом путем взаимодействия с мечеными субстанциями, обладающими аффинностью к иммуноглобулину, такими как белок А или G, или вторичные антитела. Антитело можно конъюгировать со второй субстанцией и обнаруживать с помощью меченой третьей субстанции, обладающей аффинностью ко второй субстанции, конъюгированной с антителом. Например, антитело можно конъюгировать с биотином и выявлять конъюгат антитело-биотин с использованием меченого авидина или стрептавидина. Аналогичным образом антитело можно конъюгировать с гаптеном и выявлять конъюгат антитело-гаптен с использованием меченого антитела к гаптену.
Специалисту в данной области должны быть известны эти и другие пригодные метки, которые можно применять согласно настоящему изобретению. Связывание этих меток с антителами или их фрагментами можно осуществлять с помощью стандартных методов, хорошо известных обычным специалистам в данной области. Общепринятые методы описаны у Kennedy J.Н. и др., Clin. Chim. Acta 70, 1976, сс.1-31 и у Schurs А. Н.W.М. и др., Clin. Chim Acta 81, 1977, сс.1-40. Методы сочетания, упомянутые в последней статье, представляют собой метод на основе глутарового альдегида, метод на основе перйодата, метод на основе дималеимида и другие методы, все они включены в настоящее описание в качестве ссылки.
В современных иммуноанализах применяют метод с использованием двух антител для обнаружения присутствия аналита, при этом захватывающее антитело метят косвенным образом посредством взаимодействия со вторым антителом, меченным обнаруживаемой меткой. Второе антитело предпочтительно представляет собой антитело, которое связывается с антителами животного, из которого происходит моноклональное антитело. Иными словами, если моноклональное антитело представляет собой мышиное антитело, то меченое второе антитело представляет собой антимышиное антитело. При использовании моноклонального антитела в описанном ниже анализе указанная метка предпочтительно представляет собой покрытую антителом гранулу, прежде всего магнитную гранулу. В случае применения поликлонального антитела в представленном в настоящем описании иммуноанализе метка предпочтительно представляет собой обнаруживаемую молекулу, такую как радиоактивная, флуоресцентная или электрохемилюминесцентная субстанция.
В рамках настоящего изобретения можно применять также альтернативную систему с использованием двух антител, которую часто относят к системам быстрого формата, поскольку они адаптированы для быстрого определения присутствия аналита. Для системы требуется наличие высокой аффинности между антителом и аналитом. Согласно одному из вариантов осуществления настоящего изобретения присутствие антигена IL-18 определяют с использованием пары антител, каждое из которых является специфическим в отношении антигена IL-18. В контексте настоящего описания одно из указанной пары антител обозначают как «идентифицирующее антитело», а второе из указанной пары антител обозначают как «захватывающее антитело». Моноклональное антитело, предлагаемое в настоящем изобретении, можно применять как в качестве захватывающего (иммобилизованного) антитела, так и в качестве идентифицирующего антитела. Моноклональное антитело, предлагаемое в настоящем изобретении, можно применять также одновременно и в качестве захватывающего, и в качестве идентифицирующего антитела в одном и том же анализе. Так, в одном из вариантов настоящего изобретения для обнаружения антигена IL-18 в образце биологической жидкости применяют сэндвич-метод с использованием двух антител. В этом методе аналит (антиген IL-18) помещают между идентифицирующим антителом и захватывающим антителом, при этом захватывающее антитело необратимо иммобилизовано на твердой подложке. Идентифицирующее антитело может содержать обнаруживаемую метку для выявления присутствия сэндвича антитело-аналит и, следовательно, присутствия аналита.
Примеры применяемых в качестве твердой фазы субстанций включают (но, не ограничиваясь только ими) титрационные микропланшеты, аналитические полистироловые лабораторные пробирки, магнитные, пластиковые или стеклянные гранулы и слайды, хорошо известные в области радиоиммуноанализов и ферментных иммуноанализов. Методы связывания антител с твердыми фазами также хорошо известны специалистам в данной области. В последние годы в качестве твердых подложек нашли применение многочисленные пористые материалы, такие как нейлон, нитроцеллюлоза, ацетат целлюлозы, стеклянные волокна и другие пористые полимеры.
Настоящее изобретение относится также к диагностическому набору для обнаружения антигена IL-18 в биологическом образце. Кроме того, настоящее изобретение относится также к указанному выше диагностическому набору, который в дополнение к композиции, указанной выше, содержит также реагент для обнаружения, указанный выше. Понятие «диагностический набор» относится в целом к любому диагностическому набору, известному в данной области. Более конкретно, указанное выше понятие относится к диагностическому набору, описанному у Zrein и др. (1998).
Еще одним объектом настоящего изобретения являются новые иммунозонды и тест-наборы для обнаружения и диагностирования ассоциированных с IL-18 заболеваний и состояний, указанных в настоящем описании, содержащие IL-18BP, указанный выше в настоящем описании, или IL-18ВР-специфические антитела указанные выше в настоящем описании. Для получения иммунозондов IL-18BP или антитела связывают непосредственно или косвенно с пригодной репортерной молекулой, например, ферментом или радионуклидом. Тест-набор включает контейнер, содержащий IL-18BP и/или одно или несколько антител, и инструкции по применению IL-18BP и/или антител для связывания с антигеном IL-18 с образованием иммунологического комплекса и обнаружения образования иммунологического комплекса, благодаря чему присутствие или отсутствие иммунологического комплекса коррелирует с присутствием или отсутствием антигена IL-18.
В соответствии с вышеизложенным в изобретении предложен также фармацевтический набор, который содержит фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения, в виде отдельных стандартных доз лекарственного средства, где указанные формы пригодны для введения в эффективных количествах. Такой набор может дополнительно содержать одно или несколько устройств для ингаляции для введения фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения. Например, набор может содержать одно или несколько устройств для ингаляции сухого порошка, приспособленных для введения сухого порошка из капсулы, вместе с капсулами, содержащими сухой порошок, включающий стандартную дозу фармацевтической композиции, предлагаемой в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения. В другом примере набор может включать многодозовое устройство для ингаляции сухого порошка, содержащее в своем резервуаре сухой порошок, представляющее собой многодозовое устройство для ингаляции сухого порошка, содержащее в своем резервуаре сухой порошок, который содержит фармацевтическую композицию, предлагаемую в изобретении, которая представлена в настоящем описании в различных вариантах осуществления изобретения.
Определения
Технические понятия и выражения, применяемые в настоящем описании, в целом имеют значение, общепринятое в рассматриваемой области, если ниже в настоящем описании не указано иное.
Употребляемые в настоящем описании и прилагаемых вариантах осуществления изобретения формы единственного числа включают множественное число, если из контекста ясно не следует иное. Так, например, ссылка на «соединение» означает ссылку на одно или несколько соединений.
В контексте настоящего описания понятия «лечение», «лечить» и т.п., как правило, обозначают достижение требуемого фармакологического и/или физиологического воздействия. Воздействие может быть профилактическим, заключающимся в полном или частичном предупреждении заболевания или его симптома, и/или может быть терапевтическим, заключающемся в частичном или полном излечении заболевания и/или нежелательных действий, обусловленных заболеванием. В контексте настоящего описания под понятие «лечение» подпадает любое лечение заболевания у индивидуума, и оно включает: (а) предупреждение заболевания, т.е. предотвращение нежелательного иммунного ответа у индивидуума, который может быть предрасположен к заболеванию; (б) ингибирование заболевания, т.е. прекращение его развития; или (в) ослабление заболевания, т.е. вызывание регресса заболевания; (г) реверсии симптомов заболевания, т.е. восстановление поврежденной ткани.
В контексте настоящего описания понятие «IL-18-связывающий белок (IL-18 ВР)» включает полноразмерный белок, мутеин, фрагмент, пептид, функциональное производное, функциональный фрагмент, фракцию, полученное в результате циклической перестановки производное, слитый белок, его изоформу или соль.
В контексте настоящего описания понятие «свободный IL-18» означает мономерный растворимый и не входящий в комплекс белок интерлейкин-18.
«Иммуноглобулин» представляет собой тетрамерную молекулу. В случае иммуноглобулина, встречающегося в естественных условиях, каждый тетрамер состоит из двух идентичных пар полипептидных цепей, каждая пара включает одну «легкую» (примерно 25 кДа) и одну «тяжелую» цепь (примерно 50-70 кДа). Аминоконцевая область каждой цепи включает вариабельную область, состоящую примерно из 100-110 или большего количества аминокислот, которые ответственны, прежде всего, за распознавание антигена. Карбоксиконцевая область каждой цепи содержит константную область, которая ответственна, прежде всего, за эффекторную функцию. Человеческие легкие цепи классифицируют как легкие каппа- и лямбда-цепи. Тяжелые цепи классифицируют как мю-, дельта-, гамма-, альфа- или эпсилон-цепи, определяют изотип антитела как IgM, IgD, IgG, IgA и IgE соответственно. В легких и тяжелых цепях вариабельные и константные области соединены посредством «J»-области, состоящей примерно из 12 или большего количества аминокислот, при этом тяжелая цепь включает также «D»-область, состоящую примерно из 10 или большего количества аминокислот (общие сведения изложены в: Fundamental Immunology, глава 7, под ред. Paul W., 2-е изд., изд-во Raven Press, N.Y., 1989) (публикация полностью включена в настоящее описание в качестве ссылки для всех целей). Вариабельные области каждой пары легкой/тяжелой цепей образуют антигенсвязывающий центр, в результате чего интактный иммуноглобулин имеет два сайта связывания.
Иммуноглобулиновые цепи имеют одну и ту же общую структуру, характеризующуюся наличием относительно консервативных каркасных участков (FR), соединенных тремя гипервариабельными участками, которые называют также определяющими комплементарность участками или CDR. CDR из двух цепей каждой пары выровнены с помощью каркасных участков, что позволяет связываться со специфическим эпитопом. В направлении от N-конца к С-концу как легкие, так и тяжелые цепи содержат домены FR1, CDR1, FR2, CDR.2, FR3, CDR3 и FR4. Принадлежность аминокислот каждому из доменов определяют согласно системам определений, представленным у Kabat, Sequences of Proteins of Immunological Interest, National Institutes of Health, Bethesda, Md., 1987 и 1991, или у Chothia и Lesk, J. Mol. Biol, 196, 1987, cc. 901-917; Chothia и др., Nature 342, 1989, cc. 878-883.
В контексте настоящего описания понятия «антитело» или «антитела» представляют собой общепринятые в данной области понятия, и подразумевается, что они относятся к молекулам или активным фрагментам молекул, которые связываются с известными антигенами, прежде всего, к молекулам иммуноглобулина и к иммунологически активным фрагментам молекул иммуноглобулина, т.е. молекулам, которые содержат сайт связывания, который иммуноспецифически связывается с антигеном. Согласно изобретению иммуноглобулин может представлять собой молекулу иммуноглобулина любого типа (IgG, IgM, IgD, IgE, IgA и IgY) или класса (IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2), или подкласса.
Для целей настоящего изобретения понятие «антитело» относится к интактному иммуноглобулину или его антигенсвязывающему фрагменту, который конкурирует с интактным антителом за связывание с антигеном. В частности, в контексте настоящего изобретения «антитела» включают моноклональные, поликлональные, химерные, одноцепочечные, биспецифические или биэффективные антитела, антитела с трансплантированными участками обезьяньих антител, человеческие и гуманизированные антитела.
Примерами антигенсвязывающих фрагментов могут служить, среди прочего, Fab, Fab', F(ab')2, scFv, dAb и Fv-фрагменты, включая продукты, полученные с использованием экспрессионной библиотеки Fab-фрагментов иммуноглобулина, и эпитопсвязывающие фрагменты любого из антител или фрагментов, указанных выше. Другими примерами антигенсвязывающих фрагментов являются содержащие определяющие комплементарность участки (CDR) фрагменты, димерные антитела и полипептиды, которые содержат по меньшей мере часть иммуноглобулина, достаточную для придания полипептиду способности специфически связываться с антигеном.
Такие активные фрагменты можно получать из антитела, предлагаемого в настоящем изобретении, с помощью многочисленных известных в данной области методов. Например, очищенные моноклональные антитела можно расщеплять с помощью фермента, такого как пепсин, и подвергать ЖХВР-гель-фильтрации. Затем соответствующую фракцию, содержащую Fab-фрагменты, можно собирать и концентрировать посредством фильтрации через мембрану и т.п. Дополнительное описание общих методов выделения активных фрагментов антител приведено, например, у Khaw В.А. и др., J. Nucl. Med. 23, 1982, cc. 1011-1019; Rousseaux и др., Methods Enzymology, изд-во Academic Press, 121, 1986, cc. 663-669.
Понятие «гуманизированное антитело» относится к типу сконструированного антитела, которое имеет CDR, происходящие из нечеловеческого донорского иммуноглобулина. В одном из вариантов осуществления изобретения конкретные аминокислоты в каркасном участке и константных доменах тяжелых и легких цепей подвергали мутации для того, чтобы избежать или устранить иммунный ответ у человека. В альтернативном варианте осуществления изобретения гуманизированное антитело можно получать путем слияния константных доменов из человеческого антитела с вариабельными доменами антител из видов кроме человека. Примеры методов создания гуманизированных антител представлены в патентах США 6054297, 5886152 и 5877293.
Еще в одном варианте осуществления изобретения «гуманизированное антитело» относится к типу сконструированного антитела, которое имеет CDR, происходящие из нечеловеческого донорского иммуноглобулина, встроенные в «каркас» человеческого антитела, происходящий из одного (или большего количества) человеческого(их) иммуноглобулина(ов). Кроме того, поддерживающие остатки каркасного участка можно изменять для сохранения аффинности связывания. Методы получения «гуманизированных антител» хорошо известны обычным специалистам в данной области (см., например, у Queen и др., Proc. Natl Acad Sci USA, 86, 1989, cc. 10029-10032, Hodgson и др., Bio/Technology, 9, 1991, с. 421).
«Гуманизированное антитело» можно получать также с помощью нового генетического подхода, позволяющего создавать гуманизированное поликлональные антитела с созревшей аффинностью в организме крупных животных, таких, например, как кролики (см., например, U.S. 7129084).
Понятие «моноклональное антитело» также является общепринятым в данной области, и оно относится к антителу, которое массово получают в лаборатории из единичного клона и которое распознает только один антиген. Моноклональные антитела, как правило, создают путем слияния, как правило, короткоживущей продуцирующей антитело В-клетки с быстро растущей клеткой, такой как раковая клетка (иногда ее называют «бессмертной» клеткой). Полученная в результате этого гибридная клетка, или гибридома, быстро размножается, создавая клон, который продуцирует антитело в больших количествах. Следует иметь в виду, что для целей настоящего изобретения «моноклональное антитело» включает также антитела, которые продуцируются материнским клоном, который еще не достиг полной моноклональности.
Понятие «CDR» относится к гипервариабельному участку антитела. В контексте настоящего описания понятие «гипервариабельный участок», «HVR» или «HV», относится к участкам вариабельного домена антитела, последовательность которых является гипервариабельной, и/или которые образуют структурно выраженные петли. Как правило, антитела содержат шесть гипервариабельных участков, три в VH (H1, Н2, Н3) и три в VL (L1, L2, L3). В настоящее время применяют несколько систем определения гипервариабельного участка, и они подпадают под объем настоящего изобретения. Определение определяющих комплементарность участков согласно Кэботу основано на вариабельности последовательности, и его применяют наиболее широко (Kabat и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD., 1991).
Буквы «НС» и «LC» в сочетании с понятием «CDR» служат для обозначения CDR тяжелой цепи и легкой цепи соответственно, согласно Хотиа вместо этого указывают положение структурных петель (Chothia и Lesk, J. Mol. Biol. 196, 1987, cc. 901-917). Гипервариабельные участки, определенные согласно AbM, представляют собой компромисс между CDR согласно Кэботу и структурными петлями согласно Хотиа, они используются в программе моделирования антител AbM Oxford Molecular's. «Контактные» гипервариабельные участки определяют на основе анализа пригодных сложных кристаллических структур.
Выражение «нумерация остатков вариабельного домена согласно Кэботу» или «нумерация аминокислотных положений согласно Кэботу» и их варианты относятся к системе нумерации, которую применяют для вариабельных доменов тяжелой цепи или вариабельных доменов легкой цепи, представленной в справочнике по антителам Kabat и др., Sequences of Proteins of Immunological Interest, 5-е изд., изд-во Public Health Service, National Institutes of Health, Bethesda, MD, 1991.
В контексте настоящего изобретения понятие «функционально эквивалентное антитело» относится к антителу, которое обладает практически таким же по меньшей мере одним основным функциональным свойством с рассматриваемым антителом, например, функциональные свойства, представленные в настоящем описании, включают (но, не ограничиваясь только этим): специфичность связывания со свободным белком IL-18. Антитела могут относиться к любому классу, например, IgG, IgM или IgA и т.д., или к любому подклассу, например, IgG1, IgG2a и т.д. или другим подклассам, указанным в настоящем описании или известным в данной области, но, прежде всего, к классу IgG4. Кроме того, антитела можно получать с помощью любого метода, такого как фаговый дисплей, или получать в любом организме или клеточной линии, включая клетки бактерий, насекомых, млекопитающих или другой тип клетки или линии клеток, которые продуцируют антитела с требуемыми характеристиками, такие как гуманизированные антитела. Антитела можно создавать путем объединения Fab-фрагмента и Fc-области из различных видов.
Обычные специалисты в данной области легко могут получать фрагменты или аналоги антител, руководствуясь сведениями, представленными в настоящем описании. Предпочтительные амино- и карбоксиконцы фрагментов или аналогов находятся вблизи границ функциональных доменов. Структурные и функциональные домены можно идентифицировать путем сравнения данных о нуклеотидной и/или аминокислотной последовательности с соответствующими базами данных о последовательностях. Предпочтительно для идентификации мотивов последовательности или предсказанных конформационных доменов белка, которые встречаются в других белках с известной структурой и/или функцией, используют компьютеризованные методы сравнения. Методы идентификации белковых последовательностей, которые после укладки принимают известную трехмерную структуру, являются известными (Bowie и др., Science 253, 1991, с. 164).
Понятие «человеческое антитело» включает все антитела, которые имеют одну или большее количество вариабельных и константных областей, происходящих из последовательностей человеческого иммуноглобулина. В предпочтительном варианте осуществления изобретения все вариабельные и константные домены происходят из последовательностей человеческого иммуноглобулина (полностью человеческое антитело). Такие антитела можно получать в различных клетках-хозяевах, таких, например, прокариотическая клетка, например, Е. coli. В другом варианте осуществления изобретения клетка-хозяин представляет собой эукариотическую клетку, например, клетку протиста, клетку животного, клетку растения, растительную или грибную клетку. В одном из вариантов осуществления изобретения клетка-хозяин представляет собой клетку млекопитающего, включая (но, не ограничиваясь только ими) СНО, COS, NSO, SP2, PER.C6, или грибную клетку, такую как Saccharomyces cerevisiae, или клетку насекомого, такую как Sf9. В другом варианте осуществления изобретения клетки, продуцирующие человеческие антитела, можно выращивать в хозяине в биореакторах или, в случае растений, в теплицах и в полевых условиях (см., например, у: Riechmann L., и др., Nature, 332 (6162), 1988, cc. 332-323; Queen С., и др., Proc Natl Acad Sci USA. 86 (24), декабрь 1989 г., cc. 10029-10033; Kashmiri S.V., и др., Methods 36 (1), май 2005 г., cc. 25-34; Hou S., и др., J Biochem 144 (1), июль 2008 г., cc. 115-120).
В контексте настоящего изобретения понятия «пациент» или «индивидуум» используют взаимозаменяемо, и они включают как человека, так и других животных, прежде всего млекопитающих, и другие организмы. Таким образом, способы можно применять как в терапии для человека, так и в области ветеринарии. В предпочтительном варианте осуществления изобретения пациент или индивидуум представляет собой млекопитающее, а в наиболее предпочтительном варианте осуществления изобретения пациент или индивидуум представляет собой человека.
В контексте настоящего описания выражения «фармацевтическая композиция» и «терапевтическая композиция» используются взаимозаменяемо в их наиболее широком смысле. Для целей настоящего изобретения считается, что они относятся к взятому в терапевтически эффективном количестве действующему веществу, т.е. IL-18BP, необязательно в сочетании с фармацевтически приемлемым носителем или разбавителем.
Они включают композиции, которые пригодны для лечебной обработки, контроля, ослабления, улучшения состояния или предупреждения заболевания или нарушения у человека или животного кроме человека. Таким образом, они включают фармацевтические композиции, предназначенные для применения в медицине человека или в ветеринарной медицине. Такая «терапевтическая композиция» отличается тем, что она включает по меньшей мере одно соединение IL-18BP или его физиологически приемлемую соль и необязательно носитель или эксципиент, при этом соль и носитель, и эксципиент являются переносимыми для организма-мишени, который ими обрабатывают.
Понятие «терапевтически эффективное количество» относится к количеству, которое обеспечивает терапевтическое действие для рассматриваемого состояния и схемы введения. В частности, «терапевтически эффективное количество» означает количество, эффективное в отношении предупреждения, реверсирования, облегчения или ослабления симптомов заболевания или пролонгирования выживания индивидуума, подвергающегося лечению, который может представлять собой человека или животное кроме человека. Определение терапевтически эффективного количества находится в компетенции специалиста в данной области. В частности, в рассматриваемом случае «терапевтически или профилактически эффективное количество» относится к количеству белка или пептида, мутеина, функционального производного, фракции, полученного в результате циклической перестановки производного, слитого белка, его изоформы или соли, и соединения или фармацевтической композиции, которое после введения человеку или животному приводит к терапевтическому или профилактическому действию на указанного человека или животное. Специалист в данной области легко может определять эффективное количество согласно стандартным процедурам. Терапевтически эффективное количество или доза соединения, предлагаемого в настоящем изобретении, может варьироваться в широких пределах и его можно определять методом, известным в соответствующей области. Доза может варьироваться в широких пределах и ее, естественно, следует регулировать в зависимости от индивидуальных требований в каждом конкретном случае.
Понятие «введение через слизистую оболочку» относится к различным путям введения, когда соединение абсорбируется слизистой оболочкой любой части организма. Введение через слизистую оболочку включает (но, не ограничиваясь только ими) интраназальное, трансбуккальное введение, введение через слизистую оболочку ротовой полости, внутритрахеальное введение, введение в мочевой тракт, внутриректальное, интравагинальное, подъязычное, внутрибронхиальное, внутрилегочное и чрескожное введение.
Под понятие «фармацевтически приемлемый» подпадает любой носитель, эксципиент, разбавитель или наполнитель, который не оказывает негативного влияния на эффективность проявления биологической активности действующего вещества и который не является токсичным для хозяина, которому его вводят.
Понятие «слитый белок» относится к полипептиду, который содержит IL-18ВР или вирусный IL-18BP, или его мутеин или фрагмент, слитый с другим белком, который, например, обладает более продолжительным временем нахождения в общей воде организма. Так, IL-18BP или вирусный IL-18BP можно сливать с другим белком, полипептидом или т.п., например, иммуноглобулином или его фрагментом.
Такие изоформы, мутеины, слитые белки или функциональные производные сохраняют биологическую активность IL-18BP, в частности, способность связываться с IL-18, и предпочтительно активность, практически сходную с активностью IL-18BP. В идеальном варианте такие белки обладают биологической активностью, которая даже превышает активность немодифицированного IL-18BP. Предпочтительные активные фракции обладают активностью, которая превышает активность IL-18BP, или они обладают дополнительными преимуществами, такими как более высокая стабильность или более низкая токсичность или иммуногенность, или их легче получать в больших количествах, или легче очищать.
Понятие «интерлейкин-18-связывающий белок» включает также мутеин, функциональное производное, фракцию, биологически активный пептид, полученное в результате циклической перестановки производное, слитый белок, изоформу и соль IL-18BP.
В контексте настоящего описания понятие «мутеины» относится к аналогам IL-18BP или аналогам вирусного IL-18BP, в которых один или несколько аминокислотных остатков встречающегося в естественных условиях IL-18BP или вирусного IL-18BP заменены на другие аминокислотные остатки или исключены путем делеции, или один или несколько аминокислотных остатков добавлены к последовательности встречающегося в естественных условиях IL-18ВР или вирусного IL-18BP без значительного изменения активности полученных в результате этого продуктов по сравнению с IL-18BP дикого типа или вирусным IL-18BP. Такие мутеины получают с помощью известных методов синтеза и/или сайтнаправленного мутагенеза, высокопроизводительного мутагенеза, перестановки ДНК, методов эволюции белка или других известных методов, пригодных для указанной цели.
Любой такой мутеин предпочтительно имеет аминокислотную последовательность, в достаточной степени дублирующую последовательность IL-18BP, или в достаточной степени дублирующую последовательность вирусного IL-18BP, для того, чтобы он обладал активностью, практически сходной с активностью IL-18BP. Одним из видов активности IL-18BP является его способность связываться с IL-18. Поскольку мутеин обладает значительной активностью в отношении связывания с IL-18, то его можно применять для очистки IL-18, например, с помощью аффинной хроматографии, и, таким образом, можно считать, что он обладает активностью, практически сходной с активностью IL-18BP. Таким образом, с помощью стандартных экспериментов можно определять, обладает ли любой рассматриваемый мутеин практически такой же активностью, что и IL-18BP, подвергая указанный мутеин, например, простому сэндвич-анализу в условиях конкуренции для определения того, связывается он или нет с соответствующим образом меченым IL-18, такому как радиоиммуноанализ или ELISA.
Мутеины полипептидов IL-18BP или мутеины вирусных IL-18BP, которые можно применять согласно настоящему изобретению, или нуклеиновая кислота, кодирующая их, включают ограниченный набор соответствующих в необходимой степени последовательностей в качестве замещающих пептидов или полинуклеотидов, которые обычный специалист в данной области может получать стандартными методами без излишних экспериментов на основе доктрины изобретения и указаний, представленных в настоящем описании.
Предпочтительные изменения, применяемые для получения мутеинов согласно настоящему изобретению, представляют собой изменения, известные как «консервативные» замены. Консервативные аминокислотные замены в полипептидах или белках IL-18BP, или в вирусных IL-18BP, могут включать замены синонимических аминокислот в группах, характеризующихся достаточно сходными физико-химическими свойствами, благодаря чему замены представителей группы друг на друга должны сохранять биологическую функцию молекулы (Grantham, 1974). Очевидно, что можно осуществлять также инсерции и делеции аминокислот в указанных выше последовательностях без изменения их функции, прежде всего в том случае, если инсерции или делеции затрагивают лишь небольшое количество аминокислот, например, менее тридцати, и предпочтительно менее десяти, и не приводят к удалению или смещению аминокислот, которые имеют решающее значение для функциональной конформации, например, остатков цистеина. Белки и мутеины, полученные в результате таких делеций и/или инсерций, подпадают под объем настоящего изобретения.
В контексте настоящего описания понятие «функциональные производные» включает производные IL-18BP или вирусного IL-18BP, и их мутеинов и содержащих их слитых белков, которые можно получать с использованием функциональных групп, которые присутствуют в виде боковых цепей на остатках, или N- или С-концевых групп, с помощью средств, известных в данной области, и они подпадают под объем изобретения, если они остаются фармацевтически приемлемыми, т.е., если они не нарушают активность белка, которая практически сходна с активностью IL-18BP или вирусных IL-18BP, и не придают токсические свойства композициям, содержащим их.
Такие производные могут, например, содержать полиэтиленгликолевые боковые цепи, которые могут маскировать антигенные сайты и удлинять время нахождения IL-18BP или вирусного IL-18BP в общей воде организма. Другие производные содержат алифатические сложные эфиры карбоксильных групп, амиды карбоксильных групп, полученные в результате взаимодействия с аммиаком или с первичными или вторичными аминами, N-ацильные производные свободных аминогрупп на аминокислотных остатках, образованные с использованием ацильных фрагментов (например, алканольные или карбоциклические ароильные группы), или О-ацильные производные свободных гидроксильных групп (например, групп на серильных или треонильных остатках), образованных с ацильными фрагментами.
В качестве «функционального фрагмента» IL-18BP или вирусного IL-18BP, мутеина и слитого белка, под объем настоящего изобретения подпадают любой фрагмент или предшественник полипептидной цепи молекулы белка IL-18BP индивидуально или вместе с ассоциированными молекулами или остатками, присоединенными к нему, такими, например, как сахарные или фосфатные остатки, или агрегатами молекулы белка, или самими сахарными остатками, при условии, что указанный фрагмент обладает активностью, практически сходной с активностью IL-18BP.
В контексте настоящего описания понятие «соли» относится как к солям карбоксильных групп, так и к кислотно-аддитивным солям аминогрупп молекулы IL-18BP или ее аналогов. Соли карбоксильных групп можно получать методами, известными в данной области, и они включают неорганические соли, например, соли натрия, кальция, аммония, железа или цинка и т.п. и соли с органическими основаниями, образованные, например, с аминами, такими как триэтаноламин, аргинин или лизин, пиперидин, прокаин и т.п. Кислотно-аддитивные соли включают, например, соли с минеральными кислотами, такими, например, как соляная кислота или серная кислота, и соли с органическими кислотами, такими, например, как уксусная кислота или щавелевая кислота. Очевидно, что любые такие соли должны сохранять биологическую активность IL-18BP, например, способность связываться с IL-18.
«Изоформы» IL-18BP представляют собой белки, обладающие способностью связываться с IL-18 или его фрагментом, которые можно получать путем альтернативного сплайсинга.
В контексте настоящего описания понятие «полученное с помощью циклической перестановки производное» относится к линейной молекуле, в которой концы были соединены друг с другом либо непосредственно, либо через линкер, с получением кольцевой молекулы, и затем кольцевая молекула была разомкнута в другом положении с получением новой линейной молекулы, концы которой отличны от концов исходной молекулы. Варианты с циклической перестановкой включают молекулы, структура которых эквивалентна структуре молекулы, которую подвергали циклизации и затем размыкали. Таким образом, молекулу с циклической перестановкой можно синтезировать de novo в виде линейной молекулы и не осуществлять стадию циклизации и размыкания. Получение производных с циклической перестановкой описано в WO 95/27732.
Выражение «аномальные уровни свободного IL-18» относится к уровням IL-18, повышенным или пониженным по сравнению с уровнями, присутствующими в общей воде организма здорового контрольного индивидуума. В частности, указанный аномальный уровень представляет собой повышенный уровень IL-18. В частности, указанный аномальный уровень свободного IL-18 в общей воде организма превышает уровень в общей воде организма здорового контрольного индивидуума на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100%. В конкретных вариантах осуществления изобретения референс-уровень или контрольный уровень представляет собой нормальный непатологический исходный уровень свободного IL-18, определенный у пациента, подлежащего лечению.
Выражение «аномальное соотношение свободный IL-18/IL-18BP» относится к повышенному соотношению IL-18 к IL-18BP по сравнению с величинами, обнаруженными в общей воде организма здорового контрольного индивидуума. В частности, указанное аномальное соотношение свободный IL-18/IL-18BP в общей воде организма превышает указанное соотношение в общей воде организма здорового контрольного индивидуума на 1%, 2.5%, 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100%. В конкретных вариантах осуществления изобретения референс-уровень или контрольный уровень представляет собой нормальный непатологический исходный уровень свободного IL-18, определенный у пациента, подлежащего лечению.
Выражения «молчание гена» и «посттрансляционное молчание гена» означают регуляцию, подавляющую экспрессию гена посредством механизмов, отличных от генетической модификации. Молчание возникает в результате нейтрализации мРНК на посттрансляционном уровне, при этом трансляция мРНК прекращается и происходит образование активного генного продукта, который в большинстве случаев представляет собой белок.
Понятие «предрасположенность» обозначает повышенную чувствительность индивидуума к развитию специфического заболевания. В рассматриваемом случае индивидуум классифицируется как предрасположенный, если, например, обнаружен повышенный уровень IL-18 в легких, сыворотке, мокроте, жидкости бронхоальвеолярного лаважа (BALF) или в кровотоке.
Выражения «дым», «индуцированный дымом», «сигаретный дым» или «индуцированный сигаретным дымом» относятся к табачному дыму.
«Альвеолярные макрофаги» представляют собой подтип макрофагов, присутствующий в легочных альвеолах. Они часто содержат гранулы экзогенного материала, который они захватывают с поверхностей дыхательных путей. Такие черные гранулы встречаются, прежде всего, у людей, которые в течение длительного времени подвергались воздействию мелкой пыли, мелких частиц, например, у курильщика или людей, долгое время проживающих в крупных городах.
«Цитокиновый Th2-ответ» опосредован IL-4, IL-5, IL-6, IL-8, IL-10, IL-13, и/или IL-17A, прежде всего IL-4 и/или IL-8, и/или IL-17A, в то время как «цитокиновый Тh1-ответ» опосредован интерфероном-гамма (IFN-γ), IL-2 и фактором некроза опухоли-альфа (TNF-α).
Выражение «дисбаланс IL-18/IL-18BP» относится к нарушению регуляции общего взаимодействия IL-18 и IL-18BP, которое в конечном итоге приводит к повышенному уровню несвязанного IL-18.
Понятие «заболевание» обозначает состояние здоровья животного, при котором животное не может поддерживать гомеостаз, и при котором, если заболевание не ослабляется, то здоровье животного продолжает ухудшаться. В отличие от этого, понятие «нарушение» у животного обозначает состояние здоровья, при котором животное способно поддерживать гомеостаз, но при этом состояние здоровья животного является менее благоприятным, чем оно могло бы быть в отсутствии нарушения. Без лечения нарушение не обязательно приводит к дальнейшему ухудшению состояния здоровья животного.
Заболевание или нарушение «облегчают», если уменьшают серьезность симптома заболевания или нарушения, частоту, с которой у пациента возникают указанные симптомы, или уменьшают и то, и другое.
В контексте настоящего описания понятия «с нарушенной регуляцией» или «нарушенная регуляция», относятся к ухудшению биологического процесса, что, в свою очередь, может приводить к неблагоприятным физиологическим последствиям или аномальной экспрессии гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы. В том случае, если нарушена регуляция экспрессии гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы, то уровни экспрессии, процессирования или поддержания гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы находятся вне диапазона, который рассматривается специалистом в данной области как нормальный для указанного/указанной гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы. Нарушение регуляции гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы у млекопитающего можно определять путем измерения уровня гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы в организме млекопитающего и сравнения уровня, измеренного у этого млекопитающего, с уровнем, измеренным у соответствующей популяции, в отношении которой известно, что у нее не имеет место нарушение регуляции указанного/указанной гена, нуклеиновой кислоты, белка, пептида или другой биологической молекулы. Альтернативно этому уровень можно сравнивать с уровнем, измеренным у того же самого индивидуума в другой момент времени.
В контексте настоящего описания понятия «заболевание сердца» или «сердечнососудистое заболевание» включают заболевания и нарушения, которые поражают сердечную мышцу или кровеносные сосуды сердца и всего организма. Заболевания сердца могут приводить к сердечной недостаточности и, в конечном итоге, они являются одной из самых часто встречающихся причин смерти в промышленно развитых сообществах. Примерами заболеваний сердца, индуцированных дисбалансом IL-18/IL-18BP, являются (но, не ограничиваясь только ими) обструктивное заболевание сердца, тромболитическая дисфункция, алкогольная кардиомиопатия, пролапс клапана аорты, стеноз клапана аорты, аритмии, кардиогенный шок, врожденный порок сердца, дилатационная кардиомиопатия, сердечный приступ, сердечная недостаточность, опухоль сердца, стеноз клапана легочной артерии, гипертрофическая кардиомиопатия, идиопатическая кардиомиопатия, ишемическая болезнь сердца, ишемическая кардиомиопатия, митральная регургитация, пролапс митрального клапана, перипартальная кардиомиопатия, стенокардия.
В контексте настоящего описания понятие «сахарный диабет типа 2» относится к наиболее распространенной форме диабета. Это заболевание или нарушение характеризуется либо тем, что организм не может продуцировать или продуцирует в недостаточных количествах фермент инсулин, либо тем, что клетки имеют дефекты с точки зрения их ответа на инсулин. Такие дефекты, по-видимому, зависят от инсулинового рецептора.
В контексте настоящего описания понятие «эндогенный» относится к любому материалу, происходящему из организма, клетки, ткани или системы, или продуцируемому в них. Понятие «экзогенный» относится к любому материалу, интродуцированному извне или продуцированному вне организма, клетки, ткани или системы.
В контексте настоящего описания понятие «экспрессия» относится к транскрипции и/или трансляции конкретной нуклеотидной последовательности под контролем ее промотора. В контексте настоящего описания понятие «экспрессионный вектор» относится к вектору, содержащему нуклеотидную последовательность, кодирующую по меньшей мере часть генного продукта, которая может транскрибироваться. В некоторых случаях после этого молекулы РНК транслируются в белок, полипептид или пептид. В других случаях указанные последовательности не транслируются, что имеет место, например, при производстве антисмысловых молекул, siPHK, рибозимов и т.п. Экспрессионные векторы могут содержать различные контролирующие последовательности, которые относятся к нуклеотидным последовательностям, необходимым для транскрипции и возможно для трансляции, которые функционально связаны с кодирующей последовательностью в конкретном организме-хозяине. Помимо контролирующих последовательностей, которые управляют транскрипцией и трансляцией, векторы и экспрессионные векторы могут содержать также нуклеотидные последовательности, которые выполняют другие функции. Экспрессионный вектор, предлагаемый в настоящем изобретении, можно применять в генной терапии для лечения заболевания или нарушения, указанного в настоящем описании. В частности, указанный экспрессионный вектор представляет собой вирусный вектор. Вирусы, которые можно применять в качестве носителя для доставки экспрессионного вектора, выбирают из группы, включающей ретровирус, аденовирус, лентивирус, вирус герпеса простого, вирус коровьей оспы, вирус оспы и аденоассоциированный вирус.
В контексте настоящего описания понятия «ингибирует», «нейтрализует» или «блокирует» следует понимать как синонимы, они обозначают уменьшение количества молекул, реакции, взаимодействия, генной экспрессии, экспрессии мРНК и/или белка, стабильности, функции или активности на поддающуюся измерению величину или их полное предупреждение. Ингибиторы представляют собой соединения, которые, например, связываются, частично или полностью блокируют стимуляцию, снижают, предупреждают, замедляют активацию, инактивируют, десенсибилизируют или осуществляют понижающую регуляцию стабильности, экспрессии, функции и активности белка, гена и мРНК, например, являются антагонистами.
Понятие «антисмысловой экспрессионный вектор» относится к экспрессионному вектору, кодирующему одноцепочечную или двухцепочечную РНК, которая комплементарна цепи матричной РНК (мРНК) и которая ингибирует трансляцию указанной мРНК в аминокислоты. Понятие «антисмысловая РНК» включает asPHK, siPHK, shPHK, микроРНК.
В контексте настоящего описания понятие «генная терапия» означает применение ДНК, например, экспрессионного вектора, в качестве фармацевтического агента для лечения заболевания, указанного в настоящем описании.
Краткое описание чертежей
На чертежах показано:
На фиг. 1 - Сравнение уровней общего и свободного IL-18 у отдельных пациентов, страдающих сепсисом. Взято из публикации Novick и др., 2001. Уровень свободного IL-18 (закрашенные кружки) в сыворотке страдающих сепсисом пациентов после госпитализации рассчитывали на основе концентрации общего IL-18 (незакрашенные кружки) и IL-18BPa с учетом того, что соотношение IL-18 и IL-18BPa в комплексе составляет 1:1 и рассчитанная величина KD составляет 400пМ. Каждая вертикальная линия соединяет точки, соответствующие общему и свободному IL-18 в отдельном образце сыворотки. Указанные выше анализы методом ELISA осуществляли с использованием пары антител, созданных Taniguchi и др., 1997 (1), а именно, антитела 125-2Н в качестве первичного/захватывающего антитела и антитела 159-12В в качестве вторичного/идентифицирующего антитела;
на фиг. 2 - Результаты обнаружения общего IL-18 с помощью антител 125-2Н и 159-12В. Данные свидетельствуют о том, что оба антитела позволяют количественно оценивать общий IL-18.
на фиг. 3 - Результаты титрования IL-18 в концентрации 400пг/мл в зависимости от уровня IL-18BP;
на фиг. 4 - Данные об индукции мышиного IL-18 в пространстве легочных дыхательных путей в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только полиинозиновой:полицитидиловой кислоты (р[I:С]), 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения). Пунктирной линией обозначен нижний предел обнаружения. Статистические анализы осуществляли с использованием неспаренного t-критерия;
на фиг. 5 - Данные об ингибировании общей инфильтрации клеток в пространство легочных дыхательных путей у мышей в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только р[I:С], 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения), 5-7) р[I:С] в сочетании с табачным дымом в день 4 после обработки IL-18BP в дозе 1, 3 или 10 мг/кг, 8) обработка дексаметазоном в дозе 10 мг/кг. Статистические анализы осуществляли с использованием неспаренного t-критерия;
на фиг. 6 - Данные об ингибировании общей инфильтрации клеток в пространство легочных дыхательных путей у мышей в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только р[I:С], 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения), 5) р[I:С] в сочетании с табачным дымом в день 4 после обработки IL-18BP в дозе 1, 3 или 10 мг/кг, 6) обработка дексаметазоном в дозе 10 мг/кг. Статистические анализы осуществляли с использованием дисперсионного анализа (апостериорный критерий Сидака);
на фиг. 7 - Данные об ингибировании инфильтрации нейтрофилов с помощью IL-18BP. Инфильтрацию нейтрофилов в пространство легочных дыхательных путей у мышей в оценивали в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только р[I:С], 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения), 5-7) р[I:С] в сочетании с табачным дымом в день 4 после обработки IL-18BP в дозе 1, 3 или 10 мг/кг, 8) обработка дексаметазоном в дозе 10 мг/кг. Статистические анализы осуществляли с использованием дисперсионного анализа (апостериорный критерий Сидака);
на фиг. 8 - Данные об ингибировании инфильтрации нейтрофилов с помощью IL-18BP. Инфильтрацию нейтрофилов в пространство легочных дыхательных путей у мышей в оценивали в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только р[I:С], 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения), 5) р[I:С] в сочетании с табачным дымом в день 4 после обработки IL-18BP в дозе 10 мг/кг, 8) обработка дексаметазоном в дозе 10 мг/кг. Статистические анализы осуществляли с использованием дисперсионного анализа (апостериорный критерий Сидака);
на фиг. 9 - Данные об ингибировании пути G-CSF с помощью IL-18BP. Присутствие G-CSF (пг/мл) оценивали в пространство легочных дыхательных путей у мышей с помощью ELISA в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только р[I:С], 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения), 5-7) р[I:С] в сочетании с табачным дымом в день 4 после обработки IL-18BP в дозе 1, 3 или 10 мг/кг, 8) обработка дексаметазоном в дозе 10 мг/кг. Пунктирной линией обозначен нижний предел обнаружения. Статистические анализы осуществляли с использованием t-критерия Стьюдента;
на фиг. 10 - Данные о снижении потери веса, обусловленной IL-18BP. Вес тела мышей определяли в день 5 после: 1) воздействия воздуха, 2) табачного дыма (TS), 3) только р[I:С], 4) р[I:С] в сочетании с табачным дымом в день 4 (индукция обострения), 5) р[I:С] в сочетании с табачным дымом в день 4 после обработки IL-18BP в дозе 10 мг/кг, 7) обработка дексаметазоном в дозе 10 мг/кг. Статистические анализы осуществляли с использованием дисперсионного анализа (апостериорный критерий Сидака);
на фиг. 11 - Аминокислотные последовательности вариабельной тяжелой цепи (VH) и вариабельной легкой цепи (VK) антител, полученных с использованием различных клонов. Гипервариабельные участки CDR 1, CDR 2 и CDR 3 выделены путем подчеркивания соответствующих последовательностей, определенных с помощью системы нумерации IMGT (Lefranc М.-Р. и др., Nucleic Acids Research, 27, 1999, cc. 209-212). Слева направо: первая подчеркнутая последовательность в каждой из указанных последовательностей VH и VK представляет собой CDR1, вторая подчеркнутая последовательность представляет собой CDR2, а третья подчеркнутая последовательность представляет собой CDR3. Вариабельный домен выделен жирным шрифтом.
Последовательности
SEP ID NO: 1: эпитоп 1 IL-18: Tyr-Phe-Gly-Lys-Leu-Glu-Ser-Lys-Leu-Ser-Val-Ile-Arg-Asn;
SEP ID NO: 2: эпитоп 2 IL-18: Phe-Ile-Ile-Ser-Met-Tyr-Lys-Asp-Ser-Gln-Pro-Arg-Gly-Met-Ala-Val-Thre-Ile-Ser-Val-Lys;
SEQ ID NO: 3: эпитоп 3 IL-18: Glu-Met-Asn-Pro-Pro-Asp-Asn-Ile-Lys-Asp-Thr-Lys-Ser-Asp-Ile-Ile-Phe;
SEQ ID NO: 4: эпитоп 4 IL-18: Tyr-Phe-Gly-Lys-Leu-Glu-Ser;
SEQ ID NO: 5: эпитоп 5 IL-18: Tyr-Lys-Asp-Ser-Gln-Pro-Arg-Gly-Met-Ala;
SEQ ID NO: 6: эпитоп 6 IL-18: Asp-Asn-Ile-Lys-Asp-Thr-Lys;
SEQ ID NO: 7: IL-18-связывающий белок (IL-18BP);
SEQ ID NO: 8: последовательность состоящего из 13 аминокислот линкера: Glu-Phe-Gly-Ala-Gly-Leu-Val-Leu-Gly-Gly-Gln-Phe-Met;
SEQ ID NP: 9: последовательность VH антитела 107C6;
SEQ ID NP:10: последовательность VK антитела 107C6;
SEQID NP: 11: последовательность VH антитела 108F8;
SEQ ID NP: 12: последовательность VK антитела 108F8;
SEQ ID NP: 13: последовательность VH антитела 109A6;
SEQ ID NP: 14: последовательность VK антитела 109A6;
SEQ ID NP: 15: последовательность VH антитела 111A6;
SEQ ID NP: 16: последовательность 1 VK антитела 111A6;
SEQ ID NP: 17: последовательность 2 VK антитела 111A6;
SEQ ID NP: 18: последовательность VH антитела 131B4;
SEQ ID NP: 19: последовательность VK антитела 131B4;
SEQ ID NP: 20: последовательность 1VH антитела 131E8;
SEQ ID NP: 21: последовательность 2VH антитела 131E8;
SEQ ID NP: 22: последовательность VK антитела 131E8;
SEQ ID NP: 23: последовательность VH антитела 132H4;
SEQ ID NP: 24: последовательность VK антитела 132H4;
SEQ ID NP: 25: последовательность VH антитела 133A6;
SEQ ID NP: 26: последовательность VK антитела 133A6;
SEQ ID NP: 27: последовательность CDR1 VH антитела 107C6: Gly Tyr Thr Phe Thr Asn Tyr Gly;
SEQ ID NP: 28: последовательность CDR2 VH 107C6 VH; Ile Asn Thr Tyr Ser Gly Val Pro;
SEQ ID NP: 29: последовательность CDR3 VH антитела 107C6 VH: Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr;
SEQ ID NO: 30: последовательность CDR1 VK антитела 107C6: Gln Ser Leu Leu Asp Ser Arg Thr Arg Lys Asn Tyr;
SEQ ID NO: 31: последовательность CDR2 VK антитела 107C6: Trp Ala Ser;
SEQ ID NO: 32: последовательность CDR3 VK антитела 107C6: Lys Gln Ser Tyr Asn Leu Arg Thr;
SEQ ID NP: 33: последовательность CDR1 VH антитела 108F8: Gly Tyr Thr Phe Thr Asn Tyr Gly;
SEQ ID NP: 34: последовательность CDR2 VH антитела 108F8: Ile Asn Thr Tyr Ser Gly Val Pro;
SEQ ID NP: 35: последовательность CDR3 VH антитела 108F8: Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr;
SEQ ID NP: 36: последовательность CDR1 VK антитела 108F8: Gln Ser Leu Leu Asp Ser Arg Thr Arg Lys Asn Tyr;
SEQ ID NP: 37: последовательность CDR2 VK антитела 108F8: Trp Ala Ser;
SEQ D NP: 38: последовательность CDR3 VK антитела 108F8: Lys Gln Ser Tyr Asn Leu Arg Thr;
SEQ ID NP: 39: последовательность CDR1 VH антитела 109A6: Gly Phe Lys Ile Lys Asp Thr Tyr;
SEQ ID NP: 40: последовательность CDR2 VH антитела 109A6: Ile Asp Pro Ala Asn Gly Asn Thr;
SEQ ID NP: 41: последовательность CDR3 VH антитела 109A6: Ala Gly Tyr Val Trp Phe Ala Tyr;
SEQ ID NP: 42: последовательность CDR1 VK антитела 109A6: Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr;
SEQ ID NP: 43: последовательность CDR2 VK антитела 109A6: Thr Val Ser;
SEQ D NP: 44: последовательность CDR3 VK антитела 109A6: Ser Gln Ser Thr Leu Val Pro Trp Thr;
SEQ ID NP: 45: последовательность CDR1 VH антитела 111A6: Gly Phe Lys Ile Lys Asp Thr Tyr;
SEQ ID NP: 46 последовательность CDR2 VH антитела 111A6: Ile Asp Pro Ala Asn Gly Asn Thr;
SEQ ID NP: 47: последовательность CDR3 VH антитела 111A6: Ala Gly Tyr Val Trp Phe Ala Tyr;
SEQ ID NO: 48: последовательность 1 CDR1 VK антитела 111A6: Ser Ser Val Ser Ser Ser Tyr;
SEQ ID NO: 49: последовательность 1 CDR2 VK антитела 111A6: Ser Thr Ser;
SEQ ID NO: 50: последовательность 1 CDR3 VK антитела 111A6: Gln Gln Tyr Ser Gly Tyr Pro Leu Thr;
SEQ ID NP: 51: последовательность 2 CDR1 VK антитела 111A6: Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr;
SEQID NP: 52: последовательность 2 CDR2 VK антитела 111A6: Thr Val Ser;
SEQ ID NP: 53: последовательность 2 CDR3 VK антитела 111A6: Ser Gln Ser Thr Leu Val Pro Trp Thr;
SEQ ID NP: 54: последовательность CDR1 VH антитела 131B4: Gly Phe Lys Ile Lys Asp Thr Tyr;
SEQ ID NP: 55: последовательность CDR2 VH антитела 131B4: Ile Asp Pro Ala Asn Gly Asn Thr;
SEQ ID NP: 56: последовательность CDR3 VH антитела 131B4: Ala Gly Tyr Val Trp Phe Ala Tyr;
SEQ ID NP: 57: последовательность CDR1 VK антитела 131B4: Gln Ser Leu Val His Ser Asn Gly Asn Thr Tyr;
SEQ ID NP: 58: последовательность CDR2 VK антитела 131B4: Lys Val Ser;
SEQ ID NP: 59: последовательность CDR3 VK антитела 131B4: Ser Gln Ser Ser Leu Val Pro Trp Thr;
SEQ ID NP: 60: последовательность 1 CDR1 VH антитела 131E8: Gly Phe Ser Leu Pro Asn Tyr Gly;
SEQ ID NP: 61: последовательность 1 CDR2 VH антитела 131E8: Ile Trp Ser Gly Gly Ser Thr;
SEQ ID NP: 62: последовательность 1 CDR3 VH антитела 131E8: Ala Arg Asn Phe Tyr Ser Lys Tyr Asp Tyr Ala Met Asp Tyr;
SEQ ID NP: 63: последовательность 2 CDR1 VH антитела 131E8: Gly Tyr Thr Phe Thr Ser Tyr Trp;
SEQ ID NP: 64: последовательность 2 CDR2 VH антитела 131E8: Ile Asn Pro Asn Ser Gly Ser Thr;
SEQ ID NO: 65: последовательность 2 CDR3 VH антитела 131E8: Ala Arg Leu Gly Asp Tyr;
SEQ ID NO: 66: последовательность CDR1 VK антитела 131E8: Ser Ser Val Ser Tyr;
SEQ ID NP: 67: последовательность CDR2 VK антитела 131E8: Asp Thr Ser;
SEQ ID NP: 68: последовательность CDR3 VK антитела 131E8: Phe Gln Gly Ser Gly Tyr Pro Leu Thr;
SEQ ID NP: 69: последовательность CDR1 VH антитела 132H4: Gly Phe Thr Phe Ser Asn Tyr Ala;
SEQ ID NP: 70: последовательность CDR2 VH антитела 132H4: Ile Ser Ser Gly Gly Ala Asn Ile;
SEQ ID NP: 71: последовательность CDR3 VH антитела 132H4: Ala Arg Gly Asp Tyr Phe Asn His Phe Trp Phe Ala Tyr;
SEQ ID NP: 72: последовательность CDR1 VK антитела 132H4: Gln Ser Ile Val His Ser Asn Gly Asn Thr Tyr;
SEQ ID NP: 73: последовательность CDR2 VK антитела 132H4: Lys Val Ser;
SEQ ID NP: 74: последовательность CDR3 VK антитела 132H4: Phe Gln Gly Ser His Val Pro Trp Thr;
SEQ ID NP: 75: последовательность CDR1 VH антитела 133A6: Gly Phe Thr Phe Ser Asn Tyr Ala;
SEQ ID NP: 76: последовательность CDR2 VH антитела 133A6: Ile Ser Ser Gly Gly Gly Asn Ile;
SEQ ID NP: 77: последовательность CDR3 VH антитела 133A6: Ala Arg Gly Asp Tyr Ser Asn Tyr Phe Trp Phe Ala Tyr;
SEQ ID NP: 78: последовательность CDR1 VK антитела 133A6: Gln Ser Ile Val His Ser Asn Gly Asn Thr Tyr;
SEQ ID NP: 79: последовательность CDR2 VK антитела 133A6: Lys Val Ser;
SEQ ID NP: 80: последовательность CDR3 VK антитела 133A6: Phe Gln Gly Ser His Val Pro Trp Thr.
SEQ ID NP: 81: ДНК-последовательность VH антитела 107C6
SEQ ID NP: 82: последовательность VH антитела 107C6
SEQ ID NP: 83: ДНК-последовательность VK антитела 107C6
SEQ ID NP: 84: последовательность VK антитела 108F8
SEQ ID NO: 85: ДНК-последовательность VH антитела 108F8
SEQ ID NO: 86: последовательность VH антитела 108F8
SEQ ID NO: 87: ДНК-последовательность VK антитела 108F8
SEQ ID NO: 88: последовательность VK антитела 108F8
SEQ ID NO: 89: ДНК-последовательность VH антитела 109A6
SEQ ID NO: 90: последовательность VH антитела 109A6
SEQ ID NO: 91: ДНК-последовательность VK антитела 109A6
SEQ ID NO: 92: последовательность VK антитела 109A6
SEQ ID NO: 93: ДНК-последовательность VH антитела 111A6
SEQ ID NO: 94: последовательность VH антитела 111A6
SEQ ID NO: 95: ДНК-последовательность 1 VK антитела 111A6
SEQ ID NO: 96: последовательность 1 VK антитела 111A6
SEQ ID NO: 97: ДНК-последовательность 2 VK антитела 111A6
SEQ ID NO: 98: последовательность 2 VK антитела 111A6
SEQ ID NO: 99: ДНК-последовательность 1 VH антитела 131B4
SEQ ID NO: 100: последовательность 1 VH антитела 131B4
SEQ ID NO: 101: ДНК-последовательность 2 VH антитела 131B4
SEQ ID NO: 102: последовательность 2 VH антитела 131B4
SEQ ID NO: 103: последовательность 2 вариабельного домена VH антитела 1B4
SEQ ID NO: 104: CDR1 последовательности 2 VH антитела 131B4
SEQ ID NO: 105: CDR2 последовательности 2 VH антитела 131B4
SEQ ID NO: 106: CDR3 последовательности 2 VH антитела 131B4
SEQ ID NO: 107: ДНК-последовательность 3 VH антитела 131B4
SEQ ID NO: 108: последовательность 3 VH антитела 131B4
SEQ ID NO: 109: последовательность 3 вариабельного домена VH антитела 131B4
SEQ ID NO: 110: CDR1 последовательности 3 VH антитела 131B4
SEQ ID NO: 111: CDR2 последовательности 3 VH антитела 131B4
SEQ ID NO: 112: CDR3 последовательности 3 VH антитела 131B4
SEQ ID NO: 113: ДНК-последовательность VK антитела 131B4
SEQ ID NO: 114: последовательность VK антитела 131B4
SEQ ID NO: 115: ДНК-последовательность 1 VH антитела 131E8
SEQ ID NO: 116: последовательность 1 VH антитела 131E8
SEQ ID NO: 117: ДНК-последовательность 2 VH антитела 131E8
SEQ ID NO: 118: последовательность 2 VH антитела 131E8
SEQ ID NO: 119: ДНК-последовательность 3 VH антитела 131E8
SEQ ID NO: 120: последовательность 3 VH антитела 131E8
SEQ ID NO: 121: последовательность 3 вариабельного домена VH антитела 131E8
SEQ ID NO: 122: CDR1 последовательности 3 VH антитела 131E8
SEQ ID NO: 123: CDR2 последовательности 3 VH антитела 131E8
SEQ ID NO: 124: CDR3 последовательности 3 VH антитела 131E8
SEQ ID NO: 125: ДНК-последовательность VK антитела 131E8
SEQ ID NO: 126: последовательность VK антитела 131E8
SEQ ID NO: 127: ДНК-последовательность VH антитела 131H1
SEQ ID NO: 128: последовательность VH антитела 131H1
SEQ ID NO: 129: последовательность вариабельного домена VH антитела 131H1
SEQ ID NO: 130: CDR1 последовательности VH антитела 131H1
SEQ ID NO: 131: CDR2 последовательности VH антитела 131H1
SEQ ID NO: 132: CDR3 последовательности VH антитела 131H1
SEQ ID NO: 133: ДНК-последовательность 1 VK антитела 131H1
SEQ ID NO: 134: последовательность 1 VK антитела 131H1
SEQ ID NO: 135: последовательность 1 вариабельного домена VK антитела 131H1
SEQ ID NO: 136: CDR1 последовательности 1 VK антитела 131H1
SEQ ID NO: 137: CDR2 последовательности 1 VK антитела 131H1
SEQ ID NO: 138: CDR3 последовательности 1 VK антитела 131H1
SEQ ID NO: 139: ДНК-последовательность 2 VK антитела 131H1
SEQ ID NO: 140: последовательность 2 VK антитела 131H1
SEQ ID NO: 141: последовательность 2 вариабельного домена VK антитела 131H1
SEQ ID NO: 142: CDR1 последовательности 2 VK антитела 131H1
SEQ ID NO: 143: CDR2 последовательности 2 VK антитела 131H1
SEQ ID NO: 144: CDR3 последовательности 2 VK антитела 131H1
SEQ ID NO: 145: ДНК-последовательность VH антитела 132H4
SEQ ID NO: 146: последовательность VH антитела 132H4
SEQ ID NO: 147: ДНК-последовательность VK антитела 132H4
SEQ ID NO: 148: последовательность VK антитела 132H4
SEQ ID NO: 149: ДНК-последовательность VH антитела 133A6
SEQ ID NO: 150: последовательность VH антитела 133A6
SEQ ID NO: 151: ДНК-последовательность VK антитела 133A6
SEQ ID NO: 152: последовательность VK антитела 133A6
Примеры
А. Сравнение методов обнаружения свободного IL-18 и комплекса IL-18/IL-18ВР
1. Общепринятый метод обнаружения IL-18 в организме пациентов
Количественное определение человеческого IL-18 в организме пациентов осуществляют с помощью методов ELISA, позволяющих обнаруживать общий IL-18 (как IL-18BP в свободной форме, так и IL-18BP, входящий в комплекс). ELISA включает применение поступающих в продажу антител (см. представленную ниже таблицу 8). Наиболее часто анализы методом ELISA осуществляют с использованием пары антител к IL-18, разработанных Taniguchi и др., 1997, которые поступают в продажу от нескольких поставщиков, а именно, моноклонального мышиного антитела 125-2Н в качестве первичного/захватывающего антитела и моноклонального крысиного антитела 159-12 В в качестве вторичного/идентифицирующего антитела.


2. Оценки уровней свободного IL-18
До настоящего времени не имелось публикаций об измерениях уровней свободного IL-18. Оценки уровней свободного IL-18 осуществляли путем экстраполяции с использованием метода расчета, описанного у Novick и др., 2004 (см. ниже). Представлены результаты сравнения уровней IL-18 и IL-18BP в организме человека. Авторы этих исследований применяли пару поступающих в продажу моноклональных антител к IL-18, а именно, 125-2Н и 159-12 В, при этом антитело 125-2Н использовали для захвата, было известно, что оно связывается с комплексом IL-18/IL-18BP (Argiradi и др., 2009). Для расчета уровня свободного IL-18 в сыворотке пациента исследователи применяли закон действия масс, предполагая, что связывание антител с IL-18 является обратимым. Расчет осуществляли следующим образом:
KD=0,4нМ=([IL-18]×[IL-18BP])/[IL-18-IL18BP]
или
[IL-18] (в нМ)=(0,4×[IL-18-IL18BP])/[IL-18BP],
где:
IL-18-IL-18BP представляет собой комплекс.
Константу диссоциации рассчитывали согласно Kim и др., 2000, KD=0,4нМ.
В комплексе IL-18-IL-18BP стехиометрическое соотношение равно 1:1.
Концентрацию IL-18 определяли с помощью электрохемилюминесцентного метода.
Концентрацию IL-18BP определяли с помощью ELISA.
Важно отметить, что исследователи обнаружили большие вариации между пациентами уровней свободного IL-18 относительно уровней общего IL-18, которые не отражали соотношения между IL-18 и IL-18BP. Важно отметить, что указанное соотношение IL18/IL-18BP не указано в процитированных публикациях. Кроме того, антитела к IL-18 не обладали способностью различать свободный IL-18 и IL-18 входящий в состав комплекса IL-18/IL-18BP. И, наконец, как описано у Novick и др., 2001, антитела к IL-18BP, моноклональные антитела 582.10 и 657.27, не позволяли обнаруживать IL-18BP в свободной форме, а обнаруживали только общий IL-18BP, поскольку, как было указано, они не блокировали взаимодействие между IL-18BP и IL-18 соответственно. Таким образом, расчет свободного IL-18 на основе концентрации IL-18BP является недостаточно точным. Несмотря на определенные обнадеживающие результаты, вариация данных свидетельствует о том, что точность обнаружения свободного IL-18 можно повышать с помощью более усовершенствованного анализа с использованием антител, специфически нацеленных на область IL-18, которая связывается с IL-18BP.
3. Подтверждение того, что обычно применяемые поступающие в продажу антитела не позволяют обнаруживать свободный IL-18
Было протестировано одиннадцать поступающих в продажу моноклональных антител к IL-18 в отношении их способности предупреждать любое взаимодействие между IL-18 и IL-18BP. Приведенные ниже данные демонстрируют, что они не обладали такой способностью и ни одно из протестированных антител не связывалось с сайтом, обеспечивающим взаимодействие между IL-18 и IL-18BP. Следовательно, обнаружение свободного IL-18 в полученных из организма человека образцах требует разработки специфической конструкции и подходов, нацеленных, например, на сайт связывания/эпитоп IL-18 для IL-18BP.
Обычно применяемые антитела 125-2Н и 159-12В тестировали в отношении из применимости в качестве захватывающего и идентифицирующего антител (см. фиг. 2). Полученные данные свидетельствуют о том, что оба антитела не распознают эпитоп IL-18, специфический для IL-18BP и, следовательно, позволяют количественно оценивать только общий IL-18 (обе формы, т.е. свободный и входящий в комплекс с IL-18BP).
Параллельно с антителами 125-2Н и 159-12G тестировали девять других поступающих в продажу моноклональных антител в отношении их способности обнаруживать свободный IL-18 в тех же условиях, которые описаны выше. Как указано выше, такое антитело должно позволять обнаруживать свободный IL-18 в биологических образцах. Перечень протестированных поступающих в продажу антител представлен в приведенной ниже таблице 9.

Полученные данные свидетельствуют о том, что ни одно из поступающих в продажу антител не обладало способностью отличать свободный IL-18 от IL-18, входящего в комплекс с IL-18BP.
4. Процедура на основе ELISA для обнаружения свободного IL-18
4.1. Захват свободного IL-18 с помощью IL-18BP
Лунки титрационного микропланшета сенсибилизировали взятым в соответствующем объеме забуференным фосфатом физиологическим раствором, содержащим рекомбинантный человеческий IL-18BP. Планшеты инкубировали в течение определенного периода времени при 4°С и затем стабилизировали блокирующим буфером, содержащим бычий сывороточный альбумин или другие пригодные блокирующие агенты. После завершения реакции микропланшеты запечатывали и хранили при 4°С до того, как их использовали для обнаружения свободного IL-18. Микропланшеты можно было также сушить в стабилизирующем растворе, что позволяло хранить их при комнатной температуре, и затем восстанавливать путем гидратации при подготовке для проведения анализа.
Например, для получения конечного реакционного объема 100 мкл сначала вносили первые 80 мкл конъюгата биотин/антитело. Образцы или биологические жидкости, содержащие свободный IL-18, тестировали с использованием сенсибилизированных IL-18BP микропланшетов. После этого вносили образец, содержащий биологическую жидкость или стандарт, в объеме 20 мкл на лунку микропланшета. Неразбавленная или разбавленная биологическая жидкость может представлять собой (но, не ограничиваясь только ими) сыворотку, мочу, слезы, слюну, желчь, пот, выдыхаемый или выделяемый продукт, мокроту, бронхоальвеолярную жидкость, секрет сальных желез, клеток, желез, слизистой оболочки или ткани, биопсию, гомогенизированную ткань. Концентрации применяемого в качестве стандарта свободного IL-18 составляли от 4,2 до 3000 пг/мл. Стандарт и его разведения до требуемых концентраций приготавливали с использованием поступающего в продажу рекомбинантного человеческого IL-18. Планшеты запечатывали и затем инкубировали при осторожном встряхивании для захвата свободного IL-18. Реакции давали осуществляться в течение необходимого периода времени, составлявшего от нескольких минут до нескольких часов, при комнатной температуре, при 37°С или других температурах, которые не влияли на стабильность образцов и реагентов. Лунки микропланшета интенсивно промывали соответствующим буфером и затем в каждую лунку добавляли по 100 мкл проявляющей смеси для буфера. Проявляющая смесь содержала конъюгированный со стрептавидином фермент, такой как пероксидаза или щелочная фосфатаза. Лунки микропланшета запечатывали и давали осуществляться реакции в течение определенного периода времени, составлявшего от нескольких минут до нескольких часов при комнатной температуре, при 37°С или других температурах, которые не влияли на стабильность образцов и реагентов. Затем осуществляли мониторинг результатов реакции с помощью ридера для микропланшета при соответствующей полученному реагенту длине волны абсорбции или флуоресценции, находящейся в манометровом диапазоне.
4.2. Захват свободного IL-18 антителом к IL-18
Лунки микропланшета сенсибилизировали взятым в соответствующем объеме забуференным фосфатом физиологическим раствором, содержащим антитело X. Планшеты инкубировали в течение определенного периода времени при 4°С и затем стабилизировали блокирующим буфером, содержащим бычий сывороточный альбумин или другие пригодные блокирующие агенты. После завершения реакции микропланшеты запечатывали и хранили при 4°С до того, как их использовали для обнаружения свободного IL-18. Микропланшеты можно было также сушить в стабилизирующем растворе, что позволяло хранить их при комнатной температуре, и затем восстанавливать путем гидратации при подготовке для проведения анализа.
Например, для получения конечного реакционного объема 100 мкл сначала вносили первые 80 мкл конъюгата биотин/антитело. Образцы или биологические жидкости, содержащие свободный IL-18, тестировали с использованием сенсибилизированных IL-18BP микропланшетов. После этого вносили образец, содержащий биологическую жидкость или стандарт, в объеме 20 мкл на лунку микропланшета. Неразбавленная или разбавленная биологическая жидкость может представлять собой (но, не ограничиваясь только ими) сыворотку, мочу, слезы, слюну, желчь, пот, выдыхаемый или выделяемый продукт, мокроту, бронхоальвеолярную жидкость, секрет сальных желез, клеток, желез, слизистой оболочки или ткани, биопсию, гомогенизированную ткань. Концентрации применяемого в качестве стандарта свободного IL-18 составляли от 4,2 до 3000 пг/мл. Стандарт и его разведения до требуемых концентраций приготавливали с использованием поступающего в продажу рекомбинантного человеческого IL-18. Планшеты запечатывали и затем инкубировали при осторожном встряхивании для захвата свободного IL-18. Реакции давали осуществляться в течение необходимого периода времени, составлявшего от нескольких минут до нескольких часов, при комнатной температуре, при 37°С или других температурах, которые не влияли на стабильность образцов и реагентов. Лунки микропланшета интенсивно промывали соответствующим буфером и затем в каждую лунку добавляли по 100 мкл проявляющей смеси для буфера. Проявляющая смесь содержала конъюгированный со стрептавидином фермент, такой как пероксидаза или щелочная фосфатаза. Лунки микропланшета запечатывали и давали осуществляться реакции в течение определенного периода времени, составлявшего от нескольких минут до нескольких часов при комнатной температуре, при 37°С или других температурах, которые не влияли на стабильность образцов и реагентов. Затем осуществляли мониторинг результатов реакции с помощью ридера для микропланшета при соответствующей полученному реагенту манометровой длине волны абсорбции или флуоресценции.
4.3. Титрование свободного IL-18 в зависимости от уровня IL-18BP
Постоянное количество рекомбинантного IL-18 титровали в зависимости от различных и строго определенных количеств IL-18BP для того, чтобы определить, когда становится более невозможно обнаруживать свободный IL-18. В раствор, содержащий 400 пг/мл IL-18 в ЗФР, дополненный 5% BSA, впрыскивали определенные количества IL-18BP в диапазоне от 0 до 10000 пг/мл. Молярное соотношение рассчитывали на основе соответствующих молекулярных масс IL-18 и IL-18BP. Обнаружение свободного IL-18 осуществляли с помощью ELISA с использованием IL-18BP для IL-18 как описано выше. Полученные данные, представленные на фиг. 1, свидетельствуют о том, что при концентрациях IL-18BP, равных или превышающих 6000 пг/мл, что соответствовало молярному соотношению IL-18BP/IL-18, равному ~15, обнаруживаемый IL-18, взятый в концентрации 400 пг/мл, находился вблизи соответствующего фону уровня обнаружения. В отличие от этого, при молярном соотношении меньшем 15, свободный IL-18 легко поддавался обнаружению.
4.4. Пересмотренный расчет константы диссоциации (KD) комплекса человеческий IL-18/IL-18 ВР
4.4.1 Расчет KD на основе результатов титрования
По опубликованным в литературе данным, полученным на основе измерений методом BIAcore, величина KD составляет 400пМ (Kim и др., 20008). Однако, вследствие полученных выше результатов процедура определения KD была скорректирована с использованием описанной выше процедуры на основе ELISA. Осуществляли титрование 10пМ IL-18 возрастающими концентрациями IL-18BP (60пМ-3нМ) либо в а) сыворотке здорового добровольца с истощенным эндогенным IL-18BP, либо в б) ЗФР, дополненном 5% BSA. Анализ свободного IL-18 методом ELISA в дополнение к доступным на коммерческой основе анализам общего IL-18 и общего IL-18BP позволяет определять величину Ко в растворе, что должно позволять лучше характеризовать аффинность IL-18 к связывающему его белку в общей воде организма, чем данные, полученные с помощью твердофазного метода BIAcore. Репрезентативные результаты представлены в таблице 10.
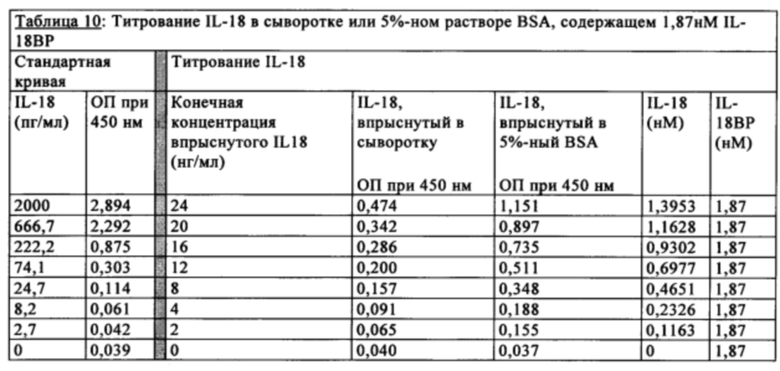
KD рассчитывали на основе следующей формулы:
KD=[свободный IL-18]×[свободный IL-18ВР]/[комплекс IL-18/IL-18BP]
[свободный IL-18BP]=[общий IL-18BP]-[свободный IL-18]
[комплекс IL-18/IL-18BP]=[общий IL-18]-[свободный IL-18]
Результат: KD=50пМ (разбавитель - сыворотка); 35пМ (разбавитель - 5%-ный BSA)
На основе результатов титрования установлено, что величина KD в применяемой в качестве разбавителя сыворотке составляла 50пМ, в ЗФР, дополненном 5% BSA - 35пМ соответственно. Новая рассчитанная величина KD, отличающаяся от предыдущих оценок величины KD для взаимодействия человеческого IL-18BP и IL-18, свидетельствует о том, что ранние оценки уровней свободного IL-18, основанные на KD, равной 400пМ, опубликованные Kim и др., 2000, являются неточными.
4.4.2 Оценки KD с помощью BIAcore
После получения с использованием титрования указанных выше величин КD при создании изобретения анализировали аффинность связывания IL-18BP с IL-18 с помощью более простого варианта метода BIAcore, заключающегося в том, что связывали IL-18 ВР с BIAcore-чипом и затем анализировали его афинность к IL-18. Этот вариант метода отличался от описанного у Kim и др., 20008, в котором IL-18 связывали с BIAcore-чипом, сенсибилизированным моноклональным антителом, и затем анализировали аффинность комплекса антитело-IL-18 к IL-18BP. Важно отметить, что полученные с помощью нового варианта метода BIAcore данные полностью соответствовали указанным выше результатам, полученным на основе титрования, т.е. величины KD находились в диапазоне от 20 до 30пМ. Результаты представлены в приведенной ниже таблице 11.

4.5. Титрование внесенного IL-18 в сыворотке или 5%-ном растворе BSA, содержащих IL-18BP
Человеческая сыворотка содержит значительные количества эндогенного IL-18, а также IL-18, входящего в комплекс с IL-18BP, уровни которых находятся в нанограммовом и пикограммовом диапазонах соответственно. Они оба могут быть обнаружены с помощью поступающих в продажу антител. Однако, в настоящее время в продаже отсутствуют анализы, которые можно применять для обнаружения свободного IL-18. Для проверки пригодности описанного выше варианта метода ELISA для обнаружения свободного IL-18, при создании изобретения вносили рекомбинантный человеческий IL-18 в человеческую сыворотку с целью определения пределов обнаружения. Для этого несколько нанограммов IL-18 вносили либо в сыворотку, содержащую эндогенный IL-18BP в концентрации 35 нг/мл, либо в раствор ЗФР, дополненный 5% BSA и 35 нг/мл IL-18BP. Мониторинг полученных уровней свободного IL-18 осуществляли с помощью описанной выше процедуры ELISA. Результаты приведены в представленной ниже таблице 12.
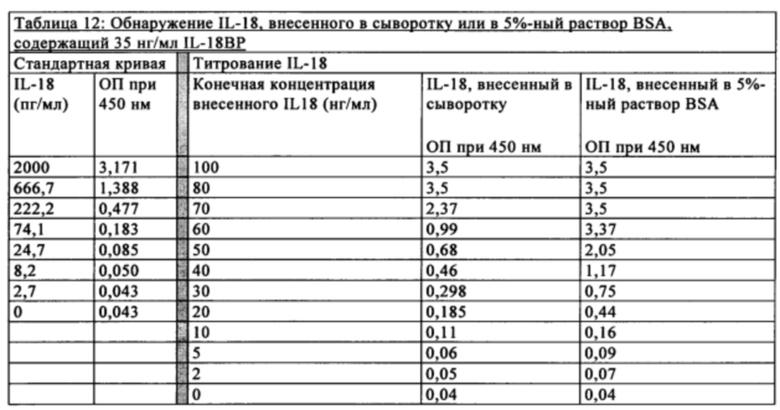
5. Обнаружение свободного IL-18 в организме пациентов
5.1. Обнаружение свободного IL-18 в сыворотке и синовиальной жидкости пациентов, страдающих различными воспалительными заболеваниями
Образцы, взятые из организма пациентов, страдающих различными воспалительными заболеваниями, анализировали с помощью описанного выше метода ELISA. Для этого были выбраны различные заболевания и условия стресса, которые, как известно, сопровождаются повышенными уровнями IL-18, такие как ревматоидный артрит, псориаз, системная красная волчанка и нахождение в отделении интенсивной терапии. По имевшимся данным у этих пациентов не проводили идентификацию свободного IL-18, а проводили только расчеты на основе закона действующих масс и величины KD, равной 400пМ, указанной в публикации Kim и др., 2000. Принимая во внимание указанные выше данные, ожидалось, что будет трудно обнаружить возможные уровни свободного IL-18, поскольку согласно научным публикациям уровни общего IL-18 в сыворотке находятся ниже или вблизи 1000 пг/мл. Кроме того, при создании изобретения протестировали образцы, взятые из организма здоровых контролей соответствующего возраста для проверки возможностей предлагаемого в изобретении варианта ELISA. Как и ожидалось, и это противоречило опубликованным оценкам, полученным на основе закона действующих масс, оказалось невозможно обнаружить уровни свободного IL-18 как в сыворотке, так и в синовиальной жидкости, в то время как уровни общего IL-18 и IL-18BP поддавались обнаружению (см. таблицу 13).
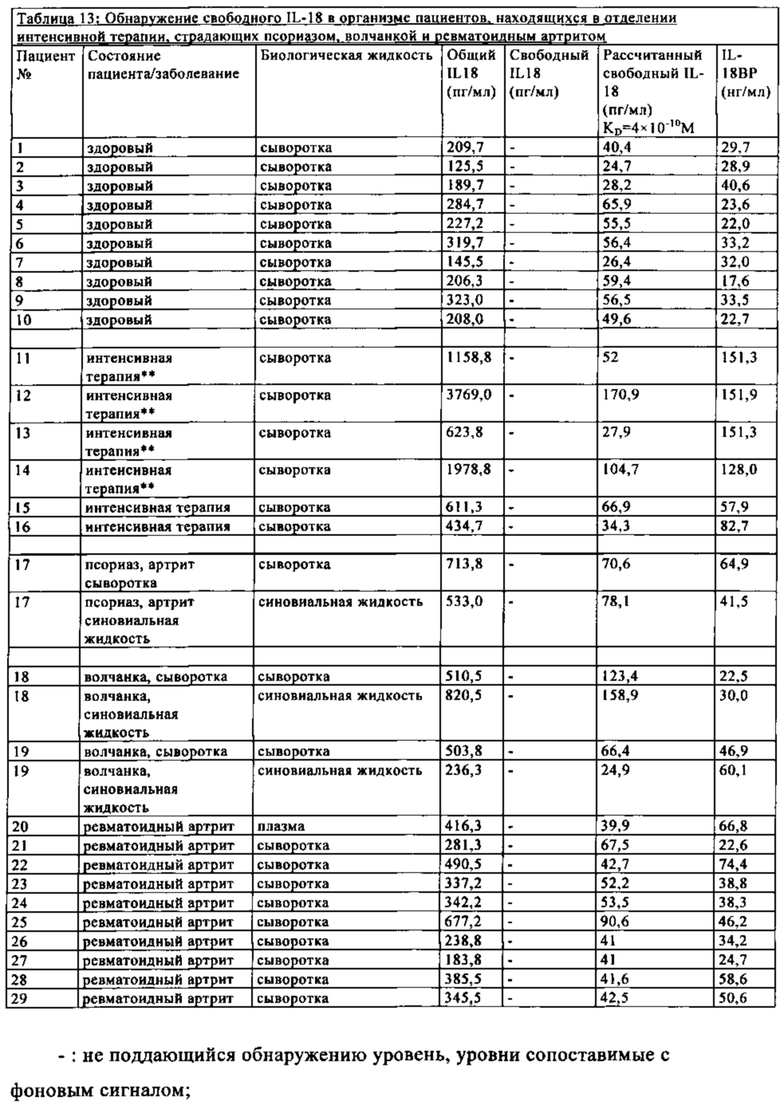
5.2. Обнаружение свободного IL-18 в сыворотке пациентов, страдающих болезнью Стилла взрослых с ранним началом
После получения указанных результатов при создании изобретения были проанализированы образцы, взятые из организма пациентов с болезнью Стилла взрослых с ранним началом, для которой, как известно, в отличие от указанных выше состояний, характеризующихся сравнительно низкими уровнями общего IL-18, характерны повышенные уровни общего IL-18 в сыворотке (Kawashima и др., 2001, и Chen и др., 2004). Как описано у Kawashima и др., 2001, и в других публикациях, повышенные уровни IL-18 в сыворотке коррелируют с симптомами болезни Стилла взрослых с ранним началом, такими как а) пирексия, артралгия, артрит, повреждения хрящей, б) повышенные уровни ферритина и в) ферменты печени (LDH). Благодаря описанному выше варианту ELISA при создании изобретения впервые были получены уровни свободного IL-18 у пациентов с болезнью Стилла взрослых с ранним началом (см. таблицу 14). Как и для других проанализированных состояний, рассчитанные уровни свободного IL-18 не соответствовали обнаруженным уровням свободного IL-18. Полученные данные свидетельствуют о том, что по меньшей мере 70% пациентов давали положительную реакцию на присутствие свободного IL-18.
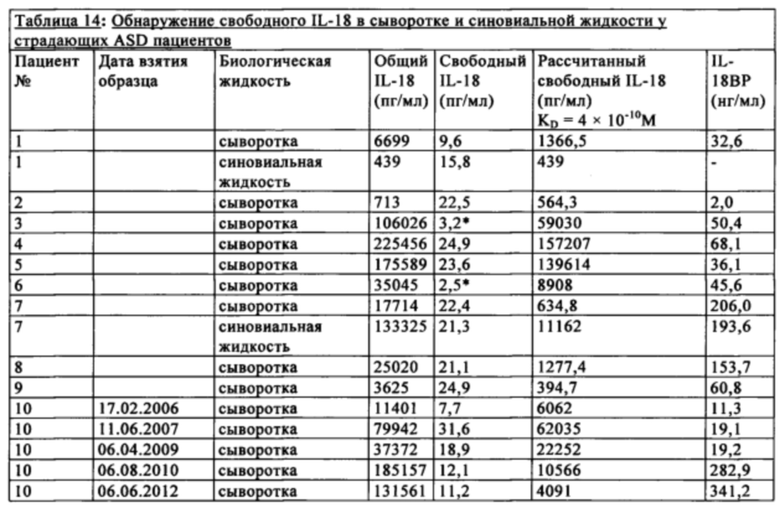
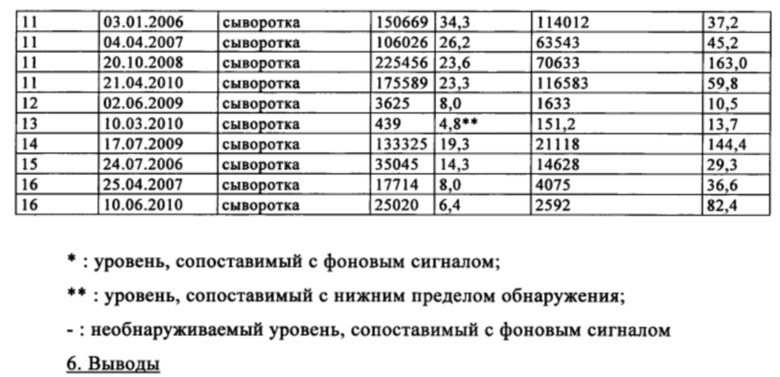
6. Выводы
Данные, приведенные в обеих публикациях, и полученные с помощью описанного выше варианта эксперимента, демонстрируют, что поступающие в продажу моноклональные антитела позволяют обнаруживать общий IL-18, но не свободный IL-18. Кроме того, подтверждено также, что наиболее широко применяемые для количественной оценки IL-18 антитела, а именно, 125-2Н и 159-12В, позволяют обнаруживать общий IL-18.
Оценка свободного IL-18 с использованием закона действующих масс представляет собой перспективный подход. Однако, получаемые при этом большие диапазоны погрешностей («усы» на графиках) не позволяют применять его для мониторинга в клинических условиях. Кроме того, антитела к IL-18BP позволяют обнаруживать общий IL-18BP, а не его свободную форму. В результате этого расчет уровня свободного IL-18 на основе концентрации IL-18 ВР является недостаточно точным.
Предложенный подход для количественной оценки свободного IL-18, основанный на использовании в качестве мишени сайта связывания IL-18 с IL-18ВР, по-видимому, является более приемлемым, и впервые продемонстрировано, что он дает более точные результаты, чем экстраполяция количественных оценок с использованием закона действующих масс. Кроме того, аффинность IL-18BP оказалась более высокой по сравнению данными, представленными в публикации Kim и др., 2000, величины KD составляют примерно 50пМ в сыворотке и с помощью нового варианта метода BIAcore установлено, что они составляют 20-30пМ.
И, наконец, у пациентов, страдающих болезнью Стилла взрослых с ранним началом, с помощью подхода на основе ELISA и варианта, предложенного в настоящем изобретении, впервые было диагностировано присутствие свободного IL-18. Эти данные подтверждают полученные ранее результаты оценок общего IL-18 при болезни Стилла взрослых с ранним началом, опубликованные Kawashima и др., 2001, и Chen и др., 2004, в этих работах сообщалось о высоких уровнях общего IL-18. Впервые новый подход на основе ELISA, представленный в настоящем описании, продемонстрировали присутствие свободного, не входящего в комплекс и биологически активного провоспалительного IL-18 у пациентов с болезнью Стилла взрослых с ранним началом.
Б. Эффективность IL-18BP на модели обострения COPD, созданной на мышах
Цель исследования заключалась в определении воздействия IL-18BP, вводимого подкожным путем при трех уровнях доз, на индуцированное полиинозиновой:полицитидиловой кислотой обострение легочного воспаления, индуцированного табачным дымом, у мышей линии C57BL/6J. В данное исследование включали в качестве референс-соединения дексаметазон, который вводили в высоких дозах оральным путем.
1. Общая методология: четырехдневное обострение/созданная с помощью табачного дыма модель на мышах
Мышам вводили либо наполнитель (ЗФР), либо IL-18BP. IL-18BP вводили подкожно трем группам животных в дозе 1, 3 или 10 мг/кг соответственно за 2 ч до первого воздействия табачным дымом в период со дня 1 по день 4. Мышам вводили орально либо наполнитель, либо дексаметазон (10 мг/кг) за 1 ч до обработки дымом, которую осуществляли дважды в день. Мышам вводили интраназально либо наполнитель, либо полиинозиновую:полицитидиловую кислоту (2 мг/кг) за 2 ч до первого воздействия воздухом или табачным дымом в день 4 для индукции обострения легочного воспаления. Воздействие табачным дымом осуществляли утром и во второй половине дня согласно следующей схеме: день 1 - в течение 15 мин, день 2 - в течение 25 мин, день 3 - в течение 30 мин и день 4 - в течение 30 мин.
Данные о группах животных и соответствующих режимах их обработки обобщены в таблице 15.

После завершения указанных выше обработок животных умерщвляли анестезией в день 5. Затем брали образцы крови из подключичной артерии (плазма) и осуществляли бронхоальвеолярный лаваж животных с использованием 3×0,4 мл ЗФР для последующего клеточного анализа и анализа цитокинов/медиаторов. Супернатанты бронхоальвеолярного лаважа хранили при -80°С до проведения анализа цитокинов/медиаторов. Клетки, выделенные из BALF, подсчитывали с использованием счетчика клеток фирмы Sysmex. И, в завершение, осуществляли статистический анализ полученных данных с помощью t-критерия Стьюдента и дисперсионного анализа (если данные удовлетворяли закону нормального распределения, то применяли критерий Сидака, если данные не удовлетворяли закону нормального распределения, то применяли критерий Крускала-Уоллеса).
2. Подтверждение активации пути IL-18 при четырехдневном обострении/на созданной с помощью табачного дыма модели на мышах
Мышиный IL-18 в BAL анализировали с помощью поступающего в продажу ELISA для подтверждения на мышиной модели пути активации IL-18. Полученные данные свидетельствуют о выраженной индукции IL-18 в пространстве легочных дыхательных путей (см. фиг. 5). IL-18 не поддавался обнаружению в контроле (только воздух). Важно отметить, что экспрессия IL-18 имела место при воздействии дыма, но при обработке только поли [I:С] индукция была незначительной (ниже нижнего предела обнаружения). В отличие от этого и в соответствии с ожидаемым комбинация дыма и поли [I:С] значительно повышала содержание IL-18 в BAL до намного более высоких уровней, чем при воздействии только дыма или только поли[I:С].
3. Ослабление с помощью IL-18BP обострения воспаления при обострении/на созданной с помощью табачного дыма модели на мышах
3.1. Ингибирование с помощью IL-18BP общей инфильтрации клеток и обострения воспаления в пространстве легочных дыхательных путей
У мышей, обработанных IL-18BP, происходило значительное ослабление общей инфильтрации клеток в легкое, имевшей место после индукции обострения воспаления. Для доз 3 и 10 мг/кг было выявлена их статистически значимая эффективность по сравнению с применявшимся в качестве положительного контроля дексаметазоном (см. фиг. 5). Важно отметить, что для дозы дексаметазона 3 мг/кг на мышиной модели не было выявлено признаков эффективного действия (данные не представлены), это свидетельствует о том, что высокая доза дексаметазона, равная 10 мг/кг, может индуцировать апоптоз клеток определенных типов, таких как макрофаги, эозинофилы и лимфоциты (данные не представлены). Сходные результаты были получены на мышиной модели при использовании рофлумиласта, т.е. [3-(циклопропилметокси)-N-(3,5-дихлорпиридин-4-ил)-4-(дифторметокси)бензамида], в этом случае не было выявлено признаков ингибирования инфильтрации при использовании дозы 2,5 мг/кг (данные не представлены). На фиг. 6 продемонстрирована выраженная и статистически достоверная эффективность IL-18BP при его применении в дозе 10 мг/кг на представленной в настоящем описании мышиной модели.
3.2. Ингибирование с помощью IL-18BP инфильтрации нейтрофилов в пространство легочных дыхательных путей
Инфильтрация нейтрофилов ингибировалась IL-18BP в легких с обострением, индуцированным дымом. Продемонстрирована статистически значимая эффективность IL-18BP в дозах 3 и 10 мг/кг по сравнению с применявшимся в качестве положительного контроля дексаметазоном (см. фиг. 7). В рассматриваемых условиях при использовании созданной на мышах модели IL-18BP в дозе 10 мг/кг обладал, по-видимому, наилучшей статистически значимой эффективностью (см. фиг. 8).
3.3. Ингибирование пути колониестимулирующего фактора гранулоцитов (G-CSF) в пространстве легочных дыхательных путей
G-CSF представляет собой широко известный цитокин, имеющий решающее значение для выживания, пролиферации, дифференцировки и функции предшественников нейтрофилов и зрелых нейтрофилов. Следовательно, ослабление индуцированного дымом-р[I:С] пути G-CSF является важным фактором, демонстрирующим влияние IL-18BP на рекрутмент нейтрофилов в пространство легочных дыхательных путей у мышей. Мониторинг присутствия G-CSF в BALF осуществляли с помощью поступающего в продажу набора для ELISA. На фиг. 9 продемонстрировано, что введение IL-18BP ослабляет высвобождение G-CSF в легочных дыхательных путях, подтверждая тем самым ингибирование инфильтрации нейтрофилов. Три протестированные на мышиной модели дозы IL-18BP обладали статистически значимым действием.
3.4. Безопасность IL-18BP: Влияние на потерю веса при обострении/на созданной с помощью табачного дыма модели на мышах
Введение IL-18BP, по-видимому, хорошо переносилось при обострении/на созданной с помощью табачного дыма модели на мышах. Например, IL-18BP снижал потерю веса даже несмотря на то, что результаты статистического анализа с использованием t-критерия Стьюдента и дисперсионного анализа не были значимыми (см. фиг. 10). У большей части мышей, которым вводили IL-18 ВР в дозах 3 и 10 мг/кг, потеря веса составляла 6-7% соответственно, в отличие от контроля, подвергавшегося воздействию табачного дыма и р[I:С], для которого потеря составляла примерно 9%. Таким образом, данные об уменьшении потери веса свидетельствуют о том, что IL-18BP не приводит к дополнительному стрессу у подопытных животных. Важно отметить, что у мышей, которых обрабатывали только р[I:С], не выявлено потери веса по сравнению с мышами, которых обрабатывали комбинацией р[I:С] и табачного дыма [см. фиг. 8, обработка 3) и 4)].
В. Создание моноклональных антител к IL-18
1. Иммунизация мышей и скрининг моноклональных антител
Мышей вакцинировали против человеческого интерлейкина-18 с применением технологии, позволяющей осуществлять иммунизацию белками, имеющими правильную укладку. Перед иммунизацией отбирали генетически модифицированных мышей по признаку главных комплексов гистосовместимости, которые могут быть чувствительными к расположенным на поверхности эпитопам IL-18, связывающимся с IL-18BP. После иммунизации выделяли В-клетки из селезенки и осуществляли гибридизацию согласно стандартной технологии создания гибридом. Гибридомы отбирали на микропланшетах и затем анализировали в отношении экспрессии моноклональных антител к IL-18, мишенью которых являлись эпитопы IL-18, содержащиеся в сайтах связывания с IL-18BP. Скрининг проводили, осуществляя 3 последовательные и избирательные стадии отбора:
Первая стадия. Попытку позитивного скрининга антител осуществляли с использованием IL-18, связанного с Luminex-гранулами, выявляя клетки, экспрессирующие моноклональные антитела к IL-18.
Вторая стадия. Антитела-кандидаты, нацеленные на находящийся на IL-18 сайт связывания с IL-18BP, подвергали повторному скринингу в условиях конкуренции с IL-18BP. Для этого моноклональные антитела связывали с Luminex-гранулами, несущими IL-18. Затем комплекс подвергали воздействию биотинилированного IL-18BP для выявления интерференции с ранее идентифицированными антителами к IL-18 (см. таблицу 1, колонка №2). В результате второго скрининга было отобрано более 300 положительных антител-кандидатов (см. таблицу 1, колонка №3). Количество позитивных кандидатов неожиданно оказалось большим, что, по-видимому, свидетельствовало об очень успешной иммунизации мышей в отношении области эпитопа-мишени. Однако уровни ингибирования были недостаточными, о чем свидетельствовали сниженные, но все еще присутствовавшие флуоресцентные сигналы, что указывало на связывание IL-18BP с входящим в комплекс антителом к IL-18. Тем не менее, и это является важным, такой стандартный описанный во многих источниках метод скрининга не учитывает возможной стерической помехи, создаваемой крупной молекулой антитела (примерно 160 кДа), для имеющего намного меньший размер IL-18BP (примерно 18 кДа, только пептид).
Третья стадия. Третью стадию скрининга осуществляли с использованием Luminex-гранул, связанных с IL-18BP и затем включенных в комплекс с интерлейкином-18, что гарантировало презентацию имеющего правильную укладку рекомбинантного IL-18 позитивным антителам-кандидатам. Описанная процедура скрининга характеризовалась значительно большей избирательностью, поскольку большинство из указанных выше антител все еще были связаны с Luminex-гранулами, несущими IL-18, это свидетельствовало о том, что их выявленное ранее ингибирующее воздействие на IL-18BP было обусловлено стерической помехой. В итоге было выявлено в общей сложности 12 антител, которые рассматривались как нацеливающие IL-18 на белок IL-18BP, поскольку они давали очень слабый флуоресцентный сигнал после связывания с IL-18 в присутствии IL-18BP, а именно, клоны №№107С6, 108F8, 109А6, 111А6, 129С3, 131 В4, 131Е8, 131Н1, 132С12, 132Н4, 133А6 и 134 В2 (см. таблицу 16, колонка №4, отобранные клоны характеризовались ингибированием, более чем в 500 раз превышающим ингибирование клонами, указанными в колонке №2). Сравнение позитивных клонов с набором негативных клонов представлено в приведенной ниже таблице 16.
Данные, полученные в результате осуществления третьей стадии скрининга (таблица 16, колонка №4), стимулировали проведение также секвенирования мРНК и операцию по разведению клонов для обогащения позитивных в отношении моноклональных антител клеток клонов # 107С6, 108F8, 109А6, 111А6, 129С3, 131В4, 131Е8, 131Н1, 132С12, 132Н4, 133А6 и 134 В2. Было подтверждено, что все эти моноклональные антитела связывались с IL-18 в сайте связывания IL-18BP.

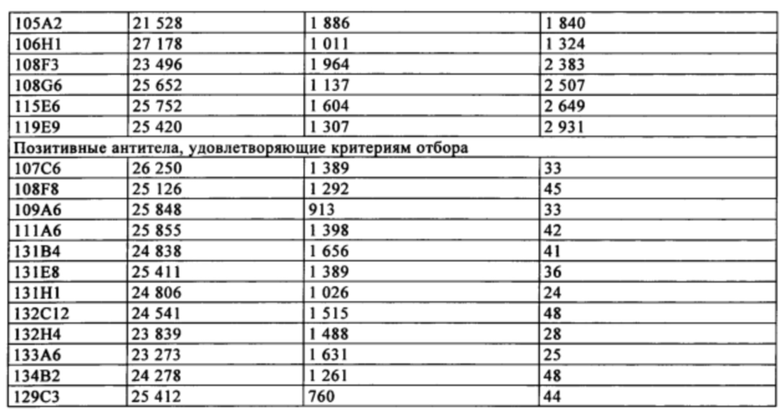
Ссылки
Argiriadi М.А., Xiang Т., Wu С, Ghayur Т. и Borhani D.W., Unusual water-mediated antigenic recognition of the proinflammatory cytokine interleukin-18. J Biol Chem; 284(36), 2009, cc. 24478-24489;
Azoulay E., Eddahibi S., Marcos E., Levame M., Harf A., Schlemmer В., Adnot S. и Delclaux C, Granulocyte colony-stimulating factor enhances alpha-naphthylthiourea-induced pulmonary hypertension. J Appl Physiol; 94, 2003, cc. 2027-2033;
Baron R.M, Choi A.J.S., Owen C.A. и Choi A.M.K., Genetically manipulated mouse models of lung disease: potential and pitfalls. Am J Physiol Lung Cell Mol Physiol; 2012, cc. 485-497;
Chen D.Y., Lan J.L., Lin F.J. и Hsieh T.Y., Proinflammatory cytokine profiles in sera and pathological tissues of patients with active untreated adult onset Still's disease. J Rheumatol; 31, 2004, cc. 2189-2198;
Chen D.Y., Lan J.L., Lin F.J., Hsieh T.Y. и Wen M.C., Predominance of Th1 cytokine in peripheral blood and pathological tissues of patients with active untreated adult onset Still's disease. Ann Rheum Dis; 63(10), 2004, cc. 1300-1306;
Cunningham R.E., Tissue disaggregation. Methods Mol Biol; 34, 1994, cc. 225-228;
Daley E., Emson C, Guignabert C, de Waal Malefyt R., Louten J., Kurup V.P., Hogaboam C, Taraseviciene-Stewart L., Voelkel N.F., Rabinovitch M. и др., Pulmonary arterial remodeling induced by a Th2 immune response. J Exp Med; 205, 2008, cc. 361-372;
Elias J.A., Kang M.J., Crothers К. и др., Mechanistic heterogeneity in chronic obstructive pulmonary disease: insights from transgenic mice. Proc Am Thorac Soc; 2006, cc. 494-498;
Eltom S., Stevenson C.S. и Rastrick J., P2X7 Receptor and Caspase - 1 Activation Are Central to Airway Inflammation Observed after Exposure to Tobacco Smoke, PLoS ONE; 6(9), 2011, e24097;
Hackett B.P., Shimizu N. и Gitlin J.D., Clara cell secretory protein gene expression in bronchiolar epithelium. Am J Physiol; 262, 1992, cc. L399-L404;
Halbower A.C., Mason R.J., Abman S.H. и Tuder R.M., Agarose infiltration improves morphology of cryostat sections of lung. Lab Invest; 71, 1994, cc. 149-153;
Hautamaki R.D., Kobayashi D.K., Senior R.M. и Shapiro S.D., Requirement for macrophage elastase for cigarette smoke-induced emphyseme in mice. Science; 277, 1997, cc. 2002-2004;
Hoshino Т., Kawase Y., Okamoto M. и др., IL-18-transgenic mice: in vivo evidence of a broad role for IL-18 in modulating immune function. J Immunol; 2001, cc. 7014-7018;
Hoshino Т., Kato S., Oka N. и др., Pulmonary inflammation and emphyseme: role of the cytokines IL-18 and IL-13. Am J Respir Crit Care Med, 2007, cc. 49-62;
Helmut Fenner. Targeting IL-18 in Chronic Obstructive Pulmonary Disease: Background and rationale. 22 марта 2013 г., CONFIDENTIAL, с. 19;
Hou S., Li В., Wang L., Qian W., Zhang D., Hong X., Wang H., Guo Y.. «Humanization of an anti-CD34 monoclonal antibody by complementarity-determining region grafting based on computer-assisted molecular modeling)). J Biochem 144 (1), 2008, cc. 115-120;
Imaoka H., Hoshino Т., Takei S., Kinoshita Т. и др., Interleukin-18 production and pulmonary function in COPD. Eur Respir J, 2008, cc. 287-297;
Jaatinen Т., Laine J., Isolation of mononuclear cells from human cord blood by Ficoll-Paque density gradient. Curr Protoc Stem Cell Biol; глава 2, том Unit 2A.1, 2007;
Kang M.J., Lee C.G., Lee J.Y., Dela Cruz C.S., Chen Z.J., Enelow R., Elias J.A., Cigarette smoke selectively enhances viral PAMP- and virus-induced pulmonary innate immune and remodeling responses in mice. J Clin Invest; 118, 2008, cc. 2771-2784;
Kang M.J., Homer R.J., Gallo А. и др., IL-18 is induced and IL-18 receptor alpha plays a critical role in the pathogenesis of cigarette smoke-induced pulmonary эмфизема and inflammation. J Immunol, 2007, cc. 1948-1959;
Kang M.J., Choi J.M., Kim B.H. и др., IL-18 induces emphyseme and airway and vascular remodeling via IFNγ, IL-17A, and IL-13. Am J Respir Crit Care Med, 2012, cc. 1205-1217;
Kashmiri S.V., De Pascalis R., Gonzales N.R., Schlom J., «SDR grafting-a new approach to antibody humanization». Methods 36 (1), май 2005, cc. 25-34;
Kawashima M. и др., Levels of interleukin-18 and its binding inhibitors in the blood circulation of patients with adult-onset Still's disease. Arthritis Rheum; 44(3), 2001, cc. 550-560;
Kim S.H. и др., Structural requirements of six naturally occurring isoforms of the IL-18 binding protein to inhibit IL-18. Proc Natl Acad Sci USA; 97(3), 2000, cc. 1190-1195;
Kratzer A., Salys J., Nold-Petry ЕЛ. и др., Role of IL-18 in second hand smoke-induced emphyseme. Am J Respir Cell Mol Biol; 48(6), 2013, cc. 725-732;
Lee C.G., Link H., Baluk P., Homer R.J., Chapoval S., Bhandari V., Kang M.J., Cohn L., Kim Y.K., McDonald D.M. и др., Vascular endothelial growth factor (VEGF) induces remodeling and enhances TH2- mediated sensitization and inflammation in the lung. Nat Med; 10, 2004, cc. 1095-1103;
Lee C.G., Hartl D., Lee G.R., Koller В., Matsuura H., Da Silva C.A., Sohn M.H., Cohn L., Homer R.J., Kozhich A.A. и др., Role of breast regression protein 39 (BRP-39)/chitinase 3-like-l in Th2 and IL-13-induced tissue responses and apoptosis. J Exp Med; 206, 2009, cc. 1149-1166;
Liu J. и др., Requirement for tumor necrosis factor-receptor 2 in alveolar chemokine expression depends upon the form of the ligand. Am J Respir Cell Mol Biol; 33, 2005, cc. 463-469;
Londhe V.A., Maisonet T.M., Lopez В., Jeng J.M., Li C., Minoo P., A subset of epithelial cells with CCSP promoter activity participates in alveolar development. Am J Respir Cell Mol Biol; 44, 2011, cc. 804-812;
Loza M.J., Watt R., Baribaud F., Barnathan E.S. и Rennard S.I., Systemic inflammatory profile and response to anti-tumor necrosis factor therapy in chronic obstructive pulmonary disease. Respir Res; 13, 2012, c. 12;
Ma В., Kang M.J., Lee C.G., Chapoval S., Liu W., Chen Q., Coyle A.J., Lora J.M., Picarella D., Homer R.J. и Elias J.A., Role of CCR5 in IFN-γ-induced and cigarette smoke-induced emphyseme. J Clin Invest; 115, 2005, cc. 3460-3472;
Nakajima Т. и Owen C., Interleukin-18: The Master Regulator Driving Destructive and Remodeling Processes in the Lungs of Patients with Chronic Obstructive Pulmonary Disease? Am J Respir Crit Care Med, 2012, cc. 1137-1138;
Novick D. и др., A novel IL-18BP ELISA shows elevated serum IL-18BP in sepsis and extensive decrease of free IL-18. Cytokine, 14, 2001, cc. 334-342;
Novick D. и др., High circulating levels of free interleukin-18 in patients with active SLE in the presence of elevated levels of interleukin-18 binding protein. J Autoimmun; 34, 2010, cc. 121-126;
Park M.C., Park Y.B. и Lee S.K., Elevated interleukin-18 levels correlated with disease activity in systemic lupus erythematosus. Clin Rheumatol; 23, 2004, cc. 225-229;
Petersen A.M.W., Penkowa M. и Iversen M., Elevated Levels of IL-18 in Plasma and Skeletal Muscle in Chronic Obstructive Pulmonary Disease. Lung, 2007, cc. 161-171;
Queen C., Schneider W.P., Selick H.E., Payne P.W., Landolfi N.F., Duncan J.F., Avdalovic N.M., Levitt M., Junghans R.P., Waldmann T.A., «A humanized antibody that binds to the interleukin 2 receptor». Proc Natl Acad Sci USA. 86 (24), декабрь 1989 г., cc. 10029-10033;
Rastrick J.M.D., Stevenson C.S., Eltom S., Grace M., Davies M. и др., Cigarette Smoke Induced Airway Inflammation Is Independent of NF-кВ Signalling. PLoS ONE; 8(1), 2013, e54128;
Ray P., Tang W., Wang P., Homer R., Kuhn С.III, Flavell R.A. и Elias J.A., Regulated overexpression of interleukin 11 in the lung: use to dissociate development-dependent and -independent phenotypes. J Clin Invest; 100, 1997, cc. 2501-2511;
Reed L.J. и Muench H., A simple method of estimating 50% endpoints. Am J Hyg; 27, 1938, cc. 493-497;
Riechmann L., Clark M., Waldmann H., Winter G., «Reshaping human antibodies for therapy». Nature 332 (6162), 1988, cc. 332-323;
Rovina N., Dima E. и Gerassimou C., Interleukin-18 in induced sputum: Association with lung function in chronic obstructive pulmonary disease. Respiratory Medicine, 2009, cc. 1056-1062;
Shapiro D.S., Transgenic and gene-targeted mice as models for chronic obstructive pulmonary disease. Eur J Respir, 2007, cc. 375-378;
Taniguchi M. и др., Characterization of anti-human interleukin-18 (IL-18)/interferon-gamma-inducing factor (IGIF) monoclonal antibodies and their application in the measurement of human IL-18 by ELISA. J Immunol Methods; 206, 1997, cc. 107-113;
Wang Z., Zheng, Zhu T.Z., Homer R.J., Riese R.J., Chapman H.A., Shapiro S.D. и Elias J.A., Interferon γ induction of pulmonary emphyseme in the adult murine lung. J Exp Med; 192, 2000, cc. 1587-1600;
Wright J.L., Cosio M. и Churg A., Animal models of chronic obstructive disease. Am J Physiol Lung Cell Mol Physiol, 2008, cc. LI-LI 5;
Wong C.K., Li E.K., Ho C.Y. и Lam C.W., Elevation of plasma interleukin-18 concentration is correlated with disease activity in systemic lupus erythematosus. Rheumatology (Oxford); 39, 2000, cc. 1078-1081;
Zhang J., Dong Z., Zhou R., Luo D., Wei H. и Tian Z., Isolation of lymphocytes and their innate immune characterizations from liver, intestine, lung and uterus. Cell Mol Immunol, 2, 2005, cc. 271-280;
Zheng Т., Zhu Z., Wang Z., Homer R.J., Ma В., Riese R., Chapman H., Shapiro S.D. и Elias J. A., Inducible targeting of IL-13 to the adult lung causes matrix metalloproteinase- and cathepsin-dependent emphyseme. J Clin Invest; 106, 2000, cc. 1081-1093;
Zheng Т. и др., Role of cathepsin S-dependent epithelial cell apoptosis in IFN-gamma-induced alveolar remodeling and pulmonary emphyseme. J Immunol; 174, 2005, cc. 8106-8115.
Дополнительные варианты осуществления изобретения
1. Ингибитор IL-18, предназначенный для применения при лечении ассоциированного с IL-18 заболевания или нарушения у индивидуума, у которого диагностированы аномальные уровни свободного IL-18 и/или аномальное соотношение свободный IL-18/IL-18BP в общей воде организма по сравнению с уровнями в общей воде организма здорового контрольного индивидуума.
2. Ингибитор IL-18, предназначенный для применения согласно варианту осуществления изобретения 1, где указанный аномальный уровень свободного IL-18 в общей воде организма превышает уровень в общей воде организма здорового контрольного индивидуума на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100%.
3. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где индивидуум, подлежащий лечению, относится к группе индивидуумов, у которых были выявлены повышенные уровни свободного IL-18 и/или аномальное соотношение свободный IL-18/IL-18BP (IL-18BP) в общей воде организма, прежде всего в сыворотке, мокроте, жидкости бронхоальвеолярного лаважа (BALF), синовиальной жидкости и/или в кровотоке, по сравнению с уровнями в общей воде организма здорового индивидуума.
4. Ингибитор IL-18, предназначенный для применения согласно варианту осуществления изобретения 2 или 3, где указанные повышенные уровни свободного IL-18 в сыворотке находятся в пределах от 5 до 10000 пг/мл, в то время как количество свободного IL-18 в сыворотке здорового индивидуума, прежде всего здорового человека, составляет ≤4 пг/мл.
5. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где указанное ассоциированное с IL-18 заболевание или нарушение представляет собой заболевание или нарушение, выбранное из группы, состоящей из хронического обструктивного заболевания легких (COPD), связанного с трансфузией повреждения легких, бронхолегочной дисплазии (BPD), острого респираторного дистресс-синдрома (ARDS), болезни Стилла взрослых, болезни Стилла детей, интерстициальной болезни легких (ILD), идиопатического легочного фиброза, муковисцидоза, легочной артериальной гипертензии, астмы, бронхоэктаза, сердечной недостаточности, амиотрофического бокового склероза (ALS), синдрома сухого глаза (DED), кератита, язвы и истирания роговицы, неоваскуляризации роговицы, патологической внутриглазной неоваскуляризации, ирита, глаукомы, дегенерации желтого пятна, синдрома Шегрена, аутоиммунного увеита, болезни Бехчета, конъюнктивита, аллергического конъюнктивита, дерматита века, диабета типа 2, болезни жирной печени неалкогольной группы (NAFLD), стеатогепатита, трансплантации солидного органа и гематологической трансплантации, повреждения, вызванного ишемией-реперфузией, семейной средиземноморской лихорадки, периодических синдромов, ассоциированных с рецептором 1 фактора некроза опухоли, криопирин-ассоциированных периодических синдромов лихорадки, гипер-IgD-синдромов, подагры, синдрома Шнитцлера, гранулематоза Вегенера, называемого также гранулематозом с полиангиитом (GPA), тиреоидита Хашимото, болезни Крона, неспецифического язвенного колита, связанных с иммуноглобулином-4 (IgG4) заболеваний и терапий на основе стволовых клеток.
6. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где указанное ассоциированное с IL-18 заболевание или нарушение индуцировано курением или воздействием пассивного курения, в частности, воздействием табачного дыма.
7. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где указанное ассоциированное с IL-18 заболевание или нарушение индуцировано вирусной инфекцией.
8. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где указанное ассоциированное с IL-18 заболевание или нарушение представляет собой индуцированное IL-18 системное проявление воспаления и ассоциированных сопутствующих заболеваний, выбранных из группы, состоящей из эмфиземы, воспаления тканей, деструкции тканей, резекции легкого, исчезновения сосудов, апоптоза эндотелиальных клеток, метаплазии слизистой оболочки, гипертрофии сердца, снижения уровня VEGF в ткани легких, утраты легочных сосудов, мускуляризации сосудов, ремоделирования сосудов, отложения коллагена, наличия патологических слоев эластина в легких, фиброзного ремоделирования дыхательных путей, увеличения воздушного пространства, хронического ремоделирования дыхательных путей и легочных сосудов и снижения легочной функции.
9. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где лечение представляет собой предупреждение, остановку, ослабление или реверсию симптомов, ассоциированных с указанным заболеванием или нарушением.
10. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где ограничивают или ингибируют связывание IL-18, прежде всего связывание свободного IL-18 с IL-18R, и, прежде всего связывание свободного IL-18 с IL-18Rα.
11. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где модифицируют, прежде всего ингибируют, IL-18-зависимые низлежащие пути передачи сигнала.
12. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где модифицируют, прежде всего ингибируют, повышенную экспрессию IFNγ, IL-13 или IL-17A по сравнению с экспрессией в организме не подвергнутых лечению индивидуумов, страдающих от указанного заболевания или нарушения.
13. Ингибитор IL-18, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где ингибитор IL-18 компенсирует дисбаланс IL-18/IL-18BP посредством улавливания и нейтрализации избытка свободного IL-18 в ткани и кровотоке.
14. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, где антитело или его фрагмент связывается с IL-18 в сайте связывания IL-18BP или вблизи сайта связывания IL-18 ВР.
15. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по варианту осуществления изобретения 14, где антитело или его фрагмент связывается со свободным белком IL-18, но не с комплексами IL-18/IL-18BP.
16. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по варианту осуществления изобретения 14 или варианту осуществления изобретения 15, где указанное антитело или его фрагмент стерически мешает или препятствует связыванию IL-18BP c IL-18.
17. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по вариантам осуществления изобретения 14-16, где указанное антитело или его фрагмент специфически связывается с одним эпитопом, комбинацией двух эпитопов или комбинацией 3 эпитопов, который(е) содержится(атся) в последовательности, выбранной из группы последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3.
18. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по варианту осуществления изобретения 17, где указанный эпитоп имеет последовательность, которая идентична на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%, 100% последовательности, выбранной из группы последовательностей, представленных в SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
19. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по варианту осуществления изобретения 18, где указанный эпитоп выбран из группы, состоящей из SEQ ID NO: 4, SEQ ID NO: 5 и SEQ ID NO: 6.
20. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент представляет собой моноклональное антитело или поликлональное антитело.
21. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент представляет собой химерное, одноцепочечное, биспецифическое антитело, антитело с трансплантированными участками обезьяньего антитела, человеческое или гуманизированное антитело.
22. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент связывается с человеческим IL-18.
23. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по одному из предыдущих вариантов осуществления изобретения, где связывание IL-18 с рецептором IL-18, прежде всего связывание с IL-18Rα, снижено по меньшей мере на 5%, прежде всего по меньшей мере на 10%, прежде всего по меньшей мере на 15%, прежде всего по меньшей мере на 20%, прежде всего по меньшей мере на 25%, прежде всего по меньшей мере на 30%, прежде всего по меньшей мере на 40%, прежде всего по меньшей мере на 45%, прежде всего по меньшей мере на 50%, прежде всего по меньшей мере на 55%, прежде всего по меньшей мере на 60%, прежде всего по меньшей мере на 65%, прежде всего по меньшей мере на 70%, прежде всего по меньшей мере на 75%, прежде всего по меньшей мере на 80%, прежде всего по меньшей мере на 85%, прежде всего по меньшей мере на 90%, прежде всего по меньшей мере на 95%, прежде всего на 100%.
24. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент нейтрализует свободный IL-18 посредством ограничения или предупреждения связывания IL-18 с рецептором IL-18 (IL-18R), прежде всего связывания свободного IL-18 с IL-18Rα.
25. IL-18-специфическое антитело, включая любое функционально эквивалентное ему антитело или его фрагменты, по одному из предыдущих вариантов осуществления изобретения, где указанное антитело или его фрагмент
а) специфически связывается с одним эпитопом, комбинацией двух эпитопов или комбинацией 3 эпитопов, который(е) содержится(атся) в последовательности, выбранной из группы последовательностей, представленных в SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3; и/или
б) специфически связывается с эпитопом, последовательность которого идентична на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или 100% последовательности, представленной в SEQ ID NO: 4, SEQ ID NO: 5 или SEQ ID NO: 6; и
в) специфически связывается с IL-18 в сайте связывания IL-18BP или вблизи сайта связывания IL-18BP; и
г) специфически связывается со свободным белком IL-18, но не с комплексами IL-18/IL-18BP; и
д) стерически препятствует связыванию IL-18BP с IL-18; и
е) снижает связывание IL-18 с рецептором IL-18, прежде всего связывание с IL-18Rα, по меньшей мере на 5%, прежде всего по меньшей мере на 10%, прежде всего по меньшей мере на 15%, прежде всего по меньшей мере на 20%, прежде всего по меньшей мере на 25%, прежде всего по меньшей мере на 30%, прежде всего по меньшей мере на 40%, прежде всего по меньшей мере на 45%, прежде всего по меньшей мере на 50%, прежде всего по меньшей мере на 55%, прежде всего по меньшей мере на 60%, прежде всего по меньшей мере на 65%, прежде всего по меньшей мере на 70%, прежде всего по меньшей мере на 75%, прежде всего по меньшей мере на 80%, прежде всего по меньшей мере на 85%, прежде всего по меньшей мере на 90%, прежде всего по меньшей мере на 95%, прежде всего на 100%.
26. Ингибитор IL-18, предназначенный для применения согласно одному из вариантов осуществления изобретения 1-13, где ингибитор представляет собой антитело, прежде всего антитело, специфическое в отношении свободного IL-18, прежде всего антагонистическое антитело, которое предупреждает связывание свободного IL-18 с рецептором IL-18, прежде всего связывание свободного IL-18 с IL-18Rα.
27. Ингибитор IL-18, предназначенный для применения согласно варианту осуществления изобретения 26, где указанное антитело представляет собой антитело по одному из вариантов осуществления изобретения 14-25.
28. Ингибитор IL-18, предназначенный для применения согласно одному из вариантов осуществления изобретения 1-13, где указанные аномальные уровни свободного IL-18 в общей воде организма определены с использованием антитела по одному из вариантов осуществления изобретения 14-25.
29. Ингибитор IL-18, предназначенный для применения согласно одному из вариантов осуществления изобретения 1-13, где ингибитор представляет собой IL-18BP, прежде всего человеческий IL-18BP (hIL-18BP), прежде всего IL-18BP, включая любой его функциональный эквивалент или его фрагменты, прежде всего IL-18BP, представленный в SEQ ID NO: 7.
30. Ингибитор IL-18, предназначенный для применения согласно вариантам осуществления изобретения 26-29, который представляет собой полноразмерный белок или мутеин, функциональное производное, функциональный фрагмент, биологически активный пептид, фракцию, полученное в результате циклической перестановки производное, слитый белок, его изоформу или соль.
31. IL-18BP, предназначенный для применения при лечении хронического обструктивного заболевания легких (COPD), болезни сердца, синдрома сухого глаза и/или диабета типа II.
32. IL-18BP, предназначенный для применения согласно варианту осуществления изобретения 31 при лечении хронического обструктивного заболевания легких (COPD).
33. IL-18BP, предназначенный для применения согласно варианту осуществления изобретения 31 при лечении болезни сердца.
34. IL-18BP, предназначенный для применения согласно варианту осуществления изобретения 31 при лечении синдрома сухого глаза.
35. IL-18BP, предназначенный для применения согласно варианту осуществления изобретения 31 при лечении диабета типа II.
36. IL-18BP, предназначенный для применения согласно вариантам осуществления изобретения 31-35, где указанное заболевание или нарушение индуцировано курением или воздействием пассивного курения, в частности воздействием табачного дыма.
37. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где указанное заболевание или нарушение индуцировано вирусной инфекцией.
38. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, где указанное заболевание или нарушение представляет собой индуцированное IL-18 системное проявление воспаления и ассоциированных сопутствующих заболеваний, выбранных из группы, состоящей из эмфиземы, воспаления тканей, деструкции тканей, резекции легкого, исчезновения сосудов, метаплазии слизистой оболочки, гипертрофии сердца, снижения уровня VEGF в ткани легких, утраты легочных сосудов, мускуляризации сосудов, отложения коллагена, наличия патологических слоев эластина в легких, фиброзного ремоделирования дыхательных путей, увеличения воздушного пространства, хронического ремоделирования дыхательных путей и легочных сосудов и снижения легочной функции.
39. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, в котором ограничивают или ингибируют связывание IL-18, прежде всего связывание свободного IL-18 с IL-18R, и прежде всего связывание свободного IL-18 с IL-18Rα.
40. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, в котором модифицируют, прежде всего ингибируют IL-18-зависимые низлежащие пути передачи сигнала.
41. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, в котором модифицируют, прежде всего ингибируют, повышенную экспрессию IFNγ, IL-13 или IL-17A по сравнению с экспрессией в организме не подвергнутых лечению индивидуумов, страдающих указанным заболеванием или нарушением.
42. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, в котором ингибитор IL-18 компенсирует дисбаланс IL-18/IL-18BP посредством улавливания избытка свободного IL-18 в ткани или кровотоке.
43. IL-18BP, предназначенный для применения согласно одному из предыдущих вариантов осуществления изобретения, в котором лечение представляет собой предупреждение, остановку, ослабление или реверсию симптомов, ассоциированных с указанным заболеванием или нарушением.
44. Фармацевтическая композиция, предназначенная для лечения заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13, у индивидуума, страдающего от такого заболевания или нарушения, или который предрасположен к развитию такого заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13, где указанная композиция содержит ингибитор IL-18 по одному из вариантов осуществления изобретения 1-13 и 26-30, прежде всего в профилактически и/или терапевтически эффективном количестве.
45. Фармацевтическая композиция по варианту осуществления изобретения 44, где указанная композиция необязательно содержит также другой ингибитор провоспалительного цитокина или его функциональный фрагмент, или регуляторный фактор, который индуцирует in-situ экспрессию указанного ингибитора провоспалительного цитокина, или его функциональный фрагмент, терапевтические средства для совместного применения, такие как противовоспалительные, бронходилататорные, антигистаминные, противозастойные или противокашлевые лекарственные субстанции.
46. Фармацевтическая композиция по варианту осуществления изобретения 44 или 45, содержащая фармацевтически приемлемый носитель и/или эксципиент.
47. Фармацевтическая композиция, предназначенная для лечения заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 31-43, у индивидуума, страдающего от такого заболевания или нарушения, или который предрасположен к развитию такого заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 31-43, где указанная композиция содержит IL-18BP по одному из вариантов осуществления изобретения 31-43, прежде всего в профилактически и/или терапевтически эффективном количестве.
48. Фармацевтическая композиция по варианту осуществления изобретения 47, где указанная композиция необязательно содержит также другой ингибитор провоспалительного цитокина или его функциональный фрагмент, или регуляторный фактор, который индуцирует in-situ экспрессию указанного ингибитора провоспалительного цитокина, или его функциональный фрагмент, терапевтические средства для совместного применения, такие как противовоспалительные, бронходилататорные, антигистаминные, противозастойные или противокашлевые лекарственные субстанции.
49. Фармацевтическая композиция по варианту осуществления изобретения 47 или 48, содержащая фармацевтически приемлемый носитель и/или эксципиент.
50. Экспрессионный вектор, содержащий кодирующую последовательность ингибитора IL-18 по одному из вариантов осуществления изобретения 1-13 и 26-30, который после введения индивидууму, страдающему от заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в предыдущих вариантах осуществления изобретения, приводит к экспрессии in situ ингибитора IL-18, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13.
51. Экспрессионный вектор, содержащий антисмысловой экспрессионный вектор IL-18, который после введения индивидууму, страдающему от заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в вариантах осуществления изобретения 1-13, приводит к ингибированию in situ экспрессии IL-18, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13.
52. Экспрессионный вектор по варианту осуществления изобретения 50 или 51, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13 и 26-43, где указанный экспрессионный вектор вводят индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, индивидуально или в сочетании с ингибитором IL-18 по одному из вариантов осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43 или фармацевтической композицией по одному из вариантов осуществления изобретения 44-49.
53. Экспрессионный вектор, содержащий кодирующую последовательность IL-18BP по одному из вариантов осуществления изобретения 31-43, который после введения индивидууму, страдающему от заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, указанного в предыдущих вариантах осуществления изобретения, приводит к экспрессии in situ IL-18BP, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 31-43.
54. Экспрессионный вектор по варианту осуществления изобретения 53, предназначенный для применения при лечении заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13 и 26-43, где указанный экспрессионный вектор вводят индивидууму, страдающему от такого заболевания или нарушения, или предрасположенному к развитию такого заболевания или нарушения, индивидуально или в сочетании с ингибитором IL-18 по одному из вариантов осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43 или фармацевтической композицией по одному из вариантов осуществления изобретения 44-49.
55. Ингибитор IL-18, предназначенный для применения согласно одному из вариантов осуществления изобретения 1-13 и 26-30, IL-18BP, предназначенный для применения согласно одному из вариантов осуществления изобретения 31-43, фармацевтическая композиция, предназначенная для применения согласно одному из вариантов осуществления изобретения 44-49, или экспрессионный вектор, предназначенный для применения согласно одному из вариантов осуществления изобретения 50-54, в котором вводят индивидууму, нуждающемуся в этом, в профилактически и/или терапевтически эффективном количестве указанный ингибитор IL-18, указанный IL-18BP, указанную фармацевтическая композиция, или указанный экспрессионный вектор, прежде всего путем системного, интраназального, трансбуккального, орального введения, введения через слизистую оболочку, внутритрахеального, внутривенного, подкожного введения, введения в мочевой тракт, интравагинального, подъязычного, внутрибронхиального, внутрилегочного, чрескожного или внутримышечного введения, прежде всего, путем бронхолегочного введения.
56. Ингибитор IL-18, IL-18BP, фармацевтическая композиция или экспрессионный вектор, предназначенный/предназначенная для применения согласно варианту осуществления изобретения 55, где указанный индивидуум представляет собой млекопитающее, прежде всего указанный индивидуум представляет собой человека.
57. Способ лечения заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13 и 26-43, у индивидуума, страдающего от такого заболевания или нарушения, или предрасположенного к развитию такого заболевания или нарушения, заключающийся в том, что вводят указанному индивидууму в терапевтически или профилактически эффективном количестве ингибитор IL-18 по одному из вариантов осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43 или фармацевтическую композицию по одному из вариантов осуществления изобретения 44-49 и/или экспрессионный вектор по одному из вариантов осуществления изобретения 50-54, прежде всего путем системного, интраназального, трансбуккального, орального введения, введения через слизистую оболочку, внутритрахеального, внутривенного, подкожного введения, введения в мочевой тракт, интравагинального, подъязычного, внутрибронхиального, внутрилегочного, чрескожного или внутримышечного введения, прежде всего, путем бронхолегочного введения.
58. Способ диагностирования заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13 и 26-43, диагностирования предрасположенности к заболеванию или нарушению, указанному в одном из вариантов осуществления изобретения 1-13 и 26-43, мониторинга минимальной остаточной болезни у индивидуума или прогнозирования чувствительности индивидуума к лечению с помощью ингибитора IL-18 по вариантам осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43 или фармацевтической композиции, содержащей ингибитор IL-18 по вариантам осуществления изобретения 44-49, заключающийся в том, что осуществляют стадии, на которых:
а) получают образец общей воды организма, прежде всего сыворотки, индивидуума;
б) анализируют указанный образец в отношении присутствия свободного IL-18 с использованием антитела к IL-18 по одному из вариантов осуществления изобретения 14-25 или IL-18BP по одному из вариантов осуществления изобретения ... в качестве захватывающей молекулы и/или анализируют указанный образец в отношении присутствия свободного IL-18BP с использованием первого моноклонального IL-18ВР-специфического захватывающего антитела и IL-18ВР-специфического идентифицирующего антитела, которое связывается с сайтом IL-18BP, отличным от сайта, с которым связывается захватывающее антитело, прежде всего одно из антител, которые связываются с сайтом IL-18BP, с которым связывается IL-18;
в) определяют количество свободного IL-18 и/или свободного IL-18BP, связанного с захватывающей молекулой в образце;
г) сравнивают количество свободного IL-18 и/или свободного IL-18BP в образце, взятом из организма индивидуума, страдающего указанным заболеванием, с количеством в образце, взятом из организма здорового индивидуума.
59. Способ диагностирования заболевания или нарушения, указанного в одном из вариантов осуществления изобретения 1-13 и 26-43, диагностирования предрасположенности к заболеванию или нарушению, указанному в одном из вариантов осуществления изобретения 1-13 и 26-43, мониторинга минимальной остаточной болезни у индивидуума или прогнозирования чувствительности индивидуума к лечению с помощью ингибитора IL-18 по вариантам осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43 или фармацевтической композиции, которая содержит ингибитор IL-18 по вариантам осуществления изобретения 44-49 и фармацевтически приемлемый носитель и/или эксципиент по одному из предыдущих вариантов осуществления изобретения, заключающийся в том, что осуществляют стадии, на которых:
а) получают образец общей воды организма, прежде всего мокроты и сыворотки, индивидуума;
б) анализируют указанный образец в отношении присутствия свободного IL-18 с использованием антитела к IL-18 по одному из вариантов осуществления изобретения 14-25 или IL-18BP в качестве захватывающей молекулы, и/или анализируют указанный образец в отношении присутствия свободного IL-18ВР с использованием первого моноклонального IL-18ВР-специфического захватывающего антитела и IL-18ВР-специфического идентифицирующего антитела, которое связывается с сайтом IL-18BP, отличным от сайта, с которым связывается захватывающее антитело, прежде всего одно из указанных IL-18BP-специфических антител, связывающихся с сайтом IL-18BP, с которым связывается IL-18;
в) анализируют указанный образец в отношении присутствия общего IL-18 и/или общего IL-18BP с использованием первого моноклонального IL-18BP-специфического антитела, которое не связывается с сайтом IL-18BP, с которым связывается IL-18, и второго IL-18-специфического антитела, которое не связывается с сайтом IL-18, с которым связывается IL-18BP;
г) определяют количество свободного и общего IL-18 и/или свободного и общего IL-18BP, связанного с захватывающей молекулой в образце;
д) сравнивают количество свободного и/или общего IL-18, и/или свободного и/или общего IL-18BP в образце, взятом из организма индивидуума, страдающего от такого заболевания, с количеством в образце, взятом из организма здорового индивидуума.
60. Способ диагностирования по одному из предыдущих вариантов осуществления изобретения, в котором количество свободного IL-18 в сыворотке, выделенной из организма индивидуума, прежде всего человека, страдающего от указанного заболевания, находится в пределах от 5 до 10000 пг/мл, в то время как количество свободного IL-18 в сыворотке здорового индивидуума, прежде всего здорового человека, составляет ≤4 пг/мл.
61. Набор биомаркеров, предназначенный для применения при диагностировании заболеваний или нарушения по одному из вариантов осуществления изобретения 1-13 и 26-43, для применения при диагностировании предрасположенности к заболеванию или нарушению по одному из вариантов осуществления изобретения 1-13 и 26-43 или для применения при мониторинге минимальной остаточной болезни у индивидуума, или для прогнозирования чувствительности индивидуума к лечению с использованием ингибитора IL-18 по вариантам осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43, или фармацевтической композиции, содержащей ингибитор IL-18 по вариантам осуществления изобретения 44-49.
62. Способ диагностирования заболеваний или нарушения по одному из вариантов осуществления изобретения 1-13 и 26-43, диагностирования предрасположенности к заболеванию или нарушению по одному из вариантов осуществления изобретения 1-13 и 26-43, или мониторинга минимальной остаточной болезни у индивидуума, или прогнозирования чувствительности индивидуума к лечению с использованием ингибитора IL-18 по вариантам осуществления изобретения 1-13 и 26-30, IL-18BP по вариантам осуществления изобретения 31-43, или фармацевтической композиции, содержащей ингибитор IL-18 по вариантам осуществления изобретения 44-49, заключающийся в том, что осуществляют стадии, на которых:
д) получают профиль биомаркеров для индивидуума, подлежащего обследованию, для чего берут образец общей воды организма у указанного индивидуума;
е) получают профиль биомаркеров для референс-популяции здоровых индивидуумов;
ж) получают профиль биомаркеров для популяции индивидуумов, страдающих от указанного заболевания или нарушения, и
з) сравнивают профиль биомаркеров, полученный на стадии а), с профилями, полученными на стадии б) и стадии в).
63. Фармацевтический набор, содержащий ингибитор IL-18 по одному из вариантов осуществления изобретения 1-13 и 26-30, IL-18BP по одному из вариантов осуществления изобретения 31-43 или фармацевтическую композицию, которая содержит ингибитор IL-18 по вариантам осуществления изобретения 44-49 и фармацевтически приемлемый носитель и/или эксципиент, предлагаемый в изобретении, в виде отдельных форм, содержащих стандартную дозу лекарственного средства, где указанные формы пригодны для введения в эффективных количествах.
64. Диагностический набор для обнаружения свободного IL-18, содержащий IL-18-специфическое антитело по одному из вариантов осуществления изобретения 14-25 в качестве захватывающего антитела или IL-18 ВР в качестве альтернативной захватывающей молекулы, и второе IL-18-специфическое идентифицирующее антитело, или IL-18-специфическое антитело по одному из вариантов осуществления изобретения 14-25 в качестве идентифицирующего антитела и второе IL-18-специфическое захватывающее антитело, где идентифицирующее антитело связывается с сайтами IL-18, отличными от сайтов, с которыми связывается захватывающая молекула.
65. Диагностический набор для обнаружения общего IL-18 или общего IL-18 ВР, содержащий первое моноклональное IL-18ВР-специфическое антитело, которое не связывается с сайтом IL-18BP, с которым связывается IL-18, и второе IL-18-специфическое антитело, которое не связывается с сайтом IL-18, с которым связывается IL-18BP.
66. Диагностический набор для обнаружения свободного IL-18BP, содержащий первое моноклональное IL-18ВР-специфическое захватывающее антитело, и IL-18ВР-специфическое идентифицирующее антитело, которое связывается с сайтом IL-18BP, отличным от сайта, с которым связывается захватывающее антитело.
67. Диагностический набор, который содержит все диагностические наборы по вариантам осуществления 64-66.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> AB2 БИО СА
<120> Применение IL-18-связывающего белка (IL-18BP)
при воспалительных заболеваниях
<130> W1568 PCT BS
<150> EP13 18 3193.5
<151> 2013-09-05
<160> 152
<170> BiSSAP 1.3
<210> 1
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> Эпитоп
<400> 1
Tyr Phe Gly Lys Leu Glu Ser Lys Leu Ser Val Ile Arg Asn
1 5 10
<210> 2
<211> 22
<212> PRT
<213> Искусственная последовательность
<220>
<223> Эпитоп
<400> 2
Phe Ile Ile Ser Met Tyr Lys Asp Ser Gln Pro Arg Gly Met Ala Val
1 5 10 15
Thr Thr Ile Ser Val Lys
20
<210> 3
<211> 17
<212> PRT
<213> Искусственная последовательность
<220>
<223> Эпитоп
<400> 3
Glu Met Asn Pro Pro Asp Asn Ile Lys Asp Thr Lys Ser Asp Ile Ile
1 5 10 15
Phe
<210> 4
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> Эпитоп
<400> 4
Tyr Phe Gly Lys Leu Glu Ser
1 5
<210> 5
<211> 10
<212> PRT
<213> Искусственная последовательность
<220>
<223> Эпитоп
<400> 5
Tyr Lys Asp Ser Gln Pro Arg Gly Met Ala
1 5 10
<210> 6
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> Эпитоп
<400> 6
Asp Asn Ile Lys Asp Thr Lys
1 5
<210> 7
<211> 164
<212> PRT
<213> Искусственная последовательность
<220>
<223> IL-18-связывающий белок
<400> 7
Thr Pro Val Ser Gln Thr Thr Thr Ala Ala Thr Ala Ser Val Arg Ser
1 5 10 15
Thr Lys Asp Pro Cys Pro Ser Gln Pro Pro Val Phe Pro Ala Ala Lys
20 25 30
Gln Cys Pro Ala Leu Glu Val Thr Trp Pro Glu Val Glu Val Pro Leu
35 40 45
Asn Gly Thr Leu Ser Leu Ser Cys Val Ala Cys Ser Arg Phe Pro Asn
50 55 60
Phe Ser Ile Leu Tyr Trp Leu Gly Asn Gly Ser Phe Ile Glu His Leu
65 70 75 80
Pro Gly Arg Leu Trp Glu Gly Ser Thr Ser Arg Glu Arg Gly Ser Thr
85 90 95
Gly Thr Gln Leu Cys Lys Ala Leu Val Leu Glu Gln Leu Thr Pro Ala
100 105 110
Leu His Ser Thr Asn Phe Ser Cys Val Leu Val Asp Pro Glu Gln Val
115 120 125
Val Gln Arg His Val Val Leu Ala Gln Leu Trp Ala Gly Leu Arg Ala
130 135 140
Thr Leu Pro Pro Thr Gln Glu Ala Leu Pro Ser Ser His Ser Ser Pro
145 150 155 160
Gln Gln Gln Gly
<210> 8
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> Линкерная последовательность
<400> 8
Glu Phe Gly Ala Gly Leu Val Leu Gly Gly Gln Phe Met
1 5 10
<210> 9
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 107C6
<400> 9
Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Leu Ser Cys Arg Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Tyr Ser Gly Val Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Gln Phe Ala Phe Ser Leu Glu Thr Ser Ala Ala Thr Ala Phe
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asp Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 10
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 107C6
<400> 10
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Val Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gly Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Asn Leu Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 11
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 108F8
<400> 11
Gln Ile Gln Leu Val Gln Ser Gly Pro Asp Ser Lys Lys Pro Gly Glu
1 5 10 15
Thr Val Lys Leu Ser Cys Arg Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Lys Trp Met
35 40 45
Gly Trp Ile Asn Thr Tyr Ser Gly Val Pro Thr Tyr Ala Asp Asp Phe
50 55 60
Lys Gly Gln Phe Ala Phe Ser Leu Glu Thr Ser Ala Ala Thr Ala Phe
65 70 75 80
Leu Gln Ile Asn Asn Leu Lys Asp Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 12
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 108F8
<400> 12
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asp Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Val Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Gly Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Asn Leu Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 13
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность антитела VH 109A6
<400> 13
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Lys Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Ile Gln Arg Pro Ala Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Gly Ser Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Ile His Leu Ser Ser Leu Thr Ser Gly Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Tyr Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 14
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность антитела VK 109A6
<400> 14
Asp Val Val Met Thr Gln Val Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Phe Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Thr Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr Leu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 15
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 111A6
<400> 15
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Lys Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Val Ile Gln Arg Pro Ala Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Gly Ser Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Ile His Leu Ser Ser Leu Thr Ser Gly Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Gly Tyr Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 16
<211> 108
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 VK антитела 111A6
<400> 16
Glu Asn Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Arg Ser Ser Val Ser Ser Ser
20 25 30
Tyr Leu His Trp Tyr Gln Gln Lys Ser Gly Ala Ser Pro Lys Leu Trp
35 40 45
Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly Val Pro Thr Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Val Glu
65 70 75 80
Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Tyr Ser Gly Tyr Pro
85 90 95
Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 17
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 VK антитела 111A6
<400> 17
Asp Val Val Met Thr Gln Val Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Phe Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Thr Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr Leu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 18
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 131B4
<400> 18
Glu Val Gln Val Gln Gln Ser Gly Ala Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Lys Ile Lys Asp Thr
20 25 30
Tyr Ile His Trp Leu Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Gly Ser Lys Phe
50 55 60
Gln Gly Lys Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Ile Gln Leu Ser Ser Leu Thr Ser Gly Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Gly Tyr Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 19
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 131B4
<400> 19
Asp Ala Val Leu Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Thr Ser Ser Gln Ser Leu Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asp Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Met Ile
65 70 75 80
Thr Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Ser Leu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Val Lys
100 105 110
<210> 20
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 VH антитела 131E8
<400> 20
Gln Val Gln Leu Lys Gln Ser Arg Pro Gly Pro Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Pro Asn Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ser Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Asn Phe Tyr Ser Lys Tyr Asp Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 21
<211> 113
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 VH антитела 131E8
<400> 21
Gln Val Gln Leu Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met His Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Asn Ile Asn Pro Asn Ser Gly Ser Thr Asn Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Leu Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
100 105 110
Ser
<210> 22
<211> 106
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 131E8
<400> 22
Glu Asn Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Ser Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Ser Thr Ser Pro Lys Leu Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Gly Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu Ala Glu
65 70 75 80
Asp Val Ala Thr Tyr Tyr Cys Phe Gln Gly Ser Gly Tyr Pro Leu Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 23
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 132H4
<400> 23
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Asn Pro Ala Lys Arg Leu Glu Trp Val
35 40 45
Ala Thr Ile Ser Ser Gly Gly Ala Asn Ile Tyr Tyr Pro Asp Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Tyr Phe Asn His Phe Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 24
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 132H4
<400> 24
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Phe Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Asn Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 25
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 133A6
<400> 25
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Thr Pro Ala Lys Arg Leu Glu Trp Val
35 40 45
Thr Thr Ile Ser Ser Gly Gly Gly Asn Ile Tyr Tyr Thr Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Tyr Ser Asn Tyr Phe Trp Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Ser Val Ser Glu
115 120
<210> 26
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 133A6
<400> 26
Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 27
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 107C6
<400> 27
Gly Tyr Thr Phe Thr Asn Tyr Gly
1 5
<210> 28
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 107C6
<400> 28
Ile Asn Thr Tyr Ser Gly Val Pro
1 5
<210> 29
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 107C6
<400> 29
Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr
1 5 10
<210> 30
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 107C6
<400> 30
Gln Ser Leu Leu Asp Ser Arg Thr Arg Lys Asn Tyr
1 5 10
<210> 31
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 107C6
<400> 31
Trp Ala Ser
1
<210> 32
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 107C6
<400> 32
Lys Gln Ser Tyr Asn Leu Arg Thr
1 5
<210> 33
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 108F8
<400> 33
Gly Tyr Thr Phe Thr Asn Tyr Gly
1 5
<210> 34
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 108F8
<400> 34
Ile Asn Thr Tyr Ser Gly Val Pro
1 5
<210> 35
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 108F8
<400> 35
Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr
1 5 10
<210> 36
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 108F8
<400> 36
Gln Ser Leu Leu Asp Ser Arg Thr Arg Lys Asn Tyr
1 5 10
<210> 37
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 108F8
<400> 37
Trp Ala Ser
1
<210> 38
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 108F8
<400> 38
Lys Gln Ser Tyr Asn Leu Arg Thr
1 5
<210> 39
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 109A6
<400> 39
Gly Phe Lys Ile Lys Asp Thr Tyr
1 5
<210> 40
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 109A6
<400> 40
Ile Asp Pro Ala Asn Gly Asn Thr
1 5
<210> 41
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 109A6
<400> 41
Ala Gly Tyr Val Trp Phe Ala Tyr
1 5
<210> 42
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 109A6
<400> 42
Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 43
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 109A6
<400> 43
Thr Val Ser
1
<210> 44
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VK антитела 109A6
<400> 44
Ser Gln Ser Thr Leu Val Pro Trp Thr
1 5
<210> 45
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 111A6
<400> 45
Gly Phe Lys Ile Lys Asp Thr Tyr
1 5
<210> 46
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 111A6
<400> 46
Ile Asp Pro Ala Asn Gly Asn Thr
1 5
<210> 47
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 111A6
<400> 47
Ala Gly Tyr Val Trp Phe Ala Tyr
1 5
<210> 48
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 CDR1 VK антитела 111A6
<400> 48
Ser Ser Val Ser Ser Ser Tyr
1 5
<210> 49
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 CDR2 VK антитела 111A6
<400> 49
Ser Thr Ser
1
<210> 50
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 CDR3 VK антитела 111A6
<400> 50
Gln Gln Tyr Ser Gly Tyr Pro Leu Thr
1 5
<210> 51
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 CDR1 VK антитела 111A6
<400> 51
Gln Arg Leu Val His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 52
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 CDR2 VK антитела 111A6
<400> 52
Thr Val Ser
1
<210> 53
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 CDR3 VK антитела 111A6
<400> 53
Ser Gln Ser Thr Leu Val Pro Trp Thr
1 5
<210> 54
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 131B4
<400> 54
Gly Phe Lys Ile Lys Asp Thr Tyr
1 5
<210> 55
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 131B4
<400> 55
Ile Asp Pro Ala Asn Gly Asn Thr
1 5
<210> 56
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 131B4
<400> 56
Ala Gly Tyr Val Trp Phe Ala Tyr
1 5
<210> 57
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 131B4
<400> 57
Gln Ser Leu Val His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 58
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 131B4
<400> 58
Lys Val Ser
1
<210> 59
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VK антитела 131B4
<400> 59
Ser Gln Ser Ser Leu Val Pro Trp Thr
1 5
<210> 60
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 CDR1 VH антитела 131E8
<400> 60
Gly Phe Ser Leu Pro Asn Tyr Gly
1 5
<210> 61
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 CDR2 VH антитела 131E8
<400> 61
Ile Trp Ser Gly Gly Ser Thr
1 5
<210> 62
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 CDR3 VH антитела 131E8
<400> 62
Ala Arg Asn Phe Tyr Ser Lys Tyr Asp Tyr Ala Met Asp Tyr
1 5 10
<210> 63
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 CDR1 VH антитела 131E8
<400> 63
Gly Tyr Thr Phe Thr Ser Tyr Trp
1 5
<210> 64
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 CDR2 VH антитела 131E8
<400> 64
Ile Asn Pro Asn Ser Gly Ser Thr
1 5
<210> 65
<211> 6
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 CDR3 VH антитела 131E8
<400> 65
Ala Arg Leu Gly Asp Tyr
1 5
<210> 66
<211> 5
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 131E8
<400> 66
Ser Ser Val Ser Tyr
1 5
<210> 67
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 131E8
<400> 67
Asp Thr Ser
1
<210> 68
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VK антитела 131E8
<400> 68
Phe Gln Gly Ser Gly Tyr Pro Leu Thr
1 5
<210> 69
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 132H4
<400> 69
Gly Phe Thr Phe Ser Asn Tyr Ala
1 5
<210> 70
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 132H4
<400> 70
Ile Ser Ser Gly Gly Ala Asn Ile
1 5
<210> 71
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 132H4
<400> 71
Ala Arg Gly Asp Tyr Phe Asn His Phe Trp Phe Ala Tyr
1 5 10
<210> 72
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 132H4
<400> 72
Gln Ser Ile Val His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 73
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 132H4
<400> 73
Lys Val Ser
1
<210> 74
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VK антитела 132H4
<400> 74
Phe Gln Gly Ser His Val Pro Trp Thr
1 5
<210> 75
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VH антитела 133A6
<400> 75
Gly Phe Thr Phe Ser Asn Tyr Ala
1 5
<210> 76
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VH антитела 133A6
<400> 76
Ile Ser Ser Gly Gly Gly Asn Ile
1 5
<210> 77
<211> 13
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VH антитела 133A6
<400> 77
Ala Arg Gly Asp Tyr Ser Asn Tyr Phe Trp Phe Ala Tyr
1 5 10
<210> 78
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR1 VK антитела 133A6
<400> 78
Gln Ser Ile Val His Ser Asn Gly Asn Thr Tyr
1 5 10
<210> 79
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR2 VK антитела 133A6
<400> 79
Lys Val Ser
1
<210> 80
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность CDR3 VK антитела 133A6
<400> 80
Phe Gln Gly Ser His Val Pro Trp Thr
1 5
<210> 81
<211> 453
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VH антитела 107C6
<400> 81
atgggttggg tgtggacctt gccattcctg atggcagctg cccaaagtat ccaagcacag 60
atccagttgg tgcagtctgg tcctgaactg aagaagcctg gagagacagt caagctctcc 120
tgcagggctt ctggatatac attcacaaac tatggaatga actgggtgaa gcaggctcca 180
ggaaagggtt taaagtggat gggctggata aacacctact ctggagtgcc aacatatgct 240
gatgacttca agggacagtt tgccttctct ttggaaacct ctgccgccac tgcctttttg 300
cagatcaaca acctcaaaga tgaggacacg gctacatatt tttgtgcaag agagggatat 360
agtactacca ggtctatgga ctactggggt caaggaacct cagtcaccgt ctcctcagcc 420
aaaacgacac ccccatctgt ctatccactg gcc 453
<210> 82
<211> 151
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 107C6
<400> 82
Met Gly Trp Val Trp Thr Leu Pro Phe Leu Met Ala Ala Ala Gln Ser
1 5 10 15
Ile Gln Ala Gln Ile Gln Leu Val Gln Ser Gly Pro Glu Leu Lys Lys
20 25 30
Pro Gly Glu Thr Val Lys Leu Ser Cys Arg Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Asn Tyr Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu
50 55 60
Lys Trp Met Gly Trp Ile Asn Thr Tyr Ser Gly Val Pro Thr Tyr Ala
65 70 75 80
Asp Asp Phe Lys Gly Gln Phe Ala Phe Ser Leu Glu Thr Ser Ala Ala
85 90 95
Thr Ala Phe Leu Gln Ile Asn Asn Leu Lys Asp Glu Asp Thr Ala Thr
100 105 110
Tyr Phe Cys Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Pro
130 135 140
Pro Ser Val Tyr Pro Leu Ala
145 150
<210> 83
<211> 501
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 107C6
<400> 83
atggagtcac agtctcaggt tcttatattg ctgctgctat gggtatctgg tacctgtggg 60
gacattgtga tgtcacagtc tccatcctcc ctggctgtgt cagcaggaga gaaggtcact 120
atgagctgca aatccagtca gagtctgctc gacagtagaa cccgaaagaa ctacttggtt 180
tggtaccagc agaaaccagg gcagtctcct aaactgctga tctactgggc atccactagg 240
ggatctgggg tccctgatcg cttcacaggc agtggatctg ggacagattt cactctcacc 300
atcagcagtg tgcaggctga agacctggca gtttattact gcaaacaatc ttataatctt 360
cggacgttcg gtggaggcac caagctggaa atcaaacggg ctgatgctgc accaactgta 420
tccatcttcc caccatccag tgagcagtta acatctggag gtgcctcagt cgtgtgcttc 480
ttgaacaact tctaccccaa a 501
<210> 84
<211> 167
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 107C6
<400> 84
Met Glu Ser Gln Ser Gln Val Leu Ile Leu Leu Leu Leu Trp Val Ser
1 5 10 15
Gly Thr Cys Gly Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala
20 25 30
Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser
35 40 45
Leu Leu Asp Ser Arg Thr Arg Lys Asn Tyr Leu Val Trp Tyr Gln Gln
50 55 60
Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg
65 70 75 80
Gly Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp
85 90 95
Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr
100 105 110
Tyr Cys Lys Gln Ser Tyr Asn Leu Arg Thr Phe Gly Gly Gly Thr Lys
115 120 125
Leu Glu Ile Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro
130 135 140
Pro Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe
145 150 155 160
Leu Asn Asn Phe Tyr Pro Lys
165
<210> 85
<211> 456
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 108F8
<400> 85
atgggttggg tgtggacctt gctattcctg atggcagctg cccaaagtat ccaatcacag 60
atccagttgg tgcagtctgg tcctgattcg aagaagcctg gagagacagt caagctctcc 120
tgcagggctt ctggatatac attcacaaac tatggaatga actgggtgaa gcaggctcca 180
ggaaagggtt taaagtggat gggctggata aacacctact ctggagtgcc aacatatgct 240
gatgacttca agggacagtt tgccttctct ttggaaacct ctgccgccac tgcctttttg 300
cagatcaaca acctcaaaga tgaggacacg gctacatatt tttgtgcaag agagggatat 360
agtactacca ggtctatgga ctactggggt caaggaacct cagtcaccgt ctcctcagcc 420
aaaacgacac ccccatctgt cttccccctg gcacct 456
<210> 86
<211> 152
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 108F8
<400> 86
Met Gly Trp Val Trp Thr Leu Leu Phe Leu Met Ala Ala Ala Gln Ser
1 5 10 15
Ile Gln Ser Gln Ile Gln Leu Val Gln Ser Gly Pro Asp Ser Lys Lys
20 25 30
Pro Gly Glu Thr Val Lys Leu Ser Cys Arg Ala Ser Gly Tyr Thr Phe
35 40 45
Thr Asn Tyr Gly Met Asn Trp Val Lys Gln Ala Pro Gly Lys Gly Leu
50 55 60
Lys Trp Met Gly Trp Ile Asn Thr Tyr Ser Gly Val Pro Thr Tyr Ala
65 70 75 80
Asp Asp Phe Lys Gly Gln Phe Ala Phe Ser Leu Glu Thr Ser Ala Ala
85 90 95
Thr Ala Phe Leu Gln Ile Asn Asn Leu Lys Asp Glu Asp Thr Ala Thr
100 105 110
Tyr Phe Cys Ala Arg Glu Gly Tyr Ser Thr Thr Arg Ser Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Pro
130 135 140
Pro Ser Val Phe Pro Leu Ala Pro
145 150
<210> 87
<211> 510
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 108F8
<400> 87
atgggcttca agatgaagtc agtcgacctg gttcttatat tgctgctgct atgggtatct 60
ggtacctgtg gggacattgt gatgtcacag tctccatcct ccctggctgt gtcagcagga 120
gagaaggtca ctatgagctg caaatccagt cagagtctgc tcgacagtag aacccgaaag 180
aactacttgg tttggtacca gcagaaacca gggcagtctc ctaaactgct gatctactgg 240
gcatccacta ggggatctgg ggtccctgat cgcttcacag gcagtggatc tgggacagat 300
ttcactctca ccatcagcag tgtgcaggct gaagacctgg cagtttatta ctgcaaacaa 360
tcttataatc ttcggacgtt cggtggaggc accaagctgg aaatcaaacg ggctgatgct 420
gcaccaactg tatccatctt cccaccatcc agtgagcagt taacatctgg aggtgcctca 480
gtcgtgtgct tcttgaacaa cttctacccc 510
<210> 88
<211> 170
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 108F8
<400> 88
Met Gly Phe Lys Met Lys Ser Val Asp Leu Val Leu Ile Leu Leu Leu
1 5 10 15
Leu Trp Val Ser Gly Thr Cys Gly Asp Ile Val Met Ser Gln Ser Pro
20 25 30
Ser Ser Leu Ala Val Ser Ala Gly Glu Lys Val Thr Met Ser Cys Lys
35 40 45
Ser Ser Gln Ser Leu Leu Asp Ser Arg Thr Arg Lys Asn Tyr Leu Val
50 55 60
Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile Tyr Trp
65 70 75 80
Ala Ser Thr Arg Gly Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly
85 90 95
Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Val Gln Ala Glu Asp
100 105 110
Leu Ala Val Tyr Tyr Cys Lys Gln Ser Tyr Asn Leu Arg Thr Phe Gly
115 120 125
Gly Gly Thr Lys Leu Glu Ile Lys Arg Ala Asp Ala Ala Pro Thr Val
130 135 140
Ser Ile Phe Pro Pro Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser
145 150 155 160
Val Val Cys Phe Leu Asn Asn Phe Tyr Pro
165 170
<210> 89
<211> 441
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VH антитела 109A6
<400> 89
atgaaatgca gctggattat gttcttcctg atggcagtgg ttacaggggt caattcagag 60
gttcagctgc agcagtctgg ggcagaactt gtgaagccag gggcctcagt caagttgtcc 120
tgcacagctt ctggcttcaa aattaaagac acctatatac actgggtgat ccagaggcct 180
gcacagggcc tggaatggat tggaaggatt gatcctgcga atggtaatac tatttatggc 240
tcaaagttcc agggcaaggc cactctaaca gcggacacat catccaacac agcctacatt 300
cacctcagca gcctgacatc tggggactct gccgtctatt actgtgcggg ctacgtttgg 360
tttgcttact ggggccaagg gactctggtc actgtctctg cagctacaac aacagcccca 420
tccgtcttcc ccctggcacc a 441
<210> 90
<211> 147
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 109A6
<400> 90
Met Lys Cys Ser Trp Ile Met Phe Phe Leu Met Ala Val Val Thr Gly
1 5 10 15
Val Asn Ser Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys
20 25 30
Pro Gly Ala Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Lys Ile
35 40 45
Lys Asp Thr Tyr Ile His Trp Val Ile Gln Arg Pro Ala Gln Gly Leu
50 55 60
Glu Trp Ile Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Gly
65 70 75 80
Ser Lys Phe Gln Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Asn
85 90 95
Thr Ala Tyr Ile His Leu Ser Ser Leu Thr Ser Gly Asp Ser Ala Val
100 105 110
Tyr Tyr Cys Ala Gly Tyr Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr
115 120 125
Leu Val Thr Val Ser Ala Ala Thr Thr Thr Ala Pro Ser Val Phe Pro
130 135 140
Leu Ala Pro
145
<210> 91
<211> 498
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 109A6
<400> 91
atgaagttgc ctgttaggct gttggtgctg atgttctgga ttcctgcctc cagcagtgat 60
gttgtgatga cccaagttcc actctccctg cctgtcagtc ttggagatca agcctccatc 120
tcttgcagat ctagtcagag acttgtgcac agtaatggaa acacctattt acattggttc 180
ttacagaagc caggccagtc tccaaagctc ctgatctaca cagtttccaa ccgattttct 240
ggggtcccag acaggttcag tggcagtgga tcagggacag atttcacact caagatcagc 300
agagtggagg ctgaggatct gggagtttat ttctgctctc aaagtacact tgttccgtgg 360
acgttcggtg gaggcaccaa gctggaaatc aaacgggctg atgctgcacc aactgtatcc 420
atcttcccac catccagtga gcagttaaca tctggaggtg cctcagtcgt gtgcttcttg 480
aacaacttct acccaaag 498
<210> 92
<211> 166
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 109A6
<400> 92
Met Lys Leu Pro Val Arg Leu Leu Val Leu Met Phe Trp Ile Pro Ala
1 5 10 15
Ser Ser Ser Asp Val Val Met Thr Gln Val Pro Leu Ser Leu Pro Val
20 25 30
Ser Leu Gly Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu
35 40 45
Val His Ser Asn Gly Asn Thr Tyr Leu His Trp Phe Leu Gln Lys Pro
50 55 60
Gly Gln Ser Pro Lys Leu Leu Ile Tyr Thr Val Ser Asn Arg Phe Ser
65 70 75 80
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
85 90 95
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys
100 105 110
Ser Gln Ser Thr Leu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu
115 120 125
Glu Ile Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
130 135 140
Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu
145 150 155 160
Asn Asn Phe Tyr Pro Lys
165
<210> 93
<211> 441
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VH антитела 111A6
<400> 93
atgaaatgca gctgggttat gttcttcctg atggcagtgg ttacaggggt caattcagag 60
gttcagctgc agcagtctgg ggcagaactt gtgaagccag gggcctcagt caagttgtcc 120
tgcacagctt ctggcttcaa aattaaagac acctatatac actgggtgat ccagaggcct 180
gcacagggcc tggaatggat tggaaggatt gatcctgcga atggtaatac tatttatggc 240
tcaaagttcc agggcaaggc cactctaaca gcggacacat catccaacac agcctacatt 300
cacctcagca gcctgacatc tggggactct gccgtctatt actgtgcggg ctacgtttgg 360
tttgcttact ggggccaagg gactctggtc actgtctctg cagctacaac aacagcccca 420
tccgtcttcc ccctggcacc a 441
<210> 94
<211> 147
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 111A6
<400> 94
Met Lys Cys Ser Trp Val Met Phe Phe Leu Met Ala Val Val Thr Gly
1 5 10 15
Val Asn Ser Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Lys
20 25 30
Pro Gly Ala Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Lys Ile
35 40 45
Lys Asp Thr Tyr Ile His Trp Val Ile Gln Arg Pro Ala Gln Gly Leu
50 55 60
Glu Trp Ile Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Gly
65 70 75 80
Ser Lys Phe Gln Gly Lys Ala Thr Leu Thr Ala Asp Thr Ser Ser Asn
85 90 95
Thr Ala Tyr Ile His Leu Ser Ser Leu Thr Ser Gly Asp Ser Ala Val
100 105 110
Tyr Tyr Cys Ala Gly Tyr Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr
115 120 125
Leu Val Thr Val Ser Ala Ala Thr Thr Thr Ala Pro Ser Val Phe Pro
130 135 140
Leu Ala Pro
145
<210> 95
<211> 495
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 1 VK антитела 111A6
<400> 95
atggattttc aggtgcagat tttcagcttc ttgctaatca gtgcctcagt tgcaatgtcc 60
agaggagaaa atgtgctcac ccagtctcca gcaatcatgt ctgcttctcc aggggagaag 120
gtcaccatga cctgcagggc caggtcaagt gtaagttcca gttacttgca ctggtaccag 180
cagaagtcag gtgcctcccc caaactctgg atttatagca catccaactt ggcttctgga 240
gtccctactc gcttcagtgg cagtgggtct gggacctctt actctctcac aatcagcagt 300
gtggaggctg aagatgctgc cacttattac tgccagcagt acagtggtta cccactcacg 360
ttcggtgctg ggaccaagct ggagctgaaa cgggctgatg ctgcaccaac tgtatccatc 420
ttcccaccat ccagtgagca gttaacatct ggaggtgcct cagtcgtgtg cttcttgaac 480
aacttctacc ccaag 495
<210> 96
<211> 165
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 VK антитела 111A6
<400> 96
Met Asp Phe Gln Val Gln Ile Phe Ser Phe Leu Leu Ile Ser Ala Ser
1 5 10 15
Val Ala Met Ser Arg Gly Glu Asn Val Leu Thr Gln Ser Pro Ala Ile
20 25 30
Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Arg Ala Arg
35 40 45
Ser Ser Val Ser Ser Ser Tyr Leu His Trp Tyr Gln Gln Lys Ser Gly
50 55 60
Ala Ser Pro Lys Leu Trp Ile Tyr Ser Thr Ser Asn Leu Ala Ser Gly
65 70 75 80
Val Pro Thr Arg Phe Ser Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu
85 90 95
Thr Ile Ser Ser Val Glu Ala Glu Asp Ala Ala Thr Tyr Tyr Cys Gln
100 105 110
Gln Tyr Ser Gly Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu
115 120 125
Leu Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser
130 135 140
Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn
145 150 155 160
Asn Phe Tyr Pro Lys
165
<210> 97
<211> 499
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 2 VK антитела 111A6
<400> 97
atgaagttgc ctgttaggct gttggtgctg atgttctgga ttcctgcctc cagcagtgat 60
gttgtgatga cccaagttcc actctccctg cctgtcagtc ttggagatca agcctccatc 120
tcttgcagat ctagtcagag acttgtgcac agtaatggaa acacctattt acattggttc 180
ttacagaagc caggccagtc tccaaagctc ctgatctaca cagtttccaa ccgattttct 240
ggggtcccag acaggttcag tggcagtgga tcagggacag atttcacact caagatcagc 300
agagtggagg ctgaggatct gggagtttat ttctgctctc aaagtacact tgttccgtgg 360
acgttcggtg gaggcaccaa gctggaaatc aaacgggctg atgctgcacc aactgtatcc 420
atcttcccac catccagtga gcagttaaca tctggaggtg cctcagtcgt gtgcttcttg 480
aacaacttct accccaaag 499
<210> 98
<211> 166
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 VK антитела 111A6
<400> 98
Met Lys Leu Pro Val Arg Leu Leu Val Leu Met Phe Trp Ile Pro Ala
1 5 10 15
Ser Ser Ser Asp Val Val Met Thr Gln Val Pro Leu Ser Leu Pro Val
20 25 30
Ser Leu Gly Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Arg Leu
35 40 45
Val His Ser Asn Gly Asn Thr Tyr Leu His Trp Phe Leu Gln Lys Pro
50 55 60
Gly Gln Ser Pro Lys Leu Leu Ile Tyr Thr Val Ser Asn Arg Phe Ser
65 70 75 80
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
85 90 95
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys
100 105 110
Ser Gln Ser Thr Leu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu
115 120 125
Glu Ile Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
130 135 140
Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu
145 150 155 160
Asn Asn Phe Tyr Pro Lys
165
<210> 99
<211> 438
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 1 VH антитела 131B4
<400> 99
atgaaatgca gctggattat gttcttcctg atggcagtgg ttacaggggt caattcagag 60
gttcaggtgc agcagtctgg ggcagagctt gtgaagccag gggcctcagt caagttgtcc 120
tgcacagctt ctggcttcaa aattaaggac acctatatac actggttaaa acagaggcct 180
gaacagggcc tggaatggat tggaaggatt gatcctgcga atggtaatac tatatatggc 240
tcaaagttcc agggcaaggc cactataaca gcagacacat catccaacac agcctacatt 300
caactcagca gcctgacatc tggggacact gccgtctatt tttgtgcggg ctacgtttgg 360
tttgcttact ggggccaagg gactctggtc actgtctctg cagccaaaac gacaccccca 420
tccgtcttcc ccctggcc 438
<210> 100
<211> 146
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 VH антитела 131B4
<400> 100
Met Lys Cys Ser Trp Ile Met Phe Phe Leu Met Ala Val Val Thr Gly
1 5 10 15
Val Asn Ser Glu Val Gln Val Gln Gln Ser Gly Ala Glu Leu Val Lys
20 25 30
Pro Gly Ala Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Lys Ile
35 40 45
Lys Asp Thr Tyr Ile His Trp Leu Lys Gln Arg Pro Glu Gln Gly Leu
50 55 60
Glu Trp Ile Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Gly
65 70 75 80
Ser Lys Phe Gln Gly Lys Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn
85 90 95
Thr Ala Tyr Ile Gln Leu Ser Ser Leu Thr Ser Gly Asp Thr Ala Val
100 105 110
Tyr Phe Cys Ala Gly Tyr Val Trp Phe Ala Tyr Trp Gly Gln Gly Thr
115 120 125
Leu Val Thr Val Ser Ala Ala Lys Thr Thr Pro Pro Ser Val Phe Pro
130 135 140
Leu Ala
145
<210> 101
<211> 453
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 2 VH антитела 131B4
<400> 101
atggctgtct tggggctgct cttctgcctg gtgacattcc caagctgtgt cctgtcccag 60
gtgcagctga agcagtcagg acctagccta gtgcagccct cacagagcct gtccataacc 120
tgcacagtct ctggtttctc attaactagc tatggtgtac actgggttcg ccagtctcca 180
ggaaagggtc tggagtggct gggagtgata tggagaggtg gaagcacaga ctacaatgca 240
gctttcatgt ccagactgag catcaccaag gacaactcca agagccaagt tttctttaaa 300
atgaacagtc tgcaagctga tgacactgcc atatactact gtgccaaaaa ttgggagtat 360
gatggttact gggggtttgc ttactggggc caagggactc tggtcactgt ctctgcagag 420
agtcagtcct tcccaaatgt cttccccctc gaa 453
<210> 102
<211> 151
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 VH антитела 131B4
<400> 102
Met Ala Val Leu Gly Leu Leu Phe Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Gln Ser Gly Pro Ser Leu Val Gln
20 25 30
Pro Ser Gln Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Thr Ser Tyr Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu
50 55 60
Glu Trp Leu Gly Val Ile Trp Arg Gly Gly Ser Thr Asp Tyr Asn Ala
65 70 75 80
Ala Phe Met Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln
85 90 95
Val Phe Phe Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr
100 105 110
Tyr Cys Ala Lys Asn Trp Glu Tyr Asp Gly Tyr Trp Gly Phe Ala Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala Glu Ser Gln Ser Phe
130 135 140
Pro Asn Val Phe Pro Leu Glu
145 150
<210> 103
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 вариабельного домена VH антитела 131B4
<400> 103
Gln Val Gln Leu Lys Gln Ser Gly Pro Ser Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Ser Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Lys Asn Trp Glu Tyr Asp Gly Tyr Trp Gly Phe Ala Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ala
115 120
<210> 104
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR1 последовательности 2 VH антитела 131B4
<400> 104
Gly Phe Ser Leu Thr Ser Tyr Gly
1 5
<210> 105
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности 2 VH антитела 131B4
<400> 105
Ile Trp Arg Gly Gly Ser Thr
1 5
<210> 106
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR3 последовательности 2 VH антитела 131B4
<400> 106
Ala Lys Asn Trp Glu Tyr Asp Gly Tyr Trp Gly Phe Ala Tyr
1 5 10
<210> 107
<211> 417
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 3 VH антитела 131B4
<400> 107
atggcagtgg ttacaggggt caattcagag gttcagctgc agcagtctgg ggctgagctt 60
gtgaggccag gggcctcagt caagttgtcc tgcacagctt ctggctttaa cattaaagac 120
gactatatgc actgggtgaa gcagaggcct gaacagggcc tggagtggat tggaaggatt 180
gatcctgcga atggtaatac taaatatgcc ccgaagttcc aggacaaggc cactataact 240
gcagacacat cctccaacac agcctacctg cagctcagca gcctgacatc tgaggacact 300
gccgtctatt actgtgctag aagctatgat ggttctctgg gggactactg gggccaaggc 360
accactctca cagtctcctc agagagtcag tccttcccaa atgtcttccc cctcgag 417
<210> 108
<211> 139
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 3 VH антитела 131B4
<400> 108
Met Ala Val Val Thr Gly Val Asn Ser Glu Val Gln Leu Gln Gln Ser
1 5 10 15
Gly Ala Glu Leu Val Arg Pro Gly Ala Ser Val Lys Leu Ser Cys Thr
20 25 30
Ala Ser Gly Phe Asn Ile Lys Asp Asp Tyr Met His Trp Val Lys Gln
35 40 45
Arg Pro Glu Gln Gly Leu Glu Trp Ile Gly Arg Ile Asp Pro Ala Asn
50 55 60
Gly Asn Thr Lys Tyr Ala Pro Lys Phe Gln Asp Lys Ala Thr Ile Thr
65 70 75 80
Ala Asp Thr Ser Ser Asn Thr Ala Tyr Leu Gln Leu Ser Ser Leu Thr
85 90 95
Ser Glu Asp Thr Ala Val Tyr Tyr Cys Ala Arg Ser Tyr Asp Gly Ser
100 105 110
Leu Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Glu
115 120 125
Ser Gln Ser Phe Pro Asn Val Phe Pro Leu Glu
130 135
<210> 109
<211> 118
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 3 вариабельного домена VH антитела 131B4
<400> 109
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asp Asp
20 25 30
Tyr Met His Trp Val Lys Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Lys Tyr Ala Pro Lys Phe
50 55 60
Gln Asp Lys Ala Thr Ile Thr Ala Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu Gln Leu Ser Ser Leu Thr Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Ser Tyr Asp Gly Ser Leu Gly Asp Tyr Trp Gly Gln Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
<210> 110
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR1 последовательности 3 VH антитела 131B4
<400> 110
Gly Phe Asn Ile Lys Asp Asp Tyr
1 5
<210> 111
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности 3 VH антитела 131B4
<400> 111
Ile Asp Pro Ala Asn Gly Asn Thr
1 5
<210> 112
<211> 11
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR3 последовательности 3 VH антитела 131B4
<400> 112
Ala Arg Ser Tyr Asp Gly Ser Leu Gly Asp Tyr
1 5 10
<210> 113
<211> 498
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 131B4
<400> 113
atgaagttgc ctgttaggct gttggtgctg atgttctgga ttcctgcttc cagcagtgat 60
gctgtgttga cccaaactcc actctccctg cctgtcagtc ttggagatca agcctccatc 120
tcttgcacat ctagtcagag ccttgtacac agtaatggaa acacctattt acattggtac 180
ctgcagaagc caggccagtc tccaaagctc ctgatctaca aagtttccga ccgattttct 240
ggggtcccag acaggttcag tggcagtgga tcaggaacag atttcacact catgatcacc 300
agagtggagg ctgaggatct gggagtttat ttctgctctc aaagttcact tgttccgtgg 360
acgttcggtg gaggcaccaa gctggaagtc aaacgggctg atgctgcacc aactgtatcc 420
atcttcccac catccagtga gcagttaaca tctggaggtg cctcagtcgt gtgcttcttg 480
aacaacttct accccaaa 498
<210> 114
<211> 166
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 131B4
<400> 114
Met Lys Leu Pro Val Arg Leu Leu Val Leu Met Phe Trp Ile Pro Ala
1 5 10 15
Ser Ser Ser Asp Ala Val Leu Thr Gln Thr Pro Leu Ser Leu Pro Val
20 25 30
Ser Leu Gly Asp Gln Ala Ser Ile Ser Cys Thr Ser Ser Gln Ser Leu
35 40 45
Val His Ser Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro
50 55 60
Gly Gln Ser Pro Lys Leu Leu Ile Tyr Lys Val Ser Asp Arg Phe Ser
65 70 75 80
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
85 90 95
Leu Met Ile Thr Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys
100 105 110
Ser Gln Ser Ser Leu Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu
115 120 125
Glu Val Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
130 135 140
Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu
145 150 155 160
Asn Asn Phe Tyr Pro Lys
165
<210> 115
<211> 452
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 1 VH антитела 131E8
<400> 115
atggctgttt tggggctgct cttctgcctg gtgacattcc caagctgtgt cctatcccag 60
gtgcagctga agcagtcaag acctggccca gtgcagccct cacagagcct gtccatcacc 120
tgcacagtct ctggtttctc attacctaac tatggtgtac actgggttcg ccagcctcca 180
ggaaagggtc tggagtggct gggagtgata tggagtggtg gaagcacaga ctataatgca 240
gctttcaaat ccagactgag catcagcaag gacaactcca agagccaagt tttctttaaa 300
atgaacagtc tgcaagctga tgacacagcc atatactact gtgccagaaa tttttatagt 360
aagtacgact atgctatgga ctactggggt caaggaacct cagtcaccgt ctcctcagcc 420
aaaacaacac ccccatccgt cttccccctg gc 452
<210> 116
<211> 150
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 VH антитела 131E8
<400> 116
Met Ala Val Leu Gly Leu Leu Phe Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Gln Ser Arg Pro Gly Pro Val Gln
20 25 30
Pro Ser Gln Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Pro Asn Tyr Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu
50 55 60
Glu Trp Leu Gly Val Ile Trp Ser Gly Gly Ser Thr Asp Tyr Asn Ala
65 70 75 80
Ala Phe Lys Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln
85 90 95
Val Phe Phe Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr
100 105 110
Tyr Cys Ala Arg Asn Phe Tyr Ser Lys Tyr Asp Tyr Ala Met Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Ser Val Thr Val Ser Ser Ala Lys Thr Thr Pro
130 135 140
Pro Ser Val Phe Pro Leu
145 150
<210> 117
<211> 411
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 2 VH антитела 131E8
<400> 117
atgttcttct tggtagcaac agctacaggt gtccactccc aggtccaact gcagcagcct 60
gggtctgtgc tggtgaggcc tggagcttca gtgaagctgt cctgcaaggc ttctggctac 120
acattcacca gctactggat gcactgggtg aagcagaggc cgggacaagg ccttgagtgg 180
attggaaata ttaatcctaa tagtggtagt actaactaca atgagaagtt caagggcaag 240
gccacactga ctgtagacac atcctccagc acagcctaca tggatctcag cagcctgaca 300
tctgaggact ctgcggtcta ttactgtgca agactgggtg actactgggg ccaaggcacc 360
actctcacag tctcctcaaa gagtcagtcc tccccatccg tcttccccct g 411
<210> 118
<211> 137
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 VH антитела 131E8
<400> 118
Met Phe Phe Leu Val Ala Thr Ala Thr Gly Val His Ser Gln Val Gln
1 5 10 15
Leu Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala Ser Val Lys
20 25 30
Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met His
35 40 45
Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Asn Ile
50 55 60
Asn Pro Asn Ser Gly Ser Thr Asn Tyr Asn Glu Lys Phe Lys Gly Lys
65 70 75 80
Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Ala Tyr Met Asp Leu
85 90 95
Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Ala Arg Leu
100 105 110
Gly Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Lys Ser
115 120 125
Gln Ser Ser Pro Ser Val Phe Pro Leu
130 135
<210> 119
<211> 435
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 3 VH антитела 131E8
<400> 119
gctgtcttgg ggctgctctt ctgcctggtt gcatttccaa gctgtgtcct gtcccaggtg 60
cagctgaagg agtcaggacc tggcctggtg gcgccctcac agagcctgtc catcacttgc 120
actgtctctg ggttttcatt aaccagctat ggtgtacact gggttcgcca gcctccagga 180
aagggtctgg agtggctggg agtaatatgg gctggtggaa gcacaaatta taattcggct 240
ctcatgtcca gactgagcat cagcaaagac aactccaaga gccaagtttt cttaaaaatg 300
aacagtctgc aaactgatga cacagccatg tactactgtg ccagagatag taactacttt 360
gactactggg gccaaggcac cactctcaca gtctcctcag agagtcagtc cttcccaaat 420
gtcttccccc tcgta 435
<210> 120
<211> 145
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 3 VH антитела 131E8
<400> 120
Ala Val Leu Gly Leu Leu Phe Cys Leu Val Ala Phe Pro Ser Cys Val
1 5 10 15
Leu Ser Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro
20 25 30
Ser Gln Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr
35 40 45
Ser Tyr Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu
50 55 60
Trp Leu Gly Val Ile Trp Ala Gly Gly Ser Thr Asn Tyr Asn Ser Ala
65 70 75 80
Leu Met Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val
85 90 95
Phe Leu Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr
100 105 110
Cys Ala Arg Asp Ser Asn Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr
115 120 125
Leu Thr Val Ser Ser Glu Ser Gln Ser Phe Pro Asn Val Phe Pro Leu
130 135 140
Val
145
<210> 121
<211> 115
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 3 вариабельного домена VH антитела 131E8
<400> 121
Gln Val Gln Leu Lys Glu Ser Gly Pro Gly Leu Val Ala Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ala Gly Gly Ser Thr Asn Tyr Asn Ser Ala Leu Met
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Asp Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Asp Ser Asn Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu Thr
100 105 110
Val Ser Ser
115
<210> 122
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR1 последовательности 3 VH антитела 131E8
<400> 122
Gly Phe Ser Leu Thr Ser Tyr Gly
1 5
<210> 123
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности 3 VH антитела 131E8
<400> 123
Ile Trp Ala Gly Gly Ser Thr
1 5
<210> 124
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR3 последовательности 3 VH антитела 131E8
<400> 124
Ala Arg Asp Ser Asn Tyr Phe Asp Tyr
1 5
<210> 125
<211> 489
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 131E8
<400> 125
atggattttc aggtgcagat tttcagcttc ctgctaatca gtgcctcagt cataatgtcc 60
agaggagaaa atgttctcac ccagtctcca gcaatcatgt ctgcatctcc aggggaaaag 120
gtcaccatga cctgcagtgc cagctcaagt gtaagttaca tgcactggta ccagcagaag 180
tcaagcacct cccccaaact ctggatttat gacacatcca aactggcttc tggagtccca 240
ggtcgcttca gtggcagtgg gtctggaaac tcttactctc tcacgatcag cagcatggag 300
gctgaagatg ttgccactta ttactgtttt caggggagtg ggtacccact cacgttcggc 360
tcggggacaa agttggaaat aaaacgggct gatgctgcac caactgtatc catcttccca 420
ccatccagtg agcagttaac atctggaggt gcctcagtcg tgtgcttctt gaacaacttc 480
taccccaaa 489
<210> 126
<211> 163
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VK антитела 131E8
<400> 126
Met Asp Phe Gln Val Gln Ile Phe Ser Phe Leu Leu Ile Ser Ala Ser
1 5 10 15
Val Ile Met Ser Arg Gly Glu Asn Val Leu Thr Gln Ser Pro Ala Ile
20 25 30
Met Ser Ala Ser Pro Gly Glu Lys Val Thr Met Thr Cys Ser Ala Ser
35 40 45
Ser Ser Val Ser Tyr Met His Trp Tyr Gln Gln Lys Ser Ser Thr Ser
50 55 60
Pro Lys Leu Trp Ile Tyr Asp Thr Ser Lys Leu Ala Ser Gly Val Pro
65 70 75 80
Gly Arg Phe Ser Gly Ser Gly Ser Gly Asn Ser Tyr Ser Leu Thr Ile
85 90 95
Ser Ser Met Glu Ala Glu Asp Val Ala Thr Tyr Tyr Cys Phe Gln Gly
100 105 110
Ser Gly Tyr Pro Leu Thr Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
115 120 125
Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu
130 135 140
Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe
145 150 155 160
Tyr Pro Lys
<210> 127
<211> 453
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VH антитела 131H1
<400> 127
atggctgtct tggggctgct cttctgcctg gtgacattcc caagctgtgt cctatcccag 60
gtgcagctga agcagtcagg acctggccta gtgcagccct cacagagcct gtccatcacc 120
tgcacagtct ctggtttctc attaactagc tatggtgtac actgggttcg ccagtctcca 180
ggaaagggtc tggagtggct gggagtgata tggagtggtg gaagcacaga ctataatgca 240
gctttcatat ccagactgag catcagcaag gacaattcca agagccaagt tttctttaaa 300
atgaacagtc tgcaagctga tgacacagcc atatattact gtgccagatc ttatgattac 360
gacgggaggg gttactttga ctactggggc caaggcacca ctctcacagt ctcctcagag 420
agtcagtcct tcccaaatgt cttccccctc gta 453
<210> 128
<211> 151
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 131H1
<400> 128
Met Ala Val Leu Gly Leu Leu Phe Cys Leu Val Thr Phe Pro Ser Cys
1 5 10 15
Val Leu Ser Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln
20 25 30
Pro Ser Gln Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu
35 40 45
Thr Ser Tyr Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu
50 55 60
Glu Trp Leu Gly Val Ile Trp Ser Gly Gly Ser Thr Asp Tyr Asn Ala
65 70 75 80
Ala Phe Ile Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln
85 90 95
Val Phe Phe Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr
100 105 110
Tyr Cys Ala Arg Ser Tyr Asp Tyr Asp Gly Arg Gly Tyr Phe Asp Tyr
115 120 125
Trp Gly Gln Gly Thr Thr Leu Thr Val Ser Ser Glu Ser Gln Ser Phe
130 135 140
Pro Asn Val Phe Pro Leu Val
145 150
<210> 129
<211> 120
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность вариабельного домена VH антитела 131H1
<400> 129
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ser Gly Gly Ser Thr Asp Tyr Asn Ala Ala Phe Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asp Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Ser Tyr Asp Tyr Asp Gly Arg Gly Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 130
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR1 последовательности VH антитела 131H1
<400> 130
Gly Phe Ser Leu Thr Ser Tyr Gly
1 5
<210> 131
<211> 7
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности VH антитела 131H1
<400> 131
Ile Trp Ser Gly Gly Ser Thr
1 5
<210> 132
<211> 14
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности VH антитела 131H1
<400> 132
Ala Arg Ser Tyr Asp Tyr Asp Gly Arg Gly Tyr Phe Asp Tyr
1 5 10
<210> 133
<211> 486
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 1 VK антитела 131H1
<400> 133
atgagtgtgc tcactcaggt cctggggttg ctgctgctgt ggcttacagg tgccagatgt 60
gacatccaga tgactcagtc tccagcctcc ctgtctgcat ctgtgggaga aactgtcacc 120
atcacatgtc gagcaagtga gaatgtttac agatatttag catggtatca gcagagacag 180
ggaaaatctc ctcagctcct ggtctatagt gcaaaaacct tagcagaagg tgtgccatca 240
aggttcagtg gcagtggatc aggcacacag ttttctctga agatcaacac cctgcagcct 300
gaagattttg ggacttatta ctgtcaacat cattataata ctcctctcac gttcggtgct 360
gggaccaagc tggagctgaa acgggctgat gctgcaccaa ctgtatccat cttcccacca 420
tccagtgagc agttaacatc tggaggtgcc tcagtcgtgt gcttcttgaa caacttctac 480
cccaaa 486
<210> 134
<211> 162
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 VK антитела 131H1
<400> 134
Met Ser Val Leu Thr Gln Val Leu Gly Leu Leu Leu Leu Trp Leu Thr
1 5 10 15
Gly Ala Arg Cys Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser
20 25 30
Ala Ser Val Gly Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Glu Asn
35 40 45
Val Tyr Arg Tyr Leu Ala Trp Tyr Gln Gln Arg Gln Gly Lys Ser Pro
50 55 60
Gln Leu Leu Val Tyr Ser Ala Lys Thr Leu Ala Glu Gly Val Pro Ser
65 70 75 80
Arg Phe Ser Gly Ser Gly Ser Gly Thr Gln Phe Ser Leu Lys Ile Asn
85 90 95
Thr Leu Gln Pro Glu Asp Phe Gly Thr Tyr Tyr Cys Gln His His Tyr
100 105 110
Asn Thr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg
115 120 125
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln
130 135 140
Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr
145 150 155 160
Pro Lys
<210> 135
<211> 107
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 1 вариабельного домена VK антитела 131H1
<400> 135
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Glu Asn Val Tyr Arg Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Arg Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Ser Ala Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Phe Ser Leu Lys Ile Asn Thr Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Thr Tyr Tyr Cys Gln His His Tyr Asn Thr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 136
<211> 6
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR1 последовательности 1 VK антитела 131H1
<400> 136
Glu Asn Val Tyr Arg Tyr
1 5
<210> 137
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности 1 VK антитела 131H1
<400> 137
Ser Ala Lys
1
<210> 138
<211> 9
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR3 последовательности 1 VK антитела 131H1
<400> 138
Gln His His Tyr Asn Thr Pro Leu Thr
1 5
<210> 139
<211> 486
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность 2 VK антитела 131H1
<400> 139
atggttctta tatggctcct gctatgggta tctggtacct gtggggacat tgtgatgtca 60
cagtctccat cctccctggc tgtgtcagca ggagagaagg tcactatgag ctgcaaatcc 120
agtcagagtc tgttcaacag taaaacccga aagaactact tggcttggtt tcagcaaaaa 180
ccagggcagt ctcctgaact gctgatctac tgggcatcca ctaggaaatc tggggtccct 240
gatcgcttca caggcagtgg atctgggaca gatttcactc tcaccatcag cagtgtgcag 300
gctgaagacc tggcagttta ttactgcaag caatcttata atctgtggac gttcggcgga 360
ggcaccaagc tggaaatcaa acgggctgat gctgcaccaa ctgtatccat cttcccacca 420
tccagtgagc agttaacatc tggaggtgcc tcagtcgtgt gcttcttgaa caacttctac 480
cccaaa 486
<210> 140
<211> 162
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 VK антитела 131H1
<400> 140
Met Val Leu Ile Trp Leu Leu Leu Trp Val Ser Gly Thr Cys Gly Asp
1 5 10 15
Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly Glu
20 25 30
Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Phe Asn Ser Lys
35 40 45
Thr Arg Lys Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Gln Ser
50 55 60
Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val Pro
65 70 75 80
Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile
85 90 95
Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln Ser
100 105 110
Tyr Asn Leu Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
115 120 125
Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro Ser Ser Glu Gln
130 135 140
Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu Asn Asn Phe Tyr
145 150 155 160
Pro Lys
<210> 141
<211> 112
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность 2 вариабельного домена VK антитела 131H1
<400> 141
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Phe Asn Ser
20 25 30
Lys Thr Arg Lys Asn Tyr Leu Ala Trp Phe Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Glu Leu Leu Ile Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Tyr Asn Leu Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 142
<211> 12
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR1 последовательности 2 VK антитела 131H1
<400> 142
Gln Ser Leu Phe Asn Ser Lys Thr Arg Lys Asn Tyr
1 5 10
<210> 143
<211> 3
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR2 последовательности 2 VK антитела 131H1
<400> 143
Trp Ala Ser
1
<210> 144
<211> 8
<212> PRT
<213> Искусственная последовательность
<220>
<223> CDR3 последовательности 2 VK антитела 131H1
<400> 144
Lys Gln Ser Tyr Asn Leu Trp Thr
1 5
<210> 145
<211> 440
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VH антитела 132H4
<400> 145
tgagctgggt tttccttgtc cttattttaa aaggtgtcca gtgtgaagtg aagctggtgg 60
agtctggggg aggcttagtg aagcctggag ggtccctgaa actctcctgt gcagcctctg 120
gattcacttt cagtaactat gccatgtctt gggttcgcca gaatccggcg aagaggctgg 180
agtgggtcgc aaccattagt agtggtggtg ctaatattta ctatccagac agtgtgaagg 240
gccgattcat catctccaga gacaatgcca ggaacaccct gtacctgcaa atgagcagtc 300
tgaggtctga ggacacggcc atgtattact gtgcaagagg cgactatttt aaccacttct 360
ggtttgctta ctggggccaa gggactcttg tcactgtctc tgcagccaaa acaacagccc 420
catcggtctt ccccctggca 440
<210> 146
<211> 146
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 132H4
<400> 146
Ser Trp Val Phe Leu Val Leu Ile Leu Lys Gly Val Gln Cys Glu Val
1 5 10 15
Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly Ser Leu
20 25 30
Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr Ala Met
35 40 45
Ser Trp Val Arg Gln Asn Pro Ala Lys Arg Leu Glu Trp Val Ala Thr
50 55 60
Ile Ser Ser Gly Gly Ala Asn Ile Tyr Tyr Pro Asp Ser Val Lys Gly
65 70 75 80
Arg Phe Ile Ile Ser Arg Asp Asn Ala Arg Asn Thr Leu Tyr Leu Gln
85 90 95
Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala Arg
100 105 110
Gly Asp Tyr Phe Asn His Phe Trp Phe Ala Tyr Trp Gly Gln Gly Thr
115 120 125
Leu Val Thr Val Ser Ala Ala Lys Thr Thr Ala Pro Ser Val Phe Pro
130 135 140
Leu Ala
145
<210> 147
<211> 481
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 132H4
<400> 147
atgaagttgc ctgttaggct gttggtgctg atgttctgga ttcctgcttc cagcagtgat 60
gttttgatga cccaaactcc actctccctg cctgtcagtc ttggagatca agcctccatc 120
tcttgtagat cgagtcagag cattgtacat agtaatggaa acacctattt agaatggtac 180
ctgcagaaac caggccagtc tccaaagttc ctgatctaca aagtttccaa ccgattttca 240
ggggtcccag acaggttcag tggcagtgga tcagggacag atttcacact caagatcaac 300
agagtggagg ctgaggatct gggaatttat tactgctttc agggttcaca tgttccgtgg 360
acgttcggtg gaggcaccaa gctggaaatc aaacgggctg atgctgcacc aactgtatcc 420
atcttcccac catccagtga gcagttaaca tctggaggtg cctcagtcgt gtgcttcttg 480
a 481
<210> 148
<211> 160
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VК антитела 132H4
<400> 148
Met Lys Leu Pro Val Arg Leu Leu Val Leu Met Phe Trp Ile Pro Ala
1 5 10 15
Ser Ser Ser Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val
20 25 30
Ser Leu Gly Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile
35 40 45
Val His Ser Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro
50 55 60
Gly Gln Ser Pro Lys Phe Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser
65 70 75 80
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
85 90 95
Leu Lys Ile Asn Arg Val Glu Ala Glu Asp Leu Gly Ile Tyr Tyr Cys
100 105 110
Phe Gln Gly Ser His Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu
115 120 125
Glu Ile Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
130 135 140
Ser Ser Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu
145 150 155 160
<210> 149
<211> 456
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VH антитела 133A6
<400> 149
atgaactttg ggttgagatt ggttttcctt gtccttgttt taaaaggtgt ccagtgtgag 60
gtgaagctag tggagtctgg aggaggctta gtgaagcctg gagggtccct gaaactctcc 120
tgtgcagcct ctggattcac tttcagtaac tatgccatgt cttgggttcg ccagactccg 180
gcgaagaggc tggagtgggt cacaaccatt agtagtggtg gtggtaacat ctactataca 240
gacagtgtga agggccgatt caccgtctcc agagacaatg ccaggaacac cctgtacctg 300
caaatgagca gtctgaggtc tgaggacacg gccatgtatt actgtgcaag aggcgactat 360
agtaactact tctggtttgc ttactggggc caagggactc tggtctctgt ctctgaagcc 420
aaaacaacag ccccatcggt cttccccctg gcacct 456
<210> 150
<211> 152
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 133A6
<400> 150
Met Asn Phe Gly Leu Arg Leu Val Phe Leu Val Leu Val Leu Lys Gly
1 5 10 15
Val Gln Cys Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys
20 25 30
Pro Gly Gly Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe
35 40 45
Ser Asn Tyr Ala Met Ser Trp Val Arg Gln Thr Pro Ala Lys Arg Leu
50 55 60
Glu Trp Val Thr Thr Ile Ser Ser Gly Gly Gly Asn Ile Tyr Tyr Thr
65 70 75 80
Asp Ser Val Lys Gly Arg Phe Thr Val Ser Arg Asp Asn Ala Arg Asn
85 90 95
Thr Leu Tyr Leu Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met
100 105 110
Tyr Tyr Cys Ala Arg Gly Asp Tyr Ser Asn Tyr Phe Trp Phe Ala Tyr
115 120 125
Trp Gly Gln Gly Thr Leu Val Ser Val Ser Glu Ala Lys Thr Thr Ala
130 135 140
Pro Ser Val Phe Pro Leu Ala Pro
145 150
<210> 151
<211> 498
<212> ДНК
<213> Искусственная последовательность
<220>
<223> ДНК-последовательность VK антитела 133A6
<400> 151
atgaagttgc ctgttaggct gttggtgctg atgttctgga ttcctgcttc cagcagtgat 60
gttttgatga cccaaactcc actctccctg cctgtcagtc ttggagatca agcctccatc 120
tcttgcagat ctagtcagag cattgtacat agtaatggaa acacctattt agaatggtac 180
ctgcagaaac caggccagtc tccaaagctc ctgatctaca aagtttccaa ccgattttct 240
ggggtcccag acaggttcag tggcagtgga tcagggacag atttcacact caagatcagc 300
agagtggagg ctgaggatct gggagtttat tactgctttc aaggttcaca tgttccgtgg 360
acgttcggtg gaggcaccaa gctggaaatc aaacgggctg atgctgcacc aactgtatcc 420
atcttcccac catccaggga gcagttaaca tctggaggtg cctcagtcgt gtgcttcttg 480
aacaacttct acccaaaa 498
<210> 152
<211> 166
<212> PRT
<213> Искусственная последовательность
<220>
<223> последовательность VH антитела 133A6
<400> 152
Met Lys Leu Pro Val Arg Leu Leu Val Leu Met Phe Trp Ile Pro Ala
1 5 10 15
Ser Ser Ser Asp Val Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val
20 25 30
Ser Leu Gly Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile
35 40 45
Val His Ser Asn Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro
50 55 60
Gly Gln Ser Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser
65 70 75 80
Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr
85 90 95
Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys
100 105 110
Phe Gln Gly Ser His Val Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu
115 120 125
Glu Ile Lys Arg Ala Asp Ala Ala Pro Thr Val Ser Ile Phe Pro Pro
130 135 140
Ser Arg Glu Gln Leu Thr Ser Gly Gly Ala Ser Val Val Cys Phe Leu
145 150 155 160
Asn Asn Phe Tyr Pro Lys
165
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| IL-18-СВЯЗЫВАЮЩИЕ БЕЛОК (IL-18BP) И АНТИТЕЛА ПРИ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЯХ | 2016 |
|
RU2755691C2 |
| IL-18-СВЯЗЫВАЮЩИЙ БЕЛОК (IL-18BP) И АНТИТЕЛА ПРИ ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЯХ | 2016 |
|
RU2810206C1 |
| АНТИ-IL-5 АНТИТЕЛА | 2017 |
|
RU2758008C2 |
| ИММУНОЦИТОКИНЫ НА ОСНОВЕ IL-15 И IL-15Rα ДОМЕНА SUSHI | 2012 |
|
RU2763298C2 |
| АНТИТЕЛА К IL-6 И ИХ СЛИТЫЕ КОНСТРУКЦИИ И КОНЪЮГАТЫ | 2019 |
|
RU2810777C2 |
| IL-12 ГЕТЕРОДИМЕРНЫЕ СЛИТЫЕ БЕЛКИ FC | 2019 |
|
RU2819097C2 |
| Анти-PD-L1 и IL-2 цитокины | 2017 |
|
RU2769282C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ СВЯЗАННЫХ С IL-8 ЗАБОЛЕВАНИЙ | 2017 |
|
RU2766112C2 |
| СЛИТЫЙ БЕЛОК, ВКЛЮЧАЮЩИЙ IL-12 И АНТИТЕЛО ПРОТИВ FAP, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2831612C1 |
| АНТИТЕЛА, НАПРАВЛЕННЫЕ ПРОТИВ ИНТЕРЛЕЙКИНА-33 (IL-33) | 2015 |
|
RU2829846C2 |
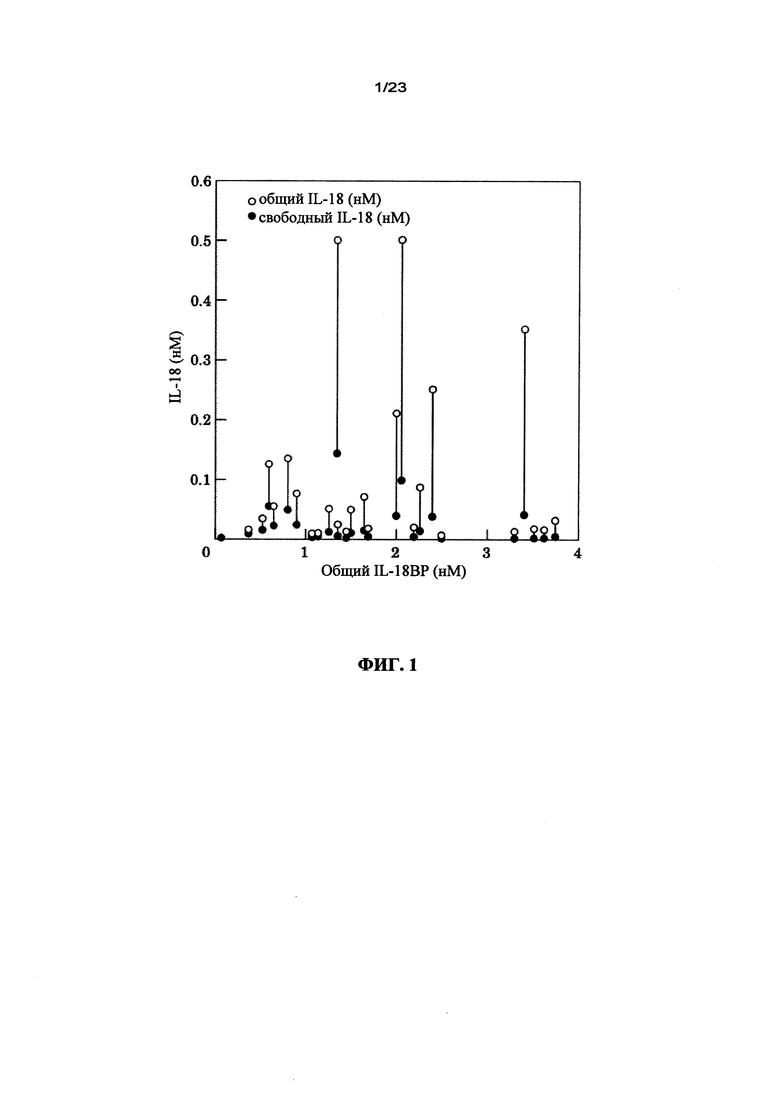
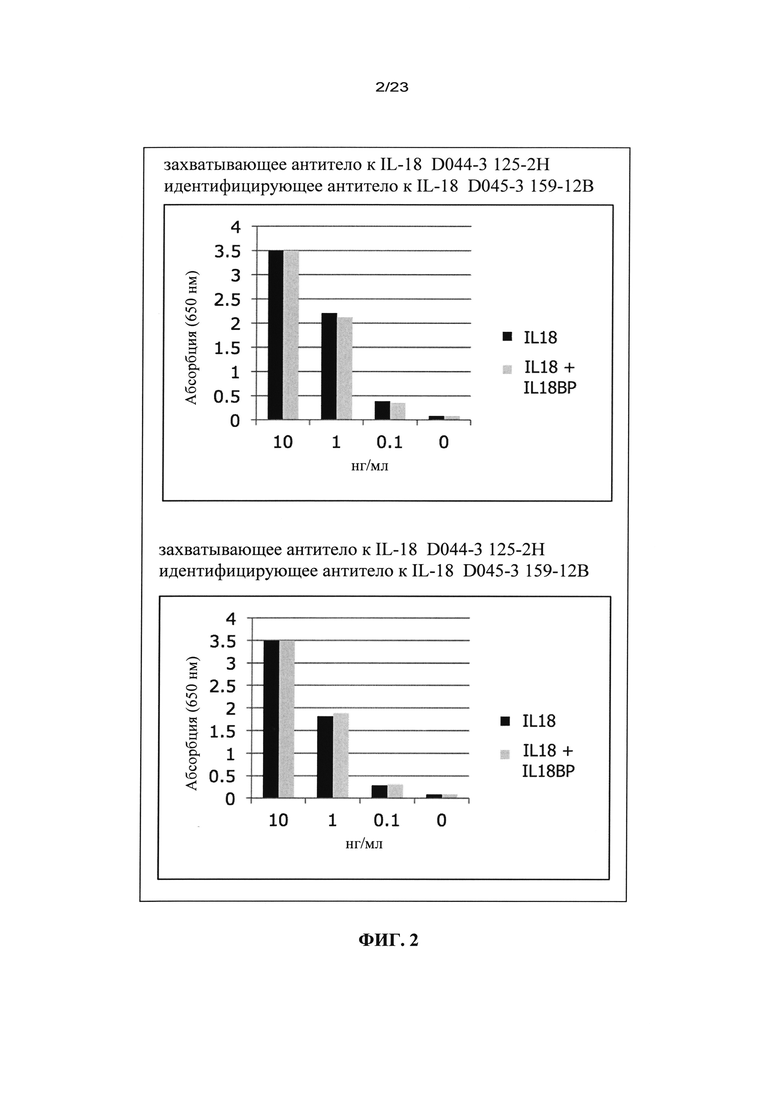
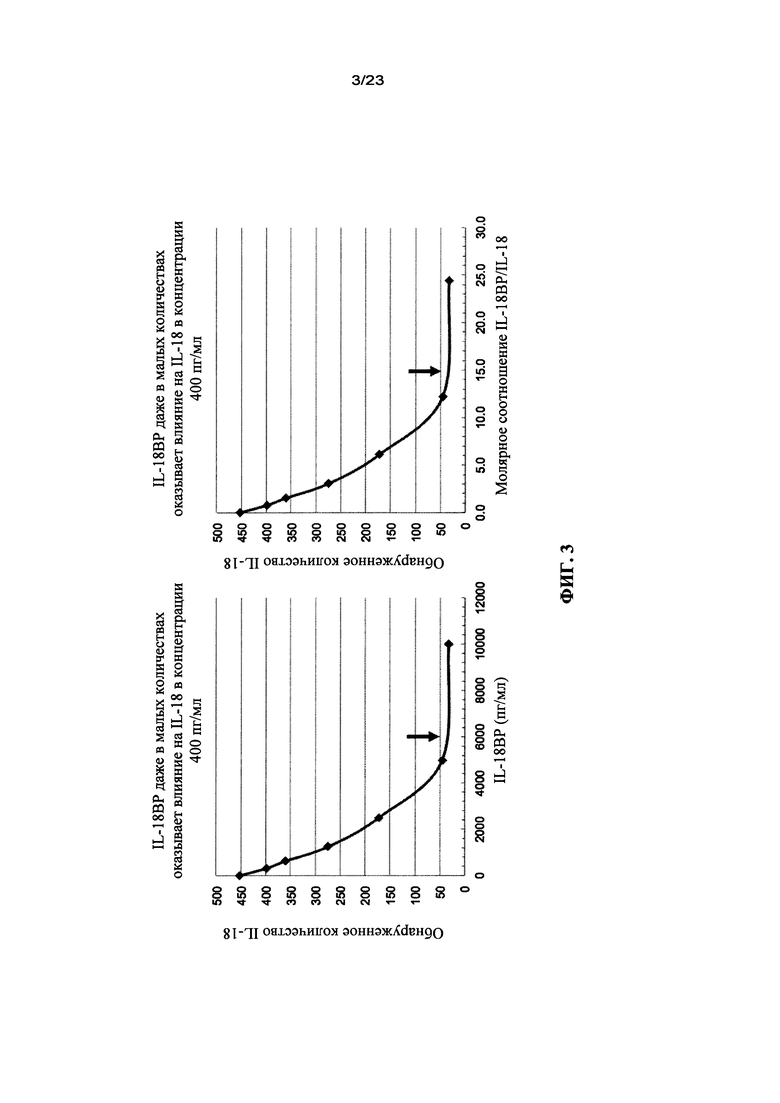
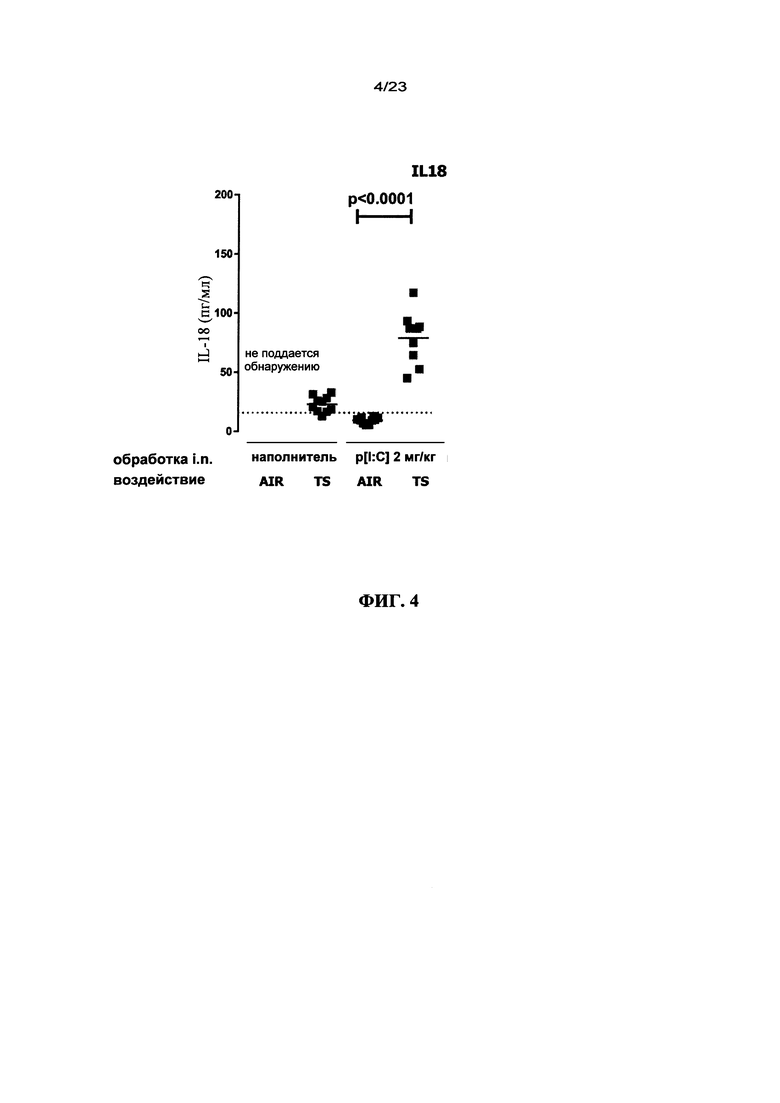
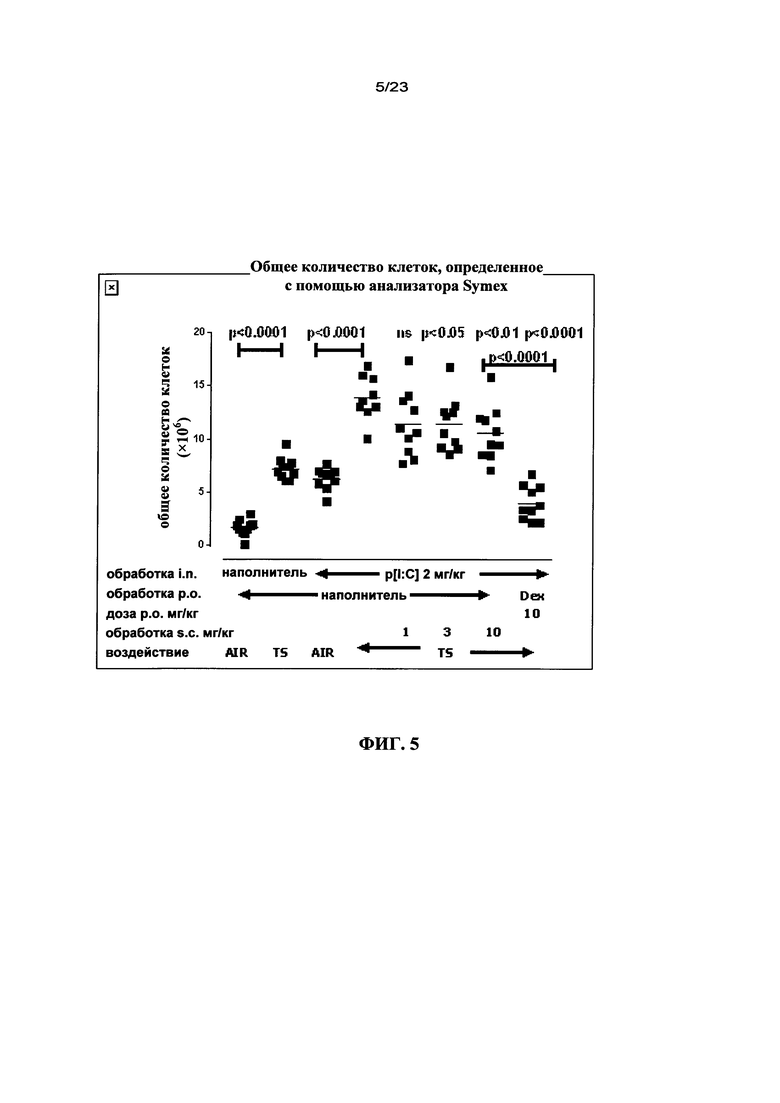
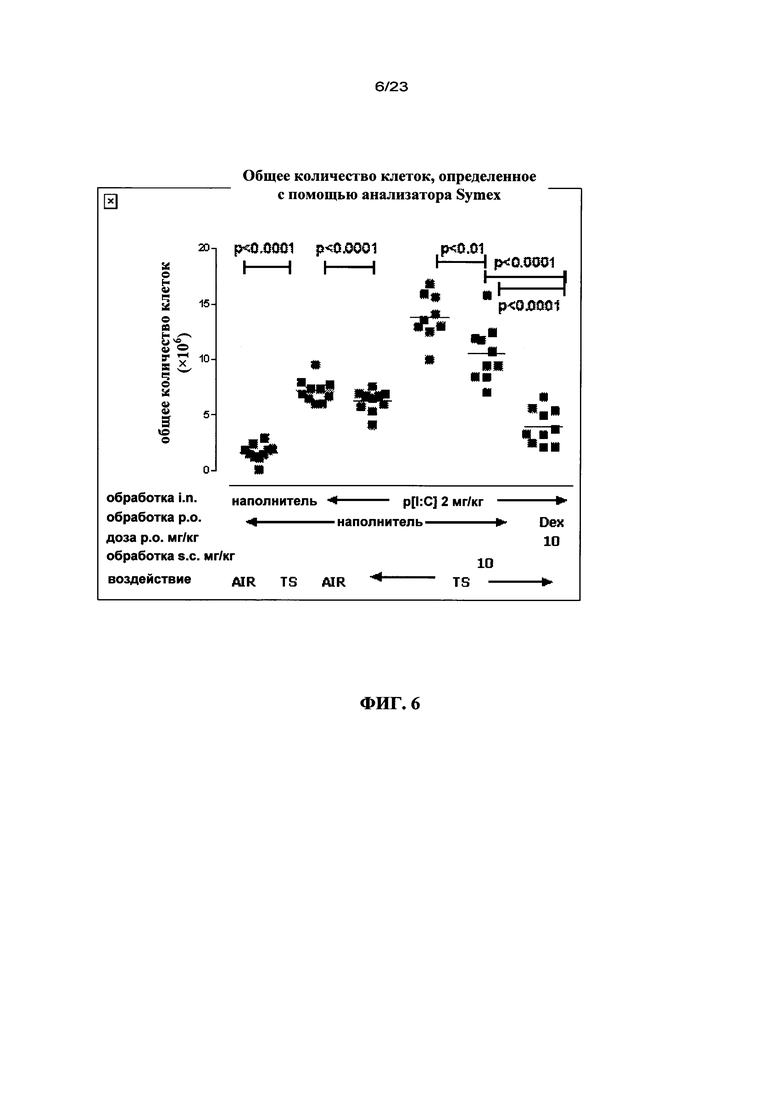
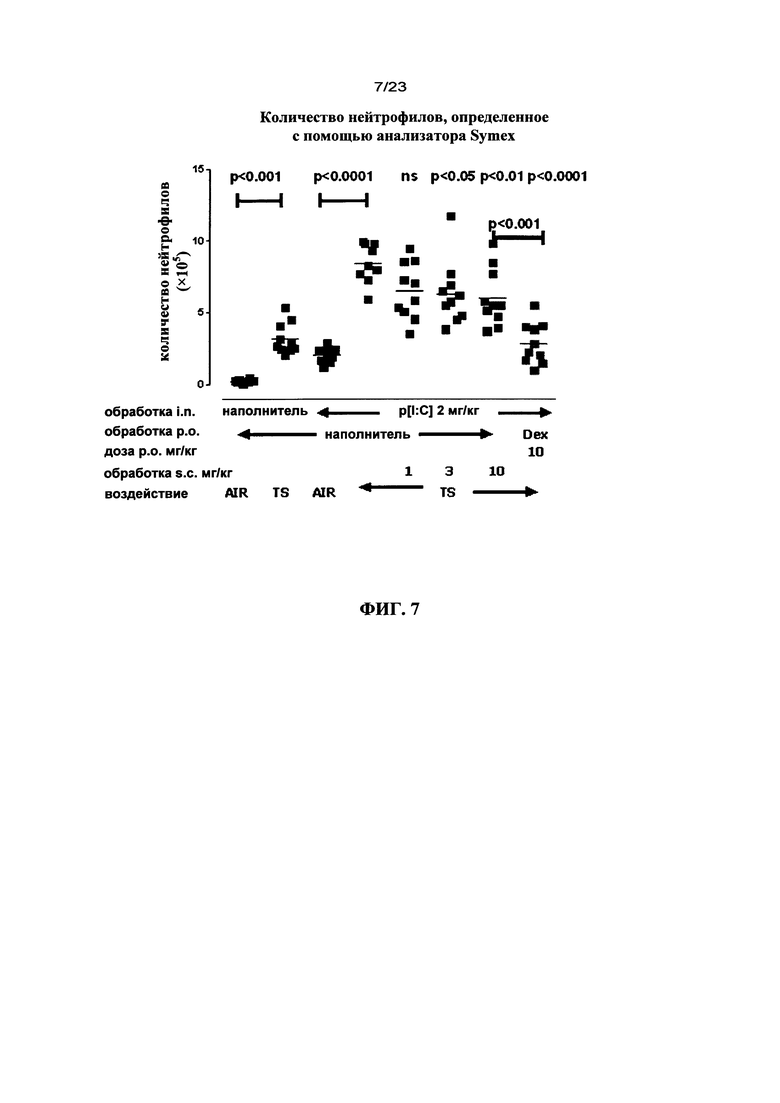
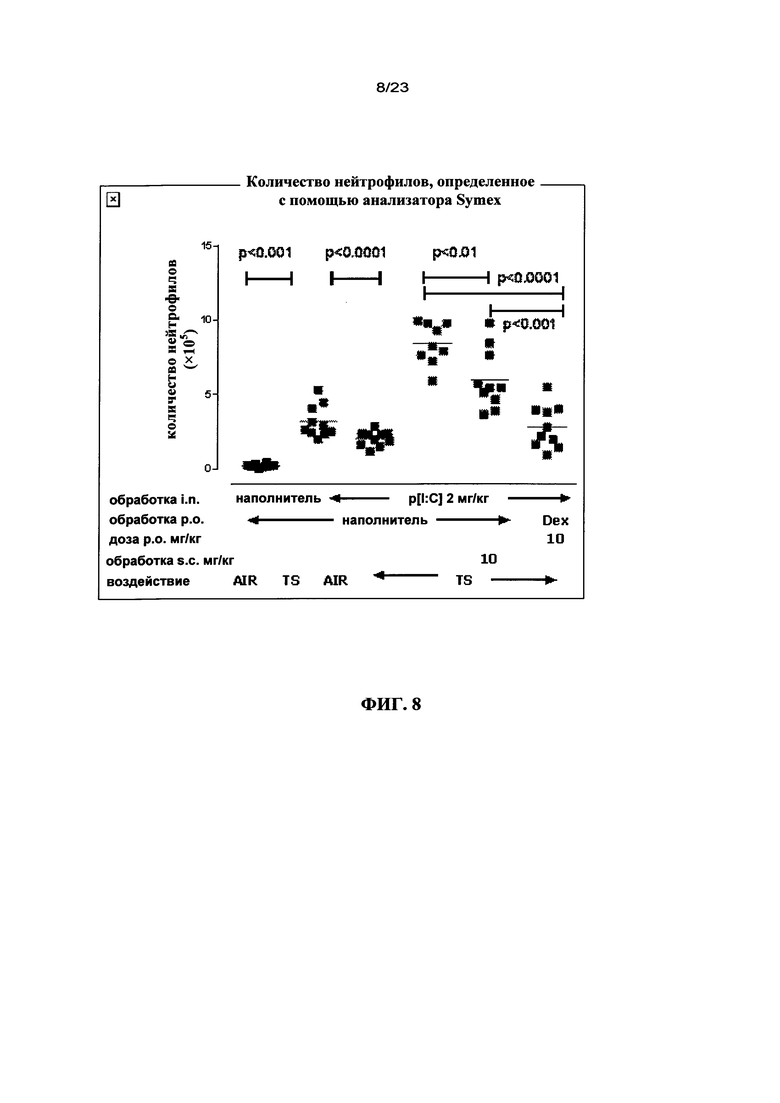
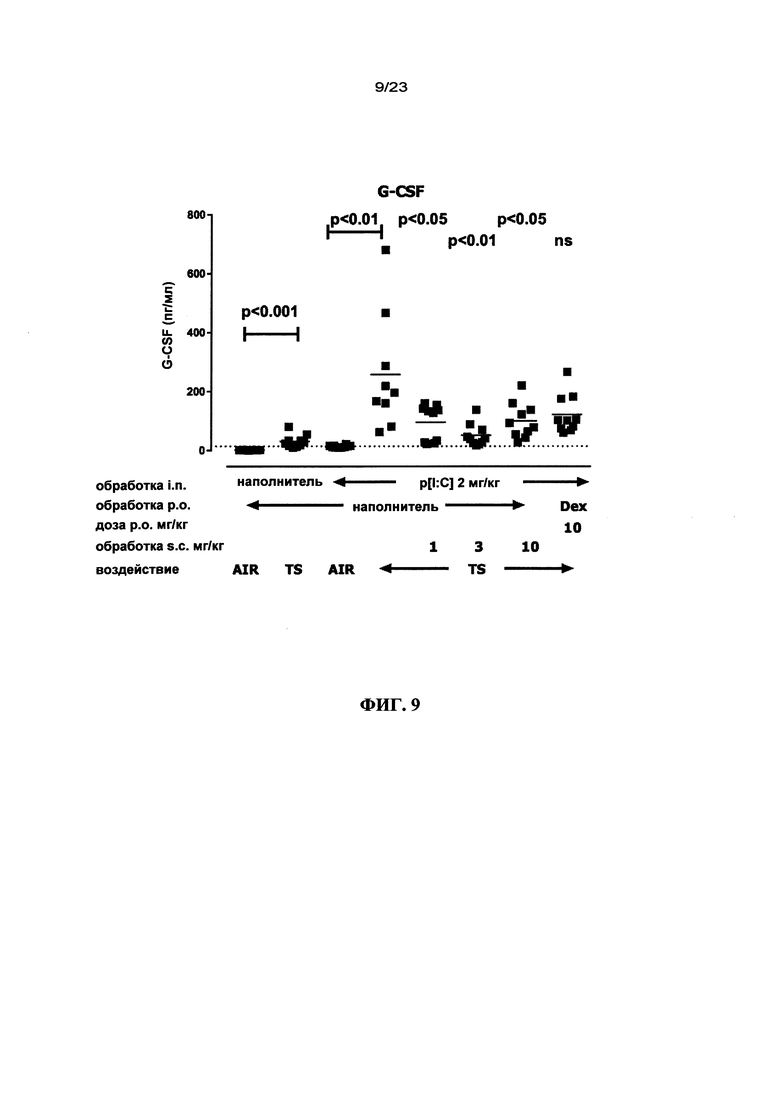
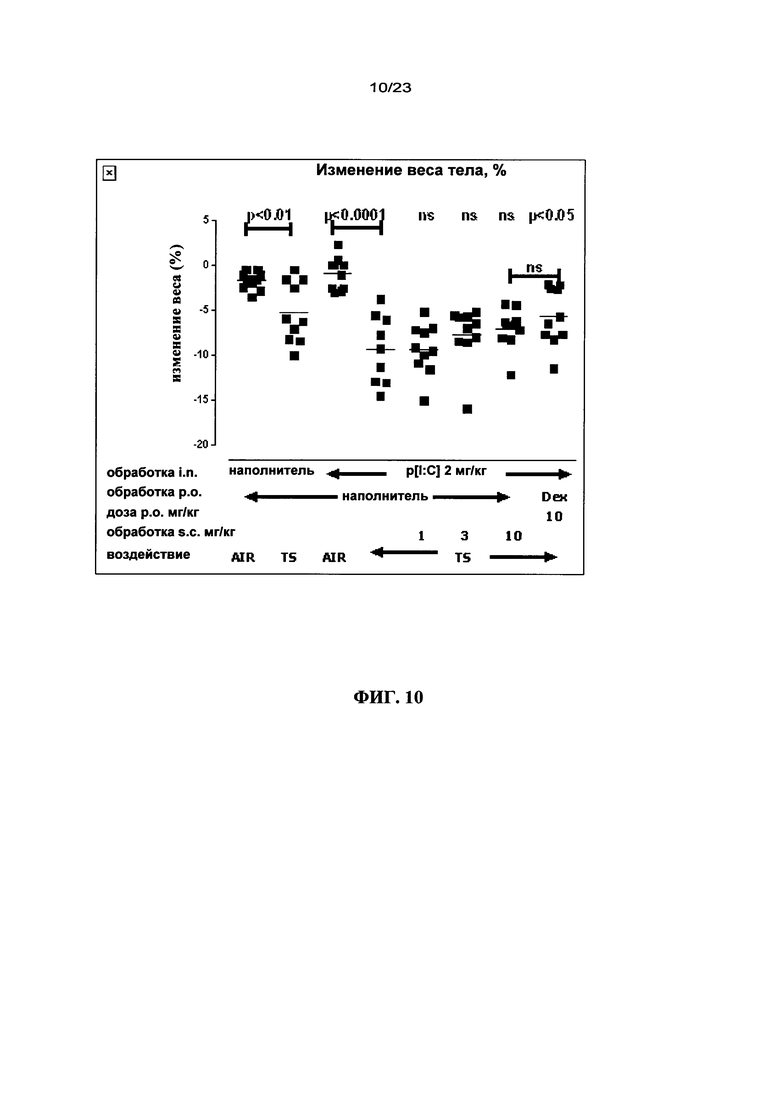













Изобретение относится к биотехнологии и медицине и представляет собой средства и способы лечения ассоциированных с интерлейкином 18 (IL-18) заболеваний и нарушений. В частности, в заявке описаны антитела, которые обладают специфичностью в отношении свободного IL-18 и IL-18-связывающего белка (IL-18BP), предназначенные для применения в указанных способах лечения и для диагностирования симптомов. 4 н. и 7 з.п. ф-лы, 16 табл., 1 пр.
1. Способ определения количества свободного IL-18 в образце in vitro, включающий обнаружение специфического связывания IL-18-связывающего белка (IL-18BP) со свободным белком IL-18 в образце, который включает стадии, на которых:
а) приводят образец или определенную часть организма или область организма, который/которая, как предполагается, содержит свободный IL-18, в контакт с IL-18-связывающим белком, который специфически связывается со свободным IL-18, но не связывается с IL-18, входящим в комплекс, и которая функционирует в качестве захватывающей молекулы для свободного IL-18;
б) дают связываться IL-18-связывающему белку со свободным IL-18;
в) обнаруживают связывание IL-18 с IL-18-связывающим белком и определяют количество свободного IL-18 в образце, где IL-18BP является IL-18BP человека.
2. Способ по п. 1, где IL-18BP является IL-18BP, как показано на SEQ ID NO: 7.
3. Применение IL-18-связывающего белка при лечении IL-18-ассоциированного заболевания или нарушения у популяции индивидуумов, у которых выявлены аномальные уровни свободного IL-18 и/или аномальное соотношение свободного IL-18 к IL-18BP в образцах, взятых из организма, по сравнению с образцами, взятыми из организма здорового контрольного индивидуума, или наличие предрасположенности к развитию такого заболевания или расстройства, где указанный аномальный уровень свободного IL-18 в образцах, взятых из организма:
а) превышает уровень в образцах, взятых из организма здорового контрольного индивидуума, на 5%, 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 100% или более чем на 100%, и
б) составляет ≥5 пг/мл и, в частности, вплоть до 10000 пг/мл, при этом количество свободного IL-18 в сыворотке здорового индивидуума, в частности здорового человека, составляет ≤4 пг/мл,
где IL-18BP является IL-18BP человека, и популяция индивидуумов, у которых выявлены аномальные уровни свободного IL-18 и/или аномальное соотношение свободного IL-18 к IL-18BP в образцах, по сравнению с образцами, взятыми из организма здорового контрольного индивидуума, определена с использованием способа по п. 1.
4. Применение по п. 3, где индивидуум, подлежащий лечению, относится к популяции индивидуумов, для которых установлено, что они имеют повышенные уровни свободного IL-18 в образцах, взятых из организма, выбранных из группы, которая состоит из жидкости бронхоальвеолярного лаважа (BALF), жидкостей кровеносной системы, секреторных жидкостей, биопсии и гомогенизированной ткани, сыворотки, плазмы, мочи, слез, слюны, желчи, пота, выделяемых продуктов, выдыхаемых продуктов, мокроты, бронхоальвеолярной жидкости, секрета сальных желез, клеточных, железистых, слизистых и тканевых секретов, по сравнению с уровнями в образцах, взятых из организма здорового индивидуума.
5. Применение по п. 3, где указанное IL-18-ассоциированное заболевание или нарушение представляет собой:
а) заболевание или нарушение, выбранное из группы, состоящей из хронического обструктивного заболевания легких (COPD), связанного с трансфузией повреждения легких, бронхолегочной дисплазии (BPD), острого респираторного дистресс-синдрома (ARDS), болезни Стилла взрослых, болезни Стилла детей, интерстициальной болезни легких (ILD), идиопатического легочного фиброза, муковисцидоза, легочной артериальной гипертензии, астмы, бронхоэктаза, сердечной недостаточности, амиотрофического бокового склероза (ALS), синдрома сухого глаза (DED), кератита, язвы и истирания роговицы, неоваскуляризации роговицы, патологической внутриглазной неоваскуляризации, ирита, глаукомы, дегенерации желтого пятна, синдрома Шегрена, аутоиммунного увеита, болезни Бехчета, конъюнктивита, аллергического конъюнктивита, дерматита века, диабета типа 2, болезни жирной печени неалкогольной группы (NAFLD), стеатогепатита, трансплантации солидного органа и гематологической трансплантации, повреждения, вызванного ишемией-реперфузией, семейной средиземноморской лихорадки, периодических синдромов, ассоциированных с рецептором 1 фактора некроза опухоли, криопирин-ассоциированных периодических синдромов лихорадки, гипер-IgD-синдромов, подагры, синдрома Шнитцлера, гранулематоза Вегенера, называемого также гранулематозом с полиангиитом (GPA), тиреоидита Хашимото, болезни Крона, неспецифического язвенного колита, связанных с иммуноглобулином-4 (IgG4) заболеваний и терапий на основе стволовых клеток; и/или
б) заболевание, индуцированное вирусной инфекцией; и/или
в) индуцированное IL-18 системное проявление воспаления и ассоциированных сопутствующих заболеваний, выбранных из группы, состоящей из эмфиземы, воспаления тканей, деструкции тканей, резекции легкого, исчезновения сосудов, апоптоза эндотелиальных клеток, метаплазии слизистой оболочки, гипертрофии сердца, снижения уровня VEGF в ткани легких, утраты легочных сосудов, мускуляризации сосудов, ремоделирования сосудов, отложения коллагена, наличия патологических слоев эластина в легких, фиброзного ремоделирования дыхательных путей, увеличения воздушного пространства, хронического ремоделирования дыхательных путей и легочных сосудов и снижения легочной функции, где лечение IL-18-ассоциированного заболевания или нарушения включает предотвращение, прекращение, облегчение или исчезновение симптомов, ассоциированных с указанным заболеванием или нарушением.
6. Применение по п. 3, где IL-18BP снижает связывание IL-18 с рецептором IL-18 (IL-18R) по меньшей мере на 5%, по меньшей мере на 10%, по меньшей мере на 15%, по меньшей мере на 20%, по меньшей мере на 25%, по меньшей мере на 30%, по меньшей мере на 40%, по меньшей мере на 45%, по меньшей мере на 50%, по меньшей мере на 55%, по меньшей мере на 60%, по меньшей мере на 65%, по меньшей мере на 70%, по меньшей мере на 75%, по меньшей мере на 80%, по меньшей мере на 85%, по меньшей мере на 90%, по меньшей мере на 95%, на 100%.
7. Применение по п. 6, где рецептор IL-18 является или IL-18Rα, IL-18Rβ, или обоими.
8. Применение IL-18-связывающего белка (IL-18BP) для получения фармацевтической композиции, предназначенной для применения при лечении IL-18-ассоциированного заболевания или нарушения у популяции индивидуумов, у которых выявлены аномальные уровни свободного IL-18 и/или аномальное соотношение свободного IL-18 к IL-18BP в образцах, взятых из организма, по сравнению с уровнями в образцах здорового контрольного индивидуума, или имеющих предрасположенность к развитию заболевания или нарушения, где указанная композиция содержит IL-18BP в профилактически и/или терапевтически эффективном количестве, где указанная композиция необязательно содержит другой ингибитор провоспалительного цитокина или его функциональный фрагмент, или регуляторный фактор, который индуцирует in-situ экспрессию указанного ингибитора провоспалительного цитокина, или его функциональный фрагмент, терапевтические средства для совместного применения, такие как противовоспалительные, бронходилататорные, антигистаминные, противозастойные или противокашлевые лекарственные субстанции.
9. Применение по п. 8, в котором указанное IL-18-ассоциированное заболевание или нарушение представляет собой:
а) заболевание или нарушение, выбранное из группы, состоящей из хронического обструктивного заболевания легких (COPD), связанного с трансфузией повреждения легких, бронхолегочной дисплазии (BPD), острого респираторного дистресс-синдрома (ARDS), болезни Стилла взрослых, болезни Стилла детей, интерстициальной болезни легких (ILD), идиопатического легочного фиброза, муковисцидоза, легочной артериальной гипертензии, астмы, бронхоэктаза, сердечной недостаточности, амиотрофического бокового склероза (ALS), синдрома сухого глаза (DED), кератита, язвы и истирания роговицы, неоваскуляризации роговицы, патологической внутриглазной неоваскуляризации, ирита, глаукомы, дегенерации желтого пятна, синдрома Шегрена, аутоиммунного увеита, болезни Бехчета, конъюнктивита, аллергического конъюнктивита, дерматита века, диабета типа 2, болезни жирной печени неалкогольной группы (NAFLD), стеатогепатита, трансплантации солидного органа и гематологической трансплантации, повреждения, вызванного ишемией-реперфузией, семейной средиземноморской лихорадки, периодических синдромов, ассоциированных с рецептором 1 фактора некроза опухоли, криопирин-ассоциированных периодических синдромов лихорадки, гипер-IgD-синдромов, подагры, синдрома Шнитцлера, гранулематоза Вегенера, называемого также гранулематозом с полиангиитом (GPA), тиреоидита Хашимото, болезни Крона, неспецифического язвенного колита, связанных с иммуноглобулином-4 (IgG4) заболеваний и терапий на основе стволовых клеток; и/или
б) заболевание, индуцированное вирусной инфекцией; и/или
в) индуцированное IL-18 системное проявление воспаления и ассоциированных сопутствующих заболеваний, выбранных из группы, состоящей из эмфиземы, воспаления тканей, деструкции тканей, резекции легкого, исчезновения сосудов, апоптоза эндотелиальных клеток, метаплазии слизистой оболочки, гипертрофии сердца, снижения уровня VEGF в ткани легких, утраты легочных сосудов, мускуляризации сосудов, ремоделирования сосудов, отложения коллагена, наличия патологических слоев эластина в легких, фиброзного ремоделирования дыхательных путей, увеличения воздушного пространства, хронического ремоделирования дыхательных путей и легочных сосудов и снижения легочной функции, где лечение IL-18-ассоциированного заболевания или нарушения включает предотвращение, прекращение, облегчение или исчезновение симптомов, ассоциированных с указанным заболеванием или нарушением.
10. Диагностический набор для обнаружения свободного IL-18 способом по п. 1, содержащий IL-18BP в качестве захватывающей молекулы и вторую IL-18-специфическую связывающую молекулу в качестве идентифицирующей молекулы, где идентифицирующая молекула связывается с сайтами IL-18, отличными от сайтов, с которыми связывается захватывающая молекула.
11. Диагностический набор по п. 10 для применения в способе по п. 1.
| WO 2004101617 A1, 25.11.2004 | |||
| ИСПОЛЬЗОВАНИЕ БИСФОСФОНАТОВ ДЛЯ ИНГИБИРОВАНИЯ РЕЗОРБЦИИ КОСТИ, ВОЗНИКАЮЩЕЙ ВСЛЕДСТВИЕ ИМПЛАНТАЦИИ ОРТОПЕДИЧЕСКИХ ПРОТЕЗОВ | 1995 |
|
RU2161032C2 |
| US 20050100965 A1, 12.05.2005 | |||
| Якушенко Е.В., ИНТЕРЛЕЙКИН-18 И ЕГО РОЛЬ В ИММУННОМ ОТВЕТЕ, Медицинская Иммунология 2005, Т | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
Авторы
Даты
2020-09-08—Публикация
2014-09-05—Подача