ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка испрашивает приоритет согласно предварительной заявке США № 62/740813, поданной 3 октября 2018 г., предварительной заявке США № 62/810038, поданной 25 февраля 2019 г., и предварительной заяв159ке США № 62/848512, поданной 15 мая 2019 г., которые все полностью включены в настоящий документ посредством ссылки для всех целей.
Уровень техники
Для того чтобы Т-клетки вызвали эффективный противоопухолевый ответ, должны произойти три события. Т-клетки сначала должны провзаимодействовать с антигенными опухолевыми пептидами, презентированными ГКГС, в среде опухоли. Во-вторых, с Т-клетками должны связаться костимулирующие молекулы. И, в-третьих, Т-клетки должны быть индуцированы цитокинами, такими как IL-12 и IL-2, чтобы выработать костимулирующие цитокины, такие как ИФН-γ, который обеспечивает дифференцировку и размножение. Распознавание только опухолевых пептидов в отсутствие индукции цитокинами приводит к тому, что Т-клетки становятся анергическими, что приводит к толерантности. Соответственно, очень многообещающим подходом в иммунотерапии рака являются разные виды лечения на основе цитокинов. Действительно, IL-2 одобрен для применения у пациентов с метастатической карциномой почек и злокачественной меланомой. Однако в настоящее время отсутствуют одобренные варианты применения рекомбинантного IL-12 у человека.Рекомбинантный IL-12 представляет собой перспективный вид лечения на основе цитокина из-за его широкого спектра действия при активации иммунной системы. Однако до настоящего времени IL-12 сталкивался с препятствиями в клинических исследованиях с участием людей из-за токсичности. Как и в случае других цитокинов короткий период полужизни IL-12 требует частых болюсных инъекций.
Кроме того, IL-12 состоит из α-цепи (субъединица p35; IL-12p35) и β-цепи (субъединица p40; IL-12p40) ковалентно связанных с образованием биологически активного гетеродимера IL-12. IL-12 осуществляет свою сигнальную функцию в клетках посредством связывания путем связывания с димерным рецепторным комплексом IL-12, состоящим из β1 рецептора IL-12 (IL-12Rβ1) и β2 рецептора IL-12 (IL-12Rβ2), на Т-клетках, и индукции секреции ИФН-γ. Однако субъединица IL-12p40 также может существовать в виде гомодимера, который, как сообщается, оказывает антагонистическое действие на активность IL-12, конкурируя за связывание с рецептором IL-12.
Настоящее изобретение относится к короткому периоду полужизни IL-12 путем обеспечения новых IL-12-Fc слитых белков, а также новых вариантов IL-12 со сниженной активностью.
Краткое описание изобретения
Согласно одному аспекту настоящего изобретения предложен гетеродимерный слитый белок Fc, содержащий: a) первый слитый белок, содержащий домен вариантной субъединицы IL-12p40 и первый домен Fc, причем указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого домена Fc; и b) второй слитый белок, содержащий домен субъединицы IL-12p35 и второй домен Fc, причем указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного домена Fc; при этом указанный первый и указанный второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc. Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из: E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная вариантная субъединица IL-12p40 по меньшей мере на 90% идентична полипептидной последовательности, выбранной из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и (или) указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная вариантная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная вариантная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из: N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная вариантная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; T366S/L368A/Y407V/Y349C и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный домен вариантной субъединицы IL-12p40 присоединен к указанному первому домену Fc с использованием первого доменного линкера и (или) указанный домен субъединицы IL-12p35 присоединен к указанному второму домену Fc с использованием второго доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc содержит:
a) указанный первый слитый белок, имеющий полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 47(XENP27201 Цепь 1), ii) SEQ ID NO: 85(XenD24752), iii) SEQ ID NO: 86(XenD24753), iv) SEQ ID NO: 87(XenD24754), v) SEQ ID NO: 88(XenD24755), vi) SEQ ID NO: 89(XenD24756), vii) SEQ ID NO: 90(XenD24757), viii) SEQ ID NO: 91(XenD24758), ix) SEQ ID NO: 92(XenD24759), x) SEQ ID NO: 93(XenD24760), xi) SEQ ID NO: 94(XenD24761), xii) SEQ ID NO: 95(XenD24762), xiii) SEQ ID NO: 96(XenD24763), xiv) SEQ ID NO: 97(XenD24764), xv) SEQ ID NO: 98(XenD24765), xvi) SEQ ID NO: 99(XenD24766), xvii) SEQ ID NO: 100(XenD24767), xviii) SEQ ID NO: 101(XenD24768), xix) SEQ ID NO: 102(XenD24769), xx) SEQ ID NO: 103(XenD24770), xxi) SEQ ID NO: 104(XenD24771), xxii) SEQ ID NO: 105(XenD24772), xxiii) SEQ ID NO: 106(XenD24773), xxiv) SEQ ID NO: 107(XenD24774), xxv) SEQ ID NO: 108(XenD24775), xxvi) SEQ ID NO: 109(XenD24776), xxvii) SEQ ID NO: 110(XenD24777), xxviii) SEQ ID NO: 111(XenD24778), xxix) SEQ ID NO: 112(XenD24792), xxx) SEQ ID NO: 215(XenD25922), xxxi) SEQ ID NO: 216(XenD25923), xxxii) SEQ ID NO: 217(XenD25924), xxxiii) SEQ ID NO: 218(XenD25925), xxxiv) SEQ ID NO: 219(XenD25926), xxxv) SEQ ID NO: 220(XenD25927), xxxvi) SEQ ID NO: 221(XenD25928), xxxvii) SEQ ID NO: 222(XenD25929), xxxviii) SEQ ID NO: 223(XenD25930), xxxix) SEQ ID NO: 224(XenD25931), xl) SEQ ID NO: XXX(XenD26411), xli) SEQ ID NO: XXX(XenD26412), xlii) SEQ ID NO: XXX(XenD26413), xliii) SEQ ID NO: XXX(XenD26414), xliv) SEQ ID NO: XXX(XenD26415), xlv) SEQ ID NO: XXX(XenD26416), xlvi) SEQ ID NO: XXX(XenD26417), xlvii) SEQ ID NO: XXX(XenD26418), xlviii) SEQ ID NO: XXX(XenD27070), xlix) SEQ ID NO: XXX(XenD27071), l) SEQ ID NO: XXX(XenD27072), li) SEQ ID NO: XXX(XenD27073), lii) SEQ ID NO: XXX(XenD27074), liii) SEQ ID NO: XXX(XenD27075), liv) SEQ ID NO: XXX(XenD27076), lv) SEQ ID NO: XXX(XenD27077), lvi) SEQ ID NO: XXX(XenD27078), lvii) SEQ ID NO: XXX(XenD28173), lviii) SEQ ID NO: XXX(XenD24876), lix) SEQ ID NO: XXX(XenD27162), lx) SEQ ID NO: XXX(XenD27163), lxi) SEQ ID NO: XXX(XenD27164), lxii) SEQ ID NO: XXX(XenD27165) lxiii) SEQ ID NO: XXX(XENP31582 Цепь 1), lxiv) SEQ ID NO: XXX(XENP31583 Цепь 1), lxv) SEQ ID NO: XXX(XENP31584 Цепь 1), lxvi) SEQ ID NO: XXX(XENP32187 Цепь 1), lxvii) SEQ ID NO: XXX(XENP32188 Цепь 1), lxviii) SEQ ID NO: XXX(XENP32189, Цепь 1), lxix) SEQ ID NO: XXX(XENP32190 Цепь 1), lxx) SEQ ID NO: XXX(XENP32191 Цепь 1), lxxi) SEQ ID NO: XXX(XENP32991 Цепь 1), lxxii) SEQ ID NO: XXX(XENP32992 Цепь 1), lxxiii) SEQ ID NO: XXX(XENP32993 Цепь 1), lxxiv) SEQ ID NO: XXX(XENP32994 Цепь 1), lxxv) SEQ ID NO: XXX(XENP32995 Цепь 1), lxxvi) SEQ ID NO: XXX(XENP32996 Цепь 1), lxxvi) SEQ ID NO: XXX(XENP32997 Цепь 1), lxxvii) SEQ ID NO: XXX(XENP32998 Цепь 1), lxxvii) SEQ ID NO: XXX(XENP32999 Цепь 1), lxxviii) SEQ ID NO: XXX(XENP33000 Цепь 1), lxxix) SEQ ID NO: XXX(XENP33001 Цепь 1), lxxx) SEQ ID NO: XXX(XENP33002 Цепь 1), lxxxi) SEQ ID NO: XXX(XENP33003 Цепь 1), lxxxii) SEQ ID NO: XXX(XENP33004 Цепь 1), lxxxiii) SEQ ID NO: XXX(XENP33005 Цепь 1), lxxxiv) SEQ ID NO: XXX(XENP33006 Цепь 1), lxxxv) SEQ ID NO: XXX (XENP33007 Цепь 1), lxxxvi) SEQ ID NO: XXX(XENP33008 Цепь 1), lxxxvii) SEQ ID NO: XXX(XENP33008 Цепь 1), lxxxviii) SEQ ID NO: XXX(XENP33009 Цепь 1), lxxxix) SEQ ID NO: XXX(XENP33010 Цепь 1) и xc) SEQ ID NO: XXX(XENP33011 Цепь 1); и
b) указанный второй слитый белок, имеющий полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 48(XENP27201 Цепь 2), ii) SEQ ID NO: 126(XenD24779), iii) SEQ ID NO: 127(XenD24780), iv) SEQ ID NO: 128(XenD24781), v) SEQ ID NO: 129(XenD24782), vi) SEQ ID NO: 130(XenD24783), vii) SEQ ID NO: 131(XenD24784), viii) SEQ ID NO: 132(XenD24785), ix) SEQ ID NO: 133(XenD24786), x) SEQ ID NO: 134(XenD24787), xi) SEQ ID NO: 135(XenD24788), xii) SEQ ID NO: 136(XenD24789), xiii) SEQ ID NO: 137(XenD24790), xiv) SEQ ID NO: 138(XenD24791), xv) SEQ ID NO: 236(XenD25911), xvi) SEQ ID NO: 237(XenD25912), xvii) SEQ ID NO: 238(XenD25913), xviii) SEQ ID NO: 239(XenD25914), xix) SEQ ID NO: 240(XenD25915), xx) SEQ ID NO: 241(XenD25916), xxi) SEQ ID NO: 242(XenD25917), xxii) SEQ ID NO: 243(XenD25918), xxiii) SEQ ID NO: 244(XenD25919), xxiv) SEQ ID NO: 245(XenD25920), xxv) SEQ ID NO: 246(XenD25921), xxvi) SEQ ID NO: XXX(XenD26427), xxvii) SEQ ID NO: XXX(XenD26428), xxviii) SEQ ID NO: XXX(XenD27089), xxix) SEQ ID NO: XXX(XenD27090), xxx) SEQ ID NO: XXX(XenD27091), xxxi) SEQ ID NO: XXX(XenD27092), xxxii) SEQ ID NO: XXX(XenD27093), xxxiii) SEQ ID NO: XXX(XenD27094), xxxix) SEQ ID NO: XXX(XenD24877), xl) SEQ ID NO: XXX(XenD27166), xli) SEQ ID NO: XXX(XENP31582 Цепь 2), xlii) SEQ ID NO: XXX(XENP31583 Цепь 2), xliii) SEQ ID NO: XXX(XENP31584 Цепь 2), xliv) SEQ ID NO: XXX(XENP32187 Цепь 2), xlv) SEQ ID NO: XXX(XENP32188 Цепь 2), xlvi) SEQ ID NO: XXX(XENP32189, Цепь 2), xlvii) SEQ ID NO: XXX(XENP32190 Цепь 2), xlviii) SEQ ID NO: XXX(XENP32191 Цепь 2), xlix) SEQ ID NO: XXX(XENP32991 Цепь 2), l) SEQ ID NO: XXX(XENP32992 Цепь 2), li) SEQ ID NO: XXX(XENP32993 Цепь 2), lii) SEQ ID NO: XXX(XENP32994 Цепь 2), liii) SEQ ID NO: XXX(XENP32995 Цепь 2), liv) SEQ ID NO: XXX(XENP32996 Цепь 2), lv) SEQ ID NO: XXX(XENP32997 Цепь 2), lvi) SEQ ID NO: XXX(XENP32998 Цепь 2), lvii) SEQ ID NO: XXX(XENP32999 Цепь 2), lviii) SEQ ID NO: XXX(XENP33000 Цепь 2), lix) SEQ ID NO: XXX(XENP33001 Цепь 2), lx) SEQ ID NO: XXX(XENP33002 Цепь 2), lxi) SEQ ID NO: XXX(XENP33003 Цепь 2), lxii) SEQ ID NO: XXX(XENP33004 Цепь 2), lxiii) SEQ ID NO: XXX(XENP33005 Цепь 2), lxiv) SEQ ID NO: XXX(XENP33006 Цепь 2), lxv) SEQ ID NO: XXX(XENP33007 Цепь 2), lxvi) SEQ ID NO: XXX(XENP33008 Цепь 2), lxvii) SEQ ID NO: XXX(XENP33008 Цепь 2), lxviii) SEQ ID NO: XXX(XENP33009 Цепь 2), lxix) SEQ ID NO: XXX(XENP33010 Цепь 2) и lxx) SEQ ID NO: XXX(XENP33011 Цепь 2).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc выбран из группы, состоящей из XENP27201, XENP28820, XENP28821, XENP28822, XENP28823, XENP28824, XENP28825, XENP28826, XENP28827, XENP28828, XENP28829, XENP28830, XENP28831, XENP28832, XENP28833, XENP28834, XENP28835, XENP28836, XENP28837, XENP28838, XENP28839, XENP28840, XENP28841, XENP28842, XENP28843, XENP28844, XENP28845, XENP28846, XENP28847, XENP28848, XENP28849, XENP28850, XENP28851, XENP28852, XENP29949, XENP29950, XENP29951, XENP29952, XENP30597, XENP30598, XENP30599, XENP30600, XENP30601, XENP30602, XENP30603, XENP30604, XENP30605, XENP30606. XENP30307, XENP30308, XENP30609, XENP31250, XENP31251, XENP31252, XENP31253, XENP31254, XENP31255, XENP31256, XENP31257, XENP31258, XENP31259, XENP31260, XENP31261, XENP31262, XENP31263, XENP31264, XENP31265, XENP31286, XENP31142, XENP31143, XENP31144, XENP31145, XENP31146, XENP31582, XENP31583, XENP31584, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190, XENP32191, XENP32991, XENP32992, XENP32993, XENP32994, XENP32995, XENP32996, XENP32997, XENP32998, XENP32999, XENP33000, XENP33001, XENP33002, XENP33003, XENP33004, XENP33005, XENP33006, XENP33007, XENP33008, XENP33008, XENP33009, XENP33010 и XENP33011.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc выбран из группы, состоящей из: XENP31251, XENP31254, XENP31258, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190, и XENP32191.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, дополнительно содержащий одну или более модификаций субъединицы IL-12p40, выбранных из группы, состоящей из: N103Q, N113Q, N200Q, и N281Q.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный слитый белок Fc, содержащий: a) первый слитый белок, содержащий первый белковый домен и первый домен Fc, причем указанный первый белковый домен ковалентно присоединен к С-концу указанного первого домена Fc; и b) второй слитый белок, содержащий второй белковый домен и второй домен Fc, причем указанный второй белковый домен ковалентно присоединен к С-концу указанного домена Fc; при этом указанный первый и указанный второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, и при этом указанный первый белковый домен содержит субъединицу IL-12p40 и указанный второй белковый домен содержит субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C) в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый белковый домен присоединен к указанному первому домену Fc с использованием первого доменного линкера и (или) указанный второй белковый домен присоединен к указанному второму домену Fc с использованием второго доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и (или) указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)). Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc содержит: a) указанный первый слитый белок, имеющий полипептидную последовательность SEQ ID NO: 49 (XENP27202 Цепь 1), и b) указанный второй слитый белок, имеющий полипептидную последовательность SEQ ID NO: 50 (XENP27202 Цепь 2).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc представляет собой XENP27202.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный слитый белок Fc, содержащий: a) слитый белок, содержащий первый белковый домен, второй белковый домен и первый домен Fc, причем указанный первый белковый домен ковалентно присоединен к указанному второму белковому домену, и при этом указанный второй белковый домен ковалентно присоединен к N-концу указанного первого домена Fc; и b) второй домен Fc; причем указанный первый и указанный второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, и при этом указанный первый белковый домен содержит субъединицу IL-12p40 и указанный второй белковый домен содержит субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C) в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый белковый домен присоединен к указанному второму белковому домену с использованием первого доменного линкера и (или) указанный второй белковый домен присоединен к указанному первому домену Fc с использованием второго доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и (или) указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, Q256, K158, C252, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc содержит: a) указанный слитый белок, имеющий полипептидную последовательность SEQ ID NO: 51 (XENP27203 Цепь 1), и b) указанный второй домен Fc, имеющий полипептидную последовательность SEQ ID NO: 52 (XENP27203 Цепь 2).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc представляет собой XENP27203.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc представляет собой XENP31290.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный слитый белок Fc, содержащий: a) слитый белок, содержащий первый белковый домен, второй белковый домен и первый домен Fc, причем указанный первый белковый домен ковалентно присоединен к указанному второму белковому домену, и при этом указанный второй белковый домен ковалентно присоединен к N-концу указанного первого домена Fc; и b) второй домен Fc; причем указанный первый и указанный второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, и при этом указанный первый белковый домен содержит субъединицу IL-12p35 и указанный второй белковый домен содержит субъединицу IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C) в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый белковый домен присоединен к указанному второму белковому домену с использованием первого доменного линкера и (или) указанный второй белковый домен присоединен к указанному первому домену Fc с использованием второго доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и (или) SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc содержит: a) указанный слитый белок, имеющий полипептидную последовательность SEQ ID NO: 53 (XENP27204 Цепь 1), и b) указанный второй домен Fc, имеющий полипептидную последовательность SEQ ID NO: 54 (XENP27204 Цепь 2).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный гетеродимерный слитый белок Fc представляет собой XENP27204.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный слитый белок Fc, содержащий: a) слитый белок, содержащий первый белковый домен, второй белковый домен и первый домен Fc, причем указанный первый белковый домен присоединен к С-концу указанного первого домена Fc, и причем указанный второй белковый домен ковалентно присоединен к указанному первому белковому домену; и b) второй домен Fc; причем указанный первый и указанный второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, и при этом указанный первый белковый домен содержит субъединицу IL-12p40 и указанный второй белковый домен содержит субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C) в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый белковый домен присоединен к указанному второму белковому домену с использованием первого доменного линкера и (или) указанный второй белковый домен присоединен к указанному первому домену Fc с использованием второго доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и (или) указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный слитый белок Fc, содержащий: a) слитый белок, содержащий первый белковый домен, второй белковый домен и первый домен Fc, причем указанный первый белковый домен присоединен к С-концу указанного первого домена Fc, и при этом указанный второй белковый домен ковалентно присоединен к указанному первому белковому домену; и b) второй домен Fc; причем указанный первый и указанный второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, и при этом указанный первый белковый домен содержит субъединицу IL-12p35 и указанный второй белковый домен содержит субъединицу IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C) в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый белковый домен присоединен к указанному второму белковому домену с использованием первого доменного линкера и (или) указанный второй белковый домен присоединен к указанному первому домену Fc с использованием второго доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и (или) указанный второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и (или) указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный комплекс, содержащий: a) субъединицу IL-12p40, и b) субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 ковалентно присоединена к указанной субъединице IL-12p35 с использованием доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и (или) указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанный первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный комплекс, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая гетеродимерный комплекс, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гетеродимерный комплекс.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гетеродимерный комплекс.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гетеродимерного комплекса, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гетеродимерный комплекс.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гетеродимерного комплекса, причем указанный способ включает: a) обеспечение композиции, содержащей гетеродимерный комплекс; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гетеродимерный комплекс.
Согласно другому аспекту настоящего изобретения предложена вариантная субъединица IL-12p40, имеющая измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p40, причем указанная вариантная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, Q256, C252, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p40, причем указанная вариантная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p40, причем указанная вариантная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p40, причем указанная вариантная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая вариантную субъединицу IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложена нуклеиновая кислота, кодирующая вариантную субъединицу IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную нуклеиновую кислоту, кодирующую вариантную субъединицу IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения вариантной субъединицы IL-12p40, причем указанный способ включает культивирование клетки-хозяина по п. H8 в условиях, при которых вырабатывается указанная вариантная субъединица IL-12p40.
Согласно другому аспекту настоящего изобретения предложена вариантная субъединица IL-12p35, имеющая измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p35, причем указанная вариантная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p35, причем указанная вариантная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p35, причем аминокислотные замены указанной вариантной субъединицы IL-12p35 выбраны из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p35, причем указанная вариантная субъединица IL-12p35 имеет аминокислотные замены N71D/N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p35, причем указанная вариантная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция, содержащая вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложена нуклеиновая кислота, кодирующая вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную нуклеиновую кислоту, кодирующую вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложена вариантная субъединица IL-12p35, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанная вариантная субъединица IL-12p35.
Согласно другому аспекту настоящего изобретения предложен гетеродимерный белок, содержащий: a) первый слитый белок, содержащий домен субъединицы IL-12p40, ковалентно присоединенный к первому домену Fc; и b) второй слитый белок, содержащий домен субъединицы IL-12p35, ковалентно присоединенный ко второму домену Fc; причем указанный первый и второй домены Fc содержат набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; и T366S/L368A/Y407V/Y349C и T366W/S354C; в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный домен субъединицы IL-12p40 присоединен к N-концу указанного первого домена Fc и указанный домен субъединицы IL-12p35 присоединен к N-концу указанного второго домена Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный домен субъединицы IL-12p40 присоединен к С-концу указанного первого домена Fc и указанный домен субъединицы IL-12p35 присоединен к С-концу указанного второго домена Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный домен субъединицы IL-12p40 присоединен к указанному первому домену Fc с использованием доменного линкера и указанный домен субъединицы IL-12p35 присоединен к указанному второму домену Fc с использованием доменного линкера.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный первый и второй домены Fc содержат петлю IgG1-CH2-CH3.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный первый слитый белок содержит, от N- к C-концу, домен субъединицы IL-12p40-доменный линкер-шарнир-CH2-CH3 и указанный второй слитый белок содержит, от N- к C-концу, домен субъединицы IL-12p35-доменный линкер-шарнир-CH2-CH3.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный первый слитый белок содержит, от N- к C-концу, шарнир-CH2-CH3-доменный линкер-домен субъединицы IL-12p40 и указанный второй слитый белок содержит, от N- к C-концу, шарнир-CH2-CH3-доменный линкер-домен субъединицы IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанная субъединица IL-12p40 имеет последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанная субъединица IL-12p35 имеет последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii) (IL-12p35(K158E)), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)),xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)),xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)),xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)),xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)),xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)),xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)),xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)),lx) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q),lxi) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)),lxii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), lxiii) SEQ ID NO: XXX (IL-12p35(N71D/N195D),lxiv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), lxv) SEQ ID NO: XXX (IL-12p35(D55Q)) и lxvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно другому аспекту настоящее изобретение включает гетеродимерный белок, содержащий: a) первый домен Fc; и b) слитый белок, содержащий: i) второй домен Fc; ii) домен субъединицы IL-12p40; и iii) домен субъединицы IL-12p35; причем указанный первый и второй домены Fc содержат набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; и T366S/L368A/Y407V/Y349C и T366W/S354C; в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный слитый белок содержит, от N- к C-концу: домен субъединицы IL-12p40-доменный линкер-домен субъединицы IL-12p35-доменный линкер-шарнир-CH2-CH3.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный слитый белок содержит, от N- к C-концу: домен субъединицы IL-12p35-доменный линкер-домен субъединицы IL-12p40-доменный линкер-шарнир-CH2-CH3.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный слитый белок содержит, от N- к C-концу: шарнир-CH2-CH3-доменный линкер-домен субъединицы IL-12p35-доменный линкер-домен субъединицы IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанный слитый белок содержит, от N- к C-концу: шарнир-CH2-CH3-доменный линкер-домен субъединицы IL-12p40-доменный линкер-домен субъединицы IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанная субъединица IL-12p40 имеет последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гетеродимерный белок, причем указанная субъединица IL-12p35 имеет последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)),xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)),xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)),xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)),xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)),xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)),xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)),xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)),lx) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q),lxi) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)),lxii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), lxiii) SEQ ID NO: XXX (IL-12p35(N71D/N195D),lxiv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), lxv) SEQ ID NO: XXX (IL-12p35(D55Q)) и lxvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен субъединицы IL-12p40-необязательный первый доменный линкер-домен субъединицы IL-12p35-необязательный второй доменный линкер-домен Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: XX (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: XX (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: XX (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: XX (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен субъединицы IL-12p35-необязательный первый доменный линкер-домен субъединицы IL-12p40-необязательный второй доменный линкер-домен Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из:
i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/C252S/K264E)), lxiv) SEQ ID NO: XXX (IL-12p40 (E59K/K99Y/C252S)), lxv)SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен Fc-необязательный первый доменный линкер-домен субъединицы IL-12p40-необязательный второй доменный линкер-домен субъединицы IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен Fc-необязательный первый доменный линкер-домен субъединицы IL-12p35-необязательный второй доменный линкер-домен субъединицы IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен субъединицы IL-12p40-первый доменный линкер-домен субъединицы IL-12p35-второй доменный линкер-домен Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из:
i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/C252S/K264E)), lxiv) SEQ ID NO: XXX (IL-12p40 (E59K/K99Y/C252S)), lxv)SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен субъединицы IL-12p35-первый доменный линкер-домен субъединицы IL-12p40-второй доменный линкер-домен Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из:
i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/C252S/K264E)), lxiv) SEQ ID NO: XXX (IL-12p40 (E59K/K99Y/C252S)), lxv)SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix) (IL-12p35(E143Q)), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен Fc-первый доменный линкер-домен субъединицы IL-12p40-второй доменный линкер-домен субъединицы IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из:
i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/C252S/K264E)), lxiv) SEQ ID NO: XXX (IL-12p40 (E59K/K99Y/C252S)), lxv)SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, каждый из которых содержит, от N- к C-концу, домен Fc-первый доменный линкер-домен субъединицы IL-12p35-второй доменный линкер-домен субъединицы IL-12p40.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанные модификации, способствующие гомодимеризации указанного домена Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный домен Fc имеет дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12) и SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем каждый указанный домен Fc дополнительно содержит аминокислотные замены M428L/N424S.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40 и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12; и (или) указанная субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252S,Q256, K158, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из:
i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/C252S/K264E)), lxiv) SEQ ID NO: XXX (IL-12p40 (E59K/K99Y/C252S)), lxv)SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в виде аминокислотных остатков, выбранных из группы, состоящей из Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет аминокислотные замены, выбранные из группы, состоящей из N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX (IL-12p35(D55Q)), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)), xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)), xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)), xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)), xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)), xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)), xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)), xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)), xl) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q), xli) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)), xlii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), xliii) SEQ ID NO: XXX (IL-12p35(N71D/N195D), xliv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), xlv) SEQ ID NO: XXX (IL-12p35(D55Q)) и xlvi) SEQ ID NO: XXX (IL-12p35(D55K)).
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31289.
Согласно некоторым вариантам реализации настоящего изобретения предложен гомодимерный слитый белок Fc, причем указанный первый и второй мономеры представляют собой XENP31291.
Согласно некоторым вариантам реализации настоящего изобретения предложена композиция гомодимерного слитого белка Fc, содержащая гомодимерный слитый белок Fc, для применения в лечении рака у субъекта.
Согласно некоторым вариантам реализации настоящего изобретения предложена одна или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложена клетка-хозяин, содержащая указанную одну или более нуклеиновых кислот, кодирующих гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ получения гомодимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина в условиях, при которых вырабатывается указанный гомодимерный слитый белок Fc.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ очистки гомодимерного слитого белка Fc, причем указанный способ включает: a) обеспечение композиции, содержащей гомодимерный слитый белок Fc; b) загрузку указанной композиции в ионообменную колонку; и c) сбор фракции, содержащей указанный гомодимерный слитый белок Fc.
Согласно другому аспекту настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем указанный способ включает введение указанному пациенту терапевтически эффективного количества гетеродимерного или гомодимерного слитого белка Fc по любому из предыдущих пунктов.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, дополнительно включающий введение терапевтически эффективного количества антитела, блокирующего контрольную точку.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем указанное антитело, блокирующее контрольную точку, выбрано из антитела к PD-1, антитела к PD-L1, антитела к TIM3, антитела к TIGIT, антитела к LAG3 и антитела к CTLA-4.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем указанное антитело к PD-1 представляет собой ниволумаб, пембролизумаб или пидилизумаб.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем указанное антитело к PD-L1 представляет собой атезолизумаб, авелумаб или дурбалумаб.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем у указанного пациента наблюдается увеличение количества лимфоцитов после введения.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем у указанного пациента наблюдается увеличение количества периферических CD8+ Т-клеток после введения.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем указанный IL-12 Fc слитый белок вводят перед ингибитором контрольной точки для увеличения экспрессии контрольной точки до лечения.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ лечения рака у пациента, нуждающегося в этом, причем указанный IL-12 Fc слитый белок вводят перед ингибитором контрольной точки для увеличения экспрессии контрольной точки до лечения.
Согласно другому аспекту настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, включающий введение указанному пациенту терапевтически эффективного количества гетеродимерного или гомодимерного слитого белка Fc по любому из предыдущих пунктов.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, дополнительно включающий введение терапевтически эффективного количества антитела, блокирующего контрольную точку.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, причем указанное антитело, блокирующее контрольную точку, выбрано из антитела к PD-1, антитела к PD-L1, антитела к TIM3, антитела к TIGIT, антитела к LAG3 и антитела к CTLA-4.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, причем указанное антитело к PD-1 представляет собой ниволумаб, пембролизумаб или пидилизумаб.
Согласно некоторым другим дополнительным вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, причем указанное антитело к PD-L1 представляет собой атезолизумаб, авелумаб или дурбалумаб.
Согласно некоторым дополнительным вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, причем указанное размножение Т-клеток представляет собой по меньшей мере 2-кратное увеличение количества Т-клеток.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, причем указанный IL-12 Fc слитый белок вводят перед ингибитором контрольной точки для увеличения экспрессии контрольной точки до лечения.
Согласно некоторым вариантам реализации настоящего изобретения предложен способ индукции размножения Т-клеток у пациента, нуждающегося в этом, причем указанный IL-12 Fc слитый белок вводят перед ингибитором контрольной точки для увеличения экспрессии контрольной точки до лечения.
Согласно одному аспекту настоящего изобретения предложена субъединица IL-12p40. Согласно другому аспекту настоящего изобретения предложена субъединица IL-12p35. Согласно дополнительному аспекту настоящего изобретения предложен гетеродимерный комплекс, содержащий a) субъединицу IL-12p40 и b) субъединицу IL-12p35.
Краткое описание чертежей
На Фигуре 1А и 1В изображены последовательности IL-12 и его рецепторов.
На Фигуре 2A-2E изображены подходящие пары наборов гетеродимеризационных вариантов Fc (включая искаженные варианты и варианты по pI). Варианты без соответствующего «мономера 2» представляют собой варианты по pI, которые можно применять по отдельности на любом мономере.
На Фигуре 3 изображен перечень изостерических вариантов константных областей антител и их соответствующих замен. pI_(-) обозначает варианты с более низким значением pI, в то время как pI_(+) обозначает варианты с более высоким значением pI. Они могут быть необязательно и независимо объединены с другими вариантами гетеродимеризации по данному изобретению (а также с другими типами вариантов, описанными в данном документе).
На Фигуре 4 изображены подходящие абляционные варианты, которые приводят к устранению связывания FcγR (иногда обозначенные как «нокауты» или варианты «КО»). Как правило, абляционные варианты встречаются на обоих мономерах, хотя в некоторых случаях они могут присутствовать только на одном мономере.
На Фигуре 5 изображены особенно пригодные варианты реализации «нецитокиновых» компонентов по данному изобретению.
На Фигуре 6 изображен ряд примерных доменных линкеров. Согласно некоторым вариантам реализации настоящего изобретения указанные линкеры находят применение в связывании субъединицы IL-12p35, субъединицы IL-12p40 или одноцепочечного комплекса IL-12 с N-концом области Fc. Согласно некоторым вариантам реализации эти линкеры находят применение в слиянии субъединицы IL-12p35 с субъединицей IL-12p40 в одноцепочечном комплексе IL-12. Важно отметить, что комплекс scIL-12 может содержать либо IL-12p35, связанную с N-концом IL-12p40, либо IL-12p40, связанную с N-концом IL-12p35. Также в некоторых случаях, описанных в данном документе, шарнирная часть домена Fc служит в качестве доменного линкера, который также можно комбинировать с любым из этих линкеров.
На Фигуре 7A-7E показаны последовательности нескольких подходящих каркасов IL-12-Fc слитых белков на основе человеческого IgG1, без последовательностей цитокина (например, субъединицы IL-12p35, субъединицы IL-12p40, или комплекса scIL-12). Каркас 1 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S в обеих цепях, искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях. Каркас 2 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S на обеих цепях, искаженные варианты S364K : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях. Каркас 3 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S на обеих цепях, искаженные варианты S364K : L368E/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368E/K370S и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях. Каркас 4 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S на обеих цепях, искаженные варианты D401K : K360E/Q362E/T411E, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами K360E/Q362E/T411E и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях. Каркас 5 основан на человеческом IgG1 (аллотип 356D/358L) и содержит C220S на обеих цепях, искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях. Каркас 6 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S на обеих цепях, искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях, а также вариант N297A на обеих цепях. Каркас 7 идентичен 6, за исключением того, что мутация представляет собой N297S.. Альтернативные форматы каркасов 6 и 7 могут исключать абляционные варианты E233P/L234V/L235A/G236del/S267K в обеих цепях. Каркас 8 основан на человеческом IgG4 и содержит искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S, а также вариант S228P (нумерация ЕС, он представляет собой S241P в Kabat) на обеих цепях, который приводит к устранению обмена фрагментами Fab, как известно в данной области техники. Каркас 9 основан на человеческом IgG2 и содержит искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S. Каркас 10 основан на человеческом IgG2 и содержит искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI Q295E/N384D/Q418E/N421D на цепи с искаженными вариантами L368D/K370S, а также вариант S267K на обеих цепях. Каркас 11 идентичен каркасу 1, за исключением того, что он содержит мутации M428L/N434S Xtend. Каркас 12 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S на обеих идентичных цепях и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих идентичных цепях. Каркас 13 основан на человеческом IgG1 (аллотип 356E/358M) и содержит C220S на обеих цепях, искаженные варианты S364K/E357Q : L368D/K370S, варианты по pI P217R/P229R/N276K на цепи с искаженными вариантами S364K/E357Q и абляционные варианты E233P/L234V/L235A/G236del/S267K на обеих цепях.
Как будет понятно специалистам в данной области техники и описано ниже, эти последовательности можно применять с любыми форматами IL-12-Fc слитых белков, описанными в данном документе, включая, но не ограничиваясь ими, форматы IL-12-heteroFc, heteroFc-IL-12 и scIL-12-Fc, схематически изображенные на Фигуре 8. Следует отметить, что для heteroFc-IL-12 слитых белков, каркасы могут дополнительно содержать делецию K447. Кроме того, любые варианты IL-12p35 и (или) IL-12p40 могут быть включены в каркасы, показанные на Фигуре 7, в любой комбинации.
В каждый из этих каркасов включены последовательности, которые на 90%, 95%, 98% и 99% идентичны (как определено в данном документе) перечисленным последовательностям и (или) содержат от 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 дополнительных аминокислотных замен (по сравнению с «исходной» последовательностью из указанной Фигуры, которая, как будет понятно специалистам в данной области техники, уже содержит ряд аминокислотных модификаций по сравнению с исходным человеческим IgG1 (или IgG2 или IgG4, в зависимости от каркаса). Таким образом, указанные каркасы могут содержать дополнительные аминокислотные модификации (как правило, аминокислотные замены) в дополнение к искаженным вариантам, вариантам по pI и абляционным вариантам, содержащимся в каркасах, представленных на данной фигуре.
На Фигурах 8A-8F изображены иллюстративные форматы IL-12-Fc слитых белков по данному изобретению. N-концевой IL-12 гетеродимерный слитый белок Fc или формат «IL-12-heteroFc» (Фигура 8A) содержит субъединицу IL-12p40, рекомбинантно слитую с N-концом одной стороны гетеродимерного Fc, и субъединицу IL-12p35, рекомбинантно слитую с N-концом другой стороны гетеродимерного Fc. Субъединицы IL-12p35 и IL-12p40 могут быть связаны с их соответствующими цепями Fc с помощью доменного линкера. C-концевой IL-12 гетеродимерный слитый белок Fc или формат «heteroFc-IL-12» (Фигура 8B) содержит субъединицу IL-12p40, рекомбинантно слитую с С-концом одной стороны гетеродимерного Fc, и субъединицу IL-12p35, рекомбинантно слитую с С-концом другой стороны гетеродимерного Fc. Субъединицы IL-12p35 и IL-12p40 могут быть связаны с их соответствующими цепями Fc с помощью доменного линкера. N-концевой одноцепочечный IL-12-Fc слитый белок или формат «scIL-12-Fc» (Фигуры 8C-D) содержит одноцепочечный комплекс IL-12 (или «комплекс scIL-12»), рекомбинантно слитый с N-концом одной стороны гетеродимерного Fc (необязательно за счет доменного линкера), при этом другая сторона молекулы представляет собой гетеродимерный Fc «только Fc» или «пустой Fc». С-концевой одноцепочечный IL-12-Fc слитый белок или формат «Fc-scIL-12» (Фигуры 8E-F) содержит комплекс scIL-12, рекомбинантно слитый с С-концом одной стороны гетеродимерного Fc (необязательно за счет доменного линкера), при этом другая сторона молекулы представляет собой гетеродимерный Fc «только Fc» или «пустой Fc». Комплекс scIL-12 может содержать либо IL-12p35, связанную с N-концом IL-12p40, либо IL-12p40, связанную с N-концом IL-12p35, необязательно, но обычно с помощью доменного линкера. Порядок двух субъединиц в комплексе scIL-12 можно обозначить следующим образом: «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом с субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом субъединицы IL-12p40.
На Фигуре 9 изображены последовательности XENP27201, иллюстративного IL-12-Fc слитого белка формата «IL-12-heteroFc», который содержит последовательности IL-12p40 дикого типа и IL-12p35 дикого типа. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 10 изображены последовательности XENP27202, иллюстративного IL-12-Fc слитого белка формата «heteroFc-IL-12», который содержит последовательности IL-12p40 дикого типа и IL-12p35 дикого типа. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 11 изображены последовательности XENP27203 и XENP27204, иллюстративных IL-12-Fc слитых белков формата «scIL-12-Fc», который содержит последовательности IL-12p40 дикого типа и IL-12p35 дикого типа. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 12A-12B изображена A) хроматограмма, иллюстрирующая часть очистки 2 XENP27201 (анионообменная хроматография после хроматографии с использованием белка A), а также чистота и гомогенность пика B, выделенного при анионообменном разделении, как изображено на Фигуре 12A, по сравнению с пиком A, определенным с помощью B) аналитической эксклюзионной хроматографии с многоугловым светорассеянием (aSEC-MALS) и C) аналитической анионообменной хроматографии (аналитическая AIEX). На Фигуре 12B также изображена молекулярная масса белковых молекул в пиках, определенная с помощью многоуглового светорассеяния.
На Фигуре 13A-13C изображена A) хроматограмма, иллюстрирующая часть очистки 2 XENP27203 (анионообменная хроматография после хроматографии с использованием белка A), а также чистота и гомогенность пика B, выделенного при анионообменном разделении, как изображено на Фигуре 13A, по сравнению с пиком A, определенным с помощью B) аналитической эксклюзионной хроматографии с многоугловым светорассеянием (SEC-MALS) и C) аналитической анионообменной хроматографии. На Фигуре 13B также изображена молекулярная масса белковых молекул в пиках, определенная с помощью многоуглового светорассеяния.
На Фигуре 14A-14B изображены схематические рисунки A) двухвалентного IL-12p40-Fc слитого белка и B) двухвалентного IL-12p35-Fc слитого белка. Каждый слитый белок содержит либо рекомбинантную субъединицу IL-12p40, либо рекомбинантную субъединицу IL-12p35, слитую с N-концом гомодимерного Fc. Субъединицы могут иметь доменный линкер между их соответствующим С-концом и N-концом области Fc.
На Фигуре 15 изображены последовательности XENP27560, двухвалентного IL-12p40-Fc слитого белка, и XENP27561, двухвалентного IL-12p35-Fc слитого белка (схематические рисунки, изображенные на Фигуре 14), который содержит последовательности IL-12p40 дикого типа и IL-12p35 дикого типа. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 16A-16D изображено фосфорилирование STAT4 на A) CD4+CD45RA-CD25hi Т-клетках, B) CD8+CD45RA-CD25hi Т-клетках, C) γδ Т-клетках и D) NK-клетках после инкубации активированных МКПК с указанными тестируемыми изделиями.
На Фигуре 17 изображены остатки на IL-12p40 (на основании последовательности зрелой формы IL-12p40), которые, как прогнозируется, вносят вклад в связывание IL-12p40 с рецепторами IL-12.
На Фигуре 18 изображены остатки аспарагиновой кислоты, глутаминовой кислоты, аспарагина и глутамина на IL-12p40 (на основании последовательности зрелой формы IL-12p40), идентифицированные с помощью пакета QuaSAR в MOE, чтобы получить оценку ASA (доступная для воды площадь поверхности, рассчитанная с использованием радиуса 1,4 Å для молекулы воды и полиэдрического представления для каждого атома) по меньшей мере 19.
На Фигуре 19 изображены остатки на IL-12p40 (на основании последовательности зрелой формы IL-12p40), которые, как прогнозируется, контактируют с рецепторами IL-23 (на основании кристаллической структуры, депонированной в PDB с номером доступа 5MZV), а также предполагаемый (ые) тип (ы) контакта. «D» обозначает контакт, прогнозируемый на основании близости. «H» обозначает контакт, прогнозируемый на основании потенциальной водородной связи. «I» обозначает контакт, прогнозируемый на основании потенциального солевого мостика. «А» обозначает контакт, прогнозируемый на основании потенциального связывания арена.
На Фигуре 20A-20I изображены последовательности иллюстративных вариантов IL-12p40, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12 и (или) удаления предполагаемых сайтов гликозилирования. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 21A-21J изображены аминокислотные последовательности иллюстративных вариантов IL-12p40 с Fc-партнерами по слиянию. Доменные линкеры подчеркнуты двойной линией и варианты IL-12p40 выделены курсивом.
На Фигуре 22 изображены остатки аспарагиновой кислоты, глутаминовой кислоты, аспарагина и глутамина на IL-12p35 (на основании последовательности зрелой формы IL-12p35), идентифицированные с помощью пакета QuaSAR в MOE, чтобы получить оценку ASA (доступная для воды площадь поверхности, рассчитанная с использованием радиуса 1,4 Å для молекулы воды и полиэдрического представления для каждого атома) по меньшей мере 103.
На Фигуре 23A-23C изображены последовательности иллюстративных вариантов IL-12p35, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12 и (или) удаления предполагаемых сайтов гликозилирования. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 24A-24D изображены аминокислотные последовательности иллюстративных вариантов IL-12p35 с Fc-партнерами по слиянию. Доменные линкеры подчеркнуты двойной линией и варианты IL-12p35 выделены курсивом.
На Фигуре 25A-25Q изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, разработанных с целью уменьшения аффинности IL-12-Fc слитых белков в отношении рецепторов IL-12 или удаления предполагаемых сайтов гликозилирования. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 26A-26B изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках и B)CD8+CD45RA+CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками, содержащими варианты IL-12p40, сконструированные с целью уменьшения аффинности и активности.
На Фигуре 27A-27B изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках и B)CD8+CD45RA+CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками, содержащими варианты IL-12p35, сконструированные с целью уменьшения аффинности и активности.
На Фигуре 28 представлены значения EC50 (для фосфорилирования STAT4) как IL-12-Fc слитые белки, содержащие варианты IL-12p40 или IL-12p35, и кратное снижение EC50 относительно WT IL-12-FcXENP27201. 27201-1 и 27201-2 представляют собой две партии XENP27201, полученные по отдельности.
На Фигуре 29A-29B изображены последовательности иллюстративных вариантов IL-12p40, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 30A-30D изображены аминокислотные последовательности иллюстративных вариантов IL-12p40 с Fc-партнером по слиянию. Доменные линкеры подчеркнуты двойной линией, а варианты IL-12p40 выделены курсивом.
На Фигуре 31A-31B изображены последовательности иллюстративных вариантов IL-12p35, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 32A-32C изображены аминокислотные последовательности иллюстративных вариантов IL-12p35 с Fc-партнерами по слиянию. Доменные линкеры подчеркнуты двойной линией, а варианты IL-12p35 выделены курсивом.
На Фигуре 33A-33P изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, разработанных с целью уменьшения аффинности IL-12-Fc слитых белков в отношении рецепторов IL-12. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 34A и 34B изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках и B)CD8+CD45RA+CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками, содержащими варианты IL-12p40, сконструированные с целью уменьшения аффинности и активности.
На Фигуре 35A и 35B изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках и B)CD8+CD45RA+CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками, содержащими варианты IL-12p40 и (или) IL-12p35, сконструированные с целью уменьшения аффинности и активности.
На Фигуре 36 представлены значения EC50 (для фосфорилирования STAT4) IL-12-Fc слитых белков, содержащих варианты IL-12p40 и (или) IL-12p35, и кратное снижение EC50 относительно WT IL-12-FcXENP27201. Данные показывают, что активность была уменьшена до 12 раз под действием IL-12-Fc слитого белка, содержащего только замену E59K в субъединице IL-12p40.
На Фигуре 37A-37B изображены последовательности иллюстративных вариантов IL-12p40, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 38 изображены последовательности иллюстративных вариантов IL-12p35, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 39A-39I изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, разработанных с целью уменьшения аффинности IL-12-Fc слитых белков в отношении рецепторов IL-12. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 40A-40B изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках и B)CD8+CD45RA+CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками, содержащими варианты IL-12p40 и (или) IL-12p35, сконструированные с целью уменьшения аффинности и активности.
На Фигуре 41 изображены значения EC50 (для фосфорилирования STAT4) IL-12-Fc слитых белков, содержащих варианты IL-12p40 и (или) IL-12p35, и кратное снижение EC50 относительно WT IL-12-FcXENP27201. Данные показывают, что активность была уменьшена до 100 раз.
На Фигуре 42A-42B изображены последовательности иллюстративных вариантов IL-12p40, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 43 изображены последовательности иллюстративных вариантов IL-12p35, разработанных с целью уменьшения аффинности гетеродимерного комплекса IL-12 в отношении рецепторов IL-12. Модифицированные аминокислоты подчеркнуты и выделены жирным шрифтом.
На Фигуре 44A-44K изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, разработанных с целью уменьшения аффинности IL-12-Fc слитых белков в отношении рецепторов IL-12. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 45A-45C изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, разработанных с целью уменьшения аффинности IL-12-Fc слитых белков в отношении рецепторов IL-12, дополнительно сконструированных с использованием Xtend Fc(M428L/N434S) для продления периода полужизни. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc. Следует отметить, что эти последовательности представлены для иллюстративных целей и что любая из последовательностей, изображенных на других Фигурах, также может включать Xtend Fc (M428L/N434S) для продления периода полужизни.
На Фигуре 46A-46D изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках, B) CD4+CD45RA-CD25+ Т-клетках, C)CD8+CD45RA+CD25+ Т-клетках и D) CD8+CD45RA-CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками, содержащими варианты IL-12p40 и (или) IL-12p35, сконструированные с целью уменьшения аффинности и активности.
На Фигуре 47 изображены значения EC50 (для фосфорилирования STAT4) IL-12-Fc слитых белков, содержащих варианты IL-12p40 и (или) IL-12p35, и кратное снижение EC50 относительно WT IL-12-FcXENP27201.
На Фигурах 48A-48D изображены иллюстративные форматы двухвалентных IL-12-Fc слитых белков по данному изобретению. Двухвалентный N-концевой одноцепочечный формат (Фигуры 48A-B) содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с N-концом цепи гомодимерного Fc (необязательно за счет доменного линкера). Двухвалентный С-концевой одноцепочечный формат (Фигуры 48C-D) содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с С-концом цепи гомодимерного Fc (необязательно за счет доменного линкера). Комплекс scIL-12 может содержать либо IL-12p35, связанную с N-концом IL-12p40, либо IL-12p40, связанную с N-концом IL-12p35, необязательно с помощью доменного линкера. Порядок двух субъединиц в комплексе scIL-12 может быть обозначен следующим образом: «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35, связана с N-концом субъединицы IL-12p40.
На Фигуре 49 изображены последовательности XENP31289 и XENP31291, иллюстративных IL-12-Fc слитых белков формата (scIL-12(p40/p35))2-Fc. XENP31289 содержит субъединицы IL-12p40 дикого типа и IL-12p35 дикого типа. XENP31291 содержит вариант IL-12p40(E59K/K99E) и субъединицы IL-12p35 дикого типа. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигуре 50 изображены последовательности XENP31290, иллюстративного IL-12-Fc слитого белка формата scIL-12(p40/p35)-Fc, который содержит вариант IL-12p40(E59K/K99E) и субъединицы IL-12p35 дикого типа. Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигурах 51A-51D изображено фосфорилирование STAT4 на A)CD4+CD45RA+CD25+ Т-клетках, B) CD4+CD45RA-CD25+ Т-клетках, C)CD8+CD45RA+CD25+ Т-клетках и D) CD8+CD45RA-CD25+ Т-клетках после инкубации активированных МКПК с IL-12-Fc слитыми белками в форматах scIL-12(p40/p35)-Fc и (scIL-12(p40/p35))2-Fc либо с субъединицами WT IL-12p40, либо вариантными субъединицами IL-12p40(E59K/K99E). Данные показывают, что IL-12-Fc слитые белки в scIL-12(p40/p35)-Fc и (scIL-12(p40/p35))2-Fc слитых белках, содержащих вариантные субъединицы IL-12p40(E59K/K99E), продемонстрировали уменьшенную активность по сравнению с IL-12-Fc слитыми белками, содержащими субъединицы WT IL-12p40.
На Фигуре 52 изображены значения EC50 (для фосфорилирования STAT4) IL-12-Fc слитых белков в форматах scIL-12(p40/p35)-Fc и (scIL-12(p40/p35))2-Fc либо с субъединицами WT IL-12p40, либо с вариантными субъединицами IL-12p40(E59K/K99E).
На Фигуре 53 изображены последовательности XENP16432, МАТ к PD-1 на основе ниволумаба и каркаса IgG1 с абляционным вариантом E233P/L234V/L235A/G236del/S267K.
На Фигурах 54A-54D изображено изменение объема опухоли (определенное с помощью измерений штангенциркулем) на A) День 11, B) День 13 и C) День 15, а также D) с течением времени у мышей NSG, которым приживляли pp65-MCF7 и человеческие МКПК и вводили ФСБ, XENP16432 (двухвалентное МАТ к PD-1) или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)). XENP29952 значительно усилил противоопухолевую активность к Дню 11, на что указывает изменение объема опухоли (статистический анализ выполняли на основе данных, скорректированных относительно исходного уровня, с использованием непарного t-критерия).
На Фигурах 55A-55F изображено количество A)CD45 клеток, B) CD3+ Т-клеток, C) CD4+ Т-клеток, D) CD8+ Т-клеток, E) NK-клеток, а также F) соотношение CD4+ Т-клеток и CD8+ Т-клеток у мышей NSG, которым приживляли pp65-MCF7 и человеческие МКПК, на День 14 после приживления МКПК и введения первой дозы ФСБ, XENP16432 (двухвалентное МАТ к PD-1) или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)). XENP29952 значительно усилил размножение CD45+, CD3+ Т-клеток, CD4+ Т-клеток, CD8+ Т-клеток и NK-клеток к Дню 14 по сравнению как с контрольным ФСБ, так и с блокадой контрольной точки с помощью XENP16432 (статистический анализ выполняли на логарифмически преобразованных данных с использованием непарного t-критерия).
На Фигурах 56A-56D изображены концентрации ИФН-γ в сыворотке на A) День 7 и B) День 14 и концентрации CD25 в сыворотке на C) День 7 и D) День 14 у мышей NSG, которым приживляли pp65-MCF7 и человеческие МКПК, после приживления МКПК и введения первой дозы ФСБ, XENP16432 (двухвалентное МАТ к PD-1), или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)). XENP29952 значительно усилил секрецию ИФН-γ и CD25 к Дню 7 по сравнению с блокадой контрольной точки с помощью XENP16432 (статистический анализ выполняли на логарифмически преобразованных данных с использованием непарного t-критерия).
На Фигурах 57A-57I изображено изменение массы тела (как индикатор РТПХ) к A) Дню 3, B) Дню 6, C) Дню 10, D) Дню 13, E) Дню 17, F) Дню 20, G) Дню 24 и H) Дню 27, а также I) с течением времени у мышей NSG, которым приживляли человеческие МКПК и вводили дозу ФСБ или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)), XENP30597 (IL-12-Fc слитый белок с уменьшенной активностью формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E)), XENP31254 (IL-12-Fc слитый белок с уменьшенной активностью формате IL-12-heteroFc, содержащий вариант IL-12p40(D18K/E59K/K99E)), XENP31251 (IL-12-Fc слитый белок с уменьшенной активностью формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99Y)), или XENP31258 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E/K264E)) при 0,3 или 0,03 мг/кг. Примечательно, что тестируемые изделия IL-12-Fc слитых белков индуцировали различные степени РТПХ, которые коррелировали с их активностью in vitro. Кроме того, данные показывают дозозависимый ответ для тестируемых изделий (т.е. усиление РТПХ при введении 0,3 мг/кг по сравнению с 0,03 мг/кг).
На Фигурах 58A-58C изображена экспрессия PD-1 на CD8+ Т-клетках (как индикатор активации) у мышей NSG с приживленными человеческими МКПК на A) День 7, B) День 10 и C) День 14 после приживления МКПК и введения первой дозы ФСБ или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)), XENP30597 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E)), XENP31254 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(D18K/E59K/K99E)), XENP31251 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99Y)), или XENP31258 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E/K264E)) при 0,3 или 0,03 мг/кг. Примечательно, что тестируемые изделия IL-12-Fc слитых белков индуцировали различные степени активации CD8+ Т-клеток, которые коррелировали с их активностью in vitro. Кроме того, данные показывают дозозависимый ответ для тестируемых изделий (т. е. усиленную активацию CD8+ Т-клеток при введении 0,3 мг/кг по сравнению с 0,03 мг/кг).
На Фигурах 59A-59C изображена экспрессия PD-1 на CD4+ Т-клетках (как индикатор активации) у мышей NSG с приживленными человеческими МКПК на A) День 7, B) День 10 и C) День 14 после приживления МКПК и введения первой дозы ФСБ или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)), XENP30597 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E)), XENP31254 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(D18K/E59K/K99E)), XENP31251 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99Y)), или XENP31258 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E/K264E)) при 0,3 или 0,03 мг/кг. Примечательно, что тестируемые изделия IL-12-Fc слитых белков индуцировали различные степени активации CD4+ Т-клеток, которые коррелировали с их активностью in vitro. Кроме того, данные показывают дозозависимый ответ для тестируемых изделий (т.е. усиленную активацию CD4+ Т-клеток при введении 0,3 мг/кг по сравнению с 0,03 мг/кг).
На Фигурах 60A-60D изображена концентрация ИФН-γ в сыворотке крови у мышей NSG с приживленными человеческими МКПК в Дни A) 7, B) 10, C) 14 и D) 31 после приживления МКПК и введения первой дозы ФСБ или XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)), XENP30597 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E)), XENP31254 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(D18K/E59K/K99E)), XENP31251 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99Y)), или XENP31258 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E/K264E)) при 0,3 или 0,03 мг/кг. Примечательно, что тестируемые изделия IL-12-Fc слитых белков индуцировали различные уровни секреции ИФН-γ, которые коррелировали с их активностью in vitro. Кроме того, данные показывают дозозависимый ответ тестируемых изделий (т. е. усиленную секрецию ИФН-γ, индуцированную при введении 0,3 мг/кг по сравнению с 0,03 мг/кг).
На Фигурах 61A-61K изображено фосфорилирование STAT4 на A) CD4+CD45RA-CD25+ Т-клетках, B)CD4+CD45RA+CD25+ Т-клетках, C) CD4+CD45RA+CD25- Т-клетках, D) CD4+CD45RA-CD25- Т-клетках, E) CD8+CD45RA-CD25+ Т-клетках, F)CD8+CD45RA+CD25+ Т-клетках, G) CD8+CD45RA+CD25- Т-клетках, H) CD8+CD45RA-CD25- Т-клетках, I) Treg, J) γδ T-клетках и K) CD56+ NK-клетках после инкубации активированных МКПК (от первого донора; донор 1) с рекомбинантным человеческим IL-12, XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)), XENP30597 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E)), XENP31254 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(D18K/E59K/K99E)), XENP31251 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99Y)), или XENP31258 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E/K264E)). Данные показывают ступенчатое изменение активности, при этом XENP29952 является наиболее активным вариантом, XENP31254 и XENP31258 являются наименее активными вариантами и XENP30597 и XENP31251 расположены между ними. Примечательно, что степень РТПХ и активации Т-клеток, индуцированная вариантами IL-12-Fc слитых белков с уменьшенной активностью in vivo, коррелировала с активностью in vitro.
На Фигурах 62A-62D изображено изменение объема опухоли (определенное с помощью измерений штангенциркулем) на A) День 14, B) День 16 и C) День 21, а также D) с течением времени у мышей NSG, которым приживляли pp65-MCF7 и человеческие МКПК и вводили ФСБ, XENP16432 (двухвалентное МАТ к PD-1), XENP31258, XENP31251, или комбинацию XENP31251 и XENP16432. XENP31258 значительно усилило противоопухолевую активность к Дню 14, XENP31251 (по отдельности или в комбинации с XENP16432) значительно усилило противоопухолевую активность к Дню 16 по сравнению с лечением ФСБ; и XENP31251 в комбинации с XENP16432 значительно усилило противоопухолевую активность к Дню 21 по сравнению с лечением XENP16432 по отдельности (статистический анализ выполняли на основании данных, скорректированных относительно исходного уровня, с использованием критерия Манна-Уитни).
На Фигурах 63A-63F изображено количество A)CD45 клеток, B) CD3+ Т-клеток, C) CD4+ Т-клеток, D) CD8+ Т-клеток, E) NK-клеток, а также F) соотношение CD8+ Т-клеток и CD4+ Т-клеток у мышей NSG с приживленными pp65-MCF7 и человеческими МКПК на День 14 после приживления МКПК и введения первой дозы ФСБ, XENP16432 (двухвалентное МАТ к PD-1), XENP31258, XENP31251 или комбинации XENP31251 и XENP16432. Примечательно, что данные показывают, что лечение XENP31251 в комбинации с XENP16432 значительно усилило размножение лимфоцитов по сравнению как с XENP31251, так и с XENP16432 по отдельности, это свидетельствует о том, что IL-12-Fc слитые белки эффективно комбинируются с блокадой контрольной точки.
На Фигурах 64A-64C изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, разработанных с целью уменьшения аффинности IL-12-Fc слитых белков в отношении рецепторов IL-12, дополнительно сконструированных с применением Xtend Fc(M428L/N434S) для продления периода полужизни. Линкеры подчеркнуты двойной чертой (хотя специалистам в данной области техники будет понятно, что указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc. Следует отметить, что эти последовательности представлены для иллюстративных целей и что любая из последовательностей, изображенных на других Фигурах, также может включать Xtend Fc (M428L/N434S) для продления периода полужизни.
На Фигурах 65A-C изображены последовательности иллюстративных вариантов IL-12p40, сконструированных с применением C252S с целью удаления свободного цистеина (в дополнение к вариантам по экспрессии и аффинности/активности).
На Фигурах 66A-66Q изображены последовательности иллюстративных вариантов IL-12-Fc слитых белков, сконструированных с применением C252S в субъединице IL-12p40 с целью удаления свободного цистеина (в дополнение к вариантам по экспрессии и аффинности/активности). Линкеры подчеркнуты двойной линией (хотя, как будет понятно специалистам в данной области техники, указанные линкеры могут быть заменены другими линкерами, некоторые из которых изображены на Фигуре 6), а косые черты (/) обозначают границу (границы) между IL-12p35, IL-12p40, линкерами и областями Fc.
На Фигурах 67A-67D изображено фосфорилирование STAT4 на A) CD8+CD45RA-CD25+ Т-клетках, B)CD8+CD45RA+CD25+ Т, C) CD4+CD45RA-CD25+ Т, D)CD4+CD45RA+CD25+ T и E) NK-клетках после инкубации активированных МКПК с IL-12-Fc, содержащими варианты IL-12p40 с дополнительной модификацией для удаления свободного цистеина или без нее. Данные показывают, что большинство вариантов, содержащих C252S в субъединице IL-12p40, продемонстрировали сходную, хотя и незначительно улучшенную, активность по сравнению с вариантами без модификации C252S
Подробное описание изобретения
I. Обзор
Настоящее изобретение направлено на новые конструкции гетеродимерных слитых белков, содержащие субъединицы IL-12 и домены Fc. Как указано выше, IL-12 состоит из α-цепи (субъединица p35; IL-12p35) и β-цепи (субъединица p40; IL-12p40), ковалентно связанных с образованием биологически активного гетеродимера IL-12. IL-12 осуществляет свою сигнальную функцию в клетках посредством связывания путем связывания с димерным рецепторным комплексом IL-12, состоящим из β1 рецептора IL-12 (IL-12Rβ1) и β2 рецептора IL-12 (IL-12Rβ2) на Т-клетках, и индукции секреции ИФН-γ. Однако субъединица IL-12p40 также может существовать в виде гомодимера, который, как сообщается, оказывает антагонистическое действие на активность IL-12 путем конкуренции за связывание с рецептором IL-12. Соответственно, настоящее изобретение относится к короткому периоду полужизни IL-12 и потенциальному образованию антагонистических гомодимеров IL12p40 с помощью обеспечения IL-12-Fc слитых белков, а также новых вариантов IL-12 со сниженной активностью. Как показано в общих чертах на Фигуре 8, гетеродимерные слитые белки по данному изобретению могут принимать различные конформации.
Настоящая заявка включает посредством ссылки 62/740813, поданную 3 октября 2018 г., и 62/828512, поданную 15 мая 2019 г., более конкретно, в отношении Фигуры 17 в 62/740813 и Фигур 62A-62K и Фигур 63A-63D в 62/828512, а также подписей к Фигурам и упоминания этих фигур в соответствующем описании.
II. Определения
С целью более полного понимания данной заявки, ниже приведены несколько определений. Такие определения предназначены для охвата грамматических эквивалентов.
Под термином «абляция» в данном документе подразумевается снижение или устранение способности к связыванию и (или) активности. Так, например, «абляция связывания FcγR» означает, что аминокислотный вариант области Fc характеризуется менее чем 50% начального связывания по сравнению с областью Fc, не содержащей специфического варианта, с потерей менее чем 70%, менее чем 80%, менее чем 90%, менее чем 95%, менее чем 98% способности к связыванию, что является предпочтительным, и, как правило, со способностью к связыванию, которая ниже уровня детектируемого связывания в анализе Biacore. Особенно применимыми при устранении связывания FcγR являются те, которые показаны на Фигуре 4. Однако, если не указано иное, мономеры Fc согласно данному изобретению сохраняют способность к связыванию с FcRn.
Под термином «АЗКЦ» (англ. «ADCC»), или «антителозависимая клеточно-опосредованная цитотоксичность», используемым в данном документе, подразумевается клеточно-опосредованная реакция, при которой неспецифические цитотоксические клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и впоследствии вызывают лизис этой клетки-мишени. АЗКЦ коррелирует со связыванием области Fc с FcγRIIIa; усиление связывания с FcγRIIIa приводит к увеличению в активности АЗКЦ. Как обсуждается в данном документе, многие варианты реализации данного изобретения приводят к полному устранению активности АЗКЦ.
Под термином «модификация», используемым в данном документе, подразумевается аминокислотная замена, вставка и (или) делеция в полипептидной последовательности или изменение фрагмента, химически связанного с белком. Например, модификация может представлять собой измененную углеводную или ПЭГ-структуру, присоединенную к белку. Под термином «аминокислотная модификация», используемым в данном документе, подразумевается аминокислотная замена, вставка и (или) делеция в полипептидной последовательности. Для ясности, если не указано иное, аминокислотная модификация всегда относится к аминокислоте, кодируемой ДНК, например, к 20 аминокислотам, которые имеют кодоны в ДНК и РНК.
Под термином «аминокислотная замена» или «замена», используемым в данном документе, подразумевается замена аминокислоты в конкретном положении в исходной полипептидной последовательности другой аминокислотой. В частности, в некоторых вариантах реализации, замена представляет собой аминокислоту, которая не встречается в природе в конкретной позиции, либо не встречается в природе в организме, либо в любом организме. Например, замена E272Y или 272Y относится к вариантному полипептиду, в данном случае к варианту Fc, в котором глутаминовая кислота в положении 272 заменена тирозином. Для ясности, белок, который был модифицирован для изменения кодирующей последовательности нуклеиновой кислоты, но не для изменения исходной аминокислоты (например, обмен CGG (кодирующего аргинин) на CGA (все еще кодирующего аргинин) для повышения уровня экспрессии в организме хозяинa), не является «аминокислотной заменой»; то есть, несмотря на создание нового гена, кодирующего тот же белок, если белок имеет ту же аминокислоту в конкретном положении, с которой он был первоначально, это не является аминокислотной заменой.
Под термином «вставка аминокислоты» или «вставка», используемым в данном документ, подразумевается добавление аминокислотного остатка или аминокислотной последовательности в конкретном положении в последовательности родительского полипептида. Например, -233E обозначает вставку глутаминовой кислоты после положения 233 и перед положением 234. Кроме того, -233ADE или A233ADE обозначает вставку AlaAspGlu после положения 233 и перед положением 234.
Под термином «делеция аминокислоты» или «делеция», используемым в данном документе, подразумевается удаление аминокислотного остатка или аминокислотной последовательности в конкретном положении в последовательности родительского полипептида. Например, E233- или E233#, E233() или E233del обозначает делецию глутаминовой кислоты в положении 233. Кроме того, EDA233- или EDA233# обозначает делецию последовательности GluAspAla, которая начинается в положении 233.
Под термином «вариантный белок» или «вариант белка», или «вариант», используемым в данном документе, подразумевается белок, который отличается от исходного белка по меньшей мере одной модификацией. Вариант белка может относиться к самому белку, композиции, содержащей указанный белок, к аминокислотной последовательности, которая его кодирует, или последовательности ДНК, которая его кодирует. Предпочтительно, вариант белка имеет по меньшей мере одну аминокислотную модификацию по сравнению с исходным белком, например, от около одной до около семидесяти аминокислотных модификаций и предпочтительно от около одной до около пяти аминокислотных модификаций по сравнению с родительским белком. Модификация может представлять собой добавление, делецию или замену. Как описано ниже, в некоторых вариантах реализации исходный полипептид, например, исходный полипептид Fc, представляет собой человеческую последовательность дикого типа, такую как область Fc из IgG1, IgG2, IgG3 или IgG4. Вариант последовательности белка в данном документе предпочтительно будет обладать по меньшей мере около 80% идентичностью с последовательностью исходного белка и наиболее предпочтительно по меньшей мере около 90% идентичностью, более предпочтительно по меньшей мере около 95-98-99% идентичностью.
Под термином «белок», используемым в данном документе, подразумевается по меньшей мере две ковалентно связанные аминокислоты, при этом указанный термин включает белки, полипептиды, олигопептиды и пептиды. В тех случаях, когда биологически функциональное звено содержит два или более белков, каждый белок может называться «мономером» или «субъединицей», или «доменом»; а биологически функциональная молекула может называться «комплексом».
Под термином «белок», используемым в данном документе, подразумевается по меньшей мере две ковалентно соединенные аминокислоты, при этом указанный термин включает белки, полипептиды, олигопептиды и пептиды. В тех случаях, когда биологически функциональная молекула или комплекс содержит два или более белков, каждый белок может называться «мономером» или «субъединицей», или «доменом»; а биологически функциональная молекула может называться «комплексом». Согласно некоторым вариантам реализации два или более белков функционального комплекса присоединены нековалентно. Согласно некоторым вариантам реализации термин «мономер» относится к полипептиду или белку, содержащему один или более компонентов, фрагментов или субъединиц белка (белков), при этом компоненты, фрагменты или субъединицы присоединены ковалентно.
Под термином «остаток», используемым в данном документе, подразумевается положение в белке и ассоциированная с ним идентичность аминокислот. Например, аспарагин 297 (также называемый Asn297 или N297) представляет собой остаток в положении 297 человеческого антитела IgG1.
Под термином «модификация подкласса IgG» или «модификация изотипа», в контексте данного документа, подразумевается аминокислотная модификация, которая превращает одну аминокислоту из одного изотипа IgG в соответствующую аминокислоту в другом, сопоставленном изотипе IgG. Например, поскольку IgG1 содержит тирозин и IgG2 содержит фенилаланин в положении 296 ЕС, замена F296Y в IgG2 считается модификацией подкласса IgG.
Карбоксиконцевая часть каждой цепи IgG определяет константную область, в первую очередь ответственную за эффекторную функцию. Kabat et al. собрали многочисленные первичные последовательности вариабельных областей тяжелых цепей и легких цепей. На основании степени консервативности последовательностей, они классифицировали отдельные первичные последовательности на последовательности CDR и последовательности каркаса, а также составили их перечень (см. SEQUENCES OF IMMUNOLOGICAL INTEREST, 5th edition, NIH publication, No. 91 - 3242, E.A. Kabat et al.; данная публикация включена в данный документ посредством ссылки в полном объеме). В данном описании система нумерации по Кабату обычно применяется для обозначения остатка в вариабельном домене (приблизительно, остатки 1 - 107 вариабельной области легкой цепи и остатки 1 - 113 вариабельной области тяжелой цепи), а система нумерации ЕС применяется для областей Fc (например, Kabat et al., выше (1991)).
В подклассе иммуноглобулинов IgG имеется несколько доменов иммуноглобулинов в тяжелой цепи. Под термином «домен иммуноглобулина (Ig)», используемым в контексте данного документа, подразумевается область иммуноглобулина, имеющая отчетливую третичную структуру. В данном изобретении представляют интерес домены тяжелой цепи, включая константные домены тяжелой цепи (СН) и шарнирные домены. В контексте антител IgG каждый изотип IgG имеет три области СН. Соответственно, «CH» домены применительно к IgG являются следующими: «CH1» относится к положениям 118 - 215 в соответствии с индексом ЕС, как по Кабату. «Шарнир» относится к положениям 216 - 230 в соответствии с индексом ЕС, как по Кабату. «CH2» относится к положениям 231 - 340 в соответствии с индексом ЕС, как по Кабату, а «CH3» относится к положениям 341 - 447 в соответствии с индексом ЕС, как по Кабату. Как показано в Таблице 1, точная нумерация и размещение доменов тяжелой цепи могут отличаться в разных системах нумерации. Как продемонстрировано в данном документе и описано ниже, варианты по pI могут находиться в одной или большем количестве областей СН, а также в шарнирной области, обсуждаемой ниже.
Другим типом домена Ig тяжелой цепи является шарнирная область. Под термином «шарнир», или «шарнирная область», или «шарнирная область антитела», или «шарнирная область иммуноглобулина», используемым в контексте данного документа, подразумевается гибкий полипептид, содержащий аминокислоты между первым и вторым константными доменами тяжелой цепи антитела. Структурно домен CH1 IgG заканчивается в положении 215 ЕС, а домен CH2 IgG начинается в положении остатка 231 ЕС. Таким образом, для IgG шарнир антитела в данном документе определен как включающий положения с 216 (E216 в IgG1) по 230 (P230 в IgG1), при этом нумерация соответствует индексу ЕС, как по Кабату. В некоторые варианты реализации данного изобретения, например, применительно к фрагменту Fc, включен шарнир, что обычно относится к положениям 216 - 230. Как отмечено в данном документе, варианты по pI также могут быть созданы в шарнирной области.
Под термином «не встречающаяся в природе модификация», используемым в контексте данного документа, подразумевается аминокислотная модификация, которая не является изотипической. Например, поскольку ни один из IgG не содержит серин в положении 434, замена 434S в IgG1, IgG2, IgG3 или IgG4 (или в их гибридах) считается не встречающейся в природе модификацией.
Под термином «аминокислота» и «идентичность аминокислоты», используемым в контексте данного документа, подразумевается одна из 20 встречающихся в природе аминокислот, которые кодируются ДНК и РНК.
Под термином «эффекторная функция», используемым в контексте данного документа, подразумевается биохимическое явление, которое возникает в результате взаимодействия области Fc антитела с рецептором Fc или лигандом Fc. Эффекторные функции включают в себя АЗКЦ, АЗКФ и КЗЦ, но не ограничиваются лишь ими.
Под термином «лиганд Fc IgG», или «лиганд Fc», используемым в контексте данного документа, подразумевается молекула, предпочтительно полипептид, из любого организма, которая связывается с областью Fc антитела IgG с образованием комплекса Fc/Fc - лиганд. Лиганды Fc включают, но не ограничиваются ими: FcγRI, FcγRII, FcγRIII, FcRn, C1q, C3, связывающий маннан лектин, рецептор маннозы, стафилококковый белок A, стрептококковый белок G и вирусный FcγR. Лиганды Fc также включают в себя гомологи рецепторов Fc (FcRH), представляющих собой семейство рецепторов Fc, которые являются гомологичными с FcγR (Davis et al., 2002, Immunological Reviews 190:123-136; включен посредством ссылки в полном объеме). Лиганды Fc могут включать в себя неизвестные молекулы, которые связывают Fc. Конкретными лигандами Fc IgG являются FcRn и Fc гамма рецепторы.
Под термином «Fc гамма рецептор», «FcγR» или «Fc гамма Р», используемым в контексте данного документа, подразумевается любой представитель семейства белков, который связывает область Fc антитела IgG и кодируется геном FcγR. У человека это семейство включает, но не ограничивается ими: FcγRI (CD64), включая изоформы FcγRIa, FcγRIb и FcγRIc; FcγRII (CD32), включая изоформы FcγRIIa (включая аллотипы H131 и R131), FcγRIIb (включая FcγRIIb-1 и FcγRIIb-2) и FcγRIIc; и FcγRIII (CD16), включая изоформы FcγRIIIa (включая аллотипы V158 и F158) и FcγRIIIb (включая аллотипы FcγRIIIb-NA1 и FcγRIIIb-NA2) (Jefferis et al., 2002, Immunol Lett 82: 57 - 65; данная публикация полностью включена в данный документ посредством ссылки), а также любые неизвестные FcγR или изоформы или аллотипы FcγR человека. FcγR может происходить из любого организма, включая, но не ограничиваясь лишь этими: организма людей, мышей, крыс, кроликов и обезьян. FcγR мыши включают, но не ограничиваются ими: FcγRI (CD64), FcγRII (CD32), FcγRIII (CD16) и FcγRIII-2 (CD16-2), а также любые неизвестные FcγR или изоформы или аллотипы FcγR мыши.
Под термином «FcRn» или «неонатальный рецептор Fc», используемым в контексте данного документа, подразумевается белок, который связывает область Fc антитела IgG и кодируется, по меньшей мере, отчасти, геном FcRn. FcRn может происходить из любого организма, включая, но не ограничиваясь ими, людей, мышей, крыс, кроликов и обезьян. Как известно в данной области техники, функциональный белок FcRn содержит два полипептида, часто обозначаемых как тяжелая цепь и легкая цепь. Легкая цепь представляет собой бета-2-микроглобулин (β2-микроглобулин), а тяжелая цепь кодируется геном FcRn. Если в данном документе не указано иное, FcRn или белок FcRn относится к комплексу тяжелой цепи FcRn с β2-микроглобулином. Для усиления связывания с FcRn и, в некоторых случаях, для увеличения периода полужизни в сыворотке, могут использоваться различные варианты Fc. В общем, если не указано иное, мономеры Fc согласно данному изобретению сохраняют способность к связыванию с FcRn (и, как указано ниже, могут включать варианты аминокислот для усиления связывания с FcRn).
Под термином «исходный полипептид», используемым в контексте данного документа, подразумевается исходный полипептид, который впоследствии модифицируют для получения варианта. Исходный полипептид может представлять собой встречающийся в природе полипептид или вариант, или сконструированный вариант встречающегося в природе полипептида. Исходный полипептид может относиться к самому полипептиду, композициям, которые содержат исходный полипептид, или к аминокислотной последовательности, которая его кодирует.
Под термином «Fc», «область Fc» или «домен Fc», используемым в контексте данного документа, подразумевается полипептид, содержащий константную область антитела, в некоторых случаях за исключением всего первого иммуноглобулинового домена константной области (например, CH1) или его части, а в некоторых случаях необязательно включая весь шарнир или его часть. В случае IgG домен Fc содержит иммуноглобулиновые домены CH2 и CH3 (Cγ2 и Cγ3) и необязательно всю шарнирную область между CH1 (Cγ1) и CH2 (Cγ2) или ее часть. Таким образом, в некоторых случаях, домен Fc содержит, от N- к C-концу, CH2-CH3 и шарнир-СН2-CH3. Согласно некоторым вариантам реализации домен Fc происходит из IgG1, IgG2, IgG3 или IgG4, при этом шарнир IgG1-CH2-CH3 и шарнир IgG4-CH2-CH3 находят особое применение во многих вариантах реализации. Кроме того, в случае доменов Fc человеческого IgG1 шарнир часто включает аминокислотную замену C220S. Кроме того, в случае доменов Fc человеческого IgG4 шарнир часто включает аминокислотную замену S228P. Несмотря на то, что границы области Fc могут варьироваться, область Fc тяжелой цепи человеческого IgG обычно определяется как включающая остатки E216, C226 или A231 на ее карбоксильном конце, при этом нумерация соответствует индексу ЕС как по Кабату. Согласно некоторым вариантам реализации настоящего изобретения, что более полно описано ниже, модификации аминокислот осуществляются в области Fc, например, для изменения связывания с одним или большим количеством рецепторов FcγR или с рецептором FcRn.
Как будет понятно специалистам в данной области техники, точная нумерация и размещение доменов тяжелых константных областей могут отличаться в разных системах нумерации. Полезное сравнение нумерации тяжелых константных областей в соответствии с EU и по Кабату приведено ниже, см. Edelman et al., 1969, Proc Natl Acad Sci USA 63: 78 - 85 и Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda, которые включены в данный документ посредством ссылки в полном объеме.
В контексте данного документа под термином «Fc-вариант» или «вариант по Fc» подразумевается белок, содержащий аминокислотную модификацию в домене Fc. Модификация может заключаться в добавлении, удалении или замене. Варианты Fc согласно данному изобретению определены в соответствии с аминокислотными модификациями, которые их составляют. Таким образом, например, N434S или 434S представляет собой вариант Fc с заменой серином в положении 434 относительно исходного полипептида Fc, при этом нумерация соответствует индексу ЕС. Аналогичным образом, M428L/N434S определяет вариант Fc с заменами M428L и N434S относительно исходного полипептида Fc. Идентичность аминокислоты ДТ может быть неопределенной и в этом случае вышеупомянутый вариант обозначается как 428L/434S. Следует отметить, что порядок, в котором представлены замены, является произвольным, т. е., к примеру, 428L/434S представляет собой тот же самый вариант по Fc, что и 434S/428L и т. д. Для всех положений, обсуждаемых в данном изобретении, которые относятся к антителам или их производным и фрагментам, если не указано иное, нумерация аминокислотных положений соответствует индексу ЕС. Индекс EU или EU-индекс, как по Кабату или схема нумерации EU, относится к нумерации антител EU (Edelman et al., 1969, Proc Natl Acad Sci USA 63: 78-85, что включено в данный документ посредством ссылки в полном объеме). Модификация может представлять собой добавление, делецию или замену.
Под термином «слитый белок», используемым в контексте данного документа, подразумевается ковалентное соединение по меньшей мере двух белков или белковых доменов. Слитые белки могут содержать искусственные последовательности, например, доменный линкер, домены вариантов Fc, домен вариантной субъединицы IL-12p40, домен вариантной субъединицы IL-12p35 и т.д., как описано в данном документе. Под термином «слитый белок Fc», или «иммуноадгезин», используемым в контексте данного документа, подразумевается белок, содержащий область Fc, обычно связанную (необязательно посредством доменного линкера, как описано в данном документе) с одним или более различными белковыми доменами. Соответственно, «IL-12-Fc слитый белок» содержит область Fc, связанную (необязательно, но обычно посредством доменного линкера) с субъединицей IL-12p40, субъединицей IL12p35 и (или) одноцепочечным комплексом IL-12 (scIL-12), как описано в данном документе. В некоторых случаях два слитых белка Fc могут образовывать гомодимерный слитый белок Fc или гетеродимерный слитый белок Fc, причем последний является предпочтительным в некоторых случаях. В некоторых случаях один мономер гетеродимерного слитого белка Fc содержит только домен Fc (например, «пустой домен Fc»), а другой мономер представляет собой слитый белок Fc, содержащий домен варианта Fc и один или два домена субъединицы IL-12, как описано в данном документе.
Под термином «положение», используемым в контексте данного документа, подразумевается местоположение в последовательности белка. Положения могут быть пронумерованы последовательно или в соответствии с установленным форматом, например, индексом EU для нумерации антител.
Под «наличием цепей» в контексте мономеров гетеродимерных белков согласно данному изобретению в данном документе подразумевается, что, подобно двум цепям ДНК, которые «совпадают», гетеродимеризационные варианты включены в каждый мономер с целью сохранения, создания и (или) усиления способности «совпадать» с образованием гетеродимеров. Например, если некоторые варианты по pI сконструированы в мономер A (например, повышая параметр pI), тогда стерические варианты, которые представляют собой «пары зарядов», которые также могут использоваться, не влияют на варианты по pI, например, варианты зарядов, которые повышают параметр pI, помещают на одну и ту же «цепь» или «мономер» с тем, чтобы сохранить обе функциональные возможности. Аналогично, для «искаженных» вариантов, которые входят в пары совокупности, как более подробно изложено ниже, специалист в данной области техники будет учитывать pI при принятии решения, в какую цепь или мономер, которые включают одну совокупность пары, направляться с тем, чтобы сделать разделение по pI максимальным также с использованием рI искаженных вариантов.
Под термином «дикий тип», или «ДТ», используемым в контексте данного документа, подразумевается аминокислотная последовательность или нуклеотидная последовательность, которая встречается в природе, включая аллельные вариации. Белок ДТ имеет аминокислотную последовательность или нуклеотидную последовательность, которая не была намеренно модифицирована.
Гетеродимерные белки согласно данному изобретению обычно являются выделенными или рекомбинантными. Термин «выделенный», при применении его для описания различных полипептидов, раскрытых в данном документе, означает полипептид, который был идентифицирован и отделен и (или) извлечен из клетки или клеточной культуры, из которой он был экспрессирован. Обычно выделенный полипептид будет получен по меньшей мере в результате одного этапа очистки. «Выделенный белок» относится к белку, который по существу не содержит других белков из клеточной культуры, например, таких как белки клетки-хозяина. Термин «рекомбинантный», используемый в контексте данного документа, означает, что белки получают с помощью методик рекомбинантных нуклеиновых кислот в экзогенных клетках-хозяевах.
«Процент (%) идентичности аминокислотной последовательности» по отношению к последовательности белка определяется в виде процента аминокислотных остатков в кандидатной последовательности, которые идентичны аминокислотным остаткам в конкретной (исходной) последовательности после выравнивания последовательностей и введения гэпов, при необходимости, для достижения максимального процента идентичности последовательности и без учета каких-либо консервативных замен в виде части идентичности последовательности. Выравнивание в целях определения процента идентичности аминокислотной последовательности может быть достигнуто различными способами, которые известны специалисту в данной области техники, например, с использованием общедоступного компьютерного программного обеспечения, такого как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить соответствующие параметры для измерения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине последовательностей, которые подлежат сравнению. Одной из конкретных программ является программа ALIGN-2, описанная в параграфах с [0279] по [0280] публикации США № 20160244525, включенной в данный документе посредством ссылки.
Степень идентичности между аминокислотной последовательностью согласно данному изобретению («последовательность согласно данному изобретению») и исходной аминокислотной последовательностью рассчитывают в виде количества точных совпадений в выравнивании двух последовательностей, деленное на длину «последовательности согласно данному изобретению» или длину исходной последовательности, в зависимости от того, какая из них является самой короткой. Полученный результат выражается в проценте идентичности.
Согласно некоторым вариантам реализации настоящего изобретения две или более аминокислотных последовательности являются, по меньшей мере, на 50%, на 60%, на 70%, на 80% или на 90% идентичными. Согласно некоторым вариантам реализации настоящего изобретения две или более аминокислотных последовательности являются, по меньшей мере, на 95%, на 97%, на 98%, на 99% или даже на 100% идентичными.
Под «доменом субъединицы IL-12p40» в данном документе подразумевают β-цепь (субъединица p40; IL-12p40). Как обсуждалось в данном документе, домен субъединицы IL-12p40 может представлять собой человеческую последовательность дикого типа (например, SEQ ID NO: XX из Фигуры 1) или ее вариант, как более подробно обсуждается ниже (например, см. Фигуры 20, 23 и 29, например).
Под «доменом субъединицы IL-12p35» в данном документе подразумевают α-цепь (субъединица p35; IL-12p35). Как обсуждалось в данном документе, домен субъединицы IL-12p35 может представлять собой человеческую последовательность дикого типа (например, SEQ ID NO: XX из Фигуры 1) или ее вариант, как более подробно обсуждается ниже (например, см. Фигуры 20, 23 и 29, например).
Домены субъединицы IL-12 по данному изобретению, когда они ассоциированы друг с другом, специфично связываются с димерным рецепторным комплексом IL-12, содержащим β1 рецептора IL-12 и β2 рецептора IL-12. Сила, или аффинность, специфического связывания может быть выражена в виде показателя константы диссоциации (KD) взаимодействия, при этом меньшая KD обозначает более высокую аффинность, а большая KD обозначает более низкую аффинность. Связывающие свойства могут быть определены с помощью методов, хорошо известных в данной области техники, таких как интерферометрия биослоя и методы на основе поверхностного плазмонного резонанса, включая методологии Biacore и Octet. Один из таких методов содержит измерение скоростей ассоциации и диссоциации комплекса антигенсвязывающий сайт - антиген или рецептор - лиганд, при этом скорости зависят от концентрации компонентов комплекса, аффинности взаимодействия и геометрических параметров, которые в равной степени влияют на скорость протекания взаимодействия в обоих направлениях. Таким образом, можно определить как скорость ассоциации (ka), так и скорость диссоциации (kd), а отношение kd/ka равно константе диссоциации KD (см., например, Nature 361:186-187 (1993) и Davies et al. (1990) Annual Rev Biochem 59:439-473), обе из которых полностью включены в данный документ посредством ссылки в отношении методов в них.
Специфичное связывание для конкретной молекулы может проявляться, например, в том, что молекула имеет показатель KD в отношении лиганда (обычно рецептора, в данном случае), составляющий по меньшей мере около 10-4 М, по меньшей мере около 10-5 М, по меньшей мере около 10-6 М, по меньшей мере около 10-7 М, по меньшей мере около 10-8 М, по меньшей мере около 10-9 М, в качестве альтернативного варианта, по меньшей мере около 10-10 М, по меньшей мере около 10-11 М, по меньшей мере около 10-12 М или выше. Как правило, молекула, которая специфично связывает ее рецептор, будет иметь значение KD, которое в 20, 50, 100, 500, 1000, 5000, 10000 или более раз выше в отношении рецептора относительно контрольной молекулы.
Кроме того, специфичное связывание для конкретной молекулы может проявляться, например, в том, что молекула имеет ka или скорость ассоциации в отношении лиганда или рецептора, которая в 20, 50, 100, 500, 1000, 5000, 10000 или более раз выше в отношении рецептора по сравнению с контролем.
Под термином «слитый» или «ковалентно связанный», используемым в контексте данного документа, подразумевается, что компоненты (например, субъединица IL-12 и домен Fc) связаны пептидными связями либо напрямую, либо опосредовано за счет доменных линкеров, описанных в данном документе.
Термин «одноцепочечная», используемый в контексте данного документа, относится к молекуле, содержащей аминокислотные домены, линейно связанные пептидными связями. Согласно определенным вариантам реализации биологически функциональный IL-12 представляет собой одноцепочечный комплекс IL-12 или «scIL-12», т.е. субъединица IL-12p35 и субъединица IL-12p40 слиты с образованием одной пептидной цепи. Согласно такому конкретному варианту реализации C-конец субъединицы IL-12p35 соединен с N-концом субъединицы IL-12p40, обозначено «scIL-12(p35/p40)». Согласно другому такому конкретному варианту реализации C-конец субъединицы IL-12p40 соединен с N-концом субъединицы IL-12p35, обозначено «scIL-12(p40/p35)». Кроме того, если эти комплексы дополнительно слиты с доменом Fc, они все еще остаются «одной цепью». Следует отметить, что эти одноцепочечные конструкции, в которых субъединицы p35 и p40 находятся на одной и той же аминокислотной цепи, все еще являются частью гетеродимерного комплекса, содержащего две аминокислотные цепи (например, как показано на Фигуре 8C и 8D, компонент scIL-12(p35/p40) и компонент «пустое плечо» Fc). Иными словами, имеются две отдельные цепи, которые составляют гетеродимерный комплекс.
Слитые белки по данному изобретению могут принимать различные форматы, включая гетеродимерные форматы, такие как те, которые изображены на Фигуре 8, а также гомодимерные форматы, такие как те, которые изображены на Фигуре 14 и Фигуре 48.
III. Гетеродимерные белки, слитые с Fc
Согласно некоторым аспектам настоящее изобретение относится к гетеродимерным слитым белкам Fc, которые включают область Fc, обычно связанную (необязательно посредством доменного линкера) с одним или более различными белковыми доменами IL-12. Эти гетеродимерные слитые белки могут принимать большое количество различных форматов, изображенных в общих чертах на Фигуре 8. Согласно одному аспекту гетеродимерный слитый белок Fc представляет собой IL-12 гетеродимерный слитый белок Fc, который включает субъединицы IL-12p40 и IL-12p35 в разных ориентациях так, что они присутствуют вместе, чтобы связываться с рецепторным комплексом IL-12 IL-12 Rβ1/β2. Домены Fc могут происходить из доменов Fc IgG, например, доменов Fc IgG1, IgG2, IgG3 или IgG4, при этом домены Fc IgG1 и IgG4 находят особое применение в данном изобретении. Как описано в данном документе, домены Fc IgG1 могут часто применяться, но не всегда, в сочетании с абляционными вариантами для устранения эффекторной функции. Аналогичным образом, если желательна низкая эффекторная функция, могут применяться домены Fc IgG4.
Как описано в данном документе и известно в данной области, гетеродимерные белки согласно данному изобретению содержат разные домены, которые также могут перекрываться. Эти домены включают, но не ограничиваются ими, домен Fc, домен CH2, домен CH3 и шарнирный домен, домен субъединицы IL-12p40 и домен субъединицы IL-12p35. Как описано в данном документе, эти домены связаны друг с другом в разных форматах, как описано в общих чертах на Фигуре 8.
Согласно некоторым из вариантов реализации в данном документе, если фрагмент белка, например, IL-12p40 или IL-12p35, присоединен к домену Fc, именно С-конец фрагмента белка присоединен ко всему или части шарнира домена Fc; например, он обычно присоединен к последовательности EPKS, которая является началом шарнира IgG1. Согласно другим вариантам реализации в данном документе, если фрагмент белка, например, IL-12p40 или IL-12p35, присоединен к домену Fc, именно N-конец фрагмента белка присоединен к C-концу домена CH3.
В некоторых из конструкций и последовательностей белка домена Fc, описанных в данном документе, C-конец фрагмента белка IL-12p40 или IL-12p35 присоединен к N-концу доменного линкера, C-конец которого присоединен к N-концу константного домена Fc (N - фрагмент белка IL-12p40 или IL-12p35 - линкер - домен Fc - C), хотя данный порядок может быть изменен (N - домен Fc - линкер - фрагмент белка IL-12p40 или IL-12p35 - С). В других конструкциях и последовательностях, описанных в данном документе, C-конец первого фрагмента белка присоединен к N-концу второго фрагмента белка, необязательно за счет доменного линкера, а C-конец второго фрагмента белка присоединен к N-концу константного домена Fc, необязательно за счет доменного линкера. В еще одной конструкции N-конец первого фрагмента белка присоединен к C-концу второго фрагмента белка, необязательно за счет доменного линкера, а N-конец второго фрагмента белка присоединен к C-концу константного домена Fc, необязательно за счет доменного линкера. В других конструкциях и последовательностях, описанных в данном документе, предусмотрен константный домен Fc, который не присоединяется к первому фрагменту белка или второму фрагменту белка. Гетеродимерный слитый белок Fc может содержать два или более иллюстративных белков мономерного домена Fc, описанных в данном документе.
Соответственно, согласно некоторым вариантам реализации настоящего изобретения предложены гетеродимерные слитые белки Fc, которые основаны на применении последовательностей двух различных вариантов Fc тяжелой цепи, которые будут самособираться с образованием гетеродимерного слитого полипептида домена Fc. В одном варианте реализации данного изобретения гетеродимерные слитые белки Fc содержат по меньшей мере два константных домена, которые могут быть сконструированы для получения гетеродимеров, например, путем инженерии pI. Другие домены Fc, которые могут применяться, включают фрагменты, которые содержат один или более из CH1, CH2, CH3, и шарнирные домены по данному изобретению, которые были сконструированы путем инженерии pI. В частности, форматы, изображенные на Фигурах 8A-F, представляют собой гетеродимерные слитые белки Fc, это означает, что белок имеет две ассоциированные последовательности Fc, самособравшиеся в гетеродимерный домен Fc, и по меньшей мере один фрагмент белка (например, 1, 2 или более фрагментов белка). В некоторых случаях первый фрагмент белка связан с первой последовательностью Fc, а второй фрагмент белка связан со второй последовательностью Fc. В некоторых случаях гетеродимерный слитый белок Fc содержит первый фрагмент белка, связанный со вторым фрагментом белка, который связан с первой последовательностью Fc и вторую последовательность Fc, которая не связана ни с первым, ни со вторым фрагментами белка.
Данное изобретение направлено на новые конструкции для получения гетеродимерных слитых белков Fc, которые позволяют обеспечить связывание с одним или более партнерами по связыванию, лигандами или рецепторами. Гетеродимерные слитые конструкции Fc основаны на самособирающейся природе двух доменов Fc тяжелых цепей антител, например, двух «мономеров», которые собираются в «димер». Гетеродимерные слитые белки Fc, получают путем изменения аминокислотной последовательности каждого мономера, что более подробно обсуждается ниже. Таким образом, данное изобретение в целом направлено на создание гетеродимерных слитых белков Fc, которые способны взаимодействовать с партнером (-ами) по связыванию или лигандом (-ами), или рецептором (-ами) и которые основаны на аминокислотных вариантах в константных областях, различающихся в каждой цепи, чтобы способствовать образованию гетеродимеров и (или) обеспечить более легкую очистку гетеродимеров по сравнению с гомодимерами. Существует ряд механизмов, которые могут быть использованы для создания гетеродимеров согласно данному изобретению. В качестве дополнения, как будет понятно специалистам в данной области техники, указанные механизмы могут быть объединены для обеспечения высокой гетеродимеризации. Таким образом, аминокислотные варианты, которые приводят к получению гетеродимеров, называются «гетеродимеризационными вариантами». Как обсуждается ниже, гетеродимеризационные варианты могут включать стерические варианты (например, варианты «выступы и впадины» или «искаженные» варианты, описанные ниже и варианты «пары зарядов», описанные ниже), а также «варианты по pI», что позволяет при очистке отделять гомодимеры от гетеродимеров. Как в целом описано в WO2014/145806, включенном в данный документ посредством ссылки в полном объеме и как конкретно описано ниже для обсуждения «гетеродимеризационных вариантов», пригодные механизмы гетеродимеризации включают «выступы и впадины» («ВИВ», англ. «KIH»; иногда называемые в данном документе «искаженными» вариантами (см. обсуждение в WO2014/145806), «электростатическое координирование» или «пары зарядов», описанные в WO2014/145806, варианты по pI, описанные в WO2014/145806 и общие дополнительные варианты Fc, описанные в WO2014/145806 и ниже.
В данном изобретении предусмотрено несколько основных механизмов, которые могут приводить к облегчению процесса очистки гетеродимерных белков и антител; каждый из них основан на использовании вариантов по pI таким образом, что каждый мономер, а впоследствии и каждая димерная молекула, имеет разное значение pI, что обеспечивает изоэлектрическую очистку димерных белков A - A, A - B и B - B. В качестве альтернативы, некоторые форматы также допускают разделение по размеру. Как дополнительно изложено ниже, также возможно «искажать» образование гетеродимеров по сравнению с гомодимерами. Таким образом, комбинация стерических гетеродимеризационных вариантов и вариантов по pI, или вариантов пары зарядов находит конкретное применение в данном изобретении.
В целом, варианты реализации, которые находят конкретное применение в данном изобретении, основаны на наборах вариантов, включающих искаженные варианты, которые способствуют образованию гетеродимеризации по сравнению с образованием гомодимеризации, в сочетании с вариантами по pI, которые увеличивают разницу pI между двумя мономерами и между каждым димерным видом.
В качестве дополнения, как более подробно изложено ниже, в зависимости от формата гетеродимерного слитого белка Fc, варианты по pI могут содержаться либо внутри константных доменов и (или) доменов Fc мономера, либо могут использоваться доменные линкеры. То есть данное изобретение предоставляет варианты по pI, которые находятся на одном или обоих мономерах, а также (или) предоставляет заряженные доменные линкеры. Кроме того, дополнительная аминокислотная инженерия для альтернативных функциональных возможностей также может вызывать изменения pI, например, в таких вариантах, как варианты Fc, FcRn и KO.
В данном изобретении, в котором значение pI используется в качестве основы для механизма разделения с целью очистки гетеродимерных белков, аминокислотные варианты могут быть введены в один или оба мономерных полипептида; это значит, что значение pI одного из мономеров (для простоты называемого в данном документе «мономер A») может быть предусмотрено таким образом, что оно будет удалено от мономера B, или могут быть изменены как мономер A, так и мономер B, при этом увеличивается значение pI мономера A и уменьшается значение pI мономера B. Как обсуждается, изменения pI одного или обоих мономеров могут быть выполнены путем удаления или добавления заряженного остатка (например, нейтральная аминокислота заменяется положительно или отрицательно заряженным аминокислотным остатком, например, глутамин заменяется глутаминовой кислотой), что приводит к изменению заряженного остатка с положительного или отрицательного на противоположный заряд (например, аспарагиновая кислота заменяется лизином) или к изменению заряженного остатка на нейтральный остаток (например, потеря заряда; лизин заменяется серином). Некоторые из таких вариантов изображены в разделе Фигуры.
Соответственно, в указанном варианте реализации данного изобретения представлено выполнение достаточного изменения pI, по меньшей мере, в одном из мономеров, таким образом, что гетеродимеры могут быть отделены от гомодимеров. Как будет понятно специалистам в данной области техники и как будет обсуждено ниже, это можно осуществить с помощью константной области тяжелой цепи «дикого типа» и вариантной области, которая была сконструирована либо для увеличения, либо для уменьшения ее значения pI (A ДТ : B+ или A ДТ : B-), или путем увеличения его в одной области и уменьшения в другой области (A+ : B- или A- : B+).
Таким образом, в целом, компонент согласно некоторым вариантам реализации настоящего изобретения представляет собой аминокислотные варианты в константных областях, которые направлены на изменение изоэлектрической точки (pI), по меньшей мере, одного, если не обоих, мономеров димерного белка путем встраивания аминокислотных замен («вариантов по pI» или «замен по pI») в один или оба мономера. Отделение гетеродимеров от двух гомодимеров может быть достигнуто, если значения pI указанных двух мономеров различаются всего на 0, 1 единицу рН, при этом все из значений 0, 2, 0, 3, 0, 4 и 0, 5 или больше находят применение в данном изобретении.
Специалистам в данной области техники будет понятно, что количество вариантов по pI, которые должны быть включены в каждый мономер или оба мономера для достижения хорошего разделения, будет частично зависеть от начального значения параметра pI компонентов. То есть, чтобы определить, какой мономер конструировать или в каком «направлении» (например, более положительный или более отрицательный), вычисляются последовательности доменов Fc и, в некоторых случаях, белковый (-е) домен (-ы), связанный (-е) с доменом Fc и на основании этого принимается решение. Как известно в данной области техники, разные домены Fc и (или) белковые домены будут иметь разные начальные значения параметра pI, которые используются в данном изобретении. В общем, как указано в данном документе, значения параметра pI рассчитаны таким образом, чтобы в результате общая разность в значениях pI для каждого мономера составляла по меньшей мере около 0,1 log и предпочтительно - от 0,2 log до 0,5 log, как указано в данном документе.
Кроме того, как будет понятно специалистам в данной области техники и как описано в данном документе, согласно некоторым вариантам реализации настоящего изобретения гетеродимеры могут быть отделены от гомодимеров на основе размера. Как показано на фигурах, например, некоторые из форматов позволяют разделить гетеродимеры и гомодимеры на основе размера.
В случае, когда варианты по pI используются для достижения гетеродимеризации, за счет использования константной (-ых) области (-ей) домена (-ов) Fc предоставляется более модульный подход к конструированию и очистке гетеродимерных слитых белков Fc. Таким образом, согласно некоторым вариантам реализации настоящего изобретения необходимо сконструировать гетеродимеризационные варианты (включая искаженные и очищающие гетеродимеризационные варианты). Кроме того, согласно некоторым вариантам реализации настоящего изобретения возможность иммуногенности, возникающая от вариантов по pI, значительно снижается путем импорта вариантов по pI из различных изотипов IgG, так что pI изменяется без введения значительной иммуногенности. Таким образом, дополнительной проблемой, которую необходимо решить, является выявление константных доменов с низким значением параметра pI и высоким содержанием последовательностей человека, например - минимизация количества или исключение остатков, происходящих не от человека, в любом конкретном положении.
Дополнительным преимуществом, которое может возникнуть при использовании данного подхода к инженерии pI, является также увеличение периода полужизни в сыворотке и увеличение связывания с FcRn. То есть, как описано в USSN 13/194904 (включенном в данный документ посредством ссылки в полном объеме), снижение параметра pI константных доменов антител (включая те, которые обнаруживаются в антителах и слитых белках Fc) может привести к более длительному удерживанию в сыворотке in vivo. Данные варианты по pI для увеличения периода полужизни в сыворотке также способствуют изменению pI для очистки.
Кроме того, следует отметить, что варианты по pI гетеродимеризационных вариантов дают дополнительное преимущество для процесса анализа и контроля качества слитых белков Fc, поскольку способность либо устранять, либо минимизировать, либо различать присутствие гомодимеров является значительной. Сходным образом важна возможность надежного тестирования воспроизводимости производства гетеродимерного слитого белка Fc.
A. Гетеродимеризационные варианты
В данном изобретении представлены гетеродимерные белки, включая гетеродимерные слитые белки Fc, в различных форматах, в которых используются гетеродимерные варианты для обеспечения образования гетеродимеров и (или) их очистки от гомодимеров. Гетеродимерные слитые конструкции основаны на самособирающейся природе двух доменов Fc, например, двух «мономеров», которые собираются в «димер».
Существует ряд подходящих пар наборов искаженных гетеродимеризационных вариантов. Указанные варианты входят в «пары» «наборов». То есть, один набор пары встроен в первый мономер, а другой набор пары встроен во второй мономер. Следует отметить, что указанные наборы не обязательно ведут себя как варианты «выступы во впадинах», с однозначным соответствием между остатком в одном мономере и остатком в другом; это значит, что указанные пары наборов образуют границу раздела между двумя мономерами, которая стимулирует образование гетеродимеров и препятствует образованию гомодимеров, способствуя тому, что процент гетеродимеров, которые спонтанно образуются в биологических условиях, будет составлять более 90%, а не ожидаемые 50% (25% гомодимер A/A : 50% гетеродимер A/B : 25% гомодимер B/B).
B. Стерические варианты
Согласно некоторым вариантам реализации, формирование гетеродимеров может быть облегчено путем добавления стерических вариантов. То есть, в результате изменения аминокислот в каждой тяжелой цепи, различные тяжелые цепи с большей вероятностью ассоциируются с образованием гетеродимерной структуры, чем с образованием гомодимеров с одинаковыми аминокислотными последовательностями в Fc. Подходящие стерические варианты включены в Фигуру 29 из USSN 15/141350, все из которых полностью включены в данный документ посредством ссылки, а также в Фигуру 2.
Один из механизмов, обычно упоминаемый в данной области техники как «выступы и впадины», относится к конструированию аминокислот, которое приводит к созданию стерических влияний, способствующих образованию гетеродимеров и препятствующих образованию гомодимеров, как описано в USSN 61/596846, Ridgway et al., Protein Engineering 9(7):617 (1996); Atwell et al., J. Mol. Biol. 1997 270:26; патент США № 8216805, все из которых полностью включены в данный документ посредством ссылки. В разделе Фиг. обозначено несколько пар «мономер A - мономер B», которые основаны на механизме «выступы и впадины». Кроме того, как описано в работе Merchant et al., Nature Biotech. 16:677 (1998), указанные мутации «выступы и впадины» можно комбинировать с дисульфидными связями для искажения образования вариантов в сторону гетеродимеризации.
Дополнительный механизм, который находит применение в создании гетеродимеров, иногда называют «электростатическим координированием», как описано в работе Gunasekaran et al., J. Biol. Chem. 285(25):19637 (2010), которая полностью включена в данный документ посредством ссылки. Данный механизм иногда обозначают в данном документе как «пары зарядов». В указанном варианте реализации данного изобретения электростатические силы используются для искажения образования вариантов в сторону гетеродимеризации. Специалистам в данной области техники будет понятно, что указанные механизмы также могут оказывать влияние на показатель pI и, следовательно, на очистку, и, таким образом, в некоторых случаях также могут рассматриваться как варианты по pI. В то же время, поскольку они были созданы для усиления гетеродимеризации и не были использованы в качестве инструментов очистки, они классифицируются как «стерические варианты». Указанные варианты включают, но не ограничиваются ими: D221E/P228E/L368E, спаренные с D221R/P228R/K409R (например, они представляют собой наборы, соответствующие «мономерам») и C220E/P228E/368E, спаренные с C220R/E224R/P228R/K409R.
Дополнительные варианты мономеров A и мономеров B, которые можно комбинировать с другими вариантами, необязательно и независимо в любом количестве, такими как варианты по pI, описанные в данном документе, или другие стерические варианты, которые представлены на Фигуре 37 в US 2012/0149876, все из которых явно включены в данный документ посредством ссылки.
Согласно некоторым вариантам реализации настоящего изобретения стерические варианты, изложенные в данном документе, могут быть необязательно и независимо встроены с любым вариантом по pI (или другими вариантами, такими как варианты по Fc, варианты по FcRn и т.д.) в один или оба мономера и могут быть независимо и необязательно включены или исключены из белков согласно данному изобретению.
Перечень подходящих искаженных вариантов приведен на Фигуре 2. Во многих вариантах реализации особое применение находят пары наборов, включая, но не ограничиваясь ими, S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411T/E360E/Q362E : D401K; L368D/K370S : S364K/E357L; K370S : S364K/E357Q; и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C). С точки зрения номенклатуры пара «S364K/E357Q : L368D/K370S» означает, что один из мономеров имеет набор с двойным вариантом S364K/E357Q, а другой имеет набор с двойным вариантом L368D/K370S; как указано выше, «наличие цепей» указанных пар зависит от исходного значения параметра pI.
C. Варианты pI (изоэлектрическая точка) для гетеродимеров
В целом, как будет понятно специалистам в данной области техники, существует две основные категории вариантов по pI: варианты, которые приводят к повышению значения pI белка (основные изменения) и варианты, которые приводят к уменьшению значения pI белка (кислотные изменения). Как описано в данном документе, могут быть использованы все комбинации указанных вариантов: один мономер может относиться к дикому типу или варианту, который не имеет существенно отличающееся от дикого типа значение pI, а другой может быть либо более основным, либо более кислым. В качестве альтернативы, каждый мономер может быть изменен, один - в более основной и один - в более кислый.
Предпочтительные комбинации вариантов по pI продемонстрированы на Фигуре 30 из USSN 15/141350, все из которых включены в данный документ посредством ссылки в полном объеме. Как описано в данном документе и показано в разделе Фигур, указанные изменения показаны относительно IgG1, но все изотипы могут быть изменены аналогичным образом, также как и гибриды изотипов. В случае если константный домен тяжелой цепи происходит из IgG2-4, также можно применять R133E и R133Q.
Согласно одному варианту реализации настоящего изобретения предпочтительная комбинация вариантов по pI содержит один мономер, содержащий варианты 208D/295E/384D/418E/421D (N208D/Q295E/N384D/Q418E/N421D по сравнению с человеческим IgG1), если один из мономеров Fc включает домен CH1. В некоторых случаях второй мономер содержит положительно заряженный доменный линкер, включительно с (GKPGS)4. В некоторых случаях первый мономер включает домен CH1, включая положение 208. Соответственно, в конструкциях, которые не включают домен CH1 (например, для гетеродимерных слитых белков Fc, в которых не используется домен CH1 на одном из доменов), предпочтительный набор варианта Fc с отрицательным значением pI включает варианты 295E/384D/418E/421D (Q295E/N384D/Q418E/N421D по сравнению с человеческим IgG1).
Согласно некоторым вариантам реализации настоящего изобретения мутации вносят в шарнир домена Fc, включая положения 216, 217, 218, 219, 220, 221, 222, 223, 224, 225, 226, 227, 228, 229 и 230. Таким образом, мутации по pI и, в частности, замены могут быть сделаны в одном или нескольких положениях 216 - 230, причем в данном изобретении находят применение 1, 2, 3, 4 или 5 мутаций. Опять же, рассматриваются все возможные комбинации, отдельно или с другими вариантами по pI в других доменах.
Конкретные замены, которые находят применение для понижения значения pI шарнирных доменов, включают следующие, но не ограничиваются ими: делеция в положении 221, ненативный валин или треонин в положении 222, делеция в положении 223, ненативная глутаминовая кислота в положении 224, делеция в положении 225, делеция в положении 235 и делеция ненативного аланина в положении 236. В некоторых случаях в шарнирном домене выполняются только замены по pI, а в других эти замены (замена) добавляются к другим вариантам по pI в других доменах в любой комбинации.
Согласно некоторым вариантам реализации настоящего изобретения мутации могут быть внесены в область CH2, включая положения 233, 234, 235, 236, 274, 296, 300, 309, 320, 322, 326, 327, 334 и 339. Следует отметить, что изменения в 233-236 могут быть внесены для увеличения эффекторной функции (наряду с 327A) в каркасе IgG2. Как упоминалось, могут быть сделаны все возможные комбинации указанных 14 положений; например, pI антитело может иметь 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 замен по pI в CH2.
Конкретные замены, которые находят применение для уменьшения значения pI в доменах CH2, включают, но не ограничиваются ими: ненативный глутамин или глутаминовую кислоту в положении 274, ненативный фенилаланин в положении 296, ненативный фенилаланин в положении 300, ненативный валин в положении 309, ненативную глутаминовую кислоту в положении 320, ненативную глутаминовую кислоту в положении 322, ненативную глутаминовую кислоту в положении 326, ненативный глицин в положении 327, ненативную глутаминовую кислоту в положении 334, ненативный треонин в положении 339 и все возможные комбинации в пределах CH2 и с другими доменами.
В данном варианте реализации данного изобретения мутации могут быть независимо и необязательно выбраны из положений 355, 359, 362, 384, 389, 392, 397, 418, 419, 444 и 447. Конкретные замены, которые находят применение для уменьшения значения pI в доменах CH3, включают, но не ограничиваются ими: ненативный глутамин или глутаминовую кислоту в положении 355, ненативный серин в положении 384, ненативный аспарагин или глутаминовую кислоту в положении 392, ненативный метионин в положении 397, ненативную глутаминовую кислоту в положении 419, ненативную глутаминовую кислоту в положении 359, ненативную глутаминовую кислоту в положении 362, ненативную глутаминовую кислоту в положении 389, ненативную глутаминовую кислоту в положении 418, ненативную глутаминовую кислоту в положении 444 и делецию или ненативную аспарагиновую кислоту в положении 447.
Изотипические варианты
В качестве дополнения, многие варианты реализации данного изобретения основаны на «импорте» pI аминокислот в определенных положениях из одного изотипа IgG в другой, тем самым уменьшая или исключая возможность внесения нежелательной иммуногенности в указанные варианты. Некоторые из них изображены на Фигуре 21 публикации США № 2014/0370013, которая включена в данный документ посредством ссылки. Это значит, что IgG1 представляет собой распространенный изотип для терапевтических антител по ряду причин, включая высокую эффекторную функцию. Однако константная область тяжелой цепи IgG1 имеет более высокое значение pI, чем таковая IgG2 (8,10 по сравнению с 7,31). В результате введения остатков IgG2 в конкретных положениях в каркас IgG1 значение pI образованного в результате мономера снижается (или увеличивается) и дополнительно у него наблюдается более длительный период полужизни в сыворотке крови. Например, IgG1 содержит глицин (pI 5,97) в положении 137, а IgG2 содержит глутаминовую кислоту (pI 3,22); импортирование глутаминовой кислоты будет влиять на значение pI образованного в результате белка. Как описано ниже, требуется, как правило, несколько аминокислотных замен для значительного влияния на значение pI вариантного слитого белка Fc. Однако следует отметить, что, как обсуждается ниже, даже изменения в молекулах IgG2 обеспечивают увеличение периода полужизни в сыворотке крови.
В других вариантах реализации данного изобретения выполняют замены неизотипных аминокислот либо с целью уменьшения общего заряженного состояния образованного в результате белка (например, путем изменения аминокислоты с более высоким значением pI на аминокислоту с более низким значением pI), либо для обеспечения приспособления в структуре с целью стабильности и т.д., как более подробно описано ниже.
Кроме того, с помощью pI инженерии константных доменов как тяжелых, так и легких цепей, можно наблюдать значительные изменения в каждом из мономеров гетеродимера. Как обсуждается в данном документе, наличие значений pI двух мономеров, отличающихся по меньшей мере на 0,5, может способствовать разделению с помощью метода ионообменной хроматографии или изоэлектрической фокусировки, или других способов, чувствительных к изоэлектрической точке.
Расчет значения pI
pI каждого мономера может зависеть от значения pI варианта константного домена тяжелой цепи и pI всего мономера, включая вариантный константный домен тяжелой цепи и партнера по слиянию. Таким образом, согласно некоторым вариантам реализации настоящего изобретения изменение в значении pI рассчитывают на основе константного домена вариантной тяжелой цепи, используя диаграмму на Фигуре 19 публикации США № 2014/0370013. Как обсуждается в данном документе, мономер, подлежащий конструированию, как правило, определяется собственным присущим значением pI каждого мономера.
Варианты по pI, которые также обеспечивают улучшенное связывание с FcRn in vivo
В случае, когда вариант по pI снижает значение pI мономера, это может иметь дополнительное преимущество в виде улучшенного удержания в сыворотке крови in vivo.
Несмотря на то, что вопрос все еще находится на изучении, считается, что области Fc имеют более длительные периоды полужизни in vivo, поскольку связывание с FcRn при рН 6 в эндосоме приводит к секвестрированию Fc (Ghetie and Ward, 1997 Immunol Today. 18 (12): 592 - 598, включена посредством ссылки в полном объеме). Затем эндосомальный компартмент рециркулирует Fc на поверхность клетки. После того, как компартмент открывается во внеклеточное пространство, более высокое значение рН - ~7,4 - способствует высвобождению Fc обратно в кровоток. Dall 'Acqua с соавт. показали на мышах, что мутантные Fc с повышенным связыванием с FcRn при pH 6 и pH 7,4 на самом деле имели пониженные концентрации в сыворотке крови и такой же период полужизни, как Fc дикого типа (Dall 'Acqua et al. 2002, J. Immunol. 169: 5171 - 5180, данная публикация включена в данный документ посредством ссылки в полном объеме). Считается, что повышенная аффинность Fc к FcRn при pH 7,4 запрещает высвобождение Fc обратно в кровоток. Следовательно, мутации в Fc, которые увеличивают время полужизни для Fc in vivo, в идеале увеличивают связывание с FcRn при более низком значении pH, в то же время позволяя высвобождать Fc при более высоком значении pH. Аминокислота гистидин меняет свое заряженное состояние в диапазоне значений pH от 6,0 до 7,4. В связи с этим неудивительно, что остатки His находятся в важных положениях в комплексе Fc - FcRn.
Существует ряд замен Fc, которые находят применение в повышенном связывании с FcRn и увеличенном периоде полужизни в сыворотке крови, как конкретно раскрыто в USSN 12/341769, который полностью включен в данный документ посредством ссылки, включая, но не ограничиваясь ими: 434A, 428L, 308F, 259I, 428L/434S, 259I/308F, 436I/428L, 436I, 434S, 252Y/428L, 252Y/434S, 428L/434S, 436V/428L и 259I/308F/428L.
Дополнительные варианты Fc для дополнительной функциональной возможности
В качестве дополнения к аминокислотным вариантам по pI существует ряд пригодных аминокислотных модификаций Fc, которые могут быть сделаны по ряду причин, включая, но не ограничиваясь ими: изменение связывания с одним или более FcγR, изменение связывания с FcRn и т. д.
Соответственно, белки согласно данному изобретению могут содержать аминокислотные модификации, включая гетеродимеризационные варианты, изложенные в данном документе, которые включают варианты по pI и стерические варианты. Каждая совокупность вариантов может быть независимо и необязательно включена или исключена из любого конкретного гетеродимерного белка.
Варианты FcγR
Соответственно, существует ряд пригодных замен в Fc, которые могут быть сделаны для изменения связывания с одним или более рецепторами FcγR. Могут быть полезными замены, которые приводят к увеличению связывания, а также к уменьшению связывания. Например, известно, что повышенное связывание с FcγRIIIa приводит к повышению АЗКЦ (антителозависимой клеточно-опосредованной цитотоксичности; клеточно-опосредованной реакции, при которой неспецифические цитотоксические клетки, которые экспрессируют FcγR, распознают связанное антитело на клетке-мишени и впоследствии вызывают лизис данной клетки-мишени). Аналогичным образом, в некоторых случаях также может быть пригодным уменьшение связывания с FcγRIIb (ингибирующий рецептор). Аминокислотные замены, которые находят применение в данном изобретении, включают замены, перечисленные в USSN 11/124620 (особенно на Фигуре 41), 11/174287, 11/396495, 11/538406, все из которых явным образом включены в данный документ посредством ссылки в полном объеме и конкретно для раскрытых в них вариантов. Конкретные варианты, которые находят применение, включают следующие, но не ограничиваясь ими: 236A, 239D, 239E, 332E, 332D, 239D/332E, 267D, 267E, 328F, 267E/328F, 236A/332E, 239D/332E/330Y, 239D, 332E/330L, 243A, 243L, 264A, 264V и 299T.
Кроме того, аминокислотные замены, которые повышают аффинность к FcγRIIc, также могут быть включены в варианты домена Fc, описанные в данном документе. Полезны замены, описанные, например, в USSN 11/124620 и 14/578305.
Абляционные варианты
Аналогичным образом, другая категория функциональных вариантов представляет собой «абляционные варианты FcγR», или «варианты нокаута Fc (Fc-KO или KO)». В указанных вариантах реализации для некоторых терапевтических приложений желательно уменьшить или устранить нормальное связывание домена Fc с одним или более, или всеми рецепторами Fcγ (например, FcγR1, FcγRIIa, FcγRIIb, FcγRIIIa и т. д.), чтобы избежать дополнительных механизмов действия. Таким образом, например, во многих вариантах реализации данного изобретения, в особенности - при использовании иммуномодулирующих белков, желательно устранять связывание с FcγRIIIa для избегания или значительного снижения активности АЗКЦ, таким образом, чтобы один из доменов Fc содержал один или более абляционных вариантов по Fcγ рецептора м. Указанные абляционные варианты изображены на Фигуре 31 в USSN 15/141350, все из которых полностью включены в данный документ посредством ссылки и каждый из них может быть независимо и необязательно включен или исключен, при этом в предпочтительных аспектах используются абляционные варианты, выбранные из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S267K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G и E233P/L234V/L235A/G236del, в соответствии с индексом ЕС. Следует отметить, что абляционные варианты, упомянутые в данном документе, устраняют связывание с FcγR, но, обычно, не связывание с FcRn.
Комбинирование гетеродимерных вариантов и вариантов Fc
Как будет понятно специалистам в данной области техники, все из перечисленных гетеродимеризационных вариантов (включая искаженных и (или) вариантов по pI) могут быть необязательно и независимо скомбинированы любым способом, при условии, что они сохраняют свое «наличие цепей» или «разделение мономеров». В качестве дополнения, все из указанных вариантов могут быть скомбинированы в любой из гетеродимеризационных форматов.
В случае вариантов по pI, несмотря на то, что варианты реализации данного изобретения, находящие особенное применение, продемонстрированы в разделе Фиг., могут быть созданы другие комбинации, на основе основного правила изменения разницы в значениях pI между двумя мономерами для облегчения очистки.
Кроме того, любой из гетеродимеризационных вариантов, искаженных вариантов и вариантов по pI также может быть независимо и необязательно скомбинирован с Fc-абляционными вариантами, вариантами Fc, вариантами FcRn, как в целом описано в данном документе.
Кроме того, мономерный домен Fc может содержать набор аминокислотных замен, который включает C220S/S267K/L368D/K370S или C220S/S267K/S364K/E357Q.
Кроме того, гетеродимерные слитые белки Fc могут содержать искаженные варианты (например, набор аминокислотных замен, показанный на Фигурах 1A - 1C из USSN 15/141350, все из которых полностью включены в данный документ посредством ссылки), при этом особенно подходящие искаженные варианты выбраны из группы, состоящей из S364K/E357Q : L368D/K370S; L368D/K370S : S364K; L368E/K370S : S364K; T411T/E360E/Q362E : D401K; L368D/K370S : S364K/E357L; K370S : S364K/E357Q; T366S/L368A/Y407V : T366W; и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C), необязательно абляционных вариантов, необязательно заряженных доменных линкеров; и необязательно вариантов по pI.
Согласно некоторым вариантам реализации домен Fc содержит одну или более аминокислотных замен, выбранных из группы, состоящей из: 236R, S239D, S239E, F243L, M252Y, V259I, S267D, S267E, S67K, S298A, V308F, L328F, L328R, 330L, I332D, I332E, M428L, N434A, N434S, 236R/L328R, S239D/I332E, 236R/L328F, V259I/V308F, S267E/L328F, M428L/N43S, Y436I/M428L, N436V/M428L, V436I/N434S, Y436V/N434S, S239D/I332E/330L, M252Y/S54T/T256E, V259I/V308F/M428L, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K в соответствии с индексом ЕС.
Согласно одному варианту реализации настоящего изобретения конкретная комбинация искаженных вариантов и вариантов по pI, которая находит применение в данном изобретении, представляет собой T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C), при этом один мономер содержит Q295E/N384D/Q418E/N481D, а другой мономер содержит положительно заряженный доменный линкер. Как будет понятно специалисту в данной области техники, варианты «выступы и впадины» не приводят к изменению параметра pI и, таким образом, могут использоваться на любом мономере.
Гетеродимерные слитые белки Fc
Согласно некоторым аспектам настоящее изобретение относится к гомодимерным слитым белкам Fc, которые включают область Fc, обычно связанную (необязательно посредством доменного линкера) с одним или более различными белковыми доменами. Эти форматы показаны в общих чертах на Фигуре 14 и Фигуре 48. Согласно одному аспекту гомодимерный слитый белок Fc представляет собой IL-12 гомодимерный слитый белок Fc, который включает субъединицы IL-12p40 и IL-12p35 в различных ориентациях так, что они присутствуют вместе, чтобы связываться с рецепторным комплексом IL-12 IL-12 Rβ1/β2. Домены Fc могут происходить из доменов Fc IgG, например, доменов Fc IgG1, IgG2, IgG3 или IgG4, при этом домены Fc IgG1 и IgG4 находят особое применение в данном изобретении. Как описано в данном документе, домены Fc IgG1 могут часто использоваться, но не всегда, в сочетании с абляционными вариантами для устранения эффекторной функции. Аналогичным образом, когда желательна низкая эффекторная функция, могут использоваться домены Fc IgG4.
Согласно одному аспекту гомодимерный слитый белок Fc содержит первый мономер и второй мономер, содержащие, от N- к C-концу, субъединицу IL-12p40-необязательный линкер-субъединицу IL-12p35-необязательный линкер-домен Fc. Согласно некоторым вариантам реализации гомодимерный слитый белок Fc содержит первый мономер и второй мономер, содержащие от N- к C-концу, субъединицу IL-12p40-линкер-субъединицу IL-12p35-линкер-домен Fc. Пример варианта реализации представлен на Фигуре 48A.
Согласно другому аспекту гомодимерный слитый белок Fc содержит первый мономер и второй мономер, содержащие, от N- к C-концу, субъединицу IL-12p35-необязательный линкер-субъединицу IL-12p40-необязательный линкер-домен Fc. Согласно некоторым вариантам реализации гомодимерный слитый белок Fc содержит первый мономер и второй мономер, содержащие от N- к C-концу, субъединицу IL-12p35-линкер-субъединицу IL-12p40-линкер-домен Fc. Пример варианта реализации представлен на Фигуре 48B.
Согласно другому аспекту гомодимерный слитый белок Fc содержит первый мономер и второй мономер, содержащие от N- к C-концу, домен Fc-необязательный линкер-субъединицу IL-12p40-необязательный линкер-субъединицу IL-12p35. Согласно некоторым вариантам реализации гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, содержит от N- к С-концу, домен Fc-линкер-субъединицу IL-12p40-линкер-субъединицу IL-12p35. Пример варианта реализации представлен на Фигуре 48C.
Согласно другому аспекту гомодимерный слитый белок Fc содержит первый мономер и второй мономер, содержащие, от N- к C-концу, домен Fc-необязательный линкер-субъединицу IL-12p35-необязательный линкер-субъединицу IL-12p40. Согласно некоторым вариантам реализации гомодимерный слитый белок Fc, содержащий первый мономер и второй мономер, содержит, от N- к С-концу, домен Fc-линкер-субъединицу IL-12p35-линкер-субъединицу IL-12p40. Пример варианта реализации представлен на Фигуре 48D.
Согласно некоторым вариантам реализации формат двухвалентного IL-12p40-Fc обеспечивает гомодимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p40; ii) необязательный первый доменный линкер; iii) белок первого вариантного домена Fc; и b) второй мономер, содержащий, от N- к C-концу: i) белок домена IL-12p40; ii) необязательный второй доменный линкер; iii) белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации формат двухвалентного IL-12p35-Fc обеспечивает гомодимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p35; ii) необязательный первый доменный линкер; iii) белок первого вариантного домена Fc; и b) второй мономер, содержащий, от N- к C-концу: i) белок домена IL-12p35; ii) необязательный второй доменный линкер; iii) белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации формат (scIL-12(p40/p35))2-Fc обеспечивает гомодимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p40; ii) необязательный первый доменный линкер; iii) белок домена IL-12p35; iv) необязательный второй доменный линкер; v) белок первого вариантного домена Fc; и b) второй мономер, содержащий, от N- к C-концу: i) белок домена IL-12p40; ii) необязательный третий доменный линкер; iii) белок домена IL-12p35; iv) необязательный четвертый доменный линкер; v) белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации формат (scIL-12(p35/p40))2-Fc обеспечивает гомодимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p35; ii) необязательный первый доменный линкер; iii) белок домена IL-12p40; iv) необязательный второй доменный линкер; v) белок первого вариантного домена Fc; и b) второй мономер, содержащий, от N- к C-концу: i) белок домена IL-12p35; ii) необязательный третий доменный линкер; iii) белок домена IL-12p40; iv) необязательный четвертый доменный линкер; v) белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации формат Fc-(scIL-12(p40/p35))2 обеспечивает гомодимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к С-концу: i) белок первого вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p40; iv) необязательный второй доменный линкер; v) белок домена IL-12p35; и b) второй мономер, содержащий, от N- к C-концу: i) белок второго вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p40; iv) необязательный второй доменный линкер; v) белок домена IL-12p35.
Согласно некоторым вариантам реализации формат Fc-(scIL-12(p35/p40))2 обеспечивает гомодимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к С-концу: i) белок первого вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p35; iv) необязательный второй доменный линкер; v) белок домена IL-12p40; и b) второй мономер, содержащий, от N- к C-концу: i) белок второго вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p35; iv) необязательный второй доменный линкер; v) белок домена IL-12p40.
Согласно некоторым вариантам реализации указанный первый доменный линкер и указанный второй доменный линкер имеют одинаковую аминокислотную последовательность. Согласно некоторым вариантам реализации первый доменный линкер и второй доменный линкер имеют разные аминокислотные последовательности.
Согласно некоторым вариантам реализации варианты Fc содержат один или более искаженных вариантов, вариантов по pI и абляционных вариантов, предусмотренных в настоящем документе. Согласно одному варианту реализации варианты Fc содержат конкретные искаженные варианты, варианты по pI и абляционные варианты. Согласно некоторым вариантам реализации модификации, способствующие гомодимеризации первого и второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S; S364K; S364K/E357L; S364K/E357Q; T411E/K360E/Q362E; D401K; T366S/L368A/Y407V; T366W; T366S/L368A/Y407V/Y349C; и T366W/S354C, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
В этом формате подходящие домены белка IL-12p40 включают, но не ограничиваются ими, SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12). В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате домены белка IL-12p35 включают SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12). В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие варианты реализации включают, но не ограничиваются ими, варианты, показанные на Фигурах 14A-14B и Фигуре 15.
В потенциальных вариантах реализации гомодимерных слитых белков Fc можно применять способы и композиции, описанные выше в разделе, озаглавленном «Гетеродимерные слитые белки Fc», в зависимости от ситуации, с целью получения гомодимера, а не гетеродимера. В потенциальных вариантах реализации гомодимерных слитых белков Fc можно применять любую комбинацию способов и композиций, описанных в данном документе.
Интерлейкин 12
Настоящее изобретение относится к биологически функциональной форме интерлейкина 12. IL-12 гетеродимерные белки Fc, содержащие вариант IL-12p40 и (или) варианты IL-12p35, имеют уменьшенную или сниженную аффинность связывания с рецепторами IL-12 по сравнению с IL-12 дикого типа, включая гетеродимер p40/p35 и гомодимер p40. IL-12 гетеродимерные белки Fc по данному изобретению обладают уменьшенной или сниженной активностью по сравнению с IL-12 дикого типа. IL-12 гетеродимерные белки Fc имеют продленный или увеличенный период полужизни в сыворотке крови. IL-12 гетеродимерные белки Fc обладают уменьшенной или сниженной потенциальной токсичностью. IL-12 гетеродимерные белки Fc по данному изобретению обладают уменьшенной или сниженной активность в отношении индукции фосфорилирования STAT4 в иммунных клетках, таких как, но не ограничиваясь ими, Т-клетки и NK-клетки. Варианты IL-12p40 содержат аминокислотные модификации (например, замены, добавления и делеции), которые удаляют потенциальные сайты N-гликозилирования. Варианты IL-12p35 содержат аминокислотные модификации (например, замены, добавления и делеции), которые удаляют потенциальные сайты N-гликозилирования. Согласно некоторым вариантам реализации IL-12 гетеродимерные белки Fc по данному изобретению обладают уменьшенным/сниженным гликозилированием по сравнению с IL-12 дикого типа. Согласно некоторым вариантам реализации статус гликозилирования IL-12 гетеродимерных белков Fc по данному изобретению отличается от белка IL-12 дикого типа. IL-12 гетеродимерные белки Fc по данному изобретению обеспечивают улучшенную фармакокинетику по сравнению с IL-12 дикого типа. Такие IL-12 гетеродимерные белки Fc также терапевтически эффективны и имеют улучшенный терапевтический индекс, например, по сравнению с IL-12 дикого типа. IL-12 гетеродимерные белки Fc по данному изобретению могут стимулировать/индуцировать активацию Т-клеток. Согласно некоторым вариантам реализации введение любого из IL-12 гетеродимерных белков Fc пациенту индуцирует активацию Т-клеток у пациента. В некоторых случаях введение индуцирует секрецию ИФН-гамма у пациента. В некоторых случаях введение IL-12 гетеродимерных белков Fc индуцирует размножение лимфоцитов у пациента. IL-12 гетеродимерные белки Fc можно применять для лечения рака, такого как разные виды рака в виде солидных опухолей или разные виды рака в виде гемобластозов. Согласно некоторым вариантам реализации введение любого из IL-12 гетеродимерных белков Fc пациенту и, в некоторых случаях, в комбинации с агентом, блокирующим контрольную точку, уменьшает размер опухоли.
Как указано выше, биологически функциональная форма интерлейкина 12 или «IL-12» представляет собой гетеродимер, состоящий из субъединицы IL-12p35 (субъединица альфа IL-12) и субъединицы IL-12p40 (субъединица бета IL-12), в данном документе обозначается как «гетеродимерный комплекс IL-12». Указанный комплекс можно применять в двух разных форматах. Как показано на Фигурах 8A-B, субъединица IL-12p40 и субъединицы IL-12p35 не соединены друг с другом ковалентно, а скорее ковалентно присоединены, соответственно, к первому и второму домену Fc, которые собираются в виде гетеродимера. В качестве альтернативы, субъединицы IL-12p35 и IL-12p40 могут быть ковалентно присоединены, необязательно с использованием доменного линкера (как описано в данном документе), как показано в общих чертах на Фигурах 8C-F, в данном документе обозначается как одноцепочечный комплекс IL-12 или «scIL-12». Порядок двух субъединиц в scIL-12 можно обозначить следующим образом: «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p40.
Согласно некоторым вариантам реализации человеческий белок IL-12p35 имеет аминокислотную последовательность, представленную в NCBI Ref. Seq. № NP_000873.2 или SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12, изображенная на Фигуре 1). В некоторых случаях кодирующая последовательность человеческой IL-12p35 представлена в NCBI Ref. Seq. № NM_000882.3. Примерный белок IL-12p35 из гетеродимерного слитого белка Fc, описанного в данном документе, может иметь аминокислотную последовательность SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12, изображенная на Фигуре 1) или аминокислоты 23-219 из SEQ ID NO: 1. Согласно некоторым вариантам реализации белок IL-12p35 имеет по меньшей мере 90%, например, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности с последовательностью SEQ ID NO: 2. Белок IL-12p35 из слитого белка Fc может иметь 1, 2, 3, 4, 5, 6, 7, 8 или 9 аминокислотных мутаций.
Согласно некоторым вариантам реализации человеческий белок IL-12p40 имеет аминокислотную последовательность, представленную в NCBI Ref. Seq. № NP_002178.3 или SEQ ID NO:3 (последовательность предшественника субъединицы бета (IL-12p40) человеческого IL-12, изображенная на Фигуре 1). В некоторых случаях кодирующая последовательность человеческой IL-12p40 представлена в NCBI Ref. Seq. № NM_002187.3. Примерный белок IL-12p40 из слитого белка Fc, описанного в данном документе, может иметь аминокислотную последовательность SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12, изображенная на Фигуре 1), или аминокислоты 23-328 из SEQ ID NO: 3. Согласно некоторым вариантам реализации белок IL-12p40 имеет по меньшей мере 90%, например, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% или более идентичности с последовательностью SEQ ID NO: 4. Белок IL-12p40 из слитого белка Fc может иметь 1, 2, 3, 4, 5, 6, 7, 8 или 9 аминокислотных мутаций.
Согласно настоящему изобретению также предложены вариантные субъединицы IL-12p40 и вариантные субъединицы IL-12p35. Эти варианты находят применение как часть биологически функционального комплекса IL-12, а также любого из IL-12-Fc слитых белков, описанных в данном документе.
A. Варианты по экспрессии
Предварительно, субъединицы IL-12p40 и IL-12p35 по данному изобретению также включают варианты для удаления потенциальных сайтов N-гликозилирования, разработанные для уменьшения гетерогенности.
Такие потенциальные сайты N-гликозилирования на IL-12p40, в которые могут быть введены модификации аминокислот, включают N103, N113, N200 и N281 (пронумерованы в соответствии с субъединицей бета человеческого IL-12 (последовательность зрелой формы IL-12p40, изображенная на Фигуре 1). Иллюстративные модификации в одном или более из этих сайтов могут быть выбраны из группы, состоящей из: N103D, N103Q, N113D, N113Q, N200D, N200Q, N281D, и N281Q. Варианты по экспрессии IL-12p40 могут включать одну или более модификаций в этих сайтах. Соответственно, согласно одному варианту реализации вариант IL-12p40 содержит N103D/N113D/N200D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N103D/N113D. Согласно одному варианту реализации вариант IL-12p40 содержит N103D/N200D. Согласно одному варианту реализации вариант IL-12p40 содержит N103D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N113D/N200D. Согласно одному варианту реализации вариант IL-12p40 содержит N113D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N200D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N103D/N113D/N200D. Согласно одному варианту реализации вариант IL-12p40 содержит N103D/N113D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N/103D/N200D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N113D/N200D/N281D. Согласно одному варианту реализации вариант IL-12p40 содержит N103Q/N113Q. Согласно одному варианту реализации вариант IL-12p40 содержит N103Q/N200Q. Согласно одному варианту реализации вариант IL-12p40 содержит N103Q/N281Q. Согласно одному варианту реализации вариант IL-12p40 содержит N113Q/N200Q. Согласно одному варианту реализации вариант IL-12p40 содержит N113Q/N281Q. Согласно одному варианту реализации вариант IL-12p40 содержит N103Q/N113Q/N200Q. Согласно одному варианту реализации вариант IL-12p40 содержит N103Q/N113Q/N281Q. Согласно одному варианту реализации вариант IL-12p40 содержит N103Q/N200Q/N281Q. Согласно одному варианту реализации вариант IL-12p40 содержит N113Q/N200Q/N281Q. Эти модификации можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по аффинности.
Такие потенциальные сайты N-гликозилирования на IL-12p35, в которых аминокислотные модификации могут быть введены в один или более сайтов, выбраны из группы, состоящей из: N71, N85 и N195 (пронумерованы в соответствии с последовательностью зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12, изображенной на Фигуре 1). Иллюстративные модификации в этих сайтах включают N71D, N71Q, N85D, N85Q, N195D, и N195Q. Варианты IL-12p35 могут включать одну или более модификаций в этих сайтах. Соответственно, согласно одному варианту реализации вариант IL-12p35 содержит N71D/N85D/N195D. Эти модификации можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p35, такими как варианты по аффинности.
Субъединица IL-12p40 имеет свободный цистеин в положении 252 (пронумеровано в соответствии с последовательностью зрелой формы субъединицы бета (IL-12p40) человеческого IL-12, изображенной на Фигуре 1), который может связываться с другими свободными цистеинами, что приводит по меньшей мере к гетерогенности, а в худшем случае приводит к иммуногенности. Соответственно, варианты IL-12p40 были разработаны для удаления свободного цистеина, например, путем введения модификации C252S (хотя можно применять и другие замены). Модификацию C252 (например, C252S) можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по аффинности или экспрессии. Иллюстративные варианты IL-12p40, содержащие модификацию в C252 для удаления свободного цистеина, изображены на Фигуре 65. Иллюстративные IL-12-Fc слитые белки создавали с дополнительными вариантными субъединицами IL-12p40, последовательности для которых изображены на Фигуре 66, и получали, как описано в общих чертах в Примере 1B. Указанные модификации можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по аффинности.
B. Варианты по аффинности и активности
Согласно настоящему изобретению предложены варианты IL-12p40 и варианты IL-12p35, которые образуют биологически функциональный IL-12 с измененной, то есть либо уменьшенной, либо увеличенной, аффинностью связывания в отношении рецепторов IL-12. В некоторых случаях вариантная субъединица IL-12p40 имеет измененную, то есть либо уменьшенную, либо увеличенную, аффинность связывания в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12. В некоторых случаях вариант IL-12p35 имеет измененную, то есть либо уменьшенную, либо увеличенную, аффинность связывания в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12. Согласно настоящему изобретению также предложены варианты IL-12p40 и варианты IL-12p35, которые образуют биологически функциональный IL-12 с измененной, то есть либо уменьшенной, либо увеличенной, активностью по сравнению с IL-12p40 и IL-12p35 дикого типа.
Подходящие сайты на IL-12p40, в которые могут быть введены аминокислотные модификации, выбраны из группы, состоящей из: E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299 (пронумерованы в соответствии с субъединицей бета (последовательность зрелой формы IL-12p40 человеческого IL-12, изображенная на Фигуре 1). Иллюстративные модификации в этих сайтах могут быть выбраны из группы, состоящей из: D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. Варианты по аффинности IL-12p40 могут включать модификации в одном или более из этих сайтов. Соответственно, согласно одному варианту реализации вариант IL-12p40 содержит N103D/N113D/N200D/N281D. Согласно другому варианту реализации вариант IL-12p40 содержит Q42E/E45Q. Согласно другому варианту реализации вариант IL-12p40 содержит E45Q/Q56E. Согласно другому варианту реализации вариант IL-12p40 содержит Q42E/E59Q. Согласно другому варианту реализации вариант IL-12p40 содержит Q56E/E59Q. Согласно другому варианту реализации вариант IL-12p40 содержит Q42E/E45Q/Q56E. Согласно другому варианту реализации вариант IL-12p40 содержит E45Q/Q56E/E59Q. Согласно другому варианту реализации вариант IL-12p40 содержит E32Q/E59Q. Согласно другому варианту реализации вариант IL-12p40 содержит D34N/E59K. Согласно другому варианту реализации вариант IL-12p40 содержит D34N/E59K/K99E. Согласно другому варианту реализации вариант IL-12p40 содержит D34K/E59K/K99E. Согласно другому варианту реализации вариант IL-12p40 содержит E32Q/D34N/E59K/K99E. Согласно другому варианту реализации вариант IL-12p40 содержит E32K/D34N/E59K/K99E. Согласно другому варианту реализации вариант IL-12p40 содержит D34N/E59Q. Согласно другому варианту реализации вариант IL-12p40 содержит E59Q/E187Q. Согласно другому варианту реализации вариант IL-12p40 содержит S43E/E59Q. Согласно другому варианту реализации вариант IL-12p40 содержит S43K/E49Q. Согласно другому варианту реализации вариант IL-12p40 содержит E59Q/K163E. Согласно другому варианту реализации вариант IL-12p40 содержит E59Q/K99E. Согласно другому варианту реализации вариант IL-12p40 содержит E59Q/K258E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59Q/K260E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E.. Согласно другому варианту реализации вариант IL-12p40 содержит D18K/E59K/K99E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/K264E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99Y.. Согласно другому варианту реализации вариант IL-12p40 содержит E59Y/K99Y.. Согласно другому варианту реализации вариант IL-12p40 содержит E59Y/K99E.. Согласно другому варианту реализации вариант IL-12p40 содержит E45K/E59K/K99E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/Q144E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/Q144K.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/R159E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/K264E.. Согласно другому варианту реализации вариант IL-12p40 содержит D18K/E59K/K99E/K264E.. Согласно другому варианту реализации вариант IL-12p40 содержит DI8K/E59K/K99E/C252S.. Согласно другому варианту реализации вариант IL-12p40 содержит D18K/E59K/K99E/C252S/K264E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99Y/C252S.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/C252S/K264E.. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/C252S.. Согласно другому варианту реализации вариант IL-12p40 содержит N103D/N113D.. Согласно другому варианту реализации вариант IL-12p40 содержит N103D/N200D.. Согласно другому варианту реализации вариант IL-12p40 содержит N103D/N281D.. Согласно другому варианту реализации вариант IL-12p40 содержит N113D/N200D.. Согласно другому варианту осущестления вариант IL-12p40 содержит N113D/N281D.. Согласно другому варианту реализации вариант IL-12p40 содержит N200D/N281D.. Согласно другому варианту реализации вариант IL-12p40 содержит N103D/N113D/N200D.. Согласно другому варианту реализации вариант IL-12p40 содержит N103D/N113D/N281D.. Согласно другому варианту реализации вариант IL-12p40 содержит N103D/N200D/N281D.. Согласно другому варианту реализации вариант IL-12p40 содержит N113D/N200D/N281D.. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N113Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N200Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N281Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N113Q/N200Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N113Q/N281Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N200Q/N281Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N113Q/N200Q.. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N113Q/N281Q,. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N200Q/N281Q. Согласно другому варианту реализации вариант IL-12p40 содержит N113Q/N200Q/N281Q. Согласно другому варианту реализации вариант IL-12p40 содержит N103Q/N113Q/N200Q/N281Q. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N113Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N200Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N281Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/N113Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/N200Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/N281Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N113Q/N200Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N113Q/N281Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N200Q/N281Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E. Согласно другому варианту реализации вариант IL-12p40 содержит E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Кроме того, эти модификации можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по экспрессии.
Субъединица IL-12p40 имеет свободный цистеин в положении 252 (пронумеровано в соответствии с последовательностью зрелой формы субъединицы бета (IL-12p40) человеческого IL-12, изображенной на Фигуре 1), который может связываться с другими свободными цистеинами, что приводит по меньшей мере к гетерогенности, а в худшем случае приводит к иммуногенности. Соответственно, варианты IL-12p40 были сконструированы для удаления свободного цистеина, например, путем введения модификации C252S (хотя могут применяться и другие замены). Модификацию C252 (например, C252S) можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по аффинности или экспрессии. Иллюстративные варианты IL-12p40, содержащие модификацию в C252 для удаления свободного цистеина, изображены на Фигуре 65. Иллюстративные IL-12-Fc слитые белки создавали с дополнительными вариантными субъединицами IL-12p40, последовательности для которых изображены на Фигуре 66, и получали, как описано в общих чертах в Примере 1B. Кроме того, эти модификации можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по экспрессии.
Подходящие сайты на IL-12p35, в которые могут быть введены аминокислотные модификации, выбраны из группы, состоящей из: Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, F96, M97, L89, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193 и A196 (пронумерованы в соответствии с последовательностью зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12, изображенной на Фигуре 1). Иллюстративные модификации выбраны из группы, состоящей из: N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. Варианты по аффинности IL-12p35 могут включать модификации в одном или более из этих сайтов. Соответственно, согласно одному варианту реализации вариант IL-12p35 содержит N71D/N85D/N195D. Согласно другому варианту реализации вариант IL-12p35 содержит N151D/E153Q. Согласно другому варианту реализации вариант IL-12p35 содержит N151D/D165N. Согласно другому варианту реализации вариант IL-12p35 содержит Q130E/N151D. Согласно другому варианту реализации вариант IL-12p35 содержит N151D/K158E. Согласно другому варианту реализации вариант IL-12p35 содержит E79Q/N151D. Согласно другому варианту реализации вариант IL-12p35 содержит D55Q/N151D. Согласно другому варианту реализации вариант IL-12p35 содержит N136D/N151D. Согласно другому варианту реализации вариант IL-12p35 содержит N21D/N151D. Согласно другому варианту реализации вариант IL-12p35 содержит E143Q/N151D. Согласно другому варианту реализации вариант IL-12p35 содержит N71Q/N85Q. Согласно другому варианту реализации вариант IL-12p35 содержит N71Q/N195Q. Согласно другому варианту реализации вариант IL-12p35 содержит N85Q/N195Q. Согласно другому варианту реализации вариант IL-12p35 содержит N71Q/N85Q/N195Q. Согласно другому варианту реализации вариант IL-12p35 содержит N71D/N85D. Согласно другому варианту реализации вариант IL-12p35 содержит N71D/N195D. Согласно другому варианту реализации вариант IL-12p35 содержит N85D/N195D.
Кроме того, эти модификации можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p35, такими как варианты по экспрессии.
Биологически функциональный гетеродимерный комплекс IL-12 может содержать субъединицу IL-12p40 дикого типа и субъединицу IL-12p35 дикого типа, вариантную субъединицу IL-12p40 и субъединицу IL-12p35 дикого типа, субъединицу IL-12p40 дикого типа и вариантную субъединицу IL-12p35 или вариантную субъединицу IL-12p40 и вариантную субъединицу IL-12p35.
Биологически функциональный двухвалентный гомодимерный комплекс IL-12 может содержать субъединицу IL-12p40 дикого типа и субъединицу IL-12p35 дикого типа, вариантную субъединицу IL-12p40 и субъединицу IL-12p35 дикого типа, субъединицу IL-12p40 дикого типа и вариантную субъединицу IL-12p35 или вариантную субъединицу IL-12p40 и вариантную субъединицу IL-12p35.
Доменные линкеры
Согласно некоторым вариантам реализации субъединицы IL-12p35 и IL-12p40 присоединены вместе за счет линкера. Необязательно субъединицы не присоединены за счет линкера. Согласно другим вариантам реализации субъединицы IL-12p35 и IL-12p40 присоединены нековалентно. Согласно некоторым вариантам реализации субъединица IL-12p35 присоединена к домену Fc за счет линкера. Согласно определенным вариантам реализации субъединица IL-12p35 непосредственно присоединена к домену Fc, например, без линкера. Согласно другим вариантам реализации субъединица IL-12p40 присоединена к домену Fc за счет линкера. Согласно другим вариантам реализации субъединица IL-12p40 непосредственно присоединена к домену Fc. В некоторых случаях линкер не используется для присоединения субъединицы IL-12p35 или субъединицы IL-12p40 к домену Fc.
Согласно некоторым вариантам реализации настоящего изобретения линкер представляет собой «доменный линкер», используемый для связывания вместе двух любых доменов, как указано в данном документе. Несмотря на то, что может быть использован любой подходящий линкер, во многих вариантах реализации используется глицин-сериновый полимер, включая, например, (GS)n, (GSGGS)n, (GGGGS)n и (GGGS)n, где n представляет собой целое число, равное по меньшей мере 0 (и обычно от 0 до 1 до 2 до 3 до 4 и до 5), а также любая пептидная последовательность, которая обеспечивает рекомбинантное присоединение двух доменов с достаточной длиной и гибкостью с тем, чтобы каждый домен сохранял свою биологическую функцию. В некоторых случаях пригодные линкеры включают (GGGGS)0 или (GGGGS)1 или (GGGGS)2. Иллюстративные доменные линкеры изображены на Фигуре 6. В некоторых случаях, и уделяя внимание «наличию цепей», как описано ниже, могут применяться заряженные доменные линкеры.
Кроме того, ранее сообщалось, что серин в линкерах Gly-Ser в слитых белках Fc может подвергаться O-гликозилированию. Соответственно, окончательный подход к снижению гетерогенности (применительно к слитым белкам Fc) заключается в замене линкеров Gly-Ser, используемых до сих пор, линкерами Gly-Ala.
Пригодные форматы согласно данному изобретению
Как показано на Фигурах 8A-F, существует ряд пригодных форматов гетеродимерных слитых белков по данному изобретению. В целом, гетеродимерные слитые белки по данному изобретению имеют два функциональных компонента: компонент гетеродимера IL-12 и компонент Fc, оба из которых могут принимать разные формы, как описано в данном документе, и оба можно комбинировать с другим компонентом в любой конфигурации.
Согласно некоторым вариантам реализации субъединицы IL-12p35 и IL-12p40 ковалентно связаны, необязательно с доменным линкером, и упоминаются в данном документе как одноцепочечный комплекс IL-12 или «scIL-12». scIL-12 может содержать либо IL-12p35, связанную с N-концом IL-12p40, либо IL-12p40, связанную с N-концом IL-12p35, необязательно с помощью доменного линкера. Порядок двух субъединиц в scIL-12 можно обозначить следующим образом: «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p340.
Согласно некоторым вариантам реализации субъединицы IL-12p35 и IL-12p40 не связаны ковалентно, а скорее ковалентно присоединены, соответственно, к первому и второму домену Fc, которые собираются в виде гетеродимера.
Первый и второй домены Fc могут иметь набор аминокислотных замен, выбранных из группы, состоящей из a) L368D/K370S и S364K; b) L368D/K370S и S364K/E357L; c) L368D/K370S и S364K/E357Q; d) S267K/L368D/K370S; e) T411E/K360E/Q362E и D401K; f) L368E/K370S и S364K; g) K370S и S364K/E357Q; и h) T366S/L368A/Y407V и T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C и T366W/S354C) в соответствии с системой нумерации ЕС.
Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС.
Необязательно первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Необязательно, первый и (или) второй домены Fc имеют варианты 428L/434S для продления периода полужизни.
A. Формат IL-12-heteroFc
Согласно одному варианту реализации настоящего изобретения предложен N-концевой IL-12 гетеродимерный слитый белок Fc или формат «IL-12-heteroFc». Согласно этому варианту реализации, как показано на Фигуре 8A, гетеродимерный слитый белок содержит два мономера. Первый мономер содержит (от N- к C-концу) IL-12p40-необязательный доменный линкер-Fc. Второй мономер содержит (от N- к C-концу) IL-12p35-необязательный доменный линкер-Fc.
В формате IL-12-heteroFc в предпочтительном варианте реализации применяется пара искаженных вариантов S364K/E357Q : L368D/K370S.
В формате IL-12-heteroFc предпочтительный вариант реализации показан на Фигуре 9 ((XENP27201, включая цепь 1 цепь 2).
Согласно некоторым вариантам реализации формат IL-12-heteroFc обеспечивает гетеродимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p40; ii) необязательный первый доменный линкер; iii) белок первого вариантного домена Fc; и b) второй мономер, содержащий, от N- к C-концу: i) белок домена IL-12p35; ii) необязательный второй доменный линкер; iii) белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации варианты Fc содержат один или более искаженных вариантов, вариантов по pI и абляционных вариантов, предусмотренных в настоящем документе. Согласно одному варианту реализации варианты Fc содержат конкретные искаженные варианты, варианты по pI и абляционные варианты. Согласно некоторым вариантам реализации модификации, способствующие гетеродимеризации первого и второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; T366S/L368A/Y407V/Y349C и T366W/S354C, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации настоящего изобретения первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
В этом формате подходящие домены белка IL-12p40 включают, но не ограничиваются ими, SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12). В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате домены белка IL-12p35 включают SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12). В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими IL-12p40(E59K/K99Y) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99Y/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2) и IL-12p40(E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2).
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p35, содержащей SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12), и вариант IL-12p40, содержащий одну или более замен, включая, но не ограничиваясь ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате подходящие комбинации вариантов IL-12p40 и IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p40, содержащей SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и IL-12p35, содержащей N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантов IL-12p40 и IL-12p35 включают, но не ограничиваются ими, комбинацию варианта IL-12p40, содержащего одну или более аминокислотных замен, выбранных из группы, состоящей из: E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E;; и варианта IL-12p35, содержащего одну или более замен, выбранных из группы, состоящей из: N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие варианты реализации включают, но не ограничиваются ими, варианты, в которых домен вариантной субъединицы IL-12p40 присоединен к указанному первому домену Fc с использованием первого доменного линкера и (или) указанный домен субъединицы IL-12p35 присоединен к указанному второму домену Fc с использованием второго доменного линкера.
В этом формате подходящие варианты реализации включают, но не ограничиваются ими: XENP31251, XENP31254, XENP31258, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190 и XENP32191. В дополнительных вариантах реализации XENP31251, XENP31254, XENP31258, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190 и XENP32191 включают дальнейшую гликоинженерию.
В этом формате подходящие варианты реализации включают, но не ограничиваются ими, варианты, показанные на Фигурах 44A-44K и Фигурах 66A-66Q.
Формат heteroFc-IL-12
Согласно другому варианту реализации настоящего изобретения предложен С-концевой IL-12 гетеродимерный слитый белок Fc или формат «heteroFc-IL-12». Согласно этому варианту реализации, как показано на Фигуре 8B, гетеродимерный слитый белок содержит два мономера. Первый мономер содержит (от N- к C-концу) Fc-необязательный доменный линкер-IL-12p40. Второй мономер содержит (от N- к C-концу) Fc-необязательный доменный линкер-IL-12p35.
В формате heteroFc-IL-12 в предпочтительном варианте реализации применяется пара искаженных вариантов S364K/E357Q : L368D/K370S.
В формате IL-12-heteroFc предпочтительный вариант реализации показан на Фигуре 10 ((XENP27202, включая цепь 1 цепь 2).
Согласно некоторым вариантам реализации формат heteroFc-IL-12 обеспечивает гетеродимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к С-концу: i) белок первого вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p40; и b) второй мономер, содержащий, от N- к C-концу: i) белок второго вариантного домена Fc; ii) необязательный второй доменный линкер; iii) белок домена IL-12p35.
Согласно некоторым вариантам реализации варианты Fc содержат один или более искаженных вариантов, вариантов по pI и абляционных вариантов, предусмотренных в настоящем документе. Согласно одному варианту реализации варианты Fc содержат конкретные искаженные варианты, варианты по pI и абляционные варианты. Согласно некоторым вариантам реализации модификации, способствующие гетеродимеризации первого и второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; T366S/L368A/Y407V/Y349C и T366W/S354C, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
В этом формате подходящие домены белка IL-12p40 включают, но не ограничиваются ими, SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12). В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате домены белка IL-12p35 включают SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12). В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими IL-12p40(E59K/K99Y) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99Y/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2) и IL-12p40(E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2).
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p35, содержащей SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12), и варианта IL-12p40, содержащего одну или более замен, включая, но не ограничиваясь ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате подходящие комбинации вариантов IL-12p40 и IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p40, содержащей SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и IL-12p35, содержащей N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантов IL-12p40 и вариантов IL-12p35 включают, но не ограничиваются ими, комбинацию варианта IL-12p40, содержащего одну или более аминокислотных замен, выбранных из группы, состоящей из: E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E;, и варианта IL-12p35, содержащего одну или более замен, выбранных из группы, состоящей из: N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие варианты реализации включают, но не ограничиваются ими, варианты, показанные на Фигуре 10.
Формат scIL-12-Fc
Согласно дополнительному варианту реализации настоящего изобретения предложен N-концевой одноцепочечный IL-12-Fc слитый белок или формат «scIL-12-Fc». Согласно этому варианту реализации, как показано на Фигурах 8C-D, гетеродимерный слитый белок содержит два мономера. Первый мономер содержит (от N- к C-концу) scIL-12-необязательный доменный линкер-Fc. Второй мономер содержит «пустой» Fc, содержащий весь шарнир или его часть - CH2 - CH3. scIL-12 может представлять собой «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p40.
В формате scIL-12-Fc в предпочтительном варианте реализации применяется пара искаженных вариантов S364K/E357Q : L368D/K370S.
В формате scIL-12-Fc предпочтительные варианты реализации показаны на Фигуре 11 как XENP24203 (включая цепь 1 и цепь 2) и XENP24204 (включая цепь 1 и цепь 2).
В формате scIL-12-Fc предпочтительный вариант реализации показан на Фигуре 50 как XENP31290 (включая цепь 1 и цепь 2).
Согласно некоторым вариантам реализации формат scIL-12-Fc представляет собой двухвалентный IL-12-Fc слитый белок. Согласно некоторым вариантам реализации формат двухвалентного IL-12-Fc слитого белка (Фигуры 48A-B) содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с N-концом цепи гомодимерного Fc (необязательно за счет доменного линкера).
Согласно некоторым вариантам реализации формат scIL-12-Fc обеспечивает гетеродимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p40; ii) необязательный первый доменный линкер; iii) белок домена IL-12p35; iv) необязательный второй линкер; v) белок первого вариантного домена Fc; и b) второй мономер, содержащий белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации формат scIL-12-Fc обеспечивает гетеродимерный слитый белок Fc, содержащий: a) первый мономер, содержащий, от N- к C-концу: i) белок домена IL-12p35; ii) необязательный первый доменный линкер; iii) белок домена IL-12p40; iv) необязательный второй линкер; v) белок первого вариантного домена Fc; и b) второй мономер, содержащий белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации варианты Fc содержат один или более искаженных вариантов, вариантов по pI и абляционных вариантов, предусмотренных в настоящем документе. Согласно одному варианту реализации варианты Fc содержат конкретные искаженные варианты, варианты по pI и абляционные варианты. Согласно некоторым вариантам реализации модификации, способствующие гетеродимеризации первого и второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; T366S/L368A/Y407V/Y349C и T366W/S354C, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
В этом формате подходящие домены белка IL-12p40 включают, но не ограничиваются ими, SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12). В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате домены белка IL-12p35 включают SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12). В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими IL-12p40(E59K/K99Y) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99Y/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2) и IL-12p40(E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2).
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p35, содержащий SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12), и варианта IL-12p40, содержащего одну или более замен, включая, но не ограничиваясь ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате подходящие комбинации вариантов IL-12p40 и IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p40, содержащей SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и IL-12p35, содержащей N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантов IL-12p40 и вариантов IL-12p35 включают, но не ограничиваются ими, комбинацию варианта IL-12p40, содержащего одну или более аминокислотных замен, выбранных из группы, состоящей из: E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E;; и варианта IL-12p35, содержащего одну или более замен, выбранных из группы, состоящей из: N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие варианты реализации включают, но не ограничиваются ими, варианты, показанные на Фигуре 11.
Формат Fc-scIL-12
Согласно дополнительному варианту реализации настоящего изобретения предложен С-концевой одноцепочечный IL-12-Fc слитый белок или формат «Fc-scIL-12». Согласно этому варианту реализации, как показано на Фигурах 8E-F, гетеродимерный слитый белок содержит два мономера. Первый мономер содержит (от N- к C-концу) Fc-необязательный линкер-scIL-12. Второй мономер содержит «пустой» Fc, содержащий весь шарнир или его часть - CH2 - CH3. Как упоминалось выше, scIL-12 может представлять собой «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p40.
В формате Fc-scIL-12 в предпочтительном варианте реализации применяется пара искаженных вариантов S364K/E357Q : L368D/K370S.
Согласно некоторым вариантам реализации формат scIL-12-Fc представляет собой двухвалентный IL-12-Fc слитый белок. Согласно некоторым вариантам реализации формат двухвалентного IL-12-Fc слитого белка (Фигуры 48C-D) содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с С-концом цепи гомодимерного Fc (необязательно за счет доменного линкера).
Согласно некоторым вариантам реализации формат scIL-12-Fc обеспечивает гетеродимерный слитый белок Fc содержащий: a) первый мономер, содержащий, от N- к С-концу: i) белок первого вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p40; iv) необязательный второй доменный линкер; v) белок домена IL-12p35; и b) второй мономер, содержащий белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации формат scIL-12-Fc обеспечивает гетеродимерный слитый белок Fc содержащий: a) первый мономер, содержащий, от N- к С-концу: i) белок первого вариантного домена Fc; ii) необязательный первый доменный линкер; iii) белок домена IL-12p35; iv) необязательный второй доменный линкер; v) белок домена IL-12p40; и b) второй мономер, содержащий белок второго вариантного домена Fc.
Согласно некоторым вариантам реализации варианты Fc содержат один или более искаженных вариантов, вариантов по pI и абляционных вариантов, предусмотренных в настоящем документе. Согласно одному варианту реализации варианты Fc содержат конкретные искаженные варианты, варианты по pI и абляционные варианты. Согласно некоторым вариантам реализации модификации, способствующие гетеродимеризации первого и второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; T366S/L368A/Y407V/Y349C и T366W/S354C, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, содержащий G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и второй домены Fc дополнительно содержат аминокислотные замены M428L/N424S.
В этом формате подходящие домены белка IL-12p40 включают, но не ограничиваются ими, SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12). В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. В этом формате подходящие варианты IL-12p40 включают, но не ограничиваются ими, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате домены белка IL-12p35 включают SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12). В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. В этом формате подходящие варианты IL-12p35, включают, но не ограничиваются ими, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими IL-12p40(E59K/K99Y) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(D18K/E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99Y/C252S) и IL-12p35 (SEQ ID NO: 2), IL-12p40(E59K/K99E/C252S/K264E) и IL-12p35 (SEQ ID NO: 2) и IL-12p40(E59K/K99E/C252S) и IL-12p35 (SEQ ID NO: 2).
В этом формате подходящие комбинации вариантной субъединицы IL-12p40 и субъединицы IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p35, содержащей SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12), и варианта IL-12p40, содержащего одну или более замен, включая, но не ограничиваясь ими, E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
В этом формате подходящие комбинации вариантов IL-12p40 и IL-12p35 включают, но не ограничиваются ими, комбинацию IL-12p40, содержащей SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и IL-12p35, содержащей N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
В этом формате подходящие комбинации вариантов IL-12p40 и IL-12p35 включают, но не ограничиваются ими, комбинацию варианта IL-12p40, содержащего одну или более аминокислотных замен, выбранных из группы, состоящей из: E59K, E59Q, D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, E299Q, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E;; и варианта IL-12p35, содержащего одну или более замен, выбранных из группы, состоящей из: N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, N195Q, N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D.
Подходящие варианты реализации данного изобретения
Как будет понятно специалистам в данной области техники и как более подробно обсуждается ниже, гетеродимерные слитые белки по данному изобретению могут принимать большое количество разнообразных конфигураций, которые в обобщенном виде изображены на Фигурах 8A-F. Аминокислотные последовательности примерных слитых белков представлены на Фигурах 9-11.
Многие из вариантов реализации, описанных в данном документе, в целом основаны на формате, который содержит первый мономер (первый слитый белок), содержащий домен субъединицы IL-12p35, ковалентно присоединенный (необязательно за счет доменного линкера) к N-концу первого домена Fc, и второй мономер (второй слитый белок), содержащий домен субъединицы IL-12p40, ковалентно присоединенный (необязательно за счет доменного линкера) к N-концу второго домена Fc. Примерные варианты реализации этого формата включают, но не ограничиваются им, XENP27201. Согласно дополнительным вариантам реализации первый мономер имеет полипептидную последовательность, выбранную из группы, состоящей из i) SEQ ID NO: XX (XENP27201 Цепь 1), ii) SEQ ID NO: XX(XenD24752), iii) SEQ ID NO: XX(XenD24753), iv) SEQ ID NO: XX(XenD24754), v) SEQ ID NO: XX(XenD24755), vi) SEQ ID NO: XX(XenD24756), vii) SEQ ID NO: XX(XenD24757), viii) SEQ ID NO: XX(XenD24758), ix) SEQ ID NO: XX(XenD24759), x) SEQ ID NO: XX(XenD24760), xi) SEQ ID NO: XX(XenD24761), xii) SEQ ID NO: XX(XenD24762), xiii) SEQ ID NO: XX(XenD24763), xiv) SEQ ID NO: XX(XenD24764), xv) SEQ ID NO: XX(XenD24765), xvi) SEQ ID NO: XX(XenD24766), xvii) SEQ ID NO: XX(XenD24767), xviii) SEQ ID NO: XX(XenD24768), xix) SEQ ID NO: XX(XenD24769), xx) SEQ ID NO: XX(XenD24770), xxi) SEQ ID NO: XX(XenD24771), xxii) SEQ ID NO: XX(XenD24772), xxiii) SEQ ID NO: XX(XenD24773), xxiv) SEQ ID NO: XX(XenD24774), xxv) SEQ ID NO: XX(XenD24775), xxvi) SEQ ID NO: XX(XenD24776), xxvii) SEQ ID NO: XX(XenD24777), xxviii) SEQ ID NO: XX(XenD24778), xxix) SEQ ID NO: XX(XenD24792), xxx) SEQ ID NO: XX(XenD25922), xxxi) SEQ ID NO: XX(XenD25923), xxxii) SEQ ID NO: XX(XenD25924), xxxiii) SEQ ID NO: XX(XenD25925), xxxiv) SEQ ID NO: XX(XenD25926), xxxv) SEQ ID NO: XX(XenD25927), xxxvi) SEQ ID NO: XX(XenD25928), xxxvii) SEQ ID NO: XX(XenD25929), xxxviii) SEQ ID NO: XX(XenD25930) и xxxix) SEQ ID NO: XX(XenD25931); и второй мономер имеет полипептидную последовательность, выбранную из группы, состоящей из i) SEQ ID NO: XX.(XENP27201 Цепь 2), ii) SEQ ID NO: XX(XenD24779), iii) SEQ ID NO: XX(XenD24780), iv) SEQ ID NO: XX(XenD24781), v) SEQ ID NO: XX(XenD24782), vi) SEQ ID NO: XX(XenD24783), vii) SEQ ID NO: XX(XenD24784), viii) SEQ ID NO: XX(XenD24785), ix) SEQ ID NO: XX(XenD24786), x) SEQ ID NO: XX(XenD24787), xi) SEQ ID NO: XX(XenD24788), xii) SEQ ID NO: XX(XenD24789), xiii) SEQ ID NO: XX(XenD24790), xiv) SEQ ID NO: XX(XenD24791), xv) SEQ ID NO: XX(XenD25911), xvi) SEQ ID NO: XX(XenD25912), xvii) SEQ ID NO: XX(XenD25913), xviii) SEQ ID NO: XX(XenD25914), xix) SEQ ID NO: XX(XenD25915), xx) SEQ ID NO: XX(XenD25916), xxi) SEQ ID NO: XX(XenD25917), xxii) SEQ ID NO: XX(XenD25918), xxiii) SEQ ID NO: XX(XenD25919), xxiv) SEQ ID NO: XX(XenD25920) и xxv) SEQ ID NO: XX(XenD25921). Конкретные такие варианты реализации включают, но не ограничиваются ими, XENP27201, XENP28820, XENP28821, XENP28822, XENP28823, XENP28824, XENP28825, XENP28826, XENP28827, XENP28828, XENP28829, XENP28830, XENP28831, XENP28832, XENP28833, XENP28834, XENP28835, XENP28836, XENP28837, XENP28838, XENP28839, XENP28840, XENP28841, XENP28842, XENP28843, XENP28844, XENP28845, XENP28846, XENP28847, XENP28848, XENP28849, XENP28850, XENP28851, XENP28852, XENP29949, XENP29950, XENP29951, XENP29952, XENP30597, XENP30598, XENP30599, XENP30600, XENP30601, XENP30602, XENP30603, XENP30604, XENP30605, XENP30606. XENP30307, XENP30308, XENP30609, XENP31250, XENP31251, XENP31252, XENP31253, XENP31254, XENP31255, XENP31256, XENP31257, XENP31258, XENP31259, XENP31260, XENP31261, XENP31262, XENP31263, XENP31264, XENP31265, XENP31286, XENP31142, XENP31143, XENP31144, XENP31145, XENP31146, XENP31582, XENP31583, XENP31584, XENP32187, XENP32188, XENP32189, XENP32190, XENP32191, XENP32991, XENP32992, XENP32993, XENP32994, XENP32995, XENP32996, XENP32997, XENP32998, XENP32999, XENP33000, XENP33001, XENP33002, XENP33003, XENP33004, XENP33005, XENP33006, XENP33007, XENP33008, XENP33008, XENP33009, XENP33010 и XENP33011. Подходящий вариант реализации гетеродимерного слитого белка Fc содержит первый мономер (первый слитый белок), содержащий домен субъединицы IL-12p35, ковалентно присоединенный (необязательно за счет доменного линкера) к С-концу первого домена Fc, и второй мономер (второй слитый белок), содержащий домен субъединицы IL-12p40, ковалентно присоединенный (необязательно за счет доменного линкера) к С-концу второго домена Fc. Примерные варианты реализации этого формата включают, но не ограничиваются им, XENP27202.
Другой подходящий вариант реализации гетеродимерного слитого белка Fc содержит первый мономер (первый слитый белок), содержащий одноцепочечный комплекс IL-12 («scIL-12») ковалентно присоединенный (необязательно за счет доменного линкера) к N-концу первого домена Fc, и второй домен Fc (например, пустой домен Fc). scIL-12 может представлять собой «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p40. Примерные варианты реализации этого формата включают, но не ограничиваются ими, XENP27203 и XENP27204.
Другой подходящий вариант реализации гетеродимерного слитого белка Fc включает первый мономер (первый слитый белок), содержащий одноцепочечный комплекс IL-12 («scIL-12»), ковалентно присоединенный (необязательно за счет доменного линкера) к С-концу первого домена Fc, и второй домен Fc (например, пустой домен Fc). scIL-12 может представлять собой «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом (с доменным линкером или без него) субъединицы IL-12p40.
Для любого из гетеродимерных слитых белков Fc, описанных в данном документе, необязательные доменные линкеры, используемые на первом мономере, на втором мономере и (или) в scIL-12, могут быть одинаковыми или разными. Кроме того, первый домен Fc и второй домен Fc гетеродимерного белка могут иметь разные аминокислотные последовательности.
Домены Fc по данному изобретению содержат домены Fc IgG, например, домены Fc IgG1. Согласно некоторым вариантам реализации первый и второй домены Fc содержат набор аминокислотных замен, выбранных из группы, состоящей из: L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q и T366S/L368A/Y407V : T366W (необязательно включая мостиковый дисульфид, T366S/L368A/Y407V/Y349C : T366W/S354C) в соответствии с системой нумерации ЕС. В некоторых случаях первый и (или) второй домены Fc любого из форматов гетеродимерных слитых белков Fc, описанных в данном документе, могут иметь дополнительный набор аминокислотных замен, содержащий Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации ЕС. Согласно некоторым вариантам реализации первый и (или) второй домены Fc имеют дополнительный набор аминокислотных замен, выбранных из группы, состоящей из G236R/L328R, E233P/L234V/L235A/G236_/S239K, E233P/L234V/L235A/G236_/S239K/A327G, E233P/L234V/L235A/G236_/S267K/A327G, E233P/L234V/L235A/G236_, и E233P/L234V/L235A/G236_/S267K, в соответствии с системой нумерации ЕС.
Дополнительные гетеродимеризационные или гомодимеризационные варианты могут быть независимо и необязательно включены и выбраны из вариантов, описанных на фигурах. Данные композиции могут дополнительно содержать абляционные варианты, варианты по pI, заряженные варианты, изотипические варианты и т. д.
А. Варианты IL-12p40
Согласно некоторым вариантам реализации субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40. Согласно некоторым конкретным таким вариантам реализации субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую уменьшенную гетерогенность. Согласно другим конкретным вариантам реализации субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную, то есть либо уменьшенную, либо увеличенную, аффинность в отношении субъединицы бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12. Согласно некоторым вариантам реализации вариантная субъединица IL-12p40 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из E3, D7, E12, D14, W15, P17, D18, A19, P20, G21, E22, M23, D29, E32, E33, D34, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Q65, Y66, E73, K84, E86, D87, G88, I89, W90, D93, D97, K99, E100, K102, N103, K104, F106, E110, N113, Y114, D129, D142, Q144, E156, R159, D161, N162, K163, D166, D170, Q172, D174, A176, C177, P178, A179, A180, E181, S183, P185, E187, N200, S204, F206, R208, D209, D214, N218, Q220, N226, Q229, E231, E235, T242, P243, S245, Y246, F247, S248, C252, Q256, K258, K260, E262, K264, D265, D270, N281, Q289, D290, R291, Y292, Y293 и E299. (пронумерованы в соответствии с последовательностью зрелой формы субъединицы бета (IL-12p40) человеческого IL-12).
Согласно некоторым вариантам реализации вариантная субъединица IL-12p40 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, E32Q, E33Q, D34N, D34K, Q42E, S43E, S43K, E45Q, Q56E, E59Q, E59K, D62N, E73Q, D87N, K99E, K99Y, E100Q, N103D, N103Q, N113D, N113Q, Q144E, D161N, R159E, K163E, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, C252S, Q256N, K258E, K260E, E262Q, K264E, N281D, N281Q, и E299Q. Согласно некоторым вариантам реализации вариантная субъединица IL-12p40 имеет аминокислотные замены, выбранные из группы, состоящей из N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E, и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
Согласно некоторым вариантам реализации вариант IL-12p40 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 57 (IL-12p40(N103D)), ii) SEQ ID NO: 58 (IL-12p40(N113D)), iii) SEQ ID NO: 59 (IL-12p40(N200D)), iv) SEQ ID NO: 60 (IL-12p40(N281D)), v) SEQ ID NO: 61 (IL-12p40(N103D/N113D/N200D/N281D)), vi) SEQ ID NO: 62 (IL-12p40(Q42E)), vii) SEQ ID NO: 63 (IL-12p40(E45Q)), viii) SEQ ID NO: 64 (IL-12p40(Q56E)), ix) SEQ ID NO: 65 (IL-12p40(E59Q)), x) SEQ ID NO: 66 (IL-12p40(D62N)), xi) SEQ ID NO: 67 (IL-12p40(Q42E/E45Q)), xii) SEQ ID NO: 68 (IL-12p40(E45Q/Q56E)), xiii) SEQ ID NO: 69 (IL-12p40(Q42E/E59Q)), xiv) SEQ ID NO: 70 (IL-12p40(Q56E/E59Q)), xv) SEQ ID NO: 71 (IL-12p40(Q42E/E45Q/Q56E)), xvi) SEQ ID NO: 72 (IL-12p40(E45Q/Q56E/E59Q)), xvii) SEQ ID NO: 73 (IL-12p40(D161N)), xviii) SEQ ID NO: 74 (IL-12p40(E73Q)), xix) SEQ ID NO: 75 (IL-12p40(Q144E)), xx) SEQ ID NO: 76 (IL-12p40(E262Q)), xxi) SEQ ID NO: 77 (IL-12p40(E100Q)), xxii) SEQ ID NO: 78 (IL-12p40(D18N)), xxiii) SEQ ID NO: 79 (IL-12p40(E33Q)), xxiv) SEQ ID NO: 80 (IL-12p40(Q229E)), xxv) SEQ ID NO: 81 (IL-12p40(E235Q)), xxvi) SEQ ID NO: 82 (IL-12p40(Q256N)), xxvii) SEQ ID NO: 83 (IL-12p40(E299Q)), xxviii) SEQ ID NO: 84 (IL-12p40(D87N)), xxix)IL-12p40(E32Q), xxx)IL-12p40(D34N), xxxi)IL-12p40(S43E), xxxii)IL-12p40(S43K), xxxiii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)), xxxiv) SEQ ID NO: 205 (IL-12p40(E59K)), xxxv)IL-12p40(K99E), xxxvi)IL-12p40(K163E), xxxvii)IL-12p40(E187Q), xxxviii)IL-12p40(K258E), xxxix)IL-12p40(K260E), xl)SEQ ID NO: 206 (IL-12p40(E32Q/E59Q)), xli) SEQ ID NO: 207 (IL-12p40(D34N/E59Q)), xlii) SEQ ID NO: 208 (IL-12p40(E59Q/E187Q)), xliii) SEQ ID NO: 209 (IL-12p40(S43E/E59Q)), xliv) SEQ ID NO: 210 (IL-12p40(S43K/E49Q)), xlv) SEQ ID NO: 211 (IL-12p40(E59Q/K163E)), xlvi) SEQ ID NO: 212 (IL-12p40(E59Q/K99E)), xlvii) SEQ ID NO: 213 (IL-12p40(E59Q/K258E)), xlviii) SEQ ID NO: 214 (IL-12p40(E59Q/K260E)), xlix) SEQ ID NO: XXX (IL-12p40(D34N/E59K)), l) SEQ ID NO: XXX (IL-12p40(E59K/K99E)), li) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E)), lii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), liii) SEQ ID NO: XXX (IL-12p40(E59K/K99Y)), liv) SEQ ID NO: XXX (IL-12p40(E59Y/K99E)), lv) SEQ ID NO: XXX (IL-12p40(E45K/E59K/K99E)), lvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144E)), lvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/Q144K)), lviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/R159E)), lix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/K264E)), lx) SEQ ID NO: XXX (IL-12p40(D18K/E59K/K99E/K264E)), lxi) SEQ ID NO: XXX (IL-12p40(C252S)), lxii) SEQ ID NO: XXX (IL-12p40(DI8K/E59K/K99E/C252S)), lxiii) SEQ ID NO: XXX (IL-12p40 (D18K/E59K/K99E/C252S/K264E)), lxiv)SEQ ID NO: XXX (IL-12p40(E59K/K99Y/C252S)), lxv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S/K264E)), lxvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/C252S)), lxvii) SEQ ID NO: XXX (IL-12p40(N103D/N113D)), lxviii) SEQ ID NO: XXX (IL-12p40(N103D/N200D)), lxix) SEQ ID NO: XXX (IL-12p40(N103D/N281D)), lxx) SEQ ID NO: XXX (IL-12p40(N113D/N200D)), lxxi) SEQ ID NO: XXX (IL-12p40(N113D/N281D)), lxxii) SEQ ID NO: XXX (IL-12p40(N200D/N281D)), lxxiii) SEQ ID NO: XXX (IL-12p50(N103D/N113D/N200D)), lxxiv) SEQ ID NO: XXX (IL-12p40(N103D/N113D/N281D)), lxxv) SEQ ID NO: XXX (IL-12p40(N103D/N200D/N281D)), lxxvi) SEQ ID NO: XXX (IL-12p40(N113D/N200D/N281D)), lxxvii) SEQ ID NO: XXX (IL-12p40(N103Q)), lxxviii) SEQ ID NO: XXX (IL-12p40(N113Q)), lxxix) SEQ ID NO: XXX (IL-12p40(N200Q)), lxxx) SEQ ID NO: XXX (IL-12p40(N281Q)), lxxxi) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q)), lxxxii) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q)), lxxxiii) SEQ ID NO: XXX (IL-12p40(N103Q/N281Q)), lxxxiv) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q)), lxxxv) SEQ ID NO: XXX (IL-12p40(N113Q/N281Q)), lxxxvi) SEQ ID NO: XXX (IL-12p40(N200Q/N281Q)), lxxxvii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q)), lxxxviii) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N281Q)), lxxxix) SEQ ID NO: XXX (IL-12p40(N103Q/N200Q/N281Q)), xc) SEQ ID NO: XXX (IL-12p40(N113Q/N200Q/N281Q)), xci) SEQ ID NO: XXX (IL-12p40(N103Q/N113Q/N200Q/N281Q)), xcii) SEQ ID NO: XXX (IL-12p40(D34N/E59K/K99E)), xciii) SEQ ID NO: XXX (IL-12p40(D34K/E59K/K99E)), xciv) SEQ ID NO: XXX (IL-12p40(E32Q/D34N/E59K/K99E)), xcv) SEQ ID NO: XXX (IL-12p40(E32K/D34N/E59K/K99E)), xcvi) SEQ ID NO: XXX (IL-12p40(E59Y/K99Y)), xcvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/C252S/K264E)), xcviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/C252S/K264E)), xcix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/C252S/K264E)), c) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N281Q/C252S/K264E)), ci) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)), cii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)), ciii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)), civ) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)), cv) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E)), cvi) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)), cvii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)), cviii) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)) и cix) SEQ ID NO: XXX (IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)).
B. Варианты IL-12p35
Согласно некоторым вариантам реализации субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35. Согласно некоторым конкретным таким вариантам реализации субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую уменьшенную гетерогенность. Согласно другим конкретным таким вариантам реализации субъединица IL-12p35 представляет собой вариантную субъединицу IL-12p35, имеющую измененную, то есть либо уменьшенную, либо увеличенную, аффинность в отношении субъединица бета-1 (IL-12Rβ1) рецептора IL-12, субъединицы бета-2 (IL-12Rβ2) рецептора IL-12 и (или) рецепторного комплекса IL-12. Согласно некоторым вариантам реализации вариантная субъединица IL-12p35 имеет одну или более аминокислотных модификаций в аминокислотных остатках, выбранных из группы, состоящей из: Q20, N21, Q35, E38, S44, E45, E46, H49, K54, D55, T59, V60, E61, C63, L64, P65, E67, L68, N71, S73, C74, L75, N76, E79, N85, L89, F96, M97, L124, M125, Q130, Q135, N136, E143, Q146, N151, E153, K158, E162, E163, D165, I171, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193, N195 и A196. (пронумерованы в соответствии с последовательностью зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12). Согласно некоторым вариантам реализации вариантная субъединица IL-12p35 имеет одну или более аминокислотных замен, выбранных из группы, состоящей из: N21D, Q35D, E38Q, D55Q, D55K, N71D, N71Q, L75A, N76D, E79Q, N85D, N85Q, L89A, F96A, M97A, L124A, M125A, Q130E, Q135E, N136D, E143Q, Q146E, N151D, N151K, E153K, E153Q, K158E, E162Q, E163Q, D165N, I171A, N195D, и N195Q. Согласно некоторым вариантам реализации вариантная субъединица IL-12p35 имеет аминокислотные замены N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, и N85D/N195D. Согласно некоторым вариантам реализации вариантная субъединица IL-12p35 имеет полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 113 (IL-12p35(N71D)), ii) SEQ ID NO: 114 (IL-12p35(N85D)), iii) SEQ ID NO: 115 (IL-12p35(N195D)), iv) SEQ ID NO: 116 (IL-12p35(N71D/N85D/N195D)), v) SEQ ID NO: 117 (IL-12p35(E153Q)), vi) SEQ ID NO: 118 (IL-12p35(E38Q)), vii) SEQ ID NO: 119 (IL-12p35(N151D)), viii) SEQ ID NO: 120 (IL-12p35(Q135E)), ix) SEQ ID NO: 121 (IL-12p35(Q35D)), x) SEQ ID NO: 122 (IL-12p35(Q146E)), xi) SEQ ID NO: 123 (IL-12p35(N76D)), xii) SEQ ID NO: 124 (IL-12p35(E162Q)), xiii) SEQ ID NO: 125 (IL-12p35(E163Q)), xiv)IL-12p35(N21D), xv) SEQ ID NO: XXX IL-12p35(D55Q), xvi)IL-12p35(E79Q), xvii)IL-12p35(Q130E), xviii)IL-12p35(N136D), xix)IL-12p35(E143Q), xx) SEQ ID NO: 227 (IL-12p35(N151K)), xxi) SEQ ID NO: 226 (IL-12p35(E153K)), xxii)IL-12p35(K158E), xxiii)IL-12p35(D165N), xxiv) SEQ ID NO: 225 (IL-12p35(N151D/E153Q)), xxv) SEQ ID NO: 228 (IL-12p35(N151D/D165N)), xxvi) SEQ ID NO: 229 (IL-12p35(Q130E/N151D)), xxvii) SEQ ID NO: 230 (IL-12p35(N151D/K158E)), xxviii) SEQ ID NO: 231 (IL-12p35(E79Q/N151D)), xxix) SEQ ID NO: 232 (IL-12p35(D55Q/N151D)), xxx) SEQ ID NO: 233 (IL-12p35(N136D/N151D)), xxxi) SEQ ID NO: 234 (IL-12p35(N21D/N151D)), xxxii) SEQ ID NO: 235 (IL-12p35(E143Q/N151D)),xxxiii) SEQ ID NO: XXX (IL-12p35(F96A)),xxxiv) SEQ ID NO: XXX (IL-12p35(M97A)), xxxv) SEQ ID NO: XXX (IL-12p35(L89A)),xxxvi) SEQ ID NO: XXX (IL-12p35(L124A)),xxxvii) SEQ ID NO: XXX (IL-12p35(M125A)),xxxviii) SEQ ID NO: XXX (IL-12p35(L75A)), xxxiv) SEQ ID NO: XXX (IL-12p35(I171A)),xxxv) SEQ ID NO: XXX (IL-12p35(N71Q)), xxxvi) SEQ ID NO: XXX (IL-12p35(N85Q)), xxxvii) SEQ ID NO: XXX (IL-12p35(N195Q)), xxxviii) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q)),xxxix) SEQ ID NO: XXX (IL-12p35(N71Q/N195Q)),lx) SEQ ID NO: XXX (IL-12p35(N85Q/N195Q),lxi) SEQ ID NO: XXX (IL-12p35(N71Q/N85Q/N195Q)),lxii) SEQ ID NO: XXX (IL-12p35(N71D/N85D)), lxiii) SEQ ID NO: XXX (IL-12p35(N71D/N195D),lxiv) SEQ ID NO: XXX (IL-12p35(N85D/N195D)), lxv) SEQ ID NO: XXX (IL-12p35(D55Q)) и lxvi) SEQ ID NO: XXX (IL-12p35(D55K)).
C. Дополнительные варианты
Согласно некоторым вариантам реализации формат scIL-12-Fc представляет собой двухвалентный IL-12-Fc слитый белок. Согласно некоторым вариантам реализации формат двухвалентного IL-12-Fc слитого белка (Фигуры 48A-B) содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с N-концом цепи гомодимерного Fc (необязательно за счет доменного линкера). Согласно некоторым вариантам реализации формат двухвалентного IL-12-Fc слитого белка (Фигуры 48C-D) содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с С-концом цепи гомодимерного Fc (необязательно за счет доменного линкера). Примеры включают, но не ограничиваются ими, XENP31289 и XENP31291 (Фигура 49).
Согласно некоторым вариантам реализации IL-12 Fc слитые белки дополнительно конструируют для продления периода полужизни с помощью замен, содержащих M428L и N434S. Согласно некоторым вариантам реализации IL-12 Fc слитые белки дополнительно конструируют для продления периода полужизни с помощью замен, содержащих M428L/N434S. Любой из IL-12 Fc слитых белков, перечисленных в данном документе, может быть сконструирован для продления периода полужизни. Примеры включают, но не ограничиваются ими, XENP31582, XENP31583 и XENP31584 (Фигура 65).
Согласно некоторым вариантам реализации примеры гетеродимерных слитых белков Fc включают XENP27201, XENP28820, XENP28821, XENP28822, XENP28823, XENP28824, XENP28825, XENP28826, XENP28827, XENP28828, XENP28829, XENP28830, XENP28831, XENP28832, XENP28833, XENP28834, XENP28835, XENP28836, XENP28837, XENP28838, XENP28839, XENP28840, XENP28841, XENP28842, XENP28843, XENP28844, XENP28845, XENP28846, XENP28847, XENP28848, XENP28849, XENP28850, XENP28851, XENP28852, XENP29949, XENP29950, XENP29951, XENP29952, XENP30597, XENP30598, XENP30599, XENP30600, XENP30601, XENP30602, XENP30603, XENP30604, XENP30605, XENP30606. XENP30307, XENP30308, XENP30609, XENP31250, XENP31251, XENP31252, XENP31253, XENP31254, XENP31255, XENP31256, XENP31257, XENP31258, XENP31259, XENP31260, XENP31261, XENP31262, XENP31263, XENP31264, XENP31265, XENP31286, XENP31142, XENP31143, XENP31144, XENP31145, XENP31146, XENP31582, XENP31583, XENP31584, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190, XENP32191, XENP32991, XENP32992, XENP32993, XENP32994, XENP32995, XENP32996, XENP32997, XENP32998, XENP32999, XENP33000, XENP33001, XENP33002, XENP33003, XENP33004, XENP33005, XENP33006, XENP33007, XENP33008, XENP33008, XENP33009, XENP33010 и XENP33011.
Согласно некоторым вариантам реализации примеры гетеродимерного слитого белка Fc включают первый слитый белок, имеющий полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 47(XENP27201 Цепь 1), ii) SEQ ID NO: 85(XenD24752), iii) SEQ ID NO: 86(XenD24753), iv) SEQ ID NO: 87(XenD24754), v) SEQ ID NO: 88(XenD24755), vi) SEQ ID NO: 89(XenD24756), vii) SEQ ID NO: 90(XenD24757), viii) SEQ ID NO: 91(XenD24758), ix) SEQ ID NO: 92(XenD24759), x) SEQ ID NO: 93(XenD24760), xi) SEQ ID NO: 94(XenD24761), xii) SEQ ID NO: 95(XenD24762), xiii) SEQ ID NO: 96(XenD24763), xiv) SEQ ID NO: 97(XenD24764), xv) SEQ ID NO: 98(XenD24765), xvi) SEQ ID NO: 99(XenD24766), xvii) SEQ ID NO: 100(XenD24767), xviii) SEQ ID NO: 101(XenD24768), xix) SEQ ID NO: 102(XenD24769), xx) SEQ ID NO: 103(XenD24770), xxi) SEQ ID NO: 104(XenD24771), xxii) SEQ ID NO: 105(XenD24772), xxiii) SEQ ID NO: 106(XenD24773), xxiv) SEQ ID NO: 107(XenD24774), xxv) SEQ ID NO: 108(XenD24775), xxvi) SEQ ID NO: 109(XenD24776), xxvii) SEQ ID NO: 110(XenD24777), xxviii) SEQ ID NO: 111(XenD24778), xxix) SEQ ID NO: 112(XenD24792), xxx) SEQ ID NO: 215(XenD25922), xxxi) SEQ ID NO: 216(XenD25923), xxxii) SEQ ID NO: 217(XenD25924), xxxiii) SEQ ID NO: 218(XenD25925), xxxiv) SEQ ID NO: 219(XenD25926), xxxv) SEQ ID NO: 220(XenD25927), xxxvi) SEQ ID NO: 221(XenD25928), xxxvii) SEQ ID NO: 222(XenD25929), xxxviii) SEQ ID NO: 223(XenD25930), xxxix) SEQ ID NO: 224(XenD25931), xl) SEQ ID NO: XXX(XenD26411),xli) SEQ ID NO: XXX(XenD26412), xlii) SEQ ID NO: XXX(XenD26413),xliii) SEQ ID NO: XXX(XenD26414), xliv) SEQ ID NO: XXX(XenD26415), xlv) SEQ ID NO: XXX(XenD26416), xlvi) SEQ ID NO: XXX(XenD26417),xlvii) SEQ ID NO: XXX(XenD26418), xlviii) SEQ ID NO: XXX(XenD27070),xlix) SEQ ID NO: XXX(XenD27071),l) SEQ ID NO: XXX(XenD27072),li) SEQ ID NO: XXX(XenD27073), lii) SEQ ID NO: XXX(XenD27074),liii) SEQ ID NO: XXX(XenD27075),liv) SEQ ID NO: XXX(XenD27076),lv) SEQ ID NO: XXX(XenD27077) lvi) SEQ ID NO: XXX(XenD27078),lvii) SEQ ID NO: XXX(XenD28173),lviii) SEQ ID NO: XXX(XenD24876),lix) SEQ ID NO: XXX(XenD27162),lx) SEQ ID NO: XXX(XenD27163),lxi) SEQ ID NO: XXX(XenD27164),lxii) SEQ ID NO: XXX(XenD27165) lxiii) SEQ ID NO: XXX(XENP31582 Цепь 1),lxiv) SEQ ID NO: XXX(XENP31583 Цепь 1),lxv) SEQ ID NO: XXX(XENP31584 Цепь 1),lxvi) SEQ ID NO: XXX(XENP32187 Цепь 1), lxvii) SEQ ID NO: XXX(XENP32188 Цепь 1),lxviii) SEQ ID NO: XXX(XENP32189, Цепь 1), lxix) SEQ ID NO: XXX(XENP32190 Цепь 1), lxx) SEQ ID NO: XXX(XENP32191 Цепь 1),lxxi) SEQ ID NO: XXX(XENP32991 Цепь 1),lxxii) SEQ ID NO: XXX(XENP32992 Цепь 1),lxxiii) SEQ ID NO: XXX(XENP32993 Цепь 1),lxxiv) SEQ ID NO: XXX(XENP32994 Цепь 1),lxxv) SEQ ID NO: XXX(XENP32995 Цепь 1),lxxvi) SEQ ID NO: XXX(XENP32996 Цепь 1), lxxvi) SEQ ID NO: XXX(XENP32997 Цепь 1), lxxvii) SEQ ID NO: XXX(XENP32998 Цепь 1),lxxvii) SEQ ID NO: XXX(XENP32999 Цепь 1),lxxviii) SEQ ID NO: XXX(XENP33000 Цепь 1), lxxix) SEQ ID NO: XXX(XENP33001 Цепь 1), lxxx) SEQ ID NO: XXX(XENP33002 Цепь 1), lxxxi) SEQ ID NO: XXX(XENP33003 Цепь 1), lxxxii) SEQ ID NO: XXX(XENP33004 Цепь 1), lxxxiii) SEQ ID NO: XXX(XENP33005 Цепь 1),lxxxiv) SEQ ID NO: XXX(XENP33006 Цепь 1), lxxxv) SEQ ID NO: XXX(XENP33007 Цепь 1), lxxxvi) SEQ ID NO: XXX (XENP33008 Цепь 1), lxxxvii) SEQ ID NO: XXX(XENP33008 Цепь 1),lxxxviii) SEQ ID NO: XXX(XENP33009 Цепь 1),lxxxix) SEQ ID NO: XXX(XENP33010 Цепь 1) и xc) SEQ ID NO: XXX(XENP33011 Цепь 1); и указанный второй слитый белок, имеющий полипептидную последовательность, выбранную из группы, состоящей из: i) SEQ ID NO: 48(XENP27201 Цепь 2),ii) SEQ ID NO: 126(XenD24779), iii) SEQ ID NO: 127(XenD24780), iv) SEQ ID NO: 128(XenD24781), v) SEQ ID NO: 129(XenD24782), vi) SEQ ID NO: 130(XenD24783), vii) SEQ ID NO: 131(XenD24784), viii) SEQ ID NO: 132(XenD24785), ix) SEQ ID NO: 133(XenD24786), x) SEQ ID NO: 134(XenD24787), xi) SEQ ID NO: 135(XenD24788), xii) SEQ ID NO: 136(XenD24789), xiii) SEQ ID NO: 137(XenD24790), xiv) SEQ ID NO: 138(XenD24791), xv) SEQ ID NO: 236(XenD25911), xvi) SEQ ID NO: 237(XenD25912), xvii) SEQ ID NO: 238(XenD25913), xviii) SEQ ID NO: 239(XenD25914), xix) SEQ ID NO: 240(XenD25915), xx) SEQ ID NO: 241(XenD25916), xxi) SEQ ID NO: 242(XenD25917), xxii) SEQ ID NO: 243(XenD25918), xxiii) SEQ ID NO: 244(XenD25919), xxiv) SEQ ID NO: 245(XenD25920), xxv) SEQ ID NO: 246(XenD25921),xxvi) SEQ ID NO: XXX(XenD26427), xxvii) SEQ ID NO: XXX(XenD26428),xxviii) SEQ ID NO: XXX(XenD27089),xxix) SEQ ID NO: XXX(XenD27090),xxx) SEQ ID NO: XXX(XenD27091),xxxi) SEQ ID NO: XXX(XenD27092), xxxii) SEQ ID NO: XXX(XenD27093),xxxiii) SEQ ID NO: XXX(XenD27094),xxxix) SEQ ID NO: XXX(XenD24877),xl) SEQ ID NO: XXX(XenD27166),xli) SEQ ID NO: XXX(XENP31582 Цепь 2),xlii) SEQ ID NO: XXX(XENP31583 Цепь 2), xliii) SEQ ID NO: XXX(XENP31584 Цепь 2), xliv) SEQ ID NO: XXX(XENP32187 Цепь 2), xlv) SEQ ID NO: XXX(XENP32188 Цепь 2), xlvi) SEQ ID NO: XXX(XENP32189, Цепь 2), xlvii) SEQ ID NO: XXX(XENP32190 Цепь 2), xlviii) SEQ ID NO: XXX(XENP32191 Цепь 2), xlix) SEQ ID NO: XXX(XENP32991 Цепь 2), l) SEQ ID NO: XXX(XENP32992 Цепь 2), li) SEQ ID NO: XXX(XENP32993 Цепь 2), lii) SEQ ID NO: XXX(XENP32994 Цепь 2), liii) SEQ ID NO: XXX(XENP32995 Цепь 2), liv) SEQ ID NO: XXX(XENP32996 Цепь 2), lv) SEQ ID NO: XXX(XENP32997 Цепь 2), lvi) SEQ ID NO: XXX(XENP32998 Цепь 2), lvii) SEQ ID NO: XXX(XENP32999 Цепь 2), lviii) SEQ ID NO: XXX(XENP33000 Цепь 2), lix) SEQ ID NO: XXX(XENP33001 Цепь 2), lx) SEQ ID NO: XXX(XENP33002 Цепь 2), lxi) SEQ ID NO: XXX(XENP33003 Цепь 2), lxii) SEQ ID NO: XXX(XENP33004 Цепь 2), lxiii) SEQ ID NO: XXX(XENP33005 Цепь 2), lxiv) SEQ ID NO: XXX(XENP33006 Цепь 2), lxv) SEQ ID NO: XXX(XENP33007 Цепь 2), lxvi) SEQ ID NO: XXX(XENP33008 Цепь 2), lxvii) SEQ ID NO: XXX(XENP33008 Цепь 2), lxviii) SEQ ID NO: XXX(XENP33009 Цепь 2), lxix) SEQ ID NO: XXX(XENP33010 Цепь 2) и lxx) SEQ ID NO: XXX(XENP33011 Цепь 2).
Предпочтительные варианты реализации включают XENP31251, XENP31254, XENP31258, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190 и XENP32191. Согласно дополнительным вариантам реализации XENP31251, XENP31254, XENP31258, XENP32186, XENP32187, XENP32188, XENP32189, XENP32190 и XENP32191 включают дальнейшую гликоинженерию.
Нуклеиновые кислоты согласно данному изобретению
Согласно настоящему изобретению также предложены композиции нуклеиновых кислот, кодирующие гетеродимерный слитый белок Fc, субъединицы IL-12 и гетеродимерный комплекс IL-12 по данному изобретению (или, в случае белка мономерного домена Fc, также нуклеиновые кислоты, кодирующие указанный белок).
Как будет понятно специалистам в данной области техники, композиции нуклеиновых кислот будут зависеть от формата гетеродимерного белка. Таким образом, например, когда для формата требуется три аминокислотные последовательности, то три последовательности нуклеиновой кислоты могут быть включены в один или более экспрессионных векторов для экспрессии. Точно так же для некоторых форматов необходимы только две нуклеиновые кислоты; опять же, они могут быть помещены в один или два экспрессионных вектора.
Как известно в данной области техники, нуклеиновые кислоты, кодирующие компоненты согласно данному изобретению, могут быть включены в экспрессионные векторы, известные в данной области техники, и, в зависимости от клеток-хозяев, использоваться для получения гетеродимерных слитых белков Fc согласно данному изобретению. Как правило, нуклеиновые кислоты функционально связаны с любым количеством регуляторных элементов (промоторов, точек начала репликации, селектируемых маркеров, сайтов связывания рибосом, индукторов и т.д.). Экспрессионные векторы могут представлять собой внехромосомные или интегрирующие векторы.
Затем нуклеиновые кислоты и (или) экспрессионные векторы по данному изобретению трансформируют в любое количество различных типов клеток-хозяев, как хорошо известно в данной области техники, включая клетки млекопитающих, бактерий, дрожжей, насекомых и (или) грибов, при этом клетки млекопитающих (например, клетки СНО) находят применение во многих вариантах реализации.
Согласно некоторым вариантам реализации каждая из нуклеиновых кислот, кодирующая каждый мономер, в зависимости от формата, содержится в одном экспрессионном векторе, как правило, под контролем различных или одинаковых промоторов. В вариантах реализации данного изобретения с особой применимостью в данном изобретении каждая из этих двух или трех нуклеиновых кислот содержится в разных экспрессионных векторах.
Гетеродимерный слитый белок Fc согласно данному изобретению получают путем культивирования клеток-хозяев, содержащих экспрессионный (экспрессионные) вектор (векторы), как хорошо известно в данной области техники. После получения выполняются традиционные стадии очистки слитых белков или антител, включая - стадия ионообменной хроматографии. Как обсуждается в данном документе, наличие значений pI двух мономеров, отличающихся по меньшей мере на 0,5, может способствовать разделению с помощью метода ионообменной хроматографии или изоэлектрической фокусировки, или других способов, чувствительных к изоэлектрической точке. То есть, вводят в состав замены по pI, которые изменяют изоэлектрическую точку (pI) каждого мономера, таким образом, что каждый мономер имеет другое значение pI и гетеродимер также имеет другое значение pI, что, таким образом, облегчает изоэлектрическую очистку гетеродимера (например, с использованием анионообменных колонок, катионообменных колонок). Указанные замены также облегчают определение и мониторинг любых загрязняющих гомодимеров после очистки (например, гели ИЭФ, кИЭФ и аналитические ионообменные (ИО) колонки).
Биологическая и биохимическая функциональная возможность IL-12 гетеродимерных иммуномодулирующих слитых белков Fc
Обычно слитые белки Fc по данному изобретению вводят пациентам, страдающим раком, и оценивают эффективность с помощью ряда способов, описанных в данном документе. Таким образом, наряду с проведением стандартных анализов эффективности, таких как определение раковой нагрузки, размера опухоли, наличия или степени метастазирования и т. д., эффективность лечения с применением иммуноонкологических препаратов также можно оценивать на основе параметров иммунного статуса. Это можно осуществлять с помощью ряда способов, включая анализы как in vitro, так и in vivo. Например, может быть проведена оценка изменений в иммунном статусе (например, наличие ICOS+ CD4+ T-клеток после лечения ipi) наряду с «традиционными» измерениями, такими как опухолевая нагрузка, размер опухоли, инвазивность, вовлечение ЛУ, метастазирование и т.д. Таким образом, можно оценить любой или все из следующих параметров: ингибирующие эффекты PVRIG на активацию или пролиферацию CD4+ T-клеток, активацию или пролиферацию CD8+ T (ЦТК) клеток, цитотоксическую активность, опосредуемую CD8+ T-клетками, и (или) ЦТК-опосредуемое истощение клеток, активность NK-клеток и истощение клеток, опосредуемое NK-клетками, потенцирующие эффекты PVRIG на дифференцировку и пролиферацию Treg-клеток и иммуносупрессию или иммунотолерантность, опосредуемую Treg- или супрессорными клетками миелоидного происхождения (СКМП), и (или) эффекты PVRIG на продукцию провоспалительных цитокинов иммунными клетками, например, продукцию IL-2, ИФН-ɣ или ФНО-α Т-клетками или другими иммунными клетками.
Согласно некоторым вариантам реализации оценку лечения выполняют путем исследования пролиферации иммунных клеток, применяя, например, метод разведения КФСЭ (англ. «CFSE»), внутриклеточное окрашивание иммунных эффекторных клеток по Ki67 и метод включения 3H-тимидина.
Согласно некоторым вариантам реализации оценку лечения выполняют путем исследования повышения экспрессии генов или повышенных уровней белков маркеров, ассоциированных с активацией, включая один или более из: CD25, CD69, CD137, ICOS, PD1, GITR, OX40, а также измерения дегрануляции клеток по поверхностной экспрессии CD107A.
Как правило, анализы экспрессии генов проводят, как известно в данной области техники.
Как правило, измерения экспрессии белка также выполняются аналогично тому, как это известно в данной области техники.
Согласно некоторым вариантам реализации настоящего изобретения оценку лечения проводят путем анализа цитотоксической активности, измеренной путем определения жизнеспособности клеток-мишеней посредством оценки многочисленных клеточных параметров, таких как ферментная активность (включая протеазную активность), проницаемость клеточной мембраны, адгезия клеток, продукция АТФ, продуцирование кофермента и активность поглощения нуклеотидов. Конкретные примеры таких анализов включают в себя, но не ограничиваются лишь этими: способ с окрашиванием трипановым синим или PI, способ с высвобождением 51Cr или 35S, анализ активности ЛДГ, анализы МТТ и (или) WST, анализ кальцеина-AM, анализ на основе люминесценции и другие.
Согласно некоторым вариантам реализации оценку лечения выполняют путем оценки активности T-клеток, измеренной по продукции цитокинов, при этом в культуральном супернатанте измеряют внутриклеточную продукцию цитокинов, включая, но не ограничиваясь ими, ИФНγ, ФНО-α, ГМ-КСФ, IL2, IL6, IL4, IL5, IL10, IL13, с применением хорошо известных методик.
Соответственно, оценку лечения можно выполнять с использованием анализов, с помощью которых исследуют один или более из следующих параметров: (i) повышение иммунного ответа, (ii) повышение активации αβ и (или) γδ T-клеток, (iii) повышение активности цитотоксических T-клеток, (iv) повышение активности NK- и (или) NKT-клеток, (v) ослабление супрессии αβ и (или) γδ Т-клеток, (vi) повышение секреции провоспалительных цитокинов, (vii) повышение секреции IL-2; (viii) повышение продукции интерферона-ɣ, (ix) повышение ответа Th1, (x) снижение ответа Th2, (xi) снижение или элиминация количества клеток и (или) активности по меньшей мере одной из регуляторных Т-клеток (Treg).
Анализы для измерения эффективности и активности
Согласно некоторым вариантам реализации настоящего изобретения активация Т-клеток оценивается с помощью анализа реакции смешанной культуры лимфоцитов (СКЛ, англ. «MLR») так, как известно в данной области техники. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение иммунного ответа, как измеряют, например, по фосфорилированию или дефосфорилированию различных факторов, или путем измерения других посттрансляционных модификаций. IL-12 опосредует экспрессию и секрецию ИФН- посредством фосфорилирования STAT4 (Morinobu et al., 2002). Соответственно, согласно некоторым вариантам реализации с помощью анализа сигнального пути измеряют повышение или снижение иммунного ответа, на что указывает фосфорилирование STAT4. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение активации αβ и (или) γδ T-клеток, как измеряют, например, по секреции цитокинов или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т.д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение активности цитотоксических Т-клеток, как измеряют, например, по непосредственному уничтожению клеток-мишеней, таких как, например, раковые клетки, или по секреции цитокинов, или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации настоящего изобретения с помощью анализа сигнального пути измеряют повышение или снижение активности NK и (или) NKT-клеток, как измеряют, например, по непосредственному уничтожению клеток-мишеней, таких как, например, раковые клетки, или по секреции цитокинов, или по изменениям в экспрессии маркеров активации, таких как, для примера, CD107a и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение супрессии αβ и (или) γδ Т-клеток, как измеряют, например, по секреции цитокинов или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т.д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение секреции провоспалительных цитокинов, как измеряют, например, с помощью ИФА, или с помощью методов на основе гранул Luminex или Multiplex, или с помощью внутриклеточного окрашивания и анализа FACS, или с помощью Alispot и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение секреции IL-2, как измеряют, например, с помощью ИФА, или с помощью методов на основе гранул Luminex или Multiplex, или с помощью внутриклеточного окрашивания и анализа FACS, или с помощью Alispot и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации данного изобретения с помощью анализа сигнального пути измеряют увеличение или уменьшение продукции интерферона-γ, как измеряют, например, с помощью ИФА, или с помощью методов на основе гранул Luminex или Multiplex, или с помощью внутриклеточного окрашивания и анализа FACS, или с помощью Alispot и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации, с помощью анализа сигнального пути измеряют повышение или снижение ответа Th1-клеток, как измеряют, например, по секреции цитокинов или по изменениям в экспрессии маркеров активации. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации, с помощью анализа сигнального пути измеряют повышение или снижение ответа Th2-клеток, как измеряют, например, по секреции цитокинов или по изменениям в экспрессии маркеров активации. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации, с помощью анализа сигнального пути измеряют увеличение или уменьшение количества клеток и (или) активности по меньшей мере одного из регуляторных Т-клеток (Treg-клеток), как измеряют, например, с помощью проточной цитометрии или ИГХ. Снижение ответа указывает на иммуностимулирующую активность. Соответствующие снижения являются такими же, как и для повышений, описанных ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение количества клеток макрофагов М2, как измеряют, например, с помощью проточной цитометрии или ИГХ. Снижение ответа указывает на иммуностимулирующую активность. Соответствующие снижения являются такими же, как и для повышений, описанных ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение проонкогенной активности макрофагов М2, как измеряют, например, по секреции цитокинов или по изменениям экспрессии маркеров активации. Снижение ответа указывает на иммуностимулирующую активность. Соответствующие снижения являются такими же, как и для повышений, описанных ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение увеличения количества нейтрофилов N2, как измеряют, например, с помощью метода проточной цитометрии или ИГХ. Снижение ответа указывает на иммуностимулирующую активность. Соответствующие снижения являются такими же, как и для повышений, описанных ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение проонкогенной активности нейтрофилов N2, как измеряют, например, по секреции цитокинов или по изменениям экспрессии маркеров активации. Снижение ответа указывает на иммуностимулирующую активность. Соответствующие снижения являются такими же, как и для повышений, описанных ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение ингибирования активации Т-клеток, как измеряют, например, по секреции цитокинов или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т.д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение ингибирования активации ЦТК, как измеряют, например, по непосредственному уничтожению клеток-мишеней, таких как, например, раковые клетки, или по секреции цитокинов, или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации, с помощью анализа сигнального пути измеряют повышение или снижение истощения αβ и (или) γδ Т-клеток, как измеряют, например, по изменениям в экспрессии маркеров активации. Снижение ответа указывает на иммуностимулирующую активность. Соответствующие снижения являются такими же, как и для повышений, описанных ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение ответа αβ и (или) γδ Т-клеток, как измеряют, например, по секреции цитокинов или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т.д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации с помощью анализа сигнального пути измеряют повышение или снижение стимуляции антигенспецифичных ответов памяти, как измеряют, например, по секреции цитокинов или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD45RA, CCR7 и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации данного изобретения с помощью анализа сигнального пути измеряют увеличение или уменьшение апоптоза или лизиса раковых клеток, как измеряют, например, с помощью анализов цитотоксичности, таких как, например, анализ MTT, анализ высвобождения Cr, анализ кальцеина AM, или с помощью анализов на основе проточной цитометрии, как в примере разведения CFSE или окрашивания йодидом пропидия и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации настоящего изобретения с помощью анализа сигнального пути измеряют повышение или снижение стимуляции цитотоксического или цитостатического эффекта на раковые клетки, как измеряют, например, с помощью анализов цитотоксичности, таких как, например, анализ MTT, анализ высвобождения Cr, анализ кальцеина AM, или с помощью анализов на основе проточной цитометрии, таких как, для примера, разведение КФСЭ или окрашивание йодидом пропидия и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации данного изобретения с помощью анализа сигнального пути измеряют увеличение или уменьшение непосредственного уничтожения раковых клеток, как измеряют, например, с помощью анализов цитотоксичности, таких как, например, анализ MTT, анализ высвобождения Cr, анализ кальцеина AM, или с помощью анализов на основе проточной цитометрии, как в примере разведения CFSE или окрашивания йодидом пропидия и т.д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации, с помощью анализа сигнального пути измеряют повышение или снижение активности Th17-клеток, как измеряют, например, по секреции цитокинов или по пролиферации, или по изменениям в экспрессии маркеров активации. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации настоящего изобретения с помощью анализа сигнального пути измеряют повышение или снижение индукции комплемент-зависимой цитотоксичности и (или) антителозависимой клеточно-опосредованной цитотоксичности, как измеряют, например, с помощью анализов цитотоксичности, таких как, например, анализ MTT, анализ высвобождения Cr, анализ кальцеина AM, или с помощью анализов на основе проточной цитометрии, таких как, для примера, разведение КФСЭ или окрашивание йодидом пропидия и т. д. Повышение активности указывает на иммуностимулирующую активность. Соответствующие повышения активности описаны ниже.
Согласно одному варианту реализации активацию Т-клеток измеряют, например, по непосредственному уничтожению клеток-мишеней, таких как, например, раковые клетки, или по секреции цитокинов, или по пролиферации, или по изменениям экспрессии маркеров активации, таких как, например, CD137, CD107a, PD1 и т. д. Для Т-клеток повышение пролиферации, повышение маркеров активации на клеточной поверхности (например, CD25, CD69, CD137, PD1), цитотоксичности (способности уничтожать клетки-мишени) и продукции цитокинов (например, IL-2, IL-4, IL-6, ИФНγ, ФНО-α, IL-10, IL-17A) могут указывать на иммунную модуляцию, которая может согласовываться с усиленным уничтожением раковых клеток.
Согласно одному варианту реализации активацию NK-клеток измеряют, например, по непосредственному уничтожению клеток-мишеней, таких как, например, раковые клетки, или по секреции цитокинов, или по изменениям экспрессии маркеров активации, таких как, например, CD107a и т. д. Для NK-клеток повышение пролиферации, цитотоксичности (способности уничтожать клетки-мишени и повышение экспрессии CD107a, гранзима и перфоринa), продукции цитокинов (например, ИФН-γ и ФНО) и экспрессии рецепторов клеточной поверхности (например, CD25) могут указывать на иммунную модуляцию, которая может согласовываться с усиленным уничтожением раковых клеток.
Согласно одному варианту реализации активацию γδ T-клеток измеряют, например, по секреции цитокинов, или по пролиферации, или по изменениям в экспрессии маркеров активации.
Согласно одному варианту реализации, активацию Th1-клеток измеряют, например, по секреции цитокинов, или по изменениям в экспрессии маркеров активации.
Соответствующие повышения активности или ответа (или снижения, в зависимости от ситуации, как описано выше) представляют собой повышения на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или от 98% до 99% по сравнению с сигналом либо в эталонном образце, либо в контрольных образцах, например, в тестовых образцах, которые не содержат IL-12 гетеродимерный слитый белок по данному изобретению. Аналогичным образом, повышение по меньшей мере в один, два, три, четыре или пять раз, по сравнению с эталонными или контрольными образцами, указывает на эффективность.
Комбинированная терапия
Согласно некоторым аспектам IL-12-Fc слитые белки, описанные в данном документе, вводят в комбинации с другим терапевтическим агентом. Фраза «вводят в комбинации с», используемая в данном документе, означает, что субъекту проводят два (или более) разных вида лечения в ходе протекания у субъекта расстройства, например, два или более вида лечения проводят после того, как у субъекта было диагностировано расстройство и до того, как расстройство было вылечено или устранено, или лечение было прекращено по другим причинам. Согласно некоторым вариантам реализации настоящего изобретения проведение одного вида лечения все еще происходит, когда начинается проведение второго вида лечения, так что существует частичное совпадение с точки зрения введения. Это иногда упоминается в данном документе как «одновременная» или «параллельная доставка». Согласно другим вариантам реализации данного изобретения один вид лечения заканчивается до того, как начинается другой вид лечения. Согласно некоторым вариантам реализации настоящего изобретения, в любом из указанных случаев лечение является более эффективным благодаря комбинированному введению. Например, второй вид лечения является более эффективным, например, эквивалентный эффект наблюдается при меньшем количестве второго вида лечения, или второй вид лечения уменьшает симптомы в большей степени, чем было бы, если бы второй вид лечения проводился в отсутствие первого вида лечения, или аналогичная ситуация наблюдается при первом виде лечения. В некоторых вариантах реализации данного изобретения лечение доставляется таким образом, что уменьшение симптома или другого параметра, связанного с расстройством, превышает то, уменьшение, которое наблюдалось бы при проведении одного вида лечения при отсутствии другого. Эффект от двух видов лечения может быть частично аддитивным, полностью аддитивным или более сильным, чем аддитивный. Доставка лечения может быть такой, что эффект от проведения первого вида лечения все еще будет обнаруживаться при проведении второго.
IL-12-Fc слитые белки (например, любую последовательность XENP, описанную в данном документе), описанные в данном документе, и по меньшей мере один дополнительный терапевтический агент можно вводить одновременно, в одной и той же или в отдельных композициях, или последовательно. В случае последовательного введения IL-12-Fc слитые белки (например, любая последовательность XENP, описанная в данном документе), описанные в данном документе, могут быть введены первыми, а дополнительный агент может быть введен вторым, или порядок введения может быть обратным.
IL-12-Fc слитые белки (например, любая последовательность XENP, описанная в данном документе), описанные в данном документе, и (или) другие терапевтические агенты, процедуры или способы воздействия могут быть введены в периоды активного нарушения или в течение периода ремиссии, или в периоды менее активного заболевания. IL-12-Fc слитые белки (например, любая последовательность XENP, описанная в данном документе) могут быть введены перед другим видом лечения, одновременно с лечением, после лечения или во время ремиссии нарушения.
Антитела, блокирующие контрольные точки
Согласно некоторым вариантам реализации IL-12-Fc слитые белки, описанные в данном документе, комбинируют с другими терапевтическими агентами, включая антитела, блокирующие контрольные точки, такие как, но не ограничиваясь ими, ингибитор PD-1, ингибитор TIM3, ингибитор CTLA4, ингибитор PD-L1, ингибитор TIGIT, ингибитор LAG3 или их комбинация.
Антитела к PD-L1
Согласно некоторым вариантам реализации IL-12-Fc слитые белки, описанные в данном документе, могут быть введены субъекту, страдающему раком, в комбинации с антителом к PD-1. В некоторых случаях антитело к PD-1 включает XENP16432 (двухвалентное МАТ к PD-1, ингибитор контрольной точки, который усиливает противоопухолевую активность путем устранения репрессии приживленных человеческих Т-клеток; последовательности, изображенные на Фигуре 53).
Согласно некоторым вариантам реализации IL-12-Fc слитые белки по данному изобретению вводят в комбинации с китруда (Keytruda®) или оптиво (Optivo®).
Иллюстративные неограничивающие молекулы антитела к PD-1 раскрыты в патентной публикации США № 2015/0210769, опубликованной 30 июля 2015 г. и озаглавленной «Молекулы антител против PD-1 и их использование» (“Antibody Molecules to PD-1 and Uses Thereof”), которая включена в данный документ посредством ссылки в полном объеме.
Согласно одному варианту реализации настоящего изобретения молекула антитела к PD-1 содержит по меньшей мере один или два вариабельных домена тяжелой цепи (необязательно включая константную область), по меньшей мере один или два вариабельных домена легкой цепи (необязательно включая константную область), или и то и другое, включая аминокислотную последовательность BAP049-Clone-A, BAP049-Clone-B, BAP049-Clone-C, BAP049-Clone-D или BAP049-Clone-E; или те, которые описаны в Таблице 1 из US 2015/0210769, или кодируется нуклеотидной последовательностью в Таблице 1; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей. Молекула антитела к PD-1, необязательно, содержит лидерную последовательность из тяжелой цепи, легкой цепи или обеих цепей, как показано в Таблице 4 из патентной публикации США № 2015/0210769; или последовательность, по существу идентичную ей.
Согласно еще одному варианту реализации молекула антитела к PD-1 содержит по меньшей мере одну, две или три области, определяющие комплементарность (CDR), из вариабельной области тяжелой цепи и (или) вариабельной области легкой цепи антитела, описанного в данном документе, например, антитела, выбранного из любого из BAP049-hum01, BAP049-hum02, BAP049-hum03, BAP049-hum04, BAP049-hum05, BAP049-hum06, BAP049-hum07, BAP049-hum08, BAP049-hum09, BAP049-hum10, BAP049-hum11, BAP049-hum12, BAP049-hum13, BAP049-hum14, BAP049-hum15, BAP049-hum16, BAP049-Clone-A, BAP049-Clone-B, BAP049-Clone-C, BAP049-Clone-D или BAP049-Clone-E; или те, которые описаны в Таблице 1, или кодируется нуклеотидной последовательностью в Таблице 1; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей.
В еще одном варианте реализации данного изобретения молекула антитела к PD-1 содержит по меньшей мере одну, две или три CDR (или в совокупности все CDR) из вариабельной области тяжелой цепи и содержит аминокислотную последовательность, продемонстрированную в Таблице 1 из патентной публикации США № 2015/0210769, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1.
В еще одном варианте реализации данного изобретения молекула антитела к PD-1 содержит по меньшей мере одну, две или три CDR (или в совокупности все CDR) из вариабельной области легкой цепи и содержит аминокислотную последовательность, продемонстрированную в Таблице 1 из патентной публикации США № 2015/0210769, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно определенным вариантам реализации настоящего изобретения молекула антитела к PD-1 содержит замену в CDR легкой цепи, например, одну или более замен в CDR1, CDR2 и (или) CDR3 легкой цепи. Согласно одному варианту реализации настоящего изобретения молекула антитела к PD-1 содержит замену в CDR3 легкой цепи в положении 102 вариабельной области легкой цепи, например, замену цистеина остатком тирозина, или цистеина остатком серина, в положении 102 вариабельной области легкой цепи в соответствии с Таблицей 1 (например, SEQ ID NO: 16 или 24 - для мышиной или химерной, немодифицированной последовательности; или любая из SEQ ID NO: 34, 42, 46, 54, 58, 62, 66, 70, 74 или 78 для модифицированной последовательности).
В другом варианте реализации данного изобретения молекула антитела к PD-1 содержит по меньшей мере одну, две, три, четыре, пять или шесть CDR (или в совокупности все CDR) из вариабельной области тяжелой и легкой цепей и содержит аминокислотную последовательность, продемонстрированную в Таблице 1 из патентной публикации США № 2015/0210769, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1.
В одном из вариантов реализации данного изобретения молекула антитела к PD-1 содержит:
(a) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1 из SEQ ID NO: 4, аминокислотную последовательность VHCDR2 из SEQ ID NO: 5 и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 13, аминокислотную последовательность VLCDR2 из SEQ ID NO: 14 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 33, каждая из которых раскрыта в Таблице 1 из US 2015/0210769;
(b) VH, содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 1; аминокислотную последовательность VHCDR2 из SEQ ID NO: 2; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 10, аминокислотную последовательность VLCDR2 из SEQ ID NO: 11 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 32, каждая из которых раскрыта в Таблице 1 из US 2015/0210769;
(c) VH, содержащую аминокислотную последовательность VHCDR1 из SEQ ID NO: 224, аминокислотную последовательность VHCDR2 из SEQ ID NO: 5 и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 13, аминокислотную последовательность VLCDR2 из SEQ ID NO: 14 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 33, каждая из которых раскрыта в Таблице 1 из US 2015/0210769; или
(d) VH, содержащую аминокислотную последовательность VHCDR1 из SEQ ID NO: 224; аминокислотную последовательность VHCDR2 из SEQ ID NO: 2; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 10, аминокислотную последовательность VLCDR2 из SEQ ID NO: 11 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 32, каждая из которых раскрыта в Таблице 1 из US 2015/0210769.
Согласно другому варианту реализации молекула антитела к PD-1 содержит (i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 1, SEQ ID NO: 4 или SEQ ID NO: 224; аминокислотную последовательность VHCDR2 из SEQ ID NO: 2 или SEQ ID NO: 5; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3; и (ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 10 или SEQ ID NO: 13, аминокислотную последовательность VLCDR2 из SEQ ID NO: 11 или SEQ ID NO: 14 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 32 или SEQ ID NO: 33, каждая из которых раскрыта в Таблице 1 из US 2015/0210769.
Согласно другим вариантам реализации данного изобретения ингибитор PD-1 представляет собой антитело к PD-1, выбранное из ниволумаба, пембролизумаба или пидилизумаба.
Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-1 представляет собой ниволумаб. Альтернативные названия ниволумаба включают MDX-1106, MDX-1106-04, ONO-4538 или BMS-936558. Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-1 представляет собой ниволумаб (регистрационный номер CAS: 946414-94-4). Ниволумаб представляет собой полностью человеческое моноклональное антитело IgG4, которое специфично блокирует PD1. Ниволумаб (клон 5C4) и другие человеческие моноклональные антитела, которые специфично связываются с PD1, раскрыты в US 8008449 и WO2006/121168. Согласно одному варианту реализации настоящего изобретения ингибитор PD-1 представляет собой ниволумаб и имеет последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере, на 85%, на 90%, на 95% или более идентична указанной последовательности). Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-1 представляет собой пембролизумаб. Пембролизумаб (также упоминается как ламбролизумаб, MK-3475, MK03475, SCH-900475 или KEYTRUDA®; Merck) представляет собой гуманизированное моноклональное антитело IgG4, которое связывается с PD-1. Пембролизумаб и другие гуманизированные антитела к PD-1 раскрыты в Hamid, O. et al. (2013) New England Journal of Medicine 369 (2): 134-44, в US 8354509 и WO2009/114335.
Согласно одному варианту реализации ингибитор PD-1 представляет собой пембролизумаб, раскрытый, например, в US 8354509 и WO 2009/114335, и имеющий последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-1 представляет собой пидилизумаб. Пидилизумаб (CT-011; Cure Tech) представляет собой гуманизированное моноклональное антитело IgG1k, которое связывается с PD1. Пидилизумаб и другие гуманизированные моноклональные антитела к PD-1 раскрыты в патентных публикациях США № 8747847 и WO 2009/101611.
Другие антитела к PD1 включают AMP 514 (Amplimmune), среди прочих, например, антитела к PD1, раскрытые в US 8609089, US 2010028330 и (или) US 20120114649.
Согласно некоторым вариантам реализации настоящего изобретения ингибитор PD-1 представляет собой иммуноадгезин (например, иммуноадгезин, содержащий внеклеточную или связывающую PD-1 часть из PD-L1 или PD-L2, слитую с константной областью (например, областью Fc из иммуноглобулиновой последовательности). Согласно некоторым вариантам реализации настоящего изобретения ингибитор PD-1 представляет собой AMP-224 (B7-DCIg; Amplimmune; например, раскрытый в WO2010/027827 и WO2011/066342), который представляет собой растворимый слитый рецептор PD-L2-Fc, который блокирует взаимодействие между PD-1 и B7-H1.
Согласно некоторым вариантам реализации настоящего изобретения антитела к PD-1 можно применять в комбинации с IL-12 Fc слитым белком по данному изобретению. Существует несколько антител к PD-1, включая, но не ограничиваясь ими, два антитела, одобренные в настоящее время Управлением по контролю качества пищевых продуктов и лекарственных средств США (FDA), пембролизумаб и ниволизумаб, а также антитела, проходящие в настоящее время клинические исследования, включая, но не ограничиваясь ими, тислелизумаб, Sym021, REGN2810 (разработано Rengeneron), JNJ-63723283 (разработано J & J), SHR-1210, пидилизумаб, AMP-224, MEDIo680, PDR001 и CT-001, а также другие, перечисленные в Liu et al., J. Hemat. & Oncol. (2017) 10: 136, указанные антитела явным образом включены в данный документ посредством ссылки.
Согласно некоторым вариантам реализации настоящего изобретения IL-12-Fc слитый белок, описанный в данном документе, можно применять в комбинации с ингибитором PD-1 (например, антителом к PD-1). Согласно определенным вариантам реализации IL-12-Fc слитый белок (например, любую последовательность XENP, описанную в данном документе), описанный в данном документе, вводят в комбинации с антителом к PD-1.
Антитела к TIM3
Согласно некоторым вариантам реализации IL-12-Fc слитые белки по данному изобретению вводят в комбинации с антителом к TIM3.
Согласно некоторым вариантам реализации IL-12-Fc слитые белки по данному изобретению вводят в комбинации с LY3321367 (Eli Lilly and Company), MBG453 (Novartis Pharmaceuticals) и TSR-022 (Tesaro, Inc.).
Иллюстративные неограничивающие молекулы антител против TIM-3 раскрыты в патентной публикации США № 2015/0218274, опубликованной 6 августа 2015 г. и озаглавленной «Молекулы антител к TIM-3 и их использование» (“Antibody Molecules to TIM-3 and Uses Thereof”), которая включена в данный документ посредством ссылки в полном объеме.
Согласно одному варианту реализации настоящего изобретения молекула антитела к TIM-3 содержит по меньшей мере один или два вариабельных домена тяжелой цепи (необязательно включая константную область), по меньшей мере один или два вариабельных домена легкой цепи (необязательно включая константную область), или и то и другое, включая аминокислотную последовательность ABTIM3, ABTIM3-hum01, ABTIM3-hum02, ABTIM3-hum03, ABTIM3-hum04, ABTIM3-hum05, ABTIM3-hum06, ABTIM3-hum07, ABTIM3-hum08, ABTIM3-hum09, ABTIM3-hum10, ABTIM3-hum11, ABTIM3-hum12, ABTIM3-hum13, ABTIM3-hum14, ABTIM3-hum15, ABTIM3-hum16, ABTIM3-hum17, ABTIM3-hum18, ABTIM3-hum19, ABTIM3-hum20, ABTIM3-hum21, ABTIM3-hum22, ABTIM3-hum23; или те, которые описаны в Таблицах 1-4 из US 2015/0218274, или кодируется нуклеотидной последовательностью в Таблицах 1-4; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей. Молекула антитела к TIM-3, необязательно, содержит лидерную последовательность из тяжелой цепи, легкой цепи или из обеих цепей, как продемонстрировано в патентной публикации США № 2015/0218274; или последовательность, по существу идентичную ей.
Согласно еще одному варианту реализации молекула антитела к TIM-3 содержит по меньшей мере одну, две или три области, определяющие комплементарность (CDR), из вариабельной области тяжелой цепи и (или) из вариабельной области легкой цепи антитела, описанного в данном документе, например, антитела, выбранного из любого из ABTIM3, ABTIM3-hum01, ABTIM3-hum02, ABTIM3-hum03, ABTIM3-hum04, ABTIM3-hum05, ABTIM3-hum06, ABTIM3-hum07, ABTIM3-hum08, ABTIM3-hum09, ABTIM3-hum10, ABTIM3-hum11, ABTIM3-hum12, ABTIM3-hum13, ABTIM3-hum14, ABTIM3-hum15, ABTIM3-hum16, ABTIM3-hum17, ABTIM3-hum18, ABTIM3-hum19, ABTIM3-hum20, ABTIM3-hum21, ABTIM3-hum22, ABTIM3-hum23; или те, которые описаны в Таблицах 1-4 из US 2015/0218274; или кодируется нуклеотидной последовательностью в Таблицах 1-4; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей.
В еще одном варианте реализации данного изобретения молекула антитела к TIM-3 содержит по меньшей мере одну, две или три CDR (или в совокупности все CDR) из вариабельной области тяжелой цепи, содержащей аминокислотную последовательность, продемонстрированную в Таблицах 1-4 из патентной публикации США № 2015/0218274, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблицах 1-4. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблицах 1-4, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблицах 1-4.
В еще одном варианте реализации данного изобретения молекула антитела к TIM-3 содержит по меньшей мере одну, две или три CDR (или в совокупности все CDR) из вариабельной области легкой цепи, содержащей аминокислотную последовательность, продемонстрированную в Таблицах 1-4 из патентной публикации США № 2015/0218274, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблицах 1-4. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблицах 1-4, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблицах 1-4. Согласно определенным вариантам реализации настоящего изобретения молекула антитела к TIM-3 содержит аминокислотную замену в CDR легкой цепи, например, одну или более замен в CDR1, CDR2 и (или) CDR3 легкой цепи.
В другом варианте реализации данного изобретения молекула антитела к TIM-3 содержит по меньшей мере одну, две, три, четыре, пять или шесть CDR (или в совокупности все CDR) из вариабельной области тяжелой и легкой цепи, содержащей аминокислотную последовательность, продемонстрированную в Таблицах 1-4 из патентной публикации США № 2015/0218274, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблицах 1-4. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблицах 1-4, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблицах 1-4.
Согласно одному варианту реализации настоящего изобретения молекула антитела к TIM-3 содержит:
(a) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 9; аминокислотную последовательность VHCDR2 из SEQ ID NO: 10; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 5; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 12, аминокислотную последовательность VLCDR2 из SEQ ID NO: 13 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 14, каждая из которых раскрыта в Таблицах 1-4 из US 2015/0218274;
(b) VH, содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 3; аминокислотную последовательность VHCDR2 из SEQ ID NO: 4; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 5; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 6, аминокислотную последовательность VLCDR2 из SEQ ID NO: 7 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 8, каждая из которых раскрыта в Таблицах 1-4 из US 2015/0218274;
(c) VH, содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 9; аминокислотную последовательность VHCDR2 из SEQ ID NO: 25; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 5; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 12, аминокислотную последовательность VLCDR2 из SEQ ID NO: 13 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 14, каждая из которых раскрыта в Таблицах 1-4 из US 2015/0218274;
(d) VH, содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 3; аминокислотную последовательность VHCDR2 из SEQ ID NO: 24; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 5; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 6, аминокислотную последовательность VLCDR2 из SEQ ID NO: 7 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 8, каждая из которых раскрыта в Таблицах 1-4 из US 2015/0218274;
(e) VH, содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 9; аминокислотную последовательность VHCDR2 из SEQ ID NO: 31; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 5; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 12, аминокислотную последовательность VLCDR2 из SEQ ID NO: 13 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 14, каждая из которых раскрыта в Таблицах 1-4 из US 2015/0218274; или
(f) VH, содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 3; аминокислотную последовательность VHCDR2 из SEQ ID NO: 30; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 5; и VL, содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 6, аминокислотную последовательность VLCDR2 из SEQ ID NO: 7 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 8, каждая из которых раскрыта в Таблицах 1-4 из US 2015/0218274.
Примерные антитела к TIM-3 раскрыты в патенте США № 8552156, WO 2011/155607, EP 2581113 и публикации США № 2014/044728.
Согласно некоторым вариантам реализации настоящего изобретения антитела к TIM-3 можно применять в комбинации с IL-12 Fc слитым белком по данному изобретению. В клинической разработке находятся несколько антител к TIM-3, включая, но не ограничиваясь ими, MBG453 и TSR-022.
Согласно некоторым вариантам реализации настоящего изобретения IL-12-Fc слитый белок, описанный в данном документе, можно применять в комбинации с ингибитором TIM-3 (например, антителом к TIM3). Согласно определенным вариантам реализации IL-12 Fc слитый белок (например, любую последовательность XENP, описанную в данном документе), описанный в данном документе, вводят в комбинации с антителом к TIM3.
Антитела к CTLA4
Примеры антител к CTLA4 включают тремелимумаб (моноклональное антитело IgG2, доступное от Pfizer, ранее известное как тицилимумаб, CP-675,206); и ипилимумаб (антитело к CTLA-4, также известное как MDX-010, номер CAS 477202-00-9). Другие иллюстративные антитела к CTLA-4 раскрыты, например, в патенте США № 5811097.
Согласно одному варианту реализации антитело к CTLA4 представляет собой ипилимумаб, раскрытый, например, в US 5811097, US 7605238, WO00/32231 и WO97/20574, и имеющий последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно одному варианту реализации антитело к CTLA4 представляет собой тремелимумаб, раскрытый, например, в US 6682736 и WO 00/37504, и имеющий последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитела к CTLA-4 можно применять в комбинации с IL-12-Fc слитым белком по данному изобретению. Таким образом, подходящие антитела к CTLA-4 для использования в комбинированной терапии, как описано в данном документе, включают, но не ограничиваются ими, ипилимумаб - антитело, одобренное в настоящее время FDA, и несколько других антител, находящихся в разработке, включая CP-675, 206 и AGEN-1884. Согласно некоторым вариантам реализации настоящего изобретения IL-12-Fc слитый белок, описанный в данном документе, можно применять в комбинации с ингибитором CTLA-4 (например, антителом к CTLA-4). Согласно определенным вариантам реализации IL-12-Fc слитые белки (например, любую последовательность XENP, описанную в данном документе), описанные в данном документе, вводят в комбинации с антителом к CTLA-4.
Антитела к PD1
Примерные неограничивающие молекулы антител к PD-1 раскрыты в US 2016/0108123, опубликованной 21 апреля 2016 г. и озаглавленной «Молекулы антител к PD-L1 и варианты их применения» (“Antibody Molecules to PD-L1 and Uses Thereof”), которая полностью включена посредством ссылки.
Согласно одному варианту реализации настоящего изобретения молекула антитела к PD-1 содержит по меньшей мере один или два вариабельных домена тяжелой цепи (необязательно включая константную область), по меньшей мере один или два вариабельных домена легкой цепи (необязательно включая константную область), или и то и другое, включая аминокислотную последовательность любого из BAP058-hum01, BAP058-hum02, BAP058-hum03, BAP058-hum04, BAP058-hum05, BAP058-hum06, BAP058-hum07, BAP058-hum08, BAP058-hum09, BAP058-hum10, BAP058-hum11, BAP058-hum12, BAP058-hum13, BAP058-hum14, BAP058-hum15, BAP058-hum16, BAP058-hum17, BAP058-Clone-K, BAP058-Clone-L, BAP058-Clone-M, BAP058-Clone-N или BAP058-Clone-O; или те, которые описаны в Таблице 1 из US 2016/0108123, или кодируется нуклеотидной последовательностью в Таблице 1; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей.
Согласно еще одному варианту реализации молекула антитела к PD-L1 содержит по меньшей мере одну, две или три области, определяющие комплементарность (CDR), из вариабельной области тяжелой цепи и (или) вариабельной области легкой цепи антитела, описанного в данном документе, например, антитела, выбранного из любого из BAP058-hum01, BAP058-hum02, BAP058-hum03, BAP058-hum04, BAP058-hum05, BAP058-hum06, BAP058-hum07, BAP058-hum08, BAP058-hum09, BAP058-hum10, BAP058-hum11, BAP058-hum12, BAP058-hum13, BAP058-hum14, BAP058-hum15, BAP058-hum16, BAP058-hum17, BAP058-Clone-K, BAP058-Clone-L, BAP058-Clone-M, BAP058-Clone-N или BAP058-Clone-O; или те, которые описаны в Таблице 1 из US 2016/0108123, или кодируется нуклеотидной последовательностью в Таблице 1; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей.
Согласно еще одному варианту реализации молекула антитела к PD-1 содержит по меньшей мере одну, две или три CDR (или в совокупности все CDR) из вариабельной области тяжелой цепи, включая аминокислотную последовательность, показанную в Таблице 1 из US 2016/0108123, или кодируется нуклеотидной последовательностью, показанной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1.
Согласно еще одному варианту реализации молекула антитела к PD-1 содержит по меньшей мере одну, две или три CDR (или в совокупности все CDR) из вариабельной области легкой цепи, включая аминокислотную последовательность, показанную в Таблице 1 из US 2016/0108123, или кодируется нуклеотидной последовательностью, показанной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно определенным вариантам реализации настоящего изобретения молекула антитела к PD-1 содержит замену в CDR легкой цепи, например, одну или более замен в CDR1, CDR2 и (или) CDR3 легкой цепи.
Согласно другому варианту реализации молекула антитела к PD-L1 содержит по меньшей мере одну, две, три, четыре, пять или шесть областей CDR (или в совокупности все CDR) из вариабельной области тяжелой и легкой цепей, включая аминокислотную последовательность, показанную в Таблице 1, или кодируется нуклеотидной последовательностью, показанной в Таблице 1 из US 2016/0108123. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1.
Согласно одному варианту реализации молекула антитела к PD-1 содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 1, SEQ ID NO: 4 или SEQ ID NO: 195; аминокислотную последовательность VHCDR2 из SEQ ID NO: 2; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3, каждая из которых раскрыта в Таблице 1 из US 2016/0108123; и
(ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 9, аминокислотную последовательность VLCDR2 из SEQ ID NO: 10 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 11, каждая из которых раскрыта в Таблице 1 из US 2016/0108123.
Согласно другому варианту реализации молекула антитела к PD-L1 содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 1, SEQ ID NO: 4 или SEQ ID NO: 195; аминокислотную последовательность VHCDR2 из SEQ ID NO: 5; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3, каждая из которых раскрыта в Таблице 1 из US 2016/0108123; и
(ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 12, аминокислотную последовательность VLCDR2 из SEQ ID NO: 13 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 14, каждая из которых раскрыта в Таблице 1 из US 2016/0108123.
Согласно одному варианту реализации настоящего изобретения молекула антитела к PD-L1 содержит аминокислотную последовательность VHCDR1 из SEQ ID NO: 1. Согласно другому варианту реализации молекула антитела к PD-L1 содержит аминокислотную последовательность VHCDR1 из SEQ ID NO: 4. Согласно еще одному варианту реализации молекула антитела к PD-L1 содержит аминокислотную последовательность VHCDR1 из SEQ ID NO: 195, каждая из которых раскрыта в Таблице 1 из US 2016/0108123.
Согласно некоторым вариантам реализации настоящего изобретения ингибитор PD-L1 представляет собой молекулу антитела. Согласно некоторым вариантам реализации настоящего изобретения ингибитор PD-L1 выбран из YW243.55.S70, MPDL3280A, MEDI-4736, MSB-0010718C, MDX-1105, атезолизумаба, дурбалумаба, авелумаба или BMS936559.
Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-L1 представляет собой атезолизумаб. Атезолизумаб (также упоминаемый как MPDL3280A и Atezo®; Roche) представляет собой моноклональное антитело, которое связывается с PD-L1. Атезолизумаб и другие гуманизированные антитела к PD-L1 раскрыты в US 8217149 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-L1 представляет собой авелумаб. Авелумаб (также упоминаемый как A09-246-2; Merck Serono) представляет собой моноклональное антитело, которое связывается с PD-L1. Авелумаб и другие гуманизированные антитела к PD-L1 раскрыты в US 9324298 и WO2013/079174 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-L1 представляет собой дурвалумаб. Дурвалумаб (также упоминаемый как MEDI4736; AstraZeneca) представляет собой моноклональное антитело, которое связывается с PD-L1. Дурвалумаб и другие гуманизированные антитела к PD-L1 раскрыты в US 8779108 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитело к PD-L1 представляет собой BMS-936559. BMS-936559 (также упоминаемый как MDX-1105; BMS) представляет собой моноклональное антитело, которое связывается с PD-L1. BMS-936559 и другие гуманизированные антитела к PD-L1 раскрыты в US 7943743 и WO2007005874 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитела к PD-1 можно применять в комбинации с IL-12-Fc слитым белком по данному изобретению. Существует несколько антител к PD-L1, включая три антитела, одобренные в настоящее время FDA, атезолизумаб, авелумаб, дурвалумаб, а также те, которые проходят клинические исследования в настоящее время, включая, но не ограничиваясь ими, LY33000054 и CS1001, а также другие, описанные в Liu et al. др., J. Hemat. & Oncol. (2017) 10: 136, указанные антитела явным образом включены в данный документ посредством ссылки.
Согласно некоторым вариантам реализации настоящего изобретения IL-12-Fc слитый белок, описанный в данном документе, можно применять в комбинации с ингибитором PD-L1 или PD-L2 (например, антителом к PD-L1).
Антитела к TIGIT
Согласно некоторым вариантам реализации настоящего изобретения антитело к TIGIT представляет собой OMP-313M32. OMP-313M32 (OncoMed Pharmaceuticals) представляет собой моноклональное антитело, которое связывается с TIGIT. OMP-313M32 и другие гуманизированные антитела к TIGIT раскрыты в US 20160376365 и WO2016191643 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитело к TIGIT представляет собой BMS-986207. BMS-986207 (также обозначаемый как ONO-4686; Bristol-Myers Squibb) представляет собой моноклональное антитело, которое связывается с TIGIT. BMS-986207 и другие гуманизированные антитела к TIGIT раскрыты в US20160176963 и WO2016106302 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитело к TIGIT представляет собой MTIG7192 MTIG7192 (Genentech) представляет собой моноклональное антитело, которое связывается с TIGIT. MTIG7192 и другие гуманизированные антитела к TIGIT раскрыты в US2017088613, WO2017053748 и WO2016011264 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Согласно некоторым вариантам реализации настоящего изобретения антитела к TIGIT можно применять в комбинации с IL-12-Fc слитым белком по данному изобретению. В клинической разработке находятся несколько антител к TIGIT, BMS-986207, OMP-313M32 и MTIG7192A.
Согласно некоторым вариантам реализации настоящего изобретения IL-12-Fc слитый белок, описанный в данном документе, можно применять в комбинации с ингибитором TIGIT (например, антителом к TIGIT). Согласно определенным вариантам реализации IL-12-Fc слитый белок (например, любую последовательность XENP, описанную в данном документе), описанный в данном документе, вводят в комбинации с антителом к TIGIT.
Антитела к LAG3
Иллюстративные неограничивающие молекулы антитела к LAG-3 раскрыты в патентной публикации США № 2015/0259420, опубликованной 17 сентября 2015 г. и озаглавленной «Молекулы антител против LAG-3 и их применения» (“Antibody Molecules to LAG-3 and Uses Thereof”), которая включена в данный документ посредством ссылки в полном объеме.
Согласно одному варианту реализации настоящего изобретения молекула антитела к LAG-3 содержит по меньшей мере один или два вариабельных домена тяжелой цепи (необязательно включая константную область), по меньшей мере один или два вариабельных домена легкой цепи (необязательно включая константную область), или и то и другое, включая аминокислотную последовательность любого из BAP050-hum01, BAP050-hum02, BAP050-hum03, BAP050-hum04, BAP050-hum05, BAP050-hum06, BAP050-hum07, BAP050-hum08, BAP050-hum09, BAP050-hum10, BAP050-hum11, BAP050-hum12, BAP050-hum13, BAP050-hum14, BAP050-hum15, BAP050-hum16, BAP050-hum17, BAP050-hum18, BAP050-hum19, BAP050-hum20, huBAP050(Ser) (например, BAP050-hum01-Ser, BAP050-hum02-Ser, BAP050-hum03-Ser, BAP050-hum04-Ser, BAP050-hum05-Ser, BAP050-hum06-Ser, BAP050-hum07-Ser, BAP050-hum08-Ser, BAP050-hum09-Ser, BAP050-hum10-Ser, BAP050-hum11-Ser, BAP050-hum12-Ser, BAP050-hum13-Ser, BAP050-hum14-Ser, BAP050-hum15-Ser, BAP050-hum18-Ser, BAP050-hum19-Ser или BAP050-hum20-Ser), BAP050-Clone-F, BAP050-Clone-G, BAP050-Clone-H, BAP050-Clone-I или BAP050-Clone-J; или те, которые описаны в Таблице 1 из US 2015/0259420, или кодируется нуклеотидной последовательностью в Таблице 1; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей.
Согласно еще одному варианту реализации молекула антитела к LAG-3 содержит по меньшей мере одну, две или три области, определяющие комплементарность (CDR), из вариабельной области тяжелой цепи и (или) вариабельной области легкой цепи антитела, описанного в данном документе, например, антитела, выбранного из любого из BAP050-hum01, BAP050-hum02, BAP050-hum03, BAP050-hum04, BAP050-hum05, BAP050-hum06, BAP050-hum07, BAP050-hum08, BAP050-hum09, BAP050-hum10, BAP050-hum11, BAP050-hum12, BAP050-hum13, BAP050-hum14, BAP050-hum15, BAP050-hum16, BAP050-hum17, BAP050-hum18, BAP050-hum19, BAP050-hum20, huBAP050(Ser) (например, BAP050-hum01-Ser, BAP050-hum02-Ser, BAP050-hum03-Ser, BAP050-hum04-Ser, BAP050-hum05-Ser, BAP050-hum06-Ser, BAP050-hum07-Ser, BAP050-hum08-Ser, BAP050-hum09-Ser, BAP050-hum10-Ser, BAP050-hum11-Ser, BAP050-hum12-Ser, BAP050-hum13-Ser, BAP050-hum14-Ser, BAP050-hum15-Ser, BAP050-hum18-Ser, BAP050-hum19-Ser или BAP050-hum20-Ser), BAP050-Clone-F, BAP050-Clone-G, BAP050-Clone-H, BAP050-Clone-I или BAP050-Clone-J; или те, которые описаны в Таблице 1 из US 2015/0259420, или кодируется нуклеотидной последовательностью в Таблице 1; или последовательность, которая по существу идентична (например, идентична по меньшей мере на 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% или более) любой из упомянутых выше последовательностей.
Согласно еще одному варианту реализации молекула антитела к LAG-3 содержит по меньшей мере одну, две или три области CDR (или в совокупности все CDR) из вариабельной области тяжелой цепи, которая содержит аминокислотную последовательность, продемонстрированную в Таблице 1 из патентной публикации США № 2015/0259420, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1.
Согласно еще одному варианту реализации молекула антитела к LAG-3 содержит по меньшей мере одну, две или три области CDR (или в совокупности все CDR) из вариабельной области легкой цепи, которая содержит аминокислотную последовательность, продемонстрированную в Таблице 1 из патентной публикации США № 2015/0259420, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно определенным вариантам реализации настоящего изобретения молекула антитела к PD-1 содержит замену в CDR легкой цепи, например, одну или более замен в CDR1, CDR2 и (или) CDR3 легкой цепи.
Согласно другому варианту реализации молекула антитела к LAG-3 содержит по меньшей мере одну, две, три, четыре, пять или шесть областей CDR (или в совокупности все CDR) из вариабельной области тяжелой и легкой цепей, которая содержит аминокислотную последовательность, продемонстрированную в Таблице 1 из патентной публикации США № 2015/0259420, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1. Согласно одному варианту реализации настоящего изобретения одна или несколько CDR (или в совокупности все CDR) имеют одно, два, три, четыре, пять, шесть или более изменений, например, аминокислотные замены или делеции, относительно аминокислотной последовательности, продемонстрированной в Таблице 1, или кодируется нуклеотидной последовательностью, продемонстрированной в Таблице 1.
Согласно одному варианту реализации молекула антитела к LAG-3 содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 1, SEQ ID NO: 4 или SEQ ID NO: 286; аминокислотную последовательность VHCDR2 из SEQ ID NO: 2; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3, каждая из которых раскрыта в Таблице 1 из US 2015/0259420; и
(ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 10, аминокислотную последовательность VLCDR2 из SEQ ID NO: 11 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 12, каждая из которых раскрыта в Таблице 1 из US 2015/0259420.
Согласно другому варианту реализации молекула антитела к LAG-3 содержит:
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность VHCDR1, выбранную из SEQ ID NO: 1, SEQ ID NO: 4 или SEQ ID NO: 286; аминокислотную последовательность VHCDR2 из SEQ ID NO: 5; и аминокислотную последовательность VHCDR3 из SEQ ID NO: 3, каждая из которых раскрыта в Таблице 1 из US 2015/0259420; и
(ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность VLCDR1 из SEQ ID NO: 13, аминокислотную последовательность VLCDR2 из SEQ ID NO: 14 и аминокислотную последовательность VLCDR3 из SEQ ID NO: 15, каждая из которых раскрыта в Таблице 1 из US 2015/0259420.
Согласно одному варианту реализации настоящего изобретения молекула антитела к LAG-3 содержит аминокислотную последовательность VHCDR1 из SEQ ID NO: 1. Согласно другому варианту реализации молекула антитела к LAG-3 содержит аминокислотную последовательность VHCDR1 из SEQ ID NO: 4. Согласно еще одному варианту реализации молекула антитела к LAG-3 содержит аминокислотную последовательность VHCDR1 из SEQ ID NO: 286, каждая из которых раскрыта в Таблице 1 из US 2015/0259420.
Согласно некоторым вариантам реализации настоящего изобретения антитело к LAG-3 представляет собой BMS-986016. BMS-986016 (также обозначаемый как BMS986016; Bristol-Myers Squibb) представляет собой моноклональное антитело, которое связывается с LAG-3. BMS-986016 и другие гуманизированные антитела к LAG-3 раскрыты в патентных публикациях US 2011/0150892, WO2010/019570 и WO2014/008218.
Согласно некоторым вариантам реализации антитело к LAG3 представляет собой LAG525. LAG525 (также упоминается как IMP701; Novartis) представляет собой моноклональное антитело, которое связывается с LAG3. LAG525 и другие гуманизированные антитела к LAG3 раскрыты в US 9244059 и WO2008132601 и имеют последовательность, раскрытую в данном документе (или последовательность, по существу идентичную или аналогичную ей, например, последовательность, которая по меньшей мере на 85%, 90%, 95% или более идентична указанной последовательности).
Другие примерные антитела к LAG3 раскрыты, например, в US2011150892 и US2018066054.
Согласно некоторым вариантам реализации настоящего изобретения антитела к LAG-3 можно применять в комбинации с IL-12-Fc слитым белком по данному изобретению. В клинической разработке находятся несколько антител к LAG-3, включая REGN3767 от Regeneron, BMS-986016 (Bristol-Myers Squibb), MK-4280 (Merck), LAG525 (Novartis) и TSR-033 (Tesaro).
Согласно некоторым вариантам реализации настоящего изобретения IL-12-Fc слитый белок, описанный в данном документе, можно применять в комбинации с ингибитором LAG3 (например, антителом к LAG3). Согласно определенным вариантам реализации IL-12-Fc слитый белок (например, любую последовательность XENP, описанную в данном документе), описанный в данном документе, вводят в комбинации с антителом к LAG3.
Виды лечения
После получения, композиции согласно данному изобретению находят применение в ряде онкологических применений при лечении онкологических заболеваний, как правило, путем стимуляции активации Т-клеток (например, Т-клетки больше не подавляются) связыванием гетеродимерных белков, слитых с Fc, согласно данному изобретению.
Соответственно, гетеродимерные композиции по данному изобретению находят применение в лечении указанных видов рака.
Композиции слитых белков для введения in vivo
Составы слитых белков, используемые в соответствии с данным изобретением, готовят для хранения путем смешивания слитого белка, имеющего целевую степень чистоты, с необязательными фармацевтически приемлемыми носителями, вспомогательными веществами или стабилизаторами (как в целом описано в Remington's Pharmaceutical Sciences 16 изд., Osol, A. Ed. [1980]), в форме лиофилизированных составов или водных растворов.
B. Способы введения
Слитые белки и химиотерапевтические агенты по данному изобретению вводят субъекту в соответствии с известными способами, такими как внутривенное введение в виде болюса или путем непрерывной инфузии в течение определенного периода времени.
Методы лечения
В способах согласно данному изобретению терапевтические средства используются для обеспечения положительного терапевтического ответа в отношении заболевания или патологического состояния. Под «положительным терапевтическим ответом» подразумевается нормализация заболевания или состояния и (или) нормализация симптомов, связанных с заболеванием или патологическим состоянием. Например, положительный терапевтический ответ может относиться к одному или нескольким из следующих видов положительной динамики заболевания: (1) снижение количества неопластических клеток; (2) повышенная гибель неопластических клеток; (3) ингибирование выживания неопластических клеток; (5) ингибирование (т.е. замедление до некоторой степени, предпочтительно остановкa) опухолевого роста; (6) повышенная выживаемость пациентов; и (7) некоторое ослабление одного или нескольких симптомов, связанных с заболеванием или патологическим состоянием.
Положительные терапевтические ответы при любом заболевании или патологическом состоянии могут быть определены с помощью стандартизированных критериев ответа, специфичных в отношении данного заболевания или патологического состояния. Реакцию опухоли можно оценивать в отношении изменений морфологии опухоли (т.е., общей опухолевой нагрузки, размера опухоли и т.п.) с использованием методик скрининга, таких как магнитно-резонансная томография (МРТ), рентгенография, компьютерная томография (КТ), сканирование костей скелета, эндоскопия и биопсия опухоли, включая аспирация костного мозга (BMA) и подсчет опухолевых клеток в кровотоке.
В дополнение к этим положительным терапевтическим ответам, субъект, проходящий лечение, может испытывать положительный эффект в виде ослабления симптомов, связанных с заболеванием.
Согласно данному изобретению, лечение содержит «терапевтически эффективное количество» используемых лекарственных препаратов. «Терапевтически эффективное количество» означает то количество, которое является эффективным для достижения желаемого терапевтического результата в дозировках и в течение требуемых периодов времени.
Терапевтически эффективное количество может варьировать в зависимости от таких факторов, как течение заболевания, возраст, пол и масса тела индивидуума, а также способность лекарственных препаратов вызывать желаемый ответ у индивидуума. Терапевтически эффективное количество также представляет собой количество, при котором любые токсические или вредные эффекты белка или части белка компенсируются терапевтически полезными эффектами.
«Терапевтически эффективное количество» в случае терапии опухолей также может быть измерено по его способности стабилизировать прогрессирование заболевания. Способность соединения ингибировать рак может быть оценена в животной модельной системе, прогнозирующей эффективность для онкологических заболеваний человека.
В качестве альтернативы, это свойство композиции может быть оценено путем исследования способности соединения ингибировать клеточный рост или индуцировать апоптоз с помощью анализов in vitro, известных специалисту в данной области техники. Терапевтически эффективное количество терапевтического соединения может приводить к уменьшению размера опухоли или иным образом ослаблять симптомы у субъекта. Рядовой специалист в данной области техники сможет определить такие количества на основе таких факторов, как размер субъекта, степень тяжести симптомов субъекта и конкретный состав композиции или выбранный способ введения.
Режимы введения доз корректируются для обеспечения оптимального желаемого ответа (например, терапевтического ответа). Например, может вводиться однократная болюсная доза, могут вводиться несколько разделенных доз в течение некоторого времени или доза может быть пропорционально понижена или повышена сообразно потребностям терапевтической ситуации. Композиции для парентерального введения могут быть составлены в виде стандартной лекарственной формы для простоты введения и единообразия введения доз. Используемое в данном документе выражение «стандартная лекарственная форма» обозначает физически раздельные единицы, подходящие в качестве однократных доз для субъектов, подлежащих лечению; каждая единица содержит заранее установленное количество активного соединения, рассчитанное на то, чтобы вызвать необходимый терапевтический эффект, в сочетании с необходимым фармацевтическим носителем.
Спецификация для стандартной лекарственной формы согласно данному изобретению обусловлена и напрямую зависит от (a) уникальных характеристик активного соединения и конкретного терапевтического эффекта, которого необходимо достичь и (b) ограничений, свойственных области техники составления такого активного соединения для лечения чувствительности у индивидуумов.
Эффективные дозы и режимы введения доз для гетеродимерных белков, используемых в данном изобретении, зависят от заболевания или патологического состояния, подлежащего лечению и могут быть определены специалистами в данной области техники.
Примерный неограничивающий диапазон терапевтически эффективного количества гетеродимерных белков, используемых в данном изобретении, составляет около 0,1-100 мг/кг.
Все цитируемые ссылки явно включены в данный документ посредством ссылки в их полном объеме.
Принимая во внимание то, что конкретные варианты реализации данного изобретения были описаны выше в иллюстративных целях, специалистам в данной области техники будет понятно, что могут быть выполнены многочисленные вариации деталей без отклонения от изобретения, описанного в прилагаемой формуле изобретения.
ПРИМЕРЫ
Ниже приведены примеры для иллюстрации данного изобретения. Эти примеры не предназначены для ограничения данного изобретения каким-либо конкретным применением или принципом работы. Для всех положений константных областей, обсуждаемых в данном изобретении, нумерация осуществляется в соответствии с индексом EU, как по Кабату (Kabat et al., 1991, Sequences of Proteins of Immunological Interest, 5th Ed., United States Public Health Service, National Institutes of Health, Bethesda; данная публикация включена в данный документ посредством ссылки в полном объеме). Специалисты в области техники антител поймут, что это соглашение состоит из непоследовательной нумерации в конкретных областях последовательности иммуноглобулина, что позволяет нормализовать ссылку на консервативные положения в семействах иммуноглобулинов. Соответственно, положения любого указанного иммуноглобулина, определенные согласно индексу EU, не обязательно будут соответствовать его последовательной последовательности.
Общие и конкретные научные методики изложены в патентных публикациях США 2015/0307629, 2014/0288275 и WO2014/145806, все из которых прямо включены в данный документ посредством ссылки во всей их полноте и, в частности, для описанных в них методик.
Пример 1:IL-12-Fc слитые белки
Как и в случае других цитокинов, IL-12 имеет короткий период полужизни, и лечение высокими дозами для преодоления короткого периода полужизни приводит к системной токсичности. Кроме того, также сообщалось, что противоопухолевый эффект требует устойчивой индукции продукции ИФН-γ с помощью IL-12 (Gollob, JA et al., 2000). Кроме того, субъединица IL-12p40, как в виде мономера, так и гомодимера, как сообщается, оказывает антагонистическое действие на активность IL-12 путем конкуренции за связывание с рецепторами IL-12 (Gillessen, S et al., 1995); соответственно, образование предварительного комплекса субъединиц IL-12p40 и IL-12p35 является предпочтительным. Чтобы устранить эти две проблемы, авторы изобретения сконструировали гетеродимер IL-12 в виде слитых белков Fc (в совокупности называемых в данном документе IL-12-Fc слитыми белками) как для усиления циркуляции посредством рециркуляции, опосредуемой FcRn, так и для образования предварительного комплекса субъединиц IL-12p40 и IL-12p35.
1A: Конструирование IL-12-Fc слитых белков в различных форматах
Авторы изобретения создали N-концевой IL-12 гетеродимерный слитый белок Fc или формат «IL-12-heteroFc», который содержит субъединицу IL-12p40, рекомбинантно слитую с N-концом одной стороны гетеродимерного Fc, и субъединицу IL-12p35, рекомбинантно слитую с N-концом другой стороны гетеродимерного Fc (Фигура 8A). Субъединицы IL-12p40 и IL-12p35 могут быть связаны с их соответствующими цепями Fc с помощью доменного линкера. Иллюстративный белок этого формата представляет собой XENP27201, последовательности для которого изображены на Фигуре 9.
Авторы изобретения также создали C-концевой IL-12 гетеродимерный слитый белок Fc или формат «heteroFc-IL-12», который содержит субъединицу IL-12p40, рекомбинантно слитую с С-концом одной стороны гетеродимерного Fc, и субъединицу IL-12p35, рекомбинантно слитую с С-концом другой стороны гетеродимерного Fc (Фигура 8B). Субъединицы IL-12p30 и IL-12p35 могут быть связаны с их соответствующими цепями Fc с помощью доменного линкера. Иллюстративный белок этого формата представляет собой XENP27202, последовательности для которого изображены на Фигуре 10.
Далее авторы изобретения создали N-концевой одноцепочечный IL-12-Fc слитый белок или формат «scIL-12-Fc», который содержит одноцепочечный комплекс IL-12 (или «комплекс scIL-12»), рекомбинантно слитый с N-концом одной стороны гетеродимерного Fc (необязательно за счет доменного линкера), при этом другая сторона молекулы представляет собой гетеродимерный Fc «только Fc» или «пустой Fc» (Фигура 8C-D). Комплекс scIL-12 может содержать либо IL-12p35, связанную с N-концом IL-12p40, либо IL-12p40, связанную с N-концом IL-12p35, необязательно с помощью доменного линкера. Порядок двух субъединиц в комплексе scIL-12 обозначен в данном документе следующим образом: «scIL-12(p40/p35)», причем субъединица IL-12p40 связана с N-концом субъединицы IL-12p35, или «scIL-12(p35/p40)», причем IL-12p35 связана с N-концом субъединицы IL-12p35. Иллюстративные белки формата scIL-12-Fc включают XENP27203 и XENP27204, последовательности для которых изображены на Фигуре 11.
Схематические рисунки дополнительных форматов IL-12, предусмотренных для применения, изображены на Фигуре 8.
1B: Получение и физическая характеристика иллюстративных IL-12-Fc слитых белков
1B (a):IL-12-heteroFc
Плазмиды, кодирующие субъединицы IL-12p35 и IL-12p40, конструировали с помощью стандартного синтеза генов с последующим субклонированием в экспрессионный вектор pTT5, содержащий Fc-партнеров по слиянию (например, константные области, изображенные на Фигуре 7). Белки получали путем временной трансфекции в клетках HEK293E и очищали с помощью двухстадийного способа очистки, включающего хроматографию с использованием белка А (часть очистки 1) с последующей анионообменной хроматографией (часть очистки 2). Хроматограмма, изображающая часть очистки 2 для иллюстративного IL-12-heteroFc XENP27201, изображена на Фигуре 12A. Хроматограмма показывает выделение двух пиков (пик A и пик B), которые были дополнительно охарактеризованы с помощью аналитической эксклюзионной хроматографии с многоугловым светорассеянием (aSEC-MALS) и аналитической анионообменной хроматографии (аналитическая AIEX) для определения идентичности, чистоты и гомогенности, как в целом описано ниже.
Пики A и B, выделенные из части очистки 2 для XENP27201, анализировали с использованием aSEC-MALS для определения составляющих их белковых молекул. Анализ проводился на системе высокоэффективной жидкостной хроматографии (ВЭЖХ) Agilent 1200. Образцы впрыскивали в колонку Superdex™ 200 10/300 GL (GE Healthcare Life Sciences) при 1,0 мл/мин, используя 1x ФСБ, pH=7,4 в качестве подвижной фазы, при 4°C в течение 25 минут с детектированием в области УФ при длине волны 280 нм. MALS выполняли на miniDAWN® TREOS® с детектором показателя преломления Optilab® T-rEX (Wyatt Technology, Санта-Барбара, Калифорния). Анализ выполняли с использованием системы хроматографических данных Agilent OpenLab (CDS) ChemStation Edition AIC, версия C.01.07, и ASTRA, версия 6.1.7.15. Хроматограммы, изображающие профили разделения пиков A и B методом aSEC, изображены на Фигуре 12B вместе с молекулярной массой составных молекул, определенной с помощью MALS. Профили показывают, что пик A содержит молекулы с молекулярными массами ~299 кДа и ~140 кДа, в то время как пик B в основном содержит молекулу с молекулярной массой ~118 кДа, что согласуется с расчетной молекулярной массой XENP27201 (на основании аминокислотной последовательности) 110,4 кДа с учетом дополнительной массы, вносимой гликанами.
Пики из части очистки 2 также анализировали с использованием аналитической AIEX для дальнейшей оценки чистоты и гомогенности пика B. Анализ выполняли на системе высокоэффективной жидкостной хроматографии (ВЭЖХ) Agilent 1200. Образцы впрыскивали в непористую колонку Proteomix SAX-NP5 5 мкМ (Sepax Technologies, Inc., Ньюарк, Делавэр) при 1,0 мл/мин с использованием градиента 0-40% NaCl в 20 мМ Трис, буфер pH=8,5 с детектированием в области УФ при длине волны 280 нМ. Анализ выполняли с использованием системы хроматографических данных Agilent OpenLab CDS ChemStation Edition AIC, версия C.01.07. Хроматограммы, изображающие разделение пиков А и В методом аналитической AIEX, изображены на Фигуре 12С. В соответствии с профилем разделения пика B методом aSEC профиль разделения пика B методом аналитической AIEX иллюстрирует чистоту и гомогенность молекул в пике B. Далее, XENP27201 относится к пику B, выделенному из части очистки 2, как изображено на Фигуре 12A.
1B(b): scIL-12(p40/p35)-Fc
Плазмиды, кодирующие IL-12p40, рекомбинантно слитую с IL-12p35 за счет линкера, конструировали с помощью стандартного синтеза генов с последующим субклонированием в экспрессионный вектор pTT5, содержащий Fc-партнеров по слиянию (например, константные области, изображенные на Фигуре 7). Белки получали путем временной трансфекции в клетках HEK293E и очищали с помощью двухстадийного способа очистки, включающего хроматографию с использованием белка А (часть очистки 1) и анионообменную хроматографию (часть очистки 2).
Хроматограмма, изображающая часть очистки 2 для иллюстративного scIL-12(p40/p35)-Fc слитого белка XENP27203, изображена на Фигуре 13A. Как указано выше, хроматограмма показывает выделение двух пиков, которые были дополнительно охарактеризованы с помощью aSEC-MALS и аналитической AIEX для определения идентичности, чистоты и гомогенности, как описано в Примере 1B (a), хроматограммы для которых изображены на Фигурах 13B-C.
Профили разделения методом aSEC для пиков A и B, выделенных из части очистки 2 XENP27203, показывают, что пик A содержит молекулы с молекулярными массами ~396 кДа, ~188 кДа и ~118 кДа, в то время как пик B в основном содержит молекулу с молекулярной массой ~118 кДа, что согласуется с расчетной молекулярной массой XENP27203 (на основании аминокислотной последовательности) 111,3 кДа с учетом дополнительной массы, вносимой гликанами. Пики также анализировали с использованием аналитической AIEX, как описано в Примере 1B (a), для дальнейшего изучения чистоты и гомогенности пика B. В соответствии с профилем пика B при разделении методом aSEC профиль пика B при разделении методом аналитической AIEX (Фигура 13C) иллюстрирует чистоту и гомогенность молекул в пике B. Далее, XENP27203 относится к пику B, выделенному в результате анионного обмена, как изображено на Фигуре 13A.
1С: Активность IL-12-Fc слитых белков в индукции фосфорилирования STAT4 in vitro
После связывания цитокинов с их рецепторами киназы Janus (JAK), ассоциированные с рецепторами цитокинов, фосфорилируют белки STAT, которые затем транслоцируются в ядро с целью дальнейшей регуляции нисходящих процессов. В частности, IL-12 опосредует экспрессию и секрецию ИФН-γ посредством фосфорилирования STAT4 (Morinobu et al., 2002). Соответственно, изучали способность IL-12-heteroFc (XENP27201) и scIL-12(p40/p35)-Fc (XENP27203), описанных выше, индуцировать фосфорилирование STAT4 в различных популяциях лимфоцитов. Двухвалентные IL-12p35-Fc слитые белки и IL-12p40-Fc слитые белки (схематические рисунки и последовательности для которых показаны на Фигурах 14-15), а также рекомбинантный IL-12 использовали в качестве контролей.
Свежеотобранные МКПК активировали путем инкубации со связанным с планшетом антителом к CD3 (100 нг/мл) в течение 3 дней. После активации МКПК инкубировали с указанными тестируемыми изделиями в указанных концентрациях в течение 15 минут при 37°C. После инкубации МКПК сначала окрашивали антителом к CD3-BUV395 (UCHT1), антителом к CD4-BV605 (RPA-T4), антителом к CD8-AF700 (SK1), антителом к CD14-APC/Fire750 (M5E2), антителом к CD20-PerCP/5.5 (2H7), антителом к CD25-BV421 (M-A251) и антителом к CD56-PE. После первого окрашивания клетки пермеабилизировали с использованием PerFix EXPOSE (Beckman Coulter, Индианаполис, Индиана). После пермеабилизации клетки окрашивали антителом к CD45RA-BV510(HI100), антителом к FoxP3-AF488(259D) и антителом к pSTAT4-AF647 (38/p-Stat4). После второго окрашивания клетки анализировали с помощью проточной цитометрии для изучения фосфорилирования STAT5 в различных популяциях лимфоцитов. Данные, изображающие среднюю интенсивность флуоресценции (СИФ) pSTAT4 на различных популяциях лимфоцитов, указывающие на передачу сигналов с помощью IL-12-Fc слитых белков за счет рецепторов IL-12, изображены на Фигуре 16.
Данные показывают, что оба XENP27201 и XENP27203 активно индуцировали фосфорилирование STAT4 в различных популяциях лимфоцитов до уровня, аналогичного уровню, индуцированному рекомбинантным IL-12, в то время как двухвалентный IL-12p40-Fc (XENP27560) и двухвалентный IL-12p35-Fc (XENP27561) слитые белки были неактивными. Примечательно, что два формата IL-12-Fc слитых белков продемонстрировали сходную активность. Кроме того, способность очищенных IL-12-Fc слитых белков индуцировать фосфорилирование STAT4 по сравнению с XENP27560 и XENP27561 подтверждает, что пик B, выделенный из части очистки 2 для обоих XENP27201 и XENP27203 (как описано в Примере 1B), состоял из активных молекул, составляющих полный гетеродимер IL-12.
Пример 2: Варианты IL-12, сконструированные для уменьшения активности
Чтобы еще больше продлить период полужизни, а также уменьшить потенциальную токсичность, авторы изобретения сконструировали варианты IL-12 со сниженной аффинностью связывания в отношении рецепторов IL-12, поскольку авторы изобретения полагали, что это снизит антигензависимое устранение (antigen sink), а также уменьшит активность.
2A(a): Конструирование вариантов IL-12p40
Сначала авторы изобретения идентифицировали W15, P17, D18, A19, P20, G21, M23, L40, D41, Q42, S43, E45, L47, T54, I55, Q56, K58, E59, F60, G61, D62, Y66 и K84 в качестве потенциальных сайтов на IL-12p40 для введения замен, модулирующих аффинность (остатки, изображенные на Фигуре 17).
В качестве второй стратегии, используя пакет QuaSAR в программном обеспечении MOE, авторы изобретения идентифицировали сильно экспонированные остатки аспарагиновой кислоты, глутаминовой кислоты, аспарагина и глутамина (в соответствии с доступной для воды площадью поверхности, рассчитанной с использованием радиуса 1,4 Å для молекулы воды и полиэдрического представления для каждого атома) в кристаллической структуре IL-12p40 (код PDB 3HMX), предполагая, что эти остатки могут вносить вклад в связывание между IL-12p40 и рецепторами IL-12. В частности, авторы изобретения сосредоточили поиск на остатках, в которые авторы могли бы включить изостерические замены (т.е. Asn и Asp; а также Gln и Glu), с целью минимизировать потенциальную иммуногенность. Соответственно, авторы изобретения идентифицировали E3, D7, E12, D14, D18, E22, D29, E32, E33, D41, Q42, E45, Q56, E59, D62, Q65, E73, E86, D93, D97, E100, N103, E110, D129, D142, Q144, E156, D161, N162, E166, E170, Q172, D174, E187, N200, D209, D214, N218, Q220, N226, Q229, E231, E235, Q256, E262, D265, D270, N281, Q289 и E299, которые имеют оценку ASA по меньшей мере 19 (остатки и оценки ASA изображены на Фигуре 18).
Как описано выше, субъединица p40 является общей для IL-12 и IL-23. Bloch et al.(2018) описали кристаллическую структуру IL-23 в комплексе с IL-23R и Nb22E11. В качестве третьей стратегии авторы изобретения предположили, что остатки на субъединице IL-12p40, контактирующие с IL-23R, также могут участвовать в связывании аналогичного рецептора IL-12Rβ2 в рецепторном комплексе IL-12. Соответственно, используя кристаллическую структуру, описанную Bloch et al. (код PDB 5MZV) и моделирование в программном обеспечении MOE, авторы изобретения идентифицировали D87, G88, I89, W90, K104 и F106 как остатки на IL-12p40, которые потенциально контактируют с IL-12Rβ2 (остатки и предполагаемый тип контакта изображены на Фигуре 19).
Наконец, чтобы гарантировать, что авторы не нарушают естественное взаимодействие между субъединицами IL-12p40 и IL-12p35, авторы изобретения идентифицировали следующие остатки на IL-12p40, которые потенциально контактируют с IL-12p35, на основании кристаллической структуры, описанной Luo et al. (2010): K102, Y114, A176, C177, P178, A179, A180, E181, S183, P185, S204, F206, R208, T242, P243, S245, Y246, F247, S248, D290, R291, Y292 и Y293.
С учетом изложенного выше, авторы изобретения разработали ряд вариантов IL-12p40, в частности, описанных выше, в остатке, в который могут быть введены изостерические замены, с целью уменьшения аффинности гетеродимера IL-12 в отношении рецепторов IL-12. Также были разработаны замены для удаления потенциальных сайтов N-гликозилирования в p40, чтобы исследовать влияние гликозилирования на гетерогенность белка. Последовательности для иллюстративных вариантов изображены на Фигуре 20. Плазмиды, кодирующие варианты IL-12p40, конструировали с помощью стандартного синтеза генов с последующим субклонированием в экспрессионный вектор pTT5, содержащий Fc-партнеров по слиянию (например, константные области, изображенные на Фигуре 7), соответствующие аминокислотные последовательности для которых изображены на Фигуре 21.
2A(b): Конструирование вариантов IL-12p35
Как и во второй стратегии, описанной выше, авторы изобретения использовали пакет QuaSAR в программном обеспечении MOE для идентификации сильно экспонированных остатков аспарагиновой кислоты, глутаминовой кислоты, аспарагина и глутамина в кристаллической структуре IL-12p35 (код PDB 3HMX), полагая, что эти остатки могут вносить вклад в связывание между гетеродимерным комплексом IL-12 и рецепторами IL-12. Как упомянуто выше, в данном документе авторы изобретения сосредоточились, в частности, на остатках, в которые авторы могли бы включить изостерические замены, чтобы минимизировать потенциальную иммуногенность. Авторы изобретения идентифицировали Q35, E38, E46, D55, E67, N71, N76, N85, Q135, Q146, N151, E153, E162 и E163, которые имеют оценку ASA по меньшей мере 103 (остатки и оценки ASA, изображенные на Фигуре 22).
Как упоминалось выше, чтобы гарантировать, что авторы не нарушают естественное взаимодействие между субъединицами IL-12p40 и IL-12p354, авторы изобретения идентифицировали следующие остатки на IL-12p35, которые потенциально контактируют с IL-12p40, на основании кристаллической структуры, описанной Luo et al. (2010): Q20, S44, E45, E46, H49, K54, T59, V60, E61, C63, L64, P65, E67, L68, S73, C74, R181, I182, R183, V185, T186, D188, R189, V190, S192, Y193 и A196.
С учетом изложенного выше, авторы изобретения разработали ряд вариантов IL-12p35 с изостерическими заменами с целью уменьшения аффинности гетеродимера IL-12 в отношении рецепторов IL-12. Также были разработаны замены для удаления потенциальных сайтов N-гликозилирования в p35, чтобы исследовать влияние гликозилирования на гетерогенность белка. Последовательности для иллюстративных вариантов изображены на Фигуре 23. Плазмиды, кодирующие варианты IL-12p35, конструировали с помощью стандартного синтеза генов с последующим субклонированием в экспрессионный вектор pTT5, содержащий Fc-партнеров по слиянию (например, константные области, изображенные на Фигуре 7), соответствующие аминокислотные последовательности для которых изображены на Фигуре 24.
2A (c): Скрининг IL-12-Fc слитых белков, имеющих уменьшенную активность
Иллюстративные вариантные IL-12-Fc слитые белки, имеющие вариантные субъединицы IL-12, описанные выше, разрабатывали с целью создания IL-12-Fc слитых белков, имеющих уменьшенную аффинность в отношении рецепторов IL-12, для уменьшения активности, последовательности для которых изображены на Фигуре 25. Авторы изобретения получили и очистили IL-12-Fc слитые белки, как описано в общих чертах в Примере 1B, и изучили их активность в анализе pSTAT4.
Человеческие МКПК активировали 100 нг/мл антитела к CD3 (ОКТ3) в течение 2 дней. Затем активированные МКПК инкубировали с указанными тестируемыми изделиями при 37C в течение 15 минут. Затем клетки окрашивали антителом к CD3-BUV395 (UCHT1), антителом к CD4-BV605 (RPAT4), антителом к CD8-AF700 (SK1), антителом к CD25-BV510 (M-A251), антителом к CD45RA-BV421(HI100), антителом к CD56-PE(N901), антителом к FoxP3-AF488(259D) и антителом к pSTAT4-AF647 (38/p-Stat4) с использованием набора PerFix EXPOSE (Beckman Coulter, Индианаполис, Индиана) и анализировали с помощью проточной цитометрии.
Данные, показывающие индукцию фосфорилирования STAT4 на CD4+CD45RA+CD25+ и CD8+CD45RA+CD25+ Т-клетках под действием IL-12-Fc слитого белка, имеющего варианты IL-12p35 или IL-12p40, изображены, соответственно, на Фигурах 26 и 27. На Фигуре 28 изображены значения EC50 различных вариантов IL-12-Fc слитых белков и кратное снижение EC50 относительно WT IL-12-Fc XENP27201. Данные показывают, что большинство IL-12-Fc слитых белков, содержащих вариантные субъединицы IL-12p40 или IL-12p30, проявляют сниженную активность в отношении индукции фосфорилирования STAT4. Примечательно, что замены E59Q и E235Q в субъединице IL-12p40 и замены E153Q и N151D в IL-12p35 были способны по отдельности обеспечивать более чем 2-кратное уменьшение активности вариантных IL-12-Fc слитых белков. Кроме того, двойные и тройные мутанты IL-12p40, содержащие E59Q, обеспечили уменьшение активности до 6,5 раза.
Два вариантных IL-12-Fc слитых белка, содержащих IL-12p40(D87N) или IL-12p40(E262Q), неожиданно проявили увеличение активности. Несмотря на то, что авторы изобретения заинтересованы в снижении активности с целью уменьшения антигензависимого устранения и увеличения посредством этого периода полужизни IL-12-Fc слитых белков, IL-12-Fc слитые белки, обладающие повышенной активностью, могут найти применение в других случаях.
2B: Конструирование вариантов IL-12p40 и IL-12p35 (Раунд 2)
Для конструирования дополнительных вариантов IL-12p40 и IL-12p35 с целью уменьшения их аффинности в отношении рецепторов IL-12 и уменьшения активности биологически активного комплекса IL-12, авторы изобретения повторно применили стратегии, описанные в Примере 2A, с расширенными критериями. Например, авторы изобретения использовали более низкий порог оценки ASA, чем тот, который определен в Примере 2A, для идентификации остатков IL-12p40 и IL-12p35, в которые можно ввести замены. Авторы изобретения также расширили критерии, чтобы включить дополнительные аминокислотные остатки, уделяя особое внимание более крупным остаткам, таким как лизин, в которых введение замен с большей вероятностью нарушало взаимодействие IL-12p35, IL-12p40, и (или) комплекса IL-12 с рецепторами IL-12.
Аналогичным образом, авторы изобретения ввели неизостерические замены, уделяя особое внимание более крупным остаткам, таким как лизин, чтобы нарушить взаимодействие IL-12p35, IL-12p40, и (или) комплекса IL-12 с рецепторами IL-12. Используя эти подходы, авторы изобретения дополнительно идентифицировали D34, K99, K163, K258 и K260 в субъединице IL-12p40; и N21, E79, Q130, N136, E143, K158 и D165 в субъединице IL-12p35 в качестве остатков, пригодных для конструирования замен. Кроме того, авторы изобретения создали дополнительные комбинированные варианты, включающие замены, идентифицированные в Примере 2, которые способствовали наибольшему уменьшению активности.
С учетом изложенного выше, авторы изобретения разработали дополнительные варианты IL-12p40 и IL-12p35, иллюстративные последовательности для которых изображены, соответственно, на Фигурах 29 и 31. Как упоминалось выше, плазмиды, кодирующие варианты IL-12p40 и IL-12p35, конструировали с помощью стандартного синтеза генов с последующим субклонированием в экспрессионный вектор pTT5, содержащий Fc-партнеров по слиянию, соответствующие аминокислотные последовательности для которых изображены, соответственно, на Фигуре 30 и 32. Создавали IL-12-Fc слитые белки с дополнительными вариантными субъединицами IL-12, последовательности для которых изображены на Фигуре 33, и получали, как описано в общих чертах в Примере 1B.
Активность дополнительных вариантных IL-12-Fc слитых белков изучали в анализе pSTAT4, как описано в общих чертах выше. В частности, человеческие МКПК активировали 100 нг/мл антитела к CD3 (ОКТ3) в течение 2 дней. Затем активированные МКПК инкубировали с указанными тестируемыми изделиями при 37C в течение 15 минут. Затем клетки окрашивали антителом к CD3-BUV395 (UCHT1), антителом к CD4-BV605 (RPAT4), антителом к CD8-AF700 (SK1), антителом к CD25-BV510 (M-A251), антителом к CD45RA-BV421(HI100) и антителом к CD56-PE(N901). Затем клетки пермеабилизировали с использованием PerFix EXPOSE (Beckman Coulter, Индианаполис, Индиана). После пермеабилизации клетки окрашивали антителом к FoxP3-AF488(259D) и антителом к pSTAT4-AF647 (38/p-Stat4) и анализировали с помощью проточной цитометрии. Данные, изображающие СИФ pSTAT4 на CD4+CD45RA+CD25+ и CD8+CD45RA+CD25+ Т-клетках изображены на Фигуре 34-35, а данные, изображающие EC50 (и кратное снижение относительно WT IL-12-Fc XENP27201), показаны на Фигуре 36. Данные показывают, что большинство из IL-12-Fc слитых белков, содержащих вариантные субъединицы IL-12p40 и (или) IL-12p30, проявляют сниженную активность в отношении индукции фосфорилирования STAT4.
2C: Конструирование вариантов IL-12p40 и IL-12p35 (Раунд 3)
В примере 2B авторы изобретения обнаружили, что IL-12-Fc слитый белок XENP29952, содержащий IL-12p40(E59K), обеспечил уменьшение в ~12 раз, в отличие от IL-12-Fc слитого белка XENP28825, содержащего IL-12p40(E59Q), активность которого уменьшилась только примерно в 2 раза. Кроме того, авторы изобретения отметили, что несколько двойных мутантов, содержащих E59Q в субъединице IL-12p40, продемонстрировали уменьшение активности в >3,5 раза (например, XENP29953, XENP29954, и XENP29959). Кроме того, авторы изобретения отметили, что в то время как XENP28846, содержащий IL-12p35(N151D), обеспечил увеличение активности, IL-12p35(D55Q/N151D) обеспечил фактически ~2-кратное уменьшение активности, что показало авторам, что модификация D55 в субъединице IL-12p35 вносит значительный вклад в уменьшение активности. Соответственно, для дальнейшего уменьшения активности IL-12-Fc слитых белков авторы изобретения создали дополнительные комбинированные варианты, включающие замены в Примере 2B, которые способствовали наибольшему уменьшению активности. Кроме того, как описано в Примере 2B, авторы изобретения дополнительно включили неизостерические замены, уделяя особое внимание более крупным остаткам, таким как лизин.
С учетом изложенного выше, авторы изобретения разработали дополнительные варианты IL-12p40 и IL-12p35, иллюстративные последовательности которых изображены, соответственно, на Фигурах 37 и 38. Создавали IL-12-Fc слитые белки с дополнительными вариантными субъединицами IL-12, последовательности для которых изображены на Фигуре 39, и получали, как описано в общих чертах в Примере 1B. Активность дополнительных вариантных IL-12-Fc слитых белков изучали в анализе pSTAT4, как описано в общих чертах выше. Данные, изображающие СИФ pSTAT4 на CD4+CD45RA+CD25+ и CD8+CD45RA+CD25+ Т-клетках, изображены на Фигуре 40, а данные, изображающие EC50 (и кратное снижение относительно WT IL-12-Fc XENP27201), показаны на Фигуре 41. Данные показывают, что все новые IL-12-Fc слитые белки, содержащие вариантные субъединицы IL-12p40 и (или) IL-12p30, проявили существенно сниженную активность в отношении индукции фосфорилирования STAT4. Примечательно, что XENP30607 и XENP30608 проявили ~100-кратное снижение активности по сравнению с XENP27201.
2D: Конструирование вариантов IL-12p40 и IL-12p35 (Раунд 4)
Авторы изобретения дополнительно сконструировали субъединицы IL-12p40 и IL-12p35 как за счет включения дополнительных вариантов, описанных в Примере 2, способствующих сдвигу активности, так и за счет дальнейшего использования неизостерических замен, уделяя особое внимание более крупным остаткам, таким как лизин и тирозин, чтобы нарушить взаимодействие IL-12p35, IL-12p40, и (или) комплекса IL-12 с рецепторами IL-12.
Кроме того, авторы изобретения выполнили дополнительный структурный анализ в программном обеспечении MOE на основе поверхностного экспонирования, чтобы идентифицировать дополнительные остатки в субъединицах IL-12p40 и IL-12p35, в которые могут быть введены модификации. Далее авторы изобретения идентифицировали остатки R159 и K264 в субъединице IL-12p40; и остатки L75, L89, F96, M97, L124, M125 и I171 в субъединице IL-12p35. Авторы изобретения использовали подходы, описанные ранее, а также замены аланином (в соответствии с методикой сканирующего аланином мутагенеза), чтобы предварительно изучить влияние модификаций в этих дополнительно идентифицированных остатках.
С учетом изложенного выше, авторы изобретения разработали дополнительные варианты IL-12p40 и IL-12p35, иллюстративные последовательности для которых изображены, соответственно, на Фигурах 42 и 43. IL-12-Fc слитые белки создавали с дополнительными вариантными субъединицами IL-12, последовательности для которых изображены на Фигуре 44, и получали, как описано в общих чертах в Примере 1B.
Активность дополнительных вариантных IL-12-Fc слитых белков изучали в анализе pSTAT4, как описано в общих чертах выше. Данные, изображающие СИФ pSTAT4 на CD4+CD45RA+CD25+, CD4+CD45RA-CD25+, CD8+CD45RA+CD25+ и CD8+CD45RA-CD25+ Т-клетках, изображены на Фигуре 46, а данные, изображающие EC50 (и кратное снижение относительно WT IL-12-Fc XENP27201), показаны на Фигуре 47. Данные показывают, что все новые IL-12-Fc слитые белки, содержащие вариантные субъединицы IL-12p40 и (или) IL-12p35, проявили существенно сниженную активность в отношении индукции фосфорилирования STAT4.
Пример 3: двухвалентные IL-12-Fc слитые белки
Авторы изобретения также разработали двухвалентные IL-12-Fc слитые белки. Одним из таких форматов является формат двухвалентного N-концевого IL-12-Fc слитого белка (Фигуры 48A-B), который содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с N-концом цепи гомодимерного Fc (необязательно за счет доменного линкера). Другой такой формат представляет собой формат двухвалентного С-конецевого IL-12-Fc слитого белка (Фигуры 48C-D), который содержит два идентичных мономера, каждый из которых содержит рекомбинантный комплекс scIL-12, слитый с С-концом цепи гомодимерного Fc (необязательно за счет доменного линкера).
Пример 4: Варианты IL-12 с уменьшенной активностью в альтернативных форматах IL-12-Fc слитых белков
Авторы изобретения также изучили варианты IL-12 применительно к дополнительным форматам IL-12-Fc слитых белков. Слитые белки в форматах scIL-12(p40/p35)-Fc и (scIL-12(p40/p35))2-Fc создавали с применением либо субъединиц WT IL-12p40, либо вариантных субъединиц IL-12p40(E59K/K99E) и получали, как описано в общих чертах в Примере 1В (и последовательности для которых изображены на Фигурах 49-50).
Активность IL-12-Fc слитых белков изучали в анализе pSTAT4, как описано в общих чертах выше. В частности, человеческие МКПК активировали 100 нг/мл антитела к CD3 (ОКТ3) в течение 2 дней при 37C. Затем активированные МКПК инкубировали с указанными тестируемыми изделиями в течение 15 минут при 37C. Затем клетки окрашивали антителом к CD3-BUV395 (UCHT1), антителом к CD4-BV605 (RPAT4), антителом к CD8-AF700 (SK1), антителом к CD25-BV711 (M-A251), антителом к CD45RA-BV421(HI100) и антителом к CD56-PE(N901). Затем клетки пермеабилизировали с использованием PerFix EXPOSE (Beckman Coulter, Индианаполис, Индиана). После пермеабилизации клетки окрашивали антителом к FoxP3-V450(259D) и антителом к pSTAT4-AF647 (38/p-Stat4) и анализировали с помощью проточной цитометрии. Данные, изображающие СИФ pSTAT4 на CD4+CD45RA+CD25+, CD4+CD45RA-CD25+, CD8+CD45RA+CD25+ и CD8+CD45RA-CD25+ Т-клетках, изображены на Фигуре 51, а данные, изображающие EC50 (и кратное снижение относительно WTIL-12-Fc XENP27201), показаны на Фигуре 52. Данные показывают, что IL-12-Fc слитые белки в различном формате продемонстрировали очень сходную активность, а IL-12-Fc слитые белки в scIL-12(p40/p35)-Fc и (scIL-12(p40/p35))2-Fc слитых белках, содержащих вариантные субъединицы IL-12p40(E59K/K99E), продемонстрировали активность, очень сходную с активностью IL-12-Fc слитых белков в формате IL-12-heteroFc, содержащем вариантную субъединицу IL-12p40(E59K/K99E).
Пример 5: IL-12-Fc слитые белки усиливают аллогенный противоопухолевый эффект Т-клеток in vivo
Затем авторы изобретения изучили противоопухолевый эффект in vivo IL-12-Fc слитых белков по данному изобретению. Мышам NOD SCID gamma (NSG) внутрикожно приживляли 3×106 клеток MCF-7, экспрессирующих pp-65, в правую часть бока на День -15. В День 0 мышам внутрибрюшинно приживляли 1,5×106 человеческих МКПК. Затем мышей (n = 15) лечили в Дни 0, 7, 14 и 21 с использованием 0,03 мг/кг XENP29952, IL-12-Fc слитого белка с уменьшенной активностью в формате IL-12-heteroFc, содержащем вариант IL-12p40(E59K). В качестве контролей (n = 10) использовали ФСБ и XENP16432 (бивалентное МАТ к PD-1, ингибитор контрольной точки, который усиливает противоопухолевую активность путем устранения репрессии приживленных человеческих Т-клеток; последовательности, изображенные на Фигуре 53). Объемы опухоли контролировали с помощью измерений штангенциркулем, данные для них показаны (дни после 1-й дозы) на Фигуре 54. Кровь и сыворотку брали в Дни 7, 14 и 21 и анализировали с помощью проточной цитометрии, чтобы изучить размножение человеческих лимфоцитов, данные для них изображены на Фигуре 55, а также с помощью анализов U-PLEX Biomarker Group 1 Human (Meso Scale, Роквилл, Мэриленд) для определения концентраций цитокинов в сыворотке крови, данные для них представлены на Фигуре 56.
Данные показывают, что IL-12-heteroFc слитый белок XENP29952 значительно усиливал размножение CD45+, CD3+ Т-клеток, CD4+ Т-клеток, CD8+ Т-клеток и NK-клеток к Дню 14 по сравнению как с контролем ФСБ, так и с блокадой контрольной точки с помощью XENP16432 (статистический анализ выполняли на логарифмически преобразованных данных с использованием непарного t-критерия). Примечательно, что XENP29952 значительно усилил противоопухолевую активность к Дню 11, на что указывает изменение объема опухоли (статистический анализ выполняли на данных, скорректированных относительно исходного уровня, с использованием непарного t-критерия). Кроме того, XENP29952 значительно усилил секрецию ИФН-γ и CD25 к Дню 7 по сравнению с блокадой контрольной точки с помощью XENP16432 (статистический анализ выполняли на логарифмически преобразованных данных с использованием непарного t-критерия).
В дополнение к противоопухолевой активности приживленные человеческие МКПК вызывают аутоиммунный ответ против мышиных клеток и впоследствии реакцию «трансплантат против хозяина» (РТПХ). Соответственно, следует отметить, что несмотря на то, что все животные, получавшие XENP29952, погибли к Дню 19, это, вероятно, было связано с их смертью в результате РТПХ, усугубленной значительно усиленным размножением человеческих лимфоцитов. Это подчеркивает важность уменьшения активности вариантов IL-12 не только для улучшения фармакокинетики, но и для улучшения терапевтического индекса.
Пример 6: IL-12-Fc слитые белки демонстрируют модулированную активность in vivo, коррелирующую с активностью in vitro
Поскольку все животные, которых лечили с использованием XENP29952 в Примере 5, погибли в результате РТПХ, авторы изобретения изучили активность in vivo IL-12-Fc слитых белков, сконструированных с вариантами IL-12 с уменьшенной активностью, в исследовании РТПХ.
Мышам NSG приживляли 10106 человеческих МКПК путем IV-OSP в День -1 и вводили внутрибрюшинно в Дни 0, 7, 14 и 21 следующие тестируемые изделия: XENP29952 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K)), XENP30597 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E)), XENP31254 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(D18K/E59K/K99E)), XENP31251 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99Y)), или XENP31258 (IL-12-Fc слитый белок с уменьшенной активностью в формате IL-12-heteroFc, содержащий вариант IL-12p40(E59K/K99E/K264E)) при 0,3 или 0,03 мг/кг. Массу тела оценивали два раза в неделю как индикатор РТПХ, эти данные изображены на Фигуре 57 как изменение массы тела (относительно исходной массы тела). Кроме того, кровь брали в День 7, 10, 14 и 31 для изучения активации различных популяций Т-клеток, на что указывают уровни экспрессии PD-1 (данные для них изображены на Фигурах 58 и 59), и сыворотку брали для изучения секреции цитокинов (данные для них изображены на Фигуре 60). Примечательно, что данные показывают дозозависимый ответ для тестируемых изделий (т.е. усиление РТПХ, активации Т-клеток и секреции ИФН-γ при введении дозы 0,3 мг/кг по сравнению с дозой 0,03 мг/кг).
XENP31251, который оказался одним из самых слабых вариантов в отношении индукции фосфорилирования STAT4 на CD4+ Т-клетках in vitro (см. Фигуры 46A-46B), неожиданно был одним из наиболее сильных индукторов РТПХ. Соответственно, авторы изобретения повторно изучили активность in vitro того же иллюстративного IL-12-Fc с уменьшенной активностью в анализе фосфорилирования STAT4, как описано в общих чертах выше, с использованием двух отдельных доноров МКПК. Человеческие МКПК активировали 1 мкг/мл антитела к CD3 (ОКТ3) в течение 2 дней при 37C. Затем активированные МКПК инкубировали с указанными тестируемыми изделиями при 37C в течение 15 минут.
Затем клетки окрашивали антителом к CD3-BUV395 (UCHT1), антителом к CD4-BV605 (RPAT4), антителом к CD8-AF700 (SK1), антителом к CD25-BV510 (M-A251), антителом к CD45-BV785, антителом к CD45RA-BV421(HI100), антителом к CD16-PE(B73) и антителом к CD56-PE(N901). Затем клетки пермеабилизировали с использованием PerFix EXPOSE (Beckman Coulter, Индианаполис, Индиана). После пермеабилизации клетки окрашивали антителом к FoxP3-AF488(259D) и антителом к pSTAT4-AF647 (38/p-Stat4) и анализировали с помощью проточной цитометрии. Индукция фосфорилирования STAT4 на различных популяциях лимфоцитов в МКПК от двух доноров изображена на Фигуре 61 (данные не показаны для второго донора, но включены посредством ссылки из Фигуры 62 в 62/848512). Данные от обоих доноров и по разным популяциям лимфоцитов показывают ступенчатое изменение активности, при этом XENP29952 является наиболее активным вариантом, XENP31254 и XENP31258 являются наименее активными вариантами, а XENP30597 и XENP31251 расположены между ними. Примечательно, что степень РТПХ, активации Т-клеток и секреции ИФН-γ in vivo, индуцированная вариантами IL-12-Fc слитых белков с уменьшенной активностью, коррелировала с активностью in vitro. Например, при дозе 0,03 мг/кг XENP29952 индуцировал более значительную РТПХ, активацию Т-клеток и секрецию ИФН-γ, чем все IL-12-Fc слитые белки с уменьшенной активностью, в то время как XENP31254 и XENP31258 индуцировали наименьшую РТПХ, активацию Т-клеток и секрецию ИФН-γ.
Пример 7: IL-12-Fc слитые белки обладают противоопухолевой активностью и эффективно комбинируются с блокадой контрольной точки
Затем авторы изобретения изучили противоопухолевый эффект in vivo комбинирования дополнительных IL-12-Fc слитых белков, а также эффект комбинирования IL-12-Fc слитых белков с блокадой контрольной точки. Мышам NSG приживляли внутрикожно 3×106 клеток MCF-7, экспрессирующих pp-65, в правый бок в День -15. В День 0 мышам внутрибрюшинно приживляли 5×106 человеческих МКПК. Затем мышей лечили в Дни 0, 7, 14 и 21 с применением 0,1 мг/кг XENP31251 по отдельности или в комбинации с 3,0 мг/кг МАТ к PD-1 XENP16432. В качестве контролей использовали ФСБ, 3,0 мг/кг XENP16432 по отдельности и XENP31258. Объемы опухоли контролировали с помощью измерений штангенциркулем, данные для них показаны (дни после 1-й дозы) на Фигуре 62. Кровь брали в Дни 7, 14 и 21 и анализировали с помощью проточной цитометрии, чтобы изучить размножение человеческих лимфоцитов, данные для них показаны на Фигуре 63 для Дня 14.
Данные показывают, что XENP31258 значительно усилил противоопухолевую активность к Дню 14, а XENP31251 (по отдельности или в комбинации с XENP16432) значительно усилил противоопухолевую активность (на что указывает изменение объема опухоли) к Дню 16 по сравнению с обработкой ФСБ (статистический анализ выполняли на данных, скорректированных относительно исходного уровня, с использованием критерия Манна-Уитни). Примечательно, что данные показывают, что XENP31251 в комбинации с XENP16432 значительно усилил противоопухолевую активность к Дню 21 по сравнению с лечением XENP16432 по отдельности; и что лечение XENP31251 в комбинации с XENP16432 значительно усилило размножение лимфоцитов по сравнению с XENP31251 или XENP16432 по отдельности, это свидетельствует о том, что IL-12-Fc слитые белки эффективно комбинируются с блокадой контрольной точки.
Пример 8: Удаление свободного цистеина в субъединице IL-12p40
Субъединица IL-12p40 имеет свободный цистеин в положении 252 (пронумеровано в соответствии с последовательностью зрелой формы субъединицы бета (IL-12p40) человеческого IL-12, изображенной на Фигуре 1), который может связываться с другими свободными цистеинами, что приводит по меньшей мере к гетерогенности, а в худшем случае приводит к иммуногенности. Соответственно, варианты IL-12p40 конструировали для удаления свободного цистеина, например, путем введения модификации C252S (хотя могут использоваться и другие замены). Модификацию C252 (например, C252S) можно применять по отдельности или в комбинации с любыми другими вариантами IL-12p40, такими как варианты по аффинности или экспрессии. Иллюстративные варианты IL-12p40, содержащие модификацию в C252 для удаления свободного цистеина, изображены на Фигуре 65. Иллюстративные IL-12-Fc слитые белки создавали с дополнительными вариантными субъединицами IL-12p40, последовательности для которых изображены на Фигуре 66, и получали, как описано в общих чертах в Примере 1B.
Активность вариантов IL-12p40, сконструированных для удаления свободного цистеина, изучали в анализе pSTAT4, как описано в общих чертах выше, чтобы убедиться, что удаление свободного цистеина не вызвало какого-либо изменения активности. Активированные МКПК инкубировали с указанными тестируемыми изделиями и оценивали СИФ STAT4 на различных популяциях, данные для них изображены на Фигуре 67. Данные показывают, что варианты, содержащие модификацию C252S, продемонстрировали активность, сходную с активностью аналогичного варианта, который не содержал модификацию C252S. Примечательно, что для 3 из 4 протестированных вариантов, для которых авторы изобретения сконструировали варианты с мутацией C252S или без нее (т.е. D18K/E59K/K99E; D18K/E59K/K99E/K264E; и E59K/K99E), мутация C252S, по-видимому, незначительно увеличивала активность IL-12-Fc слитых белков.
Приведенные выше примеры представлены для того, чтобы предоставить рядовым специалистам в данной области техники полное раскрытие и описание того, как создавать и применять варианты реализации композиций, систем и способов согласно данному изобретению и не предназначены для ограничения объема того, что авторы изобретения считают своим изобретением. Предполагается, что модификации описанных выше способов реализации данного изобретения, очевидные для специалистов в данной области техники, находятся в пределах объема прилагаемой формулы изобретения. Все патенты и публикации, упомянутые в данном описании, указывают на уровень квалификации специалистов в области техники, к которой относится данное изобретение. Все ссылки, процитированные в данном раскрытии, включены посредством ссылки в той же степени, как если бы каждая ссылка была включена индивидуально посредством ссылки в полном объеме.
Все заголовки и обозначения разделов используются только для ясности и в справочных целях и никоим образом не должны рассматриваться как ограничивающие. Например, специалисты в данной области техники оценят полезность комбинирования различных аспектов данного раскрытия из разных заголовков и разделов, в зависимости от ситуации, в соответствии с сущностью и объемом изобретения, описанного в данном документе.
Все источники, процитированные в данном документе, тем самым включены в данный документ посредством ссылки в полном объеме и для всех целей в той же степени, как если бы каждая отдельная публикация, патент или патентная заявка была специально и индивидуально указана как включенная посредством ссылки в полном объеме и для всех целей.
Многие модификации и вариации данной заявки могут быть выполнены без отклонения от ее сущности и объема, как будет очевидно для специалистов в данной области техники. Конкретные варианты реализации данного изобретения и примеры, описанные в данном документе, предлагаются только в качестве примера и данная заявка должна ограничиваться только условиями прилагаемой формулы изобретения вместе с полным объемом эквивалентов, на которые распространяется формула данного изобретения.
--->
SEQUENCE LISTING
<110> XENCOR, INC.
<120> IL-12 HETERODIMERIC FC-FUSION PROTEINS
<130> 067461-5225-WO
<140> PCT/US19/54570
<141> 2019-10-03
<150> 62/848,512
<151> 2019-05-15
<150> 62/810,038
<151> 2019-02-25
<150> 62/740,813
<151> 2018-10-03
<160> 467
<170> PatentIn version 3.5
<210> 1
<211> 219
<212> PRT
<213> Homo sapiens
<400> 1
Met Cys Pro Ala Arg Ser Leu Leu Leu Val Ala Thr Leu Val Leu Leu
1 5 10 15
Asp His Leu Ser Leu Ala Arg Asn Leu Pro Val Ala Thr Pro Asp Pro
20 25 30
Gly Met Phe Pro Cys Leu His His Ser Gln Asn Leu Leu Arg Ala Val
35 40 45
Ser Asn Met Leu Gln Lys Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys
50 55 60
Thr Ser Glu Glu Ile Asp His Glu Asp Ile Thr Lys Asp Lys Thr Ser
65 70 75 80
Thr Val Glu Ala Cys Leu Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys
85 90 95
Leu Asn Ser Arg Glu Thr Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala
100 105 110
Ser Arg Lys Thr Ser Phe Met Met Ala Leu Cys Leu Ser Ser Ile Tyr
115 120 125
Glu Asp Leu Lys Met Tyr Gln Val Glu Phe Lys Thr Met Asn Ala Lys
130 135 140
Leu Leu Met Asp Pro Lys Arg Gln Ile Phe Leu Asp Gln Asn Met Leu
145 150 155 160
Ala Val Ile Asp Glu Leu Met Gln Ala Leu Asn Phe Asn Ser Glu Thr
165 170 175
Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys
180 185 190
Ile Lys Leu Cys Ile Leu Leu His Ala Phe Arg Ile Arg Ala Val Thr
195 200 205
Ile Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
210 215
<210> 2
<211> 197
<212> PRT
<213> Homo sapiens
<400> 2
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 3
<211> 328
<212> PRT
<213> Homo sapiens
<400> 3
Met Cys His Gln Gln Leu Val Ile Ser Trp Phe Ser Leu Val Phe Leu
1 5 10 15
Ala Ser Pro Leu Val Ala Ile Trp Glu Leu Lys Lys Asp Val Tyr Val
20 25 30
Val Glu Leu Asp Trp Tyr Pro Asp Ala Pro Gly Glu Met Val Val Leu
35 40 45
Thr Cys Asp Thr Pro Glu Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln
50 55 60
Ser Ser Glu Val Leu Gly Ser Gly Lys Thr Leu Thr Ile Gln Val Lys
65 70 75 80
Glu Phe Gly Asp Ala Gly Gln Tyr Thr Cys His Lys Gly Gly Glu Val
85 90 95
Leu Ser His Ser Leu Leu Leu Leu His Lys Lys Glu Asp Gly Ile Trp
100 105 110
Ser Thr Asp Ile Leu Lys Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe
115 120 125
Leu Arg Cys Glu Ala Lys Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp
130 135 140
Leu Thr Thr Ile Ser Thr Asp Leu Thr Phe Ser Val Lys Ser Ser Arg
145 150 155 160
Gly Ser Ser Asp Pro Gln Gly Val Thr Cys Gly Ala Ala Thr Leu Ser
165 170 175
Ala Glu Arg Val Arg Gly Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu
180 185 190
Cys Gln Glu Asp Ser Ala Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile
195 200 205
Glu Val Met Val Asp Ala Val His Lys Leu Lys Tyr Glu Asn Tyr Thr
210 215 220
Ser Ser Phe Phe Ile Arg Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn
225 230 235 240
Leu Gln Leu Lys Pro Leu Lys Asn Ser Arg Gln Val Glu Val Ser Trp
245 250 255
Glu Tyr Pro Asp Thr Trp Ser Thr Pro His Ser Tyr Phe Ser Leu Thr
260 265 270
Phe Cys Val Gln Val Gln Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg
275 280 285
Val Phe Thr Asp Lys Thr Ser Ala Thr Val Ile Cys Arg Lys Asn Ala
290 295 300
Ser Ile Ser Val Arg Ala Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser
305 310 315 320
Glu Trp Ala Ser Val Pro Cys Ser
325
<210> 4
<211> 306
<212> PRT
<213> Homo sapiens
<400> 4
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 5
<211> 662
<212> PRT
<213> Homo sapiens
<400> 5
Met Glu Pro Leu Val Thr Trp Val Val Pro Leu Leu Phe Leu Phe Leu
1 5 10 15
Leu Ser Arg Gln Gly Ala Ala Cys Arg Thr Ser Glu Cys Cys Phe Gln
20 25 30
Asp Pro Pro Tyr Pro Asp Ala Asp Ser Gly Ser Ala Ser Gly Pro Arg
35 40 45
Asp Leu Arg Cys Tyr Arg Ile Ser Ser Asp Arg Tyr Glu Cys Ser Trp
50 55 60
Gln Tyr Glu Gly Pro Thr Ala Gly Val Ser His Phe Leu Arg Cys Cys
65 70 75 80
Leu Ser Ser Gly Arg Cys Cys Tyr Phe Ala Ala Gly Ser Ala Thr Arg
85 90 95
Leu Gln Phe Ser Asp Gln Ala Gly Val Ser Val Leu Tyr Thr Val Thr
100 105 110
Leu Trp Val Glu Ser Trp Ala Arg Asn Gln Thr Glu Lys Ser Pro Glu
115 120 125
Val Thr Leu Gln Leu Tyr Asn Ser Val Lys Tyr Glu Pro Pro Leu Gly
130 135 140
Asp Ile Lys Val Ser Lys Leu Ala Gly Gln Leu Arg Met Glu Trp Glu
145 150 155 160
Thr Pro Asp Asn Gln Val Gly Ala Glu Val Gln Phe Arg His Arg Thr
165 170 175
Pro Ser Ser Pro Trp Lys Leu Gly Asp Cys Gly Pro Gln Asp Asp Asp
180 185 190
Thr Glu Ser Cys Leu Cys Pro Leu Glu Met Asn Val Ala Gln Glu Phe
195 200 205
Gln Leu Arg Arg Arg Gln Leu Gly Ser Gln Gly Ser Ser Trp Ser Lys
210 215 220
Trp Ser Ser Pro Val Cys Val Pro Pro Glu Asn Pro Pro Gln Pro Gln
225 230 235 240
Val Arg Phe Ser Val Glu Gln Leu Gly Gln Asp Gly Arg Arg Arg Leu
245 250 255
Thr Leu Lys Glu Gln Pro Thr Gln Leu Glu Leu Pro Glu Gly Cys Gln
260 265 270
Gly Leu Ala Pro Gly Thr Glu Val Thr Tyr Arg Leu Gln Leu His Met
275 280 285
Leu Ser Cys Pro Cys Lys Ala Lys Ala Thr Arg Thr Leu His Leu Gly
290 295 300
Lys Met Pro Tyr Leu Ser Gly Ala Ala Tyr Asn Val Ala Val Ile Ser
305 310 315 320
Ser Asn Gln Phe Gly Pro Gly Leu Asn Gln Thr Trp His Ile Pro Ala
325 330 335
Asp Thr His Thr Glu Pro Val Ala Leu Asn Ile Ser Val Gly Thr Asn
340 345 350
Gly Thr Thr Met Tyr Trp Pro Ala Arg Ala Gln Ser Met Thr Tyr Cys
355 360 365
Ile Glu Trp Gln Pro Val Gly Gln Asp Gly Gly Leu Ala Thr Cys Ser
370 375 380
Leu Thr Ala Pro Gln Asp Pro Asp Pro Ala Gly Met Ala Thr Tyr Ser
385 390 395 400
Trp Ser Arg Glu Ser Gly Ala Met Gly Gln Glu Lys Cys Tyr Tyr Ile
405 410 415
Thr Ile Phe Ala Ser Ala His Pro Glu Lys Leu Thr Leu Trp Ser Thr
420 425 430
Val Leu Ser Thr Tyr His Phe Gly Gly Asn Ala Ser Ala Ala Gly Thr
435 440 445
Pro His His Val Ser Val Lys Asn His Ser Leu Asp Ser Val Ser Val
450 455 460
Asp Trp Ala Pro Ser Leu Leu Ser Thr Cys Pro Gly Val Leu Lys Glu
465 470 475 480
Tyr Val Val Arg Cys Arg Asp Glu Asp Ser Lys Gln Val Ser Glu His
485 490 495
Pro Val Gln Pro Thr Glu Thr Gln Val Thr Leu Ser Gly Leu Arg Ala
500 505 510
Gly Val Ala Tyr Thr Val Gln Val Arg Ala Asp Thr Ala Trp Leu Arg
515 520 525
Gly Val Trp Ser Gln Pro Gln Arg Phe Ser Ile Glu Val Gln Val Ser
530 535 540
Asp Trp Leu Ile Phe Phe Ala Ser Leu Gly Ser Phe Leu Ser Ile Leu
545 550 555 560
Leu Val Gly Val Leu Gly Tyr Leu Gly Leu Asn Arg Ala Ala Arg His
565 570 575
Leu Cys Pro Pro Leu Pro Thr Pro Cys Ala Ser Ser Ala Ile Glu Phe
580 585 590
Pro Gly Gly Lys Glu Thr Trp Gln Trp Ile Asn Pro Val Asp Phe Gln
595 600 605
Glu Glu Ala Ser Leu Gln Glu Ala Leu Val Val Glu Met Ser Trp Asp
610 615 620
Lys Gly Glu Arg Thr Glu Pro Leu Glu Lys Thr Glu Leu Pro Glu Gly
625 630 635 640
Ala Pro Glu Leu Ala Leu Asp Thr Glu Leu Ser Leu Glu Asp Gly Asp
645 650 655
Arg Cys Lys Ala Lys Met
660
<210> 6
<211> 522
<212> PRT
<213> Homo sapiens
<400> 6
Cys Arg Thr Ser Glu Cys Cys Phe Gln Asp Pro Pro Tyr Pro Asp Ala
1 5 10 15
Asp Ser Gly Ser Ala Ser Gly Pro Arg Asp Leu Arg Cys Tyr Arg Ile
20 25 30
Ser Ser Asp Arg Tyr Glu Cys Ser Trp Gln Tyr Glu Gly Pro Thr Ala
35 40 45
Gly Val Ser His Phe Leu Arg Cys Cys Leu Ser Ser Gly Arg Cys Cys
50 55 60
Tyr Phe Ala Ala Gly Ser Ala Thr Arg Leu Gln Phe Ser Asp Gln Ala
65 70 75 80
Gly Val Ser Val Leu Tyr Thr Val Thr Leu Trp Val Glu Ser Trp Ala
85 90 95
Arg Asn Gln Thr Glu Lys Ser Pro Glu Val Thr Leu Gln Leu Tyr Asn
100 105 110
Ser Val Lys Tyr Glu Pro Pro Leu Gly Asp Ile Lys Val Ser Lys Leu
115 120 125
Ala Gly Gln Leu Arg Met Glu Trp Glu Thr Pro Asp Asn Gln Val Gly
130 135 140
Ala Glu Val Gln Phe Arg His Arg Thr Pro Ser Ser Pro Trp Lys Leu
145 150 155 160
Gly Asp Cys Gly Pro Gln Asp Asp Asp Thr Glu Ser Cys Leu Cys Pro
165 170 175
Leu Glu Met Asn Val Ala Gln Glu Phe Gln Leu Arg Arg Arg Gln Leu
180 185 190
Gly Ser Gln Gly Ser Ser Trp Ser Lys Trp Ser Ser Pro Val Cys Val
195 200 205
Pro Pro Glu Asn Pro Pro Gln Pro Gln Val Arg Phe Ser Val Glu Gln
210 215 220
Leu Gly Gln Asp Gly Arg Arg Arg Leu Thr Leu Lys Glu Gln Pro Thr
225 230 235 240
Gln Leu Glu Leu Pro Glu Gly Cys Gln Gly Leu Ala Pro Gly Thr Glu
245 250 255
Val Thr Tyr Arg Leu Gln Leu His Met Leu Ser Cys Pro Cys Lys Ala
260 265 270
Lys Ala Thr Arg Thr Leu His Leu Gly Lys Met Pro Tyr Leu Ser Gly
275 280 285
Ala Ala Tyr Asn Val Ala Val Ile Ser Ser Asn Gln Phe Gly Pro Gly
290 295 300
Leu Asn Gln Thr Trp His Ile Pro Ala Asp Thr His Thr Glu Pro Val
305 310 315 320
Ala Leu Asn Ile Ser Val Gly Thr Asn Gly Thr Thr Met Tyr Trp Pro
325 330 335
Ala Arg Ala Gln Ser Met Thr Tyr Cys Ile Glu Trp Gln Pro Val Gly
340 345 350
Gln Asp Gly Gly Leu Ala Thr Cys Ser Leu Thr Ala Pro Gln Asp Pro
355 360 365
Asp Pro Ala Gly Met Ala Thr Tyr Ser Trp Ser Arg Glu Ser Gly Ala
370 375 380
Met Gly Gln Glu Lys Cys Tyr Tyr Ile Thr Ile Phe Ala Ser Ala His
385 390 395 400
Pro Glu Lys Leu Thr Leu Trp Ser Thr Val Leu Ser Thr Tyr His Phe
405 410 415
Gly Gly Asn Ala Ser Ala Ala Gly Thr Pro His His Val Ser Val Lys
420 425 430
Asn His Ser Leu Asp Ser Val Ser Val Asp Trp Ala Pro Ser Leu Leu
435 440 445
Ser Thr Cys Pro Gly Val Leu Lys Glu Tyr Val Val Arg Cys Arg Asp
450 455 460
Glu Asp Ser Lys Gln Val Ser Glu His Pro Val Gln Pro Thr Glu Thr
465 470 475 480
Gln Val Thr Leu Ser Gly Leu Arg Ala Gly Val Ala Tyr Thr Val Gln
485 490 495
Val Arg Ala Asp Thr Ala Trp Leu Arg Gly Val Trp Ser Gln Pro Gln
500 505 510
Arg Phe Ser Ile Glu Val Gln Val Ser Asp
515 520
<210> 7
<211> 862
<212> PRT
<213> Homo sapiens
<400> 7
Met Ala His Thr Phe Arg Gly Cys Ser Leu Ala Phe Met Phe Ile Ile
1 5 10 15
Thr Trp Leu Leu Ile Lys Ala Lys Ile Asp Ala Cys Lys Arg Gly Asp
20 25 30
Val Thr Val Lys Pro Ser His Val Ile Leu Leu Gly Ser Thr Val Asn
35 40 45
Ile Thr Cys Ser Leu Lys Pro Arg Gln Gly Cys Phe His Tyr Ser Arg
50 55 60
Arg Asn Lys Leu Ile Leu Tyr Lys Phe Asp Arg Arg Ile Asn Phe His
65 70 75 80
His Gly His Ser Leu Asn Ser Gln Val Thr Gly Leu Pro Leu Gly Thr
85 90 95
Thr Leu Phe Val Cys Lys Leu Ala Cys Ile Asn Ser Asp Glu Ile Gln
100 105 110
Ile Cys Gly Ala Glu Ile Phe Val Gly Val Ala Pro Glu Gln Pro Gln
115 120 125
Asn Leu Ser Cys Ile Gln Lys Gly Glu Gln Gly Thr Val Ala Cys Thr
130 135 140
Trp Glu Arg Gly Arg Asp Thr His Leu Tyr Thr Glu Tyr Thr Leu Gln
145 150 155 160
Leu Ser Gly Pro Lys Asn Leu Thr Trp Gln Lys Gln Cys Lys Asp Ile
165 170 175
Tyr Cys Asp Tyr Leu Asp Phe Gly Ile Asn Leu Thr Pro Glu Ser Pro
180 185 190
Glu Ser Asn Phe Thr Ala Lys Val Thr Ala Val Asn Ser Leu Gly Ser
195 200 205
Ser Ser Ser Leu Pro Ser Thr Phe Thr Phe Leu Asp Ile Val Arg Pro
210 215 220
Leu Pro Pro Trp Asp Ile Arg Ile Lys Phe Gln Lys Ala Ser Val Ser
225 230 235 240
Arg Cys Thr Leu Tyr Trp Arg Asp Glu Gly Leu Val Leu Leu Asn Arg
245 250 255
Leu Arg Tyr Arg Pro Ser Asn Ser Arg Leu Trp Asn Met Val Asn Val
260 265 270
Thr Lys Ala Lys Gly Arg His Asp Leu Leu Asp Leu Lys Pro Phe Thr
275 280 285
Glu Tyr Glu Phe Gln Ile Ser Ser Lys Leu His Leu Tyr Lys Gly Ser
290 295 300
Trp Ser Asp Trp Ser Glu Ser Leu Arg Ala Gln Thr Pro Glu Glu Glu
305 310 315 320
Pro Thr Gly Met Leu Asp Val Trp Tyr Met Lys Arg His Ile Asp Tyr
325 330 335
Ser Arg Gln Gln Ile Ser Leu Phe Trp Lys Asn Leu Ser Val Ser Glu
340 345 350
Ala Arg Gly Lys Ile Leu His Tyr Gln Val Thr Leu Gln Glu Leu Thr
355 360 365
Gly Gly Lys Ala Met Thr Gln Asn Ile Thr Gly His Thr Ser Trp Thr
370 375 380
Thr Val Ile Pro Arg Thr Gly Asn Trp Ala Val Ala Val Ser Ala Ala
385 390 395 400
Asn Ser Lys Gly Ser Ser Leu Pro Thr Arg Ile Asn Ile Met Asn Leu
405 410 415
Cys Glu Ala Gly Leu Leu Ala Pro Arg Gln Val Ser Ala Asn Ser Glu
420 425 430
Gly Met Asp Asn Ile Leu Val Thr Trp Gln Pro Pro Arg Lys Asp Pro
435 440 445
Ser Ala Val Gln Glu Tyr Val Val Glu Trp Arg Glu Leu His Pro Gly
450 455 460
Gly Asp Thr Gln Val Pro Leu Asn Trp Leu Arg Ser Arg Pro Tyr Asn
465 470 475 480
Val Ser Ala Leu Ile Ser Glu Asn Ile Lys Ser Tyr Ile Cys Tyr Glu
485 490 495
Ile Arg Val Tyr Ala Leu Ser Gly Asp Gln Gly Gly Cys Ser Ser Ile
500 505 510
Leu Gly Asn Ser Lys His Lys Ala Pro Leu Ser Gly Pro His Ile Asn
515 520 525
Ala Ile Thr Glu Glu Lys Gly Ser Ile Leu Ile Ser Trp Asn Ser Ile
530 535 540
Pro Val Gln Glu Gln Met Gly Cys Leu Leu His Tyr Arg Ile Tyr Trp
545 550 555 560
Lys Glu Arg Asp Ser Asn Ser Gln Pro Gln Leu Cys Glu Ile Pro Tyr
565 570 575
Arg Val Ser Gln Asn Ser His Pro Ile Asn Ser Leu Gln Pro Arg Val
580 585 590
Thr Tyr Val Leu Trp Met Thr Ala Leu Thr Ala Ala Gly Glu Ser Ser
595 600 605
His Gly Asn Glu Arg Glu Phe Cys Leu Gln Gly Lys Ala Asn Trp Met
610 615 620
Ala Phe Val Ala Pro Ser Ile Cys Ile Ala Ile Ile Met Val Gly Ile
625 630 635 640
Phe Ser Thr His Tyr Phe Gln Gln Lys Val Phe Val Leu Leu Ala Ala
645 650 655
Leu Arg Pro Gln Trp Cys Ser Arg Glu Ile Pro Asp Pro Ala Asn Ser
660 665 670
Thr Cys Ala Lys Lys Tyr Pro Ile Ala Glu Glu Lys Thr Gln Leu Pro
675 680 685
Leu Asp Arg Leu Leu Ile Asp Trp Pro Thr Pro Glu Asp Pro Glu Pro
690 695 700
Leu Val Ile Ser Glu Val Leu His Gln Val Thr Pro Val Phe Arg His
705 710 715 720
Pro Pro Cys Ser Asn Trp Pro Gln Arg Glu Lys Gly Ile Gln Gly His
725 730 735
Gln Ala Ser Glu Lys Asp Met Met His Ser Ala Ser Ser Pro Pro Pro
740 745 750
Pro Arg Ala Leu Gln Ala Glu Ser Arg Gln Leu Val Asp Leu Tyr Lys
755 760 765
Val Leu Glu Ser Arg Gly Ser Asp Pro Lys Pro Glu Asn Pro Ala Cys
770 775 780
Pro Trp Thr Val Leu Pro Ala Gly Asp Leu Pro Thr His Asp Gly Tyr
785 790 795 800
Leu Pro Ser Asn Ile Asp Asp Leu Pro Ser His Glu Ala Pro Leu Ala
805 810 815
Asp Ser Leu Glu Glu Leu Glu Pro Gln His Ile Ser Leu Ser Val Phe
820 825 830
Pro Ser Ser Ser Leu His Pro Leu Thr Phe Ser Cys Gly Asp Lys Leu
835 840 845
Thr Leu Asp Gln Leu Lys Met Arg Cys Asp Ser Leu Met Leu
850 855 860
<210> 8
<211> 599
<212> PRT
<213> Homo sapiens
<400> 8
Lys Ile Asp Ala Cys Lys Arg Gly Asp Val Thr Val Lys Pro Ser His
1 5 10 15
Val Ile Leu Leu Gly Ser Thr Val Asn Ile Thr Cys Ser Leu Lys Pro
20 25 30
Arg Gln Gly Cys Phe His Tyr Ser Arg Arg Asn Lys Leu Ile Leu Tyr
35 40 45
Lys Phe Asp Arg Arg Ile Asn Phe His His Gly His Ser Leu Asn Ser
50 55 60
Gln Val Thr Gly Leu Pro Leu Gly Thr Thr Leu Phe Val Cys Lys Leu
65 70 75 80
Ala Cys Ile Asn Ser Asp Glu Ile Gln Ile Cys Gly Ala Glu Ile Phe
85 90 95
Val Gly Val Ala Pro Glu Gln Pro Gln Asn Leu Ser Cys Ile Gln Lys
100 105 110
Gly Glu Gln Gly Thr Val Ala Cys Thr Trp Glu Arg Gly Arg Asp Thr
115 120 125
His Leu Tyr Thr Glu Tyr Thr Leu Gln Leu Ser Gly Pro Lys Asn Leu
130 135 140
Thr Trp Gln Lys Gln Cys Lys Asp Ile Tyr Cys Asp Tyr Leu Asp Phe
145 150 155 160
Gly Ile Asn Leu Thr Pro Glu Ser Pro Glu Ser Asn Phe Thr Ala Lys
165 170 175
Val Thr Ala Val Asn Ser Leu Gly Ser Ser Ser Ser Leu Pro Ser Thr
180 185 190
Phe Thr Phe Leu Asp Ile Val Arg Pro Leu Pro Pro Trp Asp Ile Arg
195 200 205
Ile Lys Phe Gln Lys Ala Ser Val Ser Arg Cys Thr Leu Tyr Trp Arg
210 215 220
Asp Glu Gly Leu Val Leu Leu Asn Arg Leu Arg Tyr Arg Pro Ser Asn
225 230 235 240
Ser Arg Leu Trp Asn Met Val Asn Val Thr Lys Ala Lys Gly Arg His
245 250 255
Asp Leu Leu Asp Leu Lys Pro Phe Thr Glu Tyr Glu Phe Gln Ile Ser
260 265 270
Ser Lys Leu His Leu Tyr Lys Gly Ser Trp Ser Asp Trp Ser Glu Ser
275 280 285
Leu Arg Ala Gln Thr Pro Glu Glu Glu Pro Thr Gly Met Leu Asp Val
290 295 300
Trp Tyr Met Lys Arg His Ile Asp Tyr Ser Arg Gln Gln Ile Ser Leu
305 310 315 320
Phe Trp Lys Asn Leu Ser Val Ser Glu Ala Arg Gly Lys Ile Leu His
325 330 335
Tyr Gln Val Thr Leu Gln Glu Leu Thr Gly Gly Lys Ala Met Thr Gln
340 345 350
Asn Ile Thr Gly His Thr Ser Trp Thr Thr Val Ile Pro Arg Thr Gly
355 360 365
Asn Trp Ala Val Ala Val Ser Ala Ala Asn Ser Lys Gly Ser Ser Leu
370 375 380
Pro Thr Arg Ile Asn Ile Met Asn Leu Cys Glu Ala Gly Leu Leu Ala
385 390 395 400
Pro Arg Gln Val Ser Ala Asn Ser Glu Gly Met Asp Asn Ile Leu Val
405 410 415
Thr Trp Gln Pro Pro Arg Lys Asp Pro Ser Ala Val Gln Glu Tyr Val
420 425 430
Val Glu Trp Arg Glu Leu His Pro Gly Gly Asp Thr Gln Val Pro Leu
435 440 445
Asn Trp Leu Arg Ser Arg Pro Tyr Asn Val Ser Ala Leu Ile Ser Glu
450 455 460
Asn Ile Lys Ser Tyr Ile Cys Tyr Glu Ile Arg Val Tyr Ala Leu Ser
465 470 475 480
Gly Asp Gln Gly Gly Cys Ser Ser Ile Leu Gly Asn Ser Lys His Lys
485 490 495
Ala Pro Leu Ser Gly Pro His Ile Asn Ala Ile Thr Glu Glu Lys Gly
500 505 510
Ser Ile Leu Ile Ser Trp Asn Ser Ile Pro Val Gln Glu Gln Met Gly
515 520 525
Cys Leu Leu His Tyr Arg Ile Tyr Trp Lys Glu Arg Asp Ser Asn Ser
530 535 540
Gln Pro Gln Leu Cys Glu Ile Pro Tyr Arg Val Ser Gln Asn Ser His
545 550 555 560
Pro Ile Asn Ser Leu Gln Pro Arg Val Thr Tyr Val Leu Trp Met Thr
565 570 575
Ala Leu Thr Ala Ala Gly Glu Ser Ser His Gly Asn Glu Arg Glu Phe
580 585 590
Cys Leu Gln Gly Lys Ala Asn
595
<210> 9
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 9
Gly Gly Gly Gly Ser
1 5
<210> 10
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 10
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 11
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 11
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 12
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 12
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 13
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 13
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 14
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 14
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
<210> 15
<211> 35
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 15
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly
20 25 30
Gly Gly Ser
35
<210> 16
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 16
Asp Pro Ala Leu Val His Gln Arg Pro Ala Pro Pro Gly Gly Gly Gly
1 5 10 15
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly
20 25 30
<210> 17
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 17
Gly Lys Pro Gly Ser
1 5
<210> 18
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 18
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser Gly Lys Pro Gly Ser
20 25
<210> 19
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 19
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser
20 25 30
<210> 20
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 20
Gly Gly Gly Glu Ser
1 5
<210> 21
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 1 monomer 1
<400> 21
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 22
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 1 monomer 2
<400> 22
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 23
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 2 monomer 1
<400> 23
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 24
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone monomer 2
<400> 24
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 25
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 3 monomer 1
<400> 25
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 26
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 3 monomer 2
<400> 26
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Glu Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 27
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 4 monomer 1
<400> 27
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Lys Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 28
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 4 monomer 2
<400> 28
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Glu
130 135 140
Asn Glu Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Glu Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 29
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 5 monomer 1
<400> 29
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Gln Leu Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 30
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 5 monomer 2
<400> 30
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 31
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 6 monomer 1
<400> 31
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 32
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 6 monomer 2
<400> 32
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Ala Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 33
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 7 monomer 1
<400> 33
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Ser Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 34
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 7 monomer 2
<400> 34
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Ser Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 35
<211> 229
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 8 monomer 1
<400> 35
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Gln Met Thr Lys Asn Gln
130 135 140
Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys
225
<210> 36
<211> 229
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 8 monomer 2
<400> 36
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Glu Glu Gly Asp Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly Lys
225
<210> 37
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 9 monomer 1
<400> 37
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
35 40 45
His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
65 70 75 80
Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn
85 90 95
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro
100 105 110
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val
130 135 140
Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
195 200 205
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Pro Gly Lys
225
<210> 38
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 9 monomer 2
<400> 38
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
35 40 45
His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Phe Asn Ser Thr
65 70 75 80
Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn
85 90 95
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro
100 105 110
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
130 135 140
Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val
195 200 205
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Pro Gly Lys
225
<210> 39
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 10 monomer 1
<400> 39
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys
35 40 45
His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr
65 70 75 80
Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn
85 90 95
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro
100 105 110
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn Gln Val
130 135 140
Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
195 200 205
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Pro Gly Lys
225
<210> 40
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 10 monomer 2
<400> 40
Glu Arg Lys Cys Cys Val Glu Cys Pro Pro Cys Pro Ala Pro Pro Val
1 5 10 15
Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
20 25 30
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys
35 40 45
His Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu
50 55 60
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Phe Asn Ser Thr
65 70 75 80
Phe Arg Val Val Ser Val Leu Thr Val Val His Gln Asp Trp Leu Asn
85 90 95
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ala Pro
100 105 110
Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Gln Pro Arg Glu Pro Gln
115 120 125
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
130 135 140
Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val
145 150 155 160
Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
165 170 175
Pro Met Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr
180 185 190
Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val
195 200 205
Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu
210 215 220
Ser Pro Gly Lys
225
<210> 41
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 11 monomer 1
<400> 41
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 42
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 11 monomer 2
<400> 42
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 43
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 12 monomer 1
<400> 43
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 44
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 12 monomer 2
<400> 44
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 45
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 13 monomer 1
<400> 45
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 46
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Backbone 13 monomer 2
<400> 46
Glu Arg Lys Ser Ser Asp Lys Thr His Thr Cys Pro Arg Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Lys Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 47
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2_Fc(216)_IgG1_
pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 47
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 48
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27201 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1_
C220S/PVA_/S267K/S364K/E357Q
<400> 48
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 49
<211> 546
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27202 Chain 1 - empty-Fc(216)_IgG1_pI(-)_Isosteric
_A_C220S/PVA_/S267K/L368D/K370S_(GGGGS)2_human_IL12p40
<400> 49
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys
130 135 140
Asn Gln Val Ser Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
225 230 235 240
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
245 250 255
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
260 265 270
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
275 280 285
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
290 295 300
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
305 310 315 320
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
325 330 335
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
340 345 350
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
355 360 365
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
370 375 380
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
385 390 395 400
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
405 410 415
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
420 425 430
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
435 440 445
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
450 455 460
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
465 470 475 480
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
485 490 495
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
500 505 510
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
515 520 525
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
530 535 540
Cys Ser
545
<210> 50
<211> 437
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27202 Chain 2 - human_IL12p40-empty-Fc(216)_IgG1_
C220S/PVA_/S267K/S364K/E357Q_(GGGGS)2_human_IL12p35
<400> 50
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
225 230 235 240
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
245 250 255
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
260 265 270
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
275 280 285
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
290 295 300
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
305 310 315 320
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
325 330 335
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
340 345 350
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
355 360 365
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
370 375 380
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
385 390 395 400
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
405 410 415
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
420 425 430
Tyr Leu Asn Ala Ser
435
<210> 51
<211> 769
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 - human_IL12p40_(GGGGS)5-human_IL12p35_(GGGGS)2
_(single-Chain)_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/
PVA_/S267K/L368D/K370S
<400> 51
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
305 310 315 320
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Asn Leu Pro Val
325 330 335
Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His His Ser Gln Asn
340 345 350
Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala Arg Gln Thr Leu
355 360 365
Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His Glu Asp Ile Thr
370 375 380
Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro Leu Glu Leu Thr
385 390 395 400
Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr Ser Phe Ile Thr Asn
405 410 415
Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe Met Met Ala Leu Cys
420 425 430
Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr Gln Val Glu Phe Lys
435 440 445
Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys Arg Gln Ile Phe Leu
450 455 460
Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu Met Gln Ala Leu Asn
465 470 475 480
Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp
485 490 495
Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu Leu His Ala Phe Arg
500 505 510
Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
515 520 525
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp
530 535 540
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
545 550 555 560
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
565 570 575
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
580 585 590
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
595 600 605
Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val
610 615 620
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
625 630 635 640
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
645 650 655
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
660 665 670
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
675 680 685
Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
690 695 700
Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
705 710 715 720
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
725 730 735
Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His Glu
740 745 750
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
755 760 765
Lys
<210> 52
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27203 Chain 2 - empty-Fc(216)_IgG1_C220S/PVA_/S267K
/S364K/E357Q
<400> 52
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 53
<211> 769
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27204 Chain 1 - human_IL12p35_(GGGGS)5-human_IL12p40
_(GGGGS)2_(single-Chain)_Fc(216)_IgG1_pI(-)_Isosteric
_A_C220S/PVA_/S267K/L368D/K370S
<400> 53
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
195 200 205
Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Ile Trp
210 215 220
Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr Pro Asp
225 230 235 240
Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu Glu Asp
245 250 255
Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly Ser Gly
260 265 270
Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly Gln Tyr
275 280 285
Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu Leu Leu
290 295 300
His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys Asp Gln
305 310 315 320
Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys Asn Tyr
325 330 335
Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr Asp Leu
340 345 350
Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln Gly Val
355 360 365
Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly Asp Asn
370 375 380
Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala Cys Pro
385 390 395 400
Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala Val His
405 410 415
Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg Asp Ile
420 425 430
Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu Lys Asn
435 440 445
Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp Ser Thr
450 455 460
Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln Gly Lys
465 470 475 480
Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr Ser Ala
485 490 495
Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala Gln Asp
500 505 510
Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro Cys Ser
515 520 525
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp
530 535 540
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
545 550 555 560
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
565 570 575
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
580 585 590
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
595 600 605
Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val
610 615 620
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
625 630 635 640
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
645 650 655
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
660 665 670
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
675 680 685
Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
690 695 700
Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
705 710 715 720
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
725 730 735
Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His Glu
740 745 750
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
755 760 765
Lys
<210> 54
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27204 Chain 2 - empty-Fc(216)_IgG1_C220S/PVA_/S267K/
S364K/E357Q
<400> 54
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<210> 55
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27560 human_IL12p40_(GGGGS)2-Fc(216)_IgG1_pI(-)_
Isosteric_A_C220S/PVA_/S267K/L368D/K370S_homodimer
<400> 55
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 56
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP27561 human_IL12p35_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_/S267K/
S364K/E357Q_homodimer
<400> 56
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 57
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D)
<400> 57
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 58
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113D)
<400> 58
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 59
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N200D)
<400> 59
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 60
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N281D)
<400> 60
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 61
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N113D/N200D/N281D)
<400> 61
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 62
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q42E)
<400> 62
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 63
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E45Q)
<400> 63
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 64
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q56E)
<400> 64
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 65
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59Q)
<400> 65
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 66
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(D62N)
<400> 66
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asn Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 67
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q42E/E45Q)
<400> 67
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 68
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E45Q/Q56E)
<400> 68
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 69
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q42E/E59Q)
<400> 69
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 70
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q56E/E59Q)
<400> 70
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 71
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q42E/E45Q/Q56E)
<400> 71
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 72
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E45Q/Q56E/E59Q)
<400> 72
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 73
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(D161N)
<400> 73
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asn Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 74
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E73Q)
<400> 74
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Gln Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 75
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q144E)
<400> 75
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Glu
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 76
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E262Q)
<400> 76
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Gln Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 77
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E100Q)
<400> 77
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Gln Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 78
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(D18N)
<400> 78
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asn Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 79
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E33Q)
<400> 79
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Gln Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 80
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q229E)
<400> 80
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Glu Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 81
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E235Q)
<400> 81
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Gln Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 82
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(Q256N)
<400> 82
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Asn
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 83
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E299Q)
<400> 83
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Gln Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 84
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(D87N)
<400> 84
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asn Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 85
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24752 human_IL12p40_N103D_(GGGGS)2-Fc(216)_IgG1
_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 85
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 86
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24753 human_IL12p40_N113D_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 86
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 87
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24754 human_IL12p40_N200D_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 87
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 88
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24755 human_IL12p40_N281D_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 88
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 89
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24756 human_IL12p40_N103D/N113D/N200D/N281D_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 89
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 90
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24757 human_IL12p40_Q42E_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 90
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 91
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24758 human_IL12p40_E45Q_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 91
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 92
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24759 human_IL12p40_Q56E_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 92
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 93
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD24760) - human_IL12p40(E59Q)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 93
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 94
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24761 human_IL12p40_D62N_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 94
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asn Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 95
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24762 human_IL12p40_Q42E/E45Q_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 95
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 96
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24763 human_IL12p40_E45Q/Q56E_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 96
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 97
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24764 human_IL12p40_Q42E/E59Q_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 97
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 98
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD24765) - human_IL12p40(Q56E/E59Q)_(GGGGS)2_Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 98
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 99
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24766 human_IL12p40_Q42E/E45Q/Q56E_(GGGGS)2-Fc(216)_IgG1_
pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 99
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 100
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24767 human_IL12p40_E45Q/Q56E/E59Q_(GGGGS)2-Fc(216)_IgG1
_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 100
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 101
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24768 human_IL12p40_D161N_(GGGGS)2-Fc(216)_IgG1_pI
(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 101
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asn Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 102
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24769 human_IL12p40_E73Q_(GGGGS)2-Fc(216)_IgG1_pI(
-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 102
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Gln Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 103
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24770 human_IL12p40_Q144E_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 103
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Glu
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 104
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24771 human_IL12p40_E262Q_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 104
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Gln Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 105
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24772 human_IL12p40_E100Q_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 105
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Gln Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 106
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24773 human_IL12p40_D18N_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 106
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asn Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 107
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24774 human_IL12p40_E33Q_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 107
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Gln Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 108
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24775 human_IL12p40_Q229E_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 108
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Glu Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 109
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24776 human_IL12p40_E235Q_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 109
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Gln Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 110
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24777 human_IL12p40_Q256E_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 110
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Glu
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 111
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24778 human_IL12p40_E299Q_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 111
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Gln Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 112
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24792 human_IL12p40_D87N_(GGGGS)2-Fc(216)_IgG1_pI(-
)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S_pTT5
<400> 112
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asn Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 113
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71D)
<400> 113
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 114
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N85D)
<400> 114
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 115
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N195D)
<400> 115
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser
195
<210> 116
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71D/N85D/N195D)
<400> 116
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser
195
<210> 117
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(E153Q)
<400> 117
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Gln Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 118
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(E38Q)
<400> 118
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Gln Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 119
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N151D)
<400> 119
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 120
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(Q135E)
<400> 120
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Glu Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 121
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(Q35D)
<400> 121
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Asp Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 122
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(Q146E)
<400> 122
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Glu Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 123
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N76D)
<400> 123
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asp Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 124
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(E162Q)
<400> 124
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Gln Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 125
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(E163Q)
<400> 125
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Gln Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 126
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24779 human_IL12p35_N71D_(GGGGS)2_Fc(216)_IgG1_C220S/PVA
_/S267K/S364K/E357Q_pTT5
<400> 126
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 127
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24780 human_IL12p35_N85D_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_
/S267K/S364K/E357Q_pTT5
<400> 127
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 128
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24781 human_IL12p35_N195D_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_
/S267K/S364K/E357Q_pTT5
<400> 128
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 129
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24782 human_IL12p35_N71D/N85D/N195D_(GGGGS)2_Fc(216)_
IgG1_C220S/PVA_/S267K/S364K/E357Q_pTT5
<400> 129
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 130
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24783 human_IL12p35_E153Q_(GGGGS)2_Fc(216)_IgG1_C220S/PVA
_/S267K/S364K/E357Q_pTT5
<400> 130
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Gln Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 131
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24784 human_IL12p35_E38Q_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_
/S267K/S364K/E357Q_pTT5
<400> 131
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Gln Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 132
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD24785) - human_IL12p35(N151D)_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 132
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 133
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24786 human_IL12p35_Q135E_(GGGGS)2_Fc(216)_IgG1_C220S/
PVA_/S267K/S364K/E357Q_pTT5
<400> 133
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Glu Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 134
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24787 human_IL12p35_Q35D_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_
/S267K/S364K/E357Q_pTT5
<400> 134
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Asp Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 135
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24788 human_IL12p35_Q146E_(GGGGS)2_Fc(216)_IgG1_C220S/PVA
_/S267K/S364K/E357Q_pTT5
<400> 135
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Glu Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 136
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24789 human_IL12p35_N76D_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_
/S267K/S364K/E357Q_pTT5
<400> 136
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asp Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 137
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24790 human_IL12p35_E162Q_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_
/S267K/S364K/E357Q_pTT5
<400> 137
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Gln Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 138
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XenD24791 human_IL12p35_E163Q_(GGGGS)2_Fc(216)_IgG1_C220S/PVA
_/S267K/S364K/E357Q_pTT5
<400> 138
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Gln Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 139
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28820 Chain 1 (XenD24756) - human_IL12p40_N103D/N113D/
N200D/N281D_(GGGGS)2-Fc(216)_IgG1_pI(-)_Isosteric_A_
C220S/PVA_/S267K/L368D/K370S
<400> 139
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 140
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28820 Chain 2 (XenD24782) - human_IL12p35_N71D/N85D/N195D
_(GGGGS)2_Fc(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 140
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 141
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28821 Chain 1 (XenD24792) - human_IL12p40_D87N_(GGGGS)
2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/
K370S
<400> 141
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asn Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 142
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28821 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 142
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 143
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28822 Chain 1 (XenD24757) - human_IL12p40_Q42E_(GGGGS)
2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/
K370S
<400> 143
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 144
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28822 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 144
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 145
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28823 Chain 1 (XenD24758) - human_IL12p40_E45Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 145
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 146
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28823 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 146
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 147
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28824 Chain 1 (XenD24759) - human_IL12p40_Q56E_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 147
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 148
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28824 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 148
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 149
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28825 Chain 1 (XenD24760) - human_IL12p40_E59Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 149
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 150
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28825 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 150
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 151
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28826 Chain 1 (XenD24761) - human_IL12p40_D62N_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 151
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asn Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 152
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28826 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 152
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 153
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28827 Chain 1 (XenD24762) - human_IL12p40_Q42E/E45Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 153
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 154
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28827 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 154
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 155
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28828 Chain 1 (XenD24763) - human_IL12p40_E45Q/Q56E_(GGGGS)
2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 155
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 156
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28828 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 156
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 157
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28829 Chain 1 (XenD24764) - human_IL12p40_Q42E/E59Q_(GGGGS)
2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 157
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 158
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28829 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 158
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 159
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28830 Chain 1 (XenD24765) - human_IL12p40_Q56E/E59Q_(GGGGS)
2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 159
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 160
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28830 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 160
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 161
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28831 Chain 1 (XenD24766) - human_IL12p40_Q42E/E45Q/Q56E_
(GGGGS)2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K
/L368D/K370S
<400> 161
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Glu Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 162
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28831 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 162
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 163
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28832 Chain 1 (XenD24767) - human_IL12p40_E45Q/Q56E/E59Q
_(GGGGS)2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 163
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Gln Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Glu Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 164
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28832 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 164
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 165
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28833 Chain 1 (XenD24768) - human_IL12p40_D161N_(GGGGS)
2-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D
/K370S
<400> 165
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asn Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 166
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28833 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 166
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 167
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28834 Chain 1 (XenD24769) - human_IL12p40_E73Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D
/K370S
<400> 167
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Gln Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 168
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28834 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 168
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 169
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28835 Chain 1 (XenD24770) - human_IL12p40_Q144E_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 169
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Glu
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 170
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28835 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 170
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 171
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28836 Chain 1 (XenD24771) - human_IL12p40_E262Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 171
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Gln Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 172
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28836 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 172
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 173
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28837 Chain 1 (XenD24772) - human_IL12p40_E100Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 173
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Gln Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 174
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28837 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 174
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 175
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28838 Chain 1 (XenD24773) - human_IL12p40_D18N_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D
/K370S
<400> 175
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asn Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 176
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28838 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 176
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 177
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28839 Chain 1 (XenD24774) - human_IL12p40_E33Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D
/K370S
<400> 177
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Gln Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 178
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28839 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 178
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 179
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28840 Chain 1 (XenD24775) - human_IL12p40_Q229E_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 179
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Glu Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 180
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28840 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 180
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 181
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28841 Chain 1 (XenD24776) - human_IL12p40_E235Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 181
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Gln Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 182
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28841 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 182
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 183
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28842 Chain 1 (XenD24777) - human_IL12p40_Q256E_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 183
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Glu
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 184
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28842 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 184
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 185
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28843 Chain 1 (XenD24778) - human_IL12p40_E299Q_(GGGGS)2
-Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 185
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Gln Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 186
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28843 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 186
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 187
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28844 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 187
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 188
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28844 Chain 2 (XenD24783) - human_IL12p35_E153Q_(GGGGS)2
_Fc(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 188
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Gln Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 189
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28845 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 189
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 190
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28845 Chain 2 (XenD24784) - human_IL12p35_E38Q_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 190
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Gln Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 191
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28846 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 191
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 192
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28846 Chain 2 (XenD24785) - human_IL12p35_N151D_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 192
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 193
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28847 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 193
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 194
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28847 Chain 2 (XenD24786) - human_IL12p35_Q135E_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 194
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Glu Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 195
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28848 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 195
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 196
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28848 Chain 2 (XenD24787) - human_IL12p35_Q35D_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 196
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Asp Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 197
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28849 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 197
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 198
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28849 Chain 2 (XenD24788) - human_IL12p35_Q146E_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 198
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Glu Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 199
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28850 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 199
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 200
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28850 Chain 2 (XenD24789) - human_IL12p35_N76D_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 200
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asp Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 201
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28851 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 201
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 202
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28851 Chain 2 (XenD24790) - human_IL12p35_E162Q_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 202
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Gln Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 203
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28852 Chain 1 (XenD22914) - human_IL12p40_(GGGGS)2-Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 203
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 204
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP28852 Chain 2 (XenD24791) - human_IL12p35_E163Q_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 204
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Gln Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 205
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K)
<400> 205
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 206
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E32Q/E59Q)
<400> 206
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 207
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(D34N/E59Q)
<400> 207
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 208
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Q/E187Q)
<400> 208
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Gln Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 209
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(S43E/E59Q)
<400> 209
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Glu Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 210
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(S43K/E59Q)
<400> 210
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Lys Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 211
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Q/K163E)
<400> 211
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Glu Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 212
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Q/K99E)
<400> 212
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 213
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Q/K258E)
<400> 213
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Glu Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 214
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Q/K260E)
<400> 214
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Glu Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 215
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25922) - human_IL12p40(E59K)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 215
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 216
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25923) - human_IL12p40(E32Q/E59Q)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 216
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 217
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25924) - human_IL12p40(D34N/E59Q)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 217
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 218
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25925) - human_IL12p40(E59Q/E187Q)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 218
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Gln Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 219
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25926) - human_IL12p40(S43E/E59Q)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 219
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Glu Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 220
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25927) - human_IL12p40(S43K/E59Q)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 220
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Lys Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 221
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25928) - human_IL12p40(E59Q/K163E)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 221
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Glu Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 222
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25929) - human_IL12p40(E59Q/K99E)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 222
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 223
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25930) - human_IL12p40(E59Q/K258E)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 223
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Glu Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 224
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD25931) - human_IL12p40(E59Q/K260E)_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 224
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Gln Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Glu Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 225
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(N151D/E153Q)
<400> 225
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Gln Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 226
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(E153K)
<400> 226
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Lys Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 227
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(N151K)
<400> 227
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Lys Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 228
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(N151D/D165N)
<400> 228
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asn Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 229
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(Q130E/N151D)
<400> 229
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Glu Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 230
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(N151D/K158E)
<400> 230
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Glu Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 231
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(E79Q/N151D)
<400> 231
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Gln Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 232
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(D55Q/N151D)
<400> 232
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Gln Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 233
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(N136D/N151D)
<400> 233
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asp Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 234
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(N21D/N151D)
<400> 234
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asp Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 235
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(E143Q/N151D)
<400> 235
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Gln Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 236
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25911) - human_IL12p35(N151D/E153Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 236
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Gln Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 237
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25912) - human_IL12p35(E153K)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 237
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Lys Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 238
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25913) - human_IL12p35(N151K)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 238
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Lys Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 239
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25914) - human_IL12p35(N151D/D165N)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 239
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asn Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 240
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25915) - human_IL12p35(Q130E/N151D)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 240
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Glu Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 241
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25916) - human_IL12p35(N151D/K158E)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 241
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Glu Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 242
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25917) - human_IL12p35(E79Q/N151D)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 242
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Gln Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 243
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25918) - human_IL12p35(D55Q/N151D)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 243
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Gln Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 244
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25919) - human_IL12p35(N136D/N151D)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 244
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asp Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 245
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25920) - human_IL12p35(N21D/N151D)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 245
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asp Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 246
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD25921) - human_IL12p35(E143Q/N151D)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 246
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Gln Leu
130 135 140
Met Gln Ala Leu Asn Phe Asp Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 247
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 247
Gly Gly Gly Gly Ala
1 5
<210> 248
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 248
Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala
1 5 10
<210> 249
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 249
Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala
1 5 10 15
<210> 250
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 250
Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly
1 5 10 15
Gly Gly Gly Ala
20
<210> 251
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 251
Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly
1 5 10 15
Gly Gly Gly Ala Gly Gly Gly Gly Ala
20 25
<210> 252
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 252
Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly
1 5 10 15
Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala
20 25 30
<210> 253
<211> 35
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<400> 253
Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly
1 5 10 15
Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly Gly Gly Ala Gly Gly
20 25 30
Gly Gly Ala
35
<210> 254
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N113D)
<400> 254
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 255
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N200D)
<400> 255
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 256
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N281D)
<400> 256
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 257
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113D/N200D)
<400> 257
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 258
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113D/N281D)
<400> 258
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 259
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N200D/N281D)
<400> 259
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 260
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N113D/N200D)
<400> 260
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 261
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N113D/N281D)
<400> 261
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 262
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103D/N200D/N281D)
<400> 262
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asp Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 263
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113D/N200D/N281D)
<400> 263
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asp Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asp Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asp Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 264
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q)
<400> 264
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 265
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113Q)
<400> 265
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 266
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N200Q)
<400> 266
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 267
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N281Q)
<400> 267
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 268
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N113Q)
<400> 268
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 269
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N200Q)
<400> 269
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 270
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N281Q)
<400> 270
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 271
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113Q/N200Q)
<400> 271
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 272
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113Q/N281Q)
<400> 272
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 273
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N200Q/N281Q)
<400> 273
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 274
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N113Q/N200Q)
<400> 274
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 275
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N113Q/N281Q)
<400> 275
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 276
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N200Q/N281Q)
<400> 276
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 277
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N113Q/N200Q/N281Q)
<400> 277
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 278
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(N103Q/N113Q/N200Q/N281Q)
<400> 278
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 279
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71Q)
<400> 279
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 280
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N85Q)
<400> 280
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 281
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N195Q)
<400> 281
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser
195
<210> 282
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71Q/N85Q)
<400> 282
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 283
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71Q/N195Q)
<400> 283
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser
195
<210> 284
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N85Q/N195Q)
<400> 284
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser
195
<210> 285
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71Q/N85Q/N195Q)
<400> 285
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser
195
<210> 286
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71D/N85D)
<400> 286
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 287
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N71D/N195D)
<400> 287
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asp Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser
195
<210> 288
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p35(N85D/N195D)
<400> 288
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asp Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asp Ala Ser
195
<210> 289
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33008 Chain 2 - human_IL12p35(N71Q/N85Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 289
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 290
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33009 Chain 2 - human_IL12p35(N71Q/N195Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 290
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 291
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD26411) - human_IL12p40_E59K/K99E_(GGGGS)2_Fc(216)
_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 291
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 292
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30598 Chain 1 (XenD26412) - human_IL12p40_D34N/E59K_(GGGGS)2
_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 292
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 293
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30599 Chain 1 (XenD26413) - human_IL12p40_D34N/E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 293
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 294
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30600 Chain 1 (XenD26414) - human_IL12p40_D34K/E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 294
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 295
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD26415) - human_IL12p40_E32Q/D34N/E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 295
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 296
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD26416) - human_IL12p40_E32Q/D34K/E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 296
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 297
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD26417) - human_IL12p40_E32K/D34N/E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 297
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Lys
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 298
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 1 (XenD26418) - human_IL12p40_E32K/D34K/E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K
/L368D/K370S
<400> 298
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Lys
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 299
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD26427) - human_IL12p35_D55Q_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 299
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Gln Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 300
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30609 Chain 2 (XenD26428) - human_IL12p35_D55K_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 300
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Lys Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 301
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31250 Chain 1 (XenD27070) - human_IL12p40(E59Y/K99E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 301
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Tyr Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 302
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31251 Chain 1 (XenD27071) - human_IL12p40(E59K/K99Y)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K
/L368D/K370S
<400> 302
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 303
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31252 Chain 1 (XenD27072) - human_IL12p40(E59Y/K99Y)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K
/L368D/K370S
<400> 303
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Tyr Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 304
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31253 Chain 1 (XenD27073) - human_IL12p40(E45K/E59K/K99E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 304
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Lys Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 305
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31254 Chain 1 (XenD27074) - human_IL12p40(D18K/E59K/K99E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 305
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 306
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31255 Chain 1 (XenD27075) - human_IL12p40(E59K/K99E/Q144E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 306
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Glu
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 307
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31256 Chain 1 (XenD27076) - human_IL12p40(E59K/K99E/Q144K)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D
/K370S
<400> 307
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Lys
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 308
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31257 Chain 1 (XenD27077) - human_IL12p40(E59K/K99E/R159E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 308
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Glu Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 309
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31258 Chain 1 (XenD27078) - human_IL12p40(E59K/K99E/K264E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/
L368D/K370S
<400> 309
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 310
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31259 Chain 2 (XenD27088) - human_IL12p35(F96A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 310
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Ala
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 311
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31260 Chain 2 (XenD27089) - human_IL12p35(M97A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 311
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Ala Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 312
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31261 Chain 2 (XenD27090) - human_IL12p35(L89A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 312
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Ala Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 313
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31262 Chain 2 (XenD27091) - human_IL12p35(L124A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 313
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Ala Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 314
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31263 Chain 2 (XenD27092) - human_IL12p35(M125A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 314
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Ala Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 315
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31264 Chain 2 (XenD27093) - human_IL12p35(L57A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 315
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Ala Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 316
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31265 Chain 2 (XenD27094) - human_IL12p35(I171A)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 316
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ala Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 317
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32186 Chain 1 (XenD28173) - human_IL12p40(D18K/E59K/K99E
/K264E)_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_
/S267K/L368D/K370S
<400> 317
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 318
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31142 Chain 1 (XenD24876) - human_IL12p40_(GGGGS)2_Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
/M428L/N434S
<400> 318
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 319
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD24877) - human_IL12p35_(GGGGS)2_IgG1_PVA
_/S267K/S364K/E357Q/M428L/N434S
<400> 319
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 320
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31143 Chain 1 (XenD27162) - human_IL12p40_E32Q/D34N/E59K/
K99E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_
/S267K/L368D/K370S/M428L/N434S
<400> 320
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 321
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31144 Chain 1 (XenD27163) - human_IL12p40_E32K/D34N/E59K/
K99E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S/M428L/N434S
<400> 321
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Lys
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 322
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> Chain 2 (XenD27166) - human_IL12p35_D55Q_(GGGGS)2_IgG1_PVA
_/S267K/S364K/E357Q/M428L/N434S
<400> 322
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Gln Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 323
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31145 Chain 1 (XenD27164) - human_IL12p40_E32K/D34K/E59K
/K99E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/
PVA_/S267K/L368D/K370S/M428L/N434S
<400> 323
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Lys
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 324
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31146 Chain 1 (XenD27165) - human_IL12p40_E59K/K99E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA
_/S267K/L368D/K370S/M428L/N434S
<400> 324
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 325
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K/K99E)
<400> 325
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 326
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(D34N/E59K)
<400> 326
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 327
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(D34N/E59K/K99E)
<400> 327
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 328
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(D34K/E59K/K99E)
<400> 328
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 329
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E32Q/D34N/E59K/K99E)
<400> 329
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 330
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E32Q/D34K/E59K/K99E)
<400> 330
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Gln
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 331
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E32K/D34N/E59K/K99E)
<400> 331
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Lys
20 25 30
Glu Asn Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 332
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E32K/D34K/E59K/K99E)
<400> 332
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Lys
20 25 30
Glu Lys Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 333
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(D55Q)
<400> 333
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Gln Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 334
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(D55K)
<400> 334
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Lys Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 335
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Y/K99E)
<400> 335
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Tyr Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 336
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K/K99Y)
<400> 336
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 337
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59Y/K99Y)
<400> 337
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Tyr Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 338
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E45K/E59K/K99E)
<400> 338
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Lys Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 339
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(D18K/E59K/K99E)
<400> 339
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 340
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K/K99E/Q144E)
<400> 340
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Glu
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 341
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K/K99E/Q144K)
<400> 341
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Lys
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 342
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K/K99E/R159E)
<400> 342
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Glu Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 343
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(E59K/K99E/K264E)
<400> 343
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 344
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p40(D18K/E59K/K99E/K264E)
<400> 344
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 345
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(F96A)
<400> 345
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Ala
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 346
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(M97A)
<400> 346
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Ala Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 347
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(L89A)
<400> 347
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Ala Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 348
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(L124A)
<400> 348
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Ala Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 349
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(M125A)
<400> 349
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Ala Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 350
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(L75A)
<400> 350
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Ala Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 351
<211> 197
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL12p35(I171A)
<400> 351
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ala Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser
195
<210> 352
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33010 Chain 2 - human_IL12p35(N85Q/N195Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 352
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 353
<211> 769
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31291 human_IL12p40(E59K/K99E)_(GGGGS)5-human_IL12p35_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K
/L368D/K370S
<400> 353
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
305 310 315 320
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Asn Leu Pro Val
325 330 335
Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His His Ser Gln Asn
340 345 350
Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala Arg Gln Thr Leu
355 360 365
Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His Glu Asp Ile Thr
370 375 380
Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro Leu Glu Leu Thr
385 390 395 400
Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr Ser Phe Ile Thr Asn
405 410 415
Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe Met Met Ala Leu Cys
420 425 430
Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr Gln Val Glu Phe Lys
435 440 445
Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys Arg Gln Ile Phe Leu
450 455 460
Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu Met Gln Ala Leu Asn
465 470 475 480
Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp
485 490 495
Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu Leu His Ala Phe Arg
500 505 510
Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
515 520 525
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp
530 535 540
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
545 550 555 560
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
565 570 575
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
580 585 590
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
595 600 605
Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val
610 615 620
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
625 630 635 640
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
645 650 655
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
660 665 670
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
675 680 685
Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
690 695 700
Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
705 710 715 720
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
725 730 735
Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His Glu
740 745 750
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
755 760 765
Lys
<210> 354
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33011 Chain 2 - human_IL12p35(N71Q/N85Q/N195Q)_
(GGGGS)2_Fc(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 354
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 355
<211> 442
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP016432 Nivolumab_H0L0_IgG1_PVA_/S267K Heavy Chain
<400> 355
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
115 120 125
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
180 185 190
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
210 215 220
Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro
225 230 235 240
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
245 250 255
Val Val Val Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp
260 265 270
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
275 280 285
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
290 295 300
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
305 310 315 320
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
325 330 335
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
340 345 350
Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
355 360 365
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
370 375 380
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
385 390 395 400
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
405 410 415
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
420 425 430
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440
<210> 356
<211> 214
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP016432 Nivolumab_H0L0_IgG1_PVA_/S267K Light Chain
<400> 356
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 357
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31582 Chain 1 - human_IL12p40(D18K/E59K/K99E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_
/S267K/L368D/K370S/M428L/N434S
<400> 357
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 358
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31583 Chain 1 - human_IL12p40(E59K/K99Y)_(GGGGS)2_Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/
K370S/M428L/N434S
<400> 358
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 359
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31584 Chain 1 - human_IL12p40(E59K/K99E/K264E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_
/S267K/L368D/K370S/M428L/N434S
<400> 359
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Leu
515 520 525
His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 360
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(C252S)
<400> 360
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Glu Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Lys Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 361
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(D18K/E59K/K99E/C252S)
<400> 361
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 362
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(D18K/E59K/K99E/C252S/K264E)
<400> 362
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 363
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99Y/C252S)
<400> 363
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 364
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/C252S/K264E)
<400> 364
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 365
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/C252S)
<400> 365
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 366
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/C252S/K264E)
<400> 366
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 367
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N113Q/C252S/K264E)
<400> 367
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 368
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N200Q/C252S/K264E)
<400> 368
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 369
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N281Q/C252S/K264E)
<400> 369
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 370
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E)
<400> 370
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 371
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E)
<400> 371
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 372
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E)
<400> 372
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 373
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E)
<400> 373
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 374
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(IL12p40_E59K/K99E/N113Q/N281Q/C252S/K264E)
<400> 374
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 375
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E)
<400> 375
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 376
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E)
<400> 376
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 377
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E)
<400> 377
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 378
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E)
<400> 378
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 379
<211> 306
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E)
<400> 379
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser
305
<210> 380
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32187 Chain 1 - human_IL12p40(D18K/E59K/K99E/C252S)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 380
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 381
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32188 Chain 1 - human_IL12p40(D18K/E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K
/L368D/K370S
<400> 381
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Lys Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 382
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32189 Chain 1 - human_IL12p40(E59K/K99Y/C252S)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA
_/S267K/L368D/K370S
<400> 382
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Tyr Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 383
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33011 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 383
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 384
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32191 Chain 1 - human_IL12p40(E59K/K99E/C252S)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA
_/S267K/L368D/K370S
<400> 384
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 385
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32991 IL-12p40(E59K/K99E/N103Q/C252S/K264E_(GGGGS)2
_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 385
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 386
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32992 IL-12p40(E59K/K99E/N113Q/C252S/K264E_(GGGGS)2
_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 386
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 387
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32993 IL-12p40(E59K/K99E/N200Q/C252S/K264E_(GGGGS)2_Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 387
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 388
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32994 IL-12p40(E59K/K99E/N281Q/C252S/K264E_(GGGGS)2_Fc
(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 388
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 389
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32995 IL-12p40(E59K/K99E/N103Q/N113Q/C252S/K264E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 389
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 390
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32996 IL-12p40(E59K/K99E/N103Q/N200Q/C252S/K264E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 390
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 391
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32997 IL-12p40(E59K/K99E/N103Q/N281Q/C252S/K264E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 391
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 392
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32998 IL-12p40(E59K/K99E/N113Q/N200Q/C252S/K264E
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 392
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 393
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32999 IL-12p40(E59K/K99E/N113Q/N281Q/C252S/K264E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 393
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 394
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33000 IL-12p40(E59K/K99E/N200Q/N281Q/C252S/K264E_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 394
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 395
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33001 IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/C252S
/K264E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S
/PVA_/S267K/L368D/K370S
<400> 395
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 396
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33002 IL-12p40(E59K/K99E/N103Q/N200Q/N281Q/C252S/
K264E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/
PVA_/S267K/L368D/K370S
<400> 396
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 397
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33003 IL-12p40(E59K/K99E/N113Q/N200Q/N281Q/C252S/
K264E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/
PVA_/S267K/L368D/K370S
<400> 397
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 398
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33004 IL-12p40(E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S
/K264E_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/
PVA_/S267K/L368D/K370S
<400> 398
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Gln Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Gln Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Gln Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Gln Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 399
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33005 Chain 2 - human_IL12p35(N71Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 399
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Gln Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 400
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33006 Chain 2 - human_IL12p35(N85Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 400
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Gln Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 401
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33007 Chain 2 - human_IL12p35(N195Q)_(GGGGS)2_Fc
(216)_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 401
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Gln Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 402
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32187 Chain 2 - IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 402
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 403
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32188 Chain 2 - IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 403
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 404
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32189 Chain 2 - IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 404
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 405
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32190 Chain 2 - IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 405
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 406
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32191 Chain 2 - IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 406
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 407
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32991 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 407
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 408
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32992 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 408
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 409
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32993 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 409
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 410
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32994 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 410
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 411
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32995 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 411
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 412
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32996 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 412
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 413
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32997 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 413
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 414
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32998 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 414
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 415
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32999 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 415
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 416
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33000 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 416
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 417
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33001 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 417
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 418
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33002 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 418
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 419
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33003 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 419
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 420
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33004 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q
<400> 420
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 421
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31582 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q/M428L/N434S
<400> 421
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 422
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31583 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q/M428L/N434S
<400> 422
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 423
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31584 Chain 2 - human_IL12p35_(GGGGS)2_Fc(216)_IgG1
_C220S/PVA_/S267K/S364K/E357Q/M428L/N434S
<400> 423
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Leu His Glu Ala Leu His Ser His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 424
<211> 769
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31290 Chain 1 - human_IL12p40(E59K/K99E)_(GGGGS)5-human_
IL12p35_(GGGGS)2_(single-chain)_Fc(216)_IgG1_pI(-)_
Isosteric_A_C220S/PVA_/S267K/L368D/K370S
<400> 424
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Cys Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Lys Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
305 310 315 320
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Arg Asn Leu Pro Val
325 330 335
Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu His His Ser Gln Asn
340 345 350
Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys Ala Arg Gln Thr Leu
355 360 365
Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp His Glu Asp Ile Thr
370 375 380
Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu Pro Leu Glu Leu Thr
385 390 395 400
Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr Ser Phe Ile Thr Asn
405 410 415
Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe Met Met Ala Leu Cys
420 425 430
Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr Gln Val Glu Phe Lys
435 440 445
Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys Arg Gln Ile Phe Leu
450 455 460
Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu Met Gln Ala Leu Asn
465 470 475 480
Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser Leu Glu Glu Pro Asp
485 490 495
Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu Leu His Ala Phe Arg
500 505 510
Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser Tyr Leu Asn Ala Ser
515 520 525
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser Ser Asp
530 535 540
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro
545 550 555 560
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
565 570 575
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His Glu Asp
580 585 590
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
595 600 605
Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr Arg Val
610 615 620
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
625 630 635 640
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
645 650 655
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
660 665 670
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
675 680 685
Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
690 695 700
Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
705 710 715 720
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
725 730 735
Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met His Glu
740 745 750
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
755 760 765
Lys
<210> 425
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32190 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)_
(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 425
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 426
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33005 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 426
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 427
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33006 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 427
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 428
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33007 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 428
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 429
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33008 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 429
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 430
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33009 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 430
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 431
<211> 547
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP33010 Chain 1 - human_IL12p40(E59K/K99E/C252S/K264E)
_(GGGGS)2_Fc(216)_IgG1_pI(-)_Isosteric_A_C220S/PVA_/
S267K/L368D/K370S
<400> 431
Ile Trp Glu Leu Lys Lys Asp Val Tyr Val Val Glu Leu Asp Trp Tyr
1 5 10 15
Pro Asp Ala Pro Gly Glu Met Val Val Leu Thr Cys Asp Thr Pro Glu
20 25 30
Glu Asp Gly Ile Thr Trp Thr Leu Asp Gln Ser Ser Glu Val Leu Gly
35 40 45
Ser Gly Lys Thr Leu Thr Ile Gln Val Lys Lys Phe Gly Asp Ala Gly
50 55 60
Gln Tyr Thr Cys His Lys Gly Gly Glu Val Leu Ser His Ser Leu Leu
65 70 75 80
Leu Leu His Lys Lys Glu Asp Gly Ile Trp Ser Thr Asp Ile Leu Lys
85 90 95
Asp Gln Glu Glu Pro Lys Asn Lys Thr Phe Leu Arg Cys Glu Ala Lys
100 105 110
Asn Tyr Ser Gly Arg Phe Thr Cys Trp Trp Leu Thr Thr Ile Ser Thr
115 120 125
Asp Leu Thr Phe Ser Val Lys Ser Ser Arg Gly Ser Ser Asp Pro Gln
130 135 140
Gly Val Thr Cys Gly Ala Ala Thr Leu Ser Ala Glu Arg Val Arg Gly
145 150 155 160
Asp Asn Lys Glu Tyr Glu Tyr Ser Val Glu Cys Gln Glu Asp Ser Ala
165 170 175
Cys Pro Ala Ala Glu Glu Ser Leu Pro Ile Glu Val Met Val Asp Ala
180 185 190
Val His Lys Leu Lys Tyr Glu Asn Tyr Thr Ser Ser Phe Phe Ile Arg
195 200 205
Asp Ile Ile Lys Pro Asp Pro Pro Lys Asn Leu Gln Leu Lys Pro Leu
210 215 220
Lys Asn Ser Arg Gln Val Glu Val Ser Trp Glu Tyr Pro Asp Thr Trp
225 230 235 240
Ser Thr Pro His Ser Tyr Phe Ser Leu Thr Phe Ser Val Gln Val Gln
245 250 255
Gly Lys Ser Lys Arg Glu Lys Glu Asp Arg Val Phe Thr Asp Lys Thr
260 265 270
Ser Ala Thr Val Ile Cys Arg Lys Asn Ala Ser Ile Ser Val Arg Ala
275 280 285
Gln Asp Arg Tyr Tyr Ser Ser Ser Trp Ser Glu Trp Ala Ser Val Pro
290 295 300
Cys Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu Pro Lys Ser
305 310 315 320
Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Pro Val Ala
325 330 335
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
340 345 350
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Lys His
355 360 365
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
370 375 380
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Glu Tyr Asn Ser Thr Tyr
385 390 395 400
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
405 410 415
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
420 425 430
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
435 440 445
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
450 455 460
Leu Thr Cys Asp Val Ser Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
465 470 475 480
Trp Glu Ser Asp Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
485 490 495
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
500 505 510
Asp Lys Ser Arg Trp Glu Gln Gly Asp Val Phe Ser Cys Ser Val Met
515 520 525
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
530 535 540
Pro Gly Lys
545
<210> 432
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<220>
<221> MISC_FEATURE
<222> (1)..(20)
<223> This sequence may encompass 0-5 "Gly Gly Gly Ser"
repeating units
<400> 432
Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Ser
20
<210> 433
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29952 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 433
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 434
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29953 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 434
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 435
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29954 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 435
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 436
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29955 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 436
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 437
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29956 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 437
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 438
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29957 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 438
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 439
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29958 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 439
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 440
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29959 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 440
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 441
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29960 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 441
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 442
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP29961 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 442
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 443
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30597 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 443
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 444
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30598 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 444
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 445
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30599 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 445
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 446
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30600 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 446
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 447
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30601 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 447
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 448
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30602 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 448
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 449
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30603 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 449
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 450
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP30604 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 450
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 451
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31250 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 451
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 452
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31251 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 452
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 453
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31252 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 453
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 454
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31253 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 454
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 455
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31254 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 455
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 456
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31255 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 456
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 457
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31255 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 457
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 458
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31256 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 458
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 459
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31257 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 459
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 460
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31258 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 460
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 461
<211> 438
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP32186 Chain 2 (XenD22915) - human_IL12p35_(GGGGS)2_Fc(216)
_IgG1_C220S/PVA_/S267K/S364K/E357Q
<400> 461
Arg Asn Leu Pro Val Ala Thr Pro Asp Pro Gly Met Phe Pro Cys Leu
1 5 10 15
His His Ser Gln Asn Leu Leu Arg Ala Val Ser Asn Met Leu Gln Lys
20 25 30
Ala Arg Gln Thr Leu Glu Phe Tyr Pro Cys Thr Ser Glu Glu Ile Asp
35 40 45
His Glu Asp Ile Thr Lys Asp Lys Thr Ser Thr Val Glu Ala Cys Leu
50 55 60
Pro Leu Glu Leu Thr Lys Asn Glu Ser Cys Leu Asn Ser Arg Glu Thr
65 70 75 80
Ser Phe Ile Thr Asn Gly Ser Cys Leu Ala Ser Arg Lys Thr Ser Phe
85 90 95
Met Met Ala Leu Cys Leu Ser Ser Ile Tyr Glu Asp Leu Lys Met Tyr
100 105 110
Gln Val Glu Phe Lys Thr Met Asn Ala Lys Leu Leu Met Asp Pro Lys
115 120 125
Arg Gln Ile Phe Leu Asp Gln Asn Met Leu Ala Val Ile Asp Glu Leu
130 135 140
Met Gln Ala Leu Asn Phe Asn Ser Glu Thr Val Pro Gln Lys Ser Ser
145 150 155 160
Leu Glu Glu Pro Asp Phe Tyr Lys Thr Lys Ile Lys Leu Cys Ile Leu
165 170 175
Leu His Ala Phe Arg Ile Arg Ala Val Thr Ile Asp Arg Val Met Ser
180 185 190
Tyr Leu Asn Ala Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Glu
195 200 205
Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
210 215 220
Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
225 230 235 240
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
245 250 255
Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly
260 265 270
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn
275 280 285
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
290 295 300
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro
305 310 315 320
Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
325 330 335
Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys Asn
340 345 350
Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
355 360 365
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
370 375 380
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys
385 390 395 400
Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys
405 410 415
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
420 425 430
Ser Leu Ser Pro Gly Lys
435
<210> 462
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 462
Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly Lys Pro Gly Ser Gly
1 5 10 15
Lys Pro Gly Ser
20
<210> 463
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<220>
<221> MISC_FEATURE
<222> (1)..(10)
<223> This sequence may encompass 0-5 "Gly Ser"
repeating units
<400> 463
Gly Ser Gly Ser Gly Ser Gly Ser Gly Ser
1 5 10
<210> 464
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<220>
<221> MISC_FEATURE
<222> (1)..(25)
<223> This sequence may encompass 0-5 "Gly Ser Gly Gly Ser"
repeating units
<400> 464
Gly Ser Gly Gly Ser Gly Ser Gly Gly Ser Gly Ser Gly Gly Ser Gly
1 5 10 15
Ser Gly Gly Ser Gly Ser Gly Gly Ser
20 25
<210> 465
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<220>
<221> MISC_FEATURE
<222> (1)..(25)
<223> This sequence may encompass 0-5 "Gly Gly Gly Gly Ser"
repeating units
<400> 465
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 466
<211> 4
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
peptide
<400> 466
Glu Pro Lys Ser
1
<210> 467
<211> 231
<212> PRT
<213> Artificial Sequence
<220>
<223> Description of Artificial Sequence: Synthetic
polypeptide
<220>
<223> XENP31290 Chain 2 - empty-Fc(216)_IgG1_C220S/PVA_/S267K/S364K
/E357Q
<400> 467
Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10 15
Pro Pro Val Ala Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
20 25 30
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
35 40 45
Asp Val Lys His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
50 55 60
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
65 70 75 80
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
85 90 95
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
100 105 110
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
115 120 125
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Gln Met Thr Lys
130 135 140
Asn Gln Val Lys Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
145 150 155 160
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
165 170 175
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
180 185 190
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
195 200 205
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
210 215 220
Leu Ser Leu Ser Pro Gly Lys
225 230
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СЛИТЫЙ БЕЛОК, ВКЛЮЧАЮЩИЙ IL-12 И АНТИТЕЛО ПРОТИВ FAP, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2831612C1 |
| АКТИВИРУЕМЫЕ ПОЛИПЕПТИДЫ ИНТЕРЛЕЙКИНА 12 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2826183C2 |
| ИММУНОЦИТОКИНЫ И ИХ ПРИМЕНЕНИЕ | 2021 |
|
RU2818371C1 |
| Слитые молекулы, происходящие от Cholix-токсина, для пероральной доставки биологически активных нагрузок | 2015 |
|
RU2723178C2 |
| АНТИТЕЛА, СОДЕРЖАЩИЕ ПОЛИПЕПТИД, ВСТРОЕННЫЙ В УЧАСТОК КАРКАСНОЙ ОБЛАСТИ 3 | 2019 |
|
RU2796254C2 |
| КОМПОЗИЦИЯ ДЛЯ КУЛЬТИВИРОВАНИЯ РЕГУЛЯТОРНЫХ Т-КЛЕТОК И ЕЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2807802C1 |
| АНТИТЕЛА, НАПРАВЛЕННЫЕ ПРОТИВ ИНТЕРЛЕЙКИНА-33 (IL-33) | 2015 |
|
RU2829846C2 |
| КОМПОЗИЦИЯ ДЛЯ ПРОТИВОРАКОВОГО ЛЕЧЕНИЯ, СОДЕРЖАЩАЯ NK-КЛЕТКИ И СЛИТЫЙ БЕЛОК, КОТОРЫЙ СОДЕРЖИТ БЕЛОК IL-2 И БЕЛОК CD80 | 2020 |
|
RU2832136C1 |
| КОМПОЗИЦИЯ ДЛЯ КУЛЬТИВИРОВАНИЯ ЕСТЕСТВЕННЫХ КЛЕТОК-КИЛЛЕРОВ И СПОСОБ ПОЛУЧЕНИЯ ЕСТЕСТВЕННЫХ КЛЕТОК-КИЛЛЕРОВ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2020 |
|
RU2824216C1 |
| Новые варианты интерлейкина-2 для лечения рака | 2020 |
|
RU2833537C2 |
















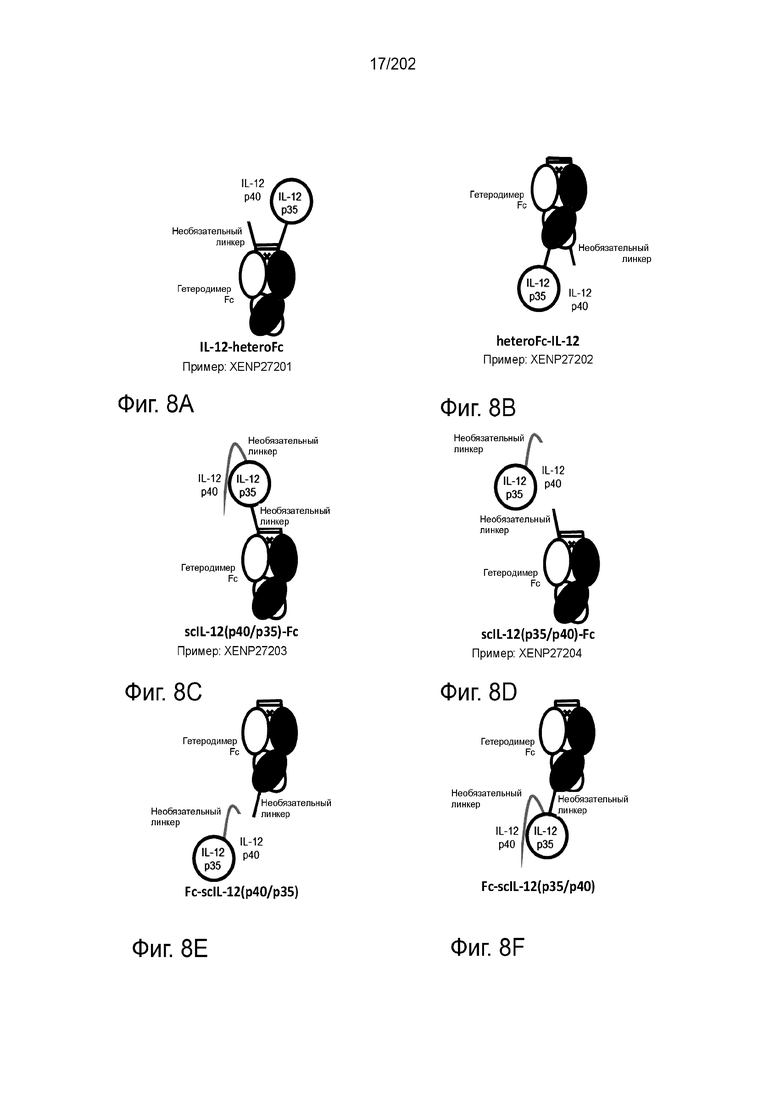



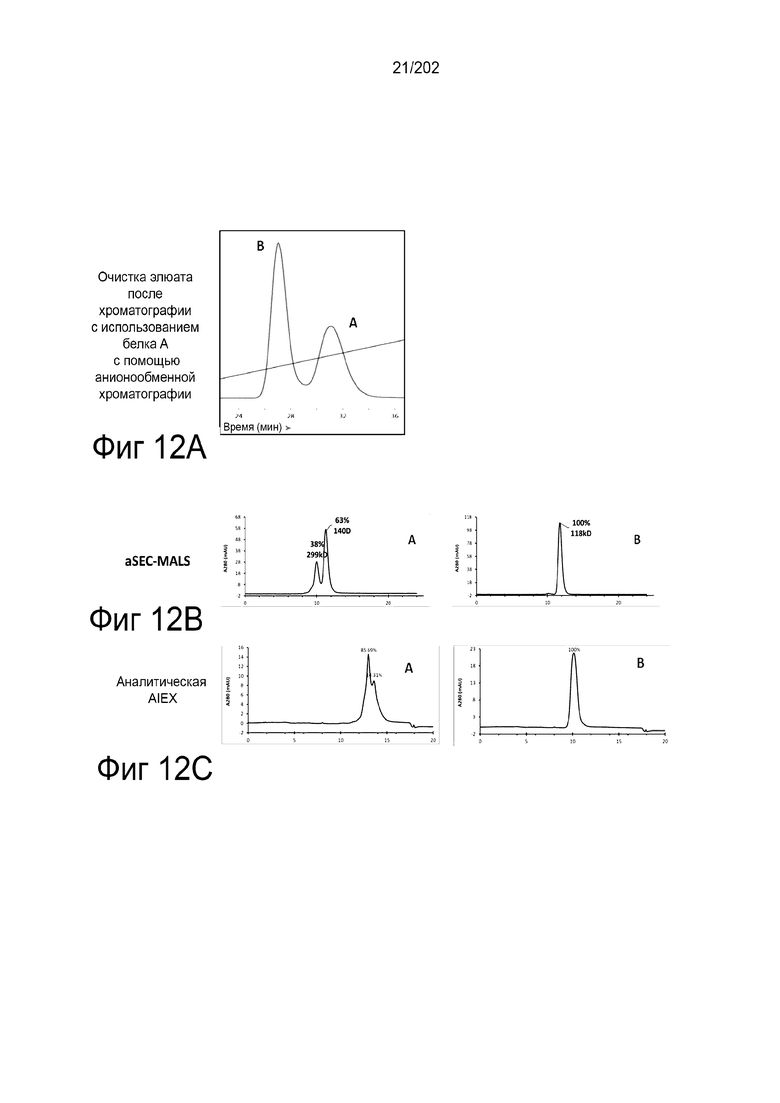
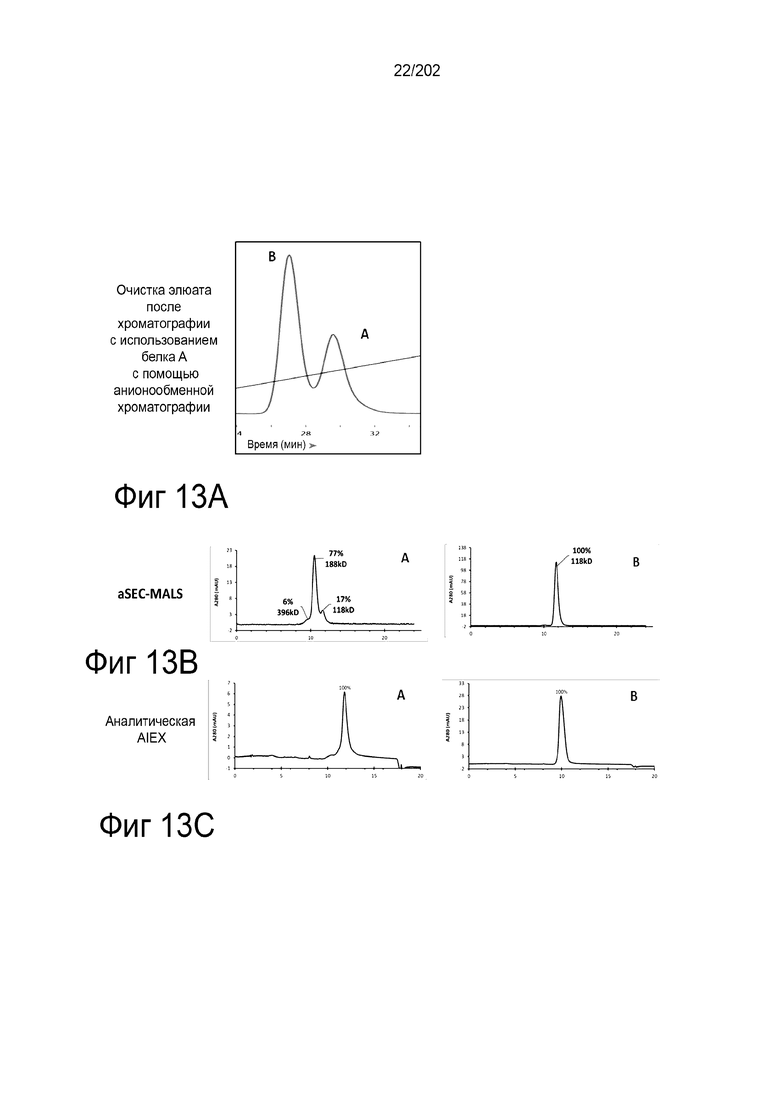
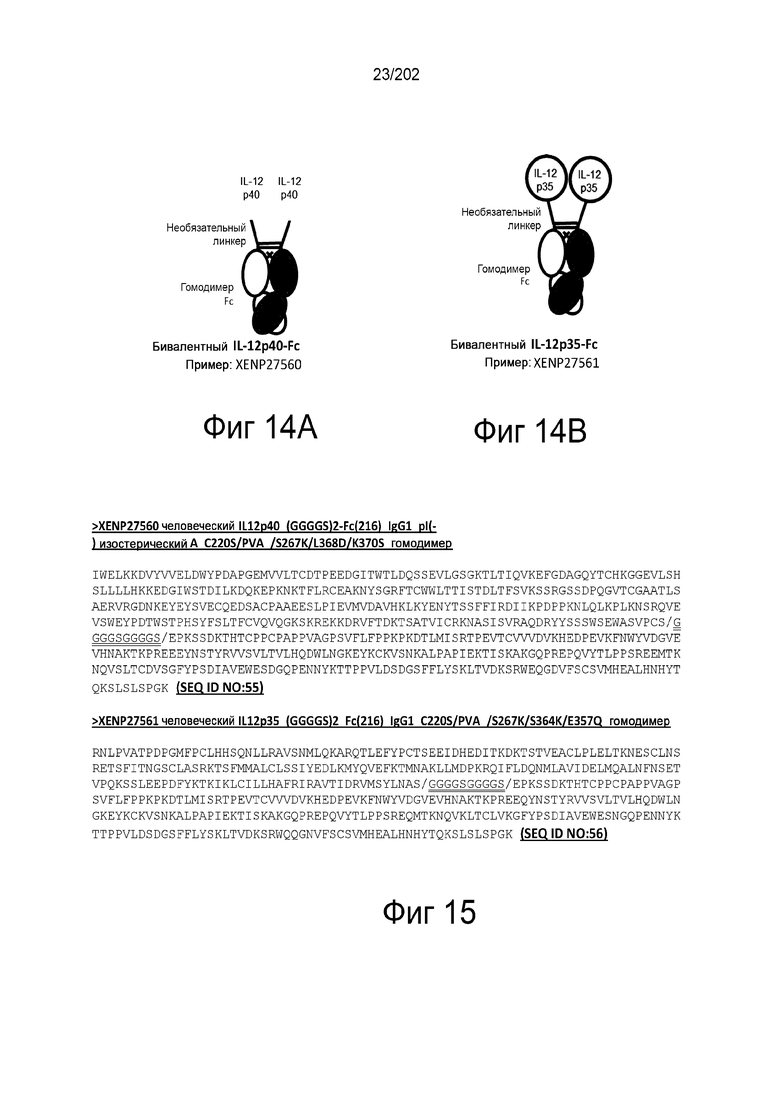
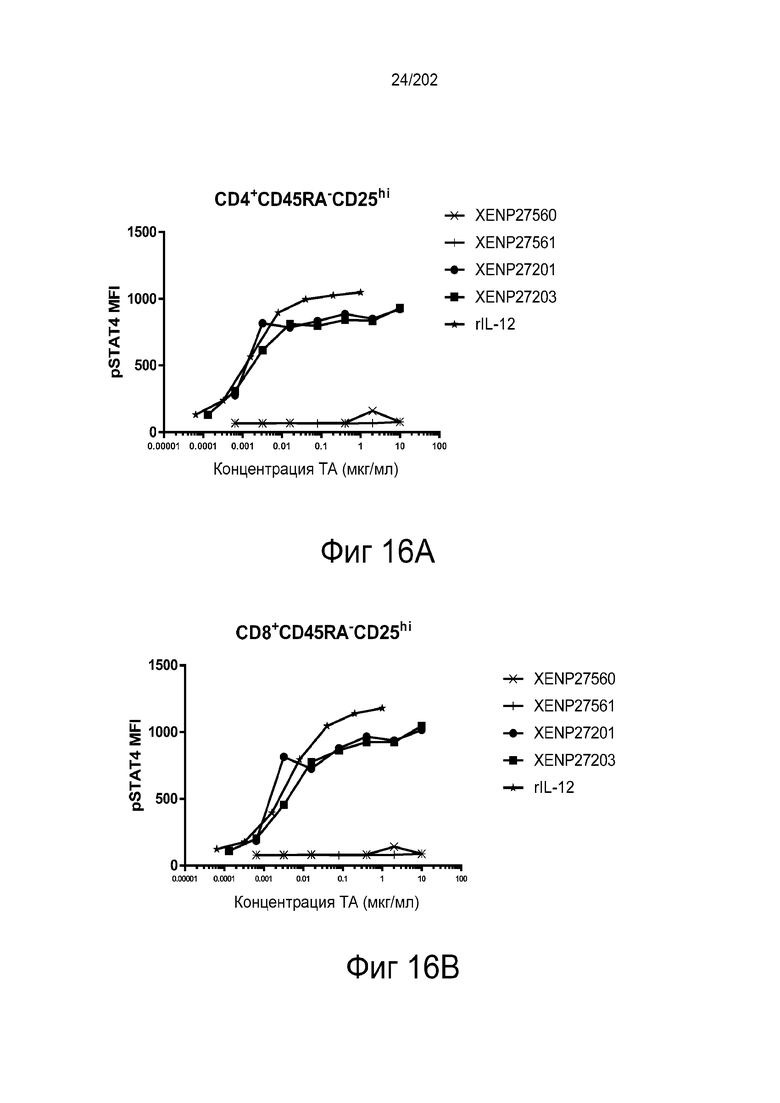
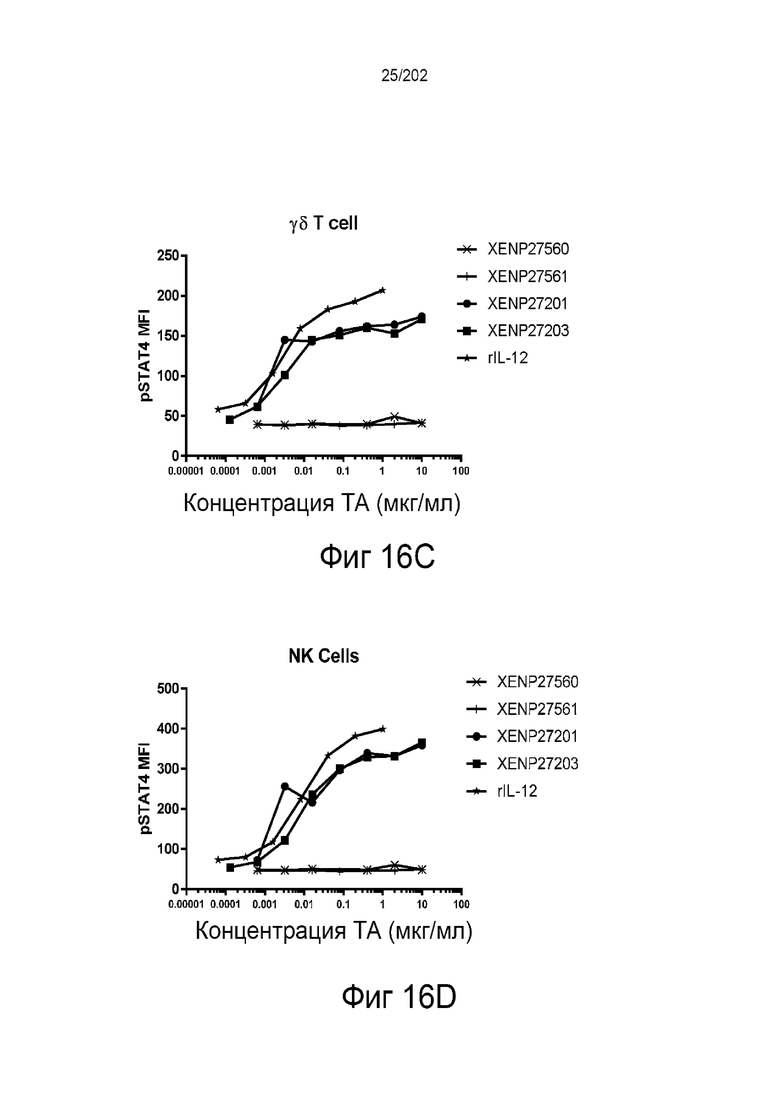

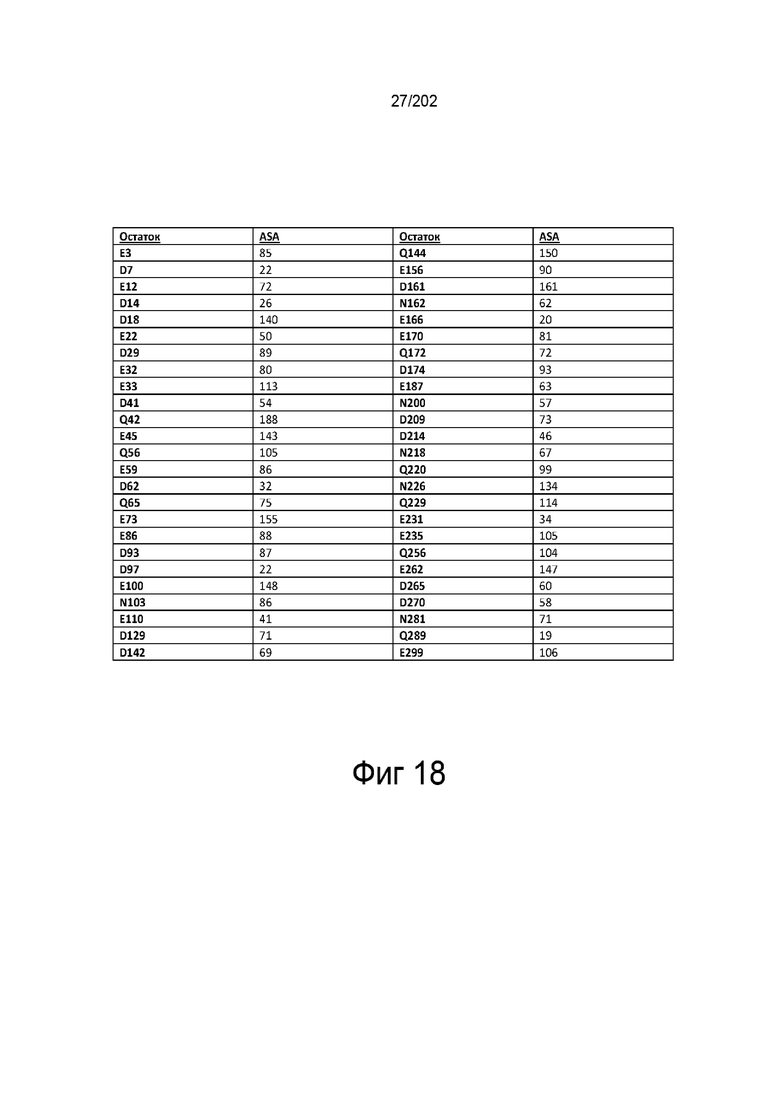


















































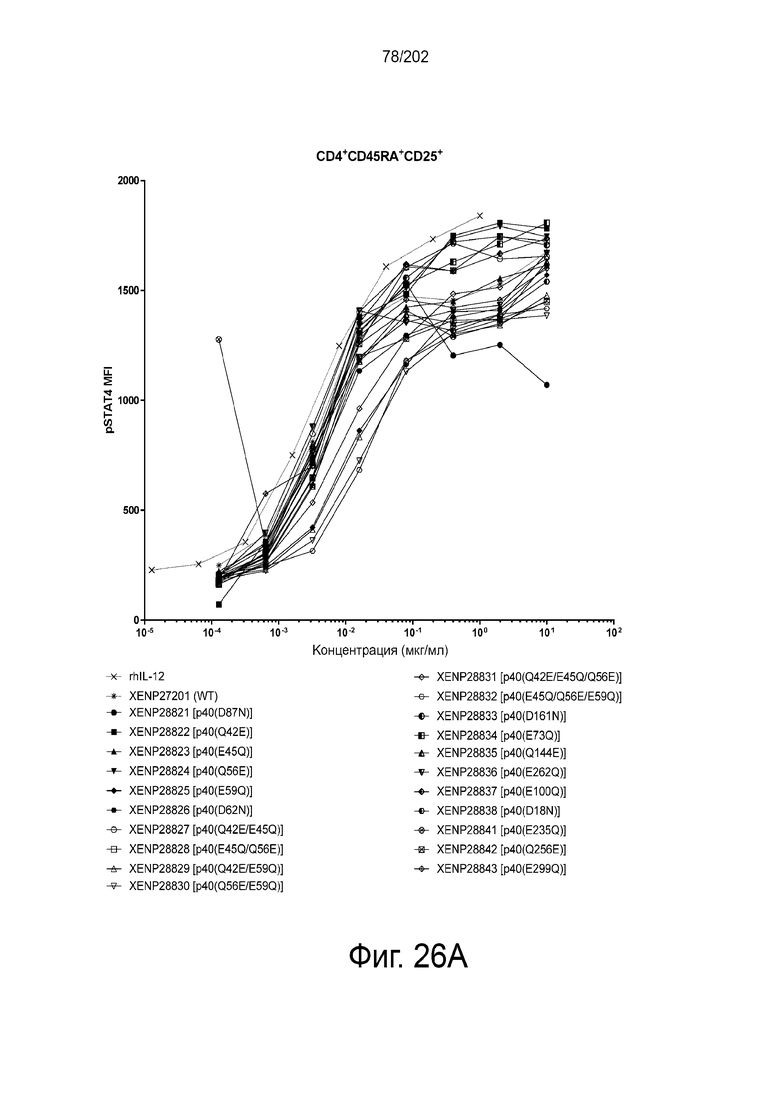
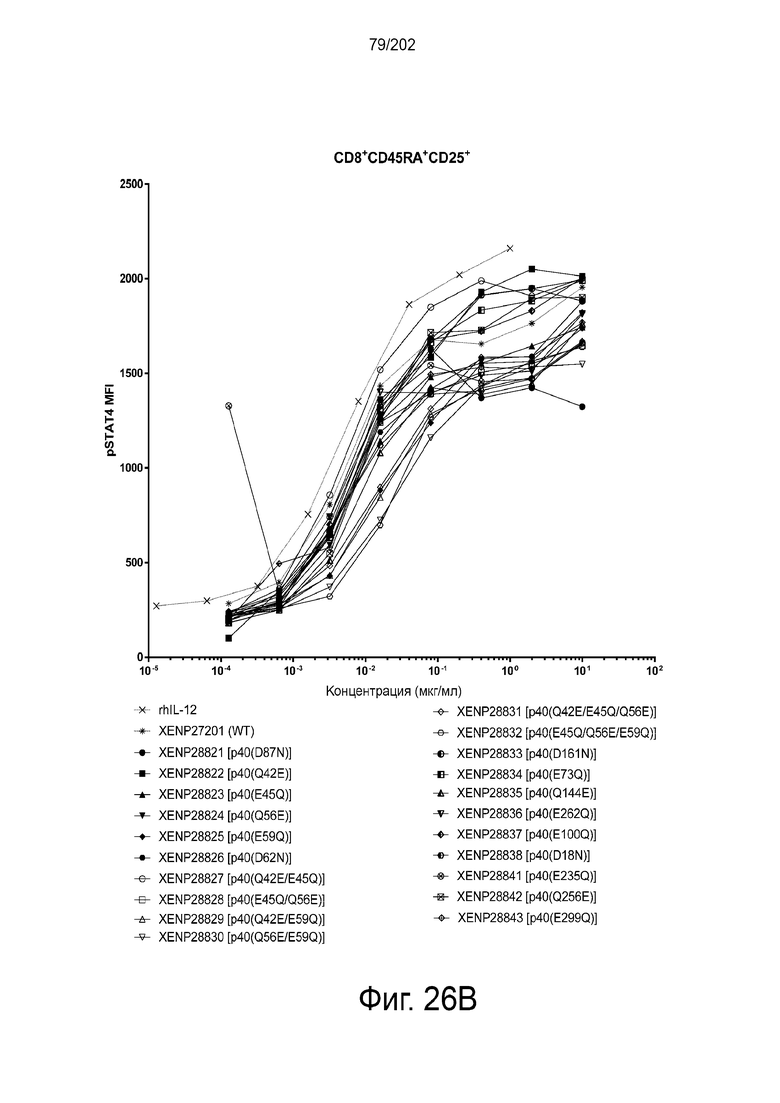
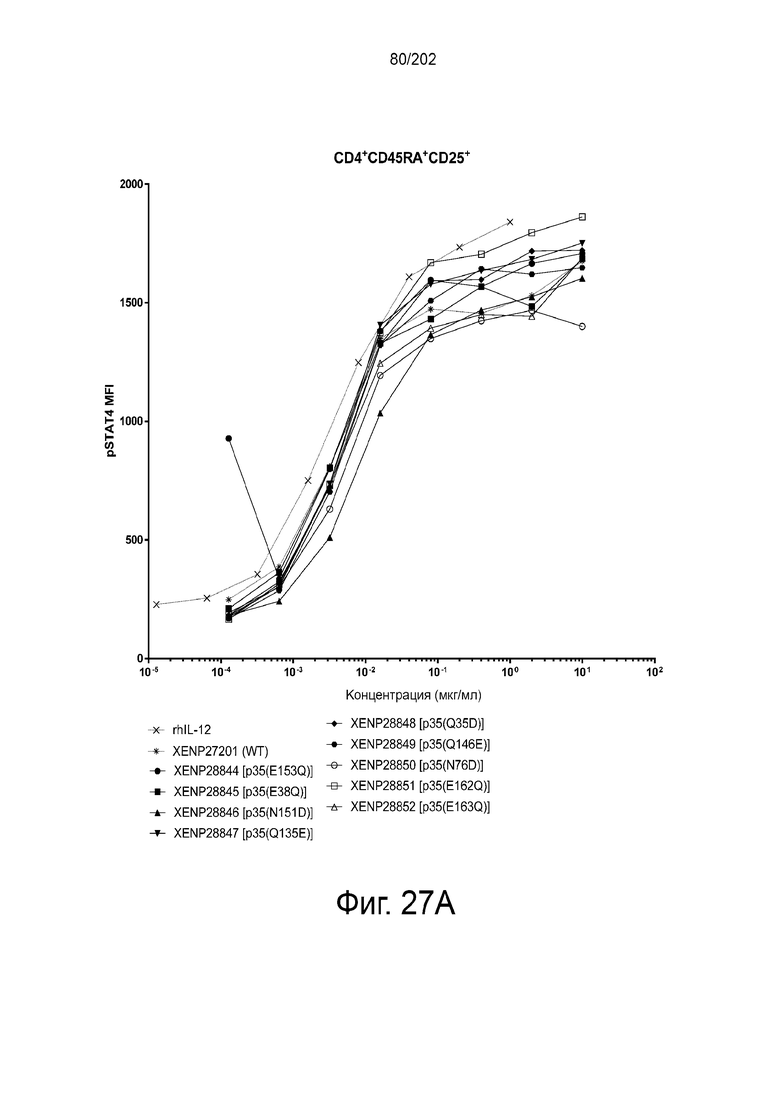
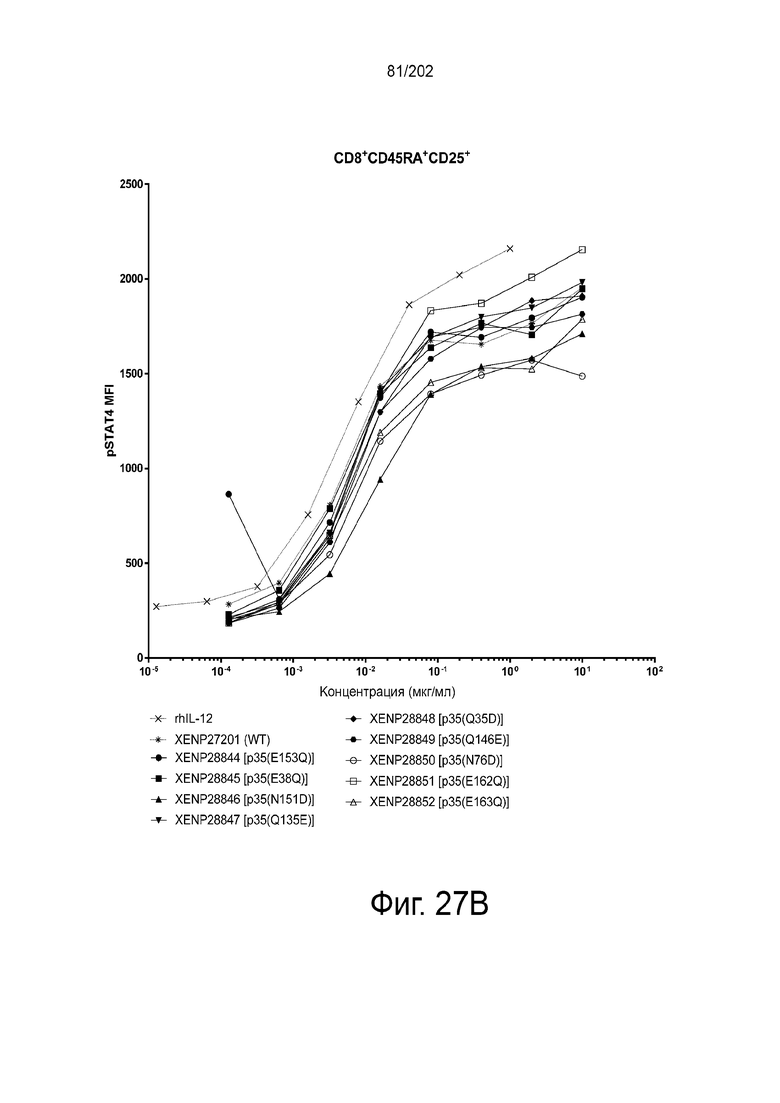
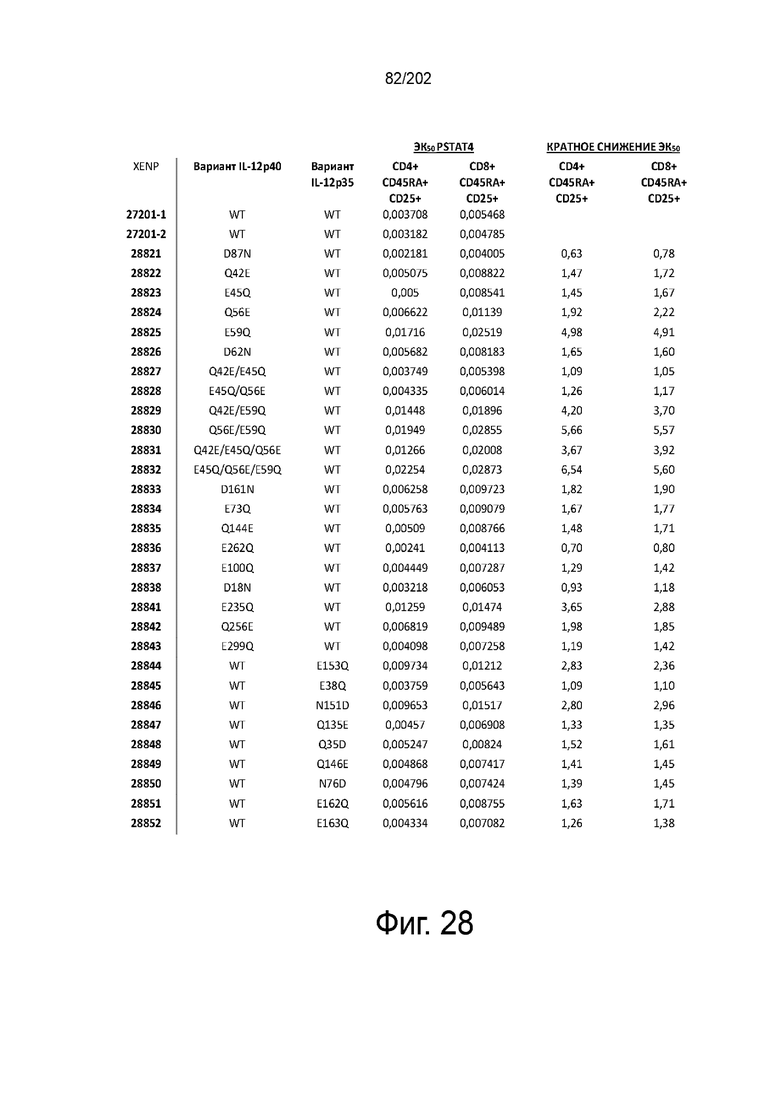




























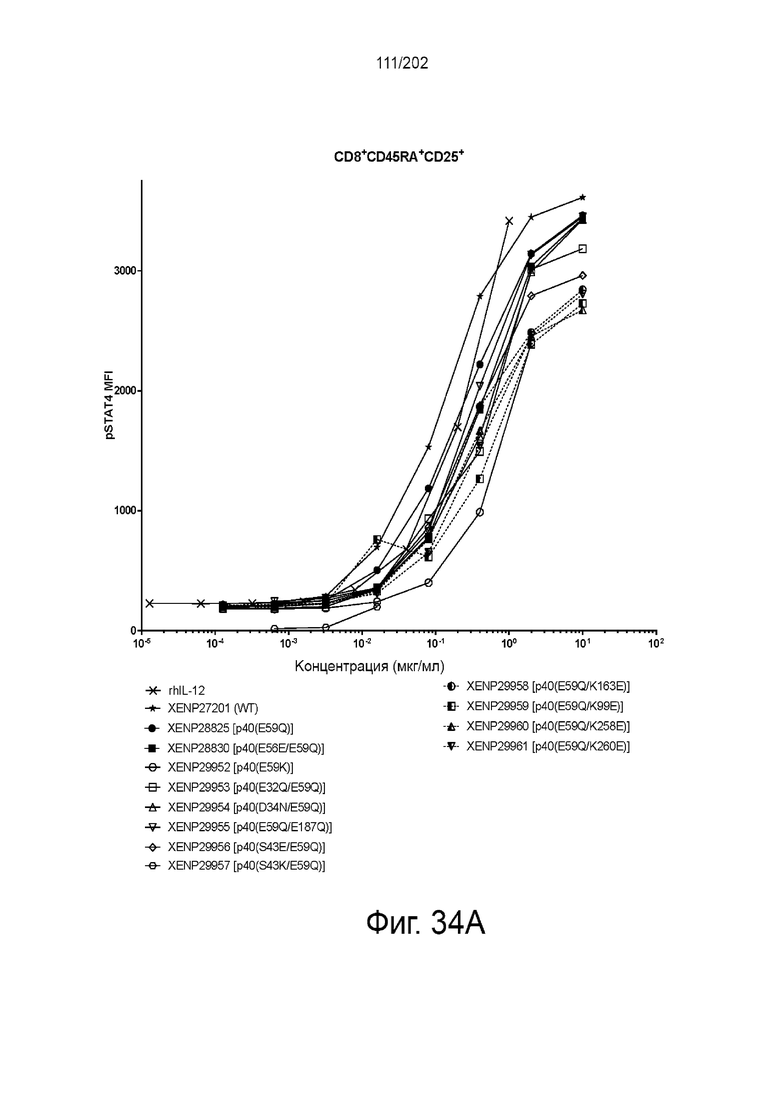
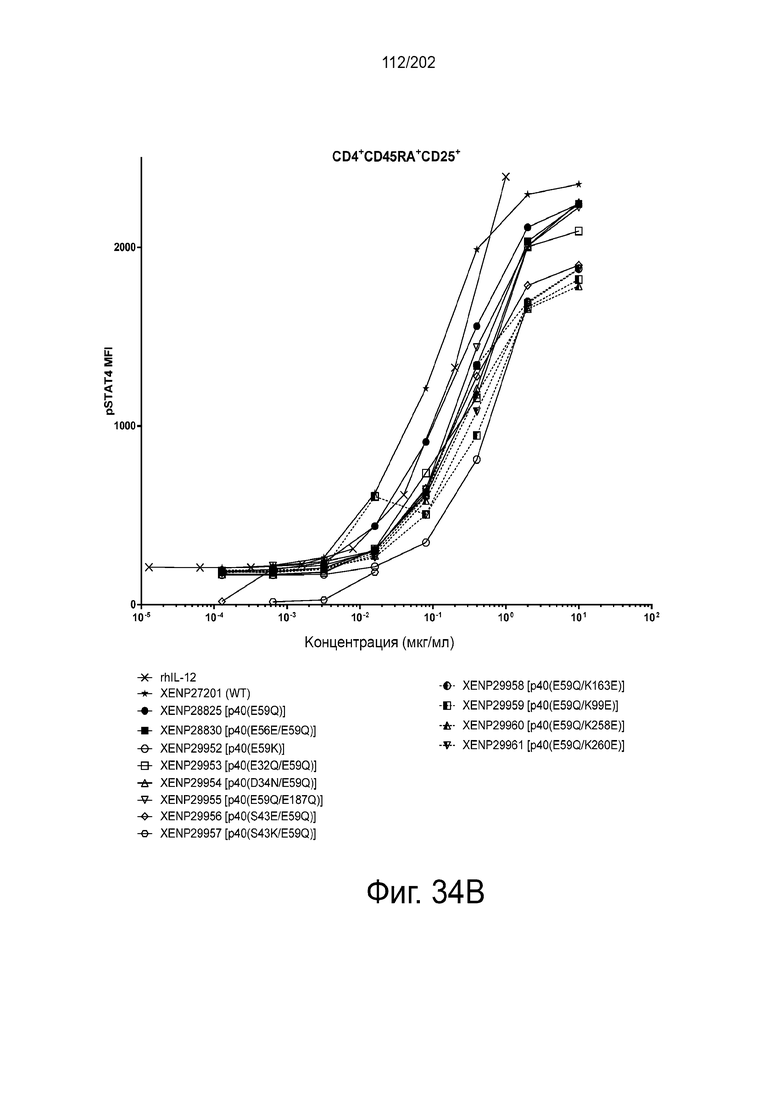
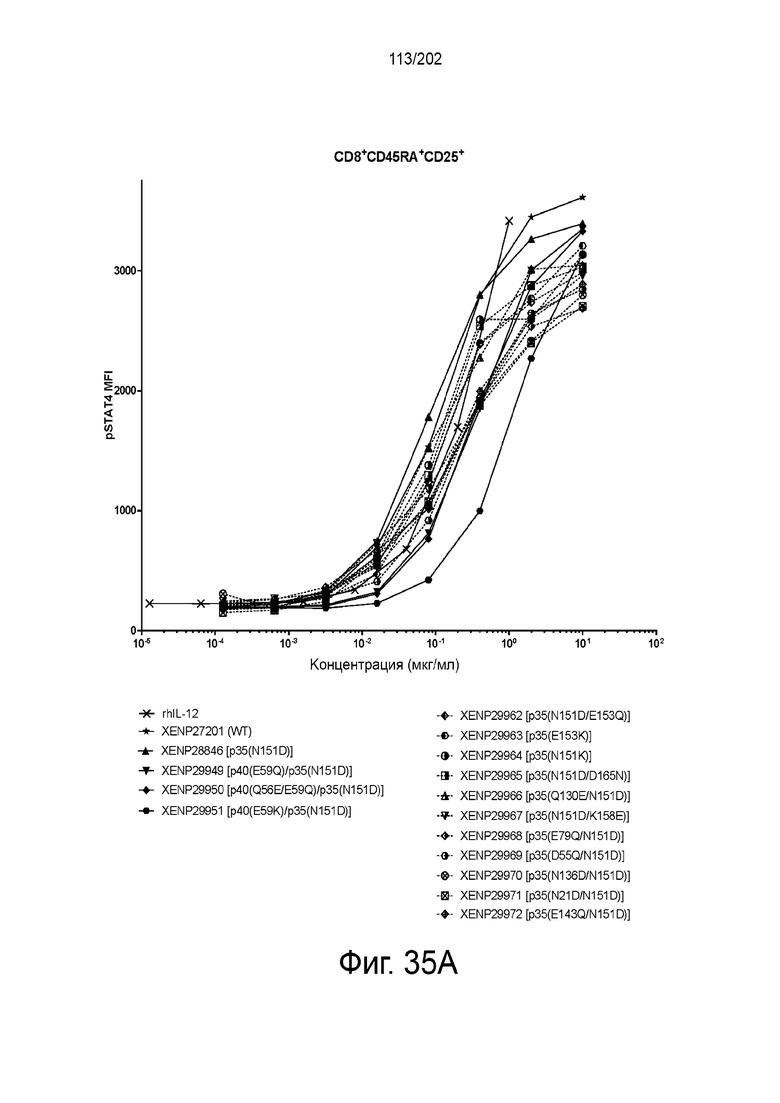
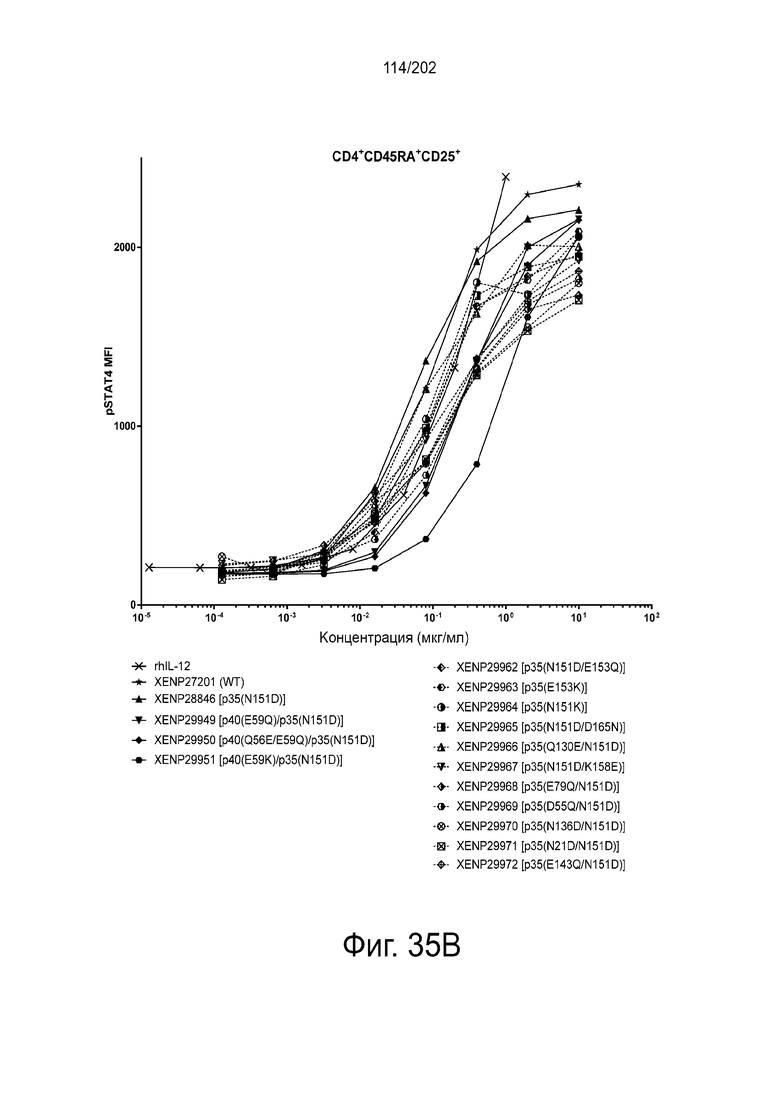
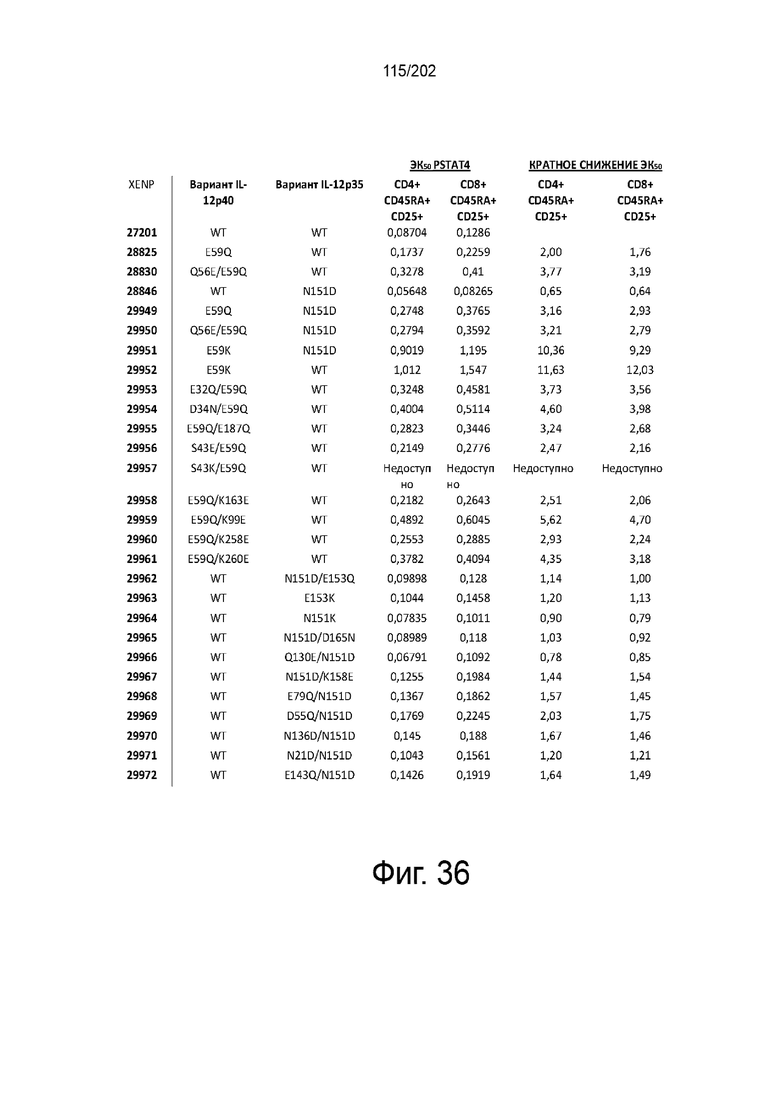












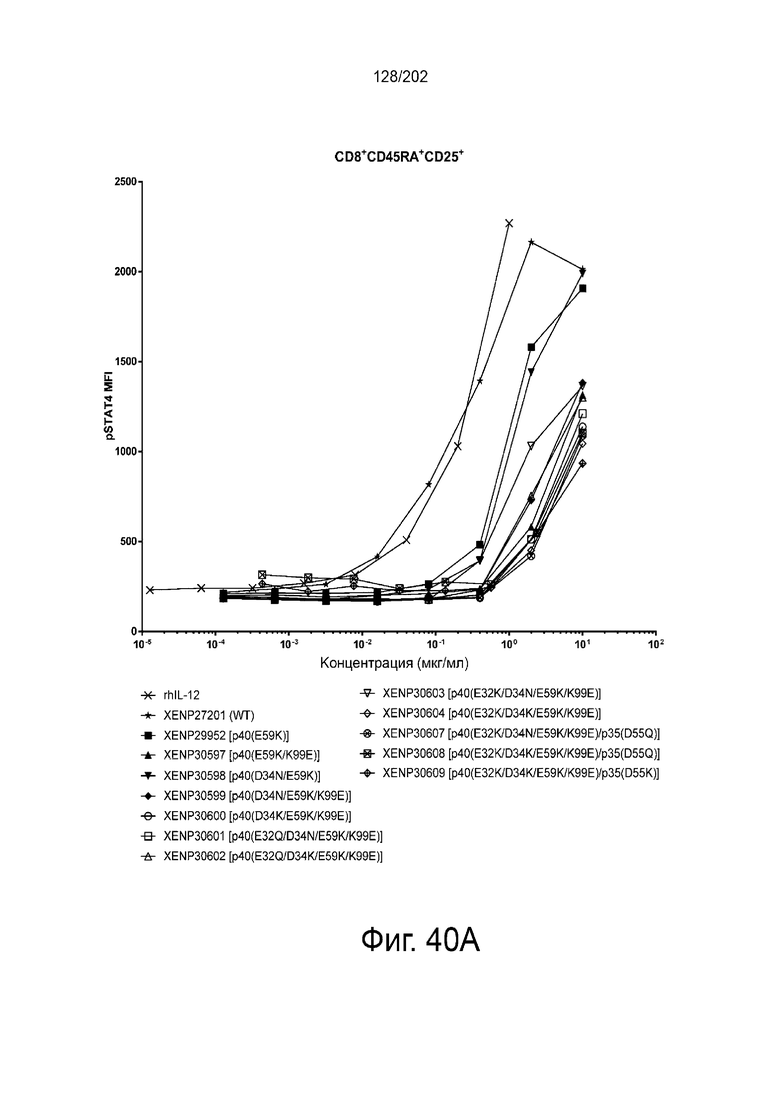
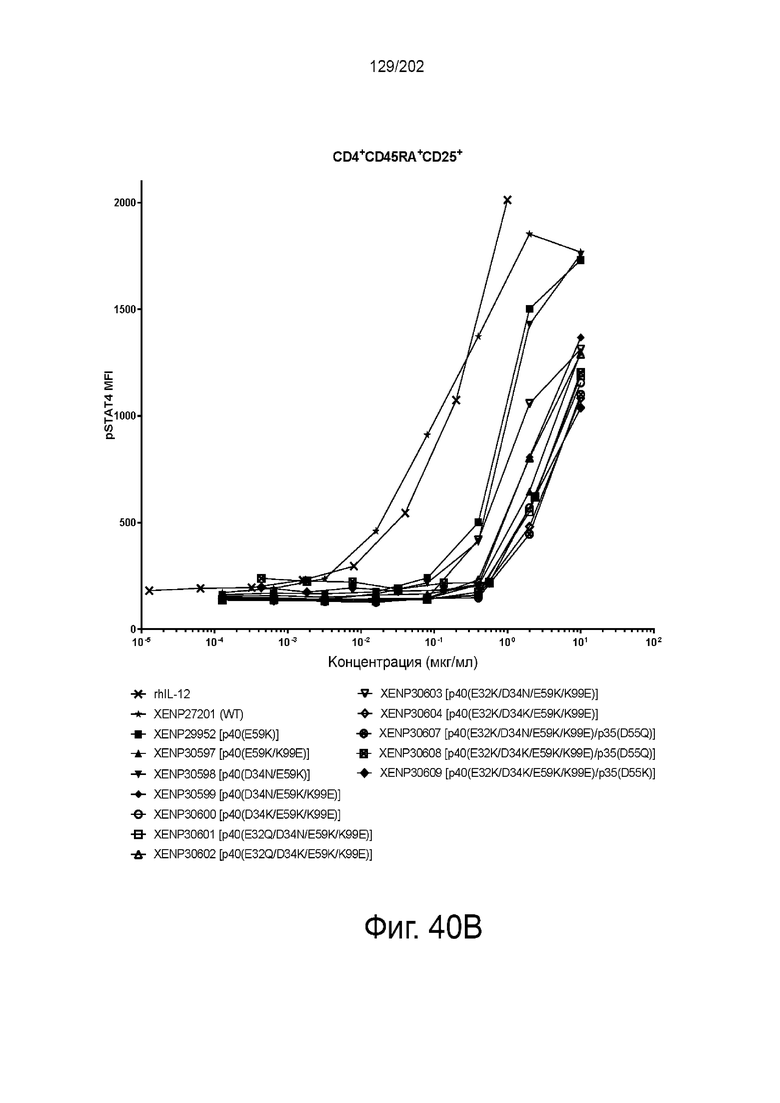
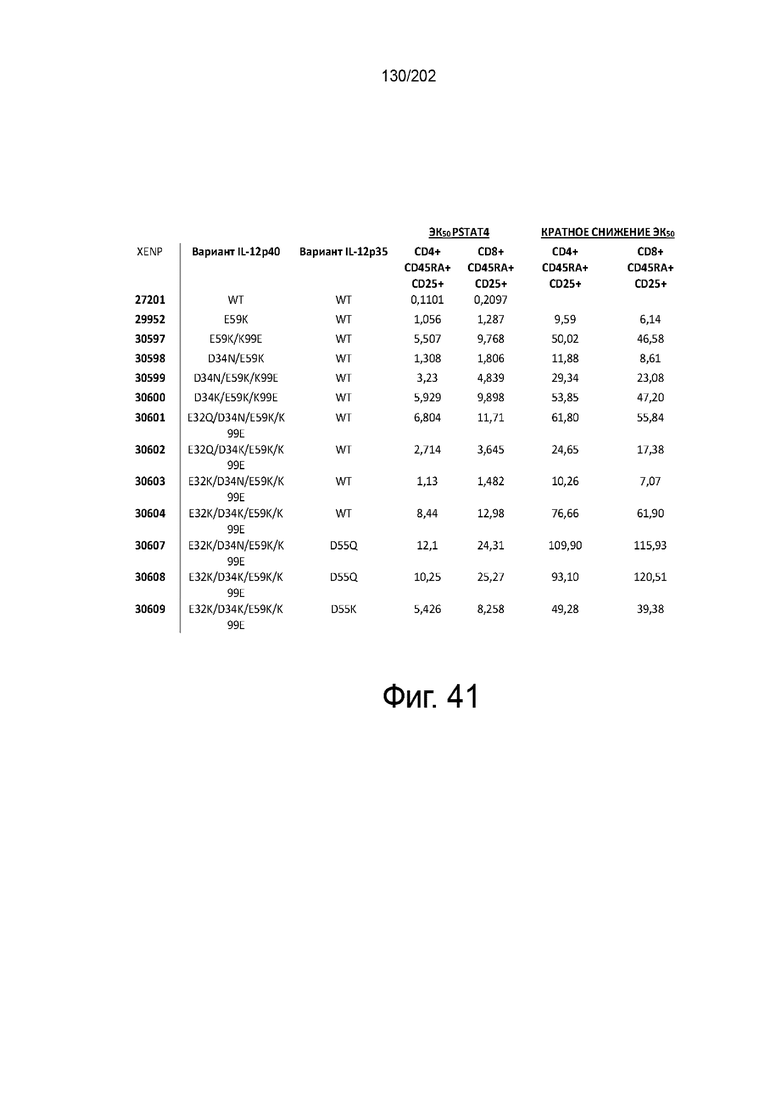


















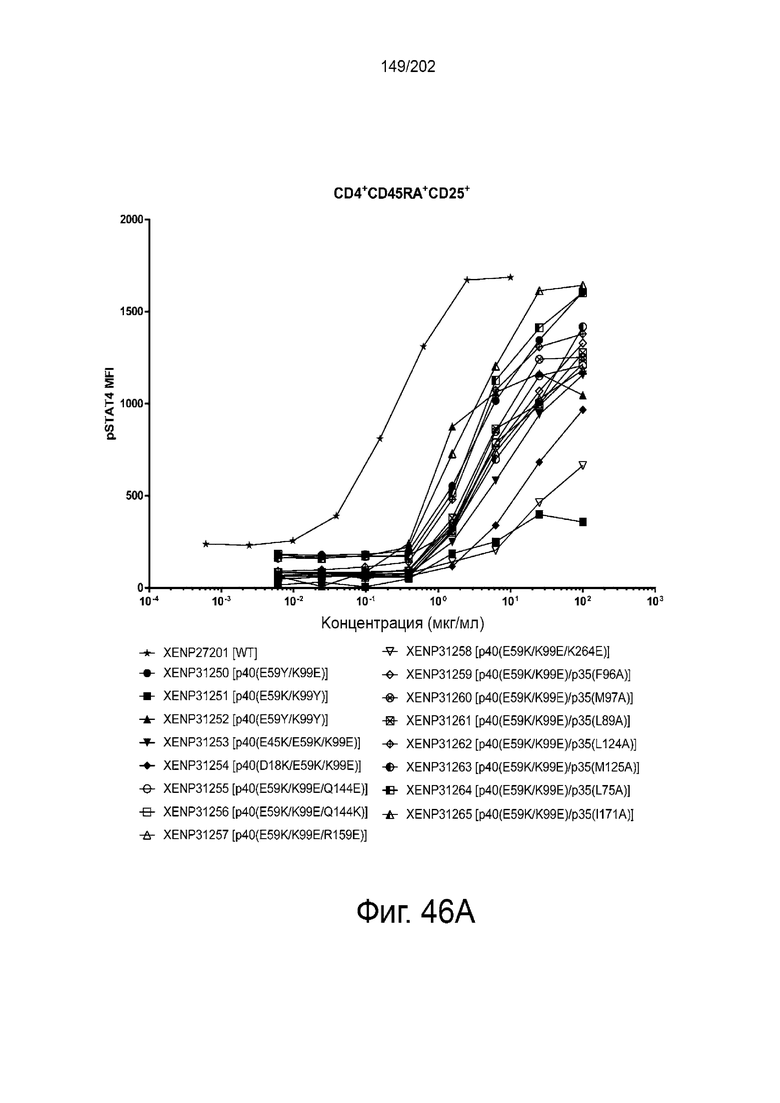
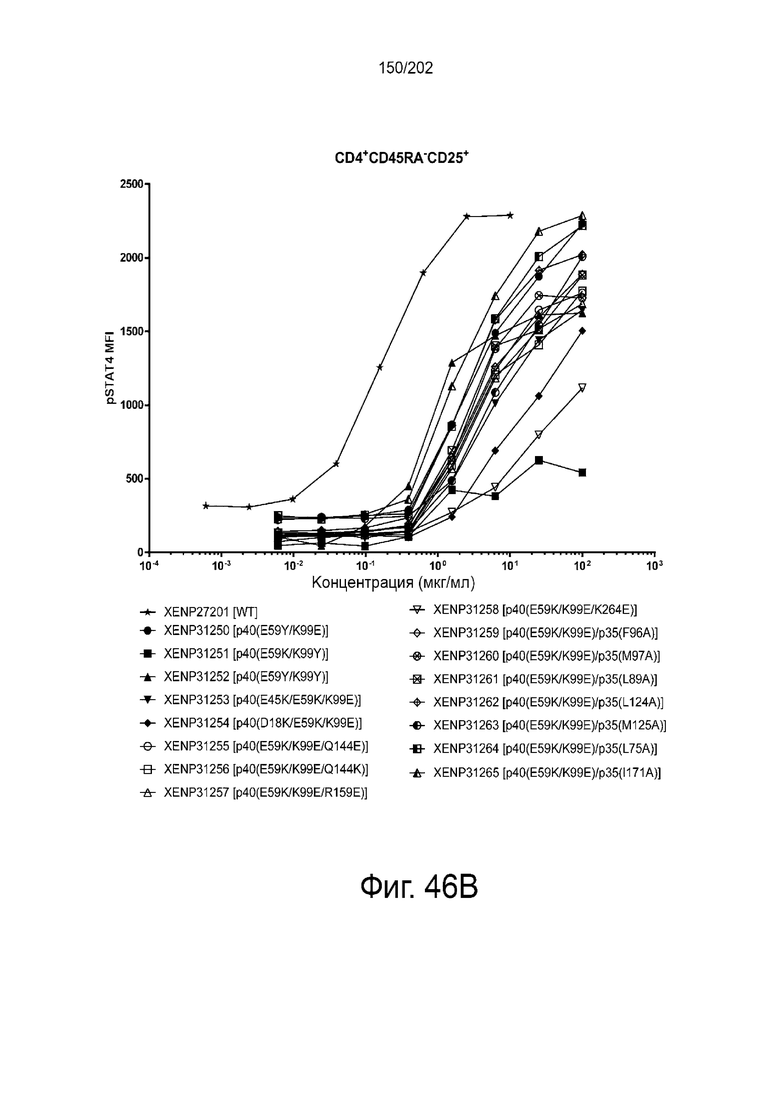
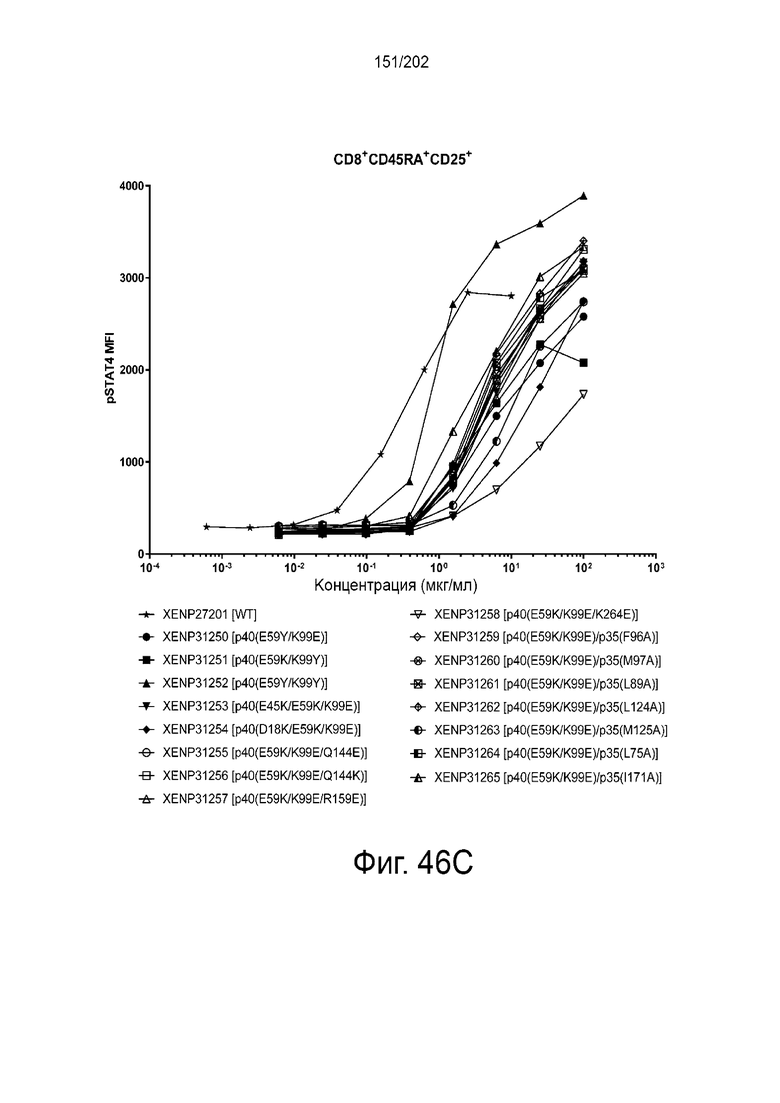
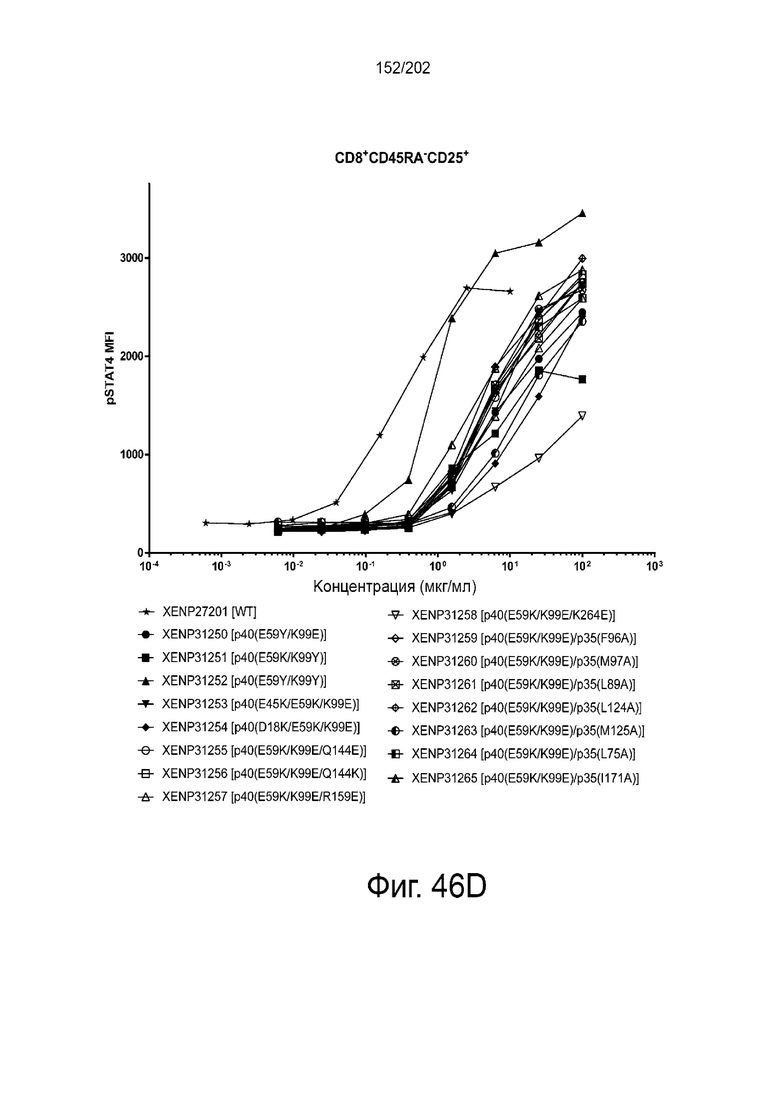
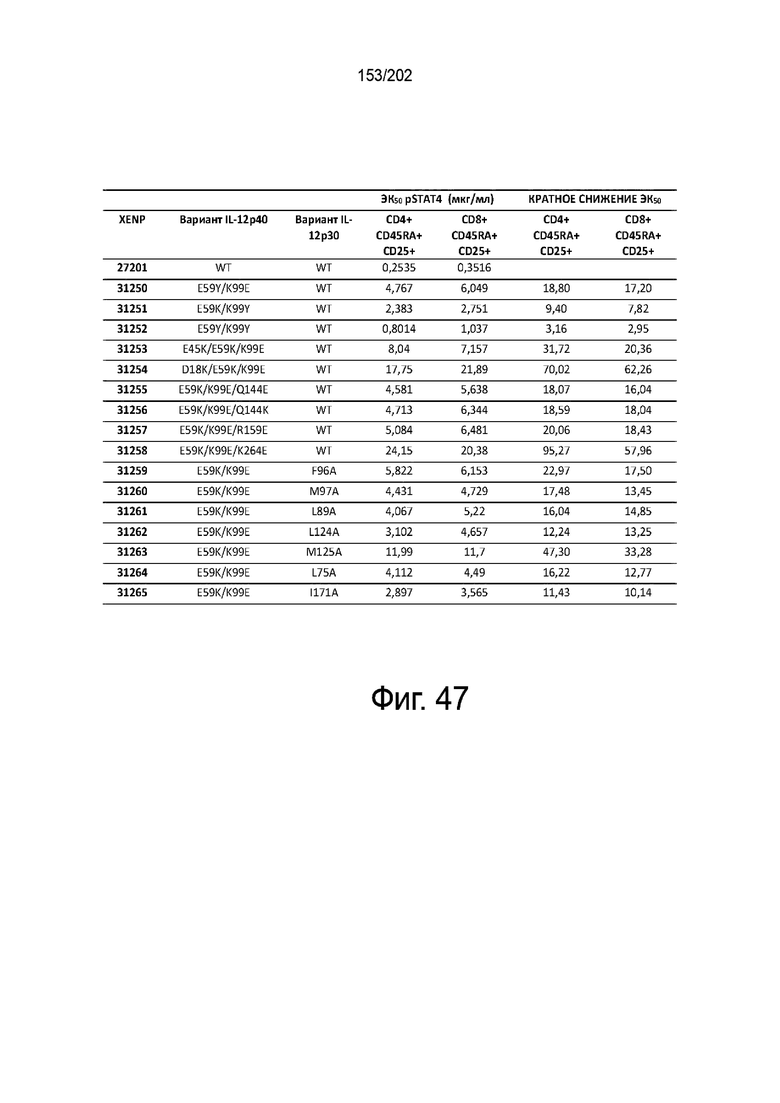
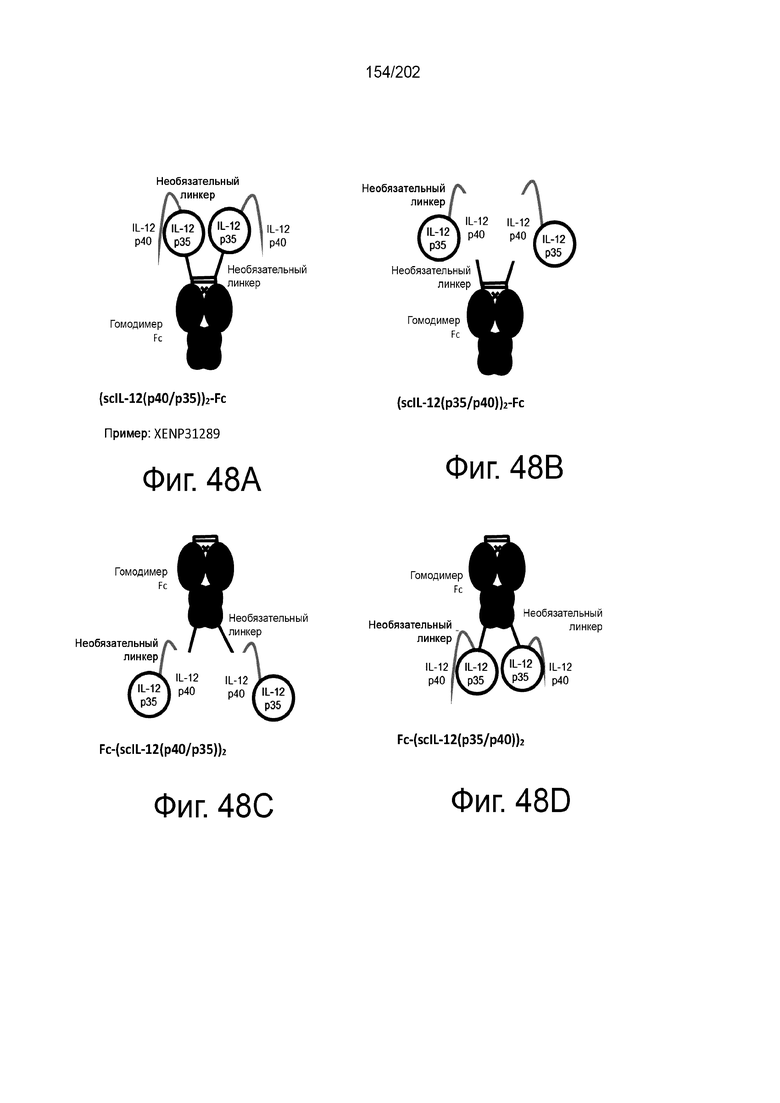


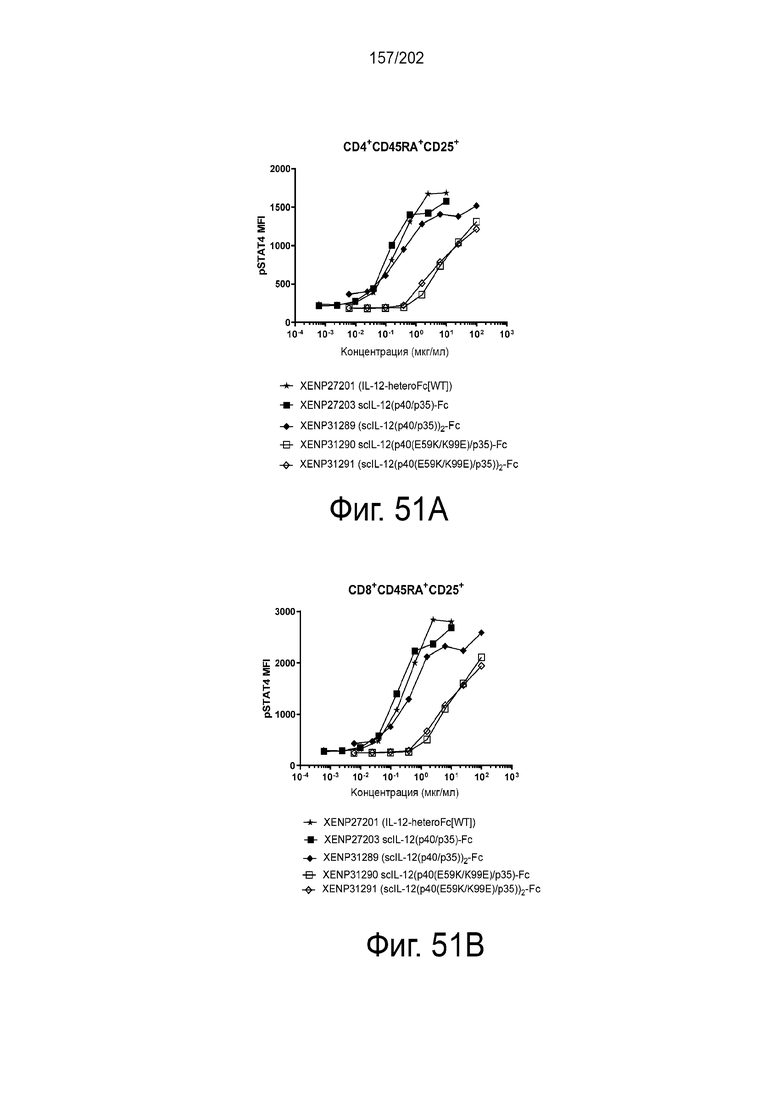
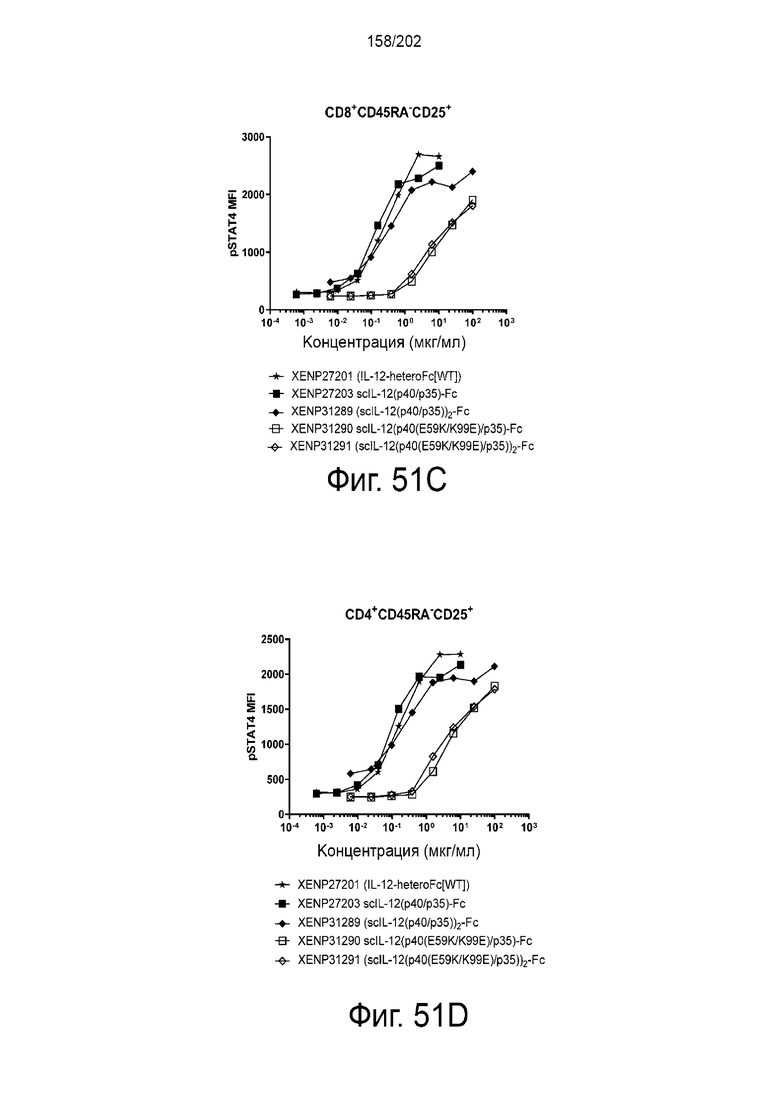
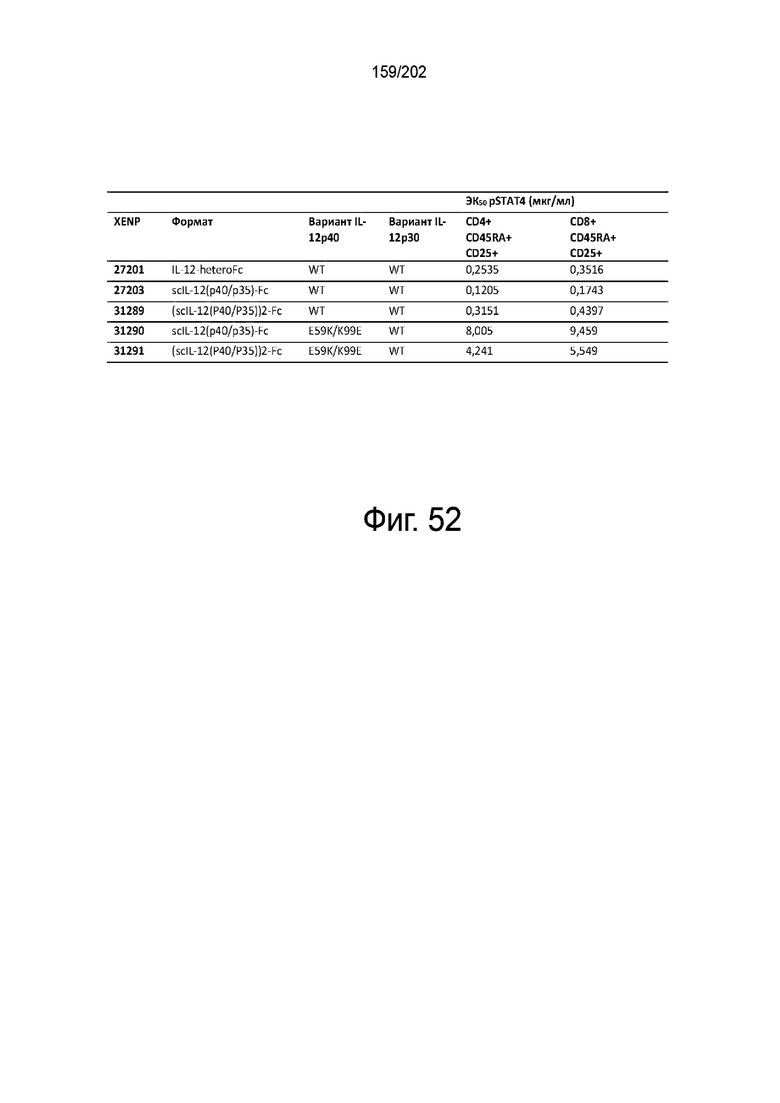

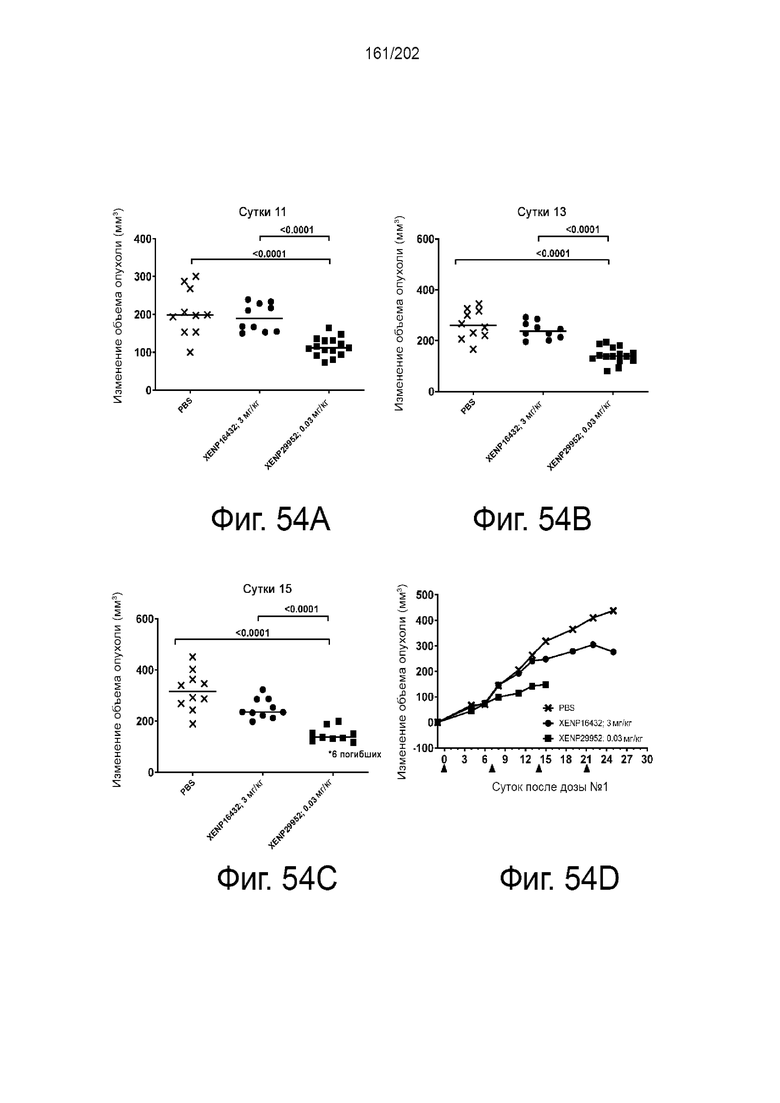
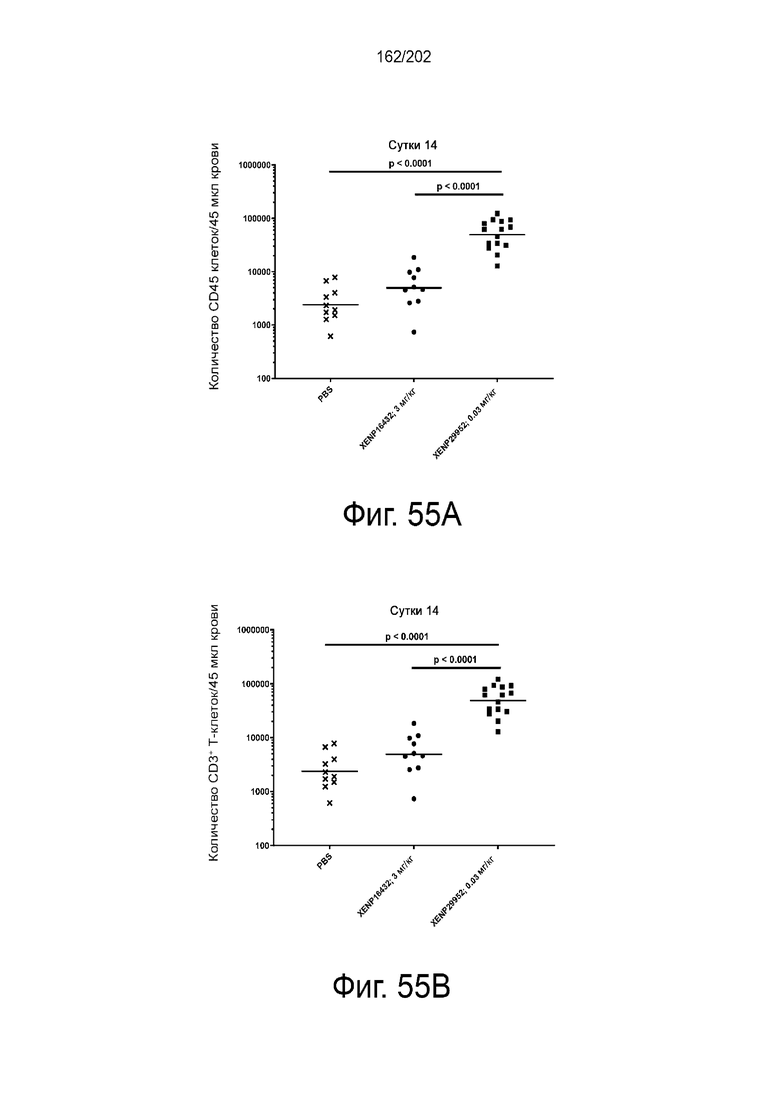
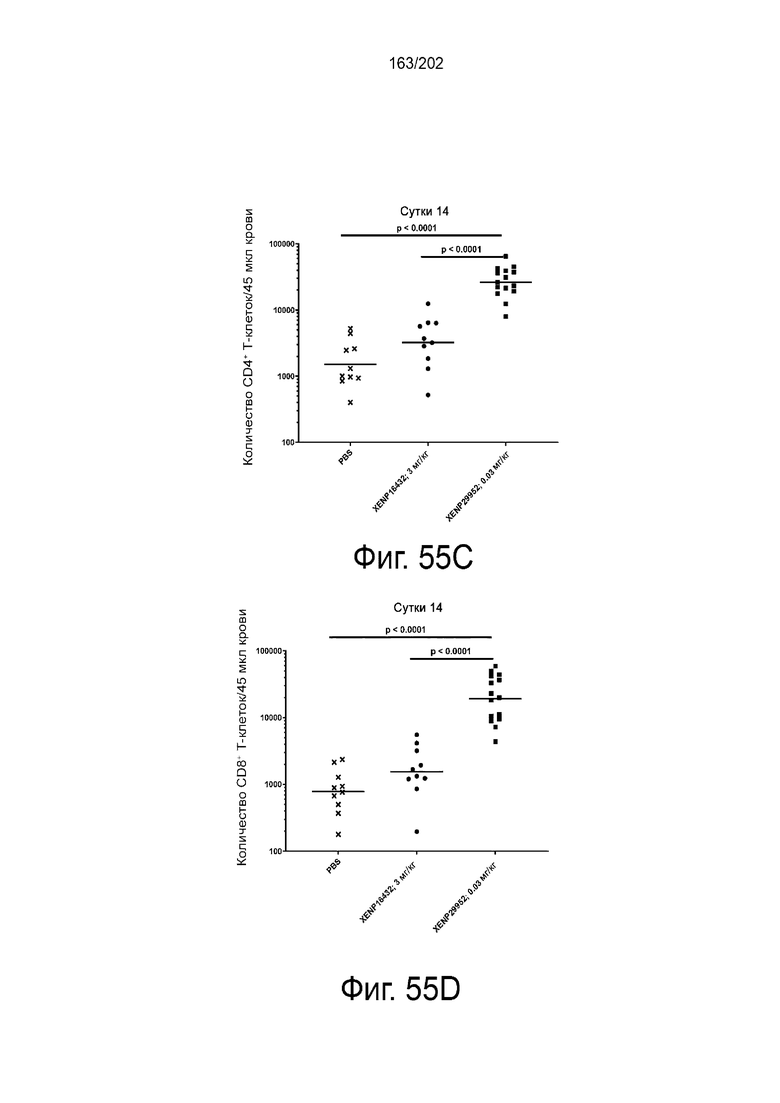
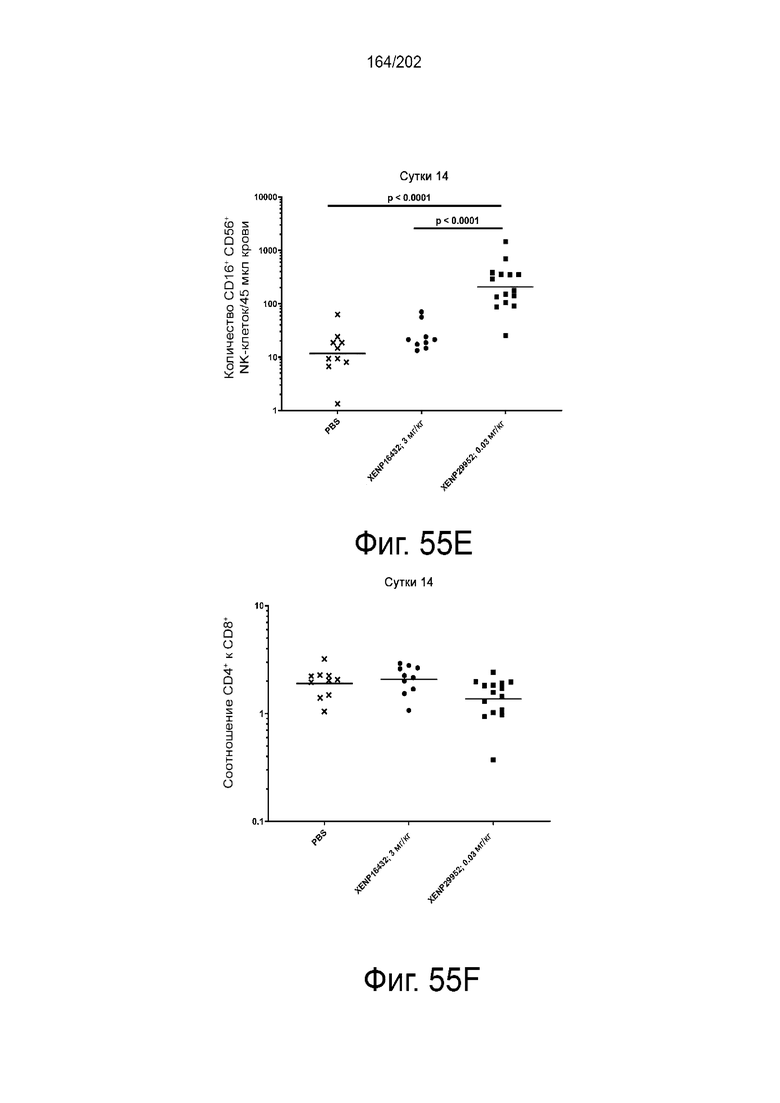
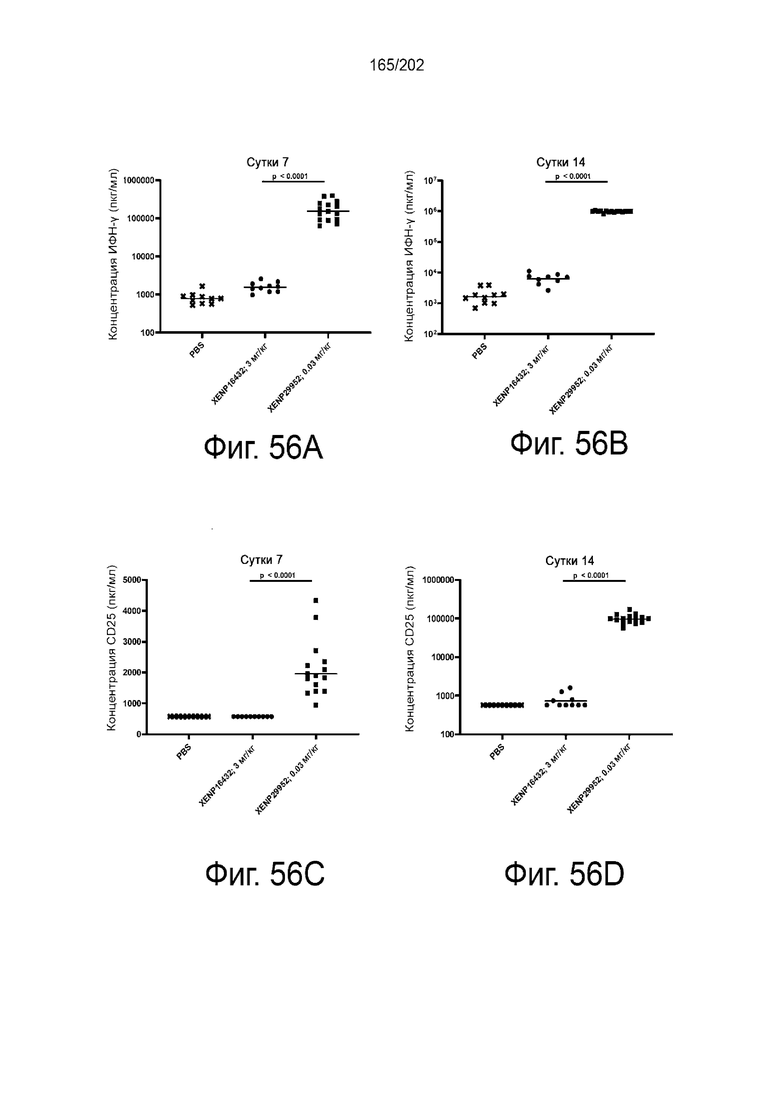
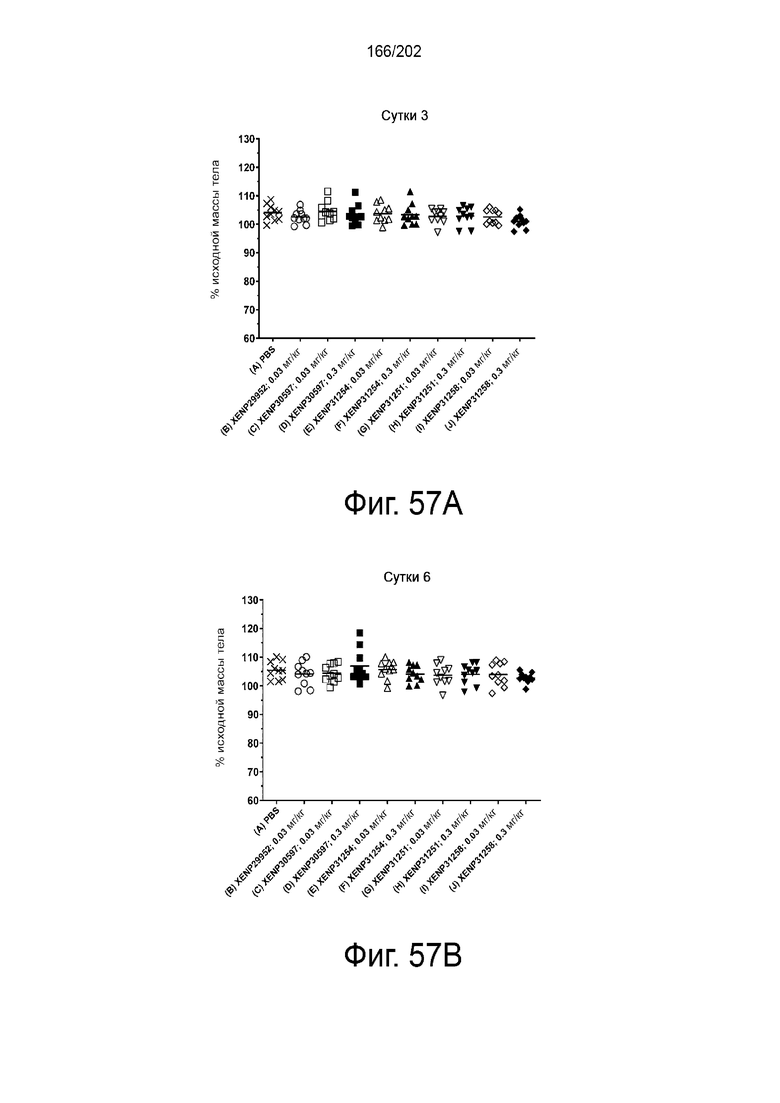

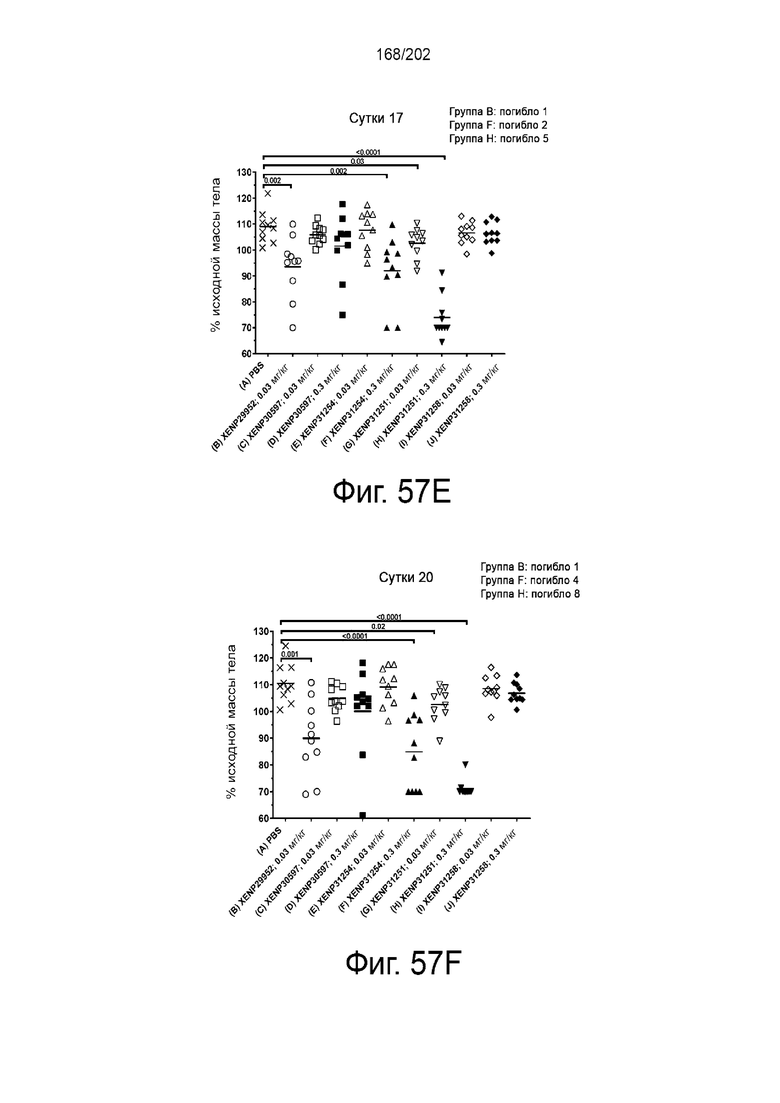
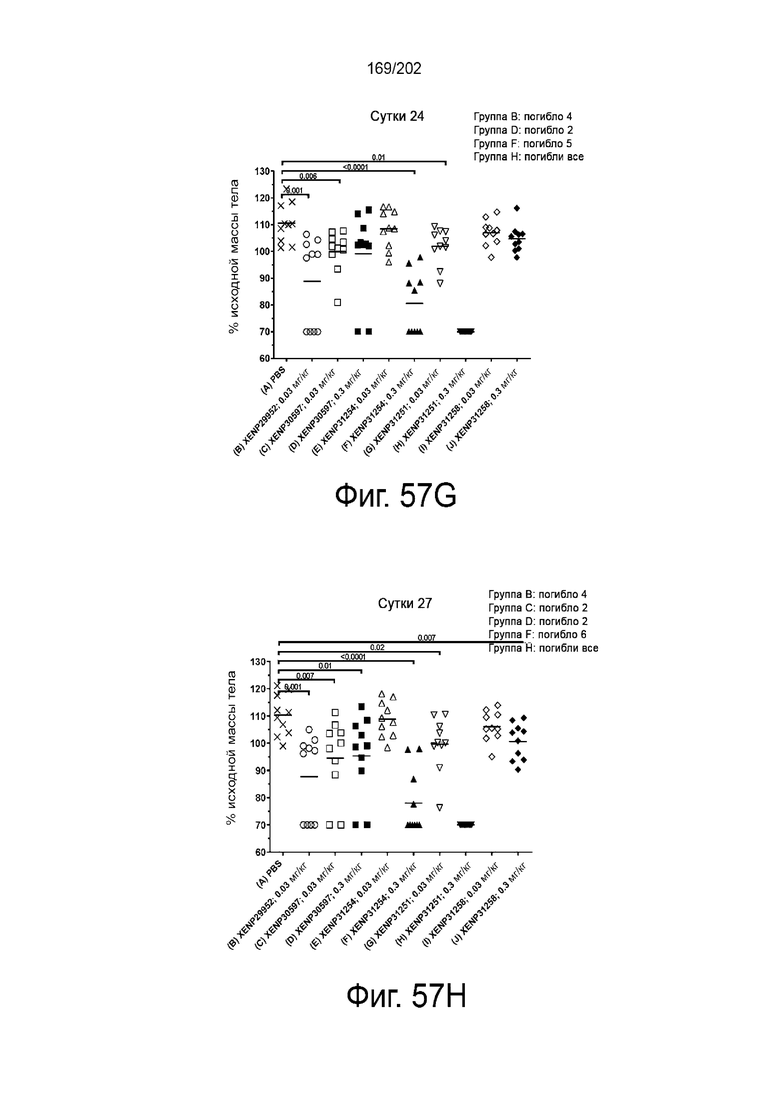
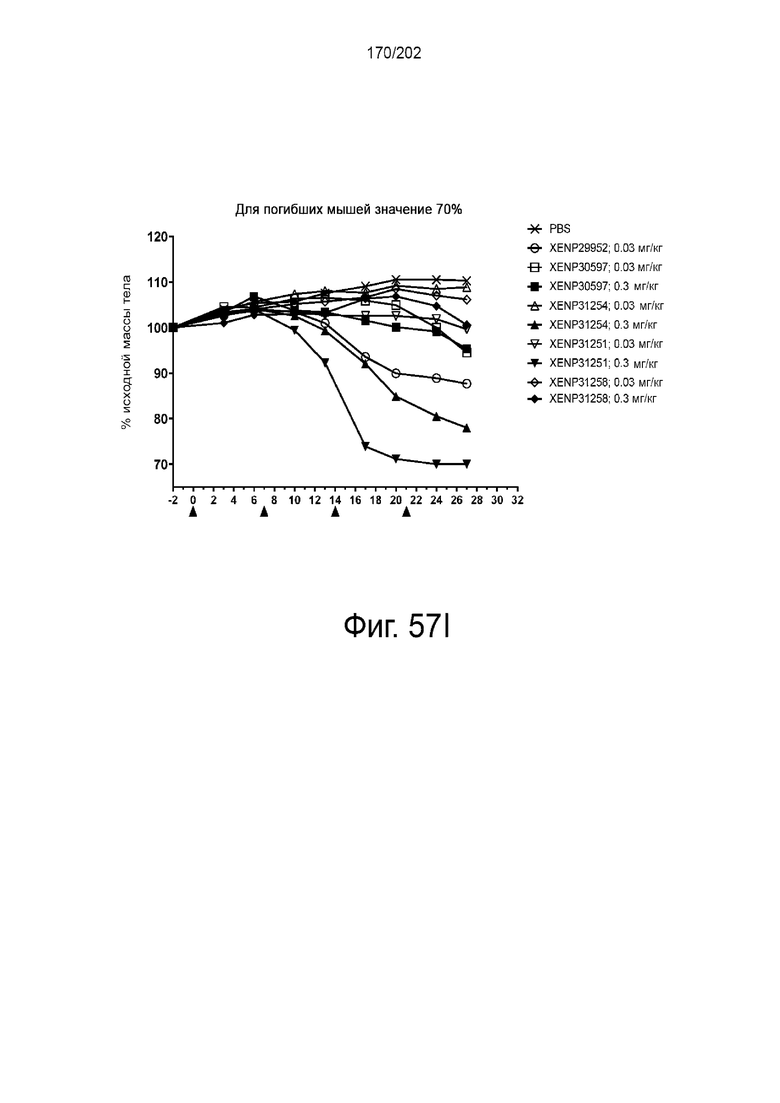
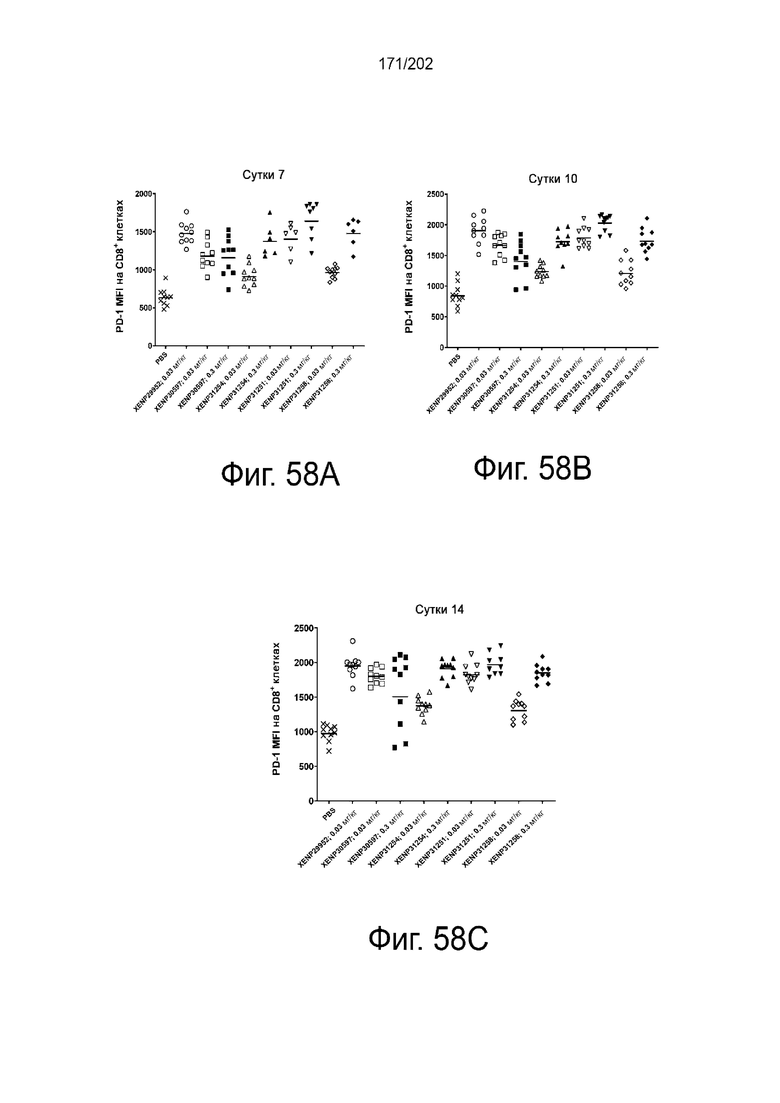
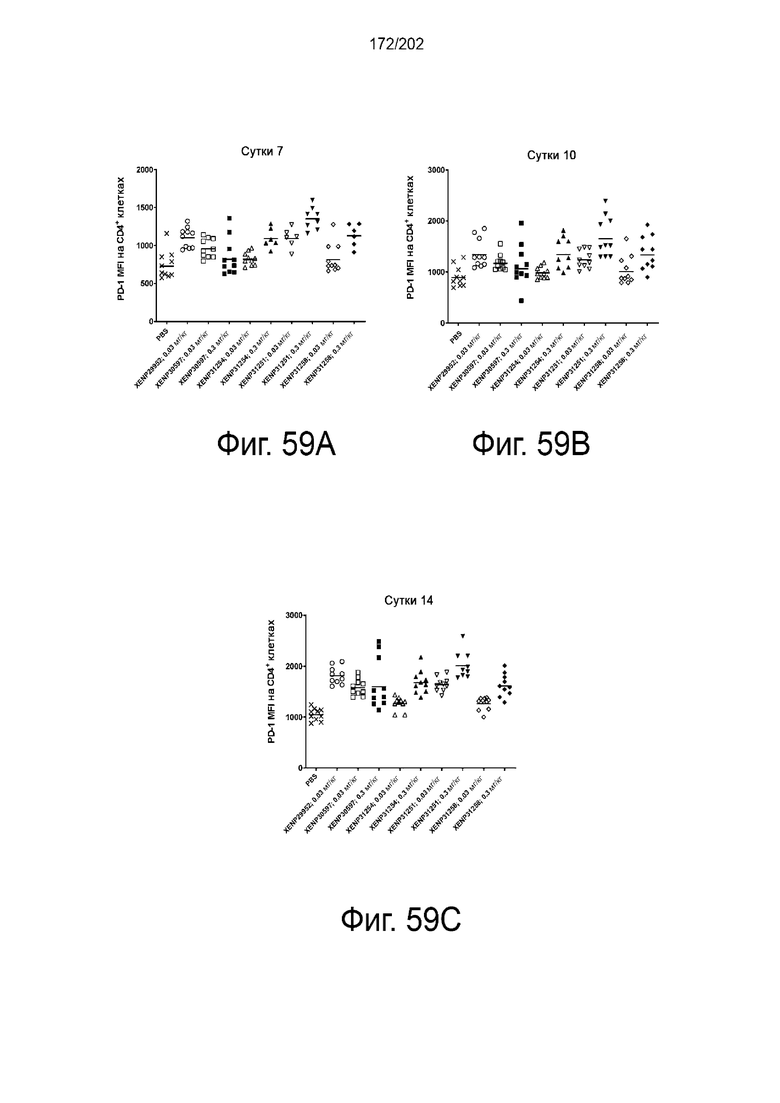
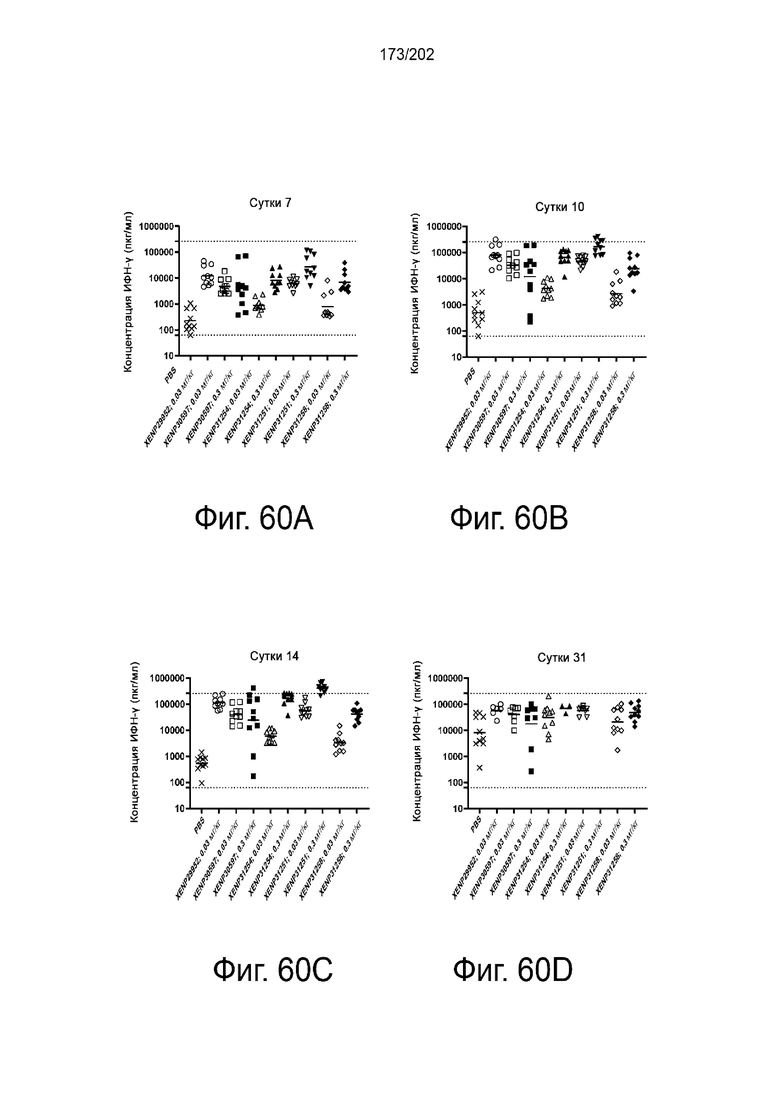
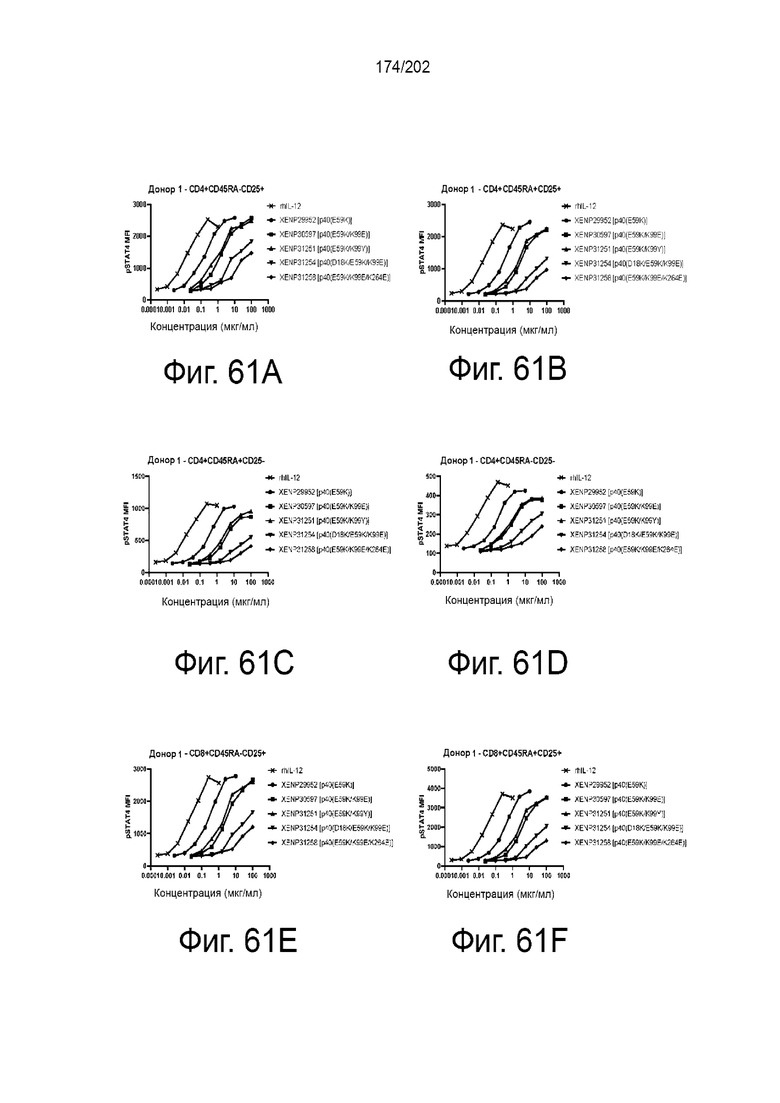
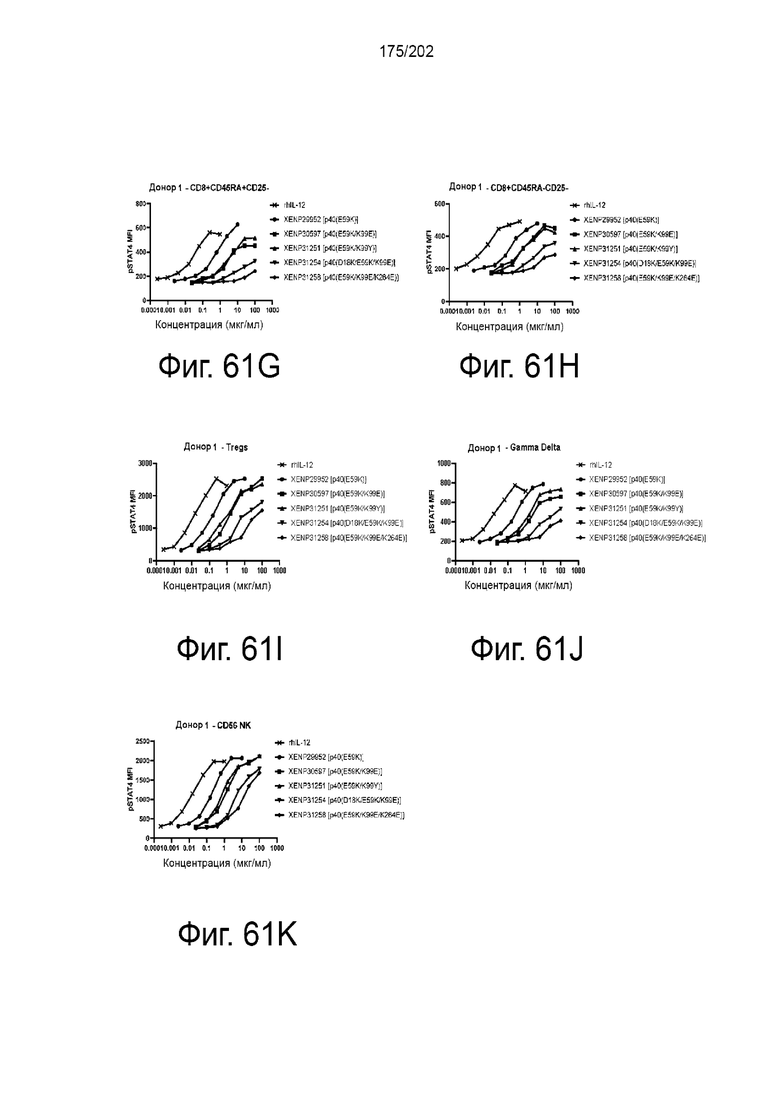
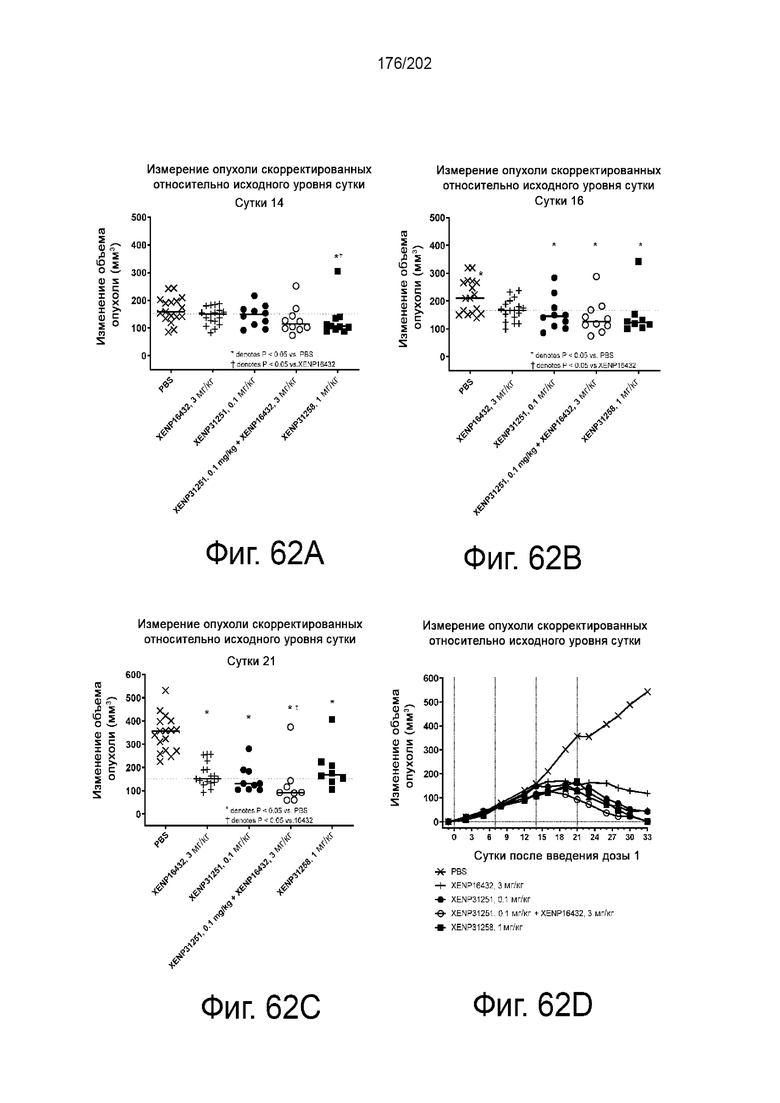
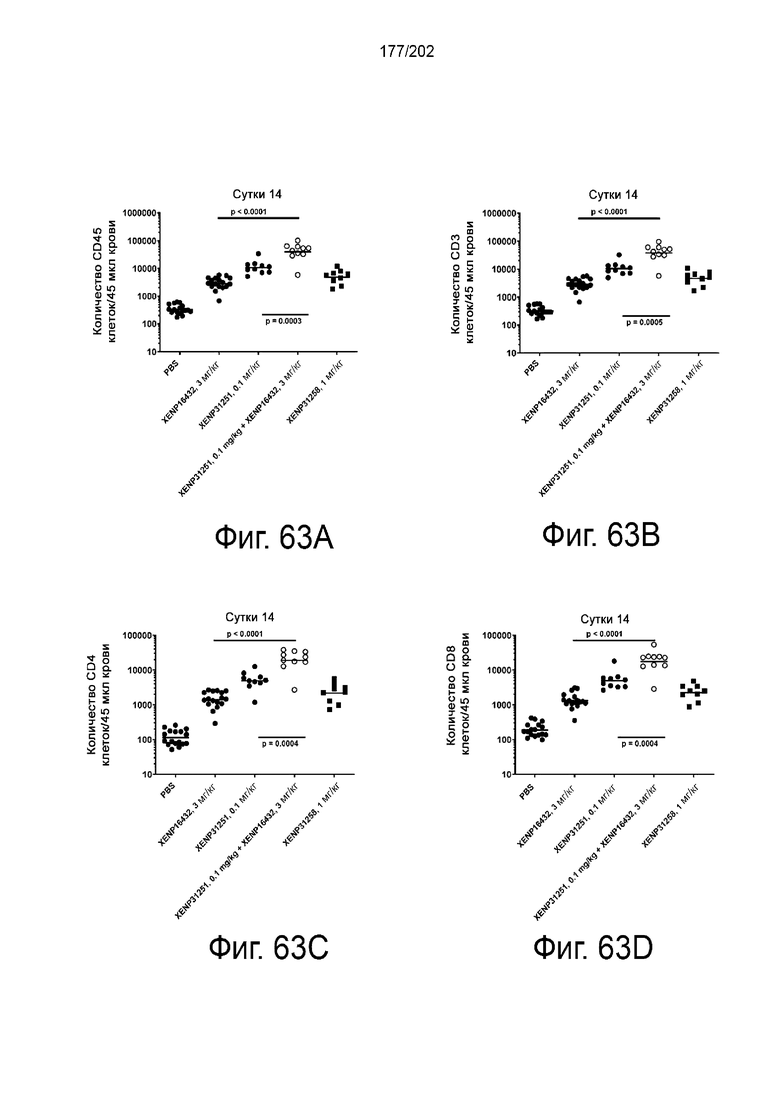
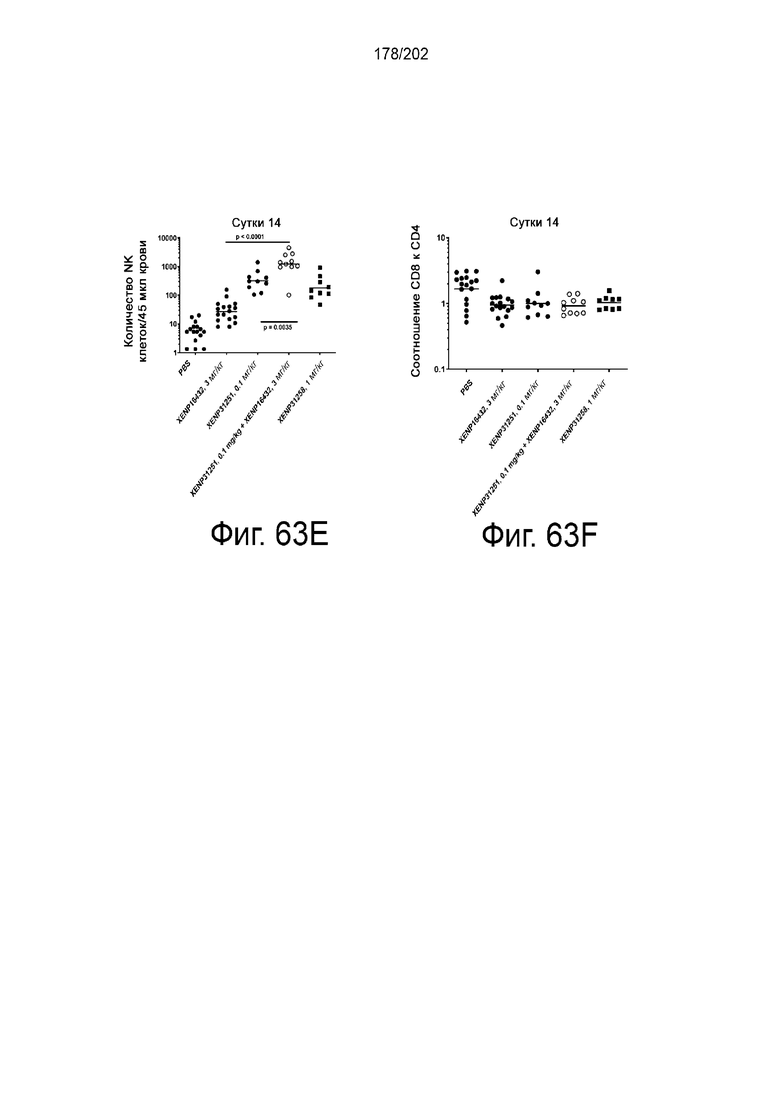























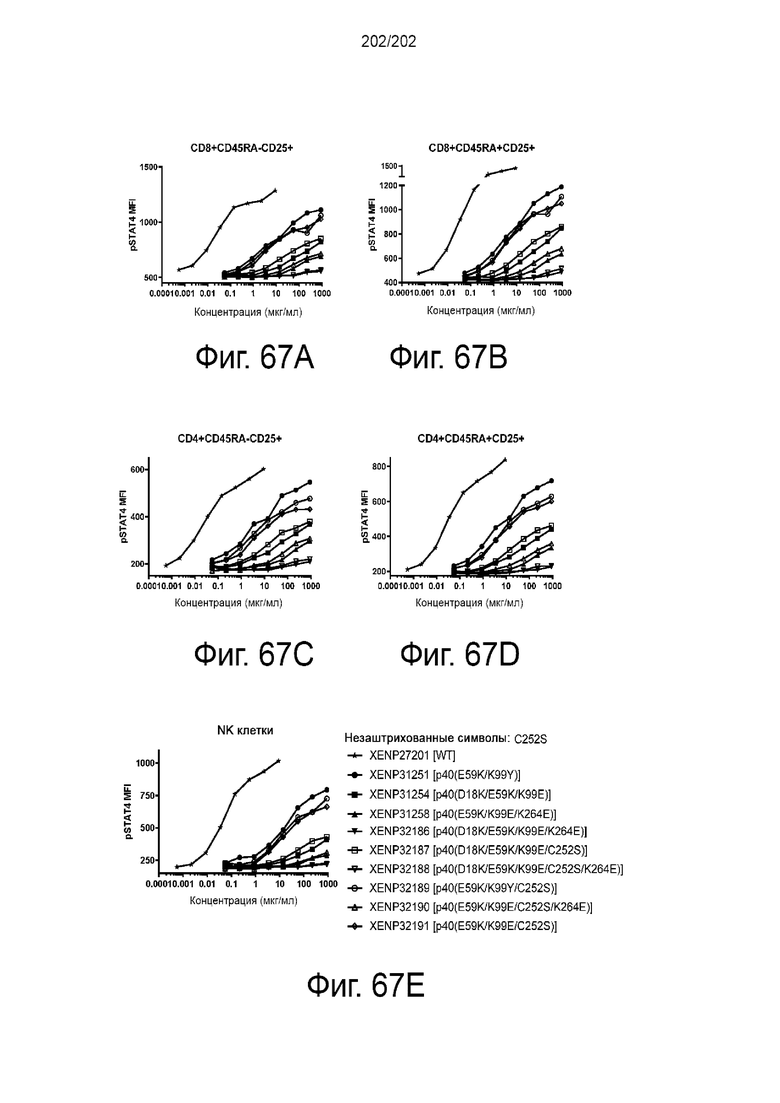
Изобретение относится к области биотехнологии, конкретно к гетеродимерным слитым белкам Fc, и может быть использовано для индукции размножения Т-клеток. Предложены гетеродимерные слитые белки Fc для индукции размножения T-клеток, в которых домены Fc содержат модификации, способствующие их гетеродимеризации. Изобретение обеспечивает получение гетеродимера IL-12 в виде слитых белков с Fc с усиленной циркуляцией в кровотоке, в котором для устранения антагонистического действия субъединицы IL-12p40 образован предварительный комплекс субъединиц IL-12p40 и IL-12p35, а также уменьшена активность вариантов IL-12 для улучшения фармакокинетики и терапевтического индекса. 8 н. и 16 з.п. ф-лы, 67 ил., 1 табл., 8 пр.
1. Гетеродимерный слитый белок Fc для индукции размножения T-клеток, содержащий:
a) первый слитый белок, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 382 с аминокислотными заменами M428L/N434S; и
b) второй слитый белок, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 404 с аминокислотными заменами M428L/N434S, где нумерация соотвествует нумерации EU.
2. Гетеродимерный слитый белок Fc для индукции размножения T-клеток, содержащий:
a) первый слитый белок, содержащий домен вариантной субъединицы IL-12p40 и первый домен Fc, где указанный домен вариантной субъединицы IL-12p40 содержит аминокислотную последовательность SEQ ID NO: 363, где указанный первый домен Fc содержит аминокислотную последовательность SEQ ID NO: 42, причем указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого домена Fc с использованием доменного линкера, содержащего аминокислоную последовательность SEQ ID NO: 10; и
b) второй слитый белок, содержащий домен субъединицы IL-12p35 и второй домен Fc, где указанный домен субъединицы IL-12p35 содержит аминокислотную последовательность SEQ ID NO: 2 и где второй домен Fc содержит аминокислотную последовательность SEQ ID NO: 41, причем указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного домена Fc с использованием доменного линкера, содержащего аминокислоную последовательность SEQ ID NO: 10.
3. Гетеродимерный слитый белок Fc для индукции размножения T-клеток, содержащий:
a) первый слитый белок, содержащий домен вариантной субъединицы IL-12p40 и первый домен Fc, причем указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого домена Fc, и где указанная вариантная субъединица IL-12p40 содержит замены E59K/K99Y/C252S и, необязательно, одну или более дополнительных аминокислотных замен, выбранных из группы, состоящей из: D18N, D18K, N21D, E32Q, E33Q, D34N, D34K, Q35D, E38Q, Q42E, S43E, S43K, E45Q, D55Q, D55K, Q56E, D62N, N71D, N71Q, E73Q, N76D, N85D, N85Q, M97A, E100Q, N103D, N103Q, N113D, N113Q, Q135E, Q144E, Q146E, N151D, N151K, E153K, E153Q, K158E, R159E, D161N, E162Q, K163E, E163Q, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, Q256N, Q256E, K258E, K260E, K264E, N281D, N281Q и E299Q по сравнению с SEQ ID NO: 4; и
b) второй слитый белок, содержащий домен субъединицы IL-12p35 и второй домен Fc, причем указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного домена Fc,
где указанный первый и второй домены Fc содержат модификации, способствующие гетеродимеризации указанного первого и указанного второго домена Fc.
4. Гетеродимерный слитый белок Fc по п. 3, также содержащий одну или более дополнительных модификаций в субъединице IL-12p40, выбранных из группы, состоящей из: N103Q, N113Q, N200Q и N281Q.
5. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что домен субъединицы IL-12p35 содержит аминокислотную последовательность SEQ ID NO: 2.
6. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанный домен субъединицы IL-12p40 содержит аминокислоные замены, выбранные из группы, состоящей из: N71D/N85D/N195D, N151D/E153Q, N151D/D165N, Q130E/N151D, N151D/K158E, E79Q/N151D, D55Q/N151D, N136D/N151D, N21D/N151D, E143Q/N151D, N71Q/N85Q, N71Q/N195Q, N85Q/N195Q, N71Q/N85Q/N195Q, N71D/N85D, N71D/N195D, N85D/N195D, N103D/N113D/N200D/N281D, Q42E/E45Q, E45Q/Q56E, Q42E/E59Q, Q56E/E59Q, Q42E/E45Q/Q56E, E45Q/Q56E/E59Q, E32Q/E59Q, D34N/E59K, D34N/E59K/K99E, D34K/E59K/K99E, E32Q/D34N/E59K/K99E, E32Q/D34K/E59K/K99E, E32K/D34K/E59K/K99E, E32K/D34N/E59K/K99E, D34N/E59Q, E59Q/E187Q, S43E/E59Q, S43K/E49Q, S43K/E59Q, E59Q/K163E, E59Q/K99E, E59Q/K258E, E59Q/K260E, E59K/K99E, D18K/E59K/K99E, E59K/K99E/K264E, E59K/K99Y, E59Y/K99Y, E59Y/K99E, E45K/E59K/K99E, E59K/K99E/Q144E, E59K/K99E/Q144K, E59K/K99E/R159E, E59K/K99E/K264E, D18K/E59K/K99E/K264E, DI8K/E59K/K99E/C252S, D18K/E59K/K99E/C252S/K264E, D18K/E59K/K99E/C252S,E59K/K99Y/C252S, E59K/K99E/C252S/K264E, E59K/K99E/C252S, N103D/N113D, N103D/N200D, N103D/N281D, N113D/N200D, N113D/N281D, N200D/N281D, N103D/N113D/N200D, N103D/N113D/N281D, N103D/N200D/N281D, N113D/N200D/N281D, N103Q/N113Q, N103Q/N200Q, N103Q/N281Q, N113Q/N200Q, N113Q/N281Q, N200Q/N281Q, N103Q/N113Q/N200Q, N103Q/N113Q/N281Q, N103Q/N200Q/N281Q, N113Q/N200Q/N281Q, N103Q/N113Q/N200Q/N281Q, E59K/K99E/N103Q/C252S/K264E, E59K/K99E/N113Q/C252S/K264E, E59K/K99E/N200Q/C252S/K264E, E59K/K99E/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/C252S/K264E, E59K/K99E/N103Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/C252S/K264E, E59K/K99E/N113Q/N281Q/C252S/K264E, E59K/K99E/N200Q/N281Q/C252S/K264E, E59K/K99E/N103Q/N113Q/N200Q/C252S/K264E, E59K/K99E/N103Q/N200Q/N281Q/C252S/K264E, E59K/K99E/N113Q/N200Q/N281Q/C252S/K264E и E59K/K99E/N103Q/N113Q/N200Q/N281Q/C252S/K264E.
7. Гетеродимерный слитый белок Fc по п. 6, отличающийся тем, что домен субъединицы IL-12p35 содержит аминокислотную последовательность SEQ ID NO: 2.
8. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанный домен вариантной субъединицы IL-12p40 содержит замены E59K/K99Y/C252S.
9. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанная вариантная субъединица IL-12p40 имеет по меньшей мере 90% идентичности с SEQ ID NO: 4 (последовательность зрелой формы субъединицы бета (IL-12p40) человеческого IL-12), и/или указанная субъединица IL-12p35 имеет по меньшей мере 90% идентичности с полипептидной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 1 (последовательность предшественника субъединицы альфа (IL-12p35) человеческого IL-12) и SEQ ID NO: 2 (последовательность зрелой формы субъединицы альфа (IL-12p35) человеческого IL-12).
10. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанная субъединица IL-12p40 представляет собой вариантную субъединицу IL-12p40, имеющую измененную аффинность в отношении субъединицы бета-1 (IL-12R131) рецептора IL-12, субъединицы бета-2 (IL-12Rig2) рецептора IL-12 и/или рецепторного комплекса IL-12.
11. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанный домен субъединицы IL-12p40 имеет аминокислотную последовательность SEQ ID NO: 363.
12. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что первый и второй Fc-домены являются вариантными IgG1 Fc-доменами.
13. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанные модификации, способствующие гетеродимеризации указанного первого и указанного второго доменов Fc, представляют собой набор аминокислотных замен, выбранных из группы, состоящей из: L368D/K370S и S364K; L368D/K370S и S364K/E357L; L368D/K370S и S364K/E357Q; T411E/K360E/Q362E и D401K; L368E/K370S и S364K; K370S и S364K/E357Q; T366S/L368A/Y407V и T366W; T366S/L368A/Y407V/Y349C и T366W/S354C, в соответствии с системой нумерации EU.
14. Гетеродимерный слитый белок Fc по п. 3, отличающийся тем, что указанный первый и/или указанный второй домены Fc имеют дополнительный набор аминокислотных замен содержащих Q295E/N384D/Q418E/N421D, в соответствии с системой нумерации EU, необязательно имеют дополнительный набор аминокислотных замен, выбранный из группы, состоящей из: G236R/L328R, E233P/L234V/L235A/G236del/S239K, E233P/L234V/L235A/G236del/S239K/A327G, E233P/L234V/L235A/G236del/S267K/A327G, E233P/L234V/L235A/G236del и E233P/L234V/L235A/G236del/S267K, в соответствии с системой нумерации EU, и необязательно имеют аминокислотные замены M428L/N434S, в соответствии с системой нумерации EU.
15. Гетеродимерный слитый белок Fc по п. 9, где указанный первый IgG1 Fc-домен содержит замены C220S/E233P/L234V/L235A/G236del/S267K/L368D/K370S и где указанный второй IgG1 Fc-домен содержит замены C220S/E233P/L234V/L235A/G236del/S267K/S364K/E357Q.
16. Гетеродимерный слитый белок Fc по п. 9, где указанный первый IgG1 Fc-домен содержит замены C220S/E233P/L234V/L235A/G236del/S267K/L368D/K370S/M428L/N434S и где указанный второй IgG1 Fc-домен содержит замены C220S/E233P/L234V/L235A/G236del/S267K/S364K/E357Q/M428L/N434S.
17. Гетеродимерный слитый белок Fc по п. 9, где указанный первый и указанный второй Fc также содержат аминокислотные замены M428L/N434S в соответствии с системой нумерации EU.
18. Гетеродимерный слитый белок Fc по п. 3, где указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого Fc-домена линкером (GGGGS)2 и где указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного второго Fc-домена линкером (GGGGS)2.
19. Гетеродимерный слитый белок Fc по п. 3, где указанный домен вариантной субъединицы IL-12p40 содержит аминокислотную последовательность SEQ ID NO: 363 и где указанный первый Fc-домен содержит аминокислотную последовательность SEQ ID NO: 42, где указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого Fc-домена с помощью доменного линкера, содержащего аминокислотную последовательность SEQ ID NO: 10, где указанный домен субъединицы IL-12p35 содержит аминокислотную последовательность SEQ ID NO: 2, где указанный второй Fc-домен содержит аминокислотную последовательность SEQ ID NO: 41 и где указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного второго Fc-домена с помощью доменного линкера, имеющего аминокислотную последовательность SEQ ID NO: 10.
20. Композиция нуклеиновых кислот, кодирующая гетеродимерный слитый белок Fc по любому из пп. 1-19, содержащая:
a) первую нуклеинорвую кислоту, кодирующую первый слитый белок, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 382 с аминокислотными заменами M428L/N434S, или слитый белок, содержащий домен вариантной субъединицы IL-12p40 и первый домен Fc, где указанный домен вариантной субъединицы IL-12p40 содержит аминокислотную последовательность SEQ ID NO: 363, где указанный первый домен Fc содержит аминокислотную последовательность SEQ ID NO: 42, причем указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого домена Fc с использованием доменного линкера, содержащего аминокислоную последовательность SEQ ID NO: 10 или слитый белок, содержащий домен вариантной субъединицы IL-12p40 и первый домен Fc, причем указанный домен субъединицы IL-12p40 ковалентно присоединен к N-концу указанного первого домена Fc, и где указанная вариантная субъединица IL-12p40 содержит замены E59K/K99Y/C252S и, необязательно, одну или более дополнительных аминокислотных замен, выбранных из группы, состоящей из D18N, D18K, N21D, E32Q, E33Q, D34N, D34K, Q35D, E38Q, Q42E, S43E, S43K, E45Q, D55Q, D55K, Q56E, D62N, N71D, N71Q, E73Q, N76D, N85D, N85Q, M97A, E100Q, N103D, N103Q, N113D, N113Q, Q135E, Q144E, Q146E, N151D, N151K, E153K, E153Q, K158E, R159E, D161N, E162Q, K163E, E163Q, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, Q256N, Q256E, K258E, K260E, K264E, N281D, N281Q и E299Q по сравнению с SEQ ID NO: 4;
b) вторую нуклеиновую кислоту, кодирующую второй слитый белок, содержащий аминокислотную последовательность, представленную в SEQ ID NO: 404 с аминокислотными заменами M428L/N434S, или слитый белок, содержащий домен субъединицы IL-12p35 и второй домен Fc, где указанный домен субъединицы IL-12p35 содержит аминокислотную последовательность SEQ ID NO: 2 и где второй домен Fc содержит аминокислотную последовательность SEQ ID NO: 41, причем указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного домена Fc с использованием доменного линкера, содержащего аминокислоную последовательность SEQ ID NO: 10, или слитый белок, содержащий домен субъединицы IL-12p35 и второй домен Fc, причем указанный домен субъединицы IL-12p35 ковалентно присоединен к N-концу указанного домена Fc.
21. Композиция экспрессионных векторов для экспрессии гетеродимерного слитого белка Fc по любому из пп. 1-19, содержащая:
a) экспрессионный вектор, содержащий первую нуклеиновую кислоту по п. 20; и
b) экспрессионный вектор, содержащий вторую нуклеиновую кислоту по п. 20.
22. Клетка-хозяин для продукции гетеродимерного слитого белка Fc по любому из пп. 1-19, содержащая композицию экспресионных векторов по п. 21.
23. Способ получения гетеродимерного слитого белка Fc, причем указанный способ включает культивирование клетки-хозяина по п. 22 в условиях, при которых экспрессируется указанный гетеродимерный слитый белок Fc, и извлечение указанного белка.
24. Композиция для индукции размножения Т-клеток, содержащая домен вариантной субъединицы IL-12p40, где указанный домен вариантной субъединицы IL-12p40 содержит замены E59K/K99Y/C252S и, необязательно, дополнительно одну или более аминокислотных замен, выбранных из группы, состоящей из: D18N, D18K, N21D, E32Q, E33Q, D34N, D34K, Q35D, E38Q, Q42E, S43E, S43K, E45Q, D55Q, D55K, Q56E, D62N, N71D, N71Q, E73Q, N76D, N85D, N85Q, M97A, E100Q, N103D, N103Q, N113D, N113Q, Q135E, Q144E, Q146E, N151D, N151K, E153K, E153Q, K158E, R159E, D161N, E162Q, K163E, E163Q, E187Q, N200D, N200Q, N218Q, Q229E, E235Q, Q256N, Q256E, K258E, K260E, K264E, N281D, N281Q и E299Q относительно SEQ ID NO: 4.
| US 2007154453 A1, 05.07.2007, WO 2018030806 A1, 15.02.2018, RU 2263118 C2, 27.10.2005, RU 2658504 C9, 21.08.2018. |
Авторы
Даты
2024-05-14—Публикация
2019-10-03—Подача