Изобретение относится к биохимии германийорганических соединений и касается биологически активного вещества 1-(герматран-1-ил)-1-оксиэтиламина, имеющего формулу: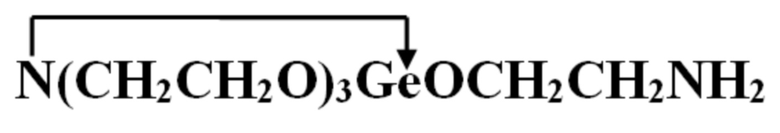 (соединение I). Изобретение также относится к медицине, фармакологии и биологии и, конкретно, может быть использовано, например, для повышения устойчивости сосудистой системы к холестерину при развитии атеросклеротического процесса.
(соединение I). Изобретение также относится к медицине, фармакологии и биологии и, конкретно, может быть использовано, например, для повышения устойчивости сосудистой системы к холестерину при развитии атеросклеротического процесса.
В последнее время доказано участие в атерогенезе лизосомальных липолитических ферментов, ответственных за деградацию липидных компонентов липопротеидов (ЛП). Определено их участие в механизме нарушений обмена липидов и липопротеидов при атеросклерозе, выявлена взаимосвязь между степенью изменений их активности в мононуклеарах крови, уровнем липидов крови и коэффициентом атерогенности [см. Серебров В.Ю., Балашов П.П., Шарыпова Н.Г. Исследование активности фосфолипаз плазматических мембран лимфоцитов при абстинентном синдроме у больных опийной наркоманией: // Сб. науч. трудов Сиб. Мед. Универ. (Томск). Актуальные проблемы биологии; - 2004. - Т. 3. - С. 209; Mallat Z, Benessiano J, Simon T, et all. Circulating secretory phospholipase A2 activity and risk of incident coronary events in healthy men and women: The EPIC-NORFOLK Study. // Arterioscler. Thromb. Vasc. Biol. - 2007; - V. 27: - P.1177-83].
Развитие атеросклероза связано с патологическими процессами в эндотелии сосудов. На раннем этапе атерогенеза активируется эндотелий, который экспрессирует на своей поверхности адгезионные молекулы для моноцитов (Мц), нейтрофилов и лейкоцитов крови и продуцирует хемоаттрактанты, привлекающие Мц в интиму сосудов. Мц, мигрирующие в субэндотелиальное пространство, дифференцируются в макрофаги, которые выступают как катализаторы образования окисленных липопротеидов низкой плотности (ЛНП), миграции и пролиферации гладкомышечных клеток из мышечной оболочки в интиму. Частицы модифицированных ЛНП захватываются макрофагами, которые трансформируются в пенистые клетки. Активированные макрофаги, продуцирующие металлопротеиназы и коллагеназу, способствуют распаду коллагена в бляшке и возникновению разрыва бляшки, образованию тромба и развитию инфаркта миокарда. Следовательно, макрофаги играют ключевую роль в развитии атеросклеротических повреждений [см. Душкин М.И. Макрофаги и атеросклероз: патофизиологические и терапевтические аспекты // Бюлл. СО РАМН (2006); №2 (120), с. 47-55]. В этом плане заслуживают внимания исследования средств, изменяющих активность гидролаз моноцитов, в частности фосфолипазы А2 (ФЛА2) (КФ 3.1.1.14) – лизосомального липолитического фермента класса гидролаз, имеющей оптимум действия при щелочных значениях рН, участвующего в атерогенезе, что обусловлено его участием в метаболизме липидов клеточных мембран, процессах перекисного окисления липидов (ПОЛ), синтезе эйкозаноидов и др. [см. Ji Huang, Hai-Yan Qian, Zhi-Zhong Li,. et all. Role of endothelial lipase in atherosclerosis // Translational Research, - 2010, vol. 156, Issue 1. - P. 1-6; Бельков В.В. С-реактивный белок и липопротеин-ассоциированная фосфолипаза А2: новые факты и новые возможности для диагностики и стратификации сердечно-сосудистых рисков // Ж. «Поликлиника» - 2010 - №1. - С. 18-21]. Следовательно, изменение активности ФЛА2 под влиянием тех или иных средств может служить критерием эффективности антиатеросклеротических препаратов. При этом существует потребность в поиске и внедрении в практику новых диагностических и лекарственных средств, обладающих указанной активностью.
Известно, что некоторые герматраны обладают адаптогенным действием [cм. Жигачёва И.В., Бинюков В.И., Миль Е.М., Генерозова И.П., Расулов М.М. Влияние германийорганического соединения на функциональное состояние митохондрий растительного и животного происхождения // Научный альманах (Биологические науки). 2015, N 7(9), 955-966].
Органические соединения германия обладают биологической активностью (см. кн. - Лукевиц Э.Я. и др. Биологическая активность соединений германия. Рига: Зинатне, 1990, стр.981). Содержащие германий органические полимеры эффективны при лечении психоневрологических нарушений (патент США 4281015, 1981 г., МПК А61К 31/28), офтальмологических расстройств (патент США 4296123, 1981 г., МПК А61К 31/28), нарушений функций печени (патент США 4309412, 1982 г., МПК А61К 31/74), фиброза легких (патент США 4321273, 1982 г., МПК А61К 31/28), аллергических заболеваний (патент США 4322402, 1982 г., МПК А61К 31/74) и гепатита (патент США 5340806, 1994 г., МПК А61К 31/79). Также они способствуют выработке интерферона в организме (патент США 4473581, 1984 г., МПК А61К 31/28) и защищают его от простуды (патент США 4898882, 1990 г., МПК А61К 31/28). Моногидрат 1-гидроксигерматрана обладает цитокинной активностью в отношении триптофанил-тРНК синтетазы (патент РФ № 2553986, 2015 г, МПК А61К 31/205).
В настоящее время существует необходимость поиска новых эффективных препаратов, обеспечивающих торможение атерогенеза.
В качестве средства, понижающего общую активность основной (щелочной) фосфолипазы А2, предлагается использовать синтезированное ранее [см. Воронков М.Г., Адамович С.Н., Мирсков Р.Г., Мирскова А.Н. Синтез новых биологически активных О-гидрометаллоатранов // ЖОХ, 2009, т. 79, №1, С. 162-163] биологически активное соединение - 1-(герматран-1-ил)-1-оксиэтиламин, который имеет формулу:
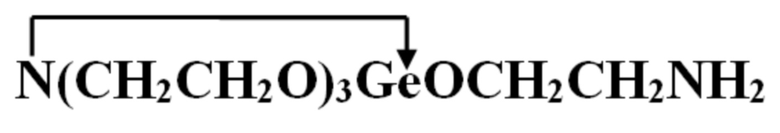
и вид:
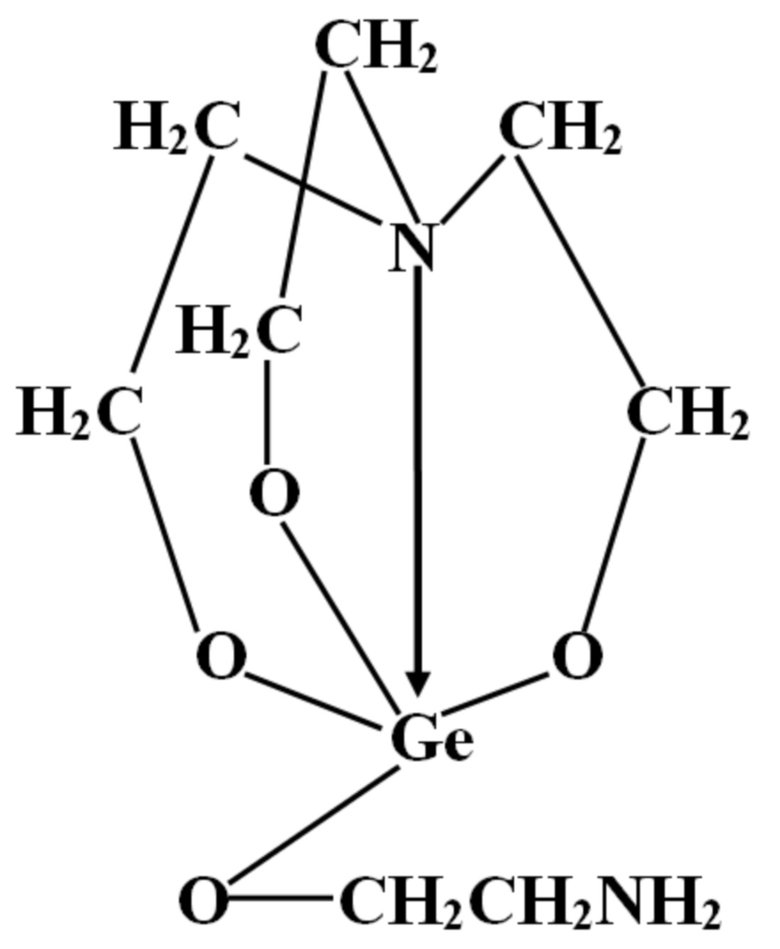
В качестве ближайшего аналога может служить хлоркрезацин [М.И. Яхкинд, М.Г. Воронков , М.И. Сусова , М.К. Нурбеков , М.М. Расулов, К.А. Абзаева, Р.М. Расулов. Применение протатран 4-хлор-2-метил-феноксиацетата для угнетения суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров // Патент на изобретение RU №2619860 от 15.04.2016].
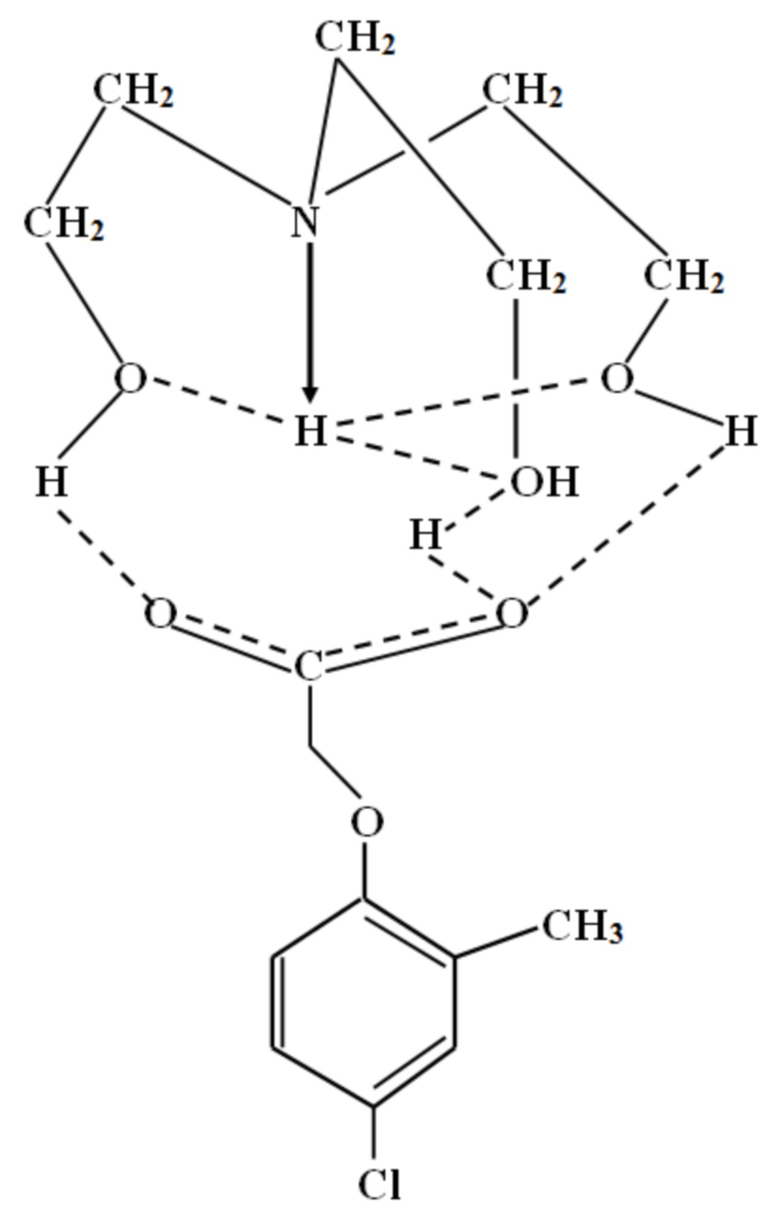
Хлоркрезацин (аналог) или протатран 4-хлор-2- метилфеноксиацетат, имеет формулу:
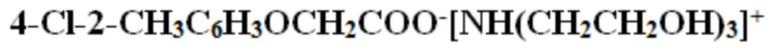
и вид:
Задачей изобретения является разработка нового средства, которое возможно применить для понижения общей активности основной фосфолипазы А2 мононуклеаров (ФЛА2).
Технический результат – расширение арсенала средств, обладающих свойством снижать суммарную активность основной (щелочной) фосфолипазы А2 мононуклеаров за счет выявленной новой биологической активности 1-(герматран-1-ил)-1-оксиэтиламина.
Предлагается применение 1-(герматран-1-ил)-1-оксиэтиламина в качестве средства, угнетающего суммарную активность основной (щелочной) фосфолипазы А2 мононуклеаров.
При этом 1-(герматран-1-ил)-1-оксиэтиламин может применяться в виде раствора в официальном растворе 0,9% натрия хлорида или в воде для инъекций.
При этом раствор может содержать 5-20 мас.% 1-(герматран-1-ил)-1-оксиэтиламина.
Заявляемая биологическая активность 1-(герматран-1-ил)-1-оксиэтил-амина в отношении угнетения активности основной (щелочной) ФЛА2 не была ранее известна.
Свойство 1-(герматран-1-ил)-1-оксиэтиламина снижать общую (суммарную) активность основной (щелочной) фосфолипазы A2 в литературе не описано.
Применение 1-(герматран-1-ил)-1-оксиэтиламина по новому назначению стало возможным благодаря выявленным нами его новым свойствам.
Впервые показано, что введение 1-(герматран-1-ил)-1-оксиэтиламина животным снижает активность лизосомального липолитического фермента из класса гидролаз (КФ 3.1.1) – щелочной ФЛА2.
Заявляемое изобретение относится к приоритетному направлению развития науки и технологий «Биомедицинские и ветеринарные технологии жизнеобеспечения и защиты человека и животных» [см. Алфавитно-предметный указатель к Международной патентной классификации по приоритетным направлениям развития науки и технологий / Ю.Г. Смирнов, Е.В. Скиданова, С.А. Краснов – М.: ПАТЕНТ, 2008. – с.15].
При разработке изобретения авторы использовали различные растворители для получения средства для воздействия на активность основной (щелочной) ФЛА2 мононуклеаров. Были испытаны различные растворы на водной основе, в частности раствор вышеуказанного активного вещества в воде для инъекций и в официальном 0,9% растворе натрия хлорида. При этом в том и в другом случае были получены аналогичные результаты. Следует отметить, что нами исследовались полученные таким образом растворы с различной концентрацией активного вещества – 1- положительные эффекты от их использования, отмеченные ниже, значимо не (герматран-1-ил)-1-оксиэтиламина (5%, 10%, 20%, 50%, 70%). При этом различались. В исследованиях использовали различные дозы активного вещества: от 0,1 мг/кг до 20 мг/кг массы животного. Эффект угнетения активности фермента ФЛА2 присутствовал во всех случаях и был прямо пропорционален дозе используемого активного вещества. Соответственно, для достижения указанного нами технического результата важным является как таковое новое свойство данного соединения, а не его доза. Поэтому ниже, в примере, приведен для демонстрации только опыт с использованием активного вещества в дозе 10 мг/кг ежедневно. В данном случае применяли раствор активного вещества, который приготовляли ex tempore, используя официальный 0,9% раствор натрия хлорида, смешивая с ним активное вещество.
Возможность осуществления изобретения может быть проиллюстрирована следующим примером.
Пример.
Исследование проводили на кроликах Шиншилла с исходной массой 1,8-2,0 кг в соответствии с «Правилами лабораторной практики в Российской Федерации». Правила утверждены приказом Министерства здравоохранения РФ от 19.06.2003 г №267 (Правила лабораторной практики в Российской Федерации Министерства здравоохранения РФ Приказ от 19 июня 2003 года № 267 http://www.kodeks.ru (24 апреля 2010г)). Животных содержали в соответствии с правилами Европейской конвенции по защите позвоночных животных, используемыми для экспериментальных и иных научных целей. По окончании эксперимента животным проводили эвтаназию цервикальной дислокацией 5 позвонка, соблюдая правила «Европейской конвенции о защите позвоночных животных, которые используются для экспериментальных и других научных целей» (Страсбург, 1986).
Гиперлипидемию у кроликов вызывали методом Аничкова-Халатова.
Испытуемые вещества для инъекций растворяли «ex tempore» в официальном растворе 0,9% натрия хлорида. Кролики были разделены на следующие группы (по 10 голов):
1) группа опыта, которым в течение 2 месяцев вводили ежедневно внутримышечно раствор 1-(герматран-1-ил)-1-оксиэтиламина, доза активного вещества 10 мг/кг массы животного, в виде свежеприготовленного раствора.
2) группа плацебо – контроля, которым вводили внутримышечно ежедневно эквиобъёмное количество официального 0,9% раствора натрия хлорида в течение 2 месяцев.
3) группа животных, получавших внутримышечно ежедневно свежеприготовленный раствор аналога – хлоркрезацина в дозе активного вещества 10 мг/кг массы животного в течение 2 месяцев.
Эталоном служили данные, полученные у интактных кроликов.
В конце экспериментов в крови животных стандартными методами определяли содержание липидов, триацилглицеринов, β-липопротеинов и холестерина.
Мононуклеары (моноциты – Мц) выделяли из крови путем последовательного центрифугирования в градиенте фикол-верографин [см. Gmelig - Meyling F., Waldman T.A. Separation of human blood monocytes and lymphocytes on a continuous percoll gradient // J. Immunol. Method. - 1980. -Vol. 26. - P. 603-308]. Гепаринизированную кровь разводили 0,9% официальным раствором натрия хлорида в соотношении 1:1 и осторожно наслаивали раствор фикола с 76% верографином, центрифугировали 45 мин. После центрифугирования отбирали Мц и вновь центрифугировали их 30 мин при 1200 g. Полученные в виде осадка Мц троекратно отмывали физиологическим раствором в соотношении 5:1 центрифугируя по 10 мин при 1200 g. Осадок гомогенизировали в 2 мл 0,25М раствора сахарозы pH 7,4 с 0,001М ЭДТА. Активность ФЛА2 определяли радиометрическим методом [см. Stoffel. W., Trabert. U. Studies on the occerence and proparties of lisosomal phospholipases Al and A2 and the degradation of posphatidie acid in rat liver lysosomes // Hoppe-Seyler's Z. Fhysiol. Chem. - 1969. - Bd/ 350. - S. 836-844] с использованием в качестве субстрата синтезированного ранее 1-ацил-2(13-Н) арахидоноил-глицеро-3sn-фосфорилхолина [см. Robertson A.F., Lends W.E.M. Positional specificities in phospholipid hydrolises // Biochemistry (Wash.). - 1962. - Vol.1. - P. 804-810]. Инкубационная смесь содержала 150 нмолей меченого лецитина, 8 ммоль CaCl2 при pH 8,0 и источник ферментов (исследуемые Мц) в конечном объеме 1,3 мл. Инкубацию проводили на водяной вибробане в течение 30 мин при 37°C. Реакцию останавливали добавлением 3 мл смеси хлороформ: метанол (1:2 об/об) и немедленно экстрагировали по методу Клайера и Дайера. Продукты реакции разделяли тонкослойной хроматографией в закрепленном слое силикагеля («Chemapol») на стеклянных пластинах размером 20×20 см в системе растворителей хлороформ: метанол:вода (65:25:4). Фракции лизолецитина, лецитина и жирных кислот экстрагировали смесью хлороформ:метанол (1:2 об/об). Экстракты помещали во флаконы с 10 мл сцинциляционной жидкости, содержащей в 100 мл толуола особой чистоты 5 г 2,5-дифенилоксазола и 300 мг 1,4-бис-(5-фенилоксазолил-2)-бензола. Радиоактивность измеряли на сцинцилляционном счетчике «Rackbeta 1215» ЛКБ (Швеция). Об активности ФЛА2 судили по образованию меченой жирной кислоты, получившейся в результате воздействия этих ферментов на 1-ацил-2(13-H)-арахидонил-глицеро-3sn-фосфорилхолин.
Активность ФЛА2 выражали в микромолях образовавшихся продуктов в минуту на 1 г белка.
Статистическую обработку данных проводили методом Стьюдента. Данные представлены в виде средних и стандартных значений ошибки – М и m, соответственно. Достоверными считаются различия при р ≤ 0,05 (см. Петри А., Сэбин К., 2009].
Результаты.
При применении 1-(герматран-1-ил)-1-оксиэтиламина в Мц снижается уровень холестерола и общих липидов (таблица 1).
Результаты ферментативного анализа, представленные в таблице 2, свидетельствуют, что развитие атеросклероза сопровождается значительным увеличением суммарной активности ФЛА2 в Мц по сравнению с эталоном. При введении 1-(герматран-1-ил)-1-оксиэтиламина достоверно снижается активность ФЛА2 в Мн по сравнению с контролем, как и при применении аналога – хлоркрезацина.
Активацию лизосомального липолиза можно рассматривать как компенсаторную реакцию ферментных систем на фоне преобладания неспецифического нерегулируемого эндоцитоза модифицированных ЛНП или надмолекулярных ЛНП-содержащих комплексов. При этом в условиях субстратного насыщения может возникнуть относительная недостаточность отдельных лизосомальных ферментов, в частности ФЛА2. ФЛА2 секретируется в виде профермента и для ее активации требуется гидролиз специфических пептидных связей. Для проявления каталитической активности ФЛА2 необходим Ca2+ в миллимолярных концентрациях. ФЛА2 имеют ключевое значение в продукции провоспалительных медиаторов - арахидоновой кислоты (АрК) и эйкозаноидов. Все метаболиты АрК называются эйкозаноидами. АрК образуется из фосфолипидов мембраны клеток (лейкоциты, тромбоциты).
Существует два основных пути метаболизма АрК – циклоксигеназный и липоксигеназный. Конечными продуктами циклоксигеназного пути являются простагландины и тромбоксаны, а липоксигеназного – гидроксиэйкозатетраеновая кислота и лейкотриены. Помимо циклооксигеназы и липоксигеназы, выявлен третий фермент – эпоксигеназа, который окисляет АрК в эпоксиэйкозатриеновую кислоту и дигидроксиэйкозатриеновую кислоту. Высвобождение АрК происходит преимущественно через активацию ФЛА2, а фосфатидилхолин является первичным субстратом. ФЛА2 принимает участие в многочисленных физиологических процессах, включая иммунные реакции, воспаление, пролиферацию, вазо- и бронхоконстрикцию [см. Zhao Y, Tong J, Не D, et all. Role of lysophosphatidic acid receptor LPA2 in the development of allergic airway inflammation in a murine model of asthma // Am. J. Respir. Crit. Care Med. - 2009. - Nov. 20, - p. 10-11].
Таким образом, применение химического соединения - 1-(герматран-1-ил)-1-оксиэтиламина приводит к достоверному снижению общей активности основной (щелочной) фосфолипазы А2 мононуклеаров.
В связи с этим, данное изобретение в дальнейшем позволит создать на основе 1-(герматран-1-ил)-1-оксиэтиламина новые фармакологические препараты для предотвращения нарушений липидного обмена.
Таблица 1
Показатели липидного обмена у кроликов при применении 1-(герматран-1-ил)-1-оксиэтиламина в физиологическом растворе
Примечание : * - p<0.05 по отношению к контролю;
** - p<0.05 по отношению к эталону.
Таблица 2
Активность ФЛА2 в моноцитах кроликов (мкмоль/мин на 1 г белка) при применении 1-(герматран-1-ил)-1-оксиэтиламина на физиологическом растворе
Примечание : * - p<0.05 по отношению к контролю;
** - p<0.05 по отношению к эталону.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ угнетения суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров с помощью 1-(герматран-1-ил)-1-оксиэтиламина | 2020 |
|
RU2732881C1 |
| Способ угнетения суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров с помощью бис(µ-тартрато)ди(µ-гидроксо) германата (IV) триэтаноламмония | 2020 |
|
RU2732880C1 |
| Применение бис(μ-тартрато)ди(μ-гидроксо) германата (IV) триэтаноламмония для угнетения суммарной активности основной (щелочной) фосфолипазы А мононуклеаров | 2020 |
|
RU2733166C1 |
| ПРИМЕНЕНИЕ ПРОТАТРАН 4-ХЛОР-2-МЕТИЛФЕНОКСИАЦЕТАТА ДЛЯ УГНЕТЕНИЯ СУММАРНОЙ АКТИВНОСТИ ОСНОВНОЙ (ЩЕЛОЧНОЙ) ФОСФОЛИПАЗЫ А2 МОНОНУКЛЕАРОВ | 2016 |
|
RU2619860C1 |
| Применение 1-(герматран-1-ил)-1-оксиэтиламина для торможения развития атеросклероза в эксперименте | 2020 |
|
RU2746321C1 |
| Способ коррекции атерогенеза в эксперименте с помощью 1-(герматран-1-ил)-1-оксиэтиламина | 2020 |
|
RU2741906C1 |
| ПРИМЕНЕНИЕ КОМПЛЕКСА-ТРИС-(2-ГИДРОКСИЭТИЛ)АМИНА С БИС-(2-МЕТИЛФЕНОКСИАЦЕТАТОМ) ЦИНКА (ЦИНКАТРАНА) В КАЧЕСТВЕ СРЕДСТВА, УГНЕТАЮЩЕГО ОБЩУЮ АКТИВНОСТЬ ОСНОВНОЙ (ЩЕЛОЧНОЙ) ФОСФОЛИПАЗЫ А2 МОНОНУКЛЕАРОВ | 2014 |
|
RU2546537C1 |
| Применение 1-гидроксигерматрана для торможения развития атеросклероза в эксперименте | 2020 |
|
RU2742972C1 |
| Способ коррекции атерогенеза в эксперименте с помощью 1-гидроксигерматрана | 2020 |
|
RU2741229C1 |
| СРЕДСТВО, МОДУЛИРУЮЩЕЕ АКТИВНОСТЬ КИСЛОЙ ФОСФОЛИПАЗЫ А1 | 2010 |
|
RU2445087C1 |
Изобретение относится к медицине и касается применения 1-(герматран-1-ил)-1-оксиэтиламина в качестве средства, угнетающего суммарную активность основной (щелочной) фосфолипазы А2 мононуклеаров. Изобретение обеспечивает угнетение суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров. 3 з.п. ф-лы, 2 табл., 1 пр.
1. Применение 1-(герматран-1-ил)-1-оксиэтиламина в качестве средства, угнетающего суммарную активность основной (щелочной) фосфолипазы А2 мононуклеаров.
2. Применение по п. 1, отличающееся тем, что 1-(герматран-1-ил)-1-оксиэтиламин используют в виде раствора в 0,9%-ном растворе натрия хлорида или в воде для инъекций.
3. Применение по п. 2, отличающееся тем, что 1-(герматран-1-ил)-1-оксиэтиламин используют в виде раствора, содержащего 5-20 мас.% активного вещества.
4. Применение по п. 1, или 2, или 3, отличающееся тем, что применяют раствор, содержащий активное вещество 1-(герматран-1-ил)-1-оксиэтиламин в дозе 10 мг/кг массы животного.
| ЖИГАЧЕВА И.В | |||
| Функциональное состояние митохондрий проростков гороха в условиях дефицита воды и обработки фосфорорганическим, германийорганическим соединениями и производным 5-гидроксибензимидазола / И | |||
| В | |||
| Жигачева, В | |||
| И | |||
| Бинюков, Е | |||
| М | |||
| Миль // Вiсник Харкiвського нацiонального аграрного унiверситету | |||
| Серiя : Бiологiя | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| - Вип | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| - С | |||
Авторы
Даты
2020-09-24—Публикация
2020-05-14—Подача