Изобретение относится к медицине, фармакологии и биологии и касается нового средства, влияющего на активность фосфолипаз.
Фосфолипазы играют важную роль в обмене липидов в живых организмах. Составной частью многих тканей и секретов живых организмов являются фосфолипазы группы А. Фосфолипазы А1 в большинстве своем - внутриклеточные ферменты, часто мембраносвязанные, не нуждаются в коферменте. Их молекулярные массы варьируют в пределах 15-90 тыс.; оптимальная каталитическая активность проявляется при pH 4,0 (для лизосомальных ферментов) или 8,0-9,5 (для ферментов микросом, плазматических мембран и цитозоля); широко распространены в животных тканях (печень, сердце, мозг) и в микроорганизмах (Bacillus subtilis, В. megateiium, Mycobacter phlei, Escherichia coli). Фосфолипазы А1 отщепляют ацильную цепь фосфолипида в sn-1 положении. При действии фосфолипазы А1 на фосфолипид образуется 1-лизофосфолипид и жирная кислота.
Доказано, что фосфолипазы являются биомаркерами активности атеросклеротического процесса [см. Душкин М.И. Макрофаги и атеросклероз: патофизиологические и терапевтические аспекты. // Бюлл. СО РАМН (2006); № 2 (120), с.47-55], эффективности проводимой терапии как у больных атеросклерозом, так и у больных с осложнениями атеросклероза, в частности ишемической болезни сердца - ИБС (стенокардией напряжения II ФК) [см. Богданова С.Н. Клинико-экспериментальное изучение влияния фактора питания на активность лизосомальных гидролаз тромбоцитов и мононуклеарных лейкоцитов при атеросклерозе. Автореф. дисс. канд., Москва (1992), 28 с., Данковцев Е.Н., Затейщиков Д.А. Биомаркеры в кардиологии: липопротеинассоциированная фосфолипаза А2. // Фарматека (2007); № 15 (149). Кардиология, неврология, с.22-28].
Известно, что на раннем этапе атерогенеза происходит активация эндотелия, который экспрессирует на своей поверхности адгезионные молекулы для моноцитов, нейтрофилов и лейкоцитов крови и продуцирует хемоаттрактанты, привлекающие моноциты в интиму сосудов. Моноциты, мигрирующие в субэндотелиальное пространство, дифференцируются в макрофаги, которые выступают как катализаторы образования окисленных ЛНП, миграции и пролиферации гладкомышечных клеток из мышечной оболочки в интиму. Частицы модифицированных ЛНП предпочтительно захватываются с помощью специфических рецепторов макрофагами, которые трансформируются в пенистые клетки. Активированные макрофаги, продуцирующие металлопротеиназы и коллагеназу, в определенных ситуациях способствуют распаду коллагена в бляшке и возникновению такого грозного осложнения, как разрыв бляшки, образование тромба и развитие инфаркта миокарда. Липидный профиль в значительной мере определяется состоянием макрофагов, их ферментативными реакциями. В этом плане заслуживают внимания исследования и разработка средств, изменяющих активность липаз макрофагов, в частности кислой фосфолипазы А1 (кФЛА1) (КФ 3.1.1.32) с оптимумом pH 4,0, вызывающей деградацию структуры фосфолипидов, отщепляя ацильные остатки от углеродных атомов C1 в молекуле лецитина и других фосфолипидов с образованием промежуточных продуктов гидролиза - лизолецитина и лизофосфолипидов, обладающих сильным мембранотоксическим действием [см. Покровский А.А., Тутельян В.А. Лизосомы. - Наука, 1976, 380 с., Брокерхоф X., Дженсен Р. Липолитические ферменты, пер. с англ., М., 1978, с.242-356.].
В литературе имеются сведения о возможности снижения общей (суммарной) активности ФЛА различными химическими соединениями [см. Губергриц Н.Б. «Эссенциале форте Н», «Эссенциале Н» в гепатологии и гастроэнтерологии. Сучасна гастроентерологiя, № 5 (43), 2008, с.79-89].
Известно также, что при введении некоторых препаратов, например, липостабила, который оказывает гиполипидемическое действие, происходит активация кислых и щелочных фосфолипаз [см. Самсонов М.А., Васильев А.В., Погожева А.В., Бобкова С.Н. Сравнительная оценка гиполипидемического действия ПНЖК w-3 и липостабила. //Вопр. питания, 1996, № 4, с.12-16].
Однако существует потребность в поиске и внедрении в практику новых диагностических и лекарственных средств, обладающих активностью в отношении фосфолипаз.
В качестве ближайшего аналога может быть указан способ снижения общей активности кФЛА1 с использованием комплекса трис-(2-гидроксиэтил)амина с бис-(2-метилфеноксиацетатом) цинка (см. Расулов М.М., Воронков М.Г., Стороженко П.А., Мирскова А.Н., Снисаренко Т.А., Абзаева К.А., Ваганов М.А. Применение комплекса трис-(2-гидроксиэтил)амина с бис-(2-метил-феноксиацетатом) цинка для снижения общей активности кислой фосфолипазы А1// Патент на изобретение RU №2545888, 10.04.2015).
Комплекс трис-(2-гидроксиэтил)амина с бис-(2-метилфеноксиацетатом) цинка (аналог), или цитримин (цинкатран), обладает широким спектром терапевтического действия и имеет формулу: (HOCH2CH2)3N⋅Zn(OOCCH2OC6H4CH3-2)2
и вид:
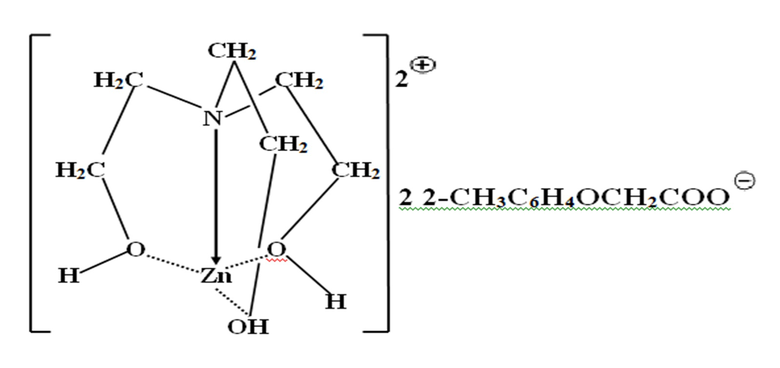
К недостатку прототипа можно отнести небольшой эффект угнетения активности фосфолипазы.
Заявляемое изобретение относится к приоритетному направлению развития науки и технологий «Биомедицинские и ветеринарные технологии жизнеобеспечения и защиты человека и животных» [см. Алфавитно-предметный указатель к Международной патентной классификации по приоритетным направлениям развития науки и технологий / Ю.Г. Смирнов, Е.В. Скиданова, С.А. Краснов - М.: ПАТЕНТ, 2008. - с.15].
Задача настоящего изобретения состоит в разработке нового средства, которое возможно использовать для понижения общей активности лизосомального липолитического фермента - кислой фосфолипазы А1.
Технический результат - расширение арсенала способов воздействия на активность кислой фосфолипазы А1 путем применения средства - 1-гидроксигерматрана, за счет его новой выявленной биологической активности, а именно, способности снижать суммарную активность кФЛА1.
Поставленная задача решается тем, что в качестве средства, понижающего общую активность кислой фосфолипазы А1, предлагается использовать синтезированное ранее (см. Воронков М.Г., Адамович С.Н. и др. Синтез новых биологически активных O-гидрометаллоатранов //ЖОХ, 2009, т.79, №1, С.162-163), биологически активное соединение - 1-гидроксигерматран, который имеет формулу:
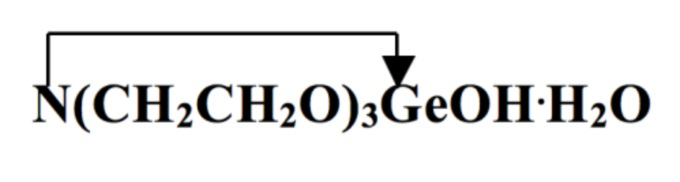
1-гидроксигерматран, или герматранол-гидрат, имеет следующий вид:
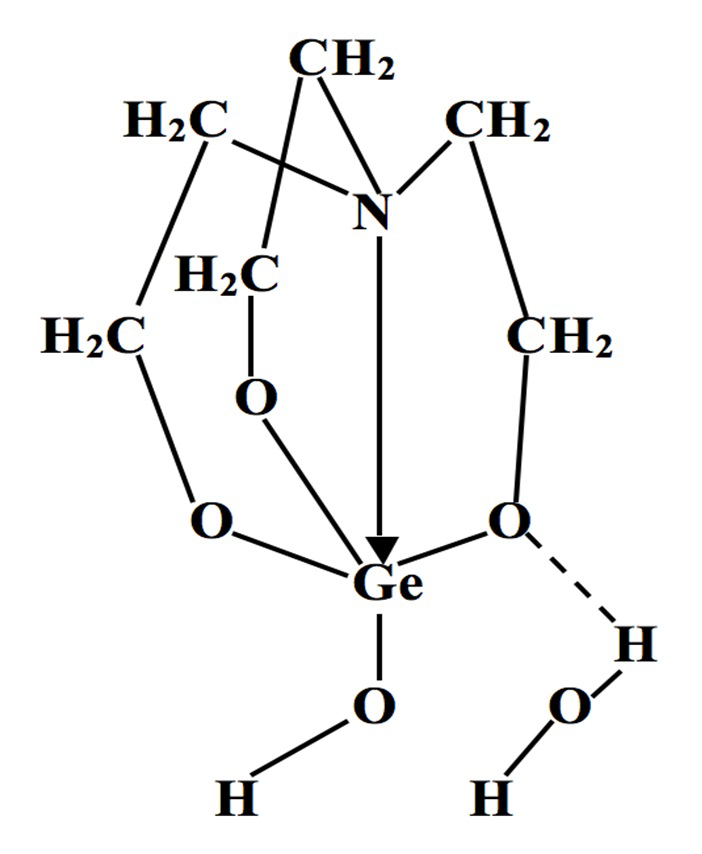
Известно свойство герматранол-гидрата стимулировать экспрессию матричной РНК триптофанил-тРНК-синтетазы [см. Расулов М.М., Стороженко П.А. и др. Герматранол-гидрат, стимулирующий экспрессию матричной РНК триптофанил-тРНК-синтетазы. Патент РФ № 2553986 С1, 20.06.2015].
1-гидроксигерматран может быть использован в клинической медицине для создания препаратов, обладающих антигиперлипидемическим действием и не имеющих побочных эффектов.
Заявляемая биологическая активность 1-гидроксигерматрана в качестве средства, обладающего свойством снижать активность кислой фосфолипазы А1, не была известна и в литературе не описана.
Впервые показано, что введение 1-гидроксигерматрана влияет на активность лизосомального липолитического фермента из класса гидролаз (КФ 3.1.1): кФЛА1 (КФ 3.1.1.32).
Таким образом, предлагается способ снижения общей (суммарной) активности лизосомального липолитического фермента - кислой фосфолипазы А1, включающий введение композиции, которая содержит 1-гидроксигерматран в качестве активного вещества, а также фармацевтически приемлемый водный носитель, экспериментальному животному внутримышечно ежедневно в течение 2 месяцев в дозе активного вещества 5,0 мг/кг массы животного.
При этом в качестве фармацевтически приемлемого водного носителя предлагается использование официальной дистиллированной воды, воды для инъекций или официального физиологического раствора - 0,9% раствора натрия хлорида.
При этом раствор готовится «ex tempore» и может содержать 5-20 мас.% 1-гидроксигерматрана.
При разработке изобретения авторы использовали различные растворители для получения средства для воздействия на активность кФЛА1. Были испытаны различные растворы на водной основе, в частности раствор вышеуказанного активного вещества в воде для инъекций, официальной дистиллированной воде и в официальном 0,9% растворе натрия хлорида. При этом во всех случаях были получены аналогичные результаты. Следует отметить, что нами исследовались полученные таким образом растворы с различной концентрацией активного вещества - 1-гидроксигерматрана (5%, 10%, 20%, 50%, 70%). При этом положительные эффекты от их использования, отмеченные ниже, значимо не различались. В исследованиях использовали различные дозы активного вещества: от 0,1 мг/кг до 20 мг/кг массы животного. Эффект угнетения активности фермента кФЛА1 присутствовал во всех случаях и был прямо пропорционален дозе используемого активного вещества. Соответственно, для достижения указанного нами технического результата важным является как таковое новое свойство данного соединения, а не его доза или конкретный водный растворитель. Поэтому ниже, в примере, приведен для демонстрации только опыт с использованием активного вещества в дозе 5,0 мг/кг массы животного ежедневно. В данном случае применяли раствор активного вещества, который приготовляли ex tempore, используя официальный физиологический раствор (0,9% натрия хлорида), смешивая с ним активное вещество.
Возможность осуществления изобретения может быть проиллюстрирована следующими данными.
Пример
Эксперименты проводили на кроликах шиншилла с исходной массой тела 1,8-2,0 кг в соответствии с «Правилами лабораторной практики в Российской Федерации». Правила утверждены приказом Министерства здравоохранения РФ от 19.06.2003 г №267 (Правила лабораторной практики в Российской Федерации Министерства здравоохранения РФ Приказ от 19 июня 2003 года № 267 http:// www. kodeks.ru (24 апреля 2010г)). Животных содержали в соответствии с правилами Европейской конвенции по защите позвоночных животных, используемыми для экспериментальных и иных научных целей. По окончании эксперимента животным проводили эвтаназию цервикальной дислокацией 5-го позвонка, соблюдая правила «Европейской конвенции о защите позвоночных животных, которые используются для экспериментальных и других научных целей» (Страсбург, 1986).
1-гидроксигерматран смешивали «ex tempore» до полного растворения в официальном 0,9% растворе натрия хлорида.
Комплекс трис-(2-гидроксиэтил)амина с бис-(2-метилфеноксиацетатом) цинка (аналог, цитримин) так же смешивали «ex tempore» до полного растворения в официальном 0,9% растворе натрия хлорида.
Гиперлипидемию вызывали методом Аничкова-Халатова (известная экспериментальная модель развития атеросклероза).
Животных группировали по 10 голов следующим образом:
1) группа опыта, которым вводили внутримышечно свежеприготовленный раствор 1-гидроксигерматрана в дозе активного вещества 5,0 мг/кг массы животного ежедневно в течение 2 месяцев.
2) группа плацебо-контроля, которым вводили внутримышечно эквиобъемное количество официального 0,9% раствора натрия хлорида ежедневно в течение 2 месяцев.
3) группа животных, получавших внутримышечно свежеприготовленный раствор аналога - цитримина (цинкатрана) в дозе активного вещества 5,0 мг/кг массы животного ежедневно в течение 2 месяцев.
Эталоном служили данные, полученные у интактных кроликов.
В конце экспериментов у животных в грудном отделе аорты стандартными методами определяли содержание липидов, триацилглицеринов, β-липопротеинов и холестерина. Для определения активности кислой фосфолипазы А1 из кусочков грудной аорты диспергированием выделяли клетки интимы известным методом [см. Нагорнев В.А. Методология в изучении проблемы атеросклероза. // Мед. акад. ж. 2005, т.5, в.3, с.121-133]. Для этого использовали раствор (0,5 мл), содержащий коллагеназу - тип 4 и эластазу - тип 3 («sigma», США). Время диспергирования - 75 мин при 37°С (1 мл/50 мг ткани). Полученную суспензию клеток промывали холодным раствором Хенкса. Осадок при последней промывке гомогенизировали в 2 мл 0,25М раствора сахарозы pH 7,4 с 0,001 м ЭДТА. Конечное разведение гомогенатов аорты соответствовало 1:20 (вес : объем). Супернатант использовали для исследования активности кислой фосфолипазы А1. Активность кФЛА1 определяли спектрофотометрически по известному методу [см. Булычев А.Г., Семенова Е.Г., Ассиновская О.А. Влияние агрегации нейтрального красного, акридинового оранжевого и хлористого аммония клетками (сублинии) на активность лизосомальных гидролаз. // Цитология. - (1986). Т.28, № 7. С.703-711], используя в качестве субстрата β-нафтилкаприлат («sigma», США). К 0,2 мл исследуемого материала добавляли 0,5 мл субстратного раствора в 0,2 М ацетатного буфера, pH 5,2, с 0,2% тритоном Х-100, инкубировали на водяной бане в течение 30 мин при 37°С. Реакцию останавливали добавлением 0,5 мл «fast blue В» («serva», ФРГ) (1 мг/мл в 0,05 М фосфатного буфера, pH 7,2), через 5 мин добавляли 1 мл 10% охлажденного раствора трихлоруксусной кислоты, еще через 3 мин - 1,5 мл этилового эфира уксусной кислоты, затем образцы встряхивали, центрифугировали на центрифуге WKH-1 при 150 g 15 мин. Отбирали 0,5 мл верхней фазы в микрокювету и проводили спектрометрию при 525 нм. Суммарную активность кФЛА1 выражали в микромолях β-нафтола, образовавшегося за 1 мин на 1 г белка.
Статистическую обработку данных проводили методом Стьюдента. Данные представляли в виде средних и стандартных значений ошибки - М и m, соответственно. Достоверными считали различия при р ≤ 0,05 (см. Петри А., Сэбин К., 2009).
Результаты ферментативного анализа представлены в таблице 1 и демонстрируют улучшение липолитических показателей и уровня кФЛА1 при использовании заявленного способа как по сравнению с группой контроля, так и по сравнению с использованием аналога (цитримина, цинкатрана).
Корреляционный анализ выявил связь средней силы между уровнем активности кФЛА1 и показателями липидного обмена после введения 1-гидроксигерматрана (таблица 2).
Активацию системы лизосомального липолиза можно рассматривать как компенсаторную реакцию ферментных систем на фоне преобладания неспецифического, нерегулируемого эндоцитоза модифицированных липопротеинов низкой плотности (ЛПНП) или надмолекулярных ЛПНП-содержащих комплексов. При этом в условиях субстратного насыщения может возникнуть относительная недостаточность отдельных лизосомальных ферментов (в частности, кФЛА1), расщепляющих этерифицированный холестерин (ЭХС), что приводит к аккумуляции ЭХС и триглицеридов в клетках крови и повышению риска развития атеросклероза [см. Нагорнев В.А. Методология в изучении проблемы атеросклероза. // Мед. акад. ж. 2005, т.5, в.3, с.121-133.]. Наряду с этим изменения в состоянии лизосомального аппарата интимы можно расценивать и как адаптационные перестройки на стадии липоидоза, и как результат функциональной недостаточности на стадии образования фиброзной бляшки.
Таким образом, реакции кислой фосфолипазы указывают на структурно- функциональные нарушения в деятельности субклеточных структур при развитии атеросклероза и, соответственно, полезными могут быть средства - модуляторы таких реакций. Установление новых свойств 1-гидроксигерматрана позволит использовать его, например, для повышения устойчивости сосудистой системы к холестерину при развитии атеросклеротического процесса, гиперлипидемии. Также он может быть использован для образования вторичных посредников или предшественников в синтезе биологически активных веществ - эйкозаноидов. Ввиду важности выявленного механизма корреляции активности ферментной системы в зависимости от состояния организма 1-гидроксигерматран можно будет использовать не только для профилактики и/или лечения состояний, связанных с нарушением нормальной функции фосфолипазы А1 макрофагов, но и при скрининге, например, соединений, обладающих аналогичной активностью.
Таблица 1.
Показатели липидного обмена при применении 1-гидроксигерматрана
Примечание: * - p<0.05 по отношению к плацебо - контролю;
** - p<0.05 по отношению к эталону.
Таблица 2.
Коэффициенты корреляции (r) активности кислой ФЛА1 в ткани аорты с показателями липидного обмена при использовании 1-гидроксигерматрана
глицерины
| название | год | авторы | номер документа |
|---|---|---|---|
| Применение 1-гидроксигерматрана для торможения развития атеросклероза в эксперименте | 2020 |
|
RU2742972C1 |
| Способ коррекции атерогенеза в эксперименте с помощью 1-(герматран-1-ил)-1-оксиэтиламина | 2020 |
|
RU2741906C1 |
| Применение 1-(герматран-1-ил)-1-оксиэтиламина для торможения развития атеросклероза в эксперименте | 2020 |
|
RU2746321C1 |
| ПРИМЕНЕНИЕ КОМПЛЕКСА-ТРИС-(2-ГИДРОКСИЭТИЛ)АМИНА С БИС-(2-МЕТИЛФЕНОКСИАЦЕТАТОМ) ЦИНКА (ЦИНКАТРАНА) ДЛЯ СНИЖЕНИЯ ОБЩЕЙ АКТИВНОСТИ КИСЛОЙ ФОСФОЛИПАЗЫ А1 | 2014 |
|
RU2545888C1 |
| Способ угнетения суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров с помощью 1-(герматран-1-ил)-1-оксиэтиламина | 2020 |
|
RU2732881C1 |
| Способ угнетения суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров с помощью бис(µ-тартрато)ди(µ-гидроксо) германата (IV) триэтаноламмония | 2020 |
|
RU2732880C1 |
| Применение 1-(герматран-1-ил)-1-оксиэтиламина для угнетения суммарной активности основной (щелочной) фосфолипазы А2 мононуклеаров | 2020 |
|
RU2732883C1 |
| Применение бис(μ-тартрато)ди(μ-гидроксо) германата (IV) триэтаноламмония для угнетения суммарной активности основной (щелочной) фосфолипазы А мононуклеаров | 2020 |
|
RU2733166C1 |
| ПРИМЕНЕНИЕ КОМПЛЕКСА-ТРИС-(2-ГИДРОКСИЭТИЛ)АМИНА С БИС-(2-МЕТИЛФЕНОКСИАЦЕТАТОМ) ЦИНКА (ЦИНКАТРАНА) В КАЧЕСТВЕ СРЕДСТВА, УГНЕТАЮЩЕГО ОБЩУЮ АКТИВНОСТЬ ОСНОВНОЙ (ЩЕЛОЧНОЙ) ФОСФОЛИПАЗЫ А2 МОНОНУКЛЕАРОВ | 2014 |
|
RU2546537C1 |
| СРЕДСТВО, МОДУЛИРУЮЩЕЕ АКТИВНОСТЬ КИСЛОЙ ФОСФОЛИПАЗЫ А1 | 2010 |
|
RU2445087C1 |
Изобретение относится к медицине, фармакологии и биологии и касается способа снижения общей (суммарной) активности лизосомального липолитического фермента – кислой фосфолипазы А1 (кФЛА1). Сущность способа заключается в том, что животному вводят внутримышечно композицию, содержащую 1-гидроксигерматран и фармацевтически приемлемый водный носитель. При этом доза активного вещества составляет 5,0 мг/кг массы животного. Препарат вводят ежедневно в течение 2 месяцев. Использование способа позволяет снизить активность кФЛА1, обеспечивая снижение гиперлипидемий и предотвращение атеросклеротических поражений кровеносных сосудов. 3 з.п. ф-лы, 2 табл., 1 пр.
1. Способ снижения общей (суммарной) активности лизосомального липолитического фермента – кислой фосфолипазы А1, включающий введение животному лекарственного средства, отличающийся тем, что в качестве такого средства используют композицию, содержащую 1-гидроксигерматран и фармацевтически приемлемый водный носитель, которую вводят животному внутримышечно в дозе 5,0 мг активного вещества/кг массы животного ежедневно в течение 2 месяцев.
2. Способ по п. 1, отличающийся тем, что используют композицию, полученную ex tempore смешиванием 1-гидроксигерматрана и фармацевтически приемлемого водного носителя.
3. Способ по любому из пп. 1 или 2, отличающийся тем, что в качестве водного носителя используют воду для инъекций, официальную дистиллированную воду или официальный физиологический раствор.
4. Способ по п. 3, отличающийся тем, что композиция может содержать 5-20 мас.% 1-гидроксигерматрана.
| ПРИМЕНЕНИЕ 1-ГИДРОКСИГЕРМАТРАНА (МОНОГИДРАТА) В КАЧЕСТВЕ СРЕДСТВА АКТОПРОТЕКТОРНОГО ДЕЙСТВИЯ И СТИМУЛИРУЮЩЕГО ТКАНЕВОЕ ДЫХАНИЕ В ОРГАНИЗМЕ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2005 |
|
RU2272624C1 |
| БИОХИМИЧЕСКИЕ КОМПЛЕКСЫ ГЕРМАНИЯ С ВЫСОКОЙ ТЕРАПЕВТИЧЕСКОЙ АКТИВНОСТЬЮ И ШИРОКИМ СПЕКТРОМ ИСПОЛЬЗОВАНИЯ | 1998 |
|
RU2233286C2 |
| CN 102250138 A, 23.11.2011 | |||
| WO 2008079055 A1, 03.07.2008 | |||
| Wakabayashi Y., Effect of germanium-132 on low-density lipoprotein oxidation and atherosclerosis in Kurosawa and Kusanagi hypercholesterolemic rabbits // Bioscience, Biotechnology, and Biochemistry, 01 Aug 2001, 65(8):1893-1896. | |||
Авторы
Даты
2021-01-22—Публикация
2020-10-12—Подача