Предлагаемое изобретение относится к способам получения новых полициклических оксирановых соединений, конкретно, к способу получения 3'-замещенных спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиранов] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранов] формулы (2):
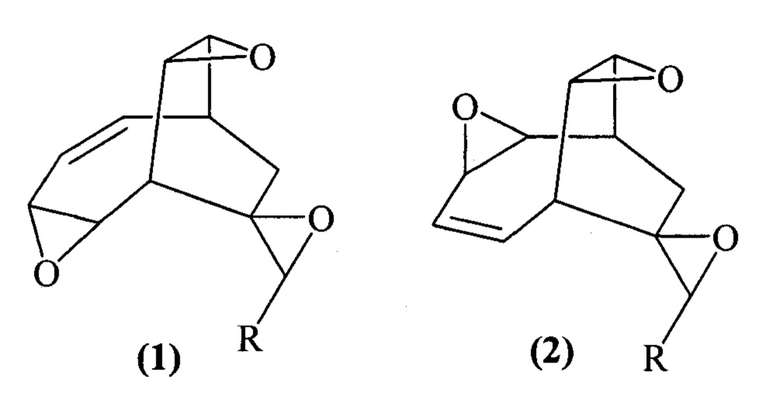
R=Ph, Hex
Указанные соединения относятся к классу оксиранов, используемых при производстве тепло, термо-, хемостойких композиций, лакокрасочных оптически прозрачных материалов, клеев (Smits J., Marx Е., Kooijmans P. et al. Pat. 20030004281 A1 USA. Publ. 2003; Сорокин М.Ф., Шоде Л.Г., Кузьмин А.И. и др. Лакокрасочные материалы и их применение. 1983. №4. С. 4-7). Оксираны находят широкое применение в органическом синтезе, благодаря уникальному строению цикла, позволяющему проводить преобразование с широким диапазоном возможностей под действием реагентов разной природы, к примеру, нуклеофильных агентов (Ю.Н. Беспалько, Е.Н Швед, Н.М. Олейник // Теор. и эспер. Химия. 2008. Т. 44, №5. с. 292-297; М.Ф. Сорокин, Э.Л. Гершанова // Кинетика и катализ. 1967. Т. 8, №3. С. 512-519).
Известен способ (F. Turecek, V. Hanus, P. Sedmera, H. Antropiusova, K. Mach. Cycloheptatriene dimers: new precursors of diamantane // Collection Czechoslovak Chem. Commun., 1981, 46, 1474) получения 8,9:12,13-диэпоксипентацикло [8.4.0.03,704,14.06,11]тетрадекана (3) реакцией эпоксидирования пентацикло[8.4.0.03,7.04,14.06,11]тетрадека-8,12-диена м-хлорнадбензойной кислотой при температуре 0°С в течение 12 ч с выходом 87% по схеме:
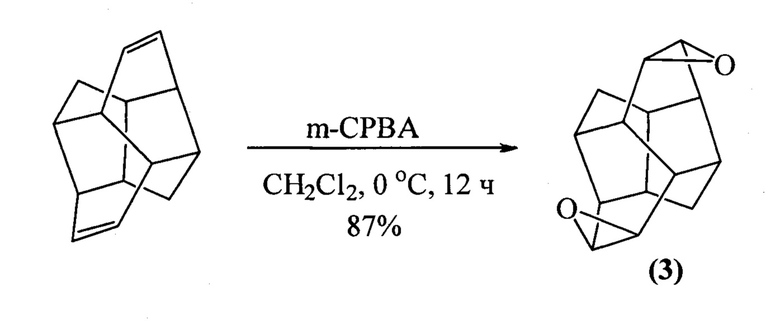
Известным способом не может быть осуществлен синтез 3'-замещенных спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиранов] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранов] формулы (2).
Известен способ (N. Toselli, D. Martin, М. Achard, A. Tenaglia, G. Buono. Highly regio- and stereocontrolled formation of functionalized tricyclo[4.2.1.02,8]non-3-enes // J. Org. Chem., 2009, 74, 3783) получения 7,8-эпокси-7-фенил(бутил)бицикло[4.2.1]нона-2,4-диена (4) реакцией эпоксидирования 7-бутил(фенил)бицикло[4.2.1]нона-2,4,7-триена м-хлорнадбензойной кислотой при температуре 0°С за 25 мин:
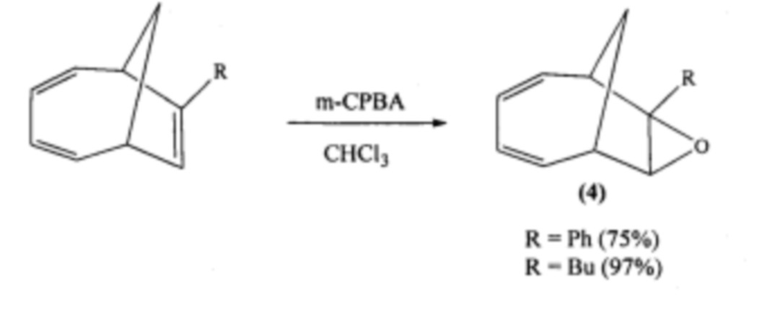
Известным способом не могут быть получены 3'-замещенные спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксираны] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксираны] формулы (2).
Таким образом, в литературе отсутствуют сведения по синтезу 3'-замещенных спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиранов] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранов] формулы (2).
Предлагается новый способ синтеза 3'-замещенных спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиранов] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранов] формулы (2).
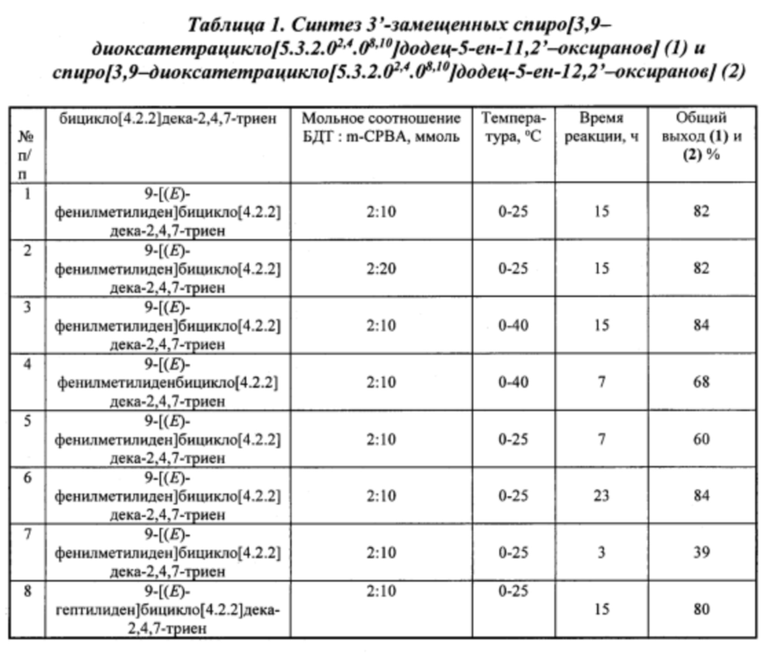
Сущность способа заключается во взаимодействии бицикло[4.2.2]дека-2,4,7-триенов (БДТ) общей формулы (5) (где R=Ph, Hex) с м-хлорнадбензойной кислотой (m-СРВА), при мольном соотношении БДТ:m-СРВА = 2:(10-20), предпочтительно 2:10. Реакцию проводят при температуре 0-40°С. Время реакции 3-23 ч, общий выход целевых продуктов (1) и (2) 39-84% в соотношении (1):(2)=1:1. В качестве растворителя необходимо использовать дихлорметан.
Реакция протекает по схеме:
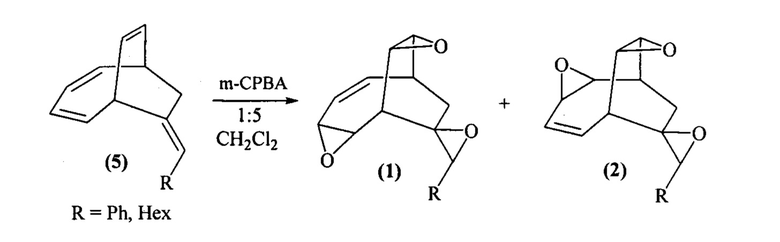
БДТ общей формулы (5) получены по способу, приведенному в работе V.A. Dyakonov, G.N. Kadikova, G.F. Gazizullina, L.M. Khalilov, U.M. Dzhemilev, Cobalt(I)-catalyzed [6π+2π]-cycloadditions of 1,2-dienes to 1,3,5,7-cyclooctatetraene // Tetrahedron Lett, 2015, 56, 2005.
Целевые продукты (1) и (2) образуются только лишь с участием бицикло[4.2.2]дека-2,4,7-триенов и м-хлорнадбензойной кислоты.
Проведение реакции в присутствии м-хлорнадбензойной кислоты больше 20 ммоль на 2 ммоль бицикло[4.2.2]дека-2,4,7-триена не приводит к увеличению выхода целевых продуктов (1) и (2). При использовании м-хлорнадбензойной кислоты в количестве 4 ммоль на 2 ммоль бицикло[4.2.2]дека-2,4,7-триена оксираны (1) и (2) не образуются, так как в данных условиях эпоксидированию подвергается одна двойная связь. Опыты проводили при температуре 0-40°С. При более высокой температуре (например, 40°С) не происходит существенного увеличения выхода целевых продуктов (1) и (2). Уменьшение продолжительности реакции (например, 3 ч) приводит к снижению выхода 3'-замещенных спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиранов] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранов] формулы (2).
Существенные отличия предлагаемого способа:
1. Способ позволяет синтезировать соединения - 3'-замещенные спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксираны] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксираны] формулы (2).
2. Предлагаемый способ базируется на использовании в качестве исходных реагентов бицикло[4.2.2]дека-2,4,7-триенов и м-хлорнадбензойной кислоты. В известных способах:
- соединение (3) получают с использованием пентацикло[8.4.0.03,7.04,14.06,11]тетрадека-8,12-диена и м-хлорнадбензойной кислоты.
- соединение (4) получают с использованием 7-бутил(фенил)бицикло[4.2.1]нона-2,4,7-триена и м-хлорнадбензойной кислоты.
Предлагаемый способ обладает следующими преимуществами:
1. Способ позволяет получать с высокими выходами 3'-замещенные спиро[3,9-диоксатетрацикло [5.3.2.02,4.08,10]додец-5-ен-11,2'-оксираны] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксираны] формулы (2), синтез которых в литературе не описан.
Способ поясняется следующими примерами:
ПРИМЕР 1. В стеклянную ампулу в атмосфере сухого аргона загружали 0.031 г (0.1 ммоль) CoI2, 0.040 г (0.1 ммоль) 1,2-бис(дифенилфосфино)этана и 0.020 г (0.3 ммоль) цинкового порошка в 1.5 мл C2H4Cl2. Смесь перемешивалась при комнатной температуре 2 минуты. Затем добавили 0.104 г (1 ммоль) 1,3,5,7-циклооктатетраена, 0.174 г (1.5 ммоль) фенилпропа-1,2-диена, 1.5 мл C2H4Cl2 и 0.064 г (0.2 ммоль) ZnI2. После нагревания при 60°С в течение 20 ч, ампулу вскрывали, содержимое отфильтровывали, легкие растворители удаляли под вакуумом, остаток хроматографировали на колонке SiO2 (элюент - петролейный эфир).
ПРИМЕР 2. В стеклянный реактор при перемешивании загружали 0.44 г (2 ммоль) 9-[(E)-фенилметилиденбицикло[4.2.2]дека-2,4,7-триена и 30 мл дихлорметана. Смесь охлаждали до 0°С и добавляли 1.73 г (10 ммоль) м-хлонадбензойной кислоты. Реакционную массу перемешивали 3 ч при 0°С и 12 ч при комнатной температуре. Затем добавляли 0.4 г (10 ммоль) гидрокарбоната натрия и перемешивали 1 ч при 0°С. Реакционную смесь промывали 1 М раствором гидроксида натрия (30 мл) и насыщенным раствором хлорида натрия (2×10 мл). Получали 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиран] (1) и 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиран] (2) (белые пластинчатые кристаллы, Тплав. = 128-129°С) с общим выходом 82%.
Структура 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксирана] (2) в кристалле приведена на рис. 1. В молекуле соединения (2), согласно рентгеноструктурному анализу, О(1') эпоксидная группа локализована за пределами бициклического каркаса, в то время как O(3) и O(9) эпоксидные группы анти-ориентированы друг относительно друга. К тому же, О(9)
группа анти-ориентирована по отношению к двойной связи С(5)-С(6) бициклического каркаса. Молекулы 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксирана] (2) стабилизированы в кристалле с помощью бифуркатных С-Н…О межмолекулярных взаимодействий между атомами кислорода эпоксидных групп и атомами водорода бициклического каркаса, что в результате приводит к Pbca пространственной группе.
Спектральные характеристики 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксирана] (1) и 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксирана] (2):
Спектр ЯМР 1Н (500 МГц, CDCl3, δ, м.д.) 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксирана] (1): 1.43-1.53 (м, 1Н), 1.58-1.70 (м, 1H), 2.88-2.95 (м, 1Н), 3.02 (т, 1Н, J=3.9 Гц), 3.10 (т, 1Н, J=5.0 МГц), 3.28 (т, 1H, J=4.4 Гц), 3.37 (т, 1Н, J=4.5 Гц), 3.61 (дд, 1H, J=4.1 Гц), 3.98 (с, 1Н), 6.12-6.21 (м, 2Н), 7.28-7.39 (м, 5Н). Спектр ЯМР 13С (125 МГц, CDCl3, δ, м.д.): 26.8, 32.0, 41.8, 50.9, 51.5, 53.2, 56.7, 62.0, 66.7, 126.5 (2С), 127.4, 127.8, 128.2 (2С), 135.4, 137.9.
Спектр ЯМР 1Н (500 МГц, CDCl3, δ, м.д.) 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксирана] (2): 1.26 (дд, 1H, J=14.9 Гц, J=1.9 Гц), 2.19 (дд, 1Н, J=14.9 Гц, J=5.6 Гц), 2.93 (дд, 1Н, J=8.4 Гц, J=2.9 Гц), 3.03 (дд, 1Н, J=6.1 Гц, J=4.1 Гц), 3.12-3.24 (м, 4Н), 3.87 (с, 1Н), 6.18-6.24 (м, 2Н), 7.16-7.20 (м, 2Н), 7.28-7.38 (м, 3Н). Спектр ЯМР 13С (125 МГц, CDCl3, δ, м.д.): 21.7, 30.8, 43.3, 49.2, 51.1, 53.3, 58.4, 62.7, 63.7, 126.4 (2С), 127.8, 128.2, 128.22 (2С), 134.5, 134.7.
Другие примеры, подтверждающие способ, приведены в таблице 1.
ПРИМЕР 3.
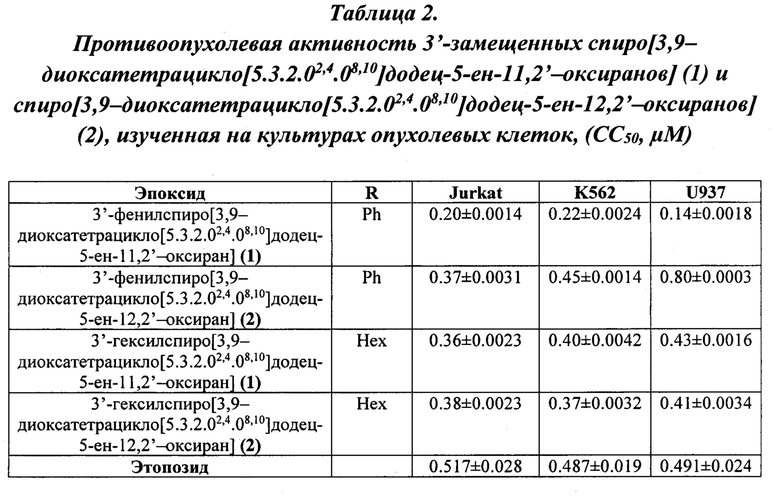
Оценка противоопухолевой активности эпоксидов общей формулы (1) и (2) осуществлена методом проточной цитофлуориметрии, по отношению к трем клеточным линиям: Jurkat, K562 и U937.
Установлено, что цитотоксическая активность имеет выраженный дозозависимый характер. В целом, значение ингибирующей концентрации СС50, полученное в результате экспозиции исследуемых соединений на упомянутых выше клеточных линиях с последующим окрашиванием клеток красителем 7AAD варьируется в зависимости от клеточной культуры в интервале 0,14-0.80 μМ для эпоксидов, где R=Ph; 0,36-0.43 μМ для эпоксидов, где R=Hex. Было установлено, что наибольшую цитотоксическую активность проявляет 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиран] (1) (СС50 0.14±0.0018 - 0.22±0.0024 μМ), и цитотоксичность тетрациклов убывает в ряду Ph (2) < Hex (1) < Hex (2) < Ph (1). При этом эпоксиды, где R=Ph (1), Hex (1), Hex (2) на всех исследуемых опухолевых клеточных линиях проявляют более высокую цитотоксическую активность по сравнению с этопозидом.
Краткое описание чертежей
Рис. 1. Структура 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксирана] (2) в кристалле.
В молекуле соединения (2), согласно рентгеноструктурному анализу, О(1') эпоксидная группа локализована за пределами бициклического каркаса, в то время как O(3) и O(9) эпоксидные группы анти-ориентированы друг относительно друга. К тому же, O(9) группа анти-ориентирована по отношению к двойной связи С(5)-С(6) бициклического каркаса. Молекулы 3'-фенилспиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксирана] (2) стабилизированы в кристалле с помощью бифуркатных С-Н…O межмолекулярных взаимодействий между атомами кислорода эпоксидных групп и атомами водорода бициклического каркаса, что в результате приводит к Pbca пространственной группе.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ АНТИ-3,9,12-ТРИОКСАПЕНТАЦИКЛО[5.3.3.0.0.0]ТРИДЕЦ-5-ЕНОВ, СИН-3,9,12-ТРИОКСАПЕНТАЦИКЛО[5.3.3.0.0.0]ТРИДЕЦ-5-ЕНОВ И 3,6,10-ТРИОКСАПЕНТАЦИКЛО[6.3.2.0.0.0]ТРИДЕЦ-12-ЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2734346C1 |
| СПОСОБ ПОЛУЧЕНИЯ 3,16,19-ТРИОКСАГЕКСАЦИКЛО[10.5.3.0.0.0.0]ИКОС-13-ЕНА, ПРОЯВЛЯЮЩЕГО ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2726355C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-МЕТИЛ-ЗАМЕЩЕННЫХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2735663C1 |
| СПОСОБ ПОЛУЧЕНИЯ (Е)-БИЦИКЛО[4.2.2]ДЕКА-2,4,7-ТРИЕНОВ | 2015 |
|
RU2605428C2 |
| СПОСОБ ПОЛУЧЕНИЯ N-СОДЕРЖАЩИХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2735662C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-АЛКИЛ(ФЕНИЛ)БИЦИКЛО[4.3.1]ДЕКА-2,4,8-ТРИЕН-7,10-ДИОЛОВ И 6-АЛКИЛБИЦИКЛО[4.3.1]ДЕКА-2,4,8-ТРИЕН-7,10-ДИОЛОВ | 2017 |
|
RU2677651C2 |
| СПОСОБ ПОЛУЧЕНИЯ Si-СОДЕРЖАЩИХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ | 2013 |
|
RU2559365C2 |
| СПОСОБ ПОЛУЧЕНИЯ Si-СОДЕРЖАЩИХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2018 |
|
RU2726195C2 |
| АЗАЦИКЛИЧЕСКИЕ СПИРО-СОЕДИНЕНИЯ | 2010 |
|
RU2550495C2 |
| Применение этил 5-арил-4-оксо-2,2,6-трифенил-1-окса-5-азаспиро[2.4]гепт-6-ен-7-карбоксилатов в качестве средств, обладающих антиоксидантной активностью | 2023 |
|
RU2813486C1 |

Изобретение относится к 3'-замещенным спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксиранам] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранам формулы (2), где R = Ph, Hex.
Изобретение также относится к способу совместного получения указанных соединений, который заключается во взаимодействии бицикло[4.2.2]дека-2,4,7-триенов с м-хлорнадбензойной кислотой при температуре 0-40°С, в дихлорметане в течение 3-23 ч. Технический результат – разработан способ получения новых соединений, которые могут найти применение в медицине в качестве биологически активных веществ, обладающих противоопухолевой активностью. 2 н.п. ф-лы, 2 табл., 3 пр., 1 ил.
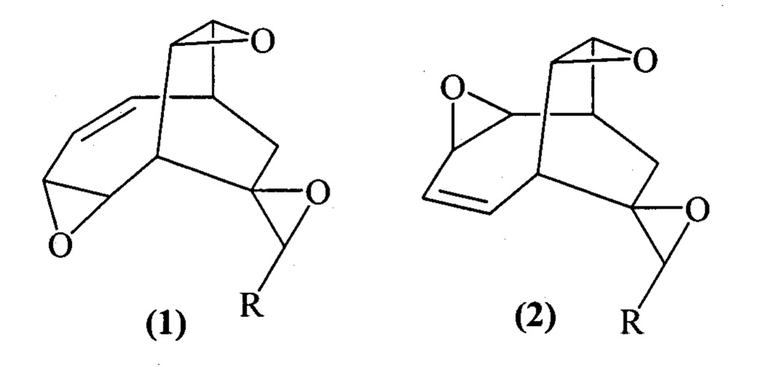
1. Способ совместного получения 3'-замещенных спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2,-оксиранов] формулы (1) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксиранов] формулы (2)
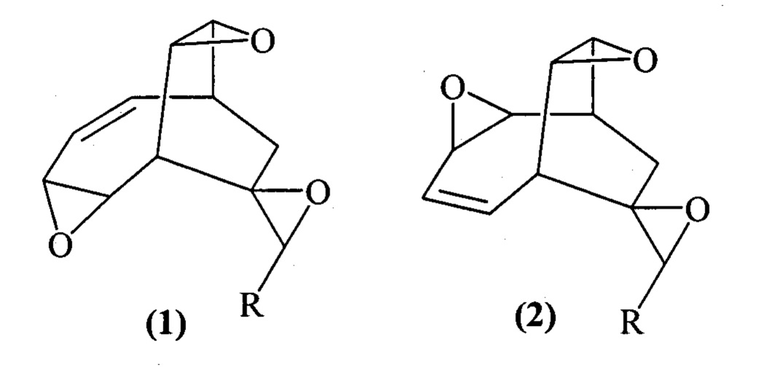
R = Ph, Hex,
отличающийся тем, что бицикло[4.2.2]дека-2,4,7-триены (БДТ) взаимодействуют с м-хлорнадбензойной кислотой (m-СРВА), при мольном соотношении БДТ:m-СРВА = 2:(10-20), при 0-40°С, в дихлорметане, в течение 3-23 ч.
2. 3'-Замещенные спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-11,2'-оксираны] формулы (1) (где R = Ph, Hex) и спиро[3,9-диоксатетрацикло[5.3.2.02,4.08,10]додец-5-ен-12,2'-оксираны] формулы (2) (где R = Ph, Hex), проявляющие противоопухолевую активность
 .
.
| N | |||
| TOSELLI et al | |||
| Org.Chem., vol | |||
| Приспособление в центрифугах для регулирования количества жидкости или газа, оставляемых в обрабатываемом в формах материале, в особенности при пробеливании рафинада | 0 |
|
SU74A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| КОНТРОЛЬНЫЙ ПРИБОР ДЛЯ ПОКАЗАНИЯ КРЕНА САМОЛЕТА | 1926 |
|
SU3783A1 |
| СПОСОБ ПОЛУЧЕНИЯ эндо-, экзо-ТЕТРАЦИКЛО[4.5.1.0.0]ДОДЕЦ-3(4)-ЕН-9-СПИРО-1'-(3'-СЕЛЕНА)ЦИКЛОПЕНТАНОВ | 2008 |
|
RU2404177C2 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ ТЕТРАЦИКЛО[5.4.1.0.0]ДОДЕЦ-3-ЕН-9-СПИРО(3'-ЭТИЛ- 3'-АЛЮМИНАЦИКЛОПЕНТАНА) И ТЕТРАЦИКЛО[5.4.1.0.0]ДОДЕЦ-4-ЕН-9-СПИРО(3'-ЭТИЛ- 3'-АЛЮМИНАЦИКЛОПЕНТАНА) | 2008 |
|
RU2376311C2 |
Авторы
Даты
2020-11-05—Публикация
2019-04-24—Подача