Настоящее изобретение относится к новым (гетеро)арил-замещенным пиперидинильным производным, к способу их получения и к фармацевтическим композициям, содержащим их.
Соединения настоящего изобретения являются новыми и обладают очень ценными фармакологическими характеристиками в области апоптоза и онкологии.
Убиквитинирование является процессом, контролирующим основные клеточные функции, такие как белковый обмен и гомеостаз, активация белка и локализация. Убиквитин представляет собой полипептид из 76 аминокислот, который ковалентно присоединен к посттрансляционно модифицированным белковым субстратам через изопептидную связь. Деубиквитинизирующие ферменты (DUB) в большинстве своем представляют собой цистеинпротеазы, которые расщепляют связь убиквитин-убиквитин или связь убиквитин-белок по Cter глицина убиквитина. Приблизительно 100 DUB регулируют тысячи убиквитинированных белков и даже наблюдается некоторая чрезмерность регуляции субстратов деубиквитиназы.
Дисрегуляцию DUB связывают с несколькими заболеваниями, такими как нейродегенеративные и инфекционные заболевания (Edelman и др., Expert Rev. Mol. Med. 2011, 13, 1-17), и злокачественные новообразования человека (Pal и др., Cancer Res. 2014, 74, 4955-4966). Соответственно, сверхэкспрессию DUB или повышение их активности связывают с многочисленными типами злокачественных заболеваний (Luise и др., Plos One 2011, 6, e15891; Rolen и др., Mol. Carcinog. 2006, 45, 260-269) и неблагоприятным прогнозом.
Убиквитин-специфическая протеаза 7 (USP7), также известная как ассоциированная с вирусом герпеса убиквитин-специфическая протеаза (HAUSP), принадлежит к семейству деубиквитинизирующих ферментов. Сообщается, что USP7 стабилизирует многочисленные онкогены, участвующие в выживании и пролиферации, посредством регуляции прогрессирования клеточного цикла, апоптоза, репарации ДНК, репликации ДНК и эпигенетических факторов (Nicholson и др., Cell Biochem. Biophys. 2011, 60, 61-68). Кроме того, было показано, что USP7 регулирует иммунный ответ посредством воспаления и Treg модуляции (Van Loosdregt и др., Immunity 2013, 39, 259-27; Colleran и др., Proc. Natl. Acad. Sci. USA 2013, 110, 618-623). USP7 также вовлечена в другие патологические состояния, такие как нарушение нервно-психического развития (Нао и др., Mol. Cell 2015, 59, 956-969) и вирусная инфекция (Holowaty и др., Biochem. Soc. Trans. 2004, 32, 731-732).
Сверхэкспрессию USP7 ассоциируют с поздними стадиями злокачественных заболеваний и неблагоприятным прогнозом при раке легких, нейробластоме, миеломе, раке предстательной железы, ободочной кишки и молочной железы. Хотя в литературе были опубликованы некоторые ингибиторы, большинство из них не были селективными и, на сегодняшний день, в клиническую практику ингибиторы USP7 не вошли (Kemp и др., Progress in Medicinal Chemistry 2016, 55, 149-192). Следовательно, существует терапевтическая потребность в соединениях, которые ингибируют активность белка USP7.
Помимо того, что соединения настоящего изобретения являются новыми, они обладают проапоптотическиими и/или антипролиферативными свойствами, что позволяет их применение при патологиях, в которые вовлечен дефект апоптоза, как, например, для лечения злокачественного новообразования и иммунопатологических и аутоиммунных заболеваний.
Более конкретно, настоящее изобретение относится к соединениям формулы (I):
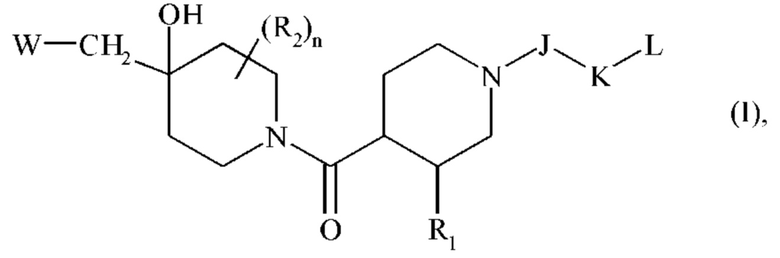
где:
 R1 представляет собой арильную группу или гетероарильную группу,
R1 представляет собой арильную группу или гетероарильную группу,
 R2 представляет собой атом водорода или атом галогена,
R2 представляет собой атом водорода или атом галогена,
 n означает целое число, равное 0, 1 или 2,
n означает целое число, равное 0, 1 или 2,
 J представляет собой -С(О)-группу, -СН(R3)-группу, или -SO2-группу,
J представляет собой -С(О)-группу, -СН(R3)-группу, или -SO2-группу,
 R3 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R3 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
 K представляет собой связь или -Cy1-группу,
K представляет собой связь или -Cy1-группу,
 L представляет собой -Су2 группу или -СН2-Су2 группу,
L представляет собой -Су2 группу или -СН2-Су2 группу,
 W представляет собой группу
W представляет собой группу
 , где:
, где:
 А представляет собой гетероарильное кольцо,
А представляет собой гетероарильное кольцо,
 X представляет собой атом углерода или атом азота,
X представляет собой атом углерода или атом азота,
 R4 представляет собой атом водорода, атом галогена, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, -Y1-N6R7 группу, -Y1-OR6 группу, линейную или разветвленную галоген(С1-С6)алкильную группу, оксо группу, -Y1-Су3 группу, -Су3-R7 группу, -Су3-OR7 группу, или -Y1-NR6-C(O)-R7 группу,
R4 представляет собой атом водорода, атом галогена, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, -Y1-N6R7 группу, -Y1-OR6 группу, линейную или разветвленную галоген(С1-С6)алкильную группу, оксо группу, -Y1-Су3 группу, -Су3-R7 группу, -Су3-OR7 группу, или -Y1-NR6-C(O)-R7 группу,
 R5 представляет собой атом водорода, атом галогена, или линейную или разветвленную (С1-С6)алкильную группу,
R5 представляет собой атом водорода, атом галогена, или линейную или разветвленную (С1-С6)алкильную группу,
 R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
 R7 представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, или -Y2-Cy4 группу,
R7 представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, или -Y2-Cy4 группу,
 Y1 и Y2 независимо друг от друга представляют собой связь или линейную или разветвленную (С1-С4)алкиленовую группу,
Y1 и Y2 независимо друг от друга представляют собой связь или линейную или разветвленную (С1-С4)алкиленовую группу,
 Cy1 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу, или гетероарильную группу, которая присоединена к группе J и к группе L,
Cy1 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу, или гетероарильную группу, которая присоединена к группе J и к группе L,
 Су2, Су3 и Су4 независимо друг от друга, представляют собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу, или гетероарильную группу,
Су2, Су3 и Су4 независимо друг от друга, представляют собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу, или гетероарильную группу,
при этом следует понимать, что:
- "арил" означает фенильную, нафтильную или инданильную группу,
- "гетероарил" означает любую моно- или конденсированную бициклическую группу, состоящую из 5-10 кольцевых членов, содержащую по меньшей мере один ароматический фрагмент и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы и азота,
- "циклоалкил" означает любую моно- или конденсированную бициклическую неароматическую карбоциклическую группу, содержащую от 3 до 7 кольцевых членов,
- "гетероциклоалкил" означает любую неароматическую моно- или конденсированную бициклическую группу, содержащую от 3 до 10 кольцевых членов и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы и азота,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, определенные таким образом, могут быть замещены 1-4 группами, выбранными из линейного или разветвленного (C1-С6)алкила, линейного или разветвленного (С2-С6)алкенила, линейного или разветвленного (С2-С6)алкинила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', -Y1-S(O)m-R', оксо (или N-оксида, в соответствующих случаях), нитро, циано, -C(O)-R', -C(O)-OR', -O-C(O)-R', -C(O)-NR'R'', -Y1-NR'-C(O)-R'', -Y1-NR'-C(O)-OR'', галогена, циклопропила, и пиридинила, который может быть замещен линейной или разветвленной (C1-С6)алкильной группой,
при этом следует понимать, что R' и R'' независимо друг от друга, представляют собой атом водорода, линейную или разветвленную (C1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С1-С6)алкокси группу, линейную или разветвленную галоген(С1-С6)алкильную группу, линейную или разветвленную гидрокси(С1-С6)алкильную группу, линейную или разветвленную (C1-С6)алкокси(С1-С6)алкильную группу, фенильную группу, циклопропилметильную группу, тетрагидропиранильную группу,
или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота, при этом следует понимать, что второй рассматриваемый азот может быть замещен 1-2 группами, представляющими собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
и при этом следует понимать, что m означает целое число, равное 0, 1 или 2,
их энантиомерам, диастереоизомерам и их солям присоединения с фармацевтически приемлемой кислотой или основанием.
Среди фармацевтически приемлемых кислот могут быть упомянуты, не подразумевая каких-либо ограничений, хлористоводородная кислота, бромистоводородная кислота, серная кислота, фосфоновая кислота, уксусная кислота, трифторуксусная кислота, молочная кислота, пировиноградная кислота, малоновая кислота, янтарная кислота, глутаровая кислота, фумаровая кислота, винная кислота, малеиновая кислота, лимонная кислота, аскорбиновая кислота, щавелевая кислота, метансульфоновая кислота, камфорная кислота и т.д.
Среди фармацевтически приемлемых оснований могут быть упомянуты, не подразумевая каких-либо ограничений, гидроксид натрия, гидроксид калия, триэтиламин, трет-бутиламин и т.д.
Среди гетероарильных групп могут быть упомянуты, не подразумевая каких-либо ограничений, пирролил, фурил, тиенил, тиазолил, изотиазолил, оксазолил, изоксазолил, пиразолил, имидазолил, пиридинил (также известный как пиридил), пиразинил, пиридазинил, пиримидинил, пиридинонил, индолил, дигидроиндолил, дигидроизоиндолил, индазолил, дигидроциклопентатиенил, бензотиенил, тетрагидробензотиенил, бензофуранил, имидазопиридинил, бензотриазолил, бензодиоксолил, дигидробензодиоксинил, хинолинил, изохинолинил, тетрагидрохинолинил, тетрагидроизохинолинил, хиноксалинил, дигидрохиноксалинил, дигидротиенодиоксинил, хиназолинонил, пирролопиридазинил, дигидропирролизинил, тетрагидроиндолизинил, и т.д.
Среди циклоалкильных групп могут быть упомянуты, не подразумевая каких-либо ограничений, циклопропил, циклобутил, циклопентил, циклогексил, и т.д.
Среди гетероциклоалкильных групп могут быть упомянуты, не подразумевая каких-либо ограничений, пирролидинил, тетрагидропиранил, пиперидинил, пиперазинил, морфолинил, и т.д.
В другом варианте осуществления изобретения, W предпочтительно представляет собой группу
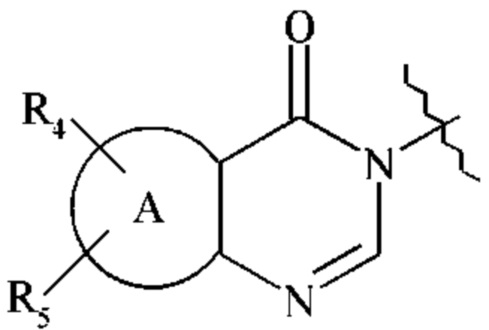 , где R4, R5 и А являются такими, как определено для формулы (I).
, где R4, R5 и А являются такими, как определено для формулы (I).
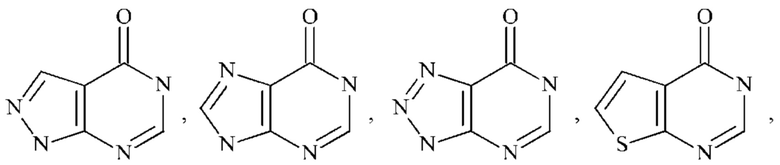
Более конкретно, 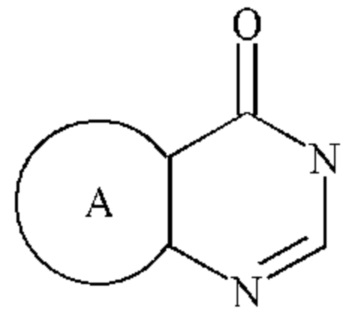 представляет собой
представляет собой 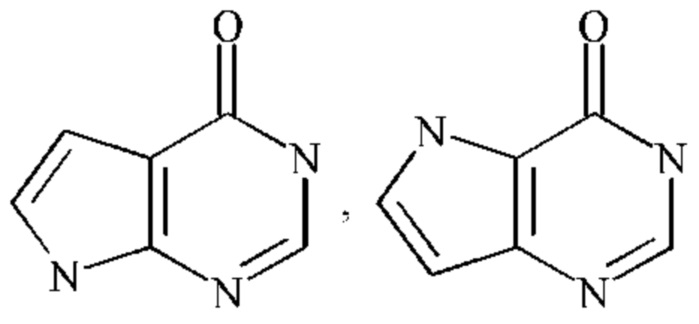 ,
, 
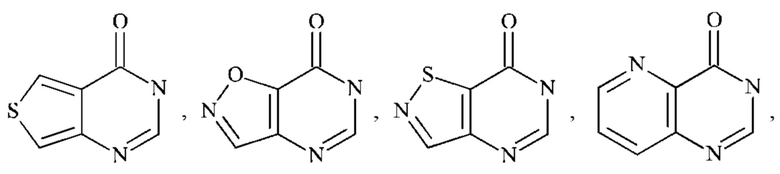
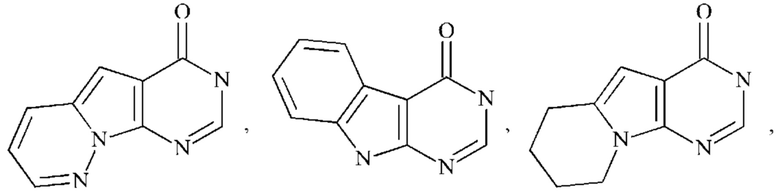
или 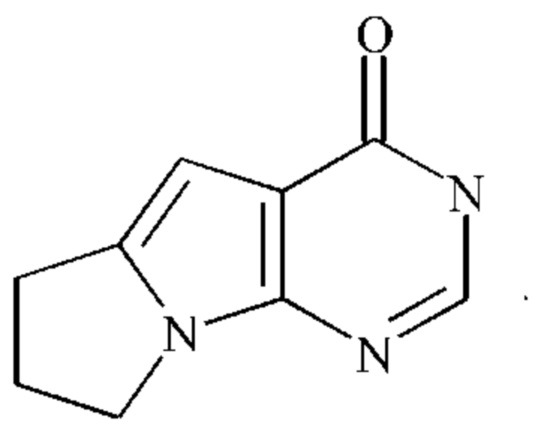
В частности,  представляет собой
представляет собой  ,
, 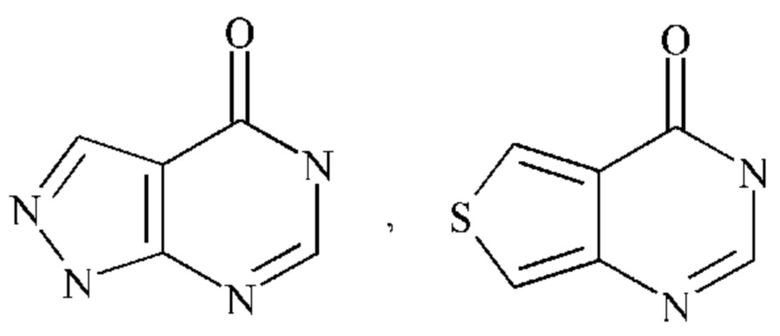 , или
, или 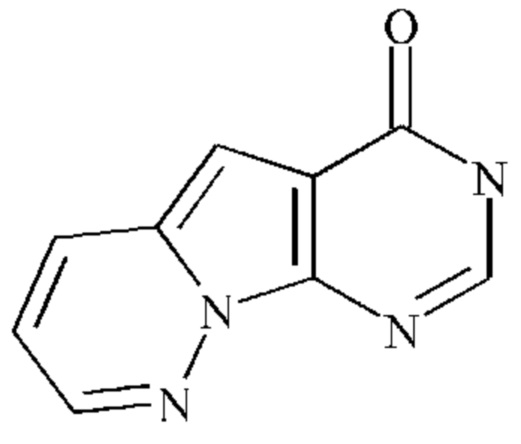 .
.
Выгодно, если 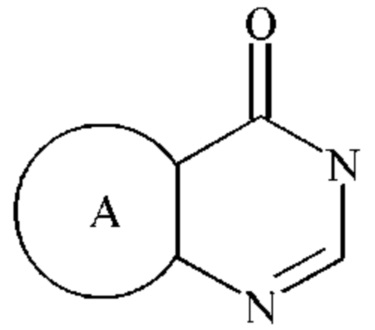 представляет собой
представляет собой 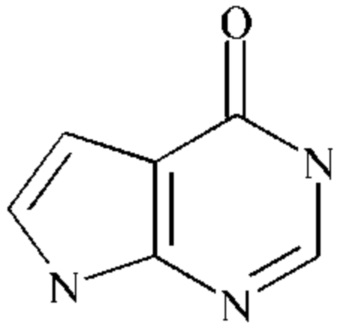 ,
,
Предпочтительно, 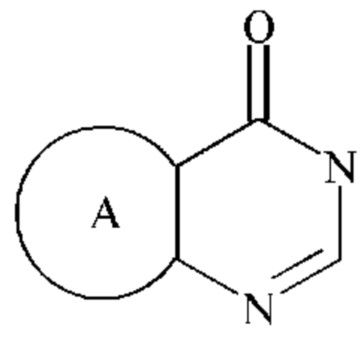 представляет собой
представляет собой 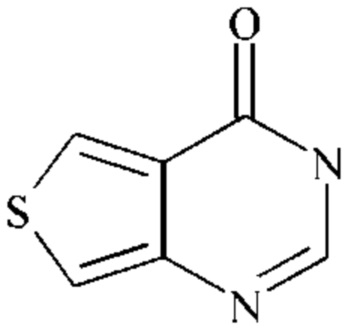 .
.
В другом варианте осуществления изобретения, W предпочтительно представляет собой группу
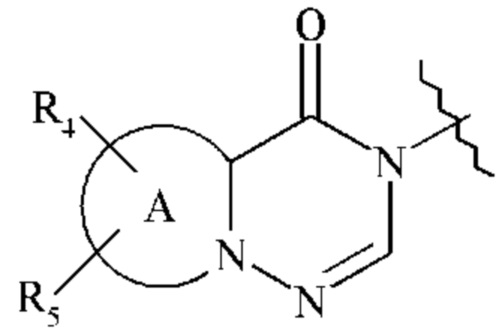 , где R4, R5 и А являются такими, как определено для формулы (I).
, где R4, R5 и А являются такими, как определено для формулы (I).
Более конкретно, 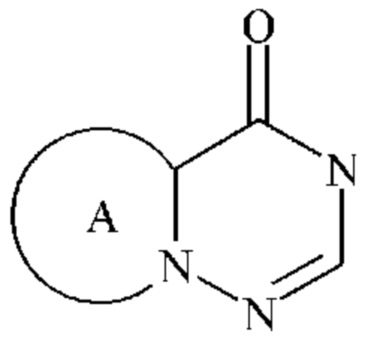 представляет собой
представляет собой  .
.
R1 предпочтительно представляет собой фенильную группу или тиенильную группу. Более предпочтительно, R1 представляет собой фенильную группу.
Предпочтительно, соединения формулы (I) демонстрируют транс-конфигурацию, как указано ниже:
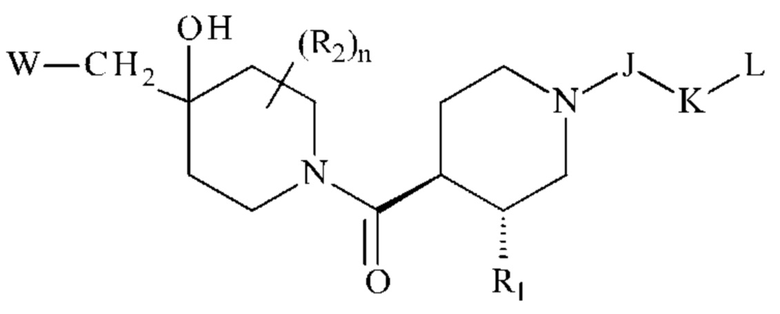
или
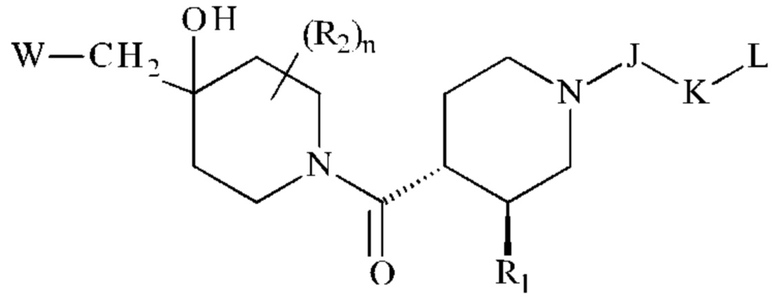
Более предпочтительно, соединения формулы (I) демонстрируют транс-конфигурацию, как указано ниже:
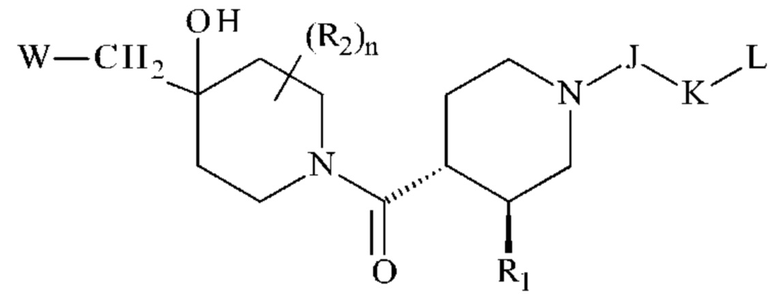
Предпочтительно, R2 представляет собой атом водорода или атом фтора. Более предпочтительно,
R2 представляет собой атом водорода. Предпочтительно, -(R2)n группа представляет собой гем-дифтор группу.
В некоторых предпочтительных вариантах осуществления изобретения, R3 представляет собой атом водорода или метильную группу. Более предпочтительно, R3 представляет собой атом водорода.
В предпочтительных соединениях изобретения, J представляет собой -С(О)-группу или -СН2-группу. Предпочтительно, J представляет собой -С(О)-группу. Предпочтительно, J представляет собой -СН2-группу.
К предпочтительно представляет собой связь или -Cy1- группу, выбранную из фенильной группы, пирролильной группы, тиенильной группы, тиазолильной группы, пиридинильной группы, тетрагидробензотиенильной группы, дигидротиенодиоксинильной группы, циклопропильной группы, циклобутильной группы, или пирролидинильной группы. Более предпочтительно, K предпочтительно представляет собой связь или -Cy1-группу, выбранную из тиенильной группы, тиазолильной группы или пиридинильной группы.
Предпочтительно, L представляет собой -Су2 группу. Более предпочтительно, Су2 представляет собой фенильную группу, инданильную группу, пирролильную группу, фурильную группу, тиенильную группу, тиазолильную группу, изотиазолильную группу, оксазолильную группу, изоксазолильную группу, пиразолильную группу, пиридинильную группу, пиразинильную группу, пиридазинильную группу, пиримидинильную группу, пиридинонильную группу, индолильную группу, дигидроиндолильную группу, дигидроизоиндолильную группу, индазолильную группу, дигидроциклопентатиенильную группу, тетрагидробензотиенильную группу, бензофуранильную группу, имидазопиридинильную группу, бензотриазолильную группу, бензодиоксолильную группу, дигидробензодиоксинильную группу, хинолинильную группу, тетрагидрохинолинильную группу, тетрагидроизохинолинильную группу, хиноксалинильную группу, дигидрохиноксалинильную группу, хиназолинонильную группу, или пирролидинильную группу. Еще более предпочтительно, Су2 представляет собой фенильную группу, пирролильную группу, фурильную группу, тиенильную группу, тиазолильную группу, оксазолильную группу, изоксазолильную группу, пиразолильную группу, пиридинильную группу, пиразинильную группу, пиридазинильную группу, пиримидинильную группу, или имидазопиридинильную группу.
Предпочтительно, Су2 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу, или гетероарильную группу, которые замещены 1 или 2 группами, выбранными из линейного или разветвленного (С1-С6)алкила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', N-оксида, циано, -C(O)-OR', -C(O)-NR'R'', галогена, где R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С1-С6)алкокси группу, тетрагидропиранильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота, при этом следует понимать, что второй рассматриваемый азот может быть замещен линейной или разветвленной (С1-С6)алкильной группой.
В некоторых предпочтительных вариантах осуществления изобретения, K представляет собой тиенильную группу, тиазолильную группу или пиридинильную группу и L представляет собой пирролильную группу, фурильную группу, тиенильную группу, пиразолильную группу, пиридинильную группу, пиримидинильную группу, или имидазопиридинильную группу, причем каждая указанная гетероарильная группа может быть замещена 1 или 2 группами, выбранными из линейного или разветвленного (С1-С6)алкила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', N-оксида, циано, -C(O)-NR'R'', галогена, где R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (C1-С6)алкильную группу, линейную или разветвленную (С1-С6)алкокси группу, линейную или разветвленную (С1-С6)алкокси(С1-С6)алкильную группу, тетрагидропиранильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота. Более предпочтительно, K представляет собой тиазолильную группу и L представляет собой пиридинильную группу.
Другими соединениями изобретения, которым отдают предпочтение, являются соединения, где K представляет собой связь и L представляет собой фенильную группу, тиазолильную группу, оксазолильную группу, изоксазолильную группу, пиразолильную группу, пиридинильную группу, пиразинильную группу, пиридазинильную группу или пиримидинильную группу, причем каждая указанная группа может быть замещена 1 или 2 группами, выбранными из линейного или разветвленного (С1-С6)алкила, -Y1-OR', -Y1-NR'R'', циано, -C(O)-OR', галогена, при этом следует понимать, что R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота, при этом следует понимать, что второй рассматриваемый азот может быть замещен 1-2 группами, представляющими собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу.
В предпочтительном варианте осуществления, -J-K-L группу, присоединенную к пиперидинильномк кольцу, определяют таким образом, что J представляет собой -С(О)-группу, К представляет собой -Cy1- группу и L представляет собой -Су2 группу.
В другом предпочтительном варианте осуществления, -J-K-L группу определяют таким образом, что J представляет собой -СН2-группу, K представляет собой связь и L представляет собой -Су2 группу.
В другом предпочтительном варианте осуществления, -J-K-L группу определяют таким образом, что J представляет собой -С(О)-группу, K представляет собой связь и L представляет собой -Су2 группу.
В другом предпочтительном варианте осуществления, -J-K-L группу определяют таким образом, что J представляет собой -СН2-группу, K представляет собой -Cy1-группу и L представляет собой -Су2 группу.
В предпочтительных соединениях изобретения, R4 представляет собой атом галогена, линейную или разветвленную (С1-С6)алкильную группу, или -Y1-Су3 группу. Предпочтительно, R4 представляет собой атом брома, метильную группу, или -Су3 группу.
Предпочтительно, Су3 представляет собой фенильную группу, нафтильную группу, пирролильную группу, фурильную группу, тиенильную группу, тиазолильную группу, пиразолильную группу, имидазолильную группу, пиридинильную группу, пиримидинильную группу, пиридинонильную группу, индолильную группу, бензодиоксолильную группу, дигидробензодиоксинильную группу, циклопропильную группу, циклобутильную группу, циклопентильную группу, циклогексильную группу, пирролидинильную группу, тетрагидропиранильную группу, или пиперидинильную группу.
Су3 предпочтительно представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу, или гетероарильную группу, которая замещена 1-3 группами, выбранными из линейного или разветвленного (С1-С6)алкила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', циано, галогена, где R' и R'' независимо друг от друга представляют собой атом водорода или линейную или разветвленную (C1-С6)алкильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота.
Предпочтительно, R5 представляет собой атом водорода или метальную группу. Более предпочтительно, R5 представляет собой атом водорода.
В предпочтительных соединениях изобретения, R6 представляет собой атом водорода или метильную группу.
R7 предпочтительно представляет собой атом водорода, метильную группу, или -СН2-Су4 группу.
Предпочтительно, Су4 представляет собой фенильную группу или дигидроиндолильную группу.
Предпочтительными соединениями изобретения являются:
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(нафталин-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(фуран-3-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(2-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(2-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[4-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(4-метилпиперазин-1-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1H-пиррол-1-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-карбонитрил;
- 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(морфолин-4-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлорфенил)-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-6,8-диметилпиримидо[5',4':4,5]пирроло[1,2-b]пиридазин-4(3H)-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метил-1-оксидопиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(пиперазин-1-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d|пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3,4-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбонитрил;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-фенил-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 4-{3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-4-оксо-3,4-дигидро-7H-пирроло[2,3-d]пиримидин-7-ил}бензонитрил;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1H-пиразол-4-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1H-пиразол-4-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[3-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-фенил-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1H-пиразол-4-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-бром-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]пирроло[2,1-f][1,2,4]триазин-4(3H)-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[4-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4(3H)-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4(3H)-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилтиено[3,4-d]пиримидин-4(3H)-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилтиено[3,4-d]пиримидин-4(3H)-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,5-дигидро-4H-пирроло[3,2-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,5-дигидро-4H-пирроло[3,2-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,5-дигидро-4H-пирроло[3,2-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[1-(дифторметил)-1H-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[1-(дифторметил)-1H-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метил-3H-имидазо[4,5-b]пиридин-6-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[2-(5-фтор-6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-3-карбоксамид;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[5-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(тетрагидро-2H-пиран-4-илокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[2-(5-амино-6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(2-бромпиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3 -метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-5-ил)-1,3 -тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3H,4H)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d|пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-3-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(6'-метил-3,3'-бипиридин-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-4-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(3-метоксифенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
- 5-[5-({(3R,4R)-4-[(4-{[7-(4-хлорфенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
- 5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(морфолин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(2-метоксиэтокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(4-метилпиперазин-1-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(2-хлор-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-[5-({(3R,4R)-4-[(4-{[7-(4-фторфенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
- метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат;
- 5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-(4-метоксифенил)-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-(4-метоксифенил)-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 5-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-(4-метоксифенил)-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(2-{6-[(2-метоксиэтил)амино]пиридин-3-ил}-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1H-пиразол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-3-карбоксилат;
- 1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-оксазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[1-({(3R,4R)-1-[(2,4-диметил-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-(1,3-оксазол-4-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-оксазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3R-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}пиридин-2-карбонитрил;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]пирроло[2,1-f][1,2,4]триазин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]тиено[3,4-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(3-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[3,3-дифтор-4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[3,3-дифтор-4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3 -фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метоксипиридазин-3-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он.
Изобретение также относится к способу получения соединений формулы (I), который отличается тем, что в качестве исходного вещества применяют соединение формулы (II):
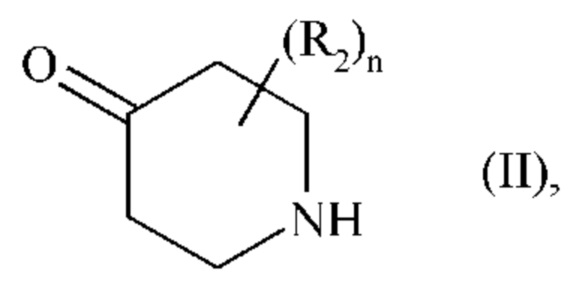
где R2 и n являются такими, как определено для формулы (I), которое подвергают сочетанию с соединением формулы (III):
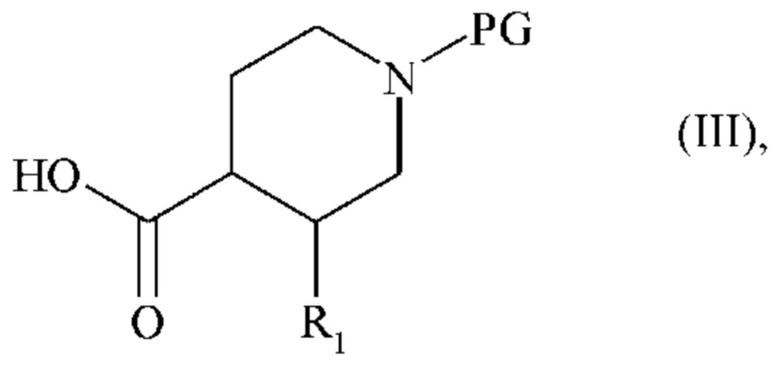
где R1 является таким, как определено для формулы (I), и PG представляет собой защитную группу аминной функции, с получением соединения формулы (IV):
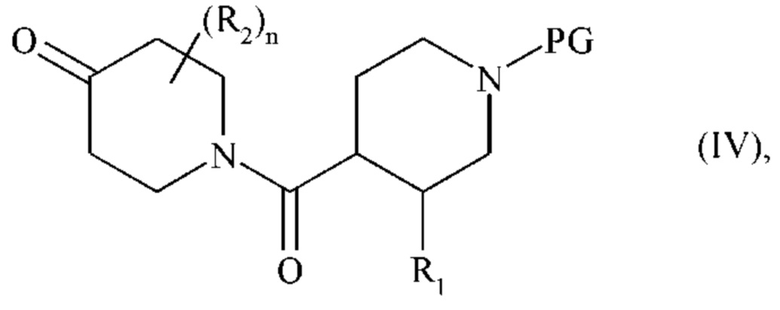
где R1, R2, n и PG являются такими, как определено выше, соединение формулы (IV) затем превращают в эпоксидное соединение формулы (V):

где R1, R2, n и PG являются такими, как определено выше, соединение формулы (V) затем подвергают сочетанию с соединением формулы (VI):

где W является таким, как определено для формулы (I), с получением соединения формулы (VII):
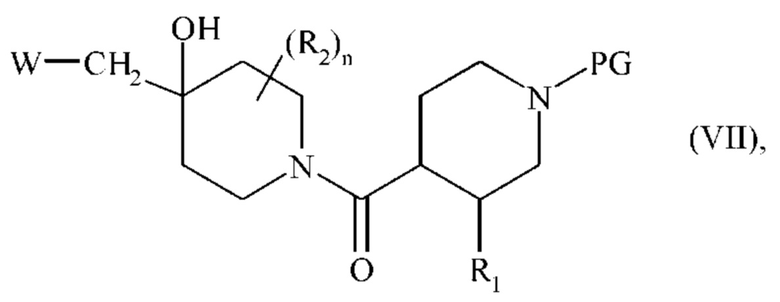
где R1, R2, n, W и PG являются такими, как определено выше, соединение формулы (VII), после реакции удаления защитной группы PG, затем подвергают:
 либо сочетанию с соединением формулы (VIII):
либо сочетанию с соединением формулы (VIII):
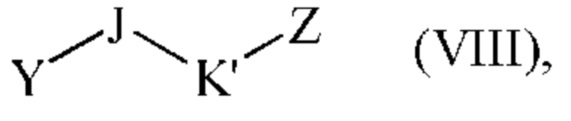
где J является таким, как определено для формулы (I), K' представляет собой -Cy1- группу, Y представляет собой гидрокси группу или атом галогена, и Z представляет собой атом галогена,
с получением соединения формулы (IX):

где R1, R2, J, K', n, W и Z являются такими, как определено выше, и соединение формулы (IX) затем подвергают сочетанию с соединением формулы (X):
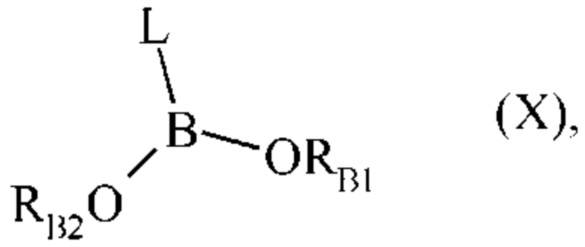
где L является таким, как определено для формулы (I), и RB1 и RB2 представляют собой атом водорода, линейную или разветвленную (C1-С6) алкильную группу, или RB1 и RB2 соединены линейной или разветвленной (С2-С6)алкиленовой группой,
с получением соединения формулы (I-а), частного случая соединений формулы (I):
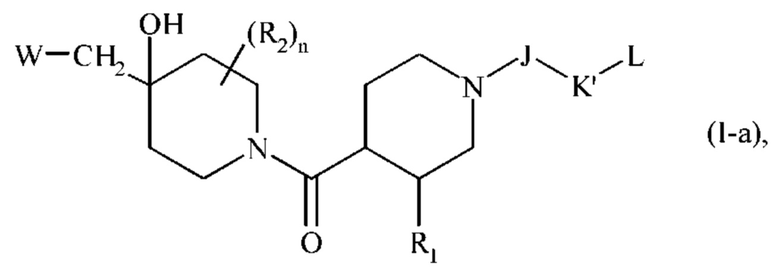
где R1, R2, J, K', L, n и W являются такими, как определено выше,
 либо сочетанию с соединением формулы (XI):
либо сочетанию с соединением формулы (XI):
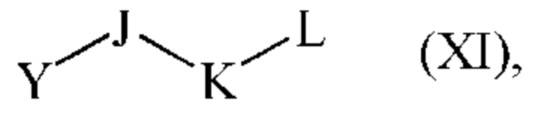
где J, K и L являются такими, как определено для формулы (I), и Y представляет собой гидрокси группу или атом галогена, с получением соединения формулы (I),
соединение формулы (I) или соединение формулы (I-а), которое является частным случаем соединения формулы (I), затем можно очистить в соответствии с обычными методиками разделения, превратить, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием и необязательно разделить на его изомеры в соответствии с обычными методиками разделения,
при этом следует понимать, что в любое время, признанное подходящим в ходе описанного выше способа, некоторые группы (гидрокси, амино …) исходных реагентов или промежуточных соединений синтеза могут быть защищены, впоследствии лишены защиты и функционализированы, как того требует синтез.
В другом варианте осуществления изобретения, соединения формулы (I) можно получить, используя альтернативный способ, который отличается тем, что в качестве исходного вещества применяют соединение формулы (XII):
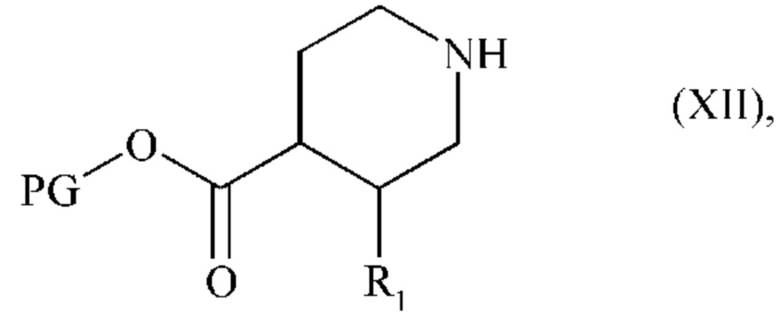
где R1 является таким, как определено для формулы (I), и PG представляет собой защитную группу функции карбоновой кислоты, которое подвергают:
 либо сочетанию с соединением формулы (VIII):
либо сочетанию с соединением формулы (VIII):
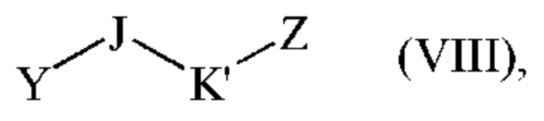
где J является таким, как определено для формулы (I), K' представляет собой -Cy1- группу, Y представляет собой гидрокси группу или атом галогена, и Z представляет собой атом галогена,
с получением соединения формулы (XIII):
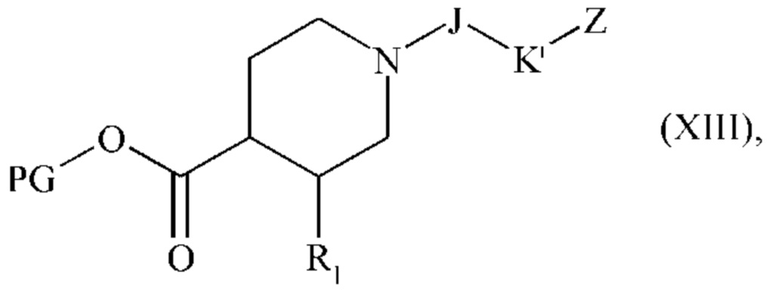
где R1, J, K', Z и PG являются такими, как определено выше, и
соединение формулы (XIII) затем подвергают сочетанию с соединением формулы (X):
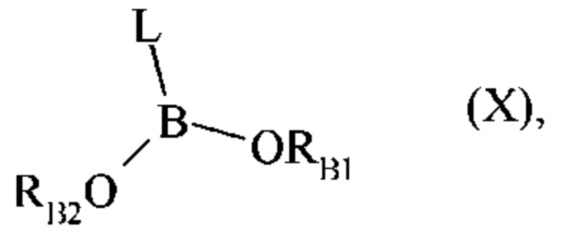
где L является таким, как определено для формулы (I), и RB1 и RB2 представляют собой атом водорода, линейную или разветвленную (C1-С6) алкильную группу, или RB1 и RB2 соединены линейной или разветвленной (С2-С6)алкиленовой группой,
с получением соединения формулы (XIV):
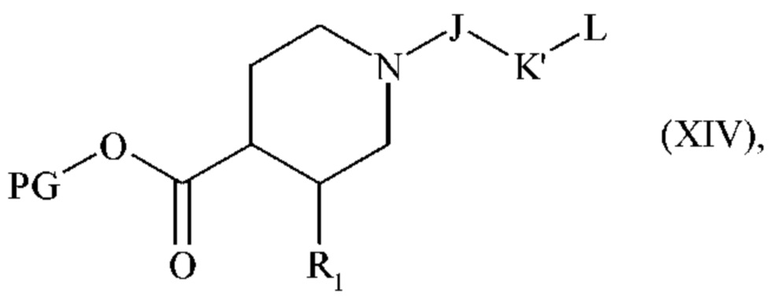
где R1, J, K', L и PG являются такими, как определено выше,
 либо сочетанию с соединением формулы (XI):
либо сочетанию с соединением формулы (XI):
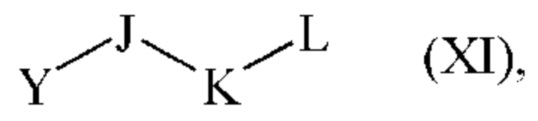
где J, K и L являются такими, как определено для формулы (I), и Y представляет собой гидрокси группу или атом галогена,
с получением соединения формулы (XV),

где R1, J, K, L и PG являются такими, как определено выше,
соединения формул (XIV) и (XV), после реакции удаления защитной группы PG, затем подвергают сочетанию с соединением формулы (II), с получением соединения формулы (XVI):
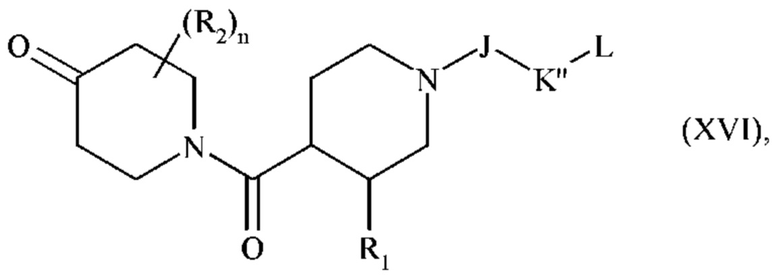
где R1, R2, J, L и n являются такими, как определено выше, и K'' означает либо K', либо K, как определено выше,
соединение формулы (XVI) затем превращают в эпоксидное соединение формулы (XVII):
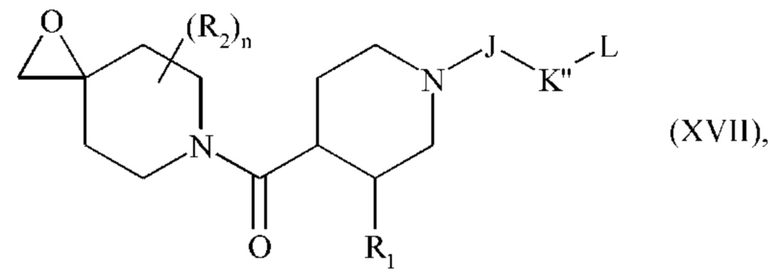
где R1, R2, J, K'', L и n являются такими, как определено выше, и
соединение формулы (XVII) затем подвергают сочетанию с соединением формулы (VI):

где W является таким, как определено для формулы (I),
с получением соединения формулы (I), которое можно очистить в соответствии с обычными методиками разделения, превратить, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием и необязательно разделить на его изомеры в соответствии с обычными методиками разделения,
при этом следует понимать, что в любое время, признанное подходящим в ходе описанного выше способа, некоторые группы (гидрокси, амино …) исходных реагентов или промежуточных соединений синтеза могут быть защищены, впоследствии лишены защиты и функционализированы, как того требует синтез.
Соединения формул (II), (III), (VI), (VIII), (X), (XI) и (XII) либо доступны для приобретения, либо могут быть получены специалистом в данной области техники с использованием обычных химических реакций, описанных в литературе.
Фармакологические исследования соединений изобретения показали проапоптотические и/или антипролиферативные свойства. Способность реактивировать апоптотический процесс в раковых клетках представляет большой терапевтический интерес для лечения злокачественных заболеваний и иммунопатологических и аутоиммунных заболеваний.
Среди намеченных противоопухолевых терапий могут быть упомянуты, не подразумевая каких-либо ограничений, терапия рака мочевого пузыря, головного мозга, молочной железы и матки, хронического лимфоидного лейкоза, рака ободочной кишки, пищевода и печени, лимфобластного лейкоза, острого миелоидного лейкоза, лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы, рака поджелудочной железы и мелкоклеточного рака легкого. Более конкретно, соединения в соответствии с изобретением будут полезными при лечении резистентных к химиотерапии, таргетной терапии или радиотерапии злокачественных заболеваний.
Настоящее изобретение также относится к фармацевтическим композициям, содержащим по меньшей мере одно соединение формулы (I) в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
Среди фармацевтических композиций в соответствии с изобретением могут быть упомянуты более конкретно те, которые подходят для перорального, парентерального, назального, чрес- или транскожного, ректального, перлингвального, офтальмологического или респираторного введения, в особенности таблетки или драже, сублингвальные таблетки, саше, пакетики, капсулы, глоссеты, пастилки, суппозитории, кремы, мази, гели для кожи и питьевые или инъекционные ампулы.
Фармацевтические композиции в соответствии с изобретением содержат один или несколько наполнителей или носителей, выбранных из разбавителей, смазывающих веществ, связующих, разрыхляющих средств, стабилизаторов, консервантов, абсорбентов, красителей, подсластителей, отдушек и т.д. В качестве неограничивающего примера могут быть упомянуты:
 в качестве разбавителей: лактоза, декстроза, сахароза, маннит, сорбит, целлюлоза, глицерин,
в качестве разбавителей: лактоза, декстроза, сахароза, маннит, сорбит, целлюлоза, глицерин,
 в качестве смазывающих веществ: кремнезем, тальк, стеариновая кислота и ее магниевые и кальциевые соли, полиэтиленгликоль,
в качестве смазывающих веществ: кремнезем, тальк, стеариновая кислота и ее магниевые и кальциевые соли, полиэтиленгликоль,
 в качестве связующих: силикат магния-алюминия, крахмал, желатин, трагакант, метилцеллюлоза, натрий-карбоксиметилцеллюлоза и поливинилпирролидон,
в качестве связующих: силикат магния-алюминия, крахмал, желатин, трагакант, метилцеллюлоза, натрий-карбоксиметилцеллюлоза и поливинилпирролидон,
 в качестве разрыхлителей: агар, альгиновая кислота и его натриевая соль, шипучие смеси.
в качестве разрыхлителей: агар, альгиновая кислота и его натриевая соль, шипучие смеси.
Дозировка варьируется в зависимости от пола, возраста и веса пациента, пути введения, природы терапевтического показания, или каких-либо сопутствующих лечений, и находится в диапазоне от 0.01 мг до 1 г в 24 часа за одно или несколько введений.
Кроме того, настоящее изобретение также относится к комбинации соединения формулы (I) с противоопухолевыми средствами, выбранными из генотоксичных средств, митотических ядов, антиметаболитов, ингибиторов протеасом, ингибиторов киназ, ингибиторов белок-белкового взаимодействия, иммуномодуляторов, ингибиторов Е3 лигазы, терапии с использованием Т-клеток с химерными антигенными рецепторами и антител, а также к фармацевтическим композициям, содержащим такой тип комбинации, и их применению для изготовления лекарственных средств для применения для лечения злокачественного новообразования.
Комбинацию соединения формулы (I) с противоопухолевым средством можно вводить одновременно или последовательно. Предпочтительным путем введения является пероральный, причем соответствующие фармацевтические композиции могут обеспечивать незамедлительное или отсроченное высвобождение активных компонентов. Кроме того, соединения комбинации можно вводить в виде двух отдельных фармацевтических композиций, каждая из которых содержит один из активных компонентов, или в виде одной фармацевтической композиции, в которой активные компоненты находятся в смеси.
Для лечения злокачественного новообразования соединения формулы (I) также можно применять в комбинации с радиотерапией.
Следующие Синтезы и Примеры иллюстрируют изобретение, но не ограничивают его каким-либо образом.
Общие методики
Все реагенты, полученные из коммерческих источников, использовали без дополнительной очистки. Безводные растворители получали из коммерческих источников и использовали без дополнительной сушки.
Флэш-хроматографию выполняли на приборе ISCO CombiFlash Rf 200i с предварительно заправленными силикагелевыми картриджами (RediSep®Rf Gold High Performance).
Тонкослойную хроматографию проводили на 5×10 см пластинах, покрытых силикагелем Merck Туре 60 F254.
Нагревание микроволновым излучением выполняли в приборе Anton Parr MonoWave или СЕМ Discover.
Операции очистки с помощью препаративной ВЭЖХ выполняли на системе HANBON NP7000 Liquid Chromatography с Gemini-NX® 5 мкм С18, 250 мм × 50 мм в.д. колонкой, работая при скорости потока 99.9 мл мин-1 с УФ детектированием на диодной матрице (210-400 нм), используя 5 мМ водный NH4HCO3 раствор и MeCN в качестве элюентов, если не указано иное.
Аналитическая ЖХ-МС: соединения настоящего изобретения характеризовали с помощью высокоэффективной жидкостной хроматографии - масс-спектроскопии (ВЭЖХ-МС) на приборе Agilent HP 1200 с Agilent 6140 квадрупольным ЖХ/МС, работая с электрораспылительной ионизацией в режиме положительных или отрицательных ионов. Диапазон сканирования молекулярных масс составлял от 100 до 1350. Параллельное УФ-детектирование проводили на 210 нм и 254 нм. Образцы вводили в виде 1 мМ раствора в MeCN, или в смеси ТГФ/H2O (1:1) с помощью 5 мкл петлевого дозатора. ЖХМС анализы выполняли на двух приборах, один из которых работал с основными, а другой с кислыми элюентами.
Основная ЖХМС: Gemini-NX, 3 мкм, С18, 50 мм × 3.00 мм в.д. колонка при 23°С, при скорости потока 1 мл мин-1, используя 5 мМ бикарбонат аммония (Растворитель А) и ацетонитрил (Растворитель В) с градиентом, начиная со 100%-ного Растворителя А и завершая 100%-ным Растворителем В в течение различных/определенных промежутков времени.
Кислая ЖХМС: Z ORBAX Eclipse XDB-C18, 1.8 мкм, 50 мм × 4.6 мм в.д. колонка при 40°С, при скорости потока 1 мл мин-1, используя 0.02% об./об. водную муравьиную кислоту (Растворитель А) и 0.02% об./об. муравьиную кислоту в ацетонитриле (Растворитель В) с градиентом, начиная со 100%-ного Растворителя А и завершая 100%-ным Растворителем В в течение различных/определенных промежутков времени.
1H-ЯМР исследования выполняли на спектрометре Bruker Avance III 500 МГц и спектрометре Bruker Avance III 400 МГц, используя ДМСО-d6 или CDCl3 в качестве растворителя. 1H ЯМР данные представлены в виде дельта-значений, приведенных в миллионных долях (м.д.), с использованием остаточного пика растворителя (2.50 м.д. для ДМСО-d6 и 7.26 м.д. для CDCl3) в качестве внутреннего стандарта. Картины расщепления обозначены в виде: s (синглет), d (дублет), t (триплет), q (квартет), quint (квинтет), sept (септет), m (мультиплет), brs (широкий синглет), brd (широкий дублет), brt (широкий триплет), brq (широкий квартет), brm (широкий мультиплет), vbrs (очень широкий синглет), dd (дублет дублетов), td (триплет дублетов), dt (дублет триплетов), dq (дублет квартетов), ddd (дублет дублета дублетов), dm (дублет мультиплетов), tm (триплет мультиплетов), qm (квартет мультиплетов).
Газовую хроматографию, комбинированную с масс-спектрометрией низкого разрешения, выполняли на газовом хроматографе Agilent 6850 и масс-спектрометре Agilent 5975С, используя 15 м × 0.25 мм колонку с 0.25 мкм покрытием HP-5MS и гелием в качестве газа-носителя. Источник ионов: EI+, 70 эВ, 230°С, квадруполь: 150°С, интерфейс: 300°С.
Данные МСВР определяли на приборе Shimadzu IT-TOF, температура источника ионов 200°С, ESI +/-, напряжение ионизации: (+-)4.5 кВ. Разрешение по массам мин. 10000.
Элементарные анализы выполняли на элементном анализаторе Thermo Flash ЕА 1112.


Общая методика 1
Стадия 1:
К перемешиваемому раствору 4-хлор-7H-пирроло[2,3-d]пиримидина (соединение Синтеза R1a; 1.84 г, 12 ммоль, 1 экв.) в абс. ДМФА (15 мл) добавляли гидрид натрия (720 мг, 60% дисп. в минеральном масле, 18 ммоль, 1.5 экв.), и перемешивали в течение 10 минут при к.т. под Ar. К реакционной смеси добавляли алкилирующий агент (13.18 ммоль) и перемешивали в течение 1-6 часов при к.т. Смесь выливали в воду (150 мл), затем ее экстрагировали с помощью ЕЕО (3×150 мл). Объединенные органические слои промывали водой, солевым раствором, сушили над MgSO4 и упаривали.
Стадия 2:
Часть соединения, полученного на приведенной выше Стадии 1, (1.36 ммоль) и моногидрат гидроксида лития (571 мг, 13.62 ммоль, 10 экв.) перемешивали в смеси PDO-вода (40 мл, 1:1 об./об.) при 110°С в течение 7-36 часов. Реакционную смесь нейтрализовали 1 н. водн. раствором HCl и полученный в результате осадок отфильтровывали, промывали водой и сушили.
Общая методика 2
Стадия 1:
Соединение Синтеза R1a (460 мг, 3 ммоль, 1 экв.), гетероарил/арил-бороновую кислоту (7.5 ммоль) и ацетат меди(II) (817 мг, 4.5 ммоль) перемешивали в пиридине (10 мл) при 50-60°С в течение 16-72 часов.
Выделение продукта реакции, путь 1:
Смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, градиент).
Выделение продукта реакции, путь 2:
Смесь фильтровали и полученный в результате фильтрат очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Стадия 2:
Полученное на приведенной выше Стадии 1 соединение (1.36 ммоль) и моногидрат гидроксида лития (571 мг, 13.62 ммоль, 10 экв.) перемешивали в смеси PDO-вода (40 мл, 1:1 об./об.) при 110°С в течение 7-24 часов. Реакционную смесь нейтрализовали 1 н. водн. раствором HCl, полученный в результате осадок отфильтровывали, промывали водой, сушили.
Общая методика 3
Стадия 1:
Соединение Синтеза R1b (746 мг, 5 ммоль, 1 экв.), гетероарил/арил-йодид (10 ммоль), CuI (286 мг, 1.5 ммоль, 0.3 экв.), R,R-диаминоциклогексан (171 мг, 1.5 ммоль, 0.3 экв.) и безводный K3PO4 (4.24 г, 20 ммоль, 4 экв.) перемешивали в диглиме (15 мл) в течение 6-16 часов при 120°С в атмосфере N2.
Выделение продукта реакции, путь 1:
После завершения реакции, смесь разбавляли водой (200 мл) (или 25% водн. NH3) и охлаждали до к.т. Смесь фильтровали, промывали водой (3×30 мл), водн. раствором NH3 (40 мл, 25%), водой (3×50 мл), гептаном (50, затем 30 мл), и сушили в вакууме.
Выделение продукта реакции, путь 2:
Реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан : ЕЕО, градиент).
Стадия 2:
Соответствующий 4-метокси-7-гетероарил/арилпирроло[2,3-d]пиримидин, полученный на приведенной выше Стадии 1 (61.3 ммоль, 1 экв.), конц. водный раствор HCl (10 мл, ~12.2 М, 122.5 ммоль, 2 экв.) и PDO (70 мл) перемешивали при 100°С в течение 0.5-2 часов. После завершения реакции, смесь частично упаривали. Образовавшуюся суспензию фильтровали и твердое вещество на фильтре промывали водой и сушили.
Общая методика 4
Стадия 1:
Соединение Синтеза R1a (154 мг, 1 ммоль, 1 экв.), ди-трет-бутил-диазодикарбоксилат (690 мг, 3 ммоль, 3 экв.), трифенилфосфин (786 мг, 3 ммоль, 3 экв.) и соответствующий спирт (3 ммоль, 3 экв.) перемешивали в абс. толуоле (10 мл) в атмосфере Ar при 50°С в течение 2 часов. Реакционную смесь упаривали, вносили в ТГФ и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Стадия 2:
Часть 4-хлор-7-арил/алкилпирроло[2,3-d]пиримидина, полученного на приведенной выше Стадии 1, (1.36 ммоль) и моногидрат гидроксида лития (571 мг, 13.62 ммоль) перемешивали в смеси PDO-вода (40 мл, 1:1 об./об.) при 110°С в течение 7-24 часов. Реакционную смесь нейтрализовали 1 н. водн. раствором HCl, полученный в результате осадок отфильтровывали, промывали водой и сушили.
Общая методика 5
Стадия 1:
Производное пиримидин-4-она (1 ммоль), эпоксидное соединение Синтеза R1f (1 ммоль) и K2CO3 (276.4 мг, 2 ммоль, 2 экв.) перемешивали в ДМФА (5 мл) при 75°С в течение 2-8 часов.
Выделение продукта реакции, путь 1:
Смесь выливали в смесь лед-вода и полученный в результате осадок отфильтровывали, промывали водой и сушили.
Выделение продукта реакции, путь 2:
Реакционную смесь фильтровали и твердое вещество промывали ДМФА. Полученный в результате фильтрат очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Стадия 2:
Часть соединения, полученного на приведенной выше Стадии 1, (1 ммоль) перемешивали в водн. растворе HCl (1 н., 10 мл, 10 ммоль, 10 экв.) и PDO (5 мл) в течение 1-3 часов при 75°С.
Выделение продукта реакции, путь 1:
Смесь охлаждали до приблизительно 0-5°С с помощью ледяной бани и белый осадок отфильтровывали и сушили в вакууме (в результате получали HCl соль).
Выделение продукта реакции, путь 2:
Смесь полностью упаривали и использовали на следующей стадии (в результате получали HCl соль).
Выделение продукта реакции, путь 3:
Смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент, в результате получали свободное основание).
Общая методика 6
Соединение, полученное при выполнении Общей методики 5, (1 ммоль, 1 экв.), арил/гетероарил-СН2-Х (1 ммоль, 1 экв.; где X представляет собой атом галогена) и K2CO3 (483 мг, 3.5 ммоль, 3.5 экв.) перемешивали в ДМФА (10 мл) при к.т. в течение 4-16 часов.
Выделение продукта реакции, путь 1:
Смесь выливали в смесь лед-вода и полученный в результате осадок отфильтровывали, промывали водой и сушили.
Выделение продукта реакции, путь 2:
Смесь фильтровали и фильтрат вводили в препаративную ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Общая методика 7
Соединение, полученное при выполнении Общей методики 5, (2.7 ммоль), EDC.HCl (1.183 г, 6.172 ммоль) и соответствующую карбоновую кислоту (2.7 ммоль) перемешивали в пиридине (25 мл) при к.т.в течение 16 часов.
Выделение продукта реакции, путь 1:
Реакционную смесь упаривали, остаток вносили в ДМФА и вводили в препаративную ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Выделение продукта реакции, путь 2:
Реакционную смесь упаривали. Остаток растирали с водой и полученное в результате твердое вещество отфильтровывали.
Общая методика 8
Соединение, полученное при выполнении Общей методики 5, (1 ммоль, 1 экв.), соответствующий сульфонилхлорид (2 ммоль, 2 экв.) и K2CO3 (553 мг, 4 ммоль, 4 экв.) перемешивали в ДМФА (10 мл) при к.т.в течение 4-28 часов.
Смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (элюент: ДХМ-МеОН).
Общая методика 9
Соответствующий галогенированный компонент (0.15 ммоль, 1 экв.), соответствующую бороновую кислоту (0.375 моль, 2.5 экв.), ATAphos*PdCl2 (10.6 мг, 0.015 ммоль, 0.1 экв.) и Cs2CO3 (171 мг, 0.525 ммоль, 3.5 экв.) разбавляли ТГФ (2.5 мл) и водой (2.5 мл). Смесь продували азотом и перемешивали в микроволновом реакторе при 80°С в течение 100-150 минут. Реакционную смесь вводили через шприцевой фильтр в колонку для препаративную ЖХ (колонка С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Общая методика 10
К перемешиваемому раствору соответствующего О-бензил- или О-метил-содержащего соединения (0.17 ммоль) в ДХМ (5 мл) по каплям добавляли трибромид бора (0.3 мл, 440 мг, 1.7 ммоль, 10 экв.) при к.т. После 3 часов перемешивания, реакционную смесь гасили EtOH и упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Общая методика 11
Данная методика аналогична описанной Общей методике 5 с использованием соединения Синтеза R1m в качестве эпоксидного компонента. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Общая методика 12
Смесь нитро соединения (1.45 ммоль), дигидрата хлорида олова(II) (1.64 г, 7.45 ммоль, 5 экв.) в EtOH (30 мл) и HCl (1 н., 5 мл, водн.) перемешивали в течение 20 часов при 80°С. К реакционной смеси добавляли насыщ. водный NaHCO3 (50 мл), затем смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (ДХМ-МеОН).
Общая методика 13
К перемешиваемой смеси амино/амидного соединения (0.105 ммоль), K2CO3 (22 мг, 0.158 ммоль, 1.5 экв.) в ДМФА (1 мл) добавляли йодметан (10 мкл) при к.т. После 18 часов перемешивания реакционную смесь фильтровали и вводили в препаративную ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Общая методика 14
N-Boc соединение (0.1 ммоль) перемешивали в водн. растворе HCl (1 н., 3 мл, 3 ммоль, 30 экв.) и PDO (2 мл) в течение 2-5 часов при 75°С.Смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент, в результате получали свободное аминное основание).
Общая методика 15
Смесь соответствующего метокси соединения (0.44 ммоль), конц. HCl (водн. 37%, 1.1 мл, 13 ммоль, 30 экв.) и PDO (7 мл) перемешивали при 100°С в течение 3 часов. К реакционной смеси добавляли раствор NaOH (водн. 2 М, 6.6 мл). Твердое соединение отфильтровывали, затем очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Синтез R1b: 4-метокси-7-H-пирроло[2,3-d]пиримидин
Соединение Синтеза R1a (100 г, 0.651 моль, 1 экв.), NaOH (31.26 г, 0.781 моль, 1.2 экв.) и МеОН (400 мл) перемешивали при 90°С в течение 24 часов. Смесь гасили водой (1200 мл) и охлаждали до к.т. с помощью ледяной бани. Смесь перемешивали в течение 30 минут, и фильтровали через стеклянный фильтр. Осадок промывали водой (3×100 мл), затем сушили и соединение Синтеза R1b получали в виде белого твердого вещества. МСВР: рассчитано для C7H7N3O: 149.0589, найдено: 150.0667 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ=12.02 (vbrs, 1 Н), 8.37 (s, 1 Н), 7.35 (d, 1 Н), 6.47 (d, 1 Н), 4.02 (s, 3 Н).
13С-ЯМР (100 МГц, MSM-d6) δ м.д. 162.6, 152.9, 150.8, 124.6, 104.8, 98.3, 53.7.
Синтез R1c: 5-[5-(хлорметил)-1,3-тиазол-2-ил]-2-метилпиридин
Стадия 1: [2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метанол
2-Бромтиазол-5-метанол (20 г, 0.103 моль, 1 экв.), 2-метилпиридин-5-бороновую кислоту (18.3 г, 0.134 моль, 1.3 экв.), ATAphos*PdCl2 (3.65 г, 5.152 ммоль, 0.05 экв.) и Cs2CO3 (67.14 г, 0.206 моль, 2 экв.) растворяли в ТГФ (800 мл) и воде (800 мл). Смесь продували азотом и перемешивали при 80°С в течение 3 часов. Смесь охлаждали до к.т. и разбавляли ЕЕО (300 мл). Слои разделяли, водный слой экстрагировали с помощью ЕЕО (3×100 мл), объединенный органический слой сушили над MgSO4 и, после фильтрования, упаривали. Остаток кристаллизовали из ЕЕО / DIPO, фильтровали и сушили в вакууме с получением коричневого твердого вещества. МСВР: рассчитано для C10H10N2OS: 206.0514, найдено: 207.0591 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ=2.52 (s, 3 Н), 4.72 (d, J=10.4 Гц, 2 Н), 5.67 (t, J=11.0 Гц, 1 Н), 7.38 (d, J=16.3 Гц, 1 Н), 7.77 (s, 1 Н), 8.14 (dd, J=16.0, 4.8 Гц, 1 Н), 8.96 (d, J=4.5 Гц, 1 Н).
Стадия 2: соединение Синтеза R1c
[2-(6-Метил-3-пиридил)тиазол-5-ил]метанол (18.23 г, 88.38 ммоль, 1 экв.) растворяли в абс. ДМФА (1.37 мл, 1.29 г, 17.68 ммоль, 0.2 экв.) и сухом ДХМ (400 мл). К реакционной смеси прикапывали (~15 мин) SOCl2 (8.36 мл, 13.67 г, 114.9 ммоль, 1.3 экв.) в виде ДХМ (50 мл) раствора при к.т. Смесь перемешивали при 50°С в течение 2 часов. Смесь охлаждали до к.т. К смеси медленно прикапывали воду (50 мл), затем ее нейтрализовали насыщ. раствором NaHCO3 (250 мл, рН 7-8). Слои разделяли. Водный слой экстрагировали с помощью ДХМ (4×50 мл). Объединенный органический слой сушили над MgSO4, фильтровали. Раствор разбавляли ЕЕО (300 мл) и фильтровали через набивку силикагеля (~20 г). Смесь упаривали с получением соединения Синтеза R1c в виде желтого твердого вещества. МСВР: рассчитано для C10H9ClN2S: 224.0175, найдено: 225.0247 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ=2.53 (s, 3 Н), 5.17 (s, 2 Н), 7.41 (d, J=16.5 Гц, 1 Н), 7.98 (s, 1 Н), 8.17 (dd, J=16.0, 5.0 Гц, 1 Н), 8.99 (d, J=5.0 Гц, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 24.5, 38.4, 124.1, 134.4, 144.4, 146.7.
Синтез R1d: 4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-карбоновая кислота
Стадия 1: этил 4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-карбоксилат
Этил 2-бром-4-метилтиазол-5-карбоксилат (26.9 г, 107.6 ммоль, 1 экв.), 2-метилпиридин-5-бороновую кислоту (19.2 г, 139.8 ммоль, 1.3 экв.), ATAphos*PdCl2 (3.05 г, 4.3 ммоль, 0.04 экв.) и Na2CO3 (34.2 г, 322.65 ммоль, 3 экв.) растворяли в ТГФ (250 мл) и воде (250 мл). Смесь продували азотом и перемешивали при 80°С в течение 2 часов. После завершения реакции, смесь охлаждали до к.т. и разбавляли ЕЕО (250 мл). Слои разделяли и водный слой экстрагировали с помощью ЕЕО (2×50 мл). Объединенный органический слой сушили над MgSO4 и, после фильтрования, упаривали. Сырой продукт растворяли в смеси ДХМ/ЕЕО/гептан (1:1:1 об./об., 600 мл) и фильтровали через силикагель (~30 г) и промывали смесью ДХМ/ЕЕО/гептан (1:1:1 об./об., 100 мл). Смесь упаривали. Остаток перекристаллизовывали из DIPO (100 мл) и сушили в вакууме с получением бежевого твердого вещества. МСВР: рассчитано для C13H14N2O2S: 262.0776, найдено: 263.0852 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ=1.31 (t, J=17.5 Гц, 3 Н), 2.54 (s, 3 Н), 2.70 (s, 3 Н), 4.30 (q, J=17.8 Гц, 2 Н), 7.42 (d, J=20.3 Гц, 1 Н), 8.24 (dd, J=20.4, 6.1 Гц, 1 Н), 9.04 (d, J=5.4 Гц, 1 Н).
Стадия 2: соединение Синтеза R1d
Этил 4-метил-2-(6-метил-3-пиридил)тиазол-5-карбоксилат (21.07 г, 80.33 ммоль, 1 экв.) растворяли в EtOH (40 мл). NaOH (4.82 г, 120.49 ммоль, 1.5 экв.) растворяли в воде (80 мл). Водн. NaOH добавляли к органической смеси и перемешивали при 80°С в течение 45 минут. После завершения реакции, смесь охлаждали до к.т. Через 1 неделю наблюдали осажденный черный осадок. Смесь фильтровали через набивку силикагеля/целита. Смесь подкисляли конц. раствором HCl (до рН~1), и полученный в результате осадок отфильтровывали, промывали водой (50 мл) и сушили в вакууме с получением соединения Синтеза R1d в виде не совсем белого твердого вещества. МСВР: рассчитано для C11H10N2O2S: 234.0463, найдено: 235.0533 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ=2.52 (s, 3 Н), 2.63 (s, 3 Н), 7.36 (d, J=16.2 Гц, 1 Н), 8.14 (dd, J=16.2, 4.8 Гц, 1 Н), 8.95 (d, J=4.8 Гц, 1 Н).
Синтез R1e: трет-бутил 1-окса-6-азаспиро[2.5]октан-6-карбоксилат
Йодид триметилсульфоксония (20.0 г, 150 ммоль) растворяли в абс. MSM (75 мл) затем последовательно добавляли дисперсию гидрида натрия (60% в минеральном масле, 6 г, 150 ммоль) и перемешивали в течение 20 минут при к.т. К смеси добавляли раствор N-Вос-пиперидин-4-она (20.0 г, 100 ммоль) в MSM (75 мл, абс.) и перемешивали в течение 15 часов при к.т. Реакционную смесь выливали в смесь лед-вода (200 мл) и экстрагировали с помощью диэтилового эфира (4×200 мл). Объединенный органический слой промывали водой, солевым раствором, затем сушили над MgSO4 и упаривали с получением соединения Синтеза R1e. МСВР: рассчитано для C11H19NO3: 213.1365, найдено: 158.0811 [(M+H-tBu)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 3.5/3.37 (brm+brm, 4 Н), 2.65 (s, 2 Н), 1.64/1.38 (m+m, 4 Н), 1.4 (s, 9 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 154.3, 79.3, 57.4, 53.3, 42.7, 33, 28.5.
Синтез R1f: трет-бутил (3R,4R)-4-(1-окса-6-азаспиро[2.5]окт-6-илкарбонил)-3-фенилпиперидин-1-карбоксилат
Стадия 1: трет-бутил (3R,4R)-4-[(4-оксопиперидин-1-ил)карбонил]-3-фенилпиперидин-1-карбоксилат
Гидрат гидрохлорида 4-пиперидона (0.969 г, 6.3 ммоль), EDC. HCl (3.623 г, 18.9 ммоль) и (3R,4R)-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновую кислоту (1.928 г, 6.3 ммоль) растворяли в пиридине (10 мл) и перемешивали при к.т. в течение 16 часов. Реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (ДХМ : МеОН, градиент) с получением указанного в заголовке продукта. МСВР: рассчитано для C22H30N2O4: 386.2206, найдено: 409.2093 [(M+Na)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ 1.42 (s, 9 Н), 4.14-1.50 (m, 16 Н), 7.32-7.15 (m, 5 Н).
Стадия 2: соединение Синтеза R1ƒ
трет-Бутил (3R,4R)-4-[(4-оксопиперидин-1-ил)карбонил]-3-фенилпиперидин-1-карбоксилат (60 г, 155 ммоль 1 экв.) и йодид триметилсульфоксония (85.41 г, 388 ммоль, 2.5 экв.) загружали в круглодонную колбу и растворяли/суспендировали в MeCN (150 мл) и МТВЕ (150 мл). Одновременно с этим NaOH (15.5 г, 388 ммоль, 2.5 экв.) растворяли в воде (21.6 мл) (-40% раствор). Водн. раствор NaOH добавляли к реакционной смеси и перемешивали при 60°С в течение 2 часов. После завершения реакции, смесь охлаждали до к.т., фильтровали через набивку целита и осадок на фильтре промывали МТВЕ (2×60 мл). К органическому слою добавляли воду (150 мл) и, после экстрагирования, слои разделяли. Водн. слой экстрагировали дополнительным МТВЕ (2×60 мл). Объединенные органические слои сушили над MgSO4 и после фильтрования упаривали с получением соединения Синтеза R1f в виде бежевой твердой пены. МСВР: рассчитано для C23H32N2O4: 400.2362, найдено: 423.2247 [(M+Na)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ=1.41 (s, 9 Н), 1.79-0.86 (m, 6 Н), 2.61-2.51 (m, 2 Н), 4.16-2.73 (m, 10 Н), 7.33-7.18 (m, 5 Н).
Синтез R1g: 3-фтор-5-йодтиофен-2-карбоновая кислота
Стадия 1: 3-фтор-5-йодтиофен-2-карбоксилат и метил 3-фтор-4,5-дийодтиофен-2-карбоксилат
К раствору метил 3-фтортиофен-2-карбоксилата (2.42 г, 15.1 ммоль) в ТГФ (10 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 25 мл, 25 ммоль) при -45°С в течение 5 минут. После 30 минут перемешивания к смеси добавляли йод (4.04 мг, 15.9 ммоль) в ТГФ (10 мл) при -45°С. После нагревания (1 час) к смеси при перемешивании добавляли насыщ. раствор NH4Cl (50 мл, водн.). Смесь экстрагировали с помощью ЕЕО (5×10 мл). Объединенный органический слой упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением 3-фтор-5-йодтиофен-2-карбоксилата и метил 3-фтор-4,5-дийодтиофен-2-карбоксилата, отдельно друг от друга.
Метил 3-фтор-5-йодтиофен-2-карбоксилат
ГХ-МС: рассчитано для C6H4FIO2S: 285.8961, найдено: 285.9 [(М, EI) форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 7.52 (s, 1 Н), 3.78 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159.4, 158.8, 128.5, 117.2, 86.4, 52.8.
Метил 3-фтор-4,5-дийодтиофен-2-карбоксилат
ГХ-МС: рассчитано для C6H4FIO2S: 411.7927, найдено: 411.9 [(М, EI) форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 3.8 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159, 158.2, 117.4, 96.1, 90.6, 53.1.
Стадия 2: соединение Синтеза R1g
Метил 3-фтор-5-йодтиофен-2-карбоксилат (1.188 г, 4.135 ммоль) и моногидрат гидроксида лития (867 мг, 20.7 ммоль) перемешивали в метаноле (10 мл) и воде (10 мл) при 70°С в течение 1 часа. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (25 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1g. ГХ-МС рассчитано для C5H2FIO2S: 271.8804, найдено: 271.9 [(М, EI) форма].
1H ЯМР (500 МГц, MSM-d6): δ м.д. 13.48 (brs), 7.74 (s, 1 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 160.4, 158.3, 128.5, 119, 85.1.
Синтез R1h: 3-фтор-4,5-дийодтиофен-2-карбоновая кислота
Метил 3-фтор-4,5-дийодтиофен-2-карбоксилат (614 мг, 1.49 ммоль) и моногидрат гидроксида лития (256 мг, 6 ммоль) перемешивали в метаноле (8 мл) и воде (8 мл) при к.т.в течение 5 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (10 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1h. МСВР: рассчитано для C5HFI2O2S: 397.7771, найдено: 352.7798 [(М-Н-CO2)+ форма].
1H ЯМР (500 МГц, MSM-d6): δ м.д. 13.72 (brs, 1 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 160, 157.7, 119.1, 95.1, 90.5.
Синтез R1i: 3-фтор-4-йод-5-метилтиофен-2-карбоновая кислота
Стадия 1: метил 3-фтор-4-йод-5-метилтиофен-2-карбоксилат
К раствору метил 3-фтор-5-йодтиофен-2-карбоксилата, соединения Синтеза R1g, (286 мг, 1 ммоль) в ТГФ (3 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 1.5 мл, 1.5 ммоль) при -45°С в течение 5 минут. После 60 минут перемешивания к смеси добавляли йодметан (123 мл, 282 мг, 2 ммоль) в ТГФ (2 мл) при -45°С и перемешивали в течение 2 часов при -40°С. После нагревания к смеси при перемешивании добавляли насыщ. раствор NH4Cl (5 мл, водн.). Смесь экстрагировали с помощью ЕЕО (4×10 мл). Объединенный органический слой упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением указанного в заголовке продукта. МСВР: рассчитано для C7H6FIO2S: 299.9117; 300.9200 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 3.8 (s, 3 Н), 2.43 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159.8, 158.5, 145.1, 109.6, 77.2, 52.8, 19.1.
Стадия 2: соединение Синтеза R1i
Метил 3-фтор-4-йод-5-метилтиофен-2-карбоксилат (40 мг, 0.133 ммоль) и моногидрат гидроксида лития (11 мг, 0.266 ммоль) перемешивали в метаноле (1 мл) и воде (1 мл) при к.т.в течение 3 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (3 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1i. 1Н ЯМР (500 МГц, MSM-d6): δ м.д. 13.41 (brs, 1 Н), 2.41 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 160.8, 158, 144.2, 76.9, 19.1.
Синтез R1i: 3-хлор-5-йодтиофен-2-карбоновая кислота
Стадия 1: сложный метиловый эфир 3-хлор-5-йодтиофен-2-карбоновой кислоты
К раствору сложного метилового эфира 3-хлортиофен-2-карбоновой кислоты (353 г, 2 ммоль) в ТГФ (5 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 3 мл, 3 ммоль) при -45°С. После 20 минут перемешивания к смеси добавляли йод (507 мг, 4 ммоль) в ТГФ (2 мл) при -45°С. После нагревания к смеси при перемешивании добавляли насыщ. раствор NH4Cl (5 мл, водн.) и раствор Na2S2O3 (5 мл, 10% водн.). Смесь экстрагировали с помощью ЕЕО (4×10 мл). Объединенный органический слой упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением указанного в заголовке продукта. МСВР: рассчитано для C6H4ClIO2S: 301.8665, найдено: 301.9000 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 37.55 (s, 1 Н), 3.8 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159.5, 139.4, 130.9, 130.6, 86.8, 53.
Стадия 2: соединение Синтеза R1j
Сложный метиловый эфир 3-хлор-5-йодтиофен-2-карбоновой кислоты (477 мг, 1.58 ммоль) и моногидрат гидроксида лития (132 мг, 3.16 ммоль) перемешивали в метаноле (5 мл) и воде (5 мл) при 50°С в течение 2.5 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. раствором HCl (4 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1j. ГХ-МС рассчитано для C5H2ClIO2S: 287.8509, найдено: 243.8 [(M-CO2, EI) форма].
1H ЯМР (500 МГц, MSM-d6): δ м.д. 13.6 (brs, 1 Н), 7.51 (s, 1 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 160.6, 139.3, 132.4, 130.1, 85.8.
Синтез R1k: 5-хлор-3-фтор-4-йодтиофен-2-карбоновая кислота
Стадия 1: метил 5-хлор-3-фтор-4-йодтиофен-2-карбоксилат
К раствору метил 3-фтор-5-йодтиофен-2-карбоксилата (286 мг, 1 ммоль) в ТГФ (5 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 1.5 мл, 1.5 ммоль) при -45°С в течение 5 минут. После 30 минут перемешивания к смеси добавляли гексахлорэтан (236 мг, 1 ммоль) в ТГФ (2 мл) при -45°С. После нагревания к смеси при перемешивании добавляли насыщ. раствор NH4Cl (5 мл, водн.). Смесь экстрагировали с помощью ЕЕО (4×10 мл) и объединенные органические слои упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением указанного в заголовке продукта. ГХ-МС рассчитано для C6H3ClFIO2S: 319.8571, найдено: 319.9 [(М, EI) форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 3.82 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159.1, 157.9, 135.9, 111.7, 81.1, 53.2.
Стадия 2: соединение Синтеза R1k
Метил 5-хлор-3-фтор-4-йодтиофен-2-карбоксилат (76 мг, 0.237 ммоль) и моногидрат гидроксида лития (20 мг, 0.474 ммоль) перемешивали в метаноле (4 мл) и воде (4 мл) при к.т. в течение 2 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (2 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1k. 1H ЯМР (400 МГц, MSM-d6): δ м.д. 13.88 (brs, 1 Н).
19F ЯМР (376.5 МГц, MSM-d6): δ м.д. -101.7.
13С ЯМР (100 МГц, MSM-d6): δ м.д. 157.4.
Синтез R1l: 5-хлор-3-фтор-4-метилтиофен-2-карбоновая кислота
Стадия 1: метил 5-хлор-3-фтортиофен-2-карбоксилат
К раствору метил 3-фтортиофен-2-карбоксилата (1826 мг, 11.4 ммоль) в ТГФ (5 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 21 мл, 21 ммоль) при -45°С в течение 5 минут. После 30 минут перемешивания при -45°С, к смеси добавляли гексахлорэтан (2.7 г, 11.4 ммоль) при -45°С и перемешивали в течение 1 часа при -40°С. После нагревания к смеси при перемешивании добавляли насыщ. раствор NH4Cl (10 мл, водн.). Смесь экстрагировали с помощью ЕЕО (4×10 мл) и объединенные органические слои упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4CO3-MeCN, градиент) с получением указанного в заголовке продукта. ГХ-МС рассчитано для C6H4ClFO2S: 193.9604, найдено: 193.9 [(М, EI) форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 7.46 (s, 1 Н), 3.81 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159.5, 157.5, 135.3, 120.2, 111.5, 53.
Стадия 2: метил 5-хлор-3-фтор-4-метилтиофен-2-карбоксилат
К раствору метил 5-хлор-3-фтортиофен-2-карбоксилата (579 мг, 3 ммоль) в ТГФ (3 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 6 мл, 6 ммоль) при -45°С в течение 5 минут. После 60 минут перемешивания к смеси добавляли йодметан (1.3 мл, 2964 мг, 20.9 ммоль) в ТГФ (2 мл) при -45°С и перемешивали в течение 2 часов при -40°С. После нагревания к смеси при перемешивании добавляли насыщ. раствор NH4Cl (5 мл, водн.). Смесь экстрагировали с помощью ЕЕО (4×10 мл) и объединенные органические слои упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением указанного в заголовке продукта. ГХ-МС рассчитано для C7H6ClFO2S: 207.9761, найдено: 207.9 [(М, EI) форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 3.81 (s, 3 Н), 2.09 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159.7, 156.4, 130.8, 127, 109.6, 53, 10.5.
Стадия 3: соединение Синтеза R1l
Метил 5-хлор-3-фтор-4-метилтиофен-2-карбоксилат (316 мг, 1.62 ммоль) и моногидрат гидроксида лития (271 мг, 6.46 ммоль) перемешивали в метаноле (5 мл) и воде (5 мл) при к.т.в течение 4 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (2 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1l. 1Н ЯМР (500 МГц, MSM-d6): δ м.д. 13.57 (brs, 1 Н), 2.07 (s, 3 Н)
13С ЯМР (125 МГц, MSM-d6): δ м.д. 160.7, 155.9, 129.8, 126.9, 111.4, 10.5
Синтез R1m: [4-метил-2-(6-метил-3-пиридил)тиазол-5-ил]-[(3R,4R)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенил-1-пиперидил]метанон
Стадия 1: гидрохлорид этил (3R,4R-3-фенилпиперидин-4-карбоксилата
1-трет-бутил 4-этил (3R,4R)-3-фенилпиперидин-1,4-дикарбоксилат (10 г, 30 ммоль) перемешивали в смеси MeCN (100 мл) и конц. раствора HCl (7.38 мл, 90 ммоль, водн.) при 80°С в течение 30 минут. Реакционную смесь упаривали, и сушили в вакууме с получением указанного в заголовке продукта.
Стадия 2: этил (3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-карбоксилат
Гидрохлорид этил (3R,4R)-3-фенилпиперидин-4-карбоксилата (7.89 г, 29.9 ммоль), 2-бром-4-метилтиазол-5-карбоновую кислоту (6.64 г, 29.9 ммоль) и EDC.HCl (17.2 г, 89.7 ммоль) растворяли в пиридине (200 мл) и перемешивали при к.т.в течение 23 часов. Реакционную смесь упаривали. К остатку добавляли воду (200 мл) и экстрагировали с помощью ДХМ (3×50 мл). Объединенный органический слой сушили над MgSO4 и упаривали с получением указанного в заголовке продукта. МСВР: рассчитано для C19H21BrN2O3S: 436.0456, найдено: 437.0546 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 7.36-7.19 (m, 5 Н), 4.96-2.74 (vbrs, 4 Н), 3.82 (q, 2 Н), 3.03 (m, 1 Н), 2.87 (m, 1 Н), 2.34 (s, 3 Н), 1.98/1.62 (m+m, 2 Н), 0.86 (t, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 160.5, 151.6, 136.3, 129.2, 60.1, 47.3, 45.3, 29.2, 16.4, 14.2.
Стадия 3: этил (3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-карбоксилат
В 8 отдельных пробирках для микроволновой печи, этил (3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-карбоксилат (8×1.87 г, 34.2 ммоль), 2-метилпиридин-5-бороновую кислоту (8×1.17 г, 68.4 ммоль), ATAphos*PdCl2 (8×303 мг, 3.4 ммоль) и Cs2CO3 (8×4.18 г, 102.6 ммоль) растворяли в ТГФ (8×25 мл) и воде (8×15 мл). 8 пробирок незамедлительно подвергали микроволновому облучению при 80°С в течение 2 часов (Anton-Paar Multiwave Pro). Органические слои 8 пробирок объединяли, частично упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением указанного в заголовке продукта. МСВР: рассчитано для C25H27N3O3S: 449.1773, найдено: 450.1860[(М+Н)+ форма].
1Н ЯМР (400 МГц, MSM-d6): δ м.д. 8.98 (d, 1 Н), 8.17 (dd, 1 Н), 7.4 (d, 1 Н), 7.36-7.16 (m, 5 Н), 5-2.75 (vbrs, 4 Н), 3.83 (q, 2 Н), 3.05 (m, 1 Н), 2.87 (m, 1 Н), 2.53 (s, 3 Н), 2.43 (s, 3 Н), 2.01/1.64 (dm+qm, 2 Н), 0.87 (t, 3 Н).
13С ЯМР (100 МГц, MSM-d6): δ м.д. 146.7, 134.4, 124, 60.1, 47.3, 45.5, 29.2, 24.3, 16.5, 14.2.
Стадия 4: (3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-карбоновая кислота
Этил (3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-карбоксилат (7.48 г, 16.64 ммоль) и гидрат гидроксида лития (1.75 г, 41.6 ммоль) перемешивали в смеси EtOH (30 мл) и воды (10 мл) при 75°С в течение 3.5 часов. Реакционную смесь частично упаривали, остаток подкисляли (до рН=4.5-5.5) раствором HCl (1 н., водн.) и полученную в результате суспензию фильтровали. Твердое соединение на фильтре промывали водой и сушили с получением указанного в заголовке продукта. МСВР: рассчитано для C23H23N3O3S: 421.146, найдено: 422.1544 [(М+Н)+ форма].
1H ЯМР (400 МГц, MSM-d6): δ м.д. 11.82 (brs, 1 Н), 8.97 (d, 1 Н), 8.15 (dd, 1 Н), 7.39 (d, 1 Н), 7.35-7.18 (m, 5 Н), 4.34-4.05 (brm, 4 Н), 3.01-2.84 (m, 2 Н), 2.54 (s, 3 Н), 2.44 (s, 3 Н), 2.06/1.66 (m+m, 2 Н).
13С ЯМР (100 МГц, MSM-d6): δ м.д. 146.8, 134.4, 123.8, 29.5, 24.3, 16.5.
Стадия 5: 1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-он
(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-карбоновую кислоту (3786 мг, 8.98 ммоль), гидрат гидрохлорида пиперидин-4-она (1518 мг, 9.88 ммоль) и EDC.HCl (5.16 г, 26.94 ммоль) перемешивали в пиридине (30 мл) при к.т.в течение 16 часов. Реакционную смесь упаривали, остаток вносили в МеОН (20 мл) и выливали в воду (120 мл) и экстрагировали с помощью ДХМ (3×60 мл). Объединенный органический слой промывали водой, солевым раствором, сушили над MgSO4 и упаривали с получением указанного в заголовке продукта. МСВР: рассчитано для C23H23N3O3S: 502.2039, найдено: 503.2088 [(М+Н)+ форма].
1Н ЯМР (400 МГц, MSM-d6): δ м.д. 8.98 (brs, 1 Н), 8.17 (dd, 1 Н), 7.4 (d, 1 Н), 7.36-7.13 (m, 5 Н), 4.92-2.76 (m, 10 Н), 2.53 (s, 3 Н), 2.45 (s, 3 Н), 2.25-1.52 (m, 6 Н).
Стадия 6: соединение Синтеза R1m
1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-он (3.89 г, 7.74 ммоль) и йодид триметилсульфоксония (2.09 г, 9.3 ммоль) перемешивали в MeCN (19 мл) при к.т.и к смеси добавляли раствор NaOH (309 мг, 9.3 ммоль) в воде (0.4 мл). Затем реакционную смесь перемешивали при 70°С в течение 2 часов. Реакционную смесь выливали в воду (200 мл) и нейтрализовали водным раствором HCl (1 н., 9 мл) и экстрагировали с помощью ДХМ (3×80 мл). Объединенный органический слой промывали водой и солевым раствором и упаривали с получением соединения Синтеза R1m в виде твердой пены. МСВР: рассчитано для C29H32N4O3S: 516.2195, найдено: 517.2267 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 8.98 (brs, 1 Н), 8.17 (dd, 1 Н), 7.4 (d, 1 Н), 7.37-7.15 (brs/brs, 5 Н), 3.82-0.88 (m, 14 Н), 3.53 (m, 1 Н), 2.97 (brm, 1 Н), 2.56 (m, 2 Н), 2.53 (s, 3 Н), 2.44 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 164.1, 160.8, 152.4, 146.8, 134.5, 125.6, 124.1, 57.4/57.1, 53.4/53.1, 42.9/42.8, 24.5, 16.7.
Синтез R1n: 3-[[4-Гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(2-триметилсилилэтоксиметил)пирроло[2,3-d]пиримидин-4-он
Стадия 1: 2-[(4-хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан
Соединение Синтеза R1a (2.81 г, 18.3 ммоль) растворяли в ТГФ (25 мл), охлаждали до 0°С, и к смеси добавляли NaH (60% дисп., 1.1 г, 27.4 ммоль) и перемешивали в течение 1 часа. Затем к смеси добавляли SEM-Cl (8.1 мл, 45.76 ммоль) и давали нагреться до к.т.Спустя 2.5 ч, к реакционной смеси добавляли воду (25 мл) и экстрагировали с помощью ЕЕО (2×30 мл). Объединенный органический слой сушили над MgSO4 и упаривали. Остаток очищали с помощью флэш-хроматографии (220 г колонка Silica Gold, гептан-ЕЕО, градиент) с получением указанного в заголовке продукта.
Стадия 2: 7-(2-триметилсилилэтоксиметил)-3Н-пирроло[2,3-d]пиримидин-4-он
2-[(4-хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (3.5 г, 12.3 ммоль) и гидрат гидроксида лития (5.17 г, 123 ммоль) перемешивали при 100°С в течение 116 часов в смеси PDO (20 мл) и воды (20 мл). Реакционную смесь фильтровали, фильтрат подкисляли водным раствором HCl (1 н., 80 мл), и полученное в результате твердое соединение отфильтровывали, промывали водой и сушили с получением указанного в заголовке продукта.
Стадия 3: трет-бутил 4-гидрокси-4-[[4-оксо-7-(2-триметилсилилэтоксиметил)пирроло [2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбоксилат
7-(2-Триметилсилилэтоксиметил)-3H-пирроло[2,3-d]пиримидин-4-он (3.11 г, 11.7 ммоль), соединение Синтеза R1e (2.75 г, 2.9 ммоль) и K2CO3 (1.78 г, 12.9 ммоль) перемешивали в ДМФА (70 мл) при 60°С в течение 40 часов. К реакционной смеси добавляли воду, полученное в результате твердое соединение отфильтровывали и промывали водой с получением указанного в заголовке продукта. МСВР: рассчитано для C23H38N4O5Si: 478.2611, найдено: 479.2694 [(М+Н)+ форма].
Стадия 4: 3-[(4-гидрокси-4-пиперидил)метил]-7-(2-триметилсилилэтоксиметил)пирроло[2,3-d]пиримидин-4-он
трет-Бутил 4-гидрокси-4-[[4-оксо-7-(2-триметилсилилэтоксиметил)пирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбоксилат (1.84 г, 3.86 ммоль) растворяли в ДХМ (50 мл) и добавляли муравьиную кислоту (5 мл) и ТФУ (1317 мг, 0.885 мл, 11.58 ммоль), и затем смесь перемешивали в течение 4 дней при к.т. К реакционной смеси добавляли водный раствор гидроксида натрия (1 н., 100 мл), затем экстрагировали с помощью ДХМ (50 мл). Органический слой сушили над MgSO4, фильтровали, и упаривали с получением указанного в заголовке продукта. МСВР: рассчитано для C18H30N4O3Si: 378.2087, найдено: 379.2176 [(М+Н)+ форма].
Стадия 5: трет-бутил (3R,4R)-4-[4-гидрокси-4-[[4-оксо-7-(2-триметилсилилэтоксиметил)пирроло [2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенилпиперидин-1-карбоксилат
3-[(4-Гидрокси-4-пиперидил)метил]-7-(2-триметилсилилэтоксиметил)пирроло[2,3-d]пиримидин-4-он (1.527 г, 3.77 ммоль), (3R,4R)-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновую кислоту (1.152 г, 3.77 ммоль) и EDC.HCl (1.446 г, 7.54 ммоль) перемешивали в пиридине (15 мл) в течение ночи при к.т. Реакционную смесь упаривали, наносили на целит, и очищали с помощью флэш-хроматографии (ДХМ-МеОН) с получением указанного в заголовке продукта. МСВР: рассчитано для C35H51N5O6Si: 665.3609, найдено: 666.3696 [(М+Н)+ форма].
Стадия 6: соединение Синтеза R1n
Раствор трет-бутил (3R,4R)-4-[4-гидрокси-4-[[4-оксо-7-(2-триметилсилилэтоксиметил)пирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенилпиперидин-1-карбоксилата (1.6 г, 2.4 ммоль), муравьиной кислоты (3 мл) и ТФУ (820 мг, 0.55 мл, 7.2 ммоль) в ДХМ (30 мл) перемешивали при к.т.в течение 4 дней. К реакционной смеси добавляли карбонат калия (15 г) в виде водного раствора, и смесь экстрагировали с помощью ДХМ. Органический слой упаривали с получением соединения Синтеза R1n. МСВР: рассчитано для C30H43N5O4Si: 565.3084, найдено: 566.3138 [(М+Н)+ форма].
Синтез R1o: 5-бром-4-(трет-бутоксикарбониламино)тиофен-2-карбоновая кислота
4-Амино-5-бромтиофен-2-карбоновую кислоту (500 мг, 2.25 ммоль) растворяли в смеси PDO (2 мл) и к реакционной смеси при 0°С добавляли воду (2 мл) и гидроксид натрия (194 мг, 4.8 ммоль). Затем к смеси добавляли ди-трет-бутил дикарбонат (1768 мг, 8.1 ммоль) и перемешивали при 0°С в течение 3 часов, затем реакционной смеси давали нагреться до к.т. и перемешивали в течение 116 часов. К реакционной смеси добавляли воду и подкисляли водным раствором HCl (1 н., 4 мл). Полученное в результате твердое вещество отфильтровывали, промывали водой и сушили. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент, в результате получали соль аммония) с получением соединения Синтеза R1o. 1Н ЯМР (500 МГц, MSM-d6): δ м.д. 8.71 (s, 1 Н), 7.44 (brs, 4 Н), 7.24 (s, 1 Н), 1.44 (s, 9 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 125.8, 28.5.
15N ЯМР (470.6 МГц, MSM-d6): δ м.д. 99.
Синтез R1p: 4-нитро-5-(4-пиридил)тиофен-2-карбоновая кислота
Используя Общую методику 9, исходили из метил 5-хлор-4-нитротиофен-2-карбоксилата и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реактанта, сырой продукт (200 мг, 0.75 ммоль) перемешивали с гидратом гидроксида лития (60 мг, 1.5 ммоль) в смести воды (2 мл) и метанола (10 мл) при к.т. в течение 4 часов. Реакционную смесь нейтрализовали водным раствором HCl (1 н., 1.5 мл). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1p. 1Н ЯМР (500 МГц, MSM-d6): δ м.д. 14.18 (vbrs, 1 Н), 8.74 (brs, 2 Н), 8.19 (s, 1 Н), 7.65 (m, 2 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 161.8, 150.4, 145.9, 143.6, 138.2, 134.4, 129.2, 124.3.
Синтез R1q-(3S,4R): (3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбоновая кислота
и
Синтез R1q-(3R,4S): (3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбоновая кислота
К перемешиваемой суспензии гидрида натрия (60% дисп., 1.4 г, 35.1 ммоль) в абс. DEE (135 мл) добавляли гидрохлорид этил 1-бензил-3-оксопиперидин-4-карбоксилата (3.54 г, 11.9 ммоль) при 0°С. После 30 минут перемешивания к реакционной смеси по каплям добавляли трифторметансульфоновый ангидрид (3.88 г, 2.28 мл, 13.5 ммоль) и перемешивали в течение 3 часов, во время чего температуре давали подняться до к.т. К реакционной смеси добавляли воду (100 мл), слои разделяли, водный слой промывали DEE. DEE слой сушили над MgSO4 и упаривали.
Часть полученного этил 1-бензил-5-(трифторметилсульфонилокси)-3,6-дигидро-2H-пиридин-4-карбоксилата (2.184 г, 5.55 ммоль), 2-тиенилбороновую кислоту (925 мг, 7.23 ммоль), ATAphos*PdCl2 (400 мг, 0.55 ммоль) и Cs2CO3 (3.63 г, 11.1 моль) растворяли в ТГФ (11 мл) и воде (11 мл). Смесь продували азотом и подвергали микроволновому обучению при 82°С в течение 140 минут. Слои разделяли, органический слой упаривали, наносили на целит и очищали с помощью флэш-хроматографии (Гептан-ЕЕО, градиент).
Ранее полученный этил 1-бензил-5-(трифторметилсульфонилокси)-3,6-дигидро-2H-пиридин-4-карбоксилат (2.184 г, 5.55 ммоль), 2-тиенилбороновую кислоту (925 мг, 7.23 ммоль), ATAphos*PdCl2 (400 мг, 0.55 ммоль) и Cs2CO3 (3.63 г, 11.1 моль) растворяли в смеси ТГФ (11 мл) и воды (11 мл). Смесь продували азотом и подвергали микроволновому обучению при 82°С в течение 140 минут. Слои разделяли, органический слой упаривали, наносили на целит и очищали с помощью флэш-хроматографии (Гептан-ЕЕО, градиент).
Полученный в результате этил 1-бензил-5-(2-тиенил)-3,6-дигидро-2Н-пиридин-4-карбоксилат (2.85 г, 8.7 ммоль), Pd на угле (3×1.5 г, 10%), раствор HCl (1 н. в эфире, 8.7 мл, 8.7 ммоль) и EtOH (65 мл) загружали в автоклав. Автоклав закрывали, инертизировали, вакуумировали и наполняли водородом (8 бар), и реакционную смесь перемешивали в автоклаве при 90°С в течение 420 часов. Во время протекания реакции катализатор отфильтровывали и дважды заменяли свежим. Реакционную смесь удаляли из автоклава и фильтровали через целит, и фильтрат упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате метил цис-1-бензил-3-(2-тиенил)пиперидин-4-карбоксилат (664 мг, 2 ммоль) растворяли в растворе NaOEt (1 н., в EtOH, свежеприготовленный, 10 мл, 10 ммоль) и перемешивали при 75°С в течение 3 часов. Затем к реакционной смеси добавляли воду (5 мл) и перемешивание продолжали при 75°С в течение 4 часов. Реакционную смесь частично упаривали, затем нейтрализовали 1 н. водным раствором HCl, твердое вещество отфильтровывали, промывали водой и сушили. Два энантиомера разделяли с помощью хиральной ЖХ с получением соединения Синтеза R1q-(3S,4R) и соединения Синтеза R1q-(3R,4S). МСВР: рассчитано для C17H19NO2S: 301.1136, найдено: 302.1217 [(М+Н)+ форма].
1Н ЯМР (400 МГц, MSM-d6): δ м.д. 12.15 (brs, 1 Н), 7.37-7.19 (m, 5 Н), 7.32 (dd, 1 Н), 6.91 (dd, 1 Н), 6.88 (dd, 1 Н), 3.51 (s, 2 Н), 3.24 (tm, 1 Н), 2.9-2.05 (m, 4 Н), 2.39 (tm, 1 Н), 1.91-1.67 (dm/qm, 2 Н).
Синтез R1s: (4-метил-2-фенилтиазол-5-ил)-[(3R,4R)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенил-1-пиперидил]метанон
Стадия 1: 1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-он гидрохлорид
трет-бутил (3R,4R)-4-(4-оксопиперидин-1-карбонил)-3-фенилпиперидин-1-карбоксилат (полученный на Стадии 1 Синтеза R1f, 4.77 г, 12.34 ммоль) перемешивали в PDO (20 мл) и водном растворе HCl (20 мл, 1 н.) при 70°С в течение 1 часа. Реакционную смесь упаривали и сушили с получением указанного в заголовке продукта. МСВР: рассчитано для C17H22N2O2: 286.1681, найдено: 287.1755 [(М+Н)+ форма].
1Н ЯМР (400 МГц, MSM-d6): δ м.д. 9.68 (brd, 1 Н), 9.14 (brq, 1 Н), 7.40-7.18 (m, 5Н), 3.73/3.31 (m/m, 2 Н), 3.73/3.31 (m/m, 2 Н), 3.56 (m, 1 Н), 3.33/3.10 (m/m, 2 Н), 3.31-3.13 (m, 2 Н), 3.26 (m, 1 Н), 2.17/1.56 (m/m, 2 Н), 2.15/1.81 (m/m, 2 Н), 2.03-1.87 (m, 2 Н).
Стадия 2: 1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]пиперидин-4-он
Гидрохлорид 1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-она (3.42 г, 10.6 ммоль), EDC.HCl (6.64 г, 34.6 ммоль) и 4-метил-2-фенилтиазол-5-карбоновую кислоту (2.32 г, 10.6 ммоль) перемешивали в пиридине (60 мл) при к.т. в течение 20 часов. Реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (ДХМ-МеОН/ДХМ, градиент) с получением указанного в заголовке продукта. МСВР: рассчитано для C28H29N3O3S: 487.1930, найдено: 488.1991 [(М+Н)+ форма].
1Н ЯМР (400 МГц, MSM-d6): δ м.д. 7.93/7.51 (brs/brs, 5 Н), 7.35/7.15 (brs/brs, 5 Н), 4.80-2.80 (brm, 4Н), 3.74/3.63 (m/brm, 2 Н), 3.74/3.32 (m/m, 2 Н), 3.56 (td, 1 Н), 2.99 (td, 1 Н), 2.44 (s, 3 Н), 2.19/1.61 (m/m, 2 Н), 2.16/1.84 (m/m, 2 Н), 1.89/1.66 (brm/brm, 2 Н).
Стадия 3: соединение Синтеза R1s
К перемешиваемой суспензии 1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]пиперидин-4-она (4.5 г, 9.23 ммоль) и йодида триметилсульфоксония (2.44 г, 11.1 ммоль) в MeCN (25 мл) добавляли водный гидроксид натрия (40 мас. %, 443 мг NaOH/0.664 мл вода) при к.т. и смесь перемешивали в течение 160 минут. Реакционную смесь разбавляли водой (20 мл) и MeCN упаривали. Остаток экстрагировали с помощью ДХМ и органический слой упаривали с получением соединения Синтеза R1s. МСВР: рассчитано для C29H31N3O3S: 501.2086, найдено: 502.2160 [(М+Н)+ форма].
1Н ЯМР (400 МГц, MSM-d6): δ м.д. 7.93 (m, 2 Н), 7.51 (m, 3 Н), 7.40-7.10 (brs/brs, 5 Н), 4.88-2.88 (brm, 4Н), 3.82-2.97 (m, 4 Н), 3.54 (m, 1 Н), 2.97 (m, 1 Н), 2.56 (m, 2 Н), 2.43 (s, 3 Н), 1.83/1.63 (brd/brq, 2 Н), 1.45-0.86 (m, 2 Н).
Синтез R1t: 1-этенил-1H-индол-2-карбоновая кислота
Смесь этил индол-2-карбоксилата (2 г, 10.57 ммоль), ацетата палладия(II) (119 мг, 0.53 ммоль), бромида меди(II) (2.37 г, 10.57 ммоль), винилацетата (20 мл, 248.7 ммоль) и ацетата натрия (2.6 г, 31.7 ммоль) нагревали при 80°С в течение 28 часов. Реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, 0-5% градиент).
Смесь полученного в результате сложного эфира (1.08 г, 5.017 ммоль) и гидрата гидроксида лития (1.05 г, 25.1 ммоль) в этаноле и воде (10-10 мл) перемешивали при 80°С в течение 90 минут. Реакционную смесь подкисляли водным раствором HCl (1 н., 30 мл) при 0-5°С, образовавшийся осадок отфильтровывали, промывали водой (5×20 мл) и сушили с получением соединения Синтеза R1t. 1Н ЯМР (400 МГц, MSM-d6): δ м.д. 13.22 (s, 1 Н), 7.75 (m, 3 Н), 7.51 (m, 1 Н), 7.22 (t, 1 Н), 5.48 (d, 1 Н), 5.28 (d, 1 Н)
Синтез R1u: 5-бром-1-винилпиррол-2-карбоновая кислота
Смесь метил 5-бром-1H-пиррол-2-карбоксилата (1.2 г, 5.88 ммоль), ацетата палладия(II) (132 мг, 0.588 ммоль), бромида меди(II) (2.63 г, 11.76 ммоль), винил-ацетата (27 мл, 294 ммоль) и ацетата натрия (2.9 г, 35.3 ммоль) нагревали при 80°С в течение 28 часов. Реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, 0-25% градиент).
Смесь полученного в результате сложного эфира (403 мг, 1.75 ммоль) и гидрата гидроксида лития (368 мг, 8.75 ммоль) в этаноле и воде (4-4 мл) перемешивали при 80°С в течение 60 минут. Реакционную смесь подкисляли водным раствором HCl (1 н., 10 мл) при 0-5°С. Образовавшийся осадок отфильтровывали, промывали водой (5×20 мл) и сушили с получением соединения Синтеза R1u. 1Н ЯМР (400 МГц, MSM-d6): δ м.д. 12.63 (s, 1 Н), 7.11 (m, 1 Н), 6.94 (d, 1 Н), 6.45 (d, 1 Н), 5.42 (m, 2 Н)
Синтез R1v: 4-бром-1-винилпиррол-2-карбоновая кислота
Смесь метил 4-бром-1H-пиррол-2-карбоксилата (1.2 г, 5.88 ммоль), ацетата палладия(II) (132 мг, 0.588 ммоль), бромида меди(II) (2.63 г, 11.76 ммоль), винил-ацетата (27 мл, 294 ммоль) и ацетата натрия (2.9 г, 35.3 ммоль) нагревали при 80°С в течение 21 часов. Реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, 0-5% градиент).
Смесь полученного в результате сложного эфира (338 мг, 1.47 ммоль) и гидрата гидроксида лития (908 мг, 7.35 ммоль) в этаноле и воде (3.5-3.5 мл) перемешивали при 80°С в течение 105 минут. Реакционную смесь подкисляли водным раствором HCl (1 н., 9 мл) при 0-5°С. Образовавшийся осадок отфильтровывали, промывали водой (2×5 мл) и сушили с получением соединения Синтеза R1v. 1H ЯМР (500 МГц, MSM-d6): δ м.д. 12.93 (brs, 1 Н), 7.85 (d, 1 Н), 7.84 (dd, 1 Н), 6.94 (d, 1 Н), 5.5/4.9 (dd+dd, 2 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 131.4, 124.1, 123.4, 120.3, 102.8, 97.9
Синтез R1w: 4,5-дихлор-3-фтортиофен-2-карбоновая кислота
Стадия 1: метил 4,5-дихлор-3-фтортиофен-2-карбоксилат
К раствору метил 3-фтортиофен-2-карбоксилата (1826 мг, 11.4 ммоль) в ТГФ (5 мл) по каплям добавляли TMP.MgCl.LiCl (1 н., в смеси ТГФ/толуол, 21 мл, 21 ммоль) при -45°С в течение 5 минут. После 30 минут перемешивания при -45°С, к смеси добавляли гексахлорэтан (2.7 г, 11.4 ммоль) при -45°С и перемешивали в течение 1 часа при -40°С. После нагревания к смеси при перемешивании добавляли насыщ. раствор NH4Cl (10 мл, водн.). Смесь экстрагировали с помощью ЕЕО (4×10 мл). Объединенный органический слой упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением указанного в заголовке продукта. ГХ-МС рассчитано для C6H3Cl2FO2S: 227.9215, найдено: 227.9 [(М, EI) форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 3.85 (s, 3 Н).
13С ЯМР (125 МГц, MSM-d6): δ м.д. 159, 152.8, 130.5, 115.5, 110.8, 53.4.
Стадия 2: соединение Синтеза R1w
Метил 4,5-дихлор-3-фтортиофен-2-карбоксилат (130 мг, 0.567 ммоль) и моногидрат гидроксида лития (95 мг, 2.27 ммоль) перемешивали в метаноле (3 мл) и воде (3 мл) при к.т.в течение 3 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (4 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1w. 13С ЯМР (125 МГц, MSM-d6): δ м.д. 160, 152.3, 129.5, 115.3, 112.8.
Синтез R1x: 2-(6-метил-3-пиридил)тиазол-5-карбоновая кислота
Этил 2-(6-метил-3-пиридил)тиазол-5-карбоксилат (745 мг, 3 ммоль) и моногидрат гидроксида лития (630 мг, 15 ммоль) перемешивали в этаноле (5 мл) и воде (5 мл) при к.т.в течение 8 часов. Смесь частично упаривали и водный остаток подкисляли 1 н. HCl (15 мл, водн.). Полученный в результате осадок отфильтровывали, промывали водой и сушили с получением соединения Синтеза R1x. МСВР: рассчитано для C10H8N2O2S: 220.0307, найдено: 221.0379 [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 13.69 (brs, 1 Н), 9.07 (d, 1 Н), 8.45 (s, 1 Н), 8.26 (dd, 1 Н), 7.44 (d, 1 Н), 2.55 (s, 3 Н). 13С ЯМР (125 МГц, MSM-d6): δ м.д. 149.3, 147.1, 134.9, 124.2, 24.5
Синтез R2b: 7-метил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и йодметана в качестве алкилирующего агента, получали соединение Синтеза R2b. МСВР: рассчитано для C7H7N3O: 149.0589, найдено: 150.0668 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.85 (brs, 1 Н), 7.88 (brs, 1 Н), 7.09 (d, 1 Н), 6.44 (d, 1 Н), 3.70 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.7, 143.8, 125.1, 108.1, 101.7, 31.8.
Синтез R2c: 7-этил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и йодэтана в качестве реагентов, получали соединение Синтеза R2c. МСВР: рассчитано для C8H9N3O: 163.0746, найдено: 164.0823 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.38 (brs, 1 Н), 7.87 (d, J=2.0 Гц, 1 Н), 7.16 (d, J=3.4 Гц, 1 Н), 6.45 (d, J=3.4 Гц, 1 Н), 4.14 (q, J=7.1 Гц, 2 Н), 1.34 (t, J=7.1 Гц, 3 Н).
Синтез R2d: 7-(пропан-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 2-йодпропана в качестве реагентов, получали соединение Синтеза R2d. МСВР: рассчитано для C9H11N3O: 177.0902, найдено: 178.0979 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.83 (brs, 1 Н), 7.87 (s, 1 Н), 7.24 (d, 1 Н), 6.47 (d, 1 Н), 4.85 (sept., 1 Н), 1.42 (d, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 146.8, 143.5, 120.7, 108.2, 102, 46.5, 23.
15N-ЯМР (50.6 МГц, MSM-d6): δ (м.д.) 168.
Синтез R2g: 7-циклопропил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и циклопропилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2g. МСВР: рассчитано для C9H9N3O: 175.0746, найдено: 176.0819 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.88 (brs, 1 Н), 7.89 (brs, 1 Н), 7.05 (d, 1 Н), 6.4 (d, 1 Н), 3.53 (m, 1 Н), 1.06-0.92 (m, 4 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 148.9, 143.8, 123.4, 108.8, 101.6, 27.5, 6.6.
Синтез R2h: 7-циклобутил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и циклобутилбромида в качестве реагентов, получали соединение Синтеза R2h. МСВР: рассчитано для C10H11N3O: 189.0902, найдено: 190.0974 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.85 (brs, 1 Н), 7.88 (brs, 1 Н), 7.09 (d, 1 Н), 6.44 (d, 1 Н), 3.70 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.7, 143.8, 125.1, 108.1, 101.7, 31.8.
Синтез R2i: 7-циклопентил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 4 исходя из соединения Синтеза R1a и циклопентанола в качестве реагентов, получали соединение Синтеза R2i. МСВР: рассчитано для C11H13N3O: 203.1059, найдено: 204.1139 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.84 (brs, 1 Н), 7.87 (d, 1 Н), 7.21 (d, 1 Н), 6.46 (d, 1 Н), 4.97 (m, 1 Н), 2.16-1.57 (m, 8 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 143.5, 121.3, 102, 55.6.
Синтез R2j: 7-циклогексил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 4 исходя из соединения Синтеза R1a и циклогексанола в качестве реагентов, получали соединение Синтеза R2j. МСВР: рассчитано для C12H15N3O: 217,1215, найдено: 218.1293 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.83 (brs, 1 Н), 7.86 (d, 1 Н), 7.23 (d, 1 Н), 6.46 (d, 1 Н), 4.45 (m, 1 Н), 1.97-1.13 (m, 10 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 143.4, 121.1, 101.8, 53.8.
Синтез R2k: 7-(1-метилпиперидин-4-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 4, исходя из соединения Синтеза R1a и 4-гидрокси-1-метилпиперидина в качестве реагентов, получали соединение Синтеза R2k. МСВР: рассчитано для C12H16N4O: 232.1324, найдено: 233.1405 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.82 (brs, 1 Н), 7.86 (d, 1 Н), 7.29 (d, 1 Н), 6.46 (d, 1 Н), 4.44 (m, 1 Н), 2.89/2.05 (m, 4 Н), 2.22 (s, 3 Н), 2.02/1.82 (m, 4 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 143.9, 121.2, 102.1, 55.1, 52.1, 46.1, 32.3.
Синтез R2l: 7-(тетрагидро-2H-пиран-4-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 4, исходя из соединения Синтеза R1a и тетрагидро-4-пиранола в качестве реагентов, получали соединение Синтеза R2l. МСВР: рассчитано для C11H13N3O2: 219.1008, найдено: 220.1082 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.88 (brs, 1 Н), 7.88 (d, 1 Н), 7.29 (d, 1 Н), 6.48 (d, 1 Н), 4.71 (m, 1 Н), 3.98/3.49 (m+m, 4 Н), 2.05/1.82 (m+m, 4 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 143.5, 121.2, 102, 66.7, 51.3, 33.3.
Синтез R2m: 7-(проп-2-ин-1-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходили из соединения Синтеза R1b (взамен соединения Синтеза R1a) и 3-бромпроп-1-ина в качестве реагентов (без стадии гидролиза), сырой метоксипиримидиновый продукт (400 мг, 2.3 ммоль) растворяли в PDO (4 мл) и добавляли водный раствор HCl (37%, 0.18 мл). Смесь нагревали при 100°С в течение 30 минут в сосуде Шленка. После охлаждения к реакционной смеси добавляли DIPO (4 мл) и полученный в результате осадок отфильтровывали и сушили с получением соединения Синтеза R2m. МСВР: рассчитано для C9H7N3O: 173.0589, найдено: 174.0665 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.98 (brs, 1 Н), 7.93 (s, 1 Н), 7.19 (d, 1 Н), 6.5 (d, 1 Н), 4.98 (d, 2 Н), 3.42 (t, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.6, 147.3, 144.3, 123.6, 102.5, 79.4, 76, 34.1.
Синтез R2n: 7-(2-метилпропил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 1-бром-2-метилпропана в качестве реагентов, получали соединение Синтеза R2n. МСВР: рассчитано для C10H13N3O: 191.1059, найдено: 192.1132 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.84 (brs, 1 Н), 7.86 (s, 1 Н), 7.12 (d, 1 Н), 6.45 (d, 1 Н), 3.92 (d, 2 Н), 2.1 (sept., 1 Н), 0.82 (d, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.7, 143.7, 124.5, 108, 101.6, 52, 29.6, 20.2.
Синтез R2o: 7-(2,2,2-трифторэтил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 2,2,2-трифторэтил трифторметансульфоната в качестве реагентов, получали соединение Синтеза R2o. МСВР: рассчитано для C8H6N3OF3: 217.0463, найдено: 218.0543 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.08 (brs, 1 Н), 7.97 (s, 1 Н), 7.19 (d, 1 Н), 6.57 (d, 1 Н), 5.06 (q, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.5, 148.4, 144.9, 124.7, 124.4, 108.8, 103.2, 45.1.
19F-ЯМР (376.5 МГц, MSM-d6): δ (м.д.) -70.3.
Синтез R2p: 7-(2,2-дифторэтил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 2-йод-1,1-дифторэтана в качестве реагентов, получали соединение Синтеза R2p. МСВР: рассчитано для C8H7N3OF2: 199.0557, найдено: 200.0634 ((М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 11.99 (brs, 1 Н), 7.93 (s, 1 Н), 7.16 (d, 1 Н), 6.53 (d, 1 Н), 6.37 (tt, 1 Н), 4.6 (td, 2 Н).
13С-ЯМР (400 МГц, MSM-d6) δ м.д. 144.4, 124.8, 114.3, 102.5, 46.2.
Синтез R2q: 7-(циклопропилметил)-3H,4H,7H-пирроло [2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и циклопропилметилбромида в качестве реагентов, получали соединение Синтеза R2q. МСВР: рассчитано для C10H11N3O: 189.0902, найдено: 190.0980 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.84 (s, 1 Н), 7.87 (s, 1 Н), 7.2 (d, 1 Н), 6.45 (d, 1 Н), 3.97 (d, 2 Н), 1.21 (m, 1 Н), 0.52-0.35 (m, 4 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.3, 143.7, 124, 108.1, 101.7, 49, 12.3, 4.07.
Синтез R2r: 7-(циклобутилметил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и бромметил)циклобутана в качестве реагентов, получали соединение Синтеза R2r. МСВР: рассчитано для C11H13N3O: 203.1059, найдено: 204.1134 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.83 (brs, 1 Н), 7.87 (d, 1 Н), 7.12 (d, 1 Н), 6.43 (d, 1 Н), 4.13 (d, 2 Н), 2.72 (m, 1 Н), 1.92/1.74 (m+m, 4 Н), 1.82 (m, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 143.7, 124.2, 101.7, 49.6, 36, 25.6, 18.
Синтез R2s: 7-(бута-2,3-диен-1-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходили из соединения Синтеза R1b (взамен соединения Синтеза R1a) и 4-бромбута-1,2-диена в качестве реагентов (без стадии гидролиза), сырой метоксипиримидиновый продукт (300 мг, 1.65 ммоль) растворяли в PDO (4 мл) и добавляли водный раствор HCl (37%, 0.18 мл). Смесь нагревали при 100°С в течение 30 минут в сосуде Шленка. После охлаждения реакционную смесь упаривали с получением соединения Синтеза R2s. МСВР: рассчитано для C10H9N3O: 187.0745, найдено: 188.0821 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.91 (brs, 1 Н), 7.89 (s, 1 Н), 7.12 (d, 1 Н), 6.46 (d, 1 Н), 5.48 (m, 1 Н), 4.87 (m, 2 Н), 4.73 (m, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 208.3, 158.7, 147.4, 143.9, 123.9, 108.2, 102.1, 88.3, 78.1, 43.
Синтез R2t: 7-[3-(диметиламино)пропил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и гидрохлорида 3-диметиламинопропилхлорида в качестве реагентов, получали соединение Синтеза R2t. МСВР: рассчитано для C11H16N4O: 220.1324, найдено: 221.1401 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.84 (brs, 1 Н), 7.88 (s, 1 Н), 7.13 (d, 1 Н), 6.44 (d, 1 Н), 4.12 (t, 2 Н), 2.15 (t, 2 Н), 2.1 (s, 6 Н), 1.85 (quint, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.4, 143.8, 124.2, 108.2, 101.7, 56.4, 45.6, 43, 28.6.
Синтез R2u: 7-(2-фторэтил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 1-фтор-2-йодэтана в качестве реагентов, получали соединение Синтеза R2u. МСВР: рассчитано для C8H8NOF: 181.0651, найдено: 182.0728 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 11.91 (brs, 1 Н), 7.9 (s, 1 Н), 7.17 (d, 1 Н), 6.49 (d, 1 Н), 4.74 (dt, 2 Н), 4.43 (dt, 2 Н).
13С-ЯМР (100 МГц, MSM-d6) δ м.д. 144, 124.3, 102, 83.1, 45.1.
Синтез R2v: 7-[2-(диметиламино)этил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и гидробромида 2-бром-N,N-диметилэтиламина в качестве реагентов, получали соединение Синтеза R2v. МСВР: рассчитано для C10H14N4O: 206.1168, найдено: 207.1242 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.84 (brs, 1 Н), 7.88 (brd, 1 Н), 7.16 (d, 1 Н), 6.44 (d, 1 Н), 4.19 (t, 2 Н), 2.6 (t, 2 Н), 2.16 (s, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.5, 143.7, 124.4, 108.1, 101.7, 59.2, 45.5, 42.6.
Синтез R2w: 7-(2-гидроксиэтил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 2-хлорэтанола в качестве реагентов, получали соединение Синтеза R2w. 1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.83 (brs, 1 Н), 7.86 (d, J=2.4 Гц, 1 Н), 7.12 (d, J=3.92 Гц, 1 H), 6.43 (d, J=3.14 Гц, 1 H), 4.92 (t, J=5.49 Гц, 1 H), 4.15 (t, J=6.28 Гц, 2 H), 3.68 (q, J=5.49 Гц, 2 H).
Синтез R2x: 7-[(4-хлорфенил)метил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 4-хлорбензилбромида в качестве реагентов, получали соединение Синтеза R2x. МСВР: рассчитано для C13H10ClN3O: 259.0512, найдено: 260.0583 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.93 (s, 7.9 (s, 1 Н), 7.39 (m, 2 Н), 7.23 (m, 2 Н), 7.22 (d, 1 Н), 6.51 (d, 1 Н), 5.34 (s, 2 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 158.7, 147.4, 144.2, 137.5, 132.5, 129.5, 129, 124.2, 108.3, 102.4, 47.5.
Синтез R2y: 7-[(3-хлорфенил)метил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 3-хлорбензилбромида в качестве реагентов, получали соединение Синтеза R2y. МСВР: рассчитано для C13H10ClN3O: 259.0512, найдено: 260.0580 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.94 (brs, 1 Н), 7.92 (d, 1 Н), 7.35 (m, 1 Н), 7.35 (m, 1 Н), 7.28 (t, 1 Н), 7.25 (d, 1 Н), 7.16 (dm, 1 Н), 6.51 (d, 1 Н), 5.35 (s, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.6, 144.3, 140.9, 133.6, 131.1, 128, 127.5, 126.4, 124.3, 108.4, 102.4,47.5.
Синтез R2z: 7-бензил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и бензилбромида в качестве реагентов, получали соединение Синтеза R2z. МСВР: рассчитано для C13H11N3O: 225.0902, найдено: 226.0986 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.91 (brs, 1 Н), 7.91 (s, 1 Н), 7.36-7.17 (m, 5 Н), 7.2 (d, 1 Н), 6.49 (d, 1 Н), 5.34 (s, 2 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.1, 124.3, 102.2, 48.1.
Синтез R2aa: 7-[(2-хлорфенил)метил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из соединения Синтеза R1a и 2-хлорбензилбромида в качестве реагентов, получали соединение Синтеза R2aa. МСВР: рассчитано для C13H10ClN3O: 2590512, найдено: 260.0587 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.95 (brs, 1 Н), 7.89 (d, 1 Н), 7.5 (dm, 1 Н), 7.32 (m, 1 Н), 7.26 (m, 1 Н), 7.17 (d, 1 Н), 6.72 (dm, 1 Н), 6.55 (d, 1 Н), 5.44 (s, 2 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.3, 129.8, 129.8, 128.8, 128.1, 124.5, 102.5, 46.
Синтез R2ab: 7-(2-оксопирролидин-1-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он
Соединение Синтеза R1b (1.74 г, 11.67 ммоль) растворяли в ДМФА (80 мл) и охлаждали до 0°С, медленно добавляли гидрид натрия (60% дисп., 1.87 г, 46.67 ммоль) и перемешивали в течение 30 минут при 0°С. К реакционной смеси добавляли гидроксиламин-О-сульфоновую кислоту (2.11 г, 18.67 ммоль) и давали нагреться до к.т., и перемешивали в течение 20 часов. К реакционной смеси добавляли воду (100 мл) и экстрагировали с помощью ДХМ (4×50 мл). Объединенный органический слой промывали водой и сушили над MgSO4 и упаривали. Остаток растворяли в MSM и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Часть полученного в результате N-аминного соединения (500 мг, 3.05 ммоль) растворяли в ДХМ (20 мл) и по каплям добавляли TEA (850 мкл, 6.09 ммоль, 2 экв.) и 4-хлорбутирил хлорид (409 мкл, 515 мг, 3.65 ммоль, 1.2 экв.), и перемешивали в течение 20 часов при к.т. Затем реакционную смесь упаривали, к остатку добавляли насыщ. раствор NaHCO3 (5 мл, водн.), MeCN (20 мл) и воду (20 мл) и смесь перемешивали в течение 3 часов при 80°С. Реакционную смесь упаривали и добавляли воду (50 мл). Раствор экстрагировали с помощью ДХМ (3×10 мл) и объединенные органические слои упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате пирролидон (200 мг, 0.862 ммоль) растворяли в растворе HCl (4 мл, 1 н., водн.) и PDO (80 мл) и перемешивали при 60°С в течение 6 часов. Реакционную смесь упаривали и остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R2ab. МСВР: рассчитано для C10H10N4O2: 218.0804, найдено: 219.0883 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.11 (brs, 1 Н), 7.91 (s, 1 Н), 7.2 (d, 1 Н), 6.53 (d, 1 Н), 3.77 (t, 2 Н), 2.47 (t, 2 Н), 2.17 (quint, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 173.7, 158.4, 146.6, 145.2, 124.2, 107, 101.3, 49.8, 28.4, 16.9.
Синтез R2ac: 7-(3,4,5-триметоксифенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 5-йод-1,2,3-триметоксибензола в качестве реагентов, получали соединение Синтеза R2ac. МСВР: рассчитано для C15H15N3O4: 301.1063, найдено: 302.1138 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.07 (brs, 1 Н), 7.95 (d, 1 Н), 7.49 (d, 1 Н), 6.99 (s, 2 Н), 6.66 (d, 1 Н), 3.82 (s, 6 Н), 3.7 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.5, 124.6, 103.2, 103, 60.6, 56.6.
Синтез R2ad: 7-(3,5-дихлорфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 3,5-дихлорфенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2ad. МСВР: рассчитано для C12H7Cl2N3O: 278.9966, найдено: 280.0040 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.03 (vbrs, 1 Н), 8.03 (s, 1 Н), 7.95 (d, 2 Н), 7.64 (t, 1 Н), 7.63 (d, 1 Н), 6.71 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 145.3, 126.7, 123.8, 122.7, 104.4.
Синтез R2ae: 7-(3-хлор-5-метоксифенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 3-хлор-5-метоксифенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2ae. МСВР: рассчитано для C13H10ClN3O2: 275.0461, найдено: 276.0541 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.18 (s, 1 Н), 8 (d, 1 Н), 7.6 (d, 1 Н), 7.51 (t, 1 Н), 7.33 (t, 1 Н), 7.08 (t, 1 Н), 6.69 (d, 1 Н), 3.85 (s, 3 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 161, 158.7, 147.5, 145, 139.7, 134.5, 124, 116.3, 112.7, 110.2, 109.4, 104, 56.4
Синтез R2af: 7-(3,5-д иметоксифенил)-3H,4H,7H-пирроло [2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 2-(3,5-диметокси)-фенил-4,4,5,5-тетраметил-(1,3,2)-диоксаборолана в качестве реагентов, получали соединение Синтеза R2af. МСВР: рассчитано для C14H13N3O3: 271.0957, найдено: 272.1030 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.11 (s, 1 Н), 7.95 (d, 1 Н), 7.52 (d, 1 Н), 6.91 (d, 2 Н), 6.66 (d, 1 Н), 6.54 (t, 1 Н), 3.8 (s, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.5, 124.2, 103.5, 103.1, 98.9.
Синтез R2ag: 7-(3,4-дихлорфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 3,4-дихлорфенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2ag. МСВР: рассчитано для C12H7Cl2N3O: 278.9966, найдено: 280.003 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.21 (brs, 1 Н), 8.15 (t, 1 Н), 8.02 (brs, 1 Н), 7.82 (d, 1 Н), 7.82 (d, 1 Н), 7.61 (d, 1 Н), 6.72 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 145.1, 131.5, 125.9, 124.3, 123.8, 104.2.
Синтез R2ah: 7-(4-хлор-3-фторфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-хлор-3-фторйодбензола в качестве реагентов, получали соединение Синтеза R2ah. МСВР: рассчитано для C12H7ClFN3O: 263.0262, найдено: 264.0339 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.21 (s, 1 Н), 8.02 (d, 1 Н), 7.97 (dd, 1 Н), 7.77 (dd, 1 Н), 7.72 (dd, 1 Н), 7.6 (d, 1 Н), 6.72 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 145.1, 131.5, 123.7, 121.5, 112.8, 104.2.
Синтез R2ai: 7-(4-хлор-3-метоксифенил)-3H,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-хлор-5-йоданизола в качестве реагентов, получали соединение Синтеза R2ai. МСВР: рассчитано для C13H10ClN3O2: 275.0461, найдено: 276.0537 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.15 (brs, 1 Н), 7.98 (brs, 1 Н), 7.58 (d, 1 Н), 7.57 (d, 1 Н), 7.49 (d, 1 Н), 7.36 (dd, 1 Н), 6.7 (d, 1 Н), 3.93 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 155.3, 147.4, 144.8, 137.7, 130.5, 124.2, 119.8, 117.3, 110, 109.4, 103.7, 56.9.
Синтез R2aj: 7-(4-фтор-3-метоксифенил)-3Н,4Н,7Н-пирроло [2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-фтор-4-йод-2-метоксибензола в качестве реагентов получали соединение Синтеза R2aj. МСВР: рассчитано для C13H10N3O2F: 259.0757, найдено: 260.0818 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.1 (s, 1 Н), 7.95 (s, 1 Н), 7.51 (d, 1 Н), 7.48 (dd, 1 Н), 7.38 (dd, 1 Н), 7.27 (ddd, 1 Н), 6.68 (d, 1 Н), 3.9 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.7, 124.5, 117, 116.5, 111, 103.4, 56.8.
Синтез R2ak: 7-(3,4-диметоксифенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и сложного пинаколового эфира 3,4-диметоксифенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2ak. МСВР: рассчитано для C14H13N3O3: 271.0957, найдено: 272.103 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 7.92 (d, 1 Н), 7.43 (d, 1 Н), 7.25 (d, 1 Н), 7.19 (dd, 1 Н), 7.08 (d, 1 Н), 6.65 (d, 1 Н), 3.8 (s, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.5, 124.6, 116.9, 112.2, 109.3, 103.1, 56.3.
Синтез R2am: 7-(4-метилфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йодтолуола в качестве реагентов, получали соединение Синтеза R2am. МСВР: рассчитано для C13H11N3O: 225.0902, найдено: 226.0987 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.06 (brs, 1 Н), 7.93 (s, 1 Н), 7.58 (dm, 1 Н), 7.44 (d, 1 Н), 7.33 (dm, 1 Н), 6.66 (d, 1 Н), 2.37 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.3, 144.5, 136.8, 135.4, 130.1, 124.5, 124.1, 109.6, 103.4,21.
Синтез R2an: 4-{4-оксо-3H,4H,7H-пирроло[2,3-d]пиримидин-7-ил}бензонитрил
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йодбензонитрила в качестве реагентов, получали соединение Синтеза R2an. МСВР: рассчитано для C13H8N4O: 236.0698, найдено: 237.0775 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.25 (brs, 1 Н), 8.05 (m, 2 Н), 8.03 (m, 2 Н), 8.02 (brs, 1 Н), 7.66 (d, 1 Н), 6.75 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 147.6, 145.2, 141.5, 134, 124.6, 123.6, 119, 110.6, 109.4, 104.7.
Синтез R2ao: 7-[4-(трифторметил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йодбензотрифторида в качестве реагентов, получали соединение Синтеза R2ao. МСВР: рассчитано для C13H8F3N3O: 279.0619, найдено: 280.0691 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.23 (brs, 1 Н), 8.02 (m, 2 Н), 8.01 (d, 1 Н), 7.92 (m, 2 Н), 7.63 (d, 1 Н), 6.74 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.6, 145.1, 126.9, 124.7, 123.8, 110.4, 104.5 15N-ЯМР (50.6 МГц, MSM-d6): δ (м.д.) 170.9.
Синтез R2ap: 7-[4-(дифторметил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-(дифторметил)-4-йодбензола в качестве реагентов, получали соединение Синтеза R2ap. МСВР: рассчитано для C13H9F2N3O: 261.0714, найдено: 262.0784 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.17 (brs, 1 Н), 7.99 (d, 1 Н), 7.91 (m, 2 Н), 7.75 (m, 2 Н), 7.58 (d, 1 Н), 7.12 (t, 1 Н), 6.72 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.9, 127.2, 124.7, 123.9, 115.1, 104.1.
Синтез R2aq: 7-[4-(гидроксиметил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йодбензилового спирта в качестве реагентов, получали соединение Синтеза R2aq. МСВР: рассчитано для C13H11N3O2: 241.0851, найдено: 242.0925 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.07 (brs, 1 Н), 7.94 (s, 1 Н), 7.66 (m, 2 Н), 7.47 (m, 2 Н), 7.45 (d, 1 Н), 6.67 (d, 1 Н), 5.31 (t, 1 Н), 4.56 (d, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.9, 147.4, 144.6, 142.2, 136.6, 127.6, 124.3, 124.2, 109.9, 103.5, 62.8.
Синтез R2ar: 7-(4-хлорфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-хлор-4-йодбензола в качестве реагентов, получали соединение Синтеза R2ar. МСВР: рассчитано для C12H8ClN3O: 245.0356, найдено: 246.0427 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.15 (brs, 1 Н), 7.97 (d, 1 Н), 7.78 (dm, 1 Н), 7.61 (dm, 1 Н), 7.53 (d, 1 Н), 6.7 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.7, 147.3, 144.8, 136.7, 131.7, 129.6, 126.1, 123.9, 109.9, 103.9.
Синтез R2as: 7-(4-фторфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-фторйодбензола в качестве реагентов, получали соединение Синтеза R2as. МСВР: рассчитано для C12H8FN3O: 229.0651, найдено: 230.0714 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.12 (brs, 1 Н), 7.95 (d, 1 Н), 7.74 (m, 2 Н), 7.48 (d, 1 Н), 7.39 (m, 2 Н), 6.68 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.7, 126.8, 124.2, 116.4, 103.5.
Синтез R2at: 7-[4-(диметиламино)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 4-(диметиламино)фенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2at. МСВР: рассчитано для C14H14N4O: 254.1168, найдено: 255.1243 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.98 (brs, 1 Н), 7.89 (d, 1 Н), 7.43 (m, 2 Н), 7.33 (d, 1 Н), 6.82 (m, 2 Н), 6.61 (d, 1 Н), 2.94 (s, 6 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.1, 125.6, 124.3, 112.7, 102.7, 40.6.
Синтез R2au: 7-[4-(4-метилпиперазин-1-ил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и сложного пинаколового эфира 4-(4-метилпиперазин-1-ил)фенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2au. МСВР: рассчитано для C17H19N5O: 309.1590, найдено: 310.1674 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.01 (brs, 1 Н), 7.9 (d, 1 Н), 7.49 (m, 2 Н), 7.37 (d, 1 Н), 7.06 (m, 2 Н), 6.63 (d, 1 Н), 3.2 (brm, 4 Н), 2.51 (brm, 4 Н), 2.27 (s, 3 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.3, 125.4, 124.2, 115.9, 102.9, 54.8, 48.3, 45.9.
Синтез R2av: 7-[4-(морфолин-4-ил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 4-морфолинофенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2av. МСВР: рассчитано для C16H16N4O2: 296.1273, найдено: 297.1361 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.01 (brs, 1 Н), 7.9 (s, 1 Н), 7.51 (m, 2 Н), 7.38 (d, 1 Н), 7.07 (m, 2 Н), 6.63 (d, 1 Н), 3.76 (m, 4 Н), 3.16 (m, 4 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 484.8, 144.3, 125.4, 124.2, 115.7, 103, 66.5.
Синтез R2ax: 7-(4-метоксифенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йоданизола в качестве реагентов, получали соединение Синтеза R2ax. МСВР: рассчитано для C13H11N3O2: 241.0851, найдено: 242.0929 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.04 (brs, 1 Н), 7.92 (d, 1 Н), 7.58 (dd, 1 Н), 7.4 (d, 1 Н), 7.08 (d, 1 Н), 6.65 (d, 1 Н), 3.81 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 158.8, 147.3, 144.4, 130.9, 126.1, 124.4, 114.8, 109.4, 103.1, 55.9.
Синтез R2ay: 7-[4-(трифторметокси)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-йод-4-(трифторметокси)бензола в качестве реагентов, получали соединение Синтеза R2ay. МСВР: рассчитано для C13H8F3N3O2: 295.0569, найдено: 296.0648 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.15 (s, 1 Н), 7.97 (d, 1 Н), 7.86 (m, 2 Н), 7.56 (m, 2 Н), 7.54 (m, 1 Н), 6.71 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.8, 126.4, 124.1, 122.5, 103.9.
Синтез R2az: 7-[4-(бензилокси)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-бензилоксийодбензола в качестве реагентов, получали соединение Синтеза R2az. MCBP: рассчитано для C19H15N3O2: 317.1164, найдено: 318.1243 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.05 (brs, 1 Н), 7.92 (d, 1 Н), 7.59 (dm, 2 Н), 7.48 (dm, 2 Н), 7.41 (d, 1 Н), 7.41 (tm, 2 Н), 7.35 (tm, 1 Н), 7.16 (dm, 2 Н), 6.65 (d, 1 Н), 5.18 (s, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 157.6, 147.3, 144.4, 137.4, 131, 129, 128.4, 128.2, 126.1, 124.3, 115.7, 109.4, 103.1, 69.9.
Синтез R2ba: 7-(5-метилтиофен-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-йод-5-метилтиофена в качестве реагентов, получали соединение Синтеза R2ba. MCBP: рассчитано для C11H9N3OS: 231.0466, найдено: 232.0541 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.17 (brs, 1 Н), 7.99 (d, 1 Н), 7.49 (d, 1 Н), 7.14 (d, 1 Н), 6.76 (dq, 1 Н), 6.67 (d, 1 Н), 2.46 (d, 3 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 145, 124.2, 123.9, 119.4, 103.9, 15.4.
Синтез R2bb: 7-(5-хлортиофен-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-хлор-5-йодтиофена в качестве реагентов, получали соединение Синтеза R2bb. MCBP: рассчитано для C10H6N3OSCl: 250.9920, найдено: 252.0005 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 12.28 (brs, 1 Н), 8.07 (d, 1 Н), 7.67 (d, 1 Н), 7.3 (d, 1 Н), 7.13 (d, 1 Н), 6.72 (d, 1 Н)
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 158.4, 146.8, 145.6, 136.4, 125.5, 124.6, 123.3, 117.5, 109.3, 104.6
Синтез R2bc: 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 1,4-бензодиоксан-6-бороновой кислоты в качестве реагентов, получали соединение Синтеза R2bc. MCBP: рассчитано для C14H11N3O3: 269.0800, найдено: 270.0881 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.05 (brs, 1 Н), 7.92 (d, 1 Н), 7.4 (d, 1 Н), 7.22 (d, 1 Н), 7.13 (dd, 1 Н), 6.99 (d, 1 Н), 6.63 (d, 1 Н), 4.33-4.25 (m, 4 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.4, 124.3, 117.7, 117.6, 113.8, 103.2.
Синтез R2bd: 7-(2H-1,3-бензодиоксол-5-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 3,4-метилендиоксифенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bd. МСВР: рассчитано для C13H9N3O3: 255.0644, найдено: 256.0719 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.05 (brs, 1 Н), 7.92 (d, 1 Н), 7.4 (d, 1 Н), 7.29 (d, 1 Н), 7.12 (dd, 1 Н), 7.05 (d, 1 Н), 6.63 (d, 1 Н), 6.11 (s, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.5, 124.5, 118.2, 108.7, 106.5, 103.1, 102.2.
Синтез R2be: 7-(нафталин-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 2-нафталинбороновой кислоты в качестве реагентов, получали соединение Синтеза R2be. МСВР: рассчитано для C16H11N3O: 261.0902, найдено: 262.0982 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.14 (s, 1 Н), 8.25 (d, 1 Н), 8.09 (d, 1 Н), 8.01 (m, 1 Н), 8.01 (m, 1 Н), 8 (s, 1 Н), 7.91 (dd, 1 Н), 7.63 (d, 1 Н), 7.6 (tm, 1 Н), 7.57 (tm, 1 Н), 6.74 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.6, 144.8, 135.4, 133.4, 132, 129.4, 128.4, 128.2, 127.4, 126.9, 124.4, 123.5, 122.3, 109.9, 103.8.
Синтез R2bf: 7-(3-метилфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 3-йодтолуола в качестве реагентов, получали соединение Синтеза R2bf. МСВР: рассчитано для C13H11N3O: 225.0902, найдено: 226.098 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.08 (brs, 1 Н), 7.95 (d, 1 Н), 7.52 (brs, 1 Н), 7.49 (dm, 1 Н), 7.46 (d, 1 Н), 7.41 (t, 1 Н), 7.22 (brd, 1 Н), 6.67 (d, 1 Н), 2.39 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.3, 144.6, 139.2, 137.8, 129.5, 128.1, 125.2, 124.2, 121.8, 109.7, 103.5, 21.4.
Синтез R2bg: 7-[3-(трифторметил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 3-йодбензотрифторида в качестве реагентов, получали соединение Синтеза R2bg. МСВР: рассчитано для C13H8F3N3O: 279.0620, найдено: 280.0699 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.19 (brs, 1 Н), 8.18 (brs, 1 Н), 8.07 (dm, 1 Н), 8.02 (d, 1 Н), 7.79 (t, 1 Н), 7.77 (dm, 1 Н), 7.65 (d, 1 Н), 6.73 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 145.1, 131.1, 128.3, 124, 123.9, 121, 104.1.
Синтез R2bh: 7-{3-[(4-метилпиперазин-1-ил)метил]фенил}-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и сложного пинаколового эфира 3-(4-метил-1-пиперазинилметил)бензолбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bh. МСВР: рассчитано для C18H21N5O: 323.1746, найдено: 324.1828 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.37/12.2/11.95 (brs, 3 Н), 8.04 (brs, 1 Н), 7.98 (s, 1 Н), 7.91 (dm, 1 Н), 7.67 (dm, 1 Н), 7.63 (d, 1 Н), 7.62 (t, 1 Н), 6.72 (d, 1 Н), 4.49 (brs, 2 Н), 3.8-3.3 (brm, 8 Н), 2.8 (brs, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.8, 130.3, 130, 127.3, 125.7, 124, 103.9, 58.7, 42.7.
Синтез R2bi: 7-[3-(гидроксиметил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 3-йодбензилового спирта в качестве реагентов, получали соединение Синтеза R2bi. MCBP: рассчитано для C13H11N3O2: 241.0851, найдено: 242.0935 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.11 (brs, 1 Н), 7.95 (d, 1 Н), 7.64 (b rt, 1 Н), 7.55 (dm, 1 Н), 7.48 (t, 1 Н), 7.46 (d, 1 Н), 7.35 (dm, 1 Н), 6.68 (d, 1 Н), 4.58 (s, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.4, 144.6, 144.4, 137.7, 129.4, 125.4, 124.2, 123, 122.5, 109.7, 103.5, 62.9.
Синтез R2bj: 7-(3-хлорфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-хлор-3-йодбензола в качестве реагентов, получали соединение Синтеза R2bj. MCBP: рассчитано для C12H8ClN3O: 245.0356, найдено: 246.0437 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.17 (brs, 1 Н), 8 (d, 1 Н), 7.92 (m, 1 Н), 7.74 (dm, 1 Н), 7.58 (d, 1 Н), 7.57 (t, 1 Н), 7.47 (dm, 1 Н), 6.7 (d, 1 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 145, 131.3, 127.2, 124.1, 123.9, 122.9, 104.
Синтез R2bk: 7-(3-фторфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-фтор-3-йодбензола в качестве реагентов, получали соединение Синтеза R2bk. MCBP: рассчитано для C12H8N3OF: 229.0651, найдено: 230.0729 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.17 (brs, 1 Н), 7.99 (d, 1 Н), 7.72 (dm, 1 Н), 7.64 (m, 1 Н), 7.58 (d, 1 Н), 7.58 (m, 1 Н), 7.25 (m, 1 Н), 6.71 (d, 1 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.9, 131.4, 130.9, 123.9, 120.2, 114, 111.6.
19F-ЯМР (376.5 МГц, MSM-d6): δ (м.д.) - 111.7.
Синтез R2bl: 7-[3-(диметиламино)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 3-(N,N-диметиламино)фенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bl. MCBP: рассчитано для C14H14N4O: 254.1168, найдено: 255.1229 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.04 (brs, 1 Н), 7.92 (d, 1 Н), 7.45 (d, 1 Н), 7.3 (t, 1 Н), 6.94 (m, 1 Н), 6.93 (dm, 1 Н), 6.74 (dm, 1 Н), 6.65 (d, 1 Н), 2.95 (s, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.3, 129.9, 124.4, 112.4, 111.4, 108.6, 103.1, 40.5.
Синтез R2bm: 7-[3-(морфолин-4-ил)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 3-(морфолино)фенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bm. 1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.05 (brs, 1 Н), 7.93 (s, 1 Н), 7.47 (d, J=3.53 Гц, 1 Н), 7.36 (t, J=8.13 Гц, 1 Н), 7.19 (t, J=2.20 Гц, 1 Н), 7.11 (dd, J=1.27, 7.93 Гц, 1 Н), 6.98 (dd, J=1.96, 8.49 Гц, 1 Н), 6.65 (d, J=3.5 Гц, 1 Н), 3.75 (t, J=4.61 Гц, 4 Н), 3.18 (t, J=4.61 Гц, 4 Н).
Синтез R2bo: 7-(3-метоксифенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 3-йоданизола в качестве реагентов, получали соединение Синтеза R2bo. MCBP: рассчитано для C13H11N3O2: 241.0851, найдено: 242.0928 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.1 (brs, 1 Н), 7.95 (d, 1 Н), 7.51 (d, 1 Н), 7.44 (t, 1 Н), 7.31 (m, 1 Н), 7.3 (m, 1 Н), 6.98 (dm, 1 Н), 6.67 (d, 1 Н), 3.82 (s, 3 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.6, 130.4, 124.2, 116.7, 112.9, 110.5, 103.5.
Синтез R2bp: 7-[3-(трифторметокси)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 3-(трифторметокси)йодбензола в качестве реагентов, получали соединение Синтеза R2bp. MCBP: рассчитано для C13H8F3N3O2: 295.0569, найдено: 296.0651 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.91 (s, 1 Н), 8 (s, 1 Н), 7.87 (t, 1 Н), 7.82 (ddd, 1 Н), 7.68 (t, 1 Н), 7.6 (d, 1 Н), 7.41 (ddd, 1 Н), 6.71 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 145.1, 131.5, 123.9, 123.2, 119.5, 117.1, 104.1.
Синтез R2bq: 7-[3-(бензилокси)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-бензилокси-3-йодбензола в качестве реагентов, получали соединение Синтеза R2bq. МСВР: рассчитано для C19H15N3O2: 317.1164, найдено: 318.1235 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.1 (brs, 1 Н), 7.95 (d, 1 Н), 7.51 (d, 1 Н), 7.51-7.31 (ш, 5 Н), 7.44 (t, 1 Н), 7.41 (m, 1 Н), 7.32 (dm, 1 Н), 7.05 (dm, 1 Н), 6.68 (d, 1 Н), 5.18 (s, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.6, 130.5, 124.1, 116.8, 113.6, 111.4, 103.6, 70.
Синтез R2br: 7-(6-метилпиридин-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-йод-6-метилпиридина в качестве реагентов, получали соединение Синтеза R2br. МСВР: рассчитано для C12H10N4O: 226.0855, найдено: 227.0933 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12 (brs, 1 Н), 8.25 (dm, 1 Н), 8.05 (s, 1 Н), 7.9 (t, 1 Н), 7.88 (d, 1 Н), 7.25 (dm, 1 Н), 6.68 (d, 1 Н), 2.52 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.9, 139.5, 122, 121.8, 113.8, 103.7, 24.4.
Синтез R2bs: 7-(6-метоксипиридин-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Смесь соединения Синтеза R1a (1.0 г, 6.51 ммоль), 2-йод-6-метоксипиридина (2.35 г, 9.77 ммоль, 1.5 экв.), йодида меди(I) (125 мг, 0.65 ммоль, 0.1 экв.), ортофосфата калия (2.76 г, 13 ммоль, 2 экв.) и (1R,2R)-(-)-1,2-диаминоциклогексана (74 мг, 0.65 ммоль, 0.1 экв.) в PDO (50 мл) перемешивали в инертной атмосфере в течение 4 часов при 100°С. Неорганические вещества отфильтровывали, фильтрат упаривали, и полученный в результате остаток очищали с помощью флэш-хроматографии (ДХМ).
Полученный арилированный продукт (920 мг, 3.5 ммоль) и моногидрат гидроксида лития (1.48 г, 35 ммоль) перемешивали в смеси PDO (15 мл) и воды (15 мл) при 110°С в течение 24 часов. Остаток подкисляли водным раствором HCl (1 н., 50 мл) и полученный в результате осадок отфильтровывали и сушили с получением соединения Синтеза R2bs.
МСВР: рассчитано для C12H10N4O2: 242.0804, найдено: 243.0884 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.21 (brs, 1 Н), 8.08 (dd, 1 Н), 8.03 (s, 1 Н), 7.94 (d, 1 Н), 7.9 (t, 1 Н), 6.78 (dd, 1 Н), 6.7 (d, 1 Н), 3.94 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 163.2, 158.5, 147.6, 147.4, 144.9, 141.9, 121.9, 111.2, 108.4, 108.4, 103.8, 53.9.
Синтез R2bt: 7-(нафталин-1-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 1-нафталинбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bt. МСВР: рассчитано для C16H11N3O: 261.0902, найдено: 262.0984 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.04 (s, 1 Н), 8.12 (d, 1 Н), 8.09 (d, 1 Н), 7.78 (d, 1 Н), 7.67 (t, 1 Н), 7.61 (dm, 1 Н), 7.6 (t, 1 Н), 7.51 (tm, 1 Н), 7.39 (d, 1 Н), 7.21 (t, 1 Н), 6.77 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.9, 149.2, 144.6, 134.2, 134.1, 130.4, 129.5, 128.7, 127.8, 127.2, 126.4, 126.3, 126, 123, 108.7, 103.1
Синтез R2bu: 7-фенил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и йодбензола в качестве реагентов, получали соединение Синтеза R2bu. МСВР: рассчитано для C12H9N3O: 211.0746, найдено: 212.083 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.1 (brs, 1 Н), 7.95 (d, 1 Н), 7.71 (m, 2 Н), 7.54 (m, 2 Н), 7.5 (d, 1 Н), 7.4 (m, 1 Н), 6.69 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.8, 147.3, 144.6, 137.8, 129.7, 127.4, 124.6, 124.1, 109.8, 103.6.
Синтез R2bv: 7-(2-метилфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 2-метилфенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bv. MCBP: рассчитано для C13H11N3O: 225.0902, найдено: 226.098 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12 (brs, 1 Н), 7.83 (d, 1 Н), 7.41 (m, 1 Н), 7.41 (m, 1 Н), 7.35 (m, 1 Н), 7.3 (d, 1 Н), 7.21 (d, 1 Н), 6.66 (d, 1 Н), 2.01 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.9, 148.2, 144.4, 136.9, 135.6, 131.2, 129.2, 128.5, 127.1, 125.3, 108.6, 102.9, 17.9.
Синтез R2bw: 7-(2-хлорфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 2-хлорфенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bw. MCBP: рассчитано для C12H8ClN3O: 245.0356, найдено: 246.0437 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.06 (brs, 1 Н), 7.86 (d, 1 Н), 7.73-7.48 (m, 4 Н), 7.27 (d, 1 Н), 6.68 (d, 1 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.7, 125.4, 102.2.
Синтез R2bx: 7-(2-фторфенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 2-фторфенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bx. MCBP: рассчитано для C12H8N3OF: 229.0651, найдено: 230.0730 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 12.09 (brs, 1 Н), 7.9 (d, 1 Н), 7.61 (m, 1 Н), 7.54 (m, 1 Н), 7.48 (m, 1 Н), 7.38 (m, 1 Н), 7.34 (dd, 1 Н), 6.7 (d, 1 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.8, 130.6, 129.6, 125.4, 125.3, 117, 103.5.
Синтез R2by: 7-[2-(диметиламино)фенил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и диметил[2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил]амина в качестве реагентов, получали соединение Синтеза R2by. MCBP: рассчитано для C14H14N4O: 254.1168, найдено: 255.1237 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12 (brs, 1 Н), 7.85 (d, 1 Н), 7.36 (m, 1 Н), 7.24 (dm, 1 Н), 7.2 (d, 1 Н), 7.13 (dm, 1 Н), 7.02 (m, 1 Н), 6.64 (d, 1 Н), 2.36 (s, 6 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 144.4, 130.1, 129.4, 125.5, 121.1, 119, 102.9, 42.4.
Синтез R2bz: 7-(2-метоксифенил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 2-метоксифенилбороновой кислоты в качестве реагентов, получали соединение Синтеза R2bz. MCBP: рассчитано для C13H11N3O2: 241.0851, найдено: 242.092 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6): δ (м.д.) 11.96 (brs, 1 Н), 7.82 (d, 1 Н), 7.46 (m, 1 Н), 7.37 (dm, 1 Н), 7.24 (dm, 1 Н), 7.18 (d, 1 Н), 7.08 (m, 1 Н), 6.6 (d, 1 Н), 3.74 (s, 3 Н).
13С-ЯМР (100 МГц, MSM-d6): δ (м.д.) 144.2, 130.2, 129.3, 126, 120.8, 113.1, 102.4.
Синтез R2ca: 7-(пиридин-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-йодпиридина в качестве реагентов, получали соединение Синтеза R2ca. MCBP: рассчитано для C11H8N4O: 212.0698, найдено: 213.0774 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.29 (s, 1 Н), 8.55 (dd, 1 Н), 8.47 (dd, 1 Н), 8.06 (brs, 1 Н), 8.03 (t, 1 Н), 7.9 (d, 1 Н), 7.4 (t, 1 Н), 6.7 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 149.1, 145, 139.4, 122.5, 122, 116.9, 104.
15N-ЯМР (50.6 МГц, MSM-d6): δ (м.д.) 171.2.
Синтез R2cb: 7-(пиридин-3-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и пиридин-3-бороновой кислоты в качестве реагентов, получали соединение Синтеза R2cb. МСВР: рассчитано для C11H8N4O: 212.0698, найдено: 213.0774 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.29 (s, 1 Н), 8.55 (dd, 1 Н), 8.47 (dd, 1 Н), 8.06 (brs, 1 Н), 8.03 (t, 1 Н), 7.9 (d, 1 Н), 7.4 (t, 1 Н), 6.7 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 149.1, 145, 139.4, 122.5, 122, 116.9, 104.
15N-ЯМР (50.6 МГц, MSM-d6): δ (м.д.) 171.2.
Синтез R2cc: 7-(тиофен-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-йодтиофена в качестве реагентов, получали соединение Синтеза R2cc. МСВР: рассчитано для C10H7N3OS: 217.0310, найдено: 218.0384 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.2 (brs, 1 Н), 8.03 (s, 1 Н), 7.58 (d, 1 Н), 7.43 (dd, 1 Н), 7.39 (dd, 1 Н), 7.07 (dd, 1 Н), 6.69 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.5, 147.2, 145.3, 138.7, 126, 124.3, 122.8, 119.2, 109.4, 104.2.
Синтез R2cd: 7-(пиридин-4-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и сложного пинаколового эфира пиридин-4-бороновой кислоты в качестве реагентов, получали соединение Синтеза R2cd. МСВР: рассчитано для C11H8N4O: 212.0698, найдено: 213.0773 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 12.31 (brs, 1 Н), 8.69 (m, 2 Н), 8.05 (s, 1 Н), 7.99 (m, 2 Н), 7.73 (d, 1 Н), 6.76 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 151.3, 145.6, 122.8, 117.3, 105.
Синтез R2ce: 7-(фуран-3-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фурана в качестве реагентов, получали соединение Синтеза R2ce. MCBP: рассчитано для C10H7N3O2: 201.0538, найдено: 202.0617 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.13 (brs, 1 Н), 8.32 (dd, 1 Н), 8 (d, 1 Н), 7.8 (dd, 1 Н), 7.52 (d, 1 Н), 7.17 (dd, 1 Н), 6.66 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.6, 147.1, 145, 143.9, 133.8, 126, 123, 109.6, 106.5, 103.8.
Синтез R2cf: 7-(тиофен-3-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 2, исходя из соединения Синтеза R1a и сложного пинаколового эфира тиофен-3-бороновой кислоты в качестве реагентов, получали соединение Синтеза R2cf. MCBP: рассчитано для C10H7N3OS: 217.0310, найдено: 218.0390 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.14 (s, 1 Н), 7.99 (d, 1 Н), 7.92 (dd, 1 Н), 7.71 (dd, 1 Н), 7.68 (dd, 1 Н), 7.57 (d, 1 Н), 6.66 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.6, 147, 144.8, 136.3, 127, 123.8, 123.3, 115.1, 109.5, 103.5.
Синтез R2cg: 7-(1-метил-1H-имидазол-4-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йод-1-метил-1H-имидазола в качестве реагентов, получали соединение Синтез R2cg. MCBP: рассчитано для C10H9N5O: 215.0807, найдено: 216.0879 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 9.24-7.3 (vbrs, 3 Н), 7.51 (d, 1 Н), 6.72 (brs, 1 Н), 3.77 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 121.7, 103.5, 35.
15N-ЯМР (50.6 МГц, MSM-d6): δ (м.д.) 153.
Синтез R2ch: 7-(1-метил-1H-пиразол-4-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 4-йод-1-метил-1Н-пиразола в качестве реагентов, получали соединение Синтеза R2ch. MCBP: рассчитано для C10H9N5O: 215.0807, найдено: 216.0889 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.12 (brs, 1 Н), 8.27 (s, 1 Н), 7.96 (s, 1 Н), 7.91 (d, 1 Н), 7.42 (d, 1 Н), 6.63 (d, 1 Н), 3.89 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.6, 146.9, 144.7, 132.1, 124.3, 123.4, 121.4, 109, 103.4, 38.5.
Синтез R2ci: 7-[1-(дифторметил)-1H-пиразол-4-ил]-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 1-(дифторметил)-4-йод-1H-пиразола в качестве реагентов, получали соединение Синтеза R2ci. МСВР: рассчитано для C10H7F2N5O: 251.0619, найдено: 252.0682 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 11.88 (brs, 1 Н), 8.83 (d, 1 Н), 8.4 (d, 1 Н), 8.03 (s, 1 Н), 7.91 (t, 1 Н), 7.58 (d, 1 Н), 6.69 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 145.2, 136.2, 123.2, 121.3, 111, 104.
Синтез R2cj: 7-(пиримидин-2-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Соединение Синтеза R1b (300 мг, 2.011 ммоль, 1 экв.), 2-хлорпиримидин (2.413 ммоль, 1.2 экв.) и безводный K2CO3 (417 мг, 3.017 ммоль, 1.5 экв.) нагревали в ДМФА (10 мл) при 150°С в течение 2 часов. Реакционную смесь фильтровали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MCN, градиент) с получением 4-метокси-7-пиримидин-2-илпирроло[2,3-d] пиримидина.
Затем полученный продукт (0.633 ммоль, 1 экв.), 1М водный раствор HCl (3 мл) и PDO (60 мл) перемешивали при 100°С в течение 1 часа. После завершения реакции, смесь упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MCN, градиент) с получением соединения Синтеза R2cj. МСВР: рассчитано для C10H7N5O: 213.0651, найдено: 214,0735 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.19 (brs, 1 Н), 8.94 (d, 1 Н), 8.01 (s, 1 Н), 7.78 (d, 1 Н), 7.54 (t, 1 Н), 6.71 (d, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 159.7, 158.7, 156, 148.1, 145.2, 123.3, 120.1, 111.4, 104.5.
Синтез R2ck: 7-(1,3-тиазол-2-ил)-3H,4Н,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и 2-йодтиазола в качестве реагентов, получали соединение Синтеза R2ck. MCBP: рассчитано для C9H6N4OS: 218.0262, найдено: 219.0335 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MeCN-d3) δ м.д. 8.5 (s, 1 Н), 7.62 (d, 1 Н), 7.52 (d, 1 Н), 7.22 (d, 1 Н), 6.51 (d, 1 Н).
13С-ЯМР (125 МГц, MeCN-d3) δ м.д. 154.5, 137.9, 116.8, 114.8, 104.2.
Синтез R2cl: 7-(1H-индол-1-ил)-3H,4Н,7H-пирроло [2,3-d]пиримидин-4-он
Соединение Синтеза R1b (1.74 г, 11.67 ммоль) растворяли в ДМФА (80 мл) и охлаждали до 0°С. Медленно добавляли гидрид натрия (60% дисп., 1.87 г, 46.67 ммоль) и смесь перемешивали в течение 30 минут при 0°С. К реакционной смеси добавляли гидроксиламин-О-сульфоновую кислоту (2.11 г, 18.67 ммоль), давали нагреться до к.т. и перемешивали в течение 20 часов. К реакционной смеси добавляли воду (100 мл) и экстрагировали с помощью ДХМ (4×50 мл). Объединенные органические слои промывали водой и сушили над MgSO4 и упаривали. Остаток растворяли в MSM и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Часть полученного в результате N-аминосоединения (500 мг, 3.05 ммоль) растворяли в PDO (5 мл) и добавляли 2,5-диметокситетрагидрофуран (454 мл, 462 мг, 3.5 ммоль). Смесь перемешивали при 100°С в течение 115 часов. Реакционную смесь разбавляли водным раствором HCl (5 н., 2 мл) и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R2cl. MCBP: рассчитано для C14H10N4O: 250.0854, найдено: 250.2000 [(М форма)].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.22 (brs, 1 Н), 7.86 (s, 1 Н), 7.71 (d, 1 Н), 7.68 (m, 1 Н), 7.58 (d, 1 Н), 7.17 (m, 1 Н), 7.17 (m, 1 Н), 6.86 (m, 1 Н), 6.73 (d, 1 Н), 6.68 (dd, 1 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.5, 147.9, 145.9, 137, 129.7, 126.3, 125.4, 123.5, 121.5, 121.5, 109, 107, 102.3, 101.8.
Синтез R2cm: 7-(1H-пиррол-1-ил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Соединение Синтеза R1b (1.74 г, 11.67 ммоль) растворяли в ДМФА (80 мл) и охлаждали до 0°С. Медленно добавляли гидрид натрия (60% дисп., 1.87 г, 46.67 ммоль) и перемешивали в течение 30 минут при 0°С. К реакционной смеси добавляли гидроксиламин-О-сульфоновую кислоту (2.11 г, 18.67 ммоль), давали нагреться до к.т. и перемешивали в течение 20 часов. К реакционной смеси добавляли воду (100 мл) и экстрагировали с помощью ДХМ (4×50 мл). Объединенные органические слои промывали водой и сушили над MgSO4, и упаривали. Остаток растворяли в MSM и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Часть полученного в результате N-аминосоединения (500 мг, 3.05 ммоль) растворяли в PDO (5 мл) и добавляли 2,5-диметокситетрагидрофуран (454 мл, 462 мг, 3.5 ммоль). Смесь перемешивали при 100°С в течение 115 часов. Реакционную смесь разбавляли водным раствором HCl (5 н., 2 мл) и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
К части полученного в результате соединения (63 мг, 0.294 ммоль) добавляли PDO (25 мл) и водный раствор HCl (1 н., 1.3 мл) и перемешивали при 60°С в течение 5 часов. Реакционную смесь упаривали и остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R2cm. MCBP: рассчитано для C10H8N4O: 200.0698, найдено: 201.0770 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ (м.д.) 12.18 (brs, 1 Н), 7.92 (s, 1 Н), 7.46 (d, 1 Н), 7.12 (m, 2 Н), 6.61 (d, 1 Н), 6.21 (m, 2 Н).
13С-ЯМР (125 МГц, MSM-d6): δ (м.д.) 158.4, 147.4, 145.8, 125.1, 122.8, 108, 106.7, 101.1.
Синтез R2de: 6-метил-7-фенил-3H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и йодбензола в качестве реагентов, получали 4-метокси-7-фенилпирроло[2,3-d]пиримидин (без гидролиза). Этот сырой продукт (450 мг, 2 ммоль) растворяли в ТГФ (18 мл), перемешиваемом при -78°С, затем добавляли LDA раствор (1.8 М, 1.7 мл, 3 ммоль). После одного часа перемешивания при -78°С, добавляли раствор йодметана (190 мкл, 3 ммоль) в ТГФ (5 мл) и перемешивание продолжали в течение 90 минут. Затем реакционную смесь разбавляли соляным раствором (10 мл) и упаривали, наносили на целит и очищали с помощью флэш-хроматографии (Гексан-ЕЕО=7-1).
Полученный в результате сырой продукт (400 мг, 1.6 ммоль) растворяли в конц. водном растворе HCl (330 мкл, ~12.2 М, 4 ммоль) и PDO (5 мл), и перемешивали при 100°С в течение 2 часов. После завершения реакции, смесь частично упаривали и образовавшуюся суспензию фильтровали. Твердое вещество на фильтре промывали водой и сушили с получением соединения Синтеза R2de. МСВР: рассчитано для C13H11N3O: 225.0902, найдено: 226.0985 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 11.94 (s, 1 Н), 7.76 (d, 1 Н), 7.55 (tm, 2 Н), 7.49 (tm, 1 Н), 7.4 (dm, 2 Н), 6.41 (d, 1 Н), 2.17 (d, 3 Н).
13С-ЯМР(125 МГц, MSM-d6): δ м.д. 158.4, 143.6, 136.2, 132.6, 129.6, 128.7, 128.5, 100.9, 13.3.
Синтез R2df: 9-метил-3H-пиримидо[4,5-6]индол-4-он
Синтез R1b (500 мг, 3.06 ммоль) и 2,5-диметокситетрагидрофуран (810 мг, 6.13 ммоль, d=1.02, 795 мкл) в PDO (5 мл) нагревали до 100°С в течение 102 часов, затем добавляли 1 н. водный раствор HCl (5 мл). Смесь растворяли в ДМФА и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R2df. МСВР: рассчитано для C11H9N3O: 199.0746, найдено: 200.0827 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 12.33 (brs, 1 Н), 8.21 (s, 1 Н), 7.63 (dm, 1 Н), 7.41 (ddd, 1 Н), 7.29 (td, 1 Н), 3.86 (s, 3 Н)
13С-ЯМР(125 МГц, MSM-d6): δ м.д. 158.5, 153.5, 148.1, 137, 124.6, 122, 121.8, 121, 110.7, 100.1, 28.5
Синтез R2dg: 6,8-диметилпиримидо[5,4-6]индолизин-4(3H)-он
Соединение Синтеза R1b (1.74 г, 11.67 ммоль) растворяли в ДМФА (80 мл) и охлаждали до 0°С. Медленно добавляли гидрид натрия (60% дисп., 1.87 г, 46.67 ммоль) и перемешивали в течение 30 минут при 0°С. К реакционной смеси добавляли гидроксиламин-О-сульфоновую кислоту (2.11 г, 18.67 ммоль), давали нагреться до к.т. и перемешивали в течение 20 часов. К реакционной смеси добавляли воду (100 мл) и экстрагировали с помощью ДХМ (4×50 мл). Объединенные органические слои промывали водой, сушили над MgSO4 и упаривали.
Часть полученного в результате N-аминосоединения (300 мг, 1.83 ммоль) и ацетилацетон (206 мкл, 201 мг 2.01 ммоль,) растворяли в 5 мл уксусной кислоты и нагревали до 120°С в течение 2.5 часов, затем добавляли ТФУ (5 мл). Смесь нагревали при 120°С в течение 18 часов. Затем добавляли воду (1 мл) и метанол (10 мл) и раствор упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), с получением соединения Синтеза R2dg. MCBP: рассчитано для C11H10N4O: 214.0855, найдено: 215.0935 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 12.16 (s, 1 Н), 8 (s, 1 Н), 6.89 (s, 1 Н), 6.68 (d, 1 Н), 2.45 (d, 3 Н), 2.44 (s, 3 Н).
13С-ЯМР(125 МГц, MSM-d6) δ м.д. 159.7, 152.5, 143.4, 141.2, 138.9, 127.7, 115.5, 109.8, 91.2, 21.9, 17.4.
Синтез R2dh: 6-хлор-7-фенил-3H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 3, исходя из соединения Синтеза R1b и йодбензола в качестве реагентов, получали 4-метокси-7-фенилпирроло[2,3-d]пиримидин (без гидролиза). Сырой продукт (394 мг, 1.75 ммоль) растворяли в ТГФ (14 мл), перемешиваемом при -78°С, затем добавляли LDA раствор (1.8 М, 1.2 мл, 2.16 ммоль). После одного часа перемешивания при -78°С, добавляли раствор гексахлорэтана (632 мг, 2.63 ммоль) в ТГФ (5 мл) и перемешивание продолжали в течение 90 минут. Затем реакционную смесь разбавляли соляным раствором (10 мл), упаривали, наносили на целит и очищали с помощью флэш-хроматографии (Гексан-ЕЕО=9-1).
Полученный в результате сырой продукт (110 мг, 0.42 ммоль) растворяли в конц. водном растворе HCl (82 мкл, ~12.2 М, 1 ммоль) и PDO (5 мл), и перемешивали при 100°С в течение 2 часов. После завершения реакции, смесь частично упаривали. Образовавшуюся суспензию фильтровали и твердое вещество на фильтре промывали водой и сушили с получением соединения Синтеза R2dh. МСВР: рассчитано для C12H8N3OCl: 245.0356, найдено: 246.043 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 12.16 (s, 1 Н), 7.88 (s, 1 Н), 7.6-7.52 (m, 5 Н), 6.78 (s, 1 Н).
13С-ЯМР(125 МГц, MSM-d6) δ м.д. 157.6, 148.2, 145.3, 101.6.
Синтез R2di: 6-йод-7-метил-3H-пирроло[2,3-d]пиримидин-4-он
Перемешиваемый раствор соединения Синтеза R1a (8 г, 52.1 ммоль) в абс. ДМФА (50 мл) охлаждали до 0°С, затем добавляли гидрид натрия (3.13 г, 60% дисп. в минеральном масле, 78.2 ммоль, 1.5 экв.) и перемешивали в течение 20 минут при к.т. под Ar. К реакционной смеси добавляли метилйодид (8.2 г, 57.2 ммоль, d=2.28, 3.6 мл) и перемешивали в течение 1.5 ч при к.т. Смесь выливали в воду (50 мл) с получением твердого соединения, которое отфильтровывали.
Часть полученного в результате твердого соединения (500 мг, 2.98 ммоль) растворяли в 5 мл абс. ТГФ и охлаждали до -78°С. Затем по каплям добавляли 2 М LDA (1.7 мл, 3.4 ммоль). Смесь перемешивали при -78°С в течение 1 часа, затем добавляли йодид (757 мг, 2.98 ммоль). Раствору давали нагреться до к.т. и перемешивали в течение 22 часов. В заключение добавляли 5 мл воды и наблюдали образование твердого соединения, которое отфильтровывали с получением соединения Синтеза R2di. МСВР: рассчитано для C7H6IN3O: 274.9556, найдено: 275.9634 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 11.97 (s, 1 Н), 7.85 (s, 1 Н), 6.79 (s, 1 Н), 3.64 (s, 3 Н).
13С-ЯМР(125 МГц, MSM-d6) δ м.д. 157.3, 149.1, 144.2, 111.4, 110.3, 80.4, 33.2.
Синтез R2dj: 5-фтор-7-метил-3H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 1, исходя из 4-хлор-5-фтор-7H-пирроло[2,3-d]пиримидина (взамен соединения Синтеза R1a) и йодметана в качестве алкилирующего агента, получали соединение Синтеза R2dj. МСВР: рассчитано для C7H6FN3O: 167.0495, найдено: 168.0574 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 11.97 (brs, 1 Н), 7.88 (s, 1 Н), 7.07 (s, 1 Н), 3.64 (s, 3 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 156.9, 144.6, 144.4, 143.1, 108.1, 97.0, 31.6.
Синтез R2dk: 3,6,7,8-тетрагидро-4H-пиримидо[5,4-b]пирролизин-4-он
Стадия 1: 4-метокси-7-((2-(триметилсилил)этокси)метил)-7Н-пирроло[2,3-d]пиримидин
В предварительно нагретой 100 мл двухгорлой сферической колбе с якорем магнитной мешалки и газовпускным патрубком соединение Синтеза R1b (2.0 г, 11.4 ммоль) растворяли в абс. ТГФ (45 мл). Раствор охлаждали до 0°С, и добавляли NaH (0.85 г, 3 экв.). Смесь перемешивали в течение 1 часа, затем добавляли SEM-Cl (3.55 мл, 1.5 экв.) с помощью шприца. Образовывался желтый раствор и белый осадок. Смеси давали нагреться до к.т., во время чего окрашивание исчезало. После обесцвечивания, реакцию гасили водой (30 мл). Смесь экстрагировали с помощью ЕЕО (3×30 мл) и собранные органические слои сушили над Na2SO4. После фильтрования, растворитель упаривали и сырой продукт очищали с помощью флэш-хроматографии (гексан:ЕЕО=20:1-9:1) с получением указанного в заголовке продукта в виде желтоватой жидкости.
Стадия 2: 6-йод-4-метокси-7-((2-(триметилсилил)этокси)метил)-7Н-пирроло[2,3-d]пиримидин
В предварительно нагретую 250 мл трехгорлую сферическую колбу с якорем магнитной мешалки и газовпускным патрубком загружали абс. ТГФ (30 мл) и диизопропиламин (2.7 мл, 1.5 экв.) в атмосфере азота. Смесь охлаждали до -78°С и добавляли n-BuLi (8.0 мл, 1.5 экв.) и перемешивали в течение 30 минут. Затем медленно в течение 30 минут добавляли 4-метокси-7-((2-(триметилсилил)этокси)метил)-7H-пирроло[2,3-d]пиримидин (3.64 г, 13.05 ммоль, 1 экв.), растворенный в абс. ТГФ (100 мл), и перемешивание продолжали в течение 1 часа. Затем медленно добавляли йод (3.95 г, 1.2 экв.), растворенный в абс. ТГФ (35 мл), и смесь перемешивали в течение дополнительных 3 часов. Затем охлаждающую баню удаляли и реакционную смесь оставляли нагреться до к.т. Добавляли солевой раствор (500 мл) и реакционный раствор три раза экстрагировали с помощью ЕЕО (150 мл). Органические фазы сушили, фильтровали, упаривали и очищали с помощью флэш-хроматографии (гексан : ЕЕО - 9:1) с получением указанного в заголовке продукта в виде желтовато-белого порошка.
Стадия 3: 6-йод-4-метокси-7Н-пирроло[2,3-d]пиримидин
В 100 мл сосуде Шленка, 6-йод-4-метокси-7-((2-(триметилсилил)этокси)метил)-7H-пирроло[2,3-d]пиримидин (4.72 г, 11.65 ммоль) растворяли в ТГФ (50 мл). К раствору добавляли TBAF.3H2O (11.34 г, 3 экв.) с 4А молекулярными ситами. Смесь нагревали при 95°С под азотом в течение ночи. После охлаждения смесь фильтровали через целит, и растворитель упаривали. К полученному в результате коричневому маслу добавляли воду и наблюдали осаждение не совсем белого порошка. Осадок отфильтровывали, промывали водой и MeCN (3×10 мл). После сушки, указанный в заголовке продукт получали в виде не совсем белого порошка.
Стадия 4: 7-аллил-6-йод-4-метокси-7Н-пирроло[2,3-d]пиримидин
В предварительно нагретой двухгорлой 100 мл сферической колбе с якорем магнитной мешалки и газовпускным патрубком 6-йод-4-метокси-7H-пирроло[2,3-d]пиримидин (900 мг, 3.27 ммоль) растворяли в абс. ТГФ (10 мл) под азотом. Затем добавляли трифенилфосфин (1.048 г, 1.2 экв.). Затем, при непрерывном перемешивании, с помощью шприца в колбу отмеряли аллиловый спирт (232 мг, 1.2 экв.). Смесь охлаждали до 0°С и с помощью шприца по каплям добавляли диизопропил-аза-дикарбоксилат (808 мг, 1.2 экв.). Смеси давали нагреться до к.т., и реакцию контролировали с помощью ТСХ. После завершения реакции, растворитель упаривали и сырой продукт очищали с помощью флэш-хроматографии (гексан : ЕЕО = 10:1) с получением указанного в заголовке продукта в виде белых кристаллов.
Стадия 5: 4-метокси-7,8-дигидро-6Н-пиримидо[5,4-b]пирролизин
В предварительно нагретый 100 мл сосуд Шленка отмеряли 7-аллил-6-йод-4-метокси-7H-пирроло[2,3-d]пиримидин (1.60 г, 5.1 ммоль) и растворяли в абс. ТГФ (50 мл). 9-Борабицикло[3.3.1]нонан (1.87 г, 3 экв.) отмеряли в перчаточной камере с двойным манифольдом, растворяли в абс. ТГФ (30 мл) и добавляли в сосуд Шленка с помощью шприца при 0°С. Реакционной смеси давали нагреться до к.т. и перемешивали в течение ночи. Затем [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (366 мг, 0.1 экв.) и K2CO3 (4.93 г, 7 экв.) отмеряли под азотом и добавляли к раствору. Смесь нагревали до 85°С в течение 4 часов. После завершения реакции растворитель упаривали и сырой продукт очищали с помощью флэш-хроматографии (гексан : ЕЕО = 3:1) с получением указанного в заголовке продукта в виде темно-красного твердого вещества.
Стадия 6: соединение Синтеза R2dk
Полученный в результате на Стадии 5, приведенной выше, метоксипирролизин (69.7 мг, 0.37 ммоль) и моногидрат гидроксида лития (155 мг, 3.7 ммоль) разбавляли в смеси PDO (2 мл) и воды (2 мл) и перемешивали при 110°С в течение 40 часов. После завершения реакции, смесь упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R2dk. МС рассчитано для C9H9N3O: 175.07, найдено: 175.2 [(М+Н)+ EI форма].
Синтез R2dl: 6,7,8,9-тетрагидро-3H-пиримидо[5,4-6]индолизин-4-он
Стадия 1: 7-(бут-3-ен-1-ил)-6-йод-4-метокси-7H-пирроло[2,3-d]пиримидин
В 100 мл сферической колбе, 6-йод-4-метокси-7H-пирроло[2,3-d]пиримидин (полученый на Стадии 3 Синтеза R2dk, 1.99 г, 7.23 ммоль) растворяли в ДМСО (70 мл), и добавляли KOH (690 мг, 1.7 экв.). Смесь обрабатывали ультразвуком в течение 10 минут, затем добавляли гомоаллилбромид (2.15 мл, 3 экв.) при 0°С. После нагревания до к.т., смесь перемешивали до завершения реакции. После завершения реакции добавляли воду (50 мл) и смесь экстрагировали с помощью ЕЕО (3×120 мл). Органические фазы собирали, сушили над сульфатом натрия и упаривали. Сырой продукт очищали с помощью флэш-хроматографии (гексан : ЕЕО = 20:1-5:1) с получением указанного в заголовке продукта в виде белого твердого вещества.
Стадия 2: 4-метикси-3,4,6,7,8,9-гексагидропиримидо[5,4-b]индолизин
7-Бут-3-енил-6-йод-4-метоксипирроло[2,3-d]пиримидин (164 мг, 0.5 ммоль) растворяли в ТГФ (2 мл) в сосуде Шленка в атмосфере азота. Смесь охлаждали до 0°С, с помощью шприца добавляли раствор 9-борабицикло[3.3.1]нонана (305 мг, 2.5 ммоль) в ТГФ (5 мл) и перемешивали в течение ночи при к.т. К реакционной смеси добавляли [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (75 мг, 0.1 ммоль) и K2CO3 (967 мг, 7 ммоль) и перемешивали в течение 3 часов при 80°С. Затем реакционную смесь упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гексан-ЕЕО=3-1).
Стадия 3: соединение Синтеза R2dl
Полученный в результате на Стадии 2, приведенной выше, метоксииндолизин (104 мг, 0.51 ммоль) и моногидрат гидроксида лития (215 мг, 5.1 ммоль), разбавляли в смеси PDO (2 мл) и воды (2 мл) и перемешивали при 110°С в течение 40 часов. После завершения реакции, смесь упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R2dl. МС: рассчитано для C10H11N3O: 189.09, найдено: 190 [(М+Н)+ EI форма].
Синтез R3a: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из 3H,4H,7H-пирроло[2,3-d]пиримидин-4-она в качестве реагента, получали соединение Синтеза R3a. МСВР: рассчитано для C24H29N5O3: 435.2270, найдено: 436.2345 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 11.91/11.9 (brs, 1 Н), 9.36/8.86 (brd+brq, 2 Н), 8.03/7.97 (s, 1 Н), 7.32-7.11 (m, 5 Н), 7.06/7.04 (dd, 1 Н), 6.47/6.43 (dd, 1 Н), 4.09-2.6 (m, 12 Н), 1.96-0.62 (m, 6 Н).
Синтез R3b: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-метил-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2b в качестве реагента, соединение Синтеза R3b получали в виде HCl соли. МСВР: рассчитано для C25H31N5O3: 449.2427, найдено: 450.2517 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.16/8.72 (brd/brq, 2 Н), 8.02/8.07 (s, 1 Н), 7.34-7.11 (m, 5 Н), 7.11/7.13 (d, 1 Н), 6.45/6.48 (d, 1 Н), 4.01/3.73 (d/s, 1 Н), 4.00-0.58 (m, 16 Н), 3.89 (d, 2 Н), 3.71 (s, 3 Н).
Синтез R3c: 7-этил-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2c в качестве реагента, соединение Синтеза R3c получали в виде HCl соли. МСВР: рассчитано для C26H33N5O3: 463.2583, найдено: 464.2654 [(М+Н)+ форма].
1H-ЯМР (500 МГц, MSM-d6) δ м.д. 9.16/8.72 (brd/brq, 2 Н), 8.01/8.07 (s, 1 Н), 7.33-7.09 (m, 5 Н), 7.18/7.19 (d, 1 Н), 6.45/6.49 (d, 1 Н), 4.13/4.15 (q, 2 Н), 4.01/3.73 (d/s, 1 Н), 4.00-0.58 (m, 16 Н), 3.89 (d, 2 Н), 1.34/1.35 (t, 3 Н).
Синтез R3d: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(пропан-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2d в качестве реагента, получали соединение Синтез R3d. MCBP: рассчитано для C27H35N5O3: 477.274, найдено: 478.2819 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.4/8.89 (brd+brq, 1+1 Н), 8.08/8.03 (s/s, 1 Н), 7.32-7.09 (m, 5 Н), 7.27/7.25 (d/d, 1 Н), 6.51/6.47 (d/d, 1 Н), 4.84 (m, 1 Н), 4.05-0.6 (m, 16 Н), 3.48/3.43 (m/m, 1 Н), 3.22 (m, 1 Н), 1.43 (d, 6 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 147.4, 121.1/121, 102.3/102.2, 46.4, 42.6/42.4, 41/40.6, 23.1.
Синтез R3e: 6-[3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-4-оксо-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-7-ил]-1,2-дигидропиридин-2-он
Используя Общую методику 15, исходя из соединения Синтеза R3bs в качестве реагента, соединение Синтез R3e получали в виде свободного основания. МСВР: рассчитано для C29H32N6O4: 528.2485, найдено: 529.2567 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 8.17/8.13 (s/s, 1 Н), 7.87/7.86 (d/d, 1 Н), 7.83/7.8 (d/d, 1 Н), 7.82 (t, 1 Н), 7.26-6.99 (m, 5 Н), 6.71/6.68 (d/d, 1 Н), 6.6 (d, 1 Н), 4.85 (brs, 1 Н), 4.12-0.75 (m, 16 Н), 3.21/3.15 (t/t, 1 Н), 2.86 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.4, 142, 122.2, 107.9, 107.1, 103.9/103.8, 46.4/46.3, 43.4/42.9.
Синтез R3g: 7-циклопропил-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2g в качестве реагента, соединение Синтеза R3g получали в виде HCl соли. МСВР: рассчитано для C27H33N5O3: 475.2583, найдено: 476.2668 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.26/8.78 (brd+brq, 2 Н), 8.12-6.38 (m, 8 Н), 4.05-0.62 (m, 23 Н).
Синтез R3h: 7-циклобутил-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2h в качестве реагента, получали соединение Синтеза R3h. МСВР: рассчитано для C28H35N5O3: 489.274, найдено: 490.2796 ((М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 8.92 (vbrs, 2 Н), 8.06/8.01 (s/s, 1 Н), 7.43/7.4 (d/d, 1 Н), 7.34-7.08 (m, 5 Н), 6.53/6.49 (d/d, 1 Н), 5.09 (m, 1 Н), 4.85 (s, 1 Н), 4.08-0.55 (m, 16 Н), 3.47/3.42 (m/m, 1 Н), 3.21 (m, 1 Н), 2.5/2.38 (m+m, 4 Н), 1.82 (m, 2 Н)
13С-ЯМР (500 МГц, MSM-d6) δ м.д. 147.6/147.5, 122/121.9, 102.5/102.4, 48.5, 42.6/42.5, 41/40.6, 31, 14.8
Синтез R3k: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(1-метилпиперидин-4-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2k в качестве реагента, соединение Синтеза R3k получали в виде HCl соли. МСВР: рассчитано для C30H40N6O3: 532.3162, найдено: 267.1658 [(М+2Н)2+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 10.87/10.67 (brs, 1 Н), 9.29/8.8 (brq+brd, 2 Н), 8.13/8.08 (s, 1 Н), 7.35-7.11 (m, 5 Н), 7.14/7.12 (d, 1 Н), 6.57/6.53 (d, 1 Н), 4.82 (brs, 1 Н), 4.76 (m, 1 Н), 4.08-2.61 (m, 16 Н), 2.78 (d, 3 Н), 2.47-1.96 (m, 4 Н), 1.95-0.59 (m, 6 Н).
Синтез R3m: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(проп-2-ин-1-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2m в качестве реагента, соединение Синтез R3m получали в виде HCl соли. МСВР: рассчитано для C27H31N5O3: 473.2427, найдено: 474.2502 [(М+Н)+ форма].
1H-ЯМР (500 МГц, MSM-d6) δ м.д. 9.32/8.83 (brd+brq, 2 Н), 8.12/8.06 (s, 1 Н), 7.33-7.12 (m, 12 Н), 7.33-7.12 (m, 5 Н), 7.22/7.2 (d, 1 Н), 6.55/6.51 (d, 1 Н), 5/4.98 (d, 2 Н), 3.44/3.43 (t, 1 Н), 1.92-0.62 (m, 6 Н).
Синтез R3n: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(2-метилпропил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2n в качестве реагента, соединение Синтеза R3n получали в виде HCl соли. МСВР: рассчитано для C28H37N5O3: 491.2896, найдено: 492.2963 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.3/8.81 (brd+brq, 2 Н), 8.07/8.01 (s, 1 Н), 7.33-7.12 (m, 5 Н), 7.15/7.13 (d, 1 Н), 6.49/6.46 (d, 1 Н), 4.05-2.61 (m, 14 Н), 2.12 (m, 1 Н), 1.92-0.61 (m, 6 Н), 0.84/0.83 (d, 6 Н).
Синтез R3o: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(2,2,2-трифторэтил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2o в качестве реагента, соединение Синтеза R3o получали в виде HCl соли. МСВР: рассчитано для C26H30F3N5O3: 517.2301, найдено: 518.2386 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.11/8.67 (brq+brd, 2 Н), 8.16-6.55 (m, 8 Н), 5.15-0.6 (m, 20 Н), 4.87 (brs, 1 Н).
Синтез R3p: 7-(2,2-дифторэтил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2p в качестве реагента, соединение Синтеза R3p получали в виде HCl соли. МСВР: рассчитано для C26H31F2N5O3: 499.2395, найдено: 500.2485 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.28/8.8 (brd+brq., 2 Н), 8.12/8.07 (s/s, 1 Н), 7.36-7.11 (m, 5 Н), 7.18/7.17 (d/d, 1 Н), 6.57/6.53 (d/d, 1 Н), 6.39 (tm, 1 Н), 4.6 (m, 2 Н), 4.07-0.6 (m, 16 Н), 3.48/3.42 (m/m, 1 Н), 3.22 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.2/148.1, 125.2, 114.4, 102.9/102.8, 46.1, 42.6/42.4, 41/40.6.
Синтез R3q: 7-(циклопропилметил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2q в качестве реагента, соединение Синтеза R3q получали в виде HCl соли. МСВР: рассчитано для C28H35N5O3: 489.2740, найдено: 490.2817 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.11/8.68 (brq+brd, 2 Н), 8.06/8 (s, 1 Н), 7.34-7.1 (m, 5 Н), 7.23/7.21 (d, 1 Н), 6.5/6.46 (d, 1 Н), 4.07-2.6 (m, 14 Н), 1.92-0.63 (m, 7 Н), 0.54-0.35 (m, 4 Н).
Синтез R3r: 7-(циклобутилметил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2r в качестве реагента, соединение Синтеза R3r получали в виде HCl соли. МСВР: рассчитано для C29H37N5O3: 503.2896, найдено: 504.2957 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 9.45/8.92 (brq+brd), 8.09/8.03 (s, 1 Н), 7.34-7.08 (m, 5 Н), 7.15/7.13 (d, 1 Н), 6.47/6.44 (d, 1 Н), 4.19-2.59 (m, 15 Н), 2.02-0.56 (m, 12 Н).
Синтез R3s: 7-(бута-2,3-диен-1-ил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2s в качестве реагента, соединение Синтеза R3s получали в виде HCl соли. МСВР: рассчитано для C28H33N5O3: 487.2583, найдено: 488.2657 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.28/8.8 (brd+brq, 2 Н), 8.09/8.03 (s, 1 Н), 7.34-7.11 (m, 5 Н), 7.15/7.14 (d, 1 Н), 6.51/6.47 (d, 1 Н), 5.5 (m, 1 Н), 4.9 (m, 2 Н), 4.88 (s, 1 Н), 4.73 (m, 2 Н), 4.06-2.63 (m, 12 Н), 1.94-0.6 (m, 6 Н).
Синтез R3t: 7-[3-(диметиламино)пропил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2t в качестве реагента, соединение Синтеза R3t получали в виде HCl соли. МСВР: рассчитано для C29H40N6O3: 520.3162, найдено: 261.1666 [(М+2Н)2+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 10.53 (brs, 1 Н), 9.33/8.83 (brs+brm, 2 Н), 8.13/8.07 (s/s, 1 Н), 7.36-7.14 (m, 5 Н), 7.23/7.21 (d/d, 1 Н), 6.53/6.5 (d/d, 1 Н), 4.2 (m, 2 Н), 4.06-0.55 (m, 16 Н), 3.48/3.43 (m/m, 1 Н), 3.22 (m, 1 Н), 3.02 (m, 2 Н), 2.72/2.71 (s/s, 6 Н), 2.17 (m, 2 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 147.9/147.8, 124.4/124.3, 102.4, 54.4, 42.6/42.4, 42.5, 42, 41/40.6, 25.6.
Синтез R3u: 7-(2-фторэтил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2u в качестве реагента, соединение Синтеза R3u получали в виде HCl соли. МСВР: рассчитано для C25H31FN5O3: 468.2411, найдено: 482.2555 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.16/8.71 (m+m, 2 Н), 8.08/8.03 (s, 1 Н), 7.34-7.11 (m, 5 Н), 7.2/7.18 (d, 1 Н), 6.53/6.49 (d, 1 Н), 4.82 (brs, 1 Н), 4.76 (dt, 2 Н), 4.44 (dt, 2 Н), 4.11-2.6 (m, 12 Н), 1.95-0.6 (m, 6 Н).
Синтез R3v: 7-[2-(диметиламино)этил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2v в качестве реагента, соединение Синтеза R3v получали в виде HCl соли. МСВР: рассчитано для C28H38N6O3: 506.3005, найдено: 254.1581 [(М+2Н)2+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 10.48 (brs, 1 Н), 9.27/8.8 (brs+brm, 2 Н), 8.16/8.11 (s/s, 1 Н), 7.37-7.16 (m, 5 Н), 7.25 (d, 1 Н), 6.57/6.54 (d/d, 1 Н), 4.9 (vbrs, 1 Н), 4.53 (m, 2 Н), 4.13-0.55 (m, 16 Н), 3.51 (m, 2 Н), 3.48/3.43 (brm/brm, 1 Н), 3.22 (m, 1 Н), 2.8/2.79 (d/d, 6 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.1, 124.4, 103, 55.9, 42.9, 42.6/42.4, 41/40.6, 39.6.
Синтез R3w: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(2-гидроксиэтил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2w в качестве реагента, получали соединение Синтеза R3w.
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 8.05/7.99 (s/s, 1 Н), 7.27-7.02 (m, 5 Н), 7.16/7.14 (d/d, 1 Н), 6.47/6.45 (d/d, 1 Н), 4.94/4.93 (t/t, 1 Н), 4.83/4.8 (s/s, 1 Н), 4.15 (m, 2 Н), 4.06-0.72 (m, 16 Н), 3.71 (m, 2 Н), 3.2/3.15 (m/m, 1 Н), 2.86 (m, 1 Н).
13С-ЯМР (100 МГц, MSM-d6) δ м.д. 147.4, 125.1, 101.8/101.7, 60.6, 47.3, 46.5/46.4, 43.4.
Синтез R3x: 7-[(4-хлорфенил)метил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2x в качестве реагента, соединение Синтеза R3x получали в виде HCl соли. МСВР: рассчитано для C31H34ClN5O3: 559.2350, найдено: 560.2418 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.04/8.63 (brd+brq, 2 Н), 8.07/8.02 (s, 1 Н), 7.44-7.07 (m, 9 Н), 7.26/7.24 (d, 1 Н), 6.54/6.5 (d, 1 Н), 5.34/5.33 (s, 2 Н), 4.81 (brs, 1 Н), 4.04-2.61 (m, 12 Н), 1.92-0.61 (m, 6 Н).
Синтез R3y: 7-[(3-хлорфенил)метил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2y в качестве реагента, соединение Синтеза R3y получали в виде HCl соли. МСВР: рассчитано для C31H34ClN5O3: 559.2350, найдено: 560.2432 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.1/8.67 (brd+brq, 2 Н), 8.09/8.03 (s, 1 Н), 7.4-7.08 (m, 9 Н), 7.29/7.27 (d, 1 Н), 6.55/6.52 (d, 1 Н), 5.35/5.34 (s, 2 Н), 4.83 (brs, 1 Н), 4.05-2.62 (m, 12 Н), 1.91-0.61 (m, 6 Н).
Синтез R3z: 7-бензил-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2z в качестве реагента, соединение Синтеза R3z получали в виде HCl соли. МСВР: рассчитано для C31H35N5O3: 525.2740, найдено: 526.2822 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.31/8.82 (brd+brq, 2 Н), 8.1/8.05 (s, 1 Н), 7.36-7.09 (m, 10 Н), 7.25/7.22 (d, 1 Н), 6.53/6.5 (d, 1 Н), 5.34/5.33 (s, 2 Н), 4.05-2.63 (m, 12 Н), 1.92-0.62 (m, 6 Н).
Синтез R3aa: 7-[(2-хлорфенил)метил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2aa в качестве реагента, соединение Синтеза R3aa получали в виде HCl соли. МСВР: рассчитано для C31H34ClN5O3: 559.2350, найдено: 560.2429 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.12/8.68 (brd+brq, 2 Н), 8.07/8.01 (s, 1 Н), 7.54-6.76 (m, 9 Н), 7.2/7.18 (d, 1 Н), 6.56/6.55 (d, 1 Н), 5.44/5.43 (s, 2 Н), 4.86/4.85 (s, 1 Н), 4.06-2.61 (m, 12 Н), 1.91-0.62 (m, 6 Н).
Синтез R3ac: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(3,4,5-триметоксифенил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ac в качестве реагента, соединение Синтеза R3ac получали в виде HCl соли. МСВР: рассчитано для C33H39N5O6: 601.2900, найдено: 602.2960 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.55/9.01 (brq+brd, 2 Н), 8.16/8.12 (s, 1 Н), 7.54/7.51 (d, 1 Н), 7.36-7.14 (m, 5 Н), 7.01/6.99 (s, 2 Н), 6.7/6.67 (d, 1 Н), 4.95 (brs, 1 Н), 4.1-2.61 (m, 12 Н), 3.83 (s, 6 Н), 3.7 (s, 3 Н), 1.98-0.62 (m, 6 Н).
Синтез R3ad: 7-(3,5-дихлорфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ad в качестве реагента, соединение Синтеза R3ad получали в виде HCl соли. МСВР: рассчитано для C30H31N5O3Cl2: 579.1804, найдено: 580.1891 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.06/8.65 (brd+brq, 2 Н), 8.18/8.14 (s, 1 Н), 7.98/7.97 (d, 2 Н), 7.71/7.68 (d, 1 Н), 7.67 (t, 1 Н), 7.34-7.14 (m, 5 Н), 6.77/6.73 (d, 1 Н), 4.88 (brs, 1 Н), 4.12-2.62 (m, 12 Н), 1.96-0.62 (m, 6 Н).
Синтез R3ae: 7-(3-хлор-5-метоксифенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ae в качестве реагента, соединение Синтеза R3ae получали в виде HCl соли. МСВР: рассчитано для C31H34ClN5O4: 575.2299, найдено: 576.2382 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 8.83 (brs, 2 Н), 8.15/8.1 (s, 1 Н), 7.64/7.62 (d, 1 Н), 7.51/7.5 (t, 1 Н), 7.36/7.34 (t, 1 Н), 7.36-7.12 (m, 5 Н), 7.09 (t, 1 Н), 6.74/6.7 (d, 1 Н), 4.87 (s, 1 Н), 4.11-2.62 (m, 12 Н), 3.85 (s, 3 Н), 1.94-0.62 (m, 6 Н).
Синтез R3af: 7-(3,5-диметоксифенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2af в качестве реагента, соединение Синтеза R3af получали в виде HCl соли. МСВР: рассчитано для C32H37N5O5: 571.2795, найдено: 572.2881 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.11/8.68 (brq+brd, 2 Н), 8.12/8.07 (s, 1 Н), 7.57/7.55 (d, 1 Н), 7.34-7.13 (m, 5 Н), 6.93/6.91 (d, 2 Н), 6.71/6.67 (d, 1 Н), 6.56/6.55 (t, 1 Н), 4.86 (brs, 1 Н), 4.09-2.62 (m, 12 Н), 3.81 (s, 6 Н), 1.94-0.64 (m, 6 Н).
Синтез R3ag: 7-(3,4-дихлорфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ag в качестве реагента, соединение Синтеза R3ag получали в виде HCl соли. МСВР: рассчитано для C30H31Cl2N5O3: 579.18042, найдено: 580.1870 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.16/8.71 (brq+brd, 2 Н), 8.2-7.79 (m, 3 Н), 8.17/8.13 (s, 1 Н), 7.65/7.63 (d, 1 Н), 7.35-7.12 (m, 5 Н), 6.76/6.72 (d, 1 Н), 4.85 (brs, 1 Н), 4.11-2.61 (m, 12 Н), 1.95-0.6 (m, 6 Н).
Синтез R3ah: 7-(4-хлор-3-фторфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ah в качестве реагента, соединение Синтеза R3ah получали в виде HCl соли. МСВР: рассчитано для C30H31N5O3FCl: 563.2100, найдено: 564.2181 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.08/8.66 (brm/brm, 2 Н), 8.16/8.12 (s, 1 Н), 7.98/7.97 (dd, 1 Н), 7.82-7.72 (m, 1 Н), 7.78 (m, 1 Н), 7.65/7.63 (d, 1 Н), 7.33-7.26 (m, 2 Н), 7.26-7.2 (m, 2 Н), 7.17 (brt, 1 Н), 6.77/6.73 (d, 1 Н), 4.86 (vbrs, 1 Н), 4.12-0.58 (, 16 Н), 4.05/3.94/3.67 (d/s, 2 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 158.3, 157.7, 148.7/148.6, 146.7/146.6, 131.6, 129/128.9, 128.3/128.1, 127.7, 124.1, 121, 112.7, 109.3/109.2, 104.5, 69.4, 53.6/53.3.
Синтез R3ai: 7-(4-хлор-3-метоксифенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ai в качестве реагента, соединение Синтеза R3ai получали в виде HCl соли. МСВР: рассчитано для C31H34ClN5O4: 575.2230, найдено: 576.2382 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 8.89 (brs, 2 Н), 8.14/8.06 (s, 1 Н), 7.62/7.6 (d, 1 Н), 7.6 (d, 1 Н), 7.51/7.5 (d, 1 Н), 7.38/7.36 (dd, 1 Н), 7.35-7.13 (m, 5 Н), 6.75/6.71 (d, 1 Н), 4.87 (s, 1 Н), 4.11-2.6 (m, 12 Н), 3.93 (s, 3 Н), 1.95-0.6 (m, 6 Н).
Синтез R3aj: 7-(4-фтор-3-метоксифенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2aj в качестве реагента, соединение Синтеза R3aj получали в виде HCl соли. МСВР: рассчитано для C31H34FN5O4: 559.2595, найдено: 560.2638 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.13/8.7 (brd+brq, 1+1 Н), 8.12/8.07 (s/s, 1 Н), 7.55/7.53 (d/d, 1 Н), 7.49 (m, 2 Н), 7.39 (m, 2 Н), 7.35-7.14 (m, 5 Н), 7.28 (m, 2 Н), 6.73/6.69 (d/d, 1 Н), 4.65-0.6 (m, 16 Н), 3.91 (s, 3 Н), 3.48/3.42 (m/m, 1 Н), 3.22 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.4/148.3, 124.8/124.7, 116.8, 116.6, 110.8, 103.7, 56.8, 42.6/42.5, 41/40.6.
Синтез R3ak: 7-(3,4-диметоксифенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ak в качестве реагента, соединение Синтеза R3ak получали в виде HCl соли. МСВР: рассчитано для C32H37N5O5: 571.2795, найдено: 572.2892 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.11/8.69 (brd+brq, 2 Н), 8.09/8.04 (s, 1 Н), 7.48/7.46 (d, 1 Н), 7.35-7.06 (m, 8 Н), 6.69/6.68 (d, 1 Н), 4.86 (brs, 1 Н), 4.11-2.6 (m, 12 Н), 3.81 (s, 6 Н), 1.96-0.62 (m, 6 Н).
Синтез R3am: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(4-метилфенил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2am в качестве реагента, соединение Синтеза R3am получали в виде HCl соли. МСВР: рассчитано для C31H35N5O3: 525.2734, найдено: 526.2816 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.31/8.82 (brd+brq, 2 Н), 8.11/8.06 (s, 1 Н), 7.6/7.58 (m, 2 Н), 7.49/7.46 (d, 1 Н), 7.35/7.34 (m, 2 Н), 7.32-7.11 (m, 5 Н), 6.71/6.67 (d, 1 Н), 4.81 (brs, 1 Н), 4.11-2.61 (m, 12 Н), 2.37 (s, 3 Н), 1.94-0.61 (m, 6 Н).
Синтез R3an: 4-[3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-4-оксо-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-7-ил]бензонитрил
Используя Общую методику 5, исходя из соединения Синтеза R2an в качестве реагента, соединение Синтеза R3an получали в виде HCl соли. МСВР: рассчитано для C31H32N6O3: 536.2536, найдено: 537.2599 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.19/8.73 (brd+brq, 2 Н), 8.18/8.14 (s/s, 1 Н), 8.12-8 (m, 4 Н), 7.71/7.69 (d/d, 1 Н), 7.35-7.13 (m, 5 Н), 6.8/6.76 (d/d, 1 Н), 4.85 (vbrs, 1 Н), 4.15-0.6 (m, 16 Н), 3.48/3.42 (m/m, 1 Н), 3.22 (m, 1 Н).
Синтез R3ao: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[4-(трифторметил)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ao в качестве реагента, соединение Синтеза R3ao получали в виде HCl соли. МСВР: рассчитано для C31H32N5O3F3: 579.2457, найдено: 580.2529 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.13/8.7 (brs+brs, 2 Н), 8.17/8.12 (s/s, 1 Н), 8.05/8.04 (d/d, 2 Н), 7.94/7.93 (d/d, 2 Н), 7.68/7.66 (d/d, 1 Н), 7.35-7.12 (m, 5 Н), 6.79/6.75 (d/d, 1 Н), 4.88 (s, 1 Н), 4.2-0.59 (m, 16 Н), 3.48/3.42 (m/m, 1 Н), 3.22 (m, 1 Н).
Синтез R3ap: 7-[4-(дифторметил)фенил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ap в качестве реагента, соединение Синтеза R3ap получали в виде HCl соли. МСВР: рассчитано для C31H33F2N5O3: 561.2551, найдено: 562.2636 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.11/8.68 (brd+brq, 2 Н), 8.14/8.09 (s, 1 Н), 7.93/7.91 (m, 2 Н), 7.76/7.75 (m, 2 Н), 7.62/7.6 (d, 1 Н), 7.34-7.12 (m, 5 Н), 7.13 (t, 1 Н), 6.77/6.73 (d, 1 Н), 4.87 (s, 1 Н), 4.11-2.61 (m, 12 Н), 1.93-0.64 (m, 6 Н).
Синтез R3aq: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[4-(гидроксиметил)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2aq в качестве реагента, соединение Синтеза R3aq получали в виде HCl соли. МСВР: рассчитано для C31H35N5O4: 541.2689, найдено: 542.2787 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.2/8.74 (brd+brq, 1+1 Н), 8.11/8.06 (s/s, 1 Н), 7.67/7.65 (dm/dm, 2 Н), 7.51/7.48 (d/d, 1 Н), 7.47 (m, 2 Н), 7.34-7.1 (m, 5 Н), 6.72/6.68 (d/d, 1 Н), 4.56 (s, 2 Н), 4.08-0.61 (m, 16 Н), 3.48/3.43 (m/m, 1 Н), 3.21 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.3/148.2, 127.8, 124.4, 124.2, 103.8, 62.8, 42.6/42.5, 41/40.6.
Синтез R3ar: 7-(4-хлорфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ar в качестве реагента, соединение Синтеза R3ar получали в виде HCl соли. МСВР: рассчитано для C30H32ClN5O3: 545.2194, найдено: 546.2288 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.38/8.87 (brs, 2 Н), 8.24-6.62 (m, 12 Н), 4.13-0.58 (m, 18 Н).
Синтез R3as: 7-(4-фторфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2as в качестве реагента, соединение Синтеза R3as получали в виде HCl соли. МСВР: рассчитано для C30H32N5O3F: 529.2489, найдено: 530.2563 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.05/8.64 (brd+brq, 2 Н), 8.11/8.06 (s, 1 Н), 7.76/7.75 (m, 2 Н), 7.52/7.5 (d, 1 Н), 7.41/7.4 (m, 2 Н), 7.34-7.13 (m, 5 Н), 6.73/6.69 (d, 1 Н), 4.84 (brs, 1 Н), 4.1-2.65 (m, 12 Н), 1.95-0.63 (m, 6 Н).
Синтез R3at: 7-[4-(диметиламино)фенил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2at в качестве реагента, соединение Синтеза R3at получали в виде HCl соли. МСВР: рассчитано для C32H38N6O3: 554.3005, найдено: 555.3076 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.15/8.71 (brd+brq, 2 Н), 8.07/8.02 (s, 1 Н), 7.52 (brm, 2 Н), 7.41/7.38 (d, 1 Н), 7.33-7.11 (m, 5 Н), 6.99 (brs, 2 Н), 6.68/6.64 (d, 1 Н), 4.07-2.62 (m, 12 Н), 2.99 (s, 6 Н), 1.93-0.64 (m, 6 Н).
Синтез R3ax: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(4-метоксифенил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ax в качестве реагента, соединение Синтеза R3ax получали в виде HCl соли. МСВР: рассчитано для C31H35N5O4: 541.2689, найдено: 542.2782 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.2/8.74 (brd+brq, 2 Н), 8.09/8.04 (s, 1 Н), 7.63-7.55 (m, 2 Н), 7.44/7.42 (d, 1 Н), 7.33-7.12 (m, 5 Н), 7.12-7.06 (m, 2 Н), 6.69/6.65 (d, 1 Н), 4.85 (brs, 1 Н), 4.07-2.63 (m, 12 Н), 3.82/3.75 (s, 3 Н), 1.95-0.61 (m, 6 Н).
Синтез R3ay: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[4-(трифторметокси)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ay в качестве реагента, соединение Синтеза R3ay получали в виде HCl соли. МСВР: рассчитано для C31H32N5O4F3: 595.2407, найдено: 596.2494 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 9.08/8.66 (brs, 2 Н), 8.13/8.08 (s, 1 Н), 7.93-7.53 (m, 4 Н), 7.59/7.57 (d, 1 Н), 7.36-7.12 (m, 5 Н), 6.75/6.72 (d, 1 Н), 4.86 (s, 1 Н), 4.14-2.59 (m, 12 Н), 1.95-0.63 (m, 6 Н).
Синтез R3az: 7-[4-(бензилокси)фенил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2az в качестве реагента, соединение Синтеза R3az получали в виде HCl соли. МСВР: рассчитано для C37H39N5O4: 617.3002, найдено: 618.3083 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.12/8.68 (brs+brs, 2 Н), 8.08/8.03 (s, 1 Н), 7.6/7.58 (m, 2 Н), 7.51-7.11 (m, 10 Н), 7.45/7.42 (d, 1 Н), 7.17 (m, 2 Н), 6.69/6.65 (d, 1 Н), 5.18 (s, 2 Н), 4.85 (s, 1 Н), 4.1-2.6 (m, 12 Н), 1.95-0.61 (m, 6 Н).
Синтез R3ba: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(5-метилтиофен-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ba в качестве реагента, соединение Синтеза R3ba получали в виде HCl соли. МСВР: рассчитано для C29H33N5O3S: 531.2304, найдено: 532.2361 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.05/8.68 (brs+brs, 2 Н), 8.14/8.1 (s, 1 Н), 7.53/7.51 (d, 1 Н), 7.33-7.11 (m, 5 Н), 7.16/7.15 (d, 1 Н), 6.77/6.76 (m, 1 Н), 6.71/6.67 (d, 1 Н), 4.88/4.87 (s, 1 Н), 4.09-2.62 (m, 12 Н), 2.46 (d, 3 Н), 1.92-0.62 (m, 6 Н).
Синтез R3bb: 7-(5-хлортиофен-2-ил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bb в качестве реагента, соединение Синтеза R3bb получали в виде HCl соли. МСВР: рассчитано для C28H30ClN5O3S: 551.1758, найдено: 552.1844 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.06/8.76 (brs+brs, 2 Н), 8.21/8.16 (s/s, 1 Н), 7.71/7.68 (d/d, 1 Н), 7.32/7.31 (d/d, 1 Н), 7.32-7.12 (m, 5 Н), 7.15/7.14 (d/d, 1 Н), 6.76/6.73 (d/d, 1 Н), 4.1-0.58 (m, 16 Н), 3.47/3.41 (m/m, 1 Н), 3.21 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 149.2/149.1, 125.6, 123.6, 117.6/117.5, 104.9, 42.6/42.5, 41/40.6.
Синтез R3bc: 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bc в качестве реагента, соединение Синтеза R3bc получали в виде HCl соли. МСВР: рассчитано для C32H35N5O5: 569.2638, найдено: 570.2709 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.42/8.89 (brd+brq, 2 Н), 8.11/8.06 (s, 1 Н), 7.44/7.41 (d, 1 Н), 7.33-7.11 (m, 5 Н), 7.23/7.22 (d, 1 Н), 7.15/7.13 (dd, 1 Н), 7/6.99 (d, 1 Н), 6.67/6.63 (d, 1 Н), 4.35-4.26 (m, 4 Н), 4.09-2.62 (m, 12 Н), 1.94-0.61 (m, 6 Н).
Синтез R3bd: 7-(2H-1,3-бензодиоксол-5-ил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bd в качестве реагента, соединение Синтеза R3bd получали в виде HCl соли. МСВР: рассчитано для C31H33N5O5: 555.2482, найдено: 570.2709 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.21/8.78 (brs+brs, 2 Н), 8.1/8.05 (s, 1 Н), 7.44/7.42 (d, 1 Н), 7.35-7.11 (m, 5 Н), 7.3/7.28 (d, 1 Н), 7.14/7.13 (dd, 1 Н), 7.07/7.06 (d, 1 Н), 6.68/6.64 (d, 1 Н), 6.12 (s, 2 Н), 4.87 (s, 1 Н), 4.09-2.62 (m, 12 Н), 1.95-0.62 (m, 6 Н).
Синтез R3be: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(нафталин-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2be в качестве реагента, соединение Синтеза R3be получали в виде HCl соли. МСВР: рассчитано для C34H35N5O3: 561.2740, найдено: 562.2831 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.16/8.72 (brd+brq, 2 Н), 8.3-7.54 (m, 7 Н), 8.16/8.11 (s, 1 Н), 7.67/7.65 (d, 1 Н), 7.35-7.13 (m, 5 Н), 6.79/6.75 (d, 1 Н), 4.89 (brs, 1 Н), 4.12-2.65 (m, 12 Н), 1.96-0.65 (m, 6 Н).
Синтез R3bf: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(3-метилфенил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bf в качестве реагента, получали соединение Синтеза R3bf. МСВР: рассчитано для C31H35N5O3: 525.2740, найдено: 526.2825 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.13/8.69 (brq+brd, 2 Н), 8.11/8.06 (s, 1 Н), 7.57-7.11 (m, 10 Н), 6.71/6.67 (d, 1 Н), 4.2-2.62 (m, 12 Н), 1.94-0.59 (m, 6 Н).
Синтез R3bg: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[3-(трифторметил)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bg в качестве реагента, соединение Синтеза R3bg получали в виде HCl соли. МСВР: рассчитано для C31H32F3N5O3: 579.2457, найдено: 580.2509 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 9.2/8.74 (brd+brq, 2 Н), 8.19/8.17 (m, 1 Н), 8.17/8.13 (s, 1 Н), 8.09/8.07 (dm, 1 Н), 7.86-7.74 (m, 2 Н), 7.7/7.67 (d, 1 Н), 7.35-7.11 (m, 5 Н), 6.78/6.74 (d, 1 Н), 4.78 (brs, 1 Н), 4.11-2.6 (m, 12 Н), 1.94-0.62 (m, 6 Н).
Синтез R3bh: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-{3-[(4-метилпиперазин-1-ил)метил]фенил}-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bh в качестве реагента, соединение Синтеза R3bh получали в виде HCl соли. МСВР: рассчитано для C36H45N7O3: 623.3584, найдено: 624.3656 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 12.37/11.6 (brs, 2 Н), 9.33/8.83 (brd+brq, 2 Н), 8.18/8.12 (s, 1 Н), 8.04-7.5 (m, 5 Н), 7.35-7.13 (m, 5 Н), 6.75/6.72 (d, 1 Н), 4.6-2.6 (m, 22 Н), 2.79 (s, 3 Н), 1.98-0.66 (m, 6 Н).
Синтез R3bi: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[3-(гидроксиметил)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bi в качестве реагента, соединение Синтеза R3bi получали в виде HCl соли. МСВР: рассчитано для C31H35N5O4: 541.2689, найдено: 542.2769 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 8.98/8.72 (brs+brs, 2 Н), 8.1/8.05 (s/s, 1 Н), 7.69-7.33 (m, 4 Н), 7.51/7.48 (d/d, 1 Н), 7.33-7.11 (m, 5 Н), 6.73/6.69 (d/d, 1 Н), 5.36 (t, 1 Н), 4.59 (d, 2 Н), 4.15-0.61 (m, 16 Н), 3.48/3.42 (m/m, 1 Н), 3.22 (m, 1 Н).
Синтез R3bj: 7-(3-хлорфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bj в качестве реагента, соединение Синтеза R3bj получали в виде HCl соли. МСВР: рассчитано для C30H32N5O3Cl: 545.2194, найдено: 546.2277 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.17/8.72 (brd+brq, 2 Н), 8.15/8.11 (s, 1 Н), 7.94-7.45 (m, 4 Н), 7.63/7.6 (d, 1 Н), 7.34-7.12 (m, 5 Н), 6.75/6.71 (d, 1 Н), 4.88 (brs, 1 Н), 4.13-2.62 (m, 12 Н), 1.95-0.62 (m, 6 Н).
Синтез R3bk: 7-(3-фторфенил)-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bk в качестве реагента, получали соединение Синтеза R3bk. МСВР: рассчитано для C30H32FN5O3: 529.2489, найдено: 530.2571 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9/8.61 (brd+brq, 1+1 Н), 8.14/8.09 (s/s, 1 Н), 7.76-7.23 (m, 4 Н), 7.62/7.6 (d/d, 1 Н), 7.34-7.13 (m, 5 Н), 6.75/6.71 (d/d, 1 Н), 4.14-0.6 (m, 16 Н), 3.47/3.42 (m/m, 1 Н), 3.2 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.6/148.5, 124.2, 104.3/104.2, 42.6/42.5, 41/40.6.
Синтез R3bl: 7-[3-(диметиламино)фенил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bl в качестве реагента, соединение Синтеза R3bl получали в виде HCl соли. МСВР: рассчитано для C32H38N6O3: 554.3005, найдено: 555.3086 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.23/8.76 (brd+brq, 1+1 Н), 8.1/8.05 (s/s, 1 Н), 7.51/7.49 (d/d, 1 Н), 7.37 (brt, 1 Н), 7.33-7.13 (m, 5 Н), 7.18-6.76 (brd, 3 Н), 6.7/6.66 (d/d, 1 H), 4.09-0.61 (m, 16 H), 3.47/3.43 (m/m, 1 H), 3.22 (m, 1 H), 2.98 (s, 6 H).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.2/148.1, 130.2, 124.7, 103.6/103.5, 42.6/42.5, 41.1, 41/40.6.
Синтез R3bm: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[3-(морфолин-4-ил)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bm в качестве реагента, соединение Синтеза R3bm получали в виде HCl соли. МСВР: рассчитано для C34H40N6O4: 596.3111, найдено: 597.3187 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.22/8.75 (brd+brq, 1+1 Н), 8.1/8.06 (s/s, 1 Н), 7.52/7.49 (d/d, 1 Н), 7.38/7.37 (t/t, 1 Н), 7.33-7.13 (m, 5 Н), 7.23/7.21 (brs/brs, 1 Н), 7.14/7.12 (d/d, 1 Н), 7 (brd., 1 Н), 6.7/6.66 (d/d, 1 Н), 4.09-0.62 (m, 16 Н), 3.76 (m, 4 Н), 3.47/3.42 (m/m, 1 Н), 3.22 (m, 1 Н), 3.19 (m, 4 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.2/148.1, 130.1, 124.7/124.6, 115.3, 114.2, 111.3/111.2, 103.6/103.5, 66.5, 48.7, 42.6, 41/40.5.
Синтез R3bo: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(3-метоксифенил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bo в качестве реагента, соединение Синтеза R3bo получали в виде HCl соли. МСВР: рассчитано для C31H35N5O4: 541.2689, найдено: 542.2762 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.21/8.75 (brd+brq, 2 Н), 8.12/8.01 (s, 1 Н), 7.56/7.54 (d, 1 Н), 7.49-6.96 (m, 9 Н), 6.72/6.68 (d, 1 Н), 4.84 (brs, 1 Н), 4.16-2.62 (m, 12 Н), 1.95-0.63 (m, 6 Н).
Синтез R3bp: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-[3-(трифторметокси)фенил]-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bp в качестве реагента, соединение Синтеза R3bp получали в виде HCl соли. МСВР: рассчитано для C31H32N5O4F3: 595.2407, найдено: 596.2491 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 8.87 (brs, 2 Н), 8.16/8.11 (s, 1 Н), 7.9/7.88 (brs, 1 Н), 7.85/7.84 (dm, 1 Н), 7.7/7.69 (t, 1 Н), 7.66/7.63 (d, 1 Н), 7.43 (dm, 1 Н), 7.34-7.11 (m, 5 Н), 6.77/6.73 (d, 1 Н), 4.87/4.86 (s, 1 Н), 4.12-2.62 (m, 12 Н), 1.97-0.61 (m, 6 Н).
Синтез R3bq: 7-[3-(бензилокси)фенил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bq в качестве реагента, соединение Синтеза R3bq получали в виде HCl соли. МСВР: рассчитано для C37H39N5O4: 617.3002, найдено: 618.3051 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.24/8.77 (brd+brq, 2 Н), 8.12/8.08 (s, 1 Н), 7.56/7.53 (d, 1 Н), 7.51-7.03 (m, 14 Н), 6.72/6.68 (d, 1 Н), 5.18 (s, 2 Н), 4.09-2.63 (m, 12 Н), 1.94-0.62 (m, 6 Н).
Синтез R3br: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(6-метилпиридин-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2br в качестве реагента, соединение Синтеза R3br получали в виде HCl соли. МСВР: рассчитано для C30H34N6O3: 526.2692, найдено: 527.2764 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.43/8.91 (brq+brd, 2 Н), 8.26/8.25 (dm, 1 Н), 8.25/8.2 (s, 1 Н), 7.92/7.9 (d, 1 Н), 7.92 (m, 1 Н), 7.34-7.11 (m, 5 Н), 7.26 (m, 1 Н), 6.73/6.69 (d, 1 Н), 4.12-2.63 (m, 12 Н), 2.53/2.52 (s, 3 Н), 1.95-0.64 (m, 6 Н).
Синтез R3bs: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(6-метоксипиридин-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bs в качестве реагента, соединение Синтеза R3bs получали в виде HCl соли. МСВР: рассчитано для C30H34N6O4: 542.2642, найдено: 543.2698 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 8.95 (brs, 2 Н), 8.8/6.81 (dd, 1 Н), 8.23/8.18 (s, 1 Н), 8.08/8.07 (dd, 1 Н), 8/7.98 (d, 1 Н), 7.93/7.92 (t, 1 Н), 7.35-7.1 (m, 5 H), 6.75/6.72 (d, 1 H), 4.14-2.62 (m, 12 H), 3.95/3.94 (s, 3 H), 1.96-0.62 (m, 6 H).
Синтез R3bt: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(нафталин-1-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bt в качестве реагента, соединение Синтеза R3bt получали в виде HCl соли. МСВР: рассчитано для C34H35N5O3: 561.2740, найдено: 562.2827 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.28/8.8 (brq+brd, 2 Н), 8.17-6.74 (m, 15 Н), 4.82 (brs, 1 Н), 4.26-0.57 (m, 18 Н).
Синтез R3bu: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-фенил-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2bu в качестве реагента, соединение Синтеза R3bu получали в виде HCl соли. МСВР: рассчитано для C30H33N5O3: 511.2583, найдено: 512.2675 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.1/8.67 (brd+brd, 2 Н), 8.11/8.06 (s/s, 1 Н), 7.75-7.38 (m, 5 Н), 7.54/7.52 (d/d, 1 Н), 7.34-7.12 (m, 5 Н), 6.73/6.69 (d/d, 1 Н), 4.86 (s, 1 Н), 4.13-0.62 (m, 16 Н), 3.47/3.42 (m/m, 1 Н), 3.22 (m, 1 Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.3/148.2, 124.5/124.4, 103.9/103.8, 42.6/42.5, 41/40.6.
Синтез R3ca: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(пиридин-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ca в качестве реагента, соединение Синтеза R3ca получали в виде HCl соли. МСВР: рассчитано для C29H32N6O3: 512.2536, найдено: 513.2612 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.07/8.65 (brd+brq, 2 Н), 8.56/8.55 (dm, 1 Н), 8.48/8.46 (dm, 1 Н), 8.22/8.17 (s, 1 Н), 8.05 (m, 1 Н), 7.94/7.92 (d, 1 Н), 7.41 (m, 1 Н), 7.33-7.12 (m, 5 Н), 6.75/6.71 (d, 1 Н), 4.9 (s, 1 Н), 4.15-2.63 (m, 12 Н), 1.92-0.65 (m, 6 Н).
Синтез R3cb: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(пиридин-3-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2cb в качестве реагента, получали соединение Синтеза R3cb. МСВР: рассчитано для C29H32N6O3: 512.2536, найдено: 513.261 [(М+Н) форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.35/8.85 (brd+brq, 1+1Н), 9.1/9.09 (d/d, 1Н), 8.68 (dd, 1Н), 8.39 (m, 1Н), 8.2/8.15 (s/s, 1Н), 7.75 (dd, 1Н), 7.69/7.67 (d/d, 1Н), 7.34-7.16 (m, 5Н), 6.81/6.77 (d/d, 1Н), 4.1-0.6 (m, 16Н), 3.49/3.43 (m/m, 1Н), 3.23 (m, 1Н)
13С-ЯМР (500 МГц, MSM-d6) δ м.д. 148.9/148.8, 146.5, 143.4, 133.6/133.5, 125.4, 124, 104.8/104.7, 42.6/42.4, 41/40.6
Синтез R3cc: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(тиофен-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2cc в качестве реагента, соединение Синтеза R3cc получали в виде HCl соли. МСВР: рассчитано для C28H31N5O3S: 517.2148, найдено: 518.2231 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.15/8.7 (brd+brq, 1+1Н), 8.18/8.13 (s/s, 1Н), 7.62/7.59 (d/d, 1Н), 7.45/7.44 (dd, 1Н), 7.4/7.39 (d/d, 1Н), 7.32-7.11 (m, 5Н), 7.09/7.08 (dd, 1Н), 6.74/6.7 (d/d, 1Н), 4.89 (brs, 1Н), 4.1-0.6 (m, 16Н), 3.47/3.42 (m/m, 1Н), 3.21 (m, 1Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.9/148.8, 126.1, 124.6, 122.9, 119.3/119.2, 104.5/104.4, 42.6/42.5, 41/40.6.
Синтез R3cd: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(пиридин-4-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2cd в качестве реагента, получали соединение Синтеза R3cd. МСВР: рассчитано для C29H32N6O3: 512.2536, найдено: 513.2609 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.46/8.94 (brs+brq, 1+1Н), 9 (dm, 2Н), 8.74 (m, 2Н), 8.4/8.36 (s/s, 1Н), 8.05/8.03 (d/d, 1Н), 7.38-7.17 (m, 5Н), 6.95/6.92 (d/d, 1Н), 4.16-0.56 (m, 16Н), 3.5/3.44 (m/m, 1Н), 3.24 (m, 1Н)
13С-ЯМР (500 МГц, MSM-d6) δ м.д. 149.8, 144.4, 123.2/123.1, 117.8, 107.4/107.3, 42.6/42.4, 41.1/40.6
Синтез R3cf: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(тиофен-3-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2cf в качестве реагента, соединение Синтеза R3cf получали в виде HCl соли. МСВР: рассчитано для C28H31N5O3S: 517.2148, найдено: 518.2233 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.29/8.8 (brd+brq, 2Н), 8.17/8.12 (s, 1Н), 7.97-7.66 (m, 3Н), 7.62/7.6 (d, 1Н), 7.33-7.11 (m, 5Н), 6.71/6.67 (d, 1Н), 4.91 (brs, 1Н), 4.12-2.63 (m, 12Н), 1.94-0.63 (m, 6Н).
Синтез R3cg: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(1-метил-1Н-имидазол-4-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2cg в качестве реагента, соединение Синтеза R3cg получали в виде HCl соли. МСВР: рассчитано для C28H33N7O3: 515.2645, найдено: 516.2728 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.3/8.81 (brq+brd), 8.19/8.14 (s, 1Н), 7.85 (brs, 1Н), 7.68 (brs, 1Н), 7.6/7.57 (d, 1Н), 7.33-7.11 (m, 5Н), 6.68/6.64 (brs, 1Н), 4.14-2.63 (brs, 12Н), 3.77 (s, 3Н), 1.95-0.63 (m, 6Н).
Синтез R3ch: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(1-метил-1Н-пиразол-4-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ch в качестве реагента, соединение Синтеза R3ch получали в виде HCl соли. МСВР: рассчитано для C28H33N7O3: 515.2645, найдено: 516.2716 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.25/8.78 (brd+brq., 2Н), 8.3/8.29 (s/s, 1Н), 8.15/8.1 (s/s, 1Н), 7.94/7.92 (d/d, 1Н), 7.47/7.44 (d/d, 1Н), 7.33-7.11 (m, 5Н), 6.68/6.64 (d/d, 1H), 4.15-0.6 (m, 16H), 3.9 (s, 3 H), 3.48/3.42 (m/m, 1H), 3.22 (m, 1H).
Синтез R3ci: 7-[1-(дифторметил)-1Н-пиразол-4-ил]-3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ci в качестве реагента, получали соединение Синтеза R3ci. МСВР: рассчитано для C28H31F2N7O3: 551.2457, найдено: 552.254 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.2/8.78 (brs+brs, 2Н), 8.87/8.85 (d, 1Н), 8.43/8.41 (d, 1Н), 8.2/8.15 (s, 1Н), 7.92 (t, 1Н), 7.61/7.59 (d, 1Н), 7.34-7.13 (m, 5Н), 6.74/6.7 (d, 1Н), 4.91 (s, 1Н), 4.1-2.63 (m, 12Н), 1.92-0.63 (m, 6Н).
Синтез R3cj: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(пиримидин-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2cj в качестве реагента, соединение Синтеза R3cj получали в виде HCl соли. МСВР: рассчитано для C28H31N7O3: 513.2488, найдено: 257.6326 [(М+2Н)2+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.24/8.77 (brd+brq, 2Н), 8.96/8.95 (brd, 1Н), 8.18/8.13 (brs, 1Н), 7.87/7.79 (d, 1Н), 7.55 (t, 1Н), 7.34-7.13 (m, 5Н), 6.76/6.72 (d, 1Н), 4.87 (brs, 1Н), 4.13-2.61 (m, 12Н), 1.93-0.63 (m, 6Н).
Синтез R3ck: 3-({4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-(1,3-тиазол-2-ил)-3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ck в качестве реагента, соединение Синтеза R3ck получали в виде HCl соли. МСВР: рассчитано для C27H30N6O3S: 518.2100, найдено: 519.2181 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.3/8.81 (brd/brq, 2Н), 8.35/8.31 (s, 1Н), 7.91/7.89 (d, 1Н), 7.7/7.69 (d, 1Н), 7.65/7.64 (d, 1Н), 7.33-7.12 (m, 5Н), 6.81/6.77 (d, 1Н), 4.14-2.61 (m, 12Н), 1.95-0.6 (m, 6Н).
Синтез R3cn: 3-[[4-гидрокси-1-[(3S,4S)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он
Используя Общую методику 5, исходя из 3H-пиридо[3,2-d]пиримидин-4-она и трет-бутил (3S,4S)-4-(1-окса-6-азаспиро[2.5]окт-6-илкарбонил)-3-фенилпиперидин-1-карбоксилата (взамен соединения Синтеза R1f) в качестве реагентов, соединение Синтеза R3cn получали в виде HCl соли. МСВР: рассчитано для C25H29N5O3: 447.227, найдено: 448.2365 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.34/8.83 (brs/brd, 2Н), 8.83 (brm, 1Н), 8.34/8.30 (s/s, 1Н), 8.14/8.12 (d/d, 1Н), 7.40-7.09 (m, 5Н), алифатические протоны: 4.13-0.52 (8×СН2), 3.49/3.42 (m, 1Н), 3.21 (m, 1Н).
13С-ЯМР (500 МГц, MSM-d6) δ м.д. 150.3/150.2, 149.8, 136.1, 129.3, 42.6/42.4, 41.0/40.5.
Синтез R3co: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он
Используя Общую методику 5, исходя из 3H-пиридо[3,2-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3co получали в виде HCl соли. МСВР: рассчитано для C25H29N5O3: 447.227, найдено: 448.2365 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.34, 8.83 (brs+brs, 2Н), 8.83 (brs, 1H), 8.34/8.30 (s/s, 1Н), 8.14/8.12 (d/d, 1Н), 7.40-7.09 (m, 5Н), алифатические протоны: 4.13-0.52 (8×СН2), 3.49/3.42 (m, 1Н), 3.21 (m, 1Н).
13С-ЯМР (500 МГц, MSM-d6) δ м.д. 150.3/150.2, 149.8, 136.1, 129.3, 42.6/42.4, 41.0/40.5.
Синтез R3cp: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперид ил]метил]тиено[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из 3H-тиено[2,3-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3cp получали в виде HCl соли. МСВР: рассчитано для C24H28N4O3S: 452.1882, найдено: 453.1933 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.23/8.76 (brs/brm, 2Н), 8.83 (brs, 1Н), 8.26/8.21 (s/s, 1H), 7.61/7.59 (d/d, 1H), 7.43/7.39 (d/d, 1Н) 7.34-7.15 (m, 5Н) 4.93/4.92 (s/s, 1Н) 4.04, 3.93/3.75 (d+d/s, 2Н) 4.00-2.60 (m, 4Н) 3.48/3.42 (m/m, 1Н) 3.41-2.98 (m, 2H) 3.33-3.00 (m, 2H) 3.21 (m, 1H) 1.94-1.80 (m, 2H) 1.51-0.57 (m, 4H).
13С-ЯМР (500 МГц, MSM-d6) δ м.д. 124.8, 122.5/122.4, 47.7/47.2, 42.7, 42.6/42.5, 41.1/40.4, 26.6/26.4.
Синтез R3cq: 6-хлор-3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он
Используя Общую методику 5, исходя из 6-хлор-3H-пиридо[3,2-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3cq получали в виде HCl соли. МСВР: рассчитано для C25H28ClN5O3: 481.1881, найдено: 482.1949 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.13, 8.69 (brs+brm, 2Н), 8.33/8.28 (s/s, 1H), 8.18/8.17 (d/d, 1H), 7.93/7.91 (d/d, 1H), 7.38-7.19 (m, 5Н), 4.09 (brm, 1H), 4.05, 3.97/3.75 (d+d/s, 2Н), 4.00-2.61 (m, 4Н), 3.40-2.99 (brm, 4Н), 3.48/3.40 (m/m, 1Н), 3.22 (m, 1Н) 1.95-1.80 (m, 2Н), 1.52-0.52 (m, 4Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 150.8/150.7, 139.9, 130.4, 42.6/42.5, 41.1/40.5.
Синтез R3cr: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-метоксипиридо[3,2-d]пиримидин-4-он
и
Синтез R3cs: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-5Н-пиридо[3,2-d]пиримидин-4,6-дион
Используя Общую методику 5, исходя из 6-метокси-3H-пиридо[3,2-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3cr и соединение Синтеза R3cs (побочный продукт) получали в виде HCl соли и разделяли их с помощью хроматографии.
Синтез R3cr: МСВР: рассчитано для C26H31N5O4: 477.2376, найдено: 478.2458 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.17, 8.72 (brs+brm, 2Н) 8.22/8.17 (s/s, 1Н) 8.02/8.00 (d/d, 1H), 7.35-7.15 (m, 5Н), 7.31/7.29 (d/d, 1H), 4.06, 3.93/3.77, 3.74 (d+d/d+d, 2Н), 4.00-2.60 (m, 4Н), 3.99/3.96 (s/s, 3Н), 3.48/3.42 (m, 1H), 3.34-2.98 (m, 4Н), 3.21 (m, 1H), 1.94-1.80 (m, 2Н), 1.52-0.57 (m, 4Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 148.2/148.1, 139.5, 119.1, 54.2, 42.6/42.4, 41.1/40.5.
Синтез R3cs: МСВР: рассчитано для C25H29N5O4: 463.222, найдено: 464.2312 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 11.67 (vbrs, 1H), 9.11, 8.68 (brs+brs, 2Н), 8.08/8.04 (s/s, 1H), 7.75/7.73 (d/d, 1H), 6.83/6.81 (d/d, 1H), 7.36-7.18 (m, 5Н), 4.89 (vbrs, 1H), 4.00-2-60 (m, 4Н), 3.99, 3.93/3.74, 3.70 (d+d/d+d, 2Н), 3.48/3.41 (m, 1Н), 3.34-3.01 (m, 4Н), 3.20 (m, 1Н), 1.92-1.80 (m, 2Н), 1.51-0.48 (m, 4Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 146.2/146.1, 140.3, 129.4, 42.6/42.5, 41.0/40.6.
Синтез R3ct: 6-(бензиламино)-3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он
Используя Общую методику 5, исходили из 6-хлор-3H-пиридо[3,2-d]пиримидин-4-она в качестве реагента без стадии снятия защиты, полученное в результате сырое Вос-защищенное соединение (0.76 ммоль) и K2CO3 (1.51 ммоль) перемешивали в бензиламине (5 мл) при 120°С в течение 17 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате сырой продукт (187 мг, 0.283 ммоль) перемешивали в водном растворе HCl (1 н., 3 мл, 3 ммоль) и PDO (3 мл) при 70°С в течение 2 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R3ct в виде HCl соли. МСВР: рассчитано для C32H36N6O3: 552.2849, найдено: 277.1497 [(М+2Н)2+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.37/8.86 (m/m, 2Н), 8.31-7.12 (m, ароматические протоны, 13 Н), 4.78-0,49 (m, алифатические протоны, 20 Н).
Синтез R3cu: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-[(4-метоксифенил)метиламино]пиридо[3,2-d]пиримидин-4-он
Используя Общую методику 5, исходили из 6-хлор-3H-пиридо[3,2-d]пиримидин-4-она в качестве реагента без стадии снятия защиты, полученное в результате сырое Вос-защищенное соединение (0.76 ммоль) и K2CO3 (1.51 ммоль) перемешивали в бензиламине (5 мл) при 120°С в течение 17 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате сырой продукт (187 мг, 0.283 ммоль) перемешивали в водном растворе HCl (1 н., 3 мл, 3 ммоль) и PDO (3 мл) при 70°С в течение 2 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением соединения Синтеза R3cu в виде HCl соли. МСВР: рассчитано для C33H38N6O4: 582.2955, найдено: 292.1552 [(М+2Н)2+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.33/8.83 (brt/brd, 2Н), 8.23/8.18 (s/s, 1Н), 7.91 (vbrs, 1Н), 7.35-7.15 (m, 5Н), 7.34 (d/d, 2Н), 7.27 (brm, 1Н), 6.92/6.91 (d/d, 2Н), 4.62/4.59 (s/s, 2Н), 4.08-0.54 (m, алифатические протоны, 8Н), 3.73 (s, 3Н), 3.48/3.42 (m/m, 1Н), 3.21 (m, 1Н).
Синтез R3cv: 6-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилтриазоло[4,5-d]пиримидин-7-он
Используя Общую методику 5, исходя из 3-фенил-6H-триазоло[4,5-d]пиримидин-7-она в качестве реагента, соединение Синтеза R3cv получали в виде HCl соли. МСВР: рассчитано для C28H31N7O3: 513.2488, найдено: 514.2576 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.28/8.79 (brd+brq, 2Н), 8.5/8.47 (s, 1Н), 8.06-7.54 (m, 5Н), 7.4-7.19 (m, 5Н), 4.98/4.96 (brs, 1Н), 4.17-2.6 (m, 12Н), 1.96-0.53 (m, 6Н).
Синтез R3cw: 1-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он
Используя Общую методику 5, исходя из 9-фенил-1H-пурин-6-она в качестве реагента, соединение Синтеза R3cw получали в виде HCl соли. МСВР: рассчитано для C29H32N6O3: 512.2536, найдено: 513.2616 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.25/8.77 (brd+brq, 2Н), 8.52/8.5 (s, 1Н), 8.28/8.23 (s, 1Н), 7.82-7.46 (m, 5Н), 7.37-7.18 (s, 5Н), 4.91 (brs, 1Н), 4.14-2.63 (m, 12Н), 1.96-0.58 (m, 6Н).
Синтез R3cx: 5-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он
Используя Общую методику 5, исходя из 1-фенил-5H-пиразоло[3,4-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3cx получали в виде HCl соли. МСВР: рассчитано для C29H32N6O3: 512.2536, найдено: 513.2627 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.22/8.76 (brs+brs, 2Н), 8.39/8.36 (s, 1Н), 8.34/8.3 (s, 1Н), 8.09-7.38 (m, 5Н), 7.36-7.16 (m, 5Н), 4.94/4.93 (s, 1Н), 4.12-2.59 (m, 12Н), 1.95-0.58 (m, 6Н).
Синтез R3cy: 7-бром-3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он
Используя Общую методику 5, исходя из 7-бром-3H-пирроло[2,1-ƒ][1,2,4]триазин-4-она в качестве реагента, соединение Синтеза R3cy получали в виде HCl соли. МСВР: рассчитано для C24H28BrN5O3: 513.1376, найдено: 514.1462 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.25/8.77 (brs+brs, 2Н), 8.03/8 (s, 1Н), 7.33-7.1 (m, 5Н), 7.03/6.99/6.77/6.75 (d, 2Н), 4.93/4.91 (s, 1Н), 4.02-2.61 (m, 12Н), 1.94-0.5 (m, 6Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 154, 120.9, 102.9.
Синтез R3cz: 6-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизотиазоло[4,5-d]пиримидин-7-он
Используя Общую методику 5, исходя из 3-фенил-6H-изотиазоло[4,5-d]пиримидин-7-она в качестве реагента, соединение Синтеза R3cz получали в виде HCl соли. МСВР: рассчитано для C29H31N5O3S: 529.2148, найдено: 530.2223 [(М+Н)+ форма].
1Н-ЯМР (400 МГц, MSM-d6) δ м.д. 9.37/8.86 (brs+brs, 2Н), 8.49/8.46 (s, 1Н), 8.43 (m, 2Н), 7.62-7.5 (m, 3Н), 7.39-7.13 (m, 5Н), 5.06/5.03 (s, 1Н), 4.2-2.6 (m, 12Н), 1.98-0.52 (m, 6Н).
Синтез R3da: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он
Используя Общую методику 5, исходили из 7-хлор-3H-тиено[3,4-d]пиримидин-4-она в качестве реагента без стадии снятия защиты, полученное в результате Вос-защищенное соединение подвергали реакции с фенилбороновой кислотой, используя Общую методику 9. Полученный в результате фенилированный сырой продукт лишали защиты в соответствии со Стадией 2 Общей методики 5 с получением соединения Синтеза R3da в виде HCl соли. МСВР: рассчитано для C30H32N4O3S: 528.2195, найдено: 529.2265 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.14/8.7 (brq+brd, 2Н), 8.51/8.47 (s, 1Н), 8.05/8.04 (m, 2Н), 8.03/7.98 (s, 1Н), 7.52-7.33 (m, 3Н), 7.32-7.1 (m, 5Н), 4.9/4.88 (s, 1Н), 4.02-2.61 (m, 12Н), 1.93-0.58 (m, 6Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 158, 143.5, 134, 127.4.
Синтез R3db: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он
Используя Общую методику 5, исходя из 7-фенил-3,5-дигидропирроло[3,2-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3db получали в виде HCl соли. МСВР: рассчитано для C30H33N5O3: 511.2583, найдено: 512.2647 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 12.35/12.3 (d, 1Н), 9.26/8.79 (brs+brs, 2Н), 8.1/8.05 (s, 1Н), 8.1/8.08 (m, 2Н), 7.92/7.9 (d, 1Н), 7.43-7.08 (m, 8Н), 4.92/4.91 (s, 1Н), 4.07-2.62 (m, 12Н), 1.97-0.63 (m, 6Н).
Синтез R3dc: 7-хлор-3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он
Используя Общую методику 5, исходя из 7-хлор-3H-тиено[3,4-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3dc получали в виде HCl соли. МСВР: рассчитано для C24H27ClN4O3S: 486.1492, найдено: 487.1544 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.16/8.71 (brd+brq, 2Н), 8.44/8.4 (s, 1Н), 8.01/7.96 (s, 1Н), 7.34-7.15 (m, 5Н), 4.87/4.85 (s, 1Н), 4-2.59 (m, 12Н), 1.93-0.52 (m, 6Н).
Синтез R3dd: 6-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизоксазоло[4,5-d]пиримидин-7-он
Используя Общую методику 5, исходя из 3-фенил-6H-изоксазоло[4,5-d]пиримидин-7-она в качестве реагента, соединение Синтеза R3dd получали в виде HCl соли. МСВР: рассчитано для C29H31N5O4: 513.2376, найдено: 514.2451 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.13/8.76 (brs+brs, 2Н), 8.44/8.4 (s, 1Н), 8.33-8.26 (m, 2Н), 7.67-7.59 (m, 3Н), 7.39-7.18 (m, 5Н), 4.99/4.97 (s, 1Н), 4.19-2.62 (m, 12Н), 1.95-0.52 (m, 6Н).
Синтез R3de: 5-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он
Используя Общую методику 5, исходя из 1-(4-метоксифенил)-5H-пиразоло[3,4-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3de получали в виде HCl соли. МСВР: рассчитано для C30H34N6O4: 542.2642, найдено: 543.2711 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 9.11/8.69 (brs+brm, 2Н), 8.34/8.3 (s/s, 1Н), 8.29/8.25 (s/s, 1Н), 7.9/7.86 (dm/dm, 2Н), 7.37-7.16 (m, 5Н), 7.13/7.12 (m/m, 2Н), 4.91 (brs, 1Н), 4.13-0.53 (m, 16Н), 3.81 (s, 3Н), 3.48/3.42 (m/m, 1Н), 3.22 (m, 1Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 152.6/152.5, 136.3/136.2, 123.8, 114.9/114.8, 55.9, 42.6/42.5, 41.1/40.5.
Синтез R3df: 1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиразоло[3,4-d]пиримидин-4-он
Используя Общую методику 5, исходя из 1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5H-пиразоло[3,4-d]пиримидин-4-она в качестве реагента, соединение Синтеза R3df получали в виде HCl соли. МСВР: рассчитано для C31H34N6O5: 570.2591, найдено: 571.2663 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 9.16/8.74 (brs+brs, 2Н), 8.3/8.26 (s, 1Н), 8.29/8.23 (s, 1Н), 7.53/7.52 (d, 1Н), 7.48/7.47 (dd, 1Н), 7.36-7.15 (m, 5Н), 7.04 (d, 1Н), 4.92/4.9 (s, 1Н), 4.35-4.26 (m, 4 Н), 4.1-2.6 (m, 12Н), 1.94-0.58 (m, 6Н).
Синтез R3dg: 6-хлор-7-(4-хлор-3-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2ah в качестве реагента, соединение Синтеза R3dg получали в виде HCl соли. МСВР: рассчитано для C30H30N5O3FCl2: 597.171, найдено: 598.1772 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 8.07/8.03 (s, 1Н), 7.85 (t, 1Н), 7.75 (dd, 1Н), 7.41 (dd, 1Н), 7.3-7.09 (m, 5Н), 6.87/6.84 (s, 1Н), 4.81/4.79 (s, 1Н), 4.06-2.51 (m, 12Н), 1.68-0.74 (m, 6Н).
Синтез R3dh: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-метил-7-фенилпирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2de в качестве реагента, соединение Синтеза R3dh получали в виде HCl соли. МСВР: рассчитано для C31H35N5O3: 525.274, найдено: 526.2827 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 9.14/8.69 (brs+brs, 2Н), 7.95/7.9 (s, 1Н), 7.61-7.37 (m, 5Н), 7.36-7.15 (m, 5Н), 6.45/6.42 (q, 1Н), 4.84/4.83 (s, 1Н), 4.06-2.61 (m, 12Н), 2.19/2.17 (d, 3Н), 1.95-0.6 (m, 6Н).
Синтез R3di: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-метилпиримидо[4,5-b]индол-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2df в качестве реагента, соединение Синтеза R3di получали в виде HCl соли. МСВР: рассчитано для C29H33N5O3: 499.2583, найдено: 500.2677 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 9.19/8.74 (brq+brd, 2Н), 8.38/8.33 (s, 1Н), 8.07/8.02 (dm, 1Н), 7.66/7.65 (dm, 1Н), 7.43/7.42 (m, 1Н), 7.37-7.12 (m, 5Н), 7.32 (m, 1Н), 4.9 (brs, 1Н), 4.21-2.62 (m, 12Н), 3.87/3.86 (s, 3Н), 1.95-0.64 (m, 6Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 158, 152.7, 137.2, 122, 99.
Синтез R3dj: 3-[(4-гидрокси-1-{[(3R,4R)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-6,8-диметилпиримидо[5,4-b]индолизин-4(3H)-он
Используя Общую методику 5, исходя из соединения Синтеза R2dg в качестве реагента, соединение Синтеза R3dj получали в виде HCl соли. МСВР: рассчитано для C29H34N6O3: 514.2692, найдено: 515.2757 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6): δ м.д. 9.25/8.77 (brq+brd, 2Н), 8.18/8.13 (s, 1Н), 7.34-7.1 (m, 5Н), 6.94/6.9 (s, 1Н), 6.71/6.7 (q, 1Н), 4.9 (brs, 1Н), 4.13-2.6 (m, 12Н), 2.47/2.45 (d, 3Н), 2.45/2.44 (s, 3Н), 1.95-0.62 (m, 6Н).
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 159.3, 152.6, 140.4, 139, 127.9, 115.4, 108.8, 91.4.
Синтез R3dk: 6-хлор-3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2dh в качестве реагента, соединение Синтеза R3dk получали в виде HCl соли. МСВР: рассчитано для C30H32ClN5O3: 545.2194, найдено: 546.2277 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 9.15/8.71 (brd+brq, 2Н), 8.05/8 (s, 1Н), 7.64-7.41 (m, 5Н), 7.37-7.18 (m, 5Н), 6.83/6.8 (s, 1Н), 4.85 (s, 1Н), 4.07-2.61 (m, 12Н), 1.94-0.61 (m, 6Н).
Синтез R3dl: 3-[[4-гидрокси-1-[(3R,4R)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-йод-7-метилпирроло[2,3-d]пиримидин-4-он
Используя Общую методику 5, исходя из соединения Синтеза R2di в качестве реагента, соединение Синтеза R3dl получали в виде HCl соли. МСВР: рассчитано для C25H30IN5O3: 575.1393, найдено: 576.1455 [(М+Н)+ форма].
1Н-ЯМР (500 МГц, MSM-d6) δ м.д. 8.02/7.97 (s/s, 1Н), 7.28-7.02 (m, 5Н), 6.84/6.83 (s/s, 1Н), 4.16-0.65 (m, 16Н), 3.65/3.64 (s/s, 3Н), 3.21/3.16 (m/m, 1Н), 2.88 (m, 1Н)
13С-ЯМР (125 МГц, MSM-d6) δ м.д. 147.9/147.8, 111.7/111.6, 80.7/80.6, 46.2, 43.2/42.8, 33.1
Синтез R3dm: 3-[[3,3-дифтор-4-гидрокси-1-[транс-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он
Йодид триметилсульфоксония (1.11 г, 5 ммоль) растворяли в абс. MSM (10 мл), затем последовательно добавляли дисперсию гидрида натрия (60% в минеральном масле, 200 мг, 5 ммоль) и перемешивали в течение 20 минут при к.т. К смеси добавляли раствор трет-бутил 3,3-дифтор-4-оксопиперидин-1-карбоксилата (783 мг, 3.33 ммоль) в MSM (5 мл, абс.) и перемешивали в течение 15 часов при к.т. Реакционную смесь выливали в смесь лед-вода (40 мл) и экстрагировали с помощью DEE (4×15 мл). Объединенный органический слой промывали водой, солевым раствором, затем сушили над MgSO4 и упаривали.
Сырой эпоксидный продукт подвергали реакции с соединением Синтеза R2bu в соответствии с Общей методикой 5.
Полученную в результате сырую HCl соль подвергали реакции с транс-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновой кислотой, используя Общую методику 7.
Сырой продукт лишали защиты в соответствии со Стадией 2 Общей методики 5 с получением соединения Синтеза R3dm. МСВР: рассчитано для C30H31F2N5O3: 547.2394, найдено: 548.2454 и 548.2490 (два диастереомера) [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 9.24/8.82 (m+m, 2Н), 8.19-8.09 (4*s, 1Н), 7.71 (m, 2Н), 7.6-7.5 (4*d, 1Н), 7.56 (m, 2Н), 7.42 (m, 1Н), 7.34-7.16 (m, 5Н), 6.79-6.67 (4*d, 1Н), 6.08 (brs, 1Н), 4.74-2.35 (m, 12Н), 2.06-1.1 (m, 4 Н)
Синтез R3dn: 3-[[3,3-дифтор-4-гидрокси-1-[транс-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он
Йодид триметилсульфоксония (1.11 г, 5 ммоль) растворяли в абс. MSM (10 мл), затем последовательно добавляли дисперсию гидрида натрия (60% в минеральном масле, 200 мг, 5 ммоль) и перемешивали в течение 20 минут при к.т. К смеси добавляли раствор трет-бутил 3,3-дифтор-4-оксопиперидин-1-карбоксилата (783 мг, 3.33 ммоль) в MSM (5 мл, абс.) и перемешивали в течение 15 часов при к.т. Реакционную смесь выливали в смесь лед-вода (40 мл) и экстрагировали с помощью DEE (4×15 мл). Объединенный органический слой промывали водой, солевым раствором, затем сушили над MgSO4 и упаривали.
Сырой эпоксидный продукт подвергали реакции с соединением Синтеза R2ax в соответствии с Общей методикой 5.
Полученную в результате сырую HCl соль подвергали реакции с транс-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновой кислотой в соответствии с Общей методикой 7.
Сырой продукт лишали защиты в соответствии со Стадией 2 Общей методики 5 с получением соединения Синтеза R3dn. МСВР: рассчитано для C31H33F2N5O4: 577.2501, найдено: 578.2547 и 578.2572 (два диастереомера) [(М+Н)+ форма].
1Н ЯМР (500 МГц, MSM-d6): δ м.д. 9.13/8.74 (m+m, 2Н), 8.16-8.05 (4*s, 1Н), 7.63-7.54 (m, 2Н), 7.48-7.41 (4*d, 1Н), 7.36-7.16 (m, 5Н), 7.14-7.06 (m, 2Н), 6.74-6.63 (4*d, 1Н), 6.17-5.95 (brs, 1Н), 4.69-2.77 (m, 12Н), 3.82/3.81 (s, 3Н), 2.05-1.15 (m, 4 Н)
ПРИМЕРЫ
Следующие Примеры иллюстрируют изобретение, но не ограничивают его каким-либо образом.
 3-[(1-{[(3S,4S)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 1)
3-[(1-{[(3S,4S)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 1)
Используя Общую методику 6, исходя из 3-[(4-гидрокси-1-{[(3S,4S)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием трет-бутил (3S,4S)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и 3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-она) и бензилбромида в качестве реагентов, получали Пример 1. МСВР: рассчитано для C31H35N5O3: 525.2739, найдено: 526.2815 [(М+Н)+ форма].
 7-(2-хлорбензил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 2)
7-(2-хлорбензил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 2)
Используя Общую методику 6, исходя из соединения Синтеза R3aa и соединения Синтеза R1c в качестве реагентов, получали Пример 2. МСВР: рассчитано для C41H42ClN7O3S: 747.2758, найдено: 374.6457 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 3)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 3)
Используя Общую методику 6, исходя из соединения Синтеза R3ac и соединения Синтеза R1c в качестве реагентов, получали Пример 3. МСВР: рассчитано для C43H47N7O6S: 789.3309, найдено: 395.6734 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 4)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 4)
Используя Общую методику 6, исходя из соединения Синтеза R3ac и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 4. МСВР: рассчитано для C43H47N7O7S: 805.3257, найдено: 403.6694 [(М+2Н)2+ форма].
 7-(3,5-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 5)
7-(3,5-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 5)
Используя Общую методику 6, исходя из соединения Синтеза R3ad и соединения Синтеза R1c в качестве реагентов, получали Пример 5. МСВР: рассчитано для C40H39N7O3SCl2: 767.2212, найдено: 768.2251 [(М+Н)+ форма].
 7-(3,5-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 6)
7-(3,5-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 6)
Используя Общую методику 6, исходя из соединения Синтеза R3ad и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 6. МСВР: рассчитано для C40H39N7O4SCl2: 783.2161, найдено: 784.2235 [(М+Н)+ форма].
 7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 7)
7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 7)
Используя Общую методику 6, исходя из соединения Синтеза R3ae и соединения Синтеза R1c в качестве реагентов, получали Пример 7. МСВР: рассчитано для C41H42ClN7O4S: 763.2708, найдено: 764.2766 [(М+Н)+ форма].
 7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 8)
7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 8)
Используя Общую методику 6, исходя из соединения Синтеза R3ae и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 8. МСВР: рассчитано для C41H42ClN7O5S: 779.2657, найдено: 780.2734 [(М+Н)+ форма].
 7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 9)
7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 9)
Используя Общую методику 6, исходя из соединения Синтеза R3af и соединения Синтеза R1c в качестве реагентов, получали Пример 9. МСВР: рассчитано для C42H45N7O5S: 759.3203, найдено: 760.3244 [(М+Н)+ форма].
 7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 10)
7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 10)
Используя Общую методику 6, исходя из соединения Синтеза R3af и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 10. МСВР: рассчитано для C42H45N7O6S: 775.3152, найдено: 776.32 [(М+Н)+ форма].
 7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 11)
7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 11)
Используя Общую методику 6, исходя из соединения Синтеза R3ah и соединения Синтеза R1c в качестве реагентов, получали Пример 11. МСВР: рассчитано для C40H39ClFN7O3S: 751.2508, найдено: 752.2564 [(М+Н)+ форма].
 7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 12)
7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 12)
Используя Общую методику 6, исходя из соединения Синтеза R3ah и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 12. МСВР: рассчитано для C40H39ClFN7O4S: 767.2457, найдено: 768.2552 [(М+Н)+ форма].
 7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 13)
7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 13)
Используя Общую методику 6, исходя из соединения Синтеза R3ai и соединения Синтеза R1c в качестве реагентов, получали Пример 13. МСВР: рассчитано для C41H42ClN7O4S: 763.2708, найдено: 764.2792 [(М+Н)+ форма].
 7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 14)
7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 14)
Используя Общую методику 6, исходя из соединения Синтеза R3ai и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 14. МСВР: рассчитано для C41H42ClN7O5S: 779.2657, найдено: 780.2729 [(М+Н)+ форма].
 7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 15)
7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 15)
Используя Общую методику 6, исходя из соединения Синтеза R3aj и соединения Синтеза R1c в качестве реагентов, получали Пример 15. МСВР: рассчитано для C41H42FN7O4S: 747.3003, найдено: 748.3047 [(М+Н)+ форма].
 7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 16)
7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 16)
Используя Общую методику 6, исходя из соединения Синтеза R3aj и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 16. МСВР: рассчитано для C41H42FN7O5S: 763.2952, найдено: 764.3029 [(М+Н)+ форма].
 7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 17)
7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 17)
Используя Общую методику 6, исходя из соединения Синтеза R3ak и соединения Синтеза R1c в качестве реагентов, получали Пример 17. МСВР: рассчитано для C42H45N7O5S: 759.3203, найдено: 380.6691 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 18)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 18)
Используя Общую методику 6, исходя из соединения Синтеза R3am и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 18. МСВР: рассчитано для C41H43N7O4S: 729.3096, найдено: 730.3162 [(М+Н)+ форма].
 4-{3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-4-оксо-3,4-дигидро-7Н-пирроло[2,3-d]пиримидин-7-ил}бензонитрил (Пример 19)
4-{3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-4-оксо-3,4-дигидро-7Н-пирроло[2,3-d]пиримидин-7-ил}бензонитрил (Пример 19)
Используя Общую методику 6, исходя из соединения Синтеза R3an и соединения Синтеза R1c в качестве реагентов, получали Пример 19. МСВР: рассчитано для C41H40N8O3S: 724.2944, найдено: 725.3009 [(М+Н)+ форма].
 4-{3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-4-оксо-3,4-дигидро-7Н-пирроло[2,3-d]пиримидин-7-ил}бензонитрил (Пример 20)
4-{3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-4-оксо-3,4-дигидро-7Н-пирроло[2,3-d]пиримидин-7-ил}бензонитрил (Пример 20)
Используя Общую методику 6, исходя из соединения Синтеза R3an и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 20. МСВР: рассчитано для C41H40N8O4S: 740.2893, найдено: 741.2984 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 21)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 21)
Используя Общую методику 6, исходя из соединения Синтеза R3ao и соединения Синтеза R1c в качестве реагентов, получали Пример 21. МСВР: рассчитано для C41H40N7O3F3S: 767.2866, найдено: 768.2899 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 22)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 22)
Используя Общую методику 6, исходя из соединения Синтеза R3ao и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 22. МСВР: рассчитано для C41H40F3N7O4S: 783.2814, найдено: 784.2887 [(М+Н)+ форма].
 7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 23)
7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 23)
Используя Общую методику 6, исходя из соединения Синтеза R3ap и соединения Синтеза R1c в качестве реагентов, получали Пример 23. МСВР: рассчитано для C41H41F2N7O3S: 749.2959, найдено: 750.3017 [(М+Н)+ форма].
 7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 24)
7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 24)
Используя Общую методику 6, исходя из соединения Синтеза R3ap и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 24. МСВР: рассчитано для C41H41F2N7O4S: 765.2909, найдено: 766.297 [(М+Н)+ форма].
 7-[4-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 25)
7-[4-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 25)
Используя Общую методику 6, исходя из соединения Синтеза R3aq и соединения Синтеза R1c в качестве реагентов, получали Пример 25. МСВР: рассчитано для C41H43N7O4S: 729.3097, найдено: 730.3137 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 26)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 26)
Используя Общую методику 6, исходя из соединения Синтеза R3aq и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 26. МСВР: рассчитано для C41H43N7O5S: 745.3046, найдено: 746.3142 [(М+Н)+ форма].
 7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 27)
7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 27)
Используя Общую методику 6, исходя из соединения Синтеза R3ar и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 27. МСВР: рассчитано для C40H40ClN7O4S: 749.2551, найдено: 750.2639 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-хлорфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 28)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-хлорфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 28)
Используя Общую методику 6, исходя из соединения Синтеза R3ar и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 28. МСВР: рассчитано для C34H34BrClN6O3S: 720.1285, найдено: 721.1355 [(М+Н)+ форма].
 7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 29)
7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 29)
Используя Общую методику 6, исходя из соединения Синтеза R3as и соединения Синтеза R1c в качестве реагентов, получали Пример 29. МСВР: рассчитано для C40H40N7O3FS: 717.2897, найдено: 718.2982 [(М+Н)+ форма].
 7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 30)
7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 30)
Используя Общую методику 6, исходя из соединения Синтеза R3as и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 30. МСВР: рассчитано для C40H40FN7O4S: 733.2847, найдено: 734.2907 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-фторфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 31)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-фторфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 31)
Используя Общую методику 6, исходя из соединения Синтеза R3as и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 31. МСВР: рассчитано для C34H34BrFN6O3S: 704.1580, найдено: 705.1642 [(М+Н)+ форма].
 7-[4-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 32)
7-[4-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 32)
Используя Общую методику 6, исходя из соединения Синтеза R3at и соединения Синтеза R1c в качестве реагентов, получали Пример 32. МСВР: рассчитано для C42H46N8O3S: 742.3414, найдено: 743.3467 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 33)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 33)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 33. МСВР: рассчитано для C41H43N7O5S: 745.3047, найдено: 746.3124 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 34)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 34)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 34. МСВР: рассчитано для C35H37BrN6O4S: 716.1780396, найдено: 717.1836 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1H-пиразол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 35)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1H-пиразол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 35)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)-1-метилпиразола в качестве реагентов, получали Пример 35. МСВР: рассчитано для C36H41N7O4: 635.3220, найдено: 636.3291 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 36)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 36)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и гидрохлорида 2-(хлорметил)пиразина в качестве реагентов, получали Пример 36. МСВР: рассчитано для C36H39N7O4: 633.3063, найдено: 634.3114 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 37)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 37)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-5-метилтиазола в качестве реагентов, получали Пример 37. МСВР: рассчитано для C36H40N6O4S: 652.2832031, найдено: 653.2891 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 38)
3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 38)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 3-бром-5-(хлорметил)пиридина в качестве реагентов, получали Пример 38. МСВР: рассчитано для C37H39BrN6O4: 710.2216, найдено: 711.2297 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-3-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 39)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-3-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 39)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и гидрохлорида 3-(хлорметил)пиридина в качестве реагентов, получали Пример 39. МСВР: рассчитано для C37H40N6O4: 632.3111, найдено: 633.3167 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 40)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 40)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)тиазола в качестве реагентов, получали Пример 40. МСВР: рассчитано для C35H38N6O4S: 638.2675, найдено: 639.2758 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 41)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 41)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)тиазола в качестве реагентов, получали Пример 41. МСВР: рассчитано для C35H38N6O4S: 638.2675, найдено: 639.2758 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 42)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 42)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-4-метилтиазола в качестве реагентов, получали Пример 42. МСВР: рассчитано для C36H40N6O4S: 652.2832, найдено: 653.2885 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4,5-диметил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 43)
3-{[1-({(3R,4R)-1-[(4,5-диметил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 43)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-4,5-диметилтиазола в качестве реагентов, получали Пример 43. МСВР: рассчитано для C37H42N6O4S: 666.2988, найдено: 667.3059 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2,4-диметил-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 44)
3-{[1-({(3R,4R)-1-[(2,4-диметил-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 44)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)-2,4-диметилтиазола в качестве реагентов, получали Пример 44. МСВР: рассчитано для C37H42N6O4S: 666.2988, найдено: 667.3047 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиразол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 45)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиразол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 45)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)-1-метилпиразола в качестве реагентов, получали Пример 45. МСВР: рассчитано для C36H41N7O4: 635.3220, найдено: 636.3288 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1,3-диметил-1Н-пиразол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 46)
3-{[1-({(3R,4R)-1-[(1,3-диметил-1Н-пиразол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 46)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)-1,3-диметилпиразола в качестве реагентов, получали Пример 46. МСВР: рассчитано для C37H43N7O4: 649.3376, найдено: 650.3455 [(М+Н)+ форма].
 4-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)пиридин-2-карбонитрил (Пример 47)
4-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)пиридин-2-карбонитрил (Пример 47)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 47. МСВР: рассчитано для C38H39N7O4: 657.3063, найдено: 658.3133 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(6-метилпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 48)
3-{[4-гидрокси-1-({(3R,4R)-1-[(6-метилпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 48)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и гидробромида 5-(бромметил)-2-метилпиридина в качестве реагентов, получали Пример 48. МСВР: рассчитано для C38H42N6O4: 646.3267, найдено: 647.3343 [(М+Н)+ форма].
 5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)пиридин-2-карбонитрил (Пример 49)
5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)пиридин-2-карбонитрил (Пример 49)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(бромметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 49. МСВР: рассчитано для C38H39N7O4: 657.3063, найдено: 658.3138 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(1,3-оксазол-4-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 50)
3-[(4-гидрокси-1-{[(3R,4R)-1-(1,3-оксазол-4-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 50)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)оксазола в качестве реагентов, получали Пример 50. МСВР: рассчитано для C35H38N6O5: 622.2903, найдено: 623.2975 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1,5-диметил-1Н-пиразол-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 51)
3-{[1-({(3R,4R)-1-[(1,5-диметил-1Н-пиразол-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 51)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 3-(хлорметил)-1,5-диметилпиразола в качестве реагентов, получали Пример 51. МСВР: рассчитано для C37H43N7O4: 649.3376, найдено: 650.3431 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-оксазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 52)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-оксазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 52)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-5-метилоксазола в качестве реагентов, получали Пример 52. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3141 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 53)
3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 53)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)-2-метилтиазола в качестве реагентов, получали Пример 53. МСВР: рассчитано для C36H40N6O4S: 652.2832, найдено: 653.2896 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 54)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 54)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 3-(хлорметил)-5-метилизоксазола в качестве реагентов, получали Пример 54. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3118 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(1,2-оксазол-3-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 55)
3-[(4-гидрокси-1-{[(3R,4R)-1-(1,2-оксазол-3-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 55)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 3-(хлорметил)изоксазола в качестве реагентов, получали Пример 55. МСВР: рассчитано для C35H38N6O5: 622.2903, найдено: 623.2961 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-оксазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 56)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-оксазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 56)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)-3-метилизоксазола в качестве реагентов, получали Пример 56. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3119 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 57)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 57)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)-5-метилизоксазола в качестве реагентов, получали Пример 57. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3139 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[6-(трифторметил)пиридин-3-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 58)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[6-(трифторметил)пиридин-3-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 58)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(бромметил)-2-(трифторметил)пиридина в качестве реагентов, получали Пример 58. МСВР: рассчитано для C38H39F3N6O4: 700.2985, найдено: 701.3082 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 59)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 59)
Используя Общую методику 6, исходя из соединения Синтеза R3ay и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 59. МСВР: рассчитано для C41H40F3N7O5S: 799.2764, найдено: 800.2855 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 60)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 60)
Используя Общую методику 6, исходя из соединения Синтеза R3ay и соединения Синтеза R1c в качестве реагентов, получали Пример 60. МСВР: рассчитано для C41H40F3N7O4S: 783.2814, найдено: 784.2904 [(М+Н)+ форма].
 7-[4-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 61)
7-[4-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 61)
Используя Общую методику 6, исходя из соединения Синтеза R3az и соединения Синтеза R1c в качестве реагентов, получали Пример 61. МСВР: рассчитано для C47H47N7O4S: 805.3410, найдено: 403.6767 [(М+2Н)2+ форма].
 7-[4-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 62)
7-[4-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 62)
Используя Общую методику 5, исходя из соединения Синтеза R3az и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 62. МСВР: рассчитано для C47H47N7O5S: 821.3359, найдено: 822.3433 [(М+Н)+ форма].
 3-[(1-{[(3S,4S)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 63)
3-[(1-{[(3S,4S)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 63)
Используя Общую методику 6, исходя из 3-({4-гидрокси-1-[(3S,4S)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-метил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием трет-бутил (3S,4S)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и соединения Синтеза R2b) и бензилбромида в качестве реагентов, получали Пример 63. МСВР: рассчитано для C32H37N5O3: 539.2896, найдено: 540.2984 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 64)
3-[(1-{[(3R,4R)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 64)
Используя Общую методику 6, исходя из соединения Синтеза R3b и бензилбромида в качестве реагентов, получали Пример 64. МСВР: рассчитано для C32H37N5O3: 539.2896, найдено: 540.2977 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 65)
3-[(1-{[(3R,4R)-1-(2-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 65)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 1-(бромметил)-2-фторбензола в качестве реагентов, получали Пример 65. МСВР: рассчитано для C32H36FN5O3: 557.2802, найдено: 558.2879 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 66)
3-[(1-{[(3R,4R)-1-(3-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 66)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 1-(бромметил)-2-метилбензола в качестве реагентов, получали Пример 66. МСВР: рассчитано для C32H36FN5O3: 557.2802, найдено: 558.2902 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 67)
3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 67)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 1-(бромметил)-2-метилбензола в качестве реагентов, получали Пример 67. МСВР: рассчитано для C33H39N5O3: 553.3053, найдено: 554.3138 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 68)
3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 68)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 1-(бромметил)-3-метилбензола в качестве реагентов, получали Пример 68. МСВР: рассчитано для C33H39N5O3: 553.3052, найдено: 554.3090 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-бромбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 69)
3-[(1-{[(3R,4R)-1-(3-бромбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 69)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 1-бром-3-(бромметил)бензола в качестве реагентов, получали Пример 69. МСВР: рассчитано для C32H36BrN5O3: 617.2001, найдено: 618.2094 [(М+Н)+ форма].
 6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1-метил-3,4-дигидрохинолин-2(1Н)-он (Пример 70)
6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1-метил-3,4-дигидрохинолин-2(1Н)-он (Пример 70)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 6-(хлорметил)-1-метил-3,4-дигидрохинолин-2-она в качестве реагентов, получали Пример 70. МСВР: рассчитано для C36H42N6O4: 622.3268, найдено: 623.3354 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-ацетилбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 71)
3-[(1-{[(3R,4R)-1-(3-ацетилбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 71)
Используя Общую методику 6, исходя из соединения Синтеза R3b и 1-[3-(хлорметил)фенил]этанона в качестве реагентов, получали Пример 71. МСВР: рассчитано для C34H39N5O4: 581.3002, найдено: 582.3054 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 72)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 72)
Используя Общую методику 6, исходя из соединения Синтеза R3ba и соединения Синтеза R1c в качестве реагентов, получали Пример 72. МСВР: рассчитано для C39H41N7O3S2: 719.2712, найдено: 720.2762 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 73)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 73)
Используя Общую методику 6, исходя из соединения Синтеза R3ba и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 73. МСВР: рассчитано для C39H41N7O4S2: 735.2661, найдено: 736.2727 [(М+Н)+ форма].
 7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 74)
7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 74)
Используя Общую методику 6, исходя из соединения Синтеза R3bb и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 74. МСВР: рассчитано для C38H38ClN7O4S2: 755.2115, найдено: 756.219 [(М+Н)+ форма].
 7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 75)
7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 75)
Используя Общую методику 6, исходя из соединения Синтеза R3bb и соединения Синтеза R1c в качестве реагентов, получали Пример 75. МСВР: рассчитано для C38H38N7O3S2Cl:739.2166, найдено: 740.2222 [(М+Н)+ форма].
 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 76)
7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 76)
Используя Общую методику 6, исходя из соединения Синтеза R3bc и соединения Синтеза R1c в качестве реагентов, получали Пример 76. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 758.3125 [(М+Н)+ форма].
 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 77)
7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 77)
Используя Общую методику 6, исходя из соединения Синтеза R3bc и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 77. МСВР: рассчитано для C42H43N7O6S: 773.2996, найдено: 774.3038 [(М+Н)+ форма].
 7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 78)
7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 78)
Используя Общую методику 6, исходя из соединения Синтеза R3bd и соединения Синтеза R1c в качестве реагентов, получали Пример 78. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 372.6517 [(М+2Н)2+ форма].
 7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 79)
7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 79)
Используя Общую методику 6, исходя из соединения Синтеза R3bd и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 79. МСВР: рассчитано для C41H41N7O6S: 759.2838, найдено: 380.6487 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он (Пример 80)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он (Пример 80)
Используя Общую методику 6, исходя из соединения Синтеза R3bf и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 80. МСВР: рассчитано для C41H43N7O4S: 729.3097, найдено: 730.3189 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 81)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 81)
Используя Общую методику 6, исходя из соединения Синтеза R3bg и соединения Синтеза R1c в качестве реагентов, получали Пример 81. МСВР: рассчитано для C41H40F3N7O3S: 767.2865, найдено: 768.2943 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 82)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 82)
Используя Общую методику 6, исходя из соединения Синтеза R3bg и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 82. МСВР: рассчитано для C41H40F3N7O4S: 783.2814, найдено: 784.2897 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-{3-[(4-метилпиперазин-1-ил)метил]фенил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 83)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-{3-[(4-метилпиперазин-1-ил)метил]фенил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 83)
Используя Общую методику 6, исходя из соединения Синтеза R3bh и соединения Синтеза R1c в качестве реагентов, получали Пример 83. МСВР: рассчитано для C46H53N9O3S:811.3992, найдено: 406.7081 [(М+2Н)2+ форма].
 7-[3-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 84)
7-[3-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 84)
Используя Общую методику 6, исходя из соединения Синтеза R3bi и соединения Синтеза R1c в качестве реагентов, получали Пример 84. МСВР: рассчитано для C41H43N7O4S: 729.3098, найдено: 730.3153 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 85)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 85)
Используя Общую методику 6, исходя из соединения Синтеза R3bi и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 85. МСВР: рассчитано для C41H43N7O5S: 745.3046, найдено: 746.313 [(М+Н)+ форма].
 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 86)
7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 86)
Используя Общую методику 6, исходя из соединения Синтеза R3bj и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 86. МСВР: рассчитано для C40H40N7O4SCl: 749.2551, найдено: 750.2624 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(3-хлорфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 87)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(3-хлорфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 87)
Используя Общую методику 6, исходя из соединения Синтеза R3bj и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 87. МСВР: рассчитано для C34H34BrClN6O3S: 720.1284, найдено: 721.1336 [(М+Н)+ форма].
 7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 88)
7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 88)
Используя Общую методику 6, исходя из соединения Синтеза R3bk и соединения Синтеза R1c в качестве реагентов, получали Пример 88. МСВР: рассчитано для C40H40FN7O3S: 717.2897, найдено: 359.6513 [(М+2Н)2+ форма].
 7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 89)
7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 89)
Используя Общую методику 6, исходя из соединения Синтеза R3bk и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 89. МСВР: рассчитано для C40H40FN7O4S: 733.2847, найдено: 734.2893 [(М+Н)+ форма].
 7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 90)
7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 90)
Используя Общую методику 6, исходя из соединения Синтеза R3bl и соединения Синтеза R1c в качестве реагентов, получали Пример 90. МСВР: рассчитано для C42H46N8O3S: 742.3413, найдено: 372.1784 [(М+2Н)2+ форма].
 7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 91)
7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 91)
Используя Общую методику 6, исходя из соединения Синтеза R3bl и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 91. МСВР: рассчитано для C42H46N8O4S: 758.3362, найдено: 380.1752 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 92)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 92)
Используя Общую методику 6, исходя из соединения Синтеза R3bm и соединения Синтеза R1c в качестве реагентов, получали Пример 92. МСВР: рассчитано для C44H48N8O4S: 784.3519, найдено: 785.3594 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 93)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 93)
Используя Общую методику 6, исходя из соединения Синтеза R3bm и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 93. МСВР: рассчитано для C44H48N8O5S: 800.3468, найдено: 801.3546 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 94)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 94)
Используя Общую методику 6, исходя из соединения Синтеза R3bo и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 94. МСВР: рассчитано для C41H43N7O5S: 745.3046, найдено: 746.3117 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 95)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 95)
Используя Общую методику 6, исходя из соединения Синтеза R3bo и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 94. МСВР: рассчитано для C35H37BrN6O4S: 745.3046, найдено: 746.3117 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 96)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 96)
Используя Общую методику 6, исходя из соединения Синтеза R3bp и соединения Синтеза R1c в качестве реагентов, получали Пример 96. МСВР: рассчитано для C41H40F3N7O4S: 783.2814, найдено: 784.2878 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 97)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 97)
Используя Общую методику 6, исходя из соединения Синтеза R3bp и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 97. МСВР: рассчитано для C41H40F3N7O5S: 799.2764, найдено: 800.2856 [(М+Н)+ форма].
 7-[3-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 98)
7-[3-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 98)
Используя Общую методику 6, исходя из соединения Синтеза R3bq и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 98. МСВР: рассчитано для C47H47N7O5S: 821.3359, найдено: 822.343 [(М+Н)+ форма].
 7-[3-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 99)
7-[3-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 99)
Используя Общую методику 6, исходя из соединения Синтеза R3bq и соединения Синтеза R1c в качестве реагентов, получали Пример 99. МСВР: рассчитано для C47H47N7O4S: 805.3410, найдено: 806.3484 (М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 100)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 100)
Используя Общую методику 6, исходя из соединения Синтеза R3bs и соединения Синтеза R1c в качестве реагентов, получали Пример 100. МСВР: рассчитано для C40H42N8O4S: 730.3049, найдено: 731.3128 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 101)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 101)
Используя Общую методику 6, исходя из соединения Синтеза R3bs и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 101. МСВР: рассчитано для C40H42N8O5S: 746.2998, найдено: 747.308 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 102)
3-[(1-{[(3R,4R)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 102)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и бензилбромида в качестве реагентов, получали Пример 102. МСВР: рассчитано для C37H39N5O3: 601.3053, найдено: 602.3155 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 103)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 103)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 103. МСВР: рассчитано для C34H35N6O3SBr: 686.1675, найдено: 687.1743 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 104)
3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 104)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 3-бром-5-(хлорметил)пиридина в качестве реагентов, получали Пример 104. МСВР: рассчитано для C36H37BrN6O3: 680.2111, найдено: 681.2179 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-4-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 105)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-4-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 105)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)пиридина в качестве реагентов, получали Пример 105. МСВР: рассчитано для C36H38N6O3: 602.3005, найдено: 603.3085 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-3-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 106)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-3-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 106)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и гидробромида 3-(бромметил)пиридина в качестве реагентов, получали Пример 106. МСВР: рассчитано для C36H38N6O3: 602.3005, найдено: 603.3062 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиразол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 107)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиразол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 107)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)-1-метилпиразола в качестве реагентов, получали Пример 107. МСВР: рассчитано для C35H39N7O3: 605.3115, найдено: 606.3188 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 108)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 108)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и гидрохлорида 2-(хлорметил)пиразина в качестве реагентов, получали Пример 108. МСВР: рассчитано для C35H37N7O3: 603.2958, найдено: 604.3021 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 109)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 109)
Используя Общую методику 9, исходя из Примера 103 и метил 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбоксилата в качестве реагентов, Пример 109 получали в результате дегалогенирования во время сочетания Сузуки. МСВР: рассчитано для C34H36N6O3S: 608.2567, найдено: 609.265 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-оксазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 110)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-оксазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 110)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-5-метилоксазола в качестве реагентов, получали Пример 110. МСВР: рассчитано для C35H38N6O4: 606.2955, найдено: 607.3016 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 111)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 111)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)тиазола в качестве реагентов, получали Пример 111. МСВР: рассчитано для C34H36N6O3S: 608.2567, найдено: 609.2651 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 112)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 112)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-5-метилтиазола в качестве реагентов, получали Пример 112. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2783 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(1,2-оксазол-3-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 113)
3-[(4-гидрокси-1-{[(3R,4R)-1-(1,2-оксазол-3-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 113)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 3-(хлорметил)изоксазола в качестве реагентов, получали Пример 113. МСВР: рассчитано для C34H36N6O4: 592.2798, найдено: 593.2864 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-оксазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 114)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-оксазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 114)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 5-(хлорметил)-3-метилизоксазола в качестве реагентов, получали Пример 114. МСВР: рассчитано для C35H38N6O4: 606.2955, найдено: 607.3046 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 115)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 115)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-4-метилтиазола в качестве реагентов, получали Пример 115. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2782 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2,4-диметил-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 116)
3-{[1-({(3R,4R)-1-[(2,4-диметил-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 116)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 5-(хлорметил)-2,4-диметилтиазола в качестве реагентов, получали Пример 116. МСВР: рассчитано для C36H40N6O3S: 636.2883, найдено: 637.2942 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4,5-диметил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 117)
3-{[1-({(3R,4R)-1-[(4,5-диметил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 117)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-4,5-диметилтиазола в качестве реагентов, получали Пример 117. МСВР: рассчитано для C36H40N6O3S: 636.2883, найдено: 637.2965 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 118)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 118)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)-5-метилизоксазола в качестве реагентов, получали Пример 118. МСВР: рассчитано для C35H38N6O4: 606.2955, найдено: 607.3009 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиразол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 119)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиразол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 119)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 5-(хлорметил)-1-метилпиразола в качестве реагентов, получали Пример 119. МСВР: рассчитано для C35H39N7O3: 605.3115, найдено: 606.3186 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 120)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,2-оксазол-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 120)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 3-(хлорметил)-5-метилизоксазола в качестве реагентов, получали Пример 120. МСВР: рассчитано для C35H38N6O4: 606.2955, найдено: 607.3011 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 121)
3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 121)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)-2-метилтиазола в качестве реагентов, получали Пример 121. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2799 [(М+Н)+ форма].
 4-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}пиридин-2-карбонитрил (Пример 122)
4-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}пиридин-2-карбонитрил (Пример 122)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 122. МСВР: рассчитано для C37H37N7O3: 627.2958, найдено: 628.3026 [(М+Н)+ форма].
 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}пиридин-2-карбонитрил (Пример 123)
5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}пиридин-2-карбонитрил (Пример 123)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 5-(бромметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 123. МСВР: рассчитано для C37H37N7O3: 627.2958, найдено: 628.3025 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(1,3-оксазол-4-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 124)
3-[(4-гидрокси-1-{[(3R,4R)-1-(1,3-оксазол-4-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 124)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)оксазола в качестве реагентов, получали Пример 124. МСВР: рассчитано для C34H36N6O4: 592.2797852, найдено: 593.2876 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(6-метилпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 125)
3-{[4-гидрокси-1-({(3R,4R)-1-[(6-метилпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 125)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и гидробромида 5-(бромметил)-2-метилпиридина в качестве реагентов, получали Пример 125. МСВР: рассчитано для C37H40N6O3: 616.3162, найдено: 617.3241 [(М+Н)+ форма].
 3-[(1-{[(3S,4S)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 126)
3-[(1-{[(3S,4S)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 126)
Используя Общую методику 6, исходя из 7-этил-3-({4-гидрокси-1-[(3S,4S)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием трет-бутил (3S,4S)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и соединения Синтеза R2c) и бензилбромида в качестве реагентов, получали Пример 126. МСВР: рассчитано для C33H39N5O3: 553.3053, найдено: 554.312 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 127)
3-[(1-{[(3R,4R)-1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 127)
Используя Общую методику 6, исходя из соединения Синтеза R3c и бензилбромида в качестве реагентов, получали Пример 127. МСВР: рассчитано для C33H39N5O3: 553.3053, найдено: 554.3122 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-(2-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 128)
7-этил-3-[(1-{[(3R,4R)-1-(2-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 128)
Используя Общую методику 6, исходя из соединения Синтеза R3c и 1-(бромметил)-2-фторбензола в качестве реагентов, получали Пример 128. МСВР: рассчитано для C33H38FN5O3: 571.2959, найдено: 572.3022 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-(3-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 129)
7-этил-3-[(1-{[(3R,4R)-1-(3-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 129)
Используя Общую методику 6, исходя из соединения Синтеза R3c и 1-(бромметил)-3-фторбензола в качестве реагентов, получали Пример 129. МСВР: рассчитано для C33H38FN5O3: 571.2959, найдено: 572.3037 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 130)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 130)
Используя Общую методику 6, исходя из соединения Синтеза R3c и 1-(бромметил)-2-метилбензола в качестве реагентов, получили Пример 130. МСВР: рассчитано для C34H41N5O3: 567.3209, найдено: 568.327 [(M+H)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 131)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 131)
Используя Общую методику 6, исходя из соединения Синтеза R3cc и соединения Синтеза R1c в качестве реагентов, получали Пример 131. МСВР: рассчитано для C38H39N7O3S2: 705.2556, найдено: 706.262 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 132)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 132)
Используя Общую методику 6, исходя из соединения Синтеза R3cc и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 132. МСВР: рассчитано для C38H39N7O4S2: 721.2505, найдено: 722.2596 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 133)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 133)
Используя Общую методику 6, исходя из соединения Синтеза R3cf и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов получали Пример 133. МСВР: рассчитано для C38H39N7O4S2: 721.2505, найдено: 722.2570 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-имидазол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 134)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-имидазол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 134)
Используя Общую методику 6, исходя из соединения Синтеза R3cg и соединения Синтеза R1c в качестве реагентов, получали Пример 134. МСВР: рассчитано для C38H41N9O3S: 703.3053, найдено: 352.6599 [(M+2H)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-имидазол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 135)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-имидазол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 135)
Используя Общую методику 6, исходя из соединения Синтеза R3cg и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 135. МСВР: рассчитано для C38H41N9O4S: 719.3002, найдено: 360.6580 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 136)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 136)
Используя Общую методику 6, исходя из соединения Синтеза R3ch и соединения Синтеза R1c в качестве реагентов, получали Пример 136. МСВР: рассчитано для C38H41N9O3S: 703.3053, найдено: 704.3095 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 137)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 137)
Используя Общую методику 6, исходя из соединения Синтеза R3ch и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 137. МСВР: рассчитано для C38H41N9O4S: 719.3002, найдено: 720.3059 [(М+Н)+ форма].
 7-[1-(дифторметил)-1Н-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 138)
7-[1-(дифторметил)-1Н-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 138)
Используя Общую методику 6, исходя из соединения Синтеза R3ci и соединения Синтеза R1c в качестве реагентов, получали Пример 138. МСВР: рассчитано для C38H39F2N9O3S: 739.2864, найдено: 740.2936 [(М+Н)+ форма].
 7-[1-(дифторметил)-1Н-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 139)
7-[1-(дифторметил)-1Н-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 139)
Используя Общую методику 6, исходя из соединения Синтеза R3ci и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 139. МСВР: рассчитано для C38H39F2N9O4S: 755.2814, найдено: 756.287 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1,3-тиазол-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 140)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1,3-тиазол-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 140)
Используя Общую методику 6, исходя из соединения Синтеза R3ck и соединения Синтеза R1c в качестве реагентов, получали Пример 140. МСВР: рассчитано для C37H38N8O3S2: 706.2509, найдено: 707.257 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1,3-тиазол-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 141)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1,3-тиазол-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 141)
Используя Общую методику 6, исходя из соединения Синтеза R3ck и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 141. МСВР: рассчитано для C37H38N8O4S2: 722.2457, найдено: 723.2535 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(проп-2-ин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 142)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(проп-2-ин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 142)
Используя Общую методику 6, исходя из соединения Синтеза R3m и соединения Синтеза R1c в качестве реагентов, получали Пример 142. МСВР: рассчитано для C37H39N7O3S: 661.2835, найдено: 662.2896 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 143)
3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 143)
Используя Общую методику 6, исходя из соединения Синтеза R3o и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 143. МСВР: рассчитано для C30H32BrF3N6O3S: 692.1392, найдено: 693.1452 [(М+Н)+ форма].
 7-(бута-2,3-диен-1-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 144)
7-(бута-2,3-диен-1-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 144)
Используя Общую методику 6, исходя из соединения Синтеза R3s и соединения Синтеза R1c в качестве реагентов, получали Пример 144. МСВР: рассчитано для C38H41N7O3S: 675.2991, найдено: 676.3089 [(М+Н)+ форма].
 7-(4-хлорбензил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 145)
7-(4-хлорбензил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 145)
Используя Общую методику 6, исходя из соединения Синтеза R3x и соединения Синтеза R1c в качестве реагентов, получали Пример 145. МСВР: рассчитано для C41H42ClN7O3S: 747.2758, найдено: 374.6462 [(М+2Н)2+ форма].
 7-(3-хлорбензил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 146)
7-(3-хлорбензил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 146)
Используя Общую методику 6, исходя из соединения Синтеза R3y и соединения Синтеза R1c в качестве реагентов, получали Пример 146. МСВР: рассчитано для C41H42ClN7O3S: 747.2758, найдено: 374.645 [(М+2Н)2+ форма].
 7-бензил-3-[(1-{[1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 147)
7-бензил-3-[(1-{[1-бензил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 147)
Используя Общую методику 6, исходя из рацемического 7-бензил-3-({4-гидрокси-1-[3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-3H,4H,7H-пирроло[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием рацемического трет-бутил 4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и 7-бензил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-она) и бензилбромида в качестве реагентов, получали Пример 147. МСВР: рассчитано для C38H41N5O3: 615.3209, найдено: 616.3308 [(М+Н)+ форма].
 7-бензил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 148)
7-бензил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 148)
Используя Общую методику 6, исходя из соединения Синтеза R3z и соединения Синтеза R1c в качестве реагентов, получали Пример 148. МСВР: рассчитано для C41H43N7O3S: 713.3148, найдено: 357.6653 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 149)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 149)
Используя Общую методику 7, исходя из соединения Синтеза R3ac и соединения Синтеза R1d в качестве реагентов, получали Пример 149. МСВР: рассчитано для C44H47N7O7S: 817.3257, найдено: 818.3322 [(М+Н)+ форма].
 7-(3,5-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 150)
7-(3,5-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 150)
Используя Общую методику 7, исходя из соединения Синтеза R3ad и соединения Синтеза R1d в качестве реагентов, получали Пример 150. МСВР: рассчитано для C41H39N7O4SCl2: 795.2161, найдено: 796.225 [(М+Н)+ форма].
 7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 151)
7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 151)
Используя Общую методику 7, исходя из соединения Синтеза R3ae и соединения Синтеза R1d в качестве реагентов, получали Пример 151. МСВР: рассчитано для C42H42N7O5SCl: 791.2657, найдено: 792.2736 [(М+Н)+ форма].
 7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 152)
7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 152)
Используя Общую методику 7, исходя из соединения Синтеза R3af и соединения Синтеза R1d в качестве реагентов, получали Пример 152. МСВР: рассчитано для C43H45N7O6S: 787.3152, найдено: 788.3224 [(М+Н)+ форма].
 7-(3,4-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 153)
7-(3,4-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 153)
Используя Общую методику 7, исходя из соединения Синтеза R3ag и соединения Синтеза R1d в качестве реагентов, получали Пример 153. МСВР: рассчитано для C41H39Cl2N7O4S: 795.2161, найдено: 796.2221 [(М+Н)+ форма].
 7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 154)
7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 154)
Используя Общую методику 7, исходя из соединения Синтеза R3ah и соединения Синтеза R1d в качестве реагентов, получали Пример 154. МСВР: рассчитано для C41H39ClFN7O4S: 779.2457, найдено: 780.2528 [(М+Н)+ форма].
 7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 155)
7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 155)
Используя Общую методику 7, исходя из соединения Синтеза R3ai и соединения Синтеза R1d в качестве реагентов, получали Пример 155. МСВР: рассчитано для C42H42ClN7O5S: 791.2657, найдено: 792.2735 [(М+Н)+ форма].
 7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 156)
7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 156)
Используя Общую методику 7, исходя из соединения Синтеза R3aj и соединения Синтеза R1d в качестве реагентов, получали Пример 156. МСВР: рассчитано для C42H42FN7O5S: 775.2952, найдено: 776.3023 [(М+Н)+ форма].
 7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 157)
7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 157)
Используя Общую методику 7, исходя из соединения Синтеза R3ak и соединения Синтеза R1d в качестве реагентов, получали Пример 157. МСВР: рассчитано для C43H45N7O6S: 787.3152, найдено: 394.6638 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 158)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 158)
Используя Общую методику 7, исходя из соединения Синтеза R3ao и соединения Синтеза R1d в качестве реагентов, получали Пример 158. МСВР: рассчитано для C42H40F3N7O4S: 795.2814, найдено: 796.2886 [(М+Н)+ форма].
 7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 159)
7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 159)
Используя Общую методику 7, исходя из соединения Синтеза R3ap и соединения Синтеза R1d в качестве реагентов, получали Пример 159. МСВР: рассчитано для C42H41F2N7O4S: 777.2909, найдено: 778.2984 [(М+Н)+ форма].
 7-[4-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 160)
7-[4-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 160)
Используя Общую методику 7, исходя из соединения Синтеза R3az и соединения Синтеза R1d в качестве реагентов, получали Пример 160. МСВР: рассчитано для C48H47N7O5S: 833.3359, найдено: 834.3447 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 161)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 161)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метил-2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 161. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2754 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-тиазол-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 162)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-тиазол-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 162)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метилизотиазол-4-карбоновой кислоты в качестве реагентов, получали Пример 162. МСВР: рассчитано для C30H34N6O4S: 574.2362, найдено: 575.2434 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он (Пример 163)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он (Пример 163)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 163. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2593 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 164)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 164)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 164. МСВР: рассчитано для C30H34N6O4S: 574.2362, найдено: 575.2437 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бензил-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 165)
3-{[1-({(3R,4R)-1-[(2-бензил-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 165)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-бензил-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 165. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2897 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 166)
3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 166)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-метилбензойной кислоты в качестве реагентов, получали Пример 166. МСВР: рассчитано для C33H37N5O4: 567.2846, найдено: 568.2904 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 167)
3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 167)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метилбензойной кислоты в качестве реагентов, получали Пример 167. МСВР: рассчитано для C33H37N5O4: 567.2846, найдено: 668.2916 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(4-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 168)
3-[(4-гидрокси-1-{[(3R,4R)-1-(4-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 168)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метилбензойной кислоты в качестве реагентов, получали Пример 168. МСВР: рассчитано для C33H37N5O4: 567.2846, найдено: 568.2919 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 169)
3-[(1-{[(3R,4R)-1-(2-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 169)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-фторбензойной кислоты в качестве реагентов, получали Пример 169. МСВР: рассчитано для C32H34FN5O4: 571.2595, найдено: 572.266 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 170)
3-[(1-{[(3R,4R)-1-(3-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 170)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-фторбензойной кислоты в качестве реагентов, получали Пример 170. МСВР: рассчитано для C32H34FN5O4: 571.2595, найдено: 572.265 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(4-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 171)
3-[(1-{[(3R,4R)-1-(4-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 171)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-фторбензойной кислоты в качестве реагентов, получали Пример 171. МСВР: рассчитано для C32H34FN5O4: 571.2595, найдено: 572.267 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 172)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 172)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метил-2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 172. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.27 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 173)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 173)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 173. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.254 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(2-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 174)
3-[(1-{[(3R,4R)-1-{[2-(2-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 174)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-(2-фторфенил)-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 174. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2668 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 175)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 175)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метил-2-(о-толил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 175. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2917 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 176)
3-{[1-({(3R,4R)-1-[(5-бромтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 176)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бромтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 176. МСВР: рассчитано для C30H32BrN5O4S: 637.1358, найдено: 638.1430 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1-бензил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 177)
3-{[1-({(3R,4R)-1-[(1-бензил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 177)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-бензилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 177. МСВР: рассчитано для C37H40N6O4: 632.3111, найдено: 633.3184 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-5-фенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 178)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-5-фенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 178)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-метил-5-фенилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 178. МСВР: рассчитано для C37H40N6O4: 632.3111, найдено: 633.3183 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1Н-пиррол-2-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 179)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1Н-пиррол-2-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 179)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1Н-пиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 179. МСВР: рассчитано для C30H34N6O4: 542.2642, найдено: 543.2711 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 180)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 180)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-метилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 180. МСВР: рассчитано для C31H36N6O4: 556.2798, найдено: 557.2862 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[1-(пиридин-3-илметил)-1Н-пиррол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 181)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[1-(пиридин-3-илметил)-1Н-пиррол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 181)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-(3-пиридилметил)пиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 181. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 317.6602 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 182)
3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 182)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-(2-амино-4-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 182. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 326.638 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 183)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 183)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метил-5-(4-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 183. МСВР: рассчитано для C36H38N6O4S: 650.2676, найдено: 651.2752 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(38,48)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 184)
3-[(4-гидрокси-1-{[(38,48)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 184)
Используя Общую методику 7, исходя из 3-({4-гидрокси-1-[(3S,4S)-3-фенилпиперидин-4-карбонил]пиперидин-4-ил}метил)-7-метил-3H,4H,7H-пирроло[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием трет-бутил (3S,4S)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и соединения Синтеза R2b) и 5-(4-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 184. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2591 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-нитро-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 185)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-нитро-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 185)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1p в качестве реагентов, получали Пример 185. МСВР: рассчитано для C35H35N7O6S: 681.2369, найдено: 682.2432 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1-этенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 186)
3-{[1-({(3R,4R)-1-[(1-этенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 186)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-винилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 186. МСВР: рассчитано для C32H36N6O4: 568.2798, найдено: 569.2884 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[1-(проп-2-ен-1-ил)-1Н-пиррол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 187)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[1-(проп-2-ен-1-ил)-1Н-пиррол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 187)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-аллилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 187. МСВР: рассчитано для C33H38N6O4: 582.2955, найдено: 583.3039 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-индол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 188)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-индол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 188)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-метилиндол-2-карбоновой кислоты в качестве реагентов, получали Пример 188. МСВР: рассчитано для C35H38N6O4: 606.2955, найдено: 607.3033 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-бром-1-метил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 189)
3-{[1-({(3R,4R)-1-[(4-бром-1-метил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 189)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-бром-1-метилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 189. МСВР: рассчитано для C31H35BrN6O4: 634.1903, найдено: 635.1981 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2,2-дифтор-1,3-бензодиоксол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 190)
3-{[1-({(3R,4R)-1-[(2,2-дифтор-1,3-бензодиоксол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 190)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2,2-дифтор-1,3-бензодиоксол-5-карбоновой кислоты в качестве реагентов, получали Пример 190. МСВР: рассчитано для C33H33F2N5O6: 633.2399, найдено: 634.2475 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(1Н-индол-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 191)
3-[(4-гидрокси-1-{[(3R,4R)-1-(1Н-индол-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 191)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1Н-индол-5-карбоновой кислоты в качестве реагентов, получали Пример 191. МСВР: рассчитано для C34H36N6O4: 592.2798, найдено: 593.2881 [(М+Н)+ форма].
 трет-бутил 6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат (Пример 192)
трет-бутил 6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидроизохинолин-2(1Н)-карбоксилат (Пример 192)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-трет-бутоксикарбонил-3,4-дигидро-1H-изохинолин-6-карбоновой кислоты в качестве реагентов, получали Пример 192. МСВР: рассчитано для C40H48N6O6: 708.3635, найдено: 709.3717 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1-ацетил-1,2,3,4-тетрагидрохинолин-6-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 193)
3-{[1-({(3R,4R)-1-[(1-ацетил-1,2,3,4-тетрагидрохинолин-6-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 193)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-ацетил-3,4-дигидро-2H-хинолин-6-карбоновой кислоты в качестве реагентов, получали Пример 193. МСВР: рассчитано для C37H42N6O5: 650.3217, найдено: 651.3306 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-бромпиридин-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 194)
3-{[1-({(3R,4R)-1-[(4-бромпиридин-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 194)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-бромпиридин-2-карбоновой кислоты в качестве реагентов, получали Пример 194. МСВР: рассчитано для C31H33BrN6O4: 632.1747, найдено: 633.1821 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бромпиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 195)
3-{[1-({(3R,4R)-1-[(2-бромпиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 195)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-бромпиридин-4-карбоновой кислоты в качестве реагентов, получали Пример 195. МСВР: рассчитано для C31H33BrN6O4: 632.1747, найдено: 633.1824 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 196)
3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 196)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бромпиридин-3-карбоновой кислоты в качестве реагентов, получали Пример 196. МСВР: рассчитано для C31H33BrN6O4: 632.1747, найдено: 633.1827 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бром-3-фтортиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 197)
3-{[1-({(3R,4R)-1-[(5-бром-3-фтортиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 197)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бром-3-фтортиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 197. МСВР: рассчитано для C30H31BrFN5O4S: 655.1264, найдено: 656.1341 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(6-бромпиридин-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 198)
3-{[1-({(3R,4R)-1-[(6-бромпиридин-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 198)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 6-бромпиридин-2-карбоновой кислоты в качестве реагентов, получали Пример 198. МСВР: рассчитано для C31H33BrN6O4: 632.1747, найдено: 633.1822 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(1Н-бензотриазол-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 199)
3-[(1-{[(3R,4R)-1-(1Н-бензотриазол-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 199)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1Н-бензотриазол-5-карбоновой кислоты в качестве реагентов, получали Пример 199. МСВР: рассчитано для C32H34N8O4: 594.2703, найдено: 595.2782 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[транс-2-фенилциклопропил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он, диастереоизомер 1 (Пример 200)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[транс-2-фенилциклопропил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он, диастереоизомер 1 (Пример 200)
Используя Общую методику 7, исходя из соединения Синтеза R3b и транс-2-фенил-1-циклопропанкарбоновой кислоты в качестве реагентов, Пример 200 получали в виде чистого диастереоизомера после очистки с помощью препаративной ЖХ (колонка С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MCN, изократический режим: 37%). МСВР: рассчитано для C35H39N5O4: 593.3002, найдено: 594.3082 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-бромбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d|пиримидин-4-он (Пример 201)
3-[(1-{[(3R,4R)-1-(3-бромбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d|пиримидин-4-он (Пример 201)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-бромбензойной кислоты в качестве реагентов, получали Пример 201. МСВР: рассчитано для C32H34BrN5O4: 631.1794, найдено: 632.1873 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[транс-2-фенилциклопропил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он, диастереоизомер 2 (Пример 202)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[транс-2-фенилциклопропил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он, диастереоизомер 2 (Пример 202)
Используя Общую методику 7, исходя из соединения Синтеза R3b и транс-2-фенилциклопропанкарбоновой кислоты в качестве реагентов, Пример 202 получали в виде чистого диастереоизомера после очистки с помощью препаративной ЖХ (колонка С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MCN, изократический режим: 37%). МСВР: рассчитано для C35H39N5O4: 593.3002, найдено: 594.3084 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(3-нитробензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 203)
3-[(4-гидрокси-1-{[(3R,4R)-1-(3-нитробензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 203)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-нитробензойной кислоты в качестве реагентов, получали Пример 203. МСВР: рассчитано для C32H34N6O6: 598.2539, найдено: 599.2625 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-бензоил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 204)
3-[(1-{[(3R,4R)-1-бензоил-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 204)
Используя Общую методику 7, исходя из соединения Синтеза R3b и бензойной кислоты в качестве реагентов, получали Пример 204. МСВР: рассчитано для C32H35N5O4: 553.2689, найдено: 554.2782 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-этинилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 205)
3-[(1-{[(3R,4R)-1-(3-этинилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 205)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-этинилбензойной кислоты в качестве реагентов, получали Пример 205. МСВР: рассчитано для C34H35N5O4: 577.2689, найдено: 578.2776 [(М+Н)+ форма].
 метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 206)
метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 206)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метоксикарбонилбензойной кислоты в качестве реагентов, получали Пример 206. МСВР: рассчитано для C34H37N5O6: 611.2744, найдено: 612.2837 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(трифторметил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 207)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(трифторметил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 207)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(трифторметил)бензойной кислоты в качестве реагентов, получали Пример 207. МСВР: рассчитано для C33H34F3N5O4: 621.2563, найдено: 622.265 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензонитрил (Пример 208)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензонитрил (Пример 208)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-цианобензойной кислоты в качестве реагентов, получали Пример 208. МСВР: рассчитано для C33H34N6O4: 578.2642, найдено: 579.272 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метоксибензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 209)
3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метоксибензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 209)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метоксибензойной кислоты в качестве реагентов, получали Пример 209. МСВР: рассчитано для C33H37N5O5: 583.2795, найдено: 584.2889 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(3-феноксибензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 210)
3-[(4-гидрокси-1-{[(3R,4R)-1-(3-феноксибензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 210)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-феноксибензойной кислоты в качестве реагентов, получали Пример 210. МСВР: рассчитано для C38H39N5O5: 645.2951, найдено: 646.3025 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-трет-бутилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 211)
3-[(1-{[(3R,4R)-1-(3-трет-бутилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 211)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-трет-бутилбензойной кислоты в качестве реагентов, получали Пример 211. МСВР: рассчитано для C36H43N5O4: 609.3315, найдено: 610.3382 [(М+Н)+ форма].
 5-бром-2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-3-карбонитрил (Пример 212)
5-бром-2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-3-карбонитрил (Пример 212)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бром-3-цианотиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 212. МСВР: рассчитано для C31H31BrN6O4S: 662.1311, найдено: 663.1384 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(хинолин-6-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 213)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(хинолин-6-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 213)
Используя Общую методику 7, исходя из соединения Синтеза R3b и хинолин-6-карбоновой кислоты в качестве реагентов, получали Пример 213. МСВР: рассчитано для C35H36N6O4: 604.2798, найдено: 605.2872 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2,3-дигидро-1,4-бензодиоксин-6-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 214)
3-[(1-{[(3R,4R)-1-(2,3-дигидро-1,4-бензодиоксин-6-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 214)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2,3-дигидро-1,4-бензодиоксин-6-карбоновой кислоты в качестве реагентов, получали Пример 214. МСВР: рассчитано для C34H37N5O6: 611.2744, найдено: 612.2822 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(5,6-дигидро-4Н-циклопента[b]тиофен-2-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 215)
3-[(1-{[(3R,4R)-1-(5,6-дигидро-4Н-циклопента[b]тиофен-2-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 215)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5,6-дигидро-4H-циклопента[b]тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 215. МСВР: рассчитано для C33H37N5O4S: 599.2567, найдено: 600.2645 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(4,5,6,7-тетрагидро-1-бензотиофен-2-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 216)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(4,5,6,7-тетрагидро-1-бензотиофен-2-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 216)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4,5,6,7-тетрагидробензотиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 216. МСВР: рассчитано для C34H39N5O4S: 613.2723, найдено: 614.2805 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бром-1-метил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 217)
3-{[1-({(3R,4R)-1-[(5-бром-1-метил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 217)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бром-1-метилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 217. МСВР: рассчитано для C31H35N6O4Br: 634.1903, найдено: 637.1959 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(3-фенилциклобутил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 218)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(3-фенилциклобутил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 218)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-фенилциклобутанкарбоновой кислоты в качестве реагентов, получали Пример 218. МСВР: рассчитано для C36H41N5O4: 607.3159, найдено: 608.3236 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-этоксибензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 219)
3-[(1-{[(3R,4R)-1-(3-этоксибензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 219)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-этоксибензойной кислоты в качестве реагентов, получали Пример 219. МСВР: рассчитано для C34H39N5O5: 597.2951, найдено: 598.3032 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(4-метилпиперазин-1-ил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 220)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(4-метилпиперазин-1-ил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 220)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(4-метилпиперазин-1-ил)бензойной кислоты в качестве реагентов, получали Пример 220. МСВР: рассчитано для C37H45N7O4: 651.3533, найдено: 652.3604 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пропан-2-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 221)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пропан-2-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 221)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-изопропилбензойной кислоты в качестве реагентов, получали Пример 221. МСВР: рассчитано для C35H41N5O4: 595.3159, найдено: 596.3251 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пирролидин-1-илметил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 222)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пирролидин-1-илметил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 222)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(пирролидин-1-илметил)бензойной кислоты в качестве реагентов, получали Пример 222. МСВР: рассчитано для C37H44N6O4: 636.3424, найдено: 637.3504 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[3-(диметиламино)бензоил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 223)
3-{[1-({(3R,4R)-1-[3-(диметиламино)бензоил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 223)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(диметиламино)бензойной кислоты в качестве реагентов, получали Пример 223. МСВР: рассчитано для C34H40N6O4: 596.3111, найдено: 597.3194 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(морфолин-4-ил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 224)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(морфолин-4-ил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 224)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-морфолинобензойной кислоты в качестве реагентов, получали Пример 224. МСВР: рассчитано для C36H42N6O5: 638.3217, найдено: 639.3282 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-(метилсульфонил)-1,2,3,4-тетрагидрохинолин-6-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 225)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-(метилсульфонил)-1,2,3,4-тетрагидрохинолин-6-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 225)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-метилсульфонил-3,4-дигидро-2H-хинолин-6-карбоновой кислоты в качестве реагентов, получали Пример 225. МСВР: рассчитано для C36H42N6O6S: 686.2886, найдено: 687.2962 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиперидин-1-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 226)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиперидин-1-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 226)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(1-пиперидил)бензойной кислоты в качестве реагентов, получали Пример 226. МСВР: рассчитано для C37H44N6O4: 636.3424, найдено: 637.3483 [(М+Н)+ форма].
 6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1-метил-3,4-дигидрохинолин-2(1Н)-он (Пример 227)
6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1-метил-3,4-дигидрохинолин-2(1Н)-он (Пример 227)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-метил-2-оксо-3,4-дигидрохинолин-6-карбоновой кислоты в качестве реагентов, получали Пример 227. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3162 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{3-[(диметиламино)метил]бензоил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 228)
3-[(1-{[(3R,4R)-1-{3-[(диметиламино)метил]бензоил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 228)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(диметиламинометил)бензойной кислоты в качестве реагентов, получали Пример 228. МСВР: рассчитано для C35H42N6O4: 610.3268, найдено: 611.335 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1-этенил-1Н-индол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 229)
3-{[1-({(3R,4R)-1-[(1-этенил-1Н-индол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 229)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1t в качестве реагентов, получали Пример 229. МСВР: рассчитано для C36H38N6O4: 618.2955, найдено: 619.3002 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бром-1-этенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 230)
3-{[1-({(3R,4R)-1-[(5-бром-1-этенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 230)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1u в качестве реагентов, получали Пример 230. МСВР: рассчитано для C32H35BrN6O4: 646.1903, найдено: 647.1989 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2-ацетилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 231)
3-[(1-{[(3R,4R)-1-(2-ацетилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 231)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-ацетилбензойной кислоты в качестве реагентов, получали Пример 231. МСВР: рассчитано для C34H37N5O5: 595.2795, найдено: 596.2861 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-фтор-4,5-дийодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 232)
3-{[1-({(3R,4R)-1-[(3-фтор-4,5-дийодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 232)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1h в качестве реагентов, получали Пример 232. МСВР: рассчитано для C30H30FI2N5O4S: 829.0092, найдено: 830.0159 [(М+Н)+ форма].
 метил 2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 233)
метил 2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 233)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-метоксикарбонилбензойной кислоты в качестве реагентов, получали Пример 233. МСВР: рассчитано для C34H37N5O6: 611.2744, найдено: 612.2823 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-фтор-4-йод-5-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 234)
3-{[1-({(3R,4R)-1-[(3-фтор-4-йод-5-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 234)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1i в качестве реагентов, получали Пример 234. МСВР: рассчитано для C31H33FIN5O4S: 717.1282, найдено: 718.1352 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-бром-1-этенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 235)
3-{[1-({(3R,4R)-1-[(4-бром-1-этенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 235)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1v в качестве реагентов, получали Пример 235. МСВР: рассчитано для C32H35BrN6O4: 646.1903, найдено: 647.198 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-хлор-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 236)
3-{[1-({(3R,4R)-1-[(3-хлор-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 236)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-хлор-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 236. МСВР: рассчитано для C31H34ClN5O4S: 607.2020, найдено: 608.2107 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-амино-4-(метилсульфонил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 237)
3-[(1-{[(3R,4R)-1-{[3-амино-4-(метилсульфонил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 237)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-амино-4-метилсульфонилтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 237. МСВР: рассчитано для C31H36N6O6S2: 652.2137, найдено: 653.2224 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-йод-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 238)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-йод-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 238)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-йод-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 238. МСВР: рассчитано для C31H34IN5O4S: 699.1376, найдено: 700.145 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бром-3-хлор-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 239)
3-{[1-({(3R,4R)-1-[(5-бром-3-хлор-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 239)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бром-3-хлор-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 239. МСВР: рассчитано для C31H33BrClN5O4S: 685.1125, найдено: 686.1217 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({1-[(метилсульфанил)метил]-1Н-пиррол-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 240)
3-[(4-гидрокси-1-{[(3R,4R)-1-({1-[(метилсульфанил)метил]-1Н-пиррол-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 240)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-(метилсульфанилметил)пиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 240. МСВР: рассчитано для C32H38N6O4S: 602.2675, найдено: 603.2756 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(хиноксалин-6-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 241)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(хиноксалин-6-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 241)
Используя Общую методику 7, исходя из соединения Синтеза R3b и хиноксалин-6-карбоновой кислоты в качестве реагентов, получали Пример 241. МСВР: рассчитано для C34H35N7O4: 605.2750, найдено: 606.2831 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1H-индол-6-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 242)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1H-индол-6-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 242)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-метилиндол-6-карбоновой кислоты в качестве реагентов, получали Пример 242. МСВР: рассчитано для C35H38N6O4: 606.2955, найдено: 607.3035 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-оксо-1-фенилпирролидин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 243)
3-{[4-гидрокси-1-({(3R,4R)-1-[(5-оксо-1-фенилпирролидин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 243)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-оксо-1-фенилпирролидин-3-карбоновой кислоты в качестве реагентов, получали Пример 243. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3129 [(М+Н)+ форма].
 трет-бутил 7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидрохиноксалин-1(2Н)-карбоксилат (Пример 244)
трет-бутил 7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидрохиноксалин-1(2Н)-карбоксилат (Пример 244)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-трет-бутоксикарбонил-2,3-дигидро-1H-хиноксалин-6-карбоновой кислоты в качестве реагентов, получали Пример 244. МСВР: рассчитано для C39H47N7O6: 709.3588, найдено: 710.3667 [(М+Н)+ форма].
 трет-бутил 7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидрохинолин-1(2Н)-карбоксилат (Пример 245)
трет-бутил 7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидрохинолин-1(2Н)-карбоксилат (Пример 245)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-трет-бутоксикарбонил-3,4-дигидро-2H-хинолин-7-карбоновой кислоты в качестве реагентов, получали Пример 245. МСВР: рассчитано для C40H48N6O6: 708.3635, найдено: 709.3715 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(гидроксиацетил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 246)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(гидроксиацетил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 246)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(2-хлорацетил)бензойной кислоты в качестве реагентов, получали Пример 246. МСВР: рассчитано для C34H37N5O6: 611.2744, найдено: 612.2817 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-бромтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 247)
3-{[1-({(3R,4R)-1-[(3-бромтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 247)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-бромтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 247. МСВР: рассчитано для C30H32BrN5O4S: 637.1359, найдено: 638.1428 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-бром-1,3-тиазол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 248)
3-{[1-({(3R,4R)-1-[(4-бром-1,3-тиазол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 248)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-бромтиазол-2-карбоновой кислоты в качестве реагентов, получали Пример 248. МСВР: рассчитано для C29H31BrN6O4S: 638.1311, найдено: 639.1389 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромтиофен-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 249)
3-{[1-({(3R,4R)-1-[(5-бромтиофен-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 249)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бромтиофен-3-карбоновой кислоты в качестве реагентов, получали Пример 249. МСВР: рассчитано для C30H32BrN5O4S: 637.1359, найдено: 638.1438 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бромтиофен-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 250)
3-{[1-({(3R,4R)-1-[(2-бромтиофен-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 250)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-бромтиофен-3-карбоновой кислоты в качестве реагентов, получали Пример 250. МСВР: рассчитано для C30H32BrN5O4S: 637.1359, найдено: 638.1443 [(М+Н)+ форма].
 3-этокси-N-(4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензил)пропанамид (Пример 251)
3-этокси-N-(4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензил)пропанамид (Пример 251)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-[(3-этоксипропаноиламино)метил]бензойной кислоты в качестве реагентов, получали Пример 251. МСВР: рассчитано для C38H46N6O6: 682.3479, найдено: 683.3559 [(М+Н)+ форма].
 трет-бутил (4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензил)карбамат (Пример 252)
трет-бутил (4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензил)карбамат (Пример 252)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-[(трет-бутоксикарбониламино)метил]бензойной кислоты в качестве реагентов, получали Пример 252. МСВР: рассчитано для C38H46N6O6: 682.3479, найдено: 683.3567 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-хлор-5-йодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 253)
3-{[1-({(3R,4R)-1-[(3-хлор-5-йодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 253)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1j в качестве реагентов, получали Пример 253. МСВР: рассчитано для C30H31ClIN5O4S: 719.0830, найдено: 720.0905 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-ацетилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 254)
3-[(1-{[(3R,4R)-1-(3-ацетилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 254)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-ацетилбензойной кислоты в качестве реагентов, получали Пример 254. МСВР: рассчитано для C34H37N5O5: 595.2795, найдено: 596.2875 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензальдегид (Пример 255)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензальдегид (Пример 255)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-формилбензойной кислоты в качестве реагентов, получали Пример 255. МСВР: рассчитано для C33H35N5O5: 581.2638, найдено: 582.271 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-этенилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 256)
3-[(1-{[(3R,4R)-1-(3-этенилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 256)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-винилбензойной кислоты в качестве реагентов, получали Пример 256. МСВР: рассчитано для C34H37N5O4: 579.2845, найдено: 580.2931 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-этилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 257)
3-[(1-{[(3R,4R)-1-(3-этилбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 257)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-этилбензойной кислоты в качестве реагентов, получали Пример 257. МСВР: рассчитано для C34H39N5O4: 581.3002, найдено: 582.3077 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(метилсульфонил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 258)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(метилсульфонил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 258)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метилсульфонилбензойной кислоты в качестве реагентов, получали Пример 258. МСВР: рассчитано для C33H37N5O6S: 631.2465, найдено: 632.2549 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4,5-дихлор-3-фтортиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 259)
3-{[1-({(3R,4R)-1-[(4,5-дихлор-3-фтортиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 259)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1w в качестве реагентов, получали Пример 259. МСВР: рассчитано для C30H30Cl2FN5O4S: 645.1379, найдено: 646.1449 [(М+Н)+ форма].
 трет-бутил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 260)
трет-бутил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 260)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-трет-бутоксикарбонилбензойной кислоты в качестве реагентов, получали Пример 260. МСВР: рассчитано для C37H43N5O6: 653.3214, найдено: 654.3298 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-хлор-3-фтор-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 261)
3-{[1-({(3R,4R)-1-[(5-хлор-3-фтор-4-метилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 261)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1l в качестве реагентов, получали Пример 261. МСВР: рассчитано для C31H33ClFN5O4S: 625.1926, найдено: 626.1997 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2,4-бис(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 262)
3-[(1-{[(3R,4R)-1-{[2,4-бис(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 262)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2,4-бис(6-метил-3-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 262. МСВР: рассчитано для C41H42N8O4S: 742.3049, найдено: 743.3126 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-хлор-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 263)
3-[(1-{[(3R,4R)-1-{[4-хлор-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 263)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-хлор-2-(6-метил-3-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 263. МСВР: рассчитано для C35H36ClN7O4S: 685.2238, найдено: 686.2299 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-хлор-2-метокси-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 264)
3-{[1-({(3R,4R)-1-[(4-хлор-2-метокси-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 264)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-хлор-2-метокситиазол-5-карбоновой кислоты в качестве реагентов получали Пример 264. МСВР: рассчитано для C30H33ClN6O5S: 624.1921, найдено: 625.2 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-бром-2-метокси-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 265)
3-{[1-({(3R,4R)-1-[(4-бром-2-метокси-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 265)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-бром-2-метокситиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 265. МСВР: рассчитано для C30H33BrN6O5S: 668.1417, найдено: 669.1494 [(М+Н)+ форма].
 6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}хиназолин-4(3Н)-он (Пример 266)
6-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}хиназолин-4(3Н)-он (Пример 266)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-оксо-3H-хиназолин-6-карбоновой кислоты в качестве реагентов, получали Пример 266. МСВР: рассчитано для C34H35N7O5: 621.2699, найдено: 622.2775 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-2-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 267)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-2-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 267)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-(2-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 267. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2603 [(М+Н)+ форма].
 7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидроизохинолин-1(2Н)-он (Пример 268)
7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидроизохинолин-1(2Н)-он (Пример 268)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 1-оксо-3,4-дигидро-2H-изохинолин-7-карбоновой кислоты в качестве реагентов, получали Пример 268. МСВР: рассчитано для C35H38N6O5: 622.2903, найдено: 623.2977 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-фтор-5-йодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 269)
3-{[1-({(3R,4R)-1-[(3-фтор-5-йодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 269)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1g в качестве реагентов, получали Пример 269. МСВР: рассчитано для C30H31N5O4FSI: 703.1125, найдено: 704.1203 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-хлор-2-(2-оксопиридин-1(2Н)-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 270)
3-[(1-{[(3R,4R)-1-{[4-хлор-2-(2-оксопиридин-1(2Н)-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 270)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-хлор-2-(2-оксо-1-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 270. МСВР: рассчитано для C34H34ClN7O5S: 687.2031, найдено: 688.2081 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-2-илметил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 271)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-2-илметил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 271)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-метил-2-(2-пиридилметил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 271. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2862 [(М+Н)+ форма].
 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1Н-индол-2,3-дион (Пример 272)
5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1Н-индол-2,3-дион (Пример 272)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2,3-диоксоиндолин-5-карбоновой кислоты в качестве реагентов, получали Пример 272. МСВР: рассчитано для C34H34N6O6: 622.2539, найдено: 623.2633 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(гидроксиметил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 273)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(гидроксиметил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 273)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(гидроксиметил)бензойной кислоты в качестве реагентов, получали Пример 273. МСВР: рассчитано для C33H37N5O5: 583.2795, найдено: 584.2875 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(2-гидроксибензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 274)
3-[(4-гидрокси-1-{[(3R,4R)-1-(2-гидроксибензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 274)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-гидроксибензойной кислоты в качестве реагентов, получали Пример 274. МСВР: рассчитано для C32H35N5O5: 569.2638, найдено: 570.2727 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-хлор-4-(диметиламино)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 275)
3-[(1-{[(3R,4R)-1-{[5-хлор-4-(диметиламино)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 275)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-хлор-4-(диметиламино)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 275. МСВР: рассчитано для C32H37ClN6O4S: 636.2286, найдено: 637.2358 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бром-4-метокситиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 276)
3-{[1-({(3R,4R)-1-[(5-бром-4-метокситиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 276)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-бром-4-метокситиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 276. МСВР: рассчитано для C31H34BrN5O5S: 667.1464, найдено: 668.153 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4,5-дибромтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 277)
3-{[1-({(3R,4R)-1-[(4,5-дибромтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 277)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4,5-дибромтиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 277. МСВР: рассчитано для C30H31Br2N5O4S: 715.0463, найдено: 716.053 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-оксо-2,3-дигидро-1Н-инден-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 278)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-оксо-2,3-дигидро-1Н-инден-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 278)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-оксоиндан-5-карбоновой кислоты в качестве реагентов, получали Пример 278. МСВР: рассчитано для C35H37N5O5: 607.2795, найдено: 608.2871 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-оксо-2,3-дигидро-1Н-изоиндол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 279)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-оксо-2,3-дигидро-1Н-изоиндол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 279)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-оксоизоиндолин-5-карбоновой кислоты в качестве реагентов, получали Пример 279. МСВР: рассчитано для C34H36N6O5: 608.2747, найдено: 609.2814 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-хлор-2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 280)
3-[(1-{[(3R,4R)-1-{[4-хлор-2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 280)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 4-хлор-2-(6-метокси-3-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 280. МСВР: рассчитано для C35H36N7O5SCl: 701.2187, найдено: 702.2257 [(М+Н)+ форма].
 метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-3-карбоксилат (Пример 281)
метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-3-карбоксилат (Пример 281)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-метоксикарбонилпиридин-3-карбоновой кислоты в качестве реагентов, получали Пример 281. МСВР: рассчитано для C33H36N6O6: 612.2697, найдено: 613.2776 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(2-гидроксиэтил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 282)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(2-гидроксиэтил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 282)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-(2-гидроксиэтил)бензойной кислоты в качестве реагентов, получали Пример 282. МСВР: рассчитано для C34H39N5O5: 597.2951, найдено: 598.3031 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(метилсульфанил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 283)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(метилсульфанил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 283)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метилсульфанилбензойной кислоты в качестве реагентов, получали Пример 283. МСВР: рассчитано для C33H37N5O4S: 599.2567, найдено: 600.2656 [(М+Н)+ форма].
 4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-2-карбонитрил (Пример 284)
4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-2-карбонитрил (Пример 284)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-цианопиридин-4-карбоновой кислоты в качестве реагентов, получали Пример 284. МСВР: рассчитано для C32H33N7O4: 579.2594, найдено: 580.2682 [(М+Н)+ форма].
 метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-5-нитробензоат (Пример 285)
метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-5-нитробензоат (Пример 285)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-метоксикарбонил-5-нитробензойной кислоты в качестве реагентов, получали Пример 285. МСВР: рассчитано для C34H36N6O8: 656.2595, найдено: 657.2679 [(М+Н)+ форма].
 диметил 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензол-1,3-дикарбоксилат (Пример 286)
диметил 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензол-1,3-дикарбоксилат (Пример 286)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3,5-бис(метоксикарбонил)бензойной кислоты в качестве реагентов, получали Пример 286. МСВР: рассчитано для C36H39N5O8: 669.2798, найдено: 670.2847 [(М+Н)+ форма].
 метил 3-бром-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 287)
метил 3-бром-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 287)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-бром-5-метоксикарбонилбензойной кислоты в качестве реагентов, получали Пример 287. МСВР: рассчитано для C34H36BrN5O6: 689.1849, найдено: 690.1936 [(М+Н)+ форма].
 трет-бутил метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензол-1,3-дикарбоксилат (Пример 288)
трет-бутил метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензол-1,3-дикарбоксилат (Пример 288)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 3-трет-бутоксикарбонил-5-метоксикарбонилбензойной кислоты в качестве реагентов, получали Пример 288. МСВР: рассчитано для C39H45N5O8: 711.3268, найдено: 712.3342 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 289)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 289)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 5-(4-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 289. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2597 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 290)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 290)
Используя Общую методику 7, исходя из соединения Синтеза R3ba и соединения Синтеза R1d в качестве реагентов, получали Пример 290. МСВР: рассчитано для C40H41N7O4S2: 747.2662, найдено: 748.2743 [(М+Н)+ форма].
 7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 291)
7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 291)
Используя Общую методику 7, исходя из соединения Синтеза R3bb и соединения Синтеза R1d в качестве реагентов, получали Пример 291. МСВР: рассчитано для C39H38ClN7O4S2: 767.2115, найдено: 768.2171 [(М+Н)+ форма].
 7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 292)
7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 292)
Используя Общую методику 7, исходя из соединения Синтеза R3bc и соединения Синтеза R1d в качестве реагентов, получали Пример 292. МСВР: рассчитано для C43H43N7O6S: 785.2996, найдено: 786.307 [(М+Н)+ форма].
 7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 293)
7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 293)
Используя Общую методику 7, исходя из соединения Синтеза R3bd и соединения Синтеза R1d в качестве реагентов, получали Пример 293. МСВР: рассчитано для C42H41N7O6S: 771.2839, найдено: 772.2895 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 294)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 294)
Используя Общую методику 7, исходя из соединения Синтеза R3bg и соединения Синтеза R1d в качестве реагентов, получали Пример 294. МСВР: рассчитано для C42H40F3N7O4S: 795.2814, найдено: 796.2883 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 295)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 295)
Используя Общую методику 7, исходя из соединения Синтеза R3bi и соединения Синтеза R1d в качестве реагентов, получали Пример 295. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 758.3124 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 296)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметокси)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 296)
Используя Общую методику 7, исходя из соединения Синтеза R3bp и соединения Синтеза R1d в качестве реагентов, получали Пример 296. МСВР: рассчитано для C42H40N7O5F3S: 811.2764, найдено: 812.2837 [(М+Н)+ форма].
 7-[3-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 297)
7-[3-(бензилокси)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 297)
Используя Общую методику 7, исходя из соединения Синтеза R3bq и соединения Синтеза R1d в качестве реагентов, получали Пример 297. МСВР: рассчитано для C48H47N7O5S: 833.3359, найдено: 834.3436 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метилпиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 298)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метилпиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 298)
Используя Общую методику 7, исходя из соединения Синтеза R3br и соединения Синтеза R1d в качестве реагентов, получали Пример 298. МСВР: рассчитано для C41H42N8O4S: 742.3049, найдено: 743.313 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 299)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 299)
Используя Общую методику 7, исходя из соединения Синтеза R3bs и соединения Синтеза R1d в качестве реагентов, получали Пример 299. МСВР: рассчитано для C41H42N8O5S: 758.2998, найдено: 759.3062 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-хлор-2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 300)
3-[(1-{[(3R,4R)-1-{[4-хлор-2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 300)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 4-хлор-2-(6-метокси-3-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 300. МСВР: рассчитано для C40H38N7O5SCl: 763.2344, найдено: 764.242 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3S,4S)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 301)
3-[(4-гидрокси-1-{[(3S,4S)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 301)
Используя Общую методику 7, исходя из 3-[(4-гидрокси-1-{[(3S,4S)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием трет-бутил (3S,4S)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и соединения Синтеза R2bu) и соединения Синтеза R1d в качестве реагентов, получали Пример 301. МСВР: рассчитано для C41H41N7O4S: 727.2941, найдено: 364.6536 [(М+2Н)2+ форма].
 3-{[1-({(3R,4R)-1-[(2-бромпиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 302)
3-{[1-({(3R,4R)-1-[(2-бромпиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 302)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 2-бромпиридин-4-карбоновой кислоты в качестве реагентов, получали Пример 302. МСВР: рассчитано для C36H35N6O4Br: 694.1903, найдено: 695.1969 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 303)
3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 303)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 5-бромпиридин-3-карбоновой кислоты в качестве реагентов, получали Пример 303. МСВР: рассчитано для C36H35N6O4Br: 694.1903, найдено: 695.1974 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 304)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 304)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 304. МСВР: рассчитано для C34H34N6O4S: 622.2362, найдено: 623.2429 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-4-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 305)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-4-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 305)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и тиазол-4-карбоновой кислоты в качестве реагентов, получали Пример 305. МСВР: рассчитано для C34H34N6O4S: 622.2362, найдено: 623.2434 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(морфолин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 306)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(морфолин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 306)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 4-метил-2-морфолинотиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 306. МСВР: рассчитано для C39H43N7O5S: 721.3046, найдено: 722.311 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 307)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 307)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 307. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2595 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 308)
3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 308)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 2-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 308. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2582 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-хлор-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 309)
3-{[1-({(3R,4R)-1-[(2-хлор-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 309)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 2-хлортиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 309. МСВР: рассчитано для C34H33ClN6O4S: 656.1973, найдено: 657.2041 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-индол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 310)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1Н-индол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 310)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 1-метилиндол-2-карбоновой кислоты в качестве реагентов, получали Пример 310. МСВР: рассчитано для C40H40N6O4: 668.3111, найдено: 669.3183 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-5-фенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 311)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-5-фенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 311)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 1-метил-5-фенилпиррол-2-карбоновой кислоты в качестве реагентов, получали Пример 311. МСВР: рассчитано для C42H42N6O4: 694.3268, найдено: 695.3331 [(М+Н)+ форма].
 метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 312)
метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 312)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 3-метоксикарбонилбензойной кислоты в качестве реагентов, получали Пример 312. МСВР: рассчитано для C39H39N5O6: 673.2900, найдено: 674.2969 [(М+Н)+ форма].
 метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-3-карбоксилат (Пример 313)
метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-3-карбоксилат (Пример 313)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 5-метоксикарбонилпиридин-3-карбоновой кислоты в качестве реагентов, получали Пример 313. МСВР: рассчитано для C38H38N6O6: 674.2853, найдено: 675.291 [(М+Н)+ форма].
 метил 4-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-2-карбоксилат (Пример 314)
метил 4-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-2-карбоксилат (Пример 314)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 2-метоксикарбонилпиридин-4-карбоновой кислоты в качестве реагентов, получали Пример 314. МСВР: рассчитано для C38H38N6O6: 674.2853, найдено: 675.2914 [(М+Н)+ форма].
 7-этил-3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 315)
7-этил-3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 315)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 4-метил-2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 315. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2903 [(М+Н)+ форма].
 7-этил-3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-тиазол-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 316)
7-этил-3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-тиазол-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 316)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 3-метилизотиазол-4-карбоновой кислоты в качестве реагентов, получали Пример 316. МСВР: рассчитано для C31H36N6O4S: 588.2519, найдено: 589.2601 [(М+Н)+ форма].
 7-этил-3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 317)
7-этил-3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 317)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 317. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2749 [(М+Н)+ форма].
 7-этил-3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 318)
7-этил-3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 318)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 318. МСВР: рассчитано для C31H36N6O4S: 588.2519, найдено: 589.259 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бензил-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 319)
3-{[1-({(3R,4R)-1-[(2-бензил-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 319)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 2-бензил-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 319. МСВР: рассчитано для C38H42N6O4S: 678.2988, найдено: 679.3065 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 320)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 320)
Используя Общую методику 6, исходя из соединения Синтеза R3c и 2-метилбензойной кислоты в качестве реагентов, получали Пример 320. МСВР: рассчитано для C34H39N5O4: 581.3002, найдено: 582.3088 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 321)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 321)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 3-метилбензойной кислоты в качестве реагентов, получали Пример 321. МСВР: рассчитано для C34H39N5O4: 581.3002, найдено: 582.3075 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(4-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 322)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-(4-метилбензоил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 322)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 4-метилбензойной кислоты в качестве реагентов, получали Пример 322. МСВР: рассчитано для C34H39N5O4: 581.3002, найдено: 582.3073 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-(2-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 323)
7-этил-3-[(1-{[(3R,4R)-1-(2-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 323)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 2-фторбензойной кислоты в качестве реагентов, получали Пример 323. МСВР: рассчитано для C33H36FN5O4: 585.2751, найдено: 586.282 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-(3-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 324)
7-этил-3-[(1-{[(3R,4R)-1-(3-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 324)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 3-фторбензойной кислоты в качестве реагентов, получали Пример 324. МСВР: рассчитано для C33H36FN5O4: 585.2751, найдено: 586.2827 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-(4-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 325)
7-этил-3-[(1-{[(3R,4R)-1-(4-фторбензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 325)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 4-фторбензойной кислоты в качестве реагентов, получали Пример 325. МСВР: рассчитано для C33H36FN5O4: 585.2751, найдено: 586.2846 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-{[2-(2-фторбензил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 326)
7-этил-3-[(1-{[(3R,4R)-1-{[2-(2-фторбензил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 326)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 2-[(2-фторфенил)метил]тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 326. МСВР: рассчитано для C37H39FN6O4S: 682.2738, найдено: 683.2804 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 327)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 327)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 4-метил-2-(о-толил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 327. МСВР: рассчитано для C38H42N6O4S: 678.2988, найдено: 679.3069 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 328)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 328)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 5-(4-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 328. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2755 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 329)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 329)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 4-метил-2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 329. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2855 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 330)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 330)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 330. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.269 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-{[2-(2-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 331)
7-этил-3-[(1-{[(3R,4R)-1-{[2-(2-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 331)
Используя Общую методику 7, исходя из соединения Синтеза R3c и 2-(2-фторфенил)-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 331. МСВР: рассчитано для C37H39FN6O4S: 682.2738, найдено: 683.2823 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 332)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 332)
Используя Общую методику 7, исходя из соединения Синтеза R3ca и соединения Синтеза R1d в качестве реагентов, получали Пример 332. МСВР: рассчитано для C40H40N8O4S: 728.2893, найдено: 729.2970 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-имидазол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 333)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-имидазол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 333)
Используя Общую методику 7, исходя из соединения Синтеза R3cg и соединения Синтеза R1d в качестве реагентов, получали Пример 333. МСВР: рассчитано для C39H41N9O4S: 731.3002, найдено: 732.3086 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 334)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 334)
Используя Общую методику 7, исходя из соединения Синтеза R3ch и соединения Синтеза R1d в качестве реагентов, получали Пример 334. МСВР: рассчитано для C39H41N9O4S: 731.3002, найдено: 732.3083 [(М+Н)+ форма].
 7-[1-(дифторметил)-1H-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 335)
7-[1-(дифторметил)-1H-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 335)
Используя Общую методику 7, исходя из соединения Синтеза R3ci и соединения Синтеза R1d в качестве реагентов, получали Пример 335. МСВР: рассчитано для C39H39F2N9O4S: 767.2814, найдено: 768.2908 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиримидин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 336)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиримидин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 336)
Используя Общую методику 7, исходя из соединения Синтеза R3cj и соединения Синтеза R1d в качестве реагентов, получали Пример 336. МСВР: рассчитано для C39H39N9O4S: 729.2845, найдено: 730.2922 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1,3-тиазол-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 337)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1,3-тиазол-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 337)
Используя Общую методику 7, исходя из соединения Синтеза R3ck и соединения Синтеза R1d в качестве реагентов, получали Пример 337. МСВР: рассчитано для C38H38N8O4S2: 734.2457, найдено: 735.2523 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метилпиперидин-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 338)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метилпиперидин-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 338)
Используя Общую методику 7, исходя из соединения Синтеза R3k и соединения Синтеза R1d в качестве реагентов, получали Пример 338. МСВР: рассчитано для C41H48N8O4S: 748.3519, найдено: 375.1823 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(проп-2-ин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 339)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(проп-2-ин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 339)
Используя Общую методику 7, исходя из соединения Синтеза R3m и соединения Синтеза R1d в качестве реагентов, получали Пример 339. МСВР: рассчитано для C38H39N7O4S: 689.2784, найдено: 690.2847 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-фтор-5-йодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 340)
3-{[1-({(3R,4R)-1-[(3-фтор-5-йодтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 340)
Используя Общую методику 7, исходя из соединения Синтеза R3o и соединения Синтеза R1g в качестве реагентов, получали Пример 340. МСВР: рассчитано для C31H30F4IN5O4S: 771.0999, найдено: 772.1074 [(М+Н)+ форма].
 7-(бута-2,3-диен-1-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 341)
7-(бута-2,3-диен-1-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 341)
Используя Общую методику 7, исходя из соединения Синтеза R3s и соединения Синтеза R1d в качестве реагентов, получали Пример 341. МСВР: рассчитано для C39H41N7O4S: 703.2941, найдено: 704.3008 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(5-бромтиофен-2-ил)сульфонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 342)
3-{[1-({(3R,4R)-1-[(5-бромтиофен-2-ил)сульфонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 342)
Используя Общую методику 8, исходя из соединения Синтеза R3b и 5-бромтиофен-2-сульфонилхлорида в качестве реагентов, получали Пример 342. МСВР: рассчитано для C29H32BrN5O5S2: 673.1028, найдено: 674.1114 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-бромфенил)сульфонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 343)
3-{[1-({(3R,4R)-1-[(3-бромфенил)сульфонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 343)
Используя Общую методику 8, исходя из соединения Синтеза R3b и 3-бромбензолсульфонилхлорида в качестве реагентов, получали Пример 343. МСВР: рассчитано для C31H34BrN5O5S: 667.1464, найдено: 668.153 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(фенилсульфонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 344)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(фенилсульфонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 344)
Используя Общую методику 8, исходя из соединения Синтеза R3bu и бензолсульфонилхлорида в качестве реагентов, получали Пример 344. МСВР: рассчитано для C36H37N5O5S: 651.2515, найдено: 652.2577 [(М+Н)+ форма].
 7-(3,4-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 345)
7-(3,4-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 345)
Используя Общую методику 6, исходя из соединения Синтеза R3ag и соединения Синтеза R1c в качестве реагентов, получали Пример 345. МСВР: рассчитано для C40H39Cl2N7O3S: 767.2212, найдено: 768.2266 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 346)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 346)
Используя Общую методику 6, исходя из соединения Синтеза R3am и соединения Синтеза R1c в качестве реагентов, получали Пример 346. МСВР: рассчитано для C41H43N7O3S: 713.3148, найдено: 714.3224 [(М+Н)+ форма].
 7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 347)
7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 347)
Используя Общую методику 7, исходя из соединения Синтеза R3ar и соединения Синтеза R1d в качестве реагентов, получали Пример 347. МСВР: рассчитано для C41H40N7O4SCl: 761.2551, найдено: 762.2622 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 348)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 348)
Используя Общую методику 7, исходя из соединения Синтеза R3ax и соединения Синтеза R1d в качестве реагентов, получали Пример 348. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 758.3117 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 349)
3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 349)
Используя Общую методику 7, исходя из соединения Синтеза R3b и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 349. МСВР: рассчитано для C30H33BrN6O4S: 652.1467, найдено: 653.1548 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)сульфонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 350)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)сульфонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 350)
Используя Общую методику 8, исходили из соединения Синтеза R3b и 2-бром-4-метил-1,3-тиазол-5-сульфонилхлорида в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 350. МСВР: рассчитано для C35H38N6O5S2: 686.2345, найдено: 687.2389 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-4-ил)-1,3-тиазол-5-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 351)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-4-ил)-1,3-тиазол-5-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 351)
Используя Общую методику 8, исходили из соединения Синтеза R3b и 2-бром-4-метил-1,3-тиазол-5-сульфонилхлорида в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 351. МСВР: рассчитано для C34H37N7O5S2: 687.2298, найдено: 344.6232 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиримидин-5-ил)-1,3-тиазол-5-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 352)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиримидин-5-ил)-1,3-тиазол-5-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 352)
Используя Общую методику 8 исходили из соединения Синтеза R3b и 2-бром-4-метил-1,3-тиазол-5-сульфонилхлорида в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с пиримидин-5-илбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 352. МСВР: рассчитано для C33H36N8O5S2: 688.2250, найдено: 689.2304 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 353)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 353)
Используя Общую методику 8 исходили из соединения Синтеза R3b и 2-бром-4-метил-1,3-тиазол-5-сульфонилхлорида в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 353. МСВР: рассчитано для C33H38N8O5S2: 690.2407, найдено: 691.2481 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 354)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 354)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с пиримидин-5-илбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 354. МСВР: рассчитано для C33H34N8O4S: 638.2424, найдено: 639.25 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 355)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 355)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 355. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.254 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 356)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 356)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 356. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.252 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 357)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 357)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 357. МСВР: рассчитано для C33H36N8O4S: 640.2580, найдено: 641.268 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)тиофен-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 358)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)тиофен-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 358)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 358. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2807 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 359)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 359)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 359. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2807 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенилтиофен-2-ил)метил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 360)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенилтиофен-2-ил)метил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 360)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 360. МСВР: рассчитано для C36H39N5O3S: 621.2773, найдено: 622.2859 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 361)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 361)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 361. МСВР: рассчитано для C34H36N7O3S: 625.2835, найдено: 626.2919 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенил-1,3-тиазол-2-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 362)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенил-1,3-тиазол-2-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 362)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 362. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2592 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)тиофен-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 363)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)тиофен-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 363)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с пиримидин-5-илбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 363. МСВР: рассчитано для C34H37N7O3S: 623.2679, найдено: 624.2761 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 364)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 364)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 364. МСВР: рассчитано для C34H38N8O4S: 654.2737, найдено: 655.2814 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 365)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 365)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 365. МСВР: рассчитано для C33H38N8O3S: 626.2787, найдено: 627.2871 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-5-фенил-1,3-тиазол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 366)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-5-фенил-1,3-тиазол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 366)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 366. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2756 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)метил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 367)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)метил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 367)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 367. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2794 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 368)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 368)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 368. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2727 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 369)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 369)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 369. МСВР: рассчитано для C34H37N7O3S: 623.2679, найдено: 624.274 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиримидин-5-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 370)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиримидин-5-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 370)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с пиримидин-5-илбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 370. МСВР: рассчитано для C34H36N8O4S: 652.2580, найдено: 653.2632 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 371)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 371)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с пиримидин-5-илбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 371. МСВР: рассчитано для C33H36N8O3S: 624.2631, найдено: 625.2706 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 372)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 372)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиазол-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 372. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2723 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 373)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 373)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 373. МСВР: рассчитано для C34H37N7O3S: 623.2679, найдено: 624.2747 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-хлор-3-фтор-4-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 374)
3-[(1-{[(3R,4R)-1-{[5-хлор-3-фтор-4-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 374)
Используя Общую методику 7, исходили из соединения Синтеза R3b и соединения Синтеза R1k в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 374. МСВР: рассчитано для C36H36ClFN6O4S: 702.2191, найдено: 703.2273 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-метил-4-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 375)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-метил-4-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 375)
Используя Общую методику 7, исходили из соединения Синтеза R3b и соединения Синтеза R1i в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 375. МСВР: рассчитано для C37H39FN6O4S: 682.2737, найдено: 683.28 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)-1,3-тиазол-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 376)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)-1,3-тиазол-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 376)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 5-бром-2-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 376. МСВР: рассчитано для C34H37N7O3S: 623.2679, найдено: 624.2737 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)-1,3-тиазол-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 377)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)-1,3-тиазол-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 377)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 5-бром-2-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с пиримидин-5-илбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 377. МСВР: рассчитано для C33H36N8O3S: 624.2631, найдено: 625.2697 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)-1,3-тиазол-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 378)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)-1,3-тиазол-2-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 378)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 5-бром-2-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 378. МСВР: рассчитано для C34H37N7O3S: 623.2679, найдено: 624.274 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенил-1,3-тиазол-2-ил)метил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 379)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенил-1,3-тиазол-2-ил)метил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 379)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 5-бром-2-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 379. МСВР: рассчитано для C35H38N6O3S: 622.2726, найдено: 623.2816 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 380)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 380)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 5-бром-2-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 380. МСВР: рассчитано для C33H38N8O3S: 626.2787, найдено: 627.2861 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 381)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 381)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 5-бром-2-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 381. МСВР: рассчитано для C35H39N7O3S: 637.2835, найдено: 638.2912 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метокси-6-метилпиридин-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 382)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метокси-6-метилпиридин-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 382)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метокси-6-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 382. МСВР: рассчитано для C36H41N7O4S: 667.2940, найдено: 668.3009 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 383)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 383)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 383. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.291 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 384)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 384)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 384. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: 681.2864 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 385)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 385)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (3-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 385. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: 681.286 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 386)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 386)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 386. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2762 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 387)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 387)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 387. МСВР: рассчитано для C36H40N6O3S: 636.2883, найдено: 637.2976 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 388)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 388)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 388. МСВР: рассчитано для C36H40N6O4S: 652.2832, найдено: 327.1501 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-(2,3'-битиофен-5-илметил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 389)
3-[(1-{[(3R,4R)-1-(2,3'-битиофен-5-илметил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 389)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 389. МСВР: рассчитано для C34H37N5O3S2: 627.2338, найдено: 628.2426 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 390)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 390)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 390. МСВР: рассчитано для C36H40N6O3S: 636.2883, найдено: 637.2964 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 391)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 391)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (3-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 391. МСВР: рассчитано для C36H40N6O4S: 652.2832, найдено: 653.2935 [(М+Н)+ форма].
 трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}тиофен-2-ил)пиридин-2-ил]карбамат (Пример 392)
трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}тиофен-2-ил)пиридин-2-ил]карбамат (Пример 392)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбаматом в соответствии с Общей методикой 9 с получением Примера 392. МСВР: рассчитано для C40H47N7O5S: 737.3359, найдено: 738.3434 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 393)
3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 393)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином в соответствии с Общей методикой 9 с получением Примера 393. МСВР: рассчитано для C35H39N7O3S: 637.2835, найдено: 638.2918 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метокси-6-метилпиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 394)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метокси-6-метилпиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 394)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции 2-метокси-6-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 394. МСВР: рассчитано для C37H42N6O4S: 666.2988, найдено: 667.3071 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 395)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 395)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 395. МСВР: рассчитано для C36H40N6O4S: 652.2832, найдено: 653.2910 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2,3'-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 396)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2,3'-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 396)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 396. МСВР: рассчитано для C35H37N5O4S2: 655.2287, найдено: 656.2362 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 397)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 397)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 397. МСВР: рассчитано для C37H39N5O4S: 649.2723, найдено: 650.2806 [(М+Н)+ форма].
 трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3-метилтиофен-2-ил)пиридин-2-ил]карбамат (Пример 398)
трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3-метилтиофен-2-ил)пиридин-2-ил]карбамат (Пример 398)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбаматом в соответствии с Общей методикой 9 с получением Примера 398. МСВР: рассчитано для C41H47N7O6S: 765.3309, найдено: 766.3374 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 399)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 399)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 399. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2922 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 400)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 400)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 400. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: 681.2854 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 401)
3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 401)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином в соответствии с Общей методикой 9 с получением Примера 401. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 333.6475 [(М+2Н)2+ форма].
 трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метилтиофен-2-ил)пиридин-2-ил]карбамат (Пример 402)
трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метилтиофен-2-ил)пиридин-2-ил]карбамат (Пример 402)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбаматом в соответствии с Общей методикой 9 с получением Примера 402. МСВР: рассчитано для C41H47N7O6S: 765.3309, найдено: 766.3381 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 403)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 403)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 403. МСВР: рассчитано для C35H37N7O5S: 667.2577, найдено: 668.2654 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 404)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 404)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (3-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 404. МСВР: рассчитано для C35H37N7O5S: 667.2577, найдено: 668.2651 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 405)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 405)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 405. МСВР: рассчитано для C35H37N7O5S: 667.2577, найдено: 668.2649 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 406)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 406)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 406. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2702 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-фтор-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 407)
3-{[1-({(3R,4R)-1-[(3-фтор-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 407)
Используя Общую методику 7, исходили из соединения Синтеза R3b и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 407. МСВР: рассчитано для C36H36FN5O4S: 653.2472, найдено: 654.2545 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({3-метил-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 408)
3-[(4-гидрокси-1-{[(3R,4R)-1-({3-метил-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 408)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридином в соответствии с Общей методикой 9 с получением Примера 408. МСВР: рассчитано для C37H37F3N6O4S: 718.2549, найдено: 719.2627 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 409)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 409)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 409. МСВР: рассчитано для C37H39N5O4S: 649.2723, найдено: 650.2803 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(тиофен-3-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 410)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(тиофен-3-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 410)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 410. МСВР: рассчитано для C33H34N6O4S2: 642.2083, найдено: 643.2166 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({5-[2-(трифторметил)пиридин-4-ил]-1,3-тиазол-2-ил}карбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 411)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({5-[2-(трифторметил)пиридин-4-ил]-1,3-тиазол-2-ил}карбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 411)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридином в соответствии с Общей методикой 9 с получением Примера 411. МСВР: рассчитано для C35H34N7O4F3S: 705.2345, найдено: 706.2421 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 412)
3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 412)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридином в соответствии с Общей методикой 9 с получением Примера 412. МСВР: рассчитано для C37H37N6O4F3S: 718.2549, найдено: 719.2622 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 413)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 413)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиофена в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридином в соответствии с Общей методикой 9 с получением Примера 413. МСВР: рассчитано для C36H37F3N6O3S: 690.2600, найдено: 691.2681 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 414)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 414)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 414. МСВР: рассчитано для C35H39N7O3S: 637.2835, найдено: 638.2893 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 415)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 415)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с [2-(трифторметил)-4-пиридил]бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 415. МСВР: рассчитано для C35H36F3N7O3S: 691.2552, найдено: 692.2610 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метилпиридин-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 416)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метилпиридин-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 416)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 416. МСВР: рассчитано для C35H39N7O3S: 637.2835, найдено: 638.2889 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-4,5-бис(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 417)
3-[(1-{[(3R,4R)-1-{[3-фтор-4,5-бис(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 417)
и
3-[(1-{[(3R,4R)-1-{[5-хлор-3-фтор-4-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 418)
Используя Общую методику 7, исходили из соединения Синтеза R3b и соединения Синтеза R1k в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 417 и Примера 418, которые разделяли с помощью хроматографии.
Пример 417: МСВР: рассчитано для C42H42FN7O4S: 759.3003, найдено: 760.3079 [(М+Н)+ форма].
Пример 418: МСВР: рассчитано для C36H36ClFN6O4S: 702.2191, найдено: 703.227 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-4,5-ди(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 419)
3-[(1-{[(3R,4R)-1-{[3-фтор-4,5-ди(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 419)
и
3-[(1-{[(3R,4R)-1-{[5-хлор-3-фтор-4-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 420)
Используя Общую методику 7, исходили из соединения Синтеза R3b и соединения Синтеза R1k в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 419 и Примера 420, которые разделяли с помощью хроматографии.
Пример 419: МСВР: рассчитано для C40H38FN7O4S: 731.2690, найдено: 732.275 [(М+Н)+ форма].
Пример 420: МСВР: рассчитано для C35H34ClFN6O4S: 688.2035, найдено: 689.212 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 421)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 421)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 4-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 421. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2608 (М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 422)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 422)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 4-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 422. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2778 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-3-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 423)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-3-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 423)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 4-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 423. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2606 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 424)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 424)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 4-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 424. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2763 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[7-(6-метилпиридин-3-ил)-2,3-дигидротиено[3,4-b][1,4]диоксин-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 425)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[7-(6-метилпиридин-3-ил)-2,3-дигидротиено[3,4-b][1,4]диоксин-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 425)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-2,3-дигидротиено[3,4-b][1,4]диоксин-7-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 425. МСВР: рассчитано для C38H40N6O6S: 708.2730, найдено: 709.2799 [(М+Н)+ форма].
 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 426)
5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 426)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбонитрилом в соответствии с Общей методикой 9 с получением Примера 426. МСВР: рассчитано для C35H36N8O3S: 648.2631, найдено: 649.2731 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(циклопропилметокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 427)
3-[(1-{[(3R,4R)-1-({2-[6-(циклопропилметокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 427)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-(циклопропилметокси)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 427. МСВР: рассчитано для C38H43N7O4S: 693.3098, найдено: 347.6613 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метоксиметил)-5-(6-метоксипиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 428)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метоксиметил)-5-(6-метоксипиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 428)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-(метоксиметил)тиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 428. МСВР: рассчитано для C38H42N6O6S: 710.2886, найдено: 711.2966 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-4-(метоксиметил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 429)
3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-4-(метоксиметил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 429)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-(метоксиметил)тиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином в соответствии с Общей методикой 9 с получением Примера 429. МСВР: рассчитано для C37H41N7O5S: 695.2890, найдено: 696.2961 [М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метиламино)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 430)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метиламино)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 430)
и
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метиламино)-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 431)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-хлор-3-(метиламино)тиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 430 (дегалогенированный побочный продукт) и Примера 431, которые разделяли с помощью хроматографии.
Пример 430: МСВР: рассчитано для C31H36N6O4S: 588.2519, найдено: 589.2593 [(М+Н)+ форма].
Пример 431: МСВР: рассчитано для C37H41N7O4S: 679.2941, найдено: 680.3015 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 432)
3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 432)
Используя Общую методику 6, исходили из соединения Синтеза R3b и 2-бром-5-(хлорметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 6-(диметиламино)-3-пиридил]бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 432. МСВР: рассчитано для C36H42N8O3S: 666.3101, найдено: 667.3171 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(6-метилпиридин-3-ил)-4,5,6,7-тетрагидро-2-бензотиофен-1-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 433)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(6-метилпиридин-3-ил)-4,5,6,7-тетрагидро-2-бензотиофен-1-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 433)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 3-йод-4,5,6,7-тетрагидро-2-бензотиофен-1-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 433. МСВР: рассчитано для C40H44N6O4S: 704.3145, найдено: 705.3219 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-амино-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 434)
3-[(1-{[(3R,4R)-1-{[4-амино-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 434)
4-Амино-5-бром-2-тиофенкарбоновую кислоту (500 мг, 2.25 ммоль) растворяли в PDO (2 мл) и воде (2 мл), затем к перемешиваемой при 0°С смеси добавляли гидроксид натрия (194 мг, 4.86 ммоль), и затем добавляли Boc2O (1768 мг, 8.1 ммоль). Реакционную смесь перемешивали в течение 116 часов, одновременно нагревая реакционную смесь до к.т. К смеси добавляли водный раствор HCl (1 н., 4 мл), осадок отфильтровывали, промывали водой и сушили.
Полученную в результате 4-(трет-бутоксикарбониламино)-5-метилтиофен-2-карбоновую кислоту (316 мг, 0.93 ммоль) и соединение Синтеза R3b (488 мг, 0.93 ммоль, в виде бис-HCl соли) сочетали, используя Общую методику 7.
Полученный в результате продукт (320 мг, 0.42 ммоль) перемешивали в PDO (3 мл) и водном растворе HCl (12.2 М, 103 мкл, 1.26 ммоль) при 50°С в течение 20 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Используя Общую методику 9, исходя из полученного в результате амино-соединения и 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 434. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 333.648 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(нафталин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 435)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(нафталин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 435)
Используя Общую методику 7, исходили из соединения Синтеза R3be и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 435. МСВР: рассчитано для C45H43N7O4S: 777.3098, найдено: 778.3185 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 436)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 436)
Используя Общую методику 6, исходили из соединения Синтеза R3bf и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 436. МСВР: рассчитано для C41H43N7O3S: 713.3148, найдено: 714.3205 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(нафталин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 437)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(нафталин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 437)
Используя Общую методику 7, исходили из соединения Синтеза R3bt и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 437. МСВР: рассчитано для C45H43N7O4S: 777.3098, найдено: 778.3177 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 438)
7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 438)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 438. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2654 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 439)
7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 439)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 439. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2661 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 440)
7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 440)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 440. МСВР: рассчитано для C37H39FN6O4S: 682.2737, найдено: 683.2819 [(М+Н)+ форма].
 7-этил-3-{[1-({(3R,4R)-1-[(4-фтор-2,3',-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 441)
7-этил-3-{[1-({(3R,4R)-1-[(4-фтор-2,3',-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 441)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 441. МСВР: рассчитано для C35H36FN5O4S2: 673.2193, найдено: 674.2272 [(М+Н)+ форма].
 7-этил-3-{[1-({(3R,4R)-1-[(3-фтор-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 442)
7-этил-3-{[1-({(3R,4R)-1-[(3-фтор-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 442)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением примера 442. МСВР: рассчитано для C37H38FN5O4S: 667.2629, найдено: 668.2702 [(М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-({3-фтор-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 443)
7-этил-3-[(1-{[(3R,4R)-1-({3-фтор-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 443)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридином в соответствии с Общей методикой 9 с получением примера 443. МСВР: рассчитано для C37H36F4N6O4S: 736.2455, найдено: 737.2524 (М+Н)+ форма].
 7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метокси-6-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 444)
7-этил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метокси-6-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 444)
Используя Общую методику 7, исходили из соединения Синтеза R3c и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метокси-6-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением примера 444. МСВР: рассчитано для C38H41FN6O5S: 712.2843, найдено: 713.2916 (М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 445)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 445)
Используя Общую методику 6, исходили из соединения Синтеза R3ca и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 445. МСВР: рассчитано для C39H40N8O3S: 700.2944, найдено: 701.2986 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 446)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 446)
Используя Общую методику 7, исходили из соединения Синтеза R3cb и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением примера 446. МСВР: рассчитано для C40H40N8O4S: 728.2893, найдено: 729.2968 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 447)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 447)
Используя Общую методику 6, исходили из соединения Синтеза R3cb и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 447. МСВР: рассчитано для C39H40N8O3S: 700.2944, найдено: 701.2985 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 448)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 448)
Используя Общую методику 7, исходили из соединения Синтеза R3cf и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 448. МСВР: рассчитано для C39H39N7O4S2: 733.2505, найдено: 734.2596 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 449)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 449)
Используя Общую методику 6, исходили из соединения Синтеза R3cf и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 449. МСВР: рассчитано для C38H39N7O3S2: 705.2556, найдено: 706.2666 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(пропан-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 450)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(пропан-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 450)
Используя Общую методику 7, исходили из соединения Синтеза R3d и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 450. МСВР: рассчитано для C38H41FN6O4S: 696.2894, найдено: 697.2968 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пропан-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 451)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пропан-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 451)
Используя Общую методику 6, исходили из соединения Синтеза R3d и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 451. МСВР: рассчитано для C37H43N7O3S: 665.3148, найдено: 333.6636 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пропан-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 452)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пропан-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 452)
Используя Общую методику 7, исходили из соединения Синтеза R3d и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реактантов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 452. МСВР: рассчитано для C38H43N7O4S: 693.3098, найдено: 694.3173 [(М+Н)+ форма].
 7-циклопропил-3-{[1-({(3R,4R)-1-[(3-фтор-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 453)
7-циклопропил-3-{[1-({(3R,4R)-1-[(3-фтор-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 453)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с фенилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 453. МСВР: рассчитано для C38H38FN5O4S: 679.2629, найдено: 680.2696 [(М+Н)+ форма].
 7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 454)
7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 454)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением примера 454. МСВР: рассчитано для C38H39FN6O4S: 694.2737, найдено: 695.2808 [(М+Н)+ форма].
 7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 455)
7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 455)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 455. МСВР: рассчитано для C37H37FN6O4S: 680.2581, найдено: 681.2645 [(М+Н)+ форма].
 7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 456)
7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 456)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 456. МСВР: рассчитано для C37H37FN6O4S: 680.2581, найдено: 681.2648 [(М+Н)+ форма].
 7-циклопропил-3-{[1-({(3R,4R)-1-[(4-фтор-2,3',-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 457)
7-циклопропил-3-{[1-({(3R,4R)-1-[(4-фтор-2,3',-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 457)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 457. МСВР: рассчитано для C36H36FN5O4S2: 685.2193, найдено: 686.2269 [(М+Н)+ форма].
 7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 458)
7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 458)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 458. МСВР: рассчитано для C38H39FN6O4S: 694.2737, найдено: 695.2812 [(М+Н)+ форма].
 7-циклопропил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 459)
7-циклопропил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 459)
Используя Общую методику 7, исходили из соединения Синтеза R3g и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 459. МСВР: рассчитано для C38H41N7O4S: 691.2941, найдено: 692.3024 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метилпиперидин-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 460)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метилпиперидин-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 460)
Используя Общую методику 6, исходили из соединения Синтеза R3k и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 460. МСВР: рассчитано для C40H48N8O3S: 720.3570, найдено: 361.1855 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метилпропил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 461)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метилпропил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 461)
Используя Общую методику 6, исходили из соединения Синтеза R3n и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 461. МСВР: рассчитано для C38H45N7O3S: 679.3304, найдено: 340.6733 [(М+2Н)2+ форма].
 7-(2,2-дифторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 462)
7-(2,2-дифторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 462)
Используя Общую методику 6, исходили из соединения Синтеза R3p и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 462. МСВР: рассчитано для C36H39F2N7O3S: 687.2803, найдено: 344.6487 [(М+2Н)2+ форма].
 7-(2,2-дифторэтил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 463)
7-(2,2-дифторэтил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 463)
Используя Общую методику 7, исходили из соединения Синтеза R3p и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением примера 463. МСВР: рассчитано для C37H37N6O4F3S: 718.2549, найдено: 719.2625 [(М+Н)+ форма].
 7-(циклопропилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 464)
7-(циклопропилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 464)
Используя Общую методику 6, исходили из соединения Синтеза R3q и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 464. МСВР: рассчитано для C38H43N7O3S: 677.3149, найдено: 339.6648 [(М+2Н)2+ форма].
 7-(циклопропилметил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 465)
7-(циклопропилметил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 465)
Используя Общую методику 7, исходили из соединения Синтеза R3q и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 465. МСВР: рассчитано для C39H41N6O4FS: 708.2894, найдено: 709.2973 [(М+Н)+ форма].
 7-(циклобутилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 466)
7-(циклобутилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 466)
Используя Общую методику 7, исходили из соединения Синтеза R3r и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 466. МСВР: рассчитано для C40H45N7O4S: 719.3254, найдено: 720.3333 [(М+Н)+ форма].
 7-(циклобутилметил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 467)
7-(циклобутилметил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 467)
Используя Общую методику 7, исходили из соединения Синтеза R3r и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 467. МСВР: рассчитано для C40H43FN6O4S: 722.3051, найдено: 723.3125 [(М+Н)+ форма].
 7-(циклобутилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 468)
7-(циклобутилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 468)
Используя Общую методику 6, исходили из соединения Синтеза R3r и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 468. МСВР: рассчитано для C39H45N7O3S: 691.3304, найдено: 692.3396 [(М+Н)+ форма].
 7-(2-фторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 469)
7-(2-фторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 469)
Используя Общую методику 6, исходили из соединения Синтеза R3u и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 469. МСВР: рассчитано для C36H40FN7O3S: 669.2897, найдено: 335.6529 [(М+2Н)2+ форма].
 7-(2-фторэтил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 470)
7-(2-фторэтил)-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 470)
Используя Общую методику 7, исходили из соединения Синтеза R3u и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 470. МСВР: рассчитано для C37H38N6O4F2S: 700.2643, найдено: 701.2725 [(М+Н)+ форма].
 7-(2-гидроксиэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 471)
7-(2-гидроксиэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 471)
Используя Общую методику 6, исходили из соединения Синтеза R3w и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением примера 471. МСВР: рассчитано для C36H41N7O4S: 667.2941, найдено: 334.6543 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(2-гидроксиэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 472)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(2-гидроксиэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 472)
Используя Общую методику 7, исходили из соединения Синтеза R3w и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 472. МСВР: рассчитано для C37H39N6O5FS: 698.2687, найдено: 699.2757 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 473)
3-[(1-{[(3R,4R)-1-(3-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 473)
Используя Общую методику 6, исходили из соединения Синтеза R1n и 1-(бромметил)-3-фторбензола в качестве реагентов, полученный в результате сырой продукт (35 мг, 0.052 ммоль) подвергали реакции с TBAF (1 M в ТГФ, 0.16 мл, 0.156 ммоль) в ТГФ (2 мл) при 75°С в течение 4 дней. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 473. МСВР: рассчитано для C31H34FN5O3: 543.2646, найдено: 544.272 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 474)
3-[(1-{[(3R,4R)-1-(2-фторбензил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 474)
Используя Общую методику 6, исходили из соединения Синтеза R1n и 1-(бромметил)-2-фторбензола в качестве реагентов, полученный в результате сырой продукт (80 мг, 0.12 ммоль) подвергали реакции с TBAF (1 M в ТГФ, 0.24 мл, 0.24 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением Примера 474. МСВР: рассчитано для C31H34FN5O3: 543.2646, найдено: 544.274 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 475)
3-[(4-гидрокси-1-{[(3R,4R)-1-(3-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 475)
Используя Общую методику 6, исходили из соединения Синтеза R1n и 1-(бромметил)-3-метилбензола в качестве реагентов, полученный в результате сырой продукт (74 мг, 0.11 ммоль) подвергали реакции с TBAF (1 M в ТГФ, 0.22 мл, 0.22 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением Примера 475. МСВР: рассчитано для C32H37N5O3: 539.2896, найдено: 540.2940 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 476)
3-[(4-гидрокси-1-{[(3R,4R)-1-(2-метилбензил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 476)
Используя Общую методику 6, исходили из соединения Синтеза R1n и 1-(бромметил)-2-метилбензола в качестве реагентов, полученный в результате сырой продукт (88 мг, 0.13 ммоль) подвергали реакции с TBAF (1 M в ТГФ, 0.26 мл, 0.26 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением Примера 476. МСВР: рассчитано для C32H37N5O3: 539.2896, найдено: 540.295 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(1-бензофуран-2-илметил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 477)
3-[(1-{[(3R,4R)-1-(1-бензофуран-2-илметил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 477)
Используя Общую методику 6, исходили из соединения Синтеза R1n и 2-(хлорметил)бензофурана в качестве реагентов, полученный в результате сырой продукт (32 мг, 0.046 ммоль) подвергали реакции с TBAF (1 M в ТГФ, 0.09 мл, 0.09 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением примера 477. МСВР: рассчитано для C33H35N5O4: 565.2689, найдено: 566.2772 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 478)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 478)
Используя Общую методику 7, исходили из соединения Синтеза R1n и 4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт (87 мг, 0.126 ммоль) подвергали реакции с TBAF (1 М в ТГФ, 0.315 мл, 0.315 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением Примера 478. МСВР: рассчитано для C29H32N6O4S: 560.2206, найдено: 561.228 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 479)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(2-фенил-1,3-тиазол-5-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 479)
Используя Общую методику 7, исходили из соединения Синтеза R1n и 2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт (86 мг, 0.11 ммоль) подвергали реакции с TBAF (1 M в ТГФ, 0.285 мл, 0.285 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением Примера 479. МСВР: рассчитано для C34H34N6O4S: 622.2362, найдено: 623.2442 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 480)
3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-2-фенил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 480)
Используя Общую методику 7, исходили из соединения Синтеза R1n и 4-метил-2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт (90 мг, 0.117 ммоль) подвергали реакции с TBAF (1 М в ТГФ, 0.293 мл, 0.293 ммоль) в ТГФ (3 мл) при 75°С в течение 1 дня. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент), затем с помощью флэш-хроматографии (МеОН-ДХМ, градиент) с получением Примера 480. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2601 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-оксопирролидин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 481)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-оксопирролидин-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 481)
Используя Общую методику 11, исходя из соединения Синтеза R2ab и соединения Синтеза R1m в качестве реагентов, получали Пример 481. МСВР: рассчитано для C39H42N8O5S: 734.2999, найдено: 735.3045 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 482)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 482)
Используя Общую методику 11, исходя из соединения Синтеза R2am и соединения Синтеза R1m в качестве реагентов, получали Пример 482. МСВР: рассчитано для C42H43N7O4S: 741.3098, найдено: 742.3167 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 483)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 483)
Используя Общую методику 11, исходя из соединения Синтеза R2aq и соединения Синтеза R1m в качестве реагентов, получали Пример 483. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 758.3122 [(М+Н)+ форма].
 7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 484)
7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 484)
Используя Общую методику 11, исходя из соединения Синтеза R2as и соединения Синтеза R1m в качестве реагентов, получали Пример 484. МСВР: рассчитано для C41H40FN7O4S: 745.2847, найдено: 373.6485 [(М+2Н)2+ форма].
 7-[4-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 485)
7-[4-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 485)
Используя Общую методику 11, исходя из соединения Синтеза R2at и соединения Синтеза R1m в качестве реагентов, получали Пример 485. МСВР: рассчитано для C43H46N8O4S: 770.3362, найдено: 771.3439 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(4-метилпиперазин-1-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 486)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(4-метилпиперазин-1-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 486)
Используя Общую методику 11, исходя из соединения Синтеза R2au и соединения Синтеза R1m в качестве реагентов, получали Пример 486. МСВР: рассчитано для C46H51N9O4S: 825.3785, найдено: 413.6974 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 487)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 487)
Используя Общую методику 11, исходя из соединения Синтеза R2av и соединения Синтеза R1m в качестве реагентов, получали Пример 487. МСВР: рассчитано для C45H48N8O5S: 812.3469, найдено: 813.3555 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиримидин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 488)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиримидин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 488)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)тиофен-2-карбоновой кислоты в качестве реагентов, полученную в результате сырую бороновую кислоту подвергали реакции с 4-бром-2-метилпиримидином в качестве галоген-соединения в соответствии с Общей методикой 9 с получением Примера 488. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2698 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(5-метилпиразин-2-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 489)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(5-метилпиразин-2-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 489)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)тиофен-2-карбоновой кислоты в качестве реагентов, полученную в результате сырую бороновую кислоту подвергали реакции с 2-бром-5-метилпиразином в качестве галоген-соединения в соответствии с Общей методикой 9 с получением Примера 489. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2703 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиразин-2-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 490)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиразин-2-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 490)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)тиофен-2-карбоновой кислоты в качестве реагентов, полученную в результате сырую бороновую кислоту подвергали реакции с 2-хлорпиразином в качестве галоген-соединения в соответствии с Общей методикой 9 с получением Примера 490. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.2547 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридазин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 491)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридазин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 491)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)тиофен-2-карбоновой кислоты в качестве реагентов, полученную в результате сырую бороновую кислоту подвергали реакции с 3-хлор-6-метилпиридазином в качестве галоген-соединения в соответствии с Общей методикой 9 с получением Примера 491. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2709 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиразин-2-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 492)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиразин-2-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 492)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)тиофен-2-карбоновой кислоты в качестве реагентов, полученную в результате сырую бороновую кислоту подвергали реакции с 2-хлор-6-метилпиразином в качестве галоген-соединения в соответствии с Общей методикой 9 с получением Примера 492. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2699 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 493)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 493)
Используя Общую методику 11, исходя из соединения Синтеза R2bf и соединения Синтеза R1m в качестве реагентов, получали Пример 493. МСВР: рассчитано для C42H43N7O4S: 741.3098, найдено: 742.3171 [(М+Н)+ форма].
 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 494)
7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 494)
Используя Общую методику 11, исходя из соединения Синтеза R3bj и соединения Синтеза R1m в качестве реагентов, получали Пример 494. МСВР: рассчитано для C41H40N7O4SCl: 761.2551, найдено: 762.2622 [(М+Н)+ форма].
 7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 495)
7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 495)
Используя Общую методику 11, исходя из соединения Синтеза R2bk и соединения Синтеза R1m в качестве реагентов, получали Пример 495. МСВР: рассчитано для C41H40FN7O4S: 745.2847, найдено: 373.6504 [(М+2Н)2+ форма].
 7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 496)
7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 496)
Используя Общую методику 11, исходя из соединения Синтеза R2bl и соединения Синтеза R1m в качестве реагентов, получали Пример 496. МСВР: рассчитано для C43H46N8O4S: 770.3362, найдено: 771.3436 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 497)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 497)
Используя Общую методику 11, исходя из соединения Синтеза R2bm и соединения Синтеза R1m в качестве реагентов, получали Пример 497. МСВР: рассчитано для C45H48N8O5S: 812.3469, найдено: 813.3544 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 498)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 498)
Используя Общую методику 10, исходя из Примера 297 и трибромида бора в качестве реагентов, получали Пример 498. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2956 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 499)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 499)
Используя Общую методику 11, исходя из соединения Синтеза R2bo и соединения Синтеза R1m в качестве реагентов, получали Пример 499. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 379.6582 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 500)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 500)
Используя Общую методику 11, исходя из соединения Синтеза R2bv и соединения Синтеза R1m в качестве реагентов, получали Пример 500. МСВР: рассчитано для C42H43N7O4S: 741.3098, найдено: 742.3169 [(М+Н)+ форма].
 7-(2-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 501)
7-(2-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 501)
Используя Общую методику 11, исходя из соединения Синтеза R2bw и соединения Синтеза R1m в качестве реагентов, получали Пример 501. МСВР: рассчитано для C41H40ClN7O4S: 761.2551, найдено: 762.2633 [(М+Н)+ форма].
 7-(2-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 502)
7-(2-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 502)
Используя Общую методику 11, исходя из соединения Синтеза R2bx и соединения Синтеза R1m в качестве реагентов, получали Пример 502. МСВР: рассчитано для C41H40N7O4FS: 745.2847, найдено: 746.2924 [(М+Н)+ форма].
 7-[2-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 503)
7-[2-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 503)
Используя Общую методику 11, исходя из соединения Синтеза R2by и соединения Синтеза R1m в качестве реагентов, получали Пример 503. МСВР: рассчитано для C43H46N8O4S: 770.3362, найдено: 771.3447 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 504)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 504)
Используя Общую методику 11, исходя из соединения Синтеза R2bz и соединения Синтеза R1m в качестве реагентов, получали Пример 504. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 758.3114 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 505)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 505)
Используя Общую методику 11, исходя из соединения Синтеза R2cc и соединения Синтеза R1m в качестве реагентов, получали Пример 505. МСВР: рассчитано для C39H39N7O4S2: 733.2505, найдено: 734.2591 [(М+Н)+ форма].
 7-(фуран-3-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 506)
7-(фуран-3-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 506)
Используя Общую методику 11, исходя из соединения Синтеза R2ce и соединения Синтеза R1m в качестве реагентов, получали Пример 506. МСВР: рассчитано для C39H39N7O5S: 717.2733, найдено: 718.2818 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1Н-индол-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 507)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1Н-индол-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 507)
Используя Общую методику 11, исходя из соединения Синтеза R2cl и соединения Синтеза R1m в качестве реагентов, получали Пример 507. МСВР: рассчитано для C43H42N8O4S: 766.3050, найдено: 767.312 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1Н-пиррол-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 508)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1Н-пиррол-1-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 508)
Используя Общую методику 11, исходя из соединения Синтеза R2cm и соединения Синтеза R1m в качестве реагентов, получали Пример 508. МСВР: рассчитано для C39H40N8O4S: 716.2893, найдено: 717.2976 [(М+Н)+ форма].
 7-циклопентил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 509)
7-циклопентил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 509)
Используя Общую методику 11, исходя из соединения Синтеза R2i и соединения Синтеза R1m в качестве реагентов, получали Пример 509. МСВР: рассчитано для C40H45N7O4S: 719.3254, найдено: 718.3195 [(М-Н)- форма].
 7-циклогексил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 510)
7-циклогексил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 510)
Используя Общую методику 11, исходя из соединения Синтеза R2j и соединения Синтеза R1m в качестве реагентов, получали Пример 510. МСВР: рассчитано для C41H47N7O4S: 733.3410, найдено: 732.3356 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тетрагидро-2Н-пиран-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 511)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тетрагидро-2Н-пиран-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 511)
Используя Общую методику 11, исходя из соединения Синтеза R2I и соединения Синтеза R1m в качестве реагентов, получали Пример 511. МСВР: рассчитано для C40H45N7O5S: 735.3203, найдено: 734.3166 [(М-Н)- форма].
 3-[(1-{[(3R,4R)-1-(3-аминобензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 512)
3-[(1-{[(3R,4R)-1-(3-аминобензоил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 512)
Используя Общую методику 12, исходя из Примера 203 в качестве исходного вещества, получали Пример 512. МСВР: рассчитано для C32H36N6O4: 568.2798, найдено: 569.2855 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(метиламино)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 513)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(метиламино)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 513)
Используя Общую методику 13, исходя из Примера 512 в качестве амино-реагента, получали Пример 513. МСВР: рассчитано для C33H38N6O4: 582.2955, найдено: 583.3036 [(М+Н)+ форма].
 трет-бутил 4-ацетил-7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидрохиноксалин-1(2Н)-карбоксилат (Пример 514)
трет-бутил 4-ацетил-7-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-3,4-дигидрохиноксалин-1(2Н)-карбоксилат (Пример 514)
Используя Общую методику 7, исходя из Примера 244 и уксусной кислоты в качестве реагентов, получали Пример 514. МСВР: рассчитано для C41H49N7O7: 751.3693, найдено: 752.3755 [(М+Н)+ форма].
 7-{4-[6-(диметиламино)пиридин-3-ил]фенил}-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 515)
7-{4-[6-(диметиламино)пиридин-3-ил]фенил}-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 515)
и
7-(4-хлорфенил)-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 516)
Используя Общую методику 9, исходя из Примера 28 и [6-(диметиламино)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 515 и Пример 516 и разделяли их с помощью хроматографии.
Пример 515: МСВР: рассчитано для C48H52N10O3S: 848.3945, найдено: 425.2060 [М+2Н)2+ форма].
Пример 516: МСВР: рассчитано для C41H43ClN8O3S: 762.2867, найдено: 382.1494 [М+2Н)2+ форма]
 5-[5-({(3R,4R)-4-[(4-{[7-(4-хлорфенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 517)
5-[5-({(3R,4R)-4-[(4-{[7-(4-хлорфенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 517)
Используя Общую методику 9, исходя из Примера 28 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 517. МСВР: рассчитано для C40H37ClN8O3S: 744.2398, найдено: 745.2471 [М+Н)+ форма].
 7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 518)
7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 518)
Используя Общую методику 9, исходя из Примера 28 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 518. МСВР: рассчитано для C40H40ClN7O3S: 733.2602, найдено: 367.6385 [(М+2Н)2+ форма].
 5-[5-({(3R,4R)-4-[(4-{[7-(4-фторфенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 519)
5-[5-({(3R,4R)-4-[(4-{[7-(4-фторфенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 519)
Используя Общую методику 9, исходя из Примера 31 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 519. МСВР: рассчитано для C40H37FN8O3S: 728.2693, найдено: 729.2757 (М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 520)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 520)
Используя Общую методику 9, исходя из Примера 34 и 2-тиенилбороновой кислоты в качестве реагентов, получали Пример 520. МСВР: рассчитано для C39H40N6O4S2: 720.2552, найдено: 721.2612 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 521)
3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 521)
Используя Общую методику 9, исходя из Примера 34 и [6-(диметиламино)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 521. МСВР: рассчитано для C42H46N8O4S: 758.3362, найдено: 380.1763 [М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 522)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 522)
Используя Общую методику 9, исходя из Примера 34 и [6-(трифторметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 522. МСВР: рассчитано для C41H40F3N7O4S: 783.2814, найдено: 784.2893 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 523)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 523)
Используя Общую методику 9, исходя из Примера 34 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 523. МСВР: рассчитано для C39H40N8O4S: 716.2893, найдено: 717.2999 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 524)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 524)
Используя Общую методику 9, исходя из Примера 34 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 524. МСВР: рассчитано для C39H42N8O4S: 718.3050, найдено: 719.3108 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 525)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 525)
Используя Общую методику 9, исходя из Примера 34 и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 525. МСВР: рассчитано для C39H42N8O4S: 718.3050, найдено: 719.3131 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 526)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 526)
Используя Общую методику 9, исходя из Примера 34 и 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиррола в качестве реагентов, получали Пример 526. МСВР: рассчитано для C40H43N7O4S: 717.3098, найдено: 718.3145 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 527)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 527)
Используя Общую методику 9, исходя из Примера 34 и 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксаборолана в качестве реагентов, получали Пример 527. МСВР: рассчитано для C39H40N6O4S2: 720.2552, найдено: 721.2649 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 528)
3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 528)
Используя Общую методику 9, исходя из Примера 34 и 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана в качестве реагентов, получали Пример 528. МСВР: рассчитано для C39H40N6O5S: 704.2781, найдено: 705.2852 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 529)
3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 529)
Используя Общую методику 9, исходя из Примера 34 и 2-фурилбороновой кислоты в качестве реагентов, получали Пример 529. МСВР: рассчитано для C39H40N6O5S: 704.2781, найдено: 705.2837 [(М+Н)+ форма].
 5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 530)
5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3Н-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 530)
Используя Общую методику 9, исходя из Примера 34 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 530. МСВР: рассчитано для C41H40N8O4S: 740.2893, найдено: 741.2956 [М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 531)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 531)
Используя Общую методику 9, исходя из Примера 34 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 531. МСВР: рассчитано для C41H43N7O4S: 729.3098, найдено: 365.6619 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(фуран-2-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 532)
3-[(1-{[(3R,4R)-1-{[5-(фуран-2-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 532)
Используя Общую методику 9, исходя из Примера 176 и 2-фурилбороновой кислоты в качестве реагентов, получали Пример 532. МСВР: рассчитано для C34H35N5O5S: 625.2359, найдено: 626.2436 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 533)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 533)
Используя Общую методику 9, исходя из Примера 176 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 533. МСВР: рассчитано для C34H37N7O4S: 639.2628, найдено: 640.2696 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 534)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 534)
Используя Общую методику 9, исходя из Примера 176 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 534. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2582 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиррол-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 535)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиррол-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 535)
Используя Общую методику 9, исходя из Примера 176 и 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиррола в качестве реагентов, получали Пример 535. МСВР: рассчитано для C35H38N6O4S: 638.2675, найдено: 639.2750 [М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(4-фторфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 536)
3-[(1-{[(3R,4R)-1-{[5-(4-фторфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 536)
Используя Общую методику 9, исходя из Примера 176 и (4-фторфенил)бороновой кислоты в качестве реагентов, получали Пример 536. МСВР: рассчитано для C36H36FN5O4S: 653.2472, найдено: 654.254 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(3-фторфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 537)
3-[(1-{[(3R,4R)-1-{[5-(3-фторфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 537)
Используя Общую методику 9, исходя из Примера 176 и (3-фторфенил)бороновой кислоты в качестве реагентов, получали Пример 537. МСВР: рассчитано для C36H36FN5O4S: 653.2472, найдено: 654.2552 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метилфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 538)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метилфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 538)
Используя Общую методику 9, исходя из Примера 176 и м-толилбороновой кислоты в качестве реагентов, получали Пример 538. МСВР: рассчитано для C37H39N5O4S: 649.2723, найдено: 650.2793 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 539)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 539)
Используя Общую методику 9, исходя из Примера 176 и о-толилбороновой кислоты в качестве реагентов, получали Пример 539. МСВР: рассчитано для C37H39N5O4S: 649.2723, найдено: 650.2793 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(4-метилфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 540)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(4-метилфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 540)
Используя Общую методику 9, исходя из Примера 176 и n-толилбороновой кислоты в качестве реагентов, получали Пример 540. МСВР: рассчитано для C37H39N5O4S: 649.2723, найдено: 650.2792 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(фуран-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 541)
3-[(1-{[(3R,4R)-1-{[5-(фуран-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 541)
Используя Общую методику 9, исходя из Примера 176 и 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана в качестве реагентов, получали Пример 541. МСВР рассчитано для C34H35N5O5S 626.2425: 625.2359, найдено: [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 542)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 542)
Используя Общую методику 9, исходя из Примера 176 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 542. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.2544 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 543)
3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 543)
Используя Общую методику 9, исходя из Примера 349 и 2-фурилбороновой кислоты в качестве реагентов, получали Пример 543. МСВР: рассчитано для C34H36N6O5S: 640.2468, найдено: 641.2544 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 544)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 544)
Используя Общую методику 9, исходя из Примера 349 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 544. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2697 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 545)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 545)
Используя Общую методику 9, исходя из Примера 349 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов получали Пример 545. МСВР: рассчитано для C34H38N8O4S: 654.2737, найдено 655.2823 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиррол-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 546)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиррол-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 546)
Используя Общую методику 9, исходя из Примера 349 и 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиррола в качестве реагентов получали Пример 546. МСВР: рассчитано для C35H39N7O4S: 653.2784, найдено 654.2848 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиразол-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 547)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(1-метил-1Н-пиразол-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 547)
Используя Общую методику 9, исходя из Примера 349 и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов получали Пример 547. МСВР: рассчитано для C34H38N8O4S: 654.2737, найдено 655.2817 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 548)
3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 548)
Используя Общую методику 9, исходя из Примера 349 и 2-фурилбороновой кислоты в качестве реагентов, получали Пример 548. МСВР рассчитано для C34H36N6O5S: 640.2468, найдено: 641.2541 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиримидин-5-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 549)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(пиримидин-5-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 549)
Используя Общую методику 9, исходя из примера 349 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 549. МСВР: рассчитано для C34H36N8O4S: 652.2580, найдено: 653.2656 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(3-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 550)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(3-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 550)
Используя Общую методику 9, исходя из Примера 349 и м-толилбороновой кислоты в качестве реагентов, получали Пример 550. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2893 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(тиофен-2-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 551)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(тиофен-2-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 551)
Используя Общую методику 9, исходя из Примера 349 и 2-тиенилбороновой кислоты в качестве реагентов, получали Пример 551. МСВР: рассчитано для C34H36N6O4S2: 656.2239, найдено: 657.2318 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(4-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 552)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(4-метилфенил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 552)
Используя Общую методику 9, исходя из Примера 349 и n-толилбороновой кислоты в качестве реагентов, получали Пример 552. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2908 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(4-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 553)
3-[(1-{[(3R,4R)-1-{[2-(4-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 553)
Используя Общую методику 9, исходя из Примера 349 и (4-фторфенил)бороновой кислоты в качестве реагентов, получали Пример 553. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2656 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(3-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 554)
3-[(1-{[(3R,4R)-1-{[2-(3-фторфенил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 554)
Используя Общую методику 9, исходя из Примера 349 и (3-фторфенил)бороновой кислоты в качестве реагентов, получали пример 554. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2659 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(тиофен-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 555)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(тиофен-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 555)
Используя Общую методику 9, исходя из Примера 349 и 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксаборолана в качестве реагентов, получали Пример 555. МСВР: рассчитано для C34H36N6O4S2: 656.2239, найдено: 657.2300 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(3-фторпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 556)
3-[(1-{[(3R,4R)-1-{[5-(3-фторпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 556)
Используя Общую методику 9, исходя из Примера 176 и (3-фтор-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 556. МСВР: рассчитано для C35H35FN6O4S: 654.2425, найдено: 655.2499 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2,2'-битиофен-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 557)
3-[(1-{[(3R,4R)-1-(2,2'-битиофен-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 557)
Используя Общую методику 9, исходя из Примера 176 и 2-тиенилбороновой кислоты в качестве реагентов, получали Пример 557. МСВР: рассчитано для C34H35N5O4S2: 641.2130, найдено: 642.2219 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2,3'-битиофен-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 558)
3-[(1-{[(3R,4R)-1-(2,3'-битиофен-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 558)
Используя Общую методику 9, исходя из примера 176 и 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксаборолана в качестве реагентов, получали Пример 558. МСВР: рассчитано для C34H35N5O4S2: 641.2131, найдено: (642.2210 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-фторфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 559)
3-[(1-{[(3R,4R)-1-{[5-(2-фторфенил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 559)
Используя Общую методику 9, исходя из Примера 176 и (2-фторфенил)бороновой кислоты в качестве реагентов, получали Пример 559. МСВР: рассчитано для C36H36FN5O4S: 653.2472, найдено: 654.2541 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенилтиофен-2-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 560)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенилтиофен-2-ил)карбонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 560)
Используя Общую методику 9, исходя из Примера 176 и фенилбороновой кислоты в качестве реагентов, получали Пример 560. МСВР: рассчитано для C36H37N5O4S: 635.2566, найдено: 636.264 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 561)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 561)
Используя Общую методику 9, исходя из Примера 176 и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 561. МСВР: рассчитано для C34H37N7O4S: 639.2628, найдено: 640.2695 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-хлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 562)
3-[(1-{[(3R,4R)-1-{[5-(2-хлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 562)
Используя Общую методику 9, исходя из Примера 176 и (2-хлор-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 562. МСВР: рассчитано для C35H35ClN6O4S: 670.2129, найдено: 671.2194 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(3-хлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 563)
3-[(1-{[(3R,4R)-1-{[5-(3-хлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 563)
Используя Общую методику 9, исходя из Примера 176 и (3-хлор-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 563. МСВР: рассчитано для C35H35ClN6O4S: 670.2129, найдено: 671.2188 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 564)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 564)
Используя Общую методику 9, исходя из Примера 176 и (3-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 564. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2742 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 565)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 565)
Используя Общую методику 9, исходя из Примера 176 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 565. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2724 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(5-хлор-2-фторпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 566)
3-[(1-{[(3R,4R)-1-{[5-(5-хлор-2-фторпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 566)
Используя Общую методику 9, исходя из Примера 176 и (5-хлор-2-фтор-4-пиридил)бороновой кислоты в качестве реагентов, получали пример 566. МСВР: рассчитано для C35H34ClFN6O4S: 688.2035, найдено: 689.2135 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2,5-дихлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 567)
3-[(1-{[(3R,4R)-1-{[5-(2,5-дихлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (пример 567)
Используя Общую методику 9, исходя из Примера 176 и 2,5-дихлор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 567. МСВР: рассчитано для C35H34N6O4SCl2: 704.1740, найдено: 705.1819 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-фторпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 568)
3-[(1-{[(3R,4R)-1-{[5-(2-фторпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 568)
Используя Общую методику 9, исходя из Примера 176 и (2-фтор-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 568. МСВР: рассчитано для C35H35N6O4S: 654.2425, найдено: 655.251 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенилтиофен-2-ил)сульфонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 569)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[(5-фенилтиофен-2-ил)сульфонил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 569)
Используя Общую методику 9, исходя из Примера 342 и фенилбороновой кислоты в качестве реагентов, получали Пример 569. МСВР: рассчитано для C35H37N5O5S2: 671.2236, найдено: 672.2297 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 570)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-2-ил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 570)
Используя Общую методику 9, исходя из Примера 342 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 570. МСВР: рассчитано для C34H36N6O5S2: 672.2189, найдено: 337.1169 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)тиофен-2-ил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 571)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиримидин-5-ил)тиофен-2-ил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 571)
Используя Общую методику 9, исходя из Примера 342 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 571. МСВР: рассчитано для C33H35N7O5S2: 673.2141, найдено: 674.221 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(1-метил-1Н-пиразол-5-ил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 572)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(1-метил-1Н-пиразол-5-ил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 572)
Используя Общую методику 9, исходя из Примера 201 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 572. МСВР: рассчитано для C36H39N7O4: 633.3063, найдено: 634.3140 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиримидин-5-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 573)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиримидин-5-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 573)
Используя Общую методику 9, исходя из Примера 201 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 573. МСВР: рассчитано для C36H37N7O4: 631.2907, найдено: 632.2982 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиридин-4-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 574)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиридин-4-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 574)
Используя Общую методику 9, исходя из Примера 201 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 574. МСВР: рассчитано для C37H38N6O4: 630.2955, найдено: 316.1552 [(М+2Н)2+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиридин-3-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 575)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиридин-3-ил)бензоил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 575)
Используя Общую методику 9, исходя из Примера 201 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 575. МСВР: рассчитано для C37H38N6O4: 630.2955, найдено: 631.3037 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(1-метил-1Н-пиразол-5-ил)пиридин-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 576)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(1-метил-1Н-пиразол-5-ил)пиридин-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 576)
Используя Общую методику 9, исходя из Примера 194 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 576. МСВР: рассчитано для C35H38N8O4: 634.3016, найдено: 635.3092 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(4,4'-бипиридин-2-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 577)
3-[(1-{[(3R,4R)-1-(4,4'-бипиридин-2-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 577)
Используя Общую методику 9, исходя из Примера 194 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 577. МСВР: рассчитано для C36H37N7O4: 631.2907, найдено: 632.2978 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)тиофен-2-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 578)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)тиофен-2-ил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 578)
Используя Общую методику 9, исходя из Примера 342 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 578. МСВР: рассчитано для C33H37N7O5S2: 675.2297, найдено: 676.2372 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиримидин-5-ил)бензил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 579)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиримидин-5-ил)бензил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 579)
Используя Общую методику 9, исходя из примера 69 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 579. МСВР: рассчитано для C36H39N7O3: 617.3115, найдено: 618.3169 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиримидин-5-ил)фенил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 580)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиримидин-5-ил)фенил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 580)
Используя Общую методику 9, исходя из Примера 343 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 580. МСВР: рассчитано для C35H37N7O5S: 667.2577, найдено: 668.2657 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(бифенил-3-илметил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 581)
3-[(1-{[(3R,4R)-1-(бифенил-3-илметил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 581)
Используя Общую методику 9, исходя из Примера 69 и фенилбороновой кислоты в качестве реагентов, получали Пример 581. МСВР: рассчитано для C38H41N5O3: 615.3209, найдено: 616.3306 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(бифенил-3-илсульфонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 582)
3-[(1-{[(3R,4R)-1-(бифенил-3-илсульфонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 582)
Используя Общую методику 9, исходя из Примера 343 и фенилбороновой кислоты в качестве реагентов, получали Пример 582. МСВР: рассчитано для C37H39N5O5S: 665.2672, найдено: 666.2747 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиридин-4-ил)бензил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 583)
3-{[4-гидрокси-1-({(3R,4R)-3-фенил-1-[3-(пиридин-4-ил)бензил]пиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 583)
Используя Общую методику 9, исходя из Примера 69 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 583. МСВР: рассчитано для C37H40N6O3: 616.3162, найдено: 309.1648 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 584)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 584)
Используя Общую методику 9, исходя из Примера 197 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 584. МСВР: рассчитано для C35H35FN6O4S: 654.2425, найдено: (655.2508 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-5-ил)пиридин-4-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 585)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1Н-пиразол-5-ил)пиридин-4-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 585)
Используя Общую методику 9, исходя из Примера 195 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 585. МСВР: рассчитано для C35H38N8O4: 634.3016, найдено: 635.3109 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2,4'-бипиридин-4-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 586)
3-[(1-{[(3R,4R)-1-(2,4'-бипиридин-4-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 586)
Используя Общую методику 9, исходя из Примера 195 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 586. МСВР: рассчитано для C36H37N7O4: 631.2907, найдено: 632.2999 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)пиридин-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 587)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(1-метил-1Н-пиразол-5-ил)пиридин-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 587)
Используя Общую методику 9, исходя из Примера 196 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 587. МСВР: рассчитано для C35H38N8O4: 634.3016, найдено: 635.3091 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(3,4'-бипиридин-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 588)
3-[(1-{[(3R,4R)-1-(3,4'-бипиридин-5-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 588)
Используя Общую методику 9, исходя из Примера 196 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 588. МСВР: рассчитано для C36H37N7O4: 631.2907, найдено: 632.2985 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[6-(1-метил-1Н-пиразол-5-ил)пиридин-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 589)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[6-(1-метил-1Н-пиразол-5-ил)пиридин-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 589)
Используя Общую методику 9, исходя из Примера 198 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 589. МСВР: рассчитано для C35H38N8O4: 634.3016, найдено: 635.3110 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-(2,4'-бипиридин-6-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 590)
3-[(1-{[(3R,4R)-1-(2,4'-бипиридин-6-илкарбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 590)
Используя Общую методику 9, исходя из Примера 198 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 590. МСВР: рассчитано для C36H37N7O4: 631.2907, найдено: 632.2996 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиридин-4-ил)фенил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 591)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиридин-4-ил)фенил]сульфонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 591)
Используя Общую методику 9, исходя из Примера 343 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 591. МСВР: рассчитано для C36H38N6O5S: 666.2625, найдено: 667.2711 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-4-фенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 592)
3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-4-фенил-1Н-пиррол-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 592)
Используя Общую методику 9, исходя из Примера 189 и фенилбороновой кислоты в качестве реагентов, получали Пример 592. МСВР: рассчитано для C37H40N6O4: 632.3111, найдено: 633.3178 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(1-метил-1Н-пиразол-5-ил)бензил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 593)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(1-метил-1Н-пиразол-5-ил)бензил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 593)
Используя Общую методику 9, исходя из Примера 69 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 593. МСВР: рассчитано для C36H41N7O3: 619.3271, найдено: 620.3359 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(1-метил-1Н-пиразол-5-ил)фенил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 594)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(1-метил-1Н-пиразол-5-ил)фенил]сульфонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 594)
Используя Общую методику 9, исходя из Примера 343 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 594. МСВР: рассчитано для C35H39N7O5S: 669.2733, найдено: 670.2827 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2,3-дихлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 595)
3-[(1-{[(3R,4R)-1-{[5-(2,3-дихлорпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 595)
Используя Общую методику 9, исходя из Примера 176 и 2,3-дихлор-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 595. МСВР: рассчитано для C35H34N6O4SCl2: 704.1740, найдено: 705.1807 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 596)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 596)
Используя Общую методику 9, исходя из Примера 176 и (2-метокси-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 596. МСВР: рассчитано для C36H38N6O5S: 666.2625, найдено: 667.2699 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 597)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 597)
Используя Общую методику 9, исходя из Примера 176 и (3-метокси-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 597. МСВР: рассчитано для C36H38N6O5S: 666.2625, найдено: 667.2702 [(М+Н)+ форма].
 2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-5-(пиридин-4-ил)тиофен-3-карбонитрил (Пример 598)
2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-5-(пиридин-4-ил)тиофен-3-карбонитрил (Пример 598)
Используя Общую методику 9, исходя из Примера 212 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 598. МСВР: рассчитано для C36H35N7O4S: 661.2471, найдено: 662.2543 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 599)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 599)
Используя Общую методику 9, исходя из Примера 197 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 599. МСВР: рассчитано для C36H37N6O4FS: 668.2581, найдено: 669.2662 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(4-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 600)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(4-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 600)
Используя Общую методику 9, исходя из Примера 176 и (4-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 600. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2756 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(5-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 601)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(5-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 601)
Используя Общую методику 9, исходя из Примера 176 и (5-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 601. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2774 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 602)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 602)
Используя Общую методику 9, исходя из Примера 176 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 602. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2757 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 603)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 603)
Используя Общую методику 9, исходя из Примера 176 и 2-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 603. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2768 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 604)
3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 604)
Используя Общую методику 9, исходя из Примера 176 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амина в качестве реагентов, получали Пример 604. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 651.2710 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 605)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 605)
Используя Общую методику 9, исходя из Примера 176 и (6-метокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 605. МСВР: рассчитано для C36H38N6O5S: 666.2625, найдено: 667.2700 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(4-хлорпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 606)
3-[(1-{[(3R,4R)-1-{[5-(4-хлорпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 606)
Используя Общую методику 9, исходя из Примера 176 и 4-хлор-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 606. МСВР: рассчитано для C35H35ClN6O4S: 670.2129, найдено: 671.2207 (М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(4-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 607)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(4-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 607)
Используя Общую методику 9, исходя из Примера 349 и (4-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 607. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2838 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(5-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 608)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(5-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 608)
Используя Общую методику 9, исходя из Примера 349 и (5-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 608. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2845 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 609)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 609)
Используя Общую методику 9, исходя из Примера 349 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 609. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2829 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 610)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 610)
Используя Общую методику 9, исходя из Примера 349 и 2-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 610. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2825 (М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(6-аминопиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 611)
3-[(1-{[(3R,4R)-1-{[2-(6-аминопиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 611)
Используя Общую методику 9, исходя из Примера 349 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амина в качестве реагентов, получали Пример 611. МСВР: рассчитано для C35H38N8O4S: 666.2737, найдено: 667.2802 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 612)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 612)
Используя Общую методику 9, исходя из Примера 349 и (6-метокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 612. МСВР: рассчитано для C36H39N7O5S: 681.2733, найдено: 682.2797 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(2-метилпиридин-4-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 613)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(2-метилпиридин-4-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 613)
Используя Общую методику 9, исходя из Примера 217 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 613. МСВР: рассчитано для C37H41N7O4: 647.3220, найдено: 648.3316 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(пиридин-3-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 614)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(пиридин-3-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 614)
Используя Общую методику 9, исходя из Примера 217 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 614. МСВР: рассчитано для C36H39N7O4: 633.3063, найдено: 634.3138 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(Пиримидин-5-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 615)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(Пиримидин-5-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 615)
Используя Общую методику 9, исходя из Примера 217 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 615. МСВР: рассчитано для C35H38N8O4: 634.3016, найдено: 635.3092 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(5-хлорпиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 616)
3-[(1-{[(3R,4R)-1-{[2-(5-хлорпиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 616)
Используя Общую методику 9, исходя из Примера 349 и 3-хлор-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 616. МСВР: рассчитано для C35H36ClN7O4S: 685.2238, найдено: 686.2306 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(1-метил-1Н-пиразол-5-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 617)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(1-метил-1Н-пиразол-5-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 617)
Используя Общую методику 9, исходя из Примера 217 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 617. МСВР: рассчитано для C35H40N8O4: 636.3173, найдено: 637.3251 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(пиридин-4-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 618)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[1-метил-5-(пиридин-4-ил)-1Н-пиррол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 618)
Используя Общую методику 9, исходя из Примера 217 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 618. МСВР: рассчитано для C36H39N7O4: 633.3063, найдено: 634.3128 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 619)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 619)
Используя Общую методику 9, исходя из Примера 197 и (2-метокси-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 619. МСВР: рассчитано для C36H37FN6O5S: 684.2530, найдено: 685.2594 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метоксипиридин-4-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 620)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метоксипиридин-4-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 620)
Используя Общую методику 9, исходя из Примера 349 и (3-метокси-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 620. МСВР: рассчитано для C36H39N7O5S: 681.2733, найдено: 682.2827 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(5-хлорпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 621)
3-[(1-{[(3R,4R)-1-{[5-(5-хлорпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 621)
Используя Общую методику 9, исходя из Примера 176 и 3-хлор-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 621. МСВР: рассчитано для C35H35ClN6O4S: 670.2129, найдено: 671.2200 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 622)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 622)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метил-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 622. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.2863 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метоксипиридин-4-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 623)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метоксипиридин-4-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 623)
Используя Общую методику 9, исходя из Примера 349 и (2-метокси-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 623. МСВР: рассчитано для C36H39N7O5S: 681.2733, найдено: 682.2807 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метокси-6-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 624)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(2-метокси-6-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 624)
Используя Общую методику 9, исходя из Примера 269 и 2-метокси-6-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 624. МСВР: рассчитано для C37H39FN6O5S: 698.2687, найдено: 699.2764 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилпиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 625)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(2-метилпиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 625)
Используя Общую методику 9, исходя из Примера 349 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 625. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 666.287 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 626)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 626)
Используя Общую методику 9, исходя из Примера 269 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 626. МСВР: рассчитано для C35H35FN6O4S: 654.2424, найдено: 655.2505 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(3-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 627)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(3-метоксипиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 627)
Используя Общую методику 9, исходя из Примера 269 и (3-метокси-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 627. МСВР: рассчитано для C36H37FN6O5S: 684.2530, найдено: 685.2598 [(М+Н)+ форма].
 трет-бутил [4-(4-фтор-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-2-ил)пиридин-2-ил]карбамат (Пример 628)
трет-бутил [4-(4-фтор-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-2-ил)пиридин-2-ил]карбамат (Пример 628)
Используя Общую методику 9, исходя из Примера 269 и трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбамата в качестве реагентов, получали Пример 628. МСВР: рассчитано для C40H44FN7O6S: 769.3058, найдено: 770.3118 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 629)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 629)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридином в соответствии с Общей методикой 9 с получением Примера 629. МСВР: рассчитано для C36H38N6O4S: найдено: 651.2752 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метоксипиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 630)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метоксипиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 630)
Используя Общую методику 9, исходя из Примера 269 и (6-метокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 630. МСВР: рассчитано для C36H37FN6O5S: 684.253, найдено: 685.2619 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 631)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метоксипиридин-3-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 631)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 631. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: 681.2868 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 632)
3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 632)
Используя Общую методику 9, исходя из Примера 269 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амина в качестве реагентов, получали Пример 632. МСВР: рассчитано для C35H36FN7O4S: 669.2534, найдено: 335.6352 (М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 633)
3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 633)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином в соответствии с Общей методикой 9 с получением Примера 633. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 333.647 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 634)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 634)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-3-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 634. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2914 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-2,3'-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 635)
3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-2,3'-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 635)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 635. МСВР: рассчитано для C35H37N5O4S2: 655.2287, найдено: 656.2362 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 636)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 636)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метил-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 636. МСВР: рассчитано для C37H40N6O4S: 664.2832, найдено: 665.2913 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 637)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метоксипиридин-4-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 637)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 637. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: [(681.2854 (М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 638)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 638)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 638. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2737 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 639)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(3-метоксипиридин-4-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 639)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-метилтиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (3-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 639. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: 681.2859 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[2-(трифторметил)пиридин-4-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 640)
3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[2-(трифторметил)пиридин-4-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 640)
Используя Общую методику 9, исходя из Примера 349 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридина в качестве реагентов, получали Пример 640. МСВР: рассчитано для C36H36F3N7O4S: 719.2502, найдено: 720.2566 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({3-фтор-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 641)
3-[(1-{[(3R,4R)-1-({3-фтор-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 641)
Используя Общую методику 9, исходя из Примера 269 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридина в качестве реагентов, получали Пример 641. МСВР: рассчитано для C36H34F4N6O4S: 722.2299, найдено: 723.2378 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(4-фтор-2,3'-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 642)
3-{[1-({(3R,4R)-1-[(4-фтор-2,3'-битиофен-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 642)
Используя Общую методику 9, исходя из Примера 269 и 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксаборолана в качестве реагентов, получали Пример 642. МСВР: рассчитано для C34H34FN5O4S2: 659.2036, найдено: 660.2108 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 643)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 643)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метил-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 643. МСВР: рассчитано для C35H37N7O4S: 651.26276, найдено: 652.2709 [(М+Н)+ форма].
 трет-бутил [4-(2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1,3-тиазол-5-ил)пиридин-2-ил]карбамат (Пример 644)
трет-бутил [4-(2-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1,3-тиазол-5-ил)пиридин-2-ил]карбамат (Пример 644)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бромтиазол-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбаматом в соответствии с Общей методикой 9 с получением Примера 644. МСВР: рассчитано для C39H44N8O6S: 752.3104, найдено: 753.318 [(М+Н)+ форма].
 трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-д игидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-ил]карбамат (Пример 645)
трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-д игидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-ил]карбамат (Пример 645)
Используя Общую методику 9, исходя из Примера 349 и трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбамата в качестве реагентов, получали Пример 645. МСВР: рассчитано для C40H46N8O6S: 766.3261, найдено: 767.3336 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-3,5-бис(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 646)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-3,5-бис(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 646)
и
3-[(1-{[(3R,4R)-1-{[3-хлор-4-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 647)
Используя Общую методику 9, исходя из Примера 239 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 646 и Пример 647 и разделяли их с помощью хроматографии.
Пример 646: МСВР: рассчитано для C43H45N7O4S: 755.3254, найдено: 756.3331 [(М+Н)+ форма].
Пример 647: МСВР: рассчитано для C37H39ClN6O4S: 698.2442, найдено: 699.253 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(3-хлор-4-метил-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 648)
3-{[1-({(3R,4R)-1-[(3-хлор-4-метил-5-фенилтиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 648)
Используя Общую методику 9, исходя из Примера 239 и фенилбороновой кислоты в качестве реагентов, получали Пример 648. МСВР: рассчитано для C37H38ClN5O4S: 683.2333, найдено: 684.241 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-хлор-4-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 649)
3-[(1-{[(3R,4R)-1-{[3-хлор-4-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 649)
Используя Общую методику 9, исходя из Примера 239 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 649. МСВР: рассчитано для C36H37ClN6O4S: 684.2286, найдено: 685.2365 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 650)
3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 650)
Используя Общую методику 9, исходя из Примера 349 и [6-(трифторметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 650. МСВР: рассчитано для C36H36F3N7O4S: 719.2502, найдено: 720.2575 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(2,6-diфторпиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 651)
3-[(1-{[(3R,4R)-1-{[2-(2,6-diфторпиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 651)
Используя Общую методику 9, исходя из Примера 349 и (2,6-дифтор-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 651. МСВР: рассчитано для C35H35F2N2O4S: 687.2440, найдено: 688.2516 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(6-фторпиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 652)
3-[(1-{[(3R,4R)-1-{[2-(6-фторпиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 652)
Используя Общую методику 9, исходя из Примера 349 и (6-фтор-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 652. МСВР: рассчитано для C35H36FN7O4S: 669.25336, найдено: 670.2603 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-4-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 653)
3-[(1-{[(3R,4R)-1-{[3-фтор-4-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 653)
и
3-[(1-{[(3R,4R)-1-{[3-фтор-4,5-ди(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 654)
Используя Общую методику 9, исходя из Примера 232 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 653 (дегалогенированный побочный продукт) и Пример 654 и разделяли их с помощью хроматографии.
Пример 653: МСВР: рассчитано для C35H35FN6O4S: 654.2424, найдено: 655.2502 [(М+Н)+ форма].
Пример 654: МСВР: рассчитано для C40H38FN7O4S: 731.2690, найдено: 732.2764 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-хлор-4-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 655)
3-[(1-{[(3R,4R)-1-{[3-хлор-4-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 655)
Используя Общую методику 9, исходя из Примера 239 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 655. МСВР: рассчитано для C37H39ClN6O4S: 698.2442, найдено: 699.2514 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({3-хлор-4-метил-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 656)
3-[(1-{[(3R,4R)-1-({3-хлор-4-метил-5-[2-(трифторметил)пиридин-4-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 656)
Используя Общую методику 9, исходя из Примера 239 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридина в качестве реагентов, получали Пример 656. МСВР: рассчитано для C37H36ClF3N6O4S: 752.2159, найдено: 753.2258 [(М+Н)+ форма].
 трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-д игидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1,3-тиазол-2-ил)пиридин-2-ил]карбамат (Пример 657)
трет-бутил [4-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-д игидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-1,3-тиазол-2-ил)пиридин-2-ил]карбамат (Пример 657)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с трет-бутил N-[4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]карбаматом в соответствии с Общей методикой 9 с получением Примера 657. МСВР: рассчитано для C39H44N8O6S: 752.3104, найдено: 753.3187 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 658)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 658)
Используя Общую методику 9, исходя из Примера 247 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 658. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2767 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 659)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиридин-4-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 659)
Используя Общую методику 9, исходя из Примера 247 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 659. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2606 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 660)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 660)
Используя Общую методику 9, исходя из Примера 247 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 660. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2762 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиридин-3-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 661)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[3-(пиридин-3-ил)тиофен-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 661)
Используя Общую методику 9, исходя из Примера 247 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 661. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2617 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-4-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 662)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-4-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 662)
Используя Общую методику 9, исходя из Примера 248 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 662. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.2564 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(6-метилпиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 663)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(6-метилпиридин-3-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 663)
Используя Общую методику 9, исходя из Примера 248 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 663. МСВР: рассчитано для C35H37N7O4S: 651.26276, найдено: 652.272 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-3-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 664)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[4-(пиридин-3-ил)-1,3-тиазол-2-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 664)
Используя Общую методику 9, исходя из Примера 248 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 664. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.256 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 665)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(2-метилпиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 665)
Используя Общую методику 9, исходя из Примера 248 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 665. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2727 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 666)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-4-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 666)
Используя Общую методику 9, исходя из Примера 249 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 666. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2601 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 667)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(6-метилпиридин-3-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 667)
Используя Общую методику 9, исходя из Примера 249 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 667. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2766 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 668)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[5-(пиридин-3-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 668)
Используя Общую методику 9, исходя из Примера 249 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 668. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.26 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 669)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[5-(2-метилпиридин-4-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 669)
Используя Общую методику 9, исходя из Примера 249 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 669. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2756 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 670)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-4-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 670)
Используя Общую методику 9, исходя из Примера 250 и 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 670. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2615 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-3-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 671)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-3-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 671)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 3-пиридилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 671. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.2542 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метилпиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 672)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метилпиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 672)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (2-метил-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 672. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2702 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 673)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 673)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 673. МСВР: рассчитано для C35H37N7O5S: 667.2577, найдено: 668.2648 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(6-аминопиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 674)
3-[(1-{[(3R,4R)-1-{[2-(6-аминопиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 674)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином в соответствии с Общей методикой 9 с получением Примера 674. МСВР: рассчитано для C34H36N8O4S: 652.2580, найдено: 327.1370 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[2-(трифторметил)пиридин-4-ил]-1,3-тиазол-5-ил}карбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 675)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[2-(трифторметил)пиридин-4-ил]-1,3-тиазол-5-ил}карбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 675)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-(трифторметил)пиридином в соответствии с Общей методикой 9 с получением Примера 675. МСВР: рассчитано для C35H34F3N7O4S: 705.2345, найдено: 706.2403 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метоксипиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 676)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метоксипиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 676)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (3-метокси-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 676. МСВР: рассчитано для C35H37N7O5S: 667.2577, найдено: 668.2638 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 677)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 677)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 677. МСВР: рассчитано для C33H34N6O4S2: 642.2083, найдено: 643.2151 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 678)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 678)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 2-бромтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 678. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 652.2696 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 679)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 679)
Используя Общую методику 9, исходя из Примера 250 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 679. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.277 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-3-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 680)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиридин-3-ил)тиофен-3-ил]карбонил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 680)
Используя Общую методику 9, исходя из Примера 250 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 680. МСВР: рассчитано для C35H36N6O4S: 636.2519, найдено: 637.2603 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метилпиридин-4-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 681)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(2-метилпиридин-4-ил)тиофен-3-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 681)
Используя Общую методику 9, исходя из Примера 250 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 681. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2761 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-хлор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 682)
3-[(1-{[(3R,4R)-1-{[3-хлор-5-(пиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 682)
Используя Общую методику 9, исходя из Примера 253 и 3-пиридилбороновой кислоты в качестве реагентов, получали Пример 682. МСВР: рассчитано для C35H35ClN6O4S: 670.2129, найдено: 671.2205 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-хлор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 683)
3-[(1-{[(3R,4R)-1-{[3-хлор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 683)
Используя Общую методику 9, исходя из Примера 253 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 683. МСВР: рассчитано для C36H37ClN6O4S: 684.2286, найдено: 685.2368 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({3-хлор-5-[6-(трифторметил)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 684)
3-[(1-{[(3R,4R)-1-({3-хлор-5-[6-(трифторметил)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 684)
Используя Общую методику 9, исходя из Примера 253 и [6-(трифторметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 684. МСВР: рассчитано для C36H34ClF3N6O4S: 738.2003, найдено: 739.2071 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({5-[6-(диметиламино)пиридин-3-ил]-3-фтортиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 685)
3-[(1-{[(3R,4R)-1-({5-[6-(диметиламино)пиридин-3-ил]-3-фтортиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 685)
Используя Общую методику 9, исходя из Примера 269 и [6-(диметиламино)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 685. МСВР: рассчитано для C37H40FN7O4S: 697.2847, найдено: 349.6491 [(М+2Н)2+ форма].
 3-{[1-({(3R,4R)-1-[(4-хлор-3-фтортиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 686)
3-{[1-({(3R,4R)-1-[(4-хлор-3-фтортиофен-2-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 686)
Используя Общую методику 9, исходя из Примера 259 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, Пример 686 получали в виде дегалогенированного побочного продукта. МСВР: рассчитано для C30H31ClFN5O4S: 611.1769, найдено: 612.1852 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({5-[6-(циклопропилметокси)пиридин-3-ил]-3-фтортиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 687)
3-[(1-{[(3R,4R)-1-({5-[6-(циклопропилметокси)пиридин-3-ил]-3-фтортиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 687)
Используя Общую методику 9, исходя из Примера 269 и 2-(циклопропилметокси)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 687. МСВР: рассчитано для C39H41FN6O5S: 724.2843, найдено: 363.1484 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(6-этоксипиридин-3-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 688)
3-[(1-{[(3R,4R)-1-{[5-(6-этоксипиридин-3-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 688)
Используя Общую методику 9, исходя из Примера 269 и (6-этокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 688. МСВР: рассчитано для C37H39FN6O5S: 698.2687, найдено: 350.1408 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[4-хлор-3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 689)
3-[(1-{[(3R,4R)-1-{[4-хлор-3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 689)
Используя Общую методику 9, исходя из Примера 259 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 689. МСВР: рассчитано для C36H36ClFN6C4S: 702.2191, найдено: 703.2265 [(М+Н)+ форма].
 5-(4-фтор-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-2-ил)пиридин-2-карбонитрил (Пример 690)
5-(4-фтор-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-2-ил)пиридин-2-карбонитрил (Пример 690)
Используя Общую методику 9, исходя из Примера 269 и (6-циано-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 690. МСВР: рассчитано для C36H34FN7O4S: 679.2377, найдено: 680.2461 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-хлор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 691)
3-[(1-{[(3R,4R)-1-{[3-хлор-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 691)
Используя Общую методику 9, исходя из Примера 253 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 691. МСВР: рассчитано для C36H37ClN6O4S: 684.2286, найдено: 685.2357 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-4-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 692)
3-[(1-{[(3R,4R)-1-{[3-фтор-4-метил-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 692)
Используя Общую методику 9, исходя из Примера 261 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 692. МСВР: рассчитано для C37H39FN6O4S: 682.2737, найдено: 683.2826 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-4-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 693)
3-[(1-{[(3R,4R)-1-{[3-фтор-4-метил-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 693)
Используя Общую методику 9, исходя из Примера 261 и (2-метил-4-пиридил)бороновой кислоты в качестве реагентов, получали Пример 693. МСВР: рассчитано для C37H39FN6O4S: 682.2737, найдено: 683.2816 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-циклопропил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 694)
3-[(1-{[(3R,4R)-1-{[4-циклопропил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 694)
Используя Общую методику 9, исходя из Примера 263 и циклопропилбороновой кислоты в качестве реагентов, получали Пример 694. МСВР: рассчитано для C38H41N7O4S: 691.2941, найдено: 692.3038 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метоксипиридин-3-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 695)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метоксипиридин-3-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 695)
Используя Общую методику 9, исходя из Примера 261 и (6-метокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 695. МСВР: рассчитано для C37H39FN6O5S: 698.2687, найдено: 350.1423 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-({3-фтор-4-метил-5-[6-(трифторметил)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 696)
3-[(1-{[(3R,4R)-1-({3-фтор-4-метил-5-[6-(трифторметил)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 696)
Используя Общую методику 9, исходя из Примера 261 и [6-(трифторметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 696. МСВР: рассчитано для C37H36F4N6O4S: 736.2455, найдено: 737.2549 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(имидазо[1,2-а]пиридин-7-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 697)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(имидазо[1,2-а]пиридин-7-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 697)
Используя Общую методику 9, исходя из Примера 269 и имидазо[1,2-а]пиридин-7-илбороновой кислоты в качестве реагентов, получали Пример 697. МСВР: рассчитано для C37H36FN7O4S: 693.2534, найдено: 694.2616 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 698)
3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 698)
Используя Общую методику 9, исходя из Примера 349 и [6-(диметиламино)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 698. МСВР: рассчитано для C37H42N8O4S: 694.3050, найдено: 695.3133 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({3-фтор-5-[6-(пиперазин-1-ил)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 699)
3-[(1-{[(3R,4R)-1-({3-фтор-5-[6-(пиперазин-1-ил)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 699)
Используя Общую методику 9, исходя из Примера 269 и 1-[5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]пиперазина в качестве реагентов, получали Пример 699. МСВР: рассчитано для C39H43FN8O4S: 738.3112, найдено: 739.3183 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(циклопропилметокси)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 700)
3-[(1-{[(3R,4R)-1-({2-[6-(циклопропилметокси)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 700)
Используя Общую методику 9, исходя из Примера 349 и 2-(циклопропилметокси)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 700. МСВР: рассчитано для C39H43N7O5S: 721.3046, найдено: 722.3118 [(М+Н)+ форма].
 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 701)
5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 701)
Используя Общую методику 9, исходя из Примера 349 и (6-циано-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 701. МСВР: рассчитано для C36H36N8C4S: 676.2580, найдено: 677.2649 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метоксиметил)-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 702)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метоксиметил)-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 702)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-(метоксиметил)тиофен-2-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 702. МСВР: рассчитано для C38H42N6O5S: 694.2938, найдено: 695.302 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метоксиметил)-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 703)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-(метоксиметил)-5-(2-метилпиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 703)
Используя Общую методику 7, исходили из соединения Синтеза R3b и 5-бром-4-(метоксиметил)тиофен-2-карбоновой кислоты в качестве реагентов. Полученный в результате сырой продукт подвергали реакции с (2-метил-4-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 703. МСВР: рассчитано для C38H42N6O5S: 694.2938, найдено: 695.3030 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({3-фтор-5-[6-(2,2,2-трифторэтокси)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 704)
3-[(1-{[(3R,4R)-1-({3-фтор-5-[6-(2,2,2-трифторэтокси)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 704)
Используя Общую методику 9, исходя из Примера 269 и [6-(2,2,2-трифторэтокси)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 704. МСВР: рассчитано для C37H36F4N6O5S: 752.2404, найдено: 753.2476 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(3-метил-3H-имидазо[4,5-b]пиридин-6-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 705)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(3-метил-3H-имидазо[4,5-b]пиридин-6-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 705)
Используя Общую методику 9, исходя из Примера 269 и 3-метил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)имидазо[4,5-b]пиридина в качестве реагентов, получали Пример 705. МСВР: рассчитано для C37H37FN8O4S: 708.2642, найдено: 709.2708 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-этил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 706)
3-[(1-{[(3R,4R)-1-{[4-этил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 706)
Используя Общую методику 9, исходя из Примера 263 и этилтрифторбората калия в качестве реагентов, получали Пример 706. МСВР: рассчитано для C37H41N7O4S: 679.2941, найдено: 680.3022 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-(диметиламино)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 707)
3-[(1-{[(3R,4R)-1-{[4-(диметиламино)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 707)
и
3-[(1-{[(3R,4R)-1-{[4-(диметиламино)-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 708)
Используя Общую методику 9, исходя из Примера 275 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 707 (дегалогенированный побочный продукт) и Пример 708 и разделяли их с помощью хроматографии.
Пример 707: МСВР: рассчитано для C32H38N6O4S: 602.2675, найдено: 603.2751 [(М+Н)+ форма].
Пример 708: МСВР: рассчитано для C38H43N7O4S: 693.3098, найдено: 694.3175 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метокси-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 709)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метокси-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 709)
Используя Общую методику 9, исходя из Примера 276 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 709. МСВР: рассчитано для C37H40N6O5S: 680.2781, найдено: 681.2860 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[4-бром-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 710)
3-[(1-{[(3R,4R)-1-{[4-бром-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 710)
и
3-[(1-{[(3R,4R)-1-{[4,5-бис(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 711)
Используя Общую методику 9, исходя из Примера 277 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 710 и Пример 711 и разделяли их с помощью хроматографии.
Пример 710: МСВР: рассчитано для C42H43N6O4SBr: 728.1780, найдено: 729.1856 [(М+Н)+ форма].
Пример 711: МСВР: рассчитано для C42H43N7O4S: 741.3098, найдено: 742.3166 [(М+Н)+ форма].
 метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-5-(6-метилпиридин-3-ил)бензоат (Пример 712)
метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-5-(6-метилпиридин-3-ил)бензоат (Пример 712)
Используя Общую методику 9, исходя из Примера 287 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 712. МСВР: рассчитано для C40H42N6O6: 702.3166, найдено: 703.323 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 713)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 713)
Используя Общую методику 9, исходя из Примера 269 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 713. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2661 [(М+Н)+ форма].
 5-[5-({(3R,4R)-4-[(4-{[7-(3-хлорфенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-(1]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 714)
5-[5-({(3R,4R)-4-[(4-{[7-(3-хлорфенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-(1]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 714)
Используя Общую методику 9, исходя из Примера 87 и (6-циано-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 714. МСВР: рассчитано для C40H37ClN8O3S: 744.2398, найдено: 745.2479 [(М+Н)+ форма].
 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 715)
7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 715)
Используя Общую методику 9, исходя из Примера 87 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 715. МСВР: рассчитано для C40H40ClN7O3S: 733.2602, найдено: 734.2693 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 716)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 716)
Используя Общую методику 9, исходя из Примера 95 и 2-тиенилбороновой кислоты в качестве реагентов, получали Пример 716. МСВР: рассчитано для C39H40N6O4S2: 720.2552, найдено: 721.2616 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 717)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 717)
Используя Общую методику 9, исходя из Примера 95 и пиримидин-5-илбороновой кислоты в качестве реагентов, получали Пример 717. МСВР: рассчитано для C39H40N8O4S: 716.2893, найдено: 717.2989 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(l-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 718)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(l-метил-1Н-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 718)
Используя Общую методику 9, исходя из Примера 95 и 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 718. МСВР: рассчитано для C39H42N8O4S: 718.3050, найдено: 719.3109 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(l-метил-1Н-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 719)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(l-метил-1Н-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 719)
Используя Общую методику 9, исходя из Примера 95 и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 719. МСВР: рассчитано для C39H42N8O4S: 718.3050, найдено: 719.3087 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(l-метил-1Н-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 720)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(l-метил-1Н-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 720)
Используя Общую методику 9, исходя из Примера 95 и 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиррола в качестве реагентов, получали Пример 720. МСВР: рассчитано для C40H43N7O4S: 717.3098, найдено: 718.3169 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-l,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 721)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-l,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 721)
Используя Общую методику 9, исходя из Примера 95 и 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксаборолана в качестве реагентов, получали Пример 721. МСВР: рассчитано для C39H40N6O4S2: 720.2552, найдено: 721.2639 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 722)
3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 722)
Используя Общую методику 9, исходя из Примера 95 и 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана в качестве реагентов, получали Пример 722. МСВР: рассчитано для C39H40N6O5S: 704.2781, найдено: 705.2823 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 723)
3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 723)
Используя Общую методику 9, исходя из Примера 95 и 2-фурилбороновой кислоты в качестве реагентов, получали Пример 723. МСВР: рассчитано для C39H40N6O5S: 704.2781, найдено: 705.2846 [(М+Н)+ форма].
 5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(3-метоксифенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 724)
5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(3-метоксифенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил (Пример 724)
Используя Общую методику 9, исходя из Примера 95 и (6-циано-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 724. МСВР: рассчитано для C41H40N8O4S: 740.2893, найдено: 741.2958 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 725)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 725)
Используя Общую методику 9, исходя из Примера 95 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 725. МСВР: рассчитано для C41H43N7O4S: 729.3098, найдено: 365.6635 [(М+2Н)2+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(6'-метил-3,3'-бипиридин-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 726)
3-{[4-гидрокси-1-({(3R,4R)-1-[(6'-метил-3,3'-бипиридин-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 726)
Используя Общую методику 9, исходя из Примера 303 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 726. МСВР: рассчитано для C42H41N7O4: 707.3220, найдено: 708.329 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 727)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 727)
Используя Общую методику 7, исходили из соединения Синтеза R3bu и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 727. МСВР: рассчитано для C41H39FN6O4S: 730.2737, найдено: 731.2812 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 728)
3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 728)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 728. МСВР: рассчитано для C35H35N6C4SBr: 714.1624, найдено: 715.1701 [(М+Н)+ форма].
 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 729)
5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 729)
Используя Общую методику 9, исходя из Примера 728 и (6-циано-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 729. МСВР: рассчитано для C41H38N8O4S: 738.2737, найдено: 739.2816 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 730)
3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 730)
Используя Общую методику 9, исходя из Примера 728 и [6-(диметиламино)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 730. МСВР: рассчитано для C42H44N8O4S: 756.3206, найдено: 757.3285 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 731)
3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 731)
Используя Общую методику 9, исходя из Примера 728 и [6-(трифторметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 731. МСВР: рассчитано для C41H38F3N7O4S: 781.2658, найдено: 782.2735 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 732)
3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 732)
Используя Общую методику 9, исходя из Примера 103 и [6-(диметиламино)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 732. МСВР: рассчитано для C41H44N8O3S: 728.3257, найдено: 365.1688 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 733)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 733)
Используя Общую методику 9, исходя из Примера 103 и (6-метокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 733. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 358.6536 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 734)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 734)
Используя Общую методику 9, исходя из Примера 728 и (6-метокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 734. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2969 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(морфолин-4-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 735)
3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(морфолин-4-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 735)
Используя Общую методику 9, исходя из Примера 103 и (6-морфолино-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 735. МСВР: рассчитано для C43H46N8O4S: 770.3362, найдено: 386.1758 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 736)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 736)
Используя Общую методику 9, исходя из Примера 103 и [6-(трифторметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 736. МСВР: рассчитано для C40H38F3N7O3S: 753.2709, найдено: 754.2786 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(пиперазин-1-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 737)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(пиперазин-1-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 737)
Используя Общую методику 9, исходя из Примера 103 и 1-[5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]пиперазина в качестве реагентов, получали Пример 737. МСВР: рассчитано для C43H47N9O3S: 769.3522, найдено: 770.3601 [(М+Н)+ форма].
 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 738)
5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбонитрил (Пример 738)
Используя Общую методику 9, исходя из Примера 103 и (6-циано-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 738. МСВР: рассчитано для C40H38N8O3S: 710.2787, найдено: 711.2881 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 739)
3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 739)
Используя Общую методику 9, исходя из Примера 103 и [6-(гидроксиметил)-3-пиридил]бороновой кислоты в качестве реагентов, получали Пример 739. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 716.3019 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метил-3H-имидазо[4,5-b]пиридин-6-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 740)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метил-3H-имидазо[4,5-b]пиридин-6-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 740)
Используя Общую методику 9, исходя из Примера 103 и 3-метил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)имидазо[4,5-b]пиридина в качестве реагентов, получали Пример 740. МСВР: рассчитано для C41H41N9O3S: 739.3053, найдено: 370.6594 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(5-фтор-6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 741)
3-[(1-{[(3R,4R)-1-{[2-(5-фтор-6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 741)
Используя Общую методику 9, исходя из Примера 103 и (5-фтор-6-гидрокси-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 741. МСВР: рассчитано для C39H38FN7O4S: 719.2690, найдено: 720.2742 [(М+Н)+ форма].
 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-3-карбоксамид (Пример 742)
5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-3-карбоксамид (Пример 742)
Используя Общую методику 9, исходя из Примера 103 и 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-3-карбоксамида в качестве реагентов, получали Пример 742. МСВР: рассчитано для C40H40N8O4S: 728.2893, найдено: 729.296 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[5-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 743)
3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[5-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 743)
Используя Общую методику 9, исходя из Примера 103 и [5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-3-пиридил]метанола в качестве реагентов, получали Пример 743. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 358.6526 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(тетрагидро-2Н-пиран-4-илокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 744)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(тетрагидро-2Н-пиран-4-илокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 744)
Используя Общую методику 9, исходя из Примера 103 и 2-тетрагидропиран-4-илокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 744. МСВР: рассчитано для C44H47N7O5S: 785.3359, найдено: 393.6745 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(5-амино-6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 745)
3-[(1-{[(3R,4R)-1-{[2-(5-амино-6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 745)
Используя Общую методику 9, исходя из Примера 103 и 2-метокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-3-амина в качестве реагентов, получали Пример 745. МСВР: рассчитано для C40H42N8O4S: 730.3050, найдено: 366.1585 [(М+2Н)2+ форма].
 метил 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбоксилат (Пример 746)
метил 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбоксилат (Пример 746)
Используя Общую методику 9, исходя из Примера 103 и метил 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбоксилата в качестве реагентов, получали Пример 746. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2954 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(2-метоксиэтокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 747)
3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(2-метоксиэтокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 747)
Используя Общую методику 9, исходя из Примера 103 и 2-(2-метоксиэтокси)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридина в качестве реагентов, получали Пример 747. МСВР: рассчитано для C42H45N7O5S: 759.3203, найдено: 760.3268 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(2-{6-[(2-метоксиэтил)амино]пиридин-3-ил}-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 748)
3-{[4-гидрокси-1-({(3R,4R)-1-[(2-{6-[(2-метоксиэтил)амино]пиридин-3-ил}-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 748)
Используя Общую методику 9, исходя из Примера 103 и N-(2-метоксиэтил)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амина в качестве реагентов, получали Пример 748. МСВР: рассчитано для C42H46N8O4S: 758.3362, найдено: 380.1717 [(М+2Н)2+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[(6'-метил-2,3'-бипиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 749)
3-{[4-гидрокси-1-({(3R,4R)-1-[(6'-метил-2,3'-бипиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 749)
Используя Общую методику 9, исходя из Примера 302 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 749. МСВР: рассчитано для C42H41N7O4: 707.3220, найдено: 708.3294 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 750)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 750)
Используя Общую методику 9, исходя из Примера 728 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 750. МСВР: рассчитано для C41H41N7O4S: 727.2941, найдено: 728.3013 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 751)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 751)
Используя Общую методику 9, исходя из Примера 103 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 751. МСВР: рассчитано для C40H41N7O3S: 699.2991, найдено: 350.6573 [(М+2Н)2+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 752)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 752)
Используя Общую методику 7, исходили из соединения Синтеза R3c и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 752. МСВР: рассчитано для C37H41N7O4S: 679.2941, найдено: 680.3014 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(6-аминопиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 753)
3-[(1-{[(3R,4R)-1-{[2-(6-аминопиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-этил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 753)
Используя Общую методику 7, исходили из соединения Синтеза R3c и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином в соответствии с Общей методикой 9 с получением Примера 753. МСВР: рассчитано для C36H40N8O4S: 680.2893, найдено: 341.1534 [(М+2Н)2+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 754)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 754)
Используя Общую методику 7, исходили из соединения Синтеза R3c и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с [6-(трифторметил)-3-пиридил]бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 754. МСВР: рассчитано для C37H38N7O4F3S: 733.2658, найдено: 734.2738 [(М+Н)+ форма].
 7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 755)
7-этил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 755)
Используя Общую методику 7, исходили из соединения Синтеза R3c и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метокси-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 755. МСВР: рассчитано для C37H41N7O5S: 695.2890, найдено: 696.2959 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 756)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-4-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 756)
Используя Общую методику 7, исходили из соединения Синтеза R3cd и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 756. МСВР: рассчитано для C40H40N8O4S: 728.2893, найдено: 729.2971 [(М+Н)+ форма].
 7-циклопропил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 757)
7-циклопропил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 757)
Используя Общую методику 6, исходили из соединения Синтеза R3g и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 757. МСВР: рассчитано для C37H41N7O3S: 663.2991, найдено: 332.6581 [(М+2Н)2+ форма].
 7-циклопропил-3-[(1-{[(3R,4R)-1-({3-фтор-5-[6-(2,2,2-трифторэтокси)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 758)
7-циклопропил-3-[(1-{[(3R,4R)-1-({3-фтор-5-[6-(2,2,2-трифторэтокси)пиридин-3-ил]тиофен-2-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 758)
Используя Общую методику 7, исходили из соединения Синтеза R3g и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с [6-(2,2,2-трифторэтокси)-3-пиридил]бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 758. МСВР: рассчитано для C39H38F4N6O5S: 778.256, найдено: 779.2595 [(М+Н)+ форма].
 7-циклобутил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 759)
7-циклобутил-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 759)
Используя Общую методику 7, исходили из соединения Синтеза R3h и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 759. МСВР: рассчитано для C39H43N7O4S: 705.3098, найдено: 706.3173 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метилпропил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 760)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2-метилпропил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 760)
Используя Общую методику 6, исходили из соединения Синтеза R3n и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 760. МСВР: рассчитано для C39H45N7O4S: 707.3254, найдено: 708.3342 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(2-метилпропил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 761)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(2-метилпропил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 761)
Используя Общую методику 7, исходили из соединения Синтеза R3n и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 761. МСВР: рассчитано для C39H43FN6O4S: 710.3051, найдено: 711.3123 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 762)
3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 762)
Используя Общую методику 7, исходя из соединения Синтеза R3o и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 762. МСВР: рассчитано для C31H32BrF3N6O4S: 720.1341, найдено: 721.1421 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 763)
3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 763)
Используя Общую методику 9, исходя из Примера 340 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 763. МСВР: рассчитано для C37H36F4N6O4S: 736.2455, найдено: 737.253 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 764)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 764)
Используя Общую методику 9, исходя из Примера 762 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 764. МСВР: рассчитано для C37H38F3N7O4S: 733.2658, найдено: 734.274 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 765)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(2,2,2-трифторэтил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 765)
Используя Общую методику 9, исходя из Примера 143 и (6-метил-3-пиридил)бороновой кислоты в качестве реагентов, получали Пример 765. МСВР: рассчитано для C36H38N7O3F3S: 705.2709, найдено: 706.2759 [(М+Н)+ форма].
 7-(2,2-дифторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 766)
7-(2,2-дифторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 766)
Используя Общую методику 7, исходили из соединения Синтеза R3p и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 766. МСВР: рассчитано для C37H39F2N7O4S: 715.2752, найдено: 716.2836 [(М+Н)+ форма].
 7-(циклопропилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 767)
7-(циклопропилметил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 767)
Используя Общую методику 7, исходили из соединения Синтеза R3q и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 767. МСВР: рассчитано для C39H43N7O4S: 705.3098, найдено: 353.6637 [(М+2Н)2+ форма].
 7-[3-(диметиламино)пропил]-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 768)
7-[3-(диметиламино)пропил]-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 768)
Используя Общую методику 7, исходили из соединения Синтеза R3t и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 768. МСВР: рассчитано для C40H46FN7O4S: 739.3316, найдено: 370.6742 [(М+2Н)2+ форма].
 7-(2-фторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 769)
7-(2-фторэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 769)
Используя Общую методику 7, исходили из соединения Синтеза R3u и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 769. МСВР: рассчитано для C37H40FN7O4S: 697.2847, найдено: 698.2920 [(М+Н)+ форма].
 7-[2-(диметиламино)этил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 770)
7-[2-(диметиламино)этил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 770)
Используя Общую методику 7, исходили из соединения Синтеза R3v и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 770. МСВР: рассчитано для C39H46N8O4S: 722.3362, найдено: 362.1756 [(М+2Н)2+ форма].
 7-[2-(диметиламино)этил]-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 771)
7-[2-(диметиламино)этил]-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 771)
Используя Общую методику 7, исходили из соединения Синтеза R3v и соединения Синтеза R1g в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 771. МСВР: рассчитано для C39H44FN7O4S: 725.3160, найдено: 363.6647 [(М+2Н)2+ форма].
 7-[2-(диметиламино)этил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 772)
7-[2-(диметиламино)этил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 772)
Используя Общую методику 6, исходили из соединения Синтеза R3v и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 772. МСВР: рассчитано для C38H46N8O3S: 694.3414, найдено: 348.1773 [(М+2Н)2+ форма].
 7-(2-гидроксиэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 773)
7-(2-гидроксиэтил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 773)
Используя Общую методику 7, исходили из соединения Синтеза R3w и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученный в результате сырой продукт подвергали реакции с (6-метил-3-пиридил)бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 773. МСВР: рассчитано для C37H41N7O5S: 695.2890, найдено: 696.2960 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 774)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 774)
Используя Общую методику 10, исходя из Примера 160 и трибромида бора в качестве реагентов, получали Пример 774. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2970 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 775)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 775)
Используя Общую методику 10, исходя из Примера 61 и трибромида бора в качестве реагентов, получали Пример 775. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 358.6539 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 776)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 776)
и
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 777)
Используя Общую методику 10, исходя из Примера 62 и трибромида бора в качестве реагентов, получали Пример 776 и Пример 777 и разделяли их с помощью хроматографии.
Пример 776: МСВР: рассчитано для C39H39N7O5S: 717.2733, найдено: 718.2818 [(М+Н)+ форма].
Пример 777: МСВР: рассчитано для C40H41N7O5S: 731.2890, найдено: 732.2963 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 778)
3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-3-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 778)
Используя Общую методику 14, исходя из Примера 402 в качестве реактанта, получали Пример 778. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 333.6468 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[4-амино-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 779)
3-[(1-{[(3R,4R)-1-{[4-амино-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 779)
Используя Общую методику 12, исходя из Примера 185 в качестве реактанта, получали Пример 779. МСВР: рассчитано для C35H37N7O4S: 651.2628, найдено: 326.6382 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,2,3,4-тетрагидроизохинолин-6-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 780)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,2,3,4-тетрагидроизохинолин-6-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 780)
Используя Общую методику 14, исходя из Примера 192 в качестве реактанта, получали Пример 780. МСВР: рассчитано для C35H40N6O4: 608.3111, найдено: 305.1639 [(М+2Н)2+ форма].
 N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)ацетамид (Пример 781)
N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)ацетамид (Пример 781)
Используя Общую методику 7, исходя из Примера 512 и уксусной кислоты в качестве реагентов, получали Пример 781. МСВР: рассчитано для C34H38N6O5: 610.2903, найдено: 611.2989 [(М+Н)+ форма].
 N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)бензамид (Пример 782)
N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)бензамид (Пример 782)
Используя Общую методику 7, исходя из Примера 512 и бензойной кислоты в качестве реагентов, получали Пример 782. МСВР: рассчитано для C39H40N6O5: 672.30603, найдено: 673.3148 [(М+Н)+ форма].
 трет-бутил(2-бром-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-3-ил)карбамат (Пример 783)
трет-бутил(2-бром-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}тиофен-3-ил)карбамат (Пример 783)
Используя Общую методику 7, исходя из соединения Синтеза R3b и соединения Синтеза R1o в качестве реагентов, получали Пример 783. МСВР: рассчитано для C35H41BrN6O6S: 752.1992, найдено: 753.2074 [(М+Н)+ форма].
 2-хлор-N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)ацетамид (Пример 784)
2-хлор-N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)ацетамид (Пример 784)
Пример 512 (100 мг, 0.176 ммоль) и хлорацетилхлорид (17 мкл, 24 мг, 0.21 ммоль), и карбонат калия (73 мг, 0.527 ммоль) перемешивали в ДМФА (2 мл) при к.т. в течение 3 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 784. МСВР: рассчитано для C34H37ClN6O5: 644.2514, найдено: 645.2606 [(М+Н)+ форма].
 N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)проп-2-енамид (Пример 785)
N-(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)проп-2-енамид (Пример 785)
Используя Общую методику 7, исходя из Примера 512 и акриловой кислоты в качестве реагентов, получали Пример 785. МСВР: рассчитано для C35H38N6O5: 622.2903, найдено: 623.2988 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 786)
3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 786)
Используя Общую методику 14, исходя из Примера 628 в качестве реактанта, получали Пример 786. МСВР: рассчитано для C35H36FN7O4S: 669.2534, найдено: 335.6337 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 787)
3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)тиофен-2-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 787)
Используя Общую методику 14, исходя из Примера 392 в качестве реактанта, получали Пример 787. МСВР: рассчитано для C35H39N7O3S: 637.2835, найдено: 319.6503 [(М+2Н)2+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,2,3,4-тетрагидрохинолин-7-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 788)
3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,2,3,4-тетрагидрохинолин-7-илкарбонил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 788)
Используя Общую методику 14, исходя из Примера 245 в качестве реактанта, получали Пример 788. МСВР: рассчитано для C35H40N6O4: 608.3111, найдено: 609.3200 [(М+Н)+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 789)
3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-1,3-тиазол-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 789)
Используя Общую методику 14, исходя из Примера 644 в качестве реактанта, получали Пример 789. МСВР: рассчитано для C34H36N8O4S: 652.2580, найдено: 327.137 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(2-аминопиридин-4-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 790)
3-[(1-{[(3R,4R)-1-{[2-(2-аминопиридин-4-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 790)
Используя Общую методику 14, исходя из Примера 645 в качестве реактанта, получали Пример 790. МСВР: рассчитано для C35H38N8O4S: 666.2737, найдено: 334.1454 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 791)
3-[(1-{[(3R,4R)-1-{[5-(2-аминопиридин-4-ил)-4-метилтиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 791)
Используя Общую методику 14, исходя из Примера 398 в качестве реактанта, получали Пример 791. МСВР: рассчитано для C36H39N7O4S: 665.2784, найдено: 333.6473 [(М+2Н)2+ форма].
 3-[(1-{[(3R,4R)-1-{[2-(2-аминопиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 792)
3-[(1-{[(3R,4R)-1-{[2-(2-аминопиридин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 792)
Используя Общую методику 14, исходя из Примера 657 в качестве реактанта, получали Пример 792. МСВР: рассчитано для C34H36N8O4S: 652.2580, найдено: 653.2646 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[4-(аминометил)бензоил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 793)
3-{[1-({(3R,4R)-1-[4-(аминометил)бензоил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 793)
Используя Общую методику 14, исходя из Примера 252 в качестве реактанта, получали Пример 793. МСВР: рассчитано для C33H38N6O4: 582.2955, найдено: 292.1560 [(М+2Н)2+ форма].
 N-(4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензил)проп-2-енамид (Пример 794)
N-(4-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензил)проп-2-енамид (Пример 794)
Используя Общую методику 7, исходя из Примера 793 и акриловой кислоты в качестве реагентов, получали Пример 794. МСВР: рассчитано для C36H40N6O5: 636.3060, найдено: 637.3134 [(М+Н)+ форма].
 3-{[1-({(3R,4R)-1-[(1-акрилоил-1,2,3,4-тетрагидрохинолин-7-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 795)
3-{[1-({(3R,4R)-1-[(1-акрилоил-1,2,3,4-тетрагидрохинолин-7-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 795)
Используя Общую методику 7, исходя из Примера 788 и акриловой кислоты в качестве реагентов, получали Пример 795. МСВР: рассчитано для C38H42N6O5: 662.3217, найдено: 663.3297 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензамид (Пример 796)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензамид (Пример 796)
Смесь Примера 208 (0.23 ммоль), ацетальдоксима (141 мкл, 137 мг, 2.3 ммоль, 10 экв.) и обработанного хлоридом меди(II) молекулярного сита (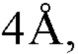 50 мг) перемешивали в МеОН (2 мл) в течение 5 часов при 60°C. Реакционную смесь фильтровали, фильтрат очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 796. МСВР: рассчитано для C33H36N6O5: 596.2747, найдено: 597.283 [(М+Н)+ форма].
50 мг) перемешивали в МеОН (2 мл) в течение 5 часов при 60°C. Реакционную смесь фильтровали, фильтрат очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 796. МСВР: рассчитано для C33H36N6O5: 596.2747, найдено: 597.283 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензойная кислота (Пример 797)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензойная кислота (Пример 797)
Смесь Примера 260 (0.66 ммоль) и хлористоводородной кислоты (водн. 1 н., 1.33 мл, 2 экв.) в MeCN (2 мл) перемешивали при 80°C в течение 4 часов. Реакционную смесь вводили в препаративную ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 797. МСВР: рассчитано для C33H35N5O6: 597.2587, найдено: 598.2659 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-N-метилбензамид (Пример 798)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-N-метилбензамид (Пример 798)
Используя Общую методику 7, исходя из Примера 797 в качестве реактанта - карбоновой кислоты и гидрохлорида метиламина в качестве аминного реактанта, получали Пример 798. МСВР: рассчитано для C34H38N6O5: 610.2903, найдено: 611.2978 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-N,N-диметилбензамид (Пример 799)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-N,N-диметилбензамид (Пример 799)
Используя Общую методику 7, исходя из Примера 797 в качестве реактанта - карбоновой кислоты и дигидрохлорида метиламина в качестве аминного реактанта, получали Пример 799. МСВР: рассчитано для C35H40N6O5: 624.3060, найдено: 625.3139 [(М+Н)+ форма].
 3-{[4-гидрокси-1-({(3R,4R)-1-[3-(морфолин-4-илкарбонил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 800)
3-{[4-гидрокси-1-({(3R,4R)-1-[3-(морфолин-4-илкарбонил)бензоил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-метил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 800)
Используя Общую методику 7, исходя из Примера 797 в качестве реактанта - карбоновой кислоты и морфолина в качестве аминного реактанта, получали Пример 800. МСВР: рассчитано для C37H42N6O6: 666.3166, найдено: 334.1668 [(М+2Н)2+ форма].
 5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-2-(6-метилпиридин-3-ил)-1,3-тиазол-4-карбонитрил (Пример 801)
5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-2-(6-метилпиридин-3-ил)-1,3-тиазол-4-карбонитрил (Пример 801)
Смесь Примера 263 (0.15 ммоль) и цианида меди(I) (156 мг, 1.74 ммоль, 12 экв.) в NMP (5 мл) подвергали микроволновому облучению в течение 4 часов при 200°C. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водная муравьиная кислота - MeCN, затем 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 801. МСВР: рассчитано для C36H36N8O4S: 676.2580, найдено: 677.266 [(М+Н)+ форма].
 (3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)(метил)сульфонийолат (Пример 802)
(3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}фенил)(метил)сульфонийолат (Пример 802)
Смесь Примера 283 (0.267 ммоль) и оксона® (164 мг, 0.267 ммоль, 1 экв) в МеОН (5 мл), воде (5 мл) и MeCN (5 мл) перемешивали при к.т. в течение 10 часов. К реакционной смеси добавляли воду (30 мл) и MSM (3 мл) и упаривали. К остатку добавляли солевой раствор (30 мл) и экстрагировали с помощью ДХМ (4×50 мл), объединенные органические слои сушили над MgSO4 и упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 802. МСВР: рассчитано для C33H37N5O5S: 615.2515, найдено: 616.2622 [(М+Н)+ форма].
 метил 3-амино-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 803)
метил 3-амино-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 803)
Используя Общую методику 12, исходя из Примера 285 в качестве реактанта, получали Пример 803. МСВР: рассчитано для C34H38N6O6: 626.2853, найдено: 627.295 [(М+Н)+ форма].
 3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-N-метокси-N-метилбензамид (Пример 804)
3-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-N-метокси-N-метилбензамид (Пример 804)
Используя Общую методику 7, исходя из Примера 797 в качестве реактанта - карбоновой кислоты и гидрохлорида N,O-диметилгидроксиламина в качестве аминного реактанта, получали Пример 804. МСВР: рассчитано для C35H40N6O6: 640.3009, найдено: 641.3089 [(М+Н)+ форма].
 метил 3-(ацетиламино)-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенил пиперидин-1-ил]карбонил}бензоат (Пример 805)
метил 3-(ацетиламино)-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенил пиперидин-1-ил]карбонил}бензоат (Пример 805)
Используя Общую методику 7, исходя из Примера 803 и уксусной кислоты в качестве реактантов, получали Пример 805. МСВР: рассчитано для C36H40N6O7: 668.2958, найдено: 669.3036 [(М+Н)+ форма].
 метил 3-(бензоиламино)-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 806)
метил 3-(бензоиламино)-5-{[(3R,4R)-4-({4-гидрокси-4-[(7-метил-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат (Пример 806)
Используя Общую методику 7, исходя из Примера 803 и бензойной кислоты в качестве реагентов, получали Пример 806. МСВР: рассчитано для C41H42N6O7: 730.3115, найдено: 731.3194 [(М+Н)+ форма].
 7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 807)
7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 807)
Используя Общую методику 10, исходя из Примера 86 в качестве реактанта, получали Пример 807. МСВР: рассчитано для C39H38N7O4SCl: 735.2394, найдено: 736.2464 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 808)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 808)
Используя Общую методику 10, исходя из Примера 99 в качестве реактанта, получали Пример 808. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 716.3012 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 809)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 809)
Используя Общую методику 10, исходя из Примера 94 в качестве реактанта, получали Пример 809. МСВР: рассчитано для C39H39N7O5S: 717.2733, найдено: 718.2805 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-оксо-1,6-дигидропиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 810)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-оксо-1,6-дигидропиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-метоксипиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 810)
Используя Общую методику 15, исходя из Примера 101 в качестве реактанта, получали Пример 810. МСВР: рассчитано для C39H40N8O5S: 732.2842, найдено: 733.2893 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метил-1-оксидопиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 811)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метил-1-оксидопиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 811)
Смесь Примера 750 (0.137 ммоль), mCPBA (24 мг, 0.137 ммоль, 1 экв.) в ДХМ (1 мл) перемешивали при к.т. в течение 25 часов. Реакционную смесь упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 811. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2959 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 812)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 812)
Используя Общую методику 10, исходя из Примера 733 в качестве реактанта, получали Пример 812. МСВР: рассчитано для C39H39N7O4S: 701.2784, найдено: 702.2841 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(4-метилпиперазин-1-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 813)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(4-метилпиперазин-1-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 813)
Смесь Примера 103 (0.391 ммоль) и N-метилпиперазина (96 мкл, 87 мг, 0.872 ммоль, 3 экв.), и PDO (5 мл) подвергали микроволновому облучению в течение в общей сложности 9 часов при 150°С. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 813. МСВР: рассчитано для C39H46N8O3S: 706.3414, найдено: 707.3487 [(М+Н)+ форма].
 5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбоновая кислота (Пример 814)
5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбоновая кислота (Пример 814)
Используя Общую методику 9, исходили из Примера 103 и метил 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-карбоксилата в качестве реагентов, сырой продукт растворяли в МеОН (5 мл) и воде (5 мл), добавляли моногидрат гидроксида лития (74 мг, 1.76 ммоль) и смесь перемешивали в течение 2 часов при к.т. Реакционную смесь упаривали до воды, нейтрализовали раствором HCl (водн., 1 н.), очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 814. МСВР: рассчитано для C40H39N7O5S: 729.2733, найдено: 730.278 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-оксо-1,6-дигидропиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-оксо-1,6-дигидропиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 815)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-оксо-1,6-дигидропиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-оксо-1,6-дигидропиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 815)
Используя Общую методику 15, исходя из Примера 101 в качестве реактанта, получали Пример 815. МСВР: рассчитано для C38H38N8O5S: 718.2686, найдено: 719.2756 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-оксо-1,6-дигидропиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 816)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(6-оксо-1,6-дигидропиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 816)
Используя Общую методику 15, исходя из Примера 100 в качестве реактанта, получали Пример 816. МСВР: рассчитано для C39H40N8O4S: 716.2893, найдено: 717.2966 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-6-оксо-1,6-дигидропиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 817)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-6-оксо-1,6-дигидропиридин-2-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он (Пример 817)
Используя Общую методику 13, исходя из Примера 816 в качестве реактанта и йодметана в качестве реагента, получали Пример 817. МСВР: рассчитано для C40H42N8O4S: 730.3050, найдено: 731.3121 [(М+Н)+ форма].
 3-[[1-[(3S,4S)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 818)
3-[[1-[(3S,4S)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 818)
Используя Общую методику 6, исходя из 3-[[4-гидрокси-1-[(3S,4S)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-она (который получали в соответствии с Общей методикой 5 с использованием трет-бутил (3S,4S)-4-(2-окса-6-азаспиро[2.5]октан-6-карбонил)-3-фенилпиперидин-1-карбоксилата и 3H-тиено[2,3-d]пиримидин-4-она) и бензилбромида в качестве реагентов, получали Пример 818. МСВР: рассчитано для C31H34N4O3S: 542.2352, найдено: 543.2419 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 819)
3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 819)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и бензилбромида в качестве реагентов, получали Пример 819. МСВР: рассчитано для C31H34N4O3S: 543.2352, найдено: 543.2401 [(М+Н)+ форма].
 3-[[1-[(3S,4S)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 820)
3-[[1-[(3S,4S)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 820)
Используя Общую методику 6, исходя из соединения Синтеза R3cn и бензилбромида в качестве реагентов, получали Пример 820. МСВР: рассчитано для C32H35N5O3: 537.274, найдено: 538.2837 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 821)
3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 821)
Используя Общую методику 6, исходя из соединения Синтеза R3co и бензилбромида в качестве реагентов, получали Пример 821. МСВР: рассчитано для C32H35N5O4: 537.2740, найдено: 538.2809 [(М+Н)+ форма].
 3-[[1-[(3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 822)
3-[[1-[(3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 822)
Используя Общую методику 5, исходили из 3H-пиридо[3,2-d]пиримидин-4-она и соединения Синтеза R1e в качестве реактантов, полученный в результате сырой пиперидиновый продукт подвергали реакции с соединением Синтеза R1q-(3R,4S) в соответствии с Общей методикой 7 с получением Примера 822. МСВР: рассчитано для C30H33N5O3S: 544.2304, найдено: 544.2381 [(М+Н)+ форма].
 3-[[1-[(3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 823)
3-[[1-[(3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 823)
Используя Общую методику 5, исходили из 3H-пиридо[3,2-d]пиримидин-4-она и соединения Синтеза R1e в качестве реактантов, полученный в результате сырой пиперидиновый продукт подвергали реакции с соединением Синтеза R1q-(3S,4R) в соответствии с Общей методикой 7 с получением Примера 823. МСВР: рассчитано для C30H33N5O3S: 544.2304, найдено: 544.2394 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 824)
3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 824)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и 1-(бромметил)-2-фторбензола в качестве реагентов, получали Пример 824. МСВР: рассчитано для C31H33FN4O3S: 560.2257, найдено: 561.2301 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(3-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 825)
3-[[1-[(3R,4R)-1-[(3-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 825)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и 1-(бромметил)-3-фторбензола в качестве реагентов, получали Пример 825. МСВР: рассчитано для C31H33FN4O3S: 560.2257, найдено: 561.2331 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(о-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 826)
3-[[4-гидрокси-1-[(3R,4R)-1-(о-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 826)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и 1-(бромметил)-2-метилбензола в качестве реагентов, получали Пример 826. МСВР: рассчитано для C32H36N4O3S: 556.2508, найдено: 557.2565 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(м-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 827)
3-[[4-гидрокси-1-[(3R,4R)-1-(м-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 827)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и 1-(бромметил)-3-метилбензола в качестве реагентов, получали Пример 827. МСВР: рассчитано для C32H36N4O3S: 556.2508, найдено: 557.2597 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 828)
3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 828)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 4-метил-2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 828. МСВР: рассчитано для C36H36N6O4S: 648.2519, найдено: 649.2583 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(2-фенилтиазол-5-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 829)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(2-фенилтиазол-5-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 829)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 829. МСВР: рассчитано для C35H34N6O4S: 634.2362, найдено: 635.2429 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-хлорпиридо[3,2-d]пиримидин-4-он (Пример 830)
3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-хлорпиридо[3,2-d]пиримидин-4-он (Пример 830)
Используя Общую методику 6, исходя из соединения Синтеза R3cq и бензилбромида в качестве реагентов, получали Пример 830. МСВР: рассчитано для C32H34ClN5O3: 571.235, найдено: 572.2416 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-метоксипиридо[3,2-d]пиримидин-4-он (Пример 831)
3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-метоксипиридо[3,2-d]пиримидин-4-он (Пример 831)
Используя Общую методику 6, исходя из соединения Синтеза R3cr и бензилбромида в качестве реагентов, получали Пример 831. МСВР: рассчитано для C33H37N5O4: 567.2846, найдено: 568.2902 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-5Н-пиридо[3,2-d]пиримидин-4,6-дион (Пример 832)
3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-5Н-пиридо[3,2-d]пиримидин-4,6-дион (Пример 832)
Используя Общую методику 6, исходя из соединения Синтеза R3cs и бензилбромида в качестве реагентов, получали Пример 832. МСВР: рассчитано для C32H35N5O4: 553.2689, найдено: 554.2762 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(3-метилизотиазол-4-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 833)
3-[[4-гидрокси-1-[(3R,4R)-1-(3-метилизотиазол-4-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 833)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 3-метилизотиазол-4-карбоновой кислоты в качестве реагентов, получали Пример 833. МСВР: рассчитано для C30H32N6O4S: 572.2206, найдено: 573.2285 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 834)
3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 834)
Используя Общую методику 6, исходя из соединения Синтеза R3co и 1-(бромметил)-2-фторбензола в качестве реагентов, получали Пример 834. МСВР: рассчитано для C32H34FN5O3: 555.2646, найдено: 556.2701 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(3-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 835)
3-[[1-[(3R,4R)-1-[(3-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 835)
Используя Общую методику 6, исходя из соединения Синтеза R3co и 1-(бромметил)-3-фторбензола в качестве реагентов, получали Пример 835. МСВР: рассчитано для C32H34FN5O4: 555.2647, найдено: 556.2702 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(о-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 836)
3-[[4-гидрокси-1-[(3R,4R)-1-(о-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 836)
Используя Общую методику 6, исходя из соединения Синтеза R3co и 1-(бромметил)-2-метилбензола в качестве реагентов, получали Пример 836. МСВР: рассчитано для C33H37N5O3: 551.2896, найдено: 552.2943 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(м-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 837)
3-[[4-гидрокси-1-[(3R,4R)-1-(м-толилметил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 837)
Используя Общую методику 6, исходя из соединения Синтеза R3co и 1-(бромметил)-3-метилбензола в качестве реагентов, получали Пример 837. МСВР: рассчитано для C33H37N5O4: 551.2897, найдено: 552.2990 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 838)
3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 838)
Используя Общую методику 7, исходя из соединения Синтеза R3cp и 4-метил-2-фенилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 838. МСВР: рассчитано для C35H35N5O4S2: 653.2130, найдено: 654.2212 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(2-бензил-4-метилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 839)
3-[[1-[(3R,4R)-1-(2-бензил-4-метилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 839)
Используя Общую методику 7, исходя из соединения Синтеза R3cp и 2-бензил-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 839. МСВР: рассчитано для C36H37N5O4S2: 667.2287, найдено: 668.2371 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(3-метилизотиазол-4-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 840)
3-[[4-гидрокси-1-[(3R,4R)-1-(3-метилизотиазол-4-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 840)
Используя Общую методику 7, исходя из соединения Синтеза R3cp и 3-метилизотиазол-4-карбоновой кислоты в качестве реагентов, получали Пример 840. МСВР: рассчитано для C29H31N5O4S2: 577.1817, найдено: 578.1901 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(бензофуран-2-илметил)-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 841)
3-[[1-[(3R,4R)-1-(бензофуран-2-илметил)-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 841)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и 2-(хлорметил)бензофурана в качестве реагентов, получали Пример 841. МСВР: рассчитано для C33H34N4O4S: 582.2301, найдено: 583.2376 [(М+Н)+ форма].
 3-[(3R,4R)-4-[4-гидрокси-4-[(4-оксотиено[2,3-d]пиримидин-3-ил)метил]пиперидин-1-карбонил]-3-фенилпиперидин-1-карбонил]-1Н-индазол-5-карбонитрил (Пример 842)
3-[(3R,4R)-4-[4-гидрокси-4-[(4-оксотиено[2,3-d]пиримидин-3-ил)метил]пиперидин-1-карбонил]-3-фенилпиперидин-1-карбонил]-1Н-индазол-5-карбонитрил (Пример 842)
Используя Общую методику 7, исходя из соединения Синтеза R3cp и 5-циано-1Н-индазол-3-карбоновой кислоты в качестве реагентов, получали Пример 842. МСВР: рассчитано для C33H31N7O4S: 621.2158, найдено: 622.2229 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(2-бензил-4-метилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 843)
3-[[1-[(3R,4R)-1-(2-бензил-4-метилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 843)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 2-бензил-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 843. МСВР: рассчитано для C37H38N6O4S: 662.2675, найдено: 663.2743 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[2-(2-фторфенил)-4-метилтиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 844)
3-[[1-[(3R,4R)-1-[2-(2-фторфенил)-4-метилтиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 844)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 2-(2-фторфенил)-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 844. МСВР: рассчитано для C36H35FN6O4S: 666.2425, найдено: 667.2498 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(о-толил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 845)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(о-толил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 845)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 4-метил-2-(о-толил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 845. МСВР: рассчитано для C37H38N6O4S: 662.2675, найдено: 663.2751 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-[2-(4-пиридил)тиазол-5-карбонил]пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 846)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-[2-(4-пиридил)тиазол-5-карбонил]пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 846)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 846. МСВР: рассчитано для C34H33N7O4S: 635.2314, найдено: 636.2401 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3S,4S)-3-фенил-1-[2-(4-пиридил)тиазол-5-карбонил]пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 847)
3-[[4-гидрокси-1-[(3S,4S)-3-фенил-1-[2-(4-пиридил)тиазол-5-карбонил]пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 847)
Используя Общую методику 7, исходя из соединения Синтеза R3cn и 2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 847. МСВР: рассчитано для C34H33N7O4S: 635.2315, найдено: 318.6241 [(М+2Н)2+ форма].
 3-[[1-[(3R,4R)-1-[2-[(2-фторфенил)метил]тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 848)
3-[[1-[(3R,4R)-1-[2-[(2-фторфенил)метил]тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 848)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 2-[(2-фторфенил)метил]тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 848. МСВР: рассчитано для C36H35FN6O4S: 666.2425, найдено: 667.2498 [(М+Н)+ форма].
 6-(бензиламино)-3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 849)
6-(бензиламино)-3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 849)
Используя Общую методику 6, исходя из соединения Синтеза R3ct и бензилбромида в качестве реагентов, получали Пример 849. МСВР: рассчитано для C39H42N6O3: 642.3318, найдено: 322.1727 [(М+2Н)2+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-[5-(4-пиридил)тиофен-2-карбонил]пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 850)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-[5-(4-пиридил)тиофен-2-карбонил]пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 850)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 5-(4-пиридил)тиофен-2-карбоновой кислоты в качестве реагентов, получали Пример 850. МСВР: рассчитано для C35H34N6O4S: 634.2362, найдено: 635.2439 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(4-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 851)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(4-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 851)
Используя Общую методику 7, исходя из соединения Синтеза R3co и 4-метил-2-(4-пиридил)тиазол-5-карбоновой кислоты в качестве реагентов, получали Пример 851. МСВР: рассчитано для C35H35N7O4S: 649.2471, найдено: 650.2547 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-[(4-метоксифенил)метиламино]пиридо[3,2-d]пиримидин-4-он (Пример 852)
3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-[(4-метоксифенил)метиламино]пиридо[3,2-d]пиримидин-4-он (Пример 852)
Используя Общую методику 6, исходя из соединения Синтеза R3cu и 1-(бромметил)-2-фторбензола в качестве реагентов, получали Пример 852. МСВР: рассчитано для C40H43FN6O4: 690.333, найдено: 346.1732 [(М+2Н)2+ форма].
 6-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 853)
6-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 853)
Используя Общую методику 5, Стадия 1, исходя из 6-хлор-3H-пиридо[3,2-d]пиримидин-4-она и соединения Синтеза R1s в качестве эпоксидного соединения, получали Пример 853. МСВР: рассчитано для C36H35ClN6O4S: 682.2129, найдено: 683.2201 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(5-пиримидин-5-илтиофен-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 854)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(5-пиримидин-5-илтиофен-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 854)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 5-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с пиримидин-5-илбороновой кислотой с получением Примера 854. МСВР: рассчитано для C33H32N6O4S2: 640.1926, найдено: 641.1995 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-пиримидин-5-илтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 855)
3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-пиримидин-5-илтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 855)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с пиримидин-5-илбороновой кислотой с получением Примера 855. МСВР: рассчитано для C33H33N7O4S2: 655.2035, найдено: 656.2132 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(5-пиримидин-5-илтиофен-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 856)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(5-пиримидин-5-илтиофен-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 856)
Используя Общую методику 7, исходили из соединения Синтеза R3co и 5-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с пиримидин-5-илбороновой кислотой с получением Примера 856. МСВР: рассчитано для C34H33N7O4S: 635.2315, найдено: 636.2387 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[5-(2-метилпиразол-3-ил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 857)
3-[[4-гидрокси-1-[(3R,4R)-1-[5-(2-метилпиразол-3-ил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 857)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 5-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом с получением Примера 857. МСВР: рассчитано для C33H34N6O4S2: 642.2083, найдено: 643.2163 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(2-метилпиразол-3-ил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 858)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(2-метилпиразол-3-ил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 858)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом с получением Примера 858. МСВР: рассчитано для C33H35N7O4S2: 657.2192, найдено: 658.2279 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[5-(2-метилпиразол-3-ил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 859)
3-[[4-гидрокси-1-[(3R,4R)-1-[5-(2-метилпиразол-3-ил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 859)
Используя Общую методику 7, исходили из соединения Синтеза R3co и 5-бромтиофен-2-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 1-метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом с получением Примера 859. МСВР: рассчитано для C34H35N7O4S: 637.2471, найдено: 638.2525 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метокси-3-пиридил)-4-метилтиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 860)
3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метокси-3-пиридил)-4-метилтиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 860)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с (6-метокси-3-пиридил)бороновой кислотой с получением Примера 860. МСВР: рассчитано для C35H36N6O5S2: 684.2189, найдено: 685.2269 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[2-(6-амино-3-пиридил)-4-метилтиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 861)
3-[[1-[(3R,4R)-1-[2-(6-амино-3-пиридил)-4-метилтиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 861)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином с получением Примера 861. МСВР: рассчитано для C34H35N7O4S2: 669.2192, найдено: 670.2245 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 862)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 862)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и 2-бром-4-метилтиазол-5-карбоновой кислоты в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с (6-метил-3-пиридил)бороновой кислотой с получением Примера 862. МСВР: рассчитано для C35H36N6O4S2: 668.2239, найдено: 669.2306 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[3-фтор-5-(6-метил-3-пиридил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 863)
3-[[1-[(3R,4R)-1-[3-фтор-5-(6-метил-3-пиридил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 863)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и соединения Синтеза R1g в качестве реагентов, полученное в результате сырое йод-соединение подвергали реакции в соответствии с Общей методикой 9 с (6-метил-3-пиридил)бороновой кислотой с получением Примера 863. МСВР: рассчитано для C35H34FN5O4S2: 671.2036, найдено: 336.6092 [(М+2Н)2+ форма].
 3-[[1-[(3R,4R)-1-[5-(6-амино-3-пиридил)-3-фтортиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 864)
3-[[1-[(3R,4R)-1-[5-(6-амино-3-пиридил)-3-фтортиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 864)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и соединения Синтеза R1g в качестве реагентов, полученное в результате сырое йод-соединение подвергали реакции в соответствии с Общей методикой 9 с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином с получением Примера 864. МСВР: рассчитано для C34H33FN6O4S2: 672.1989, найдено: 671.1926 [(М-Н)- форма].
 3-[[1-[(3R,4R)-1-[3-фтор-5-(6-пиперазин-1-ил-3-пиридил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 865)
3-[[1-[(3R,4R)-1-[3-фтор-5-(6-пиперазин-1-ил-3-пиридил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 865)
Используя Общую методику 7, исходили из соединения Синтеза R3cp и соединения Синтеза R1g в качестве реагентов, полученное в результате сырое йод-соединение подвергали реакции в соответствии с Общей методикой 9 с 1-[5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]пиперазином с получением Примера 865. МСВР: рассчитано для C38H40FN7O4S2: 741.2567, найдено: 740.2504 [(М-Н)- форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 866)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 866)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и соединения Синтеза R1c в качестве реагентов, получали Пример 866. МСВР: рассчитано для C34H36N6O3S2: 640.2290, найдено: 641.2336 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 867)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 867)
Используя Общую методику 6, исходя из соединения Синтеза R3cp и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 867. МСВР: рассчитано для C34H36N6O4S2: 656.2239, найдено: 657.2343 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-[[2-(6-пиперазин-1-ил-3-пиридил)тиазол-5-ил]метил]пиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 868)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-[[2-(6-пиперазин-1-ил-3-пиридил)тиазол-5-ил]метил]пиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 868)
Используя Общую методику 6, исходили из соединения Синтеза R3cp и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 1-[5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-2-пиридил]пиперазином с получением Примера 868. МСВР: рассчитано для C37H42N8O3S2: 710.2821, найдено: 356.1477 [(М+2Н)2+ форма].
 3-[[1-[(3R,4R)-1-[[2-(6-амино-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 869)
3-[[1-[(3R,4R)-1-[[2-(6-амино-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 869)
Используя Общую методику 6, исходили из соединения Синтеза R3cp и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-2-амином с получением Примера 869. МСВР: рассчитано для C33H35N7O3S2: 641.2243, найдено: 642.2342 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(3-метилимидазо[4,5-b]пиридин-6-ил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 870)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(3-метилимидазо[4,5-b]пиридин-6-ил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 870)
Используя Общую методику 6, исходили из соединения Синтеза R3cp и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с 3-метил-6-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)имидазо[4,5-b]пиридином с получением Примера 870. МСВР: рассчитано для C35H36N8O3S2: 680.2352, найдено: 341.1257 [(М+2Н)2+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-имидазо[1,2-а]пиридин-7-илтиазол-5-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 871)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-имидазо[1,2-а]пиридин-7-илтиазол-5-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[2,3-d]пиримидин-4-он (Пример 871)
Используя Общую методику 6, исходили из соединения Синтеза R3cp и 2-бром-5-(бромметил)тиазола в качестве реагентов, полученное в результате сырое бром-соединение подвергали реакции в соответствии с Общей методикой 9 с имидазо[1,2-a]пиридин-7-илбороновой кислотой с получением Примера 871. МСВР: рассчитано для C35H35N7O3S2: 665.2243, найдено: 333.6191 [(М+2Н)2+ форма].
 6-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилтриазоло[4,5-d]пиримидин-7-он (Пример 872)
6-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилтриазоло[4,5-d]пиримидин-7-он (Пример 872)
Используя Общую методику 7, исходя из соединения Синтеза R3cv и соединения Синтеза R1d в качестве реагентов, получали Пример 872. МСВР: рассчитано для C39H39N9O4S: 729.2845, найдено: 730.2937 [(М+Н)+ форма].
 1-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он (Пример 873)
1-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он (Пример 873)
Используя Общую методику 7, исходя из соединения Синтеза R3cw и соединения Синтеза R1d в качестве реагентов, получали Пример 873. МСВР: рассчитано для C40H40N8O4S: 728.2893, найдено: 727.2866 [(М+Н)+ форма].
 5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он (Пример 874)
5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он (Пример 874)
Используя Общую методику 6, исходя из соединения Синтеза R3cx и соединения Синтеза R1c в качестве реагентов, получали Пример 874. МСВР: рассчитано для C39H40N8O3S: 700.2944, найдено: 701.3000 [(М+Н)+ форма].
 1-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он (Пример 875)
1-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он (Пример 875)
Используя Общую методику 6, исходя из соединения Синтеза R3cw и соединения Синтеза R1c в качестве реагентов, получали Пример 875. МСВР: рассчитано для C39H40N8O3S: 700.2944, найдено: 351.1551 [(М+2Н)2+ форма].
 1-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он (Пример 876)
1-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-фенилпурин-6-он (Пример 876)
Используя Общую методику 6, исходя из соединения Синтеза R3cw и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 876. МСВР: рассчитано для C39H40N8O4S: 716.2893, найдено: 359.1535 [(М+2Н)2+ форма].
 5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он (Пример 877)
5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он (Пример 877)
Используя Общую методику 6, исходя из соединения Синтеза R3cx и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 877. МСВР: рассчитано для C39H40N8O4S: 716.2893, найдено: 717.2979 [(М+Н)+ форма].
 5-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он (Пример 878)
5-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-фенилпиразоло[3,4-d]пиримидин-4-он (Пример 878)
Используя Общую методику 7, исходя из соединения Синтеза R3cx и соединения Синтеза R1d в качестве реагентов, получали Пример 878. МСВР: рассчитано для C40H40N8O4S: 728.2893, найдено: 729.2961 [(М+Н)+ форма].
 7-бром-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 879)
7-бром-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 879)
Используя Общую методику 6, исходя из соединения Синтеза R3cy и соединения Синтеза R1c в качестве реагентов, получали Пример 879. МСВР: рассчитано для C34H36BrN7O3S: 701.1783, найдено: 702.1856 [(М+Н)+ форма].
 6-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизотиазоло[4,5-d]пиримидин-7-он (Пример 880)
6-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизотиазоло[4,5-d]пиримидин-7-он (Пример 880)
Используя Общую методику 6, исходя из соединения Синтеза R3cz и соединения Синтеза R1c в качестве реагентов, получали Пример 880. МСВР: рассчитано для C39H39N7O3S2: 717.2556, найдено: 718.2602 [(М+Н)+ форма].
 6-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизотиазоло[4,5-d]пиримидин-7-он (Пример 881)
6-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизотиазоло[4,5-d]пиримидин-7-он (Пример 881)
Используя Общую методику 7, исходя из соединения Синтеза R3cz и соединения Синтеза R1d в качестве реагентов, получали Пример 881. МСВР: рассчитано для C40H39N7O4S2: 745.2505, найдено: 746.2575 [(М+Н)+ форма].
 7-бром-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 882)
7-бром-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 882)
Используя Общую методику 7, исходя из соединения Синтеза R3cy и соединения Синтеза R1d в качестве реагентов, получали Пример 882. МСВР: рассчитано для C35H36BrN7O4S: 729.1733, найдено: 730.1797 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 883)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 883)
Используя Общую методику 7, исходя из соединения Синтеза R3da и соединения Синтеза R1d в качестве реагентов, получали Пример 883. МСВР: рассчитано для C41H40N6O4S2: 744.2552, найдено: 745.2617 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 884)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 884)
Используя Общую методику 6, исходя из соединения Синтеза R3da и соединения Синтеза R1c в качестве реагентов, получали Пример 884. МСВР: рассчитано для C40H40N6O3S2: 716.2603, найдено: 717.2680 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 885)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 885)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 885. МСВР: рассчитано для C40H40N6O4S2: 732.2552, найдено: 733.2628 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперид ил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он (Пример 886)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперид ил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он (Пример 886)
Используя Общую методику 7, исходя из соединения Синтеза R3db и соединения Синтеза R1d в качестве реагентов, получали Пример 886. МСВР: рассчитано для C41H41N7O4S: 727.2941, найдено: 728.3012 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он (Пример 887)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он (Пример 887)
Используя Общую методику 6, исходя из соединения Синтеза R3db и соединения Синтеза R1c в качестве реагентов, получали Пример 887. МСВР: рассчитано для C40H41N7O3S: 699.2991, найдено: 700.3065 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он (Пример 888)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенил-5Н-пирроло[3,2-d]пиримидин-4-он (Пример 888)
Используя Общую методику 6, исходя из соединения Синтеза R3db и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 888. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 716.3013 [(М+Н)+ форма].
 7-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 889)
7-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 889)
Используя Общую методику 7, исходя из соединения Синтеза R3dc и соединения Синтеза R1d в качестве реагентов, получали Пример 889. МСВР: рассчитано для C35H35N6O4S2Cl: 702.185, найдено: 703.1921 [(М+Н)+ форма].
 7-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперид ил]метил]тиено[3,4-d]пиримидин-4-он (Пример 890)
7-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперид ил]метил]тиено[3,4-d]пиримидин-4-он (Пример 890)
Используя Общую методику 6, исходя из соединения Синтеза R3dc и соединения Синтеза R1c в качестве реагентов, получали Пример 890. МСВР: рассчитано для C34H35ClN6O3S2: 674.1901, найдено: 675.1992 [(М+Н)+ форма].
 6-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизоксазоло[4,5-d]пиримидин-7-он (Пример 891)
6-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизоксазоло[4,5-d]пиримидин-7-он (Пример 891)
Используя Общую методику 7, исходя из соединения Синтеза R3dd и соединения Синтеза R1d в качестве реагентов, получали Пример 891. МСВР: рассчитано для C40H39N7O5S: 729.2733, найдено: 730.2806 [(М+Н)+ форма].
 6-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизоксазоло[4,5-d]пиримидин-7-он (Пример 892)
6-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-3-фенилизоксазоло[4,5-d]пиримидин-7-он (Пример 892)
Используя Общую методику 6, исходя из соединения Синтеза R3dd и соединения Синтеза R1c в качестве реагентов, получали Пример 892. МСВР: рассчитано для C39H39N7O4S: 701.2784, найдено: 702.2878 [(М+Н)+ форма].
 5-[[1-[(3R,4R)-1-[(2-бромтиазол-5-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 893)
5-[[1-[(3R,4R)-1-[(2-бромтиазол-5-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 893)
Используя Общую методику 6, исходя из соединения Синтеза R3de и 2-бром-5-(бромметил)тиазола в качестве реагентов, получали Пример 893. МСВР: рассчитано для C34H36BrN7O4S: 717.1733, найдено: 718.1792 [(М+Н)+ форма].
 5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 894)
5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 894)
Используя Общую методику 6, исходя из соединения Синтеза R3de и соединения Синтеза R1c в качестве реагентов, получали Пример 894. МСВР: рассчитано для C40H42N8O4S: 730.305, найдено: 731.3146 [(М+Н)+ форма].
 5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 895)
5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метокси-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 895)
Используя Общую методику 6, исходя из соединения Синтеза R3de и 5-(хлорметил)-2-(6-метокси-3-пиридил)тиазола в качестве реагентов, получали Пример 895. МСВР: рассчитано для C40H42N8O5S: 746.2999, найдено: 747.3071 [(М+Н)+ форма].
 5-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 896)
5-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-1-(4-метоксифенил)пиразоло[3,4-d]пиримидин-4-он (Пример 896)
Используя Общую методику 7, исходя из соединения Синтеза R3de и соединения Синтеза R1d в качестве реагентов, получали Пример 896. МСВР: рассчитано для C41H42N8O5S: 758.2999, найдено: 759.3064 [(М+Н)+ форма].
 1-(2,3-дигидро-l,4-бензодиоксин-6-ил)-5-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиразоло[3,4-d]пиримидин-4-он (Пример 897)
1-(2,3-дигидро-l,4-бензодиоксин-6-ил)-5-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиразоло[3,4-d]пиримидин-4-он (Пример 897)
Используя Общую методику 7, исходя из соединения Синтеза R3df и соединения Синтеза R1d в качестве реагентов, получали Пример 897. МСВР: рассчитано для C42H42N8O6S: 786.2948, найдено: 787.3016 [(М+Н)+ форма].
 1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиразоло[3,4-d]пиримидин-4-он (Пример 898)
1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиразоло[3,4-d]пиримидин-4-он (Пример 898)
Используя Общую методику 6, исходя из соединения Синтеза R3df и соединения Синтеза R1c в качестве реагентов, получали Пример 898. МСВР: рассчитано для C41H42N8O5S: 758.2999, найдено: 759.3077 [(М+Н)+ форма].
 6-амино-3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 899)
6-амино-3-[[1-[(3R,4R)-1-бензил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 899)
Пример 830 (8 мг, 0.013 ммоль), имин бензофенона (18 мг, 0.1 ммоль), карбонат цезия (11.1 мг, 0.033 ммоль), 4,5-бис(дифенилфосфино)-9,9-диметилксантен (1.3 мг, 0.002 ммоль), трис(дибензилиденацетон)дипалладий(0) (1.1 мг, 0.001 ммоль) перемешивали в абс. толуоле (3 мл) при 110°С в течение 5 часов. Реакционную смесь упаривали, к остатку добавляли водный раствор HCl (1 н., 2 мл) и PDO (1 мл) и смесь перемешивали при к.т. в течение 3 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 899. МСВР: рассчитано для C32H36N6O3: 552.2849, найдено: 551.2818 [(М+Н)+ форма].
 6-амино-3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 900)
6-амино-3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 900)
Раствор Примера 852 (110 мг, 0.159 ммоль) в ТФУ (3 мл) перемешивали при 70°С в течение 90 минут, затем упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 900. МСВР: рассчитано для C32H35FN6O3: 570.2755, найдено: 286.1457 [(М+2Н)2+ форма].
 N-[3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(2-оксоиндолин-6-ил)ацетамид (Пример 901)
N-[3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(2-оксоиндолин-6-ил)ацетамид (Пример 901)
Используя Общую методику 7, исходя из Примера 900 в качестве аминного компонента и 2-(2-оксоиндолин-6-ил)уксусной кислоты в качестве реактанта - карбоновой кислоты, получали Пример 901. МСВР: рассчитано для C42H42FN7O5: 743.3231, найдено: 372.6692 [(М+2Н)2+ форма].
 N-[3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(3-гидроксифенил)ацетамид (Пример 902)
N-[3-[[1-[(3R,4R)-1-[(2-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(3-гидроксифенил)ацетамид (Пример 902)
Используя Общую методику 7, исходя из Примера 900 в качестве аминного компонента и 3-гидроксифенилуксусной кислоты в качестве реактанта - карбоновой кислоты, получали Пример 902. МСВР: рассчитано для C40H41FN6O5: 704.3122, найдено: 353.1636 [(М+2Н)2+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-[(4-метоксифенил)метиламино]пиридо[3,2-d]пиримидин-4-он (Пример 903)
3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-[(4-метоксифенил)метиламино]пиридо[3,2-d]пиримидин-4-он (Пример 903)
Пример 853 (320 мг, 0.468 ммоль) перемешивали в 4-метоксибензиламине (7 мл) при 100°С в течение 4 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 903. МСВР: рассчитано для C44H45N7O5S: 783.3203, найдено: 784.326 [(М+Н)+ форма].
 6-амино-3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 904)
6-амино-3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пиридо[3,2-d]пиримидин-4-он (Пример 904)
Раствор Примера 903 (159 мг, 0.203 ммоль) в ТФУ (3 мл) перемешивали при 70°С в течение 120 минут, затем упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 904. МСВР: рассчитано для C36H37N7O4S: 663.2628, найдено: 332.6401 [(М+2Н)2+ форма].
 N-[3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(2-оксоиндолин-6-ил)ацетамид (Пример 905)
N-[3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(2-оксоиндолин-6-ил)ацетамид (Пример 905)
Используя Общую методику 7, исходя из Примера 904 в качестве аминного компонента и 2-(2-оксоиндолин-6-ил)уксусной кислоты в качестве реактанта - карбоновой кислоты, получали Пример 905. МСВР: рассчитано для C46H44N8O6S: 836.3105, найдено: 837.3173 [(М+Н)+ форма].
 N-[3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(3-гидроксифенил)ацетамид (Пример 906)
N-[3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-(3-гидроксифенил)ацетамид (Пример 906)
Используя Общую методику 7, исходя из Примера 904 в качестве аминного компонента и 3-гидроксифенилуксусной кислоты в качестве реактанта - карбоновой кислоты, получали Пример 906. МСВР: рассчитано для C44H43N7O6S: 797.2996, найдено: 798.3073 [(М+Н)+ форма].
 N-[3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-фенилацетамид (Пример 907)
N-[3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-4-оксопиридо[3,2-d]пиримидин-6-ил]-2-фенилацетамид (Пример 907)
Используя Общую методику 7, исходя из Примера 904 в качестве аминного компонента и фенилуксусной кислоты в качестве реактанта - карбоновой кислоты, получали Пример 907. МСВР: рассчитано для C44H43N7O5S: 781.3046, найдено: 782.3136 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4-он (Пример 908)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4-он (Пример 908)
Используя Общую методику 9, исходя из Примера 879 в качестве реактанта и фенилбороновой кислоты в качестве реагента, получали Пример 908. МСВР: рассчитано для C40H41N7O3S: 699.2991, найдено: 700.3034 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4-он (Пример 909)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4-он (Пример 909)
Используя Общую методику 9, исходя из Примера 882 в качестве реактанта и фенилбороновой кислоты в качестве реагента, получали Пример 909. МСВР: рассчитано для C41H41N7O4S: 727.2941, найдено: 728.3013 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-5-метил-7-фенилпирроло[3,2-d]пиримидин-4-он (Пример 910)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-5-метил-7-фенилпирроло[3,2-d]пиримидин-4-он (Пример 910)
Суспензию Примера 886 (0.052 ммоль), йодметана (6.5 мкл, 0.104 ммоль) и K2CO3 (14.4 мг, 0.104 ммоль) в ДМФА (1 мл) перемешивали при к.т. в течение ночи. Реакционную смесь фильтровали через шприцевой фильтр и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 910. МСВР: рассчитано для C42H43N7O4S: 741.3098, найдено: 742.3171 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)тиено[3,4-d]пиримидин-4-он (Пример 911)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)тиено[3,4-d]пиримидин-4-он (Пример 911)
Используя Общую методику 9, исходя из Примера 890 и 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиррола в качестве реагентов, получали Пример 911. МСВР: рассчитано для C39H41N7O3S2: 719.2712, найдено: 718.2672 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)тиено[3,4-d]пиримидин-4-он (Пример 912)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)тиено[3,4-d]пиримидин-4-он (Пример 912)
Используя Общую методику 9, исходя из Примера 890 и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразола в качестве реагентов, получали Пример 912. МСВР: рассчитано для C38H40N8O3S2: 720.2665, найдено: 721.2703 [(М+Н)+ форма].
 7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 913)
7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 913)
Используя Общую методику 9, исходя из Примера 890 и 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана в качестве реагентов, получали Пример 913. МСВР: рассчитано для C38H38N6O4S2: 706.2396, найдено: 707.2448 [(М+Н)+ форма].
 7-[4-(гидроксиметил)фенил]-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 914)
7-[4-(гидроксиметил)фенил]-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 914)
Используя Общую методику 9, исходя из Примера 890 и [4-(гидроксиметил)фенил]бороновой кислоты в качестве реагентов, получали Пример 914. МСВР: рассчитано для C41H42N6O4S2: 746.2709, найдено: 747.2782 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 915)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 915)
Используя Общую методику 9, исходя из Примера 879 в качестве реактанта и 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиррола в качестве реагента, получали Пример 915. МСВР: рассчитано для C39H42N8O3S: 702.3101, найдено: 703.3187 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 916)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 916)
Используя Общую методику 9, исходя из Примера 879 в качестве реактанта и 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразол в качестве реагента - бороновой кислоты, получали Пример 916. МСВР: рассчитано для C38H41N9O3S: 703.3053, найдено: 704.3159 [(М+Н)+ форма].
 7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 917)
7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 917)
Используя Общую методику 9, исходя из Примера 879 в качестве реактанта и 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана в качестве реагента - бороновой кислоты, получали Пример 917. МСВР: рассчитано для C38H39N7O4S: 689.2784, найдено: 690.2875 [(М+Н)+ форма].
 7-(2-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 918)
7-(2-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 918)
Используя Общую методику 9, исходя из Примера 879 в качестве реактанта и 2-фурилбороновой кислоты в качестве реагента - бороновой кислоты, получали Пример 918. МСВР: рассчитано для C38H39N7O4S: 689.2784, найдено: 690.2865 [(М+Н)+ форма].
 7-[4-(гидроксиметил)фенил]-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 919)
7-[4-(гидроксиметил)фенил]-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 919)
Используя Общую методику 9, исходя из Примера 879 в качестве реактанта и [4-(гидроксиметил)фенил]бороновой кислоты в качестве реагента - бороновой кислоты, получали Пример 919. МСВР: рассчитано для C41H43N7O4S: 729.3098, найдено: 730.3161 [(М+Н)+ форма].
 6-хлор-7-(4-хлор-3-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 920)
6-хлор-7-(4-хлор-3-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 920)
Используя Общую методику 6, исходя из соединения Синтеза R3dg и соединения Синтеза R1c в качестве реагентов, получали Пример 920. МСВР: рассчитано для C40H38Cl2FN7O3S: 785.2118, найдено: 786.2163 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-метил-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 921)
3-[[4-гидрокси-1-[(3R,4R)-1-[[2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-метил-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 921)
Используя Общую методику 6, исходя из соединения Синтеза R3dh и соединения Синтеза R1c в качестве реагентов, получали Пример 921. МСВР: рассчитано для C41H43N7O3S: 713.3148, найдено: 714.3208 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-метилпиримидо[4,5-b]индол-4-он (Пример 922)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-9-метилпиримидо[4,5-b]индол-4-он (Пример 922)
Используя Общую методику 7, исходя из соединения Синтеза R3di и соединения Синтеза R1d в качестве реагентов, получали Пример 922. МСВР: рассчитано для C40H41N7O4S: 715.2941, найдено: 716.3047 [(М+Н)+ форма].
 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-6,8-диметилпиримидо[5',4':4,5]пирроло[1,2-b]пиридазин-4(3H)-он (Пример 923)
3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-6,8-диметилпиримидо[5',4':4,5]пирроло[1,2-b]пиридазин-4(3H)-он (Пример 923)
Используя Общую методику 7, исходя из соединения Синтеза R3dj и соединения Синтеза R1d в качестве реагентов, получали Пример 923. МСВР: рассчитано для C40H42N8O4S: 730.305, найдено: 731.3134 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-метил-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 924)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6-метил-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 924)
Используя Общую методику 7, исходя из соединения Синтеза R3dh и соединения Синтеза R1d в качестве реагентов, получали Пример 924. МСВР: рассчитано для C42H43N7O4S: 741.3098, найдено: 742.3179 [(М+Н)+ форма].
 6-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 925)
6-хлор-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 925)
Используя Общую методику 7, исходя из соединения Синтеза R3dk и соединения Синтеза R1d в качестве реагентов, получали Пример 925. МСВР: рассчитано для C41H40ClN7O4S: 761.2551, найдено: 762.2633 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[3-фтор-5-(2-метил-4-пиридил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-метил-6-(2-тиенил)пирроло[2,3-d]пиримидин-4-он (Пример 926)
3-[[1-[(3R,4R)-1-[3-фтор-5-(2-метил-4-пиридил)тиофен-2-карбонил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-метил-6-(2-тиенил)пирроло[2,3-d]пиримидин-4-он (Пример 926)
Используя Общую методику 9, исходя из соединения Синтеза R3dl в качестве галогенированного реактанта и 2-тиенилбороновой кислоты в качестве реагента - бороновой кислоты, получали 3-[(4-гидрокси-1-{[(3R,4R)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-6-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он. Это промежуточное соединение подвергали реакции с соединением Синтеза R1g в соответствии с Общей методикой 7, и сырое йод-соединение подвергали реакции в соответствии с Общей методикой 9 с (2-метил-4-пиридил)бороновой кислотой с получением Примера 926. МСВР: рассчитано для C40H39FN6O4S2: 750.2458, найдено: 751.2537 [(М+Н)+ форма].
 N-[[3-[[1-[(3R,4R)-1-[(3-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-4-оксо-7Н-пирроло[2,3-d]пиримидин-6-ил]метил]ацетамид (Пример 927)
N-[[3-[[1-[(3R,4R)-1-[(3-фторфенил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-4-оксо-7Н-пирроло[2,3-d]пиримидин-6-ил]метил]ацетамид (Пример 927)
2-[(4-хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (3.5 г, 12.3 ммоль) растворяли в абс. ТГФ (55 мл) и охлаждали до -78°С, затем к смеси добавляли LDA (2.0 М, 6.8 мл, 13.6 ммоль) и перемешивали при -78°С в течение 40 минут, затем к смеси добавляли йод (3.13 г, 12.3 ммоль), и перемешивание продолжали при -78°С в течение 3 часов. К реакционной смеси добавляли воду (25 мл) и экстрагировали с помощью ЕЕО (2 × 30 мл). Объединенные органические слои упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, градиент).
Часть сырого продукта (2.38 г, 5.81 ммоль) и гидрат гидроксида лития (2.44 г, 58.1 ммоль) растворяли в смеси PDO и воды (30 мл, об./об. = 1:1) и перемешивали при 100°С в течение 70 часов. Реакционную смесь подкисляли 1 н. водным раствором HCl. Полученное в результате твердое соединение отфильтровывали, промывали водой и сушили.
Пиримидоновый продукт подвергали реакции, используя Общую методику 5, с соединением Синтеза R1e в качестве эпоксидного компонента.
Сырой продукт (3.5 г, 5.79 ммоль), цианид меди(I) (2.18 г, 24.32 ммоль), цианид тетраэтиламмония (950 мг, 6.08 ммоль), трис(дибензилиденацетон)дипалладий(0) (531 мг, 0.58 ммоль), и 1,1'-бис(дифенилфосфино)ферроцен (1.29 г, 2.32 ммоль) растворяли в абс. PDO (45 мл) и смесь перемешивали при 110°С в течение 2.3 ч. Реакционную смесь фильтровали, фильтрат упаривали, остаток разбавляли МеОН (15 мл) и затем снова фильтровали. Фильтрат упаривали, наносили на целит и очищали с помощью флэш-хроматографии (ДХМ-МеОН, градиент).
Полученный в результате Вос-защищенный циано-продукт (2.42 г, 4.81 ммоль) лишали защиты путем перемешивания в смеси ТФУ (1.11 мл, 14.47 ммоль), муравьиной кислоты (6.29 мл, 166.6 ммоль) и ДХМ (60 мл) при к.т. в течение 52 часов. К реакционной смеси добавляли K2CO3 (25 г) и ДХМ (180 мл) и экстрагировали водой (2×160 мл). Органический слой упаривали.
Сырой пиперидиновый продукт подвергали реакции с (3R,4R)-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновой кислотой, используя Общую методику 7.
Полученный в результате Вос-защищенный продукт (798 мг, 1.16 ммоль) лишали защиты путем перемешивания в смеси ТФУ (266 мкл, 3.48 ммоль), муравьиной кислоты (503 мкл, 13.3 ммоль) и ДХМ (15 мл) при к.т. в течение 164 часов. К реакционной смеси добавляли K2CO3 (2.8 г) и экстрагировали водой (2×75 мл). Органический слой упаривали.
Сырой пиперидиновый продукт подвергали реакции с 3-фторбензилхлоридом в соответствии с Общей методикой 6.
Полученный в результате сырой продукт (534 мг, 0.76 ммоль) и никель Ренея (240 мг) перемешивали в растворе аммиака в метаноле (7 М, 15 мл) в атмосфере водорода (2 бар) в течение 68 часов. Реакционную смесь фильтровали, фильтрат упаривали.
Сырой аминометильный продукт подвергали реакции с уксусной кислоты в соответствии с Общей методикой 7.
Полученный в результате продукт (85.7 мг, 0.115 ммоль) перемешивали в растворе TBAF (1 M в ТГФ, 223 мкл, 0.223 ммоль) и ТГФ (0.5 мл) при 75°С в течение 65 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 927. МСВР: рассчитано для C34H39FN6O4: 614.3017, найдено: 615.3082 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(n-толилметил)пиперидин-4-карбонил]-4-пиперидил]метил]-6-(2-тиенил)-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 928)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(n-толилметил)пиперидин-4-карбонил]-4-пиперидил]метил]-6-(2-тиенил)-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 928)
2-[(4-хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (3.5 г, 12.3 ммоль) растворяли в ТГФ (абс, 55 мл) и охлаждали до -78°С, затем к смеси добавляли LDA (2.0 М, 6.8 мл, 13.6 ммоль) и перемешивали при -78°С в течение 40 минут, затем к смеси добавляли йод (3.13 г, 12.3 ммоль) и продолжали перемешивание при -78°С в течение 3 часов. К реакционной смеси добавляли воду (25 мл) и экстрагировали с помощью ЕЕО (2×30 мл). Объединенные органические слои упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, градиент).
Часть сырого продукта (2.0 г, 4.88 ммоль) и гидрат гидроксида лития (2.05 г, 48.8 ммоль) растворяли в смеси PDO и воды (30 мл, об./об. = 1:1) и перемешивали при 100°С в течение 65 часов. Реакционную смесь подкисляли 1 н. водным раствором HCl. Полученное в результате твердое соединение отфильтровывали, промывали водой и сушили.
Пиримидоновый продукт подвергали реакции, используя Общую методику 5, с соединением Синтеза R1e в качестве эпоксидного компонента.
Полученный в результате Вос-защищенный продукт (930 мг, 1.54 ммоль) лишали защиты путем перемешивания в смеси ТФУ (363 мкл, 4.74 ммоль), муравьиной кислоты (2.06 мл, 54.6 ммоль) и ДХМ (18.6 мл) при к.т. в течение 46 часов. К реакционной смеси добавляли K2CO3 (6.5 г) и экстрагировали водой (2×80 мл). Органические слои упаривали и остаток растирали с водой (5 мл) с получением твердого соединения, которое отфильтровывали и сушили.
Сырой пиперидиновый продукт подвергали реакции с (3R,4R)-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновой кислотой, используя Общую методику 7.
Сырой Вос-защищенный продукт (647 мг, 0.82 ммоль) лишали защиты путем перемешивания в смеси ТФУ (188 мкл, 2.46 ммоль), муравьиной кислоты (356 мкл, 9.43 ммоль) и ДХМ (13 мл) при к.т. в течение 214 часов. К реакционной смеси добавляли K2CO3 (1.99 г). Раствор экстрагировали водой (2×70 мл) и органический слой упаривали.
Сырой продукт N-алкилировали 4-метилбензилхлоридом в соответствии с Общей методикой 6.
Сырое алкилированное соединение (165 мг, 0.21 ммоль), 2-тиенилбороновую кислоту (41 мг, 0.32 ммоль), хлорид лития (27 мг, 0.63 ммоль) и [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (15 мг, 0.021 ммоль) растворяли в водном растворе Na2CO3 (2 М, 265 мкл, 0.53 ммоль), толуоле (4 мл) и EtOH (4 мл) и перемешивали при 80°С в течение 23 часов. Нерастворимую часть отфильтровывали, фильтрат упаривали и остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 25 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате продукт (72 мг, 0.096 ммоль) перемешивали в растворе TBAF (1 M в ТГФ, 144 мкл, 0.144 ммоль) и ТГФ (0.5 мл) при 75°С в течение 65 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 928. МСВР: рассчитано для C36H39N5O3S: 621.2773, найдено: 622.2846 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(n-толилметил)пиперидин-4-карбонил]-4-пиперидил]метил]-6-(3-тиенил)-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 929)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(n-толилметил)пиперидин-4-карбонил]-4-пиперидил]метил]-6-(3-тиенил)-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 929)
2-[(4-Хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (3.5 г, 12.3 ммоль) растворяли в ТГФ (абс, 55 мл) и охлаждали до -78°С, затем к смеси добавляли LDA (2.0 М, 6.8 мл, 13.6 ммоль) и перемешивали при -78°С в течение 40 минут, затем к смеси добавляли йод (3.13 г, 12.3 ммоль) и продолжали перемешивание при -78°С в течение 3 часов. К реакционной смеси добавляли воду (25 мл) и экстрагировали с помощью ЕЕО (2×30 мл). Объединенные органические слои упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, градиент).
Часть сырого продукта (2.0 г, 4.88 ммоль) и гидрат гидроксида лития (2.05 г, 48.8 ммоль) растворяли в смеси PDO и воды (30 мл, об./об. = 1:1) и перемешивали при 100°С в течение 65 часов. Реакционную смесь подкисляли 1 н. водным раствором HCl. Полученное в результате твердое соединение отфильтровывали, промывали водой и сушили.
Пиримидоновый продукт подвергали реакции, используя Общую методику 5, с соединением Синтеза R1e в качестве эпоксидного компонента.
Полученный в результате Вос-защищенный продукт (930 мг, 1.54 ммоль) лишали защиты путем перемешивания в смеси ТФУ (363 мкл, 4.74 ммоль), муравьиной кислоты (2.06 мл, 54.6 ммоль) и ДХМ (18.6 мл) при к.т.в течение 46 часов. К реакционной смеси добавляли K2CO3 (6.5 г) и экстрагировали водой (2×80 мл). Органические слои упаривали и остаток растирали с водой (5 мл) с получением твердого соединения, которое отфильтровывали и сушили.
Сырой пиперидиновый продукт подвергали реакции с (3R,4R)-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновой кислотой, используя Общую методику 7.
Сырой Вос-защищенный продукт (647 мг, 0.82 ммоль) лишали защиты путем перемешивания в смеси ТФУ (188 мкл, 2.46 ммоль), муравьиной кислоты (356 мкл, 9.43 ммоль) и ДХМ (13 мл) при к.т. в течение 214 часов. К реакционной смеси добавляли K2CO3 (1.99 г). Раствор экстрагировали водой (2×70 мл) и органический слой упаривали.
Сырой продукт N-алкилировали 4-метилбензилхлоридом в соответствии с Общей методикой 6.
Сырое алкилированное соединение (170 мг, 0.21 ммоль), 4,4,5,5-тетраметил-2-(3-тиенил)-1,3,2-диоксаборолан (67 мг, 0.32 ммоль), хлорид лития (27 мг, 0.63 ммоль) и [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (15 мг, 0.021 ммоль) растворяли в водном растворе Na2CO3 (2 М, 265 мкл, 0.53 ммоль), толуоле (4 мл) и EtOH (4 мл) и перемешивали при 80°С в течение 23 часов. Нерастворимую часть отфильтровывали, фильтрат упаривали и остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате продукт (72 мг, 0.096 ммоль) перемешивали в растворе TBAF (1 M в ТГФ, 144 мкл, 0.144 ммоль) и ТГФ (0.5 мл) при 75°С в течение 60 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 929. МСВР: рассчитано для C36H39N5O3S: 621.2773, найдено: 622.2834 [(М+Н)+ форма].
 6-(2-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(n-толилметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 930)
6-(2-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(n-толилметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 930)
2-[(4-Хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (3.5 г, 12.3 ммоль) растворяли в ТГФ (абс, 55 мл) и охлаждали до -78°С, затем к смеси добавляли LDA (2.0 М, 6.8 мл, 13.6 ммоль) и перемешивали при -78°С в течение 40 минут, затем к смеси добавляли йод (3.13 г, 12.3 ммоль) и продолжали перемешивание при -78°С в течение 3 часов. К реакционной смеси добавляли воду (25 мл) и экстрагировали с помощью ЕЕО (2×30 мл). Объединенные органические слои упаривали, наносили на целит и очищали с помощью флэш-хроматографии (гептан-ЕЕО, градиент).
Часть сырого продукта (2.0 г, 4.88 ммоль) и гидрат гидроксида лития (2.05 г, 48.8 ммоль) растворяли в смеси PDO и воды (30 мл, об./об. = 1:1) и перемешивали при 100°С в течение 65 часов. Реакционную смесь подкисляли 1 н. водным раствором HCl. Полученное в результате твердое соединение отфильтровывали, промывали водой и сушили.
Пиримидоновый продукт подвергали реакции, используя Общую методику 5, с соединением Синтеза R1e в качестве эпоксидного компонента.
Полученный в результате Вос-защищенный продукт (930 мг, 1.54 ммоль) лишали защиты путем перемешивания в смеси ТФУ (363 мкл, 4.74 ммоль), муравьиной кислоты (2.06 мл, 54.6 ммоль) и ДХМ (18.6 мл) при к.т. в течение 46 часов. К реакционной смеси добавляли K2CO3 (6.5 г) и экстрагировали водой (2×80 мл). Органические слои упаривали и остаток растирали с водой (5 мл) с получением твердого соединения, которое отфильтровывали и сушили.
Сырой пиперидиновый продукт подвергали реакции с (3R,4R)-1-трет-бутоксикарбонил-3-фенилпиперидин-4-карбоновой кислотой, используя Общую методику 7.
Сырой Вос-защищенный продукт (647 мг, 0.82 ммоль) лишали защиты путем перемешивания в смеси ТФУ (188 мкл, 2.46 ммоль), муравьиной кислоты (356 мкл, 9.43 ммоль) и ДХМ (13 мл) при к.т.в течение 214 часов. К реакционной смеси добавляли K2CO3 (1.99 г). Раствор экстрагировали водой (2×70 мл) и органический слой упаривали.
Сырой продукт N-алкилировали 4-метилбензилхлоридом в соответствии с Общей методикой 6.
Сырое алкилированное соединение (170 мг, 0.21 ммоль), 2-фторфенилбороновую кислоту (44 мг, 0.32 ммоль), хлорид лития (27 мг, 0.63 ммоль) и [1,1'-бис(дифенилфосфино)ферроцен]дихлорпалладий(II) (15 мг, 0.021 ммоль) растворяли в водном растворе Na2CO3 (2 М, 265 мкл, 0.53 ммоль), толуоле (4 мл) и EtOH (4 мл) и перемешивали при 80°С в течение 22 часов. Нерастворимую часть отфильтровывали, фильтрат упаривали и остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Полученный в результате продукт (70 мг, 0.09 ммоль) перемешивали в растворе TBAF (1 M в ТГФ, 138 мкл, 0.138 ммоль) и ТГФ (0.5 мл) при 75°С в течение 60 часов. Реакционную смесь очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 5 мМ водный NH4HCO3-MeCN, градиент) с получением Примера 930. МСВР: рассчитано для C38H40FN5O3: 633.3115, найдено: 634.3194 [(М+Н)+ форма].
 5-фтор-3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-метилпирроло[2,3-d]пиримидин-4-он (Пример 931)
5-фтор-3-[[4-гидрокси-1-[(3R,4R)-1-(4-метил-2-фенилтиазол-5-карбонил)-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-метилпирроло[2,3-d]пиримидин-4-он (Пример 931)
Используя Общую методику 11, исходя из соединения Синтеза R2dj и (4-метил-2-фенил-1,3-тиазол-5-ил)[(3R,4R)-4-(1-окса-6-азаспиро[2.5]окт-6-илкарбонил)-3-фенилпиперидин-1-ил]метанона в качестве реагентов, получали Пример 931. МСВР: рассчитано для C36H37FN6O4S: 668.2581, найдено: 669.2649 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7,8-дигидро-6Н-пиримидо[5,4-b]пирролизин-4-он (Пример 932)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7,8-дигидро-6Н-пиримидо[5,4-b]пирролизин-4-он (Пример 932)
Используя Общую методику 11, исходя из соединения Синтеза R2dk и соединения Синтеза R1m в качестве реагентов, получали Пример 932. МСВР: рассчитано для C38H41N7O4S: 691.2941, найдено: 346.6539 [М+2Н)2+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6,7,8,9-тетрагидропиримидо[5,4-b]индолизин-4-он (Пример 933)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-6,7,8,9-тетрагидропиримидо[5,4-b]индолизин-4-он (Пример 933)
Используя Общую методику 11, исходя из соединения Синтеза R2dl и соединения Синтеза R1m в качестве реагентов, получали Пример 933. МСВР: рассчитано для C39H43N7O4S: 705.3098, найдено: 706.3172 [(М+Н)+ форма].
 3-[[1-[(3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 934)
3-[[1-[(3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 934)
Используя Общую методику 5, исходили из 3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-она и соединения Синтеза R1e в качестве эпоксидного компонента, сырой продукт подвергали реакции с соединением Синтеза R1q-(3R,4S) в соответствии с Общей методикой 7 с получением Примера 934. МСВР: рассчитано для C29H33N5O3S: 531.2304, найдено: 532.2388 [(М+Н)+ форма].
 3-[[1-[(3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 935)
3-[[1-[(3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 935)
Используя Общую методику 5, исходили из 3Н,4Н,7Н-пирроло[2,3-d]пиримидин-4-она и соединения Синтеза R1e в качестве эпоксидного компонента, сырой продукт подвергали реакции с соединением Синтеза R1q-(3S,4R) в соответствии с Общей методикой 7 с получением Примера 935. МСВР: рассчитано для C29H33N5O3S: 531.2304, найдено: 532.2388 [(М+Н)+ форма].
 3-[[1-[(3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-метил-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 936)
3-[[1-[(3R,4S)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-метил-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 936)
2-[(4-Хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (600 мг, 2.11 ммоль) растворяли в абс. ТГФ (12 мл) и охлаждали до -78°С, затем к смеси добавляли раствор LDA (2.0 М, 1.2 мл, 2.4 ммоль) и перемешивали при -78°С в течение 1 часа, затем к смеси добавляли йодметан (158 мкл, 2.53 ммоль), и перемешивание продолжали при -78°С в течение 3 часов. К реакционной смеси добавляли воду (10 мл) и экстрагировали с помощью ЕЕО (2×20 мл). Объединенные органические слои упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Часть сырого продукта (300 мг, 1.01 ммоль) и гидрат гидроксида лития (423 мг, 10.1 ммоль) растворяли в смеси PDO и воды (4 мл, об./об. = 1:1) и перемешивали при 100°С в течение 142 часов. Реакционную смесь подкисляли водным раствором HCl (1 н., 9.5 мл). Полученное в результате твердое соединение отфильтровывали, промывали водой и сушили.
Используя Общую методику 5, исходили из сырого продукта и соединения Синтеза R1e в качестве эпоксидного компонента, полученный в результате продукт (140 мг, 0.28 ммоль) затем перемешивали в растворе TBAF (1 M в ТГФ, 1.4 мл, 1.4 ммоль) при 90°С в течение 24 часов. К реакционной смеси добавляли воду (5 мл) и экстрагировали с помощью ЕЕО (2×10 мл). Объединенные органические слои экстрагировали водой (2×10 мл), сушили над MgSO4 и упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 25 мМ водный NH4HCO3-MeCN, ISO39).
Полученный в результате десилилилированный продукт (23.5 мг, 0.065 ммоль) перемешивали в смеси водного раствора HCl (0.65 мл) и PDO (0.5 мл) при 60°С в течение 4 часов. Реакционную смесь упаривали.
Сырой продукт подвергали реакции с соединением Синтеза R1q-(3R,4S) в соответствии с Общей методикой 7 с получением Примера 936. МСВР: рассчитано для C30H35N5O3S: 545.2460, найдено: 546.2546 [(М+Н)+ форма].
 3-[[1-[(3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-метил-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 937)
3-[[1-[(3S,4R)-1-бензил-3-(2-тиенил)пиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-6-метил-7Н-пирроло[2,3-d]пиримидин-4-он (Пример 937)
2-[(4-Хлорпирроло[2,3-d]пиримидин-7-ил)метокси]этилтриметилсилан (600 мг, 2.11 ммоль) растворяли в абс. ТГФ (12 мл) и охлаждали до -78°С, затем к смеси добавляли LDA (2.0 М, 1.2 мл, 2.4 ммоль) и перемешивали при -78°С в течение 1 часа, затем к смеси добавляли йодметан (158 мкл, 2.53 ммоль), и перемешивание продолжали при -78°С в течение 3 часов. К реакционной смеси добавляли воду (10 мл) и экстрагировали с помощью ЕЕО (2×20 мл).
Объединенные органические слои упаривали и очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 5 мкм, 5 мМ водный NH4HCO3-MeCN, градиент).
Часть сырого продукта (300 мг, 1.01 ммоль) и гидрат гидроксида лития (423 мг, 10.1 ммоль) растворяли в смеси PDO и воды (4 мл, об./об. = 1:1) и перемешивали при 100°С в течение 142 часов. Реакционную смесь подкисляли водным раствором HCl (1 н., 9.5 мл) Полученное в результате твердое соединение отфильтровывали, промывали водой и сушили.
Используя Общую методику 5, исходили из сырого продукта и соединения Синтеза R1e в качестве эпоксидного компонента, полученный в результате продукт (140 мг, 0.28 ммоль) затем перемешивали в растворе TBAF (1 M в ТГФ, 1.4 мл, 1.4 ммоль) при 90°С в течение 24 часов. К реакционной смеси добавляли воду (5 мл) и экстрагировали с помощью ЕЕО (2×10 мл). Объединенные органические слои экстрагировали водой (2×10 мл), сушили над MgSO4 и упаривали. Остаток очищали с помощью препаративной ЖХ (на колонке С-18 Gemini-NX 10 мкм, 25 мМ водный NH4HCO3-MeCN, ISO39).
Полученный в результате десилилилированный продукт (23.5 мг, 0.065 ммоль) перемешивали в смеси водного раствора HCl (0.65 мл) и PDO (0.5 мл) при 60°С в течение 4 часов. Реакционную смесь упаривали.
Сырой продукт подвергали реакции с соединением Синтеза R1q-(3S,4R) в соответствии с Общей методикой 7 с получением Примера 937. МСВР: рассчитано для C30H35N5O3S: 545.246, найдено: 546.2527 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 938)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 938)
Используя Общую методику 7, исходили из соединения Синтеза R3cy и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 938. МСВР: рассчитано для C39H41N9O4S: 731.3002, найдено: 732.3057 [(М+Н)+ форма].
 7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 939)
7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 939)
Используя Общую методику 7, исходили из соединения Синтеза R3cy и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 939. МСВР: рассчитано для C39H39N7O5S: 717.2734, найдено: 718.2804 [(М+Н)+ форма].
 7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 940)
7-(3-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 940)
Используя Общую методику 7, исходили из соединения Синтеза R3dc и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-(3-фурил)-4,4,5,5-тетраметил-1,3,2-диоксабороланом в соответствии с Общей методикой 9 с получением Примера 940. МСВР: рассчитано для C39H38N6O5S2: 734.2345, найдено: 735.2417 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)тиено[3,4-d]пиримидин-4-он (Пример 941)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиразол-4-ил)тиено[3,4-d]пиримидин-4-он (Пример 941)
Используя Общую методику 7, исходили из соединения Синтеза R3dc и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 941. МСВР: рассчитано для C39H40N8O4S2: 748.2614, найдено: 749.2704 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 942)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 942)
Используя Общую методику 7, исходили из соединения Синтеза R3cy и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с [4-(гидроксиметил)фенил]бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 942. МСВР: рассчитано для C42H43N7O5S: 757.3046, найдено: 758.3135 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]тиено[3,4-d]пиримидин-4-он (Пример 943)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]тиено[3,4-d]пиримидин-4-он (Пример 943)
Используя Общую методику 7, исходили из соединения Синтеза R3dc и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с [4-(гидроксиметил)фенил]бороновой кислотой в соответствии с Общей методикой 9 с получением Примера 943. МСВР: рассчитано для C42H42N6O5S2: 774.2658, найдено: 775.2733 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 944)
3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 944)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и соединения Синтеза R1x в качестве реагентов, получали Пример 944. МСВР: рассчитано для C40H39N7O4S: 713.2784, найдено: 714.2859 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 945)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 945)
Используя Общую методику 7, исходили из соединения Синтеза R3cy и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пирролом в соответствии с Общей методикой 9 с получением Примера 945. МСВР: рассчитано для C40H42N8O4S: 730.3050, найдено: 731.3113 [(М+Н)+ форма].
 7-(3-хлорфенил)-3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 946)
7-(3-хлорфенил)-3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 946)
Используя Общую методику 7, исходя из соединения Синтеза R3ar и соединения Синтеза R1x в качестве реагентов, получали Пример 946. МСВР: рассчитано для C40H38N7O4SCl: 747.2395, найдено: 748.2461 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(3-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 947)
3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(3-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 947)
Используя Общую методику 7, исходя из соединения Синтеза R3bo и соединения Синтеза R1x в качестве реагентов, получали Пример 947. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2968 [(М+Н)+ форма].
 7-(4-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 948)
7-(4-фторфенил)-3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 948)
Используя Общую методику 7, исходя из соединения Синтеза R3as и соединения Синтеза R1x в качестве реагентов, получали Пример 948. МСВР: рассчитано для C40H38N7O4FS: 731.2690, найдено: 732.2765 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 949)
3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 949)
Используя Общую методику 7, исходя из соединения Синтеза R3ax и соединения Синтеза R1x в качестве реагентов, получали Пример 949. МСВР: рассчитано для C41H41N7O5S: 743.2890, найдено: 744.2951 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метокси-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 950)
3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метокси-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 950)
Этил 2-(6-метокси-3-пиридил)тиазол-5-карбоксилат (0.75 ммоль) перемешивали с гидратом гидроксида лития (3 ммоль) в смести воды (2 мл) и метанола (2 мл) при 40°С в течение 4 часов. Реакционную смесь нейтрализовали 1 н. водным раствором HCl (3 мл), затем упаривали. Полученную в результате сырую 2-(6-метокси-3-пиридил)тиазол-5-карбоновую кислоту подвергали реакции с соединением Синтеза R3ax в соответствии с Общей методикой 7 с получением Примера 950. МСВР: рассчитано для C41H41N7O6S: 759.2839, найдено: 760.2908 [(М+Н)+ форма].
 7-(2-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 951)
7-(2-фурил)-3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 951)
Используя Общую методику 7, исходили из соединения Синтеза R3cy и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 2-фурилбороновой кислотой в соответствии с Общей методикой 9 с получением Примера 951. МСВР: рассчитано для C39H39N7O5S: 717.2734, найдено: 718.2801 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)тиено[3,4-d]пиримидин-4-он (Пример 952)
3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(1-метилпиррол-3-ил)тиено[3,4-d]пиримидин-4-он (Пример 952)
Используя Общую методику 7, исходили из соединения Синтеза R3dc и соединения Синтеза R1d в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пирролом в соответствии с Общей методикой 9 с получением Примера 952. МСВР: рассчитано для C40H41N7O4S2: 747.2661, найдено: 748.2722 [(М+Н)+ форма].
 3-[[3,3-дифтор-4-гидрокси-1-[транс-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он, энантиомер 1 (Пример 953)
3-[[3,3-дифтор-4-гидрокси-1-[транс-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он, энантиомер 1 (Пример 953)
и
3-[[3,3-дифтор-4-гидрокси-1-[транс-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он, энантиомер 2 (Пример 954)
Используя Общую методику 7, исходя из соединения Синтеза R3dm и соединения Синтеза R1d в качестве реагентов, получали Пример 953 и Пример 954 и их разделяли с помощью жидкостной хроматографии.
Пример 953: МСВР: рассчитано для C41H39N7O4F2S: 763.2752, найдено: 382.6463 [(М+2Н)2+ форма].
Пример 954: МСВР: рассчитано для C41H39N7O4F2S: 763.2752, найдено: 382.6463 [(М+2Н)2+ форма].
 3-[[3,3-дифтор-4-гидрокси-1-[транс-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он, энантиомер 1 (Пример 955)
3-[[3,3-дифтор-4-гидрокси-1-[транс-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он, энантиомер 1 (Пример 955)
и
3-[[3,3-дифтор-4-гидрокси-1-[транс-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он, энантиомер 2 (Пример 956)
Используя Общую методику 7, исходя из соединения Синтеза R3dn и соединения Синтеза R1d в качестве реагентов, получали Пример 955 и Пример 956 и разделяли их с помощью жидкостной хроматографии.
Пример 955: МСВР: рассчитано для C42H41N7O5F2S: 793.2858, найдено: 794.2910 [(М+Н)+ форма].
Пример 956: МСВР: рассчитано для C42H41N7O5F2S: 793.2858, найдено: 794.2960 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[4-метил-2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 957)
3-[[4-гидрокси-1-[(3R,4R)-1-[[4-метил-2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 957)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 5-(хлорметил)-4-метил-2-(6-метил-3-пиридил)тиазола в качестве реагентов, получали Пример 957. МСВР: рассчитано для C41H43N7O3S: 713.3148, найдено: 714.3215 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[[4-метил-2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 958)
3-[[4-гидрокси-1-[(3R,4R)-1-[[4-метил-2-(6-метил-3-пиридил)тиазол-5-ил]метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 958)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 5-(хлорметил)-4-метил-2-(6-метил-3-пиридил)тиазола в качестве реагентов, получали Пример 958. МСВР: рассчитано для C42H45N7O4S: 743.3254, найдено: 744.3323 [(М+Н)+ форма].
 7-(3,5-диметоксифенил)-3-[[4-гидрокси-1-[(3S,4S)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 959)
7-(3,5-диметоксифенил)-3-[[4-гидрокси-1-[(3S,4S)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,3-d]пиримидин-4-он (Пример 959)
Используя Общую методику 7, исходя из соединения Синтеза R3af и соединения Синтеза R1d в качестве реагентов, получали Пример 959. МСВР: рассчитано для C43H45N7O6S: 787.3152, найдено: 788.3226 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-4-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 960)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-4-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 960)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)пиримидина в качестве реагентов, получали Пример 960. МСВР: рассчитано для C35H37N7O3: 603.2958, найдено: 604.2303 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-4-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 961)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-4-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 961)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)пиримидина в качестве реагентов, получали Пример 961. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3140 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло [2,3-d]пиримидин-4-он (Пример 962)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло [2,3-d]пиримидин-4-он (Пример 962)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)-2-метоксипиримидина в качестве реагентов, получали Пример 962. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3126 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 963)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 963)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)-2-метоксипиримидина в качестве реагентов, получали Пример 963. МСВР: рассчитано для C37H41N7O5: 663.3169, найдено: 664.3251 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(3-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 964)
3-[[1-[(3R,4R)-1-(3-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 964)
Используя Общую методику 8, исходя из соединения Синтеза R3bu и 3-фторбензолсульфонилхлорида в качестве реагентов, получали Пример 964. МСВР: рассчитано для C36H36N5O5FS: 669.2421, найдено: 670.2489 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(3-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 965)
3-[[1-[(3R,4R)-1-(3-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 965)
Используя Общую методику 8, исходя из соединения Синтеза R3ax и 3-фторбензолсульфонилхлорида в качестве реагентов, получали Пример 965. МСВР: рассчитано для C37H38N5O6FS: 699.2527, найдено: 700.2596 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(2-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 966)
3-[[1-[(3R,4R)-1-(2-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 966)
Используя Общую методику 8, исходя из соединения Синтеза R3bu и 2-фторбензолсульфонилхлорида в качестве реагентов, получали Пример 966. МСВР: рассчитано для C36H36N5O5FS: 669.2421, найдено: 670.2492 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(2-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 967)
3-[[1-[(3R,4R)-1-(2-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 967)
Используя Общую методику 8, исходя из соединения Синтеза R3ax и 2-фторбензолсульфонилхлорида в качестве реагентов, получали Пример 967. МСВР: рассчитано для C37H38N5O6FS: 699.2527, найдено: 700.2598 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(4-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 968)
3-[[1-[(3R,4R)-1-(4-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 968)
Используя Общую методику 8, исходя из соединения Синтеза R3bu и 4-фторбензолсульфонилхлорида в качестве реагентов, получали Пример 968. МСВР: рассчитано для C36H36N5O5FS: 669.2421, найдено: 670.2494 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-(4-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 969)
3-[[1-[(3R,4R)-1-(4-фторфенил)сульфонил-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 969)
Используя Общую методику 8, исходя из соединения Синтеза R3ax и 4-фторбензолсульфонилхлорида в качестве реагентов, получали Пример 969. МСВР: рассчитано для C37H38N5O6FS: 699.2527, найдено: 700.2598 [(М+Н)+ форма].
 7-бром-3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 970)
7-бром-3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]пирроло[2,1-f][1,2,4]триазин-4-он (Пример 970)
Используя Общую методику 6, исходя из соединения Синтеза R3cy и 2-(хлорметил)пиразина в качестве реагентов, получали Пример 970. МСВР: рассчитано для C29H32N7O3Br: 605.1750, найдено: 606.1826 [(М+Н)+ форма].
 7-хлор-3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 971)
7-хлор-3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]тиено[3,4-d]пиримидин-4-он (Пример 971)
Используя Общую методику 6, исходя из соединения Синтеза R3dc и 2-(хлорметил)пиразина в качестве реагентов, получали Пример 971. МСВР: рассчитано для C29H31N6O3SCl: 578.1867, найдено: 579.1947 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 972)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 972)
Используя Общую методику 7, исходя из соединения Синтеза R3bu и пиразин-2-карбоновой кислоты в качестве реагентов, получали Пример 972. МСВР: рассчитано для C35H35N7O4: 617.2751, найдено: 618.2826 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 973)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-карбонил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 973)
Используя Общую методику 7, исходя из соединения Синтеза R3ax и пиразин-2-карбоновой кислоты в качестве реагентов, получали Пример 973. МСВР: рассчитано для C36H37N7O5: 647.2856, найдено: 648.2931 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил] метил]-7-фенилпирроло [2,3-d] пиримидин-4-он (Пример 974)
3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил] метил]-7-фенилпирроло [2,3-d] пиримидин-4-он (Пример 974)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-6-метилпиразина в качестве реагентов, получали Пример 974. МСВР: рассчитано для C36H39N7O3: 617.3114, найдено: 618.3178 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 975)
3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 975)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-6-метилпиразина в качестве реагентов, получали Пример 975. МСВР: рассчитано для C37H41N7O4: 647.3220, найдено: 648.3285 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(4,6-диметилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 976)
3-[[1-[(3R,4R)-1-[(4,6-диметилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 976)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-4,6-диметилпиримидина в качестве реагентов, получали Пример 976. МСВР: рассчитано для C37H41N7O3: 631.3271, найдено: 632.3338 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(4,6-диметилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 977)
3-[[1-[(3R,4R)-1-[(4,6-диметилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 977)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-4,6-диметилпиримидина в качестве реагентов, получали Пример 977. МСВР: рассчитано для C38H43N7O4: 661.3377, найдено: 662.3424 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4-он (Пример 978)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4-он (Пример 978)
Используя Общую методику 9, исходя из Примера 970 и фенилбороновой кислоты в качестве реагентов, получали Пример 978. МСВР: рассчитано для C35H37N7O3: 603.2958, найдено: 604.3022 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 979)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,1-f][1,2,4]триазин-4-он (Пример 979)
Используя Общую методику 9, исходя из Примера 970 и (4-метоксифенил)бороновой кислоты в качестве реагентов, получали Пример 979. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3127 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-ил метил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 980)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-ил метил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 980)
Используя Общую методику 9, исходя из Примера 971 и фенилбороновой кислоты в качестве реагентов, получали Пример 980. МСВР: рассчитано для C35H36N6O3S: 620.2570, найдено: 621.2627 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)тиено[3,4-d]пиримидин-4-он (Пример 981)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)тиено[3,4-d]пиримидин-4-он (Пример 981)
Используя Общую методику 9, исходя из Примера 971 и (4-метоксифенил)бороновой кислоты в качестве реагентов, получали Пример 981. МСВР: рассчитано для C36H38N6O4S: 650.2676, найдено: 651.2745 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиридазин-3-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло [2,3-d]пиримидин-4-он (Пример 982)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиридазин-3-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло [2,3-d]пиримидин-4-он (Пример 982)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 3-(бромметил)пиридазина в качестве реагентов, получали Пример 982. МСВР: рассчитано для C35H37N7O3: 603.2958, найдено: 604.3017 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиридазин-3-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 983)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиридазин-3-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 983)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 3-(бромметил)пиридазина в качестве реагентов, получали Пример 983. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3139 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 984)
3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 984)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-5-метилпиразина в качестве реагентов, получали Пример 984. МСВР: рассчитано для C36H39N7O3: 617.3114, найдено: 618.3172 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 985)
3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 985)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-5-метилпиразина в качестве реагентов, получали Пример 985. МСВР: рассчитано для C37H41N7O4: 647.3220, найдено: 648.3314 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло [2,3-d]пиримидин-4-он (Пример 986)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло [2,3-d]пиримидин-4-он (Пример 986)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)пиримидина в качестве реагентов, получали Пример 986. МСВР: рассчитано для C35H37N7O3: 603.2958, найдено: 604.3022 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 987)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 987)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)пиримидина в качестве реагентов, получали Пример 987. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3128 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(4-метилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 988)
3-[[4-гидрокси-1-[(3R,4R)-1-[(4-метилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 988)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-4-метилпиримидина в качестве реагентов, получали Пример 988. МСВР: рассчитано для C36H39N7O3: 617.3114, найдено: 618.3158 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(4-метилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 989)
3-[[4-гидрокси-1-[(3R,4R)-1-[(4-метилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 989)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-4-метилпиримидина в качестве реагентов, получали Пример 989. МСВР: рассчитано для C37H41N7O4: 647.3220, найдено: 648.3298 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 990)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 990)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 4-(хлорметил)-2-метилпиримидина в качестве реагентов, получали Пример 990. МСВР: рассчитано для C36H39N7O3: 617.3114, найдено: 618.3179 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 991)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 991)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 4-(хлорметил)-2-метилпиримидина в качестве реагентов, получали Пример 991. МСВР: рассчитано для C37H41N7O4: 647.3220, найдено: 648.3282 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метоксипиридазин-3-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 992)
3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метоксипиридазин-3-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 992)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 3-(хлорметил)-6-метоксипиридазина в качестве реагентов, получали Пример 992. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3129 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метоксипиридазин-3-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 993)
3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метоксипиридазин-3-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 993)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 3-(хлорметил)-6-метоксипиридазина в качестве реагентов, получали Пример 993. МСВР: рассчитано для C37H41N7O5: 663.3169, найдено: 664.3223 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метоксипиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 994)
3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метоксипиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 994)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-3-метоксипиразина в качестве реагентов, получали Пример 994. МСВР: рассчитано для C36H39N7O4: 633.3064, найдено: 634.3142 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 995)
3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он (Пример 995)
Используя Общую методику 6, исходя из соединения Синтеза R3bu и 2-(хлорметил)-3-метилпиразина в качестве реагентов, получали Пример 995. МСВР: рассчитано для C36H39N7O3: 617.3114, найдено: 618.3214 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 996)
3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 996)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-3-метилпиразина в качестве реагентов, получали Пример 996. МСВР: рассчитано для C37H41N7O4: 647.3220, найдено: 648.3265 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метоксипиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 997)
3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метоксипиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он (Пример 997)
Используя Общую методику 6, исходя из соединения Синтеза R3ax и 2-(хлорметил)-3-метоксипиразина в качестве реагентов, получали Пример 997. МСВР: рассчитано для C37H41N7O5: 663.3169, найдено: 664.3211 [(М+Н)+ форма].
 4-[[(3R,4R)-4-[4-гидрокси-4-[[4-оксо-7-(2-пиридил)пирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 998)
4-[[(3R,4R)-4-[4-гидрокси-4-[[4-оксо-7-(2-пиридил)пирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 998)
Используя Общую методику 6, исходя из соединения Синтеза R3ca и 4-(хлорметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 998. МСВР: рассчитано для C36H36N8O3: 628.2910, найдено: 629.2987 [(М+Н)+ форма].
 5-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксопирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 999)
5-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксопирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 999)
Используя Общую методику 6, исходя из соединения Синтеза R3ch и 4-(бромметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 999. МСВР: рассчитано для C35H37N9O3: 631.3019, найдено: 632.3066 [(М+Н)+ форма].
 5-[[(3R,4R)-4-[4-гидрокси-4-[[4-оксо-7-(2-пиридил)пирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1000)
5-[[(3R,4R)-4-[4-гидрокси-4-[[4-оксо-7-(2-пиридил)пирроло[2,3-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1000)
Используя Общую методику 6, исходя из соединения Синтеза R3ca и 4-(бромметил)пиридин-2-карбонитрила в качестве реагентов, получали Пример 1000. МСВР: рассчитано для C36H36N8O3: 628.2910, найдено: 629.2976 [(М+Н)+ форма].
 5-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксопирроло[2,1-f][1,2,4]триазин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1001)
5-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксопирроло[2,1-f][1,2,4]триазин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1001)
Используя Общую методику 6, исходили из соединения Синтеза R3cy и 5-(бромметил)пиридин-2-карбонитрила в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 1001. МСВР: рассчитано для C35H37N9O3: 631.3019, найдено: 632.3068 [(М+Н)+ форма].
 4-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксопирроло[2,1-f][1,2,4]триазин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1002)
4-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксопирроло[2,1-f][1,2,4]триазин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1002)
Используя Общую методику 6, исходили из соединения Синтеза R3cy и 4-(хлорметил)пиридин-2-карбонитрила в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 1002. МСВР: рассчитано для C35H37N9O3: 631.3019, найдено: 632.3071 [(М+Н)+ форма].
 4-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксотиено[3,4-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1003)
4-[[(3R,4R)-4-[4-гидрокси-4-[[7-(1-метилпиразол-4-ил)-4-оксотиено[3,4-d]пиримидин-3-ил]метил]пиперидин-1-карбонил]-3-фенил-1-пиперидил]метил]пиридин-2-карбонитрил (Пример 1003)
Используя Общую методику 6, исходили из соединения Синтеза R3dc и 4-(хлорметил)пиридин-2-карбонитрила в качестве реагентов, полученный в результате сырой продукт подвергали реакции с 1-метил-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиразолом в соответствии с Общей методикой 9 с получением Примера 1003. МСВР: рассчитано для C35H36N8O3S: 648.2631, найдено: 649.2693 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено [3,4-d]пиримидин-4-он (Пример 1004)
3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено [3,4-d]пиримидин-4-он (Пример 1004)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)-5-метилпиразина в качестве реагентов, получали Пример 1004. МСВР: рассчитано для C36H38N6O3S: 634.2726, найдено: 635.2793 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1005)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1005)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)пиримидина в качестве реагентов, получали Пример 1005. МСВР: рассчитано для C35H36N6O3S: 620.2570, найдено: 621.2619 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(4-метилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1006)
3-[[4-гидрокси-1-[(3R,4R)-1-[(4-метилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1006)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)-4-метилпиримидина в качестве реагентов, получали Пример 1006.
МСВР: рассчитано для C36H38N6O3S: 634.2726, найдено: 635.2791 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-4-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1007)
3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-4-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1007)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 4-(хлорметил)пиримидина в качестве реагентов, получали Пример 1007. МСВР: рассчитано для C35H36N6O3S: 620.2570, найдено: 621.2656 [(М+Н)+ форма].
 3-[[1-[(3R,4R)-1-[(4,6-диметилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1008)
3-[[1-[(3R,4R)-1-[(4,6-диметилпиримидин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-гидрокси-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1008)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)-4,6-диметилпиримидина в качестве реагентов, получали Пример 1008. МСВР: рассчитано для C37H40N6O3S: 648.2883, найдено: 649.2952 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1009)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1009)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 4-(хлорметил)-2-метоксипиримидина в качестве реагентов, получали Пример 1009. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2744 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d] пиримидин-4-он (Пример 1010)
3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d] пиримидин-4-он (Пример 1010)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 4-(хлорметил)-2-метилпиримидина в качестве реагентов, получали Пример 1010. МСВР: рассчитано для C36H38N6O3S: 634.2726, найдено: 635.2805 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1011)
3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1011)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)-6-метилпиразина в качестве реагентов, получали Пример 1011. МСВР: рассчитано для C36H38N6O3S: 634.2726, найдено: 635.2792 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1012)
3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1012)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)-3-метилпиразина в качестве реагентов, получали Пример 1012. МСВР: рассчитано для C36H38N6O3S: 634.2726, найдено: 635.2782 [(М+Н)+ форма].
 3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метоксипиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1013)
3-[[4-гидрокси-1-[(3R,4R)-1-[(3-метоксипиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он (Пример 1013)
Используя Общую методику 6, исходя из соединения Синтеза R3da и 2-(хлорметил)-3-метоксипиразина в качестве реагентов, получали Пример 1013. МСВР: рассчитано для C36H38N6O4S: 650.2675, найдено: 651.2764 [(М+Н)+ форма].
ФАРМАКОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ
ПРИМЕР А: Оценка ингибирования USP7 посредством считывания данных интенсивностей флуоресценции (FLINT)
Активность USP7 измеряли, используя меченый родамином-110 по с-концу убиквитин в качестве субстрата (Viva Biosciences). Инкубация с USP7 приводила к высвобождению родамина-110, что в свою очередь приводило к усилению флуоресценции, которую может использовать для непрерывного измерения активности USP7.
USP7 реакции выполняли в 50 мкл объеме, в 384 луночных черных твердых планшетах с низким связыванием (Corning #3575). Реакционный буфер состоял из 100 мМ Bicine рН 8.0, 0.01% TritonX100, 1 мМ ТСЕР и 10% ДМСО.
0.25 нМ His-His-USP7 (аа208-560, [С315А]) инкубировали с соединением (конечная концентрация ДМСО 10%) в течение 60 минут при 30°С. Реакцию затем инициировали путем добавления 500 нМ субстрата убиквитин-родамин-110 и планшеты считывали каждые 3 минуты в течение 21 минут для измерения высвобождения родамина-110. Считывание данных интенсивности флуоресценции (FLINT) выполняли, используя планшет-ридер Biomek Neo (Возбужд. 485 нм, Излуч. 535 нм).
Ингибирование возрастающими дозами соединения выражали в виде снижения в процентном выражении кинетической скорости в сравнении с кинетическими скоростями, установленными между контролями 'только ДМСО' и 'полное ингибирование' (без USP7). Ингибирующие концентрации, которые приводили к 50% снижению кинетической скорости (IC50) определяли, исходя из 11-точечных кривых доза-эффект, в XL-Fit, используя 4-параметрическую логистическую модель (сигмоидальная модель доза-ответ).
Результаты, представленные в Таблице 1 ниже, показывают, что соединения изобретения ингибируют взаимодействие между белком USP7 и флуоресцентным пептидом, описанным выше.
ПРИМЕР В: In vitro цитотоксичность
Исследования цитотоксичности проводили с помощью МТТ-анализа, используя опухолевые клеточные линии MM1S множественной миеломы или Z138 лимфомы из клеток зоны мантии. Клетки распределяли на микропланшеты и подвергали воздействию тестируемых соединений в течение 96 часов. Жизнеспособность клеток затем количественно оценивали с помощью колориметрического анализа Microculture Tetrazolium Assay (Carmichael и др., Cancer Res. 1987, 47, 936-942). Результаты выражены в IC50 (концентрация соединения, которая ингибирует жизнеспособность клетки на 50%) и представлены в Таблице 1 ниже.
Результаты показывают, что соединения изобретения являются цитотоксичными.
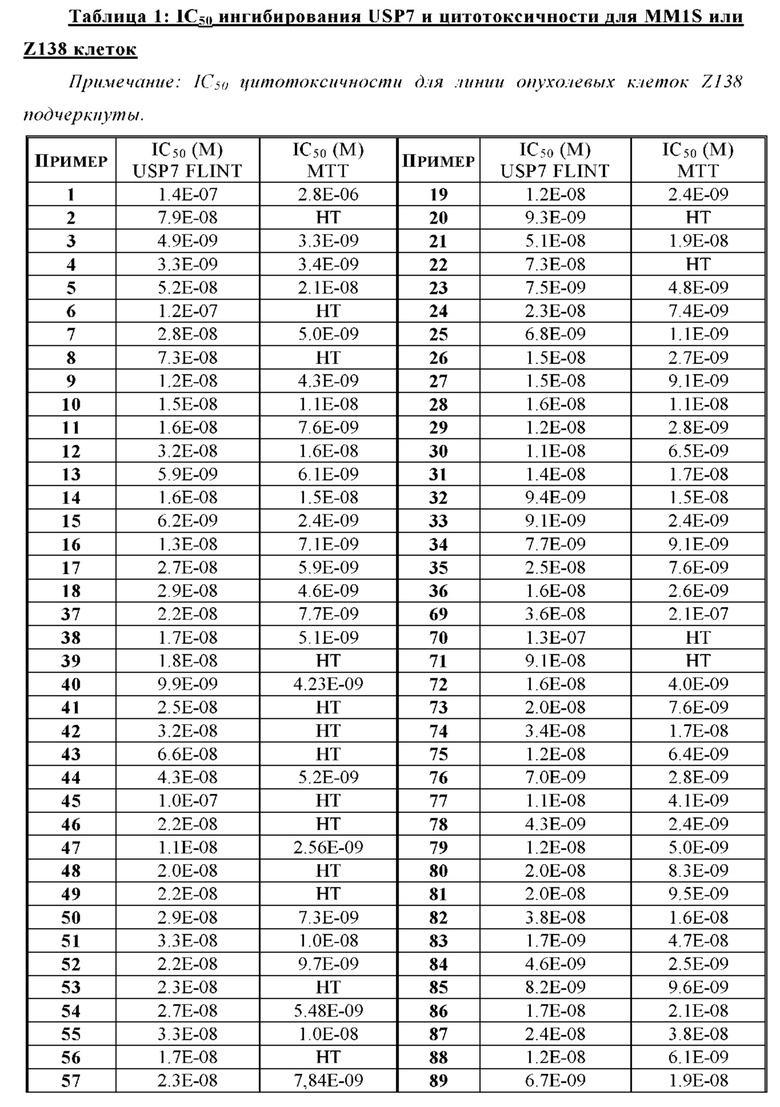
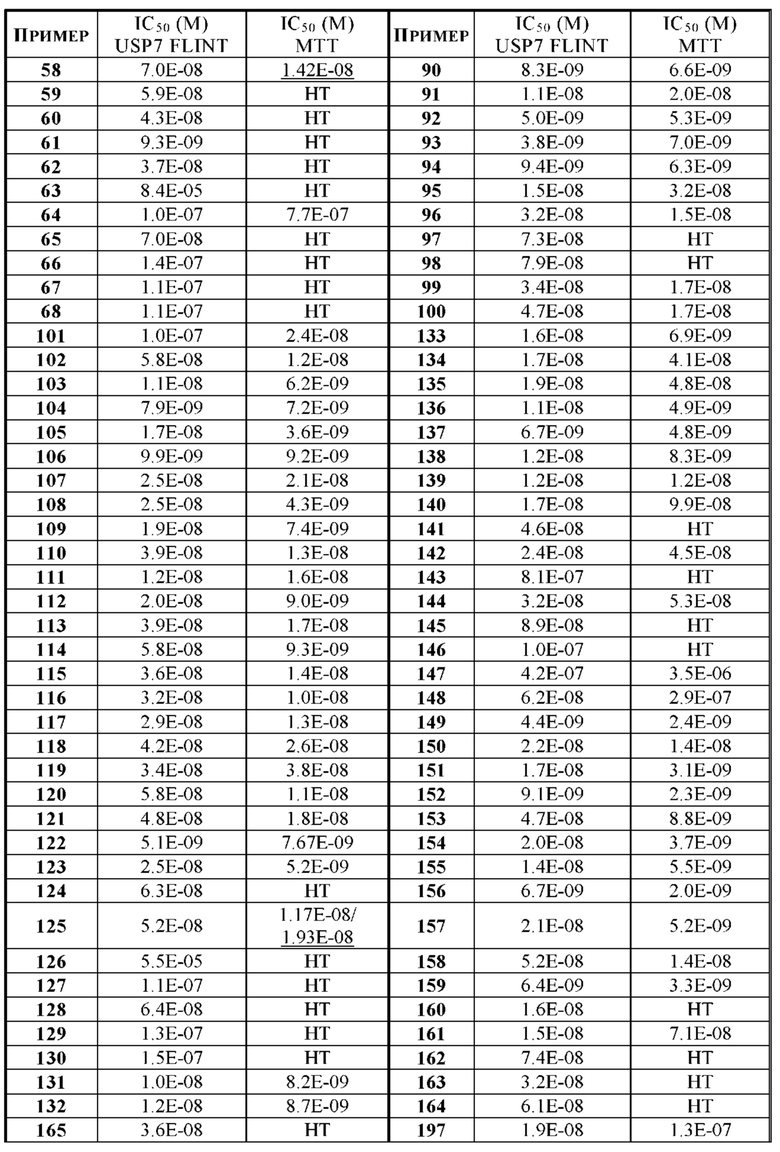
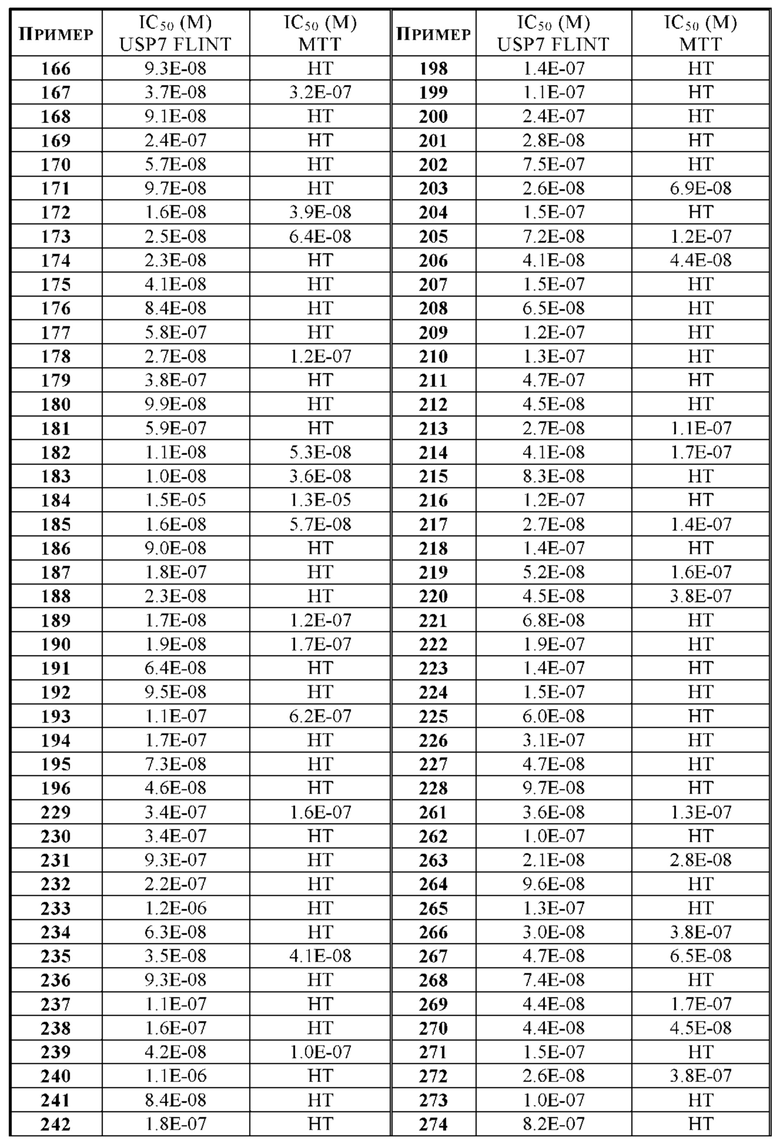
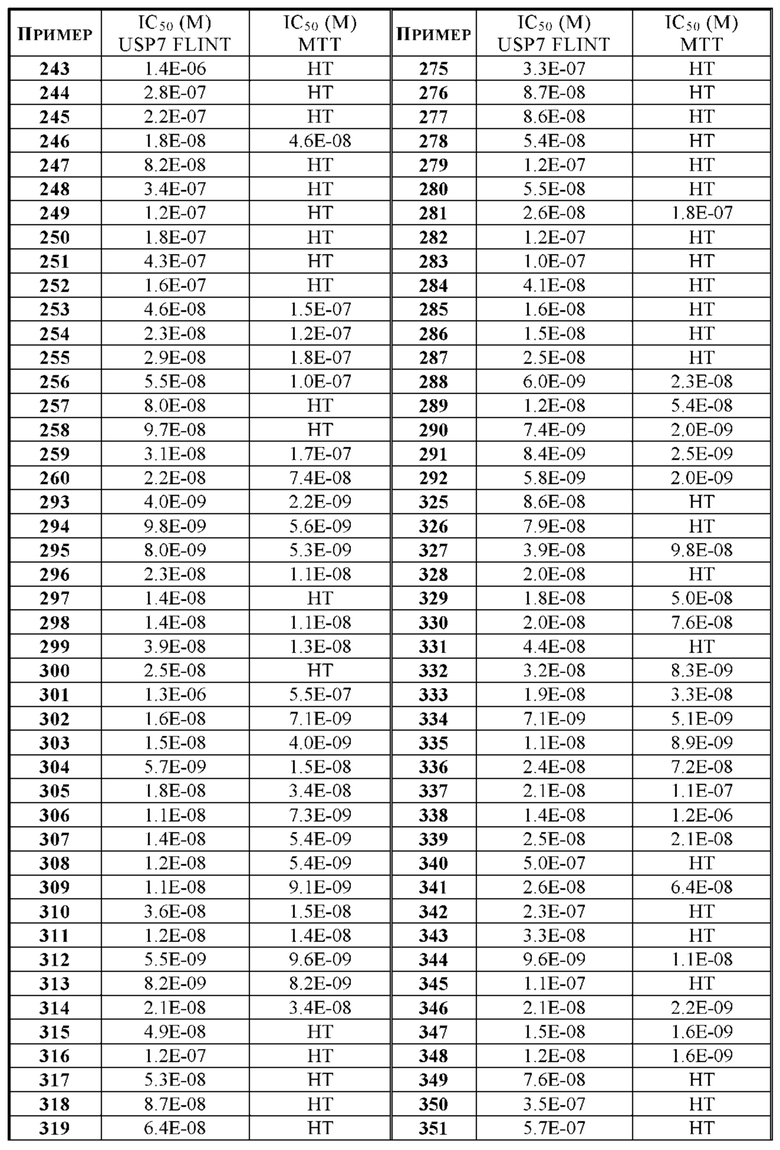
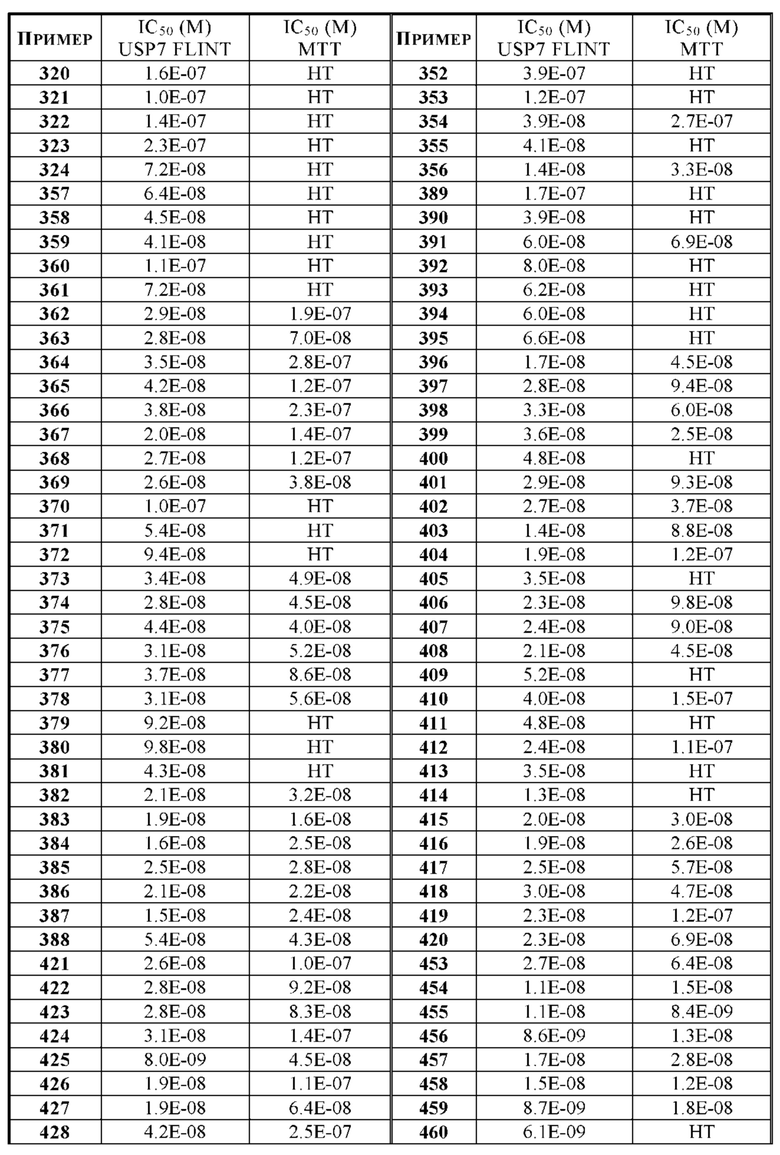
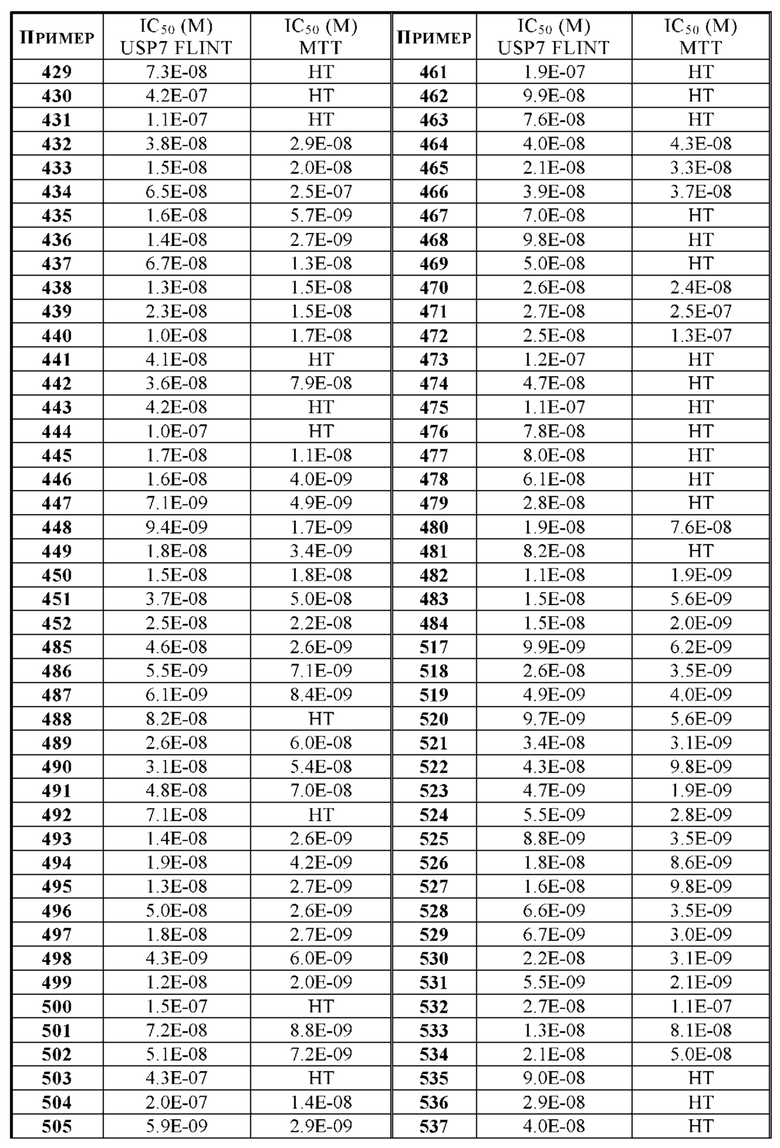
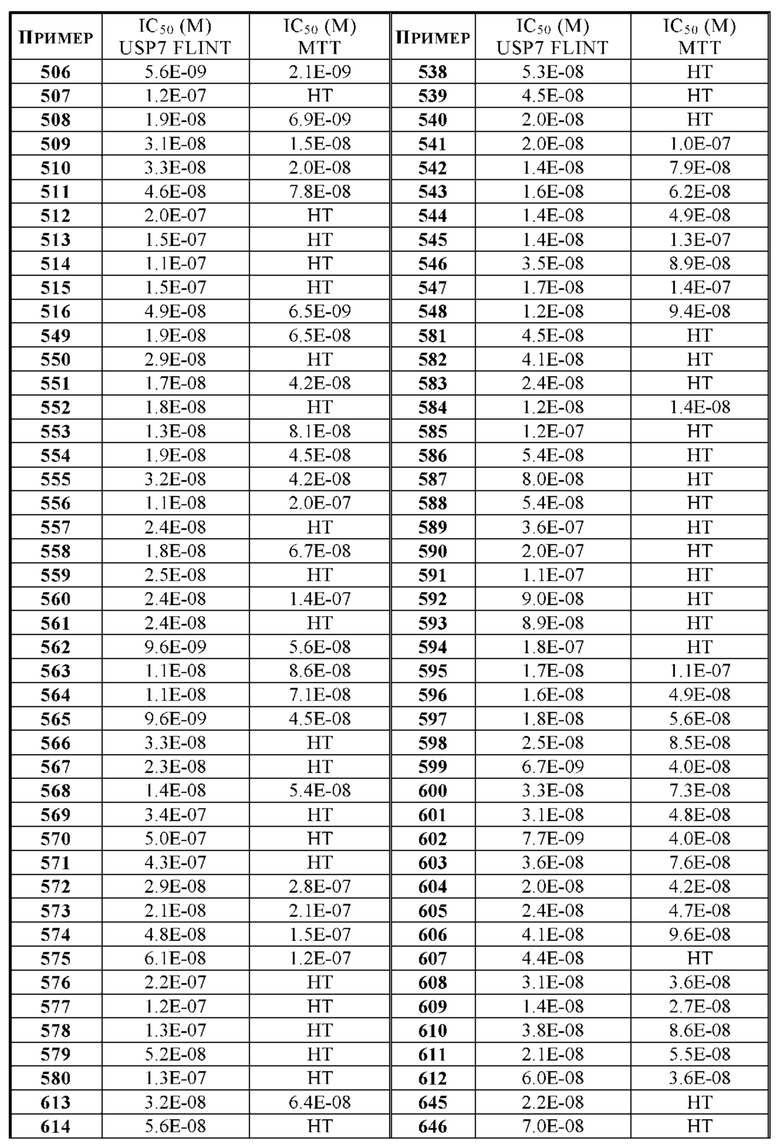
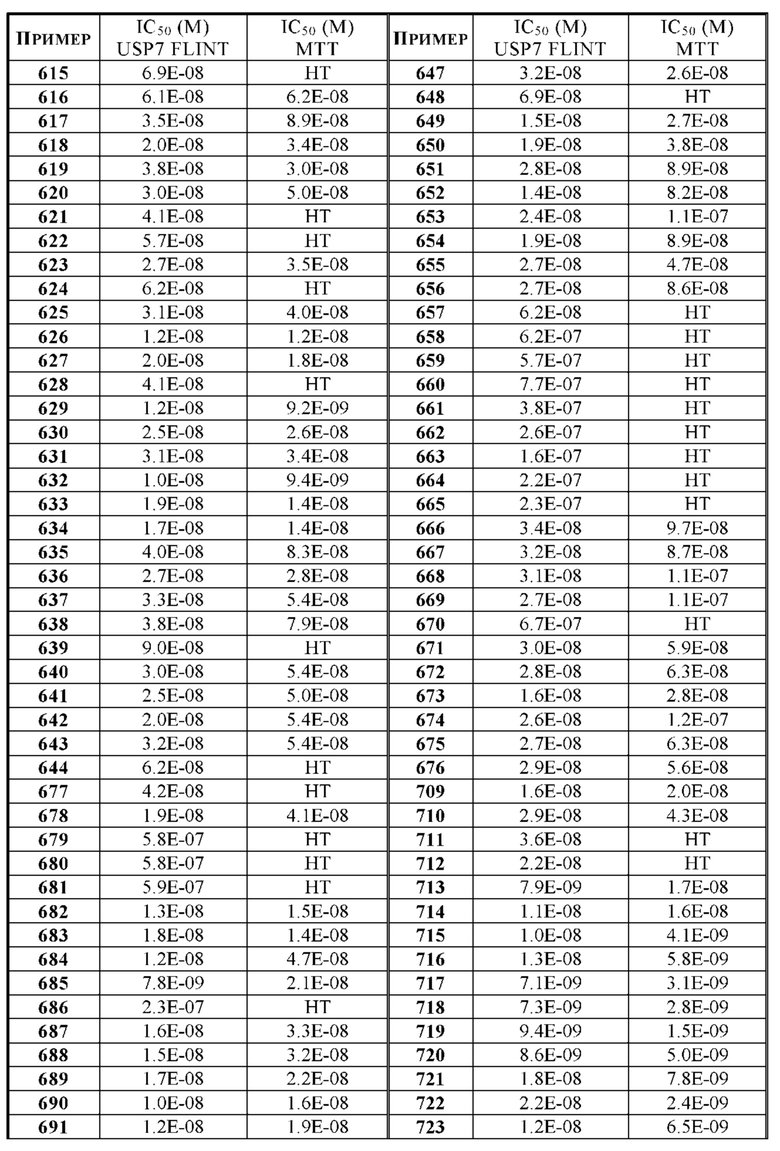


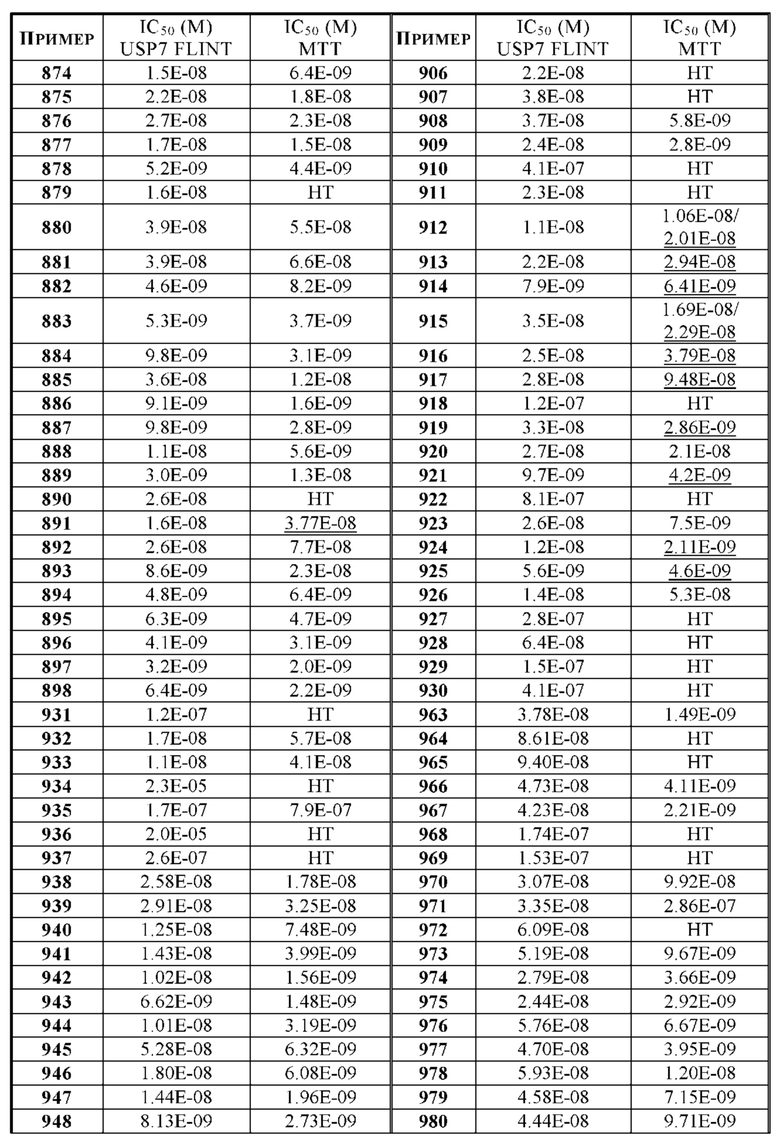
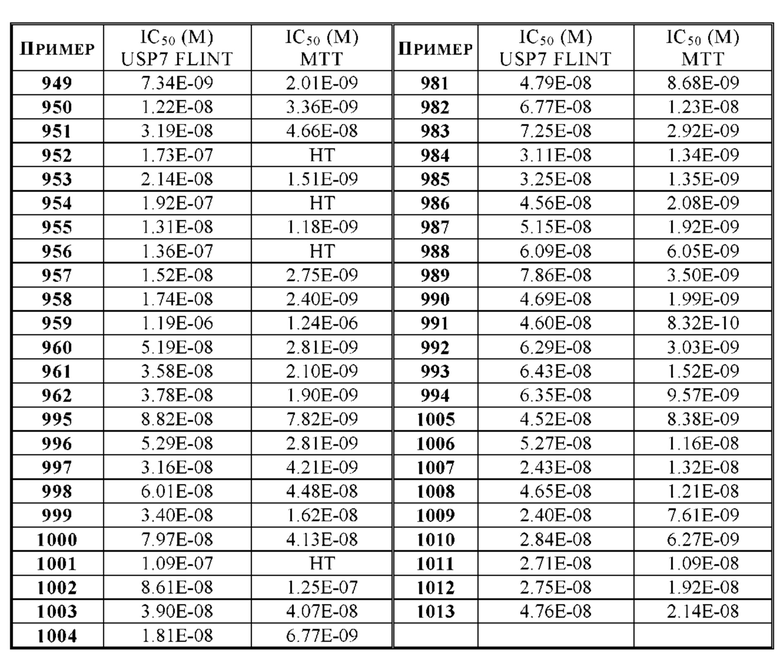
НТ: не тестировали
Для частичных ингибиторов указана процентная интенсивность флуоресценции для приведенной концентрации тестируемого соединения. Соответственно, 48.2% @400 мкМ означает, что 48.2% интенсивность флуоресценции наблюдается для концентрации тестируемого соединения, равной 400 мкМ.
ПРИМЕР С: Противоопухолевая активность in vivo
Противоопухолевую активность соединений изобретения оценивали на ксенотрансплантатной модели с использованием клеток множественной миеломы и/или острого лимфобластного лейкоза.
Иммуносупрессивным мышам подкожно пересаживали опухолевые клетки человека.
Когда объем опухоли (TV) достигал приблизительно 200 мм3, мышам в течение 3 недель один раз в день перорально вводили различные соединения в режиме 5 дней - введение/2 дня - перерыв. Массу опухоли определяли два раза в неделю с самого начала лечения.
Соединения изобретения демонстрировали противоопухолевую активность, представленную с помощью значения TGI (ингибирование роста опухоли) в конце периода лечения, в диапазоне от 40 до 133.4%. TGI определяли, как указано ниже:
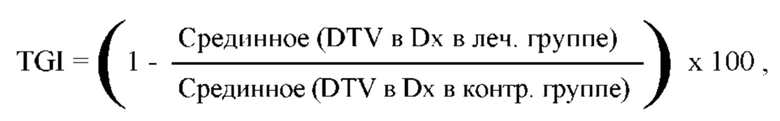
где:
DTV (дельта объем опухоли) в Dx = (TV в Dx) - (TV при рандомизации в случае каждого животного).
ПРИМЕР D: Фармацевтическая композиция: Таблетки
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ПИПЕРИДИНИЛЬНЫЕ ПРОИЗВОДНЫЕ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2017 |
|
RU2743163C2 |
| ПОЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ ЦЕЛЕНАПРАВЛЕННОЙ ДЕГРАДАЦИИ ПОЛИПЕПТИДОВ БЫСТРО УСКОРЕННОЙ ФИБРОСАРКОМЫ | 2019 |
|
RU2830173C2 |
| НОВЫЕ ИНДОЛИЗИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2693629C2 |
| 6,7-ДИГИДРО-5H-ПИРИДО[2,3-C]ПИРИДАЗИНОВЫЕ ПРОИЗВОДНЫЕ И РОДСТВЕННЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРОВ БЕЛКОВ BCLXL И ПРОАПОПТОТИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2020 |
|
RU2832191C2 |
| НОВОЕ ПРОИЗВОДНОЕ ПИПЕРИДИНА И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГИБИРОВАНИЯ АУТОТАКСИНА | 2022 |
|
RU2834850C2 |
| НОВЫЕ ИЗОИНДОЛИНОВЫЕ ИЛИ ИЗОХИНОЛИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2689305C2 |
| ЗАМЕЩЕННЫЕ ПИРРОЛИДИН-2-КАРБОКСАМИДЫ | 2011 |
|
RU2564022C2 |
| НОВЫЕ ИНДОЛИЗИНОВЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2013 |
|
RU2646223C2 |
| НОВЫЕ ФОСФАТНЫЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ИХ | 2014 |
|
RU2617682C2 |
| КЛАСС БИФУНКЦИОНАЛЬНЫХ ХИМЕРНЫХ ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ ДЛЯ НАПРАВЛЕННОГО РАЗРУШЕНИЯ АНДРОГЕННЫХ РЕЦЕПТОРОВ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2825000C2 |
Изобретение относится к соединению формулы (I):
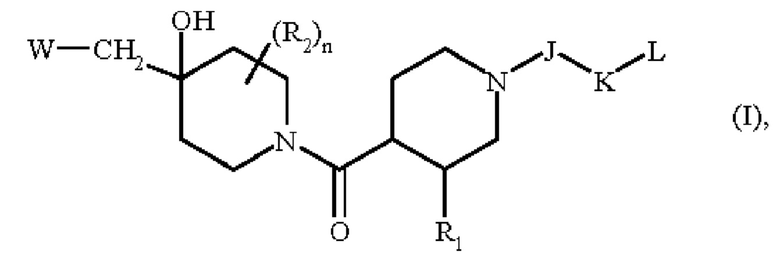
где:  R1 представляет собой фенильную группу или тиенильную группу,
R1 представляет собой фенильную группу или тиенильную группу,  R2 представляет собой атом водорода или атом галогена,
R2 представляет собой атом водорода или атом галогена,  n означает целое число, равное 0, 1 или 2,
n означает целое число, равное 0, 1 или 2,  J представляет собой -С(О)- группу, -CH(R3)- группу или -SO2- группу,
J представляет собой -С(О)- группу, -CH(R3)- группу или -SO2- группу,  R3 представляет собой атом водорода или линейную или разветвленную (C1-С6)алкильную группу,
R3 представляет собой атом водорода или линейную или разветвленную (C1-С6)алкильную группу,  K представляет собой связь или -Cy1- группу,
K представляет собой связь или -Cy1- группу,  L представляет собой -Су2 группу или -СН2-Cy2 группу,
L представляет собой -Су2 группу или -СН2-Cy2 группу,  W представляет собой группу
W представляет собой группу 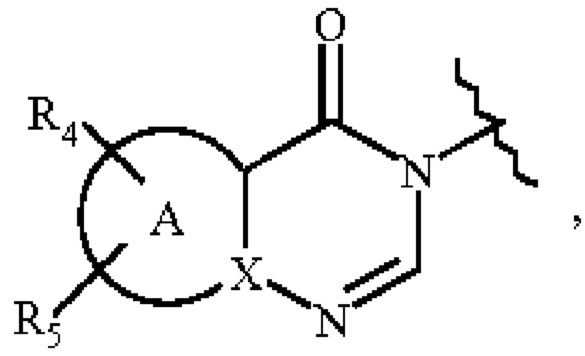 где:
где:

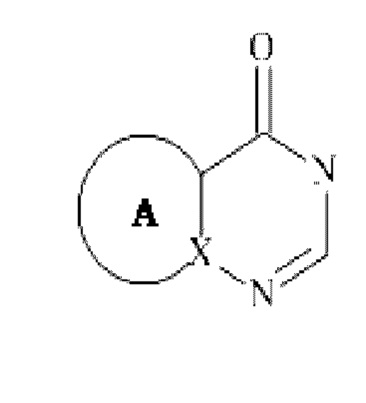 представляет собой
представляет собой 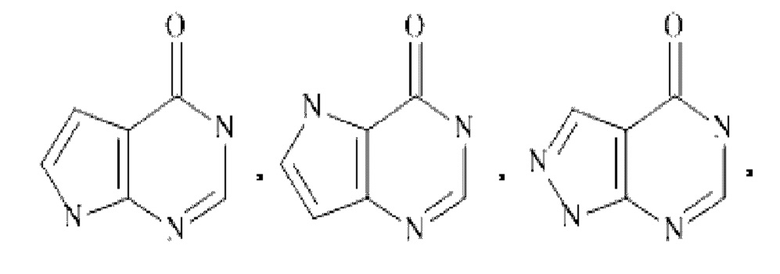
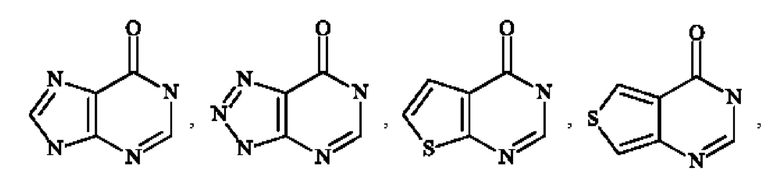
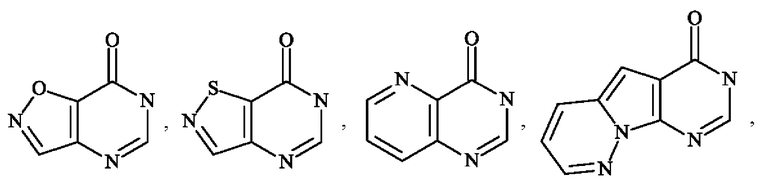
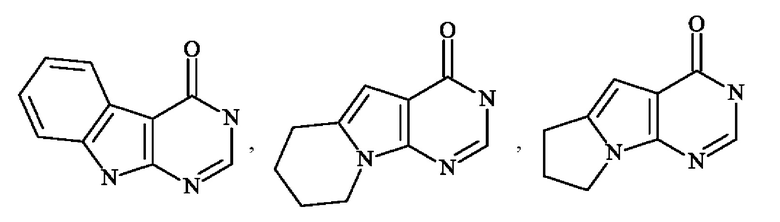 или
или 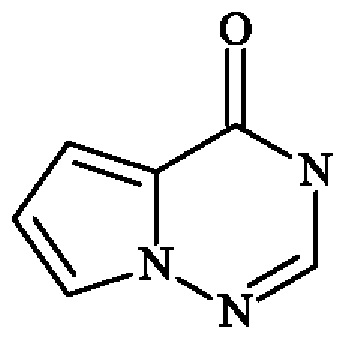 ,
,
 X представляет собой атом углерода или атом азота,
X представляет собой атом углерода или атом азота, R4 представляет собой атом водорода, атом галогена, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, -Y1-NR6R7 группу, -Y1-OR6 группу, линейную или разветвленную галоген(С1-С6)алкильную группу, оксогруппу, -Y1-Су3 группу, -Cy3-R7 группу, -Cy3-OR7 группу, или -Y1-NR6-C(O)-R7 группу,
R4 представляет собой атом водорода, атом галогена, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, -Y1-NR6R7 группу, -Y1-OR6 группу, линейную или разветвленную галоген(С1-С6)алкильную группу, оксогруппу, -Y1-Су3 группу, -Cy3-R7 группу, -Cy3-OR7 группу, или -Y1-NR6-C(O)-R7 группу,  R5 представляет собой атом водорода, атом галогена, или линейную или разветвленную (С1-С6)алкильную группу,
R5 представляет собой атом водорода, атом галогена, или линейную или разветвленную (С1-С6)алкильную группу,  R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,  R7 представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или -Y2-Cy4 группу,
R7 представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или -Y2-Cy4 группу,  Y1 и Y2 независимо друг от друга представляют собой связь или линейную или разветвленную (С1-С4)алкиленовую группу (значения остальных радикалов см. в п. 1 формулы), которое является ингибитором активности белка USP7, а также к содержащим его фармацевтическим композициям и комбинациям. 16 н. и 16 з.п. ф-лы, 1 табл., 1013 пр.
Y1 и Y2 независимо друг от друга представляют собой связь или линейную или разветвленную (С1-С4)алкиленовую группу (значения остальных радикалов см. в п. 1 формулы), которое является ингибитором активности белка USP7, а также к содержащим его фармацевтическим композициям и комбинациям. 16 н. и 16 з.п. ф-лы, 1 табл., 1013 пр.
1. Соединение формулы (I):
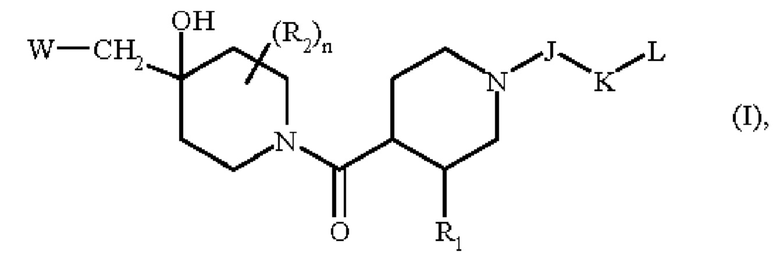
где:
 R1 представляет собой фенильную группу или тиенильную группу,
R1 представляет собой фенильную группу или тиенильную группу,
 R2 представляет собой атом водорода или атом галогена,
R2 представляет собой атом водорода или атом галогена,
 n означает целое число, равное 0, 1 или 2,
n означает целое число, равное 0, 1 или 2,
 J представляет собой -С(О)- группу, -CH(R3)- группу, или -SO2-группу,
J представляет собой -С(О)- группу, -CH(R3)- группу, или -SO2-группу,
 R3 представляет собой атом водорода или линейную или разветвленную (C1-С6)алкильную группу,
R3 представляет собой атом водорода или линейную или разветвленную (C1-С6)алкильную группу,
 K представляет собой связь или -Cy1- группу,
K представляет собой связь или -Cy1- группу,
 L представляет собой -Су2 группу или -СН2-Cy2 группу,
L представляет собой -Су2 группу или -СН2-Cy2 группу,
 W представляет собой группу
W представляет собой группу 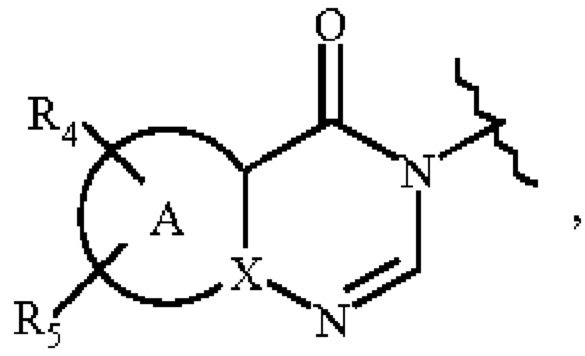 где:
где:

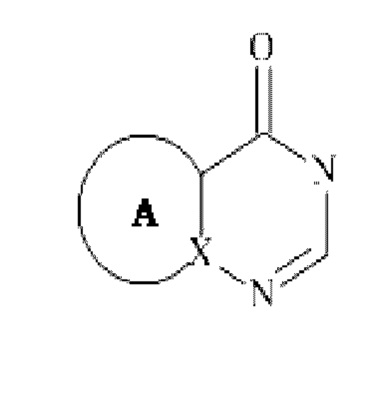 представляет собой
представляет собой 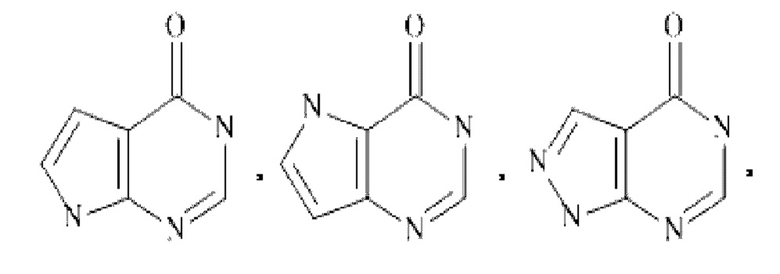
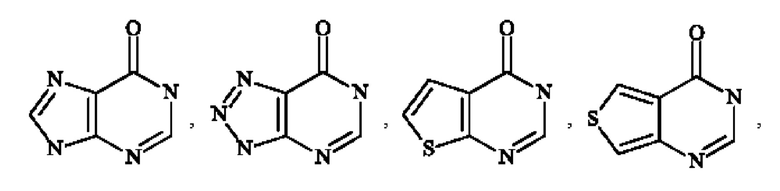
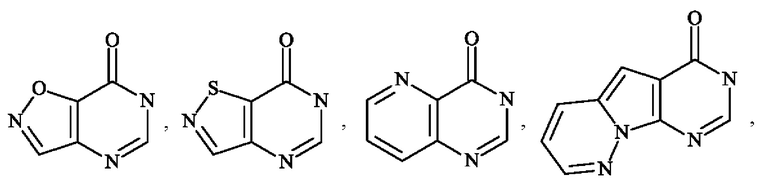
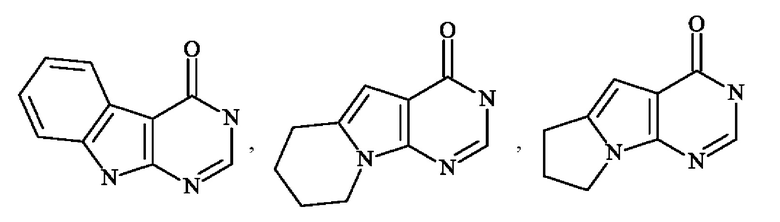
или 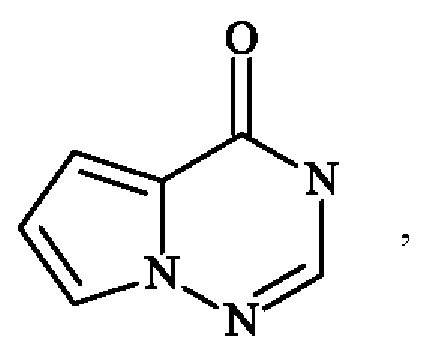
 X представляет собой атом углерода или атом азота,
X представляет собой атом углерода или атом азота,
 R4 представляет собой атом водорода, атом галогена, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, -Y1-NR6R7 группу, -Y1-OR6 группу, линейную или разветвленную галоген(С1-С6)алкильную группу, оксогруппу, -Y1-Су3 группу, -Cy3-R7 группу, -Cy3-OR7 группу или -Y1-NR6-C(O)-R7 группу,
R4 представляет собой атом водорода, атом галогена, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С2-С6)алкинильную группу, -Y1-NR6R7 группу, -Y1-OR6 группу, линейную или разветвленную галоген(С1-С6)алкильную группу, оксогруппу, -Y1-Су3 группу, -Cy3-R7 группу, -Cy3-OR7 группу или -Y1-NR6-C(O)-R7 группу,
 R5 представляет собой атом водорода, атом галогена или линейную или разветвленную (С1-С6)алкильную группу,
R5 представляет собой атом водорода, атом галогена или линейную или разветвленную (С1-С6)алкильную группу,
 R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
R6 представляет собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
 R7 представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или -Y2-Cy4 группу,
R7 представляет собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу или -Y2-Cy4 группу,
 Y1 и Y2 независимо друг от друга представляют собой связь или линейную или разветвленную (С1-С4)алкиленовую группу,
Y1 и Y2 независимо друг от друга представляют собой связь или линейную или разветвленную (С1-С4)алкиленовую группу,
 Cy1 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, пирролильной группы, тиенильной группы, тиазолильной группы, пиридинильной группы, тетрагидробензотиенильной группы, дигидротиенодиоксинильной группы, циклопропильной группы, циклобутильной группы или пирролидинильной группы, которая присоединена к группе J и к группе L,
Cy1 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, пирролильной группы, тиенильной группы, тиазолильной группы, пиридинильной группы, тетрагидробензотиенильной группы, дигидротиенодиоксинильной группы, циклопропильной группы, циклобутильной группы или пирролидинильной группы, которая присоединена к группе J и к группе L,
 Су2 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, инданильной группы, пирролильной группы, фурильной группы, тиенильной группы, тиазолильной группы, изотиазолильной группы, оксазолильной группы, изоксазолильной группы, пиразолильной группы, пиридинильной группы, пиразинильной группы, пиридазинильной группы, пиримидинильной группы, пиридинонильной группы, индолильной группы, дигидроиндолильной группы, дигидроизоиндолильной группы, индазолильной группы, дигидроциклопентатиенильной группы, тетрагидробензотиенильной группы, бензофуранильной группы, имидазопиридинильной группы, бензотриазолильной группы, бензодиоксолильной группы, дигидробензодиоксинильной группы, хинолинильной группы, тетрагидрохинолинильной группы, тетрагидроизохинолинильной группы, хиноксалинильной группы, дигидрохиноксалинильной группы, хиназолинонильной группы или пирролидинильной группы,
Су2 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, инданильной группы, пирролильной группы, фурильной группы, тиенильной группы, тиазолильной группы, изотиазолильной группы, оксазолильной группы, изоксазолильной группы, пиразолильной группы, пиридинильной группы, пиразинильной группы, пиридазинильной группы, пиримидинильной группы, пиридинонильной группы, индолильной группы, дигидроиндолильной группы, дигидроизоиндолильной группы, индазолильной группы, дигидроциклопентатиенильной группы, тетрагидробензотиенильной группы, бензофуранильной группы, имидазопиридинильной группы, бензотриазолильной группы, бензодиоксолильной группы, дигидробензодиоксинильной группы, хинолинильной группы, тетрагидрохинолинильной группы, тетрагидроизохинолинильной группы, хиноксалинильной группы, дигидрохиноксалинильной группы, хиназолинонильной группы или пирролидинильной группы,
 Су3 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, нафтильной группы, пирролильной группы, фурильной группы, тиенильной группы, тиазолильной группы, пиразолильной группы, имидазолильной группы, пиридинильной группы, пиримидинильной группы, пиридинонильной группы, индолильной группы, бензодиоксолильной группы, дигидробензодиоксинильной группы, циклопропильной группы, циклобутильной группы, циклопентильной группы, циклогексильной группы, пирролидинильной группы, тетрагидропиранильной группы или пиперидинильной группы,
Су3 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, нафтильной группы, пирролильной группы, фурильной группы, тиенильной группы, тиазолильной группы, пиразолильной группы, имидазолильной группы, пиридинильной группы, пиримидинильной группы, пиридинонильной группы, индолильной группы, бензодиоксолильной группы, дигидробензодиоксинильной группы, циклопропильной группы, циклобутильной группы, циклопентильной группы, циклогексильной группы, пирролидинильной группы, тетрагидропиранильной группы или пиперидинильной группы,
 Су4 представляет собой гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, пиперазинильной группы, морфолинильной группы, пиридинильной группы или дигидроиндолильной группы,
Су4 представляет собой гетероциклоалкильную группу, арильную группу или гетероарильную группу, выбранную из фенильной группы, пиперазинильной группы, морфолинильной группы, пиридинильной группы или дигидроиндолильной группы,
при этом следует понимать, что:
- "арил" означает фенильную, нафтильную или инданильную группу,
- "гетероарил" означает моно- или конденсированную бициклическую группу, состоящую из 5-10 кольцевых членов, содержащую по меньшей мере один ароматический фрагмент и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы и азота,
- "циклоалкил" означает моно- или конденсированную бициклическую неароматическую карбоциклическую группу, содержащую от 3 до 7 кольцевых членов,
- "гетероциклоалкил" означает неароматическую моно- или конденсированную бициклическую группу, содержащую от 3 до 10 кольцевых членов и содержащую от 1 до 3 гетероатомов, выбранных из кислорода, серы и азота,
причем арильные, гетероарильные, циклоалкильные и гетероциклоалкильные группы, определенные таким образом, могут быть замещены 1-4 группами, выбранными из линейного или разветвленного (C1-С6)алкила, линейного или разветвленного (С2-С6)алкенила, линейного или разветвленного (С2-С6)алкинила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', -Y1-S(O)m-R', оксо (или N-оксида, в соответствующих случаях), нитро, циано, -C(O)-R', -C(O)-OR', -O-C(O)-R', -C(O)-NR'R'', -Y1-NR'-C(O)-R'', -Y1-NR'-C(O)-OR'', галогена, циклопропила и пиридинила, который может быть замещен линейной или разветвленной (С1-С6)алкильной группой,
при этом следует понимать, что R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С2-С6)алкенильную группу, линейную или разветвленную (С1-С6)алкоксигруппу, линейную или разветвленную галоген(С1-С6)алкильную группу, линейную или разветвленную гидрокси(С1-С6)алкильную группу, линейную или разветвленную (C1-С6)алкокси(С1-С6)алкильную группу, фенильную группу, циклопропилметильную группу, тетрагидропиранильную группу,
или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота, при этом следует понимать, что второй рассматриваемый азот может быть замещен 1-2 группами, представляющими собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу,
и при этом следует понимать, что m означает целое число, равное 0, 1 или 2,
его энантиомеры, диастереоизомеры и их соли присоединения с фармацевтически приемлемой кислотой или основанием.
2. Соединения по п. 1, где W представляет собой группу
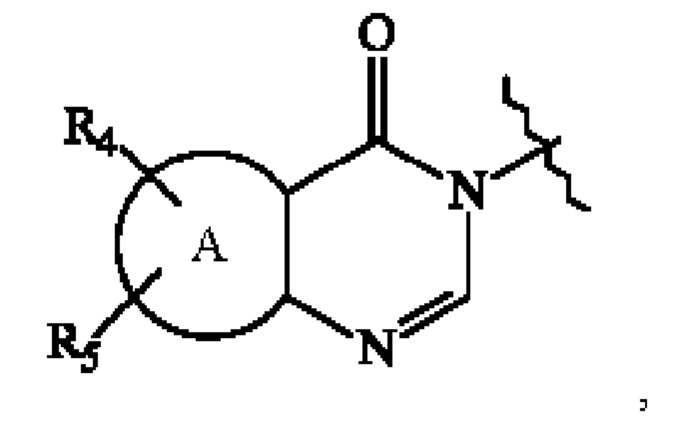
где R4, R5 являются такими, как определено в п. 1, и где
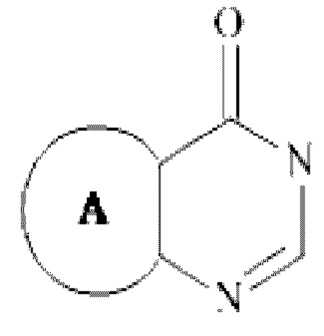 представляет собой
представляет собой 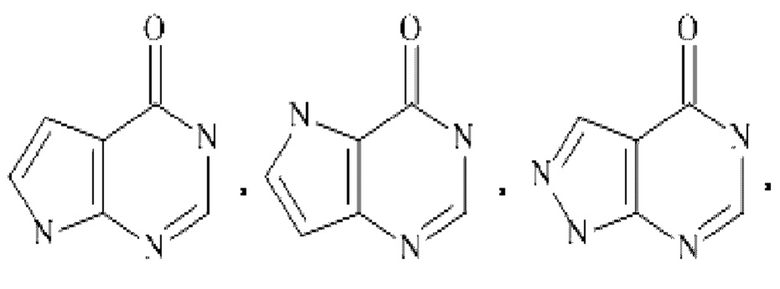
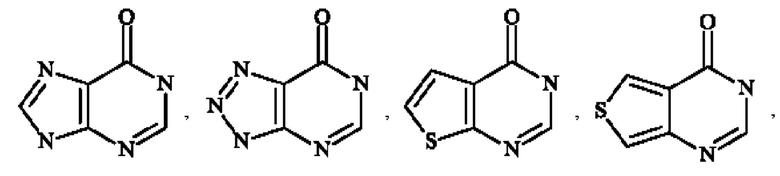
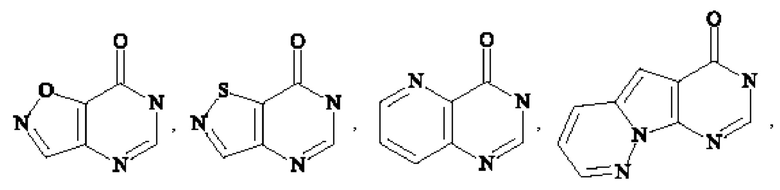
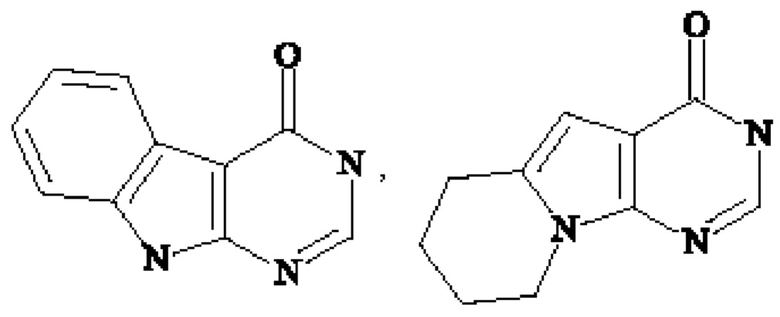 или
или 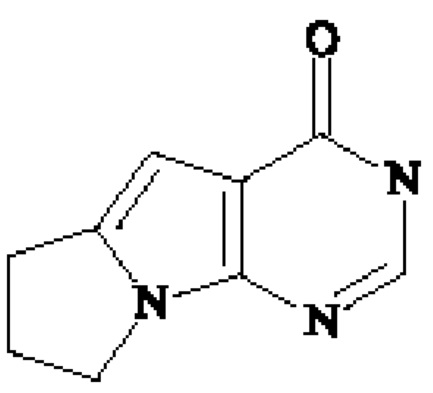 ,
,
3. Соединения по п. 1, где W представляет собой группу
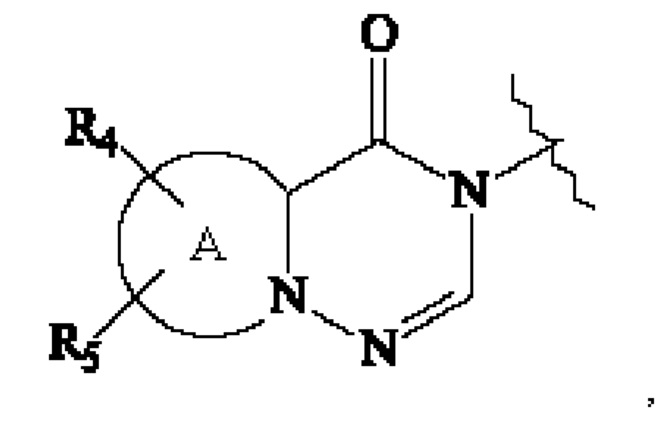
где R4, R5 являются такими, как определено в п. 1, и где
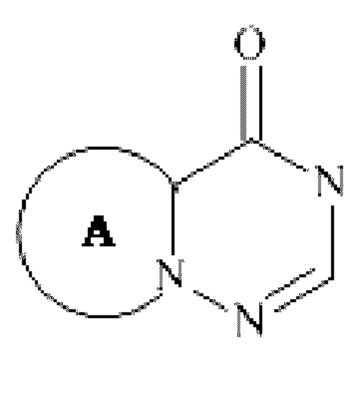 представляет собой
представляет собой 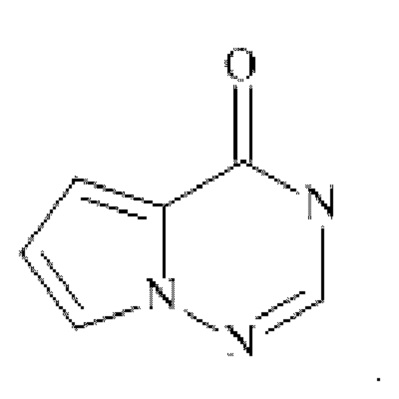
4. Соединения по п. 1, где R2 представляет собой атом водорода и атом фтора.
5. Соединения по п. 1, где R3 представляет собой атом водорода или метильную группу.
6. Соединения по п. 1, где J представляет собой -С(O)- группу или -СН3- группу.
7. Соединение по п. 1, где L представляет собой -Су2 группу.
8. Соединение по п. 1, где Cy2 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, которые замещены 1 или 2 группами, выбранными из линейного или разветвленного (С1-С6)алкила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', N-оксида, циано, -C(O)-OR', -С(O)-NR'R'', галогена, где R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С1-С6)алкокси группу, или тетрагидропиранильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота, при этом следует понимать, что второй рассматриваемый азот может быть замещен линейной или разветвленной (С1-С6)алкильной группой.
9. Соединение по п. 1, где K представляет собой тиенильную группу, тиазолильную группу или пиридинильную группу, и L представляет собой пирролильную группу, фурильную группу, тиенильную группу, пиразолильную группу, пиридинильную группу, пиримидинильную группу или имидазопиридинильную группу, причем каждая указанная гетероарильная группа может быть замещена 1 или 2 группами, выбранными из линейного или разветвленного (С1-С6)алкила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', N-оксида, циано, -C(O)-NR'R'', галогена, где R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, линейную или разветвленную (С1-С6)алкокси группу, линейную или разветвленную (С1-С6)алкокси(С1-С6)алкильную группу, или тетрагидропиранильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота.
10. Соединения по п. 1, где K представляет собой связь и L представляет собой фенильную группу, тиазолильную группу, оксазолильную группу, изоксазолильную группу, пиразолильную группу, пиридинильную группу, пиразинильную группу, пиридазинильную группу или пиримидинильную группу, причем каждая указанная гетероарильная группа может быть замещена 1 или 2 группами, выбранными из линейного или разветвленного (С1-С6)алкила, -Y1-OR', -Y1-NR'R'', циано, -C(O)-OR', галогена, при этом следует понимать, что R' и R'' независимо друг от друга представляют собой атом водорода, линейную или разветвленную (С1-С6)алкильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота, при этом следует понимать, что второй рассматриваемый азот может быть замещен 1-2 группами, представляющими собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу.
11. Соединения по п. 1, где R4 представляет собой атом галогена, линейную или разветвленную (С1-С6)алкильную группу или -Y1-Су3 группу.
12. Соединения по п. 1, где Су3 представляет собой циклоалкильную группу, гетероциклоалкильную группу, арильную группу или гетероарильную группу, которые замещены 1-3 группами, выбранными из линейного или разветвленного (С1-С6)алкила, линейного или разветвленного галоген(С1-С6)алкила, -Y1-OR', -Y1-NR'R'', циано, галогена, где R' и R'' независимо друг от друга представляют собой атом водорода или линейную или разветвленную (С1-С6)алкильную группу, или заместители пары (R', R'') вместе с атомом азота, несущим их, образуют неароматическое кольцо, состоящее из 5-7 кольцевых членов, которое может содержать в дополнение к атому азота второй гетероатом, выбранный из кислорода и азота.
13. Соединения по п. 1, где R5 представляет собой атом водорода или метильную группу.
14. Соединения по п. 1, где R6 представляет собой атом водорода или метильную группу.
15. Соединения по п. 1, где R7 представляет собой атом водорода, метильную группу, или -СН2-Су4 группу.
16. Соединения по п. 1, которые представляют собой:
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[3-метил-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-метил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[5-(6-аминопиридин-3-ил)-3-фтортиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-метил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 7-циклопропил-3-[(1-{[(3R,4R)-1-{[3-фтор-5-(пиридин-4-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(1-{[(3R,4R)-1-{[3-фтор-5-(6-метилпиридин-3-ил)тиофен-2-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3-R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(нафталин-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-7-(фуран-3-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-7-(2-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-7-(2-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-7-[4-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(4-метилпиперазин-1-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1H-пиррол-1-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(2-бром-4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}-4-метил-1,3-тиазол-2-ил)пиридин-2-карбонитрил;
-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-4-метил-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-({4-метил-2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}карбонил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-4-метил-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(морфолин-4-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлорфенил)-3-[(1-{[(3R,4R)-1-({2-[6-(диметиламино)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-6,8-диметилпиримидо[5',4':4,5]пирроло[1,2-b]пиридазин-4(3H)-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метил-1-оксидопиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(пиперазин-1-ил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(трифторметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3,4-дихлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-2-карбонитрил;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3,4-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(пиридин-3-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-фенил-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
-7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3,5-диметоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-4-{3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-4-оксо-3,4-дигидро-7H-пирроло[2,3-d]пиримидин-7-ил}бензонитрил;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1H-пиразол-4-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1H-пиразол-4-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[3-(гидрокеиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-фенил-1,5-дигидро-4H-пиразоло[3,4-d] пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(1-метил-1Н-пиразол-4-ил)-3,7-дигидро-4H-пирроло [2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлор-3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3-хлор-5-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-фтор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлор-3-метоксифенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(4-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(5-хлортиофен-2-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-бром-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]пирроло[2,1-f][1,2,4]триазин-4(3H)-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(5-метилтиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[4-(гидроксиметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[4-(гидроксиметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилпирроло[2,1-f][1,2,4]триазин-4(3H)-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилпирроло[2,1-f] [1,2,4]триазин-4(3H)-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-2-ил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилтиено[3,4-d]пиримидин-4(3H)-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенилтиено[3,4-d]пиримидин-4(3H)-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,5-дигидро-4H-пирроло[3,2-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,5-дигидро-4H-пирроло[3,2-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,5-дигидро-4H-пирроло[3,2-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метилфенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метилфенил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(тиофен-3-ил)-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(морфолин-4-ил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-[3-(трифторметил)фенил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[4-(дифторметил)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[1-(дифторметил)-1H-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-[1-(дифторметил)-1H-пиразол-4-ил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(3-метил-3H-имидазо[4,5-b]пиридин-бил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d] пиримидин-4-он;
-7-[3-(диметиламино)фенил]-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-7-(3-фторфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-{[2-(5-фтор-6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-(5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}-1,3-тиазол-2-ил)пиридин-3-карбоксамид;
-3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[5-(гидроксиметил)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-({2-[6-(тетрагидро-2H-пиран-4-илокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-{[2-(5-амино-6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4Н-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(2-бром-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(2-бромпиридин-4-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4Я-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(3-хлорфенил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-2-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(пиримидин-5-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-5-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиразол-4-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(1-метил-1H-пиррол-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-{[2-(тиофен-3-ил)-1,3-тиазол-5-ил]метил}пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-{[2-(фуран-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(1-{[(3R,4R)-1-{[2-(фуран-2-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}-4-гидроксипиперидин-4-ил)метил]-7-(3-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(2,3-дигидро-1,4-бензодиоксин-6-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-7-(1,3-бензодиоксол-5-ил)-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3,4,5-триметоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-3-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(6'-метил-3,3'-бипиридин-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиридин-4-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(3-метоксифенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
-5-[5-({(3R,4R)-4-[(4-{[7-(4-хлорфенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
-5-[5-({(3R,4R)-4-[(4-гидрокси-4-{[7-(4-метоксифенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}пиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(морфолин-4-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4,7-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-({2-[6-(2-метоксиэтокси)пиридин-3-ил]-1,3-тиазол-5-ил}метил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(4-метилпиперазин-1-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-гидроксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(3-гидроксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(4-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(2-метил-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(2-хлор-1,3-тиазол-5-ил)карбонил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(1,3-тиазол-5-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-5-[5-({(3R,4R)-4-[(4-{[7-(4-фторфенил)-4-оксо-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил]метил}-4-гидроксипиперидин-1-ил)карбонил]-3-фенилпиперидин-1-ил}метил)-1,3-тиазол-2-ил]пиридин-2-карбонитрил;
-метил 3-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}бензоат;
-5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-(4-метоксифенил)-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
-5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метоксипиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-(4-метоксифенил)-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
-5-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1-(4-метоксифенил)-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(2-{6-[(2-метоксиэтил)амино]пиридин-3-ил}-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(1-метил-1H-пиразол-4-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-3-фенил-1-(пиразин-2-илметил)пиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(5-бромпиридин-3-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- метил 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]карбонил}пиридин-3-карбоксилат;
-1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[(4-гидрокси-1-{[(3R,4R)-1-{[4-метил-2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]карбонил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1,5-дигидро-4H-пиразоло[3,4-d]пиримидин-4-он;
-1-(2,3-дигидро-1,4-бензодиоксин-6-ил)-5-[(4-гидрокси-1-{[(3R,4R)-1-{[2-(6-метилпиридин-3-ил)-1,3-тиазол-5-ил]метил}-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-1,5-дигидро-4Н-пиразоло[3,4-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-тиазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[4-гидрокси-1-({(3R,4R)-1-[(3-метил-1,2-оксазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-фенил-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-{[1-({(3R,4R)-1-[(2,4-диметил-1,3-тиазол-5-ил)метил]-3-фенилпиперидин-4-ил}карбонил)-4-гидроксипиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
-3-[(4-гидрокси-1-{[(3R,4R)-1-(1,3-оксазол-4-илметил)-3-фенилпиперидин-4-ил]карбонил}пиперидин-4-ил)метил]-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 3-{[4-гидрокси-1-({(3R,4R)-1-[(5-метил-1,3-оксазол-2-ил)метил]-3-фенилпиперидин-4-ил}карбонил)пиперидин-4-ил]метил}-7-(4-метоксифенил)-3,7-дигидро-4H-пирроло[2,3-d]пиримидин-4-он;
- 5-{[(3R,4R)-4-({4-гидрокси-4-[(4-оксо-7-фенил-4,7-дигидро-3H-пирроло[2,3-d]пиримидин-3-ил)метил]пиперидин-1-ил}карбонил)-3-фенилпиперидин-1-ил]метил}пиридин-2-карбонитрил;
- 3-[[4-гидрокси-l-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]пирроло[2,1-f][1,2,4]триазин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-[4-(гидроксиметил)фенил]тиено[3,4-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(3-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[3,3-дифтор-4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[3,3-дифтор-4-гидрокси-1-[(3R,4R)-1-[4-метил-2-(6-метил-3-пиридил)тиазол-5-карбонил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метоксипиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидии-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-3-фенил-1-(пиримидин-2-илметил)пиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилпирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(6-метоксипиридазин-3-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-(4-метоксифенил)пирроло[2,3-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(5-метилпиразин-2-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он;
- 3-[[4-гидрокси-1-[(3R,4R)-1-[(2-метилпиримидин-4-ил)метил]-3-фенилпиперидин-4-карбонил]-4-пиперидил]метил]-7-фенилтиено[3,4-d]пиримидин-4-он.
17. Способ получения соединения формулы (I) по п. 1, отличающийся тем, что в качестве исходного вещества применяют соединение формулы (II):
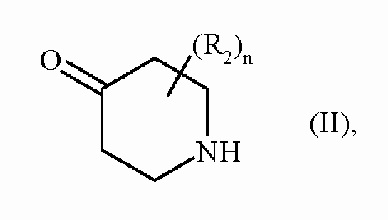
где R2 и n являются такими, как определено для формулы (I), которое подвергают сочетанию с соединением формулы (III):
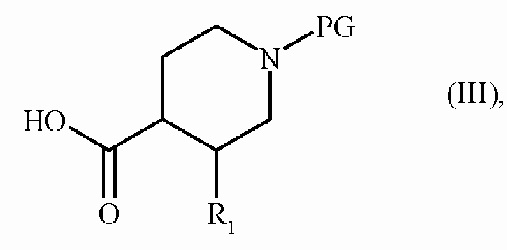
где R1 является таким, как определено для формулы (I), и PG представляет собой защитную группу аминной функции,
с получением соединения формулы (IV):
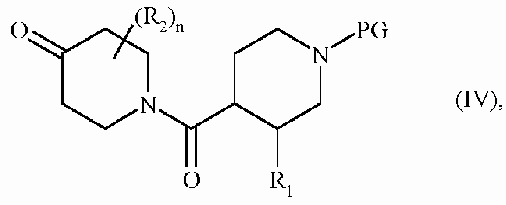
где R1, R2, n и PG являются такими, как определено выше,
соединение формулы (IV) затем превращают в эпоксидное соединение формулы (V):
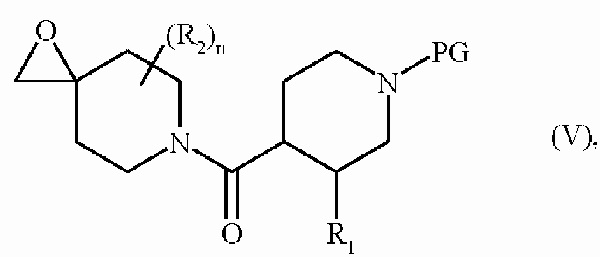
где R1, R2, n и PG являются такими, как определено выше,
соединение формулы (V) затем подвергают сочетанию с соединением формулы (VI):

где W является таким, как определено для формулы (I),
с получением соединения формулы (VII):
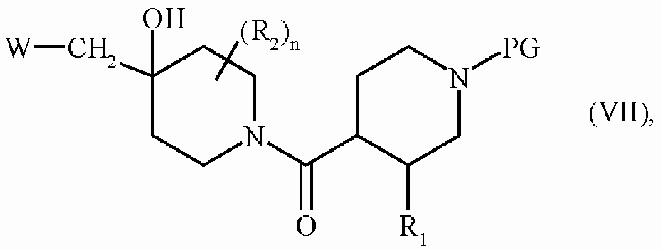
где R1, R2, n, W и PG являются такими, как определено выше,
соединение формулы (VII), после реакции удаления защитной группы PG, затем подвергают:
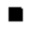 либо сочетанию с соединением формулы (VIII):
либо сочетанию с соединением формулы (VIII):
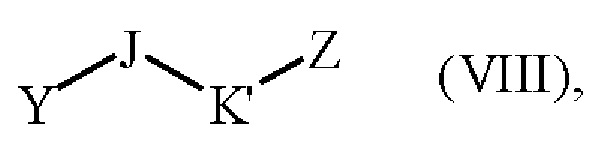
где J является таким, как определено для формулы (I), K' представляет собой -Cy1-группу, Y представляет собой гидрокси группу или атом галогена, и Z представляет собой атом галогена,
с получением соединения формулы (IX):
где R1, R2, J, K', n, W и Z являются такими, как определено выше, и
соединение формулы (IX) затем подвергают сочетанию с соединением формулы (X):
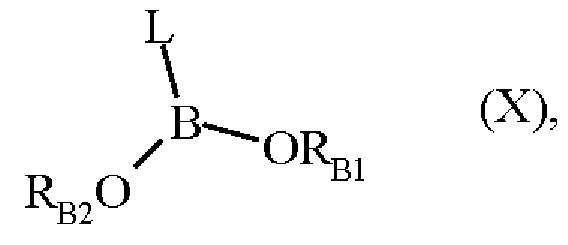
где L является таким, как определено для формулы (I), и RB1 и RB2 представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, или RB1 и RB2 соединены линейной или разветвленной (С2-С6)алкиленовой группой,
с получением соединения формулы (I-а), частного случая соединений формулы (I):

где R1, R2, J, K', L, n и W являются такими, как определено выше,
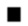 либо сочетанию с соединением формулы (XI):
либо сочетанию с соединением формулы (XI):
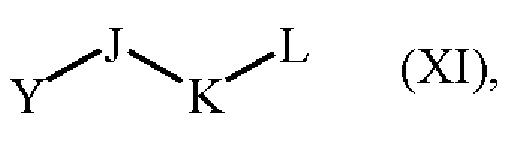
где J, K и L являются такими, как определено для формулы (I), и Y представляет собой гидроксигруппу или атом галогена,
с получением соединения формулы (I),
соединение формулы (I) или соединение формулы (I-а), которое является частным случаем соединения формулы (I), затем можно очистить в соответствии с обычными методиками разделения, превратить, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием и необязательно разделить на его изомеры в соответствии с обычными методиками разделения,
при этом следует понимать, что в любое время, признанное подходящим в ходе описанного выше способа, некоторые группы (гидрокси, амино) исходных реагентов или промежуточных соединений синтеза могут быть защищены, впоследствии лишены защиты и функционализированы, как того требует синтез.
18. Способ получения соединения формулы (I) по п. 1, отличающийся тем, что в качестве исходного вещества применяют соединение формулы (XII):
где R1 является таким, как определено для формулы (I), и PG представляет собой защитную группу функции карбоновой кислоты, которое подвергают:
 либо сочетанию с соединением формулы (VIII):
либо сочетанию с соединением формулы (VIII):
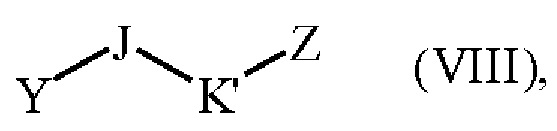
где J является таким, как определено для формулы (I), K' представляет собой -Cy1-группу, Y представляет собой гидрокси группу или атом галогена, и Z представляет собой атом галогена,
с получением соединения формулы (XIII):
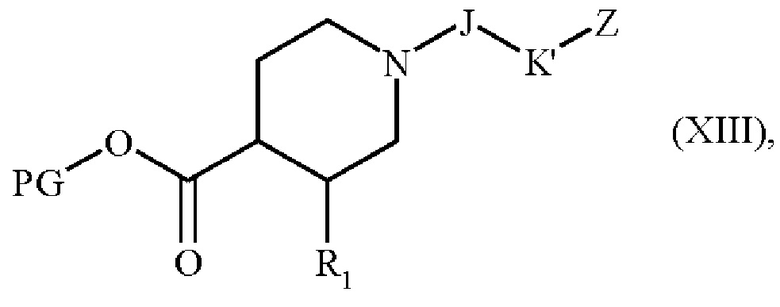
где R1, J, K', Z и PG являются такими, как определено выше, и
соединение формулы (XIII) затем подвергают сочетанию с соединением формулы (X):
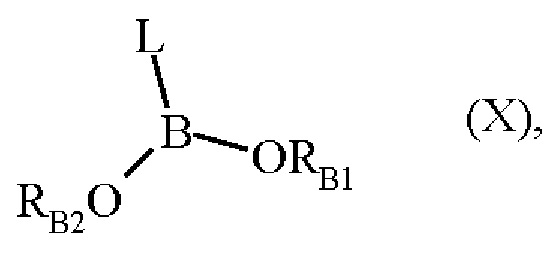
где L является таким, как определено для формулы (I), и RB1 и RB2 представляют собой атом водорода, линейную или разветвленную (C1-C6)алкильную группу, или RB1 и RB2 соединены линейной или разветвленной (С2-С6)алкиленовой группой,
с получением соединения формулы (XIV):
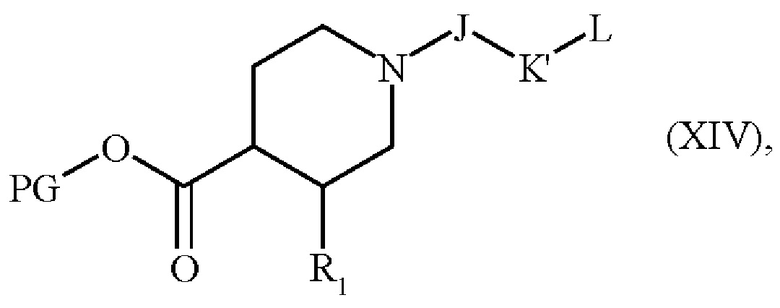
где R1, J, K', L и PG являются такими, как определено выше,
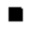 либо сочетанию с соединением формулы (XI):
либо сочетанию с соединением формулы (XI):
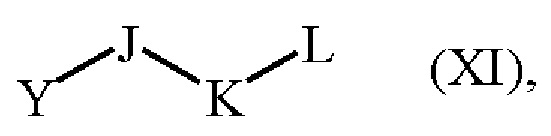
где J, K и L являются такими, как определено для формулы (I), и Y представляет собой гидрокси группу или атом галогена,
с получением соединения формулы (XV),
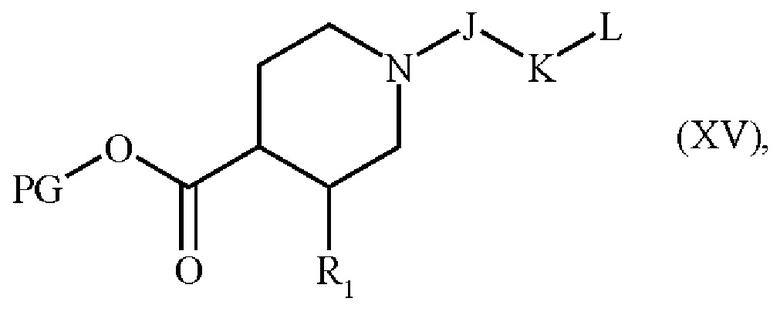
где R1, J, K, L и PG являются такими, как определено выше,
соединения формул (XIV) и (XV), после реакции удаления защитной группы PG, затем подвергают сочетанию с соединением формулы (II),
с получением соединения формулы (XVI):
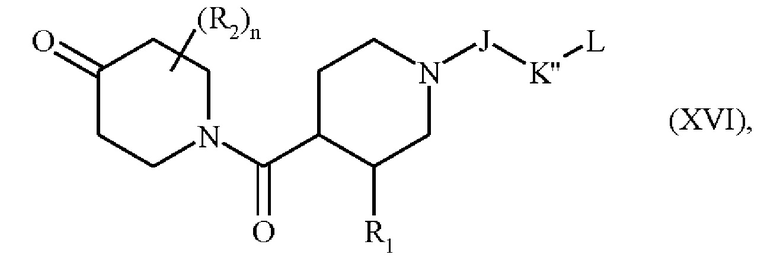
где R1, r2, J, L и n являются такими, как определено выше, и Kʺ означает либо K', либо K, как определено выше,
соединение формулы (XVI) затем превращают в эпоксидное соединение формулы (XVII):
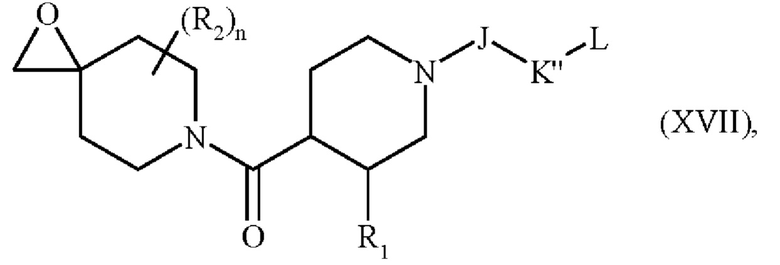
где R1, r2, J, Kʺ, L и n являются такими, как определено выше, и
соединение формулы (XVII) затем подвергают сочетанию с соединением формулы (VI):

где W является таким, как определено для формулы (I),
с получением соединения формулы (I), которое можно очистить в соответствии с обычными методиками разделения, превратить, при необходимости, в его соли присоединения с фармацевтически приемлемой кислотой или основанием и необязательно разделить на его изомеры в соответствии с обычными методиками разделения,
при этом следует понимать, что в любое время, признанное подходящим в ходе описанного выше способа, некоторые группы (гидрокси, амино) исходных реагентов или промежуточных соединений синтеза могут быть защищены, впоследствии лишены защиты и функционализированы, как того требует синтез.
19. Фармацевтическая композиция, ингибирующая активность белка USP7, содержащая соединение формулы (I) по любому из пп. 1-16 или его соль присоединения с фармацевтически приемлемой кислотой или основанием в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
20. Применение фармацевтической композиции по п. 19 в качестве проапоптотических и/или антипролиферативных средств.
21. Применение фармацевтической композиции по п. 20 для лечения злокачественных заболеваний, аутоиммунных заболеваний и заболеваний иммунной системы.
22. Применение фармацевтической композиции по п. 21 для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронического лимфоидного лейкоза, рака ободочной кишки, пищевода и печени, лимфобластного лейкоза, острого миелоидного лейкоза, лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы, рака поджелудочной железы и мелкоклеточного рака легкого.
23. Применение фармацевтической композиции по п. 19 для изготовления лекарственных средств для применения в качестве проапоптотических и/или антипролиферативных средств.
24. Применение фармацевтической композиции по п. 19 для изготовления лекарственных средств для применения для лечения злокачественных заболеваний, аутоиммунных заболеваний и заболеваний иммунной системы.
25. Применение фармацевтической композиции по п. 19 для изготовления лекарственных средств для применения для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронического лимфоидного лейкоза, рака ободочной кишки, пищевода и печени, лимфобластного лейкоза, острого миелоидного лейкоза, лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы, рака поджелудочной железы и мелкоклеточного рака легкого.
26. Применение соединения формулы (I) по любому из пп. 1-16 или его соли присоединения с фармацевтически приемлемой кислотой или основанием для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронического лимфоидного лейкоза, рака ободочной кишки, пищевода и печени, лимфобластного лейкоза, острого миелоидного лейкоза, лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы, рака поджелудочной железы и мелкоклеточного рака легкого.
27. Применение соединения формулы (I) по любому из пп. 1-16 или его соли присоединения с фармацевтически приемлемой кислотой или основанием для изготовления лекарственных средств для применения для лечения рака мочевого пузыря, головного мозга, молочной железы и матки, хронического лимфоидного лейкоза, рака ободочной кишки, пищевода и печени, лимфобластного лейкоза, острого миелоидного лейкоза, лимфом, меланом, злокачественных заболеваний крови, миелом, рака яичников, немелкоклеточного рака легкого, рака предстательной железы, рака поджелудочной железы и мелкоклеточного рака легкого.
28. Комбинация соединения формулы (I) по любому из пп. 1-16 с противоопухолевыми средствами, выбранными из генотоксичных средств, митотических ядов, антиметаболитов, ингибиторов протеасом, ингибиторов киназ, ингибиторов белок-белкового взаимодействия, иммуномодуляторов, ингибиторов Е3 лигазы, терапии с использованием Т-клеток с химерными антигенными рецепторами и антител.
29. Фармацевтическая композиция, ингибирующая активность белка USP7, содержащая комбинацию по п. 28 в комбинации с одним или несколькими фармацевтически приемлемыми наполнителями.
30. Применение комбинации по п. 28 для лечения злокачественных заболеваний.
31. Применение комбинации по п. 28 для изготовления лекарственных средств для применения для лечения злокачественных заболеваний.
32. Применение соединения формулы (I) по любому из пп. 1-16 для лечения злокачественных заболеваний, требующих проведения радиотерапии.
| RU 2014112692 A, 10.10.2015 | |||
| WO 2008108957 A2, 12.09.2008. |
Авторы
Даты
2021-02-04—Публикация
2017-06-09—Подача