Область техники
Настоящее изобретение относится к способу получения мутированных микроорганизмов, устойчивых к явлению гибели под действием лактозы, и к микроорганизмам, получаемым указанным способом. Такие сконструированные микроорганизмы могут использоваться для производства специальных продуктов, включая, например, специальные углеводы, гликолипиды и галактозилированные соединения, но не ограничиваясь ими.
Уровень техники
Гибель под действием лактозы - это хорошо известная и хорошо изученная закономерность, согласно которой рост многих организмов подавляется в присутствии лактозы и другого источника углерода. Точный механизм, лежащий в основе этого явления, тем не менее, остается неизвестным, хотя ясно, что необходимо для запуска этого механизма. Гибель под действием лактозы наблюдается, когда лактозу добавляют к микробной культуре, растущей на другом источнике углерода, например, на глицерине или сахарозе, но не ограничиваясь ими. Кроме того, это происходит, когда ген лактозного транспортера либо индуцируется, либо конститутивно экспрессируется (33, 39, 75). Впервые гибель под действием лактозы наблюдали у Е. coli, когда экспрессию лактозной пермеазы модулировали с помощью IPTG и лактозы в хемостатных условиях (28). Позднее гибель под действием лактозы наблюдали также у Rhizobium meliloti, Kluyveromyces lactis и Zymomonas mobilis (55, 70, 77). Одной из возможных причин этого явления называли "высокую цену" активности лактозного транспортера для клетки, для компенсации таких больших затрат происходило снижение или ингибирование роста, кроме того, это также связано с внеклеточной концентрацией лактозы (34), которая в большинстве технологических процессов поддерживается высокой, чтобы получить достаточно высокие титры и выходы продукта. Тем не менее в данной области техники считается, что до тех пор, пока в этих условиях происходит транспорт лактозы, будет наблюдаться и гибель под действием лактозы. Для решения проблемы гибели под действием лактозы было предложено осуществить делецию лактозной пермеазы или сильно нарушить поглощение лактозы (34). Например, Lodi et al. (55) осуществили делецию (нокаут) гена лактозной пермеазы у K. lactis и обнаружили, что гибель под действием лактозы больше не наблюдается. В ходе этих экспериментов также было показано, что спонтанные мутации приводили к появлению штаммов, отрицательных по явлению гибели под действием лактозы, у которых были обнаружены сильные нарушения поглощения лактозы. Тем не менее, поглощение лактозы важно для эффективного синтеза специальных продуктов или биопродуктов. Таким образом, очевидно, что делеция лактозной пермеазы или сильное нарушение активности лактозной пермеазы не являются решением, поскольку продукция таких биопродуктов требует 1) эффективного поглощения лактозы и 2) наличия экспрессионной кассеты, с которой не связан «фенотип гибели под действием лактозы». Лактозная пермеаза уже использовалась ранее для производства биопродуктов на основе лактозы, но без решения проблемы «фенотипа гибели под действием лактозы». В прошлом эту проблему решали либо за счет сильного снижения поглощения лактозы (и, следовательно, это приводило к тому, что продуцировалось мало специальных продуктов на основе лактозы или они не продуцировались совсем), либо за счет разъединения фазы роста и фазы продукции, чтобы вначале нарастить достаточное количество биомассы. После окончания этой фазы роста во вторую фазу добавляли лактозу для получения специального продукта. В эту вторую фазу рост прекращается или заметно уменьшается (59).
Таким образом, в настоящее время, чтобы избежать гибели под действием лактозы, поглощение лактозы должно быть прекращено или сильно нарушено, поскольку нормальное поглощение лактозы всегда будет приводить к гибели под действием лактозы. Наоборот, настоящее изобретение раскрывает методику скрининга с целью обнаружения экспрессионных кассет лактозной пермеазы, которые могли бы обеспечить эффективное поглощение лактозы без последующей гибели под действием лактозы.
Лактоза является строительным блоком для многих биопродуктов, более конкретно, для специальных углеводов (14), гликолипидов и галактозилированных соединений, таких как галактозиллипиды, галактозилцерамиды и галактозилированные агликоны. Часто остатки галактозы используются для таргетной доставки фармацевтических агентов к конкретным органам (28). Использование лактозы в качестве субстрата в комбинации с другими веществами, тем не менее, не так очевидно, как может показаться, из-за описанного выше явления «гибели под действием лактозы». В большинстве случаев для избегания явления гибели под действием лактозы требуется применять многофазные системы получения, сопряженные клеточные системы не растущих клеток (32, 48).
Основной структурный каркас многих специальных углеводов состоит из остатков лактозы или галактозы. Конкретнее, олигосахариды человеческого молока и, следовательно, олигосахариды материнского молока, обширная группа сахаридов и олигосахаридов, построены из остатков галактозы и лактозы (15). Эти углеводы далее модифицируются остатками сахаров, такими как, например, N-ацетилглюкозамин, N-ацетилгалактозамин, сиаловые кислоты (такие как N-ацетилнейраминат, N-глюкоилнейраминат, 2-кето-3-дезокси-D-глицеро-галакто-нонулосоновая кислота и другие) (21), L-фукоза и другие. Для синтеза этих соединений необходимы активированные углеводы, такие как UDP-N-ацетилглюкозамин, UDP-N-ацетилгалактозамин, CMP-сиаловая кислота, GDP-фукоза и другие, которые являются дорогостоящими и трудно синтезируемыми, но которые в оптимальном виде продуцируются живыми растущими клетками, так как для их биосинтеза требуется энергия.
Олигосахаридные компоненты человеческого/материнского молока обладают противовоспалительным и пребиотическим действиями и/или могут использоваться в терапевтических целях в качестве нутрицевтика, противовоспалительного агента, пребиотика или фармацевтического агента (15, 24, 68). Тем не менее, по-прежнему существует необходимость в разработке эффективного способа получения перечисленных высокоценных соединений.
Настоящее изобретение описывает синтетические экспрессирующие системы для лактозных транспортеров, которые не приводят к гибели под действием лактозы даже при высоких концентрациях лактозы. Мутированные организмы, содержащие указанные экспрессирующие системы, таким образом, могут использоваться для производства описанных выше биопродуктов.
Краткое описание чертежей
Фигура 1. Влияние лактозы на штамм Е. coli дикого типа. Стрелкой указан момент добавления лактозы к одной из культур, в результате чего рост этой культуры немедленно прекратился, тогда как другой штамм продолжил расти в другой культуре.
Фигура 2. Влияние лактозы на штамм Е. coli, мутантный по гену лактозного транспортера, у которого экспрессия лактозного транспортера изменена с помощью синтетического конститутивного промотора. Стрелкой указан момент добавления лактозы к среде в одной из культур. В этом случае это не оказывало никакого эффекта на рост. Таким образом, эти мутантные штаммы могут быть выбраны таким способом.
Фигура 3. Пример комбинации промотора, RBS и последовательности лактозного транспортера (SEQ ID №1), для которой при введении в мутантный штамм Е. coli не наблюдается гибели под действием лактозы.
Фигура 4. Пример последовательности гена лактозной пермеазы, трансляционно связанного с геном lacZ (SEQ ID №2).
Фигура 5. Пример последовательности гена лактозной пермеазы lacY, трансляционно связанного с геном cat (SEQ ID №3).
Фигура 6. Пример последовательности гена лактозной пермеазы K. maxianus, трансляционно связанного с геном aph 1 (SEQ ID №4).
Фигура 7. Пример последовательности гена лактозной пермеазы lacy, связанного с аптамером, который связывается с (Z)-4-(3,5-дифтор-4-гидроксибензилиден)-1,2-диметил-1Н-имидазол-5(4Н)-оном (SEQ ID №5), благодаря чему возможно обнаружение экспрессии лактозной пермеазы.
Фигура 8. Устойчивость к хлорамфениколу штамма сравнения, содержащего плазмиду сравнения pSC101 без гена лактозной пермеазы, трансляционно связанного с геном устойчивости к хлорамфениколу, и мутантного штамма с геном лактозной пермеазы, трансляционно связанным геном устойчивости к хлорамфениколу. По оси X отложены различные тестируемые концентрации хлорамфеникола, по оси Y отложены значения оптической плотности культуры после 48 часов инкубации. Штамм сравнения демонстрирует замедление роста при более низких концентрациях хлорамфеникола в процессе скрининга по сравнению с мутантным штаммом, что подтверждает, что скрининг на экспрессию лактозной пермеазы может быть осуществлен путем трансляционного связывания ее гена с геном устойчивости к антибиотику. Следовательно, организмы, экспрессирующие лактозную пермеазу, могут быть отобраны из смеси не экспрессирующих и экспрессирующих организмов описанным образом.
Фигура 9. Устойчивость к хлорамфениколу штамма сравнения, содержащего плазмиду сравнения pSC101 без гена лактозной пермеазы, трансляционно связанного с геном устойчивости к хлорамфениколу, и мутантного штамма с геном лактозной пермеазы, трансляционно связанным с геном устойчивости к хлорамфениколу. По оси X отложены различные тестируемые концентрации хлорамфеникола, по оси Y отложены значения оптической плотности культуры после 92 часов инкубации. Штамм сравнения демонстрирует замедление роста при более низких концентрациях хлорамфеникола в процессе скрининга по сравнению с мутантным штаммом, что подтверждает, что скрининг на экспрессию лактозной пермеазы может быть осуществлен путем трансляционного связывания ее гена с геном устойчивости к антибиотику. Следовательно, организмы, экспрессирующие лактозную пермеазу, могут быть отобраны из смеси не экспрессирующих и экспрессирующих организмов описанным образом.
Фигура 10. pCXP14-FT_H. pylori (SEQ ID №6).
Фигура 11. Влияние лактозы на штамм дрожжей дикого типа (Kluyveromyces marxianus lactis). Стрелкой указан момент добавления лактозы к одной из культур, в результате чего рост этой культуры немедленно прекратился, тогда как другой штамм продолжил расти в другой культуре.
Фигура 12. Влияние лактозы на штаммы дрожжей (Saccharomyces cerevisiae) с мутантным лактозным транспортером, у которых экспрессия лактозного транспортера изменена с помощью синтетического конститутивного промотора. Стрелкой указан момент добавления лактозы к среде в одной из культур. В этом случае это не оказывало никакого эффекта на рост. Таким образом, эти мутантные штаммы могут быть выбраны таким способом.
Фигура 13. Пример комбинации промотора (p1), последовательности Козак, кодирующей последовательности лактозной пермеазы K. marxianus и терминатора (SEQ ID №7), для которой при введении в мутантный штамм дрожжей не наблюдается гибели под действием лактозы.
Фигура 14. Пример комбинации промотора (р2), последовательности Козак, кодирующей последовательности лактозной пермеазы K. marxianus и терминатора (SEQ ID №8), для которой при введении в мутантный штамм дрожжей не наблюдается гибели под действием лактозы.
Фигура 15. Пример комбинации промотора, последовательности Козак, кодирующей последовательности β-галактозидазы K. marxianus и терминатора (SEQ ID №9).
Фигура 16. HR1 рДНК (SEQ ID №10).
Фигура 17. HR2 рДНК (SEQ ID №11).
Фигура 18. Примеры выбранных последовательностей, обнаруженных с помощью методики скрининга на отсутствие гибели под действием лактозы, как описано в примерах (SEQ ID №12-57).
Фигура 19. Относительная скорость роста экспрессионных кассет лактозной пермеазы, по сравнению с диким типом. Усы графика обозначают стандартное отклонение, по меньшей мере, 3 повторных измерений. Последовательности, соответствующие номерам последовательностей по оси X, приведены на Фигуре 18.
Фигура 20. Последовательность экспрессионной кассеты lacIQ_lacY, которую тестировали на наличие гибели под действием лактозы в примере 16 (SEQ ID №58).
Фигура 21. Влияние лактозы на штамм Е. coli дикого типа и мутантный штамм placIQ_lacY. Оба штамма растили с добавлением и без добавления лактозы в середине экспоненциальной фазы. Стрелкой обозначен момент добавления лактозы. Рост обоих штаммов был сильно нарушен в результате добавления лактозы.
Сущность изобретения
Настоящее изобретение относится к способу получения микроорганизмов, устойчивых к явлению гибели под действием лактозы, выращенных в окружении, в котором лактоза комбинируется с другим источником углерода, где указанный способ включает:
a. мутирование экспрессии лактозных транспортеров в микроорганизмах, где указанная мутация приводит к экспрессируемому лактозному транспортеру,
b. выращивание указанных мутированных микроорганизмов на среде, включающей источник углерода, отличный от лактозы,
c. добавление лактозы к указанной среде в процессе роста указанных мутированных микроорганизмов, и
d. отбор микроорганизмов, устойчивых к явлению гибели под действием лактозы, растущих на указанной среде, включающей лактозу.
Конкретнее, настоящее изобретение относится к способу получения микроорганизмов, устойчивых к явлению гибели под действием лактозы, выращенных в окружении, в котором лактоза комбинируется с другим источником углерода, где указанный способ включает:
a. мутирование экспрессии лактозных транспортеров в микроорганизмах, где указанная мутация приводит к экспрессии указанного лактозного транспортера
b. выращивание указанных мутированных микроорганизмов на среде, включающей источник углерода, отличный от лактозы,
c. добавление лактозы к указанной среде в процессе роста указанных мутированных микроорганизмов, и
d. отбор микроорганизмов, устойчивых к явлению гибели под действием лактозы, растущих на указанной среде, включающей лактозу, и которые сохраняют, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера.
Настоящее изобретение дополнительно относится к способу, как указано выше, где стадия а) осуществляется путем введения гетерологичного промотора перед эндогенным или экзогенным геном лактозного транспортера, и/или путем мутирования нетранслируемой области перед кодирующей последовательностью, которая содержит последовательность связывания рибосомы или последовательность Козак, и/или путем модифицирования частоты использования кодонов в эндогенном гене лактозного транспортера.
Настоящее изобретение также относится к способу, как описано выше, где указанное введение гетерологичного промотора перед эндогенным или экзогенным геном лактозного транспортера осуществляется за счет а) делеции эндогенных лактозных транспортеров из генома и введения их в другой участок в геноме указанного микроорганизма, или b) за счет введения гетерологичного промотора перед эндогенными лактозными транспортерами, или c) за счет нокаута эндогенного лактозного промотора и введения гетерологичного промотора в тот же участок генома указанного микроорганизма.
Настоящее изобретение дополнительно относится к способу, описанному выше, где экспрессия лактозной пермеазы на стадии b) обнаруживается с помощью трансляционного связывания с репортерным геном и/или через связывание с аптамером.
Настоящее изобретение относится к способу, описанному выше, где экспрессию лактозного транспортера обнаруживают посредством генетических конструкций, приведенных в SEQ ID №2, 3, 4 и/или 5.
Настоящее изобретение дополнительно относится к способу, описанному выше, где указанный лактозный транспортер представляет собой лактозную пермеазу.
Настоящее изобретение дополнительно относится к способу, описанному выше, где указанный микроорганизм представляет собой бактерию, дрожжи или грибы.
Настоящее изобретение относится также к последовательностям промотора, нетранслируемым областям перед кодирующей последовательностью, которые содержат последовательность связывания рибосомы или последовательность Козак, и/или последовательностям лактозной пермеазы, реализующим экспрессию лактозного транспортера, которая не приводит к фенотипу гибели под действием лактозы, когда микроорганизм, содержащий такую последовательность, растет в окружении, в котором лактоза комбинируется с другим (другими) источником (источниками) углерода, и получен способом, описанным выше.
Настоящее изобретение также относится к микроорганизму, устойчивому к явлению гибели под действием лактозы, выращенному в окружении, в котором лактоза комбинируется с другим источником углерода, и получен способом, описанным выше.
Более конкретно, настоящее изобретение относится к микроорганизму, описанному выше и содержащему гетерологичную последовательность перед геном лактозного транспортера, приведенную в SEQ ID №1, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46,47, 48, 49, 50, 51, 52, 53, 54, 55, 56 или 57.
Настоящее изобретение относится также к микроорганизму, устойчивому к явлению гибели под действием лактозы, в котором гены, кодирующие ферменты из путей деградации лактозы и/или галактозы, являются менее функциональными или нефункциональными.
Настоящее изобретение также относится к применению микроорганизма, описанного выше, для производства специальных продуктов на основе лактозы, таких как специальные углеводы, гликолипиды и галактозилированные соединения.
Настоящее изобретение дополнительно относится к применению микроорганизма, описанного выше, где указанные специальные углеводы представляют собой 2-фукозиллактозу, или 2'-фукозиллактозу, или 3-фукозиллактозу, или 2',3-дифукозиллактозу, или лакто-N-триозу, или лакто-N-тетраозу, или лакто-N-тетраозу, или 3'-сиалиллактозу, или 6'-сиалиллактозу.
Подробное описание изобретения
Настоящее изобретение описывает новый способ для избегания гибели под действием лактозы путем изменения экспрессии лактозного транспортера за счет применения генно-инженерного организма, мутантного организма, экспрессирующего лактозный транспортер. С этой целью экзогенный и/или эндогенный ген лактозного транспортера экспрессируют с помощью гетерологичного промотора, что не приводит к фенотипу гибели под действием лактозы, и/или модифицируют частоту использования кодонов лактозного транспортера, чтобы получить измененную экспрессию лактозного транспортера, что не приводит к фенотипу гибели под действием лактозы. Для этого природная система контроля экспрессии лактозных транспортеров должна быть удалена и/или замещена таким образом, чтобы явление гибели под действием лактозы не наблюдалось. Например, встречающуюся в природе экспрессионную кассету лактозного транспортера удаляют из генома и заново вводят ее в другой участок, и/или гетерологичный промотор вводят перед лактозным транспортером в его исходном месте расположения, и/или лактозный транспортер сначала нокаутируют, а потом вводят с гетерологичным промотором в тот же самый участок генома и/или в другой участок генома, и/или лактозный транспортер вводят в оперон, который экспрессируется под действием гетерологичного промотора.
Настоящее изобретение, таким образом, относится к способу получения микроорганизмов, устойчивых к явлению гибели под действием лактозы, выращенных в окружении, в котором лактоза комбинируется с другим источником углерода, где указанный способ включает: 1) мутирование экспрессии лактозных транспортеров в микроорганизмах, где указанная мутация приводит к экспрессии указанного лактозного транспортера, 2) выращивание указанных мутированных микроорганизмов на среде, включающей источник углерода, отличный от лактозы, 3) добавление лактозы к указанной среде в процессе роста указанных мутированных микроорганизмов и 4) отбор микроорганизмов, устойчивых к явлению гибели под действием лактозы, растущих на указанной среде, включающей лактозу, и которые сохраняют, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера.
Термин «гибель под действием лактозы» относится к явлению задержки или остановки роста организма, который выращен в окружении, в котором лактоза или галактозид комбинируется с другим (другими) источником (источниками) углерода. Источники углерода представляют собой глицерин, мальтозу, глюкозу, фруктозу, сахарозу, фукозу, маннозу, сиаловую кислоту, крахмал, целлюлозу, полиолы (такие как маннит, ксилит, сорбит), органические кислоты (лактат, сукцинат, ацетат и другие) и/или пентозы (ксилоза, арабиноза и другие), но не ограничиваясь этим.
Настоящее изобретение описывает способ идентификации экспрессирующих систем лактозной пермеазы, которые не приводят к гибели под действием лактозы. Этот способ включает анализ роста мутантного штамма, к которому добавляют лактозу в середине экспоненциальной фазы. Этот способ может быть осуществлен в высокопроизводительном формате в микротитрационных планшетах или с помощью клеточных сортеров, обеспечивающих скрининг множества промоторов, сайтов связывания рибосомы, частоты использования кодонов и других факторов, которые могут влиять на экспрессию лактозной пермеазы в мутантном микроорганизме. Настоящее изобретение описывает способ обнаружения экспрессии лактозной пермеазы посредством трансляционного связывания и/или связывания с аптамером и отбора последовательностей, которые приводят к экспрессии, с помощью репортерного гена, такого как, например, ген устойчивости к антибиотику (например, хлорамфеникол, генетицин G418, но не ограничиваясь ими), ген флуоресцентного белка, ген гидролазы (например, галактозид азы, ксиланазы, но не ограничиваясь ими) и/или последовательность аптамера, но не ограничиваясь ими. Последовательности, приводящие к экспрессии лактозной пермеазы, далее отбирают с помощью репортерного гена путем выращивания на среде с антибиотиком, колориметрическим способом (например, X-gal), и/или с помощью клеточного сортера с активацией флуоресценцией, который сортирует флуоресцентные клетки, и/или с помощью анализа аптамера, например, с использованием (Z)-4-(3,5-дифтор-4-гидроксибензилиден)-1,2-диметил-1Н-имидазол-5(4Н)-она (37, 64), но не ограничиваясь этим. Настоящее изобретение дополнительно описывает методику скрининга для обнаружения мутантных организмов, экспрессирующих лактозный транспортер, которые не подвергаются гибели под действием лактозы. Кроме того, настоящее изобретение описывает создание библиотек экспрессионных кассет лактозной пермеазы из библиотек промоторов, библиотек последовательностей RBS или последовательностей Козак, библиотек терминаторов транскрипции и/или вариантов гена лактозной пермеазы с различной частотой использования кодонов. Эти библиотеки также могут быть созданы с помощью таких способов как сборка по методу Гибсона, сборка методом Golden Gate, сборка методом Cliva, LCR или рестрикцией и лигированием (25, 36, 50, 79), но не ограничиваясь этим.
Термин «которые сохраняют, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера» относится к тому факту, что мутированные микроорганизмы по настоящему изобретению, несмотря на то, что они устойчивы к гибели под действием лактозы, должны сохранять, по меньшей мере, 50% (т.е. 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 99%) от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера.
Термин «экспрессионная кассета» относится к любой последовательности, в которой присутствуют последовательность промотора, последовательность нетранслируемой области (содержащая последовательность связывания рибосомы или последовательность Козак), кодирующую последовательность (например, последовательность гена лактозной пермеазы) и необязательно терминатор транскрипции (18).
Термин «лактозный транспортер» относится к любому белку, экспрессируемому в микроорганизме, который способен транслоцировать (транспортировать) лактозу через цитоплазматическую мембрану. Такими белками являются, например, лактозные пермеазы (транспортеры из суперсемейства MFS, или суперсемейства мембранных транспортеров Major Facilitator Superfamily).
Термин «гетерологичный промотор» относится к любому промотору, который не встречается в природе перед кодирующей последовательностью. "Промотор" представляет собой полную последовательность связывания с РНК-полимеразой, расположенную перед сайтом начала транскрипции, и нетранслируемую область перед кодирующей последовательностью. Последовательность "гетерологичного промотора", таким образом, представляет собой 1) вариант встречающейся в природе последовательности промотора, содержащей, по меньшей мере, 1 мутацию (т.е. 1, 2, 3, 4 или более), и/или 2) нативный промотор из мутантного микроорганизма, экспрессирующего лактозный транспортер, который не встречается в природе перед кодирующей последовательностью указанного транспортера, и/или 3) последовательность, которая не встречается в природе в микроорганизме, экспрессирующем лактозный транспортер, и/или 4) искусственный промотор, который представляет собой сконструированный in silico промотор. Эти промоторы могут быть найдены в библиотеках, например, описанных Alper et al. (2005), и/или НХТ7р, Hammer et al. (2006), De Mey et al. (2007), Coussement et al (2014) или Mutalik et al (2013) (3, 25, 29, 41, 60), (66), или Blount et al (2012), могут представлять собой промоторы, такие как ADH1p, TEF1p, TEF2p, GPDp, PDC1p, FBA1p, PGK1p, PGI1p, TDH2p, PYK1p, ENO2p, GPM1p, TPI1p (13), но не ограничиваясь ими, или промоторы, описанные, например, Rhodius et al. (2012). Термин «искусственный промотор» также относится к промоторам с последовательностями ДНК, которые представляют собой комбинации последовательности нативного (аутологичного) промотора с частями последовательностей других (аутологичных или гетерологичных) промоторов. Последовательности таких «искусственных промоторов» могут быть найдены в базах данных, таких как, например, partsregistry.org (19). Гетерологичные промоторы приводят либо к конститутивной экспрессии, либо к регулируемой экспрессии посредством транскрипционного фактора.
Термин «конститутивная экспрессия» означает экспрессию, которая не регулируется транскрипционными факторами, отличными от субъединиц РНК-полимеразы (например, бактериальные сигма-факторы), в определенных условиях роста. Неограничивающими примерами таких транскрипционных факторов являются CRP, LacI, ArcA, Cra, IclR и другие у Е. coli или Aft2p, Crz1p, Skn7 и другие у Saccharomyces cerevisiae, или DeoR, GntR, Fur и другие у В. subtilis. Эти транскрипционные факторы связываются с определенной последовательностью и могут блокировать или усиливать экспрессию в определенных условиях роста. РНК-полимераза связывается с определенной последовательностью для инициации транскрипции, например, посредством сигма-фактора в прокариотических клетках.
Термин «регулируемая экспрессия» означает экспрессию, которая регулируется транскрипционными факторами, отличными от субъединиц РНК-полимеразы (например, бактериальные сигма-факторы), в определенных условиях роста. Примеры таких транскрипционных факторов описаны выше.
Термин «нетранслируемая область» перед кодирующей последовательностью, которая содержит сайты связывания рибосомы или последовательности Козак, относится к последовательности между последовательностью связывания РНК- полимеразы и кодирующей последовательностью. Такой нетранслируемой областью является также последовательность, которая в природе присутствует перед кодирующей последовательностью, и/или последовательность, которая встречается в природе в микроорганизме, экспрессирующем лактозный транспортер, и/или последовательность, полученная из других организмов (прокариотов или эукариотов), и/или искусственно сконструированная последовательность, которая относится к неприродным или сконструированным in silico сайтам связывания рибосомы с известной или измеряемой скоростью трансляции, эти последовательности могут быть получены из библиотек, как описано Mutalik et al. (2013) (60), или созданы с помощью алгоритмов, например, как описано Salis et al. (2009) (67), или могут быть обнаружены в базах данных, таких как partsregistry.org (19).
Термин «модифицированная частота использования кодона» относится к изменению кодонов, использованных в кодирующей последовательности ДНК, либо на кодоны, используемые организмом чаще, либо на кодоны, используемые организмом реже. Частоту использования кодонов определяют с помощью баз данных, таких как база данных частоты использования кодонов (61), и частоту использования кодонов оптимизируют с помощью специальных алгоритмов оптимизации частоты использования кодонов (73).
Термин «трансляционно связанный» относится к связыванию экспрессии целевого гена с экспрессией репортерного гена, например, гена зеленого флуоресцентного белка, гена устойчивости к антибиотику, гена токсина (49, 53, 58, 63). Термин «трансляционный сенсор» относится к любому механизму, который может быть показателем экспрессии и трансляции гена, например, к флуоресцентным меткам и расщепленным меткам, описанным в следующих ссылках (17, 72).
Термин «связывание с аптамером» относится к введению последовательности аптамера в информационную (матричную) РНК лактозного транспортера, которая может быть обнаружена с помощью флуорофора, такого как (Z)-4-(3,5-дифтор-4- гидроксибензилиден)-1,2-диметил-1Н-имидазол-5(4Н)-он (37, 64).
Термин «анализ роста» относится к анализу кривой роста организма. Этот организм культивируется в среде для роста в условиях роста. Термин условие роста относится ко всем параметрам окружающей среды, таким как рН, температура, растворенный кислород. рН устанавливается с помощью буфера рН или за счет контроля рН и равен, например, 4, 4,5, 5, 5,5, 6, 6,5, 7, 7,5 или 8, но не ограничиваясь этим. Температура устанавливается равной, например, 25, 28, 30, 32, 34, 37, 40, 42, 45°С, но не ограничиваясь этим. Уровень растворенного кислорода соответствует анаэробным, микро-аэробным (концентрация растворенного кислорода меньше 1,5 мг/л), либо аэробным условиям.
Термин «среда» или «среда для роста» относится к любому раствору, содержащему вещества, необходимые организму для роста. Этими веществами являются источники азота, такие как соли аммония, нитраты, дрожжевой экстракт, пептон, казаминовые кислоты и/или аминокислоты, но не ограничиваясь ими, источники фосфора, такие как фосфаты, но не ограничиваясь ими, источники серы, такие как сульфаты, но не ограничиваясь ими, элементы, такие как медь, кобальт, железо, селен, иод, молибдат, магний, кальций, калий, натрий, цинк, никель, марганец, но не ограничиваясь ими, и/или борная кислота, и/или витамины, такие как тиамин, пантотеновая кислота, но не ограничиваясь ими, и/или ниацин, и/или источники углерода, такие как глицерин, мальтоза, глюкоза, фруктоза, сахароза, фукоза, манноза, сиаловая кислота, крахмал, целлюлоза, полиолы (такие как маннит, ксилит, сорбит), органические кислоты (лактат, сукцинат, ацетат и другие), и/или пентозы (ксилоза, арабиноза и другие), но не ограничиваясь ими.
Термин «организм» или «клетка», как указано выше, относится к микроорганизму, выбранному из списка, состоящего из бактерий, дрожжей или грибов, или относится к растительной или животной клетке. Бактерии предпочтительно принадлежат филуму Proteobacteria, или филуму Firmicutes, или филуму Cyanobactria, или филуму Deinococcus-Thermus. Бактерии, принадлежащие филуму Proteobacteria, предпочтительно принадлежит семейству Enterobacteriaceae, предпочтительно виду Escherichia coli. Бактерии предпочтительно относятся к любому штамму, принадлежащему виду Escherichia coli, например, включая, но не ограничиваясь, Escherichia coli В, Escherichia coli С, Escherichia coli W, Escherichia coli K12, Escherichia coli Nissle. Конкретнее, последний термин относится к культивируемым штаммам Escherichia coli, обозначаемым как штаммы Е. coli K12, которые хорошо адаптированы к лабораторному окружению, и, в отличие от штаммов дикого типа, потеряли свою способность расти в кишечнике. Хорошо известными примерами штаммов Е. coli K12 являются K12 дикого типа, W3110, MG1655, М182, МС1000, МС1060, МС1061, МС4100, JM101, NZN111 и АА200. Таким образом, настоящее изобретение, в частности, относится к мутированному и/или трансформированному штамму Escherichia coli, как указано выше, где указанный штамм Е. coli представляет собой штамм K12. Конкретнее, настоящее изобретение относится мутированному и/или трансформированному штамму Escherichia coli, как указано выше, где указанный штамм K12 представляет собой Е. coli MG1655. Бактерии, принадлежащие к филуму Firmicutes, предпочтительно принадлежат к Bacilli, предпочтительно к видам Bacillus. Дрожжи предпочтительно принадлежат к филуму Ascomycota, или филуму Basidiomycota, или филуму Deuteromycota, или филуму Zygomycetes. Дрожжи предпочтительно принадлежат к роду Saccharomyces, Pichia, Hansunella, Kluyveromyces, Yarrowia или Starmerella. Грибы предпочтительно принадлежат к роду Rhizopus, Dictyostelium или Aspergillus.
Настоящее изобретение описывает организмы, которые способны осуществлять поглощение лактозы и не подвергаться гибели под действием лактозы и которые способны превращать лактозу или остатки галактозы в ее составе в специальный продукт. Более конкретно, указанные специальные продукты или биопродукты представляют собой специальные углеводы, гликолипиды, включая галактолипиды и/или лактолипиды, но не ограничиваясь ими, и/или галактозилированные соединения, такие как галактозиллипиды, галактозилцерамиды и/или галактозилированные агликоны.
Настоящее изобретение описывает организмы, которые способны осуществлять поглощение лактозы, не подвергаясь гибели под действием лактозы, и превращать указанную лактозу в олигосахариды человеческого молока, такие как 3-фукозиллактоза, 2'-фукозиллактоза, 6-фукозиллактоза, 2',3-дифукозиллактоза, 2',2-дифукозиллактоза, 3,4-дифукозиллактоза, 6'-сиалиллактоза, 3'-сиалиллактоза, 3,6-дисиалиллактоза, 6,6'-дисиалиллактоза, 3,6-дисиалиллакто-N-тетраоза, лактодифукотетраоза, лакто-N-тетраоза, лакто-N-неотетраоза, лакто-N-фукопентаоза II, лакто-N-фукопентаоза I, лакто-N-фукопентаоза III, сиалиллакто-N-тетраоза с, сиалиллакто-N-тетраоза b, сиалиллакто-N-тетраоза а, лакто-N-дифукогексаоза I, лакто-N-дифукогексаоза II, лакто-N-гексаоза, лакто-N-неогексаоза, пара-лакто-N-гексаоза, монофукозилмоносиалиллакто-N-тетраоза с, монофукозил пара-лакто-N-гексаоза, монофукозиллакто-N-гексаоза III, изомерная фукозилированная лакто-N-гексаоза III, изомерная фукозилированная лакто-N-гексаоза I, сиалиллакто-N-гексаоза, сиалиллакто-N-неогексаоза II, дифукозил-пара-лакто-N-гексаоза, дифукозиллакто-N-гексаоза, дифукозиллакто-N-гексаоза а, дифукозиллакто-N-гексаоза с, галактозилированный хитозан, фукозилированные олигосахариды и/или сиалилированные олигосахариды, но не ограничиваясь ими.
Настоящее изобретение дополнительно описывает организмы, которые не подвергаются гибели под действием лактозы и которые синтезируют сахара, входящие в состав нуклеотидов, такие как GDP-L-фукоза, GDP-манноза, GDP-глюкоза, CMP-сиаловая кислота, UDP-глюкоза, UDP-галактоза, UDP-N-ацетилглюкозамин, UDP-N-ацетилманнозамин, UDP-N-ацетилгалактозамин, UDP-глюкуроновая кислота, UDP-галактуроновая кислота, UDP-ксилоза, UDP-арабиноза и/или dTDP-рамноза, но не ограничиваясь ими. Термин "сиаловая кислота", согласно определению Varki (1992) (71), относится к группе соединений, таких как нейраминовая кислота, N-ацетилнейраминовая кислота или N-гликозилнейраминовая кислота, но не ограничиваясь ими. Внутриклеточная концентрация или пул GDP-фукозы увеличивается за счет повышающей регуляции метаболического пути синтеза de novo и/или усиления реутилизации. Метаболический путь синтеза de novo состоит из GDP-4- кето-6-дезоксиманноза-3,5-эпимеразы-4-редуктазы или синтазы GDP-фукозы, 4,6-дегидратазы GDP-маннозы, пирофосфорилазы GDP-D-маннозы, изомеразы фосфоманнозы и/или фосфоманномутазы, экспрессия которых увеличивается индивидуально с помощью генетических элементов, таких как промоторы и/или сайты связывания рибосомы, но не ограничиваясь ими, и/или за счет изменения частоты использования кодонов в моноцистроне или полицистроне (структура оперона), и/или с помощью регуляторов arcA iclR в Enter obacteriaceae, и/или с помощью транскрипционного регулятора RcsA в Enterobacteriaceae или гомологичных генов в бактериях, или Xbp1, Spt20, Sfp1, Rpd3, Rap1, Gcr1, Gcn5, Cst6, Abf1, Hsf1, Reb1, Cad1, Sin4, Ash1, Ixr1, Met32, Pho2, Rgr1, Spt7, Swi4 в Saccharomyces cerevisiae, или гомологичных генов в дрожжах или грибах. Метаболический путь реутилизации состоит из киназы L-фукозы и/или пирофосфорилазы GDP-L-фукозы. Пул GDP-маннозы увеличивается за счет повышающей регуляции генов, кодирующих пирофосфорилазу GDP-D-маннозы, изомеразу фосфоманнозы и/или фосфоманномутазу; и/или генов, кодирующих маннокиназу и пирофосфорилазу GDP-D-маннозы. Пул UDP-галактозы увеличивается за счет повышающей регуляции генов, кодирующих галактокиназу, и/или галактоза-1-фосфат-уридилтрансферазу, и/или UDP-галактоза-4-эпимеразу, и/или UDP-галактоза/глюкоза пирофосфорилазу, и/или синтазу лактозы, и/или фосфорилазу лактозы, и/или фосфорилазы сахарозы. Пул UDP-глюкозы увеличивается за счет повышающей регуляции генов, кодирующих глюкокиназу, и/или пирофосфорилазу UDP-глюкозы, и/или фосфорилазу сахарозы, и/или фосфоглюкомутазу, и/или синтазу сахарозы. Пул СМР-сиаловой кислоты увеличивается за счет повышающей регуляции генов, кодирующих L-глутамин:D-фруктоза-6-фосфат-аминотрансферазу, и/или мутазу фосфоглюкозамина, и/или глюкозамин-1-фосфат-ацетилтрансферазу, и/или N-ацетилглюкозамин-1-фосфат-уридилтрансферазу, и/или UDR-N-ацетилглюкозамин-2-эпимеразу, и/или синтазу N-ацетилнейраминовой кислоты, и/или синтетазу цитидин-5'-монофосфат-N-ацетилнейрамината. Пул UDP-N-ацетилглюкозамина увеличивается за счет повышающей регуляции генов, кодирующих L-глутамин : D-фруктоза-6-фосфат-аминотрансферазу, и/или мутазу фосфоглюкозамина, и/или глюкозамин-1-фосфат- ацетилтрансферазу, и/или N-ацетилглюкозамин-1-фосфат-уридилтрансферазу, и/или глюкозамин-6-фосфат-N-ацетилтрансферазу, и/или мутазу фосфоацетилглюкозамина, и/или UDP-N-ацетилглюкозамин-пирофосфорилазу. Пул UDP-N-ацетилманнозамина увеличивается за счет повышающей регуляции генов, опосредующих увеличение пула UDP-N-ацетилглюкозамина, и/или генов, кодирующих UDP-N-ацетилглюкозамин-2-эпимеразу. Пул UDP-N-ацетилглюкозамина увеличивается за счет повышающей регуляции генов, опосредующих увеличение пула UDP-N-ацетилглюкозамина, и/или генов, кодирующих UDP-N-ацетилглюкозамин-С4-эпимеразу. Пул UDP-глюкуроновой кислоты увеличивается за счет повышающей регуляции генов, опосредующих увеличение пула UDP-глюкозы, и/или генов, кодирующих дегидрогеназу UDP-глюкозы. Пул UDP-ксилозы увеличивается за счет повышающей регуляции генов, опосредующих увеличение пула UDP-глюкуроновой кислоты, и/или генов, кодирующих синтазу UDP-D-ксилозы. Пул UDP-галактуроновой кислоты увеличивается за счет повышающей регуляции генов, опосредующих увеличение пула UDP-глюкуроновой кислоты, и/или генов, кодирующих UDP-D-глюкуроновая кислота-4-эпимеразу. Пул UDP-арабинозы увеличивается за счет повышающей регуляции генов, опосредующих увеличение пула UDP-глюкуроновой кислоты, и/или генов, кодирующих UDP-D-ксилоза-4-эпимеразу, и/или киназу арабинозы, и/или пирофосфорилазу UDP-L-арабинозы. Пул dTDP-рамнозы увеличивается за счет повышающей регуляции генов, кодирующих пирофосфорилазу dTDP-глюкозы, и/или dTDP-глюкоза-4,6-дегидратазу, и/или dTDP-4-дегидрорамноза-3,5-эпимеразу, и/или dTDP-4-дегидрорамноза редуктазу, и/или глюкоза-1-фосфат-тимидилтрансферазу, и/или синтазу нуклеотид-рамнозы.
Термин "пул" дополнительно относится к концентрациям метаболитов, которые в естественных условиях встречаются в организме дикого типа, например, концентрации пула сахара, входящего в состав нуклеотидов. Термин "увеличенный пул" относится к значительно увеличенной концентрации указанного пула метаболита по сравнению с пулом метаболита в организме дикого типа.
Термин "повышающая регуляция гена" относится к каждой генетической модификации, которая приводит к усиленной экспрессии гена и/или активности продукта указанного гена. Указанная генетическая модификация представляет собой модификацию промотора, в нетранслируемой области, сайта связывания рибосомы, кодирующей последовательности, локализации гена, структуры интрона/экзона и/или терминатора транскрипции, которая приводит к указанному повышению экспрессии и/или активности.
Кроме того, настоящее изобретение описывает генетически модифицированные организмы, которые способны переносить эти сахара в составе нуклеотидов в моно-, ди- или олигосахариды, такие как галактоза, лактоза, лакто-N-биоза, лакто-N-триоза, лакто-N-тетраоза, лакто-N-неотетраоза, глоботриоза, 2'-фукозиллактоза, 3-фукозиллактоза, 3-сиалиллактоза, 6-сиалиллактоза, олигосахариды человеческого молока, гепарозаны, хитозаны, факторы образования клубеньков (Nod-факторы), гликолипиды и/или агликоны, но не ограничиваясь ими, с помощью фермента гликозилтрансферазы.
Настоящее изобретение также описывает организмы, которые не подвергаются гибели под действием лактозы и которые дополнительно могут модифицировать указанную лактозу с помощью ферментов, таких как гидролазы углеводов, трансферазы углеводов, синтазы углеводов, ацетилазы, ацилтрансферазы, фосфатазы углеводов, лиазы полисахаридов, киназы, пирувилазы (pyruvylases) и/или сульфотрансферазы, но не ограничиваясь ими.
Настоящее изобретение дополнительно описывает организмы, которые не подвергаются гибели под действием лактозы и которые больше не деградируют лактозу в результате того, что ген гидролазы лактозы у этих организмов становится менее функциональным или не функциональным.
Термин «гены, которые становятся менее функциональными или нефункциональными» относится к методикам, хорошо известным специалистам в данной области технике, таким как использование миРНК, интерферирующих РНК, микроРНК, асРНК, мутированных генов, нокаута генов, транспозонного мутагенеза, CrispR/CAS и т.п., которые используются для изменения генов таким образом, что они обладают меньшей способностью (т.е. статистически значимой «меньшей способностью» по сравнению с функциональным геном дикого типа) или полностью теряют способность (например, нокаутированные гены) продуцировать функционально активные конечные продукты. Термин «нокаут (гена)», таким образом, относится к гену, который становится нефункциональным. Термин «удаленный ген» или «делеция гена» также относится к гену, который становится нефункциональным (2, 4-9, 22, 27, 30, 43, 45, 46, 51, 65, 74).
Настоящее изобретение описывает организмы, в которых гены введены/нокаутированы/повышающе регулированы с целью производства биопродуктов, описанных выше. Такие гены можно найти с помощью генетических баз данных, таких как, например, genbank, но не ограничиваясь этим, или белковых баз данных, таких как, например, uniprot, но не ограничиваясь этим, или баз данных ферментов, таких как, например, база данных ферментов Brenda, но не ограничиваясь этим (16, 23, 38), а метаболические пути синтеза биопродуктов описаны в таких базах данных как, например, KEGG, Biocyc, Metacyc (20, 44, 47), но не ограничиваясь ими. Метаболические пути синтеза некоторых биопродуктов, описанных выше, можно установить с помощью нескольких математических инструментов, описанных в данной области техники (35, 54, 57, 76).
Примеры
1. Материалы и методы для работы с Escherichia coli
Штаммы и плазмиды
Escherichia coli MG1655 [λ-, F-, rph-1] и JM109 были получены из Нидерландской коллекции культур бактерий (NCCB). Все мутантные штаммы были созданы с использованием способа Datsenko & Wanner (27).
Среды
Среда Luria Broth (LB) состояла из 1% триптона пептона (Difco, Эрембодегем, Бельгия), 0,5% дрожжевого экстракта (Difco) и 0,5% хлорида натрия (VWR, Лёвен, Бельгия). Среда для встряхиваемой колбы содержала 2 г/л NH4Cl, 5 г/л (NH4)2SO4, 2,993 г/л KH2PO4, 7,315 г/л K2HPO4, 8,372 г/л MOPS, 0,5 г/л NaCl, 0,5 г/л MgSO4⋅7H2O, 15 г/л глицерина (если не указано иное), 1 мл/л раствора витаминов, 100 мкл/л раствора молибдата и 1 мл/л раствора селена. рН среды доводили до 7 с помощью 1М KOH.
Раствор витаминов состоял из 3,6 г/л FeCl2⋅4H2O, 5 г/л CaCl2⋅2H2O, 1,3 г/л MnCl2⋅2H2O, 0,38 г/л CuCl2⋅2H2O, 0,5 г/л CoCl2⋅6H2O, 0,94 г/л ZnCl2, 0,0311 г/л Н3ВО4, 0,4 г/л Na2EDTA⋅2H2O и 1,01 г/л тиамина ⋅ HCl. Раствор молибдата содержал 0,967 г/л Na2MoO4⋅2H2O. Раствор селена содержал 42 г/л SeO2.
Минимальная среда для ферментации содержала 6,75 г/л NH4Cl, 1,25 г/л (NH4)2SO4, 1,15 г/л KH2PO4, 0,5 г/л NaCl, 0,5 г/л MgSO4⋅7H2O, 30 г/л лактозы и 20 г/л сахарозы (или другие концентрации, если указано иное), 1 мл/л раствора витаминов, 100 мкл/л раствора молибдата и 1 мл/л раствора селена такого же состава, как описано выше.
Условия культивирования
Предварительную культуру от одной колонии на чашке со средой LB инкубировали в 5 мл среды LB на протяжении 8 часов при 37°C на орбитальном встряхивателе при 200 rpm. Из этой культуры 2 мл переносили в 100 мл минимальной среды во встряхиваемую колбу объемом 500 мл и инкубировали в течение 16 часов при 37°C на орбитальном встряхивателе при 200 rpm. 4% инокулят использовали в 2 или 5 л сосуде для культивирования Biostat В Plus с рабочим объемом 1,5 л или 4 л (Sartorius Stedim Biotech, Мельзунген, Германия). Условия культивирования были следующими: 37°C, перемешивание при 800 rpm и скорость подачи газа 1,5 л/мин. Аэробные условия поддерживали барботированием воздуха. рН поддерживали на уровне 7 с помощью 0,5 М H2SO4 и 35% М раствора аммония. Выходящий газ охлаждали до 4°C при помощи устройства для охлаждения выходящих газов (Frigomix 1000, Sartorius Stedim Biotech, Мельзунген, Германия). Когда в процессе ферментации образовывалась пена, добавляли 10% раствор кремнийорганического противовспенивающего агента (BDH 331512К, VWR Int Ltd., Пул, Англия) (приблизительно 10 мкл). Отходящий газ анализировали при помощи анализатора отходящего газа EL3020 (ABB Automation GmbH, 60488 Франкфурт-на-Майне, Германия).
Все данные регистрировали с помощью системы Sartorius MFCS/win, версия 3.0 (Sartorius Stedim Biotech, Мельзунген, Германия).
Методика отбора проб
Внутри биореактора находится собирательная трубка (BD Spinal Needle, 1,2×152 мм (BDMedical Systems, Franklin Lakes, NJ - США), которая соединена с портом реактора, а снаружи соединена с гибкой трубкой Masterflex-14 (Cole-Parmer, Антверпен, Бельгия), заканчивающейся собирательным портом с перегородкой для отбора проб. С другой стороны этот собирательный порт обратно соединен с реакционным сосудом с помощью гибкой трубки Masterflex-16. Такая система называется петлей для быстрого отбора проб. Во время отбора проб реакционный бульон прокачивается по петле для отбора проб. Было посчитано, что при скорости потока 150 мл/мин реакционный бульон достигает собирательного порта за 0,04 с и за 3,2 с возвращается обратно в реактор. При уровне рО2, равным 50%, содержание кислорода в жидкости составляет примерно 3 мг/л при 37°C. Уровень рО2 никогда не должен падать ниже 20%, чтобы избегать микроаэробных условий. Таким образом, во время прохождения через собирательную петлю может поглощаться 1,8 мг/л кислорода. Если предположить, что скорость поглощения кислорода составляет 0,4 г кислорода/г биомассы/ч (максимальная скорость поглощения кислорода при μmax), то для 5 г/л биомассы скорость поглощения кислорода будет составлять 2 г/л/ч или 0,56 мг/л/с, с учетом 3,2 с (время пребывания биомассы в петле) поглощение кислорода составит 1,8 мг/л.
Для подавления метаболизма клеток во время отбора проб реакционный бульон засасывали из собирательного порта с помощью шприца, заполненного 62 г шариков из нержавеющей стали, предварительно охлажденных до -20°C, чтобы немедленно охладить 5 мл бульона до 4°C. После отбора пробы немедленно центрифугировали с охлаждением (15000 g, 5 мин, 4°C). Во время периодических экспериментов образцы для измерения OD600нм отбирали, используя петлю для быстрого отбора проб и способ отбора проб с охлажденными стальными шариками. Способы анализа
Плотность клеток культуры постоянно контролировали путем измерения оптической плотности при 600 нм (спектрофотометр Uvikom 922, BRS, Брюссель, Бельгия). Сухую массу клеток получали центрифугированием (15 мин, 5000g, ротор GSA, Sorvall RC-5B, Goffin Meyvis, Капеллен, Бельгия) 20 г реакционного бульона в предварительно высушенных и взвешенных пробирках типа Falcon. Далее осадок один раз промывали 20 мл физиологического раствора (9 г/л NaCl) и высушивали при 70°C до постоянного веса. Чтобы иметь возможность преобразовывать результаты измерений OD600нм в значения концентрации биомассы, была построена кривая корреляции между OD600нм и концентрацией биомассы. Концентрации глюкозы и органических кислот определяли с помощью системы HPLC Varian Prostar (Varian, Синт-Кателейне-Вавер, Бельгия), используя колонку Aminex НРХ-87Н (Bio-Rad, Эке, Бельгия), нагретую до 65°C, оснащенную предколонкой длинной 1 см, и используя в качестве подвижной фазы 5 мМ H2SO4 (0,6 мл/мин). Для детектирования пика использовали двухволновой UV-VIS (210 нм и 265 нм) детектор (Varian Prostar 325) и дифференциальный рефрактометрический детектор (Merck LaChrom L-7490, Merck, Левен, Бельгия). Пики можно идентифицировать, разделив значение поглощения для пика при 265 на значения поглощения пика при 210 нм. Результаты деления представляют собой постоянную величину, характерную для определенного соединения (формула Ламберта-Бера).
Глюкозу, фруктозу, сахарозу, олигосахариды и глюкозу-1-фосфат измеряли методом HPLC с использованием колонки Hypercarb и обнаруживали с помощью детектора MSMS (Antonio et al., 2007; Nielsen et al., 2006).
Генетические способы
Способы, используемые для получения мутантов, описаны ниже.
Плазмиды поддерживали в клетка-хозяевах Е. coli DH5α (F-, ϕ80dlacZΔM15, Δ(lacZYA-argF)U169, deoR, recA1, endA1, hsdR17(rk-, mk+), phoA, supE44, λ-, thi-1, gyrA96, relA1).
Плазмиды
Плазмиды pKD46 (вспомогательная плазмида Red, устойчивость к ампициллину), pKD3 (содержит фланкированный FRT-сайтами ген устойчивости к хлорамфениколу (cat)), pKD4 (содержит фланкированный FRT-сайтами ген устойчивости к канамицину (kan)) и рСР20 (экспрессирует FLP рекомбиназу) использовали для получения мутантных конструкций. Плазмиду pBluescript (Fermentas, Санкт-Леон-Рот, Германия) использовали для получения производных pKD3 и pKD4 с библиотекой промоторов или с аллелями, несущими точечную мутацию.
Мутации
Мутации заключались в нарушении функции гена (нокаут, KO). Они были введены с использованием концепции Datsenko и Warmer (27).
Трансформантов, содержащих вспомогательную плазмиду Red, выращивали в 10 мл среды LB с ампициллином (100 мг/л) и L-арабинозой (10 мМ) при 30°C до OD600нм, равной 0,6. Для получения электрокомпетентных клеток клетки промывали сначала 50 мл ледяной воды, затем 1 мл ледяной воды. Далее клетки ресуспендировали в 50 мкл ледяной воды. Электропорацию проводили, используя 50 мкл клеток, 10-100 нг линейного двухцепочечного ДНК продукта и Gene Pulser™ (BioRad) (600 Ω, 25 мкФ и 250 вольт).
После электропорации клетки добавляли к 1 мл среды LB и инкубировали 1 ч при 37°C, после чего высевали на LB-агар, содержащий 25 мг/л хлорамфеникола или 50 мг/л канамицина для отбора трансформантов, устойчивых к антибиотику. Наличие мутаций в отобранных мутантах подтверждали методом ПЦР с праймерами к участкам последовательности, расположенным выше и ниже модифицированной области, далее отобранных мутантов выращивали на LB-агаре при 42°C, чтобы они утратили вспомогательную плазмиду. Мутантов тестировали на чувствительность к ампициллину.
Линейная двухцепочечная ДНК
Линейные дц-ДНК ампликоны получали с помощью ПЦР, используя в качестве матрицы pKD3, pKD4 и их производные. Часть последовательности используемых праймеров была комплементарна матрице, а другая часть комплементарна участку на хромосомной ДНК, где должна произойти рекомбинация. Для KO была сконструирована область гомологии 50 нуклеотидов до стартового кодона целевого гена и область гомологии 50 нуклеотидов после стоп- кодона целевого гена. Для KI необходимо было сохранить точку начала транскрипции (+1). ПЦР продукты очищали после ПЦР, расщепляли DpnI, вторично очищали в агарозном геле и суспендировали в элюирующем буфере (5 мМ Tris, рН 8,0).
Удаление гена устойчивости к антибиотику. Отобранных мутантов (устойчивых к хлорамфениколу или канамицину) трансформировали плазмидой рСР20, представляющей собой плазмиду с устойчивостью к ампициллину и хлорамфениколу, обладающей чувствительной к температуре репликацией и термической индукцией синтеза FLP. Устойчивых к ампициллину трансформантов отбирали при 30°C, после чего несколько колоний очищали на LB при 42°C и далее проверяли, утратили ли они всю устойчивость к антибиотикам и вспомогательную плазмиду FLP. Нокауты и вставки генов проверяли с помощью контрольных праймеров (Fw/Rv-gene-out).
Трансформация
Плазмиды трансформировали в CaCl2 компетентные клетки по упрощенной методике Hanahan (42) или электропорацией, как описано выше.
2. Материалы и методы для работы с дрожжами
2.1. Штаммы
Saccharomyces cerevisiae BY4742 были получены из коллекции культур Euroscarf. Все мутантные штаммы были созданы путем гомологичной рекомбинации или путем трансформации плазмидой с использованием способа Gietz (40). Kluyveromyces marxianus lactis были получены из коллекции культур Лаборатории промышленной биотехнологии и биокатализа.
2.2. Среды
Штаммы выращивали на синтетической среде с точно установленным составом для дрожжей с полной смесью добавок (Synthetic Defined yeast medium with Complete Supplement Mixture, SD CSM) или CSM drop-out (SD CSM-Ura), содержащей 6,7 г.л-1 основы азотного агара для дрожжей без аминокислот (YNB w/o АА, Difco), 20 г.л-1 агара (Difco) (твердые культуры), 22 г.л-1 глюкозы моногидрата или 20 г.л-1 лактозы и 0,79 г.л-1 CSM или 0,77 г.л-1 CSM-Ura (MP Biomedicals).
2.3. Условия культивирования
Культуры дрожжей сначала инокулировали в 5 мл подходящей среды и инкубировали в течение ночи при 30°C и 200 rpm. Для увеличения объема культуры 2% (или больше) предварительной культуры инокулировали в 50-200 мл среды. Эти культуры снова инкубировали при 30°C и 200 rpm.
Эксперименты по анализу роста проводили в 96-луночном планшете или колбе Эрленмейера. Чтобы получить одиночные колонии в качестве стартового материала для экспериментов по анализу роста и продукции, штаммы высевали на чашки с селективной средой SD CSM и инкубировали в течение 2-3 дней при 30°C. Затем отбирали одну колонию и переносили в 5 мл среды для проведения экспериментов в колбе Эрленмейера или в 1 мл среды для проведения экспериментов в микротитрационных планшетах.
Для проведения экспериментов в колбе Эрленмейера предварительные культуры инкубировали в течение ночи при 30°C и 200 rpm и 2% от этих предварительных культур добавляли к 100 мл среды, чтобы начать эксперименты по анализу роста.
Для экспериментов по анализу роста МТР колонии добавляли к 150 мкл среды и инкубировали в течение 24 часов при 30°C. После инкубации 2 мкл предварительных культур МТР добавляли к 150 мкл свежей среды, содержащей МТР. OD измеряли каждые пятнадцать минут в течение 48 часов с помощью Infinite® 200 Pro Tecan.
2.4. Методика отбора проб
Пробы для измерения OD, клеточной фракции (0,2 мл) и фракции супернатанта (1 мл) культуры отбирали каждые два часа до достижения стационарной фазы и каждую пару часов на протяжении стационарной фазы. Пробу объемом 1 мл сначала центрифугировали (11), после чего клеточный осадок и супернатант разделяли и хранили отдельно при -20°C. Супернатант хранили для проведения анализа внеклеточных продуктов, а клеточный осадок использовали для анализа внутриклеточных метаболитов.
2.5. Способы анализа
Плотность клеток культуры постоянно контролировали путем измерения оптической плотности при 600 нм (спектрофотометр Uvikom 922, BRS, Брюссель, Бельгия) или с помощью микротитрационного планшетного ридера Biochrom Anthos Zenyth 340. Сухую массу клеток получали центрифугированием (15 мин, 5000g, ротор GSA, Sorvall RC-5B, Goffin Meyvis, Капеллен, Бельгия) 20 г реакционного бульона в предварительно высушенных и взвешенных пробирках типа Falcon. Далее осадок один раз промывали 20 мл физиологического раствора (9 г/л NaCl) и высушивали при 70°C до постоянного веса. Чтобы иметь возможность преобразовывать результаты измерений OD600нм в значения концентрации биомассы, была построена кривая корреляции между OD600нм и концентрацией биомассы. Концентрации глюкозы и органических кислот определяли с помощью системы HPLC Varian Prostar (Varian, Синт-Кателейне-Вавер, Бельгия), используя колонку Aminex НРХ-87Н (Bio-Rad, Эке, Бельгия), нагретую до 65°C, оснащенную предколонкой длинной 1 см и используя в качестве подвижной фазы 5 мМ H2SO4 (0,6 мл/мин). Для детектирования пика использовали двухволновой детектор UV-VIS (210 нм и 265 нм) (Varian Prostar 325) и дифференциальный рефрактометрический детектор (Merck LaChrom L-7490, Merck, Левен, Бельгия). Пики можно идентифицировать, разделив значение поглощения для пика при 265 на значения поглощения пика при 210 нм. Результаты деления представляют собой постоянную величину, характерную для определенного соединения (формула Ламберта-Бера).
Глюкозу, фруктозу, сахарозу, олигосахариды и глюкозу-1-фосфат измеряли методом HPLC с использованием колонки Hypercarb и обнаруживали с помощью детектора MSMS (Antonio et al., 2007; Nielsen et al., 2006).
2.6. Генетические способы
Способы, используемые для получения мутантов, описаны ниже.
Плазмиды поддерживали в клетках-хозяевах Е. coli DH5α (F-, ϕ80dlacZΔM15, Δ(lacZYA-argF)U169, deoR, recA1, endA1, hsdR17 (rk-, mk+), phoA, supE44, λ-, thi-1, gyrA96, relAX).
Плазмиды
Экспрессионную плазмиду дрожжей p2a_2μ_Lac4, полученную из Лаборатории промышленной биотехнологии и биокатализа, использовали, чтобы обеспечить рост Saccharomyces на лактозе в качестве единственного источника С.Эта плазмида содержит ген устойчивости к ампициллину и бактериальную точку начала репликации, чтобы можно было осуществлять селекцию и поддерживать плазмиду в Е. coli. Плазмида также содержит 2μ ori дрожжей и селективный маркер Ura3, чтобы можно было осуществлять селекцию и поддерживать плазмиду в дрожжах. И последнее, плазмида содержит экспрессионную кассету β-галактозидазы (SEQ ID 9, Фигура 15).
Мутации
Мутации заключались во введении плазмиды p2a_2μ_Lac4 (как описано выше) и во вставке гена (KI) (KI в локусе рДНК) с использованием двухцепочечной линейной ДНК (как описано выше). Трансформантов высевали на среду SD CSM-Ura после трансформации плазмидной ДНК или на среду SD CSM-Ura с лактозой в качестве единственного источника С после трансформации двухцепочечной линейной ДНК. Наличие плазмид в отобранных мутантах подтверждали с помощью ПЦР с праймерами, соответствующими p2a_2μ_Lac4. Наличие геномной вставки в отобранных мутантах подтверждали с помощью ПЦР с праймерами к участкам выше и ниже модифицированной области, а также подтверждали секвенированием (проводили в LGC Genomics (LGC group, Германия)).
Линейная двухцепочечная ДНК
Линейные дц-ДНК ампликоны получали с помощью ПЦР, используя в качестве матрицы плазмиды pJet_KI_p1_Lac12_t@rDNA или pJet_KI_p2_Lac12_t@rDNA. Эти плазмиды содержат области гомологии размером 2500 пар оснований (HR1 (SEQ ID 10, Фигура 16) и HR2 (SEQ ID 11, Фигура 17)), фланкирующие SEQ ID 7 и SEQ ID 8, соответственно, вставленные по сайту множественного клонирования клонирующего вектора pJET (Thermoscientific). Используемые праймеры гомологичны 5'-концу HR1 (прямой праймер) и 3'-концу HR2 (обратный праймер). Перед трансформацией продукты ПЦР очищали после ПЦР.
Трансформация
Плазмиды и линейную двухцепочечную ДНК трансформировали, используя способ Gietz (40).
3. Результаты
Пример 1. Вставка лактозной пермеазы lacYE. coli в локус agp.
Первый штамм MG1655ΔlacY был создан в соответствии со способом Datsenko и Wanner, как описано выше. Для этого MG1655 трансформировали плазмидой pKD46 и линейную ДНК конструировали из основных плазмид pKD3 и pKD4 с фланкированными областями гомологии к гену lacY. Успешных рекомбинантов далее подвергали скринингу с соответствующими антибиотиками. Чтобы убедиться, что этот штамм не способен поглощать лактозу, штамм выращивали на минимальной среде, содержащей только лактозу в качестве источника углерода. В ходе этого эксперимента рост не наблюдался, следовательно, эта клетка не может больше транспортировать лактозу через свою мембрану.
Чтобы далее получить синтетическую экспрессирующую систему, синтетический промотор и RBS были синтезированы в комбинации с геном lacY (был заказан в IDT и Geneart). Эта последовательность показана на Фигуре 3. Эта последовательность также была введена в геном в локусе гена agp, следуя адаптированной методике Datsenko и Wanner. Кратко, конструкцию лактозной пермеазы сначала собирали со скрининговой кассетой из плазмиды pKD3, в результате чего была получена новая плазмида pCX_lacY-kan. Из этой плазмиды линейная ДНК может быть амплифицирована методом ПЦР с гомологией к геномной области agp. Эта полученная линейная ДНК далее может быть трансформирована в MG1655ΔlacY Е coli, в которой присутствует плазмида pKD46. В результате происходит рекомбинация экспрессионной кассеты лактозного транспортера в геном и образуется организм, экспрессирующей лактозную пермеазу, MG1655ΔlacYΔagp::lacYsynthetic. Чтобы подтвердить восстановление способности расти на лактозе, этот штамм выращивали на минимальной среде, содержащей лактозу, как описано выше. Способность расти на лактозе была восстановлена полностью, а скорость роста была аналогична скорости роста штамма дикого типа.
Пример 2. Влияние лактозы на штамм Е. coli дикого типа и мутантный штамм Е. coli, который не подвергается гибели под действием лактозы
Эксперимент во встряхиваемой колбе, как описано в материалах и методах, проводили на MG1655 дикого типа и MG1655ΔlacYΔagp::lacYsynthetic. Эти штаммы выращивали во встряхиваемой колбе в среде с глицерином (15 г/л глицерина, как описано в материалах и методах), и в середине экспоненциальной фазы (приблизительно при OD 0,8) к штаммам добавляли лактозу (200 г/л концентрированного раствора добавляли до конечной концентрации 10 г/л). Как можно видеть на Фигуре 1 и Фигуре 2, мутантный штамм не подвергается гибели под действием лактозы.
Пример 3. Использование трансляционного связывания или трансляционных сенсоров для подтверждения экспрессии лактозного транспортера
Поскольку штамм с полностью нокаутированным геном лактозной пермеазы также не будет подвергаться гибели под действием лактозы, а целью является получение функциональной, активной, экспрессируемой лактозной пермеазы, необходимо проводить скрининг на экспрессию лактозной пермеазы. С этой целью могут быть созданы варианты последовательностей промоторов, сайтов связывания рибосом, последовательностей Козак, варианты с измененной частотой использования кодонов и варианты терминаторов транскрипции. Тем не менее, с этими вариантами последовательностей могут получиться конструкции с нулевой экспрессией, в результате чего образуются мутантные штаммы, у которых отсутствует лактозный транспортер. Поэтому должна быть создана система для обнаружения экспрессии лактозного транспортера, предпочтительно с репортерным геном, по которому легко можно провести скрининг, например, таким как lacZ, гены флуоресцентных белков или гены устойчивости к антибиотикам.
Создание трансляционно связанной системы, которая повторно инициирует трансляцию репортерного гена для обнаружения экспрессии лактозного транспортера
Два гена могут быть трансляционно связаны путем введения области повторной инициации трансляции, расположенной с 3' конца от целевого гена и с 5' конца от репортерного гена. Трансляция может быть повторно инициирована с помощью нескольких кодонов, таких как AUG, UUG, GUG или AUA (63). Последовательность такой конструкции, которая трансляционно связывает ген лактозной пермеазы и ген lacZ, показана на Фигуре 4. Для создания этой последовательности последовательности lacY и lacZ амплифицируют из генома Е. coli с использованием праймеров с сайтами рестрикции golden gate (BsaI, получены из NEB). Межгенная область, обеспечивающая трансляционное связывание, может быть заказана в любой компании, занимающейся синтезом генов, например, в IDT или Geneart. Все части далее собираются методом Golden Gate, как описано Engler et al. (2013) (36), в плазмиду pUC54 вместе с промотором и последовательностью RBS, как показано на Фигуре 3 (для Е. coli), или в плазмиду pGK12, которая реплицируется в Bacillus sp. и содержит промотор и сайт связывания рибосомы Bacillus.
Создание трансляционно связанной системы, инициирующей трансляцию репортерного гена, для обнаружения экспрессии лактозного транспортера посредством раскрытия петли на сайте связывания рибосомы
Второй способ проведения скрининга на наличие экспрессии, основанный на трансляционном связывании, описан Mendez-Perez et al. (2012) (58). Этот способ был адаптирован для скрининга на наличие экспрессии лактозной пермеазы с репортерным геном устойчивости к хлорамфениколу. В этом случае лактозный транспортер lacY связан посредством HIS-tag и сайта связывания рибосомы с репортерным геном устойчивости к хлорамфениколу. Части последовательности для этой конструкции также заказаны в IDT или Geneart и собраны по методу сборки Golden gate. Полученная последовательность приведена на Фигуре 5.
Создание трансляционно связанной системы, связывающей лактозный транспортер дрожжей с репортерным геном
Несмотря на то что у дрожжей нет цистронов, возможно провести скрининг на наличие экспрессии посредством трансляционного связывания через вирусные сайты внутренней посадки рибосомы (так называемые последовательности IRES) (56). Примером такой последовательности является последовательность Т2А (10), которая обеспечивает полностью независимую (это означает, что белки не представляют собой белок слияния), но связанную трансляцию двух белков в цистроне. Это означает, что если последний белок цистрона экспрессируется, то первый белок тоже экспрессируется.
В дрожжах, например, Kluyveromyces marxianus, ген лактозной пермеазы может использоваться для транспорта лактозы внутрь клетки. Этот ген может быть связан через последовательность Т2А с геном aph 1, кодирующим устойчивость к генетицину. Эта последовательность создана аналогично тому, как описано выше. Конечная последовательность приведена на Фигуре 6.
Создание системы, связанной с аптамером, с помощью которой аптамер вводится в матричную РНК лактозной пермеазы
Экспрессия лактозной пермеазы также может быть обнаружена на уровне матричной РНК. Для этого аптамер, связывающий (Z)-4-(3,5-дифтор-4-гидроксибензилиден)-1,2-диметил-1Н-имидазол-5(4Н)-он, клонируют после кодирующей последовательности лактозной пермеазы, как показано на фигуре 7. Экспрессия этой конструкции модулируется так же, как описано в Примере 6. По окончании роста клеток в среду добавляют (Z)-4-(3,5-дифтор-4-гидроксибензилиден)-1,2-диметил-1Н-имидазол-5(4Н)-он, как описано Pothoulakis et al (2013) (64), и мутантные штаммы, экспрессируюшие лактозную пермеазу, отбирают на клеточном сортере с активацией флуоресценции (FACS).
Пример 4. Обнаружение экспрессии лактозного транспортера, трансляционно связанного с геном устойчивости к хлорамфениколу
Были сконструированы два штамма, в которых лактозная пермеаза была удалена (нокаутирована) из генома. Оба штамма трансформировали плазмидой pSC101, содержащей ген устойчивости к канамицину, с тем отличием, что одна из плазмид содержала конститутивно экспрессируемую лактозную пермеазу, как описано в Примере 1 и 2, в результате чего были получены штамм сравнения MG1655ΔlacY pSC101_kan и штамм MG1655ΔlacY pSC101_kan_ lacYsynthetic_cat с трансляционным связыванием lacY_cat, как описано в Примере 4 и на Фигуре 5. Оба штамма выращивали на минимальной среде, как описано выше, при разных концентрациях хлорамфеникола (между 0 и 30 мг/л). На Фигурах 8 и 9 показано, что после 48 и 92 часов рост штамма сравнения ингибируется при более низкой концентрации хлорамфеникола по сравнению с мутантным штаммом с трансляционным связыванием lacY_cat, что говорит о том, что такая система является отличным вариантом проведения скрининга генетических конструкций, экспрессирующих лактозную пермеазу.
Пример 5. Методика скрининга на наличие мутантов, экспрессирующих лактозную пермеазу, и не подвергающихся гибели под действием лактозы
Как и в Примере 2, выращивали смесь двух штаммов, устойчивых к хлорамфениколу, где один штамм не гибнет под действием лактозы и экспрессирует лактозную пермеазу, трансляционно связанную с хлорамфениколом, а второй штамм имеет кассету устойчивости к хлорамфениколу, но содержит природную экспрессирующую систему лактозной пермеазы. Оба штамма выращивали в среде, как описано в Примере 2, и лактозу добавляли в середине экспоненциальной фазы, как показано в Примере 2. Мутантный штамм, который не подвергается гибели под действием лактозы, продолжал расти, тогда как другой штамм, чувствительный к гибели под действием лактозы, прекращал расти. В конце экспоненциальной фазы 0,1 мл этой культуры инокулировали во вторую встряхиваемую колбу с аналогичной средой, как описано выше. Снова, при OD 0,8 добавляли лактозу, что приводило к остановке роста штамма, чувствительного к гибели под действием лактозы, и накоплению мутантного штамма, не подвергающегося гибели под действием лактозы. После 5-кратного повторения этой процедуры доля мутантного штамма, не подвергающегося гибели под действием лактозы, составляла 99%, что позволяло легко выделить его из культуры.
Пример 6. Создание мутантных экспрессионных кассет лактозной пермеазы
Варианты последовательностей промоторов, сайтов связывания рибосом, последовательностей Козак, терминаторов транскрипции и варианты гена лактозной пермеазы (с разной частотой использования кодонов) были заказаны в компаниях, предлагающих услугу по синтезу генов, например, IDT, Geneart, Genscript, Gen9 и другие. Дизайн библиотеки промоторов для бактерий основан на консенсусной последовательности бактериальных промоторов с двумя консервативными областями в районе -10 и -35 пар оснований от точки начала транскрипции. Основания между этими консервативными областями, перед ними и после них далее случайным образом изменяли на А, Т, G или С, в результате чего получали промоторы с разной силой экспрессии. Альтернативно, изменяли консервативные области, а окружающие последовательности сохраняли, в результате чего также были получены промоторы разной силы. Эти смеси последовательностей далее клонировали (либо методом сборки по Гибсону, либо методом сборки Golden Gate, либо методом сборки Cliva, либо LCR, либо рестрикцией и лигированием) (25, 36, 50, 79) перед трансляционно связанной лактозной пермеазой, в результате чего получали библиотеку экспрессионных кассет лактозной пермеазы, которую можно подвергнуть скринингу, используя протокол, описанный в Примере 5.
Библиотеку эукариотических промоторов создавали на основе корового промотора (13). Для Saccharomyces cerevisiae этот промотор может быть гетерологичным TEF промотором pTEF1, который усилен с помощью последовательностей UAS и видоизменен мутациями для изменения силы промотора (12). Такой промотор заказывали и клонировали, как описано выше, перед трансляционно связанной лактозной пермеазой, и конечной конструкцией трансформировали дрожжи, такие как Saccharomyces cerevisiae, с использованием плазмиды или путем интеграции в хромосому.
Нетранслируемая область у прокариот состоит из сайта связывания рибосомы, а у эукариот из последовательности Козак. Обе последовательности рандомизировали и клонировали перед кодирующей последовательностью, как описано выше, в результате чего получали библиотеку экспрессионных кассет с разной трансляционной эффективностью. Рандомизация может быть рационализирована с помощью таких инструментов, как калькулятор RBS, который вычисляет корреляцию эффективности трансляции последовательности и уменьшает количество вариантов, которые должны быть включены в библиотеку (67).
Частоту использования кодонов изменяли путем изменения кодирующей последовательности гена без изменения аминокислотной последовательности белка. Это называется адаптацией кодонов. Частоту использования кодонов на протяжении последовательности изменяли таким образом, что в определенные области вводили более или менее редкие кодоны, что приводило к изменению эффективности экспрессии и эффективности фолдинга. Для пермеазы, последовательность которой содержит только редкие кодоны (определяется для организма с помощью базы данных частоты использования кодонов (61)), характерна низкая скорость трансляции по сравнению с пермеазой с полностью кодон-оптимизированной последовательностью (содержит только те кодоны, которые часто встречаются в целевом организме). Кроме того, первые кодоны кодирующей последовательности также влияют на эффективность последовательности Козак или сайта связывания рибосомы (62, 69, 78).
Область терминатора транскрипции изменяли, используя эндогенные или экзогенные последовательности терминатора транскрипции из базы данных (18, 26). Эти терминаторы транскрипции также клонировали способом, аналогичным описанному выше.
Пример 7. Обогащение экспрессионных кассет, которые экспрессируют лактозную пермеазу и не приводят к гибели под действием лактозы
Экспрессионные кассеты были созданы в соответствии с Примером 3 и 7. В результате была получена библиотека экспрессионных кассет лактозной пермеазы. Экспрессионные кассеты, которые приводили к экспрессии лактозной пермеазы, были отобраны в соответствии со способами из Примеров 3 и 4. Экспрессионные кассеты, экспрессирующие лактозную пермеазу, которые не приводили к гибели под действием лактозы, были отобраны в соответствии со способами, описанными в Примерах 2 и 5. Отобранные экспрессионные кассеты также анализировали с помощью секвенирования и способом, описанным в Примере 2.
Пример 8. Ферментативная продукция 2-фукозиллактозы бактериями Е. coli с фукозилтрансферазой из Helicobacter pylori
Мутантный штамм, в котором нокаутированы гены lacZ, glgC, agp, pfkA, pfkB, pgi, arcA, iclR, wcaJ и конститутивно экспрессируется lacY, как описано в Примере 1 и Примере 2, чтобы обеспечить экспрессию при всех условиях культивирования, далее трансформировали фукозилтрансферазой из Helicobacter pylori и фосфорилазой сахарозы из Bifidobacterium adolescentis, которые также экспрессируются конститутивно. Конститутивные промоторы были выбраны из библиотеки промоторов, описанной De Mey et al., 2007. Этот штамм культивировали в среде, как описано в материалах и методах, но с 30 г/л сахарозы и 50 г/л лактозы. В результате было получено до 1,5 г/л 2'-фукозиллактозы
Пример 9. Продукция 2-фукозиллактозы бактериями Е. coli с периодической подпиткой
Методами генной инженерии согласно методикам, описанным выше, создавали мутантный штамм с генотипом:
ΔlacZYAΔglgCΔagpΔpgiΔpfkA-P22-baSPΔpfkBΔarcAΔiclR::slΔwcaJAΔlonΔadhE-P14-frk+pCXP14-FT_H. pylori (вектор с последовательностью SEQ ID №6, смотрите Фигуру 10). Экспрессию лактозной пермеазы изменяли, как описано в Примере 1 и Примере 2. Промоторы Р22 и Р14 были получены из библиотеки промоторов, сконструированной De Mey et al. (29), и их клонировали по аналогии с методикой, описанной Aerts et al. (1). "::sl" означает «безрубцовая» делеция гена, то есть без сайта FRT, который остается на хромосоме.
Этот штамм культивировали в биореакторе, как описано выше в материалах и методах, в минеральной среде с 30 г/л сахарозы и 50 г/л лактозы. После порционной фазы в биореактор добавляли 500 г/л сахарозы, 50 г/л лактозы и 1 г/л гептагидрата сульфата магния. В результате этого в супернатанте накапливалось 27,5 г/л фукозиллактозы.
Пример 10. Продукция лакто-N-триозы бактериями Е. coli
Мутантный штамм конструировали методами генной инженерии по методикам, описанным выше, для экспрессии UDP-N-ацетилглюкозамин-трансферазы, фосфорилазы сахарозы, L-глутамин:D-фруктоза-6-фосфат-аминотрансферазы и глюкозамин-уридилтрансферазы с помощью плазмиды pBR322, в которой каждый ген экспрессировался под контролем конститутивного промотора из библиотеки промоторов De Mey et al. (29), и содержался селективный маркер бета-лактамаза. Этот вектор трансформировали в мутантный штамм Е. Coli, имеющий генотип ΔlacZYAΔglgCΔagp::Р14-frk-¥22-BaSPΔpgiΔpfkAΔpfkBΔnagABCDEΔmanAΔnanATEKΔmanXYZ, конститутивно экспрессирующий лактозную пермеазу, как описано выше. Этот штамм культивировали во встряхиваемой колбе, как описано выше, с лактозой и сахарозой в качестве источников углерода с добавлением глицерина или без него. Этот хозяин-продуцент не подвергался гибели под действием лактозы и продуцировал 62,5 и 55,3 мг/л лакто-N-триозы, соответственно, из добавляемой лактозы.
Пример 11. Конструкция лактозной пермеазы дрожжей K. marxianus (pi), введенная в локус рДНК
Сначала плазмидой p2a_2μ_Lac4 трансформировали штамм Saccharomyces cerevisiae BY4742 дикого типа. Трансформацию осуществляли, используя в общей сложности 4 мкг плазмиды, по протоколу (40). Трансформированные дрожжевые клетки высевали на чашки с SD-CSM drop-out (без урацила). Через два дня на чашках наблюдался рост, и колонии дрожжей тестировали на наличие нужной плазмиды. ПЦР для отбора колоний проводили для всех 33 колоний. Все протестированные колонии содержали плазмиду p2a_2μ_Lac4. Для дальнейшего использования была отобрана колония 5. Эту колонию трансформировали 2 мкг двухцепочечной линейной ДНК, полученной из pJet_KI_p1_Lac12_t@rDNA. Трансформированные клетки выращивали на чашках SD-CSM-Ura с лактозой в качестве единственного источника С.Через три дня после трансформации несколько колоний достаточно выросли, чтобы можно было протестировать их на наличие экспрессионной кассеты Lac12 в рДНК Saccharomyces. Для всех колоний проводили ПЦР для отбора колоний. Все протестированные колонии содержали экспрессионную кассету Lac12. Для дальнейшего использования была отобрана колония 6 {Saccharomyces KI_p1_Lac12_t@rDNA).
Пример 12. Конструкция лактозной пермеазы дрожжей K. marxianus (р2), введенная в локус рДНК
Сначала плазмидой p2a_2μ_Lac4 трансформировали штамм Saccharomyces cerevisiae BY4742 дикого типа. Трансформацию осуществляли, используя в общей сложности 4 мкг плазмиды, по протоколу Gietz (40). Трансформированные дрожжевые клетки высевали на чашки с SD-CSM drop-out (без урацила). Через два дня на чашках наблюдался рост, и колонии дрожжей тестировали на наличие нужной плазмиды. ПЦР для отбора колоний проводили для всех 33 колоний. Все протестированные колонии содержали плазмиду p2a_2μ_Lac4. Для дальнейшего использования была отобрана колония 5. Эту колонию трансформировали 2 мкг двухцепочечной линейной ДНК, полученной из pJet_KI_p2_Lac12_t@rDNA. Трансформированные клетки выращивали на чашках SD-CSM-Ura с лактозой в качестве единственного источника С. Через три дня после трансформации несколько колоний достаточно выросли, чтобы можно было протестировать их на наличие экспрессионной кассеты Lac12 в рДНК Saccharomyces. Для всех колоний проводили ПЦР для отбора колоний. Все протестированные колонии содержали экспрессионную кассету Lac12. Для дальнейшего использования была отобрана колония 7 (Saccharomyces KI_p2_Lac12_t@rDNA).
Пример 13. Рост на лактозе штамма дрожжей дикого типа и 2 мутантных штаммов дрожжей
Эксперимент во встряхиваемой колбе, как описано в материалах и методах, проводили на штаммах Kluyveromyces дикого типа, Saccharomyces KI_p1_Lac12_t@rDNA и Saccharomyces KI_p2_Lac12_t@rDNA. Эти штаммы выращивали во встряхиваемой колбе в среде, содержащей лактозу в качестве единственного источника С (20 г/л). Как можно видеть в Таблице 1, мутантные штаммы Saccharomyces растут так же быстро, как штамм Kluyveromyces marcianus lactis дикого типа, который, как известно, способен к быстрому росту на лактозе (31). Таким образом, конститутивно экспрессируемая лактозная пермеаза обеспечивает быстрый и эффективный приток лактозы в клетку дрожжей.

Пример 14. Влияние лактозы на штамм дрожжей дикого типа и мутантный штамм дрожжей, который не подвергается гибели под действием лактозы
Эксперимент во встряхиваемой колбе, как описано в материалах и методах, проводили на штаммах Kluyveromyces дикого типа, Saccharomyces KI_p1_Lac12_t@rDNA и Saccharomyces KI_p2_Lac12_t@rDNA. Эти штаммы выращивали во встряхиваемой колбе в среде с глюкозой (20 г/л глюкозы, как описано в материалах и методах), и в середине экспоненциальной фазы роста к штаммам добавляли лактозу (200 г/л концентрированного раствора добавляли до конечной концентрации 10 г/л). Как можно видеть на Фигуре 11 и Фигуре 12, мутантные штаммы не подвергаются гибели под действием лактозы. Более того, в Примере 13 было подтверждено наличие быстрого и эффективного потока лактозы внутрь этих дрожжевых клеток.
Пример 15. Секвенирование экспрессионных кассет лактозной пермеазы, которые не приводят к гибели под действием лактозы
46 колоний, отобранных в результате скрининга, как описано выше, были секвенированы, в результате чего были получены последовательности SEQ ID №12 - 57 (Фигура 18). Эти последовательности представляют собой варианты промотора и RBS, которые не приводят к гибели под действием лактозы, когда они экспрессируются в Е. coli. Следует обратить внимание на то, что было отобрано огромное количество колоний, которые были секвенированы, следовательно, с помощью этой методики скрининга было получено намного больше последовательностей, чем показано на Фигуре 18, а альтернативные методики получения библиотек, описанные выше, также приведут к последовательностям, отличным от тех, что показаны на Фигуре 18.
Пример 16. Определение μMAX для мутантных штаммов с экспрессионной кассетой лактозной пермеазы
Все штаммы брали либо из чашек с LB-агаром, на которых они росли, либо из криопробирок, и инокулировали в 5,0 мл среды Luria broth (10 г триптона; 5 г дрожжевого экстракта; 10 г NaCl). После выращивания в течение ночи при 37°C 1 мл этой предварительной культуры добавляли во встряхиваемую колбу объемом 500 мл, содержащую 100 мл минимальной среды с лактозой (2,0 г/л NH4Cl; 5,0 г/л; (NH4)2SO4; 3,0 г/л KH2PO4, 7,3 г/л K2HPO4; 8,4 г/л MOPS; 0,5 г/л MgSO4×7H2O; 0,5 г/л NaCl; 10 г/л лактозы; 0,4 мг/л Na2EDTA×2H2O; 0,03 мг/л Н3ВО3; 1,01 мг/л тиамина HCl; 0,94 мг/л ZnCl2; 0,5 мг/л CoCl2×6H2O; 0,38 мг/л CuCl2×2H2O; 1,59 мг/л MnCl2×4H2O; 3,6 мг/л CaCl2 и 0,096 мг/л Na2MoO4×2H2O); рН 7,0. После выращивания в течение ночи при 37°C обе предварительные культуры разбавляли минимальной средой с лактозой до OD600, равной 0,050. Суспензию далее переносили в 96-луночный планшет МТР (n=32), закрывали пленкой Easyseal. Измерения OD проводили каждые 10 минут на протяжении 24 часов с помощью Infinite М200 pro (TECAN) при следующих условиях: температура: 37°C+/-0,5; встряхивание 597 секунд; амплитуда встряхивания 2 мм; 280 rpm; длина волны OD600; вспышки #10; время вспышки 150 мс).
Пример 17. Характеристика экспрессионных кассет лактозной пермеазы
Один из способов снизить или устранить гибель под действием лактозы заключается в значительном снижении или устранении активности лактозной пермеазы (смотрите Пример 16). Но с точки зрения продукции биопродуктов на основе лактозы или галактозы необходимо, чтобы в клетку поступало много лактозы. Здесь мы подтверждаем, что приток лактозы в клетку у мутантных штаммов, устойчивых к гибели под действием лактозы, сопоставим, равен или даже превышает приток лактозы в клетку у организма дикого типа, подвергающегося гибели под действием лактозы. С этой целью в штамм MG1655ΔlacY были введены новые экспрессионные кассеты лактозной пермеазы, по-прежнему экспрессирующие бета-галактозидазу. Показателем притока лактозы внутрь клетки является скорость роста этих новых штаммов, поскольку любой штамм с заметно сниженной экспрессией лактозной пермеазы будет иметь значительно более низкую скорость роста.
Результаты этого анализа показаны на Фигуре 19. Почти все штаммы, показанные на этой фигуре, имеют скорость роста, равную или более высокую по сравнению со штаммом дикого типа, что свидетельствует о том, что активность и экспрессия лактозной пермеазы для них равна или выше, чем у штамма дикого типа, тем не менее, в отличие от экспрессирующей системы дикого типа, эти экспрессионные кассеты не приводят к гибели под действием лактозы. Этот способ, тем не менее, ограничен экспрессией гена бета-галактозидазы, которая становится стадией, лимитирующей рост. Поэтому экспрессию гена лактозной пермеазы измеряли с помощью описанной выше трансляционно связанной системы. Минимальная ингибирующая концентрация (MIC) для хлорамфеникола является показателем экспрессии гена лактозной пермеазы, и MIC определяли для каждой кассеты. В качестве показателя экспрессии лактозной пермеазы дикого типа использовали самую низкую MIC, для которой по-прежнему была характерна такая же скорость роста, как и для штамма дикого типа.
Для штаммов, содержащих кассеты с наименьшей MIC и имеющих такую же скорость роста, как и штамм дикого типа, MIC составляет приблизительно 20 мг/л хлорамфеникола. Для мутантных штаммов с несколько более низкой скорость роста MIC находится в диапазоне между 15 и 20 мг/л, а для мутантных штаммов с такой же или более высокой скорость роста MIC находится в диапазоне между 20 и 80 мг/л. 85% последовательностей относятся к последней категории, что означает, что большинство последовательностей, идентифицированных как экспрессионные кассеты, не приводящие к гибели под действием лактозы, демонстрируют более высокую экспрессию лактозной пермеазы, что противоречит описанному ранее в литературе.
Пример 18. Создание экспрессионной кассеты с промотором lacIq
По аналогии с методикой, описанной выше, промотор placIQ клонировали перед геном lacY Е. coli. Финальная последовательность этой конструкции приведена на Фигуре 20.
Пример 19. Другие промоторы, используемые в уровне техники, которые приводят к гибели под действием лактозы
Промотор placIQ представляет собой промотор, который использовался в данной области техники для экспрессии лактозной пермеазы в Е. coli. При использовании этого промотора происходит поглощение лактозы внутрь клетки. Тем не менее эффект от такого поглощения не проверяли. Скорость роста на лактозе штамма дикого типа значительно не отличается от скорости роста штамма с промотором lacIq (μmax составляет 0,1 и 0,11 ч-1, соответственно), что свидетельствует о примерно равных скоростях поглощения лактозы. Скрининг на наличие явления гибели под действием лактозы у штаммов с такой экспрессионной кассетой lacIQ подтвердил, что этот промотор также приводит к гибели под действием лактозы (смотрите Фигуру 21). Это подтверждает тот факт, что существуют определенные последовательности промоторов, которые приводят к гибели под действием лактозы, и другие последовательности, которые не приводят к гибели под действием лактозы. Рационализация последовательностей невозможна, а подбор индивидуальных последовательностей (путем проб и ошибок) - это кропотливая работа, требующая огромных затрат, таким образом, описанная выше методика идентификации экспрессионных кассет, которые не приводят к гибели под действием лактозы, является лучшей альтернативой длительной и дорогостоящей работе по скринингу.
Пример 20. Продукция лакто-N-тетраозы дрожжами S. cerevisiae
Мутантные штаммы, сконструированные в Примерах 11 и 12, далее трансформировали β-1,4-галактозилтрансферазой и β-1,3-N-ацетилглюкозаминилтрансферазой из Neisseria meningitidis, которые также конститутивно экспрессировали, используя стандартный экспрессионный вектор дрожжей, например, описанный Lee et al. (52). Штаммы культивировали в среде, как описано в материалах и методах, но с 20 г/л сахарозы и 20 г/л лактозы. В результате было получено до 30 мг/л лакто-N-тетраозы.
Пример 21. Продукция 2-фукозиллактозы дрожжами S. cerevisiae
Мутантные штаммы, сконструированные в Примерах 11 и 12, далее трансформировали синтазой GDP-фукозы и GDP-манноза-4,6-дегидратазой Е. coli и фукозилтрансферазой из Helicobacter pylori, которые также конститутивно экспрессировали, используя стандартный экспрессионный вектор дрожжей, например, описанный Lee et al. (52). Штаммы культивировали в среде, как описано в материалах и методах, но с 20 г/л сахарозы и 20 г/л лактозы. В результате было получено до 10 мг/л 2-фукозиллактозы.
Ссылки
1. Aerts, D., Т. Verhaeghe, M. De Mey, Т. Desmet, and W. Soetaert. 2010. A constitutive expression system for high throughput screening. Engineering in Life Sciences 10:DOI: 10.1002/elsc.201000065.
2. Agrawal, N., P.V.N. Dasaradhi, A. Mohmmed, P. Malhotra, R.K. Bhatnagar, and S.K. Mukherjee. 2003. RNA Interference: Biology, Mechanism, and Applications. Microbiology and Molecular Biology Reviews 67:657-685.
3. Alper, H., C. Fischer, E. Nevoigt, and G. Stephanopoulos. 2005. Tuning genetic control through promoter engineering. Proceedings of the national academy of sciences of the United States of America 102:12678-12683.
4. Avihoo, A., I. Gabdank, M. Shapira, and D. Barash. 2007. In silico design of small RNA switches. IEEE Transactions on Nanobioscience 6:4-11.
5. Ayres, E.K., V.J. Thomson, G. Merino, D. Balderes, and D.H. Figurski. 1993. Precise deletions in large bacterial genomes by Vector-mediated Excision (VEX): The trfA gene of promiscuous plasmid RK2 is essential for replication in several gram-negative hosts. Journal of Molecular Biology 230:174-185.
6.  , P., M. Alexeyev, I. Shokolenko, F. Bolivar, and F. Valle. 1996. A pBRINT family of plasmids for integration of cloned DNA into the Escherichia coli chromosome. Gene 172:65-69.
, P., M. Alexeyev, I. Shokolenko, F. Bolivar, and F. Valle. 1996. A pBRINT family of plasmids for integration of cloned DNA into the Escherichia coli chromosome. Gene 172:65-69.
7. Balbas, P., and G. Gosset. 2001. Chromosomal editing in Escherichia coli. Molecular Biotechnology 19:1-12.
8. Barrett, A.R., Y. Kang, K.S. Inamasu, M.S. Son, J.M. Vukovich, and Т.T. Hoang. 2008. Genetic tools for allelic replacement in Burkholderia species. Applied and Environmental Microbiology 74:4498-4508.
9. Beauprez, J. 2010. Metabolic modelling and engineering of Escherichia coli for succinate production. PhD. Ghent University, Ghent.
10. Beekwilder, J., H.M. van Rossum, F. Koopman, F. Sonntag, M. Buchhaupt, J. Schrader, R.D. Hall, D. Bosch, J. T. Pronk, A. J. A. van Maris, and J.-M. Daran. 2014. Polycistronic expression of a b-carotene biosynthetic pathway in Saccharomyces cerevisiae coupled to b-ionone production.
11. Biofuge, H. Thermo.
12. Blazeck, J., R. Garg, B. Reed, and H.S. Alper. 2012. Controlling promoter strength and regulation in Saccharomyces cerevisiae using synthetic hybrid promoters. Biotechnology And Bioengineering 109:2884-2895.
13. Blount, В.A., T. Weenink, S. Vasylechko, and T. Ellis. 2012. Rational Diversification of a Promoter Providing Fine-Tuned Expression and Orthogonal Regulation for Synthetic Biology. PLoS ONE 7:e33279.
14. Bode, L. 2012. Human milk oligosaccharides: Every baby needs a sugar mama. Glycobiology 22:1147-1162.
15. Bode, L. 2006. Recent Advances on Structure, Metabolism, and Function of Human Milk Oligosaccharides. The Journal of Nutrition 136:2127-2130.
16. Brenda Database 2006, в соответствии с датой публикации на веб-сайте, [доступно онлайн]
17. Cabantous, S., Т.С. Terwilliger, and G.S. Waldo. 2005. Protein tagging and detection with engineered self-assembling fragments of green fluorescent protein. Nat Biotech 23:102-107.
18. Cambray, G., J.C. Guimaraes, V.K. Mutalik, C. Lam, Q.-A. Mai, T. Thimmaiah, J.M. Carothers, A.P. Arkin, and D. Endy. 2013. Measurement and modeling of intrinsic transcription terminators. Nucleic Acids Research 41:5139-5148.
19. Canton, В., A. Labno, and D. Endy. 2008. Refinement and standardization of synthetic biological parts and devices. Nat Biotech 26:787-793.
20. Caspi, R., T. Altman, R. Billington, K. Dreher, H. Foerster, C.A. Fulcher, T.A. Holland, I.M. Keseler, A. Kothari, A. Kubo, M. Krummenacker, M. Latendresse, L.A. Mueller, Q. Ong, S. Paley, P. Subhraveti, D.S. Weaver, D. Weerasinghe, P. Zbang, and P.D. Karp. 2014. The MetaCyc database of metabolic pathways and enzymes and the BioCyc collection of Pathway/Genome Databases. Nucleic Acids Research 42:D459-D471.
21. Chen, X., and A. Varki. 2009. Advances in the Biology and Chemistry of Sialic Acids. ACS Chemical Biology 5:163-176.
22. Cherepanov, P.P., and W. Wackernagel. 1995. Gene disruption in Escherichia coli: TcR and KmR cassettes with the option of Flp-catalyzed excision of the antibiotic- resistance determinant. Gene 158:9-14.
23. Consortium, T.U. 2015. UniProt: a hub for protein information. Nucleic Acids Research 43:D204-D212.
24. Coppa, G.V., L. Zampini, T. Galeazzi, and O. Gabrielli. 2006. Prebiotics in human milk: a review. Digestive and Liver Disease 38:S291-S294.
25. Coussement, P., J. Maertens, J. Beauprez, W. Van Bellegem, and M. De Mey. 2014. One step DNA assembly for combinatorial metabolic engineering, p.70-77, vol. 23.
26. Curran, K.A., A.S. Karim, A. Gupta, and H.S. Alper. 2013. Use of expression-enhancing terminators in Saccharomyces cerevisiae to increase mRNA half-life and improve gene expression control for metabolic engineering applications, p.88-97, vol. 19.
27. Datsenko, K.A., and B.L. Wanner. 2000. One-step inactivation of chromosomal genes in Escherichia coli K-12 using PCR products. Proceedings of the national academy of sciences of the United States of America 97:6640-6645.
28. Davis, S.S. 1997. Biomedical applications of nanotechnology - implications for drug targeting and gene therapy. Trends in Biotechnology 15:217-224.
29. De Mey, M., J. Maertens, G.J. Lequeux, W.K. Soetaert, and E.J. Vandamme. 2007. Construction and model-based analysis of a promoter library for E.coli: an indispensable tool for metabolic engineering. BMC Biotechnology 7:34-48.
30. DiCarlo, J.E., J.E. Norville, P. Mali, X. Rios, J. Aach, and G.M. Church. 2013. Genome engineering in Saccharomyces cerevisiae using CRISPR-Cas systems. Nucleic Acids Research.
31.  , E., M.
, E., M.  , Z.
, Z.  , M.
, M. 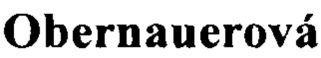 , and I. Hapala. 2015. Production of squalene by lactose-fermenting yeast Kluyveromyces lactis with reduced squalene epoxidase activity. Letters in Applied Microbiology 61:77-84.
, and I. Hapala. 2015. Production of squalene by lactose-fermenting yeast Kluyveromyces lactis with reduced squalene epoxidase activity. Letters in Applied Microbiology 61:77-84.
32. Dumon, С, B. Priem, S.L. Martin, A. Heyraud, C. Bosso, and E. Samain. 2001. In vivo fucosylation of lactoN-neotetraose and lactoN-neohexaose by heterologous expression of Helicobacter pylori α-1,3 fucosyltransferase in engineered Escherichia coli. Glycoconjugate Journal 18:465-474.
33. Dykhuizen, D., and D. Hartl. 1978. Transport by the lactose permease of Escherichia coli as the basis of lactose killing. Journal of Bacteriology 135:876-882.
34. Eames, M., and T. Kortemme. 2012. Cost-Benefit Tradeoffs in Engineered lac Operons. Science 336:911-915.
35. Edwards, J.S., R. Ramakrishna, С.H. Schilling, and В.O. Palsson. 1999. Metabolic flux balance analysis. Metabolic Engineering: 13-57.
36. Engler, С, R. Gruetzner, R. Kandzia, and S. Marillonnet. 2009. Golden Gate Shuffling: A One-Pot DNA Shuffling Method Based on Type lis Restriction Enzymes. PLoS ONE 4:e5553.
37. Filonov, G.S., J.D. Moon, N. Svensen, and S. R. Jaffrey. 2014. Broccoli: Rapid Selection of an RNA Mimic of Green Fluorescent Protein by Fluorescence-Based Selection and Directed Evolution. Journal of the American Chemical Society.
38. Galperin, M.Y., and G.R. Cochrane. 2009. Nucleic Acids Research annual Database Issue and the NAR online Molecular Biology Database Collection in 2009. Nucleic Acid Research 37:Dl-4.
39. Ghazi, A., H. Therisod, and E. Shechter. 1983. Comparison of lactose uptake in resting and energized Escherichia coli cells: high rates of respiration inactivate the lac carrier. Journal of Bacteriology 154:92-103.
40. Gietz, R.D., R.H. Schiestl, A.R. Willems, and R.A. Woods. 1995. Studies on the transformation of intact yeast cells by the LiAc/SS-DNA/PEG procedure. Yeast 11:355-360.
41. Hammer, K., I. Mijakovic, and P.R. Jensen. 2006. Synthetic promoter libraries - tuning of gene expression. TRENDS in Biotechnology 24:53-55.
42. Hanahan, D., J. Jessee, and F.R. Bloom. 1991. Plasmid transformation of Escherichia coli and other bacteria. Methods in Enzymology 204:63-113.
43. Hebert, C.G., J.J. Valdes, and W. E. Bentley. 2008. Beyond silencing- engineering applications of RNA interference and antisense technology for altering cellular phenotype. Current opinion in biotechnology 19:500-505.
44. Heinemann, M., A. Kummel, R. Ruinatscha, and S. Panke. 2005. KEGG: Kyoto Encyclopedia of Genes and Genomes. In silico genome-scale reconstruction and validation of the Staphylococcus aureus metabolic network. Biotechnol Bioeng 92:850-864.
45. Hoang, Т.Т., R.R. Karkhoff-Schweizer, A.J. Kutchma, and H.P. Schweizer. 1998. A broad-host-range Flp-FRT recombination system for site-specific excision of chromosomally-located DNA sequences: application for isolation of unmarked Pseudomonas aeruginosa mutants. Gene 212:77-86.
46. Jiang, W., D. Bikard, D. Cox, F. Zhang, and L. A. Marraffini. 2013. RNA-guided editing of bacterial genomes using CRISPR-Cas systems. Nat Biotech 31:233-239.
47. Kanehisa, M., M. Araki, S. Goto, M. Hattori, M. Hirakawa, M. Itoh, T. Katayama, S. Kawashima, S. Okuda, T. Tokimatsu, and Y. Yamanishi. 2008. KEGG for linking genomes to life and the environment. Nucleic Acid Research 36:D480-484.
48. Koizumi, S., T. Endo, K. Tabata, and A. Ozaki. 1998. Large-scale production of UDP-galactose and globotriose by coupling metabolically engineered bacteria. Nat Biotech 16:847-850.
49. Kojima, K.K., T. Matsumoto, and H. Fujiwara. 2005. Eukaryotic Translational Coupling in UAAUG Stop-Start Codons for the Bicistronic RNA Translation of the Non-Long Terminal Repeat Retrotransposon SART1. Molecular and Cellular Biology 25:7675-7686.
50. Kok, S.d., L.H. Stanton, T. Slaby, M. Durot, V.F. Holmes, K.G. Patel, D. Piatt, E.B. Shapland, Z. Serber, J. Dean, J.D. Newman, and S.S. Chandran. 2014. Rapid and Reliable DNA Assembly via Ligase Cycling Reaction. ACS Synthetic Biology 3:97-106.
51. Kristensen, C.S., L. Eberl, J. M. Sanchez-Romero, M. Givskov, S. Molin, and V. De Lorenzo. 1995. Site-specific deletions of chromosomally located DNA segments with the multimer resolution system of broad-host-range plasmid RP4. Journal of Bacteriology 177:52-58.
52. Lee, M.E., W.C. DeLoache, B. Cervantes, and J.E. Dueber. 2015. A Highly Characterized Yeast Toolkit for Modular, Multipart Assembly. ACS Synthetic Biology 4:975-986.
53. Levin-Karp, A., U. Barenholz, T. Bareia, M. Dayagi, L. Zelcbuch, N. Antonovsky, E. Noor, and R. Milo. 2013. Quantifying Translational Coupling in E.coli Synthetic Operons Using RBS Modulation and Fluorescent Reporters. ACS Synthetic Biology 2:327-336.
54. Llaneras, F., and J.  . 2008. Stoichiometric modelling of cell metabolism. Journal of Bioscience and Bioengineering 105:1-11.
. 2008. Stoichiometric modelling of cell metabolism. Journal of Bioscience and Bioengineering 105:1-11.
55. Lodi, Т., and C. Donnini. 2005. Lactose-induced cell death of b-galactosidase mutants in Kluyveromyces lactis. FEMS Yeast Research 5:727-734.
56. Martin, P., O. Albagli, M. Poggi, K. Boulukos, and P. Pognonec. 2006. Development of a new bicistronic retroviral vector with strong IRES activity. BMC Biotechnology 6:4.
57. McShan, D.С, S. Rao, and I. Shah. 2003. PathMiner: predicting metabolic pathways by heuristic search. Bioinformatics 19:1692-1698.
58. Mendez-Perez, D., S. Gunasekaran, V.J. Orler, and B.F. Pfleger. 2012. A translation-coupling DNA cassette for monitoring protein translation in Escherichia coli. Metabolic Engineering 14:298-305.
59. Merighi, M., J.M. Mccoy, and M.I. Heidtman. 2012. Biosynthesis of human milk oligosaccharides in engineered bacteria. WO 2012112777
60. Mutalik, V.K., J.C. Guimaraes, G. Cambray, C. Lam, M.J. Christoffersen, Q.-A. Mai, A.B. Tran, M. Paull, J.D. Keasling, A.P. Arkin, and D. Endy. 2013. Precise and reliable gene expression via standard transcription and translation initiation elements. Nat Meth 10:354-360.
61. Nakamura, Y., T. Gojobori, and T. Ikemura. 2000. Codon usage tabulated from international DNA sequence databases: status for the year 2000. Nucleic Acids Research 28:292.
62. Pechmann, S., and J. Frydman. 2012. Evolutionary conservation of codon optimality reveals hidden signatures of cotranslational folding. Nat Struct Mol Biol 20:237-243.
63. Peijnenburg, А. С.M., G. Venema, and S. Bron. 1990. Translational coupling in a penP-lacZ gene fusion in Bacillus subtilis and Escherichia coli: Use of AUA as a restart codon. 1990 221:267-272.
64. Pothoulakis, G., F. Ceroni, B. Reeve, and T. Ellis. 2014. The Spinach RNA Aptamer as a Characterization Tool for Synthetic Biology. ACS Synthetic Biology 3:182-187.
65. Rasmussen, L., H. Sperling-Petersen, and K. Mortensen. 2007. Hitting bacteria at the heart of the central dogma: sequence-specific inhibition. Microbial Cell Factories 6:24.
66. Rhodius, V.A., V.K. Mutalik, and C.A. Gross. Predicting the strength of UP-elements and full-length E. coli SigmaE promoters. Nucleic Acids Research 40:2907-2924.
67. Salis, H.M., E.A. Mirsky, and C.A. Voigt. 2009. Automated design of synthetic ribosome binding sites to control protein expression. Nat Biotech 27:946-950.
68. Seed, В., and J. Holgersson. 1999. Fucosyltransferase genes and uses thereof. Патент US 5858752
69. Supek, F., and T. muc. 2010. On Relevance of Codon Usage to Expression of Synthetic and Natural Genes in Escherichia coli. Genetics 185:1129-1134.
70. Timblin, C.R., and M.L. Kahn. 1984. Lactose inhibits the growth of Rhizobium meliloti cells that contain an actively expressed Escherichia coli lactose operon. Journal of Bacteriology 158:1204-1207.
71. Varki, A. 1992. Diversity in the sialic acids. Glycobiology 2:25-40.
72. Waldo, G.S., В.M. Standish, J. Berendzen, and Т.C. Terwilliger. 1999. Rapid protein-folding assay using green fluorescent protein. Nat Biotech 17:691-695.
73. Welch, M., S. Govindarajan, J.E. Ness, A. Villalobos, A. Gurney, J. Minshull, and C. Gustafsson. 2009. Design Parameters to Control Synthetic Gene Expression in Escherichia coli. PLoS ONE 4:e7002.
74. Williams, J., J. Luke, and C. Hodgson. 2009. Strain engineering by genome mass transfer: Efficient chromosomal trait transfer method utilizing donor genomic DNA and recipient recombineering hosts. Molecular Biotechnology 43:41-51.
75. Wilson, D.M., R.M. Putzrath, and Т.H. Wilson. 1981. Inhibition of growth of Escherichia coli by lactose and other galactosides. Biochimica et Biophysica Acta (BBA) - Biomembranes 649:377-384.
76. Xu, X.J., L.M. Cao, and X. Chen. 2008. Elementary flux mode analysis for optimized ethanol yield in anaerobic fermentation of glucose with Saccharomyces cerevisiae. Chinese Journal of Chemical Engineering 16:135-142.
77. Yanase, H., J. Kurii, and K. Tonomura. 1988. Fermentation of lactose by Zymomonas mobilis carrying a Lac+ recombinant plasmid. Journal of Fermentation Technology 66:409-415.
78. Zhou, M., J. Guo, J. Cha, M. Chae, S. Chen, J. M. Barral, M. S. Sachs, and Y. Liu. 2013. Non-optimal codon usage affects expression, structure and function of clock protein FRQ. Nature 495:111-115.
79. Zou, R., K. Zhou, G. Stephanopoulos, and H.P. Too. 2013. Combinatorial Engineering of 1-Deoxy-D-Xylulose 5-Phosphate Pathway Using Cross-Lapping In Vitro Assembly (CLIVA) Method. PLoS ONE 8:e79557.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ЮНИВЕРСИТЕЙТ ГЕНТ
<120> МУТАНТНЫЕ МИКРООРГАНИЗМЫ, УСТОЙЧИВЫЕ К ГИБЕЛИ ПОД ДЕЙСТВИЕМ ЛАКТОЗЫ
<130> P2013/049PCT
<150> EP14193151.9
<151> 2014-11-14
<160> 58
<170> PatentIn version 3.5
<210> 1
<211> 1460
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 1
agcgcaacgc aattaatgtg agttagctca ctcattaggc accccaggct tgtgtaggct 60
ggagctgctt cgaagttcct atactttcta gagaatagga acttcggaat aggaactaag 120
gaggatattc atatggaccg atatcccggg cggccgctct agaagaagct tgggatccgt 180
cgacctcgaa ttcggaggaa acaaagatgt actatttaaa aaacacaaac ttttggatgt 240
tcggtttatt ctttttcttt tactttttta tcatgggagc ctacttcccg tttttcccga 300
tttggctaca tgacatcaac catatcagca aaagtgatac gggtattatt tttgccgcta 360
tttctctgtt ctcgctatta ttccaaccgc tgtttggtct gctttctgac aaactcgggc 420
tgcgcaaata cctgctgtgg attattaccg gcatgttagt gatgtttgcg ccgttcttta 480
tttttatctt cgggccactg ttacaataca acattttagt aggatcgatt gttggtggta 540
tttatctagg cttttgtttt aacgccggtg cgccagcagt agaggcattt attgagaaag 600
tcagccgtcg cagtaatttc gaatttggtc gcgcgcggat gtttggctgt gttggctggg 660
cgctgtgtgc ctcgattgtc ggcatcatgt tcaccatcaa taatcagttt gttttctggc 720
tgggctctgg ctgtgcactc atcctcgccg ttttactctt tttcgccaaa acggatgcgc 780
cctcttctgc cacggttgcc aatgcggtag gtgccaacca ttcggcattt agccttaagc 840
tggcactgga actgttcaga cagccaaaac tgtggttttt gtcactgtat gttattggcg 900
tttcctgcac ctacgatgtt tttgaccaac agtttgctaa tttctttact tcgttctttg 960
ctaccggtga acagggtacg cgggtatttg gctacgtaac gacaatgggc gaattactta 1020
acgcctcgat tatgttcttt gcgccactga tcattaatcg catcggtggg aaaaacgccc 1080
tgctgctggc tggcactatt atgtctgtac gtattattgg ctcatcgttc gccacctcag 1140
cgctggaagt ggttattctg aaaacgctgc atatgtttga agtaccgttc ctgctggtgg 1200
gctgctttaa atatattacc agccagtttg aagtgcgttt ttcagcgacg atttatctgg 1260
tctgtttctg cttctttaag caactggcga tgatttttat gtctgtactg gcgggcaata 1320
tgtatgaaag catcggtttc cagggcgctt atctggtgct gggtctggtg gcgctgggct 1380
tcaccttaat ttccgtgttc acgcttagcg gccccggccc gctttccctg ctgcgtcgtc 1440
aggtgaatga agtcgcttaa 1460
<210> 2
<211> 4432
<212> DNA
<213> Artificial sequence
<220>
<223> Genetic constructs detecting expressed lactose transporters
<400> 2
atgtactatt taaaaaacac aaacttttgg atgttcggtt tattcttttt cttttacttt 60
tttatcatgg gagcctactt cccgtttttc ccgatttggc tacatgacat caaccatatc 120
agcaaaagtg atacgggtat tatttttgcc gctatttctc tgttctcgct attattccaa 180
ccgctgtttg gtctgctttc tgacaaactc gggctgcgca aatacctgct gtggattatt 240
accggcatgt tagtgatgtt tgcgccgttc tttattttta tcttcgggcc actgttacaa 300
tacaacattt tagtaggatc gattgttggt ggtatttatc taggcttttg ttttaacgcc 360
ggtgcgccag cagtagaggc atttattgag aaagtcagcc gtcgcagtaa tttcgaattt 420
ggtcgcgcgc ggatgtttgg ctgtgttggc tgggcgctgt gtgcctcgat tgtcggcatc 480
atgttcacca tcaataatca gtttgttttc tggctgggct ctggctgtgc actcatcctc 540
gccgttttac tctttttcgc caaaacggat gcgccctctt ctgccacggt tgccaatgcg 600
gtaggtgcca accattcggc atttagcctt aagctggcac tggaactgtt cagacagcca 660
aaactgtggt ttttgtcact gtatgttatt ggcgtttcct gcacctacga tgtttttgac 720
caacagtttg ctaatttctt tacttcgttc tttgctaccg gtgaacaggg tacgcgggta 780
tttggctacg taacgacaat gggcgaatta cttaacgcct cgattatgtt ctttgcgcca 840
ctgatcatta atcgcatcgg tgggaaaaac gccctgctgc tggctggcac tattatgtct 900
gtacgtatta ttggctcatc gttcgccacc tcagcgctgg aagtggttat tctgaaaacg 960
ctgcatatgt ttgaagtacc gttcctgctg gtgggctgct ttaaatatat taccagccag 1020
tttgaagtgc gtttttcagc gacgatttat ctggtctgtt tctgcttctt taagcaactg 1080
gcgatgattt ttatgtctgt actggcgggc aatatgtatg aaagcatcgg tttccagggc 1140
gcttatctgg tgctgggtct ggtggcgctg ggcttcacct taatttccgt gttcacgctt 1200
agcggccccg gcccgctttc cctgctgcgt cgtcaggtga atgaagtcgc tgataaaaac 1260
tggaggcgtc ataggggatc ccgtcgtttt acaacgtcgt gactgggaaa accctggcgt 1320
tacccaactt aatcgccttg cagcacatcc ccctttcgcc agctggcgta atagcgaaga 1380
ggcccgcacc gatcgccctt cccaacagtt gcgcagcctg aatggcgaat ggcgctttgc 1440
ctggtttccg gcaccagaag cggtgccgga aagctggctg gagtgcgatc ttcctgaggc 1500
cgatactgtc gtcgtcccct caaactggca gatgcacggt tacgatgcgc ccatctacac 1560
caacgtgacc tatcccatta cggtcaatcc gccgtttgtt cccacggaga atccgacggg 1620
ttgttactcg ctcacattta atgttgatga aagctggcta caggaaggcc agacgcgaat 1680
tatttttgat ggcgttaact cggcgtttca tctgtggtgc aacgggcgct gggtcggtta 1740
cggccaggac agtcgtttgc cgtctgaatt tgacctgagc gcatttttac gcgccggaga 1800
aaaccgcctc gcggtgatgg tgctgcgctg gagtgacggc agttatctgg aagatcagga 1860
tatgtggcgg atgagcggca ttttccgtga cgtctcgttg ctgcataaac cgactacaca 1920
aatcagcgat ttccatgttg ccactcgctt taatgatgat ttcagccgcg ctgtactgga 1980
ggctgaagtt cagatgtgcg gcgagttgcg tgactaccta cgggtaacag tttctttatg 2040
gcagggtgaa acgcaggtcg ccagcggcac cgcgcctttc ggcggtgaaa ttatcgatga 2100
gcgtggtggt tatgccgatc gcgtcacact acgtctgaac gtcgaaaacc cgaaactgtg 2160
gagcgccgaa atcccgaatc tctatcgtgc ggtggttgaa ctgcacaccg ccgacggcac 2220
gctgattgaa gcagaagcct gcgatgtcgg tttccgcgag gtgcggattg aaaatggtct 2280
gctgctgctg aacggcaagc cgttgctgat tcgaggcgtt aaccgtcacg agcatcatcc 2340
tctgcatggt caggtcatgg atgagcagac gatggtgcag gatatcctgc tgatgaagca 2400
gaacaacttt aacgccgtgc gctgttcgca ttatccgaac catccgctgt ggtacacgct 2460
gtgcgaccgc tacggcctgt atgtggtgga tgaagccaat attgaaaccc acggcatggt 2520
gccaatgaat cgtctgaccg atgatccgcg ctggctaccg gcgatgagcg aacgcgtaac 2580
gcgaatggtg cagcgcgatc gtaatcaccc gagtgtgatc atctggtcgc tggggaatga 2640
atcaggccac ggcgctaatc acgacgcgct gtatcgctgg atcaaatctg tcgatccttc 2700
ccgcccggtg cagtatgaag gcggcggagc cgacaccacg gccaccgata ttatttgccc 2760
gatgtacgcg cgcgtggatg aagaccagcc cttcccggct gtgccgaaat ggtccatcaa 2820
aaaatggctt tcgctacctg gagagacgcg cccgctgatc ctttgcgaat acgcccacgc 2880
gatgggtaac agtcttggcg gtttcgctaa atactggcag gcgtttcgtc agtatccccg 2940
tttacagggc ggcttcgtct gggactgggt ggatcagtcg ctgattaaat atgatgaaaa 3000
cggcaacccg tggtcggctt acggcggtga ttttggcgat acgccgaacg atcgccagtt 3060
ctgtatgaac ggtctggtct ttgccgaccg cacgccgcat ccagcgctga cggaagcaaa 3120
acaccagcag cagtttttcc agttccgttt atccgggcaa accatcgaag tgaccagcga 3180
atacctgttc cgtcatagcg ataacgagct cctgcactgg atggtggcgc tggatggtaa 3240
gccgctggca agcggtgaag tgcctctgga tgtcgctcca caaggtaaac agttgattga 3300
actgcctgaa ctaccgcagc cggagagcgc cgggcaactc tggctcacag tacgcgtagt 3360
gcaaccgaac gcgaccgcat ggtcagaagc cgggcacatc agcgcctggc agcagtggcg 3420
tctggcggaa aacctcagtg tgacgctccc cgccgcgtcc cacgccatcc cgcatctgac 3480
caccagcgaa atggattttt gcatcgagct gggtaataag cgttggcaat ttaaccgcca 3540
gtcaggcttt ctttcacaga tgtggattgg cgataaaaaa caactgctga cgccgctgcg 3600
cgatcagttc acccgtgcac cgctggataa cgacattggc gtaagtgaag cgacccgcat 3660
tgaccctaac gcctgggtcg aacgctggaa ggcggcgggc cattaccagg ccgaagcagc 3720
gttgttgcag tgcacggcag atacacttgc tgatgcggtg ctgattacga ccgctcacgc 3780
gtggcagcat caggggaaaa ccttatttat cagccggaaa acctaccgga ttgatggtag 3840
tggtcaaatg gcgattaccg ttgatgttga agtggcgagc gatacaccgc atccggcgcg 3900
gattggcctg aactgccagc tggcgcaggt agcagagcgg gtaaactggc tcggattagg 3960
gccgcaagaa aactatcccg accgccttac tgccgcctgt tttgaccgct gggatctgcc 4020
attgtcagac atgtataccc cgtacgtctt cccgagcgaa aacggtctgc gctgcgggac 4080
gcgcgaattg aattatggcc cacaccagtg gcgcggcgac ttccagttca acatcagccg 4140
ctacagtcaa cagcaactga tggaaaccag ccatcgccat ctgctgcacg cggaagaagg 4200
cacatggctg aatatcgacg gtttccatat ggggattggt ggcgacgact cctggagccc 4260
gtcagtatcg gcggaattcc agctgagcgc cggtcgctac cattaccagt tggtctggtg 4320
tcaaaaataa gctggtttga agggtattgg tcggtcagtt tcacctgatt tacgtaaaaa 4380
cccgcttcgg cgggtttttg cttttggagg ggcagaaaga tgaatgactg tc 4432
<210> 3
<211> 2093
<212> DNA
<213> Artificial sequence
<220>
<223> Genetic constructs detecting expressed lactose transporters
<400> 3
atgtactatt taaaaaacac aaacttttgg atgttcggtt tattcttttt cttttacttt 60
tttatcatgg gagcctactt cccgtttttc ccgatttggc tacatgacat caaccatatc 120
agcaaaagtg atacgggtat tatttttgcc gctatttctc tgttctcgct attattccaa 180
ccgctgtttg gtctgctttc tgacaaactc gggctgcgca aatacctgct gtggattatt 240
accggcatgt tagtgatgtt tgcgccgttc tttattttta tcttcgggcc actgttacaa 300
tacaacattt tagtaggatc gattgttggt ggtatttatc taggcttttg ttttaacgcc 360
ggtgcgccag cagtagaggc atttattgag aaagtcagcc gtcgcagtaa tttcgaattt 420
ggtcgcgcgc ggatgtttgg ctgtgttggc tgggcgctgt gtgcctcgat tgtcggcatc 480
atgttcacca tcaataatca gtttgttttc tggctgggct ctggctgtgc actcatcctc 540
gccgttttac tctttttcgc caaaacggat gcgccctctt ctgccacggt tgccaatgcg 600
gtaggtgcca accattcggc atttagcctt aagctggcac tggaactgtt cagacagcca 660
aaactgtggt ttttgtcact gtatgttatt ggcgtttcct gcacctacga tgtttttgac 720
caacagtttg ctaatttctt tacttcgttc tttgctaccg gtgaacaggg tacgcgggta 780
tttggctacg taacgacaat gggcgaatta cttaacgcct cgattatgtt ctttgcgcca 840
ctgatcatta atcgcatcgg tgggaaaaac gccctgctgc tggctggcac tattatgtct 900
gtacgtatta ttggctcatc gttcgccacc tcagcgctgg aagtggttat tctgaaaacg 960
ctgcatatgt ttgaagtacc gttcctgctg gtgggctgct ttaaatatat taccagccag 1020
tttgaagtgc gtttttcagc gacgatttat ctggtctgtt tctgcttctt taagcaactg 1080
gcgatgattt ttatgtctgt actggcgggc aatatgtatg aaagcatcgg tttccagggc 1140
gcttatctgg tgctgggtct ggtggcgctg ggcttcacct taatttccgt gttcacgctt 1200
agcggccccg gcccgctttc cctgctgcgt cgtcaggtga atgaagtcgc tcatcatcac 1260
caccatcatt aggatggtgg tgatgataat ggagaaaaaa atcactggat ataccaccgt 1320
tgatatatcc caatggcatc gtaaagaaca ttttgaggca tttcagtcag ttgctcaatg 1380
tacctataac cagaccgttc agctggatat tacggccttt ttaaagaccg taaagaaaaa 1440
taagcacaag ttttatccgg cctttattca cattcttgcc cgcctgatga atgctcatcc 1500
ggagttccgt atggcaatga aagacggtga gctggtgata tgggatagtg ttcacccttg 1560
ttacaccgtt ttccatgagc aaactgaaac gttttcatcg ctctggagtg aataccacga 1620
cgatttccgg cagtttctac acatatattc gcaagatgtg gcgtgttacg gtgaaaacct 1680
ggcctatttc cctaaagggt ttattgagaa tatgtttttc gtcagcgcca atccctgggt 1740
gagtttcacc agttttgatt taaacgtggc caatatggac aacttcttcg cccccgtttt 1800
cactatgggc aaatattata cgcaaggcga caaggtgctg atgccgctgg cgattcaggt 1860
tcatcatgcc gtttgtgatg gcttccatgt cggcagaatg cttaatgaat tacaacagta 1920
ctgcgatgag tggcagggcg gggcgtaagg atccaaaggt acctctagag tcgacctgca 1980
ggccttcgta aatctggcga gtggggaact gccagacatc aaataaaaca aaaggctcag 2040
tcggaagact gggccttttg ttttatctgt tgtttgtcgg tgaacactct ccc 2093
<210> 4
<211> 2628
<212> DNA
<213> Artificial sequence
<220>
<223> Genetic constructs detecting expressed lactose transporters
<400> 4
atggcagatc attcgagcag ctcatcttcg ctgcagaaga agccaattaa tactatcgag 60
cataaagaca ctttgggcaa tgatcgggat cacaaggaag ccttgaacag tgataatgat 120
aatacttctg gattgaaaat caatggtgtc cccatcgagg acgctagaga ggaagtgctc 180
ttaccaggtt acttgtcgaa gcaatattac aaattgtacg gtttatgttt tataacatat 240
ctgtgtgcta ctatgcaagg ttatgatggg gctttaatgg gttctatcta taccgaagat 300
gcatatttga aatactacca tttggatatt aactcatcct ctggtactgg tctagtgttc 360
tctattttca acgttggtca aatttgcggt gcattctttg ttcctcttat ggattggaaa 420
ggtagaaaac ctgctatttt aattgggtgt ctgggtgttg ttattggtgc tattatttcg 480
tctttaacaa caacaaagag tgcattaatt ggtggtagat ggttcgtggc ctttttcgct 540
acaatcgcta atgcagcagc tccaacatac tgtgcagaag tggctccagc tcacttaaga 600
ggtaaggttg caggtcttta taacaccctt tggtctgtcg gttccattgt tgctgccttt 660
agcacttacg gtaccaacaa aaacttccct aactcctcca aggcttttaa gattccatta 720
tacttacaaa tgatgttccc aggtcttgtg tgtatatttg gttggttaat cccagaatct 780
ccaagatggt tggttggtgt tggccgtgag gaagaagctc gtgaattcat tatcaaatac 840
cacttaaatg gcgatagaac tcatccatta ttggatatgg agatggcaga aataatagaa 900
tctttccatg gtacagattt atcaaaccct ctagaaatgt tagatgtaag gagcttattc 960
agaacgagat cggataggta cagagcaatg ttggttatac ttatggcttg gttcggtcaa 1020
ttttccggta acaatgtgtg ttcgtactat ttgcctacca tgttgagaaa tgttggtatg 1080
aagagtgtct cattgaatgt gttaatgaat ggtgtttatt ccatcgtcac ttggatttct 1140
tcaatttgcg gtgcattctt tattgataag attggtagaa gggaaggttt ccttggttct 1200
atctcaggtg ctgcattagc attgacaggt ctatctatct gtactgctcg ttatgagaag 1260
actaagaaga agagtgcttc caatggtgca ttggtgttca tttatctctt tggtggtatc 1320
ttttcttttg ctttcactcc aatgcaatcc atgtactcaa cagaagtgtc tacaaacttg 1380
acgagatcta aggcccaact cctcaacttt gtggtttctg gtgttgccca atttgttaat 1440
caatttgcta ctccaaaggc aatgaagaat atcaaatatt ggttctatgt gttctacgtt 1500
ttcttcgata ttttcgaatt tattgttatc tacttcttct tcgttgaaac taagggtaga 1560
agcttagaag aattagaagt tgtctttgaa gctccaaacc caagaaaggc atccgttgat 1620
caagcattct tggctcaagt cagggcaact ttggtccaac gaaatgacgt tagagttgca 1680
aatgctcaaa atttgaaaga gcaagagcct ctaaagagcg atgctgatca tgtcgaaaag 1740
ctttcagagg cagaatctgt tagagcagaa ggaaggggtt ctttgttgac ttgtggagat 1800
gttgaggaga atccaggacc aggtaaggaa aagactcacg tttcgaggcc gcgattaaat 1860
tccaacatgg atgctgattt atatgggtat aaatgggctc gcgataatgt cgggcaatca 1920
ggtgcgacaa tctatcgatt gtatgggaag cccgatgcgc cagagttgtt tctgaaacat 1980
ggcaaaggta gcgttgccaa tgatgttaca gatgagatgg tcagactaaa ctggctgacg 2040
gaatttatgc ctcttccgac catcaagcat tttatccgta ctcctgatga tgcatggtta 2100
ctcaccactg cgatccccgg caaaacagca ttccaggtat tagaagaata tcctgattca 2160
ggtgaaaata ttgttgatgc gctggcagtg ttcctgcgcc ggttgcattc gattcctgtt 2220
tgtaattgtc cttttaacag cgatcgcgta tttcgtctcg ctcaggcgca atcacgaatg 2280
aataacggtt tggttgatgc gagtgatttt gatgacgagc gtaatggctg gcctgttgaa 2340
caagtctgga aagaaatgca taagcttttg ccattctcac cggattcagt cgtcactcat 2400
ggtgatttct cacttgataa ccttattttt gacgagggga aattaatagg ttgtattgat 2460
gttggacgag tcggaatcgc agaccgatac caggatcttg ccatcctatg gaactgcctc 2520
ggtgagtttt ctccttcatt acagaaacgg ctttttcaaa aatatggtat tgataatcct 2580
gatatgaata aattgcagtt tcatttgatg ctcgatgagt ttttctaa 2628
<210> 5
<211> 1457
<212> DNA
<213> Artificial sequence
<220>
<223> Genetic constructs detecting expressed lactose transporters
<400> 5
atgtactatt taaaaaacac aaacttttgg atgttcggtt tattcttttt cttttacttt 60
tttatcatgg gagcctactt cccgtttttc ccgatttggc tacatgacat caaccatatc 120
agcaaaagtg atacgggtat tatttttgcc gctatttctc tgttctcgct attattccaa 180
ccgctgtttg gtctgctttc tgacaaactc gggctgcgca aatacctgct gtggattatt 240
accggcatgt tagtgatgtt tgcgccgttc tttattttta tcttcgggcc actgttacaa 300
tacaacattt tagtaggatc gattgttggt ggtatttatc taggcttttg ttttaacgcc 360
ggtgcgccag cagtagaggc atttattgag aaagtcagcc gtcgcagtaa tttcgaattt 420
ggtcgcgcgc ggatgtttgg ctgtgttggc tgggcgctgt gtgcctcgat tgtcggcatc 480
atgttcacca tcaataatca gtttgttttc tggctgggct ctggctgtgc actcatcctc 540
gccgttttac tctttttcgc caaaacggat gcgccctctt ctgccacggt tgccaatgcg 600
gtaggtgcca accattcggc atttagcctt aagctggcac tggaactgtt cagacagcca 660
aaactgtggt ttttgtcact gtatgttatt ggcgtttcct gcacctacga tgtttttgac 720
caacagtttg ctaatttctt tacttcgttc tttgctaccg gtgaacaggg tacgcgggta 780
tttggctacg taacgacaat gggcgaatta cttaacgcct cgattatgtt ctttgcgcca 840
ctgatcatta atcgcatcgg tgggaaaaac gccctgctgc tggctggcac tattatgtct 900
gtacgtatta ttggctcatc gttcgccacc tcagcgctgg aagtggttat tctgaaaacg 960
ctgcatatgt ttgaagtacc gttcctgctg gtgggctgct ttaaatatat taccagccag 1020
tttgaagtgc gtttttcagc gacgatttat ctggtctgtt tctgcttctt taagcaactg 1080
gcgatgattt ttatgtctgt actggcgggc aatatgtatg aaagcatcgg tttccagggc 1140
gcttatctgg tgctgggtct ggtggcgctg ggcttcacct taatttccgt gttcacgctt 1200
agcggccccg gcccgctttc cctgctgcgt cgtcaggtga atgaagtcgc tgataactct 1260
acgacaacct cttcacagcc aatctcgccc ggatagctca gtcggtagag cagcggccgg 1320
acgcaactga atgaaatggt gaaggacggg tccaggtgtg gctgcttcgg cagtgcagct 1380
tgttgagtag agtgtgagct ccgtaactag tcgcgtccgg ccgcgggtcc agggttcaag 1440
tccctgttcg ggcgcca 1457
<210> 6
<211> 3638
<212> DNA
<213> Artificial sequence
<220>
<223> Vector
<400> 6
cgcgttggat gcaggcatgc aagcttggct gttttggcgg atgagagaag attttcagcc 60
tgatacagat taaatcagaa cgcagaagcg gtctgataaa acagaatttg cctggcggca 120
gtagcgcggt ggtcccacct gaccccatgc cgaactcaga agtgaaacgc cgtagcgccg 180
atggtagtgt ggggtctccc catgcgagag tagggaactg ccaggcatca aataaaacga 240
aaggctcagt cgaaagactg ggcctttcgt tttatctgtt gtttgtcggt gaacgctctc 300
ctgagtagga caaatccgcc gggagcggat ttgaacgttg cgaagcaacg gcccggaggg 360
tggcgggcag gacgcccgcc ataaactgcc aggcatcaaa ttaagcagaa ggccatcctg 420
acggatggcc tttttgcgtt tctacaaact ctttttgttt atttttctaa atacattcaa 480
atatgtatcc gctcatgaga caataaccct gataaatgct tcaataatat tgaaaaagga 540
agagtatgag tattcaacat ttccgtgtcg cccttattcc cttttttgcg gcattttgcc 600
ttcctgtttt tgctcaccca gaaacgctgg tgaaagtaaa agatgctgaa gatcagttgg 660
gtgcacgagt gggttacatc gaactggatc tcaacagcgg taagatcctt gagagttttc 720
gccccgaaga acgttttcca atgatgagca cttttaaagt tctgctatgt ggcgcggtat 780
tatcccgtgt tgacgccggg caagagcaac tcggtcgccg catacactat tctcagaatg 840
acttggttga gtactcacca gtcacagaaa agcatcttac ggatggcatg acagtaagag 900
aattatgcag tgctgccata accatgagtg ataacactgc ggccaactta cttctgacaa 960
cgatcggagg accgaaggag ctaaccgctt ttttgcacaa catgggggat catgtaactc 1020
gccttgatcg ttgggaaccg gagctgaatg aagccatacc aaacgacgag cgtgacacca 1080
cgatgcctac agcaatggca acaacgttgc gcaaactatt aactggcgaa ctacttactc 1140
tagcttcccg gcaacaatta atagactgga tggaggcgga taaagttgca ggaccacttc 1200
tgcgctcggc ccttccggct ggctggttta ttgctgataa atctggagcc ggtgagcgtg 1260
ggtctcgcgg tatcattgca gcactggggc cagatggtaa gccctcccgt atcgtagtta 1320
tctacacgac ggggagtcag gcaactatgg atgaacgaaa tagacagatc gctgagatag 1380
gtgcctcact gattaagcat tggtaactgt cagaccaagt ttactcatat atactttaga 1440
ttgatttaaa acttcatttt taatttaaaa ggatctaggt gaagatcctt tttgataatc 1500
tcatgaccaa aatcccttaa cgtgagtttt cgttccactg agcgtcagac cccgtagaaa 1560
agatcaaagg atcttcttga gatccttttt ttctgcgcgt aatctgctgc ttgcaaacaa 1620
aaaaaccacc gctaccagcg gtggtttgtt tgccggatca agagctacca actctttttc 1680
cgaaggtaac tggcttcagc agagcgcaga taccaaatac tgtccttcta gtgtagccgt 1740
agttaggcca ccacttcaag aactctgtag caccgcctac atacctcgct ctgctaatcc 1800
tgttaccagt ggctgctgcc agtggcgata agtcgtgtct taccgggttg gactcaagac 1860
gatagttacc ggataaggcg cagcggtcgg gctgaacggg gggttcgtgc acacagccca 1920
gcttggagcg aacgacctac accgaactga gatacctaca gcgtgagcta tgagaaagcg 1980
ccacgcttcc cgaagggaga aaggcggaca ggtatccggt aagcggcagg gtcggaacag 2040
gagagcgcac gagggagctt ccagggggaa acgcctggta tctttatagt cctgtcgggt 2100
ttcgccacct ctgacttgag cgtcgatttt tgtgatgctc gtcagggggg cggagcctat 2160
ggaaaaacgc cagcaacgcg gcctttttac ggttcctggc cttttgctgg ccttttgctc 2220
acatgttctt tcctgcgtta tcccctgatt ctgtggataa ccgtattacc gcctttgagt 2280
gagctgatac cgctcgccgc agccgaacga ccgagcgcag cgagtcagtg agcgaggaag 2340
cggaagagcg cctgatgcgg tattttctcc ttacgcatct gtgcggtatt tcacaccgca 2400
tatggtgcac tctcagtaca atctgctctg atgccgcata gttaagccag tatacactcc 2460
gctatcgcta cgtgactggg tcatggctgc gccccgacac ccgccaacac ccgctgacgc 2520
gccctgacgg gcttgtctgc tcccggcatc cgcttacaga caagctgtga ccgtctccgg 2580
gagagctcga tatcccgggc ggccgccttc attctataag tttcttgaca tcttggccgg 2640
catatggtat aatagggaaa tttccatggc ggccgctcta gaagaagctt gggatccgtc 2700
gacctcgaat tcggaggaaa caaagatggc ctttaaagtt gttcagattt gtggtggtct 2760
gggcaatcag atgtttcagt atgcatttgc aaaaagcctg cagaaacata gcaatacacc 2820
ggttctgctg gatattacca gctttgattg gagcaatcgt aaaatgcagc tggaactgtt 2880
tccgattgat ctgccgtatg caagcgaaaa agaaattgca attgccaaaa tgcagcatct 2940
gccgaaactg gttcgtaatg ttctgaaatg catgggtttt gatcgtgtga gccaagaaat 3000
cgtgtttgaa tatgaaccga aactgctgaa aaccagccgt ctgacctatt tttatggcta 3060
ttttcaggat ccgcgttatt ttgatgcaat tagtccgctg atcaaacaga cctttaccct 3120
gcctccgcct ccggaaaatg gtaataacaa aaaaaaagaa gaagagtatc atcgtaaact 3180
ggcactgatt ctggcagcaa aaaatagcgt gtttgtgcat attcgtcgcg gtgattatgt 3240
tggtattggt tgtcagctgg gcatcgatta tcagaaaaaa gcactggaat acatggcaaa 3300
acgtgttccg aatatggaac tgtttgtgtt ttgcgaggac ctggaattta cccagaatct 3360
ggatctgggc tatccgttta tggatatgac cacccgtgat aaagaggaag aggcatattg 3420
ggatatgctg ctgatgcaga gctgtaaaca tggtattatt gccaacagca cctatagttg 3480
gtgggcagca tatctgatta ataacccgga aaaaatcatt attggtccga aacattggct 3540
gtttggccat gaaaacatcc tgtgtaaaga atgggtgaaa atcgaaagcc actttgaagt 3600
gaaaagccag aaatataatg cctaataaga gctcccaa 3638
<210> 7
<211> 2660
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 7
tattttagat tcctgacttc aactcaagac gcacagatat tataacatct gcagaatagg 60
catttgcaag aattactcgt gagtaaggaa agagtgagga actatcgcat acctgcattt 120
aaagatgccg atttgggcgc gaatccttta ttttggcttc accctcatac tattatcagg 180
gccagaaaaa ggaagtgttt ccctccttct tgaattgatg ttaccctcat aaagcacgtg 240
gcctcttatc gagaaagaaa ttaccgtcgc tcgtgatttg tttgcaaaaa gaacaaaact 300
gaaaaaaccc agacacgctc gacttcctct cttcctattg attgcagctt ccaatttcgt 360
cacacaacaa ggtcctagcg acggctcaca ggttttgtaa caagcaatcg aaggttctgg 420
aatggcggga aagggtttag taccacatgc tatgatgccc actgtgatca ccagagcaaa 480
gttcgttcga tcgtactgtt actctctctc tttcaaacag aattgtccga atcgtgtgac 540
aacaacagcc tgttctcaca cactcttttc ttctaaccaa gggggtggtt tagtttagta 600
gaacctcgtg aaacttacat ttacatatat ataaacttgc ataaattggt caatgcaaga 660
aatacatatt tggtcttttc taattcgtag ttttttcaag ttcttagatg ctttcttttt 720
ctcttttttt acagatcatc aaggaagtaa ttatctactt tttacaacaa atataaaaaa 780
aatggcagat cattcgagca gctcatcttc gctgcagaag aagccaatta atactatcga 840
gcataaagac actttgggca ttgatctgga tcacaaggaa gccttgaaca gtgataatga 900
taatacttct ggattgaaaa tcaatggtgt ccccatcgag gacgctagag aggaagtgct 960
cttaccaggt tacttgtcga agcaatatta caaattgtac agtttatgtt ttgtaacata 1020
tctgtgtgct actatgcaag gttatgatgg ggctttaatg ggttctatct ataccgaaaa 1080
tgcatatttg gaatactacc atttggatat taactcatcc agtggtactg gtctagtgtt 1140
ctctattttc aacgttggtc aaatttgcgg tgcattcttt gttcctctta tggattggaa 1200
aggtagaaaa cctgctattt taattgggtg tctgggtgtt gttattggtg gtattattac 1260
gtctgtaaca acaacaaaga gtgcattaat tggtggtaga tggttcatgg cctttttcgc 1320
tacaatcgct aattcagcag ctccagcata ctgtgcagaa gtggctccag ctcacttaag 1380
aggtaaggtt gcaggtcttt ataacaccct ttggtctgtc ggttccattg ttgctgcctt 1440
taccactctc ggtaccaaca aaaacttccc taactcctcc aaggctttta agattccatt 1500
atacttacaa atgatgttcc caggtcttgt gtgtatattt ggttggttaa tcccagaatc 1560
tccaagatgg ttggttggtg ttggccgtga ggaagaagct cgtgaattca ttatcaaata 1620
ccacttaaat ggcgatagaa ctcatccatt attggatatg gagatggcag aaataataga 1680
atctttccat ggtacagatt tatcaaaccc tctagaaatg ttagatgtaa ggatcttatt 1740
cagaacgaga tcggataggt acagagcaat gttggttata cttatggctt ggttcggtca 1800
attttccggt aacaatgtgt gttcgtacta tttgcctacc atgttgagaa atgttggtat 1860
gaagagtgtc tcattgaatg tgttaatgaa tggtgtttat tccatcgtct cttggatttc 1920
ttcaatttgc ggtgcattct ttattgataa gattggtaga agggaaggtt tccttggttc 1980
tatctcaggt gctgcattag cattgacagg tctatctatc tgtactgctc gttatgagaa 2040
gactaagaag aagagtgctt ccaatggtgc attggtgttc atttatctct ttggtgttat 2100
cttttctttt gctttcactc caatgcaatc catgtactca acagaagtgt ctacaaactt 2160
gacgagatct aaggcccaac tcctcaacgg tgtggtttct ggtgttgccc aatttgttaa 2220
tcaatttgct actccaaagg caatgaagaa tatcaaatat tggttctatg tgttctacgt 2280
tttcttcgat attttcgaat ttattgttat ctacttcttc ttcgttgaaa ctaagggtag 2340
aagcttagaa gaattagaag ctgtctttga agctccaaac ccaagaaagg catccgttga 2400
tcaagcattc ttggctcaag ccagggcaac tttggtccaa caaaatgacg ttagagttgc 2460
aaatgctcaa aatttgaaag agcaagagct tctaaagagc gatgctgatc atgtcgaaaa 2520
gctttcagag gcagaatctg tttaaagagt cttttgtaac gaccccgtct ccaccaactt 2580
ggtatgcttg aaatctcaag gccattacac attcagttat gtgaacgaaa ggtctttatt 2640
taacgtagca taaactaaat 2660
<210> 8
<211> 2554
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 8
aggaataagg atacttcaag actagattcc cccctgcatt cccatcagaa ccgtaaacct 60
tggcgctttc cttgggaagt attcaagaag tgccttgtcc ggtttctgtg gctcacaaac 120
cagcgcgccc gatatggctt tcttttcact tatgaatgta ccagtacggg acaattagaa 180
cgctcctgta acaatctctt tgcaaatgtg gggttacatt ctaaccatgt cacactgctg 240
acgaaattca aagtaaaaaa aaatgggacc acgtcttgag aacgatagat tttctttatt 300
ttacattgaa cagtcgttgt ctcagcgcgc tttatgtttt cattcatact tcatattata 360
aaataacaaa agaagaattt catattcacg cccaagaaat caggctgctt tccaaatgca 420
attgacactt cattagccat cacacaaaac tctttcttgc tggagcttct tttaaaaaag 480
acctcagtac accaaacacg ttacccgacc tcgttatttt acgacaacta tgataaaatt 540
ctgaagaaaa aataaaaaaa ttttcatact tcttgctttt atttaaacca ttgaatgatt 600
tcttttgaac aaaactacct gtttcaccaa aggaaataga aagaaaaaat caattagaag 660
aaaacaaaaa acaaaatggc agatcattcg agcagctcat cttcgctgca gaagaagcca 720
attaatacta tcgagcataa agacactttg ggcattgatc tggatcacaa ggaagccttg 780
aacagtgata atgataatac ttctggattg aaaatcaatg gtgtccccat cgaggacgct 840
agagaggaag tgctcttacc aggttacttg tcgaagcaat attacaaatt gtacagttta 900
tgttttgtaa catatctgtg tgctactatg caaggttatg atggggcttt aatgggttct 960
atctataccg aaaatgcata tttggaatac taccatttgg atattaactc atccagtggt 1020
actggtctag tgttctctat tttcaacgtt ggtcaaattt gcggtgcatt ctttgttcct 1080
cttatggatt ggaaaggtag aaaacctgct attttaattg ggtgtctggg tgttgttatt 1140
ggtggtatta ttacgtctgt aacaacaaca aagagtgcat taattggtgg tagatggttc 1200
atggcctttt tcgctacaat cgctaattca gcagctccag catactgtgc agaagtggct 1260
ccagctcact taagaggtaa ggttgcaggt ctttataaca ccctttggtc tgtcggttcc 1320
attgttgctg cctttaccac tctcggtacc aacaaaaact tccctaactc ctccaaggct 1380
tttaagattc cattatactt acaaatgatg ttcccaggtc ttgtgtgtat atttggttgg 1440
ttaatcccag aatctccaag atggttggtt ggtgttggcc gtgaggaaga agctcgtgaa 1500
ttcattatca aataccactt aaatggcgat agaactcatc cattattgga tatggagatg 1560
gcagaaataa tagaatcttt ccatggtaca gatttatcaa accctctaga aatgttagat 1620
gtaaggatct tattcagaac gagatcggat aggtacagag caatgttggt tatacttatg 1680
gcttggttcg gtcaattttc cggtaacaat gtgtgttcgt actatttgcc taccatgttg 1740
agaaatgttg gtatgaagag tgtctcattg aatgtgttaa tgaatggtgt ttattccatc 1800
gtctcttgga tttcttcaat ttgcggtgca ttctttattg ataagattgg tagaagggaa 1860
ggtttccttg gttctatctc aggtgctgca ttagcattga caggtctatc tatctgtact 1920
gctcgttatg agaagactaa gaagaagagt gcttccaatg gtgcattggt gttcatttat 1980
ctctttggtg ttatcttttc ttttgctttc actccaatgc aatccatgta ctcaacagaa 2040
gtgtctacaa acttgacgag atctaaggcc caactcctca acggtgtggt ttctggtgtt 2100
gcccaatttg ttaatcaatt tgctactcca aaggcaatga agaatatcaa atattggttc 2160
tatgtgttct acgttttctt cgatattttc gaatttattg ttatctactt cttcttcgtt 2220
gaaactaagg gtagaagctt agaagaatta gaagctgtct ttgaagctcc aaacccaaga 2280
aaggcatccg ttgatcaagc attcttggct caagccaggg caactttggt ccaacaaaat 2340
gacgttagag ttgcaaatgc tcaaaatttg aaagagcaag agcttctaaa gagcgatgct 2400
gatcatgtcg aaaagctttc agaggcagaa tctgtttaaa gagtcttttg taacgacccc 2460
gtctccacca acttggtatg cttgaaatct caaggccatt acacattcag ttatgtgaac 2520
gaaaggtctt tatttaacgt agcataaact aaat 2554
<210> 9
<211> 4141
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 9
tattttagat tcctgacttc aactcaagac gcacagatat tataacatct gcagaatagg 60
catttgcaag aattactcgt gagtaaggaa agagtgagga actatcgcat acctgcattt 120
aaagatgccg atttgggcgc gaatccttta ttttggcttc accctcatac tattatcagg 180
gccagaaaaa ggaagtgttt ccctccttct tgaattgatg ttaccctcat aaagcacgtg 240
gcctcttatc gagaaagaaa ttaccgtcgc tcgtgatttg tttgcaaaaa gaacaaaact 300
gaaaaaaccc agacacgctc gacttcctct cttcctattg attgcagctt ccaatttcgt 360
cacacaacaa ggtcctagcg acggctcaca ggttttgtaa caagcaatcg aaggttctgg 420
aatggcggga aagggtttag taccacatgc tatgatgccc actgtgatca ccagagcaaa 480
gttcgttcga tcgtactgtt actctctctc tttcaaacag aattgtccga atcgtgtgac 540
aacaacagcc tgttctcaca cactcttttc ttctaaccaa gggggtggtt tagtttagta 600
gaacctcgtg aaacttacat ttacatatat ataaacttgc ataaattggt caatgcaaga 660
aatacatatt tggtcttttc taattcgtag ttttttcaag ttcttagatg ctttcttttt 720
ctcttttttt acagatcatc aaggaagtaa ttatctactt tttacaacaa atataaaaaa 780
aatgtcttgc cttattcctg agaatttaag gaaccccaaa aaggttcacg aaaatagatt 840
gcctactagg gcttactact atgatcagga tattttcgaa tctctcaatg ggccttgggc 900
ttttgcgttg tttgatgcac ctcttgacgc tccggatgct aagaatttag actgggaaac 960
ggcaaagaaa tggagcacca tttctgtgcc atcccattgg gaacttcagg aagactggaa 1020
gtacggtaaa ccaatttaca cgaacgtaca gtaccctatc ccaatcgaca tcccaaatcc 1080
tcccactgta aatcctactg gtgtttatgc tagaactttt gaattagatt cgaaatcgat 1140
tgagtcgttc gagcacagat tgagatttga gggtgtggac aattgttacg agctttatgt 1200
taatggtcaa tatgtgggtt tcaataaggg gtcccgtaac ggggctgaat ttgatatcca 1260
aaagtacgtt tctgagggcg aaaacttagt ggtcgtcaag gttttcaagt ggtccgattc 1320
cacttatatc gaggaccaag atcaatggtg gctctctggt atttacagag acgtttcttt 1380
actaaaattg cctaagaagg cccatattga agacgttagg gtcactacaa cttttgtgga 1440
ctctcagtat caggatgcag agctttctgt gaaagttgat gtccagggtt cttcttatga 1500
tcacatcaat ttcacacttt acgaacctga agatggatct aaagtttacg atgcaagctc 1560
tttgttgaac gaggagaatg ggaacacgac tttttcaact aaagaattta tttccttctc 1620
caccaaaaag aacgaagaaa cagctttcaa gatcaacgtc aaggccccag aacattggac 1680
cgcagaaaat cctactttgt acaagtacca gttggattta attggatctg atggcagtgt 1740
gattcaatct attaagcacc atgttggttt cagacaagtg gagttgaagg acggtaacat 1800
tactgttaat ggcaaagaca ttctctttag aggtgtcaac agacatgatc accatccaag 1860
gttcggtaga gctgtgccat tagattttgt tgttagggac ttgattctaa tgaagaagtt 1920
taacatcaat gctgttcgta actcgcatta tccaaaccat cctaaggtgt atgacctctt 1980
cgataagctg ggcttctggg tcattgacga ggcagatctt gaaactcatg gtgttcaaga 2040
gccatttaat cgtcatacga acttggaggc tgaatatcca gatactaaaa ataaactcta 2100
cgatgttaat gcccattact tatcagataa tccagagtac gaggtcgcgt acttagacag 2160
agcttcccaa cttgtcctaa gagatgtcaa tcatccttcg attattatct ggtccttggg 2220
taacgaagct tgttatggca gaaaccacaa agccatgtac aagttaatta aacaattgga 2280
tcctaccaga cttgtgcatt atgagggtga cttgaacgct ttgagtgcag atatctttag 2340
tttcatgtac ccaacatttg aaattatgga aaggtggagg aagaaccaca ctgatgaaaa 2400
tggtaagttt gaaaagcctt tgatcttgtg tgagtacggc catgcaatgg gtaacggtcc 2460
tggctctttg aaagaatatc aagagttgtt ctacaaggag aagttttacc aaggtggctt 2520
tatctgggaa tgggcaaatc acggtattga attcgaagat gttagtactg cagatggtaa 2580
gttgcataaa gcttatgctt atggtggtga ctttaaggaa gaggttcatg acggagtgtt 2640
catcatggat ggtttgtgta acagtgagca taatcctact ccgggccttg tagagtataa 2700
gaaggttatt gaacccgttc atattaaaat tgcgcacgga tctgtaacaa tcacaaataa 2760
gcacgacttc attacgacag accacttatt gtttatcgac aaggacacgg gaaagacaat 2820
cgacgttcca tctttaaagc cagaagaatc tgttactatt ccttctgata caacttatgt 2880
tgttgccgtg ttgaaagatg atgctggtgt tctaaaggca ggtcatgaaa ttgcctgggg 2940
ccaagctgaa cttccattga aggtacccga ttttgttaca gagacagcag aaaaagctgc 3000
gaagatcaac gacggtaaac gttatgtctc agttgaatcc agtggattgc attttatctt 3060
ggacaaattg ttgggtaaaa ttgaaagcct aaaggtcaag ggtaaggaaa tttccagcaa 3120
gtttgagggt tcttcaatca ctttctggag acctccaacg aataatgatg aacctaggga 3180
ctttaagaac tggaagaagt acaatattga tttaatgaag caaaacatcc atggagtgag 3240
tgtcgaaaaa ggttctaatg gttctctagc tgtagtcacg gttaactctc gtatatcccc 3300
agttgtattt tactatgggt ttgagactgt tcagaagtac acgatctttg ctaacaaaat 3360
aaacttgaac acttctatga agcttactgg cgaatatcag cctcctgatt tcccaagagt 3420
tgggtacgaa ttctggctag gagatagtta tgaatcattt gaatggttag gtcgcgggcc 3480
cggcgaatca tatccggata agaaggaatc tcaaagattc ggtctttacg attccaaaga 3540
tgtagaggaa ttcgtatatg actatcctca agaaaatgga aatcatacag atacccactt 3600
tttgaacatc aaatttgaag gtgcaggaaa actatcgatc ttccaaaagg agaagccatt 3660
taacttcaag atttcagacg aatacggggt tgatgaagct gcccacgctt gtgacgttaa 3720
aagatacggc agacactatc taaggttgga ccatgcaatc catggtgttg gtagcgaagc 3780
atgcggacct gctgttctgg accagtacag attgaaagct caagatttca actttgagtt 3840
tgatctcgct tttgaataag ccggccattg aattgaattg aaatcgatag atcaattttt 3900
ttcttttctc tttccccatc ctttacgcta aaataatagt ttattttatt ttttgaatat 3960
tttttattta tatacgtata tatagactat tatttatctt ttaatgatta ttaagatttt 4020
tattaaaaaa aaattcgcac ctcttttaat gcctttatgc agtttttttt tcccattcga 4080
tatttctatg ttcgggttca gcgtatttta agtttaataa ctcgaaaatt ctgcgtttcg 4140
a 4141
<210> 10
<211> 1187
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 10
ttaatctcag cagatcgtaa caacaaggct actctactgc ttacaatacc ccgttgtaca 60
tctaagtcgt atacaaatga tttatcccca cgcaaaatga cattgcaatt cgccagcaag 120
cacccaaggc ctttccgcca agtgcaccgt tgctagcctg ctatggttca gcgacgccac 180
aaggacgcct tattcgtatc catctatatt gtgtggagca aagaaatcac cgcgttctag 240
catggattct gacttagagg cgttcagcca taatccagcg gatggtagct tcgcggcaat 300
gcctgatcag acagccgcaa aaaccaatta tccgaatgaa ctgttcctct cgtactaagt 360
tcaattacta ttgcggtaac attcatcagt agggtaaaac taacctgtct cacgacggtc 420
taaacccagc tcacgttccc tattagtggg tgaacaatcc aacgcttacc gaattctgct 480
tcggtatgat aggaagagcc gacatcgaag aatcaaaaag caatgtcgct atgaacgctt 540
gactgccaca agccagttat ccctgtggta acttttctgg cacctctagc ctcaaattcc 600
gagggactaa aggatcgata ggccacactt tcatggtttg tattcacact gaaaatcaaa 660
atcaaggggg cttttaccct tttgttctac tggagatttc tgttctccat gagcccccct 720
taggacatct gcgttatcgt ttaacagatg tgccgcccca gccaaactcc ccacctgaca 780
atgtcttcaa cccggatcag ccccgaatgg gaccttgaat gctagaacgt ggaaaatgaa 840
ttccagctcc gcttcattga ataagtaaag aaactataaa ggtagtggta tttcactggc 900
gccgaagctc ccacttattc tacaccctct atgtctcttc acaatgtcaa actagagtca 960
agctcaacag ggtcttcttt ccccgctgat tctgccaagc ccgttccctt ggctgtggtt 1020
tcgctagata gtagataggg acagtgggaa tctcgttaat ccattcatgc gcgtcactaa 1080
ttagatgacg aggcatttgg ctaccttaag agagtcatag ttactcccgc cgtttacccg 1140
cgcttggttg aatttcttca ctttgacatt cagagcactg ggcagaa 1187
<210> 11
<211> 2010
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 11
agtagtccgc ctagcagagc aagccccacc aagcagtcca caagcacgcc cgctgcgtct 60
gaccaaggcc ctcactaccc gacccttaga gccaatcctt atcccgaagt tacggatcta 120
ttttgccgac ttcccttatc tacattattc tatcaactag aggctgttca ccttggagac 180
ctgctgcggt tatcagtacg acctggcatg aaaactattc cttcctgtgg attttcacgg 240
gccgtcacaa gcgcaccgga gccagcaaag gtgctggcct cttccagcca taagacccca 300
tctccggata aaccaattcc ggggtgataa gctgttaaga agaaaagata actcctccca 360
gggctcgcgc cgacgtctcc acattcagtt acgttaccgt gaagaatcca tatccaggtt 420
ccggaatctt aaccggattc cctttcgatg gtggcctgca taaaatcagg cctttgaaac 480
ggagcttccc catctcttag gatcgactaa cccacgtcca actgctgttg acgtggaacc 540
tttccccact tcagtcttca aagttctcat ttgaatattt gctactacca ccaagatctg 600
cactagaggc cgttcgaccc gaccttacgg tctaggcttc gtcactgacc tccacgcctg 660
cctactcgtc agggcatcat atcaaccctg acggtagagt ataggtaaca cgcttgagcg 720
ccatccattt tcagggctag ttcattcggc cggtgagttg ttacacactc cttagcggat 780
tccgacttcc atggccaccg tccggctgtc tagatgaact aacacctttt gtggtgtctg 840
atgagcgtgt attccggcac cttaactcta cgttcggttc atcccgcatc gccagttctg 900
cttaccaaaa atggcccact aaaagctctt cattcaaatg tccacgttca attaagtaac 960
aaggacttct tacatattta aagtttgaga ataggtcaag gtcatttcga ccccggaacc 1020
tctaatcatt cgctttacct cataaaactg atacgagctt ctgctatcct gagggaaact 1080
tcggcaggaa ccagctacta gatggttcga ttagtctttc gcccctatac ccaaattcga 1140
cgatcgattt gcacgtcaga accgctacga gcctccacca gagtttcctc tggcttcacc 1200
ctattcaggc atagttcacc atctttcggg tcccaacagc tatgctctta ctcaaatcca 1260
tccgaagaca tcaggatcgg tcgattgtgc acctcttgcg aggccccaac ctacgttcac 1320
tttcattacg cgtatgggtt ttacacccaa acactcgcat agacgttaga ctccttggtc 1380
cgtgtttcaa gacgggcggc atataaccat tatgccagca tccttgactt acgtcgcagt 1440
cctcagtccc agctggcagt attcccacag gctataatac ttaccgaggc aagctacatt 1500
cctatggatt tatcctgcca ccaaaactga tgctggccca gtgaaatgcg agattcccct 1560
acccacaagg agcagagggc acaaaacacc atgtctgatc aaatgccctt ccctttcaac 1620
aatttcacgt actttttcac tctcttttca aagttctttt catctttcca tcactgtact 1680
tgttcgctat cggtctctcg ccaatattta gctttagatg gaatttacca cccacttaga 1740
gctgcattcc caaacaactc gactcttcga aggcacttta caaagaaccg cactcctcgc 1800
cacacgggat tctcaccctc tatgacgtcc tgttccaagg aacatagaca aggaacggcc 1860
ccaaagttgc cctctccaaa ttacaactcg ggcaccgaag gtaccagatt tcaaatttga 1920
gcttttgccg cttcactcgc cgttactaag gcaatcccgg ttggtttctt ttcctccgct 1980
tattgatatg cttaagttca gcgggtactc 2010
<210> 12
<211> 1558
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 12
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcttactgt cgggaattcg cgttggccaa ttcattaatg gtataaggtt 180
cttgacatct tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa 240
aggagatcaa caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt 300
ttctatgtac tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta 360
cttttttatc atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca 420
tatcagcaaa agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt 480
ccaaccgctg tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat 540
tattaccggc atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt 600
acaatacaac attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa 660
cgccggtgcg ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga 720
atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg 780
catcatgttc accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat 840
cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa 900
tgcggtaggt gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca 960
gccaaaactg tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt 1020
tgaccaacag tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg 1080
ggtatttggc tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc 1140
gccactgatc attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat 1200
gtctgtacgt attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa 1260
aacgctgcat atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag 1320
ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca 1380
actggcgatg atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca 1440
gggcgcttat ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac 1500
gcttagcggc cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1558
<210> 13
<211> 1551
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 13
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacacttac tgtcgggaat tcgcgttggc caattaatta atggtataag gttcttgaca 180
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 240
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 300
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 360
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 420
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 480
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 540
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 600
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 660
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 720
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 780
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 840
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 900
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 960
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 1020
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 1080
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1140
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1200
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1260
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1320
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1380
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1440
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1500
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1551
<210> 14
<211> 1398
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 14
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtacatgtac tatttaaaaa acacaaactt ttggatgttc 180
ggtttattct ttttctttta cttttttatc atgggagcct acttcccgtt tttcccgatt 240
tggctacatg acatcaacca tatcagcaaa agtgatacgg gtattatttt tgccgctatt 300
tctctgttct cgctattatt ccaaccgctg tttggtctgc tttctgacaa actcgggctg 360
cgcaaatacc tgctgtggat tattaccggc atgttagtga tgtttgcgcc gttctttatt 420
tttatcttcg ggccactgtt acaatacaac attttagtag gatcgattgt tggtggtatt 480
tatctaggct tttgttttaa cgccggtgcg ccagcagtag aggcatttat tgagaaagtc 540
agccgtcgca gtaatttcga atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg 600
ctgtgtgcct cgattgtcgg catcatgttc accatcaata atcagtttgt tttctggctg 660
ggctctggct gtgcactcat cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc 720
tcttctgcca cggttgccaa tgcggtaggt gccaaccatt cggcatttag ccttaagctg 780
gcactggaac tgttcagaca gccaaaactg tggtttttgt cactgtatgt tattggcgtt 840
tcctgcacct acgatgtttt tgaccaacag tttgctaatt tctttacttc gttctttgct 900
accggtgaac agggtacgcg ggtatttggc tacgtaacga caatgggcga attacttaac 960
gcctcgatta tgttctttgc gccactgatc attaatcgca tcggtgggaa aaacgccctg 1020
ctgctggctg gcactattat gtctgtacgt attattggct catcgttcgc cacctcagcg 1080
ctggaagtgg ttattctgaa aacgctgcat atgtttgaag taccgttcct gctggtgggc 1140
tgctttaaat atattaccag ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc 1200
tgtttctgct tctttaagca actggcgatg atttttatgt ctgtactggc gggcaatatg 1260
tatgaaagca tcggtttcca gggcgcttat ctggtgctgg gtctggtggc gctgggcttc 1320
accttaattt ccgtgttcac gcttagcggc cccggcccgc tttccctgct gcgtcgtcag 1380
gtgaatgaag tcgcttaa 1398
<210> 15
<211> 1558
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 15
cccgtcttac tgtcgggaat tcgcgttggc caattaatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcttactgt cgggaattcg cgttggccga ttcattaatg gtataaggtt 180
cttgacatct tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa 240
aggagatcaa caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt 300
ttctatgtac tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta 360
cttttttatc atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca 420
tatcagcaaa agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt 480
ccaaccgctg tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat 540
tattaccggc atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt 600
acaatacaac attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa 660
cgccggtgcg ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga 720
atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg 780
catcatgttc accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat 840
cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa 900
tgcggtaggt gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca 960
gccaaaactg tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt 1020
tgaccaacag tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg 1080
ggtatttggc tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc 1140
gccactgatc attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat 1200
gtctgtacgt attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa 1260
aacgctgcat atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag 1320
ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca 1380
actggcgatg atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca 1440
gggcgcttat ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac 1500
gcttagcggc cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1558
<210> 16
<211> 1558
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 16
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcttactgt cgggaattcg cgttggccga ttcttataaa tcattatctt 180
cttgacattt tagaaacaat atggtataat ataacgataa gggcccaagt tcacttaaaa 240
aggagatcaa caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt 300
ttctatgtac tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta 360
cttttttatc atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca 420
tatcagcaaa agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt 480
ccaaccgctg tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat 540
tattaccggc atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt 600
acaatacaac attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa 660
cgccggtgcg ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga 720
atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg 780
catcatgttc accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat 840
cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa 900
tgcggtaggt gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca 960
gccaaaactg tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt 1020
tgaccaacag tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg 1080
ggtatttggc tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc 1140
gccactgatc attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat 1200
gtctgtacgt attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa 1260
aacgctgcat atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag 1320
ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca 1380
actggcgatg atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca 1440
gggcgcttat ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac 1500
gcttagcggc cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1558
<210> 17
<211> 1471
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 17
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcttat taacaatatc cttcttgaca ttttgcaggg attgtgatat 120
aatcaataag tatgggccca agttcactta aaaaggagat caacaatgaa agcaattttc 180
gtactgaaac atcttaatca tgcgtaggat tttttctatg tactatttaa aaaacacaaa 240
cttttggatg ttcggtttat tctttttctt ttactttttt atcatgggag cctacttccc 300
gtttttcccg atttggctac atgacatcaa ccatatcagc aaaagtgata cgggtattat 360
ttttgccgct atttctctgt tctcgctatt attccaaccg ctgtttggtc tgctttctga 420
caaactcggg ctgcgcaaat acctgctgtg gattattacc ggcatgttag tgatgtttgc 480
gccgttcttt atttttatct tcgggccact gttacaatac aacattttag taggatcgat 540
tgttggtggt atttatctag gcttttgttt taacgccggt gcgccagcag tagaggcatt 600
tattgagaaa gtcagccgtc gcagtaattt cgaatttggt cgcgcgcgga tgtttggctg 660
tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg ttcaccatca ataatcagtt 720
tgttttctgg ctgggctctg gctgtgcact catcctcgcc gttttactct ttttcgccaa 780
aacggatgcg ccctcttctg ccacggttgc caatgcggta ggtgccaacc attcggcatt 840
tagccttaag ctggcactgg aactgttcag acagccaaaa ctgtggtttt tgtcactgta 900
tgttattggc gtttcctgca cctacgatgt ttttgaccaa cagtttgcta atttctttac 960
ttcgttcttt gctaccggtg aacagggtac gcgggtattt ggctacgtaa cgacaatggg 1020
cgaattactt aacgcctcga ttatgttctt tgcgccactg atcattaatc gcatcggtgg 1080
gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta cgtattattg gctcatcgtt 1140
cgccacctca gcgctggaag tggttattct gaaaacgctg catatgtttg aagtaccgtt 1200
cctgctggtg ggctgcttta aatatattac cagccagttt gaagtgcgtt tttcagcgac 1260
gatttatctg gtctgtttct gcttctttaa gcaactggcg atgattttta tgtctgtact 1320
ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct tatctggtgc tgggtctggt 1380
ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc ggccccggcc cgctttccct 1440
gctgcgtcgt caggtgaatg aagtcgctta a 1471
<210> 18
<211> 1632
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 18
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat tcgcgttggc caattaatta 120
atggtataag gttcttgaca tcttacaatc aatatggtat aataatttag ttagggccca 180
agttcactta aaaaggagat caacacttac tgtcgggaat tcgcgttggc caattaatta 240
atggtataag gttcttgaca tcttacaatc aatatggtat aaataattta gttagggccc 300
aagttcactt aaaaaggaga tcaacaatga aagcaatttt cgtactgaaa catcttaatc 360
atgcgtagga ttttttctat gtactattta aaaaacacaa acttttggat gttcggttta 420
ttctttttct tttacttttt tatcatggga gcctacttcc cgtttttccc gatttggcta 480
catgacatca accatatcag caaaagtgat acgggtatta tttttgccgc tatttctctg 540
ttctcgctat tattccaacc gctgtttggt ctgctttctg acaaactcgg gctgcgcaaa 600
tacctgctgt ggattattac cggcatgtta gtgatgtttg cgccgttctt tatttttatc 660
ttcgggccac tgttacaata caacatttta gtaggatcga ttgttggtgg tatttatcta 720
ggcttttgtt ttaacgccgg tgcgccagca gtagaggcat ttattgagaa agtcagccgt 780
cgcagtaatt tcgaatttgg tcgcgcgcgg atgtttggct gtgttggctg ggcgctgtgt 840
gcctcgattg tcggcatcat gttcaccatc aataatcagt ttgttttctg gctgggctct 900
ggctgtgcac tcatcctcgc cgttttactc tttttcgcca aaacggatgc gccctcttct 960
gccacggttg ccaatgcggt aggtgccaac cattcggcat ttagccttaa gctggcactg 1020
gaactgttca gacagccaaa actgtggttt ttgtcactgt atgttattgg cgtttcctgc 1080
acctacgatg tttttgacca acagtttgct aatttcttta cttcgttctt tgctaccggt 1140
gaacagggta cgcgggtatt tggctacgta acgacaatgg gcgaattact taacgcctcg 1200
attatgttct ttgcgccact gatcattaat cgcatcggtg ggaaaaacgc cctgctgctg 1260
gctggcacta ttatgtctgt acgtattatt ggctcatcgt tcgccacctc agcgctggaa 1320
gtggttattc tgaaaacgct gcatatgttt gaagtaccgt tcctgctggt gggctgcttt 1380
aaatatatta ccagccagtt tgaagtgcgt ttttcagcga cgatttatct ggtctgtttc 1440
tgcttcttta agcaactggc gatgattttt atgtctgtac tggcgggcaa tatgtatgaa 1500
agcatcggtt tccagggcgc ttatctggtg ctgggtctgg tggcgctggg cttcacctta 1560
atttccgtgt tcacgcttag cggccccggc ccgctttccc tgctgcgtcg tcaggtgaat 1620
gaagtcgctt aa 1632
<210> 19
<211> 1558
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 19
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcttactgt cgggaattcg cgttggccga ttcattaatg gtataaggtt 180
cttgacatct tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa 240
aggagatcaa caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt 300
ttctatgtac tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta 360
cttttttatc atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca 420
tatcagcaaa agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt 480
ccaaccgctg tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat 540
tattaccggc atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt 600
acaatacaac attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa 660
cgccggtgcg ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga 720
atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg 780
catcatgttc accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat 840
cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa 900
tgcggtaggt gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca 960
gccaaaactg tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt 1020
tgaccaacag tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg 1080
ggtatttggc tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc 1140
gccactgatc attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat 1200
gtctgtacgt attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa 1260
aacgctgcat atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag 1320
ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca 1380
actggcgatg atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca 1440
gggcgcttat ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac 1500
gcttagcggc cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1558
<210> 20
<211> 1571
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 20
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaggctta cccgtcttac tgtcgggaat tcgcgttggc cgattcatta 180
atggtataag gttcttgaca tcttacaatc aatatggtat aataatttag ttagggccca 240
agttcactta aaaaggagat caacaatgaa agcaattttc gtactgaaac atcttaatca 300
tgcgtaggat tttttctatg tactatttaa aaaacacaaa cttttggatg ttcggtttat 360
tctttttctt ttactttttt atcatgggag cctacttccc gtttttcccg atttggctac 420
atgacatcaa ccatatcagc aaaagtgata cgggtattat ttttgccgct atttctctgt 480
tctcgctatt attccaaccg ctgtttggtc tgctttctga caaactcggg ctgcgcaaat 540
acctgctgtg gattattacc ggcatgttag tgatgtttgc gccgttcttt atttttatct 600
tcgggccact gttacaatac aacattttag taggatcgat tgttggtggt atttatctag 660
gcttttgttt taacgccggt gcgccagcag tagaggcatt tattgagaaa gtcagccgtc 720
gcagtaattt cgaatttggt cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg 780
cctcgattgt cggcatcatg ttcaccatca ataatcagtt tgttttctgg ctgggctctg 840
gctgtgcact catcctcgcc gttttactct ttttcgccaa aacggatgcg ccctcttctg 900
ccacggttgc caatgcggta ggtgccaacc attcggcatt tagccttaag ctggcactgg 960
aactgttcag acagccaaaa ctgtggtttt tgtcactgta tgttattggc gtttcctgca 1020
cctacgatgt ttttgaccaa cagtttgcta atttctttac ttcgttcttt gctaccggtg 1080
aacagggtac gcgggtattt ggctacgtaa cgacaatggg cgaattactt aacgcctcga 1140
ttatgttctt tgcgccactg atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg 1200
ctggcactat tatgtctgta cgtattattg gctcatcgtt cgccacctca gcgctggaag 1260
tggttattct gaaaacgctg catatgtttg aagtaccgtt cctgctggtg ggctgcttta 1320
aatatattac cagccagttt gaagtgcgtt tttcagcgac gatttatctg gtctgtttct 1380
gcttctttaa gcaactggcg atgattttta tgtctgtact ggcgggcaat atgtatgaaa 1440
gcatcggttt ccagggcgct tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa 1500
tttccgtgtt cacgcttagc ggccccggcc cgctttccct gctgcgtcgt caggtgaatg 1560
aagtcgctta a 1571
<210> 21
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 21
cccgtcttac tgtcgggaat tcgcgttggc cgattcattt aaccgataag cttcttgaca 60
tgtttagggt gttatgatat aatcacccaa ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 22
<211> 1951
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 22
ggcacctgag tcgctgtctt tttcgtgaca ttcagttcgc tgcgctcacg gctctggcag 60
tgaatggggg taaatggcac tacaggcgcc ttttatggat tcatgcaagg aaactaccca 120
taatacaaga aaagcccgtc acgggcttct cagggcgttt tatggcgggt ctgctatgtg 180
gtgctatctg actttttgct gttcagcagt tcctgccctc tgattttcca gtctgaccac 240
ttcggattat cccgtgacag gtcattcaga ctggctaatg cacccagtaa ggcagcggta 300
tcatcaacag gcttacccgt cttactgtcg ggaattcgcg ttggccgatt aaaggagatc 360
aacaatgaaa gcactgtcgg gaattcgcgt tggccgattc attaatggta taaggttctt 420
gacatcttac aatcaatatg gtataataat ttagttaggg cccaagttca cttaaaaagg 480
agatcaacaa tgaaagcaag cggtatcatc aacaggctta cccgtcttac tgtcgggaat 540
tcgcgttggc cgattcatta atggtataag gttcttgaca tcttacaatc aatatggtat 600
aataatttag ttagggccca agttcactta aaaaggagat caacaatgaa agcaattttc 660
gtactgaaac atcttaatca tgcgtaggat tttttctatg tactatttaa aaaacacaaa 720
cttttggatg ttcggtttat tctttttctt ttactttttt atcatgggag cctacttccc 780
gtttttcccg atttggctac atgacatcaa ccatatcagc aaaagtgata cgggtattat 840
ttttgccgct atttctctgt tctcgctatt attccaaccg ctgtttggtc tgctttctga 900
caaactcggg ctgcgcaaat acctgctgtg gattattacc ggcatgttag tgatgtttgc 960
gccgttcttt atttttatct tcgggccact gttacaatac aacattttag taggatcgat 1020
tgttggtggt atttatctag gcttttgttt taacgccggt gcgccagcag tagaggcatt 1080
tattgagaaa gtcagccgtc gcagtaattt cgaatttggt cgcgcgcgga tgtttggctg 1140
tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg ttcaccatca ataatcagtt 1200
tgttttctgg ctgggctctg gctgtgcact catcctcgcc gttttactct ttttcgccaa 1260
aacggatgcg ccctcttctg ccacggttgc caatgcggta ggtgccaacc attcggcatt 1320
tagccttaag ctggcactgg aactgttcag acagccaaaa ctgtggtttt tgtcactgta 1380
tgttattggc gtttcctgca cctacgatgt ttttgaccaa cagtttgcta atttctttac 1440
ttcgttcttt gctaccggtg aacagggtac gcgggtattt ggctacgtaa cgacaatggg 1500
cgaattactt aacgcctcga ttatgttctt tgcgccactg atcattaatc gcatcggtgg 1560
gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta cgtattattg gctcatcgtt 1620
cgccacctca gcgctggaag tggttattct gaaaacgctg catatgtttg aagtaccgtt 1680
cctgctggtg ggctgcttta aatatattac cagccagttt gaagtgcgtt tttcagcgac 1740
gatttatctg gtctgtttct gcttctttaa gcaactggcg atgattttta tgtctgtact 1800
ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct tatctggtgc tgggtctggt 1860
ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc ggccccggcc cgctttccct 1920
gctgcgtcgt caggtgaatg aagtcgctta a 1951
<210> 23
<211> 1749
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 23
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 120
tcgcgttggc cgattcgaat tcgcgttggc cgattaaagg agatcaacaa tgaaagctta 180
ctgtcgggaa ttcgcgttgg ccgattcgaa ttcgcgttgg ccgattcatt aatggtataa 240
ggttcttgac atcttacaat caatatggta taataattta gttagggccc aagttcactt 300
aaaaaggaga tcaacaatga aagcttactg tcgggaattc gcgttggccg attcattaat 360
ggtataaggt tcttgacatc ttacaatcaa tatggtataa taatttagtt agggcccaag 420
ttcacttaaa aaggagatca acaatgaaag caattttcgt actgaaacat cttaatcatg 480
cgtaggattt tttctatgta ctatttaaaa aacacaaact tttggatgtt cggtttattc 540
tttttctttt acttttttat catgggagcc tacttcccgt ttttcccgat ttggctacat 600
gacatcaacc atatcagcaa aagtgatacg ggtattattt ttgccgctat ttctctgttc 660
tcgctattat tccaaccgct gtttggtctg ctttctgaca aactcgggct gcgcaaatac 720
ctgctgtgga ttattaccgg catgttagtg atgtttgcgc cgttctttat ttttatcttc 780
gggccactgt tacaatacaa cattttagta ggatcgattg ttggtggtat ttatctaggc 840
ttttgtttta acgccggtgc gccagcagta gaggcattta ttgagaaagt cagccgtcgc 900
agtaatttcg aatttggtcg cgcgcggatg tttggctgtg ttggctgggc gctgtgtgcc 960
tcgattgtcg gcatcatgtt caccatcaat aatcagtttg ttttctggct gggctctggc 1020
tgtgcactca tcctcgccgt tttactcttt ttcgccaaaa cggatgcgcc ctcttctgcc 1080
acggttgcca atgcggtagg tgccaaccat tcggcattta gccttaagct ggcactggaa 1140
ctgttcagac agccaaaact gtggtttttg tcactgtatg ttattggcgt ttcctgcacc 1200
tacgatgttt ttgaccaaca gtttgctaat ttctttactt cgttctttgc taccggtgaa 1260
cagggtacgc gggtatttgg ctacgtaacg acaatgggcg aattacttaa cgcctcgatt 1320
atgttctttg cgccactgat cattaatcgc atcggtggga aaaacgccct gctgctggct 1380
ggcactatta tgtctgtacg tattattggc tcatcgttcg ccacctcagc gctggaagtg 1440
gttattctga aaacgctgca tatgtttgaa gtaccgttcc tgctggtggg ctgctttaaa 1500
tatattacca gccagtttga agtgcgtttt tcagcgacga tttatctggt ctgtttctgc 1560
ttctttaagc aactggcgat gatttttatg tctgtactgg cgggcaatat gtatgaaagc 1620
atcggtttcc agggcgctta tctggtgctg ggtctggtgg cgctgggctt caccttaatt 1680
tccgtgttca cgcttagcgg ccccggcccg ctttccctgc tgcgtcgtca ggtgaatgaa 1740
gtcgcttaa 1749
<210> 24
<211> 1556
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 24
cccgtcttac tgtcgggaat tcgcgttggc cgattcatac taagcattat attcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcactgtcg ggaattcgcg ttggccaatt aattaatggt ataaggttct 180
tgacatctta caatcaatat ggtataataa tttagttagg gcccaagttc acttaaaaag 240
gagatcaaca atgaaagcaa ttttcgtact gaaacatctt aatcatgcgt aggatttttt 300
ctatgtacta tttaaaaaac acaaactttt ggatgttcgg tttattcttt ttcttttact 360
tttttatcat gggagcctac ttcccgtttt tcccgatttg gctacatgac atcaaccata 420
tcagcaaaag tgatacgggt attatttttg ccgctatttc tctgttctcg ctattattcc 480
aaccgctgtt tggtctgctt tctgacaaac tcgggctgcg caaatacctg ctgtggatta 540
ttaccggcat gttagtgatg tttgcgccgt tctttatttt tatcttcggg ccactgttac 600
aatacaacat tttagtagga tcgattgttg gtggtattta tctaggcttt tgttttaacg 660
ccggtgcgcc agcagtagag gcatttattg agaaagtcag ccgtcgcagt aatttcgaat 720
ttggtcgcgc gcggatgttt ggctgtgttg gctgggcgct gtgtgcctcg attgtcggca 780
tcatgttcac catcaataat cagtttgttt tctggctggg ctctggctgt gcactcatcc 840
tcgccgtttt actctttttc gccaaaacgg atgcgccctc ttctgccacg gttgccaatg 900
cggtaggtgc caaccattcg gcatttagcc ttaagctggc actggaactg ttcagacagc 960
caaaactgtg gtttttgtca ctgtatgtta ttggcgtttc ctgcacctac gatgtttttg 1020
accaacagtt tgctaatttc tttacttcgt tctttgctac cggtgaacag ggtacgcggg 1080
tatttggcta cgtaacgaca atgggcgaat tacttaacgc ctcgattatg ttctttgcgc 1140
cactgatcat taatcgcatc ggtgggaaaa acgccctgct gctggctggc actattatgt 1200
ctgtacgtat tattggctca tcgttcgcca cctcagcgct ggaagtggtt attctgaaaa 1260
cgctgcatat gtttgaagta ccgttcctgc tggtgggctg ctttaaatat attaccagcc 1320
agtttgaagt gcgtttttca gcgacgattt atctggtctg tttctgcttc tttaagcaac 1380
tggcgatgat ttttatgtct gtactggcgg gcaatatgta tgaaagcatc ggtttccagg 1440
gcgcttatct ggtgctgggt ctggtggcgc tgggcttcac cttaatttcc gtgttcacgc 1500
ttagcggccc cggcccgctt tccctgctgc gtcgtcaggt gaatgaagtc gcttaa 1556
<210> 25
<211> 1802
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 25
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattaaagg agatcaacaa tgaaagctta 120
ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa ggttcttgac atcttacaat 180
caatatggta taataattta gttagggccc aagttcactt aaaaaggaga tcaacactta 240
ctgtcgggaa ttcgcgttgg ccaattaatt aatggtataa ggttcttgac atcttacaat 300
caatatggta taataattta gttagggccc aagttcactt aaaaaggaga tcaacaatga 360
aagcaggctt acccgtctta ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa 420
ggttcttgac atcttacaat caatatggta taataattta gttagggccc aagttcactt 480
aaaaaggaga tcaacaatga aagcaatttt cgtactgaaa catcttaatc atgcgtagga 540
ttttttctat gtactattta aaaaacacaa acttttggat gttcggttta ttctttttct 600
tttacttttt tatcatggga gcctacttcc cgtttttccc gatttggcta catgacatca 660
accatatcag caaaagtgat acgggtatta tttttgccgc tatttctctg ttctcgctat 720
tattccaacc gctgtttggt ctgctttctg acaaactcgg gctgcgcaaa tacctgctgt 780
ggattattac cggcatgtta gtgatgtttg cgccgttctt tatttttatc ttcgggccac 840
tgttacaata caacatttta gtaggatcga ttgttggtgg tatttatcta ggcttttgtt 900
ttaacgccgg tgcgccagca gtagaggcat ttattgagaa agtcagccgt cgcagtaatt 960
tcgaatttgg tcgcgcgcgg atgtttggct gtgttggctg ggcgctgtgt gcctcgattg 1020
tcggcatcat gttcaccatc aataatcagt ttgttttctg gctgggctct ggctgtgcac 1080
tcatcctcgc cgttttactc tttttcgcca aaacggatgc gccctcttct gccacggttg 1140
ccaatgcggt aggtgccaac cattcggcat ttagccttaa gctggcactg gaactgttca 1200
gacagccaaa actgtggttt ttgtcactgt atgttattgg cgtttcctgc acctacgatg 1260
tttttgacca acagtttgct aatttcttta cttcgttctt tgctaccggt gaacagggta 1320
cgcgggtatt tggctacgta acgacaatgg gcgaattact taacgcctcg attatgttct 1380
ttgcgccact gatcattaat cgcatcggtg ggaaaaacgc cctgctgctg gctggcacta 1440
ttatgtctgt acgtattatt ggctcatcgt tcgccacctc agcgctggaa gtggttattc 1500
tgaaaacgct gcatatgttt gaagtaccgt tcctgctggt gggctgcttt aaatatatta 1560
ccagccagtt tgaagtgcgt ttttcagcga cgatttatct ggtctgtttc tgcttcttta 1620
agcaactggc gatgattttt atgtctgtac tggcgggcaa tatgtatgaa agcatcggtt 1680
tccagggcgc ttatctggtg ctgggtctgg tggcgctggg cttcacctta atttccgtgt 1740
tcacgcttag cggccccggc ccgctttccc tgctgcgtcg tcaggtgaat gaagtcgctt 1800
aa 1802
<210> 26
<211> 1947
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 26
cctgagtcgc tgtctttttc gtgacattca gttcgctgcg ctcacggctc tggcagtgaa 60
tgggggtaaa tggcactaca ggcgcctttt atggattcat gcaaggaaac tacccataat 120
acaagaaaag cccgtcacgg gcttctcagg gcgttttatg gcgggtctgc tatgtggtgc 180
tatctgactt tttgctgttc agcagttcct gccctctgat tttccagtct gaccacttcg 240
gattatcccg tgacaggtca ttcagactgg ctaatgcacc cagtaaggca gcggtatcat 300
caacaggctt acccgtctta ctgtcgggaa ttcgcgttgg ccgattaaag gagatcaaca 360
atgaaagcac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 420
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 480
caacaatgaa agcaagcggt atcatcaaca ggcttacccg tcttactgtc gggaattcgc 540
gttggccgat tcattaatgg tataaggttc ttgacatctt acaatcaata tggcataata 600
atttagttag ggcccaagtt cacttaaaaa ggagatcaac aatgaaagca attttcgtac 660
tgaaacatct taatcatgcg taggattttt tctatgtact atttaaaaaa cacaaacttt 720
tggatgttcg gtttattctt tttcttttac ttttttatca tgggagccta cttcccgttt 780
ttcccgattt ggctacatga catcaaccat atcagcaaaa gtgatacggg tattattttt 840
gccgctattt ctctgttctc gctattattc caaccgctgt ttggtctgct ttctgacaaa 900
ctcgggctgc gcaaatacct gctgtggatt attaccggca tgttagtgat gtttgcgccg 960
ttctttattt ttatcttcgg gccactgtta caatacaaca ttttagtagg atcgattgtt 1020
ggtggtattt atctaggctt ttgttttaac gccggtgcgc cagcagtaga ggcatttatt 1080
gagaaagtca gccgtcgcag taatttcgaa tttggtcgcg cgcggatgtt tggctgtgtt 1140
ggctgggcgc tgtgtgcctc gattgtcggc atcatgttca ccatcaataa tcagtttgtt 1200
ttctggctgg gctctggctg tgcactcatc ctcgccgttt tactcttttt cgccaaaacg 1260
gatgcgccct cttctgccac ggttgccaat gcggtaggtg ccaaccattc ggcatttagc 1320
cttaagctgg cactggaact gttcagacag ccaaaactgt ggtttttgtc actgtatgtt 1380
attggcgttt cctgcaccta cgatgttttt gaccaacagt ttgctaattt ctttacttcg 1440
ttctttgcta ccggtgaaca gggtacgcgg gtatttggct acgtaacgac aatgggcgaa 1500
ttacttaacg cctcgattat gttctttgcg ccactgatca ttaatcgcat cggtgggaaa 1560
aacgccctgc tgctggctgg cactattatg tctgtacgta ttattggctc atcgttcgcc 1620
acctcagcgc tggaagtggt tattctgaaa acgctgcata tgtttgaagt accgttcctg 1680
ctggtgggct gctttaaata tattaccagc cagtttgaag tgcgtttttc agcgacgatt 1740
tatctggtct gtttctgctt ctttaagcaa ctggcgatga tttttatgtc tgtactggcg 1800
ggcaatatgt atgaaagcat cggtttccag ggcgcttatc tggtgctggg tctggtggcg 1860
ctgggcttca ccttaatttc cgtgttcacg cttagcggcc ccggcccgct ttccctgctg 1920
cgtcgtcagg tgaatgaagt cgcttaa 1947
<210> 27
<211> 1511
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 27
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat tcgcgttggc caattaatta 120
atggtataag gttcttgaca tcttacaatc aatatggtat aataatttag ttagggccca 180
agttcactta aaaaggagat caacaatgaa agcaattttc gtactgaaac atcttaatca 240
tgcgtaggat tttttctatg tactatttaa aaaacacaaa cttttggatg ttcggtttat 300
tctttttctt ttactttttt atcatgggag cctacttccc gtttttcccg atttggctac 360
atgacatcaa ccatatcagc aaaagtgata cgggtattat ttttgccgct atttctctgt 420
tctcgctatt attccaaccg ctgtttggtc tgctttctga caaactcggg ctgcgcaaat 480
acctgctgtg gattattacc ggcatgttag tgatgtttgc gccgttcttt atttttatct 540
tcgggccact gttacaatac aacattttag taggatcgat tgttggtggt atttatctag 600
gcttttgttt taacgccggt gcgccagcag tagaggcatt tattgagaaa gtcagccgtc 660
gcagtaattt cgaatttggt cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg 720
cctcgattgt cggcatcatg ttcaccatca ataatcagtt tgttttctgg ctgggctctg 780
gctgtgcact catcctcgcc gttttactct ttttcgccaa aacggatgcg ccctcttctg 840
ccacggttgc caatgcggta ggtgccaacc attcggcatt tagccttaag ctggcactgg 900
aactgttcag acagccaaaa ctgtggtttt tgtcactgta tgttattggc gtttcctgca 960
cctacgatgt ttttgaccaa cagtttgcta atttctttac ttcgttcttt gctaccggtg 1020
aacagggtac gcgggtattt ggctacgtaa cgacaatggg cgaattactt aacgcctcga 1080
ttatgttctt tgcgccactg atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg 1140
ctggcactat tatgtctgta cgtattattg gctcatcgtt cgccacctca gcgctggaag 1200
tggttattct gaaaacgctg catatgtttg aagtaccgtt cctgctggtg ggctgcttta 1260
aatatattac cagccagttt gaagtgcgtt tttcagcgac gatttatctg gtctgtttct 1320
gcttctttaa gcaactggcg atgattttta tgtctgtact ggcgggcaat atgtatgaaa 1380
gcatcggttt ccagggcgct tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa 1440
tttccgtgtt cacgcttagc ggccccggcc cgctttccct gctgcgtcgt caggtgaatg 1500
aagtcgctta a 1511
<210> 28
<211> 1950
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 28
cctgagtcgc tgtctttttc gtgacattca gttcgctgcg ctcacggctc tggcagtgaa 60
tgggggtaaa tggcactaca ggcgcctttt atggattcat gcaaggaaac tacccataat 120
acaagaaaag cccgtcacgg gcttctcagg gcgttttatg gcgggtctgc tatgtggtgc 180
tatctgactt tttgctgttc agcagttcct gccctctgat tttccagtct gaccacttcg 240
gattatcccg tgacaggtca ttcagactgg ctaatgcacc cagtaaggca gcggtatcat 300
caacaggctt acccgtctta ctgtcgggaa ttcgcgttgg ccgattaaag gagatcaaca 360
atgaaagcac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 420
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 480
caacaatgaa agcaagcggt atcatcaaca ggcttacccg tcttactgtc gggaattcgc 540
gttggccgat tcattaatgg tataaggttc tttgacatct tacaatcaat atggtataat 600
aatttagtta gggcccaagt tcacttaaaa aaggagatca acaatgaaag caattttcgt 660
actgaaacat cttaatcatg cgtaggattt ttttctatgt actatttaaa aaacacaaac 720
ttttggatgt tcggtttatt ctttttcttt tactttttta tcatgggagc ctacttcccg 780
tttttcccga tttggctaca tgacatcaac catatcagca aaagtgatac gggtattatt 840
tttgccgcta tttctctgtt ctcgctatta ttccaaccgc tgtttggtct gctttctgac 900
aaactcgggc tgcgcaaata cctgctgtgg attattaccg gcatgttagt gatgtttgcg 960
ccgttcttta tttttatctt cgggccactg ttacaataca acattttagt aggatcgatt 1020
gttggtggta tttatctagg cttttgtttt aacgccggtg cgccagcagt agaggcattt 1080
attgagaaag tcagccgtcg cagtaatttc gaatttggtc gcgcgcggat gtttggctgt 1140
gttggctggg cgctgtgtgc ctcgattgtc ggcatcatgt tcaccatcaa taatcagttt 1200
gttttctggc tgggctctgg ctgtgcactc atcctcgccg ttttactctt tttcgccaaa 1260
acggatgcgc cctcttctgc cacggttgcc aatgcggtag gtgccaacca ttcggcattt 1320
agccttaagc tggcactgga actgttcaga cagccaaaac tgtggttttt gtcactgtat 1380
gttattggcg tttcctgcac ctacgatgtt tttgaccaac agtttgctaa tttctttact 1440
tcgttctttg ctaccggtga acagggtacg cgggtatttg gctacgtaac gacaatgggc 1500
gaattactta acgcctcgat tatgttcttt gcgccactga tcattaatcg catcggtggg 1560
aaaaacgccc tgctgctggc tggcactatt atgtctgtac gtattattgg ctcatcgttc 1620
gccacctcag cgctggaagt ggttattctg aaaacgctgc atatgtttga agtaccgttc 1680
ctgctggtgg gctgctttaa atatattacc agccagtttg aagtgcgttt ttcagcgacg 1740
atttatctgg tctgtttctg cttctttaag caactggcga tgatttttat gtctgtactg 1800
gcgggcaata tgtatgaaag catcggtttc cagggcgctt atctggtgct gggtctggtg 1860
gcgctgggct tcaccttaat ttccgtgttc acgcttagcg gccccggccc gctttccctg 1920
ctgcgtcgtc aggtgaatga agtcgcttaa 1950
<210> 29
<211> 1551
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 29
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggcataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacacttac tgtcgggaat tcgcgttggc caattaatta atggtataag gttcttgaca 180
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 240
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtatgat tttttctatg 300
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 360
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 420
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 480
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 540
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 600
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 660
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 720
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 780
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 840
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 900
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 960
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 1020
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 1080
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1140
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1200
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1260
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1320
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1380
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1440
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1500
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1551
<210> 30
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 30
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 31
<211> 1551
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 31
cccgtcttac tgtcgggaat tcgcgttggc cgattcattc aatccaatag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacacttac tgtcgggaat tcgcgttggc caattaatta atggtataag gttcttgaca 180
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 240
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 300
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 360
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 420
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 480
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 540
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 600
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 660
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 720
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 780
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 840
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 900
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 960
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 1020
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 1080
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1140
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1200
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1260
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1320
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1380
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1440
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1500
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1551
<210> 32
<211> 1558
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 32
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatgggat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcttactgt cgggaattcg cgttggccga ttcttataaa tcattatctt 180
cttgacattt tagaaacaat atggtataat ataacgataa gggcccaagt tcacttaaaa 240
aggagatcaa caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt 300
ttctatgtac tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta 360
cttttttatc atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca 420
tatcagcaaa agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt 480
ccaaccgctg tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat 540
tattaccggc atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt 600
acaatacaac attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa 660
cgccggtgcg ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga 720
atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg 780
catcatgttc accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat 840
cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa 900
tgcggtaggt gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca 960
gccaaaactg tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt 1020
tgaccaacag tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg 1080
ggtatttggc tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc 1140
gccactgatc attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat 1200
gtctgtacgt attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa 1260
aacgctgcat atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag 1320
ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca 1380
actggcgatg atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca 1440
gggcgcttat ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac 1500
gcttagcggc cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1558
<210> 33
<211> 1542
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 33
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgctggc cgattcgaat tcgcgttggc cgattaaagg agatcaacta tgaaagctta 120
ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa ggctcttgac atcttacaat 180
caatatggta taataattta gttagggccc aagttcactt aaaaaggaga tcaacaatga 240
aagcaatttt cgtactgaaa catcttaatc atgcgtagga ttttttctat gtactattta 300
aaaaacacaa acttttggat gttcggttta ttctttttct tttacttttt tatcatggga 360
gcctacttcc cgtttttccc gatttggcta catgacatca accatatcag caaaagtgat 420
acgggtatta tttttgccgc tatttctctg ttctcgctat tattccaacc gctgtttggt 480
ctgctttctg acaaactcgg gctgcgcaaa tacctgctgt ggattattac cggcatgtta 540
gtgatgtttg cgccgttctt tatttttatc ttcgggccac tgttacaata caacatttta 600
gtaggatcga ttgttggtgg tatttatcta ggcttttgtt ttaacgccgg tgcgccagca 660
gtagaggcat ttattgagaa agtcagccgt cgcagtaatt tcgaatttgg tcgcgcgcgg 720
atgtttggct gtgttggctg ggcgctgtgt gcctcgattg tcggcatcat gttcaccatc 780
aataatcagt ttgttttctg gctgggctct ggctgtgcac tcatcctcgc cgttttactc 840
tttttcgcca aaacggatgc gccctcttct gccacggttg ccaatgcggt aggtgccaac 900
cattcggcat ttagccttaa gctggcactg gaactgttca gacagccaaa actgtggttt 960
ttgtcactgt atgttattgg cgtttcctgc acctacgatg tttttgacca acagtttgct 1020
aatttcttta cttcgttctt tgctaccggt gaacagggta cgcgggtatt tggctacgta 1080
acgacaatgg gcgaattact taacgcctcg attatgttct ttgcgccact gatcattaat 1140
cgcatcggtg ggaaaaacgc cctgctgctg gctggcacta ttatgtctgt acgtattatt 1200
ggctcatcgt tcgccacctc agcgctggaa gtggttattc tgaaaacgct gcatatgttt 1260
gaagtaccgt tcctgctggt gggctgcttt aaatatatta ccagccagtt tgaagtgcgt 1320
ttttcagcga cgatttatct ggtctgtttc tgcttcttta agcaactggc gatgattttt 1380
atgtctgtac tggcgggcaa tatgtatgaa agcatcggtt tccagggcgc ttatctggtg 1440
ctgggtctgg tggcgctggg cttcacctta atttccgtgt tcacgcttag cggccccggc 1500
ccgctttccc tgctgcgtcg tcaggtgaat gaagtcgctt aa 1542
<210> 34
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 34
cccgtcttac tgtcgggaat tcgcgttggc cgattcatac tacccataat gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 35
<211> 1551
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 35
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacacttac tgtcgggaat tcgcgttggc caattaatta atggtataag gttcttgaca 180
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 240
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 300
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 360
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 420
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 480
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 540
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 600
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 660
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 720
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 780
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 840
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 900
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 960
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 1020
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 1080
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1140
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1200
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1260
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1320
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1380
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1440
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1500
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1551
<210> 36
<211> 1491
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 36
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgatggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattcttac acgatatata cttcttgaca 120
ttttgcggga attatggtat aatcacaagg ttagggccca agttcactta aaaaggagat 180
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 240
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 300
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 360
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 420
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 480
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 540
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 600
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 660
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 720
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 780
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 840
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 900
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 960
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 1020
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1080
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1140
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1200
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1260
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1320
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1380
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1440
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1491
<210> 37
<211> 1405
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 37
cccgtcttac tgtcgggaat tcgcgttggc caattaatta atggtataag gttcttgaca 60
tcttacaggg cccaagttca cttaaaaagg agatcaacaa tgaaagcaat tttcgtactg 120
aaacatctta atcatgcgta ggattttttc tatgtactat ttaaaaaaca caaacttttg 180
gatgttcggt ttattctttt tcttttactt ttttatcatg ggagcctact tcccgttttt 240
cccgatttgg ctacatgaca tcaaccatat cagcaaaagt gatacgggta ttatttttgc 300
cgctatttct ctgttctcgc tattattcca accgctgttt ggtctgcttt ctgacaaact 360
cgggctgcgc aaatacctgc tgtggattat taccggcatg ttagtgatgt ttgcgccgtt 420
ctttattttt atcttcgggc cactgttaca atacaacatt ttagtaggat cgattgttgg 480
tggtatttat ctaggctttt gttttaacgc cggtgcgcca gcagtagagg catttattga 540
gaaagtcagc cgtcgcagta atttcgaatt tggtcgcgcg cggatgtttg gctgtgttgg 600
ctgggcgctg tgtgcctcga ttgtcggcat catgttcacc atcaataatc agtttgtttt 660
ctggctgggc tctggctgtg cactcatcct cgccgtttta ctctttttcg ccaaaacgga 720
tgcgccctct tctgccacgg ttgccaatgc ggtaggtgcc aaccattcgg catttagcct 780
taagctggca ctggaactgt tcagacagcc aaaactgtgg tttttgtcac tgtatgttat 840
tggcgtttcc tgcacctacg atgtttttga ccaacagttt gctaatttct ttacttcgtt 900
ctttgctacc ggtgaacagg gtacgcgggt atttggctac gtaacgacaa tgggcgaatt 960
acttaacgcc tcgattatgt tctttgcgcc actgatcatt aatcgcatcg gtgggaaaaa 1020
cgccctgctg ctggctggca ctattatgtc tgtacgtatt attggctcat cgttcgccac 1080
ctcagcgctg gaagtggtta ttctgaaaac gctgcatatg tttgaagtac cgttcctgct 1140
ggtgggctgc tttaaatata ttaccagcca gtttgaagtg cgtttttcag cgacgattta 1200
tctggtctgt ttctgcttct ttaagcaact ggcgatgatt tttatgtctg tactggcggg 1260
caatatgtat gaaagcatcg gtttccaggg cgcttatctg gtgctgggtc tggtggcgct 1320
gggcttcacc ttaatttccg tgttcacgct tagcggcccc ggcccgcttt ccctgctgcg 1380
tcgtcaggtg aatgaagtcg cttaa 1405
<210> 38
<211> 1491
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 38
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattcttac acgatatata cttcttgaca 120
ttttgcggga attatggtat aatcacaagg ttagggccca agttcactta aaaaggagat 180
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 240
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 300
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 360
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 420
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 480
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 540
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 600
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 660
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 720
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 780
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 840
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 900
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 960
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 1020
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1080
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1140
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1200
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1260
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1320
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1380
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1440
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1491
<210> 39
<211> 2116
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 39
cctgagtcgc tgtctttttc gtgacattca gttcgctgcg ctcacggctc tggcagtgaa 60
tgggggtaaa tggcactaca ggcgcctttt atggattcat gcaaggaaac tacccataat 120
acaagaaaag cccgtcacgg gcttctcagg gcgttttatg gcgggtctgc tatgtggtgc 180
tatctgactt tttgctgttc agcagttcct gccctctgat tttccagtct gaccacttcg 240
gattatcccg tgacaggtca ttcagactgg ctaatgcacc cagtaaggca gcggtatcat 300
caacaggctt acccgtctta ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa 360
ggttcttgac atcttacaat caatatggta taataattta gttagggccc aagttcactt 420
aaaaaggaga tcaacaatga aagcttactg tcgggaattc gcgttggccg attcattaat 480
ggtataaggt tcttgacatc ttacaatcaa tatggtataa taatttagtt agggcccaag 540
ttcacttaaa aaggagatca acaatgaaag cttactgtcg ggaattcgcg ttggccgatt 600
cattaatggt ataaggttct tgacatctta caatcaatat ggtataataa tttagttagg 660
gcccaagttc acttaaaaag gagatcaaca cttactgtcg ggaattcgcg ttggccaatt 720
aattaatggt ataaggttct tgacatctta caatcaatat ggtataataa tttagttagg 780
gcccaagttc acttaaaaag gagatcaaca atgaaagcaa ttttcgtact gaaacatctt 840
aatcatgcgt aggatttttt ctatgtacta tttaaaaaac acaaactttt ggatgttcgg 900
tttattcttt ttcttttact tttttatcat gggagcctac ttcccgtttt tcccgatttg 960
gctacatgac atcaaccata tcagcaaaag tgatacgggt attatttttg ccgctatttc 1020
tctgttctcg ctattattcc aaccgctgtt tggtctgctt tctgacaaac tcgggctgcg 1080
caaatacctg ctgtggatta ttaccggcat gttagtgatg tttgcgccgt tctttatttt 1140
tatcttcggg ccactgttac aatacaacat tttagtagga tcgattgttg gtggtattta 1200
tctaggcttt tgttttaacg ccggtgcgcc agcagtagag gcatttattg agaaagtcag 1260
ccgtcgcagt aatttcgaat ttggtcgcgc gcggatgttt ggctgtgttg gctgggcgct 1320
gtgtgcctcg attgtcggca tcatgttcac catcaataat cagtttgttt tctggctggg 1380
ctctggctgt gcactcatcc tcgccgtttt actctttttc gccaaaacgg atgcgccctc 1440
ttctgccacg gttgccaatg cggtaggtgc caaccattcg gcatttagcc ttaagctggc 1500
actggaactg ttcagacagc caaaactgtg gtttttgtca ctgtatgtta ttggcgtttc 1560
ctgcacctac gatgtttttg accaacagtt tgctaatttc tttacttcgt tctttgctac 1620
cggtgaacag ggtacgcggg tatttggcta cgtaacgaca atgggcgaat tacttaacgc 1680
ctcgattatg ttctttgcgc cactgatcat taatcgcatc ggtgggaaaa acgccctgct 1740
gctggctggc actattatgt ctgtacgtat tattggctca tcgttcgcca cctcagcgct 1800
ggaagtggtt attctgaaaa cgctgcatat gtttgaagta ccgttcctgc tggtgggctg 1860
ctttaaatat attaccagcc agtttgaagt gcgtttttca gcgacgattt atctggtctg 1920
tttctgcttc tttaagcaac tggcgatgat ttttatgtct gtactggcgg gcaatatgta 1980
tgaaagcatc ggtttccagg gcgcttatct ggtgctgggt ctggtggcgc tgggcttcac 2040
cttaatttcc gtgttcacgc ttagcggccc cggcccgctt tccctgctgc gtcgtcaggt 2100
gaatgaagtc gcttaa 2116
<210> 40
<211> 2122
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 40
tgtctttttc gtgacattca gttcgctgcg ctcacggctc tggcagtgaa tgggggtaaa 60
tggcactaca ggcgcctttt atggattcat gcaaggaaac tacccataat acaagaaaag 120
cccgtcacgg gcttctcagg gcgttttatg gcgggtctgc tatgtggtgc tatctgactt 180
tttgctgttc agcagttcct gccctctgat tttccagtct gaccacttcg gattatcccg 240
tgacaggtca ttcagactgg ctaatgcacc cagtaaggca gcggtatcat caacaggctt 300
acccgtctta ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa ggttcttgac 360
atcttacaat caatatggta taataattta gttagggccc aagttcactt aaaaaggaga 420
tcaacaatga aagcttactg tcgggaattc gcgttggccg attcattaat ggtataaggt 480
tcttgacatc ttacaatcaa tatggtataa taatttagtt agggcccaag ttcacttaaa 540
aaggagatca acaatgaaag cactgtcggg aattcgcgtt ggccgattca ttaatggtat 600
aaggttcttg acatcttaca atcaatatgg tataataatt tagttagggc ccaagttcac 660
ttaaaaagga gatcaacaat gaaagcttac tgtcgggaat tcgcgttggc cgattcatta 720
atggtataag gttcttgaca tcttacaatc aatatggtat aataatttag ttagggccca 780
agttcactta aaaaggagat caacacttta ctgtcgggga attcgccgtt gggccaattt 840
aattaatggg tataagggtt ccttgacaat gtactattta aaaaacacaa acttttggat 900
gttcggttta ttctttttct tttacttttt tatcatggga gcctacttcc cgtttttccc 960
gatttggcta catgacatca accatatcag caaaagtgat acgggtatta tttttgccgc 1020
tatttctctg ttctcgctat tattccaacc gctgtttggt ctgctttctg acaaactcgg 1080
gctgcgcaaa tacctgctgt ggattattac cggcatgtta gtgatgtttg cgccgttctt 1140
tatttttatc ttcgggccac tgttacaata caacatttta gtaggatcga ttgttggtgg 1200
tatttatcta ggcttttgtt ttaacgccgg tgcgccagca gtagaggcat ttattgagaa 1260
agtcagccgt cgcagtaatt tcgaatttgg tcgcgcgcgg atgtttggct gtgttggctg 1320
ggcgctgtgt gcctcgattg tcggcatcat gttcaccatc aataatcagt ttgttttctg 1380
gctgggctct ggctgtgcac tcatcctcgc cgttttactc tttttcgcca aaacggatgc 1440
gccctcttct gccacggttg ccaatgcggt aggtgccaac cattcggcat ttagccttaa 1500
gctggcactg gaactgttca gacagccaaa actgtggttt ttgtcactgt atgttattgg 1560
cgtttcctgc acctacgatg tttttgacca acagtttgct aatttcttta cttcgttctt 1620
tgctaccggt gaacagggta cgcgggtatt tggctacgta acgacaatgg gcgaattact 1680
taacgcctcg attatgttct ttgcgccact gatcattaat cgcatcggtg ggaaaaacgc 1740
cctgctgctg gctggcacta ttatgtctgt acgtattatt ggctcatcgt tcgccacctc 1800
agcgctggaa gtggttattc tgaaaacgct gcatatgttt gaagtaccgt tcctgctggt 1860
gggctgcttt aaatatatta ccagccagtt tgaagtgcgt ttttcagcga cgatttatct 1920
ggtctgtttc tgcttcttta agcaactggc gatgattttt atgtctgtac tggcgggcaa 1980
tatgtatgaa agcatcggtt tccagggcgc ttatctggtg ctgggtctgg tggcgctggg 2040
cttcacctta atttccgtgt tcacgcttag cggccccggc ccgctttccc tgctgcgtcg 2100
tcaggtgaat gaagtcgctt aa 2122
<210> 41
<211> 2130
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 41
tcgctgtctt tttcgtgaca ttcagttcgc tgcgctcacg gctctggcag tgaatggggg 60
taaatggcac tacaggcgcc ttttatggat tcatgcaagg aaactaccca taatacaaga 120
aaagcccgtc acgggcttct cagggcgttt tatggcgggt ctgctatgtg gtgctatctg 180
actttttgct gttcagcagt tcctgccctc tgattttcca gtctgaccac ttcggattat 240
cccgtgacag gtcattcaga ctggctaatg cacccagtaa ggcagcggta tcatcaacag 300
gcttacccgt cttactgtcg ggaattcgcg ttggccgatt cattaatggt ataaggttct 360
tgacatctta caatcaatat ggtataataa tttagttagg gcccaagttc acttaaaaag 420
gagatcaaca atgaaagctt actgtcggga attcgcgttg gccgattcat taatggtata 480
aggttcttga catcttacaa tcaatatggt ataataattt agttagggcc caagttcact 540
taaaaaggag atcaacaatg aaagcactgt cgggaattcg cgttggccga ttcattaatg 600
gtataagggt cttgacatct tacaatcaat atggtataat aatttaggta ggggccaagt 660
tcacttagaa aggagatcaa caatgaaagc ttactgtcgg gaattcgcgt tggccgattc 720
attaatggta taaggttctt gacatcttac aatctatatg gtatcataat atacttaggg 780
cccaagttca cttaaaaagg agatcaacac ttactgtcgc gaattcgcgt tggccaatta 840
attcatggta taaggttctt gacatcttac aatcaaatgt actatttaaa aaacacaaac 900
ttttggatgt tcggtttatt ctttttcttt tactttttta tcatgggagc ctacttcccg 960
tttttcccga tttggctaca tgacatcaac catatcagca aaagtgatac gggtattatt 1020
tttgccgcta tttctctgtt ctcgctatta ttccaaccgc tgtttggtct gctttctgac 1080
aaactcgggc tgcgcaaata cctgctgtgg attattaccg gcatgttagt gatgtttgcg 1140
ccgttcttta tttttatctt cgggccactg ttacaataca acattttagt aggatcgatt 1200
gttggtggta tttatctagg cttttgtttt aacgccggtg cgccagcagt agaggcattt 1260
attgagaaag tcagccgtcg cagtaatttc gaatttggtc gcgcgcggat gtttggctgt 1320
gttggctggg cgctgtgtgc ctcgattgtc ggcatcatgt tcaccatcaa taatcagttt 1380
gttttctggc tgggctctgg ctgtgcactc atcctcgccg ttttactctt tttcgccaaa 1440
acggatgcgc cctcttctgc cacggttgcc aatgcggtag gtgccaacca ttcggcattt 1500
agccttaagc tggcactgga actgttcaga cagccaaaac tgtggttttt gtcactgtat 1560
gttattggcg tttcctgcac ctacgatgtt tttgaccaac agtttgctaa tttctttact 1620
tcgttctttg ctaccggtga acagggtacg cgggtatttg gctacgtaac gacaatgggc 1680
gaattactta acgcctcgat tatgttcttt gcgccactga tcattaatcg catcggtggg 1740
aaaaacgccc tgctgctggc tggcactatt atgtctgtac gtattattgg ctcatcgttc 1800
gccacctcag cgctggaagt ggttattctg aaaacgctgc atatgtttga agtaccgttc 1860
ctgctggtgg gctgctttaa atatattacc agccagtttg aagtgcgttt ttcagcgacg 1920
atttatctgg tctgtttctg cttctttaag caactggcga tgatttttat gtctgtactg 1980
gcgggcaata tgtatgaaag catcggtttc cagggcgctt atctggtgct gggtctggtg 2040
gcgctgggct tcaccttaat ttccgtgttc acgcttagcg gccccggccc gctttccctg 2100
ctgcgtcgtc aggtgaatga agtcgcttaa 2130
<210> 42
<211> 1865
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 42
gcccgtcacg ggcttctcag ggcgttttat ggcgggtctg ctatgtggtg ctatctgact 60
ttttgctgtt cagcagttcc tgccctctga ttttccagtc tgaccacttc ggattatccc 120
gtgacaggtc attcagactg gctaatgcac ccagtaaggc agcggtatca tcaacaggct 180
tacccgtctt actgtcggga attcgcgttg gccgattcat taatggtata aggttcttga 240
catcttacaa tcaatatggt ataataattt agttagggcc caagttcact taaaaaggag 300
atcaacaatg aaagcttact gtcgggaatt cgcgttggcc gattcattaa tggtataagg 360
ttcttgacat cttacaatca atatggtata ataatttagt tagggcccaa gttcacttaa 420
aaaggagatc aacaatgaaa gcactgtcgg gaattcgcgt tggccaatta attaatggta 480
taaggttctt gacatcttac aatcaatatg gtataataat ttagttaggg cccaagttca 540
cttaaaaagg agatcaacaa tgaaagcaat tttcgtactg aaacatctta atcatgcgta 600
ggattttttc tatgtactat ttaaaaaaca caaacttttg gatgttcggt ttattctttt 660
tcttttactt ttttatcatg ggagcctact tcccgttttt cccgatttgg ctacatgaca 720
tcaaccatat cagcaaaagt gatacgggta ttatttttgc cgctatttct ctgttctcgc 780
tattattcca accgctgttt ggtctgcttt ctgacaaact cgggctgcgc aaatacctgc 840
tgtggattat taccggcatg ttagtgatgt ttgcgccgtt ctttattttt atcttcgggc 900
cactgttaca atacaacatt ttagtaggat cgattgttgg tggtatttat ctaggctttt 960
gttttaacgc cggtgcgcca gcagtagagg catttattga gaaagtcagc cgtcgcagta 1020
atttcgaatt tggtcgcgcg cggatgtttg gctgtgttgg ctgggcgctg tgtgcctcga 1080
ttgtcggcat catgttcacc atcaataatc agtttgtttt ctggctgggc tctggctgtg 1140
cactcatcct cgccgtttta ctctttttcg ccaaaacgga tgcgccctct tctgccacgg 1200
ttgccaatgc ggtaggtgcc aaccattcgg catttagcct taagctggca ctggaactgt 1260
tcagacagcc aaaactgtgg tttttgtcac tgtatgttat tggcgtttcc tgcacctacg 1320
atgtttttga ccaacagttt gctaatttct ttacttcgtt ctttgctacc ggtgaacagg 1380
gtacgcgggt atttggctac gtaacgacaa tgggcgaatt acttaacgcc tcgattatgt 1440
tctttgcgcc actgatcatt aatcgcatcg gtgggaaaaa cgccctgctg ctggctggca 1500
ctattatgtc tgtacgtatt attggctcat cgttcgccac ctcagcgctg gaagtggtta 1560
ttctgaaaac gctgcatatg tttgaagtac cgttcctgct ggtgggctgc tttaaatata 1620
ttaccagcca gtttgaagtg cgtttttcag cgacgattta tctggtctgt ttctgcttct 1680
ttaagcaact ggcgatgatt tttatgtctg tactggcggg caatatgtat gaaagcatcg 1740
gtttccaggg cgcttatctg gtgctgggtc tggtggcgct gggcttcacc ttaatttccg 1800
tgttcacgct tagcggcccc ggcccgcttt ccctgctgcg tcgtcaggtg aatgaagtcg 1860
cttaa 1865
<210> 43
<211> 1802
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 43
gctgttcagc agttcctgcc ctctgatttt ccagtctgac cacttcggat tatcccgtga 60
caggtcattc agactggcta atgcacccag taaggcagcg gtatcatcaa caggcttacc 120
cgtcttactg tcgggaattc gcgttggccg attcattaat ggtataaggt tcttgacatc 180
ttacaatcaa tatggtataa taatttagtt agggcccaag ttcacttaaa aaggagatca 240
acaatgaaag cttactgtcg ggaattcgcg ttggccgatt cattaatggt ataaggttct 300
tgacatctta caatcaatat gggtataata atttagttag ggcccaagtt cacttaaaaa 360
ggagatcaac aatgaaagca ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa 420
ggttcttgac atcttacaat caatatggta taataattta gttagggccc aagttcactt 480
aaaaaggaga tcaacaatga aagcaatttt cgtactgaaa catcttaatc atgcgtagga 540
ttttttctat gtactattta aaaaacacaa acttttggat gttcggttta ttctttttct 600
tttacttttt tatcatggga gcctacttcc cgtttttccc gatttggcta catgacatca 660
accatatcag caaaagtgat acgggtatta tttttgccgc tatttctctg ttctcgctat 720
tattccaacc gctgtttggt ctgctttctg acaaactcgg gctgcgcaaa tacctgctgt 780
ggattattac cggcatgtta gtgatgtttg cgccgttctt tatttttatc ttcgggccac 840
tgttacaata caacatttta gtaggatcga ttgttggtgg tatttatcta ggcttttgtt 900
ttaacgccgg tgcgccagca gtagaggcat ttattgagaa agtcagccgt cgcagtaatt 960
tcgaatttgg tcgcgcgcgg atgtttggct gtgttggctg ggcgctgtgt gcctcgattg 1020
tcggcatcat gttcaccatc aataatcagt ttgttttctg gctgggctct ggctgtgcac 1080
tcatcctcgc cgttttactc tttttcgcca aaacggatgc gccctcttct gccacggttg 1140
ccaatgcggt aggtgccaac cattcggcat ttagccttaa gctggcactg gaactgttca 1200
gacagccaaa actgtggttt ttgtcactgt atgttattgg cgtttcctgc acctacgatg 1260
tttttgacca acagtttgct aatttcttta cttcgttctt tgctaccggt gaacagggta 1320
cgcgggtatt tggctacgta acgacaatgg gcgaattact taacgcctcg attatgttct 1380
ttgcgccact gatcattaat cgcatcggtg ggaaaaacgc cctgctgctg gctggcacta 1440
ttatgtctgt acgtattatt ggctcatcgt tcgccacctc agcgctggaa gtggttattc 1500
tgaaaacgct gcatatgttt gaagtaccgt tcctgctggt gggctgcttt aaatatatta 1560
ccagccagtt tgaagtgcgt ttttcagcga cgatttatct ggtctgtttc tgcttcttta 1620
agcaactggc gatgattttt atgtctgtac tggcgggcaa tatgtatgaa agcatcggtt 1680
tccagggcgc ttatctggtg ctgggtctgg tggcgctggg cttcacctta atttccgtgt 1740
tcacgcttag cggccccggc ccgctttccc tgctgcgtcg tcaggtgaat gaagtcgctt 1800
aa 1802
<210> 44
<211> 2245
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 44
ggcacctgag tcgctgtctt tttcgtgaca ttcagttcgc tgcgctcacg gctctggcag 60
tgaatggggg taaatggcac tacaggcgcc ttttatggat tcatgcaagg aaactaccca 120
taatacaaga aaagcccgtc acgggcttct cagggcgttt tatggcgggt ctgctatgtg 180
gtgctatctg actttttgct gttcagcagt tcctgccctc tgattttcca gtctgaccac 240
ttcggattat cccgtgacag gtcattcaga ctggctaatg cacccagtaa ggcagcggta 300
tcatcaacag gcttacccgt cttactgtcg ggaattcgcg ttggccgatt cattaatggt 360
ataaggttct tgacatctta caatcaatat ggtataataa tttagttagg gcccaagttc 420
acttaaaaag gagatcaaca atgaaagctt actgtcggga attcgcgttg gccgattcat 480
taatggtata aggttcttga catcttacaa tcaatatggt ataataattt agttagggcc 540
caagttcact taaaaaggag atcaacaatg aaagcactgt cgggaattcg cgttggccga 600
ttcattaatg gtataaggtt cttgacatct tacaatcaat atggtataat aatttagtta 660
gggcccaagt tcacttaaaa aggagatcaa caatgaaagc ttactgtcgg gaattcgcgt 720
tggccgattc attaatggta taaggttctt gacatcttac aatcaatatg gtataataat 780
ttagttaggg cccaagttca cttaaaaagg agatcaacac ttactgtcgg gaattcgcgt 840
tggccaatta attaatggta taaggttctt gacatcttac aatcaatatg gtataataat 900
ttagttaggg cccaagttca cttaaaaagg agatcaacaa tgaaagcaat tttcgtactg 960
aaacatctta atcatgcgta ggattttttc tatgtactat ttaaaaaaca caaacttttg 1020
gatgttcggt ttattctttt tcttttactt ttttatcatg ggagcctact tcccgttttt 1080
cccgatttgg ctacatgaca tcaaccatat cagcaaaagt gatacgggta ttatttttgc 1140
cgctatttct ctgttctcgc tattattcca accgctgttt ggtctgcttt ctgacaaact 1200
cgggctgcgc aaatacctgc tgtggattat taccggcatg ttagtgatgt ttgcgccgtt 1260
ctttattttt atcttcgggc cactgttaca atacaacatt ttagtaggat cgattgttgg 1320
tggtatttat ctaggctttt gttttaacgc cggtgcgcca gcagtagagg catttattga 1380
gaaagtcagc cgtcgcagta atttcgaatt tggtcgcgcg cggatgtttg gctgtgttgg 1440
ctgggcgctg tgtgcctcga ttgtcggcat catgttcacc atcaataatc agtttgtttt 1500
ctggctgggc tctggctgtg cactcatcct cgccgtttta ctctttttcg ccaaaacgga 1560
tgcgccctct tctgccacgg ttgccaatgc ggtaggtgcc aaccattcgg catttagcct 1620
taagctggca ctggaactgt tcagacagcc aaaactgtgg tttttgtcac tgtatgttat 1680
tggcgtttcc tgcacctacg atgtttttga ccaacagttt gctaatttct ttacttcgtt 1740
ctttgctacc ggtgaacagg gtacgcgggt atttggctac gtaacgacaa tgggcgaatt 1800
acttaacgcc tcgattatgt tctttgcgcc actgatcatt aatcgcatcg gtgggaaaaa 1860
cgccctgctg ctggctggca ctattatgtc tgtacgtatt attggctcat cgttcgccac 1920
ctcagcgctg gaagtggtta ttctgaaaac gctgcatatg tttgaagtac cgttcctgct 1980
ggtgggctgc tttaaatata ttaccagcca gtttgaagtg cgtttttcag cgacgattta 2040
tctggtctgt ttctgcttct ttaagcaact ggcgatgatt tttatgtctg tactggcggg 2100
caatatgtat gaaagcatcg gtttccaggg cgcttatctg gtgctgggtc tggtggcgct 2160
gggcttcacc ttaatttccg tgttcacgct tagcggcccc ggcccgcttt ccctgctgcg 2220
tcgtcaggtg aatgaagtcg cttaa 2245
<210> 45
<211> 2029
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 45
gcaaggaaac tacccataat acaagaaaag cccgtcacgg gcttctcagg gcgttttatg 60
gcgggtctgc tatgtggtgc tatctgactt tttgctgttc agcagttcct gccctctgat 120
tttccagtct gaccacttcg gattatcccg tgacaggtca ttcagactgg ctaatgcacc 180
cagtaaggca gcggtatcat caacaggctt acccgtctta ctgtcgggaa ttcgcgttgg 240
ccgattaatt aatggtataa ggttcttgac atcttacaat caatatggta taataattta 300
gttagggccc aagttcactt aaaaaggaga tcaacaatga aagcttactg tcgggaattc 360
gcgttggccg attcattaat ggtataaggt tcttgacatc ttacaatcaa tatggtataa 420
taatttagtt agggcccaag ttcacttaaa aaggagatca acaatgaaag caggcttacc 480
cgtcttactg tcgggaattc gcgttggccg attcattaat ggtataaggt tcttgacatc 540
ttacaatcaa tatggtataa taatttagtt agggcccaag ttcacttaaa aaggagatca 600
acacttactg tcgggaattc gcgttggcca attaattaat ggtataaggt tcttgacatc 660
ttacaatcaa tatggtataa taatttagtt agggcccaag ttcacttaaa aaggagatca 720
acaatgaaag caattttcgt actgaaacat cttaatcatg cgtaggattt tttctatgta 780
ctatttaaaa aacacaaact tttggatgtt cggtttattc tttttctttt acttttttat 840
catgggagcc tacttcccgt ttttcccgat ttggctacat gacatcaacc atatcagcaa 900
aagtgatacg ggtattattt ttgccgctat ttctctgttc tcgctattat tccaaccgct 960
gtttggtctg ctttctgaca aactcgggct gcgcaaatac ctgctgtgga ttattaccgg 1020
catgttagtg atgtttgcgc cgttctttat ttttatcttc gggccactgt tacaatacaa 1080
cattttagta ggatcgattg ttggtggtat ttatctaggc ttttgtttta acgccggtgc 1140
gccagcagta gaggcattta ttgagaaagt cagccgtcgc agtaatttcg aatttggtcg 1200
cgcgcggatg tttggctgtg ttggctgggc gctgtgtgcc tcgattgtcg gcatcatgtt 1260
caccatcaat aatcagtttg ttttctggct gggctctggc tgtgcactca tcctcgccgt 1320
tttactcttt ttcgccaaaa cggatgcgcc ctcttctgcc acggttgcca atgcggtagg 1380
tgccaaccat tcggcattta gccttaagct ggcactggaa ctgttcagac agccaaaact 1440
gtggtttttg tcactgtatg ttattggcgt ttcctgcacc tacgatgttt ttgaccaaca 1500
gtttgctaat ttctttactt cgttctttgc taccggtgaa cagggtacgc gggtatttgg 1560
ctacgtaacg acaatgggcg aattacttaa cgcctcgatt atgttctttg cgccactgat 1620
cattaatcgc atcggtggga aaaacgccct gctgctggct ggcactatta tgtctgtacg 1680
tattattggc tcatcgttcg ccacctcagc gctggaagtg gttattctga aaacgctgca 1740
tatgtttgaa gtaccgttcc tgctggtggg ctgctttaaa tatattacca gccagtttga 1800
agtgcgtttt tcagcgacga tttatctggt ctgtttctgc ttctttaagc aactggcgat 1860
gatttttatg tctgtactgg cgggcaatat gtatgaaagc atcggtttcc agggcgctta 1920
tctggtgctg ggtctggtgg cgctgggctt caccttaatt tccgtgttca cgcttagcgg 1980
ccccggcccg ctttccctgc tgcgtcgtca ggtgaatgaa gtcgcttaa 2029
<210> 46
<211> 2088
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 46
ttcagttcgc tgcgctcacg gctctggcag tgaatggggg taaatggcac tacaggcgcc 60
ttttatggat tcatgcaagg aaactaccca taatacaaga aaagcccgtc acgggcttct 120
cagggcgttt tatggcgggt ctgctatgtg gtgctatctg actttttgct gttcagcagt 180
tcctgccctc tgattttcca gtctgaccac ttcggattat cccgtgacag gtcattcaga 240
ctggctaatg cacccagtaa ggcagcggta tcatcaacag gcttacccgt cttactgtcg 300
ggaattcgcg ttggccgatt cattaatggt ataaggttct tgacatctta caatcaatat 360
ggtataataa tttagttagg gcccaagttc acttaaaaag gagatcaaca atgaaagctt 420
actgtcggga attcgcgttg gccgattcat taatggtata aggttcttga catcttacaa 480
tcaatatggt ataataattt agttagggcc caagttcact taaaaaggag atcaacaatg 540
aaagcactgt cgggaattcg cgttggccga ttcattaatg gtataaggtt cttgacatct 600
tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa aggagatcaa 660
cacttactgt cgggaattcg cgttggccaa ttaattaatg gtataaggtt cttgacatct 720
tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa aggagatcaa 780
caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt ttctatgtac 840
tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta cttttttatc 900
atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca tatcagcaaa 960
agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt ccaaccgctg 1020
tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat tattaccggc 1080
atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt acaatacaac 1140
attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa cgccggtgcg 1200
ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga atttggtcgc 1260
gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg catcatgttc 1320
accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat cctcgccgtt 1380
ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa tgcggtaggt 1440
gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca gccaaaactg 1500
tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt tgaccaacag 1560
tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg ggtatttggc 1620
tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc gccactgatc 1680
attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat gtctgtacgt 1740
attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa aacgctgcat 1800
atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag ccagtttgaa 1860
gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca actggcgatg 1920
atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca gggcgcttat 1980
ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac gcttagcggc 2040
cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 2088
<210> 47
<211> 2102
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 47
gctgcgctca cggctctggc agtgaatggg ggtaaatggc actacaggcg ccttttatgg 60
attcatgcaa ggaaactacc cataatacaa gaaaagcccg tcacgggctt ctcagggcgt 120
tttatggcgg gtctgctatg tggtgctatc tgactttttg ctgttcagca gttcctgccc 180
tctgattttc cagtctgacc acttcggatt atcccgtgac aggtcattca gactggctaa 240
tgcacccagt aaggcagcgg tatcatcaac aggcttaccc gtcttactgt cgggaattcg 300
cgttggccga ttcgaattcg cgttggccga ttcgaattcg cgttggccga ttcgaattcg 360
cgttggccga ttcgaattcg cgttggccga ttcgaattcg cgttggccga ttcgaattcg 420
cgttggccga ttcgaattcg cgttggccga ttcattaatg gtataaggtt cttgacatct 480
tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa aggagatcaa 540
caatgaaagc ttactgtcgg gaattcgcgt tggccgattc attaatggta taaggttctt 600
gacatcttac aatcaatatg gtataataat ttagttaggg cccaagttca cttaaaaagg 660
agatcaacaa tgaaagctta ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa 720
ggttcttgac atcttacaat caatatggta taataattta gttagggccc aagttcactt 780
aaaaaggaga tcaacaatga aagcaatttt cgtactgaaa catcttaatc atgcgtagga 840
ttttttctat gtactattta aaaaacacaa acttttggat gttcggttta ttctttttct 900
tttacttttt tatcatggga gcctacttcc cgtttttccc gatttggcta catgacatca 960
accatatcag caaaagtgat acgggtatta tttttgccgc tatttctctg ttctcgctat 1020
tattccaacc gctgtttggt ctgctttctg acaaactcgg gctgcgcaaa tacctgctgt 1080
ggattattac cggcatgtta gtgatgtttg cgccgttctt tatttttatc ttcgggccac 1140
tgttacaata caacatttta gtaggatcga ttgttggtgg tatttatcta ggcttttgtt 1200
ttaacgccgg tgcgccagca gtagaggcat ttattgagaa agtcagccgt cgcagtaatt 1260
tcgaatttgg tcgcgcgcgg atgtttggct gtgttggctg ggcgctgtgt gcctcgattg 1320
tcggcatcat gttcaccatc aataatcagt ttgttttctg gctgggctct ggctgtgcac 1380
tcatcctcgc cgttttactc tttttcgcca aaacggatgc gccctcttct gccacggttg 1440
ccaatgcggt aggtgccaac cattcggcat ttagccttaa gctggcactg gaactgttca 1500
gacagccaaa actgtggttt ttgtcactgt atgttattgg cgtttcctgc acctacgatg 1560
tttttgacca acagtttgct aatttcttta cttcgttctt tgctaccggt gaacagggta 1620
cgcgggtatt tggctacgta acgacaatgg gcgaattact taacgcctcg attatgttct 1680
ttgcgccact gatcattaat cgcatcggtg ggaaaaacgc cctgctgctg gctggcacta 1740
ttatgtctgt acgtattatt ggctcatcgt tcgccacctc agcgctggaa gtggttattc 1800
tgaaaacgct gcatatgttt gaagtaccgt tcctgctggt gggctgcttt aaatatatta 1860
ccagccagtt tgaagtgcgt ttttcagcga cgatttatct ggtctgtttc tgcttcttta 1920
agcaactggc gatgattttt atgtctgtac tggcgggcaa tatgtatgaa agcatcggtt 1980
tccagggcgc ttatctggtg ctgggtctgg tggcgctggg cttcacctta atttccgtgt 2040
tcacgcttag cggccccggc ccgctttccc tgctgcgtcg tcaggtgaat gaagtcgctt 2100
aa 2102
<210> 48
<211> 2056
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<220>
<221> misc_feature
<222> (616)..(616)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (656)..(656)
<223> n is a, c, g, or t
<220>
<221> misc_feature
<222> (674)..(674)
<223> n is a, c, g, or t
<400> 48
gctgttcagc agttcctgcc ctctgatttt ccagtctgac cacttcggat tatcccgtga 60
caggtcattc agactggcta atgcacccag taaggcagcg gtatcatcaa caggcttacc 120
cgtcttactg tcgggaattc gcgttggccg attaattaat ggtataaggt tcttgacatc 180
ttacaatcaa tatggtataa taatttagtt agggcccaag ttcacttaaa aaggagatca 240
acaatgaaag cttactgtcg ggaattcgcg ttggccgatt cattaatggt ataaggttct 300
tgacatctta caatcaatat ggtataataa tttagttagg gcccaagttc acttaaaaag 360
gagatcaaca atgaaagcag gcttacccgt cttactgtcg ggaattcgcg ttggccgatt 420
cattaatggt ataaggttct tgacatctta caatcaatat ggtataataa tttagttagg 480
gcccaagttc acttaaaaag gagatcaaca cttactgtcg ggaattcgcg ttggccaatt 540
aattaatggt ataaggttct tgacatctta caatcaatat ggtataataa tttagttagg 600
gcccaagttc acttanaaag gagatcaaca cttactgtcg ggaattcgcg ttggcncatt 660
aattaatggt atanagttct tgacatctta ccaatcatat ggtataataa tttagttagg 720
gcccaagttc acttaaaaag gagatcaaca atgaaagcaa ttttcgtact gaaacatctt 780
aatcatgcgt aggatttttt ctatgtacta tttaaaaaac acaaactttt ggatgttcgg 840
tttattcttt ttcttttact tttttatcat gggagcctac ttcccgtttt tcccgatttg 900
gctacatgac atcaaccata tcagcaaaag tgatacgggt attatttttg ccgctatttc 960
tctgttctcg ctattattcc aaccgctgtt tggtctgctt tctgacaaac tcgggctgcg 1020
caaatacctg ctgtggatta ttaccggcat gttagtgatg tttgcgccgt tctttatttt 1080
tatcttcggg ccactgttac aatacaacat tttagtagga tcgattgttg gtggtattta 1140
tctaggcttt tgttttaacg ccggtgcgcc agcagtagag gcatttattg agaaagtcag 1200
ccgtcgcagt aatttcgaat ttggtcgcgc gcggatgttt ggctgtgttg gctgggcgct 1260
gtgtgcctcg attgtcggca tcatgttcac catcaataat cagtttgttt tctggctggg 1320
ctctggctgt gcactcatcc tcgccgtttt actctttttc gccaaaacgg atgcgccctc 1380
ttctgccacg gttgccaatg cggtaggtgc caaccattcg gcatttagcc ttaagctggc 1440
actggaactg ttcagacagc caaaactgtg gtttttgtca ctgtatgtta ttggcgtttc 1500
ctgcacctac gatgtttttg accaacagtt tgctaatttc tttacttcgt tctttgctac 1560
cggtgaacag ggtacgcggg tatttggcta cgtaacgaca atgggcgaat tacttaacgc 1620
ctcgattatg ttctttgcgc cactgatcat taatcgcatc ggtgggaaaa acgccctgct 1680
gctggctggc actattatgt ctgtacgtat tattggctca tcgttcgcca cctcagcgct 1740
ggaagtggtt attctgaaaa cgctgcatat gtttgaagta ccgttcctgc tggtgggctg 1800
ctttaaatat attaccagcc agtttgaagt gcgtttttca gcgacgattt atctggtctg 1860
tttctgcttc tttaagcaac tggcgatgat ttttatgtct gtactggcgg gcaatatgta 1920
tgaaagcatc ggtttccagg gcgcttatct ggtgctgggt ctggtggcgc tgggcttcac 1980
cttaatttcc gtgttcacgc ttagcggccc cggcccgctt tccctgctgc gtcgtcaggt 2040
gaatgaagtc gcttaa 2056
<210> 49
<211> 1558
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 49
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcttactgt cgggaattcg cgttggccga ttcttataaa tcattatctt 180
cttgacattt tagaaacaat atggtataat ataacgataa gggcccaagt tcacttaaaa 240
aggagatcaa caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt 300
ttctatgtac tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta 360
cttttttatc atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca 420
tatcagcaaa agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt 480
ccaaccgctg tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat 540
tattaccggc atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt 600
acaatacaac attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa 660
cgccggtgcg ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga 720
atttggtcgc gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg 780
catcatgttc accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat 840
cctcgccgtt ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa 900
tgcggtaggt gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca 960
gccaaaactg tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt 1020
tgaccaacag tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg 1080
ggtatttggc tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc 1140
gccactgatc attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat 1200
gtctgtacgt attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa 1260
aacgctgcat atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag 1320
ccagtttgaa gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca 1380
actggcgatg atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca 1440
gggcgcttat ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac 1500
gcttagcggc cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1558
<210> 50
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 50
cccgtcttac tgtcgggaat tcgcgttggc cgattcattt aaccgataag cttcttgaca 60
tgtttagggt gttatgatat aatcacccaa ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 51
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 51
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 52
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 52
cccgtcttac tgtcgggaat tcgcgttggc cgattcttaa attcaataac tttcttgaca 60
tgttattaga tttatggtat aatgacccga tatgggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 53
<211> 1571
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 53
cccgtcttac tgtcgggaat tcgcgttggc cgattaatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaggctta cccgtcttac tgtcgggaat tcgcgttggc caattaatta 180
atggtataag gttcttgaca tcttacaatc aatatggtat aataatttag ttagggccca 240
agttcactta aaaaggagat caacaatgaa agcaattttc gtactgaaac atcttaatca 300
tgcgtaggat tttttctatg tactatttaa aaaacacaaa cttttggatg ttcggtttat 360
tctttttctt ttactttttt atcatgggag cctacttccc gtttttcccg atttggctac 420
atgacatcaa ccatatcagc aaaagtgata cgggtattat ttttgccgct atttctctgt 480
tctcgctatt attccaaccg ctgtttggtc tgctttctga caaactcggg ctgcgcaaat 540
acctgctgtg gattattacc ggcatgttag tgatgtttgc gccgttcttt atttttatct 600
tcgggccact gttacaatac aacattttag taggatcgat tgttggtggt atttatctag 660
gcttttgttt taacgccggt gcgccagcag tagaggcatt tattgagaaa gtcagccgtc 720
gcagtaattt cgaatttggt cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg 780
cctcgattgt cggcatcatg ttcaccatca ataatcagtt tgttttctgg ctgggctctg 840
gctgtgcact catcctcgcc gttttactct ttttcgccaa aacggatgcg ccctcttctg 900
ccacggttgc caatgcggta ggtgccaacc attcggcatt tagccttaag ctggcactgg 960
aactgttcag acagccaaaa ctgtggtttt tgtcactgta tgttattggc gtttcctgca 1020
cctacgatgt ttttgaccaa cagtttgcta atttctttac ttcgttcttt gctaccggtg 1080
aacagggtac gcgggtattt ggctacgtaa cgacaatggg cgaattactt aacgcctcga 1140
ttatgttctt tgcgccactg atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg 1200
ctggcactat tatgtctgta cgtattattg gctcatcgtt cgccacctca gcgctggaag 1260
tggttattct gaaaacgctg catatgtttg aagtaccgtt cctgctggtg ggctgcttta 1320
aatatattac cagccagttt gaagtgcgtt tttcagcgac gatttatctg gtctgtttct 1380
gcttctttaa gcaactggcg atgattttta tgtctgtact ggcgggcaat atgtatgaaa 1440
gcatcggttt ccagggcgct tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa 1500
tttccgtgtt cacgcttagc ggccccggcc cgctttccct gctgcgtcgt caggtgaatg 1560
aagtcgctta a 1571
<210> 54
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 54
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 55
<211> 1968
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 55
cccgtcttac tgtcgggaat tcgcgttggc cgattcgaat tcgcgttggc cgattcgaat 60
tcgcgttggc cgattcgaat tcgcgttggc cgattcatta atggtataag gttcttgaca 120
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 180
caacacttac tgtcgggaat tcgcgttggc cgattcatta atggtataag gttcttgaca 240
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 300
caacaatgaa agcttactgt cgggaattcg cgttggccga ttcattaatg gtataaggtt 360
cttgacatct tacaatcaat atggtataat aatttagtta gggcccaagt tcacttaaaa 420
aggagatcaa caatgaaagc ttactgtcgg gaattcgcgt tggccgattc attaatggta 480
taaggttctt gacatcttac aatcaatatg gtataataat ttagttaggg cccaagttca 540
cttaaaaagg agatcaacac ttactgtcgg gaattcgcgt tggccaatta attaatggta 600
taaggttctt gacatcttac catcaatatg gggcccaagt tcacttaaaa aggagatcaa 660
caatgaaagc aattttcgta ctgaaacatc ttaatcatgc gtaggatttt ttctatgtac 720
tatttaaaaa acacaaactt ttggatgttc ggtttattct ttttctttta cttttttatc 780
atgggagcct acttcccgtt tttcccgatt tggctacatg acatcaacca tatcagcaaa 840
agtgatacgg gtattatttt tgccgctatt tctctgttct cgctattatt ccaaccgctg 900
tttggtctgc tttctgacaa actcgggctg cgcaaatacc tgctgtggat tattaccggc 960
atgttagtga tgtttgcgcc gttctttatt tttatcttcg ggccactgtt acaatacaac 1020
attttagtag gatcgattgt tggtggtatt tatctaggct tttgttttaa cgccggtgcg 1080
ccagcagtag aggcatttat tgagaaagtc agccgtcgca gtaatttcga atttggtcgc 1140
gcgcggatgt ttggctgtgt tggctgggcg ctgtgtgcct cgattgtcgg catcatgttc 1200
accatcaata atcagtttgt tttctggctg ggctctggct gtgcactcat cctcgccgtt 1260
ttactctttt tcgccaaaac ggatgcgccc tcttctgcca cggttgccaa tgcggtaggt 1320
gccaaccatt cggcatttag ccttaagctg gcactggaac tgttcagaca gccaaaactg 1380
tggtttttgt cactgtatgt tattggcgtt tcctgcacct acgatgtttt tgaccaacag 1440
tttgctaatt tctttacttc gttctttgct accggtgaac agggtacgcg ggtatttggc 1500
tacgtaacga caatgggcga attacttaac gcctcgatta tgttctttgc gccactgatc 1560
attaatcgca tcggtgggaa aaacgccctg ctgctggctg gcactattat gtctgtacgt 1620
attattggct catcgttcgc cacctcagcg ctggaagtgg ttattctgaa aacgctgcat 1680
atgtttgaag taccgttcct gctggtgggc tgctttaaat atattaccag ccagtttgaa 1740
gtgcgttttt cagcgacgat ttatctggtc tgtttctgct tctttaagca actggcgatg 1800
atttttatgt ctgtactggc gggcaatatg tatgaaagca tcggtttcca gggcgcttat 1860
ctggtgctgg gtctggtggc gctgggcttc accttaattt ccgtgttcac gcttagcggc 1920
cccggcccgc tttccctgct gcgtcgtcag gtgaatgaag tcgcttaa 1968
<210> 56
<211> 1431
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 56
cccgtcttac tgtcgggaat tcgcgttggc cgattcatta atgggataag gttcttgaca 60
tcttacaatc aatatggtat aataatttag ttagggccca agttcactta aaaaggagat 120
caacaatgaa agcaattttc gtactgaaac atcttaatca tgcgtaggat tttttctatg 180
tactatttaa aaaacacaaa cttttggatg ttcggtttat tctttttctt ttactttttt 240
atcatgggag cctacttccc gtttttcccg atttggctac atgacatcaa ccatatcagc 300
aaaagtgata cgggtattat ttttgccgct atttctctgt tctcgctatt attccaaccg 360
ctgtttggtc tgctttctga caaactcggg ctgcgcaaat acctgctgtg gattattacc 420
ggcatgttag tgatgtttgc gccgttcttt atttttatct tcgggccact gttacaatac 480
aacattttag taggatcgat tgttggtggt atttatctag gcttttgttt taacgccggt 540
gcgccagcag tagaggcatt tattgagaaa gtcagccgtc gcagtaattt cgaatttggt 600
cgcgcgcgga tgtttggctg tgttggctgg gcgctgtgtg cctcgattgt cggcatcatg 660
ttcaccatca ataatcagtt tgttttctgg ctgggctctg gctgtgcact catcctcgcc 720
gttttactct ttttcgccaa aacggatgcg ccctcttctg ccacggttgc caatgcggta 780
ggtgccaacc attcggcatt tagccttaag ctggcactgg aactgttcag acagccaaaa 840
ctgtggtttt tgtcactgta tgttattggc gtttcctgca cctacgatgt ttttgaccaa 900
cagtttgcta atttctttac ttcgttcttt gctaccggtg aacagggtac gcgggtattt 960
ggctacgtaa cgacaatggg cgaattactt aacgcctcga ttatgttctt tgcgccactg 1020
atcattaatc gcatcggtgg gaaaaacgcc ctgctgctgg ctggcactat tatgtctgta 1080
cgtattattg gctcatcgtt cgccacctca gcgctggaag tggttattct gaaaacgctg 1140
catatgtttg aagtaccgtt cctgctggtg ggctgcttta aatatattac cagccagttt 1200
gaagtgcgtt tttcagcgac gatttatctg gtctgtttct gcttctttaa gcaactggcg 1260
atgattttta tgtctgtact ggcgggcaat atgtatgaaa gcatcggttt ccagggcgct 1320
tatctggtgc tgggtctggt ggcgctgggc ttcaccttaa tttccgtgtt cacgcttagc 1380
ggccccggcc cgctttccct gctgcgtcgt caggtgaatg aagtcgctta a 1431
<210> 57
<211> 2296
<212> DNA
<213> Artificial sequence
<220>
<223> Heterologous sequences in front of a lactose transporter gene
<400> 57
ggcacctgag tcgctgtctt tttcgtgaca ttcagttcgc tgcgctcacg gctctggcag 60
tgaatggggg taaatggcac tacaggcgcc ttttatggat tcatgcaagg aaactaccca 120
taatacaaga aaagcccgtc acgggcttct cagggcgttt tatggcgggt ctgctatgtg 180
gtgctatctg actttttgct gttcagcagt tcctgccctc tgattttcca gtctgaccac 240
ttcggattat cccgtgacag gtcattcaga ctggctaatg cacccagtaa ggcagcggta 300
tcatcaacag gcttacccgt cttactgtcg ggaattcgcg ttggccgatt cgaattcgcg 360
ttggccgatt cttagagata aaaaatttct tgacatgttc tatgttttgt gatataatcg 420
tgagataagg gcccaagttc acttaaaaag gagatcaaca atgaaagcaa gcggtatcat 480
caacaggctt acccgtctta ctgtcgggaa ttcgcgttgg ccgattcatt aatggtataa 540
ggttcttgac atcttacaat caatatggta taataattta gttagggccc aagttcactt 600
aaaaaggaga tcaacaatga aagcttactg tcgggaattc gcgttggccg attcattaat 660
ggtataaggt tcttgacatc ttacaatcaa tatggtataa taatttagtt agggcccaag 720
ttcacttaaa aaggagatca acaatgaaag cttactgtcg ggaattcgcg ttggccgatt 780
cattaatggt ataaggttct tgacatctta caatcaatat ggtataataa tttagttagg 840
gcccaagttc acttaaaaag gagatcaaca cttactgtcg ggaattcgcg ttggccaatt 900
aattaatggt ataaggttct tgacatctta caatcaatat tgtataataa tttagttagg 960
gcccaagttc acttaaaaag gagatcaaca atgaaagcaa ttttcgtact gaaacatctt 1020
aatcatgcgt aggatttttt ctatgtacta tttaaaaaac acaaactttt ggatgttcgg 1080
tttattcttt ttcttttact tttttatcat gggagcctac ttcccgtttt tcccgatttg 1140
gctacatgac atcaaccata tcagcaaaag tgatacgggt attatttttg ccgctatttc 1200
tctgttctcg ctattattcc aaccgctgtt tggtctgctt tctgacaaac tcgggctgcg 1260
caaatacctg ctgtggatta ttaccggcat gttagtgatg tttgcgccgt tctttatttt 1320
tatcttcggg ccactgttac aatacaacat tttagtagga tcgattgttg gtggtattta 1380
tctaggcttt tgttttaacg ccggtgcgcc agcagtagag gcatttattg agaaagtcag 1440
ccgtcgcagt aatttcgaat ttggtcgcgc gcggatgttt ggctgtgttg gctgggcgct 1500
gtgtgcctcg attgtcggca tcatgttcac catcaataat cagtttgttt tctggctggg 1560
ctctggctgt gcactcatcc tcgccgtttt actctttttc gccaaaacgg atgcgccctc 1620
ttctgccacg gttgccaatg cggtaggtgc caaccattcg gcatttagcc ttaagctggc 1680
actggaactg ttcagacagc caaaactgtg gtttttgtca ctgtatgtta ttggcgtttc 1740
ctgcacctac gatgtttttg accaacagtt tgctaatttc tttacttcgt tctttgctac 1800
cggtgaacag ggtacgcggg tatttggcta cgtaacgaca atgggcgaat tacttaacgc 1860
ctcgattatg ttctttgcgc cactgatcat taatcgcatc ggtgggaaaa acgccctgct 1920
gctggctggc actattatgt ctgtacgtat tattggctca tcgttcgcca cctcagcgct 1980
ggaagtggtt attctgaaaa cgctgcatat gtttgaagta ccgttcctgc tggtgggctg 2040
ctttaaatat attaccagcc agtttgaagt gcgtttttca gcgacgattt atctggtctg 2100
tttctgcttc tttaagcaac tggcgatgat ttttatgtct gtactggcgg gcaatatgta 2160
tgaaagcatc ggtttccagg gcgcttatct ggtgctgggt ctggtggcgc tgggcttcac 2220
cttaatttcc gtgttcacgc ttagcggccc cggcccgctt tccctgctgc gtcgtcaggt 2280
gaatgaagtc gcttaa 2296
<210> 58
<211> 2210
<212> DNA
<213> Artificial sequence
<220>
<223> Terminator construct
<400> 58
tcgcgttggc cgattcggaa taggacacca tcgaatggtg caaaaccttt cgcggtatgg 60
catgatagcg cccggaagag agtcaattca gggtggtgaa tatgtactat ttaaaaaaca 120
caaacttttg gatgttcggt ttattctttt tcttttactt ttttatcatg ggagcctact 180
tcccgttttt cccgatttgg ctacatgaca tcaaccatat cagcaaaagt gatacgggta 240
ttatttttgc cgctatttct ctgttctcgc tattattcca accgctgttt ggtctgcttt 300
ctgacaaact cgggctgcgc aaatacctgc tgtggattat taccggcatg ttagtgatgt 360
ttgcgccgtt ctttattttt atcttcgggc cactgttaca atacaacatt ttagtaggat 420
cgattgttgg tggtatttat ctaggctttt gttttaacgc cggtgcgcca gcagtagagg 480
catttattga gaaagtcagc cgtcgcagta atttcgaatt tggtcgcgcg cggatgtttg 540
gctgtgttgg ctgggcgctg tgtgcctcga ttgtcggcat catgttcacc atcaataatc 600
agtttgtttt ctggctgggc tctggctgtg cactcatcct cgccgtttta ctctttttcg 660
ccaaaacgga tgcgccctct tctgccacgg ttgccaatgc ggtaggtgcc aaccattcgg 720
catttagcct taagctggca ctggaactgt tcagacagcc aaaactgtgg tttttgtcac 780
tgtatgttat tggcgtttcc tgcacctacg atgtttttga ccaacagttt gctaatttct 840
ttacttcgtt ctttgctacc ggtgaacagg gtacgcgggt atttggctac gtaacgacaa 900
tgggcgaatt acttaacgcc tcgattatgt tctttgcgcc actgatcatt aatcgcatcg 960
gtgggaaaaa cgccctgctg ctggctggca ctattatgtc tgtacgtatt attggctcat 1020
cgttcgccac ctcagcgctg gaagtggtta ttctgaaaac gctgcatatg tttgaagtac 1080
cgttcctgct ggtgggctgc tttaaatata ttaccagcca gtttgaagtg cgtttttcag 1140
cgacgattta tctggtctgt ttctgcttct ttaagcaact ggcgatgatt tttatgtctg 1200
tactggcggg caatatgtat gaaagcatcg gtttccaggg cgcttatctg gtgctgggtc 1260
tggtggcgct gggcttcacc ttaatttccg tgttcacgct tagcggcccc ggcccgcttt 1320
ccctgctgcg tcgtcaggtg aatgaagtcg ctcatcatca ccaccatcat taggatggtg 1380
gtgatgataa tggagaaaaa aatcactgga tataccaccg ttgatatatc ccaatggcat 1440
cgtaaagaac attttgaggc atttcagtca gttgctcaat gtacctataa ccagaccgtt 1500
cagctggata ttacggcctt tttaaagacc gtaaagaaaa ataagcacaa gttttatccg 1560
gcctttattc acattcttgc ccgcctgatg aatgctcatc cggagttccg tatggcaatg 1620
aaagacggtg agctggtgat atgggatagt gttcaccctt gttacaccgt tttccatgag 1680
caaactgaaa cgttttcatc gctctggagt gaataccacg acgatttccg gcagtttcta 1740
cacatatatt cgcaagatgt ggcgtgttac ggtgaaaacc tggcctattt ccctaaaggg 1800
tttattgaga atatgttttt cgtcagcgcc aatccctggg tgagtttcac cagttttgat 1860
ttaaacgtgg ccaatatgga caacttcttc gcccccgttt tcactatggg caaatattat 1920
acgcaaggcg acaaggtgct gatgccgctg gcgattcagg ttcatcatgc cgtttgtgat 1980
ggcttccatg tcggcagaat gcttaatgaa ttacaacagt actgcgatga gtggcagggc 2040
ggggcgtaag gatccaaagg tacctctaga gtcgacctgc aggccttcgt aaatctggcg 2100
agtggggaac tgccagacat caaataaaac aaaaggctca gtcggaagac tgggcctttt 2160
gttttatctg ttgtttgtcg gtgaacactc tcccgtgtag gctggagctg 2210
<---
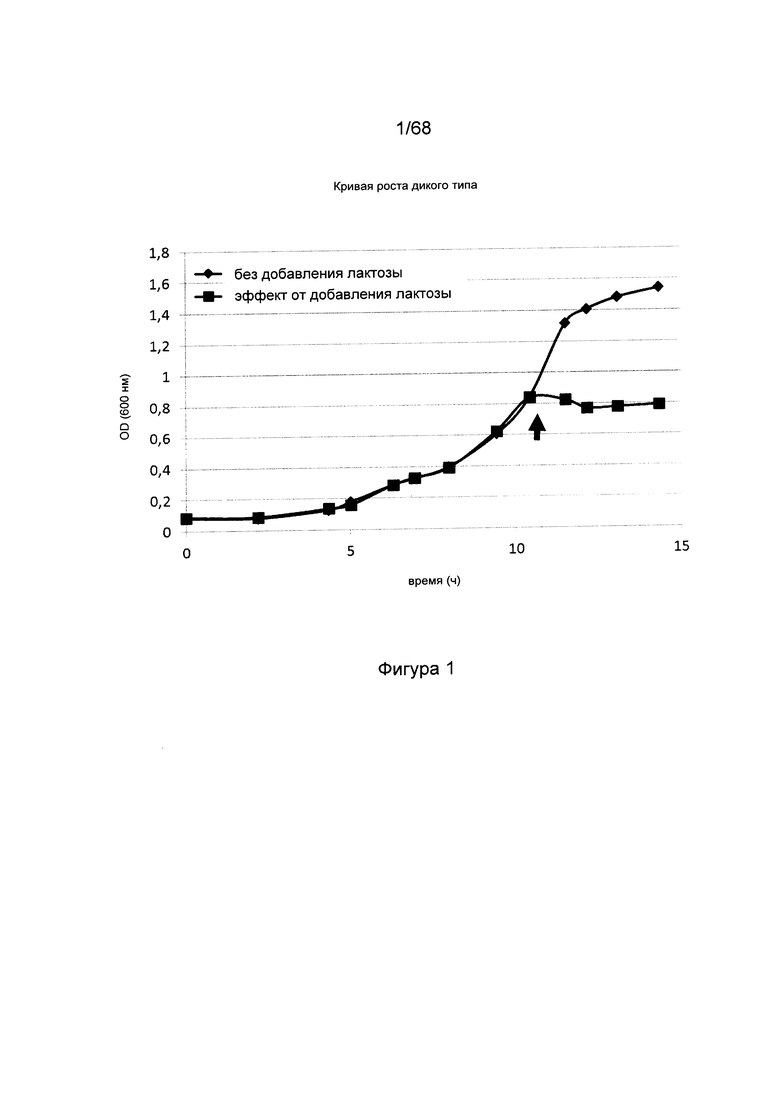
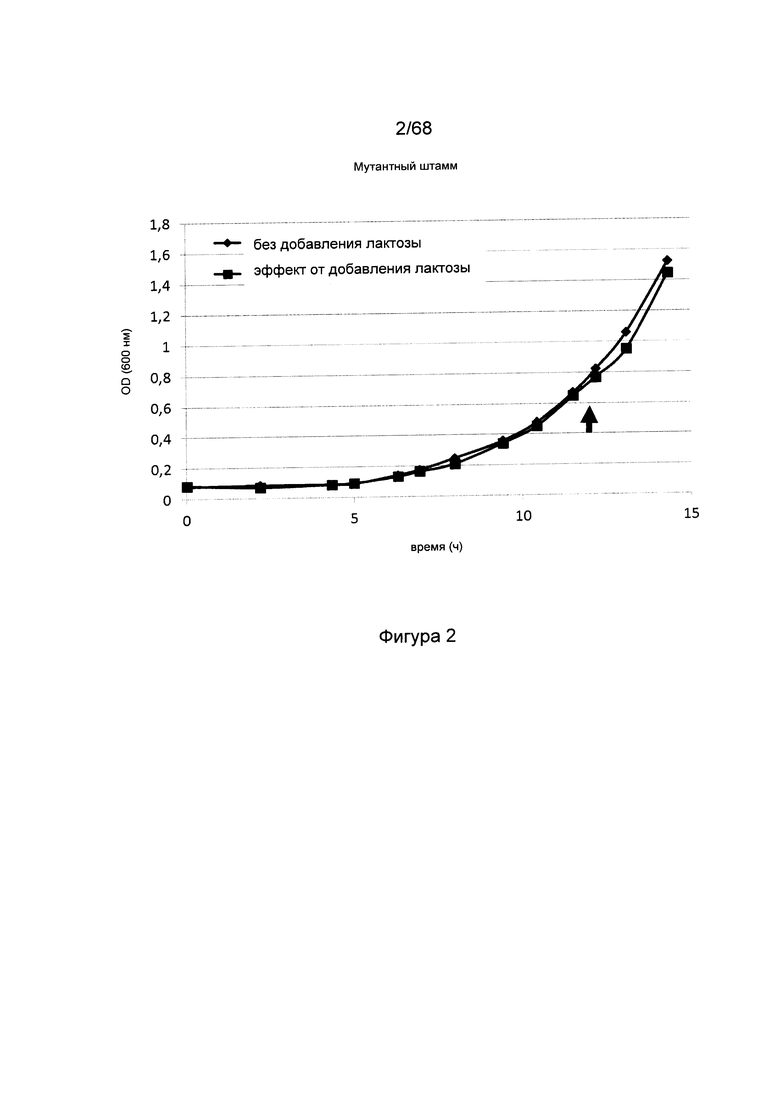






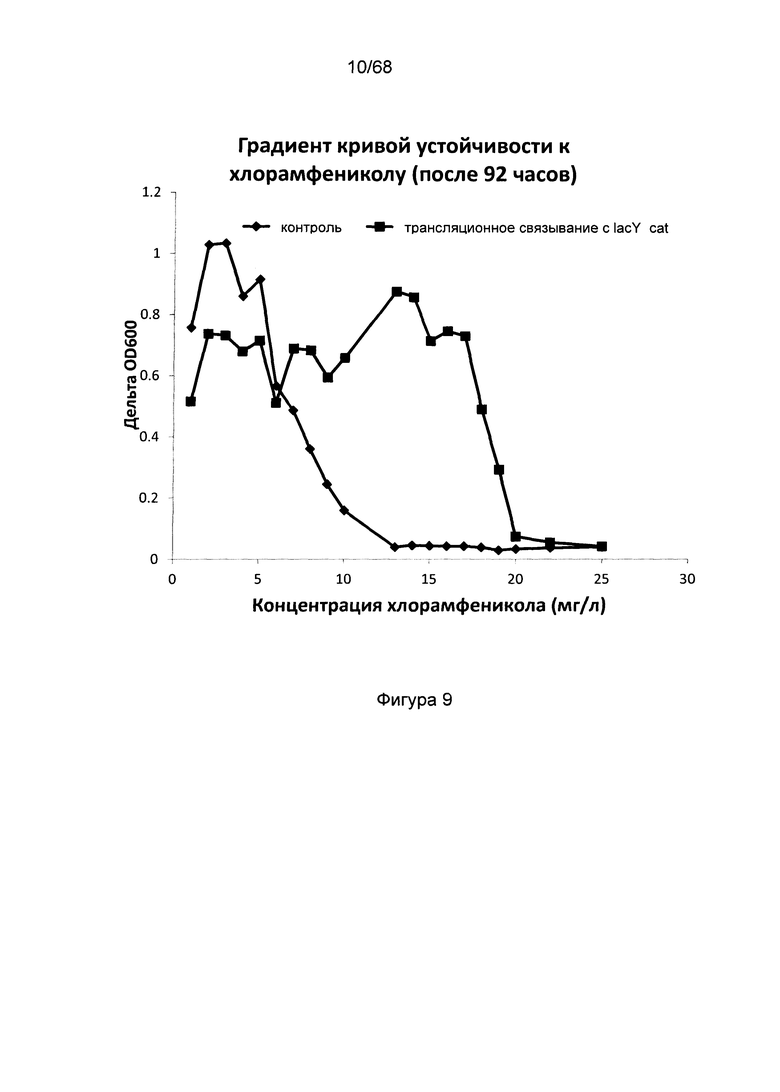


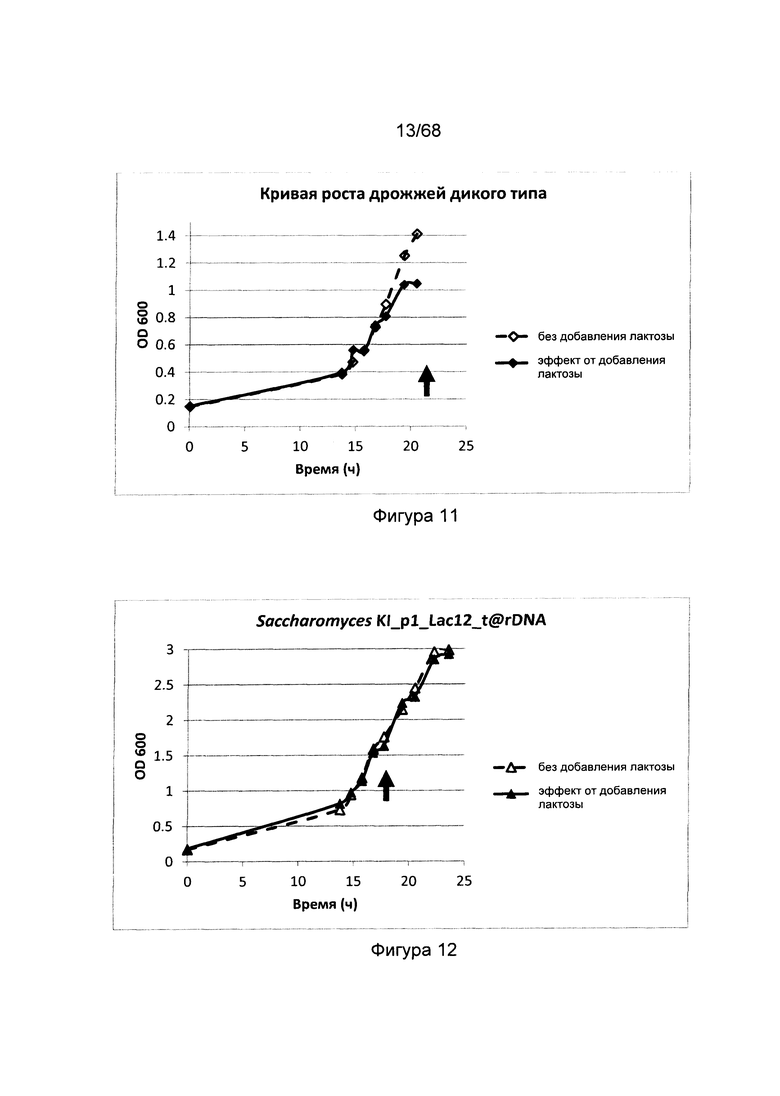






















































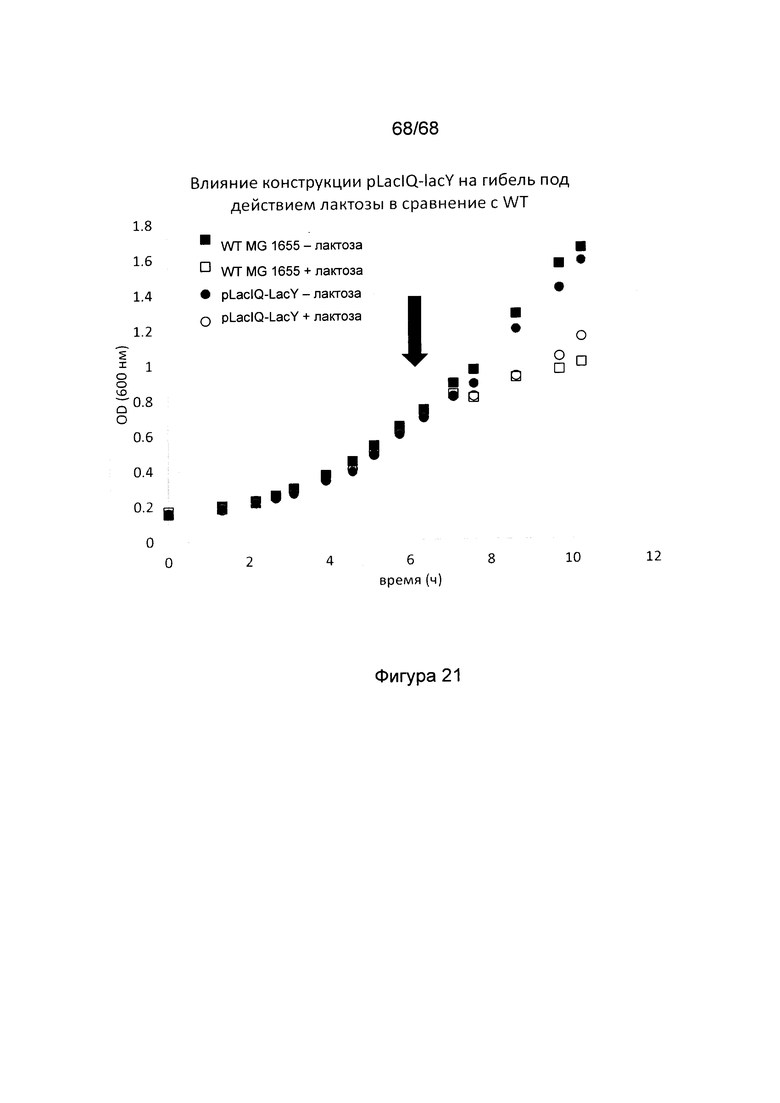
Изобретение относится к способу получения микроорганизмов, устойчивых к явлению подавления действием лактозы, к микроорганизмам, полученным указанным способом. Способ получения микроорганизмов, устойчивых к явлению подавления действием лактозы, выращенных в окружении, в котором лактоза комбинируется с другим источником углерода, включает изменение экспрессии лактозного транспортера в микроорганизмах путем введения гетерологичного промотора перед эндогенным или экзогенным геном лактозного транспортера или путем изменения кодонов эндогенного гена лактозного транспортера на кодоны, используемые микроорганизмом чаще, или на кодоны, используемые микроорганизмом реже, последующее выращивание указанных микроорганизмов на среде, включающей источник углерода, отличный от лактозы, а также добавление лактозы к указанной среде, включающей источник углерода, отличный от лактозы, в процессе роста указанных микроорганизмов и обнаружение экспрессии лактозного транспортера. Осуществляют отбор микроорганизмов, устойчивых к явлению подавления действием лактозы, растущих на указанной среде, включающей лактозу и другой источник углерода, которые сохраняют, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера, на основании обнаруженной экспрессии лактозного транспортера. При этом указанный источник углерода, отличный от лактозы, выбран из группы, состоящей из глицерина, мальтозы, глюкозы, фруктозы, сахарозы, фукозы, маннозы, сиаловой кислоты, крахмала, целлюлозы, полиолов, органических кислот и пентоз. Предложены также варианты микроорганизмов, полученные указанным способом. Предложена также экспрессионная кассета лактозного транспортера, приводящая к экспрессии лактозного транспортера, которая не приводит к фенотипу подавления действием лактозы, которая выделенная из варианта указанного микроорганизма. Указанную экспрессионную кассету и указанные варианты микроорганизмов применяют для производства 2-фукозиллактозы, 2'-фукозиллактозы, 3-фукозиллактозы, 2',3-дифукозиллактозы, лакто-N-триозы, лакто-N-тетраозы, лакто-nN-тетраозы, 3'-сиалиллактозы, 6'-сиалиллактозы, гликолипидов или галактозилированных соединений. Предложен также способ получения экспрессионной кассеты. Изобретение обеспечивает сохранение в полученном микроорганизме, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера, на основании обнаруженной экспрессии лактозного транспортера. 6 н. и 8 з.п. ф-лы, 1 табл., 21 пр., 21 ил.
1. Способ получения микроорганизмов, устойчивых к явлению подавления действием лактозы, выращенных в окружении, в котором лактоза комбинируется с другим источником углерода, где способ включает:
a. изменение экспрессии лактозного транспортера в микроорганизмах путем введения гетерологичного промотора перед эндогенным или экзогенным геном лактозного транспортера или путем изменения кодонов эндогенного гена лактозного транспортера на кодоны, используемые микроорганизмом чаще, или на кодоны, используемые микроорганизмом реже,
b. выращивание указанных микроорганизмов на среде, включающей источник углерода, отличный от лактозы,
c. добавление лактозы к указанной среде, включающей источник углерода, отличный от лактозы, в процессе роста указанных микроорганизмов и
d. обнаружение экспрессии лактозного транспортера, и
e. отбор микроорганизмов, устойчивых к явлению подавления действием лактозы, растущих на указанной среде, включающей лактозу и другой источник углерода, которые сохраняют, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера, на основании обнаруженной экспрессии лактозного транспортера,
причем указанный источник углерода, отличный от лактозы, выбран из группы, состоящей из глицерина, мальтозы, глюкозы, фруктозы, сахарозы, фукозы, маннозы, сиаловой кислоты, крахмала, целлюлозы, полиолов, органических кислот и пентоз.
2. Способ по п. 1, где введение гетерологичного промотора перед эндогенным или экзогенным геном лактозного транспортера осуществляют за счет а) делеции эндогенных лактозных транспортеров из генома и введения их в другой участок в геноме указанного микроорганизма, или b) за счет введения гетерологичного промотора перед эндогенными лактозными транспортерами, или с) за счет нокаута эндогенного лактозного промотора и введения гетерологичного промотора в тот же участок генома указанного микроорганизма.
3. Способ по пп. 1, 2, где указанный экспрессированный лактозный транспортер обнаруживают с помощью трансляционного связывания с репортерным геном и/или через связывание с аптамером.
4. Способ по пп. 1-3, где указанный экспрессированный лактозный транспортер обнаруживают посредством генетических конструкций, приведенных в SEQ ID NO 2, 3, 4 и/или 5.
5. Способ по пп. 1, 2, где указанный экспрессированный лактозный транспортер обнаруживают путем измерения скорости роста мутированных микроорганизмов.
6. Способ по пп. 1, 2, где указанный экспрессированный лактозный транспортер обнаруживают путем измерения скорости роста мутированных микроорганизмов на среде, включающей лактозу в качестве единственного источника углерода.
7. Способ по пп. 1-6, где указанный лактозный транспортер представляет собой лактозную пермеазу.
8. Способ по пп. 1-7, где указанный микроорганизм представляет собой бактериальную, дрожжевую или грибную клетку.
9. Микроорганизм, устойчивый к явлению подавления действием лактозы, выращенный в окружении, в котором лактоза комбинируется с другим (другими) источником (источниками) углерода, выбранным(и) из группы, состоящей из глицерина, мальтозы, глюкозы, фруктозы, сахарозы, фукозы, маннозы, сиаловой кислоты, крахмала, целлюлозы, полиолов, органических кислот и пентоз, причем указанный микроорганизм получают способом по пп. 1-8, и причем указанный микроорганизм содержит гетерологичный промотор перед эндогенным или экзогенным геном лактозного транспортера или эндогенный ген лактозного транспортера, в котором кодоны изменены на кодоны, используемые микроорганизмом чаще, или на кодоны, используемые микроорганизмом реже.
10. Микроорганизм, устойчивый к явлению подавления действием лактозы, выращенный в окружении, в котором лактоза комбинируется с другим (другими) источником (источниками) углерода, выбранным(и) из группы, состоящей из глицерина, мальтозы, глюкозы, фруктозы, сахарозы, фукозы, маннозы, сиаловой кислоты, крахмала, целлюлозы, полиолов, органических кислот и пентоз, содержащий экспрессионную кассету лактозного транспортера, содержащую последовательность, приведенную в SEQ ID NO 1, 7, 8, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56 или 57, причем указанный микроорганизм получают способом по пп. 1-8.
11. Микроорганизм по пп. 9, 10, в котором гены, кодирующие ферменты из путей деградации лактозы и/или галактозы, являются менее функциональными по сравнению с функциональным геном дикого типа или нефункциональными.
12. Экспрессионная кассета лактозного транспортера, приводящая к экспрессии лактозного транспортера и которая не приводит к фенотипу подавления действием лактозы, причем указанную экспрессионную кассету лактозного транспортера получают путем выделения из микроорганизма по п. 10, и где указанная экспрессионная кассета содержит последовательность, приведенную в SEQ ID NO 1, 7, 8, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36, 37, 38, 39, 40, 41, 42, 43, 44, 45, 46, 47, 48, 49, 50, 51, 52, 53, 54, 55, 56 или 57.
13. Применение микроорганизма по любому из пп. 9-11 или экспрессионной кассеты лактозного транспортера по п. 12 для производства 2-фукозиллактозы, 2'-фукозиллактозы, 3-фукозиллактозы, 2',3-дифукозиллактозы, лакто-N-триозы, лакто-N-тетраозы, лакто-nN-тетраозы, 3'-сиалиллактозы, 6'-сиалиллактозы, гликолипидов или галактозилированных соединений.
14. Способ получения экспрессионной кассеты лактозного транспортера, которая не приводит к фенотипу подавления действием лактозы, включающий:
- создание мутантов экспрессионной кассеты лактозного транспортера путем введения гетерологичного промотора перед геном лактозного транспортера или путем изменения кодонов гена лактозного транспортера на кодоны, используемые микроорганизмом чаще, или на кодоны, используемые микроорганизмом реже, причем указанные мутанты демонстрируют измененную экспрессию гена лактозного транспортера по сравнению с экспрессией соответствующего гена лактозного транспортера дикого типа;
- скрининг мутантных экспрессионных кассет на наличие экспрессионных кассет, которые обеспечивают экспрессию лактозного транспортера в микроорганизме, трансформированном указанной экспрессионной кассетой;
- скрининг мутантных экспрессионных кассет, которые обеспечивают экспрессию лактозного транспортера на наличие экспрессионных кассет, которые не приводят к подавлению действием лактозы в микроорганизме, трансформированном указанной экспрессионной кассетой путем выращивания микроорганизмов, трансформированных указанными экспрессионными кассетами в среде, включающей источник углерода, отличный от лактозы, и добавления лактозы во время середины экспоненциальной фазы, причем указанный источник углерода, отличный от лактозы, выбран из группы, состоящей из глицерина, мальтозы, глюкозы, фруктозы, сахарозы, фукозы, маннозы, сиаловой кислоты, крахмала, целлюлозы, полиолов, органических кислот и пентоз; и
- выделение указанной экспрессионной кассеты из указанных трансформированных микроорганизмов, которые (i) устойчивы к явлению подавления действием лактозы и которые (ii) сохраняют, по меньшей мере, 50% от уровня транспорта лактозы в клетку, достигаемого с экспрессионной кассетой дикого типа указанного лактозного транспортера.
| EAMES М | |||
| ET AL., Cost-Benefit Tradeoffs in Engineered lac Operons, Science 336, 911-915 (2012) | |||
| Найдено онлайн: https://science.sciencemag.org/content/336/6083/911/tab-pdf Supplementary Materials | |||
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| LODI T ET AL., | |||
Авторы
Даты
2021-04-13—Публикация
2015-11-12—Подача