Область техники, к которой относится изобретение
Изобретение относится к медицине, ветеринарной медицине, предназначено для терапии внутрибрюшинных инфекционных процессов с целью применения оптимальной схемы лечения патологий бактериального генеза.
Уровень техники
Известен способ лечения послеоперационных инфекционных процессов, в частности абсцессов брюшной полости, включающий общепринятую медикаментозную терапию, отличающийся тем, что больному в первые один-два дня после операции в курс лечения дополнительно назначают химопсин, который вводят местно 2-3 раза в дневное время суток в концентрации 0,5-1,0 мг на 1 мл 10%-ного раствора натрия хлорида с экспозицией 1,5-2 ч в количестве от 1/4 до 1/3 объема удаленного из полости абсцесса гноя, после чего в курс лечения/ включают бактериофаг, который при суточной дозе не более 200 мл вводят местно 2 раза в дневное время суток с экспозицией 1,5-2 ч в количестве от 1/10 до 1/5 объема удаленного из полости абсцесса гноя, вид бактериофага выбирают в соответствии с результатами бактериологического исследования содержимого полости абсцесса, курс лечения составляет 6-9 дней (см. патент RU 2243780).
Рассмотренный способ требует индивидуального подхода (расчет объема удаленного гноя, выбора бактериофага) и значительных материальных затрат.
Применение транскутанного облучения инфицированных животных в области передней брюшной стенки аппаратом АЛТ «Узор» через 3 и 6 часов после заражения изменяло цитокиновый статус экспериментальных животных в динамике модельного инфекционного процесса. Отмечено снижение гиперпродукции ИЛ-1 и ФНО-α, наиболее выраженное при стафилококковой инфекции. Интересен факт определения через 6 и 12 часов после транскутанного облучения в сыворотке крови инфицированных мышей ИФН-γ и ИЛ-8 в небольших концентрациях (в сыворотках крови животных из контрольных групп он не обнаруживался). Макрофаги, выделенные из перитонеального экссудата мышей через 1 и 6 часов после облучения, имели необычную морфологию - были крупные, раздутые, деформированные. В то же время процессы адгезии и внутриклеточного киллинга ими бактерий проходили активно, (см. Применение низкоинтенсивного лазерного излучения для коррекции цитокинового баланса и активности фагоцитоза возбудителей внутрибольничных инфекций (экспериментальное обоснование на модели лабораторных животных) / Водянова, Татьяна Викторовна // диссертация на соиск. канд. мед. наук. - Саратов, 2007. - с. 145).
Рассмотренный способ характеризуется следующими недостатками: проводится только патогенетическая терапия, без воздействия на причину возникновения инфекции; применение низкоинтенсивного лазерного излучения, особенно в ветеринарной медицине, экономически неоправданно.
Способ лечения инфекции, вызываемой штаммами рода Staphylococcus, Streptococcus или Enterococcus с множественной лекарственной устойчивостью, отличающийся тем, что лечение проводят лантоцином, выбранным из группы: низин, субтилин, эпидермин, галлидермин, рер-5, причем указанный лантоцин вводят в количестве, превышающем его минимальную ингибирующую концентрацию. В качестве лантоцина выбирают низин, который вводят в количестве, равном дозе приблизительно 2-200 мг/кг/сутки (см. патент RU 2202360).
Рассмотренный способ имеет ряд существенных недостатков: широкий терапевтический диапазон лантоцина; низин, как было обнаружено исследователями ранее, является недостаточно действенным для терапевтического применения в медицине и ветеринарии. Актагардин и мерсацидин являются более современными лантионинсодержащими антимикробными пептидами, но обладают только умеренной активностью в отношении стафилококков и энтерококков по сравнению с используемыми в настоящее время терапевтическими агентами.
Известен способ лечения инфекции Staphylococcus epidermidis с помощью внутрибрюшинного введения даптомицина, пациенту на перитонеальном диализе. После первоначального внутривенного введения даптомицина в дозе 9 мг/кг массы тела каждые 48 часов, поменяли на внутрибрюшинное введение 5,3 мг/кг массы тела каждые 48 часов. Терапевтический лекарственный мониторинг проводили через 4 часа и 24 часа после введения дозы. Из-за высокой пиковой концентрации доза была снижена до конечной поддерживающей дозы 3,2 мг/кг массы тела. Данные свидетельствуют о том, что концентрация препарата в сыворотке крови выше минимальной ингибирующей концентрации, может быть достигнута при внутрибрюшинном введении даптомицина каждые 48 часов (см. Successful Treatment of a Pacemaker Infection with Intraperitoneal Daptomycin / Anne В Taegtmeyer, Nina Kononowa, Dominique Fasel, Manuel Haschke, Felix Burkhalter // Peritoneal dialysis international: journal of the International Society for Peritoneal Dialysis Jan-Feb 2016; 36(1):114-7. doi: 10.3747/pdi.2014.00271.).
Рассмотренный способ имеет ряд существенных недостатков: обязательным является измерение концентрации препарата в сыворотке крови и коррекция дозы.
Наиболее близким изобретением к описываемому способу по технической сущности является способ лечения, смоделированного перитониального процесса, который заключается в введении зараженным крысам диализирующего раствора (смесь: гемодез + 0,9% раствор NaCl + 40% раствор глюкозы) с добавлением амоксиклава (40 мг/кг). При этом диализирующий раствор в брюшную полость вводили каждые 8 часов через дренажную систему, которую подшивали к вентральной брюшной стенке. Раствор в брюшной полости оставляли на 15 минут, а затем удаляли путем аспирации шприцем (см. Динамика морфофункциональных показателей и разработка оперативного лечения при перитоните у мелких домашних животных / Слинько Вадим Владимирович // автореферат на соиск. канд. биол. наук. - Ставрополь, 2006. - с. 24).
Рассмотренный способ имеет ряд недостатков, основными из которых является частота и способ введения препаратов, сложность проведения терапевтических манипуляций, в связи с этим возможность рецидивов или осложнений, длительность лечения.
Раскрытие изобретения
Задачей изобретения являлась разработка способа лечения интраперитонеального стафилококкового инфекционного процесса ниосомальным офлоксацином, который позволяет быстро создать необходимую концентрацию антибактериального препарата в брюшной полости лабораторных животных, за счет более реактивного подавления патогенной микрофлоры повысить эффективность терапии внутрибрюшинных инфекционных процессов, а это приводит к сокращению длительности курса антибиотикотерапии, что в свою очередь способствует клиническому выздоровлению животных и позволяет снизить временные и финансовые затраты.
Технический результат, который может быть достигнут с помощью предложенного способа, сводится к сокращению времени достижения терапевтической концентрации антибактериального препарата в брюшной полости параллельно с временем достижения таковой в сыворотке крови, сокращению длительности системного воздействия антибактериальных средств на организм и снижению вероятности возникновения рецидивов.
Технический результат достигается с помощью способа лечения интраперитонеального стафилококкового инфекционного процесса ниосомальным офлоксацином, в котором производят введение антибактериального препарата, при этом антибактериальный препарат вводят подкожно два раза в сутки и в качестве антибактериального препарата используют ниосомальный офлоксацин в дозе 2 мл/кг.
Сущность способа лечения интраперитонеального стафилококкового инфекционного процесса ниосомальным офлоксацином, включающий введение антибактериального препарата, при этом антибактериальный препарат вводят подкожно два раза в сутки и в качестве антибактериального препарата используют ниосомальный офлоксацин в дозе 2 мл/кг.
Краткое описание чертежей и их материалов
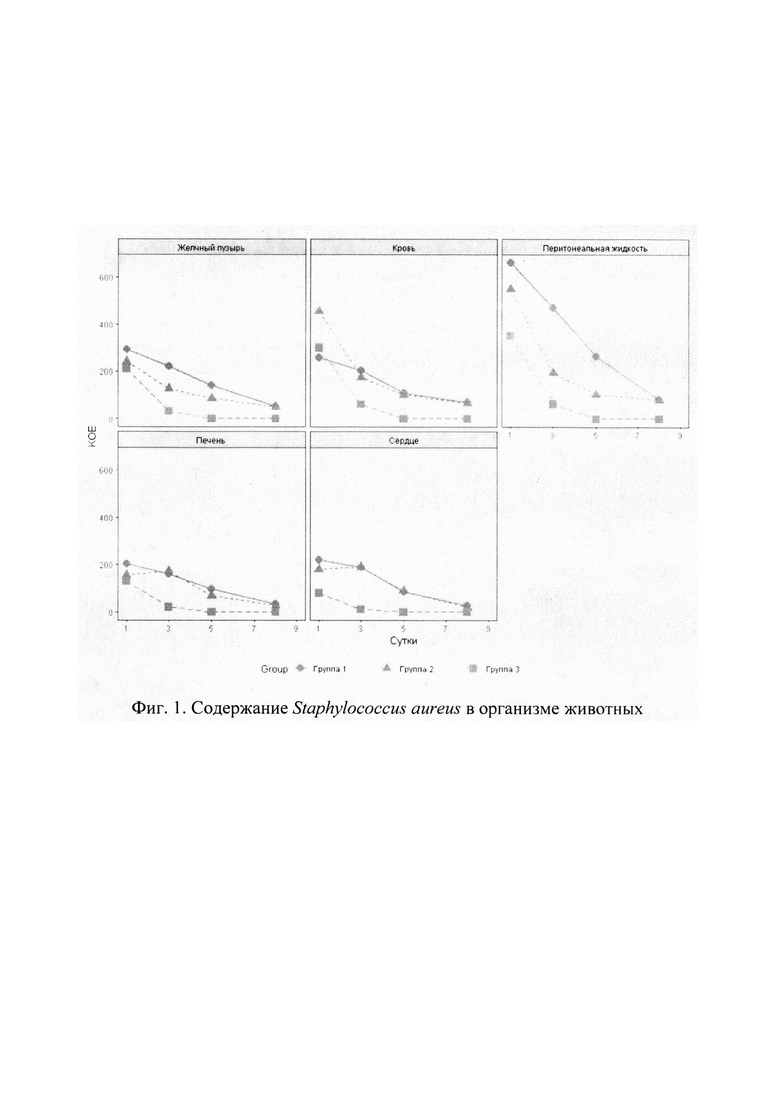
На фиг. 1 дан способ лечения интраперитонеального стафилококкового инфекционного процесса ниосомальным офлоксацином, содержание Staphylococcus aureus в организме животных.
Осуществление изобретения
Эксперименты на животных проводили согласно правилам, принятым Директивой 2010/63/eu Европейского парламента и Совета Европейского Союза от 22 сентября 2010 года, по охране животных, используемых в научных целях (DIRECTIVE 2010/63/EU OF THE EUROPEAN PARLIAMENT AND OF THE COUNCIL on the protection of animals used for scientific purposes. 22 September 2010), Европейской Конвенции по защите позвоночных животных, используемых для экспериментальных и иных научных целей (European Convention for the Protection of Vertebrate Animals Used for Experimental and other Scientific Purposes (ETS 123). Strasbourg, 1986) и приказу МЗ СССР №755 от 12.08.1977.
Объектом исследования служили беспородные кролики, с экспериментально смоделированным инфекционным процессом, вызванным стафилококком (патент 2723745).
Проводился подсчет количества высеваемых колоний из перитонеальной жидкости, желчного пузыря, крови, печени, сердца при моделировании интраперитонеального стафилококкового инфекционного процесса.
Микробиологическое исследование проводили в первый, третий, пятый и восьмой дни патологического процесса. Для разведений смывов использовали стерильный 0,9% физиологический раствор. Затем готовили стерильными пипетками возрастающие десятикратные разведения от 10-1 до 10-7. Из разведений 10-7 и 10-6 проводили высев на поверхность МПА в чашки Петри. Каждое разведение высевали на две чашки с МПА и инкубировали при температуре 37-38°С в течение 18-20 часов, при этом чашки переворачивали дном вверх. По истечении срока культивирования подсчитывали колонии.
При определении чувствительности культуры Staphylococcus aureus к офлоксацину аптечному и инкапсулированному в ниосомы выявлена задержка роста от 1 до 1,5 см.
Лечение лабораторных животных, у которых смоделирован интраперитонеальный стафилококковый инфекционный процесс проводили офлоксацином, лекарственная форма: раствор для инфузий (в растворе натрия хлорида 0,9%); производитель ОАО «Акционерное Курганское общество медицинских препаратов и изделий Синтез», а также ниосомальной формой офлоксацина (патент 2583135) синтезированного в лаборатории биохимии ФКУЗ «Ставропольского научно-исследовательского противочумного института. Эффективность включения офлоксацина в ниосомы составила 76,1%.
Примеры конкретного выполнения способа лечения интраперитонеального стафилококкового инфекционного процесса ниосомальным офлоксацином.
Пример №1
Оценку терапевтической эффективности проводят на кроликах с интраперитонеальным инфекционным процессом. Терапию животных начинали одномоментно, спустя 24 часа после введения взвеси, при условии клинического проявления заболевания. Клинические признаки регистрировали у всех животных. Применяют подкожно аптечный офлоксацин, в дозе 3 мл/кг массы животного, вводят 3 раза в сутки.
К окончанию эксперимента у 2 животных при осмотре брюшной стенки обнаружены свищи, из которых вытекает гной при надавливании.
Пример №2
Выполняется аналогично примеру 1, но применяют подкожно ниосомальный офлоксацин, в дозе 1 мл/кг массы животного, вводят 3 раза в сутки.
При подсчете высеваемых колоний из печени, желчного пузыря, крови, сердца и перитонеальной жидкости инфицированных животных наблюдалось значительное уменьшение данного показателя к 8 суткам терапии (фиг. 1).
Падеж не регистрировался при введении Staphylococcus aureus кроликам и при последующем лечении.
Пример №3
Выполняется аналогично примеру 1, но применяют подкожно ниосомальный офлоксацин, в дозе 2 мл/кг массы животного, вводят 2 раза в сутки.
На протяжении всего эксперимента гибель животных отсутствовала. К 5 суткам после начала лечения клиническое выздоровление наступало у всех кроликов, что выражалось нормализацией общего состояния животных. Такие показатели как температура тела, частота пульса и дыхания в пределах физиологической нормы. К завершению исследования рост микробных клеток отсутствовал во всех органах и биологических жидкостях, что свидетельствует о высокой лечебной эффективности офлоксацина, инкапсулированного в ниосомы.
Таким образом, оптимальным является пример 3. Рассмотренный способ прост в исполнении, позволяет быстро создать необходимую концентрацию офлоксацина в организме лабораторных животных, что способствует высокой эффективности терапии интраперитонеального стафилококкового инфекционного процесса. Это позволяет сократить длительность курса антибиотикотерапии, его токсическое воздействие на организм и снизить риск вероятности возникновения осложнений и рецидивов.
Предлагаемое изобретение по сравнению с прототипом и другими известными техническими решениями имеет следующие преимущества: сокращена частота введения препарата, длительность лечения, отсутствует сложность проведения терапевтических манипуляций.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ моделирования интраперитонеального стафилококкового инфекционного процесса | 2019 |
|
RU2723745C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИИ, ВЫЗЫВАЕМОЙ ШТАММАМИ РОДА STAPHYLOCOCCUS, STREPTOCOCCUS ИЛИ ENTEROCOCCUS С МНОЖЕСТВЕННОЙ ЛЕКАРСТВЕННОЙ УСТОЙЧИВОСТЬЮ | 1996 |
|
RU2202360C2 |
| Способ моделирования внутрибрюшного синегнойного инфекционного процесса | 2019 |
|
RU2725136C1 |
| СПОСОБ ЛЕЧЕНИЯ СТАФИЛОКОККОВЫХ ИНФЕКЦИЙ У МЛЕКОПИТАЮЩЕГО (ВАРИАНТЫ) | 1998 |
|
RU2234940C2 |
| СПОСОБ МОДЕЛИРОВАНИЯ МОЛНИЕНОСНОГО СЕПСИСА, ВЫЗВАННОГО МИКСТИНФЕКЦИЕЙ НА ФОНЕ ОЖОГОВОЙ ТРАВМЫ | 2012 |
|
RU2507601C1 |
| НОВОЕ ПОЛУСИНТЕТИЧЕСКОЕ ПРОИЗВОДНОЕ ЭРЕМОМИЦИНА И ЕГО ПРИМЕНЕНИЕ | 2016 |
|
RU2641912C1 |
| Способ диагностики стафилококковой абдоминальной хирургической инфекции | 2019 |
|
RU2705415C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ ЗАБОЛЕВАНИЙ ТЕЛЯТ | 1992 |
|
RU2045281C1 |
| СПОСОБ КОРРЕКЦИИ ЭНДОТЕЛИАЛЬНОЙ ДИСФУНКЦИИ АЗИТРОМИЦИНОМ ПРИ МОДЕЛИРОВАНИИ ХРОНИЧЕСКОГО ГРАМПОЛОЖИТЕЛЬНОГО СЕПСИСА | 2009 |
|
RU2400826C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СОПРОВОЖДАЮЩИХСЯ ИЗМЕНЕНИЯМИ КАЧЕСТВЕННОГО И/ИЛИ КОЛИЧЕСТВЕННОГО СОСТАВА ВНЕКЛЕТОЧНОЙ ДНК КРОВИ (ВАРИАНТЫ) | 2004 |
|
RU2267329C2 |
Изобретение относится к области медицины, а именно к ветеринарной медицине, и предназначено для терапии внутрибрюшинных инфекционных процессов с целью применения оптимальной схемы лечения патологий бактериального генеза. Для лечения интраперитонеального стафилококкового инфекционного процесса у кроликов вводят антибактериальный препарат. При этом антибактериальный препарат вводят подкожно два раза в сутки и в качестве антибактериального препарата используют ниосомальный офлоксацин в дозе 2 мл/кг. Использование изобретения позволяет сократить частоту введения препарата, длительность лечения, обеспечивает простоту проведения терапевтических манипуляций. 3 пр., 1 ил.
Способ лечения интраперитонеального стафилококкового инфекционного процесса ниосомальным офлоксацином у кроликов, включающий введение антибактериального препарата, причем антибактериальный препарат вводят подкожно два раза в сутки и в качестве антибактериального препарата используют ниосомальный офлоксацин в дозе 2 мл/кг.
| СЛИНЬКО В.В | |||
| Динамика морфофункциональных показателей и разработка оперативного лечения при перитоните у мелких домашних животных | |||
| Автореферат | |||
| канд | |||
| биол | |||
| наук, 2006, Ставрополь, с | |||
| Пишущая машина для тюркско-арабского шрифта | 1922 |
|
SU24A1 |
| СОСТАВ ОФЛОКСАЦИНА ДЛЯ ИНЪЕКЦИЙ | 2003 |
|
RU2245134C1 |
| СВЕТЛАКОВА Е.В | |||
| и др | |||
| Определение чувствительности Staphylococcus aureus к аптечной и ниосомальной формам офлоксацина | |||
| Фундаментальные | |||
Авторы
Даты
2021-06-09—Публикация
2020-10-29—Подача