Изобретение относится к новым биологически активным соединениям - комплексным соединениям меди(II) на основе арилметиленбиспиран-2-онов, обладающим цитотоксическим действием, в частности - способностью подавлять метаболическую активность клеточной линии карциномы шейки матки человека (HeLa), которые могут найти применение в медицинской практике для лечения раковых заболеваний.
Известны комплексные соединения, проявляющие цитотоксическую активность по отношению к различным видам опухолевых клеток.
К таким соединениям относится известный препарат цисплатин, а также бензаннелированные аналоги 2H-пиран-2-онов - 2Н(4H)-хромен-2-оны, и комплексы на их основе (см. патент США № 5858780, по кл. МПК C12N 5/22, опубл. 12.01.1999).
Недостатками цисплатина и его производных (см. J. Oncology&Hematology, 2007, 20) является наличие нежелательных побочных эффектов при применении in vivo, таких как анемия, нейротоксичность и нефротоксичность, а также наличие лекарственной устойчивости.
Известны комплексные соединения цинка(II), меди(II), никеля(II), кобальта(II) на основе 4H-хромен-2-онов, обладающие цитотоксическими свойствами и низкой токсичностью по сравнению с цисплатином (LD50 13,5 мг/кг) (см. Saif M. at al. Synthesis, characterization, and antioxidant/cytotoxic activity of new chromone Schiff base nano-complexes of Zn(II), Cu(II), Ni(II) and Co(II) // J. Molecular Structure. - 2016. - Т. 1118. - С. 75-82.). Цитотоксические эффекты данных комплексов были проверены in vitro на клеточных линиях асцитной карциномы Эрлиха (EAC), выделенных из асцитной жидкости самок швейцарских мышей-альбиносов. Наиболее эффективным оказался комплекс меди(II) со значениями IC50 равным 4,76 мкг/мл.

В отношении клеток аденокарциномы легкого (клетки LA795) немелкоклеточного рака легкого была испытана противоопухолевая активность комплекса меди(II), на основе производного 2H-хромен-2-она и фенантролина in vitro и in vivo (см. Zhu T. at al. Antitumor effect of a copper (II) complex of a coumarin derivative and phenanthroline on lung adenocarcinoma cells and the mechanism of action // Molecular medicine reports. - 2014. - Т. 10. - №5. - С. 2477-2482).
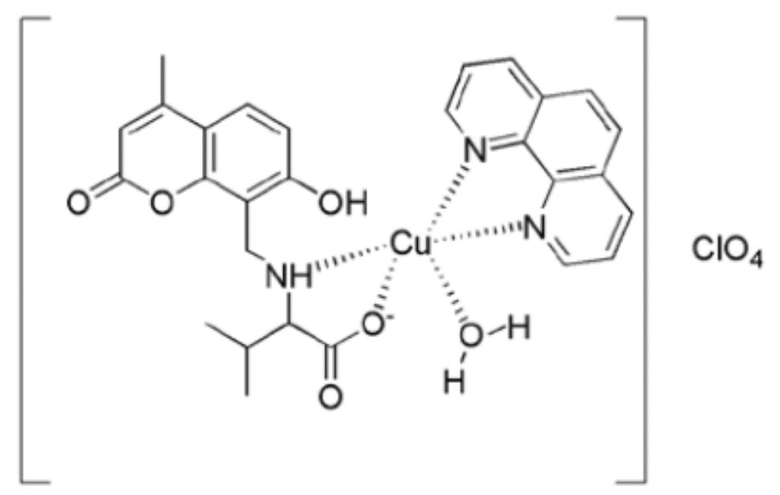
Обнаружено, что комплекс ингибирует пролиферацию клеток аденокарциномы легкого LA795 в зависимости от концентрации и времени. Полумаксимальная ингибирующая концентрация комплекса после 48 и 72-часовой обработки составляла 2,5 мкмоль/л.
Известны также комплексы Cu(II) и Ni(II) (E)-N'-(2-гидроксибензилиден)-3-оксо-3H-бензо[f]хромен-2-карбоксигидразида с формулой:
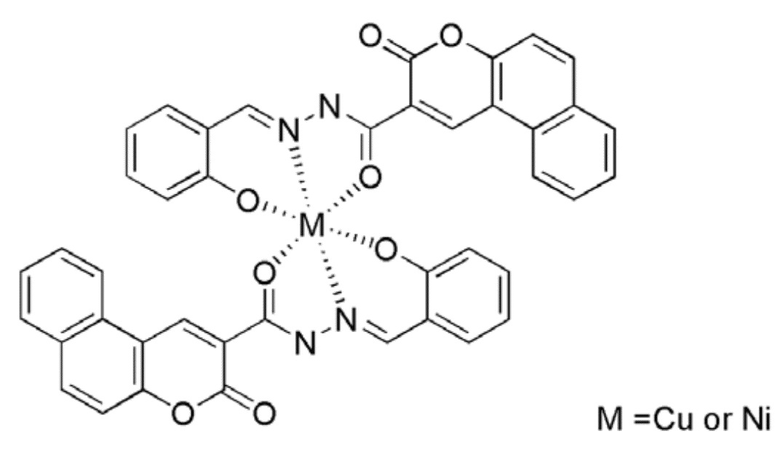
где М=Cu, Ni.
обладающие выраженными цитотоксическими свойствами, которые были исследованы в отношении клеточных линий HepG2 (гепатоцеллярная карцинома человека), HL60 (промиелоцинтарная лейкемия) и PC3 (предстательная железа) (см. Zhu T. at al. Anticancer activity and DNA-binding investigations of the Cu(II) and Ni(II) complexes with Coumarin Derivative // Chem Biol Drug Des. - 2015. - Т.85. - №3. - С. 385-393).
Наиболее близким по назначению к предлагаемому изобретению относится комплексное соединение палладия(II) с формулой
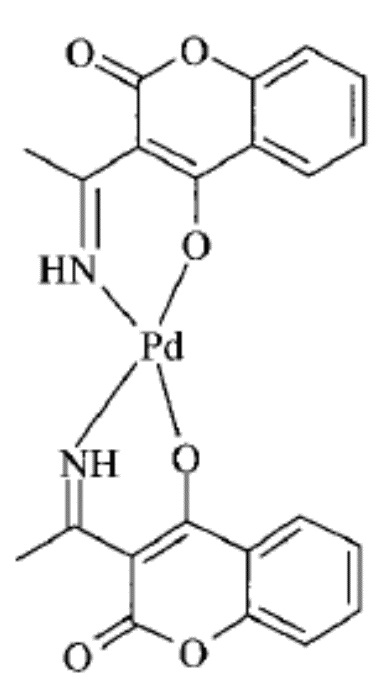
обладающее цитотоксической активностью в отношении клеток А549 (карцинома легкого), HeLa (карцинома шейки матки человека) и К562 (миелогенная лейкемия) (см. Budzisz E. et al, Synthesis, crystal structure and biological characterization of a novel palladium(II) complex with a coumarin-derived ligand // European Journal of Inorganic Chemistry. – 2004. - T. 22. - C. 4412-4419). Значения IC50 0,0097, 0,0078 и 0,0078 мкМ, соответственно, превосходят значения препарата сравнения карбоплатина (105,98, 73,49 и 60,92 мкМ).
Изобретение направлено на решение проблемы расширения арсенала средств, обладающих цитотоксическим действием, которые могут быть использованы в качестве активных компонентов противоопухолевых лекарственных средств.
Заявляемая проблема решается тем, что комплексные соединения меди(II) на основе арилметиленбиспиран-2-онов, обладающие цитотоксической активностью, представляют собой соединения формулы:

где при n = 4 R=H (1) или R=3-NO2 (2) или при n = 3 R= 4-OCH3 (3)
Заявляемые соединения меди(II) на основе арилметиленбиспиран-2-онов синтезированы впервые с использованием термической активации (кипячение на колбонагревателе при температуре 78°С) с хорошими выходами 51-66% за 1,5-2,5 часа, что определяет технологичность их получения.

При этом, соединение № 1 - комплекс меди(II) 3,3'-(фенилметилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) синтезирован одностадийным методом в результате двухкомпонентной реакции 3,3'-(фенилметилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) и моногидрата ацетата меди(II) в этаноле при термической активации.

Соединение № 2 - комплекс меди(II) 3,3'-((3-нитрофенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) синтезирован одностадийным методом в результате двухкомпонентной реакции 3,3'-((3-нитрофенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) и моногидрата ацетата меди(II) в этаноле при термической активации.

Соединение № 3 - комплекс меди(II) 3,3'-((4-метоксифенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) синтезирован одностадийным методом в результате двухкомпонентной реакции 3,3'-((4-метоксифенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) и моногидрата ацетата меди(II) в этаноле при термической активации.

Состав полученных комплексных соединений и их строение подтверждены данными элементного анализа, ЯМР 1Н, 13С, ИК, УФ - спектроскопии, дифференциально-термического анализа.
Изобретение иллюстрируется чертежами, где представлены графики метаболической активности клеточной линии HELA при воздействии на неё заявляемых соединений, при этом:
- на фиг. 1 представлен график метаболической активности при воздействии на неё соединения № 1;
- на фиг. 2 представлен график метаболической активности при воздействии на неё соединения № 2;
- на фиг. 3 представлен график метаболической активности при воздействии на неё соединения № 3.
Получение новых комплексных соединений и испытание их цитотоксической активности иллюстрируется следующими примерами.
Пример 1. Синтез комплекса меди(II) 3,3'-(фенилметилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) (1)
В круглодонную колбу объемом 50 мл, снабженную обратным холодильником, помещают 0,5 г (1 ммоль) 3,3'-(фенилметилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) в 10 мл этанола, нагревают до 50°С и приливают нагретый до 50°С раствор 0,26 г (1 ммоль) моногидрата ацетата меди(II) в 22 мл этанола. Кипятят смесь в течение 2 часов. По окончании реакции смесь упаривают на воздухе, образовавшиеся зеленые кристаллы промывают водой, этанолом, сушат. Получают 0.61 г (66%) комплекса меди(II) 3,3'-(фенилметилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) (1) Т.пл. 184-186°С. Спектр ЯМР 1Н (ацетон-d6), δ, м.д.: 2.22 (с 3Н, СН3) 2.34 (уш. с 9Н, СН3), 4.04 (уш. с 2Н, H2O), 5.67 (уш. с 2Н, СНметин), 6.27 (уш. с 4Н, =СН), 6.89-7.93 (м 10Н, CHAr.), 10.06 (с 2Н, ОН). Найдено, %: С 56.96, Н 4.19. CuC38H38O16. Вычислено, %: С 56.69, Н 4.23.
Пример 2. Синтез комплекса меди(II) 3,3'-((3-нитрофенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) (2)
Аналогично методике синтеза в примере 1 к 0.5 г (1 ммоль) 3,3'-((3-нитрофенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) добавляют 0.26 г (1 ммоль) моногидрата ацетата меди(II). Получают 0.50 г (51%) комплекса меди(II) 3,3'-((3-нитрофенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) (2). Время реакции составляет 1.5 часа. Т.пл. 199-200°С. Спектр ЯМР 1Н (ацетон-d6), δ, м.д.: 2.21, 2.26, 2.34, 2.40 (с 3Н, СН3), 4.04 (уш. с 2Н, H2O), 5.73 (уш. с 2Н, СН), 6.27 (уш. с 4Н, =СН), 7.45-8.74 (м 8Н, CHAr.), 10.22 (с 2Н, ОН). Найдено, %: С 49.82, Н 3.7, N 3.01 CuC38H36N2O20. Вычислено, %: С 49.74, Н 3.52, N 3.10.
Пример 3. Синтез комплекса меди(II) 3,3'-((4-метоксифенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) (3)
Аналогично методике синтеза в примере 1 к 0.5 г (1 ммоль) 3,3'-((4-метоксифенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) добавляют 0.26 г (1 ммоль) моногидрата ацетата меди(II). Получают 0.52 г (53%) комплекса меди(II) 3,3'-((4-метоксифенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) (3). Время реакции составляет 2.5 часа. Т.пл. 163-164°С. Спектр ЯМР 1Н (ацетон-d6), δ, м.д.: 2.24, 2.21, 2.26, 2.32 (с 3Н, СН3), 3.83, 3.92 (с 3Н, ОСН3), 4.03 (уш. с 1.5Н, H2O), 5.65 (уш. с 2Н, СН), 6.23 (уш. с 4Н, =СН), 6.86-8.02 (м 8Н, CHAr.), 9.90 (с 2Н, ОН). Найдено, %: С 59.65, Н 4.20. CuC40H40O17. Вычислено, %: С 59.89, Н 4.27.
Контроль за ходом реакций осуществлялся методом ТСХ, элюент - гексан:этилацетат:ацетон (3:1:1), проявитель - пары йода.
Пример 4. Биологические испытания заявленных соединений.
Цитотоксичность комплексов меди(II) на основе арилметиленбиспиран-2-онов определяли с помощью МТТ-теста на клеточной линии раковой опухоли шейки матки человека (HeLa). В основе МТТ-теста лежит способность живых клеток восстанавливать нитротетразолевый синий (([3-(4.5-диметилтиазол-2-ил)]-2.5-дифенилтетразолиумбромид) до формазана.
Клетки линий HeLa, суспендированные в питательной среде, вносили в лунки 96-луночных полистироловых планшетов по достижении клеточного монослоя 70-90%, удаляли старую питательную среду и вносили новую, содержащую исследуемое вещество. В качестве контрольного препарата использовали ДМСО или этанол, в концентрации, соответствующей исследуемому образцу. Питательная среда представляла собой среду ДМЕМ с добавлением 10% эмбриональной телячьей сыворотки.
Лиофильно высушенные тестируемые вещества ресуспендировали в ДМСО с получением насыщенных растворов (5-10 мг/мл).
Через 24 часа удаляли старую питательную среду и вносили раствор нитротетразолевого синего (0,5 мг на 100 мл забуференного физиологического раствора), культивировали 1 час. Содержимое лунок удаляли и вносили ДМСО. Далее измеряли оптическую плотность лунок с помощью Tecan Spark 10M (Tecan, Австрия) при 540 нм и вычисляли измеренное фоновое поглощение при длине волны 690 нм. Дыхательную активность контрольных образцов принимали за 100%.
Тестируемые вещества вносились в 5 повторах, эксперимент повторяли 3 раза.
На фиг. 1, 2, 3 и в таблице представлены результаты определения метаболической активности клеточной линии HeLa при воздействии на них соединений 1, 2 и 3 в максимальной использованной концентрации.
Из приведенных данных следует, что соединение № 1 комплекс меди(II) 3,3'-(фенилметилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) в максимальной использованной концентрации подавляет метаболическую активность клеточной линии HeLa до 89.4%, а соединения 2 и 3 комплексы меди(II) 3,3'-((3-нитрофенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она) и 3,3'-((4-метоксифенил)метилен)бис(4-гидрокси-6-метил-2Н-пиран-2-она), соответственно, значительно подавляют метаболическую активность клеточной линии HeLa (до 47.9% и 59.6%).
Проведенный нами виртуальный скрининг биологической активности полученных структур при помощи программы PASS также подтвердил вероятность проявления противоопухолевой (Ра = 72%, Ра = 69%) активности у соединений 2 и 3.
Таким образом, заявляемые соединения могут быть перспективны для создания препаратов, направленных на лечение раковых заболеваний.
| название | год | авторы | номер документа |
|---|---|---|---|
| АЛЬГИЦИДНОЕ СРЕДСТВО ПРОТИВ КУЛЬТУРЫ МИКРОВОДОРОСЛЕЙ DUNALIELLA SALINA | 2022 |
|
RU2788987C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ КУЛЬТУРЫ КЛЕТОК ESCHERICHIA COLI | 2022 |
|
RU2786842C1 |
| 4-(2,4-ДИМЕТОКСИФЕНИЛ)-2-(2-ГИДРОКСИФЕНИЛ)-5,6-ДИГИДРО-4Н-БЕНЗО[H]ХРОМЕН-3-КАРБОНОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2707972C1 |
| 4-ГИДРОКСИПИРАН-2-ОНЫ, ЦИКЛООКТИЛ-ИЛИ БЕНЗОПИРАН-2-ОНЫ, 4-ГИДРОКСИ-2Н-ПИРАН-2-ОНЫ И 4-ГИДРОКСИ-ЦИКЛООКТАПИРАН-2-ОНЫ | 1995 |
|
RU2139284C1 |
| ПРОИЗВОДНЫЕ ДИГИДРОНАФТОПИРАНОВ ИЛИ ИХ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПОДАВЛЯЮЩАЯ ПРОЛИФЕРАЦИЮ КЛЕТОК | 1993 |
|
RU2083572C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2714932C1 |
| Метил-3-арил-3a-нитро-4-(трифторметил)-1,2,3,3a,4,9b-гексагидрохромено[3,4-c]пиррол-1-карбоксилаты, обладающие цитотоксической активностью в отношении к клеткам линии карциномы шейки матки человека HeLa, и способ их получения | 2023 |
|
RU2818191C1 |
| ВЕЩЕСТВО С ПРОТИВОВИРУСНОЙ И АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ НА ОСНОВЕ ПРОИЗВОДНЫХ 2,8-ДИТИОКСО-1H-ПИРАНО[2,3-D, 6,5-D`] ДИПИРИМИДИНА И ИХ 10-АЗА-АНАЛОГОВ | 2003 |
|
RU2246496C1 |
| СПОСОБ ИДЕНТИФИКАЦИИ ПРОТИВООПУХОЛЕВЫХ ЦЕЛЕВЫХ ФЕРМЕНТОВ | 2002 |
|
RU2319482C2 |
| ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ 2-{4-[(3S)-ПИПЕРИДИН-3-ИЛ]ФЕНИЛ}-2Н-ИНДАЗОЛ-7-КАРБОКСАМИДА | 2009 |
|
RU2495035C2 |

Изобретение относится к новым биологически активным соединениям, а именно к комплексным соединениям меди(II) на основе арилметиленбиспиран-2-онов, формулы
 ,
,
где при n = 4 R=H (1) или R=3-NO2 (2) или при n = 3 R= 4-OCH3 (3). Предложенные комплексные соединения обладают цитотоксическим действием, в частности - способностью подавлять метаболическую активность клеточной линии карциномы шейки матки человека (HeLa), и могут найти применение в медицинской практике для лечения раковых заболеваний. 3 ил., 1 табл., 4 пр.
Комплексные соединения меди(II) на основе арилметиленбиспиран-2-онов, обладающие цитотоксической активностью в отношении клеток Hela, формулы
 ,
,
где при n = 4 R=H (1) или R=3-NO2 (2) или при n = 3 R= 4-OCH3 (3).
| BUDZISZ E | |||
| et al., Synthesis, Crystal Structure and Biological Characterization of a Novel Palladium(II) Complex with a Coumarin-Derived Ligand, European Journal of Inorganic Chemistry, 2004, v | |||
| Машина для добывания торфа и т.п. | 1922 |
|
SU22A1 |
| ВОДЯНЫЕ ЧАСЫ | 1926 |
|
SU4412A1 |
| ZHU T | |||
| et al., Anticancer activity and DNA-binding investigations of the Cu(II) and Ni(II) complexes with Coumarin Derivative, Chem | |||
Авторы
Даты
2021-08-24—Публикация
2020-03-16—Подача