Изобретение относится к микробиологии и биотехнологии и касается получения штаммов дрожжей Komagataella phaffii (Pichia pastoris), способных продуцировать фермент фитазу.
Фосфор является важным химическим элементом, необходимым для роста и развития животных. В большинстве используемых в животноводстве растительных кормов, таких как зерновые и бобовые культуры, фосфор содержится, в основном, в форме фитата (мио-инозитол гексакисфосфат) [Advanced Food Research, 1982, 28, 1-92.]. Моногастричные животные не способны усваивать фитатный фосфор из-за отсутствия в пищеварительном тракте необходимого фермента [Can. J. Anim. Sci., 2013, 93, 9-21.].
Присутствие в составе комбикорма фитата препятствует также эффективному усвоению кальция, магния, цинка, железа и других минеральных веществ и приводит к связыванию белков корма в недоступные для переваривания комплексы [Current Topics In Nutraceutical Research, 2008, 6(3), 131-144.].
Фитазы (мио-инозитол гексакисфосфат фосфогидролазы) гидролизуют фитат с отщеплением фосфатных групп. Эти ферменты с успехом используют в качестве кормовой добавки, значительно повышая усвоение фосфора [J. Sci. Food Agric., 2015, 95, 878-896.]. Они обеспечивают высвобождение не только фитат-связанного фосфора, но также белков, макро- и микроэлементов, повышая питательные свойства кормов [British Poultry Science, 2004, 45(1), 101-108.].
Природными источниками фитаз являются различные микроорганизмы: бактерии, грибы [FEMS Microbiology Reviews, 2005, 29 (1), 3-23.].
В промышленности фитазы получают путем микробиологического синтеза с использованием штаммов-продуцентов, потребность промышленности в которых постоянно растет [Afr. J. Biotechnol., 2009, 8(17), 4229-4232.]. Наиболее перспективные продуценты фитазы получены на основе рекомбинантных штаммов метилотрофных дрожжей Komagataella phaffii (Pichia pastoris) [J. Mol. Recognit., 2005, 18(2), 119-138. doi: 10.1002/jmr.687], которые обладают мощными системами экспрессии и секреции рекомбинантных белков (включая фитазы) и для которых разработаны питательные среды и отработан процесс ферментации с использованием культуры высокой плотности. Процесс культивирования метилотрофных дрожжей достаточно прост, поскольку их рост не блокируется продуктами метаболизма [FEMS Microbiol. Rev., 2000, 24:45-66, doi: 10.1111/j.1574-6976.2000.tb00532.x].
На основе дрожжей K. phaffii сконструированы продуценты фитаз: Citrobacter amalonaticus [ВМС Biotechnology, 2015, 15, 88.], Escherichia coli [J. Agric. Food Chem., 2013, 61(25), 6007-6015., CN 102586294, CN 102943083], Peniophora lycii [Appl. Microbiol. Biotechnol., 2006, 72(5), 1039-47.], Citrobacter braakii [Acta Microbiologica Sinica, 46(6), 945-950.], Yersinia rohdei, Yersinia pestis, Y. intermedia [Appl. Microbiol. Biotechnol., 2008, 80(3), 417-426.] и других.
Гены, кодирующие фитазы различного происхождения, экспрессируются в дрожжах K. phaffii с различной эффективностью. При экспрессии генов, кодирующих фитазы из Yersinia rohdei, Yersinia pestis, Y. intermedia, E. coli или Aspergillus niger, в дрожжах K. phaffii фитазная активность в культуральной жидкости на 4 сутки культивирования составляет соответственно 313, 19, 270, 219 и 16 ед/мл. [Appl. Microbiol. Biotechnol., 2008, 80(3), 417-426.]. При этом, фитазы различного происхождения отличаются между собой по свойствам, существенным для использования в промышленности, таким как, оптимальный рабочий диапазон рН, устойчивость к действию протеолитических ферментов, температуры, рН и другим [J. Agric. Food Chem., 2013, 61(25), 6007-6015; Annu. Rev. Anim. Biosci., 2013, 1, 283-309.].
Получение новых фитаз, обладающих промышленно-ценными свойствами и способных эффективно экспрессироваться в дрожжах K. phaffii является актуальной задачей.
Технической проблемой, на решение которой направлено заявляемое изобретение является расширение арсенала рекомбинантных микроорганизмов, продуцирующих фитазу.
Техническим результатом, достигаемым при реализации заявляемого изобретения является получение трансформанта дрожжей Komagataella phaffii - продуцента фитазы PhyCt из Cronobacter turicensis.
Получение заявляемого трансформанта включает введение ДНК последовательности гена m-phyCt, кодирующего фитазу PhyCt из С. Turicensis (или одного из вариантов его ДНК последовательности, обусловленного вырожденностью генетического кода) в клетки дрожжей K. phaffii с помощью экспрессионной кассеты, включающей ген m-phyCt или один из вариантов его последовательности, промотор, работающий в дрожжах K. phaffii, сигнальный пептид для осуществления секреции фермента в культуральную жидкость, а также терминатор, маркерный ген и, предпочтительно, сайт для гомологичной интеграции в хромосому.
Нуклеотидная последовательность гена m-phyCt, кодирующего фитазу PhyCt из С. turicensis, представлена в международной базе Genbank под номером МТ489463. В силу «вырожденности» генетического кода одна и та же аминокислотная последовательность может кодироваться большим числом нуклеотидных последовательностей, поэтому для клонирования может быть использована не только сама нуклеотидная последовательность (ген m-phyCt), но и все ее варианты, определяемые вырожденностью генетического кода.
Интеграцию нуклеотидной последовательности осуществляют путем или гомологичной, или негомологичной рекомбинации. Трансформацию экспрессионной кассеты в клетки дрожжей K. phaffii проводят в частности, методом электропорации [http://tools.thermofisher.com/content/sfs/manuals/pich_man.pdf], методом с использованием полиэтиленгликоля или протопластов [http://www.thermofisher.com/order/catalog/product/K173001].
Конструирование экспрессионных кассет осуществляют стандартными методами генетической инженерии [Рыбчин В.Н. Основы генетической инженерии. - СПб.: СПбГТУ, 1999; Sambrook J., Maniatis Т., Fritsch Е. Molecular cloning: a laboratory manual. - N.Y.: Cold Spring Harbor Laboratory, 1989.] с использованием генетических элементов, подходящих для работы с дрожжами K. phaffii. В качестве промоторов используют AOX1, DAS, FLD1, ICL1, PHO89, THI11, ADH1, ENO1, GUT1, GAP, TEF1, PGK1, GCW14, G1, G6 или другие [Appl. Microbiol. Biotechnol., 2014, 98, 5301-5317.]. В качестве сигнальных пептидов используют α-фактор, PHO1, SUC2, РНА-Е, KILM1, pGKL, CLY, CLY-L8, K28 pre-pro-toxin или другие [Appl. Microbiol. Biotechnol., 2014, 98, 5301-5317.]. В качестве селективных маркеров используют любые подходящие маркеры, например, гены резистентности к антибиотикам зеоцину, генетицину (G418) или бластицидину С, а также гены комплементирующие ауксотрофные мутации в геноме K. phaffii, например, HIS4, МЕТ2, ADE1, ARG4, URA3, URA5, GUT1 [Yeast, 2005, 22, 249-270.]. В качестве плечей для гомологичной интеграции используют последовательности генов АОХ1, HIS4 [http://www.thermofisher.com/order/catalog/product/V17520] или другие последовательности, гомологичные участкам хромосомы дрожжей K. phaffii.
Полученные трансформанты тестируют на наличие целевого гена в составе хромосомной ДНК и способность проявлять фитазную активность.
Изобретение проиллюстрировано следующими фигурами.
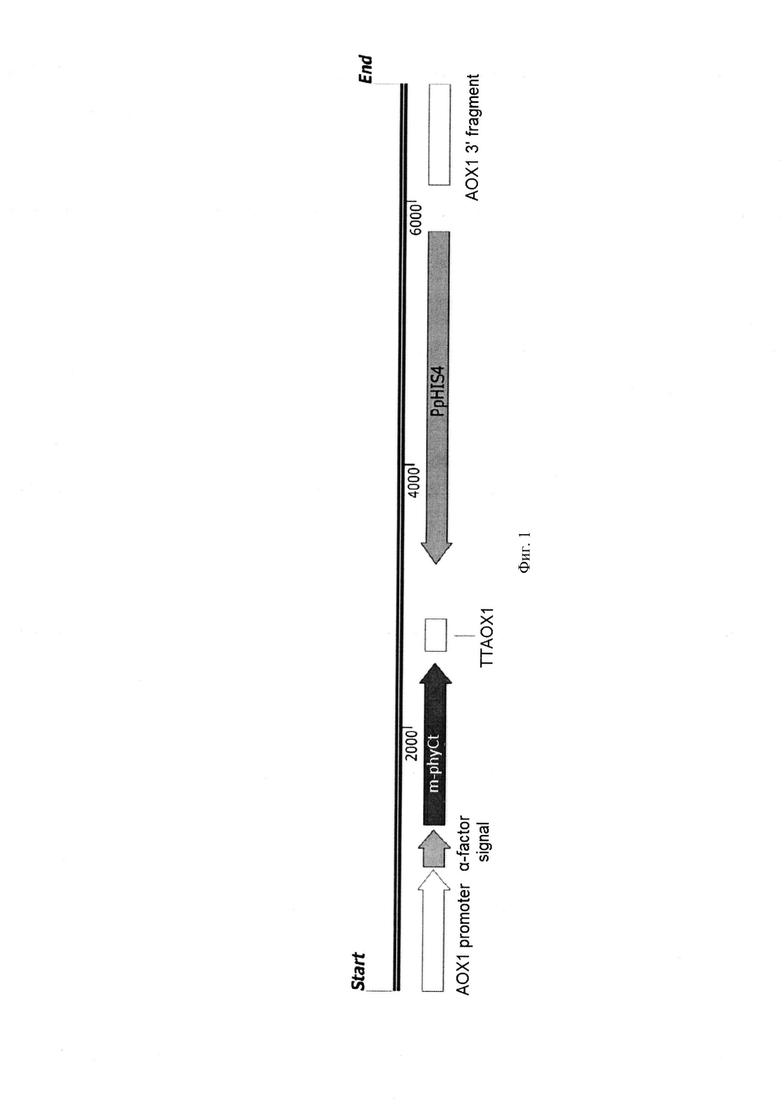
Фиг. 1. Экспрессионная кассета
Фиг. 2. Электрофореграмма фрагмента ПЦР, соответствующего гену m-phyCt
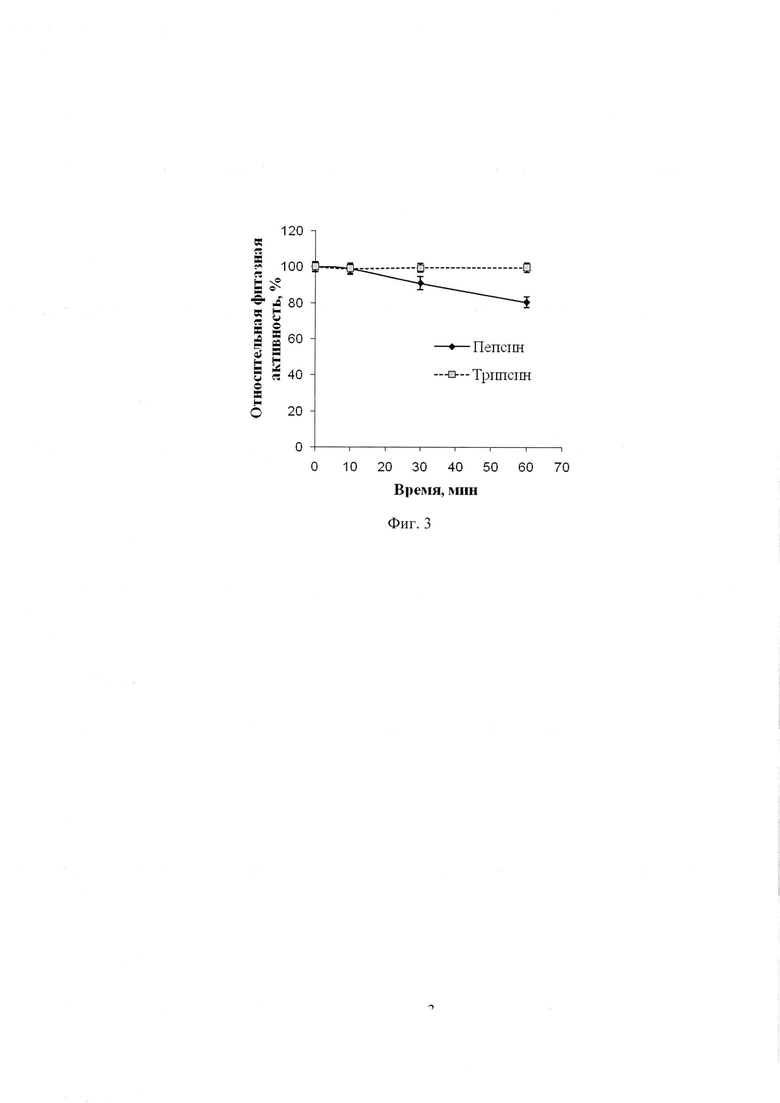
Фиг. 3. Устойчивость фитазы С. turicensis к действию протеолитических ферментов (пепсина и трипсина).
Пример 1. Конструирование трансформанта дрожжей K. phaffii, продуцирующего фитазу С. turicensis
При конструировании интегративной экспрессионной кассеты используют метод "фьюжн-пцр" [Gene., 1989, 77(1), 61-68.].
Последовательность гена m-phyCt, представленную в международной базе данных GenBank под номером МТ489463 и кодирующую фитазу из С. turicensis, синтезируют методом, описанным в [J. Microbiol. Methods, 2010, 81(2), 147-152.]. Получают ДНК последовательность, на 3'- и 5'-концах которой предусмотрены сайты рестрикции EcoRI и NotI, приведенную в перечне последовательностей под номером SEQ ID NO: 1.
Полученную последовательность ДНК встраивают в состав экспрессионной кассеты (фиг. 1), в состав которой входят следующие генетические элементы:
- ген m-phyCt, встроенный в единую рамку считывания с нуклеотидной последовательностью сигнального пептида α-фактора из Saccharomyces cerevisiae, под контролем АОХ1 промотора;
- терминатор транскрипции ТТАОХ1;
- дрожжевой селективный маркер HIS4, комплементирующий у дрожжей K. phaffii мутацию в гене HIS4;
- область интеграции - 3'-фрагмент нуклеотидной последовательности гена АОХ1.
Полученную интегративную экспрессионную кассету трансформируют в штамм K. phaffii Y-2837, который предварительно выращивают в жидкой питательной среде YP (мас. %: дрожжевой экстракт - 1, пептон - 2, вода - остальное) с добавлением глюкозы (2 мас. %) до концентрации 1×108 клеток на 1 мл. Клетки отделяют центрифугированием, промывают в ледяной стерильной воде, а затем в ледяном растворе 1М сорбитола. Затем клетки инкубируют в 25 мМ растворе дитиотрейтола в течение 15 минут и промывают в ледяном растворе 1М сорбитола. Далее клетки ресуспендируют в ледяном растворе 1 М сорбитола в концентрации 1-5×109 клеток на 1 мл. Аликвоту, объемом 40 мкл клеточной суспензии, переносят в охлажденный эппендорф, добавляют 400 нг ДНК экспрессионной интеграционной кассеты, и инкубируют во льду 5 минут. Смесь клеток и ДНК переносят в предварительно охлажденную кювету для электропорации. Электропорацию проводят при следующих условиях: 1,5 кВ, 400 Ом, 25 uF. После порации добавляют 1 мл ледяного раствора 1М сорбитола.
Селекцию трансформантов ведут в течение 5 суток при температуре 30°С на агаризованной среде следующего состава (мас. %): Na2HPO4 - 0,6; KH2PO4 - 0,3; NaCl - 0,05; NH4Cl - 0,1; MgSO47H2O - 0,065; агар - 2; глюкоза - 2; CaCl2 - 0,07; биотин, мг - 0,0002; кальций пантотенат - 0,04; фолиевая кислота - 0,0002; ниацин - 0,04; р-аминобензойная к-та - 0,02; пиридоксин гидрохлорид - 0,04; рибофлавин - 0,02; тиамин гидрохлорид - 0,04; борная кислота - 0,05; CuSO4 - 0,004; KJ - 0,01; FeCl3 - 0,02; натрий молибдат - 0,02; ZnSO4 - 0,04, вода - остальное.
Наличие целевого гена в составе хромосомной ДНК полученных трансформантов определяют методом ПЦР с использованием праймеров PhyCt-F (5'-gaagtttctgacgaaatgaa-3'), PhyCt-R (5'-ttatctgttgatgtgagcca-3').
Режим реакции ПЦР: 94°С - 3 мин - 1 цикл; 30 циклов: 94°С - 30 с, 57°С - 30 с, 72°С - 90 с; 72°С - 5 мин - 1 цикл.
Для контроля величины амплифицированного фрагмента ДНК при электрофорезе используют молекулярный маркер GeneRuler 1 kb DNA Ladder (Fermentas) (линия 2, фиг. 2, размер фрагментов снизу вверх 10000, 8000, 6000, 5000, 4000, 3500, 3000, 2500, 2000, 1500, 1000, 750, 500, 250 п.н.).
Наличие ПЦР-фрагмента размером 1245 п.н. (линия 1 фиг. 2) подтверждает присутствие гена m-phyCt, кодирующего фитазу из С. turicensis, в составе хромосомы полученных трансформантов.
Пример 2. Оценка уровня фитазной активности трансформантов дрожжей Komagataella phaffii
Отбор наиболее продуктивного трансформанта проводят при культивировании в жидкой питательной среде по следующей схеме.
Посевную культуру каждого из трансформантов в отдельности выращивают в пробирках (50 мл) с 5 мл жидкой питательной среды YP с добавлением глюкозы (2 мас. %) при 30°С в течение 24 ч на качалке (250 об/мин). Засев ферментационной среды осуществляют в соотношении 1/10 для каждого трансформанта в отдельности.
Ферментацию проводят при 30°С на качалке (250 об/мин) в питательной среде YP с добавлением 1% глюкозы в течение 24 ч. Экспрессию гена фитазы индуцируют путем добавления метанола до конечной концентрации 1% каждые 24 ч в течение 2 суток. Продуктивность каждого из полученных трансформантов K. phaffii оценивают по активности фитазы, накопившейся в культуральной жидкости. Для этого клетки трансформанта осаждают центрифугированием, а супернатант используют для определения фитазной активности модифицированным методом Фиске-Субарроу [J. Microbiol. Methods, 1999, 39(1), 17-22.].

Представленные в таблице значения фитазной активности свидетельствуют о достаточно высоком уровне продуктивности полученных трансформантов K. Phaffii по фитазе С. turicensis, а также об эффективной экспрессии фитазы PhyCt в дрожжах K. phaffii.
Отобранный по результатам ферментации наиболее продуктивный трансформант №10, который синтезирует фитазу в количестве 382 ед/мл, депонируют в Биоресурсном центре Всероссийская Коллекция Промышленных Микроорганизмов (БРЦ ВКПМ) НИЦ «Курчатовский институт» - ГосНИИгенетика (117545 Москва, 1-ый Дорожный проезд, д. 1) как Komagataella phaffii Cron10 ВКПМ Y-4840.
Штамм характеризуется следующими признаками
Культурально-морфологические признаки
При культивировании при температуре 28°С в течение 48 часов на агаризованной среде YP следующего состава (мас. %: пептон - 2, дрожжевой экстракт - 1, агар - 2, вода - остальное) с добавлением глюкозы (2 мас. %), клетки имеют овальную форму, 3-4 мкм в диаметре. Клетки почкуются, при этом почкование истинное, многостороннее. Истинного мицелия не образуют. Споруляция происходит при инкубации культуры на агаризованной среде следующего состава (мас. %): хлорид калия - 1.0, ацетат натрия - 0.5, глюкоза - 1.0, агар - 2.0, вода - остальное. Аски имеют тетраэдрическую форму, включают 4 аскоспоры.
На агаризованной среде YP с добавлением глюкозы (2 мас. %) колонии светло-бежевого цвета с ровным краем, матовой поверхностью, линзовидным профилем и пастообразной консистенцией. При росте в жидкой среде YP с добавлением глюкозы (2 мас. %), при 28°С в течение 24 ч культивирования - жидкость мутная, осадок белый, коагуляции не наблюдается, пристеночных пленок не образует.
Физиолого-биохимические признаки
Способен к росту как в аэробных, так и в анаэробных условиях.
В качестве единственного источника углерода способен использовать метанол, этанол, глюкозу, глицерин, лактат, сукцинат, не способен ассимилировать мальтозу, сахарозу, ацетат, крахмал, лактозу.
При культивировании в присутствии метанола способен синтезировать фитазу.
Пример 3. Устойчивость фитазы PhyCt, синтезированной заявляемым трансформантом, к действию протеаз (пепсина и трипсина)
По окончании процесса ферментации, проведенной как описано в примере 2, клетки заявляемого трансформанта осаждают центрифугированием, а супернатант используют для выделения и очистки фитазы методом катионообменной хроматографии [Биотехнология. 2019, 35(4), 33-41.]. Очищенный фермент инкубируют в 0,25 М глицин - HCl буфере (рН 2,0) с пепсином или в 0,25 М трис-HCl буфере (рН 7,0) с трипсином при 37°С. Соотношение протеаза/фермент составляет 0,1 (по массе). Устойчивость к протеазам оценивают путем измерения остаточной относительной фитазной активности модифицированным методом Фиске-Субарроу [J. Microbiol. Methods, 1999, 39(1), 17-22.] после инкубации фермента в течение 10, 30 и 60 мин.
На фиг. 3 показана относительная остаточная активность фитазы PhyCt при действии протеаз (пепсина и трипсина) в течение 1 часа при 37°С и соотношении протеаза/фермент 0,1 (по массе). За 100% принимают начальное значение фитазной активности.
Из представленных результатов видно, что остаточная фитазная активность фитазы PhyCt при действии трипсина составляет практически 100%, а при действии пепсина - 80%, что не уступает соответствующим показателям при тех же условиях (времени и температуре) для известных коммерческих фитаз или превосходит их.
Так, например, наиболее устойчивая к трипсину фитаза из Y. intermedia сохраняет 90% своей активности [Biochem. Biophys. Res. Commun., 2006, 350(4), 884-889.].
Коммерческая фитаза из A. Niger под влиянием трипсина теряет 60% своей активности уже при соотношении трипсин/фитаза 0,01 (по массе). [Arch Biochem Biophys. 1999, 365(2):262-7.], а под влиянием пепсина, в зависимости от соотношения пепсин/фермент, теряет 49-61% активности [In: International Phytase Summit. 2012, AB Vista, 96-107].
Известная коммерческая фитаза из Escherichia coli при воздействии пепсина (при различном соотношении протеаза/фермент) проявляет остаточную активность 93-97% [In: International Phytase Summit. 2012, AB Vista, 96-107], но при воздействии трипсина (даже при соотношении протеаза/фермент 0,025) ее остаточная активность составляет 80% [Arch Biochem Biophys. 1999, 365(2):262-7.].
При этом известно, что рекомбинантная фитаза из E. coli, экспрессируемая в K. phaffii (P. pastoris), теряет около 70% своей активности при воздействии пепсина уже при соотношении протеаза/фитаза 0,002 (по массе) [J Agric Food Chem 2013, 61(25):6007-6015.].
Высокая устойчивость продуцируемой заявляемым трансформантом фитазы PhyCt к действию протеолитических ферментов делает ее привлекательной для промышленного применения, в частности, для использования в качестве кормовой добавки.
--->
Перечень последовательностей
<110> Федеральное государственное бюджетное учреждение "Государственный научно-
исследовательский институт генетики и селекции промышленных микроорганизмов
Национального исследовательского центра "Курчатовский институт" (НИЦ
«Курчатовский институт» - ГосНИИгенетика).
State Research Institute for Genetics and Selection of Industrial
Microorganisms of National Research Center «Kurchatov Institute» (NRC
«Kurchatov Institute» – GOSNIIGENETIKA).
<120> Трансформант дрожжей Komagataella phaffii, продуцирующий фитазу Cronobacter
turicensis
<130> 20-04
<160> 1
<210> 1
<211> 1263
<212> DNA
<213> Artificial Sequence
<220>
<223> ген m-phyCt, кодирующий фитазу PhyCt бактерий Cronobacter turicensis
<400> 1
aagaattcga agtttctgac gaaatgaagt tggaaagagt tgttatcgtt tctagacacg 60
gtgttagagc tccaactaag ttcactccat tgatgcaaga agttactcca tacccatggc 120
cacaatggga cgttccattg ggttggttga ctactagagg tggtgaattg gttactgaat 180
tgggtagata ccaaaagtct gttttcgttg acaagggtat cttggaaggt aacgaatgtc 240
catctccaga acaagttgct gttatcgctg acactgacca aagaactaga aagactggtg 300
aagctttctt ggctggtttc gctccaggtt gtcaaaacaa ggttcactac caaaaggaac 360
acgacaagaa ggacccattg ttcaacccgg ttaagacggg tgtgtgtagc ttcaacgttt 420
ctaagactca agaagctatc ttgactagag ctggtggtaa cgttgaaaga tacactcaaa 480
gatacgactc tgctttcaga actttggaac aagttttgaa cttctctcaa tctgctgctt 540
gtaagtctac tagacaacca ggctgcactc tcccaggtgc tctcccatct gaattgaaga 600
cttcttctga caacgtttct ttgtctggtg cttggtcttt gtcttctatg ttgactgaaa 660
tcttcttgtt gcaagaagct caaggtatgc cagaagttgc ttggggtaga atccacggtg 720
aaaaggaatg gactgaattg ttgtctttgc acaacgctca attcgacttg ttgcaaagaa 780
ctccagaagt tgctagaact agagctactc cattgttgga cttgatctct agagctttgg 840
tttctaacgg ttctactgaa aaccactacg gtatcaagtt gccagtttct ttgttgttca 900
tcgctggtca cgacactaac ttggctaact tgtctggtgc tttcgacttg aactggtctt 960
tgccaggtca accagacaac actccaccag gcggcgaatt ggtcttcgag agatggaaga 1020
gagtttctga caacactgac tggattcaag tttctttcgt ttaccagact ctccaacaaa 1080
tgcgtgagtt caagccatct tcttcttctc catctccaca taagatagtt ttgactctcc 1140
catcttgtca ggacaagaac ccagaaggta tgtgcagctt gaagggtttc aatgacatcg 1200
ttcaaagagt tagaatccca caatgtgctg ttatggctca catcaacaga taagcggссg 1260
ctt 1263
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Трансформант дрожжей Komagataella phaffi - продуцент фитазы Citrobacter gillenii | 2020 |
|
RU2771582C1 |
| Штамм дрожжей Komagataella phaffii с инактивированным геном HIS4 - реципиент для конструирования безмаркерных штаммов-продуцентов гетерологичных белков | 2022 |
|
RU2787584C1 |
| Штамм дрожжей Komagataella phaffii с инактивированным геном LEU2 - реципиент для конструирования штаммов-продуцентов гетерологичных белков | 2022 |
|
RU2788528C1 |
| Интегративная кассета для экспрессии генов и ее использование при конструировании трансформанта дрожжей Komagataella mondaviorum | 2023 |
|
RU2836330C1 |
| Трансформант Komagataella phaffii, содержащий ген HAC1, продуцент рекомбинантного химозина Vicugna pacos в активной форме | 2023 |
|
RU2828277C1 |
| Трансформант Komagataella phaffii - продуцент рекомбинантного химозина в активной форме | 2022 |
|
RU2805486C1 |
| Трансформант дрожжей Pichia pastoris, продуцирующий фитазу Escherichia coli | 2019 |
|
RU2737621C1 |
| Трансформант дрожжей Pichia pastoris, продуцирующий фитазу | 2019 |
|
RU2708446C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris - продуцент фитазы | 2018 |
|
RU2701498C1 |
| Рекомбинантный штамм дрожжей Pichia pastoris с увеличенной продукцией фитазы Escherichia coli | 2019 |
|
RU2737623C1 |

Изобретение относится к биотехнологии. Предложен трансформант дрожжей Komagataella phaffii, продуцирующий фитазу Cronobacter turicensis. Трансформант содержит ДНК-последовательность гена m-phyCt, кодирующего фитазу Cronobacter turicensis, или один из вариантов такой последовательности, обусловленный вырожденностью генетического кода. Полученная фитаза сохраняет не менее 80% и около 100% активности при воздействии на нее соответственно пепсина или трипсина в течение 1 ч при 37°С и соотношении протеаза/фермент 0,1 по массе. 3 ил., 1 табл., 3 пр.
Трансформант дрожжей Komagataella phaffii, продуцирующий фитазу Cronobacter turicensis и содержащий ДНК-последовательность гена m-phyCt, кодирующего фитазу Cronobacter turicensis, или один из вариантов такой последовательности, обусловленный вырожденностью генетического кода.
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА ДЛЯ ЭКСПРЕССИИ В ДРОЖЖАХ PICHIA PASTORIS ГЕНА ФИТАЗЫ (ВАРИАНТЫ), ШТАММ ДРОЖЖЕЙ PICHIA PASTORIS - ПРОДУЦЕНТ ФИТАЗЫ (ВАРИАНТЫ) | 2009 |
|
RU2409670C1 |
| GenBank: MT489463.1, 13.12.2020 | |||
| Synthetic construct phytase (m-phyCt) gene, partial cds | |||
| Найдено онлайн: https://www.ncbi.nlm.nih.gov/nuccore/1940855166 Дата обращения 09.08.2021 | |||
| LI C | |||
| ET AL | |||
| Combined strategies for improving expression of Citrobacter amalonaticus phytase in Pichia pastoris | |||
| BMC Biotechnol | |||
Авторы
Даты
2021-09-29—Публикация
2021-01-22—Подача