Область техники, к которой относится изобретение
Это раскрытие относится к вакцине против Mycoplasma spp.; в частности, к субъединичной вакцине против Mycoplasma spp.
Уровень техники
Mycoplasma spp. является известной в настоящее время мельчайшей бактерией, способной к саморепликации вне клеток хозяина. Хотя энзоотическая пневмония свиней не должна вызывать смерть свиньи, она снижает эффективность кормления и вызывает замедление роста, воспаление и иммуносупрессию, а также делает свинью более восприимчивой к инфекции другими патогенами, что вследствие этого приводит к экономическому ущербу для производства.
На настоящий момент энзоотическую пневмонию свиней предотвращают тремя главными стратегиями, включая: введение лекарственного средства, контроль состояния окружающей среды и вакцинацию. Учитывая плохую предотвращающую эффективность антибиотиков от Mycoplasma hyopneumoniae, введение лекарственного средства может быть использовано только в целях лечения, и удовлетворение потребностей в профилактике представляет сложность. Кроме того, принимая во внимание то, что лекарственная зависимость может привести к более сильной инфекции, вызываемой посредством резистентных к лекарственным средствам бактерий, для введения лекарственного средства требуются меры предосторожности и существует множество ограничений.
Контроль состояния окружающей среды формирует основу профилактики инфекции Mycoplasma spp. Хорошая санитарная обработка и управление свиноводческими помещениями были бы полезными для снижения частоты инфекции. С другой стороны, профилактика могла бы быть более полноценной при вакцинации.
В обычных вакцинах в данной области используются неактивные/мертвые бактерии в качестве активного ингредиента. Однако стоимость обычных вакцин является слишком высокой из-за того, что Mycoplasma spp. являются прихотливыми бактериями и их трудно культивировать в лаборатории. Для того, чтобы снизить стоимость вакцин Mycoplasma spp., ученые непрерывно пытаются разработать вакцины различных типов, такие как: (1) аттенуированные вакцины, (2) векторные вакцины, (3) субъединичные вакцины и (4) ДНК вакцины. Среди них, субъединичные вакцины демонстрируют наибольшую эффективность из-за преимуществ в легкости производства и высокой безопасности.
К настоящему времени существует несколько потенциальных белков-кандидатов, которые могли бы быть использованы для вакцин M. hyopneumoniae; однако нет дополнительных сообщений, подтверждающих, что такие белки пригодны для вакцин M. hyopneumoniae.
Краткое описание изобретения
В свете вышеприведенного, одна из задач настоящего изобретения заключается в получении антигенов, пригодных для использования в вакцинах M. hyopneumoniae, с получением, посредством этого новых вакцин M. Hyopneumoniae, так, что стоимость профилактики может быть снижена.
Другая задача настоящего изобретения заключается в получении комбинации антигенов, которые пригодны для использования в вакцинах M. hyopneumoniae, с получением, посредством этого, субъединичных вакцин с лучшими характеристиками; вследствие этого будет иметь место большее количество вариантов для целей профилактики.
Для решения вышеуказанных задач, настоящее изобретение относится к рекомбинантному белку для профилактики инфекции Mycoplasma spp., включающему аминокислотную последовательность SEQ ID NO: 08, SEQ ID NO: 09, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или их комбинацию.
Настоящее изобретение также относится к композиции для профилактики инфекции Mycoplasma spp., содержащей: активный ингредиент, содержащий белок PdhA, XylF, EutD, Mhp145, P78, P132, Mhp389 или их комбинацию; и фармацевтически приемлемый адъювант.
Предпочтительно указанный активный ингредиент имеет концентрацию от 50 до 3500 мкг/мл в расчете на общий объем указанной композиции.
Предпочтительно, указанный активный ингредиент содержит по меньшей мере два белка, выбранных из группы, состоящей из PdhA, XylF, EutD, Mhp145, P78, P132 и Mhp389.
Предпочтительно, указанный активный ингредиент содержит PdhA и P78.
Предпочтительно, указанный активный ингредиент содержит XylF и Mhp145.
Предпочтительно, указанный фармацевтически приемлемый адъювант представляет собой полный адъювант Фрейнда, неполный адъювант Фрейнда, алюмогель, поверхностно-активное вещество, полианионный адъювант, пептид, масляную эмульсию или их комбинацию.
Предпочтительно, указанная композиция дополнительно содержит фармацевтически приемлемую добавку.
Предпочтительно, указанная фармацевтически приемлемая добавка представляет собой растворитель, стабилизатор, разбавитель, консервант, антибактериальный агент, противогрибковый агент, изотонический агент, замедляющий абсорбцию агент или их комбинацию.
Настоящее изобретение дополнительно относится к композиции для профилактики инфекции Mycoplasma spp., содержащей: активный ингредиент, содержащий аминокислотную последовательность SEQ ID NO: 08, SEQ ID NO: 09, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или их комбинацию; и фармацевтически приемлемый адъювант.
Предпочтительно, указанный активный ингредиент имеет концентрацию от 50 до 3500 мкг/мл в расчете на общий объем указанной композиции.
Предпочтительно, указанный активный ингредиент содержит по меньшей мере две аминокислотные последовательности, выбранные из группы, состоящей из SEQ ID NO: 08, SEQ ID NO: 09, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13 и SEQ ID NO: 14.
Предпочтительно, указанный активный ингредиент содержит аминокислотные последовательности SEQ ID NO: и SEQ ID NO: 12.
Предпочтительно, указанный активный ингредиент содержит аминокислотные последовательности SEQ ID NO: 09 и SEQ ID NO: 11.
Предпочтительно, указанная композиция дополнительно содержит фармацевтически приемлемую добавку. Предпочтительно, указанная фармацевтически приемлемая добавка представляет собой растворитель, стабилизатор, разбавитель, консервант, антибактериальный агент, противогрибковый агент, изотонический агент, замедляющий абсорбцию агент или их комбинацию.
Настоящее изобретение также относится к экспрессионному вектору для профилактики инфекции Mycoplasma spp., содержащему: плазмиду; где указанная плазмида содержит: нуклеотидную последовательность, содержащую по меньшей мере одну последовательность, выбранную из группы, состоящей из SEQ ID NO: 01, SEQ ID NO: 02, SEQ ID NO: 03, SEQ ID NO: 04, SEQ ID NO: 05, SEQ ID NO: 06 и SEQ ID NO: 07; и регуляторный элемент.
Предпочтительно, указанный регуляторный элемент содержит промотор и сайт связывания рибосомы.
Предпочтительно, указанная плазмида представляет собой pET-MSY, pET-YjgD, pET-D или pET-SUMO.
Предпочтительно, указанная плазмида дополнительно содержит ген, кодирующий партнер слияния.
Предпочтительно, указанный партнер слияния представляет собой MsyB E. coli, YjgD E. coli, белок D бактериофага лямбда или SUMO S. cerevisiae.
Предпочтительно, указанный экспрессионный вектор используется в системе экспрессии генов E. coli.
В целом, настоящее изобретение относится к антигенам, которые пригодны для использования в качестве активного ингредиента субъединичной вакцины/композиции M. hyopneumoniae, и к субъединичной вакцине M. hyopneumoniae, полученной с их использованием. Субъединичная вакцина по настоящему изобретению может быть не только эффективно использована в целях профилактики для снижения ее стоимости, раскрытие настоящего изобретения также демонстрирует, что ʺкоктейльнаяʺ субъединичная вакцина (т.е. имеющая по меньшей мере два антигена в качестве активных ингредиентов) с использованием по меньшей мере двух антигенов по настоящему изобретению имеет улучшенную индукцию иммунного ответа.
Краткое описание чертежей
Фигура 1 демонстрирует результат двумерного электрофореза белков в геле, проведенного в 1-м примере данного изобретения.
Фигура 2 демонстрирует результат цветной реакции Вестерн-блота, проведенного в 1-м примере данного изобретения.
Фигура 3 демонстрирует результат электрофореза продуктов ПЦР, полученных во 2-м примере данного изобретения.
Фигура 4 демонстрирует записи стимуляционных экспериментов, проведенных в 3-м примере данного изобретения.
Подробное описание изобретения
Одна из ключевых целей данного изобретения заключалась в обзоре потенциальных кандидатных антигенов, пригодных для субъединичных вакцин, с использованием двумерного электрофореза белков в геле наряду с технологией иммунологического скринирования, и в идентифицировании антигенов посредством масс-спектрометра. Затем, характеристики субъединичных вакцин по данному изобретению подтверждали экспериментами с моделями на животном.
Кратко, ход выполнения данного изобретения являлся следующим:
(1) Индуцирование иммунного ответа экспериментальных свиней инъецированием общепринятой вакциной M. hyopneumoniae и получением сыворотки, содержащей антитела к M. hyopneumoniae. (2) Получение тотального белка M. hyopneumoniae для двумерного электрофореза белков в геле. (3) Проведение гибридизации результата двумерного электрофореза белков в геле этапа (2) с использованием сыворотки этапа (1) в качестве 1ого антитела и затем сбор белков, являющихся позитивными (т.е. кандидатными антигенами) из геля после амплификации 2ым антителом и последующей процедуры визуализации. (4) Идентификация кандидатных антигенов, полученных в этапе (3). (5) Экспрессирование указанных кандидатных антигенов в больших количествах с использованием системы экспрессии генов E. coli. (6) Исследование эффективности субъединичных вакцин по данному изобретению в уменьшении патологических проявлений в легком экспериментами стимуляции свиньи и, посредством этого проверяя ценность указанных кандидатных антигенов при использовании в качестве активного ингредиента субъединичной вакцины.
Композиция для профилактики инфекции Mycoplasma spp. по данному изобретению содержит активный ингредиент и фармацевтически приемлемый адъювант. В одном варианте осуществления данного изобретения, указанный активный ингредиент может представлять собой PdhA, XylF, EutD, Mhp145, P78, P132 или Mhp389. В альтернативном варианте осуществления при условии, что антигенная детерминанта любого из вышеуказанных белков не нарушается, указанный активный ингредиент может представлять собой слитый белок любых двух из вышеуказанных белков. В другом альтернативном варианте осуществления указанный активный ингредиент содержит по меньшей мере два из вышеуказанных белков; то есть является так называемой ʺкоктейльнойʺ вакциной по данному изобретению.
В другом варианте осуществления данного изобретения указанный активный ингредиент может содержать аминокислотную последовательность SEQ ID NO: 08, SEQ ID NO: 09, SEQ ID NO: 10, SEQ ID NO: 11, SEQ ID NO: 12, SEQ ID NO: 13, SEQ ID NO: 14 или их комбинацию. В альтернативном варианте осуществления при условии, что антигенная детерминанта, образованная укладкой пептида указанной аминокислотной последовательности, не нарушается, указанный активный ингредиент может представлять собой слитый белок с по меньшей мере двумя указанными последовательностями. В другом альтернативном варианте осуществления указанный активный ингредиент содержит два или более белков, соответственно содержащих одну из вышеуказанных аминокислотных последовательностей; то есть является так называемой ʺкоктейльнойʺ вакциной по данному изобретению.
Указанный фармацевтически приемлемый адъювант используется для улучшения иммунного эффекта указанного активного ингредиента, стабилизируя указанный активный ингредиент и/или увеличивая безопасность вакцин. Указанный фармацевтически приемлемый адъювант по данному изобретению включает в себя, но не ограничен ими: полный адъювант Фрейнда, неполный адъювант Фрейнда, алюмогель, поверхностно-активное вещество, полианионный адъювант, пептид, масляную эмульсию или их комбинацию.
Композиция по данному изобретению может иметь один или по меньшей мере два указанных активных ингредиента (т.е. коктейльная вакцина). В одном примере композиции по данному изобретению указанный активный ингредиент имеет концентрацию от 50 до 3500 мкг/мл в расчете на общий объем указанной композиции. В предпочтительном варианте осуществления данного изобретения, когда указанная композиция содержит только один указанный активный ингредиент, указанный активный ингредиент имеет концентрацию от 50 до 500 мкг/мл в расчете на общий объем указанной композиции. В альтернативном варианте осуществления данного изобретения, композиция по данному изобретению содержит по меньшей мере один указанный активный ингредиент; где общая концентрация указанного активного ингредиента(ов), содержащаяся в указанной композиции, составляет от 50 до 1000 мкг/мл, от 50 до 1500 мкг/мл, от 50 до 2000 мкг/мл, от 50 до 2500 мкг/мл, от 50 до 3000 мкг/мл или от 50 до 3500 мкг/мл в расчете на общий объем указанной композиции.
Другой аспект данного изобретения заключается в предоставлении экспрессионного вектора для профилактики инфекции Mycoplasma spp. Конкретно, указанный экспрессионный вектор может быть использован для системы экспрессии генов E. coli. Тем не менее, не выходя за рамки основной идеи данного изобретения, рядовой специалист в данной области может модифицировать указанные векторы на основании данного открытия и сделать указанный вектор пригодным для другой системы экспрессии генов, что все еще будет находиться в рамках объема данного изобретения.
Указанный экспрессионный вектор содержит плазмиду. Указанная плазмида содержит: нуклеотидную последовательность, содержащую по меньшей мере одну последовательность, выбранную из группы, состоящей из SEQ ID NO: 01, SEQ ID NO: 02, SEQ ID NO: 03, SEQ ID NO: 04, SEQ ID NO: 05, SEQ ID NO: 06, SEQ ID NO: 07 и их комбинацию; и регуляторный элемент.
Указанный вектор используется в системе экспрессии генов E. coli и для продуцирования антигенов по данному изобретению посредством E. coli. Другими словами, указанная нуклеотидная последовательность может быть транслирована в последовательность аминокислот антигена по данному изобретению посредством системы экспрессии генов E. coli, и затем аминокислотная последовательность может быть уложена в антиген по данному изобретению.
В альтернативном варианте осуществления при условии, что функционирование системы экспрессии генов E. coli не блокировано и производство указанной нуклеотидной последовательности и укладка являющейся ее результатом аминокислотной последовательности не нарушены, указанная плазмида может содержать две или более указанных нуклеотидных последовательностей.
Указанный регуляторный элемент относится к элементу, требующемуся для инициирования транскрипции и трансляции в системе экспрессии. Указанный регуляторный элемент должен по меньшей мере содержать промотор и сайт связывания рибосомы. Предпочтительно указанный регуляторный элемент может дополнительно содержать: операторную, энхансерную последовательность или их комбинацию.
В предпочтительном варианте осуществления данного изобретения, указанная плазмида дополнительно содержит ген, кодирующий партнер слияния. Указанный партнер слияния включает в себя, но не ограничен ими MsyB E. coli, YjgD E. coli, белок D бактериофага лямбда или SUMO S. cerevisiae. Указанный MsyB имеет высокое содержание кислотных аминокислот и должен способствовать улучшению растворимости белков, которые должны быть продуцированы.
Последующие примеры, излагают испытания и эксперименты данного изобретения для того, чтобы дополнительно объяснить признаки и преимущества данного изобретения. Необходимо отметить, что последующие примеры являются иллюстративными и не должны быть использованы для ограничения объема притязаний данного изобретения.
Пример 1: Скринирование на кандидатные антигены, пригодные для использования в качестве активного ингредиента субъединичной вакцины.
Приготовление сыворотки, содержащей антитело против свиного Mycoplasm spp.
В соответствии с исследованиями из свиньи может быть выделено семь Mycoplasm spp.: Mycoplasm hyopneumoniae, Mycoplasma hyorhinis, Mycoplasma hyosynoviae, Mycoplasma flocculare, Mycoplasma hyopharyngis, Mycoplasma sualvi, Mycoplasma bovigenitalium (Gourlay et al., 1978; Blank et al., 1996; Assuncao et al., 2005). Среди них, M. hyopneumoniae является главным патогеном энзоотической пневмонии свиней с уровнем заболеваемости от 25 до 93%. Вследствие этого в данном изобретении использовали M. hyopneumoniae (штамм PRIT-5) для иммунных протеомных исследований и в качестве источников генов, кодирующих антигены. Среду Фриза (Friis et al., 1975) использовали для культивирования M. hyopneumoniae. В соответствии со схемой эксперимента соответствующее количество антибиотика или агар 1,5% добавляли для формирования твердой среды.
Три SPF свиньи возрастом 4 недели были доставлены из Научно-исследовательского института сельскохозяйственной технологии и их кормили одинаковым кормом и держали при одинаковых окружающих условиях и условиях роста в свинарнике перед экспериментами. После того, как свиней вскармливали до возраста 32 дня, 46 дней и 60 дней, свиньям вводили 2 мл вакцины Bayovac® MH-PRIT-5 (PRIT-5 M. hyopneumoniae) посредством внутримышечной инъекции. Затем свиней непрерывно вскармливали до возраста 74 дня и отбирали кровь из их яремной вены. Отобранную кровь помещали в условия комнатной температуры на 1 час и хранили при 4°C. На следующий день отобранную кровь центрифугировали при 1107×g в течение 30 минут и супернатант удаляли для очистки пробирки и хранили при -20°C.
Двумерный белковый электрофорез в геле тотального белка Mycoplasm spp.
Набор для выделения белка ReadyPrepTM (тотальный белок) (Bio-Rad, CA, USA) использовали для выделения тотального белка Mycoplasm spp. Впоследствии концентрацию собранного белка определяли с использованием Bio-Rad RC DC Protein Assay Kit (CA, USA). Подробный протокол может быть взят из описания продукта или может быть модифицирован из хорошо известных протоколов в данной области.
Двумерный электрофорез белков в геле проводили в два этапа: изоэлектрическое фокусирование (ИЭФ) и электрофорез в геле в присутствии додецилсульфата натрия (ДСН-ПААГ-электрофорез). ИЭФ проводили для разделения белков в образце в зависимости от их изоэлектрической точки; ДСН-ПААГ-электрофорез проводили для разделения белков в соответствии с их молекулярной массой. См. фигуру 1, которая демонстрирует результат двумерного электрофореза белков в геле.
Гибридизация.
Сыворотку, полученную в этапе (1), использовали в качестве 1го антитела для гибридизирования с результатом двумерного электрофореза белков в геле в этапе (2). После того, как белки подвергали амплифицированию 2ым антителом и визуализации последующей процедурой визуализации, собирали белки, являвшиеся позитивными. Эти белки распознавались антителом к Mycoplasm spp. и вследствие этого могли быть пригодны в качестве кандидатных антигенов для активного ингредиента субъединичных вакцин.
Гибридизацию проводили посредством Вестерн-блотинга. Кратко, 2D гель после электрофореза переносили на PVDF мембрану. Затем мембрану инкубировали и гибридизировали последовательно с 1ым антителом (сыворотка, содержащая антитело к Mycoplasm spp.) и 2ым антителом (конъюгированные с AP анти-свиные IgG). Впоследствии проводили цветную реакцию с использованием раствора NBT/BCIP.
Результат цветной реакции Вестерн-блотинга показан на фигуре 2; где 10 белков, позитивных в иммуногибридизации с антителом к Mycoplasm spp., обозначали как кандидатные антигены для использования в качестве активных ингредиентов субъединичных вакцин.
Идентификация полученных кандидатных антигенов.
В соответствии с цветной реакцией Вестерн-блотинга гель, соответствующий позитивному положению на мембране, разрезали на микропептид и анализировали посредством масс-спектроскопии. Полученные данные масс-спектроскопии затем совмещали с аминокислотной последовательностью и базой данных белков для идентификации этих белков.
См. следующую таблицу 1, приведены указанные 10 белков, позитивных к иммуногибридизации с антителом к Mycoplasm spp.
10 белков, позитивных к иммуногибридизации с антителом к Mycoplasm spp. и их амино последовательность.
Пример 2: Экспрессирование указанных кандидатных антигенов в большом количестве посредством системы экспрессии генов E. coli.
Escherichia coli JM109 использовали в качестве клеток хозяина для клонирования и Escherichia coli BL21 (DE3) использовали в качестве клеток хозяина для экспрессии белка. Клетки Escherichia coli культивировали в среде LB (Luria-Bertani; Difco, Michigan, USA). В соответствии с планом эксперимента соответствующее количество антибиотика или агар 1,5% добавляли для формирования твердой среды.
Амплификация генов, кодирующих кандидатные антигены.
После того, как кандидатные антигены были идентифицированы, искали гены, кодирующие такие антигены в базе данных NCBI (National Center for Biotechnology Information). Специфичные праймеры, нацеленные на гены антигена были сконструированы соответствующим образом. Затем гены антигена амплифицировали с использованием специфичных праймеров и хромосомы M. hyopneumoniae PRIT-5 в качестве матрицы. Использованные специфичные праймеры приведены в последующей таблице 2.
Набор праймеров.
5'-GATATAGGATCCATGGACAAATTTCGCTATGTAAAGCCT G-3'
PdhAR (SEQ ID NO: 16)
5'-CAATATGTCGACTTATTTTACTCCTTTAAAAAATTCAAGCG CTTC-3'
5'-GATATAGGATCCATGAATGGAATAAATTTCTTGGCTTAGGC TTAGTTTTTC-3'
XylFR (SEQ ID NO: 18)
5'-CAATATGTCGACTTAATTTTTATTAATATCGGTAATTAGTT TGTCTAAGC-3'
5'-GATATAGGATCCATGACATACCAAGAATATCTTCAAGCAA
G-3'
EUTDR (SEQ ID NO: 20)
5'-CAATATGTCGACCTATTTACCTTCTTCAAC
TTGTAGAGCGCT-3'
5'-GATATAGGATCCATAGCTTCAAGGTCGAA TACAACTGC-3'
Mhp145R (SEQ ID NO: 22)
5'-CAATATGTCGACTTAATTTACCTTTTGGAG TATCCCATTTTC-3'
5'-GATATAGGATCCTTATCCTATAAATTTAGG CGTTTTTTCC-3'
P78R (SEQ ID NO: 24)
5'-CAATATGTCGACTTATTTTGATTTAAAAGCAGGACCTAA AT-3'
5'-GATATAGGATCCATTGGACTAACAATTTTTGAGAAATCATT TAG-3'
P132R (SEQ ID NO: 26)
5'-CAATATGTCGACTTATTCCTAAATAGCCCC ATAAAGTG-3'
5'-GATATAGGATCCATGGACAAATTTTCACGA ACTGTTCT-3'
Mhp389R (SEQ ID NO: 28)
5'-CAATATGTCGACCTAGATTTTAAAGGATTTTTTTAATTCAA TAATATAATC-3'
Полимеразную цепную реакцию (ПЦР) проводили с наборами праймеров, приведенных в таблице 2 выше, для амплификации генов кандидатных антигенов. Амплифицированные гены затем использовали системе экспрессии генов E. coli. Условия ПЦР были следующими: 5 минут при 98°C (один цикл); 30 секунд при 94°C, 30 секунд при 55°C, X секунд при 68°C (35 циклов); 5 минут при 68°C (один цикл). Указанный X являлся временем элонгации для ДНК полимеразы и его устанавливали в зависимости от размера фрагмента, который должен быть амплифицирован. После ПЦР проводили электрофорез для проверки того, если продукты ПЦР содержали фрагменты ДНК ожидаемого размера. См. фигуру 3, которая демонстрирует результат электрофореза продуктов ПЦР; где трек 1 являлся геном eutD; трек 2 являлся pdhA; трек 3 являлся xylF; трек 4 являлся геном P78; трек 5 являлся геном P132; трек 6 являлся mhp145; трек 7 являлся mhp389.
Клонирование продуктов ПЦР.
Клонирование проводили с использованием набора для клонирования ПЦР CloneJET и лигационную смесь трансформировали в E. coli ECOSTM 9-5 (Yeastern, Taipei, Taiwan). Подробный протокол может быть получен из описания продукта или модифицирован из хорошо известного протокола в данной области.
После трансформации бактерии культивировали на твердой среде LB, содержащей ампициллин (100 мкг/мл) до формирования их колонии. Затем проводили ПЦР по колониям для скринирования штаммов с успешной трансформацией. Условия ПЦР были следующими: 5 минут при 95°C (один цикл); 30 секунд при 95°C, 30 секунд при 55°C, X секунд при 72°C (25 циклов); 7 минут при 72°C (один цикл). Указанный X являлся временем элонгации для ДНК полимеразы и был установлен в зависимости от размера фрагмента, который должен быть амплифицирован. Скорость элонгации Taq ДНК полимеразы (Genomics, Taipei, Taiwan) составляет 1 т.н./мин; вследствие этого, если Taq ДНК полимераза используется для амплифицирования фрагмента ДНК 1 т.н., указанный X будет установлен на 1 минуту.
Плазмиды из штаммов, для которых было подтверждено наличие вставки ДНК в рекомбинантной плазмиде, затем подвергали ДНК секвенированию (Total Solution Provider of Systems Biology and Chemoinformatics Ltd.). Плазмиды, содержащие eutD, pdhA, xylF, ген P78, ген P132, mhp145 и mhp389 были названы pJET-eutD, pJET-pdhA, pJET-xylF, pJET-P78, pJET-P132, pJET-mhp145, pJET-mhp389, соответственно.
Точечная мутация и клонирование генов антигена M. hyopneumoniae.
Перед амплифицированием кандидатных антигенов в системе экспрессии генов E. coli необходимо рассмотреть значение кодона в различных организмах. При этом, если ген содержит кодон, который будет неодинаково кодироваться в организме, из которого он происходит, и E. coli, ген должен быть модифицирован точечной мутацией.
Гены антигена M. hyopneumoniae, pdhA, xylF, ген P78, ген P132, mhp145 и mhp389, содержат кодон TGA (eutD не имеет проблем со значением кодона подобно другими). Кодон TGA транслировался в триптофан в Mycoplasma spp., но транслировался как стоп-кодон в E. coli. Для того чтобы предотвратить невозможность продуцирования целого белка в системе экспрессии генов E. coli, сконструировали праймеры, нацеленные на сайт TGA, и проводили точечную мутацию, замещающую TGA на TGG с использованием полимеразной цепной реакции с перекрывающимися удлинениями. В результате, гены, которые должны быть экпрессированы в системе экспрессии генов E. coli, могут быть безошибочно транслированы в кандидатный антиген данного изобретения. Кроме того, сайты рестрикции BamHI гена P78, гена P132 и mhp389, были подвержены молчащей мутации для удобства клонирования.
Праймеры, использованные для точечной мутации, сконструировали, чтобы сайт точечной мутации был расположен в центральной части праймера и чтобы значение Tm было выше 78°C. Значение Tm праймеров для точечной мутации рассчитывали с использованием формулы, предоставленной Invitrogene Co.: Tm=81,5+0,41 (%GC) - 675/N - % несоответствия; где %GC обозначает процентное содержание GC относительно общего количества нуклеотидов, содержащихся в рассматриваемом праймере; N обозначает длину рассматриваемого праймера; %несоответствие обозначает процентное содержание основания, которое должно подвергнуться мутации относительно общего содержания нуклеотидов, содержащихся в рассматриваемом праймере. Наборы праймеров, использованных для вышеуказанных генов, приведены в последующих таблицах 3-8.
Наборы праймеров для точечной мутации pdhA.
SEQ ID NO: 29
SEQ ID NO: 30
SEQ ID NO: 31
SEQ ID NO: 32
SEQ ID NO: 33
SEQ ID NO: 34
SEQ ID NO: 35
SEQ ID NO: 36
SEQ ID NO: 37
SEQ ID NO: 38
SEQ ID NO: 39
SEQ ID NO: 40
SEQ ID NO: 41
SEQ ID NO: 42
SEQ ID NO: 43
SEQ ID NO: 44
Наборы праймеров для точечной мутации xylF.
SEQ ID NO: 45
SEQ ID NO: 46
SEQ ID NO: 47
SEQ ID NO: 48
SEQ ID NO: 49
SEQ ID NO: 50
SEQ ID NO: 51
SEQ ID NO: 52
SEQ ID NO: 53
SEQ ID NO: 54
SEQ ID NO: 55
SEQ ID NO: 56
SEQ ID NO: 57
SEQ ID NO: 58
Наборы праймеров для точечной мутации гена P78.
SEQ ID NO: 59
SEQ ID NO: 60
SEQ ID NO: 61
SEQ ID NO: 62
SEQ ID NO: 63
SEQ ID NO: 64
SEQ ID NO: 65
SEQ ID NO: 66
SEQ ID NO: 67
SEQ ID NO: 68
Наборы праймеров для точечной мутации гена P132.
SEQ ID NO: 69
SEQ ID NO: 70
SEQ ID NO: 71
SEQ ID NO: 72
SEQ ID NO: 73
SEQ ID NO: 74
SEQ ID NO: 75
SEQ ID NO: 76
SEQ ID NO: 77
SEQ ID NO: 78
SEQ ID NO: 79
SEQ ID NO: 80
SEQ ID NO: 81
SEQ ID NO: 82
SEQ ID NO: 83
SEQ ID NO: 84
SEQ ID NO: 85
SEQ ID NO: 86
SEQ ID NO: 87
SEQ ID NO: 88
Наборы праймеров для точечной мутации mhp145.
SEQ ID NO: 89
SEQ ID NO: 90
SEQ ID NO: 91
SEQ ID NO: 92
Наборы праймеров для точечной мутации mhp389.
SEQ ID NO: 93
SEQ ID NO: 94
SEQ ID NO: 95
SEQ ID NO: 96
SEQ ID NO: 97
SEQ ID NO: 98
SEQ ID NO: 99
SEQ ID NO: 100
Способ точечной мутации кратко разъяснен ниже. Хромосому M. hyopneumoniae PRIT-5 использовали в качестве матрицы и ДНК фрагменты амплифицировали с использованием наборов праймеров, приведенных в таблицах 3-8 выше.
Реакционная смесь для ПЦР объемом 50 мкл содержала буфер для ПЦР 1× GDP-HiFi, 200 мкМ смеси dATP, dTTP, dGTP и dCTP, 1 мкМ праймеров, 100 нг хромосомы M. hyopneumoniae PRIT-5 и 1 Ед ДНК полимеразы GDP-HiFi. Условия ПЦР были следующими: 5 минут при 98°C (один цикл); 30 секунд при 94°C, 30 секунд при 55°C, X секунд при 68°C (35 циклов); 5 минут при 68°C (один цикл). Указанный X являлся временем элонгации для ДНК полимеразы и был установлен в зависимости от размера фрагмента, который должен быть амплифицирован. Скорость элонгации ДНК полимеразы GDP-HIFI (GeneDirex, Las Vegas, USA) составляет 1 т.н./15 секунд; вследствие этого, если ДНК полимераза GDP-HIFI используется для амплифицирования фрагмента ДНК 1 т.н., указанный X будет составлять 15 секунд. После ПЦР проводили электрофорез для проверки того, если продукты ПЦР содержали фрагменты ДНК ожидаемого размера. Затем продукт ПЦР был рециркулирован с использованием набора системы для выделения из геля Gel-MTM.
Впоследствии продукт ПЦР использовали в качестве матрицы и амплифицировали с использованием наборов праймеров, приведенных в таблице 2 выше. Условия ПЦР были следующими: 2 минуты при 98°C (один цикл); 30 секунд при 94°C, 30 секунд при 55°C, X секунд при 68°C (35 циклов); 5 минут при 68°C (один цикл). Указанный X являлся временем элонгации для ДНК полимеразы и был установлен в зависимости от размера фрагмента, который должен быть амплифицирован. Скорость элонгации ДНК полимеразы GDP-HIFI (GeneDirex, Las Vegas, USA) составляет 1 т.н./15 секунд; вследствие этого, если ДНК полимераза GDP-HIFI используется для амплифицирования фрагмента ДНК 1 т.н., указанный X будет составлять 15 секунд. После вышеуказанного этапа амплификации может быть получена полноразмерная последовательность кандидатных генов антигена с точечной мутацией.
Затем продукт ПЦР выделяли с использованием набора системы очистки PCR-MTM (GeneMark, Taichung, Taiwan) и проводили его клонирование использованием набора для клонирования ПЦР CloneJET. Проводили ПЦР по колониям для подтверждения того, что штаммы после трансформации, содержали плазмиду, имеющую вставку ДНК, и затем плазмиды выделяли для ДНК секвенирования (Total Solution Provider of Systems Biology and Chemoinformatics Ltd.). Плазмиды, содержащие мутированные кандидатные гены антигена, были названы pJET-pdhAM, pJET-xylFM, pJET-P78M, pJET-P132M, pJET-mhp145M, pJET-mhp389M, соответственно.
В соответствии с результатом секвенирования ДНК последовательности кандидатных генов антигена после точечной мутации являлись такими, как показано в SEQ ID NO:01 (pdhA), SEQ ID NO:02 (xylF), SEQ ID NO:03 (eutD, был без точечной мутации), SEQ ID NO:04 (mhp145), SEQ ID NO:05 (ген P78), SEQ ID NO:06 (ген P132), SEQ ID NO:07 (mhp389).
Конструирование экспрессионных векторов для экспрессирования антигенов M. hyopneumoniae
В этой части экспериментов плазмиду pET-MSY использовали в качестве остова для конструирования экспрессионного вектора для экспрессирования антигена M. hyopneumoniae. pET-MSY является производной pET29a и имеет MsyB E. coli. Вследствие этого, экспрессированный рекомбинантный антиген будет иметь партнера слияния MsyB. MsyB имеет большое содержание кислотных аминокислот и способен к увеличению растворимости экспрессированного белка.
После того, как pJET-eutD, pJET-pdhA, pJET-xylF, pJET-P78, pJET-P132, pJET-mhp145 и pJET-mhp389 были расщеплены BamHI и SalI, полученный фрагмент ДНК встраивали в pET-Msy, расщепленную предварительно с такими же рестрикционными ферментами, посредством лигазы. Затем pET-Msy с ДНК фрагментом трансформировали в E. coli ECOS 9-5. Проводили ПЦР по колониям для подтверждения штаммов после трансформации, содержащих плазмиду, имеющую вставку ДНК, и затем плазмиды выделяли из них для секвенирования ДНК (Total Solution Provider of Systems Biology and Chemoinformatics Ltd.). Плазмиды c подтвержденной корректной ДНК последовательностью были названы pET-MSYEutD, pET-MSYPdhA, pET-MSYXylF, pET-MSYP78, pET-MSYP132, pET-MSYMhp145 и pET-MSYMhp389, соответственно. Такие полученные плазмиды являлись примерами экспрессионных векторов для профилактики инфекции Mycoplasma spp. по данному изобретению.
Экспрессия и выделение антигенов M. hyopneumoniae
Векторы для экспрессии антигена трансформировали в E. coli BL21 (DE3). Единичные колонии штаммов, являющихся результатом трансформации, инокулировали в жидкую среду LB, содержащую канамицин (рабочая концентрация: 30 мкг/мл). После культивирования в течение ночи 37°C, 180 об./мин. суспензию бактерий разбавляли в соотношении 1:100 и инокулировали снова в другую жидкую среду LB, содержащую канамицин (рабочая концентрация: 30 мкг/мл). Бактерии культивировали при 37°C, 180 об./мин. до OD600 вследствие этого достигая приблизительно от 0,6 до 0,8. Затем добавляли 0,1 мМ IPTG для индуцирования экспрессии. После индукции в течение 4 часов осадок собирали центрифугированием (10000×g, 10 минут, 4°C) и экспрессию проверяли посредством белкового электрофореза.
Впоследствии использовали аффинную хроматографию с иммобилизованными металлами (IMAC) для выделения белка посредством ковалентного связывания между His tag N-конца рекомбинантного белка и ионами никеля или ионами кобальта. Протокол выделения белка соответствовал описанию продукта QIAexpressionistTM (fourth edition, Qiagen). Осадок суспендировали в буфере для лизиса (50 мМ NaH2PO4, 300 мМ NaCl, 10 мМ имидазол, pH 8,0) и разрушали ультразвуковым гомогенизатором. После центрифугирования (8000×g, 15 минут) отбирали супернатант для введения в колонку с 1 мл смолы Ni-NTA. Рекомбинантные антигены должны были связаться на указанной смоле. Затем в колонку вводили 15 мл промывочного буфера (50 мМ NaH2PO4, 300 мМ NaCl, 20 мМ имидазол, pH 8,0) для промывки смолы, чтобы неспецифически связанные белки были удалены. В заключение, добавляли 20 мл элюирующего буфера (50 мМ NaH2PO4, 300 мМ NaCl, 250 мМ имидазол, pH 8,0) для вымывания рекомбинантных антигенов со смолы; в которой имидазол с высокой концентрацией может конкурировать за сайт связывания на смоле с рекомбинантными белками и посредством этого вызывая вымывание рекомбинантных белков. Результат выделения затем проверяли электрофорезом белков.
Кандидатные антигены данного изобретения, собранные посредством выделения, могут затем быть использованы для последующих иммунных испытаний для подтверждения возможности их использования в качестве активного ингредиента субъединичных вакцин против Mycoplasm spp.
Пример 3: Эксперименты иммунной стимуляции свиней кандидатными антигенами данного изобретения.
В этом примере кандидатные антигены данного изобретения использовали в качестве активного ингредиента для приготовления субъединичных вакцин и тестировали на их иммунные эффекты в живой свинье.
Приготовление вакцины
Один выделенный рекомбинантный антиген или несколько выделенных рекомбинантных антигенов смешивали с алюмогелем в качестве адъюванта для приготовления субъединичной вакцины или коктейльной субъединичной вакцины. Каждая доза приготовленной вакцины имела объем 2 мл, и содержание каждого вида антигена составляло 100 мкг.
В последующей таблице 9 приведены образцы, приготовленные в этом примере для экспериментов иммунной стимуляции.
Образцы вакцины, приготовленные в примере 3
Эксперименты иммунной стимуляции свиней проводили с использованием Bayovac® MH-PRIT-5 (изготовлен с использованием M. hyopneumoniae PRIT-5, в качестве позитивной контрольной группы), субъединичных вакцин (образцы 1-7 данного изобретения) и коктейльных вакцин (образцы 8 и 9 данного изобретения).
33 свиньи SPF возрастом 4 недели доставляли из Научно-исследовательского института сельскохозяйственной технологии и кормили с одинаковыми кормом, окружающими условиями и условиями роста в свинарнике перед экспериментами.
После того, как свиней вскармливали до возраста 35 дней и 49 дней, свиньям вводили 2 мл вышеприведенной вакцины посредством внутримышечной инъекции.
Стимуляционные эксперименты
Вышеуказанных свиней, подвергаемых индуцированию иммунного ответа, стимулировали Mycoplasm spp. в возрасте 109 дней для подтверждения иммунного эффекта вышеуказанных вакцин.
Сначала легкое, отобранное у свиней, инфицированных Mycoplasm spp., измельчали в 20 мл среды Фриза и центрифугировали при 148,8×g в течение 10 минут. Супернатант удаляли для очистки пробирки и центрифугировали снова при 7870×g в течение 40 минут. Затем супернатант удаляли и осадок суспендировали в 6 мл среды Фриза для получения суспензии. Впоследствии суспензию фильтровали через мембраны 5 мкм и 0,45 мкм последовательно для получения растворов бактерий, требующихся для стимуляционных экспериментов.
Раствор бактерий (5 мл) вводили подвергнутым наркозу свиньям через их трахею. После 28 дней введения свиней умерщвляли и вскрывали для отбора их легкого. Иммунный эффект проверяли посредством наблюдения за легким и регистрировали в соответствии со следующими критериями: наблюдаемый патологический признак в любой из средних верхних долей и верхних долей любой стороны легкого оценивали как 10 баллов; наблюдаемый патологический признак в любой средней верхней доле и диафрагмальных долях любой стороны легкого, оценивали как 5 баллов. Общая оценка составляла 55 баллов. Запись результатов наблюдения представлена на фигуре 4.
По сравнению с результатами неинъецированных свиней семь кандидатных антигенов данного изобретения были способны обеспечивать иммунные эффекты, эквивалентные общепринятой вакцине (Bayovac® MH-PRIT-5). Если принимать во внимание более высокую безопасность субъединичных вакцин, то вакцины, содержащие кандидатные антигены данного изобретения, должны иметь большую ценность.
С другой стороны не являлось обычным использование двух или более антигенов, которые должны индуцировать иммунные эффекты в одной вакцине из-за того, что два или более антигенов могут не обеспечивать двойной иммунный эффект. В действительности имеет место более высокая вероятность того, что два или более антигенов будут препятствовать друг другу и в результате снижать иммунный эффект вакцины. В соответствии с результатом этого примера, образец 8 и образец 9 данного изобретения (т.е. коктейльная вакцина) неожиданно обеспечивали существенное возрастание иммунного эффекта. При этом субъединичные вакцины данного изобретения не только имеют высокую безопасность, но также предоставляют больший иммунный эффект, когда кандидатные антигены данного изобретения использованы в комбинации.
Рядовой специалист в данной области может легко понять любые возможные модификации на основании открытия данного изобретения без выхода за рамки основной идеи данного изобретения. Вследствие этого примеры выше не должны быть использованы для ограничения данного изобретения, но подразумевают охватывание любых возможных модификации в рамках основной идеи и объема данного изобретения в соответствии с приведенной далее формулой изобретения.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ СЕЛЬСКОХОЗЯЙСТВЕННОЙ ТЕХНОЛОГИИ
<120> Субъединичная вакцина против Mycoplasma Spp
<130> GPI13TW0261-RU-1
<160> 100
<170> PatentIn version 3.5
<210> 1
<211> 1125
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> мутированный ген pdhA
<400> 1
atggacaaat ttcgctatgt aaagcctggt caaattatgg caaaagatga agaaatgatt 60
cgctttcttg atattgatgg taatctttta tcttcaactg tttttggacc aatcgacgaa 120
acaaatgata ttcgcttatc aaaacaggaa atcaaaaaag cttatgaatt tatggtttta 180
tctcgccaac aagatacgta tatgacacaa ctacagcgac aaggtagaat gttgactttt 240
gcccctaact ttggtgaaga agctcttcaa gtagcctcag ggatggcgct aacaaaagat 300
gactggtttg tcccagcttt tcgttcaaat gcaacaatgt tatatcttgg cgtgccaatg 360
atcttgcaaa tgcaatattg gaatggtagc gaaaaaggta atgtaattcc cgaaaatgtt 420
aatgttttac ctattaacat tcccatcgga acgcagtttt cccatgctgc cggaattgct 480
tatgcagcaa aactaacagg taaaaaaata gtttcaatga gttttattgg aaacggggga 540
actgccgaag gcgagtttta cgaggcgcta aatattgcaa gtatttggaa atgaccagtt 600
gttttttgcg taaataacaa tcaatgggca atttcaaccc caaataaata tgaaaacggt 660
gcctcaacaa ttgctgcaaa agcaatggca gccggaattc ctggaattcg tgtagacgga 720
aatgaccttt tagcttctta tgaagtaatc aaggaagctg ttgattatgc tcgttctgga 780
aacggtcctg ttcttgttga gtttgtaact tggcgtcaag gtgttcatac ctcttctgat 840
aatccacgaa tttatcgtac tgttgaagag gaaagagaac acgaaaaatg ggaaccaatg 900
caccggattg aaaaatatat gtttgaccgc ggaattcttg attctgccga aaaacaaaaa 960
atttgggatg aagcgcttgc gattgtcaaa gaaacttatg aaaaatctct tgttgggctt 1020
gagtcaacaa ttgatgaaat tttcgatcat acctacaagg ttttaccacc agaacttgaa 1080
gaacaaaaac aagaagcgct tgaatttttt aaaggagtaa aataa 1125
<210> 2
<211> 1344
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> мутированный ген xylF
<400> 2
atgaaatgga ataaatttct tggcttaggc ttagtttttc cgctttcagc aatcgcgaca 60
atctctgccg gatgttggga taaagaaaca actaaagaag aaaaatcagc cgataatcaa 120
aataaacaaa tcactgatgt ctcaaaaatt tcaggactag ttaatgagcg aaaatccgaa 180
attatggccg caaaagctga tgcaaacaaa cattttgggc taaatatggc aattgtaacc 240
gctgatggaa cggtaaatga taattcattt aaccaatcaa gttgggaggc aattcaacaa 300
cttggcgctc ttactggagg tgagattact tcagtagata gttcaactgc tgaacttgaa 360
ggaaaatata gctcacttgc taataccaac aaaaatgttt gggtactttc tggttttcaa 420
cacggtgatg cgatcacaaa atggttaaaa atccctgaaa ataagcaatt atttactgaa 480
aaaaatatta tcatactcgg aattgactgg actgatactg aaaatgtaat tccaacaggt 540
cgatatatta atttaaccta taaaactgaa gaagccggat ggcttgcagg atatgcgaat 600
gcttcctttt tggcaaaaaa attcccaagt gatccaacta aaagatcagc aattgttatc 660
ggtggtggga ttttcccagc tgtaactgat tttatcgctg gttatctagc cggaattaaa 720
gcttggaatc taaaaaattc tgataaaaaa acaaagataa caactgataa aatcgaaata 780
aatcttgggt ttgattttca aaatacttca acaaaagaaa gacttgaaca aattgcttca 840
aaagataaac cttcaacact attagcagtc gctggaccac ttactgaaat tttctcggat 900
ataatcgcaa accaaaatga tcgttatctc attggtgttg acaccgacca atcacttgtt 960
tatacaaaaa ctaaaaataa atttttcacc tcaattttga aaaatttagg ttactccgtt 1020
ttcagtgttc ttagtgattt atataccaaa aaatcaaatt caagaaattt agccggcttt 1080
gaatttggta aaaaaagtgc aaccgtttat cttggaatta aagacaagtt tgtcgatatt 1140
gctgatactt ctttagaagg aaatgataaa aaactcgcaa ctgaagccat ttctgaagct 1200
aaaaaagaat ttgaagaaaa aactaagaca actcctgccg aagaagttcg taaaacttta 1260
gaaattccgg aaatgactga taaacaacct gataaacaac aggaaagctt agacaaacta 1320
attaccgata ttaataaaaa ttaa 1344
<210> 3
<211> 954
<212> ДНК
<213> Mycoplasma hyopneumoniae
<400> 3
atgacatacc aagaatatct tcaagcaaga cttgagcaac aaaatgagac aaaaagttta 60
cgctcagttc taattattga tggtgctgat ccgcgagcaa ttgccgcggc aaaactttta 120
aaggaaaaaa atttagtaaa accggtttta ctagttgatg aagaaattcc aaatcttgac 180
gttgatcaac atatagttaa ttttcaagaa aaaatggaat ttattaagga atttcttaaa 240
ttccgcaagg gaaaagaaac tcctgagtca gccgaaattc aatttcaatc aaatgctttt 300
tatggaacaa tgctactaag aaagaaaaaa gtagatgcag ttgtcggggg tcttaattac 360
ccaacagccg aaattttacg agcagctttt aaaataatcg ggccaaaacc aaatataaaa 420
acaatttcat cagtaatgat tatgcataaa gatcaggaaa aatatttatt tagtgatatt 480
tcagtaaata ttgctccaaa tgagaatcaa cttgttgata ttgctaaaaa tgcccttgat 540
tttgctattc agttaggttt tgatccaaaa ccagcttttc tttccttttc aacaaaagga 600
tcagcaaaat caccgcagtc agaattagtg gctaaagcga cgcaaatgtt taatgcaaca 660
tccccaattg aagcttatgg tgaaattcag cttgatgccg cccttgatat tgaagttcgc 720
cgccaaaaat atgaagtaaa tgtaggtaaa aacgccaata ttttaatttt cccgaatctt 780
gatgcaggaa atattggcta taaaattgcc caaagattgg gaaattttgg ggcaattggc 840
ccaataatta ccggaattaa tgccccaatt aatgatttat cccggggatc aacaactcaa 900
gatgtcttta ataccgtgct aattagcgct ctacaagttg aagaaggtaa atag 954
<210> 4
<211> 1122
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> мутированный ген mhp145
<400> 4
atagcttcaa ggtcgaatac aactgccaaa gttgccccag ttgctgttgt tttctcaaca 60
agaaataatc cttttttcca aaatgttgaa aaagggattg aaacagcggc aaaagaatta 120
ggagttgact atgaagtcta tgactctgaa aatgactcgg ataaagaagc aagaaatatt 180
tcaaatatta ttgcaaaaca acaaaaagtt gtaattttta acgatgttaa tgaagattca 240
ggaatctcag ctgttaaaaa attaaatcaa gctggaattc cggtaattgc cactgatcat 300
ttactaaatt cgccaaaagc cttagaagca aaaattaaag ttgaagccaa tattgcttct 360
gataataaac aagcaggagt aattcttgcc cagtttatgg cccaaaaaat cggacttcct 420
caagattcac ttacttattc agtctatgga attcccggaa ctgaatcagg ggaatcccga 480
gctcaagggt ttattgaaac agttaaaaat ctaaataatc aagcaataaa atacaacctt 540
ttttcttatg gaaaatacgg aaaagaaaat gcaaatggaa aaacttacat cggaagacaa 600
gctgatgata atcgcgatct agcaaatcaa agagttgcaa atgatgcaac gcaagtattc 660
caagatgctc aaaaaaggcc acttttggtt tttgggacta atgatgaagc tgccttaggt 720
tcaatttctg cccttgaaag tgcccagatt ccattaggag gtggagataa attccttcca 780
ggttcaggaa aagtttatat taccggagtt gattatacaa atgatgctca aaaagcggta 840
ttaaataata aattatcagc aactgttgaa caagatactg atcttttagg aagactttct 900
ttaataattg cagaaaaaat tcttaaagat caatggaaaa caagtaaata ttctgatttt 960
tattcacaat ttcctcagct tgataaagac aaaaatcctg atgatcaagt tgagcaagga 1020
tattatttta aagtaggaac aaaacttttc tggaaaggac cagatggaaa aggtgaaaaa 1080
cttcaagccg atgaaaatgg gatactccaa aaggtaaatt aa 1122
<210> 5
<211> 2076
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> мутированный ген P78
<400> 5
ttatcctata aatttaggcg ttttttccta accagcgcac ttagttttgc tcccttggct 60
ttagttgcaa gttgtgttaa taattcccga tttgattcaa atgaggataa taaattagtt 120
tttggtcata ctttttcatc ttcaggaaaa gaggcaaaag cacttgagaa aattattgaa 180
gtctggaata aaactgcaac taatcaaaaa gattttatca aaatggaagc acaatatttc 240
cagaatggct ataatggatc agcggcttca attacaaact ttttacagac aaaagatcgg 300
ataaaactgc caaatattgt cacaaattat ccttcacttc tggcaatagt taataaatat 360
tcaatgactt ttccgcttgt taaagatttt agttctaatc aagaaccaca agatgaaaat 420
gaaaaagcaa taaaaaagtt cctaaaagag caaggaattt ctgatttcct tgagattaat 480
aaagaagttc ctttccttga tacaaaggga gtttataccc ttccatttgg aaaatcaact 540
gaagttctta caattaataa agttttgttt ggttggatga ttaataaagc acttgctgat 600
ccaaaaaagc cagcaaaaat taaagaagaa gataaacctt attttgccga atttcaaaaa 660
ttaggcaagg aaaaaactgg tgatattaaa gaaattgaaa gaatctggaa aaaatatgtc 720
tccgatgatc aaggacttgc aggctatgaa tttcgccgat ccgatcttga aaattttact 780
gacctacaga aattatcatc acgaattctt cgttcttttc cagaggccct ttcaggaggc 840
tccactgatt cggcaaaatc agttttagga attgataatc aagcaacgct agtttttgct 900
cttgccagat cagtttcaga aggtaatcga tcccaggaag ttactgttct tgataggcaa 960
aagaatttaa ttgattatat atcttttata gataaacctg attcaattag atataaaaat 1020
ttagaaaaaa tttttaattt attaagccaa gggataaaag atcgctcaat ttattataca 1080
tctgcagggg agtataattc aacttttttc cggaatcatc agcaggtttt ctcaattggt 1140
tcaacttcag gctatttcca taattttgtc aaaccaacag cgacaaatta tcaaatcgga 1200
tttaagaaaa atgatggtct taagtcagtt tatagcgtta gctatcccaa atttagcgca 1260
attgtatcac ttgaagatct caaggatata accaaagatc tagaaataac agcaaccgat 1320
ggtagctcta aattaaaaat tgatgctaaa tttttaggaa aactcaaaga atatgcacag 1380
caaaatccag ttaaaaaagt gttttatttt actgatcgat cagaaaaacc ttcaggtatc 1440
ttcgaaaaag attatattgt tttaggcaaa tacaaaaatg ataaaaatga agaatttaat 1500
ggccttgtaa ttccaactta tacagaactc tataaaaatt ctggatcaaa tgcccttaat 1560
gatgatgaac ttgcacttga agccccaccg cataaattcg atgcaaatag taaaatcacc 1620
cccattgtcg cccaaggtcc tgatctaatt tttattcatt caactgaaaa agaagataaa 1680
gccgcaaaag cttttgttaa atggcttttg acagaaaaaa tagtctttga ggaaaatagt 1740
caggaaaaaa tgactccgct tgagtatttt gccagagcaa cctcatattt attgccaata 1800
aaatcaacgc ttgataaaac ccattttagt ccaaaaaata gatctcagaa attcatactt 1860
gaccaattta gtaaatttct taatgctgat tcaaaaggaa aatattcgct tgtctatgat 1920
aatgccgatg caaatgcttc atccttccgt gaatcactag attcttcagt tgcccagatg 1980
caatcattaa aagccagcga tggaaaacta cgtagtttta aagagttttt agaaaaacta 2040
gagggaaatt taggtcctgc ttttaaatca aaataa 2076
<210> 6
<211> 3549
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> мутированный ген P132
<400> 6
attggactaa caatttttga gaaatcattt agttcccaag tttcaggagg ggtcgataag 60
aacaaagttg tggatttaaa atcagattca gatcaaatct tctcagaaga agattttata 120
agagcagttg agaatcttaa actttttgat aaatataaac atctaacagc aagaatggca 180
ttaggacttg ctagggaagc agctaatgcc tttaactttt tagatactta tgactacacc 240
ccaattacaa aacattcatt taagatttct ttggatattt ccgatgcctt tgcggctaat 300
aaagaagtaa aagcggtagt ggttagtgca tattcccaaa aatatcaagt tacctattca 360
agactaactt ctctaaaagg ttggaaagaa gaagatgatt ttggcgatga tattatagat 420
tatcaaatta atcaagagct ttcaggtcta tcactttctt ccttagcccc tgaaagcgcg 480
catcttttag cctcagaaat ggcttttcgg cttgataatg actttcaagt tgcatataaa 540
aaaacaggat caagagccga ggcttttcgt caggccttga taaagaatta tcttggttat 600
aacttagtta accgccaagg tttgcccact atgctccaaa agggttatgt gctagccccc 660
aaaacaattg aaaataaaaa tgcaagcgaa gaaaaattag taaatataaa tgaaaatgac 720
cgtgcaaggg ttaataaact acaaaaagta gaaaatctag cctttaaaaa cttaagtgat 780
ccaaatggaa cgctttctat tacttttgaa ctctgggacc caaatggtaa attagtatcc 840
gaatacgatt ttaaaattaa gggaatcaaa aaacttgatt ttgatcttaa aaaacaagag 900
gaaaaagtac ttcaaaaagt aactgaattt gttgagatta aaccttatgt tcaattaggt 960
ttaatccgtg ataatttatc attgtctgaa attatctata aaaatgataa taatccggag 1020
tatcttagga aaatattagc taaactaaaa gaacacaata acaacaaaag ggtggataat 1080
aatacatcca ctactaaatt tcaagaagag gatcttaaaa acgaaccaaa ttctaatgga 1140
tcagaacaag attctttcga gaaagcaaag gaaaatttcc ttagtttttt tgatctaagg 1200
tcgagactaa ttcctattcc cgatcttcct ttatattatc ttaaagttaa ttcaattaat 1260
tttgatagaa atattgaaga aaatgaaaaa gaaaaattat taaaaaatga acaagtagta 1320
ctcaaagtag attttagtct taaaaaagtt gttagcgata ttagagctcc ttacctagtt 1380
tctagtcagg ttagatcaaa ttatcccccg gttttaaaag cttcgctagc aaaaataggt 1440
aaggggtcaa attcaaaagt tgtcctttta gatcttggaa atttatcttc aagatttaaa 1500
gttcaacttg attatagtgc aaaacaaaga gaaataatta atactttatt aaaggaaaat 1560
ccagaaagag aaaaagaatt acaagctaaa attgaaagta agacgtttag tccaatagat 1620
cttaacaatg atgatctatt agcaatcgaa tttcaatatg aggataaccc tgaaggagat 1680
tggataactt tagggagaat ggaaaagtta gtcaaagagg ttatccaata taaaaaagaa 1740
ggtaaaacct tcttagatga tgaagtcgcg aaaacacttt attatttaga tttccatcat 1800
ctacctcaaa gtaaaaaaga cctcgaagaa tataaagaaa aacacaaaaa caagtttatc 1860
agcgaaataa aacctgctac accagcaagt caagcaaaaa caagtcaagc aaaaaatgaa 1920
aaagaagtaa aacctgaatc agcccaagca gaagcttcat cttcaaattc taatgattct 1980
agtagtaaaa ccacttcttc ttcaagtatg gcgggtacaa cccaaaataa atctacagaa 2040
actccaaatt caagttcaaa ttcaacacca acaagttcag caacaacttc agcaacaact 2100
tcaacaacaa gttcaaattc aagttcaaca acaagttcaa caacaacaac aacttcaaca 2160
caagcagcaa caacttcagc ctcttcggct aaagtaaaaa caactaaatt ccaagaacaa 2220
gtaaaagaac aagaacaaaa acaagaaaaa gcaaaagaaa ctaaccaatt attagatact 2280
aaaagaaata aagaagactc agggcttgga ttaattcttt gggatttcct agtaaattca 2340
aaatataaaa ctctaccagg aactacctgg gatttccatg ttgaaccaga taatttcaat 2400
gatcgtctaa aaataacagc gattctaaaa gaaaatacat cccaggcaaa gtcaaaccca 2460
gatagtaaaa acctaacttc cctatcacga aaccttataa taaaaggggt tatggctaat 2520
aaatacattg actacttagt ccaagaagat ccagtacttc ttgtagatta tacaagaaga 2580
aaccagatta aaaccgaaag agaaggacaa ctaatttgga gccagttagc ttcccctcaa 2640
atggcatctc ctgaatctag tcccgaaaag gctaagctcg agatcaccga ggaaggactc 2700
cgtgttaaaa aaggtggcac taagataaaa gagacaagaa aaagcacaac cagcaatgct 2760
aaaagcaata ctaactccaa accaaataaa aagttagtcc tactaaaagg gtctataaaa 2820
aacccgggaa caaaaaagga atggattctt gtaggatctg ggaataaggc caccaaaaac 2880
ggaagctcca gcaacaactc caatacgcaa atatggataa cccgtctagg aacatctgtt 2940
ggttcattaa aaaccgaagg tgagacagtc cttggaattt cgaataataa ttcccaaggg 3000
gaagttctct ggactactat taaatccaaa ctcgaaaacg aaaataactc agataacaat 3060
caaatccaat actccccaag tacgcatagt ttaacaacca attctcgatc aaatacccaa 3120
caatcagggc gaaatcaaat taaaattaca aacacgcaaa ggaaaacaac aacttcgcca 3180
agccaaaatc taagtcaaaa tcctgatctc aaccaaattg atgtaagact tggtctacta 3240
gtacaagaca aaaaacttca cctttggtgg attgctaatg atagctctga tgagcctgag 3300
catataacaa ttgatttcgc tgaagggaca aaatttaatt atgatgattt aaattatgtc 3360
ggagggcttt taaaaaatac tacaaataat aacaatatgc aaacccaaga cgatgaaggt 3420
gatggatatc ttgccctaaa aggattaggt atctatgaat ttcctgatga tgaaagtatt 3480
gatcaacccg ctactgttga aaaggcagag agattatata aacactttat ggggctattt 3540
agggaataa 3549
<210> 7
<211> 1053
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> мутированный ген mhp389
<400> 7
atggacaaat tttcacgaac tgttctcggt gatattcacc catcggaatt aggtgttgtt 60
gactgtcatg atcatttaat taaaaattat ggaccaaaag ctcacgaaca tccggatttt 120
gtaatgttat caaatgaggc tgcaattgct gaatcacttg aatatgcttc ccggggtgga 180
aaaacaatag tgacaatgga ccccccaaat gttggtcggg atgtctatcg aatgttaaag 240
attgccaaag ctcttgaagg aaaagtgcat attattatgg caactggatt tcataaagcg 300
gctttctatg ataaaggcgc atcatggctt gcgcttgcac caacagatga aattgtaaaa 360
atggttgttg ctgaaattac acagggaatg gatgaatata attattcagg tcctgtggtt 420
agacgttcaa aagccaaagc aggaattatc aaagccggaa ctggatatgg agcaattgat 480
cgacttgaat taaaatcact tgaggttgca gcaagagcct caattgaaac cggggcaccg 540
attttggttc atacccaatt aggaacaatg gcctatgaag cggcaaaata tttaattgat 600
tttggtgcaa atccacggaa aattcagatc tcacatctta ataaaaaccc tgataaatat 660
tattatgcaa aaataattaa agaacttggg gtatctttat gttttgatgg tcctgatcgg 720
gttaagtatt ttcctgatac aactcttgct gaaaatatta aatatcttgt cgatttagga 780
ctagaaaaac atattacctt atcacttgat gccggtcgtg ttttatatca gcgaaattat 840
ggaaaactta aaggtaaatg gacttttgga ctaacctatt tattcgatcg gtttattccg 900
cttttagaac aagttggaat tagcaaggaa acaattaata atattcttgt taataatcca 960
gctgaaattc ttgcctttga tcagccaaga aaatttgatc catcaattct tccagattat 1020
attattgaat taaaaaaatc ctttaaaatc tag 1053
<210> 8
<211> 374
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 8
Met Asp Lys Phe Arg Tyr Val Lys Pro Gly Gln Ile Met Ala Lys Asp
1 5 10 15
Glu Glu Met Ile Arg Phe Leu Asp Ile Asp Gly Asn Leu Leu Ser Ser
20 25 30
Thr Val Phe Gly Pro Ile Asp Glu Thr Asn Asp Ile Arg Leu Ser Lys
35 40 45
Gln Glu Ile Lys Lys Ala Tyr Glu Phe Met Val Leu Ser Arg Gln Gln
50 55 60
Asp Thr Tyr Met Thr Gln Leu Gln Arg Gln Gly Arg Met Leu Thr Phe
65 70 75 80
Ala Pro Asn Phe Gly Glu Glu Ala Leu Gln Val Ala Ser Gly Met Ala
85 90 95
Leu Thr Lys Asp Asp Trp Phe Val Pro Ala Phe Arg Ser Asn Ala Thr
100 105 110
Met Leu Tyr Leu Gly Val Pro Met Ile Leu Gln Met Gln Tyr Trp Asn
115 120 125
Gly Ser Glu Lys Gly Asn Val Ile Pro Glu Asn Val Asn Val Leu Pro
130 135 140
Ile Asn Ile Pro Ile Gly Thr Gln Phe Ser His Ala Ala Gly Ile Ala
145 150 155 160
Tyr Ala Ala Lys Leu Thr Gly Lys Lys Ile Val Ser Met Ser Phe Ile
165 170 175
Gly Asn Gly Gly Thr Ala Glu Gly Glu Phe Tyr Glu Ala Leu Asn Ile
180 185 190
Ala Ser Ile Trp Lys Trp Pro Val Val Phe Cys Val Asn Asn Asn Gln
195 200 205
Trp Ala Ile Ser Thr Pro Asn Lys Tyr Glu Asn Gly Ala Ser Thr Ile
210 215 220
Ala Ala Lys Ala Met Ala Ala Gly Ile Pro Gly Ile Arg Val Asp Gly
225 230 235 240
Asn Asp Leu Leu Ala Ser Tyr Glu Val Ile Lys Glu Ala Val Asp Tyr
245 250 255
Ala Arg Ser Gly Asn Gly Pro Val Leu Val Glu Phe Val Thr Trp Arg
260 265 270
Gln Gly Val His Thr Ser Ser Asp Asn Pro Arg Ile Tyr Arg Thr Val
275 280 285
Glu Glu Glu Arg Glu His Glu Lys Trp Glu Pro Met His Arg Ile Glu
290 295 300
Lys Tyr Met Phe Asp Arg Gly Ile Leu Asp Ser Ala Glu Lys Gln Lys
305 310 315 320
Ile Trp Asp Glu Ala Leu Ala Ile Val Lys Glu Thr Tyr Glu Lys Ser
325 330 335
Leu Val Gly Leu Glu Ser Thr Ile Asp Glu Ile Phe Asp His Thr Tyr
340 345 350
Lys Val Leu Pro Pro Glu Leu Glu Glu Gln Lys Gln Glu Ala Leu Glu
355 360 365
Phe Phe Lys Gly Val Lys
370
<210> 9
<211> 447
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 9
Met Lys Trp Asn Lys Phe Leu Gly Leu Gly Leu Val Phe Pro Leu Ser
1 5 10 15
Ala Ile Ala Thr Ile Ser Ala Gly Cys Trp Asp Lys Glu Thr Thr Lys
20 25 30
Glu Glu Lys Ser Ala Asp Asn Gln Asn Lys Gln Ile Thr Asp Val Ser
35 40 45
Lys Ile Ser Gly Leu Val Asn Glu Arg Lys Ser Glu Ile Met Ala Ala
50 55 60
Lys Ala Asp Ala Asn Lys His Phe Gly Leu Asn Met Ala Ile Val Thr
65 70 75 80
Ala Asp Gly Thr Val Asn Asp Asn Ser Phe Asn Gln Ser Ser Trp Glu
85 90 95
Ala Ile Gln Gln Leu Gly Ala Leu Thr Gly Gly Glu Ile Thr Ser Val
100 105 110
Asp Ser Ser Thr Ala Glu Leu Glu Gly Lys Tyr Ser Ser Leu Ala Asn
115 120 125
Thr Asn Lys Asn Val Trp Val Leu Ser Gly Phe Gln His Gly Asp Ala
130 135 140
Ile Thr Lys Trp Leu Lys Ile Pro Glu Asn Lys Gln Leu Phe Thr Glu
145 150 155 160
Lys Asn Ile Ile Ile Leu Gly Ile Asp Trp Thr Asp Thr Glu Asn Val
165 170 175
Ile Pro Thr Gly Arg Tyr Ile Asn Leu Thr Tyr Lys Thr Glu Glu Ala
180 185 190
Gly Trp Leu Ala Gly Tyr Ala Asn Ala Ser Phe Leu Ala Lys Lys Phe
195 200 205
Pro Ser Asp Pro Thr Lys Arg Ser Ala Ile Val Ile Gly Gly Gly Ile
210 215 220
Phe Pro Ala Val Thr Asp Phe Ile Ala Gly Tyr Leu Ala Gly Ile Lys
225 230 235 240
Ala Trp Asn Leu Lys Asn Ser Asp Lys Lys Thr Lys Ile Thr Thr Asp
245 250 255
Lys Ile Glu Ile Asn Leu Gly Phe Asp Phe Gln Asn Thr Ser Thr Lys
260 265 270
Glu Arg Leu Glu Gln Ile Ala Ser Lys Asp Lys Pro Ser Thr Leu Leu
275 280 285
Ala Val Ala Gly Pro Leu Thr Glu Ile Phe Ser Asp Ile Ile Ala Asn
290 295 300
Gln Asn Asp Arg Tyr Leu Ile Gly Val Asp Thr Asp Gln Ser Leu Val
305 310 315 320
Tyr Thr Lys Thr Lys Asn Lys Phe Phe Thr Ser Ile Leu Lys Asn Leu
325 330 335
Gly Tyr Ser Val Phe Ser Val Leu Ser Asp Leu Tyr Thr Lys Lys Ser
340 345 350
Asn Ser Arg Asn Leu Ala Gly Phe Glu Phe Gly Lys Lys Ser Ala Thr
355 360 365
Val Tyr Leu Gly Ile Lys Asp Lys Phe Val Asp Ile Ala Asp Thr Ser
370 375 380
Leu Glu Gly Asn Asp Lys Lys Leu Ala Thr Glu Ala Ile Ser Glu Ala
385 390 395 400
Lys Lys Glu Phe Glu Glu Lys Thr Lys Thr Thr Pro Ala Glu Glu Val
405 410 415
Arg Lys Thr Leu Glu Ile Pro Glu Met Thr Asp Lys Gln Pro Asp Lys
420 425 430
Gln Gln Glu Ser Leu Asp Lys Leu Ile Thr Asp Ile Asn Lys Asn
435 440 445
<210> 10
<211> 317
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 10
Met Thr Tyr Gln Glu Tyr Leu Gln Ala Arg Leu Glu Gln Gln Asn Glu
1 5 10 15
Thr Lys Ser Leu Arg Ser Val Leu Ile Ile Asp Gly Ala Asp Pro Arg
20 25 30
Ala Ile Ala Ala Ala Lys Leu Leu Lys Glu Lys Asn Leu Val Lys Pro
35 40 45
Val Leu Leu Val Asp Glu Glu Ile Pro Asn Leu Asp Val Asp Gln His
50 55 60
Ile Val Asn Phe Gln Glu Lys Met Glu Phe Ile Lys Glu Phe Leu Lys
65 70 75 80
Phe Arg Lys Gly Lys Glu Thr Pro Glu Ser Ala Glu Ile Gln Phe Gln
85 90 95
Ser Asn Ala Phe Tyr Gly Thr Met Leu Leu Arg Lys Lys Lys Val Asp
100 105 110
Ala Val Val Gly Gly Leu Asn Tyr Pro Thr Ala Glu Ile Leu Arg Ala
115 120 125
Ala Phe Lys Ile Ile Gly Pro Lys Pro Asn Ile Lys Thr Ile Ser Ser
130 135 140
Val Met Ile Met His Lys Asp Gln Glu Lys Tyr Leu Phe Ser Asp Ile
145 150 155 160
Ser Val Asn Ile Ala Pro Asn Glu Asn Gln Leu Val Asp Ile Ala Lys
165 170 175
Asn Ala Leu Asp Phe Ala Ile Gln Leu Gly Phe Asp Pro Lys Pro Ala
180 185 190
Phe Leu Ser Phe Ser Thr Lys Gly Ser Ala Lys Ser Pro Gln Ser Glu
195 200 205
Leu Val Ala Lys Ala Thr Gln Met Phe Asn Ala Thr Ser Pro Ile Glu
210 215 220
Ala Tyr Gly Glu Ile Gln Leu Asp Ala Ala Leu Asp Ile Glu Val Arg
225 230 235 240
Arg Gln Lys Tyr Glu Val Asn Val Gly Lys Asn Ala Asn Ile Leu Ile
245 250 255
Phe Pro Asn Leu Asp Ala Gly Asn Ile Gly Tyr Lys Ile Ala Gln Arg
260 265 270
Leu Gly Asn Phe Gly Ala Ile Gly Pro Ile Ile Thr Gly Ile Asn Ala
275 280 285
Pro Ile Asn Asp Leu Ser Arg Gly Ser Thr Thr Gln Asp Val Phe Asn
290 295 300
Thr Val Leu Ile Ser Ala Leu Gln Val Glu Glu Gly Lys
305 310 315
<210> 11
<211> 373
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 11
Ile Ala Ser Arg Ser Asn Thr Thr Ala Lys Val Ala Pro Val Ala Val
1 5 10 15
Val Phe Ser Thr Arg Asn Asn Pro Phe Phe Gln Asn Val Glu Lys Gly
20 25 30
Ile Glu Thr Ala Ala Lys Glu Leu Gly Val Asp Tyr Glu Val Tyr Asp
35 40 45
Ser Glu Asn Asp Ser Asp Lys Glu Ala Arg Asn Ile Ser Asn Ile Ile
50 55 60
Ala Lys Gln Gln Lys Val Val Ile Phe Asn Asp Val Asn Glu Asp Ser
65 70 75 80
Gly Ile Ser Ala Val Lys Lys Leu Asn Gln Ala Gly Ile Pro Val Ile
85 90 95
Ala Thr Asp His Leu Leu Asn Ser Pro Lys Ala Leu Glu Ala Lys Ile
100 105 110
Lys Val Glu Ala Asn Ile Ala Ser Asp Asn Lys Gln Ala Gly Val Ile
115 120 125
Leu Ala Gln Phe Met Ala Gln Lys Ile Gly Leu Pro Gln Asp Ser Leu
130 135 140
Thr Tyr Ser Val Tyr Gly Ile Pro Gly Thr Glu Ser Gly Glu Ser Arg
145 150 155 160
Ala Gln Gly Phe Ile Glu Thr Val Lys Asn Leu Asn Asn Gln Ala Ile
165 170 175
Lys Tyr Asn Leu Phe Ser Tyr Gly Lys Tyr Gly Lys Glu Asn Ala Asn
180 185 190
Gly Lys Thr Tyr Ile Gly Arg Gln Ala Asp Asp Asn Arg Asp Leu Ala
195 200 205
Asn Gln Arg Val Ala Asn Asp Ala Thr Gln Val Phe Gln Asp Ala Gln
210 215 220
Lys Arg Pro Leu Leu Val Phe Gly Thr Asn Asp Glu Ala Ala Leu Gly
225 230 235 240
Ser Ile Ser Ala Leu Glu Ser Ala Gln Ile Pro Leu Gly Gly Gly Asp
245 250 255
Lys Phe Leu Pro Gly Ser Gly Lys Val Tyr Ile Thr Gly Val Asp Tyr
260 265 270
Thr Asn Asp Ala Gln Lys Ala Val Leu Asn Asn Lys Leu Ser Ala Thr
275 280 285
Val Glu Gln Asp Thr Asp Leu Leu Gly Arg Leu Ser Leu Ile Ile Ala
290 295 300
Glu Lys Ile Leu Lys Asp Gln Trp Lys Thr Ser Lys Tyr Ser Asp Phe
305 310 315 320
Tyr Ser Gln Phe Pro Gln Leu Asp Lys Asp Lys Asn Pro Asp Asp Gln
325 330 335
Val Glu Gln Gly Tyr Tyr Phe Lys Val Gly Thr Lys Leu Phe Trp Lys
340 345 350
Gly Pro Asp Gly Lys Gly Glu Lys Leu Gln Ala Asp Glu Asn Gly Ile
355 360 365
Leu Gln Lys Val Asn
370
<210> 12
<211> 691
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 12
Leu Ser Tyr Lys Phe Arg Arg Phe Phe Leu Thr Ser Ala Leu Ser Phe
1 5 10 15
Ala Pro Leu Ala Leu Val Ala Ser Cys Val Asn Asn Ser Arg Phe Asp
20 25 30
Ser Asn Glu Asp Asn Lys Leu Val Phe Gly His Thr Phe Ser Ser Ser
35 40 45
Gly Lys Glu Ala Lys Ala Leu Glu Lys Ile Ile Glu Val Trp Asn Lys
50 55 60
Thr Ala Thr Asn Gln Lys Asp Phe Ile Lys Met Glu Ala Gln Tyr Phe
65 70 75 80
Gln Asn Gly Tyr Asn Gly Ser Ala Ala Ser Ile Thr Asn Phe Leu Gln
85 90 95
Thr Lys Asp Arg Ile Lys Leu Pro Asn Ile Val Thr Asn Tyr Pro Ser
100 105 110
Leu Leu Ala Ile Val Asn Lys Tyr Ser Met Thr Phe Pro Leu Val Lys
115 120 125
Asp Phe Ser Ser Asn Gln Glu Pro Gln Asp Glu Asn Glu Lys Ala Ile
130 135 140
Lys Lys Phe Leu Lys Glu Gln Gly Ile Ser Asp Phe Leu Glu Ile Asn
145 150 155 160
Lys Glu Val Pro Phe Leu Asp Thr Lys Gly Val Tyr Thr Leu Pro Phe
165 170 175
Gly Lys Ser Thr Glu Val Leu Thr Ile Asn Lys Val Leu Phe Gly Trp
180 185 190
Met Ile Asn Lys Ala Leu Ala Asp Pro Lys Lys Pro Ala Lys Ile Lys
195 200 205
Glu Glu Asp Lys Pro Tyr Phe Ala Glu Phe Gln Lys Leu Gly Lys Glu
210 215 220
Lys Thr Gly Asp Ile Lys Glu Ile Glu Arg Ile Trp Lys Lys Tyr Val
225 230 235 240
Ser Asp Asp Gln Gly Leu Ala Gly Tyr Glu Phe Arg Arg Ser Asp Leu
245 250 255
Glu Asn Phe Thr Asp Leu Gln Lys Leu Ser Ser Arg Ile Leu Arg Ser
260 265 270
Phe Pro Glu Ala Leu Ser Gly Gly Ser Thr Asp Ser Ala Lys Ser Val
275 280 285
Leu Gly Ile Asp Asn Gln Ala Thr Leu Val Phe Ala Leu Ala Arg Ser
290 295 300
Val Ser Glu Gly Asn Arg Ser Gln Glu Val Thr Val Leu Asp Arg Gln
305 310 315 320
Lys Asn Leu Ile Asp Tyr Ile Ser Phe Ile Asp Lys Pro Asp Ser Ile
325 330 335
Arg Tyr Lys Asn Leu Glu Lys Ile Phe Asn Leu Leu Ser Gln Gly Ile
340 345 350
Lys Asp Arg Ser Ile Tyr Tyr Thr Ser Ala Gly Glu Tyr Asn Ser Thr
355 360 365
Phe Phe Arg Asn His Gln Gln Val Phe Ser Ile Gly Ser Thr Ser Gly
370 375 380
Tyr Phe His Asn Phe Val Lys Pro Thr Ala Thr Asn Tyr Gln Ile Gly
385 390 395 400
Phe Lys Lys Asn Asp Gly Leu Lys Ser Val Tyr Ser Val Ser Tyr Pro
405 410 415
Lys Phe Ser Ala Ile Val Ser Leu Glu Asp Leu Lys Asp Ile Thr Lys
420 425 430
Asp Leu Glu Ile Thr Ala Thr Asp Gly Ser Ser Lys Leu Lys Ile Asp
435 440 445
Ala Lys Phe Leu Gly Lys Leu Lys Glu Tyr Ala Gln Gln Asn Pro Val
450 455 460
Lys Lys Val Phe Tyr Phe Thr Asp Arg Ser Glu Lys Pro Ser Gly Ile
465 470 475 480
Phe Glu Lys Asp Tyr Ile Val Leu Gly Lys Tyr Lys Asn Asp Lys Asn
485 490 495
Glu Glu Phe Asn Gly Leu Val Ile Pro Thr Tyr Thr Glu Leu Tyr Lys
500 505 510
Asn Ser Gly Ser Asn Ala Leu Asn Asp Asp Glu Leu Ala Leu Glu Ala
515 520 525
Pro Pro His Lys Phe Asp Ala Asn Ser Lys Ile Thr Pro Ile Val Ala
530 535 540
Gln Gly Pro Asp Leu Ile Phe Ile His Ser Thr Glu Lys Glu Asp Lys
545 550 555 560
Ala Ala Lys Ala Phe Val Lys Trp Leu Leu Thr Glu Lys Ile Val Phe
565 570 575
Glu Glu Asn Ser Gln Glu Lys Met Thr Pro Leu Glu Tyr Phe Ala Arg
580 585 590
Ala Thr Ser Tyr Leu Leu Pro Ile Lys Ser Thr Leu Asp Lys Thr His
595 600 605
Phe Ser Pro Lys Asn Arg Ser Gln Lys Phe Ile Leu Asp Gln Phe Ser
610 615 620
Lys Phe Leu Asn Ala Asp Ser Lys Gly Lys Tyr Ser Leu Val Tyr Asp
625 630 635 640
Asn Ala Asp Ala Asn Ala Ser Ser Phe Arg Glu Ser Leu Asp Ser Ser
645 650 655
Val Ala Gln Met Gln Ser Leu Lys Ala Ser Asp Gly Lys Leu Arg Ser
660 665 670
Phe Lys Glu Phe Leu Glu Lys Leu Glu Gly Asn Leu Gly Pro Ala Phe
675 680 685
Lys Ser Lys
690
<210> 13
<211> 1182
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 13
Ile Gly Leu Thr Ile Phe Glu Lys Ser Phe Ser Ser Gln Val Ser Gly
1 5 10 15
Gly Val Asp Lys Asn Lys Val Val Asp Leu Lys Ser Asp Ser Asp Gln
20 25 30
Ile Phe Ser Glu Glu Asp Phe Ile Arg Ala Val Glu Asn Leu Lys Leu
35 40 45
Phe Asp Lys Tyr Lys His Leu Thr Ala Arg Met Ala Leu Gly Leu Ala
50 55 60
Arg Glu Ala Ala Asn Ala Phe Asn Phe Leu Asp Thr Tyr Asp Tyr Thr
65 70 75 80
Pro Ile Thr Lys His Ser Phe Lys Ile Ser Leu Asp Ile Ser Asp Ala
85 90 95
Phe Ala Ala Asn Lys Glu Val Lys Ala Val Val Val Ser Ala Tyr Ser
100 105 110
Gln Lys Tyr Gln Val Thr Tyr Ser Arg Leu Thr Ser Leu Lys Gly Trp
115 120 125
Lys Glu Glu Asp Asp Phe Gly Asp Asp Ile Ile Asp Tyr Gln Ile Asn
130 135 140
Gln Glu Leu Ser Gly Leu Ser Leu Ser Ser Leu Ala Pro Glu Ser Ala
145 150 155 160
His Leu Leu Ala Ser Glu Met Ala Phe Arg Leu Asp Asn Asp Phe Gln
165 170 175
Val Ala Tyr Lys Lys Thr Gly Ser Arg Ala Glu Ala Phe Arg Gln Ala
180 185 190
Leu Ile Lys Asn Tyr Leu Gly Tyr Asn Leu Val Asn Arg Gln Gly Leu
195 200 205
Pro Thr Met Leu Gln Lys Gly Tyr Val Leu Ala Pro Lys Thr Ile Glu
210 215 220
Asn Lys Asn Ala Ser Glu Glu Lys Leu Val Asn Ile Asn Glu Asn Asp
225 230 235 240
Arg Ala Arg Val Asn Lys Leu Gln Lys Val Glu Asn Leu Ala Phe Lys
245 250 255
Asn Leu Ser Asp Pro Asn Gly Thr Leu Ser Ile Thr Phe Glu Leu Trp
260 265 270
Asp Pro Asn Gly Lys Leu Val Ser Glu Tyr Asp Phe Lys Ile Lys Gly
275 280 285
Ile Lys Lys Leu Asp Phe Asp Leu Lys Lys Gln Glu Glu Lys Val Leu
290 295 300
Gln Lys Val Thr Glu Phe Val Glu Ile Lys Pro Tyr Val Gln Leu Gly
305 310 315 320
Leu Ile Arg Asp Asn Leu Ser Leu Ser Glu Ile Ile Tyr Lys Asn Asp
325 330 335
Asn Asn Pro Glu Tyr Leu Arg Lys Ile Leu Ala Lys Leu Lys Glu His
340 345 350
Asn Asn Asn Lys Arg Val Asp Asn Asn Thr Ser Thr Thr Lys Phe Gln
355 360 365
Glu Glu Asp Leu Lys Asn Glu Pro Asn Ser Asn Gly Ser Glu Gln Asp
370 375 380
Ser Phe Glu Lys Ala Lys Glu Asn Phe Leu Ser Phe Phe Asp Leu Arg
385 390 395 400
Ser Arg Leu Ile Pro Ile Pro Asp Leu Pro Leu Tyr Tyr Leu Lys Val
405 410 415
Asn Ser Ile Asn Phe Asp Arg Asn Ile Glu Glu Asn Glu Lys Glu Lys
420 425 430
Leu Leu Lys Asn Glu Gln Val Val Leu Lys Val Asp Phe Ser Leu Lys
435 440 445
Lys Val Val Ser Asp Ile Arg Ala Pro Tyr Leu Val Ser Ser Gln Val
450 455 460
Arg Ser Asn Tyr Pro Pro Val Leu Lys Ala Ser Leu Ala Lys Ile Gly
465 470 475 480
Lys Gly Ser Asn Ser Lys Val Val Leu Leu Asp Leu Gly Asn Leu Ser
485 490 495
Ser Arg Phe Lys Val Gln Leu Asp Tyr Ser Ala Lys Gln Arg Glu Ile
500 505 510
Ile Asn Thr Leu Leu Lys Glu Asn Pro Glu Arg Glu Lys Glu Leu Gln
515 520 525
Ala Lys Ile Glu Ser Lys Thr Phe Ser Pro Ile Asp Leu Asn Asn Asp
530 535 540
Asp Leu Leu Ala Ile Glu Phe Gln Tyr Glu Asp Asn Pro Glu Gly Asp
545 550 555 560
Trp Ile Thr Leu Gly Arg Met Glu Lys Leu Val Lys Glu Val Ile Gln
565 570 575
Tyr Lys Lys Glu Gly Lys Thr Phe Leu Asp Asp Glu Val Ala Lys Thr
580 585 590
Leu Tyr Tyr Leu Asp Phe His His Leu Pro Gln Ser Lys Lys Asp Leu
595 600 605
Glu Glu Tyr Lys Glu Lys His Lys Asn Lys Phe Ile Ser Glu Ile Lys
610 615 620
Pro Ala Thr Pro Ala Ser Gln Ala Lys Thr Ser Gln Ala Lys Asn Glu
625 630 635 640
Lys Glu Val Lys Pro Glu Ser Ala Gln Ala Glu Ala Ser Ser Ser Asn
645 650 655
Ser Asn Asp Ser Ser Ser Lys Thr Thr Ser Ser Ser Ser Met Ala Gly
660 665 670
Thr Thr Gln Asn Lys Ser Thr Glu Thr Pro Asn Ser Ser Ser Asn Ser
675 680 685
Thr Pro Thr Ser Ser Ala Thr Thr Ser Ala Thr Thr Ser Thr Thr Ser
690 695 700
Ser Asn Ser Ser Ser Thr Thr Ser Ser Thr Thr Thr Thr Thr Ser Thr
705 710 715 720
Gln Ala Ala Thr Thr Ser Ala Ser Ser Ala Lys Val Lys Thr Thr Lys
725 730 735
Phe Gln Glu Gln Val Lys Glu Gln Glu Gln Lys Gln Glu Lys Ala Lys
740 745 750
Glu Thr Asn Gln Leu Leu Asp Thr Lys Arg Asn Lys Glu Asp Ser Gly
755 760 765
Leu Gly Leu Ile Leu Trp Asp Phe Leu Val Asn Ser Lys Tyr Lys Thr
770 775 780
Leu Pro Gly Thr Thr Trp Asp Phe His Val Glu Pro Asp Asn Phe Asn
785 790 795 800
Asp Arg Leu Lys Ile Thr Ala Ile Leu Lys Glu Asn Thr Ser Gln Ala
805 810 815
Lys Ser Asn Pro Asp Ser Lys Asn Leu Thr Ser Leu Ser Arg Asn Leu
820 825 830
Ile Ile Lys Gly Val Met Ala Asn Lys Tyr Ile Asp Tyr Leu Val Gln
835 840 845
Glu Asp Pro Val Leu Leu Val Asp Tyr Thr Arg Arg Asn Gln Ile Lys
850 855 860
Thr Glu Arg Glu Gly Gln Leu Ile Trp Ser Gln Leu Ala Ser Pro Gln
865 870 875 880
Met Ala Ser Pro Glu Ser Ser Pro Glu Lys Ala Lys Leu Glu Ile Thr
885 890 895
Glu Glu Gly Leu Arg Val Lys Lys Gly Gly Thr Lys Ile Lys Glu Thr
900 905 910
Arg Lys Ser Thr Thr Ser Asn Ala Lys Ser Asn Thr Asn Ser Lys Pro
915 920 925
Asn Lys Lys Leu Val Leu Leu Lys Gly Ser Ile Lys Asn Pro Gly Thr
930 935 940
Lys Lys Glu Trp Ile Leu Val Gly Ser Gly Asn Lys Ala Thr Lys Asn
945 950 955 960
Gly Ser Ser Ser Asn Asn Ser Asn Thr Gln Ile Trp Ile Thr Arg Leu
965 970 975
Gly Thr Ser Val Gly Ser Leu Lys Thr Glu Gly Glu Thr Val Leu Gly
980 985 990
Ile Ser Asn Asn Asn Ser Gln Gly Glu Val Leu Trp Thr Thr Ile Lys
995 1000 1005
Ser Lys Leu Glu Asn Glu Asn Asn Ser Asp Asn Asn Gln Ile Gln
1010 1015 1020
Tyr Ser Pro Ser Thr His Ser Leu Thr Thr Asn Ser Arg Ser Asn
1025 1030 1035
Thr Gln Gln Ser Gly Arg Asn Gln Ile Lys Ile Thr Asn Thr Gln
1040 1045 1050
Arg Lys Thr Thr Thr Ser Pro Ser Gln Asn Leu Ser Gln Asn Pro
1055 1060 1065
Asp Leu Asn Gln Ile Asp Val Arg Leu Gly Leu Leu Val Gln Asp
1070 1075 1080
Lys Lys Leu His Leu Trp Trp Ile Ala Asn Asp Ser Ser Asp Glu
1085 1090 1095
Pro Glu His Ile Thr Ile Asp Phe Ala Glu Gly Thr Lys Phe Asn
1100 1105 1110
Tyr Asp Asp Leu Asn Tyr Val Gly Gly Leu Leu Lys Asn Thr Thr
1115 1120 1125
Asn Asn Asn Asn Met Gln Thr Gln Asp Asp Glu Gly Asp Gly Tyr
1130 1135 1140
Leu Ala Leu Lys Gly Leu Gly Ile Tyr Glu Phe Pro Asp Asp Glu
1145 1150 1155
Ser Ile Asp Gln Pro Ala Thr Val Glu Lys Ala Glu Arg Leu Tyr
1160 1165 1170
Lys His Phe Met Gly Leu Phe Arg Glu
1175 1180
<210> 14
<211> 350
<212> PRT
<213> Mycoplasma hyopneumoniae
<400> 14
Met Asp Lys Phe Ser Arg Thr Val Leu Gly Asp Ile His Pro Ser Glu
1 5 10 15
Leu Gly Val Val Asp Cys His Asp His Leu Ile Lys Asn Tyr Gly Pro
20 25 30
Lys Ala His Glu His Pro Asp Phe Val Met Leu Ser Asn Glu Ala Ala
35 40 45
Ile Ala Glu Ser Leu Glu Tyr Ala Ser Arg Gly Gly Lys Thr Ile Val
50 55 60
Thr Met Asp Pro Pro Asn Val Gly Arg Asp Val Tyr Arg Met Leu Lys
65 70 75 80
Ile Ala Lys Ala Leu Glu Gly Lys Val His Ile Ile Met Ala Thr Gly
85 90 95
Phe His Lys Ala Ala Phe Tyr Asp Lys Gly Ala Ser Trp Leu Ala Leu
100 105 110
Ala Pro Thr Asp Glu Ile Val Lys Met Val Val Ala Glu Ile Thr Gln
115 120 125
Gly Met Asp Glu Tyr Asn Tyr Ser Gly Pro Val Val Arg Arg Ser Lys
130 135 140
Ala Lys Ala Gly Ile Ile Lys Ala Gly Thr Gly Tyr Gly Ala Ile Asp
145 150 155 160
Arg Leu Glu Leu Lys Ser Leu Glu Val Ala Ala Arg Ala Ser Ile Glu
165 170 175
Thr Gly Ala Pro Ile Leu Val His Thr Gln Leu Gly Thr Met Ala Tyr
180 185 190
Glu Ala Ala Lys Tyr Leu Ile Asp Phe Gly Ala Asn Pro Arg Lys Ile
195 200 205
Gln Ile Ser His Leu Asn Lys Asn Pro Asp Lys Tyr Tyr Tyr Ala Lys
210 215 220
Ile Ile Lys Glu Leu Gly Val Ser Leu Cys Phe Asp Gly Pro Asp Arg
225 230 235 240
Val Lys Tyr Phe Pro Asp Thr Thr Leu Ala Glu Asn Ile Lys Tyr Leu
245 250 255
Val Asp Leu Gly Leu Glu Lys His Ile Thr Leu Ser Leu Asp Ala Gly
260 265 270
Arg Val Leu Tyr Gln Arg Asn Tyr Gly Lys Leu Lys Gly Lys Trp Thr
275 280 285
Phe Gly Leu Thr Tyr Leu Phe Asp Arg Phe Ile Pro Leu Leu Glu Gln
290 295 300
Val Gly Ile Ser Lys Glu Thr Ile Asn Asn Ile Leu Val Asn Asn Pro
305 310 315 320
Ala Glu Ile Leu Ala Phe Asp Gln Pro Arg Lys Phe Asp Pro Ser Ile
325 330 335
Leu Pro Asp Tyr Ile Ile Glu Leu Lys Lys Ser Phe Lys Ile
340 345 350
<210> 15
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 15
gatataggat ccatggacaa atttcgctat gtaaagcctg 40
<210> 16
<211> 45
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 16
caatatgtcg acttatttta ctcctttaaa aaattcaagc gcttc 45
<210> 17
<211> 51
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 17
gatataggat ccatgaatgg aataaatttc ttggcttagg cttagttttt c 51
<210> 18
<211> 50
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 18
caatatgtcg acttaatttt tattaatatc ggtaattagt ttgtctaagc 50
<210> 19
<211> 41
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 19
gatataggat ccatgacata ccaagaatat cttcaagcaa g 41
<210> 20
<211> 42
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 20
caatatgtcg acctatttac cttcttcaac ttgtagagcg ct 42
<210> 21
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 21
gatataggat ccatagcttc aaggtcgaat acaactgc 38
<210> 22
<211> 42
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 22
caatatgtcg acttaattta ccttttggag tatcccattt tc 42
<210> 23
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 23
gatataggat ccttatccta taaatttagg cgttttttcc 40
<210> 24
<211> 41
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 24
caatatgtcg acttattttg atttaaaagc aggacctaaa t 41
<210> 25
<211> 44
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 25
gatataggat ccattggact aacaattttt gagaaatcat ttag 44
<210> 26
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 26
caatatgtcg acttattcct aaatagcccc ataaagtg 38
<210> 27
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 27
gatataggat ccatggacaa attttcacga actgttct 38
<210> 28
<211> 51
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 28
caatatgtcg acctagattt taaaggattt ttttaattca ataatataat c 51
<210> 29
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 29
gatataggat ccatggacaa atttcgctat gtaaagcctg 40
<210> 30
<211> 36
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 30
gctaacaaaa gatgactggt ttgtcccagc ttttcg 36
<210> 31
<211> 36
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 31
cgaaaagctg ggacaaacca gtcatctttt gttagc 36
<210> 32
<211> 36
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 32
cttgcaaatg caatattgga atggtagcga aaaagg 36
<210> 33
<211> 36
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 33
cctttttcgc taccattcca atattgcatt tgcaag 36
<210> 34
<211> 58
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 34
cgaggcgcta aatattgcaa gtatttggaa atggccagtt gttttttgcg taaataac 58
<210> 35
<211> 58
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 35
gttatttacg caaaaaacaa ctggccattt ccaaatactt gcaatattta gcgcctcg 58
<210> 36
<211> 52
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 36
gttttttgcg taaataacaa tcaatgggca atttcaaccc caaataaata tg 52
<210> 37
<211> 52
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 37
catatttatt tggggttgaa attgcccatt gattgttatt tacgcaaaaa ac 52
<210> 38
<211> 36
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 38
gttgagtttg taacttggcg tcaaggtgtt catacc 36
<210> 39
<211> 36
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 39
ggtatgaaca ccttgacgcc aagttacaaa ctcaac 36
<210> 40
<211> 32
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 40
gagaacacga aaaatgggaa ccaatgcacc gg 32
<210> 41
<211> 32
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 41
ccggtgcatt ggttcccatt tttcgtgttc tc 32
<210> 42
<211> 39
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 42
ccgaaaaaca aaaaatttgg gatgaagcgc ttgcgattg 39
<210> 43
<211> 39
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 43
caatcgcaag cgcttcatcc caaatttttt gtttttcgg 39
<210> 44
<211> 45
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 44
caatatgtcg acttatttta ctcctttaaa aaattcaagc gcttc 45
<210> 45
<211> 52
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 45
gatataggat ccatgaaatg gaataaattt cttggcttag gcttagtttt tc 52
<210> 46
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 46
catttaacca atcaagttgg gaggcaattc aacaacttgg 40
<210> 47
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 47
ccaagttgtt gaattgcctc ccaacttgat tggttaaatg 40
<210> 48
<211> 45
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 48
ctaataccaa caaaaatgtt tgggtacttt ctggttttca acacg 45
<210> 49
<211> 45
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 49
cgtgttgaaa accagaaagt acccaaacat ttttgttggt attag 45
<210> 50
<211> 44
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 50
cggtgatgcg atcacaaaat ggttaaaaat ccctgaaaat aagc 44
<210> 51
<211> 44
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 51
gcttattttc agggattttt aaccattttg tgatcgcatc accg 44
<210> 52
<211> 45
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 52
ttatcatact cggaattgac tggactgata ctgaaaatgt aattc 45
<210> 53
<211> 45
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 53
gaattacatt ttcagtatca gtccagtcaa ttccgagtat gataa 45
<210> 54
<211> 29
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 54
gaagaagccg gatggcttgc aggatatgc 29
<210> 55
<211> 29
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 55
gcatatcctg caagccatcc ggcttcttc 29
<210> 56
<211> 53
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 56
ggttatctag ccggaattaa agcttggaat ctaaaaaatt ctgataaaaa aac 53
<210> 57
<211> 53
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 57
gtttttttat cagaattttt tagattccaa gctttaattc cggctagata acc 53
<210> 58
<211> 50
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 58
caatatgtcg acttaatttt tattaatatc ggtaattagt ttgtctaagc 50
<210> 59
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 59
gatataggat ccttatccta taaatttagg cgttttttcc 40
<210> 60
<211> 52
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 60
caattaataa agttttgttt ggttggatga ttaataaagc acttgctgat cc 52
<210> 61
<211> 52
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 61
ggatcagcaa gtgctttatt aatcatccaa ccaaacaaaa ctttattaat tg 52
<210> 62
<211> 53
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 62
gatattaaag aaattgaaag aatctggaaa aaatatgtct ccgatgatca agg 53
<210> 63
<211> 53
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 63
ccttgatcat cggagacata ttttttccag attctttcaa tttctttaat atc 53
<210> 64
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 64
gccctttcag gaggctccac tgattcggca 30
<210> 65
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 65
tgccgaatca gtggagcctc ctgaaagggc 30
<210> 66
<211> 46
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 66
gccgcaaaag cttttgttaa atggcttttg acagaaaaaa tagtct 46
<210> 67
<211> 46
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 67
agactatttt ttctgtcaaa agccatttaa caaaagcttt tgcggc 46
<210> 68
<211> 41
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 68
caatatgtcg acttattttg atttaaaagc aggacctaaa t 41
<210> 69
<211> 44
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 69
gatataggat ccattggact aacaattttt gagaaatcat ttag 44
<210> 70
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 70
ctaacttctc taaaaggttg gaaagaagaa gatgattttg 40
<210> 71
<211> 40
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 71
caaaatcatc ttcttctttc caacctttta gagaagttag 40
<210> 72
<211> 47
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 72
ctttctatta cttttgaact ctgggaccca aatggtaaat tagtatc 47
<210> 73
<211> 47
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 73
gatactaatt taccatttgg gtcccagagt tcaaaagtaa tagaaag 47
<210> 74
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 74
ccctgaagga gattggataa ctttagggag 30
<210> 75
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 75
ctccctaaag ttatccaatc tccttcaggg 30
<210> 76
<211> 34
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 76
ctaccaggaa ctacctggga tttccatgtt gaac 34
<210> 77
<211> 34
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 77
gttcaacatg gaaatcccag gtagttcctg gtag 34
<210> 78
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 78
ggacaactaa tttggagcca gttagcttcc 30
<210> 79
<211> 30
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 79
ggaagctaac tggctccaaa ttagttgtcc 30
<210> 80
<211> 35
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 80
ggaacaaaaa aggaatggat tcttgtagga tctgg 35
<210> 81
<211> 35
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 81
ccagatccta caagaatcca ttcctttttt gttcc 35
<210> 82
<211> 34
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 82
ccaatacgca aatatggata acccgtctag gaac 34
<210> 83
<211> 34
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 83
gttcctagac gggttatcca tatttgcgta ttgg 34
<210> 84
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 84
ccaaggggaa gttctctgga ctactattaa atccaaac 38
<210> 85
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 85
gtttggattt aatagtagtc cagagaactt ccccttgg 38
<210> 86
<211> 37
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 86
caaaaaactt cacctttggt ggattgctaa tgatagc 37
<210> 87
<211> 37
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 87
gctatcatta gcaatccacc aaaggtgaag ttttttg 37
<210> 88
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 88
caatatgtcg acttattcct aaatagcccc ataaagtg 38
<210> 89
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 89
gatataggat ccatagcttc aaggtcgaat acaactgc 38
<210> 90
<211> 68
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 90
aataattgca gaaaaaattc ttaaagatca atggaaaaca agtaaatatt ctgattttta 60
ttcacaat 68
<210> 91
<211> 68
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 91
attgtgaata aaaatcagaa tatttacttg ttttccattg atctttaaga attttttctg 60
caattatt 68
<210> 92
<211> 42
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 92
caatatgtcg acttaattta ccttttggag tatcccattt tc 42
<210> 93
<211> 38
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 93
gatataggat ccatggacaa attttcacga actgttct 38
<210> 94
<211> 34
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 94
caatagtgac aatggacccc ccaaatgttg gtcg 34
<210> 95
<211> 34
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 95
cgaccaacat ttggggggtc cattgtcact attg 34
<210> 96
<211> 35
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 96
gataaaggcg catcatggct tgcgcttgca ccaac 35
<210> 97
<211> 35
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 97
gttggtgcaa gcgcaagcca tgatgcgcct ttatc 35
<210> 98
<211> 41
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 98
ggaaaactta aaggtaaatg gacttttgga ctaacctatt t 41
<210> 99
<211> 41
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 99
aaataggtta gtccaaaagt ccatttacct ttaagttttc c 41
<210> 100
<211> 51
<212> ДНК
<213> Синтетическая последовательность
<220>
<223> праймер
<400> 100
caatatgtcg acctagattt taaaggattt ttttaattca ataatataat c 51
<---



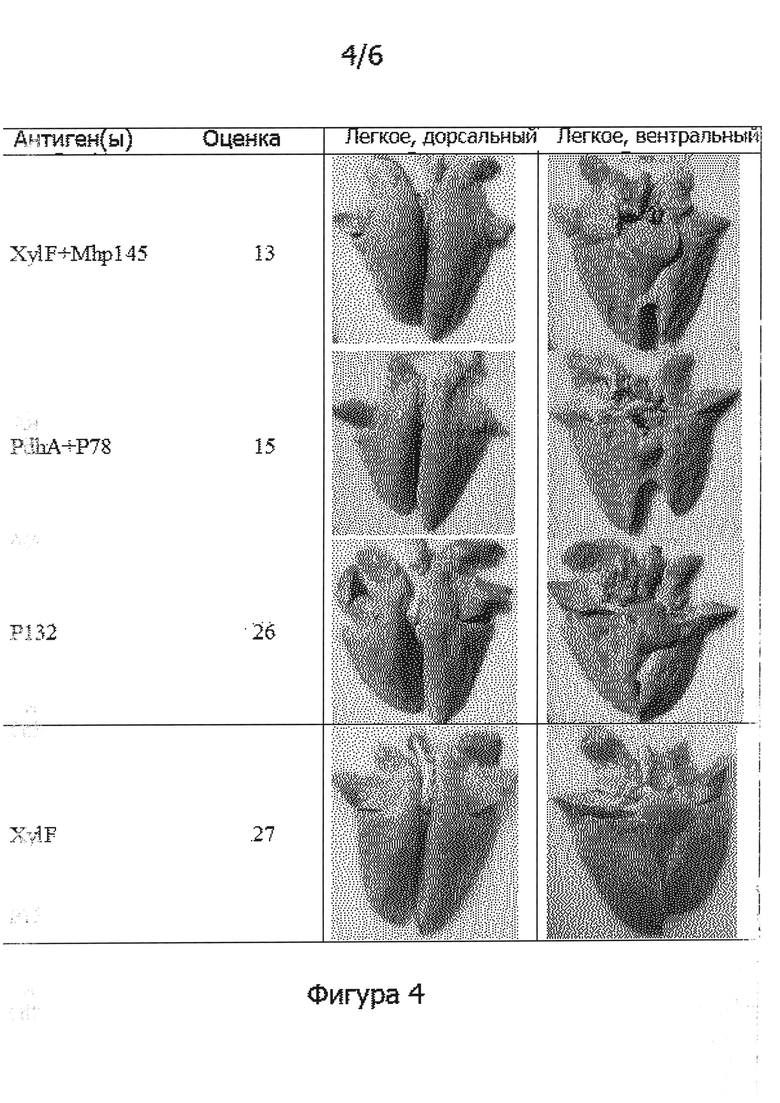


Изобретение относится к области биотехнологии, конкретно к получению субъединичных вакцин против Mycoplasma spp., и может быть использовано в медицине для профилактики инфекции Mycoplasma spp. Предложены вакцинные композиции на основе белка EutD с SEQ ID NO: 10 в сочетании с фармацевтически приемлемым адъювантом или фармацевтически приемлемой добавкой. Изобретение обеспечивает достижение сильных иммунных эффектов против Mycoplasma spp. 2 н. и 4 з.п. ф-лы, 4 ил., 9 табл., 3 пр.
1. Композиция для профилактики инфекции Mycoplasma spp., содержащая:
эффективное количество белка EutD в качестве активного ингредиента указанной композиции; и
фармацевтически приемлемый адъювант,
где указанный EutD имеет последовательность SEQ ID NO: 10.
2. Композиция по п. 1, в которой концентрация указанного активного ингредиента составляет от 50 до 3500 мкг/мл из расчета на общий объем указанной композиции.
3. Композиция по п. 1, в которой указанный фармацевтически приемлемый адъювант представляет собой полный адъювант Фрейнда, неполный адъювант Фрейнда, гель оксида алюминия, поверхностно-активное вещество, полианионный адъювант, пептид, масляную эмульсию или их комбинацию.
4. Композиция для профилактики инфекции Mycoplasma spp., содержащая:
эффективное количество белка EutD в качестве активного ингредиента указанной композиции;
фармацевтически приемлемый адъювант и
фармацевтически приемлемую добавку,
где указанный EutD имеет последовательность SEQ ID NO: 10.
5. Композиция по п. 4, в которой указанный фармацевтически приемлемый адъювант представляет собой полный адъювант Фрейнда, неполный адъювант Фрейнда, гель оксида алюминия, поверхностно-активное вещество, полианионный адъювант, пептид, масляную эмульсию или их комбинацию.
6. Композиция по п. 4, в которой указанная фармацевтически приемлемая добавка представляет собой растворитель, стабилизатор, разбавитель, консервант, антибактериальный агент, противогрибковый агент, изотонический агент, замедляющий абсорбцию агент или их комбинацию.
| EP 359919 A2, 28.03.1990 | |||
| Динамометрическая втулка | 1921 |
|
SU600A1 |
| Устройство лазов в резервуарах для пара высокого давления | 1926 |
|
SU9901A1 |
Авторы
Даты
2021-11-12—Публикация
2019-07-08—Подача