Область техники
Настоящее изобретение согласно вариантам его осуществления относится к пептидам и их применению в лечении заболеваний, нарушений или состояний, ассоциированных с мутантным p53.
Злокачественная опухоль является основной причиной смерти в развитых странах, и средний возраст населения продолжает увеличиваться вместе с числом диагностированных случаев и экономических последствий. Злокачественная опухоль представляет собой не отдельное заболевание, в скорее группу из более чем 200 заболеваний, характеризующихся неконтролируемым ростом и распространением аномальных клеток. Злокачественная опухоль является высоко гетерогенным заболеванием с основными молекулярными различиями в экспрессии и распределении маркеров поверхности опухолевых клеток даже среди больных с одинаковым типом и степенью злокачественной опухоли. Более того, клеточные мутации, как правило, накапливаются по мере прогрессирования злокачественной опухоли, что еще больше увеличивает гетерогенность опухоли. Большинство опухолевых клеток проявляют геномную нестабильность с повышенной экспрессией онкогенов и инактивацией генов-супрессоров опухолей.
Ген p53 считают наиболее важным геном-супрессором опухолей, который действует как главный барьер против прогрессирования злокачественной опухоли. Белок p53 отвечает за различные типы клеточного стресса, а также запускает арест клеточного цикла, апоптоз или старение. Это достигается транскрипционной трансактивацией специфических целевых генов, несущих мотивы связывания ДНК p53. Широко признано, что путь р53 нарушается практически во всех злокачественных опухолях человека. Мутацию р53 рассматривают как критический шаг в процессе злокачественных превращений, и в более 50% случаев злокачественные опухоли несут мутации в своих генах р53. Большинство этих мутаций являются бессмысленными точковыми мутациями, которые нацелены на ДНК-связывающий коровый домен (DBD) p53, что тем самым отменяет специфическое связывание ДНК p53 с ее целевым сайтом. Эти мутации предупреждают р53-зависимую транскрипцию и, следовательно, опосредованное р53 подавление опухолей. Исключительно высокая частота мутаций p53 в опухолях человека различных типов делает p53 уникальным среди генов, вовлеченных в развитии опухолей, что делает мутированный p53 (Mut-p53) привлекательной мишенью для новых методов терапии злокачественных опухолей.
Структурные исследования показали, что полученные из опухоли бессмысленные мутации в DBD p53 вызывают общий эффект: дестабилизацию фолдинга DBD при физиологической температуре (Joerger, A.C., M.D. Allen, and A.R. Fersht, Crystal structure of a superstable mutant of human p53 core domain. Insights into the mechanism of rescuing oncogenic mutations. J Biol Chem, 2004 279(2): p. 1291-6). Эта дестабилизация может быть обратимой, поскольку некоторые мутанты могут возвращаться к конформации дикого типа и связывать ДНК при пониженных температурах. Таким образом, большинство мутаций р53 дестабилизируют фолдинг белка р53, вызывая частичную денатурацию при физиологической температуре.
Мутантные белки p53 накапливаются с высоким содержанием в опухолевых клетках, главным образом из-за их неспособности активировать экспрессию собственного деструктора p53 Mdm2. Более того, многие активирующие стрессовые сигналы р53 (такие как гипоксия, геномная нестабильность и экспрессия онкогена) конститутивно индуцируются в клетках злокачественной опухоли. Поэтому, предполагают, что реактивация Mut-p53 будет оказывать значительные противоопухолевые эффекты. Кроме того, на мышиной модели показали, что восстановление функций р53 хорошо переносится в нормальных тканях и не вызывает видимых токсических эффектов (Ventura, A., et al., Restoration of p53 function leads to tumour regression in vivo. Nature, 2007. 445(7128): p. 661-5).
Структурные исследования показывают, что степень нарушенного фолдинга различается у мутантов; однако происходит не определенный альтернативный фолдинг, а скорее частичная денатурация. Это говорит о том, что «низкомолекулярный» подход для обращения эффекта мутации р53 при фолдинге может быть применим к широкому спектру мутантных форм. Другим важным прогнозом структурных исследований является то, что ожидается, что лиганд, который связывается с правильно сложенной фракцией белка, будет сдвигать равновесие по направлению к нативному фолдингу в соответствии с законом действия масс.
Несколько попыток коррекции были предприняты в области конформации р53. Доказательство принципа для стабилизирующих конформацию пептидов предоставили Фридлер и его коллеги (Friedler, A., et al., A peptide that binds and stabilizes p53 core domain: chaperone strategy for rescue of oncogenic mutants. Proc. Natl. Acad. Sci. USA, 2002. 99(2): p. 937-42). Пептид с девятью остатками CDB3 сконструировали на основе кристаллической структуры комплекса между DBD p53 и ASPP (Samuels-Lev, Y., et al., ASPP proteins specifically stimulate the apoptotic function of p53. Mol. Cell, 2001. 8(4): p. 781-94). Показали, что этот пептид связывает Mut-p53 и действует как шаперон, смещая равновесие по направлению к конформации WT, о чем свидетельствует повышенная реакционная способность по отношению к PAb1620. Однако биологические эффекты CDB3 (Issaeva, N., et al., Rescue of mutants of the tumor suppressor p53 in cancer cells by a designed peptide. Proc. Natl. Acad. Sci. USA, 2003. 100(23): p. 13303-7) являются всего лишь частичными, поскольку конформация комплекса Mut-p53/CDB3 находится в промежуточном состоянии между WT и мутантом.
Идентифицировали низкомолекулярные соединения, нацеливающиеся на Mut-p53, с использованием либо белковых, либо клеточных анализов (Peng, Y., et al., Rescue of mutant p53 transcription function by ellipticine. Oncogene, 2003. 22(29): p. 4478-87). CP-31398 идентифицировали с помощью скрининга молекул, которые защищают выделенный DBD p53 от тепловой денатурации, что оценивали по поддержанию реакционной способности PAb1620 при нагревании белков (Foster, B.A., et al., Pharmacological rescue of mutant p53 conformation and function. Science, 1999. 286(5449): p. 2507-10). Механизм действия CP-31398 остается неясным. ЯМР-исследования не выявили никакой связи CP-31398 с DBD p53 Rippin, T.M., et al., Characterization of the p53-rescue drug CP-31398 in vitro and in living cells. Oncogene, 2002. 21(14): p. 2119-29). CP-31398 влияет на экспрессию генов и индуцирует гибель клеток как зависимым от p53, так и независимым образом. Таким образом, похоже, что CP-3138 имеет другие клеточные цели, чем р53, которые могут объяснить его клеточную токсичность.
Обнаружили две другие малые молекулы, которые сохраняют функцию р53 в живых клетках злокачественной опухоли, PRIMA-1 и MIRA-1, с использованием клеточных скрининговых анализов. PRIMA-1 и MIRA-1 имеют сходные профили активности (Bykov, V.J., et al., Reactivation of mutant p53 and induction of apoptosis in human tumor cells by maleimide analogs. J Biol Chem, 2005. 280(34): p. 30384-91), но структурно не являются родственными. PRIMA-1 является пролекарством, которое превращается в активное соединение, которое связывается с мутантным р53, а также с другими молекулами (Cell Death Dis. 2015 Jun 18;6:e1794. doi: 10,1038/cddis,2015,143), и некоторые из его эффектов, по-видимому, не зависят от статуса мутантного p53 (BMC Cancer. 2015 Oct 13;15:684. doi: 10.1186/s12885-015-1667-1).
Авторы вариантов осуществления настоящего изобретения ранее описывали применение фагового дисплея для отбора реактивирующих mutp53 пептидов (WO2015/019318). Пептидные библиотеки фагового дисплея гораздо сложнее библиотек химических веществ. Процесс отбора основывался на связывании пептидов с иммобилизованной целью, элюировании и амплификации и, наконец, идентификации путем секвенирования, что позволяло скринировать большое количество молекул за короткое время. Объединили различные стратегии отбора для отбора лидеров из различных пептидных библиотек и глубокого секвенирования отобранных пулов. Показали, что лидерные пептиды обеспечивают для mutp53 подобные WTp53 активности in vitro и в живых клетках, и приводят к регрессии несущих mutp53 опухолей на некоторых моделях ксенотрансплантатов.
Сущность изобретения
Согласно аспекту вариантов осуществления настоящего изобретения представлен выделенный пептид, содержащий аминокислотную последовательность, расположенную в пространстве и конфигурации, которые обеспечивают взаимодействие пептида с доменом связывания с ДНК (DBD) в p53 через по меньшей мере один остаток DBD, посредством которого pCAP 250 (SEQ ID NO: 1) связывает DBD, при этом пептид по меньшей мере частично реактивирует мутантный белок p53, при условии, что пептид не является SEQ ID NO: 59-382.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется через Helix-2 и L1 в DBD.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие влияет на структурную стабильность Helix-2 и/или L1 в DBD, как анализировали с помощью ЯМР.
Согласно некоторым вариантам осуществления настоящего изобретения по меньшей мере один остаток выбран из группы, состоящей из H115, G117 из L1 и Y126, и V274, и G279, и R280 из p53.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере одной аминокислоты аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере двух аминокислот аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере трех аминокислот аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере четырех аминокислот аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения пептид содержит аминокислотную последовательность
X1-X2-X3-X4-X5-X6 (SEQ ID NO: 53),
в которой
X1 и X5 представляют собой положительно заряженную аминокислоту;
X2 выбран из группы, состоящей из Ser, Thr, Asn, Gln, Pro, Ala и Gly;
X3 представляет собой любую аминокислоту;
X4 и X6 выбраны из группы, состоящей из альфа-метиламинокислоты и аминокислоты, нарушающей структуру бета-листов.
Согласно некоторым вариантам осуществления настоящего изобретения пептид содержит аминокислотную последовательность
X1-X2-X3-X4-X5-X6 (SEQ ID NO: 54),
в которой
X1 и X5 выбраны из группы, состоящей из His, Arg и Lys;
X2 выбран из группы, состоящей из Ser, Thr, Asn, Gln, Pro, Ala и Gly;
X3, X4, X6 представляют собой любую аминокислоту.
Согласно некоторым вариантам осуществления настоящего изобретения положительно заряженная аминокислота выбрана из группы, состоящей из His, диаминомасляной кислоты (Dab), Arg и Lys.
Согласно некоторым вариантам осуществления настоящего изобретения X3 представляет собой D-аминокислоту.
Согласно некоторым вариантам осуществления настоящего изобретения X3 представляет собой фосфорилированную аминокислоту.
Согласно некоторым вариантам осуществления настоящего изобретения X3 представляет собой нефосфорилируемую аминокислоту.
Согласно некоторым вариантам осуществления настоящего изобретения X3 представляет собой не связывающуюся с водородом аминокислоту.
Согласно некоторым вариантам осуществления настоящего изобретения X3 выбран из группы, состоящей из полярной незаряженной аминокислоты и гидрофобной аминокислоты.
Согласно некоторым вариантам осуществления настоящего изобретения X2 представляет собой Ser.
Согласно некоторым вариантам осуществления настоящего изобретения X4 представляет собой альфа-метиламинокислоту, а X6 представляет собой аланин.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид имеет аминокислотную последовательность HSAPHP (SEQ ID NO: 49) или HSEPHP (SEQ ID NO: 50).
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид содержит по меньшей мере одну дополнительную аминокислоту (X7), присоединенную к С-концу аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения по меньшей мере одна дополнительная аминокислота является отрицательно заряженной аминокислотой.
Согласно некоторым вариантам осуществления настоящего изобретения по меньшей мере одна дополнительная аминокислота выбрана из группы, состоящей из Asp, Glu, Gly, Ala и Ser.
Согласно некоторым вариантам осуществления настоящего изобретения по меньшей мере одна дополнительная аминокислота содержит две дополнительных аминокислоты (X7-X8), и при этом X8 выбран из группы, состоящей из His, Dab, Asp и Glu.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид содержит по меньшей мере одну дополнительную аминокислоту, присоединенную к N-концу аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид содержит по меньшей мере две дополнительных аминокислоты, присоединенных к N-концу аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения по меньшей мере одна дополнительная аминокислота, присоединенная к N-концу аминокислотной последовательности, представляет собой Arg.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид дополнительно содержит проникающий в клетку фрагмент.
Согласно некоторым вариантам осуществления настоящего изобретения проникающий в клетку фрагмент присоединяется к N-концу пептида.
Согласно некоторым вариантам осуществления настоящего изобретения проникающий в клетку фрагмент выбран из группы, состоящей из фрагмента жирной кислоты, белкового фрагмента и их комбинации.
Согласно некоторым вариантам осуществления настоящего изобретения фрагмент жирной кислоты содержит миристоильную жирную кислоту, а белковый фрагмент содержит по меньшей мере одну положительно заряженную аминокислоту.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид в длину составляет не более 20 аминокислот.
Согласно некоторым вариантам осуществления настоящего изобретения пептид по меньшей мере частично изменяет конформацию мутантного белка p53 на конформацию белка p53 дикого типа (WT).
Согласно некоторым вариантам осуществления настоящего изобретения пептид по меньшей мере частично изменяет конформацию мутантного белка p53 так, что мутантный белок p53 распознается моноклональным антителом против белка p53 WT.
Согласно некоторым вариантам осуществления настоящего изобретения мутантный белок p53 не распознается моноклональным антителом против белка p53 WT.
Согласно некоторым вариантам осуществления настоящего изобретения мутантный белок p53 при связывании с пептидом распознается моноклональным антителом против белка p53 WT.
Согласно некоторым вариантам осуществления настоящего изобретения моноклональным антителом является Ab1620.
Согласно некоторым вариантам осуществления настоящего изобретения пептид по меньшей мере частично восстанавливает активность мутантного белка p53 до активности белка p53 WT.
Согласно некоторым вариантам осуществления настоящего изобретения активность заключается в снижении жизнеспособности клеток, экспрессирующих мутантный белок p53.
Согласно некоторым вариантам осуществления настоящего изобретения активность заключается в обеспечении апоптоза клеток, экспрессирующих мутантный белок p53.
Согласно некоторым вариантам осуществления настоящего изобретения активность заключается в связывании с элементом связывания с консенсусной ДНК p53 в клетках, экспрессирующих мутантный белок p53.
Согласно некоторым вариантам осуществления настоящего изобретения элемент связывания с консенсусной ДНК содержит последовательности нуклеиновой кислоты, изложенные в SEQ ID NO: 55 и 56.
Согласно некоторым вариантам осуществления настоящего изобретения связывание приводит к по меньшей мере частичной активация эндогенного целевого гена p53.
Согласно некоторым вариантам осуществления настоящего изобретения эндогенный целевой ген выбран из группы, состоящей из p21, MDM2 и PUMA.
Согласно некоторым вариантам осуществления настоящего изобретения мутантный белок p53 характеризуется конформацией, отличной от таковой белка p53 WT.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид изложен в SEQ ID NO: 429 или 448.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид изложен в SEQ ID NO: 429, 448, 446, 449 или 462.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид выбран из группы, состоящей из SEQ ID NO: 8 и 412-464.
Согласно некоторым вариантам осуществления настоящего изобретения выделенный пептид не является каким-либо из пептидов, изложенных в SEQ ID NO: 59-382.
Согласно аспекту вариантов осуществления настоящего изобретения представлен способ лечения заболевания, нарушения или состояния, ассоциированных с мутантным белком p53, предусматривающий введение субъекту при необходимости этого терапевтически эффективного количества выделенного пептида, описываемого в настоящем документе, с лечением тем самым заболевания, нарушения или состояния.
Согласно некоторым вариантам осуществления настоящего изобретения способ дополнительно предусматривает введение субъекту терапевтически эффективного количества химиотерапии на основе платины.
Согласно аспекту вариантов осуществления настоящего изобретения представлен способ лечения заболевания, нарушения или состояния, ассоциированных с мутантным белком p53, предусматривающий введение субъекту при необходимости этого терапевтически эффективного количества химиотерапии на основе платины и выделенного пептида, содержащего аминокислотную последовательность, имеющего пространство и конфигурацию, которые обеспечивают связывание пептида с доменом связывания с ДНК (DBD) p53 тем же образом, как и pCAP 250 (SEQ ID NO: 1) связывает DBD, при этом пептид по меньшей мере частично реактивирует мутантный белок p53, с лечением тем самым заболевания, нарушения или состояния.
Согласно аспекту вариантов осуществления настоящего изобретения представлен способ лечения заболевания, нарушения или состояния, ассоциированных с мутантным белком p53, предусматривающий введение субъекту при необходимости этого терапевтически эффективного количества выделенного пептида, содержащего аминокислотную последовательность, имеющую пространство и конфигурацию, которые обеспечивают связывание пептида с доменом связывания с ДНК (DBD) p53 тем же образом, как и pCAP 250 (SEQ ID NO: 1) связывает DBD, при этом пептид по меньшей мере частично реактивирует мутантный белок p53, и при этом терапевтически эффективное количество составляет 0,01-0,3 мг/кг в сутки, с лечением тем самым заболевания, нарушения или состояния.
Согласно некоторым вариантам осуществления настоящего изобретения пептидом является пептид, описываемый в настоящем документе.
Согласно некоторым вариантам осуществления настоящего изобретения пептидом является pCAP 250 (SEQ ID NO: 1).
Согласно некоторым вариантам осуществления настоящего изобретения введение включает в себя подкожное введение.
Согласно некоторым вариантам осуществления настоящего изобретения введение включает в себя непрерывную инфузию.
Согласно некоторым вариантам осуществления настоящего изобретения заболеванием является злокачественная опухоль.
Если не указано иное, все технические и/или научные термины, используемые в настоящем документе, имеют то же значение, что традиционно известно рядовому специалисту в области, к которой относится настоящее изобретение. Хотя в осуществлении или тестировании вариантов осуществления настоящего изобретения могут быть использованы способы и материалы, подобные или эквивалентные описываемым в настоящем документе, ниже описываются иллюстративные способы и/или материалы. В случае конфликта контролем будет служить патентное описание. Кроме того, материалы, способы и примеры приведены исключительно с иллюстративной целью и не должны считаться ограничивающими.
Краткое описание чертежей
Варианты осуществления настоящего изобретения описываются в настоящем документе исключительно в качестве примера со ссылкой на прилагаемые графические материалы. С конкретной ссылкой на подробные графические материалы подчеркивается, что показанные данные приведены в качестве примера и с целью иллюстративного обсуждения вариантов осуществления настоящего изобретения. В этом отношении описание в сочетании с графическими материалами позволит специалистам в данной области понять, как можно реализовать варианты осуществления настоящего изобретения.
На фиг. 1 представлен дозозависимый эффект pCAP-250 (SEQ ID NO: 1) отдельно или в комбинации с цисплатином в анализе жизнеспособности клеток злокачественной опухоли яичника ES2. Клетки культивировали в 96-луночных планшетах с 3000 клеток/лунка. Серийные разведения pCAP-250 добавляли либо отдельно, либо вместе с 1 мкг/мл цисплатина и планшеты инкубировали еще 48 часов при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм. Жизнеспособность клеток ES2, обработанных 1 мкг/мл, составляла 39%. IC50 для pCAP-250 оценивали как 3,2 мкM, а в комбинации с цисплатином IC50 для pCAP-250 оценивали как 1,9 мкМ, что указывает на синергетический эффект двух соединений.
На фиг. 2 представлена столбцовая диаграмма, демонстрирующая эффект pCAP-250 (SEQ ID NO: 1) и разных производных (SEQ ID NO: 2-19) в анализе жизнеспособности клеток злокачественной опухоли яичника ES2 и в отношении связывания с p53 DBD, как определяли с помощью MST. Клетки ES2 Con, экспрессирующие эндогенный mp53S241F, и клетки ES2 KO, в которых p53 был стабильно нокаутирован с использованием CRISPR/Cas9 (ES2 p53KO), для контроля специфичности по отношению к mutp53, культивировали в 96-луночных планшетах с 3000 клеток/лунка. Указанные пептиды добавляли при концентрации 8 мкг/мл и планшеты инкубировали еще 48 часов при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм. Различие в эффекте конкретного пептида по отношению к ES2 Con по сравнению с ES KO указывает на специфичность пептида по отношению к экспрессии mutp53. Некоторые пептидные производные, в которых аминокислоты, которые были заменены аланином (серин и гистидин, например), демонстрировали сниженный эффект по отношению к клеткам ES2 Con, что указывает на важное значение этих аминокислот для эффективности пептида.
На фиг. 3A-K представлены графики анализа микромасштабного термофореза (MST) на предмет связывания флуоресцентно меченого WTp53DBD (фиг. 3A) или p53 полной длины (фиг. 3B) и указанных пептидов (SEQ ID NO: 1, 4, 9). Эксперимент выполняли согласно инструкциям изготовителя; получали 10 серийных разведений каждого указанного пептида (фиг. 3A - pCAP-250) (фиг. 3A, F, H, I, K pCAP402, pCAP 404, pCAP409 и pCAP 364), добавляли меченый белок к каждому пептидному образцу и загружали на капилляры. Образцы анализировали на предмет передвижения флуоресцентного wtp53DBD в температурном градиенте с различными концентрациями пептидов. Результаты анализа MST представлены в виде кривой, полученной с помощью программного обеспечения изготовителя для анализа данных.
На фиг. 4A-D представлены фармакокинетические показатели различных путей введения. Фиг. 4A – Концентрация в плазме против временных профилей pCAP-250 после введения 1 мг/кг iv (среднее ± SD, n = 3). Фиг. 4B - Концентрация в плазме против временных профилей pCAP-250 после непрерывного подкожного введения в течение 7 суток (среднее ± SD, n = 3). Фиг. 4C - Концентрация в плазме против временных профилей pCAP-250 после введения 1 мг/кг iv (среднее ± SD, n = 3). Фиг. 4D - Концентрация в плазме против временных профилей pCAP-250 после подкожного введения 1 мг/кг (среднее ± SD, n = 3).
На фиг. 5A-D представлен in vivo эффект пептида pCAP-250 на мышиной модели ксенотрансплантата.
Клетки 2*105 ES2, экспрессирующие люциферазу, вводили инъекцией в бедра голых мышей. Измеряли биолюминесценцию. Через 12 суток после инъекции мышей рандомно делили на 4 группы и вводили инъекцию внутрь опухоли, три раза в неделю, либо со смесью 2 контрольных пептидов (pCAP 76 и 12; 5 мкг каждого пептида), либо с pCAP-250 (10 мкг). В качестве альтернативы, мышам трансплантировали мининасосы Alzet, содержащие 0,8 мг в PBS контрольных пептидов или 0,8 мг в PBS pCAP-250. На фиг. 5A показано прямое изображение мышей контрольной группы и обработанных pCAP-250 внутрь опухоли мышей по окончании эксперимента (день 21). На фиг. 5B показано прямое изображение мышей контрольной группы и обработанных pCAP-250 с помощью мининасосов Alzet мышей по окончании эксперимента (день 14). На фиг. 5C показаны контрольные мыши и группа эффективного pCAP-250: показаны блочная диаграмма, демонстрирующая считывания люциферазы в опухолях как функцию времени; среднее значение (горизонтальная линия), стандартное отклонение (рамка), самое высокое и самое низкое считывания до (до дня 0) и после начала обработки. Фоновый пороговый уровень выявления системы IVIS составлял приблизительно 5 × 106 фотонов. На фиг. 5D показаны контрольные мыши и группа эффективного pCAP-250: показаны блочная диаграмма, демонстрирующая считывания люциферазы в опухолях как функцию времени; среднее значение (горизонтальная линия), стандартное отклонение (рамка), самое высокое и самое низкое считывания до (до дня 0) и после начала обработки. Фоновый пороговый уровень выявления системы IVIS составлял приблизительно 5 × 106 фотонов.
На фиг. 6A-C показано необязательное прогнозируемое положение связывания пептида для пептидной последовательности HSTPHPD на поверхности домена связывания с ДНК (DBD) P53. DBD представлен в виде нарисованного бирюзым изображения, а прогнозируемый пептид показан как пурпурные веточки. На фиг. 6A представлена общая схема пептидного комплекса DBD. На фиг. 6B представлено более близкое рассмотрение области связывания DBD-пептид. На фиг. 6C представлен подробный атомический перечень невалентного взаимодействия между DBD (цепь B) и положением связывания прогнозируемого пептида (цепь A).
На фиг. 7 показаны дозозависимые эффекты реактивирующих p53 пептидов в трех повторностях. Линия клеток SW480, содержащая мутантный p53R273H p53. Клетки культивировали в 96-луночных планшетах с 3000 клеток/лунка. Добавляли серийные разведения разных пептидов и планшеты инкубировали еще 72 часа при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм. Результаты нормализовали по 100% жизнеспособности необработанных клеток.
На фиг. 8 показаны дозозависимые эффекты реактивирующих p53 пептидов в трех повторностях. Линия клеток ES2, содержащая мутант S241F p53. Клетки культивировали в 96-луночных планшетах с 3000 клеток/лунка. Добавляли серийные разведения разных пептидов и планшеты инкубировали еще 48 часов при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм. Результаты нормализовали по 100% жизнеспособности необработанных клеток.
На фиг. 9 показаны спектры 1H–15N HSQC корового домена (DBD) p53 дикого типа, полученные при 293 K, спектры DBD (94-312 из SEQ ID NO: 44) и определение остатков, полученное Wong et al., показано черным (Wong, K.B., et al., Hot-spot mutants of p53 core domain evince characteristic local structural changes. Proc Natl Acad Sci U S A, 1999. 96(15): p. 8438-42). ЯМР-спектры, полученные для свободного DBD (94-296) и для комплекса DBD-pCAP 250, показаны синими и красными, соответственно. Примеры умеренных (C277 и R280) и сильных пиковых изменений (G117) выделены пурпурным и коричневым, соответственно. Пиковые области H115 и Y126 выделены желтым.
На фиг. 10 представлено картирование структуры DBD по изменению спектров 1H–15N HSQC в результате связывания pCAP 250 (SEQ ID NO: 1) с DBD. Структура DBD представлена в виде рисунка, а ДНК окрашена желтым. Неопределяемые остатки из анализа Wong et al. (выше) окрашены зеленым, а остатки, обеспечивающие пиковые изменения при добавлении pCAP 250, окрашены пурпурным.
На фиг. 11A-B представлена структурная реорганизация H115, G117 и Y126. Структура DBD представлена в виде рисунка, а ДНК окрашена желтым. H115, G117 и Y126 показаны в виде зеленых веточек, а петля L1 окрашена пурпурным. На фиг. 11A и 11B представлены верхние и вторые верхние энергетически наилучшие конформации DBD, расшифрованные с помощью ЯМР (pdb код 2FEJ), соответственно.
На фиг. 12 представлены спектры 1H–15N HSQC комплексов DBD p53 дикого типа-пептид, полученные при 293 K. ЯМР-спектры, полученные для белково-пептидных комплексов DBD-pCAP 250 и для DBD-pCAP 615 (SEQ ID NO: 465) показаны красным и зеленым, соответственно. Пики H115 и Y126 обозначены кружочками.
На фиг. 13 представлены спектры 1H–15N HSQC комплексов DBD p53 дикого типа и DBD-pCAP 553 (SEQ ID NO: 429), полученные при 293 K. ЯМР-спектры, полученные для свободного DBD и для белково-пептидного комплекса DBD-pCAP 553, показаны синим и красным, соответственно. Сильные неопределяемые пики, которые особенно проявляются при пересмотре пептида pCAP 553, обозначаются зелеными овалами. Несколько примеров пиков, которые становятся более уплотненными и округлыми, в комплексе DBD-pCAP 553 обозначаются коричневыми овалами.
На фиг. 14 представлены верхние части двух моделей связывания прогнозируемого пептида для комплекса DBD-pCAP 250. Структура DBD представлена в виде рисунка, а ДНК окрашена желтым. H115, G117 и Y126 показаны в виде зеленых веточек, а петля L1 окрашена пурпурным. Верхние части двух моделей связывания прогнозируемого пептида для комплекса DBD-pCAP 250 окрашены бирюзовым.
Подробное описание настоящего изобретения
Настоящее изобретение согласно вариантам его осуществления относится к пептидам и их применению в лечении заболеваний, нарушений или состояний, ассоциированных с мутантным p53.
Перед подробным объяснением по меньшей мере одного варианта осуществления настоящего изобретения следует отметить, что настоящее изобретение не должно обязательно ограничиваться его применением с подробностями, изложенными в следующем описании или проиллюстрированными примерами. Настоящее изобретение может предусматривать другие варианты осуществления или осуществляться, или выполняться различными путями.
Авторы вариантов осуществления настоящего изобретения ранее описывали применение фагового дисплея для отбора реактивирующих mutp53 пептидов (WO2015/019318, которая тем самым включена посредством ссылки во всей своей полноте). Показали, что лидерные пептиды, в том числе pCAP 250 (SEQ ID NO: 1), обеспечивают для mutp53 подобные WTp53 активности in vitro и в живых клетках, и приводят к регрессии несущих mutp53 опухолей на некоторых моделях ксенотрансплантатов.
При осуществлении настоящего изобретения на практике авторы настоящего изобретения обнаружили, что pCAP 250 связывает домен связывания с ДНК (DBD) p53. Структурно-функциональный анализ с использованием сканирования аланина выявил консенсус для связывания pCAP 250 с DBD.
Экспериментальные результаты ЯМР обеспечивают дополнительные доказательства явного связывания pCAP 250 и его пептидных вариантов с DBD WT белка p53. Эти результаты подтверждают выводы о связывании pCAP 250 с DBD с использованием анализа микромасштабного термофореза (MST) (фиг. 3A-K). Результаты ЯМР дополнительно указывают на то, что связывание pCAP 250 и его пептидных вариантов индуцирует структурные изменения в DBD, которые непосредственно влияют на целостность и стабильность области связывания DBD-ДНК, а именно структурные мотивы Helix-2 и петли L1, которые необходимы для способности DBD связывать ДНК. Связывание pCAP 250 и его пептидных вариантов дополнительно влияет на дополнительные остатки в окружении структурных мотивов Helix-2 и петли L1, создавая относительно большой, но при этом существенно нарушенный участок поверхности DBD.
Эти результаты позволяют разработать новые пептиды, которые демонстрируют одинаковое взаимодействие с DBD p53 и способны, по меньшей мере частично, реактивировать мутантный белок p53, при этом такие пептиды, наделенные противораковой активностью, показаны в примере 5.
Таким образом, согласно аспекту настоящего изобретения представлен выделенный пептид, содержащий аминокислоту последовательность, расположенную в пространстве и конфигурации, которые обеспечивают взаимодействие пептида доменом связывания с ДНК (DBD) p53 через по меньшей мере один остаток DBD, посредством которого pCAP 250 (SEQ ID NO: 1) связывает DBD, при этом указанный пептид по меньшей мере частично реактивирует мутантный белок p53.
Согласно конкретному варианту осуществления пептид не является SEQ ID NO: 1-338, 368-382 из WO2015/019318 (т.е. SEQ ID NO: 59-382 в настоящем документе).
Согласно конкретному варианту осуществления пептид не является каким-либо из пептидов, описанных в WO2015/019318, включенной тем самым посредством ссылки во всей своей полноте, поскольку обладает активностью реактивации мутантного p53.
Используемый в настоящем документе термин «выделенный» относится, по меньшей мере частично, к отделенному от естественной среды, например, от организма или от пептидной библиотеки.
Используемый в настоящем документе термин «p53», также известный как «TP53», относится к генной последовательности, кодирующей белковый продукт EC 2.7.1.37, как правило, функционирующий как фактор транскрипции, регулирующий клеточный цикл, следовательно, функционирующий в своей форме дикого типа как ген-супрессор опухолей. Согласно конкретному варианту осуществления p53 представляет собой человеческий p53.
Используемые в настоящем документе термины «p53 дикого типа», «p53 wt» и «p53 WT» могут быть использованы взаимозаменяемо и относятся к белку p53 дикого типа, обладающему конформацией белка p53 дикого типа и, следовательно, активностью белка p53 дикого типа. Согласно вариантам осуществления p53 дикого типа может быть идентифицирован с помощью специфического моноклонального антитела. Согласно некоторым вариантам осуществления моноклональным антителом является Ab1620.
Структурные данные для белка доступны из PDBe RCSB.
Термин «конформация» по отношению к белку относится к структурному расположению (фолдингу) белка в пространстве.
Используемые в настоящем документе термины «мутантный p53», «Mut-p53», «мутантировавший p53» и «мутант p53» могут быть использованы взаимозаменяемо и относятся к мутантному белку p53, неспособному эффективно функционировать в целевой клетке. Согласно вариантам осуществления Mut-p53 не может связываться со своим целевым сайтом. Согласно вариантам осуществления Mut-p53 является мутантным по области домена связывания с ДНК (DBD). Согласно вариантам осуществления Mut-p53 неправильно свернут в неактивную конформацию. Согласно некоторым типичным вариантам осуществления Mut-p53 является чувствительным к температуре (ts) mut p53 R249S (R249S p53), мутантным p53 Mut-p53 R175H (R175H p53) полной длины с «горячей точкой» или каким-либо другим белком Mut-p53. Согласно вариантам осуществления Mut-p53 идентифицируют с помощью специфического моноклонального антитела, способного распознавать неправильно свернутую конформацию p53 (индуцированную мутацией p53). Согласно вариантам осуществления Mut-p53 идентифицируют с помощью специфического моноклонального антитела. Согласно некоторым вариантам осуществления моноклональным антителом является Ab420.
Согласно некоторым вариантам осуществления мутантный белок p53 содержит мутацию, выбранную из группы, состоящей из R175H, V143A, R249S, R273H, R280K, P309S, P151S, P151H, C176S, C176F, H179L, Q192R, R213Q, Y220C, Y220D, R245S, R282W, D281G, S241F, C242R, R248Q, R248W, D281G, R273C и V274F. Каждый вариант представляет отдельный вариант осуществления настоящего изобретения.
Используемые в настоящем документе термины «реактивирующий пептид», «Реактивирующий Mut-p53 пептид» или «пептид» могут быть использованы взаимозаменяемо и относятся к пептиду, способному, по меньшей мере частично, восстанавливать активность Mut-p53. Используемая в настоящем документе фраза «реактивирующий мутантный белок p53» относится к пептиду, который при взаимодействии его с мутантным белком p53 увеличивает у мутантного белка p53 по меньшей мере одну из его активностей, при этом активностями являются активности белка p53 дикого типа. Например, при взаимодействии с пептидом, представленным в настоящем изобретении, мутантный белок p53 может усиливать, непосредственно или опосредованно, экспрессию проапоптических белков, таких как каспазы, в клетке злокачественной опухоли, подобно тому, как это делает белок p53 дикого типа с подобной ситуации, или подавлять опухоли in vivo, как можно проанализировать с использованием мышиной модели заболевания с использованием ксенотрансплантата.
Без углубления в теорию полагают, что реактивирующий пептид связывает mut p53 в DBD, термодинамически стабилизирует фолдинг белка WTp53 и, следовательно, восстанавливает функцию подавления опухоли.
Согласно вариантам осуществления реактивирующий пептид может реактивировать Mut-p53 путем воздействия на конформацию Mut-p53 с обеспечением конформации, которая более подобна или идентична нативному p53 WT. Согласно вариантам осуществления реактивирующий пептид может реактивировать Mut-p53 с восстановлением связывания Mut-p53 с сайтом связывания p53 WT в целевой ДНК. Согласно вариантам осуществления реактивирующий пептид может восстанавливать биохимические свойства Mut-p53. Согласно вариантам осуществления реактивирующий пептид может индуцировать проявление белком Mut-p53 p53-селективного ингибирования клеток злокачественной опухоли. Согласно вариантам осуществления реактивирующий пептид может реактивировать Mut-p53 с наличием структурных свойств, биохимических свойств, физиологических свойств и/или функциональных свойств, подобных (т.е. ± 10%, 20%, 30% различия между Mut-p53 и p53 WT) или идентичных таковым в белке p53 WT, как определено в анализах связывания/структурных анализах, описываемых в настоящем документе, например, MST и ЯМР.
Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 3-30 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-30 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 12-30 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 3-25 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-25 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 12-25 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 3-22 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-22 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 12-22 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-9 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 6-9 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-10 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 6-10 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 9-10 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 8-10 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 6-9 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 6-8 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 6-7 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-8 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7-9 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 5-20 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 6-15 аминокислот в длину. Согласно вариантам осуществления реактивирующим пептидом является пептид, имеющий 7 или 12 аминокислот в длину.
Термин «способный, по меньшей мере частично, реактивировать мутантный белок p53» или «по меньшей мере частично реактивировать мутантный белок p53», как взаимозаменяемо используется в настоящем документе, относится к пептиду, при этом при связывании пептида с мутантным белком p53 у мутантного белка p53 усиливается или повышается активность, подобная соответствующей активности белка p53 дикого типа.
Используемый в настоящем документе термин «домен связывания с ДНК» или «DBD» в p53 относится к домену в p53, который связывает соответствующий элемент p53 в целевом белке (например, элемент связывания с консенсусной ДНК содержит аминокислотную последовательность, изложенную в SEQ ID NO: 44, или состоит из таковой), как правило, относящийся к остаткам 94-292, 91-292, 94-293, 94-296, 91-296, 91-293, 94-312 или 92-312 человеческого p53 (GenBank p53 полной длины: BAC16799,1, SEQ ID NO: 44). Согласно конкретному варианту осуществления DBD принадлежит мутантному p53.
Как упоминалось, пептид содержит аминокислотную последовательность, расположенную в пространстве и конфигурации, которые обеспечивают взаимодействие пептида с DBD в p53 по меньшей мере через один остаток DBD, с помощью которого pCAP 250 (SEQ ID NO: 1) связывает DBD.
Таким образом, реактивирующий пептид согласно некоторым вариантам осуществления настоящего изобретения, как правило, ассоциируется с доменом DBD в p53 так, что реакционно способная группа(ы) пептида располагается достаточно близко к соответствующей реакционно способной группе(ам) (как правило, боковым цепям аминокислотных остатков) в DBD с тем, чтобы обеспечить наличие эффективной концентрация пептида в DBD, и, кроме того, реакционно способные группы пептида располагаются в надлежащей ориентации, чтобы обеспечить перекрывание и, таким образом, сильное химическое взаимодействие и низкую диссоциацию. Поэтому, реактивирующий пептид согласно некоторым вариантам осуществления настоящего изобретения, как правило, включает в себя структурные элементы, которые, как известно, вовлечены во взаимодействия, а также может характеризоваться рестрикцией своей конформационной гибкости, чтобы избежать конформационных изменений, которые могут влиять на его ассоциацию с DBD в p53 или ослаблять ее.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется через Helix-2 и L1 указанного DBD.
Как правило, Helix-2 располагается между аминокислотами 276-289, а L1 располагается между аминокислотами 112-124.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие влияет на структурную стабильность Helix-2 и/или L1 указанного DBD, как анализировали с помощью ЯМР.
Согласно некоторым вариантам осуществления по меньшей мере один остаток в DBD, с помощью которого опосредуется взаимодействие с пептидом, выбран из группы, состоящей из H115, G117 из L1 в p53 и Y126, и V274, и G279, и R280 в p53 (wt или мутантном, в котором различие в аминокислотах, как правило, заключается в отдельных аминокислотах, что не существенно влияет на нумерацию аминокислот). Однако специалисту в данной области будет известно, как найти соответствующую аминокислоту (с точки зрения состава и положения в мутантном p53).
Согласно некоторым вариантам осуществления взаимодействие пептида с DBD является нековалентным, например, опосредованные водородной связью в воде взаимодействия.
Согласно некоторым вариантам осуществления взаимодействие осуществляется с помощью по меньшей мере одной аминокислоты аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере двух аминокислот аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере трех аминокислот аминокислотной последовательности.
Согласно некоторым вариантам осуществления настоящего изобретения взаимодействие осуществляется с помощью по меньшей мере четырех аминокислот аминокислотной последовательности.
Согласно конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Trp146 и/или Gln144 человеческого p53. Данное взаимодействие, вероятно, осуществляется через Ser в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Tyr126, Asn128 и/или Asp268 человеческого p53.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Lys101 человеческого p53 через Asp10 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Thr102 человеческого p53 через Asp10 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Phe113 человеческого p53 через Thr6 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Trp146 человеческого p53 через Ser5 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Ser5 человеческого p53 через Thr6 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой His8 человеческого p53 через Thr6 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Gly112 человеческого p53 через Ser5 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Согласно другому конкретному варианту осуществления взаимодействием является взаимодействие с аминокислотой Gly112 человеческого p53 через Thr6 в pCAP 250 или его аналоги в аналогичных структурах, как далее описывается в настоящем документе ниже.
Другие предполагаемые положения для взаимодействий на поверхности DBD p53 представлены на фиг. 6A-C, которые считаются частью настоящего описания, где каждый вариант представляет независимый вариант осуществления.
Другие предполагаемые положения для взаимодействий на поверхности DBD p53 представлены на фиг. 9-14, которые считаются частью настоящего описания, где каждый вариант представляет независимый вариант осуществления.
Способы изучения аминокислот либо в пептиде, либо в DBD, которые важны для взаимодействия, хорошо известны в уровне техники и включают в себя без ограничения кристаллографию, а также применение компьютерных алгоритмов, например, AnchorDock (Ben Shimon Structure. 2015 May 5;23(5):929-40), Virtual Crystallographic Calculators V.2 и т.п.
Согласно конкретному варианту осуществления пептид содержит консенсусный мотив.
Используемый в настоящем документе термин «консенсусный мотив» относится к аминокислотной последовательности по меньшей мере из 3 аминокислот, 4, 5 или 6 аминокислот, которые могут быть последовательными или непоследовательными. Согласно конкретному варианту осуществления консенсусный мотив имеет в длину 6 последовательных аминокислот.
Согласно некоторым вариантам осуществления настоящего изобретения пептид содержит аминокислотную последовательность
X1-X2-X3-X4-X5-X6 (SEQ ID NO: 53),
в которой
X1 и X5 представляют собой положительно заряженную аминокислоту;
X2 выбран из группы, состоящей из Ser, Thr, Asn, Gln, Pro, Ala и Gly;
X3 представляет собой любую аминокислоту;
X4 и X6 выбраны из группы, состоящей из альфа-метиламинокислоты и аминокислоты, нарушающей структуру бета-листов.
Согласно некоторым вариантам осуществления настоящего изобретения пептид содержит аминокислотную последовательность
X1-X2-X3-X4-X5-X6 (SEQ ID NO: 54),
в которой
X1 и X5 выбраны из группы, состоящей из His, Arg и Lys;
X2 выбран из группы, состоящей из Ser, Thr, Asn, Gln, Pro, Ala и Gly;
X3, X4, X6 представляют собой любую аминокислоту.
Используемый в настоящем документе термин «положительно заряженная аминокислота» представляет аминокислоту, которая может быть положительной (т.e. протонированной) при физиологическом pH.
Согласно варианту осуществления положительно заряженная аминокислота выбрана из группы, состоящей из диаминомасляной кислоты (Dab), Arg и Lys.
Согласно конкретному варианту осуществления X3 представляет собой D-аминокислоту.
Согласно конкретному варианту осуществления X3 является фосфорилированным (например, фосфосерин) или его фосфомиметиком (например, Glu или Asp).
Согласно конкретному варианту осуществления X3 представляет собой нефосфорилируемую аминокислоту (например, Val).
Согласно конкретному варианту осуществления X3 представляет собой не связывающуюся с водородом аминокислоту (например Ala).
Согласно конкретному варианту осуществления X3 выбран из группы, состоящей из полярной незаряженной аминокислоты (например, Ser) и гидрофобной аминокислоты (например Ile).
Согласно конкретному варианту осуществления X2 представляет собой Ser.
Согласно конкретному варианту осуществления X4 и X6 выбраны из группы, состоящей из Ser, Thr, Pro, Ala и Gly.
Согласно конкретному варианту осуществления X4 представляет собой альфа-метиламинокислоту или аминокислоту, нарушающую структуру бета-листов, например, Pro, Aib или Ala.
Согласно конкретному варианту осуществления X4 представляет собой альфа-метиламинокислоту.
Согласно конкретному варианту осуществления X6 представляет собой Ala.
Согласно конкретному варианту осуществления пептид имеет аминокислотную последовательность HSAPHP (SEQ ID NO: 46).
Согласно конкретному варианту осуществления пептид содержит по меньшей мере одну дополнительную аминокислоту (X7), присоединенную к С-концу указанной аминокислотной последовательности.
Согласно конкретному варианту осуществления по меньшей мере одна дополнительная аминокислота является отрицательно заряженной аминокислотой (т.е. аминокислотой, которая, как правило, является отрицательной (т.e. депротонированной) при физиологическом pH), или малой аминокислотой (например, Gly, Ala, Val).
Согласно конкретному варианту осуществления по меньшей мере одна дополнительная аминокислота выбрана из группы, состоящей из Asp, Glu, Gly, Ala и Ser.
Согласно конкретному варианту осуществления по меньшей мере одна отрицательно заряженная аминокислота представляет собой Asp.
Согласно конкретному варианту осуществления по меньшей мере одна дополнительная аминокислота содержит две дополнительных аминокислоты (X7-X8), и при этом указанный X8 выбран из группы, состоящей из His, Dab, Asp и Glu.
Согласно конкретному варианту осуществления по меньшей мере одна отрицательно заряженная аминокислота представляет собой Asp или два последовательных остатка Asp.
Согласно конкретному варианту осуществления пептид содержит по меньшей мере одну дополнительную аминокислоту, присоединенную к N-концу указанной аминокислотной последовательности.
Согласно конкретному варианту осуществления пептид содержит по меньшей мере две дополнительных аминокислоты, присоединенных к N-концу указанной аминокислотной последовательности.
Согласно конкретному варианту осуществления по меньшей мере одна дополнительная аминокислота, присоединенная к N-концу указанной аминокислотной последовательности, представляет собой Arg или два последовательных остатка Arg.
Связывание пептида с DBD может быть определено с использованием любого способа, известного в уровне техники, такого как конкурентный анализ, при котором растворимый DBD используют в качестве конкурирующего средства.
Используемый в настоящем документе термин «рекомбинантный или синтетический пептид» относится к пептиду, полученному с помощью стандартных биотехнологических способов, известных в уровне техники, таких как экспрессия в бактериях или твердофазный пептидный синтез (SPPS).
Согласно конкретному варианту осуществления пептид дополнительно содержит проникающий в клетку фрагмент, который может быть присоединен к N-концу пептида, C-концу пептида или к обоим концам пептида. Будет понятно, что этот фрагмент также может быть связан с основной частью пептида, а не с его концами в случае, если это не влияет на связывание пептида с DBD. Будет понятно, что такой фрагмент является гетерологичным фрагментом, который не связывается с пептидом в природе тем же способом (т.е. в отношении положения или химии).
Используемый в настоящем документе термин «проницаемость» относится к способности средства или вещества проникать, проходить или диффундировать через барьер, мембрану или слой кожи. Фрагмент «клеточной проницаемости» или «клеточного проникновения» относится к любой молекуле, известной в уровне техники, которая способна облегчать или усиливать проникновение молекул через мембраны.
Используемая в настоящем документе фраза «усиливающий проницаемость фрагмент» относится к средству, которое усиливает транслокацию любого присоединенного пептида через клеточную мембрану.
Любой фрагмент, известный в уровне техники для облегчения, активно или пассивно, или для усиления проницаемости композиций в клетки, может быть использован для конъюгации с пептидным ядром в соответствии с настоящим изобретением. Неограничивающие примеры включают в себя гидрофобные фрагменты, такие как жирные кислоты, стероиды и объемные ароматические или алифатические соединения; фрагменты, которые могут иметь рецепторы клеточной мембраны, или носители, такие как стероиды, витамины и сахара, встречающиеся в природе (например, положительно заряженные аминокислоты, например, Lys или Arg) и не встречающиеся в природе аминокислоты, и белковый фрагмент, например, транспортерные пептиды, также называемые «проникающими в клетку пептидами» или CPP, поли-аргинин или поли-лизин их комбинацию или антитело. Согласно некоторым вариантам осуществления белковым фрагментом является CPP. Согласно некоторым вариантам осуществления белковым фрагментом является поли-аргинин. Согласно некоторым вариантам осуществления гидрофобным фрагментом является липидный фрагмент или аминокислотный фрагмент. Согласно некоторым вариантам осуществления настоящего изобретения проникающий в клетку фрагмент представляет собой комбинацию белкового фрагмента и фрагмента на основе липида (например, один с N-конца, а другой с C-конца пептида).
Проникающие в клетку пептиды (CPP) являются короткими пептидами (≤ 40 аминокислот) со способностью получать доступ во внутренне пространство почти любой клетки. Они являются высоко катионными и обычно богаты аминокислотами аргинин и лизин. В этой связи авторы настоящего изобретения использовали положительно заряженные аминокислоты (на обоих концах пептида) или поликатионные аминокислоты (по меньшей мере 2, например, 2-12) poly-Arg для обеспечения проникновения пептидов в клетку. Они обладают исключительным свойством переноса в клетки обширного ряда ковалентно и нековалентно конъюгированных грузов, таких как белки, олигонуклеотиды и даже 200-нм липосомы. Поэтому, согласно дополнительному типичному варианту осуществления CPP могут быть использованы для транспортировки пептидов во внутренне пространство клеток.
TAT (активатор транскрипции из HIV-1), pAntp (также называемый пенетратином, гомеодоменным фактором транскрипции Drosophila antennapedia) и VP22 (из вируса Herpes Simplex) являются примерами CPP, которые могут попадать в клетки нетоксическим и эффективном путем и могут быть подходящими для применения согласно вариантам осуществления настоящего изобретения. Протоколы для получения конъюгатов CPP-груз и для инфицирования клеток такими конъюгатами можно найти, например, у L Theodore et al. (The Journal of Neuroscience, (1995) 15(11): 7158-7167), Fawell S, et al. (Proc Natl Acad Sci USA, (1994) 91:664–668) и Jing Bian et al. (Circulation Research (2007) 100: 1626-1633).
Однако настоящее раскрытие не является ограничивающим, и может быть использовано любое подходящее проницающее средство, известное специалистам в данной области.
Если пептиды в соответствии с настоящим изобретением присоединяются к проникающим в клетку пептидам, предполагается, что пептид полной длины состоит из не более 50 аминокислот, не более 40 аминокислот, не более 35 аминокислот, не более 30 аминокислот, не более 25 аминокислот, не более 22 аминокислот, не более 20 аминокислот, не более 15 аминокислот, не более 12 аминокислот, не более 10 аминокислот, не более 9 аминокислот, не более 8 аминокислот или не более 7 аминокислот.
Неограничивающие примеры небелковых проникающих в клетку фрагментов включают в себя гидрофобные фрагменты, такие как липиды, жирные кислоты, стероиды и объемные ароматические или алифатические соединения; фрагменты, которые могут иметь рецепторы клеточной мембраны, или носители, такие как стероиды, витамины и сахара, наночастицы и липосомы.
Используемый в настоящем документе термин «фрагмент жирной кислоты» относится к части жирной кислоты, которая демонстрирует конкретный набор химических и фармакологических характеристик, подобных соответствующей полной исходной молекуле жирной кислоты. Термин, кроме того, относится к любым молекулярным частицам и/или молекулярному фрагменту, содержащим ацильный компонент жирной (карбоновой) кислоты.
Усиливающий проницаемость фрагмент в соответствии с настоящим изобретением предпочтительно ковалентно соединяется с пептидной последовательностью посредством прямой связи или через линкер с образованием пептидного конъюгата. Усиливающий проницаемость фрагмент может быть присоединен к любому положению в пептидном фрагменте, непосредственно или через спейсер, предпочтительно к аминоконцу пептида. Согласно определенным вариантам осуществления усиливающим проницаемость фрагментом является жирная кислота.
Гидрофобный фрагмент в соответствии с настоящим изобретением предпочтительно может содержать липидный фрагмент или аминокислотный фрагмент. Согласно конкретному варианту осуществления гидрофобной фрагмент выбран из группы, состоящей из фосфолипидов, стероидов, сфингозинов, церамидов, октил-глицина, 2-циклогексилаланина, бензоилфенилаланина, пропионоила (C3); бутаноила (C4); пентаноила (C5); капроила (C6); гептаноила (C7); каприлоила (C8); нонаноила (C9); каприла (C10); ундеканоила (C11); лауроила (C12); тридеканоила (C13); миристоила (C14); пентадеканоила (C15); пальмитоила (C16); фтаноила ((CH3)4); гептадеканоила (C17); стеароила (C18); нонадеканоила (C19); арахидоила (C20); генэйкозаноила (C21); бехеноила (C22); руцизаноила (C23) и лигноцероила (C24); при этом указанный гидрофобной фрагмент присоединяется к указанному химерному полипептиду амидными связями, сульфгидрилами, аминами, спиртами, фенольными группами или связями углерод-углерод.
Другими примерами липидных фрагментов, которые могут быть использованы в соответствии с настоящим изобретением, являются липофектамин, трансфектак, трансфектам, цитофектин, DMRIE, DLRIE, GAP-DLRIE, DOTAP, DOPE, DMEAP, DODMP, DOPC, DDAB, DOSPA, EDLPC, EDMPC, DPH, TMADPH, CTAB, lysyl-PE, DC-Cho, аланилхолестерин; DCGS, DPPES, DCPE, DMAP, DMPE, DOGS, DOHME, DPEPC, Pluronic, Tween, BRIJ, плазмалоген, фосфатидилэтаноламин, фосфатидилхолин, глицерин-3-этилфосфатидилхолин, диметиламмония пропан, триметиламмония пропан, диэтиламмония пропан, триэтиламмония пропан, диметилдиоктадециламмония бромид, сфинголипид, сфингомиелин, лизолипид, гликолипид, сульфатид, гликосфинголипид, холестерин, сложный эфир холестерина, соль холестерина, масло, N-сукцинилдиолеоилфосфатидилэтаноламин, 1,2-диолеоил-sn-глицерин, 1,3-дипальмитоил-2-сукцинилглицерин, 1,2-дипальмитоил-sn-3-сукцинилглицерин, 1-гексадецил-2-пальмитоилглицерофосфатидилэтаноламин, пальмитоилгомоцистеин, N,N'-бис(додециаминокарбонилметилен)-N,N'-бис((-N,N,N-триметиламмоний-этил-аминокарбонилметилен)этилендиамина тетрайодид; N,N"-бис(гексадециламинокарбонилметилен)-N,N',N"-трис((-N,N,N-триметиламмоний-этиламинокарбонилметилендиэтилентриамина гексайодид; N,N'-бис(додециламинокарбонилметилен)-N,N"-бис((-N,N,N-триметиламмоний-этиламинокарбонилметилен)циклогексилен-1,4-диамина тетрайодид; 1,7,7-тетра-((N,N,N,N-тетраметиламмоний-этиламино-карбонилметилен)-3-гексадециламинокарбонил-метилен-1,3,7-триазагептана гептайодид; N,N,N',N'-тетра-((N,N,N-триметиламмоний-этиламинокарбонилметилен)-N'-(1,2-диолеоилглицеро-3-фосфоэтаноламинокарбонилметилен)диэтилентриамина тетрайодид; диолеоилфосфатидилэтаноламин, жирная кислота, лизолипид, фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, фосфатидилглицерин, фосфатидилинозит, сфинголипид, гликолипид, глюколипид, сульфатид, гликосфинголипид, фосфатидная кислота, пальмитиновая кислота, стеариновая кислота, арахидоновая кислота, олеиновая кислота, несущий липид полимер, несущий липид сульфонированный сахарид, холестерин, токоферола гемисукцинат, липид со связанной с эфиром жирной кислотой, липид со связанной со сложным эфиром жирной кислотой, полимеризованный липид, диацетилфосфат, стеариламин, карбиолипин, фосфолипид с жирной кислотой длиной 6-8 углеродов, фосфолипид с асимметричными ацильными цепями, 6-(5-холестен-3b-илокси)-1-тио-b-D-галактопиранозид, дигалактозилдиглицерид, 6-(5-холестен-3b-илокси)гексил-6-амино-6-деокси-1-тио-b-D-галактопиранозид, 6-(5-холестен-3b-илокси)гексил-6-амино-6-деоксил-1-тио-a-D-маннопиранозид, 12-(((7'-диэтиламино-кумарин-3-ил)карбонил)метиламино)-октадекановая кислота; N-[12-(((7'-диэтиламино-кумарин-3-ил)карбонил)метил-амино)окстадеканоил]-2-аминопальмитиновая кислота; холестерил-4'-триметил-аммонио)бутаноат; N-сукцинилдиолеоил-фосфатидилэтаноламин; 1,2-диолеоил-sn-глицерин; 1,2-дипальмитоил-sn-3-сукцинил-глицерин; 1,3-дипальмитоил-2-сукцинилглицерин, 1-гексадецил-2-пальмитоилглицеро-фосфоэтаноламин и пальмитоилгомоцистеин.
Термины «полипептид» и «пептид» используют взаимозаменяемо в настоящем документе в отношении полимера из аминокислотных остатков. Данные термины применяют к аминокислотным полимерам, в которых один или несколько аминокислотных остатков являются искусственными химическими аналогами соответствующей встречающейся в природе аминокислоты, а также к встречающимся в природе аминокислотным полимерам.
Используемый в настоящем документе термин «пептид» охватывает нативные пептиды (либо продукты разложения, синтетически синтезированные пептиды, либо рекомбинантные пептиды) и пептидомиметики (как правило, синтетически синтезированные пептиды), а также пептоиды и полупептоиды, являющиеся пептидными аналогами, которые могут иметь, например, модификации, придающие пептидам бóльшую стабильность в организме или бóльшую способность к проникновению в клетки. Такие модификации включают в себя без ограничения N-концевую модификацию, C-концевую модификацию, модификацию пептидной связи, модификации каркаса и модификацию остатков. Способы получения пептидомиметических соединений хорошо известны в уровне техники и описаны, например, в Quantitative Drug Design, C.A. Ramsden Gd., Chapter 17.2, F. Choplin Pergamon Press (1992), которая включена посредством ссылки, как если бы полностью была изложена в настоящем документе. Дополнительные подробности в этом отношении представлены в настоящем документе ниже.
Пептидные связи (-CO-NH-) в пептиде могут быть замещены, например, N-метилированными амидными связями (-N(CH3)-CO-), сложноэфирными связями (-C(=O)-O-), кетометиленовыми связями (-CO-CH2-), сульфинилметиленовыми связями (-S(=O)-CH2-), _-аза-связями (-NH-N(R)-CO-), при этом R представляет собой любой алкил (например, метил), аминовыми связями (-CH2-NH-), сульфидными связями (-CH2-S-), этиленовыми связями (-CH2-CH2-), гидроксиэтиленовыми связями (-CH(OH)-CH2-), тиоамидными связями (-CS-NH-), олефиновыми двойными связями (-CH=CH-), фторированными олефиновыми двойными связями (-CF=CH-), ретроамидными связями (-NH-CO-), пептидными производными (-N(R)-CH2-CO-), при этом R представляет собой «нормальную» боковую цепь, в естественных условиях присутствующую на атоме углерода.
Такие модификации могут встречаться при любой из связей вдоль пептидной цепи и даже при нескольких (2-3) связях одновременно.
Термин «консервативная замена» относится к замене аминокислоты из одного класса аминокислотой того же класса, при этом класс определяют по общим физико-химическим свойствам боковой цепи аминокислоты и по высоким частотам замены в гомологичных белках, обнаруженных в природе, как определяют, например, с помощью стандартной матрицы частоты замещений Дайхоффа или матрицы BLOSUM. Боковые цепи аминокислот классифицировали на шесть общих классов, которые включают в себя класс I (Cys); класс II (Ser, Thr, Pro, Ala, Gly); класс III (Asn, Asp, Gin, Glu); класс IV (His, Arg, Lys); класс V (He, Leu, Val, Met) и класс VI (Phe, Tyr, Trp). Например, замена другого остатка класса III, такого как Asn, Gin или Glu на Asp является консервативной заменой.
Другие классификации включают в себя положительные аминокислоты (Arg, His, Lys), отрицательные аминокислоты (Asp, Glu), полярные незаряженные (Ser, Thr, Asn, Gln), гидрофобные боковые цепи (Ala, Val, Ile, Leu, Met, Phe, Tyr, Trp).
Термин «неконсервативная замена» относится к замене аминокислоты в одном классе аминокислотой из другого класса; например, замена Ala, остатка из класса II, остатком из класса III, таким как Asp, Asn, Glu или Gin.
Встречающиеся в природе ароматические аминокислоты Trp, Tyr и Phe могут быть замещены не встречающимися в природе ароматическими аминокислотами, такими как 1,2,3,4-тетрагидроизохинолин-3-карбоновая кислота (Tic), нафтилаланин, производные Phe с метилированным кольцом, галогенированные производные Phe или O-метил-Tyr. Другие синтетические варианты приводятся далее в настоящем документе в таблице 2.
Пептиды согласно вариантам осуществления настоящего изобретения также могут включать в себя одну или несколько модифицированных аминокислот либо один или несколько неаминокислотных мономеров (например, жирных кислот, комплексных углеводов и т.д.).
Термин «аминокислота» или «аминокислоты» включает в себя 20 встречающихся в природе аминокислот, такие аминокислоты, которые зачастую модифицированы послетрансляционно in vivo, в том числе, например, гидроксипролин, фосфосерин и фосфотреонин, и другие необычные аминокислоты, в том числе без ограничения 2-аминоадипиновую кислоту, гидроксилизин, изодесмозин, норвалин, норлейцин и орнитин. Кроме того, термин «аминокислота» включает в себя как D-, так и L-аминокислоты.
В приведенных ниже таблицах 1 и 2 перечисляются встречающиеся в природе аминокислоты (таблица 1) и нетипичные или модифицированные аминокислоты (например, синтетические, таблица 2), которые могут быть использованы согласно вариантам осуществления настоящего изобретения.
Таблица 1
Таблица 2
Пептиды согласно вариантам осуществления настоящего изобретения предпочтительно используют в линейной форме, хотя будет понятно, что в случаях, если циклизация серьезно не нарушает характеристики пептида, также могут быть использованы циклические формы пептида.
Для улучшения биодоступности пептид может содержать по меньшей мере одну D-аминокислоту (например, 2-7, 2-6, 2-5, 2-4, 2-3). Согласно конкретному варианту осуществления все аминокислоты в пептиде являются D-аминокислотами.
Согласно вариантам осуществления пептид является химически модифицированным.
Термин «химически модифицированная» относится к аминокислоте, которая является модифицированной либо естественными процессами, либо методиками химической модификаций, которые хорошо известны в уровне техники. Типичные, но не исключительные примеры многочисленных известных модификаций включают в себя ацетилирование, ацилирование, амидирование, АДФ-рибозилирование, гликозилирование, гликозаминогликанирование, формирование GPI якоря, ковалентное присоединение липида или липидного производного, метилирование, миристилирование, пегилирование, пренилирование, фосфорилирование, убиквитинилирование или любой подобный процесс (см., например, SEQ ID NO: 2, 17-19).
Согласно конкретному варианту осуществления пептид может предусматривать C-концевое амидирование.
В качестве альтернативы или дополнения, пептид может быть конъюгирован с небелковым нетоксичным фрагментом, таким как без ограничения полиэтиленгликоль (PEG), пливинилпирролидон (PVP), поли(малеиновый ангидрид стирола) (SMA) и сополимер дивинилового эфира и малеинового ангидрида (DIVEMA).
Будет понятно, что в качестве пептидов в соответствии с настоящим изобретением также могут быть использованы пептидные гомологи, которые обладают желаемой активностью (например, реактивация мутантов p53), также называемые в настоящем документе функциональными эквивалентами, в силу чего активность пептидного гомолога определяют согласно способам, известным в уровне техники, таким как описываемые в настоящем документе. Такие гомологи могут быть, например, по меньшей мере на 80%, по меньшей мере на 81%, по меньшей мере на 82%, по меньшей мере на 83%, по меньшей мере на 84%, по меньшей мере на 85%, по меньшей мере на 86%, по меньшей мере на 87%, по меньшей мере на 88%, по меньшей мере на 89%, по меньшей мере на 90%, по меньшей мере на 91%, по меньшей мере на 92%, по меньшей мере на 93%, по меньшей мере на 94%, по меньшей мере на 95%, по меньшей мере на 96%, по меньшей мере на 97%, по меньшей мере на 98%, по меньшей мере на 99% или на 100% идентичны SEQ ID NO: 53, или 54, или 1 (при условии, что это не пептиды, раскрытые в WO2015/019318 (например, SEQ ID NO: 286-321).
Согласно конкретному варианту осуществления пептид содержит аминокислотную последовательность или изложен в SEQ ID NO: 8, 412-464.
Согласно конкретному варианту осуществления пептид выбран из группы последовательностей SEQ ID NO: 429, 448, 449, 446 и 462.
Согласно некоторым вариантам осуществления пептид по меньшей мере частично изменяет конформацию мутантного белка p53 до конформации белка p53 дикого типа (WT).
В уровне техники известны антитела, которые специфически распознают только белки p53 дикого типа. Такие антитела высоко применимы в определении того, может ли определенный белок p53, либо дикого типа, либо мутант сохранять конформацию функционального белка p53 дикого типа. Таким образом, согласно некоторым вариантам осуществления пептид по меньшей мере частично изменяет конформацию мутантного белка p53 так, что мутантный белок p53 распознается моноклональным антителом, направленным исключительно против белка p53 WT или против белка p53, сохраняющего конформацию белка p53 WT. Согласно некоторым вариантам осуществления моноклональным антителом является Ab1620.
Следует учитывать, что, поскольку p53 экспрессируется из обоих аллелей, суммарное содержание внутриклеточного p53 может быть представлено диким типом (wt/wt) или смесью wt и мутантного p53 (wt/mut), или только мутантным p53 (если оба аллеля являются мутантными (mut/mut), или удалением одного аллеля (mut/-)). При злокачественной опухоли ситуация зачастую представляет собой wt/mut, mut/mut или mut/-. Поскольку p53 действует как тетрамер, мутантные белки p53 могут отменять активность белков p53 дикого типа, которые могут существовать в клетках злокачественной опухоли. Поэтому, пептиды, обеспечиваемые в соответствии с настоящим изобретением, особенно применимы в лечении злокачественных опухолей, при котором повышение содержания белков p53 дикого типа не приносит пользы.
Согласно некоторым вариантам осуществления пептид, по меньшей мере частично, восстанавливает активность мутантного белка p53 по меньшей мере до одной из активностей белка p53 WT.
Используемый в настоящем документе термин «уменьшение» относится к статистически значимому снижению определенного фенотипа по меньшей мере на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%75%, 80%, 95% или даже 100% по сравнению с контролем (например, той же клеточной/животной системой, обрабатываемой контрольной средой-носителем или вовсе не обрабатываемой) при тех же условиях анализа.
Используемый в настоящем документе термин «увеличение» или «улучшение» относится к статистически значимому повышению определенного фенотипа по меньшей мере на приблизительно 10%, 20%, 30%, 40%, 50%, 60%, 70%75%, 80%, 95% или даже 100% по сравнению с контролем (например, той же клеточной/животной системой, обрабатываемой контрольной средой-носителем или вовсе не обрабатываемой) при тех же условиях анализа.
Используемый в настоящем документе термин «клетки, экспрессирующие мутантный белок p53» относится к клеткам, которые экспрессируют мутантный белок p53 по меньшей мере по одному аллелю. Согласно некоторым вариантам осуществления термин «клетки, экспрессирующие мутантный белок p53» является взаимозаменяемым с термином «клетки злокачественной опухоли».
Термин «проапоптические гены» относится к гену или множеству генов, вовлеченных в апоптоз, либо непосредственно (например, определенные каспазы), либо опосредованно (например, как часть каскада передачи сигнала).
Согласно некоторым вариантам осуществления активность заключается в снижении жизнеспособности клеток, экспрессирующих мутантный белок p53. Согласно некоторым вариантам осуществления активность заключается в обеспечении апоптоза клеток, экспрессирующих мутантный белок p53. Согласно некоторым вариантам осуществления активность заключается в активации проапоптических генов клеток, экспрессирующих указанный мутантный белок p53. Согласно некоторым вариантам осуществления проапоптические гены выбраны из группы, состоящей из CD95, Bax, DR4, DR5, PUMA, NOXA, Bid, 53AIP1 и PERP. Каждый вариант представляет отдельный вариант осуществления настоящего изобретения.
Согласно некоторым вариантам осуществления активность заключается в связывании элемента связывания с консенсусной ДНК p53 в клетках, экспрессирующих мутантный белок p53. Согласно некоторым вариантам осуществления элемент связывания с консенсусной ДНК содержит нуклеотидные последовательности, изложенные в SEQ ID NO: 55 и 56, или состоит из таковых.
Способы мониторинга клеточных изменений, индуцированных любым из пептидов в соответствии с настоящим изобретением, известны в уровне техники и включают в себя, например, тест MTT, который основан на избирательной способности живых клеток восстанавливать желтую соль MTT (3-(4,5-диметилтиазолил-2)-2,5-дифенилтетразолия бромид) (Sigma, Aldrich St Louis, MO, USA) до багрово-синего нерастворимого осадка формазана; анализ с помощью BrDu (колориметрического набора Cell Proliferation ELISA BrdU (Roche, Mannheim, Germany)); анализ TUNEL (Roche, Mannheim, Germany); анализ с помощью Annexin V (ApoAlert® Annexin V Апоптоз Kit (Clontech Laboratories, Inc., CA, USA)); анализ ассоциированного с β-галактозидазой старения (Dimri GP, Lee X, et al. 1995. A biomarker that identifies senescent human cells in culture and in aging skin in vivo. Proc Natl Acad Sci U S A 92:9363-9367); а также различные способы выявления РНК и белка (выявляющие уровни экспрессии и/или активности), которые далее описываются в настоящем документе ниже.
Согласно некоторым вариантам осуществления связывание приводит к по меньшей мере частичной активации эндогенного целевого гена p53. Согласно некоторым вариантам осуществления эндогенный целевой ген выбран из группы, состоящей из p21, MDM2 и PUMA. Каждый вариант представляет отдельный вариант осуществления настоящего изобретения.
Согласно некоторым вариантам осуществления мутантный белок p53 характеризуется конформацией, отличной от таковой белка p53 WT. Согласно некоторым вариантам осуществления мутантный белок p53 является, по меньшей мере частично, неактивным по сравнению с белком p53 WT.
Согласно некоторым вариантам осуществления мутантный белок p53 не распознается моноклональным антителом против белка p53 WT. Согласно некоторым вариантам осуществления мутантный белок p53 при связывании с пептидом распознается моноклональным антителом против белка p53 WT. Согласно некоторым вариантам осуществления моноклональным антителом является Ab1620.
Согласно вариантам осуществления реактивирующий пептид может реактивировать Mut-p53 с наличием структурных свойств, биохимических свойств, физиологических свойств и/или функциональных свойств, подобных или идентичных таковым в белке p53 WT.
Согласно некоторым вариантам осуществления представлены реактивирующие пептиды Mut-p53, при этом пептиды имеют длину приблизительно 3-25 аминокислот. Согласно вариантам осуществления реактивирующие пептиды Mut-p53 имеют длину приблизительно 4-15 аминокислот. Согласно вариантам осуществления реактивирующие пептиды Mut-p53 имеют длину приблизительно 7-12 аминокислот. Согласно вариантам осуществления реактивирующие пептиды Mut-p53 имеют длину 7 аминокислот. Согласно вариантам осуществления реактивирующие пептиды Mut-p53 имеют длину 12 аминокислот. Каждый вариант представляет отдельный вариант осуществления настоящего изобретения.
По всей настоящей заявке упоминаются другие длины пептидов. Каждый вариант представляет отдельный вариант осуществления настоящего изобретения.
Согласно некоторым вариантам осуществления реактивирующий Mut-p53 пептид может поражать Mut-p53 таким образом, что он может трансактивировать репортерный ген (такой как, люциферазу), имеющий связывающий p53 WT элемент в своем промоторе. Согласно вариантам осуществления трансактивация репортерного гена может быть выполнена in vitro (например, в аналитической пробирке или лунке), или in vivo в клетке, содержащей конструкцию репортерного гена.
Согласно некоторым вариантам осуществления реактивирующий Mut-p53 пептид может связываться с доменом связывания с ДНК (DBD) в мутантном p53. Согласно вариантам осуществления мутантный p53 содержит мутацию в своем домене связывания с ДНК (DBD).
Используемый в настоящем документе термин «фармацевтическая композиция» относится к любой композиции, содержащий по меньшей мере один фармацевтически активный ингредиент.
Используемый в настоящем документе термин «ассоциированное с мутантным белком p53» относится к любому заболеванию, нарушению или состоянию, которое вызывается мутантным белком p53, или его прогрессирование связано с наличием мутантного белка p53 в клетке или органе.
Следует учитывать, что, поскольку p53 экспрессируется из обоих аллелей, суммарное содержание внутриклеточного p53 может быть представлено диким типом (wt/wt) или смесью wt и мутантного p53 (wt/mut), или только мутантным p53 (если оба аллеля являются мутантными (mut/mut), или удалением одного аллеля (mut/-)). При злокачественной опухоли ситуация зачастую представляет собой wt/mut, mut/mut или mut/-. Поскольку p53 действует как тетрамер, мутантные белки p53 могут отменять активность белков p53 дикого типа, которые могут существовать в клетках злокачественной опухоли. Поэтому, пептиды, обеспечиваемые в соответствии с настоящим изобретением, особенно применимы в лечении злокачественных опухолей. Следует отметить, что клетка может иметь больше двух аллелей p53, по меньшей мере один из которых является мутантным p53.
Используемый в настоящем документе термин «терапевтически эффективное количество» относится к количеству композиции, содержащей пептид в соответствии с настоящим изобретением, которое является достаточным для уменьшения, снижения и/или подавления заболевания, нарушения или состояния у индивидуума.
Согласно аспекту настоящего изобретения представлен способ лечения заболевания, нарушения или состояния, ассоциированных с мутантным белком p53, предусматривающий введение субъекту при необходимости этого терапевтически эффективного количества выделенного пептида, описываемого в настоящем документе (например, SEQ ID NO: 8, 412-464), с лечением тем самым указанного заболевания, нарушения или состояния.
Согласно аспекту настоящего изобретения представлен способ лечения заболевания, нарушения или состояния, ассоциированных с мутантным белком p53, предусматривающий введение субъекту при необходимости этого терапевтически эффективного количества выделенного пептида, содержащего аминокислотную последовательность, имеющую пространство и конфигурацию, которые обеспечивают связывание пептида с доменом связывания с ДНК (DBD) в p53 тем же образом, как и pCAP 250 (SEQ ID NO: 1) связывает указанный DBD, при этом указанный пептид по меньшей мере частично реактивирует мутантный белок p53, и при этом указанное терапевтически эффективное количество составляет 0,01-0,3 мг/кг в сутки или 0,01-0,2 мг/кг в сутки (например, 0,01-0,35 мг/кг в сутки, 0,01-0,35 мг/кг в сутки, 0,01-0,15 мг/кг в сутки, 0,01-0,1 мг/кг в сутки, 0,01-0,095 мг/кг в сутки, 0,01-0,09 мг/кг в сутки, 0,01-0,085 мг/кг в сутки, 0,01-0,08 мг/кг в сутки, 0,01-0,075 мг/кг в сутки, 0,01-0,07 мг/кг в сутки, 0,01-0,065 мг/кг в сутки, 0,01-0,06 мг/кг в сутки, 0,01-0,055 мг/кг в сутки, 0,01-0,05 мг/кг в сутки, 0,01-0.45 мг/кг в сутки, 0,01-0,04 мг/кг в сутки, 0,01-0,035 мг/кг в сутки, 0,01-0,03 мг/кг в сутки), с лечением тем самым указанного заболевания, нарушения или состояния.
Используемый в настоящем документе термин «лечение заболевания» или «лечение состояния» относится к введению композиции, которая включает в себя по меньшей мере одно средство, эффективное для облегчения симптомов, ассоциированных с заболеванием, уменьшения тяжести или излечения заболевания, или для предупреждения проявления заболевания у субъекта. Введение может включать в себя любой путь введения. Согласно вариантам осуществления заболеванием является заболевание, которое вызвано или связано с наличием мутантного p53 в клетке, ткани, органе, организме и т.п. Согласно вариантам осуществления заболеванием является злокачественная опухоль. Согласно вариантам осуществления злокачественная опухоль выбрана из группы, состоящей из злокачественной опухоли молочной железы, злокачественной опухоли толстой кишки, злокачественной опухоли яичника и злокачественной опухоли легкого.
Согласно вариантам осуществления злокачественная опухоль является метастатической злокачественной опухолью.
Согласно вариантам осуществления злокачественная опухоль является метастатической злокачественной опухолью молочной железы, метастатической злокачественной опухолью толстой кишки, метастатической злокачественной опухолью яичника или метастатической злокачественной опухолью легкого.
Каждый вариант представляет отдельный вариант осуществления настоящего изобретения. Согласно вариантам осуществления субъектом является млекопитающее, такое как человек. Согласно вариантам осуществления субъектом является млекопитающее животное. Согласно вариантам осуществления субъектом является отличное от млекопитающего животное. Согласно вариантам осуществления у субъекта диагностировали заболевание, состояние или нарушение.
Согласно вариантам осуществления злокачественной опухолью является адренокортикальная карцинома, анальная злокачественная опухоль, злокачественная опухоль мочевого пузыря, опухоль головного мозга, глиома ствола головного мозга, опухоль головного мозга, астроцитома мозжечка, эпендимома, медуллобластома, супратенториальная примитивная нейроэктодермальная опухоль, опухоли шишковидной железы, гипоталамическая глиома, злокачественная опухоль молочной железы, карциноидная опухоль, карцинома, злокачественная опухоль шейки матки, злокачественная опухоль толстой кишки, эндометриальная злокачественная опухоль, злокачественная опухоль пищевода, злокачественная опухоль внепеченочного желчного протока, опухоли семейства Юинга (pnet), экстракраниальная герминогенная опухоль, злокачественная опухоль глаза, интраокулярная меланома, злокачественная опухоль желчного пузыря, злокачественная опухоль желудка, герминогенная опухоль, внегонадная, гестационная трофобластическая опухоль, злокачественная опухоль головы и шеи, гипофаренгиальная злокачественная опухоль, карцинома островковых клеток, злокачественная опухоль гортани, лейкоз, острый лимфобластный лейкоз, злокачественная опухоль ротовой полости, злокачественная опухоль печени, злокачественная опухоль легкого, мелкоклеточная лимфома, связанная с AIDS лимфома, лимфома центральной нервной системы (первичная), кожная T-клеточная лимфома, болезнь Ходжкина, неходжкинское заболевание, злокачественная мезотелиома, меланома, карцинома из клеток Меркеля, метастатическая сквамозная карцинома, множественная миелома, злокачественные новообразования плазматических клеток, фунгоидный микоз, миелодиспластический синдром, миелопролиферативные нарушения, злокачественная опухоль носоглотки, нейробластома, злокачественная опухоль ротоглотки, остеосаркома, злокачественная опухоль эпителия яичника, герминогенная опухоль яичников, злокачественная опухоль яичника с низким потенциалом, злокачественная опухоль поджелудочной железы, экзокринная злокачественная опухоль поджелудочной железы, карцинома островковых клеток, злокачественная опухоль параназального синуса и носовой полости, злокачественная опухоль паращитовидной железы, злокачественная опухоль полового члена, феохромоцитомная злокачественная опухоль, злокачественная опухоль гипофиза, злокачественное новообразование плазматических клеток, злокачественная опухоль предстательной железы, рабдомиосаркома, злокачественная опухоль прямой кишки, почечноклеточная злокачественная опухоль, злокачественная опухоль слюнной железы, синдром Сезари, злокачественная опухоль кожи, кожная T-клеточная лимфома, злокачественная опухоль кожи, саркома Капоши, злокачественная опухоль кожи, меланома, злокачественная опухоль тонкого кишечника, саркома мягких тканей, злокачественная опухоль яичка, тимома, злокачественная опухоль щитовидной железы, уретральная злокачественная опухоль, злокачественная опухоль матки, саркома, редкая злокачественная опухоль детского возраста, злокачественная опухоль влагалища, злокачественная опухоль наружных женским половых органов или опухоль Вильмса.
Согласно вариантам осуществления злокачественной опухолью является злокачественная опухоль легкого.
Согласно вариантам осуществления злокачественной опухолью является злокачественная опухоль яичника.
Согласно вариантам осуществления злокачественной опухолью является трижды негативная злокачественная опухоль молочной железы.
Согласно вариантам осуществления злокачественной опухолью является метастатическая злокачественная опухоль легкого.
Согласно вариантам осуществления злокачественной опухолью является метастатическая злокачественная опухоль яичника.
Согласно вариантам осуществления злокачественной опухолью является метастатическая трижды негативная злокачественная опухоль молочной железы.
Согласно вариантам осуществления злокачественной опухолью является несолидная опухоль, такая как злокачественная опухоль крови. Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является лейкоз или лимфома. Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является острый лимфобластный лейкоз (ALL). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является острый миелогенный лейкоз (AML). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является хронический лимфоцитарный лейкоз (CLL). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является мелкоклеточная лимфоцитарная лимфома (SLL). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является хронический миелогенный лейкоз (CML). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является острый моноцитарный лейкоз (AMOL). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является лимфома Ходжкина (любая из четырех подтипов). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является неходжкинская лимфома (любая из подтипов). Согласно другому варианту осуществления несолидной опухолью или злокачественной опухолью крови является миелоидный лейкоз.
Для применения в способах в соответствии с настоящим изобретением реактивирующие пептиды могут быть составлены традиционным образом с использованием одного или нескольких фармацевтически приемлемых носителей, стабилизаторов или вспомогательных средств (сред-носителей) для образования фармацевтической композиции, известной в уровне техники, в частности, в отношении белковых активных средств. Носитель(и) является «приемлемым» в смысле совместимости с другими ингредиентами композиции и безвредности для его реципиента. Подходящие носители, как правило, включают в себя физиологический солевой раствор или этаноловые многоатомные спирты, такие как глицерин или пропиленгликоль.
Реактивирующие пептиды могут быть составлены в нейтральных или солевых формах. Фармацевтически приемлемые соли включают в себя соли присоединения кислоты (образованные со свободными аминогруппами) и образованные неорганическими кислотами, такими как хлористоводородная или фосфорная кислоты, или органическими кислотами, такими как уксусная, оксалиновая, виноградная и малеиновая. Соли, образованные со свободными карбоксильными группами, также могут быть получены из неорганических оснований, таких как гидроксиды натрия, калия, аммония, кальция или трехвалентного железа, и органических оснований, таких как изопропиламин, триметиламин, 2-этиламиноэтанол, гистидин и прокаин.
Композиции могут быть соответствующим образом составлены для внутривенного, внутримышечного, подкожного или внутриперитонеального введения и обычно содержат стерильные водные растворы реактивирующих пептидов, которые предпочтительно являются изотоническими с кровью реципиента. Такие составы, как правило, получают путем растворения твердого активного ингредиента в воде, содержащей физиологически совместимые вещества, такие как хлорид натрия, глицин и т.п., и имеющей буферный pH, совместимый с физиологическими условиями, для получения водного раствора и обеспечения стерильности указанного раствора. Они могут быть получены в контейнерах для одной или нескольких доз, например, запечатанные ампулы или флаконы.
Композиции могут включать в себя стабилизатор, такой как, например, полиэтиленгликоль, белки, сахариды (например, трегалозу), аминокислоты, неорганические кислоты и их смеси. Стабилизаторы используют в водных растворах при соответствующих концентрации и pH. pH водного раствора регулируют в диапазоне 5,0-9,0, предпочтительно в диапазоне 6-8. При составлении реактивирующих пептидов может быть использовано антиадсорбционное средство. Другие подходящие вспомогательные средства, как правило, могут включать в себя антиоксидант, такой как аскорбиновая кислота.
Композиции могут быть составлены в виде препаратов контролированного высвобождения, которое может быть достигнуто посредством применения полимера для образования комплекса или для абсорбирования белков. Соответствующие полимеры для составов контролированного высвобождения включают в себя, например, сложный полиэфир, полиаминокислоты, поливинил, пирролидон, этиленвинилацетат и метилцеллюлозу. Другим возможным способом контролированного высвобождения является включение реактивирующих пептидов в частицы из полимерного материала, такого как сложные полиэфиры, полиаминокислоты, гидрогели, поли(молочной кислоты) или этиленвинилацетатные coполимеры. В качестве альтернативы, вместо включения этих средств в полимерные частицы, можно захватывать такие материалы в микрокапсулы, полученные, например, с помощью методик коацервации или с помощью межфазной полимеризации, например, гидроксиметилцеллюлозные или желатиновые микрокапсулы и поли(метилметакрилатные) микрокапсулы, соответственно, или в коллоидные системы доставки лекарственного средства, например, липосомы, альбуминовые микросферы, микроэмульсии, каночастицы и нанокапсулы, или в макроэмульсии.
Согласно вариантам осуществления реактивирующие пептиды в соответствии с настоящим изобретением могут быть составлены в пероральные или оральные композиции и согласно вариантам осуществления включают в себя жидкие растворы, эмульсии, суспензии и т.п. Согласно вариантам осуществления фармацевтически приемлемые носители, подходящие для получения таких композиций, хорошо известны в уровне техники. Согласно вариантам осуществления жидкие оральные композиции содержат от приблизительно 0,001% до приблизительно 0,9% реактивирующих пептидов или согласно другому варианту осуществления от приблизительно 0,01% до приблизительно 10%.
Согласно вариантам осуществления композиции для применения в способах в соответствии с настоящим изобретением включают в себя растворы или эмульсии, которые согласно вариантам осуществления являются водными растворами или эмульсиями, содержащими безопасное и эффективное количество реактивирующего пептида и необязательно другие соединения, предназначенные для местного интраназального введения.
Согласно вариантам осуществления инъекционные растворы в соответствии с настоящим изобретением составляют в водных растворах. Согласно одному варианту осуществления инъекционные растворы в соответствии с настоящим изобретением составляют в физиологически совместимых буферах, таких как раствор Хэнка, раствор Рингера или физиологический солевой буфер. Согласно вариантам осуществления для чресслизистого введения в составе используют пенетранты, подходящие для проникновения через барьер. Такие пенетранты, как правило, известны в уровне техники.
Согласно одному варианту осуществления препараты, описываемые в настоящем документе, составляют для парентерального введения, например, с помощью болюсной инъекции или непрерывной инфузии. Согласно вариантам осуществления составы для инъекции представлены в единичной дозированной форме, например, в ампулах, или контейнерах с несколькими дозами, необязательно с добавлением консерванта. Согласно вариантам осуществления композиции представляют собой суспензии, растворы или эмульсии в масляных или водных средах-носителях и содержат вспомогательные вещества, такие как суспендирующие, стабилизирующие и/или диспергирующие средства.
Реактивирующие пептиды в соответствии с настоящим изобретением могут быть введены любым подходящим путем введения, выбранным из орального, местного, чрескожного или парентерального введения. Согласно некоторым вариантам осуществления путь введения включает в себя местное применение, выбранное из кожного, вагинального, ректального, ингаляционного, интраназального, глазного, ушного и буккального. Согласно некоторым вариантам осуществления путь введения включает в себя парентеральную инъекцию. Согласно различным вариантам осуществления стадию введения выполняют парентеральным путем, выбранным из группы, состоящей из внутривенного, внутримышечного, подкожного, внутрикожного, внутриперитонеального, внутриартериального, интрацеребрального, интрацеребровентрикулярного, внутрикостного и интратекального. Например, реактивирующие пептиды могут быть введены системно, например, парентеральными путями, такими как, внутриперитонеальный (i.p.), внутривенный (i.v.), подкожный или внутримышечный пути. Реактивирующие пептиды в соответствии с настоящим изобретением и/или любое необязательное дополнительное средство могут быть введены системно, например, путем интраназального введения. Реактивирующие пептиды в соответствии с настоящим изобретением и/или любое необязательное дополнительное средство могут быть введены системно, например, путем орального введения, с использованием определенных композиций или составов, способных обеспечивать для белков оральную биодоступность. Реактивирующие пептиды в соответствии с настоящим изобретением и/или любое необязательное дополнительное средство могут быть введены локально.
Согласно конкретному варианту осуществления введение включает в себя подкожное введение.
В качестве альтернативы или дополнения, согласно конкретному варианту осуществления введение включает в себя непрерывную инфузию.
Таким образом, реактивирующие пептиды (например, SEQ ID NO: 1, 8 или 412-464, или 429, 448, 449, 446, 462) также может быть доставлены с помощью систем доставки медленного высвобождения, насосов и других известных систем доставки для непрерывной инфузии, например, в следующих дозах, например, 0,01-0,3 мг/кг в сутки, 0,01-0,15 мг/кг в сутки, 0,01-0,1 мг/кг в сутки, 0,01-0,095 мг/кг в сутки, 0,01-0,09 мг/кг в сутки, 0,01-0,085 мг/кг в сутки, 0,01-0,08 мг/кг в сутки, 0,01-0,075 мг/кг в сутки, 0,01-0,07 мг/кг в сутки, 0,01-0,065 мг/кг в сутки, 0,01-0,06 мг/кг в сутки, 0,01-0,055 мг/кг в сутки, 0,01-0,05 мг/кг в сутки, 0,01-0.45 мг/кг в сутки, 0,01-0,04 мг/кг в сутки, 0,01-0,035 мг/кг в сутки, 0,01-0,03 мг/кг в сутки. Режимы введения дозы могут варьировать для обеспечения желаемых уровней циркулирующих в крови конкретных реактивирующих пептидов на основании их фармакокинетических показателей. Таким образом, дозы рассчитывают так, чтобы поддерживать желаемый уровень циркулирующего в крови терапевтического средства.
Как правило, эффективную дозу определяют по активности реактивирующих пептидов и по состоянию субъекта, а также по массе тала или площади поверхности подлежащего лечению субъекта. Размер дозы и режим введения дозы также определяют по наличию, природе и степени каких-либо нежелательных побочных эффектов, которые сопровождают введение реактивирующих пептидов конкретному субъекту.
Согласно вариантам осуществления представлен набор для лечения или предупреждения связанного с p53 состояния. Согласно вариантам осуществления набор содержит контейнер (такой как флакон), содержащий реактивирующий Mut-p53 пептид в подходящем буфере и инструкции по применению путем введения реактивирующего пептида.
Предполагают, что эффективность лечения пептидами в соответствии с настоящим изобретением может быть повышена при объединении с общепринятыми стандартными терапевтическими методами (например, с противораковой терапией). Таким образом, пептид может быть использован для лечения заболеваний или состояний, ассоциированных с p53 (описываемых в настоящем документе выше), отдельно или в комбинации с другим признанным или экспериментальным терапевтическим режимом для таких нарушений. Будет понятно, что лечение дополнительными терапевтическими способами или композициями обладает потенциалом существенного снижения эффективных клинических доз таких методов лечения со снижением тем самым зачастую изнуряющих негативных побочных эффектов и высокой стоимости лечения.
Терапевтический режим лечения злокачественной опухоли, подходящий для комбинации с пептидами согласно вариантам осуществления настоящего изобретения или полинуклеотидом, кодирующим их, включает в себя без ограничения химиотерапию, лучевую терапию, фототерапию и фотодинамическую терапию, хирургическое вмешательство, диетотерапию, аблативную терапию, объединенную лучевую терапию и химиотерапию, брахиотерапию, протонную терапию, иммунотерапию, клеточную терапию и протонную радиохирургическую терапию. Согласно конкретному варианту осуществления химиотерапия основывается на платине.
Противораковые лекарственные средства
Противораковые лекарственные средства, которые могут быть введены совместно с соединениями в соответствии с настоящим изобретением включают в себя без ограничения ацивицин; акларубицин; акодазол гидрохлорид; акронин; адриамицин; адозелезин; альдезлейкин, альтретамин; амбомицин; аметантрон ацетат; аминоглутетимид; амсакрин; анастрозол; антрамицин; аспарагиназу; асперлин; азацитидин; азетепа; азотомицин; батимастат; бензодепа; бикалутамид; бисантрен гидрохлорид; биснафид димезилат; бицелезин; блеомицин сульфат; брехинар натрий; бропиримин; бусульфан; кактиномицин; калустерон; карацемид; карбетимер; карбоплатин; кармустин; карубицин гидрохлорид; карцелезин; цедефингол; хлорамбуцил; циролемицин; цисплатин; кладрибин; криснатол мезилат; циклофосфамид; цитарабин; декарбазин; дактиномицин; даунорубицин гидрохлорид; децитабин; дексормаплатин; дезагуанин; дезагуанин мезилат; диазихон; доцетаксел; доксорубицин; доксорубицин гидрохлорид; дролоксифен; дролоксифен цитрат; дромостанолон пропионат; дуазомицин; эдатрексат; эфлорнитин гидрохлорид; эльзамитруцин; энлоплатин; энпромат; эпипропидин; эпирубицин гидрохлорид; эрбулозол; эзорубицин гидрохлорид; эстрамустин; эстрамустин фосфат натрий; этанидазол; этопозид; этопозид фосфат; этоприн; фадрозол гидрохлорид; фазарабин; фенретинид; флоксуридин; флударабин фосфат; флуороурацил; флуроцитабин; фосхидон; фостриецин натрий; гемцитабин; гемцитабин гидрохлорид; гидроксимочевину; идарубицин гидрохлорид; ифосфамид; илмофозин; альфа-2а интерферон; альфа-2b интерферон; альфа-n1 интерферон; альфа-n3 интерферон; бета-Ia интерферон; гамма-Ib интерферон; ипроплатин; иринотекан гидрохлорид; ланреотид ацетат; летрозол; лейпролид ацетат; лиарозол гидрохлорид; лометрексол натрий; ломустин; лозоксантрон гидрохлорид; мазопрокол; маитанзин; мехлоретамин гидрохлорид; мегестрол ацетат; меленгестрол ацетат; мелфалан; меногарил; меркаптопурин; метотрексат; метотрексат натрий; метоприн; метуредепа; митиндомид; митокарцин; митокромин; митогиллин; митомалцин; митомицин; митоспер; митотан; митоксантрон гидрохлорид; микофеноловую кислоту; нокодазол; ногаламицин; ормаплатин; оксизуран; паклитаксел; пегаспаргазу; пелиомицин; пентамустин; пепломицин сульфат; перфосфамид; пипоброман; пипосульфан; пироксантрон гидрохлорид; пликамицин; пломестан; порфимер натрий; порфиромицин; преднимустин; прокарбазин гидрохлорид; пуромицин; пуромицин гидрохлорид; пиразофурин; рибоприн; роглетимид; сафингол; сафингол гидрохлорид; семустин; симтразен; спарфозат натрий; спарзомицин; спирогерманий гидрохлорид; спиромустин; спироплатин; стрептонигрин; стрептозоцин; сулофенур; тализомицин; текогалан натрий; тегафур; телоксантрон гидрохлорид; темопорфин; тенипозид; тероксирон; тестолактон; тиамиприн; тиогуанин; тиотепа; тиазофурин; тирапазамин; топотекан гидрохлорид; торемифен цитрат; трестолон ацетат; трицирибин фосфат; триметрексат; триметрексат глюкуронат; трипторелин; тубулозол гидрохлорид; урацил мустард; уредепа; вапреотид; вертепорфин; винбластин сульфат; винкристин сульфат; виндезин; виндезин сульфат; винепидин сульфат; винглицинат сульфат; винлейрозин сульфат; винорельбин тартрат; винросидин сульфат; винзолидин сульфат; ворозол; цениплатин; циностатин; цорубицин гидрохлорид. Дополнительные противонеопластические средства включают в себя раскрытые в части 52 «Antineoplastic Agents» (Paul Calabresi and Bruce A. Chabner) и во введении к ней, 1202-1263, в Goodman and Gilman's "The Pharmacological Basis of Therapeutics", Eighth Edition, 1990, McGraw-Hill, Inc. (Health Professions Division).
Согласно другому аспекту настоящего изобретения представлен способ лечения заболевания, нарушения или состояния, ассоциированных с мутантным белком p53, предусматривающий введение субъекту при необходимости этого терапевтически эффективного количества химиотерапии на основе платины и выделенного пептида, содержащего аминокислотную последовательность, имеющую пространство и конфигурацию, которые обеспечивают связывание пептида с доменом связывания с ДНК (DBD) в p53 тем же образом, как и pCAP 250 (SEQ ID NO: 1) связывает указанный DBD (например, SEQ ID NO: 1, 8, 412-464, 429, 448, 449, 446, 462), при этом указанный пептид, по меньшей мере частично, реактивирует мутантный белок p53, с лечением тем самым указанного заболевания, нарушения или состояния.
Конкретные примеры химиотерапевтических средств на основе платины включают в себя без ограничения цисплатин, первый из разработанных, карбоплатин, противонеопластическое средство на основе платины второго поколения, оксалиплатин, сатраплатин, пикоплатин, недаплатин, триплатин, липоплатин, липосомальную версию цисплатина.
Также в настоящем документе предусматриваются наборы и изделия или изготовление для осуществления комбинированных методов лечения, описываемых в настоящем документе (например, пептид вместе с химиотерапией на основе платины).
Будет понятно, что пептид, содержащий аминокислотную последовательность, выбранную из группы, состоящей из 59-382, также может быть обеспечен в описанных выше способах.
Используемый в настоящем документе термин «приблизительно» относится к ± 10%.
Термины «содержит», «содержащий», «включает в себя», «включающий в себя», «имеющий» и их сочетания означают «включающий в себя без ограничения».
Термин «состоящий из» означает «включающий в себя и ограничивающийся таковым».
Термин «состоящий по сути из» означает, что композиция, способ или структура могут включать в себя дополнительные ингредиенты, стадии и/или части, но только если дополнительные ингредиенты, стадии и/или части не изменяют существенно основные и новые характеристики заявляемых композиции, способа или структуры.
Используемая в настоящем документе форма единственного числа предусматривает использование множественного числа, если в контексте четко не указано иное. Например, термин «соединение» или «по меньшей мере одно соединение» может включать в себя множество соединений, в том числе их смеси.
По всей настоящей заявке различные варианты осуществления настоящего изобретения могут быть представлены в формате диапазона. Следует учитывать, что описание в формате диапазона служит исключительно для удобства и краткости и не должно истолковываться как жесткое ограничение объема настоящего изобретения. Следовательно, описание диапазона следует рассматривать как конкретно раскрывающее все возможные поддиапазоны, а также отдельные числовые значения в этом диапазоне. Например, описание диапазона, такого как от 1 до 6, следует рассматривать как конкретно раскрытые поддиапазоны, такие как от 1 до 3, от 1 до 4, от 1 до 5, от 2 до 4, от 2 до 6, от 3 до 6 и т.д., а также отдельные числа в этом диапазоне, например, 1, 2, 3, 4, 5 и 6. Это применяется независимо от широты диапазона.
Всякий раз, когда в настоящем документе указывается числовой диапазон, предполагается включение любого указанного числа (дробного или целого) в указанном диапазоне. Фразы «диапазон/диапазон между» первым указанным числом и вторым указанным числом и «диапазон/диапазон от» первого указанного числа «до» второго указанного числа используются в настоящем документе взаимозаменяемо и означают включение первого и второго указанных чисел и всех дробных или целых чисел между ними.
Используемый в настоящем документе термин «способ» относится к путям, средствам, методикам и процедурам для выполнения данной задачи, в том числе без ограничения к таким путям, средствам, методикам и процедурам, которые либо известны, либо легко разрабатываются из известных путей, средств, методик и процедур специалистами, практикующими в химической, фармакологической, биологической, биохимической и медицинской областях.
Используемый в настоящем документе термин «лечение» включает в себя устранение, существенное подавление, замедление или обращение прогрессирования состояния, существенное облегчение клинических или эстетических симптомов состояния или существенное предупреждение проявления клинических или эстетических симптомов состояния.
При упоминании перечней конкретных последовательностей такую ссылку следует понимать как также охватывающую последовательности, которые, по сути, соответствуют комплементарной им последовательности, включающей в себя незначительные вариации последовательности, возникающие, например, из-за ошибок секвенирования, ошибок клонирования или других изменений, приводящих к замене основания, делеции основания или добавлению основания, при условии, что частота таких изменений составляет менее 1 в 50 нуклеотидах, в качестве альтернативы, менее 1 в 100 нуклеотидах, в качестве альтернативы, менее 1 в 200 нуклеотидах, в качестве альтернативы, менее 1 в 500 нуклеотидах, в качестве альтернативы, менее 1 в 1000 нуклеотидах, в качестве альтернативы, менее 1 в 5000 нуклеотидах, в качестве альтернативы, менее 1 в 10000 нуклеотидах.
Следует принимать во внимание, что некоторые признаки настоящего изобретения, которые для ясности описаны в контексте отдельных вариантов осуществления, также могут быть представлены в комбинации в одном варианте осуществления. И наоборот, разные признаки настоящего изобретения, которые для краткости описаны в контексте одного варианта осуществления, также могут быть предусмотрены отдельно или в любой подходящей подкомбинации или в любом другом описанном варианте осуществления настоящего изобретения. Некоторые признаки, описанные в контексте разных вариантов осуществления, не должны считаться существенными признаками этих вариантов осуществления, если только этот вариант осуществления не осуществляется без этих элементов.
Различные варианты осуществления и аспекты настоящего изобретения, описанные выше и заявленные в приведенном ниже разделе формулы изобретения, получают экспериментальную поддержку в следующих примерах.
Примеры
Далее делается ссылка на следующие примеры, которые вместе с приведенными выше описаниями иллюстрируют нестоящее изобретение неограничивающим образом.
Как правило, номенклатура, используемая в настоящем документе, и лабораторные процедуры, используемые в настоящем изобретении, включают в себя молекулярные, биохимические, микробиологические и методики рекомбинантной ДНК. Такие методики подробно разъясняются в литературе. См., например, "Molecular Cloning: A laboratory Manual" Sambrook et al., (1989); "Current Protocols in Molecular Biology" Volumes I-III Ausubel, R. M., ed. (1994); Ausubel et al., "Current Protocols in Molecular Biology", John Wiley and Sons, Baltimore, Maryland (1989); Perbal, "A Practical Guide to Molecular Cloning", John Wiley & Sons, New York (1988); Watson et al., "Recombinant DNA", Scientific American Books, New York; Birren et al. (eds) "Genome Analysis: A Laboratory Manual Series", Vols. 1-4, Cold Spring Harbor Laboratory Press, New York (1998); методы, изложенные в патентах США №№ 4666828, 4683202, 4801531, 5192659 и 5272057; "Cell Biology: A Laboratory Handbook", Volumes I-III Cellis, J. E., ed. (1994); "Current Protocols in Immunology" Volumes I-III Coligan J. E., ed. (1994); Stites et al. (eds), "Basic and Clinical Immunology" (8th Edition), Appleton & Lange, Norwalk, CT (1994); Mishell and Shiigi (eds), "Selected Methods in Cellular Immunology", W. H. Freeman and Co., New York (1980); общедоступные иммуноoанализы широко описываются в патентной и научной литературе, см., например, патенты США №№ 3791932, 3839153, 3850752, 3850578, 3853987, 3867517, 3879262, 3901654, 3935074, 3984533, 3996345, 4034074, 4098876, 4879219, 5011771 и 5281521; "Oligonucleotide Synthesis" Gait, M. J., ed. (1984); “Nucleic Acid Hybridization" Hames, B. D., and Higgins S. J., eds. (1985); "Transcription and Translation" Hames, B. D., and Higgins S. J., Eds. (1984); "Animal Cell Culture" Freshney, R. I., ed. (1986); "Immobilized Cells and Enzymes" IRL Press, (1986); "A Practical Guide to Molecular Cloning" Perbal, B., (1984) and "Methods in Enzymology" Vol. 1-317, Academic Press; "PCR Protocols: A Guide To Methods And Applications", Academic Press, San Diego, CA (1990); Marshak et al., "Strategies for Protein Purification and Characterization - A Laboratory Course Manual" CSHL Press (1996); все из которых включены посредством ссылки, как если бы полностью были изложены в настоящем документе. Другие общие ссылки представлены по всему настоящему документу. Предполагают, что процедуры в них хорошо известны в уровне техники и представлены для удобства читателя. Вся информация, содержащаяся в них, включена в настоящий документ посредством ссылки.
Экспериментальные процедуры
Анализ жизнеспособность с помощью кристаллического фиолетового
Клетки культивировали в 96-луночных планшетах с 2500-4000 клеток/лунка. Добавляли серийные разведения различных пептидов и планшеты инкубировали еще 48 часов при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм.
Анализ с помощью ChIP
Клетки сшивали с формальдегидом (1% конечная концентрация) при комнатной температуре в течение 10 минут. Формальдегид нейтрализовали глицином 0,25 M в течение 5 минут. Клетки дважды промывали 10 мл охлажденного до температуры льда PBS и собирали путем соскабливания. Затем клетки повторно суспендировали в 0,3 мл буфера для лизиса (1% SDS, 10 мM EDTA, 50 мM Tris-HCl, pH 8,1, смесь ингибиторов протеаз) и обрабатывали ультразвуком в течение 6 минут в ультразвуковой бане с последующим центрифугированием в течение 10 минут на льду с получением фрагментов 200-500 п.о. Супернатанты собирали и разбавляли в 10 раз в буфере для разбавления ChIP (1% Triton X-100, 2 мM EDTA, 150 мM NaCl, 20 мM Tris-HCl, pH 8,1) с последующей иммуноочисткой с помощью 40 мкл предварительно блокированной протеин А-сефарозы с 2 мкг ДНК спермы лосося, фрагментированной в результате гидродинамического сдвига, и 10 мкг BSA в течение 2 часов при 4°C. Выполняли иммуноосаждение на протяжении ночи при 4°C со специфическими поликлональными антителами против αp53 или αRNApolII. После иммуноосаждения добавляли 40 мкл протеин А-сефарозы и далее инкубировали еще 1 час. Осадки последовательно промывали в TSE I (0,1% SDS, 1% Triton X-100, 2 мM EDTA, 20 мM Tris-HCl, pH 8,1, 150 мM NaCl), TSE II (500 мM NaCl) и буфере III (0,25 M LiCl, 1% NP-40, 1% дезоксихолата, 1 мM EDTA, 10 мM Tris-HCl, pH 8,1). Осадки промывали три раза с помощью буфера TE и дважды экстрагировали с помощью 1% SDS, 0,1 M NaHCO3. Элюаты объединяли и нагревали при 65°C на протяжении ночи для обращения сшивания формальдегидом. Фрагменты ДНК очищали с помощью набора QIAquick Spin (Qiagen, CA). Выполняли реакции иммуноосаждения в трех повторностях. Гранулы использовали только в качестве неспецифического контроля. Количественный анализ активных и репрессивных гистоновых меток в продуктах ChIP из клонов выполняли с помощью количественной RT-PCR. Для нормализации эффективности иммуноосаждения (IP) выполняли нормализацию хроматина IP с использованием специфических праймеров для промоторной области necdin и 5’-области.
Нокаут CRISPR p53
Плазмиду № 42230, содержащую единичную направляющую РНК (sgRNA) экзона 3 TP53, получали от компании Addgene. Клетки ES2 трансфицировали с использованием реагента jetPEI (Polyplus) согласно протоколу изготовителя. Через 48 часов клетки высевали в 96-луночный планшет как клоны отдельной клетки. Наращивали клоны отдельной клетки и проверяли их статус в отношении p53 с помощью анализа вестерн-блоттинга с использованием антитела DO-1 против p53.
Последовательности sgRNA
F: 5’-CACCGCCATTGTTCAATATCGTCCG-3’ (SEQ ID NO: 47),
R: 5’-AACCGGACGATATTGAACAATGG-3’ (SEQ ID NO: 48).
Доклиническое тестирование пептидов
Мышам (голым мышам Athymic возрастом 6 недель) вводили инъекцией подкожно 2 × 105–106 клеток в каждое бедро. Все клеточные линии, используемые в данных экспериментах, стабильно экспрессировали репортерный ген люциферазы для обеспечения мониторинга роста опухоли с помощью прямой визуализации. Через 4-18 суток, когда опухоли достигали видимого размера, мышей рандомно делили на несколько групп: контрольная группа, обрабатываемая каким-либо одним контрольным пептидом, и группы, обрабатываемые эффективным пептидом, каким-либо одним пептидом. Пептиды вводили либо инъекцией внутрь опухоли 10 мкг пептида на опухоль в 40 мкл PBS три раза в неделю, либо с помощью мининасосов Alzet 0,8 мг в течение двух недель. Рост опухоли со временем измеряли с помощью прямой визуализации с использованием системы IVIS2000. Время экспозиции калибровали до 20 секунд. Получали 16 изображений за 8 минут и регистрировали пиковые значения люминесценции для каждой опухоли. Эксперименты проводили до достижения опухолями максимально допустимого размера 1 см3, при этом мышей умерщвляли, а опухоли извлекали, измеряли и взвешивали.
RT-PCR
РНК получали с использованием набора Macherey-Nagel NucleoSpin RNA II на клеточном осадке согласно протоколу изготовителя. Аликвоты 0,4-1 мкг обратно транскрибировали с использованием Bio-RT 2000 (Bio-Lab) и рандомных гексамерных праймеров. QRT-PCR выполняли на аппарате ABI 7300 (Applied Biosystems) с использованием SYBR Green FastMix ROX (Quanta). Праймерами RT-PCR являются следующие (все праймерные последовательности представлены от 5’ до 3’).
Перечень праймеров
ЯМР
Очищенный меченный 15N коровый домен p53, 1 мл 40 мкM (aa 94-296), диализировали против 1 л буфера для ЯМР (157,5 мM натрий-фосфатного буфера, содержащего 52,5 мM NaCl и 2,625 мM DTT, pH 7,2) в течение 48 часов, буфер заменяли и образец диализировали против 1 л буфера для ЯМР еще 24-48 часов (всего 72 часа). 0,5 мл образца подвергали ЯМР высокого разрешения. Анализ ЯМР выполняли в научном институте Weizmann.
Двухмерные спектры 1H-15N Heteronuclear Single Quantum Coherence (HSQC) 15N-p53 самого по себе и при образовании комплекса с указанными пептидами регистрировали при 293 K. Спектры получали на ЯМР-спектрометре Bruker AVIII-800, оснащенном 5-мм датчиком тройного резонанса с инверсным детектированием CryoProbe (TCI). Подавления сигнала растворителя достигали с использованием последовательности WATERGATE.
Пример 1
pCAP-250 синергезирует с цисплатином в отношении снижения жизнеспособности клеток злокачественной опухоли яичника ES2
Клетки ES2 культивировали в 96-луночных планшетах с 3000 клеток/лунка. Добавляли серийные разведения pCAP-250 либо отдельно, либо вместе с 1 мкг/мл цисплатина и планшеты инкубировали еще 48 часов при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм. Жизнеспособность клеток ES2, обработанных с помощью 1 мкг/мл, составляла 39%. IC50 для pCAP-250 оценивали при 3,2 мкM и в комбинации с цисплатином IC50 для pCAP-250 оценивали при 1,9 мкM, что указывает на синергетический эффект между двумя соединениями.
На фиг. 1 представлены результаты эксперимента. Затем жизнеспособность клеток злокачественной опухоли существенно снижалась в присутствии pCAP 250. Синергизм обеспечивается комбинированным лечением pCAP 250 с химиотерапией на основе платины.
Пример 2
Характеристика активности pCAP-250 и различных производных
Клетки ES2 Con, экспрессирующие эндогенный mp53S241F, и клетки ES2 KO, в которых p53 был стабильно нокаутирован с использованием CRISPR/Cas9 (ES2 p53KO) для контроля на предмет специфичности по отношению к mutp53, культивировали в 96-луночных планшетах с 3000 клеток/лунка. Указанные пептиды добавляли при концентрации 8 мкг/мл и планшеты инкубировали еще 48 часов при 37°C. Затем среду удаляли и определяли жизнеспособность клеток с помощью окрашивания клеток кристаллическим фиолетовым (0,05%) в метаноле/PBS (1:5, объем/объем), в течение 10 минут, с последующими 3 промываниями с помощью PBS. Добавляли 10% уксусную кислоту в каждую лунку в течение 10 минут. OD определяли при 595 нм.
На фиг. 2 показано различие в эффекте конкретного пептида по отношению к ES2 Con по сравнению с ES KO, что указывает на специфичность пептида по отношению к экспрессии mutp53. Некоторые пептидные производные, в которых аминокислоты, которые были заменены аланином (серин и гистидин, например), демонстрировали сниженный эффект по отношению к клеткам ES2 Con, что указывает на важное значение этих аминокислот для эффективности пептида.
Результаты далее дополняли анализом аффинности связывания, описанным ниже.
Пример 3
Связывание pCAP 250 с DBD p53
На фиг. 3A-K представлен анализ микромасштабного термофореза на предмет связывания флуоресцентно меченого WTp53DBD и pCAP-250. Эксперимент выполняли согласно инструкциям изготовителя; получали 10 серийных разведений pCAP-250, добавляли меченый белок к каждому пептидному образцу и загружали на капилляры. Образцы анализировали на предмет передвижения флуоресцентного wtp53DBD в температурном градиенте с различными концентрациями pCAP-250. Результаты анализа микромасштабного термофореза представлены в виде кривой, полученной с помощью программного обеспечения изготовителя для анализа данных.
Пример 4
Фармакокинетическое исследование – способ введения pCAP 250 и время полужизни в плазме
Результаты на фиг. 4A-D показывают, что время полужизни в плазме pCAP 250 (SEQ ID NO: 1) составляет 0,8-1,8 часа при внутривенном введении. Кроме того, результаты показывают, что время полужизни в плазме pCAP 250 (SEQ ID NO: 1) составляет 3-8 часов при подкожном введении.
Пример 5
In vivo эффект пептида pCAP-250 на мышиной модели ксенотрансплантата
На фиг. 5A-D показано, что pCAP 250 (SEQ ID NO: 1) при введении инъекциями внутрь опухоли при дозе 0,4 мг/кг 3 раза в неделю оказывает существенный эффект по отношению к развитию опухоли клетками ES2 на модели ксенотрансплантата злокачественной опухоли яичника. Кроме того, показано, что pCAP 250 при подкожном введении с помощью мининасосов Alzet при дозе 2,3 мг/кг в сутки оказывает существенный эффект по отношению к развитию опухоли клетками ES2 на модели ксенотрансплантата злокачественной опухоли яичника.
Пример 6
Противораковая активность вариантов пептида pCAP 250, определяемая с помощью in vitro анализа жизнеспособности клеток
Таблица 3
Таблица 3. Перечень 53 вариантов пептида pCAP-250. myr означает миристоильную группу, буквы в верхнем и нижнем регистре означают аминокислоты L-типа и D-типа, соответственно. L-DAB означает диаминомасляную кислоту L-типа. PSER и pser означают фосфосерин L-типа и D-типа, соответственно. AIB означает аминоизомасляную кислоту.
Пептиды тестировали в противораковых анализах на двух клеточных линиях. Как можно видеть на фиг. 7-8, указанные пептиды обладают противораковой активностью, определяемой по жизнеспособности клеток (анализ жизнеспособности с помощью кристаллического фиолетового).
Пример 7
ЯМР эксперименты с комплексом pCAP-250-DBD и вариантами его пептида
Выполняли ЯМР-эксперименты (спектры 1H–15N HSQC) для оценивания структурных эффектов, которые индуцировали путем связывания пептида pCAP-250 (PCAP 250) с DBD p53. Поскольку оценку пиков остатков ранее получали для DBD WT (94-312 из SEQ ID NO: 44) (Wong et al., выше), ЯМР-эксперименты проводили с использованием DBD WT (94-296, SEQ ID NO: 44), придерживаясь тех же условий, что описаны у Wong et al (выше).
На фиг. 9 представлена оценка ЯМР пиков, полученная Wong et al. (выше), вместе с картой ЯМР пиков, полученной для свободного DBD и для комплекса DBD-pCAP 250. На фиг. 9 можно видеть, что, в целом, карту Wong et al. (supra) успешно воспроизвели, несмотря на различия в длинах C-концов конструкций DBD, 296 против 312. Наблюдаются многочисленные пиковые изменения в ряде интенсивностей между картами свободного DBD и DBD-pCAP 250, в том числе исчезновение и появление нескольких не определенных пиков, что, таким образом, указывает на связывание pCAP 250 с DBD WT. Картирование этих изменений в структуре DBD обеспечивает четкую картину относительно трехмерной структурной области, на которую влияет связывание pCAP 250. Эта область в основном включает в себя Helix-2 и петлю L1 мотивов области контакта DBD-ДНК, и она далее расширяется в центральную область белка (см. пурпурный цвет на фиг. 10). C277 и R280 являются примерами умеренных пиковых движений остатков, расположенных на Helix-2, где наблюдается наиболее резкое пиковое движение для G117, расположенного на петле L1 (см. пурпурные и коричневые кружочки на фиг. 9).
Интересно, что пики относительно низкой интенсивности, изначально наблюдаемые Wong et al. (выше) для H115 и Y126, не наблюдаются для свободного DBD, но появляются при добавлении пептида pCAP 250 (см. желтые кружочки на фиг. 10). Такое существенное различие в определяемых пиках можно рассматривать как наиболее доминирующие пиковые изменения, индуцированные pCAP 250. Низкая интенсивность исходных пиков и отсутствие пиков из спектров свободных DBD указывают на то, что эти остатки расположены в структурной области низкой стабильности белка, которая может принимать более чем одну доминирующую стабильную конформацию и, таким образом, очень чувствительна к небольшим изменениям состояний белка. Действительно, резкая структурная реорганизация показана для H115 и Y126 при сравнении двух верхних низкоэнергетических конформаций структуры DBD, расшифрованные с помощью ЯМР (pdb код 2FEJ). Примечательно, что трехмерная организация H115 и Y126 находится в непосредственной близости от G117 и может непосредственно влиять на нее, и вместе эти три остатка в высокой степени связаны со структурной целостностью петли L1 (см. фиг. 11A-B). Появление пиков H115 и Y126 при добавлении пептида далее подтверждали дополнительным ЯМР-экспериментом с использованием другого варианта пептида pCAP 250 pCAP-615 (RRHSTP{DAB}PD), SEQ ID NO: 465 (см. фиг. 12).
Обнаружили, что вариант пептида pCAP 250 pCAP-553 (myr-RRHSvP(L-DAB)PD, где v обозначает валин D-типа, SEQ ID NO: 429) был в два раза сильнее, чем P-250 в анализе с клетками SW-480, содержащими мутантный p53R273H (см. фиг. 7). ЯМР-анализ указывает на то, что pCAP-553 (P553) имеет тенденцию связывать DBD с улучшенной аффинностью. Это в первую очередь отражается в появлении семи разных новых и очень сильных не определенных пиков на карте пиков ЯМР, созданной для комплекса DBD-pCAP 553, по сравнению со свободным DBD. Кроме того, формы пиков, полученных для комплекса DBD-pCAP 553, как правило, являются более унифицированными и повторяющимися, что указывает на то, что связывание пептида P553 улучшает структурную стабильность DBD (см. фиг. 13).
Результаты ЯМР-эксперимента свидетельствуют о явном связывании pCAP 250 и его вариантов пептидов с DBD WT в белке p53. Эти результаты подтверждают выводы о связывании pCAP 250 с DBD с использованием метода MST (фиг. 3A-K). Результаты ЯМР также указывают на то, что связывание pCAP 250 и его пептидных вариантов индуцирует структурные изменения в DBD, которые непосредственно влияют на целостность и стабильность области связывания DBD-ДНК, а именно структурных мотивов Helix-2 и L1, которые необходимы для способности DBD связывать ДНК. Связывание pCAP 250 и его пептидных вариантов, кроме того, влияет на дополнительные остатки в окружении структурных мотивов Helix-2 и петли L1, что создает относительно большой, но явно пораженный участок на поверхности DBD.
Хотя настоящее изобретение описано в сочетании с конкретными вариантами его осуществления, очевидно, что многие альтернативы, модификации и вариации будут понятны специалистам в данной области. Следовательно, оно предусматривает все такие альтернативы, модификации и вариации, которые охватываются идеей и широким объемом прилагаемой формулы изобретения.
Все публикации, патенты и заявки на выдачу патента, упомянутые в настоящем раскрытии, включены в настоящее раскрытие во всей своей полноте, в той же степени, как если бы каждые отдельные публикация, патент и заявка на выдачу патента были специально и индивидуально включены в настоящий документ посредством ссылки. Кроме того, цитирование или идентификация любой ссылки в настоящей заявке не должны толковаться как признание того, что такая ссылка предлагается в виде предшествующего уровня техники для настоящего изобретения. В той степени, в которой используются заголовки разделов, их не следует понимать как обязательно ограничивающие.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ИЕДА РИСЕЧ ЭНД ДЕВЕЛОПМЕНТ КО. ЛТД.
РОТТЕР, Варда
ОРЕН, Моше
ТАЛ, Перри
АЙЗЕНБЕРГЕР, Шей
БЕН-ШИМОН, Ави
<120> ПЕПТИДЫ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ,
НАРУШЕНИЙ ИЛИ СОСТОЯНИЙ, АССОЦИИРОВАННЫХ С МУТАНТНЫМ P53
<130> 68699
<150> US 62/291,003
<151> 2016-02-04
<160> 465
<170> PatentIn version 3.5
<210> 1
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristlyated
<400> 1
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 2
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristlyated
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> Amidated c terminus
<400> 2
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 3
<211> 7
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 3
His Ser Thr Pro His Pro Asp
1 5
<210> 4
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristlyated
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> DOTA conjugate
<400> 4
Arg Arg His Ser Thr Pro His Pro Asp Lys
1 5 10
<210> 5
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 5
Arg Arg Ala Ser Thr Pro His Pro Asp
1 5
<210> 6
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 6
Arg Arg His Ala Thr Pro His Pro Asp
1 5
<210> 7
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 7
Arg Arg His Ser Ala Pro His Pro Asp
1 5
<210> 8
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 8
Arg Arg His Ser Thr Ala His Pro Asp
1 5
<210> 9
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 9
Arg Arg His Ser Thr Pro Ala Pro Asp
1 5
<210> 10
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 10
Arg Arg His Ser Thr Pro His Ala Asp
1 5
<210> 11
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 11
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 12
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 12
Arg Arg His Ser Thr Pro His Pro Ala
1 5
<210> 13
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 13
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 14
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 14
Arg Arg His Ser Thr Pro His Pro Asp Cys
1 5 10
<210> 15
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 15
Arg Arg His Ser Thr Pro His Pro Asp Tyr
1 5 10
<210> 16
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 16
Arg Arg His Ser Thr Pro His Pro Asp Lys
1 5 10
<210> 17
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristoylation
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> Acetylated C terminus
<400> 17
Arg Arg His Ser Thr Pro His Pro Asp Lys
1 5 10
<210> 18
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 18
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 19
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristoylation
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> Biotin conjugate
<400> 19
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 20
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 20
cccaagcaat ggatgatttg a 21
<210> 21
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 21
ggcagaccag catgacagat t 21
<210> 22
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 22
gacctcaacg cacagtacga g 21
<210> 23
<211> 22
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 23
aggcaaatgt gcaataccaa ca 22
<210> 24
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 24
actgtgaccc ttgcaccaaa t 21
<210> 25
<211> 24
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 25
aggcactcac agagcactac aaac 24
<210> 26
<211> 20
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 26
acccactcct ccacctttga 20
<210> 27
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 27
gtggctctga ttggctttct g 21
<210> 28
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 28
gcgagactgt ggccttgtgt c 21
<210> 29
<211> 23
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 29
ggttgactca gcttttcctc ttg 23
<210> 30
<211> 22
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 30
ggataattag acgtacgtgg gc 22
<210> 31
<211> 20
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 31
gtattccccc aggtttacat 20
<210> 32
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 32
ggcattctgg gagcttcatc t 21
<210> 33
<211> 20
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 33
gcggattagg gcttcctctt 20
<210> 34
<211> 22
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 34
aggagtccca tgatgagatt gt 22
<210> 35
<211> 26
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 35
ggttacagca ccatcagtag gtacag 26
<210> 36
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 36
gccaccccaa gttagatctg g 21
<210> 37
<211> 18
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 37
gcccttggac ggcttttc 18
<210> 38
<211> 22
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 38
ctgttgctgt agccaaattc gt 22
<210> 39
<211> 20
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 39
cttgggctgc ctgttttcag 20
<210> 40
<211> 20
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 40
actttgtgga ccctggaacg 20
<210> 41
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 41
tatttaaacc atgcattttc c 21
<210> 42
<211> 23
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 42
ggacaattga caaaatcagt atc 23
<210> 43
<211> 21
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 43
aggagtgagt ggaagacaga a 21
<210> 44
<211> 393
<212> PRT
<213> homo sapiens
<400> 44
Met Glu Glu Pro Gln Ser Asp Pro Ser Val Glu Pro Pro Leu Ser Gln
1 5 10 15
Glu Thr Phe Ser Asp Leu Trp Lys Leu Leu Pro Glu Asn Asn Val Leu
20 25 30
Ser Pro Leu Pro Ser Gln Ala Met Asp Asp Leu Met Leu Ser Pro Asp
35 40 45
Asp Ile Glu Gln Trp Phe Thr Glu Asp Pro Gly Pro Asp Glu Ala Pro
50 55 60
Arg Met Pro Glu Ala Ala Pro Arg Val Ala Pro Ala Pro Ala Ala Pro
65 70 75 80
Thr Pro Ala Ala Pro Ala Pro Ala Pro Ser Trp Pro Leu Ser Ser Ser
85 90 95
Val Pro Ser Gln Lys Thr Tyr Gln Gly Ser Tyr Gly Phe Arg Leu Gly
100 105 110
Phe Leu His Ser Gly Thr Ala Lys Ser Val Thr Cys Thr Tyr Ser Pro
115 120 125
Ala Leu Asn Lys Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln
130 135 140
Leu Trp Val Asp Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met
145 150 155 160
Ala Ile Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys
165 170 175
Pro His His Glu Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln
180 185 190
His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp
195 200 205
Arg Asn Thr Phe Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu
210 215 220
Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser
225 230 235 240
Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr
245 250 255
Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val
260 265 270
His Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn
275 280 285
Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr
290 295 300
Lys Arg Ala Leu Ser Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys
305 310 315 320
Lys Pro Leu Asp Gly Glu Tyr Phe Thr Leu Gln Ile Arg Gly Arg Glu
325 330 335
Arg Phe Glu Met Phe Arg Glu Leu Asn Glu Ala Leu Glu Leu Lys Asp
340 345 350
Ala Gln Ala Gly Lys Glu Pro Gly Gly Ser Arg Ala His Ser Ser His
355 360 365
Leu Lys Ser Lys Lys Gly Gln Ser Thr Ser Arg His Lys Lys Leu Met
370 375 380
Phe Lys Thr Glu Gly Pro Asp Ser Asp
385 390
<210> 45
<211> 199
<212> PRT
<213> homo sapiens
<400> 45
Ser Ser Ser Val Pro Ser Gln Lys Thr Tyr Gln Gly Ser Tyr Gly Phe
1 5 10 15
Arg Leu Gly Phe Leu His Ser Gly Thr Ala Lys Ser Val Thr Cys Thr
20 25 30
Tyr Ser Pro Ala Leu Asn Lys Met Phe Cys Gln Leu Ala Lys Thr Cys
35 40 45
Pro Val Gln Leu Trp Val Asp Ser Thr Pro Pro Pro Gly Thr Arg Val
50 55 60
Arg Ala Met Ala Ile Tyr Lys Gln Ser Gln His Met Thr Glu Val Val
65 70 75 80
Arg Arg Cys Pro His His Glu Arg Cys Ser Asp Ser Asp Gly Leu Ala
85 90 95
Pro Pro Gln His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr
100 105 110
Leu Asp Asp Arg Asn Thr Phe Arg His Ser Val Val Val Pro Tyr Glu
115 120 125
Pro Pro Glu Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met
130 135 140
Cys Asn Ser Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr
145 150 155 160
Ile Ile Thr Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser
165 170 175
Phe Glu Val His Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu
180 185 190
Glu Glu Asn Leu Arg Lys Lys
195
<210> 46
<211> 6
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 46
His Ser Ala Pro His Pro
1 5
<210> 47
<211> 18
<212> RNA
<213> Artificial sequence
<220>
<223> single guide RNA (sgRNA)
<400> 47
caccgccagc aaacgccg 18
<210> 48
<211> 19
<212> RNA
<213> Artificial sequence
<220>
<223> single guide RNA (sgRNA)
<400> 48
aaccggacga agaacaagg 19
<210> 49
<211> 6
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 49
His Ser Ala Pro His Pro
1 5
<210> 50
<211> 6
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<400> 50
His Ser Glu Pro His Pro
1 5
<210> 51
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristoylation
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> BSA conjugate
<400> 51
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 52
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristoylation
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> KLH conjugate
<400> 52
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 53
<211> 6
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> selected from the group consisting of positively charged amino
acid
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> selected from the group consisting of Ser, Thr, Asn, Gln, Pro,
Ala and Gly
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> any amino acid
<220>
<221> MISC_FEATURE
<222> (4)..(4)
<223> selected from the group consisting of an alpha methyl amino and a
beta-breaker amino acid
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> selected from the group consisting of positively charged amino
acid
<220>
<221> MISC_FEATURE
<222> (6)..(6)
<223> selected from the group consisting of an alpha methyl amino and a
beta-breaker amino acid
<400> 53
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 54
<211> 6
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> selected from the group consisting of His, Arg and Lys
<220>
<221> MISC_FEATURE
<222> (2)..(2)
<223> selected from the group consisting of Ser, Thr, Asn, Gln, Pro,
Ala and Gly
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> X is any amino acid
<220>
<221> misc_feature
<222> (4)..(4)
<223> Xaa can be any amino acid
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> selected from the group consisting of His, Arg and Lys
<220>
<221> misc_feature
<222> (6)..(6)
<223> Xaa can be any amino acid
<400> 54
Xaa Xaa Xaa Xaa Xaa Xaa
1 5
<210> 55
<211> 47
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 55
catgcccaga catgtccttg ctgctgcgaa catgtcccaa catgttg 47
<210> 56
<211> 47
<212> DNA
<213> Artificial sequence
<220>
<223> Single strand DNA oligonucleotide
<400> 56
caacatgttg ggacatgttc gcagcagcaa ggacatgtct gggcatg 47
<210> 57
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristoylation
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> folate conjugate
<400> 57
Arg Arg His Ser Thr Pro His Pro Asp Lys
1 5 10
<210> 58
<211> 15
<212> PRT
<213> Artificial sequence
<220>
<223> synthetic peptide
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristoylation
<400> 58
Arg Arg His Ser Thr Pro His Pro Asp His Ala Tyr Pro His Ala
1 5 10 15
<210> 59
<211> 21
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (12)..(21)
<223> X= Arg or absent
<400> 59
Ile Arg Ile Leu Met Phe Leu Ile Gly Cys Gly Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa
20
<210> 60
<211> 28
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (19)..(28)
<223> X=Arg or absent
<400> 60
Leu Arg Cys Leu Leu Leu Leu Ile Gly Arg Val Gly Arg Lys Lys Arg
1 5 10 15
Arg Gln Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
20 25
<210> 61
<211> 17
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (8)..(17)
<223> X=Arg or absent
<400> 61
Tyr Pro Thr Gln Gly His Leu Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa
<210> 62
<211> 22
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (13)..(22)
<223> X=Arg or absent
<400> 62
Ser Trp Gln Ala Leu Ala Leu Tyr Ala Ala Gly Trp Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 63
<211> 20
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (11)..(20)
<223> X=Arg or absent
<400> 63
Thr Leu Tyr Leu Pro His Trp His Arg His Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa
20
<210> 64
<211> 16
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (7)..(16)
<223> X=Arg or absent
<400> 64
Ile Arg Gly Arg Ile Ile Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
<210> 65
<211> 22
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (13)..(22)
<223> X=Arg or absent
<400> 65
Ser Phe Ile Leu Phe Ile Arg Arg Gly Arg Leu Gly Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 66
<211> 22
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (13)..(22)
<223> X=Arg or absent
<400> 66
His Ser Ser His His His Pro Val His Ser Trp Asn Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa
20
<210> 67
<211> 17
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (8)..(17)
<223> X=Arg or absent
<400> 67
His Ala Asn Leu His His Thr Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa
<210> 68
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (11)..(20)
<223> X=Arg or absent
<400> 68
Trp Asn His His His Ser Thr Pro His Pro Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa
20
<210> 69
<211> 16
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (7)..(16)
<223> X=Arg or absent
<400> 69
His Ser Thr Pro His Pro Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
<210> 70
<211> 14
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (5)..(14)
<223> X=Arg or absent
<400> 70
Ser Ile Leu Thr Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10
<210> 71
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (11)..(20)
<223> X=Arg or absent
<400> 71
Tyr Arg Arg Leu Leu Ile Gly Met Met Trp Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa
20
<210> 72
<211> 20
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (11)..(20)
<223> X=Arg or absent
<400> 72
Tyr Arg Arg Leu Leu Ile Gly Met Met Trp Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa
20
<210> 73
<211> 17
<212> PRT
<213> Artificial
<220>
<223> Peptide
<220>
<221> MISC_FEATURE
<222> (8)..(17)
<223> X=Arg or absent
<400> 73
Phe Pro Gly His Thr Ile His Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
1 5 10 15
Xaa
<210> 74
<211> 22
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MISC_FEATURE
<222> (1)..(10)
<223> X=Arg or absent
<220>
<221> MISC_FEATURE
<222> (1)..(22)
<223> D-amino_acid_peptide
<400> 74
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Gly Leu Arg Gly Arg Arg
1 5 10 15
Ile Phe Leu Ile Phe Ser
20
<210> 75
<211> 12
<212> PRT
<213> Artificial
<220>
<223> Peptide
<400> 75
Leu Thr Phe Glu His Tyr Trp Ala Gln Leu Thr Ser
1 5 10
<210> 76
<211> 12
<212> PRT
<213> Artificial
<220>
<223> Peptide
<400> 76
Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly Gly
1 5 10
<210> 77
<211> 12
<212> PRT
<213> Artificial
<220>
<223> Peptide
<400> 77
Asn Pro Asn Thr Tyr Val Pro His Trp Met Arg Gln
1 5 10
<210> 78
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 78
Tyr Arg Arg Leu Leu Ile Gly Met Met Trp
1 5 10
<210> 79
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 79
Asp Glu Phe His Ser Phe Tyr Thr Ala Arg Gln Thr Gly
1 5 10
<210> 80
<211> 7
<212> PRT
<213> Artificial
<220>
<223> Peptide
<400> 80
Lys Pro Asp Ser Pro Arg Val
1 5
<210> 81
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 81
Pro Pro Tyr Ser Gln Phe Leu Gln Trp Tyr Leu Ser
1 5 10
<210> 82
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 82
Ser Glu Phe Pro Arg Ser Trp Asp Met Glu Thr Asn
1 5 10
<210> 83
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 83
His Asp Thr His Asn Ala His Val Gly
1 5
<210> 84
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 84
Trp Ser Glu Tyr Asp Ile Pro Thr Pro Gln Ile Pro Pro
1 5 10
<210> 85
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 85
Ser Ile Leu Thr Leu Ser Arg Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
<210> 86
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 86
Ser Cys Arg Cys Arg Leu Arg Gly Asp Arg Gly Asp Arg
1 5 10
<210> 87
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 87
Gly Gly Gly Gly Gly Gly Gly Gly Gly Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
<210> 88
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 88
Ser Glu Tyr Leu Cys Ser Ser Leu Asp Ala Ala Gly
1 5 10
<210> 89
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 89
Gly Glu Ser Phe Val Gln His Val Phe Arg Gln Asn
1 5 10
<210> 90
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 90
Ser Val His His His His Arg Met His Leu Val Ala
1 5 10
<210> 91
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 91
Gly Arg Arg Arg Phe Cys Met
1 5
<210> 92
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 92
Lys Leu Thr Ile His His His
1 5
<210> 93
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 93
Phe Gly Ser His His Glu Leu
1 5
<210> 94
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 94
Gly Thr Val Asp His His Ala
1 5
<210> 95
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 95
Asp Arg Leu Ser Val Phe Leu Phe Ile Met
1 5 10
<210> 96
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 96
Ala Ile Ser His His Thr Arg
1 5
<210> 97
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 97
Lys His His Pro Phe Asp His Arg Leu Gly Asn Gln
1 5 10
<210> 98
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 98
His Ser Ala His His Thr Met
1 5
<210> 99
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 99
Glu Leu Gly Leu His Arg His
1 5
<210> 100
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 100
Arg Arg Leu Arg Ile Cys Val
1 5
<210> 101
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 101
Val Pro His Ile His Glu Phe Thr Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
<210> 102
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 102
Pro Leu Thr Leu Ile
1 5
<210> 103
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 103
Ser Leu Leu Ile Gly
1 5
<210> 104
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 104
Lys Pro Pro Glu Arg
1 5
<210> 105
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 105
Cys Arg Ile Ile Arg
1 5
<210> 106
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 106
Ser Phe Ile Leu Ile
1 5
<210> 107
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 107
Pro His His His Ser
1 5
<210> 108
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 108
Glu Phe His Ser
1
<210> 109
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 109
Arg Leu Arg Arg Leu
1 5
<210> 110
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 110
Asp Ser Pro Arg
1
<210> 111
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 111
His Pro Trp Thr His
1 5
<210> 112
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 112
His Phe Ser His His
1 5
<210> 113
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 113
Arg Arg Val Ile
1
<210> 114
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 114
Ile Leu Val Ile
1
<210> 115
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 115
Arg Arg Ser Arg Ser Asn Glu Asp Val Glu Asp Lys Thr Glu Asp Glu
1 5 10 15
<210> 116
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 116
Arg Arg Ile Arg Ser Gly Gly Lys Asp His Ala Trp Thr Pro Leu His
1 5 10 15
Glu Asn His
<210> 117
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 117
His Thr Pro His Pro Pro Val Ala Arg Thr Ser Pro Leu Gln Thr Pro
1 5 10 15
Arg Arg
<210> 118
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 118
Pro Asp Ser Glu Pro Pro Arg Met Glu Leu Arg Arg Arg
1 5 10
<210> 119
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 119
Arg Arg Asp Thr Phe Asp Ile Arg Ile Leu Met Ala Phe
1 5 10
<210> 120
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 120
Arg Arg Glu Val Thr Glu Leu His His Thr His Glu Asp Arg Arg
1 5 10 15
<210> 121
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 121
Ser Pro Trp Thr His Glu Arg Arg Cys Arg Gln Arg
1 5 10
<210> 122
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 122
Arg Ser Arg Ser Ser His Leu Arg Asp His Glu Arg Thr His Thr
1 5 10 15
<210> 123
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 123
Arg Arg Arg Ser Thr Asn Thr Phe Leu Gly Glu Asp Phe Asp Gln
1 5 10 15
<210> 124
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 124
Leu Ile Gly Leu Ser Thr Ser Pro Arg Pro Arg Ile Ile Arg
1 5 10
<210> 125
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 125
Glu Ile Tyr Gly Glu Ser Gly Lys Thr Asp Glu His Ala Leu Asp Thr
1 5 10 15
Glu Tyr Arg Arg
20
<210> 126
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 126
Arg Arg Val Ile Leu Arg Ser Tyr Asp Gly Gly His Ser Thr Pro His
1 5 10 15
Pro Asp
<210> 127
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 127
Thr Gly Lys Thr Phe Val Lys Arg His Leu Thr Glu Phe Glu Lys Lys
1 5 10 15
Tyr Arg
<210> 128
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 128
Asn His Phe Asp Tyr Asp Thr Ile Glu Leu Asp Thr Ala Gly Glu Tyr
1 5 10 15
Ser Arg Arg Arg
20
<210> 129
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 129
Asp Pro Glu Pro Pro Arg Tyr Leu Pro Pro Pro Pro Glu Arg Arg
1 5 10 15
<210> 130
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 130
Arg Arg Thr Phe Ile Arg His Arg Ile Asp Ser Thr Glu Val Ile Tyr
1 5 10 15
Gln Asp Glu Asp
20
<210> 131
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 131
Glu Ser Lys Thr Gly His Lys Ser Glu Glu Gln Arg Leu Arg Arg Tyr
1 5 10 15
Arg
<210> 132
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 132
Tyr Asp Asp Glu His Asn His His Pro His His Ser Thr His Arg Arg
1 5 10 15
Arg
<210> 133
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 133
Arg Arg Arg Arg Glu Val His Thr Ile His Gln His Gly Ile Val His
1 5 10 15
Ser Asp
<210> 134
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 134
Asp Glu Pro Leu Pro Pro Pro Glu Arg Arg Arg
1 5 10
<210> 135
<211> 6
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 135
Ser Pro His Pro Pro Tyr
1 5
<210> 136
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 136
Ser Pro His Pro Pro Tyr Ser Pro His Pro Pro Tyr Ser Pro His Pro
1 5 10 15
Pro Tyr Pro
<210> 137
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 137
Arg Arg Pro His Asn Leu His His Asp
1 5
<210> 138
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 138
Leu Arg Asp Pro His Pro Pro Glu Arg Arg Ile Arg
1 5 10
<210> 139
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 139
Arg Arg Pro Ala Asp Gln Ile Ser Tyr Leu His Pro Pro Glu Arg
1 5 10 15
<210> 140
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 140
Asp Leu Gln Tyr Asp Phe Pro Arg Ile Arg Arg
1 5 10
<210> 141
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 141
Tyr Asp Glu Leu Tyr Gln Lys Glu Asp Pro His Arg Arg Arg
1 5 10
<210> 142
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 142
Phe Lys Pro Glu Arg Phe Pro Gln Asn Asp Arg Arg Arg
1 5 10
<210> 143
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 143
Arg Pro Ala Asp Arg Ile Arg Arg
1 5
<210> 144
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 144
His Asp Phe Asp Pro Arg Tyr Arg Asp Arg Arg
1 5 10
<210> 145
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 145
Arg Ile Arg Arg Asp Pro Asp Ser Pro Leu Pro His Pro Glu
1 5 10
<210> 146
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 146
Xaa Arg Arg Ile Arg Ile Leu Met Phe Leu Ile Gly Cys Gly Arg Val
1 5 10 15
<210> 147
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 147
His Pro His Val Ile Leu Pro Arg Ile Arg Ile Arg Ile Arg
1 5 10
<210> 148
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 148
Glu Ile His Thr Ile His Leu Leu Pro Glu Arg Arg
1 5 10
<210> 149
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 149
Glu Pro Ser His Pro Arg Ser Arg Tyr Pro Arg Thr Phe
1 5 10
<210> 150
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 150
Arg Asn Ile Ile Ile Arg Asp Phe Ile His Phe Ser His Ile Asp Arg
1 5 10 15
<210> 151
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (10)..(10)
<223> X=MYRISTATE
<400> 151
Arg Arg Ile Arg Asp Pro Gln Ile Lys Xaa Leu Glu Ile His Phe Ser
1 5 10 15
His Ile Asp
<210> 152
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 152
Xaa Asp Leu His Thr Ile His Ile Pro Arg Asp Arg Arg
1 5 10
<210> 153
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 153
Ser His Asp Phe Pro His Arg Glu Pro Arg Pro Glu Arg Arg
1 5 10
<210> 154
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 154
Ser Tyr Arg His Tyr Ser Asp His Trp Glu Asp Arg Arg Arg
1 5 10
<210> 155
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 155
Val Trp Val His Asp Ser Cys His Ala Asn Leu Gln Asn Tyr Arg Asn
1 5 10 15
Tyr Leu Leu Pro
20
<210> 156
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 156
Glu His Asp Phe Glu Val Arg Gly Asp Val Val Asn Gly Arg Asn His
1 5 10 15
Gln Gly Pro Lys
20
<210> 157
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 157
Leu Glu Val Ile Tyr Met Ile
1 5
<210> 158
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 158
Trp Thr Leu Ser Asn Tyr Leu
1 5
<210> 159
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 159
Asp Ser Leu His Ser Thr Tyr
1 5
<210> 160
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 160
Trp His His Arg Gln Gln Ile Pro Arg Pro Leu Glu
1 5 10
<210> 161
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 161
Ala Pro Ser Ile Phe Thr Pro His Ala Trp Arg Gln
1 5 10
<210> 162
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 162
Thr His Phe Ser His His Leu Lys Gly Gly Gly Arg Arg Gln Arg Arg
1 5 10 15
Arg Pro
<210> 163
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 163
Leu His Ser Lys Thr Leu Val Leu Gly Gly Gly Arg Arg Arg Arg Gly
1 5 10 15
Asp Arg
<210> 164
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 164
Trp Thr Leu Ser Asn Tyr Leu Gly Gly Arg Lys Lys Arg Arg Gln Arg
1 5 10 15
Arg Arg Arg
<210> 165
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 165
Val Arg Cys Ile Phe Arg Gly Ile Trp Val Arg Leu
1 5 10
<210> 166
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 166
His Ser Ser Gly His Asn Phe Val Leu Val Arg Gln
1 5 10
<210> 167
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 167
Leu Phe Ile Leu Val Phe Arg
1 5
<210> 168
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 168
Thr Thr Ser His His Pro Lys
1 5
<210> 169
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 169
Val Met Val Leu Phe Arg Ile Leu Arg Gly Ser Met
1 5 10
<210> 170
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 170
Ser Ile Leu Thr
1
<210> 171
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 171
Arg Arg Arg Glu Ser Glu Gln Arg Ser Ile Ser Leu His His His Ser
1 5 10 15
Thr
<210> 172
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 172
Xaa His Phe Asn His Tyr Thr Phe Glu Ser Thr Cys Arg Arg Arg Arg
1 5 10 15
Cys
<210> 173
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 173
His Ser Thr Pro His Pro Pro Gln Pro Pro Glu Arg Arg Arg
1 5 10
<210> 174
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 174
Arg Arg Lys Ser Glu Pro His Ser Leu Ser Gly Gly Tyr Gln Thr Gly
1 5 10 15
Ala Asp
<210> 175
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 175
His Arg Thr Gly His Tyr Thr Arg Cys Arg Gln Arg Cys Arg Ser Arg
1 5 10 15
Ser His Asn Arg His
20
<210> 176
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 176
Arg Arg Cys Arg Ser Ile Leu Pro Leu Leu Leu Leu Ser Arg
1 5 10
<210> 177
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 177
Arg Thr Leu His Gly Arg Arg Val Ile Leu His Glu Gly Gly His Ser
1 5 10 15
Ile Ser Asp Leu Lys
20
<210> 178
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 178
His His Arg Leu Ser Tyr Phe Ile Val Arg Arg His Ser Thr His Ala
1 5 10 15
Ser Arg
<210> 179
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 179
Arg Arg Ile Arg Ile Asp Pro Gln His Asp
1 5 10
<210> 180
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 180
Ile Leu Gln Pro Asp Phe Leu Ile Arg Pro Glu
1 5 10
<210> 181
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 181
His Asp Pro Arg Ile Ile Arg Ile Arg
1 5
<210> 182
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 182
Ser Pro Tyr Pro Ile Arg Thr
1 5
<210> 183
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 183
Ile Leu Val Ile Ile Gln Arg Ile Met
1 5
<210> 184
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 184
Ile Arg Phe Ile Leu Ile Arg
1 5
<210> 185
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 185
Ser Ser Val His His Arg Gly
1 5
<210> 186
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 186
Leu Arg Arg Gln Leu Gln Leu
1 5
<210> 187
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 187
His Thr Thr Ala His Thr His
1 5
<210> 188
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 188
His Pro His Asn His Thr Val His Asn Val Val Tyr
1 5 10
<210> 189
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 189
Asp His Ser Lys Phe Val Pro Leu Phe Val Arg Gln
1 5 10
<210> 190
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 190
Ser Ile Arg Thr Leu Gly Arg Phe Leu Ile Ile Arg Val
1 5 10
<210> 191
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 191
Gly Leu Cys Arg Ile Ile Leu
1 5
<210> 192
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 192
Ser Pro Pro Ile Arg His His
1 5
<210> 193
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 193
His Pro Thr His Pro Ile Arg Leu Arg Asp Asn Leu Thr Arg
1 5 10
<210> 194
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 194
Xaa Arg Glu Glu Glu Thr Ile Leu Ile Ile Arg Arg Arg
1 5 10
<210> 195
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 195
His Thr Ile His Ser Ile Ser Asp Phe Pro Glu Pro Pro Asp Arg Arg
1 5 10 15
Arg Arg
<210> 196
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 196
Asp Glu Asp Ala Ala His Ser Thr Gly His Pro His Asn Ser Gln His
1 5 10 15
Arg Arg Arg Arg
20
<210> 197
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 197
Thr Glu Gln His His Tyr Ile Pro His Arg Arg Arg
1 5 10
<210> 198
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 198
Arg Leu Arg Arg Val Ile Leu Arg Ser Tyr His Glu
1 5 10
<210> 199
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 199
Glu Glu Pro Asp Arg Gln Pro Ser Gly Lys Arg Gly Gly Arg Lys Arg
1 5 10 15
Arg Ser Arg
<210> 200
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 200
Arg Asp Phe His Thr Ile His Pro Ser Ile Ser Arg Arg
1 5 10
<210> 201
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 201
Arg Arg Val Asp Ile His Asp Gly Gln Arg Arg
1 5 10
<210> 202
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 202
Asp Gln Pro Tyr Pro His Arg Arg Ile Arg
1 5 10
<210> 203
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 203
Xaa Arg Asp Phe Ile Leu Phe Ile Arg Arg Leu Gly Arg Arg
1 5 10
<210> 204
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 204
Leu Asp Leu Tyr His Pro Arg Glu Arg Arg
1 5 10
<210> 205
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 205
Arg Arg Ile Arg Asp Pro Leu Gly Asn Glu His Glu
1 5 10
<210> 206
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 206
Ile Val Glu Phe Arg Ile Arg Arg
1 5
<210> 207
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 207
Arg Arg Pro Arg Ile Pro Asp Tyr Ile Leu
1 5 10
<210> 208
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 208
Arg Ser Thr Pro His Ile His Glu Phe Ile Arg Arg
1 5 10
<210> 209
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 209
Ser His Asp Phe Tyr Pro His Trp Met Arg Glu Arg Ile Arg
1 5 10
<210> 210
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 210
His Phe Ser His His Leu Lys
1 5
<210> 211
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 211
Thr Ser Pro Leu Gln Ser Leu Lys
1 5
<210> 212
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 212
Ala Ile Leu Thr Leu Ile Leu Arg Arg Val Ile Trp Pro
1 5 10
<210> 213
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 213
Leu Arg Phe Ile Asp Tyr Pro
1 5
<210> 214
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 214
Gly Pro Ile Lys His His Leu Gln His His
1 5 10
<210> 215
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 215
Leu Thr Leu Ser
1
<210> 216
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 216
Arg Tyr Glu Glu Asn Asn Gly Val Asn Pro Pro Val Gln Val Phe Glu
1 5 10 15
Ser Arg Thr Arg
20
<210> 217
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 217
Arg Glu Gly Phe Tyr Gly Pro Trp His Glu Gln Arg Arg Arg
1 5 10
<210> 218
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 218
Arg Arg Asp Ile Ile Arg His Asn Ala His Ser
1 5 10
<210> 219
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 219
His Asp Phe His Asp Tyr Leu Glu Arg Arg
1 5 10
<210> 220
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 220
Ile Arg Glu Phe Asp Pro Arg Arg Ile Arg
1 5 10
<210> 221
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 221
Arg Leu Arg Cys Leu Leu Leu Leu Ile Gly Arg Val Gly Arg Arg
1 5 10 15
<210> 222
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 222
Leu Gly Ile Asp Glu Asp Glu Glu Thr Glu Thr Ala Pro Glu
1 5 10
<210> 223
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 223
Ser Leu Leu Ile Gly Phe Gly Ile Ile Arg Ser Arg
1 5 10
<210> 224
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 224
Val His Glu Val Thr His His Trp Leu
1 5
<210> 225
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 225
Ala Thr Pro Phe His Gln Thr
1 5
<210> 226
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 226
Ser Ile Leu Pro Leu Phe Leu Ile Arg Arg Ser Gly
1 5 10
<210> 227
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 227
Ser Cys Arg Cys Arg Leu Arg Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
<210> 228
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 228
Ser Arg Ile Val Leu Gly Trp
1 5
<210> 229
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 229
Ser Asn Ile His His Gln Val
1 5
<210> 230
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 230
Leu Thr Leu Met Arg Leu Arg Ile Ile Gly
1 5 10
<210> 231
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 231
His Ser Tyr Ser Pro Tyr Tyr Thr Phe Arg Gln His
1 5 10
<210> 232
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 232
Phe Ile Leu Ile Arg
1 5
<210> 233
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 233
Arg Cys Arg Asn Arg Lys Lys Glu Lys Thr Glu Cys Leu Gln Lys Glu
1 5 10 15
Ser Glu Lys
<210> 234
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 234
Arg Arg Ile Lys Met Ile Arg Thr Ser Glu Ser Phe Ile Gln His Ile
1 5 10 15
Val Ser
<210> 235
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 235
Arg Arg Val Ser Glu Leu Gln Arg Asn Lys His Gly Arg Lys His Glu
1 5 10 15
Leu
<210> 236
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 236
Arg Arg Arg Leu Asp Asp Glu Asp Val Gln Thr Pro Thr Pro Ser Glu
1 5 10 15
Tyr Gln Asn
<210> 237
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 237
Arg Arg Arg Gln Pro Leu Pro Ser Ala Pro Glu Asn Glu Glu
1 5 10
<210> 238
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 238
Ser Pro Leu Gln Thr Pro Ala Ala Pro Gly Ala Ala Ala Gly Pro Ala
1 5 10 15
Leu Ser Pro Val
20
<210> 239
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 239
Ser His Gln Val His Thr His His Asn Asn
1 5 10
<210> 240
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 240
Lys Leu Gln Val Pro Ile Lys
1 5
<210> 241
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 241
Ile Arg Gly Arg Ile Ile Arg Arg Lys Lys Arg Arg Gln Arg Arg Arg
1 5 10 15
Arg Gly Asp Arg
20
<210> 242
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 242
Gln Ile Pro His Arg Ser Ser Thr Ala Leu Gln Leu
1 5 10
<210> 243
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 243
Ser Tyr Gln Thr Met Gln Pro
1 5
<210> 244
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 244
Thr Asp Ser His Ser His His Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 245
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 245
Ile Pro Met Asn Phe Thr Ser His Ser Leu Arg Gln Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg Arg
20
<210> 246
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 246
Tyr Trp Ser Ala Pro Gln Pro Ala Thr Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg
20
<210> 247
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 247
Ser Thr Thr His Pro His Pro Gly Thr Ser Ala Pro Glu Pro Ala Thr
1 5 10 15
Arg Arg Arg
<210> 248
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 248
Asp Asp Ser Asp Asn Arg Ile Ile Arg Tyr Arg Arg
1 5 10
<210> 249
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 249
Thr Ser Pro His Pro Ser Leu Pro Arg His Ile Tyr Pro Arg Arg
1 5 10 15
<210> 250
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 250
Arg Arg Ile Thr Glu Ile Arg Gly Arg Thr Gly Lys Thr Thr Leu Thr
1 5 10 15
Tyr Ile Glu Asp
20
<210> 251
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 251
Xaa Asp Glu Arg Thr Gly Lys Thr Arg Arg Tyr Ile Asp Thr Arg Asp
1 5 10 15
Ile Arg Arg
<210> 252
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 252
Xaa Met Thr Tyr Ser Asp Met Pro Arg Arg Ile Ile Thr Asp Glu Asp
1 5 10 15
Arg Arg Arg
<210> 253
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 253
Arg Arg Tyr Asp Thr Val Ile Asp Asp Ile Glu Tyr Arg Arg
1 5 10
<210> 254
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 254
Arg Asp Thr Ile Glu Arg Pro Glu Ile Arg Arg
1 5 10
<210> 255
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 255
Xaa Arg Tyr Arg Arg Leu Ile Leu Glu Ile Trp Arg Arg
1 5 10
<210> 256
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 256
Xaa Arg His Asp Thr His Asn Ala His Ile Arg Arg
1 5 10
<210> 257
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 257
Thr His Asp Phe Asp Arg Leu Leu Arg Ile Arg Arg Arg
1 5 10
<210> 258
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 258
Arg His Asn His Ile Arg Pro Asp Asn Gln
1 5 10
<210> 259
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 259
Arg Tyr Lys Glu Pro Arg Ile Thr Pro Arg Glu
1 5 10
<210> 260
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 260
Leu Arg Ile Glu Pro Ile Arg Ile Arg
1 5
<210> 261
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 261
Xaa Arg Leu Ile Arg Ile Arg Ile Leu Met
1 5 10
<210> 262
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 262
Arg Pro Glu Phe His Ser Phe His Pro Ile Tyr Glu Arg Arg
1 5 10
<210> 263
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 263
Ser Thr Thr His Ile His Ala
1 5
<210> 264
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 264
Phe Pro His Leu Val Ser Ser Leu Thr Thr
1 5 10
<210> 265
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 265
Gly Leu His Leu Phe Thr Thr Asp Arg Gln Gly Trp
1 5 10
<210> 266
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 266
Asn His Pro Trp Gln Phe Pro Asn Arg Trp Thr Arg Arg Arg Arg Arg
1 5 10 15
Arg
<210> 267
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 267
His Ser Ser His His His Pro Val His Ser Trp Asn Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 268
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 268
Xaa Asp Ile His Thr Ile His Leu Pro Asp Thr His Arg Arg
1 5 10
<210> 269
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 269
Val Ala Glu Phe Ala Gln Ser Ile Gln Ser Arg Ile Val Glu Trp Lys
1 5 10 15
Glu Arg Leu Asp
20
<210> 270
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 270
Thr Arg Ile Leu Cys Ile Val Met Met
1 5
<210> 271
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 271
Phe Leu Leu Pro Glu Pro Asp Glu Asn Thr Arg Trp
1 5 10
<210> 272
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 272
Leu Met Ser Asn Ala Gln Tyr
1 5
<210> 273
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 273
Ser Ile Leu Thr Leu Ser Cys Arg Cys Arg Leu Arg Leu Trp Arg
1 5 10 15
<210> 274
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 274
His Gln Ile His Arg Asn His Thr Tyr
1 5
<210> 275
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 275
Leu Ile Arg Arg Cys Ser Leu Gln Arg
1 5
<210> 276
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 276
Gly Ala Met His Leu Pro Trp His Met Gly Thr Arg Arg Arg Arg Arg
1 5 10 15
Arg
<210> 277
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 277
Asp Glu Asp Ala Lys Phe Arg Ile Arg Ile Leu Met Arg Arg
1 5 10
<210> 278
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 278
Asn His Ile Thr Asn Gly Gly Glu Glu Asp Ser Asp Cys Ser Ser Arg
1 5 10 15
Arg Arg Arg Leu
20
<210> 279
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 279
Xaa His Ser Ser His His His Pro Thr Val Gln His Arg Arg
1 5 10
<210> 280
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 280
Arg Asp Phe Glu Arg Thr Ile Val Asp Ile
1 5 10
<210> 281
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 281
Xaa Arg Arg Arg Glu Ile Leu His Pro Glu Phe Arg Ile Leu Tyr Glu
1 5 10 15
<210> 282
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 282
His His Phe Ser His His Trp Lys Thr
1 5
<210> 283
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 283
Phe Leu Ile Arg Arg Ser Gly
1 5
<210> 284
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 284
His Asn His His His Ser Gln His Thr Pro Gln His
1 5 10
<210> 285
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 285
His Leu His Lys His His Tyr Lys Asp Ser Arg Met
1 5 10
<210> 286
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 286
His Arg Thr Gln Ser Thr Leu Ile Leu Phe Ile Arg Arg Gly Arg Glu
1 5 10 15
Thr
<210> 287
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 287
Leu His Phe Ser His Ile Asp Arg Arg
1 5
<210> 288
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 288
Tyr Glu Leu Pro His His Ala Tyr Pro Ala
1 5 10
<210> 289
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 289
Ser Leu Leu Ile Gly Phe Gly Ile Ile Arg Ser Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 290
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 290
His Thr Asp Ser His Pro His His His His Pro His Arg Arg Arg Arg
1 5 10 15
Arg
<210> 291
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 291
Ala Thr Gln His His Tyr Ile Lys Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 292
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 292
Phe Arg Ser Phe Ala Ile Pro Leu Val Val Pro Phe Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 293
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 293
Tyr Pro Thr Gln Gly His Leu Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 294
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 294
His Ala Asn Leu His His Thr Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 295
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 295
Tyr Arg Arg Leu Leu Ile Gly Met Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg
20
<210> 296
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 296
Ser His Tyr His Thr Pro Gln Asn Pro Pro Ser Thr Arg Arg Arg
1 5 10 15
<210> 297
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 297
Arg Ser Tyr Ser Lys Leu Leu Cys Leu Leu Glu Arg Leu Arg Ile Ser
1 5 10 15
Pro
<210> 298
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 298
Phe Trp Thr Gln Ser Ile Lys Glu Arg Lys Met Leu Asn Glu His Asp
1 5 10 15
Phe Glu Val Arg
20
<210> 299
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 299
Thr His Phe Ser His His Leu Lys His
1 5
<210> 300
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 300
Ser Cys Arg Cys Arg Leu Arg
1 5
<210> 301
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 301
Met His Pro Pro Asp Trp Tyr His His Thr Pro Lys Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 302
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 302
His Thr Ile His Val His Tyr Pro Gly Asn Arg Gln Pro Asn Pro Pro
1 5 10 15
Leu Ile Leu Gln Arg
20
<210> 303
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 303
Thr Pro Ser Tyr Gly His Thr Pro Ser His His Arg Arg Arg
1 5 10
<210> 304
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 304
Xaa Ile Arg Gly Arg Ile Arg Ile Ile Arg Arg Ile Arg
1 5 10
<210> 305
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 305
His His Pro Trp Thr His His Gln Arg Trp Ser
1 5 10
<210> 306
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 306
Ile Pro Met Asn Phe Thr Ser His Ser Leu Arg Gln
1 5 10
<210> 307
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 307
Ser Asn His His His Arg His His Thr Asn Thr His
1 5 10
<210> 308
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 308
Glu Val Thr Phe Arg His Ser Val Val Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg
20
<210> 309
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 309
Phe Pro Gly His Thr Ile His Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 310
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 310
Ser Ile Leu Thr Leu Ser Arg Ile Val Leu Gly Trp Trp
1 5 10
<210> 311
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 311
Thr Leu Tyr Leu Pro His Trp His Arg His
1 5 10
<210> 312
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 312
Ser Ile Leu Thr Leu Arg Leu Arg Arg Leu Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 313
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 313
Thr Leu Tyr Leu Pro His Trp His Arg His Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg
20
<210> 314
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 314
Thr Asp Ser His Ser His His
1 5
<210> 315
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 315
Glu Trp Lys Glu Arg Leu Asp Lys Glu Phe Ser Leu Ser Val Tyr Gln
1 5 10 15
Lys Met Lys Phe
20
<210> 316
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 316
Thr Ile His Pro Ser Ile Ser
1 5
<210> 317
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 317
Ser Ile Leu Thr Leu Arg Leu Arg Arg Leu Arg Arg
1 5 10
<210> 318
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 318
Val Pro His Ile His Glu Phe Thr
1 5
<210> 319
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 319
Thr Ile Ile His Arg Glu Asp Glu Asp Glu Ile Glu Trp
1 5 10
<210> 320
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 320
Lys Asp Leu Pro Phe Tyr Ser His Leu Ser Arg Gln
1 5 10
<210> 321
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 321
Thr His Phe Ser His His Leu Lys His Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 322
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 322
Ala Thr Gln His His Tyr Ile Lys
1 5
<210> 323
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 323
Ile Ile Arg Gly Asn Phe Leu Ile Gly Gly Arg Leu
1 5 10
<210> 324
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 324
Leu Pro Asn Pro Pro Glu Arg His His Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg
20
<210> 325
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 325
Ser Phe Ile Leu Phe Ile Arg Arg Gly Arg Leu Gly Arg Gly Asp Arg
1 5 10 15
<210> 326
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 326
Phe Pro Gly His Thr Ile His
1 5
<210> 327
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 327
Cys Ile Leu Arg Leu Trp Trp
1 5
<210> 328
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 328
Arg Arg Arg Ser His Ser Gln Glu Asn Val Asp Gln Asp Thr Asp Glu
1 5 10 15
<210> 329
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 329
Met Ser Thr Glu Ser Asn Met Pro Arg Leu Ile Gln Asn Asp Asp Arg
1 5 10 15
Arg Arg
<210> 330
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 330
Leu Leu Arg Leu Gly Leu Ile
1 5
<210> 331
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 331
Ile Arg Ile Leu Met Phe Leu Ile Gly Cys Gly Arg
1 5 10
<210> 332
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 332
Leu His Ser Lys Thr Leu Val Leu
1 5
<210> 333
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 333
Leu Arg Cys Leu Leu Leu Leu Ile Gly Arg Val Gly
1 5 10
<210> 334
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 334
Phe Leu Ile Gly Pro Asp Arg Leu Ile Arg Ser Arg
1 5 10
<210> 335
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 335
Leu Pro Asn Pro Pro Glu Arg His His
1 5
<210> 336
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 336
His Thr Asp Ser His Pro His His His His Pro His
1 5 10
<210> 337
<211> 22
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> Fluorescein isothiocyanate (FITC)
<222> (1)..(1)
<223> X=Fluorescein isothiocyanate (FITC)
<400> 337
Xaa Ser Phe Ile Leu Phe Ile Arg Arg Gly Arg Leu Gly Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg Arg Arg
20
<210> 338
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 338
His Ser Ser His His His Pro Val His Ser Trp Asn
1 5 10
<210> 339
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 339
Xaa Arg Thr Leu Ile Gly Ile Ile Arg Ser His His Leu Thr Leu Ile
1 5 10 15
Arg Arg
<210> 340
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 340
Ile Arg Gly Arg Ile Ile Arg
1 5
<210> 341
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 341
Ile Ile Arg Gly Asn Phe Leu Ile Gly Gly Arg Leu Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg Arg
20
<210> 342
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 342
Ile Arg Ile Leu Met
1 5
<210> 343
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 343
Gly Ala Met His Leu Pro Trp His Met Gly Thr Leu
1 5 10
<210> 344
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 344
Lys Arg Gly Gly Arg Lys Arg Arg Gly Gly Gly His Arg Leu Ser Tyr
1 5 10 15
Phe Ile Arg Arg
20
<210> 345
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 345
Asn His Pro Trp Gln Phe Pro Asn Arg Trp Thr Val
1 5 10
<210> 346
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 346
Met His Pro Pro Asp Trp Tyr His His Thr Pro Lys His
1 5 10
<210> 347
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 347
Ser Trp Gln Ala Leu Ala Leu Tyr Ala Ala Gly Trp Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 348
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 348
His Asn Ala His
1
<210> 349
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 349
Asp Glu Phe Glu Arg Tyr Arg Arg Phe Ser Thr Ser Arg Arg Arg
1 5 10 15
<210> 350
<211> 9
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 350
Glu Val Thr Phe Arg His Ser Val Val
1 5
<210> 351
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 351
Thr Arg Ile Leu Cys Ile Val Arg Lys Lys Arg Arg Gln Arg Arg Arg
1 5 10 15
Arg Gly Asp Arg
20
<210> 352
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 352
Ser Ile Leu Thr Leu Ser Arg Gly Arg Lys Lys Arg Arg Gln Arg Arg
1 5 10 15
Arg Arg
<210> 353
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 353
Cys Ile Leu Arg Leu Trp Trp Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg
<210> 354
<211> 13
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 354
Ala Ser Trp Gln Ala Leu Ala Leu Tyr Ala Ala Gly Trp
1 5 10
<210> 355
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 355
Xaa Pro Arg Val Leu Pro Ser Pro His Thr Ile His Pro Ser Gln Tyr
1 5 10 15
Pro
<210> 356
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 356
His Ala Asn Leu His His Thr
1 5
<210> 357
<211> 22
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 357
Ser Phe Ile Leu Phe Ile Arg Arg Gly Arg Leu Gly Arg Lys Lys Arg
1 5 10 15
Arg Gln Arg Arg Arg Pro
20
<210> 358
<211> 8
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 358
Tyr Pro Thr Gln Gly His Leu Arg
1 5
<210> 359
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 359
Tyr Arg Arg Leu Leu Ile Gly Met Met Trp Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg Arg
20
<210> 360
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 360
Ser Phe Ile Leu Phe Ile Arg Arg Gly Arg Leu Gly
1 5 10
<210> 361
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 361
Ile Arg Ile Leu Met Phe Leu Ile Gly Cys Gly Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg
<210> 362
<211> 14
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 362
Xaa Arg Arg Ile Cys Arg Phe Ile Arg Ile Cys Arg Val Arg
1 5 10
<210> 363
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 363
Ile Arg Gly Arg Ile Ile Arg Arg Arg Arg Arg Arg Arg Arg Arg Arg
1 5 10 15
<210> 364
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 364
Arg Arg Arg His Asp Ser Cys His Asn Gln Leu Gln Asn Tyr Asp His
1 5 10 15
Ser Thr Glu
<210> 365
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 365
Trp Asn His His His Ser Thr Pro His Pro Arg Arg Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg
20
<210> 366
<211> 19
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 366
Xaa Arg Arg Pro Val Ala Pro Asp Leu Arg His Thr Ile His Ile Pro
1 5 10 15
Pro Glu Arg
<210> 367
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 367
Arg Arg Asp Ile His Thr Ile His Pro Phe Tyr Gln
1 5 10
<210> 368
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 368
Trp Asn His His His Ser Thr Pro His Pro Ala His
1 5 10
<210> 369
<211> 21
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 369
Ser Phe Ile Leu Phe Ile Arg Arg Gly Arg Leu Gly Arg Arg Arg Arg
1 5 10 15
Arg Arg Arg Arg Arg
20
<210> 370
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> D-amino_acid
<222> (1)..(20)
<400> 370
Arg Arg Arg Arg Arg Arg Arg Arg Gly Leu Arg Gly Arg Arg Ile Phe
1 5 10 15
Leu Ile Phe Ser
20
<210> 371
<211> 16
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 371
Xaa Arg Arg His Asn Ala His His Ser Thr Pro His Pro Asp Asp Arg
1 5 10 15
<210> 372
<211> 6
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 372
His Ser Thr Pro His Pro
1 5
<210> 373
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 373
Leu Arg Cys Leu Leu Leu Leu Ile Gly Arg Val Gly Arg Lys Lys Arg
1 5 10 15
Arg Gln Arg Arg
20
<210> 374
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 374
Xaa Arg Arg Lys His Asn Lys His Arg Pro Glu Pro Asp Ser Asp Glu
1 5 10 15
Arg
<210> 375
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 375
Xaa Arg Arg Ile Arg Asp Pro Arg Ile Leu Leu Leu His Phe Asp
1 5 10 15
<210> 376
<211> 20
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 376
Arg Lys Arg Gly Lys Ser Tyr Ala Phe Phe Val Pro Pro Ser Glu Ser
1 5 10 15
Lys Glu Arg Trp
20
<210> 377
<211> 15
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 377
Xaa Arg Arg Lys Ile Leu Phe Ile Arg Leu Met His Asn Lys His
1 5 10 15
<210> 378
<211> 17
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 378
Xaa Arg Arg Leu Ile Val Arg Ile Leu Lys Leu Pro Asn Pro Pro Glu
1 5 10 15
Arg
<210> 379
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> MYRISTATE
<222> (1)..(1)
<223> X=MYRISTATE
<400> 379
Xaa Arg Arg His Ser Thr Pro His Pro Asp
1 5 10
<210> 380
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 380
Lys Pro Pro Asp Arg Leu Trp His Tyr Thr Gln Pro
1 5 10
<210> 381
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 381
Ala Thr Leu Pro Phe Val Thr Asp Arg Gln Gly Trp
1 5 10
<210> 382
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 382
Phe Tyr Ser His Ser Thr Ser Pro Ala Pro Ala Lys
1 5 10
<210> 383
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 383
Cys Tyr Ser His Ser Tyr Pro Thr Gln Gly His Leu
1 5 10
<210> 384
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 384
Glu Phe His Ser Phe Tyr Thr Ala Arg Gln Thr Gly
1 5 10
<210> 385
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 385
Ser Asp Gly Phe Val Pro His Phe Lys Arg Gln His
1 5 10
<210> 386
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 386
Leu Pro Asn Pro Pro Glu Arg
1 5
<210> 387
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 387
Leu His Ser Lys Thr Leu Val
1 5
<210> 388
<211> 6
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 388
His Val His Thr His Gln
1 5
<210> 389
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 389
Ser Ser Ser Leu Gly Thr His
1 5
<210> 390
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 390
His Glu Val Thr His His Trp
1 5
<210> 391
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 391
Ser Ala Pro Gln Pro Ala Thr
1 5
<210> 392
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 392
Thr Pro Pro Leu Thr Leu Ile
1 5
<210> 393
<211> 6
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 393
His Pro Trp Thr His His
1 5
<210> 394
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 394
Ser Ala Ala Ser Asp Leu Arg
1 5
<210> 395
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 395
Ser Pro Leu Gln Ser Leu Lys
1 5
<210> 396
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 396
Arg Pro Thr Gln Val Leu His
1 5
<210> 397
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 397
Phe Arg Ser Phe Ala Ile Pro Leu Val Val Pro Phe
1 5 10
<210> 398
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 398
Lys Ile Leu Phe Ile Arg Leu Met His Asn Lys His
1 5 10
<210> 399
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 399
His His His Pro
1
<210> 400
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 400
His Thr Ile His
1
<210> 401
<211> 4
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 401
His Asn Lys His
1
<210> 402
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 402
Leu Leu Leu Ile Gly
1 5
<210> 403
<211> 5
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 403
Ile Leu Phe Ile Arg
1 5
<210> 404
<211> 6
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 404
Ile Arg Gly Arg Ile Ile
1 5
<210> 405
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 405
Ser Phe Ile Leu Phe Ile Arg
1 5
<210> 406
<211> 7
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 406
Tyr Pro Thr Gln Gly His Leu
1 5
<210> 407
<211> 10
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 407
Trp Asn His His His Ser Thr Pro His Pro
1 5 10
<210> 408
<211> 11
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 408
Ile Arg Ile Leu Met Phe Leu Ile Gly Cys Gly
1 5 10
<210> 409
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 409
Ser Trp Gln Ala Leu Ala Leu Tyr Ala Ala Gly Trp
1 5 10
<210> 410
<211> 12
<212> PRT
<213> Artificial
<220>
<223> peptide
<220>
<221> D-amino_acids
<222> (1)..(12)
<400> 410
Gly Leu Arg Gly Arg Arg Ile Phe Leu Ile Phe Ser
1 5 10
<210> 411
<211> 18
<212> PRT
<213> Artificial
<220>
<223> peptide
<400> 411
Leu Arg Cys Leu Leu Leu Leu Ile Gly Arg Val Gly Arg Lys Lys Arg
1 5 10 15
Arg Gln
<210> 412
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (1)..(1)
<223> N terminus myristlyated
<400> 412
Arg Arg His Ser Thr Pro His Pro Gly Glu
1 5 10
<210> 413
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 413
Arg Arg His Ser Thr Pro His Pro Ser Glu
1 5 10
<210> 414
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 414
Arg Arg His Ser Thr Pro His Pro Ala Asp
1 5 10
<210> 415
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 415
Arg Arg His Ser Thr Pro His Pro Ala Glu
1 5 10
<210> 416
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 416
Arg Arg His Ser Ser Pro His Pro Asp
1 5
<210> 417
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 417
Arg Arg His Ser Val Pro His Pro Asp
1 5
<210> 418
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 418
Arg Arg His Ser Cys Pro His Pro Asp
1 5
<210> 419
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Glutamic Acid
<400> 419
Arg Arg His Ser Glu Pro His Pro Asp
1 5
<210> 420
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Threonine
<400> 420
Arg Arg His Ser Thr Pro His Pro Asp
1 5
<210> 421
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Serine
<400> 421
Arg Arg His Ser Ser Pro His Pro Asp
1 5
<210> 422
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Valine
<400> 422
Arg Arg His Ser Val Pro His Pro Asp
1 5
<210> 423
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 423
Arg Arg Xaa Ser Thr Pro His Pro Asp
1 5
<210> 424
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 424
Arg Arg His Ser Thr Pro Xaa Pro Asp
1 5
<210> 425
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> Methylated Amino Acid Residue
<400> 425
Arg Arg His Ser Thr Pro His Pro Asp Asp
1 5 10
<210> 426
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 426
Arg Arg His Ser Thr Pro His Ala Asp
1 5
<210> 427
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 427
Arg Arg His Ser Lys Pro His Pro Asp
1 5
<210> 428
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 428
Arg Arg His Ser Ser Pro Xaa Pro Asp
1 5
<210> 429
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Valine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 429
Arg Arg His Ser Val Pro Xaa Pro Asp
1 5
<210> 430
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 430
Arg Arg His Ser Thr Pro Xaa Ala Asp
1 5
<210> 431
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Serine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 431
Arg Arg His Ser Ser Pro Xaa Pro Asp
1 5
<210> 432
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (10)..(10)
<223> C-Terminal Amidation
<400> 432
Arg Arg His Ser Lys Pro His Pro Asp Asp
1 5 10
<210> 433
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 433
Arg Arg Xaa Ser Thr Pro Xaa Pro Asp
1 5
<210> 434
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 434
Arg Arg His Ser Lys Pro Xaa Pro Asp
1 5
<210> 435
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 435
Arg Arg Xaa Ser Lys Pro His Pro Asp
1 5
<210> 436
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 436
Arg Arg Xaa Ser Lys Pro Xaa Pro Asp
1 5
<210> 437
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 437
Arg Arg His Ser Lys Pro His Ala Asp
1 5
<210> 438
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 438
Arg Arg His Ser Lys Pro His Ala Ser Glu
1 5 10
<210> 439
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 439
Arg Arg His Ser Lys Pro His Pro Ser Glu
1 5 10
<210> 440
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Serine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 440
Arg Arg Xaa Ser Ser Pro Xaa Pro Asp
1 5
<210> 441
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Valine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 441
Arg Arg Xaa Ser Val Pro Xaa Pro Asp
1 5
<210> 442
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 442
Arg Arg His Ser Thr Pro His Ala Ser Glu
1 5 10
<210> 443
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Lysine
<400> 443
Arg Arg His Ser Lys Pro His Pro Asp
1 5
<210> 444
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (5)..(5)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 444
Arg Arg His Ser Xaa Pro His Pro Asp
1 5
<210> 445
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (5)..(5)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 445
Arg Arg His Ser Xaa Pro His Ala Asp
1 5
<210> 446
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 446
Arg Arg His Ser Glu Pro Xaa Pro Asp
1 5
<210> 447
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 447
Arg Arg Xaa Ser Glu Pro His Pro Asp
1 5
<210> 448
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D Valine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> C-Terminal Amidation
<400> 448
Arg Arg His Ser Val Pro Xaa Pro Asp
1 5
<210> 449
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (6)..(6)
<223> X is 2-Aminoisobutyric acid ( Aib)
<400> 449
Arg Arg His Ser Thr Xaa His Ala Asp
1 5
<210> 450
<211> 13
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 450
Arg Arg His Ser Thr Pro His Pro Asp Ile Glu Gly Arg
1 5 10
<210> 451
<211> 21
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 451
Arg Arg His Ser Thr Pro His Pro Asp Ile Glu Gly Arg Gly Trp Gln
1 5 10 15
Arg Pro Ser Ser Trp
20
<210> 452
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 452
Arg Arg Xaa Ser Glu Pro Xaa Pro Asp
1 5
<210> 453
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> C-Terminal Amidation
<400> 453
Arg Arg His Ser Glu Pro Xaa Pro Asp
1 5
<210> 454
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 454
Arg Arg Xaa Ser Glu Pro His Pro Asp
1 5
<210> 455
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> L-Phosphoserine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 455
Arg Arg His Ser Ser Pro Xaa Pro Asp
1 5
<210> 456
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D-Phosphoserine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 456
Arg Arg His Ser Ser Pro Xaa Pro Asp
1 5
<210> 457
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> L-Phosphoserine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<220>
<221> MISC_FEATURE
<222> (9)..(9)
<223> C-Terminal Amidation
<400> 457
Arg Arg His Ser Ser Pro Xaa Pro Asp
1 5
<210> 458
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 458
Arg Arg His Ser Lys Pro Xaa Pro Asp
1 5
<210> 459
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (3)..(3)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 459
Arg Arg Xaa Ser Lys Pro His Pro Asp
1 5
<210> 460
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 460
Arg Arg His Ser Thr Pro His Pro Ala His
1 5 10
<210> 461
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> misc_feature
<222> (10)..(10)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 461
Arg Arg His Ser Thr Pro His Pro Ala Xaa
1 5 10
<210> 462
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 462
Arg Arg His Ser Thr Pro His Pro Asp His
1 5 10
<210> 463
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<220>
<221> MISC_FEATURE
<222> (5)..(5)
<223> D-Valine
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is L- Diaminobutyric Acid (L-DAB)
<400> 463
Arg Arg His Ser Val Pro Xaa Pro Asp His
1 5 10
<210> 464
<211> 10
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> LIPID
<222> (1)..(1)
<223> MYRISTATE group attached
<400> 464
Arg Arg His Ser Thr Pro His Ala Asp His
1 5 10
<210> 465
<211> 9
<212> PRT
<213> Artificial sequence
<220>
<223> pCAP 250 peptide variant
<220>
<221> misc_feature
<222> (7)..(7)
<223> X is Diaminobutyric Acid (DAB)
<400> 465
Arg Arg His Ser Thr Pro Xaa Pro Asp
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИ-PVRIG АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2732042C2 |
| АНТИ-PVRIG АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2827926C2 |
| ПЕПТИДНЫЕ АНТАГОНИСТЫ ПЕПТИДНЫХ ГОРМОНОВ ИЗ СЕМЕЙСТВА КАЛЬЦИТОНИНА (CGRP) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2742826C2 |
| ПЕПТИДЫ, СПОСОБНЫЕ РЕАКТИВИРОВАТЬ МУТАНТЫ Р53 | 2014 |
|
RU2721423C2 |
| ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) С АНТИГЕНСВЯЗЫВАЮЩИМИ ДОМЕНАМИ К КОНСТАНТНОЙ ОБЛАСТИ β Т-КЛЕТОЧНОГО РЕЦЕПТОРА | 2015 |
|
RU2830064C2 |
| УЛУЧШЕННЫЕ ПЕПТИДНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ NASH И ДРУГИХ РАССТРОЙСТВ | 2019 |
|
RU2790209C2 |
| IL-17A-связывающие полипептиды | 2016 |
|
RU2749712C2 |
| АФФИМЕРЫ, СВЯЗЫВАЮЩИЕСЯ С НЕОНАТАЛЬНЫМ FC РЕЦЕПТОРОМ | 2020 |
|
RU2817008C1 |
| Фармацевтическая композиция, содержащая инсулин и глюкагон | 2019 |
|
RU2823246C2 |
| ИСКУССТВЕННЫЕ НЕИЗБИРАТЕЛЬНЫЕ ЭПИТОПЫ КЛЕТОК Т-ХЕЛПЕРОВ КАК ИММУННЫЕ СТИМУЛЯТОРЫ ДЛЯ СИНТЕТИЧЕСКИХ ПЕПТИДНЫХ ИММУНОГЕНОВ | 2019 |
|
RU2839585C2 |
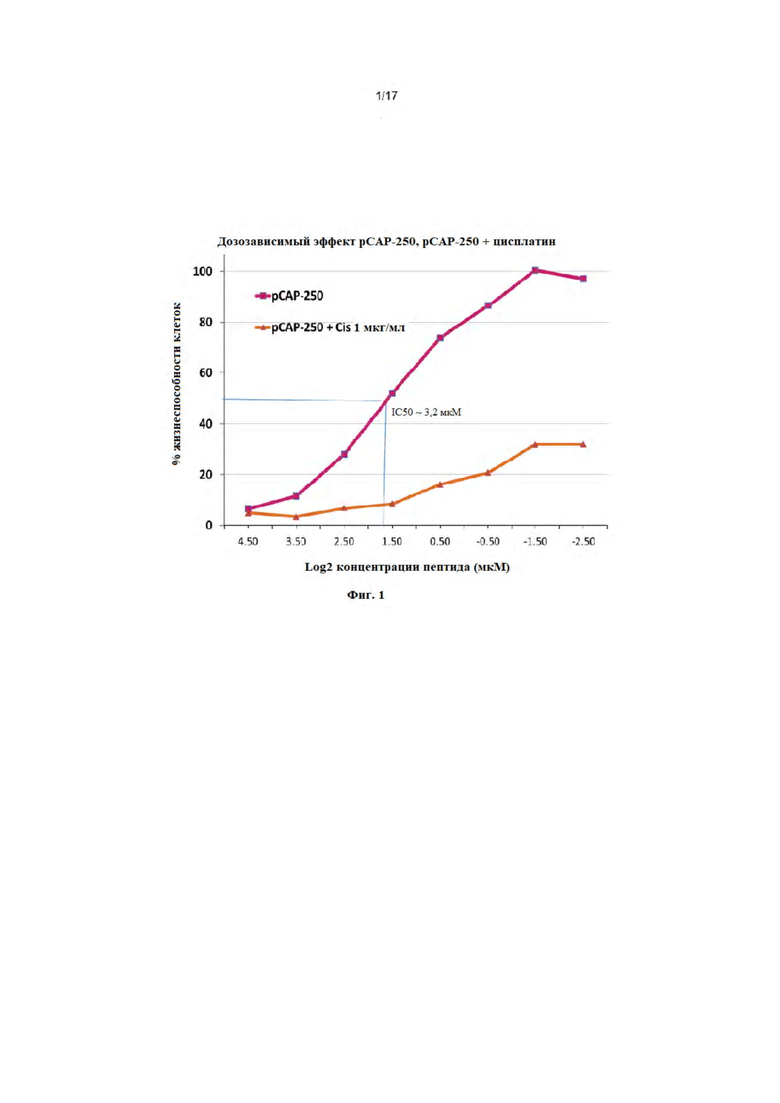
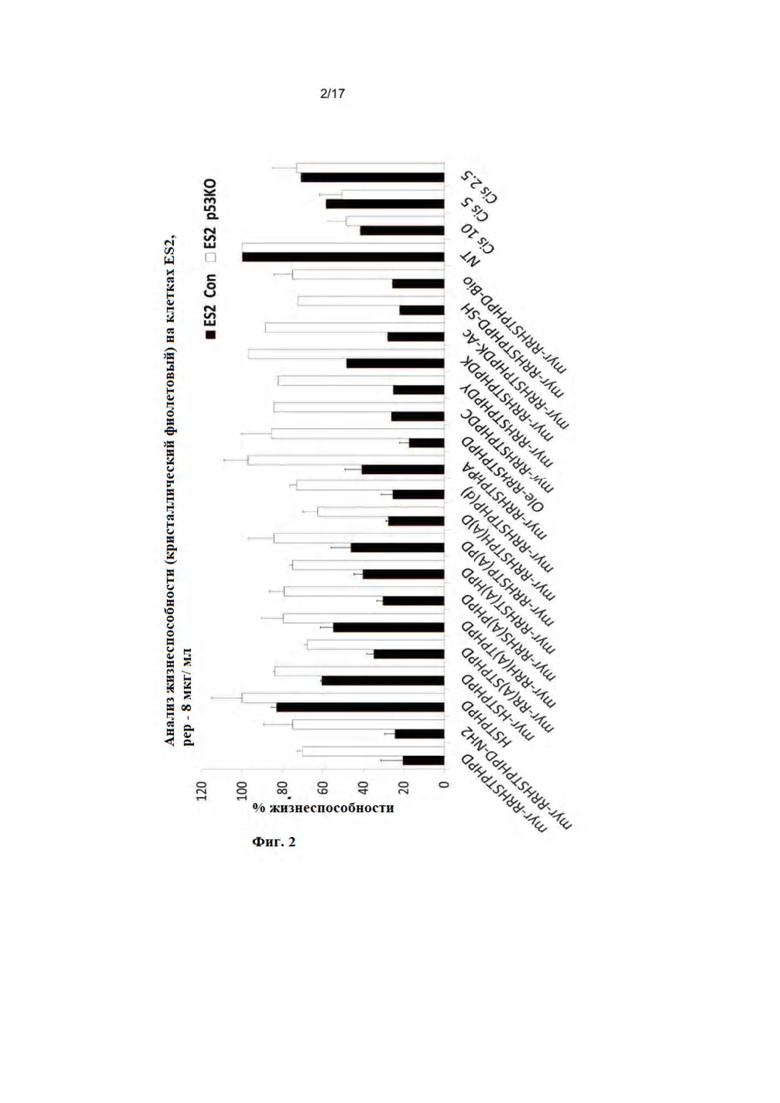
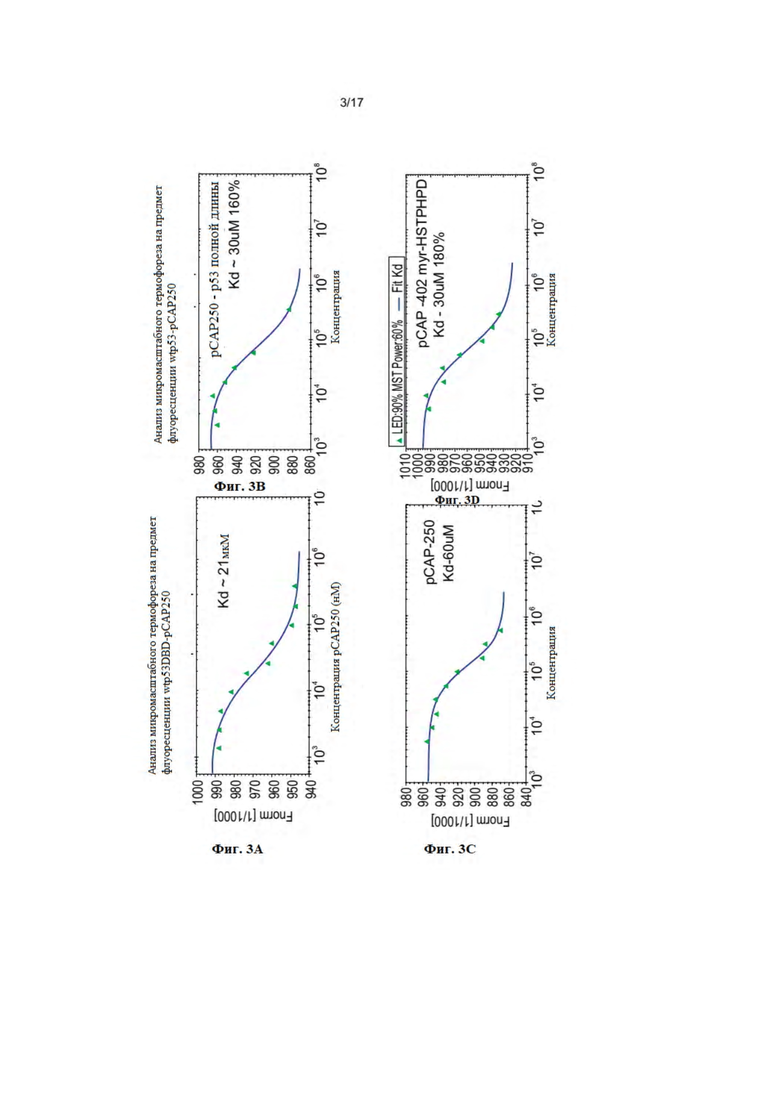

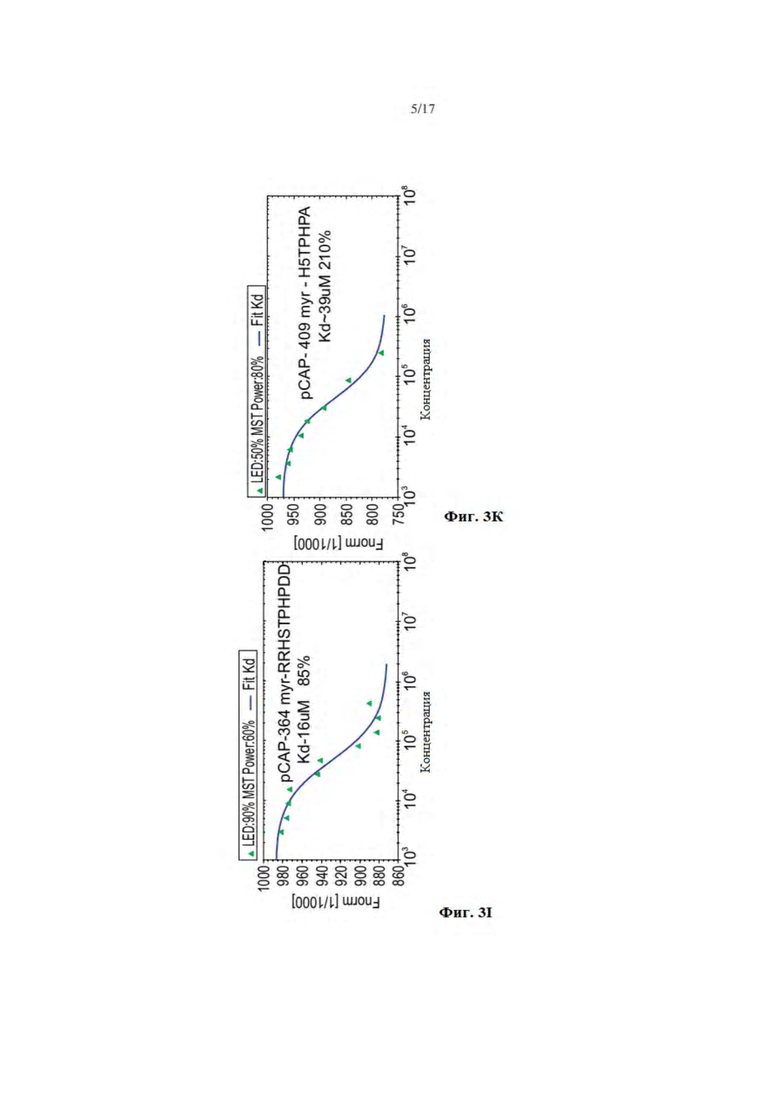
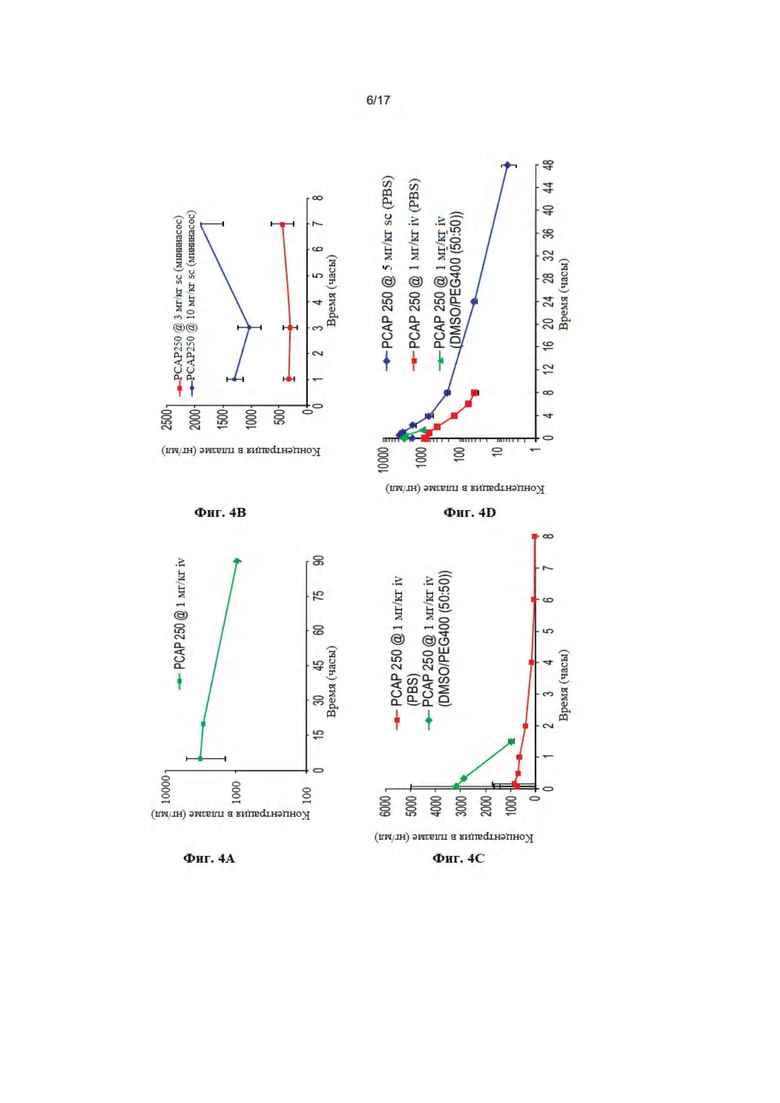

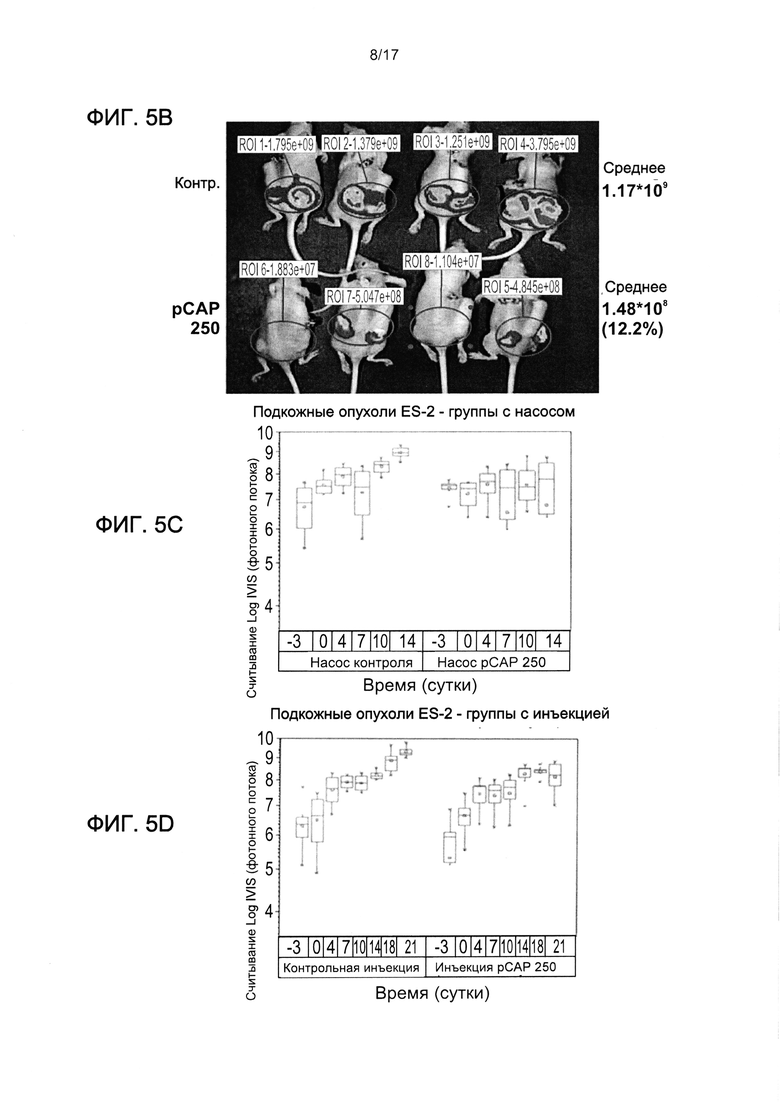




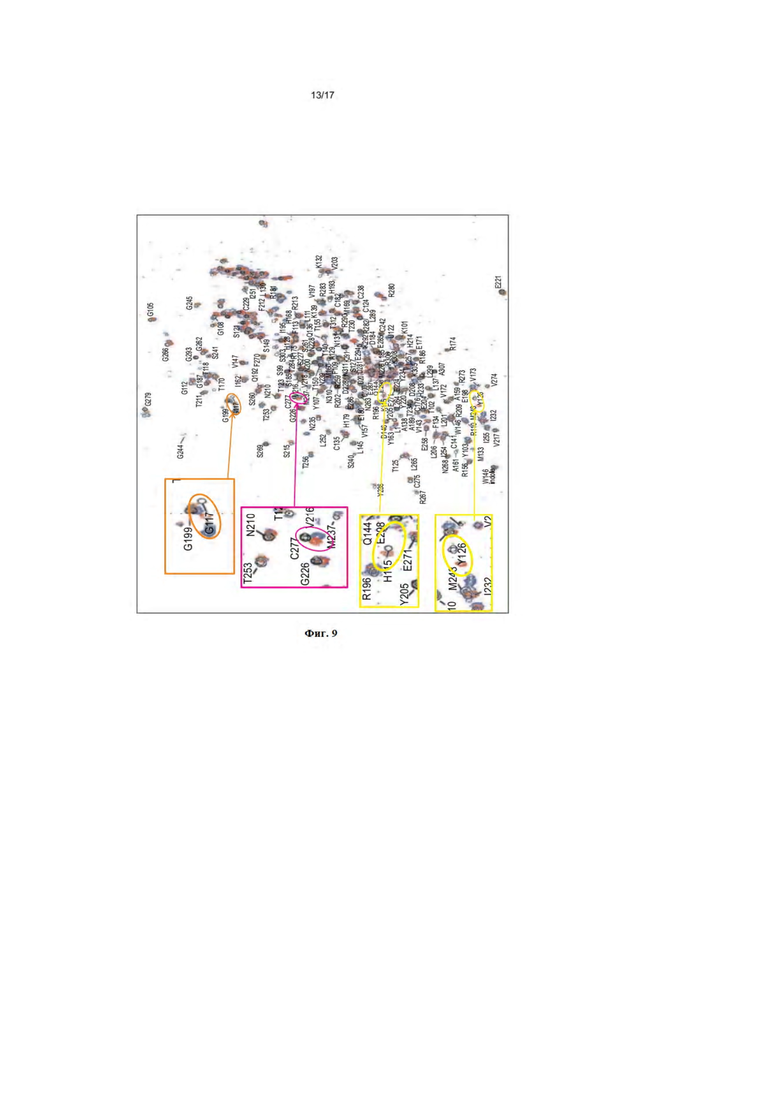




Изобретение относится к области биотехнологии, конкретно к получению пептидов, связывающихся с мутантным белком p53, и может быть использовано в медицине. Полученные пептиды с SEQ ID NO: 426, 427, 429-431, 446, 448, 449, 452-455 457-464 индуцируют проявление белком Mut-p53 p53-селективного ингибирования клеток злокачественной опухоли, экспрессирующих мутантный белок p53, и могут быть использованы для эффективной терапии злокачественных опухолей, вызванных мутантным белком p53. 4 н. и 8 з.п. ф-лы, 14 ил., 3 табл., 7 пр.
1. Выделенный пептид, состоящий из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOs: 426, 427, 429-431, 446, 448, 449, 452-455 и 457-464, при этом указанный пептид связывает мутантный белок p53 и, тем самым, индуцирует проявление мутантным белком p53 p53-селективного ингибирования клеток злокачественной опухоли, экспрессирующих мутантный белок p53.
2. Выделенный пептид по п. 1, выбранный из группы, состоящей из SEQ ID NOs: 426, 427, 429-431 и 446.
3. Выделенный пептид по п. 1, выбранный из группы, состоящей из SEQ ID NOs: 429, 448, 449, 452-455 и 457-464.
4. Применение выделенного пептида по п. 1 для лечения злокачественной опухоли, которая вызывается мутантным белком p53 или ее прогрессирование связано с наличием мутантного белка p53 в клетке или органе.
5. Применение по п. 4, где злокачественная опухоль выбрана из злокачественной опухоли молочной железы, злокачественной опухоли толстой кишки, злокачественной опухоли яичника и злокачественной опухоли легкого.
6. Применение по п. 4, где злокачественная опухоль является метастатической злокачественной опухолью.
7. Применение выделенного пептида в терапевтически эффективном количестве, состоящего из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOs: 426, 427, 429-431, 446, 448, 449, 452-455 и 457-464, при этом указанный пептид связывает мутантный белок p53 и, тем самым, индуцирует проявление мутантным белком p53 p53-селективного ингибирования клеток злокачественной опухоли, экспрессирующих мутантный белок p53, в комбинации с терапевтически эффективным количеством химиотерапии на основе платины для лечения злокачественной опухоли, которая вызывается мутантным белком p53 или ее прогрессирование связано с наличием мутантного белка p53 в клетке или органе.
8. Применение по п. 7, где злокачественная опухоль выбрана из злокачественной опухоли молочной железы, злокачественной опухоли толстой кишки, злокачественной опухоли яичника и злокачественной опухоли легкого.
9. Применение по п. 7, где злокачественная опухоль является метастатической злокачественной опухолью.
10. Применение выделенного пептида в терапевтически эффективном количестве, состоящего из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NOs: 426, 427, 429-431, 446, 448, 449, 452-455 и 457-464, при этом указанный пептид связывает мутантный белок p53 и, тем самым, индуцирует проявление мутантным белком p53 p53-селективного ингибирования клеток злокачественной опухоли, экспрессирующих мутантный белок p53, и при этом указанное терапевтически эффективное количество составляет 0,01-0,3 мг/кг в сутки, для лечения злокачественной опухоли, которая вызывается мутантным белком p53 или ее прогрессирование связано с наличием мутантного белка p53 в клетке или органе.
11. Применение по п. 10, где злокачественная опухоль выбрана из злокачественной опухоли молочной железы, злокачественной опухоли толстой кишки, злокачественной опухоли яичника и злокачественной опухоли легкого.
12. Применение по п. 10, где злокачественная опухоль является метастатической злокачественной опухолью.
| WO 2013036208 A1, 14.03.2013 | |||
| MADHUMALAR A | |||
| et al | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| QIU S | |||
| et al | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| Приспособление для постепенного включения и выключения фрикционных муфт в самодвижущихся экипажах и т.п. | 1919 |
|
SU356A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2021-12-15—Публикация
2017-02-03—Подача