Область техники
Настоящее изобретение относится к моноклональным антителам против FZD10, способам диагностирования связанных с FZD10 заболеваний с использованием такого антитела, способам обнаружения белка FZD10, способам определения лекарственного эффекта после лечения ингибитором FZD10, способам скрининга субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, и диагностическим реактивам, содержащим такое антитело.
Уровень техники
Белки Frizzled представляют собой семейство сопряженных с G-белком рецепторов, которые имеют сайт связывания для белковых лигандов Wnt. В генетических анализах до сих пор идентифицированы 18 генов Wnt и 10 генов Frizzled (от FZD1 до FZD10), и о них известно, что все они обладают высоким структурным сходством.
Белки Frizzled представляют собой семь трансмембранных белков, которые имеют внеклеточный богатый цистеином домен на N-конце. Этот богатый цистеином домен представляет собой сайт связывания для лигандов Wnt. Связывание между лигандам Wnt и рецепторами Frizzled не обязательно происходит один к одному. Обнаружено, что один лиганд Wnt связывается с несколькими рецепторами Frizzled, и множество лигандов Wnt с одним рецептором Frizzled.
Считают, что связывание между лигандом Wnt и рецептором Frizzled активирует путь передачи сигнала Wnt. Существует множество путей передачи сигнала Wnt, которые или активируют путь β-катенина или не затрагивают β-катенин, и полагают, что различные комбинации лиганда Wnt/рецептора Frizzled активируют различные пути.
Путь передачи сигнала Wnt/β-катенина, активируемый при связывании рецептора, опосредован цитоплазматическим белком Dishevelled (Dsh), взаимодействующим непосредственно с рецептором Frizzled, и ведет к цитоплазматической стабилизации и накоплению β-катенина в цитоплазме. В отсутствие сигнала Wnt, β-катенин локализован в цитоплазматическом деградационном комплексе, содержащем белки супрессоров опухоли аденоматозного полипоза толстой кишки (APC) и ауксин. Эти белки выполняют функцию необходимых каркасов для киназы гликогенсинтазы (GSK) 3β для связывания и фосфорилирования β-катенина, чтобы помечать его для деградации через убиквитин-протеасомный путь (патентный документ 1). Показано, что β-катенин-независимый путь участвует во многих процессах, которые включают поляризацию плоских клеток (PCP), которая участвует в регуляции цитоскелетной системы, путь Wnt/Ca2+, участвующий в клеточной моторике и адгезии, и пути, участвующие в регуляции миогенеза через протеинкиназу A. Рецепторы Frizzled могут образовывать димеры, и сообщалось, что эта димеризация вовлечена в активацию пути передачи сигнала Wnt (непатентный документ 1).
Сообщалось о повышающей регуляции мРНК FZD10 (эталонная последовательность: номер доступа Genbank NM_007197.3 (SEQ ID NO: 21)) во многих линиях клеток злокачественных опухолей, включая клеточные линии цервикальной области, пищеварительного тракта и глиобластомы, и приблизительно в 40% первичных злокачественных опухолей желудка и первичных злокачественных опухолей ободочной кишки, и большинстве тканей синовиальной саркомы (патентные документы 1 и 2 и непатентные документы 2 и 3). Примеры заболеваний, связанных со сверхэкспрессией белка FZD10, включают синовиальную саркому, злокачественную опухоль толстой кишки (карциному толстой кишки), злокачественную опухоль желудка, хронический миелолейкоз (CML) и острый миелолейкоз (AML) (патентные документы с 3 до 5). Следовательно, FZD10 считают подходящей мишенью для средств против злокачественных опухолей, и показано, что FZD10-специфическая миРНК подавляет пролиферацию клеток синовиальной саркомы, и показано, что антитела против FZD10 обладают противоопухолевой активностью в модели трансплантации синовиальной саркомы на мышах (патентные документы 3 и 4). Кроме того, можно предсказывать эффективность моноклональных антител против FZD10 в качестве диагностических средств при терапии. В дополнение к успешным случаям клинического применения моноклональных антител, таких как диагностические средства для трастузумаба, ритуксимаба и бевацизумаба против злокачественной опухоли молочной железы, злокачественной лимфомы и злокачественной опухоли ободочной кишки, идет разработка нескольких моноклональных антител против других молекулярных мишеней, и их диагностические эффекты проходят оценку. С точки зрения отбора пациентов, эффективно отвечающих на терапевтические средства, эти диагностические средства предположительно ведут к более эффективной терапии.
Документы известного уровня техники
[Патентные документы]
[Патентный документ 1] WO2007/053577
[Патентный документ 2] WO2004/020668
[Патентный документ 3] WO2005/004912
[Патентный документ 4] WO2006/013733
[Патентный документ 5] WO2007/148417
[Непатентные документы]
[Непатентный документ 1] Charles E. Dann et al., Nature (2001), 412:86-90
[Непатентный документ 2] H. Terasaki et al., Int. J. Mol. Med. (2002) 9, 107-112
[Непатентный документ 3] S. Nagayama et al., Oncogene (2005) 24, 6201-6212
Сущность изобретения
[Проблемы, подлежащие решению с помощью изобретения]
При лечении опухоли с использованием лекарственного средства для молекулярной мишени, для диагностического средства важно обнаруживать белок клетки, который сверхэкспрессирован в основной части целевой опухоли и не экспрессирован или только минимально экспрессирован в нормальных тканях. Однако специфическое высокочувствительное обнаружение белка, экспрессируемого в опухолях является сложным, и антитела против такого белка также сложно получать. Например, для FZD10, который считают мишенью для средств против злокачественной опухоли, коммерчески доступно несколько антител. Однако когда коммерчески доступные антитела, полученные авторами настоящего изобретения, использовали для окрашивания FZD10-экспрессирующих клеток, даже клетки с низкими уровнями экспрессии FZD10 иногда давали положительный сигнал (ложный положительный). Таким образом, встает вопрос о том, что антитела с недостаточной иммунологической специфичностью могут не позволять четко обнаруживать различные уровни экспрессии FZD10 с использованием интенсивности реакции антитела в качестве показателя. Следовательно, цель настоящего изобретения состоит в том, чтобы предоставить антитела, которые связываются с FZD10 со специфичностью и высокой чувствительностью.
[Средство решения проблем]
Соответственно, авторы настоящего изобретения исследовали антитела, которые специфически связывают с FZD10, среди моноклональных антител, полученных посредством иммунизации мышей антигеном FZD10, и преуспели в идентификации конкретного клона антитела, который может специфически связываться с рекомбинантным белком FZD10 человека и может специфически обнаруживать белок FZD10, экспрессируемый в клетках и тканях.
В частности, настоящее изобретение относится к следующему:
[1] антитело или его антигенсвязывающий фрагмент, способные к связыванию с белком FZD10 или его частичным пептид, которые содержат любую или обе из:
вариабельной области тяжелой цепи, содержащей
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 1,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 2, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 3; и
вариабельной области легкой цепи, содержащей
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 4,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 5, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 6;
[2] антитело или его антигенсвязывающий фрагмент по [1], которые содержат одну или обе из вариабельной области тяжелой цепи, содержащей аминокислотную последовательность из SEQ ID NO: 7, и вариабельной области легкой цепи, содержащей аминокислотную последовательность из SEQ ID NO: 8;
[3] антитело или его антигенсвязывающий фрагмент по [1] или [2], которые специфически распознают полипептид, состоящий из аминокислотной последовательности из SEQ ID NO: 9;
[4] антитело или его антигенсвязывающий фрагмент, которые конкурируют с антителом по любому из [1]-[3] за специфическое связывание с FZD10;
[5] антитело или его антигенсвязывающий фрагмент по любому из [1]-[4], которые конъюгируют с аффинной меткой, ферментативной меткой, радиоизотопной меткой или флуоресцентной меткой;
[6] полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по любому из [1]-[5];
[7] реактив для диагностирования связанного с FZD10 заболевания, определения лекарственного эффекта после лечения ингибитором FZD10 или скрининга субъекта, у которого лечение ингибитором FZD10 является высокоэффективным, где реактив содержит антитело или его антигенсвязывающий фрагмент по любому из [1]-[5];
[8] способ диагностирования связанного с FZD10 заболевания или предрасположенности к развитию заболевания у субъекта, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5];
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с контролем, где более высокий уровень белка FZD10, чем контроль, указывает на то, что субъект страдает заболеванием или имеет риск развития заболевания;
[9] реактив по [7] или способ по [8], где связанное с FZD10 заболевание представляет собой злокачественную опухоль, экспрессирующую FZD10;
[10] реактив или способ по [9], где злокачественную опухоль выбирают из группы, состоящей из синовиальной саркомы, злокачественной опухоли легких, злокачественной опухоли пищевода, злокачественной опухоли толстой кишки (карциномы толстой кишки), злокачественной опухоли желудка, хронического миелолейкоза (CML) и острого миелолейкоза (AML);
[11] способ обнаружения белка FZD10 в образце, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5]; и
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом;
[12] способ определения лекарственного эффекта после лечения ингибитором FZD10 у субъекта, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5];
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с уровнем экспрессии перед введением лекарственного средства, где уровень белка FZD10 ниже такового перед введением лекарственного средства указывает на то, что лекарственное средство эффективно у субъекта;
[13] способ скрининга субъекта, у которого лечение ингибитором FZD10 является высокоэффективным, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5];
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с контролем, где уровень белка FZD10, который равен или выше чем контроль, указывает на то, что лечение ингибитором FZD10 является высокоэффективным у субъекта;
[14] способ по любому из [8]-[13], в котором образец представляет собой клетку или ткань, выделенные у субъекта;
[15] способ получения антитела, которое может связываться с белком FZD10 или его частичным пептидом, включающий стадии:
(a) культивирования клетки, содержащей вектор со вставленным полинуклеотидом по [6]; и
(b) сбора антитела из культуры или среды для культивирования клетки.
Настоящее изобретение дополнительно относится к следующему:
[16] способ обнаружения диагностического маркера для связанного с FZD10 заболевания или предрасположенности к развитию заболевания, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5]; и
(b) обнаружения белка FZD10 в образце в качестве маркера посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом;
[17] антитело или его антигенсвязывающий фрагмент по любому из [1]-[5] для использования в диагностировании связанного с FZD10 заболевания или предрасположенности к развитию заболевания;
[18] использование антитела или его антигенсвязывающего фрагмента по любому из [1]-[5] при изготовлении реактива для диагностирования связанного с FZD10 заболевания или предрасположенности к развитию заболевания;
[19] способ обнаружения маркера лекарственного эффекта для ингибитора FZD10, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5]; и
(b) обнаружения белка FZD10 в образце в качестве маркера посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом;
[20] антитело или его антигенсвязывающий фрагмент по любому из [1]-[5] для использования при определении лекарственного эффекта после лечения ингибитором FZD10;
[21] использование антитела или его антигенсвязывающего фрагмента по любому из [1]-[5] при изготовлении реактива для определения лекарственного эффекта после лечения ингибитором FZD10;
[22] способ обнаружения маркера восприимчивости к лечению ингибитором FZD10, включающий стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из [1]-[5]; и
(b) обнаружения белка FZD10 в образце в качестве маркера посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом;
[23] антитело или его антигенсвязывающий фрагмент по любому из [1]-[5], которые служат для использования в скрининге субъекта, у которого лечение ингибитором FZD10 является высокоэффективным; и
[24] использование антитела или его антигенсвязывающего фрагмента по любому из [1]-[5] при изготовлении реактива для скрининга субъекта, у которого лечение ингибитором FZD10 является высокоэффективным.
В дополнение к приведенному выше, другие цели и признаки настоящего изобретения будут более полно видны из следующего подробного описания при прочтении в сочетании с сопроводительными фиг. и примерами. Однако следует понимать, что как вышеуказанное краткое изложение настоящего изобретения, так и нижеследующее подробное описание являются образцовыми вариантами осуществления и не ограничивают настоящее изобретение или другие альтернативные варианты осуществления настоящего изобретения. В частности, хотя настоящее изобретение описано в настоящем описании со ссылкой на многие конкретные варианты осуществления, следует принимать во внимание, что описание является иллюстрацией к настоящему изобретению, и его не создавали в качестве ограничения настоящего изобретения. Различные модификации и применения могут приходить на ум специалистам в данной области, не отступая от сущности и объема настоящего изобретения, как описано с помощью приложенной формулы изобретения. Аналогичным образом, другие цели, признаки, эффекты и преимущества настоящего изобретения будут видны из этого краткого изложения и определенных вариантов осуществления, описанных далее, и будут без труда видны специалистам в данной области. Такие цели, признаки, эффекты и преимущества будут видны из указанного выше в сочетании с сопроводительными примерами, данными, фиг. и всеми обоснованными выводами, проистекающими из них, отдельно или при рассмотрении источников, включенных в настоящее описание.
[Краткое описание фигур]
На фиг. 1 представлена экспрессия мРНК FZD10 в клеточных линиях злокачественных опухолей каждого типа в Cancer Cell Line Encyclopedia (CCLE), которая представляет собой базу данных об анализах экспрессии мРНК с использованием клеточных линий злокачественных опухолей каждого типа.
На фиг. 2 представлен набор микрофотографий, показывающих специфичность антитела против FZD10 (10A8H4G4) при иммуногистохимическом окрашивании с использованием клеточной линии, принудительно экспрессировавшей FZD10. В результате иммуногистохимического окрашивания антителом против FZD10 (10A8H4G4), специфическое окрашивание наблюдали на парафиновом срезе, полученном из клеточной линии с принудительной экспрессией FZD10 (FZD10/DLD1), но окрашивание не наблюдали в клеточной линии, в которую вводили пустой вектор (Mock/DLD1) в качестве отрицательного контроля. С другой стороны, в результате иммуногистохимического окрашивания с использованием коммерчески доступных антител (FZD10(L164)Ab и FZD10PolyclonalAb), окрашивание наблюдали как в FZD10/DLD1, так и в Mock/DLD1. Это раскрывало специфичность антитела против FZD10 (10A8H4G4) по сравнению с коммерчески доступными антителами. Кроме того, график под фотографиями показывает долю (%) FZD10-положительных клеток от числа клеток с принудительной экспрессией, которую вычисляли по результату иммуногистохимического окрашивания.
На фиг. 3 представлена корреляция между экспрессией, которую анализировали посредством проточной цитометрии и посредством иммуногистохимического окрашивания с использованием различных клеточных линий с различными уровнями экспрессии FZD10. A: гистограммы, показывающие результаты проточной цитометрии с использованием 10A8H4G4, которое обнаруживало экспрессию FZD10 на клеточной мембране каждой клеточной линии. SYO-1, T.T и H727 представляли собой клеточные линии, экспрессирующие FZD10, и LoVo представляла собой клеточную линию не экспрессирующую FZD10. B: микрофотографии, показывающие результаты иммуногистохимического окрашивания с использованием парафиновых срезов, полученных из каждой клеточной линии. График под фотографиями показывает долю (%) FZD10-положительных клеток в каждой клеточной линии, которую вычисляли по результату иммуногистохимического окрашивания. Окрашивание наблюдали в FZD10-экспрессирующих клеточных линиях, таких как SYO-1, T.T и H727, но не в LoVo (клеточная линия без экспрессии). Анализы с использованием клеточных линий раскрывали специфичность антитела против FZD10 (10A8H4G4) при иммуногистохимическом окрашивании.
На фиг. 4 представлена корреляция между экспрессией, которую анализировали посредством иммуногистохимического окрашивания и посредством ПЦР в реальном времени с использованием парафиновых срезов, полученных из ксенотрансплантатных опухолей мыши из клеточных линий SYO-1 и COLO201 и образцов клинических злокачественных опухолей легких от 1 до 6. A: при иммуногистохимическом окрашивании с использованием антитела против FZD10 по настоящему изобретению (10A8H4G4), обнаруживали, что SYO-1 и образец 5 являлись FZD10-положительными. С другой стороны, имело место небольшое окрашивание в образцах с низкой экспрессией. B: доля FZD10-положительных клеток среди опухолевых клеток, которую вычисляли по результатам иммуногистохимического окрашивания с A, представлена в виде графика. C: анализы экспрессии тех же случаев посредством ПЦР в реальном времени давали результаты, которые коррелировали с иммуногистохимическим окрашиванием. Анализы с использованием клинических образцов раскрывали высокую специфичность антитела против FZD10 по настоящему изобретению (10A8H4G4) при иммуногистохимическом окрашивании.
[Описание вариантов осуществления]
Несмотря на то что любые способы и материалы, подобные или эквивалентные тем, что описаны в настоящем описании, можно использовать при практической реализации или тестировании вариантов осуществления настоящего изобретения, предпочтительные способы, устройства и материалы описаны далее. Однако прежде, чем будут описаны данные материалы и способы, следует понимать, что настоящее изобретение не ограничено конкретными размерами, геометрическими формами, измерениями, материалами, приемами, протоколами и т. д., описанными в настоящем описании, поскольку они могут варьировать в соответствии со стандартными экспериментами и оптимизацией. Также следует понимать, что терминология, используемая в описании, служит лишь цели описания конкретных версий или вариантов осуществления, и не предназначена для ограничения объема настоящего изобретения, который ограничен только приложенной формулой изобретения.
Настоящее изобретение предусматривает моноклональные антитела против FZD10, которые могут специфически связываться с белком FZD10 или его частичным пептидом. Настоящее изобретение предоставляет доказательство того, что моноклональное антитело против FZD10 по настоящему изобретению обладает высокой специфичностью при обнаружении белка FZD10 при иммуногистохимическом окрашивании.
Антитело против FZD10 (10A8H4G4) по настоящему изобретению имеет по меньшей мере следующие аминокислотные последовательности в вариабельных областях:
10A8H4G4, аминокислотная последовательность вариабельной области тяжелой цепи (за исключением сигнальной последовательности):
QVTLKESGPGILQPSQTLSLTCSFSGFSLSTSGLGVSWIRQPSGKGLEWLAHIYWDDDKRYNPSLKSRLTISKDTSSNQVFLKITSVDTADTATYYCARRAYYGNYYALDYWGQGTSVTVSS (SEQ ID NO: 7);
10A8H4G4, аминокислотная последовательность вариабельной области легкой цепи (за исключением сигнальной последовательности): DIVMTQSPSSLTVTAGEKVTMSCKSSQSLLNSGNQKNYLTWYQQKPGQPPKLLIYWASTRKSGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCQNDYSYPVTFGAGTKLELKRAD (SEQ ID NO: 8).
Антитела по настоящему изобретению можно получать рекомбинантными способами с использованием ДНК, которая кодирует указанные выше аминокислотные последовательности.
Антитела по настоящему изобретению получали посредством скрининга и отбора антител, связывающих FZD10, посредством ELISA среди множества антителопродуцирующих гибридом, полученных путем иммунизации мышей. Антитела, отобранные посредством ELISA, подвергали дальнейшему отбору посредством иммунологического окрашивания. Отбирали антитела, с помощью которых клетки с принудительной экспрессией (положительные контрольные клетки) показывали в качестве положительных и отрицательные контрольные клетки в качестве отрицательных. Среди этих отобранных антител, дополнительно отбирали те, с помощью которых эндогенные FZD10-экспрессирующие клетки (положительные контрольные клетки) показывали в качестве положительных и отрицательные контрольные клетки в качестве отрицательных. Если взаимодействие с FZD10 не является очень сильным, антитела, обладающие низкой способностью к связыванию, будут вести себя приблизительно как фон. Следовательно, скрининг осуществляли посредством иммунологического окрашивания с использованием клеточной линии, у которой предварительно определяли уровень экспрессии эндогенного FZD10. Таким образом, успешно отбирали антитело, представляющее интерес, которое обладает высокой способностью к связыванию с FZD10.
Антитела по настоящему изобретению специфически связываются с FZD10. Следовательно, антитела по настоящему изобретению можно использовать в качестве инструментов для обнаружения FZD10 или FZD10-экспрессирующих клеток или тканей. Кроме того, антитела по настоящему изобретению можно конъюгировать с меткой, которую можно использовать для того, чтобы обнаруживать антитела, и такие меченные антитела более предпочтительны для обнаружения FZD10-экспрессирующих клеток злокачественной опухоли или тканей злокачественной опухоли, например, злокачественной опухоли толстой кишки. Метка, подлежащая конъюгации с антителами по настоящему изобретению, может представлять собой любую метку до тех пор, пока она может обнаруживать антитело, связанное с FZD10, и включает аффинные метки (например, биотин и авидин), ферментативные метки (например, пероксидазу хрена и щелочную фосфатазу) и флуоресцентные метки (например, FITC и родамин).
Когда антитела по настоящему изобретению используют в качестве диагностических средств для того, чтобы выбирать пациентов для терапии злокачественной опухоли, антитела по настоящему изобретению можно использовать непосредственно или получать в виде композиции, подходящей для различных типов использования.
I. Определения
Формы единственного числа, как используют в настоящем описании, подразумевают «по меньшей мере один», пока иное не указано конкретно.
Термины «выделенное» и «очищенное», используемые в отношении вещества (например, пептида, антитела, полинуклеотида или т. п.), указывают на то, что вещество по существу не содержит по меньшей мере одно вещество, которое может содержаться в природном источнике. Таким образом, выделенное или очищенное антитело относится к антителу, которое по существу не содержит другой клеточный материал, например, углевод, липид и другие контаминирующие белки из клеточного или тканевого источника, из которого происходит антитело. В предпочтительном варианте осуществления антитела по настоящему изобретению являются выделенными или очищенными.
Термины «полипептид» и «белок» используют взаимозаменяемо в настоящем описании, и они относятся к полимерам аминокислотных остатков. Эти термины применят ко встречаемым в природе аминокислотным полимерам, а также к не встречаемым в природе аминокислотным полимерам, содержащим один или несколько не встречаемых в природе аминокислотных остатков. Не встречаемые в природе аминокислоты включают аналоги аминокислот, миметики аминокислот и т. п.
Термины «полинуклеотид», «олигонуклеотид» и «нуклеиновая кислота» используют взаимозаменяемо в настоящем описании, и они относятся к полимеру нуклеотидов.
Если не указано иное, термин «связанное с FZD10 заболевание» обозначает злокачественную опухоль, экспрессирующую FZD10.
Если не указано иное, термин «злокачественная опухоль» относится к злокачественной опухоли, экспрессирующей FZD10, и предпочтительно к злокачественной опухоли, чрезмерно экспрессирующей ген FZD10, и ее примеры включают, но не ограничиваясь этим, синовиальную саркому, злокачественную опухоль легких, злокачественную опухоль пищевода, злокачественную опухоль толстой кишки (карциному толстой кишки), злокачественную опухоль желудка, хронический миелолейкоз (CML) и острый миелолейкоз (AML). Например, возможно узнавать, какие клетки злокачественной опухоли экспрессируют FZD10, используя Cancer Cell Line Encyclopedia (CCLE), которая представляет собой базу данных об анализах экспрессии мРНК, используя клеточные линии злокачественных опухолей каждого типа. В настоящей заявке также обнаружена выдающаяся повышающая регуляция в злокачественной опухоли легких, злокачественной опухоли пищевода и злокачественной опухоли толстой кишки (карциноме толстой кишки) (фиг. 1).
Термин «антитело», как используют в настоящем описании, предназначен включать иммуноглобулины и их фрагменты, которые обладают специфической реактивностью к обозначенному белку или его пептиду. Антитело может включать антитела, слитые с другими белками или метками, и фрагменты антител. Кроме того, антитело в настоящем описании используют в самом широком смысле, и оно в частности охватывает интактные моноклональные антитела, поликлональные антитела, полиспецифические антитела (например, биспецифические антитела), образованные из по меньшей мере двух интактных антител, и фрагменты антител, при условии, что они проявляют желательную биологическую активность. «Антитело» обозначает все классы (например, IgA, IgD, IgE, IgG и IgM).
«Фрагменты антител» представляют собой часть интактного антитела, в целом содержат одну или несколько антигенсвязывающих областей или вариабельных областей интактного антитела. Следовательно, в настоящем изобретении, фрагменты антител могут содержать одну или несколько антигенсвязывающих частей интактного антитела. Термин «антигенсвязывающая часть» или «антигенсвязывающий фрагмент» антитела, как используют в настоящем описании, относится к одному или нескольким иммунологически активным фрагментам антитела, которые сохраняют способность к специфическому связыванию с антигеном (например, FZD10). Показано, что антигенсвязывающую функцию антитела можно реализовать с помощью фрагментов полноразмерного антитела. Примеры фрагментов антител включают фрагменты Fab, Fab', F(ab')2, и Fv; линейные антитела; и молекулы одноцепочечных антител. Независимо от структуры, фрагмент антитела связывается с тем же антигеном, который распознает интактное антитело. Термин «фрагмент антитела» также включает синтетически или генетически сконструированный полипептид, который связывается с конкретным антигеном, такой как полипептиды, состоящие из вариабельной области легкой цепи, фрагменты «Fv», состоящие из вариабельных областей тяжелых и легких цепей, рекомбинантные одноцепочечные полипептидные молекулы, в которых легкие и тяжелые вариабельные области соединяют пептидным линкером («белки scFv»), и минимальные распознающие единицы, состоящие из аминокислотных остатков, которые имитируют гипервариабельная область.
Если не указано иное, все технические термины и научные термины, используемые в настоящем описании, имеют те же значение, что и термины в обычном понимании специалиста в области, к которой относится настоящее изобретение.
В настоящем изобретении специфическое связывание антитела с белком FZD10 можно оценивать, например, по конкуренции между антителами. В частности, специфичность рассматриваемого антитела можно оценивать с использованием антитела по настоящему изобретению, например, антитела, содержащего вариабельную область тяжелой цепи, содержащую аминокислотную последовательность из SEQ ID NO: 7, и вариабельную область легкой цепи, содержащую аминокислотную последовательность из SEQ ID NO: 8, в качестве эталонного антитела. Репрезентативным эталонным антителом является 10A8H4G4. Если рассматриваемое антитело конкурирует с реакцией антиген-антитело между эталонным антителом и белком FZD10 человека, то можно подтверждать, что рассматриваемое антитело содержит эквивалент специфичности эталонного антитела. Например, возникновение конкуренции между антителами можно определять, если количество связывания эталонного антитела с белком FZD10 в отсутствие рассматриваемого антитела ингибировано на 10%, 20%, 30% или 40% или более предпочтительно на 50% или больше, когда эталонное антитело и белок FZD10 вступают в реакцию в присутствии рассматриваемого антитела. Конкуренцию между антителами можно оценивать с использованием не только белка FZD10, но также его частичного пептида, до тех пор пока эталонное антитело может связываться с ним. Предпочтительный частичный пептид представляет собой пептид N-концевого внеклеточного домена белка FZD10, например, частичный пептид, содержащий аминокислотную последовательность из SEQ ID NO: 9.
II. Получение антител
В настоящем изобретении используют моноклональные антитела против FZD10. Антитела предоставляют с помощью способов, хорошо известных в данной области.
Образцовые приемы для получения антител, которые используют в соответствии с настоящим изобретением, описаны далее.
(i) Моноклональные антитела
Моноклональные антитела получают из популяции по существу гомогенных антител, т. е. отдельные антитела, содержащиеся в популяции, являются идентичными, за исключением возможных встречаемых в природе мутаций, которые могут присутствовать в незначительных количествах. Таким образом, модификатор «моноклональный» указывает на характер антитела как не являющегося смесью дискретных антител.
Например, моноклональные антитела можно создавать с использованием гибридомного способа, впервые описанного в Kohler et al., Nature, 256: 495 (1975), или можно создавать посредством способов с рекомбинантной ДНК (патент США № 4816567).
В гибридомном способе мышь или другое подходящее животное-хозяина, например, хомяка, иммунизируют полипептидом FZD10 (белком FZD10 или его частичным полипептидом) для того, чтобы индуцировать лимфоциты, которые продуцируют или способны продуцировать антитела, которые будут специфически связываться с полипептидами FZD10. Альтернативно, лимфоциты можно иммунизировать полипептидом FZD10 in vitro. Затем лимфоциты можно сливать с миеломными клетками, используя подходящее средство для слияния, такое как полиэтиленгликоль, чтобы формировать гибридомную клетку (Goding, Monoclonal Antibodies: Principles and Practice, стр. 59-103 (Academic Press, 1986)).
Полученные гибридомные клетки высевают и растят в подходящей среде для культивирования, которая предпочтительно содержит одно или несколько веществ, которые ингибируют рост или выживаемость не слитых родительских миеломных клеток. Например, если родительские миеломные клетки не имеют фермент гипоксантингуанинфосфорибозилтрансферазу (HGPRT или HPRT), то среда для культивирования для гибридом обычно может содержать гипоксантин, аминоптерин и тимидин (среда HAT), эти вещества предотвращают рост HGPRT-дефицитных клеток.
Предпочтительные миеломные клетки представляют собой те, которые эффективны для слияния, поддерживают стабильное и на высоком уровне продуцирование антител отобранными антителопродуцирующими клетками и чувствительны к среде, такой как среда HAT. Предпочтительные линии миеломных клеток включают линии миеломы мыши, такие как те, которые происходят из опухолей MOPC-21 и MPC-11 мыши, доступных в Salk Institute Cell Distribution Center, San Diego, California USA, и клетки SP-2 или X63-Ag8-653, доступные в American Type Culture Collection, Manassas, Virginia, USA. Также описаны линии миеломы человека и гетеромиеломных клеток мыши-человека для получения моноклональных антител человека (Kozbor, J. Immunol., 133: 300 1 (1984); Brodeur et al., Monoclonal Antibody Production Techniques and Applications, стр. 51-63 (Marcel Dekker, Inc., New York, 1987)).
Среда для культивирования, в которой растят гибридомные клетки, анализируют на продуцирование моноклональных антител, направленных против антигена. Предпочтительно, специфичность связывания моноклональных антител, продуцируемых гибридомными клетками, определяют посредством иммунопреципитации или посредством анализа связывания in vitro, такого как радиоиммунный анализ (RIA) или твердофазный иммуноферментный анализ (ELISA).
Аффинность связывания моноклонального антитела, например, можно определять с помощью анализа Скетчарда из Munson et al., Anal. Biochem., 107: 220 (1980).
После того как идентифицируют гибридомные клетки, которые продуцируют антитела желаемой специфичности, аффинности и/или активности, клоны можно субклонировать с помощью процедур предельного разведения и растить стандартными способами (Goding, Monoclonal Antibodies: Principles and Practice, стр. 59-103 (Academic Press, 1986)). Подходящие среды для культивирования для этой цели включают, например, среды D-MEM или RPML-1640. Кроме того, гибридомные клетки можно растить in vivo в виде асцитных опухолей в животном.
Моноклональные антитела, секретируемые субклонами, можно очищать до однородности. Например, разделение и очистку антител можно осуществлять в соответствии со способами разделения и способами очистки, используемыми для белков в целом. Например, антитело можно надлежащим образом выделять и отделять от среды для культивирования, асцита или сыворотки крови посредством надлежащего отбора и комбинированного использования колоночной хроматографии, такой как аффинная хроматография, фильтрования, ультрафильтрования, высаливания, диализа, SDS-электрофореза в полиакриламидном геле и электрофореза с изоэлектрическим фокусированием (Antibodies: A Laboratory Manual. Ed Harlow and David Lane, Cold Spring Harbor Laboratory (1988)), но без ограничения этим. Колонку с белком A и колонку с белком G можно использовать в качестве аффинной колонки. Образцовые колонки с белком A, подлежащие использованию, включают, например, Hyper D, POROS и Sepharose F.F. (Pharmacia).
Помимо аффинной хроматографии, образцовая хроматография включает, например, ионообменную хроматографию, гидрофобную хроматографию, гель-фильтрацию, хроматографию с обращенными фазами, адсорбционную хроматографию и т. п. (Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Marshak et al., Cold Spring Harbor Laboratory Press (1996)). Хроматографические процедуры можно осуществлять посредством хроматографии с обращенной фазой, такой как HPLC и FPLC.
ДНК, кодирующая моноклональные антитела, уже выделена и секвенирована с использованием стандартных процедур (например, с использованием олигонуклеотидных зондов, которые способны к специфическому связыванию с генами, кодирующими тяжелые и легкие цепи мышиных антител). Гибридомные клетки служат в качестве предпочтительного источника такой ДНК. После выделения ДНК можно помещать в экспрессирующие векторы, которые затем трансфицируют в клетки-хозяева, такие как клетки E. coli, клетки COS обезьяны, клетки яичника китайского хомяка (CHO) или миеломные клетки, которые иначе не продуцируют белок иммуноглобулина, чтобы добиваться синтеза моноклональных антител в рекомбинантных клетках-хозяевах. Обзорные статьи по рекомбинантной экспрессии ДНК, кодирующей антитело, в бактериях включают Skerra et al., Curr. Opinion in Immunol., 5: 256-262 (1993) и Pluckthun, Immunol. Revs., 130: 151-188 (1992).
Другой способ создания специфических антител или фрагментов антител с реактивностью против FZD10 состоит в скрининге экспрессионных библиотек, кодирующих гены иммуноглобулинов или их частей, которые экспрессированы в бактериях, с использованием белка FZD10 или его частичного пептида. Например, полные фрагменты Fab, области VH и области Fv можно экспрессировать в бактериях с использованием фаговых экспрессионных библиотек. См., например, Ward et al., Nature 341: 544-546 (1989); Huse et al., Science 246: 1275-1281 (1989); и McCafferty et al., Nature 348: 552-554 (1990). Скрининг таких библиотек, например, с использованием пептида FZD10, позволяет идентифицировать фрагменты иммуноглобулинов с реактивностью к FZD10. Альтернативно, мышь SCID-hu (доступную в Genpharm) можно использовать для получения антител или их фрагментов.
В дополнительном варианте осуществления антитела или фрагменты антител можно выделять из фаговых библиотек антител, созданных с использованием приемов, описанных в McCafferty et al., Nature, 348: 552-554 (1990). Clackson et al., Nature, 352: 624-628 (1991) и Marks et al., J MoL BioL, 222: 581-597 (1991), где описано выделение антител мыши и человека, соответственно, с использованием фаговых библиотек. Следующие публикации описывают получения высокоаффинных (в нМ диапазоне) антител человека посредством перетасовки цепей (Marks et al., BioTechnology, 10: 779-783 (1992)), а также комбинаторной инфекции и рекомбинации in vivo в качестве стратегии для конструирования очень больших фаговых библиотек (Waterhouse et al., Nuc. Acids. Res., 21: 2265-2266 (1993)). Таким образом, эти приемы представляют собой жизнеспособные альтернативы для традиционных гибридомных приемов получения моноклональных антител для выделения моноклональных антител.
Настоящее изобретение предусматривает антитела, подходящие для диагностирования связанных с FZD10 заболеваний, определения лекарственного эффекта после лечения ингибитором FZD10 и скрининга субъектов, у которых лечение ингибитором FZD10 является высокоэффективным. В настоящем изобретении успешно создан клон моноклонального антитела мыши (10A8H4G4), который может обнаруживать белок FZD10 с высокой специфичностью при иммуногистохимическом окрашивании и проточной цитометрии. Продемонстрировано, что этот клон антитела, когда используют при иммуногистохимическом окрашивании образцов клинических злокачественных опухолей легких, давал положительные результаты в образцах злокачественных опухолей легких, в которых подтверждали экспрессию FZD10 на высоких уровнях посредством ПЦР в реальном времени, но небольшое окрашивание в образцах злокачественных опухолей легких, в которых подтверждали экспрессию FZD10 на низких уровнях посредством ПЦР в реальном времени. Кроме того, тогда как коммерчески доступные антитела против FZD10 окрашивали как образец, полученный из клеточной линии с принудительной экспрессией FZD10, так и образец, полученный из не экспрессирующей FZD10 клеточной линии, было показано, что антитело против FZD10 по настоящему изобретению специфически окрашивает образец, получаемый из клеточной линии с принудительной экспрессией FZD10. Антитела по настоящему изобретению, которые обладают такой высокой антигенной специфичностью, благоприятны при выборе пациентов с высокими уровнями экспрессии FZD10, а также при выборе пациентов, у которых лечение ингибитором FZD10 вероятно эффективно.
Аминокислотные последовательности вариабельной области тяжелой цепи (V область H цепи) и вариабельной области легкой цепи (V область L цепи) клона моноклонального антитела мыши против FZD10 по настоящему изобретению (10A8H4G4) представлены в SEQ ID NO: 7 и 8, соответственно.
Определяющие комплементарность области (CDR), входящие в вариабельную область тяжелой цепи и вариабельную область легкой цепи, можно определять в соответствии со способами, хорошо известными в данной области. Например, способ, описанный Kabat et al. (Kabat E. A. et al. (1991) Sequence of Proteins of Immunological Interest. 5-е изд.) или Chothia et al. (Chothia et al. J. Mol. Biol. (1987) 196; 901-917) в целом используют для определения CDR. CDR 1, 2 и 3 вариабельной области тяжелой цепи клона моноклонального антитела мыши против FZD10 по настоящему изобретению (10A8H4G4), как определяют в соответствии с определением Kabat, приведены в SEQ ID NO: 1, 2 и 3, соответственно, и CDR 1, 2 и 3 вариабельной области легкой цепи этого клона приведены в SEQ ID NO: 4, 5 и 6, соответственно.
Следовательно, настоящее изобретение предусматривает антитела или их антигенсвязывающие фрагменты, способные к связыванию с белком FZD10 или его частичным пептидом, которые содержат одну или обе из вариабельной области тяжелой цепи и вариабельной области легкой цепи, где вариабельная область тяжелой цепи содержит:
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 1,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 2, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 3;
и вариабельная область легкой цепи содержит:
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 4,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 5, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 6.
В настоящем изобретении, частичный пептид белка FZD10, с которым связываются антитела по настоящему изобретению, предпочтительно представляет собой пептид N-концевого внеклеточного домена белка FZD10, который, например, состоит из аминокислотной последовательности, которая содержит аминокислотную последовательность (SEQ ID NO: 9), соответствующую положениям с 21 до 161 белка FZD10 (SEQ ID NO: 22), и которую выбирают из SEQ ID NO: 22. Более предпочтительно, частичный пептид белка FZD10 в настоящем изобретении может состоять из аминокислотной последовательности из SEQ ID NO: 9.
Пример указанной выше вариабельной области тяжелой цепи, содержащей «CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 1; CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 2; и CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 3», представляет собой вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность из SEQ ID NO: 7. Пример указанной выше вариабельной области легкой цепи, содержащей «CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 4; CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 5; и CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 6», представляет собой вариабельную область легкой цепи, содержащую аминокислотную последовательность из SEQ ID NO: 8.
Следовательно, в одном из вариантов осуществления настоящее изобретение предусматривает антитела или их антигенсвязывающие фрагменты, которые содержат одну или обе из вариабельной области тяжелой цепи, содержащей аминокислотную последовательность из SEQ ID NO: 7, и вариабельной области легкой цепи, содержащей аминокислотную последовательность из SEQ ID NO: 8.
Антитела по настоящему изобретению можно получать стандартными способами. Например, антитело можно получать посредством встраивания полинуклеотида, кодирующего полипептид антитела, в подходящий вектор, введения вектора в организм-хозяин и получения антитела из организма-хозяина в соответствии со стандартными приемами генетической рекомбинации (см., например, Vandamme, A. M. et al., Eur. J. Biochem. (1990) 192, 767-75).
Последовательности нуклеиновой кислоты полинуклеотидов, кодирующих вариабельные области (V области) антител по настоящему изобретению, можно выводить из аминокислотных последовательностей V областей антител по настоящему изобретению. Например, последовательности нуклеиновой кислоты, представленные SEQ ID NO: 10 и 11, можно использовать в качестве последовательностей нуклеиновой кислоты, кодирующих вариабельную область тяжелой цепи (VH) и вариабельную область легкой цепи (VL), соответственно, клона антитела по настоящему изобретению. Полинуклеотид, кодирующий V область антител по настоящему изобретению, можно синтезировать на основе информации о последовательности стандартными способами, такими как твердофазные приемы (Beaucage SL & Iyer RP, Tetrahedron (1992) 48, 2223-311; Matthes et al., EMBO J (1984) 3, 801-5) и приемы синтеза олигонуклеотидов (Jones et al. Nature (1986) 321, 522-5).
Полинуклеотид, кодирующий V область антитела, встраивают в экспрессирующий вектор, содержащий полинуклеотид, кодирующий константную (C) область антитела.
Для получения антитела, используемого в настоящем изобретении, полинуклеотид, кодирующий антитело (ген антитела), встраивают в экспрессирующий вектор с тем, чтобы ген антитела можно было экспрессировать под управлением управляющих экспрессией элементов (например, энхансера, промотора). Клетку-хозяина трансформируют экспрессирующим вектором, чтобы экспрессировать антитело.
При экспрессии гена антитела, полинуклеотид, кодирующий H цепь, и полинуклеотид, кодирующий L цепь антитела, можно встраивать в отдельные экспрессирующие векторы и затем клетку-хозяина совместно трансформируют получаемыми рекомбинантными экспрессирующими векторами. Альтернативно, как полинуклеотид, кодирующий H цепь, так и полинуклеотид, кодирующий L цепь антитела, можно встраивать вместе в один экспрессирующий вектор, и затем клетку-хозяина трансформируют получаемым рекомбинантным экспрессирующим вектором (например, WO 94/11523).
Ген антитела можно экспрессировать известными способами. Для экспрессии в клетке млекопитающего можно функционально связывать стандартный эффективный промотор, ген антитела, подлежащий экспрессии, и сигнал поли(A) (расположенный по направлению считывания ниже 3'-конца гена антитела). Например, в качестве системы эффективного промотора/энхансера, можно использовать систему предраннего промотора/энхансера цитомегаловируса человека.
Другие системы промоторов/энхансеров, например, те, которые происходят из вирусов (например, ретровируса, вируса полиомы, аденовируса и вируса обезьян 40 (SV40)), и те, которые происходят из клеток млекопитающих (например, фактор элонгации 1α человека (HEF1α)), также можно использовать для экспрессии антитела в настоящем изобретении.
Когда используют систему промотора/энхансера SV40, экспрессию гена можно осуществлять без труда способом из Mulligan et al. (Nature (1979) 277, 108-14). Когда используют систему промотора/энхансера HEF1α, экспрессию гена можно осуществлять без труда способом из Mizushima et al. (Nucleic Acids Res. (1990) 18, 5322).
Для экспрессии в E. coli можно функционально связывать стандартный эффективный промотор, сигнальную последовательность для секреции антитела, представляющего интерес, и ген антитела. В качестве промотора можно использовать промотор lacZ или промотор araB. Когда используют промотор lacZ, экспрессию гена можно осуществлять с помощью способа из Ward et al. (Nature (1098) 341, 544-6.; FASBE J. (1992) 6, 2422-7.), тогда как при использовании промотора araB экспрессию гена можно осуществлять с помощью способа из Better et al. (Science (1988) 240, 1041-3.).
В отношении сигнальной последовательности для секреции антитела, когда антитело, представляющее интерес, предназначено для секреции в периплазматическое пространство E. coli, можно использовать сигнальную последовательность pelB (Lei, S.P. et al, J. Bacteriol. (1987) 169, 4379-83.). Антитело, секретируемое в периплазматическое пространство, выделают и затем осуществляют его повторную укладку с тем, чтобы антитело принимало подходящую конфигурацию.
Можно использовать сайт начала репликации, происходящий из вирусов (например, SV40, вируса полиомы, аденовируса, вирус папилломы крупного рогатого скота (BPV)), или тому подобное. Для того чтобы увеличивать число копий гена в системе клетки-хозяина, экспрессирующий вектор дополнительно может содержать ген селективного маркера, такой как ген аминогликозидфосфотрансферазы (APH), ген тимидинкиназы (TK), ген ксантингуанинфосфорибозилтрансферазы E. coli (Ecogpt) и ген дигидрофолатредуктазы (dhfr). Для получения антитела, используемого в настоящем изобретении, можно использовать любую экспрессирующую систему, включающую эукариотические и прокариотические клеточные системы. Эукариотическая клетка включает стабильные клеточные линии животных (например, млекопитающих, насекомых, плесени и грибов, дрожжей). Прокариотическая клетка включает бактериальные клетки, такие как клетки E. coli. Предпочтительно антитело, используемое в настоящем изобретении, экспрессируют в клетке млекопитающего, такой как клетка CHO, COS, миелома, BHK, Vero и HeLa.
Затем трансформированную клетку-хозяина культивируют in vitro или in vivo для получения антитела, представляющего интерес. Культивирование клетки-хозяина можно осуществлять любым известным способом. Можно использовать среду для культивирования, которая в настоящем описании может представлять собой среду DMEM, MEM, RPMI-1640 или IMDM. Среда для культивирования может содержать добавку сыворотки, такой как эмбриональная телячья сыворотка (FCS).
При получении рекомбинантного антитела, помимо указанных выше клеток-хозяев, трансгенное животное также можно использовать в качестве организма-хозяина. Например, ген антитела вставляют в предварительно определяемый сайт гена, кодирующего белок, неотъемлемо продуцируемый с молоком животного (например, β-казеин), чтобы получать слитый ген. Фрагмент ДНК, содержащий слитый ген со введенным геном антитела инъецируют в зародыш не относящегося к человеку животного, и затем зародыш вводят в самку животного. Самка животного, имеющая зародыш в себе, вынашивает трансгенное не относящееся к человеку животное. Происходит секреция антитела, представляющего интерес, в молоко от трансгенного не относящегося к человеку животного или его потомства. С целью увеличения количества антителосодержащего молока, трансгенному животному можно вводить подходящий гормон (Ebert, K.M. et al, Bio/Technology (1994) 12, 699-702).
Антитело, которое экспрессируют и получают, как описано выше, можно выделять из клеток или организма животного-хозяина и очищать. Выделение и очистку антитела, используемого в настоящем изобретении, можно осуществлять на аффинной колонке. Также можно использовать другие способы, стандартно используемые для выделения и очистки антител; таким образом, способ конкретно не ограничен. Например, различную хроматографию, фильтрование, ультрафильтрование, высаливание и диализ можно использовать по отдельности или в комбинации для того, чтобы выделять и очищать антитело, представляющее интерес (Antibodies A Laboratory Manual. Ed. Harlow, David Lane, Cold Spring Harbor Laboratory, 1988).
(ii) Фрагменты антител
Разработаны различные приемы для получения фрагментов антител. Стандартно эти фрагменты традиционно получали через протеолитическое расщепление интактных антител (см., например, Morimoto et al., Journal of Biochemical and Biophysical Methods 24: 107-117 (1992); и Brennan et al., Science, 229: 81 (1985)). Однако в настоящее время эти фрагменты можно получать непосредственно с помощью рекомбинантных клеток-хозяев. Например, фрагменты антител можно выделять из фаговой библиотеки антитела. Альтернативно, фрагменты Fab'-SH можно собирать непосредственно из Escherichia coli, а фрагменты F(ab')2 можно формировать посредством химического сопряжения (Carter et al., Bio/Technology 10: 163-167 (1992)). В другом подходе фрагменты F(ab')2 можно выделять непосредственно из клеточной культуры рекомбинантного хозяина. Другие приемы для получения фрагментов антител должны быть ясны специалистам в данной области. В другом варианте осуществления наиболее подходящие антитела представляют собой одноцепочечные Fv фрагменты (scFv). См. WO93/16185; US5571894; и US5587458. Кроме того, фрагменты антител могут представлять собой «линейные антитела», как описано, например, в US5641870. Такие фрагменты линейных антител могут быть моноспецифическими или биспецифическими.
(iii) Меченные антитела
Антитела по настоящему изобретению необязательно конъюгируют с аффинной меткой, ферментативной меткой, радиоизотопной меткой, флуоресцентной меткой или хемилюминесцентной меткой. Например, присутствие метки, которая присутствует и поддается обнаружению в ткани FZD10-экспрессирующей злокачественной опухоли, делает возможным определение присутствия или отсутствия злокачественной опухоли или опухоли у диагностируемого субъекта. Локализация метки в ткани злокачественной опухоли также позволяет определять распространение заболевания.
Метки, подходящие для использования, включают, например, флуоресцентные метки, такие как флуоресцеин и родамин; и ферментативные метки, такие как люцифераза. Поддающиеся обнаружению метки/метки для обнаружения, подлежащие использованию, отбирают в соответствии с используемым способом визуализации. Конъюгаты между такими метками и антителами можно получать с использованием протоколами и приемами, известными в данной области. В настоящем изобретении, антитела по настоящему изобретению можно конъюгировать с желаемой меткой непосредственно перед использованием, или можно предоставлять в виде конъюгированных с меткой антител.
Конъюгаты между антителами и метками можно получать с использованием различных бифункциональных средств для сопряжения с белком, таких как N-сукцинимидил-3-(2-пириилдитриол)пропионат (SPDP), сукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат, иминотиолан (IT), бифункциональные производные имидоэфира (такие как диметиладипимидат HCL), активные сложные эфиры (такие как дисукцинимидилсуберат), альдегиды (такие как глутаральдегид), бис-азидосоединения (такие как бис(п-азидобензоил)гександиамин), производные бис-диазония (такие как бис-(п-диазонийбензоил)-этилендиамин), диизоцианаты (такие как толуол-2,6-диизоцианат) и бис-активные соединения фтора (такие как 1,5-дифтор-2,4-динитробензол). Альтернативно, слитые белки, содержащие антитело и метку, можно получать, например, посредством приемов рекомбинации или синтеза пептидов. Подходящие примеры таких слитых белков включают слитые белки, сформированные между антителом и метящим белком, таким как ECFP, EYFP или EGFP.
III. Диагностирование связанных с FZD10 заболеваний, скрининг субъектов, у которых лечение ингибитором FZD10 является высокоэффективным (диагностирование перед лечением), или определении лекарственного эффекта после лечения ингибитором FZD10 (диагностирование после лечения)
FZD10 можно использовать в качестве диагностического маркера для связанных с FZD10 заболеванием и в качестве маркера для оценки восприимчивости к ингибиторам FZD10 и лекарственного эффекта ингибиторов у субъектов, которые страдают заболеваниями. Следовательно, антитела по настоящему изобретению можно использовать в качестве реактивов для обнаружения маркера, чтобы диагностировать связанные с FZD10 заболевания, такие как злокачественная опухоль, осуществлять скрининг субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, или определять лекарственный эффект после лечения ингибитором FZD10.
Более конкретно, антитела по настоящему изобретению можно использовать для того, чтобы обнаруживать белок FZD10 в образцах, выделенных у субъектов, и диагностировать связанные с FZD10 заболевания, осуществлять скрининг субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, или определять лекарственный эффект после лечения ингибитором FZD10. Следовательно, настоящее изобретение предусматривает способы диагностирования связанных с FZD10 заболеваний или предрасположенностей к развитию таких заболеваний у субъектов, способы скрининга субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, и способы определения лекарственного эффекта после лечения ингибитором FZD10, которые осуществляют посредством обнаружения белка FZD10 в образцах, выделенных у субъектов, с использованием антитела по настоящему изобретению. Эти способы включают следующие стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по настоящему изобретению;
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с контролем.
В типичном варианте осуществления, образец представляет собой клетку или ткань, выделенную у указанного выше субъекта, и предпочтительно представляет собой ткань, выделенную у субъекта. Следовательно, обычно, все способы по настоящему изобретению осуществляют in vitro на образцах, выделенных у субъектов. Известны способы выделения тканей и клеток у субъектов с помощью таких приемов, как биопсия и взятие крови. Альтернативно также можно использовать биологические образцы, удаленные у субъектов через медицинские процедуры для терапии (такие как хирургическая операция). Клетки и ткани, выделенные у субъектов, можно обрабатывать надлежащим образом перед приведением в контакт с антителами. Например, в целом, образцы тканей, получаемые у субъектов, замораживают, делают срезы и затем фиксируют спиртом, формалином и т. п. для того, чтобы получать образцы для иммуногистологического анализа. Альтернативно образцы тканей, культивируемые клетки и т. п. можно фиксировать формалином и т. п. и затем заливать парафином, чтобы получать срезы для иммуногистологического анализа.
Связывание антитела или его антигенсвязывающего фрагмента по настоящему изобретению с образцом или, более конкретно, с антигенным белком в образце можно обнаруживать способами, известными специалистам в данной области. Более конкретно, после приведения антитела по настоящему изобретению в контакт с указанным выше образцом, антитело, не связанное с FZD10 в образце, удаляют посредством промывания, и затем связывание между антителом по настоящему изобретению и белком FZD10 в образце можно обнаруживать посредством обнаружения антитела, остающегося в образце. Поступая так, когда антитело является непосредственно меченным, присутствие антитела по настоящему изобретению, связанного с белком FZD10, можно обнаруживать посредством обнаружения метки. Если метка представляет собой фермент, флуоресцентное вещество, люминесцентное вещество, частицу или т. п., которые поддаются обнаружению, метку можно обнаруживать непосредственно. Кроме того, когда антитело по настоящему изобретению метят аффинным веществом (связывающим веществом), таким как биотин (аффинная метка), присутствие антитела можно захватывать с использованием партнера связывания, такого как меченный авидин. Альтернативно, когда антитело по настоящему изобретению не является меченным непосредственно, антитело по настоящему изобретению можно обнаруживать с использованием антителосвязывающего реактив. Например, в качестве антителосвязывающего реактива, белок A или антитело против антитела можно метить и использовать для обнаружения антитела.
При диагностировании связанных с FZD10 заболеваний, если уровень белка FZD10 выше контрольного уровня (нормального контрольного уровня, предпочтительно уровня экспрессии белка FZD10 в образце, выделенном у здорового субъекта, который не страдает связанными с FZD10 заболеваниями) на указанной выше стадии (c), это указывает на то, что субъект страдает связанным с FZD10 заболеванием или имеет риск развития заболевания.
Кроме того, при скрининге субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, если уровень белка FZD10 приблизительно равен или превышает контрольный уровень (предпочтительно, уровень экспрессии белка FZD10 в ткани субъекта, у которого диагностировали связанное с FZD10 заболевание) на указанной выше стадии (c), это указывает на то, что лечение ингибитором FZD10 является высокоэффективным у субъекта.
С другой стороны, при определении лекарственного эффекта после лечения ингибитором FZD10, если уровень белка FZD10 ниже контрольного уровня (предпочтительно уровня экспрессии белка FZD10 в образце, выделенному у субъекта перед введением лекарственного средства) на указанной выше стадии (c), это указывает на то, что лекарственное средство эффективно у субъекта.
Пациенты, у которых продемонстрировано наличие связанного с FZD10 заболевания в соответствии с диагностическим способом по настоящему изобретению, способны стать субъектами лечения ингибитором FZD10. Следовательно, после диагностического способа по настоящему изобретению, ингибитор FZD10 можно вводить пациентам, у которых продемонстрировано наличие связанного с FZD10 заболевания. Альтернативно, после скрининга, ингибитор FZD10 также можно вводить пациентам, у которых продемонстрировано, что лечение ингибитором FZD10 способно быть высокоэффективным. Кроме того, если продемонстрировано, что ингибитор FZD10 имеет терапевтический эффект у пациента, которому вводили ингибитор FZD10, введение ингибитора FZD10 тому же пациенту можно продолжать.
Таким образом, настоящее изобретение относится к способам лечения связанных с FZD10 заболеваний, которые включают идентификацию какого-либо пациента, выбранного из следующей группы, с помощью способа по настоящему изобретению, и введение ингибитора FZD10 пациенту:
пациент, у которого продемонстрировано наличие связанного с FZD10 заболевания с помощью диагностического способа по настоящему изобретению;
пациент, у которого показано, что лечение ингибитором FZD10 способно быть эффективным; и
пациент, который получал введение ингибитора FZD10, и у которого показано, что ингибитор имеет терапевтический эффект.
В настоящем изобретении, ингибитор FZD10, подлежащий введению пациентам, может представлять собой любое известное соединение. В настоящем описании ингибитор FZD10 также включает антитела, проявляющие цитотоксическую активность против FZD10-экспрессирующих клеток, и двухцепочечные молекулы РНК, которые супрессируют экспрессию FZD10. Примеры таких антител и двухцепочечных молекул РНК представляют собой антитела против FZD10, раскрытые в WO2005/004912 или WO2007/148417, и FZD10-специфическую миРНК, раскрытую в WO2006/013733.
В контексте настоящего изобретения, контрольный уровень, измеряемый в биологическом образце, который заведомо не содержит связанных с FZD10 заболеваний (например, без злокачественных опухолей), называют «нормальным контрольным уровнем». Когда уровень белка FZD10 в образце, выделенном у субъекта, выше нормального контрольного уровня, у субъекта можно диагностировать связанное с FZD10 заболевание, которое следует лечить.
С другой стороны, контрольный уровень, определяемый у биологического образца, заведомого имеющего связанное с FZD10 заболевание (например, злокачественную опухоль), называют «патологическим контрольным уровнем (например, контрольным уровнем злокачественной опухоли)». Когда уровень белка FZD10 в образце, выделенном у субъекта перед лечением ингибитором FZD10, равен или выше патологического контрольного уровня, можно диагностировать, что лечение ингибитором FZD10 является высокоэффективным у субъекта.
Кроме того, когда уровень белка FZD10 в образце, выделенном у субъекта после лечения ингибитором FZD10, ниже патологического контрольного уровня у того же субъекта перед введением лекарственного средства, можно диагностировать, что лечение было эффективным, другими словами, лечение ингибитором FZD10 является высокоэффективным.
В определенном варианте осуществления нормальные клетки (или ткани), получаемые из не пораженной области (например, область не злокачественной опухоли) органа со связанным с FZD10 заболеванием, подлежащим лечению (например, злокачественной опухолью), можно использовать в качестве нормального контроля. В другом варианте осуществления контрольный уровень можно определять статистическим способом на основе результатов, полученных посредством анализа уровня белка FZD10, измеряемого предварительно в образцах, полученных у субъектов, у которых известно состояние заболевания (например, злокачественная опухоль или не злокачественная опухоль). Кроме того, контрольный уровень можно получать из базы данных о профилях экспрессии, получаемых из ранее тестированных образцов (клеток или тканей). Когда образцы, подлежащие оценке, представляют собой образцы ткани, образец, происходящий из той же ткани, предпочтительно используют в качестве контрольного образца.
Кроме того, по одному из аспектов по настоящему изобретению, уровень белка FZD10 в биологическом образце можно сравнивать с множеством контрольных уровней, измеряемых во множестве эталонных образцов. Предпочтительно использовать контрольные уровни, измеряемые в эталонных образцах, извлекаемых из ткани того типа, который схож с типом ткани биологического образца, полученного у субъекта. Кроме того, предпочтительно использовать эталонное значение уровня белка FZD10 в популяции, у которой известно состояние заболевания. Эталонное значение можно получать любым известным в данной области способом. Например, используемое эталонное значение может представлять собой диапазон среднего +/- 2 S.D. или среднего +/- 3 S.D.
Уровень белка FZD10 в образце можно считать высоким, когда уровень, например, на 10%, 25% или 50% выше контрольного уровня или больше в 1,1 раза, больше чем в 1,5 раза, больше чем в 2,0 раза, больше чем в 5,0 раза или больше чем в 10,0 раза выше контрольного уровня или даже выше. Уровень белка FZD10 в образце можно считать низким, когда уровень, например, на 10%, 25% или 50% ниже контрольного уровня или больше чем в 1,1 раза, больше чем в 1,5 раза, больше чем в 2,0 раза, больше чем в 5,0 раза или больше чем в 10,0 раза ниже контрольного уровня или даже ниже.
В типичном варианте осуществления, связанное с FZD10 заболевание представляет собой FZD10-экспрессирующую злокачественную опухоль. FZD10-экспрессирующие злокачественные опухоли представляют собой, например, синовиальную саркому, злокачественную опухоль легких, злокачественную опухоль пищевода, злокачественную опухоль толстой кишки (карциному толстой кишки), злокачественную опухоль желудка, хронический миелолейкоз (CML) и острый миелолейкоз (AML), но не ограничены этим.
В дополнительном варианте осуществления настоящее изобретение предусматривает способы обнаружения диагностического маркера для связанного с FZD10 заболевания или предрасположенности к развитию заболевания, где способы включают обнаружение белка FZD10 в образце в качестве диагностического маркера с использованием антитела или его антигенсвязывающего фрагмента по настоящему изобретению. Показано, что экспрессия FZD10 усилена в клетках злокачественной опухоли определенных типов по сравнению с нормальными тканями. Следовательно, если уровень экспрессии FZD10 можно обнаруживать специфически, это будет полезно в качестве диагностического маркера для связанных с FZD10 заболеваний. В контексте настоящего изобретения, диагностический маркер для связанного с FZD10 заболевания или предрасположенности к развитию заболевания относится к белку FZD10 в образце, выделенном у субъекта, который обнаруживают посредством связывания с антителом или его антигенсвязывающим фрагментом по настоящему изобретению, и он отличается тем, что когда его уровень экспрессии выше контрольного уровня, то демонстрируют, что субъект страдает заболеванием или имеет риск развития заболевания. Здесь указанный выше контрольный уровень представляет собой нормальный контрольный уровень и предпочтительно уровень экспрессии белка FZD10 в образце, выделенном у здорового субъекта, который не страдает связанным с FZD10 заболеванием. В целом, контрольный уровень предпочтительно представляет собой уровень экспрессии в той же ткани, что и ткань, из которой происходят клетки злокачественной опухоли, подвергаемые обнаружению диагностического маркера.
Настоящее изобретение также относится к антителу или его антигенсвязывающему фрагменту по настоящему изобретению для использования в диагностировании связанного с FZD10 заболевания или предрасположенности к развитию заболевания. Альтернативно, настоящее изобретение предусматривает использование антитела или его антигенсвязывающего фрагмента по настоящему изобретению при изготовлении реактива для диагностирования связанного с FZD10 заболевания или предрасположенности к развитию заболевания.
Кроме того, настоящее изобретение предусматривает способы обнаружения маркера для восприимчивости к лечению ингибитором FZD10, где способы включают стадию обнаружения белка FZD10 в образце в качестве маркера восприимчивости, используя антитело или его антигенсвязывающий фрагмент по настоящему изобретению. Показано, что экспрессия FZD10 усилена, в частности, в определенных клетках злокачественной опухоли и рост таких клеток злокачественной опухоли подавляют ингибиторы FZD10 (WO2005/004912, WO2006/013733 и WO2007/148417). То есть, экспрессию FZD10 можно использовать в качестве показателя для предсказания восприимчивости к ингибиторам FZD10. Это обусловлено тем, что, если FZD10 экспрессирован на высоком уровне, то можно ожидать, что ингибиторы FZD10 обладают эффектом ингибирования клеточного роста. Следовательно, если уровень экспрессии FZD10 можно обнаруживать специфически, это будет полезно в качестве маркера для восприимчивости к лечению ингибитором FZD10. В контексте настоящего изобретения, маркер для восприимчивости к лечению ингибитором FZD10 относится к белку FZD10 в образце, выделенном у субъекта, который обнаруживают посредством связывания с антителом или его антигенсвязывающим фрагментом по настоящему изобретению, и отличается тем, что, когда его уровень экспрессии равен или превышает контрольный уровень, показывают, что эффект лечения ингибитором FZD10 будет высоким у субъекта. Здесь указанный выше контрольный уровень предпочтительно представляет собой патологический контрольный уровень, т. е. уровень экспрессии белка FZD10 в образце, выделенном из патологического места у субъекта, который заведомо страдает связанным с FZD10 заболеванием, и особенно предпочтительно представляет собой уровень экспрессии белка FZD10 в образце, выделенном перед лечением у субъекта, у которого лечение ингибитором FZD10 является высокоэффективным.
Настоящее изобретение также относится к антителу или его антигенсвязывающему фрагменту по настоящему изобретению для использования в скрининге субъекта, у которого лечение ингибитором FZD10 является высокоэффективным. Альтернативно, настоящее изобретение предусматривает использование антитела или его антигенсвязывающего фрагмента по настоящему изобретению при изготовлении реактива для скрининга субъекта, у которого лечение ингибитором FZD10 является высокоэффективным.
Настоящее изобретение также относится к способам обнаружения маркера для лекарственного эффекта ингибитора FZD10, где способы включают стадию обнаружения белка FZD10 в образце в качестве маркера лекарственного эффекта с использованием антитела или его антигенсвязывающего фрагмента по настоящему изобретению. Показано, что экспрессия FZD10 усилена, в частности, в определенных клетках злокачественной опухоли, и рост таких клеток злокачественной опухоли супрессируют ингибиторы FZD10 (WO2005/004912, WO2006/013733 и WO2007/148417). Следовательно, ткани злокачественной опухоли, содержащие такие клетки злокачественной опухоли, можно уменьшать или уничтожать с помощью ингибиторов FZD10. То есть, уровень экспрессии FZD10 можно использовать в качестве показателя для того, чтобы оценивать лекарственный эффект ингибиторов FZD10 у субъектов, несущих такие клетки злокачественной опухоли. Это обусловлено тем, что, если уровень экспрессии FZD10 в образце, выделенном из ткани, имеющей FZD10-положительные клетки злокачественной опухоли, снижают по сравнению с уровнем образца, выделенного перед лечением ингибитором FZD10, то можно считать, что ингибитор FZD10 снизил FZD10-положительные клетки злокачественной опухоли. Следовательно, если уровень экспрессии FZD10 можно обнаруживать специфически, это будет полезно в качестве маркера для лекарственного эффекта ингибиторов FZD10. В контексте настоящего изобретения, маркер для лекарственного эффекта ингибиторов FZD10 относится к белку FZD10 в образце, выделенному у субъекта, который получал введение ингибитора FZD10, который обнаруживают посредством связывания с антителом или его антигенсвязывающим фрагментом по настоящему изобретению, и который отличается тем, что когда его уровень экспрессии ниже контрольного уровня, то показывают, что ингибитор FZD10 эффективен у субъекта. Здесь указанный выше контрольный уровень предпочтительно представляет собой уровень экспрессии белка FZD10 в образце, выделенном из патологического места у субъекта перед введением лекарственного средства.
Настоящее изобретение также относится к антителу или его антигенсвязывающему фрагменту по настоящему изобретению для использования при определении лекарственного эффекта после лечения ингибитором FZD10. Альтернативно, настоящее изобретение предусматривает использование антитела или его антигенсвязывающего фрагмента по настоящему изобретению при изготовлении реактива для определения лекарственного эффекта после лечения ингибитором FZD10.
IV. Реактивы или наборы для диагностирования связанных с FZD10 заболеваний, скрининга субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, или определения лекарственного эффекта после лечения ингибитором FZD10
Настоящее изобретение предусматривает реактивы или наборы для диагностирования связанных с FZD10 заболеваний, скрининга субъектов, у которых лечение ингибитором FZD10 является высокоэффективным, или определения лекарственного эффекта после лечения ингибитором FZD10. В частности, эти наборы содержат антитело или его антигенсвязывающий фрагмент по настоящему изобретению в качестве реактива для обнаружения белка FZD10. В одном из вариантов осуществления антитело для диагностического реактива или набора по настоящему изобретению можно метить флуоресцентным веществом, люминесцентным веществом или радиоизотопом. Способы мечения антитела и способы обнаружения меченного антитела хорошо известны в данной области, и любые метку и способ можно использовать для настоящего изобретения.
Данные наборы могут включать комбинацию антитела или его антигенсвязывающего фрагмента по настоящему изобретению и другого реактива для обнаружения маркера. Наборы дополнительно могут включать реактивы положительного и отрицательного контроля для FZD10 и вторичное антитело для обнаружения антитела по настоящему изобретению. Например, культуральные срезы клеточных линий или образцов ткани, которые заведомо высоко экспрессируют FZD10, могут служить в качестве эффективных реактивов положительного контроля. Кроме того, например, образцы ткани, полученные у здоровых субъектов, или ткани не злокачественной опухоли могут служить в качестве эффективных реактивов отрицательного контроля. Вторичное антитело для обнаружения антитела по настоящему изобретению предпочтительно метят флуоресцентным веществом, люминесцентным веществом, радиоизотопом или ферментом. Наборы по настоящему изобретению дополнительно могут включать другие материалы, желательные с точки зрения пользователя или коммерческой точки зрения, в том числе буфер, раствор для разведения, фильтр, иглу, шприц и приложенный документ с инструкциями для использования (например, письменный документ, ленту и CD-ROM). Эти реактивы и т. п. можно содержать в меченном контейнере. Подходящие контейнеры включают бутылки, флаконы и пробирки. Контейнеры можно создавать из различных материалов, таких как стекло или пластмасса.
В настоящем описании приведено подробное объяснение настоящего изобретения со ссылкой на его конкретные варианты осуществления. Однако следует понимать, что приведенное выше объяснение фактически представляет собой иллюстративное и разъясняющее объяснение и предназначено для того, чтобы объяснять настоящее изобретение и его предпочтительные варианты осуществления. Экспериментальным путем специалист в данной области без труда узнает, что в нем можно выполнять различные изменения и модификации, не отступая от сущности и объема настоящего изобретения. Таким образом, настоящее изобретение не ограничено вышеприведенным объяснение, но предполагаемо определено в приложенной формуле изобретения и ее эквивалентах.
Ниже в настоящем описании настоящее изобретение описано более подробно со ссылкой на примеры. Тем не менее, хотя следующие материалы, способ и примеры могут служить для содействия среднему специалисту при выполнении и использовании определенных вариантов осуществления настоящего изобретения, они предназначены только для того, чтобы иллюстрировать аспекты настоящего изобретения и, таким образом, ни коим образом не ограничивают объем настоящего изобретения. Специалист в данной области может использовать способы и материалы, подобные или эквивалентные тем, что описаны в настоящем описании, при практической реализации или тестировании настоящего изобретения.
Все документы известного уровня техники, цитируемые в настоящем описании, включены по ссылке в настоящее описание.
Примеры
Далее настоящее изобретение в частности описано со ссылкой на примеры, но его не следует толковать в качестве ограниченного ими.
[Материалы и способы]
Клеточная культура
Экспрессирующий FZD10 вектор вводили в клеточную линию злокачественной опухоли толстой кишки человека DLD1, приобретенную в ATCC, чтобы получать клеточную линию с принудительной экспрессией FZD10 (FZD10/DLD1). Клеточную линию, в которую вводили пустой вектор (Mock/DLD1), получали в качестве отрицательного контроля. Клеточные линии поддерживали в RPMI-1640 с добавлением 10% эмбриональной телячьей сыворотки (FBS), 1% пенициллина/стрептомицина и 0,8 мг/мл генетицина при 37°C в увлажненной атмосфере 5% CO2. Клеточную линию синовиальной саркомы человека SYO-1, предоставленную в Rare Cancer Center of the National Cancer Center, поддерживали в DMEM с добавлением 10% эмбриональной телячьей сыворотки (FBS) и 1% пенициллина/стрептомицина при 37°C в увлажненной атмосфере 5% CO2. Линию клеток злокачественной опухоли пищевода человека T.T, приобретенную в JCRB, поддерживали в DMEM/F12 (1:1) с добавлением 10% эмбриональной телячьей сыворотки (FBS) и 1% пенициллина/стрептомицина при 37°C в увлажненной атмосфере 5% CO2. Линию клеток злокачественной опухоли легких человека H727, приобретенную в ATCC, поддерживали в RPMI-1640 с добавлением 10% эмбриональной телячьей сыворотки (FBS) и 1% пенициллина/стрептомицина при 37°C в увлажненной атмосфере 5% CO2. Клеточную линию злокачественной опухоли толстой кишки человека COLO201, приобретенную в ATCC, поддерживали в RPMI-1640 с добавлением 10% эмбриональной телячьей сыворотки (FBS), 1% пенициллина/стрептомицина, 10 мМ HEPES, 1 мМ пирувата натрия и 4,5 г/л глюкозы при 37°C в увлажненной атмосфере 5% CO2. Клеточную линию злокачественной опухоли толстой кишки человека LoVo, приобретенную в ATCC, поддерживали в F12 с добавлением 20% эмбриональной телячьей сыворотки (FBS) и 1% пенициллина/стрептомицина при 37°C в увлажненной атмосфере CO2.
Клинические образцы
Образцы ткани из хирургически удаленной злокачественной опухоли легких (фиксированные формалином парафиновые срезы и замороженные ткани) и соответствующую им клиническую информацию получали из Kanagawa Cancer Center с письменного информированного согласия.
Иммуногистохимическое окрашивание (IHC)
Фиксированные формалином парафиновые срезы FZD10/DLD1, Mock/DLD1, SYO1, T.T, H727, LoVo, COLO201 и клинические образцы депарафинизировали посредством погружения в ксилол на три минуты три раза и затем погружали в 100% этанол на одну минуту два раза, после чего следовал 90%, 70% и 50% этанол на одну минуту каждый для регидратации. Для обработки по извлечению антигенов срезы, погруженные в Antigen Retrieval Solution pH 9 (Nichirei Biosciences Inc.), инкубировали при 125°C в течение 30 с для FZD10/DLD1 и Mock/DLD1 и при 95°C в течение 40 минут для SYO1, T.T, H727, LoVo, COLO201 и клинических образцов. После инкубации, их оставляли стоять при комнатной температуре в течение 20 минут и затем промывали проточной водой в течение 5 минут. Срезы погружали в 3,0% пероксид водорода на 10 минут, чтобы блокировать эндогенные пероксидазы, и промывали в Wash Buffer (TBS-T(Takara Bio)) в течение 5 минут три раза. Кроме того, чтобы блокировать неспецифические реакции, подходящее количество Protein Block Solution (Dako) добавляли по каплям на срезы, и их оставляли стоять в течение 10 минут. Во влажной камере подходящее количество каждого первичного антитела (FZD10Ab(10A8H4G4), FZD10(L164)pAb и FZD10 PolyclonalAb) добавляли по каплям и после срезы оставляли стоять в течение 60 минут, их подвергали трем 5-минутным промываниям в Wash Buffer. Во влажной камере, подходящее количество Histofine Simple Stain MAX-PO (Nichirei Biosciences Inc.), в качестве вторичного антитела, добавляли по каплям и оставляли стоять в течение 30 минут. Срезы промывали в Wash Buffer в течение 5 минут три раза. Реакцию развития окраски осуществляли с использованием DAB Substrate Solution (Nichirei Biosciences Inc.). Препараты срезов погружали в гематоксилин (Dako) на 20 с и промывали проточной водой. Дегидратацию осуществляли посредством погружения в 50%, 70%, и 90% этанол на 1 минуту каждый и в 100% этанол на 1 минуту два раза. Наконец, срезы очищали посредством погружения в ксилол на 3 минуты два раза и заливали в Mount-Quick (DAIDO SANGYO).
ПЦР в реальном времени (RT)
Общую РНК экстрагировали из линии клеток злокачественной опухолиs (SYO-1 и COLO201) с использованием набора RNeasy Mini (QIAGEN). Для клинической замороженной ткани (сквамозная злокачественная опухоль легких), замороженные тканевые срезы погружали в реактив TRIzol (Invitrogen) и измельчали и подвергали экстрагированию хлороформом. В получаемый экстракт добавляли приблизительно равное количество 70% этанола и экстрагировали общую РНК с использованием набора RNeasy Mini (QIAGEN). Используя транскриптазу SuperScript III Reverse Transcriptase (Invitrogen), из общей РНК синтезировали кДНК. Используя кДНК в качестве матрицы, осуществляли ПЦР с использованием набора KAPA SYBR FAST ABI Prism qPCR (KAPA Biosystems). Целевым геном для анализа экспрессии был FZD10, а геном домашнего хозяйства был глицеральдегид-3-фосфатдегидрогеназа (GAPDH). ПЦР в реальном времени осуществляли с использованием, для FZD10, набора праймеров FZD10-11F: 5'-GTGTGCAGCCGTAGGTTAAAG-3' (SEQ ID NO: 12) и FZD10 R5: 5'-GACTGGGCAGGGATCTCATA-3' (SEQ ID NO: 13) и, для GAPDH, набора праймеров GAPDH RT-ПЦР Fw: 5'-ACAACAGCCTCAAGATCATCAG-3' (SEQ ID NO: 14) и GAPDH RT-ПЦР Re: 5'-GGTCCACCACTGACACGTTG-3' (SEQ ID NO: 15). Осуществляли мониторинг количество продукта ПЦР амплификации с течением времени и вычисляли значение Ct, задавая порог в области, где продукт ПЦР амплификации амплифицировали экспоненциально. Концентрацию неизвестного образца вычисляли посредством применения значения Ct к калибровочной кривой. Количество матрицы стандартизовали среди образцов посредством деления количественного значения для гена FZD10 на количественное значение для гена GAPDH и сравнивали уровни экспрессии гена FZD10.
Проточная цитометрия (FCM)
SYO1, T.T, H727 и LoVo поддерживали в соответствующих рекомендованных средах для культивирования до ранней конфлюентности. Для того чтобы избегать дегенерации антигенов клеточной поверхности, клетки после этого разделяли с использованием Cell Dissociation Solution (SIGMA, MO) и суспендировали в 0,5% BSA/PBS. Суспендированные клетки пропускали через клеточное сито для того, чтобы удалять агрегаты, и посчитывали число клеток. Клетки распределяли в 96-луночный планшет для анализа (2×105 клеток/50 мкл). Добавляли 50 мкл разведенного тестового антитела или культурального супернатанта и оставляли стоять при 4°C в течение одного часа. Планшет центрифугировали при 1500 об./мин в течение 5 минут при 4°C, удаляли супернатант и затем планшет промывали два раза в 150 мкл 0,5% BSA/PBS. Клетки смешивали с 20 мкг/мл IgG козы против антитела мыши с Alexa Fluor 488 (H+L) (Invitrogen, CA) и оставляли стоять в темноте при 4°C в течение одного часа. Планшет центрифугировали на 1500 об./мин в течение 5 минут при 4°C, удаляли супернатант, затем планшет промывали два раза в 150 мкл 0,5% BSA/PBS и суспендировали клетки в 120 мкл 0,5% BSA/PBS. Характер связывания и специфичность тестового антитела оценивали с использованием FACS Calibur (Becton Dickinson, NJ) по инструкциям производителя.
[Пример 1] Получение моноклональные антитела против FZD10
(1) Получение продуцирующих антитело против FZD10 гибридом с использованием растворимого белка FZD10 в качестве иммуногена
FZD10 представляет собой мембранный белок. Для получения антител, которые реагируют с фиксированным мембранным белком, его внеклеточная область может быть иммуногеном. Поскольку внеклеточные области FZD10, за исключением N-концевой области, столь коротки, что их может быть трудно использовать в качестве антигенов, N-концевую внеклеточную область (аминокислоты с 1 до 161) выбирали в качестве иммуногена. Растворимый белок FZD10 без сигнального пептида (область аминокислот с 21 до 161) (SEQ ID NO: 9) использовали в качестве иммуногена для получения моноклональных антител. 50 мкг пептида антигена добавляли в адъювант Фрейнда, эмульсифицировали и инъецировали подкожно мышам Balb/c (Japan SLC, Inc.) для первичной иммунизации. Вторую и последующие иммунизации осуществляли посредством подкожной инъекции количества, эквивалентного 25 мкг пептида антигена, полученного аналогичным образом. Через 3 суток после конечной иммунизации спленоциты асептически получали у мышей. В соответствии со стандартным способом, их сливали с миеломными клетками мыши SP2/0 с использованием способа с полиэтиленгликолем.
(2) Отбор продуцирующих антитело против FZD10 гибридом
Для отбора антител против FZD10, сначала осуществляли способ ELISA с использованием растворимого белка FZD10 для скрининга антител, связывающихся с FZD10. Дополнительно осуществляли скрининг антител, отобранных с помощью способа ELISA, посредством иммунологического окрашивания. Отбор посредством иммунологического окрашивания осуществляли посредством иммуногистохимического окрашивания с использованием клеточной линии FZD10/DLD1 с принудительной экспрессией FZD10, которая экспрессирует полноразмерный белок FZD10 (SEQ ID NO: 22). В частности, получали фиксированный формалином парафиновый срез клеточной линии FZD10/DLD1 с принудительной экспрессией полноразмерного белка FZD10. Затем осуществляли иммунологическое окрашивание и отбирали гибридомы, у которых наблюдали сильную реакцию.
Среди тестированных гибридом обнаруживали, что клон гибридомы 10A8H4G4 продуцирует FZD10-специфическое антитело на высоком уровне, и результаты ее иммуногистохимического окрашивания представлены на фиг. 2. Как показано на фотографиях и графиках на фиг. 2, парафиновый срез, полученный из клеточной линии FZD10/DLD1 с принудительной экспрессией FZD10, показывал окрашивание с использованием 10A8H4G4, что указывает на высокую долю FZD10-положительных клеток. С другой стороны, парафиновый срез, полученный из клеточной линии, в которую вводили пустой вектор в качестве отрицательного контроля (Mock/DLD1), показывал небольшое окрашивание, что указывает на малую долю FZD10-положительных клеток. Эти результаты демонстрируют, что клон гибридомы 10A8H4G4 можно использовать в качестве гибридомы, продуцирующей антитело, которое специфически обнаруживает FZD10 при иммуногистохимическом окрашивании.
С другой стороны, когда для окрашивания использовали коммерчески доступные антитела (FZD10(L164)Ab и FZD10PolyclonalAb), окрашивание наблюдали как в FZD10/DLD1, так и в Mock/DLD1 (сигнал обнаруживали в большой доле клеток). Следовательно, результаты обнаружения с использованием этих коммерческих антител предположительно включают ложноположительные сигналы.
По указанным выше результатам, обнаруживали, что антитело против FZD10 по настоящему изобретению (10A8H4G4) обладает благоприятным свойством в виде способности обнаруживать FZD10 с более высокой специфичностью, чем коммерчески доступные антитела против FZD10, при иммуногистохимическом окрашивании.
Этот клон гибридомы 10A8H4G4 выбирали для получения антитела для дальнейших экспериментов. Клон гибридомы 10A8H4G4 культивировали в большом масштабе и позднее культуральное текучее вещество собирали от двух до трех недель. Антитело очищали от культурального текучего вещества с использованием колонки с белком A (GE Healthcare, NJ). В настоящем описании антитело по настоящему изобретению также обозначают как клон 10A8H4G4.
[Пример 2] Оценка специфичности моноклонального антитела против FZD10
Затем специфичность 10A8H4G4 оценивали с использованием различных клеточных линий с различными уровнями экспрессии FZD10. В частности, результаты иммуногистохимического окрашивания и проточной цитометрии с использованием 10A8H4G4 сравнивали для того, чтобы исследовать, находится ли окрашивание в соответствии с уровнем экспрессии белка FZD10. Cancer Cell Line Encyclopedia (CCLE), база данных об анализах экспрессии мРНК для клеточных линий злокачественных опухолей каждого типа, показывает, что повышающая регуляция экспрессии удивительным образом имеет место в злокачественной опухоли легких, злокачественной опухоли пищевода и злокачественной опухоли толстой кишки (карциноме толстой кишки) (фиг. 1). Соответственно, клеточные линии, происходящие из злокачественных опухолей этих типов, использовали в дальнейшем анализе.
Сначала проточную цитометрию с использованием 10A8H4G4 осуществляли для того, чтобы подтверждать экспрессию эндогенного белка FZD10 на клеточной мембране различных клеточных линий, происходящих из тканей злокачественных опухолей человека. Как показано на фиг. 3, положительные сигналы обнаруживали посредством проточной цитометрии с использованием 10A8H4G4 в SYO-1, происходящей из синовиальной саркомы человека, у которой продемонстрирована экспрессия белка FZD10 эндогенно, а также в клеточной линии T.T, происходящей из злокачественной опухоли пищевода человека, и клеточной линии H727, происходящей из злокачественной опухоли легких человека. С другой стороны, положительный сигнал не обнаруживали с помощью проточной цитометрии при использовании 10A8H4G4 в клеточной линии LoVo, происходящей из злокачественной опухоли толстой кишки человека, которая известна как клеточная линия, не экспрессирующая FZD10.
Затем, используя 10A8H4G4, осуществляли иммуногистохимическое окрашивание парафиновых срезов, полученных из этих клеточных линий. Как показано на фиг. 3B, в результате окрашивания с использованием 10A8H4G4, окрашивание наблюдали в парафиновых срезах, полученных из клеточных линий SYO-1, T.T и H727, у которых обнаружена экспрессия FZD10. На этих парафиновых срезах положительные сигналы обнаруживали в высокой доле клеток в корреляции с результатами проточной цитометрии. С другой стороны, имело место небольшое окрашивание парафинового среза, полученного из клеточной линии LoVo, не экспрессирующей FZD10, причем положительные сигналы почти не обнаруживали.
Указанные выше результаты демонстрируют, что антитело против FZD10 по настоящему изобретению (10A8H4G4), представляет собой эффективный инструмент, который может обнаруживать белок FZD10 в образцах как в проточной цитометрии, так и в иммуногистохимическом окрашивании с высокой специфичностью.
[Пример 3] Обнаружение белка FZD10 в модели трансплантата опухоли и клинических образцах
Специфичность антитела против FZD10 по настоящему изобретению (10A8H4G4) при иммуногистохимическом окрашивании оценивали с использованием парафиновых срезов, полученных из ксенотрансплантатных опухолей мыши из линий клеток злокачественной опухоли, и образцов клинических злокачественных опухолей легких. Экспрессию белка FZD10 и РНК в парафиновых срезах, полученных из ксенотрансплантатных опухолей мыши из SYO-1 и COLO201, и в областях злокачественных опухолей и не злокачественных опухолей из образцов клинических злокачественных опухолей легких от 1 до 6 обнаруживали посредством иммуногистохимического окрашивания и ПЦР в реальном времени, соответственно, и результаты представлены на фиг. 4.
Как показано на фиг. 4, в парафиновом срезе, полученном из ксенотрансплантатной опухоли мыши из клеточной линии SYO-1, у которой обнаруживали высокую экспрессию РНК FZD10, обнаруживали клетки, окрашенные 10A8H4G4, т. е. FZD10-положительные клетки. Однако в парафиновом срезе, полученном из ксенотрансплантатной опухоли мыши из клеточная линия COLO201, в которой количество экспрессии РНК FZD10 мало, число клеток, окрашенных 10A8H4G4, т.е. FZD10-положительных клеток, также мало. Этот результат демонстрирует, что антитело против FZD10 по настоящему изобретению (10A8H4G4) представляет собой эффективный инструмент для получения результатов обнаружения при иммуногистохимическом окрашивании, которые коррелируют с уровнями экспрессии белка FZD10 в образцах.
Кроме того, в клиническом образце злокачественной опухоли легких 5, в котором наблюдали специфическую экспрессию РНК FZD10 в область опухоли, обнаруживали клетки, окрашенные 10A8H4G4, т.е. FZD10-положительные клетки. Однако другие образцы клинических злокачественных опухолей легких, в которых не наблюдали специфическую экспрессию РНК FZD10 в области опухоли, были едва ли окрашены, причем FZD10-положительные клетки почти не обнаруживали. Этот результат демонстрирует, что 10A8H4G4 также может специфически обнаруживать белок FZD10 в клинических образцах.
[Пример 4] Анализ аминокислотных последовательностей вариабельных областей моноклонального антитела против FZD10
Анализировали аминокислотные последовательности вариабельных областей антитела против FZD10 по настоящему изобретению (10A8H4G4).
Используя набор RNeasy mini (QIAGEN), из гибридомы 10A8H4G4 экстрагировали общую РНК. Из общей РНК синтезировали кДНК с использованием Super Script II Reverse Transcriptase (Invitrogen). Праймеры для синтеза кДНК представляют собой следующее.
mIGCUniRv в качестве 3'-праймера тяжелой цепи:
5'-CTGGGAAGGTGTGCACAC-3' (SEQ ID NO: 16)
mIGKRv2 в качестве 3'-праймера легкой цепи:
5'-GTTGTTCAAGAAGCACACGAC-3' (SEQ ID NO: 17)
Полимер dC добавляли на конец кДНК с использованием 5' RACE System for Rapid Amplification of cDNA Ends (Invitrogen) и полинуклеотиды, кодирующие вариабельные области моноклонального антитела, амплифицировали с использованием Platinum Taq DNA Polymerase High Fidelity (Invitrogen). Праймеры для амплификации представляют собой следующее. Нуклеотид «I» в последовательности праймера представляет инозин.
5' RACE Abridged Anchor Primer в качестве 5' праймеров тяжелой цепи и легкой цепи:
5'-GGCCACGCGTCGACTAGTACGGGIIGGGIIGGGIIG-3' (SEQ ID NO: 18);
mIGCUniRv2 в качестве 3'-праймера тяжелой цепи:
5'-TGGACAGGGATCCAGAGTTCC-3' (SEQ ID NO: 19); и
mIGKNesRv2 в качестве 3'-праймера легкой цепи:
5'-CAGATGTTAACTGCTCACTGGATGG-3' (SEQ ID NO: 20).
ПЦР продукты клонировали в вектор pGEM-T Easy (Promega). Определяли последовательности областей вставляемых фрагментов и определяли нуклеотидные последовательности вариабельных областей 10A8H4G4 (за исключением сигнальной последовательности).
Аминокислотные последовательности и нуклеотидные последовательности вариабельной области тяжелой цепи и вариабельной области легкой цепи моноклонального антитела мыши определяли как следующее:
10A8H4G4, аминокислотная последовательность вариабельной области тяжелой цепи (за исключением сигнальной последовательности):
QVTLKESGPGILQPSQTLSLTCSFSGFSLSTSGLGVSWIRQPSGKGLEWLAHIYWDDDK
RYNPSLKSRLTISKDTSSNQVFLKITSVDTADTATYYCARRAYYGNYYALDYWGQGTSV
TVSS (SEQ ID NO: 7) (кодируется нуклеотидной последовательностью SEQ ID NO: 10);
10A8H4G4, нуклеотидная последовательность вариабельной области тяжелой цепи:
5'-
CAGGTTACTCTGAAAGAGTCTGGCCCTGGGATATTGCAGCCCTCCCAGACC
CTCAGTCTGACTTGTTCTTTCTCTGGGTTTTCACTGAGCACTTCTGGTCTG
GGTGTGAGCTGGATTCGTCAGCCTTCAGGAAAGGGTCTGGAGTGGCTGGCA
CACATTTACTGGGATGATGACAAGCGCTATAACCCATCCCTGAAGAGCCGG
CTCACAATCTCCAAGGATACCTCCAGCAACCAGGTATTCCTCAAGATCACC
AGTGTGGACACTGCAGATACTGCCACATACTACTGTGCTCGAAGAGCCTAC
TATGGTAATTACTATGCTTTGGACTACTGGGGTCAAGGAACCTCAGTCACC
GTCTCCTCA-3' (SEQ ID NO: 10);
10A8H4G4, аминокислотная последовательность вариабельной области легкой цепи (за исключением сигнальной последовательности):
DIVMTQSPSSLTVTAGEKVTMSCKSSQSLLNSGNQKNYLTWYQQKPGQPPKLLIYWAST
RKSGVPDRFTGSGSGTDFTLTISSVQAEDLAVYYCQNDYSYPVTFGAGTKLELKRAD (SEQ ID NO: 8) (кодируется нуклеотидной последовательностью SEQ ID NO: 11);
10A8H4G4, нуклеотидная последовательность вариабельной области легкой цепи:
5'-
GACATTGTGATGACACAGTCTCCATCCTCCCTGACTGTGACAGCAGGAGAG
AAGGTCACTATGAGCTGCAAGTCCAGTCAGAGTCTGTTAAACAGTGGAAAT
CAAAAGAACTACTTGACCTGGTACCAGCAGAAACCAGGGCAGCCTCCTAAA
CTGTTGATCTACTGGGCATCCACTAGGAAATCTGGGGTCCCTGATCGCTTC
ACAGGCAGTGGATCTGGAACAGATTTCACTCTCACCATCAGCAGTGTGCAG
GCTGAAGACCTGGCAGTTTATTACTGTCAGAATGATTATAGTTATCCGGTC
ACGTTCGGTGCTGGGACCAAGCTGGAGCTGAAACGGGCTGAT-3' (SEQ ID NO: 11).
Последовательности CDR антитела по настоящему изобретению (10A8H4G4), которые определяли в соответствии с определением Kabat, представляют собой следующее:
CDR1 тяжелой цепи (CDR-H1): TSGLGVS (SEQ ID NO: 1);
CDR2 тяжелой цепи (CDR-H2): HIYWDDDKRYNPSLKS (SEQ ID NO: 2);
CDR3 тяжелой цепи (CDR-H3): RAYYGNYYALDY (SEQ ID NO: 3);
CDR1 легкой цепи (CDR-L1): KSSQSLLNSGNQKNYLT (SEQ ID NO: 4);
CDR2 легкой цепи (CDR-L2): WASTRKS (SEQ ID NO: 5); и
CDR3 легкой цепи (CDR-L3): QNDYSYPVT (SEQ ID NO: 6).
Промышленная применимость
В настоящем изобретении достигнут успех в получении антитела против FZD10, способного обнаруживать белок FZD10 в образцах, выделенных из таких мишеней, как клинические образцы, с высокой специфичностью. Использование антитела против FZD10 по настоящему изобретению делает возможным высокочувствительное обнаружение белка FZD10 в образцах при низком фоне. Следовательно, антитело по настоящему изобретению можно использовать при диагностировании связанных с FZD10 заболеваний, таких как FZD10-экспрессирующие злокачественные опухоли. Кроме того, поскольку антитело по настоящему изобретению может обнаруживать FZD10 в соответствии с уровнем экспрессии FZD10 в образцах, его также можно использовать при скрининге субъектов, у которых лечение ингибитором FZD10 является высокоэффективным (диагностирование перед лечением) и определении лекарственного эффекта после лечения ингибитором FZD10 у субъектов (диагностирование после лечения).
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ONCOTHERAPY SCIENCE, INC.
<120> МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ FZD10 ЕГО ИСПОЛЬЗОВАНИЕ
<130> ONC-A1605P
<150> JP 2016-197881
<151> 2016-10-06
<160> 22
<170> PatentIn версии 3.5
<210> 1
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH CDR1
<400> 1
Thr Ser Gly Leu Gly Val Ser
1 5
<210> 2
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH CDR2
<400> 2
His Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 3
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> VH CDR3
<400> 3
Arg Ala Tyr Tyr Gly Asn Tyr Tyr Ala Leu Asp Tyr
1 5 10
<210> 4
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL CDR1
<400> 4
Lys Ser Ser Gln Ser Leu Leu Asn Ser Gly Asn Gln Lys Asn Tyr Leu
1 5 10 15
Thr
<210> 5
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL CDR2
<400> 5
Trp Ala Ser Thr Arg Lys Ser
1 5
<210> 6
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> VL CDR
<400> 6
Gln Asn Asp Tyr Ser Tyr Pro Val Thr
1 5
<210> 7
<211> 122
<212> Белок
<213> Искусственная последовательность
<220>
<223> вариабельная область H-цепи
<400> 7
Gln Val Thr Leu Lys Glu Ser Gly Pro Gly Ile Leu Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Phe Ser Gly Phe Ser Leu Ser Thr Ser
20 25 30
Gly Leu Gly Val Ser Trp Ile Arg Gln Pro Ser Gly Lys Gly Leu Glu
35 40 45
Trp Leu Ala His Ile Tyr Trp Asp Asp Asp Lys Arg Tyr Asn Pro Ser
50 55 60
Leu Lys Ser Arg Leu Thr Ile Ser Lys Asp Thr Ser Ser Asn Gln Val
65 70 75 80
Phe Leu Lys Ile Thr Ser Val Asp Thr Ala Asp Thr Ala Thr Tyr Tyr
85 90 95
Cys Ala Arg Arg Ala Tyr Tyr Gly Asn Tyr Tyr Ala Leu Asp Tyr Trp
100 105 110
Gly Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 8
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> вариабельная область L-цепи
<400> 8
Asp Ile Val Met Thr Gln Ser Pro Ser Ser Leu Thr Val Thr Ala Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Gly Asn Gln Lys Asn Tyr Leu Thr Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Lys Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Gln Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Asn
85 90 95
Asp Tyr Ser Tyr Pro Val Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu
100 105 110
Lys Arg Ala Asp
115
<210> 9
<211> 141
<212> Белок
<213> Искусственная последовательность
<220>
<223> фрагмент FZD10 в качестве иммуногена
<400> 9
Ile Ser Ser Met Asp Met Glu Arg Pro Gly Asp Gly Lys Cys Gln Pro
1 5 10 15
Ile Glu Ile Pro Met Cys Lys Asp Ile Gly Tyr Asn Met Thr Arg Met
20 25 30
Pro Asn Leu Met Gly His Glu Asn Gln Arg Glu Ala Ala Ile Gln Leu
35 40 45
His Glu Phe Ala Pro Leu Val Glu Tyr Gly Cys His Gly His Leu Arg
50 55 60
Phe Phe Leu Cys Ser Leu Tyr Ala Pro Met Cys Thr Glu Gln Val Ser
65 70 75 80
Thr Pro Ile Pro Ala Cys Arg Val Met Cys Glu Gln Ala Arg Leu Lys
85 90 95
Cys Ser Pro Ile Met Glu Gln Phe Asn Phe Lys Trp Pro Asp Ser Leu
100 105 110
Asp Cys Arg Lys Leu Pro Asn Lys Asn Asp Pro Asn Tyr Leu Cys Met
115 120 125
Glu Ala Pro Asn Asn Gly Ser Asp Glu Pro Thr Arg Gly
130 135 140
<210> 10
<211> 366
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность нуклеиновой кислоты вариабельной области
H-цепи
<400> 10
caggttactc tgaaagagtc tggccctggg atattgcagc cctcccagac cctcagtctg 60
acttgttctt tctctgggtt ttcactgagc acttctggtc tgggtgtgag ctggattcgt 120
cagccttcag gaaagggtct ggagtggctg gcacacattt actgggatga tgacaagcgc 180
tataacccat ccctgaagag ccggctcaca atctccaagg atacctccag caaccaggta 240
ttcctcaaga tcaccagtgt ggacactgca gatactgcca catactactg tgctcgaaga 300
gcctactatg gtaattacta tgctttggac tactggggtc aaggaacctc agtcaccgtc 360
tcctca 366
<210> 11
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> последовательность нуклеиновой цепи вариабельной области
L-цепи
<400> 11
gacattgtga tgacacagtc tccatcctcc ctgactgtga cagcaggaga gaaggtcact 60
atgagctgca agtccagtca gagtctgtta aacagtggaa atcaaaagaa ctacttgacc 120
tggtaccagc agaaaccagg gcagcctcct aaactgttga tctactgggc atccactagg 180
aaatctgggg tccctgatcg cttcacaggc agtggatctg gaacagattt cactctcacc 240
atcagcagtg tgcaggctga agacctggca gtttattact gtcagaatga ttatagttat 300
ccggtcacgt tcggtgctgg gaccaagctg gagctgaaac gggctgat 348
<210> 12
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность прямого
праймера для FZD10
<400> 12
gtgtgcagcc gtaggttaaa g 21
<210> 13
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность обратного
праймера для FZD10
<400> 13
gactgggcag ggatctcata 20
<210> 14
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность прямого
праймера для GAPDH
<400> 14
acaacagcct caagatcatc ag 22
<210> 15
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность обратного
праймера для GAPDH
<400> 15
ggtccaccac tgacacgttg 20
<210> 16
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность 3’-праймера
для VH
<400> 16
ctgggaaggt gtgcacac 18
<210> 17
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность 3’-праймера
для VL
<400> 17
gttgttcaag aagcacacga c 21
<210> 18
<211> 36
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность 5’-праймера
для VH и VL
<220>
<221> смешанные признаки
<222> (24)..(25)
<223> n представляет собой инозин
<220>
<221> смешанные признаки
<222> (29)..(30)
<223> n представляет собой инозин
<220>
<221> смешанные признаки
<222> (34)..(35)
<223> n представляет собой инозин
<400> 18
ggccacgcgt cgactagtac gggnngggnn gggnng 36
<210> 19
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность 3’-праймера
для VH
<400> 19
tggacaggga tccagagttc c 21
<210> 20
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Искусственно синтезированная последовательность 3’-праймера
для VL
<400> 20
cagatgttaa ctgctcactg gatgg 25
<210> 21
<211> 3288
<212> ДНК
<213> Homo sapiens
<220>
<221> CDS
<222> (485)..(2230)
<300>
<308> № доступа Genbank NM_007197.3
<309> 2015-12-31
<313> (1)..(3288)
<400> 21
cgagtcttct catcccggga cgcaaacctc gaaacagctg ccggctggtc ccggccgagg 60
ccggcgcagg gagggaggag ccgcccgggc tgtgggggcg ccgcgagctg ggccggcctc 120
ggtgtgcccg cgccgccagc ccgctccaga cgcgccacct gggcgctcca agaagaggcc 180
gaagtttgcc gcggccgtga gttggagctc gcgccgggcc gctgcgccgg gagctccggg 240
ggcttccctc gcttcccggt attgtttgca aactttgctg ctctccgccg cggcccccaa 300
ctcggcggac gccgggcgcg gagagccgag ccgggggcgc tgtgcgcagc gctcgggcca 360
ggccgggcgg gcatgggcgg gggcccgagc aggggtggag agccggggcc agcagcagcc 420
cgtgcccggg agcggcggcg ctgaggggcg cggagctccc cgcgaggaca cgtccaacgc 480
cagc atg cag cgc ccg ggc ccc cgc ctg tgg ctg gtc ctg cag gtg atg 529
Met Gln Arg Pro Gly Pro Arg Leu Trp Leu Val Leu Gln Val Met
1 5 10 15
ggc tcg tgc gcc gcc atc agc tcc atg gac atg gag cgc ccg ggc gac 577
Gly Ser Cys Ala Ala Ile Ser Ser Met Asp Met Glu Arg Pro Gly Asp
20 25 30
ggc aaa tgc cag ccc atc gag atc ccg atg tgc aag gac atc ggc tac 625
Gly Lys Cys Gln Pro Ile Glu Ile Pro Met Cys Lys Asp Ile Gly Tyr
35 40 45
aac atg act cgt atg ccc aac ctg atg ggc cac gag aac cag cgc gag 673
Asn Met Thr Arg Met Pro Asn Leu Met Gly His Glu Asn Gln Arg Glu
50 55 60
gca gcc atc cag ttg cac gag ttc gcg ccg ctg gtg gag tac ggc tgc 721
Ala Ala Ile Gln Leu His Glu Phe Ala Pro Leu Val Glu Tyr Gly Cys
65 70 75
cac ggc cac ctc cgc ttc ttc ctg tgc tcg ctg tac gcg ccg atg tgc 769
His Gly His Leu Arg Phe Phe Leu Cys Ser Leu Tyr Ala Pro Met Cys
80 85 90 95
acc gag cag gtc tct acc ccc atc ccc gcc tgc cgg gtc atg tgc gag 817
Thr Glu Gln Val Ser Thr Pro Ile Pro Ala Cys Arg Val Met Cys Glu
100 105 110
cag gcc cgg ctc aag tgc tcc ccg att atg gag cag ttc aac ttc aag 865
Gln Ala Arg Leu Lys Cys Ser Pro Ile Met Glu Gln Phe Asn Phe Lys
115 120 125
tgg ccc gac tcc ctg gac tgc cgg aaa ctc ccc aac aag aac gac ccc 913
Trp Pro Asp Ser Leu Asp Cys Arg Lys Leu Pro Asn Lys Asn Asp Pro
130 135 140
aac tac ctg tgc atg gag gcg ccc aac aac ggc tcg gac gag ccc acc 961
Asn Tyr Leu Cys Met Glu Ala Pro Asn Asn Gly Ser Asp Glu Pro Thr
145 150 155
cgg ggc tcg ggc ctg ttc ccg ccg ctg ttc cgg ccg cag cgg ccc cac 1009
Arg Gly Ser Gly Leu Phe Pro Pro Leu Phe Arg Pro Gln Arg Pro His
160 165 170 175
agc gcg cag gag cac ccg ctg aag gac ggg ggc ccc ggg cgc ggc ggc 1057
Ser Ala Gln Glu His Pro Leu Lys Asp Gly Gly Pro Gly Arg Gly Gly
180 185 190
tgc gac aac ccg ggc aag ttc cac cac gtg gag aag agc gcg tcg tgc 1105
Cys Asp Asn Pro Gly Lys Phe His His Val Glu Lys Ser Ala Ser Cys
195 200 205
gcg ccg ctc tgc acg ccc ggc gtg gac gtg tac tgg agc cgc gag gac 1153
Ala Pro Leu Cys Thr Pro Gly Val Asp Val Tyr Trp Ser Arg Glu Asp
210 215 220
aag cgc ttc gca gtg gtc tgg ctg gcc atc tgg gcg gtg ctg tgc ttc 1201
Lys Arg Phe Ala Val Val Trp Leu Ala Ile Trp Ala Val Leu Cys Phe
225 230 235
ttc tcc agc gcc ttc acc gtg ctc acc ttc ctc atc gac ccg gcc cgc 1249
Phe Ser Ser Ala Phe Thr Val Leu Thr Phe Leu Ile Asp Pro Ala Arg
240 245 250 255
ttc cgc tac ccc gag cgc ccc atc atc ttc ctc tcc atg tgc tac tgc 1297
Phe Arg Tyr Pro Glu Arg Pro Ile Ile Phe Leu Ser Met Cys Tyr Cys
260 265 270
gtc tac tcc gtg ggc tac ctc atc cgc ctc ttc gcc ggc gcc gag agc 1345
Val Tyr Ser Val Gly Tyr Leu Ile Arg Leu Phe Ala Gly Ala Glu Ser
275 280 285
atc gcc tgc gac cgg gac agc ggc cag ctc tat gtc atc cag gag gga 1393
Ile Ala Cys Asp Arg Asp Ser Gly Gln Leu Tyr Val Ile Gln Glu Gly
290 295 300
ctg gag agc acc ggc tgc acg ctg gtc ttc ctg gtc ctc tac tac ttc 1441
Leu Glu Ser Thr Gly Cys Thr Leu Val Phe Leu Val Leu Tyr Tyr Phe
305 310 315
ggc atg gcc agc tcg ctg tgg tgg gtg gtc ctc acg ctc acc tgg ttc 1489
Gly Met Ala Ser Ser Leu Trp Trp Val Val Leu Thr Leu Thr Trp Phe
320 325 330 335
ctg gcc gcc ggc aag aag tgg ggc cac gag gcc atc gaa gcc aac agc 1537
Leu Ala Ala Gly Lys Lys Trp Gly His Glu Ala Ile Glu Ala Asn Ser
340 345 350
agc tac ttc cac ctg gca gcc tgg gcc atc ccg gcg gtg aag acc atc 1585
Ser Tyr Phe His Leu Ala Ala Trp Ala Ile Pro Ala Val Lys Thr Ile
355 360 365
ctg atc ctg gtc atg cgc agg gtg gcg ggg gac gag ctc acc ggg gtc 1633
Leu Ile Leu Val Met Arg Arg Val Ala Gly Asp Glu Leu Thr Gly Val
370 375 380
tgc tac gtg ggc agc atg gac gtc aac gcg ctc acc ggc ttc gtg ctc 1681
Cys Tyr Val Gly Ser Met Asp Val Asn Ala Leu Thr Gly Phe Val Leu
385 390 395
att ccc ctg gcc tgc tac ctg gtc atc ggc acg tcc ttc atc ctc tcg 1729
Ile Pro Leu Ala Cys Tyr Leu Val Ile Gly Thr Ser Phe Ile Leu Ser
400 405 410 415
ggc ttc gtg gcc ctg ttc cac atc cgg agg gtg atg aag acg ggc ggc 1777
Gly Phe Val Ala Leu Phe His Ile Arg Arg Val Met Lys Thr Gly Gly
420 425 430
gag aac acg gac aag ctg gag aag ctc atg gtg cgt atc ggg ctc ttc 1825
Glu Asn Thr Asp Lys Leu Glu Lys Leu Met Val Arg Ile Gly Leu Phe
435 440 445
tct gtg ctg tac acc gtg ccg gcc acc tgt gtg atc gcc tgc tac ttt 1873
Ser Val Leu Tyr Thr Val Pro Ala Thr Cys Val Ile Ala Cys Tyr Phe
450 455 460
tac gaa cgc ctc aac atg gat tac tgg aag atc ctg gcg gcg cag cac 1921
Tyr Glu Arg Leu Asn Met Asp Tyr Trp Lys Ile Leu Ala Ala Gln His
465 470 475
aag tgc aaa atg aac aac cag act aaa acg ctg gac tgc ctg atg gcc 1969
Lys Cys Lys Met Asn Asn Gln Thr Lys Thr Leu Asp Cys Leu Met Ala
480 485 490 495
gcc tcc atc ccc gcc gtg gag atc ttc atg gtg aag atc ttt atg ctg 2017
Ala Ser Ile Pro Ala Val Glu Ile Phe Met Val Lys Ile Phe Met Leu
500 505 510
ctg gtg gtg ggg atc acc agc ggg atg tgg att tgg acc tcc aag act 2065
Leu Val Val Gly Ile Thr Ser Gly Met Trp Ile Trp Thr Ser Lys Thr
515 520 525
ctg cag tcc tgg cag cag gtg tgc agc cgt agg tta aag aag aag agc 2113
Leu Gln Ser Trp Gln Gln Val Cys Ser Arg Arg Leu Lys Lys Lys Ser
530 535 540
cgg aga aaa ccg gcc agc gtg atc acc agc ggt ggg att tac aaa aaa 2161
Arg Arg Lys Pro Ala Ser Val Ile Thr Ser Gly Gly Ile Tyr Lys Lys
545 550 555
gcc cag cat ccc cag aaa act cac cac ggg aaa tat gag atc cct gcc 2209
Ala Gln His Pro Gln Lys Thr His His Gly Lys Tyr Glu Ile Pro Ala
560 565 570 575
cag tcg ccc acc tgc gtg tga acagggctgg agggaagggc acaggggcgc 2260
Gln Ser Pro Thr Cys Val
580
ccggagctaa gatgtggtgc ttttcttggt tgtgtttttc tttcttcttc ttcttttttt 2320
ttttttataa aagcaaaaga gaaatacata aaaaagtgtt taccctgaaa ttcaggatgc 2380
tgtgatacac tgaaaggaaa aatgtactta aagggttttg ttttgttttg gttttccagc 2440
gaagggaagc tcctccagtg aagtagcctc ttgtgtaact aatttgtggt aaagtagttg 2500
attcagccct cagaagaaaa cttttgttta gagccctccc taaatataca tctgtgtatt 2560
tgagttggct ttgctaccca tttacaaata agaggacaga taactgcttt gcaaattcaa 2620
gagcctcccc tgggttaaca aatgagccat ccccagggcc cacccccagg aaggccacag 2680
tgctgggcgg catccctgca gaggaaagac aggacccggg gcccgcctca caccccagtg 2740
gatttggagt tgcttaaaat agactccggc cttcaccaat agtctctctg caagacagaa 2800
acctccatca aacctcacat ttgtgaactc aaacgatgtg caatacattt ttttctcttt 2860
ccttgaaaat aaaaagagaa acaagtattt tgctatatat aaagacaaca aaagaaatct 2920
cctaacaaaa gaactaagag gcccagccct cagaaaccct tcagtgctac attttgtggc 2980
tttttaatgg aaaccaagcc aatgttatag acgtttggac tgatttgtgg aaaggagggg 3040
ggaagaggga gaaggatcat tcaaaagtta cccaaagggc ttattgactc tttctattgt 3100
taaacaaatg atttccacaa acagatcagg aagcactagg ttggcagaga cactttgtct 3160
agtgtattct cttcacagtg ccaggaaaga gtggtttctg cgtgtgtata tttgtaatat 3220
atgatatttt tcatgctcca ctattttatt aaaaataaaa tatgttcttt agtttgctgc 3280
taaaaaaa 3288
<210> 22
<211> 581
<212> Белок
<213> Homo sapiens
<400> 22
Met Gln Arg Pro Gly Pro Arg Leu Trp Leu Val Leu Gln Val Met Gly
1 5 10 15
Ser Cys Ala Ala Ile Ser Ser Met Asp Met Glu Arg Pro Gly Asp Gly
20 25 30
Lys Cys Gln Pro Ile Glu Ile Pro Met Cys Lys Asp Ile Gly Tyr Asn
35 40 45
Met Thr Arg Met Pro Asn Leu Met Gly His Glu Asn Gln Arg Glu Ala
50 55 60
Ala Ile Gln Leu His Glu Phe Ala Pro Leu Val Glu Tyr Gly Cys His
65 70 75 80
Gly His Leu Arg Phe Phe Leu Cys Ser Leu Tyr Ala Pro Met Cys Thr
85 90 95
Glu Gln Val Ser Thr Pro Ile Pro Ala Cys Arg Val Met Cys Glu Gln
100 105 110
Ala Arg Leu Lys Cys Ser Pro Ile Met Glu Gln Phe Asn Phe Lys Trp
115 120 125
Pro Asp Ser Leu Asp Cys Arg Lys Leu Pro Asn Lys Asn Asp Pro Asn
130 135 140
Tyr Leu Cys Met Glu Ala Pro Asn Asn Gly Ser Asp Glu Pro Thr Arg
145 150 155 160
Gly Ser Gly Leu Phe Pro Pro Leu Phe Arg Pro Gln Arg Pro His Ser
165 170 175
Ala Gln Glu His Pro Leu Lys Asp Gly Gly Pro Gly Arg Gly Gly Cys
180 185 190
Asp Asn Pro Gly Lys Phe His His Val Glu Lys Ser Ala Ser Cys Ala
195 200 205
Pro Leu Cys Thr Pro Gly Val Asp Val Tyr Trp Ser Arg Glu Asp Lys
210 215 220
Arg Phe Ala Val Val Trp Leu Ala Ile Trp Ala Val Leu Cys Phe Phe
225 230 235 240
Ser Ser Ala Phe Thr Val Leu Thr Phe Leu Ile Asp Pro Ala Arg Phe
245 250 255
Arg Tyr Pro Glu Arg Pro Ile Ile Phe Leu Ser Met Cys Tyr Cys Val
260 265 270
Tyr Ser Val Gly Tyr Leu Ile Arg Leu Phe Ala Gly Ala Glu Ser Ile
275 280 285
Ala Cys Asp Arg Asp Ser Gly Gln Leu Tyr Val Ile Gln Glu Gly Leu
290 295 300
Glu Ser Thr Gly Cys Thr Leu Val Phe Leu Val Leu Tyr Tyr Phe Gly
305 310 315 320
Met Ala Ser Ser Leu Trp Trp Val Val Leu Thr Leu Thr Trp Phe Leu
325 330 335
Ala Ala Gly Lys Lys Trp Gly His Glu Ala Ile Glu Ala Asn Ser Ser
340 345 350
Tyr Phe His Leu Ala Ala Trp Ala Ile Pro Ala Val Lys Thr Ile Leu
355 360 365
Ile Leu Val Met Arg Arg Val Ala Gly Asp Glu Leu Thr Gly Val Cys
370 375 380
Tyr Val Gly Ser Met Asp Val Asn Ala Leu Thr Gly Phe Val Leu Ile
385 390 395 400
Pro Leu Ala Cys Tyr Leu Val Ile Gly Thr Ser Phe Ile Leu Ser Gly
405 410 415
Phe Val Ala Leu Phe His Ile Arg Arg Val Met Lys Thr Gly Gly Glu
420 425 430
Asn Thr Asp Lys Leu Glu Lys Leu Met Val Arg Ile Gly Leu Phe Ser
435 440 445
Val Leu Tyr Thr Val Pro Ala Thr Cys Val Ile Ala Cys Tyr Phe Tyr
450 455 460
Glu Arg Leu Asn Met Asp Tyr Trp Lys Ile Leu Ala Ala Gln His Lys
465 470 475 480
Cys Lys Met Asn Asn Gln Thr Lys Thr Leu Asp Cys Leu Met Ala Ala
485 490 495
Ser Ile Pro Ala Val Glu Ile Phe Met Val Lys Ile Phe Met Leu Leu
500 505 510
Val Val Gly Ile Thr Ser Gly Met Trp Ile Trp Thr Ser Lys Thr Leu
515 520 525
Gln Ser Trp Gln Gln Val Cys Ser Arg Arg Leu Lys Lys Lys Ser Arg
530 535 540
Arg Lys Pro Ala Ser Val Ile Thr Ser Gly Gly Ile Tyr Lys Lys Ala
545 550 555 560
Gln His Pro Gln Lys Thr His His Gly Lys Tyr Glu Ile Pro Ala Gln
565 570 575
Ser Pro Thr Cys Val
580
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОКЛОНАЛЬНОЕ АНТИТЕЛО ПРОТИВ MELK И ЕГО ИСПОЛЬЗОВАНИЕ | 2017 |
|
RU2756982C2 |
| НАЦЕЛЕННЫЕ НА uPARAP КОНЪЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2017 |
|
RU2740311C2 |
| СТАБИЛЬНЫЕ СОСТАВЫ АНТИТЕЛ ПРОТИВ TIGIT, ОТДЕЛЬНО И В КОМБИНАЦИИ С АНТИТЕЛАМИ ПРОТИВ РЕЦЕПТОРА 1 ПРОГРАММИРУЕМОЙ СМЕРТИ (PD-1), И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2820576C2 |
| АНТИТЕЛА И МЕТОДЫ АНАЛИЗА ДЛЯ ОБНАРУЖЕНИЯ РЕЦЕПТОРА ФОЛИЕВОЙ КИСЛОТЫ 1 | 2014 |
|
RU2725825C2 |
| БИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2839153C2 |
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800923C2 |
| АНТИТЕЛА В7-Н4 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2809243C2 |
| АНТИТЕЛА К БЕЛКУ CD38 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2776795C2 |
| ЧЕЛОВЕЧЕСКИЕ АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С ROR2 | 2018 |
|
RU2784586C2 |
| КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ МОДУЛЯЦИИ ПЕРЕДАЧИ СИГНАЛА LAIR | 2017 |
|
RU2757394C2 |
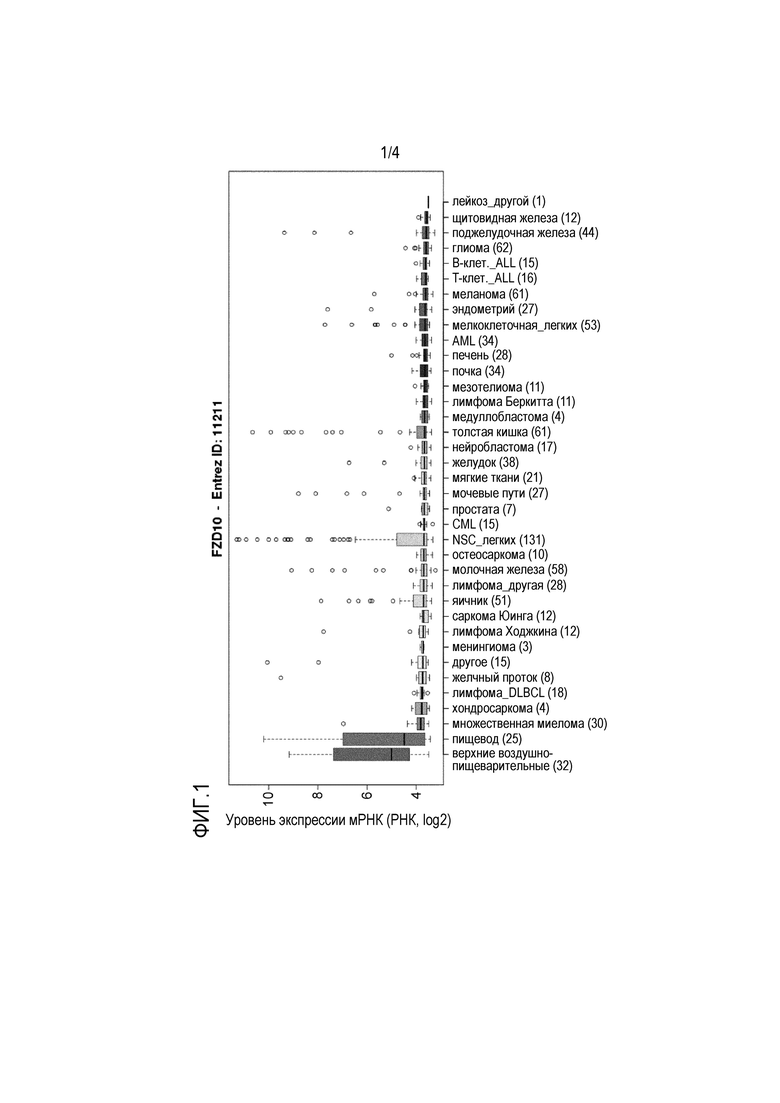

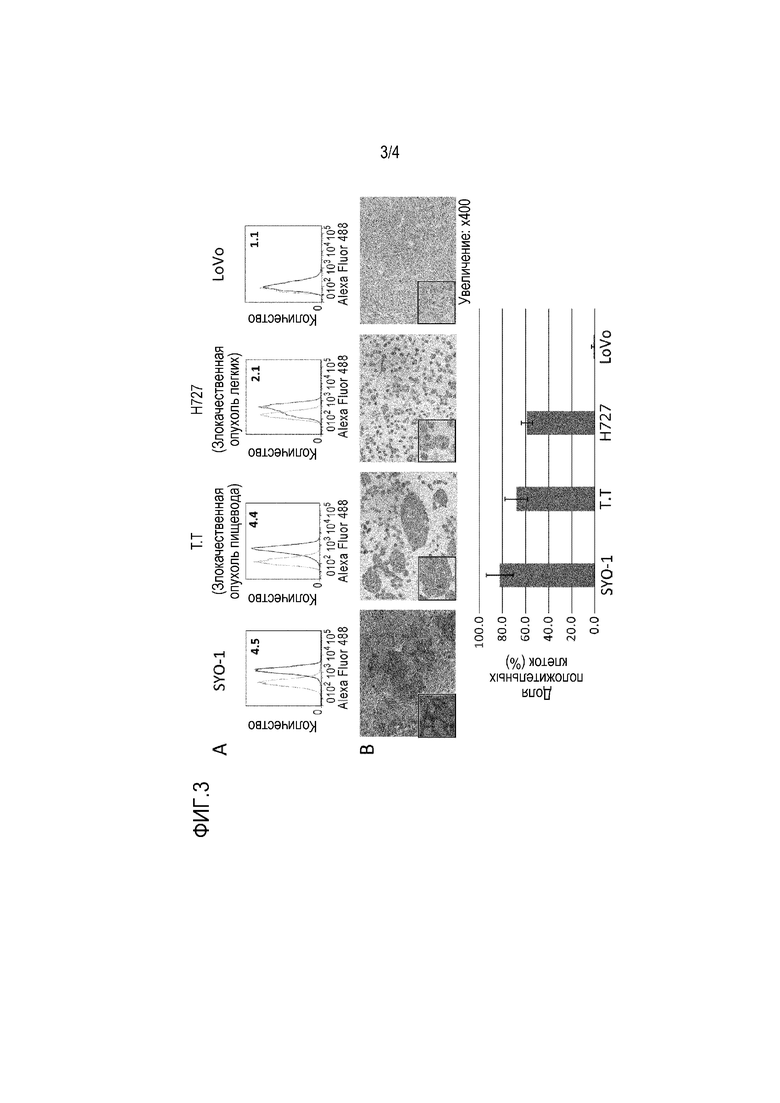
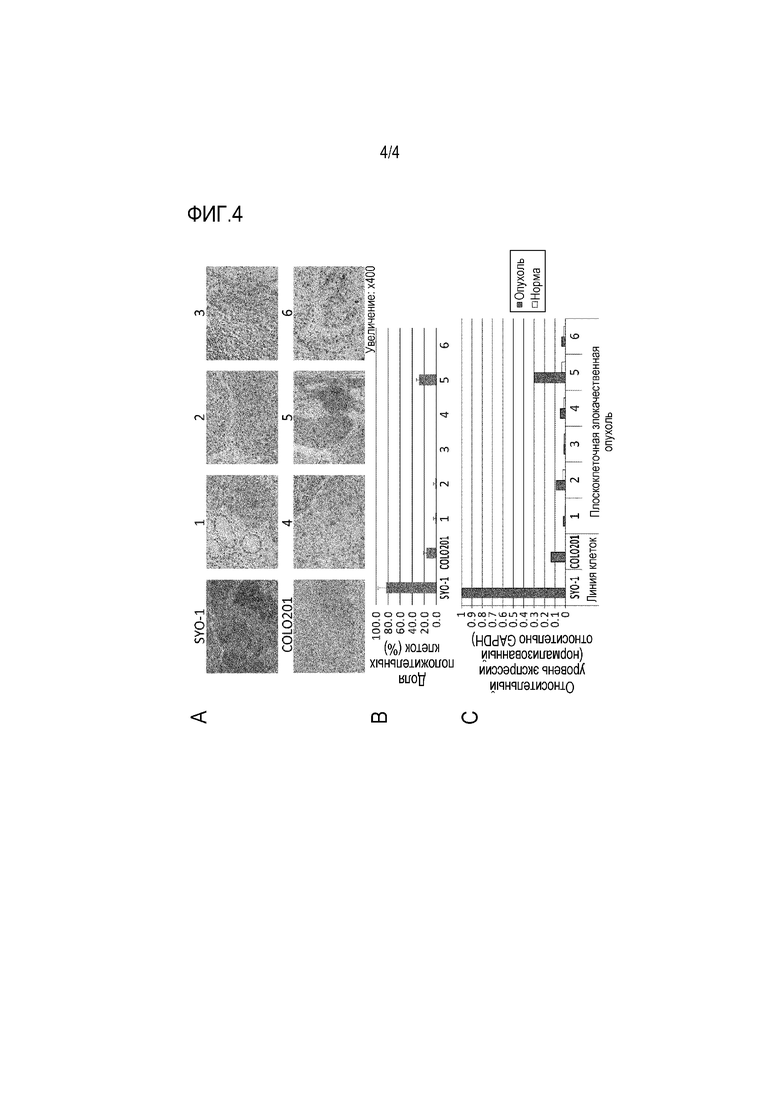
Изобретение относится к области биохимии, в частности к антителу, которое специфически связывается с белком FZD10. Также раскрыты полинуклеотид, кодирующий указанное антитело. Раскрыты способ диагностирования, связанного с FZD10 заболевания, способ обнаружения белка FZD10, способ скрининга субъекта, способ получения антитела, с помощью указанного антитела. Изобретение обладает способностью эффективно лечить заболевания, ассоциированные с белком FZD10. 8 н. и 6 з.п. ф-лы, 4 ил., 4 пр.
1. Антитело или его антигенсвязывающий фрагмент, отличающиеся тем, что антитело или его антигенсвязывающий фрагмент специфически связывается с белком FZD10 или его частичным пептидом, который содержит аминокислотную последовательность SEQ ID NO: 9, где антитело или его антигенсвязывающий фрагмент содержит обе из:
вариабельной области тяжелой цепи, содержащей
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 1,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 2, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 3; и
вариабельной области легкой цепи, содержащей
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 4,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 5, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 6.
2. Антитело или его антигенсвязывающий фрагмент по п. 1, отличающиеся тем, что антитело или его антигенсвязывающий фрагмент содержит обе из вариабельной области тяжелой цепи, содержащей аминокислотную последовательность из SEQ ID NO: 7, и вариабельной области легкой цепи, содержащей аминокислотную последовательность из SEQ ID NO: 8.
3. Антитело или его антигенсвязывающий фрагмент по п. 1 или 2, отличающиеся тем, что антитело или его антигенсвязывающий фрагмент специфически распознает полипептид, состоящий из аминокислотной последовательности из SEQ ID NO: 9.
4. Антитело или его антигенсвязывающий фрагмент по любому из пп. 1–3, которые конъюгируют с аффинной меткой, ферментативной меткой, радиоизотопной меткой или флуоресцентной меткой.
5. Полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент, по любому из пп. 1-3.
6. Меченое антитело для обнаружения FZD10 в соответствии с экспрессией уровня FZD10, где меченое антитело содержит подходящее количество антитела или его антигенсвязывающего фрагмента, достаточное для обнаружения белка FZD10, где антитело или его антигенсвязывающий фрагмент специфически связывается с белком FZD10 или его частичным пептидом, который содержит аминокислотную последовательность SEQ ID NO: 9, где антитело или его антигенсвязывающий фрагмент содержит обе из:
вариабельной области тяжелой цепи, содержащей
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 1,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 2, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 3; и
вариабельной области легкой цепи, содержащей
CDR1, содержащую аминокислотную последовательность из SEQ ID NO: 4,
CDR2, содержащую аминокислотную последовательность из SEQ ID NO: 5, и
CDR3, содержащую аминокислотную последовательность из SEQ ID NO: 6.
7. Способ диагностирования связанного с FZD10 заболевания или предрасположенности к развитию заболевания у субъекта, где способ включает стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из пп. 1-4;
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с контролем, где более высокий уровень белка FZD10, чем контроль, указывает на то, что субъект страдает заболеванием или имеет риск развития заболевания.
8. Способ по п. 7, где связанное с FZD10 заболевание представляет собой злокачественную опухоль, экспрессирующую FZD10.
9. Способ по п. 8, где злокачественную опухоль выбирают из группы, состоящей из синовиальной саркомы, злокачественной опухоли легких, злокачественной опухоли пищевода, злокачественной опухоли толстой кишки (карциномы толстой кишки), злокачественной опухоли желудка, хронического миелолейкоза (CML) и острого миелолейкоза (AML).
10. Способ обнаружения белка FZD10 в образце, который включает стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из пп. 1-4; и
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом.
11. Способ определения лекарственного эффекта после лечения ингибитором FZD10 у субъекта, где способ включает стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из пп. 1-4;
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с уровнем экспрессии перед введением лекарственного средства, где уровень белка FZD10 ниже такового перед введением лекарственного средства указывает на то, что лекарственное средство эффективно у субъекта.
12. Способ скрининга субъекта, у которого лечение ингибитором FZD10 является высокоэффективным, где способ включает стадии:
(a) приведения в контакт образца, выделенного у субъекта, с антителом или его антигенсвязывающим фрагментом по любому из пп. 1-4;
(b) обнаружения белка FZD10 в образце посредством обнаружения связывания между антителом или его антигенсвязывающим фрагментом и образцом; и
(c) сравнения уровня белка FZD10 в образце с контролем, где уровень белка FZD10, который равен или выше чем контроль, указывает на то, что лечение ингибитором FZD10 является высокоэффективным у субъекта.
13. Способ по любому из пп. 7-12, в котором образец представляет собой клетку или ткань, выделенные у субъекта.
14. Способ получения антитела или его антигенсвязывающего фрагмента по любому из пп. 1-3, где способ включает стадии:
(a) культивирования клетки, содержащей вектор, в который введен полинуклеотид по п. 5; и
(b) сбора антитела из культуры или среды для культивирования клетки.
| НАПРАВЛЕННЫЕ НА ОПУХОЛЬ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА ПРОТИВ FZD10 И ИХ ПРИМЕНЕНИЕ | 2006 |
|
RU2412203C2 |
| Огнепреградитель | 1988 |
|
SU1648506A2 |
| WO 2013025446 A3, 21.02.2013. | |||
Авторы
Даты
2022-01-31—Публикация
2017-10-04—Подача