ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к составам терапевтических антител и к их использованию для лечения различных нарушений. В одном аспекте изобретение относится к составам, содержащим антитела или их антигенсвязывающие фрагменты, которые связываются с T-клеточным иммунорецептором с доменами Ig и ITIM (TIGIT). В другом аспекте такой состав дополнительно содержит антитело против рецептора 1 программируемой смерти (PD-1) или его антигенсвязывающий фрагмент. Настоящее изобретение относится также к способам лечения различных злокачественных опухолей и хронических инфекций с использованием составов по изобретению.
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет по U.S.S.N. 62/500278, поданной 2 мая 2017 г., полное содержание которой приведено в настоящем описании в качестве ссылки.
ССЫЛКА НА СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ, ПРИНЯТЫЙ В ЭЛЕКТРОННОЙ ФОРМЕ
Список последовательностей настоящей заявки принят в электронной форме через EFS-Web как список последовательностей в формате ASCII, с наименованием файла «24453WOPCT-SEQTXT-01MAY2018.TXT», датой создания 1 мая 2018 г. и размером 227 кб. Этот список последовательностей, принятый через EFS-Web, является частью описания, и его полное содержание приведено в настоящем описании в качестве ссылки.
УРОВЕНЬ ТЕХНИКИ ДЛЯ ИЗОБРЕТЕНИЯ
Лекарственные средства на основе антител для использования у человека могут несколько отличаться по аминокислотной последовательности их константных доменов или по их каркасным последовательностям внутри вариабельных доменов, однако, они, как правило, наиболее существенно отличаются по последовательностям CDR. Даже антитела, связывающие один и тот же белок, один и тот же полипептид или даже, потенциально, один и тот же эпитоп, могут содержать полностью различные последовательности CDR. Терапевтические антитела для использования у человека можно также получать из зародышевой последовательности антитела человека или из зародышевых последовательностей из не относящихся к человеку (например, грызунов) антител, например, как в гуманизированных антителах, что приводит к дополнительному разнообразию потенциальных последовательностей CDR. Эти различия последовательности приводят к различной стабильности в растворе и к различной способности реагировать на параметры раствора. Кроме того, небольшие изменения в аранжировке аминокислот или изменения в одном или нескольких остатках аминокислот могут приводить к очень сильно отличающейся стабильности антитела и его чувствительности к путям специфической для последовательности деградации. Следовательно, в настоящее время не является возможным прогнозировать условия раствора, необходимые для оптимизации стабильности антитела. Каждое антитело необходимо исследовать индивидуально для определения оптимального состава раствора. Bhambhani et al. (2012) J. Pharm. Sci. 101:1120.
Антитела также представляют собой относительно высокомолекулярные белки (~150000 Да), например, по сравнению с другими терапевтическими белками, такими как гормоны и цитокины. Следовательно, часто является необходимым дозирование с относительно высокими весовыми количествами лекарственных средств на основе антител для достижения желательных молярных концентраций лекарственного средства. Кроме того, часто является желательным подкожное введение лекарственных средств на основе антител, поскольку это позволяет самостоятельное введение. Самостоятельное введение исключает затрату времени и средств, ассоциированную с посещением медицинского учреждения для введения, например, внутривенно. Подкожная доставка ограничена объемом раствора, который практически можно доставлять в участок инъекции в однократной инъекции, который, как правило, составляет приблизительно 1-1,5 мл. Подкожное самостоятельное введение, как правило, осуществляют с использованием предварительно заполненного шприца или автоинжектора, заполненного жидким раствором состава лекарственного средства, а не лиофилизированной формой, чтобы избежать необходимости для пациента ресуспендировать лекарственное средство перед инъекцией. Лекарственные средства на основе антител должны являться стабильными во время хранения, для обеспечения эффективности и единообразного дозирования, таким образом, является критическим, чтобы любой выбранный состав поддерживал желательные свойства, такие как высокая концентрация, прозрачность и приемлемая вязкость, и чтобы он также поддерживал эти свойства и эффективность лекарственного средства на протяжении приемлемо длительного срока хранения в типичных условиях хранения.
TIGIT (T-клеточный иммунорецептор с доменами Ig и ITIM) представляет собой иммуномодулирующий рецептор, экспрессированный, в первую очередь, на активированных T-клетках и клетках NK. TIGIT также известен как VSIG9; VSTM3; и WUCAM. В его структуре показаны один внеклеточный иммуноглобулиновый домен, трансмембранная область типа 1 и два мотива ITIM. TIGIT формирует часть костимулирующей сети, которая состоит из положительного (CD226) и отрицательного (TIGIT) иммуномодулирующих рецепторов на T-клетках, и лигандов, экспрессировванных на APC (CD155 и CD112).
Важным признаком структуры TIGIT является присутствие иммунорецепторного связывающего тирозин ингибирующего мотива (ITIM) в его цитоплазматическом хвостовом домене. Как и для PD-1 и TIGIT, прогнозируют, что домен ITIM в цитоплазматической области TIGIT привлекает тирозинфосфатазы, такие как SHP-1 и SHP-2, и за этим следует дефосфорилирование остатков тирозина внутри иммунорецепторных активирующих мотивов на основе тирозина (ITAM) на субъединицах T-клеточного рецептора (TCR). Таким образом, связывание TIGIT посредством рецепторов-лигандов CD155 и CD112, экспрессированных клетками опухолей или TAM, может вносить вклад в супрессию передачи сигналов TCR и активации T-клеток, которые являются необходимыми для поддержания эффективного противоопухолевого иммунитета. Таким образом, антагонистическое антитело, специфическое для TIGIT, может ингибировать индуцированную CD155 и CD112 супрессию ответов T-клеток и усиливать противоопухолевый иммунитет.
Существует необходимость в стабильных составах антител против TIGIT для фармацевтического использования, например, для лечения различных злокачественных опухолей и инфекционных заболеваний, так же как в стабильных составах антител против TIGIT, в совместном составе с антителами против PD-1 человека. Предпочтительно, такие составы могут иметь длительный срок хранения, являться стабильными при хранении и транспортировке, и могут, предпочтительно, иметь стабильность в течение от нескольких месяцев до нескольких лет в условиях, типичных для хранения лекарственных средств для самостоятельного введения, т.е. при температуре холодильника в шприце, что приводит к длительному сроку хранения соответствующего продукта лекарственного средства.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте изобретение относится к составу антитела против TIGIT или его антигенсвязывающего фрагмента, содержащему (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент; (ii) буфер, (iii) невосстанавливающий сахар; (iv) неионное поверхностно-активное вещество; и (v) антиоксидант. В другом варианте осуществления, состав дополнительно содержит антитело против PD-1, например, пембролизумаб или ниволумаб. В другом варианте осуществления, состав дополнительно содержит хелатирующий агент.
В одном варианте осуществления, состав содержит (i) от приблизительно 10 мг/мл до приблизительно 200 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента; (ii) от приблизительно 5 мМ до приблизительно 20 мМ буфера; (iii) от приблизительно 6% до приблизительно 8% по массе/объему (масс./об.) невосстанавливающего сахара; (iv) от приблизительно 0,01% до приблизительно 0,10% (масс./об.) неионного поверхностно-активного вещества; и (v) от приблизительно 1 мМ до приблизительно 20 мМ антиоксиданта. В одном варианте осуществления, состав дополнительно содержит антитело против PD-1, например, пембролизумаб или ниволумаб. В другом варианте осуществления, состав дополнительно содержит хелатирующий агент. В одном варианте осуществления, состав имеет pH между 4,5-6,5. В конкретных вариантах осуществления, pH состава составляет от приблизительно pH 5,5 до приблизительно pH 6,2. В следующем варианте осуществления, pH состава составляет от приблизительно pH 5,6 до приблизительно pH 6,0. В другом варианте осуществления, pH состава составляет приблизительно 5,7. В другом варианте осуществления, pH состава составляет приблизительно 5,8. В другом варианте осуществления, pH состава составляет приблизительно 5,9. В другом варианте осуществления, pH состава составляет приблизительно 6,0. В другом варианте осуществления, pH состава составляет приблизительно 6,1. В другом варианте осуществления, pH состава составляет приблизительно 6,2.
В одном варианте осуществления состава, буфер представляет собой L-гистидиновый буфер или ацетат натрия, невосстанавливающий сахар представляет собой сахарозу, неионное поверхностно-активное вещество представляет собой полисорбат 80, и антиоксидант представляет собой метионин или его фармацевтически приемлемую соль. В одном варианте осуществления, антиоксидант представляет собой L-метионин. В другом варианте осуществления, антиоксидант представляет собой фармацевтически приемлемую соль L-метионина, например, такую как метионин HCl.
В другом варианте осуществления, состав содержит (i) от приблизительно 10 мг/мл до приблизительно 200 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента; (ii) от приблизительно 5 мМ до приблизительно 20 мМ L-гистидинового буфера или буфер от приблизительно 5 мМ до приблизительно 20 мМ ацетат натрия; (iii) от приблизительно 6% до приблизительно 8% масс./об. сахарозы; (iv) от приблизительно 0,01% до приблизительно 0,10% масс./об. полисорбата 80; и (v) от приблизительно 1 мМ до приблизительно 20 мМ L-метионина. В другом варианте осуществления, состав дополнительно содержит антитело против PD-1, например, пембролизумаб или ниволумаб. В одном варианте осуществления, состав дополнительно содержит хелатирующий агент. В одном варианте осуществления, хелатирующий агент присутствует в количестве от приблизительно 1 мкМ до приблизительно 50 мкМ. В одном варианте осуществления, хелатирующий агент представляет собой ДТПА. В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА. В одном варианте осуществления, буфер представляет собой L-гистидиновый буфер. В одном варианте осуществления, состав содержит от приблизительно 5 мМ до приблизительно 20 мМ L-гистидинового буфера. В другом варианте осуществления, состав содержит от приблизительно 5 мМ до приблизительно 10 мМ L-метионина. В следующем варианте осуществления, состав содержит полисорбат 80 в массовой доле приблизительно 0,02% масс./об. В одном варианте осуществления, состав антитела против TIGIT содержит сахарозу в массовой доле приблизительно 7% (масс./об.). В любом из этих вариантов осуществления, метионин представляет собой L-метионин.
В вариантах осуществления состава, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет от приблизительно 10 мг/мл до приблизительно 100 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 10 мг/мл, 12,5 мг/мл, 15 мг/мл, 20 мг/мл, 25 мг/мл, 50 мг/мл, 75 мг/мл или 100 мг/мл. В одном варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 20 мг/мл. В одном варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 25 мг/мл. В одном варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 50 мг/мл. В одном варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 75 мг/мл. В одном варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 100 мг/мл.
В одном аспекте, настоящее изобретение относится к составу, содержащему приблизительно 20 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном аспекте, настоящее изобретение относится к составу, содержащему приблизительно 25 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном аспекте, настоящее изобретение относится к составу, содержащему приблизительно 50 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном аспекте, настоящее изобретение относится к составу, содержащему приблизительно 75 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном аспекте, настоящее изобретение относится к составу, содержащему приблизительно 100 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном аспекте любого из вышеуказанных составов, состав имеет pH от приблизительно 5,4 до приблизительно 6,2. В другом аспекте состав имеет pH приблизительно 5,5-6,2. В другом варианте осуществления, состав имеет pH приблизительно 5,8-6,1. В другом варианте осуществления, pH составляет приблизительно 5,8. В одном варианте осуществления, pH составляет 5,9. В другом варианте осуществления pH составляет 6,0. В следующем варианте осуществления pH составляет 6,1.
В одном аспекте любого из вышеуказанных составов, состав содержит антитело против PD1 или его антигенсвязывающий фрагмент. В одном варианте осуществления, антитело против PD1 представляет собой пембролизумаб. В другом аспекте, антитело против PD1 представляет собой ниволумаб.
В другом аспекте, состав может дополнительно содержать хелатирующий агент. В одном варианте осуществления, хелатирующий агент представляет собой ДТПА. В одном варианте осуществления, хелатирующий агент представляет собой ЭДТА. В одном аспекте, хелатирующий агент присутствует в количестве от приблизительно 1мкМ до приблизительно 50 мкМ. В одном варианте осуществления, состав содержит приблизительно 5 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 10 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 15 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 20 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 25 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 30 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 35 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 40 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 45 мкМ хелатирующий агент. В одном варианте осуществления, состав содержит приблизительно 50 мкМ хелатирующий агент. В одном варианте осуществления, хелатирующий агент представляет собой ДТПА, присутствующую в любом из количеств, указанных выше. В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА, присутствующую в любом из количеств, указанных выше.
В одном варианте осуществления, состав содержится в стеклянном флаконе. В другом варианте осуществления, состав содержится в устройстве для инъекций. В другом варианте осуществления, состав представляет собой жидкий состав. В одном аспекте состав является замороженным при по меньшей мере ниже -70°C. В другом варианте осуществления, состав представляет собой раствор, разведенный из лиофилизированного состава.
В конкретных вариантах осуществления, состав является стабильным при температуре холодильника (2-8°C) в течение по меньшей мере 3 месяцев, предпочтительно, 6 месяцев, и более предпочтительно, 1 года, и даже более предпочтительно, вплоть до 2 лет. В одном варианте осуществления состава, через 12 месяцев при 5°C % мономера антитела против TIGIT составляет ≥ 90%, как определено посредством эксклюзионной хроматографии. В другом варианте осуществления состава, через 12 месяцев при 5°C % тяжелой цепи и легкой цепи антитела против TIGIT составляет ≥ 90%, как определено посредством восстанавливающего CE-SDS. В другом варианте осуществления состава, через 12 месяцев при 5°C % тяжелой цепи и легкой цепи антитела против TIGIT составляет ≥ 95%, как определено посредством восстанавливающего CE-SDS. В другом варианте осуществления состава, через 12 месяцев при 5°C % интактного антитела IgG против TIGIT составляет ≥ 90%, как определено посредством невосстанавливающего CE-SDS. В другом варианте осуществления состава, через 12 месяцев при 5°C % интактного антитела IgG против TIGIT составляет ≥ 95%, как определено посредством невосстанавливающего CE-SDS.
В одном аспекте любого из составов, описанных выше, состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:111 или ее вариант, CDRL2 из SEQ ID NO:112 или ее вариант, CDRL3 из SEQ ID NO:113 или ее вариант, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:108 или ее вариант, CDRH2 из SEQ ID NO:154 или ее вариант и CDHR3 из SEQ ID NO:110 или ее вариант. В одном аспекте любого из составов, описанных выше, состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:111, CDRL2 из SEQ ID NO:112, CDRL3 из SEQ ID NO:113, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:108, CDRH2 из SEQ ID NO:154 и CDHR3 из SEQ ID NO:110. В другом аспекте состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148 или ее вариант, и вариабельную область легкой цепи, содержащую SEQ ID NO:152 или ее вариант. В другом аспекте состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и вариабельную область легкой цепи, содержащую SEQ ID NO:152. В одном аспекте, анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:291 или ее вариант, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293 или ее вариант. В одном аспекте анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:291, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293. В другом аспекте анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG4 человека, содержащий аминокислотную последовательность из SEQ ID NO:292, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293. В другом аспекте, анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG4 человека, содержащий аминокислотную последовательность из SEQ ID NO:292 или ее вариант, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293 или ее вариант.
В одном аспекте настоящее изобретение относится к совместному составу антитела против TIGIT или его антигенсвязывающего фрагмента, и антитела против PD-1 человека или его антигенсвязывающего фрагмента, содержащему (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент; (ii) антитело против PD-1 человека, или его антигенсвязывающий фрагмент, (ii) буфер, (iii) невосстанавливающий сахар; (iv) неионное поверхностно-активное вещество; и (v) антиоксидант. В одном варианте осуществления, совместный состав дополнительно содержит хелатирующий агент. В одном варианте осуществления хелатирующий агент представляет собой ЭДТА. В другом варианте осуществления, хелатирующий агент представляет собой ДТПА. В одном варианте осуществления совместного состава, соотношение антитела против PD-1 человека к антителу против TIGIT составляет 1:2. В одном варианте осуществления совместного состава, соотношение антитела против PD-1 человека к антителу против TIGIT составляет 1:1. В одном варианте осуществления совместного состава, соотношение антитела против PD-1 человека к антителу против TIGIT составляет 2:1.
В одном варианте осуществления изобретения, совместный состав содержит (i) от приблизительно 1 мг/мл до приблизительно 200 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента; (ii) от приблизительно 1 мг/мл до приблизительно 200 мг/мл антитела против PD-1 человека; (iii) от приблизительно 5 мМ до приблизительно 20 мМ буфера; (iv) от приблизительно 6% до приблизительно 8% по массе/объему (масс./об.) невосстанавливающего сахара; (v) от приблизительно 0,01% до приблизительно 0,10% (масс./об.) неионного поверхностно-активного вещества; и (vi) от приблизительно 1 мМ до приблизительно 20 мМ антиоксиданта. В одном варианте осуществления, совместный состав дополнительно содержит хелатирующий агент. В одном варианте осуществления, хелатирующий агент присутствует в количестве от приблизительно 1 мкМ до приблизительно 50 мкМ. В одном варианте осуществления, хелатирующий агент представляет собой ДТПА. В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА. В одном варианте осуществления совместного состава, соотношение антитела против PD-1 человека к антителу против TIGIT составляет 1:2. В одном варианте осуществления совместного состава, соотношение антитела против PD-1 человека к антителу против TIGIT составляет 1:1. В одном варианте осуществления совместного состава, соотношение антитела против PD-1 человека к антителу против TIGIT составляет 2:1. В одном варианте осуществления, совместный состав имеет pH между 4,5 и 6,5. В конкретных вариантах осуществления, pH состава составляет от приблизительно pH 5,5 до приблизительно pH 6,2. В следующем варианте осуществления, pH состава составляет приблизительно pH 5,8-6,0.
В одном варианте осуществления совместного состава, буфер представляет собой гистидиновый буфер или буфер ацетат натрия, невосстанавливающий сахар представляет собой сахарозу, неионное поверхностно-активное вещество представляет собой полисорбат 80, и антиоксидант представляет собой L-метионин. В другом варианте осуществления, совместный состав содержит (i) от приблизительно 1 мг/мл до приблизительно 100 мг/мл антитела против TIGIT или его антигенсвязывающего фрагмента; (ii) от приблизительно 1 мг/мл до приблизительно 100 мг/мл антитела против PD-1 человека или его антигенсвязывающего фрагмента; (iii) от приблизительно 5 мМ до приблизительно 20 мМ L-гистидин или буфер ацетат натрия от приблизительно 5 мМ до приблизительно 20 мМ; (iv) от приблизительно 6% до приблизительно 8% масс./об. сахарозы; (v) от приблизительно 0,01% до приблизительно 0,10% (масс./об.) полисорбата 80; и (vi) от приблизительно 1 мМ до приблизительно 20 мМ L-метионина. В одном варианте осуществления, совместный состав, необязательно, содержит хелатирующий агент. В одном варианте осуществления, хелатирующий агент присутствует в количестве от приблизительно 1 мкМ до приблизительно 50 мкМ. В одном варианте осуществления, хелатирующий агент представляет собой ДТПА. В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА. В одном варианте осуществления, буфер представляет собой L-гистидиновый буфер. В одном варианте осуществления, совместный состав содержит от приблизительно 8 мМ до приблизительно 12 мМ L-гистидинового буфера. В другом варианте осуществления, совместный состав содержит от приблизительно 5 мМ до приблизительно 10 мМ L-метионина. В следующем варианте осуществления, совместный состав содержит полисорбат 80 в массовой доле приблизительно 0,02% масс./об. В одном варианте осуществления, совместный состав содержит сахарозу в массовой доле приблизительно 7% (масс./об.).
В вариантах осуществления совместного состава, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет от приблизительно 1 мг/мл до приблизительно 100 мг/мл. В вариантах осуществления совместного состава, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет от приблизительно 10 мг/мл до приблизительно 100 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 10 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 12,5 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 20 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 25 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 50 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 75 мг/мл. В другом варианте осуществления, концентрация антитела против TIGIT или его антигенсвязывающего фрагмента составляет приблизительно 100 мг/мл.
В некоторых вариантах осуществления совместного состава, концентрация антитела против PD-1 человека составляет от приблизительно 1 мг/мл до приблизительно 100 мг/мл. В одном варианте осуществления совместного состава, концентрация антитела против PD-1 человека составляет от приблизительно 10 мг/мл до приблизительно 100 мг/мл. В другом варианте осуществления, концентрация антитела против PD-1 человека составляет 20 мг/мл. В другом варианте осуществления, концентрация антитела против PD-1 человека составляет 25 мг/мл.
В одном варианте осуществления, совместный состав содержит приблизительно 20 мг/мл антитела против PD1, приблизительно 20 мг/мл антитела против TIGIT, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном варианте осуществления, совместный состав содержит приблизительно 25 мг/мл антитела против PD1, приблизительно 25 мг/мл антитела против TIGIT, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном варианте осуществления, совместный состав содержит приблизительно 50 мг/мл антитела против PD1, приблизительно 50 мг/мл антитела против TIGIT, 10 мМ L-гистидинового буфера, приблизительно 7% масс./об. сахарозы, приблизительно 0,02% масс./об. полисорбата 80 и приблизительно 10 мМ L-метионина.
В одном аспекте любого из составов, описанных выше, состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:111 или ее вариант, CDRL2 из SEQ ID NO:112 или ее вариант, CDRL3 из SEQ ID NO:113 или ее вариант, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:108 или ее вариант, CDRH2 из SEQ ID NO:154 или ее вариант и CDHR3 из SEQ ID NO:110 или ее вариант. В одном аспекте любого из составов, описанных выше, состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:111, CDRL2 из SEQ ID NO:112, CDRL3 из SEQ ID NO:113, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:108, CDRH2 из SEQ ID NO:154 и CDHR3 из SEQ ID NO:110. В другом аспекте состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148 или ее вариант, и вариабельную область легкой цепи, содержащую SEQ ID NO:152 или ее вариант. В другом аспекте состав содержит анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и вариабельную область легкой цепи, содержащую SEQ ID NO:152. В одном аспекте анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:291 или ее вариант, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293 или ее вариант. В одном аспекте анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:291, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293. В другом аспекте анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG4 человека, содержащий аминокислотную последовательность из SEQ ID NO:292 или ее вариант, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293 или ее вариант. В другом аспекте анти-TIGIT антитело или его антигенсвязывающий фрагмент дополнительно содержит константный домен тяжелой цепи IgG4 человека, содержащий аминокислотную последовательность из SEQ ID NO:292, и константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293.
В одном аспекте любого из составов, описанных выше, антитело против PD-1 человека или его антигенсвязывающий фрагмент содержит три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:1 или ее вариант, CDRL2 из SEQ ID NO:2 или ее вариант, CDRL3 из SEQ ID NO:3 или ее вариант, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:6 или ее вариант, CDRH2 из SEQ ID NO:7 или ее вариант и CDHR3 из SEQ ID NO:8 или ее вариант. В одном аспекте любого из составов, описанных выше, антитело против PD-1 человека или его антигенсвязывающий фрагмент содержит три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:1, CDRL2 из SEQ ID NO:2, CDRL3 из SEQ ID NO:3, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:6, CDRH2 из SEQ ID NO:7 и CDHR3 из SEQ ID NO:8. В другом аспекте составы содержат антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие вариабельную область легкой цепи, содержащую SEQ ID NO:4 или ее вариант, и вариабельную область тяжелой цепи, содержащую SEQ ID NO:9 или ее вариант. В другом аспекте составы содержат антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие вариабельную область легкой цепи, содержащую SEQ ID NO:4, и вариабельную область тяжелой цепи, содержащую SEQ ID NO:9. В другом аспекте составы содержат антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие легкую цепь, содержащую SEQ ID NO:5, и тяжелую цепь, содержащую SEQ ID NO:10. В другом аспекте составы содержат антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие легкую цепь, содержащую SEQ ID NO:5 или ее вариант, и тяжелую цепь, содержащую SEQ ID NO:10 или ее вариант. В одном аспекте любого из составов, описанных выше, антитело против PD1 человека или его антигенсвязывающий фрагмент представляет собой пембролизумаб. В другом аспекте антитело против PD1 человека или его антигенсвязывающий фрагмент представляет собой ниволумаб.
В одном аспекте любого из совместных составов, описанных выше, состав содержит (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:111, CDRL2 из SEQ ID NO:112, CDRL3 из SEQ ID NO:113, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:108, CDRH2 из SEQ ID NO:154 и CDHR3 из SEQ ID NO:110, и (ii) антитело против PD-1 человека или его антигенсвязывающий фрагмент, содержащие три CDR легкой цепи и три CDR тяжелой цепи, где CDR легкой цепи содержат CDRL1 из SEQ ID NO:1, CDRL2 из SEQ ID NO:2, CDRL3 из SEQ ID NO:3, и CDR тяжелой цепи содержат CDRH1 из SEQ ID NO:6, CDRH2 из SEQ ID NO:7, и CDHR3 из SEQ ID NO:8.
В одном аспекте любого из совместных составов, описанных выше, состав содержит (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и вариабельную область легкой цепи, содержащую SEQ ID NO:152, и (ii) антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие вариабельную область легкой цепи, содержащую SEQ ID NO:4, и вариабельную область тяжелой цепи, содержащую SEQ ID NO:9.
В другом аспекте любого из совместных составов, описанных выше, состав содержит (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и дополнительно содержащие константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:291, и вариабельную область легкой цепи, содержащую SEQ ID NO:152, и дополнительно содержащие константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293, и (ii) антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие легкую цепь, содержащую SEQ ID NO:5, и тяжелую цепь, содержащую SEQ ID NO:10.
В другом аспекте любого из совместных составов, описанных выше, состав содержит (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, содержащие вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и дополнительно содержащие константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:292, и вариабельную область легкой цепи, содержащую SEQ ID NO:152, и дополнительно содержащие константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293, и (ii) антитело против PD1 человека или его антигенсвязывающий фрагмент, содержащие легкую цепь, содержащую SEQ ID NO:5, и тяжелую цепь, содержащую SEQ ID NO:10.
В одном варианте осуществления любого из составов, описанных выше, состав содержится в стеклянном флаконе. В другом варианте осуществления, состав содержится в устройстве для инъекций. В другом варианте осуществления, состав представляет собой жидкий состав. В одном аспекте состав является замороженным при по меньшей мере ниже -70°C. В другом варианте осуществления, состав представляет собой раствор, разведенный из лиофилизированного состава.
Настоящее изобретение относится к способу лечения хронической инфекции или злокачественной опухоли у нуждающегося в этом субъекта-млекопитающего (например, человека), включающим: введение эффективного количества состава антитела против TIGIT или совместного состава, указанного в настоящем описании.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На ФИГУРЕ 1 показана стабильность pH составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 2 показана стабильность концентрации полисорбата 80 для составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 3 показаны данные стабильности активности в ELISA для составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 4 показаны данные стабильности мономера (%) по UP-SEC для составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 5 показаны данные стабильности высокомолекулярных (HMW) молекул (%) по UP-SEC для составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 6 показаны данные стабильности низкомолекулярных (LMW) молекул (%) по UP-SEC для составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 7 показаны данные стабильности чистоты тяжелой цепи+легкой цепи (%) по восстанавливающему CE-SDS для составов в течение 9 месяцев в различных условиях хранения.
На ФИГУРЕ 8 показаны данные стабильности чистоты интактного IgG (%)по невосстанавливающему CE-SDS для составов в течение 9 месяцев в различных условиях хранения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном аспекте изобретение относится к составам, содержащим антитела против TIGIT и их антигенсвязывающие фрагменты, содержащим метионин. Настоящее изобретение относится также к совместным составам антитела против TIGIT или его антигенсвязывающего фрагмента и антитела против PD-1 человека или его антигенсвязывающего фрагмента, содержащим метионин. В каждом случае, состав и совместный состав, необязательно, содержит хелатирующий агент.
I. Определение и сокращенные обозначения
Как используют на протяжении описания и прилагаемой формулы изобретения, приняты следующие сокращенные обозначения:
API активный фармацевтический ингредиент
CDR определяющая комплементарность область в вариабельных областях иммуноглобулина, определенная с использованием системы нумерации Kabat, если не указано иное
CHO яичники китайского хомяка
CI доверительный интервал
ДТПА диэтилентриаминпентауксусная кислота
EC50 концентрация, приводящая к 50% эффективности или связыванию
ELISA твердофазный иммуноферментный анализ
FFPE фиксированный формалином, погруженный в парафин
FR каркасная область
HRP пероксидаза хрена
HNSCC плоскоклеточная карцинома головы и шеи
IC50 концентрация, приводящая к 50% ингибированию
IgG иммуноглобулин G
IHC иммуногистохимия или иммуногистохимический
mAb моноклональное антитело
MES 2-(N-морфолино)этансульфоновая кислота
NCBI Национальный центр биотехнологической информации
NSCLC немелкоклеточный рак легкого
ПЦР полимеразная цепная реакция
PD-1 белок программируемой смерти 1 (называемый также белок-1 программируемой клеточной смерти и рецептор 1 программируемой смерти)
PD-L1 лиганд 1 рецептора 1 программируемой клеточной смерти
PD-L2 лиганд 2 рецептора 1 программируемой клеточной смерти
PS80 полисорбат 80
TNBC трижды отрицательный рак молочной железы
VH вариабельная область тяжелой цепи иммуноглобулина
VK вариабельная область легкой цепи каппа иммуноглобулина
VL вариабельная область легкой цепи иммуноглобулина
об./об. объем на объем
WFI вода для инъекций
масс./об. масса на объем
Чтобы изобретение можно было легче понять, определенные технические и научные термины конкретно определены ниже. Если конкретно не определено иное в другом месте этого описания, все другие технические и научные термины, используемые в настоящем описании, имеют значение, которое является общепринятым для специалиста в области, к которой относится это изобретение.
Как используют на протяжении описания и прилагаемой формулы изобретения, неконкретизированные и конкретизированные формы единственного числа включают ссылки на множественное число, если контекст явно не требует иного.
Ссылка на «или» обозначает любую или обе возможности, если контекст явно не требует одной из указанных возможностей. В некоторых случаях, «и/или» используют для выделения любой или обеих возможностей.
«Лечить» или «лечение» злокачественной опухоли, в рамках изобретения, обозначает введение состава по изобретению субъекту, который имеет иммунное состояние или злокачественное состояние, или у которого диагностирована злокачественная опухоль или патогенная инфекция (например, вирусная, бактериальная, грибковая), для достижения по меньшей мере одного положительного терапевтического эффекта, например, такого как уменьшение количества клеток злокачественных опухолей, уменьшение размера опухоли, уменьшение скорости инфильтрации злокачественных клеток в периферические органы, или уменьшение скорости метастазирования опухоли или роста опухоли. «Лечение» может включать одно или несколько из следующего: индукции/увеличения противоопухолевого иммунного ответа, стимуляции иммунного ответа на патоген, токсин и/или собственный антиген, стимуляции иммунного ответа на вирусную инфекцию, уменьшения количества одного или нескольких маркеров опухолей, ингибирования роста или выживаемости клеток опухолей, уничтожения или уменьшения размера одного или нескольких злокачественных очагов или опухолей, уменьшения уровня одного или нескольких маркеров опухолей, облегчения, уменьшения тяжести или длительности злокачественной опухоли, продления выживаемости пациента относительно ожидаемой выживаемости для сходного не подвергаемого лечению пациента.
«Иммунное состояние» или «иммунное нарушение» включает, например, патологическое воспаление, воспалительное нарушение и аутоиммунное нарушение или заболевание. «Иммунное состояние» также относится к инфекции, персистирующей инфекции и пролиферативным состояниям, таким как злокачественная опухоль, опухоли и ангиогенез, включая инфекции, опухоли и злокачественные опухоли, устойчивые к уничтожению иммунной системой. «Злокачественное состояние» включает, например, злокачественную опухоль, клетки злокачественных опухолей, опухоли, ангиогенез и предзлокачественные состояния, такие как дисплазия.
Положительные терапевтические эффекты при злокачественной опухоли можно измерять рядом способов (См., W. A. Weber, J. Nucl. Med. 50:1S-10S (2009)). Например, применительно к ингибированию роста опухоли, в соответствии со стандартами NCI, T/C ≤42% представляет собой минимальный уровень противоопухолевой активности. T/C < 10% считают высоким уровнем противоопухолевой активности, где T/C (%) = медиана объема опухоли после лечения/медиана объема опухоли в контроле × 100. В некоторых вариантах осуществления, лечение, достигнутое посредством введения состава по изобретению, представляет собой любое из выживаемости без прогрессирования (PFS), свободной от заболевания выживаемости (DFS) или общей выживаемости (OS). PFS, также обозначаемая как «время до прогрессирования опухоли», показывает длительность времени во время и после лечения, в которое злокачественная опухоль не растет, и включает количество времени, которое пациенты испытывают полный ответ или частичный ответ, так же как количество времени, которое пациенты испытывают стабильное заболевание. DFS относится к длительности времени во время и после лечения, которое пациент остается свободным от заболевания. OS относится к продлению ожидаемой продолжительности жизни, по сравнению с наивными или не подвергаемыми лечению индивидуумами или пациентами. В то время как вариант осуществления составов, способов лечения и применений по настоящему изобретению может не являться эффективным для достижения положительного терапевтического эффекта у каждого пациента, он должен являться эффективным для статистически значимого количества субъектов, как определено посредством любого статистического теста, известного в данной области, такого как t-критерий Стьюдента, критерий хи2, U-критерий согласно Манну и Уитни, критерий Крускала-Уоллиса (H-критерий), критерий Джонкхиера-Терпстры и критерий Уилкоксона.
Термин «пациент» (альтернативно обозначаемый как «субъект» или «индивидуум» в настоящем описании) относится к млекопитающему (например, крысе, мыши, собаке, кошке, кролику), которого можно лечить с использованием составов по изобретению, наиболее предпочтительно, человеку. В некоторых вариантах осуществления, пациент представляет собой взрослого пациента. В других вариантах осуществления, пациент представляет собой пациента детского возраста.
Термин «антитело» относится к любой форме антитела, обладающей желательной биологической активностью. Таким образом, он использован в самом широком смысле и конкретно включает, но без ограничения, моноклональные антитела (включая полноразмерные моноклональные антитела), поликлональные антитела, гуманизированные, полностью человеческие антитела и химерные антитела. «Исходные антитела» представляют собой антитела, полученные посредством подвергания иммунной системы воздействию антигена, до модификации антител для намеченного использования, например, гуманизации антитела для использования в качестве человеческого терапевтического антитела.
Как правило, основная структурная единица антитела содержит тетрамер. Каждый тетрамер включает две идентичные пары полипептидных цепей, где каждая пара имеет одну «легкую» (приблизительно 25 кДа) и одну «тяжелую» цепь (приблизительно 50-70 кДа). Амино-концевая часть каждой цепи включает вариабельную область приблизительно от 100 до 110 или более аминокислот, в первую очередь ответственных за узнавание антигена. Вариабельные области каждой пары легкая/тяжелая цепь формируют связывающий участок антитела. Таким образом, как правило, интактное антитело имеет два связывающих участка. Карбокси-концевая часть тяжелой цепи может определять константную область, в первую очередь ответственную за эффекторную функцию. Как правило, человеческие легкие цепи классифицируют как легкие цепи каппа и лямбда. Кроме того, человеческие тяжелые цепи, как правило, классифицируют как мю, дельта, гамма, альфа или эпсилон, и они определяют изотип антитела как IgM, IgD, IgG, IgA и IgE, соответственно. Внутри легких и тяжелых цепей, вариабельные и константные области соединены посредством области «J» из приблизительно 12 или более аминокислот, где тяжелая цепь включает также область «D» из приблизительно 10 и более аминокислот. См. в общем, Fundamental Immunology Ch. 7 (Paul, W., ed., 2nd ed. Raven Press, N.Y. (1989).
Как правило, вариабельные домены как тяжелых, так и легких цепей, содержат три гипервариабельные области, называемые также определяющими комплементарность областями (CDR), локализованные внутри относительно консервативных каркасных областей (FR). CDR обычно выровнены посредством каркасных областей, что позволяет их связывание со специфическим эпитопом. Как правило, от N-конца до C-конца, вариабельные домены как легких, так и тяжелых цепей, содержат FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Приписывание аминокислоты каждому домену осуществляют, как правило, в соответствии с определениями из Sequences of Proteins of Immunological Interest, Kabat, et al.; National Institutes of Health, Bethesda, Md. ; 5th ed.; NIH Publ. No. 91-3242 (1991); Kabat (1978) Adv. Prot. Chem. 32:1-75; Kabat, et al., (1977) J. Biol. Chem. 252:6609-6616; Chothia, et al., (1987) J Mol. Biol. 196:901-917 или Chothia, et al., (1989) Nature 342:878-883.
Антитело, которое «специфически связывается с» указанным белком-мишенью, представляет собой антитело, для которого показано предпочтительное связывание с этой мишенью по сравнению с другими белками, но эта специфичность не требует абсолютной специфичности связывания. Антитело считают «специфическим» для намеченной для него мишени, если его связывание является определяющим присутствие белка-мишени в образце, например, без получения нежелательных результатов, таких как ложноположительные. Антитела или их связывающие фрагменты, которые можно использовать по настоящему изобретению, могут связываться с белком-мишенью с аффинностью, по меньшей мере в два раза большей, предпочтительно, по меньшей мере в десять раз большей, более предпочтительно, по меньшей мере в 20 раз большей, и наиболее предпочтительно, по меньшей мере в 100 раз большей, чем аффинность для нецелевых белков. В рамках изобретения, говорят, что антитело специфически связывается с полипептидом, содержащим данную аминокислотную последовательность, например, аминокислотную последовательность молекулы зрелого TIGIT человека или PD-1 человека, если оно связывается с полипептидами, содержащим эту последовательность, но не связывается с белками, лишенными этой последовательности.
«Химерное антитело» относится к антителу, в котором часть тяжелой и/или легкой цепи является идентичной или гомологичной соответствующим последовательностям в антителе, происходящем из конкретного вида (например, человека) или принадлежащем к конкретному классу или подклассу антитела, в то время как остальная часть цепи(цепей) является идентичной или гомологичной соответствующим последовательностям в антителе, происходящем из другого вида (например, мыши) или принадлежащем к другому классу или подклассу антитела, так же как к фрагментам таких антител, при условии, что они имеют желательную биологическую активность.
«Введенные в совместный состав» или «совместный состав», или «получение совместного состава», или «составленные совместно», в рамках изобретения, относится по меньшей мере к двум различным антителам или их антигенсвязывающим фрагментам, которые составляют совместно и хранят в форме комбинированного продукта в одном флаконе или сосуде (например, устройстве для инъекции), вместо того, чтобы составлять и хранить индивидуально и затем смешивать перед введением или вводить отдельно. В одном варианте осуществления, совместный состав содержит два различных антитела или их антигенсвязывающие фрагменты.
Термин «фармацевтически эффективное количество» или «эффективное количество» обозначает количество, на основании которого достаточно терапевтической композиции или состава вводят пациенту для лечения заболевания или состояния. Специалисту в данной области известно, что этот уровень можно менять в соответствии с такими характеристиками пациента, как возраст, масса и т.д.
Термин «приблизительно», при определении количества (например, мМ, или M) вещества или композиции, процента (об./об. или масс./об.) компонента состава, pH раствора/состава или значения параметра, характеризующего стадию способа, или т.п. относится к варианту числового количества, который может возникнуть, например, в ходе типичных способов измерения, манипуляций и отбора образцов, включенных в получение, характеризацию и/или использование вещества или композиции; из-за экспериментальной ошибки в этих способах; из-за различий в изготовлении, источнике или чистоте ингредиентов, используемых для получения или использования композиций, или осуществления способов; и т.п. В конкретных вариантах осуществления, «приблизительно» может обозначать изменение на ±0,1%, 0,5%, 1%, 2%, 3%, 4%, 5% или 10%.
В рамках изобретения, «x% (масс./об.)» является эквивалентным x г/100 мл (например, 5% масс./об. эквивалентно 50 мг/мл).
Составы по настоящему изобретению включают антитела и их фрагменты, которые являются биологически активными после разведения или в жидкой форме.
Термины «злокачественная опухоль», «раковый» или «злокачественный» обозначают или описывают физиологическое состояние у млекопитающих, которое, как правило, характеризуется нерегулируемым ростом клеток. Примеры злокачественных опухолей включают, но без ограничения, карциному, лимфому, лейкоз, бластому и саркому. Более конкретные примеры таких злокачественных опухолей включают плоскоклеточную карциному, миелому, мелкоклеточный рак легкого, немелкоклеточный рак легкого, глиому, лимфому Ходжкина, неходжскинскую лимфому, желудочно-кишечную злокачественную опухоль (злокачественную опухоль желудочно-кишечного тракта), рак почки, рак яичника, рак печени, лимфобластный лейкоз, лимфоцитарный лейкоз, колоректальный рак, рак эндометрия, рак почки, рак предстательной железы, рак щитовидной железы, меланому, хондросаркому, нейробластому, рак поджелудочной железы, мультиформную глиобластому, рак шейки матки, злокачественную опухоль мозга, рак желудка, рак мочевого пузыря, гепатому, рак молочной железы, карциному ободочной кишки и рак головы и шеи.
«Chothia» обозначает систему нумерации антител, описанную в Al-Lazikani et al., JMB 273:927-948 (1997).
«Kabat», в рамках изобретения обозначает систему выравнивания и нумерации иммуноглобулинов, впервые представленную в Elvin A. Kabat ((1991) Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md.).
«Ингибирующее рост средство», в рамках изобретения, относится к соединению или композиции, которые ингибируют рост клетки, особенно, злокачественной клетки, экспрессирующей любой из генов, идентифицированных в настоящем описании, либо in vitro, либо in vivo. Таким образом, ингибирующее рост средство представляет собой средство, которое значительно уменьшает процент клеток со сверхэкспрессией таких генов в S-фазе. Примеры ингибирующих рост средств включают средства, блокирующие прохождение клеточного цикла (в точке, отличной от S-фазы), такие как средства, индуцирующие арест в G1-фазе и арест в M-фазе. Классические блокаторы M-фазы включают алкалоиды барвинка (винкристин и винбластин), таксаны и ингибиторы топоизомеразы II, такие как доксорубицин, эпирубицин, даунорубицин и этопозид. Средства, осуществляющие арест в G1-фазе, также распространяются на арест в S-фазе, например, алкилирующие ДНК средства, такие как декарбазин, мехлорэтамин и цисплатин. Дополнительную информацию можно обнаружить в The Molecular Basis of Cancer, Mendelsohn and Israel, eds., Chapter 1, entitled «Cell cycle regulation, oncogens, and antineoplastic drugs» by Murakami et al. (WB Saunders: Philadelphia, 1995).
Термины «связывающий TIGIT фрагмент», «его антигенсвязывающий фрагмент», «его связывающий фрагмент» или «его фрагмент» включают фрагмент или производное антитела, которые еще по существу сохраняют его биологическую активность связывания антигена (TIGIT человека) и ингибирования его активности (например, блокирования связывания TIGIT человека с его нативными лигандами). Таким образом, термин «фрагмент антитела» или связывающий TIGIT фрагмент относится к части полноразмерного антитела, как правило, его антигенсвязывающей или вариабельной области. Примеры фрагментов антител против TIGIT включают фрагменты Fab, Fab', F(ab')2 и Fv. Как правило, связывающий фрагмент или производное сохраняет по меньшей мере 10% его активности ингибирования TIGIT. В некоторых вариантах осуществления, связывающий фрагмент или производное сохраняет по меньшей мере 25%, 50%, 60%, 70%, 80%, 90%, 95%, 99% или 100% (или более) его активности ингибирования TIGIT, хотя можно использовать любой связывающий фрагмент с достаточной аффинностью, чтобы оказывать желательный биологический эффект. В некоторых вариантах осуществления, антигенсвязывающий фрагмент связывается со своим антигеном с аффинностью, по меньшей мере в два раза большей, предпочтительно, по меньшей мере в десять раз большей, более предпочтительно, по меньшей мере в 20 раз большей, и наиболее предпочтительно, по меньшей мере в 100 раз большей, чем аффинность для неродственных антигенов. В одном варианте осуществления антитело имеет аффинность, превышающую приблизительно 109 литров/моль, как определено, например, посредством анализа Скэтчарда. Munsen et al. (1980) Analyt. Biochem. 107:220-239. Предусмотрено также, чтобы связывающий TIGIT фрагмент мог включать варианты, имеющие консервативные аминокислотные замены, по существу не изменяющие его биологическую активность.
Термины «связывающий PD-1 фрагмент», «его антигенсвязывающий фрагмент», «его связывающий фрагмент» или «его фрагмент» включают фрагмент или производное антитела, которые еще по существу сохраняют его биологическую активность связывания антигена (PD-1 человека) и ингибирования его активности (например, блокирования связывания PD-1 с PDL1 и PDL2). Таким образом, термин «фрагмент антитела» или связывающий PD-1 фрагмент относится к части полноразмерного антитела, как правило, его антигенсвязывающей или вариабельной области. Примеры фрагментов антител включают фрагменты Fab, Fab', F(ab')2 и Fv. Как правило, связывающий фрагмент или производное сохраняет по меньшей мере 10% его активности ингибирования PD-1. В некоторых вариантах осуществления, связывающий фрагмент или производное сохраняет по меньшей мере 25%, 50%, 60%, 70%, 80%, 90%, 95%, 99% или 100% (или более) его активности ингибирования PD-1, хотя можно использовать любой связывающий фрагмент с достаточной аффинностью, чтобы оказывать желательный биологический эффект. В некоторых вариантах осуществления, антигенсвязывающий фрагмент связывается со своим антигеном с аффинностью, по меньшей мере в два раза большей, предпочтительно, по меньшей мере в десять раз большей, более предпочтительно, по меньшей мере в 20 раз большей, и наиболее предпочтительно, по меньшей мере в 100 раз большей, чем аффинность для неродственных антигенов. В одном варианте осуществления антитело имеет аффинность, превышающую приблизительно 109 литров/моль, как определено, например, посредством анализа Скэтчарда. Munsen et al. (1980) Analyt. Biochem. 107:220-239. Предусмотрено также, чтобы связывающий PD-1 фрагмент мог включать варианты, имеющие консервативные аминокислотные замены, по существу не изменяющие его биологическую активность.
«Человеческое антитело» относится к антителу, содержащему белковые последовательности только человеческого иммуноглобулина. Человеческое антитело может содержать мышиные углеводные цепи, если продуцировано у мыши, в клетке мыши или в гибридоме, происходящей из клетки мыши. Подобным образом, «мышиное антитело» или «крысиное антитело» относятся к антителу, содержащему последовательности только мышиного или крысиного иммуноглобулина, соответственно.
«Гуманизированное антитело» относится к формам антител, содержащим последовательности из не относящихся к человеку (например, мышиных) антител, так же как из человеческих антител. Такие антитела содержат минимальную последовательность, происходящую из не относящегося к человеку иммуноглобулина. Как правило, гуманизированное антитело может содержать по существу все из по меньшей мере одного, и как правило, двух, вариабельных доменов, в которых все или в основном все из гипервариабельных петель соответствуют гипервариабельным петлям из не относящегося к человеку иммуноглобулина, и все или в основном все из областей FR представляют собой области из последовательностей иммуноглобулина человека. Гуманизированное антитело также может, необязательно, содержать по меньшей мере часть константной области (Fc) иммуноглобулина, как правило, из иммуноглобулина человека. Гуманизированные формы антител грызунов могут, как правило, содержать такие же последовательности CDR из исходных антител грызунов, хотя определенные аминокислотные замены можно включать для увеличения аффинности, увеличения стабильности гуманизированного антитела или по другим причинам.
Антитела по настоящему изобретению включают также антитела с модифицированными (или блокированными) областями Fc для обеспечения измененных эффекторных функций. См., например, Патент США No. 5624821; WO2003/086310; WO2005/120571; WO2006/0057702; Presta (2006) Adv. Drug Delivery Rev. 58:640-656. Такие модификации можно использовать для усиления или супрессии различных реакций иммунной системы, с возможными благоприятными эффектами для диагностики и терапии. Изменения в области Fc включают изменения аминокислот (замены, делеции и вставки), гликозилирование или дегликозилирование и добавление множественных Fc. Изменения в Fc могут также изменять время полужизни антител в терапевтических антителах, и более длительное время полужизни может приводить к менее частому дозированию, с сопутствующим увеличением удобства и уменьшением использования материала. См. Presta (2005) J. Allergy Clin. Immunol.116:731 at 734-35.
«Полностью человеческое антитело» относится к антителу, содержащему белковые последовательности только человеческого иммуноглобулина. Полностью человеческое антитело может содержать мышиные углеводные цепи, если продуцировано у мыши, в клетке мыши или в гибридоме, происходящей из клетки мыши. Подобным образом, «мышиное антитело» относится к антителу, содержащему последовательности только мышиного иммуноглобулина. Полностью человеческое антитело можно получать у человека, в трансгенном животном, имеющем зародышевые последовательности иммуноглобулина человека, посредством фагового дисплея или других молекулярно-биологических способов.
«Гипервариабельная область» относится к остаткам аминокислот антитела, ответственным за связывание антигена. Гипервариабельная область содержит остатки аминокислот из «определяющей комплементарность области» или «CDR» (например, остатки 24-34 (CDRL1), 50-56 (CDRL2) и 89-97 (CDRL3) в вариабельном домене легкой цепи, и остатки 31-35 (CDRH1), 50-65 (CDRH2) и 95-102 (CDRH3) в вариабельном домене тяжелой цепи, как определено посредством системы нумерации Kabat (Kabat et al. (1991) Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md.), и/или такие остатки из «гипервариабельной петли» (т.е. остатки 26-32 (L1), 50-52 (L2) и 91-96 (L3) в вариабельном домене легкой цепи и 26-32 (H1), 53-55 (H2) и 96-101 (H3) в вариабельном домене тяжелой цепи (Chothia and Lesk (1987) J. Mol. Biol. 196: 901-917). В рамках изобретения, термин «каркасные» или «FR» остатки относится к остаткам вариабельного домена, отличным от остатков гипервариабельной области, определенных в настоящем описании как остатки CDR. Остатки CDR и FR определяют в соответствии со стандартным определением последовательности по Kabat. Kabat et al. (1987) Sequences of Proteins of Immunological Interest, National Institutes of Health, Bethesda Md.
«Консервативно модифицированные варианты» или «консервативная замена», относящиеся к заменам аминокислот, известны специалисту в данной области и могут быть осуществлены, в основном, без изменения биологической активности полученной молекулы, даже в необходимых областях полипептида. Такие иллюстративные замены, предпочтительно, осуществляют в соответствии с заменами, указанными в таблице 1, следующим образом:
Таблица 1. Иллюстративные консервативные аминокислотные замены
Кроме того, специалисту в данной области известно, что, как правило, одиночные аминокислотные замены в не являющихся необходимыми областях полипептида существенно не изменяют биологическую активность. См., например, Watson et al. (1987) Molecular Biology of the Gene, The Benjamin/Cummings Pub. Co., p. 224 (4th Edition).
Фраза «в основном состоит из», или варианты, такие как «в основном состоят из» или «в основном состоящий из», как используют на протяжении описания и формулы изобретения, указывают на включение любых перечисленных элементов или групп элементов, и необязательное включение других элементов, сходной или отличной природы, по отношению к перечисленным элементам, которые существенно не изменяют основные или новые свойства указанных режима дозирования, способа или композиции. В качестве неограничивающего примера, связывающее соединение, которое в основном состоит из перечисленной аминокислотной последовательности, может также включать одну или несколько аминокислот, включая замены одного или нескольких остатков аминокислот, которые существенно не влияют на свойства связывающего соединения.
«Содержащий» или варианты, такие как «содержат», «содержит» или «содержится», используют на протяжении описания и формулы изобретения во включительном смысле, т.е., для указания присутствия указанных признаков, но не для исключения присутствия или добавления дополнительных признаков, которые могут существенно улучшать способ или полезность любого из вариантов осуществления изобретения, если контекст не требует иного посредством явно выраженного или необходимого подразумеваемого утверждения.
«Выделенное антитело» и «выделенный фрагмент антитела» относится к статусу очистки и в таком контексте означает, что указанная молекула является в основном свободной от других биологических молекул, таких как нуклеиновые кислоты, белки, липиды, углеводы, или другой материал, такой как клеточный дебрис и среда для выращивания. Как правило, термин «выделенный» не предназначен для обозначения полного отсутствия такого материала или отсутствия воды, буферов или солей, если они не присутствуют в количествах, создающих существенные помехи для экспериментального или терапевтического использования связывающего соединения, как описано в настоящем описании.
«Моноклональное антитело» или «mAb», или «Mab», в рамках изобретения, относится к популяции по существу гомогенных антител, т.е., молекулы антител, содержащиеся в популяции, являются идентичными по аминокислотной последовательности, за исключением возможных природных мутаций, которые могут присутствовать в незначительных количествах. В отличие от этого, общепринятые (поликлональные) препараты антител, как правило, включают в себя множество различных антител, обладающих различными аминокислотными последовательностями в их вариабельных доменах, в частности, в их CDR, которые часто являются специфическими для различных эпитопов. Определение «моноклональное» указывает на характер антитела, как полученного из по существу гомогенной популяции антител, и его не следует истолковывать как требующее получения антитела каким-либо конкретным способом. Например, моноклональные антитела для использования в соответствии с настоящим изобретением можно получать способом гибридомы, впервые описанным в Kohler et al. (1975) Nature 256: 495, или их можно получать способами рекомбинантной ДНК (см., например, Патент США No. 4816567). «Моноклональные антитела» можно выделять также из фаговых библиотек антител с использованием способов, описанных в Clackson et al. (1991) Nature 352: 624-628 и Marks et al. (1991) J. Mol. Biol. 222: 581-597, например. См. также Presta (2005) J. Allergy Clin. Immunol. 116:731.
«Опухоль», применительно к субъекту, у которого диагностирована злокачественная опухоль, или у которого подозревают наличие злокачественной опухоли, относится к злокачественной или потенциально злокачественной неоплазии или массе ткани любого размера, и включает первичные опухоли и вторичные неоплазии. Солидная опухоль представляет собой аномальный рост или массу ткани, которая обычно не содержит кист или жидких областей. Различные типы солидных опухолей названы по типу образующих их клеток. Примерами солидных опухолей являются саркомы, карциномы и лимфомы. Лейкозы (злокачественные опухоли крови) обычно не формируют солидные опухоли (Национальный институт онкологии США, Словарь онкологических терминов).
Термин «размер опухоли» относится к общему размеру опухоли, который можно измерять как длину и ширину опухоли. Размер опухоли можно определять множеством способов, известных в данной области, например, таких как определение измерений опухоли(опухолей) после удаления у субъекта, например, с использованием штангенциркуля, или во время нахождения в организме, с использованием способов визуализации, например, сканирования костей, ультразвука, сканирования КТ или МРТ.
«Вариабельные области» или «V-область», в рамках изобретения, обозначают фрагмент цепей IgG, различающийся по последовательности между различными антителами. Он простирается до остатка по Kabat 109 в легкой цепи и 113 в тяжелой цепи.
Термин «буфер» включает средства, поддерживающие pH раствора составов по изобретению в приемлемом диапазоне, или, для лиофилизированных составов по изобретению, обеспечивающие приемлемый pH раствора перед лиофилизацией.
Термины «лиофилизация», «лиофилизированный» и «сублимированный» относятся к способу, посредством которого материал, подлежащий высушиванию, сначала замораживают, и затем лед или замороженный растворитель удаляют посредством сублимации в условиях вакуума. Наполнитель можно включать в составы до лиофилизации для увеличения стабильности лиофилизированного продукта при хранении.
Термин «фармацевтический состав» относится к препаратам, которые находятся в такой форме, чтобы позволять активным ингредиентам являться эффективными, и которые не содержат дополнительных компонентов, являющихся токсичными для субъектов, которым будут вводить состав. Термин «состав» и «фармацевтический состав» используют взаимозаменяемо на протяжении описания.
«Фармацевтически приемлемый» относится к наполнителям (носителям, добавкам) и композициям, которые можно целесообразно вводить субъекту для обеспечения эффективной дозы используемого активного ингредиента и которые «рассматривают как в основном безопасные» например, которые являются физиологически переносимыми и, как правило, не приводят к аллергической или сходной неблагоприятной реакции, такой как расстройство желудка и т.п., при введении человеку. В другом варианте осуществления, этот термин относится к молекулам и композициям, одобренным регулирующим органом федерального или регионального правительства, или перечисленным в фармакопее США или другой общепринятой фармакопее для использования у животных, и более конкретно, у человека.
«Разведенный» состав представляет собой состав, полученный посредством разведения лиофилизированного белкового состава в разбавителе, таким образом, что белок распределяется в разведенном составе. Разведенный состав является пригодным для введения, например, парентерального введения), и может, необязательно, являться пригодным для подкожного введения.
«Время разведения» представляет собой время, необходимое для регидратации лиофилизированного состава с использованием раствора до свободного от частиц осветленного раствора.
«Стабильный» состав представляет собой состав, в котором белок в основном сохраняет свою физическую стабильность и/или химическую стабильность, и/или биологическую активность при хранении. Различные аналитические способы измерения стабильности белка доступны в данной области, и их обзор приведен в Peptide and Protein Drug Delivery, 247-301, Vincent Lee Ed., Marcel Dekker, Inc., New York, N.Y., Pubs. (1991) и Jones, A. Adv. Drug Delivery Rev. 10:29-90 (1993). Стабильность можно измерять при выбранной температуре в течение выбранного периода времени. Например, в одном варианте осуществления, стабильный состав представляет собой состав без значительных изменений, наблюдаемых при температуре холодильника (2-8°C), в течение по меньшей мере 12 месяцев. В другом варианте осуществления, стабильный состав представляет собой состав без значительных изменений, наблюдаемых при температуре холодильника (2-8°C), в течение по меньшей мере 18 месяцев. В другом варианте осуществления, стабильный состав представляет собой состав без значительных изменений, наблюдаемых при комнатной температуре (23-27°C) в течение по меньшей мере 3 месяцев. В другом варианте осуществления, стабильный состав представляет собой состав без значительных изменений, наблюдаемых при комнатной температуре (23-27°C) в течение по меньшей мере 6 месяцев. В другом варианте осуществления, стабильный состав представляет собой состав без значительных изменений, наблюдаемых при комнатной температуре (23-27°C) в течение по меньшей мере 12 месяцев. В другом варианте осуществления, стабильный состав представляет собой состав без значительных изменений, наблюдаемых при комнатной температуре (23-27°C) в течение по меньшей мере 18 месяцев. Критерии стабильности состава антитела являются следующими. Как правило, не более 10%, предпочтительно, 5% мономера антитела является деградированным, как измерено посредством SEC-HPLC. Как правило, состав является бесцветным, или от прозрачного до немного опалесцирующего по визуальному анализу. Как правило, концентрация, pH и осмоляльность состава не изменяются более, чем на +/-10%. Активность, как правило, находится в пределах 60-140%, предпочтительно 80-120%, от контроля или эталона. Как правило, наблюдают не более, чем 10%, предпочтительно, 5% укороченных антител, т.е., % низкомолекулярных молекул, как определено, например, посредством HP-SEC. Как правило, наблюдают не более, чем 10%, предпочтительно, не более, чем 5% агрегации антител, т.е. % высокомолекулярных молекул, как определено, например, посредством HP-SEC.
Антитело «сохраняет свою физическую стабильность» в фармацевтическом составе, если для него не показано значительного увеличения агрегации, преципитации и/или денатурации при визуальном обследовании цвета и/или прозрачности, или как измерено посредством УФ светорассеяния, эксклюзионной хроматографии (SEC) и динамического светорассеяния. Изменения конформации белка можно оценивать посредством флуоресцентной спектроскопии, которая определяет третичную структуру белка, и посредством спектроскопии FTIR, которая определяет вторичную структуру белка.
Антитело «сохраняет свою химическую стабильность» в фармацевтическом составе, если для него не показано значительного химического изменения. Химическую стабильность можно оценивать посредством детекции и количественной оценки химически измененных форм белка. Процессы деградации, которые часто изменяют химическую структуру белка, включают гидролиз или укорочение (оцененные такими способами, как эксклюзионная хроматография и SDS-PAGE), окисление (оцененные такими способами, как пептидное картирование в сочетании с масс-спектроскопией или MALDI/TOF/MS), дезамидирование (оцененные такими способами, как ионообменная хроматография, капиллярное изоэлектрическое фокусирование, пептидное картирование, измерение содержания изоаспарагиновой кислоты) и изомеризацию (оцененную посредством измерения содержания изоаспарагиновой кислоты, пептидного картирования и т.д.).
Антитело «сохраняет свою биологическую активность» в фармацевтическом составе, если биологическая активность антитела в данное время находится в пределах предопределенного диапазона биологической активности, показанного на время получения фармацевтического состава. Биологическую активность антитела можно определять, например, посредством анализа связывания антигена.
Термин «изотонический» означает, что представляющий интерес состав имеет по существу такое же осмотическое давление, как человеческая кровь. Изотонические составы, как правило, имеют осмотическое давление приблизительно 270-328 мОсм. Немного гипотоническое давление составляет 250-269, и немного гипертоническое давление составляет 328-350 мОсм. Осмотическое давление можно измерять, например, с использованием осмометра парового или определяющего точку замерзания типа.
II. Составы и совместные составы по изобретению.
В одном аспекте, изобретение относится к стабильным биологическим составам, содержащим антитела против TIGIT или их антигенсвязывающие фрагменты, которые специфически связываются с TIGIT человека, в качестве активного фармацевтического ингредиента. Включение метионина в такие составы уменьшает окисление остатков метионина, присутствующих в области Fc антитела против TIGIT, и, в примере антитела против TIGIT, содержащего CDRH3 из SEQ ID NO:110, триптофан. Такие составы могут дополнительно содержать хелатирующий агент, такой как ДТПА, который может дополнительно уменьшать окисление.
В одном аспекте изобретение относится также к совместному составу антитела против TIGIT с антителом против PD-1. Главные пути деградации пембролизумаба включают окисление метионина 105 (Met105) в CDR3 тяжелой цепи (например, M105 из SEQ ID NO:10) при пероксидном стрессе, и окисление Met105 и остатков метионина Fc при воздействии света. Пембролизумаб сохранял свою биоактивность в большинстве из условий стресса для тестированных уровней деградации. однако, уменьшение аффинности к PD-1 наблюдали для подвергнутых пероксидному стрессу образцов посредством поверхностного плазмонного резонанса (SPR). Экспонированный остаток метионина или остаток метионина в CDR антитела имеет потенциал для влияния на биологическую активность антитела посредством окисления. Добавление метионина может уменьшать окисление Met105 в CDR тяжелой цепи пембролизумаба.
Антитела против PD-1 и их антигенсвязывающие фрагменты
В одном аспекте изобретение относится к стабильным биологическим составам, содержащим антитела против TIGIT или их антигенсвязывающие фрагменты, в совместном составе с антителами против PD-1 человека или их антигенсвязывающими фрагментами, которые специфически связываются с PD-1 человека (например, человеческим или гуманизированным антителом против PD-1), в качестве активного фармацевтического ингредиента (API PD-1), так же как к способам использования составов по изобретению. Любое антитело против PD-1 или его антигенсвязывающий фрагмент можно использовать в совместных составах и способах по изобретению. В конкретных вариантах осуществления, API PD-1 представляет собой антитело против PD-1, выбранное из пембролизумаба и ниволумаба. В конкретных вариантах осуществления, антитело против PD-1 представляет собой пембролизумаб. В альтернативных вариантах осуществления, антитело против PD-1 представляет собой ниволумаб. В таблице 2 представлены аминокислотные последовательности иллюстративных антител против PD-1 человека пембролизумаба и ниволумаба. Альтернативные антитела против PD-1 и антигенсвязывающие фрагменты, которые можно использовать в совместных составах и способах по изобретению, показаны в таблице 3.
В некоторых вариантах осуществления, антитело против PD-1 человека или его антигенсвязывающий фрагмент для использования в совместных составах по изобретению содержит три CDR легкой цепи из CDRL1, CDRL2 и CDRL3, и/или три CDR тяжелой цепи из CDRH1, CDRH2 и CDRH3.
В одном варианте осуществления изобретения, CDRL1 представляет собой SEQ ID NO:1 или вариант SEQ ID NO:1, CDRL2 представляет собой SEQ ID NO:2 или вариант SEQ ID NO:2, и CDRL3 представляет собой SEQ ID NO:3 или вариант SEQ ID NO:3.
В одном варианте осуществления, CDRH1 представляет собой SEQ ID NO:6 или вариант SEQ ID NO:6, CDRH2 представляет собой SEQ ID NO:7 или вариант SEQ ID NO:7, и CDRH3 представляет собой SEQ ID NO:8 или вариант SEQ ID NO:8.
В одном варианте осуществления, три CDR легкой цепи представляют собой SEQ ID NO:1, SEQ ID NO:2 и SEQ ID NO:3, и три CDR тяжелой цепи представляют собой SEQ ID NO:6, SEQ ID NO:7 и SEQ ID NO:8.
В альтернативном варианте осуществления изобретения, CDRL1 представляет собой SEQ ID NO:11 или вариант SEQ ID NO:11, CDRL2 представляет собой SEQ ID NO:12 или вариант SEQ ID NO:12, и CDRL3 представляет собой SEQ ID NO:13 или вариант SEQ ID NO:13.
В одном варианте осуществления, CDRH1 представляет собой SEQ ID NO:16 или вариант SEQ ID NO:16, CDRH2 представляет собой SEQ ID NO:17 или вариант SEQ ID NO:17, и CDRH3 представляет собой SEQ ID NO:18 или вариант SEQ ID NO:18.
В одном варианте осуществления, три CDR легкой цепи представляют собой SEQ ID NO:1, SEQ ID NO:2 и SEQ ID NO:3, и три CDR тяжелой цепи представляют собой SEQ ID NO:6, SEQ ID NO:7 и SEQ ID NO:8.
В альтернативном варианте осуществления, три CDR легкой цепи представляют собой SEQ ID NO:11, SEQ ID NO:12 и SEQ ID NO:13, и три CDR тяжелой цепи представляют собой SEQ ID NO:16, SEQ ID NO:17 и SEQ ID NO:18.
В следующем варианте осуществления изобретения, CDRL1 представляет собой SEQ ID NO:21 или вариант SEQ ID NO:21, CDRL2 представляет собой SEQ ID NO:22 или вариант SEQ ID NO:22, и CDRL3 представляет собой SEQ ID NO:23 или вариант SEQ ID NO:23.
В другом варианте осуществления, CDRH1 представляет собой SEQ ID NO:24 или вариант SEQ ID NO:24, CDRH2 представляет собой SEQ ID NO:25 или вариант SEQ ID NO:25, и CDRH3 представляет собой SEQ ID NO:26 или вариант SEQ ID NO:26.
В другом варианте осуществления, три CDR легкой цепи представляют собой SEQ ID NO:21, SEQ ID NO:22 и SEQ ID NO:23, и три CDR тяжелой цепи представляют собой SEQ ID NO:24, SEQ ID NO:25 и SEQ ID NO:26.
Некоторые антитела против PD-1 человека и антигенсвязывающие фрагменты по изобретению содержат вариабельную область легкой цепи и вариабельную область тяжелой цепи. В некоторых вариантах осуществления, вариабельная область легкой цепи содержит SEQ ID NO:4 или вариант SEQ ID NO:4, и вариабельная область тяжелой цепи содержит SEQ ID NO:9 или вариант SEQ ID NO:9. В следующих вариантах осуществления, вариабельная область легкой цепи содержит SEQ ID NO:14 или вариант SEQ ID NO:14, и вариабельная область тяжелой цепи содержит SEQ ID NO:19 или вариант SEQ ID NO:19. В следующих вариантах осуществления, вариабельная область тяжелой цепи содержит SEQ ID NO:27 или вариант SEQ ID NO:27 и вариабельная область легкой цепи содержит SEQ ID NO:28 или вариант SEQ ID NO:28, SEQ ID NO:29 или вариант SEQ ID NO:29, или SEQ ID NO:30 или вариант SEQ ID NO:30. В таких вариантах осуществления, вариант последовательности вариабельной области легкой цепи или тяжелой цепи является идентичным контрольной последовательности, за исключением наличия одной, двух, трех, четырех или пяти аминокислотных замен. В некоторых вариантах осуществления, замены находятся в каркасной области (т.е., вне CDR). В некоторых вариантах осуществления, одна, две, три, четыре или пять из аминокислотных замен представляют собой консервативные замены.
В одном варианте осуществления совместных составов по изобретению, антитело против PD-1 человека или антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, содержащую или состоящую из SEQ ID NO:4, и вариабельную область тяжелой цепи, содержащую или состоящую из SEQ ID NO:9. В следующем варианте осуществления, антитело против PD-1 человека или антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, содержащую или состоящую из SEQ ID NO:14, и вариабельную область тяжелой цепи, содержащую или состоящую из SEQ ID NO:19. В одном варианте осуществления составов по изобретению, антитело против PD-1 человека или антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, содержащую или состоящую из SEQ ID NO:28, и вариабельную область тяжелой цепи, содержащую или состоящую из SEQ ID NO:27. В следующем варианте осуществления, антитело против PD-1 человека или антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, содержащую или состоящую из SEQ ID NO:29, и вариабельную область тяжелой цепи, содержащую или состоящую из SEQ ID NO:27. В другом варианте осуществления, антитело или антигенсвязывающий фрагмент содержит вариабельную область легкой цепи, содержащую или состоящую из SEQ ID NO:30, и вариабельную область тяжелой цепи, содержащую или состоящую из SEQ ID NO:27.
В другом варианте осуществления, совместные составы по изобретению содержат антитело против PD-1 человека или антигенсвязывающий белок, имеющий домен VL и/или домен VH c по меньшей мере 95%, 90%, 85%, 80%, 75% или 50% гомологией последовательности с одним из доменов VL или доменов VH, описанных выше, и имеющий специфическое связывание с PD-1. В другом варианте осуществления, антитело против PD-1 человека или антигенсвязывающий белок из совместных составов по изобретению содержит домены VL и VH, имеющие вплоть до 1, 2, 3, 4 или 5, или более аминокислотных замен, и имеет специфическое связывание с PD-1.
В любом из вариантов осуществления выше, API PD-1 может представлять собой полноразмерное антитело против PD-1 или его антигенсвязывающий фрагмент, который специфически связывается с PD-1 человека. В конкретных вариантах осуществления, API PD-1 представляет собой полноразмерное антитело против PD-1, выбранное из любого класса иммуноглобулинов, включая IgM, IgG, IgD, IgA и IgE. Предпочтительно, антитело представляет собой антитело IgG. Можно использовать любой изотип IgG, включая IgG1, IgG2, IgG3 и IgG4. Различные константные домены можно присоединять к областям VL и VH, представленным в настоящем описании. Например, если конкретное намеченное использование антитела (или фрагмента) по настоящему изобретению предусматривает измененные эффекторные функции, можно использовать константный домен тяжелой цепи, отличной от IgG1. Несмотря на то, что антитела IgG1 обеспечивают длительное время полужизни и эффекторные функции, такие как активация комплемента и антителозависимая клеточная цитотоксичность, такие виды активности могут не являться желательными для всех применений антитела. В таких случаях, можно использовать, например, константный домен IgG4.
В вариантах осуществления по изобретению, API PD-1 представляет собой антитело против PD-1, содержащее легкую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:5, и тяжелую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:10. В альтернативных вариантах осуществления, API PD-1 представляет собой антитело против PD-1, содержащее легкую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:15, и тяжелую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:20. В следующих вариантах осуществления, API PD-1 представляет собой антитело против PD-1, содержащее легкую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:32, и тяжелую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:31. В дополнительных вариантах осуществления, API PD-1 представляет собой антитело против PD-1, содержащее легкую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:33, и тяжелую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:31. В дополнительных вариантах осуществления, API PD-1 представляет собой антитело против PD-1, содержащее легкую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:34, и тяжелую цепь, содержащую или состоящую из последовательности остатков аминокислот, как указано в SEQ ID NO:31. В некоторых совместных составах по изобретению, API PD-1 представляет собой пембролизумаб или биоаналогичный пембролизумаб. В некоторых совместных составах по изобретению, API PD-1 представляет собой ниволумаб или биоаналогичный ниволумаб.
Обычно, варианты аминокислотной последовательности антител против PD-1 и антигенсвязывающих фрагментов по изобретению или антител против TIGIT и антигенсвязывающих фрагментов по изобретению могут иметь аминокислотную последовательность, имеющую по меньшей мере 75% идентичность аминокислотной последовательности с аминокислотной последовательностью эталонного антитела или антигенсвязывающего фрагмента (например, тяжелой цепью, легкой цепью, VH, VL или гуманизированной последовательностью), более предпочтительно, по меньшей мере 80%, более предпочтительно, по меньшей мере 85%, более предпочтительно, по меньшей мере 90%, и наиболее предпочтительно, по меньшей мере 95, 98 или 99%. Идентичность или гомологию, применительно к последовательности, определяют в настоящем описании как процент остатков аминокислот в последовательности-кандидате, которые являются идентичными остаткам антитела против PD-1, после выравнивания последовательностей и внесения пропусков, при необходимости, для достижения максимальной процентной идентичности последовательностей, и не рассматривая никаких консервативных замен в качестве части идентичности последовательности. Никакие из N-концевых, C-концевых или внутренних удлинений, делеций или вставок в последовательности антитела не следует рассматривать как влияющие на идентичность или гомологию последовательности.
Идентичность последовательности относится к степени, в которой аминокислоты из двух полипептидов являются одинаковыми в эквивалентных положениях, когда две последовательности оптимально выровнены. Идентичность последовательности можно определять с использованием алгоритма BLAST, где параметры алгоритма выбраны для получения наибольшего совпадения между соответствующими последовательностями на протяжении полной длины соответствующих эталонных последовательностей. Следующие ссылки относятся к алгоритмам BLAST, часто используемым для анализа последовательностей: BLAST ALGORITHMS: Altschul, S.F., et al., (1990) J. Mol. Biol. 215:403-410; Gish, W., et al., (1993) Nature Genet. 3:266-272; Madden, T.L., et al., (1996) Meth. Enzymol. 266:131-141; Altschul, S.F., et al., (1997) Nucleic Acids Res. 25:3389-3402; Zhang, J., et al., (1997) Genome Res. 7:649-656; Wootton, J.C., et al., (1993) Comput. Chem. 17:149-163; Hancock, J.M. et al., (1994) Comput. Appl. Biosci. 10:67-70; ALIGNMENT SCORING SYSTEMS: Dayhoff, M.O., et al., «A model of evolutionary change in proteins.» in Atlas of Protein Sequence and Structure, (1978) vol. 5, suppl. 3. M.O. Dayhoff (ed.), pp. 345-352, Natl. Biomed. Res. Found., Washington, DC; Schwartz, R.M., et al., «Matrices for detecting distant relationships.» in Atlas of Protein Sequence and Structure, (1978) vol. 5, suppl. 3.» M.O. Dayhoff (ed.), pp. 353-358, Natl. Biomed. Res. Found., Washington, DC; Altschul, S.F., (1991) J. Mol. Biol. 219:555-565; States, D.J., et al., (1991) Methods 3:66-70; Henikoff, S., et al., (1992) Proc. Natl. Acad. Sci. USA 89:10915-10919; Altschul, S.F., et al., (1993) J. Mol. Evol. 36:290-300; ALIGNMENT STATISTICS: Karlin, S., et al., (1990) Proc. Natl. Acad. Sci. USA 87:2264-2268; Karlin, S., et al., (1993) Proc. Natl. Acad. Sci. USA 90:5873-5877; Dembo, A., et al., (1994) Ann. Prob. 22:2022-2039; и Altschul, S.F. «Evaluating the statistical significance of multiple distinct local alignments.» in Theoretical and Computational Methods in Genome Research (S. Suhai, ed.), (1997) pp. 1-14, Plenum, New York.
Подобным образом, любой класс легких цепей можно использовать в композициях и способах в настоящем описании. Конкретно, каппа, лямбда или их варианты можно использовать в настоящих композициях и способах.
Таблица 2. Иллюстративные последовательности антител против PD-1
Таблица 3. Дополнительные антитела против PD-1 и антигенсвязывающие фрагменты, которые можно использовать в совместных составах, способах и применениях по изобретению.
В некоторых вариантах осуществления совместного состава по изобретению, API PD-1 (т.е. антитело против PD-1 или его антигенсвязывающий фрагмент) присутствует в концентрации от приблизительно 25 мг/мл до приблизительно 100 мг/мл. В альтернативных вариантах осуществления, API присутствует в концентрации приблизительно 10 мг/мл, приблизительно 25 мг/мл, приблизительно 50 мг/мл, приблизительно 75 мг/мл или приблизительно 100 мг/мл.
Антитела против TIGIT их антигенсвязывающие фрагменты
В одном аспекте изобретение относится к стабильным биологическим составам, содержащим антитела против TIGIT или их антигенсвязывающие фрагменты, которые специфически связываются с TIGIT человека (например, человеческое или гуманизированное анти-TIGIT антитело), в качестве активного фармацевтического ингредиента (TIGIT API), так же как к способам использования составов по изобретению.
В другом аспекте изобретение относится также к биологическим совместным составам, содержащим (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, которые специфически связываются с TIGIT человека (например, человеческое или гуманизированное анти-TIGIT антитело) и (ii) антитело против PD-1 человека или его антигенсвязывающий фрагмент, которые специфически связываются с PD-1 человека. Любое анти-TIGIT антитело или его антигенсвязывающий фрагмент можно использовать в составе, включая совместный состав, и в способах по изобретению. Иллюстративные последовательности антитела против TIGIT указаны ниже в таблицах 4 и 5.
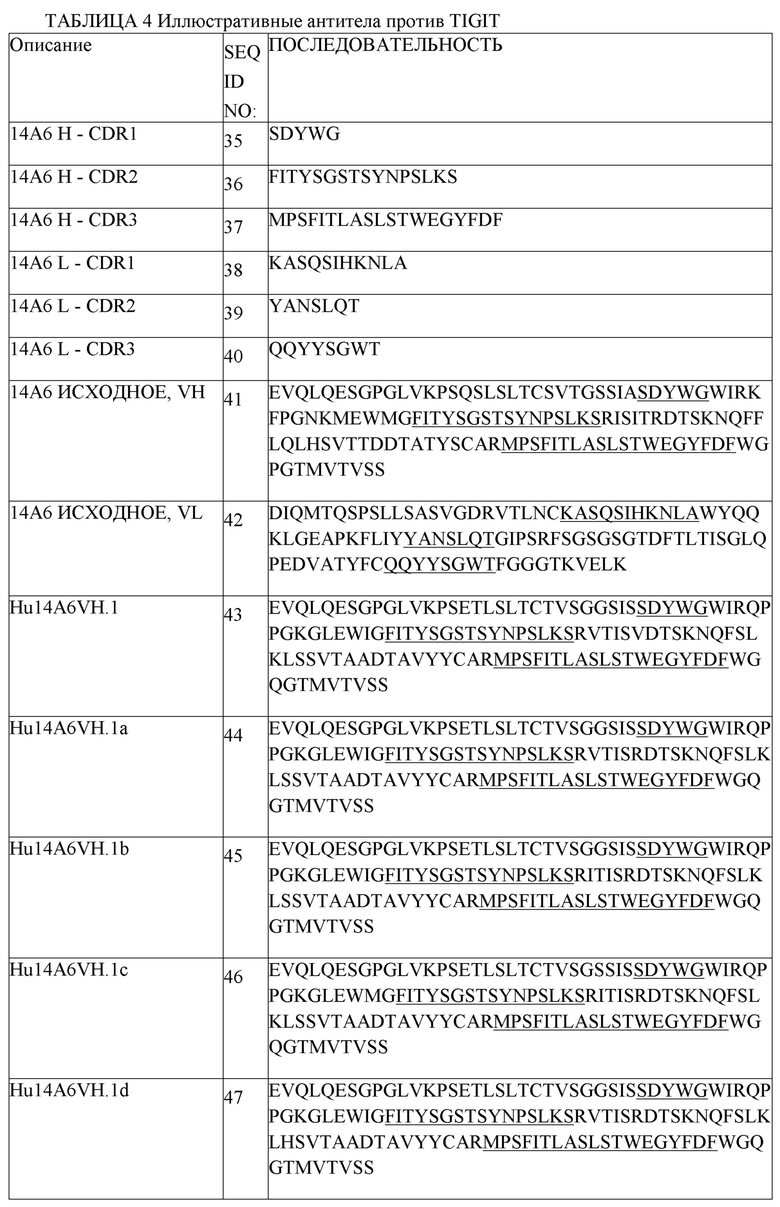
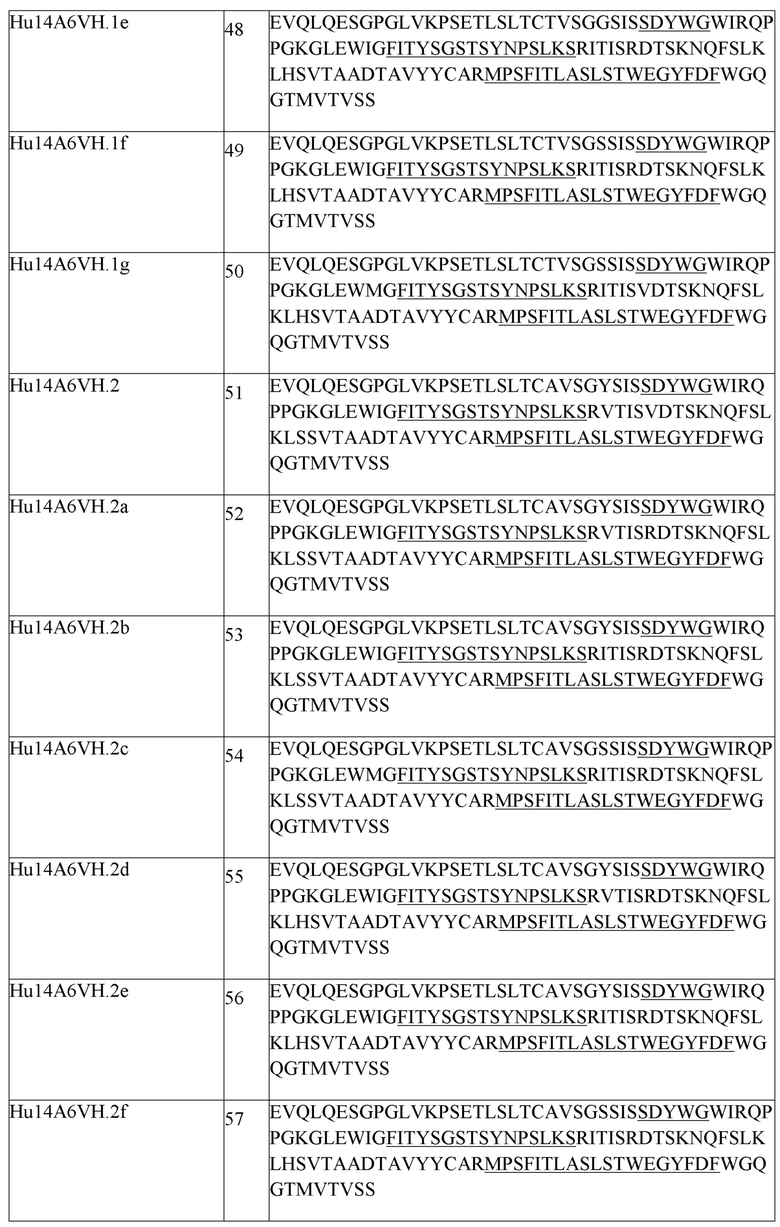
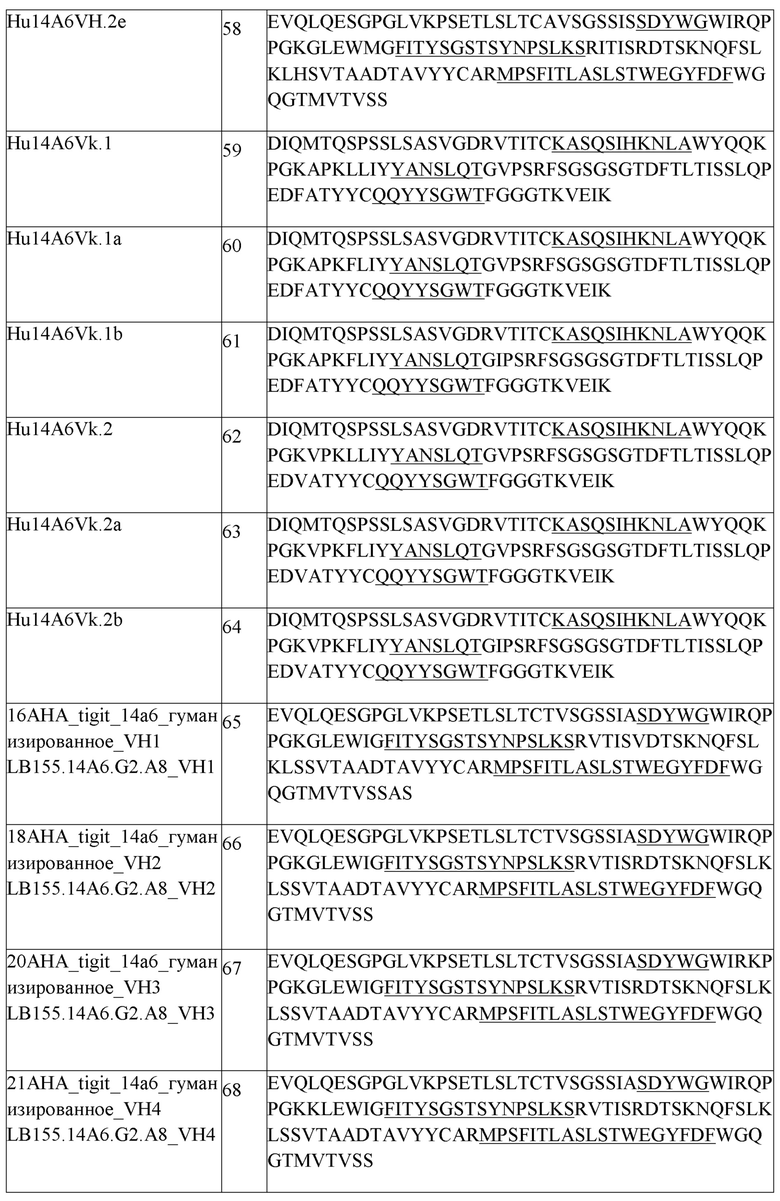

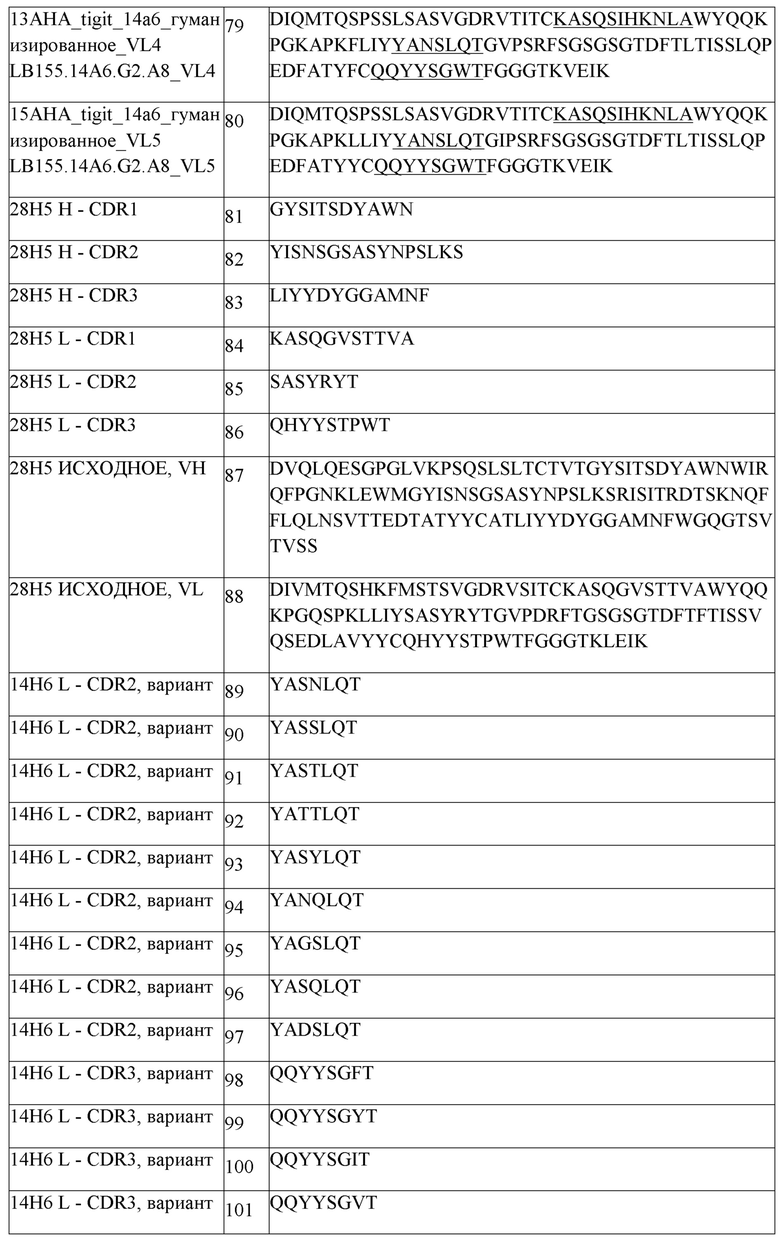

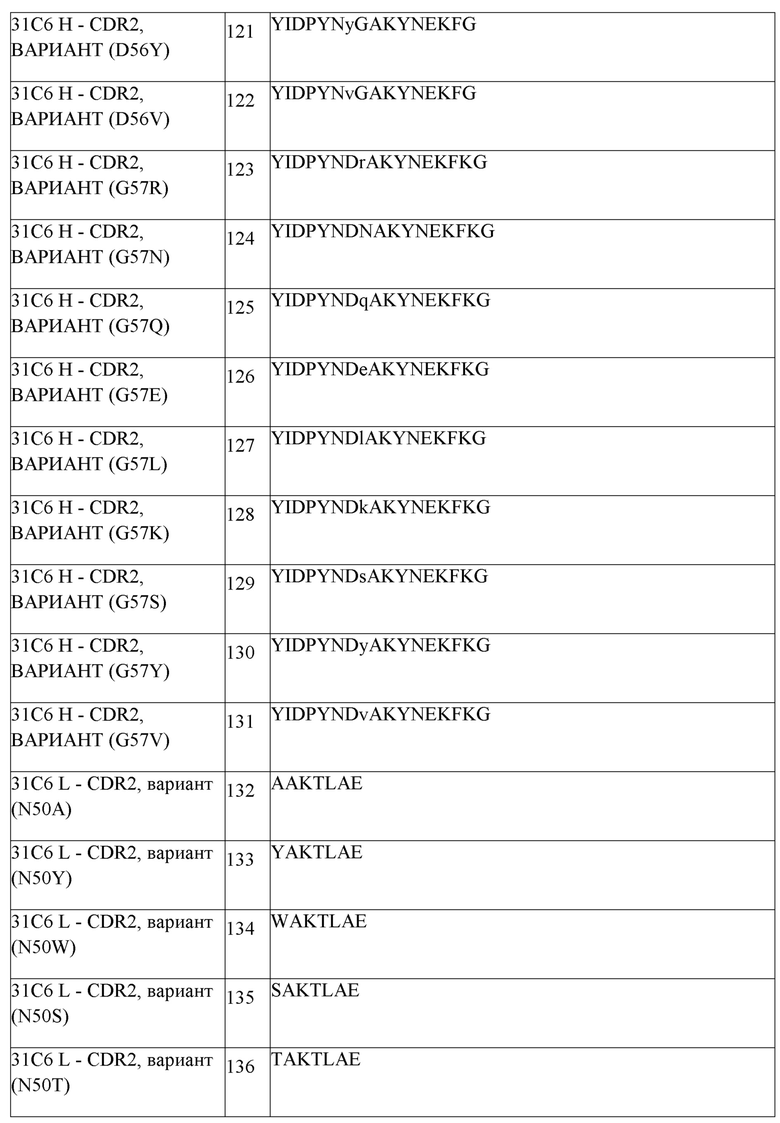

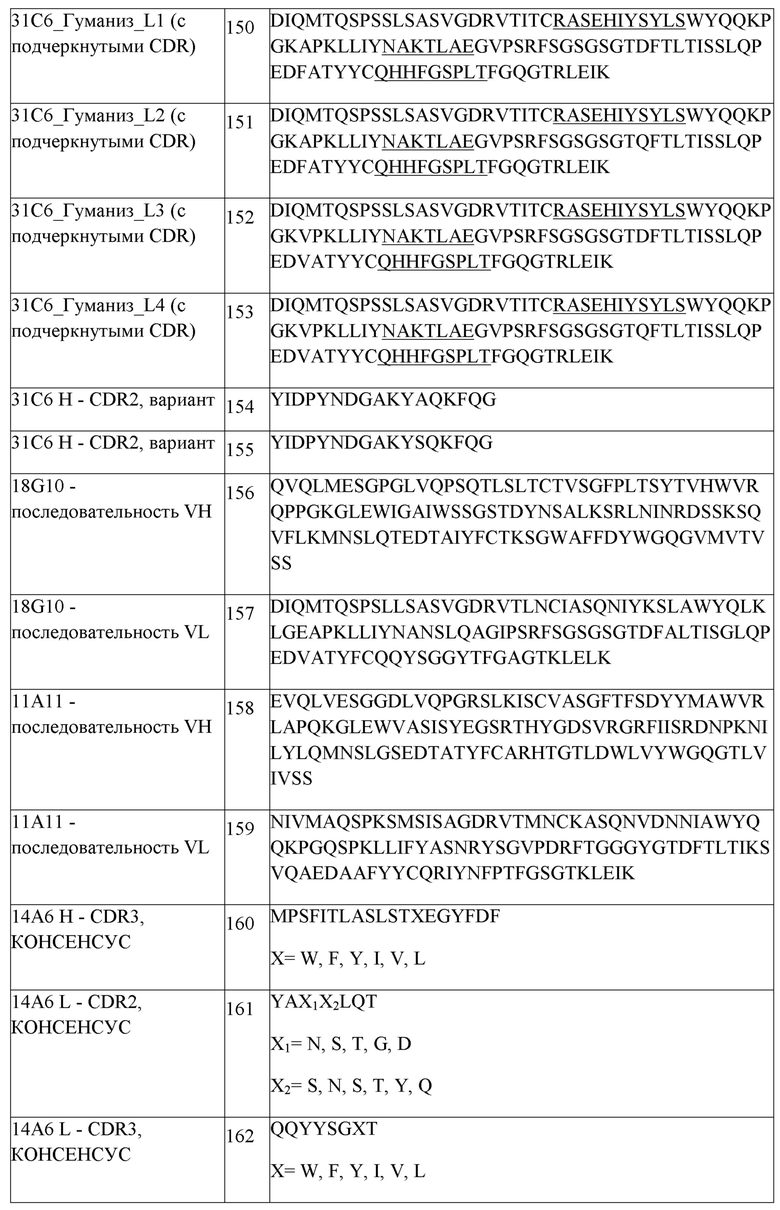





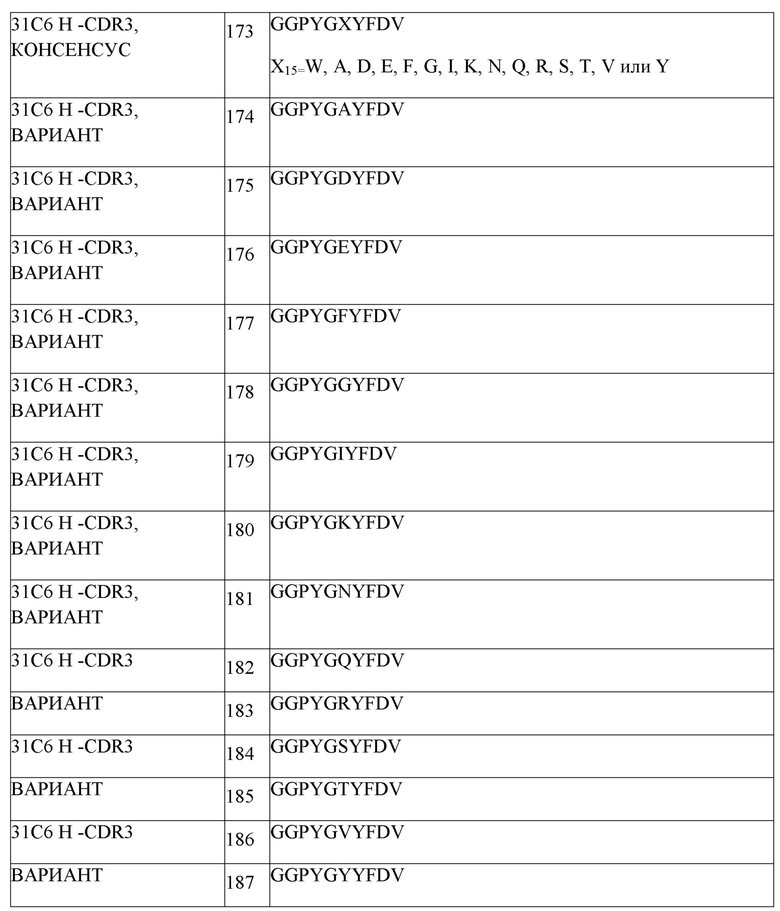
В некоторых вариантах осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит три CDR легкой цепи из CDRL1, CDRL2 и CDRL3, и/или три CDR тяжелой цепи из CDRH1, CDRH2 и CDRH3.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:35, CDRH2, содержащую SEQ ID NO:36, CDRH3, содержащую любую из SEQ ID NO:37, 103, 104, 105, 106, 107 или 160, CDRL1, содержащую SEQ ID NO:38, CDRL2, содержащую любую из SEQ ID NO:39, 89, 90, 91, 92, 93, 94, 95, 96, 97 или 69, и CDRL3, содержащую любую из SEQ ID NO:40, 98, 99, 100, 101, 102 или 162.
В другом варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:81, CDRH2, содержащую SEQ ID NO:82, CDRH3, содержащую SEQ ID NO:83, CDRL1, содержащую SEQ ID NO:84, CDRL2, содержащую SEQ ID NO:85, и CDRL3, содержащую SEQ ID NO:86.
В другом варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:108, CDRH2, содержащую любую из SEQ ID NO:109, 116, 117, 118, 119, 120, 121, 122, 123, 124, 125, 126, 127, 128, 129, 130, 131, 154, 155 или 167, CDRH3, содержащую любую из SEQ ID NO:110, 173, 174, 175, 176, 177, 178, 179, 180, 181, 182, 183, 184, 185, 186 или 187, CDRL1, содержащую SEQ ID NO:111, CDRL2, содержащую любую из SEQ ID NO:112, 132, 133, 134, 135, 136, 137, 138, 139, 140, 141, 142 или 168, и CDRL3, содержащую аминокислотную последовательность из SEQ ID NO:113.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:35, CDRH2, содержащую из SEQ ID NO:36, CDRH3, содержащую SEQ ID NO:37, CDRL1, содержащую SEQ ID NO:38, CDRL2, содержащую SEQ ID NO:39, и CDRL3, содержащую аминокислотную последовательность из SEQ ID NO:40.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:108, CDRH2, содержащую любую из SEQ ID NO:109, 154 или 145, CDRH3, содержащую SEQ ID NO:110, CDRL1, содержащую SEQ ID NO:111, CDRL2, содержащую SEQ ID NO:112, и CDRL3, содержащую аминокислотную последовательность из SEQ ID NO:113.
В другом варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую аминокислотную последовательность из SEQ ID NO:108, CDRH2, содержащую SEQ ID NO:154, CDRH3, содержащую SEQ ID NO:110, CDRL1, содержащую SEQ ID NO:111, CDRL2, содержащую SEQ ID NO:112, и CDRL3, содержащую SEQ ID NO:113.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи. В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:41, и вариабельную область легкой цепи, содержащую SEQ ID NO:42.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:87, и вариабельную область легкой цепи, содержащую SEQ ID NO:88.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:114, и вариабельную область легкой цепи, содержащую SEQ ID NO:115.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую любую из SEQ ID NO:43-58, 65-75 и 87, и вариабельную область легкой цепи, содержащую любую из SEQ ID NO:59-64, 76-80 и 88.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую любую из SEQ ID NO:144-149, и вариабельную область легкой цепи, содержащую любую из SEQ ID NO:150-153.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и вариабельную область легкой цепи, содержащую SEQ ID NO:152.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:147, и вариабельную область легкой цепи, содержащую SEQ ID NO:150.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:148, и вариабельную область легкой цепи, содержащую SEQ ID NO:153.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:163, и вариабельную область легкой цепи, содержащую SEQ ID NO:165.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:169, и вариабельную область легкой цепи, содержащую SEQ ID NO:171.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:164, и вариабельную область легкой цепи, содержащую SEQ ID NO:166.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:170, и вариабельную область легкой цепи, содержащую SEQ ID NO:172.



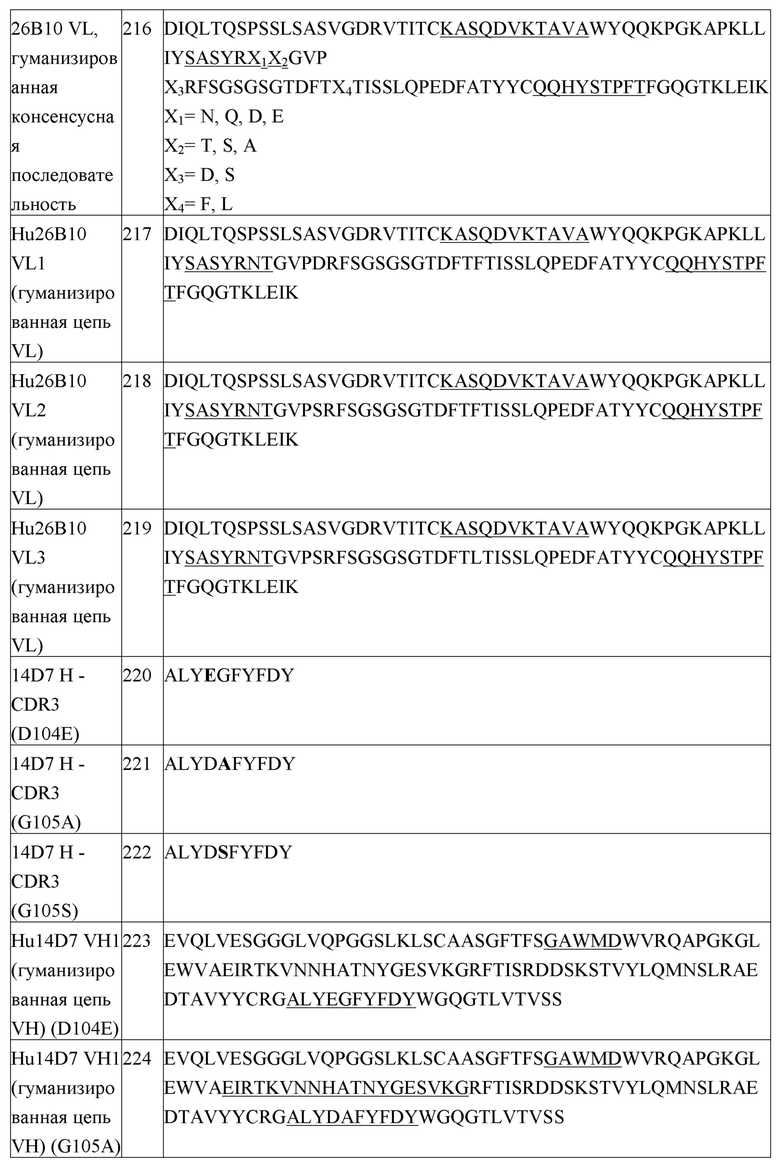

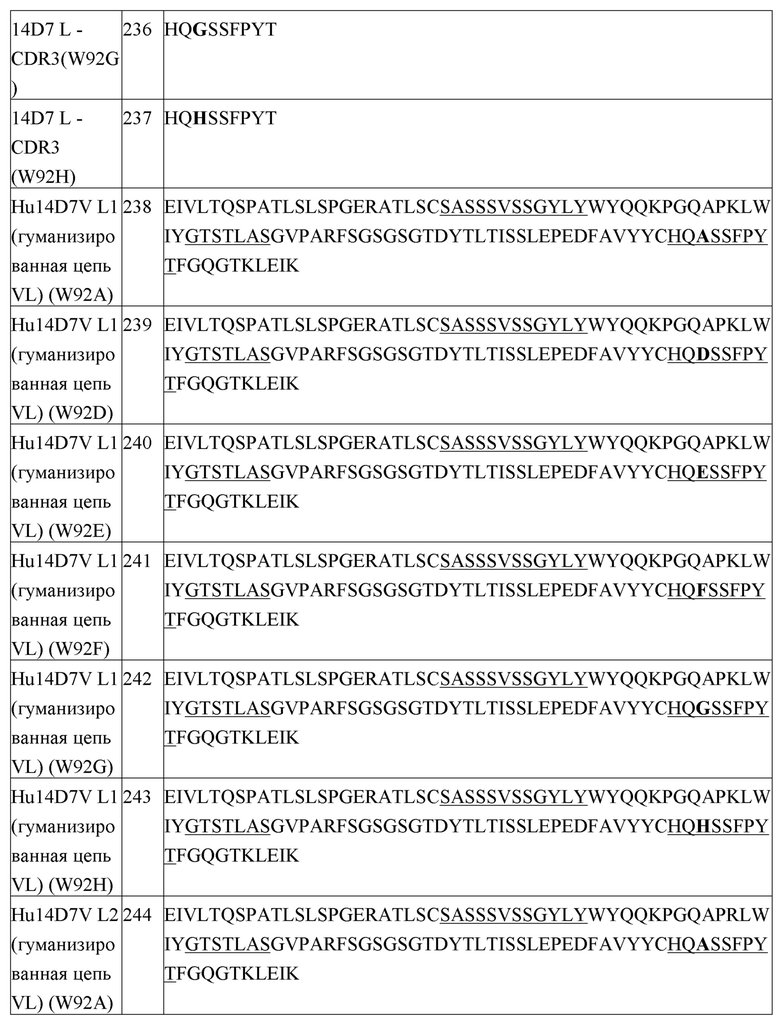
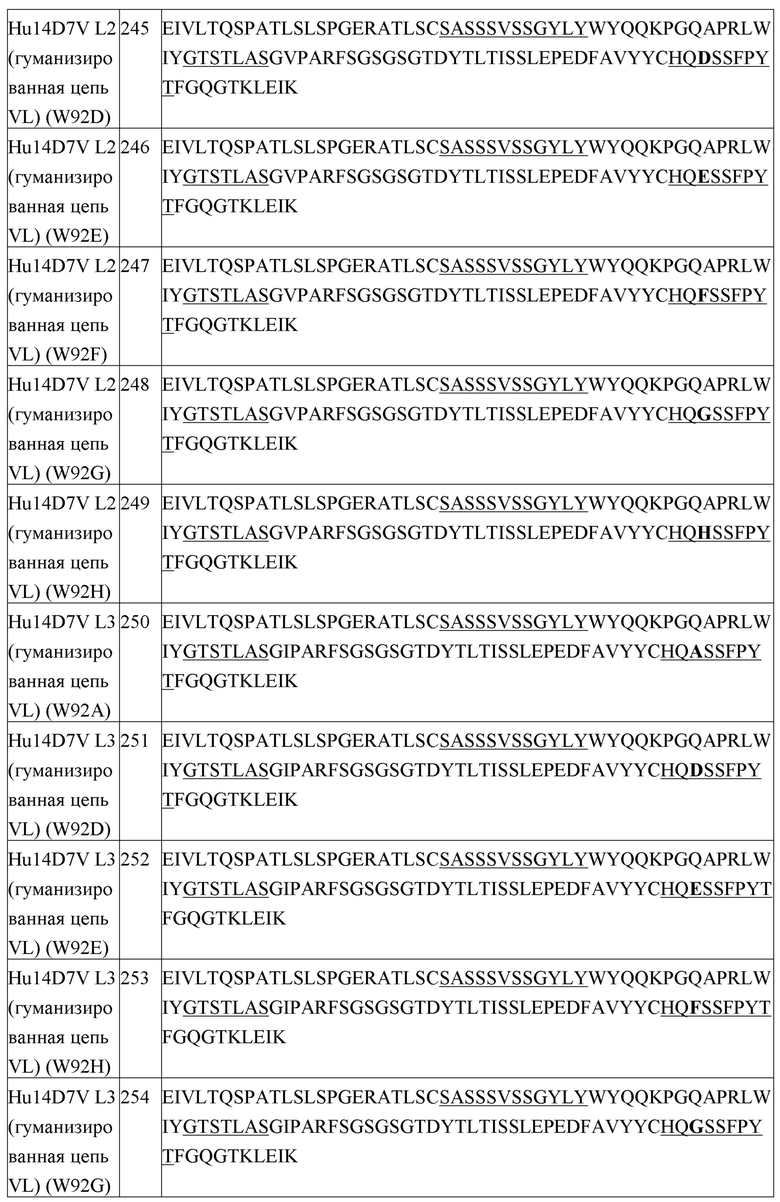
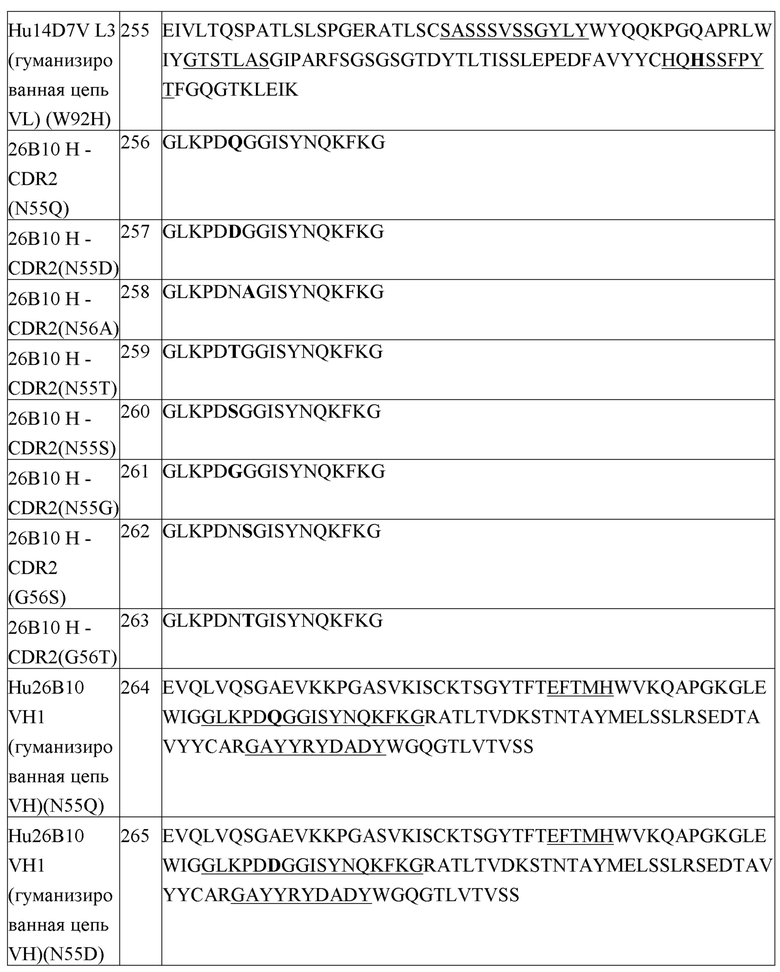
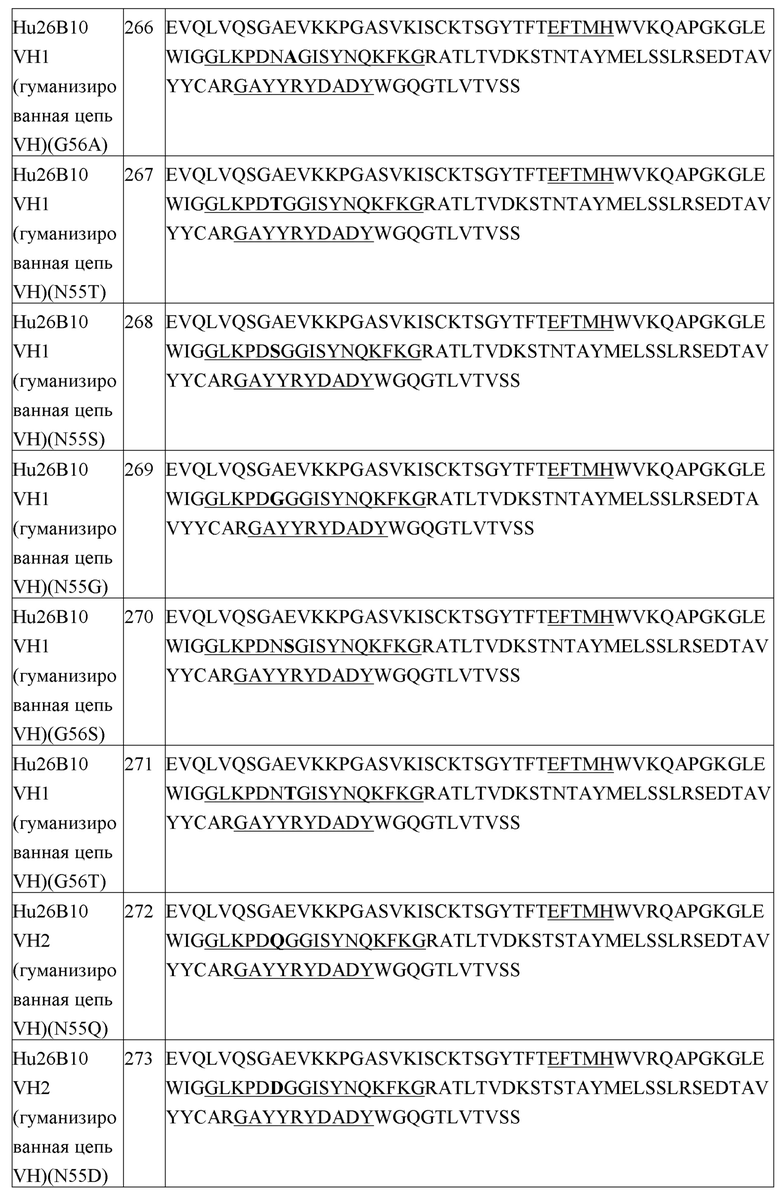


В одном варианте осуществления, анти-TIGIT антитело или антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:188, CDRH2, содержащую SEQ ID NO:189, CDRH3, содержащую любую из SEQ ID NO:190, 220, 221 или 222, CDRL1, содержащую SEQ ID NO:191, CDRL2, содержащую SEQ ID NO:192, и CDRL3, содержащую любую из SEQ ID NO:193, 232, 233, 234, 235, 236 или 237.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит CDRH1, содержащую SEQ ID NO:204, CDRH2, содержащую любую из SEQ ID NO:205, 256, 257, 258, 259, 260, 261, 262 или 263, CDRH3, содержащую SEQ ID NO:206, CDRL1, содержащую SEQ ID NO:207, CDRL2, содержащую SEQ ID NO:208, и CDRL3, содержащую SEQ ID NO:209.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи. В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:194, и вариабельную область легкой цепи, содержащую SEQ ID NO:195.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:196, и вариабельную область легкой цепи, содержащую SEQ ID NO:200.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:210, и вариабельную область легкой цепи, содержащую SEQ ID NO:211.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую SEQ ID NO:212, и вариабельную область легкой цепи, содержащую SEQ ID NO:216.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую любую из SEQ ID NO:197, 198, 199, 223, 224, 225, 226, 227, 228, 229, 230 и 231, и вариабельную область легкой цепи, содержащую любую из SEQ ID NO:201, 202, 203, 238, 239, 240, 241, 242, 243, 244, 245, 246, 247, 248, 249, 250, 251, 252, 253, 254 и 255.
В одном варианте осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит вариабельную область тяжелой цепи, содержащую любую из SEQ ID NO:213, 214, 215, 264, 265, 266, 267, 268, 269, 270, 271, 272, 273, 274, 275, 276, 277, 278, 279, 280, 281, 282, 283, 284, 285 и 286, и вариабельную область легкой цепи, содержащую любую из SEQ ID NO:217, 218 и 219.
Дополнительные антитела против TIGIT, которые можно использовать в составах, описанных в настоящем описании, включают антитела, описанные, например, в Международной заявке PCT No. WO 2016/106302; WO 2016/011264; и WO 2009/126688.
ТАБЛИЦА 6: Иллюстративные последовательности тяжелой цепи
В любом из вышеупомянутых вариантов осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент представляет собой антитело, содержащее любую из вариабельных тяжелых цепей, описанных выше, и константный домен любой человеческой тяжелой цепи. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению относится к изотипу IgG и содержит константный домен тяжелой цепи IgG1, IgG2, IgG3 или IgG4 человека. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен тяжелой цепи IgG1 человека (SEQ ID NO:291) или его вариант, где вариант содержит вплоть до 20 модифицированных аминокислотных замен. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению представляет собой антитело, содержащее константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность из SEQ ID NO:291. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен тяжелой цепи IgG1 человека где константный домен IgG1 является афукозилированным. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен тяжелой цепи IgG4 человека или его вариант, где вариант содержит вплоть до 20 модифицированных аминокислотных замен. В другом варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен тяжелой цепи IgG4 человека, где аминокислота в положении 228 (с использованием схемы нумерации EU) заменена с Ser на Pro. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен тяжелой цепи IgG4 человека, содержащий аминокислотную последовательность из SEQ ID NO:292.
В любом из вышеупомянутых вариантов осуществления, анти-TIGIT антитело или его антигенсвязывающий фрагмент может содержать любую из вариабельных легких цепей, описанных выше, и константный домен человеческой легкой цепи. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен легкой цепи каппа человека или его вариант, где вариант содержит вплоть до 20 модифицированных аминокислотных замен. В другом варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен легкой цепи лямбда человека или его вариант, где вариант содержит вплоть до 20 модифицированных аминокислотных замен. В одном варианте осуществления, антитело или его антигенсвязывающий фрагмент по изобретению содержит константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность из SEQ ID NO:293.
Составы
Составы по изобретению, минимизируют формирование агрегатов антитела (высокомолекулярных молекул) и частиц, высокомолекулярных и низкомолекулярных молекул, минимизируют окисление остатков метионина, и обеспечивают то, что антитело сохраняет биологическую активность с течением времени.
В одном аспекте изобретение относится к различным составам антитела против TIGIT или его антигенсвязывающего фрагмента. Например, настоящее изобретение относится к составам, содержащим (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, (ii) буфер (например, L-гистидин или ацетат), (iii) невосстанавливающий сахар (например, сахарозу); (iv) неионное поверхностно-активное вещество (например, полисорбат 80); и (v) антиоксидант (например, L-метионин). В одном варианте осуществления, состав дополнительно содержит антитело против PD-1. В одном аспекте состав дополнительно содержит хелатирующий агент. В одном варианте осуществления, хелатирующий агент присутствует в количестве от приблизительно 1 мкМ до приблизительно 50 мкМ. В одном варианте осуществления, хелатирующий агент представляет собой диэтилентриаминпентауксусную кислоту (ДТПА). В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА.
В другом аспекте настоящее изобретение относится также к различным совместным составам антитела против TIGIT или его антигенсвязывающего фрагмента и антитела против PD-1 человека или его антигенсвязывающего фрагмента. В одном варианте осуществления состав содержит (i) анти-TIGIT антитело или его антигенсвязывающий фрагмент, (ii) антитело против PD-1 человека или его антигенсвязывающий фрагмент, (iii) буфер (например, L-гистидин или ацетат), (iv) невосстанавливающий сахар (например, сахарозу), (v) неионное поверхностно-активное вещество (например, полисорбат 80) и (vi) антиоксидант (например, L-метионин). В одном варианте осуществления, состав дополнительно содержит хелатирующий агент В одном варианте осуществления, хелатирующий агент присутствует в количестве от приблизительно 1 мкМ до приблизительно 50 мкМ. В одном варианте осуществления, хелатирующий агент представляет собой диэтилентриаминпентауксусную кислоту (ДТПА). В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА.
Фармацевтические составы по настоящему изобретению могут включать буферы.
Буферы, которые можно использовать в фармацевтических составах и способах по изобретению, включают сукцинат (натрия или калия), L-гистидин, фосфат (натрия или калия), трис (трис(гидроксиметил)аминометан), диэтаноламин, цитрат (натрия), ацетат (натрия) и т.п. В одном варианте осуществления изобретения, буфер присутствует в составе в концентрации приблизительно 1-20 мМ (1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 и 20 мМ). В конкретных вариантах осуществления изобретения, буфер представляет собой гистидиновый, например, L-гистидиновый буфер.
Буфер по этому изобретению имеет pH в диапазоне от приблизительно 4,5 до приблизительно 6,5; приблизительно 5,0-6,2; приблизительно 5,5-6,0; и предпочтительно, имеет pH приблизительно 5,8. При установлении иллюстративного состава, гистидиновые и ацетатные буферы в диапазоне pH 5,0-6,0 исследовали по применимости. Когда указан диапазон значений pH, например, «pH между pH 5,5 и 6,0», диапазон предназначен для включения указанных значений. Например, диапазон от приблизительно 5,0 до приблизительно 6,0 включает 5,0, 5,1, 5,2, 5,3, 5,4, 5,5, 5,6, 5,7, 5,8, 5,9 и 6,0. Если не указано иное, pH относится к pH после разведения лиофилизированных составов по настоящему изобретению. pH, как правило, измеряют при 25°C с использованием стандартного pH-метра со стеклянным электродом. В рамках изобретения, раствор, содержащий «гистидиновый буфер при pH X», относится к раствору при pH X и содержащему гистидиновый буфер, т.е. pH предназначен для обозначения pH раствора.
В одном варианте осуществления изобретения, состав антитела против TIGIT, и совместный состав антитела против TIGIT и антитела против PD-1 человека содержит невосстанавливающий сахар. В рамках изобретения, «невосстанавливающий сахар» представляет собой сахар, неспособный действовать в качестве восстанавливающего средства, поскольку он не содержит или не может быть переведен в форму, содержащую свободную альдегидную группу или свободную кетоновую группу. Примеры невосстанавливающих сахаров включают, но без ограничения дисахариды, такие как сахароза и трегалоза. В одном варианте осуществления изобретения, невосстанавливающий сахар присутствует в количестве приблизительно 1-10% (масс./об.) (1, 2, 3, 4, 5, 6, 7, 8, 9 или 10%). В другом варианте осуществления, невосстанавливающий сахар присутствует в количестве от приблизительно 6% до приблизительно 8% (масс./об.) (6, 7 или 8%). В следующем варианте осуществления, невосстанавливающий сахар присутствует в количестве приблизительно 6% (масс./об.). В следующем варианте осуществления, невосстанавливающий сахар присутствует в количестве приблизительно 7% (масс./об.). В следующем варианте осуществления, невосстанавливающий сахар присутствует в количестве приблизительно 8% (масс./об.). В одном варианте осуществления, невосстанавливающий сахар представляет собой сахарозу, трегалозу или рафинозу. В другом варианте осуществления, невосстанавливающий сахар представляет собой сахарозу. В следующем варианте осуществления, сахароза присутствует при 6-8% масс./об. В одном варианте осуществления, сахароза присутствует при приблизительно 6% (масс./об.). В одном варианте осуществления, сахароза присутствует при приблизительно 7% (масс./об.). В одном варианте осуществления, сахароза присутствует при приблизительно 8% (масс./об.).
Составы по изобретению содержат также поверхностно-активное вещество. В рамках изобретения, поверхностно-активное вещество представляет собой поверхностно действующее вещество, являющееся амфипатическим по характеру. Поверхностно-активные вещества можно добавлять в составы в настоящем описании для обеспечения стабильности, уменьшения и/или предотвращения агрегации, или для предотвращения и/или ингибирования повреждения белка в условиях переработки, таких как очистка, фильтрация, лиофилизация, транспортировка, хранение и доставка. По настоящему изобретению, поверхностно-активное вещество можно использовать для обеспечения дополнительной стабильности активного ингредиента(ингредиентов).
Неионные поверхностно-активные вещества, которые можно использовать в составах, включая совместные составы, по изобретению, включают, но без ограничения, сложные эфиры жирных кислот и полиоксиэтиленсорбитана (полисорбаты, продаваемые под торговым наименованием Tween® (Uniquema Americas LLC, Wilmington, DE)) включая полисорбат-20 (полиоксиэтиленсорбитанмонолаурат), полисорбат-40 (полиоксиэтиленсорбитанмонопальмитат), полисорбат-60 (полиоксиэтиленсорбитанмоностеарат) и полисорбат-80 (полиоксиэтиленсорбитанмоноолеат); сложные алкиловые эфиры полиоксиэтилена, такие как Brij® 58 (Uniquema Americas LLC, Wilmington, DE) и Brij® 35; полоксамеры (например, полоксамер 188); Triton® X-100 (Union Carbide Corp., Houston, TX) и Triton® X-114; NP40; Span 20, Span 40, Span 60, Span 65, Span 80 и Span 85; сополимеры этилена и пропиленгликоля (например, серии неионных поверхностно-активных веществ плюроник®, таких как плюроник® F68, плюроник® 10R5, плюроник® F108, плюроник® F127, плюроник® F38, плюроник® L44, плюроник® L62 (BASF Corp., Ludwigshafen, Germany); и додецилсульфат натрия (SDS). В одном варианте осуществления, неионное поверхностно-активное вещество представляет собой полисорбат 80 или полисорбат 20. В одном варианте осуществления, неионное поверхностно-активное вещество представляет собой полисорбат 20. В другом варианте осуществления, неионное поверхностно-активное вещество представляет собой полисорбат 80.
Количество неионного поверхностно-активного вещества для включения в составы по изобретению представляет собой количество, достаточное для осуществления желательной функции, т.е. минимальное количество, необходимое для стабилизации активного фармацевтического ингредиента (т.е. антитела против TIGIT или его антигенсвязывающего фрагмента, или как антитела против TIGIT или его антигенсвязывающего фрагмента, так и антитела против PD-1 человека или его антигенсвязывающего фрагмента) в составе. Все проценты неионного поверхностно-активного вещества приведены как % масс./об. Как правило, поверхностно-активное вещество присутствует в концентрации от приблизительно 0,008% до приблизительно 0,1% масс./об. В некоторых вариантах осуществления этого аспекта изобретения, поверхностно-активное вещество присутствует в составе в количестве от приблизительно 0,01% до приблизительно 0,1%; от приблизительно 0,01% до приблизительно 0,09%; от приблизительно 0,01% до приблизительно 0,08%; от приблизительно 0,01% до приблизительно 0,07%; от приблизительно 0,01% до приблизительно 0,06%; от приблизительно 0,01% до приблизительно 0,05%; от приблизительно 0,01% до приблизительно 0,04%; от приблизительно 0,01% до приблизительно 0,03%, от приблизительно 0,01% до приблизительно 0,02%, от приблизительно 0,015% до приблизительно 0,04%; от приблизительно 0,015% до приблизительно 0,03%, от приблизительно 0,015% до приблизительно 0,02%, от приблизительно 0,02% до приблизительно 0,04%, от приблизительно 0,02% до приблизительно 0,035% или от приблизительно 0,02% до приблизительно 0,03%. В конкретных вариантах осуществления, поверхностно-активное вещество присутствует в количестве приблизительно 0,02%. В альтернативных вариантах осуществления, поверхностно-активное вещество присутствует в количестве приблизительно 0,01%, приблизительно 0,015%, приблизительно 0,025%, приблизительно 0,03%, приблизительно 0,035% или приблизительно 0,04%.
В иллюстративных вариантах осуществления изобретения, поверхностно-активное вещество представляет собой неионное поверхностно-активное вещество, выбранное из группы, состоящей из: полисорбата 20 и полисорбата 80. В предпочтительных вариантах осуществления, поверхностно-активное вещество представляет собой полисорбат 80.
В конкретных вариантах осуществления, составы, включая совместные составы, по изобретению, содержат от приблизительно 0,01% до приблизительно 0,04% масс./об. полисорбата 80. В следующих вариантах осуществления, составы, описанные в настоящем описании, содержат полисорбат 80 в количестве приблизительно 0,008% масс./об., приблизительно 0,01% масс./об. В одном варианте осуществления, количество полисорбата 80 составляет приблизительно 0,015 масс./об.%. В другом варианте осуществления, количество полисорбата 80 составляет приблизительно 0,02% масс./об. В следующем варианте осуществления, количество полисорбата 80 составляет приблизительно 0,025% масс./об. В другом варианте осуществления, количество полисорбата 80 составляет приблизительно 0,03% масс./об. В следующем варианте осуществления, количество полисорбата 80 составляет приблизительно 0,035% масс./об. В другом варианте осуществления, количество полисорбата 80 составляет приблизительно 0,04% масс./об. В следующем варианте осуществления, количество полисорбата 80 составляет приблизительно 0,045% масс./об. В конкретных вариантах осуществления, составы по изобретению содержат приблизительно 0,02% масс./об. полисорбата 80.
Составы, включая совместные составы, по настоящему изобретению содержат также метионин или его фармацевтически приемлемую соль, в качестве антиоксиданта. В одном варианте осуществления изобретения, метионин представляет собой L-метионин. В другом варианте осуществления, метионин представляет собой фармацевтически приемлемую соль L-метионина, например, такую как метионин HCl. В одном варианте осуществления, метионин присутствует в составе в концентрации приблизительно 1-20 мМ (1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 и 20 мМ). В другом варианте осуществления, метионин присутствует от приблизительно 5 мМ до приблизительно 10 мМ (5, 6, 7, 8, 9 и 10 мМ). В другом варианте осуществления, метионин присутствует при приблизительно 10 мМ.
Составы, включая совместные составы, по настоящему изобретению могут также дополнительно содержать хелатирующий агент. В одном варианте осуществления изобретения, хелатирующий агент присутствует в составе в концентрации приблизительно 5-30 мкМ (например, 5, 10, 15, 20, 25, или 30 мкМ). В одном варианте осуществления, хелатирующий агент представляет собой ДТПА. В другом варианте осуществления, хелатирующий агент представляет собой ЭДТА.
Лиофилизированные фармацевтические композиции
Лиофилизированные составы терапевтических белков обеспечивают несколько преимуществ. Лиофилизированные составы, как правило, обеспечивают лучшую химическую стабильность, чем растворы составов, и таким образом, увеличивают время полужизни. Лиофилизированный состав можно также разводить в различных концентрациях, в зависимости от клинических факторов, таких как способ введения или дозирования. Например, лиофилизированный состав можно разводить в высокой концентрации (т.е. в небольшом объеме), при необходимости, для подкожного введения, или в более низкой концентрации, при внутривенном введении. Высокие концентрации могут также являться необходимыми, если высокие дозы необходимы для конкретного субъекта, в частности при подкожном введении, где объем инъекции необходимо минимизировать. Один из таких лиофилизированных составов антитела описан в Патенте США No. 6267958, полное содержание которого, таким образом, приведено в качестве ссылки. Лиофилизированные составы другого терапевтического белка описаны в Патенте США No. 7247707, полное содержание которого, таким образом, приведено в качестве ссылки.
Как правило, лиофилизированный состав получают, предусматривая разведение при высокой концентрации продукта лекарственного средства (DP, в одном иллюстративном варианте осуществления, гуманизированного антитела против PD-1 пембролизумаба или его антигенсвязывающего фрагмента), т.е., предусматривая разведение в низком объеме воды. Последующее разведение водой или изотоническим буфером затем можно легко использовать для разведения DP до более низкой концентрации. Как правило, наполнители включают в лиофилизированный состав по настоящему изобретению на уровнях, которые обеспечивают приблизительно изотонический состав при разведении при высокой концентрации DP, например, для подкожного введения. Разведение в большем объеме воды для получения более низкой концентрации DP неизбежно уменьшает тоничность разведенного раствора, однако, такое уменьшение может не иметь большой важности при не подкожном, например, внутривенном, введении. Если изотоничность является желательной при более низкой концентрации DP, лиофилизированный порошок можно разводить в стандартном низком объеме воды, и затем дополнительно разводить изотоническим разбавителем, таким как 0,9% хлорид натрия.
Лиофилизированные составы по настоящему изобретению получают посредством лиофилизации (сублимации) подготовленного для лиофилизации раствора. Сублимацию осуществляют посредством замораживания состава и последующей сублимации воды при температуре, подходящей для первичной сушки. В этих условиях, температура продукта ниже эвтектической точки или температуры коллапса состава. Как правило, температура стеллажей для первичной сушки лежит в диапазоне приблизительно от -30 до 25°C (при условии, что продукт остается замороженным в ходе первичной сушки) при подходящем давлении, лежащем в диапазоне, как правило, приблизительно от 50 до 250 мторр (от 6,7 до 33,3 Па). Состав, размер и тип контейнера, содержащего образец (например, стеклянного флакона), и объем жидкости определяют время, необходимое для сушки, которое может лежать в диапазоне от нескольких часов до нескольких суток (например, 40-60 час). Стадию вторичной сушки можно проводить при приблизительно 0-40°C, в зависимости, в первую очередь, от типа и размера контейнера, и типа используемого белка. Время вторичной сушки определяется желательным уровнем остаточной влажности в продукте и, как правило, занимает по меньшей мере приблизительно 5 часов. Как правило, содержание влажности в лиофилизированном составе составляет менее, чем приблизительно 5%, и предпочтительно, менее, чем приблизительно 3%. Давление может являться таким же, как давление, используемое на стадии первичной сушки. Условия сублимации можно менять, в зависимости от состава и размера флакона.
В некоторых случаях, может являться желательной лиофилизация белкового состава в контейнере, в котором необходимо проводить разведение белка, чтобы избежать стадии переноса. Контейнер, в этом случае, может, например, представлять собой флакон 3, 5, 10, 20, 50 или 100 см3.
Лиофилизированные составы по настоящему изобретению разводят перед введением. Белок можно разводить до концентрации приблизительно 10, 15, 20, 25, 30, 40, 50, 60, 75, 80, 90 или 100 мг/мл, или более высоких концентраций, таких как 150 мг/мл, 200 мг/мл, 250 мг/мл или 300 мг/мл, вплоть до приблизительно 500 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 10-300 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 20-250 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 150-250 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 180-220 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 50-150 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 100 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 75 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 50 мг/мл. В одном варианте осуществления, концентрация белка после разведения составляет приблизительно 25 мг/мл. Высокие концентрации белка являются особенно полезными, когда намечена подкожная доставка разведенного состава. Однако, для других способов введения, таких как внутривенное введение, более низкие концентрации белка могут являться желательными (например, приблизительно 5-50 мг/мл).
Разведение, как правило, проводят при температуре приблизительно 25°C для обеспечения полной гидратации, хотя другие температуры можно использовать, как желательно. Время, необходимое для разведения, зависит, например, от типа разбавителя, количества наполнителя(наполнителей) и белка. Иллюстративные разбавители включают стерильную воду, бактериостатическую воду для инъекций (BWFI), раствор для забуферивания pH (например, фосфатно-солевой буфер), стерильный солевой раствор, раствор Рингера или раствор декстрозы.
Жидкие фармацевтические композиции
Жидкий состав антитела можно получать посредством взятия лекарственного вещества (например, гуманизированного антитела против PD-1), которое находится в жидкой форме (например, пембролизумаба в водном фармацевтическом составе), и замены его буфера на желательный буфер на последней стадии способа очистки. Стадия лиофилизации не присутствует в этом варианте осуществления. Лекарственное вещество в конечном буфере концентрируют до желательной концентрации. Наполнители, такие как сахароза и полисорбат 80, добавляют к лекарственному веществу и разводят его с использованием подходящего буфера до конечной концентрации белка. Конечный состав лекарственного вещества фильтруют с использованием фильтров 0,22 мкм, и заполняют им конечный контейнер (например, стеклянные флаконы).
III. Способы применения
Изобретение также относится к способу лечения злокачественной опухоли у субъекта, включающему введение эффективного количества любого из составов по изобретению; т.е., любого состава, описанного в настоящем описании, субъекту. В некоторых конкретных вариантах осуществления этого способа, состав вводят субъекту посредством внутривенного введения. В других вариантах осуществления, состав вводят субъекту посредством подкожного введения. В одном варианте осуществления, изобретение относится к способу лечения злокачественной опухоли у пациента-человека, включающему введение любого состава по изобретению пациенту.
В любом из способов по изобретению, злокачественная опухоль может быть выбрана из группы, состоящей из: меланомы, рака легкого, рака головы и шеи, рака мочевого пузыря, рака молочной железы, злокачественной опухоли желудочно-кишечного тракта, множественной миеломы, печеночноклеточного рака, лимфомы, рака почки, мезотелиомы, рака яичника, рака пищевода, рака анального канала, злокачественной опухоли рака желчных протоков, колоректального рака, рака шейки матки, рака щитовидной железы, злокачественной опухоли слюнных желез, рака предстательной железы (например, невосприимчивой к гормонам аденокарциномы предстательной железы), рака поджелудочной железы, рака ободочной кишки, рака пищевода, рака печени, рака щитовидной железы, глиобластомы, глиомы и других неопластических злокачественных новообразований.
В некоторых вариантах осуществления, рак легкого представляет собой немелкоклеточный рак легкого.
В альтернативных вариантах осуществления, рак легкого представляет собой мелкоклеточный рак легкого.
В некоторых вариантах осуществления, лимфома представляет собой лимфому Ходжкина.
В других вариантах осуществления, лимфома представляет собой неходжскинскую лимфому. В конкретных вариантах осуществления, лимфома представляет собой медиастинальную крупноклеточную В-клеточную лимфому.
В некоторых вариантах осуществления, рак молочной железы представляет собой трижды отрицательный рак молочной железы.
В следующих вариантах осуществления, рак молочной железы представляет собой ER+/HER2- рак молочной железы.
В некоторых вариантах осуществления, рак мочевого пузыря представляет собой уротелиальную злокачественную опухоль.
В некоторых вариантах осуществления, рак головы и шеи представляет собой злокачественную опухоль носоглотки. В некоторых вариантах осуществления, злокачественная опухоль представляет собой рак щитовидной железы. В других вариантах осуществления, злокачественная опухоль представляет собой злокачественную опухоль слюнных желез. В других вариантах осуществления, злокачественная опухоль представляет собой плоскоклеточную карциному головы и шеи.
В одном варианте осуществления, изобретение относится к способу лечения метастазирующего немелкоклеточного рака легкого (NSCLC) у пациента-человека, включающему введение состава по изобретению пациенту. В конкретных вариантах осуществления, пациент имеет опухоль с высокой экспрессией PD-L1 [(показатель доли опухоли (TPS) ≥50%)], и его ранее не подвергали лечению с использованием химиотерапии содержащими платину средствами. В других вариантах осуществления, пациент имеет опухоль с экспрессией PD-L1 (TPS ≥1%), и его ранее подвергали лечению с использованием химиотерапии содержащими платину средствами. В других вариантах осуществления, пациент имеет опухоль с экспрессией PD-L1 (TPS ≥1%), и его ранее не подвергали лечению с использованием химиотерапии содержащими платину средствами. В конкретных вариантах осуществления, пациент имел прогрессирование заболевания во время или после проведения химиотерапии содержащими платину средствами. В конкретных вариантах осуществления, TPS PD-L1 определяют посредством одобренного FDA тестирования. В конкретных вариантах осуществления, опухоль пациента не имеет геномных аберраций EGFR или ALK. В конкретных вариантах осуществления, опухоль пациента имеет геномную аберрацию EGFR или ALK, и пациент имел прогрессирование заболевания во время или после проведения лечения аберрации(аберраций) EGFR или ALK, до введения антитела против PD-1 или его антигенсвязывающего фрагмента.
В некоторых вариантах осуществления, злокачественная опухоль представляет собой метастазирующий колоректальный рак с высокими уровнями микросателлитной нестабильности (MSI-H).
В некоторых вариантах осуществления, злокачественная опухоль представляет собой метастазирующий колоректальный рак с высокими уровнями микросателлитной нестабильности (MSI-H).
В некоторых вариантах осуществления, злокачественная опухоль представляет собой солидную опухоль с высоким уровнем микросателлитной нестабильности (MSI-H).
В некоторых вариантах осуществления, злокачественная опухоль представляет собой солидную опухоль с высокой нагрузкой мутаций.
В некоторых вариантах осуществления, злокачественная опухоль выбрана из группы, состоящей из: меланомы, немелкоклеточного рака легкого, рецидивирующей или невосприимчивой классической лимфомы Ходжкина, плоскоклеточной карциномы головы и шеи, уротелиальной злокачественной опухоли, рака пищевода, рака желудка и печеночноклеточного рака.
В других вариантах осуществления вышеуказанных способов лечения, злокачественная опухоль представляет собой гематологическое злокачественное новообразование. В конкретных вариантах осуществления, гематологическое злокачественное новообразование представляет собой острый лимфобластный лейкоз (ALL), острый миелоидный лейкоз (AML), хронический лимфоцитарный лейкоз (CLL), хронический миелоидный лейкоз (CML), диффузную крупноклеточную В-клеточную лимфому (DLBCL), положительную по EBV DLBCL, первичную медиастинальную крупноклеточную В-клеточную лимфому, крупноклеточную В-клеточную лимфому с высоким содержанием T-клеток/гистиоцитов, фолликулярную лимфому, лимфому Ходжкина (HL), лимфому из клеток мантийной зоны (MCL), множественную миелому (MM), злокачественную опухоль с экспрессией белка-1 лейкоза миелоидных клеток (Mcl-1), миелодиспластический синдром (MDS), неходжскинскую лимфому (NHL) или мелколимфоцитарную лимфому (SLL).
Злокачественные новообразования, для которых показана улучшенная свободная от заболевания и общая выживаемость, применительно к присутствию инфильтрующих опухоль лимфоцитов в биоптате или хирургическом материале, например, при меланоме, колоректальном раке, раке печени, почки, желудка/пищевода, молочной железы, поджелудочной железы и яичника, охвачены способами и видами лечения, описанными в настоящем описании. Известно, что такие подтипы злокачественных опухолей являются чувствительными к иммунному контролю T-лимфоцитов. Кроме того, охвачены невосприимчивые или рецидивирующие злокачественные новообразования, рост которых можно ингибировать с использованием антител, описанных в настоящем описании.
Дополнительные злокачественные опухоли, при которых можно получать преимущество от лечения с использованием составов, описанных в настоящем описании, включают злокачественные опухоли, ассоциированные с персистирующей инфекцией вирусами, такими как вирусы иммунодефицита человека, вирусы гепатита класса A, B и C, вирус Эпштейна-Барр, вирусы папилломы человека, как известно, имеющие причинно-следственную связь, например, с саркомой Капоши, раком печени, злокачественной опухолью носоглотки, лимфомой, злокачественными опухолями шейки матки, вульвы, анального канала, пениса и полости рта.
Составы можно использовать также для предотвращения или лечения инфекции и инфекционного заболевания. Таким образом, изобретение относится к способу лечения хронической инфекции у субъекта-млекопитающего, включающему введение эффективного количества состава по изобретению субъекту. В некоторых конкретных вариантах осуществления этого способа, состав вводят субъекту посредством внутривенного введения. В других вариантах осуществления, состав вводят субъекту посредством подкожного введения.
Эти средства можно использовать отдельно, или в комбинации с вакцинами, для стимуляции иммунного ответа на патогены, токсины и собственные антигены. Антитела или их антигенсвязывающие фрагменты можно использовать для стимуляции иммунного ответа на вирусы, инфекционные для человека, включая, но без ограничения: вирусы иммунодефицита человека, вирусы гепатита класса A, B и C, вирус Эпштейна-Барр, цитомегаловирус человека, вирусы папилломы человека и вирусы герпеса. Антагонистические антитела против PD-1 или фрагменты антител можно использовать для стимуляции иммунного ответа на инфекцию бактериальных или грибковых паразитов и других патогенов. Вирусные инфекции гепатитом B и C и HIV присутствуют среди инфекций, как считают, являющихся хроническими вирусными инфекциями.
Составы по изобретению можно вводить пациенту в комбинации с одним или несколькими «дополнительными лекарственными средствами». Дополнительное лекарственное средство может представлять собой биологическое лекарственное средство (включая, но без ограничения, антитела против VEGF, EGFR, Her2/neu, рецепторов VEGF, других рецепторов факторов роста, CD20, CD40, CD-40L, OX-40, 4-1BB и ICOS), иммуногенное средство (например, ослабленные злокачественные клетки, антигены опухолей, антигенпредставляющие клетки, такие как дендритные клетки, сенсибилизированные происходящими из опухоли антигеном или нуклеиновыми кислотами, иммуностимулирующие цитокины (например, IL-2, IFNα2, GM-CSF), и клетки, трансфицированные генами, кодирующими иммуностимулирующие цитокины, такие как, но без ограничения, GM-CSF).
Как отмечено выше, в некоторых вариантах осуществления способов по изобретению, способ дополнительно включает введение дополнительного лекарственного средства. В конкретных вариантах осуществления, дополнительное лекарственное средство представляет собой антитело против LAG3 или его антигенсвязывающий фрагмент, антитело против GITR или его антигенсвязывающий фрагмент, антитело против CTL4 или его антигенсвязывающий фрагмент, антитело против CD27 или его антигенсвязывающий фрагмент. В одном варианте осуществления, дополнительное лекарственное средство представляет собой вектор на основе вируса болезни Ньюкасла, экспрессирующий IL-12. В следующем варианте осуществления, дополнительное лекарственное средство представляет собой динациклиб. В дополнительных вариантах осуществления, дополнительное лекарственное средство представляет собой агонист STING.
Пригодные способы введения могут, например, включать парентеральную доставку, включая внутримышечную, подкожную, так же как интратекальную, прямую интравентрикулярную, внутривенную, внутрибрюшинную. Лекарственные средства можно вводить множеством общепринятых способов, таких как внутрибрюшинная, парентеральная, внутриартериальная или внутривенная инъекция. Способы введения, в которых объем раствора должен являться ограниченным (например, подкожное введение) требуют лиофилизированного состава, чтобы позволять разведение в высокой концентрации.
Выбор дозы дополнительного лекарственного средства зависит от нескольких факторов, включая скорость оборота молекулы в сыворотке или ткани, уровень симптомов, иммуногенность молекулы, и доступность мишеней - клеток, ткани или органа, у индивидуума, подвергаемого лечению. Доза дополнительного лекарственного средства должна представлять собой количество, обеспечивающее приемлемый уровень побочных эффектов. Соответственно, уровень дозы и частота дозирования каждого дополнительного лекарственного средства (например, биотерапевтического или химиотерапевтического средства) могут зависеть, частично, от конкретного лекарственного средства, тяжести злокачественной опухоли, подвергаемой лечению, и характеристик пациента. Доступны руководства по выбору соответствующих доз антител, цитокинов и малых молекул. См., например, Wawrzynczak (1996) Antibody Therapy, Bios Scientific Pub. Ltd, Oxfordshire, UK; Kresina (ed.) (1991) Monoclonal Antibodies, Cytokines and Arthritis, Marcel Dekker, New York, NY; Bach (ed.) (1993) Monoclonal Antibodies and Peptide Therapy in Autoimmune Diseases, Marcel Dekker, New York, NY; Baert et al. (2003) New Engl. J. Med. 348:601-608; Milgrom et al. (1999) New Engl. J. Med. 341:1966-1973; Slamon et al. (2001) New Engl. J. Med. 344:783-792; Beniaminovitz et al. (2000) New Engl. J. Med. 342:613-619; Ghosh et al. (2003) New Engl. J. Med. 348:24-32; Lipsky et al. (2000) New Engl. J. Med. 343:1594-1602; Physicians' Desk Reference 2003 (Physicians' Desk Reference, 57th Ed); Medical Economics Company; ISBN: 1563634457; 57th edition (November 2002). Определение соответствующего режима дозирования может осуществлять клиницист, например, с использованием параметров или факторов, как известно или как подозревают в данной области, влияющих на лечение, или как прогнозируют, влияющих на лечение, и определение может зависеть, например, от клинического анамнеза пациента (например, предшествующей терапии), типа и стадии злокачественной опухоли, подлежащей лечению, и биомаркеров ответа на одно или несколько из лекарственных средств при комбинированной терапии.
Доступно множество литературных источников для облегчения выбора фармацевтически приемлемых носителей или наполнителей для дополнительного лекарственного средства. См., например, Remington's Pharmaceutical Sciences and U.S. Pharmacopeia: National Formulary, Mack Publishing Company, Easton, PA (1984); Hardman et al. (2001) Goodman and Gilman’s The Pharmacological Basis of Therapeutics, McGraw-Hill, New York, NY; Gennaro (2000) Remington: The Science and Practice of Pharmacy, Lippincott, Williams, and Wilkins, New York, NY; Avis et al. (eds.) (1993) Pharmaceutical Dosage Forms: Parenteral Medications, Marcel Dekker, NY; Lieberman, et al. (eds.) (1990) Pharmaceutical Dosage Forms: Tablets, Marcel Dekker, NY; Lieberman et al. (eds.) (1990) Pharmaceutical Dosage Forms: Disperse Systems, Marcel Dekker, NY; Weiner and Kotkoskie (2000) Excipient Toxicity and Safety, Marcel Dekker, Inc., New York, NY.
Фармацевтический состав антитела можно вводить посредством непрерывной инфузии, или в дозах с интервалами, например, одни сутки, 1-7 раз в неделю, одна неделя, две недели, три недели, один раз в месяц, один раз в два месяца и т.д. Предпочтительный способ дозирования представляет собой способ, включающий максимальную дозу или частоту дозирования, исключающую значительные нежелательные побочные эффекты. Общая еженедельная доза, как правило, составляет по меньшей мере 0,05 мкг/кг, 0,2 мкг/кг, 0,5 мкг/кг, 1 мкг/кг, 10 мкг/кг, 100 мкг/кг, 0,2 мг/кг, 1,0 мг/кг, 2,0 мг/кг, 10 мг/кг, 25 мг/кг, 50 мг/кг массы тела или более. См., например, Yang et al. (2003) New Engl. J. Med. 349:427-434; Herold et al. (2002) New Engl. J. Med. 346:1692-1698; Liu et al. (1999) J. Neurol. Neurosurg. Psych. 67:451-456; Portielji et al. (20003) Cancer Immunol. Immunother. 52:133-144. Желательная доза низкомолекулярного лекарственного средства, например, пептидного миметика, природного продукта или органического химического соединения, является приблизительно такой же, как для антитела или полипептида, на основании моль/кг.
Варианты осуществления по изобретению включают также один или несколько из биологических составов, описанных в настоящем описании, (i) для использования в, (ii) для использования в качестве лекарственного средства или композиции для, или (iii) для использования в получении лекарственного средства для: (a) терапии (например, организма человека); (b) медицины; (c) индукции или увеличения противоопухолевого иммунного ответа (d) уменьшения количества одного или нескольких маркеров опухолей у пациента; (e) остановки или замедления роста опухоли или злокачественной опухоли клеток крови; (f) остановки или замедления прогрессирования связанного с PD-1 заболевания или связанного с антителами против TIGIT заболевания; (g) остановки или замедления прогрессирования злокачественной опухоли; (h) стабилизации связанного с PD-1 заболевания или связанного с антителами против TIGIT заболевания; (i) ингибирования роста или выживаемости клеток опухолей; (j) уничтожения или уменьшения размера одного или нескольких злокачественных очагов или опухолей; (k) уменьшения прогрессирования, начала или тяжести связанного с PD-1 заболевания или связанного с антителами против TIGIT заболевания; (l) уменьшения тяжести или длительности клинических симптомов связанного с PD-1 или связанного с антителами против TIGIT заболевания, такого как злокачественная опухоль, (m) продления выживаемости пациента относительно ожидаемой выживаемости для сходного не подвергаемого лечению пациента, n) индукции полной или частичной ремиссии злокачественного состояния или другого связанного с PD-1 или связанного с антителами против TIGIT заболевания, o) лечения злокачественной опухоли; или p) лечения хронических инфекций.
ОБЩИЕ СПОСОБЫ
Стандартные способы молекулярной биологии описаны в Sambrook, Fritsch and Maniatis (1982 & 1989 2nd Edition, 2001 3rd Edition) Molecular Cloning, A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY; Sambrook and Russell (2001) Molecular Cloning, 3rd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY; Wu (1993) Recombinant DNA, Vol. 217, Academic Press, San Diego, CA). Стандартные способы представлены также в Ausbel, et al. (2001) Current Protocols in Molecular Biology, Vols.1-4, John Wiley and Sons, Inc. New York, NY, где описано клонирование в бактериальных клетках и мутагенез ДНК (том 1), клонирование в клетках млекопитающих и дрожжах (том 2), гликоконъюгаты и экспрессия белка (том 3), и биоинформатика (том 4).
Описаны способы очистки белка, включая иммунопреципитацию, хроматографию, электрофорез, центрифугирование и кристаллизацию (Coligan, et al. (2000) Current Protocols in Protein Science, Vol. 1, John Wiley and Sons, Inc., New York). Описаны химический анализ, химическая модификация, посттрансляционная модификация, получение слитых белков, гликозилирование белков (см., например, Coligan, et al. (2000) Current Protocols in Protein Science, Vol. 2, John Wiley and Sons, Inc., New York; Ausubel, et al. (2001) Current Protocols in Molecular Biology, Vol. 3, John Wiley and Sons, Inc., NY, NY, pp. 16,0,5-16,22,17; Sigma-Aldrich, Co. (2001) Products for Life Science Research, St. Louis, MO; pp. 45-89; Amersham Pharmacia Biotech (2001) BioDirectory, Piscataway, N.J., pp. 384-391). Описаны продукция, очистка и фрагментация поликлональных и моноклональных антител (Coligan, et al. (2001) Current Protocols in Immunology, Vol. 1, John Wiley and Sons, Inc., New York; Harlow and Lane (1999) Using Antibodies, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY; Harlow and Lane, выше). Доступны стандартные способы характеризации взаимодействий лиганд/рецептор (см., например, Coligan, et al. (2001) Current Protocols in Immunology, Vol. 4, John Wiley, Inc., New York).
Можно получать моноклональные, поликлональные и гуманизированные антитела (см., например, Sheperd and Dean (eds.) (2000) Monoclonal Antibodies, Oxford Univ. Press, New York, NY; Kontermann and Dubel (eds.) (2001) Antibody Engineering, Springer-Verlag, New York; Harlow and Lane (1988) Antibodies A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY, pp. 139-243; Carpenter, et al. (2000) J. Immunol. 165:6205; He, et al. (1998) J. Immunol. 160:1029; Tang et al. (1999) J. Biol. Chem. 274:27371-27378; Baca et al. (1997) J. Biol. Chem. 272:10678-10684; Chothia et al. (1989) Nature 342:877-883; Foote and Winter (1992) J. Mol. Biol. 224:487-499; Патент США No. 6329511).
Альтернативой гуманизации является использование библиотек человеческих антител, экспонированных на фагах, или библиотек человеческих антител в трансгенных мышах (Vaughan et al. (1996) Nature Biotechnol. 14:309-314; Barbas (1995) Nature Medicine 1:837-839; Mendez et al. (1997) Nature Genetics 15:146-156; Hoogenboom and Chames (2000) Immunol. Today 21:371-377; Barbas et al. (2001) Phage Display: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, New York; Kay et al. (1996) Phage Display of Peptides and Proteins: A Laboratory Manual, Academic Press, San Diego, CA; de Bruin et al. (1999) Nature Biotechnol. 17:397-399).
Очистка антигена не является необходимой для получения антител. Животных можно иммунизировать клетками, несущими представляющий интерес антиген. Затем можно выделять спленоциты от иммунизированных животных, и спленоциты можно сливать с линией клеток миеломы для получения гибридомы (см., например, Meyaard et al. (1997) Immunity 7:283-290; Wright et al. (2000) Immunity 13:233-242; Preston et al., выше; Kaithamana et al. (1999) J. Immunol. 163:5157-5164).
Антитела можно конъюгировать, например, с небольшими молекулами лекарственного средства, ферментами, липосомами, полиэтиленгликолем (PEG). Антитела являются полезными для терапии, диагностики, наборов или других целей, и включают антитела, присоединенные, например, к красителям, радиоактивным изотопам, ферментам или металлам, например, коллоидному золоту (см., например, Le Doussal et al. (1991) J. Immunol. 146:169-175; Gibellini et al. (1998) J. Immunol. 160:3891-3898; Hsing and Bishop (1999) J. Immunol. 162:2804-2811; Everts et al. (2002) J. Immunol. 168:883-889).
Доступны способы проточной цитометрии, включая активированную флуоресценцией сортировку клеток (FACS) (см., например, Owens, et al. (1994) Flow Cytometry Principles for Clinical Laboratory Practice, John Wiley and Sons, Hoboken, NJ; Givan (2001) Flow Cytometry, 2nd ed.; Wiley-Liss, Hoboken, NJ; Shapiro (2003) Practical Flow Cytometry, John Wiley and Sons, Hoboken, NJ). Доступны флуоресцентные реагенты, пригодные для модификации нуклеиновых кислот, включая праймеры и зонды на основе нуклеиновой кислоты, полипептиды и антитела, для использования, например, в качестве диагностических реагентов (Molecular Probesy (2003) Catalogue, Molecular Probes, Inc., Eugene, OR; Sigma-Aldrich (2003) Catalogue, St. Louis, MO).
Описаны стандартные способы гистологии иммунной системы (см., например, Muller-Harmelink (ed.) (1986) Human Thymus: Histopathology and Pathology, Springer Verlag, New York, NY; Hiatt, et al. (2000) Color Atlas of Histology, Lippincott, Williams, and Wilkins, Phila, PA; Louis, et al. (2002) Basic Histology: Text and Atlas, McGraw-Hill, New York, NY).
Доступны пакеты программного обеспечения и базы данных для определения, например, антигенных фрагментов, лидерных последовательностей, сворачивания белка, функциональных доменов, участков гликозилирования, и для выравнивания последовательностей (см., например, GenBank, Vector NTI® Suite (Informax, Inc, Bethesda, MD); GCG Wisconsin Package (Accelrys, Inc., San Diego, CA); DeCypher® (TimeLogic Corp., Crystal Bay, Nevada); Menne, et al. (2000) Bioinformatics 16: 741-742; Menne, et al. (2000) Bioinformatics Applications Note 16:741-742; Wren, et al. (2002) Comput. Methods Programs Biomed. 68:177-181; von Heijne (1983) Eur. J. Biochem. 133:17-21; von Heijne (1986) Nucleic Acids Res. 14:4683-4690).
Аналитические способы
Аналитические способы, пригодные для оценки стабильности продукта, включают эксклюзионную хроматографию (SEC), тест динамического светорассеяния (DLS), дифференциальную сканирующую калориметрию (DSC), количественное определение изо-asp, анализ активности, анализ УФ при 340 нм, УФ-спектроскопию и FTIR. SEC (J. Pharm. Scien., 83:1645-1650, (1994); Pharm. Res., 11:485 (1994); J. Pharm. Bio. Anal., 15:1928 (1997); J. Pharm. Bio. Anal., 14:1133-1140 (1986)) измеряет процент мономера в продукте и дает информацию о количестве растворимых агрегатов. DSC (Pharm. Res., 15:200 (1998); Pharm. Res., 9:109 (1982)) дает информацию о температуре денатурации белка и температуре стеклования. DLS (American Lab., November (1991)) измеряет средний коэффициент диффузии и дает информацию о количестве растворимых и нерастворимых агрегатов. Анализ УФ при 340 нм измеряет интенсивность рассеянного света при 340 нм и дает информацию о приблизительных количествах растворимых и нерастворимых агрегатов. УФ-спектроскопия измеряет оптическую плотность при 278 нм и дает информацию о концентрации белка. FTIR (Eur. J. Pharm. Biopharm., 45:231 (1998); Pharm. Res., 12:1250 (1995); J. Pharm. Scien., 85:1290 (1996); J. Pharm. Scien., 87:1069 (1998)) измеряет ИК-спектр в области амида один, и дает информацию о вторичной структуре белка.
Содержание изо-asp в образцах измеряют с использованием системы детекции изоаспартата Isoquant (Promega). В наборе используют фермент изоаспартил-метилтрансферазу белка (PIMT) для специфической детекции присутствия остатков изоаспарагиновой кислоты в белке-мишени. PIMT катализирует перенос метильной группы от S-аденозил-L-метионина к изоаспарагиновой кислоте в положении альфа-карбоксила, с получением в процессе S-аденозил-L-гомоцистеина (SAH). Это относительно небольшая молекула, и обычно ее можно выделять и количественно оценивать посредством обращеннофазовой HPLC с использованием стандартов SAH для HPLC, предоставленных в наборе.
Активность или биоидентичность антитела можно измерять по его способности связываться со своим антигеном. Специфическое связывание антитела с его антигеном можно количественно оценивать посредством любого способа, известного специалисту в данной области, например, иммуноанализа, такого как ELISA (твердофазный иммуноферментный анализ).
Содержание всех публикаций, упомянутых в настоящем описании, приведено в качестве ссылки с целью описания и раскрытия способов и материалов, которые можно использовать в сочетании с настоящим изобретением.
При наличии описания различных вариантов осуществления по изобретению в настоящем описании со ссылкой на сопутствующие чертежи, следует понимать, что изобретение не является ограниченным этими точными вариантами осуществления, и что специалист в данной области может осуществлять различные их изменения и модификации без отклонения от объема или содержания изобретения, как определено в прилагаемой формуле изобретения.
ПРИМЕРЫ
ПРИМЕР 1
Скрининг буфера состава антитела против TIGIT
Широкомасштабное исследование разработки составов проводили для трех антител против TIGIT, где каждое анти-TIGIT антитело имеет следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, для оценки (1) биофизической/биохимической лабильности; (2) условий получения предварительного состава (pH, соль и буфер) и (3) совместимости с платформой среди составов. Образцы анализировали посредством спектрофотометрии УФ/видимой областей спектра по мутности (A350) в качестве суррогата более крупных агрегатов, эксклюзионной хроматографии (UP-SEC) для детекции высокомолекулярных молекул, капиллярного изоэлектрического фокусирования (cIEF) для измерения эффекта стресса на распределение зарядов на поверхности молекулы, восстанавливающего капиллярного электрофореза с додецилсульфатом натрия (CE-SDS) для детекции протеолитического расщепления тяжелых или легких цепей, анализа не видимых невооруженным глазом частиц для детекции не видимых невооруженным глазом агрегатов.
Широкомасштабный скрининг составов включал 1 мг/мл антитела против TIGIT, составленного в выборке трех видов буферов: Ацетатный буфер с значениями pH в диапазоне от 5,0 до 6,2, цитратный буфер с значениями pH в диапазоне от 5,6 до 6,8 и L-гистидиновый буфер с значениями pH в диапазоне от 5,0 до 6,8. Таким образом, проверяли значения pH в диапазоне от 5,0 до 6,8 и ионнную силу 0-150 мМ NaCl. Образцы подвергали стрессу при 50°C в течение 10 суток и анализировали по термостабильности с использованием дифференциальной сканирующей флуориметрии (DSF), коллоидной стабильности с использованием эксклюзионной хроматографии (UP-SEC), предрасположенности к агрегации с использованием Guava (анализ характеризации не видимых невооруженным глазом частиц на основе проточной цитометрии), мутности (измерения A350), профилю вариантов заряда (cIEF) и профилю фрагментации с использованием Caliper.
На основании результатов, полученных в исследовании, состав, обеспечивающий максимальную стабильность белка, представлял собой 10 мМ L-гистидин в диапазоне pH от 5,6 до 6,2. Для 10 мМ L-гистидина в диапазоне pH от 5,6 до 6,2 показана минимальная агрегация, мониторируемая по UP-SEC, с ΔSEC главного пика в диапазоне между -1,63 и -1,85% (по сравнению с SEC главного пика в диапазоне от -2,0 до -5,0% в условиях другого буфера и pH) (данные не представлены). Профиль cIEF показал, что отмечено уменьшение относительной площади пика для главного пика и основных молекул, и увеличение относительной площади пика кислых вариантов для образцов через 10 суток при 50°C (cIEF главного пика в диапазоне между -9,0 и -11,3%) (данные не представлены). Уменьшение количества основных вариантов и увеличение количества кислых вариантов при воздействии повышенной температуры является общераспространенным для mAb. Добавление соли уменьшало стабильность белка среди исследованных композиций.
ПРИМЕР 2
Исследование диапазона pH для состава антитела против TIGIT
В этом исследовании, анти-TIGIT антитело, имеющее следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, тестировали в концентрации 50 мг/мл в 10 мМ L-гистидиновом буфере. 7% (масс./об.) сахарозы добавляли в состав для увеличения объемной стабильности (в качестве стабилизатора и неионного модификатора тоничности) молекулы. Анти-TIGIT антитело составляли в 10 мМ L-гистидиновом буфере, 7% сахарозе при pH 5,5, pH 6,0 и pH 6,5. Стабильность таких составов оценивали следующим образом:
(1) Стабильность молекулы мониторировали по термостабильности и стабильности при хранении в условиях ускоренного старения (5°C, 25°C и 40°C в течение вплоть до 6 месяцев), с защитой от света.
(2) Проводили также исследования стабильности для стресса при замораживании-размораживании и стресса при встряхивании.
(3) Исследование встряхивания проводили в составах, содержащих различные концентрации полисорбата 80 (PS-80) для оценки концентрации PS-80 в составе.
(4) Исследование светового стресса проводили для оценки необходимости L-метионина в составах.
Материалы и способы
Исследование термостабильности (3 месяца)
50 мг/мл антитела против TIGIT составляли в 10 мМ L-гистидиновом буфере, 7% сахарозе, 0,2 мг/мл полисорбате 80 при pH 5,5, pH 6,0 или pH 6,5. Полученные составы стерилизовали фильтрацией и заполняли ими флаконы 2R, закрытые хлорбутиловыми пробками и защищенные алюминиевыми герметизирующими ободками. Проводили ступенчатое исследование стабильности при 5°C (влажность окружающего воздуха), 25°C (60% относительная влажность) и 40°C/ (75% относительная влажность). Образцы анализировали с использованием UP-SEC, HP-IEX, cIEF (избранные образцы), MFI, CE-SDS (невосстанавливающего «NR» и восстанавливающего «R»), восстанавливающего пептидного картирования (MFI и восстанавливающее пептидное картирование проводили в избранных временных точках).
1-месячное исследование термостабильности разрабатывали для 25 мг/мл антитела против TIGIT, составленного в 10 мМ L-гистидиновом буфере, 7% сахарозе, 0,2 мг/мл PS-80, pH 6,0. Полученные составы стерилизовали фильтрацией и заполняли ими флаконы 2R, закрытые хлорбутиловыми пробками и защищенные алюминиевыми герметизирующими ободками. Проводили ступенчатое исследование стабильности при 5°C (влажность окружающего воздуха), 25°C (60% относительная влажность) и 40°C/ (75% относительная влажность) в течение одного месяца. Образцы анализировали с использованием UP-SEC, cIEF и CE-SDS (NR и R).
Исследование стабильности при встряхивании
50 мг/мл антитела против TIGIT составляли в 10 мМ L-гистидиновом буфере, 7% сахарозе, pH 6,0 с различными концентрациями полисорбата 80 (0, 0,1, и 0,2 мг/мл). Полученные составы стерилизовали фильтрацией и заполняли ими флаконы 2R (объем заполнения 1,2 мл), закрытые хлорбутиловыми пробками и защищенные алюминиевыми герметизирующими ободками. Образцы подвергали встряхиванию в горизонтальном положении при 300 об./мин в течение вплоть до 7 суток при 18-22°C. The образцы анализировали с использованием UP-SEC, MFI, CE-SDS (NR и R).
Стабильность при замораживании-размораживании
50 мг/мл анти-TIGIT антитело составляли в 10 мМ L-гистидиновом буфере, 7% сахарозе, 0,2 мг/мл полисорбате 80, pH 6,0. Полученные составы стерилизовали фильтрацией и заполняли ими флаконы 2R, закрытые хлорбутиловыми пробками и защищенные алюминиевыми герметизирующими ободками. Образцы подвергали 5 циклам замораживания-размораживания от -80°C до 18-22°C (по меньшей мере 24 часов в условиях замораживания и при комнатной температуре до полного размораживания). Образцы анализировали с использованием UP-SEC, MFI, CE-SDS (NR и R).
Исследование стабильности при световом стрессе
Ранние исследования разработки показали присутствие экспонированного остатка триптофана, так же как нескольких остатков метионина, подверженных окислению при световом стрессе. Исследования разрабатывали в условиях светового стресса ICH при видимом свете (CWF, 0,1x ICH, 0,2x ICH, 0,5x ICH, 1x ICH) в составах в присутствии и в отсутствие L-метионина (состав 1: 10 мМ L-гистидинового буфера, 7% сахарозы, 0,2 мг/мл полисорбата 80, pH 6,0, и состав 2: 10 мМ L-гистидинового буфера, 10 мМ L-метионина, 7% сахарозы, 0,2 мг/мл полисорбата 80, pH 6,0). Образцы анализировали с использованием UP-SEC, cIEF, CE-SDS (NR и R) и восстанавливающего пептидного картирования.
Результаты
Результаты для термостабильности
Состав при 50 мг/мл: Для всех тестированных показывающих стабильность анализов, значительных изменений не наблюдали при 5°C при всех значениях pH через 3 месяца (данные не представлены). При 25°C и 40°C, pH 5,5 и pH 6,0 показана сходная стабильность, и эти условия приводили к большей стабильности, чем pH 6,5 (данные не представлены). Скорости деградации при pH 6,5 для анализов UP-SEC, CE-SDS (NR) и cIEF при 25°C и 40°C были относительно более высокими, чем наблюдали при pH 5,5 и pH 6,0, а также по сравнению со сравнительной молекулой. Таким образом, диапазон pH от 5,5 до 6,0 (pI 8,7) сочли приемлемым. Окисления, дезамидирования или изомеризации не наблюдали для антитела против TIGIT через 3 месяца при всех температурах и значениях pH.
Состав при 25 мг/мл: Деградацию наблюдали при 25° C и 40° C для всех тестируемых анализов. Обнаружено, что скорости деградации являлись сходными со скоростями в условиях 50 мг/мл (см. выше).
Исследование стабильности при встряхивании
Для составов, не содержащих полисорбат 80, показаны видимые частицы к концу 7 суток. Анализ не видимых невооруженным глазом частиц показал, что количество частиц 10 мкм или более было значительно уменьшено в составе, содержащем полисорбат 80 в концентрации 0,2 мг/мл. Значительных различий между образцами не наблюдали с использованием других анализов.
Стабильность при замораживании-размораживании
Не наблюдали изменений стабильности молекулы после 5 циклов замораживания-размораживания во всех тестированных анализах.
Исследование стабильности при световом стрессе
Деградацию наблюдали, когда образцы обоих составов подвергали воздействию светового стресса при 0,5x ICH или выше, при тестировании посредством UP-SEC, cIEF, CE-SDS (NR и R). При установке условий ниже 0,5x ICH, не показано значительной деградации для обоих составов. Данные восстанавливающего пептидного картирования в условиях светового стресса при 0,5x и выше показали окисление остатков триптофана и метионина. 10 мМ L-метионина в составе уменьшал уровни окисления остатков метионина, но не влиял на уровни окисления триптофана.
Заключение
На основании вышеизложенного, 10 мМ L-гистидинового буфера, 10 мМ L-метионина, 7% сахарозы, 0,2 мг/мл полисорбата 80, pH 5,5-6,0, сочли адекватными для придания стабильности для поддержания хранения в условиях холодильника.
ПРИМЕР 3
Дополнительные исследования pH
Анти-TIGIT антитело, имеющее следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, и на остове IgG1, составляли в шести 10 мМ гистидиновых буферах с различным pH (в диапазоне от 5,0 до 6,5). Термостабильность в различных составах исследовали при 2~8°C, 25°C и 40°C в течение 8 недель.
Гистидиновые буферы различного pH (5,0~6,5) получали посредством титрования 10 мМ L-гистидинового буфера до буфера 10 мМ L-гистидин-HCl. Буфер для антитела против TIGIT меняли на шесть различных гистидиновых буферов с различными pH посредством четырех - пяти циклов ультрафильтрации с использованием устройства для центрифугирования в условиях 4°C и 4500 об./мин~5000 об./мин (105~260 мин в каждом цикле). После замены буфера, определенное количество сахарозы и раствора для хранения полисорбата 80 (1%, масс./масс.) добавляли в растворы с различным pH для достижения целевого количества, и подходящее количество соответствующего гистидинового буфера добавляли таким образом, чтобы довести концентрацию антитела до приблизительно 50 мг/мл.
Затем составы подвергали асептической фильтрации с использованием 0,22-мкм мембранного фильтра. По 3 мл каждого образца асептически заполняли 6-мл стеклянные флаконы для исследования термостабильности в течение T0, 4 недель (4Н) и 8 недель (8Н). По 1 мл каждого образца асептически заполняли 6-мл стеклянные флаконы для исследования термостабильности в течение двух недель (2Н) исследование термостабильности. Заполненные флаконы закрывали пробками и герметично обжимали немедленно после заполнения. Все вышеуказанные стадии проводили в ламинарном шкафу биологической защиты. Эти флаконы помещали в закрытые коробки и хранили в условиях различной температуры для исследования термостабильности.
Результаты и обсуждение
Внешний вид всех образцов оставался таким же в течение четырех недель во всех условиях.
Однако, через 8 недель, для образцов при 2~8°C и 25°C показано небольшое желтоватое окрашивание, и для образцов при 40°C показано более глубокое желтоватое окрашивание. Все образцы являлись немного опалесцирующими и свободными от видимых частиц на протяжении периода исследования. Значительного измерения концентрации белка во всех образцах не наблюдали на протяжении исследования.
Коллоидную стабильность образцов оценивали по чистоте посредством эксклюзионной хроматографии (SEC), в которой определяли процент мономера, так же как проценты высокомолекулярных молекул (HMW) и пики поздней элюции (LMW молекулы). Анализ проводили с использованием системы Agilent 1260 Infinity с колонкой для эксклюзионной хроматографии TSKGel G3000SWXL (300 × 7,8 мм, 5 мкм). Подвижная фаза представляла собой 50 мМ PB, 300 мМ NaCl, pH 7,0±0,2, и скорость потока устанавливали на 1,0 мл/мин. Образцы разводили до 10 мг/мл для инъекции и детектировали при 280 нм с использованием детектора УФ.
Данные UPSEC указаны в таблице ниже:
Как показано в таблице выше, % главного пика по SEC являлся стабильным при 2~8°C во всех образцах, однако, при 25°C и 40°C, наблюдали значительное уменьшение % главного пика. Скорость уменьшения % главного пика была выше в образцах при 40°C, чем при 25°C. При 40°C в течение восьми недель, % HMW был больше в образцах при pH 6,2 и 6,5, в то время как % LMW был больше в образцах при pH 5,0 и 5,3.
Для оценки химической стабильности составов, капиллярное изоэлектрическое фокусирование (cIEF) проводили для оценки химической стабильности и для мониторирования изменения профиля варианта заряда с течением времени. Кратко, 20 мкл (2,0 мг/мл) эталонного стандарта или образца смешивали с 0,5 мкл маркера с pI 5,85, 0,5 мкл маркера с pI 9,77, 1 мкл фармалита 3-10, 0,5 мкл фармалита 5-8, 0,5 мкл фармалита 8-10,5, 35 мкл 1% метилцеллюлозы, 37,5 мкл 8 M мочевины. Очищенную воду добавляли для доведения конечного объема до 100 мкл. Затем смесь анализировали с использованием анализатора для капиллярного изоэлектрического фокусирования iCE-3, оборудованного покрытым фторуглеродом детектором по всей длине капилляра. Фокусирование проводили в две стадии: (1) 1,5 кВ в течение 1 мин и (2) 3 кВ в течение 8 мин. На протяжении эксперимента, штатив автодозатора поддерживали при 5°C.
Данные cIEF для оценки уровней кислых вариантов, % главного пика и % основных вариантов приведены в таблице ниже.
Как видно в таблице выше, при 2~8°C, % главного пика, % кислого пика и % основного пика по cIEF являлись относительно стабильными и сравнимыми во всех образцах.
При 2~8°C, % основного пика по cIEF также увеличивался; увеличение в образцах при pH буфера 5,0 и 5,3 было выше, чем в других образцах. При 25°C, % главного пика, % кислого пика и % основного пика являлись стабильными в течение первых двух недель, но немного изменялись через четыре недели, где % главного пика уменьшался, в то время как % кислого пика увеличивался соответственно). Скорость изменения в различных составах являлась сравнимой. При 40°C, значительное уменьшение % главного пика и заметное увеличение % кислого пика обнаружено во всех составах даже через две недели, однако, степень изменения являлась сходной в каждом составе. % основного пика также увеличивался; увеличение в образцах в буфере pH 5,0 и 5,3 было больше, чем в других образцах.
Для оценки чистоты составов, проводили невосстанавливающий анализ Caliper. Кратко, закупленный буфер для образцов смешивали с раствором 10% додецилсульфата натрия (SDS) в соотношении объемов 20 к 1, и 100 мМ раствора N-этилмалеинимида добавляли в смешанный раствор в соотношении объемов 0,7 к 20 (относительно раствора для денатурации образцов). Стандарт или образец сначала разводили до 1 мг/мл, и 2 мкл разведенного стандарта или образца смешивали с 7 мкл раствора для денатурации образцов. Смесь инкубировали при 70°C в течение 10 мин. 35 мкл очищенной воды добавляли к инкубируемому раствору, и 42 мкл смешанного раствора переносили в 96-луночный планшет для анализа. Планшет с образцами анализировали с помощью LabChip GX II HT, с использованием анализа HT Antibody Analysis 200.
Данные невосстанавливающего анализа Caliper для оценки % чистоты показаны в таблице ниже:
Как показано в таблице выше - при 2~8°C в течение восьми недель, чистота по невосстанавливающему Caliper каждого состава являлась относительно стабильной. При 25°C в течение восьми недель, чистота каждого состава немного уменьшалась. При 40°C, чистота уменьшалась значительно, особенно, когда образцы находились в буфере pH 5,0 и 5,3, уменьшение было намного более быстрым, чем для других. Размер молекул являлся стабильным на протяжении исследования (данные не представлены).
Для дополнительной оценки чистоты составов, проводили также восстанавливающий анализ Caliper. Кратко, закупленный буфер для образцов смешивали с раствором 10% SDS в соотношении объемов 20 к 1, и раствор 1M дитиотреитола добавляли в смешанный раствор в соотношении объемов 0,7 к 20 (относительно раствора для денатурации образцов). Стандарт или образец сначала разводили до 1 мг/мл, и 2 мкл разведенного стандарта или образца смешивали с 7 мкл раствора для денатурации образцов. Смесь инкубировали при 70°C в течение 10 мин. 35 мкл очищенной воды добавляли к инкубируемому раствору, и 42 мкл смешанного раствора переносили в 96-луночный планшет для анализа. Планшет с образцами анализировали с помощью LabChip GX II HT, с использованием анализа HT Antibody Analysis 200.
Данные восстанавливающего анализа Caliper для оценки % чистоты показаны в таблице ниже:
Как видно выше, при 2~8°C и 25°C в течение восьми недель, чистота по восстанавливающему Caliper каждого состава являлась относительно стабильной. При 40°C, явное уменьшение чистоты по Caliper_восст. обнаружено во всех составах. Чистота образцов в буфере pH 5,0 уменьшалась наиболее сильно, за этим следовали образцы в буфере pH 5,3. Скорость уменьшения в буферах pH 5,6, 5,9 и 6,2 являлась сравнимой, но более низкой. Чистота образцов в буфере pH 6,5 уменьшалась наиболее медленно. Уменьшение чистоты, вероятно, было обусловлено уменьшением % тяжелой цепи (HC), в то время как % легкой цепи (LC) являлся стабильным в исследовании. Размер легкой цепи и тяжелой цепи антитела являлся стабильным во всех образцах в течение 8Н.
ПРИМЕР 4
Состав антитела против TIGIT без метионина
Анти-TIGIT антитело, имеющее следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, тестировали в концентрации 50 мг/мл в 10 мМ L-гистидиновом буфере, 7% сахарозе, 0,2 мг/мл PS-80 с pH в диапазоне от 5,0 до 6,5. Стабильность молекулы мониторировали по термостабильности и стабильности при хранении в условиях ускоренного старения, с защитой от света. В дополнение к термостабильности, проводили также исследования стабильности при замораживании-размораживании, стабильности при встряхивании, стабильности при световом стрессе. Тестирование стабильности включало UP-SEC, cIEF, CE-SDS, MFI и восстанавливающее пептидное картирование.
Результаты
Исследование термостабильности (8 недель)
Для всех тестированных показывающих стабильность анализов, анти-TIGIT антитело являлось стабильным при 5°C для всех тестированных лабильностей. Скорости деградации, как наблюдали с использованием UP-SEC, Caliper CE-SDS, cIEF, MFI, были выше при 40°C, чем при 25°C. При 25°C и 40°C, отмечены следующие результаты:
UP-SEC: Уменьшение % мономера наблюдали для всех значений pH от 5,0 до 6,5. При более низких значениях pH (5,0 и 5,3), уменьшение главного пика было в первую очередь обусловлено увеличением % низкомолекулярных (LMW) молекул, в то время как уменьшение % мономера при pH 6,5 было главным образом обусловлено % высокомолекулярных (HMW) молекул. Уменьшение % мономера было наивысшим при pH 6,5 через 8 недель анализа стабильности в условиях ускоренного старения. (данные не представлены)
cIEF: Уменьшение главного пика cIEF наблюдали для всех значений pH от 5,0 до 6,5 при 25°C и 40°C. При более высоких значениях pH (6,3-6,5), уменьшение главного пика было главным образом обусловлено увеличением содержания кислых вариантов, в то время как при pH 5,0 и 5,3, уменьшение главного пика было обусловлено увеличением содержания как кислых, так и основных вариантов. (данные не представлены)
CE-SDS (Caliper): При невосстанавливающем CE-SDS уменьшение главного пика главным образом наблюдали при 40°C, из-за присутствия фрагментированных молекул. Для составов при более низких значениях pH (5,0 и 5,3) показана относительно более высокая скорость фрагментации, чем для остальных значений pH.
Восстанавливающий анализ CE-SDS (Caliper) выявил, что при 5°C и 25°C в течение восьми недель, чистота каждого состава являлась относительно стабильной. При 40°C, явное уменьшение чистоты обнаружено во всех составах. Чистота образцов в буфере pH 5,0 уменьшалась наиболее сильно, за этим следовали образцы в буфере pH 5,3.
MFI: Увеличение содержания не видимых невооруженным глазом частиц наблюдали для всех составов при 40°C. При pH 6,3 и 6,5 присутствовало наивысшее увеличение содержания не видимых невооруженным глазом частиц, относительно остальных буферов.
Восстанавливающее пептидное картирование: Среди идентифицированных лабильностей, только для M254 показано относительное увеличение окисления через 8 недель при 40°C, по сравнению с исходными образцами.
Заключение: 10 мМ L-гистидинового буфера, 7% сахарозы, 0,2 мг/мл PS-80, pH 5,6-6,3 адекватно поддерживали стабильность при хранении антитела против TIGIT в течение 8 недель.
Исследование стабильности при встряхивании
Не наблюдали изменений содержания растворимых агрегатов, заряженных вариантов, фрагментации или не видимых невооруженным глазом частиц, когда состав 50 мг/мл антитела против TIGIT (в 10 мМ L-гистидиновом буфере, 7% сахарозе, pH 5,8 и любом из 0, 0,1, 0,2 и 0,3 мг/мл PS-80) подвергали умеренному встряхиванию в течение вплоть до 7 суток при 100 об./мин при 18-22°C.
Стабильность при замораживании-размораживании
Не наблюдали изменений содержания растворимых агрегатов, заряженных вариантов, фрагментации или не видимых невооруженным глазом частиц, когда 50 мг/мл антитела против TIGIT (в 10 мМ L-гистидиновом буфере, 7% сахарозе, 0,2 мг/мл PS-80, pH 5,8) подвергали 5 циклам замораживания/размораживания (замораживания при -80°C в течение 2 часов и размораживания при комнатной температуре в течение 1 часа).
Исследование стабильности при световом стрессе
Состав при 50 мг/мл подвергали в течение 48 часов стрессу под воздействием видимого света (5000 люкс). В этих условиях, присутствовало минимальное изменение содержания растворимых агрегатов, заряженных вариантов, не видимых невооруженным глазом частиц, pH, концентрации, фрагментации и окисления в условиях ~0,2x ICH (воздействие света 12 час). В условиях ~1x (воздействие света 48 час), присутствовало увеличение содержания растворимых агрегатов, кислых вариантов, фрагментации, не видимых невооруженным глазом частиц и окисления метионина.
Заключение
На основании этих исследований, 10 мМ L-гистидинового буфера, 7% сахарозы, 0,2 мг/мл PS-80 pH 5,3-6,3 являлись способными поддерживать стабильность антитела против TIGIT. Окисление метионина наблюдали при воздействии сильного светового стресса. Как отмечено в примере 2, добавление 10 мМ L-метионинаа уменьшает окисление остатков метионина.
ПРИМЕР 5
Скрининг полисорбата 80
Для антитела против TIGIT, имеющего следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, получали четыре (4) состава при pH 5,8, в 10 мМ L-гистидиновом буфере, и с различными концентрациями PS-80 (как показано ниже). Стабильность белка в различных составах исследовали в условиях присутствия или отсутствия встряхивания в течение периода 7 суток при 20°C.
Составы получали в 10 мМ L-гистидиновом буфере при pH 5,8 с использованием системы замены буфера TFF в лабораторном масштабе. Белки, составленные с различным содержанием полисорбата 80, затем подвергали асептической фильтрации с использованием 0,22-мкм мембранного фильтра. По 2 мл каждого образец асептически заполняли 6-мл стеклянные флаконы. Заполненные флаконы закрывали пробками и обжимали немедленно после заполнения. Образцы разделяли на группу встряхивания и группу без встряхивания. В группе встряхивания, эти флаконы переносили в закрытые коробки и затем помещали в термостатируемый встряхиватель, и встряхивали при 100 об./мин, 20°C в течение вплоть до 7 суток. В группе без встряхивания, эти флаконы переносили в закрытые коробки и помещали в термостатируемый встряхиватель, но встряхиватель не включали при 20°C в течение вплоть до 7 суток.
Стабильность антитела в различных составах в присутствии или в отсутствие встряхивания исследовали через 3 и 7 суток.
Данные UPSEC для оценки уровней высокомолекулярных молекул (HMW или агрегатов), % мономера и LMW (низкомолекулярных молекул) представлены в таблице ниже:
Как можно видеть, содержание полисорбата 80 не оказывало значительного влияния на чистоту по SEC в условиях присутствия или отсутствия встряхивания. Содержание полисорбата 80 не оказывало значительного влияния на pI, процент главного пика, кислого пика и основного пика в анализе cIEF, в условиях присутствия или отсутствия встряхивания, вплоть до 7 суток.
Содержание полисорбата 80 не оказывало значительного влияния на чистоту по невосстанавливающему Caliper, в присутствии или в отсутствие встряхивания, вплоть до 7 суток, как показано в таблице ниже.
Проводили также восстанавливающий анализ Caliper. Содержание PS-80 не оказывало значительного влияния на чистоту по восстанавливающему Caliper, в присутствии или в отсутствие встряхивания, в течение 7 суток.
Для измерения содержания не видимых невооруженным глазом частиц, приблизительно по 1500 мкл каждого образца отбирали из контейнера - стеклянного флакона и тестировали посредством микропроточной визуализации (MFI), в соответствии с руководством для пользователя. Зарегистрированы концентрации частиц в различных диапазонах размера, включая 1~2 мкм, 2~5 мкм, 5~10 мкм, 10~25 мкм и >25 мкм (см. ниже). Содержание полисорбата 80 не оказывало значительного влияния на концентрацию частиц в присутствии или в отсутствие встряхивания вплоть до 7 суток.
ПРИМЕР 6
Добавление хелатирующего агента
В этом исследовании сравнивали стабильность антитела против TIGIT, имеющего следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, в 10 мМ L-гистидиновом буфере (pH=5,8), 0,02% (масс./об.) полисорбате 80, 10 мМ L-метионинае («L-Met»), 7% масс./об. сахарозе в присутствии или в отсутствие 20 мкМ или 50 мкМ ДТПА.
Тремя составами заполняли флаконы и проводили ступенчатое исследование стабильности при 5°C (влажность окружающего воздуха), 25°C (60% относительная влажность), и 40°C (75% относительная влажность) в течение восемнадцати недель с защитой от света.
Коллоидную стабильность образцов оценивали по чистоте посредством эксклюзионной хроматографии (SEC), в которой определяли процент мономера, так же как проценты высокомолекулярных молекул (HMW) и пики поздней элюции (LMW молекулы). Данные UPSEC для оценки уровней % HMW (агрегатов), % мономера и %LMW представлены в таблице ниже:
Как показано в таблице выше, при 5°C, 25°C и 40°C, для всех трех составов показана тенденция к увеличению % пика HMW и % пика LMW (и, следовательно, уменьшению % пика мономера), вплоть до временной точки 18 недель. При 25°C, для обоих составов показаны сходные тенденции, но меньшие изменения, по сравнению с 40°C. При 5°C, не наблюдали существенных изменений. Для состава 1 показано большее увеличение % HMW и % LMW по сравнению с составом 2 (20 мкМ ДТПА) и составом 3 (50 мкМ ДТПА). Кроме того, для состава 1 показано большее уменьшение % мономера по сравнению с составами 2 и 3. Сходные результаты наблюдали в анализе HP-IEX (данные не представлены).
Для оценки того, может ли ДТПА защищать составы от окислительного стресса, тремя составами заполняли флаконы и подвергали воздействию света (0,5X ICH и 1X ICH). Как видно в таблице ниже, для состава 1 показано большее увеличение % окисления M254, M430 и W104 (остатков метионина и триптофана, чувствительных к окислению), по сравнению с составом 2 (20 мкМ ДТПА) и составом 3 (мкМ ДТПА). Таким образом, ДТПА может дополнительно улучшать стабильность состава антитела против TIGIT.
ПРИМЕР 7
Долгосрочная стабильность составов антитела против TIGIT
В этом примере описаны данные долгосрочной стабильности для антитела против TIGIT, составленного в L-гистидиновом буфере, L-метионине, сахарозе, полисорбате 80 и воде для инъекции, следующим образом:
Составами заполняли стеклянные флаконы USP типа 1 с эластомерной пробкой и алюминиевым герметизирующим ободком. Затем флаконы инкубировали в трех различных условиях хранения: 5°C (влажность окружающего воздуха), 25°C (60% относительная влажность), и 40°C (75% относительная влажность). Данные собирали на время ноль, 1 месяц, 3 месяца, 6 месяцев для всех условий хранения, 9 месяцев (для условий хранения при 5°C и 25°C), 12 месяцев (для условий хранения при 5°C и 25°C), 18 месяцев (для условий хранения при 5°C), 24 месяца (для условий хранения при 5°C) и 36 месяцев (для условий хранения при 5°C).
Результаты
Результаты показывают общую физическую и химическую стабильность антитела против TIGIT при хранении в рекомендованных условиях долгосрочного хранения при 5°C в течение 18 месяцев. Не наблюдали поддающейся измерению потери активности, и чистота соответствовала спецификациям в рекомендованных условиях хранения. Результаты показаны в следующих таблицах:
* значение составляет 98,2
Концентрация белка
Для данных стабильности концентрации белка для всех временных точек и условий не показано каких-либо значительных изменений как функции от времени или условий хранения, и все результаты находились в пределах критериев приемлемости 45-55 мг/мл.
pH
Не присутствовало значительных изменений pH для условий 5 C, 25 C, и 40 C. На Фигуре 1 показаны данные pH для временных точек от 0 до 9 месяцев.
Полисорбат 80
Содержание полисорбата 80 в рекомендованных условиях хранения 5°C немного уменьшалось до 0,13 мг/мл через 9 месяцев и 18 месяцев (данные для 18 месяцев не представлены). Тенденцию уменьшения содержания полисорбата 80 наблюдали при 25°C (в условиях ускоренного старения) и 40°C (в условиях стресса). При 40°C концентрация полисорбата 80 уменьшалась до 0,06 мг/мл через 6 месяцев, и при 25°C содержание полисорбата 80 уменьшалось до 0,07 мг/мл через 9 месяцев. Данные концентрации полисорбата 80 в течение вплоть до 9 месяцев указаны на фигуре 2.
Активность связывания по ELISA
Не присутствовало явной тенденции в какой-либо временной точки или в каких-либо условиях для полученных результатов ELISA. Данные активности в течение вплоть до 9 месяцев указаны на фигуре 3.
Чистота по UP-SEC
Данные чистоты по UP-SEC проиллюстрированы ниже на фигуре 4 для % мономера, на фигуре 5 для % высокомолекулярных молекул, и на фигуре 6 для % низкомолекулярных молекул, вплоть до 9 месяцев.
В рекомендованных условиях хранения при 5°C, присутствует небольшое уменьшение % мономера с соответствующим небольшим увеличением % высокомолекулярных молекул в течение 18 месяцев исследования стабильности. % низкомолекулярных молекул от исходной точки до 18 месяцев находится ниже предела количественного определения (< QL), который равен 0,4%. В условиях 25°C, % мономера уменьшался от исходной точки до 12 месяцев с соответствующим увеличением % высокомолекулярных молекул. Через 9 и 12 месяцев, зарегистрированы % низкомолекулярных молекул выше QL.
В условиях стресса при 40°C, % мономера уменьшался от 98,7% до 93,8% с соответствующим увеличением содержания высокомолекулярных молекул от 1,33% до 2,63% и низкомолекулярных молекул от <QL до 3,53%. Этот результат не являлся неожиданным, с учетом характера условий хранения.
Восстанавливающий и невосстанавливающий CD-SDS
На фигурах 7 и 8 показаны данные чистоты вплоть до 9 месяцев, как определено посредством восстанавливающего и невосстанавливающего CD-SDS. Не присутствовало заметных тенденций в восстанавливающем (% тяжелой и легкой цепи) или невосстанавливающем (% интактного IgG) CE-SDS в условиях долгосрочного хранения при 5°C, и результаты находились в пределах критериев приемлемости GMP продукта лекарственного средства ≥ 90,0%. В условиях ускоренного старения при 25°C, тенденцию к уменьшению наблюдали для невосстанавливающих условий. Для CE-SDS в восстанавливающих условиях, также наблюдали тенденцию к уменьшению. Как для восстанавливающего, так и для невосстанавливающего CE-SDS, все результаты, вплоть до временной точки 9 месяцев, находились в пределах критериев приемлемости GMP. В условиях стресса при 40°C, через 6 месяцев, результаты как восстанавливающего, так и невосстанавливающего CD-SDS были ниже критериев приемлемости ≥ 90,0%, установленных GMP для продукта лекарственного средства. Результат невосстанавливающего CE-SDS выпадал из спецификации через 3 месяца с результатом 88,9%, и затем далее уменьшался через 6 месяцев до 79,6%. Для восстанавливающего CE-SDS, % тяжелой цепи и % легкой цепи уменьшался от 94,2% через 3 месяца до 87,7% через 6 месяцев. Это уменьшение не являлось неожиданным при 40°C, с учетом характера этих условий.
Варианты заряда по HP-IEX
При 5°C (долгосрочное хранение), присутствует небольшое увеличение % кислых вариантов от исходного 21,46% до 22,49% через 9 месяцев, с соответствующим небольшим уменьшением общего количества главного пика от 68,8% до 67,1% через 9 месяцев. % основных вариантов начинает немного увеличиваться через 9 месяцев, с увеличением от 10,15% через 6 месяцев до 10,38% через 9 месяцев. При 25°C (в условиях ускоренного старения), общее количество главного пика уменьшалось от 68,8% в исходной временной точке до 47,6% через 9 месяцев. Вместе с уменьшением общего количества главного пика, наблюдали соответствующее увеличение содержания кислых вариантов от 21,46% до 39,86% и небольшое увеличение содержания основных вариантов от 9,70% до 11,51%. При 40°C (в условиях стресса), присутствовало уменьшение общего количества главного пика до 10,1% через 6 месяцев, вместе с соответствующим значительным увеличением содержания кислых вариантов до 80,02% и основных вариантов до 9,95%.
Частицы
Частицы измеряли посредством mHIAC. Результаты в условиях 5°C были сильно ниже критериев приемлемости ≤ 6000 частиц на контейнер для ≥ 10 мкм и ≤ 600 частиц на контейнер для ≥ 25 мкм от исходной точки до 9 месяцев. При 25°C, зарегистрировано увеличение содержания частиц >= 10 мкм от 13 частиц на контейнер в исходной временной точке до 460 частиц на контейнер через 9 месяцев. Присутствовало уменьшение содержания частиц для частиц >= 25 мкм с результатом 3 частицы на контейнер через 9 месяцев. Данные для всех временных точек при 25C находились в пределах критериев приемлемости для анализа как >=10 мкм, так и >= 25 мкм. Данные в условиях 40°C показали очень сильное увеличение содержания частиц >=10 мкм с 8258 частиц на контейнер через 9 месяцев. Этот результат находился вне критериев приемлемости <=600 частиц на контейнер. Результат для частиц >= 25 мкм увеличивался во временной точке анализа стабильности 9 месяцев до 124 частиц на контейнер, что соответствует критериям приемлемости >= 25 мкм (<=600 частиц на контейнер).
Мутность
Мутность определяли по спектрофотометрическому поглощению при 350 нм. При более длительном хранении в условиях 5°C, не присутствовало заметного изменения вплоть до временной точки 9. В условиях 25C, присутствует небольшое увеличение через 3 месяца с результатом 0,163 AU, он продолжает увеличиваться до 9 месяцев с результатом 0,196 AU. При 40C, присутствует более выраженное увеличение, начиная с 1 месяца с 0,188 AU, и затем сильное увеличение до 0,453 AU через 9 месяцев.
Заключения
На основании этих данных, на время тестирования 18 месяцев, не наблюдали значительных изменений или тенденций в условиях хранения 5 C в ходе исследований стабильности для pH, концентрации белка, внешнего вида и видимых частиц (данные не представлены), и активности и частиц (данные не представлены). За исключением небольшого увеличения окрашивания и уменьшения содержания PS-80 до 0,13 мг/мл, не наблюдали значительных изменений или тенденций в каком-либо тесте стабильности при 5°C.
На основании данных долгосрочной стабильности при 5C, состав антитела против TIGIT, содержащий L-гистидиновый буфер, сахарозу, полисорбат 80 и L-метионин, имеет ожидаемый срок хранения 30 месяцев. Для составов, дополнительно содержащих хелатирующий агент, ожидают уменьшение деградации полисорбата 80, которую наблюдали.
ПРИМЕР 8
Совместный состав антитела против TIGIT и антитела против PD-1.
Совместное составление двух антител в один состав является более удобным для пациентов и увеличивает соблюдение режима с помощью совместного дозирования двух антител. Совместное составление двух антител в один состав является более удобным для пациентов и увеличивает соблюдение режима с помощью совместного дозирования двух антител. Анти-TIGIT антитело, имеющее следующие CDR: HCDR1 из SEQ ID NO:108, HCDR2 из SEQ ID NO:154, HCDR3 из SEQ ID NO:110, LCDR1 из SEQ ID NO:111, LCDR2 из SEQ ID NO:112 и LCDR3 из SEQ ID NO:113, на остове IgG1, совместно составляли с пембролизумабом. На основании белок-белковых взаимодействий (показано ниже), обнаружено, что совместный состав (показано ниже) является стабильным при pH 5,0-6,0. Таким образом, совместный состав (P1T1) при pH 5,0, 5,5 и 6,0 выбран и помещен для дополнительных исследований термостабильности при 5°C, 25°C и 40°C, вместе с двумя контрольными составами (антитела против PD1 и антитела против TIGIT).
Составы получали в форме жидких составов следующим образом:
По 1 мл каждого состава заполняли флаконы 2R. Стабильность измеряли посредством визуальной проверки, концентрации белка, микропроточной визуализации (MFI) (оценки частиц), эксклюзионной хроматографии (SEC) в смешанном режиме (оценки агрегации), IEX (оценки вариантов заряда) и UP-SEC (оценки агрегации). Способ исследования термостабильности является следующим:
(влажность окружающего воздуха)
(60% относительная влажность)
(75% относительная влажность)
Измеряли белок-белковые взаимодействия, показательные для коллоидности и термостабильности, различных совместных составов. Отталкивающее белок-белковое взаимодействие, как показано по положительному значению параметра диффузионного взаимодействия (KD) KD >0, указывает на стабильный состав с низкой предрасположенностью к агрегации. Обнаружили, что Kd для совместного состава имеет положительное значение KD, которое является показательным для отталкивающего и стабилизирующего белок-белкового взаимодействия, что может указывать на меньшую предрасположенность к агрегации и на стабильный совместный состав.
На основании положительного параметра диффузионного взаимодействия (KD) или KD >0, ожидают, что антитела при совместном составлении могут иметь хорошее поведение в совместном составе, подобно составам одного антитела.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> НАРАСИМХАН, Чакраварти Начу
ДЕ, Арнаб
<120> СТАБИЛЬНЫЕ СОСТАВЫ АНТИТЕЛ ПРОТИВ TIGIT, ОТДЕЛЬНО И В
КОМБИНАЦИИ С АНТИТЕЛАМИ ПРОТИВ РЕЦЕПТОРА 1 ПРОГРАММИРУЕМОЙ СМЕРТИ
(PD-1), И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
<130> 24453
<150> 62/500,278
<151> 2017-05-02
<160> 293
<170> PatentIn версии 3.5
<210> 1
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 1
Arg Ala Ser Lys Gly Val Ser Thr Ser Gly Tyr Ser Tyr Leu His
1 5 10 15
<210> 2
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 2
Leu Ala Ser Tyr Leu Glu Ser
1 5
<210> 3
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 3
Gln His Ser Arg Asp Leu Pro Leu Thr
1 5
<210> 4
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 4
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 5
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 5
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 6
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 6
Asn Tyr Tyr Met Tyr
1 5
<210> 7
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 7
Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe Lys
1 5 10 15
Asn
<210> 8
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 8
Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr
1 5 10
<210> 9
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 9
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 10
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 10
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 11
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 11
Arg Ala Ser Gln Ser Val Ser Ser Tyr Leu Ala
1 5 10
<210> 12
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 12
Asp Ala Ser Asn Arg Ala Thr
1 5
<210> 13
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 13
Gln Gln Ser Ser Asn Trp Pro Arg Thr
1 5
<210> 14
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 14
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 15
<211> 214
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 15
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Ser Asn Trp Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 16
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 16
Asn Ser Gly Met His
1 5
<210> 17
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 17
Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 18
<211> 4
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 18
Asn Asp Asp Tyr
1
<210> 19
<211> 113
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 19
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser
<210> 20
<211> 440
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 20
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Asp Cys Lys Ala Ser Gly Ile Thr Phe Ser Asn Ser
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Lys Arg Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Thr Asn Asp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
100 105 110
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser
115 120 125
Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
130 135 140
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
145 150 155 160
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
165 170 175
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys
180 185 190
Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp
195 200 205
Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala
210 215 220
Pro Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro
225 230 235 240
Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val
245 250 255
Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val
260 265 270
Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln
275 280 285
Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln
290 295 300
Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly
305 310 315 320
Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro
325 330 335
Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr
340 345 350
Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser
355 360 365
Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr
370 375 380
Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr
385 390 395 400
Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe
405 410 415
Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys
420 425 430
Ser Leu Ser Leu Ser Leu Gly Lys
435 440
<210> 21
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 21
Arg Ala Ser Lys Ser Val Ser Thr Ser Gly Phe Ser Tyr Leu His
1 5 10 15
<210> 22
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 22
Leu Ala Ser Asn Leu Glu Ser
1 5
<210> 23
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 23
Gln His Ser Trp Glu Leu Pro Leu Thr
1 5
<210> 24
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 24
Ser Tyr Tyr Leu Tyr
1 5
<210> 25
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 25
Gly Val Asn Pro Ser Asn Gly Gly Thr Asn Phe Ser Glu Lys Phe Lys
1 5 10 15
Ser
<210> 26
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 26
Arg Asp Ser Asn Tyr Asp Gly Gly Phe Asp Tyr
1 5 10
<210> 27
<211> 120
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 28
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 28
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 29
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 29
Glu Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
35 40 45
Gln Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 30
<211> 111
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 30
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
35 40 45
Gln Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Leu Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 31
<211> 447
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 31
Gln Val Gln Leu Val Gln Ser Gly Val Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Tyr Met Tyr Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Asn Pro Ser Asn Gly Gly Thr Asn Phe Asn Glu Lys Phe
50 55 60
Lys Asn Arg Val Thr Leu Thr Thr Asp Ser Ser Thr Thr Thr Ala Tyr
65 70 75 80
Met Glu Leu Lys Ser Leu Gln Phe Asp Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Asp Tyr Arg Phe Asp Met Gly Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 32
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 32
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Arg Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Ser Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 33
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 33
Glu Ile Val Leu Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
35 40 45
Gln Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 34
<211> 218
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 34
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ala Ser Lys Gly Val Ser Thr Ser
20 25 30
Gly Tyr Ser Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser Pro
35 40 45
Gln Leu Leu Ile Tyr Leu Ala Ser Tyr Leu Glu Ser Gly Val Pro Asp
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Ala Phe Thr Leu Lys Ile Ser
65 70 75 80
Arg Val Glu Ala Glu Asp Val Gly Leu Tyr Tyr Cys Gln His Ser Arg
85 90 95
Asp Leu Pro Leu Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 35
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 35
Ser Asp Tyr Trp Gly
1 5
<210> 36
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 36
Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 37
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 37
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 38
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 38
Lys Ala Ser Gln Ser Ile His Lys Asn Leu Ala
1 5 10
<210> 39
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 39
Tyr Ala Asn Ser Leu Gln Thr
1 5
<210> 40
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 40
Gln Gln Tyr Tyr Ser Gly Trp Thr
1 5
<210> 41
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 41
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Ser Val Thr Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Phe Pro Gly Asn Lys Met Glu Trp Met
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe Leu
65 70 75 80
Gln Leu His Ser Val Thr Thr Asp Asp Thr Ala Thr Tyr Ser Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Pro Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 42
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 42
Asp Ile Gln Met Thr Gln Ser Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Leu Gly Glu Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Gly Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Phe Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Leu Lys
100 105
<210> 43
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 43
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 44
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 44
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 45
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 45
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 46
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 46
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 47
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 47
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 48
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 48
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Gly Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 49
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 49
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 50
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 50
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 51
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 51
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 52
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 52
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 53
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 53
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 54
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 54
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Ser Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 55
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 55
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 56
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 56
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Tyr Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 57
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 57
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Ser Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 58
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 58
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ala Val Ser Gly Ser Ser Ile Ser Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Met
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu His Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 59
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 59
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 60
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 60
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 61
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 61
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 62
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 62
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 63
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 63
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 64
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 64
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 65
<211> 129
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 65
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser Ala
115 120 125
Ser
<210> 66
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 66
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 67
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 67
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 68
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 68
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Lys Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 69
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 69
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Met Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 70
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 70
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Pro Pro Gly Lys Lys Met Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 71
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 71
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Phe Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Asp Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 72
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 72
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Lys Pro Pro Gly Lys Lys Met Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 73
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 73
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 74
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 74
Glu Val Gln Leu Gln Gln Ser Gly Ala Gly Leu Leu Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Ile Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 75
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 75
Glu Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Pro Gly
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Ser Ser Ile Ala Ser Asp
20 25 30
Tyr Trp Gly Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Trp Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Met Val Thr Val Ser Ser
115 120 125
<210> 76
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 76
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 77
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 77
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 78
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 78
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 79
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 79
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 80
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 80
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Asn Ser Leu Gln Thr Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 81
Gly Tyr Ser Ile Thr Ser Asp Tyr Ala Trp Asn
1 5 10
<210> 82
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 82
Tyr Ile Ser Asn Ser Gly Ser Ala Ser Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 83
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 83
Leu Ile Tyr Tyr Asp Tyr Gly Gly Ala Met Asn Phe
1 5 10
<210> 84
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 84
Lys Ala Ser Gln Gly Val Ser Thr Thr Val Ala
1 5 10
<210> 85
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 85
Ser Ala Ser Tyr Arg Tyr Thr
1 5
<210> 86
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 86
Gln His Tyr Tyr Ser Thr Pro Trp Thr
1 5
<210> 87
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 87
Asp Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Ser Leu Ser Leu Thr Cys Thr Val Thr Gly Tyr Ser Ile Thr Ser Asp
20 25 30
Tyr Ala Trp Asn Trp Ile Arg Gln Phe Pro Gly Asn Lys Leu Glu Trp
35 40 45
Met Gly Tyr Ile Ser Asn Ser Gly Ser Ala Ser Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Phe Phe
65 70 75 80
Leu Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Thr Leu Ile Tyr Tyr Asp Tyr Gly Gly Ala Met Asn Phe Trp Gly
100 105 110
Gln Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 88
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 88
Asp Ile Val Met Thr Gln Ser His Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Gly Val Ser Thr Thr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln His Tyr Tyr Ser Thr Pro Trp
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 89
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 89
Tyr Ala Ser Asn Leu Gln Thr
1 5
<210> 90
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 90
Tyr Ala Ser Ser Leu Gln Thr
1 5
<210> 91
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 91
Tyr Ala Ser Thr Leu Gln Thr
1 5
<210> 92
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 92
Tyr Ala Thr Thr Leu Gln Thr
1 5
<210> 93
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 93
Tyr Ala Ser Tyr Leu Gln Thr
1 5
<210> 94
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 94
Tyr Ala Asn Gln Leu Gln Thr
1 5
<210> 95
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 95
Tyr Ala Gly Ser Leu Gln Thr
1 5
<210> 96
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 96
Tyr Ala Ser Gln Leu Gln Thr
1 5
<210> 97
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 97
Tyr Ala Asp Ser Leu Gln Thr
1 5
<210> 98
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 98
Gln Gln Tyr Tyr Ser Gly Phe Thr
1 5
<210> 99
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 99
Gln Gln Tyr Tyr Ser Gly Tyr Thr
1 5
<210> 100
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 100
Gln Gln Tyr Tyr Ser Gly Ile Thr
1 5
<210> 101
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 101
Gln Gln Tyr Tyr Ser Gly Val Thr
1 5
<210> 102
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 102
Gln Gln Tyr Tyr Ser Gly Leu Thr
1 5
<210> 103
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 103
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Phe Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 104
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 104
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Tyr Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 105
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 105
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Ile Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 106
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 106
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Val Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 107
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 107
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Leu Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 108
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 108
Ser Tyr Val Met His
1 5
<210> 109
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 109
Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 110
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 110
Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val
1 5 10
<210> 111
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 111
Arg Ala Ser Glu His Ile Tyr Ser Tyr Leu Ser
1 5 10
<210> 112
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 112
Asn Ala Lys Thr Leu Ala Glu
1 5
<210> 113
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 113
Gln His His Phe Gly Ser Pro Leu Thr
1 5
<210> 114
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 114
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Lys Gln Lys Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Ser Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Ala Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 115
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 115
Asp Ile Gln Met Thr Gln Ser Pro Ala Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Glu Thr Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Gln Gly Lys Ser Pro Gln Leu Leu Val
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Phe Ser Leu Lys Ile Asn Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Gly Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Thr Leu Glu Leu Lys
100 105
<210> 116
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 116
Tyr Ile Asp Pro Tyr Asn Arg Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 117
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 117
Tyr Ile Asp Pro Tyr Asn Leu Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 118
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 118
Tyr Ile Asp Pro Tyr Asn Lys Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 119
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 119
Tyr Ile Asp Pro Tyr Asn Phe Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 120
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 120
Tyr Ile Asp Pro Tyr Asn Ser Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 121
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 121
Tyr Ile Asp Pro Tyr Asn Tyr Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 122
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 122
Tyr Ile Asp Pro Tyr Asn Val Gly Ala Lys Tyr Asn Glu Lys Phe Gly
1 5 10 15
<210> 123
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 123
Tyr Ile Asp Pro Tyr Asn Asp Arg Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 124
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 124
Tyr Ile Asp Pro Tyr Asn Asp Asn Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 125
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 125
Tyr Ile Asp Pro Tyr Asn Asp Gln Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 126
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 126
Tyr Ile Asp Pro Tyr Asn Asp Glu Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 127
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 127
Tyr Ile Asp Pro Tyr Asn Asp Leu Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 128
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 128
Tyr Ile Asp Pro Tyr Asn Asp Lys Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 129
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 129
Tyr Ile Asp Pro Tyr Asn Asp Ser Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 130
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 130
Tyr Ile Asp Pro Tyr Asn Asp Tyr Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 131
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 131
Tyr Ile Asp Pro Tyr Asn Asp Val Ala Lys Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 132
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 132
Ala Ala Lys Thr Leu Ala Glu
1 5
<210> 133
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 133
Tyr Ala Lys Thr Leu Ala Glu
1 5
<210> 134
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 134
Trp Ala Lys Thr Leu Ala Glu
1 5
<210> 135
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 135
Ser Ala Lys Thr Leu Ala Glu
1 5
<210> 136
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 136
Thr Ala Lys Thr Leu Ala Glu
1 5
<210> 137
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 137
Ile Ala Lys Thr Leu Ala Glu
1 5
<210> 138
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 138
Val Ala Lys Thr Leu Ala Glu
1 5
<210> 139
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 139
Asn Asn Lys Thr Leu Ala Glu
1 5
<210> 140
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 140
Asn Ile Lys Thr Leu Ala Glu
1 5
<210> 141
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 141
Asn Leu Leu Thr Leu Ala Glu
1 5
<210> 142
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 142
Asn Thr Lys Thr Leu Ala Glu
1 5
<210> 143
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 143
Asn Val Lys Thr Leu Ala Glu
1 5
<210> 144
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 144
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 145
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 145
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ser Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ser Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 146
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 146
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 147
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 147
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ser Asp Lys Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 148
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 148
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ser Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 149
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 149
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ser Asp Lys Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Thr Val Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Trp Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 150
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 150
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 151
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 151
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 152
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 152
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 153
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 153
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Val Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Ala Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Gln Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 154
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 154
Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 155
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 155
Tyr Ile Asp Pro Tyr Asn Asp Gly Ala Lys Tyr Ser Gln Lys Phe Gln
1 5 10 15
Gly
<210> 156
<211> 116
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 156
Gln Val Gln Leu Met Glu Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Phe Pro Leu Thr Ser Tyr
20 25 30
Thr Val His Trp Val Arg Gln Pro Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Ala Ile Trp Ser Ser Gly Ser Thr Asp Tyr Asn Ser Ala Leu Lys
50 55 60
Ser Arg Leu Asn Ile Asn Arg Asp Ser Ser Lys Ser Gln Val Phe Leu
65 70 75 80
Lys Met Asn Ser Leu Gln Thr Glu Asp Thr Ala Ile Tyr Phe Cys Thr
85 90 95
Lys Ser Gly Trp Ala Phe Phe Asp Tyr Trp Gly Gln Gly Val Met Val
100 105 110
Thr Val Ser Ser
115
<210> 157
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 157
Asp Ile Gln Met Thr Gln Ser Pro Ser Leu Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Leu Asn Cys Ile Ala Ser Gln Asn Ile Tyr Lys Ser
20 25 30
Leu Ala Trp Tyr Gln Leu Lys Leu Gly Glu Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asn Ala Asn Ser Leu Gln Ala Gly Ile Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Ala Leu Thr Ile Ser Gly Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Phe Cys Gln Gln Tyr Ser Gly Gly Tyr Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 158
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 158
Glu Val Gln Leu Val Glu Ser Gly Gly Asp Leu Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Lys Ile Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Ala Trp Val Arg Leu Ala Pro Gln Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Tyr Glu Gly Ser Arg Thr His Tyr Gly Asp Ser Val
50 55 60
Arg Gly Arg Phe Ile Ile Ser Arg Asp Asn Pro Lys Asn Ile Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Gly Ser Glu Asp Thr Ala Thr Tyr Phe Cys
85 90 95
Ala Arg His Thr Gly Thr Leu Asp Trp Leu Val Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Ile Val Ser Ser
115
<210> 159
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 159
Asn Ile Val Met Ala Gln Ser Pro Lys Ser Met Ser Ile Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Met Asn Cys Lys Ala Ser Gln Asn Val Asp Asn Asn
20 25 30
Ile Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Phe Tyr Ala Ser Asn Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Gly Gly Tyr Gly Thr Asp Phe Thr Leu Thr Ile Lys Ser Val Gln Ala
65 70 75 80
Glu Asp Ala Ala Phe Tyr Tyr Cys Gln Arg Ile Tyr Asn Phe Pro Thr
85 90 95
Phe Gly Ser Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 160
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (13)..(13)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (13)..(13)
<223> белок
<400> 160
Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Xaa Glu Gly Tyr
1 5 10 15
Phe Asp Phe
<210> 161
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (3)..(3)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (4)..(4)
<223> белок
<400> 161
Tyr Ala Xaa Xaa Leu Gln Thr
1 5
<210> 162
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (7)..(7)
<223> белок
<400> 162
Gln Gln Tyr Tyr Ser Gly Xaa Thr
1 5
<210> 163
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (6)..(6)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (9)..(9)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (12)..(12)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (15)..(15)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (16)..(16)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (17)..(17)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (23)..(23)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (25)..(25)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (27)..(27)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (30)..(30)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (37)..(37)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (39)..(39)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (40)..(40)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (43)..(43)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (44)..(44)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (45)..(45)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (48)..(48)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (67)..(67)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (68)..(68)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (70)..(70)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (71)..(71)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (79)..(79)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (81)..(81)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (83)..(83)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (87)..(87)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (88)..(88)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (92)..(92)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (94)..(94)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (110)..(110)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (119)..(119)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (122)..(122)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (123)..(123)
<223> белок
<400> 163
Glu Val Gln Leu Gln Xaa Ser Gly Xaa Gly Leu Xaa Lys Pro Xaa Xaa
1 5 10 15
Xaa Leu Ser Leu Thr Cys Xaa Val Xaa Gly Xaa Ser Ile Xaa Ser Asp
20 25 30
Tyr Trp Gly Trp Xaa Arg Xaa Xaa Pro Gly Xaa Xaa Xaa Glu Trp Xaa
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Xaa Xaa Ile Xaa Xaa Asp Thr Ser Lys Asn Gln Phe Xaa Leu
65 70 75 80
Xaa Leu Xaa Ser Val Thr Xaa Xaa Asp Thr Ala Xaa Tyr Xaa Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Xaa Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Xaa Gly Thr Xaa Xaa Thr Val Ser Ser
115 120 125
<210> 164
<211> 127
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (6)..(6)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (9)..(9)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (12)..(12)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (15)..(15)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (16)..(16)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (23)..(23)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (25)..(25)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (27)..(27)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (30)..(30)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (37)..(37)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (39)..(39)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (40)..(40)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (44)..(44)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (45)..(45)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (48)..(48)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (67)..(67)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (71)..(71)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (83)..(83)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (88)..(88)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (110)..(110)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (122)..(122)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (123)..(123)
<223> белок
<400> 164
Glu Val Gln Leu Gln Xaa Ser Gly Xaa Gly Leu Xaa Lys Pro Xaa Xaa
1 5 10 15
Thr Leu Ser Leu Thr Cys Xaa Val Xaa Gly Xaa Ser Ile Xaa Ser Asp
20 25 30
Tyr Trp Gly Trp Xaa Arg Xaa Xaa Pro Gly Lys Xaa Xaa Glu Trp Xaa
35 40 45
Gly Phe Ile Thr Tyr Ser Gly Ser Thr Ser Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Xaa Thr Ile Ser Xaa Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Xaa Ser Val Thr Ala Xaa Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Met Pro Ser Phe Ile Thr Leu Ala Ser Leu Ser Thr Xaa Glu Gly
100 105 110
Tyr Phe Asp Phe Trp Gly Gln Gly Thr Xaa Xaa Thr Val Ser Ser
115 120 125
<210> 165
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (10)..(10)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (21)..(21)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (22)..(22)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (40)..(40)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (42)..(42)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (43)..(43)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (46)..(46)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (52)..(52)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (53)..(53)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (58)..(58)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (77)..(77)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (83)..(83)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (87)..(87)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (95)..(95)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (105)..(105)
<223> белок
<400> 165
Asp Ile Gln Met Thr Gln Ser Pro Ser Xaa Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Xaa Xaa Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Xaa Gly Xaa Xaa Pro Lys Xaa Leu Ile
35 40 45
Tyr Tyr Ala Xaa Xaa Leu Gln Thr Gly Xaa Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Xaa Leu Gln Pro
65 70 75 80
Glu Asp Xaa Ala Thr Tyr Xaa Cys Gln Gln Tyr Tyr Ser Gly Xaa Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Xaa Lys
100 105
<210> 166
<211> 106
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> неопределенный признак
<222> (43)..(43)
<223> белок
<220>
<221> неопределенный признак
<222> (46)..(46)
<223> белок
<220>
<221> неопределенный признак
<222> (52)..(52)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (53)..(53)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (56)..(56)
<223> белок
<220>
<221> неопределенный признак
<222> (58)..(58)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (62)..(62)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (63)..(63)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (68)..(68)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (83)..(83)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (95)..(95)
<223> белок
<400> 166
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Ile His Lys Asn
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Xaa Pro Lys Xaa Leu Ile
35 40 45
Tyr Tyr Ala Xaa Xaa Leu Gln Thr Gly Xaa Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Xaa Ala Thr Tyr Tyr Cys Gln Gln Tyr Tyr Ser Gly Xaa Thr
85 90 95
Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 167
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (7)..(7)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (8)..(8)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (12)..(12)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (13)..(13)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (16)..(16)
<223> белок
<400> 167
Tyr Ile Asp Pro Tyr Asn Xaa Xaa Ala Lys Tyr Xaa Xaa Lys Phe Xaa
1 5 10 15
Gly
<210> 168
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> неопределенный признак
<222> (1)..(1)
<223> белок
<220>
<221> неопределенный признак
<222> (2)..(2)
<223> белок
<400> 168
Xaa Xaa Lys Thr Leu Ala Glu
1 5
<210> 169
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (5)..(5)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (9)..(9)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (11)..(11)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (12)..(12)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (16)..(16)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (20)..(20)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (38)..(38)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (40)..(40)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (44)..(44)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (56)..(56)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (57)..(57)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (61)..(61)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (62)..(62)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (65)..(65)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (67)..(67)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (68)..(68)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (72)..(72)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (74)..(74)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (76)..(76)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (79)..(79)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (85)..(85)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (87)..(87)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (89)..(89)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (91)..(91)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (92)..(92)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (104)..(104)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (111)..(111)
<223> белок
<400> 169
Glu Val Gln Leu Xaa Gln Ser Gly Xaa Glu Xaa Xaa Lys Pro Gly Xaa
1 5 10 15
Ser Val Lys Xaa Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Xaa Gln Xaa Pro Gly Gln Xaa Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Xaa Xaa Ala Lys Tyr Xaa Xaa Lys Phe
50 55 60
Xaa Gly Xaa Xaa Thr Leu Thr Xaa Asp Xaa Ser Xaa Ser Thr Xaa Tyr
65 70 75 80
Met Glu Leu Ser Xaa Leu Xaa Ser Xaa Asp Xaa Xaa Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Xaa Tyr Phe Asp Val Trp Gly Xaa Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 170
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (16)..(16)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (44)..(44)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (56)..(56)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (57)..(57)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (61)..(61)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (62)..(62)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (65)..(65)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (72)..(72)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (74)..(74)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (76)..(76)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (79)..(79)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (85)..(85)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (89)..(89)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (92)..(92)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (104)..(104)
<223> белок
<400> 170
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Xaa
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Tyr
20 25 30
Val Met His Trp Val Arg Gln Ala Pro Gly Gln Xaa Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Asp Pro Tyr Asn Xaa Xaa Ala Lys Tyr Xaa Xaa Lys Phe
50 55 60
Xaa Gly Arg Val Thr Leu Thr Xaa Asp Xaa Ser Xaa Ser Thr Xaa Tyr
65 70 75 80
Met Glu Leu Ser Xaa Leu Arg Ser Xaa Asp Thr Xaa Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Tyr Gly Xaa Tyr Phe Asp Val Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 171
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (9)..(9)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (17)..(17)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (18)..(18)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (40)..(40)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (43)..(43)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (45)..(45)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (48)..(48)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (50)..(50)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (51)..(41)
<223> белок
<220>
<221> неопределенный признак
<222> (51)..(51)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (70)..(70)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (72)..(72)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (74)..(74)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (76)..(76)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (83)..(83)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (84)..(84)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (100)..(100)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (103)..(103)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (106)..(106)
<223> белок
<400> 171
Asp Ile Gln Met Thr Gln Ser Pro Xaa Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Xaa Xaa Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Xaa Gly Lys Xaa Pro Xaa Leu Leu Xaa
35 40 45
Tyr Xaa Xaa Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Xaa Phe Xaa Leu Xaa Ile Xaa Ser Leu Gln Pro
65 70 75 80
Glu Asp Xaa Xaa Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Xaa Gly Thr Xaa Leu Glu Xaa Lys
100 105
<210> 172
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (43)..(43)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (50)..(50)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (51)..(51)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (70)..(70)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (83)..(83)
<223> белок
<400> 172
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Glu His Ile Tyr Ser Tyr
20 25 30
Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Xaa Pro Lys Leu Leu Ile
35 40 45
Tyr Xaa Xaa Lys Thr Leu Ala Glu Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Xaa Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Xaa Ala Thr Tyr Tyr Cys Gln His His Phe Gly Ser Pro Leu
85 90 95
Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 173
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (6)..(6)
<223> белок
<400> 173
Gly Gly Pro Tyr Gly Xaa Tyr Phe Asp Val
1 5 10
<210> 174
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 174
Gly Gly Pro Tyr Gly Ala Tyr Phe Asp Val
1 5 10
<210> 175
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 175
Gly Gly Pro Tyr Gly Asp Tyr Phe Asp Val
1 5 10
<210> 176
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 176
Gly Gly Pro Tyr Gly Glu Tyr Phe Asp Val
1 5 10
<210> 177
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 177
Gly Gly Pro Tyr Gly Phe Tyr Phe Asp Val
1 5 10
<210> 178
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 178
Gly Gly Pro Tyr Gly Gly Tyr Phe Asp Val
1 5 10
<210> 179
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 179
Gly Gly Pro Tyr Gly Ile Tyr Phe Asp Val
1 5 10
<210> 180
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 180
Gly Gly Pro Tyr Gly Lys Tyr Phe Asp Val
1 5 10
<210> 181
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 181
Gly Gly Pro Tyr Gly Asn Tyr Phe Asp Val
1 5 10
<210> 182
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 182
Gly Gly Pro Tyr Gly Gln Tyr Phe Asp Val
1 5 10
<210> 183
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 183
Gly Gly Pro Tyr Gly Arg Tyr Phe Asp Val
1 5 10
<210> 184
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 184
Gly Gly Pro Tyr Gly Ser Tyr Phe Asp Val
1 5 10
<210> 185
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 185
Gly Gly Pro Tyr Gly Thr Tyr Phe Asp Val
1 5 10
<210> 186
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 186
Gly Gly Pro Tyr Gly Val Tyr Phe Asp Val Ser Glu Gln Ile Asp
1 5 10 15
<210> 187
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 187
Gly Gly Pro Tyr Gly Tyr Tyr Phe Asp Val
1 5 10
<210> 188
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 188
Gly Ala Trp Met Asp
1 5
<210> 189
<211> 19
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 189
Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu Ser
1 5 10 15
Val Lys Gly
<210> 190
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 190
Ala Leu Tyr Asp Gly Phe Tyr Phe Asp Tyr
1 5 10
<210> 191
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 191
Ser Ala Ser Ser Ser Val Ser Ser Gly Tyr Leu Tyr
1 5 10
<210> 192
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 192
Gly Thr Ser Thr Leu Ala Ser
1 5
<210> 193
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 193
His Gln Trp Ser Ser Phe Pro Tyr Thr
1 5
<210> 194
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 194
Glu Val Lys Leu Glu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Met Lys Leu Ser Cys Val Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ser Pro Glu Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Asn Leu Arg Ala Glu Asp Ser Gly Ile Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Gly Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 195
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 195
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Asn Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Asn Met Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Met Lys
100 105
<210> 196
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (33)..(33)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (34)..(34)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (76)..(76)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (79)..(79)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (80)..(80)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (85)..(85)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (86)..(86)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (87)..(87)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (93)..(93)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (104)..(104)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (105)..(105)
<223> белок
<400> 196
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Xaa Xaa Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Xaa Ser Lys Xaa Xaa
65 70 75 80
Val Tyr Leu Gln Xaa Xaa Xaa Leu Arg Ala Glu Asp Xaa Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Xaa Xaa Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 197
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 197
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Gly Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 198
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 198
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Gly Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 199
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 199
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Gly Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 200
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (20)..(20)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (46)..(46)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (48)..(48)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (59)..(59)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (79)..(79)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (84)..(84)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (92)..(92)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (107)..(107)
<223> белок
<400> 200
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Xaa Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Xaa Leu Xaa
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Xaa Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Xaa Glu
65 70 75 80
Pro Glu Asp Xaa Ala Val Tyr Tyr Cys His Gln Xaa Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Xaa Lys
100 105
<210> 201
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 201
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 202
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 202
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 203
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 203
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Trp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 204
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 204
Glu Phe Thr Met His
1 5
<210> 205
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 205
Gly Leu Lys Pro Asp Asn Gly Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 206
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 206
Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr
1 5 10
<210> 207
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 207
Lys Ala Ser Gln Asp Val Lys Thr Ala Val Ala
1 5 10
<210> 208
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 208
Ser Ala Ser Tyr Arg Asn Thr
1 5
<210> 209
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 209
Gln Gln His Tyr Ser Thr Pro Phe Thr
1 5
<210> 210
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 210
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Ala Val Asp Lys Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 211
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 211
Asp Ile Val Leu Thr Gln Ser His Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Lys Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Ser Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Asn Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Asp Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln His Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Thr Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 212
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (11)..(11)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (12)..(12)
<223> белок
<220>
<221> неопределенный признак
<222> (24)..(24)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (30)..(30)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (33)..(33)
<223> белок
<220>
<221> неопределенный признак
<222> (34)..(34)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (37)..(37)
<223> белок
<220>
<221> неопределенный признак
<222> (38)..(38)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (47)..(47)
<223> белок
<220>
<221> неопределенный признак
<222> (55)..(56)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (61)..(61)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (62)..(62)
<223> белок
<220>
<221> неопределенный признак
<222> (74)..(74)
<223> белок
<220>
<221> неопределенный признак
<222> (77)..(77)
<223> белок
<220>
<221> неопределенный признак
<222> (81)..(81)
<223> белок
<220>
<221> неопределенный признак
<222> (91)..(91)
<223> белок
<220>
<221> неопределенный признак
<222> (105)..(106)
<223> белок
<400> 212
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Xaa Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Xaa His Trp Val Xaa Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Xaa Xaa Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Xaa Ser Thr Xaa Thr Ala Tyr
65 70 75 80
Xaa Glu Leu Ser Ser Leu Arg Ser Glu Asp Xaa Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Xaa Xaa Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 213
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 213
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 214
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 214
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 215
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 215
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 216
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (55)..(55)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (56)..(56)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (60)..(60)
<223> белок
<220>
<221> НЕОПРЕДЕЛЕННЫЙ ПРИЗНАК
<222> (73)..(73)
<223> белок
<400> 216
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Lys Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Xaa Xaa Gly Val Pro Xaa Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Xaa Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 217
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 217
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Lys Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Asn Thr Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 218
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 218
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Lys Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Asn Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 219
<211> 107
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 219
Asp Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asp Val Lys Thr Ala
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Asn Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln His Tyr Ser Thr Pro Phe
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 220
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 220
Ala Leu Tyr Glu Gly Phe Tyr Phe Asp Tyr
1 5 10
<210> 221
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 221
Ala Leu Tyr Asp Ala Phe Tyr Phe Asp Tyr
1 5 10
<210> 222
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 222
Ala Leu Tyr Asp Ser Phe Tyr Phe Asp Tyr
1 5 10
<210> 223
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 223
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Glu Gly Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 224
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 224
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Ala Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 225
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 225
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Ser Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 226
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 226
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Glu Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 227
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 227
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Ala Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 228
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 228
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Ser Ser
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Ser Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 229
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 229
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Glu Gly Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 230
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 230
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Ala Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 231
<211> 121
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 231
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Gly Ala
20 25 30
Trp Met Asp Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Glu Ile Arg Thr Lys Val Asn Asn His Ala Thr Asn Tyr Gly Glu
50 55 60
Ser Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Val Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Arg Gly Ala Leu Tyr Asp Ser Phe Tyr Phe Asp Tyr Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 232
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 232
His Gln Ala Ser Ser Phe Pro Tyr Thr
1 5
<210> 233
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 233
His Gln Asp Ser Ser Phe Pro Tyr Thr
1 5
<210> 234
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 234
His Gln Glu Ser Ser Phe Pro Tyr Thr
1 5
<210> 235
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 235
His Gln Phe Ser Ser Phe Pro Tyr Thr
1 5
<210> 236
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 236
His Gln Gly Ser Ser Phe Pro Tyr Thr
1 5
<210> 237
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 237
His Gln His Ser Ser Phe Pro Tyr Thr
1 5
<210> 238
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 238
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Ala Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 239
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 239
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Asp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 240
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 240
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Glu Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 241
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 241
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Phe Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 242
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 242
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Gly Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 243
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 243
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Lys Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln His Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 244
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 244
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Ala Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 245
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 245
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Asp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 246
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 246
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Glu Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 247
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 247
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Phe Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 248
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 248
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Gly Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 249
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 249
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln His Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 250
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 250
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Ala Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 251
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 251
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Asp Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 252
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 252
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Glu Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 253
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 253
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Phe Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 254
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 254
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln Gly Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 255
<211> 108
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 255
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Ser Ala Ser Ser Ser Val Ser Ser Gly
20 25 30
Tyr Leu Tyr Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Trp
35 40 45
Ile Tyr Gly Thr Ser Thr Leu Ala Ser Gly Ile Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Tyr Thr Leu Thr Ile Ser Ser Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys His Gln His Ser Ser Phe Pro
85 90 95
Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 256
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 256
Gly Leu Lys Pro Asp Gln Gly Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 257
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 257
Gly Leu Lys Pro Asp Asp Gly Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 258
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 258
Gly Leu Lys Pro Asp Asn Ala Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 259
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 259
Gly Leu Lys Pro Asp Thr Gly Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 260
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 260
Gly Leu Lys Pro Asp Ser Gly Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 261
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 261
Gly Leu Lys Pro Asp Gly Gly Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 262
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 262
Gly Leu Lys Pro Asp Asn Ser Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 263
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 263
Gly Leu Lys Pro Asp Asn Thr Gly Ile Ser Tyr Asn Gln Lys Phe Lys
1 5 10 15
Gly
<210> 264
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 264
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Gln Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 265
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 265
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asp Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 266
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 266
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Ala Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 267
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 267
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Thr Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 268
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 268
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Ser Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 269
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 269
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Gly Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 270
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 270
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Ser Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 271
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 271
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Lys Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Thr Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 272
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 272
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Gln Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 273
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 273
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asp Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 274
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 274
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Ala Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 275
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 275
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Thr Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 276
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 276
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Ser Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 277
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 277
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Gly Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 278
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 278
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Ser Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 279
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 279
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Thr Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 280
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 280
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Gln Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 281
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 281
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asp Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 282
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 282
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Ala Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 283
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 283
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Thr Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 284
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 284
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Ser Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 285
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 285
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Gly Gly Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 286
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 286
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Ser Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 287
<211> 119
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 287
Glu Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Val Ser Gly Tyr Thr Phe Thr Glu Phe
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Gly Leu Lys Pro Asp Asn Thr Gly Ile Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Ala Tyr Tyr Arg Tyr Asp Ala Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 288
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 288
Ser Ser Thr Thr Ala Gln Val Asn Trp Glu Gln Gln Asp Gln Leu
1 5 10 15
<210> 289
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 289
Ile Tyr His Thr Tyr Pro Asp Gly Thr
1 5
<210> 290
<211> 5
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 290
Gly Arg Ile Phe Leu
1 5
<210> 291
<211> 330
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
IgG1
<400> 291
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 292
<211> 325
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 292
Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr
1 5 10 15
Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro
20 25 30
Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val
35 40 45
His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser
50 55 60
Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr
65 70 75 80
Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val
85 90 95
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
100 105 110
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
115 120 125
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
130 135 140
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
145 150 155 160
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
165 170 175
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
180 185 190
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
195 200 205
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
210 215 220
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
225 230 235 240
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
245 250 255
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
260 265 270
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
275 280 285
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
290 295 300
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
305 310 315 320
Leu Ser Leu Gly Lys
325
<210> 293
<211> 105
<212> Белок
<213> Искусственная последовательность
<220>
<223> белок
<400> 293
Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu
1 5 10 15
Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro
20 25 30
Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly
35 40 45
Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr
50 55 60
Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His
65 70 75 80
Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val
85 90 95
Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИ-PD-1 АНТИТЕЛА | 2019 |
|
RU2788095C2 |
| АНТИ-TIGIT АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2817838C2 |
| АНТИТЕЛО К TIGIT И ЕГО ИСПОЛЬЗОВАНИЕ | 2019 |
|
RU2786434C2 |
| АНТИТЕЛО ПРОТИВ LILRB1 И ЕГО ПРИМЕНЕНИЯ | 2021 |
|
RU2813373C1 |
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| АНТИТЕЛА К PD-1 И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2761640C2 |
| АНТИГЕНСВЯЗЫВАЮЩИЕ БЕЛКИ ПРОТИВ TIGIT И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2776714C2 |
| АНТИТЕЛА ПРОТИВ GUCY2C И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2812113C2 |
| ГУМАНИЗИРОВАННОЕ АНТИТЕЛО ПРОТИВ РЕЦЕПТОРА IGF-1 | 2021 |
|
RU2836869C1 |
| АНТИ-TIGIT АНТИТЕЛА И СПОСОБЫ ПРИМЕНЕНИЯ | 2016 |
|
RU2732591C2 |
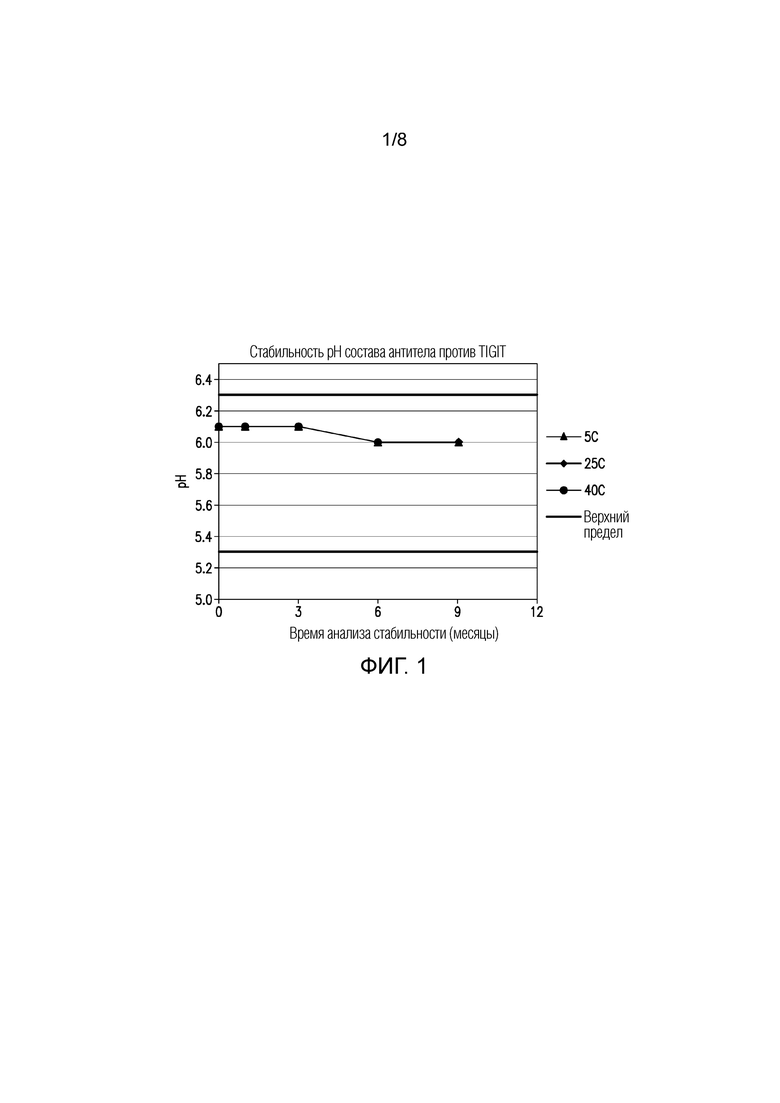
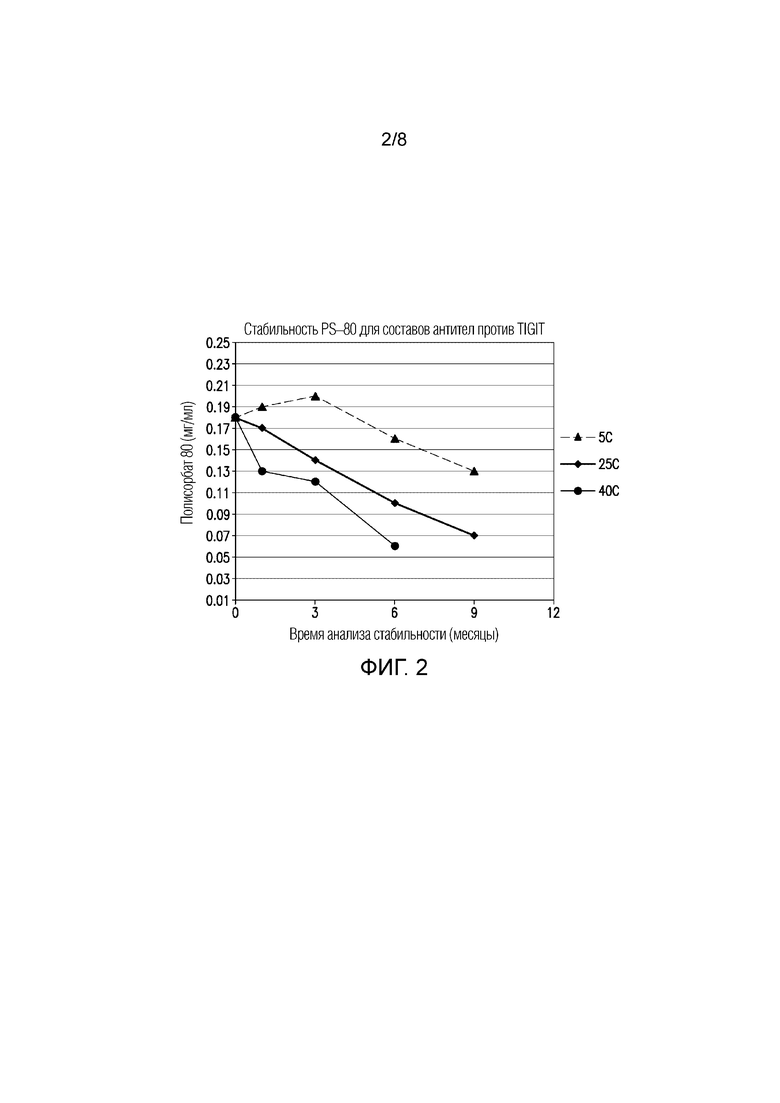
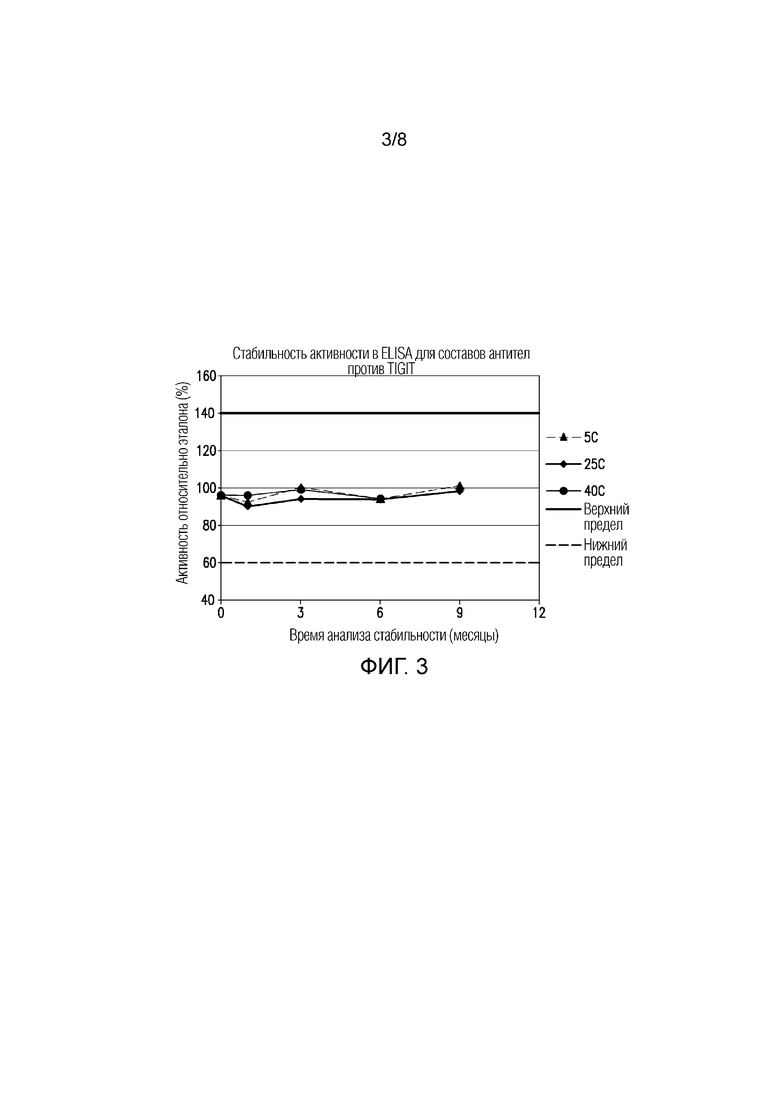

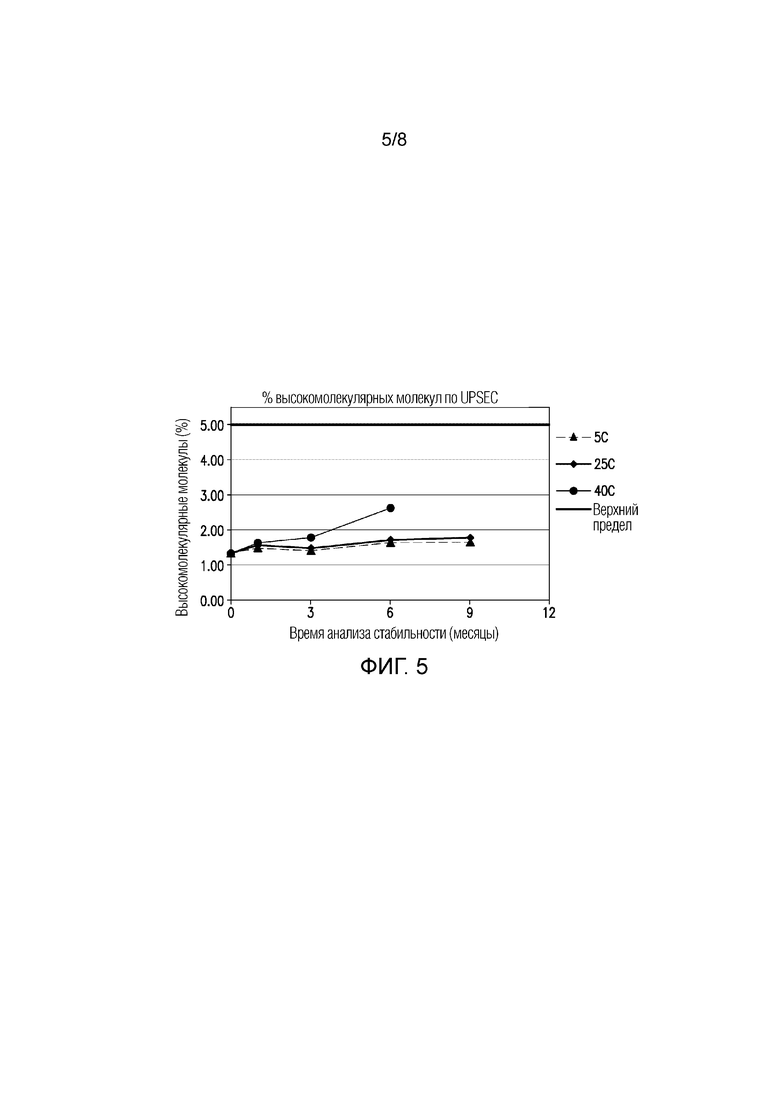
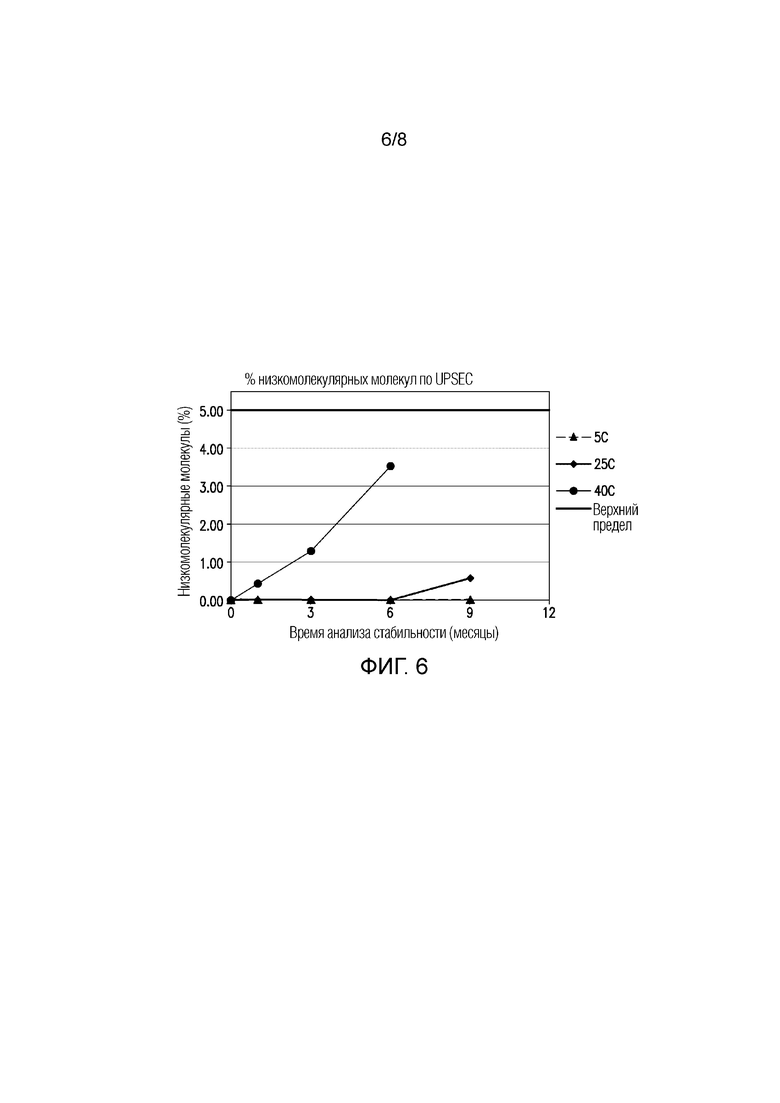
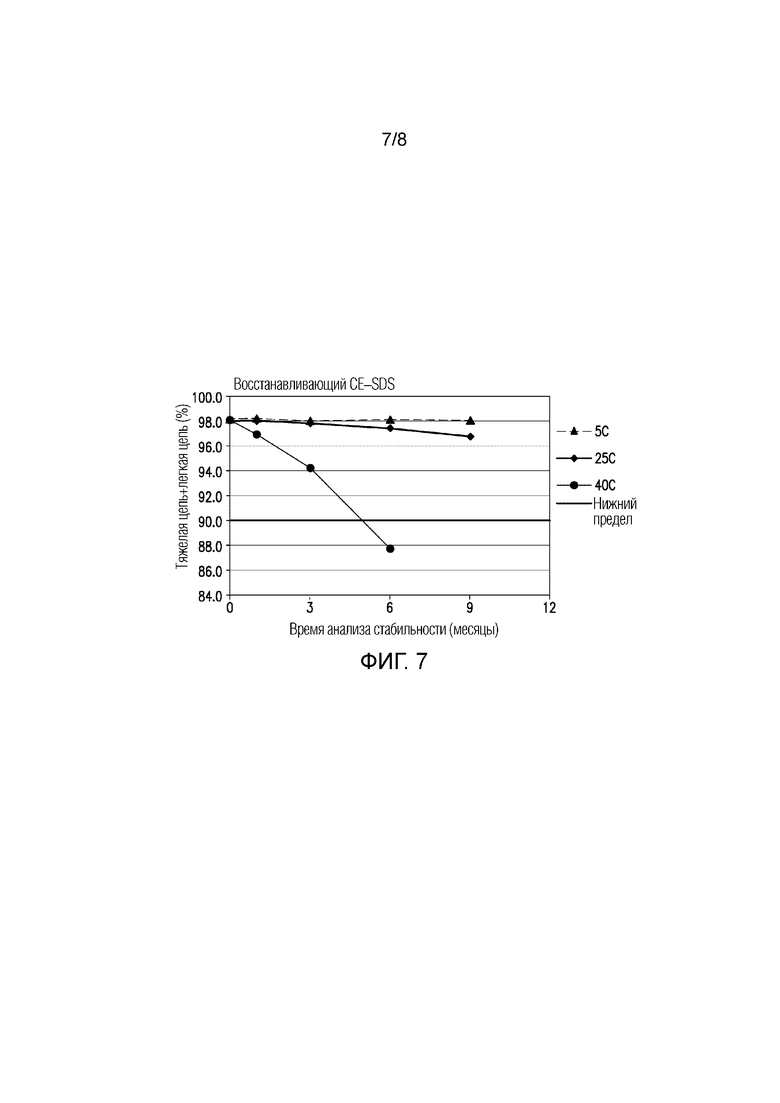

Изобретение относится к области биотехнологии, в частности к стабильному составу, содержащему от около 10 мг/мл до около 200 мг/мл анти-TIGIT антитела или его антигенсвязывающего фрагмента, от около 5 мM до около 20 мM L-гистидинового буфера, от около 6% до около 8% (масс./об.) сахарозы, от около 0,01% до около 0,10% (масс./об.) полисорбата 80, от около 1 мM до около 20 мM L-метионина и от 10 около мг/мл до около 200 мг/мл анти-PD1 антитела или его антигенсвязывающего фрагмента, где состав является совместным составом и где рН стабильного состава равно от 5,3 до 6,2. Изобретение эффективно для лечения злокачественной опухоли и для лечения хронической инфекции. 4 н. и 15 з.п. ф-лы, 8 ил., 6 табл., 8 пр.
1. Стабильный состав для лечения злокачественной опухоли у пациента, где стабильный состав содержит:
(i) от около 10 мг/мл до около 200 мг/мл анти-TIGIT антитела или его антигенсвязывающего фрагмента,
где анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит:
три CDR легкой цепи, содержащие CDRL1 c SEQ ID NO: 111, CDRL2 c SEQ ID NO: 112 и CDRL3 c SEQ ID NO: 113, и
три CDR тяжелой цепи, содержащие CDRH1 c SEQ ID NO: 108, CDRH2 c SEQ ID NO: 154 и CDRH3 c SEQ ID NO: 110;
(ii) от около 5 мM до около 20 мM L-гистидинового буфера;
(iii) от около 6% до около 8% (масс./об.) сахарозы;
(iv) от около 0,01% до около 0,10% (масс./об.) полисорбата 80;
(v) от около 1 мM до около 20 мM L-метионина; и
(vi) от 10 около мг/мл до около 200 мг/мл анти-PD1 антитела или его антигенсвязывающего фрагмента,
где анти-PD-1 антитело или его антигенсвязывающий фрагмент содержит:
три CDR легкой цепи с SEQ ID NO: 1, SEQ ID NO: 2 и SEQ ID NO: 3 и
три CDR тяжелой цепи с SEQ ID NO: 6, SEQ ID NO: 7 и SEQ ID NO: 8,
где состав является совместным составом и
где рН стабильного состава равно от 5,3 до 6,2.
2. Состав по п.1, где анти-PD–1 антитело или его антигенсвязывающий фрагмент содержит
вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 4, и
вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 9.
3. Состав по любому из пп.1, 2, где состав содержит анти-PD–1 антитело, представляющее собой пембролизумаб.
4. Состав по любому из пп.1-3, содержащий
около 10 мг/мл анти-PD1 антитела и
около 10 мг/мл анти-TIGIT антитела.
5. Состав по любому из пп.1–4, дополнительно содержащий хелатирующий агент.
6. Состав по п.5, где хелатирующий агент представляет собой ДТПА.
7. Состав по любому из пп.1–6, где состав содержится в стеклянном флаконе или в устройстве для инъекций.
8. Состав по любому из пп.1–7, где состав является жидким составом, состав заморожен по меньшей мере при ниже –70°C или состав представляет собой раствор, разведенный из лиофилизированного состава.
9. Состав по любому из пп.1–8, где через 12 месяцев при 5°C:
(i) % мономера анти-TIGIT антитела составляет ≥ 95%, как определено посредством эксклюзионной хроматографии;
(ii) % тяжелой цепи и легкой цепи анти-TIGIT антитела составляет ≥ 90%, как измерено посредством восстанавливающего CE–SDS;
(iii) % тяжелой цепи и легкой цепи анти-TIGIT антитела составляет ≥ 95%, как измерено посредством восстанавливающего CE – SDS;
(iv) % интактного IgG анти-TIGIT антитела составляет ≥ 90%, как измерено посредством невосстанавливающего CE–SDS; и/или
(v) % интактного IgG анти-TIGIT антитела составляет ≥ 95%, как измерено посредством невосстанавливающего CE–SDS.
10. Состав по пп.1-9, где анти-TIGIT антитело или его антигенсвязывающий фрагмент содержит
вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 148, и
вариабельную область легкой цепи, содержащую аминокислотная последовательность SEQ ID NO: 152.
11. Состав по пп.1-9, где анти-TIGIT антитело содержит
(i) константный домен тяжелой цепи IgG1 человека, содержащий аминокислотную последовательность SEQ ID NO: 291, и
константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность SEQ ID NO: 293; или
(ii) константный домен тяжелой цепи IgG4 человека, содержащий аминокислотную последовательность SEQ ID NO: 292, и
константный домен легкой цепи каппа человека, содержащий аминокислотную последовательность SEQ ID NO: 293.
12. Состав по пп.1-11, где рН состава равен от 5,5 до 6,3.
13. Состав по пп.1-12, содержащий от около 8 мМ до около 12 мМ L-гистидинового буфера; и/или содержащий около 0,02% (масс./об.) полисорбата 80.
14. Состав по пп.1-13, содержащий от около 10 мг/мл до около 100 мг/мл анти-TIGIT антитела или его антигенсвязывающего фрагмента или где концентрация анти-TIGIT антитела или его антигенсвязывающего фрагмента составляет около 10 мг/мл, 12,5 мг/мл, 25 мг/мл, 50 мг/мл, 75 мг/мл или 100 мг/мл.
15. Состав по п.14, где соотношение анти-PD-1 антитела и анти-TIGIT равно 1:1.
16. Состав по пп.1-15, где состав представляет собой жидкий состав, состав заморожен по крайней мере до температуры ниже -70°C или состав представляет собой раствор, восстановленный из лиофилизированного состава.
17. Способ лечения злокачественной опухоли у пациента–человека, включающий введение эффективного количества состава по любому из пп.1–16.
18. Способ лечения хронической инфекции у пациента–человека, включающий введение эффективного количества состава по любому из пп.1–16.
19. Применение стабильного состава по любому из пп.1–16 для получения лекарственного средства для лечения злокачественной опухоли.
| US 2008112953 A1, 15.05.2008 | |||
| US 2012183531 A1, 19.07.2012 | |||
| WEI WANG et al., Antibody Structure, Instability, and Formulation, JOURNAL OF PHARMACEUTICAL SCIENCES, 2007, Vol | |||
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| WEI WANG, Instability, stabilization, and formulation of liquid protein pharmaceuticals, International Journal of Pharmaceutics, 1999, Vol | |||
| Способ укрепления под покрышкой пневматической шины предохранительного слоя или манжеты | 1917 |
|
SU185A1 |
| Способ применения резонанс конденсатора, подключенного известным уже образом параллельно к обмотке трансформатора, дающего напряжение на анод генераторных ламп | 1922 |
|
SU129A1 |
| LENE | |||
Авторы
Даты
2024-06-05—Публикация
2018-05-01—Подача