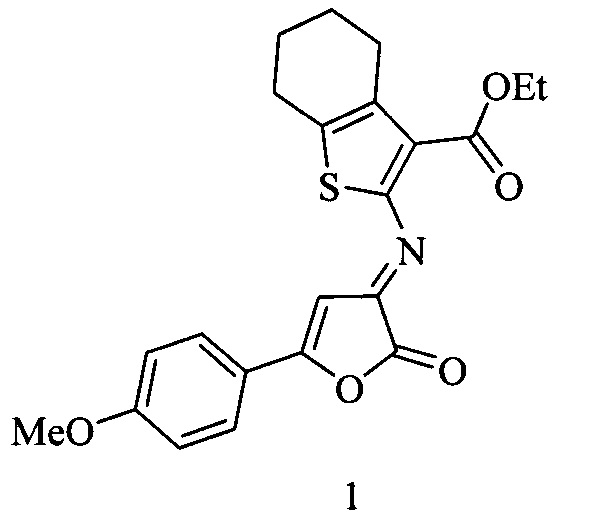
Изобретение относится к области органической и медицинской химии, а именно к применению биологически активных веществ класса замещенных 3-имино-3Н-фуран-2-онов, а именно к этиловому эфиру 2-[(5-(4-метоксифенил)-2-оксофуран-3(2Н)-илиден)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты 1 формулы:

в медицине в качестве лекарственного средства с противогрибковыми свойствами и низкой токсичностью.
Аналогом по структуре заявляемому соединению является 5-(4-феноксифенил)-3-(3,4,5-триметоксибензилиден)фуран-2(3Н)-он [Asif Husain, M.S.Y. Khan, S.M. Hasan, M.M. Alam (2005). 2-Arylidene-4-(4-phenoxy-phenyl)but-3-en-4-olides:Synthesis, reactions and biological activity. European Journal of Medicinal Chemistry. №40, 1394-1404] формулы:


Эталоном сравнения биологической активности был выбран тербинафин формулы:
который широко применяется в лечебной практике, и является аналогом по действию [Машковский М.Д. Лекарственные средства. - 16-е изд., перераб., испр. и доп. - М.: Новая волна, 2012. - с. 925].
Из уровня техники известна структурная формула соединения 1 (Shipilovskikh, S.А., Rubtsov, А.Е., Zalesov, V.V. (2009). Chemistry of iminofurans 3.*Synthesis and intramolecular cyclization of (Z)-4-aryl-2-[3-(ethoxycarbonyl)-4,5,6,7-tetra-hydrobenzo[b]thiophen-2-ylamino]-4-oxobuten-2-oic acids. Chemistry of Heterocyclic Compounds, 45(6), 658-661. doi: 10.1007/sl0593-009-0334-3). Осуществлен способ получения соединения 1 внутримолекулярной циклизацией 4-(4-Метоксифенил)-4-оксо-2-[(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)амино]бут-2-еновой кислоты в среде уксусного ангидрида при 120°С с последующим выделением целевого продукта известными методами по схеме:
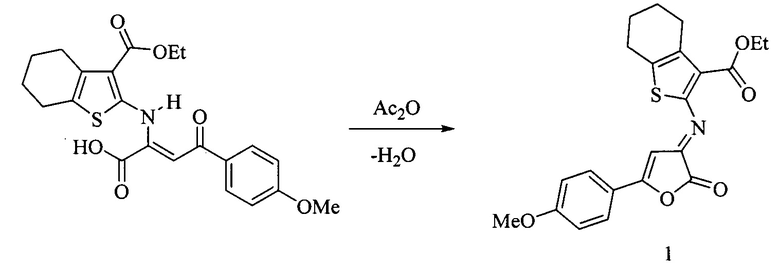
Однако из патентной и научно-технической литературы не выявлено применение соединения 1 в качестве средств с противогрибковыми свойствами.
Задачей изобретения является расширение арсенала противогрибковых средств по отношению к кандидозу, в частности разработка средства, обладающего выраженной противогрибковой активностью по отношению к candida albicans, низкой токсичностью и превышающего по указанной активности применяемые в медицинской практике препараты.
Поставленная задача достигается применением этилового эфира 2-[(5-(4-метоксифенил)-2-оксофуран-3(2Н)-илиден)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты, который обладает противогрибковой активностью.
Технический результат: получено соединение с высокими выходами, обладающее выраженной противогрибковой активностью, а также низкой токсичностью.
Изобретение иллюстрируется примерами исследования фармакологических свойств.
Пример 1. Получение соединения 1. 4.29 г (0.01 моль) 4-(4-Метоксифенил)-4-оксо-2-[(3-(этоксикарбонил)-4,5,6,7-тетрагидробензо[b]тиофен-2-ил)амино]бут-2-еновой кислоты в 10 мл уксусного ангидрида медленно нагревали до 120°С и перемешивали в течение 60 мин. Полученный раствор охлаждали до 0°С, выпавший осадок отфильтровывали и промывали безводным диэтиловым эфиром. Выход 87%. Тразл.=168-170°С (толуол). Найдено, %: С 66.10, Н 5.03, N 3.67, S 8.44. C21H19NO4S. Вычислено, %: С 66.12, Н 5.02, N 3.67, S 8.41. ИК спектр (ФСМ 1202, вазелиновое масло, ν, см-1): 1607 (C=N), 1715 (COOEt), 1796 (СОлакт). Спектр ЯМР 1Н, (Varian Mercury 300, 300 МГц, DMSOd6), ν, м.д.: 1.40 (т, J 7.1 Гц, 3Н, Me), 1.82 (м, 2Н, СН2), 1.88 (м, 2Н, СН2), 2.75 (м, 2Н, СН2), 2.81 (м, 2Н, СН2), 4.39 (кв, J 7.1, 2Н Гц, CH2O), 6.90 (с, 1Н, HAr), 7.51 (м, J 7.4 Гц, 2Н, HAr), 7.56 (м, J 7.3 Гц, 1Н, HAr), 7.85 (м, J 7.2 Гц, 2Н, HAr). Спектр ЯМР 13С (75 МГц, CDCl3), δ, м.д.: 14.3, 22.3, 22.8, 25.1, 25.8, 61.3, 98.0, 126.6, 127.2, 129.2, 131.7, 132.9, 136.3, 139.3, 145.7, 149.1, 163.0, 164.0, 166.4. Полученное соединение 1 представляет собой насыщенно-красное кристаллическое вещество, растворимое в хлороформе, толуоле, ацетоне, не растворимое в воде и гексане.
Пример 2. Для характеристики противогрибковой активности соединения использовали стандартные параметры: минимальная подавляющая концентрация (МПК), которую определяли модифицированным методом двукратных серийных разведений [МУК 4.2.1890-04 Определение чувствительности микроорганизмов к антибактериальным препаратам] и минимальная бактерицидная концентрация (МБК) [Медицинские лабораторные технологии: Руководство по клинической лабораторной диагностике, п/р Каприщенко, 2013, Т. 2, стр. 407]. Тесты проводили с использованием культуры модельного микроорганизма Candida albicans АТСС 10231 (Всероссийская коллекция патогенных микроорганизмов) на питательной среде Мюллера-Хинтона с добавлением 0,4% глюкозы в 96-луночных полистироловых планшетах. Концентрация микроорганизмов в лунках перед началом культивирования составляла 5*105 КОЕ/мл. Культивирование проводили при 37°С без перемешивания. Определение МПК и высевы для определения МБК производили через 24 ч. Исследуемые соединения растворяли в диметилсульфоксиде (ДМСО) в концентрации 20 мг/мл до полного растворения. Максимальная действующая концентрация составляла 1000 мкг/мл.
Пример 3. Острую токсичность (ЛД50, мг/мл) соединения 1 определяли по методу Г.Н. Першина [Першин Г.Н. Методы экспериментальной химиотерапии // М., С. 100, 109-117 (1971)]. Соединение 1 вводили внутрибрюшинно белым мышам массой 16-18 г в виде взвеси в 2% крахмальной слизи и наблюдали за поведением и гибелью животных в течение 10 суток. Для исследуемого соединения 1 ЛД50 составляет >1500 мг/кг.
Согласно классификации токсичности препаратов соединение 1 относится к V классу практически нетоксичных препаратов [Измеров Н.Ф., Саноцкий И.В., Сидоров К.К. Параметры токсикометрии промышленных ядов при однократном воздействии: Справочник. М., 1977. - с. 196]. Результаты испытаний представлены в таблице:
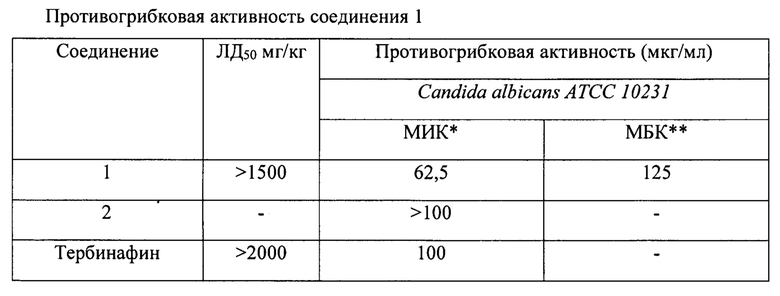

Как видно из таблицы, заявляемое соединение 1 превышает по противогрибковой активности препарат сравнения (тербинафин) в более чем в 1,5 раза по отношению к Candida albicans АТСС 10231, а также показывает низкую токсичность. Таким образом, этиловый эфир 2-[(5-(4-метоксифенил)-2-оксофуран-3(2Н)-илиден)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты 1 проявляет более высокую активность по сравнению со структурным аналогом и эталоном сравнения, что делает возможным ее использование для создания новых лекарственных средств целенаправленного действия.
Изобретение относится к применению этилового эфира 2-[(5-(4-метоксифенил)-2-оксофуран-3(2Н)-илиден)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты формулы 1 в качестве противогрибкового средства. 3 пр.

Применение этилового эфира 2-[(5-(4-метоксифенил)-2-оксофуран-3(2Н)-илиден)амино]-4,5,6,7-тетрагидробензо[b]тиофен-3-карбоновой кислоты 1 формулы:

в качестве противогрибкового средства.
| Asif Husain, M.S.Y | |||
| Khan, S.M | |||
| Hasan, M.M | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| European Journal of Medicinal Chemistry", 2005, No.40, pp.1394-1404 | |||
| (Z)-2((4-R-5-R-3-(ЭТОКСИКАРБОНИЛ)ТИОФЕН-2-ИЛ)АМИНО)-4-ОКСО-4-R-БУТ-2-ЕНОВЫЕ КИСЛОТЫ, ОБЛАДАЮЩИЕ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ | 2019 |
|
RU2722176C1 |
| S | |||
| A | |||
| Shipilovskikha, V | |||
| Y | |||
| Vaganova, R | |||
| R | |||
| Makhmudova "Synthesis and Antinociceptive Activity of | |||
Авторы
Даты
2022-03-15—Публикация
2021-06-29—Подача