Для настоящей заявки испрашивается приоритет Китайской патентной заявки 202010076729.2, поданной 23 января 2020 года и Китайской патентной заявки 20201128639.8, поданной 3 ноября 2020 года, полное содержание которых включено в данный документ посредством ссылки.
Область техники
Изобретение относится к области биомедицины и относится к мишени, имеющей отношение к лечению фиброзирующих заболеваний, и ее применению, в частности к применению Pear1 в качестве мишени в лечении связанных с фиброзом заболеваний, и относится к антителу, направленно воздействующему на Pear1, для лечения связанных с фиброзом заболеваний, и его применению.
Предшествующий уровень техники
Все повреждения органов или тканей будут запускать сложные клеточные и молекулярные реакции, в конечном счете приводящие к фиброзу тканей. Несмотря на то, что такая реакция фиброза тканей может иметь характерное свойство адаптивной регенерации тканей в течение короткого срока, рубец органа или ткани будет возникать, когда фиброз прогрессирует долгое время, что в конечном счете приводит к тканевой и клеточной дисфункции и органной недостаточности. По известным или неизвестным причинам большинство органов и тканей человека, таких как кожа, легкое, печень, сердце, почка, поджелудочная железа, селезенка, нервная система и костный мозг могут становиться фиброзными, что серьезно вредит здоровью человека. Основным патологическим изменением при фиброзе является увеличение соединительных тканей и уменьшение паренхимальных клеток в тканях органов. Непрерывное прогрессирование может вызывать повреждение структуры и нарушение функции, даже вызывать органную недостаточность, и это представляет серьезную угрозу здоровью и жизни человека. Фиброз тканей является основной причиной нетрудоспособности и летальности при многих заболеваниях во всем мире. Почти 45% смертельных случаев от различных заболеваний можно отнести к состояниям гиперплазии тканевых волокон. Основной механизм фиброза органа по существу связан с пролиферацией фибробластов, огромным количеством накопленного внеклеточного матрикса с сопутствующими воспалительными повреждениями и разрушением тканевых структур.
Однако в настоящее время повреждение структуры и нарушение функции фибробластов и внеклеточного матрикса в нормальных тканях не может быть предотвращено или реверсировано. Для данной области крайне необходимо разработать лекарственное средство для улучшения состояния при возникновении, прогрессировании и ухудшении фиброзирующих заболеваний и тем самым восстановления нормальной функции тканей и органов.
Краткое изложение сущности изобретения
Для того чтобы преодолеть недостатки предшествующего уровня техники, в котором не было разработано лекарственное средство для улучшения состояния при возникновении, развитии и ухудшении фиброзирующих заболеваний и тем самым восстановления нормальной функции тканей и органов, согласно настоящему изобретению предложена мишень, а именно Pear1, для лечения фиброзирующего заболевания и ее применение; в частности, предложено антитело, направленно воздействующее на Pear1, для лечения связанных с фиброзом заболеваний.
В первом аспекте настоящего изобретения предложено применение гена, белка Pear1 (эндотелиальный рецептор агрегации тромбоцитов 1) и его агониста в 1) получении лекарственного средства для лечения фиброзирующих заболеваний; 2) получении лекарственного средства для понижающей регуляции и/или ингибирования сигнального пути активации фибробластов; и/или 3) получении лекарственного средства для ингибирования активации фибробластов.
В другом воплощении фиброзирующее заболевание включает в себя фиброз легких, фиброз печени, фиброз сердца, фиброз почек, фиброз костного мозга, рубец на коже и/или фиброз мягких тканей.
В другом воплощении фиброз легких представляет собой идиопатический фиброз легких (IPF). Предпочтительно, фиброз легких дополнительно включает в себя рестриктивное заболевание легких, сопровождающееся фиброзом легких.
В другом воплощении фиброз сердца представляет собой фиброз миокарда, в частности фиброз миокарда после инфаркта миокарда.
В другом воплощении фиброз кожи представляет собой заболевание, при котором нормальные тканевые клетки заменяются фибробластами вследствие травматических факторов на коже или в мягких тканях.
В другом воплощении травматические факторы включают в себя рубцы, образовавшиеся на коже в результате травмы, эмпироза, хирургического вмешательства или пластической хирургии, или келоидные или склеродермические рубцы, образовавшиеся на коже пациентов с рубцовым диатезом, или и т.д.
В другом воплощении агонист представляет собой агонист белка Pear1.
В другом воплощении агонист усиливает экспрессию и/или активность Pear1.
В другом воплощении агонист включает в себя антитело, направленно воздействующее на Pear1, или его вариант, FcεR1α, декстрана сульфат, фукозу или их комбинацию.
В другом воплощении агонист включает в себя антитело, направленно воздействующее на Pear1, или его вариант.
В другом воплощении агонист включает в себя антитело или его вариант согласно второму аспекту настоящего изобретения.
В другом воплощении Pear1 представляет собой ген Pear1 и/или кодируемый им
белок.
В другом воплощении ген Pear1 или кодируемый им белок имеет происхождение от млекопитающего.
В другом воплощении ген Pear1 или кодируемый белок имеет происхождение от человека, мыши, крысы, собаки, обезьяны, верблюда, альпаки или их комбинации.
В другом воплощении ген Pear1 или кодируемый им белок имеет происхождение от человека или мыши.
В другом воплощении сигнальный путь активации фибробластов включает в себя сигнальный путь PI3K/AKT, сигнальный путь MAPK и/или сигнальный путь SMAD.
Согласно второму аспекту настоящего изобретения предложено выделенное антитело или его вариант, направленно воздействующее(ий) на Pear1, где антитело содержит вариабельную область тяжелой цепи и/или вариабельную область легкой цепи; аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи представлены как SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 28 соответственно; аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи представлены как SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно, или аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи представлены как SEQ ID NO: 47, GTS и SEQ ID NO: 48 соответственно, или аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи представлены как SEQ ID NO: 49, DTS и SEQ ID NO: 50 соответственно, или аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи представлены как SEQ ID NO: 51, GAT и SEQ ID NO: 52 соответственно, или аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи представлены как SEQ ID NO: 53, LVS и SEQ ID NO: 54 соответственно.
В другом воплощении вариант представляет собой последовательность с добавлением, делецией или заменой одной-нескольких, предпочтительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, аминокислотных остатков в CDR, FR или полноразмерной последовательности антитела.
В другом воплощении вариант имеет или по существу имеет активность направленного воздействия на Pear1.
В другом воплощении HCDR1 варианта мутирована с S на А или Т в третьей позиции, с G на D в шестой позиции и/или с Р на Т или Y в восьмой позиции аминокислотной последовательности, которая представлена в SEQ ID NO: 26, и/или HCDR2 варианта мутирована с Р на S или G в третьей позиции, с Y на N в четвертой позиции и/или с Т на А в восьмой позиции аминокислотной последовательности, которая представлена в SEQ ID NO: 27, и/или HCDR3 варианта мутирована с А на D в девятой позиции и/или с Y на F в десятой позиции аминокислотной последовательности, которая представлена в SEQ ID NO: 28.
В другом воплощении HCDR1 антитела или его варианта содержит любую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 26, SEQ ID NO: 31, SEQ ID NO: 33, SEQ ID NO: 36 и SEQ ID NO: 39. HCDR2 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 27, SEQ ID NO:30, SEQ ID NO: 34, SEQ ID NO: 37 и SEQ ID NO: 40-44; и HCDR3 содержит любую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 28, SEQ ID NO: 29, SEQ ID NO: 32, SEQ ID NO: 35 и SEQ ID NO: 38; и/или
LCDR 1 антитела или его варианта содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 45, SEQ ID NO: 47, SEQ ID NO: 49, SEQ ID NO: 51 и SEQ ID NO: 53; LCDR2 содержит любую аминокислотную последовательность, выбранную из GAT, SAS, DTS и LVS; и LCDR3 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 46, SEQ ID NO: 48, SEQ ID NO:50, SEQ ID NO: 52 и SEQ ID NO: 54.
В другом воплощении HFR (каркасный участок вариабельной области тяжелой цепи) 1 антитела или его варианта содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 114, SEQ ID NO: 115 и SEQ ID NO: 116. HFR2 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 117, SEQ ID NO: 118, SEQ ID NO: 119, SEQ ID NO:120, SEQ ID NO: 121, SEQ ID NO: 122, SEQ ID NO: 123, SEQ ID NO: 124 и SEQ ID NO: 125; и HFR3 содержит любую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 126, SEQ ID NO: 127, SEQ ID NO: 128, SEQ ID NO: 129, SEQ ID NO:130, SEQ ID NO: 131, SEQ ID NO: 132, SEQ ID NO: 133, SEQ ID NO: 134 и SEQ ID NO: 135; и HFR4 содержит любую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 136 и SEQ ID NO: 137; и/или
В другом воплощении LFR (каркасный участок вариабельной области легкой цепи) 1 антитела или его варианта содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 138, SEQ ID NO: 139, SEQ ID NO:140, SEQ ID NO: 141, SEQ ID NO: 142 и SEQ ID NO: 143. LFR2 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 144, SEQ ID NO: 145, SEQ ID NO: 146, SEQ ID NO: 147, SEQ ID NO: 148 и SEQ ID NO: 149; и LFR3 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 150, SEQ ID NO: 151, SEQ ID NO: 152, SEQ ID NO: 153, SEQ ID NO: 154, SEQ ID NO: 155, SEQ ID NO: 156 и SEQ ID NO: 157; и LFR4 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 158, SEQ ID NO: 159, SEQ ID NO: 160, SEQ ID NO: 161 и SEQ ID NO: 162.
В другом воплощении антитело или его вариант содержит аминокислотные последовательности, которые представлены соответственно:
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 28, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 29, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 30 и SEQ ID NO: 28, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 47, GTS и SEQ ID NO: 48,
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 29, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, DTS и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 40 и SEQ ID NO: 28, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, GAT и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 41 и SEQ ID NO: 28, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, SAS и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 42 и SEQ ID NO: 28, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, LVS и SEQ ID NO: 52; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 26, SEQ ID NO: 43 и SEQ ID NO: 32, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 31, SEQ ID NO: 27 и SEQ ID NO: 32, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 51, GAT и SEQ ID NO: 52; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 31, SEQ ID NO: 37 и SEQ ID NO: 32, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 53, LVS и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3 SEQ ID NO: 31, SEQ ID NO: 34 и SEQ ID NO: 32, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, SAS и SEQ ID NO: 50,
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 31, SEQ ID NO: 30 и SEQ ID NO: 35, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 47, GAT и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 31, SEQ ID NO: 42 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, DTS и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 33, SEQ ID NO: 34 и SEQ ID NO: 35, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 33, SEQ ID NO: 37 и SEQ ID NO: 32, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 53, LVS и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 33, SEQ ID NO: 30 и SEQ ID NO: 35, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 47, GAT и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 33, SEQ ID NO: 42 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, DTS и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 36, SEQ ID NO: 37 и SEQ ID NO: 38, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 53, LVS и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 36, SEQ ID NO: 34 и SEQ ID NO: 32, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, SAS и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 36, SEQ ID NO: 30 и SEQ ID NO: 35, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 47, GAT и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 36, SEQ ID NO: 42 и SEQ ID NO: 28, LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, DTS и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 27 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39 и SEQ ID NO: 32, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, SAS и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 30 и SEQ ID NO: 35, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 47, GAT и SEQ ID NO: 50; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 42 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, DTS и SEQ ID NO: 54; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 37 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 49, GAT и SEQ ID NO: 48; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 40 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 41 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 42 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 43 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46; или
HCDR1, HCDR2 и HCDR3, как представлено в SEQ ID NO: 39, SEQ ID NO: 44 и SEQ ID NO: 28, и LCDR1, LCDR2 и LCDR3, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46.
В другом воплощении аминокислотные последовательности указанной вариабельной области легкой цепи и указанной вариабельной области тяжелой цепи представлены как SEQ ID NO: 16 и SEQ ID NO: l соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 16 и SEQ ID NO: 2 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи соответственно такие представлены в SEQ ID NO: 17 и SEQ ID NO: 3; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 18 и SEQ ID NO: 2 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 19 и SEQ ID NO: 4 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 20 и SEQ ID NO: 5 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 21 и SEQ ID NO: 6 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 23 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 24 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 25 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 23 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 24 и SEQ ID NO соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 25 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 23 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 24 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 25 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 22 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 23 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 24 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 25 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 22 и SEQ ID NO: 11 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 22 и SEQ ID NO: 12 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 22 и SEQ ID NO: 13 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 14 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 15 соответственно.
В другом воплощении вариант имеет идентичность 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% с аминокислотной последовательностью антитела.
В другом воплощении антитело представляет собой полноразмерное антитело, Fab, Fab', F (ab') 2, Fv, такой как scFv, биспецифическое антитело, мультиспецифическое антитело, или однодоменное антитело, или моноклональное антитело или поликлональное антитело, производное от антитела.
В другом воплощении антитело или его вариант представляет собой полноразмерное антитело, и константная область тяжелой цепи полноразмерного антитела выбрана из константной области тяжелой цепи hIgG1, hIgG2, hIgG3, hIgG4 и производной от них последовательности.
В другом воплощении константная область легкой цепи антитела выбрана из к-цепи или %-цепи или производной от них последовательности.
В другом воплощении производная последовательность константной области тяжелой цепи содержит последовательность с добавлением, делецией или заменой одного-нескольких, предпочтительно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10, аминокислотных остатков, в константной области тяжелой цепи hIgG1, hIgG2, hIgG3 или hIgG4.
В другом воплощении константная область тяжелой цепи константной области тяжелой цепи имеет идентичность 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% с константной областью тяжелой цепи hIgG1, hIgG2, hIgG3 или hIgG4.
В другом воплощении константная область тяжелой цепи полноразмерного антитела представляет собой константную область тяжелой цепи hIgG3 или hIgG4 или производную от них последовательность.
В другом воплощении производная последовательность представляет собой аминокислотную последовательность, имеющую замену 1-2 аминокислот в константной области тяжелой цепи hIgG1, hIgG2, hIgG3 или hIgG4.
В другом воплощении производная последовательность представляет собой мутацию hIgG4 S228P.
В другом воплощении константная область легкой цепи представляет собой κ-цепь человека.
Согласно третьему аспекту настоящего изобретения предложена выделенная нуклеиновая кислота, кодирующая любое антитело или его вариант согласно второму аспекту настоящего изобретения.
Согласно четвертому аспекту настоящего изобретения предложен рекомбинантный экспрессионный вектор, содержащий выделенную нуклеиновую кислоту согласно третьему аспекту настоящего изобретения.
Согласно пятому аспекту настоящего изобретения предложен трансформант, содержащий выделенную нуклеиновую кислоту согласно третьему аспекту настоящего изобретения или рекомбинантный экспрессионный вектор согласно четвертому аспекту настоящего изобретения.
В другом воплощении хозяином трансформанта является прокариотическая клетка или эукариотическая клетка.
В другом воплощении прокариотическая клетка включает в себя Е coli.
В другом воплощении эукариотическая клетка включает в себя дрожжи, такие как Saccharomyces cerevisiae, Pichia pastoris, Aspergillus или Trichoderma или их комбинацию.
Согласно шестому аспекту настоящего изобретения предложено лекарственное средство, содержащее антитело или его вариант согласно второму аспекту настоящего изобретения.
В другом воплощении лекарственное средство представляет собой фармацевтическую композицию.
В другом воплощении фармацевтическая композиция дополнительно содержит фармацевтически приемлемый носитель.
В другом воплощении фармацевтическая композиция содержит один или более агонистов Pear1.
В другом воплощении фармацевтическая композиция дополнительно содержит один или более из Fc εR1α, декстрана сульфата, фукозы, аптамера и имеющего небольшую молекулу соединения в качестве агонистов Pear1; более предпочтительно FcεR1α, декстрана сульфат или фукозу.
В другом воплощении фармацевтическая композиция содержит антитело, направленно воздействующее на Pear1, как описано выше, где антитело включает в себя полноразмерное антитело, Fab, Fab', F (ab ') 2, Fv, такой как scFv, биспецифическое антитело, мультиспецифическое антитело, однодоменное антитело, или моноклональное или поликлональное антитело, полученное из антитела, как оно описано выше; предпочтительно дополнительно содержит FcεR1α, декстрана сульфат, фукозу, аптамер и имеющее небольшую молекулу соединение; или содержит антитело, направленно воздействующее на Pear1, как описано выше, и это антитело включает в себя полноразмерное антитело, Fab, Fab', F (ab ') 2, Fv, такой как scFv, биспецифическое антитело, мультиспецифическое антитело, однодоменное антитело, или моноклональное антитело или поликлональное антитело, полученное из антитела, предпочтительно дополнительно содержит FcεR1α, декстрана сульфат, фукозу, аптамер и имеющую небольшую молекулу соединение; более предпочтительно, включает введение FcεR1α, декстрана сульфата или фукозы.
Согласно седьмому аспекту настоящего изобретения предложено применение антитела или его варианта согласно любому из второго аспекта настоящего изобретения, или трансформанта согласно пятому аспекту настоящего изобретения, или лекарственного средства согласно шестому аспекту настоящего изобретения в 1) получении лекарственного средства для лечения фиброзирующих заболеваний; 2) получении лекарственного средства для понижающей регуляции и/или ингибирования сигнального пути активации фибробластов; и/или 3) получении лекарственного средства для ингибирования активации фибробластов.
В другом воплощении фиброзирующее заболевание включает в себя фиброз легких, фиброз печени, фиброз сердца, фиброз почек, фиброз костного мозга, рубец на коже и/или фиброз мягких тканей.
В другом воплощении фиброз легких дополнительно включает в себя рестриктивное заболевание легких, сопровождающееся фиброзом легких.
В другом воплощении фиброз кожи включает в себя заболевание, при котором нормальные тканевые клетки заменяются фибробластами из-за травматических факторов в коже или мягких тканях.
В другом воплощении различные факторы дополнительно включают одно или более из: инфекция, травма, медикаментозная терапия, облучение, инородные тела или иммунная гиперфункция.
Согласно восьмому аспекту настоящего изобретения предложен нетерапевтический способ ингибирования активации клеток-фибробластов in vitro, включающий стадии добавления гена Pear1, его продукта экспрессии или его агониста к культивированным фибробластам, тем самым ингибируя активацию фибробластов.
В другом воплощении активация фибробластов включает в себя эпителиально-мезенхимальный перенос фибробластов и замену нормальных тканевых клеток.
В другом воплощении ген Pear1, его белок или его агонист имеет концентрацию 0,001 нМ-1M.
Согласно девятому аспекту настоящего изобретения предложен способ введения антитела или его варианта согласно второму аспекту настоящего изобретения или лекарственного средства согласно шестому аспекту настоящего изобретения нуждающемуся индивидууму или объекту для лечения фиброзирующих заболеваний.
В другом воплощении согласно изобретению предложено применение антитела или его варианта согласно любому из второго аспекта, трансформанта согласно пятому аспекту изобретения или лекарственного средства согласно шестому аспекту изобретения в 1) лечении фиброзирующих заболеваний; 2) понижающей регуляции и/или ингибировании сигнальных путей активации фибробластов; и/или 3) ингибировании активации фибробластов.
В другом воплощении нуждающийся индивидуум или объект представляет собой индивидуум или объект, который имеет фиброзирующее заболевание.
В другом воплощении нуждающийся индивидуум или объект представляет собой индивидуум или объект, который страдает или страдал пневмонией, гепатитом, нефритом, инфарктом миокарда, хирургическим вмешательством и/или травмой, обусловленной различными факторами.
В другом воплощении вводимая или применяемая композиция включает в себя композицию для ингаляции, композицию для местного введения, композицию для парентерального введения или их комбинацию.
В другом воплощении композиция для ингаляции включает в композицию для пульверизации, композицию в форме спрея, капли в нос, порошка или их комбинацию.
В другом воплощении композиция для парентерального введения включает в себя композицию в форме капли, геля, эмульсии, мази, пластыря, пленки, инъекции или их комбинации.
В другом воплощении парентеральное введение включает в себя местное введение, инсталляцию, инъекцию или их комбинацию, например подкожную инъекцию.
Согласно десятому аспекту изобретения предложен способ конструирования гуманизированной трансгенной по Pear1 животной модели, включающий стадию замены гена Pear1 животного геном Pear1 человека.
В другом воплощении способ включает в себя стадии (1) выбора экзона гена Pear1 животного; (2) проведения гомологичной рекомбинации по экзону гена Pear1 животного, заменяя тем самым ген Pear1 животного геном Pear1 человека.
В другом воплощении животное представляет собой млекопитающее, не являющееся человеком.
В другом воплощении животное включает в себя мышь, крысу, кошачьих, собачьих, обезьяну, верблюда, альпаку или их комбинацию.
В другом воплощении экзон гена Pear1 представляет собой один или более экзонов 4-6 гена Pear1 мыши.
В другом воплощении способ включает в себя стадии (1) проектирования мишени вблизи экзона 1-ATG мышиной кодирующей области и замены гена Pear1 мыши в присутствии матрицы для гомологичной рекомбинации.
В другом воплощении добавление сигнала терминации транскрипции SV40 polyA после кДНК Pear1 человека, обеспечивая тем самым полную замену транскриптов Pear1 мыши на кДНК Pear1 человека, и размещение гена Pear1 человека после промотора гена Pear1 мыши, обеспечивая тем самым нормальную экспрессию гена Pear1 человека в каждой ткани и каждом органе мыши.
Предпочтительно, способ дополнительно включает в себя (3) стадию определения, успешно ли сконструирована гуманизированная мышь: амплификацию гена Pear1 человека праймерами и определение успешного конструирования, если ген Pear1 человека может быть амплифицирован; более предпочтительно, праймеры являются такими, как представлено в SEQ ID NO: 110-113.
Согласно одиннадцатому аспекту изобретения предложена также гуманизированная трансгенная по Pear1 мышиная модель.
Согласно двенадцатому аспекту настоящего изобретения предложено применение гуманизированной трансгенной по Pear1 мышиной модели по одиннадцатому аспекту настоящего изобретения в скрининге/оценке лекарственного средства для лечения заболеваний, связанных с Pear1 человека.
Согласно тринадцатому аспекту настоящего изобретения предложено применение гуманизированной трансгенной по Pear1 мышиной модели по одиннадцатому аспекту настоящего изобретения в оценке лечебного эффекта лекарственного средства, направленно воздействующего на Pear1 человека в животной модели.
Согласно четырнадцатому аспекту изобретения предложен способ скрининга агониста Pear1, включающий стадии (1) добавления или не добавления молекул-кандидатов в систему культивирования фибробластов тестируемой группы или контрольной группы соответственно; (2) сравнения активации фибробластов в тестируемой группе и контрольной группе; и (3) подтверждения, что молекула-кандидат является агонистом Pear1, если активация фибробластов в тестируемой группе значительно ниже, чем в контрольной группе.
В другом воплощении активация фибробластов означает, что соотношение количеств (А1) эпителиально-мезенхимального переноса в тестируемой группе и количеств (А0) фибробластов в контрольной группе составляет по меньшей мере более 1,2, или по меньшей мере более 1,5, или по меньшей мере более 2,0-10,0.
В другом воплощении активация фибробластов означает, что соотношение количеств (Е1) внеклеточного матрикса фибробластов в тестируемой группе и количеств (Е0) внеклеточного матрикса фибробластов в контрольной группе составляет по меньшей мере более 1,2, или по меньшей мере более 1,5, или по меньшей мере более 2,0-10,0.
Согласно пятнадцатому аспекту настоящего изобретения предложен способ скрининга кандидата-лекарственного средства, направленно воздействующего на Pear1, для лечения фиброзирующих заболеваний, включающий стадии (1) получения гуманизированной трансгенной по Pear1 животной модели согласно одиннадцатому аспекту настоящего изобретения или гуманизированной трансгенной по Pear1 животной модели, полученной способом согласно десятому аспекту настоящего изобретения; (2) индуцирования симптомов фиброзирующего заболевания у животных из стадии (1); (3) введения молекулы-кандидата животным стадии (2); и (4) наблюдения облегчения фиброзирующего заболевания у животного, определяя тем самым, является ли молекула-кандидат лекарственным средством, направленно воздействующим на Pear1, для лечения фиброзирующих заболеваний.
В другом воплощении животное представляет собой млекопитающее, не являющееся человеком.
В другом воплощении стадии (2) и (3) можно менять местами.
В другом воплощении индуцирование включает в себя одно или более из лекарственного индуцирования, химического индуцирования, индуцирования облучением.
В другом воплощении индуцирование осуществляют блеомицином. Согласно изобретению предложено антитело, направленно воздействующее на Pear1, и его (Fab) 2, Fab фрагмент или FcR1, декстрана сульфат, фукоза, аптамер или имеющее небольшую молекулу соединение.
Согласно изобретению предложена фармацевтическая композиция. Фармацевтическая композиция содержит антитело, направленно воздействующее на Pear1, и его (Fab) 2, Fab фрагмент или FcR1, декстрана сульфат, фукозу, аптамер или имеющее небольшую молекулу соединение.
Согласно изобретению предложено применение Pear1 в качестве мишени в ингибировании активации фибробластов, лечении фиброза легких, рестриктивных заболеваний легких, сопровождающихся фиброзом легких, и других связанных с фиброзом заболеваний, стимулировании регенерации повреждений и/или заживления ран.
Согласно изобретению предложено применение антитела, направленно воздействующего на Pear1, и его (Fab) 2, Fab фрагмента или FcR1, декстрана сульфата, фукозы, аптамера или имеющего небольшую молекулу соединения в ингибировании активации фибробластов, лечении фиброза легких, рестриктивных заболеваний легких, сопровождающихся фиброзом легких, и других связанных с фиброзом заболеваний, стимулировании регенерации повреждений и/или заживления ран.
Согласно изобретению предложен способ направленного воздействия на Pear1 для ингибирования активации фибробластов, лечения фиброза легких, рестриктивных заболеваний легких, сопровождающихся фиброзом легких, и других связанных с фиброзом заболеваний, стимулировании регенерации повреждений и/или заживления ран. Способ включает в себя введение антитела, направленно воздействующего на Pear1, и его (Fab) 2, Fab фрагмента или FcR1, декстрана сульфата, фукозы, аптамера или имеющего небольшую молекулу соединения нуждающемуся индивидууму.
В другом воплощении введение включает в себя ингаляционное введение, легочную пульверизацию, местную инъекцию, трансдермальное всасывание, подкожную инъекцию или местное нанесение.
Следует иметь в виду, что в рамках объема настоящего изобретения вышеуказанные технические признаки настоящего изобретения и технические признаки, конкретно описанные ниже (например, в воплощениях), можно комбинировать с любыми другими с образованием нового или предпочтительного технического решения. Это не будет повторяться в данном документе ввиду ограниченного объема настоящего изобретения.
Краткое описание графических материалов
ФИГ. 1. Делеция гена Pear1 индуцирует снижение функции легких старых мышей, а) Стратегия конструирования мыши с нокаутом гена Pear1. b) Уровень экспрессии Pear1, обнаруженный в эксперименте методом иммунноблоттинга, и результат показывает, что белок Pear1 полностью утерян у мыши с нокаутом Pear1. с) Делеция гена Pear1 индуцирует значительное снижение форсированной жизненной емкости (FVC) и объем форсированного выдоха за 0,1 секунды (FEV 0,1) у старых мышей, d) Делеция гена Pear1 вызывает значительное накопление легочных коллагеновых компонентов у мышей.
ФИГ. 2. Делеция гена Pear1 усугубляет фиброз легких мышей, индуцированный блеомицином. а) Делеция гена Pear1 увеличивает уровень смертности индуцированных блеомицином мышей. b) Делеция гена Pear1 увеличивает потерю массы тела индуцированных блеомицином мышей, с) Делеция гена Pear1 явно усугубляет снижение форсированной жизненной емкости и объема форсированного выдоха за 0,1 секунды (FEV 0,1) индуцированной блеомицином мыши, d) Делеция гена Pear1 значительно усиливает накопление коллагеновых компонентов в легких у индуцированных блеомицином мыши.
ФИГ. 3. Pear1 регулирует активацию фибробластов и синтез внеклеточного матрикса посредством эпителиально-мезенхимального перехода (ЕМТ) фибробластов. а) Делеция Pear1 оказывает очевидное влияние на увеличение доли легочных фибробластов (CD140 а+) и уменьшение доли эпителиальных клеток (CD326+) у индуцированных блеомицином мышей, но мало влияет на клетки CD45+ и эндотелиальные клетки (CD31+). b) Pear1 в значительной степени экспрессируется на мышиных легочных фибробластах, культивированных in vitro, с) Иммуноблоттинг подтверждает, что Pear1 экспрессируется на легочных фибробластах. d) Экспрессия гена на легочных фибробластах у индуцированной блеомицином мыши в анализе RNA-SEQ (секвенирование РНК); и делеция Pear1 явно стимулируют эпителиально-мезенхимальный переход легочных фибробластов у индуцированной блеомицином мыши, е) qPCR (количественная полимеразная цепная реакция) также подтверждает, что делеция Pear1 явно способствует синтезу белков внеклеточного матрикса легочными фибробластами у индуцированной блеомицином мыши.
ФИГ. 4. Делеция Pear1 может в значительной степени стимулировать внутриклеточные сигналы, опосредованные трансформацией рецепторов фактора роста β (TGFβ), рецепторов тромбоцитарного фактора роста (PDGF) и рецепторов фактора роста фибробластов (FGF). Делеция Pear1 может в значительной степени стимулировать опосредованное рецептором TGF(3 фосфорилирование и фосфорилирование SMAD2/3 и ERK1/2, JNK, Р38; стимулировать опосредованное рецептором PDGF фосфорилирование ERK1/2, JNK, Р38 и фосфорилирование Akt; стимулировать опосредованное рецептором FGF фосфорилирование ERK1/2, JNK, Р 38 и фосфорилирование Akt.
ФИГ. 5. Активированный Pear1 ингибирует белки внеклеточного матрикса, экспрессированные фибробластами. FcεR1α, декстрана сульфат и фукоза способны ингибировать экспрессию внеклеточного матриксного гена периостина (Postn), Col5a3 и Timp1 легочных фибробластов человека.
ФИГ. 6. Сравнение аффинности антител к Pear1 человека. Планшет для ELISA покрывали белками ECD (внеклеточный домен) Pear1 человека и проводили реакции между антителами в разных концентрациях (2000 нг/мл, 1000 нг/мл, 500 нг/мл, 250 нг/мл, 125 нг/мл, 62,5 нг/мл, 31,25 нг/мл, 15,625 нг/мл, 7,8125 нг/мл, 3,90625 нг/мл, 1,953125 нг/мл, 0,9765625 нг/мл) и белками ECD Pear1 человека. Определяли значение OD (оптическая плотность) для получения значения ЕС 50 для комбинации антиген-антитело.
ФИГ. 7. Антитело к Pear1 человека явно вызывает регрессию индуцированного блеомицином процесса фиброза легких у гуманизированной трансгенной по Pear1 мыши, а) Стратегия конструирования гуманизированной трансгенной по Pear1 мыши. b) Лизат легочных фибробластов мыши получали и тестировали в отношении уровней экспрессии Pear1 мыши и Pear1 человека методом иммуноблоттинга. Результат показывает, что гуманизированная трансгенная по Pear1 мышь была успешно сконструирована.
ФИГ. 8. Моноклональное антитело к Pear1 человека ингибирует экспрессию белков внеклеточного матрикса в фибробластах человека из различных тканей, а) Моноклональное антитело LF2 ингибирует почечные фибробласты человека, экспрессирующие белки внеклеточного матрикса. b) Моноклональное антитело LF2 ингибирует сердечные фибробласты человека, экспрессирующие белки внеклеточного матрикса. с) Моноклональное антитело LF2 ингибирует печеночные фибробласты человека, экспрессирующие белки внеклеточного матрикса. d) Моноклональное LF2 антитело ингибирует фибробласты кожи человека, экспрессирующие белки внеклеточного матрикса.
Подробное описание
Благодаря обширным и интенсивным исследованиям авторы изобретения неожиданно обнаружили, что ген Pear1 и его белок экспрессируются в фибробластах и играют ключевую роль в фиброзирующих заболеваниях. Конкретно, по сравнению с мышами дикого типа у мыши с нокаутом гена Pear1, сконструированной автором изобретения, существенно усугублялись индуцированные блеомицином симптомы фиброза легких и снижение функции легких. Кроме того, авторы изобретения также продемонстрировали в патологии, что делеция гена Pear1 может в значительной степени способствовать эпителиально-мезенхимальному переходу фибробластов, способствовать способности фибробластов синтезировать внеклеточный матрикс, тем самым заставляя нормальные органы и ткани презентировать состояние избыточной соединительной ткани и вызывая фиброз легких. Более важно, авторы изобретения продемонстрировали, что активация Pear1 может снижать синтез внеклеточного матрикса фибробластами, снижать симптомы фиброза и даже реверсировать фиброз.
Авторы изобретения также исследовали влияние гена Pear1 на связанный с фиброзирующим заболеванием сигнальный путь. Эксперименты доказывают, что делеция гена Pear1 может приводить к повышающей регуляции связанного с фиброзом сигнального пути, о котором сообщается в предшествующем уровне техники, включая одно или более из повышающей регуляции сигнального пути PI3K/AKT, сигнального пути MAPK и сигнального пути SMAD. Следовательно, делеция гена Pear1 приводит к повышающей регуляции связанных с фиброзом сигнальных путей и играет ключевую роль в сбалансировании сверхактивации фибробластов, высвобождения внеклеточного матрикса и образования/разрушения клеточного матрикса.
Базируясь на вышеуказанном исследовании, авторы изобретения сконструировали антитела, направленно воздействующие на Pear1, в качестве агониста. Было доказано, что антитела по настоящему изобретению или их варианты имеют выраженную функцию активации Pear1, модулирования связанных с фиброзным заболеванием путей передачи сигналов (в частности, понижающей регуляции одного или более из сигнального пути PI3K/Akt, сигнального пути MAPK и сигнального пути SMAD) и превосходный противофиброзный эффект, а также демонстрируют важность Pear1 при фиброзных заболеваниях с другой точки зрения.
Настоящее изобретение осуществлено исходя из вышеуказанного.
Термины
В данном документе, если конкретно не указано иное, формы единственного числа включают в себя форму множественного числа определяемых объектов.
Используемый в данном документе термин "по существу" означает присущую неопределенность, которая может быть отнесена к любым количественным сравнениям, значениям, измерениям или в других формах. Термин "по существу" также относится к количественной оценке или степени упоминаемого изменения, которая не приведет к изменению основной функции обсуждаемого предмета изобретения. Например, "по существу имеет активность направленного воздействия на активацию Pear1" означает, что антитела способны взаимодействовать с Pear1, например объединяться с белком Pear1 и ингибировать сигнальные пути активации фибробластов в разной степени. Согласно данным о взаимосвязи между Pear1 и активацией фибробластов специалист в данной области способен получить агонист Pear1 стандартными методами и с использованием скрининговой модели по настоящему изобретению.
Используемый в данном документе термин "антитело или его вариант" относится к белку, фрагменту антитела или полипептидной последовательности из молекулы иммуноглобулина, которая специфически связывается с антигеном. Антитело может представлять собой поликлональное или моноклональное, многонитевое или однонитевое антитело или интактный иммуноглобулин, и может иметь происхождение из природных источников или рекомбинантных источников. В одном воплощении "антитело или вариант" по настоящему изобретению выделен(о) и имеет происхождение из рекомбинантного источника.
Используемый в данном документе термин "фрагмент антитела" относится к по меньшей мере участку антитела, который сохраняет способность специфически взаимодействовать с антигеном (например, путем связывания, стерического затруднения, стабилизации/дестабилизации, пространственного распределения). Примеры фрагментов антитела включают, но без ограничения, Fab, Fab', F(ab')2, Fv фрагмент, scFv фрагмент антитела, связанный дисульфидной связью FVS (sdFV), Fd фрагмент, состоящий из VH и СН1 доменов, линейные антитела, однодоменные антитела, мультиспецифические антитела, образованные фрагментами антитела (например, бивалентные фрагменты из двух Fab фрагментов, связанных дисуфидными связями в шарнирной области) и выделенные CDR или другие эпитопсвязывающие фрагменты. Антигенсвязывающий фрагмент может быть также встроен в однодоменное антитело, максимальное антитело, микро-антитело, нано-антитело, внутриклеточное антитело, биспецифическое антитело и химерное антитело.
Используемый в данном документе термин "производная последовательность" относится к новой последовательности после добавления, делеции или консервативной замены одной или более (например, не более 10) аминокислот первоначальной последовательности антитела/белка/полипептида; и/или к новой последовательности после модификации первоначальной последовательности антитела/белка/полипептида без изменения или по существу без изменения активности первоначального антитела/белка/полипептида. Консервативные замены, как правило, общеизвестны специалистам в данной области, например:
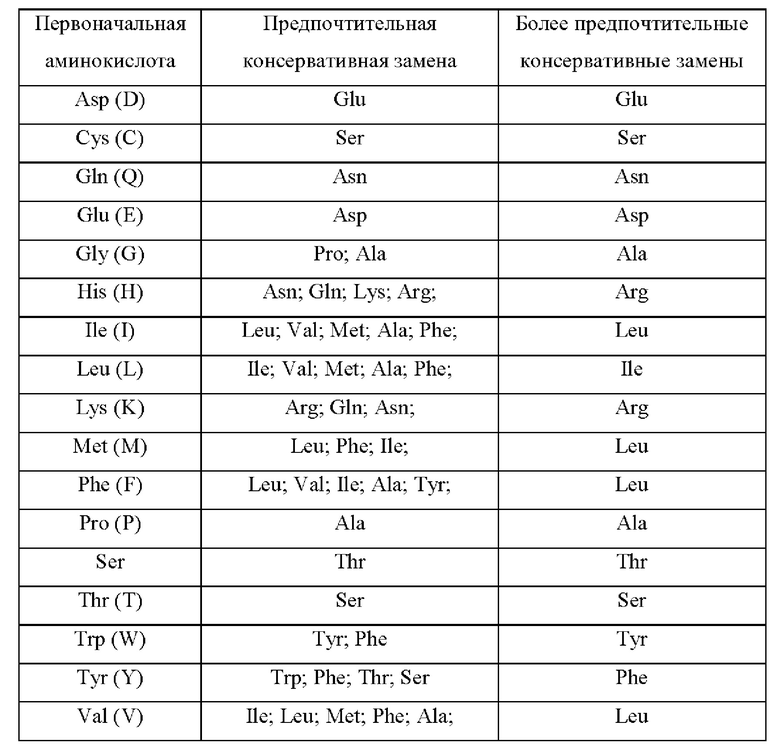
Используемый в данном документе термин "нуклеиновая кислота" или "полинуклеотид" относится к однонитевой или двухнитевой форме дезоксирибонуклеиновой кислоты (ДНК) или рибонуклеиновой кислоты (РНК) и их полимеру. Если конкретно не указано иное, конкретная нуклеиновокислотная последовательность также предусматривает ее вариант (например, замена вырожденного кодона), аллель, прямой гомолог, SNP (однонуклеотидный полиморфизм) и комплементарную последовательность, и четко определенную последовательность.
Используемые в данном документе термины "экспрессионный вектор" и "рекомбинантный экспрессионный вектор" могут быть использованы взаимозаменяемым образом и относятся к вектору, содержащему рекомбинантный полинуклеотид, который содержит последовательность контроля экспрессии, функционально связанную с нуклеотидной последовательностью, которая должна быть экспрессирована. Экспрессионный вектор содержит достаточно унодействующих элементов для экспрессии; другие элементы для экспрессии могут быть предоставлены клеткой-хозяином или в in vitro экспрессионной системе. Экспрессионные векторы включают все векторы, известные в данной области, в том числе те, которые встроены в рекомбинантные космиды, плазмиды (например, "голые" или в липосомах) и вирусы (например, лентивирусы, ретровирусы, аденовирусы и аденоассоциированные вирусы).
Используемые в данном документе термины "сигнальный путь" и "путь передачи сигналов" могут быть использованы взаимозаменяемым образом и относятся к биохимической связи между множеством молекул сигнальной трансдукции, которые передают сигнал от одной части клетки к другой части клетки, которая должна быть функциональной. Термин "рецептор клеточной поверхности" охватывает молекулы и молекулярные комплексы, способные получать сигналы и передавать сигналы через клеточную мембрану.
Используемый в данном документе термин "специфически связываются" относится к антителу или лиганду, который распознает и связывается с белком-партнером связывания (например, Pear1), присутствующим в образце, но антитело или лиганд по существу не идентифицирует или связывает другие молекулы в образце.
Используемые в данном документе термины "субъект" и "объект" могут быть использованы взаимозаменяемым образом и относятся к живому организму (например, млекопитающему, такому как мышь, крыса, кошачьи, собачьи, овца, верблюд, обезьяна, альпака или человек), у которого может быть индуцирован иммунный ответ.
Используемые в данном документе термины "эффективное количество", "безопасное эффективное количество" или "терапевтически эффективное количество" могут быть использованы взаимозаменяемым образом и относятся к количеству вещества, препарата, лекарственного средства или фармацевтической композиции, которое эффективно обеспечивает конкретный биологический результат и имеет приемлемую побочную реакцию у субъекта, как описано в данном документе. Например, специалист в данной области, такой как опытный клиницист, может скорректировать "безопасное эффективное количество" в соответствии с субъектом.
Используемый в данном документе термин "направленная активация" ("направленное воздействие на активацию") относится к молекуле, подлежащей тестированию, которая оказывает активирующее воздействие на ген, белок или активность мишени, осуществляя тем самым повышающую регуляцию его экспрессии или активности. Как правило, "направленная активация" может быть определена одним или более методами, такими как количественное определение экспрессии, определение уровней активности, пути нисходящего влияния или секреции гена или его белка.
Используемый в данном документе термин "лечение" ("проведение лечения" или "лечить") относится к облегчению или регрессии прогрессирования, тяжести и/или продолжительности фиброзирующего заболевания или ослаблению одного или более симптомов (предпочтительно, одного или более четко выраженных симптомов) фиброзирующего заболевания путем введения одного или более терапевтических средств (например, одного или более терапевтических агентов, таких как агонисты или антитела или их варианты).
Объем: В всем описании изобретения различные аспекты изобретения могут быть представлены в форме диапазонов. Следует иметь в виду, что описание в форме диапазонов дано для удобства и краткости и не должно толковаться как ограничивающее объем изобретения. Соответственно, описание диапазонов следует рассматривать как конкретное раскрытие всех возможных субдиапазонов и индивидуальных числовых значений в пределах этого диапазона. Например, описание диапазона, такое как от 1 до 6, следует считать конкретно раскрывающим такие субдиапазоны, как 1-3, 1-4, 1-5, 2-4, 2-6, 3-6 и т.д., а также индивидуальные числовые значения в пределах этого диапазона, такие как 1, 2, 2,7, 3,4, 5, 5,3 и 6. В качестве другого примера, диапазон, такой как имеющий идентичность 95-99%, включает в себя диапазон идентичности 95%, 96%, 97%, 98% или 99%, включая субдиапазоны, такие как идентичность 96-99%, 96-98%, 96-97%, 97-99%, 97-98% и 98-99%. Это применимо независимо от ширины диапазона.
Фиброзирующее заболевание
Используемый в данном документе термин "фиброзирующее заболевание" относится к заболеванию, которое возникает в результате чрезмерной или аномальной активации фибробластов вследствие повреждений нормальной ткани или клетки, регенерации ткани или органа, инициированной фибробластами, в результате эпителиально-мезенхимального перехода фибробластов, повышенного синтеза внеклеточного матрикса, замещения нормальных тканей рубцовой тканью и утери функции нормальных тканей.
Как правило, поскольку фибробласты широко распределены в различных нормальных тканях, в случае, если нормальные тканевые клетки повреждены, может быть индуцирована чрезмерная или аномальная активация фибробластов, такая как значительный фиброз легких, фиброз печени или фиброз почек после воспаления легких, печени или почек; или такая как пролиферативные рубцы на коже, мышце или соединительной ткани, вызванные хирургическим вмешательством, травмой или т.п.; или фиброз миокарда после инфаркта миокарда и миелофиброз, ассоциированный с миелопролиферативными заболеваниями и т.д. Указано, что "фиброзирующее заболевание" представляет собой "рубец", который распространяется по органам или тканям всего организма и вызван чрезмерной или аномальной активацией фибробластов из-за повреждения нормальных тканей, и этот рубец непосредственно ограничивает первоначальные нормальные функции органов и тканей.
С точки зрения механизма, фиброзирующее заболевание характеризуется миграцией фибробластов (FB) в рану и/или пролиферацией и массивной агрегацией внеклеточного матрикса, сопровождающейся воспалительными повреждениями и повреждениями структуры тканей. Следовательно, FB играют очень важную роль в протекании фиброзных заболеваний. FB являются основными клеточными компонентами в соединительных тканях и дифференцируются из мезенхимальных клеток в эмбриональном периоде. Фибробласт может также существовать в форме фиброцита, который находится в его зрелом и покоящемся состоянии. Фибробласты и фиброциты могут превращаться друг в друга в определенных условиях. Кроме того, известно, что FB могут преобразовываться из эпителиальных клеток, макрофагов, кровяных мононуклеарных клеток, эндотелиальных клеток и других нормальных клеток посредством эпителиально-мезенхимального перехода (ЕМТ), и эти процессы транс дифференциации могут представлять собой важный режим генерации FB при фиброзирующих заболеваниях.
В физиологических условиях FB синтезируют и высвобождают компоненты внеклеточного матрикса (ЕСМ) для формирования тканей, поддержания морфологии органов и физиологических функций, и используются в регенерации после повреждения тканей. При патологических состояниях FB могут трансформироваться в активированные фибробласты посредством аномальной пролиферации и могут синтезировать и секретировать массивные белки ЕСМ, вызывая тем самым образование избыточных соединительных тканей и фиброз органов. Кроме того, уровень ЕСМ дополнительно регулируется и контролируется установлением равновесия между расщепляющим его ферментом, а именно матриксной металлопротеиназой (ММП), и тканевым ингибитором матриксной металлопротеиназы (TIMPS). В физиологическом состоянии синтез и расщепление ЕСМ в легких находятся в равновесии; в то время как во время протекания процесса фиброза легких равновесие в системе MMP/TIMP нарушается, и ЕСМ чрезмерно накапливается, образуя рубцовую структуру, которая является ключевым фактором развития фиброза. Это указывает на то, что FB, а также равновесие MMP/TIMPS играют важную роль в фиброзирующих заболеваниях.
Фиброз легких
Фиброз легких является наиболее распространенным и самым тяжелым фиброзным заболеванием и относится к легочным заболеваниям, вызываемым аномальной активацией фибробластов и образованием рубцов, вызываемым аномальной регенерацией повреждения альвеолярной ткани. Фиброз легких, который характеризуется в основном сухим кашлем и прогрессирующей одышкой, серьезно ухудшает дыхательную функцию организма человека. Повреждение легких усугубляется с развитием заболевания, и снижение дыхательной функции пациента сохраняется. Основные причины смерти включают в себя острое обострение дыхательной функции и связанные с этим осложнения.
Причина фиброза легких у большинства пациентов не известна, и поэтому его называют идиопатической интерстициальной пневмонией. Тип заболевания, охарактеризованного как фиброз легких, в числе идиопатической интерстициальной пневмонии называется идиопатическим фиброзом легких (IPF). Непрерывное диффузное альвеолярное воспаление и нарушение альвеолярной структуры при IPF приводят к легочному интерстициальному фиброзу с образованием постоянных рубцов, и функция легких необратимо снижается. В конечном итоге это приводит к дыхательной недостаточности и становится причиной смерти пациентов. IPF обычно встречается у людей среднего или пожилого возраста, в частности в мужских группах от 50 до 70 лет. Статистика сообщает, что распространенность среди всего населения каждый год составляет около (2-29)/10 миллионов, и тенденция роста увеличивается примерно на 11% из года в год. Причина IPF не ясна и в настоящее время считается связанной с факторами окружающей среды или применением химиотерапевтических лекарственных средств. Острый приступ также может быть вызван повторными инфекциями, вызванными вирусами, бактериями, грибками, паразитами и тому подобным. Кроме того, аутоиммунные заболевания, такие как красная волчанка и другие аутоиммунные заболевания, являются одной из причин заболевания. Прогноз IPF неблагоприятный, медианный срок выживаемости больного составляет 2-3 года, 5-летняя выживаемость ниже 30%, в связи с чем его называют "опухолеподобным заболеванием".
Поскольку IPF прогрессирует непредсказуемо, его довольно трудно лечить. Лечение IPF в основном включает в себя нелекарственную терапию, включая отказ от курения, кислородотерапию, искусственную вентиляцию легких, паллиативное лечение и обучение реабилитации легких и т.д.; и лекарственную терапию, включая гормональную терапию, кислотоподавляющую терапию, лечение N-ацетилцистеином и т.п. Хотя глюкокортикоиды применяются для лечения фиброза легких более 50 лет, последние исследования доказывают, что они эффективны только у 20% пациентов, а длительное применение глюкокортикоидов может вызвать тяжелые побочные реакции. Кроме того, мета-анализ результатов исследований показал, что однократное применение N-ацетилцистеина не может снизить смертность пациента от болезни или улучшить значения изменения форсированной жизненной емкости (FVC) или качество жизни. В последние годы FDA (Управление по контролю за качеством пищевых продуктов и лекарственных средств США) один за другим одобрило противоопухолевые лекарственные средства пирфенидон и нинтеданиб в качестве орфанных лекарственных средств для лечения IPF, причем пирфенидон представляет собой обладающее множественным действием соединение пиридина, имеющее небольшую молекулу, с противовоспалительным, антифиброзным и антиокислительным свойствами. Пирфенидон может существенно уменьшать скорость снижения жизненной емкости форсированного выдоха. После непрерывного введения пирфенидона в течение 52 недель снижение индекса функции легких пациента может быть замедлено, выживаемость без прогрессирования (PFS) пациента продлевается, и риск смерти пациента уменьшается, но побочные эффекты включают фоточувствительность, слабость, сыпь, дискомфорт в желудке и анорексию. Нинтеданиб является многоцелевым низкомолекулярным ингибитором тирозинкиназы, и нинтеданиб позволяет значительно снизить абсолютное значение падения FVC у больного IPF и в определенной степени облегчить болезненный процесс. Хотя и нинтеданиб, и пирфенидон могут снижать скорость ухудшения функции легких и улучшать качество жизни пациентов, они подходят только для замедления скорости ухудшения функции легких пациентов, но не для улучшения показателей дыхательной системы. Таким образом, они применимы только к пациентам с IPF с легкой и умеренной легочной дисфункцией и не могут применяться у пациентов с тяжелой IPF. Кроме того, пирфенидон нельзя применять у пациентов с почечной дисфункцией, а нинтеданиб нельзя применять у пациентов с дисфункцией печени, что еще больше ограничивает применение этих двух лекарственных средств.
Фиброзы других органов
Фиброз печени представляет собой патологический процесс, вызываемый регенерацией поврежденной печени. Аномальная пролиферация звездчатых клеток в соединительных тканях (т.е. печеночных фибробластов) и большое количество секретированного внеклеточного матрикса, обусловленное повреждениями печени, являются основными причинами. Долговременный фиброз печени может развиться в цирроз печени, высокое давление в воротной вене, рак печени и т.п.
Фиброз миокарда относится к рубцам, образовавшимся в результате аномальной пролиферации миокардиальных фибробластов и образования огромного количества внеклеточного матрикса, индуцированного некрозом клеток миокарда. Фиброз миокарда будет приводить в результате к ригидности миокарда, расширению сердца и вызывать аритмию, сердечную недостаточность и т.п.
Фиброз почек относится к рубцам, образовавшимся в результате аномального отложения внеклеточного матрикса (ЕСМ) фибробластами соединительной ткани почек вследствие повреждения почечных клеток, вызванного травмой, инфекцией, нарушением кровотока, иммунным воспалительным ответом и т.д., и приводящего в результате к склерозу почечной паренхимы и утрате функции.
Фиброз костного мозга представляет собой заболевание, вызванное аномальным отложением внеклеточного матрикса (ЕСМ) тканей волокон костного мозга, и является типом миелопролиферативного заболевания, серьезно поражающего гематопоэтическую функцию.
Образование рубцов на коже или рубцов мягких тканей обусловлено огромным количеством ЕСМ, продуцированного и отложенного фибробластами, мигрировавшими из соединительных тканей кожи в раненные участки кожи или мягких тканей. Аномальное образование рубцов может затруднять заживление хронических ран и вызывать фиброз. Как правило, все причины повреждения кожи или мягких тканей, такие как хирургическое вмешательство, травма, эмпироз, локальное или диффузное воспаление (т.е. аутоиммунные заболевания, склеродермия и т.д.) могут приводить к аномальным рубцам или избыточным соединительным тканям мягких тканей.
Ген Pear1 или его белки
Pear1, эндотелиальный рецептор агрегации тромбоцитов 1 (Gene ID: 375033), представляет собой трансмембранный белок I типа, 150 кДа, и является членом семейства рецепторных белков, содержащих множественные эпидермальный фактор роста-подобные домены (MEGF). Pear1 человека содержит 1037 аминокислот (АА), включающих сигнальную последовательность из 20 АА, внеклеточный домен (ECD) из 735 АА, трансмембранную область из 21 АА и цитоплазматическую область из 261 АА. Pear1 экспрессируются у всех млекопитающих и имеют высокое сходство. Например, сходство между Pear1 человека и Pear1 мыши (Gene ID II: 73182) составляет 84%.
Сначала было обнаружено, что Pear1 экспрессируется в эндотелиальных клетках сосудов и тромбоцитах. Когда тромбоцит напрямую контактирует с другим тромбоцитом, рецепторы Pear1 на поверхности тромбоцитов соединяются с потенциальным лигандом на контактирующей поверхности тромбоцитов в другой фазе через его домен EMI, приводя тем самым к внутриклеточному сигналу и активации тромбоцитов. Однако в последние годы в литературе сообщалось, что однонуклеотидный полиморфизм Pear1 может быть не напрямую связан с активностью тромбоцитов человека. За исключением того, что Pear1 в основном связан с процессом активации тромбоцитов, сообщается, что Pear1 имеет функцию регуляции неоваскуляризации и устранения мертвых нейронов. Таким образом, из приведенных выше исследований видно, что Pear1 может выполнять совершенно разные биологические функции в разных тканях и органах.
В то же время авторы изобретения впервые обнаружили, что помимо экспрессии в сосудистых эндотелиальных клетках, что подтверждено в настоящее время, Pear1 также экспрессируется в фибробластах и оказывает отрицательное регуляционное воздействие на активацию фибробластов.
В результате нокаутирования гена Pear1 у мыши и конструирования гуманизированной трансгенной по гену Pear1 мыши и тому подобного стало ясно, что делеция гена Pear1 может приводить к повышающей регуляции одного или более описанных сигнальных путей, связанных с фиброзом (включая повышающую регуляцию одного или более путей, включающих сигнальный путь PI3K/AKT, сигнальный путь MAPK и сигнальный путь SMAD), и в результате к повышающей регуляции сигнального пути активации фибробластов. Можно видеть, что ген Pear1 играет ключевую роль в активации фибробластов, высвобождении клеточного матрикса и уравновешивании продуцирования/расщепления клеточного матрикса.
Поэтому с использованием Pear1 в качестве мишени конструируется антитело, способное усиливать активность Pear1 настолько, чтобы ингибировать чрезмерную активацию фибробластов, достигая тем самым цели лечения фиброзирующих заболеваний.
Сигнальный путь активации клеток волокон
Известно, что фибробласты регулируются внутриклеточными сигналами, опосредованными различными цитокинами через их рецепторы. Эти сигнальные пути этих активированных фибробластов включают в основном трансформированный опосредованный рецептором фактора роста бета (TGFβ) сигнальный путь SMAD и сигнальный путь MAPK (включая сигнальный путь ERK1/2, JNK, Р38); опосредованный рецептором тромбоцитарного фактора роста (PDGF) сигнальный путь MAPK (включая сигнальный путь ERK1/2, JNK, Р38) и сигнальный путь PI3K/AKT; опосредованный рецептором фактора роста фибробластов (FGF) сигнальный путь MAPK (включая сигнальный путь ERK1/2, JNK, Р38) и сигнальный путь PI3K/AKT и т.д.
Эти пути являются клеточными сигнальными путями, которые в значительной степени присутствуют in vivo и играют важную роль в пролиферации и дифференцировке клеток. Например, сигнальный путь TGF-J3 играет существенную роль в раннем эмбриональном развитии и образовании тканевых органов, иммунизации, регенерации тканей и сбалансировании гомеостаза. В качестве другого примера, сигнальные пути MAPK содержат в основном четыре расположенных ниже по ходу сигнальных молекулы: ERK1/2, JNKS, P38S и ERK5. ERK1/2, JNKS, P38S и ERK5 являются близкородственными в процессах иммунитета и воспаления, клеточной дифференцировки, апоптоза, пролиферации и т.п. Кроме того, сигнальный путь PI3K/AKT может регулировать пролиферацию, дифференцировку и апоптоз клеток и играет решающую роль в миграции, адгезии клеток, ангиогенезе и синтезе и секреции внеклеточного матрикса. Существующие лекарственные средства или большинство исследуемых обладают эффектом ингибирования активации сигнальных путей; такой как нинтеданиб, разрешенный для лечения фиброза легких, может ингибировать как рецептор фактора роста эндотелия сосудов (VEGFR), указанный сигнальный путь MAPK и сигнальный путь PI3K/Akt, опосредованный рецептором тромбоцитарного фактора роста (PDGFR), так и сигнальный путь рецептора фактора роста фибробластов (FGFR), а также вызывает серьезные системные побочные эффекты.
Авторы изобретения доказывают экспериментами, что ген Pear1 напрямую связан с вышеуказанными сигнальными путями, что отличается от эффекта непосредственного ингибирования или понижающей регуляции активации путей у известных лекарственных средств. Авторы изобретения определяют эффекты отрицательной регуляции гена Pear1 или его белка на указанные сигнальные пути, то есть активации этих сигнальных путей может способствовать нокаутирование Pear1, и агонист Pear1 может частично осуществлять понижающую регуляцию активации этих сигнальных путей, тем самым регулируя аномальную активацию фибробластов, лечить или улучшать состояние при фиброзных заболеваниях.
Агонист и лекарственные средства
Используемые в данном документе термины "агонист", "агонист Pear1" или "агонист гена Pear1 или его белка" могут быть использованы взаимозаменяемым образом и относятся к веществам, способным усиливать активность гена Pear1 или его белка, и/или связывать белок Pear1, и/или содействовать Pear1 в ингибировании сигнальных путей активации сигнального пути фибробластов, и/или снижать высвобождение ЕСМ из фибробластов. В дополнение к известному агонисту Pear1, согласно настоящему изобретению предложено новое антитело, которое специфически связывается с Pear1.
Предпочтительно, агонист, предусмотренный настоящим изобретением, представляет собой агонист, который способен связываться с геном Pear1 или его белком и вызывать структурное изменение Pear1, тем самым ингибируя активацию фибробластов. Предпочтительно, указанный агонист представляет собой агонист, который направленно воздействует на белок Pear1 и связывается с белком Pear1, экспрессированным на фибробластах.
В предпочтительном воплощении, в дополнение к антителу по настоящему изобретению, агонист по настоящему изобретению может также содержать вещество, известное в данной области, которое обладает функцией активирования Pear1, такое как FcεR1α (т.е. Fc-фрагмент рецептора IgE Ia), декстрана сульфат, фукоза или их комбинация, и может также включать в себя природный аптамер к Pear1 и/или имеющее небольшую молекулу соединение, более предпочтительно FcεR1α, декстрана сульфат и фукозу, которые могут в значительной степени ингибировать ЕСМ, синтезируемый легочными фибробластами, улучшать легочную функцию и увеличивать выживаемость.
Используя Pear1 в качестве мишени по настоящему изобретению, специалист в данной области сможет разработать множество разных агонистов, направленно воздействующих на Pear1, включая, но без ограничения, имеющие небольшую молекулу агонисты, антитела или их активные фрагменты, микроРНК и т.п. В настоящем изобретении имеющее небольшую молекулу соединение может также относиться к встречающемуся в природе или искусственно разработанному имеющему небольшую молекулу агонисту к рецептору Pear1.
В настоящем изобретении аптамер относится к скрининговой технологии in vitro: систематическая эволюция лигандов путем экспоненциального обогащения (SELEX). Полученная структурированная олигонуклеотидная последовательность (РНК или ДНК) имеет высокую способность распознавания и высокую аффинность к соответствующим молекулам-мишеням (белки, вирусы, бактерии, клетки, ионы тяжелых металлов и т.п.).
Согласно изобретению также предложено лекарственное средство, содержащее безопасное и эффективное количество антитела по изобретению или его варианта. Лекарственное средство по настоящему изобретению может также представлять собой фармацевтическую композицию, содержащую один или более агонистов Pear1. В другом воплощении фармацевтическая композиция содержит антитело по настоящему изобретению, направленно воздействующее на Pear1, или его вариант, такой как F(ab)2 и Fab фрагмент антитела, FcεR1α, декстрана сульфат, фукозу, аптамер или имеющее небольшую молекулу соединение.
В другом воплощении лекарственное средство представляет собой фармацевтическую композицию, т.е. дополнительно содержит фармацевтически приемлемый носитель или эксципиент.Фармацевтически приемлемый носитель по настоящему изобретению может быть использован для сохранения структуры и функции агониста по настоящему изобретению и облегчения его применения. Специалист в данной области может выбирать и комбинировать согласно потребностям. Такие носители включают, но без ограничения, физиологический раствор, буфер, глюкозу, воду, глицерин, этанол и их комбинации.
Агонисты, антитела и их варианты и лекарственное средства и/или фармацевтические композиции, содержащие их, можно вводить (доставлять) нуждающимся субъектам различными путями, включающими, но без ограничения, ингаляцию, местное введение и/или парентеральное введение.
В предпочтительном воплощении специалист в данной области может определить тип препарата, подлежащего введению, согласно пути введения, например включая ингаляционное введение, местное введение, парентеральное введение или их комбинацию. Препарат для ингаляционного введения включает препарат для пульверизации, препарат-спрей, капли в нос, порошок или их комбинацию. Препарат для местного введения и/или препарат для парентерального введения включает каплю, гель, эмульсию, мазь, пластырь, пленку, инъекцию или их комбинацию. В предпочтительном воплощении лекарственное средство можно вводить различными путями, такими как местное нанесение, инсталляция, внутримышечная инъекция, местная инъекция и т.д.
Антитело или его вариант
Согласно настоящему изобретению предложено антитело или его вариант, которое(ый) специфически связывается с белком Pear1 /направленно воздействует на белок Pear1. Предпочтительно, антитела или их варианты по изобретению представляют собой мышиные моноклональные антитела и могут представлять собой рекомбинантные, поликлональные, многоцепочечные или одноцепочечные антитела или интактный иммуноглобулин. Предпочтительно, антитела по изобретению или их варианты являются гуманизированными. Предпочтительно, антитела по изобретению представляют собой химерные антитела. Предпочтительные антитела по изобретению или их варианты представлены в Таблицах 3.2, 3.3, 4 и 5.
Антитело, направленно воздействующее на Pear1, включает в себя полноразмерное антитело и фрагмент антитела (такой как Fab', Fab', F(ab')2, Fv, такой как scFv), а также включает в себя биспецифическое антитело, мультиспецифическое антитело, однодоменное антитело или моноклональное антитело или поликлональное антитело, полученное из этого антитела.
В настоящем изобретении Fab-фрагмент антитела также называется фрагментом связывания с антигеном и относится к домену в структуре антитела, который связывается с антигеном. Fab-фрагмент состоит из полной легкой цепи и VH и СН1 домена тяжелой цепи. Под действием папаина антитело может распадаться на два Fab-фрагмента и Fc-фрагмент.
FR фрагмента Fab, которая может быть использована в антителе по изобретению или его варианте, конкретно не ограничена; предпочтительно, в настоящем изобретении используются FR IgG4 человека и многие мутантные последовательности FR. Результат показывает, что изменение последовательности FR практически не влияет на связывание антигена и антитела. Можно видеть, что фрагменты CDR антитела по настоящему изобретению обладают превосходной способностью специфически и стабильно связываться с белком Pear1. Специалист в данной области в состоянии использовать антитела по настоящему изобретению или их варианты согласно идее использовать Pear1 в качестве мишени по настоящему изобретению и его релевантности в отношении фиброзирующих заболеваний, и использовать множество известных в настоящее время FR для скрининга сконструированного антитела, тем самым получая антитело, имеющее активность, согласующуюся или по существу согласующуюся с активностью антител по настоящему изобретению или их вариантов, и это также входит в объем настоящего изобретения.
Константные области, которые могут быть использованы в антителах или их вариантах по настоящему изобретению, конкретно не ограничены. Специалист в данной области в состоянии произвести скрининг фрагмента константной области, подходящего для антитела, содержащего антитело или его вариант, согласно идее использовать Pear1 в качестве мишени настоящего изобретения и его релевантности в отношении фиброзирующих заболеваний, тем самым получая полное антитело, имеющее активность, согласующуюся или по существу согласующуюся с активностью антитела или его вариантов по настоящему изобретению.
Способ лечения
Согласно изобретению предложен способ лечения фиброзных заболеваний. Способ включает в себя введение нуждающемуся индивидууму или субъекту антитела по изобретению или его варианта или лекарственного средства по изобретению. В другом воплощении способ лечения представляет собой лечения фиброза легких, рестриктивных заболеваний легких, сопровождающихся фиброзом легких. Способ включает в себя, но без ограничения, введение антител по изобретению или их вариантов или лекарственного средства по изобретению пульверизацией.
В другом воплощении способ лечения представляет собой способ лечения фиброза кожи и мягких тканей. Способ включает в себя, но без ограничения, введение антител по изобретению или их вариантов таким путем, как местная инъекция, наружное нанесение, покрытие, инфильтрация, транс дермальная аппликация или т.п. Предпочтительно, например, рубец на коже образовался после процессов лечения травмы, эмпироза, хирургических вмешательств или пластической хирургии и т.п., или келоид, склеродерма и т.п.образовались в коже субъектов с рубцовым диатезом. Способ также подходит для регенерации поврежденной ткани или органа и/или заживления раны.
В другом воплощении способ лечения представляет собой способ лечения фиброза печени, сердца или почек. Способ включает в себя, но без ограничения, введение антитела по изобретению или его варианта или содержащего его лекарственного средства таким путем, как местная инъекция, нанесение, инфильтрация или т.п.
Время введения антитела или его варианта или лекарственного средства по изобретению конкретно не ограничено, предпочтительно немедленно после возникновения фиброза. Антитело или его вариант или лекарственное средство по изобретению также можно вводить совместно с другим системным или местным применением, и порядок введения конкретно не ограничен.
Трансгенная по гену Pear1 человека животная модель и способ скрининга лекарственных средств
Согласно изобретению дополнительно предложена новая модель для скрининга и идентификации лекарственных средств против фиброза. Авторы изобретения заменили ген Pear1 мыши геном Pear1 человека путем гомологичной рекомбинации, основанной на обнаружении корреляции между геном Pear1 и его белком и фиброзирующим заболеванием, и таким образом получили модель. Следует иметь в виду, что согласно данным настоящего изобретения специалист в данной области также может сконструировать других трансгенных животных, у которых произведена замена на ген Pear1 человека другими разными способами, и использовать трансгенное животное в качестве модели для исследования фиброзного заболевания и скрининга лекарственных средств против фиброза.
Кроме того, согласно изобретению также предложен способ скрининга лекарственных средств, например способ скрининга агониста Pear1. Способ позволяет исследовать действие кандидата-агониста Pear1 в системе культивирования фибробластов, используя Pear1 в качестве мишени, и его воздействие на фибробласты. Когда ясна корреляция между активацией Pear1, механизмом эпителиально-мезенхимального перехода фибробластов и высвобождением внеклеточного матрикса фибробластами, агонист Pear1 может быть отсеян способом скрининга лекарственных средств. Разумеется, способ осуществления оценки фармакодинамики с использованием трансгенной животной модели по настоящему изобретению также охвачен, то есть введение кандидата-агониста Pear1 трансгенной по Pear1 животной модели по изобретению, установка контроля и подтверждение потенциального агониста Pear1, когда симптомы фиброза у животного ослабляются. Симптомы фиброза включают, но без ограничения, структурные и функциональные изменения, которые имеют место в таких частях или органах, как легкие, сердце, почки, костный мозг, кожа, мягкие ткани и т.д. Указанные структурные и функциональные изменения могут быть определены специалистами в данной области техники (например, экспериментирующим персоналом или клиницистами) с учетом состояния различных частей или органов.
Настоящее изобретение дополнительно подробно описано нижеследующими воплощениями и графическими материалами. Объем защиты настоящего изобретения не ограничивается нижеследующими воплощениями. Вариации и преимущества, ожидаемые специалистом в данной области, могут быть охвачены изобретением как не выходящие за рамки замысла и объема изобретения, и объем защиты определен в прилагаемой формуле изобретения. Как правило, соблюдаются обычные условия, такие как в Sambrook et al. Molecular Cloning: A Laboratory Manual (New York: Cold Spring Harbor Laboratory Press, 2002), или условия, предложенные производителем
Экспериментальные материалы и методы
1. Реагент, получение антитела и клеточная линия
Моноклональные антитела к Pear1 мыши и к Pear1 человека были получены в лаборатории путем иммунизации нокаутных мышей и мышей BALB/c человеческим внеклеточным доменом соответственно. Высокоаффиные моноклональные гибридомные клетки получали по стандартной технологии слияния клеток селезенки мыши и клеток миеломы мыши, и затем гибридомные клетки инъецировали иммунодефицитным мышам для получения асцита. Асцит очищали шариками с белком A/G, и полученное антитело использовали для соответствующих экспериментов. Белок FcεR1α с его меткой был приобретен в R&D Corporation. Полипептид синтезирован GL Biochem (Shanghai) Co. Ltd. Фибробласты легких человека, фибробласты кожи человека, сердечные фибробласты, почечные фибробласты и печеночные фибробласты приобретены в клеточной библиотеке АТСС (Американская коллекция типовых культур).
2. Измерение функции легких мыши
Мышей анестезируют интраперитонеальной инъекцией пентобарбитала (100 мг/кг), и каждую мышь соединяют с контролируемым компьютером дыхательным аппаратом для мелких животных через воздухопроводный шланг согласно описанию системы для анализа функции легких AniRes2005 (BestLab version 2.0, AniRes2005, China) производителя. Изменение давления в плетизмографической камере измеряют через порт в соединительной трубке датчиком давления для определения форсированной жизненной емкости (FVC) и объема форсированного выдоха за 0,1 секунды (FEV 0,1) в качестве показателя функции легких.
3. Выделение и культура первичных мышиных легочных фибробластов
Этот метод включает в себя следующие стадии: Свежие ткани легких индуцированных блеомицином и не индуцированных мышей измельчали и затем подвергали энзимолизу в течение 2 часов в культуральной среде DMEM/F12 (содержащей 100 ед./мл коллагензы типа I, 2,5 мг/мл коллагеназы IV, 0,3 мг/мл гиалуронидазы и 0,1 мг/мл ДНКазы). После добавления 2% бычьего сывороточного альбумина ферментационную суспензию центрифугировали при 800 об/мин. Затем осадок суспендировали в культуральной среде DMEM/F12 с 10% фетальной бычьей сыворотки и культивировали в чашке для культивирования клеток при 37°С с 5% СО2 в течение 2 суток. Первичные мышиные легочные фибробласты в экспериментах представляют собой клетки 2-3 поколений.
4. Конструирование плазмиды и экспрессия белка
Конструировали плазмиды сверэкспрессии Pear1 –рсДНК3.1 человека и мыши с FLAG-маркером и his-меткой, плазмиды трансфицировали в клетки 293S с PEI, и клетки 293S культивировали в суспензии, не содержащей сыворотку. Надосадочную жидкость экстрагировали, и белок очищали на никелевой колонке.
5. Проточная цитометрия
В эксперименте с проведением анализа методом проточной цитометрии использовали свежую ткань легких. Выполняли приготовление мышиных одиночных клеток легких путем измельчения и ферментирования свежего мышиного легкого и собирали одиночные клетки мышиного легкого с помощью клеточного фильтра и центрифуги. Долю каждой клеточной популяции анализировали путем инкубирования с флуоресцентно-меченым антителом к CD45, CD31, CD326, CD140a и Pear1. Все эксперименты методом проточной цитометрии проводили с использованием Aria III на общей технической платформе в Shanghai Jiao Tong University (Шанхайский университет Цзяо Тун), и анализ методом проточной цитометрии проводили с использованием программного обеспечения FlowJo.
6. Окрашивание гематоксилином и эозином (НЕ) и окрашивание по Массону Легкое и печень мыши фиксировали в 4% параформальдегиде в течение 48 часов.
После заделки в парафин для нарезки срезов использовали полуавтоматическую роторную резательную машину (Leica; rm2235 и cm1950), депарафинизацию проводили при комнатной температуре, для регидратации использовали градиентный этанол, затем осуществляли окрашивание НЕ и окрашивание по Массону.
7. Анализ методами RNA-seq и биоинформатики
Общую мРНК экстрагировали из мышиных легочных CD140+ фибробластов с использованием раствора Trizol (hivitrogen, Carlsbad, Calif.) согласно стандартным экспериментальным методам. Анализ методами RNA-SEQ (секвенирование РНК) и биоинформатики, дифференциальную идентификация экспрессии генов (DEG), анализ сигнального пути, анализ представленности генов (GSEA) выполняли с использование! общей технической сервисной платформы Shanghai Jiao Tong University School о Medicine (Медицинская школа Шанхайского университета Цзяо Тун). 8. Количественная PCR в режиме реального времени
Общую мРНК экстрагировали из фибробластов в соответствии со стандартным] протоколами с использованием раствора Trizol (mvitrogen, Carlsbad, Calif.] Комплементарную ДНК синтезировали обратной транскрипазой (Takara). Экспрессии генов детектировали прибором ABI 7000 Real-Time PCR (Life Technologies] Последовательности праймеров для PCR (полимеразная цепная реакция, ПЦР перечислены в Таблице 1. Человеческую глицерилальдегид-3-фосфонатдегидрогеназ; (Gapdh) или ген 18 сРНК использовали в качестве контроля.
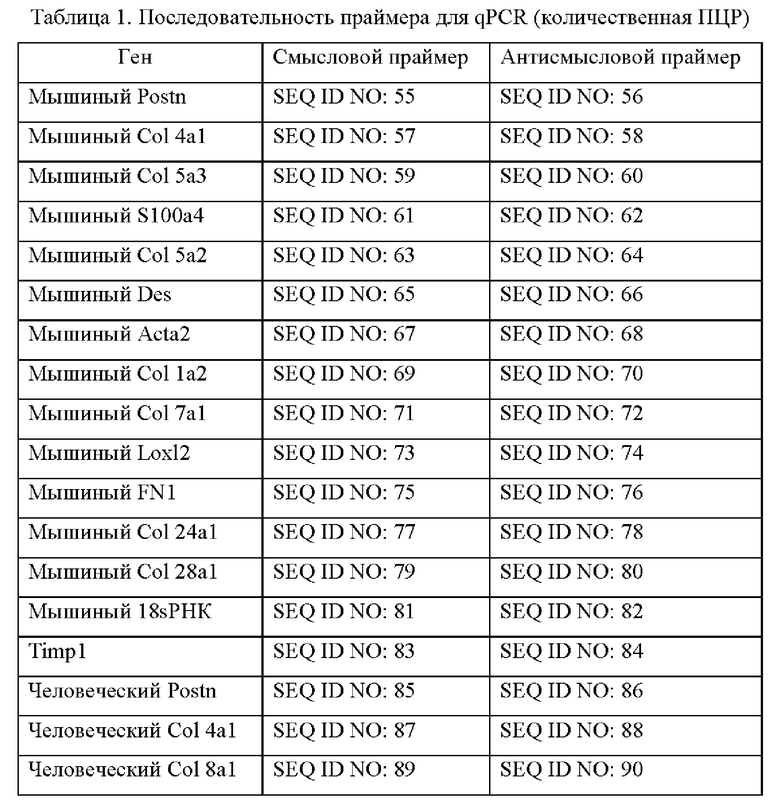
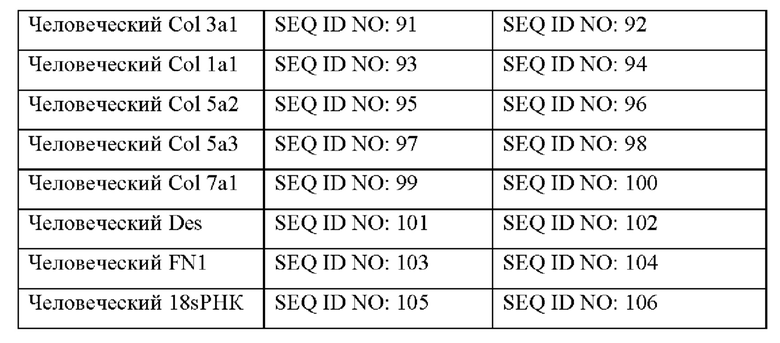
9. Статистический метод
Все данные подвергали статистическому анализу с использованием программного обеспечения SPSS 13.0 для Windows. Двусторонний t-критерий Стьюдента использовали для двух совокупностей данных. Анализ Каплана-Мейера использовали для анализа выживаемости. При всех сравнениях данных считалось, что значение Р менее 0,05 имеет статистическую значимость.
Пример 1. Конструирование мышей с нокаутом гена Pear1
Мышь с нокаутом гена Pear1 (мышь с делецией гена Pear1) конструируют по технологии генного нокаута First-Knockout technology. Стратегия конструирования показана на ФИГ. 1а, где фрагмент IRES (содержащий репортерный ген lacZ и один управляемый промотором neo) вставляют в интрон исходного гена, тем самым разрушая функцию гена Pear1. Мышиные генотипы идентифицируют с использованием общепризнанных в данной области PCR-методов. Как показано в последовательности из Таблицы 2, прямой праймер (Pear1-F) предусмотрен в области экзона 6 гена Pear1, и обратный праймер предусмотрен в области вставочного фрагмента Frt (Pear1 KO-R) или в области интрона 6 (Pear1 WT-R) для амплификации KO полосы или WT полосы соответственно. В данном изобретении использовали 8-10-недельных мышей, и мышей кормили в специфических беспатогенных условиях (SPF). Использование мышей одобрено Комитетом по этике Shanghai Jiao Tong University School of Medcine. Конструкционная диаграмма показана на ФИГ. 1a. Данные вестерн-блоттинга подтвердили, что белок у мышей с нокаутом гена Pear1 был полностью удален (ФИГ. 1b). 
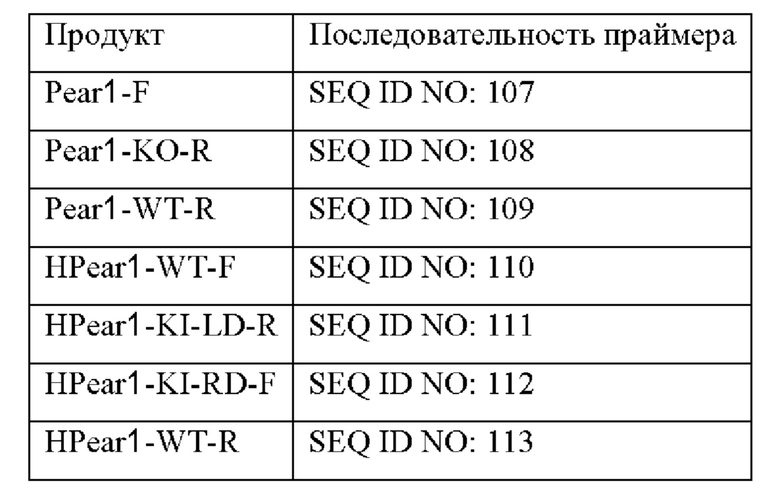
Pear1 -F, Pear1 -KO-R и Pear1 -WT-R используют для идентификации генотипа мышей с нокаутом Pear1. HPEAR-1-WT-F, Н Pear1-KI-LD-R, Н Pear1-KI-RD-F и Н Pear1-WT-R используют для идентификации генотипа гуманизированных по Pear1 мышей.
Пример 2. Влияние делеции Pear1 на функцию легких мышей
Определяют функцию легких мыши с нокаутом гена Pear1 из Примера 1. В первую очередь изобретение сравнивает функцию легких и отложение коллагена старых мышей дикого типа (WT) и старых мышей с нокаутом гена Pear1.
Результаты показывают, что утрата Pear1 явно вызывает снижение форсированной жизненной емкости (FVC) и количество объема форсированного выдоха (FEV 0,1) за 0,1 секунды у 12-месячных мышей (смотри ФИГ. 1c). FVC и FEV являются важными показателями функции легких. Среднее значение FVC и FEV0.1 у контрольных 12-месячных мышей дикого типа (WT) составляет 0,56 и 0,78, а среднее значение FVC и FEV 0,1 у 12-месячных мышей с нокаутом гена Pear1 составляет 0,79 и 0,69 (р <0,1), и поэтому дыхательная функция старых мышей с нокаутом гена Pear1 значительно хуже, чем дыхательная функция контрольных мышей WT.
Иммуногистохимический эксперимент доказывает, что мышь с нокаутом гена Pear1 имеет коллагеновые компоненты (смотри ФИГ. 1D). Окрашивание по Массону является классическим методом окрашивания коллагена, и коллаген может окрашиваться в зеленый цвет; следовательно, состояние отложения коллагена может быть отражено процентом площади зеленых зон; коэффициент отложения коллагена у 12-месячных мышей WT составляет 3%, а доля отложения коллагена у мышей с нокаутом гена Pear1 составляет 7%, что явно превышает отложение коллагена у контрольных мышей дикого типа (WT).
Результаты показывают, что у старых мышей с делецией Pear1 может развиваться спонтанный фиброз тканей легких с поражением дыхательной функции.
Пример 3: Конструирование мышиной модели фиброза легких и выявление влияния делеции Pear1 на фиброз у мыши.
3. Способ конструирования мышиной модели фиброза легких
Блеомицин представляет собой многокомпонентный комплексный антибиотик, обладающий противоопухолевым действием, и одним из его токсических и побочных эффектов является то, что он вызывает фиброз легких. Блеомицин вводят в трахею мыши, чтобы вызвать фиброз легких у мыши, и поскольку патологические гистологические изменения наиболее близки к фиброзу легких человека, мышиная модель является общепризнанной для индуцирования фиброза легких.
В этом эксперименте мышиную модель фиброза легких конструируют путем введения 2 мкг/г блеомицина впрыскиванием в трахею самцам мышей WT (в возрасте 8-12 недель) и мышам с нокаутом Pear1 из Примера 1 для индуцирования повреждения легких соответственно.
3.2. Выявление влияния делеции Pear1 на фиброз у мышей
Определено, что смертность мышей с нокаутом гена Pear1 намного выше, чем выживаемость контрольных мышей дикого типа (WT) за период наблюдения 21 сутки. Выживаемость контрольных мышей дикого типа (WT) составляет 0,6, тогда как выживаемость контрольных мышей дикого типа (WT) составляет 0,6 после 15 суток индуцирования блеомицином, тогда как выживаемость мышей с нокаутом гена Pear1 составляет только 0,2.
Делеция Pear1 способствует потере массы тела индуцированной блеомицином мыши (смотри ФИГ. 2b). Массу тела мышей измеряли с использованием электронных весов на 7, 14 и 21 сутки после индуцирования блеомицином. Вес мышей дикого типа снижается с первоначальных 26 г (сутки 0) до 23,5 г (сутки 7), 22,5 г (сутки 14), 21,5 г (сутки 21), тогда как вес мышей с нокаутом гена Pear1 снижается с 26 г (сутки 0) до 22 г (сутки 7), 20,5 г (сутки 14), 17,5 г (сутки 21).
Делеция Pear1 значительно усугубляла снижение форсированной жизненной емкости и объем форсированного выдоха за 0,1 секунды у мышей, индуцированных блеомицином (смотри ФИГ. 2с). Средние значения FVC и FEV0,1 у выживших контрольных мышей дикого типа (WT) составляли 0,56 и 0,49, тогда как средние значения FVC и FEV 0,1 у мышей с нокаутом гена Pear1 составляли 0,47 и 0,41 (Р <0,01) соответственно. Так что дыхательная функция у мышей с нокаутом гена значительно хуже, чем дыхательная функция у контрольных мышей дикого типа.
Иммуногистохимический эксперимент доказывает, что мышь с нокаутом гена Pear1 имеет больше коллагеновых компонентов (смотри ФИГ. 2d). Окрашивание по Массону является классическим методом окрашивания коллагена, и коллаген может окрашиваться в зеленый цвет; следовательно, состояние отложения коллагена может быть выражено через процент площади зеленой зоны; и относительный показатель отложения коллагена у мышей дикого типа на 21 сутки после индуцирования блеомицином составляет 25%, а доля отложения коллагена у мышей с нокаутом гена Pear1 составляет 48%, что намного выше, чем у контрольных мышей дикого типа (WT).
Согласно результату эксперимента делеция Pear1 может в значительной степени способствовать фиброзу легких мыши, индуцированный блеомицином, функция легких заметно снижается, отложение коллагена сильно увеличивается, и очевидно, что смертность увеличивается.
Пример 4. Pear1 регулирует активацию фибробластов и синтез внеклеточного матрикса в результате эпителиально-мезенхимального перехода
После 21-суточного индуцирования блеомицином контрольных мышей дикого типа (WT) и мышей с нокаутом гена Pear1 подвергали промывке перфузией PBS (забуференный фосфатами физиологический раствор), легкое извлекали и затем ферментировали в одноклеточную суспензию коллагеназой. При определении методом проточной цитометрии экспрессии лейкоцитарного маркера CD45, сосудистого эндотелиального маркера CD31, эпителиального маркера CD326 и маркера фибробластов CD 140а авторы изобретения обнаружили, что доля фибробластов у контрольных мышей дикого типа (WT) на 21-е сутки после индуцирования блеомицином составляет 16%, а доля фибробластов у мышей с нокаутом гена Pear1 составляет 22%, что свидетельствует о том, что делеция Pear1 явно может стимулировать индуцированное блеомицином увеличение количества клеток-фибробластов (см. ФИГ. 3а).
Затем методом культивирования суспензии одиночных клеток легких на стенке определяют первичные легочные клетки-фибробласты. Результаты проточной цитометрии показали, что Pear1 в высокой степени экспрессируется в фибробластах легких контрольных мышей дикого типа (WT) (см. ФИГ. 3b); вестерн-иммуноблоттинг также подтверждает этот результат (см. ФИГ. 3с).
Далее, экспрессию гена в клетках-фибробластах легких индуцированных блеомицином и не индуцированных контрольных легких мышей дикого типа (WT) и мышей с нокаутом гена Pear1 исследовали с использованием технологии RNA-seq; разностный ген впоследствии подвергают анализу представленности групп генов GSEA, и результаты показывают, что в случае индуцирования блеомицином делеция Pear1 может в значительной степени способствовать эпителиально-мезенхимальному переходу (ЕМТ) фибробластов (см. ФИГ. 3d).
Затем используют технологию количественной PCR в режиме реального времени для определения генов синтеза белков внеклеточного матрикса, таких как коллаген, фибронектин, периостин (Postn) и т.д., и результаты показали, что в случае индуцирования блеомицином делеция Pear1 в значительной степени повышает способность фибробластов синтезировать внеклеточный матрикс.
Таким образом, результаты настоящего примера показали, что Pear1 является важным отрицательным регуляторным рецептором, который естественным образом ингибирует ЕМТ-конверсию фибробластов и синтез белков внеклеточного матрикса, и делеция Pear1 в значительной степени способствует ЕМТ-конверсии фибробластов и способности синтезировать внеклеточный матрикс.
Пример 5. Исследование регуляции сигнального пути активации фибробластов тканей легких посредством Pear1
Получали фибробласты легких мышей с делецией Pear1 и без делеции, и затем фибробласты обрабатывали TGFβ, PDGF и FGF соответственно и определяли условия фосфорилирования (активации) сигнальной молекулы в активации сигнального пути фибробластов (общеизвестные основные сигнальные пути активированных фибробластов включают опосредованный рецептором TGFβ сигнальный путь Smad, сигнальный путь MAPK (включая сигнальные пути ERK1/2, JNK, Р38); опосредованный рецептором PDGF сигнальный путь MAPK (включая сигнальные пути ERK1/2, JNK, Р38) и сигнальный путь PI3K/AKT; опосредованный рецептором FGF сигнальный путь MAPK (включая сигнальные пути ERK1/2, JNK, Р38) и сигнальный путь PI3K/Akt и т.д.). Было установлено, что делеция Pear1 делеция может в значительной степени повышать уровень фосфорилирования сигнальных молекул, то есть внутриклеточную передачу сигналов, опосредованную рецептором TGFβ, рецептором PDGF и рецептором FGF (ФИГ. 4). На ФИГ. 4 показано, что в этих сигнальных путях цвет полосы для мышей с нокаутом Pear1 (KO) глубже, чем цвет для мышей дикого типа (WT), у которых Pear1 нормально экспрессировался. Поэтому можно видеть, что после нокаутирования Pear1 сигнальный путь сверхактивируется.
Результаты этого примера показали, что Pear1 может ингибировать активацию фибробластов, опосредованную различными цитокиновыми рецепторами посредством внутриклеточных сигналов.
Пример 6. Активация Pear1 ингибирует фибробласты, экспрессирующие экспрессию белков внеклеточного матрикса
Результаты вышеуказанного исследования показали, что рецептор Pear1 обладает способностью ингибировать пролиферацию фибробластов и синтез внеклеточного матрикса, и поэтому авторы изобретения полагают, что лиганд к Pear1 можно использовать для лечения фиброза легких, действуя на него.
Чтобы исследовать, может ли лиганд к Pear1, о котором сообщалось в литературе, такой как FcεR1α, декстрана сульфат и природные фукоиданы, ингибировать способность фибробластов синтезировать внеклеточный матрикс, согласно настоящему изобретению фибробласты легких человека обрабатывали FcεR1α, декстрана сульфатом и природными фукоиданами в концентрациях, о которых сообщалось в литературе: 1 мкг/мл или 5 мкг/мл FcεR1α, 5 нМ или 20 нМ декстрана сульфата, 30 мкг/мл или 300 мкг/мл природных фукоиданов.
Результаты показали, что FcεR1α, декстрана сульфат и природные фукоиданы могут ингибировать экспрессию гена внеклеточного матрикса фибробластов легких человека, такого как костный мембранный белок (периостин), Col5a3 и Timp1 (см. ФИГ. 5). Таким образом, результаты этого примера свидетельствуют о том, что активация Pear1 может снижать способность фибробластов синтезировать внеклеточный матрикс.
Пример 7. Конструирование гуманизированных трансгенных по Pear1 мышей
Мышь с нокином гена Pear1 человека конструировали по технологии CRISPR/Cas9, намечали целевую точку у экзона 1-ATG кодирующего участка мыши, и в присутствии гомологичной рекомбинационной матрицы экзогенный ген человека интегрировали в целевое положение и заменяли последовательность мышиного гена Pear1. Мышиный Pear1 имеет множество транскриптов. Поэтому экзон 4-6 мышиного гена Pear1 был выбран для замены на кДНК Pear1 человека, и сигнал терминации транскрипции SV40 polyA добавляли позади кДНК Pear1 человека, чтобы мышиный Pear1 был полностью заменен человеческим Pear1 (см. ФИГ. 7а).
Сконструированный гуманизированный трансгенный по Pear1 мышиный генотип идентифицируют методом PCR, общепризнанным в данной области. Фибробласты легких собирали, уровень мышиного Pear1 и уровень человеческого Pear1 определяли методом иммуноблоттинга, и результат показал, что человеческий Pear1 полностью заменил мышиный у гуманизированной трансгенной мыши (см. ФИГ. 7b).
В изобретении использовали 8-10-недельных мышей, и мышей кормили в условиях отсутствия специфических патогенов (SPF). Комитет по этике исследований на животных Shanghai Jiao Tong University School of Medicine одобрил использование этих мышей.
Пример 8. Получение и функциональная идентификация антитела к Pear1 человека
8.1. Получение антитела к Pear1 человека
По сравнению с белком и соединением моноклональное антитело имеет преимущества сильного направленного воздействия, невысокой токсичности и небольших побочных эффектов, хорошей стабильности, длительного периода полувыведения in vivo и т.п.и стало популярной областью современных исследований и разработок лекарственных средств. Изобретение обеспечивает противофиброзный эффект активации Pear1 фибробластов с использованием моноклонального антитела.
Этот способ включает в себя следующие стадии: сначала конструирование плазмиды и затем трансфицирование в суспензию культивированных клеток 293S для экспрессии 6 х His-меченого внеклеточного сегмента Pear1 человека (Leu-21-Ser; 754); белок очищали на никелевой колонке и смешивали с иммунным адъювантом для иммунизации мышей Balb/c; сепарация селезенки мыши с помощью стандартного иммунного процесса; и получение моноклональных гибридомных клеток по стандартной технологии получения моноклональных антител.
В изобретении используется твердофазный иммуноферментный анализ (ELISA) для скрининга гибридомных клеток-продуцентов моноклональных антител, способных связываться с Pear1 человека. Гибридомный клеточный штамм, способный секретировать высокоаффинное моноклональное антитело, которое может связывать Pear1 человека, имеет 53 штамма.
Идентификация влияния антитела на внеклеточный матрикс.Воздействие антитела на уровень экспрессии внеклеточного матриксного белка периостина (Postn), коллагена (Col.4 al), Col8al, Col3al, Col1a1, Col5a2, Col5a3, Col7a1, десмина (Des) и актина альфа 2 (Acta2) в фибробластах легких человека (NhLF) определяли методом qPCR (см. праймеры в Таблице 1).
Шесть антител LF2, LF3, LF7, LF11, LF15 и LF16 могут в значительной степени ингибировать фибробласты легких человека, экспрессирующие белки внеклеточного матрикса (см. Таблицу 3.1).
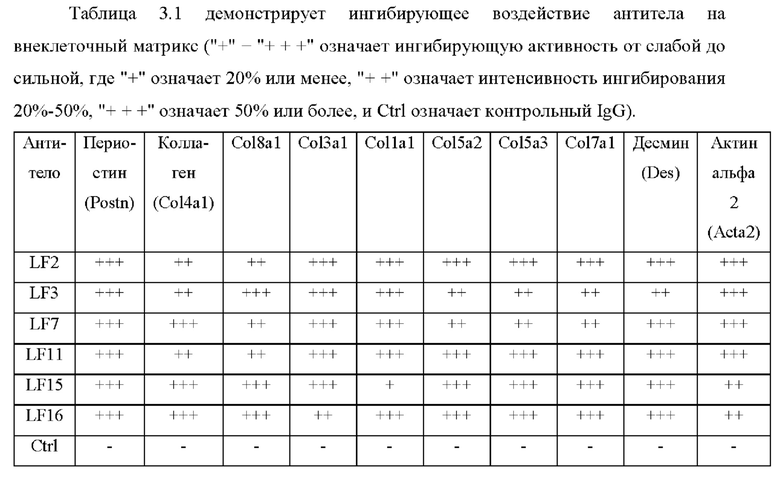
Результаты показывают, что мышиное моноклональное антитело, направленно воздействующее на Pear1 человека, может ингибировать фибробласты, синтезирующие внеклеточного матрикса, и ингибирующее воздействие антитела согласно изобретению исчезает в условиях делеции гена Pear1.
В Таблице 3.2 перечислены последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи антител LF2, LF3, LF7, LF11, LF15, LF16, и последовательности их CDR показаны в Таблице 3.3.
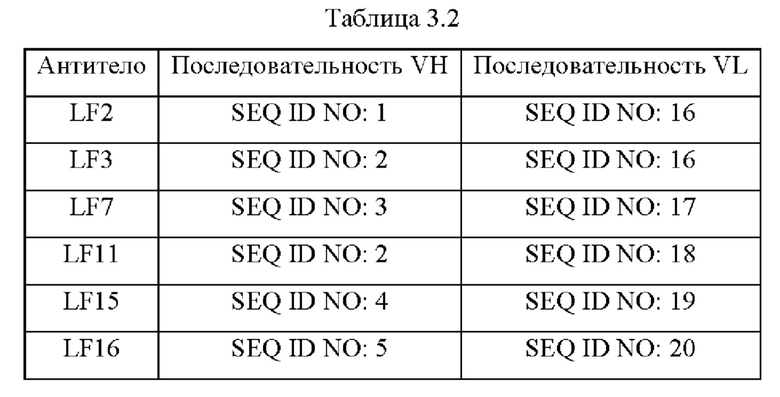
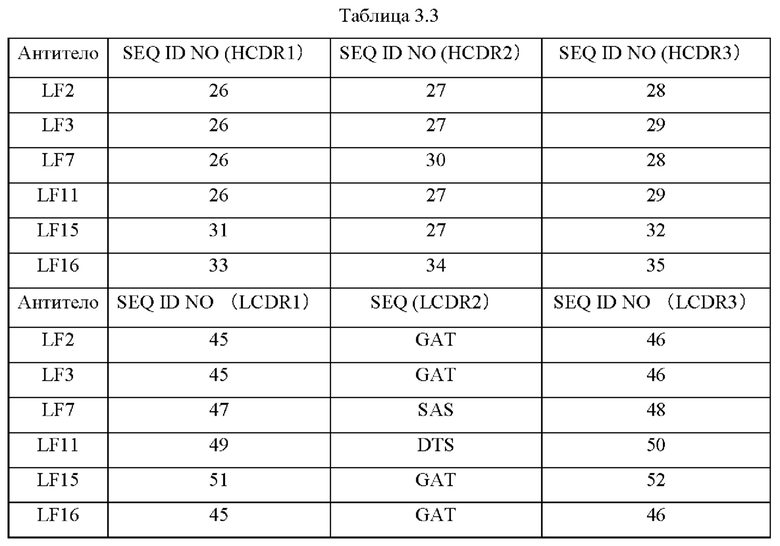
8.2. Идентификации функции антитела к Pear1 человека
8.2.1. Сравнение антигенсвязывающей способности этих антител. Набор для ELISA покрывали белком ECD Pear1 человека и затем подвергали взаимодействию с антителом к Pear1 в разных концентрациях (2000 нг/мл, 1000 нг/мл, 500 нг/мл, 250 нг/мл, 125 нг/мл, 62,5 нг/мл, 31,25 нг/мл, 15,625 нг/мл, 7,8125 нг/мл, 3,90625 нг/мл, 1,953125 нг/мл, 0,9765625 нг/мл) для получения значения ЕС50 для комбинации антиген-антитело (см. ФИГ. 6 и Таблицу 3.4 ниже).
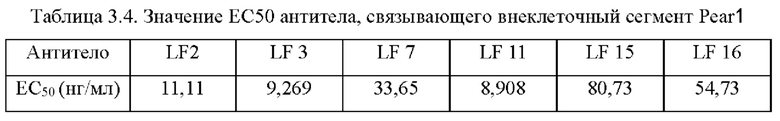
Результаты показывают, что связывающая с Pear1 ЕС50 антитела к Pear1 человека составляет менее 100 нг/мл, имеет хороший эффект связывания с мишенью, и ЕС50 различных антител даже достигает 15 нг/мл или менее, и можно видеть, что специфичность к мишени антитела по изобретению очень сильная.
8.2.2. Антитело к Pear1 человека обладает эффектом против фиброза легких и улучшает функцию легких
Для определения эффекта антитела к Pear1 человека в лечения фиброза легких согласно настоящему изобретению дополнительно сконструирована трансгенная мышь, в которой Pear1 человека заменяет мышиный Pear1, то есть гуманизированная трансгенная по Pear1 мышь, и способ конструирования описан в Примере 7 (ФИГ. 7а). Моноклональные антитела LF2, LF3, LF7, LF11, LF15 и LF16 суспендировали в обычном физиологическом растворе, и распылитель использовали для распыления 1 мкг/г антитела для введения в легкие индуцированной блеомицином гуманизированной трансгенной по Pear1 мыши каждые 7 суток (см. Пример 3). У мышей анализировали функцию легких и патологические изменения на 21-е сутки. Результаты исследования показывают, что LF2, LF3, LF7, LF11, LF15 и LF16 все способны эффективно улучшать функцию легких мыши (форсированная жизненная емкость, FVC), и данные, при которых лечение антителом повышает форсированную жизненную емкость, показаны в Таблице 3.5. Данные по форсированной жизненной емкости и отложению коллагена в тканях легких в процентах для группы лечения антителом LF2 представлены на ФИГ. 7 с и ФИГ. 7d. 

Результаты эксперимента показывают, что специфичность моноклонального антитела, направленно воздействующего на Pear1 человека, значительная, и этот способ может быть использован для облегчения индуцированного блеомицином фиброза легких мышей и улучшения функции легких.
Пример 9. Гуманизированная трансформация и идентификация функции антитела к Pear1 человека
9.1. Конструирование гуманизированного антитела
Гуманизированную трансформацию вышеуказанного антитела проводили методом трансплантации CDR согласно изобретению и осуществляли разные обратные мутации (последовательности гуманизированных антител hLF 101-116, hLF-N55 S, hLF-N55 D, hLF-N55 Q, hLF-G56 А и hLF-G56 V также представлены в Таблице 4) в каркасной области.
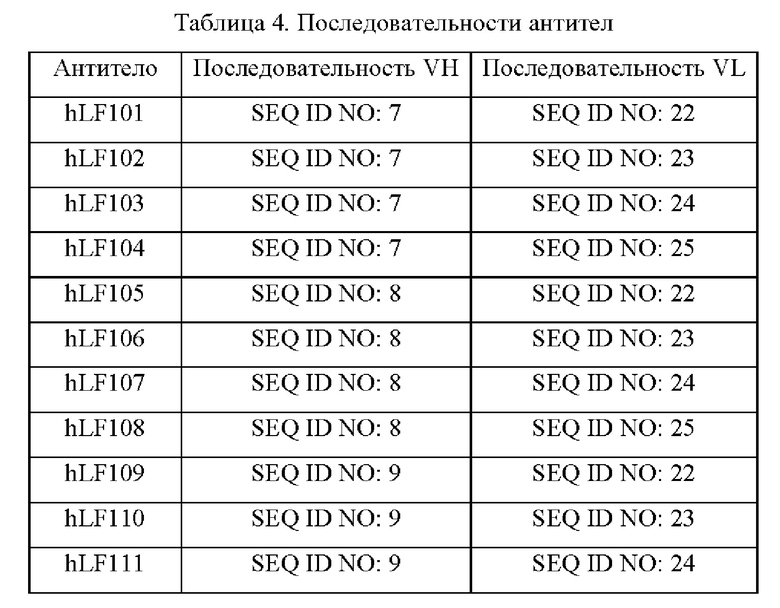
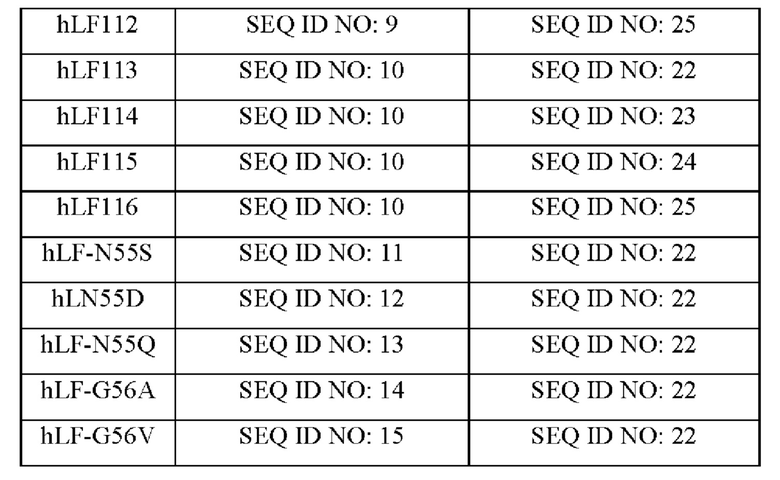
Последовательность CDR антитела представлена в SEQ ID NO: 26-55 в Таблице 5, и последовательность CDR антитела пронумерована в соответствии с правилом нумерации IMGT.
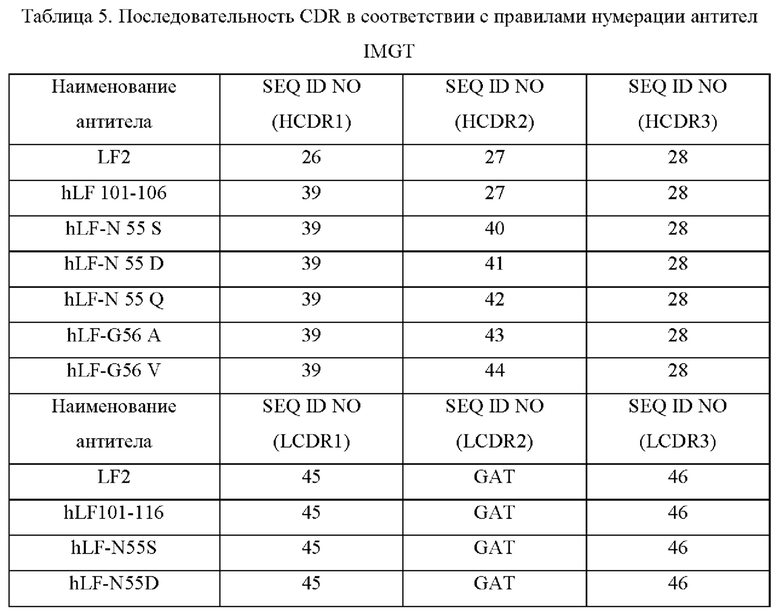
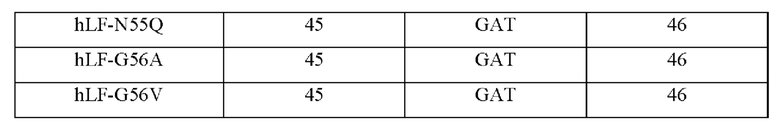
9.2. Тест на аффинность связывания гуманизированного антитела к Pear1 человека с внеклеточным сегментом Pear1 (см. Таблицу 6)
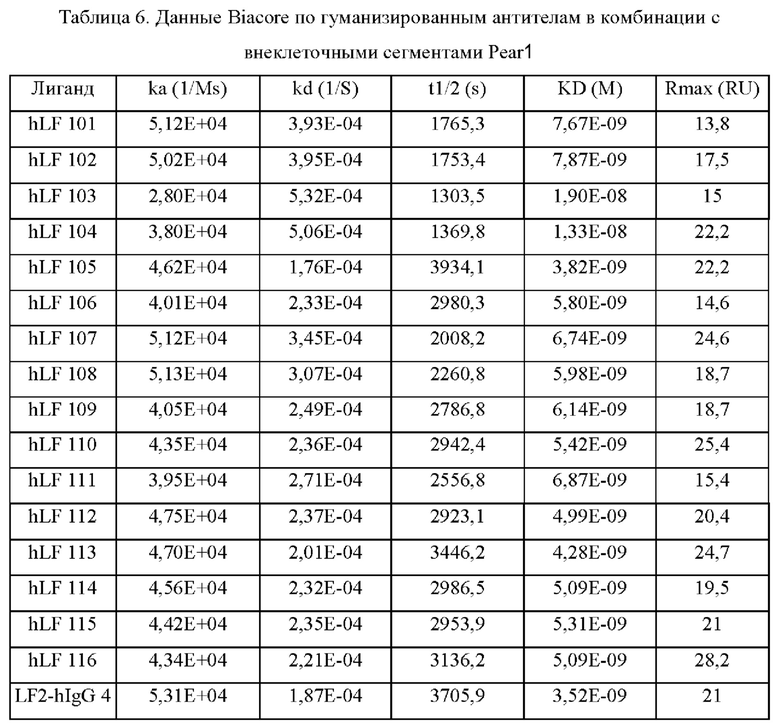
Результаты показывают, что каждое гуманизированное антитело обладает активностью связывания с внеклеточным сегментом Pear1, и замена и обратная мутация FR области антитела незначительно влияют на аффинность CDR.
9.3. Роль гуманизированного антитела к Pear1 в индуцированном блеомицином фиброзе легких мышей
В изобретении вышеуказанное гуманизированное модифицированное антитело суспендировали в нормальном физиологическом растворе, и распылитель использовали для распыления 1 мкг/г гуманизированного модифицированного антитела в легкие индуцированных блеомицином гуманизированных трансгенных по Pear1 мышей (см. Пример 3). У мышей анализировали функцию легких на 21-е сутки. Результаты исследования показывают, что вышеуказанное антитело может эффективно улучшать функцию легких мышей (форсированная жизненная емкость FVC), и данные представлены в Таблице 7.
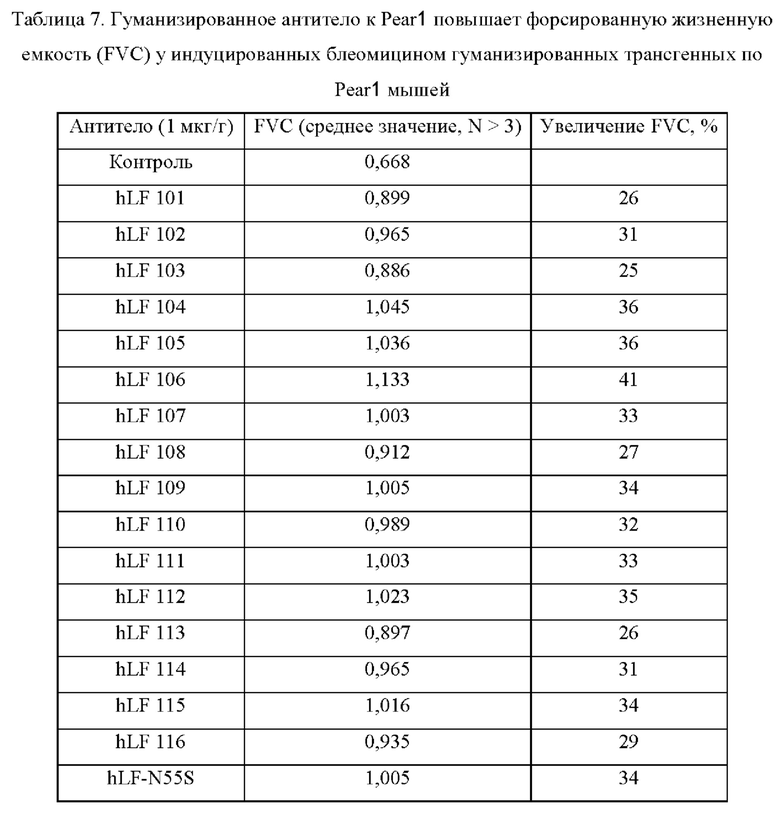
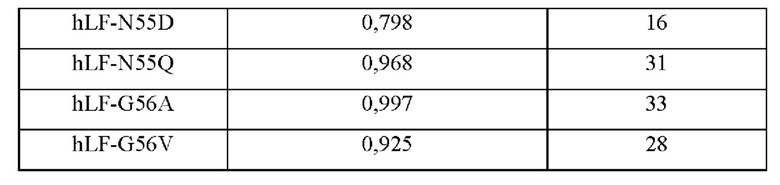
Результаты показывают, что все гуманизированные антитела могут эффективно повышать форсированную жизненную емкость у индуцированных блеомицином гуманизированных трансгенных по Pear1 мышей.
Пример 10. Моноклональное антитело к Pear1 человека ингибирует фибробласты из различных тканей, экспрессирующие белки внеклеточного матрикса
Для дополнительного исследования эффекта Pear1 в фибробластах из других источников в изобретении использовали технологию количественной PCR в режиме реального времени и исследовали влияние моноклонального антитела к Pear1 на способность синтезировать внеклеточный матрикс человеческих кожных фибробластов, сердечных фибробластов, почечных фибробластов и печеночных фибробластов.
Результаты исследования показывают, что антитело к Pear1 человека согласно этому изобретению может также ингибировать культивированные человеческие кожные фибробласты, сердечные фибробласты, почечные фибробласты и печеночные фибробласты, экспрессирующие белки внеклеточного матрикса. Моноклональное антитело LF 3 ингибирует человеческие почечные фибробласты, экспрессирующие белки внеклеточного матрикса (см. ФИГ. 8а). Моноклональное антитело LF 3 ингибирует человеческие сердечные фибробласты, экспрессирующие белки внеклеточного матрикса (см. ФИГ. 8b). Моноклональное антитело LF 3 ингибирует человеческие печеночные фибробласты, экспрессирующие белки внеклеточного матрикса (см. ФИГ. 8с). Моноклональное антитело LF 3 ингибирует человеческие кожные фибробласты, экспрессирующие белки внеклеточного матрикса (см. ФИГ. 8d).
Вышеуказанные результаты таже подтверждают, что антитело к Pear1, действующее на фибробласты, также может быть использовано для лечения рубцов на коже, образовавшихся вследствие травмы, эмпироза, хирургического вмешательства или придания формы и красоты, для лечения фиброза сердца, сердечной недостаточности, снижения диастолической функции или фракции выброса и аритмии, вызванных повреждением миокарда, вызванным старением или другими причинами, для лечения фиброза почек, вызванного повреждением почек, для лечения фиброза печени, вызванного различными инфекционными и химическими повреждениями, и для лечения фиброза печени, индуцированного высоким давлением в воротной вене, печеночным асцитом, циррозом печени, зависимой легочной гипертензией, для лечения фиброза костного мозга, вызванного трансплантацией или химиотерапией, для лечения фиброза поджелудочной железы и т.д. и для лечения фиброза селезенки, нервной системы и т.д.
Хотя конкретные примеры настоящего изобретения были описаны выше, специалисту в данной области техники должно быть понятно, что это всего лишь примеры, и различные изменения или модификации могут быть сделаны в этих примерах без отклонения от принципов и замысла изобретения. Таким образом, изобретения определяется прилагаемой формулой изобретения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Shanghai Jiaoton University, School of Medicine
<120> Соответствующая мишень для лечения фиброзирующих заболеваний и ее применение
<130> P20406151CF
<150> 2020100767292
<151> 2020-01-23
<150> 2020112126398
<151> 2020-11-03
<160> 162
<170> PatentIn version 3.5
<210> 1
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2-VH
<400> 1
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ser His Val Lys Asn Leu Glu Trp Ile
35 40 45
Gly Val Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Ile Glu Leu Leu Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ala
115
<210> 2
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> LF3-VH
<400> 2
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Lys Gln Thr His Gly Lys Asn Leu Glu Trp Ile
35 40 45
Gly Leu Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Asp Glu Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ala
115
<210> 3
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> LF7-VH
<400> 3
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ser His Gly Lys Asn Leu Glu Trp Ile
35 40 45
Gly Val Ile Asn Ser Tyr Asn Gly Gly Ala Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Ile Val His
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ala
115
<210> 4
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> LF15-VH
<400> 4
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Glu Asn Leu Glu Trp Ile
35 40 45
Gly Val Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Phe Ser Thr Ala Tyr
65 70 75 80
Met Glu Ile Leu Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ser Arg Gly Gly Gly Asn Ser Trp Phe Ala Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 5
<211> 118
<212> PRT
<213> Artificial Sequence
<220>
<223> LF16-VH
<400> 5
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser Gly Tyr Ala Phe Thr Gly Tyr
20 25 30
Thr Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Asp Trp Ile
35 40 45
Gly Val Ile Asn Gly Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Leu Ser Leu Thr Ser Glu Asp Ser Ala Ile Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Pro Thr Thr Gly Phe Val Tyr Trp Gly Gln Gly Thr
100 105 110
Leu Val Thr Val Ser Ala
115
<210> 6
<211> 115
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1-VH
<400> 6
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Asn Trp Val Lys Gln Ser His Gly Glu Ser Leu Glu Trp Ile
35 40 45
Gly Asp Ile Asn Pro Asn Asn Gly Gly Ala Thr Tyr Asn Gln Lys Phe
50 55 60
Glu Gly Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Gly Gln Leu Leu Gly Phe Ala Ser Trp Gly Gln Gly Thr Leu Val Thr
100 105 110
Val Ser Ala
115
<210> 7
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF101-104-VH
<400> 7
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Gln Asn Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Arg Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 8
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF105-108-VH
<400> 8
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 9
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF109-112-VH
<400> 9
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Gln Asn Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Val Thr Leu Thr Val Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 10
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-113-116-VH
<400> 10
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Asn Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asn Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Lys Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 11
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-N55S-VH
<400> 11
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Ser Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 12
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-N55D-VH
<400> 12
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asp Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 13
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-N55Q-VH
<400> 13
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Gln Gly Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 14
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-G56A-VH
<400> 14
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asn Ala Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 15
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-G56V-VH
<400> 15
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Pro Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met
35 40 45
Gly Val Ile Asn Pro Tyr Asn Val Gly Thr Ser Tyr Asn Gln Lys Phe
50 55 60
Lys Gly Arg Ala Thr Leu Thr Val Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 16
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2/LF3-VL
<400> 16
Asp Ile Gln Met Thr Gln Thr Ser Ser Ser Phe Ser Val Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asp Ile Tyr Asn Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Ser Ile Thr Ser Leu Gln Thr
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Thr Pro Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Gln
100 105
<210> 17
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> LF7-VL
<400> 17
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Asp Thr Asn
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ala Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Glu Tyr Phe Cys Gln Gln Tyr Asp Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Arg
100 105
<210> 18
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> LF11-VL
<400> 18
Asp Ile Val Ile Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Arg Ser Ser Val Ser Tyr Met
20 25 30
Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Arg Leu Leu Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Val Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Arg Met Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Phe Cys Gln Gln Trp Ser Ser Tyr Pro Pro Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 19
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> LF15-VL
<400> 19
Asp Ile Gln Met Thr Gln Thr Ser Ser Tyr Leu Ser Val Ser Leu Gly
1 5 10 15
Gly Arg Val Thr Ile Thr Cys Lys Ala Ser Asp His Ile Asn Asn Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Tyr Ser Leu Thr Ile Thr Ser Leu Gln Thr
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Ile Pro Thr
85 90 95
Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 20
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> LF16-VL
<400> 20
Asp Ile Gln Met Thr Gln Thr Ser Ser Ser Phe Ser Val Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asp Ile Tyr Asn Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Lys Asp Tyr Thr Leu Ser Ile Thr Ser Leu Gln Thr
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Thr Pro Thr
85 90 95
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 21
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1-VL
<400> 21
Asp Val Val Leu Thr Gln Thr Pro Leu Ser Leu Pro Val Asn Ile Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Thr Gln Ser Leu Leu Asn Ser
20 25 30
Asp Arg Phe Thr Tyr Leu Asp Trp Tyr Leu Gln Arg Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Leu Val Ser Tyr Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Leu Tyr Tyr Cys Leu Gln Ser
85 90 95
Ser Tyr Leu Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 22
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF101\105\109\113\N55-G56 МУТАНТ-VL
<400> 22
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asp Ile Tyr Asn Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Thr Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 23
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF102\106\110\114-VL
<400> 23
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asp Ile Tyr Asn Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Thr Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 24
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF103\107\111\115-VL
<400> 24
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asp Ile Tyr Asn Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Thr Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 25
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF104\108\112\116-VL
<400> 25
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Glu Asp Ile Tyr Asn Arg
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Lys Leu Leu Ile
35 40 45
Ser Gly Ala Thr Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Trp Ser Thr Pro Thr
85 90 95
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 26
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2/3/7/11 HCDR1
<400> 26
Gly Tyr Ser Phe Thr Gly Tyr Pro
1 5
<210> 27
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2/3/11/15/hLF101-116 HCDR2
<400> 27
Ile Asn Pro Tyr Asn Gly Gly Thr
1 5
<210> 28
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2/7/hLF101-116 HCDR3
<400> 28
Ala Arg Gly Gly Val Arg Pro Phe Ala Tyr
1 5 10
<210> 29
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LF3/11 HCDR3
<400> 29
Ala Arg Gly Gly Val Arg Pro Phe Asp Phe
1 5 10
<210> 30
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF7 HCDR2
<400> 30
Ile Asn Ser Tyr Asn Gly Gly Ala
1 5
<210> 31
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF15 HCDR1
<400> 31
Gly Tyr Ser Phe Thr Gly Tyr Thr
1 5
<210> 32
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> LF15 HCDR3
<400> 32
Ser Arg Gly Gly Gly Asn Ser Trp Phe Ala Tyr
1 5 10
<210> 33
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF16 HCDR1
<400> 33
Gly Tyr Ala Phe Thr Gly Tyr Thr
1 5
<210> 34
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF16 HCDR2
<400> 34
Ile Asn Gly Tyr Asn Gly Gly Thr
1 5
<210> 35
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> LF16 HCDR3
<400> 35
Ala Arg Gly Gly Pro Thr Thr Gly Phe Val Tyr
1 5 10
<210> 36
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1 HCDR1
<400> 36
Gly Tyr Thr Phe Thr Asp Tyr Tyr
1 5
<210> 37
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1 HCDR2
<400> 37
Ile Asn Pro Asn Asn Gly Gly Ala
1 5
<210> 38
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1 HCDR3
<400> 38
Gly Gln Leu Leu Gly Phe Ala Ser
1 5
<210> 39
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF101 HCDR1
<400> 39
Gly Tyr Thr Phe Thr Gly Tyr Pro
1 5
<210> 40
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-N55S HCDR2
<400> 40
Ile Asn Pro Tyr Ser Gly Gly Thr
1 5
<210> 41
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-N55D HCDR2
<400> 41
Ile Asn Pro Tyr Asp Gly Gly Thr
1 5
<210> 42
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-N55Q HCDR2
<400> 42
Ile Asn Pro Tyr Gln Gly Gly Thr
1 5
<210> 43
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-G56A HCDR2
<400> 43
Ile Asn Pro Tyr Asn Ala Gly Thr
1 5
<210> 44
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> hLF-G56V HCDR2
<400> 44
Ile Asn Pro Tyr Asn Val Gly Thr
1 5
<210> 45
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2/3/16/hLF101-116 LCDR1
<400> 45
Glu Asp Ile Tyr Asn Arg
1 5
<210> 46
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF2/3/16/hLF101-116 LCDR3
<400> 46
Gln Gln Tyr Trp Ser Thr Pro Thr
1 5
<210> 47
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> LF7 LCDR1
<400> 47
Gln Asn Val Asp Thr Asn
1 5
<210> 48
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> LF7 LCDR3
<400> 48
Gln Gln Tyr Asp Ser Tyr Pro Tyr Thr
1 5
<210> 49
<211> 5
<212> PRT
<213> Artificial Sequence
<220>
<223> LF11 LCDR1
<400> 49
Ser Ser Val Ser Tyr
1 5
<210> 50
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> LF11 LCDR3
<400> 50
Gln Gln Trp Ser Ser Tyr Pro Pro Thr
1 5
<210> 51
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> LF15 LCDR1
<400> 51
Asp His Ile Asn Asn Trp
1 5
<210> 52
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> LF15 LCDR3
<400> 52
Gln Gln Tyr Trp Ser Ile Pro Thr
1 5
<210> 53
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1 HCDR1
<400> 53
Gln Ser Leu Leu Asn Ser Asp Arg Phe Thr Tyr
1 5 10
<210> 54
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> LFm1 LCDR3
<400> 54
Leu Gln Ser Ser Tyr Leu Pro Tyr Thr
1 5
<210> 55
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Postn-F мыши
<400> 55
ggggttgtca ctgtgaactg 20
<210> 56
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Postn-R мыши
<400> 56
cggctgctct aaatgatgaa 20
<210> 57
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 4a1-F мыши
<400> 57
ctggcacaaa agggacgag 19
<210> 58
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 4a1-R мыши
<400> 58
acgtggccga gaatttcacc 20
<210> 59
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a3-F мыши
<400> 59
ggcaaagatg gtattccagg acc 23
<210> 60
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a3-R мыши
<400> 60
tgcttccttt gtgaccaggc atc 23
<210> 61
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> S100a4-F мыши
<400> 61
agctcaagga gctactgacc ag 22
<210> 62
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> S100a4-R мыши
<400> 62
gctgtccaag ttgctcatca cc 22
<210> 63
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a2-F мыши
<400> 63
gtggcatagg agagaaaggt gc 22
<210> 64
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a2-R мыши
<400> 64
gccaactaag cctctaggac ca 22
<210> 65
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Des-F мыши
<400> 65
gtggatgcag ccactctagc 20
<210> 66
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Des-R мыши
<400> 66
ttagccgcga tggtctcata c 21
<210> 67
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Acta2-F мыши
<400> 67
tgctgacaga ggcaccactg aa 22
<210> 68
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Acta2-R мыши
<400> 68
cagttgtacg tccagaggca tag 23
<210> 69
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 1a2-F мыши
<400> 69
ttctgtgggt cctgctggga aa 22
<210> 70
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 1a2-R мыши
<400> 70
ttgtcacctc ggatgccttg ag 22
<210> 71
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 7a1-F мыши
<400> 71
caggcattgg tgccagtgaa ca 22
<210> 72
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 7a1-R мыши
<400> 72
tggacctcca tcctcacagt ca 22
<210> 73
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Loxl2-F мыши
<400> 73
attaacccca actatgaagt gcc 23
<210> 74
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Loxl2-R мыши
<400> 74
ctgtctcctc actgaaggct c 21
<210> 75
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> FN1-F мыши
<400> 75
ccaggtcgaa aagggtatat ggg 23
<210> 76
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> FN1-R мыши
<400> 76
cggttatccc tacttctcca gg 22
<210> 77
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 24a1-F мыши
<400> 77
ccaggtcgaa aagggtatat ggg 23
<210> 78
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 24a1-R мыши
<400> 78
cggttatccc tacttctcca gg 22
<210> 79
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 28a1-F мыши
<400> 79
gcctggtctt aaaggagaac ctg 23
<210> 80
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 28a1-R мыши
<400> 80
agccatcacc tttgagtcct gg 22
<210> 81
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> 18sRNA-F мыши
<400> 81
ttgactcaac acgggaaacc 20
<210> 82
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> 18sRNA-R мыши
<400> 82
agacaaatcg ctccaccaac 20
<210> 83
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Timp1-F
<400> 83
ggagagtgtc tgcggatact tc 22
<210> 84
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Timp1-R
<400> 84
gcaggtagtg atgtgcaaga gtc 23
<210> 85
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Postn -F человека
<400> 85
cagcaaacca ccttcacgga tc 22
<210> 86
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Postn-R человека
<400> 86
ttaaggaggc gctgaaccat gc 22
<210> 87
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 4a1 -F человека
<400> 87
tgttgacggc ttacctggag ac 22
<210> 88
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 4a1-R человека
<400> 88
ggtagaccaa ctccaggctc tc 22
<210> 89
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 8a1-F человека
<400> 89
aggaagccgt acccaagaaa gg 22
<210> 90
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 8a1-R человека
<400> 90
ggtatcccat gacctggcaa ac 22
<210> 91
<211> 24
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 3a1-F человека
<400> 91
cccactatta ttttggcaca acag 24
<210> 92
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 3a1-R человека
<400> 92
aacggatcct gagtcacaga ca 22
<210> 93
<211> 26
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 1a1-F человека
<400> 93
tagggtctag acatgttcag ctttgt 26
<210> 94
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 1a1-R человека
<400> 94
gtgattggtg ggatgtcttc gt 22
<210> 95
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a2-F человека
<400> 95
taggaactga tggtactcct gg 22
<210> 96
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a2-R человека
<400> 96
ggcctatcgg accctgaata c 21
<210> 97
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a3-F человека
<400> 97
gtggccgtca gcatagatgg 20
<210> 98
<211> 23
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 5a3-R человека
<400> 98
tgaatgtctc cctcgaaagt ctt 23
<210> 99
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 7a1-F человека
<400> 99
ttacgccgct gacattgtgt t 21
<210> 100
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> Col 7a1-R человека
<400> 100
accagccctt cgagaaagc 19
<210> 101
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Des-F человека
<400> 101
tccagtccta cacctgcgag at 22
<210> 102
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> Des-R человека
<400> 102
cgcaatgttg tcctggtagc ca 22
<210> 103
<211> 22
<212> DNA
<213> Artificial Sequence
<220>
<223> FN1-F человека
<400> 103
gagctgcacc tgtcttggga ac 22
<210> 104
<211> 21
<212> DNA
<213> Artificial Sequence
<220>
<223> FN1-R человека
<400> 104
ggagcaaatg gcaccgagat a 21
<210> 105
<211> 24
<212> DNA
<213> Artificial Sequence
<220>
<223> 18sRNA-F человека
<400> 105
gagcggtcgg cgtcccccaa cttc 24
<210> 106
<211> 24
<212> DNA
<213> Artificial Sequence
<220>
<223> 18sRNA-R человека
<400> 106
gcgcgtgcag ccccggacat ctaa 24
<210> 107
<211> 25
<212> DNA
<213> Artificial Sequence
<220>
<223> Pear1-F
<400> 107
gctactgtct gctccttcag ttccc 25
<210> 108
<211> 25
<212> DNA
<213> Artificial Sequence
<220>
<223> Pear1-KO-R
<400> 108
ctcctacata gttggcagtg tttgg 25
<210> 109
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> Pear1-WT-R
<400> 109
gagggaaggg ttgtgtcagg 20
<210> 110
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> HPear1-WT-F
<400> 110
gcagtgggct gatttcttc 19
<210> 111
<211> 20
<212> DNA
<213> Artificial Sequence
<220>
<223> HPear1-KI-LD-R
<400> 111
tgctacagtt gactccccat 20
<210> 112
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> HPear1-KI-RD-F
<400> 112
ggcagtttgg agaaggttg 19
<210> 113
<211> 19
<212> DNA
<213> Artificial Sequence
<220>
<223> HPear1-WT-R
<400> 113
ccaaccccag ctacagtta 19
<210> 114
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR1
<400> 114
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Met Lys Ile Ser Cys Lys Ala Ser
20 25
<210> 115
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR1
<400> 115
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Ala Ser
20 25
<210> 116
<211> 25
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR1
<400> 116
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser
20 25
<210> 117
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 117
Met Asn Trp Val Lys Gln Ser His Gly Glu Asn Leu Glu Trp Ile Gly
1 5 10 15
Val
<210> 118
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 118
Met Asn Trp Val Lys Gln Ser His Gly Glu Ser Leu Glu Trp Ile Gly
1 5 10 15
Asp
<210> 119
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 119
Met Asn Trp Val Lys Gln Ser His Gly Lys Asn Leu Asp Trp Ile Gly
1 5 10 15
Val
<210> 120
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 120
Met Asn Trp Val Lys Gln Thr His Gly Lys Asn Leu Glu Trp Ile Gly
1 5 10 15
Leu
<210> 121
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 121
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Asn Leu Glu Trp Met Gly
1 5 10 15
Val
<210> 122
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 122
Met Asn Trp Val Arg Gln Ala Pro Gly Lys Arg Leu Glu Trp Met Gly
1 5 10 15
Val
<210> 123
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 123
Met Asn Trp Val Arg Gln Ala Pro Gly Gln Asn Leu Glu Trp Met Gly
1 5 10 15
Val
<210> 124
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 124
Met Asn Trp Val Arg Gln Ser His Gly Lys Asn Leu Glu Trp Ile Gly
1 5 10 15
Val
<210> 125
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR2
<400> 125
Met Asn Trp Val Arg Gln Ser His Val Lys Asn Leu Glu Trp Ile Gly
1 5 10 15
Val
<210> 126
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 126
Ser Tyr Asn Gln Lys Phe Lys Gly Arg Val Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ala Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 127
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 127
Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Phe Ser Thr Ala Tyr Met Glu Ile Leu Ser Leu Thr Ser Glu Asp
20 25 30
Ser Ala Val Tyr Tyr Cys
35
<210> 128
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 128
Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ser Asn Ile Val His Met Glu Leu Leu Ser Leu Thr Ser Glu Asp
20 25 30
Ser Ala Val Tyr Tyr Cys
35
<210> 129
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 129
Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ser Ser Thr Ala Tyr Ile Glu Leu Leu Ser Leu Thr Ser Asp Asp
20 25 30
Ser Ala Val Tyr Tyr Cys
35
<210> 130
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 130
Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ser Ser Thr Ala Tyr Met Glu Leu Leu Ser Leu Thr Ser Asp Glu
20 25 30
Ser Ala Val Tyr Tyr Cys
35
<210> 131
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 131
Ser Tyr Asn Gln Lys Phe Lys Gly Lys Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ser Ser Thr Ala Tyr Met Glu Leu Leu Ser Leu Thr Ser Glu Asp
20 25 30
Ser Ala Ile Tyr Tyr Cys
35
<210> 132
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 132
Ser Tyr Asn Gln Lys Phe Lys Gly Arg Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ala Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 133
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 133
Ser Tyr Asn Gln Lys Phe Lys Gly Arg Ala Thr Leu Thr Val Asp Thr
1 5 10 15
Ser Ala Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 134
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 134
Ser Tyr Asn Gln Lys Phe Lys Gly Arg Val Thr Leu Thr Arg Asp Lys
1 5 10 15
Ser Ala Ser Thr Ala Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp
20 25 30
Thr Ala Val Tyr Tyr Cys
35
<210> 135
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR3
<400> 135
Thr Tyr Asn Gln Lys Phe Glu Gly Lys Ala Thr Leu Thr Val Asp Lys
1 5 10 15
Ser Ser Ser Thr Ala Tyr Met Glu Leu Arg Ser Leu Thr Ser Glu Asp
20 25 30
Ser Ala Val Tyr Tyr Cys
35
<210> 136
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR4
<400> 136
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
1 5 10
<210> 137
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> HFR4
<400> 137
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
1 5 10
<210> 138
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR1
<400> 138
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser
20 25
<210> 139
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR1
<400> 139
Asp Ile Gln Met Thr Gln Thr Ser Ser Ser Phe Ser Val Ser Leu Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser
20 25
<210> 140
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR1
<400> 140
Asp Ile Gln Met Thr Gln Thr Ser Ser Tyr Leu Ser Val Ser Leu Gly
1 5 10 15
Gly Arg Val Thr Ile Thr Cys Lys Ala Ser
20 25
<210> 141
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR1
<400> 141
Asp Ile Val Ile Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Arg
20 25
<210> 142
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR1
<400> 142
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser
20 25
<210> 143
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR1
<400> 143
Asp Val Val Leu Thr Gln Thr Pro Leu Ser Leu Pro Val Asn Ile Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Thr
20 25
<210> 144
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR2
<400> 144
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
1 5 10 15
Ser
<210> 145
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR2
<400> 145
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Lys Leu Leu Ile
1 5 10 15
Ser
<210> 146
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR2
<400> 146
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Asn Ala Pro Arg Leu Leu Ile
1 5 10 15
Ser
<210> 147
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR2
<400> 147
Leu Asp Trp Tyr Leu Gln Arg Pro Gly Gln Ser Pro Gln Leu Leu Ile
1 5 10 15
Tyr
<210> 148
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR2
<400> 148
Met Tyr Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Arg Leu Leu Ile
1 5 10 15
Tyr
<210> 149
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR2
<400> 149
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ala Leu Ile
1 5 10 15
Tyr
<210> 150
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 150
Lys Leu Ala Ser Gly Val Pro Val Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Ser Tyr Ser Leu Thr Ile Ser Arg Met Glu Ala Glu Asp Ala Ala
20 25 30
Thr Tyr Phe Cys
35
<210> 151
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 151
Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Lys Asp Tyr Thr Leu Ser Ile Thr Ser Leu Gln Thr Glu Asp Val Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 152
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 152
Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Asn Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 153
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 153
Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Asn Asp Tyr Thr Leu Ser Ile Thr Ser Leu Gln Thr Glu Asp Val Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 154
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 154
Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Asn Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro Glu Asp Phe Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 155
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 155
Ser Leu Glu Thr Gly Val Pro Ser Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Tyr Ser Leu Thr Ile Thr Ser Leu Gln Thr Glu Asp Val Ala
20 25 30
Thr Tyr Tyr Cys
35
<210> 156
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 156
Tyr Arg Phe Ser Gly Val Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Lys Ile Ser Arg Val Glu Ala Glu Asp Leu Gly
20 25 30
Leu Tyr Tyr Cys
35
<210> 157
<211> 36
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR3
<400> 157
Tyr Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly
1 5 10 15
Thr Asp Phe Thr Leu Thr Ile Ser Asn Val Gln Ser Glu Asp Leu Ala
20 25 30
Glu Tyr Phe Cys
35
<210> 158
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR4
<400> 158
Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
1 5 10
<210> 159
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR4
<400> 159
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
1 5 10
<210> 160
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR4
<400> 160
Phe Gly Gly Gly Thr Lys Leu Glu Ile Arg
1 5 10
<210> 161
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR4
<400> 161
Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
1 5 10
<210> 162
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> LFR4
<400> 162
Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
1 5 10
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТЕЛА ПРОТИВ БЕЛКА-1 ЗАПРОГРАММИРОВАННОЙ КЛЕТОЧНОЙ СМЕРТИ (PD-1) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2725950C1 |
| Антитела против лиганда-1 запрограммированной смерти (PD-L1) и их применение | 2017 |
|
RU2721582C1 |
| Антитела против CXCR2 и их применение | 2019 |
|
RU2807067C2 |
| ЭЛЕМЕНТЫ, СВЯЗЫВАЮЩИЕСЯ С ИЛ-1 БЕТА | 2013 |
|
RU2711118C2 |
| МУЛЬТИСПЕЦИФИЧЕСКАЯ АНТИГЕНСВЯЗЫВАЮЩАЯ МОЛЕКУЛА, ОБЛАДАЮЩАЯ ЗАМЕЩАЮЩЕЙ ФУНКЦИОНАЛЬНОЙ АКТИВНОСТЬЮ КОФАКТОРА КОАГУЛИРУЮЩЕГО ФАКТОРА КРОВИ VIII, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ УКАЗАННУЮ МОЛЕКУЛУ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2018 |
|
RU2812909C2 |
| Композиция для предупреждения и лечения заболевания кожи, содержащая вещество, специфично связывающееся с пептидом, имеющим происхождение из виментина | 2018 |
|
RU2751486C1 |
| АНТИТЕЛА К C10ORF54 И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2819627C1 |
| Биспецифическое антитело анти-HER2/анти-4-1BB и его применение | 2020 |
|
RU2831838C2 |
| АНТИТЕЛА ПРОТИВ PD-L1 И ИХ ВАРИАНТЫ | 2017 |
|
RU2770590C2 |
| ЛЕЧЕНИЕ ГОЛОВНОЙ БОЛИ ПРИ ИЗБЫТОЧНОМ ПРИМЕНЕНИИ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ АНТИТЕЛАМИ К CGRP ИЛИ CGRP-R | 2020 |
|
RU2826186C2 |
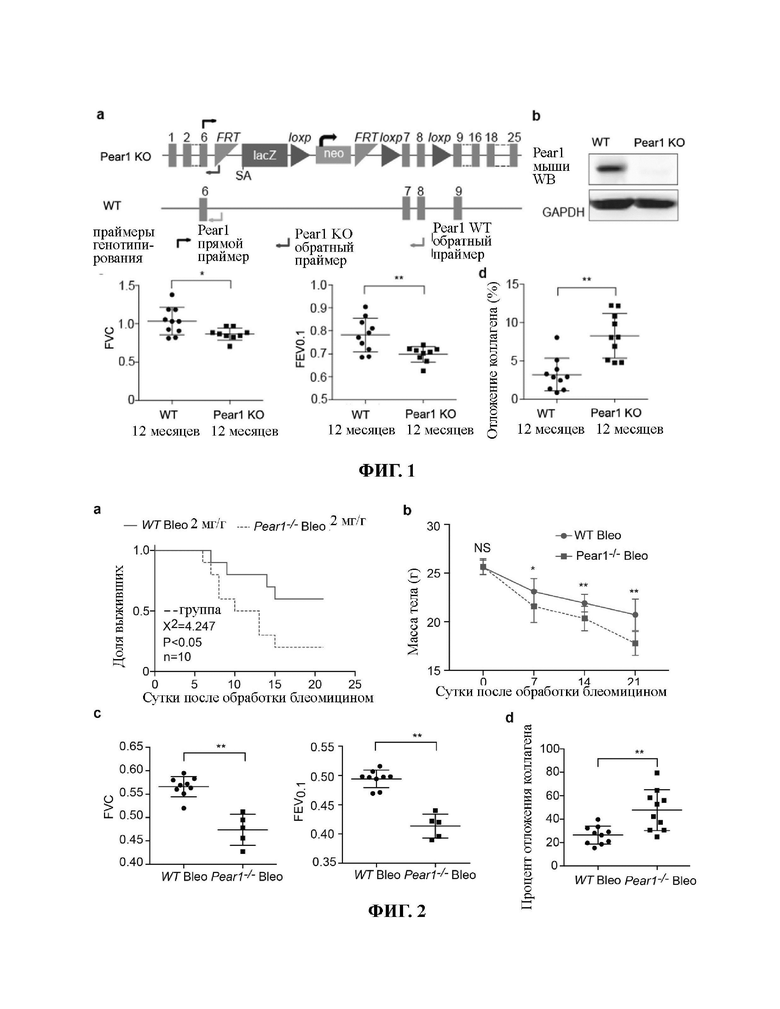
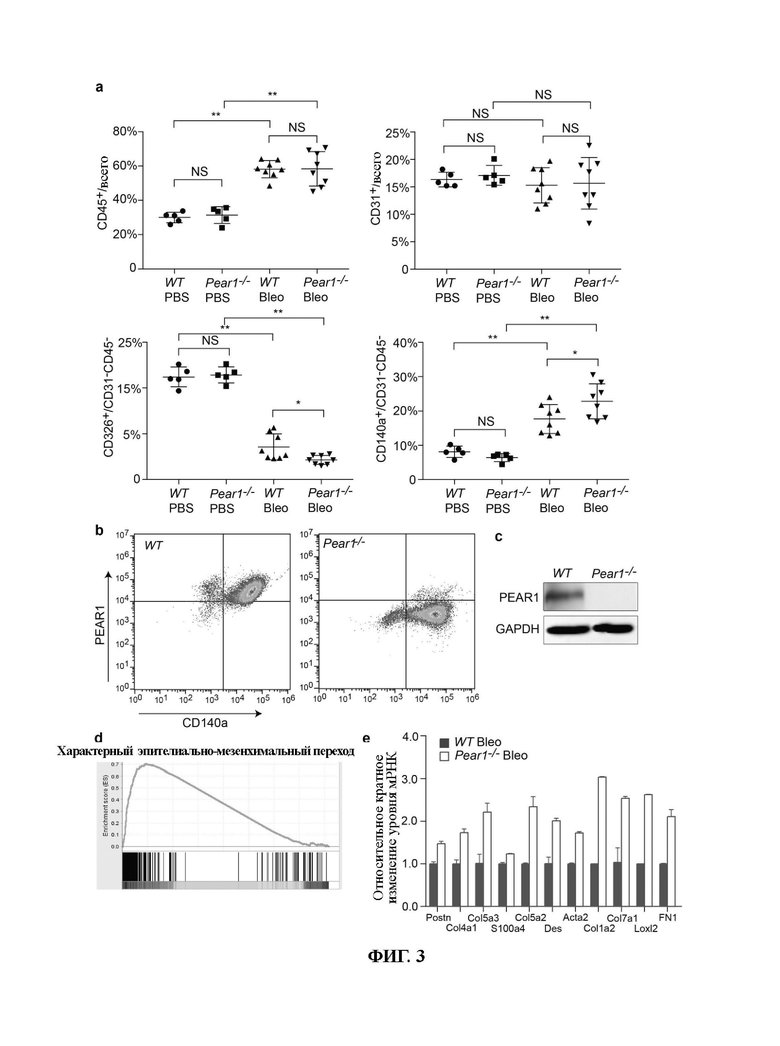
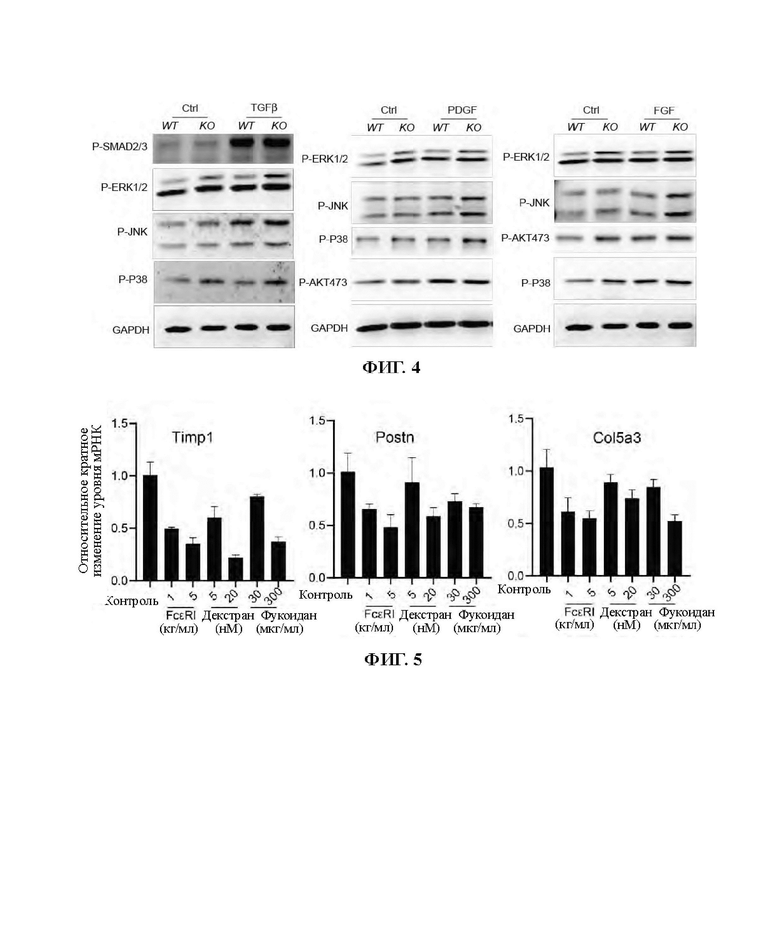
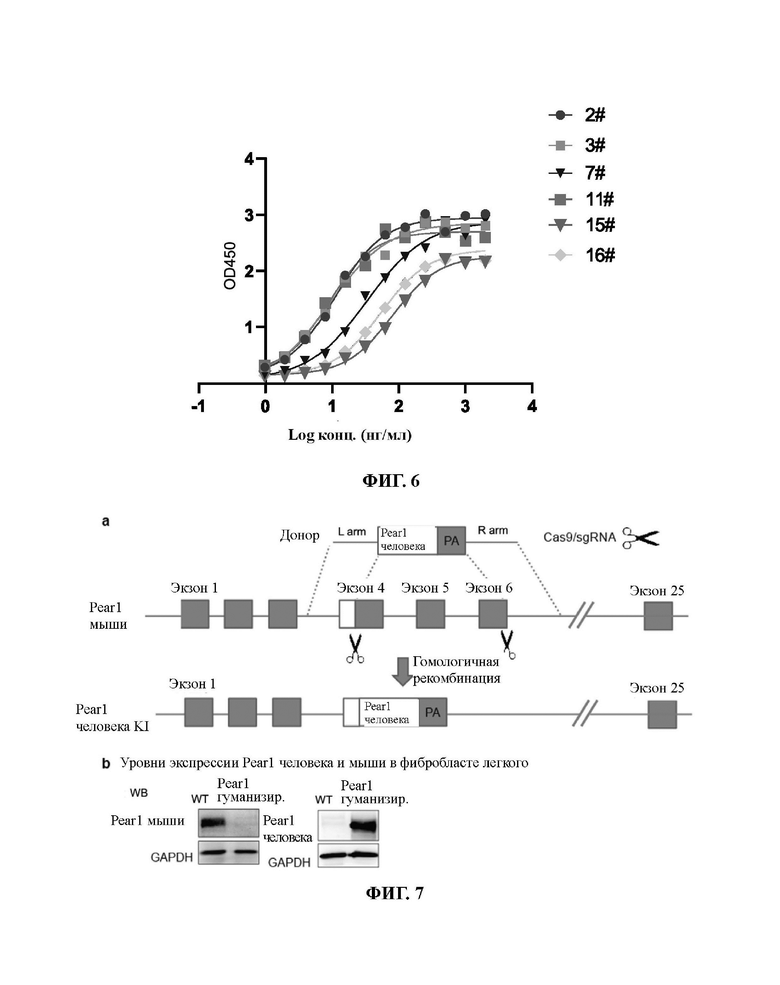
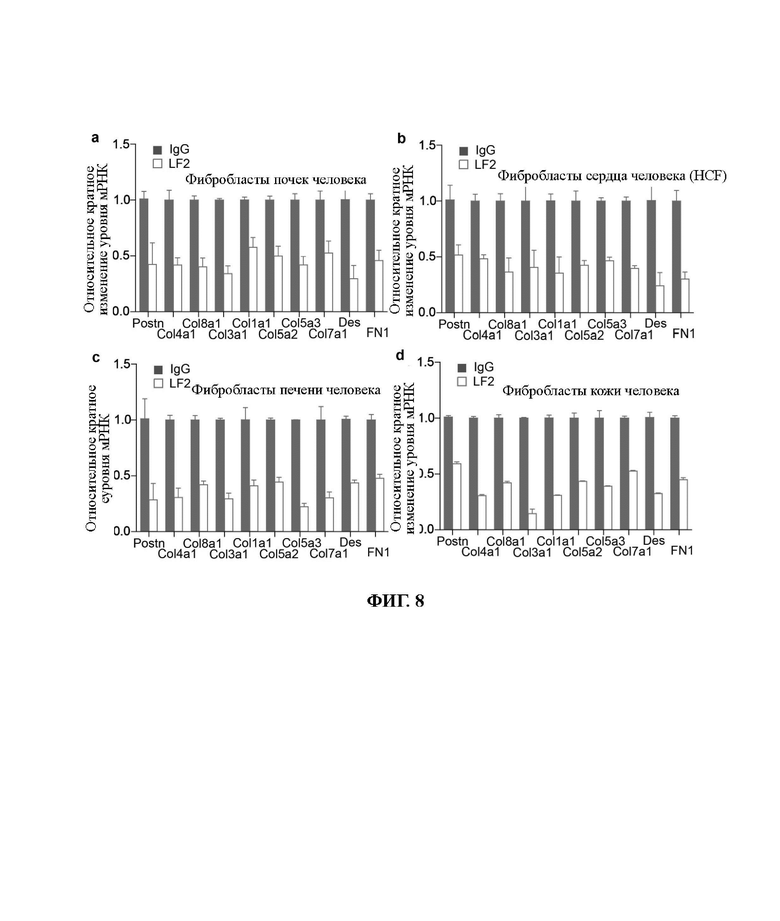
Группа изобретений относится к области биотехнологии и медицины. Предложено применение агониста Pear1 в получении лекарственного средства для ингибирования активации фибробластов. Также раскрыты направленно воздействующие на Pear1 антитело и его антигенсвязывающий фрагмент и их получение и применение. Раскрыт способ скрининга лекарственного средства для ингибирования активации фибробластов. Изобретения обеспечивают противофиброзный эффект активации Pear1 фибробластов с использованием агонистов Pear1 и, в частности, антитела, направленно воздействующего на Pear1, ингибирующих способность фибробластов синтезировать внеклеточный матрикс, имеют широкие перспективы применения в лечении фиброзирующих заболеваний и сопутствующих тяжело протекающих заболеваний. 9 н. и 18 з.п. ф-лы, 8 ил., 7 табл., 10 пр.
1. Применение агониста Pear1 (эндотелиальный рецептор агрегации тромбоцитов 1) в получении лекарственного средства для ингибирования активации фибробластов.
2. Применение по п. 1, где указанное лекарственное средство предназначено для понижающей регуляции и/или ингибирования сигнального пути активации фибробластов.
3. Применение по п. 1 или 2, где указанное лекарственное средство предназначено для лечения фиброзирующих заболеваний, стимулирования регенерации повреждений и/или заживления ран.
4. Применение по п. 3, где фиброзирующее заболевание включает в себя фиброз легких, фиброз печени, фиброз сердца, фиброз почек, фиброз костного мозга, рубец на коже и/или рубец мягких тканей.
5. Применение по п. 4, где фиброз легких представляет собой идиопатический фиброз легких; предпочтительно фиброз легких дополнительно включает в себя рестриктивное заболевание легких, сопровождающееся фиброзом легких.
6. Применение по п. 1, где агонист усиливает экспрессию и/или активность Pear1 или агонист содержит антитело, направленно воздействующее на Pear1, или его антигенсвязывающий фрагмент, FcεR1α, декстрана сульфат, фукозу или их комбинацию.
7. Выделенное антитело или его антигенсвязывающий фрагмент, направленно воздействующее(ий) на Pear1, где антитело содержит вариабельную область тяжелой цепи и вариабельную область легкой цепи; где указанные области содержат совокупности CDR, имеющие следующие аминокислотные последовательности:
(1) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(2) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 29 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(3) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 26, SEQ ID NO: 30 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 47, SAS и SEQ ID NO: 48 соответственно; или
(4) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 26, SEQ ID NO: 27 и SEQ ID NO: 29 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 49, DTS и SEQ ID NO: 50 соответственно; или
(5) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 31, SEQ ID NO: 27 и SEQ ID NO: 32 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 51, GAT и SEQ ID NO: 52 соответственно; или
(6) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 33, SEQ ID NO: 34 и SEQ ID NO: 35 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(7) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 39, SEQ ID NO: 27 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(8) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 39, SEQ ID NO: 40 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(9) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 39, SEQ ID NO: 41 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(10) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 39, SEQ ID NO: 42 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(11) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 39, SEQ ID NO: 43 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно; или
(12) аминокислотные последовательности HCDR1, HCDR2 и HCDR3 вариабельной области тяжелой цепи, как представлено в SEQ ID NO: 39, SEQ ID NO: 44 и SEQ ID NO: 28 соответственно; и
аминокислотные последовательности LCDR1, LCDR2 и LCDR3 вариабельной области легкой цепи, как представлено в SEQ ID NO: 45, GAT и SEQ ID NO: 46 соответственно.
8. Выделенное антитело или его антигенсвязывающий фрагмент, направленно воздействующее(ий) на Pear1, по п. 7, где указанный антигенсвязывающий фрагмент имеет идентичность 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99% с аминокислотной последовательностью антитела.
9. Выделенное антитело или его антигенсвязывающий фрагмент, направленно воздействующее(ий) на Pear1, по п. 7, где антитело представляет собой полноразмерное антитело, Fab, Fab', F(ab')2, Fv, такой как scFv, биспецифическое антитело, мультиспецифическое антитело, или однодоменное антитело, или моноклональное антитело, или поликлональное антитело; или антитело или его антигенсвязывающий фрагмент представляет собой полноразмерное антитело, и константная область тяжелой цепи полноразмерного антитела выбрана из константной области тяжелой цепи hIgG1, hIgG2, hIgG3, hIgG4.
10. Выделенное антитело или его антигенсвязывающий фрагмент, направленно воздействующее(ий) на Pear1, по п. 7, где HCDR1 антигенсвязывающего фрагмента мутирована с S на A или T в третьей позиции, с G на D в шестой позиции и/или с P на T или Y в восьмой позиции аминокислотной последовательности, которая представлена в SEQ ID NO: 26, и/или HCDR2 антигенсвязывающего фрагмента мутирована с P на S или G в третьей позиции, с Y на N в четвертой позиции и/или с T на A в восьмой позиции аминокислотной последовательности, которая представлена в SEQ ID NO: 27, и/или HCDR3 антигенсвязывающего фрагмента мутирована с A на D в девятой позиции и/или с Y на F в десятой позиции аминокислотной последовательности, которая представлена в SEQ ID NO: 28.
11. Выделенное антитело или его антигенсвязывающий фрагмент, направленно воздействующее(ий) на Pear1, по п. 7, где HFR (каркасный участок вариабельной области тяжелой цепи) 1 антитела или его антигенсвязывающего фрагмента содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 114, 115 и SEQ ID NO: 116; HFR2 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 117, 118, 119, 120, 121, 122, 123, 124 и SEQ ID NO: 125; и HFR3 содержит любую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 126, 127, 128, 129, 130, 131, 132, 133, 134 и SEQ ID NO: 135; и HFR4 содержит любую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 136 и SEQ ID NO: 137; и LFR (каркасный участок вариабельной области легкой цепи) 1 антитела или его антигенсвязывающего фрагмента содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 138, 139, 140, 141, 142 и SEQ ID NO: 143; LFR2 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 144, 145, 146, 147, 148 и SEQ ID NO: 149; и LFR3 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 150, 151, 152, 153, 154, 155, 156 и SEQ ID NO: 157; и LFR4 содержит любую аминокислотную последовательность, выбранную из SEQ ID NO: 158, 159, 160, 161 и SEQ ID NO: 162.
12. Выделенное антитело или его антигенсвязывающий фрагмент, направленно воздействующее(ий) на Pear1, по п. 7, где аминокислотные последовательности указанной вариабельной области легкой цепи и указанной вариабельной области тяжелой цепи представлены как SEQ ID NO: 16 и SEQ ID NO: 1 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 16 и SEQ ID NO: 2 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи соответственно такие, как представлено в SEQ ID NO: 17 и SEQ ID NO: 3; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 18 и SEQ ID NO: 2 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 19 и SEQ ID NO: 4 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 20 и SEQ ID NO: 5 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 21 и SEQ ID NO: 6 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 23 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 24 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 25 и SEQ ID NO: 7 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 23 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 24 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 25 и SEQ ID NO: 8 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 23 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 24 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 25 и SEQ ID NO: 9 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 22 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 23 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 24 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 25 и SEQ ID NO: 10 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 22 и SEQ ID NO: 11 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены как SEQ ID NO: 22 и SEQ ID NO: 12 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи представлены в SEQ ID NO: 22 и SEQ ID NO: 13 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 14 соответственно; или аминокислотные последовательности вариабельной области легкой цепи и вариабельной области тяжелой цепи такие, как представлено в SEQ ID NO: 22 и SEQ ID NO: 15 соответственно.
13. Выделенная нуклеиновая кислота, кодирующая антитело или его антигенсвязывающий фрагмент по пп. 7-12.
14. Рекомбинантный экспрессионный вектор, содержащий выделенную нуклеиновую кислоту по п. 13.
15. Трансформант для экспрессии антитела, направленно воздействующего на Pear1, содержащий выделенную нуклеиновую кислоту по п. 13 или рекомбинантный экспрессионный вектор по п. 14.
16. Лекарственное средство для ингибирования активации фибробластов, содержащее антитело или его антигенсвязывающий фрагмент по любому из пп. 7-12 в эффективном количестве.
17. Лекарственное средство по п. 16, где указанное лекарственное средство представляет собой фармацевтическую композицию; предпочтительно фармацевтическая композиция дополнительно содержит фармацевтически приемлемый носитель; предпочтительно фармацевтическая композиция содержит один или более агонистов Pear1.
18. Применение антитела или его антигенсвязывающего фрагмента по любому из пп. 7-12, нуклеиновой кислоты по п. 13, рекомбинантного экспрессионного вектора по п. 14 или трансформанта по п. 15 в получении лекарственного средства для ингибирования активации фибробластов.
19. Применение по п. 18, где указанное лекарственное средство предназначено для понижающей регуляции и/или ингибирования сигнального пути активации фибробластов.
20. Применение по п. 18 или 19, где указанное лекарственное средство предназначено для лечения фиброзирующих заболеваний, стимулирования регенерации повреждений и/или заживления ран.
21. Применение по п. 20, где фиброзирующее заболевание включает в себя фиброз легких, фиброз печени, фиброз сердца, фиброз почек, фиброз костного мозга, рубец на коже и/или рубец мягких тканей; предпочтительно фиброз легких представляет собой идиопатический фиброз легких; предпочтительно фиброз легких дополнительно включает в себя рестриктивное заболевание легких, сопровождающееся фиброзом легких.
22. Способ скрининга лекарственного средства для ингибирования активации фибробластов, включающий стадии (1) добавления или не добавления антитела, направленно воздействующего на Pear1, в систему культивирования фибробластов тестируемой группы или контрольной группы соответственно; (2) сравнение активации фибробластов в тестируемой группе и контрольной группе путем тестирования аффинности связывания антитела c внеклеточным сегментом Pear1; и (3) подтверждение, что данное антитело является агонистом Pear1, если активация фибробластов в тестируемой группе значительно ниже, чем в контрольной группе, указанный агонист Pear1 представляет собой лекарственное средство для ингибирования активации фибробластов.
23. Способ по п. 22, где указанное лекарственное средство предназначено для понижающей регуляции и/или ингибирования сигнального пути активации фибробластов.
24. Способ по п. 22 или 23, где указанное лекарственное средство предназначено для лечения фиброзирующих заболеваний, стимулирования регенерации повреждений и/или заживления ран.
25. Способ направленного воздействия на Pear1 для ингибирования активации фибробластов, включающий введение нуждающемуся индивидууму агониста Pear1, где указанный агонист представляет собой антитело, направленно воздействующее на Pear1 или его (Fab)2 или Fab фрагмента или FcR1, декстрана сульфат, фукозу или их комбинацию.
26. Способ по п. 25, где указанное ингибирование активации фибробластов предназначено для лечения фиброза легких, рестриктивных заболеваний легких, сопровождающихся фиброзом легких, и других связанных с фиброзом заболеваний, стимулирования регенерации повреждений и/или заживления ран.
27. Способ по п. 25 или 26, где введение включает ингаляционное введение, легочную пульверизацию, местную инъекцию, трансдермальное всасывание, подкожную инъекцию или местное нанесение.
| CN 109486943 A, 19.03.2019 | |||
| CN 109055530 A, 21.12.2018 | |||
| CN 0105671142 A, 15.06.2016 | |||
| NCBI Reference Sequence: XP_016856729.1, 06.12.2019, platelet endothelial aggregation receptor 1 isoform X6 [Homo sapiens] | |||
| NCBI Reference Sequence: XP_009241123.2, 28.02.2018, platelet endothelial aggregation receptor 1 isoform X3 [Pongo abelii] | |||
| КОМПОЗИЦИИ И СПОСОБЫ ПРОФИЛАКТИКИ ИЛИ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, СОСТОЯНИЙ ИЛИ ПРОЦЕССОВ, ХАРАКТЕРИЗУЕМЫХ АБЕРРАНТНОЙ ПРОЛИФЕРАЦИЕЙ ФИБРОБЛАСТОВ И ОТЛОЖЕНИЕМ ВНЕКЛЕТОЧНОГО МАТРИКСА | 2012 |
|
RU2620066C2 |
Авторы
Даты
2024-11-25—Публикация
2021-01-25—Подача