ОБЛАСТЬ ТЕХНИКИ
[0001] Настоящее изобретение относится к новому способу обнаружения воздействия зеараленона (ZEN), включающему определение уровня экспрессии по меньшей мере одной микроРНК в тестируемом образце, а также к новому применению по меньшей мере одной микроРНК для обнаружения воздействия зеараленона (ZEN) в тестируемом образце.
ОПИСАНИЕ
[0002] Микотоксины представляют собой вторичные метаболиты плесеней, которые приводят к зависимым от концентрации эффектам, неблагоприятным для здоровья животных. В Северной и Центральной Европе микотоксины, продуцируемые полевыми грибами, такими как Fusarium graminearum или F. culmorum, чаще всего обнаруживают в кормах для животных (Streit et al. 2012. Toxins, 4, 788-809). Зеараленон (ZEN) считается одним из наиболее значимых микотоксинов Fusarium, особенно в свиноводстве. ZEN часто загрязняет кукурузу, но может также встречаться в различных других продуктах, таких как пшеница, ячмень или овес. В недавнем исследовании 88% протестированных образцов корма показали положительный результат в отношении наличия ZEN с медианной и максимальной концентрациями 20 мкг/кг и 11192 мкг/кг, соответственно (Kovalsky et al. 2016. Toxins, 8, E363). Свиньи особенно восприимчивы к воздействию ZEN, что объясняется видоспецифическим метаболизмом этого микотоксина (Fink-Gremmels and Malekinejad. 2007. Animal Feed Science and Technology, 137, 326-341). ZEN демонстрирует низкую острую токсичность, но действует как полный и частичный агонист рецепторов эстрогена α и β, соответственно (Zinedine et al. 2007. Food and Chemical Toxicology, 45, 1-18). Как следствие, воздействие ZEN на свиней приводит к нарушениям репродуктивной функции и фертильности. Например, у неполовозрелых свиней начинается развитие молочных желез при применении кормов, содержащих 1-5 ppm ZEN. Также наблюдаются вульвовагинит, отек вульвы и пролапсы прямой кишки (Osweiler, G. 1999. Mycotoxins. In: STRAW, В., DALLAIRE, S., MENGELING, W. & TAYLOR, D. (eds.) 8th Diseases of swine. Ames, Iowa, USA: Iowa State University Press; Osweiler, G. D. 2000. Mycotoxins: Contemporary issues of food animal health and productivity. Veterinary Clinics of North America: Food Animal Practice, 16, 511-530). У зрелых свиноматок результаты действия ZEN зависят от концентрации в корме, продолжительности воздействия и фазы гестации и варьируются от анэструса до уменьшения количества живых эмбрионов, увеличения количества мертворожденных поросят и выкидышей (Kordic et al. 1992. Journal of environmental pathology, toxicology and oncology: official organ of the International Society for Environmental Toxicology and Cancer, 11, 53-55). У новорожденных поросят от подвергшихся воздействию свиноматок было зафиксировано увеличение наружных половых органов и более высокая заболеваемость поросят дисплазией тазобедренных сустаов и тремором (Osweiler, G. 1999. Mycotoxins. In: STRAW, В., DALLAIRE, S., MENGELING, W. & TAYLOR, D. (eds.) 8th Diseases of swine. Ames, Iowa, USA: Iowa State University Press). Кроме того, ZEN активирует различные рецепторы, особенно прегнан-Х-рецептор, участвующий в регуляции изоформ цитохрома Р450 in vitro, тем самым потенциально оказывая влияние на фазу I метаболизма различных эндо- и ксенобиотиков (Ayed-Boussema et al. 2011. Environmental Toxicology and Pharmacology, 31, 79-87).
[0003] До настоящего момента обнаружение микотоксикоза ZEN в основном основывалось на наблюдении клинических признаков и анализе корма. Тем не менее, ZEN, как и многие другие микотоксины, демонстрирует воздействия, неблагоприятные для здоровья скота до того, как клинические симптомы становятся очевидными. Анализ образцов корма сопровождается определенными проблемами: Репрезентативные образцы корма необходимо отбирать с учетом неоднородного распределения микотоксинов в партии, а также момента времени отбора проб, поскольку партии корма могли измениться между отбором проб и началом появления эффектов, вызванных микотоксином. Кроме того, необходимо учитывать сопутствующее загрязнение образцов корма микотоксином, которое может привести к аддитивному, синергическому или антагонистическому эффектам у животных (Grenier and Oswald. 2011. World Mycotoxin Journal, 4, 285-313). Более того, наличие модифицированных форм ZEN не отслеживается регулярно, а суммируется с общей нагрузкой ZEN на индивидуум (Binder et al. 2017. Toxins, 9, 56). В отличие от анализа кормов, обнаружение специфичных биомаркеров в биологических матрицах свиней, таких как моча, фекалии, желчь или ткани, позволило бы обнаружить микотоксикоз на уровне индивидуума. В исследованиях микотоксинов применяют два типа биомаркеров: биомаркеры, основанные на воздействии, и биомаркеры, основанные на механизме (Baldwin et al. 2011. World Mycotoxin Journal, 4, 257-270). В то время как первые относятся к измерению самого микотоксина и/или его метаболитов, вторые относятся к специфичному биологическому ответу, например, увеличению/уменьшению уровней белка или клеточного метаболита, которые могут быть связаны с потреблением микотоксина. Что касается ZEN, то в последние годы предпринимались усилия по определению у свиней биомаркера, основанного на воздействии. В контролируемых условиях в многочисленных исследованиях изучали влияние увеличения концентраций токсинов на уровни ZEN и/или его метаболитов в крови, моче и желчи, а также в кале, спинномозговой жидкости, печени или спинном жире. Как правило, самые высокие концентрации ZEN и его метаболитов были извлечены из желчи и мочи с наилучшими коэффициентами корреляции, т.е. отношением употребленного ZEN к извлеченному ZEN, для желчи и мочи в качестве матриц, чем для других матриц, таких как кровь ( et al. 2003. Archives of Animal Nutrition, 57, 311-334; Goyarts et al. 2007. Food Additives and Contaminants, 24, 369-380; Brezina et al. 2014. Archives of animal nutrition, 68, 425-447). В соответствии с этим в недавнем полевом исследовании не удалось сопоставить уровни ZEN в корме для свиноматок с уровнями в плазме, поскольку концентрации токсинов в плазме были ниже предела количественного определения в большинстве образцов (Van Limbergen et al. 2017. Veterinary Record, 181, 539). Биомаркеры, основанные на воздействии, все еще не могут быть рекомендованы для прогнозирования употребления ZEN в полевых условиях, поскольку сопоставимые концентрации ZEN в желчи, крови или моче могут быть получены из широкого диапазона уровней воздействия ZEN (
et al. 2003. Archives of Animal Nutrition, 57, 311-334; Goyarts et al. 2007. Food Additives and Contaminants, 24, 369-380; Brezina et al. 2014. Archives of animal nutrition, 68, 425-447). В соответствии с этим в недавнем полевом исследовании не удалось сопоставить уровни ZEN в корме для свиноматок с уровнями в плазме, поскольку концентрации токсинов в плазме были ниже предела количественного определения в большинстве образцов (Van Limbergen et al. 2017. Veterinary Record, 181, 539). Биомаркеры, основанные на воздействии, все еще не могут быть рекомендованы для прогнозирования употребления ZEN в полевых условиях, поскольку сопоставимые концентрации ZEN в желчи, крови или моче могут быть получены из широкого диапазона уровней воздействия ZEN ( and Winkler. 2015. Food and Chemical Toxicology, 84, 225-249). Чаще всего остатки ZEN не указывают на тяжесть эффектов, неблагоприятных для здоровья, вызванных ZEN, о чем свидетельствует, например, отсутствие корреляции между общими уровнями ZEN в желчи и массой матки после воздействия ZEN (
and Winkler. 2015. Food and Chemical Toxicology, 84, 225-249). Чаще всего остатки ZEN не указывают на тяжесть эффектов, неблагоприятных для здоровья, вызванных ZEN, о чем свидетельствует, например, отсутствие корреляции между общими уровнями ZEN в желчи и массой матки после воздействия ZEN ( and Winkler. 2015. Food and Chemical Toxicology, 84, 225-249). Что касается биомаркеров ZEN, основанных на механизме, было обнаружено изменение некоторых биологических параметров, таких как гематологические и биохимические параметры (Goyarts et al. 2007. Food Additives and Contaminants, 24, 369-380;
and Winkler. 2015. Food and Chemical Toxicology, 84, 225-249). Что касается биомаркеров ZEN, основанных на механизме, было обнаружено изменение некоторых биологических параметров, таких как гематологические и биохимические параметры (Goyarts et al. 2007. Food Additives and Contaminants, 24, 369-380;  et al. 2016. Research in Veterinary Science, 109, 169-180) или экспрессия мРНК (Dai et al. 2016. Animal Reproduction Science, 168, 126-137; Reddy et al. 2017. Asian-Australasian Journal of Animal Sciences, 31, 595-606; Zhou et al. 2018. Asian-Australasian Journal of Animal Sciences, 31, 32), при воздействии ZEN in vivo. Однако воспроизводимость и специфичность исследуемых параметров ограничена в той степени, что пока не удалось установить четкую зависимость «доза-ответ» между увеличением/уменьшением этих биологических параметров в крови, моче или желчи и употреблением ZEN. Не et al. (Не et al. 2018. Endocrinology, 159, 2993-3006) описывают повышение экспрессии микроРНК (miRNA) miR-7 в ткани гипофиза свиней с овариэктомией после внутрибрюшинной инъекции 112,5 мг ZEN в сутки. Тем не менее, Не et al. применяли экспериментальную схему, которая не отражает естественное воздействие ZEN вследствие загрязненного корма, поскольку количество 112,5 мг ZEN намного превышает реальный уровень воздействия. Кроме того, введение путем инъекций не отражает естественное употребление корма. Кроме того, свиньи с овариэктомией не являются хорошими моделями воздействия ZEN на здоровых свиней, не подвергшихся овариэктомии, поскольку воздействие ZEN обычно коррелирует с нарушениями репродуктивной функции и фертильности. Кроме того, было бы желательно идентифицировать биомаркер, который был бы подходящим для обнаружения воздействия ZEN, в более доступном образце, чем ткань гипофиза, таком как сыворотка.
et al. 2016. Research in Veterinary Science, 109, 169-180) или экспрессия мРНК (Dai et al. 2016. Animal Reproduction Science, 168, 126-137; Reddy et al. 2017. Asian-Australasian Journal of Animal Sciences, 31, 595-606; Zhou et al. 2018. Asian-Australasian Journal of Animal Sciences, 31, 32), при воздействии ZEN in vivo. Однако воспроизводимость и специфичность исследуемых параметров ограничена в той степени, что пока не удалось установить четкую зависимость «доза-ответ» между увеличением/уменьшением этих биологических параметров в крови, моче или желчи и употреблением ZEN. Не et al. (Не et al. 2018. Endocrinology, 159, 2993-3006) описывают повышение экспрессии микроРНК (miRNA) miR-7 в ткани гипофиза свиней с овариэктомией после внутрибрюшинной инъекции 112,5 мг ZEN в сутки. Тем не менее, Не et al. применяли экспериментальную схему, которая не отражает естественное воздействие ZEN вследствие загрязненного корма, поскольку количество 112,5 мг ZEN намного превышает реальный уровень воздействия. Кроме того, введение путем инъекций не отражает естественное употребление корма. Кроме того, свиньи с овариэктомией не являются хорошими моделями воздействия ZEN на здоровых свиней, не подвергшихся овариэктомии, поскольку воздействие ZEN обычно коррелирует с нарушениями репродуктивной функции и фертильности. Кроме того, было бы желательно идентифицировать биомаркер, который был бы подходящим для обнаружения воздействия ZEN, в более доступном образце, чем ткань гипофиза, таком как сыворотка.
[0004] Настоящее изобретение было осуществлено с учетом уровня техники, описанного выше. В целом, авторы настоящей заявки обнаружили, что биомаркеры, основанные на механизме, были бы более подходящими для применения в области обнаружения микотоксикоза, чем биомаркеры, основанные на воздействии, вследствие более простых способов обнаружения и прямой корреляции с действием микотоксина у индивидуума, но до сих пор подходящий биомаркер, основанный на воздействии или биомаркер, основанный на механизме, не был идентифицирован.
[0005] Настоящее изобретение относится к способу обнаружения воздействия зеараленона (ZEN), при этом способ включает определение в тестируемом образце уровня экспрессии по меньшей мере одной микроРНК, описанной в настоящей заявке; и сравнение уровня экспрессии с уровнем экспрессии указанной по меньшей мере одной микроРНК в контрольном образце. МикроРНК (также называемые microRNA) представляют собой короткие молекулы РНК длиной обычно от приблизительно 19 до приблизительно 24 нуклеотидов. МикроРНК представляют собой отрицательные регуляторы экспрессии генов, способные блокировать трансляцию мРНК в белки или деградировать молекулы мРНК. Посредством обеспечения способа обнаружения воздействия ZEN, включающего определение в тестируемом образце уровня экспрессии по меньшей мере одной микроРНК, описанной в настоящей заявке; и сравнение уровня экспрессии с референсным значением, авторы неожиданно идентифицировали надежный способ обнаружения воздействия ZEN с помощью биомаркера, основанного на воздействии, который подходит для применения в данной области техники.
[0006] Термин "уровень экспрессии" полинуклеотида, такого как, например, молекула мРНК или микроРНК, относится к относительному или абсолютному количеству указанного полинуклеотида. Уровни экспрессии полинуклеотидов могут быть определены с помощью соответствующих стратегий, известных специалисту в данной области техники, включая, но не ограничиваясь ими, эксперименты с применением биочипов, количественную ПЦР в реальном времени или так называемые технологии секвенирования следующего поколения (NGS), предлагаемые, например, Illumina, Pacific Biosciences, Oxford Nanopore Technologies etc.
[0007] Зеараленон (ZEN) представляет собой нестероидный макроциклический лактон со следующей структурной формулой, который может быть синтезирован посредством метаболического пути поликетидов:
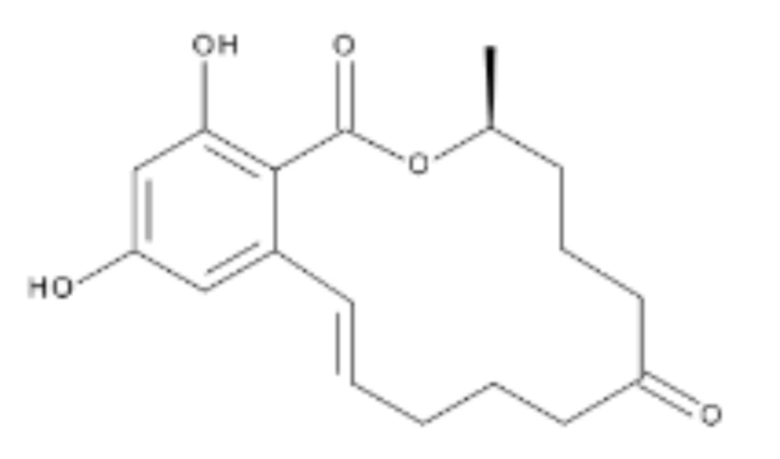
Его название в соответствии с номенклатурой ИЮПАК представляет собой: (2E,11S)-15,17-дигидрокси-11-метил-12-оксабицикло[12.4.0]октадека-1(18),2,14,16-тетраен-7,13-дион. Различные производные ZEN также встречаются в природе и могут быть образованы ферментативными или химическими модификациями ZEN. Примеры включают, но не ограничиваются ими, гликозидные конъюгаты ZEN или конъюгаты, содержащие сульфат, образованные при метаболизме грибов, растений или млекопитающих, а также метаболиты ZEN, образованные в организме человека или животных, среди прочего. Под производными ZEN ниже понимают конъюгаты ZEN или метаболиты ZEN, которые встречаются в природе или синтезированы путем химического или биохимического синтеза, но, в частности, α-зеараленол (α-ZEL; (2E,7R,11S)-7,15,17-тригидрокси-11-метил-12-оксабицикло[12.4.0]-октадека-1(18),2,14,16-тетраен-13-он), β-зеараленол (β-ZEL; (2Е,78,118)-7,15,17-тригидрокси-11-метил-12-оксабицикло[12.4.0]октадека-1(18),2,14,16-тетраен-13-он), α-зеараланол (α-ZAL; (7R,11S)-7,15,17-тригидрокси-11-метил-12-оксабицикло[12.4.0]октадека-1(18), 14,16-триен-13-он), β-зеараланол(β-ZAL; (78,118)-7,15,17-тригидрокси-11-метил-12-оксабицикло[12.4.0]октадека-1(14),15,17-триен-13-он), зеараленон 14-сульфат (Z14S; [(2Е, 11S)-15-гидрокси-11-метил-7,13-диоксо-12-оксабицикло[12.4.0]октадека-1(18),2,14,16-тетраен-17-ил]гидросульфат), зеараленон-14-гликозид (Z14G; (2E,11S)-15-гидрокси-11-метил-17-[(3R,4S,5S,6R)-3,4,5-тригидрокси-6-(гидроксиметил)-тетрагидропиран-2-ил]окси-12-оксабицикло[12.4.0]октадека 1(18)2,14,16-тетраен-7,13-дион), а также зеараланон (ZAN; (118)-15,17-дигидрокси-11-метил-12-оксабицикло-[12.4.0]октадека-1(18),14,16-триен-7,13-дион). ZEN, а также производные ZEN, в частности α-ZEL, β-ZEL, Z14S, α-ZAL, β-ZAL, Z14G и ZAN, также могут быть обнаружены в обработанных пищевых продуктах и продуктах питания для животных, таких как хлеб или пиво, вследствие их высокой химической и физической стабильности.
[0008] В данном контексте термин "воздействие/эффект зеараленона" или "воздействие ZEN" относится к воздействию зеараленона на биологическую систему или к (физиологическому) влиянию зеараленона на биологическую систему. Биологическая система может представлять собой любую биологическую систему, такую как клетка, культура клеток, ткань или животное. В некоторых вариантах реализации "эффект зеараленона" может дополнительно относиться к воздействию на биологическую систему производного или аналога зеараленона или к (физиологическому) эффекту производного или аналога зеараленона на биологическую систему. Производное зеараленона предпочтительно представляет собой производное, описанное в настоящей заявке выше. Следует понимать, что производное или аналог зеараленона предпочтительно имеет такой же или аналогичный эффект, что и зеараленон, на биологическую систему. Предпочтительно, "эффект зеараленона" относится к воздействию зеараленона.
[0009] В настоящей заявке "тестируемый образец" предпочтительно относится к образцу, для которого необходимо определить, вступал ли он в контакт с ZEN (или аналогом или производным ZEN) или нет, или подвергался ли субъект, у которого он получен, воздействию ZEN (или аналога или производного ZEN) или нет. Способы согласно настоящему изобретению могут, таким образом, включать стадию (b) получения тестируемого образца.
[0010] Референсное значение может соответствовать уровню экспрессии указанной по меньшей мере одной микроРНК согласно настоящему изобретению, который был определен в одном или более контрольных образцах. В зависимости от типа образца, такой контрольный образец мог вступать в контакт с (предпочтительно с известным количеством) ZEN или аналогом или производным ZEN, или контрольный образец не вступал в контакт с ZEN или аналогом или производным ZEN. Такой контрольный образец мог быть получен у субъекта, который подвергался воздействию (предпочтительно известного количества) ZEN или аналога или производного ZEN, или мог быть получен у субъекта, который не подвергался воздействию ZEN или аналога или производного ZEN. В настоящей заявке контакт образца с ZEN или аналогом или производным ZEN, которые не являются биодоступными, например, вследствие связывания с другим веществом, что предотвращает взаимодействие ZEN или аналога или производного ZEN с биологической системой, или воздействие на субъект ZEN или аналога или производного ZEN, которые не являются биодоступными, эквивалентно отсутствию контакта ZEN или аналога или производного ZEN с образцом или отсутствию воздействия на субъект ZEN или аналога или производного ZEN. Референсное значение также может представлять собой усредненное или среднее значение, которое было определено в нескольких контрольных образцах. По меньшей мере одна микроРНК согласно настоящему изобретению может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-125a, ssc-miR-125b, ssc-miR-127, ssc-miR-129a, ssc-miR-133a-5p, ssc-miR-135, ssc-miR-136, ssc-miR-140-3р, ssc-miR-142-3р, ssc-miR-143-5p, ssc-miR-146b, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-miR-187, ssc-miR-195, ssc-miR-204, ssc-miR-206, ssc-miR-22-3p, ssc-miR-22-5p, ssc-miR-335, ssc-miR-34a, ssc-miR-369, ssc-miR-378, ssc-miR-424-5p, ssc-miR-432-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-486, ssc-miR-493-3р, ssc-miR-493-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-708-3р, ssc-miR-758, ssc-miR-7135-3р, hsa-miR-135b-5p, hsa-miR-301a-5p, put-miR-300. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183, ssc-miR-140-3р, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497. По меньшей мере одна микроРНК согласно настоящему изобретению также может представлять собой комбинацию двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати или даже более или всех микроРНК, выбранных из вышеуказанной группы.
[0011] Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183 и ssc-miR-140-3р. По меньшей мере одна микроРНК согласно настоящему изобретению также может представлять собой комбинацию двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати, четырнадцати или всех пятнадцати микроРНК, выбранных из вышеуказанной группы. Таким образом, эффект зеараленона может быть определен с особенно высокой надежностью. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению выбрана из группы, состоящей из ssc-miR-542-3р, ssc-miR-1, ssc-miR-493-3р, ssc-miR-135, ssc-miR-432-5p и ssc-miR-455-5р. По меньшей мере одна микроРНК согласно настоящему изобретению также может представлять собой комбинацию двух, трех, четырех, пяти или всех шести микроРНК, выбранных из вышеуказанной группы. Предпочтительные комбинации двух микроРНК, выбранных из вышеуказанной группы, содержат пару, выбранную из группы, состоящей из ssc-miR-542-3р и ssc-miR-1, ssc-miR-542-3р и ssc-miR-493-3р, ssc-miR-135 и ssc-miR-432-5р, и ssc-miR-455-5p и ssc-miR-493-3р. Предпочтительные комбинации могут также содержать две, три или четыре из вышеуказанных пар. Таким образом, точность результатов способа может быть увеличена.
[0012] Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p и ssc-miR-497. По меньшей мере одна микроРНК согласно настоящему изобретению также может представлять собой комбинацию двух, трех, четырех, пяти, шести, семи, восьми, девяти, десяти, одиннадцати, двенадцати, тринадцати, четырнадцати, пятнадцати или всех шестнадцати микроРНК, выбранных из вышеуказанной группы. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению представляет собой ssc-miR-542-3р и/или ssc-miR-1.
[0013] В настоящей заявке, если не указано иное, микроРНК обозначены номерами доступа базы данных последовательностей miRBase в версии от 21 июня 2014 г. (Kozomara A, Griffiths-Jones S. Nucleic Acids Res. 2014 42:D68-D73; Kozomara A, Griffiths-Jones S. Nucleic Acids Res. 2011 39:D152-D157; Griffiths-Jones S, Saini HK, van Dongen S, Enright AJ. Nucleic Acids Res. 2008 36:D154-D158;Griffiths-Jones S, Grocock RJ, van Dongen S, Bateman A, Enright AJ. Nucleic Acids Res. 2006 34:D140-D144; Griffiths-Jones S. Nucleic Acids Res. 2004 32:D109-D111). В следующей таблице кратко охарактеризованы некоторые микроРНК согласно настоящему изобретению.

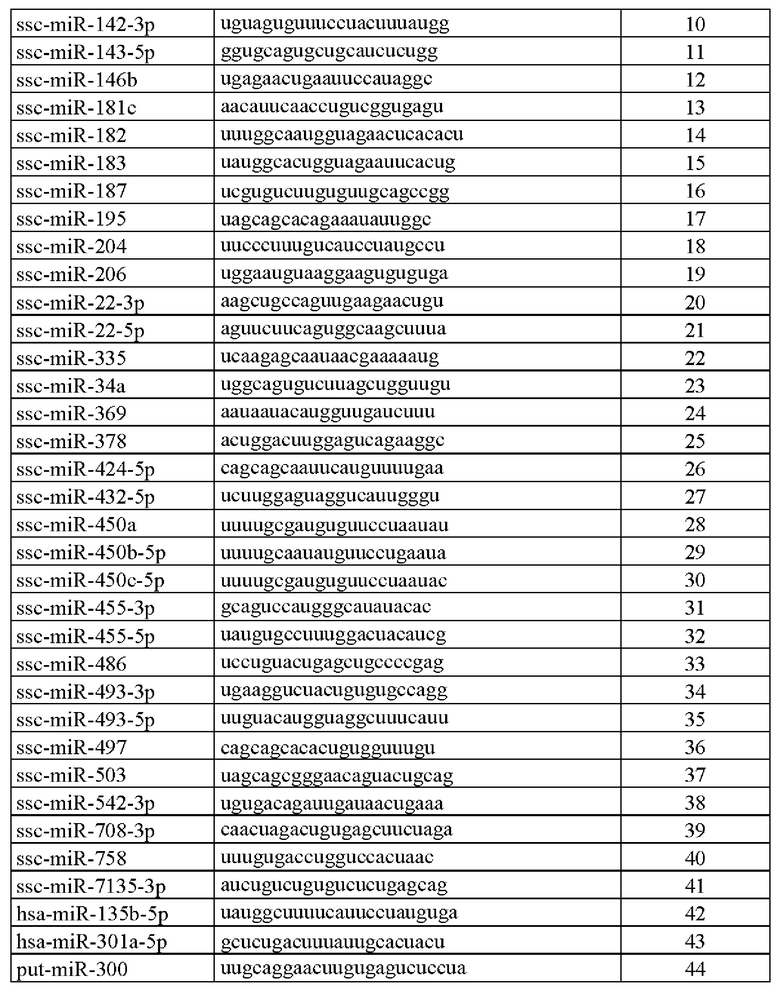
[0014] Способы согласно настоящему изобретению могут включать сравнение уровня по меньшей мере одной микроРНК, определенной в тестируемом образце, с референсным значением. Если по меньшей мере одна микроРНК включает более одной микроРНК, сравнение уровня между этими микроРНК может включать сравнение соотношения между двумя микроРНК. Например, если по меньшей мере одна микроРНК включает две, три, четыре или пять микроРНК, выбранных из группы, состоящей из или содержащей по меньшей мере некоторые, предпочтительно все из ssc-miR-542-3р, ssc-miR-1, ssc-miR-493-3р, ssc-miR-135, ssc-miR-432-5p и ssc-miR-455-5p, сравнение уровня может относиться к сравнению соотношения между ssc-miR-542-3р и ssc-miR-1, ssc-miR-542-3р и ssc-miR-493-3р, ssc-miR-135 и ssc-miR-432-5p и/или ssc-miR-455-5p и ssc-miR-493-3р. Сравнение уровня также может относиться к сравнению соотношения между любыми парами микроРНК, показанными на Фигуре 7.
[0015] Сравнение уровня указанной по меньшей мере одной микроРНК может быть основано на сравнении отдельных значений одной или более микроРНК. Например, отклонение уровней экспрессии микроРНК между тестируемым образцом и референсным значением может указывать на эффект зеараленона (например, воздействие зеараленона), в частности, если референсное значение соответствует уровню экспрессии указанной микроРНК в контрольном образце, который не вступал в контакт с зеараленоном или который был получен у субъекта, который не подвергался воздействию зеараленона. Отклонение уровней экспрессии может быть показательным в отношении воздействия зеараленона. Отклонение может быть выражено в нормальной шкале или предпочтительно в логарифмической шкале, такой как log2-шкала. Отклонение предпочтительно является статистически значимым. Специалисту в данной области техники известно несколько способов проверки статистической значимости результатов, и специалист в данной области техники может выбрать и применить наиболее подходящий способ анализа статистической значимости. Статистическая значимость может быть, например, выражена р-величиной или FDR скорректированной р-величиной, а уровень значимости может составлять ≤0,07, предпочтительно ≤0,05 или более предпочтительно ≤0,001. Отклонение может представлять собой увеличение или уменьшение. Отклонение, указывающее на воздействие ZEN, может, например, составлять по меньшей мере приблизительно 1,3 раза, более предпочтительно по меньшей мере приблизительно 1,5 раза и наиболее предпочтительно по меньшей мере приблизительно 2 раза по сравнению с референсным значением, соответствующим образцу, не вступавшему в контакт с зеараленоном или полученному от субъекта, не подвергавшегося воздействию зеараленона.
[0016] В качестве альтернативы, если референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, вступавшем в контакт с ZEN или аналогом ZEN или производным ZEN, или был получен у субъекта, который подвергался воздействию ZEN или аналога ZEN или производного ZEN, отсутствие отклонения, незначительное отклонение или (нетипично) низкое отклонение между значениями тестируемого образца и референсного значения может быть показательным в отношении воздействия зеараленона, такого как воздействие зеараленона.
[0017] Термин "обнаружение" или "детектирование" в настоящей заявке в контексте обнаружения воздействия зеараленона может в целом относиться к количественному или качественному обнаружению. Например, "обнаружение" может относиться к качественному обнаружению, то есть, присутствует ли эффект зеараленона на основании стадии сравнения. "Обнаружение" может также относиться к количественному обнаружению, т.е. к степени воздействия зеараленона на основании стадии сравнения.
[0018] В настоящей заявке термин "образец" относится к биологическому образцу. Образец может содержать клетку. Образец может быть получен у субъекта. Биологические образцы включают, но не ограничиваются ими, кровь, сыворотку, мононуклеарные клетки периферической крови (МКПК), мочу, фекалии, сперму или ткани, такие как ткань матки. Чтобы обеспечить быстрое обнаружение воздействия ZEN у субъекта и, таким образом, достичь максимальной применимости в полевых условиях, способ обнаружения предпочтительно применяют к образцу, который может быть получен с минимальными усилиями. Следовательно, образец предпочтительно представляет собой образец крови, в частности образец сыворотки крови. Путем обеспечения способа, в котором образец представляет собой образец сыворотки крови, потенциальное воздействие ZEN на субъект можно оценить наиболее удобным образом. Образец сыворотки крови можно получить, например, пункцией краниальной полой вены (Vena cava cranialis) или яремной вены (Vena jugalaris). Образцы сыворотки можно хранить при -80 °С для последующего анализа. Еще один предпочтительный образец представляет собой образец матки. Образец также может представлять собой образец клеточной культуры. Образец клеточной культуры может содержать интактные клетки, но может также содержать или состоять из разрушенных клеток и/или супернатанта интактных или разрушенных клеток. Клетки, содержащиеся в клеточной культуре, могут экспрессировать рецепторы эстрогена а и/или (3, предпочтительно рецепторы эстрогена а и/или р млекопитающих, таких как человек или свинья. Предпочтительные клеточные линии для образца клеточной культуры могут представлять собой MCF-7, T47D, SUM159, HeLa или Ishikawa. Кроме того, первичные клетки, такие как, например, зернистые клетки свиньи, могут представлять собой предпочтительные клетки для образца клеточной культуры.
[0019] Если образец представляет собой образец ткани матки, по меньшей мере одна микроРНК предпочтительно выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181с, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p и ssc-miR-497, причем по меньшей мере одна микроРНК предпочтительно представляет собой ssc-miR-542-3р и/или ssc-miR-1.
[0020] Если образец представляет собой образец крови, такой как образец сыворотки, по меньшей мере одна микроРНК может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183 и ssc-miR-140-3р, предпочтительно выбрана из группы, состоящей из ssc-miR-542-3р, ssc-miR-1, ssc-miR-493-3р, ssc-miR-135, ssc-miR-432-5p и ssc-miR-455-5p.
[0021] Сравнение уровня указанной по меньшей мере одной микроРНК также может быть основано на сравнении отдельных значений нескольких микроРНК. В данном случае относительные (или менее предпочтительные абсолютные) отклонения уровня экспрессии в тестируемом образце от референсного значения могут быть объединены для получения еще более значимого результата, чем сравнение уровня только одной микроРНК. В качестве альтернативы, значения отклонений могут быть умножены или разделены друг на друга, в зависимости от ожидаемого направления отклонения в случае воздействия зеараленона.
[0022] Сравнение уровня указанной по меньшей мере одной микроРНК также может относиться к сравнению соотношения двух микроРНК. Соотношение может быть определено путем деления уровня одной микроРНК на уровень второй микроРНК, как известно специалистам в данной области техники. Авторы настоящего изобретения обнаружили, что определение отклонения соотношений микроРНК, как описано выше, позволяет на удивление хорошо различать образцы, которые подвергались воздействию зеараленона (ZEN), и образцы, которые не подвергались воздействию зеараленона (ZEN). Если отдельные измеренные микроРНК анализируют с помощью кПЦР, возможным способом расчета соотношения является определение ΔCt (например, Ct микроРНК - Ct UniSp4) для каждой микроРНК для расчета соотношения. В качестве иллюстративного примера, соотношение между miR-135a и miR-1a может быть рассчитано с помощью ΔCt микроРНК 135а - ΔCt микроРНК 1а.
[0023] Исключительно хорошее обнаружение воздействия ZEN может быть достигнуто, когда по меньшей мере одно соотношение уровней экспрессии между двумя микроРНК выбрано из группы, состоящей из соотношений между miR-542-3р и miR-1, miR542-3p и miR493-3p, miR-135a-5p и miR-432-5p, и miR-455-5p и miR-493-3р. Соотношение может считаться предпочтительным для способа, описанного в настоящей заявке, если анализ рабочих характеристик (ROC) (Grand and Sabin. 2010. Current Opinion in HIV and AIDS, 5, 473-479) для различия воздействия ZEN по сравнению с отсутствием воздействия ZEN приводит к значению площади под кривой (AUC), которое составляет более или равное 0,7. В качестве альтернативы или дополнительно, кратное изменение соотношения микроРНК в образце, содержащем ZEN, предпочтительно составляет по меньшей мере приблизительно 1,3 раза, более предпочтительно по меньшей мере приблизительно 1,5 раза, наиболее предпочтительно по меньшей мере приблизительно 2 раза по сравнению с образцом, не вступавшим в контакт с ZEN или полученным от субъекта, не подвергавшегося воздействию ZEN. Кратное изменение может быть как положительным, так и отрицательным, т.е. положительно или отрицательно регулируемым по сравнению с контрольным образцом. Уровень по меньшей мере одной микроРНК еще более предпочтительно содержит по меньшей мере одно соотношение уровней экспрессии между двумя микроРНК, выбранными из группы, состоящей из miR-542-3р и miR-1, miR-542-3р и miR-493-3р, miR-135a-5p и miR-432-5p, и miR-455-5p и miR-493-3р. Таким образом, можно обнаружить воздействие ZEN с особенно хорошей надежностью и воспроизводимостью.
[0024] Сравнение уровня указанной по меньшей мере одной микроРНК с референсным значением, в частности, если задействовано несколько микроРНК, также может быть осуществлено с применением сложных способов, таких как компьютеризованные способы, в частности, способы, включающие машинное обучение. В качестве иллюстративного примера, система искусственной нейронной сети может быть использована для сравнения уровня(ей) экспрессии с референсным значением. Нейронная сеть может быть обучена путем обеспечения значения одного или более референсных значений, которые могут соответствовать уровням микроРНК из одного или более образцов. Предпочтительно, для обучения нейронной сети могут быть использованы как референсные значения воздействия ZEN, так и референсные значения отсутствия воздействия ZEN. Обученная нейронная сеть затем может быть использована для обнаружения воздействия зеараленона. Для этой цели значения уровня (уровней) микроРНК соответствующей микроРНК тестируемого образца могут быть использованы в качестве входных данных для нейронной сети, и нейронная сеть может обеспечивать выявление воздействия зеараленона, такое как качественная информация, количественная информация, оценка, вероятность или любой другой тип информации, подходящей для обнаружения или характеристики воздействия зеараленона. Способы построения, обучения и применения нейронной сети хорошо известны специалисту в данной области техники. Другие (компьютеризированные) подходы также могут быть пригодны для применения в настоящем изобретении и также известны специалисту в данной области техники, такие как, например, байесовские сети или деревья решений.
[0025] Как правило, результатом стадии сравнения (d) может быть любой тип информации, указывающей, вступал ли ли образец в контакт с ZEN (или аналогом или производным ZEN) или подвергался ли субъект, у которого был получен образец, воздействию ZEN (или аналога или производного ZEN). Информация может представлять собой качественную информацию, количественную информацию, оценку, вероятность или любой другой тип полезной информации. Способ согласно настоящему изобретению может, таким образом, включать дополнительную стадию(и) обеспечения информации относительно воздействия зеараленона. Информация может быть предоставлена с помощью любого подходящего средства, известного специалисту в данной области техники.
[0026] В настоящей заявке "субъект" относится к позвоночному, предпочтительно к млекопитающему. В настоящей заявке термин "млекопитающее" относится к любому животному, классифицируемому как млекопитающее, включая, не ограничиваясь ими, людей, домашних и сельскохозяйственных животных и животных зоопарка, спортивных животных или домашних животных, таких как овцы, собаки, лошади, кошки, коровы, крысы, свиньи, приматы, такие как яванские макаки, если привести только несколько иллюстративных примеров. Предпочтительный субъект относится к роду Sus, предпочтительно к виду Sus scrofa. Другим предпочтительным субъектом является человек.
[0027] Эффект ZEN, в частности воздействие ZEN, проявляется в виде эффектов, неблагоприятных для здоровья, таких как нарушения репродуктивной функции и фертильности, особенно у млекопитающих и особенно существенно у субъектов рода Sus. Для обеспечения наиболее быстрого обнаружения воздействия ZEN у указанных субъектов в настоящем изобретении также предложен способ, описанный выше, где субъект предпочтительно является млекопитающим, более предпочтительно из рода Sus.
[0028] Способы согласно настоящему изобретению могут быть использованы для диагностики, в частности, диагностики воздействия зеараленона на субъект. Такие способы могут быть предназначены для определения состояния здоровья субъекта, чтобы принять решение о необходимости принятия мер для поддержания или улучшения здоровья субъекта.
[0029] Способы согласно настоящему изобретению также могут быть недиагностическими. В качестве иллюстративного примера, недиагностический способ может представлять собой способ отбора проб корма. Отбор проб корма обычно не является очень точным вследствие неоднородного распределения микотоксинов в корме и типичных размеров проб, используемых для этого анализа. Вследствие поглощения сравнительно большого количества корма субъектом, таким как свинья, определение воздействия ZEN на субъект может обеспечить более надежный результат теста на загрязнение корма зеараленоном, чем анализ корма непосредственно. Таким образом, способы согласно настоящему изобретению могут представлять собой способы обнаружения зеараленона в корме или пище. Способы согласно настоящему изобретению могут включать, до получения тестируемого образца у субъекта, стадию (а) кормления субъекта кормом или пищей, предположительно содержащей зеараленон.
[0030] Чтобы избежать нежелательных последствий длительного воздействия зеараленона, может потребоваться обработка загрязненного ZEN корма или пищи нейтрализующим ZEN агентом или применение способа нейтрализации ZEN в случае обнаружения воздействия зеараленона у субъекта. Следовательно, в настоящем изобретении дополнительно предложен способ, описанный выше, отличающийся тем, что способ предназначен для выбора пищи или корма для приведения в контакт с нейтрализующим зеараленон агентом или для применения способа нейтрализации зеараленона. Посредством применения описанного способа выбора пищи или корма для приведения в контакт с нейтрализующим ZEN агентом или для применения способа нейтрализации ZEN можно по меньшей мере смягчить или полностью избежать эффектов, неблагоприятных для здоровья. Способы согласно настоящему изобретению могут, таким образом, включать стадию (а) кормления субъекта кормом, предположительно содержащим зеараленон, до получения тестируемого образца у субъекта. Способы согласно настоящему изобретению также могут включать стадию (f) выбора корма для приведения в контакт с нейтрализующим зеараленон агентом или применение способа нейтрализации зеараленона, если отклонение уровней экспрессии по меньшей мере одной микроРНК между тестируемым образцом и контрольным образцом указывает на воздействие зеараленона. Способы согласно настоящему изобретению, таким образом, могут включать обеспечение нейтрализующего зеараленон агента или применение способа нейтрализации зеараленона. Способы согласно настоящему изобретению могут также включать приведение корма или пищи, выбранной указанным способом, в контакт с нейтрализующим зеараленон агентом или применение способа нейтрализации зеараленона к корму.
[0031] Нейтрализующий зеараленон агент или способ может относиться к агенту или способу, который деградирует зераленон, например, путем изменения его молекулярной структуры, что может быть осуществлено путем химического, ферментативного или физического взаимодействия с нейтрализующим зеараленон агентом. Результатом такой обработки может являться менее токсичная молекула. Нейтрализующий зеараленон агент или способ также может снижать биодоступность зеараленона, например, зеараленон становится недоступным для субъекта, предпочтительно для системы пищеварения субъекта. Это может быть достигнуто, например, с помощью агента, который связывает или адсорбирует зеараленон. Как правило, нейтрализующий зеараленон агент может представлять собой любой подходящий тип агента, который может быть выбран из группы, состоящей из одного или более полипептидов, одного или более микроорганизмов и одного или более зеараленон-связывающих агентов.
[0032] Нейтрализующий зеараленон агент также может представлять собой α/β-гидролазу, способную трансформировать зеараленон или его производные или аналоги. Специалисту в данной области техники известны различные α/β-гидролазы, которые, среди прочего, описаны у Lenfant et al. (2013) 'ESTHER, the database of the α/β-hydrolase fold superfamily of proteins: tools to explore diversity of functions' Nucleic Acids Research, Volume 41, Issue D1, D423-D429 and Mindrebo et al. (2016) 'Unveiling the functional diversity of the Alpha-Beta hydrolase fold in plants' Curr Opin Struct Biol. 233-246. Вкратце, все α/β-гидролазы имеют свойство специфичной укладки, называемой α/β-укладкой (альфа/бета-укладка), α/β-укладка является общей для ряда гидролитических ферментов самого разного филогенетического происхождения и каталитической функции. Ядро каждого фермента представляет собой α/β-структуру (а не цилиндр), содержащую 8 β-нитей (b1-b8), соединенных а-спиралями (aA-aF) (Ollis et al. (1992) 'The alpha/beta hydrolase fold' Protein Eng. 5(3): 197-211). Следовательно, описанная в настоящей заявке α/β-гидролаза может содержать α/β-укладку. Описанная в настоящей заявке α/β-гидролаза предпочтительно включает основной домен α/β-гидролазы, состоящий из 8 β-нитей (b1-b8), расположенных на центральном β-листе, и дополнительно включает 6 перекрещивающихся α-спиралей (аА-aF).
[0033] Члены различных классов α/β-гидролаз, а также их структурные характеристики, среди прочего, описаны в Kourist et al. (2010) 'The alpha/beta-hydrolase fold 3DM database (ABHDB) as a tool for protein engineering.' Chembiochem. 11(12): 1635-43).
[0034] α/β-гидролазы часто описывают как ферменты, ответственные за гидролиз сложноэфирных и пептидных связей. Однако α/β-гидролазы также участвуют в разрыве углерод-углеродных связей, реакциях декарбоксилирования и кофакторнезависимом диоксигенировании гетероароматических колец. Таким образом, α/β-гидролазы могут включать каталитические члены (ферменты) в данном суперсемействе. Неограничивающими примерами являются гидролазы (ацетилхолинэстераза, карбоксилэстераза, диенелактонгидролаза, липаза, кутиназа, тиоэстераза, серинкарбоксипептидаза, пролиниминопептидаза, пролинолигопептидаза, эпоксидгидролаза) вместе с ферментами, которые требуют активации реакции HCN, H2O2 или О2 вместо Н2О для механизма реакции (галогеналкандегалогеназа, галопероксидаза, гидроксинитриллиаза). Некаталитические члены могут включать нейролигины, глутактин, нейротактин, С-концевой домен тиреоглобулина, желточные белки, CCG1-взаимодействующий фактор-В и дипептидиламинопептидазу VI.
[0035] В базе данных ESTHER собрана и прокомментирована опубликованная информация, относящаяся к последовательностям генов и белков данного суперсемейства. Таким образом, специалист в данной области может также получить α/β-гидролазы из ESTHER (http://bioweb.supagro.inra.fr/ESTHER/general?what=index), базы данных суперсемейства белков α/β-гидролаз с укладкой.
[0036] В настоящей заявке α/β-гидролаза может содержать последовательность SEQ ID NO: 45 или последовательность, которая имеет 60% или более идентичности с последовательностью SEQ ID NO: 45. Таким образом, любая α/β-гидролаза, содержащая эту последовательность, охватывается термином α/β-гидролаза.
[0037] Дополнительно или в качестве альтернативы, α/β-гидролаза в настоящем изобретении также может содержать последовательность SEQ ID NO: 46 или последовательность, которая имеет 60% или более идентичности с последовательностью SEQ ID NO: 46. Таким образом, любая α/β-гидролаза, содержащая эту последовательность, охватывается термином α/β-гидролаза.
[0038] Дополнительно или в качестве альтернативы, α/β-гидролаза в настоящем изобретении также может содержать последовательность SEQ ID NO: 47, 48 или 49 или последовательность, которая имеет 60% или более идентичности с последовательностью SEQ ID NO: 47, 48 или 49. Таким образом, любая α/β-гидролаза, содержащая эту последовательность, охватывается термином α/β-гидролаза.
[0039] Дополнительно или в качестве альтернативы, α/β-гидролаза в настоящем изобретении также может содержать последовательность SEQ ID NO: 50 или последовательность, которая имеет 60% или более идентичности с последовательностью SEQ ID NO: 50. Таким образом, любая α/β-гидролаза, содержащая эту последовательность, охватывается термином α/β-гидролаза.
[0040] Например, α/β-гидролаза может содержать последовательность, имеющую по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% идентичности с последовательностью SEQ ID NO: 45. Дополнительно или в качестве альтернативы, α/β-гидролаза может содержать последовательность, имеющую по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% идентичности с последовательностью SEQ ID NO: 46. Дополнительно или в качестве альтернативы, α/β-гидролаза может содержать последовательность, имеющую по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% идентичности с последовательностью SEQ ID NO: 47, 48 и/или 49. Дополнительно или в качестве альтернативы, α/β-гидролаза может содержать последовательность, имеющую по меньшей мере 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 97%, 98%, 99% идентичности с последовательностью SEQ ID NO: 50.



[0042] Термин «идентичный» или «процент идентичности» в контексте двух или более последовательностей полипептидов, таких как SEQ ID NO: 45-50, относится к двум или более последовательностям или подпоследовательностям, которые являются одинаковыми или которые имеют указанный процент одинаковых аминокислот (например, идентичны по меньшей на 85%, 90%, 95%, 96%, 97%, 98% или 99%) при сравнении и выравнивании для максимального соответствия в окне сравнения или в обозначенной области, при определении с применением алгоритма сравнения последовательностей, известного в данной области техники, или путем выравнивания вручную и визуального контроля. Последовательности, имеющие, например, идентичность последовательностей от 80% до 95% или более, считаются по существу идентичными. Специалистам в данной области техники известно, как определить процент идентичности между последовательностями, используя, например, алгоритмы, такие как алгоритмы, основанные на компьютерной программе CLUSTALW (Thompson Nucl. Acids Res. 2 (1994), 4673-4680) или FASTDB (Brutlag Сотр. App. Biosci. 6 (1990), 237-245), как известно в данной области техники.
[0043] Также для специалистов в данной области техники доступны алгоритмы BLAST и BLAST 2.6 (Altschul Nucl. Acids Res. 25 (1977), 3389-3402). Программа BLASTP для аминокислотных последовательностей использует по умолчанию длину сегмента (W), равную 6, ожидаемый порог, равный 10, и сравнение обеих цепей. Кроме того, можно применять оценочную матрицу BLOSUM62 (Henikoff Proc. Natl. Acad. Sci., USA, 89, (1989), 10915; Henikoff and Henikoff (1992) 'Amino acid substitution matrices from protein blocks.' Proc Natl Acad Sci USA. 1992 Nov 15;89(22):10915-9).
[0044] Например, BLAST2.6, что означает инструмент поиска базового локального выравнивания (Altschul, Nucl. Acids Res. 25 (1997), 3389-3402; Altschul, J. Mol. Evol. 36 (1993), 290-300; Altschul, J. Mol. Biol. 215 (1990), 403-410), можно применять для поиска локального выравнивания последовательностей.
[0045] Нейтрализующий зеараленон агент также может представлять собой озон, как, например, описано в Qi L et al. Food Addit Contam Part A Chem Anal Control Expo Risk Assess. 2016 Nov;33(11):1700-1710. Нейтрализующий зеараленон агент также может представлять собой микроорганизм, такой как, например, Clonostachys rosea, как описано в Kosawang С et al., Fungal Biol. 2014 Apr; 118(4):364-73, или Lactobacillus pentosus, как описано в Arunrussamee Sangsila et al., Food Control, Volume 62, April 2016, Pages 187-192, или штамм дрожжей, такой как Trichosporon mycotoxinivorans MTV, как описано в Schatzmayr et al. Mycot. Res. 2003 19: 124-128. Дополнительные нейтрализующие зеараленон агенты, например, описаны в Zinedine A et al., Food Chem Toxicol. 2007 Jan;45(l):1-18 or Ji С et al., Animal Nutrition Volume 2, Issue 3, 2016, Pages 127-133.
[0046] Как описано выше, нейтрализующий зеараленон агент также может снижать биодоступность зеараленона, например, путем связывания и/или адсорбции. Примеры таких агентов могут включать холестирамин, дивинилбензол-стирол, бентониты, богатые монтмориллонитом глины, цеолиты, органоглины, активированный уголь, дрожжи или продукты, полученные из стенок дрожжевых клеток.
[0047] Способы нейтрализации зеараленона могут включать, но не ограничиваются ими, способы приведения в контакт нейтрализующего зеараленон агента с кормом. Способы могут также включать термообработку или ультразвуковую обработку.
[0048] Оценка продуктивности и/или эффективности нейтрализующих микотоксин агентов или способов нейтрализации микотоксина представляет собой значительную проблему вследствие отсутствия подходящих способов, позволяющих определить, достигает ли применяемый нейтрализующий микотоксин агент или способ желаемого эффекта. Таким образом, способы согласно настоящему изобретению также могут служить для оценки способности способа или (тестируемого) соединения к нейтрализации ZEN. Другими словами, способ согласно настоящему изобретению можно применять для оценки способности способа или соединения к нейтрализации ZEN. Такое соединение может быть выбрано из группы, состоящей из одного или более полипептидов, одного или более микроорганизмов, включая живые, мертвые, лиофилизированные, автолизированные и/или покоящиеся микроорганизмы, и одного или более зеараленон-связывающих агентов, включая органический и/или неорганический зеараленон-связывающий агент(ы). С помощью способов согласно настоящему изобретению оценка продуктивности и/или эффективности нейтрализующего ZEN агента или способа может быть получена особенно быстрым и оперативным образом.
[0049] В случаях, когда образец был получен у субъекта, способ согласно настоящему изобретению может, таким образом, включать, до получения тестируемого образца у субъекта, стадию (а3) кормления субъекта кормом, вступавшим в контакт с зеараленоном и тестируемым соединением. В таком случае способ может дополнительно включать стадии приведения корма в контакт с зеараленоном, приведения корма в контакт с тестируемым соединением и/или приведения зеараленона в контакт с тестируемым соединением. Как правило, такие стадии могут быть осуществлены в любом порядке. Соответственно, способ перед стадией (а3) может включать стадии: (a1) приведение корма в контакт с зеараленоном, и (а2) приведение корма, вступавшего в контакт с зеараленоном, в контакт с тестируемым соединением; или (а1') приведение корма в контакт с тестируемым соединением, и (а2') приведение корма, вступавшего в контакт с тестируемым соединением, в контакт с зеараленоном; или (a1'') приведение зеараленона с в контакт тестируемым соединением, и (а2'') приведение зеараленона, вступавшего в контакт с тестируемым соединением, в контакт с кормом.
[0050] В некоторых случаях, которые могут представлять случай, когда тестируемый образец представляет собой культуру клеток, образец мог непосредственно вступать в контакт с зеараленоном и тестируемым соединением. Контрольный образец, используемый в таком способе, может представлять собой отрицательный контрольный образец или положительный контрольный образец. Отрицательный контрольный образец, используемый в данном контексте, относится к образцу, который вступал в контакт с зеараленоном и необязательно к соединению, которое не нейтрализует зеараленон. Положительный контрольный образец, используемый в данном контексте, относится к образцу, который вступал в контакт с зеараленоном, и к соединению, которое нейтрализует зеараленон, или к образцу, который не вступал в контакт с зеараленоном. В таком способе отсутствие отклонения или незначительного отклонения уровней экспрессии между тестируемым образцом и положительным контрольным образцом может указывать на способность тестируемого соединения к нейтрализации зеараленона. В качестве альтернативы или дополнительно, наличие (предпочтительно значительного) отклонения уровней экспрессии между тестируемым образцом и отрицательным контрольным образцом может указывать на способность тестируемого соединения к нейтрализации зеараленона. В таких способах образец может представлять собой образец, который не был получен у субъекта.
[0051] Чтобы избежать длительных, трудоемких и затратных испытаний на животных, предпочтительно проводят исследовательские эксперименты на культивируемых клетках. Следовательно, тестируемый образец, положительный контрольный образец и/или отрицательный контрольный образец могут представлять собой клеточную культуру. В качестве иллюстративного примера, клеточная культура может содержать MCF-7, T47D, SUM159, HeLa или Ishikawa. Кроме того, первичные клетки, такие как, например, зернистые клетки свиньи, могут содержаться в клеточной культуре. Путем обеспечения способа, описанного в настоящей заявке, отличающегося тем, что тестируемый образец, контрольный образец, такой как положительный контрольный образец или отрицательный контрольный образец, представляет собой культуру клеток, можно получить ценные данные, например, о способности способа или соединения к нейтрализации ZEN, особенно эффективным образом.
[0052] Настоящее изобретение также относится к применению по меньшей мере одной микроРНК согласно настоящему изобретению для обнаружения воздействия зеараленона в тестируемом образце. По меньшей мере одна микроРНК может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-125a, ssc-miR-125b, ssc-miR-127, ssc-miR-129a, ssc-miR-133a-5p, ssc-miR-135, ssc-miR-136, ssc-miR-140-3р, ssc-miR-142-3р, ssc-miR-143-5p, ssc-miR-146b, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-miR-187, ssc-miR-195, ssc-miR-204, ssc-miR-206, ssc-miR-22-3р, ssc-miR-22-5p, ssc-miR-335, ssc-miR-34a, ssc-miR-369, ssc-miR-378, ssc-miR-424-5p, ssc-miR-432-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-486, ssc-miR-493-3р, ssc-miR-493-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-708-3р, ssc-miR-758, ssc-miR-7135-3р, hsa-miR-135b-5p, hsa-miR-301a-5p, put-miR-300. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183, ssc-miR-140-3р, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497. Применение можно осуществлять в любом способе согласно настоящему изобретению. Такое применение можно осуществлять с целью обнаружения воздействия зеараленона на субъект, оценки способности тестируемого соединения или способа нейтрализации зеараленона или выбора пищи для обработки с помощью нейтрализующего зеараленон агента или способа. С применением по меньшей мере одной микроРНК, как описано в настоящей заявке, для обнаружения воздействия зеараленона в тестируемом образце, эффект ZEN может быть обнаружен с особенно высокой надежностью и специфичностью.
[0053] Для обеспечения быстрой реакции, такой как, например, при подаче противодействующего агента в случае воздействия ZEN, необходима быстрая доступность результатов испытаний. Это может быть достигнуто, например, если определение уровня экспрессии по меньшей мере одной микроРНК в тестируемом образце и сравнение уровня экспрессии с референсным значением осуществляют с помощью интегрированной системы. Таким образом, способы согласно настоящему изобретению могут представлять собой способы, выполняемые с помощью компьютера, которые могут быть осуществлены устройством для выполнения такого способа.
[0054] Таким образом, настоящее изобретение также относится к системе обработки данных, содержащей процессор, выполненный с возможностью осуществления способа, включающего стадии сравнения уровня экспрессии по меньшей мере одной микроРНК в соответствии с изобретением, определенного в тестируемом образце, полученном у субъекта, с референсным значением. Необходим ввод уровня экспрессии по меньшей мере одной микроРНК. Информация может быть передана в систему обработки данных через устройство, которое способно определять такую информацию, например, по некоторой среде передачи, такой как электрический провод или кабель, по оптоволоконному кабелю или с помощью электромагнитного излучения. Такое устройство может быть интегрировано в систему обработки данных или подключено к ней. Информация, касающаяся уровня экспрессии по меньшей мере одной микроРНК, также может быть передана в систему обработки данных посредством ввода через пользовательский интерфейс. Если референсное значение соответствует уровню экспрессии указанной микроРНК в контрольном образце, который был получен у субъекта, не подвергавшегося воздействию зеараленона, (значительное) отклонение уровней экспрессии микроРНК между тестируемым образцом и референсным значением может указывать на эффект зеараленона (такой как воздействие зеараленона). В таком случае способ может включать выявление воздействия зеараленона на субъект, если определено отклонение. В качестве альтернативы, если референсное значение соответствует уровню экспрессии, который был определен, соответствует контрольному образцу, который был получен у субъекта, подвергшегося воздействию зеараленона, отсутствие отклонения между значениями тестируемого образца и референсным значением не может указывать на эффект зеараленона, такой как воздействие зеараленона. В таком случае способ может включать выявление воздействия зеараленона на субъект, если не обнаружено отклонения или существенного отклонения. "Отсутствие отклонения" в данном контексте может также включать незначительное отклонение или (нетипично) низкое отклонение. По меньшей мере одна микроРНК может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-125a, ssc-miR-125b, ssc-miR-127, ssc-miR-129a, ssc-miR-133a-5p, ssc-miR-135, ssc-miR-136, ssc-miR-140-3р, ssc-miR-142-3р, ssc-miR-143-5p, ssc-miR-146b, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-miR-187, ssc-miR-195, ssc-miR-204, ssc-miR-206, ssc-miR-22-3р, ssc-miR-22-5p, ssc-miR-335, ssc-miR-34a, ssc-miR-369, ssc-miR-378, ssc-miR-424-5p, ssc-miR-432-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-486, ssc-miR-493-3р, ssc-miR-493-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-708-3р, ssc-miR-758, ssc-miR-7135-3р, hsa-miR-135b-5p, hsa-miR-301a-5p, put-miR-300. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3p, ssc-miR-183, ssc-miR-140-3р, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497.
[0055] В идеале, система обработки данных соединена или интегрирована в устройство, которое способно определять уровень экспрессии по меньшей мере одной микроРНК согласно настоящему изобретению в тестируемом образце. Устройство может обеспечивать системе обработки данных информацию относительно уровня экспрессии указанной по меньшей мере одной микроРНК. Такое устройство может, например, представлять собой устройство для секвенирования, такое как устройство количественного секвенирования в реальном времени. Устройства для секвенирования известны специалисту в данной области техники и, например, являются коммерчески доступными от Illumina, Pacific Biosciences, Oxford Nanopore Technologies и т.д. Особенно подходящими являются портативные устройства для секвенирования, такие как секвенирование MinION (Oxford Nanopore Technologies). Устройство, способное определять уровень экспрессии по меньшей мере одной микроРНК в соответствии с настоящим изобретением, также может представлять собой считывающее устройство для микрочипов.
[0056] Соответственно, настоящее изобретение также относится к устройству для секвенирования, способному определять уровень по меньшей мере одной микроРНК согласно настоящему изобретению, содержащему систему обработки данных согласно настоящему изобретению. По меньшей мере одна микроРНК может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-125a, ssc-miR-125b, ssc-miR-127, ssc-miR-129a, ssc-miR-133a-5p, ssc-miR-135, ssc-miR-136, ssc-miR-140-3р, ssc-miR-142-3р, ssc-miR-143-5p, ssc-miR-146b, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-miR-187, ssc-miR-195, ssc-miR-204, ssc-miR-206, ssc-miR-22-3р, ssc-miR-22-5p, ssc-miR-335, ssc-miR-34a, ssc-miR-369, ssc-miR-378, ssc-miR-424-5p, ssc-miR-432-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-486, ssc-miR-493-3р, ssc-miR-493-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-708-3р, ssc-miR-758, ssc-miR-7135-3р, hsa-miR-135b-5p, hsa-miR-301a-5p, put-miR-300. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183, ssc-miR-140-3р, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497.
[0057] Настоящее изобретение также относится к компьютерной программе, содержащей инструкции по выполнению системой обработки данных, описанной в настоящей заявке, или устройством для секвенирования, описанным в настоящей заявке, стадий (а) сравнения уровня экспрессии по меньшей мере одной микроРНК в соответствии с изобретением, определенного в тестируемом образце, полученном у субъекта, с референсным значением и (b) выявления воздействия зеараленона на субъект, если определено отклонение, причем референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, полученном у субъекта, который не подвергался воздействию зеараленона; или выявления воздействия зеараленона на субъект, если отклонение не определено, причем референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, полученном у субъекта, который подвергался воздействию зеараленона. Когда компьютерная программа загружается и выполняется системой обработки данных, система обработки данных становится устройством для осуществления способов, описанных в настоящей заявке.
[0058] Компьютерная программа может представлять собой компьютерный программный продукт, доступный с используемого компьютером или машиночитаемого носителя, обеспечивающий программный код для использования компьютером или любой системой выполнения инструкций или в связи с ними. Настоящее изобретение, таким образом, также относится к машиночитаемому носителю, хранящему на нем компьютерную программу, описанную в настоящей заявке. Используемый компьютером или машиночитаемый носитель может представлять собой любое устройство, которое может содержать, хранить, передавать, распространять или перемещать программу для использования системой, устройством или устройством выполнения инструкций или в связи с ними. Носитель может представлять собой электронную, магнитную, оптическую, электромагнитную, инфракрасную, полупроводниковую или бумажную систему (или аппарат или устройство) или среду распространения. Носитель может представлять собой любой подходящий материальный носитель, такой как дискета, CD, DVD, BD, жесткий диск, карта памяти, карта памяти или любой другой машиночитаемый носитель данных.
[0059] Для достижения особенно экономически эффективного и быстрого обнаружения воздействия ZEN предложен набор для осуществления способа обнаружения воздействия ZEN в смысле настоящего изобретения, содержащий специфичный связывающий агент по меньшей мере для одной микроРНК согласно настоящему изобретению, содержащейся на твердой подложке или конъюгированной с ней. По меньшей мере одна микроРНК может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-125a, ssc-miR-125b, ssc-miR-127, ssc-miR-129a, ssc-miR-133a-5p, ssc-miR-135, ssc-miR-136, ssc-miR-140-3р, ssc-miR-142-3р, ssc-miR-143-5p, ssc-miR-146b, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-miR-187, ssc-miR-195, ssc-miR-204, ssc-miR-206, ssc-miR-22-3р, ssc-miR-22-5p, ssc-miR-335, ssc-miR-34a, ssc-miR-369, ssc-miR-378, ssc-miR-424-5p, ssc-miR-432-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-486, ssc-miR-493-3р, ssc-miR-493-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-708-3р, ssc-miR-758, ssc-miR-7135-3р, hsa-miR-135b-5p, hsa-miR-301a-5p, put-miR-300. Предпочтительно, по меньшей мере одна микроРНК согласно настоящему изобретению может быть выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183, ssc-miR-140-3р, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497. Набор может содержать немеченого специфичного связывающего партнера и меченого специфичного партнера по меньшей мере одной микроРНК. Предпочтительно немеченый специфичный связывающий партнер конъюгирован с твердой подложкой. Набор может содержать специфичные связывающие партнеры не более чем для 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 или 26 микроРНК. В некоторых вариантах применения набор может содержать специфичных связывающих партнеров не более чем 24, 48, 96 или 384 микроРНК. Набор может содержать специфичных связывающих партнеров не более чем для 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 или 26 микроРНК согласно настоящему изобретению. Набор может содержать только специфичных связывающих партнеров для микроРНК в соответствии со способами согласно настоящему изобретению.
[0060] Такой набор может быть предназначен для теста бокового потока. Схематическое изображение устройства бокового потока показано на Фиг.8. Набор может содержать устройство бокового потока (LFD), которое содержит носитель (твердую опору), который имеет по меньшей мере две зоны, подушку конъюгата и зону проведения испытания. Подушка конъюгата содержит меченый связующий агент для по меньшей мере одной микроРНК согласно настоящему изобретению, который может быть мобилизован в растворителе (например, растворителе, который содержит молекулу-мишень) и транспортирован в ней к зоне проведения испытания. Зона проведения испытания содержит немеченый связующий агент, который также способен связывать молекулу-мишень. Таким образом, мишени (по меньшей мере одна микроРНК), которые также связаны меченым агентом из подушки конъюгата, иммобилизованы в зоне проведения испытания. Необязательная дополнительная контрольная зона может содержать другой иммобилизованный связующий агент, способный связывать меченый связующий агент из подушки конъюгата, который не удерживается в зоне проведения испытаний. Примеры устройств бокового потока описаны в Koczula and Gallotta. Essays Biochem. 2016 Jun 30;60(1):111-20 or Krska and Molinelli. Anal Bioanal Chem. 2009 Jan; 393(l):67-71.
[0061] Кроме того, иммунохимическое обнаружение может быть выполнено с помощью ИФА, например, сэндвич-ИФА. Таким образом, набор может содержать (предпочтительно немеченый) специфичный связывающий агент для целевой микроРНК, который может быть иммобилизован на твердой подложке или иммобилизован на твердой подложке. Тестируемый образец может быть добавлен на подложку. Кроме того, может быть добавлен меченый связывающий агент для целевой микроРНК. Затем метку, связанную с микроРНК, можно применять для количественного определения микроРНК.
[0062] Специфичный связывающий агент может представлять собой, например, нуклеиновую кислоту, антитело, антигенсвязывающий фрагмент антитела или белковоподобную молекулу, обладающую антителоподобными свойствами. В тех случаях, когда в наборе используют как меченый, так и немеченый специфичный связывающий партнер, предпочтительно, чтобы оба связывающих партнера могли одновременно связываться с целевой микроРНК. Это может быть достигнуто, например, если один специфичный связывающий партнер может связываться (например, гибридизоваться) с одной частью целевой микроРНК, тогда как другой специфичный связывающий партнер может связываться (например, гибридизоваться) с другой частью целевой микроРНК.
[0063] Набор может дополнительно содержать средство для обнаружения микроРНК, которое связано со специфичным связывающим агентом, таким как немеченый специфичный связывающий агент, описанный в настоящей заявке, который предпочтительно конъюгирован с твердой подложкой. Такое средство может содержать зонд, конъюгированный с детектируемой меткой. Например, такое средство может представлять собой меченый специфичный связующий агент, как описано в настоящей заявке. Как правило, такая "детектируемая метка" может представлять собой любое подходящее химическое вещество или фермент, которое прямо или косвенно генерирует детектируемое соединение или сигнал в химической, физической, оптической или ферментативной реакции. Например, флуоресцентная или радиоактивная метка может быть использована для генерации флуоресценции или рентгеновского излучения в качестве детектируемого сигнала. Краситель может быть использован для генерации оптического сигнала. Щелочная фосфатаза, пероксидаза хрена и β-галактозидаза являются примерами ферментных меток (и в то же время оптических меток), которые катализируют образование хромогенных продуктов реакции. Предпочтительно, метка не оказывает негативного влияния на характеристики связывающего партнера, с которым конъюгирована метка. Предпочтительной детектируемой меткой является оптически детектируемая метка, такая как хромофор или флуоресцентная метка.
[0064] Настоящее изобретение дополнительно характеризуется следующими пунтами:
[0065] Пункт 1. Способ обнаружения воздействия зеараленона, включающий: (с) определение в тестируемом образце уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183, ssc-miR-140-3р, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497; и (d) сравнение уровня экспрессии с референсным значением.
[0066] Пункт 2. Способ по п. 1, отличающийся тем, что референсное значение соответствует уровню экспрессии указанной по меньшей мере одной микроРНК в контрольном образце.
[0067] Пункт 3. Способ по п. 1 или 2, отличающийся тем, что эффект зеараленона представляет собой воздействие зеараленона.
[0068] Пункт 4. Способ по любому из предшествующих пунктов, отличающийся тем, что тестируемый образец получают у субъекта.
[0069] Пункт 5. Способ по любому из предшествующих пунктов, отличающийся тем, что отклонение уровня экспрессии от референсного значения указывает на воздействие зеараленона.
[0070] Пункт 6. Способ по любому из предшествующих пунктов, отличающийся тем, что отклонение включает увеличение и/или уменьшение уровня экспрессии по меньшей мере одной из микроРНК по п. 1.
[0071] Пункт 7. Способ по любому из предшествующих пунктов, отличающийся тем, что отклонение включает увеличение и/или уменьшение по меньшей мере одного соотношения уровней экспрессии по меньшей мере двух из микроРНК по п. 1.
[0072] Пункт 8. Способ по любому из предшествующих пунктов, отличающийся тем, что отклонение является статистически значимым.
[0073] Пункт 9. Способ по любому из предшествующих пунктов, отличающийся тем, что контрольный образец был получен у субъекта, который не подвергался воздействию зеараленона, или представляет собой среднее значение нескольких образцов, которые были получены у одного или более субъектов, которые не подвергались воздействию зеараленона.
[0074] Пункт 10. Способ по любому из предшествующих пунктов, отличающийся тем, что образец представляет собой образец крови или образец ткани.
[0075] Пункт 11. Способ по любому из предшествующих пунктов, отличающийся тем, что образец представляет собой образец сыворотки крови.
[0076] Пункт 12. Способ по любому из предшествующих пунктов, отличающийся тем, что по меньшей мере одна микроРНК выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3р, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3р, ssc-miR-455-3р, ssc-miR-183 и ssc-miR-140-3р.
[0077] Пункт 13. Способ по п. 11 или 12, отличающийся тем, что по меньшей мере одна микроРНК включает две микроРНК, выбранные из группы, состоящей из ssc-miR-542-3р и ssc-miR-1, ssc-miR-542-3р и ssc-miR-493-3р, ssc-miR-135 и ssc-miR-432-5p, и ssc-miR-455-5p и ssc-miR-493-3р.
[0078] Пункт 14. Способ по любому из пунктов 11-13, отличающийся тем, что уровень экспрессии по меньшей мере одной микроРНК включает по меньшей мере одно соотношение уровней экспрессии между двумя микроРНК, выбранными из группы, состоящей из ssc-miR-542-3р и ssc-miR-1, ssc-miR-542-3р и ssc-miR-493-3р, ssc-miR-135 и ssc-miR-432-5p, и ssc-miR-455-5p и ssc-miR-493-3р.
[0079] Пункт 15. Способ по п. 14, отличающийся тем, что по меньшей мере одно соотношение уровней экспрессии между двумя микроРНК выбрано из группы, состоящей из соотношения между ssc-miR-542-3р и ssc-miR-1, ssc-miR-542-3р и ssc-miR-493-3р, ssc-miR-135 и ssc-miR-432-5p, и ssc-miR-455-5p и ssc-miR-493-3р.
[0080] Пункт 16. Способ по любому из пунктов 1-10, отличающийся тем, что образец представляет собой образец ткани матки.
[0081] Пункт 17. Способ по любому из предшествующих пунктов, отличающийся тем, что по меньшей мере одна микроРНК выбрана из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3р, ssc-miR-135, ssc-miR-7135-3р, ssc-miR-204, ssc-miR-143-5p, ssc-miR-187, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p и ssc-miR-497.
[0082] Пункт 18. Способ по п. 16 или 17, отличающийся тем, что по меньшей мере одна микроРНК содержит miR-542-3р и miR-1.
[0083] Пункт 19. Способ по п. 18, отличающийся тем, что уровень экспрессии по меньшей мере одной микроРНК включает соотношение уровней экспрессии между miR-542-3р и miR-1.
[0084] Пункт 20. Способ по любому из пп. 4-19, отличающийся тем, что субъект представляет собой млекопитающее.
[0085] Пункт 21. Способ по любому из пп. 4-20, отличающийся тем, что субъект представляет собой субъект рода Sus.
[0086] Пункт 22. Способ по п. 21, отличающийся тем, что субъект относится к виду Sus scrofa.
[0087] Пункт 23. Способ по любому из предшествующих пунктов, дополнительно включающий (е) обеспечение информации относительно воздействия зеараленона.
[0088] Пункт 24. Способ по любому из предшествующих пунктов, дополнительно включающий (b) обеспечение тестируемого образца.
[0089] Пункт 25. Способ по любому из предшествующих пунктов, отличающийся тем, что способ предназначен для диагностики.
[0090] Пункт 26. Способ по любому из предшествующих пунктов, отличающийся тем, что способ предназначен для диагностики воздействия зеараленона.
[0091] Пункт 27. Способ по любому из пп. 1-24, отличающийся тем, что способ не предназначен для диагностики.
[0092] Пункт 28. Способ по любому из пунктов 4-24 и 27, отличающийся тем, что способ предназначен для обнаружения зеараленона в корме или пище.
[0093] Пункт 29. Способ по п. 28, отличающийся тем, что способ включает, перед получением тестируемого образца от субъекта, (а) кормление субъекта кормом, предположительно содержащим зеараленон.
[0094] Пункт 30. Способ по любому из пунктов 4-24 и 27-29, отличающийся тем, что способ предназначен для выбора корма для приведения в контакт с нейтрализующим зеараленон агентом или применении способа нейтрализации зеараленона.
[0095] Пункт 31. Способ по п. 29 или 30, включающий (а) кормление субъекта кормом, предположительно содержащим зеараленон, до получения тестируемого образца у субъекта; и/или (f) выбор корма для приведения в контакт с нейтрализующим зеараленон агентом или применение способа нейтрализации зеараленона, если отклонение уровней экспрессии по меньшей мере одной микроРНК между тестируемым образцом и контрольным образцом указывает на воздействие зеараленона.
[0096] Пункт 32. Способ по п. 30 или 31, отличающийся тем, что нейтрализующий зеараленон агент выбран из группы, состоящей из одного или более полипептидов, одного или более микроорганизмов и одного или более зеараленон-связывающих агентов.
[0097] Пункт 33. Способ по любому из п. 30-32, дополнительно включающий обеспечение нейтрализующего зеараленон агента.
[0098] Пункт 34. Способ по любому из пунктов 30-33, дополнительно включающий приведение в контакт корма или пищи, выбранной с применением способа, с нейтрализующим зеараленон агентом или применение способа нейтрализации зеараленона к корму.
[0099] Пункт 35. Способ по любому из пунктов 4-22 и 25-27, отличающийся тем, что способ предназначен для оценки способности способа или тестируемого соединения к нейтрализации зеараленона.
[0100] Пункт 36. Способ по п. 35, отличающийся тем, что тестируемое соединение выбрано из группы, состоящей из одного или более полипептидов, одного или более микроорганизмов и одного или более зеараленон-связывающих агентов.
[0101] Пункт 37. Способ по п. 35 или 36, отличающийся тем, что способ включает, перед получением тестируемого образца у субъекта, (а3) кормление субъекта кормом, вступавшим в контакт с зеараленоном и тестируемым соединением.
[0102] Пункт 38. Способ по п. 37, отличающийся тем, что способ перед (а3) включает стадии: (a1) приведение корма в контакт с зеараленоном, и (а2) приведение корма, вступавшего в контакт с зеараленоном, в контакт с тестируемым соединением; или (а1') приведение корма в контакт с тестируемым соединением, и (а2') приведение корма, вступавшего в контакт с тестируемым соединением, в контакт с зеараленоном; или (a1'') приведение зеараленона с в контакт тестируемым соединением, и (а2'') приведение зеараленона, вступавшего в контакт с тестируемым соединением, в контакт с кормом.
[0103] Пункт 39. Способ по любому из пунктов 1-3, отличающийся тем, что способ предназначен для оценки способности способа или тестируемого соединения к нейтрализации зеараленона.
[0104] Пункт 40. Способ по п. 39, отличающийся тем, что тестируемое соединение выбрано из группы, состоящей из одного или более полипептидов, одного или более микроорганизмов и одного или более зеараленон-связывающих агентов.
[0105] Пункт 41. Способ по п. 39 или 40, отличающийся тем, что тестируемый образец вступал в контакт с зеараленоном и тестируемым соединением.
[0106] Пункт 42. Способ по любому из пунктов 39-41, отличающийся тем, что контрольный образец представляет собой отрицательный контрольный образец или положительный контрольный образец.
[0107] Пункт 43. Способ по п. 42, отличающийся тем, что отсутствие отклонения уровней экспрессии между тестируемым образцом и положительным контрольным образцом или наличие отклонения уровней экспрессии между тестируемым образцом и отрицательным контрольным образцом указывает на способность тестируемого соединения к нейтрализации зеараленона.
[0108] Пункт 44. Способ по любому из пунктов 40-43, отличающийся тем, что тестируемый образец, контрольный образец, положительный контрольный образец или отрицательный контрольный образец представляет собой культуру клеток.
[0109] Пункт 45. Способ по пп. 30-44, отличающийся тем, что нейтрализацию осуществляют путем деградации.
[0110] Пункт 46. Способ по пп. 30-44, отличающийся тем, что нейтрализацию осуществляют путем связывания.
[0111] Пункт 47. Применение по меньшей мере одной микроРНК, выбранной из группы, состоящей из miR-1, miR-181c, miR-206, miR-503, miR-542-3р, miR-135, miR-135a-5p, miR-129a-3p, miR-142-3р, miR-432-5p, miR-455-5p, miR-182, miR-493-3р, miR-455-3p, miR-183, miR-140-3р, miR-7135-3р, miR-204, miR-143-5p, miR-187, miR-335, miR-424-5p, miR-450a, miR-450b-5p, miR-450c-5p, miR-497, для обнаружения воздействия зеараленона в тестируемом образце.
[0112] Пункт 48. Применение по п. 47, отличающееся тем, что указанное применение предназначено для обнаружения воздействия зеараленона на субъект.
[0113] Пункт 49. Система обработки данных, содержащая процессор, выполненный с возможностью осуществления способа, включающего стадии (а) сравнения уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из miR-1, miR-181c, miR-206, miR-503, miR-542-3р, miR-135, miR-135a-5p, miR-129a-3p, miR-142-3p, miR-432-5p, miR-455-5p, miR-182, miR-493-3р, miR-455-3р, miR-183, miR-140-3р, miR-7135-3p, miR-204, miR-143-5p, miR-187, miR-335, miR-424-5p, miR-450a, miR-450b-5p, miR-450c-5p и miR-497, определенного в тестируемом образце, полученном у субъекта с референсным значением; и (b) выявления воздействия зеараленона на субъект, если определено отклонение, причем референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, полученном у субъекта, который не подвергался воздействию зеараленона; или выявления воздействия зеараленона на субъект, если отклонение не определено, причем референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, полученном у субъекта, который подвергался воздействию зеараленона.
[0114] Пункт 50. Устройство для секвенирования, способное определять уровень по меньшей мере одной микроРНК, выбранной из группы, состоящей из miR-1, miR-181с, miR-206, miR-503, miR-542-3р, miR-135, miR-135a-5p, miR-129a-3p, miR-142-3р, miR-432-5p, miR-455-5p, miR-182, miR-493-3р, miR-455-3р, miR-183, miR-140-3р, miR-7135-3р, miR-204, miR-143-5p, miR-187, miR-335, miR-424-5p, miR-450a, miR-450b-5p, miR-450c-5p и miR-497, содержащее систему обработки данных по п. 49.
[0115] Пункт 51. Компьютерная программа, содержащая инструкции по выполнению системой обработки данных по п. 49 или устройством для секвенирования по п. 50 стадий (b) сравнения уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из miR-1, miR-181с, miR-206, miR-503, miR-542-3р, miR-135, miR-135a-5p, miR-129a-3p, miR-142-3р, miR-432-5p, miR-455-5p, miR-182, miR-493-3p, miR-455-3р, miR-183, miR-140-3р, miR-7135-3р, miR-204, miR-143-5p, miR-187, miR-335, miR-424-5p, miR-450a, miR-450b-5p, miR-450c-5p и miR-497, определенного в образце, полученном у субъекта, с референсным значением; и (с) выявления воздействия зеараленона на субъект, если определено отклонение, причем референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, полученном у субъекта, который не подвергался воздействию зеараленона; или выявления воздействия зеараленона на субъект, если отклонение не определено, причем референсное значение соответствует уровню экспрессии, который был определен в контрольном образце, полученном у субъекта, который подвергался воздействию зеараленона.
[0116] Пункт 52. Машиночитаемый носитель, хранящий на нем компьютерную программу по п. 51.
[0117] Пункт 53. Набор для осуществления способа по любому из пунктов 1-38, содержащий специфичный связывающий агент для по меньшей мере одной микроРНК, выбранной из группы, состоящей из miR-1, miR-181с, miR-206, miR-503, miR-542-3р, miR-135, miR-135a-5p, miR-129a-3p, miR-142-3р, miR-432-5p, miR-455-5p, miR-182, miR-493-3p, miR-455-3р, miR-183, miR-140-3р, miR-7135-3р, miR-204, miR-143-5p, miR-187, miR-335, miR-424-5p, miR-450a, miR-450b-5p, miR-450c-5p и miR-497, находящийся на твердой подложке или конъюгированный с ней.
[0118] Пункт 54. Набор по п. 53, отличающийся тем, что специфичный связывающий агент представляет собой нуклеиновую кислоту, антитело, антигенсвязывающий фрагмент антитела или белковоподобную молекулу, обладающую антителоподобными свойствами.
[0119] Пункт 55. Набор по п. 53 или 54, дополнительно содержащий средство для обнаружения микроРНК, которая связана со специфичным связывающим агентом.
[0120] Пункт 56. Набор по п. 55, отличающийся тем, что средство для обнаружения микроРНК, которая связана со специфичным связывающим агентом, содержит зонд, конъюгированный с детектируемой меткой.
[0121] Пункт 57. Набор по п. 56, отличающийся тем, что детектируемая метка представляет собой оптически детектируемую метку.
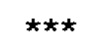
[0122] Следует отметить, что в настоящей заявке неопределенные и определенные артикли единственного числа включают ссылки на множественное число и наоборот, если контекст явно не предписывает иное. Таким образом, например, ссылка на "микроРНК" или "способ" включает одну или более таких микроРНК или способов, соответственно, а ссылка на "способ" включает эквивалентные стадии и способы, которые могут быть модифицированы или заменены, как известно рядовым специалистам в данной области техники. Аналогично, например, ссылка на "микроРНК" во множественном числе включает "микроРНК" в единственном числе.
[0123] Если не указано иное, термин «по меньшей мере», предшествующий серии элементов, следует понимать как относящийся к каждому элементу в серии. Специалисты в данной области техники смогут понять или установить, используя не более чем рутинное экспериментирование, многие эквиваленты конкретных вариантов реализации изобретения, описанных в настоящей заявке. Подразумевается, что такие эквиваленты входят в объем настоящего изобретения.
[0124] Термин "более" включает конкретное число. Например, "более 20" означает ≥20.
[0125] Во всей настоящей заявке и формуле изобретения или пунктах, если контекст не требует иного, слово "содержать" и варианты, такие как "содержит" и "содержащий", будут пониматься как подразумевающие включение указанного целого числа (или стадии) или группы целых чисел (или стадий). Оно не исключает любое другое целое число (или стадию) или группу целых чисел (или стадий). При применении в настоящей заявке термин "содержащий" может быть заменен термином "содержащий", "состоящий из", "включающий", "имеющий" или "несущий".
[0126] Используемый в настоящей заявке термин «примерно» или «приблизительно» означает в пределах 20%, предпочтительно в пределах 10% и более предпочтительно в пределах 5% от заданного значения или диапазона. Он включает, однако, также конкретное число, например, приблизительно 20 включает 20.
[0127] При использовании в настоящей заявке термин «состоящий из» исключает любой элемент, стадию или ингредиент, не указанный в формуле изобретения. При использовании в настоящей заявке термин "состоящий по существу из" не исключает материалы или стадии, которые существенно не влияют на основные и новые характеристики формулы изобретения.
[0128] В каждом случае в настоящей заявке любой из терминов "содержащий", "состоящий по существу из" и "состоящий из" может быть заменен любым из двух других терминов. Возможность замены терминов друг на друга не следует понимать, что эти термины обязательно являются синонимами.
[0129] Следует понимать, что настоящее изобретение не ограничивается конкретной методологией, протоколами, материалами, реагентами и веществами и т.д., описанными в настоящей заявке, и как таковое может варьироваться. Терминология, используемая в настоящей заявке, предназначена только для описания конкретных вариантов реализации и не предназначена для ограничения объема настоящего изобретения, которое определено только формулой изобретения.
[0130] Все публикации, цитируемые по всему тексту настоящей заявки (включая все патенты, патентные заявки, научные публикации, спецификации производителей, инструкции и т.д.) полностью включены в настоящую заявку посредством ссылки. В настоящей заявке ничего не следует толковать как признание того, что настоящее изобретения не датировано более ранним числом на основании предшествующего изобретения. В той степени, в которой материал, включенный посредством ссылки, противоречит или не согласуется с настоящей заявкой, настоящая заявка заменяет любой такой материал.
[0131] Для дальнейшего разъяснения всех аспектов настоящего изобретения, ниже изобретение описано с помощью фигур и примеров. В нем:
[0132] На ФИГ. 1 показаны средние площади поверхности вульвы животных (n=6) из четырех групп лечения в течение времени эксперимента.
[0133] На ФИГ. 2 показано количество дифференциально экспрессированных микроРНК в образцах матки поросят, подвергшихся воздействию ZEN (с скорректированными р-величинами ≤0,07).
[0134] На ФИГ. 3А и В показаны значения кратного изменения S. scrofa-специфичных микроРНК в ткани матки, на которые оказано значительное влияние, (т.е. с скорректированным значением FDR р ≤0,07) по меньшей мере в одной группе ZEN при воздействии ZEN. Значения кратного изменения могут быть как положительными, так и отрицательными, т.е. положительно или отрицательно регулируемыми по сравнению с контрольным образцом.
[0135] На ФИГ. 3С-3Е показаны значения кратного изменения S. scrofa-специфичных микроРНК в ткани матки, на которые не было оказано значительного влияния (т.е. с скорректированным значением FDR р >0,07). Значения кратного изменения могут быть как положительными, так и отрицательными, т.е. положительно или отрицательно регулируемыми по сравнению с контрольным образцом.
[0136] На ФИГ. 4 показаны log2-преобразованные кратные изменения и уровни экспрессии (измеренные как метки на миллион, ТРМ) предполагаемых и прогнозируемых микроРНК, значительно увеличенные или уменьшенные (скорректированное значение FDR р ≤0,07) при воздействии ZEN в ткани матки.
[0137] На ФИГ. 5 показаны результаты целевого анализа сыворотки на основе кПЦР на 6 и 28 день, для сравнения группы контроля и группы с высоким ZEN. Были рассмотрены только микроРНК с количественно определяемыми уровнями по меньшей мере у четырех индивидуумов в каждой группе лечения.
[0138] На ФИГ. 6 показаны значения кратного изменения микроРНК из целевого анализа сыворотки на основе кПЦР. Значения кратного изменения могут быть как положительными, так и отрицательными, т.е. положительно или отрицательно регулируемыми по сравнению с контрольным образцом.
[0139] На ФИГ. 7 показаны значения кратного изменения соотношений микроРНК из целевого анализа сыворотки на основе кПЦР для всех трех групп ZEN, а также комбинированное значение трех групп ZEN по сравнению с контролем (т.е. ZEN по сравнению с отсутствием ZEN). Отношения считались подходящими, когда площадь под кривой (AUC) составляла ≥0,7 в течение по меньшей мере одного дня отбора образца. Значения кратного изменения могут быть как положительными, так и отрицательными, т.е. положительно или отрицательно регулируемыми по сравнению с контрольным образцом.
[0140] На ФИГ. 8 проиллюстрировано схематическое изображение устройства бокового потока.
ПРИМЕРЫ
[0141] Пример 1: Животные и дизайн исследования
[0142] Самки поросят-отъемышей (свиноматка: Landrace х Large White, кабан: Pietrain; возраст 30 +/- 2 дня) были получены от местного производителя и помечены индивидуально. Поросят помещали в загоны с решетчатым полом в контролируемых условиях окружающей среды. После семидневного периода акклиматизации двадцать четыре самки поросят были отобраны на основании массы тела и размера вульвы и распределены в одну из четырех групп (6 животных на группу). Поросята получали либо холостой корм (отрицательный контроль; Ctrl), либо корм, загрязненный ZEN в трех возрастающих концентрациях (низкий ZEN: 0,17 мг/кг питания; средний ZEN: 1,5 мг/кг питания; высокий ZEN: 4,6 мг/кг питания). В течение 28-дневного экспериментального периода каждой группе обработки был предоставлен свободный доступ к воде и назначенному питанию. Свиней ежедневно наблюдали и еженедельно взвешивали.
[0143] Питание было изготовлено на BIOMIN AN (Herzogenburg, Австрия) и составлено в соответствии с требованиями к энергии и аминокислотам для поросят. Были приготовлены четыре разные серии, одна контрольная серия и три серии, искусственно загрязненные ZEN (Fermentek LTD, Israel; чистота >99,2%). Однородное распределение ZEN в питании достигалось путем приготовления премиксов мальтодекстрина, которые содержали соответствующее количество ZEN и которые добавляли к основному корму с содержанием 0,9% (масс./масс). Окончательные концентрации ZEN были проверены с помощью ВЭЖХ-МС (Romer Labs GmbH) и подтверждены.
[0144] Кровь собирали еженедельно (день 0, 6, 14, 21 и 28) у отдельных животных посредством пункции краниальной полой вены vena cava cranialis (Primavette® EDTA, Kabe Labortechnik GmbH, Numbrecht-Elsenroth, Германия). После центрифугирования (1500 x g, 20 мин) образцы сыворотки хранили при -80 °С для последующего анализа. Длину и ширину вульвы измеряли через равные промежутки времени с помощью штангенциркуля для определения эффектов ZEN в питании. Площадь вульвы рассчитывали как длина вульвы х ширина вульвы, как сообщалось ранее (Jiang et al. 2011. Journal of animal science, 89, 3008-3015). За экспериментальный период было проведено восемь измерений для поросенка.
[0145] После 28 дней воздействия экспериментального питания свиней анестезировали внутримышечной инъекцией кетамина (0,1 мл/кг массы тела (м.т.) Narketan®, Vetoquinol GmbH, Ravensburg, Германия) и азаперона (0,03 мл/кг м. т.; Stresnil®, Janssen-Cilag, Neuss, Германия). Впоследствии животных умерщвляли путем внутрисердечной инъекции Т61® (Intervet, Unterschlei*Bheim, Германия; 0,1 мл/кг м. т.). Весь репродуктивный тракт собирали, взвешивали и исследовали на наличие каких-либо клинических признаков. Небольшие кусочки тела матки и средней части тощей кишки рассекали, помещали в 1 мл RNAlater и хранили в течение ночи при 4 °С. На следующий день все образцы тканей переносили в -80 °С для долгосрочного хранения и до обработки для транскриптомного анализа.
[0146] Результаты: Воздействие ZEN увеличивало поверхность вульвы дозозависимым и зависящим от времени образом (см. ФИГ. 1). В частности, поросята из групп со средни и высоким ZEN показали значительное увеличение поверхности вульвы после тринадцати и шести дней воздействия, соответственно. На 26 день увеличение поверхности вульвы по сравнению с контрольной группой составляло +90% для группы со средним ZEN и +230% для группы с высоким ZEN. Аналогично, масса всего репродуктивного тракта (включая влагалище, матку, маточные трубы, яичники) была значительно увеличена у поросят группы с высоким ZEN. Массу репродуктивного тракта выражали относительно индивидуальной массы тела ([репродуктивный тракт (в граммах)/масса тела (в кг)]*100), и расчетное среднее значение (±СО) было следующим: 51,8 ± 20,6, 55,8 ± 17,2, 121,4 ± 43,4 и 353,4 ± 110,6 в группах контроля, низкого ZEN, среднего ZEN и высокого ZEN, соответственно. Значительные различия наблюдались между группой с высоким ZEN и контрольной группой (р-величины <0,001). Независимо от концентрации, воздействие ZEN не влияло на массу тела поросят.
[0147] Пример 2: анализ микроРНК в тканях
[0148] Экстракция микроРНК и подготовка библиотеки: В общей сложности 18 животных применяли для исследований профиля микроРНК в тканях: 6 из группы контроля, 4 из группы с низким ZEN, 4 из группы со средним ZEN и 4 из группы с высоким ZEN. Приблизительно 30 мг ткани из матки или тощей кишки разрушали с помощью шариковой мельницы, и общую РНК, включая РНК из приблизительно 18 нуклеотидов и более, экстрагировали и очищали с помощью набора miRNeasy Mini Kit (Qiagen, Hilden, Германия), следуя инструкциям производителя. Концентрацию РНК сначала оценивали на Nanodrop (Termo Scientific NanoDrop 2000, США), и снова с применением биоанализатора Agilent 2100 (Технологии Agilent, Германия) во время измерения RIN для определения качества РНК. В общей сложности 1 мкг общей РНК использовали для построения библиотек секвенирования небольших РНК с использованием набора препаратов NEBNext Multiplex SmallRNA Library для Illumina (New England Biolabs). Лигированную с помощью адаптера общую РНК обратно транскрибировали в кДНК, которую использовали в качестве матрицы для ПЦР-амплификации (15 циклов) с использованием праймера SR Illumina и индексных праймеров 1-18. Библиотеки баркодированных ДНК очищали с использованием протокола очистки QIAQuick PCR (Qiagen, Hilden, Германия) и количественно определяли с использованием высокочувствительного чипа DNA 1000 (Agilent Technologies, Германия). Очищенные образцы объединяли при эквимолярной (50 нМ) концентрации. Выбор размера проводили с применением выделения из геля для выбора размеров вставки от 18 до 50 нуклеотидов. Конечные мультиплексированные (n=18) библиотеки секвенировали на приборе для секвенирования NextSeq 500 в соответствии с инструкциями производителя. Необработанные данные демультиплексировали, и файлы FASTQ для каждого образца генерировали с помощью программного обеспечения bcl2fastq (Illumina inc.). Данные FASTQ проверяли с применением онлайн инструмента FastQC (http://www.bioinformatics.babraham.ac.uk/projects/fastqc/).
[0149] Биоинформатический анализ секвенирования РНК (RNA-Seq): Для общего количества прочтений последовательности адаптера обрезали с помощью Cutadapt и проводили фильтрацию по качеству (Q-Score >30) с применением инструмента FastQC. Обрезанные и отфильтрованные по качеству прочтения выравнивали с референсными последовательностями микроРНК в miRBase release 21 (www.mirbase.org; Kozomora and Griffiths-Jones. 2014. Nucleid Acids Research, 42, D68-D73) с применением bowtie2. Впоследствии прочтения картировали относительно геномной сборки Sus scrofa Sscrofal0.2, а также небольших некодирующих референсных баз данных РНК Ensembl. Прочтения были нормализованы к общему количеству прочтений в библиотеке, чтобы генерировать значения меток на миллион (ТРМ). Clustvis применяли для анализа неконтролируемой кластеризации. EdgeR (Robinson et al. 2010. Bioinformatics, 26, 139-140) применяли для анализа дифференциальной экспрессии на основе значений ТРМ. Полученные р-величины были скорректированы для многократного тестирования с использованием коэффициента ложного обнаружения Бенджамини-Хохберга (FDR). Скорректированные р-величины ≤0,07 считали значимыми.
[0150] Валидация РНК-последовательности: Полимеразную цепную реакцию в реальном времени, также называемую количественной полимеразной цепной реакцией (кПЦР), использовали для верификации некоторых результатов, полученных для РНК-последовательности из матки. Начиная с тех же образцов общей РНК, которые применяли для анализа секвенирования, кДНК синтезировали с применением универсального набора для синтеза кДНК Universal cDNA Synthesis Kit II (Exiqon, Дания) в реакции обратной транскрипции (ОТ) с использованием 50 нг общей РНК. Условия реакции применяли в соответствии с рекомендациями производителя. Для контроля эффективности ОТ и наличия примесей с ингибирующей активностью, к реакции ОТ добавляли синтетический spike-in РНК (cel-miR-39-3р). ПЦР-амплификацию проводили в формате 96-луночного планшета в приборе Roche LC480 II (Roche, Германия) и с использованием EXiLENT SYBR Green mastermix (Exiqon, Дания) со следующими настройками: 95 °С в течение 10 мин, 45 циклов 95 °С в течение 10 с и 60 °С в течение 60 с с последующим анализом кривой плавления. Для расчета цикла значений количественного определения (Cq-значения) применяли способ второй производной. Значения Cq нормировали к среднему значению Cq в каждом образце (global mean normalization) путем вычитания индивидуального значения Cq микроРНК из среднего значения Cq, рассчитанного для этого образца.
[0151] Результаты: Секвенирование малых РНК выявило наличие 224 микроРНК (с >1 меток на миллион), известных у видов свиней (ssc) в образцах матки, из в общей сложности 461 зрелой микроРНК, которые в настоящее время известны в miRBase для свиней. Из них на 16 (средний ZEN) и 74 (высокий ZEN) микроРНК было оказано значительное влияние после воздействия ZEN. На ФИГ. 2 представлен обзор количества микроРНК с повышенной и пониженной регуляцией в различных группах обработки. В группе со средним ZEN достигнуты кратные изменения видоспецифичных микроРНК, на которые оказано значительное влияние, от -3,4 (ssc-miRNA-187) до +3,9 (ssc-miRNA-542-3р) по сравнению с контрольной группой (ФИГ. 3А и 3В). В группе с высоким ZEN эффекты были более выраженными, с кратными изменениями, достигающими от-4,1 (ssc-miRNA-204) до +12,6 (ssc-miRNA-542-3р). В общей сложности на 14 микроРНК (ssc-miR-1, ssc-miR-143-5p, ssc-miR-181c, ssc-miR-187, ssc-miR-206, ssc-miR-335, ssc-miR-424-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-7135-3р) было оказано влияние в группе со средним ZEN и высоким ZEN. Воздействие ZEN приводило к значительному отклонению экспрессии 13 предполагаемых или прогнозируемых микроРНК (ФИГ. 4). Из них, на put-miR-300 было оказано значительное врияние при среднем ZEN и высоком ZEN. Для валидации результатов секвенирования РНК следующего поколения ssc-miR-542-3р, ssc-miR-450c-5p, ssc-miR-503, ssc-miR-424-5p, ssc-miR-181c были успешно количественно определены в образцах матки с помощью кПЦР для всех групп.
[0152] Пример 3: анализ микроРНК в образцах сыворотки крови
[0153] Экстракция микроРНК и анализ кПЦР: В отличие от анализа малых РНК-последовательностей, всех животных из исследования кормления использовали для исследований профиля микроРНК в сыворотке (6 на группу; всего 24 животных). РНК выделяли из образцов сыворотки с помощью набора miRNeasy Mini Kit (Qiagen, Германия). Образцы сыворотки размораживали на льду и центрифугировали при 12000 g в течение 5 минут для удаления любых клеточных остатков. Для каждого образца 200 мкл сыворотки смешивали с 1000 мкл Qiazol и 1 мкл синтетических spike-in (Exiqon, Дания). После 10-минутной инкубации при комнатной температуре к лизатам добавляли 200 мкл хлороформа с последующим центрифугированием с охлаждением при 12000 g в течение 15 минут при 4 °С. Объем 650 мкл верхней водной фазы смешивали с 7 мкл гликогена (50 мг/мл) для усиления осаждения. Образцы переносили в мини-колонку miRNeasy, и РНК осаждали с применением 750 мкл этанола с последующей промывкой буфером RPE и RWT. РНК элюировали в 30 мкл не содержащей нуклеаз воды и хранили при -80 °С до дальнейшего анализа. Начиная с образцов общей РНК, кДНК синтезировали с использованием универсального набора для синтеза кДНК Universal cDNA Synthesis Kit II (Exiqon, Дания). Условия реакции были выбраны в соответствии с рекомендациями производителя. В общей сложности использовали 2 мкл очищенной общей РНК на 10 мкл реакции обратной транскрипции (ОТ). Для контроля эффективности ОТ и наличия примесей с ингибирующей активностью, к реакции ОТ добавляли синтетический spike-in РНК (cel-miR-39-3р). ПЦР-амплификацию проводили в формате 384-луночного планшета с использованием специальных планшетов Pick&Mix (Exiqon, Дания) в приборе Roche LC480 II (Roche, Германия) и EXiLENT SYBR Green mastermix (Exiqon, Дания) со следующими настройками: 95 °С в течение 10 мин, 45 циклов 95 °С в течение 10 с и 60 °С в течение 60 с с последующим анализом кривой плавления. Для расчета цикла значений количественного определения (Cq-значения) применяли способ второй производной, как известно специалисту в данной области техники. Значения Cq нормировали к среднему значению Cq в каждом образце (global mean normalization) путем вычитания индивидуального значения Cq микроРНК из среднего значения Cq, рассчитанного для этого образца. МикроРНК, выбранные для целевого анализа, их ответы на обработку ZEN в образцах матки и их релевантность показаны в Таблице 1.
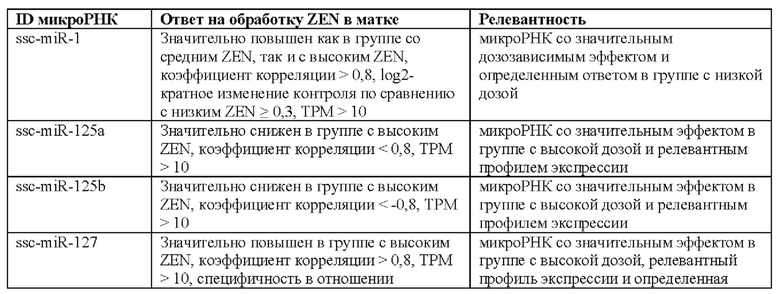
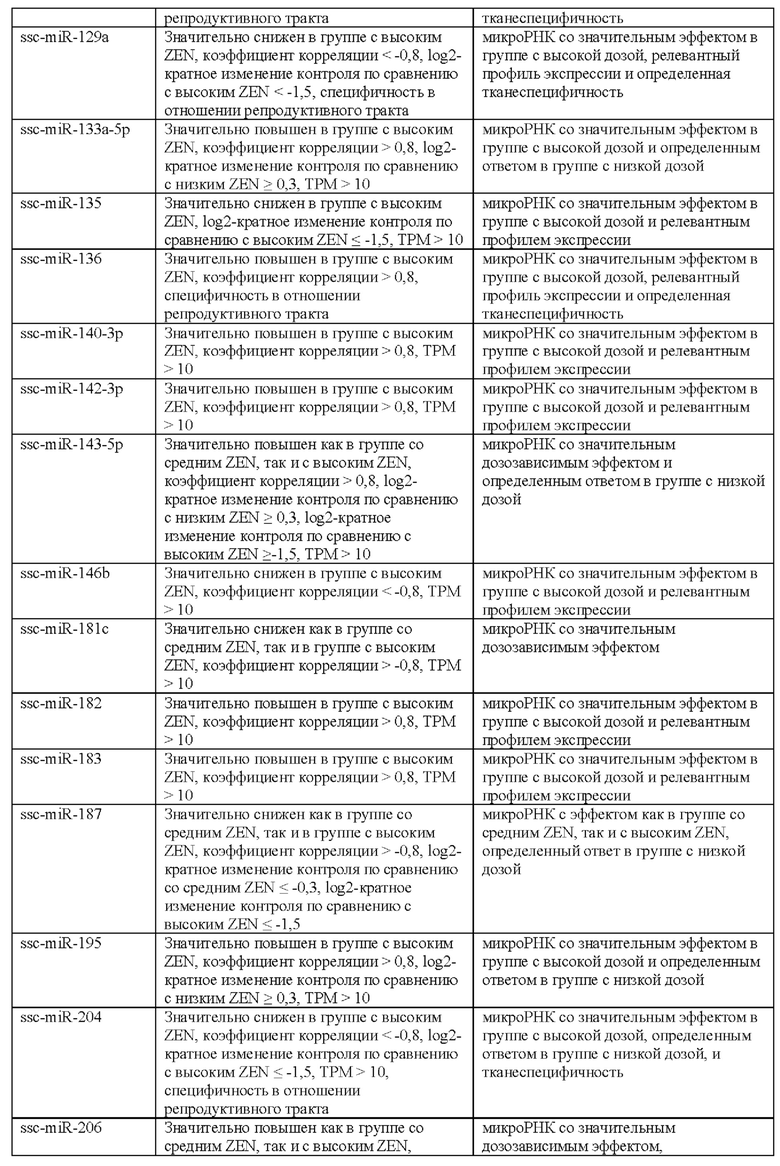
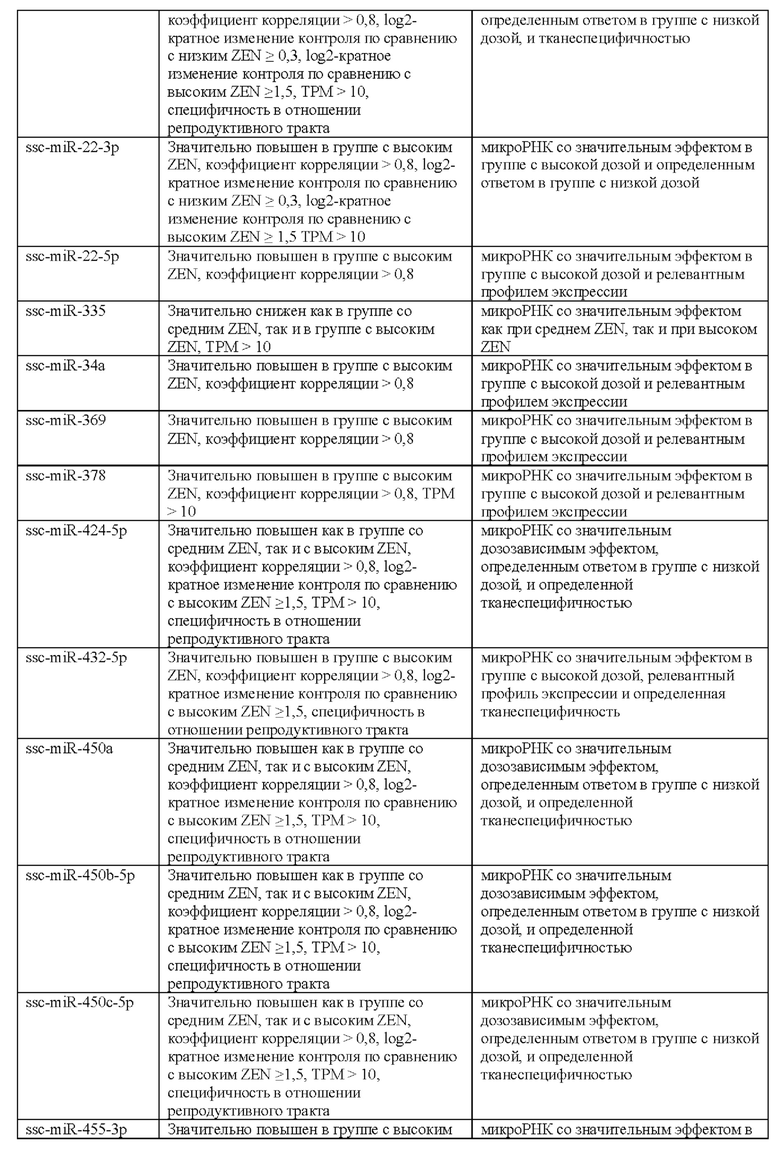
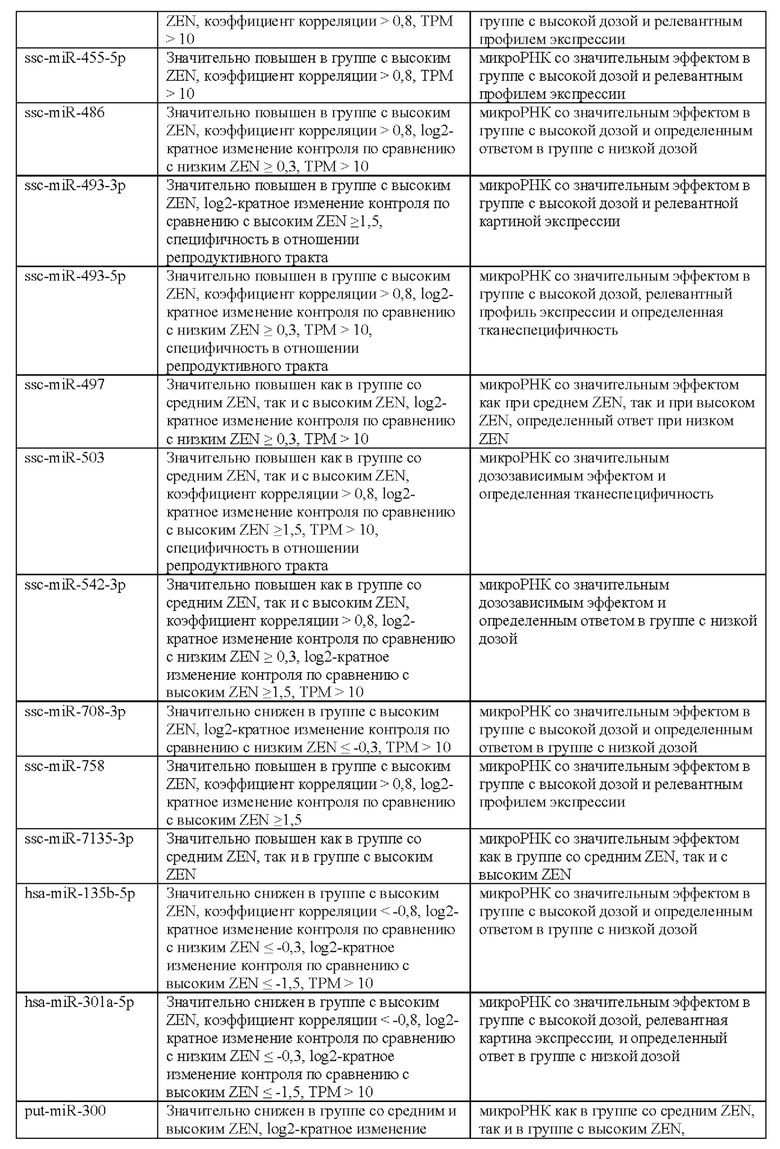

[0154] Результаты: Целевой анализ ssc-miR-1, ssc-miR-125a, ssc-miR-125b, ssc-miR-127, ssc-miR-129a, ssc-miR-133a-5p, ssc-miR-135, ssc-miR-136, ssc-miR-140-3р, ssc-miR-142-3p, ssc-miR-143-5p, ssc-miR-146b, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-miR-187, ssc-miR-195, ssc-miR-204, ssc-miR-206, ssc-miR-22-3р, ssc-miR-22-5p, ssc-miR-335, ssc-miR-34a, ssc-miR-369, ssc-miR-378, ssc-miR-424-5p, ssc-miR-432-5p, ssc-miR-450a, ssc-miR-450b-5p, ssc-miR-450c-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-486, ssc-miR-493-3р, ssc-miR-493-5p, ssc-miR-497, ssc-miR-503, ssc-miR-542-3р, ssc-miR-708-3р, ssc-miR-758, ssc-miR-7135-3р, hsa-miR-135b-5p, hsa-miR-301a-5p, put-miR-300 проводили в образцах сыворотки, собранных через 6 и 28 дней после воздействия ZEN. Для ssc-miR-135, ssc-miR-187, ssc-miR-195, ssc-miR-497 амплификацию с помощью кПЦР проводили с помощью праймеров, предназначенных для ортологических последовательностей человека. Однако идентичность последовательностей между последовательностью свиньи и последовательности человека для этих четырех микроРНК составляла 100%. После удаления нескольких микроРНК из набора данных вследствие слишком низкого количества прочтений (ssc-miR-143-5p, ssc-miR-187, ssc-miR-493-5p, ssc-miR-708-3р, ssc-miR-7135-3р, ssc-miR-135b-5p, hsa-miR-301a-5p, put-miR-300), акцент был сделан на сравнении поддающихся количественному определению уровней микроРНК между группой контроля и группой с высоким ZEN. Три (день 6) и пять (день 28) микроРНК продемонстрировали повышенную или пониженную регуляцию после воздействия ZEN (нескорректированная р-величина ≤0,1). МикроРНК с повышенной регуляцией включают ssc-miR-140-3р, ssc-miR-455-3р, ssc-miR-455-5p и ssc-miR-542-3р, в то время как микроРНК с пониженной регуляцией включают ssc-miR-1, ssc-miR-142-3р, ssc-miR-181c и ssc-miR-182. На ФИГ. 5 приведена подробная информация о log2-преобразованных кратных изменениях уровней микроРНК в сыворотке после воздействия ZEN. В дополнение к вышеуказанным микроРНК, ZEN оказывал значительный эффект на log2-преобразованные кратные изменения (≤-0,8 или ≥0,8) шести микроРНК, а именно ssc-miR-129а, ssc-miR-135, ssc-miR-206, ssc-miR-432-5p, ssc-miR-493-3р и ssc-miR-503. Для дальнейшего изучения глобальных эффектов ZEN вне зависимости от концентраций были проведены анализы основных компонентов (РСА) на данных (кратные изменения) для всех групп и для всех микроРНК. Это позволило обнаружить микроРНК, которые не являются постоянными во всех видах обработки. Таким образом, были обнаружены некоторые микроРНК, на которые, как уже сообщалось, было оказано влияние, а также новые микроРНК, такие как ssc-miR-183. Исходя из полученных данных, ssc-miR-1, ssc-miR-129a, hsa-miR-135a-3p, ssc-140-3р, ssc-miR-142-3р, ssc-miR-181c, ssc-miR-182, ssc-miR-183, ssc-206, ssc-miR-432-5p, ssc-miR-455-3р, ssc-miR-455-5p, ssc-miR-493-3р, ssc-miR-503 and ssc-miR-542-3р были идентифицированы как подходящие микроРНК для применения в качестве биомаркеров, основанных на механизме, для определения воздействия ZEN на основе значимой повышающей или понижающей регуляции и релевантного профиля экспрессии, который учитывает как относительное кратное изменение, так и абсолютные уровни экспрессии.
[0155] Пример 4: Корреляция уровней микроРНК в ткани и сыворотке
[0156] Для сравнения результатов микроРНК, полученных для матки (количество прочтений NGS) и сыворотки (значения кПЦР dCq), был проведен корреляционный анализ. С этой целью прочтения NGS подвергали log2-преобразованию, а остатки (разница со средним) рассчитывали и использовали для корреляции. Две микроРНК продемонстрировали тенденцию корреляции уровней экспрессии в тканях и сыворотке: ssc-miR-455-5p (размер выборки: 17; коэффициент корреляции r=0,4045; уровень значимости Р=0,1073; 95% доверительный интервал для г: от -0,09449 до 0,7411) и ssc-miR-542-3р (размер выборки: 17; коэффициент корреляции r=0,4244; уровень значимости Р=0,0895; 95% доверительный интервал для r: от -0,07066 до 0,7517).
[0157] Пример 5: соотношения микроРНК и анализ рабочих характеристик (ROC)
[0158] Были определены соотношения между выбранными микроРНК, которые были идентифицированы как подверженные воздействию ZEN в образцах сыворотки, и впоследствии для них применяли подход ROC (анализа рабочих характеристик) в качестве валидированного и распространенного способа оценки биомаркеров (Grand and Sabin. 2010. Current Opinion in HIV and AIDS, 5, 473-479). Таким образом, были определены подходящие соотношения, которые допускали различие между свиньями, не подвергавшимися воздействию ZEN (контроль), и свиньями, подвергавшимися воздействию ZEN (низкий ZEN, средний ZEN, высокий ZEN): ssc-miR-135/ssc-miR-432-5p, ssc-miR-455-5p/ssc-miR-493-3p, ssc-miR-542-3p/ssc-miR-1 и ssc-miR-542-3p/ssc-miR-493-3p (ФИГ. 6).
[0159] В дополнение к 15 микроРНК сыворотки, идентифицированным как микроРНК, подходящие для применения в качестве биомаркеров, основанных на механизме, в отношении воздействия ZEN, описанным в Примере 3, было обнаружено, что соотношения микроРНК ssc-miR-135/ssc-miR-432-5p, ssc-miR-455-5p/ssc-miR-493-3p, ssc-miR-542-3p/ssc-miR-1 и ssc-miR-542-3p/ssc-miR-493-3p являются особенно надежными и хорошо выраженными биомаркерами, позволяющими обнаруживать воздействие ZEN.
[0160] Изобретение, иллюстративно описанное в настоящей заявке, может быть соответствующим образом реализовано в отсутствие какого-либо элемента или элементов, ограничения или ограничений, конкретно не описанных в настоящей заявке. Кроме того, термины и выражения, используемые в настоящей заявке, применялись в качестве терминов для описания, а не ограничения, и нет намерения использовать такие термины и выражения для исключения любых эквивалентов показанных и описанных признаков или их частей, но необходимо признать, что различные модификации возможны в пределах объема заявленного изобретения. Таким образом, следует понимать, что, хотя настоящее изобретение было конкретным образом раскрыто с помощью иллюстративных вариантов реализации изобретения и необязательных признаков, специалисты в данной области техники могут прибегнуть к модификации и вариации изобретений, воплощенных в настоящей заявке, и что такие модификации и вариации считаются входящими в объем настоящего изобретения.
[0161] Настоящее изобретение описано в широком и общем виде в настоящей заявке. Каждый из более узких видов и подгрупп, подпадающих под общее описание, также являются частью настоящего изобретения. Оно включает в себя общее описание настоящего изобретения с условием или отрицательным ограничением удаления любого субъекта из рода, независимо от того, указан ли конкретно в настоящей заявке исключаемый предмет.
[0162] Другие варианты реализации находятся в пределах следующей формулы изобретения. Кроме того, если признаки или аспекты настоящего изобретения описаны терминами групп Маркуша, специалистам в данной области техники будет понятно, что настоящее изобретение также описано терминами любого отдельного члена или подгруппы членов группы Маркуша.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Erber Aktiengesellschaft
<120> Биомаркер
<130> ERB16374PCT
<150> EP18210684.9
<151> 2018-12-06
<160> 50
<170> BiSSAP 1.3.6
<210> 1
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 1
uggaauguaa agaaguaugu a 21
<210> 2
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 2
ucccugagac ccuuuaaccu gug 23
<210> 3
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 3
ucccugagac ccuaacuugu ga 22
<210> 4
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 4
ucggauccgu cugagcuugg cu 22
<210> 5
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 5
aagcccuuac cccaaaaagc au 22
<210> 6
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 6
agcugguaaa auggaaccaa au 22
<210> 7
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 7
uauggcuuuu uauuccuaug uga 23
<210> 8
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 8
acuccauuug uuuugaugau gga 23
<210> 9
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 9
uaccacaggg uagaaccacg gac 23
<210> 10
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 10
uguaguguuu ccuacuuuau gg 22
<210> 11
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 11
ggugcagugc ugcaucucug g 21
<210> 12
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 12
ugagaacuga auuccauagg c 21
<210> 13
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 13
aacauucaac cugucgguga gu 22
<210> 14
<211> 24
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 14
uuuggcaaug guagaacuca cacu 24
<210> 15
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 15
uauggcacug guagaauuca cug 23
<210> 16
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 16
ucgugucuug uguugcagcc gg 22
<210> 17
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 17
uagcagcaca gaaauauugg c 21
<210> 18
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 18
uucccuuugu cauccuaugc cu 22
<210> 19
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 19
uggaauguaa ggaagugugu ga 22
<210> 20
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 20
aagcugccag uugaagaacu gu 22
<210> 21
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 21
aguucuucag uggcaagcuu ua 22
<210> 22
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 22
ucaagagcaa uaacgaaaaa ug 22
<210> 23
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 23
uggcaguguc uuagcugguu gu 22
<210> 24
<211> 21
<212> РНК
<213> Sus scrofa
<400> 24
aauaauacau gguugaucuu u 21
<210> 25
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 25
acuggacuug gagucagaag gc 22
<210> 26
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 26
cagcagcaau ucauguuuug aa 22
<210> 27
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 27
ucuuggagua ggucauuggg u 21
<210> 28
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 28
uuuugcgaug uguuccuaau au 22
<210> 29
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 29
uuuugcaaua uguuccugaa ua 22
<210> 30
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 30
uuuugcgaug uguuccuaau ac 22
<210> 31
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 31
gcaguccaug ggcauauaca c 21
<210> 32
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 32
uaugugccuu uggacuacau cg 22
<210> 33
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 33
uccuguacug agcugccccg ag 22
<210> 34
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 34
ugaaggucua cugugugcca gg 22
<210> 35
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 35
uuguacaugg uaggcuuuca uu 22
<210> 36
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 36
cagcagcaca cugugguuug u 21
<210> 37
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 37
uagcagcggg aacaguacug cag 23
<210> 38
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 38
ugugacagau ugauaacuga aa 22
<210> 39
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 39
caacuagacu gugagcuucu aga 23
<210> 40
<211> 21
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 40
uuugugaccu gguccacuaa c 21
<210> 41
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 41
aucugucugu gucucugagc ag 22
<210> 42
<211> 23
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 42
uauggcuuuu cauuccuaug uga 23
<210> 43
<211> 22
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 43
gcucugacuu uauugcacua cu 22
<210> 44
<211> 24
<212> РНК
<213> Sus scrofa
<220>
<223> микроРНК
<400> 44
uugcaggaac uugugagucu ccua 24
<210> 45
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Домен альфа/бета гидролазы
<400> 45
Met Val Thr Ser Pro Ala Leu Arg Asp Val His Val Pro His Ala Tyr
1 5 10 15
Pro Glu Gln Gln Val Asp Leu Gly Glu Ile Thr Met Asn Tyr Ala Glu
20 25 30
Ala Gly Asp Pro Asp Arg Pro Ala Val Leu Leu Ile Pro Glu Gln Thr
35 40 45
Gly Ser Trp Trp Ser Tyr Glu Glu Ala Met Gly Leu Leu Ser Glu His
50 55 60
Phe His Val Tyr Ala Val Asp Leu Arg Gly Gln Gly Arg Ser Ser Trp
65 70 75 80
Thr Pro Lys Arg Tyr Ser Leu Asp Asn Phe Gly Asn Asp Leu Val Arg
85 90 95
Phe Ile Ala Leu Val Val Lys Arg Pro Val Val Val Ala Gly Asn Ser
100 105 110
Ser Gly Gly Val Leu Ala Ala Trp Leu Ser Ala Tyr Ser Met Pro Gly
115 120 125
Gln Leu Arg Gly Val Leu Cys Glu Asp Pro Pro Phe Phe Ala Ser Glu
130 135 140
Leu Val Pro Ala His Gly His Ser Val Arg Gln Gly Ala Gly Pro Val
145 150 155 160
Phe Glu Leu Phe Arg Thr Tyr Leu Gly Asp Gln Trp Ser Val Gly Asp
165 170 175
Trp Glu Gly Phe Cys Arg Ala Ala Gly Ala Ser Ala Ser Pro Met Ala
180 185 190
Arg Ser Phe Val Ala Asp Gly Ile Pro Gln His Leu Gln Glu Tyr Asp
195 200 205
Pro Glu Trp Ala Arg Val Phe Tyr Glu Gly Thr Val Gly Leu Ser Cys
210 215 220
Pro His Glu Arg Met Leu Gly Gln Val Lys Thr Pro Val Leu Leu Thr
225 230 235 240
His His Met Arg Gly Ile Asp Pro Glu Thr Gly Asn Leu Leu Gly Ala
245 250 255
Leu Ser Asp Glu Gln Ala Leu Arg Ala Arg Arg Leu Met Asp Ser Ala
260 265 270
Gly Val Thr Val Asp Tyr Glu Ser Val Pro Asp Ala Ser His Met Met
275 280 285
His Gln Ser Ala Pro Ala Arg Tyr Val Glu Ile Phe Thr Arg Trp Ala
290 295 300
Ala Ala Leu Ala Pro
305
<210> 46
<211> 308
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Домен альфа/бета гидролазы
<400> 46
Met Ala Asp Pro Ala Gln Arg Asp Val Tyr Val Pro His Ala Tyr Pro
1 5 10 15
Glu Lys Gln Ala Asp Leu Gly Glu Ile Thr Met Asn Tyr Ala Glu Ala
20 25 30
Gly Glu Pro Asp Met Pro Ala Val Leu Leu Ile Pro Glu Gln Thr Gly
35 40 45
Ser Trp Trp Gly Tyr Glu Glu Ala Met Gly Leu Leu Ala Glu Asn Phe
50 55 60
His Val Tyr Ala Val Asp Leu Arg Gly Gln Gly Arg Ser Ser Trp Ala
65 70 75 80
Pro Lys Arg Tyr Ser Leu Asp Asn Phe Gly Asn Asp Leu Val Arg Phe
85 90 95
Ile Ala Leu Val Val Lys Arg Pro Val Ile Val Ala Gly Asn Ser Ser
100 105 110
Gly Gly Val Leu Ala Ala Trp Leu Ser Ala Tyr Ser Met Pro Gly Gln
115 120 125
Val Arg Gly Ala Leu Cys Glu Asp Ala Pro Phe Phe Ala Ser Glu Leu
130 135 140
Val Thr Thr Cys Gly His Ser Ile Arg Gln Ala Ala Gly Pro Met Phe
145 150 155 160
Glu Leu Phe Arg Thr Tyr Leu Gly Asp Gln Trp Ser Val Gly Asp Trp
165 170 175
Thr Gly Tyr Cys Arg Ala Ala Asp Ala Ser Ser Ser Pro Met Ala Arg
180 185 190
Tyr Phe Val Ala Asp Glu Ile Pro Gln His Met Arg Glu Tyr Asp Pro
195 200 205
Glu Trp Ala Arg Ala Phe Trp Glu Gly Thr Val Ala Leu His Cys Pro
210 215 220
His Glu Gln Leu Leu Thr Gln Val Lys Thr Pro Val Leu Leu Thr His
225 230 235 240
His Met Arg Asp Ile Asp Pro Asp Thr Gly His Leu Val Gly Ala Leu
245 250 255
Ser Asp Glu Gln Ala Ala Arg Ala Arg Leu Leu Met Glu Ser Ala Gly
260 265 270
Val Lys Val Asp Tyr Ala Ser Val Pro Asp Ala Leu His Met Met His
275 280 285
Gln Phe Asp Pro Pro Arg Tyr Val Glu Ile Phe Thr Gln Trp Ala Ala
290 295 300
Thr Leu Ala Ala
305
<210> 47
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Домен альфа/бета гидролазы
<400> 47
Met Val Thr Ser Pro Ala Leu Arg Asp Val His Val Pro His Ala Tyr
1 5 10 15
Pro Glu Gln Gln Val Asp Leu Gly Glu Ile Thr Met Asn Tyr Ala Glu
20 25 30
Ala Gly Asp Pro Gly Arg Pro Ala Val Leu Leu Ile Pro Glu Gln Thr
35 40 45
Gly Ser Trp Trp Ser Tyr Glu Glu Ala Met Gly Leu Leu Ala Glu His
50 55 60
Phe His Val Tyr Ala Val Asp Leu Arg Gly Gln Gly Arg Ser Ser Trp
65 70 75 80
Thr Pro Lys Arg Tyr Ser Leu Asp Asn Phe Gly Asn Asp Leu Val Arg
85 90 95
Phe Ile Ala Leu Val Val Arg Arg Pro Val Val Val Ala Gly Asn Ser
100 105 110
Ser Gly Gly Val Leu Ala Ala Trp Leu Ser Ala Tyr Ser Met Pro Gly
115 120 125
Gln Ile Arg Gly Val Leu Cys Glu Asp Pro Pro Phe Phe Ala Ser Glu
130 135 140
Leu Val Pro Ala His Gly His Ser Val Arg Gln Gly Ala Gly Pro Val
145 150 155 160
Phe Glu Leu Phe Arg Thr Tyr Leu Gly Asp Gln Trp Ser Val Gly Asp
165 170 175
Trp Glu Gly Phe Arg Ser Ala Ala Asp Ala Ser Ala Ser Pro Met Ala
180 185 190
Arg Ser Phe Val Ala Asp Thr Ile Pro Gln His Leu Lys Glu Tyr Asp
195 200 205
Pro Glu Trp Ala Arg Ala Phe Tyr Glu Gly Thr Val Gly Leu Asn Cys
210 215 220
Pro His Glu Arg Met Leu Asn Arg Val Asn Thr Pro Val Leu Leu Thr
225 230 235 240
His His Met Arg Gly Thr Asp Pro Glu Thr Gly Asn Leu Leu Gly Ala
245 250 255
Leu Ser Asp Glu Gln Ala Ala Gln Val Arg Arg Leu Met Glu Ser Ala
260 265 270
Gly Val Lys Val Asp Tyr Glu Ser Val Pro Asp Ala Ser His Met Met
275 280 285
His Gln Ser Asp Pro Ala Arg Tyr Ala Glu Ile Leu Thr Pro Trp Thr
290 295 300
Ala Ala Leu Ala Pro
305
<210> 48
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Домен альфа/бета гидролазы
<400> 48
Met Val Thr Ser Pro Ala Leu Arg Asp Val His Val Pro His Ala Tyr
1 5 10 15
Pro Glu Gln Gln Val Asp Leu Gly Glu Ile Thr Met Asn Tyr Ala Glu
20 25 30
Ala Gly Asp Pro Asp Arg Pro Ala Val Leu Leu Ile Pro Glu Gln Thr
35 40 45
Gly Ser Trp Trp Ser Tyr Glu Glu Ala Met Gly Leu Leu Ala Glu His
50 55 60
Phe His Val Tyr Ala Val Asp Leu Arg Gly Gln Gly Arg Ser Ser Trp
65 70 75 80
Thr Pro Lys Arg Tyr Ser Leu Asp Asn Phe Gly Asn Asp Leu Val Arg
85 90 95
Phe Ile Ala Leu Val Val Lys Arg Pro Val Val Val Ala Gly Asn Ser
100 105 110
Ser Gly Gly Val Leu Ala Ala Trp Leu Ser Ala Tyr Ser Met Pro Gly
115 120 125
Gln Leu Arg Gly Val Leu Cys Glu Asp Pro Pro Phe Phe Ala Ser Glu
130 135 140
Leu Val Pro Ala His Gly His Ser Val Arg Gln Gly Ala Gly Pro Val
145 150 155 160
Phe Glu Leu Phe Arg Thr Tyr Leu Gly Asp Gln Trp Ser Val Ser Asp
165 170 175
Trp Glu Gly Phe Cys Arg Ala Ala Gly Ala Ser Ala Ser Pro Met Ala
180 185 190
Arg Ser Phe Val Ala Asp Gly Ile Pro Gln His Leu Lys Glu Tyr Asp
195 200 205
Pro Glu Trp Ala Arg Ala Phe His Glu Gly Thr Val Gly Leu Asn Cys
210 215 220
Pro His Glu Arg Met Leu Gly Arg Val Asn Thr Pro Val Leu Leu Thr
225 230 235 240
His His Met Arg Gly Thr Asp Pro Glu Thr Gly Asn Leu Leu Gly Ala
245 250 255
Leu Ser Asp Glu Gln Ala Ala Gln Ala Arg Leu Leu Met Glu Ser Ala
260 265 270
Gly Val Arg Val Asp Tyr Glu Ser Val Pro Asp Ala Ser His Met Met
275 280 285
His Gln Ser Asp Pro Ala Arg Tyr Ala Glu Ile Phe Thr Arg Trp Ala
290 295 300
Ala Ala Leu Ala Pro
305
<210> 49
<211> 309
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Домен альфа/бета гидролазы
<400> 49
Met Val Thr Ser Pro Ala Leu Arg Asp Val His Val Pro His Ala Tyr
1 5 10 15
Pro Glu Gln Gln Val Asp Leu Gly Glu Ile Thr Met Asn Tyr Ala Glu
20 25 30
Ala Gly Asp Pro Gly Arg Pro Ala Val Leu Leu Ile Pro Glu Gln Thr
35 40 45
Gly Ser Trp Trp Ser Tyr Glu Glu Ala Met Gly Leu Leu Ala Glu His
50 55 60
Phe His Val Tyr Ala Val Asp Leu Arg Gly Gln Gly Arg Ser Ser Trp
65 70 75 80
Thr Pro Lys Arg Tyr Ser Leu Asp Asn Phe Gly Asn Asp Leu Val Arg
85 90 95
Phe Met Ala Leu Val Val Arg Arg Pro Val Val Val Ala Gly Asn Ser
100 105 110
Ser Gly Gly Val Leu Ala Ala Trp Leu Ser Ala Tyr Ser Met Pro Gly
115 120 125
Gln Ile Arg Gly Val Leu Cys Glu Asp Pro Pro Phe Phe Ala Ser Glu
130 135 140
Leu Val Pro Ala His Gly His Ser Val Arg Gln Gly Ala Gly Pro Val
145 150 155 160
Phe Glu Leu Phe Arg Thr Tyr Leu Gly Asp Gln Trp Ser Val Gly Asp
165 170 175
Trp Glu Gly Phe Arg Ser Ala Ala Gly Ala Ser Ala Ser Pro Met Ala
180 185 190
Arg Ser Phe Val Ala Asp Thr Ile Pro Gln His Leu Lys Glu Tyr Asp
195 200 205
Pro Glu Trp Ala Arg Ala Phe Tyr Glu Gly Thr Val Gly Leu Asn Cys
210 215 220
Pro His Glu Arg Met Leu Asn Arg Val Asn Thr Pro Val Leu Leu Thr
225 230 235 240
His His Met Arg Gly Thr Asp Pro Glu Thr Gly Asn Leu Leu Gly Ala
245 250 255
Leu Ser Asp Glu Gln Ala Ala Gln Ala Arg Arg Leu Met Glu Ser Ala
260 265 270
Gly Val Lys Val Asp Tyr Glu Ser Val Pro Asp Ala Ser His Met Met
275 280 285
His Gln Ser Asp Pro Ala Arg Tyr Ala Glu Ile Leu Thr Pro Trp Ala
290 295 300
Ala Ala Leu Ala Pro
305
<210> 50
<211> 328
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<223> Домен альфа/бета гидролазы
<400> 50
Met Ala Glu Glu Gly Thr Arg Ser Glu Ala Ala Asp Ala Ala Thr Gln
1 5 10 15
Ala Arg Gln Leu Pro Asp Ser Arg Asn Ile Phe Val Ser His Arg Phe
20 25 30
Pro Glu Arg Gln Val Asp Leu Gly Glu Val Val Met Asn Phe Ala Glu
35 40 45
Ala Gly Ser Pro Asp Asn Pro Ala Leu Leu Leu Leu Pro Glu Gln Thr
50 55 60
Gly Ser Trp Trp Ser Tyr Glu Pro Val Met Gly Leu Leu Ala Glu Asn
65 70 75 80
Phe His Val Phe Ala Val Asp Ile Arg Gly Gln Gly Arg Ser Thr Trp
85 90 95
Thr Pro Arg Arg Tyr Ser Leu Asp Asn Phe Gly Asn Asp Leu Val Arg
100 105 110
Phe Ile Ala Leu Val Ile Lys Arg Pro Val Val Val Ala Gly Asn Ser
115 120 125
Ser Gly Gly Leu Leu Ala Ala Trp Leu Ser Ala Tyr Ala Met Pro Gly
130 135 140
Gln Ile Arg Ala Ala Leu Cys Glu Asp Ala Pro Phe Phe Ala Ser Glu
145 150 155 160
Leu Val Pro Ala Tyr Gly His Ser Val Leu Gln Ala Ala Gly Pro Ala
165 170 175
Phe Glu Leu Tyr Arg Asp Phe Leu Gly Asp Gln Trp Ser Ile Gly Asp
180 185 190
Trp Lys Gly Phe Val Glu Ala Ala Lys Ala Ser Pro Ala Lys Ala Met
195 200 205
Gln Leu Phe Pro Thr Pro Asp Glu Ala Pro Gln Asn Leu Lys Glu Tyr
210 215 220
Asp Pro Glu Trp Gly Arg Ala Phe Phe Glu Gly Thr Val Ala Leu His
225 230 235 240
Cys Pro His Asp Arg Met Leu Ser Gln Val Lys Thr Pro Ile Leu Ile
245 250 255
Thr His His Ala Arg Thr Ile Asp Pro Glu Thr Gly Glu Leu Leu Gly
260 265 270
Ala Leu Ser Asp Leu Gln Ala Glu His Ala Gln Asp Ile Ile Arg Ser
275 280 285
Ala Gly Val Arg Val Asp Tyr Gln Ser His Pro Asp Ala Leu His Met
290 295 300
Met His Leu Phe Asp Pro Ala Arg Tyr Ala Glu Ile Leu Thr Ser Trp
305 310 315 320
Ser Ala Thr Leu Pro Ala Asn Asp
325
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| Полинуклеотиды, кодирующие релаксин | 2017 |
|
RU2795683C2 |
| Синергетическое действие SMN1 и miR-23a при лечении спинальной мышечной атрофии | 2021 |
|
RU2839898C2 |
| ОНКОЛИТИЧЕСКИЙ HSV-ВЕКТОР | 2014 |
|
RU2719190C2 |
| ДОСТАВКА ТЕРАПЕВТИЧЕСКИХ ПОЛИПЕПТИДОВ ПОСРЕДСТВОМ ПСЕВДОТИПИРОВАННЫХ ОНКОЛИТИЧЕСКИХ ВИРУСОВ | 2017 |
|
RU2758007C2 |
| ЭКЗОСОМАЛЬНЫЕ БИОМАРКЕРЫ | 2015 |
|
RU2712223C2 |
| Средства и способы расщепления зеараленона | 2019 |
|
RU2826156C2 |
| ЛЕЧЕНИЕ РАКА С ИСПОЛЬЗОВАНИЕМ ХИМЕРНОГО АНТИГЕНСПЕЦИФИЧЕСКОГО РЕЦЕПТОРА НА ОСНОВЕ ГУМАНИЗИРОВАННОГО АНТИТЕЛА ПРОТИВ EGFRvIII | 2014 |
|
RU2831418C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ТРАНСДУКЦИИ И ЭКСПАНСИИ ЛИМФОЦИТОВ И РЕГУЛЯЦИИ ИХ АКТИВНОСТИ | 2018 |
|
RU2820974C1 |
| СИНЦИТИАЛЬНЫЕ ОНКОЛИТИЧЕСКИЕ МУТАНТЫ HERPES SIMPLEX В КАЧЕСТВЕ МОЩНЫХ ТЕРАПЕВТИЧЕСКИХ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ РАКА | 2020 |
|
RU2821999C2 |
| ВЕКТОРЫ AAV, НАЦЕЛЕННЫЕ НА ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ | 2015 |
|
RU2727015C2 |
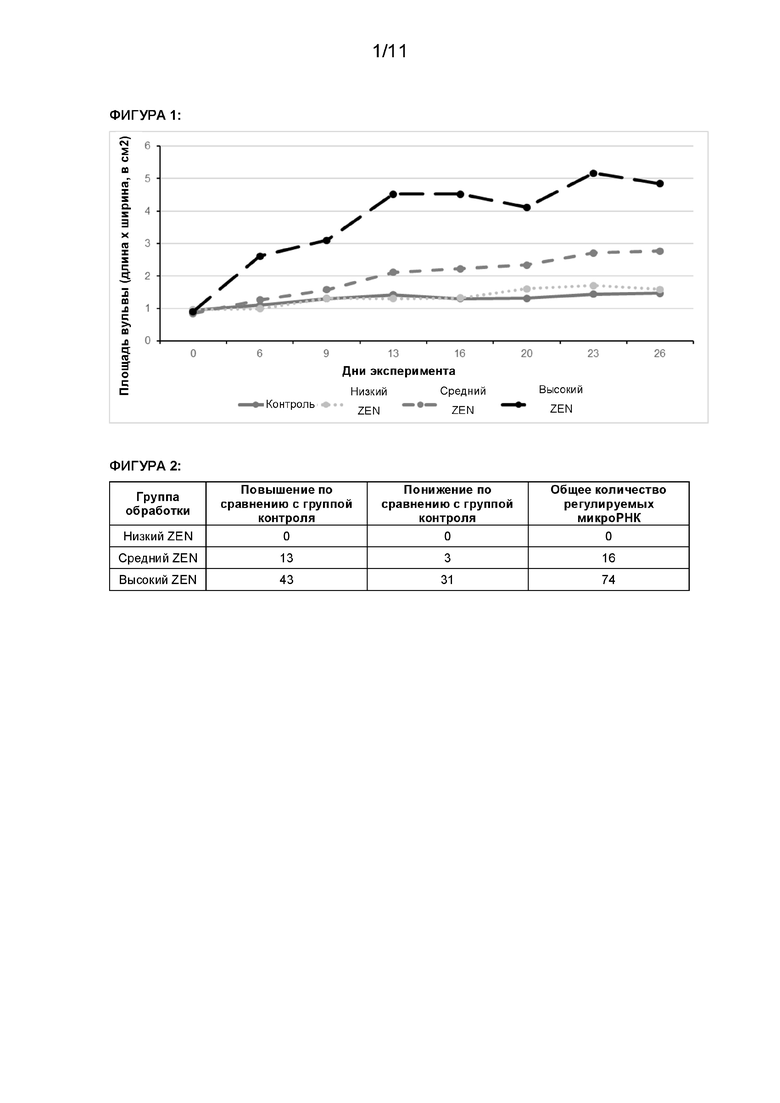
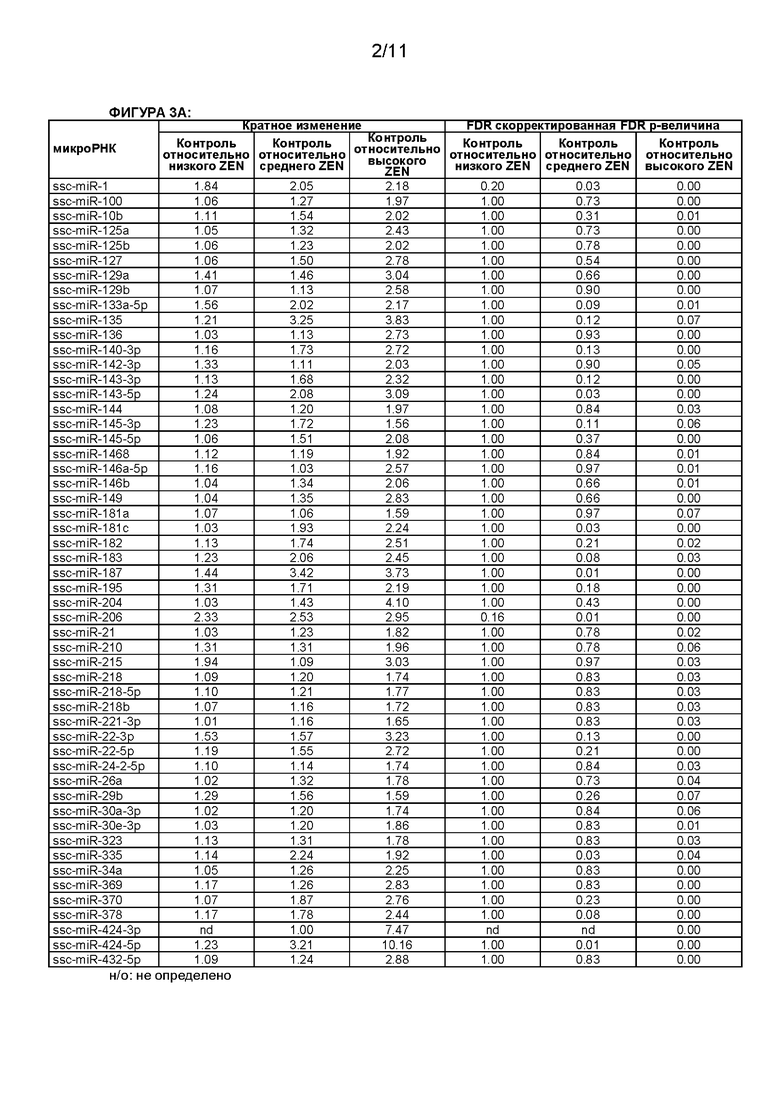
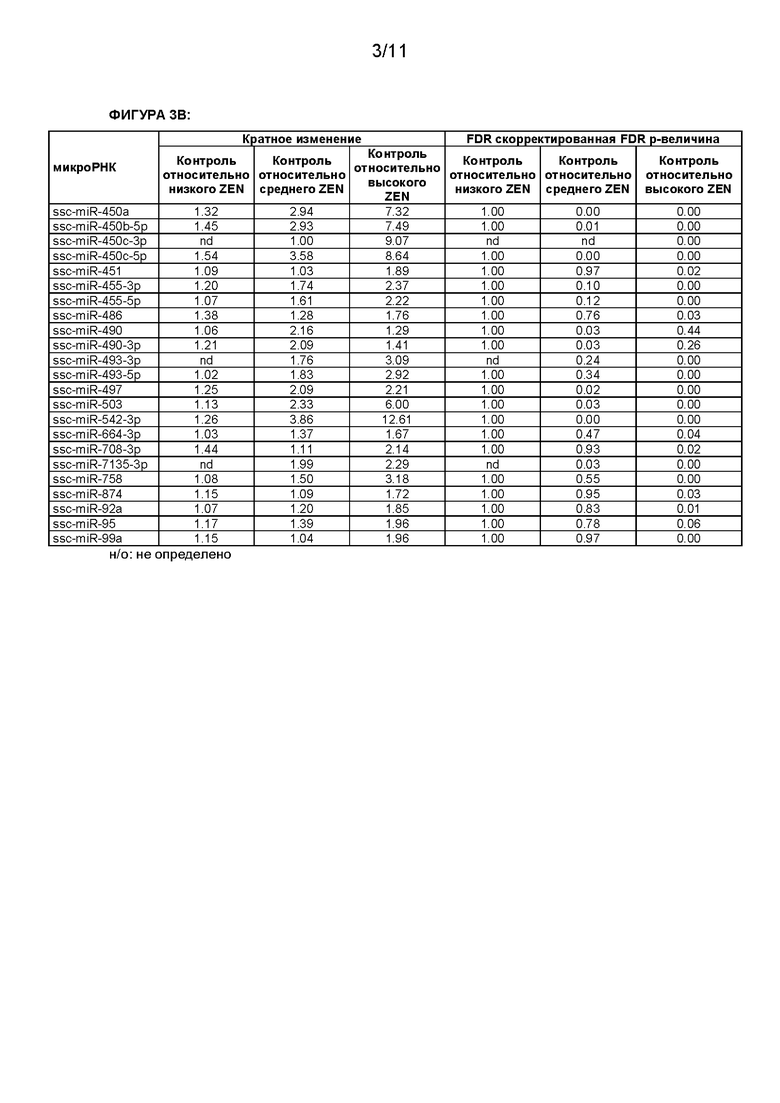
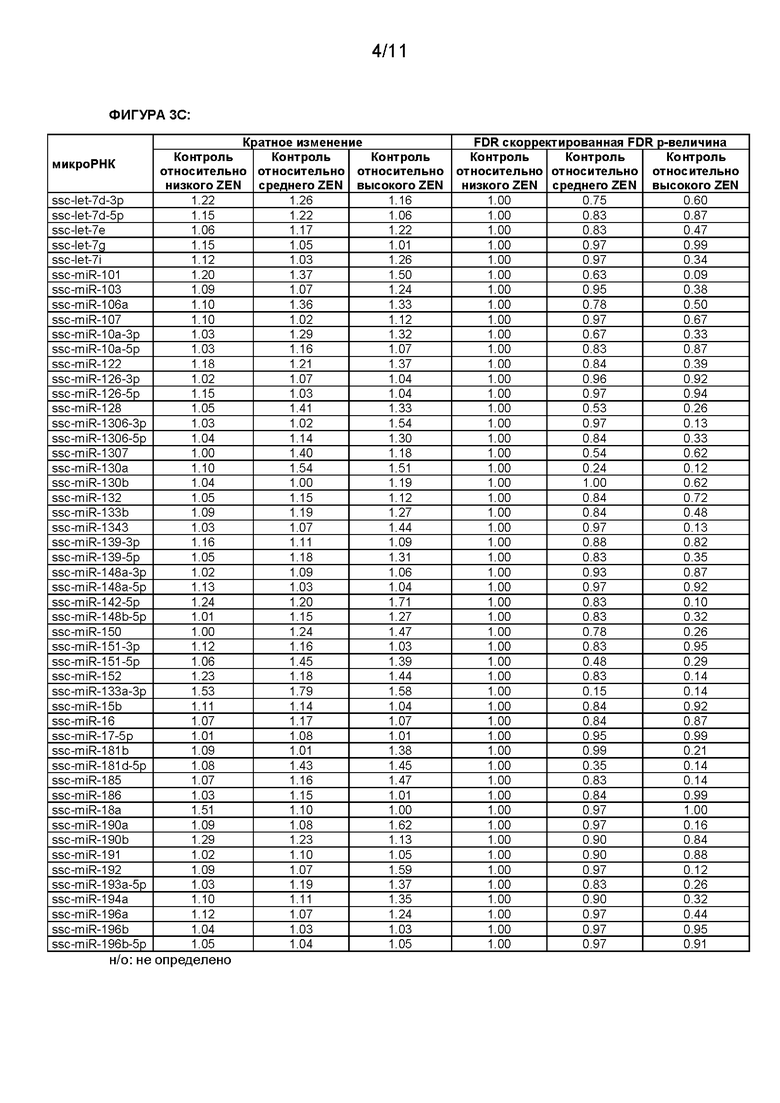
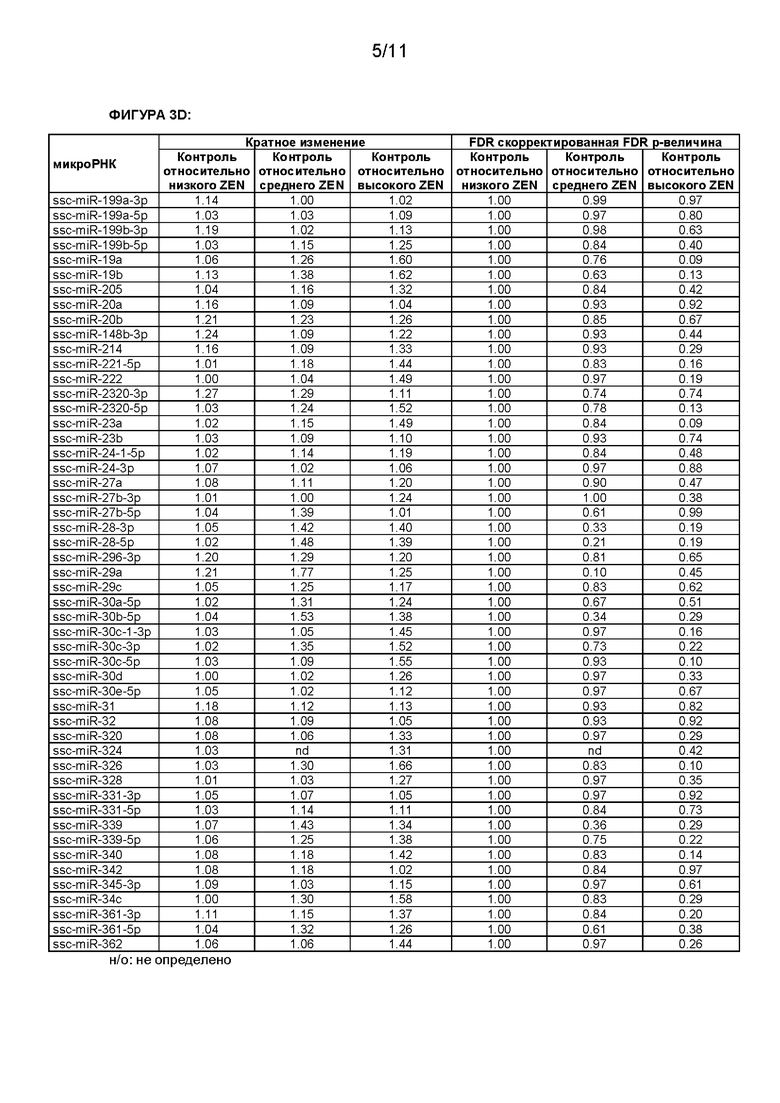
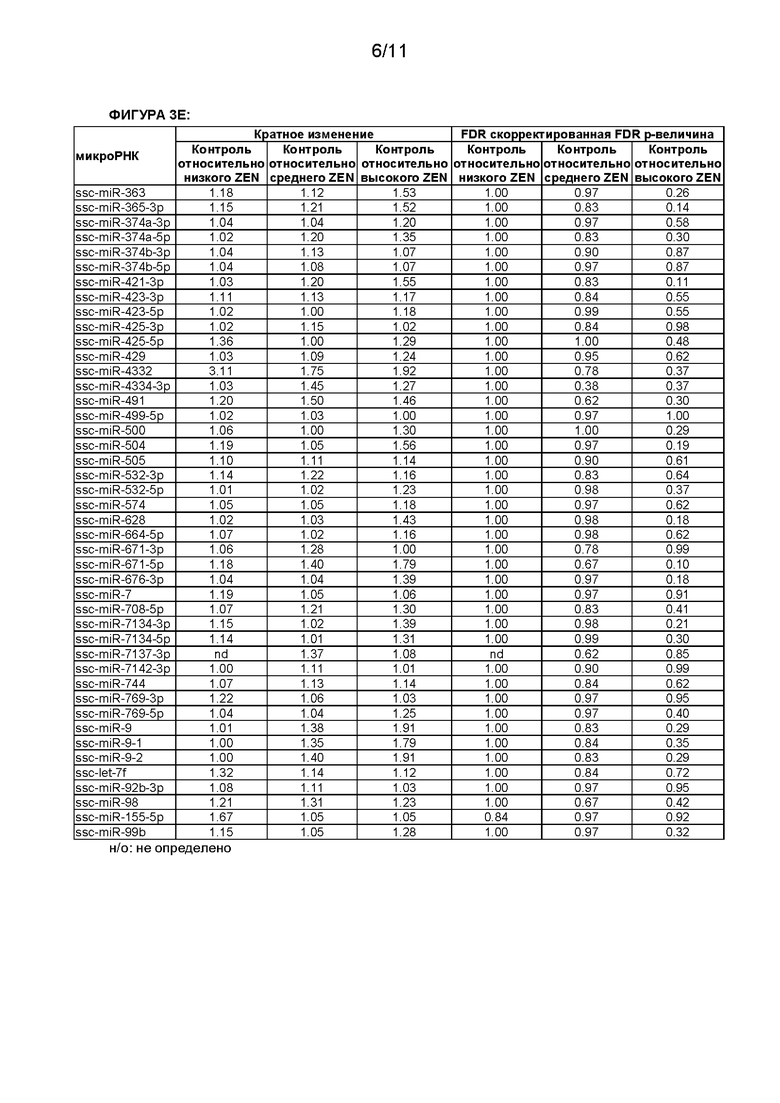
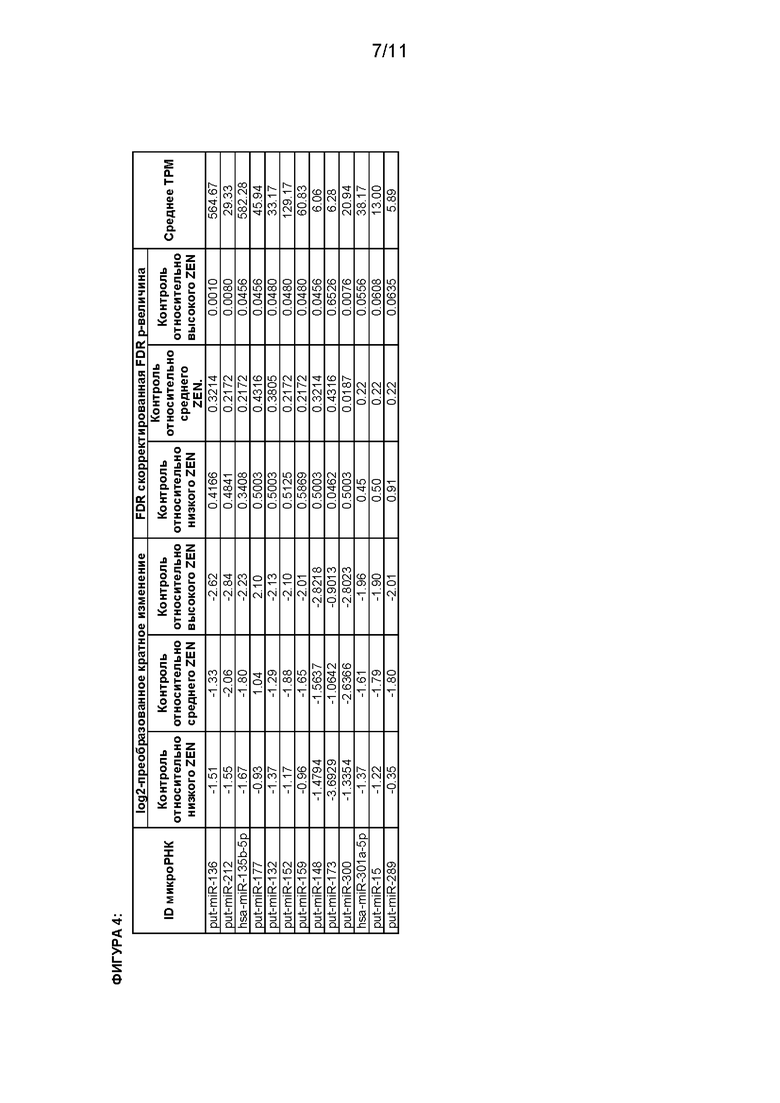
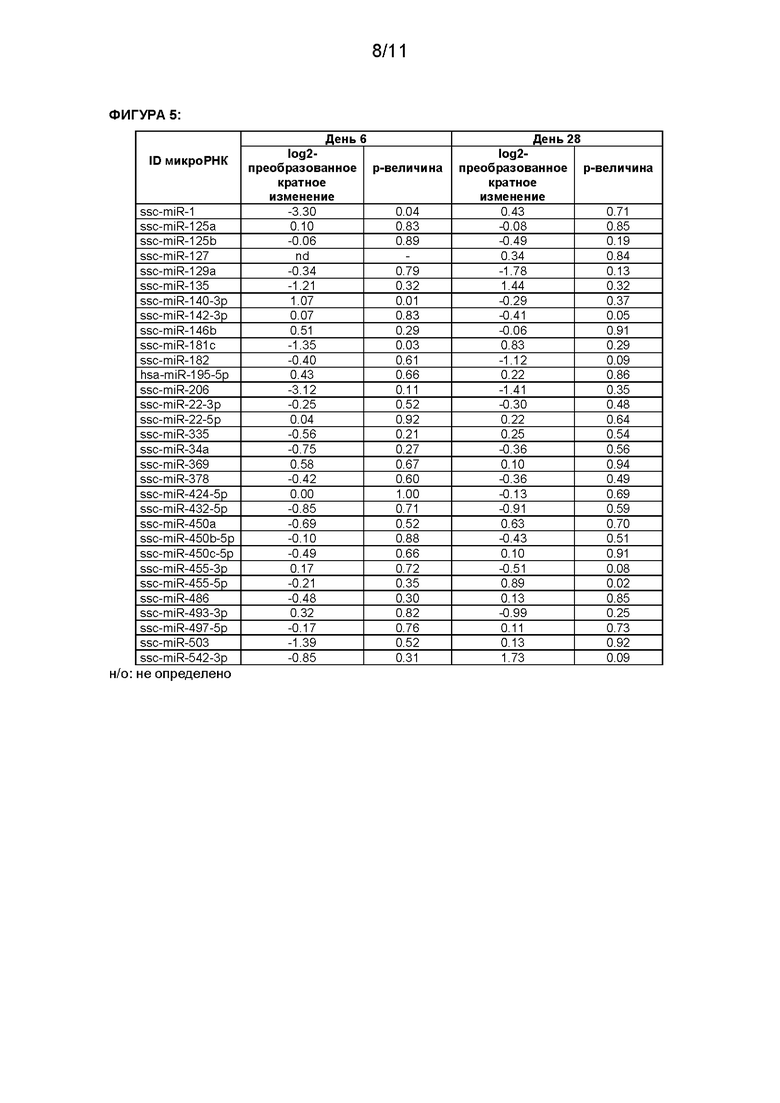
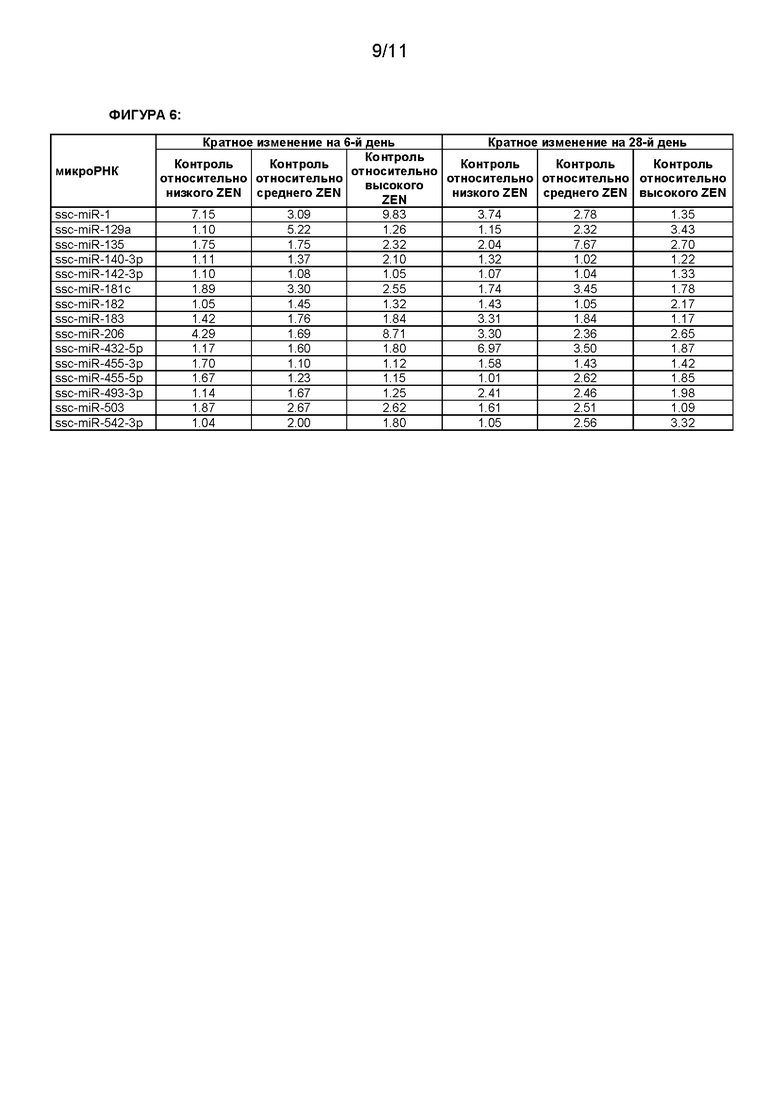
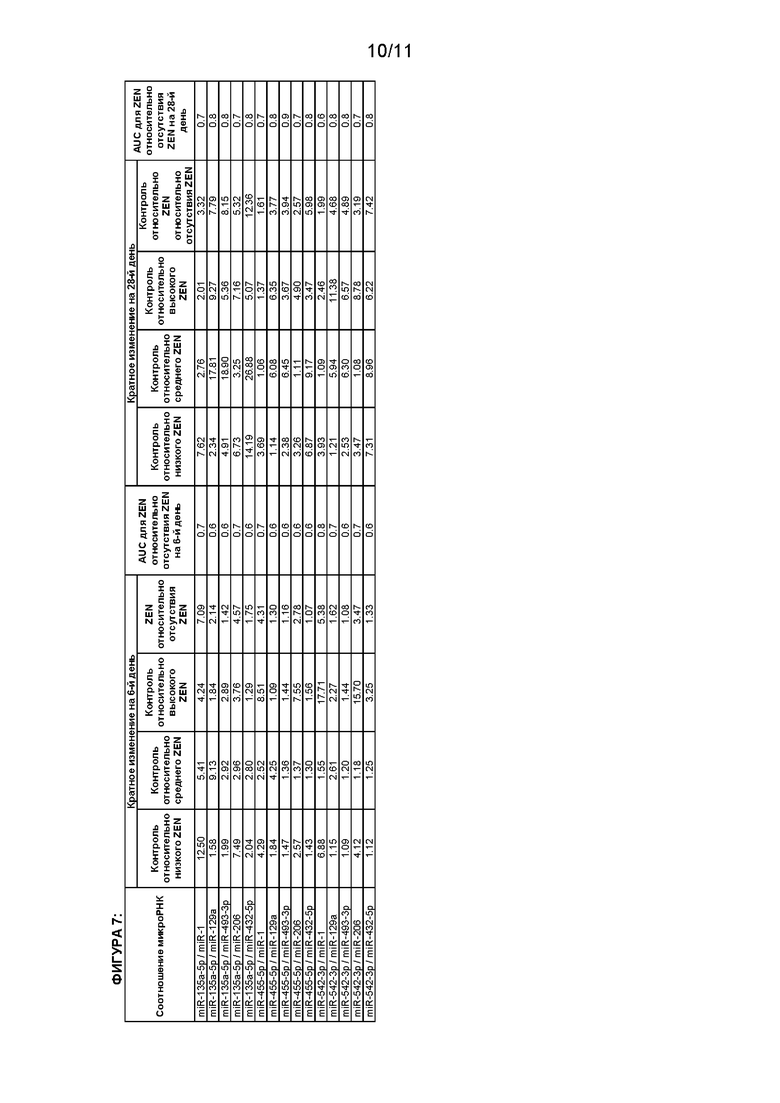

Изобретение относится к биотехнологии. Описан способ обнаружения эффекта зеараленона, включающий: определение в тестируемом образце уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, или по меньшей мере одного соотношения уровней экспрессии между двумя из указанных микроРНК, причем указанный тестируемый образец представляет собой образец крови; и сравнение указанного уровня экспрессии или указанного по меньшей мере одного соотношения уровней экспрессии с референсным значением. Также описана система обработки данных, содержащая процессор, выполненный с возможностью осуществления указанного способа. Предложено Устройство для секвенирования, способное определять уровень по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-135a-5p, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, содержащее систему обработки данных. Предложен машиночитаемый носитель, хранящий на нем компьютерную программу, содержащую инструкции для обеспечения работы указанной системы или устройства для секвенирования. Представлен набор для осуществления указанного способа. Группа изобретений относится к способу обнаружения воздействия зеараленона (ZEN), включающему определение уровня экспрессии по меньшей мере одной микроРНК в тестируемом образце, а также к новому применению по меньшей мере одной микроРНК для обнаружения воздействия зеараленона (ZEN) в тестируемом образце. 6 н. и 8 з.п. ф-лы, 8 ил., 1 табл., 5 пр.
1. Способ обнаружения эффекта зеараленона, включающий:
(c) определение в тестируемом образце уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, или по меньшей мере одного соотношения уровней экспрессии между двумя из указанных микроРНК, причем указанный тестируемый образец представляет собой образец крови; и
(d) сравнение указанного уровня экспрессии или указанного по меньшей мере одного соотношения уровней экспрессии с референсным значением.
2. Способ по п. 1, отличающийся тем, что указанное референсное значение соответствует уровню экспрессии указанной по меньшей мере одной микроРНК в контрольном образце.
3. Способ по п. 1, отличающийся тем, что указанное по меньшей мере одно соотношение уровней экспрессии между двумя микроРНК включает по меньшей мере одно соотношение уровней экспрессии между двумя микроРНК, выбранными из группы, состоящей из ssc-miR-542-3p и ssc-miR-1, ssc-miR-542-3p и ssc-miR-493-3p, ssc-miR-135 и ssc-miR-432-5p, и ssc-miR-455-5p и ssc-miR-493-3p.
4. Способ по любому из пп. 1-3, отличающийся тем, что указанный тестируемый образец получен у субъекта, причем указанный субъект предпочтительно представляет собой млекопитающее, предпочтительно рода Sus, предпочтительно вида Sus scrofa.
5. Способ по любому из пп. 1-4, дополнительно включающий
b) обеспечение тестируемого образца; и/или
e) обеспечение информации относительно эффекта зеараленона.
6. Способ по любому из пп. 1-5, отличающийся тем, что указанный способ предназначен для диагностики, предпочтительно воздействия зеараленона.
7. Способ по любому из пп. 1-5, отличающийся тем, что указанный способ предназначен для обнаружения зеараленона в корме или пище, причем указанный способ предпочтительно предназначен для выбора корма для приведения в контакт с нейтрализующим зеараленон агентом или для применения способа нейтрализации зеараленона.
8. Способ по любому из пп. 4-7, включающий
(а) кормление указанного субъекта кормом, предположительно содержащим зеараленон, до получения тестируемого образца от указанного субъекта;
и/или
(f) выбор корма для приведения в контакт с нейтрализующим зеараленон агентом или применение способа нейтрализации зеараленона, если отклонение уровней экспрессии указанной по меньшей мере одной микроРНК между тестируемым образцом и контрольным образцом указывает на воздействие зеараленона.
9. Способ по любому из пп. 1-8, отличающийся тем, что указанный способ обнаружения эффекта зеараленона осуществляют для оценки способности способа или тестируемого соединения нейтрализовать зеараленон.
10. Применение по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-135a-5p, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, для обнаружения эффекта зеараленона в тестируемом образце, причем указанный тестируемый образец представляет собой образец крови.
11. Система обработки данных, содержащая процессор, выполненный с возможностью осуществления способа, включающего стадии
(a) сравнения уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-135a-5p, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, определенного в тестируемом образце, полученном от субъекта, или по меньшей мере одного соотношения уровней экспрессии между двумя из указанных микроРНК с референсным значением, причем указанный тестируемый образец представляет собой образец крови; и
(b) выявления воздействия зеараленона на указанный субъект, если определено отклонение, где указанное референсное значение соответствует уровню экспрессии или соотношению уровней экспрессии, который(ое) был(о) определен(о) в контрольном образце, полученном у субъекта, который не подвергался воздействию зеараленона; или выявления воздействия зеараленона на указанный субъект, если отклонение не определено, где указанное референсное значение соответствует уровню экспрессии или соотношению уровней экспрессии, который(ое) был(о) определен(о) в контрольном образце, полученном у субъекта, который подвергался воздействию зеараленона.
12. Устройство для секвенирования, способное определять уровень по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-135a-5p, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, содержащее систему обработки данных по п. 11.
13. Машиночитаемый носитель, хранящий на нем компьютерную программу, содержащую инструкции для обеспечения выполнения системой обработки данных по п. 11 или устройством для секвенирования по п. 12 стадий
(b) сравнения уровня экспрессии по меньшей мере одной микроРНК, выбранной из группы, состоящей из ssc-miR-1, ssc-miR-181c, ssc-miR-206, ssc-miR-503, ssc-miR-542-3p, ssc-miR-135, ssc-miR-135a-5p, ssc-miR-129a-3p, ssc-miR-142-3p, ssc-miR-432-5p, ssc-miR-455-5p, ssc-miR-182, ssc-miR-493-3p, ssc-miR-455-3p, ssc-miR-183, и ssc-miR-140-3p, или по меньшей мере одного соотношения уровней экспрессии между двумя из указанных микроРНК определенного в образце, полученном от субъекта, причем указанный образец представляет собой образец крови, с референсным значением; и
(c) выявления воздействия зеараленона на указанный субъект, если определено отклонение, где указанное референсное значение соответствует уровню экспрессии или соотношению уровней экспрессии, который(ое) был(о) определен(о) в контрольном образце, полученном у субъекта, который не подвергался воздействию зеараленона; или выявления воздействия зеараленона на указанный субъект, если отклонение не определено, где указанное референсное значение соответствует уровню экспрессии или соотношению уровней экспрессии, который(ое) был(о) определен(о) в контрольном образце, полученном у субъекта, который подвергался воздействию зеараленона.
14. Набор для осуществления способа по любому из пп. 1-9, содержащий специфичный связывающий агент для по меньшей мере одной микроРНК, выбранной из группы, состоящей из miR-1, miR-181c, miR-206, miR-503, miR-542-3p, miR-135, miR-135a-5p, miR-129a-3p, miR-142-3p, miR-432-5p, miR-455-5p, miR-182, miR-493-3p, miR-455-3p, miR-183, и miR-140-3p, причем указанный специфичный связывающий агент представляет собой молекулу нуклеиновой кислоты, которая гибридизуется с указанной по меньшей мере одной микроРНК, конъюгированную с твердой подложкой.
| Адаптивная система обработки данных | 1987 |
|
SU1455342A1 |
| RU 2015139609 A, 24.03.2017 | |||
| СПОСОБ ОСУЩЕСТВЛЕНИЯ КОММУНИКАЦИЙ И ВИРТУАЛЬНЫХ ПУТЕШЕСТВИЙ | 2012 |
|
RU2498396C1 |
| BRZUZAN ET AL, "MicroRNA expression profiles in liver and colon of sexually immature gilts after exposure to Fusarium mycotoxins", POL J VET SCI.,Vol | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| ПОГЛОЩАЮЩИЙ НЕЙТРОНЫ МАТЕРИАЛ НА ОСНОВЕ ГАФНАТА ДИСПРОЗИЯ | 2012 |
|
RU2522747C2 |
| СПОСОБ ПРОИЗВОДСТВА ГРАНУЛ ЖАРОПРОЧНЫХ СПЛАВОВ | 2011 |
|
RU2468891C1 |
| EP 3246398 A4, | |||
Авторы
Даты
2023-11-23—Публикация
2019-12-06—Подача