Область техники, к которой относится изобретение
Изобретение относится к области медицины и фармакологии и может быть использовано для получения и применения лекарственных средств и биоматериалов для нейропротекции и стимуляции регенерации ткани мозга после повреждений различного генеза: механических, термических, химических (токсических, метаболических), радиационных, сочетанных, вызванных острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, а также инфекционных, в том числе вызванных микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2.
Уровень техники
Повреждения головного мозга (острые нарушения мозгового кровообращения, травмы, токсические повреждения и т.д.) являются одной из основных причин смертности и инвалидизации людей в мире, причем количество таких патологий, согласно оценкам экспертов, будет только расти в связи с увеличением продолжительности жизни и общим старением населения Земли [Суслина З.А. Клиническое руководство по ранней диагностике, лечению и профилактике сосудистых заболеваний головногомозга / З.А. Суслина, Ю.Я. Варакин. - М.: МЕДпресс-информ, 2017. - 352 с; Strong, K. Preventinq stroke: savinq lives around the world / K. Strong, C. Mathers, R. Bonita // Lancet Neurol. - 2007. - Vol. 6. - P. 182-187]. В то же время доступных и эффективных терапевтических подходов, способных приостановить прогрессирование патологического процесса и стимулировать восстановление мозговой ткани, не существует.
В патогенезе острых повреждений головного мозга различного генеза выделяют общие ключевые патогенетические механизмы: ишемическое повреждение нейронов и клеток глии, токсическое действие крови и метаболитов, глутамат-опосредованная эксайтотоксичность, воспаление и вторичное повреждение мозговой ткани. Основным недостатком существующих препаратов и терапевтических подходов является их направленность на купирование симптоматики (проявлений болезни) или воздействие лишь на часть патогенетических механизмов заболевания: чаще всего, это подавление гибели нейронов при ишемическом, токсическом или эксайтотоксическом действии. Существующие препараты (ввиду отсутствия соответствующих компонентов или своего происхождения из клеток и тканей животных) не обладают способностью подавлять активацию клеток микроглии, воспаление в очаге повреждения и вторичное повреждение мозговой ткани. Именно комплексное противодействие патогенетическим механизмам, названным выше, позволит увеличить резистентность ткани мозга к негативному действию повреждающего фактора, приостановит прогрессирование заболевания и ускорит процесс регенерации мозговой ткани, причем данный подход можно считать эффективным для широкого спектра патологий ввиду общности их патогенетических механизмов. К тому же, абсолютное большинство существующих патентов и публикаций не описывают ключевых параметров (состав композиции или средства, соотношение его компонентов, способ и кратность введения, дозировка и временное терапевтическое окно), необходимых для эффективной терапии повреждения мозга.
Из уровня техники известны композиции для стимуляции восстановления нервной ткани после повреждения (в т.ч. инфаркт головного мозга, церебральный инсульт, энцефалоррагию, субарахноидальное кровоизлияние, опухоль головного мозга, травматические, ишемические, дегенеративные заболевания черепных нервов) путем введения (в т.ч. локально и внутривенно) мезенхимальных клеток (в т.ч. аутологичных), полученных из костного мозга, пуповинной крови или периферической крови [US20070178591]. Модификацией данной композиции является применение мезенхимальных клеток, в которую введен ген BDNF, ген PLGF, ген GDNF или ген IL-2; или иммортализованная мезенхимальная клетка, введенная с геном hTERT. Однако, в источнике не раскрыта информация о диапазоне терапевтических концентраций и соотношении факторов роста, не содержится данных о возможности их применения для нейропротекции мозговой ткани и стимуляции восстановления мозга при термических, химических (токсических, метаболических), радиационных и сочетанных повреждениях, а также повреждениях, вызванных инфекционными агентами (в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2) и острым нарушением мозгового кровообращения по геморрагическому типу, а также не представлены режимы введения композиции, а именно не указано временное терапевтическое окно, дозу и кратность введения, к тому же, введение клеток в область повреждения мозга возможно только в ходе сложного хирургического вмешательства в рамках стационара; внутривенное введение клеток ассоциировано с высоким риском тромбозов и эмболий; а применение аутологичных клеток делает невозможным применение данной композиции в острейшем периоде, что сильно снижает эффективность лечения состояний после острых повреждений головного мозга.
Из уровня техники известна композиция для стимуляции восстановления нервной ткани после геморрагического инсульта, включающая компоненты культуральной среды (в т.ч. экзосомы или другим микровезикулы (например, апоптотические тельца)), в которой росли фибробласты, выделенные из костного мозга, жировой ткани, плаценты, пуповины с путем их введения в область повреждения [WO2021097423]. Композиция включает: фактор ингибирования лейкемии (LIF), нейротрофический фактор головного мозга (BDNF), рецептор эпидермального фактора роста (EGF), основной фактор роста фибробластов (bFGF), FGF-6, глиальный нейротрофический фактор (GDNF), гранулоцитарный колониестимулирующий фактор (GCSF), фактор роста гепатоцитов (HGF), IFN-g, белок, связывающий инсулиноподобный фактор роста (IGFBP-2), IGFBP-6, IL-1ra, IL-6, IL-8, хемотаксический белок моноцитов (MCP-1), колониестимулирующий фактор мононуклеарных фагоцитов (M-CSF), нейротрофические факторы (NT3), тканевой ингибитор металлопротеиназ (TIMP-1), TIMP-2, фактор некроза опухоли (TNF-b), фактор роста эндотелия сосудов (VEGF), VEGF-D, рецептор активатора плазминогена урокиназы (uPAR), костный морфогенетический белок 4 (BMP4), IL1-a, IL-3, лептин, фактор стволовых клеток (SCF), фактор-1, полученный из стромальных клеток (SDF-1), фактор роста тромбоцитов-BB (PDGF-BB), трансформирующие факторы роста бета (TGF-b). Также композиция может включать культуральную среду с одной или несколькими клетками гематопоэтическими (могут быть получены из одного или нескольких источников, включая жировую ткань, костный мозг, периферическую кровь, мобилизованную периферическую кровь и пуповинную кровь) или мезенхимальными стволовыми клетками (могут быть получены из жировой ткани, костного мозга, периферической крови и др.), в т.ч. генетически модифицированными (не экспрессируют HLA, CD34 или CD14). Однако, в источнике не раскрыта информация о диапазоне терапевтических концентраций факторов роста, а также не указано временное терапевтическое окно и кратность введения, к тому же используемые клетки являются фибробластами, что ограничивает регенераторный потенциал их кондиционной среды, поскольку фибробласты в большом количестве синтезируют профибротические факторы роста (TGF-b) и компоненты внеклеточного матрикса, в том числе и коллагены, которые тормозят регенерацию нервной ткани и стимулируют глиоз.
Из уровня техники известно средство для стимуляции регенерации тканей на основе компонентов бессывороточной культуральной среды (продуктов секреции), в которой росли МСК человека, выделенные из жировой ткани и способ его получения [RU2620167]. Средство содержит продукты секреции МСК человека, включающие факторы роста: VEGF в концентрации не менее 200 пкг/мл, HGF в концентрации не менее 150 пкг/мл, FGF basic в концентрации не менее 0,29 пкг/мл, ангиопоэтин-1 в концентрации не менее 145 пкг/мл, PDGF в концентрации не менее 500 пкг/мл. Однако, данное средство не содержит факторы роста с нейропротективной активностью (например, мозговой нейротрофический фактор BDNF) или молекулы, регулирующими процессы нейритогенеза (например, урокиназный активатор плазминогена), а также молекулы с противовоспалительной активностью (интерлейкины, IDO, TNF), что не предполагает возможность воздействия компонентов данного средства на ключевые патогенетические механизмы при повреждении головного мозга и не предполагает возможность его применения для терапии повреждений мозга. Для получения средства используют культивирование МСК человека, выделенных из жировой ткани, в среде AdvanceSTEM Cell Culture Media, культивирование в которой дает меньшую продуктивность клеточной культуры, чем при культивировании в среде DMEM с низким содержанием глюкозы без фенолового красного. К тому же способ применения данного средства не описывает его применение для осуществления нейропротекции, а также критические параметры терапии повреждений мозга: временное терапевтическое окно, дозу и кратность введения.
Из уровня техники известна композиция для лечения, ингибирования, уменьшения, облегчения и/или предотвращения воспалительного состояния, аутоиммунного заболевания, аутовоспалительного заболевания, метаболического нарушения или воспаления, представляющая собой культуральную среду, в которой росли мультипотенциальные стромальные клетки, выделенные из жировой ткани [WO2021011935]. Однако, применение данной композиции не предполагается с целью нейропротекции и стимуляции регенерации ткани мозга после механических, термических, химических (токсических, метаболических), радиационных и сочетанных повреждений, а также повреждений, вызванных острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, и инфекционными агентами, в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2, не представлена информация о диапазоне терапевтических концентраций факторов роста, не указано временное терапевтическое окно, доза и кратность введения.
Из уровня техники известно терапевтическое средство для нейропротекции после поражений центральной и периферической нервной системы различного происхождения с помощью введения в область повреждения компонентов кондиционированной среды мезенхимальных стромальных клеток (МСК), выделенные из пупочного канатика человека [RU2742034]. Кондиционированная среда при этом содержит G-CSF (гранулоцитарный колониестимулирующий фактор), HGF (фактор роста гепатоцитов), IFN-a2 (интерферон альфа-2), IL-6 (интерлейкин-6), IL-8 (интерлейкин-8), SCF (фактор стволовых клеток), SCGF (фактор роста стволовых клеток), VEGF (фактор роста сосудистого эндотелия), FGF (фактор роста фибробластов). Однако, предложенное средство не учитывает тот факт, что основную нейропротективную функцию в составе кондиционированной среды выполняют нейротрофические факторы, не учитывает их вклад и не оценивает их терапевтические концентрации. Описание данной композиции не содержит информации о временном терапевтическом окне, дозе и кратности введения с целью нейропротекции и стимуляции регенерации ткани мозга после повреждений, к тому же используемые клетки получены из ткани пуповины, что накладывает на их применение ряд этических ограничений.
Наиболее близкой к заявляемой является композиция клеток, полученных из амниотической жидкости, или факторов, продуцируемых указанными стволовыми клетками, а также способ индукции и ускорения неврологического восстановления после ишемического и геморрагического инсультов, травмы головного мозга и др. с помощью введения указанной композиции [US2018071342]. Указанные факторы могут включать белки, пептиды, кондиционированные среды, экзосомы или микровезикулы. Компоненты среды при этом могут включать активин А, адреномедуллин, aFGF, ALK1, ALK5, ANF, ангиогенин, ангиопоэтин-1, ангиопоэтин-2, ангиопоэтин-3, ангиопоэтин-4, bFGF, B61, кадгерины, CAM-RF, аналоги цГМФ, ChDI, CLAF, клаудины, коллаген, коллагеновые рецепторы α1β1 и α2β1, коннексины, Cox-2, ECDGF (эндотелиальноклеточный фактор роста), ECG, ECI, EDM, EGF, EMAP, эндоглин, эндотелины, эндостатин, ингибитор роста эндотелиальных клеток, фактор поддержания жизнеспособности эндотелиальных клеток, сфинголипид G-белок-связанный рецептор-1 (EDG1), эфрин, Epo, HGF, TGF-бета, PD-ECGF, PDGF, IGF, IL8, гормон роста, фрагмент фибрина E, FGF-5, фибронектин и рецептор фибронектина α5.beta.1, фактор X, HB-EGF, HBNF, HGF, HUAF, сердечный ингибитор пролиферации клеток сосудов, IL1, IGF-2 IFN-gamma, интегриновые рецепторы, K-FGF, LIF, фактор роста, полученный из лейомиомы, MCP-1, фактор роста, полученный из макрофагов, фактор роста, полученный из моноцитов, MD-ECI, ME CIF, MMP 2, MMP3, MMP9, урокиазный активатор плазминогена, нейропилин (NRP1, NRP2), нейротелин, доноры оксида азота, синтазы оксида азота (NOS), Notch, окклюдины, зональные окклюдины, онкостатин М, PDGF, PDGF-B, PDGF рецепторы, PDGFR-β, PD-ECGF, PAI-2, PD-ECGF, PF4, P1GF, PKR1, PKR2, PPAR-гамма, лиганды PPAR-гамма, фосфодиэстераза, пролактин, простациклин, протеин S, гладкомышечные клетки- фактор роста, полученный из клеток гладкой мускулатуры, сфингозин-1-фосфат-1 (SIP1), Syk, SLP76, тахикинины, TGF-бета, Tie 1, Tie2, TGF-(и TGF-(рецепторы, TIMP, TNF-альфатрансферрин, тромбоспондин, урокиназа, VEGF-A, VEGF-B, VEGF-C, VEGF-D, VEGF-E, VEGF, VEGF164, VEGI, EG-VEGF. Однако, в описании композиции перечислен широкий спектр ростовых факторов и низкомолекулярных соединений без указания диапазона их концентраций или их соотношений, а также одновременно указаны факторы нейтрализующие активность друг друга (MMP 2, MMP3, MMP9 и TIMP; TGF-(и TGF-(рецепторы; PDGF-B и PDGF-рецепторы; урокиназа, VEGF-A/B/C/D/E и сердечный ингибитор пролиферации клеток сосудов и т.д.), что не позволяет ожидать от предлагаемой композиции (особенно в отсутствии информации о соотношении концентраций факторов) реальной терапевтической активности (способности оказывать нейпротективный и прорегенераторный эффект) в отношении поврежденной мозговой ткани. Физиологический эффекты факторов роста и цитокинов и терапевтическая активность препарата на их основе во многом определяются их концентрациями и соотношением по сравнению с их антагонистами, поскольку для реализации своего эффекта они должны проникнуть в область повреждения, преодолеть ингибирующее влияние антагониста и насытить соответствующий рецептор, оказывать необходимое по длительности и силе воздействие. Также в источнике не раскрыты детали способа получения данной композиции, в частности не указана среда для культивирования МСК, хотя известно, что состав культуральной среды роста для МСК влияет на качественный и количественный состав получаемого секретома. Помимо этого, в источнике не раскрыты путь введения, временное терапевтическое окно, доза и кратность введения для профилактики и лечения острых повреждений мозговой ткани. Данная информация является неотъемлемой при разработке подходов для терапии повреждений мозга и профилактики осложнений, особенно, острых нарушений мозгового кровообращения, поскольку своевременное оказание медицинской помощи, адекватный путь доставки и доза терапевтического препарата являются основой снижения смертности и тяжести неврологических нарушений при таких состояниях. Помимо этого, для наработки композиции использованы клетки, выделенные из амниотической жидкости, получение которых требует применения инвазивных и болезненных методов и является менее перспективным по своей доступности и безопасности для донора, а также сопряжено с рядом этических ограничений.
Технической проблемой, на решение которой направлено заявляемое изобретение является разработка композиции для нейропротекции и стимуляции нейрорегенерации головного мозга после повреждения, средства на его основе, а также способов его получения и применения, с целью снижения смертности и инвалидизации среди таких пациентов, обладающее комплексным действием. Повреждения мозга включает в себя механические, термические, химические (токсических, метаболических), радиационные и сочетанные повреждения, а также повреждения, вызванные острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, и инфекционными агентами, в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2.
Раскрытие изобретения
Техническим результатом заявляемого изобретения является выживаемость экспериментальных животных до 100%, снижение тяжести неврологических нарушений - до 100% животных визуально здоровы через 14 дней после моделирования инсульта, и уменьшение объема повреждения головного мозга в среднем в 2 раза по данным МРТ и гистологического исследования по сравнению с группой контроля (без композиции), а также снижение активации клеток микроглии до базального уровня в модели острого нарушения мозгового кровообращения по геморрагическому типу в эксперименте in vivo. Помимо этого, заявляемая композиция стимулирует поляризацию клеток моноцитарно-макрофагального ряда в противовоспалительном направлении (М2-фенотип), в том числе и в провоспалительных условиях, в 2-6 раз (в зависимости от измеряемого маркера) более эффективно по сравнению с группой контроля (без композиции); а также стимулирует выживаемость клеток нейробластомы SH-SY5Y в условиях глутамат-опосредованной токсичности в 4-40 раз (в зависимости от состава композиции и времени исследования) более эффективно по сравнению с группой контроля (без композиции) - в экспериментах in vitro.
Полноценное сравнение терапевтической активности заявляемого изобретения с прототипом невозможно ввиду отсутствия в открытом доступе экспериментально подтвержденной информации о наличии такой активности в текстовом или графическом виде.
Эффективность заявляемой композиции достигается за счет сбалансированного действия компонентов кондиционированной среды (КС) мезенхимных стромальных клеток (МСК) человека или ее отдельных фракций на ключевых участников повреждения нервной ткани при повреждении мозга: на нейроны, клетки микро- и макроглии, а также на клетки моноцитарно/макрофагального звена гематогенного происхождения.
Технический результат достигается композицией для нейропротекции и стимуляции нейрорегенерации головного мозга на основе компонентов секретома МСК человека, характеризующаяся наличием факторов роста и цитокинов в культуральной среде, включая BDNF в количестве не менее 3 нг/мл, GDNF - не менее 0.03 нг/мл, VEGF - не менее 0.2 нг/мл, HGF - не менее 0.15 нг/мл, uPA - не менее 0.34 нг/мл и TGFb (суммарно по изоформам TGFb1, TGFb2 и TGFb3) - не менее 0.055 нг/мл и содержащая не менее 5 мкг/мл по тотальному белку. Композиция дополнительно может содержать противовоспалительные цитокины, включая антагонист рецептора IL-1 IL-1Ra в количестве не менее 0.4 нг/мл, IL-4 - не менее 0.08 нг/мл, IL-6 - не менее 1 нг/мл, IL-10 - не менее 0.01 нг/мл, IL-11 - не менее 0.4 нг/мл, IL-13 - не менее 0.7 пг/мл, и молекулы, обладающие противовоспалительным эффектом, включая IDO - не менее 0.08 нг/мл, растворимые формы рецепторов IL-1 - не менее 0.01 нг/мл и TNF - не менее 0.01 нг/мл. Также композиция дополнительно может содержать микроРНК hsa-miR-23a-3p (SEQ ID NO: 1), hsa-miR-101 (SEQ ID NO: 2 и/или SEQ ID NO: 3), hsa-miR-146a (SEQ ID NO: 4 и/или SEQ ID NO: 5), hsa-miR-491-5p (SEQ ID NO: 6), hsa-miR-19b (SEQ ID NO: 7 и/или SEQ ID NO: 8), hsa-miR-21 (SEQ ID NO: 9 и/или SEQ ID NO: 10), hsa-miR-25 (SEQ ID NO: 11 и/или SEQ ID NO: 12), hsa-miR-125b (SEQ ID NO: 13 и/или SEQ ID NO: 14), hsa-miR-126a-3p (SEQ ID NO: 15). При этом композиция представляет собой концентрированный раствор цитокинов и факторов роста в культуральной среде, замороженный или лиофильно высушенный раствор, характеризующаяся наличием комплекса свойств, включающего способность препятствовать глутамат-опосредованной гибели нейральных клеток, способность стимулировать поляризацию клеток моноцитарно-макрофагального звена в противовоспалительном направлении (M2-фенотип), предотвращение активации клеток микроглии.
Технический результат также достигается применением заявляемой композиции в качестве средства предотвращающего глутамат-опосредованную гибель нейральных клеток, стимулирующего поляризацию клеток моноцитарно-макрофагального звена в противовоспалительном направлении (M2-фенотип), предотвращающего активацию клеток микроглии.
Также технический результат достигается способом получения заявляемой композиции, включающим культивирование и кондиционирование первично выделенных аллогенных мезенхимных стромальных клеток (МСК) человека 2 - 5 пассажа в среде роста в течение 72-144 ч, отбор и очистку среды культивирования от остатков клеток, концентрирование среды культивирования до уменьшения исходного объема по меньшей мере в 10 раз, очищение среды культивирования с получением стерильного концентрата. При этом в качестве среды роста используют среду Игла, модифицированную Дульбекко (DMEM) с низким содержанием глюкозы (не более 1 г/л) без фенолового красного с добавлением пенициллина/стрептомицина, а также растворов заменимых аминокислот и витаминов. Полученный стерильный концентрат замораживают при температуре от минус 80°С до минус 18°С или лиофильно высушивают. Лиофильную сушку проводят в 6-10 стадий при давлении 0.013-0.027 кПа, температуре от минус 45°С до 25°С, время лиофилизации составляет не более 24 часов при максимальной загрузке лиофильной сушки. В качестве первично выделенных аллогенных МСК человека используют жировую ткань, при этом культивирование МСК и кондиционирование среды проводят при содержании кислорода 1-21 об.%.
Технический результат достигается также средством для нейропротекции и стимуляции нейрорегенерации, включающим заявляемую композицию в терапевтически эффективном количестве и вспомогательные компоненты, в качестве которых используют любые терапевтические приемлемые добавки, наполнители, изотонические агенты, стабилизаторы и/или консерванты. Дополнительно средство может содержать альбумин человека в количестве не менее 5 мкг/мл. Заявляемое средство представляет собой концентрированный раствор цитокинов и факторов роста в культуральной среде, замороженный или лиофильно высушенный раствор.
Также технический результат достигается способом стимуляции нейропротекции и регенерации головного мозга после повреждения, включающий введение заявляемой композиции или средства в организм человека в терапевтически эффективном количестве. При этом композицию или средство вводят локально в область повреждения головного мозга в дозе 5-30 мкг/мл (по белку) или интраназально в дозе 25-250 мкг по белку на 1 кг массы тела, или внутривенно струйно или капельно в дозе 30-300 мкг по белку на 1 кг массы тела, или в спинномозговой канал в дозе 30-300 мкг по белку на 1 кг массы тела. Композицию или средство вводят однократно или многократно в течение одного или нескольких дней с равными интервалами в течение первых трех недель после повреждения головного мозга, при этом в острейшей фазе повреждения головного мозга композицию или средство вводят не позднее 6 часов от момента повреждения, в острой фазе повреждения головного мозга композицию или средство вводят в период от 6 до 120 часов от момента повреждения, в подострой фазе повреждения головного мозга композицию или средство вводят в период от 5 до 21 суток от момента повреждения. Повреждение головного мозга может быть вызвано острым нарушением мозгового кровообращения (ОНМК) по геморрагическому типу вне зависимости от его этиологии или по ишемическому типу вне зависимости от этиологии данного нарушения, или повреждение вызвано воздействием механического фактора вне зависимости от его природы, или воздействием термического фактора вне зависимости от его природы, или химического фактора вне зависимости от его природы (токсическое воздействие, метаболические нарушения), или проникающего излучения (радиации) вне зависимости от его природы, или сочетанием факторов в любых сочетаниях вне зависимости от их природы, а также повреждение головного мозга вызвано воздействием инфекционного агента. При этом, ОНМК по геморрагическому типу являются следствием врожденных или приобретенных дефектов сосудистого русла головного мозга. В качестве инфекционного агента может выступать бактериальная или вирусная инфекция, а именно бактериальная инфекция может быть вызвана микроорганизмами родов Neisseria и Borrelia, вирусная инфекция - вирусом SARS-Cov2.
Краткое описание чертежей
Изобретение поясняется следующими чертежами.
На фиг. 1 представлены результаты исследований in vivo нейропротекторной активности неконцентрированного секретома МСК человека (чМСК1x) при его введении непосредственно в область повреждения через 5 минут после моделирования геморрагического инсульта: А - выживаемость экспериментальных животных; Б - неврологический статус экспериментальных животных (ЛО - ложнооперированный); когнитивный статус экспериментальных животных: В - кратковременная память (через 24 часа после внутримозгового кровоизлияния); Г - долговременная память (10 дней после внутримозгового кровоизлияния). Пунктирная линия соответствует показателям памяти животных ЛО. Данные представлены как среднее значение (25%; 75%). n=10; достоверных различий между группами нет.
На фиг. 2 представлены результаты исследований in vivo нейропротекторной активности 10-кратно концентрированного секретома МСК человека (чМСК10x) при его введении непосредственно в область повреждения через 5 минут после моделирования геморрагического инсульта: А - выживаемость экспериментальных животных; Б - неврологический статус подопытных животных через 3 и 10 суток после внутримозгового кровоизлияния (ЛО - ложнооперированный). Данные представлены как среднее значение (25%; 75%). [* - p<0.01; n ≥ 10; двусторонний точный тест Фишера].
На фиг. 3 представлены результаты МРТ головного мозга на 11-е сутки после внутримозгового кровоизлияния: неконцентрированный секретом МСК человека (чМСК1x), 10-кратно концентрированный секретом МСК человека (чМСК10x), рекомбинантный BDNF (3.5 нг/мкл) и неконцентрированный секретом МСК человека, содержащий рекомбинантный BDNF в концентрации 3.5 нг/мкл (чМСК-B) вводили непосредственно в область повреждения через 5 минут после моделирования геморрагического инсульта. На диаграмме: синяя пунктирная линия соответствует объему очага поражения головного мозга у ложнооперированных животных. Данные представлены как среднее значение (25%; 75%). [* - р<0.05; n ≥ 8; ANOVA on ranks].
На фиг. 4 представлены результаты гистохимического исследования головного мозга на 14 сутки после внутримозгового кровоизлияния: неконцентрированный секретом МСК человека (чМСК1x), 10-кратно концентрированный секретом МСК человека (чМСК10x), рекомбинантный BDNF (3.5 нг/мкл) и неконцентрированный секретом МСК человека, содержащий рекомбинантный BDNF в концентрации 3.5 нг/мкл (чМСК-B) вводили непосредственно в область повреждения через 5 минут после моделирования геморрагического инсульта. На фотографиях: красной пунктирной линией отмечен очаг поражения. На схеме: синяя пунктирная линия соответствует площади поражения головного мозга у ложнооперированных животных. Данные представлены как среднее значение (25%; 75%). n=5; достоверных различий между группами нет.
На фиг. 5 представлены гистологические признаки поражения мозговой ткани (гематоксилин-эозин): А и Б - очаг некроза, сдерживаемый инфильтрацией нейтрофилов (ИН) и глиальным рубцом (ГР); В - признаки застоя крови и миграции лейкоцитов через стенку капилляров.
На фиг. 6 представлены результаты гистологического исследования срезов головного мозга: неконцентрированный секретом МСК человека (чМСК1x), 10-кратно концентрированный секретом МСК человека (чМСК10x), 10-кратно концентрированный секретом МСК крысы (кМСК10x), рекомбинантный BDNF (3.5 нг/мкл) и неконцентрированный секретом МСК человека, содержащий рекомбинантный BDNF в концентрации 3.5 нг/мкл (чМСК-B) вводили непосредственно в область повреждения через 5 минут после моделирования геморрагического инсульта. Окраска по Перлсу показывает отложения гемосидерина (синие зерна). Окрашивание по Нисслю отражает функциональное состояние нейронов в полутени: красные стрелки - живые, но гипоксические нейроны, черные стрелки - погибшие нейроны (тени нейронов).
На фиг. 7 представлены результаты иммуногистохимического окрашивания срезов головного мозга через 14 суток после внутримозгового кровоизлияния: а - иммуногистохимическое окрашивание на CD68; (б) - иммуногистохимическое окрашивание на CD163. Все препараты вводили непосредственно в область повреждения через 5 минут после моделирования геморрагического инсульта. На фото: зеленое окрашивание соответствует окрашиванию CD68 или CD163; синее окрашивание соответствует ядрам клеток. На диаграмме: синяя пунктирная линия соответствует площади очага поражения головного мозга у животных СО. Данные представлены в виде медианы (25%; 75%). [* - p<0.05, n ≥ 9, ANOVA on ranks; # - p<0.005, n ≥ 9, ANOVA on ranks].
На фиг. 8 представлены результаты исследования нейропротективной активности 10-кратно концентрированного крысиного (аллогенного) секретома МСК крысы (кМСК10x) in vivo, введенного в область повреждения через 5 минут после моделирования геморрагического инсульта: (а) - динамика выживаемости экспериментальных животных; (б) - неврологический статус экспериментальных животных на 3 и 10 сутки после внутримозгового кровоизлияния (ЛО - ложнооперированный) [* - р<0.01, n=10, двусторонний точный критерий Фишера; ** - p<0.0005, n=18, двусторонний точный критерий Фишера]; (в) - образцы МР-изображений и гистологических срезов головного мозга, полученных от экспериментальных животных; (г) - результаты МРТ головного мозга на 11-е сутки после внутримозгового кровоизлияния [# - р<0.005; n ≥ 8; ANOVA on ranks]; (д) - результаты гистохимического исследования головного мозга на 14-е сутки после внутримозгового кровоизлияния [## - р<0.05; n=5; ANOVA on ranks]. Данные представлены в виде медианы (25%; 75%).
На фиг. 9 представлены результаты исследования in vitro нейропротективной активности секретомов МСК (чМСК1x, чМСК10x, чМСК-В и кМСК10x): (а) - динамика выживаемости клеток нейробластомы SH-SY5Y в условиях глутамат-индуцированной нейротоксичности [* - р<0.001 по сравнению с контролем (K+); n=12; ANOVA on ranks]; (б) - рост нейритов в культуре клеток нейробластомы SH-SY5Y [** - р<0.004 по сравнению с контролем; n=5; ANOVA on ranks]. Данные представлены в виде медианы (25%; 75%).
На фиг. 10 представлены образцы изображений (необработанные данные), полученных при изучении нейропротекторной активности секретомов МСК на модели глутамат-индуцированной нейротоксичности in vitro. Зеленая окраска соответствует погибшим клеткам (апоптоз).
На фиг. 11 представлены образцы изображений (необработанные данные), полученных при изучении способности секретомов МСК стимулировать нейритогенез.
На фиг. 12 представлены результаты исследования способности секретома МСК человека влиять на поляризацию клеток моноцитарно/макрофагального звена периферической крови человека. Секретом МСК человека снижает экспрессию маркеров провоспалительного фенотипа (CD80, CD86) и увеличивает экспрессию маркеров противовоспалительного фенотипа (CD206, CD209) в клетках моноцитарно-макрофагального звена человека (n≥3).
На фиг. 13 представлены результаты оценки неврологических дефицитов у крыс с различными способами введения (n=5). Наиболее выраженный нейропротективный эффект секретома наблюдается при локальном введении секретома МСК в область повреждения, а также при внутривенном и интраназальном введении секретома МСК.
На фиг. 14 представлены результаты сравнения терапевтической активности секретома МСК крыс при внутривенном введении и введении в область инсульта (* - p<0.05, n ≥ 5) - МРТ-исследование.
На фиг. 15 представлены результаты оценки неврологических дефицитов у крыс в зависимости от времени введения секретома (n=5). Наиболее выраженный нейропротективный эффект секретома МСК наблюдается при его введении через 1 и 3 часа после моделирования геморрагического инсульта.
На фиг. 16 представлены результаты оценки объема повреждения мозга у крыс с моделью геморрагического инсульта (по данным МРТ-исследования) в зависимости от времени введения секретома (n=3). Наименьший объем повреждения головного мозга наблюдается при внутривенном введении секретома МСК через 1-3 часа после моделирования геморрагического инсульта.
На фиг. 17 представлены результаты оценки неврологических дефицитов (А) и объема повреждения мозга (по данным МРТ-исследования) (Б) у крыс с моделью геморрагического инсульта в зависимости от дозы секретома аллогенных МСК, введенного внутривенно через 1 час после моделирования ОНМК по геморрагическому типу (n=4). Наилучший неврологический статус (100% животных визуально здоровы) наблюдается в группах 5x-25x. Наилучший терапевтический эффект наблюдается при внутривенном введении секретома МСК крыс в дозе 5x-25x - 15-75 мкг/кг (по белку) через 1 час после моделирования геморрагического инсульта.
Осуществление изобретения
Ниже представлено более подробное описание заявляемого изобретения. Настоящее изобретение может подвергаться различным изменениям и модификациям, понятным специалисту на основе прочтения данного описания. Такие изменения не ограничивают объем притязаний.
Для получения средства в заявленном изобретении используются МСК жировой ткани, получение которых не требует применения инвазивных и болезненных методов. Следует также учитывать, что именно жировая ткань считается одним из основных источников внеклеточных везикул, циркулирующих в организме человека. Для заявленной композиции показаны выраженные нейропротективные и антивоспалительные свойства, как на in vitro моделях глутамат-опосредованной эксайтотоксичности, поляризации моноцитов/макрофагов, так и на in vivo модели геморрагического инсульта у крыс. Механизмы повреждения мозговой ткани, такие как ишемическое повреждение нейронов и клеток глии, токсическое действие крови и метаболитов, глутамат-опосредованная эксайтотоксичность, воспаление и вторичное повреждение мозговой ткани - являются универсальными механизмами повреждениями мозговой ткани и характерны в тех или иных комбинациях для механических, термических, химических (токсических, метаболических), радиационных и сочетанных повреждений головного мозга, а также повреждений, вызванных острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, и инфекционными агентами, в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2. Композиции и средства на их основе, способные смягчать и тормозить действие основных патогенетических компонентов повреждений мозга, таких как ишемическое повреждение нейронов и клеток глии, токсическое действие крови и метаболитов, глутамат-опосредованная эксайтотоксичность, воспаление и вторичное повреждение мозговой ткани, в острейшей, острой и подострой стадии повреждения могут быть с успехом применены для лечения широкого спектра патологий, ассоциированных с острым повреждением головного мозга вне зависимости от его генеза.
Техническая проблема получения такой композиции и получаемого из него средства решается путем культивирования и кондиционирования первичных МСК жировой ткани человека 2 - 5 пассажей в бессывороточной среде роста DMEM с низким содержанием глюкозы без фенолового красного, содержащей 1% антибиотика/антимикотика, 1% глутамина, в том числе, с добавками, поддерживающих жизнеспособность клеток не менее 90% и пригодных для терапевтического применения. В отличие от прототипа в настоящем изобретении для получения секретома использованы мезенхимные стромальные клетки, полученные из жировой ткани, что является менее инвазивным и болезненным, а также более безопасным и этически обоснованным подходом, чем получение клеток амниотической жидкости. Для получения кондиционированной среды в заявляемом изобретении использованы мультипотентные мезенхимные стволовые/стромальные клетки (МСК) человека, отвечающие за репарацию и регенерацию тканей и органов как в норме, так и при повреждениях. МСК могут быть легко выделены в результате ферментативной обработки образцов жировой ткани, полученной в результате косметической липосакции или в ходе хирургического удаления жирового отложения. Культивирование изолированных МСК ЖТ приводит к получению относительно гомогенной популяции мультипотентных стромальных фибробластоподобных клеток. Следует также учитывать, что именно жировая ткань считается одним из основных источников внеклеточных везикул, циркулирующих в организме человека.
В заявленном изобретении могут быть использованы МСК, полученные самостоятельно по любому известному из уровня техники способу (например, из хирургических биопсий, липоаспирата и др.), так и в виде коммерческих препаратов МСК, имеющих сертификат качества и предназначенных, в том числе, для клинического применения, например, такие как продукт ATCC (ATCC® PCS-500-011), представляющий собой МСК человека, выделенные из липоаспирата, культивированные до 2 пассажа и подвергнутые криоконсервации.
В большинстве протоколов выделения и культивирования МСК жировой ткани используется среда с добавлением эмбриональной телячьей сыворотки (ЭТС) или фетальной бычьей сыворотки (ФБС). Эти сыворотки содержат необходимый коктейль факторов роста, гормонов и витаминов, стимулирующих клеточную адгезию и пролиферацию в условиях культивирования in vitro. В состав среды культивирования по умолчанию также входит феноловый красный, который является pH-индикатором. Однако попытки трансляции in vitro данных в in vivo модели и клинику показали, что феноловый красный снижает продуктивность клеточных культур и оказывает местное раздражающее действие при введении концентрированных бесклеточных продуктов в месте трансплантации.
Отличительной особенностью заявляемого изобретения является использование для культивирования МСК среды, не содержащей фенолового красного: DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA) с добавлением 10% фетальной бычьей сыворотки FBS (HyClone, USA) с добавлением раствора антибиотиков Penicillin-Streptomycin (HyClone, USA), раствора L-Glutamine 200 mM (Gibco, USA), об.%:
DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA) - 87.4- 88.6;
Фетальная бычья сыворотка FBS (HyClone, USA) - 9.5-10.5;
Раствор антибиотиков Penicillin-Streptomycin (HyClone, USA) - 0.95 - 1.05;
Раствор L-Glutamine 200 mM (Gibco, USA) - 0.95 - 1.05;
МСК выделяют из подкожной жировой ткани человека и культивируют в приготовленной по указанной выше схеме среде роста до 2-5 пассажа. Затем клетки тщательно отмывают от компонентов среды роста раствором Хэнкса (фирмы ПанЭко или аналогичным) и подвергают кондиционированию. В ряде протоколов кондиционирование клеток-продуцентов происходит в этих же условиях, что и культивирование - это приводит к тому, что основным компонентом полученного «секретома» является ксеногенная сыворотка, способная активировать выраженную иммунную реакцию со стороны организма реципиента или даже вызвать реакцию «трансплантат против хозяина». В других протоколах в качестве среды для кондиционирования используются бессывороточные среды, но нет никакого указания на содержание или отсутствие в них фенолового красного.
Дополнительной отличительной особенностью заявляемого изобретения является использование для кондиционирования клеток-продуцентов бессывороточной среды, не содержащей фенолового красного: DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA) с добавлением раствора антибиотиков Penicillin-Streptomycin (HyClone, USA), раствора L-Glutamine 200 mM (Gibco, USA), раствора незаменимых аминокислот MEM NEAA (100x) (Gibco, USA), раствора витаминов MEM Vitamin Solution (100X) (Gibco, USA) в следующих соотношениях по объему, об.%:
DMEM с низким содержанием глюкозы (не более 1 г/л) без фенолового красного (Gibco, USA) - 96.2 - 95.8;
Раствор антибиотиков Penicillin-Streptomycin (HyClone, USA) - 0.95 - 1.05;
Раствор L-Glutamine 200 mM (Gibco, USA) - 0.95 - 1.05;
Раствор незаменимых аминокислот MEM NEAA (100x) (Gibco, USA) - 0.95 - 1.05;
Раствор витаминов MEM Vitamin Solution (100X) (Gibco, USA) - 0.95 - 1.05.
Использование добавок заменимых аминокислот и витаминов призвано компенсировать отсутствие в среде кондиционирования фетальной бычьей сыворотки и увеличить продуктивность кондиционируемых клеток.
Указанную среду для кондиционирования клеткам добавляют в объеме 0.1-0.2 мл/см2 и культивируют в условиях СО2 инкубатора при 37±1°С, 5%-ом содержании СО2, содержании O2 в атмосфере не ниже 1% и относительной влажности ≥ 95% в течение 72-144 часов. Полученную таким образом кондиционированную среду МСК, содержащую все продукты секреции МСК человека, собирают в стерильные емкости для центрифугирования, удаляют путем центрифугирования остатки клеток, а полученный супернатант подвергают концентрированию методом центрифугирования или тангенциальной фильтрации с использованием мембран и фильтров, пропускающих молекулы не более 10 кДа, с уменьшением исходного объема очищенной среды и получением композиции, сконцентрированной в 1-50 раз от исходного объема и содержащей не менее 1 мкг/мл тотального белка (https://www.thermofisher.com/order/catalog/product/23225), BDNF (не менее 3 нг/мл), GDNF (не менее 0.03 нг/мл), VEGF (не менее 0.2 нг/мл), HGF (не менее 0.15 нг/мл), uPA (не менее 0.34 нг/мл), TGFb (суммарно по изоформам TGFb1, TGFb2 и TGFb3 не менее 0.055 нг/мл), антагонист рецептора IL-1 IL-1Ra (не менее 0.4 нг/мл), IL-4 (не менее 0.08 нг/мл), IL-6 (не менее 1 нг/мл), IL-10 (не менее 0.01 нг/мл), IL-11 (не менее 0.4 нг/мл), IL-13 (не менее 0.7 пг/мл), IDO (не менее 0.08 нг/мл), растворимые формы рецепторов IL-1 (не менее 0.01 нг/мл) и TNF (не менее 0.01 нг/мл), а также микроРНК обладающие нейропротективной и противовоспалительной активностью: hsa-miR-23a-3p (SEQ ID NO: 1), hsa-miR-101 (SEQ ID NO: 2 и/или SEQ ID NO: 3), hsa-miR-146a (SEQ ID NO: 4 и/или SEQ ID NO: 5), hsa-miR-491-5p (SEQ ID NO: 6), обладающие противовоспалительным эффектом, и hsa-miR-19b (SEQ ID NO: 7 и/или SEQ ID NO: 8), hsa-miR-21 (SEQ ID NO: 9 и/или SEQ ID NO: 10), hsa-miR-25 (SEQ ID NO: 11 и/или SEQ ID NO: 12), hsa-miR-125b (SEQ ID NO: 13 и/или SEQ ID NO: 14), hsa-miR-126a-3p (SEQ ID NO: 15), что устанавливается методами анализа содержания общего белка или отдельных белков/микроРНК в смеси. При характеристике и оценке качества композиции оценивают качественный состав указанных микроРНК, поскольку их количество в единицах массы (нг) не представляется возможным измерять. Их уровень измеряют и указывают относительно уровня представленности другого транскрипта (мРНК), который тоже в свою очередь может сильно меняться в зависимости от условий культивирования, типа и источника получения клеток и т.д.
В отличие от прототипа полученная композиция, характеризуется тем, что она обладает способностью препятствовать глутамат-опосредованной гибели нейральных клеток, способностью стимулировать поляризацию клеток моноцитарно-макрофагального звена в противовоспалительном направлении (M2-фенотип), а также предотвращать активацию клеток микроглии, что было продемонстрировано на моделях in vitro и in vivo.
Полученная композиция служит основой для получения средства для нейропротекции и стимуляции регенерации мозговой ткани после повреждения. Средство содержит композицию в терапевтически эффективном количестве и вспомогательные компоненты, стабилизирующие, консервирующие или улучшающие реологические свойства композиции в составе лекарственного средства. Для поддержания стабильности компонентов, входящих в состав средства, последнее может быть заморожено (-80…-18°С), с последующей разморозкой перед использованием или лиофилизировано в 6-10 стадий при давлении 0.013-0.027 кПа, температуре от минус 45°С до 25°С в течение не более 24 часов при максимальной загрузке лиофильной сушки, с последующим восстановлением лиофилизата в воде для инъекций или аналоге перед использованием.
Полученное средство обладает комплексным действием на основные компоненты патогенеза (ишемическое повреждение нейронов и клеток глии, токсическое действие крови и метаболитов, глутамат-опосредованная эксайтотоксичность, воспаление и вторичное повреждение мозговой ткани) широкого спектра острых повреждений головного мозга вне зависимости от механизма и этиологии данного повреждения, в том числе таких как механические, термические, химические (токсических, метаболических), радиационные и сочетанные повреждения головного мозга, а также повреждения, вызванные острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, и инфекционными агентами, в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2, что позволяет применять его с целью снижения смертности и инвалидизации среди таких пациентов. В заявленном изобретении терапевтический потенциал полученного средства демонстрируют на модели острого нарушения мозгового кровообращения по геморрагическому типу (геморрагический инсульт) у крыс, поскольку геморрагический инсульт объединяет все названные выше компоненты патогенеза, характерные для повреждения мозговой ткани.
Геморрагический инсульт у крыс моделируют механическим повреждением внутренней капсулы головного мозга (кзади от брегмы -2.0 мм, вправо от сигмы - 3.5 мм) [Paxinos G. and Watson C. The rat brain in stereotaxic coordinates. 2007] с последующим введением 20-40 мкл аутологичной крови из подъязычной вены в область повреждения. Затем экспериментальным животным через 5 минут в область кровоизлияния вводят секретом МСК, сконцентрированный в 10 раз, содержащий факторы роста: BDNF (не менее 3 нг/мл), GDNF (не менее 0.03 нг/мл), VEGF (не менее 0.2 нг/мл), HGF (не менее 0.15 нг/мл), uPA (не менее 0.34 нг/мл), TGFb (суммарно по изоформам TGFb1, TGFb2 и TGFb3 не менее 0.055 нг/мл), цитокины: IL-4 (не менее 0.08 нг/мл), IL-6 (не менее 1 нг/мл), IL-10 (не менее 0.01 нг/мл), IL-11 (не менее 0.4 нг/мл), IL-13 (не менее 0.7 пг/мл), противовоспалительные молекулы: антагонист рецептора IL-1 IL-1Ra (не менее 0.4 нг/мл), IDO (не менее 0.08 нг/мл), растворимые формы рецепторов IL-1 (не менее 0.01 нг/мл) и TNF (не менее 0.01 нг/мл), а также микроРНК обладающие нейропротективной и противовоспалительной активностью: hsa-miR-23a-3p (SEQ ID NO: 1), hsa-miR-101 (SEQ ID NO: 2 и SEQ ID NO: 3), hsa-miR-146a (SEQ ID NO: 4 и SEQ ID NO: 5), hsa-miR-491-5p (SEQ ID NO: 6), обладающие противовоспалительным эффектом, и hsa-miR-19b (SEQ ID NO: 7 и SEQ ID NO: 8), hsa-miR-21 (SEQ ID NO: 9 и SEQ ID NO: 10), hsa-miR-25 (SEQ ID NO: 11 и SEQ ID NO: 12), hsa-miR-125b (SEQ ID NO: 13 и SEQ ID NO: 14), hsa-miR-126a-3p (SEQ ID NO: 15) в дозе не менее 1 мкг/кг (по тотальному белку). Модификацией данного способа является введение описанного выше секретома МСК в дозе не менее 1 мкг/кг (по тотальному белку) однократно интраназально, внутривенно или интратекально через 6 часов и менее после моделирования инсульта. Модификацией данного способа является повторное введение описанного выше секретома МСК в дозе не менее 1 мкг/кг (по тотальному белку) одним из описанных выше способов через 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21 дней после инсульта. Диапазон терапевтических доз при клиническом применении заявляемых композиции и средства на его основе должен быть установлен дополнительно, поскольку сильно зависит от объема повреждения, локализации и тяжести инсульта, а также пути введения и времени введения после инсульта.
Восстановление животных после геморрагического инсульта оценивают по параметрам выживаемости, сохранности неврологических показателей, и объему области повреждения головного мозга по данным магнитно-резонансной томографии (МРТ) и гистологического исследования. Выживаемость животных оценивают и регистрируют ежедневно в течение всего эксперимента, неврологические показатели оценивают через 3 и 10, 21 и 45 суток после моделирования геморрагического инсульта по шкале Stroke-index McGraw, модифицированной для грызунов И.В. Ганушкиной [McGraw C.P. et al., Stroke, 1976; Gannushkina I.V., Vestn Ross Akad Med Nauk, 2000]. «Визуально здоровые животные» не имеют признаков неврологического дефицита. Животными с «легкими неврологическими нарушениями» считают животных с признаками вялости, слабости конечностей, тремора, птоза и/или полуптоза. Животных с признаками пареза и/или паралича конечностей, нарушением координации или в коматозном состоянии учитывают, как животных с «тяжелыми неврологическими нарушениями».
Объем повреждения головного мозга по МРТ оценивают через 11 и 45 дней после моделирования геморрагического инсульта с использованием системы Clinscan 7T (Bruker Biospin, США), снабженной катушкой для анализа мозга крысы с TurboS Spin Echo и подавлением сигнала от жировой ткани. Коронарные проекции получают при следующих параметрах: TR (время повторения)=5220 мс; TE (время до эха)=53 мс; продолжительность эха сигнала=9; базовое разрешение 230х320; FoV (поле зрения)=32 (40 мм; толщина среза=0.5 мм; расстояние между срезами=0.75 мм. Поперечные проекции получают при следующих параметрах: TR=4000 мс; TE=40 мс; продолжительность эха сигнала=9; базовое разрешение 288х320; FoV=40 (40 мм; толщина среза=0.5 мм; расстояние между срезами=0.6 мм.
Объем повреждения головного мозга с помощью гистологического исследования оценивают через 14 и 45 дней после моделирования геморрагического инсульта. Для этого крыс умерщвляют в среде CO2. Головной мозг извлекают, фиксируют в 4% растворе формальдегида и заливают парафином. Срезы головного мозга, содержащие очаг повреждения, депарафинизируют и антигены демаскируют.Часть срезов окрашивают гематоксилин-эозином, крезиловым фиолетовым (окраска по Нисслю) или берлинской лазурью Перлса (окраска по Перлсу). Комбинация этих красителей позволяет оценить различные аспекты морфологических изменений в поврежденном мозге: размер поражения, нейрональный статус, скорость инфильтрации лейкоцитов и размер отложений гемосидерина.
Для иммуногистохимического окрашивания срезы обрабатывают 50 мМ раствором ацетата аммония и блокируют 10% козьей сывороткой для уменьшения фоновой флуоресценции. После блокирования их инкубируют с антителами к CD68 (Abcam, #ab125212, США) и CD163 (Abcam, #ab182422, США) с последующей инкубацией с флуоресцентно меченными вторичными козьими антикроличьими антителами (Invitrogen, #A11034, США). Ядра окрашивают раствором 4',6-диамидино-2-фенилиндола (DAPI) (Sigma, #MBD0015-10ML, США). Образцы исследуют с помощью микроскопа Leica DM600, оснащенного камерой DFC360 FX и DFC420C (Leica Microsystems GmbH, Германия) или аналогичного, с использованием репрезентативных полей зрения для получения фотографий. Обработку и анализ изображений проводят с использованием программного обеспечения LasX (Leica Microsystems GmbH, Германия) и FiJi.»
В настоящем изобретении на основании данных исследования эффективности предлагаемой композиции в модели геморрагического инсульта in vivo приведены данные о качественном и количественном составе применяемой композиции, об оптимальном пути введения, временном терапевтическом окне и дозе, что является неотъемлемой информацией при разработке подходов для терапии повреждений мозга и профилактики осложнений, особенно, острых нарушений мозгового кровообращения.
Техническая проблема стимуляции нейропротекции и регенерации ткани мозга после повреждения решается применением лекарственного средства указанным в изобретении способом, который подразумевает введение комплексного препарата, разработанного на основе секретома МСК, сконцентрированного в 1-50 раз, содержащего факторы роста: BDNF (не менее 3 нг/мл), GDNF (не менее 0.03 нг/мл), VEGF (не менее 0.2 нг/мл), HGF (не менее 0.15 нг/мл), uPA (не менее 0.34 нг/мл), TGFb (суммарно по изоформам TGFb1, TGFb2 и TGFb3 не менее 0.055 нг/мл), цитокины: IL-4 (не менее 0.08 нг/мл), IL-6 (не менее 1 нг/мл), IL-10 (не менее 0.01 нг/мл), IL-11 (не менее 0.4 нг/мл), IL-13 (не менее 0.7 пг/мл), противовоспалительные молекулы: антагонист рецептора IL-1 IL-1Ra (не менее 0.4 нг/мл), IDO (не менее 0.08 нг/мл), растворимые формы рецепторов IL-1 (не менее 0.01 нг/мл) и TNF (не менее 0.01 нг/мл), а также микроРНК обладающие нейропротективной и противовоспалительной активностью: hsa-miR-23a-3p (SEQ ID NO: 1), hsa-miR-101 (SEQ ID NO: 2 и SEQ ID NO: 3), hsa-miR-146a (SEQ ID NO: 4 и SEQ ID NO: 5), hsa-miR-491-5p (SEQ ID NO: 6), обладающие противовоспалительным эффектом, и hsa-miR-19b (SEQ ID NO: 7 и SEQ ID NO: 8), hsa-miR-21 (SEQ ID NO: 9 и SEQ ID NO: 10), hsa-miR-25 (SEQ ID NO: 11 и SEQ ID NO: 12), hsa-miR-125b (SEQ ID NO: 13 и SEQ ID NO: 14), hsa-miR-126a-3p (SEQ ID NO: 15), измеренных методами иммуноферментного анализа (для белков), ПЦР в реальном времени (для микроРНК) или аналогичными. Применяемая композиция содержит комбинацию факторов роста, внеклеточных везикул, переносящих определенные микроРНК, или других биологически активных компонентов, секретированных МСК человека в оптимальном сочетании активных компонентов различной природы, не содержит белков животного происхождения и бактериальных фрагментов, а также обеспечивает сбалансированный эффект за счет наличия различных по природе и механизму действия факторов.
Указанный секретом МСК получают при культивировании МСК человека в бессывороточной среде Игла, модифицированной Дульбекко (DMEM), лишенной животных компонентов, с содержанием глюкозы не более 1 г/л без фенолового красного с добавлением растворов Penicillin-Streptomycin solution (HyClone, #SV30010) 0.95-1.05%, L-Glutamine (200 mM) (Gibco, #25030081) 0.95-1.05%, MEM Non-Essential Amino Acids Solution (100X) (Gibco, #11140076) 0.95-1.05%, MEM Vitamin Solution (100X) (Gibco, #11120052) 0.95-1.05%), с потенциально безопасным для клинического применения составом, поддерживающей жизнеспособность клеток в течение подобранного срока кондиционирования, путем сбора кондиционированной среды, содержащей биологически активные факторы и внеклеточные везикулы, секретируемые клетками в культуральную среду, очистки полученной среды и ее фракционирования с помощью центрифугирования и ультрафильтрации. Средство на основе заявляемой композиции включает композицию в терапевтически эффективном количестве, а также терапевтические приемлемые добавки, наполнители (глюкоза, лактоза, цитрат натрия, альбумин человека и др.), стабилизаторы изотонические агенты (хлористый натрий) и/или консерванты (парабены, хлорбутанол, сорбиновая кислота и др.). Стабилизацию полученных композиции или средства осуществляют путем лиофилизации. Полученный лиофилизат, разведенный в стерильной воде для инъекций или аналоге, можно использовать как лекарственное средство для лечения или профилактики осложнений острых нарушениях мозгового кровообращения по геморрагическому типу.
Таким образом, технический результат достигается за счет того, что предлагаемое применение композиции, включающее локальное, интраназальное, внутривенное или интратекальное введение в дозе не менее 1 мкг/кг (по тотальному белку) в течение 6 часов и менее после повреждения ткани мозга (в острейшем периоде), в диапазоне 6-120 часов при повреждении ткани мозга (острый период), в диапазоне от 5 до 21 суток при повреждении ткани мозга (подострый период) после механического, термического, химического (токсических, метаболических), радиационного и сочетанного повреждения, а также повреждения, вызванного острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, и инфекционными агентами, в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2, оказывает комплексное действие, по крайней мере, на нейроны, клетки макро- и микроглии, а также клетки моноцитарно/макрофагального звена гематогенного происхождения. Эффективность заявляемого средства предполагает наличие целого комплекса воздействий, направленных на лечение или профилактику осложнений при острых повреждениях мозговой ткани вне зависимости от механизма и этиологии данного повреждения. Будучи введенной в острейшем периоде после повреждения мозга, предлагаемая композиция предотвращает гибель нейронов, вызванную гипоксией, выбросом глутамата и прямым токсическим действием крови, за счет снижения активности проапоптотических белков Bax и увеличения активности антиапоптотических белков Bcl-2. Будучи введенной в острейшем и остром периоде после повреждения мозга, предлагаемая композиция подавляет гиперактивацию клеток микроглии, что препятствует миграции из крови в очаг повреждения избыточного количества клеток моноцитарно/макрофагального звена и стимулирует поляризацию последних в противовоспалительном направлении. Будучи введенной в остром и подостром периоде после повреждения мозга, предлагаемая композиция предотвращает гибель нейронов, вызванную воспалением и вторичным повреждением головного мозга, за счет снижения активности проапоптотических белков Bax и увеличения активности антиапоптотических белков Bcl-2 в нейральных клетках и поляризации клеток микроглии и клеток моноцитарно/макрофагального звена в противовоспалительном направлении. Вторичное повреждение ткани головного мозга развивается в результате первичной массированной гибели нервной ткани, что приводит к нарушению гематоэнцефалического барьера, воспалению и отеку, что приводит к сдавлению и нарушению кровоснабжения прилежащей мозговой ткани, ее ишемии и гибели с расширением первичного очага повреждения. Своевременная нейротрофическая поддержка и подавление воспалительных процессов способны разорвать порочный круг вторичного повреждения нервной ткани.
Пример 1. Метод культивирования МСК жировой ткани (МСК ЖТ). Метод получения секретома.
Культуры клеток МСК человека, полученные из жировой ткани здоровых доноров (n=3), были получены из биобанка Института регенеративной медицины МГУ им. М.В. Ломоносова, идентификатор коллекции: MSU_МСК_AD (https://human.depo.msu.ru). Их культивировали в среде DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA), содержащей 10% фетальной бычьей сыворотки (HyClone, USA) и 1% антибиотика/антимикотика (Gibco, USA), 1% глутамина (Gibco, USA). Все процедуры, выполняемые с образцами тканей пациентов, соответствовали Хельсинкской декларации и одобрены Этическим комитетом МГУ им. М.В. Ломоносова (IRB00010587), протокол №4 (2018).
МСК крыс, получали из жировой ткани половозрелых самцов крыс линии Wistar в соответствии с ранее описанным протоколом [Aleksandrushkina NA, Danilova NV, Grigorieva OA, Mal'kov PG, Popov VS, Efimenko AY, et al. Bulletin of Experimental Biology and Medicine. 2019;167(1):159-63] и культивированы в среде среде DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA), содержащей 10% фетальной бычьей сыворотки (HyClone, USA) и 1% антибиотика/антимикотика (HyClone, USA), 1% глутамина (Gibco, USA). Полученные МСК характеризовали в соответствии с критериями Международного общества клеточной терапии (ISCT) по способности адгезироваться к пластику, экспрессировать CD73, CD90 и CD105, отсутствию гемопоэтических и эндотелиальных маркеров CD14, CD19, CD34, CD45 и HLA-DR и способности дифференцироваться in vitro в адипогенном, хондрогенном и остеогенном направлении [Viswanathan S, Shi Y, Galipeau J, Krampera M, Leblanc K, Martin I, Nolta J, Phinney DG, Sensebe L. Mesenchymal stem versus stromal cells: International Society for Cell & Gene Therapy (ISCT®) Mesenchymal Stromal Cell committee position statement on nomenclature. Cytotherapy. 2019 Oct;21(10):1019-1024. doi: 10.1016/j.jcyt.2019.08.002; Sagaradze G, Grigorieva O, Nimiritsky P, Basalova N, Kalinina N, Akopyan Z, Efimenko A. Conditioned Medium from Human Mesenchymal Stromal Cells: Towards the Clinical Translation. Int J Mol Sci. 2019 Apr 3;20(7):1656. doi: 10.3390/ijms20071656]. Среду меняли каждые 3-4 дня. Все эксперименты проводились с клетками в пределах 5 пассажей.
Кондиционированную среду, содержащую компоненты секретома МСК человека или крысы, получали согласно опубликованному ранее протоколу [Karagyaur M, Dzhauari S, Basalova N, et al. MSC Secretome as a Promising Tool for Neuroprotection and Neuroregeneration in a Model of Intracerebral Hemorrhage. Pharmaceutics. 2021; 13(12):2031, doi:10.3390/pharmaceutics13122031; RU2620167; RU2766707]. Вкратце, субконфлюентные МСК человека или крысы на пассажах 2-5 тщательно промывали раствором Хенкса (ПанЭко, Россия), а затем культивировали в течение 144 часов в среде DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA) с добавлением 1% раствора антибиотиков Penicillin-Streptomycin (HyClone, USA), 1% раствора L-Glutamine 200 mM (Gibco, USA), 1% раствора незаменимых аминокислот MEM NEAA (100x) (Gibco, USA), 1% раствора витаминов MEM Vitamin Solution (100X) (Gibco, USA). По окончании кондиционирования среду собирали и центрифугировали в течение 10 минут при 300 g для удаления клеточного дебриса (группа чМСК1x), а часть образцов дополнительно концентрировали в 10 раз (группа чМСК10x), используя картриджи для ультрафильтрации с отсечкой молекулярной массы менее 10 кДа (Merck, Германия).
Секретом МСК крыс концентрировали в 10 раз таким же образом (группа кМСК10x). В качестве отрицательного контроля (контрольная группа) мы DMEM с низким содержанием глюкозы без фенолового красного (Gibco, USA) с добавлением 1% раствора антибиотиков Penicillin-Streptomycin (HyClone, USA), 1% раствора L-Glutamine 200 mM (Gibco, USA), 1% раствора незаменимых аминокислот MEM NEAA (100x) (Gibco, USA), 1% раствора витаминов MEM Vitamin Solution (100X) (Gibco, USA). В качестве положительного контроля использовали ту же контрольную среду с добавлением 3.5 нг/мкл рекомбинантного мозгового нейротрофического фактора человека (группа BDNF) (#ab206642-2, Abcam, США) [Karagyaur M, Dzhauari S, Basalova N, et al. MSC Secretome as a Promising Tool for Neuroprotection and Neuroregeneration in a Model of Intracerebral Hemorrhage. Pharmaceutics. 2021;13(12):2031, doi:10.3390/pharmaceutics13122031]. Для повышения нейропротекторной активности секретом 1x дополняли человеческим BDNF до конечной концентрации 3.5 нг / мкл (группа чМСК-B).
В полученных секретомах МСК человека и крыс с помощью иммуноферментного анализа оценивали концентрации ключевых факторов, обладающих нейропротективной и противовоспалительной активностью: BDNF, GDNF, VEGF, HGF, uPA, TGFb, IL-1Ra, IL-4, IL-6, IL-10, IL-11, IL-13, IDO, растворимые формы рецепторов IL-1 и TNF, а также микроРНК: miR-23a-3p, miR-101, miR-146a, miR-491, miR-19b, miR-21, miR-25, miR-125b, 126a-3p.Их концентрации для неконцентрированного секретома МСК человека/крыс находились в количестве BDNF (не менее 3 нг/мл), GDNF (не менее 0.03 нг/мл), VEGF (не менее 0.2 нг/мл), HGF (не менее 0.15 нг/мл), uPA (не менее 0.34 нг/мл), TGFb (суммарно по изоформам TGFb1, TGFb2 и TGFb3 не менее 0.055 нг/мл), антагонист рецептора IL-1 IL-1Ra (не менее 0.4 нг/мл), IL-4 (не менее 0.08 нг/мл), IL-6 (не менее 1 нг/мл), IL-10 (не менее 0.01 нг/мл), IL-11 (не менее 0.4 нг/мл), IL-13 (не менее 0.7 пг/мл), IDO (не менее 0.08 нг/мл), растворимые формы рецепторов IL-1 (не менее 0.01 нг/мл) и TNF (не менее 0.01 нг/мл).
В ходе проведения данного исследования изучалось несколько композиций, различающихся по составу и концентрации действующих веществ (на основании 3 измерений):
Вариант 1 - (BDNF). Рекомбинантный BDNF человека в концентрации 3.2 нг/мкл на DMEM с низким содержанием глюкозы и без фенолового красного.
Вариант 2 - (чМСК1x). BDNF (3.2 (1.2 нг/мл), GDNF (0.03 (0.018 нг/мл), VEGF (0.27 (0.13 нг/мл), HGF (0.15 (0.07 нг/мл), uPA (0.34 (0.16 нг/мл), TGF-b (0.055 (0.027 нг/мл) на DMEM с низким содержанием глюкозы и без фенолового красного.
Вариант 3 - (чМСК-B). BDNF (3.2 (1.2 нг/мл), GDNF (0.03 (0.018 нг/мл), VEGF (0.27 (0.13 нг/мл), HGF (0.15 (0.07 нг/мл), uPA (0.34 (0.16 нг/мл), TGF-b (0.055 (0.027 нг/мл) на DMEM с низким содержанием глюкозы и без фенолового красного.
Вариант 4 - (чМСК10х). Компоненты секретома МСК человека (ксеногенный для крысиной модели): BDNF (28.9 (14.3 нг/мл), GDNF (0.27 (0.11 нг/мл), VEGF (2.3 (0.7 нг/мл), HGF (1.4 (0.3 нг/мл), uPA (2.7 (0.74 нг/мл), TGF-b (0.45 (0.17 нг/мл), антагонист рецептора IL-1 IL-1Ra (3.3 (0.7 нг/мл), IL-4 (0.77 (0.14 нг/мл), IL-6 (6 (0.7 нг/мл), IL-10 (0.13 (0.07 нг/мл), IL-11 (2.4 (0.88 нг/мл), IL-13 (6.5 (0.7 пг/мл), IDO (0.8 (0.27 нг/мл), растворимые формы рецепторов IL-1 (0.08 (0.05 нг/мл) и TNF (0.12 (0.067 нг/мл), а также микроРНК: hsa-miR-23a-3p (SEQ ID NO: 1), hsa-miR-101 (SEQ ID NO: 2 и SEQ ID NO: 3), hsa-miR-146a (SEQ ID NO: 4 и SEQ ID NO: 5), hsa-miR-491-5p (SEQ ID NO: 6), hsa-miR-19b (SEQ ID NO: 7 и SEQ ID NO: 8), hsa-miR-21 (SEQ ID NO: 9 и SEQ ID NO: 10), hsa-miR-25 (SEQ ID NO: 11 и SEQ ID NO: 12), hsa-miR-125b (SEQ ID NO: 13 и SEQ ID NO: 14), hsa-miR-126a-3p (SEQ ID NO: 15) - на DMEM с низким содержанием глюкозы и без фенолового красного.Вариант 5 - (кМСК10х). Компоненты секретома МСК крыс (аллогенный для крысиной модели): BDNF (21.6 (6.8 нг/мл), GDNF (0.51 (0.19 нг/мл), VEGF (2.8 (1.2 нг/мл), HGF (0.94 (0.36 нг/мл), uPA (4.9 (1.8 нг/мл), TGF-b (0.73 (0.24 нг/мл), антагонист рецептора IL-1 IL-1Ra (4.6 (1.4 нг/мл), IL-4 (0.86 (0.21 нг/мл), IL-6 (4.8 (0.9 нг/мл), IL-10 (0.24 (0.15 нг/мл), IL-11 (1.9 (0.69 нг/мл), IL-13 (16.9 (4.9 пг/мл), IDO (1.4 (0.39 нг/мл), растворимые формы рецепторов IL-1 (0.12 (0.07 нг/мл) и TNF (0.19 (0.081 нг/мл), а также микроРНК: rno-miR-23a-3p (SEQ ID NO: 16), rno-miR-101 (SEQ ID NO: 17 и SEQ ID NO: 18), rno-miR-146a (SEQ ID NO: 19 и SEQ ID NO: 20), rno-miR-19b (SEQ ID NO: 21 и SEQ ID NO: 22), rno-miR-21 (SEQ ID NO: 23 и SEQ ID NO: 24), rno-miR-25 (SEQ ID NO: 25 и SEQ ID NO: 26), rno-miR-125b (SEQ ID NO: 27 и SEQ ID NO: 28), rno-miR-126a-3p (SEQ ID NO: 29) - на DMEM с низким содержанием глюкозы и без фенолового красного.
Вариант 6 - (кМСК50х). Компоненты секретома МСК крыс (аллогенный для крысиной модели): BDNF (86.4 (14.5 нг/мл), GDNF (2.24 (0.87 нг/мл), VEGF (12.3 (4.9 нг/мл), HGF (4.57 (1.39 нг/мл), uPA (20.6 (4.6 нг/мл), TGF-b (3.3 (1.13 нг/мл), антагонист рецептора IL-1 IL-1Ra (15.7 (3.9 нг/мл), IL-4 (3.8 (0.95 нг/мл), IL-6 (21.4 (4.3 нг/мл), IL-10 (1.22 (0.48 нг/мл), IL-11 (7.6 (1.94 нг/мл), IL-13 (0.06 (0.012 нг/мл), IDO (6.8 (1.6 нг/мл), растворимые формы рецепторов IL-1 (0.48 (0.19 нг/мл) и TNF (1.4 (0.37 нг/мл), а также микроРНК: rno-miR-23a-3p (SEQ ID NO: 16), rno-miR-101 (SEQ ID NO: 17 и SEQ ID NO: 18), rno-miR-146a (SEQ ID NO: 19 и SEQ ID NO: 20), rno-miR-19b (SEQ ID NO: 21 и SEQ ID NO: 22), rno-miR-21 (SEQ ID NO: 23 и SEQ ID NO: 24), rno-miR-25 (SEQ ID NO: 25 и SEQ ID NO: 26), rno-miR-125b (SEQ ID NO: 27 и SEQ ID NO: 28), rno-miR-126a-3p (SEQ ID NO: 29) - на DMEM с низким содержанием глюкозы и без фенолового красного.
Концентрирование более, чем в 50 раз (вариант композиции 6) по нашим данным, является неэффективным, что обусловлено высокой вязкостью образующегося концентрата и практической невозможностью дальнейшего концентрирования. Таким образом, верхняя граница возможных концентраций факторов роста в композициях, полученных в ходе концентрирования секретома МСК жировой ткани, является естественной и соответствует концентрациям, полученным для варианта композиции 6.
Пример 2. Метод моделирования внутримозгового кровоизлияния (геморрагического инсульта) и введение секретома в область повреждения.
Механизмы повреждения мозговой ткани, такие как ишемическое повреждение нейронов и клеток глии, токсическое действие крови и метаболитов, глутамат-опосредованная эксайтотоксичность, воспаление и вторичное повреждение мозговой ткани - являются универсальными механизмами повреждениями мозговой ткани и характерны в тех или иных комбинациях для механических, термических, химических (токсических, метаболических), радиационных и сочетанных повреждений головного мозга, а также повреждений, вызванных острым нарушением мозгового кровообращения по геморрагическому или ишемическому типу, и инфекционными агентами, в том числе микроорганизмами родов Neisseria, Borrelia и коронавирусными инфекциями, в том числе вирусом SARS-Cov2 [Ng SY, Lee AYW. Traumatic Brain Injuries: Pathophysiology and Potential Therapeutic Targets. Front Cell Neurosci. 2019;13:528. doi: 10.3389/fncel.2019.00528; Walter EJ, Carraretto M. The neurological and cognitive consequences of hyperthermia. Crit Care. 2016;20(1):199. doi: 10.1186/s13054-016-1376-4; Dang J, Chen J, Bi F, Tian F. The clinical and pathological features of toxic encephalopathy caused by occupational 1,2-dichloroethane exposure. Medicine (Baltimore). 2019 Apr;98(17):e15273. doi: 10.1097/MD.0000000000015273; Kuriakose D, Xiao Z. Pathophysiology and Treatment of Stroke: Present Status and Future Perspectives. Int J Mol Sci. 2020 Oct 15;21(20):7609. doi: 10.3390/ijms21207609; Shao Z, Tu S, Shao A. Pathophysiological Mechanisms and Potential Therapeutic Targets in Intracerebral Hemorrhage. Front Pharmacol. 2019 Sep 19;10:1079. doi: 10.3389/fphar.2019.01079; Hoffman O, Weber RJ. Pathophysiology and treatment of bacterial meningitis. Ther Adv Neurol Disord. 2009;2(6):1-7. doi:10.1177/1756285609337975; Wijeratne T, Gillard Crewther S, Sales C, Karimi L. COVID-19 Pathophysiology Predicts That Ischemic Stroke Occurrence Is an Expectation, Not an Exception-A Systematic Review. Front Neurol. 2021 Jan 28;11:607221. doi: 10.3389/fneur.2020.607221].
Вторичное повреждение ткани головного мозга развивается в результате первичной массированной гибели нервной ткани, что приводит к нарушению гематоэнцефалического барьера, воспалению и отеку, что приводит к сдавлению и нарушению кровоснабжения прилежащей мозговой ткани, ее ишемии и гибели с расширением первичного очага повреждения [Ng SY, Lee AYW. Traumatic Brain Injuries: Pathophysiology and Potential Therapeutic Targets. Front Cell Neurosci. 2019;13:528. doi: 10.3389/fncel.2019.00528; Walter EJ, Carraretto M. The neurological and cognitive consequences of hyperthermia. Crit Care. 2016;20(1):199. doi: 10.1186/s13054-016-1376-4]. Своевременная нейротрофическая поддержка и подавление воспалительных процессов способны разорвать порочный круг вторичного повреждения нервной ткани.
Композиции и средства на их основе, способные смягчать и тормозить действие этих основных патогенетических звеньев повреждения мозга в острейшей, острой и подострой стадии повреждения могут быть с успехом применены для лечения широкого спектра патологий, ассоциированных с острым повреждением головного мозга вне зависимости от его генеза.
В заявленном изобретении терапевтический потенциал полученного средства демонстрируют на модели острого нарушения мозгового кровообращения по геморрагическому типу (геморрагический инсульт) у крыс, поскольку геморрагический инсульт объединяет все названные выше компоненты патогенеза, характерные для повреждения мозговой ткани, а композиции или средства, продемонстрировавшие высокую терапевтическую эффективность на модели геморрагического инсульта, с высокой долей вероятности окажутся эффективными при лечении других острых повреждений мозга вне зависимости от их генеза.
Моделирование геморрагического инсульта осуществляли согласно описанной ранее модели внутримозгового кровоизлияния во внутреннюю капсулу правого полушария по А.Н. Макаренко и др. [Makarenko, A.N.; Kositsyn, N.S.; Pasikova, N.V.; Svinov, M.M. Metod modelirovaniia lokal'nogo krovoizliianiia v razlich-nykh strukturakh golovnogo mozga u éksperimental'nykh zhivotnykh [Simulation of local cerebral hemorrhage in different brain structures of experimental animals]. Zh Vyssh Nerv Deiat Im I P Pavlova, 2002, 52(6), 765-768]. Для моделирования внутримозгового кровоизлияния крыс анестезировали раствором, содержащим 2% Zoletil(50 (VirBac, Испания) и 1.5% ксилазина (InterChemie, Нидерланды) в физиологическом растворе в дозе 1 мл/кг массы тела и помещали в стереотаксический аппарат.
Рассекали кожу и сухожильный апоневроз, череп перфорировали (кзади от брегмы -2.0 мм, вправо от сигмы - 3.5 мм) [Paxinos, G.; Watson, C. The rat brain in stereotaxic coordinates. 6th Edition. Cambridge: Academic Press, 2007]. Ткань головного мозга в области перфорации разрушали, а поверхностные вены головного мозга на соответствующей стороне были повреждены для моделирования кровотечения. Для стандартизации объема излившейся крови в очаг повреждения медленно вводили 20 мкл аутологичной крови, взятой из подъязычной вены. Через 5 мин вводили 20 мкл соответствующей концентрированной пробы среды, и рану ушивали. В ходе исследования терапевтической активности композиции для нейропротекции и стимуляции регенерации нервной ткани в модели in vivo исследовали варианты композиций 1, 2, 3, 4, 5 и 6 (см. Пример 1).
Животным из группы ЛО (ложнооперированные) делали перфорацию черепа без какого-либо последующего повреждения головного мозга или инъекций образца крови/секретома.
Пример 3. Метод оценки эффективности восстановления морфологии и функций мозга после моделирования геморрагического инсульта.
Оценка неврологического статуса
За животными наблюдали в течение 14 дней после моделирования внутримозгового кровоизлияния с ежедневной регистрацией гибели крыс и оценкой неврологического статуса через 3 и 10 дней после кровоизлияния (по шкале Stroke-index McGraw, модифицированной для грызунов И.В. Ганушкиной) [McGraw, C.P.; Pashayan, A.G.; Wendel, O.T.; Cerebral infarction in the Mongolian gerbil exacerbated by phenoxyben-zamine treatment. Stroke, 1976, 7(5), 485-488. doi: 10.1161/01.str.7.5.485.; Gannushkina, I.V.; Mozgovoe krovoobrashchenie pri razlichnykh vidakh tsirkuliatornoĭ gipoksii mozga [Cerebral circula-tion in different types of brain hypoxia]. Vestn Ross Akad Med Nauk, 2000, 9, 22-27. Russian.]. Вкратце, «визуально здоровые животные» не имели признаков неврологического дефицита. Животные с признаками вялости, слабости конечностей, тремора, птоза и/или полуптоза считались животными «с легкими неврологическими нарушениями». Животные, у которых наблюдались признаки пареза и/или паралича конечностей, нарушения координации или находились в коме, считались животными «с тяжелыми неврологическими нарушениями». Когнитивные нарушения оценивали с помощью теста пассивного избегания [Fabbri, R., Furini, C. R., Passani, M. B., Provensi, G., Baldi, E., Bucherelli, C., et al. (2016). Memory retrieval of inhibitory avoidance requires histamine H1 receptor activation in the hippocampus. Proc. Natl. Acad. Sci. U. S. A. 113, E2714-E2720]. У животных вырабатывали рефлекс за 24 часа до внутримозгового кровоизлияния. Для этого каждое животное помещали в аппарат пассивного избегания (San Diego Instruments, США) и регистрировали время до его входа в темную камеру аппарата. В камере крыса получала 8 болевых электрических раздражителей (0,4 мА, 1 сек каждый). Через 24 часа и 10 дней после внутримозгового кровоизлияния (кратковременная и долговременная память соответственно) животных повторно обследовали - фиксировали время избегания темной камеры с электрическим полом. Максимальное время наблюдения за каждым животным составляло 180 секунд (100%). Полученные результаты были нормированы на 180 секунд, и вычисляли «эффективность» краткосрочной и долгосрочной памяти в %.
Оценка объема повреждения головного мозга с помощью МРТ
МР-изображения были получены через 11 дней после моделирования внутримозгового кровоизлияния с использованием системы Clinscan 7T (Bruker Biospin, США), снабженной катушкой для анализа мозга крысы с TurboS Spin Echo и подавлением сигнала от жировой ткани. Коронарные проекции были получены с использованием следующих параметров: TR (время повторения)=5220 мс; TE (время до эха)=53 мс; продолжительность эха сигнала=9; базовое разрешение 230х320; FoV (поле зрения)=32 (40 мм; толщина среза=0.5 мм; расстояние между срезами=0.75 мм. Поперечные проекции были получены с использованием следующих параметров: TR=4000 мс; TE=40 мс; продолжительность эха сигнала=9; базовое разрешение 288х320; FoV=40 (40 мм; толщина среза=0.5 мм; расстояние между срезами=0.6 мм.
Оценка объема повреждения головного мозга с помощью гистохимических и иммуногистохимических методов
Для гистологических исследований крыс на 14 день после моделирования внутримозгового кровоизлияния умерщвляли в среде CO2. Головной мозг извлекали, фиксировали в 4% растворе формальдегида и заливали парафином. Срезы головного мозга, содержащие очаг повреждения, депарафинизировали и антигены демаскировали. Часть срезов окрашивали гематоксилин-эозином, крезиловым фиолетовым (окраска по Нисслю) или берлинской лазурью Перлса (окраска по Перлсу). Комбинация этих красителей позволяет оценить различные аспекты морфологических изменений в поврежденном мозге: размер поражения, нейрональный статус, скорость инфильтрации лейкоцитов и размер отложений гемосидерина.
Для иммуногистохимического окрашивания срезы обрабатывали 50 мМ раствором ацетата аммония и блокировали 10% козьей сывороткой для уменьшения фоновой флуоресценции. После блокирования их инкубировали с антителами к CD68 (Abcam, #ab125212, США) и CD163 (Abcam, #ab182422, США) с последующей инкубацией с флуоресцентно меченными вторичными козьими антикроличьими антителами (Invitrogen, #A11034, США). Ядра окрашивали раствором 4',6-диамидино-2-фенилиндола (DAPI) (Sigma, #MBD0015-10ML, США). Образцы исследовали с помощью микроскопа Leica DM600, оснащенного камерой DFC360 FX и DFC420C (Leica Microsystems GmbH, Германия), с использованием репрезентативных полей зрения для получения фотографий. Обработку и анализ изображений проводили с использованием программного обеспечения LasX (Leica Microsystems GmbH, Германия) и FiJi.
Пример 4. Метод оценки нейропротективной и нейротрофической активности аллогенного и ксеногенного секретомов МСК при их введении в область геморрагического инсульта.
Для оценки нейропротективной и нейротрофической активности аллогенного и ксеногенного секретомов МСК при их введении в область геморрагического инсульта использовали описанную выше модель геморрагического инсульта. В исследование были включены 98 животных: 40 крыс для пилотного исследования (группы ложнооперированных (SO), контрольная, BDNF и чМСК1x, по 10 крыс в каждой), 30 крыс для исследования нейропротекторной активности секретома MSC человека (контроль, чМСК10x и Группы чМСК-B, по 10 крыс в каждой) и 28 крыс для исследования видовой специфичности (10 крыс для контрольной группы и 18 для группы кМСК10x). Ни одна из крыс не была исключена из исследования.
Результаты пилотного исследования показали, что секретом чМСК1x обладает потенциальной терапевтической активностью, но является менее эффективным, чем препарат BDNF из группы положительного контроля (Фиг. 1Б). Хотя секретом чМСК1x не оказал значительного влияния на выживаемость и облегчение неврологического дефицита у экспериментальных животных, он способствовал сохранению долговременной памяти у крыс [100% (94.4%; 100%) по сравнению с 79.2% (12.2%; 100%) в контрольной группе, n≥8] (Фиг. 1Г). В то время как BDNF обеспечивал лучший неврологический результат (Фиг. 1Б), он был менее эффективен, чем чМСК1x в когнитивном тесте: 80.6% (42.8%; 100%) (Фиг. 1Г). Предположительно, это связано с различием в действии секретома BDNF и чМСК1x: BDNF - это белок с прямой (немедленной) нейротрофической активностью, в то время как секретом чМСК1x состоит из большого числа молекулярных комплексов (особенно микровезикул, которые имеют отсроченное действие на программу транскрипции клеток-мишеней) с более низким содержанием нейротрофических факторов (например, концентрация BDNF 3 (1.2 пг/мкл, n=9).
Было сделано предположение, что слабый эффект секретома чМСК1x связан с низкой концентрацией биологически активных компонентов внутри секретома, поэтому было проведено расширенное исследование с использованием комбинации чМСК1x, дополненной человеческим BDNF 3.5 нг/мкл (чМСК-B) и 10-кратно концентрированного секретома МСК человека (чМСК10x). Добавление группы чМСК-B к эксперименту связано с ожиданием аддитивного терапевтического эффекта белка BDNF (немедленный эффект) и микровезикул МСК (замедленный эффект) во время длительного процесса восстановления мозга после внутримозгового кровоизлияния.
Секретом чМСК10x способствовал сохранению неврологических показателей (через 10 дней после внутримозгового кровоизлияния) и обеспечивал выживание 100% экспериментальных животных (до 14 дней после внутримозгового кровоизлияния), в то время как в группе отрицательного контроля (контроль) 30% животных погибли, а 20% животных имели тяжелый неврологический дефицит (через 10 дней после внутримозгового кровоизлияния) [p<0,01; n (10; двусторонний точный тест Фишера] (Фиг. 2). Снижение выраженности неврологического дефицита без значительного увеличения выживаемости (80%) наблюдалось в экспериментальной группе чМСК-B (а также в группах BDNF и чМСК1x).
По данным МРТ-исследования достоверных различий в объеме поражения головного мозга в экспериментальных группах по сравнению с контролем не выявлено. В группе чМСК1x наблюдали тенденцию к уменьшению, а в группе чМСК10x - тенденцию к увеличению объема поражения головного мозга через 11 дней после внутримозгового кровоизлияния: 70.1 (53.5; 155.8) мм3 и 261.4 (232.0; 337.4) мм3, соответственно, против 176.6 (138.5; 201.5) мм3 в контрольной группе (Фиг. 3). Однако значительная разница в размере объема поражения наблюдалась между группами чМСК1x и чМСК10x [р<0.05; n (8; ANOVA on ranks].
Окрашивание гематоксилином-эозином срезов головного мозга, в области повреждения, показало аналогичное результатам МРТ распределение размеров поражения головного мозга по группам (Фиг. 4). Существенной разницы между группами не наблюдалось, хотя, как и в исследовании МРТ, участок поражения имел тенденцию к уменьшению в группах чМСК1x и чМСК-B: 4.9% (3.9%; 6.2%) и 6.6% (2.8%; 7.7%), соответственно, против 9.8% (6.6%; 13.4%) в контрольной группе [р=0.220; n=5; ANOVA on ranks].
Окрашивание срезов мозга гематоксилин-эозином и по Нисслю также подтвердило наличие микроскопических признаков повреждения ткани головного мозга: некроза, ишемии, отека, глиального рубца, нейтрофильной инфильтрации и застоя крови в капиллярном русле (Фиг. 5 и 6). Признаки повреждения были более выражены в контрольной группе, но количественный анализ не проводился. Окраска берлинской лазурью (по Перлсу) позволила выявить отложения гемосидерина (синего цвета) в ткани мозга, прилегающей к участку поражения, во всех группах, но они были менее выражены в контрольной группе и группе чМСК10x (Фиг. 6). Было предположено, что это обусловлено расширением очага повреждения в контрольной группе и группе чМСК10x, что привело к поглощению отложений гемосидерина некротическими массами.
Иммуногистохимическое окрашивание срезов мозга на CD68, маркер провоспалительных клеток M1-микроглии и маркер лизосомальной активности, выявило его значительно более высокое представительство в срезах мозга группы чМСК10x: так в данной группе область, окрашенная специфически CD68, занимает на срезах мозга 18.0% (6.5%; 25.6%) против 5.9%. % (5.0%; 7.4%) в контрольной группе [р<0.05; n (9; ANOVA on ranks] (Фиг. 7А). Не наблюдалось значительной разницы в площади, окрашенной антителами к CD68, в группах BDNF, чМСК1x и чМСК-B по сравнению с Контролем, хотя наблюдалась тенденция к увеличению количества клеток CD68+в этих группах.
Окрашивание на CD163, маркер клеток M2-микроглии, показало заметное (но не статистически значимое) снижение уровня CD163+клеток в группе чМСК10x - 1.7% (0.6%; 5.3%) по сравнению с 9.7% (4.6%; 15.0%) в контрольной группе [р=0.052; n (8; ANOVA on ranks] (Фиг. 7Б). Аналогичное снижение наблюдалось в группах BDNF, чМСК1x и чМСК-B, однако они существенно не отличались от контрольной группы.
Поскольку площадь срезов, специфически окрашенная антителами к CD68, в группе чМСК10x была значительно выше, чем в других группах, и коррелировала с объемом поражения головного мозга согласно МРТ и гистохимическим исследованиям, было предположено, что этот негативный эффект связан с действием отдельных компонентов секретома ксеногенных (человеческих) МСК. Чтобы проверить эту гипотезу, был изучен потенциальный терапевтический эффект аллогенного секретома МСК крыс кМСК10x и сравнили его эффективность с таковой ксеногенного секретома МСК человека чМСК10x. Выявлено, что секретом кМСК10x обеспечивает 100% выживаемость и отличное неврологическое восстановление животных после внутримозгового кровоизлияния, как и секретом чМСК10x [p<0.01 (n=10) для чМСК10x по сравнению с контролем; p<0.0005 (n=18) для кМСК10x по сравнению с контролем; двусторонний точный тест Фишера] (Фиг. 8). Согласно МРТ-исследованию, секретом кМСК10x эффективно уменьшал объем поражения головного мозга, в отличие от чМСК10x: 90.2 (48.3; 144.3) мм3 для кМСК10x против 261.4 (232.0; 337.4) мм3 для чМСК10x [р<0.005; n (8; ANOVA on ranks]. Аналогичные результаты были получены при гистологическом исследовании головного мозга крыс: площадь повреждения головного мозга в группе кМСК10x была значительно меньше (3.9% (2.6%; 4.2%)), чем в контрольной группе (9.8% (6.6%; 13.4%)). [р<0.05; n=5; ANOVA on ranks] (Фиг. 8).
Это уменьшение размера поражения также коррелировало со снижением иммуноокрашивания CD68 в срезах мозга крыс кМСК10x: 5.6% (1.1%; 7.7%) [p<0.005 для кМСК10x по сравнению с чМСК10x; n (9; ANOVA on ranks] (Фиг. 7А). Окрашивание CD163 в срезах крыс кМСК10x существенно не отличалось от других групп: 5.3% (2.2%; 5.5%) [р=0.06; n (8; ANOVA on ranks] (Фиг. 7Б).
По результатам данного исследования было установлено, что секретомы МСК человека и крысы, сконцентрированные в 10 раз, обладают выраженной нейропротективной и нейротрофической активностью (по показателям выживаемости, неврологического статуса), однако, ксеногенные компоненты секретома МСК (в данном случае - секретом МСК человека) способны вызывать гиперактивацию иммунных клеток, что приводит к разрастанию очага повреждения и в перспективе может привести к снижению выживаемости и прогрессированию неврологических дефицитов. В то же время, применение аллогенного секретома (в данном случае - секретом МСК крыс) приводит к уменьшению объема очага повреждения по данным МРТ и гистологического исследования и не приводит к гиперактивации иммунных клеток, окружающих область повреждения, что вкупе с прекрасной выживаемостью и предотвращением развития неврологических дефицитов соответствует позитивному прогнозу терапии геморрагического инсульта с помощью введения аллогенного секретома МСК, сконцентрированного в 10 раз (в дозе 15 мкг/кг по белку) - вариант композиции 5, в область кровоизлияния. Остальные варианты композиций не позволяют добиться желаемого терапевтического эффекта, что проявляется в более низкой выживаемости животных (по сравнению с действием варианта композиции 5), худшим восстановлением неврологических показателей, большем очаге повреждения по данным МРТ и гистологического исследования. Стоит обратить особое внимание на эффект вариантов композиций 4 (ксеногенный секретом МСК клеток человека) и 5 (аллогенный секретом МСК клеток человека): терапевтическая эффективность данных вариантов по показателям выживаемости экспериментальных животных и восстановлению неврологического статуса практически идентична, но размер очага повреждения в группе с ксеногенным секретомом выше, что согласно нашим данным (увеличение экспрессии CD68 и снижение экспрессии CD163), а также данным литературы обусловлено активацией иммунно-компетентных клеток в организме реципиента. Сама по себе композиция 4 способна поляризовать аллогенные иммунные клетки (моноциты и макрофаги периферической крови человека) в противовоспалительный М2-фенотип (см. Пример 6), а наблюдаемый эффект активации микроглии и увеличения очага повреждения в эксперименте in vivo обусловлен иммуногенным действием ксеногенных молекул/белков. Совокупность результатов in vivo и in vitro исследований позволяют предположить высокую терапевтическую активность аллогенной по отношению к человеку композиции 4 при повреждениях мозга.
Пример 5. Метод оценки нейропротективной и нейротрофической активности секретома МСК in vitro.
Для оценки нейропротективной и нейротрофической активности клеточного секретома in vitro клетки нейробластомы SH-SY5Y (ATCC (CRL-2266™)) высевали в 48-луночные планшеты в полную питательную среду (DMEM/F12 с добавлением 10% FBS и 1% пенициллин-стрептомицина (Gibco, США)) в количестве 40000 клеток/лунку в четырех повторах. На следующий день среду удаляли и образцы бессывороточной среды (К+), бессывороточной среды с 3.5 нг / мкл человеческого BDNF (BDNF) или секретома MSC (чМСК1x, чМСК10x, чМСК-B или кМСК10x) (варианты композиций 1, 2, 3, 4, 5 и 6 - см. Пример 1), в каждую добавляли 100 мМ L-глутамата [Nampoothiri, M.; Reddy, N.D.; John, J.; Kumar, N.; Kutty Nampurath, G.; Rao Chamallamudi M. Insulin blocks glutamate-induced neurotoxicity in differentiated SH-SY5Y neuronal cells. Behav Neurol, 2014, 2014, 674164. doi:10.1155/2014/674164] и 5 мкМ реагента для апоптоза IncuCyte(Caspase-3/7 (Essen Bioscience, #4440, США). В контрольной группе (К-) не добавляли L-глутамат, BDNF или секретом MSC, чтобы отслеживать спонтанную гибель клеток в бессывороточной среде. Глутамат вызывает быстрое увеличение цитозольной концентрации Са2+в клетках SH-SY5Y (аналогично тому, что происходит в нейронах) с последующей активацией каспазы. Реагент IncuCyte(Caspase-3/7 для апоптоза, расщепленный активированным Caspase-3/7, окрашивает ядерную ДНК (зеленая флуоресценция). Чтобы контролировать гибель клеток SH-SY5Y, планшет помещали в систему анализа живых клеток Incucyte(ZOOM (Essen Bioscience), расположенную внутри инкубатора с CO2. Покадровую визуализацию девяти полей зрения (фазовый и зеленый канал) каждой лунки выполняли через 1, 3, 6, 12, 24, 48 и 72 часа после замены среды.
Для оценки способности секретомов МСК стимулировать рост нейритов клетки SH-SY5Y высевали в 48-луночные планшеты в полную питательную среду по 40000 клеток/лунку в четырех повторностях. На следующий день среду удаляли и добавляли бессывороточную среду (контроль), бессывороточную среду с 3.5 нг/мкл человеческого BDNF (BDNF) или секретома MSC (чМСК1x, чМСК10x, чМСК-B или кМСК10x). Чтобы контролировать рост нейритов из клеток SH-SY5Y, планшет помещали в систему анализа живых клеток Incucyte(ZOOM (Essen Bioscience), расположенную внутри инкубатора с CO2. Покадровую визуализацию девяти полей зрения каждой лунки выполняли через 0, 6 и 24 часа после замены среды.
Микрофотографии для расчета процента живых клеток (по сравнению с исходным числом клеток) и оценки скорости роста нейритов анализировали с помощью программного обеспечения ImageJ (NIH, США). Клеточные отростки длиной более двух диаметров клеток считались нейритами.
При исследовании нейропротективной и нейротрофической активности секретома МСК in vitro обнаружили, что секретомы чМСК1x, чМСК10x, кМСК10x и чМСК-B поддерживают выживание линии клеток нейробластомы человека SH-SY5Y в условиях нейротоксичности, индуцированной глутаматом (Фиг. 9А и 10). Так, количество живых клеток в группах чМСК1x, чМСК10x, кМСК10x и чМСК-B было значительно выше через 3-24 часа после добавления глутамата, чем в группе положительного контроля «К+» без секретома [p<0.001 по сравнению с контролем (К+); n=12; ANOVA on ranks]. Выживание SH-SY5Y в этих группах было сравнимо с таковым, наблюдаемым в группе положительного контроля BDNF. Не наблюдалось значимых различий в выживаемости SH-SY5Y между группами МСК, за исключением кМСК10x. Его нейропротективная активность была значительно выше по сравнению с группой «К+» и даже по сравнению с чМСК1x, чМСК-B и чМСК10x в определенные моменты времени. Секретомы чМСК1x, чМСК10x и кМСК10x поддерживали выживание SH-SY5Y до 72 часов в нейротоксических условиях: 7% (0%; 9%), 8% (4%; 10%) и 19% (11%; 27%) живых клеток, соответственно. Тогда как в группе «К+» живых клеток через 24 часа эксперимента не наблюдалось. В дополнение к гибели клеток SH-SY5Y, вызванной глутаматом, наблюдалась их спонтанная гибель. Она значительно увеличивалась только через 24 часа после начала эксперимента in vitro - это можно было наблюдать в группе отрицательного контроля «К-» (бессывороточная среда без глутамата).
Изучение динамики роста нейритов SH-SY5Y в течение 24 часов эксперимента показало спонтанный рост нейритов во всех экспериментальных группах. Секретомы чМСК1x, чМСК10x, чМСК-B и кМСК10x увеличивали рост нейритов по сравнению с контрольной группой через 6 часов от момента начала эксперимента, однако разница не была статистически значимой. Только в группе BDNF рост нейритов был значительно выше по сравнению с контрольной группой [р<0.005 по сравнению с контролем; n=5; ANOVA on ranks] (Фиг. 9Б и 11).
Таким образом, в результате исследования нейропротективной и нейротрофической активности секретома МСК in vitro было установлено, что что секретомы чМСК1x, чМСК10x (вариант композиции 4), кМСК10x (вариант композиции 5) и чМСК-B (вариант композиции 3) поддерживают выживание линии клеток нейробластомы человека SH-SY5Y в условиях нейротоксичности, индуцированной глутаматом, но не оказывают достоверного влияния на рост нейритов линии клеток нейробластомы человека SH-SY5Y в течение 24 часов.
Пример 6. Метод оценки способности секретома МСК влиять на активность клеток моноцитарно-макрофагального ряда гематогенного происхождения in vitro.
В модели нейротоксичности, индуцированной глутаматом, in vitro секретомы МСК крыс кМСК10x и человека чМСК10x поддерживают выживание клеток линии нейробластомы человека SH-SY5Y, однако введение этих секретомов оказывает противоположный эффект на объем повреждения в головном мозге: секретом аллогенных крысиных МСК уменьшает объем повреждения, а секретом ксеногенных человеческих МСК приводит к увеличению объема повреждения.
Было предположено, что разница в наблюдаемом эффекте аллогенного и ксеногенного секретомов обусловлена участием некоего иммунного компонента в организме крыс и для этого окрасили срезы мозга после воздействия секретомов МСК крыс и человека антителами к маркеру фагоцитоза CD68 (маркер активированной микроглии). На срезах головного мозга крыс после введения секретома МСК человека наблюдали выраженную экспрессию CD68, маркера фагоцитоза и активации микроглии, в то время как введение секретома МСК крыс такого эффекта не вызывало и уровень экспрессии CD68 в мозгу таких крыс не отличался от контрольных образцов (Фиг. 7А). Таким образом, согласно нашим данным введение секретома ксеногенных клеток, в частности МСК, в мозг может активировать клетки микроглии и процессы фагоцитоза, что может привести к разрастанию очага повреждения, при этом для аллогенного секретома такого негативного эффекта не было обнаружено.
Для оценки способности секретома МСК влиять на активность клеток моноцитарно-макрофагального ряда гематогенного происхождения использовали модель поляризации моноцитов/макрофагов в М1- и М2-фенотип in vitro.
Для этого донорскую кровь (20 мл) собирали в пробирки объемом 50 мл, тщательно и аккуратно перемешивали с 200 мкл 0.5М раствора ЭДТА*К2 (антикоагулянт) и центрифугировали при 400g в течение 10 минут для того, чтобы отделить форменные элементы крови от плазмы. Плазму отбирали, а к осадку клеток добавляли эквивалентный объем стерильного фосфатно-солевого буфера (PBS). Суспензию форменных элементов крови в PBS наслаивали на раствор фиколла с удельной плотностью 1,077 г/мл и затем центрифугировали при 400g в течение 30 минут без активного торможения. На границе разделения фаз фикола и PBS собирали слой мононуклеаров, их отмывали два раза PBS, осаждали центрифугированием и ресуспендировали в среде роста RPMI, содержащей 10% фетальной бычьей сыворотки FBS и 1% раствора антибиотика/антимикотика. Клетки высаживали на культуральные планшеты с высокоадгезионной поверхностью BD Primaria в концентрации 1.5*106 клеток/мл, а планшеты помещали в CO2-инкубатор на 35-40 минут.После окончания времени инкубации, неприкрепившиеся клетки отмывали, а к оставшимся добавляли бессывороточную культуральную среду X-VIVO(15 (Lonza, #BE02-060F) с колониестимулирующим фактором макрофагов (GM-CSF) (SciStore, #PSG030-10) в концентрации 50 нг/мл. Клетки культивировали в течение 8 дней. На 6-й день после выделения популяции моноцитов/макрофагов осуществляли их поляризацию в М1-фенотип путем добавления в среду роста рекомбинантного IFN((R&D Systems, #285-IF-100/CF) человека (50 нг/мл) и липополисахарида (10 нг/мл) (SigmaAldrich, #297-473-0) или в М2-фенотип путем добавления в среду роста рекомбинантных IL-4 (R&D Systems, #204-IL-010/CF) (20 нг/мл) и TGF((Peprotech, #100-21) (20 нг/мл) человека. В часть образцов добавляли секретом МСК человека чМСК10х (вариант композиции 4) до достижения конечной концентрации 1 мкг/мл (по белку) - 1х в среде роста.
Клетки инкубировали в поляризующих средах в течение 48 часов, после чего их снимали с пластика культуральными скребками, окрашивали на маркеры M1- и M2-фенотипов и анализировали состав популяций с помощью проточной цитометрии FACSCantoTM II (BD Biosciences, США). Оценивали также прямое и боковое светорассеяние клеток, для визуализации степени чистоты полученных клеточных популяций. Для оценки эффективности поляризации макрофагов в M1-фенотипа в присутствии или отсутствии CD-008-0045 использовали антитела к маркерам CD80 (BD, #566992) и CD86 (BD, #555660). Для оценки эффективности поляризации макрофагов в M2-фенотип в присутствии или отсутствии секретома МСК человека использовали антитела к маркерам CD206 (BioLegend, #141720) и CD209 (BioLegend, #343006).
Проведенное исследование показало, что добавление в среду культивирования секретома МСК человека достоверно тормозит поляризацию моноцитов/макрофагов в провоспалительный M1-фенотип по сравнению с группой контроля (n=4; p<0.05) (Фиг. 12). Так, в группе без секретома МСК человека (контроль) средняя интенсивность окраски (арифметическое среднее интенсивности сигнала) клеток, поляризованных в M1-фенотип и окрашенных антителами к CD86 (M1) составила 60.3 (53.5;72.1) %, в то время как добавление секретома МСК человека снижало среднюю интенсивность окраски таких клеток до 50.5 (43.4;55.9) %.
Добавление секретома МСК человека в среду культивирования стимулировало поляризацию моноцитов/макрофагов в противовоспалительный M2-фенотип: средняя интенсивность окраски (арифметическое среднее интенсивности сигнала) клеток, поляризованных в M2-фенотип и окрашенных антителами к CD209 (M2) в группе контроля составила 51.8 (18.7;54.1) %, в то время как в группе секретома МСК человека - 68.8 (61.2;72.5) % (n (4) (Фиг. 12).
Таким образом, секретом МСК человека снижает экспрессию маркеров провоспалительного фенотипа (CD80, CD86) и увеличивает экспрессию маркеров противовоспалительного фенотипа (CD206, CD209) на клетках моноцитарно-макрофагального ряда человека in vitro, что свидетельствует об иммуносупрессивной активности секретома МСК (Фиг. 12) в отношении аллогенных иммунных клеток.
Пример 7. Метод оценки нейропротективной и нейротрофической активности секретома МСК при различных способах его введения.
Введение аллогенного секретома МСК непосредственно в очаг кровоизлияния после повреждения стимулирует выживаемость, уменьшает тяжесть неврологических нарушений и приводит к уменьшению очага повреждения, однако этот способ доставки терапевтического препарата практически нереализуем в клинике, поэтому нами была изучена возможность применения клинически релевантных путей введения препарата: интраназального, внутривенного, а также интрактекального (введение в спиномозговой канал).
Для оценки нейропротективной и нейротрофической активности секретома МСК при различных способах его введения использовали описанную выше модель геморрагического инсульта, однако, для этого использовали секретом МСК крыс, сконцентрированный в 50 раз (вариант композиции 6), который вводили крысам интраназально, внутривенно или интратекально (в спинномозговой канал) через 5 минут после моделирования геморрагического инсульта. В исследование были включены 20 животных: по 5 животных в группах внутривенного введения секретома МСК, интраназального введения секретома МСК, интратекального введения секретома МСК, группе контроля (внутривенное введение соответствующего объема пустой среды роста). Ни одна из крыс не была исключена из исследования.
Для интраназального введения наркотизированную крысу после моделирования геморрагического инсульта клали брюхом вверх и в каждую из ноздрей вводили по 40 мкл секретома МСК крыс, сконцентрированного в 50 раз (в дозе 20 мкг/ноздрю (по белку)). Внутривенное введение секретома кМСК50х осуществляли в объеме 100 мкл в хвостовую вену в дозе 150 мкг/кг (по белку) - согласно стандартной методике. Для введения в спинномозговой канал наркотизированную крысу после моделирования геморрагического инсульта помещали на высокий валик спиной вверх, кожу в области поясничного отдела позвоночника разрезали, а секретом кМСК50х в объеме 100 мкл и в дозе 150 мкг/кг (по белку) медленно вводили в спинномозговой канал между позвонками L5-S1.
Для оценки эффективности восстановления структуры и функции головного мозга в зависимости от способа введения лекарственного препарата использовали описанные выше методы: выживаемость, неврологический статус, объем повреждения головного мозга по данным МРТ.
Ввиду небольшой выборки (по 5 животных в группе) во всех группах наблюдали 100% выживаемость, однако на основании результатов неврологического исследования и данных МРТ удалось установить, что наиболее выраженный терапевтический эффект секретома наблюдался при его внутривенном введении (Фиг. 13 и 14). Нейропротективный эффект от внутривенного введения секретома МСК оказался практически таким же выраженным, как и при локальной инъекции секретома МСК крыс в область инсульта - как по результатам неврологического исследования (Фиг. 13), так и по результатам МРТ (n≥5) (Фиг. 14). Интраназальное введение препарата оказало менее выраженный эффект на восстановление структуры и функции головного мозга после инсульта и сопровождалось значительными разбросами показателей среди животных, что, по-видимому, связано с трудностями дозирования и удержания препарата в носовой полости. Интратекальное введение препарата не оказало эффекта на восстановление структуры и функции головного мозга, что, по-видимому, обусловлено током спинномозговой жидкости в каудальном направлении.
Таким образом, в результате оценки нейропротективной и нейротрофической активности секретома МСК при различных способах его введения было установлено, что нейропротективная, противовоспалительная и прорегенераторная активность секретома МСК в наибольшей степени проявляется при внутривенном или интраназальном его введении.
Пример 8. Метод оценки нейропротективной и нейротрофической активности секретома МСК в зависимости от сроков его введения после инсульта.
Принципиально важным шагом для перехода к практическому использованию секретома в лечении инсультов является установление терапевтической эффективности секретома в зависимости от времени его применения после геморрагического инсульта (так называемое, «терапевтическое окно»). Для этого нами была изучена эффективность внутривенного и интраназального введения секретома МСК через 1, 3 и 6 часов после геморрагического инсульта на описанной выше модели геморрагического инсульта. Секретом МСК крыс, сконцентрированный в 50 раз (вариант композиции 6), вводили интраназально (в дозе 20 мкг/ноздрю (по белку)) или внутривенно (в дозе 150 мкг/кг (по белку)) через 1, 3 или 6 часов после моделирования геморрагического инсульта. В исследование были включены 21 животных (7 групп по 3 животных в каждой: интраназальное введение через 1 или 3 или 6 часов после моделирования геморрагического инсульта, внутривенное введение через 1 или 3 или 6 часов после моделирования геморрагического инсульта, группа контроля (внутривенное введение соответствующего объема пустой среды роста через 1 час после моделирования геморрагического инсульта). Ни одна из крыс не была исключена из исследования.
Для оценки эффективности восстановления структуры и функции головного мозга в зависимости от сроков введения лекарственного препарата использовали описанные выше методы: выживаемость, неврологический статус, объем повреждения головного мозга по данным МРТ.
По результатам неврологического исследования секретом МСК оказывал нейропротективный эффект даже через 6 часов после инсульта (при внутривенном введении), что выражалось в снижении тяжести неврологических нарушений у экспериментальных животных (Фиг. 15). Однако, по данным МРТ наблюдается снижение нейропротективной активности секретома МСК с увеличением срока введения от момента инсульта. Наименьший объем очага инсульта наблюдается при внутривенном введении секретома МСК через 1 час после инсульта (Фиг. 16).
Таким образом, в результате оценки нейропротективной и нейротрофической активности секретома МСК в зависимости от сроков его введения после инсульта было установлено, что наилучший терапевтический эффект достигается при введении первой дозы препарата в период 6 часов и менее от момента острого нарушения мозгового кровообращения по геморрагическому типу.
Пример 9. Метод оценки нейропротективной и нейротрофической активности секретома МСК в зависимости от дозы при внутривенном введении
Для оценки нейропротективной и нейротрофической активности секретома МСК в зависимости от дозы при внутривенном введении использовали описанную выше модель геморрагического инсульта, а препарат вводили внутривенно (в дозах 5х, 10х, 25х, 50х - 15-150 мкг/кг (по белку)) через 1 час после моделирования геморрагического инсульта в объеме 100 мкл. Дозы 5х, 10х и 25х были получены разведением секретома МСК 50х (вариант композиции 6) в среде DMEM с низким соодержанием глюкозы и без фенолового красного и без фетальной бычьей сыворотки (FBS). В исследование были включены 20 животных: (5 групп по 4 крысы в каждой: дозировки 15, 30, 75, 150 мкг/кг (по белку) и группа контроля (внутривенное введение соответствующего объема пустой среды роста через 1 час после моделирования геморрагического инсульта)). Ни одна из крыс не была исключена из исследования.
Для оценки эффективности восстановления структуры и функции головного мозга в зависимости от дозы при внутривенном введении использовали описанные выше методы: выживаемость, неврологический статус, объем повреждения головного мозга по данным МРТ.
Во всех экспериментальных группах выживаемость составила 100% (по 4 животных в группе). По результатам неврологического исследования тяжелые неврологические нарушения наблюдались у 25% животных (1 крыса из 4) из группы контроля и 25% (1 крыса из 4) из группы 50х. Легкие неврологические нарушения наблюдались у 25% животных (1 крыса из 4) из группы контроля, остальные животные - визуально здоровы. По данным МРТ наилучший терапевтический эффект наблюдается при использовании секретома МСК крыс в дозах 5x-10x - 15-30 мкг/кг (по белку), а по результатам снижения тяжести неврологических нарушений в дозах 5x-25x - 15-75 мкг/кг (по белку) (Фиг. 17).
Таким образом, в результате оценки нейропротективной и нейротрофической активности секретома МСК в зависимости от дозы при внутривенном введении на модели геморрагического инсульта у крыс было установлено, что наилучший терапевтический эффект достигается при внутривенном введении секретома МСК в диапазоне доз 5x-10x - 15-75 мкг/кг (по белку)). Диапазон терапевтических доз при клиническом применении заявляемых композиции и средства на его основе должен быть установлен дополнительно, поскольку сильно зависит от объема повреждения, локализации и тяжести инсульта, а также пути введения и времени введения после инсульта.
Заявляемое лекарственное средство обладает комплексным действием, по крайней мере, на нейроны, клетки микро- и макроглии, клетки моноцитарно/макрофагального звена гематогенного происхождения, как на ключевых участников повреждения нервной ткани.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Федеральное государственное бюджетное образовательное
учреждение высшего профессионального образования
"Московский государственный университет имени М.В.Ломоносова" (МГУ)
<120> КОМПОЗИЦИЯ ДЛЯ НЕЙРОПРОТЕКЦИИ И СТИМУЛЯЦИИ НЕЙРОРЕГЕНЕРАЦИИ
ГОЛОВНОГО МОЗГА ПОСЛЕ ПОВРЕЖДЕНИЯ, СРЕДСТВО НА ЕЕ ОСНОВЕ,
СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
<160> SEQ ID NО:1
<210> 1
<211> 21
<212> human microRNA
<213> natural sequence
<223> miR-23a-3p
<400> 1
1 aucacauugc cagggauuuc c
<160> SEQ ID NО:2
<210> 2
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-101-5p
<400> 2
1 caguuaucac agugcugaug cu
<160> SEQ ID NО:3
<210> 3
<211> 21
<212> human microRNA
<213> natural sequence
<223> miR-101-3p
<400> 3
1 uacaguacug ugauaacuga a
<160> SEQ ID NО:4
<210> 4
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-146a-5p
<400> 4
1 ugagaacuga auuccauggg uu
<160> SEQ ID NО:5
<210> 5
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-146a-3p
<400> 5
1 ccucugaaau ucaguucuuc ag
<160> SEQ ID NО:6
<210> 6
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-491-5p
<400> 6
1 aguggggaac ccuuccauga gg
<160> SEQ ID NО:7
<210> 7
<211> 23
<212> human microRNA
<213> natural sequence
<223> miR-19b-1-5p
<400> 7
1 aguuuugcag guuugcaucc agc
<160> SEQ ID NО:8
<210> 8
<211> 23
<212> human microRNA
<213> natural sequence
<223> miR-19b-3p
<400> 8
1 ugugcaaauc caugcaaaac uga
<160> SEQ ID NО:9
<210> 9
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-21-5p
<400> 9
1 uagcuuauca gacugauguu ga
<160> SEQ ID NО:10
<210> 10
<211> 21
<212> human microRNA
<213> natural sequence
<223> miR-21-3p
<400> 10
1 caacaccagu cgaugggcug u
<160> SEQ ID NО:11
<210> 11
<211> 21
<212> human microRNA
<213> natural sequence
<223> miR-25-5p
<400> 11
1 aggcggagac uugggcaauu g
<160> SEQ ID NО:12
<210> 12
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-25-3p
<400> 12
1 cauugcacuu gucucggucu ga
<160> SEQ ID NО:13
<210> 13
<211>22
<212> human microRNA
<213> natural sequence
<223> miR-125b-5p
<400> 13
1 ucccugagac ccuaacuugu ga
<160> SEQ ID NО:14
<210> 14
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-125b-3p
<400> 14
1 acggguuagg cucuugggag cu
<160> SEQ ID NО:15
<210> 15
<211> 22
<212> human microRNA
<213> natural sequence
<223> miR-126a-3p
<400> 15
1 ucguaccgug aguaauaaug cg<160> SEQ ID NО:16
<210> 1
<211> 21
<212> rat microRNA
<213> natural sequence
<223> miR-23a-3p
<400> 1
1 AUCACAUUGC CAGGGAUUUC C
<160> SEQ ID NО:17
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-101-5p
<400> 1
1 UCAGUUAUCA CAGUGCUGAU GC
<160> SEQ ID NО:18
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-101-3p
<400> 1
1 UACAGUACUG UGAUAACUG AA
<160> SEQ ID NО:19
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-146a-5p
<400> 1
1 UGAGAACUGA AUUCCAUGGG UU
<160> SEQ ID NО:20
<210> 1
<211> 21
<212> rat microRNA
<213> natural sequence
<223> miR-146a-3p
<400> 1
1 ACCUGUGAAG UUCAGUUCUU U
<160> SEQ ID NО:21
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-19b-5p
<400> 1
1 AGUUUUGCAG GUUUGCAUCC AG
<160> SEQ ID NО:22
<210> 1
<211> 23
<212> rat microRNA
<213> natural sequence
<223> miR-19b-3p
<400> 1
1 UGUGCAAAUC CAUGCAAAAC UGA
<160> SEQ ID NО:23
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-21-5p
<400> 1
1 UAGCUUAUCA GACUGAUGUU GA
<160> SEQ ID NО:24
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-21-3p
<400> 1
1 CAACAGCAGU CGAUGGGCUG UC
<160> SEQ ID NО:25
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-25-5p
<400> 1
1 AGGCGGAGAC ACGGGCAAUU GC
<160> SEQ ID NО:26
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-25-3p
<400> 1
1 CAUUGCACUU GUCUCGGUCU GA
<160> SEQ ID NО:27
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-125b-5p
<400> 1
1 UCCCUGAGAC CCUAACUUGU GA
<160> SEQ ID NО:28
<210> 1
<211> 22
<212> rat microRNA
<213> natural sequence
<223> miR-125b-3p
<400> 1
1 ACGGGUUAGG CUCUUGGGAG CU
<160> SEQ ID NО:29
<210> 1
<211> 21
<212> rat microRNA
<213> natural sequence
<223> miR-126a-3p
<400> 1
1 CAUUAUUACU UUUGGUACGC G
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ФИБРОЗА ТКАНЕЙ НА ОСНОВЕ КОМПОНЕНТОВ СЕКРЕТОМА МЕЗЕНХИМНЫХ СТРОМАЛЬНЫХ КЛЕТОК, СПОСОБ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ СРЕДСТВА | 2020 |
|
RU2766707C1 |
| БИОМАРКЕРЫ ТРАВМАТИЧЕСКОГО ПОВРЕЖДЕНИЯ ГОЛОВНОГО МОЗГА | 2017 |
|
RU2771757C2 |
| Способ получения глиальных производных индуцированных плюрипотентных стволовых клеток с повышенной экспрессией BDNF для терапии ишемического инсульта | 2023 |
|
RU2829361C1 |
| ВАРИАНТЫ РЕКОМБИНАНТНЫХ AAV И ИХ ПРИМЕНЕНИЯ | 2015 |
|
RU2738421C2 |
| СПОСОБЫ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ СОСТОЯНИЙ С ПРИМЕНЕНИЕМ ГЕМАТОПОЭТИЧЕСКИХ ФАКТОРОВ РОСТА | 2003 |
|
RU2353385C2 |
| Способ получения кондиционной среды, обладающей регенераторным потенциалом, для интраназального введения при лечении заболеваний центральной нервной системы | 2016 |
|
RU2637407C1 |
| ПРИМЕНЕНИЕ СТВОЛОВЫХ КЛЕТОК, ЭКСПРЕССИРУЮЩИХ МЕЗЕНХИМАЛЬНЫЕ И НЕЙРОНАЛЬНЫЕ МАРКЕРЫ, И ИХ КОМПОЗИЦИЙ ДЛЯ ЛЕЧЕНИЯ НЕВРОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ (ВАРИАНТЫ) | 2017 |
|
RU2742828C2 |
| СПОСОБ ЛЕЧЕНИЯ ИНСУЛЬТА | 2004 |
|
RU2283121C2 |
| Рекомбинантная плазмидная ДНК, кодирующая микроРНК hsa-mir-143-3p, и ее применение в качестве положительного контроля при ПЦР-РВ для диагностики сердечно-сосудистых заболеваний и выявления риска их развития | 2025 |
|
RU2837882C1 |
| СТВОЛОВЫЕ КЛЕТКИ, ЭКСПРЕССИРУЮЩИЕ МЕЗЕНХИМАЛЬНЫЕ И НЕЙРОНАЛЬНЫЕ МАРКЕРЫ, ИХ КОМПОЗИЦИИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ | 2017 |
|
RU2741839C2 |
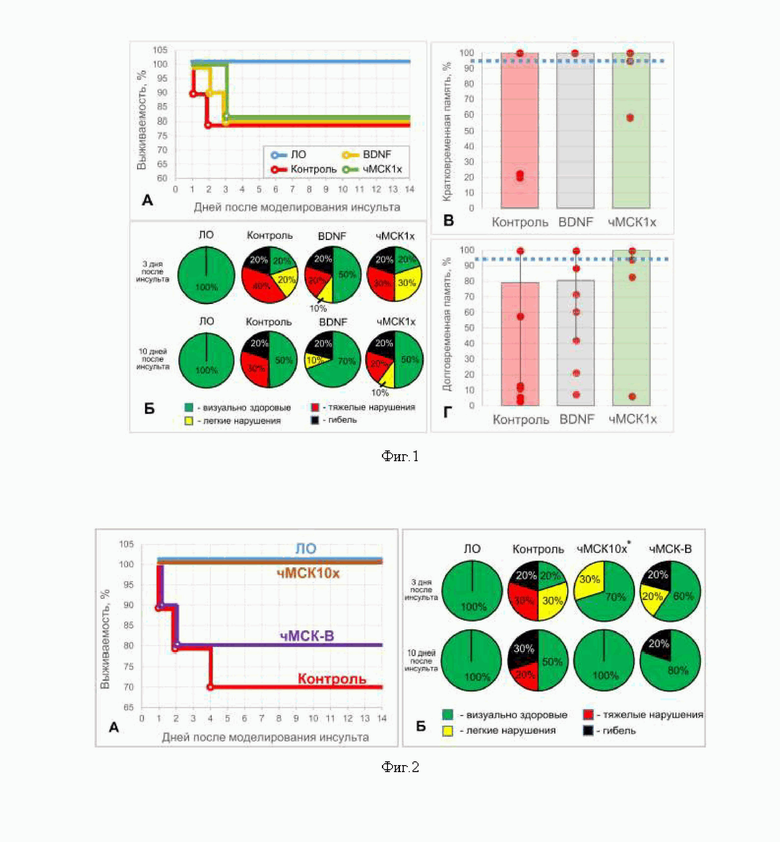
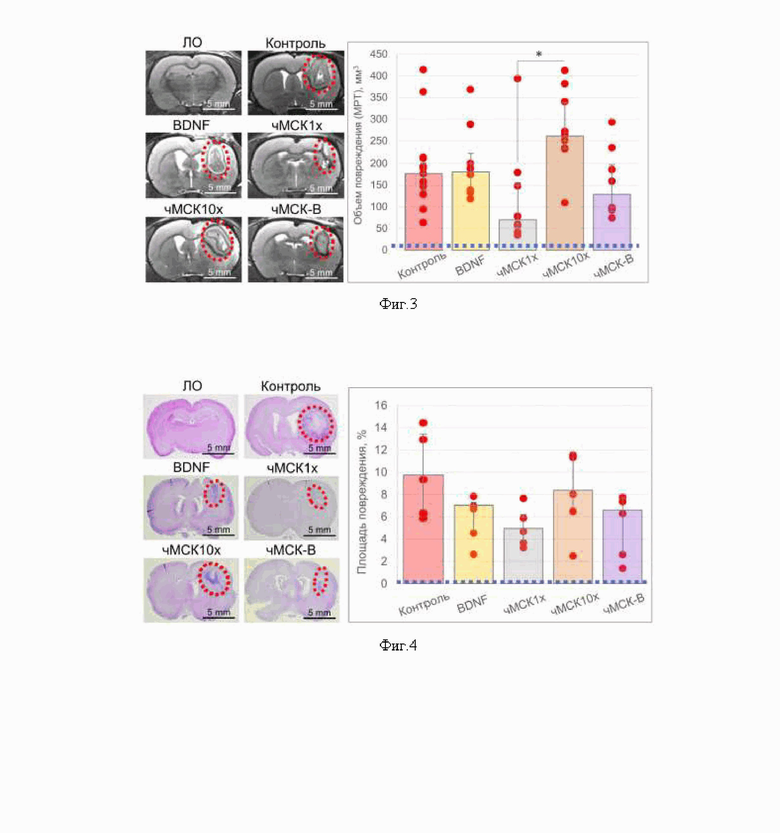
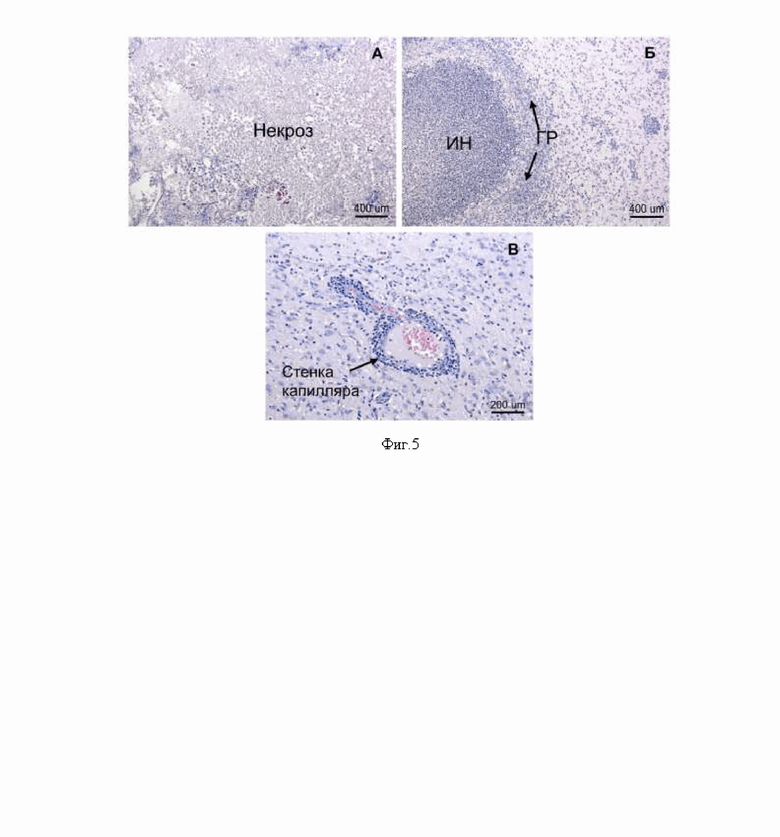
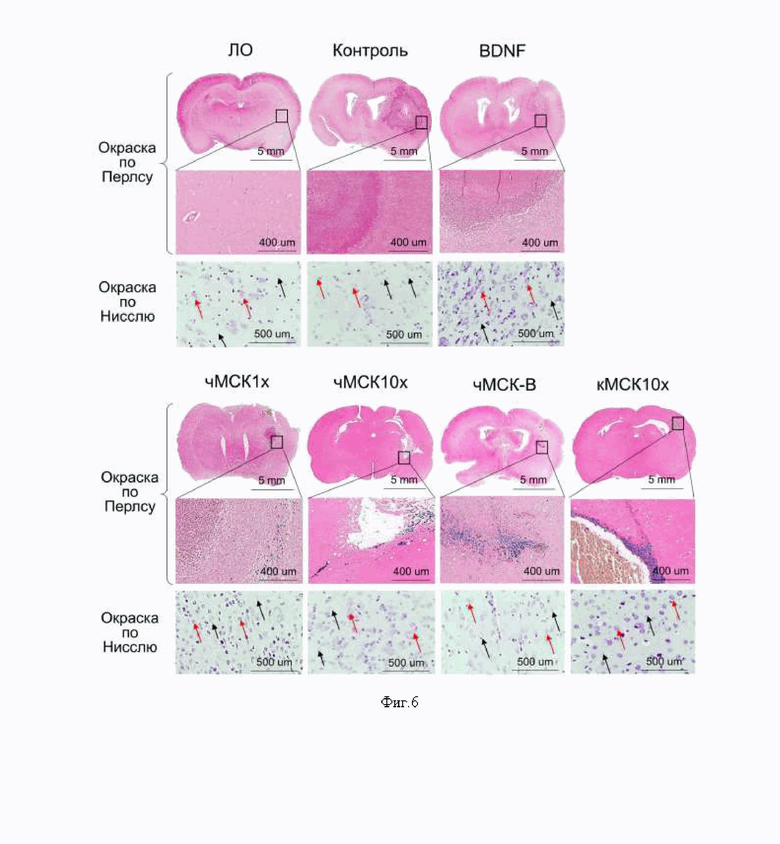

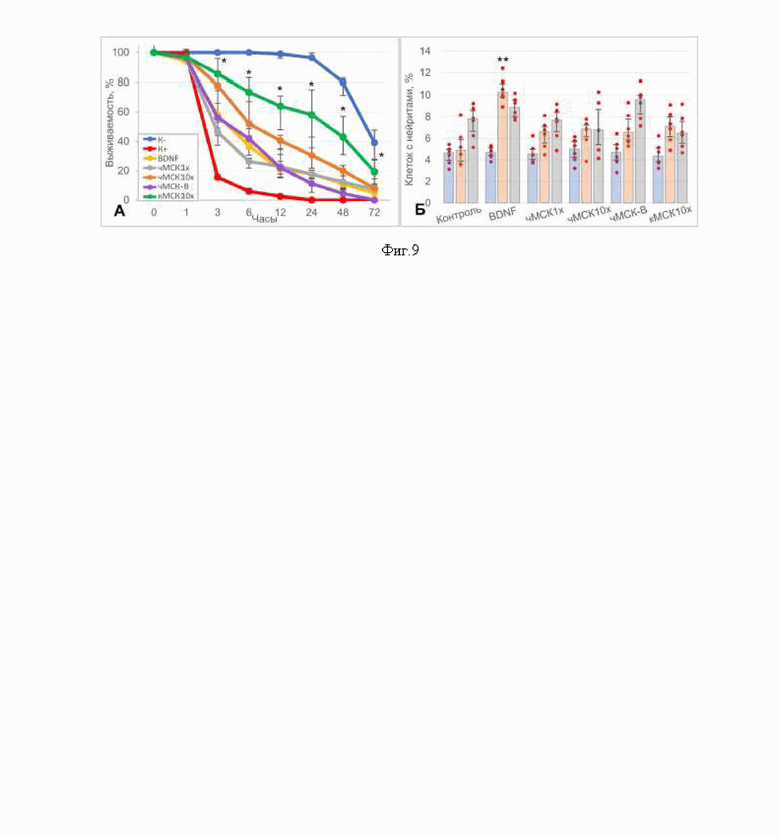

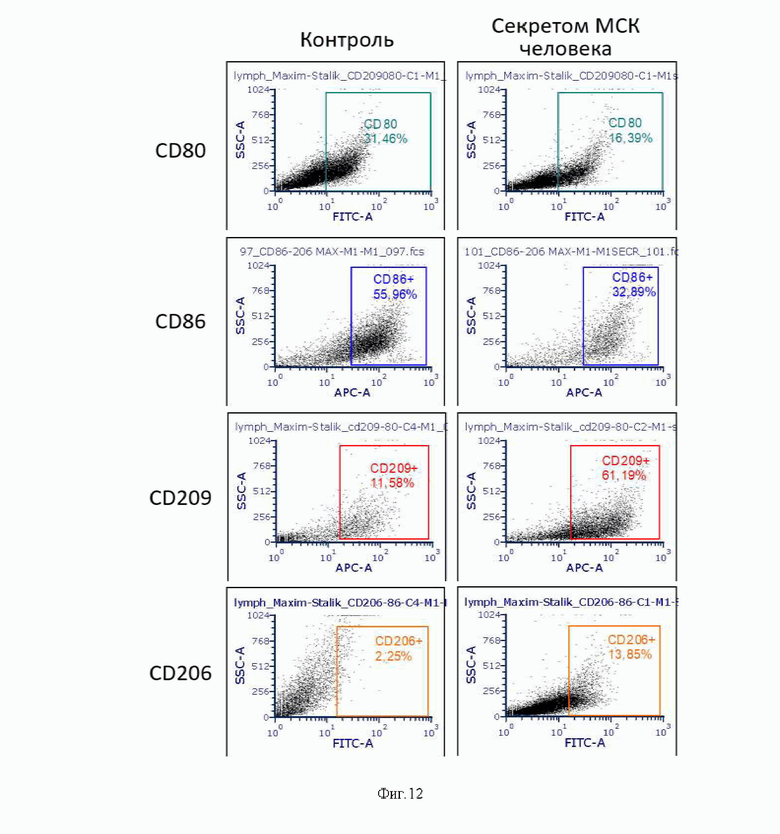

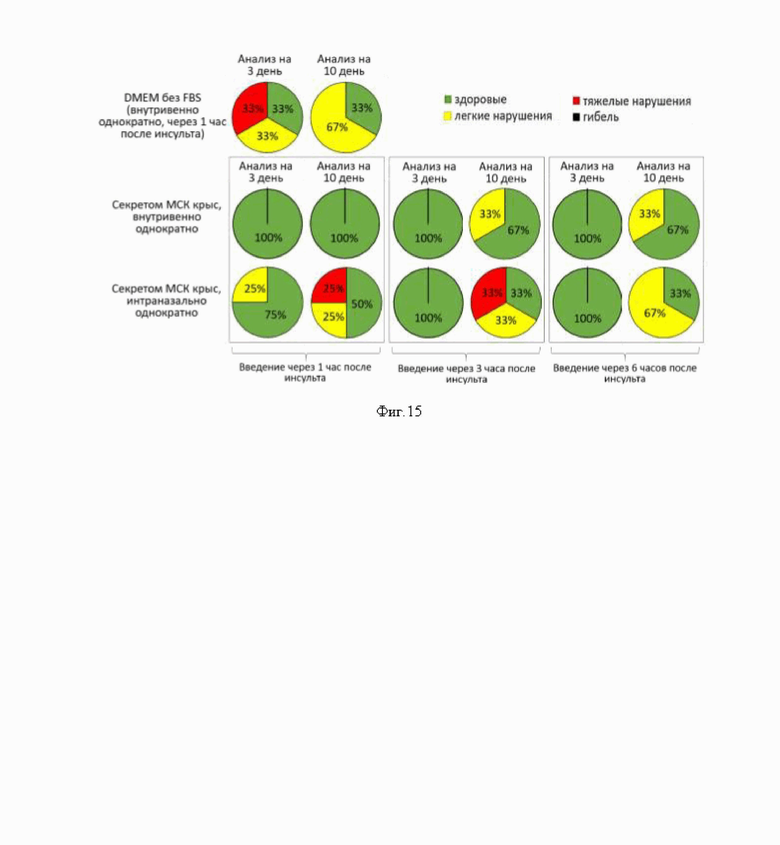
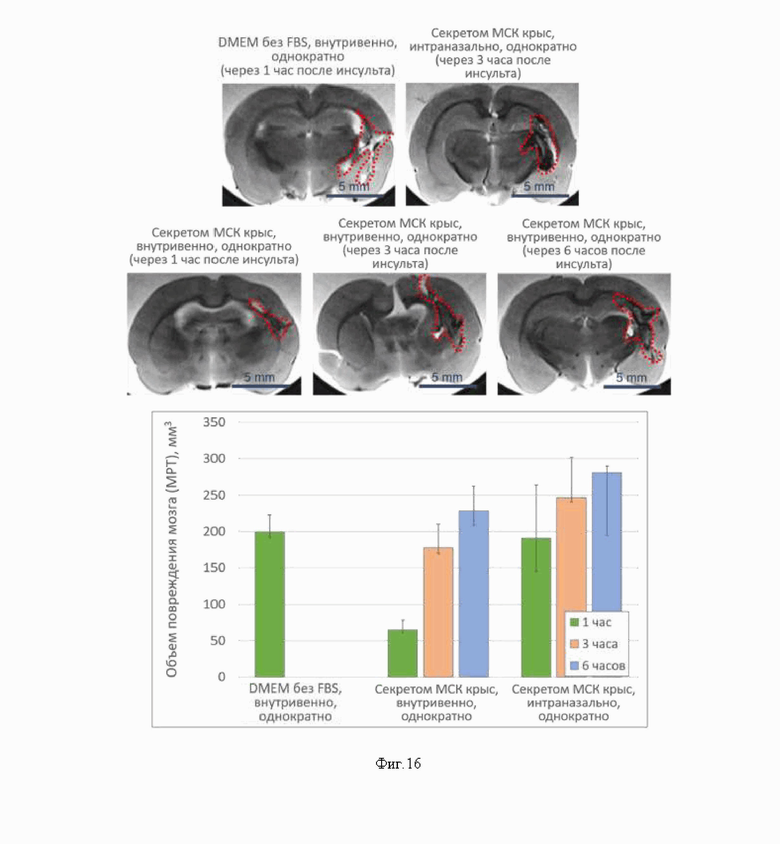
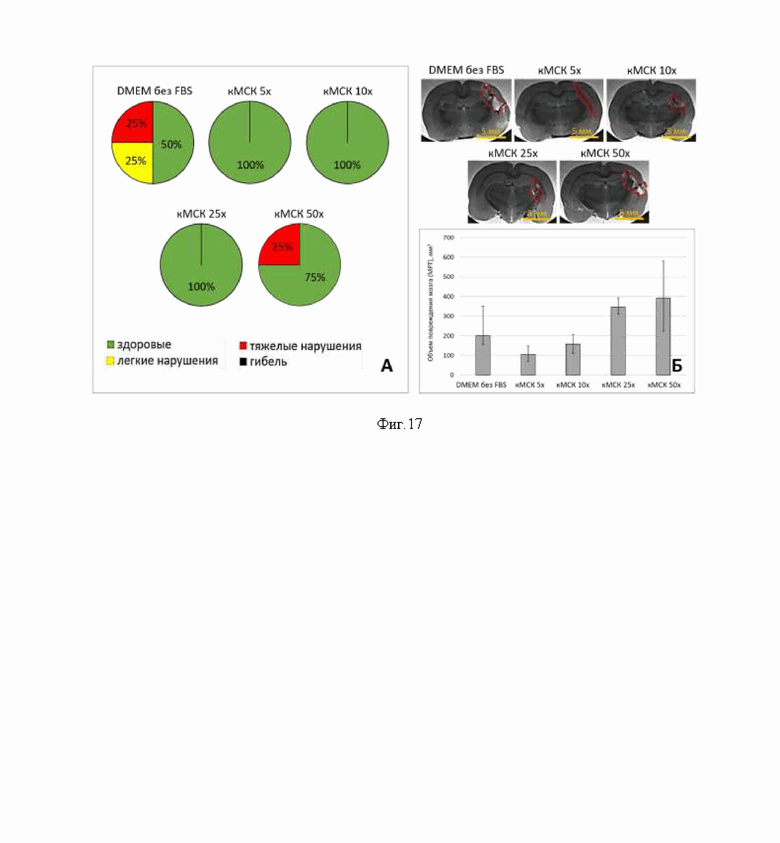
Группа изобретений относится к области медицины и фармакологии и может быть использована для получения и применения лекарственных средств и биоматериалов для нейропротекции и стимуляции регенерации ткани мозга после повреждений различного генеза. Предлагается композиция для нейропротекции и стимуляции нейрорегенерации головного мозга на основе компонентов секретома мезенхимных стромальных клеток (МСК) человека, характеризующаяся наличием факторов роста и цитокинов в культуральной среде, включая BDNF в количестве не менее 3 нг/мл, GDNF – не менее 0,03 нг/мл, VEGF – не менее 0,2 нг/мл, HGF – не менее 0,15 нг/мл, uPA – не менее 0,34 нг/мл и TGFb – не менее 0,055 нг/мл, а также применение указанной композиции в качестве средства, предотвращающего глутамат-опосредованную гибель нейральных клеток, стимулирующего поляризацию клеток моноцитарно-макрофагального звена в противовоспалительном направлении (M2-фенотип), предотвращающего активацию клеток микроглии. Способ получения композиции включает культивирование и кондиционирование первично выделенных из жировой ткани аллогенных МСК человека в течение 2–5 пассажей в среде роста Игла, модифицированной Дульбекко (DMEM) с содержанием глюкозы не более 1 г/л без фенолового красного с добавлением пенициллина/стрептомицина, растворов незаменимых аминокислот и витаминов, в течение 72–144 ч, отбор и очистку среды культивирования от остатков клеток, концентрирование и очищение указанной среды с получением стерильного концентрата. Предлагается также средство для нейропротекции и стимуляции нейрорегенерации, включающее указанную композицию в терапевтически эффективном количестве и вспомогательные компоненты, и способ стимуляции нейропротекции и регенерации головного мозга после повреждения, включающий введение указанных выше композиции или средства в организм человека в терапевтически эффективном количестве. Технический результат: снижение тяжести неврологических нарушений в течение 14 дней после моделирования инсульта у экспериментальных животных, и уменьшение объема повреждения головного мозга в среднем в 2 раза по данным МРТ и гистологического исследования по сравнению с группой контроля (без композиции), а также снижение активации клеток микроглии до базального уровня в модели острого нарушения мозгового кровообращения по геморрагическому типу в эксперименте in vivo. 5 н. и 19 з.п. ф-лы, 17 ил., 9 пр.
1. Композиция для нейропротекции и стимуляции нейрорегенерации головного мозга на основе компонентов секретома мезенхимных стромальных клеток (МСК) человека, характеризующаяся наличием факторов роста и цитокинов в культуральной среде, включая BDNF в количестве не менее 3 нг/мл, GDNF - не менее 0.03 нг/мл, VEGF - не менее 0.2 нг/мл, HGF - не менее 0.15 нг/мл, uPA - не менее 0.34 нг/мл и TGFb - не менее 0.055 нг/мл.
2. Композиция по п. 1, характеризующаяся тем, что содержание TGFb указано суммарно по изоформам TGFb1, TGFb2 и TGFb3.
3. Композиция по п. 1, характеризующаяся тем, что она дополнительно содержит противовоспалительные цитокины, включая антагонист рецептора IL-1 IL-1Ra в количестве не менее 0.4 нг/мл, IL-4 - не менее 0.08 нг/мл, IL-6 - не менее 1 нг/мл, IL-10 - не менее 0.01 нг/мл, IL-11 - не менее 0.4 нг/мл, IL-13 - не менее 0.7 пг/мл, и молекулы, обладающие противовоспалительным эффектом, включая IDO - не менее 0.08 нг/мл, растворимые формы рецепторов IL-1 - не менее 0.01 нг/мл и TNF - не менее 0.01 нг/мл.
4. Композиция по п. 1, характеризующаяся тем, что она дополнительно содержит микроРНК hsa-miR-23a-3p, hsa-miR-101, hsa-miR-146a, hsa-miR-491-5p, hsa-miR-19b, hsa-miR-21, hsa-miR-25, hsa-miR-125b, hsa-miR-126a-3p.
5. Композиция по п. 4, характеризующаяся тем, что используют микроРНК hsa-miR-23a-3p с последовательностью SEQ ID NO: 1, hsa-miR-101 - SEQ ID NO: 2 и/или SEQ ID NO: 3, hsa-miR-146a - SEQ ID NO: 4 и/или SEQ ID NO: 5, hsa-miR-491-5p - SEQ ID NO: 6, hsa-miR-19b - SEQ ID NO: 7 и/или SEQ ID NO: 8, hsa-miR-21 - SEQ ID NO: 9 и/или SEQ ID NO: 10, hsa-miR-25 - SEQ ID NO: 11 и/или SEQ ID NO: 12, hsa-miR-125b - SEQ ID NO: 13 и/или SEQ ID NO: 14, hsa-miR-126a-3p - SEQ ID NO: 15.
6. Композиция по п. 1, характеризующаяся тем, что представляет собой концентрированный раствор цитокинов и факторов роста в культуральной среде, замороженный или лиофильно высушенный раствор.
7. Применение композиции по п. 1 в качестве средства, предотвращающего глутамат-опосредованную гибель нейральных клеток, стимулирующего поляризацию клеток моноцитарно-макрофагального звена в противовоспалительном направлении (M2-фенотип), предотвращающего активацию клеток микроглии.
8. Способ получения композиции по п. 1, характеризующийся тем, что включает культивирование и кондиционирование первично выделенных аллогенных мезенхимных стромальных клеток (МСК) человека, выделенных из жировой ткани, в течение 2–5 пассажей в среде роста Игла, модифицированной Дульбекко (DMEM) с содержанием глюкозы не более 1 г/л без фенолового красного с добавлением пенициллина/стрептомицина, растворов незаменимых аминокислот и витаминов, в течение 72-144 ч, отбор и очистку среды культивирования от остатков клеток, концентрирование среды культивирования до, по меньшей мере, 10-кратного уменьшения исходного объема, очищение среды культивирования с получением стерильного концентрата.
9. Способ по п. 8, характеризующийся тем, что стерильный концентрат замораживают при температуре от минус 80°С до минус 18°С или лиофильно высушивают.
10. Способ по п. 8, характеризующийся тем, что лиофильную сушку проводят в 6-10 стадий при давлении 0.013-0.027 кПа, температуре от минус 45°С до 25°С, время лиофилизации составляет не более 24 часов при максимальной загрузке лиофильной сушки.
11. Способ по п. 8, характеризующийся тем, что культивирование МСК и кондиционирование среды проводят при содержании кислорода 1-21 об.%.
12. Средство для нейропротекции и стимуляции нейрорегенерации, включающее композицию по п. 1 в терапевтически эффективном количестве и вспомогательные компоненты.
13. Средство по п. 12, характеризующееся тем, что в качестве вспомогательных компонентов использованы терапевтические приемлемые добавки, наполнители, изотонические агенты, стабилизаторы и/или консерванты.
14. Средство по п. 12, характеризующееся тем, что дополнительно содержит альбумин человека в количестве не менее 5 мкг/мл.
15. Средство по п. 12, характеризующееся тем, что представляет собой концентрированный раствор цитокинов и факторов роста в культуральной среде, замороженный или лиофильно высушенный раствор.
16. Способ стимуляции нейропротекции и регенерации головного мозга после повреждения, включающий введение композиции по п. 1 или средства по п. 12 в организм человека в терапевтически эффективном количестве.
17. Способ по п. 16, характеризующийся тем, что композицию или средство вводят локально в область повреждения головного мозга, интраназально, внутривенно струйно или капельно, интратекально (в спинномозговой канал).
18. Способ по п. 16, характеризующийся тем, что композицию или средство вводят однократно или многократно в течение одного или нескольких дней с равными интервалами в течение первых трех недель после повреждения головного мозга.
19. Способ по п. 16, характеризующийся тем, что в острейшей фазе повреждения головного мозга композицию или средство вводят не позднее 6 часов от момента повреждения, в острой фазе повреждения головного мозга композицию или средство вводят в период от 6 до 120 часов от момента повреждения, в подострой фазе повреждения головного мозга композицию или средство вводят в период от 5 до 21 суток от момента повреждения.
20. Способ по п. 16, характеризующийся тем, что повреждение головного мозга вызвано острым нарушением мозгового кровообращения (ОНМК) по геморрагическому типу вне зависимости от его этиологии или по ишемическому типу вне зависимости от этиологии данного нарушения, или повреждение вызвано воздействием механического фактора вне зависимости от его природы, или воздействием термического фактора вне зависимости от его природы, или химического фактора вне зависимости от его природы (токсическое воздействие, метаболические нарушения), или проникающего излучения (радиации) вне зависимости от его природы, или сочетанием факторов в любых сочетаниях вне зависимости от их природы, а также повреждение головного мозга вызвано воздействием инфекционного агента.
21. Способ по п. 20, характеризующийся тем, что ОНМК по геморрагическому типу являются следствием врожденных или приобретенных дефектов сосудистого русла головного мозга.
22. Способ по п. 20, характеризующийся тем, что в качестве инфекционного агента может выступать бактериальная или вирусная инфекция.
23. Способ по п. 22, характеризующийся тем, что бактериальная инфекция может быть вызвана микроорганизмами родов Neisseria и Borrelia.
24. Способ по п. 22, характеризующийся тем, что вирусная инфекция может быть вызвана вирусом SARS-Cov2.
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА ДЛЯ СТИМУЛЯЦИИ РЕГЕНЕРАЦИИ НА ОСНОВЕ ПРОДУКТОВ СЕКРЕЦИИ МУЛЬТИПОТЕНТНЫХ МЕЗЕНХИМНЫХ СТРОМАЛЬНЫХ КЛЕТОК ЧЕЛОВЕКА | 2015 |
|
RU2620167C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ОЖОГОВ И РАН НА ОСНОВЕ ЦИТОКИНОВ И ФАКТОРОВ РОСТА, СЕКРЕТИРУЕМЫХ МЕЗЕНХИМНЫМИ КЛЕТКАМИ ЧЕЛОВЕКА, СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА И СПОСОБ ЛЕЧЕНИЯ ОЖОГОВ И РАН | 2014 |
|
RU2574017C1 |
| Бесклеточные терапевтические средства для регенеративной медицины и способы их получения | 2018 |
|
RU2742034C2 |
| Способ получения кондиционной среды, обладающей регенераторным потенциалом, для интраназального введения при лечении заболеваний центральной нервной системы | 2016 |
|
RU2637407C1 |
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| SAGARADZE G | |||
| et al | |||
| Conditioned Medium from Human Mesenchymal Stromal Cells: Towards the Clinical Translation | |||
Авторы
Даты
2023-09-12—Публикация
2022-05-23—Подача