Изобретение относится к медицине, а именно к травматологии и ортопедии, гнойной хирургии и может быть использовано в комплексе хирургического лечения глубокой перипротезной инфекции тазобедренного сустава при наличии перипротезного перелома.
Количество выполняемого первичного эндопротезирования тазобедренного сустава (ТБС) повышается в геометрической прогрессии (см. Травматизм, ортопедическая заболеваемость, состояние травматолого-ортопедической- помощи населению России в 2018 году: сборник. Под ред. Н.А. Еськина. М: ЦИТО им. Н.Н. Приорова, 2019. 166 с). Аналогично возрастает количество осложнений и последующих ревизионных вмешательств. Именно перипротезная инфекция (ПЛИ) является третьей по частоте причиной ревизионного эндопротезирования, а по некоторым источникам - второй (27,6%) (см. Шубняков И.И., Тихилов P.M., Денисов А.О., Ахмедилов М.А., Черный А.Ж., Тотоев З.А., Джавадов А.А., Карпухин А.С., Муравьёва Ю.В. Что изменилось в структуре ревизионного эндопротезирования тазобедренного сустава в последние годы? Травматология и ортопедия России. 2019; 25(4):9-27).
Инфекционные осложнения в ортопедии являются одними из самых грозных, обусловливают увеличение сроков госпитализации пациентов, приводят к инвалидизации их или ее усугублению, увеличивают экономические затраты на лечение пациентов (см. Мурылев В.Ю., Куковенко Г.А., Елизаров П.М., Иваненко Л.Р., Сорокина Г.Л., Рукин Я.А. и др. Алгоритм первого этапа лечения поздней глубокой перипротезной инфекции тазобедренного сустава. Травматология и ортопедия России. 2018;24(4):95-104. doi: 10.21823/2311-2905-2018-24-4-95-104).
Двухэтапный метод является наиболее популярной формой лечения пациентов с ППИ. Процент успешного исхода, по данным различных авторов, при применении такой методики варьирует от 60 до 95% (см. Лю Б., Тихилов Р.М., Шубняков И.И., Божкова С.А., Артюх В.А., Денисов А.О. Анализ эффективности санирующих операций при параэндопротезной инфекции. Травматология и ортопедия России. 2014;(2):22-29; см. Uchiyama К., Takahira N., Fukushima К., Moriya М., Yamamoto Т., Minegishi Y. at al. Two-stage revision total hip arthroplasty for periprosthetic infections using antibiotic-impregnated cement spacers of various types and materials. Scientific World Journal. 2013; 147-248. doi: 10.1155/2013/147248). При указанной технологии реэндопротезирование проводится вторым этапом, на фоне массивной антибиотикотерапии как после удаления, так и после повторной имплантации эндопротеза.
Добиться максимально необходимой концентрации антибиотиков в околосуставных тканях для санации гнойного очага, а также сохранить хороший функциональный результат, облегчить повторную имплантацию компонентов эндопротеза помогает установка цементного спейсера или «временного» протеза, изготовленного из костного цемента (порошковый компонент - полиметилметакрилат, жидкий компонент - мономер метилметакрилат), содержащего высокую концентрацию антибиотика (см. Клинические рекомендации. Перипротезная инфекция в области крупных суставов конечностей. СПб. Общероссийская общественная организация Ассоциация травматологов-ортопедов России (ATOP). 2016. 43 с.).
Спейсер - приспособление на основе биосовместимых материалов (полиметилметакрилата, полиэтилена, металлов) с включением в состав веществ с антимикробной активностью, применяемое для временного заполнения полости сустава в период между удалением инфицированного эндопротеза и установкой ревизионного эндопротеза у пациентов с перипротезной инфекцией.
Следующей по частоте причиной ревизионных вмешательств (примерно 6% всех ревизий) является перипротезный перелом бедра (ППБ) - тяжелое осложнение после тотального эндопротезирования тазобедренного сустава (см. Marsland D., Mears S.C. A review of periprosthetic femoral fractures associated with total hip arthroplasty. Geriatr. Orthop. Surg. Rehabil. 2012. V.3. P. 107-120. DOI:10.1177/21514585124628702). Частота интраоперационных ППБ варьирует от 0,1 до 27,8%, а послеоперационных - от 0,07 до 18% (см. Малыгин Р.В., Сивков В.С., Цыбин А.В., Воронкевич В.А., Любчак В.В., Шубняков М.И. Современный подход в лечении перипротезных переломов бедренной кости //Современные проблемы науки и образования. - 2020. - № 1). Ожидается, что количество случаев ППБ возрастет к 2030 году в связи с увеличением ожидаемой продолжительности жизни населения (см. Delia Valle C.J., Haidukewych G.J., Callaghan J.J. Periprosthetic fractures of the hip and knee: a problem on the rise but better solutions. Instr. Course Lect. 2010. V.59. P. 563-575.).
Хирургическое лечение ППБ в зависимости от типа перелома согласно унифицированной классификации всех перипротезных переломов - UCS (см. Duncan С.Р., Haddad F.S. The Unified Classification system (UCS): improving our understanding of periprosthetic fractures. Bone Joint J. 2014. V.96- B. P. 713-716) может включать как открытую репозицию и фиксацию перелома с использованием пластин, серкляжей и винтов или ретроградных интрамедуллярных штифтов, так и сложные ревизионные операции, связанные с удалением эндопротезов (см. Малыгин Р.В., Сивков В.С., Цыбин А.В., Воронкевич В.А., Любчак В.В., Шубняков М.И. Современный подход в лечении перипротезных переломов бедренной кости //Современные проблемы науки и образования. - 2020. - № 1).
Сочетание перипротезного перелома бедра и перипротезной инфекции приводит к огромной проблеме выбора оптимального метода лечения и тактики хирургического вмешательства, которые должны привести к таким целям, как: купирование инфекции, стабильная фиксация и сохранение хорошего функционального результата.
В доступных литературных источниках не найдено публикаций, посвященных лечению комбинации перипротезного перелома и инфекции.
Из патентных источников известен «Способ для борьбы с инфекцией глубоких слоёв мягких тканей при эндопротезировании тазобедренного сустава» (см. патент RU № 2697989 С1, опубл. 21.08.2019, Бюл. № 24). С целью сохранения эндопротеза пациента, обеспечения минимального объема хирургического повреждения анатомических структур, предотвращения развития осложнений в пораженном эндопротезированном суставе, снижения риска повторного оперативного вмешательства на пораженном суставе пациента, а также обеспечения восстановления функциональных возможностей конечности пациента, промывают полость раны растворами антисептиков системой двойных дренажей раздельно для подвода и отвода антисептика. В рану устанавливают максимально близко к эндопротезу два редон-дренажа в виде силиконовых перфорированных трубок, один из которых предназначен для введения антисептиков и источника ультразвукового излучения в рану, а второй - для эвакуации содержимого из раны, внутри редон-дренажей размещают трубки с перфорированными концами, которые вводят в рану через дополнительные разрезы- контрапертуры, отсоединяют систему подачи антисептика, перекрывают отток через отводящий дренаж, оставляя в полости раны антисептик, в полость раны вводят источник ультразвукового излучения для подачи волновых колебаний и создают эффект кавитации в течение 5-7 дней послеоперационного периода. Способ позволяет обеспечить минимальный объём хирургического повреждения анатомических структур, снизить риск повторного оперативного вмешательства на пораженном суставе. Однако применение известного способа ограничено сроками до 3 - 4 недель с момента возникновения инфекции (согласно материалам второй международной согласительной конференции по скелетно-мышечной инфекции (председатели: проф. Дж. Парвизи, проф. Т. Герке. Под общ. ред. Р.М. Тихилова, С.А. Божковой, И.И. Шубнякова. СПб.: РНИИТО им. Р.Р. Вредена, 2019)), кроме того, способ исключает замену мобильных компонентов эндопротеза, что значительно увеличивает риск рецидива инфекции. Указанный способ возможен только при стабильных компонентах эндопротеза тазобедренного сустава.
Так же известен «Способ хирургического лечения перипротезной инфекции крупных суставов с использованием поливалентного бактериофага фагодерм и вакуумного дренирования продуктов воспаления» (см. патент RU 2631052 С1, опубл. 15.09.2017, Бюл. № 26). Для хирургического лечения перипротезной инфекции крупных суставов иссекают некротически измененные ткани с удалением патологически измененных мягких тканей, в том числе из полости металлического эндопротеза, с обнажением поверхности металлического эндопротеза. Выполняют разъединение металлического эндопротеза и удаляют его головку и полиэтиленовый вкладыш. Промывают поверхность полости раны и обнаженные поверхности разъединенного металлического эндопротеза. Выполняют размещение новой головки эндопротеза и нового полиэтиленового вкладыша соответствующего размера в металлическом эндопротезе и восстанавливают целостность эндопротеза. Промывают поверхность полости раны и поверхности собранного металлического эндопротеза. На поверхность полости раны и на поверхность собранного металлического эндопротеза наносят гель с поливалентными бактериофагами Фагодерм, равномерно распределяя его по всей поверхности полости раны и поверхности собранного металлического эндопротеза. На раневую поверхность полости раны и поверхность металлического эндопротеза укладывают в качестве раневого заполнителя выполненную из гидрофильной полиуретановой основы пропитанную 1% раствором бактериофага Фагодерм пористую губку. Открытую раневую поверхность прооперированного пациента накрывают изолятором с самоклеющимися краями, изолятор с самоклеющимися краями оснащают вакуумной системой. Выполняют в послеоперационном периоде вакуумное дренирование продуктов воспаления костных и мягких тканей раневой поверхности через предварительно уложенную пористую губку. Способ позволяет сохранить эндопротез, уменьшить объём хирургического повреждения анатомических структур, уменьшить риск повторного оперативного вмешательства. Однако, применение известного способа в связи с сохранением статических компонентов эндопротеза ограничено сроками до 3 - 4 недель с момента возникновения инфекции (согласно материалам второй международной согласительной конференции по скелетно-мышечной инфекции). Указанный способ возможен только при стабильных компонентах эндопротеза. Недостатком способа так же является необходимость ревизии раны после осуществления каждого вакуумного дренирования раневой поверхности и раскрытия пленочного изолятора, что в свою очередь повышает риски бактериальной контаминации раны и металлоконструкций и повторного нагноения.
При изучении патентной литературы нами выявлены следующие способы формирования спейсера тазобедренного сустава из костного цемента.
Известны типы спейсеров, изготовленные заранее, или преформированные (см. патент RU 110262 U1 МПК A61F 2/32, опубл. 20.11.2011; см. патент RU 115652 U1 МПК A61F 2/32 опубл. 10.05.2012).
Недостатками преформированных спейсеров являются ограниченное антибактериальное воздействие, обусловленное использованием производителями узкого круга антибактериальных веществ (Гентамицин, Ванкомицин, Тобрамицин); негативные характеристики пары трения «цемент - кость», приводящие к болевому синдрома при трении спейсера о вертлужную впадину во время движения в суставе и деструкции костной ткани.
Известен «Двухкомпонентный цементный спейсер тазобедренного сустава» (см. патент RU 110263 U1 МПК A61F 2/32, опубл. 20.11.2011), который имеет вертлужную составляющую, представляющую собой цементную сферу, диаметр которой на 1-2 мм меньше диаметра кольца вертлужной впадины, и бедренную составляющую - армированный цилиндрический стержень, повторяющий диаметр костномозгового канала бедренной кости после римирования, проксимальный конец спейсера выстоит из костномозгового канала на 1-2 см, а полусферическая вогнутая его форма является повторением формы и размера вертлужного компонента спейсера.
«Спейсер тазобедренного сустава» (см. патент RU 123662 U1 МПК A61F 2/32, опубл. 10.01.2013) выполнен из костного цемента, имеющего в составе антибиотик. Спейсер содержит три элемента, отличающийся тем, что первый элемент выполнен в виде шара, второй - в виде «седловидной» ножки бедренного компонента, третий элемент, расположенный между первыми двумя, имеет форму полусферической шайбы.
Недостатками вышеуказанных устройств являются нестабильность компонентов спейсера, недостаточная конгруэнтность, которая вызывает ограничение движений, низкие прочностные характеристики пар трения «цемент - цемент» и «цемент - кость», последняя вызывает так же болевой синдром и деструкцию костной ткани.
Известен «Спейсер тазобедренного сустава» (см. патент RU 174697 U1 МПК A61F 2/32, опубл. 26.10.2017), включающий бедренный компонент, металлическую головку и тазовый компонент, изготовленный из костного цемента с антибиотиком, при этом в тазовый компонент установлена металлическая головка с возможностью ее вращения, отличающийся тем, что спейсер выполнен тотальным, металлическая головка - съемной, а тазовый компонент - в виде полусферы, верхнезадняя часть которого смещена за его пределы на 0,4 см, образуя, так называемый «козырек». Недостатки этой модели, заключаются в низкой прочности тазового компонента, обусловленная техникой изготовления последнего, что является причиной последующей нестабильности спейсера.
Известен «Тотальный спейсер тазобедренного сустава» (см. патент RU 176945 U1 МПК А61В 17/56, опубл. 02.02.2018, Бюл. № 4), состоящий из бедренного, армированного по оси, и тазового компонентов, выполненных из костного цемента с антибиотиком с нанесенными по поверхности насечками, отличающийся тем, что на бедренном компоненте между шейкой и ножкой выполнен опорный валик, а насечки имеют форму ребер и располагаются вдоль оси бедренного компонента. Недостатками являются низкая стабильность компонентов спейсера, недостаточная конгруэнтность, которая вызывает ограничение движений, низкие прочностные характеристики пары трения «цемент-цемент».
Известен «Спейсер тазобедренного сустава» (см. патент RU 2663628 С1 МПК А61В 17/56, опубл. 07.08.2018, Бюл. № 22), состоящий из головки, шейки, ножки, изготовленных из костного цемента с расположенным внутри металлическим стержнем, отличающийся тем, что дополнительно введены последовательно соединенные приемопередатчик, блок управления, шаговый двигатель и коммутатор, три цилиндрические емкости с разными антибиотиками, выход каждой из которых посредством трубки подключен к соответствующему входу коммутатора, причем в каждой емкости имеется поршень, к входу каждой емкости присоединена трубка, выходящая на поверхность спейсера в области нижней части ножки, также введены последовательно соединенные элемент питания и насос, второй вход которого соединен со вторым выходом блока управления, второй вход которого соединен с выходом элемента питания, причем выход коммутатора посредством трубки подключен к третьему входу насоса, к выходу которого присоединена трубка, выходящая на поверхность спейсера в области его шейки. Недостатки изобретения заключаются в неполной конгруэнтности артикулирующих поверхностей, низкой фиксационной стабильности, снижении прочности за счет каналов и емкостей, имеющихся в нем, что может способствовать механическому повреждению компонента спейсера при полной нагрузке, в отрицательных характеристиках пары трения «цемент - кость», приводящих к болевому синдрому и деструкции костной ткани вертлужной впадины. Главными недостатками данного вида спейсера являются его трудность и дороговизна изготовления, ограничения в эксплуатации в связи с необходимостью использования персонального компьютера и радиопередатчиков.
Все вышеуказанные виды спейсеров не решают проблему лечения и тактику хирургического вмешательства при комбинации перипротезного перелома и инфекции.
Задачей изобретения является достижение стабильной фиксации перипротезного перелома, снижение частоты возможных интра- и послеоперационных осложнений, связанных с нестабильностью спейсера тазобедренного сустава и его механическим разрушением, улучшение качества жизни пациента в период ожидания второго этапа реэндопротезирования.
Техническим результатом заявляемого изобретения является разработка способа, позволяющего лечить глубокую перипротезную инфекцию тазобедренного сустава при наличии перипротезного перелома.
Технический результат достигается тем, что после осуществления хирургического доступа к тазобедренному суставу удаляют головку эндопротеза тазобедренного сустава, затем бедренный компонент, после чего удаляют вертлужный компонент эндопротеза и другие имеющиеся металлоконструкции в области инфекционного процесса, далее осуществляют дебридмент, промывание полости сустава растворами антисептиков, затем выполняют ревизию перелома бедренной кости, устраняют межкостную интерпозицию мягких тканей, промывают рану раствором антисептика и затем устанавливают устройство - артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием, таким образом, что используя дозу костного цемента: 40 г с термостабильным антибиотиком чашку устанавливают в вертлужную впадину, далее заполняют стерильную силиконовую трубку костным цементом, насыщенным термостабильными антибиотиками, в фазе аппликации костного цемента в указанную трубку вводят сердечник, после полимеризации костного цемента силиконовую трубку срезают, затем соединяют плечо тела и стержень, проксимальную часть канала бедренной кости заполняют дозой костного цемента: 40 г с термостабильным антибиотиком, в фазе аппликации костного цемента единые тело и интрамедуллярный стержень погружают в канал бедренной кости, так чтобы верхний край плеча был на уровне большого вертела бедренной кости, при этом производят открытую репозицию перипротезного перелома бедренной кости и дополнительную его фиксацию проволочным серкляжом, далее производят дистальное блокирование стержня, подбирают размер длины металлической головки с конусом посадки 12/14 мм, на шейку надевают стерильную металлическую головку и вправляют головку в чашку, после окончания полимеризации костного цемента проверяют стабильность фиксации компонентов, синтеза перелома бедра, амплитуду движений в суставе, осуществляют гемостаз, рану промывают раствором антисептика, устанавливают низковакуумную дренажную систему, рану ушивают послойно.
Для осуществления предложенного способа нами разработано устройство - артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием, выполненный в виде стержня с дистальным широким наконечником. Стержень покрывается цементной антибактериальной мантией, что увеличивает активную площадь антибактериального эффекта спейсера. В свою очередь широкий наконечник имеет отверстие для дистального блокирования стержня, что повышает стабильность фиксации перелома бедренной кости. При последующем удалении спейсера из канала бедренной кости (во время второго этапа ревизионного эндопротезирования) широкий наконечник стержня будет препятствовать задержке фрагментов костного цемента в канале бедра.
Устройство выполнено из нержавеющей медицинской стали (марки 12Х18Н9Т ГОСТ 5632-72) состоит из тела (см. Фиг. 1, цифра 3; см. Фиг. 3) и интрамедуллярного стержня (см. Фиг. 1, цифра 4; см. Фиг. 2) с наконечником (см. Фиг. 2, цифра 16). Тело имеет шейку (см. Фиг. 2, цифра 14) с конусом 12/14 мм для фиксации головки эндопротеза (см. Фиг. 1, цифра 2), плеча (см.
Фиг. 3, цифра 18). В нижнем отделе тела имеется отверстие с резьбой М6х0,75 (см. Фиг. 3, цифра 17) для фиксации с интрамедуллярным стержнем, на котором в проксимальном отделе так же имеется резьбовая часть (см. Фиг. 2, цифра 19). Высота резьбовой части 8 мм. Интрамедуллярный стержень длиной 250 - 300 мм представлен сердечником (см. Фиг. 2, цифра 12) диаметром 6 мм и имеет в дистальном отделе наконечник (см. Фиг. 2, цифра 16) в виде конуса со сквозным отверстием (см. Фиг. 2, цифра 15) в поперечном направлении. Диаметр основания конуса 10 - 12 мм (в зависимости от диаметра канала бедренной кости). Таким образом, создается уступ между сердечником и наконечником для опоры цементной мантии. В собранном виде изделие представлено на фигуре № 1.
Представляем фигуры для лучшего понимания способа.
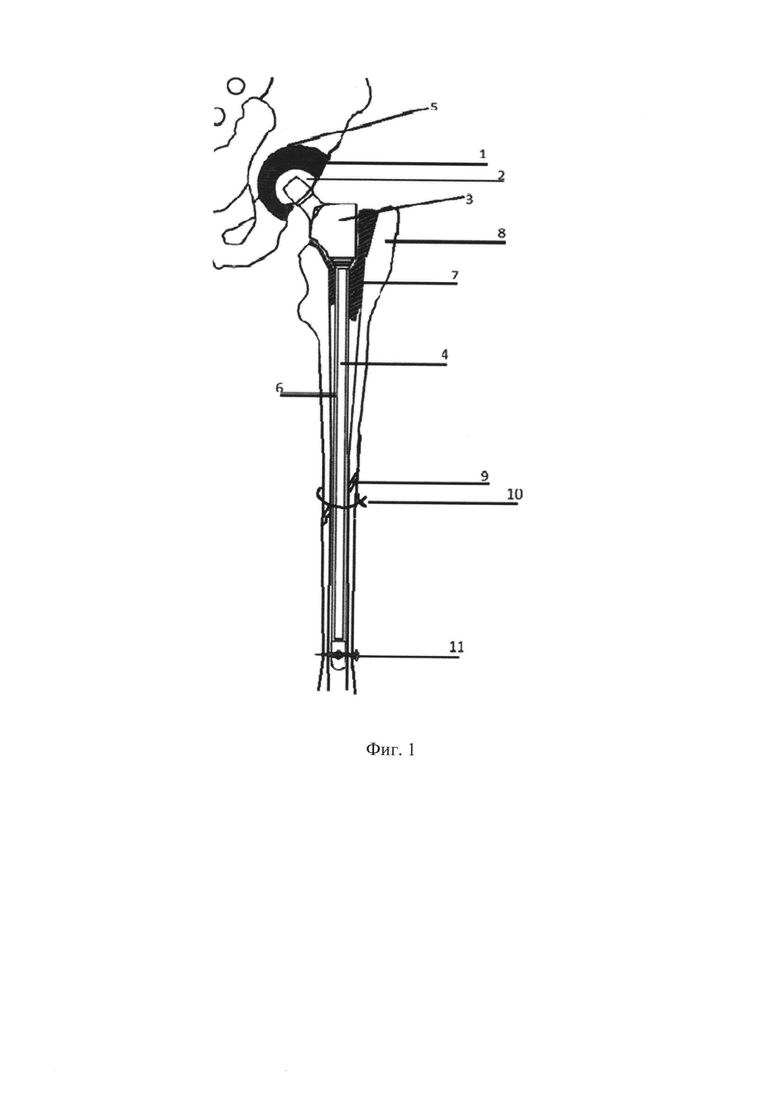
На Фиг. 1 изображен вид спейсера спереди назад, установленного на место удаленного эндопротеза. Цифрами обозначены:
1 - тазовый компонент (чашка);
2 - металлическая головка;
3 - тело спейсера;
4 - интрамедуллярный стержень;
5 - вертлужная впадина;
6 - антибактериальная цементная мантия;
7 - костный цемент в проксимальной части канала бедренной кости;
8 - большой вертел бедренной кости;
9 - перипротезный перелом бедренной кости;
10 - проволочный серкляж;
11 - блокирующий винт.
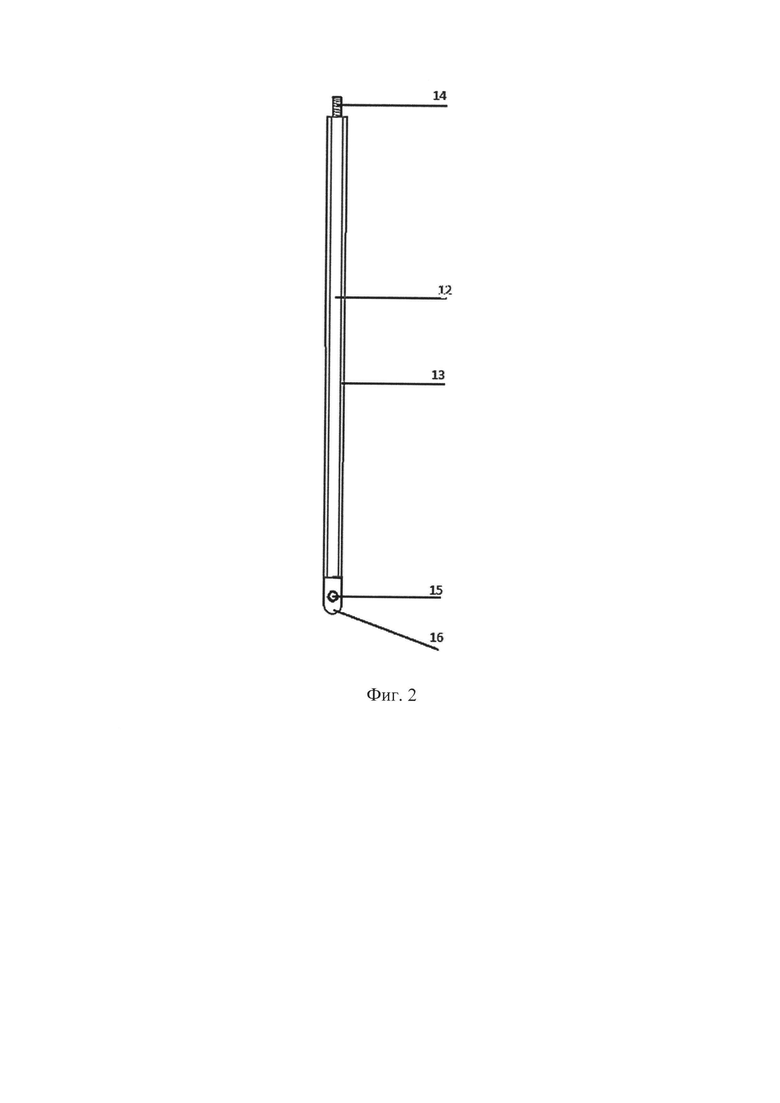
На Фиг. 2 изображен интрамедуллярный стержень. Цифрами обозначены:
12 - сердечник;
13 - антибактериальная цементная мантия;
14 - резьбовая часть;
15 - сквозное отверстие для дистального блокирования;
16 - наконечник.
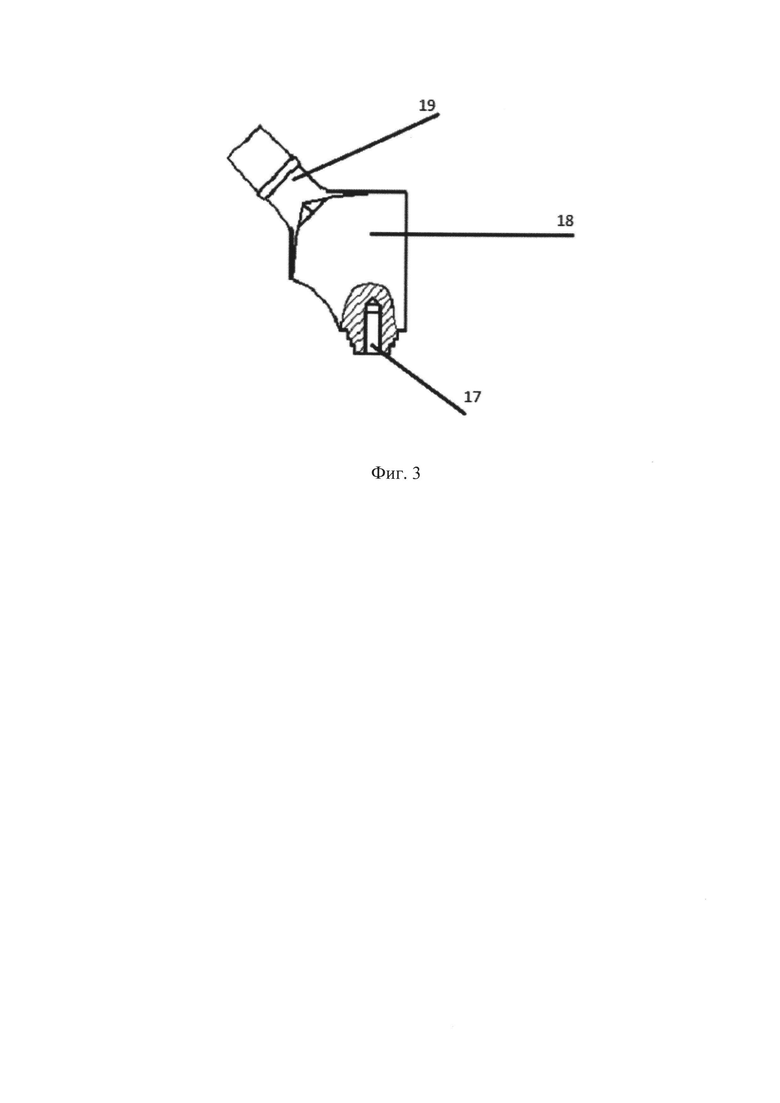
На Фиг. 3 изображено тело спейсера. Цифрами обозначены:
17 - резьбовая часть;
18 - плечо;
19 - шейка.
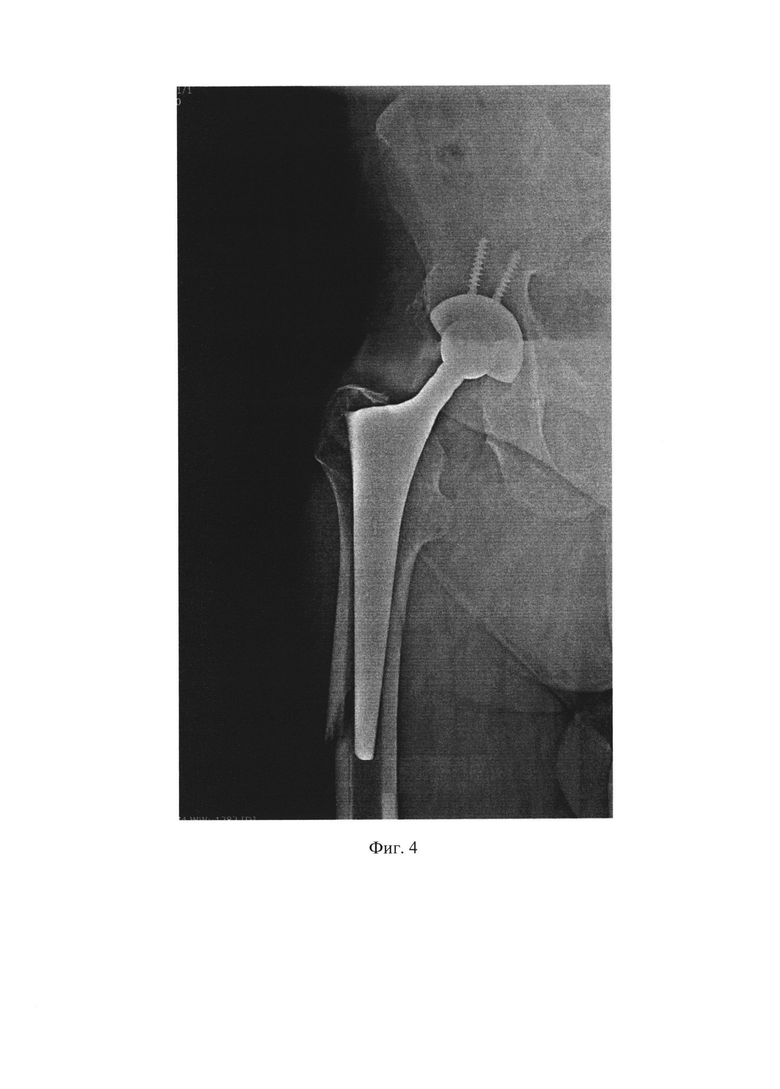
На Фиг. 4 представлена рентгенограмма правого тазобедренного сустава и верхней трети бедренной кости с перипротезным переломом (при поступлении в отделение травматологии и ортопедии). Клинический пример.
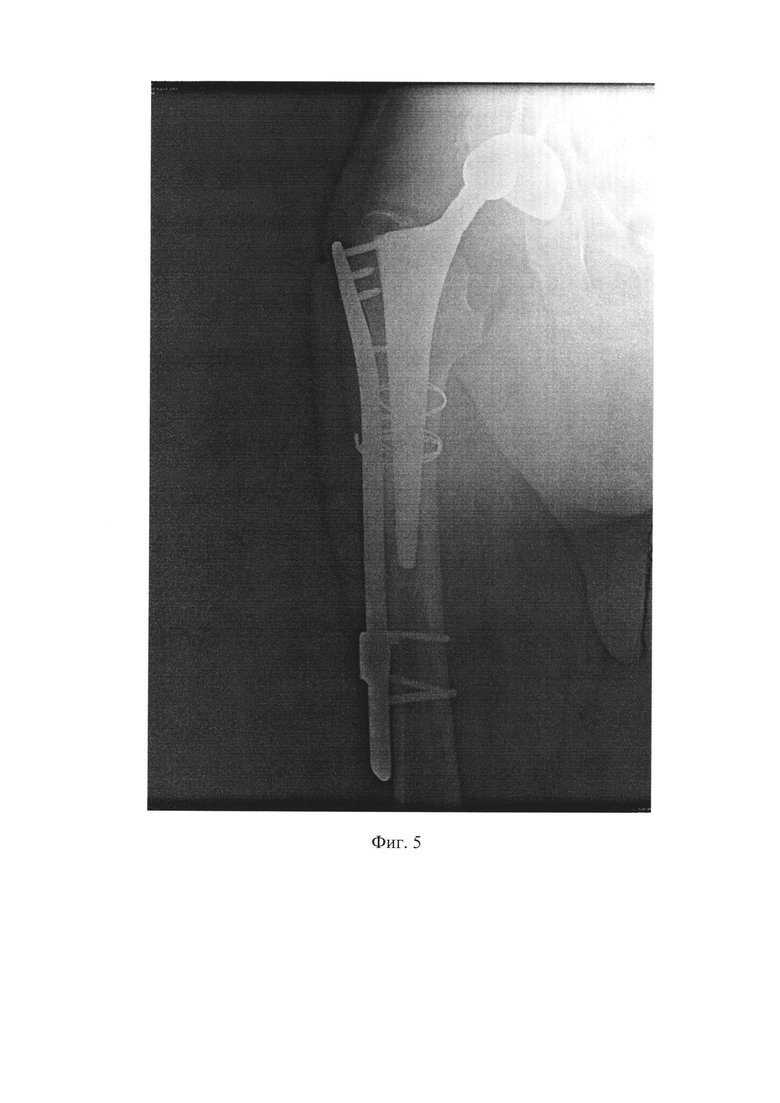
На Фиг. 5 представлена рентгенограмма правого тазобедренного сустава и верхне-средней трети бедренной кости после металлоостеосинтеза перипротезного перелома и вывихом головки эндопротеза (при поступлении в отделение гнойной хирургии). Клинический пример.
На Фиг. 6 изображено интраоперационное фото интрамедуллярного стержня, покрытого цементной антибактериальной мантией и соединенного с телом спейсера. Клинический пример.
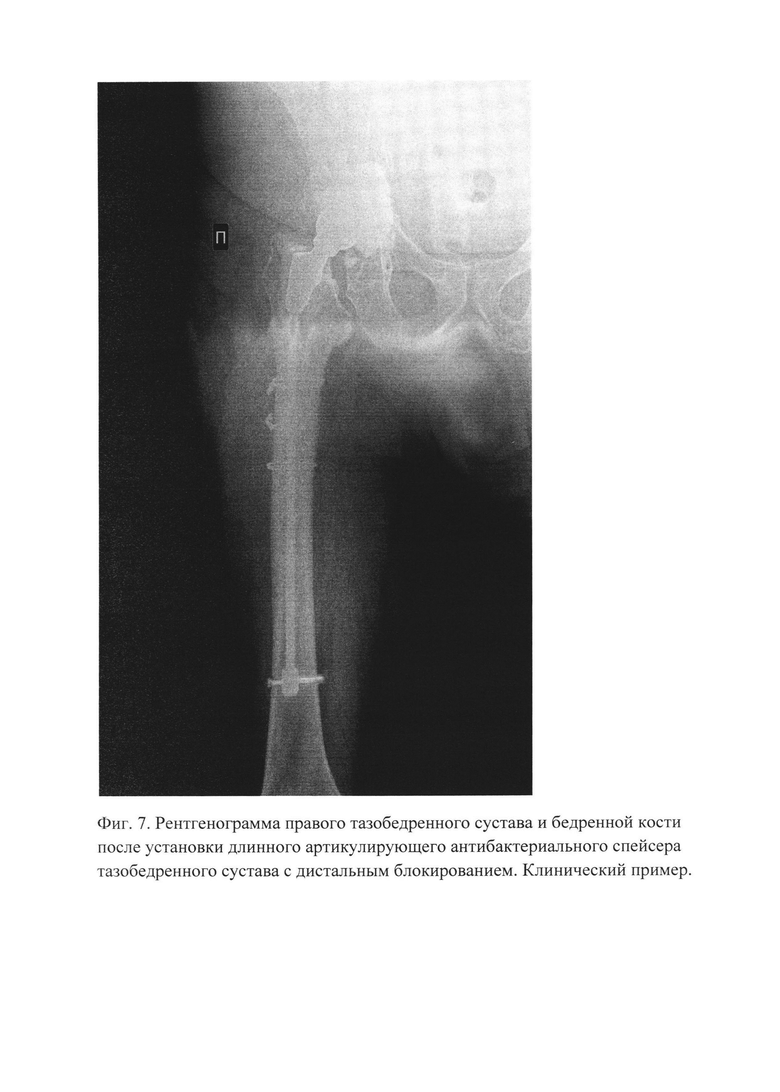
На Фиг. 7 изображена рентгенограмма правого тазобедренного сустава и бедренной кости после установки артикулирующего антибактериального спейсера тазобедренного сустава с дистальным блокированием. Клинический пример.
Способ осуществляется следующим образом.
При наличии свищевого хода, после обработки операционного поля в него вводят 0,1% водный раствор бриллиантового зеленого. Далее выполняют разрез кожи с иссечением послеоперационного рубца, рассекают подкожно-жировую клетчатку, фасцию. Затем производят передне- наружнюю артротомию. Первым удаляют головку эндопротеза тазобедренного сустава, затем бедренный компонент, после чего удаляют вертлужный компонент эндопротеза и другие имеющиеся
металлоконструкции в области инфекционного процесса. Далее приступают к дебридменту: удаляют костный цемент (при его наличии), некротизированные фрагменты кости, синовиальную оболочку и мягкие ткани, прокрашенные 0,1% водным раствором бриллиантового зеленого. Дебридмент сопровождается промыванием полости сустава растворами антисептиков: 3,0% раствор перекиси водорода, затем 0,02 % раствор хлоргексидина, затем, 0,1 % раствор полигексонида. Производится смена операционного белья и медицинских перчаток. Далее выполняется ревизия перелома бедренной кости, устранение межкостной интерпозиции мягких тканей, промывание раны 0,02 % раствором хлоргексидина (либо 3,0% раствором перекиси водорода, либо 0,1 % раствором полигексонида).
Устанавливают артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием, состоящий из тазового компонента (чашки) (см. Фиг. 1, цифра 1), металлической головки (см. Фиг. 1, цифра 2), тела (см. Фиг. 1, цифра 3, Фиг. 3.) и стержня (см. Фиг. 1, цифра 4, Фиг. 2). При этом используют интраоперационно изготовленный в фабричной пресс-форме тазовый компонент (чашку) (см. Фиг. 1, цифра 1) из костного цемента, насыщенного термостабильными антибиотиками, с активностью соответствующей данным бактериологического исследования. Геометрические размеры чашки соответствуют аналогичным удаленного компонента.
С помощью дозы костного цемента (40 г) с термостабильным антибиотиком устанавливают изготовленную чашку (см. Фиг. 1, цифра 1) в вертлужную впадину (см. Фиг. 1, цифра 5).
Далее стерильная силиконовая трубка необходимого диаметра (в зависимости от диаметра канала бедренной кости: 10 мм, 12 мм) заполняется костным цементом насыщенным термостабильными антибиотиками, с активностью соответствующей данным бактериологического исследования. В фазе аппликации костного цемента в указанную трубку вводится сердечник (см. Фиг. 2, цифра 12) стержня (см. Фиг. 1, цифра 4).
После полимеризации костного цемента силиконовую трубку срезают. Тем самым на сердечнике (см. Фиг. 2, цифра 12) стержня (см. Фиг. 1, цифра 4) создается антибактериальная цементная мантия (см. Фиг. 1, цифра 6; см. Фиг. 2, цифра 13).
Следующим этапом посредством резьбового соединения (см. Фиг. 2, цифра 14; см. Фиг. 3, цифра 17), соединяются плечо тела (см. Фиг. 1, цифра 3; см. Фиг. 3, цифра 18) и стержень (см. Фиг. 1, цифра 4; см. Фиг. 2). Проксимальная часть канала бедренной кости заполняется дозой костного цемента (40г) (см. Фиг. 1, цифра 7) с термостабильным антибиотиком и в фазе его аппликации единые тело (см. Фиг. 1, цифра 3; см. Фиг. 3) и интрамедуллярный стержень (см. Фиг. 1. цифра 4; см. Фиг. 2) погружается в канал бедренной кости так чтобы верхний край плеча тела (см. Фиг. 1. цифра 3; см. Фиг. 3. цифра 18) был на уровне большого вертела бедренной кости (см. Фиг. 1, цифра 8), при этом производится открытая репозиция перипротезного перелома бедренной кости (см. Фиг. 1, цифра 9) и дополнительная его фиксация проволочным серкляжом (см. Фиг. 1, цифра 10).
Далее производится дистальное блокирование стержня (см. Фиг. 1, цифра 4). Для этого под рентгеновским контролем в имеющееся отверстие (см. Фиг. 2, цифра 15) в наконечнике (см. Фиг. 2, цифра 16) интрамедуллярного стержня вводится блокирующий винт (см. Фиг. 1, цифра 11) диаметром 5 мм после просверливания канала сверлом диаметром 4 мм.
Подбирается размер длины металлической головки с конусом посадки 12/14 мм (см. Фиг. 1, цифра 2), с целью выравнивания длины ног и достижения нормального тонуса мышц, окружающих тазобедренный сустав (профилактика вывихов). На шейку (см. Фиг. 3, цифра 19), которая имеет конус 12/14 мм, надевают стерильную металлическую головку (см. Фиг. 1, цифра 2). Вправляют головку в тазовый компонент (чашку) (см. Фиг. 1, цифра 1).
После окончания полимеризации проверяют стабильность фиксации компонентов, синтеза перелома бедра, амплитуду движений в суставе.
Осуществляют гемостаз. Рану промывают 0,02 % раствором хлоргексидина (либо 3,0% раствором перекиси водорода, либо 0,1 % раствором полигексонида), устанавливают низковакуумную дренажную систему. Рану ушивают послойно. Через 72 часа после операции пациент начинает ходить с дополнительной опорой на костыли и без нагрузки на оперированную конечность. С 5 суток начинают занятия лечебной физкультурой, электростимуляцию мышц бедра.
Способ апробирован в отделении гнойной хирургии и травматологии ГБУ РО «Областная клиническая больница № 2», г. Ростов-на-Дону.
Приводим клинический пример выполнения способа.
Больной М., 61 год, в 2008 году выполнено тотальное
эндопротезирование правого ТБС по поводу посттравматического коксартроза. В последующем происходили неоднократные вывихи головки эндопротеза (со слов пациента около 20 раз в сумме).
25.08.2020 в результате падения у пациента произошел перипротезный перелом правого бедра (см. Фиг. 4). В травматолого-ортопедическом отделении ОКБ № 2 08.09.2020 выполнена открытая репозиция, накостный МОС перипротезного перелома правого бедра.
26.10.2020 - повторный вывих эндопротеза правого тазобедренного сустава (см. Фиг. 5). Течение заболевания осложнилось глубокой инфекцией области хирургического вмешательства, периимплантной/перипротезной инфекцией.
С 29.10.2020 по 16.11.2020 проходил лечение в отделении гнойной хирургии и травматологии ГБУ РО ОКБ № 2, где на основании данных клинико-лабораторного, рентгенологического (см. Фиг. 5), микробиологического обследований (бактериологический посев биоптатов стенок свищевого хода и пунктата правого ТБС - Staphylococcus aureus 105), консультаций смежных специалистов установлены диагнозы:
- основной: тотальный эндопротез правого тазобедренного сустава (2008 г.). Перипротезный перелом правого бедра в условиях накостного МОС (08.09.2020 г.). Привычный вывих эндопротеза, рецидив вывиха 26.10.2020 г.
Глубокая перипротезная инфекция II типа.
- сопутствующий: гипертоническая болезнь 3 ст., группа риска 4. ИБС: стенокардия напряжения ФК 2. Постинфарктный (БДУ) кардиосклероз. ХСН 1 ст., ФК 2. Приходящее нарушение ритма по типу частой желудочковой экстрасистолии.
Операция выполнена 02.11.2020- ревизия, удаление металлоконструкций правого бедра, компонентов тотального эндопроетеза правого тазобедренного сустава, секвестрнекрэктомия. Пульс-лаваж. Имплантация артикулирующего антибактериального спейсера тазобедренного сустава с дистальным блокированием.
Ход операции: под спинномозговой анестезией в положении больного на левом боку в свищевой ход по наружной поверхности средней трети правого бедра введен 0,1% водный раствор бриллиантового зеленого. По наружной поверхности правого тазобедренного сустава, верхней и средней трети бедра выполнен разрез по старому послеоперационному рубцу длиной 35 см с иссечением последнего и фистулы. Рассечены кожа, клетчатка, фасция. По ходу выполнялась некрэктомия мягких тканей. Визуализированы металлоконструкции, передним трансглютеальным доступом обнажена шейка протеза.
Ревизия: выявлено тотальное рубцовое изменение, прокрашивание 0,1% водным раствором бриллиантового зеленого капсулы сустава, участка кости проксимального отдела бедра и мягких тканей вдоль пластины, патологические грануляции.
Некротизированные мягкие ткани радикально иссечены, произведена остеонекрэктомия прокрашенных участков кости (материал отправлен на гистологическое и бактериологическое исследование). Удалены винты, серкляжные петли, накостная пластина. Визуализирован несросшийся косой перелом бедренной кости.
Далее произведен вывих головки эндопротеза, её удаление. После безуспешных попыток удаления ножки эндопротеза была произведена резекционная трепанация проксимальной части бедренной кости размерами 1x12 см, выполнено удаление бедренного компонента эндопротеза. Канал кости обработан. Удалена чашка эндопротеза, обработка вертлужной впадины. Выполнена повторная ревизия раны, окончательная некрэктомия.
Рана, канал, впадина промыты 0,1 % раствором полигексонида в объеме 9 литров. Гемостаз. Смена операционного белья и хирургических перчаток.
В фабричной пресс-форме изготовлен тазовый компонент (чашка) из костного цемента, насыщенного термостабильными антибиотиками (использовано 20 г костного цемента с Гентамицином + 2 г. Ванкомицина). С помощью аналогичной дозы костного цемента в вертлужную впадину установлена изготовленная чашка.
Далее стерильная силиконовая трубка внутренним диаметром 10 мм, заполнена 20 г костного цемента с Гентамицином + 2 г. Ванкомицина.
В фазе аппликации костного цемента в указанную трубку введен сердечник стержня изделия. Создана антибактериальная цементная мантия, стержень соединен с телом спейсера (см. Фиг. 6).
Проксимальная часть канала бедренной кости заполнена 1 дозой костного цемента 40 г с 1 г Гентамицина + 4 г Ванкомицина.
Произведена репозиция перелома средней трети бедра. Интрамедуллярный стержень погружен в канал бедренной кости. Трепанационный фрагмент верхней трети бедренной кости помещен в ложе сформированной трепанации. Фиксация последнего 1 проволочным серкляжом, дополнительная фиксация линии перелома 2 аналогичными серкляжами.
Произведено дистальное блокирование стержня под рентгеновским контролем винтом диаметром 5 мм.
Установлена металлическая головка и вправлена в тазовый компонент (чашку). Поверхности артикулировали, компоненты стабильны, вывихивания нет, остеосинтез относительно стабилен (см. Фиг. 7).
Через контрапертуры установлена низковакуумная дренажная система.
Рана послойно ушита наглухо. Асептическая повязка.
Проводилась медикаментозная терапия: антибиотикотерапия, профилактика тромбоэмболических осложнений, коррекция кардиальной патологии.
Дренажи удалены на 3 и 5 день после операции. На 10-е сутки после операции выполнена пункция тазобедренного сустава, содержимое направлено на посев. Бактериологический посев пунктата правого тазобедренного сустава - стерилен. Рана зажила первичным натяжением, швы сняты на 14 сутки. Пациент выписан на амбулаторное лечение с рекомендациями: длительная антибиотикопрофилактика в течение 6 недель.
Через 2 недели после окончания приема пероральных антибиотиков пациент осмотрен в амбулаторном режиме: клинических и лабораторных показателей воспаления не выявлено, выполнена трехкратная пункция правого тазобедренного сустава с последующим посевом пунктата: роста микрофлоры не выявлено.
Больному планируется второй этап оперативного вмешательства - ревизионное эндопротезирование правого тазобедренного сустава.
Технико-экономическая эффективность способа заключается в том, что его применение предусматривает артикуляцию поверхностей, что улучшает качество жизни пациента, сохраняя объем движений в тазобедренном суставе, предотвращает дислокацию бедра.
Наличие цементной антибактериальной мантии по всей длине интрамедуллярного стержня увеличивает активную площадь антибактериального эффекта спейсера, повышает концентрацию противомикробных химических препаратов, что в свою очередь снижает вероятность рецидива инфекции.
Дистальное блокирование стержня описанного изделия повышает стабильность фиксации перипротезного перелома бедренной кости, предотвращая как ротационное, так и смещение по длине костных отломков.
Наличие широкого наконечника стержня препятствует задержке фрагментов костного цемента в канале бедра при последующем удалении спейсера из канала бедренной кости (во время второго этапа ревизионного эндопротезирования).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗГОТОВЛЕНИЯ АРТИКУЛИРУЮЩЕГО АРМИРОВАННОГО ЦЕМЕНТНОГО АНТИБАКТЕРИАЛЬНОГО СПЕЙСЕРА КОЛЕННОГО СУСТАВА | 2018 |
|
RU2711608C1 |
| Способ лечения перипротезной инфекции при операциях эндопротезирования | 2023 |
|
RU2818150C1 |
| Способ лечения больных с перипротезной инфекцией после эндопротезирования тазобедренного сустава | 2023 |
|
RU2825106C1 |
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ С ВОСПОЛНЕНИЕМ КАВИТАРНЫХ ДЕФЕКТОВ ВЕРТЛУЖНОЙ ВПАДИНЫ | 2023 |
|
RU2821558C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ БОЛЬНЫХ С ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ ТАЗОБЕДРЕННОГО СУСТАВА | 2018 |
|
RU2675338C1 |
| Способ изготовления спейсера тазобедренного сустава при неопороспособной вертлужной впадине | 2017 |
|
RU2675551C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ СПЕЙСЕРА ТАЗОБЕДРЕННОГО СУСТАВА ПРИ НЕОПОРОСПОСОБНОЙ ВЕРТЛУЖНОЙ ВПАДИНЕ И ВЕРТЛУЖНЫЙ КОМПОНЕНТ СПЕЙСЕРА ТАЗОБЕДРЕННОГО СУСТАВА | 2020 |
|
RU2759655C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ ПЕРИПРОТЕЗНОЙ ИНФЕКЦИЕЙ КОЛЕННОГО СУСТАВА | 2024 |
|
RU2838762C1 |
| Способ лечения перипротезной инфекции при эндопротезировании коленного сустава | 2020 |
|
RU2725272C1 |
| СПОСОБ АРТРОДЕЗИРОВАНИЯ КОЛЕННОГО СУСТАВА В УСЛОВИЯХ ПЕРИПРОТЕЗНОЙ ИНФЕКЦИИ И НАЛИЧИЯ КОСТНЫХ ДЕФЕКТОВ | 2024 |
|
RU2840189C1 |

Группа изобретений относится к медицине, а именно к травматологии и ортопедии, гнойной хирургии, и может быть использована в комплексе хирургического лечения глубокой перипротезной инфекции тазобедренного сустава при наличии перипротезного перелома. Осуществляют хирургический доступ к тазобедренному суставу и удаляют головку эндопротеза тазобедренного сустава, бедренный компонент, затем вертлужный компонент эндопротеза и другие имеющиеся металлоконструкции в области инфекционного процесса. Затем выполняют ревизию перелома бедренной кости, устраняют межкостную интерпозицию мягких тканей, промывают рану раствором антисептика и устанавливают устройство - артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием. Артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием состоит из чашки, металлической головки, тела и стержня. Чашку изготавливают интраоперационно из костного цемента, насыщенного термостабильными антибиотиками, а головка, тело и стержень с наконечником выполнены из нержавеющей медицинской стали. Тело имеет шейку с конусом для фиксации головки эндопротеза и плечо, в котором имеется отверстие с резьбой для фиксации с интрамедуллярным стержнем. Группа изобретений позволяет снизить вероятность рецидива инфекции за счет увеличения активной площади антибактериального эффекта спейсера, повысить стабильность фиксации перипротезного перелома за счет дистального блокирования стержня, улучшить качество жизни пациента, сохраняя объем движений в тазобедренном суставе и предотвращая дислокацию бедра за счет артикуляции поверхностей. 2 н. и 1 з.п. ф-лы, 7 ил., 1 пр.
1. Способ лечения глубокой перипротезной инфекции тазобедренного сустава при наличии перипротезного перелома, включающий осуществление хирургического доступа к тазобедренному суставу, удаление головки эндопротеза тазобедренного сустава, затем бедренного компонента, после чего удаляют вертлужный компонент эндопротеза и другие имеющиеся металлоконструкции в области инфекционного процесса, далее осуществляют дебридмент, промывание полости сустава растворами антисептиков, затем выполняют ревизию перелома бедренной кости, устраняют межкостную интерпозицию мягких тканей, промывают рану раствором антисептика и затем устанавливают артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием по п.2 таким образом, что с помощью 40 г костного цемента с термостабильным антибиотиком устанавливают чашку в вертлужную впадину, далее на сердечнике стержня спейсера создают антибактериальную цементную мантию, для этого заполняют стерильную силиконовую трубку 10 мм или 12 мм костным цементом, насыщенным термостабильными антибиотиками, в фазе аппликации костного цемента в указанную трубку вводят сердечник, после полимеризации костного цемента силиконовую трубку срезают, затем соединяют плечо тела и стержень спейсера, проксимальную часть канала бедренной кости заполняют 40 г костного цемента с термостабильным антибиотиком, в фазе аппликации костного цемента единые тело и интрамедуллярный стержень погружают в канал бедренной кости, так чтобы верхний край плеча был на уровне большого вертела бедренной кости, при этом производят открытую репозицию перипротезного перелома бедренной кости и дополнительную его фиксацию проволочным серкляжом, далее выполняют дистальное блокирование стержня, подбирают размер длины металлической головки с конусом посадки 12/14 мм, на шейку надевают стерильную металлическую головку и вправляют головку в чашку, после окончания полимеризации костного цемента проверяют стабильность фиксации компонентов, синтеза перелома бедра, амплитуду движений в суставе, осуществляют гемостаз, рану промывают раствором антисептика, устанавливают низковакуумную дренажную систему, рану ушивают послойно.
2. Артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием для осуществления способа по п.1, включающий чашку, металлическую головку, тело и стержень, отличающийся тем, что чашку изготавливают интраоперационно в фабричной пресс-форме из костного цемента, насыщенного термостабильными антибиотиками, а головка, тело и стержень с наконечником выполнены из нержавеющей медицинской стали, при этом тело имеет шейку с конусом 12/14 мм для фиксации головки эндопротеза и плечо, в котором имеется отверстие с резьбой М6х0,75 для фиксации с интрамедуллярным стержнем, интрамедуллярный стержень 250-300 мм представлен сердечником диаметром 6 мм и имеет в проксимальном отделе резьбовую часть высотой 8 мм для соединения с телом, а в дистальном отделе наконечник в виде конуса со сквозным отверстием в поперечном направлении и диаметром основания 10-12 мм, при этом сердечник интрамедуллярного стержня покрывают цементной антибактериальной мантией с использованием силиконовой трубки с внутренним диаметром 10 мм или 12 мм.
3. Артикулирующий антибактериальный спейсер тазобедренного сустава с дистальным блокированием по п.2, отличающийся тем, что для дистального блокирования стержня под рентгеновским контролем в имеющееся отверстие в наконечнике интрамедуллярного стержня вводят винт диаметром 5 мм после просверливания канала сверлом диаметром 4 мм.
| Спейсер тазобедренного сустава | 2018 |
|
RU2680771C1 |
| СПОСОБ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СВАРНЫХ ШВОВ АУСТЕНИТНО-ФЕРРИТНБ1Х СТАЛЕЙ | 0 |
|
SU176945A1 |
| US 2009069899 A1, 12.03.2009 | |||
| CN 211750285 U, 27.10.2020 | |||
| КУКОВЕНКО Г.А | |||
| Двухэтапное ревизионное эндопротезирование в лечении глубокой перипротезной инфекции тазобедренного сустава | |||
| Диссертация на соискание ученой степени к.м.н | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Приспособление для получения кинематографических стерео снимков | 1919 |
|
SU67A1 |
| SPORER S.M | |||
| et al | |||
| Spacer Design | |||
Авторы
Даты
2022-03-15—Публикация
2021-05-04—Подача