Область техники
Настоящее изобретение относится к фармацевтической композиции, пищевой композиции и композиции корма для предупреждения или лечения неалкогольной жировой инфильтрации печени, содержащей лиганды сопряженного с G-белком рецептора 119 (GPR119) в качестве эффективных ингредиентов; к способу лечения и облегчения неалкогольной жировой инфильтрации печени; или к их применению для предупреждения или лечения неалкогольной жировой инфильтрации печени.
Уровень техники
Жировая инфильтрация печени представляет собой патологическое состояние, при котором триглицериды в избыточной степени накапливаются в гепатоцитах, и она с медицинской точки зрения определяется как состояние, при котором триглицериды составляют 5% или более массы печени. Жировую инфильтрацию печени классифицируют на алкогольную и неалкогольную жировую инфильтрацию печени в зависимости от того, вызвана ли жировая инфильтрация печени чрезмерным употреблением алкоголя или нет. Неалкогольная жировая инфильтрация печени (NAFLD) представляет собой группу заболеваний, которые охватывают все аспекты данного заболевания в диапазоне от неалкогольной жировой инфильтрации печени до стеатогепатита и цирроза. Простая неалкогольная жировая инфильтрация печени, которая охватывает только жировые отложения в печени и демонстрирует увеличение жировых отложений в тканях печени, вызванное резистентностью к инсулину и т.д. без каких-либо признаков повреждения гепатоцитов и фиброза, прогрессирует в неалкогольный стеатогепатит (NASH), который сопровождается повреждением гепатоцитов, вызванным воспалительными ответами вследствие оксидативного стресса, и иногда фиброзом, и может прогрессировать в цирроз печени, который без надлежащего лечения сопровождается необратимым повреждением печени.
В последнее время распространенность неалкогольной жировой инфильтрации печени заболевание быстро возросла по всему миру и, согласно оценке, распространенность простой жировой инфильтрации печени составляет от 6,3 до 33%, и распространенность неалкогольного стеатогепатита, сопровождающегося воспалением, составляет, согласно сообщениям, от 3 до 5% (Hepatology, 2012(55): 2005-2023). Простая жировая инфильтрация печени очень медленно прогрессирует в серьезное заболевание печени и не повышает смертность, ассоциированную с заболеваниями печени, однако стеатогепатит может приводить к циррозу и раку печени и повышает смертность, ассоциированную с заболеваниями печени, а также общую смертность. Кроме того, простая жировая инфильтрация печени может быть без труда смягчена посредством снижения массы тела на 3-5% путем изменения повседневных привычек, однако рекомендуется снижение массы тела по меньшей мере на 10% для уменьшения воспаления. Однако неясно, может ли это снижение массы тела индуцировать уменьшение воспаления или фиброза в печени (Korean J Gastroenterol, 2012(60): 64-66).
На настоящий момент не существует терапевтического средства против неалкогольного стеатогепатита. При ухудшении заболевания проводят трансплантацию печени. В соответствии со статистическими данными в США на 2013 год гепатит C считался наиболее частой причиной трансплантации печени, за которым следовал неалкогольный гепатит. Кроме того, повышение частоты трансплантаций печени за 10 лет с 2004 года составляло 14% для гепатита C, в то время как для неалкогольного стеатогепатита оно составляло 170%, демонстрируя быстрый рост, и также ожидалось, что к в 2020 году NASH станет основной причиной трансплантации печени, обогнав гепатит C, и, таким образом, существует острая необходимость в разработке эффективного терапевтического средства против неалкогольной инфильтрации печени, включая неалкогольный стеатогепатит.
В настоящее время медикаментозная терапия против неалкогольного стеатогепатита включает способ введения средства, усиливающего резистентность к инсулину (например, пиоглитазон), или антиоксиданта (например, витамин E), для которых были подтверждены данные о снижении накопления жира и воспаления посредством мелкомасштабных клинических испытаний у пациентов с неалкогольным стеатогепатитом. Однако такой способ не продемонстрировал явного эффекта смягчения воспаления и фиброза, и все еще невозможно предоставить эти лекарственные средства в качестве интенсивной терапии вследствие опасения по поводу безопасности при долговременном применении.
Сопряженный с G-белком рецептор 119 (GPR119) распространен в L- и K-клетках тонкого кишечника. Если GPR119 активируется триглицеридными метаболитами (2-моноацилглицерин) и т.д., GPR119 повышает секрецию гормонов-инкретинов, таких как глюкагон-подобный пептид-1 (GLP-1) или зависимый от глюкозы инсулинотропный полипептид (GIP). GPR119 также распространен в бета-клетках и альфа-клетках поджелудочной железы и участвует в поддержании уровня сахара в крови посредством контроля секреции инсулина и глюкагона зависимым от глюкозы образом. Кроме того, сообщается, что, если GPR119 сверхэкспрессируется в линии макрофагов человека, экспрессия рецептора GLP-1 возрастает, повышая уровень ATP-связывающего кассетного белка A1 (ABCA1), который является переносчиком, выводящим холестерин из клеток, тем самым повышая ApoA1-опосредуемй рефлюкс холестерина, повышая метаболизм липидов и снижая концентрацию воспалительных цитокинов в крови (J Lipid Res, 2014(55): 681-697).
Однако до настоящего времени не сообщалось, ингибирует ли лиганд GPR119 прямо воспалительный ответ и, таким образом, ингибирует ли он воспалительный ответ, который является основой повреждения гепатоцитов при неалкогольной жировой инфильтрации печени. Также не было описано, смягчает ли лиганд GPR119 воспаление и фиброз после индукции неалкогольной жировой инфильтрации печени.
Подробное описание изобретения
Техническая проблема
Задачей настоящего изобретения является предоставление фармацевтической композиции для предупреждения или лечения неалкогольной жировой инфильтрации, содержащей лиганд GPR119 в качестве эффективного ингредиента.
Техническое решение
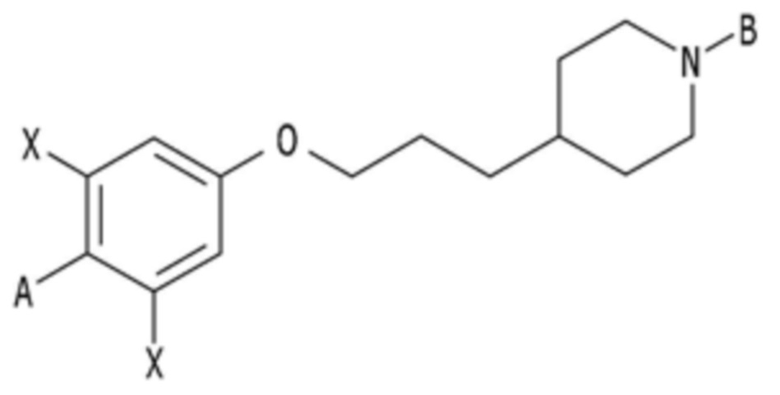
Настоящее изобретение может относиться к фармацевтической композиции для предупреждения или лечения неалкогольной жировой инфильтрации печени, которая содержит соединение, соответствующее приведенной ниже химической формуле 1, его фармацевтически приемлемые соли, их оптические изомеры, их гидраты или сольваты, или их смеси в качестве эффективного ингредиента:
[Химическая формула 1]
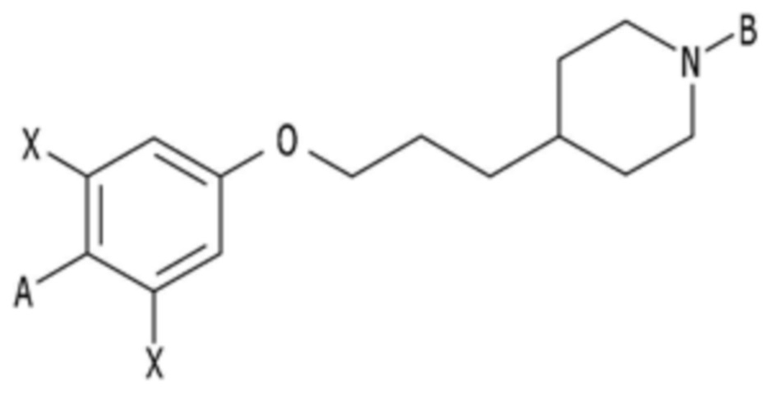
Фармацевтическая композиция в соответствии с настоящим изобретением может быть пригодна для предупреждения или лечения неалкогольной жировой инфильтрации печени посредством значительного ингибирования отложения триглицеридов, воспаления и фиброза в тканях печени.
В химической формуле 1
A представляет собой оксадиазол, дигидрооксазол, тиазол или тиадиазол, A независимо не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из галогена, прямого или разветвленного C1-C6 алкила и C1-C6 спирта, и алкильная или спиртовая группа независимо не замещена или замещена галогеном или C1-C6 алкоксигруппой;
B представляет собой пиридин, пиримидин, пиразин или оксадиазол, B независимо не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из галогена, группы прямого или разветвленного C1-C6 алкила, C1-C6 спирта, C1-C6 алкокси и оксадиазола, и группа прямого или разветвленного C1-C6 алкила, C1-C6 спирта, C1-C6 алкокси или оксадиазола независимо не замещена или замещена группой галогена, C1-C6 алкила или C1-C6 алкокси; и
каждый X независимо представляет собой F, Cl, Br или I, но не ограничивается ими.
Согласно одному варианту осуществления настоящего изобретения, может предусматриваться, что в химической формуле 1
A представляет собой
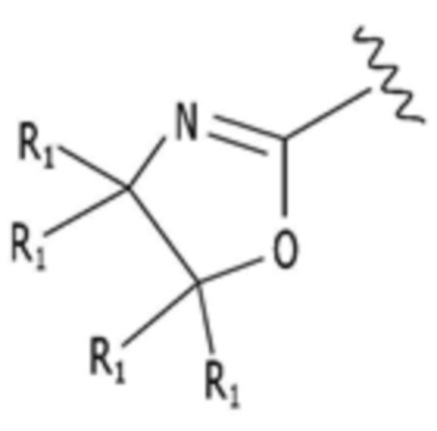 ,
, 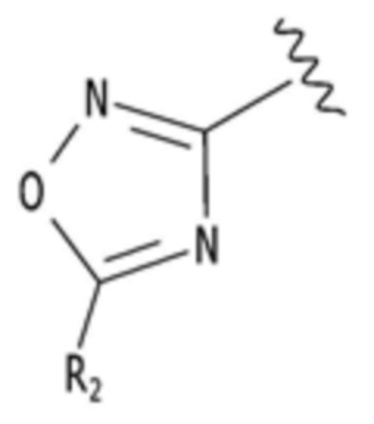 ,
, 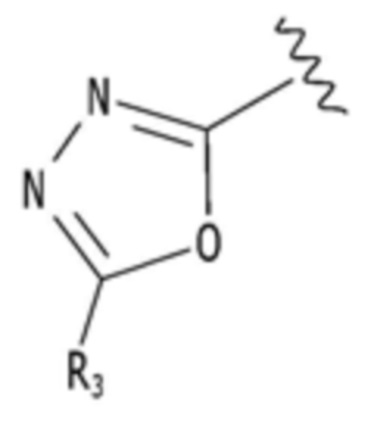 ,
, 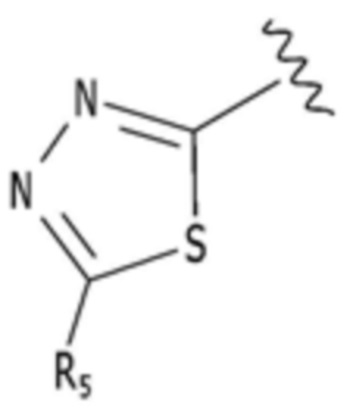 или
или 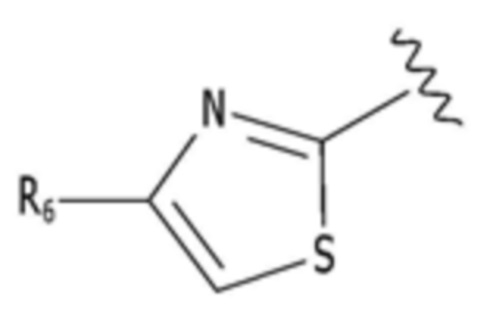 ; и
; и
каждый из R1-R3, R5 и R6 независимо представляет собой один или несколько заместителей, выбранных из группы, состоящей из водорода, галогена, прямого или разветвленного C1-C6 алкила и C1-C6 спирта, и алкильная или спиртовая группа независимо не замещена или замещена галогеном или C1-C6 алкоксигруппой.
Согласно другому варианту осуществления настоящего изобретения, может предусматриваться, что в химической формуле
B представляет собой 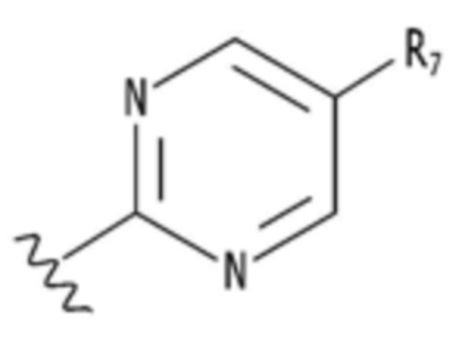 ,
, 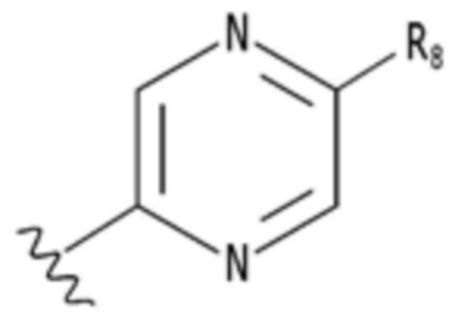 ,
, 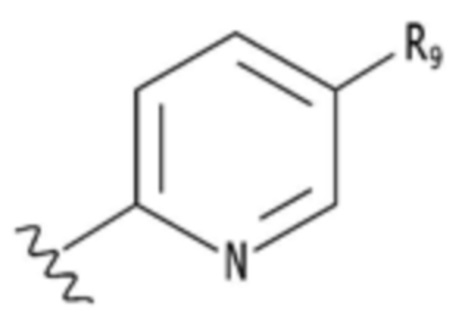 ,
, 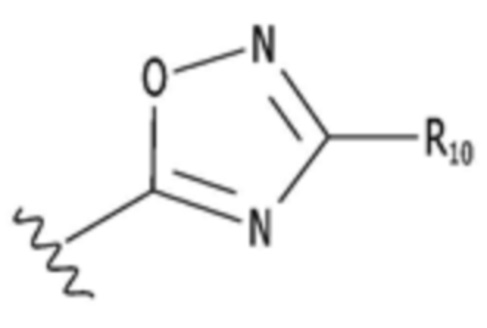 или
или 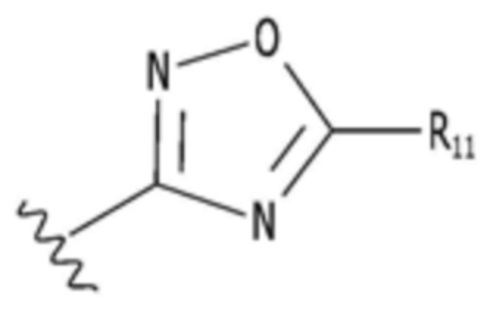 ; и
; и
R7-R11 независимо замещены по меньшей мере одним заместителем, выбранным из группы, состоящей из водорода, галогена, группы прямого или разветвленного C1-C6 алкила, C1-C6 спирта, C1-C6 алкокси и оксадиазола, и группа алкила, спирта, алкокси или оксадиазола независимо не замещена или замещена галогеном, C1-C6 алкилом или C1-C6 алкоксигруппой.
Согласно одному варианту осуществления настоящего изобретения, может предусматриваться, что в химической формуле 1 A представляет собой оксадиазол, замещенный прямым или разветвленным C1-C6 алкилом, B представляет собой пиримидин, замещенный прямым или разветвленным C1-C6 алкилом, и X представляет собой F.
В рамках настоящего изобретения термин "галоген" может относиться к фтору, хлору, брому или йоду.
В рамках настоящего изобретения термин "алкил" может относиться к прямому или разветвленному углеводородному остатку, если нет иных указаний. Пример C1-C6 алкила может включать метил, этил, пропил, изопропил, бутил, изобутил, пентил, гексил и т.д.
В рамках настоящего изобретения термин "алкокси" может включать алкил-кислородный радикал, имеющий алкил, как определено выше, если нет иных указаний. Пример C1-C6 алкокси может включать метокси, этокси, пропокси, бутокси, пентокси и т.д.
В рамках настоящего изобретения термин "гетероцикл" или "гетероциклический" может относиться к 5-13-члеенному гетероароматическому или неароматическому соединению, включающему от одного до трех гетероатомов, выбранных из группы, состоящей из N, O и S, если нет иных указаний.
В рамках настоящего изобретения соединение, соответствующее химической формуле 1, может представлять собой соединение, выбранное конкретно из группы, состоящей из следующих соединений:
2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-4,5-дигидрооксазол,
(R)-2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-4-метил-4,5-дигидрооксазол,
(S)-2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-4-метил-4,5-дигидрооксазол,
(S)-2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-метил-4,5-дигидрооксазол,
(R)-2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-метил-4,5-дигидрооксазол,
2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5,5-диметил-4,5-дигидрооксазол,
(R)-(2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-4,5-дигидрооксазол-5-ил)метанол,
(S)-(2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-4,5-дигидрооксазол-5-ил)метанол,
(R)-3-(2-(4-(3-(3,5-дифтор-4-(5-метил-4,5-дигидрооксазол-2-ил)фенокси)пропил)пиперидин-1-ил)пиримидин-5-ил)-5-изобутил-1,2,4-оксадиазол,
(R)-5-(4-(3-(3,5-дифтор-4-(4-метил-4,5-дигидрооксазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-изопропил-1,2,4-оксадиазол,
(S)-5-(4-(3-(3,5-дифтор-4-(5-метил-4,5-дигидрооксазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-изопропил-1,2,4-оксадиазол,
5-(4-(3-(4-(5,5-диметил-4,5-дигидрооксазол-2-ил)-3,5-дифторфенокси)пропил)пиперидин-1-ил)-3-изопропил-1,2,4-оксадиазол,
3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-метил-1,2,4-оксадиазол,
3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-пропил-1,2,4-оксадиазол,
3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол,
5-(трет-бутил)-3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол,
(3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол-5-ил)метанол,
2-(3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол-5-ил)этан-1-ол,
(S)-1-(3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол-5-ил)пропан-1-ол,
(R)-1-(3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол-5-ил)пропан-2-ол,
(S)-1-(3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол-5-ил)пропан-2-ол,
2-(3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,2,4-оксадиазол-5-ил)-2-метилпропан-1-ол,
3-(2,6-дифтор-4-(3-(1-(5-пропилпиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-пентилпиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-метоксипиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-изопропоксипиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
3-(4-(3-(1-(5-хлорпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол,
3-(4-(3-(1-(5-бромпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-метил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-этил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
5-(sec-бутил)-3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-(метоксиметил)-1,2,4-оксадиазол,
(S)-1-(3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-1,2,4-оксадиазол-5-ил)пропан-1-ол,
2-(3-(2,6-дифтор-4-(3-(1-(5-(5-изобутил-1,2,4-оксадиазол-3-ил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-1,2,4-оксадиазол-5-ил)-2-метилпропан-1-ол,
3-(4-(3-(1-(5-хлорпиразин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиридин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(3-изопропил-1,2,4-оксадиазол-5-ил)пиперидин-4-ил)пропокси)фенил)-5-метил-1,2,4-оксадиазол,
3-(2,6-дифтор-4-(3-(1-(3-изопропил-1,2,4-оксадиазол-5-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,2,4-оксадиазол,
(3-(2,6-дифтор-4-(3-(1-(3-изопропил-1,2,4-оксадиазол-5-ил)пиперидин-4-ил)пропокси)фенил)-1,2,4-оксадиазол-5-ил)метанол,
2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-метил-1,3,4-оксадиазол,
2-этил-5-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-1,3,4-оксадиазол,
2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,3,4-оксадиазол,
5-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-N-изопропил-1,3,4-оксадиазол-2-амин,
2-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-метил-1,3,4-оксадиазол,
2-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-этил-1,3,4-оксадиазол,
2-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,3,4-оксадиазол,
2-(4-(3-(1-(5-хлорпиразин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-метил-1,3,4-оксадиазол,
2-(4-(3-(1-(5-хлорпиразин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-этил-1,3,4-оксадиазол,
2-(4-(3-(1-(5-хлорпиразин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,3,4-оксадиазол,
5-(4-(3-(3,5-дифтор-4-(5-метил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-пропил-1,2,4-оксадиазол,
5-(4-(3-(3,5-дифтор-4-(5-этил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-пропил-1,2,4-оксадиазол,
5-(4-(3-(3,5-дифтор-4-(5-изопропил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-пропил-1,2,4-оксадиазол,
5-(4-(3-(3,5-дифтор-4-(5-метил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-изопропил-1,2,4-оксадиазол,
5-(4-(3-(4-(5-этил-1,3,4-оксадиазол-2-ил)-3,5-дифторфенокси)пропил)пиперидин-1-ил)-3-изопропил-1,2,4-оксадиазол,
5-(4-(3-(3,5-дифтор-4-(5-изопропил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-изопропил-1,2,4-оксадиазол,
5-(4-(3-(3,5-дифтор-4-(5-метил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-3-(2,2,2-трифторэтил)-1,2,4-оксадиазол,
3-(4-(3-(3,5-дифтор-4-(5-изопропил-1,3,4-оксадиазол-2-ил)фенокси)пропил)пиперидин-1-ил)-5-изопропил-1,2,4-оксадиазол,
2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,3,4-тиадиазол,
2-(2,6-дифтор-4-(3-(1-(5-пропилпиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,3,4-тиадиазол,
2-(2,6-дифтор-4-(3-(1-(5-пентилпиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,3,4-тиадиазол,
2-(2,6-дифтор-4-(3-(1-(5-фторпиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,3,4-тиадиазол,
2-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиримидин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,3,4-тиадиазол,
2-(2,6-дифтор-4-(3-(1-(5-(трифторметил)пиридин-2-ил)пиперидин-4-ил)пропокси)фенил)-5-изопропил-1,3,4-тиадиазол, и
4-этил-2-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)тиазол.
В одном варианте осуществления настоящего изобретения соединение, соответствующее химической формуле 1 по настоящему изобретению, в частности, может представлять собой 3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол.
В рамках настоящего изобретения неограничивающий пример фармацевтически приемлемой соли соединения, соответствующего химической формуле 1, может включат соли неорганических кислот, таких как хлористоводородная кислота, бромноватая кислота, фосфорная кислота или серная кислота; соли органических карбоновых кислот, таких как уксусная кислота, трифторуксусная кислота, лимонная кислота, малеиновая кислота, щавелевая кислота, янтарная кислота, бензойная кислота, виннокаменная кислота, фумаровая кислота, миндальная кислота, аскорбиновая кислота или яблочная кислота, или соли сульфоновых кислот, таких как метансульфоновая кислота или паратолуолсульфоновая кислота; соли щелочных металлов, таких как натрий, калий или литий; соли различных кислот, о которых известно, что они способны образовывать другие фармацевтически приемлемые соли; и т.п.
В одном конкретном варианте осуществления настоящего изобретения было подтверждено посредством эксперимента, состоящего в проведении гистологической оценки, измеряющей концентрацию ALT и AST в крови, измеряющей уровень экспрессии генов и белков, ассоциированных с воспалением и фиброзом, и т.п., что повреждение тканей печени, отложение триглицеридов в тканях печени, инфильтрация воспалительных клеток и фиброз в значительной степени ингибируются в модели на мышах ob/ob, у которых неалкогольную жировую инфильтрацию печени индуцировали специальным рационом, посредством введения соединения, соответствующего химической формуле 1, в ходе процесса индукции заболевания (пример 1).
В одном конкретном варианте осуществления настоящего изобретения было впервые подтверждено, что соединение, соответствующее химической формуле 1, ингибирует дифференцировку моноцитов человека и активацию дифференцированных макрофагов посредством воспалительного фактора зависимым от концентрации образом через механизм ингибирования воспалительных ответов (пример 2).
В одном конкретном варианте осуществления настоящего изобретения было подтверждено, что повреждение тканей печени, отложение триглицеридов в тканях печени, инфильтрация воспалительных клеток и фиброз значительно снижаются в модели на мышах C57BL6, в которой неалкогольная жировая инфильтрация печени индуцируется специальным рационом, путем введения соединения, соответствующего химической формуле 1, после индукции заболевания (Пример 3).
Фармацевтическую композицию для предупреждения или лечения неалкогольной жировой инфильтрации печени в соответствии с настоящим изобретением можно использовать в форме обычного фармацевтического препарата. Фармацевтический препарат можно вводить в различных пероральных и парентеральных дозированных формах при введении, и дозированные формы могут быть разными в зависимости от способа применения.
Если фармацевтический препарат составляют в виде различных пероральных и парентеральных дозированных форм, является возможным применение обычно используемых эксципиентов, таких как наполнители, разбавители, сухие разбавители, связующие вещества, увлажнители, разрыхлители, поверхностно-активные вещества и т.д.
Твердый препарат для перорального введения может включать таблетки, пилюли, порошки, гранулы, капсулы и т.д., и этот твердый препарат можно получать путем смешения по меньшей мере одного эксципиента, например, крахмала, карбоната кальция, сахарозы, лактозы, желатина и т.п. в фармацевтической композиции. Кроме того, в дополнение к простым эксципиентам можно использовать смазывающие вещества, такие как стеарат магния, тальк и т.д.
Более того, жидкий препарат для перорального введения может включать суспендирующие вещества, жидкости для внутреннего применения, эмульсии, сиропы и т.д., однако также он может включать различные эксципиенты, например, увлажнители, подсластители, вкусовые добавки, консерванты и т.д., в дополнение к воде и вазелиновому маслу, которые являются часто используемыми простыми разбавителями.
Препарат для парентерального введения может включать стерильные водные растворы, неводные растворители, суспензии, эмульсии, лиофилизированные препараты и суппозитории. Неводный растворитель и суспендирующее вещество могут включать пропиленгликоль, полиэтиленгликоль, растительное масло, такое как оливковое масло, инъекционный сложный эфир, такой как этилолеат и т.д. Основа суппозитория может включать витепсол, макрогол, tween 61, масло какао, лауриний, глицерожелатин и т.д.
Кроме того, фармацевтическая композиция для предупреждения или лечения неалкогольной жировой инфильтрации печени в соответствии с настоящим изобретением может включать эффективное количество в диапазоне введения от приблизительно 1 до приблизительно 1000 мг. Вводимое количество или принимаемое количество может быть введено посредством различных вводимых доз и способов, например, один раз в сутки или несколько раз в сутки, путем разделения композиции в зависимости от массы тела индивидуума, возраста, пола, состояния здоровья, рациона, времени введения, способа введения, скорости экскреции и тяжести заболевания.
В рамках настоящего изобретения неалкогольная жировая инфильтрация печени (NAFLD) может включать как первичную, так и вторичную неалкогольную жировую инфильтрацию печени. В частности, в рамках настоящего изобретения неалкогольная жировая инфильтрация печени (NAFLD) может включать, но не ограничивается ими, простой стеатоз, неалкогольный стеатогепатит (NASH) и фиброз печени и цирроз печени, вызываемые прогрессированием этих заболеваний.
Фармацевтическая композиция по настоящему изобретению может содержать соединение, соответствующее химической формуле 1, или один или несколько эффективных ингредиентов, которые демонстрируют сходную с ним функцию.
Настоящее изобретение также может относиться к способу предупреждения или лечения неалкогольной жировой инфильтрации печени, который включает введение терапевтически эффективного количества соединения, соответствующего химической формуле 1, его фармацевтически приемлемых солей, их оптических изомеров, их гидратов или сольватов, или их смесей индивидууму, нуждающемуся в лечении.
В рамках настоящего изобретения, термин "индивидуум, нуждающийся в лечении," может относиться к млекопитающим, включающим людей, и термин "введение" может относиться к предоставлению определенного материала индивидуумам любым подходящим способом. Термин "терапевтически эффективное количество" может относиться к количеству активного ингредиента или фармацевтической композиции, которое индуцирует проявление у животных или человека биологического или медицинского ответа, изучаемого исследователями, ветеринарами, докторами или другими клиницистами, и такое количество может включать количество для индукции облегчения заболевания или нарушения, подвергаемого лечению. Специалистам в данной области понятно, что терапевтически эффективная дозировка и количество введений для эффективных ингредиентов по настоящему изобретению может варьироваться в зависимости от желаемого эффекта.
В рамках настоящего изобретения путь введения фармацевтической композиции по настоящему изобретению может представлять собой любой обычный путь при условии, что он позволяет достигнуть ткани-мишени.
Введение можно проводить перорально, внутрибрюшинно, внутривенно, внутримышечно, подкожно, эндотелиально, интраназально, внутрилегочным путем, ректально, внутрь полости, внутрибрюшинно и интратекально, но не ограничиваясь ими.
Фармацевтическую композицию по настоящему изобретению можно вводить один раз в сутки или по меньшей мере два раза в сутки с определенным временным интервалом.
Фармацевтическую композицию по настоящему изобретению можно использовать отдельно или в комбинации с хирургической операцией, эндокринотерапией, медикаментозным лечением и способом с использованием модификатора биологического ответа для предупреждения и лечения неалкогольной жировой инфильтрации печени.
Настоящее изобретение также может относиться к пищевой композиции для предупреждения или облегчения неалкогольной жировой инфильтрации печени, которая содержит соединение, соответствующее химической формуле 1, его фармацевтически приемлемые соли, их оптические изомеры, их гидраты или сольваты или их смеси в качестве эффективного ингредиента.
В рамках настоящего изобретения термин "облегчение" может относиться ко всем действиям, при которых происходит улучшение заболевания или происходит благоприятное изменение в результате введение композиции.
В рамках настоящего изобретения термин "продукт питания" может относиться к мясу, сосискам, хлебу, шоколаду, конфетам, закускам, кондитерским изделиям, пицце, лапше быстрого приготовления, другим макаронным изделиям, жевательным резинкам, молочным продуктам, включающим мороженое, различные типы супов, напитков, чаев, полезным для здоровья напиткам, алкогольным напиткам, витаминным комплексам, полезным для здоровья функциональным продуктам питания, продуктам диетического питания, продуктам питания с биологически активными пищевыми добавками и т.п., и он может включать все продукты питания в общепринятом значении.
Термин "полезный для здоровья функциональный продукт питания" может иметь то же значение, что и продукт питания для специального оздоровительного использования (FoSHU), и он относится к продукту питания, имеющему высокий медицинский и лечебный эффект, который переработан так, чтобы он эффективно демонстрировал биологическую функцию регуляции в дополнение к предоставлению питательных веществ. В этом случае термин "функция(функциональность)" может относиться к контролю питательных веществ или достижению благоприятного эффекта на здоровье, такого как физиологическое действие и т.д. в отношении структуры и функции организма человека.
"Продукт диетического питания" может относиться к продукту питания, имеющему эффект активного поддержания или улучшения здоровья по сравнению с обычным продуктом питания, и "продукт питания с биологически активными пищевыми добавками" может относиться к продукту для цели улучшения здоровья. В некоторых случаях термины "полезный для здоровья функциональный продукт питания", "продукт диетического питания" и "продукт питания с биологически активными пищевыми добавками" могут использоваться взаимозаменяемо.
Продукт питания по настоящему изобретению можно получать способом, обычно используемым в данной области, и можно добавлять исходные материалы и ингредиенты, обычно добавляемые в данной области, для получения продукта питания в процессе приготовления. В частности, могут быть включены белки, углеводы, жиры, пищевые добавки, приправы и вкусовые добавки, и пример углеводов может включать глюкозу, фруктозу, мальтозу, сахарозу, олигосахарид, декстрин, циклодекстрин, ксилит, сорбит, эритрол, сахарин или синтетические вкусовые добавки, но не ограничиваясь ими. Пищевую композицию по настоящему изобретению можно приготавливать в виде различных дозированных форм без ограничений, при условии, что дозированная форма признана продуктом питания.
Настоящее изобретение также может относиться к способу предупреждения или облегчения неалкогольной жировой инфильтрации печени, который включает введение пищевой композиции, содержащей соединение, соответствующее химической формуле 1, его фармацевтически приемлемые соли, их оптические изомеры, их гидраты или сольваты, или их смеси, в качестве эффективного ингредиента индивидууму, нуждающемуся облегчении.
Настоящее изобретение также может относиться к композиции корма для предупреждения или облегчения неалкогольной жировой инфильтрации печени, которая содержит соединение, соответствующее химической формуле 1, его фармацевтически приемлемые соли, их оптические изомеры, их гидраты или сольваты, или их смеси в качестве эффективного ингредиента.
В рамках настоящего изобретения термин "корм" может относиться к любому природному или искусственному рациону, одному приему пищи и т.д., или к ингредиенту одного приема пищи, который подлежит употреблению или перевариванию сельскохозяйственными животными или является пригодным для этого. Кром может содержат кормовые добавки или вспомогательные корма.
Тип корма конкретно не ограничен, и можно использовать корм, обычно используемый в данной области. Неограничивающий пример корма может включать растительные корма, такие как злаки, корнеплоды, побочные продукты переработки пищевых продуктов, водоросли, волокна, фармацевтические побочные продукты, масла и жиры, крахмалы, жмыховую муку, побочные продукты производства круп и т.п.; корма для животных, такие как белки, неорганические материалы, масла и жиры, минералы, белки одноклеточных организмов, зоопланктон, пищевые продукты и т.п. Корм можно использовать отдельно или путем смешения по меньшей мере двух из них.
Настоящее изобретение также может относиться к применению соединения, соответствующего химической формуле 1, его фармацевтически приемлемых солей, их оптических изомеров, гидратов или сольватов, или их смесей, для предупреждения или лечения неалкогольной жировой инфильтрации печени.
Настоящее изобретение также может относиться к применению соединения, соответствующего химической формуле 1, его фармацевтически приемлемых солей, их оптических изомеров, их гидратов или сольватов, или их смесей для получения фармацевтического препарата для предупреждения или лечения неалкогольной жировой инфильтрации печени.
В терапевтическом способе, пищевой композиции, способе облегчения, композиции корма и их применении соединение, соответствующее химической формуле 1, в частности, может представлять собой 3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол.
Вещества, упоминаемые для фармацевтической композиции, терапевтического способа, пищевой композиции, способа облегчения, композиции корма и их применения в соответствии с настоящим изобретением подразумевают одно и то же, если это не противоречит одно другому.
Преимущественные эффекты
Фармацевтическая композиция в соответствии с настоящим изобретением демонстрирует превосходный эффект облегчения метаболизма липидов, снижения накопления жиров в тканях печени и предупреждения гистологического повреждения, вызываемого воспалением и фиброзом тканей печени, и, таким образом, она может использоваться для предупреждения или лечения неалкогольной жировой инфильтрации печени.
Краткое описание чертежей
На фиг.1 представлено изображение образца ткани, демонстрирующее эффект уменьшения количества триглицеридов и ингибирования инфильтрации воспалительных клеток посредством соединения по настоящему изобретению в модели на мышах с индуцированным неалкогольным стеатогепатитом.
На фиг.2 представлен аналитический график, демонстрирующий эффект ингибирования инфильтрации воспалительных клеток и ингибирования фиброза посредством соединения по настоящему изобретению в модели на мышах с индуцированным неалкогольным стеатогепатитом (#, p<0,05 против нормальных; * и **, p<0,05 и p<0,01 против Ob-NASH).
На фиг.3 представлено изображение образца ткани, демонстрирующее эффект ингибирования фиброза посредством соединения по настоящему изобретению в модели на мышах с индуцированным неалкогольным стеатогепатитом.
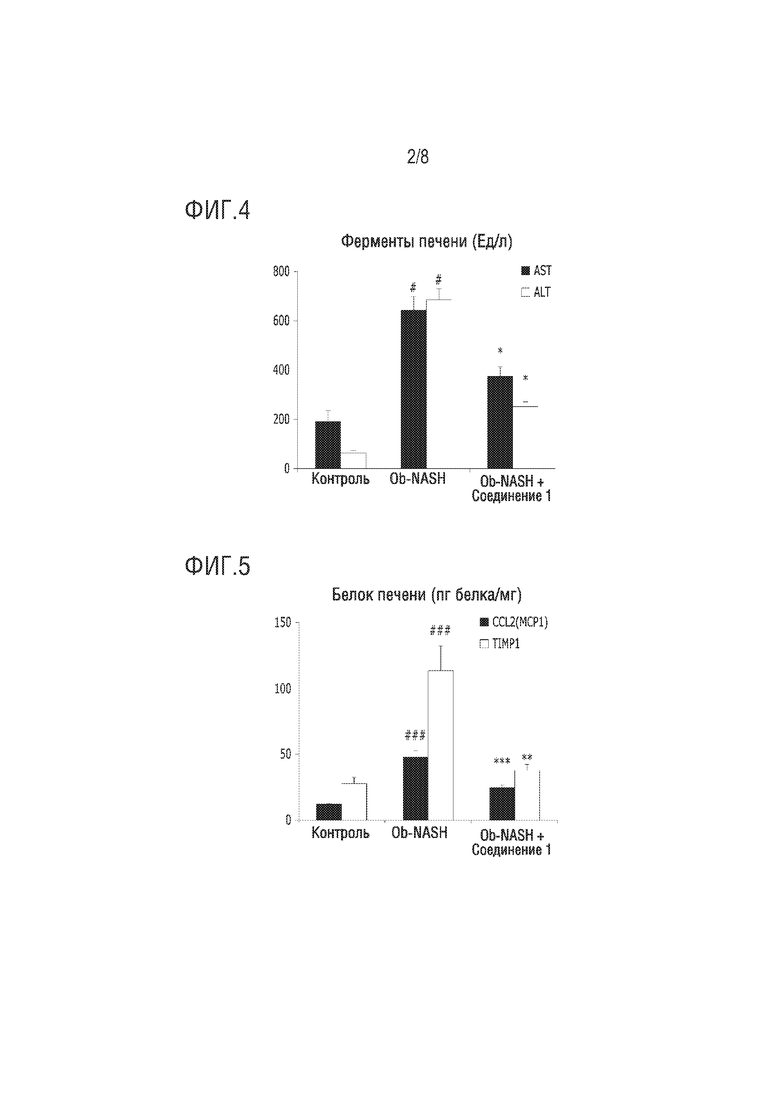
На фиг.4 представлено изображение, демонстрирующее эффект уменьшения уровня AST и ALT посредством соединения по настоящему изобретению в модели на мышах с индуцированным неалкогольным стеатогепатитом (#, p<0,05 против нормы; *, p<0,05 против Ob-NASH).
На фиг.5 представлено изображение, демонстрирующее результаты измерения концентрации белков, ассоциированных с воспалением и фиброзом, в модели на мышах с индуцированным неалкогольным стеатогепатитом (###, p<0,001 против нормы; ** и ***, p<0,01 и p<0,001 против Ob-NASH).
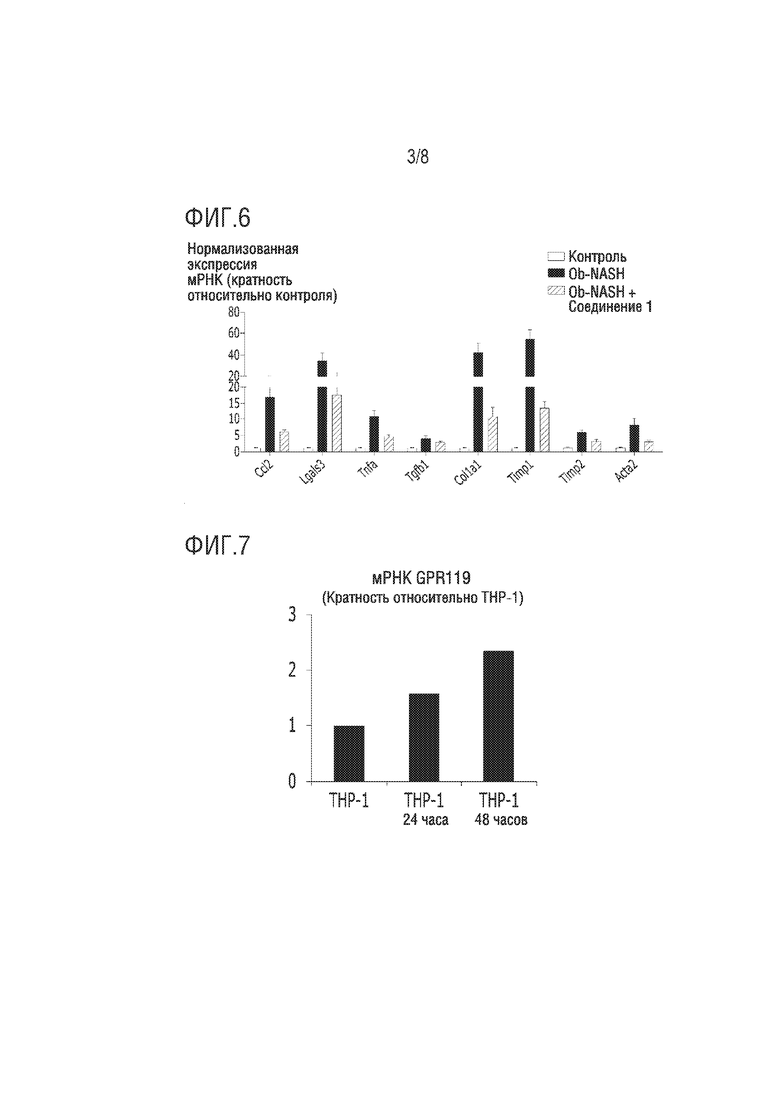
На фиг.6 представлено изображение, демонстрирующее результаты измерения уровня экспрессии генов, ассоциированных с воспалением и фиброзом, в модели на мышах с индуцированным неалкогольным стеатогепатитом.
На фиг.7 представлено изображение, демонстрирующее результаты оценки экспрессии генов GPR119 в клетках в момент времени до дифференцировки моноцитов человека в макрофаги и после дифференцировки в течение 24 и 48 часов.
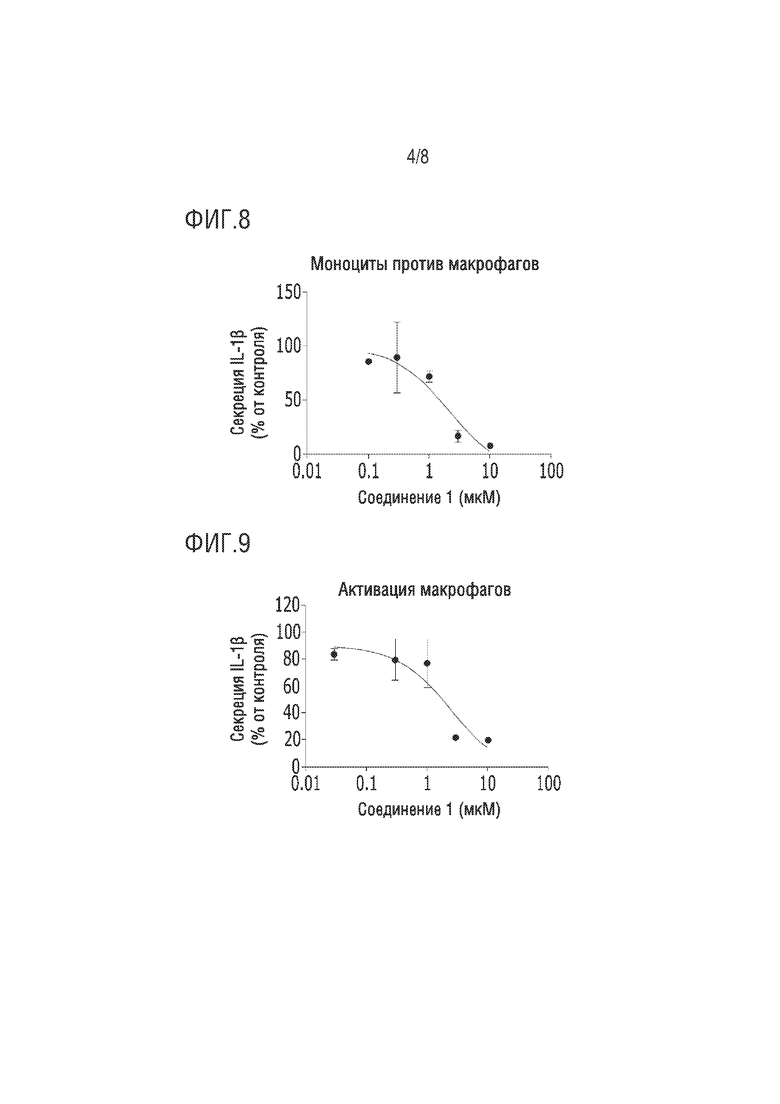
На фиг.8 представлено изображение, демонстрирующее результаты оценки эффекта на дифференцировку моноцитов человека в макрофаги в зависимости от лечения соединением по настоящему изобретению.
На фиг.9 представлено изображение, демонстрирующее результаты оценки эффекта на активацию дифференцированных макрофагов в зависимости от лечения соединением по настоящему изобретению.
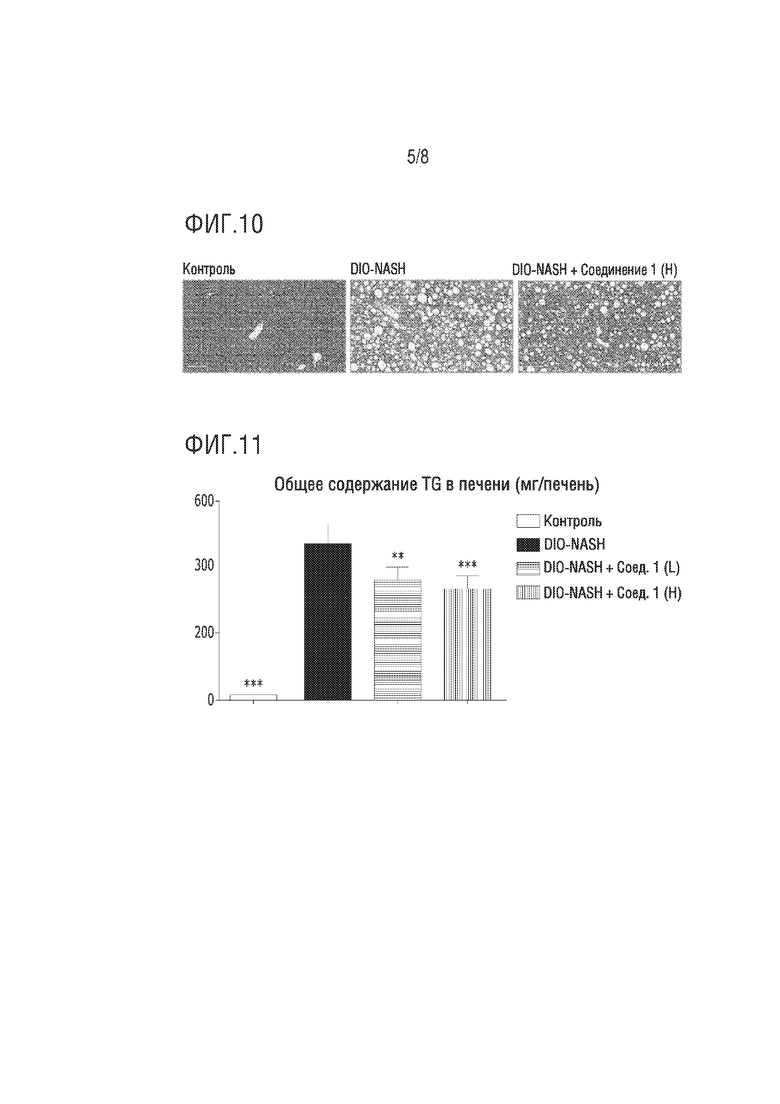
На фиг.10 представлено изображение образца ткани, демонстрирующее эффект уменьшения уровня триглицеридов и ингибирования инфильтрации воспалительных клеток в ткани печени посредством соединения по настоящему изобретению в модели на мышах с индуцированным неалкогольным стеатогепатитом.
На фиг.11 представлено изображение, демонстрирующее результаты измерения содержания триглицеридов в тканях печени в модели на мышах с индуцированным неалкогольным стеатогепатитом (** и ***, p<0,01 и p<0,001 против DIO-NASH).
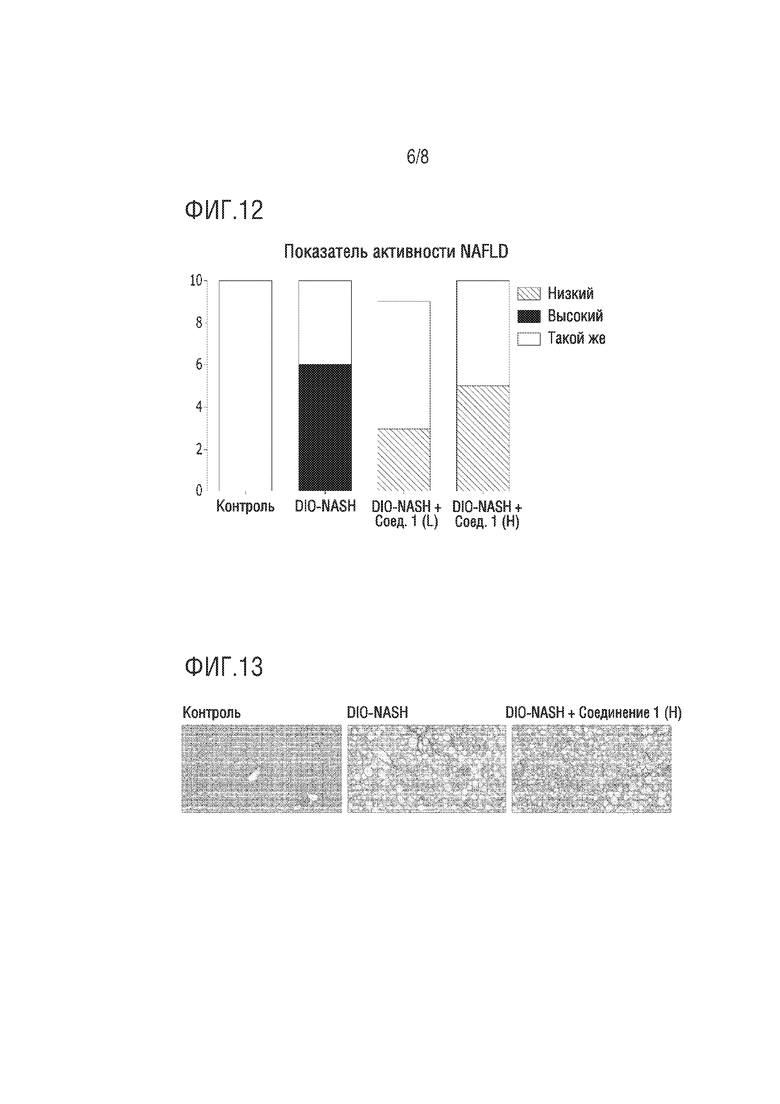
На фиг.12 представлено изображение, демонстрирующее изменение показателя активности NAFLD (NAS) до и после введения одному и тому же индивидууму в модели на мышах с индуцированным неалкогольным стеатогепатитом.
На фиг.13 представлено изображение образца ткани, демонстрирующее эффект ингибирования фиброза посредством соединения по настоящему изобретению в модели на мышах с индуцированным неалкогольным стеатогепатитом.
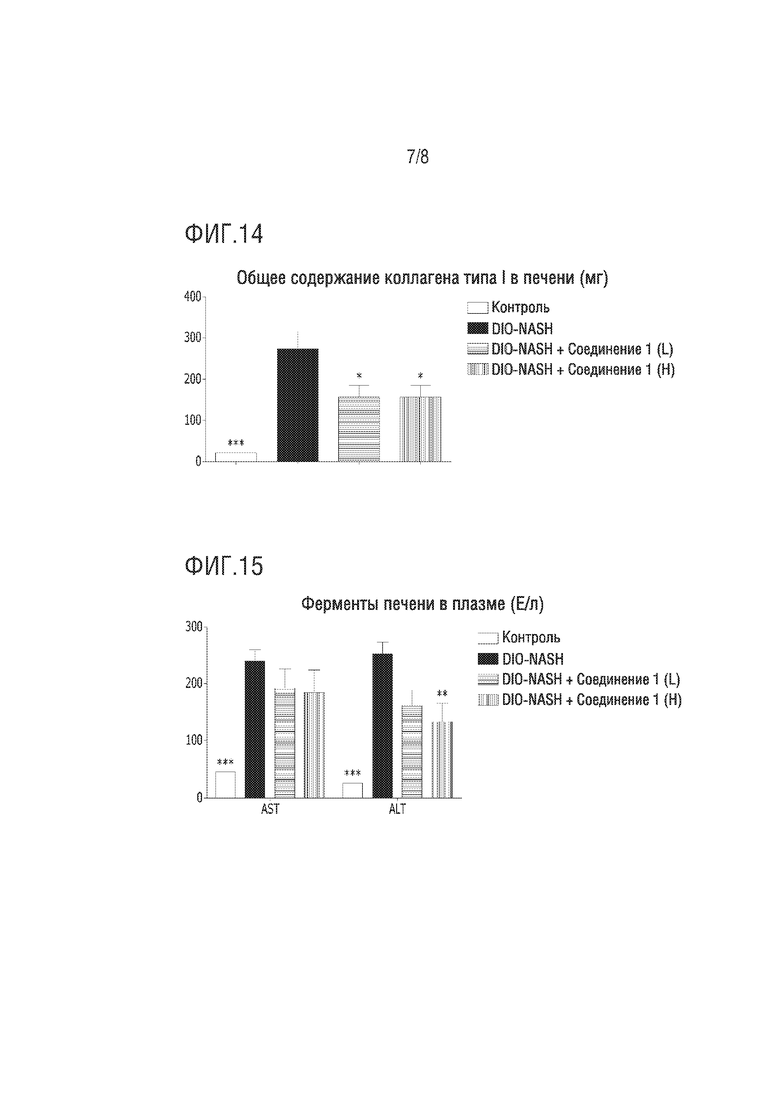
На фиг.14 представлено изображение, демонстрирующее результаты измерения содержания коллагена типа I в тканых печени в модели на мышах с индуцированным неалкогольным стеатогепатитом (* и ***, p<0,05 и p<0,001 против DIO-NASH).
На фиг.15 представлено изображение, демонстрирующее результаты измерения концентрации AST и ALT в крови в модели на мышах с индуцированным неалкогольным стеатогепатитом (** и ***, p<0,01 и p<0,001 против DIO-NASH).
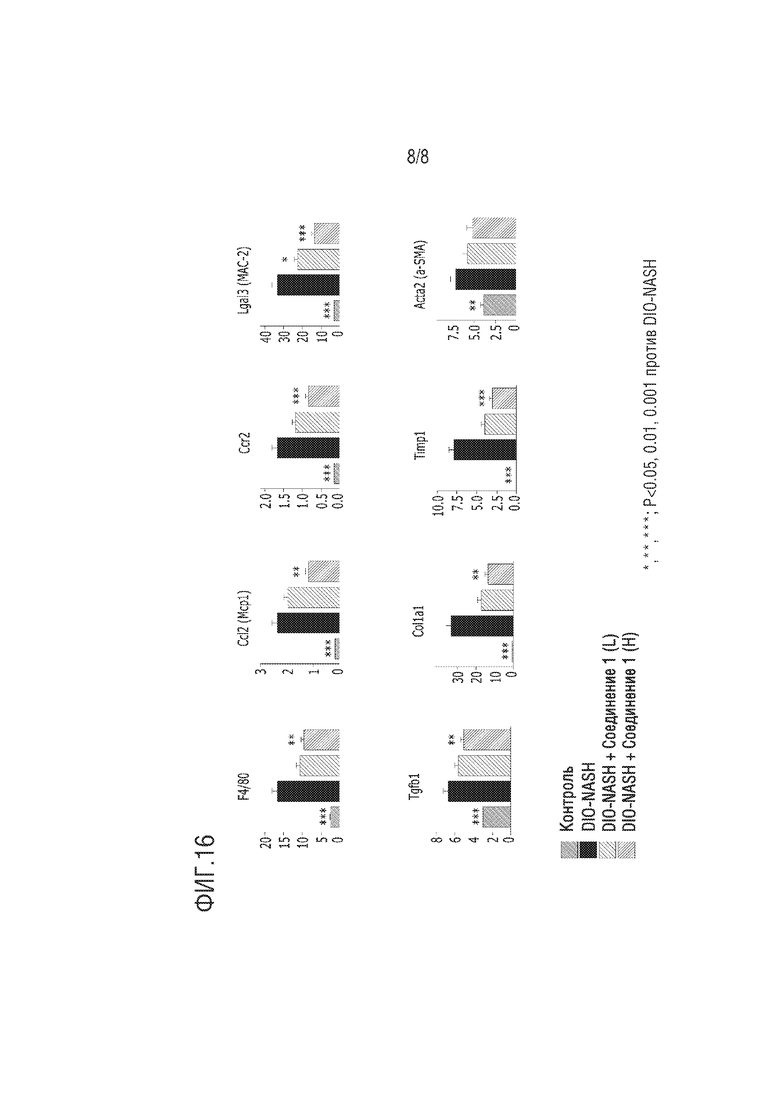
На фиг.16 представлено изображение, демонстрирующее результаты измерения уровня экспрессии генов аттрактанта моноцитов, маркеров макрофагов и маркеров фиброза в тканях печени в модели на мышах с индуцированным неалкогольным стеатогепатитом (*, ** и ***, p<0,05, p<0,01 и p<0,001 против DIO-NASH).
Способ осуществления изобретения
Признаки и преимущества настоящего изобретения, а также способы их достижения станут понятными с помощью иллюстративных вариантов осуществления, подробно описанных в настоящем описании далее. Однако настоящее изобретение не ограничивается примерами, описанными в настоящем описании далее, а может быть осуществлено в различных формах. Далее, приведенные ниже примеры приводятся для лучшего понимания настоящего изобретения и предоставлены только для полной иллюстрации объема настоящего изобретения специалистам в данной области, и, таким образом, настоящее изобретение определяется только объемом его формулы изобретения.
<Пример 1> Подтверждение эффективности лиганда GPR119 в модели на мышах с индуцированным стеатогепатитом вследствие предоставления специального рациона
Для подтверждения эффекта соединения лиганда GPR119 в соответствии с настоящим изобретением на предупреждение неалкогольной жировой инфильтрации печени проводили следующий эксперимент.
Подготовка модели на мышах с неалкогольным стеатогепатитом
Самцов мышей ob/ob в возрасте шести недель кормили специальным рационом, содержащим высокий уровень жиров, высокое содержание фруктозы, и высокий уровень холестерина в течение 10 недель, и, таким образом, у них индуцировали развитие неалкогольного стеатогепатита. Смешанную форму рациона подготавливали так, чтобы суточная доза (3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазола (далее "соединение 1") достигала 100 мг/кг/сутки, и предоставляли мыши в момент начала предоставления специального рациона на 10 недель.
Гистологическое исследование
Для гистологического исследования подготовленных модельных мышей с индуцированным неалкогольным стеатогепатитом подвергали аутопсии для фиксации выделенной ткани печени в 10% формалине и получения парафинового блока, тем самым получая срез ткани толщиной 2 мкм. Для подтверждения инфильтрации воспалительных клеток проводили окрашивание гематоксилином и эозином (HE) с использованием автоматического устройства для окрашивания (Autostainner XL, Leica), и его результаты представлены на фиг.1 и 2.
Как понятно из фиг.1 и 2, мышь ob/ob (Ob-NASH), которую кормили специальным рационом в течение 10 недель, продемонстрировала заметное увеличение количества триглицеридных липидных капель в тканях печени по сравнению с мышью C57BL/6, которую кормили нормальным рационом (нормальная), и также была подтверждена инфильтрация воспалительных клеток. Напротив, было подтверждено, что инфильтрация воспалительных клеток в значительной степени ингибировалась, когда соединение 1 по настоящему изобретению предоставляли одновременно со специальным рационом (Ob-NASH+соединение 1).
Затем для оценки фиброза волокна в ткани печени подвергали специфическому окрашиванию с использованием трихромного окрашивания по Массону или красителя Сириуса красного, и его результаты представлены на фиг.2 и 3.
Как понятно из фиг.2 и 3, было подтверждено, что мышь ob/ob, которую кормили специальным рационом в течение 10 недель, демонстрирует окрашенные фиолетовым ткани печени в целом со значительным прогрессированием фиброза в отличие от мыши C57BL/6, которую кормили нормальным рационом, но фиброз тканей печени значительно ингибировался, когда одновременно со специальным рационом предоставляли соединение 1 по настоящему изобретению.
Измерение уровней AST и ALT в крови
Модельных мышей с индуцированным неалкогольным стеатогепатитом подвергали аутопсии, после которой выделяли плазму для количественного определения аспартатаминотрансферазы (AST) и аланинаминотрансферазы (ALT) с использованием автоматического анализатора крови (Konelab 20i), и его результаты представлены на фиг.4.
Как показано на фиг.4, было подтверждено, что мышь ob/ob, которую кормили специальным рационом в течение 10 недель, демонстрировала значительное повышение уровней ALT и AST в крови, которое является маркером повреждения печени, вследствие повреждения тканей печени, в отличие от мыши C57BL/6, которую кормили нормальным рационом. С другой стороны, было подтверждено, что мышь ob/ob, которой вводили соединение 1 по настоящему изобретению вместе со специальным рационом, демонстрировала значительное ингибирование повышения уровней ALT и AST, что означает, что повреждение гепатоцитов снижается.
Подтверждение концентрации белков, ассоциированных с воспалением и фиброзом
Для оценки эффекта на экспрессию связанных с воспалением генов и связанных с фиброзом белков в тканях печени ткани печени, полученные из модельных мышей, помещали в буфер RIPA (Cell Signaling) и на них разбрызгивали TissueLyser IITM (Quiagen), после чего проводили количественное определение концентрации тотального белка с использованием набора Pierce BCA Protein Assay Kit (Thermo Fisher Scientific) и концентрации белка Ccl2 (=Mcp1; R&D Systems, MJE00) и Timp1 (R&D Systems, MTM100) мыши в тканях печени количественно определяли с использованием коммерчески доступного набора ELISA, так что его результаты представлены на фиг.5.
Как показано на фиг.5, было подтверждено, что мышь, которую кормили специальным рационом, демонстрирует повышение концентраций в тканях печени белка Ccl2 (=Mcp1), который является фактором, индуцирующим воспалительные клетки в тканях печени, и Timp1, который является эндогенным ингибитором ферментов, деградирующих волокна, отложенные в тканях печени, в то время как уровни белков Ccl2 и Timp1 значительно ингибируются, когда соединение 1 по настоящему изобретению вводят вместе со специальным рационом.
Подтверждение экспрессии генов, ассоциированных с воспаление и фиброзом
Для измерения уровня экспрессии связанных с воспалением генов и связанных с фиброзом генов в тканях печени Trizol® (Invitrogen) добавляли к тканям печени, полученным из модельных мышей, после чего тотальную РНК экстрагировали из тканей способом, описанным изготовителем, а затем синтезировали кДНК с использованием обратной транскриптазы. Затем проводили полимеразную цепную реакцию в реальном времени на устройстве LightCycler®480 Instrument II (RocheLifeScience) с использованием реагента SYBR Green I Master Mix (Roche, 04707516001), и ее результаты представлены на фиг.6.
Как показано на фиг.6, было подтверждено, что мышь, которую кормили специальным рационом в течение 10 недель, демонстрирует увеличение экспрессии связанных с воспалением генов мыши (Ccl2, Lgals3, Tnfa) и связанных с фиброзом генов (Tgfb1, Col1a, Timp1, Timp2, Acta2), в то время как увеличение экспрессии генов, ассоциированных с воспалением и фиброзом, значительно ингибируется когда вводят соединение 1 по настоящему изобретению вместе со специальным рационом.
Указанные выше результаты показывают, что соединение по настоящему изобретению имеет превосходный эффект на неалкогольную жировую инфильтрацию печени посредством ингибирования повреждения, воспаления и фиброза тканей печени.
<Пример 2> Подтверждение ингибиторного эффекта на дифференцировку моноцитов человека и активацию дифференцированных макрофагов
Для оценки прямого противовоспалительного эффекта соединения в соответствии с настоящим изобретением, подтверждали эффект на дифференцировку моноцитов человека и их активацию.
Сначала, в результате оценки экспрессии гена GPR119 в клетках в момент времени перед дифференцировкой моноцитов человека (THP-1, ATCC® TIB-202™) в макрофаги и после дифференцировки в течение 24 и 48 часов с использованием форбола 12-миристата 13-ацетата (PMA), было подтверждено, что экспрессия рецептора GPR119 возрастает с течением времени по мерее дифференцировки моноцитов в макрофаги (фиг.7).
Затем моноциты THP-1 обрабатывали PMA (50 нг/мл) в течение 48 часов для дифференцировки в макрофаги, одновременно также обрабатывая соединением 1, затем проводили замену на бессывороточную среду, а затем обрабатывали липополисахаридами (LPS, 0,5 нг/мл) в течение четырех часов для количественного определения интерлейкина-1β (IL-1β, R&D Systems, DY201), секретируемого в среду, с использованием коммерческого набора ELISKA, и оценки эффекта на дифференцировку моноцитов, и его результаты приведены на фиг.8.
Как показано на фиг.8, было подтверждено, что секреция IL-1β, вызванная активацией макрофагов, снижается зависимым от концентрации образом при обработке соединение по настоящему изобретению в процессе дифференцировки моноцитов в макрофаги.
Кроме того, после обработки дифференцированных макрофагов соединением 1 в течение 48 часов секретируемый IL-1β количественно определяли тем же способом, который описан выше в отношении активации иммунных клеток посредством LPS, для оценки эффекта на активацию дифференцированных макрофагов. Таким образом, результаты представлены на фиг.9.
Как показано на фиг.9, было подтверждено, что секреция IL-1β, вызванная активацией макрофагов, снижается зависимым от концентрации образом, даже когда дифференцированные макрофаги обрабатывают соединением по настоящему изобретению.
Указанные выше результаты указывают на то, что соединение по настоящему изобретению обладает превосходным эффектом на предупреждение и лечение неалкогольной жировой инфильтрации печени посредством прямого ингибирования дифференцировки и активации иммунных клеток.
<Пример 3> Подтверждение эффективности лиганда GPR119 у модельных мышей с индуцированным стеатогепатитом вследствие предоставления специального рациона
Для подтверждения эффекта соединения лиганда GPR119 в соответствии с настоящим изобретением на лечение неалкогольной жировой инфильтрации печени проводили следующий эксперимент.
Подготовка модельной мыши с неалкогольным стеатогепатитом и схема исследования
Самцов мышей C57BL/6J в возрасте шести недель кормили специальным рационом, содержавшим высокий уровень жиров, высокое содержание фруктозы, и высокий уровень холестерина в течение 26 недель, и, таким образом, у них индуцировали развитие неалкогольного стеатогепатита. Индукцию жировой инфильтрации печени и воспалительного фиброза подтверждали посредством биопсии тканей печени за три недели до предоставления лекарственного средства, и мышей равномерно распределяли в каждую из групп на основе площади окрашенного коллагена в тканях печени. Корм получали путем смешения соединения в соответствии с настоящим изобретением с кормом специального рациона и предоставляли в течение дополнительных восьми недель. В зависимости от рациона, предоставляемого мышам, каждую из групп классифицировали на контрольную группу, которую кормили нормальным рационом (нормальная), группу положительного контроля, в которой мышам с индуцированным неалкогольным стеатогепатитом вследствие специального рациона не предоставляли лекарственное средство (DIO-NASH), и группу, в которой мышам с индуцированным неалкогольным стеатогепатитом предоставляли соединение 1 в количестве 30 мг/кг/сутки (L) и 100 мг/мг/сутки (H) (Cmpd1 (L) и Cmpd1 (H), соответственно).
Гистологическое исследование
Для гистологического исследования подготовленных модельных мышей C57BL/6J подвергали аутопсии для фиксации выделенной ткани печени в 10% формалине и получения парафинового блока, тем самым получая срез ткани толщиной 2 мкм. Затем проводили окрашивание гематоксилином и эозином (HE) с использованием автоматического устройства для окрашивания (Autostainner XL, Leica), и его результаты представлены на фиг.10. Кроме того, ткань печени, выделенную из модельных мышей C57BL/6J, использовали для измерения содержания триглицеридов ткани печени с использованием триглицеридного реагента (Roche Diagnotics, #22-045-795), и результаты представлены на фиг.11.
Как понятно из фиг.10 и 11, мыши, которых кормили только специальным рационом (DIO-NASH), продемонстрировали значительное увеличение жировых отложений и инфильтрации воспалительных клеток в тканях печени по сравнению с мышами, которых кормили нормальным рационом (нормальные), в то время как группа DIO-NASH_Compd1 (H), которую кормили соединением 1 по настоящему изобретению вместе со специальным рационом, продемонстрировала значительное снижение жировых отложений и инфильтрации воспалительных клеток.
Кроме того, в результате вычисления показателя активности NAFLD (NAS), отражающего долю жировых клеток, инфильтрацию воспалительных клеток и повреждение гепатоцитов на основе описанного выше гистологического исследования до и после введения, ухудшение заболевания происходило у 50% группы DIO-NASH, в то время как ни одной из особей не происходило ухудшение в случае введения соединения, и происходило смягчение заболевания приблизительно у 50% группы DIO-NASH_Compd1 (фиг.12).
Затем для оценки фиброза волокна в ткани печени подвергали специфическому окрашиванию с использованием красителя Сириуса красного у мышей в каждой группы, и содержание коллагена типа I в тканях печени определяли способом визуализирующего анализа после иммунного окрашивания, так что его результаты представлены на фиг.13 и 14.
Как показано на фиг.13 и 14, мыши, которых кормили только специальным рационом (DIO-NASH), продемонстрировали выраженное прогрессирование фиброза в тканях печени по сравнению с мышами, которых кормили нормальным рационом (нормальные), в то время как группа, которую кормили соединением 1 по настоящему изобретению вместе со специальным рационом (DIO-NASH_Compd1), продемонстрировала выраженное снижение формирования сшивок волокон в тканях печени, а также продемонстрировала значительное снижение уровня коллагена типа I.
Измерение уровней AST и ALT в крови
Каждую из групп мышей подвергали аутопсии, после которой выделяли плазму для количественного определения аспартатаминотрансферазы (AST) и аланинаминотрансферазы (ALT) с использованием автоматического анализатора крови (Konelab 20i). Таким образом, его результаты представлены на фиг.15.
Как показано на фиг.15, группа мышей, которых кормили только специальным рационом (DIO-NASH), продемонстрировала значительное увеличение концентрации ALT и AST в крови по сравнению с мышами, которых кормили нормальным рационом, в то время как группа мышей, которых кормили соединением 1 по настоящему изобретению вместе со специальным рационом (DIO-NASH_Compd1), продемонстрировала значительное ингибирование повышения ALT и AST.
Подтверждение изменения экспрессии генов
Для анализа изменения общей экспрессии генов в тканях печени, выделенных из описанных выше модельных мышей через восемь недель после введения лекарственного средства, фракцию выделенной РНК использовали для получения библиотеки с использованием NeoPrep (Illumina), и подвергали определению профиля RNAseq посредством NexSeq 500 (Illumina), после чего проводили биоинформатический анализ и изменения основных групп генов классифицировали для каждой функции, так что результаты представлены на фиг.16.
Как показано на фиг.16, мыши, которых кормили только специальным рационом (DIO-NASH), продемонстрировали повышение экспрессии аттрактантов моноцитов, маркеров макрофагов и маркеров фиброза в тканях печени по сравнению с мышами, которых кормили нормальным рационом (нормальные), в то время как группа мышей DIO-NASH_Compd1, которых кормили соединением 1 по настоящему изобретению вместе со специальным рационом, продемонстрировала выраженное снижение уровня указанных выше маркеров.
Приведенные выше результаты указывают на то, что соединение по настоящему изобретению обладает эффектом на неалкогольную жировую инфильтрацию печени посредством ингибирования повреждения, воспаления и фиброза тканей печени, и имеет более превосходный терапевтический эффект посредством сопутствующего введения ингибитора DPPIV.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА | 2021 |
|
RU2803733C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРЕДУПРЕЖДЕНИЯ ИЛИ ЛЕЧЕНИЯ ДИАБЕТА И СВЯЗАННЫХ С НИМ МЕТАБОЛИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2021 |
|
RU2809286C1 |
| Соединение, обладающее агонистической активностью в отношении GPR119, способ его получения и фармацевтическая композиция, содержащая его в качестве эффективного компонента | 2015 |
|
RU2670197C1 |
| КОМБИНАЦИИ ДЛЯ ЛЕЧЕНИЯ НАСГ/НАЖБП И СВЯЗАННЫХ С НИМИ ЗАБОЛЕВАНИЙ | 2019 |
|
RU2776369C1 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ ВЕЩЕСТВА - АГОНИСТЫ GPR119 | 2017 |
|
RU2734500C2 |
| СОЕДИНЕНИЯ И КОМПОЗИЦИИ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ GPR119 | 2008 |
|
RU2443699C2 |
| НОВОЕ ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ СОЕДИНЕНИЙ ТИЕНО[3,2-D]ПИРИМИДИН-4-ОНА | 2019 |
|
RU2768828C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ НЕАЛКОГОЛЬНОГО СТЕАТОГЕПАТИТА У КРЫС | 2009 |
|
RU2394281C1 |
| НОВОЕ ПРОИЗВОДНОЕ ПИПЕРИДИНА И СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНГИБИРОВАНИЯ АУТОТАКСИНА | 2022 |
|
RU2834850C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПЕЧЕНИ | 2018 |
|
RU2723686C1 |
Группа изобретений относится к области фармакологии и медицины и направлена на предупреждение или лечение неалкогольной жировой инфильтрации печени. В частности описано применение соединения, соответствующего следующей химической формуле 1, или его фармацевтически приемлемых солей для предупреждения или лечения неалкогольной жировой инфильтрации печени: где A представляет собой оксадиазол, причем A независимо не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из прямого и разветвленного C1-C6 алкила; B представляет собой пиримидин, B независимо не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из прямого и разветвленного C1-C6 алкила; и X независимо представляет собой F. Кроме того, описаны способы предупреждения или лечения неалкогольной жировой инфильтрации печени и применение соединения формулы 1, или его фармацевтически приемлемых солей, для изготовления лекарственного средства для предупреждения или лечения неалкогольной жировой инфильтрации печени. Технический результат: обеспечение эффективного предупреждения или лечения неалкогольной жировой инфильтрации печени. 4 н. и 5 з.п. ф-лы, 16 ил., 3 пр.
[Химическая формула 1]
1. Применение соединения, соответствующего следующей химической формуле 1, или его фармацевтически приемлемых солей для предупреждения или лечения неалкогольной жировой инфильтрации печени:
[Химическая формула 1]
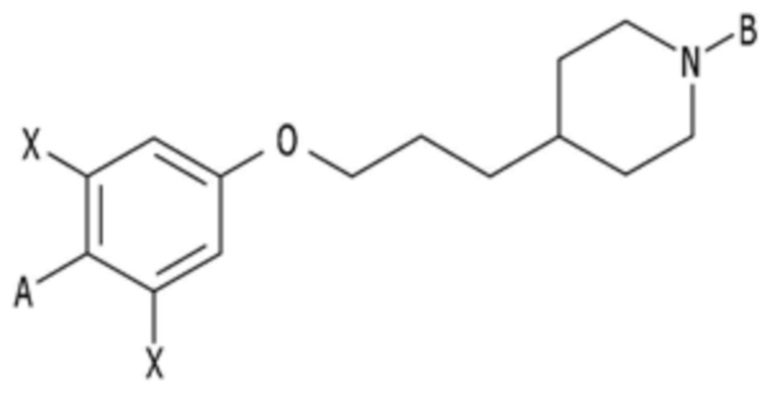 ,
,
где A представляет собой оксадиазол, причем A независимо не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из прямого и разветвленного C1-C6 алкила;
B представляет собой пиримидин, B независимо не замещен или замещен по меньшей мере одним заместителем, выбранным из группы, состоящей из прямого и разветвленного C1-C6 алкила; и
X независимо представляет собой F.
2. Применение по п.1, где соединение, соответствующее химической формуле 1, представляет собой 3-(4-(3-(1-(5-этилпиримидин-2-ил)пиперидин-4-ил)пропокси)-2,6-дифторфенил)-5-изопропил-1,2,4-оксадиазол.
3. Применение по п.1, где неалкогольная жировая инфильтрация печени выбрана из группы, состоящей из простой жировой инфильтрации печени, неалкогольного стеатогепатита, фиброза печени и цирроза.
4. Применение по п.1, где соединение химической формулы 1 или его фармацевтически приемлемые соли ингибирует отложение триглицеридов в тканях печени.
5. Применение по п.1, где соединение химической формулы 1 или его фармацевтически приемлемые соли ингибирует инфильтрацию воспалительных клеток в ткани печени.
6. Применение по п.1, где соединение химической формулы 1 или его фармацевтически приемлемые соли ингибирует фиброз тканей печени.
7. Способ предупреждения или лечения неалкогольной жировой инфильтрации печени, причем способ включает введение терапевтически эффективного количества соединения, соответствующего приведенной ниже химической формуле 1, или его фармацевтически приемлемых солей индивидууму, нуждающемуся в лечении:
[Химическая формула 1]
 ,
,
где A, B и X являются такими, как показано в п.1.
8. Способ предупреждения или облегчения неалкогольной жировой инфильтрации печени, причем способ включает введение терапевтически эффективного количества пищевой композиции, содержащей соединение, соответствующее приведенной ниже химической формуле 1, или его фармацевтически приемлемых солей индивидууму, нуждающемуся в облегчении:
[Химическая формула 1]
 ,
,
где A, B и X являются такими, как в п.1.
9. Применение соединения, соответствующего приведенной ниже химической формуле 1, или его фармацевтически приемлемых солей для изготовления лекарственного средства для предупреждения или лечения неалкогольной жировой инфильтрации печени:
[Химическая формула 1]
 ,
,
где A, B и X являются такими же, как и в п.1.
| WO 2016068453 A, 06.05.2016 | |||
| US 2017049773 A1, 23.02.2017 | |||
| WO 2010004347 A, 14.01.2010 | |||
| RU 2012145116 A, 27.04.2014. |
Авторы
Даты
2022-03-25—Публикация
2019-09-11—Подача