Перекрестная ссылка на родственную заявку
Данная патентная заявка заявляет приоритет по первоначальной патентной заявке США №62/867619, поданной 27 июня 2019 года, которая включена в данный документ посредством ссылки во всей своей полноте.
Утверждение относительно исследования или разработки, финансируемых из федерального бюджета
Данное изобретение было создано при поддержке правительства под номером проекта ВС010985 национальными институтами здравоохранения, национальным институтом онкологии. Государство имеет определенные права в данном изобретении.
Включение посредством ссылки материала, представленного в электронной форме
В данный документ посредством ссылки во всей своей полноте включен машиночитаемый перечень нуклеотидных/аминокислотных последовательностей, поданный наряду с этим и идентифицированный следующим образом: один (текстовый) файл, размером 357775 байт ASCII, с названием «749338_ST25.txt», датированный 23 июня 2020 года.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Некоторые виды рака могут иметь очень ограниченные варианты лечения, в частности, когда рак становится метастатическим и неоперабельным. Несмотря на прогресс в видах лечения, таких как, например, хирургическое вмешательство, химиотерапия и лучевая терапия, прогноз в случае многих видов рака, таких как, например, рак поджелудочной железы, коло ректальных рак, рак легкого, рак эндометрия, рак яичника и рак предстательной железы, может быть неблагоприятным. Соответственно, существует неудовлетворенная потребность в дополнительных видах лечения рака.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Согласно одному воплощению изобретения предложен выделенный или очищенный Т-клеточный рецептор (TCR - от англ. Т cell receptor), обладающий антигенной специфичностью в отношении аминокислотной последовательности человеческого p53R175H или человеческого p53Y220C, где TCR содержит следующие аминокислотные последовательности: (1) все из SEQ ID NO: 3-8; (2) все из SEQ ID NO: 14-19; (3) все из SEQ ID NO: 25-30; (4) все из SEQ ID NO: 36-41; (5) все из SEQ ID NO: 47-52; (6) все из SEQ ID NO: 58-63; (7) все из SEQ ID NO: 69-74; (8) все из SEQ ID NO: 80-85; или (9) все из SEQ ID NO: 131-136.
В одном воплощении изобретения TCR обладает антигенной специфичностью в отношении аминокислотной последовательности человеческого p53R175H или человеческого p53Y220C, где аминокислотная последовательность человеческого p53R175H представляет собой SEQ ID NO: 2 или SEQ ID NO: 96.
В одном воплощении изобретения TCR обладает антигенной специфичностью в отношении аминокислотной последовательности человеческого p53R175H или человеческого p53Y220C, где аминокислотная последовательность человеческого p53Y220C представляет собой SEQ ID NO: 113.
В одном воплощении изобретения TCR не обладает антигенной специфичностью в отношении аминокислотной последовательности человеческого р53 дикого типа SEQ ID NO: 95.
В одном воплощении изобретения TCR не обладает антигенной специфичностью в отношении аминокислотной последовательности человеческого р53 дикого типа SEQ ID NO: 112.
Согласно еще одним воплощениям изобретения предложены родственные полипептиды и белки, а также родственные нуклеиновые кислоты, рекомбинантные экспрессионные векторы, клетки-хозяева, популяции клеток и фармацевтические композиции, связанные с TCR по изобретению.
Согласно воплощению изобретения предложена выделенная или очищенная нуклеиновая кислота, содержащая, от 5' к 3', первую последовательность нуклеиновой кислоты и вторую нуклеотидную последовательность, где первая и вторая нуклеотидная последовательность, соответственно, кодируют аминокислотные последовательности SEQ ID NO: 9 и 10; 10 и 9; 20 и 21; 21 и 20; 31 и 32; 32 и 31; 42 и 43; 43 и 42; 53 и 54; 54 и 53; 64 и 65; 65 и 64; 75 и 76; 76 и 75; 86 и 87; 87 и 86; 137 и 138; 138 и 137; 142 и 143; 143 и 142; 144 и 145; 145 и 144; 146 и 147; 147 и 146; 148 и 149; 149 и 148; 150 и 151; 151 и 150; 152 и 153; 153 и 152; 154 и 155; 155 и 154; 156 и 157; 157 и 156; 159 и 158; 158 и 159; 178 и 10; 10 и 178; 181 и 21; 21 и 181; 184 и 32; 32 и 184; 187 и 43; 43 и 187; 190 и 54; 54 и 190; 193 и 65; 65 и 193; 196 и 76; 76 и 196; 199 и 87; 87 и 199; 137 и 202; 202 и 137; 9 и 205; 205 и 9; 20 и 207; 207 и 20; 31 и 209; 209 и 31; 42 и 211; 211 и 42; 53 и 213; 213 и 53; 64 и 215; 215 и 64; 75 и 217; 217 и 75; 86 и 219; 219 и 86; 137 и 221; 221 и 137; 223 и 202; 202 и 223; 223 и 221; 221 и 223; 20 и 226; 226 и 20; 181 и 226; или 226 и 181.
Согласно воплощению изобретения предложена выделенная или очищенная нуклеиновая кислота, содержащая, от 5' к 3', первую последовательность нуклеиновой кислоты и вторую нуклеотидную последовательность, где первая и вторая нуклеотидная последовательность, соответственно, кодируют аминокислотные последовательности SEQ ID NO: 11 и 12; 12 и 11; 22 и 23; 23 и 22; 33 и 34; 34 и 33; 44 и 45; 45 и 44; 55 и 56; 56 и 55; 66 и 67; 67 и 66; 77 и 78; 78 и 77; 88 и 89; 89 и 88; 139 и 140; 140 и 139; 160 и 161; 161 и 160; 162 и 163; 163 и 162; 164 и 165; 165 и 164; 166 и 167; 167 и 166; 168 и 169; 169 и 168; 170 и 171; 171 и 170; 172 и 173; 173 и 172; 174 и 175; 175 и 174; 176 и 177; 177 и 176; 179 и 12; 12 и 179; 182 и 23; 23 и 182; 185 и 34; 34 и 185; 188 и 45; 45 и 188; 191 и 56; 56 и 191; 194 и 67; 67 и 194; 197 и 78; 78 и 197; 200 и 89; 89 и 200; 139 и 203; 203 и 139; 11 и 206; 206 и 11; 22 и 208; 208 и 22; 33 и 210; 210 и 33; 44 и 212; 212 и 44; 55 и 214; 214 и 55; 66 и 216; 216 и 66; 77 и 218; 218 и 77; 88 и 220; 220 и 88; 139 и 222; 222 и 139; 224 и 203; 203 и 224; 224 и 222; 222 и 224; 22 и 227; 227 и 22; 182 и 227; или 227 и 182.
В одном воплощении изобретения выделенная или очищенная нуклеиновая кислота дополнительно содержит третью нуклеотидную последовательность, размещенную между первой и второй нуклеотидной последовательностью, где третья нуклеотидная последовательность кодирует расщепляемый линкерный пептид.
В одном воплощении изобретения расщепляемый линкерный пептид содержит аминокислотную последовательность SEQ ID NO: 94.
В одном воплощении изобретения выделенная или очищенная нуклеотидная кислота кодирует аминокислотную последовательность, выделенную из группы, состоящей из: SEQ ID NO: 13, 24, 35, 46, 57, 68, 79, 90, 141, 180, 183, 186, 189, 192, 195, 198, 201, 204, 225, 228 и 229.
В одном воплощении изобретения рекомбинантный экспрессионный вектор представляет собой транспозон или лентивирусный вектор.
Согласно еще одному воплощению изобретения предложен выделенный или очищенный TCR, полипептид или белок, кодируемый любой из нуклеиновых кислот или векторов, описанных в данном документе.
Согласно еще одному воплощению изобретения предложен выделенный или очищенный TCR, полипептид или белок, которые получен в результате экспрессии любой их нуклеиновых кислот или векторов, описанных в данном документе, в клетке.
Согласно еще одному воплощению изобретения предложен способ получения клетки-хозяина, экспрессирующей TCR, который обладает антигенной специфичностью в отношении пептида с SEQ ID NO: 2, 96 или 113, причем способ включает приведение клетки в контакт с любым из векторов, описанных в данном документе, в условиях, допускающих введение вектора в клетку.
Согласно еще одному воплощению изобретения предложена выделенная или очищенная клетка-хозяин, содержащая любую из нуклеиновых кислот или рекомбинантных экспрессионных векторов, описанных в данном документе.
В одном воплощении изобретения клетка-хозяин представляет собой человеческий лимфоцит.
В одном воплощении изобретения клетка-хозяин выбрана из группы, состоящей из Т-клетки, Т-клетки - естественного киллера (NKT - от англ. natural killer Т cell), инвариантной Т-клетки - естественного киллера (iNKT) и естественного киллера (NK - от англ. natural killer).
Согласно еще одному воплощению изобретения предложен способ получения любого из TCR, полипептидов или белков, описанных в данном документе, причем способ включает культивирование любой из клеток-хозяев или популяций клеток-хозяев, описанных в данном документе, таким образом, что получают TCR, полипептид или белок.
Согласно еще одному воплощению изобретения предложен любой из TCR, полипептидов, белков, нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев, популяций клеток или фармацевтических композиций, описанных в данном документе, для применения в индукции иммунного ответа на рак у млекопитающего. В одном воплощении согласно изобретению предложен способ индукции иммунного ответа на рак у млекопитающего, включающий введение любого из TCR, полипептидов, белков, нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев, популяций клеток или фармацевтических композиций, описанных в данном документе.
Согласно еще одним воплощениям изобретения предложены способы выявления наличия рака у млекопитающего и способы лечения или предупреждения рака у млекопитающего. В одном воплощении согласно изобретению предложен способ лечения или предупреждения рака у млекопитающего, включающий введение любого из TCR, полипептидов, белков, нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев, популяций клеток или фармацевтических композиций, как описано в данном документе. В одном воплощении рак представляет собой холангиокарциному, меланому, рак толстой кишки, рак прямой кишки, рак яичника, рак эндометрия, немелкоклеточный рак легкого (NSCLC - от англ. non-small cell lung cancer), глиобластому, рак шейки матки, рак головы и шеи, рак молочной железы, рак поджелудочной железы или рак мочевого пузыря.
В одном воплощении изобретения при раке, как известно, имеется мутация R175H или Y220C в человеческом р53.
КРАТКОЕ ОПИСАНИЕ НЕСКОЛЬКИХ ПРЕДСТАВЛЕНИЙ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фиг. 1А представляет собой схему, показывающую схему эксперимента, где исходные ворота выглядели следующим образом: лимфоциты → одиночные клетки → живые (PI (от англ. propidium iodide - йодид пропидия)-негативные) → CD3+ (Т-клетки).
Фиг. 1В-1С представляют собой графики, показывающие процентное содержание 4-1ВВ позитивных клеток, выявляемое после IVS (от англ. in vitro stimulation - стимуляция in vitro) (TP53-TMG-IVS (В) или p53-LP-IVS (С)) и обогащения 4-1ВВ/ОХ40. Культуры, считающиеся позитивными, выделены жирным шрифтом. Показаны ответы на мутантный ТР53 (TMG (закрашенные круги); LP (закрашенные квадраты)) и аналоги дикого типа (WT) (TMG (незакрашенные круги); LP (незакрашенные квадраты)).
На Фиг. 1D показаны репрезентативные графики проточной цитометрии от культуры 4141-CD8 TP53-TMG-IVS после совместного культивирования с аутологичными антигенпрезентирующими клетками, которых подвергали электропорации с использованием тандемных минигенов (TMG - от англ. tandem minigene) WT или мутантного (MUT) ТР53.
На Фиг. 1Е показана секреция интерферона-гамма (левая ось) или повышающая регуляция 4-1ВВ (правая ось), измеренная после сортировки CD4 Т-клеток после контакта с антигеном и стимуляции in vitro незрелыми дендритными клетками, которых подвергали электропорации с использованием мутантного ТР53-TMG. Затем культуру культивировали с незрелыми дендритными клетками, которых подвергали электропорации с использованием мутантного TP53-TMG, и на следующие сутки 4-1ВВ+ и/или ОХ40+ клетки сортировали и размножали посредством протокола быстрого размножения. После 12-14 суток размножения культуру (4285-CD4 TP53-TMG-IVS) тестировали в отношении специфичности к неоантигену p53-R175H посредством ELISPOT интерферона-гамма (левая ось) или повышающей регуляции 4-1ВВ посредством цитометрии (правая ось).
Фиг. 1F представляет собой график, показывающий секрецию интерферона-γ, как измерено посредством ELISA, в супернатанты сокультуры аутологичных антигенпрезентирующих клеток, в которые по действием импульса вводили 4285-CD4 TP53-TMG-IVS и пептид. Культуру 4285-CD4 TP53-TMG-IVS совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили снижающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи, супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (от англ. Standard Error Of Mean - стандартная ошибка среднего) (n=3, технические повторности).
Фиг. 2А представляет собой график, показывающий клональность общей численности популяций, которая представляет собой нормированную оценку разнородности образца, где числа, ближе к 1, являются менее различными. Секвенирование TCRB проводили на PBL до и после размножения с использованием IVS и обогащения 4-1ВВ/ОХ40 или с LP или TMG. Культуры с подтвержденными ответами на неоантиген р53 выделены с помощью звездочки.
Фиг. 2В представляет собой график, показывающий максимальную продуктивную уникальную частоту CDR3B из каждой популяции. Секвенирование TCRB проводили на PBL до и после размножения с использованием IVS и обогащения 4-1ВВ/ОХ40 или с LP или с TMG. Культуры с подтвержденными ответами на неоантиген р53 выделены звездочкой.
Фиг. 2С представляет собой график, показывающий результаты эксперимента, в котором нетрансдуцированные Т-клетки (отрицательный контроль для TCR-трансдуцированных Т-клеток) совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175 длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2D представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR1, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2Е представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR2, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2F представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR3, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2G представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR5, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2Н представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR6, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2I представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR7, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2J представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, трансдуцированные 4285-PBL-TCR9, совместно культивировали с незрелыми дендритными клетками, в которые под действием импульса вводили уменьшающиеся концентрации или WT (незакрашенные круги) или мутантных (закрашенные квадраты) пептидов p53-R175, длиной 25 аминокислот. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 2K-2L представляют собой графики, показывающие процентное содержание клонотипов TCRB, измеренное после мечения CDR3B с известной специфичностью в отношении мутантного ТР53 до (PBL) и после протокола (IVS/обогащение) IVS и обогащения 4-1ВВ. P53R175H-специфичные клонотипы показаны на K. P53R248W-специфичные клонотипы показаны на L.
Фиг. 3А представляет собой график, показывающий процентное содержание 4-1ВВ-позитивных клеток, измеренное после трансфекции линии клеток обезьяны COS7 указанным HLA (от англ. human leukocyte antigen - человеческий лейкоцитарный антиген) и в которые под действием импульса вводили указанный минимальный пептид р53 (WT (незакрашенные столбцы); мутантный (закрашенные столбцы)). Показаны результаты по культуре 4141-CD8 TP53-TMG-IVS. В TMG-wtR175 имелся мутантный ТР53 во всех положениях, за исключением R175H. Последовательность HMTEWRRC представляет собой SEQ ID NO: 95. Последовательность HMTEWRJHC представляет собой SEQ ID NO: 96.
Фиг. 3В представляет собой график, показывающий количество IFN-γ, измеренное после трансфекции линии клеток обезьяны COS7 указанным HLA и в которые под действием импульса вводили указанный минимальный пептид р53 (WT (незакрашенные столбцы); мутантный (закрашенные столбцы)). Показаны результаты по культуре 4266-CD8 TP53-TMG-IVS. Последовательность SSCMGGMNRR представляет собой SEQ ID NO: 97. Последовательность SSCMGGMNWR представляет собой SEQ ID NO: 98.
Фиг. 3С представляет собой график, показывающий результаты эксперимента, в котором линию опухолевых клеток обезьяны COS7 трансфицировали плазмидной ДНК HLA, соответствующей гаплотипу пациента 4285, и или только WT ТР53 TMG в положении R175H (WT-R175-TMG; незакрашенные столбцы) или мутантным TP53-TMG, содержащим неоантиген р53-R175H (закрашенные столбцы). На следующие сутки культуру 4285-CD4 TP53-TMG-IVS добавляли и совместно культивировали. После инкубации в течение ночи супернатанты сокультуры добавляли и совместно культивировали. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма Данные представляют собой среднее ± SEM (n=3).
На Фиг. 3D показаны графики по проточной цитометрии, показывающие повышающую регуляцию 4-1ВВ на CD8+ Т-клетках из культур TP53-TMG-IVS (4266-CD8 слева и 4141-CD8 справа) после совместного культивирования с ТС#4266 (аутологичный трансплантат от пациента 4266; А*68:01; p53R248W) и клетками Saos2 (А*02:01), сверхэкспрессирующими полноразмерный ген p53R175H.
Фиг. 4 представляет собой график, показывающий результаты эксперимента, в котором линию опухолевых клеток обезьяны COS7 трансфицировали DRA1*01:01:01 и DRB1*13:01:01 и или нерелевантным (незакрашенные столбцы), или WT ТР53 TMG только в положении R175H (WT-R175-TMG; серые столбцы) или мутантным TP53-TMG, содержащим неоантиген p53-R175H (закрашенные столбцы). На следующие сутки Т-клетки, трансдуцированные 4285-PBL-TCR или нетрансдуцированные, добавляли и совместно культивировали. После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 5 представляет собой график, показывающий результаты эксперимента, в котором клоны Т-клетки получали посредством предельного разведения после сортировки CD8+ Т-клеток из культуры фрагмента опухоли 4259-F1. 24 Культуры совместно культивировали с опухолевыми клетками Т2 (HLA-A*02:01), в которые под действием импульса вводили ДМСО (носитель пептида), пептид WT p53-Y220 или пептид MUT p53-Y220C. После инкубации в течение ночи клетки окрашивали на CD3, CD8 и 4-1ВВ, затем анализировали посредством проточной цитометрии. Изображены частоты встречаемости CD8+4-1BB+ Т-клеток из культур.
Фиг. 6 представляет собой график, показывающий результаты эксперимента, в котором 4259-F1-TCR трансдуцировали в донорские Т-клетки периферической крови, затем совместно культивировали с опухолевыми клетками Т2 (HLA-А*02:01), в которые под действием импульса вводили уменьшающиеся концентрации или пептида WT p53-Y220 (WPYEPPEV) (SEQ ID NO: 112) или пептида MUT p53-Y220C (WPCEPPEV) (SEQ ID NO: 113). После инкубации в течение ночи супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Данные представляют собой среднее ± SEM (n=3).
Фиг. 7 представляет собой график, показывающий результаты эксперимента, в котором Т-клетки, или не экспрессирующие TCR (нетрансдуцированные), или экспрессирующие р53-R175H-специфичный TCR или 4259-F1-TCR, совместно культивировали с опухолевыми клетками, которые или с или без экспрессии HLA-А*02:01, p53-R175H или p53-Y220C. После инкубации в течение ночи клетки окрашивали на CD3, CD8 и 4-1ВВ, затем анализировали посредством проточной цитометрии. Изображены частоты встречаемости CD8+4-1ВВ+ Т-клеток из культур. Данные представляют собой среднее ± SEM (n=3).
На Фиг. 8 показано выравнивание аминокислотных последовательностей девяти вариантов сплайсинга р53. SP|P04637|P53_HUMAN (SEQ ID NO: 1); SP|P04637-2|P53_HUMAN (SEQ ID NO: 114); SP|P04637-3|P53_HUMAN (SEQ ID NO: 115); SP|P04637-4|P53_HUMAN (SEQ ID NO: 116); SP|P04637-5|P53_HUMAN (SEQ ID NO: 117); SP|P04637-6|P53_HUMAN (SEQ ID NO: 118); SP|P04637-7|P53_HUMAN (SEQ ID NO: 119); SP|P04637-8|P53_HUMAN (SEQ ID NO: 120); и SP|P04637-9|P53_HUMAN (SEQ ID NO: 121).
На Фиг. 9 показано выравнивание аминокислотных последовательностей частей последовательности TRBV7-9*03 с аминокислотной последовательностью TRBV7-9*01. «L36092|TRBV7-9*01|Homo» представляет собой SEQ ID NO: 129. «AF009663|TRBV7-9*03|Homo» представляет собой SEQ ID NO: 130.
Фиг. 10 представляет собой график, показывающий процентное содержание 4-1ВВ-позитивных клеток (%CD8+) (правая у-ось; черные столбцы) и IFN-γ (пятна/ 2×104 клеток) (левая у-ось; заштрихованные столбцы), измеренное после совместного культивирования TIL от Пациента 4141 (культуры фрагмента 12) с аутологичными АРС, трансфицированными TMG, кодирующим нерелевантные мутации (TMG-IRR), последовательностью р53 WT (TP53-wt-TMG) или последовательностью мутантного р53, включающей R175H (TP53-mut-TMG). Только среда и РМА и иономицин представляли собой отрицательный и положительный контроли, соответственно.
Фиг. 11 представляет собой график, показывающий число IFN-γ-позитивных пятен на 2×104 эффекторных клеток, измеренное после совместного культивирования TIL от Пациента 4141 (культура фрагмента 12) с клетками Cos7, совместно трансфицированными указанными аллелями HLA и или без дополнительного гена (только HLA; незакрашенные столбцы), или WT ТР53 TMG (серые заштрихованные столбцы) или мутантным ТР53 TMG (черные столбцы), содержащим последовательность p53-R175H.
Фиг. 12 представляет собой график, показывающий концентрацию IFN-γ (пг/мл), измеренную после совместного культивирования Т-клеток, экспрессирующих имитацию (отсутствие TCR) или 4141-TCR1a2, с опухолевыми клетками Т2 (экспрессирующими HLA-A*02:01). В клетки Т2 под действием импульса вводили носитель пептида (ДМСО; серые столбики) или очищенные (больше 95% посредством ВЭЖХ (высокоэффективная жидкостная хроматография)) пептиды, состоящие из пептида WT p53-R175 (заштрихованные серые столбцы) или мутантного пептида p53-R175H (черные столбцы). Только среда (незакрашенные столбцы) и РМА и Иономицин (решетчатые столбцы) представляли собой отрицательный и положительный контроли, соответственно. Данные представляют собой среднее ± SEM (n=3).
Фиг. 13 представляет собой график, показывающий процентное содержание клеток, позитивных в отношении экспрессии одного из указанных маркеров после совместной культивации Т-клеток, экспрессирующих 4141-TCR1a2, с клетками Saos2 (p53-NULL и HLA-A*02:01+), которые были или неманипулированными (незаштрихованные столбцы) или сделаны сверхэкспрессирующими полноразмерный белок p53-R175H (заштрихованные столбцы). Данные представляют собой среднее ± SEM (n=3). Двусторонние t-критерии Стьюдента осуществляли для каждого цитокина между двумя клеточными линиями для статистических анализов (***р<0,001).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Опухолевый белок Р53 (также называемый «ТР53» или «р53») действует как супрессор опухоли, например, посредством регуляции деления клеток. Белок р53 расположен в ядре клетки, где он связывается непосредственно с ДНК. Когда ДНК повреждается, белок р53 участвует в определении того, будет ли ДНК восстановлена, или поврежденная клетка будет подвергаться апоптозу. Если ДНК может быть восстановлена, белок р53 активирует другие гены для устранения повреждения. Если ДНК не может быть восстановлена, белок р53 предотвращает деление клетки и подает ей сигнал для того, чтобы подвергаться апоптозу. Посредством остановки деления клеток с мутированной или поврежденной ДНК, р53 помогает предотвратить развитие опухоли. WT (нормальный) полноразмерный р53 содержит аминокислотную последовательность SEQ ID NO: 1.
Мутации в белке р53 могут уменьшать или исключать функцию белка р53 - супрессора опухоли. В качестве альтернативы или дополнительно, мутация р53 может представлять собой мутацию с приобретением функции, влияя на белок р53 WT доминантно-негативным образом. Мутантный белок р53 может экспрессироваться при любом из множества раковых заболеваний человека, например, при холангиокарциноме, меланоме, раке толстой кишки, раке прямой кишки, раке яичника, раке эндометрия, немелкоклеточном раке легкого (NSCLC), глиобластоме, раке шейки матки, раке головы и шеи, раке молочной железы, раке поджелудочной железы или раке мочевого пузыря.
Согласно воплощению изобретения предложен выделенный или очищенный Т-клеточный рецептор (TCR), обладающий антигенной специфичностью в отношении мутантного человеческого р53 (далее в данном документе, «мутантного р53»). Ниже в данном документе ссылки на «TCR» также относятся к функциональным частям и функциональным вариантам TCR, если не указано иное. Мутации р53 определены в данном документе посредством ссылки на аминокислотную последовательность полноразмерного р53 WT (SEQ ID NO: 1). Мутации р53 описаны в данном документе посредством ссылки на аминокислотный остаток, находящийся в конкретном положении, с последующим номером положения, за которым следует аминокислота, которой заменен тот остаток при конкретной обсуждаемой мутации. Аминокислотная последовательность р53 (например, пептид р53) может содержать меньше, чем все из аминокислотных остатков полноразмерного белка р53 WT. Соответственно, номера положения определены в данном документе посредством ссылки на полноразмерный белок р53 WT (а именно, SEQ ID NO: 1) с пониманием того, что фактическое положение соответствующего остатка в конкретном примере аминокислотной последовательности р53 может отличаться. Поскольку положения представляют собой такие, как определено SEQ ID NO: 1, термин «R175» относится к аргинину, находящемуся в положении 175 SEQ ID NO: 1, «R175H» указывает на то, что аргинин, находящийся в положении 175 SEQ ID NO: 1, заменен гистидином, в то время как «Y220C» указывает на то, что тирозин, находящийся в положении 220 SEQ ID NO: 1, заменен цистеином. Например, когда конкретный пример аминокислотной последовательности р53 представляет собой, например, YKQSQHMTEVVRRCPHHERCSDSDG (SEQ ID NO: 110) (иллюстративный пептид р53 WT, соответствующий смежным аминокислотным остаткам 163-187 SEQ ID NO: 1), «R175H» относится к замене подчеркнутого аргинина в SEQ ID NO: 110 гистидином, даже несмотря на то, что фактическое положение подчеркнутого аргинина в SEQ ID NO: 110 представляет собой 13. Человеческие аминокислотные последовательности р53 с мутацией R175H ниже в данном документе называются «R175H» или «p53R175H». Человеческие аминокислотные последовательности р53 с мутацией Y220C называются ниже в данном документе «Y220C» или «p53Y220C». В том виде, в котором он используется в данном документе, термин «мутантный р53» относится к человеческому p53R175H или человеческому p53Y220C.
Р53 имеет девять известных вариантов сплайсинга. Мутации р53, описанные в данном документе, являются консервативными у всех девяти вариантов сплайсинга р53. Выравнивание девяти вариантов сплайсинга р53 показано на Фиг. 8. Соответственно, TCR по изобретению могут обладать антигенной специфичностью в отношении любой мутантной аминокислотной последовательности р53, описанной в данном документе, кодируемой любым из девяти вариантов сплайсинга р53. Поскольку положения представляют собой такие, как определено SEQ ID NO: 1, в таком случае фактические положения аминокислотной последовательности определенного варианта сплайсинга р53 определены относительно соответствующих положений SEQ ID NO: 1, и положения, как определено SEQ ID NO: 1, могут отличаться от фактических положений в конкретном варианте сплайсинга. Таким образом, например, мутации относятся к замене аминокислотного остатка в аминокислотной последовательности конкретного варианта сплайсинга р53, соответствующей указанному положению аминокислотной последовательности из 393 аминокислот SEQ ID NO: 1 с пониманием того, что фактические положения в варианте сплайсинга могут отличаться.
В одном воплощении изобретения TCR обладает антигенной специфичностью в отношении человеческого р53 с мутацией в положении 175, как определено SEQ ID NO: 1. Мутация р53 в положении 175 может представлять собой любую миссенс-мутацию. Соответственно, мутация в положении 175 может представлять собой замену нативного остатка аргинина (WT), находящегося в положении 175, любым аминокислотным остатком, отличным от аргинина. В одном воплощении изобретения TCR обладает антигенной специфичностью в отношении человеческого р53 с мутацией R175H. Например, TCR по изобретению может обладать антигенной специфичностью в отношении одной или более мутантных аминокислотных последовательностей р53, выбранных из группы, состоящей из: EVVRHCPHHER (SEQ ID NO: 2), HMTEVVRHC (SEQ ID NO: 96), KQSQHMTEVVRHCPH (SEQ ID NO: 100), QSQHMTEVVRHCPHH (SEQ ID NO: 101), SQHMTEVVRHCPHHE (SEQ ID NO: 102), QHMTEVVRHCPHHER (SEQ ID NO: 103), HMTEVVRHCPHHERC (SEQ ID NO: 104), MTEVVRHCPHHERCS (SEQ ID NO: 105), TEVVRHCPHHERCSD (SEQ ID NO: 106), EVVRHCPHHERCSDS (SEQ ID NO: 107), VVRHCPHHERCSDSD (SEQ ID NO: 108), VRHCPHHERCSDSDG (SEQ ID NO: 109), YKQSQHMTEVVRHCPHHERCSDSDG (SEQ ID NO: 111).
В одном воплощении изобретения TCR обладает антигенной специфичностью в отношении человеческого р53 с мутацией в положении 220, как определено SEQ ID NO: 1. Мутация р53 в положении 220 может представлять собой миссенс-мутацию. Соответственно, мутация в положении 220 может представлять собой замену нативного остатка тирозина (WT), находящегося в положении 220, любым аминокислотным остатком, отличным от тирозина. В одном воплощении изобретения TCR обладает антигенной специфичностью в отношении человеческого р53 с мутацией Y220C. Например, TCR по изобретению может обладать антигенной специфичностью в отношении мутантной аминокислотной последовательности р53 VVPCEPPEV (SEQ ID NO: 113).
В одном воплощении изобретения TCR по изобретению могут быть способны распознавать мутантный р53 HLA (человеческий лейкоцитарный антиген) - молекулозависимым образом. Фраза «HLA-молекулозависимым образом», в том виде, в котором она используется в данном документе, означает, что TCR вызывает иммунный ответ при связывании с мутантным р53 в контексте молекулы HLA, которая экспрессируется пациентом, у которого был выделен TCR. TCR по изобретению могут быть способны распознавать мутантный р53, который презентирован применяемой молекулой HLA, и могут связываться с молекулой HLA помимо мутантного р53.
В одном воплощении изобретения TCR по изобретению могут распознавать R175H, презентированный молекулой HLA II класса. В данном отношении, TCR может вызывать иммунный ответ при связывании с R175H в контексте молекулы HLA II класса. TCR по изобретению могут распознавать R175H, который презентирован молекулой HLA класса II, и могут связываться с молекулой HLA класса II помимо R175H.
В одном воплощении изобретения молекула HLA класса II представляет собой HLA-DR гетеродимер. HLA-DR гетеродимер представляет собой рецептор клеточной поверхности, включающий цепь α и цепь β. Цепь α HLA-DR кодируется геном HLA-DRA. В одном воплощении цепь альфа молекулы HLA класса II экспрессируется аллелью HLA-DRA1*01:01:01. Цепь β HLA-DR кодируется геном HLA-DRB1, геном HLA-DRB3, геном HLA-DRB4 или геном HLA-DRB5. Примеры молекул, кодируемых геном HLA-DRB1, могут включать HLA-DR1, HLA-DR2, HLA-DR3, HLA-DR4, HLA-DR5, HLA-DR6, HLA-DR7, HLA-DR8, HLA-DR9, HLA-DR10, HLA-DR11, HLA-DR12, HLA-DR13, HLA-DR14, HLA-DR15, HLA-DR16 и HLA-DR17, но не ограничиваются ими. Ген HLA-DRB3 кодирует HLA-DR52. Ген HLA-DRB4 кодирует HLA-DR53. Ген HLA-DRB5 кодирует HLA-DR51. В одном воплощении изобретения молекула HLA класса II представляет собой гетеродимер HLA-DRB1:HLA-DRA. Цепь бета молекулы HLA класса II может экспрессироваться аллелью HLA-DRB1*13:01, HLA-DRB1*13:02, HLA-DRB1*13:03, HLA-DRB1*13:04, HLA-DRB1*13:05, HLA-DRB1*13:06, HLA-DRB1*13:07, HLA-DRB1*13:08, HLA-DRB1*13:09 или HLA-DRB1*13:10. Водном особенно предпочтительном воплощении цепь бета молекулы HLA класса II экспрессируется аллелью HLA-DRB1*13:01.
В одном воплощении изобретения один из TCR по изобретению может распознавать Y220C, презентированный молекулой HLA класса I. В данном отношении, TCR может вызывать иммунный ответ при связывании с Y220C в контексте HLA-молекулы класса I. TCR по изобретению может распознавать Y220C, который презентирован молекулой HLA класса I, и может связываться с молекулой HLA класса I помимо Y220C.
В одном воплощении изобретения молекула HLA класса I представляет собой молекулу HLA-A. Молекула HLA-A представляет собой гетеродимер цепи α и микроглобулина β2. Цепь α HLA-A может кодироваться геном HLA-A. Микроглобулин β2 связывается нековалентно с доменами альфа 1, альфа 2 и альфа 3 цепи альфа с построением комплекса HLA-A. Молекула HLA-A может представлять собой любую молекулу HLA-A. В одном воплощении изобретения молекула HLA класса I представляет собой молекулу HLA-A2. Молекула HLA-A2 может представлять собой любую молекулу HLA-A2. Примеры молекул HLA-A2 могут включать, но не ограничиваются HLA-A*02:01, HLA-A*02:02, HLA-A*02:03, HLA-A*02:05, HLA-A*02:06, HLA-A*02:07 или HLA-A*02:11. Предпочтительно, молекула HLA класса I представляет собой молекулу HLA-A*02:01.
TCR по изобретению могут обеспечивать любое одно или более из многих преимуществ, включая случаи экспрессии клетками, используемыми для адоптивного переноса клеток. Мутантный р53 экспрессируется раковыми клетками и не экспрессируется нормальными, нераковыми клетками. Без привязки к конкретной теории или механизму, полагают, что TCR по изобретению преимущественно нацелены на разрушение раковых клеток при минимизации или исключении разрушения нормальных, нераковых клеток, таким образом, уменьшая, например, посредством минимизации или исключения токсичности. Кроме того, TCR по изобретению могут, преимущественно, успешно лечить или предупреждать раковые заболевания, позитивные в отношении мутантного р53, которые не отвечают на другие типы лечения, такие как, например, химиотерапия, оперативное вмешательство или облучение. Кроме того, TCR по изобретению могут обеспечивать высокоавидное распознавание мутантного р53, которое может обеспечивать способность распознавать неманипулированные опухолевые клетки (например, опухолевые клетки, которые не были обработаны интерфероном (IFN)-γ, трансфицированы вектором, кодирующим один или оба из мутантного р53 и применимой молекулы HLA, которым не вводили под действием импульса пептид р53 с мутацией р53 или их комбинация). Приблизительно половина всех опухолей несет мутацию в р53, приблизительно половина которых будет представлять собой миссенс-мутацию. Мутация R175H экспрессируется примерно 4,5% всех раковых заболеваний, и аллель HLA-DRB1*13:01 экспрессируется примерно 15% популяции США. Мутация Y220C встречается у примерно 1,5% всех раковых заболеваний, и аллель HLA-А*02:01 экспрессируется от примерно 40% до примерно 50% популяции США. Мутации R175H и Y220C возникают во многих гистологиях опухоли, что указывает на то, что неоднородная группа пациентов могла получать пользу от TCR по изобретению. Соответственно, TCR по изобретению могут увеличивать число пациентов, которые могут подходить для лечения посредством иммунотерапии.
Фраза «антигенная специфичность», в том виде, в котором она используется в данном документе, означает, что TCR может специфично связываться с и иммунологически распознавать мутантный р53 с высокой авидностью. Например, считается, что TCR может обладать «антигенной специфичностью» в отношении мутантного р53, если примерно от 1×104 до примерно 1×105 Т-клеток, экспрессирующих TCR, секретируют по меньшей мере примерно 200 пг/мл или больше (например, 200 пг/мл или больше, 300 пг/мл или больше, 400 пг/мл или больше, 500 пг/мл или больше, 600 пг/мл или больше, 700 пг/мл или больше, 1000 пг/мл или больше, 5000 пг/мл или больше, 7000 пг/мл или больше, 10000 пг/мл или больше, 20000 пг/мл или больше, или интервал, определенный любыми двумя из приведенных выше значений) IFN-γ при совместном культивировании с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые под действием импульса вводили низкую концентрацию мутантного пептида р53 (например, от примерно 0,05 нг/мл до примерно 5 нг/мл, 0,05 нг/мл, 0,1 нг/мл, 0,5 нг/мл, 1 нг/мл, 5 нг/мл или интервал, определенный любыми двумя из указанных выше значений), или (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые была введена нуклеотидная последовательность, кодирующая мутантный р53, таким образом, что клетка-мишень экспрессирует мутантный р53. Клетки, экспрессирующие TCR по изобретению, могут также секретировать IFN-γ при совместной культивации с клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые под действием импульса вводили более высокие концентрации мутантного пептида р53.
В качестве альтернативы или дополнительно, считается, что TCR может обладать «антигенной специфичностью» в отношении мутантного р53, если Т-клетки, экспрессирующие TCR, секретируют по меньшей мере в два раза больше IFN-γ при совместном культивировании с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые под действием импульса вводили низкую концентрацию мутантного пептида р53, или (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые введена нуклеотидная последовательность, кодирующая мутантный р53, таким образом, что клетка-мишень экспрессирует мутантный р53, по сравнению с количеством IFN-γ, экспрессируемым отрицательным контролем. Отрицательный контроль может представлять собой, например, (i) Т-клетки, экспрессирующие TCR, совместно культивируемые с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые посредством импульса вводили такую же концентрацию нерелевантного пептида (например, некоторого другого пептида с последовательностью, отличной от мутантного пептида р53), или (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые введена нуклеотидная последовательность, кодирующая нерелевантный пептид, таким образом, что клетка-мишень экспрессирует нерелевантный пептид, или (ii) нетрансдуцированные Т-клетки (например, происходящие из РВМС (от англ. human peripheral blood mononuclear cell - мононуклеарная клетка периферической крови человека), которые не экспрессируют TCR), совместно культивируемые с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулой HLA, в которые под действием импульса вводили такую же концентрацию мутантного пептида р53, или (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые введена нуклеотидная последовательность, кодирующая мутантный р53, таким образом, что клетка-мишень экспрессирует мутантный р53. Секрецию IFN-γ можно измерять способами, известными в данной области, такими как, например, твердофазный иммуноферментный анализ (ELISA - от англ. enzyme-linked immunosorbent assay).
В качестве альтернативы или дополнительно считается, что TCR может обладать «антигенной специфичностью» в отношении мутантного р53, если по меньшей мере в два раза больше по числу Т-клеток, экспрессирующих TCR, секретируют IFN-γ при совместной культивации с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые под действием импульса вводили низкую концентрацию мутантного пептида р53, или с (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые была введена нуклеотидная последовательность, кодирующая мутантный р53, таким образом, что клетка-мишень экспрессирует мутантный р53, по сравнению с числом Т-клеток отрицательного контроля, которые секретируют IFN-γ. Концентрация пептида и отрицательного контроля может представлять собой такую, как описано в данном документе, в отношении других аспектов изобретения. Число клеток, секретирующих IFN-γ, может быть измерено способами, известными в данной области, такими как, например, иммуноферментный спот-анализ (ELISOT).
В качестве альтернативы или дополнительно считается, что TCR может обладать «антигенной специфичностью» в отношении мутантного р53, если по меньшей мере в два раза больше пятен выявляется посредством ELISPOT для Т-клеток, экспрессирующих TCR при совместной культивации с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые под действием импульса вводили низкую концентрацию мутантного пептида р53, или с (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые была введена нуклеотидная последовательность, кодирующая мутантный р53, таким образом, что клетка-мишень экспрессирует мутантный р53, по сравнению с числом пятен, выявляемых посредством ELISPOT для Т-клеток отрицательного контроля, совместно культивируемых с теми же клетками-мишенями. Концентрация пептида и отрицательного контроля может представлять собой такую, как описано в данном документе, в отношении других аспектов изобретения.
В качестве альтернативы или дополнительно считается, что TCR может обладать «антигенной специфичностью» в отношении мутантного р53, если больше чем примерно 50 пятен выявляют посредством ELISPOT для Т-клеток, экспрессирующих TCR, при совместной культивации с (а) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые под действием импульса вводили низкую концентрацию мутантного пептида р53, или с (b) клетками-мишенями, негативными в отношении антигена, позитивными в отношении применимой молекулы HLA, в которые была введена нуклеотидная последовательность, кодирующая мутантный р53, таким образом, что клетка-мишень экспрессирует мутантный р53. Концентрация пептида может представлять собой такую, как описано в данном документе, в отношении других аспектов изобретения.
В качестве альтернативы или дополнительно считается, что TCR может обладать «антигенной специфичностью» в отношении мутантного р53, если Т-клетки, экспрессирующие TCR, осуществляют повышающую регуляцию экспрессии одного или обоих из 4-1ВВ и ОХ40, как измерено посредством, например, проточной цитометрии после стимуляции клетками-мишенями, экспрессирующими мутантный р53.
Согласно воплощению изобретения предложен TCR, содержащий два полипептида (а именно, полипептидные цепи), таких как цепь альфа (α) TCR, цепь бета (β) TCR, цепь гамма (γ) TCR, цепь дельта (δ) TCR, их комбинацию. Полипептиды TCR по изобретению могут содержать любую аминокислотную последовательность, при условии, что TCR обладает антигенной специфичностью в отношении мутантного р53.
В одном воплощении изобретения TCR содержит две полипептидных цепи, каждая из которых содержит вариабельную область, содержащую гипервариабельную область (CDR - от англ. complementarity determining region)1, CDR2 и CDR3 TCR. В одном воплощении изобретения TCR содержит первую полипептидную цепь, содержащую CDR1 цепи α (CDR1α), CDR2 цепи α (CDR2α) и CDR3 цепи α (CDR3α), и вторую полипептидную цепь, содержащую CDR1 цепи β (CDR1β), CDR2 цепи β (CDR2β) и CDR3 цепи β (CDR3β). В одном воплощении изобретения TCR содержит аминокислотные последовательности: (1) все из SEQ ID NO: 3-8; (2) все из SEQ ID NO: 14-19; (3) все из SEQ ID NO: 25-30; (4) все из SEQ ID NO: 36-41; (5) все из SEQ ID NO: 47-52; (6) все из SEQ ID NO: 58-63; (7) все из SEQ ID NO: 69-74; (8) все из SEQ ID NO: 80-85; или (9) все из SEQ ID NO: 131-136. Каждая из указанных выше девяти коллекций аминокислотных последовательностей в данном абзаце представляет шесть областей CDR каждого из девяти разных TCR, обладающих антигенной специфичностью в отношении мутантного человеческого р53. Шесть аминокислотных последовательностей в каждой коллекции соответствуют CDR1α, CDR2α, CDR3α, CDR1β, CDR2β и CDR3β TCR, соответственно.
В одном воплощении изобретения TCR содержит аминокислотную последовательность вариабельной области цепи α и аминокислотную последовательность вариабельной области цепи β, которые вместе содержат одну из коллекций CDR, изложенных выше. В данном отношении TCR может, например, содержать аминокислотные последовательности любой из SEQ ID NO: 9, 10, 20, 21, 31, 32, 42, 43, 53, 54, 64, 65, 75, 76, 86, 87, 137, 138, 142-159, 178, 181, 184, 187, 190, 193, 196, 199, 202, 205, 207, 209, 211, 213, 215, 217, 219, 221, 223 и 226. Например, TCR может содержать: (1) обе SEQ ID NO: 9 и 10; (2) обе SEQ ID NO: 20 и 21; (3) обе SEQ ID NO: 31 и 32; (4) обе SEQ ID NO: 42 и 43; (5) обе SEQ ID NO: 53 и 54; (6) обе SEQ ID NO: 64 и 65; (7) обе SEQ ID NO: 75 и 76; (8) обе SEQ ID NO: 86 и 87; (9) обе SEQ ID NO: 137 и 138; (10) обе SEQ ID NO: 142 и 143; (11) обе SEQ ID NO: 144 и 145; (12) обе SEQ ID NO: 146 и 147; (13) обе SEQ ID NO: 148 и 149; (14) обе SEQ ID NO: 150 и 151; (15) обе SEQ ID NO: 152 и 153; (16) обе SEQ ID NO: 154 и 155; (17) обе SEQ ID NO: 156 и 157; (18) обе SEQ ID NO: 159 и 158; (19) обе SEQ ID NO: 178 и 10; (20) обе SEQ ID NO: 181 и 21; (21) обе SEQ ID NO: 184 и 32; (22) обе SEQ ID NO: 187 и 43; (23) обе SEQ ID NO: 190 и 54; (24) обе SEQ ID NO: 193 и 65; (25) обе SEQ ID NO: 196 и 76; (26) обе SEQ ID NO: 199 и 87; (27) обе SEQ ID NO: 137 и 202; (28) обе SEQ ID NO: 9 и 205; (29) обе SEQ ID NO: 20 и 207; (30) обе SEQ ID NO: 31 и 209; (31) обе SEQ ID NO: 42 и 211; (32) обе SEQ ID NO: 53 и 213; (33) обе SEQ ID NO: 64 и 215; (34) обе SEQ ID NO: 75 и 217; (35) обе SEQ ID NO: 86 и 219; (36) обе SEQ ID NO: 137 и 221; (37) обе SEQ ID NO: 223 и 202; (38) обе SEQ ID NO: 223 и 221; (39) обе SEQ ID NO: 20 и 226; или (40) обе SEQ ID NO: 181 и 226. Каждая из указанных выше коллекций аминокислотных последовательностей в данном абзаце представляет две вариабельные области каждого из разных TCR, обладающих антигенной специфичностью в отношении мутантного человеческого р53. Данные две аминокислотные последовательности в каждой коллекции соответствуют вариабельной области цепи α и вариабельной области цепи β TCR, соответственно.
TCR по изобретению могут дополнительно содержать константную область. Константная область может происходить из любого подходящего вида, такого как, например, человек или мышь. В одном воплощении изобретения TCR дополнительно содержат мышиную константную область. В том виде, в котором он используется в данном документе, термин «мышиный» или «человеческий», при ссылке на TCR или любой компонент TCR, описанный в данном документе (например, гипервариабельная область (CDR), вариабельная область, константная область, цепь альфа и/или цепь бета), означает TCR (или его компонент), который происходит из мыши или человека, соответственно, а именно, TCR (или его компонент), который происходил из или, одновременно, экспрессировался мышиной Т-клеткой или человеческой Т-клеткой, соответственно. В одном воплощении изобретения TCR может содержать мышиную константную область цепи α и мышиную константную область цепи β. Мышиная константная область цепи α может быть модифицирована или не модифицирована. Модифицированная мышиная константная область цепи α может быть, например, цистеин-замещенной, LVL-модифицированной или как цистеин-замещенной, так и LVL-модифицированной, как описано, например, в патенте США №10174098. Мышиная константная область цепи β может быть модифицирована или немодифицирована. Модифицированная мышиная константная область цепи р может быть, например, цистеин-замещенной, как описано, например, в патенте США №10174098. В одном воплощении изобретения TCR содержит цистеин-замещенную, LVL-модифицированную мышиную константную область цепи α, содержащую аминокислотную последовательность SEQ ID NO: 91 или 92. В одном воплощении изобретения TCR содержит цистеин-замещенную мышиную константную область цепи β, содержащую аминокислотную последовательность SEQ ID NO: 93.
В одном воплощении изобретения TCR по изобретению может содержать цепь α TCR и цепь β TCR. Цепь α TCR может содержать вариабельную область цепи α или константную область цепи α. С цепью α данного типа может образовывать пару любая цепь β TCR. Цепь β может содержать вариабельную область цепи β и константную область цепи β.
В некоторых воплощениях аминокислотная последовательность любой из цепей α и/или цепей β, раскрытых в данном документе, дополнительно содержит аминокислотную последовательность RAKR (SEQ ID NO: 230) на С-конце.
В одном воплощении изобретения TCR содержит аминокислотные последовательности любой из SEQ ID NO 11, 12, 22, 23, 33, 34, 44, 45, 55, 56, 66, 67, 77, 78, 88, 89, 139, 140, 160-177, 179, 182, 185, 188, 191, 194, 197, 200, 203, 206, 208, 210, 212, 214, 216, 218, 220, 222, 224 и 227. Например, TCR может содержать: (1) обе из SEQ ID NO: 11 и 12; (2) обе из SEQ ID NO: 22 и 23; (3) обе из SEQ ID NO: 33 и 34; (4) обе из SEQ ID NO: 44 и 45; (5) обе из SEQ ID NO: 55 и 56; (6) обе из SEQ ID NO: 66 и 67; (7) обе из SEQ ID NO: 77 и 78; (8) обе из SEQ ID NO: 88 и 89; (9) обе из SEQ ID NO: 139 и 140; (10) обе из SEQ ID NO: 160 и 161; (11) обе из SEQ ID NO: 162 и 163; (12) обе из SEQ ID NO: 164 и 165; (13) обе из SEQ ID NO: 166 и 167; (14) обе из SEQ ID NO: 168 и 169; (15) обе из SEQ ID NO: 170 и 171; (16) обе из SEQ ID NO: 172 и 173; (17) обе из SEQ ID NO: 174 и 175; (18) обе из SEQ ID NO: 176 и 177; (19) обе из SEQ ID NO: 179 и 12; (20) обе из SEQ ID NO: 182 и 23; (21) обе из SEQ ID NO: 185 и 34; (22) обе из SEQ ID NO: 188 и 45; (23) обе из SEQ ID NO: 191 и 56; (24) обе из SEQ ID NO: 194 и 67; (25) обе из SEQ ID NO: 197 и 78; (26) обе из SEQ ID NO: 200 и 89; (27) обе из SEQ ID NO: 139 и 203; (28) обе из SEQ ID NO: 11 и 206; (29) обе из SEQ ID NO: 22 и 208; (30) обе из SEQ ID NO: 33 и 210; (31) обе из SEQ ID NO: 44 и 212; (32) обе из SEQ ID NO: 55 и 214; (33) обе из SEQ ID NO: 66 и 216; (34) обе из SEQ ID NO: 77 и 218; (35) обе из SEQ ID NO: 88 и 220; (36) обе из SEQ ID NO: 139 и 222; (37) обе из SEQ ID NO: 224 и 203; (38) обе из SEQ ID NO: 224 и 222; (39) обе из SEQ ID NO: 22 и 227; или (40) обе из SEQ ID NO: 182 и 227. Каждая из указанных выше коллекций аминокислотных последовательностей в данном абзаце представляет цепь α и цепь β каждого из разных TCR, обладающих антигенной специфичностью в отношении мутантного человеческого р53. Две аминокислотные последовательности в каждой коллекции соответствуют цепи α и цепи β TCR, соответственно.
В объем изобретения включены функциональные варианты TCR по изобретению, описанные в данном документе. Термин «функциональный вариант», в том виде, в котором он используется в данном документе, относится к TCR, полипептиду или белку, обладающему существенной или значимой идентичностью или сходством последовательностей с исходным TCR, полипептидом или белком, функциональный вариант которого сохраняет биологическую активность TCR, полипептида или белка, чьим вариантом он является. Функциональные варианты охватывают, например, данные варианты TCR, полипептида или белка, описанные в данном документе (исходные TCR, полипептид или белок), которые сохраняют способность к специфичному связыванию с мутантным р53, в отношении которого исходный TCR обладает антигенной специфичностью, или с которым специфично связывается исходный полипептид или белок, в похожей степени, в той же степени или в большей степени, чем исходный TCR, полипептид или белок. В отношении исходного TCR, полипептида или белка, функциональный вариант может, например, быть на по меньшей мере примерно 30%, на по меньшей мере примерно 50%, на по меньшей мере примерно 75%, на по меньшей мере примерно 80%, на по меньшей мере примерно 90%, на по меньшей мере примерно 95%, на по меньшей мере примерно 96%, на по меньшей мере примерно 97%, на по меньшей мере примерно 98%, на по меньшей мере примерно 99% или более идентичным по аминокислотной последовательности исходному TCR, полипептиду или белку, соответственно.
Функциональный вариант может, например, содержать аминокислотную последовательность исходного TCR, полипептида или белка с по меньшей мере одной консервативной заменой аминокислоты. Консервативные замены аминокислоты известны в данной области и включают замены аминокислот, в которых одна аминокислота, обладающая определенными физическими и/или химическими свойствами, заменена другой аминокислотой, которая обладает такими же химическими или физическими свойствами. Например, консервативная замена аминокислоты может представлять собой кислую аминокислоту, замененную другой кислой аминокислотой (например, Asp или Glu), аминокислоту с неполярной боковой цепью, замененную другой аминокислотой с неполярной боковой цепью (например, Ala, Gly, Val, Ile, Leu, Met, Phe, Pro, Trp, Val и т.д.), основную аминокислоту, замененную другой основной аминокислотой (Lys, Arg и т.д.), аминокислоту с полярной боковой цепью, замененную другой аминокислотой с полярной боковой цепью (Asn, Cys, Gln, Ser, Thr, Tyr, и т.д.), и т.д.
В качестве альтернативы или дополнительно, функциональные варианты могут содержать аминокислотную последовательность исходного TCR, полипептида или белка с по меньшей мере одной неконсервативной заменой аминокислоты. В данном случае предпочтительно, чтобы неконсервативная замена аминокислоты не затрагивала или не ингибировала биологическую активность функционального варианта. Предпочтительно, неконсервативная замена аминокислоты усиливает биологическую активность функционального варианта, таким образом, что биологическая активность функционального варианта повышается, по сравнению с исходным TCR, полипептидом или белком.
TCR, полипептид или белок может по существу состоять из конкретно указанной аминокислотной последовательности или последовательностей, описанных в данном документе, таким образом, что другие компоненты TCR, полипептида или белка, например, другие аминокислоты, существенно не меняют биологическую активность TCR, полипептида или белка.
Также согласно изобретению предложен полипептид, содержащий функциональную часть любого из TCR, описанных в данном документе. Термин «полипептид», в том виде, в котором он используется в данном документе, включает олигопептиды и относится к одиночной цепи аминокислот, соединенных одной или более пептидными связями.
В отношении полипептидов по изобретению, функциональная часть может представлять собой любую часть, содержащую смежные аминокислоты TCR, частью которого она является, при условии, что функциональная часть специфично связывается с мутантным р53. Термин «функциональная часть», при использовании по отношению к TCR, относится к любой часть или фрагменту TCR по изобретению, чья часть или фрагмент сохраняет биологическую активность TCR, чей частью она является (исходный TCR). Функциональные части охватывают, например, такие части TCR, которые сохраняют способность специфично связываться с мутантным р53 (например, образом, зависимым от применимой молекулы HLA) или выявлять, лечить или предупреждать рак, в похожей степени, той же степени или в большей степени, по сравнению с исходным TCR. В отношении исходного TCR, функциональная часть может содержать, например, примерно 10%, примерно 25%, примерно 30%, примерно 50%, примерно 68%, примерно 80%, примерно 90%, примерно 95% или больше исходного TCR.
Функциональная часть может содержать дополнительные аминокислоты на N- или С-конце данной части или на обоих концах, которые не обнаружены в аминокислотной последовательности исходного TCR. Желательно, дополнительные аминокислоты не мешают биологической функции функциональной части, например, специфичному связыванию с мутантным р53; и/или обладанию способностью выявлять рак, лечить или предупреждать рак и т.д. Более желательно, дополнительные аминокислоты усиливают биологическую активность, по сравнению с биологической активностью исходного TCR.
Полипептид может содержать функциональную часть одной из двух или обеих цепей аир TCR по изобретению, такую как функциональная часть, содержащая одну или более из CDR1, CDR2 и CDR3 вариабельной(ых) области(ей) цепи α и/или цепи β TCR по изобретению. В одном воплощении изобретения полипептид может содержать функциональную часть, содержащую следующие аминокислотные последовательности: (1) все из SEQ ID NO: 3-8; (2) все из SEQ ID NO: 14-19; (3) все из SEQ ID NO: 25-30; (4) все из SEQ ID NO: 36-41; (5) все из SEQ ID NO: 47-52; (6) все из SEQ ID NO: 58-63; (7) все из SEQ ID NO: 69-74; (8) все из SEQ ID NO: 80-85; или (9) все из SEQ ID NO: 131-136.
В одном воплощении изобретения полипептид по изобретению может содержать, например, вариабельную область TCR по изобретению, содержащую комбинацию областей CDR, изложенных выше. В данном отношении, полипептид может содержать, например, следующие аминокислотные последовательности: (1) обе из SEQ ID NO: 9 и 10; (2) обе из SEQ ID NO: 20 и 21; (3) обе из SEQ ID NO: 31 и 32; (4) обе из SEQ ID NO: 42 и 43; (5) обе из SEQ ID NO: 53 и 54; (6) обе из SEQ ID NO: 64 и 65; (7) обе из SEQ ID NO: 75 и 76; (8) обе из SEQ ID NO: 86 и 87; (9) обе из SEQ ID NO: 137 и 138; (10) обе из SEQ ID NO: 142 и 143; (11) обе из SEQ ID NO: 144 и 145; (12) обе из SEQ ID NO: 146 и 147; (13) обе из SEQ ID NO: 148 и 149; (14) обе из SEQ ID NO: 150 и 151; (15) обе из SEQ ID NO: 152 и 153; (16) обе из SEQ ID NO: 154 и 155; (17) обе из SEQ ID NO: 156 и 157; (18) обе из SEQ ID NO: 159 и 158; (19) обе из SEQ ID NO: 178 и 10; (20) обе из SEQ ID NO: 181 и 21; (21) обе из SEQ ID NO: 184 и 32; (22) обе из SEQ ID NO: 187 и 43; (23) обе из SEQ ID NO: 190 и 54; (24) обе из SEQ ID NO: 193 и 65; (25) обе из SEQ ID NO: 196 и 76; (26) обе из SEQ ID NO: 199 и 87; (27) обе из SEQ ID NO: 137 и 202; (28) обе из SEQ ID NO: 9 и 205; (29) обе из SEQ ID NO: 20 и 207; (30) обе из SEQ ID NO: 31 и 209; (31) обе из SEQ ID NO: 42 и 211; (32) обе из SEQ ID NO: 53 и 213; (33) обе из SEQ ID NO: 64 и 215; (34) обе из SEQ ID NO: 75 и 217; (35) обе из SEQ ID NO: 86 и 219; (36) обе из SEQ ID NO: 137 и 221; (37) обе из SEQ ID NO: 223 и 202; (38) обе из SEQ ID NO: 223 и 221; (39) обе из SEQ ID NO: 20 и 226; или (40) обе из SEQ ID NO: 181 и 226.
В одном воплощении изобретения полипептид по изобретению может дополнительно содержать константную область TCR по изобретению, изложенную выше. В данном отношении, полипептид может содержать, например, аминокислотную последовательность (i) одну из SEQ ID NO 91-93 или (ii) SEQ ID NO: 93 и одну из SEQ ID NO: 91 и 92.
В одном воплощении изобретения полипептид по изобретению может содержать цепь α и цепь β TCR по изобретению. В данном отношении, полипептид может содержать, например, следующие аминокислотные последовательности: (1) обе из SEQ ID NO: 11 и 12; (2) обе из SEQ ID NO: 22 и 23; (3) обе из SEQ ID NO: 33 и 34; (4) обе из SEQ ID NO: 44 и 45; (5) обе из SEQ ID NO: 55 и 56; (6) обе из SEQ ID NO: 66 и 67; (7) обе из SEQ ID NO: 77 и 78; (8) обе из SEQ ID NO: 88 и 89; (9) обе из SEQ ID NO: 139 и 140; (10) обе из SEQ ID NO: 160 и 161; (11) обе из SEQ ID NO: 162 и 163; (12) обе из SEQ ID NO: 164 и 165; (13) обе из SEQ ID NO: 166 и 167; (14) обе из SEQ ID NO: 168 и 169; (15) обе из SEQ ID NO: 170 и 171; (16) обе из SEQ ID NO: 172 и 173; (17) обе из SEQ ID NO: 174 и 175; (18) обе из SEQ ID NO: 176 и 177; (19) обе из SEQ ID NO: 179 и 12; (20) обе из SEQ ID NO: 182 и 23; (21) обе из SEQ ID NO: 185 и 34; (22) обе из SEQ ID NO: 188 и 45; (23) обе из SEQ ID NO: 191 и 56; (24) обе из SEQ ID NO: 194 и 67; (25) обе из SEQ ID NO: 197 и 78; (26) обе из SEQ ID NO: 200 и 89; (27) обе из SEQ ID NO: 139 и 203; (28) обе из SEQ ID NO: 11 и 206; (29) обе из SEQ ID NO: 22 и 208; (30) обе из SEQ ID NO: 33 и 210; (31) обе из SEQ ID NO: 44 и 212; (32) обе из SEQ ID NO: 55 и 214; (33) обе из SEQ ID NO: 66 и 216; (34) обе из SEQ ID NO: 77 и 218; (35) обе из SEQ ID NO: 88 и 220; (36) обе из SEQ ID NO: 139 и 222; (37) обе из SEQ ID NO: 224 и 203; (38) обе из SEQ ID NO: 224 и 222; (39) обе из SEQ ID NO: 22 и 227; или (40) обе из SEQ ID NO: 182 и 227.
Согласно изобретению дополнительно предложен белок, содержащий по меньшей мере один из полипептидов, описанных в данном документе. Под термином «белок» подразумевают молекулу, содержащую одну или более полипептидных цепей. В одном воплощении белок по изобретению может содержать: (1) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 3-5, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 6-8; (2) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 14-16, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 17-19; (3) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 25-27, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 28-30; (4) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 36-38, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 39-41; (5) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 47-49, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 50-52; (6) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 58-60, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 61-63; (7) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 69-71, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 72-74; (8) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 80-82, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 83-85; или (9) первую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 131-133, и вторую полипептидную цепь, содержащую аминокислотные последовательности всех из SEQ ID NO: 134-136.
В одном воплощении изобретения белок содержит: (1) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 9, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 10; (2) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 21; (3) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 31, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 32; (4) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 42, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 43; (5) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 53, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 54; (6) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 64, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 65; (7) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 75, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 76; (8) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 86, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 87; (9) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 137, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 138; (10) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 142, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 143; (11) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 144, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 145; (12) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 146, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 147; (13) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 148, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 149; (14) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 150, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 151; (15) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 152, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 153; (16) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 154, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 155; (17) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 156, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 157; (18) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 158, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 159; (19) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 178, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 10; (20) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 181, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 21; (21) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 184, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 32; (22) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 187, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 43; (23) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 190, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 54; (24) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 193, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 65; (25) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 196, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 76; (26) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 199, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 87; (27) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 137, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 202; (28) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 9, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 205; (29) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 207; (30) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 31, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 209; (31) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 42, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 211; (32) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 53, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 213; (33) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 64, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 215; (34) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 75, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 217; (35) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 86, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 219; (36) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 137, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 221; (37) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 223, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 202; (38) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 223, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 221; (39) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 20, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 226; или (40) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 181, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 226.
В одном воплощении изобретения белок содержит: (1) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 11, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 12; (2) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 23; (3) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 33, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 34; (4) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 44, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 45; (5) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 55, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 56; (6) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 66, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 67; (7) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 77, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 78; (8) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 88, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 89; (9) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 139, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 140; (10) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 160, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 161; (11) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 162, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 163; (12) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 164, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 165; (13) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 166, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 167; (14) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 168, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 169; (15) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 170, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 171; (16) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 172, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 173; (17) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 174, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 175; (18) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 176, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 177; (19) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 179, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 12; (20) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 182, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 23; (21) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 185, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 34; (22) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 188, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 45; (23) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 191, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 56; (24) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 194, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 67; (25) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 197, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 78; (26) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 200, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 89; (27) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 139, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 203; (28) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 11, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 206; (29) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 208; (30) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 33, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 210; (31) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 44, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 212; (32) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 55, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 214; (33) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 66, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 216; (34) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 77, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 218; (35) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 88, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 220; (36) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 139, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 222; (37) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 224, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 203; или (38) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 224, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 222; (39) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 22, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 227; или (40) первую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 182, и вторую полипептидную цепь, содержащую аминокислотную последовательность SEQ ID NO: 227.
Белок по изобретению может представлять собой TCR. В качестве альтернативы, если первая и/или вторая полипептидная цепь(и) белка дополнительно содержит(ат) другие аминокислотные последовательности, например, аминокислотную последовательность, кодирующую иммуноглобулин или его часть, затем белок по изобретению может представлять собой слитый белок. В данном отношении согласно изобретению также предложен слитый белок, содержащий по меньшей мере один из полипептидов по изобретению, описанных в данном документе, вместе с по меньшей мере одним другим полипептидом. Другой полипептид может существовать в виде отдельного полипептида слитого белка или может существовать в виде полипептида, который экспрессируется в рамке (в тандеме) с одним из полипептидов по изобретению, описанных в данном документе. Другой полипептид может кодировать любую пептидную или белковую молекулу или ее часть, включая, но не, ограничиваясь иммуноглобулином, CD3, CD4, CD8, молекулой МНС, молекулой CD1, например, CD1a, CD1b, CD1c, CD1d и т.д.
Слитый белок может содержать одну или более копий полипептида по изобретению и/или одну или более копий другого полипептида. Например, слитый белок может содержать 1, 2, 3, 4, 5 или больше копий полипептида по изобретению и/или другого полипептида. Подходящие способы получения слитых белков известны в данной области и включают, например, способы генной инженерии.
В некоторых воплощениях изобретения TCR, полипептиды и белки по изобретению могут экспрессироваться в виде одного белка, содержащего линкерный пептид, связывающий цепь α и цепь β. В данном отношении, TCR, полипептиды и белки по изобретению могут дополнительно содержать линкерный пептид. Линкерный пептид может преимущественно облегчать экспрессию рекомбинантного TCR, полипептида и/или белка в клетке-хозяине. Линкерный пептид может содержать любую подходящую аминокислотную последовательность. Например, линкерный пептид может содержать аминокислотную последовательность SEQ ID NO: 94. При экспрессии конструкции, включающей линкерный пептид, клеткой-хозяином, линкерный пептид может расщепляться, приводя к получению отдельных цепей α и β. В одном воплощении изобретения TCR, полипептид или белок может содержать аминокислотную последовательность, содержащую полноразмерную цепь α, полноразмерную цепь β и линкерный пептид, расположенный между цепями α и β.
В некоторых воплощениях TCR, полипептид или белок, раскрытый в данном документе, содержит цепь α и/или цепь β, как раскрыто в данном документе, содержащий один пептид. В некоторых воплощениях последовательность сигнального пептида любой из цепей α и/или цепей β, раскрытых в данном документе, содержит остаток аланина или гистидина, заменяющий остаток дикого типа в положении 2.
В некоторых воплощениях TCR, полипептид или белок, раскрытый в данном документе, содержит зрелую версию цепи α и/или цепи β, как раскрыто в данном документе, которая не имеет одного пептида.
Белок по изобретению может представлять собой рекомбинантное антитело или его антигенсвязывающий фрагмент, содержащее по меньшей мере один из полипептидов по изобретению, описанных в данном документе. В том виде, в котором он используется в данном документе, термин «рекомбинантное антитело» относится к рекомбинантному (например, генетически сконструированному) белку, содержащему по меньшей мере один из полипептидов по изобретению и полипептидную цепь антитела или его антигенсвязывающего фрагмента. Полипептид антитела или его антигенсвязывающего фрагмента может представлять собой тяжелую цепь, легкую цепь, вариабельную или константную область тяжелой или легкой цепи, одноцепочечный вариабельный фрагмент (scFv - от англ. chain variable fragment) или фрагмент Fc, Fab или F(ab)2' антитела и т.д. Полипептидная цепь антитела или его антигенсвязывающего фрагмента может существовать в виде отдельного полипептида рекомбинантного антитела. В качестве альтернативы полипептидная цепь антитела или его антигенсвязывающего фрагмента может существовать в виде полипептида, который экспрессируется в рамке (в тандеме) с полипептидом по изобретению. Полипептид антитела или его антигенсвязывающего фрагмента может представлять собой полипептид любого антитела или любого фрагмента антитела, включая любое из антител и фрагментов антител, раскрытых в данном документе.
TCR, полипептиды и белки по изобретению могут иметь любую длину, а именно, могут содержать любое число аминокислот, при условии, что TCR, полипептиды или белки сохраняют свою биологическую активность, например, способность к специфичному связыванию с мутантным р53; выявлять рак у млекопитающего; или лечить или предупреждать рак у млекопитающего и т.д. Например, длина полипептида может находиться в интервале от примерно 50 до примерно 5000 аминокислот, как например, 50, 70, 75, 100, 125, 150, 175, 200, 300, 400, 500, 600, 700, 800, 900, 1000 или более аминокислот в длину. В данном отношении, полипептиды по изобретению также включают олигопептиды.
TCR, полипептиды и белки по изобретению могут содержать синтетические аминокислоты вместо одной или более встречающихся в природе аминокислот. Такие синтетические аминокислоты известны в данной области и включают, например, аминоциклогексанкарбоновую кислоту, норлейцин, α-амино-n-декановую кислоту, гомосерин, S-ацетиламинометилцистеин, транс-3- и транс-4-гидроксипролин, 4-аминофенилаланин, 4-нитрофенилаланин, 4-хлорфенилаланин, 4-карбоксифенилаланин, β-фенилсерин, β-гидроксифенилаланин, фенилглицин, α-нафтилаланин, циклогексилаланин, циклогексил глицин, индолин-2-карбоновую кислоту, 1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту, аминомалоновую кислоту, моноамид аминомалоновой кислоты, N'-бензил-N'-метиллизин, N',N'-дибензиллизин, 6-гидроксилизин, орнитин, α-аминоциклопентанкарбоновую кислоту, α-аминоциклогексанкарбоновую кислоту, α-аминоциклогептанкарбоновую кислоту, α-(2-амино-2-норборнан)-карбоновую кислоту, α,γ-диаминомасляную кислоту, α,β-диаминопропионовую кислоту, гомофенилаланин и α-трет-бутилглицин.
TCR, полипептиды и белки по изобретению могут, например, быть гликозилированы, амидированы, карбоксилированы, фосфорилированы, этерифицированы, N-ацилированы, циклизированы посредством, например, дисульфидного мостика, или превращены в соль присоединения кислоты и/или возможно димеризованы или полимеризованы или конъюгированы.
TCR, полипептид и/или белок по изобретению может быть получен способами, известными в данной области, такими как, например, синтез de novo. Кроме того, полипептиды и белки могут быть рекомбинантно получены с использованием нуклеиновых кислот, описанных в данном документе, используя стандартные способы генной инженерии. См., например, Green and Sambrook, Molecular Cloning: A Laboratory Manual, 4th ed., Cold Spring Harbor Press, Cold Spring Harbor, NY (2012). В качестве альтернативы, TCR, полипептиды и/или белки, описанные в данном документе, могут быть коммерчески синтезированы компаниями, такими как Synpep (Dublin, СА), Peptide Technologies Corp. (Gaithersburg, MD) и Multiple Peptide Systems (San Diego, СА). В данном отношении, TCR, полипептиды и белки по изобретению могут быть синтетическими, рекомбинантными, выделенными и/или очищенными.
Согласно одному воплощению изобретения предложена нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую любой из TCR, полипептидов или белков, описанных в данном документе. Термин «нуклеиновая кислота», в том виде, в котором он используется в данном документе, включает «полинуклеотид», «олигонуклеотид» и «молекулу нуклеиновой кислоты» и обычно означает полимер ДНК или РНК, который может быть одноцепочечным или двухцепочечным, который может содержать природные, неприродные или измененные нуклеотиды, и который может содержать природную, неприродную или измененную межнуклеотидную связь, такую как фосфорамидатная связь или фосфортиоатная связь, вместо фосфодиэфира, обнаруженного между нуклеотидами немодифицированного олигонуклеотида. В одном воплощении нуклеиновая кислота содержит комплементарную ДНК (кДНК). Обычно предпочтительно, чтобы нуклеиновая кислота не содержала никаких вставок, делеций, инверсий и/или замен. Однако, может быть подходящим в некоторых примерах, как описано в данном документе, чтобы нуклеиновая кислота содержала одну или более вставок, делеций, инверсий и/или замен.
Предпочтительно, нуклеиновые кислоты по изобретению являются рекомбинантными. В том виде, в котором он используется в данном документе, термин «рекомбинантный» относится к (i) молекулам, которые конструируют за пределами живых клеток посредством присоединения сегментов природных или синтетических нуклеиновых кислот к молекулам нуклеиновой кислоты, которые могут реплицироваться в живой клетке, или (ii) молекулам, которые получены в результате репликации молекул, описанных выше в (i). В целях данного документа, репликация может представлять собой репликацию in vitro или репликацию in vivo.
Нуклеиновые кислоты могут быть сконструированы на основе химического синтеза и/или ферментативных реакций лигирования с использованием способов, известных в данном документе. См. выше, например, Green and Sambrook et al. Например, нуклеиновая кислота может быть химически синтезирована с использованием встречающихся в природе нуклеотидов или по-разному модифицированных нуклеотидов, сконструированных для повышения биологической стабильности молекул или для увеличения физической стабильности дуплекса, образованного при гибридизации (например, производные фосфортиоата и акридин-замещенные нуклеотиды). Примеры модифицированных нуклеотидов, которые могут быть использованы для образования нуклеиновых кислот, включают, но не ограничиваются нижеследующим: 5-фторурацил, 5-бромурацил, 5-хлорурацил, 5-йодурацил, гипоксантин, ксантин, 4-ацетилцитозин, 5-(карбоксигидроксиметил) урацил, 5-карбоксиметиламинометил-2-тиоуридин, 5-карбоксиметиламинометилурацил, дигидроурацил, бета-D-галактозилквеозин, инозин, N6-изопентениладенин, 1-метилгуанин, 1-метилинозин, 2,2-диметилгуанин, 2-метиладенин, 2-метилгуанин, 3-метилцитозин, 5-метилцитозин, N6-замещенный аденин, 7-метилгуанин, 5-метиламинометиламинометилурацил, 5-метоксиаминометил-2-тиоулурацил, бета-D-маннозилквеозин, 5'-метоксикарбоксиметилурацил, 5-метоксиурацил, 2-метилтио-N6-изопентениладенин, урацил-5-оксиуксусная кислота (v), вибутоксозин, псевдоурацил, квеозин, 2-тиоцитозин, 5-метил-2-тиоурацил, 2-тиоурацил, 4-тиоурацил, 5-метилурацил, сложный метиловый эфир урацил-5-оксиуксусной кислоты, 3-(3-амино-3-N-2-карбоксипропил) урацил и 2,6-диаминопурин. В качестве альтернативы одна или более из нуклеиновых кислот по изобретению может быть приобретена у компаний, таких как Macromolecular Resources (Fort Collins, CO) и Synthegen (Houston, TX).
В одном воплощении изобретения нуклеиновая кислота содержит нуклеотидную последовательность с оптимизированными кодонами, кодирующую любые из TCR, полипептидов или белков, описанных в данном документе. Без связывания какой-либо конкретной теорией или механизмом, полагают, что оптимизация кодонов нуклеотидной последовательности повышает эффективность трансляции транскриптов мРНК (матричная РНК). Оптимизация кодонов нуклеотидной последовательности может включать замену нативного кодона другим кодоном, который кодирует ту же аминокислоту, но может транслироваться тРНК (транспортная РНК), которая более легко доступна в клетке, с повышением, таким образом, эффективности трансляции.
Оптимизация нуклеотидной последовательности также может сокращать вторичные структуры мРНК, которые могли бы мешать трансляции, повышая, таким образом, эффективность трансляции.
Согласно изобретению также предложена нуклеиновая кислота, содержащая нуклеотидную последовательность, которая комплементарна нуклеотидной последовательности любой из нуклеиновых кислот, описанных в данном документе, или нуклеотидную последовательность, которая гибридизуется в жестких условиях с нуклеотидной последовательностью любой из нуклеиновых кислот, описанных в данном документе.
Нуклеотидная последовательность, которая гибридизуется в жестких условиях, предпочтительно гибридизуется в условиях высокой жесткости. Под фразой «условия высокой жесткости» подразумевается, что нуклеотидная последовательность специфично гибридизуется с целевой последовательностью (нуклеотидной последовательностью любой из нуклеиновых кислот, описанных в данном документе) в количестве, которое заметно сильнее, чем при неспецифичной гибридизации. Условия высокой жесткости включают условия, которые будут отличать полинуклеотид с точной комплементарной последовательностью или полинуклеотид, содержащий только несколько разрозненных ошибок спаривания, от случайной последовательности, которая, как оказалось, имеет несколько маленьких областей (например, 3-10 оснований), которые совпадали с нуклеотидной последовательностью. Такие маленькие области комплементарности легче плавятся, чем полноразмерный комплемент из 14-17 или более оснований, и гибридизация в условиях высокой жесткости делает их легко различимыми. Условия относительно высокой жесткости будут включать, например, низкосолевые и/или высокотемпературные условия, как например, обеспеченные примерно 0,02-0,1 М NaCl или эквивалентом, при температурах примерно 50-70°С. Такие условия высокой жесткости допускают мало, если вообще допускают, ошибок спаривания между нуклеотидной последовательностью и матрицей или целевой цепью, особенно подходят для выявления экспрессии любого из TCR по изобретению. Обычно следует принимать во внимание, что условия могут становиться более жесткими в результате добавления увеличивающихся количеств формамида.
Согласно изобретению также предложена нуклеиновая кислота, содержащая нуклеотидную последовательность, которая по меньшей мере на примерно 70% или более, например, примерно 80%, примерно 90%, примерно 91%, примерно 92%, примерно 93%, примерно 94%, примерно 95%, примерно 96%, примерно 97%, примерно 98% или примерно 99% идентична любой из нуклеиновых кислот, описанных в данном документе. В связи с этим, нуклеиновая кислота может по существу состоять из любых нуклеотидных последовательностей, описанных в данном документе.
Нуклеиновые кислоты по изобретению могут быть включены в рекомбинантный экспрессионный вектор. В этом отношении, согласно изобретению предложен рекомбинантный экспрессионный вектор, содержащий любую из нуклеиновых кислот по изобретению. В одном воплощении изобретения рекомбинантный экспрессионный вектор содержит нуклеотидную последовательность, кодирующую цепь α, цепь β и линкерный пептид.
В целях данного документа, термин «рекомбинантный экспрессионный вектор» обозначает конструкцию генетически модифицированного олигонуклеотида или полинуклеотида, которая делает возможной экспрессию мРНК, белка, полипептида или пептида клеткой-хозяином, когда конструкция содержит нуклеотидную последовательность, кодирующую мРНК, белок, полипептид или пептид, и вектор приводится в контакт с клеткой в условиях, достаточных для экспрессии мРНК, белка, полипептида или пептида в клетке. Векторы по изобретению не встречаются в природе как единое целое. Однако, части векторов могут встречаться в природе. Рекомбинантные экспрессионные векторы по изобретению могут содержать любой тип нуклеотида, включая, но, не ограничиваясь ДНК и РНК, которые могут являться одноцепочечными или двухцепочечными, синтезированными или полученными отчасти из природных источников, и которые могут содержать природные, неприродные или измененные нуклеотиды. Рекомбинантные экспрессионные векторы могут содержать встречающиеся в природе, не встречающиеся в природе межнуклеотидные связи или оба типа связей. Предпочтительно, не встречающиеся в природе или измененные нуклеотиды или межнуклеотидные связи не препятствуют транскрипции или репликации вектора.
Рекомбинантный экспрессионный вектор по изобретению может представлять собой любой подходящий рекомбинантный экспрессионный вектор и может быть использован для трансформации или трансфекции любой подходящей клетки-хозяина. Подходящие векторы включают векторы, сконструированные для наработки и размножения или для экспрессии или и того и другого, такие как плазмиды и вирусы. Вектор может быть выбран из группы, состоящей из серии транспозон/транспозаза, серии pUC (Fermentas Life Sciences), серии pBluescript (Stratagene, LaJolla, СА), серии pET (Novagen, Madison, WI), серии pGEX (Pharmacia Biotech, Uppsala, Швеция) и серии pEX (Clontech, Palo Alto, СА). Также можно использовать векторы на основе бактериофагов, такие как λGT10, λGT11, λZapll (Stratagene), λEMBL4 и λNM1149. Примеры экспрессионных векторов растений включают pBI01, pBI101.2, pBI101.3, pBI121 и pBIN19 (Clontech). Примеры экспрессионных векторов животных включают pEUK-CI, рМАМ и pMAMneo (Clontech). Предпочтительно рекомбинантный экспрессионный вектор представляет собой транспозонный вектор или вирусный вектор, например, ретровирусный вектор.
Рекомбинантные экспрессионные векторы по изобретению могут быть получены, используя стандартные методики генной инженерии, описанные, например, в Green and Sambrook et al., см. выше. Конструкции экспрессионных векторов, которые являются кольцевыми или линейными, могут быть получены содержащими систему репликации, являющуюся функциональной в прокариотической или эукариотической клетке-хозяине. Системы репликации могут происходить, например, из ColEI, 2 μ плазмизы, λ, SV40, вируса папилломы крупного рогатого скота и т.п.
Желательно, чтобы рекомбинантный экспрессионный вектор содержал регуляторные последовательности, такие как старт-кодон и стоп-кодон транскрипции и трансляции, которые специфичны в отношении типа клетки-хозяина (например, бактерия, гриб, растение или животное), в которую вектор должен быть введен, исходя из конкретного случая и принимая во внимание то, основан ли вектор на ДНК или РНК.
Рекомбинантный экспрессионный вектор может включать один или более маркерных генов, которые делают возможной селекцию трансформированных или трансфицированных клеток-хозяев. Маркерные гены включают устойчивость к биоциду, например, устойчивость к антибиотикам, тяжелым металлам и т.д., дополнение в ауксотрофной клетке-хозяине для обеспечения прототрофности и т.д. Подходящие маркерные гены для экспрессионных векторов по изобретению включают, например, гены устойчивости к неомицину/G418, гены устойчивости к гигромицину, гены устойчивости к гистидинолу, гены устойчивости к тетрациклину и гены устойчивости к ампициллину.
Рекомбинантный экспрессионный вектор может содержать нативный или ненативный промотор, функционально связанный с нуклеотидной последовательностью, кодирующей TCR, полипептид или белок, или с нуклеотидной последовательностью, которая комплементарна или которая гибридизуется с нуклеотидной последовательностью, кодирующей TCR, полипептид или белок. Отбор промоторов, например, сильных, слабых, индуцибельных, тканеспецифичных и специфичных в отношении стадии развития, находится в компетенции обычного специалиста в данной области. Аналогично, объединение нуклеотидной последовательности с промотором также находится в компетенции специалиста в данной области. Промотор может представлять собой невирусный промотор, например, промотор человеческого фактора элонгации-1α, или вирусный промотор, например, промотор цитомегаловируса (CMV - от англ. cytomegalovirus), промотор SV40, промотор RSV и промотор, обнаруженный в длинном концевом повторе вируса стволовых клеток мыши.
Рекомбинантные экспрессионные векторы по изобретению могут быть сконструированы или для временной экспрессии, или для стабильной экспрессии или для того и другого. Кроме того, рекомбинантные экспрессионные векторы могут быть сделаны для конститутивной экспрессии или для индуцибельной экспрессии.
Кроме того, рекомбинантные экспрессионные векторы могут быть сделаны таким образом, чтобы они включали ген самоубийства. В том виде, в котором он используется в данном документе, термин «ген самоубийства» относится к гену, который вызывает гибель клетки, экспрессирующей данный ген самоубийства. Ген самоубийства может представлять собой ген, который придает клетке, в которой экспрессируется данный ген, чувствительность к агенту, например, лекарственному средству, и вызывает гибель клетки, когда клетка контактирует с или подвергается воздействию данного агента. Гены самоубийства известны в данной области и включают, например, ген тимидинкиназы (TK - от англ. thymidine kinase) вируса простого герпеса (HSV - от англ. herpes simplex virus), цитозиндеаминазы, пуриннуклеозидфосфорилазы и нитроредуктазы.
Согласно другому воплощению изобретения дополнительно предложена клетка-хозяин, содержащая любой из рекомбинантных экспрессионных векторов, описанных в данном документе. В том виде, в котором он используется в данном документе, термин «клетка-хозяин» относится к любому типу клетки, который может содержать рекомбинантный экспрессионный вектор по изобретению. Клетка-хозяин может представлять собой эукариотическую клетку, например, растения, животного, грибов или водорослей, или может представлять собой прокариотическую клетку, например, бактерий или простейших. Клетка-хозяин может представлять собой культивируемую клетку или первичную клетку, то есть выделенную непосредственно из организма, например, человека. Клетка-хозяин может представлять собой адгезивную клетку или суспензионную клетку, то есть клетку, которая растет в суспензии. Подходящие клетки-хозяева известны в данной области и включают, например, клетки Е. coli DH5α, клетки яичника китайского хомяка, клетки VERO мартышки, клетки COS, клетки HEK293 и т.п. В целях амплификации или репликации рекомбинантного экспрессионного вектора клетка-хозяин предпочтительно представляет собой прокариотическую клетку, например, клетку DH5α. В целях получения рекомбинантного TCR, полипептида или белка, клетка-хозяин предпочтительно представляет собой клетку млекопитающего. Наиболее предпочтительно, клетка-хозяин представляет собой клетку человека. В то время как клетка-хозяин может быть клеткой любого типа клетки, может происходить из любого типа ткани и может находиться на любой стадии развития, клетка-хозяин предпочтительно представляет собой лимфоцит периферической крови (PBL - от англ. peripheral blood lymphocyte) или мононуклеарную клетку периферической крови (РВМС). Более предпочтительно, клетка-хозяин представляет собой Т-клетку.
В целях данного документа Т-клетка может представлять собой любую Т-клетку, такую как культивируемая Т-клетка, например, первичная Т-клетка или Т-клетка из культивируемой линии Т-клеток, например, Jurkat, SupT1 и т.д., или Т-клетка, полученная от млекопитающего. В случае получения от млекопитающего Т-клетка может быть получена из многих источников, включая, но, не ограничиваясь кровью, костным мозгом, лимфатическим узлом, тимусом или другими тканями или жидкостями. Т-клетки могут быть также обогащены или очищены. Предпочтительно, Т-клетка представляет собой Т-клетку человека. Т-клетка может быть любого типа Т-клетки и может находиться на любой стадии развития, включая CD4+/CD8+ дважды позитивные Т-клетки, CD4+ Т-хелперы, например, клетки Th1 и Th2, CD4+ Т-клетки, CD8+ Т-клетки (например, цитотоксические Т-клетки), опухоль-инфильтрирующие лимфоциты (TIL), Т-клетки памяти (например, центральные Т-клетки памяти и эффекторные Т-клетки памяти), интактные Т-клетки и т.п., но, не ограничиваясь ими.
Также согласно изобретению предложена популяция клеток, содержащая по меньшей мере одну клетку-хозяина, описанную в данном документе. Популяция клеток может представлять собой гетерогенную популяцию, содержащую клетку-хозяина, содержащую любой из описанных рекомбинантных экспрессионный векторов, помимо по меньшей мере одной другой клетки, например, клетки-хозяина (например, Т-клетки), которая не содержит никакого из рекомбинантных экспрессионных векторов, или клетки, отличной от Т-клетки, например, В-клетки, макрофага, нейтрофила, эритроцита, гепатоцита, эндотелиальной клетки, эпителиальной клетки, мышечной клетки, клетки головного мозга и т.д. В качестве альтернативы, популяция клеток может представлять собой по существу однородную популяцию, где популяция содержит в основном клетки-хозяева (например, по существу состоящие из), содержащие рекомбинантный экспрессионный вектор. Популяция также может представлять собой клональную популяцию клеток, в которой все клетки популяции представляют собой клоны одной единственной клетки-хозяина, содержащей рекомбинантный экспрессионный вектор, таким образом, что все клетки популяции содержат рекомбинантный экспрессионный вектор. В одном воплощении изобретения популяция клеток представляет собой клональную популяцию, содержащую клетки-хозяева, содержащие рекомбинантный экспрессионный вектор, как описано в данном документе.
В одном воплощении изобретения число клеток в популяции может быстро увеличиваться. Увеличение числа Т-клеток может осуществляться любым из целого ряда способов, известных в данной области, как описано, например, в патенте США 8034334; патенте США 8383099; публикации патентной заявки США №2012/0244133; Dudley et al., J. Immunother., 26: 332-42 (2003); и Riddell et al., J. Immunol. Methods, 128: 189-201 (1990). В одном воплощении увеличение числа Т-клеток осуществляют посредством культивирования Т-клеток с антителом ОКТЗ, IL-2 и фидерными РВМС (например, облученными аллогенными РВМС).
TCR, полипептиды, белки, нуклеиновые кислоты, рекомбинантные экспрессионные векторы и клетки-хозяева (включая их популяции) по изобретению могут быть выделены и/или очищены. Термин «выделенный», в том виде, в котором он используется в данном документе, означает удаленный из его природной окружающей среды. Термин «очищенный», в том виде, в котором он используется в данном документе, означает с повышенной чистотой, где «чистота» является относительным термином и не обязательно понимается как абсолютная чистота. Например, чистота может составлять по меньшей мере примерно 50%, по меньшей мере примерно 60%, по меньшей мере примерно 70%, по меньшей мере примерно 80%, по меньшей мере примерно 90%, по меньшей мере примерно 95% или может составлять примерно 100%.
TCR, полипептиды, белки, нуклеиновые кислоты, рекомбинантные экспрессионные векторы и клетки-хозяева (включая их популяции) по изобретению, все из которых далее в данном документе в совокупности называются «TCR материалами по изобретению», могут быть приготовлены в композиции, такой как фармацевтическая композиция. В связи с этим, согласно изобретению предложена фармацевтическая композиция, содержащая любой из TCR, полипептидов, белков, нуклеиновых кислот, экспрессионных векторов и клеток-хозяев (включая их популяции), описанных в данном документе, и фармацевтически приемлемый носитель. Фармацевтические композиции по изобретению, содержащие любой из TCR материалов по изобретению, могут содержать более одного TCR материала по изобретению, например, полипептид и нуклеиновую кислоту, или два или более разных TCR. В качестве альтернативы, фармацевтическая композиция может содержать TCR материал по изобретению в комбинации с другим(и) фармацевтически активным(и) агентом(ами) или лекарственным(и) средством(ами), таким(и) как химиотерапевтический агент, например, аспарагиназа, бусульфан, карбоплатин, цисплатин, даунорубицин, доксорубицин, фторурацил, гемцитабин, гидроксимочевина, метотрексат, паклитаксел, ритуксимаб, винбластин, винкристин и т.д.
Предпочтительно, носитель представляет собой фармацевтически приемлемый носитель. В отношении фармацевтических композиций носитель может представлять собой любой из носителей, традиционно используемых для конкретного рассматриваемого TCR материала по изобретению. Способы получения вводимых композиций известны или очевидны специалистам в данной области и описаны более подробно, например, в Remington: The Science and Practice of Pharmacy, 22nd Ed., Pharmaceutical Press (2012). Предпочтительно, чтобы фармацевтически приемлемый носитель представлял собой носитель, который не обладает вредными побочными эффектами или токсичностью в применяемых условиях.
Выбор носителя будет определяться отчасти конкретным TCR материалом по изобретению, а также конкретным способом, используемым для введения TCR материала по изобретению. Соответственно, существует множество подходящих препаратов фармацевтической композиции по изобретению. Подходящие препараты могут включать любой из препаратов для парентерального, подкожного, внутривенного, внутримышечного, внутриартериального, интратекального, внутриопухолевого или внутрибрюшинного введения. Более чем один путь может быть использован для введения TCR материалов по изобретению, и, в определенных примерах, конкретный путь может обеспечивать более немедленную и более эффективную реакцию, чем в случае другого пути.
Предпочтительно, TCR материал по изобретению вводят посредством инъекции, например, внутривенно. Когда TCR материал по изобретению представляет собой клетку-хозяина, экспрессирующую TCR по изобретению, фармацевтически приемлемый носитель для клеток для инъекции может включать любой изотонический носитель, такой как, например, нормальный физиологический раствор (примерно 0,90 масс./об. % NaCl в воде, примерно 300 мосмоль/л NaCl в воде или примерно 9,0 г NaCl на литр воды), раствор электролита NORMOSOL R (Abbott, Chicago, IL), PLASMA-LYTE A (Baxter, Deerfield, IL), примерно 5%-ную декстрозу в воде или Рингера-лактат. В одном воплощении фармацевтически приемлемый носитель дополняют человеческим сывороточным альбумином.
В целях изобретения количество или доза (например, число клеток, когда TCR материал по изобретению представляет собой одну или более клеток) вводимого TCR материала по изобретению должны быть достаточными для эффекта, например, терапевтического или профилактического ответа, у субъекта или животного за разумный период времени. Например, доза TCR материала по изобретению должна быть достаточной для связывания с раковым антигеном (например, мутантным р53) или выявления, лечения или предупреждения рака за период от примерно 2 часов или больше, например, от 12 до 24 или более часов, с момента введения. В конкретных воплощениях период времени мог бы быть даже больше. Доза будет определяться эффективностью конкретного TCR материала по изобретению и состоянием животного (например, человека), а также массой тела данного животного (например, человека), подлежащего лечению.
Многие анализы для определения вводимой дозы известны в данной области. В целях изобретения анализ, который включает сравнение степени, до которой лизируются клетки-мишени или секретируется IFN-γ Т-клетками, экспрессирующими TCR, полипептид или белок по изобретению при введении данной дозы таких Т-клеток млекопитающему у целого ряда млекопитающих, каждому из которых дается разная доза Т-клеток, можно было бы использовать для определения исходной дозы, подлежащей введению млекопитающему. Степень, до которой лизируются клетки-мишени или секретируется IFN-γ при введении определенной дозы, можно анализировать способами, известными в данной области.
Доза TCR материала по изобретению также будет определяться существованием, природой и степенью любых вредных побочных эффектов, которые могут сопутствовать введению конкретного TCR материала по изобретению. Обычно, лечащий врач будет принимать решение относительно дозировки TCR материала по изобретению, посредством которой лечить каждого отдельного пациента, учитывая множество факторов, таких как возраст, масса тела, общее состояние здоровья, рацион, пол, TCR материал по изобретению, подлежащий введению, способ введения и тяжесть рака, подлежащего лечению. В одном воплощении, в котором TCR материал по изобретению представляет собой популяцию клеток, число клеток, вводимых за инфузию, может варьировать, например, от примерно 1×106 до примерно 1×1012 клеток или больше. В конкретных воплощениях можно вводить меньше чем 1×106 клеток.
Одному из обычных специалистов в данной области будет сразу понятно, что TCR материалы по изобретению могут быть модифицированы множеством путей, таким образом, чтобы терапевтическая или профилактическая эффективность TCR материалов по изобретению увеличивалась посредством данной модификации. Например, TCR материалы по изобретению могут быть конъюгированы или прямо, или опосредовано через мостик с химиотерапевтическим агентом. В данной области известно практическое применение конъюгации соединений с химиотерапевтическим агентом. Один из обычных специалистов в данной области признает, что сайты на TCR материалах по изобретению, которые не являются необходимыми для функции TCR материалов по изобретению, являются сайтами, идеальными для присоединения мостика и/или химиотерапевтического агента, при условии, что мостик и/или химиотерапевтический агент, будучи присоединенным(и) к TCR материалам по изобретению, не препятствует(ют) функции TCR материалов по изобретению, то есть способности связываться с мутантным р53 или выявлять, лечить или предупреждать рак.
Предполагается, что фармацевтические композиции, TCR, полипептиды, белки, нуклеиновые кислоты, рекомбинантные экспрессионные векторы, клетки-хозяева или популяции клеток по изобретению могут быть использованы в способах лечения или предупреждения рака. Без привязки к конкретной теории, полагают, что TCR по изобретению специфично связываются с мутантным р53, таким образом, что TCR (или родственный полипептид или белок по изобретению), при экспрессии клеткой, способен опосредовать иммунный ответ на клетку-мишень, экспрессирующую мутантный р53. В этой связи, согласно одному воплощению изобретения предложен способ лечения или предупреждения рака у млекопитающего, включающий введение млекопитающему любой из фармацевтических композиций, TCR, полипептидов или белков, описанных в данном документе, любой нуклеиновой кислоты или рекомбинантного экспрессионного вектора, содержащего нуклеотидную последовательность, кодирующую любой из TCR, полипептидов, белков, описанных в данном документе, или любой клетки-хозяина или популяции клеток, содержащих рекомбинантный вектор, который кодирует любой из TCR, полипептидов или белков, описанных в данном документе, в количестве, эффективном для лечения или предупреждения рака у млекопитающего.
Согласно одному воплощению изобретения предложена любая из фармацевтических композиций, TCR, полипептидов или белков, описанных в данном документе, любая нуклеиновая кислота или рекомбинантный экспрессионный вектор, содержащий нуклеотидную последовательность, кодирующую любой из TCR, полипептидов, белков, описанных в данном документе, или любая клетка-хозяин или популяция клеток, содержащих рекомбинантный вектор, который кодирует любой из TCR, полипептидов или белков, описанных в данном документе, для применения в лечении или предупреждении рака у млекопитающего.
Термины «лечить» и «предупреждать», а также слова, происходящие от них, в том виде, в котором они используются в данном документе, не обязательно подразумевают 100%-ое или полное вылечивание или предупреждение. Вернее, существуют варьирующие степени лечения или предупреждения, которые обычный специалист в данной области расценивает как приносящие возможную пользу или терапевтический эффект. В связи с этим, способы по изобретению могут обеспечивать любое количество любого уровня лечения или предупреждения рака у млекопитающего. Кроме того, лечение или предупреждение, предложенные согласно способу по изобретению, могут включать лечение или предупреждение одного или более состояний или симптомов рака, подлежащего лечению или предупреждению. Например, лечение или предупреждение может включать стимулирование регрессии опухоли. Кроме того, в целях данного документа, термин «предупреждение» может охватывать задержку начала рака или его симптома или состояния. В качестве альтернативы или дополнительно, термин «предупреждение» может охватывать предупреждение или задержку рецидива рака или его симптома или патологического состояния.
Также согласно воплощению изобретения предложен способ выявления наличия рака у млекопитающего. Способ включает (i) приведение образца, содержащего одну или более клеток от млекопитающего, в контакт с любым из TCR, полипептидов, белков, нуклеиновых кислот, рекомбинантных экспрессионных векторов, клеток-хозяев, популяций клеток или фармацевтических композиций по изобретению, описанных в данном документе, с образованием, посредством этого, комплекса, и (ii) выявление данного комплекса, где выявление комплекса свидетельствует о наличии рака у млекопитающего.
Относительно способа выявления рака у млекопитающего по изобретению, образец клеток может представлять собой образец, содержащий цельные клетки, их лизаты или фракцию лизатов цельных клеток, например, ядерную или цитоплазматическую фракцию, фракцию общего белка или фракцию нуклеиновой кислоты.
В целях способа выявления по изобретению, приведение в контакт может происходить in vitro или in vivo относительно млекопитающего. Предпочтительно, приведение в контакт происходит in vitro.
Кроме того, выявление комплекса может происходить посредством любого числа путей, известных в данной области. Например, TCR, полипептиды, белки, нуклеиновые кислоты, рекомбинантные экспрессионные векторы, клетки-хозяева или популяции клеток по изобретению, описанные в данном документе, могут быть мечены выявляемой меткой, такой как, например, радиоизотоп, флуорофор (например, флуоресцеин изотиоцианат (FITC - от англ. fluorescein isothiocyanate), фикоэритрин (РЕ - от англ. phycoerythrin)), фермент (например, щелочная фосфатаза, пероксидаза хрена) и элементарные частицы (например, частицы золота).
В целях способов по изобретению, в которых вводят клетки-хозяева или популяции клеток, клетки могут представлять собой клетки, которые являются аллогенными или аутологичными в отношении млекопитающего. Предпочтительно, клетки являются аутологичными в отношении млекопитающего.
В отношении способов по изобретению рак может представлять собой любой рак, включая, например, любой из следующих видов рака: острый лимфоцитарный рак, острый миелоидный лейкоз, альвеолярная рабдомиосаркома, рак кости, рак головного мозга, рак молочной железы, рак ануса и анального канала или прямой кишки, рак глаза, рак внутрипеченочного желчного протока, рак суставов, рак шеи, желчного пузыря или плевры, рак носа, носовой полости или среднего уха, рак ротовой полости, рак влагалища, рак вульвы, хронический лимфоцитарный лейкоз, хронический миелоидный рак, рак толстой кишки, коло ректальный рак, рак эндометрия, рак пищевода, рак шейки матки, карциноидная опухоль желудочно-кишечного тракта, глиома, лимфома Ходжкина, рак гортаноглотки, рак почки, рак гортани, рак печени, рак легкого, злокачественная мезотелиома, меланома, множественная миелома, рак носоглотки, неходжкинская лимфома, рак ротоглотки, рак яичника, рак пениса, рак поджелудочной железы, брюшины, сальника и рак брыжейки тонкой кишки, рак глотки, рак предстательной железы, рак прямой кишки, рак почки, рак кожи, рак тонкой кишки, рак мягкой ткани, рак желудка, рак яичка, рак щитовидной железы, рак матки, рак мочеточника и рак мочевого пузыря. В одном предпочтительном воплощении рак представляет собой рак, при котором экспрессируется мутантный р53. При раке может экспрессироваться р53 с мутацией в одном или обоих положениях 175 и 220, как определено SEQ ID NO: 1. При раке может экспрессироваться р53 с одной или обеими из следующих мутаций человеческого р53: R175H и Y220C. Предпочтительно, рак представляет собой эпителиальный рак или холангиокарциному, меланому, рак толстой кишки, рак прямой кишки, рак яичника, рак эндометрия, немелкокпеточный рак легкого (NSCLC), глиобластому, рак шейки матки, рак головы и шеи, рак молочной железы, рак поджелудочной железы или рак мочевого пузыря.
Млекопитающее, на которое ссылаются в способах по изобретению, может представлять собой любое млекопитающее. В том виде, в котором он используется в данном документе, термин «млекопитающее» относится к любому млекопитающему, включая млекопитающих отряда Rodentia, таких как мыши и хомяки, и млекопитающих отряда Logomorpha, таких как кролики, но, не ограничиваясь ими. Предпочтительным является то, чтобы млекопитающие происходили из отряда Carnivora, включая Felines (кошки) и Canines (собаки). Более предпочтительно, чтобы млекопитающие происходили из отряда Artiodactyla, включая Bovines (коровы) и Swines (свиньи), или из отряда Perssodactyla, включая Equines (лошади). Наиболее предпочтительно, чтобы млекопитающие принадлежали к отряду Primates, Ceboids или Simoids (обезьяны) или к отряду Anthropoids (человек и человекообразные обезьяны). Особенно предпочтительным млекопитающим является человек.
Следующие примеры дополнительно иллюстрируют изобретение, но, конечно, никоим образом не должны рассматриваться как ограничивающие его объем.
ПРИМЕРЫ
Следующие материалы и методы использовали в экспериментах, описанных в Примерах 1-7.
Субъекты и образцы
Продукты лейкафереза и образцы опухоли получали у индивидов с эпителиальными метастатическими раковыми заболеваниями, отобранных Национальным институтом здоровья в протоколе NCT01174121, который был одобрен экспертным советом медицинского учреждения (IRB - от англ. institutional-review board) Национального института онкологии (NCI - от англ. National Cancer Institute). Пациентов выбирали на основе доступности результатов по предварительному лечению, лейкаферезу и TIL скринингу, и они получали предшествующие терапии (хирургическое вмешательство, химиотерапию, лучевую терапию) по стандарту медицинской помощи (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019); Deniger et al., Clin. Cancer Res., 24 (22): 5562-73 (2018)). Ficoll-Hypaque использовали для выделения PBL (от англ. Peripheral Blood Leukocyte -лимфоцит периферической крови) из продукта лейкафереза, и клетки криоконсервировали для дальнейшего использования. Все исследуемые пациенты имели мутацию ТР53, подтвержденную посредством полноэкзомного секвенирования в линии с использованием клинических протоколов, как описано ранее (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)).
Антитела и FACS
Проточная цитометрия на основе флуоресцентно меченых антител подробно описана в Таблице 1. Аналитическую проточную цитометрию проводили в системе FACS (от англ. fluorescence-activated cell sorting - сортировка клеток с активированной флуоресценцией) CANTO II (BD Biosciences, San Jose, СА) с анализом посредством программного обеспечения FLOWJO (TreeStar, Ashland, OR). Все клетки сортировали по лимфоцитам и живым клеткам по исключению клеток, окрашенных йодидом пропидия (PI). Клетки сортировали для IVS и 4-1ВВ/ОХ40 на клеточном сортере FACS ARIA II (BD Biosciences). 4-1BB+ и/или ОХ40+ клетки сортировали по отдельности через CD3+CD4+CD8- (CD4) и CD3+CD4-CD8+ (CD8) ворота. Сокультуры сортировали посредством клеточного сортера SH800S (Sony Biotechnology) для ПЦР на одиночной клетке для идентификации генов TCR.
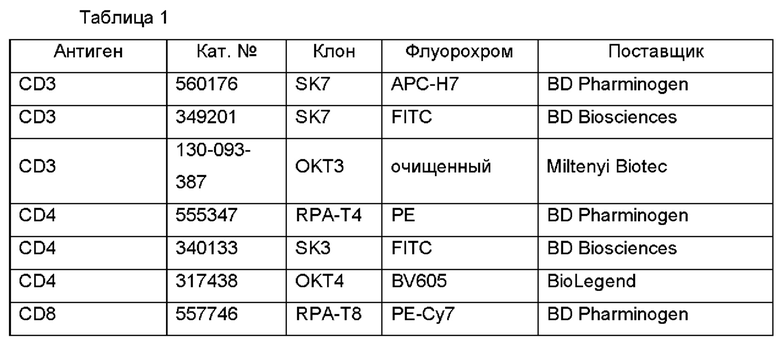
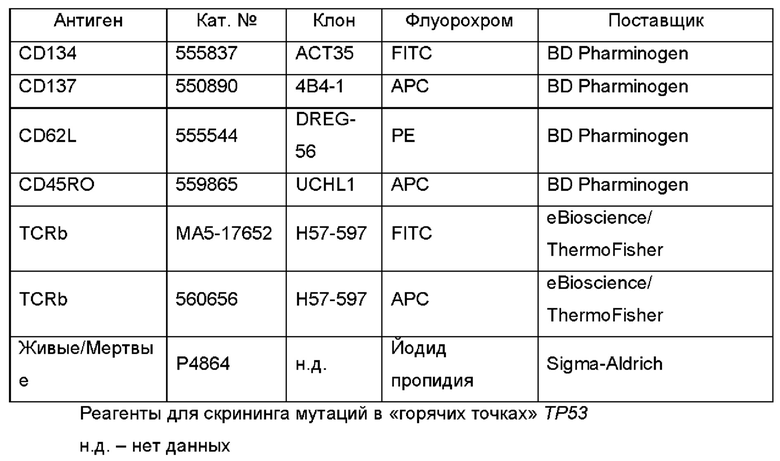
Конструкции TMG WT (дикий тип) (TMG-WT-TP53) и мутантного ТР53 (TMG-MUT-ТР53) получали для TIL скрининга, как описано ранее (Malekzadeh et al., J. Clin, invest 129 (3): 1109-14 (2019)). Кратко, каждую мутацию в «горячей точке» ТР53 (R175H, Y220C, G245S, G245D, R248L, R248Q, R248W, R249S, R273C, R273H, R273L и R282W) создавали в минигене с мутантным кодоном посередине и на 12 нормальных кодонов выше и ниже, и данные минигены объединяли в TMG. Также получали похожую последовательность, соответствующую последовательностям WT. TMG синтезировали в виде ДНК и клонировали в рамку с сигнальной последовательностью LAMP и последовательностью локализации DC-LAMP, затем транскрибировали in vitro до мРНК с использованием набора mMESSAGE mMACHINE Т7 Ultra в соответствии с инструкциями изготовителя (Thermo-Fisher; Waltham, MA). Кроме того, WT и мутантные пептиды синтезировали для p53R175H, p53R248W и p53Y220C и очищали до чистоты больше 95% посредством высокоэффективной жидкостной хроматографии (Genscript; Piscataway, NJ). Все пептиды восстанавливали повторно растворяли в ДМСО (диметилсульфоксид).
Антигенпрезентирующие клетки
Моноцитарные незрелые дендритные клетки (DC - от англ. dendritic cell) получали посредством способа адгезии (Tran et al., Science, 350 (6266): 1387-90 (2015)). Кратко, PBL высевали в среду AIM-V (Life Technologies, Waltham, MA), содержащую ДНКазу (Genentech Inc., San Francisco, СА), и инкубировали в течение 1,5-2 часов при 37°С. Неприлипшие клетки удаляли и использовали свежими или криоконсервированными. Прилипшие клетки промывали в AIM-V, инкубировали один час при 37°С, и среду заменяли на среду DC (RPMI-1640, 2 мМ L-глутамин, с 5%-ной человеческой сывороткой, 100 Ед/мл пенициллина, 100 мкг/мл стрептомицина, амфотерицина В, 800 МЕд/мл гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF - от англ. granulocyte-macrophage colony-stimulating factor) и 200 Ед/мл интерлейкина-4 (IL-4 - от англ. intereleukin-4) (Peprotech, Rocky Hill, NJ)). Клетки подпитывали каждые 2-3 суток и собирали в сутки 5-6.
IVS, сокультура, мутантная в отношении ТР53, обогащение 4-1ВВ/ОХ40 и REP
Для проведения сортировки клеток после контакта с антигеном предварительную обработку PBL проводили, как описано ранее (Cafri et al., Nat. Commun., 10 (1): 449 (2019)). Криоконсервированные образцы афереза размораживали, промывали, доводили до 5-10×106 клеток/мл средой AIM-V, содержащей ДНКазу, и жизнеспособные клетки 1,75-2×108 высевали в колбы Т175 (Corning Inc., Corning, NY) и инкубировали при 37°С, 5% CO2 в течение 90 минут. После 90 минут неприлипшие, обедненные моноцитами PBL собирали, центрифугировали и инкубировали в течение ночи при 37°С и 5% CO2 в среде 50/50 (среда AIM-V, среда RPMI-1640 (Lonza, Walkersville, MD), содержащая 5%-ную сыворотку АВ человека, 100 Ед/мл пенициллина и 100 мкг/мл стрептомицина (Life Technologies), 2 мМ L-глутамин (Life Technologies), 10 мкг/мл гентамицина (Quality Biological Inc., Gaithersburg, MD), 12,5 мМ HEPES (Life Technologies)). Прилипшие моноциты дифференцировались в незрелые DC, как описано выше. После покоя неприлипших клеток в течение ночи клетки собирали, и 1-2×108 клеток ресуспендировали в 50 мкл окрашивающего буфера (PBS (от англ. phosphate buffered saline - фосфатно-солевой буферный раствор), 0,5% BSA (от англ. bovine serum albumin - бычий сывороточный альбумин, 2 мМ ЭДТА (Этилендиаминтетрауксусная кислота)) с антителами против CD3, CD8, CD4, CD62L, CD45RO. Клетки инкубировали в течение 30 минут при 4°С и два раза промывали перед приобретением. Для определения популяции сортировки сортировку осуществляли на живых клетках (негативных в отношении йодида пропидия), одиночных клетках, CD3+ Т-клетках, затем клетках после контакта с антигенами (CD62L-CD45RO+, CD62L+CD45RO+, CD62L-CD45RO-), которые были дополнительно подразделены на CD4+ или CD8+. CD8+ и CD4+ Т-клетки памяти после контакта с антигеном сортировали отдельно, собирали, считали и ресуспендировали в средах 50/50, содержащих концентрацию 60нг/мл интерлейкина-21 (IL-21). Аутологичные DC подвергали электропорации 18-24 часов предварительно с TMG-MUT-TP53 или под действие импульса в течение 2-4 часов в день сортировки FACS вводили специфичный в отношении пациента мутантный p53-LP. Клетки-мишени (DC) два раза промывали в средах 50/50 и ресуспендировали в средах 50/50 без цитокинов. Проводили стимуляцию in vitro (IVS) сокультуры в соотношении 1:3 - 1:6 (DC:T-клетка) в конечной концентрации 30нг/мл IL-21 после добавления DC. После 14 суток роста и 3-х подпиток IL-21 и интерлейкином-2 (IL-2; алдеслейкин), как описано ранее (Cafri et al., Nat. Commun., 10 (1): 449 (2019)), аутологичные DC еще раз подвергали электропорации или по действием импульса вводили TMG-MUT-TP53 или мутантный длинный пептид (LP - от англ. long peptide), соответственно, и совместно культивировали IVS культуры в течение 18-24 часов при 37°С и 5% CO2. Параллельно, IVS культуры совместно культивировали с DC, которых подвергали электропорации с использованием нерелевантного TMG или в которые посредством импульса вводили ДМСО в случае отрицательных контролей во время сортировки обогащения 4-1ВВ/ОХ40. После совместного культивирования клетки собирали и ресуспендировали в 50 мкл окрашивающего буфера (PBS, 0,5% BSA, 2 мМ ЭДТА), содержащего антитела против CD3, CD4, CD8, 4-1ВВ и ОХ40, инкубировали в течение 30 минут при 4°С и промывали два раза перед приобретением. Отсортированные 4-1ВВ+/ОХ40+ обогащенные Т-клетки размножали посредством REP с использованием питающих устройств облученных PBL, 30 нг/мл антитела ОКТЗ (Miltenyi Biotec, Bergisch Gladbach, Германия) и 3000 МЕд/мл IL-2 в средах 50/50. Быстро размножаемые (REP) культуры подпитывали 3 раза и тестировали в отношении реактивности или криоконсервировали в сутки 14.
Сокультура
Скрининг IVS и обогащенных Т-клеток выполняли посредством той же стратегии, используемой для скрининга TIL фрагментов (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)). Кратко, аутологичные DC подвергали электропорации с использованием TMG (105 клеток/лунка) и оставляли покоиться в течение ночи или в них посредством импульса вводили пептид или ДМСО (8×104 клеток/лунка) в течение 2-4 часов. Клетки-мишени два раза промывали и ресуспендировали в средах 50/50 и совместно культивировали с 2×104 Т-клетками в планшетах для метода иммуноферментных пятен (ELISPOT) для оценки интерферона-γ (IFNγ) (EMD Millipore, Burlington, MA). Форбол 12-миристат 13-ацетат (РМА - от англ. Phorbol 12-myristate 13-acetate) и иономицин (Thermo Fisher) использовали в качестве положительного контроля, и только среда представляла собой отрицательный контроль. Совместно культивируемые клетки удаляли, окашивали и анализировали посредством проточной цитометрии, как указано выше, в то время как планшет ELISPOT обрабатывали в соответствии с инструкциями изготовителя. Линии опухолевых клеток выращивали по меньшей мере в течение недели из криоконсервированных стоков перед совместной культивацией, и их поколение описано в другом месте (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)). Опухолевые клетки совместно культивировали в соотношении 1:1 с Т-клетками (общее количество клеток 2×105) в течение ночи в круглодонных 96-луночных планшетах. После сбора супернатанта сокультуры для оценки секреции IFNγ посредством твердофазного иммуноферментного анализа (ELISA; Thermo Fisher), совместно культивируемые клетки анализировали посредством проточной цитометрии.
Анализ минимальных пептидов и рестрикционное картирование HLA
Похожий способ, описанный ранее, использовали для идентификации минимальных пептидов и определения рестрикций HLA (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)). Кратко, использовали алгоритм аффинности связывания пептида NetMHC (v3.4) (Lundegaard et al., Bio informatics, 24 (11): 1397-8 (2008)) для предсказания неоэпитопов для аллелей HLA класса I. Пептиды - кандидаты из 9-11 аминокислот совместно культивировали, как описано выше. Для исследования CD4+ минимальных неоантигенов, пептиды из 15 аминокислот с перекрыванием 14 аминокислот, совместно культивировали, как описано выше. Для определения рестрикций HLA, опухолевые клетки COS7 высевали в количестве 2,5×104 клеток/лунка в RPMI-1640, содержащей 2 мМ L-глутамин и 10%-ную фетальную телячью сыворотку, в плоскодонные 96-луночные планшеты и инкубировали в течение ночи при 37°С. Отдельные аллели HLA класса-I, специфичные в отношении пациента (300 нг/лунка), или обе цепи α и β HLA класса-II (каждой 150 нг/лунка) в ДНК-плазмидах (каркас pcDNA3.1) подвергали трансфекции с помощью реагента для тансфекции LIPOFECTAMINE 2000 в соответствии с инструкциями изготовителя (ThermoFisher). Когда TMG совместно трансфицировали с HLA, концентрация HLA уменьшалась до 150 нг/лунка в случае класса-I и до 100 нг/лунка класса-II. TMG WT, используемые для данных экспериментов, представляли собой TMG-MUT-TP53, возвращенные к WT только в исследуемом положении, например, R175H. После 24-часовой инкубации среду для трансфекции удаляли, пептиды или ДМСО вводили под действием импульса в течение 2-4 часов в среде 50/50, лунки два раза промывали средой 50/50 и 105 Т-клеток инкубировали в течение ночи. Супернатанты сокультуры анализировали в отношении секреции IFNγ посредством ELISA, и клетки окрашивали в отношении повышающей регуляции 4-1ВВ и анализировали посредством проточной цитометрии.
Секвенирование TCRB
Секвенирование для исследования TCRB проводилось на основе геномной ДНК Adaptive Biotechnologies (Seattle, WA). Минимум 5×104 клеток направляли на секвенирование. Анализ продуктивных перестроек TCR проводили, используя инструмент IMMUNOSEQ ANALYZER 3.0 (Adaptive Biotechnologies).
Идентификация и реконструкция TCR
TCR идентифицировали посредством сортировки сокультур Т-клеток и DC, экспрессирующих неоантигены р53, в одиночные лунки с последующим проведением полимеразной цепной реакции с обратной транскриптазой на одиночной клетке (ОТ-ПЦР) генов TCR, аналогично предыдущим исследованиям (Pasetto et al., Cancer Immunol. Res., doi 10.1158/2326-6066.CIR-16-0001 (2016); Deniger et al., Clin. Cancer Res., 23 (2): 351-62 (2017)). ПЦР-продукты хранили раздельно в случае TCRα и TCRβ и анализировали посредством секвенирования методом Сэнгера Данные частичные последовательности TCR анализировали посредством веб-сайтов IMGT/V-Quest (imgt.org/IMGT) и IGBLAST (ncbi.nlm.nih.gov/igblast), которые идентифицировали точные CDR3 и J или D/J области и с наибольшей вероятностью семейство TRAV и TRBV. Человеческие полноразмерные вариабельные последовательности сливали с мышиными константными цепями, как было сделано в других исследованиях (Deniger et al., Clin. Cancer Res., 23 (2): 351-62 (2017); Cohen et al., J. Clin. Invest., 125 (10): 3981-91 (2015). Гены муринизированных TCRα и TCRβ связывали с RAKR-SGSG (SEQ ID NO: 128) и последовательностью с «проскоком» рибосомы Р2А с получением стехиометрической экспрессии цепей TCR в одиночном цистроне. Данную последовательность синтезировали и клонировали в вектор MSGV1 для образования временных ретровирусных супернатантов.
Трансдукция TCR
Доноров PBL доводили до 3×106 клеток/мл в среде 50/50 с добавлением 50 нг/мл растворимого OKT3 и 300 МЕд/мл IL-2, и активировали в планшетах с низкой адгезией в течение двух суток перед ретровирусной трансдукцией. Плазмиду pMSGN/1, кодирующую TCR, специфичный в отношении мутации (1,5 мкг/лунка), и плазмиду RD114, кодирующую оболочку (0,75 мкг/лунка), совместно трансфицировали в 106 HEK293GP клеток/лунка 6-луночного планшета, покрытого поли-D-лизином, с использованием реагента для трансфекции LIPOFECTAMINE 2000 (Life Technologies). Ретровирусные супернатанты собирали через двое суток после трансфекции, разводили в соотношении 1:1 средой DMEM (от англ. Dulbecco modified Eagle's medium - среда Иглу, модифицированная по Дульбекко) и центрифугировали в 6-луночном необработанном планшете для культур тканей, покрытом реагентом RETRONECTIN (10 мкг/лунка, Takara, Rockville, MD) при 2000×g в течение 2 часов при 32°С. Супернатанты отсасывали, и 2×106 стимулированных Т-клеток в количестве 5×105 клеток/мл добавляли в каждую лунку в среде 50/50 с использованием 300 МЕд/мл IL-2. Т-клетки центрифугировали в планшетах, покрытых реагентом RETRONECTIN, в течение 10 мин при 300×g. Среду заменяли, спустя 3-4 суток, 300 МЕд/мл IL-2, и трансдуцированные клетки анализировали через 10-14 суток после трансдукции.
ПРИМЕР 1
Данный пример демонстрирует IVS Т-клеток периферической крови после контакта с антигеном с мутациями ТР53.
Т-клетки после контакта с антигеном из PBL оценивали у 7 пациентов с раком толстой кишки, 1 пациента с раком прямой кишки и 1 пациента с раком яичника с опухолью с мутацией ТР53 (Таблица 2). У пациентов 4217 (p53R175H), 4213 (p53R248Q), 4257 (p53R248W) и 4254 (p53R273H) не было TIL-ответов на неоантигены р53. Напротив, TIL были реактивными в отношении мутации аутологичного ТР53 у пациентов 4141 (p53R175H), 4285 (p53R175H), 4149 (p53Y220C), 4266 (p53R248W) и 4273 (p53R248W) (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019); Deniger et al., Clin. Cancer Res., 24 (22): 5562-73 (2018)). Криоконсервированные продукты афереза (до какого-либо действия) использовали для сортировки CD4+ или CD8+ Т-клеток после контакта с антигеном из PBL (Фиг. 1А, слева). Отсортированные CD4+ или CD8+ Т-клетки стимулировали in vitro DC, экспрессирующими мРНК TP53-TMG с мутацией (TP53-TMG-IVS), или в них посредством импульса вводили мутантный p53-LP, специфичный в отношении пациента (p53-LP-IVS). После 12 суток культивирования в присутствии IL-21 и IL-2, in vitro стимулированные CD4+ и CD8+ клетки памяти совместно культивировали с DC, которых подвергали электропорации с использованием мРНК TP53-TMG с мутацией, в случае TP53-TMG-IVS, или совместно культивировали с мутантным p53-LP, специфичным в отношении пациента, в случае p53-LP-IVS, и осуществляли сортировку на следующий день на основе экспрессии маркеров активации Т-клеток 4-1ВВ и/или ОХ40 (Фиг. 1А, посередине). Биомасса клеток после TP53-TMG-IVS и p53-LP-IVS была сопоставима как в случае CD4+, так и CD8+ Т-клеток, составляя от 0,9×107 до 18,3×107 клеток, с 0,3×107 до 15,6×107 исходных Т-клеток (Таблица 3). Часть CD4+4-1ВВ+/ОХ40+ и CD8+4-1ВВ+/ОХ40+Т-клеток сортировали из всех популяций для завершенности и симметрии эксперимента, которая составляла от 2×102 до 1,7×105 клеток и 0,1% -6,9% от исходных CD4 или CD8 ворот (Таблица 3). Отсортированные Т-клетки подвергались REP и их анализировали, спустя 14 суток быстрого размножения. Конечные массы клеток находились в интервале от 7×106 до 4,2×108 Т-клеток, на что вероятно влияло исходное количество клеток в REP (Таблица 3).

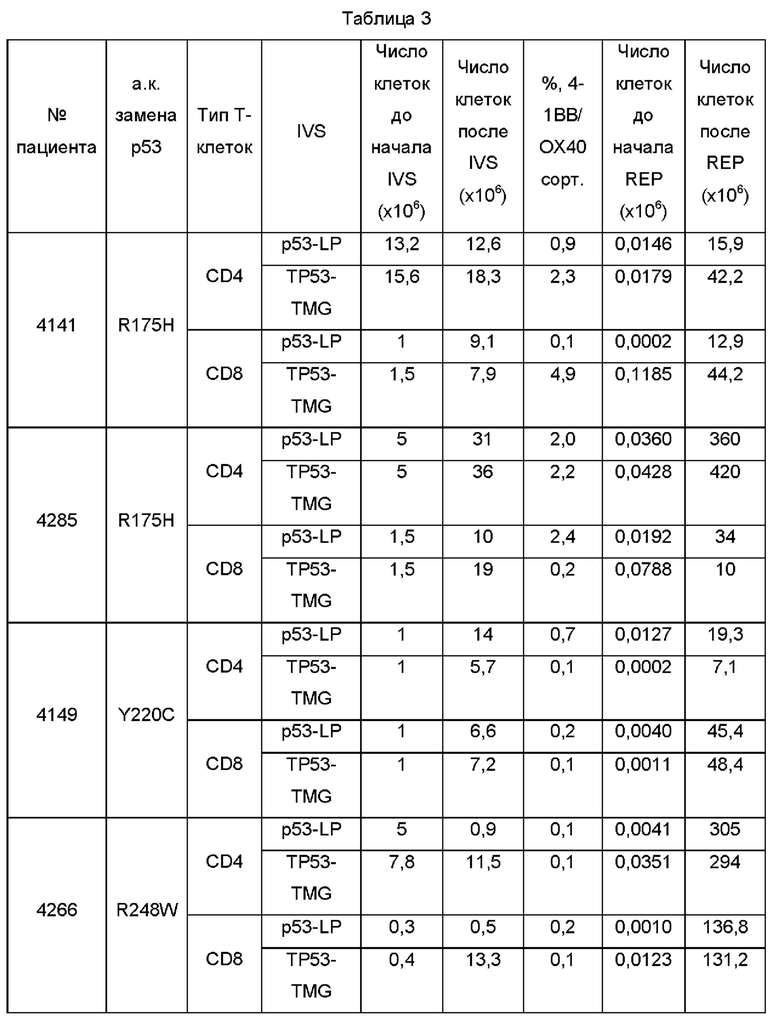

Таблица 3. Биомассы Т-клеток после IVS, обогащения 4-1ВВ/ОХ40 и быстрого размножения у пациентов с культурой, реактивной в отношении неоантигена р53. Число клеток до начала IVS зависело от частоты встречаемости Т-клеток после контакта с антигеном CD4 и CD8 в PBL. Процентное содержание отсортированных 4-1ВВ/ОХ40 Т-клеток зависело от контрольной сортировки для исключения как можно большего числа неспецифичных Т-клеток, и, вероятно, занижен процент реактивных Т-клеток в популяции. Все обогащенные клетки помещались в REP.
ПРИМЕР 2
Данный пример демонстрирует, что Т-клетки, реактивные в отношении мутации ТР53, присутствовали в PBL пациентов с внутриопухолевыми TIL ответами на неоантигены р53.
Аналитический скрининг выполняли на культурах Примера 1 после IVS, обогащения 4-1ВВ/ОХ40 и REP, где реакционные способности оценивали по повышающей регуляции маркера клеточной поверхности 4-1ВВ посредством цитометрии и секреции IFNγ с использованием анализа ELISPOT (Фиг. 1А, справа). Т-клетки периферической крови не были реактивными в отношении неоантигенов р53 у пациентов 4213, 4217, 4254 и 4257, которые подтверждали результаты скрининга TIL (Таблица 2). Данные пациенты, возможно, не имели иммуногенной комбинации HLA и неоэпитопа р53. Напротив, Т-клетки, специфичные в отношении мутации ТР53, идентифицировали в Т-клетках после контакта с антигеном из PBL 5 пациентов (4141 и 4285: p53R175H, 4149: p53Y220C, 4266 и 4273: p53R248W), у которых были внутриопухолевые Т-клеточные ответы на мутантный ТР53 за свет TIL (Фиг. 1В-1С и Таблица 2) (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)). TP53-TMG-IVS приводила к получению Т-клеток, специфичных к неоантигену р53, в 4141-CD8, 4285-CD4, 4149-CD4 и 4266-CD8 культурах (Фиг. 1В), и p53-LP-IVS приводила к получению Т-клеток, специфичных в отношении неоантигена р53, в 4285-CD4 и 4273-CD4 культурах (Фиг. 1С). Специфичность ответов на мутантный ТР53 (Фиг. 1В-1С, закрашенные фигуры) характеризовалась отсутствием ответа на аналог WT (Фиг. 1В-1С, незакрашенные фигуры). Самая высокая частота встречаемости клеток, реактивных в отношении мутации ТР53, составляла 78% в 4141-CD8 ТР53-TMG-IVS культуре против p53R175H (Фиг. 1D). 4285-CD4 TP53-TMG-IVS культура иллюстрировала положительный результат скрининга секреции IFNγ, поскольку Т-клетки были реактивными в отношении мутантных TMG-MUT-ТР53 и p53R175H LP, но не против WT TMG-MUT-ТР53, нерелевантного TMG, ДМСО (носитель пептида) или WT p53R175 LP (Фиг. 1Е). p53R175H LP имел аминокислотную последовательность YKQSQHMTEVVRHCPHHERCSDSDG (SEQ ID NO: 111). WT p53R175 LP имел аминокислотную последовательность YKQSQHMTEVVRRCPHHERCSDSDG (SEQ ID NO: 110). Отобранные культуры считались реактивными, исходя из повышающей регуляции 4-1ВВ и/или секреции IFNγ, и далее исследовались (Таблицы 4А-4В). Культура 4285-CD4 TP53-TMG-IVS демонстрировала специфичное когнатное распознавание p53R175H LP с концентрациями пептидов вплоть до 10 нг/мл (Фиг. 1F). Таким образом, посредством IVS и обогащения 4-1ВВ/ОХ40 высоко специфичные CD8+ и CD4+ Т-клетки, нацеленные на общедоступные мутации ТР53, могли быть идентифицированы.



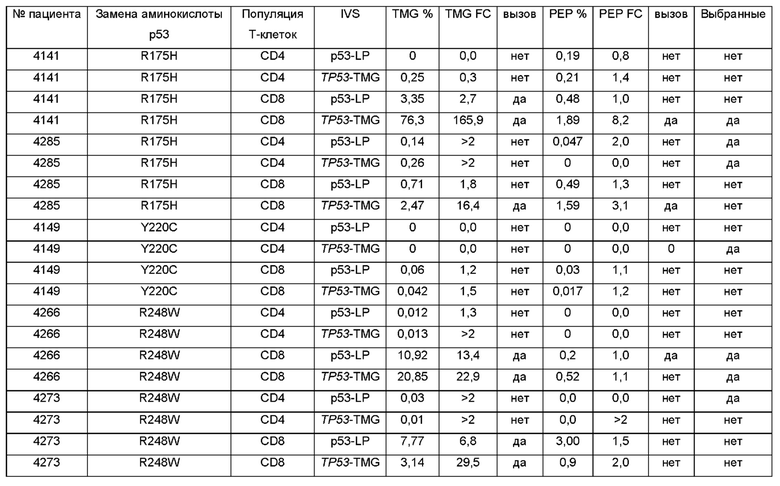
ПРИМЕР З
Данный пример демонстрирует, что отслеживание TCRB демонстрировало обогащение Т-клеток, реактивных в отношении неоантигена р53, из PBL.
Было желательным дополнительно охарактеризовать разнообразие TCR в случае популяции Т-клеток, реактивных в отношении мутации ТР53, каждого пациента, и определить, изменяли ли IVS и обогащение 4-1ВВ/ОХ40 репертуар Т-клеток. Для осуществления этого, проводили глубокое секвенирование TCRB (Pasetto et al., Cancer Immunol. Res., 4 (9): 734-43 (2016)), и частоты встречаемости клонотипа продуктивных Т-клеток измеряли на основе уникальных последовательностей CDR3B и суммарной клональности образцов, что представляет собой нормированное измерение разнообразия популяции, где больше олигокпональных образцов достигают 1 (Boyd et al., Sci. Transl. Med., 1 (12): 12ra23) (2009); Howie et al., Sci. Transl. Med., 7 (301): 301ra131 (2015)). Клональность TCRB значимо увеличивалась в культурах TP53-TMG-IVS и p53-LP-IVS, образованных из образцов PBL всех пациентов, относительно PBL до IVS (Фиг. 2А). Аналогично, наиболее часто встречающийся уникальный клонотип TCRB в каждом образце TP53-TMG-IVS и p53-LP-IVS имел более высокую частоту, чем в pre-IVS PBL (Фиг. 2В). Ранжирование последовательностей TCRB, реактивных в отношении неоантигена р53, находилось в интервале от 1 до 167 в конечных культурах p53-LP-IVS или TP53-TMG-IVS, но не выявлялись или ранг 5020 в исходных PBL (Таблица 5). Увеличенная клональность или максимальные частоты встречаемости клонотипа TCRB не ограничивались культурами с Т-клеточными ответами на неоантигены р53 (Фиг. 2А-2В; звездочки обозначали позитивные культуры). Это указывало на то, что имел место репертуар Т-клеток, искаженный в результате IVS и обогащения 4-1ВВ/ОХ40, но оценки максимальной частоты и клональности не были достаточными для предсказания ответа культуры на мутантный ТР53.
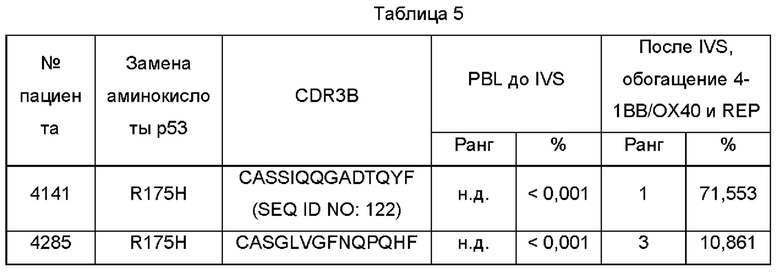
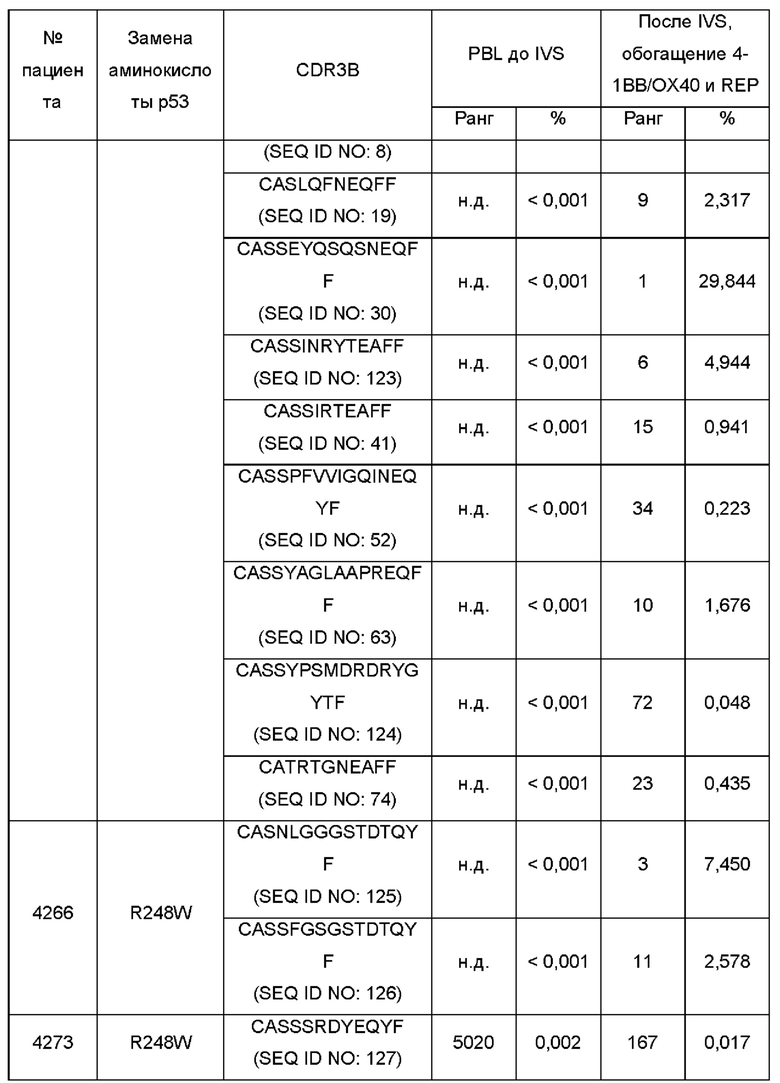
Таблица 5. Отслеживание TCRB клеток, реактивных в отношении неоантигена р53, до и после IVS, совместного культивирования, сортировки 4-1ВВ/ОХ40 и REP. Секвенирование при исследовании TCRB Adadptive Biotechnologies проводили с по меньшей мере 50000 клетками.
ПРИМЕР 4
Данный пример демонстрирует выделение TCR, реактивных в отношении неоантигена р53, и отслеживание посредством секвенирования TCRB.
Затем TCR идентифицировали из IVS популяций, реактивных в отношении неоантигена р53, для возможного терапевтического и исследовательского применения и для отслеживания клонотипов TCRB на протяжении периода культивирования для оценки степени обогащения Т-клеток, реактивных в отношении мутации ТР53. TCR идентифицировали после совместной культивации реактивных культур IVS с конгатным неоантигеном р53 (TMG или LP), сортировки 4-1ВВ+ Т-клеток и ОТ-ПЦР на одиночной клетке генов альфа и бета TCR, аналогично предыдущим исследованиям (Pasetto et al., Cancer Immunol. Res., 4 (9): 734-43 (2016)). Пары TCR реконструировали, клонировали в ретровирусные векторы и трансдуцировали в донорные PBL. Второй аминокислотный остаток заменяли на аланин (А) для того, чтобы иметь более сильную последовательность Козака для высоко эффективной трансляции. Константные области цепи α TCR заменяли цистеин-замещенной, LVL-модифицированной мышиной константной областью цепи α. Константные области цепи β TCR заменяли цистеин-замещенной мышиной константной областью цепи β.
В общей сложности идентифицировали 11 TCR, нацеленных на неоантиген p53R175H (пациенты 4141 и 4285) и p53R248W (пациенты 4266 и 4273) (Таблица 5). TCR для пациента 4149 не мог быть определен из-за ограниченной доступности Т-клеток. TCR, реактивные в отношении того же неоантигена р53, из TIL (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)) идентифицировали в PBL после IVS и обогащения 4-1BB/OX40 у пациентов 4141, 4266 и 4273, нацеленные на p53R175H/HLA-A*02:01, p53R248W/HLA-A*68:01 и p53R248W/HLA-DPB1*02:01, соответственно. Никаких дополнительных Т-клеток, реактивных в отношении мутации ТР53, не идентифицировали у данных пациентов. Напротив, 7 уникальных TCR, специфичных в отношении неоантигена p53R175H, от пациента 4285 идентифицировали из PBL, которые отсутствовали в исследовании TIL, и TCR, происходящий из TIL, не был обнаружен в популяциях PBL. Функциональные авидности TCR, происходящих из PBL (4285-PBL-TCR), были сопоставимы с TCR, происходящими из TIL (4285-TIL-TCR), с распознаванием p53R175H LP до 10 нг/мл и отсутствием ответа на p53R175 LP WT (Фиг. 2C-2J). Отслеживание клонотипов TCRB, специфичных в отношении неоантигена p53R175H, от пациентов 4141 и 4285 продемонстрировало экспоненциальное размножение после IVS и обогащения 4-1ВВ/ОХ40, по сравнению с исходными PBL (Фиг. 2K). Кроме того, последовательности CDR3B от пациента 4285 были ниже предела обнаружения (меньше 0,001% от 2×105 считываний) в объеме PBL, но имели достаточные частоты встречаемости после IVS и обогащения 4-1ВВ/ОХ40, включая четыре TCR в первых 10 из общего количества кпонотипов CDR3B (Таблица 5). TCR, специфичные в отношении неоантигена p53R248W, от пациента 4266 также были ниже порога обнаружения в PBL, но составляли 2,6% (4266-PBL-TCR3) и 7,5% (4266-PBL-TCR2) в культуре 4266-CD8 TP53-TMG-IVS (Фиг. 2L). TCR со специфичностью в отношении неоантигена p53R248W обогащались с 0,002% по 0,017% в культуре 4273-CD4 p53-LP-IVS (Фиг. 2L). Обобщенно, данные демонстрировали, что PBL могут являться источником общедоступных TCR, реактивных в отношении мутации ТР53, идентичных или сравнимых с внутриопухолевыми TCR.
ПРИМЕР 5
Данный пример демонстрировал, что обычные рестрикционные элементы HLA и неоэпитопы р53 являлись иммуногенными.
Затем оценивали распознанные минимальные неоэпитопы р53 и соответствующие рестрикции HLA. Картирование HLA выполняли посредством трансфекции ДНК-плазмид, соответствующих каждой из отдельных аллелей HLA пациента, в линию клеток обезьяны COS7 (не имеющую HLA) и введения под действием импульса пептидов или совместной трансфекции с TMG, аналогично предыдущим отчетам (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019); Deniger et al., Clin. Cancer Res., 24 (22): 5562-73 (2018)). Культура 4141-CD8 TP53-TMG-IVS являлась специфичной в отношении неоэпитопа p53R175H HMTEVVRHC (SEQ ID NO: 96) в контексте HLA-A*02:01, высокочастотного HLA в популяции США (Gonzales et al., Hisp. Health Care Int., 15 (4): 180-8 (2017)), как измерено по экспрессии 4-1ВВ (Фиг. 3А). HLA-A*68:01 ограничивал неоэпитоп p53R248W SSCMGGMNWR (SEQ ID NO: 98), распознаваемый культурой CD8 TP53-TMG-IVS, как измерено по секреции IFNγ (Фиг. 3В). Это было ожидаемо, поскольку TCR из TIL у пациентов 4141 и 4266 были обнаружены в данных культурах IVS и уже установили минимальные неоэпитопы и элементы рестрикции HLA (Malekzadeh et al., J. Clin. Invest. 129 (3): 1109-14 (2019)). Аналогично, 4273-PBL-TCR был обнаружен в культуре 4273-CD4 p53-LP-IVS и имел известную комбинацию p53R248W и HLA-DPB1*02:01 из исследований TIL. Даже несмотря на то, что существовало различие в TCR между PBL и TIL в случае пациента 4285, культура 4285-CD4 TP53-TMG-IVS была специфичной в отношении той же комбинации p53R175H и HLA-DBR1*13:01, обнаруженной в TIL (Фиг. 3С). Кроме того, все 4285-PBL-TCR были специфичными в отношении p53R175H и HLA-DBR1*13:01 и все присутствовали в культуре 4285-CD4 TP53-TMG-IVS на основе секвенирования TCRB (Таблица 5; Фиг. 4). Пептиды из пятнадцати аминокислот p53R175H с перекрыванием 14 аминокислот вводили под действием импульса в DC от пациента 4285 и совместно культивировали с TCR-трансдуцированными Т-клетками, и определяли, что коровый пептид EVVRHCPHHER (SEQ ID NO: 2) являлся общей последовательностью, распознаваемой 4285-PBL-TCR в контексте HLA-DRB1*13:01 (Таблица 6). В итоге, те же TCR из TIL в PBL, которые распознавали тот же HLA и минимальные неоэпитопы р53, обнаруживали в трех случаях, и в одном случае обнаруживали дополнительные TCR с такой же специфичностью в отношении неоантигена р53, как и в случае внутриопухолевых Т-клеток.
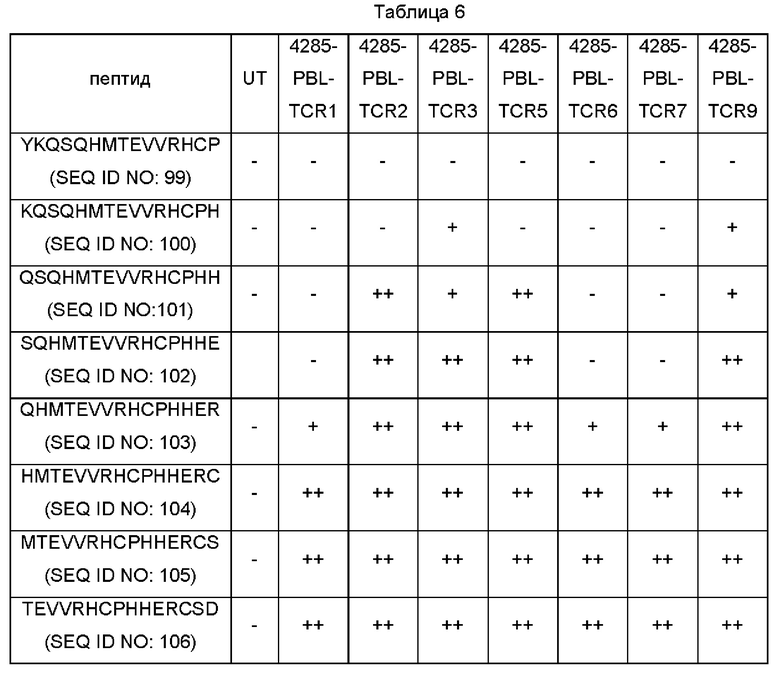
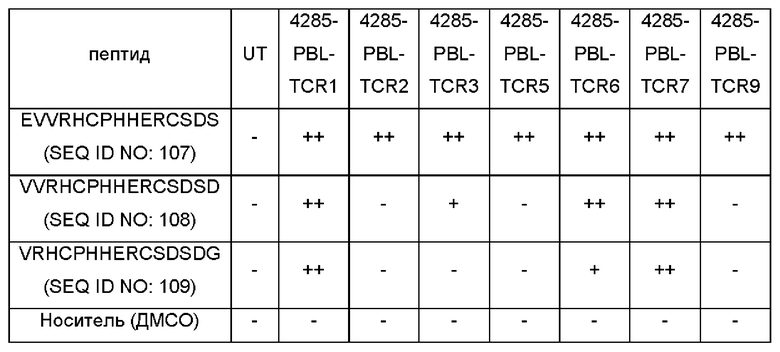
ПРИМЕР 6
В данном примере продемонстрировано, что опухолевые клетки обрабатывают и презентируют неоэпитопы р53 на HLA, которые распознаются Т-клетками, происходящими из PBL, после IVS.
Т-клетки, реактивные в отношении мутации ТР53, оценивали в отношении способности распознавать естественным образом обрабатываемый и презентируемый антиген, экспрессируемый на поверхности опухолевой клетки. Линию опухолевых клеток остеосаркомы Saos2-R175H (HLA-А*02:01 и сверхэкспрессирующих полноразмерный p53R175H) и линию опухолевых клеток ксенотрансплантата человека ТС#4266 (p53R248W и HLA-А*68:01:02 рак толстой кишки) использовали в качестве моделей. После ночного совместного культивирования CD8+ Т-клетки из культур 4141-CD8 TP53-TMG-IVS и 4266-CD8 TP53-TMG-IVS осуществляли повышающую регуляцию 4-1ВВ в ответ на клеточные линии Saos2-R175H и ТС#4266, соответственно, с минимальной активацией перекрестно совместимой клеточной линии (Фиг. 3D). Таким образом, Т-клетки, специфичные в отношении мутации ТР53, из PBL могли распознавать опухолевые клетки с естественным образом обработанными и презентируемыми неоэпитопами р53.
ПРИМЕР 7
В данном примере продемонстрированы аминокислотные последовательности TCR, сконструированные в Примере 4 и названные в заголовке Таблицы 6. Аминокислотные последовательности вариабельных областей цепей альфа и бета TCR данных TCR показаны в Таблице 7. CDR подчеркнуты.











Название TCR: 4285-PBL-TCR1

Последовательность TCR 4285-PBL-TCR1, которую выделяли у Пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 6), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 7), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 8), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 3), пятая подчеркнутая область представляет собой CDR2aльфa (SEQ ID NO: 4) и шестая подчеркнутая область представляет собой CDR3aльфa (SEQ ID NO: 5). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 10) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 9) включает последовательность, начинающуюся непосредственно после линкера и кончающуюся непосредственно перед началом константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 12) включает последовательность, начинающуюся от N-конца и кончающуюся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 11) включает последовательность, начинающуюся непосредственно после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR1, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 180. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 178. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 179.
Еще один вариант 4285-PBL-TCR1 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 205. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 206.
Предсказанные зрелые последовательности вариабельных областей альфа и бета цепей 4285-PBL-TCR1 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого сигнального пептида показана в SEQ ID NO: 142. Предсказанная полноразмерная цепь альфа (включая вариабельные и константные области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 160. Предсказанная вариабельная область цепи бета без N-концевого сигнального пептида показана в SEQ ID NO: 143. Предсказанная полноразмерная цепь бета (включая вариабельную и константную области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 161.
Название TCR: 4285-PBL-TCR2


Последовательность TCR 4285-PBL-TCR2, которую выделяли у Пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 17), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 18), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 19), четвертая подчеркнутая область представляет сбой CDR1альфа (SEQ ID NO: 14), пятая подчеркнутая область представляет собой CDR2альфа (SEQ ID NO: 15) и шестая подчеркнутая область представляет собой CDR3альфа (SEQ ID NO: 16). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 21) включает последовательность, начинающуюся от N-конца и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 20) включает последовательность, начинающуюся непосредственно после линкера и заканчивающуюся непосредственно до начала константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 23) включает последовательность, начинающуюся от N-конца и заканчивающуюся непосредственно до начала линкера. Полноразмерная цепь альфа (SEQ ID NO: 22) включает последовательность, начинающуюся непосредственно после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR2, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 183. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 181. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 182.
Еще один вариант 4285-PBL-TCR2 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 207. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 208.
Предсказанные зрелые последовательности вариабельных областей цепи альфа и бета 4285-PBL-TCR2 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого сигнального пептида показана в SEQ ID NO: 144. Предсказанная полноразмерная цепь альфа (включая вариабельные и константные области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 162. Предсказанная вариабельная область цепи бета без N-концевых сигнальных пептидов показана в SEQ ID NO: 145. Предсказанная полноразмерная цепь бета (включая вариабельную и константную области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 163.
Название TCR: 4285-PBL-TCR3

Последовательность TCR 4285-PBL-TCR3, которую выделяли у пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 28), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 29), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 30), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 25), пятая подчеркнутая область представляет собой CDR2aльфa (SEQ ID NO: 26) и шестая подчеркнутая область представляет собой CDR3aльфa (SEQ ID NO: 27). Выделенная жирным шрифтом область представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область бета цепи (SEQ ID NO: 93) и вторая выделенная курсивом область представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 32) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 31) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся непосредственно перед началом константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 34) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 33) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR3, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 186. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 184. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 185.
Еще один вариант 4285-PBL-TCR3 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 209. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 210.
Предсказанные зрелые последовательности вариабельной области цепи альфа и бета 4285-PBL-TCR3 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого пептида показана в SEQ ID NO: 146. Предсказанная полноразмерная цепь альфа (включая вариабельную и константную области цепи альфа) без N-коневого сигнального пептида показана в SEQ ID NO: 164. Предсказанная вариабельная область цепи бета без N-концевого сигнального пептида показана в SEQ ID NO: 147. Предсказанная полноразмерная цепь бета (включая вариабельные и константные области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 165.
Название TCR: 4285-PBL-TCR5

Последовательность TCR 4285-PBL-TCR5, которую выделяли у Пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 39), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 40), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 41), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 36), пятая подчеркнутая область представляет собой CDR2aльфa (SEQ ID NO: 37) и шестая подчеркнутая область представляет собой CDR3aльфa (SEQ ID NO: 38). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 43) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно до начала константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 42) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся непосредственно перед началом константной области цепи альфа. Полно размерная цепь бета (SEQ ID NO: 45) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 44) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR5, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 189. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 187. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 188.
Еще один вариант 4285-PBL-TCR5 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 211. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 212.
Предсказанные зрелые последовательности вариабельной области цепи альфа и бета 4285-PBL-TCR5 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого сигнального пептида показана в SEQ ID NO: 148. Предсказанная полноразмерная цепь альфа (включая вариабельную и константную области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 166. Предсказанная вариабельная область цепи бета без N-концевого сигнального пептида показана в SEQ ID NO: 149. Предсказанная полноразмерная цепь бета (включая вариабельную и константную области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 167.
Название TCR: 4285-PBL-TCR6

Последовательность TCR 4285-PBL-TCR6, которая была выделена у Пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 50), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 51), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 52), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 47), пятая подчеркнутая область представляет собой CDR2альфа (SEQ ID NO: 48) и шестая подчеркнутая область представляет собой CDR3aльфa (SEQ ID NO: 49). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 54) включает последовательность, начинающуюся от N-конца и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи бета (SEQ ID NO: 53) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся непосредственно перед началом константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 56) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 55) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR6, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 192. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 190. Полноразмерная цепь варианта изложена в SEQ ID NO: 191.
Еще один вариант 4285-PBL-TCR6 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 213. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 214.
Предсказанные зрелые последовательности вариабельной области цепи альфа и бета 4285-PBL-TCR6 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого сигнального пептида показана в SEQ ID NO: 150. Предсказанная полноразмерная цепь альфа (включая вариабельные и константные области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 168. Предсказанная вариабельная область цепи бета без N-концевого сигнального пептида показана в SEQ ID NO: 151. Предсказанная полноразмерная цепь бета (включая вариабельные и константные области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 169.
Название TCR: 4285-PBL-TCR7

Последовательность TCR 4285-PBL-TCR7, которую выделяли у Пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 61), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 62), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 63), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 58), пятая подчеркнутая область представляет собой CDR2aльфa (SEQ ID NO: 59) и шестая подчеркнутая область представляет собой CDR3aльфa (SEQ ID NO: 60). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 65) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 64) включает последовательность, начинающуюся сразу после линкера и кончающуюся непосредственно перед началом константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 67) включает последовательность, начинающуюся с N-конца и кончающуюся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 66) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR7, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 195. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 193. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 194.
Еще один вариант 4285-PBL-TCR7 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 215. Полноразмерная цепь бета изложена в SEQ ID NO: 216.
Предсказанные зрелые последовательности вариабельных областей цепи альфа и бета 4285-PBL-TCR7 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого сигнального пептида показана в SEQ ID NO: 152. Предсказанная полноразмерная цепь альфа (включая вариабельную и константную области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 170. Предсказанная вариабельная область цепи бета без N-концевого сигнального пептида показана в SEQ ID NO: 153. Предсказанная полноразмерная цепь бета (включая вариабельную и константную области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 171.
Название TCR: 4285-PBL-TCR9


Последовательность TCR 4285-PBL-TCR9, которую выделяли у Пациента 4285, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 72), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 73), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 74), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 69), пятая подчеркнутая область представляет собой CDR2aльфa (SEQ ID NO: 70) и шестая подчеркнутая область представляет собой CDR3aльфa (SEQ ID NO: 71). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 76) включает последовательность, начинающуюся с N-конца, и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 75) включает последовательность, начинающуюся срезу после линкера и заканчивающуюся непосредственно до начала константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 78) включает последовательность, начинающуюся с N-конца и заканчивающаяся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 77) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся С-концом.
Вариант 4285-PBL-TCR9, содержащий сигнальный пептид цепи альфа дикого типа, изложен в SEQ ID NO: 198. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 196. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 197.
Еще один вариант 4285-PBL-TCR9 содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 217. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 218.
Предсказанные зрелые последовательности вариабельной области цепи альфа и бета 4285-PBL-TCR9 без N-концевых сигнальных пептидов показаны в Таблице 7. Предсказанная вариабельная область цепи альфа для зрелой последовательности без N-концевого сигнального пептида показана в SEQ ID NO: 154. Предсказанная полноразмерная цепь альфа (включая вариабельную и константную области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 172. Предсказанная вариабельная область цепи бета без N-концевого сигнального пептида показана в SEQ ID NO: 155. Предсказанная полноразмерная цепь бета (включая вариабельную и константную области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 173.
ПРИМЕР 8
Данный пример демонстрирует частоты встречаемости CD8+4-1BB+ Т-клеток, выявляемых после совместного культивирования Т-клеток из образца опухоли от Пациента 4259 с мутантным пептидом p53-Y220C.
Клоны Т-клеток получали посредством предельного разведения после сортировки CD8+ Т-клеток из культуры фрагмента опухоли 4259-F1. 24 Культуры совместно культивировали с опухолевыми клетками Т2 (HLA-А*02:01), в которые посредством импульса вводили ДМСО (носитель пептидов), пептид WT p53-Y220 (VVPYEPPEV) (SEQ ID NO: 112) или пептид MUT p53-Y220C (VVPCEPPEV) (SEQ ID NO: 113). После инкубирования в течение ночи клетки окрашивали на CD3, CD8 и 4-1ВВ, затем анализировали посредством проточной цитометрии. Частоты встречаемости CD8+4-1BB+ Т-клеток из культур показаны на Фиг. 5. Как показано на Фиг. 5, получали клоны реактивных Т-клеток.
ПРИМЕР 9
Данный пример демонстрирует выделение Т-клеточного рецептора, реактивного в отношении неоантигена p53-Y220C, 4259-F1-TCR.
Последовательность TCR со специфичностью в отношении p53-Y220C и HLA-А*02:01 (из культуры фрагмента F1 пациента 4259 Примера 8) было трудно определить. Последовательность нельзя было определить, используя классическую методику ПЦР на одиночной клетке. Два ограничения методики ПЦР на одиночной клетке заключаются в том, что (1) она устанавливает только последовательность короткой части гена TCR, окружающую гипервариабельную область CDR3, что приводит к тому, что исследователь делает заключение об остальной части TCR, используя менее полиморфные области TCR, например, вариабельное семейство, и (2) только одна последовательность может присутствовать для получения считывания функциональной последовательности методом секвенирования Сэнгера. Данные проблемы преодолевали, получая клоны Т-клеток посредством предельного разведения и затем секвенирования полноразмерных генов TCRальфа и TCRбета, как экспрессируется транскриптами мРНК посредством 5'RACE. Затем определяли, что клонотип Т-клеток со специфичностью в отношении p53-Y220C и HLA-А*02:01 экспрессировал две цепи TCRальфа и две цепи TCRбета. Это противоречит большей части Т-клеток, которые только экспрессируют одну цепь TCRальфа и одну цепь TCRбета. Только одна из цепей TCRбета была функциональной, поскольку другая имела сдвиг рамки, который приводил к преждевременному стоп-кодону. Кроме того, данная цепь TCRбета принадлежала к семейству TRBV7-9*03, а не к семейству TRBV7-9*01, о чем было сообщено посредством ПЦР на одиночной клетке и секвенирования для исследования TCRB семейства TRBV7-9 (низкое разрешение) Adaptive Biotechnologies. Существует неконсервативная замена аминокислоты между двумя вариабельными цепями (N или D в положении 26), что указывает на то, что выбор TRBV7-9*03 был полезным (см. Фиг. 9). Было две идентифицированные функциональные цепи TCRaльфa, и только одна из них образовывала пару правильным образом с функциональной TCRбета, придавая специфичность в отношении p53-Y220C и HLA-А*02:01.
Пары TCR реконструировали и клонировали в ретровирусные векторы. Второй аминокислотный остаток заменяли на аланин (А) для получения более сильной последовательности Козака для высоко эффективной трансляции. Константные области цепи α TCR заменяли цистеин-замещенной, LVL-модифицированной мышиной константной областью цепи α. Константные области цепи β TCR заменяли цистеин-замещенной мышиной константной областью цепи β.
Название TCR: 4259-F1-TCR

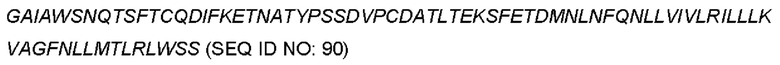
Последовательность TCR, реактивного в отношении неоантигена p53-Y220C, 4259-F1-TCR, который выделяли у Пациента 4259, изложена непосредственно выше. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 83), вторая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 84), третья подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 85), четвертая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 80), пятая подчеркнутая область представляет собой CDR2альфа (SEQ ID NO: 81) и шестая подчеркнутая область представляет собой CDR3альфа (SEQ ID NO: 82). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая область, выделенная курсивом, представляет собой константную область цепи бета (SEQ ID NO: 93) и вторая область, выделенная курсивом, представляет собой константную область цепи альфа (SEQ ID NO: 91). Вариабельная область цепи бета (SEQ ID NO: 87) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом константной области цепи бета. Вариабельная область цепи альфа (SEQ ID NO: 86) включает последовательность, начинающуюся непосредственно после линкера и заканчивающуюся непосредственно перед началом константной области цепи альфа. Полноразмерная цепь бета (SEQ ID NO: 89) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом линкера. Полноразмерная цепь альфа (SEQ ID NO: 88) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся С-концом.
Вариант 4259-F1-TCR, содержащий цепь альфа с сигнальным пептидом дикого типа, изложен в SEQ ID NO: 201. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 199. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 200.
Еще один вариант 4259-F1-TCR содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 219. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 220.
Аминокислотные последовательности вариабельных областей цепей альфа и бета 4259-F1-TCR показаны в Таблице 8. CDR подчеркнуты. Предсказанная полноразмерная цепь альфа (включая вариабельные и константные области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 174. Предсказанная полноразмерная цепь бета (включая вариабельные и константные области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 175.


ПРИМЕР 10
Данный пример демонстрирует, что 4259-F1-TCR Примера 9 специфично распознает мутантный пептид p53-Y220C и не соответствующий пептид WT.
4259-F1-TCR Примера 9 трансдуцировали в Т-клетки периферической крови донора, затем совместно культивировали с опухолевыми клетками Т2 (HLA-А*02:01), в которые под действием импульса вводили уменьшающиеся концентрации или пептида WT p53-Y220 (VVPYEPPEV) (SEQ ID NO: 112) или пептида MUT p53-Y220C (VVPCEPPEV) (SEQ ID NO: 113). После инкубации в течение ночи, супернатанты сокультуры анализировали посредством ELISA в отношении секреции интерферона-гамма. Результаты показаны на Фиг. 6.
ПРИМЕР 11
Данный пример демонстрирует, что 4259-F1-TCR специфично распознает опухолевые клетки, экспрессирующие p53-Y220C, презентируемый HLA-A*02:01.
Т-клетки, или не экспрессирующие TCR (нетрансдуцированные), или экспрессирующие TCR, специфичный к p53-R175H, или 259-F1-TCR Примера 9, совместно культивировали с опухолевыми клетками, или с или без экспрессии HLA-А*02:01, p53-R175H или p53-Y220C. После инкубации в течение ночи, клетки окрашивали на CD3, CD8 и 4-1ВВ, затем анализировали посредством проточной цитометрии. Частоты встречаемости CD8+4-1BB+ Т-клеток из культур показаны на Фиг. 7.
ПРИМЕР 12
Данный пример демонстрирует выделение и специфичную реактивность TCR от пациента 4141.
Обобщенные результаты лечения пациентов TIL, реактивными в отношении мутации р53, предложены в Таблице 9.
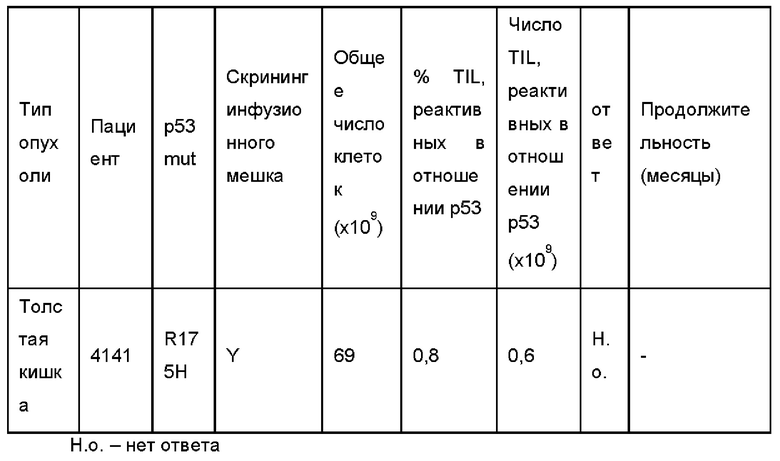
Аутологичные АРС (от англ. antigen-presenting cell - антигенпрезентирующая клетка) трансфицировали TMG, кодирующим нерелевантные мутации, последовательностью р53 WT или последовательностью мутантного р53, включающей R175H. Только среда и РМА и иономицин представляли собой отрицательный и положительный контроли, соответственно. На следующий день, TIL от пациента 4141 (культура фрагмента 12) совместно культивировали в течение ночи при 37°С с TMG-трансфицированными АРС. Секрецию IFN-γ оценивали посредством ELISPOT. Экспрессию 4-1ВВ оценивали посредством проточной цитометрии после сортировки посредством ворот следующим образом: лимфоциты → живые клетки (PI-негативные) → CD3+ (Т-клетки) → CD4-CD8+. Результаты показаны на Фиг. 10.
Клетки Cos7 (2,5×104/лунка) высевали в лунки плоскодонных 96-луночных планшетов. На следующие сутки клетки совместно трансфицировали отдельными аллелями HLA от пациента 4141 и или без дополнительного гена, или WT ТР53 TMG или мутантным ТР53 TMG, содержащим последовательность p53-R175H. TIL со специфичностью в отношении p53-R175H от Пациента 4141 (культура фрагмента 12) совместно культивировали на следующие сутки с трансфицированными клетками Cos7 и инкубировали в течение ночи при 37°С. Секрецию IFN-γ оценивали посредством ELISPOT. Результаты показаны на Фиг. 11.
Т-клетки, экспрессирующие имитацию (отсутствие TCR) или 4141-TCR1a2, совместно культивировали с опухолевыми клетками (экспрессирующими HLA-А*02:01). В клетки Т2 под действием импульса вводили в течение 2 часов при 37°С носитель пептидов (ДМСО) или очищенные (чистота больше 95% посредством ВЭЖХ) пептиды, состоящие из пептида WT p53-R175 HMTEVVRRC (SEQ ID NO: 95) или мутантного пептида p53-R175H HMTEVVRHC (SEQ ID NO: 96). Только среды и PMA и иономицин представляли собой отрицательный и положительный контроли, соответственно. Совместное культивирование проводили в течение ночи при 37°С. Секрецию IFN-γ оценивали посредством ELISA. Результаты показаны на Фиг. 12.
Т-клетки, экспрессирующие 4141-TCR1a2, совместно культивировали в течение ночи при 37°С с клетками Saos2 (p53-NULL и HLA-A*02:01+), которые или представляли собой неманипулированные клетки или клетки, сделанные сверхэкспрессирующими полноразмерный белок p53-R175H. Ингибиторы секреции (монензин и брефелдин А) добавляли к сокультурам для захвата цитокинов в Т-клетках. После 6 часов совместного культивирования клетки фиксировали и пермеабилизировали, затем окрашивали на IL-2, CD107a, IFN-γ и фактор некроза опухоли-альфа (TNFα - от англ. tumor necrosis factor-alpha). Проточную цитометрию использовали для анализа сокультур на основе ворот лимфоцитов. Результаты показаны на Фиг. 13.
Последовательность TCR 4141-TCR1a2, которую выделяли у Пациента 4141, изложена ниже. Начиная с N-конца, первая подчеркнутая область представляет собой CDR1альфа (SEQ ID NO: 131), вторая подчеркнутая область представляет собой CDR2aльфa (SEQ ID NO: 132), третья подчеркнутая область представляет собой CDR3альфа (SEQ ID NO: 133), четвертая подчеркнутая область представляет собой CDR1бета (SEQ ID NO: 134), пятая подчеркнутая область представляет собой CDR2бета (SEQ ID NO: 135) и шестая подчеркнутая область представляет собой CDR3бета (SEQ ID NO: 136). Область, выделенная жирным шрифтом, представляет собой линкер (SEQ ID NO: 94). Начиная с N-конца, первая выделенная курсивом область представляет собой константную область цепи альфа (SEQ ID NO: 91) и вторая выделенная курсивом область представляет собой константную область цепи бета (SEQ ID NO: 93). Вариабельная область цепи альфа (SEQ ID NO: 137) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом константной области цепи альфа. Вариабельная область цепи бета (SEQ ID NO: 138) включает последовательность, начинающуюся сразу после линкера и заканчивающуюся непосредственно перед началом константной области цепи бета. Полноразмерная цепь альфа (SEQ ID NO: 139) включает последовательность, начинающуюся с N-конца и заканчивающуюся непосредственно перед началом линкера. Полноразмерная цепь бета (SEQ ID NO: 140) включает последовательность, начинающуюся непосредственно после линкера и заканчивающуюся С-концом.
Т-клетки, реактивные в отношении опухоли, идентифицированы, как описано ниже. TCR выделяли, как описано ниже.
Название TCR: 4141-TCR1a2
Распознавание мутации р53: R175H
Способ скрининга: универсальный скрининг мутации в «горячей точке» р53
Совместное культивирование для идентификации TCR: Сокультура 4141 TIL инфузионного мешка с p53mutTMG и отсортированных CD8+41BB+ Т-клеток
Способ идентификации TCR: ОТ-ПЦР на одиночной клетке, затем набор для клонирования ТА ТОРО (Thermo Fisher Scientific, Waltham, MA) для цепи альфа
Ориентация TCR: альфа-бета
Экспрессионный вектор: транспозон SB

Вариант 4141-TCR1a2, содержащий цепь бета с сигнальным пептидом дикого типа, изложен в SEQ ID NO: 204. Вариант содержит вариабельную область цепи бета (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 202. Полноразмерная цепь бета варианта изложена в SEQ ID NO: 203.
Еще один вариант 4141-TCR1a2, содержащий цепь альфа с сигнальным пептидом дикого типа, изложен в SEQ ID NO: 225. Вариант содержит вариабельную область цепи бета, как изложено в SEQ ID NO: 221. Полноразмерная цепь варианта изложена в SEQ ID NO: 222. Вариант содержит вариабельную область цепи альфа (с сигнальным пептидом дикого типа), как изложено в SEQ ID NO: 223. Полноразмерная цепь альфа варианта изложена в SEQ ID NO: 224.
Аминокислотные последовательности вариабельных областей цепи альфа и бета 4141-TCR1a2 показаны в Таблице 10. CDR подчеркнуты. Предсказанная полноразмерная цепь альфа (включая вариабельную и константную области цепи альфа) без N-концевого сигнального пептида показана в SEQ ID NO: 176. Предсказанная полноразмерная цепь бета (включая вариабельную и константную области цепи бета) без N-концевого сигнального пептида показана в SEQ ID NO: 177.
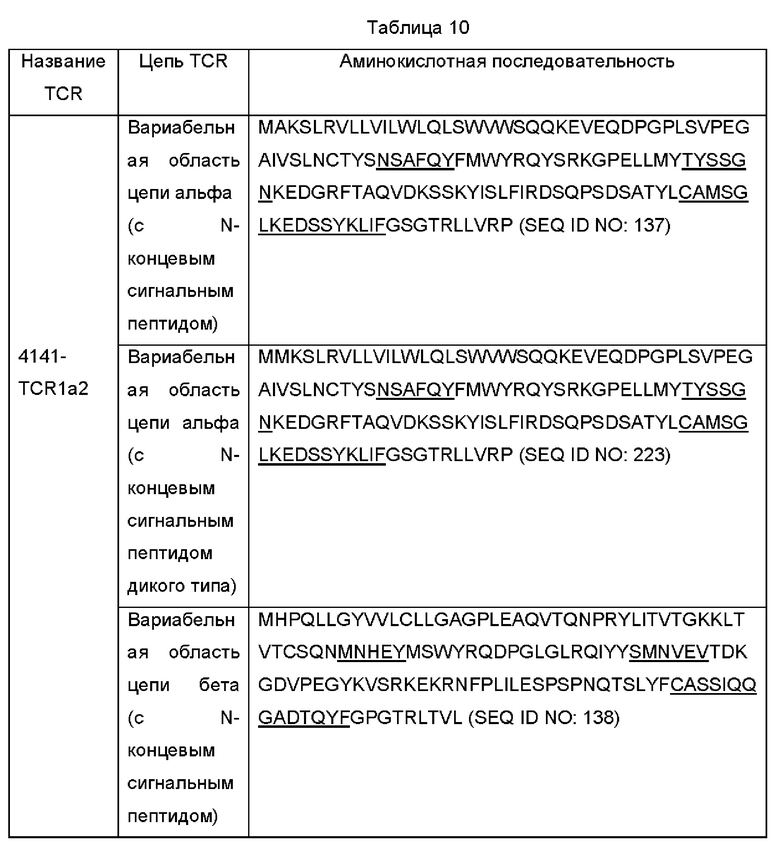

Статистика для 4141-TCR1a2 от пациента 4141 изложена ниже в Таблице 11.
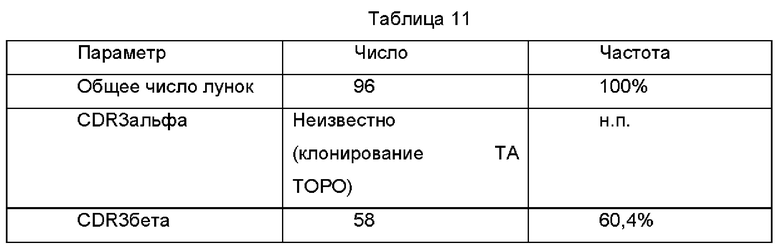
TCR 4141-TCR1a2 выделяли, экспрессировали в Т-клетках и анализировали в сравнении с релевантным антигеном. Краткое изложение результатов показано в Таблице 12.

Все ссылки, включая публикации, патентные заявки и патенты, процитированные в данном документе, включены в данный документ посредством ссылки в равной мере, как если бы каждая ссылка была отдельно и конкретно указана включенной посредством ссылки и была изложена в данном документе во всей своей полноте.
Применение терминов в единственном числе и «по меньшей мере один» и похожих объектов ссылки в контексте описания изобретения (особенно в контексте следующей формулы изобретения) следует истолковывать как охватывающее и термины в единственном числе и термины во множественном числе, если в данном документе не указано иное или оно явно не противоречит контексту. Применение термина «по меньшей мере один» с последующим перечислением одного или более пунктов (например, «по меньшей мере один из А и В») следует истолковывать как означающее один пункт, выбранный из перечисленных пунктов (А или В), или любую комбинацию двух или более из перечисленных пунктов (А или В), если в данном документе не указано иное или оно явно не противоречит контексту. Термины «содержащий», «имеющий», «включающий» и «содержащий» следует истолковывать как открытые термины (то есть, означающие «включающий, но не ограниченный…»), если не указано иное. Раскрытие диапазонов значений в данном документе предназначено только для того, чтобы служить в качестве сокращенного способа ссылки в отдельности на каждое отдельное значение, попадающее в данный диапазон, если в данном документе не указано иное, и каждое отдельное значение включено в описание изобретения, как если бы оно было по отдельности перечислено в данном документе. Все способы, описанные в данном документе, можно осуществлять в любом подходящем порядке, если в данном документе не указано иное или иначе нет явных противоречий контексту. Применение всех возможных примеров или вводных слов перед примером (например, «такой как»), предоставленных в данном документе, предназначено только для лучшего освещения изобретения и не накладывает ограничения на объем изобретения, если не заявлено иное. Язык в описании изобретения не следует истолковывать как указывающий на какой-либо незаявленный элемент в качестве существенного для практического осуществления данного изобретения.
Предпочтительные воплощения данного изобретения описаны в данном документе, включая наилучший способ, известный авторам изобретения, для осуществления изобретения. Изменения данных предпочтительных воплощений могут стать очевидными обычным специалистам в данной области при чтении изложенного выше описания. Авторы изобретения ожидают, что специалисты в данной области будут использовать такие изменения в соответствующих случаях, и авторы изобретения намерены осуществлять на практике данное изобретение иначе, чем конкретно описано в данном документе. Соответственно, данное изобретение включает все модификации и эквиваленты предмета, перечисленные в формуле изобретения, приложенной к данному документу, как разрешено применяемым законом. Кроме того, любая комбинация описанных выше элементов во всех их возможных вариантах охвачена изобретением, если в данном документе не указано иное или она иначе явно не противоречит контексту.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> THE UNITED STATES OF AMERICA, AS REPRESENTED BY THE
SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES
<120> T-КЛЕТОЧНЫЕ РЕЦЕПТОРЫ, РАСПОЗНАЮЩИЕ МУТАЦИЮ R175H ИЛИ Y220C В P53
<130> 749338
<150> US 62/867,619
<151> 2019-06-27
<160> 230
<170> PatentIn version 3.5
<210> 1
<211> 393
<212> ПРТ
<213> Homo sapiens
<400> 1
Met Glu Glu Pro Gln Ser Asp Pro Ser Val Glu Pro Pro Leu Ser Gln
1 5 10 15
Glu Thr Phe Ser Asp Leu Trp Lys Leu Leu Pro Glu Asn Asn Val Leu
20 25 30
Ser Pro Leu Pro Ser Gln Ala Met Asp Asp Leu Met Leu Ser Pro Asp
35 40 45
Asp Ile Glu Gln Trp Phe Thr Glu Asp Pro Gly Pro Asp Glu Ala Pro
50 55 60
Arg Met Pro Glu Ala Ala Pro Pro Val Ala Pro Ala Pro Ala Ala Pro
65 70 75 80
Thr Pro Ala Ala Pro Ala Pro Ala Pro Ser Trp Pro Leu Ser Ser Ser
85 90 95
Val Pro Ser Gln Lys Thr Tyr Gln Gly Ser Tyr Gly Phe Arg Leu Gly
100 105 110
Phe Leu His Ser Gly Thr Ala Lys Ser Val Thr Cys Thr Tyr Ser Pro
115 120 125
Ala Leu Asn Lys Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln
130 135 140
Leu Trp Val Asp Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met
145 150 155 160
Ala Ile Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys
165 170 175
Pro His His Glu Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln
180 185 190
His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp
195 200 205
Arg Asn Thr Phe Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu
210 215 220
Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser
225 230 235 240
Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr
245 250 255
Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val
260 265 270
Arg Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn
275 280 285
Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr
290 295 300
Lys Arg Ala Leu Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys
305 310 315 320
Lys Pro Leu Asp Gly Glu Tyr Phe Thr Leu Gln Ile Arg Gly Arg Glu
325 330 335
Arg Phe Glu Met Phe Arg Glu Leu Asn Glu Ala Leu Glu Leu Lys Asp
340 345 350
Ala Gln Ala Gly Lys Glu Pro Gly Gly Ser Arg Ala His Ser Ser His
355 360 365
Leu Lys Ser Lys Lys Gly Gln Ser Thr Ser Arg His Lys Lys Leu Met
370 375 380
Phe Lys Thr Glu Gly Pro Asp Ser Asp
385 390
<210> 2
<211> 11
<212> ПРТ
<213> Homo sapiens
<400> 2
Glu Val Val Arg His Cys Pro His His Glu Arg
1 5 10
<210> 3
<211> 7
<212> ПРТ
<213> Homo sapiens
<400> 3
Thr Ile Ser Gly Thr Asp Tyr
1 5
<210> 4
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 4
Gly Leu Thr Ser Asn
1 5
<210> 5
<211> 12
<212> ПРТ
<213> Homo sapiens
<400> 5
Cys Ile Leu Arg Asp Asn Asn Ala Arg Leu Met Phe
1 5 10
<210> 6
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 6
Met Asn His Glu Tyr
1 5
<210> 7
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 7
Ser Met Asn Val Glu Val
1 5
<210> 8
<211> 14
<212> ПРТ
<213> Homo sapiens
<400> 8
Cys Ala Ser Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe
1 5 10
<210> 9
<211> 126
<212> ПРТ
<213> Homo sapiens
<400> 9
Met His Leu Val Thr Ser Ile Thr Val Leu Leu Ser Leu Gly Ile Met
1 5 10 15
Gly Asp Ala Lys Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu
20 25 30
Glu Pro Val His Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp
35 40 45
Tyr Ile His Trp Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val
50 55 60
Ile His Gly Leu Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala
65 70 75 80
Ile Ala Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr
85 90 95
Leu Arg Asp Ala Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala
100 105 110
Arg Leu Met Phe Gly Asp Gly Thr Gln Leu Val Val Lys Pro
115 120 125
<210> 10
<211> 132
<212> ПРТ
<213> Homo sapiens
<400> 10
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg
115 120 125
Leu Ser Ile Leu
130
<210> 11
<211> 263
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 11
Met His Leu Val Thr Ser Ile Thr Val Leu Leu Ser Leu Gly Ile Met
1 5 10 15
Gly Asp Ala Lys Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu
20 25 30
Glu Pro Val His Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp
35 40 45
Tyr Ile His Trp Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val
50 55 60
Ile His Gly Leu Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala
65 70 75 80
Ile Ala Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr
85 90 95
Leu Arg Asp Ala Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala
100 105 110
Arg Leu Met Phe Gly Asp Gly Thr Gln Leu Val Val Lys Pro Asn Ile
115 120 125
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
130 135 140
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
145 150 155 160
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
165 170 175
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
180 185 190
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
195 200 205
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
210 215 220
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
225 230 235 240
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
245 250 255
Thr Leu Arg Leu Trp Ser Ser
260
<210> 12
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 12
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg
115 120 125
Leu Ser Ile Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 13
<211> 595
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 13
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg
115 120 125
Leu Ser Ile Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
305 310 315 320
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Leu Val
325 330 335
Thr Ser Ile Thr Val Leu Leu Ser Leu Gly Ile Met Gly Asp Ala Lys
340 345 350
Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu Glu Pro Val His
355 360 365
Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp Tyr Ile His Trp
370 375 380
Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val Ile His Gly Leu
385 390 395 400
Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala Ile Ala Glu Asp
405 410 415
Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr Leu Arg Asp Ala
420 425 430
Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala Arg Leu Met Phe
435 440 445
Gly Asp Gly Thr Gln Leu Val Val Lys Pro Asn Ile Gln Asn Pro Glu
450 455 460
Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu
465 470 475 480
Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met
485 490 495
Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala
500 505 510
Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser
515 520 525
Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser
530 535 540
Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr
545 550 555 560
Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile
565 570 575
Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu
580 585 590
Trp Ser Ser
595
<210> 14
<211> 7
<212> ПРТ
<213> Homo sapiens
<400> 14
Thr Ile Ser Gly Asn Glu Tyr
1 5
<210> 15
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 15
Gly Leu Lys Asn Asn
1 5
<210> 16
<211> 19
<212> ПРТ
<213> Homo sapiens
<400> 16
Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys
1 5 10 15
Leu Thr Phe
<210> 17
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 17
Leu Asn His Asp Ala
1 5
<210> 18
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 18
Ser Gln Ile Val Asn Asp
1 5
<210> 19
<211> 11
<212> ПРТ
<213> Homo sapiens
<400> 19
Cys Ala Ser Leu Gln Phe Asn Glu Gln Phe Phe
1 5 10
<210> 20
<211> 133
<212> ПРТ
<213> Homo sapiens
<400> 20
Met His Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro
130
<210> 21
<211> 131
<212> ПРТ
<213> Homo sapiens
<400> 21
Met Ala Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu
1 5 10 15
Gly Ala Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu
20 25 30
Phe Arg Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu
35 40 45
Asn His Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu
50 55 60
Arg Leu Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp
65 70 75 80
Ile Ala Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro
85 90 95
Leu Thr Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys
100 105 110
Ala Ser Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu
130
<210> 22
<211> 270
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 22
Met His Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 23
<211> 304
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 23
Met Ala Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu
1 5 10 15
Gly Ala Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu
20 25 30
Phe Arg Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu
35 40 45
Asn His Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu
50 55 60
Arg Leu Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp
65 70 75 80
Ile Ala Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro
85 90 95
Leu Thr Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys
100 105 110
Ala Ser Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
130 135 140
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln
180 185 190
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
195 200 205
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
210 215 220
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
225 230 235 240
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
245 250 255
Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala
260 265 270
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
275 280 285
Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 24
<211> 601
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 24
Met Ala Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu
1 5 10 15
Gly Ala Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu
20 25 30
Phe Arg Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu
35 40 45
Asn His Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu
50 55 60
Arg Leu Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp
65 70 75 80
Ile Ala Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro
85 90 95
Leu Thr Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys
100 105 110
Ala Ser Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
130 135 140
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln
180 185 190
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
195 200 205
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
210 215 220
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
225 230 235 240
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
245 250 255
Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala
260 265 270
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
275 280 285
Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
305 310 315 320
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Leu Val Ala
325 330 335
Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr
340 345 350
Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu
355 360 365
Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr
370 375 380
Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys
385 390 395 400
Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg
405 410 415
Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala
420 425 430
Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser
435 440 445
Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro
450 455 460
Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
465 470 475 480
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
485 490 495
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
500 505 510
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
515 520 525
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
530 535 540
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
545 550 555 560
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
565 570 575
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
580 585 590
Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 25
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 25
Val Ser Asn Ala Tyr Asn
1 5
<210> 26
<211> 4
<212> ПРТ
<213> Homo sapiens
<400> 26
Gly Ser Lys Pro
1
<210> 27
<211> 13
<212> ПРТ
<213> Homo sapiens
<400> 27
Cys Ala Val Glu Asp Arg Arg Arg Thr Ala Leu Ile Phe
1 5 10
<210> 28
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 28
Ser Asn His Leu Tyr
1 5
<210> 29
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 29
Phe Tyr Asn Asn Glu Ile
1 5
<210> 30
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 30
Cys Ala Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe
1 5 10 15
<210> 31
<211> 131
<212> ПРТ
<213> Homo sapiens
<400> 31
Met His Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu
1 5 10 15
Asn Ser Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro
20 25 30
Ser Thr Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn
35 40 45
His Ser Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro
50 55 60
Gly Cys Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln
65 70 75 80
Gly Arg Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile
85 90 95
Leu Gln Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Val Glu
100 105 110
Asp Arg Arg Arg Thr Ala Leu Ile Phe Gly Lys Gly Thr Thr Leu Ser
115 120 125
Val Ser Ser
130
<210> 32
<211> 134
<212> ПРТ
<213> Homo sapiens
<400> 32
Met Ala Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu
130
<210> 33
<211> 268
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 33
Met His Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu
1 5 10 15
Asn Ser Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro
20 25 30
Ser Thr Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn
35 40 45
His Ser Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro
50 55 60
Gly Cys Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln
65 70 75 80
Gly Arg Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile
85 90 95
Leu Gln Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Val Glu
100 105 110
Asp Arg Arg Arg Thr Ala Leu Ile Phe Gly Lys Gly Thr Thr Leu Ser
115 120 125
Val Ser Ser Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys
130 135 140
Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp
145 150 155 160
Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr
165 170 175
Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly
180 185 190
Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe
195 200 205
Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala
210 215 220
Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln
225 230 235 240
Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly
245 250 255
Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 34
<211> 307
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 34
Met Ala Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser
305
<210> 35
<211> 602
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 35
Met Ala Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser
305 310 315 320
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met His
325 330 335
Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu Asn Ser
340 345 350
Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro Ser Thr
355 360 365
Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn His Ser
370 375 380
Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro Gly Cys
385 390 395 400
Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln Gly Arg
405 410 415
Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile Leu Gln
420 425 430
Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Val Glu Asp Arg
435 440 445
Arg Arg Thr Ala Leu Ile Phe Gly Lys Gly Thr Thr Leu Ser Val Ser
450 455 460
Ser Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro
465 470 475 480
Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln
485 490 495
Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys
500 505 510
Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile
515 520 525
Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu
530 535 540
Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu
545 550 555 560
Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu
565 570 575
Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn
580 585 590
Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 36
<211> 7
<212> ПРТ
<213> Homo sapiens
<400> 36
Thr Ile Ser Gly Asn Glu Tyr
1 5
<210> 37
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 37
Gly Leu Lys Asn Asn
1 5
<210> 38
<211> 19
<212> ПРТ
<213> Homo sapiens
<400> 38
Cys Ile Val Arg Gly Ser Pro Gly Ala Gly Gly Thr Ser Tyr Gly Lys
1 5 10 15
Leu Thr Phe
<210> 39
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 39
Leu Asn His Asp Ala
1 5
<210> 40
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 40
Ser Gln Ile Val Asn Asp
1 5
<210> 41
<211> 11
<212> ПРТ
<213> Homo sapiens
<400> 41
Cys Ala Ser Ser Ile Arg Thr Glu Ala Phe Phe
1 5 10
<210> 42
<211> 133
<212> ПРТ
<213> Homo sapiens
<400> 42
Met His Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Gly Ser Pro Gly
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro
130
<210> 43
<211> 129
<212> ПРТ
<213> Homo sapiens
<400> 43
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Ile Arg Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val
<210> 44
<211> 270
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 44
Met His Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Gly Ser Pro Gly
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 45
<211> 302
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 45
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Ile Arg Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 46
<211> 599
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 46
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Ile Arg Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser Arg Ala
290 295 300
Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
305 310 315 320
Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Leu Val Ala Arg Val
325 330 335
Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr Thr Gln
340 345 350
Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu Pro Cys
355 360 365
Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr Arg Gln
370 375 380
Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys Asn Asn
385 390 395 400
Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg Lys Ser
405 410 415
Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala Val Tyr
420 425 430
Tyr Cys Ile Val Arg Gly Ser Pro Gly Ala Gly Gly Thr Ser Tyr Gly
435 440 445
Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asn Ile
450 455 460
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
465 470 475 480
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
485 490 495
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
500 505 510
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
515 520 525
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
530 535 540
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
545 550 555 560
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
565 570 575
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
580 585 590
Thr Leu Arg Leu Trp Ser Ser
595
<210> 47
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 47
Thr Thr Leu Ser Asn
1 5
<210> 48
<211> 7
<212> ПРТ
<213> Homo sapiens
<400> 48
Leu Val Lys Ser Gly Glu Val
1 5
<210> 49
<211> 14
<212> ПРТ
<213> Homo sapiens
<400> 49
Cys Ala Gly Pro Gly Gly Ala Gly Ser Tyr Gln Leu Thr Phe
1 5 10
<210> 50
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 50
Met Asn His Glu Tyr
1 5
<210> 51
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 51
Ser Met Asn Val Glu Val
1 5
<210> 52
<211> 17
<212> ПРТ
<213> Homo sapiens
<400> 52
Cys Ala Ser Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr
1 5 10 15
Phe
<210> 53
<211> 130
<212> ПРТ
<213> Homo sapiens
<400> 53
Met His Leu Ile Thr Ser Met Leu Val Leu Trp Met Gln Leu Ser Gln
1 5 10 15
Val Asn Gly Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln
20 25 30
Glu Gly Glu Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser
35 40 45
Asn Ile Gln Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu
50 55 60
Ile Gln Leu Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr
65 70 75 80
Phe Gln Phe Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala
85 90 95
Thr Gln Thr Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly
100 105 110
Ala Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val
115 120 125
Ile Pro
130
<210> 54
<211> 135
<212> ПРТ
<213> Homo sapiens
<400> 54
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro
115 120 125
Gly Thr Arg Leu Thr Val Thr
130 135
<210> 55
<211> 267
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 55
Met His Leu Ile Thr Ser Met Leu Val Leu Trp Met Gln Leu Ser Gln
1 5 10 15
Val Asn Gly Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln
20 25 30
Glu Gly Glu Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser
35 40 45
Asn Ile Gln Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu
50 55 60
Ile Gln Leu Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr
65 70 75 80
Phe Gln Phe Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala
85 90 95
Thr Gln Thr Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly
100 105 110
Ala Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val
115 120 125
Ile Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
130 135 140
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
145 150 155 160
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
165 170 175
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
180 185 190
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
195 200 205
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
210 215 220
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 56
<211> 308
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 56
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro
115 120 125
Gly Thr Arg Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro
130 135 140
Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys
180 185 190
Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp
225 230 235 240
Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys
290 295 300
Arg Lys Asn Ser
305
<210> 57
<211> 602
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 57
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro
115 120 125
Gly Thr Arg Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro
130 135 140
Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys
180 185 190
Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp
225 230 235 240
Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys
290 295 300
Arg Lys Asn Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe
305 310 315 320
Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met
325 330 335
His Leu Ile Thr Ser Met Leu Val Leu Trp Met Gln Leu Ser Gln Val
340 345 350
Asn Gly Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln Glu
355 360 365
Gly Glu Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser Asn
370 375 380
Ile Gln Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu Ile
385 390 395 400
Gln Leu Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr Phe
405 410 415
Gln Phe Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala Thr
420 425 430
Gln Thr Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly Ala
435 440 445
Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val Ile
450 455 460
Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro
465 470 475 480
Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln
485 490 495
Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys
500 505 510
Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile
515 520 525
Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu
530 535 540
Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu
545 550 555 560
Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu
565 570 575
Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn
580 585 590
Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 58
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 58
Thr Thr Ser Asp Arg
1 5
<210> 59
<211> 7
<212> ПРТ
<213> Homo sapiens
<400> 59
Leu Leu Ser Asn Gly Ala Val
1 5
<210> 60
<211> 14
<212> ПРТ
<213> Homo sapiens
<400> 60
Cys Ala Val Ala His Met Asp Ser Asn Tyr Gln Leu Ile Trp
1 5 10
<210> 61
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 61
Met Asn His Glu Tyr
1 5
<210> 62
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 62
Ser Val Gly Glu Gly Thr
1 5
<210> 63
<211> 16
<212> ПРТ
<213> Homo sapiens
<400> 63
Cys Ala Ser Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe
1 5 10 15
<210> 64
<211> 130
<212> ПРТ
<213> Homo sapiens
<400> 64
Met His Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu
1 5 10 15
Ser Gly Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln
20 25 30
Glu Gly Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp
35 40 45
Arg Leu Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu
50 55 60
Phe Val Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met
65 70 75 80
Ala Ser Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala
85 90 95
Ala Val His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met
100 105 110
Asp Ser Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile
115 120 125
Lys Pro
130
<210> 65
<211> 134
<212> ПРТ
<213> Homo sapiens
<400> 65
Met Ala Leu Gly Leu Leu Cys Cys Gly Ala Phe Ser Leu Leu Trp Ala
1 5 10 15
Gly Pro Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu
20 25 30
Lys Thr Gly Gln Ser Met Thr Leu Leu Cys Ala Gln Asp Met Asn His
35 40 45
Glu Tyr Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu
50 55 60
Ile His Tyr Ser Val Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro
65 70 75 80
Asp Gly Tyr Asn Val Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly
85 90 95
Leu Glu Ser Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser
100 105 110
Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu
130
<210> 66
<211> 267
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 66
Met His Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu
1 5 10 15
Ser Gly Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln
20 25 30
Glu Gly Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp
35 40 45
Arg Leu Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu
50 55 60
Phe Val Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met
65 70 75 80
Ala Ser Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala
85 90 95
Ala Val His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met
100 105 110
Asp Ser Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile
115 120 125
Lys Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
130 135 140
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
145 150 155 160
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
165 170 175
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
180 185 190
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
195 200 205
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
210 215 220
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 67
<211> 307
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 67
Met Ala Leu Gly Leu Leu Cys Cys Gly Ala Phe Ser Leu Leu Trp Ala
1 5 10 15
Gly Pro Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu
20 25 30
Lys Thr Gly Gln Ser Met Thr Leu Leu Cys Ala Gln Asp Met Asn His
35 40 45
Glu Tyr Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu
50 55 60
Ile His Tyr Ser Val Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro
65 70 75 80
Asp Gly Tyr Asn Val Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly
85 90 95
Leu Glu Ser Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser
100 105 110
Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser
305
<210> 68
<211> 601
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 68
Met Ala Leu Gly Leu Leu Cys Cys Gly Ala Phe Ser Leu Leu Trp Ala
1 5 10 15
Gly Pro Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu
20 25 30
Lys Thr Gly Gln Ser Met Thr Leu Leu Cys Ala Gln Asp Met Asn His
35 40 45
Glu Tyr Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu
50 55 60
Ile His Tyr Ser Val Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro
65 70 75 80
Asp Gly Tyr Asn Val Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly
85 90 95
Leu Glu Ser Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser
100 105 110
Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser
305 310 315 320
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met His
325 330 335
Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu Ser Gly
340 345 350
Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln Glu Gly
355 360 365
Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp Arg Leu
370 375 380
Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu Phe Val
385 390 395 400
Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met Ala Ser
405 410 415
Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala Ala Val
420 425 430
His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met Asp Ser
435 440 445
Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile Lys Pro
450 455 460
Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
465 470 475 480
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
485 490 495
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
500 505 510
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
515 520 525
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
530 535 540
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
545 550 555 560
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
565 570 575
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
580 585 590
Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 69
<211> 7
<212> ПРТ
<213> Homo sapiens
<400> 69
Thr Ile Ser Gly Asn Glu Tyr
1 5
<210> 70
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 70
Gly Leu Lys Asn Asn
1 5
<210> 71
<211> 19
<212> ПРТ
<213> Homo sapiens
<400> 71
Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser Tyr Gly Lys
1 5 10 15
Leu Thr Phe
<210> 72
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 72
Leu Asn His Asp Ala
1 5
<210> 73
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 73
Ser Gln Ile Val Asn Asp
1 5
<210> 74
<211> 11
<212> ПРТ
<213> Homo sapiens
<400> 74
Cys Ala Thr Arg Thr Gly Asn Glu Ala Phe Phe
1 5 10
<210> 75
<211> 133
<212> ПРТ
<213> Homo sapiens
<400> 75
Met His Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro
130
<210> 76
<211> 129
<212> ПРТ
<213> Homo sapiens
<400> 76
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr
100 105 110
Arg Thr Gly Asn Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val
<210> 77
<211> 270
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 77
Met His Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 78
<211> 302
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 78
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr
100 105 110
Arg Thr Gly Asn Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 79
<211> 599
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 79
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr
100 105 110
Arg Thr Gly Asn Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser Arg Ala
290 295 300
Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
305 310 315 320
Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Leu Val Ala Arg Val
325 330 335
Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr Thr Gln
340 345 350
Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu Pro Cys
355 360 365
Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr Arg Gln
370 375 380
Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys Asn Asn
385 390 395 400
Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg Lys Ser
405 410 415
Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala Val Tyr
420 425 430
Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser Tyr Gly
435 440 445
Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asn Ile
450 455 460
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
465 470 475 480
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
485 490 495
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
500 505 510
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
515 520 525
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
530 535 540
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
545 550 555 560
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
565 570 575
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
580 585 590
Thr Leu Arg Leu Trp Ser Ser
595
<210> 80
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 80
Val Ser Gly Asn Pro Tyr
1 5
<210> 81
<211> 8
<212> ПРТ
<213> Homo sapiens
<400> 81
Tyr Ile Thr Gly Asp Asn Leu Val
1 5
<210> 82
<211> 17
<212> ПРТ
<213> Homo sapiens
<400> 82
Cys Ala Val Arg Asp Gly Ser Ala Thr Ser Gly Thr Tyr Lys Tyr Ile
1 5 10 15
Phe
<210> 83
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 83
Ser Glu His Asn Arg
1 5
<210> 84
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 84
Phe Gln Asn Glu Ala Gln
1 5
<210> 85
<211> 13
<212> ПРТ
<213> Homo sapiens
<400> 85
Cys Ala Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe
1 5 10
<210> 86
<211> 136
<212> ПРТ
<213> Homo sapiens
<400> 86
Met His Ser Ala Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser
1 5 10 15
Gly Leu Arg Ala Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val
20 25 30
Ala Glu Gly Asn Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly
35 40 45
Asn Pro Tyr Leu Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln
50 55 60
Phe Leu Leu Lys Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr
65 70 75 80
Gly Phe Glu Ala Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys
85 90 95
Lys Pro Ser Ala Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val
100 105 110
Arg Asp Gly Ser Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr
115 120 125
Gly Thr Arg Leu Lys Val Leu Ala
130 135
<210> 87
<211> 132
<212> ПРТ
<213> Homo sapiens
<400> 87
Met Ala Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr
130
<210> 88
<211> 273
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 88
Met His Ser Ala Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser
1 5 10 15
Gly Leu Arg Ala Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val
20 25 30
Ala Glu Gly Asn Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly
35 40 45
Asn Pro Tyr Leu Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln
50 55 60
Phe Leu Leu Lys Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr
65 70 75 80
Gly Phe Glu Ala Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys
85 90 95
Lys Pro Ser Ala Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val
100 105 110
Arg Asp Gly Ser Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr
115 120 125
Gly Thr Arg Leu Lys Val Leu Ala Asn Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 89
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 89
Met Ala Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 90
<211> 605
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 90
Met Ala Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
305 310 315 320
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Ser Ala
325 330 335
Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser Gly Leu Arg Ala
340 345 350
Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val Ala Glu Gly Asn
355 360 365
Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly Asn Pro Tyr Leu
370 375 380
Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln Phe Leu Leu Lys
385 390 395 400
Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr Gly Phe Glu Ala
405 410 415
Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys Lys Pro Ser Ala
420 425 430
Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val Arg Asp Gly Ser
435 440 445
Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr Gly Thr Arg Leu
450 455 460
Lys Val Leu Ala Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu
465 470 475 480
Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe
485 490 495
Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile
500 505 510
Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn
515 520 525
Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile
530 535 540
Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp
545 550 555 560
Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe
565 570 575
Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala
580 585 590
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600 605
<210> 91
<211> 137
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 91
Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
1 5 10 15
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
20 25 30
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
35 40 45
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
50 55 60
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
65 70 75 80
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
85 90 95
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
100 105 110
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
115 120 125
Leu Met Thr Leu Arg Leu Trp Ser Ser
130 135
<210> 92
<211> 137
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 92
Asp Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
1 5 10 15
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
20 25 30
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
35 40 45
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
50 55 60
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
65 70 75 80
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
85 90 95
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
100 105 110
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
115 120 125
Leu Met Thr Leu Arg Leu Trp Ser Ser
130 135
<210> 93
<211> 173
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 93
Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro
1 5 10 15
Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu
20 25 30
Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn
35 40 45
Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys
50 55 60
Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala
65 70 75 80
Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe
85 90 95
His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro
100 105 110
Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly
115 120 125
Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu
130 135 140
Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser
145 150 155 160
Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
165 170
<210> 94
<211> 27
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 94
Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
1 5 10 15
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro
20 25
<210> 95
<211> 9
<212> ПРТ
<213> Homo sapiens
<400> 95
His Met Thr Glu Val Val Arg Arg Cys
1 5
<210> 96
<211> 9
<212> ПРТ
<213> Homo sapiens
<400> 96
His Met Thr Glu Val Val Arg His Cys
1 5
<210> 97
<211> 10
<212> ПРТ
<213> Homo sapiens
<400> 97
Ser Ser Cys Met Gly Gly Met Asn Arg Arg
1 5 10
<210> 98
<211> 10
<212> ПРТ
<213> Homo sapiens
<400> 98
Ser Ser Cys Met Gly Gly Met Asn Trp Arg
1 5 10
<210> 99
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 99
Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg His Cys Pro
1 5 10 15
<210> 100
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 100
Lys Gln Ser Gln His Met Thr Glu Val Val Arg His Cys Pro His
1 5 10 15
<210> 101
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 101
Gln Ser Gln His Met Thr Glu Val Val Arg His Cys Pro His His
1 5 10 15
<210> 102
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 102
Ser Gln His Met Thr Glu Val Val Arg His Cys Pro His His Glu
1 5 10 15
<210> 103
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 103
Gln His Met Thr Glu Val Val Arg His Cys Pro His His Glu Arg
1 5 10 15
<210> 104
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 104
His Met Thr Glu Val Val Arg His Cys Pro His His Glu Arg Cys
1 5 10 15
<210> 105
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 105
Met Thr Glu Val Val Arg His Cys Pro His His Glu Arg Cys Ser
1 5 10 15
<210> 106
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 106
Thr Glu Val Val Arg His Cys Pro His His Glu Arg Cys Ser Asp
1 5 10 15
<210> 107
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 107
Glu Val Val Arg His Cys Pro His His Glu Arg Cys Ser Asp Ser
1 5 10 15
<210> 108
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 108
Val Val Arg His Cys Pro His His Glu Arg Cys Ser Asp Ser Asp
1 5 10 15
<210> 109
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 109
Val Arg His Cys Pro His His Glu Arg Cys Ser Asp Ser Asp Gly
1 5 10 15
<210> 110
<211> 25
<212> ПРТ
<213> Homo sapiens
<400> 110
Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys Pro His
1 5 10 15
His Glu Arg Cys Ser Asp Ser Asp Gly
20 25
<210> 111
<211> 25
<212> ПРТ
<213> Homo sapiens
<400> 111
Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg His Cys Pro His
1 5 10 15
His Glu Arg Cys Ser Asp Ser Asp Gly
20 25
<210> 112
<211> 9
<212> ПРТ
<213> Homo sapiens
<400> 112
Val Val Pro Tyr Glu Pro Pro Glu Val
1 5
<210> 113
<211> 9
<212> ПРТ
<213> Homo sapiens
<400> 113
Val Val Pro Cys Glu Pro Pro Glu Val
1 5
<210> 114
<211> 341
<212> ПРТ
<213> Homo sapiens
<400> 114
Met Glu Glu Pro Gln Ser Asp Pro Ser Val Glu Pro Pro Leu Ser Gln
1 5 10 15
Glu Thr Phe Ser Asp Leu Trp Lys Leu Leu Pro Glu Asn Asn Val Leu
20 25 30
Ser Pro Leu Pro Ser Gln Ala Met Asp Asp Leu Met Leu Ser Pro Asp
35 40 45
Asp Ile Glu Gln Trp Phe Thr Glu Asp Pro Gly Pro Asp Glu Ala Pro
50 55 60
Arg Met Pro Glu Ala Ala Pro Pro Val Ala Pro Ala Pro Ala Ala Pro
65 70 75 80
Thr Pro Ala Ala Pro Ala Pro Ala Pro Ser Trp Pro Leu Ser Ser Ser
85 90 95
Val Pro Ser Gln Lys Thr Tyr Gln Gly Ser Tyr Gly Phe Arg Leu Gly
100 105 110
Phe Leu His Ser Gly Thr Ala Lys Ser Val Thr Cys Thr Tyr Ser Pro
115 120 125
Ala Leu Asn Lys Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln
130 135 140
Leu Trp Val Asp Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met
145 150 155 160
Ala Ile Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys
165 170 175
Pro His His Glu Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln
180 185 190
His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp
195 200 205
Arg Asn Thr Phe Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu
210 215 220
Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser
225 230 235 240
Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr
245 250 255
Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val
260 265 270
Arg Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn
275 280 285
Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr
290 295 300
Lys Arg Ala Leu Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys
305 310 315 320
Lys Pro Leu Asp Gly Glu Tyr Phe Thr Leu Gln Asp Gln Thr Ser Phe
325 330 335
Gln Lys Glu Asn Cys
340
<210> 115
<211> 346
<212> ПРТ
<213> Homo sapiens
<400> 115
Met Glu Glu Pro Gln Ser Asp Pro Ser Val Glu Pro Pro Leu Ser Gln
1 5 10 15
Glu Thr Phe Ser Asp Leu Trp Lys Leu Leu Pro Glu Asn Asn Val Leu
20 25 30
Ser Pro Leu Pro Ser Gln Ala Met Asp Asp Leu Met Leu Ser Pro Asp
35 40 45
Asp Ile Glu Gln Trp Phe Thr Glu Asp Pro Gly Pro Asp Glu Ala Pro
50 55 60
Arg Met Pro Glu Ala Ala Pro Pro Val Ala Pro Ala Pro Ala Ala Pro
65 70 75 80
Thr Pro Ala Ala Pro Ala Pro Ala Pro Ser Trp Pro Leu Ser Ser Ser
85 90 95
Val Pro Ser Gln Lys Thr Tyr Gln Gly Ser Tyr Gly Phe Arg Leu Gly
100 105 110
Phe Leu His Ser Gly Thr Ala Lys Ser Val Thr Cys Thr Tyr Ser Pro
115 120 125
Ala Leu Asn Lys Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln
130 135 140
Leu Trp Val Asp Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met
145 150 155 160
Ala Ile Tyr Lys Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys
165 170 175
Pro His His Glu Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln
180 185 190
His Leu Ile Arg Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp
195 200 205
Arg Asn Thr Phe Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu
210 215 220
Val Gly Ser Asp Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser
225 230 235 240
Ser Cys Met Gly Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr
245 250 255
Leu Glu Asp Ser Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val
260 265 270
Arg Val Cys Ala Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn
275 280 285
Leu Arg Lys Lys Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr
290 295 300
Lys Arg Ala Leu Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys
305 310 315 320
Lys Pro Leu Asp Gly Glu Tyr Phe Thr Leu Gln Met Leu Leu Asp Leu
325 330 335
Arg Trp Cys Tyr Phe Leu Ile Asn Ser Ser
340 345
<210> 116
<211> 354
<212> ПРТ
<213> Homo sapiens
<400> 116
Met Asp Asp Leu Met Leu Ser Pro Asp Asp Ile Glu Gln Trp Phe Thr
1 5 10 15
Glu Asp Pro Gly Pro Asp Glu Ala Pro Arg Met Pro Glu Ala Ala Pro
20 25 30
Pro Val Ala Pro Ala Pro Ala Ala Pro Thr Pro Ala Ala Pro Ala Pro
35 40 45
Ala Pro Ser Trp Pro Leu Ser Ser Ser Val Pro Ser Gln Lys Thr Tyr
50 55 60
Gln Gly Ser Tyr Gly Phe Arg Leu Gly Phe Leu His Ser Gly Thr Ala
65 70 75 80
Lys Ser Val Thr Cys Thr Tyr Ser Pro Ala Leu Asn Lys Met Phe Cys
85 90 95
Gln Leu Ala Lys Thr Cys Pro Val Gln Leu Trp Val Asp Ser Thr Pro
100 105 110
Pro Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys Gln Ser Gln
115 120 125
His Met Thr Glu Val Val Arg Arg Cys Pro His His Glu Arg Cys Ser
130 135 140
Asp Ser Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg Val Glu Gly
145 150 155 160
Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg His Ser
165 170 175
Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys Thr Thr
180 185 190
Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly Met Asn
195 200 205
Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser Gly Asn
210 215 220
Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys Pro Gly
225 230 235 240
Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly Glu Pro
245 250 255
His His Glu Leu Pro Pro Gly Ser Thr Lys Arg Ala Leu Pro Asn Asn
260 265 270
Thr Ser Ser Ser Pro Gln Pro Lys Lys Lys Pro Leu Asp Gly Glu Tyr
275 280 285
Phe Thr Leu Gln Ile Arg Gly Arg Glu Arg Phe Glu Met Phe Arg Glu
290 295 300
Leu Asn Glu Ala Leu Glu Leu Lys Asp Ala Gln Ala Gly Lys Glu Pro
305 310 315 320
Gly Gly Ser Arg Ala His Ser Ser His Leu Lys Ser Lys Lys Gly Gln
325 330 335
Ser Thr Ser Arg His Lys Lys Leu Met Phe Lys Thr Glu Gly Pro Asp
340 345 350
Ser Asp
<210> 117
<211> 302
<212> ПРТ
<213> Homo sapiens
<400> 117
Met Asp Asp Leu Met Leu Ser Pro Asp Asp Ile Glu Gln Trp Phe Thr
1 5 10 15
Glu Asp Pro Gly Pro Asp Glu Ala Pro Arg Met Pro Glu Ala Ala Pro
20 25 30
Pro Val Ala Pro Ala Pro Ala Ala Pro Thr Pro Ala Ala Pro Ala Pro
35 40 45
Ala Pro Ser Trp Pro Leu Ser Ser Ser Val Pro Ser Gln Lys Thr Tyr
50 55 60
Gln Gly Ser Tyr Gly Phe Arg Leu Gly Phe Leu His Ser Gly Thr Ala
65 70 75 80
Lys Ser Val Thr Cys Thr Tyr Ser Pro Ala Leu Asn Lys Met Phe Cys
85 90 95
Gln Leu Ala Lys Thr Cys Pro Val Gln Leu Trp Val Asp Ser Thr Pro
100 105 110
Pro Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys Gln Ser Gln
115 120 125
His Met Thr Glu Val Val Arg Arg Cys Pro His His Glu Arg Cys Ser
130 135 140
Asp Ser Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg Val Glu Gly
145 150 155 160
Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg His Ser
165 170 175
Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys Thr Thr
180 185 190
Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly Met Asn
195 200 205
Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser Gly Asn
210 215 220
Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys Pro Gly
225 230 235 240
Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly Glu Pro
245 250 255
His His Glu Leu Pro Pro Gly Ser Thr Lys Arg Ala Leu Pro Asn Asn
260 265 270
Thr Ser Ser Ser Pro Gln Pro Lys Lys Lys Pro Leu Asp Gly Glu Tyr
275 280 285
Phe Thr Leu Gln Asp Gln Thr Ser Phe Gln Lys Glu Asn Cys
290 295 300
<210> 118
<211> 307
<212> ПРТ
<213> Homo sapiens
<400> 118
Met Asp Asp Leu Met Leu Ser Pro Asp Asp Ile Glu Gln Trp Phe Thr
1 5 10 15
Glu Asp Pro Gly Pro Asp Glu Ala Pro Arg Met Pro Glu Ala Ala Pro
20 25 30
Pro Val Ala Pro Ala Pro Ala Ala Pro Thr Pro Ala Ala Pro Ala Pro
35 40 45
Ala Pro Ser Trp Pro Leu Ser Ser Ser Val Pro Ser Gln Lys Thr Tyr
50 55 60
Gln Gly Ser Tyr Gly Phe Arg Leu Gly Phe Leu His Ser Gly Thr Ala
65 70 75 80
Lys Ser Val Thr Cys Thr Tyr Ser Pro Ala Leu Asn Lys Met Phe Cys
85 90 95
Gln Leu Ala Lys Thr Cys Pro Val Gln Leu Trp Val Asp Ser Thr Pro
100 105 110
Pro Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys Gln Ser Gln
115 120 125
His Met Thr Glu Val Val Arg Arg Cys Pro His His Glu Arg Cys Ser
130 135 140
Asp Ser Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg Val Glu Gly
145 150 155 160
Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe Arg His Ser
165 170 175
Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp Cys Thr Thr
180 185 190
Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly Gly Met Asn
195 200 205
Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser Ser Gly Asn
210 215 220
Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala Cys Pro Gly
225 230 235 240
Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys Gly Glu Pro
245 250 255
His His Glu Leu Pro Pro Gly Ser Thr Lys Arg Ala Leu Pro Asn Asn
260 265 270
Thr Ser Ser Ser Pro Gln Pro Lys Lys Lys Pro Leu Asp Gly Glu Tyr
275 280 285
Phe Thr Leu Gln Met Leu Leu Asp Leu Arg Trp Cys Tyr Phe Leu Ile
290 295 300
Asn Ser Ser
305
<210> 119
<211> 261
<212> ПРТ
<213> Homo sapiens
<400> 119
Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln Leu Trp Val Asp
1 5 10 15
Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys
20 25 30
Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys Pro His His Glu
35 40 45
Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg
50 55 60
Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe
65 70 75 80
Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp
85 90 95
Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly
100 105 110
Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser
115 120 125
Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala
130 135 140
Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys
145 150 155 160
Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr Lys Arg Ala Leu
165 170 175
Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys Lys Pro Leu Asp
180 185 190
Gly Glu Tyr Phe Thr Leu Gln Ile Arg Gly Arg Glu Arg Phe Glu Met
195 200 205
Phe Arg Glu Leu Asn Glu Ala Leu Glu Leu Lys Asp Ala Gln Ala Gly
210 215 220
Lys Glu Pro Gly Gly Ser Arg Ala His Ser Ser His Leu Lys Ser Lys
225 230 235 240
Lys Gly Gln Ser Thr Ser Arg His Lys Lys Leu Met Phe Lys Thr Glu
245 250 255
Gly Pro Asp Ser Asp
260
<210> 120
<211> 209
<212> ПРТ
<213> Homo sapiens
<400> 120
Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln Leu Trp Val Asp
1 5 10 15
Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys
20 25 30
Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys Pro His His Glu
35 40 45
Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg
50 55 60
Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe
65 70 75 80
Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp
85 90 95
Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly
100 105 110
Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser
115 120 125
Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala
130 135 140
Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys
145 150 155 160
Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr Lys Arg Ala Leu
165 170 175
Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys Lys Pro Leu Asp
180 185 190
Gly Glu Tyr Phe Thr Leu Gln Asp Gln Thr Ser Phe Gln Lys Glu Asn
195 200 205
Cys
<210> 121
<211> 214
<212> ПРТ
<213> Homo sapiens
<400> 121
Met Phe Cys Gln Leu Ala Lys Thr Cys Pro Val Gln Leu Trp Val Asp
1 5 10 15
Ser Thr Pro Pro Pro Gly Thr Arg Val Arg Ala Met Ala Ile Tyr Lys
20 25 30
Gln Ser Gln His Met Thr Glu Val Val Arg Arg Cys Pro His His Glu
35 40 45
Arg Cys Ser Asp Ser Asp Gly Leu Ala Pro Pro Gln His Leu Ile Arg
50 55 60
Val Glu Gly Asn Leu Arg Val Glu Tyr Leu Asp Asp Arg Asn Thr Phe
65 70 75 80
Arg His Ser Val Val Val Pro Tyr Glu Pro Pro Glu Val Gly Ser Asp
85 90 95
Cys Thr Thr Ile His Tyr Asn Tyr Met Cys Asn Ser Ser Cys Met Gly
100 105 110
Gly Met Asn Arg Arg Pro Ile Leu Thr Ile Ile Thr Leu Glu Asp Ser
115 120 125
Ser Gly Asn Leu Leu Gly Arg Asn Ser Phe Glu Val Arg Val Cys Ala
130 135 140
Cys Pro Gly Arg Asp Arg Arg Thr Glu Glu Glu Asn Leu Arg Lys Lys
145 150 155 160
Gly Glu Pro His His Glu Leu Pro Pro Gly Ser Thr Lys Arg Ala Leu
165 170 175
Pro Asn Asn Thr Ser Ser Ser Pro Gln Pro Lys Lys Lys Pro Leu Asp
180 185 190
Gly Glu Tyr Phe Thr Leu Gln Met Leu Leu Asp Leu Arg Trp Cys Tyr
195 200 205
Phe Leu Ile Asn Ser Ser
210
<210> 122
<211> 14
<212> ПРТ
<213> Homo sapiens
<400> 122
Cys Ala Ser Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe
1 5 10
<210> 123
<211> 13
<212> ПРТ
<213> Homo sapiens
<400> 123
Cys Ala Ser Ser Ile Asn Arg Tyr Thr Glu Ala Phe Phe
1 5 10
<210> 124
<211> 17
<212> ПРТ
<213> Homo sapiens
<400> 124
Cys Ala Ser Ser Tyr Pro Ser Met Asp Arg Asp Arg Tyr Gly Tyr Thr
1 5 10 15
Phe
<210> 125
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 125
Cys Ala Ser Asn Leu Gly Gly Gly Ser Thr Asp Thr Gln Tyr Phe
1 5 10 15
<210> 126
<211> 15
<212> ПРТ
<213> Homo sapiens
<400> 126
Cys Ala Ser Ser Phe Gly Ser Gly Ser Thr Asp Thr Gln Tyr Phe
1 5 10 15
<210> 127
<211> 12
<212> ПРТ
<213> Homo sapiens
<400> 127
Cys Ala Ser Ser Ser Arg Asp Tyr Glu Gln Tyr Phe
1 5 10
<210> 128
<211> 8
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 128
Arg Ala Lys Arg Ser Gly Ser Gly
1 5
<210> 129
<211> 115
<212> ПРТ
<213> Homo sapiens
<400> 129
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asn Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Leu
115
<210> 130
<211> 115
<212> ПРТ
<213> Homo sapiens
<400> 130
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Leu
115
<210> 131
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 131
Asn Ser Ala Phe Gln Tyr
1 5
<210> 132
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 132
Thr Tyr Ser Ser Gly Asn
1 5
<210> 133
<211> 16
<212> ПРТ
<213> Homo sapiens
<400> 133
Cys Ala Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe
1 5 10 15
<210> 134
<211> 5
<212> ПРТ
<213> Homo sapiens
<400> 134
Met Asn His Glu Tyr
1 5
<210> 135
<211> 6
<212> ПРТ
<213> Homo sapiens
<400> 135
Ser Met Asn Val Glu Val
1 5
<210> 136
<211> 14
<212> ПРТ
<213> Homo sapiens
<400> 136
Cys Ala Ser Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe
1 5 10
<210> 137
<211> 136
<212> ПРТ
<213> Homo sapiens
<400> 137
Met Ala Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asn Ser Ala Phe Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys
50 55 60
Gly Pro Glu Leu Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu
85 90 95
Phe Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser
115 120 125
Gly Thr Arg Leu Leu Val Arg Pro
130 135
<210> 138
<211> 132
<212> ПРТ
<213> Homo sapiens
<400> 138
Met His Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu
130
<210> 139
<211> 273
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 139
Met Ala Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asn Ser Ala Phe Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys
50 55 60
Gly Pro Glu Leu Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu
85 90 95
Phe Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser
115 120 125
Gly Thr Arg Leu Leu Val Arg Pro Asn Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 140
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 140
Met His Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 141
<211> 605
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 141
Met Ala Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asn Ser Ala Phe Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys
50 55 60
Gly Pro Glu Leu Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu
85 90 95
Phe Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser
115 120 125
Gly Thr Arg Leu Leu Val Arg Pro Asn Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
275 280 285
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Pro Gln
290 295 300
Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala Gly Pro Leu Glu
305 310 315 320
Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys
325 330 335
Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser
340 345 350
Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser
355 360 365
Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys
370 375 380
Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro
385 390 395 400
Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Ser Ile Gln Gln
405 410 415
Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val Leu
420 425 430
Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro
435 440 445
Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu
450 455 460
Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn
465 470 475 480
Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys
485 490 495
Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala
500 505 510
Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe
515 520 525
His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro
530 535 540
Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly
545 550 555 560
Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu
565 570 575
Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser
580 585 590
Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
595 600 605
<210> 142
<211> 107
<212> ПРТ
<213> Homo sapiens
<400> 142
Lys Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu Glu Pro Val
1 5 10 15
His Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp Tyr Ile His
20 25 30
Trp Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val Ile His Gly
35 40 45
Leu Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala Ile Ala Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr Leu Arg Asp
65 70 75 80
Ala Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala Arg Leu Met
85 90 95
Phe Gly Asp Gly Thr Gln Leu Val Val Lys Pro
100 105
<210> 143
<211> 111
<212> ПРТ
<213> Homo sapiens
<400> 143
Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys Lys
1 5 10 15
Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser Met
35 40 45
Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys Val
50 55 60
Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro Ser
65 70 75 80
Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Gly Leu Val Gly Phe
85 90 95
Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg Leu Ser Ile Leu
100 105 110
<210> 144
<211> 114
<212> ПРТ
<213> Homo sapiens
<400> 144
Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala
1 5 10 15
Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr
20 25 30
Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly
35 40 45
Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp
65 70 75 80
Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly
85 90 95
Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val
100 105 110
His Pro
<210> 145
<211> 108
<212> ПРТ
<213> Homo sapiens
<400> 145
Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg Lys Glu Gly Gln Asn
1 5 10 15
Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His Asp Ala Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu Ile Tyr Tyr Ser Gln
35 40 45
Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala Glu Gly Tyr Ser Val
50 55 60
Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr Val Thr Ser Ala Gln
65 70 75 80
Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser Leu Gln Phe Asn Glu
85 90 95
Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val Leu
100 105
<210> 146
<211> 106
<212> ПРТ
<213> Homo sapiens
<400> 146
Lys Asp Gln Val Phe Gln Pro Ser Thr Val Ala Ser Ser Glu Gly Ala
1 5 10 15
Val Val Glu Ile Phe Cys Asn His Ser Val Ser Asn Ala Tyr Asn Phe
20 25 30
Phe Trp Tyr Leu His Phe Pro Gly Cys Ala Pro Arg Leu Leu Val Lys
35 40 45
Gly Ser Lys Pro Ser Gln Gln Gly Arg Tyr Asn Met Thr Tyr Glu Arg
50 55 60
Phe Ser Ser Ser Leu Leu Ile Leu Gln Val Arg Glu Ala Asp Ala Ala
65 70 75 80
Val Tyr Tyr Cys Ala Val Glu Asp Arg Arg Arg Thr Ala Leu Ile Phe
85 90 95
Gly Lys Gly Thr Thr Leu Ser Val Ser Ser
100 105
<210> 147
<211> 115
<212> ПРТ
<213> Homo sapiens
<400> 147
Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr Gln Met Gly
1 5 10 15
Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His Leu Tyr Phe
20 25 30
Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe Leu Val Ser
35 40 45
Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe Asp Asp Gln
50 55 60
Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu Lys Ile Arg
65 70 75 80
Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala Ser Ser Glu
85 90 95
Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
100 105 110
Thr Val Leu
115
<210> 148
<211> 114
<212> ПРТ
<213> Homo sapiens
<400> 148
Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala
1 5 10 15
Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr
20 25 30
Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly
35 40 45
Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp
65 70 75 80
Thr Ala Val Tyr Tyr Cys Ile Val Arg Gly Ser Pro Gly Ala Gly Gly
85 90 95
Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val
100 105 110
His Pro
<210> 149
<211> 108
<212> ПРТ
<213> Homo sapiens
<400> 149
Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg Lys Glu Gly Gln Asn
1 5 10 15
Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His Asp Ala Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu Ile Tyr Tyr Ser Gln
35 40 45
Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala Glu Gly Tyr Ser Val
50 55 60
Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr Val Thr Ser Ala Gln
65 70 75 80
Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser Ser Ile Arg Thr Glu
85 90 95
Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val Val
100 105
<210> 150
<211> 111
<212> ПРТ
<213> Homo sapiens
<400> 150
Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln Glu Gly Glu
1 5 10 15
Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser Asn Ile Gln
20 25 30
Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu Ile Gln Leu
35 40 45
Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr Phe Gln Phe
50 55 60
Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala Thr Gln Thr
65 70 75 80
Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly Ala Gly Ser
85 90 95
Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val Ile Pro
100 105 110
<210> 151
<211> 114
<212> ПРТ
<213> Homo sapiens
<400> 151
Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys Lys
1 5 10 15
Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser Met
35 40 45
Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys Val
50 55 60
Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro Ser
65 70 75 80
Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Ser Pro Phe Val Val
85 90 95
Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr
100 105 110
Val Thr
<210> 152
<211> 112
<212> ПРТ
<213> Homo sapiens
<400> 152
Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln Glu Gly
1 5 10 15
Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp Arg Leu
20 25 30
Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu Phe Val
35 40 45
Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met Ala Ser
50 55 60
Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala Ala Val
65 70 75 80
His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met Asp Ser
85 90 95
Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile Lys Pro
100 105 110
<210> 153
<211> 113
<212> ПРТ
<213> Homo sapiens
<400> 153
Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu Lys Thr Gly Gln Ser
1 5 10 15
Met Thr Leu Leu Cys Ala Gln Asp Met Asn His Glu Tyr Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu Ile His Tyr Ser Val
35 40 45
Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro Asp Gly Tyr Asn Val
50 55 60
Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly Leu Glu Ser Ala Ala
65 70 75 80
Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser Ser Tyr Ala Gly Leu
85 90 95
Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
100 105 110
Leu
<210> 154
<211> 114
<212> ПРТ
<213> Homo sapiens
<400> 154
Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala
1 5 10 15
Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr
20 25 30
Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly
35 40 45
Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp
65 70 75 80
Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly
85 90 95
Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val
100 105 110
His Pro
<210> 155
<211> 108
<212> ПРТ
<213> Homo sapiens
<400> 155
Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg Lys Glu Gly Gln Asn
1 5 10 15
Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His Asp Ala Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu Ile Tyr Tyr Ser Gln
35 40 45
Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala Glu Gly Tyr Ser Val
50 55 60
Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr Val Thr Ser Ala Gln
65 70 75 80
Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr Arg Thr Gly Asn Glu
85 90 95
Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val Val
100 105
<210> 156
<211> 116
<212> ПРТ
<213> Homo sapiens
<400> 156
Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val Ala Glu Gly Asn
1 5 10 15
Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly Asn Pro Tyr Leu
20 25 30
Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln Phe Leu Leu Lys
35 40 45
Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr Gly Phe Glu Ala
50 55 60
Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys Lys Pro Ser Ala
65 70 75 80
Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val Arg Asp Gly Ser
85 90 95
Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr Gly Thr Arg Leu
100 105 110
Lys Val Leu Ala
115
<210> 157
<211> 113
<212> ПРТ
<213> Homo sapiens
<400> 157
Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr Lys Arg Gly
1 5 10 15
Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His Asn Arg Leu
20 25 30
Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe Leu Thr Tyr
35 40 45
Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu Ser Asp Arg
50 55 60
Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu Glu Ile Gln
65 70 75 80
Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala Ser Ser Pro
85 90 95
Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val
100 105 110
Thr
<210> 158
<211> 111
<212> ПРТ
<213> Homo sapiens
<400> 158
Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys Lys
1 5 10 15
Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser Met
35 40 45
Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys Val
50 55 60
Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro Ser
65 70 75 80
Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Ser Ile Gln Gln Gly
85 90 95
Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val Leu
100 105 110
<210> 159
<211> 115
<212> ПРТ
<213> Homo sapiens
<400> 159
Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro Leu Ser Val Pro Glu
1 5 10 15
Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser Asn Ser Ala Phe Gln
20 25 30
Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys Gly Pro Glu Leu Leu
35 40 45
Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp Gly Arg Phe Thr Ala
50 55 60
Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu Phe Ile Arg Asp Ser
65 70 75 80
Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala Met Ser Gly Leu Lys
85 90 95
Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr Arg Leu Leu
100 105 110
Val Arg Pro
115
<210> 160
<211> 244
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 160
Lys Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu Glu Pro Val
1 5 10 15
His Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp Tyr Ile His
20 25 30
Trp Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val Ile His Gly
35 40 45
Leu Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala Ile Ala Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr Leu Arg Asp
65 70 75 80
Ala Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala Arg Leu Met
85 90 95
Phe Gly Asp Gly Thr Gln Leu Val Val Lys Pro Asn Ile Gln Asn Pro
100 105 110
Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr
115 120 125
Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr
130 135 140
Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys
145 150 155 160
Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr
165 170 175
Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro
180 185 190
Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu
195 200 205
Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg
210 215 220
Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg
225 230 235 240
Leu Trp Ser Ser
<210> 161
<211> 284
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 161
Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys Lys
1 5 10 15
Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser Met
35 40 45
Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys Val
50 55 60
Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro Ser
65 70 75 80
Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Gly Leu Val Gly Phe
85 90 95
Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg Leu Ser Ile Leu Glu
100 105 110
Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro Ser
115 120 125
Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu Ala
130 135 140
Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly
145 150 155 160
Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys Glu
165 170 175
Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr
180 185 190
Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe His
195 200 205
Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro Val
210 215 220
Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Ile
225 230 235 240
Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr
245 250 255
Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Thr
260 265 270
Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
275 280
<210> 162
<211> 251
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 162
Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala
1 5 10 15
Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr
20 25 30
Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly
35 40 45
Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp
65 70 75 80
Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly
85 90 95
Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val
100 105 110
His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
115 120 125
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
130 135 140
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
145 150 155 160
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
165 170 175
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
180 185 190
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
195 200 205
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
210 215 220
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
225 230 235 240
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
245 250
<210> 163
<211> 281
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 163
Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg Lys Glu Gly Gln Asn
1 5 10 15
Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His Asp Ala Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu Ile Tyr Tyr Ser Gln
35 40 45
Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala Glu Gly Tyr Ser Val
50 55 60
Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr Val Thr Ser Ala Gln
65 70 75 80
Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser Leu Gln Phe Asn Glu
85 90 95
Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val Leu Glu Asp Leu Arg
100 105 110
Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu
115 120 125
Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe
130 135 140
Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val
145 150 155 160
His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr
165 170 175
Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His
180 185 190
Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser
195 200 205
Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn
210 215 220
Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala
225 230 235 240
Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu
245 250 255
Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val
260 265 270
Met Ala Met Val Lys Arg Lys Asn Ser
275 280
<210> 164
<211> 243
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 164
Lys Asp Gln Val Phe Gln Pro Ser Thr Val Ala Ser Ser Glu Gly Ala
1 5 10 15
Val Val Glu Ile Phe Cys Asn His Ser Val Ser Asn Ala Tyr Asn Phe
20 25 30
Phe Trp Tyr Leu His Phe Pro Gly Cys Ala Pro Arg Leu Leu Val Lys
35 40 45
Gly Ser Lys Pro Ser Gln Gln Gly Arg Tyr Asn Met Thr Tyr Glu Arg
50 55 60
Phe Ser Ser Ser Leu Leu Ile Leu Gln Val Arg Glu Ala Asp Ala Ala
65 70 75 80
Val Tyr Tyr Cys Ala Val Glu Asp Arg Arg Arg Thr Ala Leu Ile Phe
85 90 95
Gly Lys Gly Thr Thr Leu Ser Val Ser Ser Asn Ile Gln Asn Pro Glu
100 105 110
Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu
115 120 125
Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met
130 135 140
Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala
145 150 155 160
Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser
165 170 175
Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser
180 185 190
Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr
195 200 205
Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile
210 215 220
Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu
225 230 235 240
Trp Ser Ser
<210> 165
<211> 288
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 165
Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr Gln Met Gly
1 5 10 15
Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His Leu Tyr Phe
20 25 30
Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe Leu Val Ser
35 40 45
Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe Asp Asp Gln
50 55 60
Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu Lys Ile Arg
65 70 75 80
Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala Ser Ser Glu
85 90 95
Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
100 105 110
Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
115 120 125
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
130 135 140
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
145 150 155 160
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln
165 170 175
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
180 185 190
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
195 200 205
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
210 215 220
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
225 230 235 240
Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala
245 250 255
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
260 265 270
Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
275 280 285
<210> 166
<211> 251
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 166
Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala
1 5 10 15
Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr
20 25 30
Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly
35 40 45
Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp
65 70 75 80
Thr Ala Val Tyr Tyr Cys Ile Val Arg Gly Ser Pro Gly Ala Gly Gly
85 90 95
Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val
100 105 110
His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
115 120 125
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
130 135 140
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
145 150 155 160
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
165 170 175
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
180 185 190
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
195 200 205
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
210 215 220
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
225 230 235 240
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
245 250
<210> 167
<211> 281
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 167
Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg Lys Glu Gly Gln Asn
1 5 10 15
Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His Asp Ala Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu Ile Tyr Tyr Ser Gln
35 40 45
Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala Glu Gly Tyr Ser Val
50 55 60
Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr Val Thr Ser Ala Gln
65 70 75 80
Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser Ser Ile Arg Thr Glu
85 90 95
Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val Val Glu Asp Leu Arg
100 105 110
Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu
115 120 125
Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe
130 135 140
Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val
145 150 155 160
His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr
165 170 175
Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His
180 185 190
Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser
195 200 205
Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn
210 215 220
Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala
225 230 235 240
Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu
245 250 255
Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val
260 265 270
Met Ala Met Val Lys Arg Lys Asn Ser
275 280
<210> 168
<211> 248
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 168
Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln Glu Gly Glu
1 5 10 15
Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser Asn Ile Gln
20 25 30
Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu Ile Gln Leu
35 40 45
Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr Phe Gln Phe
50 55 60
Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala Thr Gln Thr
65 70 75 80
Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly Ala Gly Ser
85 90 95
Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val Ile Pro Asn
100 105 110
Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser
115 120 125
Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn
130 135 140
Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val
145 150 155 160
Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp
165 170 175
Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn
180 185 190
Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu
195 200 205
Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val
210 215 220
Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu
225 230 235 240
Met Thr Leu Arg Leu Trp Ser Ser
245
<210> 169
<211> 287
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 169
Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys Lys
1 5 10 15
Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser Met
35 40 45
Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys Val
50 55 60
Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro Ser
65 70 75 80
Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Ser Pro Phe Val Val
85 90 95
Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr
100 105 110
Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe
115 120 125
Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val
130 135 140
Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp
145 150 155 160
Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala
165 170 175
Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val
180 185 190
Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val
195 200 205
Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro
210 215 220
Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp
225 230 235 240
Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr
245 250 255
Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu
260 265 270
Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
275 280 285
<210> 170
<211> 249
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 170
Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln Glu Gly
1 5 10 15
Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp Arg Leu
20 25 30
Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu Phe Val
35 40 45
Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met Ala Ser
50 55 60
Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala Ala Val
65 70 75 80
His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met Asp Ser
85 90 95
Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile Lys Pro
100 105 110
Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
115 120 125
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
130 135 140
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
145 150 155 160
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
165 170 175
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
180 185 190
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
195 200 205
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
210 215 220
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
225 230 235 240
Leu Met Thr Leu Arg Leu Trp Ser Ser
245
<210> 171
<211> 286
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 171
Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu Lys Thr Gly Gln Ser
1 5 10 15
Met Thr Leu Leu Cys Ala Gln Asp Met Asn His Glu Tyr Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu Ile His Tyr Ser Val
35 40 45
Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro Asp Gly Tyr Asn Val
50 55 60
Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly Leu Glu Ser Ala Ala
65 70 75 80
Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser Ser Tyr Ala Gly Leu
85 90 95
Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
100 105 110
Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
115 120 125
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
130 135 140
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
145 150 155 160
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
165 170 175
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
180 185 190
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
195 200 205
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
210 215 220
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
225 230 235 240
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
245 250 255
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
260 265 270
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
275 280 285
<210> 172
<211> 251
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 172
Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala
1 5 10 15
Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr
20 25 30
Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly
35 40 45
Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu
50 55 60
Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp
65 70 75 80
Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly
85 90 95
Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val
100 105 110
His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
115 120 125
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
130 135 140
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
145 150 155 160
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
165 170 175
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
180 185 190
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
195 200 205
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
210 215 220
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
225 230 235 240
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
245 250
<210> 173
<211> 281
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 173
Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg Lys Glu Gly Gln Asn
1 5 10 15
Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His Asp Ala Met Tyr Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu Ile Tyr Tyr Ser Gln
35 40 45
Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala Glu Gly Tyr Ser Val
50 55 60
Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr Val Thr Ser Ala Gln
65 70 75 80
Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr Arg Thr Gly Asn Glu
85 90 95
Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val Val Glu Asp Leu Arg
100 105 110
Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu
115 120 125
Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe
130 135 140
Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val
145 150 155 160
His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr
165 170 175
Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His
180 185 190
Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser
195 200 205
Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn
210 215 220
Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala
225 230 235 240
Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu
245 250 255
Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val
260 265 270
Met Ala Met Val Lys Arg Lys Asn Ser
275 280
<210> 174
<211> 253
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 174
Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val Ala Glu Gly Asn
1 5 10 15
Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly Asn Pro Tyr Leu
20 25 30
Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln Phe Leu Leu Lys
35 40 45
Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr Gly Phe Glu Ala
50 55 60
Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys Lys Pro Ser Ala
65 70 75 80
Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val Arg Asp Gly Ser
85 90 95
Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr Gly Thr Arg Leu
100 105 110
Lys Val Leu Ala Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu
115 120 125
Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe
130 135 140
Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile
145 150 155 160
Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn
165 170 175
Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile
180 185 190
Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp
195 200 205
Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe
210 215 220
Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala
225 230 235 240
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
245 250
<210> 175
<211> 286
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 175
Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr Lys Arg Gly
1 5 10 15
Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His Asn Arg Leu
20 25 30
Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe Leu Thr Tyr
35 40 45
Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu Ser Asp Arg
50 55 60
Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu Glu Ile Gln
65 70 75 80
Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala Ser Ser Pro
85 90 95
Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val
100 105 110
Thr Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
115 120 125
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
130 135 140
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
145 150 155 160
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
165 170 175
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
180 185 190
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
195 200 205
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
210 215 220
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
225 230 235 240
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
245 250 255
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
260 265 270
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
275 280 285
<210> 176
<211> 252
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 176
Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro Leu Ser Val Pro Glu
1 5 10 15
Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser Asn Ser Ala Phe Gln
20 25 30
Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys Gly Pro Glu Leu Leu
35 40 45
Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp Gly Arg Phe Thr Ala
50 55 60
Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu Phe Ile Arg Asp Ser
65 70 75 80
Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala Met Ser Gly Leu Lys
85 90 95
Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr Arg Leu Leu
100 105 110
Val Arg Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys
115 120 125
Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp
130 135 140
Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr
145 150 155 160
Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly
165 170 175
Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe
180 185 190
Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala
195 200 205
Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln
210 215 220
Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly
225 230 235 240
Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
245 250
<210> 177
<211> 284
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 177
Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys Lys
1 5 10 15
Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser Trp
20 25 30
Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser Met
35 40 45
Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys Val
50 55 60
Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro Ser
65 70 75 80
Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Ser Ile Gln Gln Gly
85 90 95
Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val Leu Glu
100 105 110
Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro Ser
115 120 125
Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu Ala
130 135 140
Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn Gly
145 150 155 160
Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys Glu
165 170 175
Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala Thr
180 185 190
Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe His
195 200 205
Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro Val
210 215 220
Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly Ile
225 230 235 240
Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu Tyr
245 250 255
Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser Thr
260 265 270
Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
275 280
<210> 178
<211> 126
<212> ПРТ
<213> Homo sapiens
<400> 178
Met Lys Leu Val Thr Ser Ile Thr Val Leu Leu Ser Leu Gly Ile Met
1 5 10 15
Gly Asp Ala Lys Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu
20 25 30
Glu Pro Val His Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp
35 40 45
Tyr Ile His Trp Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val
50 55 60
Ile His Gly Leu Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala
65 70 75 80
Ile Ala Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr
85 90 95
Leu Arg Asp Ala Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala
100 105 110
Arg Leu Met Phe Gly Asp Gly Thr Gln Leu Val Val Lys Pro
115 120 125
<210> 179
<211> 263
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 179
Met Lys Leu Val Thr Ser Ile Thr Val Leu Leu Ser Leu Gly Ile Met
1 5 10 15
Gly Asp Ala Lys Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu
20 25 30
Glu Pro Val His Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp
35 40 45
Tyr Ile His Trp Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val
50 55 60
Ile His Gly Leu Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala
65 70 75 80
Ile Ala Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr
85 90 95
Leu Arg Asp Ala Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala
100 105 110
Arg Leu Met Phe Gly Asp Gly Thr Gln Leu Val Val Lys Pro Asn Ile
115 120 125
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
130 135 140
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
145 150 155 160
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
165 170 175
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
180 185 190
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
195 200 205
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
210 215 220
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
225 230 235 240
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
245 250 255
Thr Leu Arg Leu Trp Ser Ser
260
<210> 180
<211> 595
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 180
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg
115 120 125
Leu Ser Ile Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
305 310 315 320
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Lys Leu Val
325 330 335
Thr Ser Ile Thr Val Leu Leu Ser Leu Gly Ile Met Gly Asp Ala Lys
340 345 350
Thr Thr Gln Pro Asn Ser Met Glu Ser Asn Glu Glu Glu Pro Val His
355 360 365
Leu Pro Cys Asn His Ser Thr Ile Ser Gly Thr Asp Tyr Ile His Trp
370 375 380
Tyr Arg Gln Leu Pro Ser Gln Gly Pro Glu Tyr Val Ile His Gly Leu
385 390 395 400
Thr Ser Asn Val Asn Asn Arg Met Ala Ser Leu Ala Ile Ala Glu Asp
405 410 415
Arg Lys Ser Ser Thr Leu Ile Leu His Arg Ala Thr Leu Arg Asp Ala
420 425 430
Ala Val Tyr Tyr Cys Ile Leu Arg Asp Asn Asn Ala Arg Leu Met Phe
435 440 445
Gly Asp Gly Thr Gln Leu Val Val Lys Pro Asn Ile Gln Asn Pro Glu
450 455 460
Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu
465 470 475 480
Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met
485 490 495
Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala
500 505 510
Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser
515 520 525
Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser
530 535 540
Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr
545 550 555 560
Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile
565 570 575
Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu
580 585 590
Trp Ser Ser
595
<210> 181
<211> 133
<212> ПРТ
<213> Homo sapiens
<400> 181
Met Arg Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro
130
<210> 182
<211> 270
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 182
Met Arg Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 183
<211> 601
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 183
Met Ala Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu
1 5 10 15
Gly Ala Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu
20 25 30
Phe Arg Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu
35 40 45
Asn His Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu
50 55 60
Arg Leu Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp
65 70 75 80
Ile Ala Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro
85 90 95
Leu Thr Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys
100 105 110
Ala Ser Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu
115 120 125
Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu
130 135 140
Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu
145 150 155 160
Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp
165 170 175
Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln
180 185 190
Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg
195 200 205
Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln
210 215 220
Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser
225 230 235 240
Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala
245 250 255
Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala
260 265 270
Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val
275 280 285
Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys
305 310 315 320
Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Arg Leu Val Ala
325 330 335
Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr
340 345 350
Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu
355 360 365
Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr
370 375 380
Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys
385 390 395 400
Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg
405 410 415
Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala
420 425 430
Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser
435 440 445
Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro
450 455 460
Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
465 470 475 480
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
485 490 495
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
500 505 510
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
515 520 525
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
530 535 540
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
545 550 555 560
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
565 570 575
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
580 585 590
Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 184
<211> 131
<212> ПРТ
<213> Homo sapiens
<400> 184
Met Ala Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu
1 5 10 15
Asn Ser Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro
20 25 30
Ser Thr Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn
35 40 45
His Ser Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro
50 55 60
Gly Cys Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln
65 70 75 80
Gly Arg Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile
85 90 95
Leu Gln Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Val Glu
100 105 110
Asp Arg Arg Arg Thr Ala Leu Ile Phe Gly Lys Gly Thr Thr Leu Ser
115 120 125
Val Ser Ser
130
<210> 185
<211> 268
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 185
Met Ala Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu
1 5 10 15
Asn Ser Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro
20 25 30
Ser Thr Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn
35 40 45
His Ser Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro
50 55 60
Gly Cys Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln
65 70 75 80
Gly Arg Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile
85 90 95
Leu Gln Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Val Glu
100 105 110
Asp Arg Arg Arg Thr Ala Leu Ile Phe Gly Lys Gly Thr Thr Leu Ser
115 120 125
Val Ser Ser Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys
130 135 140
Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp
145 150 155 160
Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr
165 170 175
Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly
180 185 190
Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe
195 200 205
Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala
210 215 220
Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln
225 230 235 240
Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly
245 250 255
Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 186
<211> 602
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 186
Met Ala Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser
305 310 315 320
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Ala
325 330 335
Leu Gln Ser Thr Leu Gly Ala Val Trp Leu Gly Leu Leu Leu Asn Ser
340 345 350
Leu Trp Lys Val Ala Glu Ser Lys Asp Gln Val Phe Gln Pro Ser Thr
355 360 365
Val Ala Ser Ser Glu Gly Ala Val Val Glu Ile Phe Cys Asn His Ser
370 375 380
Val Ser Asn Ala Tyr Asn Phe Phe Trp Tyr Leu His Phe Pro Gly Cys
385 390 395 400
Ala Pro Arg Leu Leu Val Lys Gly Ser Lys Pro Ser Gln Gln Gly Arg
405 410 415
Tyr Asn Met Thr Tyr Glu Arg Phe Ser Ser Ser Leu Leu Ile Leu Gln
420 425 430
Val Arg Glu Ala Asp Ala Ala Val Tyr Tyr Cys Ala Val Glu Asp Arg
435 440 445
Arg Arg Thr Ala Leu Ile Phe Gly Lys Gly Thr Thr Leu Ser Val Ser
450 455 460
Ser Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro
465 470 475 480
Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln
485 490 495
Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys
500 505 510
Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile
515 520 525
Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu
530 535 540
Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu
545 550 555 560
Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu
565 570 575
Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn
580 585 590
Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 187
<211> 133
<212> ПРТ
<213> Homo sapiens
<400> 187
Met Arg Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Gly Ser Pro Gly
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro
130
<210> 188
<211> 270
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 188
Met Arg Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Gly Ser Pro Gly
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 189
<211> 599
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 189
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Ile Arg Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser Arg Ala
290 295 300
Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
305 310 315 320
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Arg Leu Val Ala Arg Val
325 330 335
Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr Thr Gln
340 345 350
Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu Pro Cys
355 360 365
Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr Arg Gln
370 375 380
Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys Asn Asn
385 390 395 400
Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg Lys Ser
405 410 415
Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala Val Tyr
420 425 430
Tyr Cys Ile Val Arg Gly Ser Pro Gly Ala Gly Gly Thr Ser Tyr Gly
435 440 445
Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asn Ile
450 455 460
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
465 470 475 480
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
485 490 495
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
500 505 510
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
515 520 525
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
530 535 540
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
545 550 555 560
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
565 570 575
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
580 585 590
Thr Leu Arg Leu Trp Ser Ser
595
<210> 190
<211> 130
<212> ПРТ
<213> Homo sapiens
<400> 190
Met Leu Leu Ile Thr Ser Met Leu Val Leu Trp Met Gln Leu Ser Gln
1 5 10 15
Val Asn Gly Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln
20 25 30
Glu Gly Glu Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser
35 40 45
Asn Ile Gln Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu
50 55 60
Ile Gln Leu Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr
65 70 75 80
Phe Gln Phe Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala
85 90 95
Thr Gln Thr Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly
100 105 110
Ala Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val
115 120 125
Ile Pro
130
<210> 191
<211> 267
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 191
Met Leu Leu Ile Thr Ser Met Leu Val Leu Trp Met Gln Leu Ser Gln
1 5 10 15
Val Asn Gly Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln
20 25 30
Glu Gly Glu Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser
35 40 45
Asn Ile Gln Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu
50 55 60
Ile Gln Leu Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr
65 70 75 80
Phe Gln Phe Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala
85 90 95
Thr Gln Thr Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly
100 105 110
Ala Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val
115 120 125
Ile Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
130 135 140
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
145 150 155 160
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
165 170 175
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
180 185 190
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
195 200 205
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
210 215 220
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 192
<211> 602
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 192
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro
115 120 125
Gly Thr Arg Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro
130 135 140
Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys
180 185 190
Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp
225 230 235 240
Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys
290 295 300
Arg Lys Asn Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe
305 310 315 320
Ser Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met
325 330 335
Leu Leu Ile Thr Ser Met Leu Val Leu Trp Met Gln Leu Ser Gln Val
340 345 350
Asn Gly Gln Gln Val Met Gln Ile Pro Gln Tyr Gln His Val Gln Glu
355 360 365
Gly Glu Asp Phe Thr Thr Tyr Cys Asn Ser Ser Thr Thr Leu Ser Asn
370 375 380
Ile Gln Trp Tyr Lys Gln Arg Pro Gly Gly His Pro Val Phe Leu Ile
385 390 395 400
Gln Leu Val Lys Ser Gly Glu Val Lys Lys Gln Lys Arg Leu Thr Phe
405 410 415
Gln Phe Gly Glu Ala Lys Lys Asn Ser Ser Leu His Ile Thr Ala Thr
420 425 430
Gln Thr Thr Asp Val Gly Thr Tyr Phe Cys Ala Gly Pro Gly Gly Ala
435 440 445
Gly Ser Tyr Gln Leu Thr Phe Gly Lys Gly Thr Lys Leu Ser Val Ile
450 455 460
Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro
465 470 475 480
Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln
485 490 495
Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys
500 505 510
Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile
515 520 525
Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu
530 535 540
Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu
545 550 555 560
Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu
565 570 575
Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn
580 585 590
Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 193
<211> 130
<212> ПРТ
<213> Homo sapiens
<400> 193
Met Lys Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu
1 5 10 15
Ser Gly Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln
20 25 30
Glu Gly Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp
35 40 45
Arg Leu Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu
50 55 60
Phe Val Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met
65 70 75 80
Ala Ser Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala
85 90 95
Ala Val His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met
100 105 110
Asp Ser Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile
115 120 125
Lys Pro
130
<210> 194
<211> 267
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 194
Met Lys Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu
1 5 10 15
Ser Gly Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln
20 25 30
Glu Gly Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp
35 40 45
Arg Leu Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu
50 55 60
Phe Val Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met
65 70 75 80
Ala Ser Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala
85 90 95
Ala Val His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met
100 105 110
Asp Ser Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile
115 120 125
Lys Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp
130 135 140
Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser
145 150 155 160
Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp
165 170 175
Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala
180 185 190
Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys
195 200 205
Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr
210 215 220
Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn
225 230 235 240
Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe
245 250 255
Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265
<210> 195
<211> 601
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 195
Met Ala Leu Gly Leu Leu Cys Cys Gly Ala Phe Ser Leu Leu Trp Ala
1 5 10 15
Gly Pro Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu
20 25 30
Lys Thr Gly Gln Ser Met Thr Leu Leu Cys Ala Gln Asp Met Asn His
35 40 45
Glu Tyr Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu
50 55 60
Ile His Tyr Ser Val Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro
65 70 75 80
Asp Gly Tyr Asn Val Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly
85 90 95
Leu Glu Ser Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser
100 105 110
Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser
305 310 315 320
Leu Leu Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Lys
325 330 335
Lys Leu Leu Ala Met Ile Leu Trp Leu Gln Leu Asp Arg Leu Ser Gly
340 345 350
Glu Leu Lys Val Glu Gln Asn Pro Leu Phe Leu Ser Met Gln Glu Gly
355 360 365
Lys Asn Tyr Thr Ile Tyr Cys Asn Tyr Ser Thr Thr Ser Asp Arg Leu
370 375 380
Tyr Trp Tyr Arg Gln Asp Pro Gly Lys Ser Leu Glu Ser Leu Phe Val
385 390 395 400
Leu Leu Ser Asn Gly Ala Val Lys Gln Glu Gly Arg Leu Met Ala Ser
405 410 415
Leu Asp Thr Lys Ala Arg Leu Ser Thr Leu His Ile Thr Ala Ala Val
420 425 430
His Asp Leu Ser Ala Thr Tyr Phe Cys Ala Val Ala His Met Asp Ser
435 440 445
Asn Tyr Gln Leu Ile Trp Gly Ala Gly Thr Lys Leu Ile Ile Lys Pro
450 455 460
Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg
465 470 475 480
Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile
485 490 495
Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys
500 505 510
Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala
515 520 525
Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr
530 535 540
Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr
545 550 555 560
Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu
565 570 575
Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu
580 585 590
Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600
<210> 196
<211> 133
<212> ПРТ
<213> Homo sapiens
<400> 196
Met Arg Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro
130
<210> 197
<211> 270
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 197
Met Arg Leu Val Ala Arg Val Thr Val Phe Leu Thr Phe Gly Thr Ile
1 5 10 15
Ile Asp Ala Lys Thr Thr Gln Pro Pro Ser Met Asp Cys Ala Glu Gly
20 25 30
Arg Ala Ala Asn Leu Pro Cys Asn His Ser Thr Ile Ser Gly Asn Glu
35 40 45
Tyr Val Tyr Trp Tyr Arg Gln Ile His Ser Gln Gly Pro Gln Tyr Ile
50 55 60
Ile His Gly Leu Lys Asn Asn Glu Thr Asn Glu Met Ala Ser Leu Ile
65 70 75 80
Ile Thr Glu Asp Arg Lys Ser Ser Thr Leu Ile Leu Pro His Ala Thr
85 90 95
Leu Arg Asp Thr Ala Val Tyr Tyr Cys Ile Val Arg Ala Arg Ala Asn
100 105 110
Ala Gly Gly Thr Ser Tyr Gly Lys Leu Thr Phe Gly Gln Gly Thr Ile
115 120 125
Leu Thr Val His Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln
130 135 140
Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp
145 150 155 160
Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe
165 170 175
Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser
180 185 190
Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp
195 200 205
Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys
210 215 220
Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn
225 230 235 240
Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val
245 250 255
Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
260 265 270
<210> 198
<211> 599
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 198
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr
100 105 110
Arg Thr Gly Asn Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser Arg Ala
290 295 300
Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
305 310 315 320
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Arg Leu Val Ala Arg Val
325 330 335
Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr Thr Gln
340 345 350
Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu Pro Cys
355 360 365
Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr Arg Gln
370 375 380
Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys Asn Asn
385 390 395 400
Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg Lys Ser
405 410 415
Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala Val Tyr
420 425 430
Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser Tyr Gly
435 440 445
Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asn Ile
450 455 460
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
465 470 475 480
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
485 490 495
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
500 505 510
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
515 520 525
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
530 535 540
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
545 550 555 560
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
565 570 575
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
580 585 590
Thr Leu Arg Leu Trp Ser Ser
595
<210> 199
<211> 136
<212> ПРТ
<213> Homo sapiens
<400> 199
Met Ala Ser Ala Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser
1 5 10 15
Gly Leu Arg Ala Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val
20 25 30
Ala Glu Gly Asn Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly
35 40 45
Asn Pro Tyr Leu Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln
50 55 60
Phe Leu Leu Lys Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr
65 70 75 80
Gly Phe Glu Ala Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys
85 90 95
Lys Pro Ser Ala Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val
100 105 110
Arg Asp Gly Ser Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr
115 120 125
Gly Thr Arg Leu Lys Val Leu Ala
130 135
<210> 200
<211> 273
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 200
Met Ala Ser Ala Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser
1 5 10 15
Gly Leu Arg Ala Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val
20 25 30
Ala Glu Gly Asn Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly
35 40 45
Asn Pro Tyr Leu Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln
50 55 60
Phe Leu Leu Lys Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr
65 70 75 80
Gly Phe Glu Ala Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys
85 90 95
Lys Pro Ser Ala Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val
100 105 110
Arg Asp Gly Ser Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr
115 120 125
Gly Thr Arg Leu Lys Val Leu Ala Asn Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 201
<211> 605
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 201
Met Ala Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
305 310 315 320
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Ala Ser Ala
325 330 335
Pro Ile Ser Met Leu Ala Met Leu Phe Thr Leu Ser Gly Leu Arg Ala
340 345 350
Gln Ser Val Ala Gln Pro Glu Asp Gln Val Asn Val Ala Glu Gly Asn
355 360 365
Pro Leu Thr Val Lys Cys Thr Tyr Ser Val Ser Gly Asn Pro Tyr Leu
370 375 380
Phe Trp Tyr Val Gln Tyr Pro Asn Arg Gly Leu Gln Phe Leu Leu Lys
385 390 395 400
Tyr Ile Thr Gly Asp Asn Leu Val Lys Gly Ser Tyr Gly Phe Glu Ala
405 410 415
Glu Phe Asn Lys Ser Gln Thr Ser Phe His Leu Lys Lys Pro Ser Ala
420 425 430
Leu Val Ser Asp Ser Ala Leu Tyr Phe Cys Ala Val Arg Asp Gly Ser
435 440 445
Ala Thr Ser Gly Thr Tyr Lys Tyr Ile Phe Gly Thr Gly Thr Arg Leu
450 455 460
Lys Val Leu Ala Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu
465 470 475 480
Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe
485 490 495
Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile
500 505 510
Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn
515 520 525
Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile
530 535 540
Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp
545 550 555 560
Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe
565 570 575
Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala
580 585 590
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600 605
<210> 202
<211> 132
<212> ПРТ
<213> Homo sapiens
<400> 202
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu
130
<210> 203
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 203
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 204
<211> 605
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 204
Met Ala Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asn Ser Ala Phe Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys
50 55 60
Gly Pro Glu Leu Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu
85 90 95
Phe Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser
115 120 125
Gly Thr Arg Leu Leu Val Arg Pro Asn Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
275 280 285
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Gly Pro Gln
290 295 300
Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala Gly Pro Leu Glu
305 310 315 320
Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr Val Thr Gly Lys
325 330 335
Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His Glu Tyr Met Ser
340 345 350
Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln Ile Tyr Tyr Ser
355 360 365
Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro Glu Gly Tyr Lys
370 375 380
Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile Leu Glu Ser Pro
385 390 395 400
Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser Ser Ile Gln Gln
405 410 415
Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg Leu Thr Val Leu
420 425 430
Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu Pro
435 440 445
Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys Leu
450 455 460
Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val Asn
465 470 475 480
Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr Lys
485 490 495
Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser Ala
500 505 510
Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln Phe
515 520 525
His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys Pro
530 535 540
Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys Gly
545 550 555 560
Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile Leu
565 570 575
Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val Ser
580 585 590
Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
595 600 605
<210> 205
<211> 132
<212> ПРТ
<213> Homo sapiens
<400> 205
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg
115 120 125
Leu Ser Ile Leu
130
<210> 206
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 206
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Gly Leu Val Gly Phe Asn Gln Pro Gln His Phe Gly Asp Gly Thr Arg
115 120 125
Leu Ser Ile Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 207
<211> 129
<212> ПРТ
<213> Homo sapiens
<400> 207
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Leu
<210> 208
<211> 302
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 208
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 209
<211> 134
<212> ПРТ
<213> Homo sapiens
<400> 209
Met Asp Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu
130
<210> 210
<211> 307
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 210
Met Asp Thr Trp Leu Val Cys Trp Ala Ile Phe Ser Leu Leu Lys Ala
1 5 10 15
Gly Leu Thr Glu Pro Glu Val Thr Gln Thr Pro Ser His Gln Val Thr
20 25 30
Gln Met Gly Gln Glu Val Ile Leu Arg Cys Val Pro Ile Ser Asn His
35 40 45
Leu Tyr Phe Tyr Trp Tyr Arg Gln Ile Leu Gly Gln Lys Val Glu Phe
50 55 60
Leu Val Ser Phe Tyr Asn Asn Glu Ile Ser Glu Lys Ser Glu Ile Phe
65 70 75 80
Asp Asp Gln Phe Ser Val Glu Arg Pro Asp Gly Ser Asn Phe Thr Leu
85 90 95
Lys Ile Arg Ser Thr Lys Leu Glu Asp Ser Ala Met Tyr Phe Cys Ala
100 105 110
Ser Ser Glu Tyr Gln Ser Gln Ser Asn Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser
305
<210> 211
<211> 129
<212> ПРТ
<213> Homo sapiens
<400> 211
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Ile Arg Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val
<210> 212
<211> 302
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 212
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Ser Ile Arg Thr Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 213
<211> 135
<212> ПРТ
<213> Homo sapiens
<400> 213
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro
115 120 125
Gly Thr Arg Leu Thr Val Thr
130 135
<210> 214
<211> 308
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 214
Met Gly Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Pro Phe Val Val Ile Gly Gln Ile Asn Glu Gln Tyr Phe Gly Pro
115 120 125
Gly Thr Arg Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro
130 135 140
Lys Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln
145 150 155 160
Lys Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val
165 170 175
Glu Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys
180 185 190
Thr Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser
195 200 205
Ser Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His
210 215 220
Phe Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp
225 230 235 240
Pro Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala
245 250 255
Trp Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly
260 265 270
Val Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr
275 280 285
Leu Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys
290 295 300
Arg Lys Asn Ser
305
<210> 215
<211> 134
<212> ПРТ
<213> Homo sapiens
<400> 215
Met Ser Leu Gly Leu Leu Cys Cys Gly Ala Phe Ser Leu Leu Trp Ala
1 5 10 15
Gly Pro Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu
20 25 30
Lys Thr Gly Gln Ser Met Thr Leu Leu Cys Ala Gln Asp Met Asn His
35 40 45
Glu Tyr Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu
50 55 60
Ile His Tyr Ser Val Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro
65 70 75 80
Asp Gly Tyr Asn Val Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly
85 90 95
Leu Glu Ser Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser
100 105 110
Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu
130
<210> 216
<211> 307
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 216
Met Ser Leu Gly Leu Leu Cys Cys Gly Ala Phe Ser Leu Leu Trp Ala
1 5 10 15
Gly Pro Val Asn Ala Gly Val Thr Gln Thr Pro Lys Phe Arg Val Leu
20 25 30
Lys Thr Gly Gln Ser Met Thr Leu Leu Cys Ala Gln Asp Met Asn His
35 40 45
Glu Tyr Met Tyr Trp Tyr Arg Gln Asp Pro Gly Met Gly Leu Arg Leu
50 55 60
Ile His Tyr Ser Val Gly Glu Gly Thr Thr Ala Lys Gly Glu Val Pro
65 70 75 80
Asp Gly Tyr Asn Val Ser Arg Leu Lys Lys Gln Asn Phe Leu Leu Gly
85 90 95
Leu Glu Ser Ala Ala Pro Ser Gln Thr Ser Val Tyr Phe Cys Ala Ser
100 105 110
Ser Tyr Ala Gly Leu Ala Ala Pro Arg Glu Gln Phe Phe Gly Pro Gly
115 120 125
Thr Arg Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys
130 135 140
Val Ser Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys
145 150 155 160
Ala Thr Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu
165 170 175
Leu Ser Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr
180 185 190
Asp Pro Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser
195 200 205
Arg Leu Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe
210 215 220
Arg Cys Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro
225 230 235 240
Glu Gly Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp
245 250 255
Gly Arg Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val
260 265 270
Leu Ser Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu
275 280 285
Tyr Ala Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg
290 295 300
Lys Asn Ser
305
<210> 217
<211> 129
<212> ПРТ
<213> Homo sapiens
<400> 217
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr
100 105 110
Arg Thr Gly Asn Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val
<210> 218
<211> 302
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 218
Met Ser Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Thr
100 105 110
Arg Thr Gly Asn Glu Ala Phe Phe Gly Gln Gly Thr Arg Leu Thr Val
115 120 125
Val Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 219
<211> 132
<212> ПРТ
<213> Homo sapiens
<400> 219
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr
130
<210> 220
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 220
Met Gly Thr Ser Leu Leu Cys Trp Met Ala Leu Cys Leu Leu Gly Ala
1 5 10 15
Asp His Ala Asp Thr Gly Val Ser Gln Asp Pro Arg His Lys Ile Thr
20 25 30
Lys Arg Gly Gln Asn Val Thr Phe Arg Cys Asp Pro Ile Ser Glu His
35 40 45
Asn Arg Leu Tyr Trp Tyr Arg Gln Thr Leu Gly Gln Gly Pro Glu Phe
50 55 60
Leu Thr Tyr Phe Gln Asn Glu Ala Gln Leu Glu Lys Ser Arg Leu Leu
65 70 75 80
Ser Asp Arg Phe Ser Ala Glu Arg Pro Lys Gly Ser Phe Ser Thr Leu
85 90 95
Glu Ile Gln Arg Thr Glu Gln Gly Asp Ser Ala Met Tyr Leu Cys Ala
100 105 110
Ser Ser Pro Gly Leu Ala Tyr Glu Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Thr Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 221
<211> 132
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 221
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu
130
<210> 222
<211> 305
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 222
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser
305
<210> 223
<211> 136
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 223
Met Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asn Ser Ala Phe Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys
50 55 60
Gly Pro Glu Leu Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu
85 90 95
Phe Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser
115 120 125
Gly Thr Arg Leu Leu Val Arg Pro
130 135
<210> 224
<211> 273
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 224
Met Met Lys Ser Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu
1 5 10 15
Ser Trp Val Trp Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro
20 25 30
Leu Ser Val Pro Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser
35 40 45
Asn Ser Ala Phe Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys
50 55 60
Gly Pro Glu Leu Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp
65 70 75 80
Gly Arg Phe Thr Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu
85 90 95
Phe Ile Arg Asp Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala
100 105 110
Met Ser Gly Leu Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser
115 120 125
Gly Thr Arg Leu Leu Val Arg Pro Asn Ile Gln Asn Pro Glu Pro Ala
130 135 140
Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu
145 150 155 160
Phe Thr Asp Phe Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser
165 170 175
Gly Thr Phe Ile Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp
180 185 190
Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr
195 200 205
Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp
210 215 220
Val Pro Cys Asp Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met
225 230 235 240
Asn Leu Asn Phe Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu
245 250 255
Leu Lys Val Ala Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser
260 265 270
Ser
<210> 225
<211> 605
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 225
Met Ala Pro Gln Leu Leu Gly Tyr Val Val Leu Cys Leu Leu Gly Ala
1 5 10 15
Gly Pro Leu Glu Ala Gln Val Thr Gln Asn Pro Arg Tyr Leu Ile Thr
20 25 30
Val Thr Gly Lys Lys Leu Thr Val Thr Cys Ser Gln Asn Met Asn His
35 40 45
Glu Tyr Met Ser Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Gln
50 55 60
Ile Tyr Tyr Ser Met Asn Val Glu Val Thr Asp Lys Gly Asp Val Pro
65 70 75 80
Glu Gly Tyr Lys Val Ser Arg Lys Glu Lys Arg Asn Phe Pro Leu Ile
85 90 95
Leu Glu Ser Pro Ser Pro Asn Gln Thr Ser Leu Tyr Phe Cys Ala Ser
100 105 110
Ser Ile Gln Gln Gly Ala Asp Thr Gln Tyr Phe Gly Pro Gly Thr Arg
115 120 125
Leu Thr Val Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser
130 135 140
Leu Phe Glu Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr
145 150 155 160
Leu Val Cys Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser
165 170 175
Trp Trp Val Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro
180 185 190
Gln Ala Tyr Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu
195 200 205
Arg Val Ser Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys
210 215 220
Gln Val Gln Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly
225 230 235 240
Ser Pro Lys Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg
245 250 255
Ala Asp Cys Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser
260 265 270
Ala Thr Ile Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala
275 280 285
Val Leu Val Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn
290 295 300
Ser Arg Ala Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu
305 310 315 320
Lys Gln Ala Gly Asp Val Glu Glu Asn Pro Gly Pro Met Met Lys Ser
325 330 335
Leu Arg Val Leu Leu Val Ile Leu Trp Leu Gln Leu Ser Trp Val Trp
340 345 350
Ser Gln Gln Lys Glu Val Glu Gln Asp Pro Gly Pro Leu Ser Val Pro
355 360 365
Glu Gly Ala Ile Val Ser Leu Asn Cys Thr Tyr Ser Asn Ser Ala Phe
370 375 380
Gln Tyr Phe Met Trp Tyr Arg Gln Tyr Ser Arg Lys Gly Pro Glu Leu
385 390 395 400
Leu Met Tyr Thr Tyr Ser Ser Gly Asn Lys Glu Asp Gly Arg Phe Thr
405 410 415
Ala Gln Val Asp Lys Ser Ser Lys Tyr Ile Ser Leu Phe Ile Arg Asp
420 425 430
Ser Gln Pro Ser Asp Ser Ala Thr Tyr Leu Cys Ala Met Ser Gly Leu
435 440 445
Lys Glu Asp Ser Ser Tyr Lys Leu Ile Phe Gly Ser Gly Thr Arg Leu
450 455 460
Leu Val Arg Pro Asn Ile Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu
465 470 475 480
Lys Asp Pro Arg Ser Gln Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe
485 490 495
Asp Ser Gln Ile Asn Val Pro Lys Thr Met Glu Ser Gly Thr Phe Ile
500 505 510
Thr Asp Lys Cys Val Leu Asp Met Lys Ala Met Asp Ser Lys Ser Asn
515 520 525
Gly Ala Ile Ala Trp Ser Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile
530 535 540
Phe Lys Glu Thr Asn Ala Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp
545 550 555 560
Ala Thr Leu Thr Glu Lys Ser Phe Glu Thr Asp Met Asn Leu Asn Phe
565 570 575
Gln Asn Leu Leu Val Ile Val Leu Arg Ile Leu Leu Leu Lys Val Ala
580 585 590
Gly Phe Asn Leu Leu Met Thr Leu Arg Leu Trp Ser Ser
595 600 605
<210> 226
<211> 129
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 226
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Leu
<210> 227
<211> 302
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 227
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser
290 295 300
<210> 228
<211> 599
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 228
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser Arg Ala
290 295 300
Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
305 310 315 320
Gly Asp Val Glu Glu Asn Pro Gly Pro Met His Leu Val Ala Arg Val
325 330 335
Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr Thr Gln
340 345 350
Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu Pro Cys
355 360 365
Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr Arg Gln
370 375 380
Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys Asn Asn
385 390 395 400
Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg Lys Ser
405 410 415
Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala Val Tyr
420 425 430
Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser Tyr Gly
435 440 445
Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asn Ile
450 455 460
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
465 470 475 480
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
485 490 495
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
500 505 510
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
515 520 525
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
530 535 540
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
545 550 555 560
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
565 570 575
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
580 585 590
Thr Leu Arg Leu Trp Ser Ser
595
<210> 229
<211> 599
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 229
Met Ala Asn Gln Val Leu Cys Cys Val Val Leu Cys Phe Leu Gly Ala
1 5 10 15
Asn Thr Val Asp Gly Gly Ile Thr Gln Ser Pro Lys Tyr Leu Phe Arg
20 25 30
Lys Glu Gly Gln Asn Val Thr Leu Ser Cys Glu Gln Asn Leu Asn His
35 40 45
Asp Ala Met Tyr Trp Tyr Arg Gln Asp Pro Gly Gln Gly Leu Arg Leu
50 55 60
Ile Tyr Tyr Ser Gln Ile Val Asn Asp Phe Gln Lys Gly Asp Ile Ala
65 70 75 80
Glu Gly Tyr Ser Val Ser Arg Glu Lys Lys Glu Ser Phe Pro Leu Thr
85 90 95
Val Thr Ser Ala Gln Lys Asn Pro Thr Ala Phe Tyr Leu Cys Ala Ser
100 105 110
Leu Gln Phe Asn Glu Gln Phe Phe Gly Pro Gly Thr Arg Leu Thr Val
115 120 125
Leu Glu Asp Leu Arg Asn Val Thr Pro Pro Lys Val Ser Leu Phe Glu
130 135 140
Pro Ser Lys Ala Glu Ile Ala Asn Lys Gln Lys Ala Thr Leu Val Cys
145 150 155 160
Leu Ala Arg Gly Phe Phe Pro Asp His Val Glu Leu Ser Trp Trp Val
165 170 175
Asn Gly Lys Glu Val His Ser Gly Val Cys Thr Asp Pro Gln Ala Tyr
180 185 190
Lys Glu Ser Asn Tyr Ser Tyr Cys Leu Ser Ser Arg Leu Arg Val Ser
195 200 205
Ala Thr Phe Trp His Asn Pro Arg Asn His Phe Arg Cys Gln Val Gln
210 215 220
Phe His Gly Leu Ser Glu Glu Asp Lys Trp Pro Glu Gly Ser Pro Lys
225 230 235 240
Pro Val Thr Gln Asn Ile Ser Ala Glu Ala Trp Gly Arg Ala Asp Cys
245 250 255
Gly Ile Thr Ser Ala Ser Tyr Gln Gln Gly Val Leu Ser Ala Thr Ile
260 265 270
Leu Tyr Glu Ile Leu Leu Gly Lys Ala Thr Leu Tyr Ala Val Leu Val
275 280 285
Ser Thr Leu Val Val Met Ala Met Val Lys Arg Lys Asn Ser Arg Ala
290 295 300
Lys Arg Ser Gly Ser Gly Ala Thr Asn Phe Ser Leu Leu Lys Gln Ala
305 310 315 320
Gly Asp Val Glu Glu Asn Pro Gly Pro Met Arg Leu Val Ala Arg Val
325 330 335
Thr Val Phe Leu Thr Phe Gly Thr Ile Ile Asp Ala Lys Thr Thr Gln
340 345 350
Pro Pro Ser Met Asp Cys Ala Glu Gly Arg Ala Ala Asn Leu Pro Cys
355 360 365
Asn His Ser Thr Ile Ser Gly Asn Glu Tyr Val Tyr Trp Tyr Arg Gln
370 375 380
Ile His Ser Gln Gly Pro Gln Tyr Ile Ile His Gly Leu Lys Asn Asn
385 390 395 400
Glu Thr Asn Glu Met Ala Ser Leu Ile Ile Thr Glu Asp Arg Lys Ser
405 410 415
Ser Thr Leu Ile Leu Pro His Ala Thr Leu Arg Asp Thr Ala Val Tyr
420 425 430
Tyr Cys Ile Val Arg Ala Arg Ala Asn Ala Gly Gly Thr Ser Tyr Gly
435 440 445
Lys Leu Thr Phe Gly Gln Gly Thr Ile Leu Thr Val His Pro Asn Ile
450 455 460
Gln Asn Pro Glu Pro Ala Val Tyr Gln Leu Lys Asp Pro Arg Ser Gln
465 470 475 480
Asp Ser Thr Leu Cys Leu Phe Thr Asp Phe Asp Ser Gln Ile Asn Val
485 490 495
Pro Lys Thr Met Glu Ser Gly Thr Phe Ile Thr Asp Lys Cys Val Leu
500 505 510
Asp Met Lys Ala Met Asp Ser Lys Ser Asn Gly Ala Ile Ala Trp Ser
515 520 525
Asn Gln Thr Ser Phe Thr Cys Gln Asp Ile Phe Lys Glu Thr Asn Ala
530 535 540
Thr Tyr Pro Ser Ser Asp Val Pro Cys Asp Ala Thr Leu Thr Glu Lys
545 550 555 560
Ser Phe Glu Thr Asp Met Asn Leu Asn Phe Gln Asn Leu Leu Val Ile
565 570 575
Val Leu Arg Ile Leu Leu Leu Lys Val Ala Gly Phe Asn Leu Leu Met
580 585 590
Thr Leu Arg Leu Trp Ser Ser
595
<210> 230
<211> 4
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Синтетический
<400> 230
Arg Ala Lys Arg
1
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ВАКЦИНА И СПОСОБЫ ОБНАРУЖЕНИЯ И ПРОФИЛАКТИКИ ФИЛЯРИОЗА | 2021 |
|
RU2832185C1 |
| CD20 ТЕРАПИЯ, CD22 ТЕРАПИЯ И КОМБИНИРОВАННАЯ ТЕРАПИЯ КЛЕТКАМИ, ЭКСПРЕССИРУЮЩИМИ ХИМЕРНЫЙ АНТИГЕННЫЙ РЕЦЕПТОР (CAR) K CD19 | 2016 |
|
RU2752918C2 |
| ХИМЕРНЫЕ РЕЦЕПТОРЫ АНТИГЕНА ПРОТИВ МЕЗОТЕЛИНА ЧЕЛОВЕКА И ИХ ПРИМЕНЕНИЕ | 2014 |
|
RU2714902C2 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ | 2016 |
|
RU2770001C2 |
| МАТЕРИАЛЫ И МЕТОДЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ У СОБАК | 2020 |
|
RU2811752C2 |
| НЕ ВСТРЕЧАЮЩИЙСЯ В ПРИРОДЕ ВИРУС РЕПРОДУКТИВНО-РЕСПИРАТОРНОГО СИНДРОМА СВИНЕЙ (BPPCC) И СПОСОБЫ ПРИМЕНЕНИЯ | 2015 |
|
RU2687150C2 |
| Т-КЛЕТКИ, МОДИФИЦИРОВАННЫЕ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, НАЦЕЛЕННЫМ НА CS1, ДЛЯ ЛЕЧЕНИЯ АМИЛОИДОЗА AL | 2018 |
|
RU2774895C2 |
| Т-КЛЕТКИ, МОДИФИЦИРОВАННЫЕ ХИМЕРНЫМ РЕЦЕПТОРОМ АНТИГЕНА, НАЦЕЛЕННЫМ НА CS1 | 2015 |
|
RU2727451C2 |
| КОНСТРУКЦИИ ДНК-АНТИТЕЛ ДЛЯ ПРИМЕНЕНИЯ ПРОТИВ БОЛЕЗНИ ЛАЙМА | 2017 |
|
RU2813829C2 |
| КОМПОЗИЦИИ И СПОСОБЫ РЕДАКТИРОВАНИЯ ГЕНОВ | 2019 |
|
RU2804665C2 |
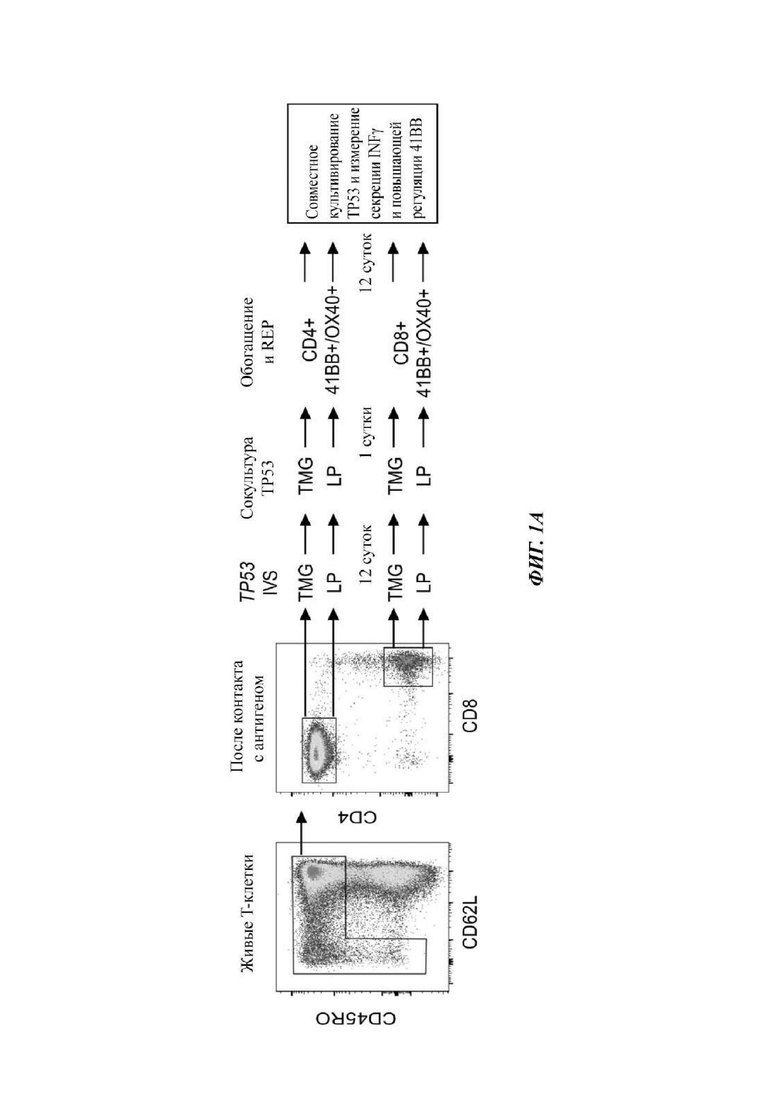
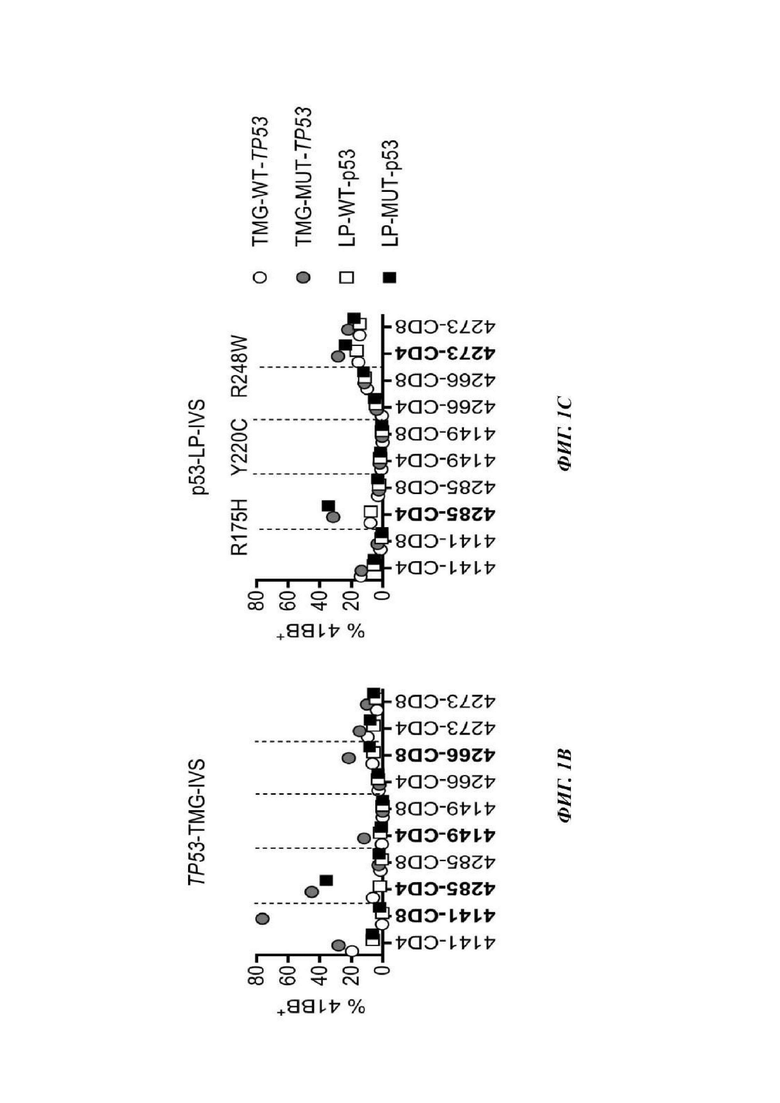
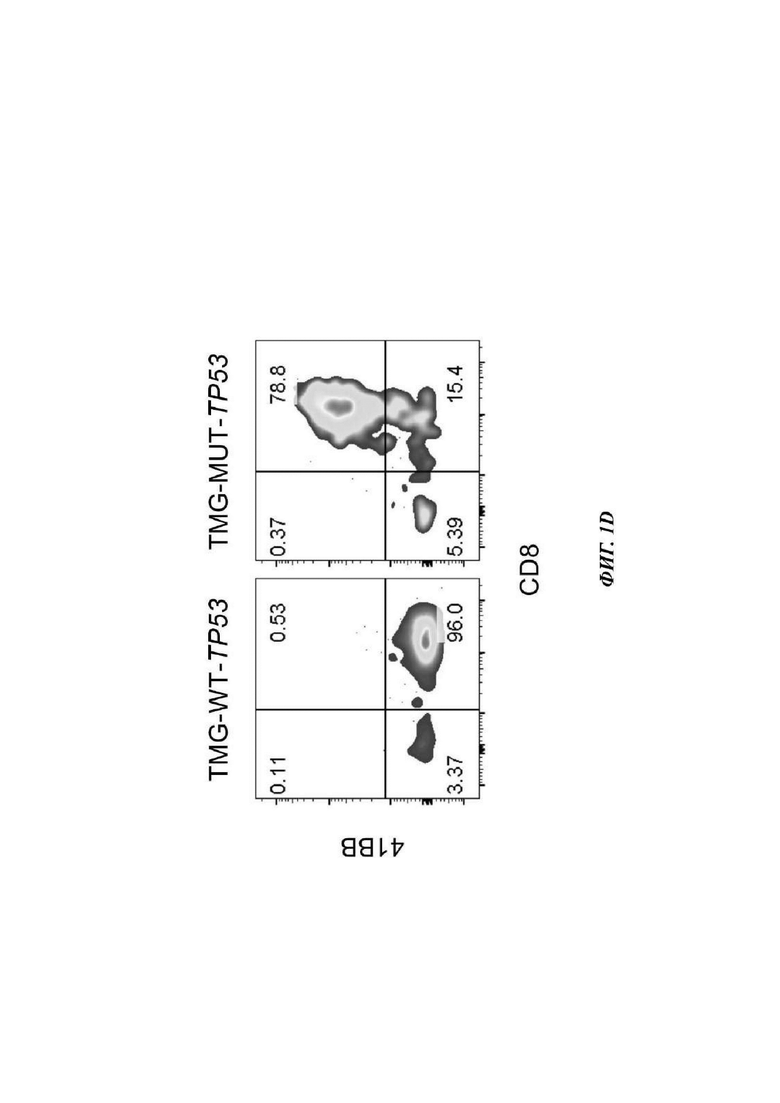
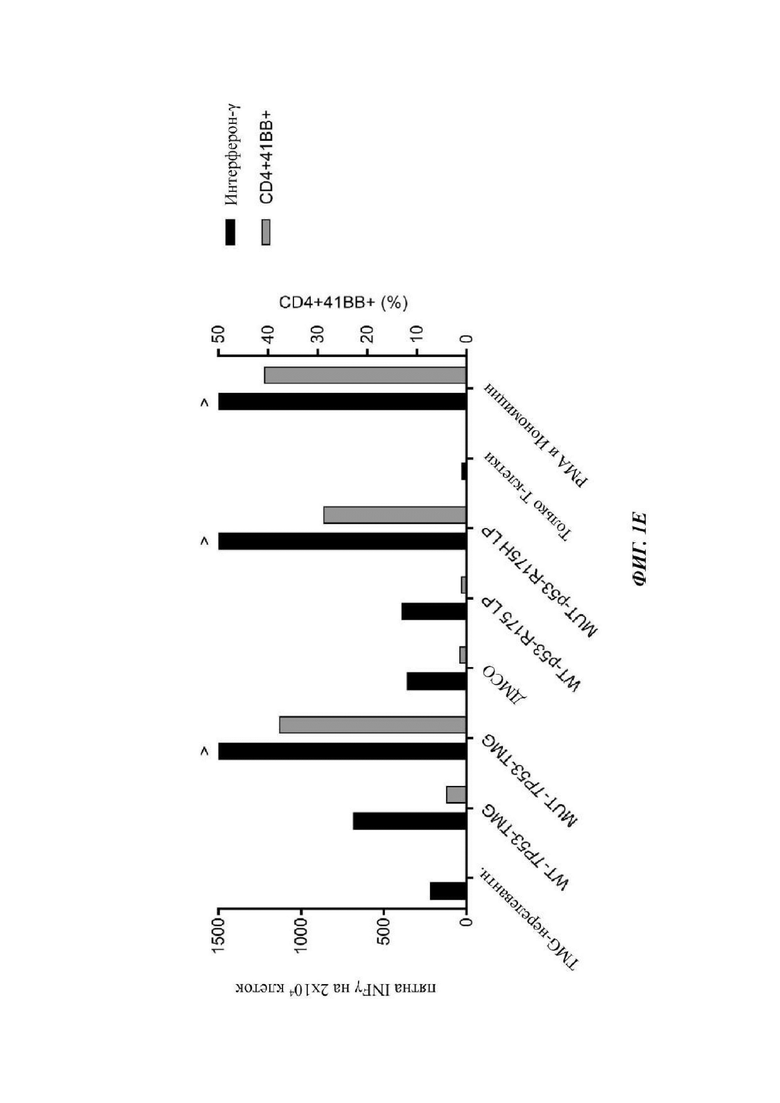
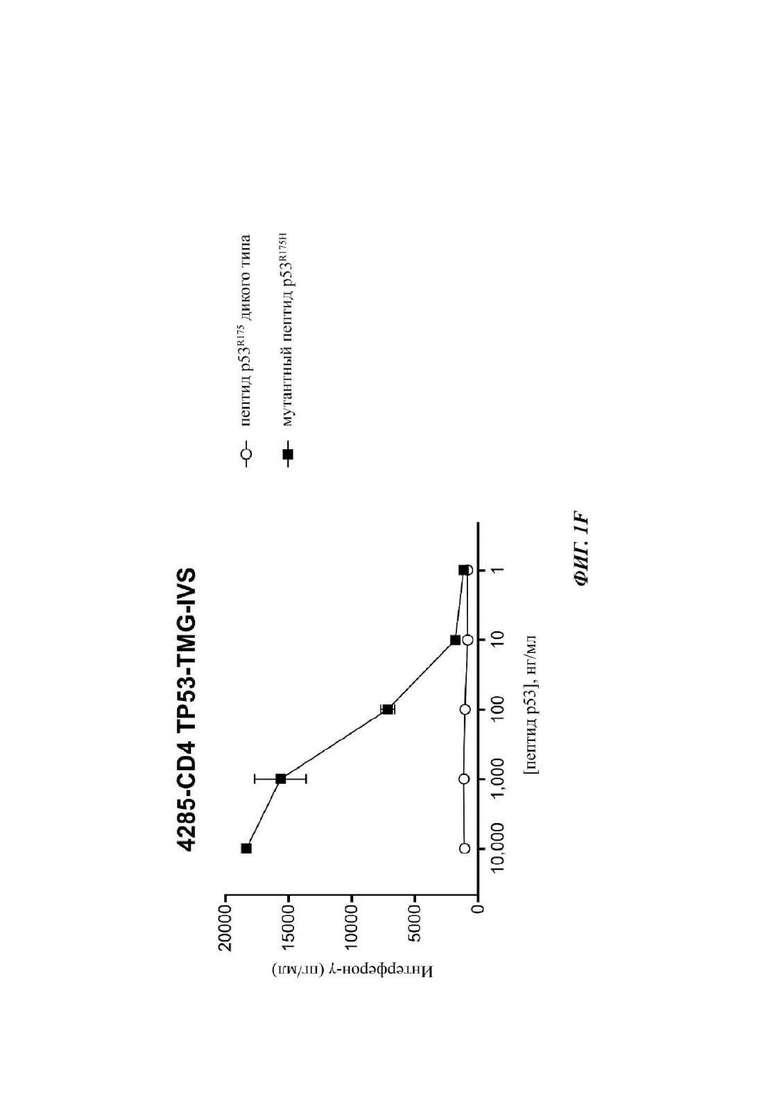
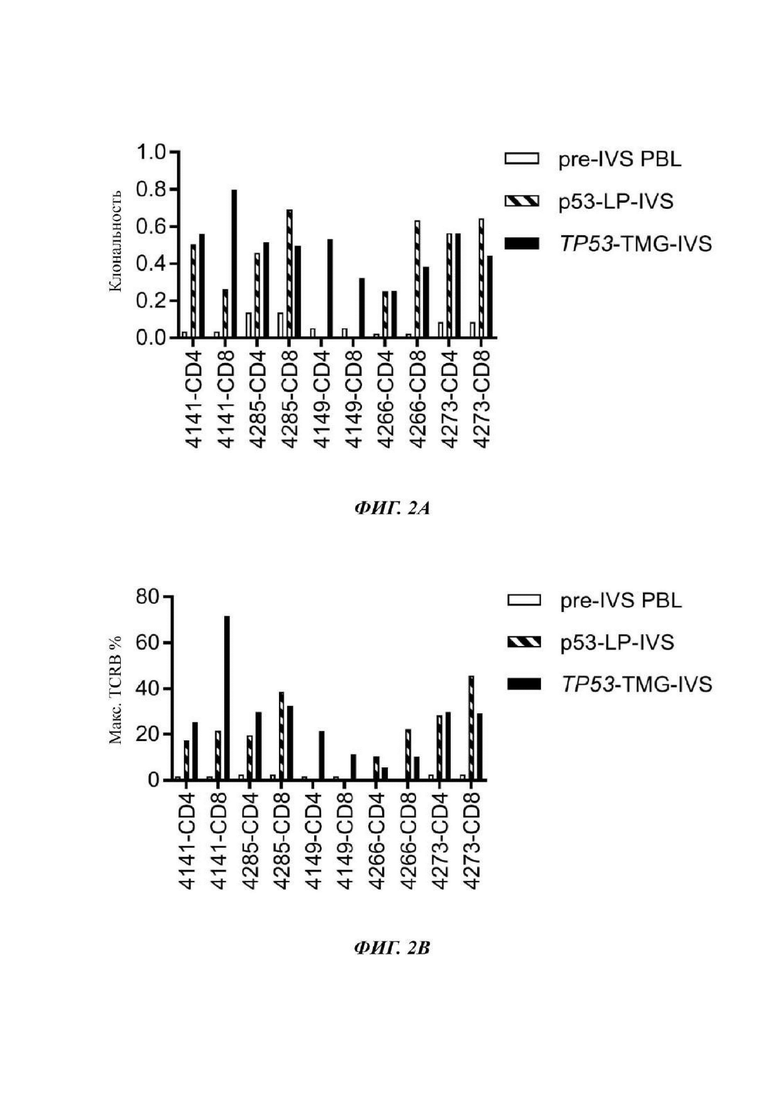
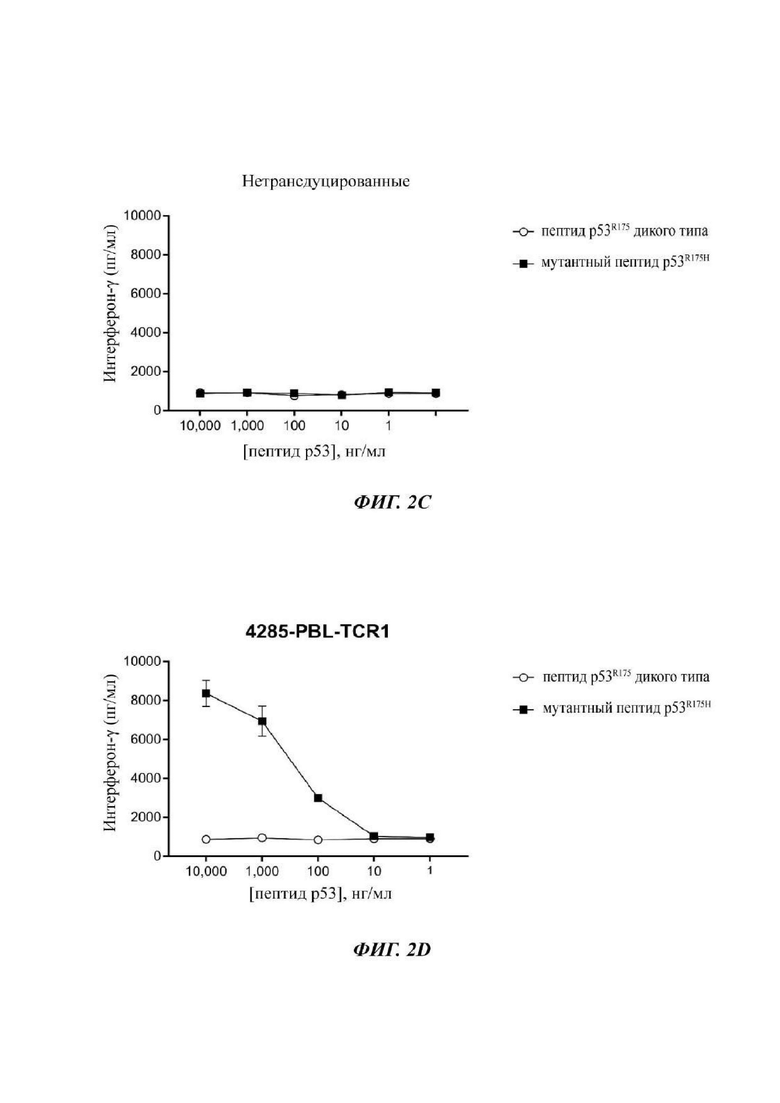
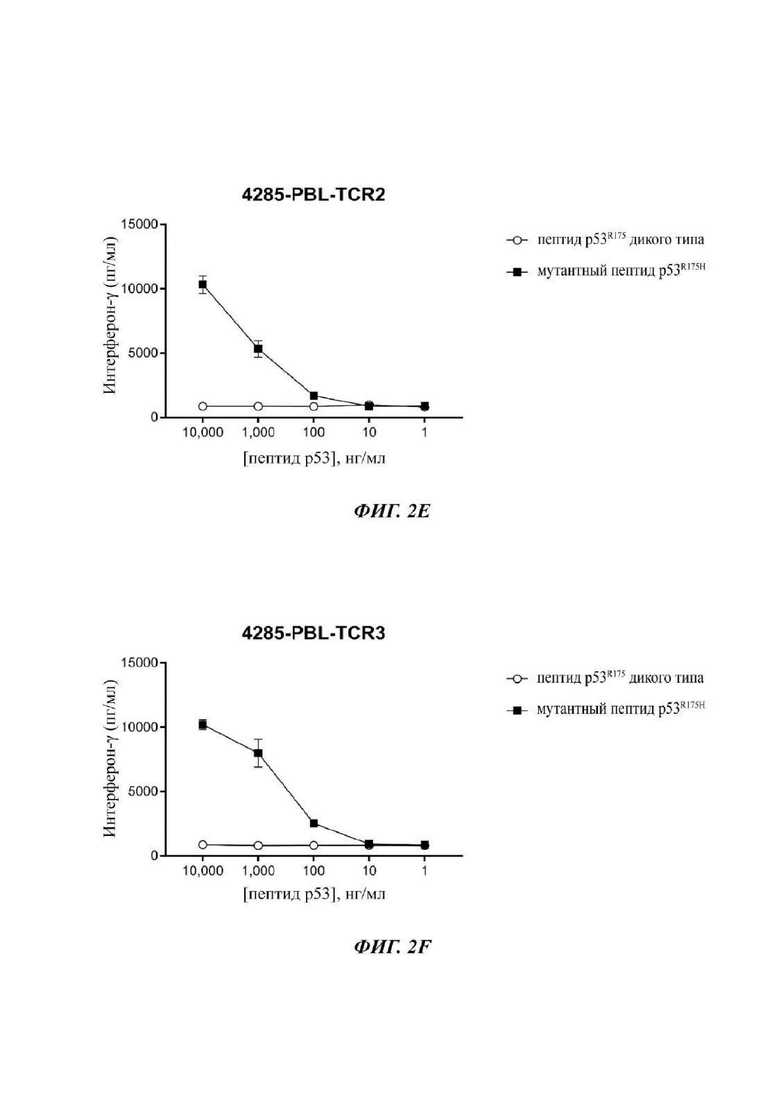
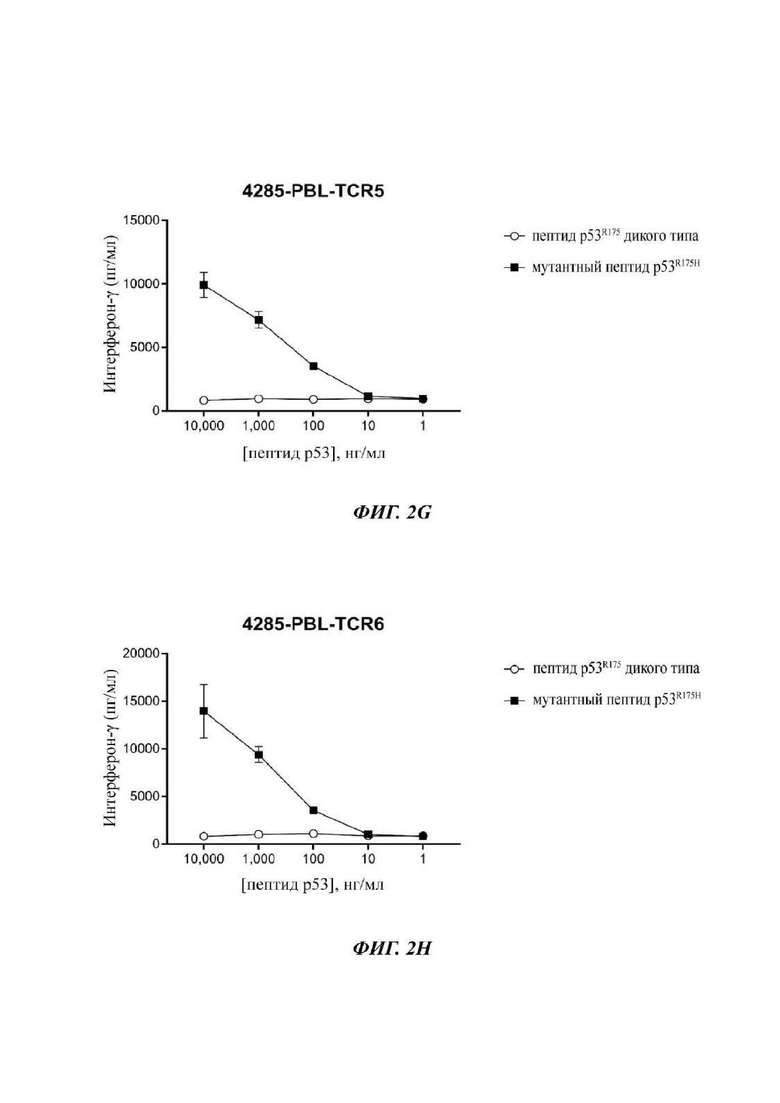
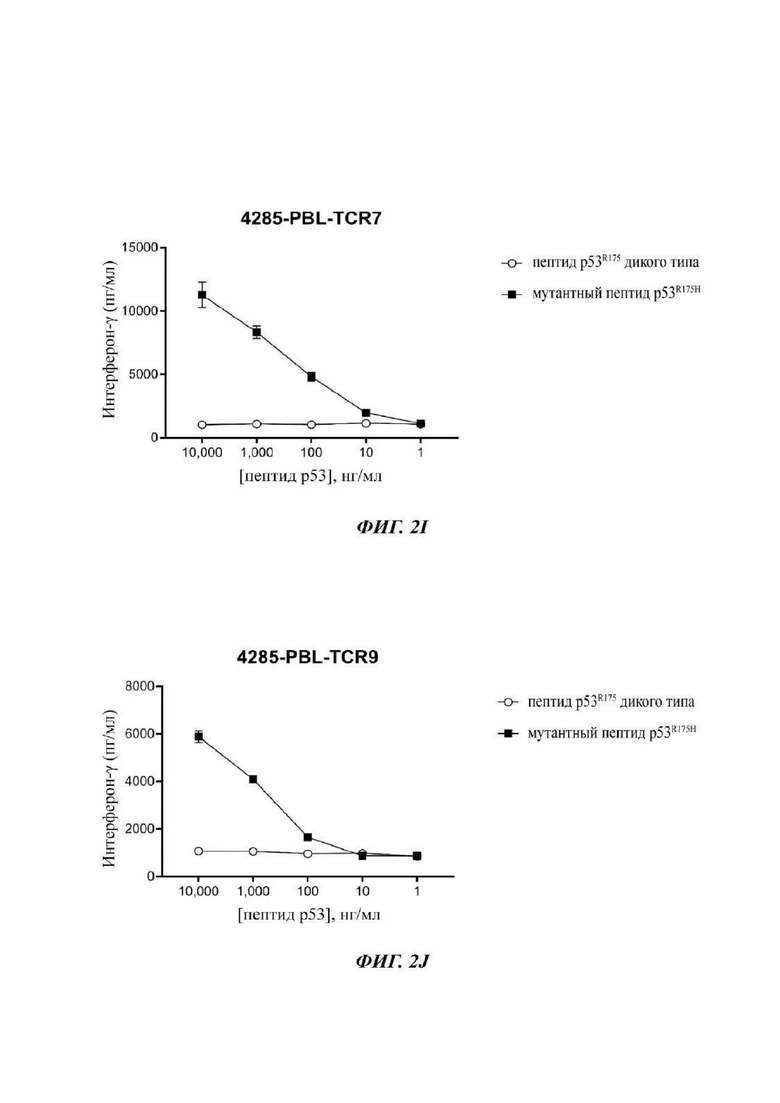
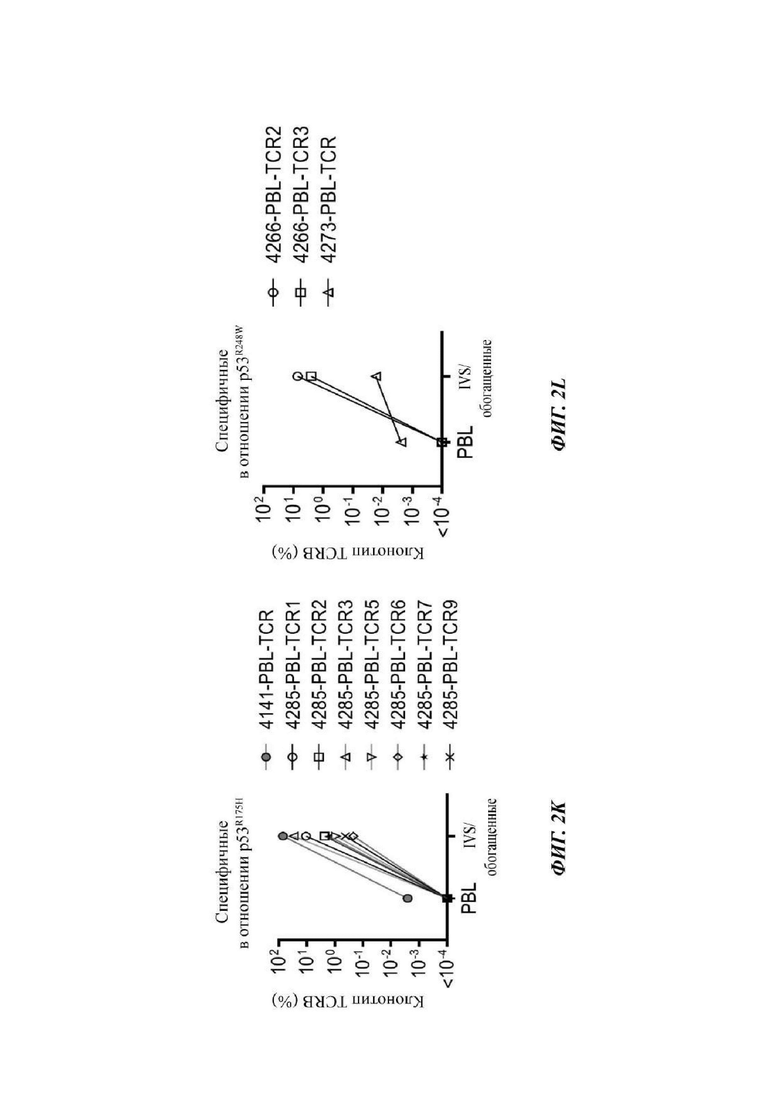
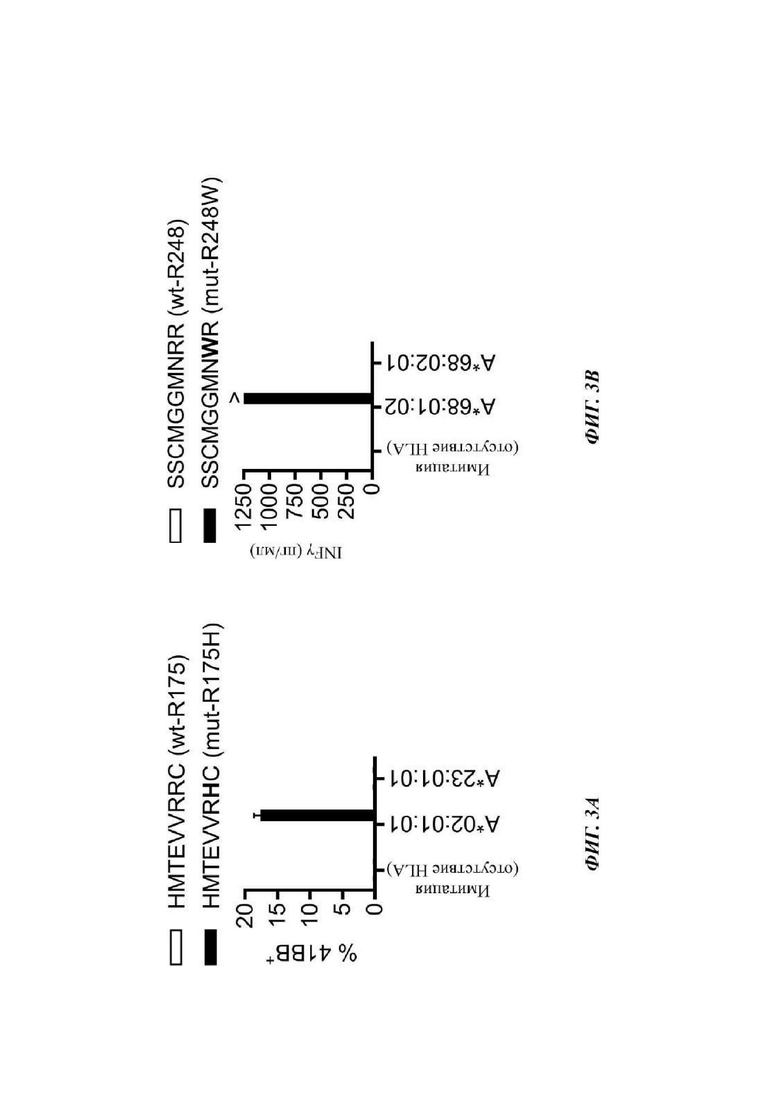
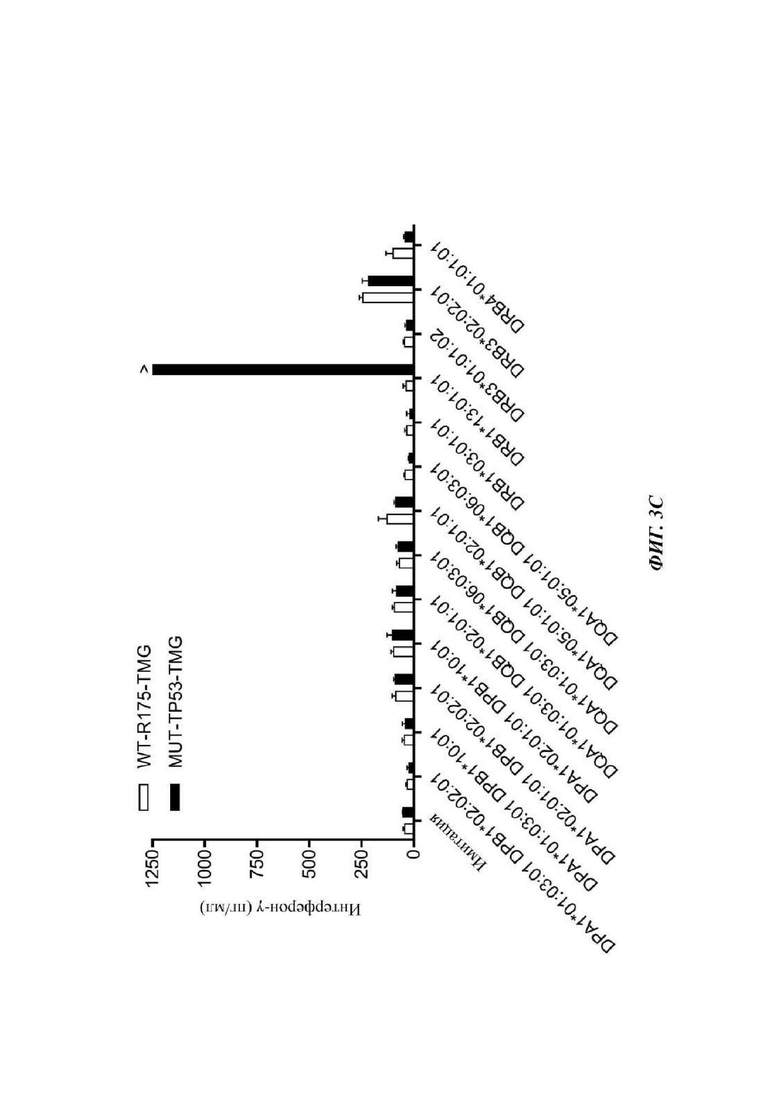
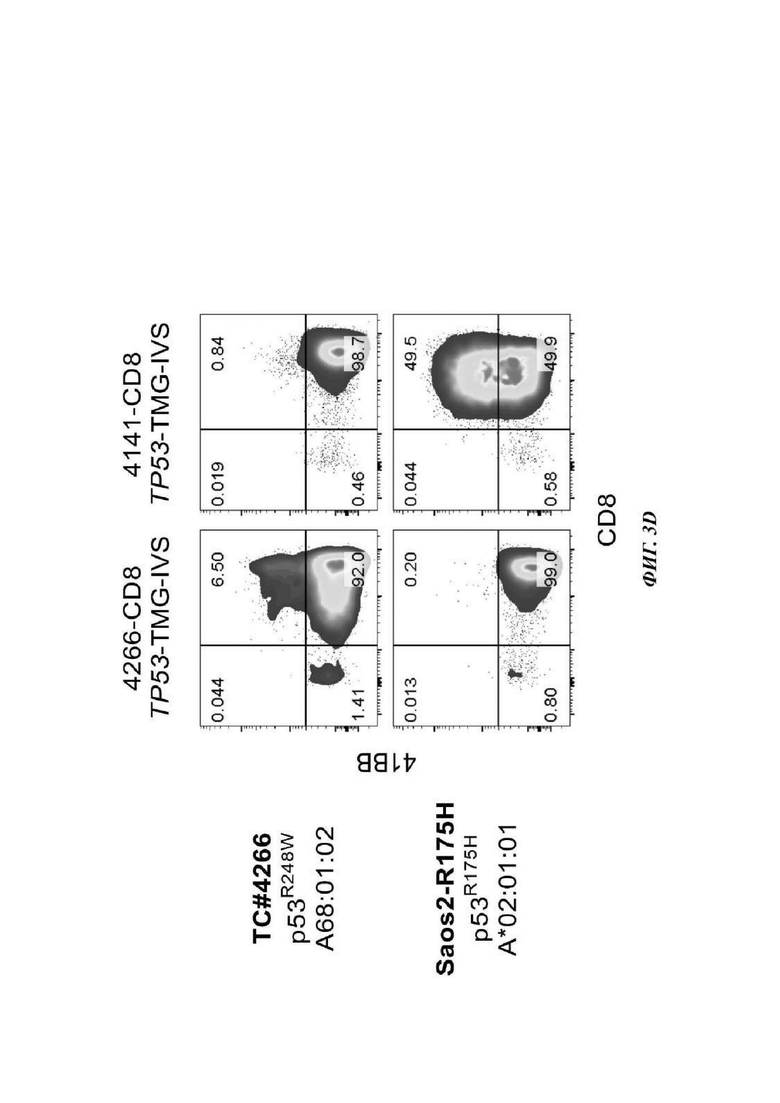
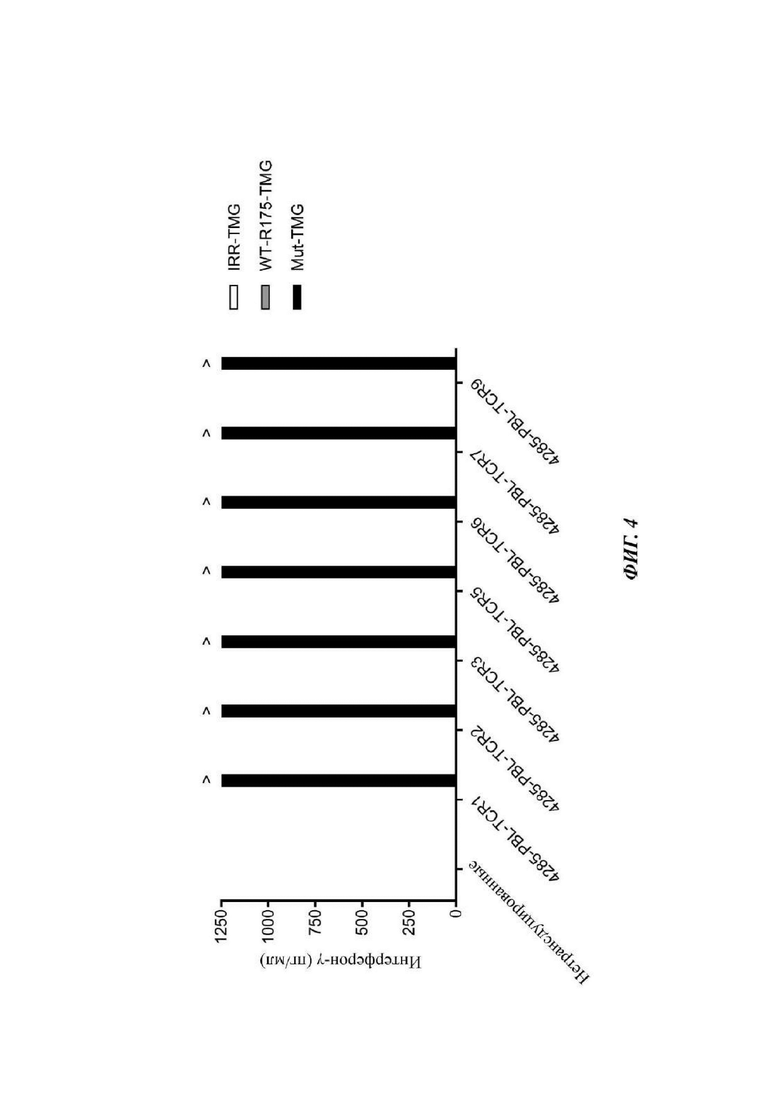
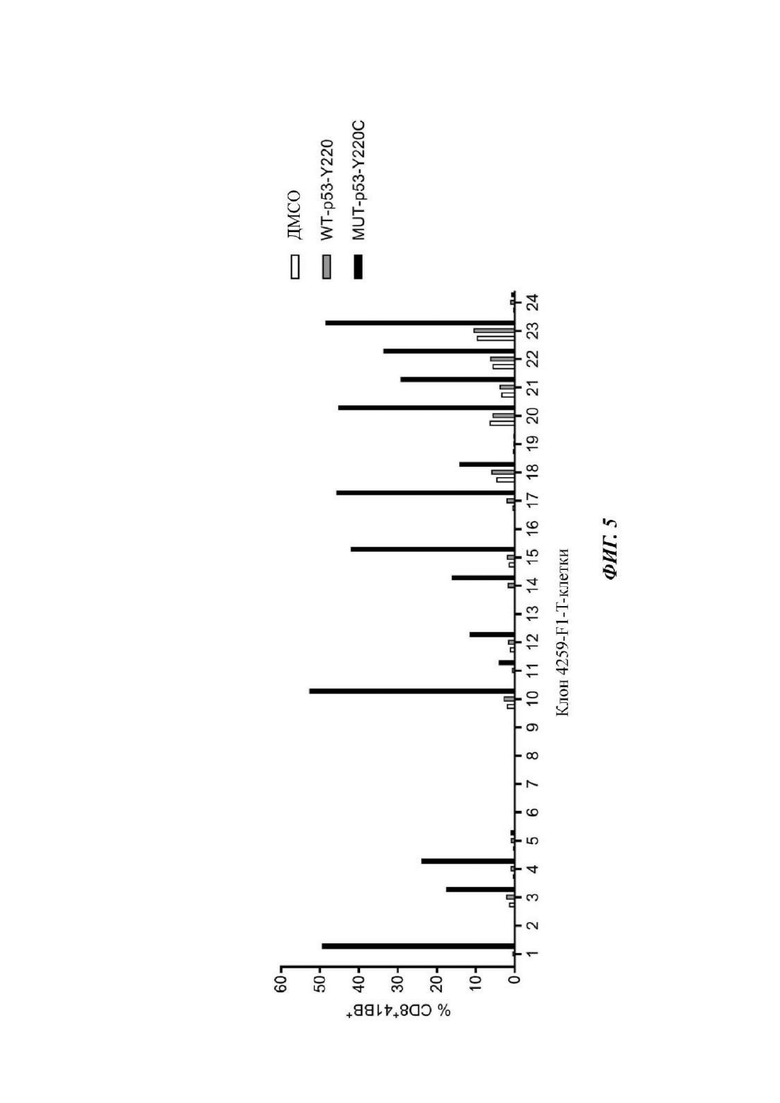
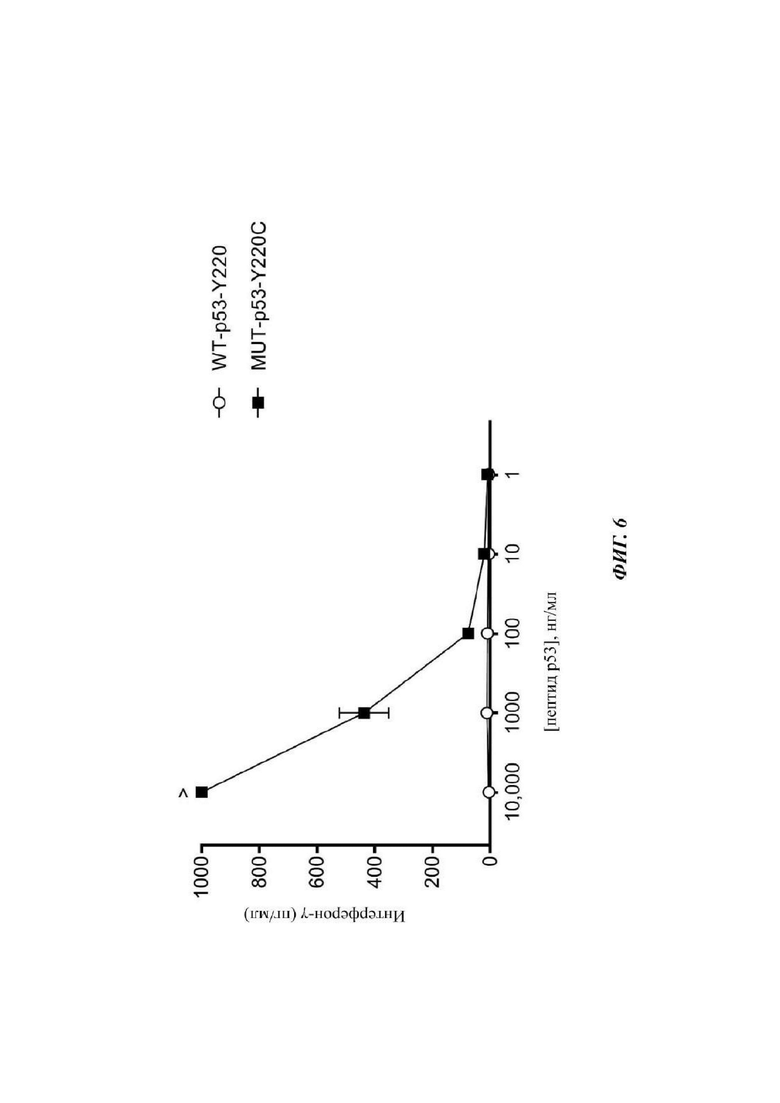
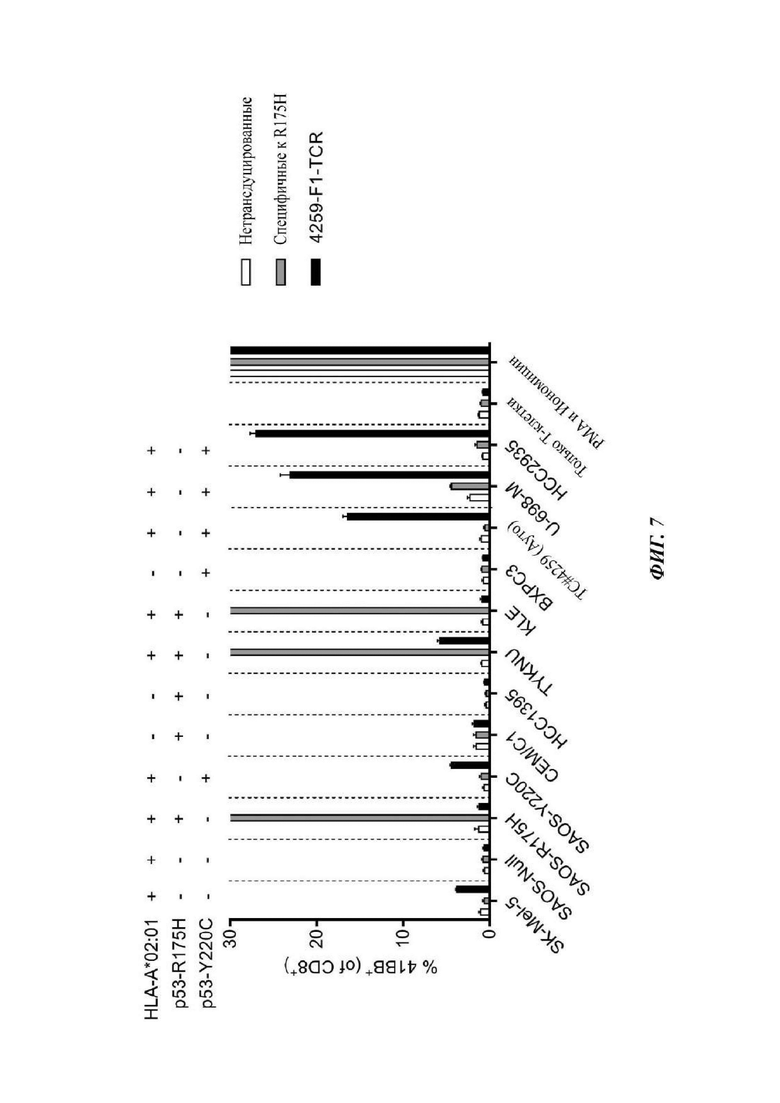


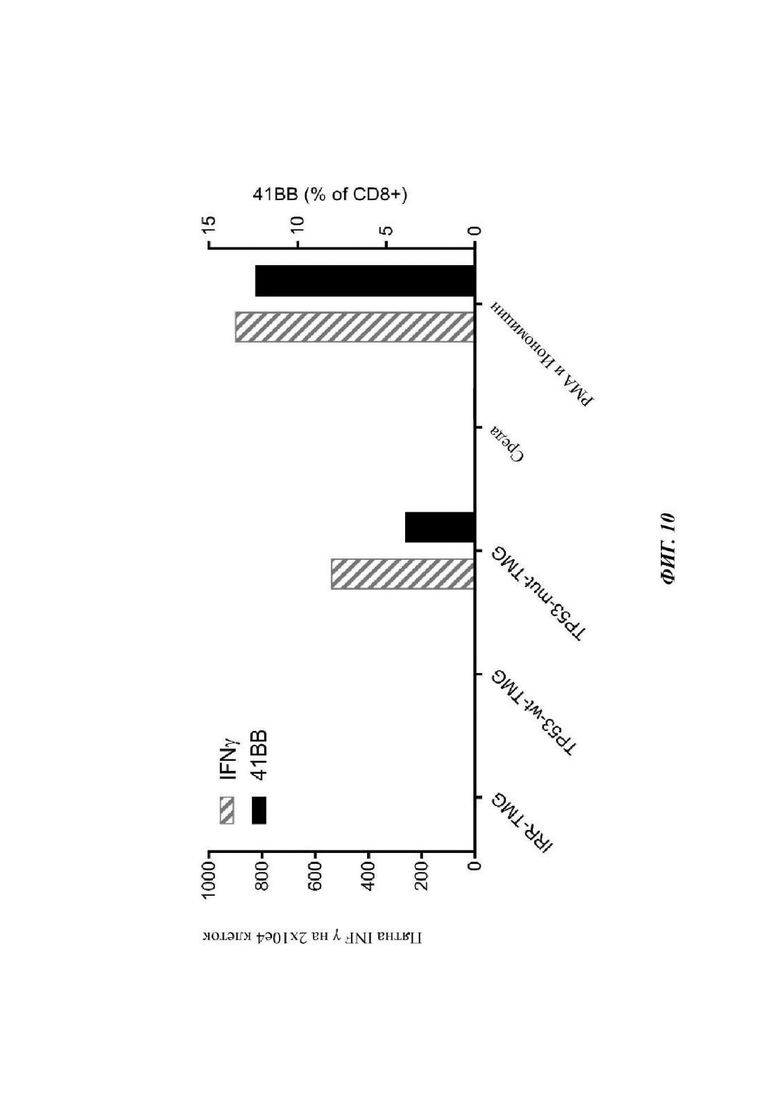
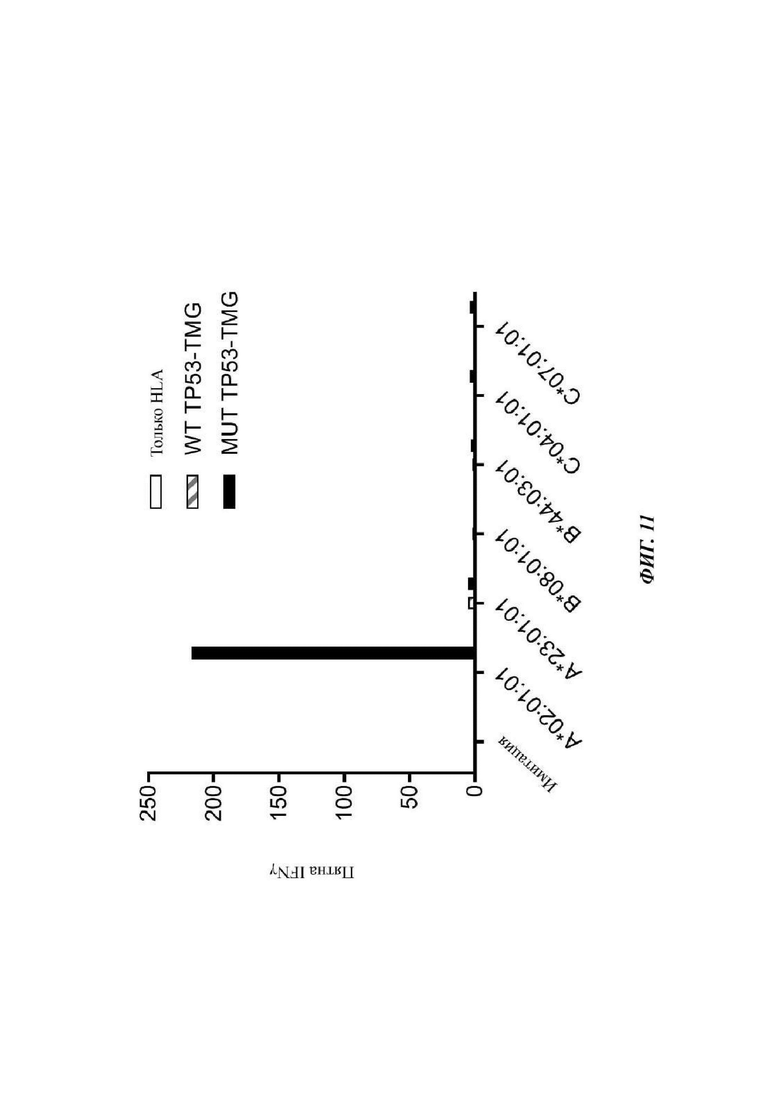
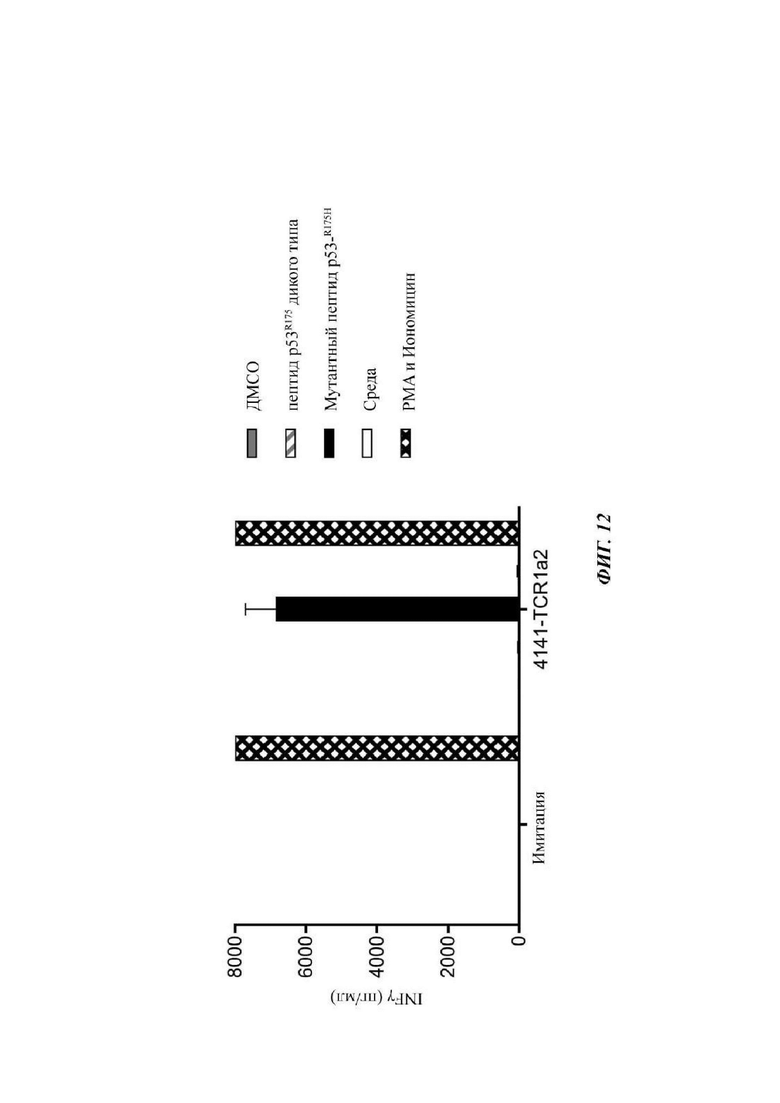
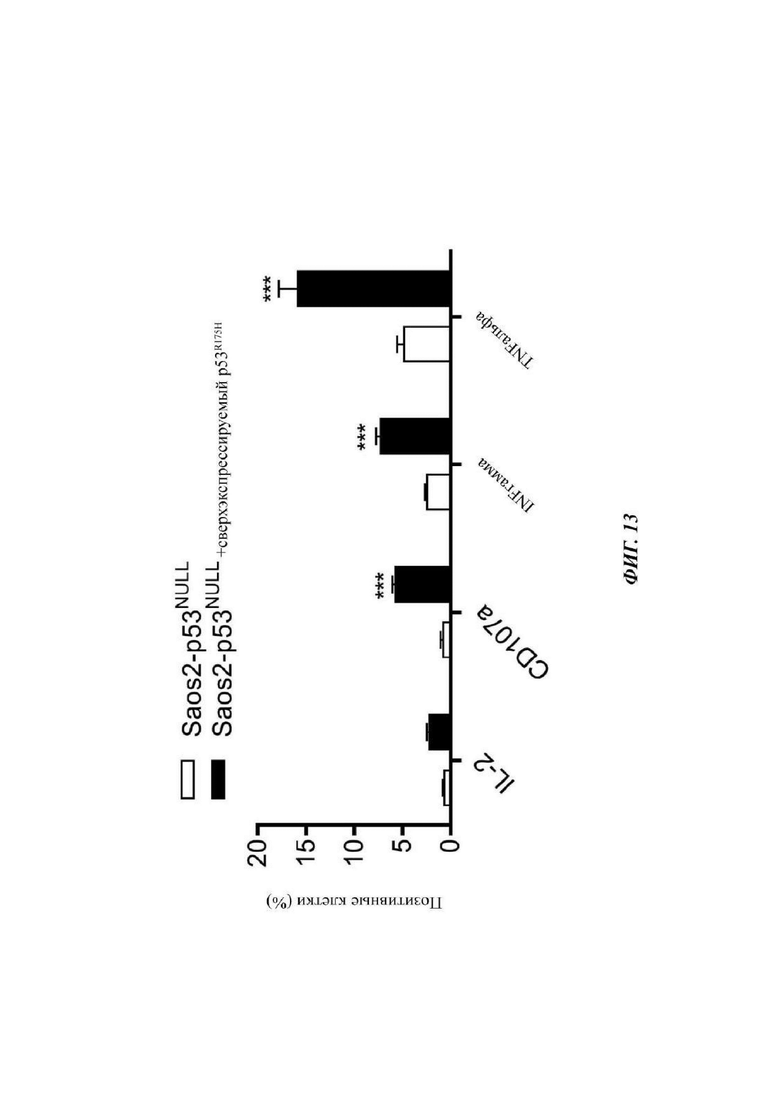
Изобретение относится к области биотехнологии, конкретно к получению Т-клеточных рецепторов (TCR), распознающих мутантный белок p53, и может быть использовано в медицине для выявления и лечения рака, который экспрессирует аминокислотную последовательность человеческого p53Y220C, презентированного молекулой HLA-А*02:01. Предложен TCR, обладающий антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой человеческого лейкоцитарного антигена (HLA)-А*02:01. Также предложены средства и методы для рекомбинантного получения TCR и для использования его в терапии и диагностике. Изобретение обеспечивает получение TCR для экспрессии клетками, используемыми для адоптивного переноса клеток, которые преимущественно нацелены на разрушение раковых клеток при минимизации или исключении разрушения нормальных, нераковых клеток, таким образом уменьшая побочные эффекты посредством минимизации или исключения токсичности. 25 н. и 14 з.п. ф-лы, 13 ил., 12 табл., 12 пр. 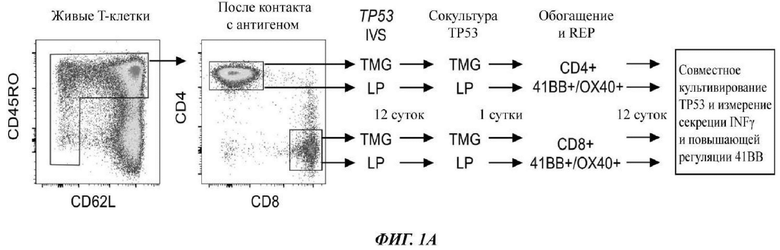
1. Выделенный или очищенный T-клеточный рецептор (TCR), обладающий антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой человеческого лейкоцитарного антигена (HLA)-А*02:01, где указанный TCR содержит определяющую комплементарность область (CDR)1 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 80, CDR2 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 81, CDR3 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 82, CDR1 цепи бета согласно аминокислотной последовательности SEQ ID NO: 83, CDR2 цепи бета согласно аминокислотной последовательности SEQ ID NO: 84 и CDR3 цепи бета согласно аминокислотной последовательности SEQ ID NO: 85.
2. TCR по п. 1, где указанный TCR содержит следующие аминокислотные последовательности:
(1) обе SEQ ID NO: 86 и 87;
(2) обе SEQ ID NO: 156 и 157;
(3) обе SEQ ID NO: 199 и 87; или
(4) обе SEQ ID NO: 86 и 219.
3. TCR по п. 1 или 2, где указанный TCR содержит следующие аминокислотные последовательности:
(1) обе SEQ ID NO: 88 и 89;
(2) обе SEQ ID NO: 174 и 175;
(3) обе SEQ ID NO: 200 и 89; или
(4) обе SEQ ID NO: 88 и 220.
4. TCR по любому из пп. 1-3, в котором аминокислотная последовательность человеческого p53Y220C представляет собой SEQ ID NO: 113.
5. TCR по любому из пп. 1-4, где указанный TCR не обладает антигенной специфичностью в отношении аминокислотной последовательности человеческого p53 дикого типа SEQ ID NO: 112.
6. Выделенный или очищенный полипептид для получения рекомбинантного TCR, обладающего антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой HLA- А*02:01, где указанный полипептид содержит аминокислотную последовательность цепи альфа TCR, содержащую CDR1 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 80, CDR2 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 81, CDR3 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 82, и аминокислотную последовательность цепи бета TCR, содержащую CDR1 цепи бета согласно аминокислотной последовательности SEQ ID NO: 83, CDR2 цепи бета согласно аминокислотной последовательности SEQ ID NO: 84 и CDR3 цепи бета согласно аминокислотной последовательности SEQ ID NO: 85, и расщепляемый линкер, расположенный между аминокислотной последовательностью цепи альфа TCR и аминокислотной последовательностью цепи бета TCR.
7. Полипептид по п. 6, где указанный полипептид содержит следующие аминокислотные последовательности:
(1) обе SEQ ID NO: 86 и 87;
(2) обе SEQ ID NO: 156 и 157;
(3) обе SEQ ID NO: 199 и 87; или
(4) обе SEQ ID NO: 86 и 219.
8. Полипептид по п. 6 или 7, где указанный полипептид содержит следующие аминокислотные последовательности:
(1) обе SEQ ID NO: 88 и 89;
(2) обе SEQ ID NO: 174 и 175;
(3) обе SEQ ID NO: 200 и 89; или
(4) обе SEQ ID NO: 88 и 220.
9. Выделенный или очищенный белок, обладающий антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой HLA-А*02:01, где указанный белок содержит:
первую полипептидную цепь, содержащую CDR1 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 80, CDR2 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 81, CDR3 цепи альфа согласно аминокислотной последовательности SEQ ID NO: 82, и вторую полипептидную цепь, содержащую CDR1 цепи бета согласно аминокислотной последовательности SEQ ID NO: 83, CDR2 цепи бета согласно аминокислотной последовательности SEQ ID NO: 84 и CDR3 цепи бета согласно аминокислотной последовательности SEQ ID NO: 85.
10. Белок по п. 9, где:
(1) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 86, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 87;
(2) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 156, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 157;
(3) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 199, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 87; или
(4) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 86, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 219.
11. Белок по п. 9 или 10, где:
(1) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 88, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 89;
(2) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 174, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 175;
(3) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 200, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 89; или
(4) указанная первая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 88, и указанная вторая полипептидная цепь содержит аминокислотную последовательность SEQ ID NO: 220.
12. Выделенная или очищенная нуклеиновая кислота для экспрессии CD8+ Т клеткой, где указанная нуклеиновая кислота содержит нуклеотидную последовательность, кодирующую TCR по любому из пп. 1-5.
13. Нуклеиновая кислота для экспрессии CD8+ Т клеткой, где указанная нуклеиновая кислота содержит, от 5’ к 3’, первую нуклеотидную последовательность, вторую нуклеотидную последовательность и третью нуклеотидную последовательность, где первая и вторая нуклеотидная последовательность, соответственно, кодируют аминокислотные последовательности SEQ ID NO: 86 и 87; 87 и 86; 156 и 157; 157 и 156; 199 и 87; 87 и 199; 86 и 219; или 219 и 86, где третья нуклеотидная последовательность размещена между первой и второй нуклеотидной последовательностью, при этом указанная третья нуклеотидная последовательность кодирует расщепляемый линкерный пептид.
14. Выделенная или очищенная нуклеиновая кислота для экспрессии CD8+ Т клеткой, где указанная нуклеиновая кислота содержит нуклеотидную последовательность, кодирующую полипептид по любому из пп. 6-8.
15. Выделенная или очищенная нуклеиновая кислота для экспрессии CD8+ Т клеткой, где указанная нуклеиновая кислота содержит нуклеотидную последовательность, кодирующую белок по любому из пп. 9-11.
16. Рекомбинантный экспрессионный вектор для экспрессии CD8+ Т клеткой, где вектор содержит нуклеиновую кислоту по п. 12.
17. Рекомбинантный экспрессионный вектор для экспрессии CD8+ Т клеткой, где вектор содержит нуклеиновую кислоту по п. 13.
18. Рекомбинантный экспрессионный вектор для экспрессии CD8+ Т клеткой, где вектор содержит нуклеиновую кислоту по п. 14.
19. Рекомбинантный экспрессионный вектор для экспрессии CD8+ Т клеткой, где вектор содержит нуклеиновую кислоту по п. 15.
20. Рекомбинантный экспрессионный вектор по п. 16, который представляет собой транспозон или лентивирусный вектор.
21. Способ получения CD8+ Т клетки, экспрессирующей TCR, который обладает антигенной специфичностью в отношении пептида с SEQ ID NO: 113, презентированного молекулой HLA-А*02:01, включающий приведение CD8+ Т клетки в контакт с вектором по п. 16 в условиях, допускающих введение вектора в CD8+ Т клетку.
22. CD8+ Т клетка, содержащая рекомбинантный экспрессионный вектор по п. 16, для получения TCR, обладающего антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой HLA-А*02:01.
23. CD8+ Т клетка, содержащая рекомбинантный экспрессионный вектор по п. 18, для получения полипептида для получения рекомбинантного TCR.
24. CD8+ Т клетка, содержащая рекомбинантный экспрессионный вектор по п. 19, для получения белка, обладающего антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой HLA-А*02:01.
25. CD8+ Т клетка по п. 22, где указанная клетка представляет собой человеческую CD8+ Т клетку.
26. Популяция клеток, содержащая CD8+ Т клетку по п. 22, для получения TCR, обладающего антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой HLA- А*02:01.
27. Популяция клеток, содержащая CD8+ Т клетку по п. 23, для получения полипептида для получения рекомбинантного TCR.
28. Популяция клеток, содержащая CD8+ Т клетку по п. 24, для получения белка, обладающего антигенной специфичностью в отношении аминокислотной последовательности человеческого p53Y220C, презентированного молекулой HLA- А*02:01.
29. Способ получения TCR по любому из пп. 1-5, причем указанный способ включает культивирование CD8+ Т клетки по п. 22 или популяции CD8+ Т клеток по п. 26 таким образом, что получают TCR.
30. Способ получения полипептида по любому из пп. 6-8, причем указанный способ включает культивирование CD8+ Т клетки по п. 23 или популяции CD8+ Т клеток по п. 27 таким образом, что получают полипептид.
31. Способ получения белка по любому из пп. 9-11, причем указанный способ включает культивирование CD8+ Т клетки по п. 24 или популяции CD8+ Т клеток по п. 28 таким образом, что получают белок.
32. Фармацевтическая композиция для лечения или предупреждения рака у млекопитающего, содержащая эффективное количество (a) CD8+ Т клетки по п. 22 или популяции CD8+ Т клеток по п. 26 и (b) фармацевтически приемлемый носитель, где рак экспрессирует аминокислотную последовательность человеческого p53Y220C, презентированного молекулой HLA-А*02:01.
33. Способ выявления наличия рака у млекопитающего, включающий:
(a) приведение образца, содержащего раковые CD8+ Т клетки, в контакт с CD8+ Т клеткой по п. 22 или популяцией CD8+ Т клеток по п. 26, с образованием, посредством этого, комплекса, и
(b) выявление указанного комплекса,
где выявление комплекса свидетельствует о наличии рака у млекопитающего, и где рак экспрессирует аминокислотную последовательность человеческого p53Y220C, презентированного молекулой HLA-А*02:01.
34. Способ индукции иммунного ответа на рак у млекопитающего, включающий введение млекопитающему эффективного количества CD8+ Т клетки по п. 22, популяции CD8+ Т клеток по п. 26 или фармацевтической композиции, содержащей указанную CD8+ Т клетку или популяцию CD8+ Т клеток, где рак экспрессирует аминокислотную последовательность человеческого p53Y220C, презентированного молекулой HLA-А*02:01.
35. Способ лечения или предупреждения рака у млекопитающего, включающий введение млекопитающему эффективного количества CD8+ Т клетки по п. 22, популяции CD8+ Т клеток по п. 26 или фармацевтической композиции, содержащей указанную CD8+ Т клетку или популяцию CD8+ Т клеток, где рак экспрессирует аминокислотную последовательность человеческого p53Y220C, презентированного молекулой HLA-А*02:01.
36. Способ по п. 34 или 35, где способ включает введение популяции CD8+ Т клеток млекопитающему, при этом указанная популяция CD8+ Т клеток является аутологичной в отношении млекопитающего.
37. Способ по п. 34 или 35, где способ включает введение популяции CD8+ Т клеток млекопитающему, при этом указанная популяция CD8+ Т клеток является аллогенной в отношении млекопитающего.
38. Способ по любому из пп. 33-37, где рак представляет собой эпителиальный рак.
39. Способ по любому из пп. 33-37, где рак представляет собой холангиокарциному, меланому, рак толстой кишки, рак прямой кишки, рак яичника, рак эндометрия, немелкоклеточный рак легкого (NSCLC), глиобластому, рак шейки матки, рак головы и шеи, рак молочной железы, рак поджелудочной железы или рак мочевого пузыря.
| WO 2019067243 A1, 04.04.2019 | |||
| WO 2019067242 A1, 04.04.2019 | |||
| LO W | |||
| et al | |||
| Веникодробильный станок | 1921 |
|
SU53A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Ножной переключатель для перемены направления вращения электродвигателя | 1921 |
|
SU534A1 |
| EA 201792420 A1, 30.04.2018 | |||
| HOLLER P.D | |||
| et al | |||
| Quantitative analysis of the contribution | |||
Авторы
Даты
2024-11-12—Публикация
2020-06-26—Подача