Область техники
Изобретение относится к областям молекулярной биологии, вирусологии и клеточных технологий. Изобретение потенциально может быть использовано для лечения ВИЧ.
Работа выполнена при финансовой поддержке Министерства Науки и Высшего образования Российской Федерации в рамках Соглашения № 075-15-2019-1661 от 31.10.2019 и при финансовой поддержке РФФИ по соглашению 18-29-07052.
Уровень техники
Выбор gp41-зависимого слияния в качестве мишени для противовирусной терапии.
В терапии вируса иммунодефицита человека (ВИЧ) широко используются пептидные ингибиторы слияния. Они препятствуют последнему этапу проникновения ВИЧ в клетку-мишень за счет блокирования образования шестиспирального пучка, который участвует в слиянии вирусной и клеточной мембраны.
Первым одобренным препаратом этой группы стал Энфувиртид (Lalezari et al., 2003), короткий пептид из С-концевого гептадного повтора gp41 (С-пептид). Этот препарат обладает рядом недостатков, включая появление резистентных штаммов ВИЧ и развитием побочных эффектов у пациентов.
После его одобрения эта сфера науки стала активно развиваться, появилось большое количество исследований. Однако ни один из опубликованных растворимых пептидов (US2005089840A1, WO2016171980A1) не может полностью и пожизненно защитить клетки от инфицирования.
Вследствие этого начали появляться системы доставки пептида на мембрану клетки-мишени.
Описан метод экспонирования пептидного ингибитора слияния на мембране в контексте хемокинового корецептора ВИЧ CXCR4 (Lesli et al., 2016), при котором слияние пептида с рецептором происходит через связку из двух аминокислот, лейцина и лизина, а в качестве способа доставки ингибитора используется лентивирусный вектор. Ведутся клинические испытания.
Также описан способ доставки пептида 2P23 на поверхность мембраны в контексте GPI-заякоренного белка (Xiaoran et al., 2019), однако описанная конструкция имеет больший размер, в качестве способа доставки предлагается только лентивирусный вектор. Заякоривание ингибитора слияния 2P23 на клеточной мембране может полностью блокировать инфекцию ВИЧ-1 и группы мутантов, устойчивых к энфувиртиду. Связанный с мембраной 2P23 эффективно блокирует инфекцию ВИЧ и делает CD4+ Т-клетки устойчивыми к заражению вирусом.
В 2019 году в нашей лаборатории была разработана система доставки эпитопных тагов на мембрану, позволяющая быстро изолировать клетки с CRISPR/Cas9-индуцированной целевой генетической модификацией методом иммунофлюоресценции и клеточной сортировки. При этом было выявлено, что наиболее короткой и эффективной конструкцией является GPI-заякоренный белок CD52, куда между сигналом экспорта и сигналом GPI-заякоривания была вставлена последовательность эпитопного тага Flag или HA (Zotova et al., 2019). Мы модифицировали экспонируемую последовательность эпитопного тага в системе доставки путем замены ее на последовательность одного из С-пептидов, ингибирующих слияние ВИЧ с клеточной мембраной, и, таким образом, придали системе не только возможность селекции редактированных клеток, но и обеспечили устойчивость модифицированных клеток к заражению ВИЧ различной тропности.
Чтобы добиться наиболее высокой эффективности, нами разработана технология, позволяющая экспонировать на мембране одновременно два пептида и проводить селекцию клеток по двум защитным пептидам.
Разработанная технология позволяет получать популяции клеток, невосприимчивых к инфицированию ВИЧ, внося минимальные внетаргетные изменения в геном нативной клетки за счет использования рибонуклеопротеинового (RNP) комплекса нуклеазы Cas9 с направляющей (гидовой) РНК. Благодаря малому размеру встраиваемой генетической конструкции, предлагаемая нами технология имеет ряд преимуществ. Во-первых, процесс наработки донорной ДНК является экономичным. Во-вторых, более эффективной оказывается доставка конструкции в клетки и ее интеграция по механизму гомологичной рекомбинации. Совместимость технологии с разными системами редактирования генома на основе CRISPR/Cas9 и других позволяет легко адаптировать ее к последним разработкам в этой области.
Раскрытие сущности изобретения
Настоящее изобретение представляет собой технологию генотерапии ВИЧ, при которой защитный пептид из gp41 доставляется на поверхность плазматической мембраны клетки - мишени за счет внесения кодирующей его нуклеотидной последовательности в геном с помощью CRISPR/Cas9 в составе генетической конструкции, представляющей собой белок CD52, между двумя частями которого (сигналом экспорта белка и сигналом GPI-заякоривания) встроен целевой пептид, либо путем слияния целевого пептида с N-концом CXCR4.
В альтернативном варианте доставка генетической конструкции, представляющей собой белок CD52, между двумя частями которого (сигналом экспорта белка и сигналом заякоривания) встроен целевой пептид, осуществляется с помощью лентивирусного вектора.
Для осуществления изобретения в клетки вводится три компонента: нуклеаза Cas9, гидовая РНК (gRNA) и донорная ДНК. Гидовая РНК направляет Cas9 на определенное место в геноме. Донорная ДНК содержит целевую генетическую конструкцию и плечи гомологии, окружающие место встраивания, и служит матрицей для гомологичной рекомбинации. В одном из вариантов осуществления изобретения направленное редактирование можно осуществлять путем трансфекции кодирующими Cas9 и gRNA плазмидами (например, pcDNA3.3-hCas9 (Addgene #41815)), в других вариантах осуществления изобретения - с помощью комплекса RNP, включающего рекомбинантный белок Cas9 в комплексе с gRNA, полученной путем транскрипции in vitro.
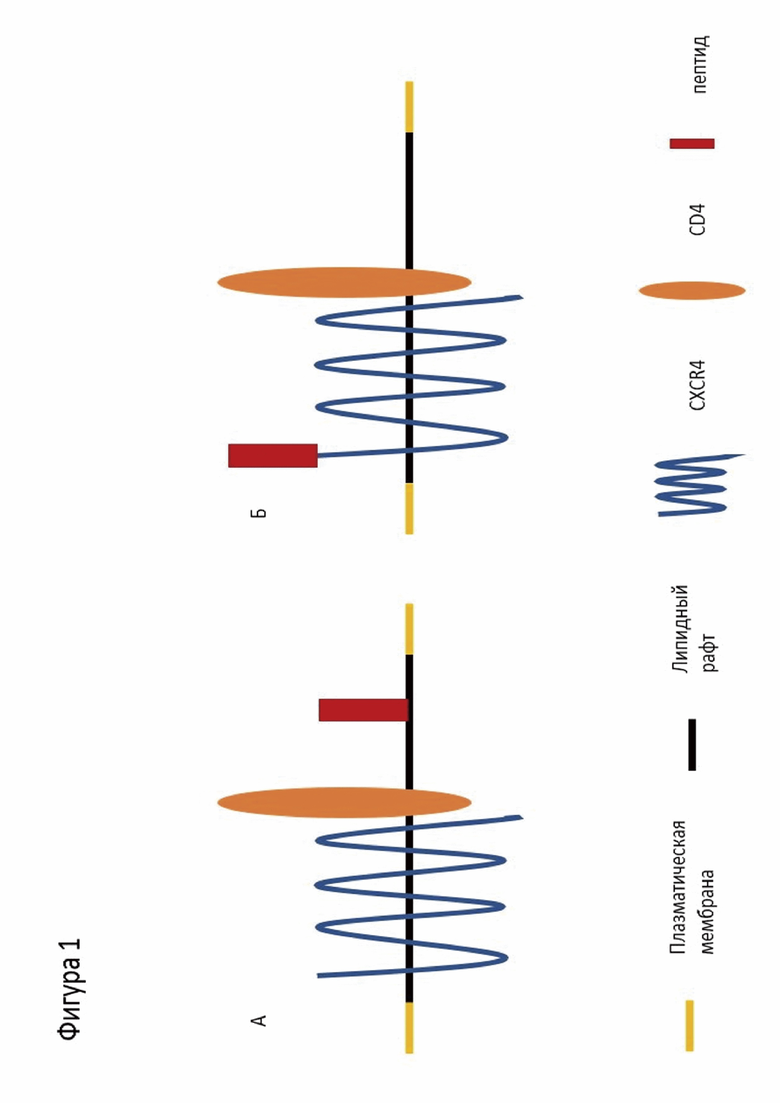
В одном варианте осуществления изобретения целевая генетическая конструкция, закодированная в донорной ДНК, основана на последовательности GPI-заякоренного белка CD52. SEQ ID № 1 или 2 являются сигналом экспорта белка. SEQ ID № 3 служит сигналом для мембранного заякоривания конструкции. Между SEQ ID № 1/2 и № 3 находится последовательность, кодирующая один из защитных пептидов из gp41 (SEQ ID № 4-9). Такая конструкция доставляет пептид на поверхность клетки в специфическую зону - липидный рафт, где локализуются рецептор CD4 и корецепторы CCR5 и CXCR4, распознаваемые ВИЧ и используемые им для проникновения в клетку. Пептид, экспонируемый на поверхности клетки, взаимодействует с N-концевым гептадным повтором gp41 вирусного белка слияния, и препятствует образованию шестиспирального пучка, таким образом, защищая клетку от проникновения ВИЧ (фиг. 1А).
В другом варианте осуществления изобретения пептид из gp41, слитый с N-концом корецептора CXCR4, действует по такому же принципу, препятствуя образованию шестиспирального пучка (фиг. 1Б).
Наибольшую эффективность в качестве защитных пептидов в конструкциях проявили С34, MT-C34, HP23L, 2p23, nHP23L и n2p23 (SEQ ID № 4-9 соответственно).
Настоящее изобретение также предлагает способы эффективной доставки целевых генетических конструкций на мембрану клетки:
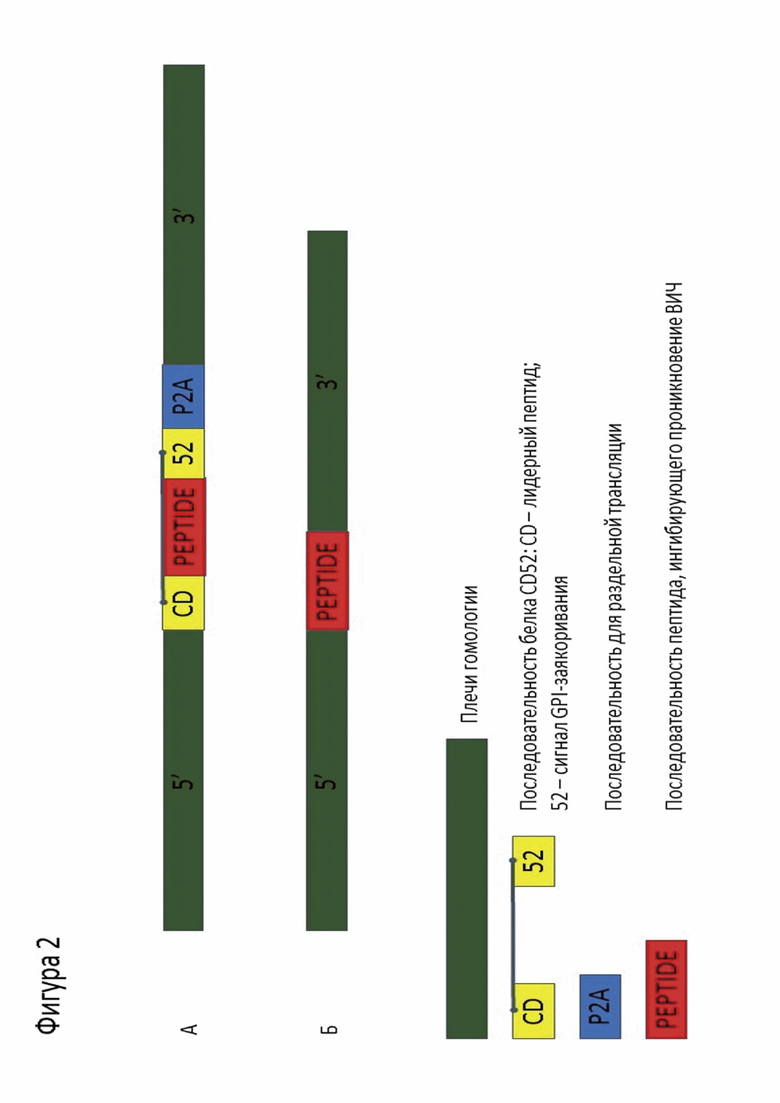
- встраивание в геном посредством CRISPR/Cas9 под эндогенный промотор, например, гена CXCR4, для которого подобрана gRNA (SEQ ID № 10), донорная ДНК включает в себя 5’ и 3’ плечи гомологии SEQ ID № 11 и 12 соответственно, между которыми заключена целевая последовательность CD52-пептид, после которой стоит последовательность Р2А (SEQ ID № 13), позволяющая рибосоме пропускать образование ковалентной связи между глицином и пролином, иначе говоря, позволяющей получить с одной РНК раздельную трансляцию пептида и белка CXCR4 (фиг. 2А);
- слияние пептида с N-концом хемокинового рецептора CXCR4 (фиг. 1Б) с помощью системы геномного редактирования CRISPR/Cas9. При этом для нацеливания Cas9 используется гидовая РНК (SEQ ID № 10), донорская ДНК в этом случае включает в себя 5’ и 3’ плечи гомологии SEQ ID № 11 и 12 соответственно, между которыми расположен один из целевых пептидов (SEQ ID № 5, 6-9, фиг. 2Б). В этом случае непосредственно после трансляции пептида начинается трансляция CXCR4, что приводит к слиянию пептида с его N-концом.
Поскольку имеется возможность внесения модификации в два аллеля гена, то одновременно можно экспрессировать на поверхности клетки два пептида из gp41, в том числе сочетая в клетке слитый с корецептором и заякоренный на мембране пептиды, два слитых с корецептором или два заякоренных пептида. Для этого при внесении конструкций в клетку при электропорации используется одновременно две донорные ДНК, представленные на фиг. 2, в соотношении 1:1.
В качестве слитых с корецептором пептидов могут быть использованы, но не ограничиваются ими, MT-C34, HP23L, 2p23, nHP23L и n2p23 (SEQ ID № 5, 6-9 соответственно).
В качестве заякоренного на мембране может быть использованы, но не ограничиваются им, MT-C34 (SEQ ID № 5).
Высокую эффективность показало сочетание заякоренного пептида MT-С34 и 2р23 или HP23L, слитого с CXCR4.
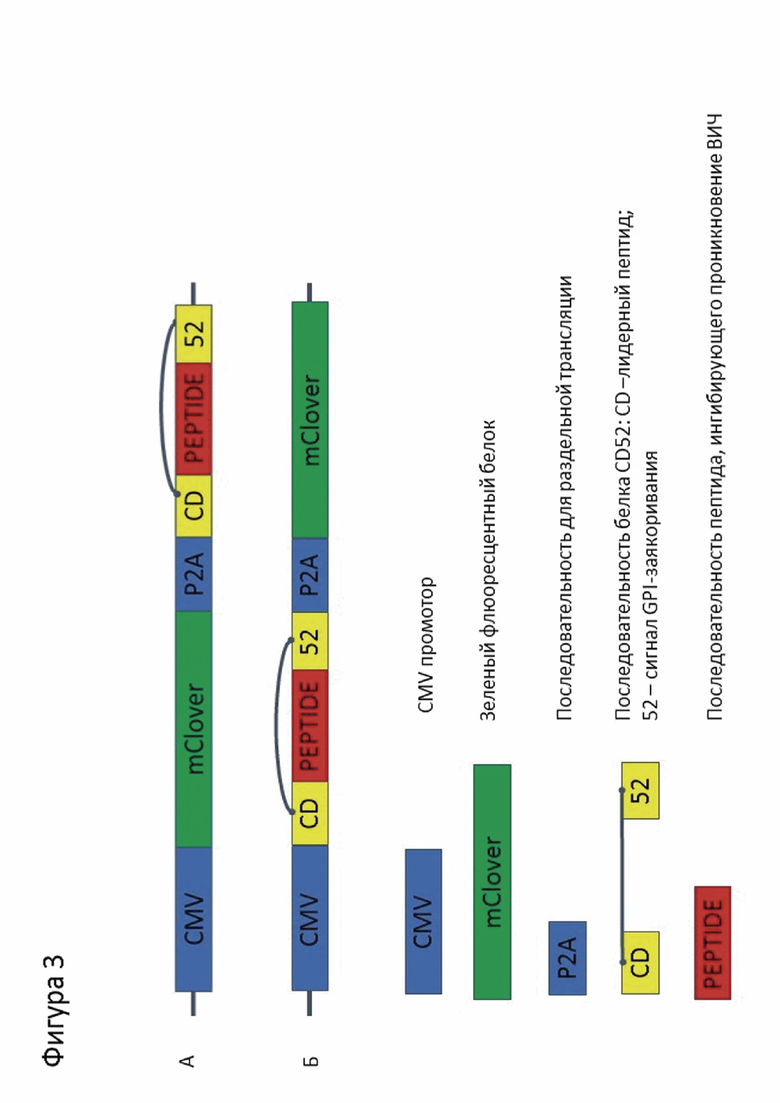
Для осуществления альтернативного варианта доставки генетической конструкции, представляющей собой белок CD52, между двумя частями которого встроен целевой пептид C34, MT-C34, HP23L, 2p23, nHP23L и n2p23 (SEQ ID № 4-9 соответственно), используется лентивирусный вектор (фиг. 3А). Для облегчения сортировки клеток, несущих целевую конструкцию, в вектор внесена последовательность флюоресцирующего белка mClover, разделенного с целевой конструкцией последовательностью Р2А. Такая система позволяет осуществлять трансляцию mClover и защитную конструкцию с одной матричной РНК. Благодаря этому трансдуцированные клетки флюоресцируют и могут быть отсортированы.
Краткое описание чертежей
Фигура 1. Схема расположения защитных пептидов на поверхности клеточной мембраны: А - в контексте GPI-заякоренного белка CD52, Б - слитый с N-концом белка CXCR4.
Фигура 2. Схемы последовательностей, используемых в качестве донорных ДНК для внесения целевых мутаций: А - защитный пептид из gp41 в контексте GPI-заякоренного белка CD52 встраивается перед CXCR4 через P2A, Б - пептид сливается с N-концом CXCR4.
Фигура 3. Схема лентивирусного вектора, используемого для внесения защитного пептида из gp41 в контексте GPI-заякоренного белка CD52 с возможностью сортировки клеток, несущих целевую мутацию по зеленому флюоресцентному белку mClover (A), а также вектора, который используется в качестве матрицы для ПЦР-амплификации донорной ДНК (Б).
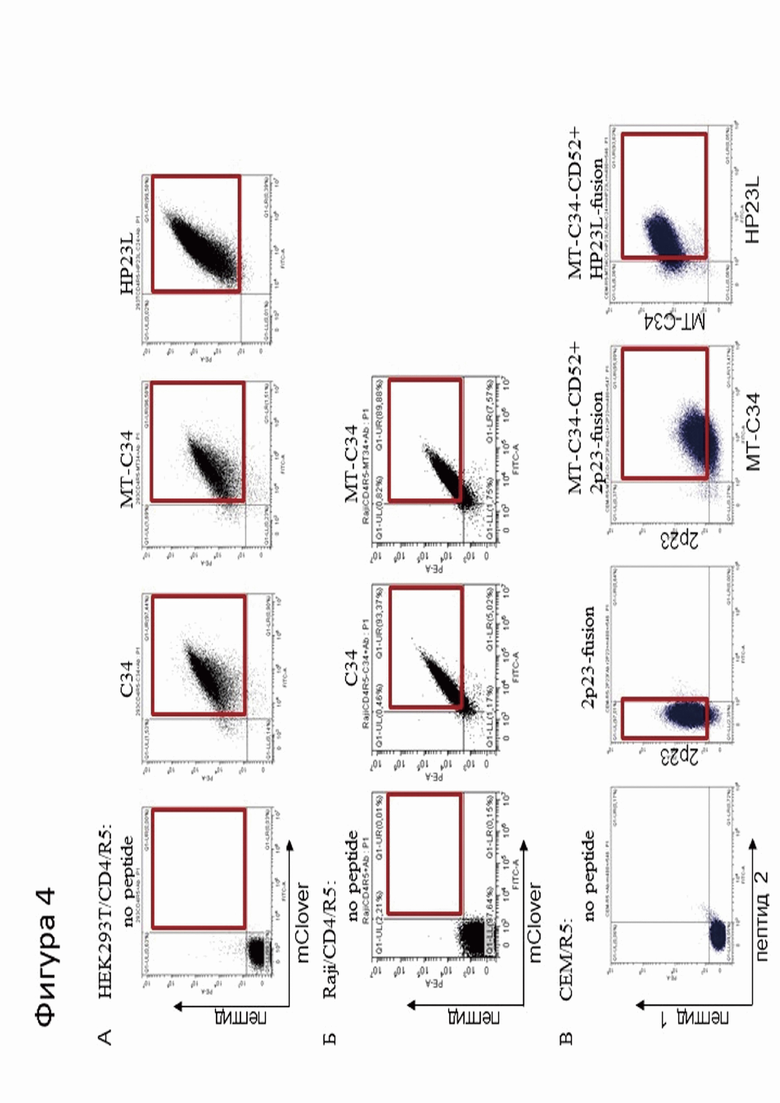
Фигура 4. Примеры иммунофлюоресцентного окрашивания клеточных линий, несущих пептид, ингибирующий проникновение ВИЧ: А - клеточные линии, полученные путем лентивирусной трансдукции на основе HEK293T/CD4/R5 с пептидами С34 и MT-C34, HP23L Б - клеточные линии, полученные путем лентивирусной трансдукции на основе Raji/CD4/R5 с пептидами C34 и MT-C34. В - клеточные линии, полученные на основе CEM/R5 путем CRISPR/Cas9-опосредованного биаллельного нокина пептидов 2P23, слитого с CXCR4, и MT-C34, экспрессирующегося в липидных рафтах отдельно от CXCR4.
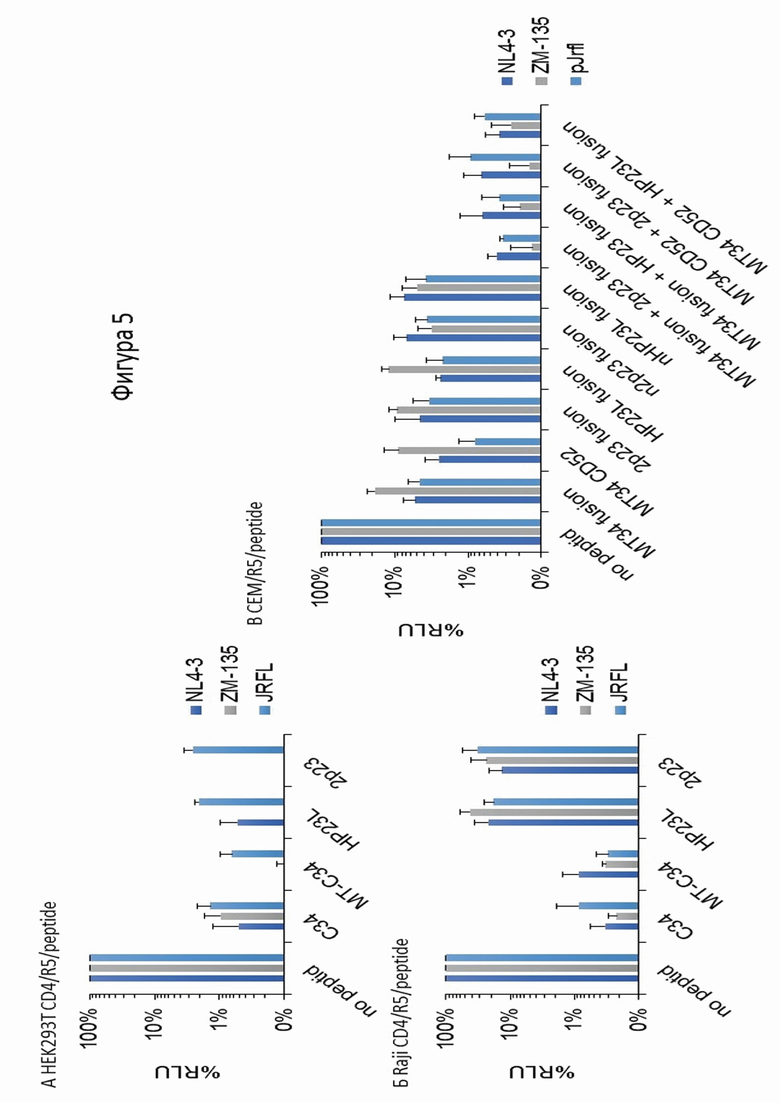
Фигура 5. Графическое представление результатов инфекционных тестов: А - Инфекция свободными вирусными частицами на клетках HEK293T/CD4/R5/peptide, Б - тест на межклеточную инфекцию от Raji к Raji/CD4/R5/peptide, В - тест на межклеточную инфекцию от Raji к CEM/R5/peptide.
Осуществление изобретения
Пример 1. Получение клеточных линий, несущих целевые конструкции, с помощью CRISPR/Cas9 и исследование эффективности
На основе клеточной линии CD4+ лимфобластов CEM-CCRF (CEM) была получена сублиния клеток CEM/R5, чувствительных к инфицированию ВИЧ-1 разной тропности за счет экспрессии молекул CD4, CCR5 и CXCR4, одна из которых была превнесена путем лентивирусной трансдукции CCR5-экспрессирующей конструкции.
На основе этой сублинии путем нокина были получены клеточные линии, несущие целевые конструкции с пептидом. Для этого использовали электропорацию с помощью прибора Neon Thermo Fisher в режиме, рекомендуемом производителем.
Смесь для электропорации включала следующие компоненты:
- pcDNA3.3-hCas9 (Addgene #41815) - плазмида, кодирующая Cas9 дикого типа;
- вектор pKS gRNA BB, экспрессирующий гидовую РНК, в состав которого включена gRNA SEQ ID №11;
- матрица-донор, полученный путем амплификации ПЦР, и представляющий собой последовательность, описанную выше (фиг. 2).
Получение ПЦР-донора:
ПЦР- доноры получены методом, описанным ранее Мазуровым Д.В. (Мазуров, 2020). В качестве матрицы для ПЦР выступают лентивирусные векторы (фиг. 3Б), несущие целевой пептид. В качестве праймеров использовались последовательности SEQ ID № 14-23, содержащие плечи гомологии (Таблица 1).
Таблица 1
3’-CXCR4start-in: SEQ ID № 15
3’-CXCR4start-in: SEQ ID № 15
3’-CXCR4start-in: SEQ ID № 15
3’-MT34-X4-in: SEQ ID № 17
3’-2P23-X4-in: SEQ ID № 19
3’-HP23L -X4-in: SEQ ID № 21
3’-n2P23-X4-in:
use 3’-2P23-X4-in (SEQ ID № 19)
3’-nHP23L -X4-in:
use 3’-HP23L-X4-in (SEQ ID № 21)
Амплификация проводилась при следующем режиме:
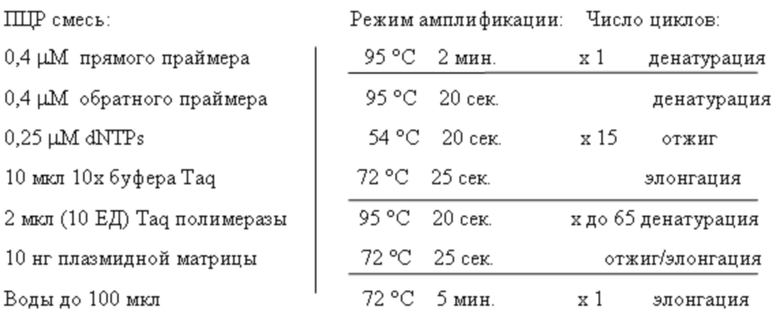
Описанным способом были получены клеточные линии с пептидом в контексте CD52: CEM/R5/MT34-CD52, слитым с CXCR4: CEM/R5/MT34-fusion, CEM/R5/2p23-fusion, CEM/R5/HP23L-fusion, CEM/R5/n2p23-fusion, CEM/R5/nHP23L-fusion и клеточные линии с биаллельным нокином: CEM/R5/MT34-CD52/2p23-fusion, CEM/R5/MT34-fusion/2p23-fusion, CEM/R5/MT34-CD52/HP23L-fusion, CEM/R5/MT34-fusion/HP23L-fusion (фиг. 4В). Сортировка клеток с целевой конструкцией проводилась путем иммунофлюоресцентного окрашивания. В качестве первичных антител были использованы антитела к соответствующим пептидам, полученные в нашей лаборатории; в качестве вторичных антител использовались коммерческие антитела, коньюгированные с флюоресцентной меткой. Выделение клеток с целевой конструкцией проводилось методом FACS - сортировки до достижения чистоты культуры не менее 98%.
С помощью RNP была получена клеточная линия CEM/R5/MT34-CD52/2p23-fusion-RNP путем электропорации клеток CEM/R5. Смесь для электропорации включала:
- белок RNP-gRNA
- ПЦР-донор, включающий пептид МТ34, соответствующий схеме фиг. 2А
- ПЦР-донор, включающий пептид 2р23, соответствующий схеме фиг. 2Б
Использовался режим, рекомендованный Neon Thermo Fisher.
Для исследования эффективности работы внесенных в клетку генетических конструкций, были проведены инфекционные тесты на межклеточную передачу с вирусами ВИЧ с разным тропизмом.
Для этого клетки Raji электропорировали с помощью прибора Neon Thermo Fisher, используя рекомендуемый производителем режим. Смесь для электропорации включала плазмиды pUCHR-inLuc-mR, pCMV-d8.2R и одним из энвелопов: NL4-3, JRFL или ZM135. Через 6 часов электропорированные клетки смешивали с тестируемыми клетками CEM/R5/peptide в соотношении 2:1. Все результаты были получены в трех независимых экспериментах. Проведенные инфекционные тесты показали, что технология эффективно защищает клетки от проникновения ВИЧ (фиг. 5В).
Благодаря совместимости технологии с разными системами на основе CRISPR/Cas9, технология легко адаптируема в соответствии с последними разработками в этой области.
Пример 2. Внесение целевой конструкции в клетку с помощью лентивирусного вектора и исследование эффективности
Для осуществления альтернативного варианта внесения конструкции в клетку на основе клеточных линий HEK293T и Raji были получены линии, чувствительные к инфицированию ВИЧ разной тропности - HEK293T/CD4/R5 и Raji/CD4/R5, экспрессирующие CD4, CCR5 и CXCR4, где CD4 и CCR5 были экзогенными и стабильно интегрированы с помощью лентивирусного вектора. Затем на их основе с помощью лентивирусного вектора, были получены клеточные линии, несущие на мембране один из GPI-заякоренных пептидов: HEK293T/CD4/R5/С34, HEK293T/CD4/R5/MT-C34, HEK293T/CD4/R5/MT-C34-R, HEK293T/CD4/R5/HP23L, HEK293T/CD4/R5/2p23 (фиг. 4А); Raji/CD4/R5/C34, Raji/CD4/R5/MT-C34, Raji/CD4/R5/HP23L, Raji/CD4/R5/2p23, Raji/CD4/R5nHP23L и Raji/CD4/R5n2p23 (фиг. 4Б).
Для это этого были получены лентивирусные псевдочастицы путем липофектной трансфекции HEK293T тремя плазмидами: pUCHR-mClover-P2A-CDpeptide52, содержащей последовательность целевого пептида в контексте CD52 (фиг. 3А), pCMVΔ8.2R - упаковочной плазмиды ВИЧ (Addgene # 12263) и pCMV-VSV-G (Addgene # 8454), экспрессирующей белок оболочки G вируса везикулярного стоматита. После трансфекции клетки инкубировали в течении 48 часов, после чего супернатант собирали и добавляли к клеточным линиям HEK293T/CD4/R5 и Raji/CD4/R5 в дозе, необходимой для получения не более чем 30% клеток с целевой конструкцией. Клетки с целевой конструкцией сортировали по mClover до достижения чистоты культуры не менее 98%.
Для оценки степени защиты клеток от ВИЧ, полученные клетки были проанализированы в одноцикловом псевдовирусном тесте. На клетках HEK293T/CD4/R5/peptide были поставлены инфекционные тесты с выделенными вирусными частицами. Для этого были наработаны псевдовирусные частицы, покрытые одним из трех оболочечных белков ВИЧ-1: CXCR4 - тропный NL4-3 и CCR5 - тропные JRFL и ZM-135. Клетки HEK293T были трансфицированы с помощью реагента Lipofectamine 2000 (ThermoFisher) в соответствии с инструкцией производителя тремя плазмидами: pUCHR-inLuc-mR, несущей ген люциферазы и необходимой для детекции проникновения вируса в клетку; упаковочной pCMV-d8.2R, и одним из оболочечных белков NL4-3, JRFL или ZM135. Спустя 48 часов вирусный супернатант собирали и фильтровали. Инфекционный тест проводили путем добавления вирусного супернатанта к тестируемой клеточной линии HEK293T/CD4/R5/peptide. В качестве контроля использовали клеточную линию HEK293T/CD4/R5. Спустя 48 часов клетки собирали, лизировали и измеряли люциферазную активность. Результаты представлены на фигуре 5А. Тест показал, что большинство GPI-заякоренных gp41 пептидов эффективно защищают клетку от проникновения ВИЧ-1.
Для теста на межклеточную передачу ВИЧ-1 клетки Raji электропорировали плазмидами pUCHR-inLuc-mR, pCMV-d8.2R и одним из оболочечных белков Env из штаммов ВИЧ-1 NL4-3, JRFL или ZM135. Трансфецированные клетки инкубировали 6 часов и смешивали с клетками-мишенями Raji/CD4/R5/peptide в соотношении 2:1 (фиг. 5Б). Через 72 часа совместного культивирования уровень инфекции измеряли по активности люциферазы к лизированных клетках. Результаты теста показали, что изобретенные конструкции эффективно защищают клетки от проникновения ВИЧ не только при инфекции свободными вирусными частицами, но блокируют межклеточную инфекцию ВИЧ-1, передающуюся при непосредственном контакте клетки-продуцента вируса с клеткой-мишенью. Все показанные результаты были получены как минимум в трех независимых экспериментах, что подтверждает описанные эффекты и их статистическую значимость.
Изобретение потенциально может быть использовано на CD4+ клетках человека для терапии ВИЧ.
Цитируемая литература
1. Мазуров Д.В. Селекция редактированных клеток методом SORTS. Глава 22 в монографии "Методы редактирования генов и геномов", Новосибирск, Издательство Сибирского отделения РАН, 2020.
2. Lalezari J.P., DeJesus E., Northfelt D.W. et al. A controlled phase II trial assessing three doses of enfuvirtide (T-20) in combination with abacavir, amprenavir, ritonavir and efavirenz in nonnucleoside reverse transcriptase inhibitor-naive HIV-infected adults. Antivir. Ther. 2003; 8: 279-287.
3. Leslie GJ, Wang J, Richardson MW, Haggarty BS, Hua KL, Duong J, Secreto AJ, Jordon AP, Romano J, Kumar KE, DeClercq JJ, Gregory PD, June CH, Root MJ, Riley JL, Holmes MC, Hoxie JA. Potent and Broad Inhibition of HIV-1 by a Peptide from the gp41 Heptad Repeat-2 Domain Conjugated to the CXCR4 Amino Terminus. PLoS Pathog. 2016 Nov 17;12(11): e1005983. doi: 10.1371/journal.ppat.1005983
4. Xiaoran Tang, Hongliang Jin, Yue Chen, Li Li, Yuanmei Zhu, Huihui Chong, Yuxian He. A Membrane-Anchored Short-Peptide Fusion Inhibitor Fully Protects Target Cells from Infections of Human Immunodeficiency Virus Type 1 (HIV-1), HIV-2, and Simian Immunodeficiency Virus, Journal of Virology Oct 2019, 93 (22) e01177-19; DOI: 10.1128/JVI.01177-19
5. Zotova, A., Pichugin, A., Atemasova, A. et al. Isolation of gene-edited cells via knock-in of short glycophosphatidylinositol-anchored epitope tags. Sci Rep 9, 3132 (2019). https://doi.org/10.1038/s41598-019-40219-z
--->
<110> Федеральное государственное бюджетное учреждение науки Институт биологии
гена Российской академии наук (Institute of Gene Biology Russian Academy of
Sciences)
<120> Технология создания Т-клеточной устойчивости к ВИЧ-1 на основе
генетически-кодируемых GPI-заякоренных пептидов из gp41
<160> 24
<210> 1
<211> 28
<212> PRT
<213> H.sapiens
<400> 1
Lys Arg Phe Leu Phe Leu Leu Leu Thr Ile Ser Leu Leu Val Met Val 16
1 5 10 15
Gln Ile Gln Thr Gly Leu Ser Gly Gln Asn Asp Thr 28
20 25
<210> 2
<211> 23
<212> PRT
<213> H.sapiens
<400> 2
Lys Arg Phe Leu Phe Leu Leu Leu Thr Ile Ser Leu Leu Val Met Val 16
1 5 10 15
Gln Ile Gln Thr Gly Leu Ser 23
20
<210> 3
<211> 27
<212> PRT
<213> H.sapiens
<223> Umb – стоп-кодон
<400> 3
Ser Ala Ser Ser Asn Ile Ser Gly Gly Ile Phe Leu Phe Phe Val Ala 16
1 5 10 15
Asn Ala Ile Ile His Leu Phe Cys Phe Ser Umb 27
20 25
<210> 4
<211> 34
<212> PRT
<213> artificial sequence
<220> PEPTIDE
<223> C-34
<400> 4
Trp Met Glu Trp Asp Arg Glu Ile Asn Asn Tyr Thr Ser Leu Ile His 16
1 5 10 15
Ser Leu Ile Glu Glu Ser Gln Asn Gln Gln Glu Lys Asn Glu Gln Glu 32
20 25 30
Leu Leu 34
<210> 5
<211> 36
<212> PRT
<213> artificial sequence
<220> PEPTIDE
<223> MT C-34
<400> 5
Met Thr Trp Met Glu Trp Asp Arg Glu Ile Asn Asn Tyr Thr Ser Leu 16
1 5 10 15
Ile His Ser Leu Ile Glu Glu Ser Gln Asn Gln Gln Glu Lys Asn Glu 32
20 25 30
Gln Glu Leu Leu 36
35
<210> 6
<211> 23
<212> PRT
<213> artificial sequence
<220> PEPTIDE
<223> HP23L
<400> 6
Glu Leu Thr Trp Glu Glu Trp Glu Lys Lys Ile Glu Glu Tyr Thr Lys 16
1 5 10 15
Lys Ile Glu Glu Ile Leu Lys 23
20
<210> 7
<211> 23
<212> PRT
<213> artificial sequence
<220> PEPTIDE
<223> 2P23
<400> 7
Glu Met Thr Trp Glu Glu Trp Glu Lys Lys Ile Glu Glu Tyr Thr Lys 16
1 5 10 15
Lys Ile Glu Glu Ile Leu Lys 23
20
<210> 8
<211> 24
<212> PRT
<213> artificial sequence
<220> PEPTIDE
<223> nHP23L
<400> 8
Gly Asn Leu Thr Trp Glu Glu Trp Glu Lys Lys Ile Glu Glu Tyr Thr 16
1 5 10 15
Lys Lys Ile Glu Glu Ile Leu Lys 24
20
<210> 9
<211> 24
<212> PRT
<213> artificial sequence
<220> PEPTIDE
<223> n2p23
<400> 9
Gly Asn Met Thr Trp Glu Glu Trp Glu Lys Lys Val Glu Glu Leu Glu 16
1 5 10 15
Lys Lys Ile Glu Glu Leu Leu Lys 24
20
<210> 10
<211> 21
<212> ДНК
<213> H.sapiens
<400> 10
gagaaccagc ggttaccatg g 21
<210> 11
<211> 89
<212> ДНК
<213> H.sapiens
<400> 11
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacc 89
<210> 12
<211> 96
<212> ДНК
<213> H.sapiens
<400> 12
gag ggg atc agt gta agt cca gtt tca acc tgc ttt gtc ata aat gta caa acg ttt gaa 60
ctt aga gcg cag ccc ctc tcc gag cgg gca gaa gcg 96
<210> 13
<211> 66
<212> ДНК
<213> H.sapiens
<400> 17
ggatccggcg caacaaactt ctctctgctg aaacaagccg gagatgtcga agagaatcct 60
ggaccg 66
<210> 14
<211> 105
<212> ДНК
<213> artificial sequence
<220>
<223> 5’-CXCR4start-in
<400> 14
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacca ccatgaagcg cttcc 105
<210> 15
<211> 114
<212> ДНК
<213> artificial sequence
<220>
<223> 3’-CXCR4start-in
<400> 15
cgcttctgcc cgctcggaga ggggctgcgc tctaagttca aacgtttgta catttatgac 60
aaagcaggtt gaaactggac ttacactgat cccctcggcc ggtccaggat tctc 114
<210> 16
<211> 106
<212> ДНК
<213> artificial sequence
<220>
<223> 5’-MT34-X4-in
<400> 16
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacca tgacctggat ggagtg 106
<210> 17
<211> 112
<212> ДНК
<213> artificial sequence
<220>
<223> 3’-MT34-X4-in
<400> 17
cgcttctgcc cgctcggaga ggggctgcgc tctaagttca aacgtttgta catttatga 60
aaagcaggtt gaaactggac ttacactgat cccctccagg agctcctgct cg 112
<210> 18
<211> 110
<212> ДНК
<213> artificial sequence
<220>
<223> 5’-2P23-X4-in
<400> 18
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacca tggagatgac ctgggaagag 110
<210> 19
<211> 115
<212> ДНК
<213> artificial sequence
<220>
<223> 3’-2P23-X4-in
<400> 19
cgcttctgcc cgctcggaga ggggctgcgc tctaagttca aacgtttgta catttatgac 60
aaagcaggtt gaaactggac ttacactgat cccctccttg agcagctctt cgatt 115
<210> 20
<211> 110
<212> ДНК
<213> artificial sequence
<220>
<223> 5’-HP23L-X4-in
<400> 20
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacca tggagctgac ctgggaagag 110
<210> 21
<211> 116
<212> ДНК
<213> artificial sequence
<220>
<223> 3’-HP23L -X4-in
<400> 21
cgcttctgcc cgctcggaga ggggctgcgc tctaagttca aacgtttgta catttatgac 60
aaagcaggtt gaaactggac ttacactgat cccctccttg aggatctctt cgattt 116
<210> 22
<211> 110
<212> ДНК
<213> artificial sequence
<220>
<223> 5’-n2P23-X4-in
<400> 22
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacca tgggcaacat gacctgggaa 110
<210> 23
<211> 110
<212> ДНК
<213> artificial sequence
<220>
<223> 5’-nHP23L-X4-in
<400> 23
agtttgttgg ctgcggcagc aggtagcaaa gtgacgccga gggcctgagt gctccagtag 60
ccaccgcatc tggagaacca gcggttacca tgggcaacct gacctgggaa 110
<---
Изобретение относится к области биотехнологии, в частности к способам редактирования клеточного гена CXCR4 в целях предотвращения инфицирования CD4 лимфобластов человека ВИЧ-1 с помощью системы редактирования CRISPR/Cas. Способы предусматривают электропорацию клеток CD4 лимфобластов смесью для электропорации, состоящей из эффективного количества гидовой РНК, эндонуклеазы Cas9 и донорной ДНК, а также нокин или направленное встраивание нуклеотидной последовательности, кодирующей защитный пептид группы gp41, под эндогенный промотор гена CXCR4. Изобретение эффективно для терапии ВИЧ-1. 3 н.п. ф-лы, 5 ил., 1 табл., 2 пр.
1. Способ редактирования клеточного гена CXCR4 в целях предотвращения инфицирования CD4 лимфобластов человека ВИЧ-1 с помощью системы редактирования CRISPR/Cas,
включающий следующие стадии:
а) электропорация клеток CD4 лимфобластов смесью для электропорации, состоящей из эффективного количества гидовой РНК последовательностью SEQ ID 10, эндонуклеазы Cas9 и донорной ДНК, несущей нуклеотидную последовательность, кодирующую защитный пептид группы gp41 и встроенную между лидерной последовательностью белка CD52 и сигналом GPI-заякоривания белка CD52;
при этом донорная ДНК имеет следующую формулу:
- плечо гомологии 5’ последовательностью SEQ ID 11;
- лидерная последовательность CD52 последовательностью SEQ ID 1 или SEQ ID 2;
- защитный пептид группы gp41 MT-C34 последовательностью SEQ ID 5;
- сигнал GPI-заякоривания последовательностью CD52 SEQ ID 3;
- последовательность Р2А, позволяющая получить с одной РНК трансляцию двух белковых продуктов, последовательностью SEQ ID 13;
- плечо гомологии 3’ последовательностью SEQ ID 12;
б) нокин или направленное встраивание нуклеотидной последовательности, кодирующей защитный пептид группы gp41, под эндогенный промотор гена CXCR4;
в) экспонирование защитного пептида группы gp41 на поверхности клетки в липидных рафтах.
2. Способ редактирования клеточного гена CXCR4 в целях предотвращения инфицирования CD4 лимфобластов человека ВИЧ-1 с помощью системы редактирования CRISPR/Cas,
включающий следующие стадии:
а) электропорацию клеток CD4 лимфобластов смесью для электропорации, состоящей из эффективного количества гидовой РНК последовательностью SEQ ID 10, эндонуклеазы Cas9 и донорной ДНК, несущую нуклеотидную последовательность, кодирующую защитный пептид группы gp41,
при этом донорная ДНК имеет формулу:
плечо гомологии 5’ последовательностью SEQ ID 11;
защитный пептид группы gp41, выбранный из С34, MT-C34, HP23L, 2p23, nHP23L, n2p23 последовательностями SEQ ID 4, 5, 6, 7, 8 и 9 соответственно;
плечо гомологии 3’ последовательностью SEQ ID 12;
б) нокин или направленное встраивание нуклеотидной последовательности, кодирующей защитный пептид группы gp41, под эндогенный промотор гена CXCR4;
в) слияние защитного пептида группы gp41 с N-концом эндогенного CXCR4.
3. Способ редактирования клеточного гена CXCR4 в целях предотвращения инфицирования CD4 лимфобластов человека ВИЧ-1 с помощью системы редактирования CRISPR/Cas, включающий редактирование клеточного гена CXCR4 способом по п. 1 или 2, отличающийся тем, что при электропорации используются одновременно две донорные ДНК в соотношении 1:1, что приводит к сочетанию заякоренного пептида и пептида, слитого с CXCR4.
| МАСЛЕННИКОВА А.К.Ю | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| МАЗУРОВ Д.В | |||
| и др | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| PANPAN HOU et al., | |||
Авторы
Даты
2022-04-04—Публикация
2020-12-24—Подача