Область техники, к которой относится изобретение
Настоящее изобретение относится к получению жидкого топлива с применением синтез-газа, и, в частности, оно относится к катализатору и способу прямой конверсии синтез-газа для получения жидкого топлива.
Уровень техники
По мере развития экономики и повышения уровня жизни также с каждым годом стремительно увеличивается необходимое количество жидкого топлива и химической продукции. На сегодняшний день производство бензина в целом основано на каталитическом риформинге тяжелого лигроина. По мере того как мировые нефтяные ресурсы с каждым днем истощаются, цена на сырую нефть остается высокой. В частности, недостаток в нефтяных ресурсах испытывает Китай, в котором каждый год больше чем приблизительно 60% объема потребления нефти зависит от импорта, и поиск технологических процессов, которые могут стать альтернативой, а также разработка и применение способов, позволяющих получать жидкое топливо из угля, биомассы и прочих источников углерода, не основанных на нефти, имеют важное социальное и стратегическое значение.
Китай богат угольными ресурсами, и из угля в качестве сырья с помощью газификации получают синтез-газ (а именно смесь газов CO и H2); синтез-газ превращают в метанол; внедренный технологический процесс, в котором из метанола затем посредством диметилового эфира получают бензин, был завершен, и при внедрении для целей индустриализации этот процесс обеспечил важный путь в отношении угля, природного газа и прочих источников углерода для получения жидкого топлива. Тем не менее, если бы можно было осуществить прямую конверсию синтез-газа, то прямой путь, в котором не выполняется синтез метанола и дегидрирование метанола для получения диметилового эфира, позволил бы не только упростить технологический процесс, но и позволил бы сократить количество отдельных операций и тем самым снизить объем капиталовложений и потребления энергии. Традиционный процесс Фишера-Тропша позволяет осуществлять прямую конверсию синтез-газа для получения жидкого топлива, однако он ограничен своим механизмом реакции; молекулы CO и H2 на поверхности катализатора подвергаются диссоциативной адсорбции и на поверхности возникают атомы C и атомы O; атомы C и атомы O вступают в реакцию с водородом, адсорбированным на поверхности катализатора, с образованием промежуточного продукта в виде метилена (CH2), при этом высвобождаются молекулы воды. Промежуточный продукт в виде метилена мигрирует и подвергается реакции внедрения, и на поверхности катализатора осуществляется свободная полимеризация с образованием продукта в виде алкана, содержащего разное число атомов углерода (от одного до тридцати, а то и до сотен атомов углерода). Распределение числа атомов углерода для продукта в виде алкана после всей реакции является широким, при этом селективность в отношении целевого продукта является низкой, например селективность в отношении бензина составляет менее 50%. С помощью двухфункционального катализатора, состоящего из оксида и молекулярного сита, можно разделить активацию CO и сопряжение C-C в двух активных центрах, чтобы тем самым преодолеть ограничение селективности в отношении продукта в традиционном процессе Фишера-Тропша, и можно было получить высокую селективность в отношении бензина. Тем не менее в случае некоторых молекулярных сит, подходящих для синтеза бензиновой фракции, например молекулярного сита ZSM-5, которое применяется чаще всего, легко образуются ароматические углеводороды, из-за чего в полученном бензине содержание ароматических углеводородов чрезмерно высокое, что нарушает экологические требования. Поэтому крайне необходимо разработать катализатор, который предназначен для получения жидкого топлива в виде бензиновой фракции (C5-C11) с применением высокоактивного синтез-газа, при этом обеспечивается высокая селективность в отношении бензина при сравнительно низкой селективности в отношении ароматических углеводородов в бензине.
Суть изобретения
Для решения вышеуказанных проблем согласно настоящему изобретению предложены катализатор и способ прямой конверсии синтез-газа для получения жидкого топлива.
Технические решения согласно настоящему изобретению являются следующими.
Согласно одному аспекту настоящего изобретения предложен двухфункциональный смешанный катализатор, при этом указанный катализатор содержит компонент Ⅰ и компонент Ⅱ; указанные компонент Ⅰ и компонент Ⅱ объединены друг с другом путем механического перемешивания; активная составляющая компонента Ⅰ представляет собой оксид металла; компонент II представляет собой одно, два или более из молекулярного сита с образованными десятичленными кольцами одномерными каналами и с топологической структурой TON, или AEL, или MTT, или MRE или молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE, модифицированное металлом; указанный оксид металла представляет собой один, два или более из MnOx, MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnO, ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CeO2, CoAlyO(1+1,5y), FeAlyO(1+1,5y), Ga2O3, Bi2O3, In2O3, InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z); диапазон значений указанного x составляет 1-3,5; диапазон значений y составляет 0,1-10; диапазон значений z составляет 0,1-10;
удельная площадь поверхности указанных MnOx, ZnO, CeO2, Ga2O3, Bi2O3, In2O3 составляет 1-100 м2/г;
удельная площадь поверхности указанных MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CoAlyO(1+1,5y), FeAlyO(1+1,5y), InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z) составляет 5-150 м2/г.
Указанное молекулярное сито с образованными десятичленными кольцами одномерными каналами представляет собой молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE; молекулярное сито с TON, или AEL, или MTT, или MRE содержит образованные десятичленными кольцами одномерные каналы.
Согласно рассмотренному выше техническому решению является предпочтительным, если указанное молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE содержит структуру с образованными десятичленными кольцами одномерными каналами, при этом элементный состав его каркаса может представлять собой один, два или более из Si-O, Si-Al-O, Si-Al-P-O, Al-P-O, Ga-P-O, Ga-Si-Al-O, Zn-Al-P-O, Mg-Al-P-O, Co-Al-P-O, при этом молекулярное сито этого типа предпочтительно представляет собой одно, два или более из SAPO-11, или ZSM-22, или ZSM-23, или ZSM-48.
Согласно рассмотренному выше техническому решению является предпочтительным, если указанное молекулярное сито AEL содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,05-0,5 моль/кг; предпочтительно составляет 0,05-0,4 моль/кг, более предпочтительно составляет 0,05-0,3 моль/кг; указанное молекулярное сито TON содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,005-0,6 моль/кг; предпочтительно составляет 0,005-0,4 моль/кг, более предпочтительно составляет 0,005-0,2 моль/кг.
Молекулярное сито в указанном компоненте II может быть самостоятельно синтезированным, а также может быть имеющимся на рынке продуктом, который должен удовлетворять требования, определенные в объеме настоящего изобретения.
Указанная концентрация кислоты определена на основании пиков TPD NH3 и включает три типа кислотности, а именно слабую кислоту, кислоту средней силы и сильную кислоту;
TPD NH3 основана на положениях десорбционных пиков NH3, при этом под положениями десорбционных пиков подразумевается то, что в стандартных условиях испытания, то есть в условиях испытания, при которых отношение массы образца w к расходу газа-носителя f (w/f) равно 100 г⋅ч./л, а скорость прироста тепла составляет 10°C/мин., на основании сигнала теплопроводности в отношении десорбции NH3, регистрируемого с помощью TCD, строится кривая десорбции, и на основании положений самых верхних точек пиков на кривой неорганические твердые вещества разделяются по трем типам силы кислоты; слабая кислота подразумевает кислотные центры с температурой десорбции NH3, которая составляет менее 275°C; кислота средней силы подразумевает кислотные центры с температурой десорбции NH3 200-500°C; сильная кислота подразумевает кислотные центры с температурой десорбции NH3, которая составляет более 500°C. Указанное молекулярное сито может быть получено в лаборатории, а также может быть приобретено у поставщиков и удовлетворяет требованиям, определенным в настоящем изобретении.
При применении ацетона в качестве молекулярного зонда химический сдвиг 13C-ЯМР находится в диапазоне 210-220 ppm.
Согласно рассмотренному выше техническому решению является предпочтительным, если весовое отношение активной составляющей в компоненте Ⅰ к компоненту Ⅱ составляет 0,1-20, предпочтительно составляет 0,3-5.
Согласно рассмотренному выше техническому решению является предпочтительным, если в указанный компонент I также добавлено диспергирующее средство, при этом оксид металла диспергирован в диспергирующем средстве; указанное диспергирующее средство представляет собой одно, два или более из Al2O3, SiO2, Cr2O3, ZrO2, TiO2, Ga2O3, активированного угля, графена и углеродных нанотрубок.
Согласно рассмотренному выше техническому решению является предпочтительным, если содержание диспергирующего средства в указанном компоненте I составляет 0,05-90 вес. %, остальное представляет собой оксид металла.
Согласно рассмотренному выше техническому решению является предпочтительным, если элемент O каркаса указанного молекулярного сита, представляющего собой компонент II, может быть соединен или не соединен с H; и указанный H посредством метода ионного обмена может быть полностью или частично замещен одним, двумя или более из Na, Mg, K, Mn, Ag, Mo, Cr, Fe, Co, Ca, Pt, Pd, Ti, Zn, Ga, Ba и Ge, при этом после замещения общее молярное отношение металла к кислороду составляет 0,0002-0,02.
Согласно другому аспекту настоящего изобретения предложен способ прямой конверсии синтез-газа для получения жидкого топлива, в котором с синтез-газом в качестве сырья для реакции в условиях неподвижного слоя или подвижного слоя проводят реакцию конверсии, при этом применяемый катализатор представляет собой вышеуказанный двухфункциональный смешанный катализатор.
Согласно рассмотренному выше техническому решению является предпочтительным, если давление указанного синтез-газа составляет 0,5-10 МПа, предпочтительно 1-8 МПа; температура реакции составляет 300-600°C, предпочтительно 350-450°C; объемная скорость составляет 300-12000 ч.−1, предпочтительно 1000-9000 ч.−1, более предпочтительно 3000-9000 ч.−1; указанный синтез-газ представляет собой смесь газов H2/CO, отношение H2/CO составляет 0,2-3,5, предпочтительно 0,3-2,5.
Согласно рассмотренному выше техническому решению является предпочтительным, если с применением указанного двухфункционального смешанного катализатора путем одноэтапной прямой конверсии синтез-газа получают жидкое топливо, при этом селективность в отношении жидкого топлива может достигать 50-80%, предпочтительно составляет 65-80%; селективность в отношении ароматических C5-C11-углеводородов составляет менее 40%, предпочтительно составляет менее 30%; при этом селективность в отношении метана как побочного продукта составляет менее 15%, предпочтительно составляет менее 10%.
Настоящее изобретение характеризуется следующими преимуществами.
1. Предложенная технология получения жидкого топлива отличается от традиционного процесса Фишера-Тропша в том, что с высокой эффективностью осуществляется одноэтапная прямая конверсия синтез-газа в жидкое топливо и при этом значительно снижается селективность в отношении ароматических углеводородов в жидком топливе.
2. Селективность в отношении жидкого топлива в продукте является высокой и может достигать 50-80%, при этом продукт не нужно подвергать глубокому охлаждению и можно сразу разделять, что значительно снижает потребление энергии и расходы в отношении разделения.
3. В катализаторе оксид металла в качестве активной составляющей компонента I обладает относительно высокой удельной площадью поверхности, поэтому на поверхности оксида металла расположено больше активных центров, что больше способствует прохождению каталитической реакции.
4. Компонент II в катализаторе, с одной стороны, предназначен для обеспечения за счет взаимодействия с компонентом I дополнительной конверсии промежуточного продукта в активной газовой фазе, полученного с помощью компонента I, с получением жидкого топлива, при этом действие компонента II, приводящее каскадную реакцию к равновесию, может способствовать активной конверсии синтез-газа со стороны компонента I и повышать степень конверсии; с другой стороны, особая структура с образованными десятичленными кольцами каналами молекулярного сита, которым является компонент II в соответствии с настоящим изобретением, характеризуется уникальным эффектом отбора, и можно с высокой селективностью получать больше продукта в виде жидкого топлива, при этом значительно снижается содержание ароматических углеводородов в жидком топливе.
5. Применение по отдельности компонента I или компонента II в соответствии с настоящим изобретением абсолютно не может обеспечить выполнение цели настоящего изобретения. Например, селективность в отношении метана в продукте, полученном с применением исключительно компонента I, является очень высокой, а степень конверсии - очень низкой, тогда как при применении исключительно компонента II практически невозможна активная конверсия синтез-газа, поэтому только за счет катализа, обеспечиваемого взаимодействием компонента I с компонентом II, можно получить высокоэффективную конверсию синтез-газа, а также получить отличную селективность. Это обусловлено тем, что компонент I может активировать синтез-газ с получением особого промежуточного продукта в активной газовой фазе; промежуточный продукт за счет газовой диффузии попадает в каналы в компоненте II; поскольку молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE, выбранное в соответствии с настоящим изобретением, характеризуется особой структурой с образованными десятичленными кольцами одномерными каналами и кислотностью, можно эффективно осуществлять активную конверсию промежуточного продукта в активной газовой фазе, полученного с помощью компонента I, в жидкое топливо, при этом поддерживается сравнительно низкая селективность в отношении ароматических углеводородов (<40%). Указанное молекулярное сито отличается от молекулярного сита с восьмичленными кольцами для образования одномерной структуры и от молекулярного сита с двенадцатичленными кольцами, а также с десятичленными кольцами для образования двухмерной и трехмерной структуры, при этом в случае продукта с восьмичленными кольцами для образования одномерной структуры в целом основными являются углеводороды с короткой цепью (C2-C4); несмотря на то что в продукте, полученном с применением молекулярного сита с двенадцатичленными кольцами для образования одномерной структуры, доля продукта с длинной углеродной цепью является относительно высокой, содержание ароматических углеводородов в таком продукте, однако, выше, чем в продукте, полученном с применением молекулярного сита с десятичленными кольцами для образования одномерной структуры; несмотря на то что в случае молекулярных сит с десятичленными кольцами для образования двухмерной структуры и десятичленными кольцами для образования трехмерной структуры можно получить сравнительно большое количество высокоуглеродистого продукта, селективность в отношении ароматических углеводородов с длинной цепью, однако, является высокой, что нарушает экологические требования. Благодаря особой структуре с каналами компонента II получают продукт, характеризующийся особой селективностью.
6. Способ получения заявленного смешанного катализатора характеризуется простыми и умеренными условиями; кроме того, реакционный процесс характеризуется высокими выходом продукта и селективностью; селективность в отношении жидкого топлива, образованного фракцией C5-C11, может достигать 50-80%, при этом селективность в отношении ароматических C5-C11-углеводородов составляет менее 40%, а селективность в отношении метана как побочного продукта является низкой (<15%).
Конкретные варианты осуществления
Ниже настоящее изобретение описано более подробно с помощью вариантов осуществления, но объем правовой охраны настоящего изобретения этими вариантами осуществления не ограничивается. При этом в этих вариантах осуществления представлена только часть условий для осуществления основных целей, но это не означает, что для достижения этих основных целей эти условия необходимо выполнить обязательно.
Удельная площадь поверхности образцов может быть испытана путем проведения физической адсорбции азота или аргона.
Оксиды металла, указанные в настоящем изобретении, можно обеспечивать путем закупки оксидов металла с высокой удельной площадью поверхности, имеющихся на рынке, а также они могут быть получены с применением следующих нескольких способов.
1. Получение компонента Ⅰ катализатора
(I). Синтезирование материала ZnO с высокой удельной поверхностью с применением метода осаждения
(1). В 3 сосуда соответственно отвешивали 3 части Zn(NO3)2·6H2O, при этом масса каждой части составляла 0,446 г (1,5 ммоль); затем соответственно отвешивали 0,795 г (7,5 ммоль), 1,272 г (12 ммоль), 1,908 г (18 ммоль) NaCO3 и последовательно добавляли в вышеуказанные 3 сосуда; затем в 3 сосуда добавляли деионизированную воду в количестве 30 мл; при температуре 70°C перемешивали в течение 0,5 ч. или дольше с обеспечением равномерного смешивания раствора; обеспечивали естественное охлаждение до комнатной температуры. Реакционный раствор центрифугировали, собирали осадок после центрифугирования и промывали 2 раза деионизированной водой с получением предшественника оксида металла ZnO.
(2). Прокаливание: вышеуказанный полученный продукт после горячей сушки в атмосфере воздуха подвергали прокаливанию в определенной атмосфере с получением материала ZnO с высокой удельной поверхностью. Атмосфера представляет собой инертный газ, восстановительный газ или окислительный газ; инертный газ представляет собой один, два или более из N2, He и Ar; восстановительный газ представляет собой один или два из H2 и CO, при этом восстановительный газ также может содержать инертный газ; окислительный газ представляет собой один, два или более из O2, O3 и NO2, при этом окислительный газ также может содержать инертный газ. Температура прокаливания составляет 300-700°C, а его длительность составляет от 0,5 ч. до 12 ч.
Цель прокаливания заключается в том, чтобы в условиях высокой температуры разложить предшественник оксида металла после осаждения на наночастицы оксида с высокой удельной площадью поверхности; кроме того, путем высокотемпературной обработки при прокаливании поверхность полученного в результате разложения оксида можно очистить от адсорбирующего вещества.
Конкретные образцы и условия их получения приведены в таблице 1, при этом в таблице в качестве сравнительного образца представлен ZnO4, который представляет собой доступный для приобретения монокристаллический ZnO с низкой удельной площадью поверхности.
Таблица 1. Получение материала ZnO и его рабочие параметры

(II). Синтезирование материала MnOx с высокой удельной площадью поверхности с применением метода совместного осаждения
Способ получения такой же, как и для вышеуказанного ZnO2, и разница заключается в том, что содержащий Zn предшественник заменили на соответствующий содержащий Mn предшественник, который может быть одним из нитрата марганца, хлорида марганца и ацетата марганца; в данном случае это нитрат марганца; соответствующий продукт определен как MnOx; x=1; удельная площадь поверхности составляет 43 м2/г.
(III). Синтезирование материала CeO2 с высокой удельной площадью поверхности с применением метода совместного осаждения
Способ получения такой же, как и для вышеуказанного ZnO2, и разница заключается в том, что содержащий Zn предшественник заменили на соответствующий содержащий Ce предшественник, который может быть одним из нитрата церия, хлорида церия и ацетата церия; в данном случае это нитрат церия; соответствующий продукт определен как CeO2; удельная площадь поверхности составляет 92 м2/г.
(IV). Синтезирование материала Ga2O3 с высокой удельной площадью поверхности с применением метода совместного осаждения
Способ получения такой же, как и для вышеуказанного ZnO2, и разница заключается в том, что содержащий Zn предшественник заменили на соответствующий содержащий Ga предшественник, который может быть одним из нитрата галлия, хлорида галлия и ацетата галлия; в данном случае это нитрат галлия; соответствующий продукт определен как Ga2O3; удельная площадь поверхности составляет 55 м2/г.
(V). Синтезирование материала Bi2O3 с высокой удельной площадью поверхности с применением метода совместного осаждения
Способ получения такой же, как и для вышеуказанного ZnO2, и разница заключается в том, что содержащий Zn предшественник заменили на соответствующий содержащий Bi предшественник, который может быть одним из нитрата висмута, хлорида висмута и ацетата висмута; в данном случае это нитрат висмута. Соответствующий продукт определен как Bi2O3; удельная площадь поверхности соответственно составляет 87 м2/г.
(VI). Синтезирование материала In2O3 с высокой удельной площадью поверхности с применением метода совместного осаждения
Способ получения такой же, как и для вышеуказанного ZnO2, и разница заключается в том, что содержащий Zn предшественник заменили на соответствующий содержащий In предшественник, который может быть одним из нитрата индия, хлорида индия и ацетата индия; в данном случае это нитрат индия; соответствующий продукт определен как In2O3; удельная площадь поверхности составляет 52 м2/г.
(VII). Синтезирование материала MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CoAlyO(1+1,5y), FeAlyO(1+1,5y), InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z) с высокой удельной площадью поверхности с применением метода осаждения:
В качестве предшественника применяли нитрат цинка, нитрат алюминия, нитрат хрома, нитрат марганца, нитрат циркония, нитрат галлия, нитрат индия, нитрат кобальта и нитрат железа, которые при комнатной температуре смешивали в воде с карбонатом аммония (при этом карбонат аммония используется в качестве осаждающего реагента; отношение сырья при загрузке предусматривает избыток карбоната аммония, или предпочтительно отношение ионов аммония к ионам металла составляет 1:1); вышеуказанную смесь выдерживали, затем извлекали, промывали, фильтровали и высушивали; полученное твердое вещество прокаливали в атмосфере воздуха и получали оксид металла с высокой удельной поверхностью. Конкретные образцы и условия их получения приведены в таблице 2.
Таблица 2. Получение оксида металла с высокой удельной площадью поверхности и его рабочие параметры

(VIII). Оксид металла, диспергированный в диспергирующем средстве Cr2O3, Al2O3 или ZrO2
С диспергирующим средством Cr2O3, Al2O3 или ZrO2 в качестве носителя, посредством способа осаждения седиментацией получали оксид металла, диспергированный в Cr2O3, Al2O3 или ZrO2. В качестве примера приведено получение диспергированного ZnO, в соответствии с которым доступный на рынке Cr2O3 (удельная площадь поверхности составляла приблизительно 5 м2/г), Al2O3 (удельная площадь поверхности составляла приблизительно 20 м2/г) или ZrO2 (удельная площадь поверхности составляла приблизительно 10 м2/г) в качестве носителя предварительно диспергировали в воде; затем с применением нитрата цинка в качестве сырья при комнатной температуре смешивали с осаждающим реагентом, представляющим собой карбонат натрия, для осаждения, при этом молярная концентрация Zn2+ составляла 0,067 М, а числовое соотношение мольных долей Zn2+ и осаждающего реагента составляло 1:8; затем при температуре 160°C выдерживали 24 часа и получали ZnO, диспергированный в Cr2O3, Al2O3 или ZrO2 в качестве носителя (содержание диспергирующего средства в компоненте I составляло соответственно 0,1 вес. %, 20 вес. % и 85 вес. %). Полученные образцы в атмосфере воздуха при температуре 500°C прокаливали в течение 1 ч.; продукты соответственно определяли как дисперсные оксиды 1-3, у которых удельная площадь поверхности составляла соответственно 148 м2/г, 115 м2/г и 127 м2/г.
Аналогичным образом можно получать оксид MnO, диспергированный в SiO2 (удельная площадь поверхности составляла приблизительно 2 м2/г), Ga2O3 (удельная площадь поверхности составляла приблизительно 10 м2/г) или TiO2 (удельная площадь поверхности составляла приблизительно 15 м2/г) в качестве носителя (содержание диспергирующего средства в компоненте Ⅰ составляло соответственно 5 вес. %, 30 вес. %, 60 вес. %); продукты соответственно определяли как дисперсные оксиды 4-6. У них удельная площадь поверхности составляла соответственно 97 м2/г, 64 м2/г, 56 м2/г.
Аналогичным образом можно получать оксид ZnO, диспергированный в активированном угле (удельная площадь поверхности составляла приблизительно 1000 м2/г), графене (удельная площадь поверхности составляла приблизительно 500 м2/г) и углеродных нанотрубках (удельная площадь поверхности составляла приблизительно 300 м2/г) в качестве носителя (содержание диспергирующего средства в компоненте I составляло соответственно 5 вес. %, 30 вес. %, 60 вес. %); продукты соответственно определяли как дисперсные оксиды 7-9. У них удельная площадь поверхности составляла соответственно 177 м2/г, 245 м2/г и 307 м2/г.
2. Получение компонента II (молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE)
Указанное молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE содержит одномерные каналы, образованные десятичленными кольцами.
Кислота средней силы, указанная в настоящем изобретении, может быть проверена с применением спектра ядерного магнитного резонанса Н, TPD NH3, ИК-спектрометрии, химического титрования и т.п. в отношении твердых веществ. Тем не менее, способы проверки кислотности не ограничиваются вышеуказанными способами проверки.
Молекулярное сито согласно настоящему изобретению может представлять собой молекулярное сито с топологической структурой TON, или AEL, или MTT, или MRE, у которого плотность товарной кислоты соответствует требованиям настоящего изобретения, а также может представлять собой самостоятельно синтезированное молекулярное сито; в данном документе в качестве примера выбрано молекулярное сито, полученное методом гидротермального синтеза.
1) Молекулярное сито с топологической структурой AEL, конкретный способ получения которого является следующим.
Исходя из SiO2:Al2O3:H3PO4:R:H2O = 4:10:10:9:300 (соотношение по массе) для оксидов отвешивали сырье: золь кремниевой кислоты 30% (концентрация по массе); изопропилат алюминия; фосфорную кислоту; DPA и/или DIPA (R); деионизированную воду; после смешивания при комнатной температуре добавляли вспомогательную добавку HF в молярном количестве, которое составляет 0,5 от матричного средства; перемешивали при 30°C и выдерживали, через 2 ч. перемещали в сосуд для гидротермальной реакции, в котором при 200°C в течение 24 ч. обеспечивали кристаллизацию. Резко охлаждали до комнатной температуры на водяной бане, несколько раз промывали в центробежной мойке с получением надосадочной жидкости с pH, равным 7, после завершения промывания; осадок после горячей сушки в течение 17 ч. при 110°C прокаливали в течение 3 ч. в атмосфере воздуха с температурой 600°C с получением заполняемой неорганической твердой кислоты с кремнием, фосфором и алюминием, характеризующейся многоуровневой пористой структурой.
2) Молекулярное сито с топологической структурой TON, конкретный способ получения которого является следующим.
Исходя из SiO2:Al2O3:K2O:R:H2O = 70:1:7,5:25:500 (соотношение по массе) для оксидов отвешивали сырье: золь кремниевой кислоты 30% (концентрация по массе); сульфат алюминия; гидроксид калия; HDA (R); деионизированную воду; после смешивания при комнатной температуре добавляли вспомогательную добавку HF в молярном количестве, которое составляет 0,5 от матричного средства; перемешивали при 30°C и выдерживали, через 2 ч. перемещали в сосуд для гидротермальной реакции, в котором при 180°C в течение 48 ч. обеспечивали кристаллизацию. Резко охлаждали до комнатной температуры на водяной бане, несколько раз промывали в центробежной мойке с получением надосадочной жидкости с pH, равным 7, после завершения промывания; осадок после горячей сушки в течение 17 ч. при 110°C прокаливали в течение 3 ч. в атмосфере воздуха с температурой 600°C с получением молекулярного сита.
3) Молекулярное сито с топологической структурой MTT, конкретный способ получения которого является следующим.
0,4 г сульфата алюминия растворяли в 60,75 г воды; после добавления 0,26 г NaOH и 2,4 г пиридина добавляли 4,5 г белой сажи. После перемешивания в течение 2 ч. перемещали в футерованный тетрафторэтиленом сосуд для гидротермальной реакции и при 160 в течение 3 дней проводили кристаллизацию. Продукт, который подвергали центробежному отделению, промыванию, высушиванию и прокаливанию, снова подвергали центробежному отделению, промыванию, высушиванию и прокаливанию после того, как подвергали ионному обмену в течение 2 ч. в 1 М растворе нитрата аммония при 70 с получением продукта.
4) Молекулярное сито с топологической структурой MRE, конкретный способ получения которого является следующим.
С PMBr2 в качестве матричного средства 0,15 г нитрата алюминия растворяли в 17,93 г воды, добавляли 0,64 г 50 вес. % гидроксида натрия, после чего добавляли 1,24 г матричного средства. Наконец, добавляли 4,96 г TEOS (тетраэтилортосиликата) и перемешивали в течение 2 ч.; переносили 45 мл в сосуд для гидротермальной реакции и при 160 7 дней со скоростью вращения 37 об./мин. осуществляли кристаллизацию. Продукт после резкого охлаждения подвергали центробежному отделению, промыванию, высушиванию и прокаливанию. Аналогично его снова подвергали центробежному отделению, промыванию, высушиванию и прокаливанию после того, как подвергали ионному обмену в течение 2 ч. в 1 М растворе нитрата аммония при 70 с получением продукта.
Элементный состав каркаса указанного молекулярного сита с топологической структурой TON, или AEL, или MTT, или MRE может представлять собой один, два или более из Si-O, Si-Al-O, Si-Al-P-O, Al-P-O, Ga-P-O, Ga-Si-Al-O, Zn-Al-P-O, Mg-Al-P-O, Co-Al-P-O; элемент O частей каркаса соединен с H; соответствующие продукты последовательно определяли как части 1-6.
Таблица 3. Получение молекулярного сита с топологической структурой TON, или AEL, или MTT, или MRE и его рабочие параметры

2) H, соединенный с вышеуказанным элементом O каркаса в продуктах в виде частей 1-6, методом ионного обмена частично замещали следующими ионами металла: Na, Mg, K, Mn, Ag, Mo, Cr, Fe, Co, Ca, Pt, Pd, Ti, Zn, Ga, Ba и Ge; способ получения являлся следующим.
Исходя из SiO2:Al2O3:H3PO4:R:H2O=4:16:32:55:150, при этом R представляет собой матричное средство.
Сульфат алюминия смешивали с раствором гидроксида натрия; затем добавляли золь кремниевой кислоты, фосфорную кислоту, DPA и/или DIPA (R); деионизированную воду; перемешивали в течение 1 ч. с получением однородного исходного геля; затем его перемещали в реактор для синтеза под высоким давлением; после стационарной кристаллизации в течение 48 ч. при 190 подвергали резкому охлаждению, промыванию и высушиванию с получением образца молекулярного сита с топологической структурой AEL.
Исходя из SiO2:Al2O3:K2O:R:H2O=70:1:7,5:25:500, при этом R представляет собой матричное средство.
Сульфат алюминия смешивали с раствором гидроксида калия; затем добавляли золь кремниевой кислоты, HDA (R); деионизированную воду; перемешивали в течение 1 ч. с получением однородного исходного геля; затем его перемещали в реактор для синтеза под высоким давлением; после стационарной кристаллизации в течение 48 ч. при 190 подвергали резкому охлаждению, промыванию и высушиванию с получением образца молекулярного сита с топологической структурой TON.
Исходя из SiO2:Al2O3:Na2O:R:H2O=9:1:0,5:5:130, при этом R представляет собой матричное средство.
Сульфат алюминия растворяли в воде; затем добавляли NaOH, пиридин (R) и белую сажу; после перемешивания в течение 2 ч. перемещали в футерованный тетрафторэтиленом гидротермальный сосуд и при 160 в течение 3 дней осуществляли кристаллизацию. После центробежного отделения, промывания, высушивания и прокаливания продукта получали продукт в виде образца молекулярного сита с топологической структурой MTT.
Исходя из SiO2:Al2O3:Na2O:R:H2O=25:1:1,5:6:90, при этом R представляет собой матричное средство.
Нитрат алюминия смешивали с раствором гидроксида натрия; затем добавляли TEOS, PMBr2 (R), деионизированную воду; после перемешивания в течение 2 ч. его перемещали в реактор для синтеза под высоким давлением; после стационарной кристаллизации в течение 84 ч. при 160 подвергали резкому охлаждению, промыванию и высушиванию с получением образца молекулярного сита с топологической структурой MRE.
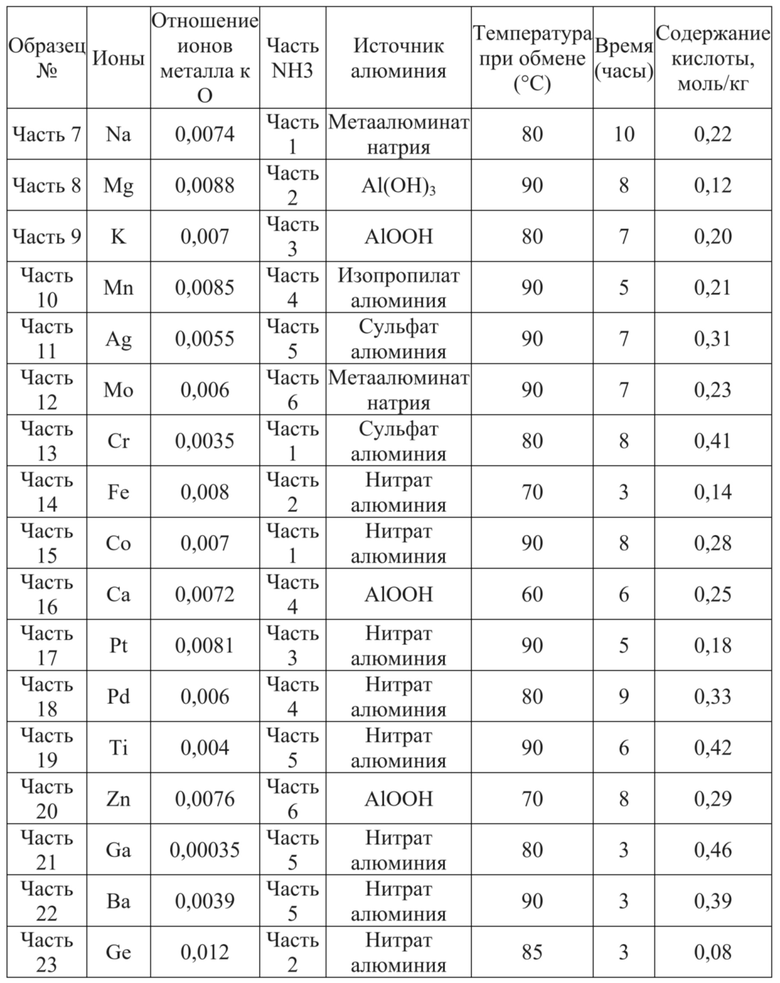
Брали вышеуказанные образцы; в соответствии с пропорцией, в которой соотношение по массе твердых и жидких веществ составляет 1:30, их смешивали с раствором соли азотной кислоты, содержащим ионы металла, предназначенные для обмена, в количестве 0,5 моль/л; при 80°C перемешивали в течение 6 ч., промывали, подвергали горячей сушке, что последовательно повторяли 2 раза; при температуре 550 градусов прокаливали в течение 3 ч. и получали TON, или AEL, или MTT, или MRE, содержащие ионы металла в результате обмена. Соответствующие продукты соответственно определяли как части 7-23.
Таблица 4. Получение молекулярного сита с топологической структурой TON, или AEL, или MTT, или MRE и его рабочие параметры
3) Молекулярное сито с другим элементным составом

3. Получение катализатора
Компонент I и компонент II в необходимых пропорциях добавляли в сосуд; используя одну, две или более из силы сжатия, силы удара, силы резания, силы трения и т. д., вызванных быстрым движением этих материалов и/или сосуда, обеспечивали выполнение отделения, разбивания, равномерного перемешивания и др.; путем изменения температуры и атмосферы газа-носителя осуществляли преобразование механической энергии, тепловой энергии и химической энергии и дополнительно регулировали взаимодействие разных компонентов.
В процессе механического перемешивания температура перемешивания может быть установлена на уровне 20-100°C, и способ может проводиться в определенной атмосфере или непосредственно в атмосфере воздуха, при этом в качестве атмосферы выбран любой из следующих газов:
a) азот и/или инертный газ;
b) смесь газов водорода с азотом и/или инертным газом, при этом объем водорода в смеси газов составляет 5-50%;
c) смесь газов CO с азотом и/или инертным газом, при этом объем CO в смеси газов составляет 5-20%;
d) смесь газов из O2 с азотом и/или инертным газом, при этом объем O2 в смеси газов составляет 5-20%; указанный инертный газ представляет собой один, два или более из гелия, аргона и неона.
Механическое перемешивание для объединения компонентов может предусматривать одно, два или более из механического смешивания, перемешивания при измельчении в шаровой мельнице, перемешивания во встряхивающем устройстве и перемешивания при механическом растирании, в частности, следующее.
Механическое смешивание: в мешалке посредством перемешивающих лопастей осуществляют смешивание компонента I с компонентом II, при этом путем регулирования времени перемешивания (от 5 мин. до 120 мин.) и частоты вращения (30-300 об./мин.) можно регулировать степень перемешивания компонента I и компонента II и относительное расстояние.
Перемешивание при измельчении в шаровой мельнице: катализатор быстро перемешивают в размольной емкости с применением размольных тел, при этом катализатор подвергается сильным ударам и раздавливанию, что приводит к измельчению и смешиванию компонентов I и II. Проводили контроль размольных тел (могут быть выполнены из нержавеющей стали, агата, кварца; с диапазоном размера от 5 мм до 15 мм) и на основании их отношения к катализаторам (диапазон отношения по массе - 20-100:1) в отношении катализаторов можно регулировать размер частиц и относительное расстояние.
Перемешивание во встряхивающем устройстве: компонент I и компонент II предварительно смешивают и помещают в сосуд; путем регулирования возвратно-поступательных вибраций или круговых вибраций встряхивающего устройства осуществляют смешивание компонента I с компонентом II, при этом путем регулирования скорости (в диапазоне 1-70 об./мин.) и времени (в диапазоне от 5 мин. до 120 мин.) вибрирования осуществляют их равномерное смешивание и регулирование относительного расстояния между ними.
Механическое растирание: компонент Ⅰ и компонент Ⅱ предварительно смешивали и помещали в сосуд; при определенном давлении (в диапазоне от 5 килограмм до 20 килограмм) посредством растирающего устройства обеспечивали относительное перемещение перемешанных катализаторов (число оборотов в диапазоне 30-300 об./мин.) с осуществлением регулирования размера частиц и относительного расстояния в отношении катализаторов, а также с осуществлением равномерного смешивания.
Конкретный способ получения катализатора и его рабочие параметры представлены в таблице 6.
Таблица 6. Получение катализатора и его рабочие параметры



Пример каталитической реакции
В качестве примера рассмотрена реакция в неподвижном слое, но катализатор также используется в реакторе с подвижным слоем. Установка оснащена устройством измерения массового расхода газа и хроматографом для анализа продукта в непрерывном режиме (отходящий газ из реактора непосредственно попадает в дозирующий клапан хроматографа, и осуществляется циклический анализ образцов в реальном времени).
Помещали 2 г вышеуказанного катализатора согласно настоящему изобретению в реактор с неподвижным слоем; заменяли воздух в реакторе атмосферой Ar; затем в атмосфере H2 нагревали до 300°C и подавали синтез-газ (молярное отношение H2/CO = 0,2-3,5), при этом давление синтез-газа составляло 0,5-10 МПа; нагревали до температуры реакции 300-600°C; регулировали объемную скорость исходного газа для реакции до 300-12000 мл/г/ч. Полученный продукт анализировали в непрерывном режиме с помощью хроматографии.
Изменение температуры, давления, объемной скорости и молярного отношения H2/CO в синтез-газе может изменить характеристики реакции. При этом селективность в отношении жидкого топлива, полученного из C5-C11, может достигать 50-80%; поскольку гидрирующая активность поверхности соединений металлов в катализаторе является невысокой, предотвращается образование большого количества метана, поэтому селективность в отношении метана является низкой. В таблице 7 приведены данные в отношении конкретного применения катализаторов и его результатов.
Таблица 7. Данные в отношении конкретного применения катализаторов и его результатов

 В сравнительном образце 1 компонент A катализатора представляет собой ZnO3, а компонент B представляет собой MOR, предлагаемый к приобретению компанией «Шеньтань», который характеризуется одномерными каналами, образованными восьмичленными кольцами и двенадцатичленными кольцами.
В сравнительном образце 1 компонент A катализатора представляет собой ZnO3, а компонент B представляет собой MOR, предлагаемый к приобретению компанией «Шеньтань», который характеризуется одномерными каналами, образованными восьмичленными кольцами и двенадцатичленными кольцами.
В сравнительном образце 2 используемое в катализаторе молекулярное сито представляет собой имеющийся в продаже продукт ZSM-12, который характеризуется прямыми одномерными каналами, образованными двенадцатичленными кольцами.
В сравнительном образце 3 используемое в катализаторе молекулярное сито представляет собой имеющийся в продаже продукт SAPO-34, который характеризуется трехмерными пересекающимися каналами и диаметром отверстия, образованного восьмичленными кольцами.
В сравнительном образце 4 используемое в катализаторе молекулярное сито представляет собой имеющийся в продаже продукт ZSM-5, который характеризуется трехмерной топологической структурой с десятичленными кольцами.
В сравнительном образце 5 используемое в катализаторе молекулярное сито представляет собой имеющийся в продаже продукт ZSM-35 с топологической структурой, в которой имеются как восьмичленные кольца, так и десятичленные кольца для образования двухмерной структуры.
В сравнительном образце 6 используемое в катализаторе молекулярное сито представляет собой имеющийся в продаже продукт MCM-22, который характеризуется двухмерной топологической структурой с десятичленными кольцами.
В сравнительном образце 7 используемое в катализаторе молекулярное сито представляет собой имеющийся в продаже продукт ZSM-11, который характеризуется трехмерной топологической структурой с десятичленными кольцами.
Результаты реакции со сравнительными образцами 1-7 говорят о том, что молекулярные сита с разной топологической структурой явно влияют на селективность в отношении продукта. В случае имеющихся в продаже молекулярных сит MOR, в которых имеются как восьмичленные кольца, так и двенадцатичленные кольца для образования одномерной структуры, основным продуктом в целом являются углеводороды с короткой цепью (C2-C4), тогда как селективность в отношении продукта с длинной цепью относительно низкая. Несмотря на то что в случае ZSM-12 с двенадцатичленными кольцами для образования одномерной структуры в продукте селективность в отношении бензина также относительно высокая, содержание ароматических углеводородов в бензине, тем не менее, сравнительно высокое (>40%). ZSM-35, в котором имеются как восьмичленные кольца, так и десятичленные кольца для образования двухмерной структуры, и SAPO-34 с трехмерной структурой, содержащей восьмичленные кольца, не способствуют образованию C5-алканов или выше и подходят для продуктов в виде углеводородов с короткой цепью. Кроме того, несмотря на то что MCM-22 с двухмерными каналами, образованными десятичленными кольцами, а также ZSM-5 с трехмерными каналами, образованными десятичленными кольцами, и молекулярное сито ZSM-11 подходят для получения бензиновой фракции, селективность в отношении ароматических углеводородов в бензине, тем не менее, высокая (>50%). Только молекулярные сита с топологической структурой типа TON, или AEL, или MTT, или MRE с одномерными каналами, образованными десятичленными кольцами, подходят для получения бензина с низким содержанием ароматических углеводородов.
В сравнительном образце 8 компонент I катализатора представляет собой ZnO4, при этом удельная площадь поверхности сравнительно низкая (<1 м2/г), а компонент II представляет собой часть 1, при этом степень конверсии CO сравнительно низкая и активность во время реакции сравнительно низкая, поэтому удельная площадь поверхности оксида слишком мала, что не способствует осуществлению реакции.
Катализатор, используемый в сравнительном образце 9, содержит только компонент I в виде ZnO1 и не содержит образца молекулярного сита с топологической структурой TON, или AEL, или MTT, или MRE, при этом степень конверсии при реакции сравнительно низкая, а основной продукт в целом представлен диметиловым эфиром, метаном и другими побочными продуктами, и при этом жидкое топливо почти не образуется.
Катализатор, который применяли в качестве сравнительного образца 10, содержал только молекулярное сито в качестве компонента II и не содержал образца компонента I; каталитическая реакция практически не является активной.
Сравнительные образцы 9 и 10 указывают на то, что результаты реакции являются очень низкими, если применяют только компонент I или компонент II, и совершенно не обладают отличными характеристиками реакции, как у настоящего изобретения.
Из приведенных выше таблиц можно понять структуру молекулярного сита, в том числе топологическую структуру TON, или AEL, или MTT, или MRE, а также концентрацию кислот и содержание кислот; кроме того, крайне важным является сочетание оксида металла с молекулярным ситом, поскольку оно непосредственно влияет на степень конверсии монооксида углерода и селективность в отношении жидкого топлива.
| название | год | авторы | номер документа |
|---|---|---|---|
| СМЕШАННЫЙ КАТАЛИЗАТОР, МОДИФИЦИРОВАННЫЙ ОРГАНИЧЕСКИМ ОСНОВАНИЕМ, И СПОСОБ ПОЛУЧЕНИЯ ЭТИЛЕНА ПУТЕМ ГИДРИРОВАНИЯ МОНООКСИДА УГЛЕРОДА | 2019 |
|
RU2749513C1 |
| КАТАЛИЗАТОР И СПОСОБ ПРЯМОЙ КОНВЕРСИИ СИНТЕЗ-ГАЗА ДЛЯ ПОЛУЧЕНИЯ МАЛОУГЛЕРОДИСТЫХ ОЛЕФИНОВ | 2019 |
|
RU2758849C1 |
| КАТАЛИТИЧЕСКИЙ ВЫСОКОСЕЛЕКТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВ С НИЗКИМ ЧИСЛОМ АТОМОВ УГЛЕРОДА С ПРИМЕНЕНИЕМ ЛЕГИРОВАННОГО ГЕТЕРОАТОМАМИ МОЛЕКУЛЯРНОГО СИТА И СИНТЕЗ-ГАЗА | 2019 |
|
RU2778293C1 |
| Катализатор изодепарафинизации углеводородного сырья С10+ для получения низкозастывающих масел и дизельных топлив и способ получения низкозастывающих масел и топлив с его использованием | 2016 |
|
RU2627770C1 |
| КАТАЛИЗАТОР И СПОСОБ ПРЯМОЙ КОНВЕРСИИ СИНТЕЗ-ГАЗА ДЛЯ ПОЛУЧЕНИЯ МАЛОУГЛЕРОДИСТЫХ ОЛЕФИНОВ | 2018 |
|
RU2736729C1 |
| Способ получения катализатора для изодепарафинизации дизельных фракций нефти | 2020 |
|
RU2734969C1 |
| Катализатор изодепарафинизации углеводородного сырья и способ его получения | 2021 |
|
RU2764599C1 |
| КАТАЛИЗАТОР ГИДРОИЗОМЕРИЗАЦИИ | 2018 |
|
RU2780344C2 |
| Способ получения базового масла | 2021 |
|
RU2781062C1 |
| Способ получения катализатора изодепарафинизации дизельных фракций для использования в каталитической системе, состоящей из катализаторов гидроочистки и изодепарафинизации и катализатор, полученный этим способом | 2020 |
|
RU2739566C1 |
Изобретения относятся к конверсии синтез-газа. Описан катализатор для прямой конверсии синтез-газа для получения жидкого топлива, который содержит компонент Ⅰ и компонент Ⅱ; указанные компонент Ⅰ и компонент Ⅱ объединены друг с другом путем механического перемешивания; активная составляющая компонента Ⅰ представляет собой оксид металла, а компонент II представляет собой молекулярное сито с одномерными каналами, образованными десятичленными кольцами; указанный оксид металла представляет собой один, два или более из MnOx, MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnO, ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CeO2, CoAlyO(1+1,5y), FeAlyO(1+1,5y), Ga2O3, Bi2O3, In2O3, InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z); диапазон значений указанного x составляет 1-3,5; диапазон значений y составляет 0,1-10; диапазон значений z составляет 0,1-10; удельная площадь поверхности указанных MnOx, ZnO, CeO2, Ga2O3, Bi2O3, In2O3 составляет 1-100 м2/г;
удельная площадь поверхности указанных MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CoAlyO(1+1,5y), FeAlyO(1+1,5y), InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z) составляет 5-150 м2/г; при этом указанное молекулярное сито представляет собой молекулярное сито с топологической структурой TON, AEL, MTT или MRE, и представляет собой одно из SAPO-11, ZSM-23 или ZSM-48. Описан способ прямой конверсии синтез-газа для получения жидкого топлива, в котором синтез-газом в качестве сырья для реакции в условиях неподвижного слоя или подвижного слоя проводят реакцию конверсии, при этом применяют указанный выше катализатор. Технический результат-получение жидкого топлива с пониженным содержанием ароматических соединений. 2 н. и 19 з.п. ф-лы, 7 табл., 2 пр.
1. Катализатор для прямой конверсии синтез-газа для получения жидкого топлива, отличающийся тем, что указанный катализатор содержит компонент Ⅰ и компонент Ⅱ; указанные компонент Ⅰ и компонент Ⅱ объединены друг с другом путем механического перемешивания; активная составляющая компонента Ⅰ представляет собой оксид металла, а компонент II представляет собой молекулярное сито с одномерными каналами, образованными десятичленными кольцами; указанный оксид металла представляет собой один, два или более из MnOx, MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnO, ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CeO2, CoAlyO(1+1,5y), FeAlyO(1+1,5y), Ga2O3, Bi2O3, In2O3, InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z); диапазон значений указанного x составляет 1-3,5; диапазон значений y составляет 0,1-10; диапазон значений z составляет 0,1-10;
удельная площадь поверхности указанных MnOx, ZnO, CeO2, Ga2O3, Bi2O3, In2O3 составляет 1-100 м2/г;
удельная площадь поверхности указанных MnCryO(x+1,5y), MnAlyO(x+1,5y), MnZryO(x+2y), MnInyO(x+1,5y), ZnCryO(1+1,5y), ZnAlyO(1+1,5y), ZnGayO(1+1,5y), ZnInyO(2+1,5y), CoAlyO(1+1,5y), FeAlyO(1+1,5y), InyAlzMnO(x+1,5y+1,5z), InyGazMnO(x+1,5y+1,5z) составляет 5-150 м2/г;
при этом указанное молекулярное сито представляет собой молекулярное сито с топологической структурой TON, AEL, MTT или MRE, и представляет собой одно из SAPO-11, ZSM-23 или ZSM-48.
2. Катализатор по п. 1, отличающийся тем, что элементный состав каркаса указанного молекулярного сита представляет собой один, два или более из Si-O, Si-Al-O, Si-Al-P-O, Al-P-O, Ga-P-O, Ga-Si-Al-O, Zn-Al-P-O, Mg-Al-P-O, Co-Al-P-O.
3. Катализатор по п. 1, отличающийся тем, что весовое отношение активной составляющей в компоненте Ⅰ к компоненту Ⅱ составляет 0,1-20.
4. Катализатор по п. 1, отличающийся тем, что весовое отношение активной составляющей в компоненте Ⅰ к компоненту Ⅱ составляет 0,3-5.
5. Катализатор по п. 1, отличающийся тем, что в указанный компонент Ⅰ также добавлено диспергирующее средство, при этом оксид металла диспергирован в диспергирующем средстве; указанное диспергирующее средство представляет собой одно, два или более из Al2O3, SiO2, Cr2O3, ZrO2, TiO2, Ga2O3, активированного угля, графена и углеродных нанотрубок.
6. Катализатор по п. 1, отличающийся тем, что указанное молекулярное сито с топологической структурой AEL содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,05-0,5 моль/кг; при этом диапазон значений температуры, которому соответствуют пики в виде десорбционных пиков указанных кислот средней силы по TPD NH3, составляет 200-500°С; при применении ацетона в качестве молекулярного зонда химический сдвиг 13C-ЯМР находится в диапазоне 210-220 ppm.
7. Катализатор по п. 6, отличающийся тем, что указанное молекулярное сито с топологической структурой AEL содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,05-0,4 моль/кг.
8. Катализатор по п. 6, отличающийся тем, что указанное молекулярное сито с топологической структурой AEL содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,05-0,3 моль/кг.
9. Катализатор по п. 6, отличающийся тем, что указанное молекулярное сито характеризуется топологической структурой TON, MTT или MRE и содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,005-0,6 моль/кг.
10. Катализатор по п. 6, отличающийся тем, что указанное молекулярное сито характеризуется топологической структурой TON, MTT или MRE и содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,005-0,4 моль/кг.
11. Катализатор по п. 6, отличающийся тем, что указанное молекулярное сито характеризуется топологической структурой TON, MTT или MRE и содержит кислотные центры средней силы, при этом количество кислотных центров средней силы составляет 0,005-0,2 моль/кг.
12. Катализатор по п. 2, отличающийся тем, что элемент O каркаса молекулярного сита может быть соединен или не соединен с H; и указанный H посредством метода ионного обмена может быть полностью или частично замещен одним, двумя или более из Na, Mg, K, Mn, Ag, Mo, Cr, Fe, Co, Ca, Pt, Pd, Ti, Zn, Ga, Ba, Ge, при этом после замещения общее молярное отношение металла к кислороду составляет 0,0002-0,02.
13. Катализатор по п. 5, отличающийся тем, что в указанном компоненте Ⅰ содержание диспергирующего средства составляет 0,05-90 вес. %, а остальное представляет собой оксид металла.
14. Способ прямой конверсии синтез-газа для получения жидкого топлива, отличающийся тем, что с синтез-газом в качестве сырья для реакции в условиях неподвижного слоя или подвижного слоя проводят реакцию конверсии, при этом применяемый катализатор представляет собой катализатор по любому из пп. 1-13.
15. Способ по п. 14, отличающийся тем, что давление указанного синтез-газа составляет 0,5-10 МПа; температура реакции составляет 300-600°C; объемная скорость составляет 300-12000 ч.-1, указанный синтез-газ представляет собой смесь газов H2/CO; отношение H2/CO составляет 0,2-3,5.
16. Способ по п. 15, отличающийся тем, что давление указанного синтез-газа составляет 1-8 МПа.
17. Способ по п. 15, отличающийся тем, что температура реакции составляет 320-450°C.
18. Способ по п. 15, отличающийся тем, что объемная скорость составляет 1000-9000 ч.-1.
19. Способ по п. 15, отличающийся тем, что объемная скорость составляет 3000-9000 ч.-1.
20. Способ по п. 15, отличающийся тем, что отношение H2/CO составляет 0,3-2,5.
21. Способ по п. 14, отличающийся тем, что в указанном способе с синтез-газом в качестве сырья для реакции путем одноэтапной прямой конверсии получают жидкое топливо, при этом селективность в отношении жидкого топлива может достигать 50-80%; селективность в отношении ароматических C5-C11-углеводородов составляет менее 40%; при этом селективность в отношении метана как побочного продукта составляет менее 15%.
| СИНТЕЗ ЖИДКОГО ТОПЛИВА И ХИМИЧЕСКИХ РЕАКТИВОВ ИЗ КИСЛОРОДСОДЕРЖАЩИХ УГЛЕВОДОРОДОВ | 2008 |
|
RU2472840C2 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПОЛИМЕРИЗАЦИИ МОНОМЕРОВ | 1999 |
|
RU2251453C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ И МОДИФИКАЦИИ ЭЛЕКТРОХИМИЧЕСКИХ КАТАЛИЗАТОРОВ НА УГЛЕРОДНОМ НОСИТЕЛЕ | 2015 |
|
RU2595900C1 |
| КОБАЛЬТ-МОЛИБДЕНОВЫЙ КАТАЛИЗАТОР НА УГЛЕРОДНОЙ ПОДЛОЖКЕ | 2012 |
|
RU2598844C2 |
| WO 2018103603 A1, 14.06 | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| CN 106947511 А, 14.07.2017 | |||
| CN 107971026 А, 01.05.2018 | |||
| Автоматический железнодорожный тормоз с электромагнитным управлением | 1930 |
|
SU26722A1 |
| Приспособление для обрезки обвертки и стеблей ворсовальных шишек | 1930 |
|
SU28645A1 |
Авторы
Даты
2022-05-19—Публикация
2019-12-10—Подача